Impuretés de nitrosamine dans les médicaments : Méthodes d'analyses et résultats des analyses
Sur cette page
- Méthode d'analyse pour les sartans ou antagoniste des récepteurs de l'angiotensine II (ARA)
- Méthode d'analyse pour les produits contenant de la ranitidine
- Méthodes d'analyse pour les produits contenant de la metformine
- Résultats des analyses pour les sartans ou récepteurs de l'angiotensine II (ARBs)
- Résultats pour les ranitidines
- Résulats des analyses pour les produits de metformine
Les méthodes d'analyses suivantes ont été élaborées par Santé Canada et peuvent servir d'option analytique potentielle pour les organismes de réglementation et l'industrie afin de détecter les impuretés de nitrosamines dans certaines substances et certains produits pharmaceutiques. Ces méthodes doivent être validées par l'utilisateur si les données résultantes sont utilisées pour étayer une évaluation de la qualité de l'IPA ou du produit pharmaceutique requise, ou si les résultats sont utilisés dans une présentation réglementaire. Les méthodes sont susceptibles d'être modifiées à mesure que de nouveaux renseignements sont disponibles.
Méthode d'analyse pour les sartans ou antagonistes des récepteurs de l'angiotensine II (ARA)
Détection de la N-Nitrosodiméthylamine (NDMA) et de la N-Nitrosodiéthylamine (NDEA) par GC-MS/MS (injection directe) dans les produits finis et les substances médicamenteuses de la classe des sartans
1. Principe et portée
La présente méthode a été dévelopée afin de détecter et quantifier les impuretés nitrosamine N-nitrosodiméthylamine (NDMA) et N-nitrosodiéthylamine (NDEA) dans les produits finis de valsartan, irbésartan et losartan. Cette méthode est effectuée par un chromatographe en phase gazeuse couplé à un spectromètre de masse en tandem (GC-MS/MS) à injection directe.
La méthode peut également être utilisée pour détecter et quantifier la NDMA et la NDEA dans les produits finis de candersartan et olmésartan et les substances médicamenteuses de sartans (par ex. valsartan, ibésartan, losartan, candesartan et olmésartan). Par contre, s'il y a des interférences d'observer, une validation supplémentaire serait requise.
2. Réactifs et étalons de référence
- Méthanol grade HPCL MeOH (nº du CAS : 67-56-1)
- NDMA : Solution de N-Nitrosodiméthylamine (5000 μg/mL dans du méthanol; nº du CAS : 62-75-9)
- NDEA : Solution de N-Nitrosodiéthylamine, (100 μg/mL dans du méthanol; nº du CAS : 55-18-5)
- Solution de NDMA-d6 : Solution de N-nitrosodiméthylamine-d6 (1000 μg/mL dans du méthanol; nº du CAS : 17829-05-9)
3. Instruments et équipements
- Agilent GC 7890A avec MSMS 7000 avec source EI source ou l'équivalent
- Agilent DB-624 25 m x 0.32 μm 1.8 μm ou l'équivalent
- Vials pour CG ambrés de 2 mL à bouchon fileté et membrane de PTFE/silicone
- Tubes en verre filetés de 20 x 125 mm avec bouchons vissables
- Pipettes automatiques, volumes variés
- Balance à chargement supérieur d'une précision de ± 0,01 g et balance analytique permettant une lecture à ± 0,0001 g
- Ballons volumétriques (catégorie A), volumes variés ou l'équivalent
- Pipettes Pasteur et poires à pipette
- Spatule
- Vials ambrés en verre de 15 mL avec bouchon
- Vials ambrés en verre de 40 mL avec bouchon
- Mélangeur Vortex, à un et à plusieurs tubes
- Supports pour vials et supports de rangement
- Chiffons Kimwipe
- Mortier et pilon
- Bain à ultrason
- Centrifugeuse, Beckmann-Coulter Allegra X-15R ou équivalente
4. Préparation des solutions
Solutions étalons
- Solutions étalons de référence (telles qu'achetées)
-
- Solution étalon de NDMA dans du méthanol (5000 ppm)
- Solution étalon de NDEA dans du méthanol (100 ppm)
- Solution étalon interne (telle qu'achetée)
-
- Solution étalon de NDMA-d6 dans du méthanol (1000 ppm)
Solutions étalons diluées
- Solution étalon de NDMA (200 ppm) :
-
Transférer 800 μL de solution étalon de référence de NDMA (5000 ppm) dans un ballon volumétrique de 20 mL, diluer jusqu'à la jauge avec du méthanol.
- Solution étalon diluée (NDMA : 40 ppm, NDEA : 20 ppm) :
-
Transférer 800 μL de solution étalon de NDMA (200 ppm) et 800 μL de solution étalon de NDEA (100 ppm) dans un ballon volumétrique de 4 mL, diluer jusqu'à la jauge avec du méthanol.
- Solution-étalon interne-1 (20 ppm) :
-
Transférer 500 μL de solution étalon de NDMA-d6 (1000 ppm) dans un ballon volumétrique de 25 mL, diluer jusqu'à la jauge avec du méthanol.
- Solution-étalon interne-2 (0,2 ppm) :
-
Transférer 5 μL de solution étalon de NDMA-d6 (20 ppm) dans un ballon volumétrique de 500 mL, diluer jusqu'à la jauge avec du méthanol.
Solutions d'étalonnage
- STD-12 :
-
Transférer 500 μL de solution étalon diluée (NDMA : 40 ppm, NDEA : 20 ppm) et 50 μL de solution étalon interne-1 (20 ppm) dans un ballon volumétrique de 5 mL, diluer au volume avec du méthanol. Bien mélanger.
- STD-7 :
-
Transférer 1000 μL de STD-12 dans un ballon volumétrique de 20 mL, diluer au volume avec la solution étalon interne-2 (0,2 ppm). Bien mélanger. Cette solution servira à effectuer l'évaluation de la performance du système et la vérification de la dérive du système.
- STD-11 :
-
Dilution 1:1 de STD-12 avec la solution étalon interne-2
- STD-10 :
-
Dilution 1:1 de STD-11 avec la solution étalon interne-2
- STD-9 :
-
Dilution 1:1 de STD-10 avec la solution étalon interne-2
- STD-8 :
-
Dilution 3:2 de STD-9 avec la solution étalon interne-2
- STD-6 :
-
Dilution 1:1 de STD-7 avec la solution étalon interne-2
- STD-5 :
-
Dilution 1:1 de STD-6 avec la solution étalon interne-2
- STD-4 :
-
Dilution 2:3 de STD-5 avec la solution étalon interne-2
- STD-3 :
-
Dilution 1:1 de STD-4 avec la solution étalon interne-2
- STD-2 :
-
Dilution 1:1 de STD-3 avec la solution étalon interne-2
- STD-1 :
-
Dilution 2:3 de STD-2 avec la solution étalon interne-2
| Description | Concentration de NDMA (µg/mL) | Concentration de NDEA (µg/mL) | Concentration de NDMA-d6 (µg/mL) |
|---|---|---|---|
| STD-1 | 0,002 | 0,001 | 0,2 |
| STD-2 | 0,005 | 0,0025 | 0,2 |
| STD-3 | 0,01 | 0,005 | 0,2 |
| STD-4 | 0,02 | 0,01 | 0,2 |
| STD-5 | 0,05 | 0,025 | 0,2 |
| STD-6 | 0,1 | 0,05 | 0,2 |
| STD-7 | 0,2 | 0,1 | 0,2 |
| STD-8 | 0,3 | 0,15 | 0,2 |
| STD-9 | 0,5 | 0,25 | 0,2 |
| STD-10 | 1 | 0,5 | 0,2 |
| STD-11 | 2 | 1 | 0,2 |
| STD-12 | 4 | 2 | 0,2 |
Pour la NDMA, les solutions STD-1 à STD-6 sont utilisées pour la plage de travail allant de 0,002 à 0,1 µg/mL; les solutions STD-6 à STD-12 sont utilisées pour la plage de travail allant de 0,1 à 4,0 µg/mL.
Pour la NDEA, les solutions STD-1 à STD-5 sont utilisées pour la plage de travail allant de 0,001 à 0,025 µg/mL; les solutions STD-5 à STD-11 sont utilisées pour la plage de travail allant de 0,025 à 1,0 µg/mL.
Les plages de travail de la NDMA et de la NDEA peuvent être ajustées au besoin.
Préparation des échantillons
Pour les produits finis :
Peser au minimum 20 comprimés et calculer le poids moyen d'un comprimé. Moudre au minimum 20 comprimés en une poudre fine à l'aide du mortier et du pilon.
Préparer trois réplicats par échantillon. Peser précisément l'équivalent de 250 mg d'ingrédient pharmaceutique actifde la poudre d'échantillon homogénéisée dans un tube en verre fileté à fond rond.
À l'aide d'une pipette automatique, ajouter 5 mL de solution étalon interne-2 de NDMA-d6 à chaque tube d'échantillon. Bien refermer les tubes, soumettre à l'ultrason pendant 5 minutes, puis déposer le support de tubes dans l'agitateur vortex à tubes multiples et agiter à 2000 rpm pendant 5 minutes. Centrifuger les tubes pendant au moins 5 minutes à 1500 rpm. Délicatement, retirer les tubes de la centrifugeuse. À l'aide d'une pipette Pasteur, transférer un aliquot de chaque tube dans un vial GC en verre de 2 mL.
Remarque : La précision de la méthode a été évaluée par des études de récupération. Les valsartan, irbésartan et losartan dans les produits finis ont été ensemencés avec une solution d'étalon de référence de la façon suivante :
- Pour les échantillons contenant de la NDMA à un taux supérieur à 0,3 ppm ou de la NDEA à un taux supérieur à 0,08 ppm :
-
Ensemencer la solution d'échantillon avec la solution étalon qui correspond le mieux à celle de l'échantillon et calculer la récupération.
- Pour les échantillons contenant de la NDMA à un taux inférieur à 0,3 ppm ou de la NDEA à un taux inférieur à 0,08 ppm :
-
Ensemencer la solution de l'échantillon avec la solution STD-3 (1:1) afin d'obtenir une solution contenant 0,05 ppm de la NDMA et 0,025 ppm de la NDEA. Vérifier le ratio signal/bruit et calculer la limite de détection (LOD) et la limite de quantification (LOQ).
Pour les substances médicamenteuses :
Préparer trois échantillons de chaque substance. Peser précisément 250 mg de la poudre homogénéisée de l'échantillon dans un tube fileté à fond rond en verre.
Continuer la préparation selon les instructions pour les produits finis ci-dessus. Il est recommandé d'ensemencer l'échantillon pour déterminer la précision de la méthode.
5. Paramètres de fonctionnement des instruments :
Paramètres suggérés pour le GC :
Paramètres de l'injecteur :
- Mode d'injection :
- Injecteur « pulsed splitless »
- Température d'injecteur :
- 240 °C
- Débit :
- 1,8 mL/min
- Débit de vidange de la membrane (septum) :
- 3 mL/min
- Débit de vidange :
- 50 mL/min après 0,75 minute
- Volume d'injection :
- 2,0 µL
- Programmation du four :
- Température initiale : 60 °C
Attente : 2 min
| No de rail (ramp #) |
Débit (°C/min) (Rate) |
Température finale (°C) | Durée d'attente (minutes) |
|---|---|---|---|
| 1 | 5 | 130 | 0 |
| 2 | 40 | 240 | 5 |
Durée totale : 24 min
Paramètres suggérés pour le détecteur MS
- Ligne de transfert de la MS (température auxiliaire) :
- 250 °C
- Source d'ions :
- EI
- Température de la source :
- 250 °C
- Délai du solvant :
- 6 min
- Temps d'arrêt :
- 15 min
- Gaz d'injection (quench gas):
- Hélium à 2,25 mL/min
- Gaz de collision :
- Azote à 1,5 mL/min
| Analyte | Temps de rétention (minutes) | Segment | Fenêtre du temps de rétention (minutes) | Ion précurseur (m/z) | Ion produit (m/z) | CE (V) |
Résolution | Temporisation (ms) (dwell) |
|---|---|---|---|---|---|---|---|---|
| NDMA-d6 (étalon interne) | 7,8 | 1 | 7,5-8,1 | 80 | 50 | 5 | Étendue / étendue | 100 |
| NDMA | 7,8 | 1 | 7,5-8,1 | 74 | 42 | 15 | Étendue / étendue | 100 |
| 74 | 44 | 4 | 100 | |||||
| NDEA | 12,7 | 2 | 12,4-13,0 | 102 | 44 | 12 | Étendue / étendue | 150 |
| 102 | 85 | 2 | 150 |
6. Performance du système
Le coefficient de détermination (R2) de chaque courbe d'étalonnage est d'au moins 0,995.
Le ratio signal/bruit de la solution STD-1 (NDMA = 0,002 µg/mL; NDEA = 0,001 µg/mL) devrait être au moins 10.
7. Calculs
Établir les courbes d'étalonnage pour la NDMA et la NDEA en utilisant le ratio de facteur de réponse (surface du pic de NDMA ou NDEA divisée par la surface du pic de l'étalon interne) par rapport à la concentration étalon (µg/mL). À l'aide des pentes et ordonnées à l'origine des courbes d'étalonnage, déterminer la teneur en NDMA et en NDEA de chaque échantillon en fonction de l'équation suivante.
Pour les produits finis :
Les résultats, en ppm relatif à la quantité déclarée de la substance médicamenteuse sartan dans le produit, sont calculés comme suit :
Équation 1
![(ppm) = [(y-b)÷m] x AVGwt x V ÷ Wtspl ÷ LC](/content/dam/hc-sc/images/services/drug-and-health-products/compliance-enforcement/information-health-product/nitrosamine-impurities/test-methods/math1.jpg)
Où,
- y =
- rapport de la surface du pic de NDMA ou de NDEA à la surface du pic de NDMA-d6
- b =
- ordonnée à l'origine de la courbe linéaire
- m =
- pente de la courbe linéaire
- AVGwt =
- poids moyen d'un comprimé (g)
- V =
- 5 mL (volume)
- Wtspl =
- poids de l'échantillon (g)
- LC =
- quantité déclarée sur l'étiquette (g) de l'échantillon
Description textuel
Parties par million est égale à y moins b sur m, qui représente la différence entre le rapport de la surface du pic d'impureté à la surface du pic de l'étalon interne moins l'ordonnée à l'origine de la courbe linéaire sur la pente de la courbe linéaire. Cette valeur est multipliée par le poids moyen d'un comprimé, ensuite multipliée par le volume, divisée par le poids de l'échantillon et ensuite divisée par la quantité déclarée sur l'étiquette de l'échantillon.
Pour les substances médicamenteuses :
Les résultats, en ppm relatif à la substance médicamenteuse testée, sont calculés comme suit :
Équation 2
![(ppm) = [(y-b)÷m] x V ÷ Wtspl](/content/dam/hc-sc/images/services/drug-and-health-products/compliance-enforcement/information-health-product/nitrosamine-impurities/test-methods/math2.jpg)
Où,
- y =
- rapport de la surface du pic de NDMA ou de NDEA à la surface du pic de NDMA-d6
- b =
- ordonnée à l'origine de la courbe linéaire
- m =
- pente de la courbe linéaire
- Wtspl =
- poids de l'échantillon (g)
- V =
- 5 mL (volume)
Description textuel
Parties par million est égale à y moins b sur m, qui représente la différence entre le rapport de la surface du pic d'impureté à la surface du pic de l'étalon interne moins l'ordonnée à l'origine de la courbe linéaire sur la pente de la courbe linéaire. Cette valeur est multipliée par le volume et ensuite divisée par le poids de l'échantillon.
8. Résultats de la LOD et de la LOQ
Les limites de détection (LOD) et les limites de quantification (LOQ) peuvent être calculées en utilisant le ratio signal/bruit de la solution d'échantillon ensemencé (ensemencé avec la solution STD-3 à 1 :1).
LOD et LOQ théoriques :
Si aucun résultat de solution ensemencée n'est disponible, les LOD et LOQ théoriques peuvent être calculées en utilisant le signal/bruit de la STD-1 (NDMA : 0,002 µg/mL; NDEA 0,001 µg/mL).
À des fins de référence, les résultats des LOD et LOQ théoriques de Santé Canada sont les suivants :
| Concentration substance médicamenteuse µg/mL | NDMA | NDEA | ||||||
|---|---|---|---|---|---|---|---|---|
| µg/mL | Signal/bruit | LOD (calc.) ppm | LOQ (calc.) ppm | µg/mL | Signal/bruit | LOD (calc.) ppm | LOQ (calc.) ppm | |
| 50 | 0,002 | 74 | 0,002 | 0,0054 | 0,001 | 55 | 0,002 | 0,0073 |
9. Chromatogrammes des échantillons
Figure 1 : Chromatogrammes d'un échantillon dans lequel a été détecté de la NDMA et de la NDEA
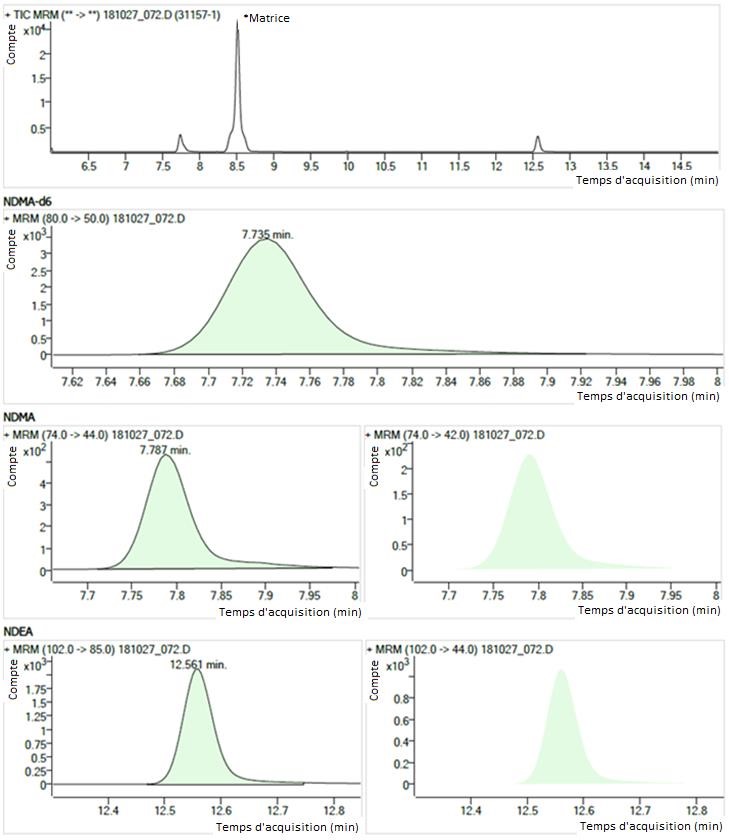
Description textuel
La figure montre des chromatogrammes d'un échantillon montrant des pics typiques de la NDMA et de la NDEA. Les chromatogrammes sont organisés en quatre rangées.
- La première rangée montre un chromatogramme du courant total ionique de 6,0 à 15,0 minutes. Il y a un large pic à 8,5 minutes (étiqueté « matrice ») et des pics plus petits à 7,7 minutes (NDMA, NDMA-d6) et à 12,6 minutes (NDEA).
- La deuxième rangée montre des chromatogrammes de surveillance de réactions multiples (m/z 80,0 → 50,0) avec un seul pic pour l'étalon interne de la NDMA-d6 à 7,735 minutes.
- La troisième rangée montre deux chromatogrammes de surveillance de réactions multiples (m/z 74,0 → 44,0 and m/z 74,0 → 42,0), chacun avec un seul pic pour la NDMA à 7,787 minutes.
- La quatrième rangée montre deux chromatogrammes de surveillance de réactions multiples (m/z 102,0 → 85,0 and m/z 102,0 → 44,0) avec un seul pic pour la NDEA à 12,561 minutes.
Figure 2 : Chromatogramme de la solution STD-1
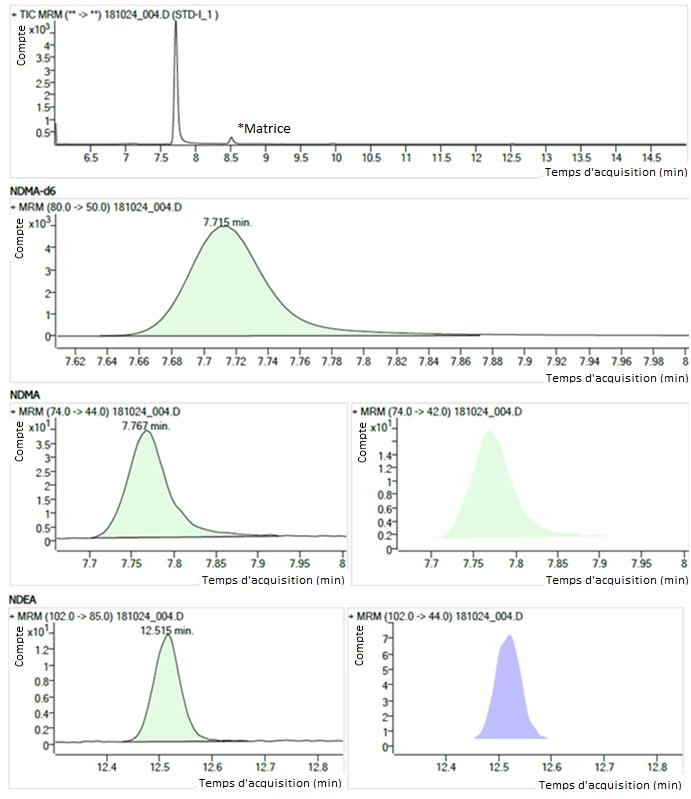
Description textuel
La figure montre des chromatogrammes de la solution étalon STD-1. Les chromatogrammes sont organisés en quatre rangées.
- La première rangée montre des chromatogrammes du courant total ionique de 6,0 à 15,0 minutes. Il y a un large pic à 7,7 minutes (NDMA, NDMA-d6) et un petit pic à 8,5 minutes (étiqueté « matrice »).
- La deuxième rangée montre deux chromatogrammes de surveillance de réactions multiples (m/z 80.0 → 50.0) avec un seul pic pour la solution d'étalon interne NDMA-d6 à 7,715 minutes.
- La troisième rangée montre deux chromatogrammes de surveillance de réactions multiples (m/z 74.0 → 44.0 and m/z 74.0 → 42.0) avec un seul pic pour la NDMA à 7,767 minutes.
- La quatrième rangée montre deux chromatogrammes de surveillance de réactions multiples (m/z 102.0 → 85.0 and m/z 102.0 → 44.0) avec un seul pic pour la NDEA à 12,515.
Méthode d'analyses pour les produits contenant de la ranitidine
Détermination de la N-Nitrosodiméthylamine (NDMA) dans les médicaments contenant de la ranitidine par UPLC-MS/MS.
1. Principe et portée
La présente méthode a été conçue afin de détecter et de quantifier la N-nitrosodiméthylamine (NDMA) présente dans les médicaments contenant de la ranitidine à l'aide de la chromatographie liquide haute performance couplée à la spectrométrie de masse en tandem (UPLC MS/MS).
2. Réactifs et étalons de références
- Solution de NDMA, N-Nitrosodiméthylamine (200 ppm), CAS nº 62-75-9
- Méthanol, grade LC-MS (CAS nº 67-56-1)
- Acide formique, grade LC-MS, CAS nº 64-18-6
- Eau déionisée
3. Instruments et équipements
- UPLC-TQ-S avec source APCI de Waters ou l'équivalent
- Colonne ACQUITY UPLC HSS T3, 100Å, 1,8 µm, 3 mm sur 150 mm, ou équivalente.
- Tubes en verre de 125 x 16 mm avec bouchons vissables
- Microtubes 2,0 mL pour centrifugeuse
- Pipettes Eppendorf, volumes variés, ou l'équivalent
- Balance analytique
- Ballons volumétriques (catégorie A), volumes variés, ou l'équivalent
- Mélangeur Vortex, à un et à plusieurs tubes
- Mortier et pilon
- Bain à ultrason
- Vials pour HPLC
- Centrifugeuse
4. Préparation des solutions
Entreposage
Les solutions d'étalonnage et d'échantillons sont conservées au réfrigérateur.
Préparation des phases mobiles
- Phase mobile A : 0,1 % d'acide formique dans l'eau
- Préparation : Mélanger l'acide formique à de l'eau dans un ratio volumétrique de 1 pour 1 000.
- Phase mobile B : 0,1 % d'acide formique dans le méthanol
- Préparation : Mélanger l'acide formique au méthanol dans un ratio volumétrique de 1 pour 1 000.
Préparation du diluant
- Diluant : 5 % de méthanol dans l'eau
- Préparation : Mélanger le méthanol et l'eau dans un ratio volumétrique de 5 pour 95.
Préparation des solutions étalons
- Solutions étalons mère (telles qu'achetées)
- Solution étalon de NDMA dans du méthanol (200 ppm).
Solutions étalons pour l'étalonnage
- STD-1 :
-
Transférer 50 μL de la solution étalon mère de NDMA (200 ppm) dans un ballon volumétrique de 50 mL, diluer au volume avec le diluant. Bien mélanger. Cette solution servira à effectuer l'évaluation de la performance du système ansi que la dérive du système.
- STD-2 :
- Dilution 1 pour 1 de la solution STD-1 avec le diluant. Bien mélanger.
- STD-3 :
- Dilution 1 pour 1 de la solution STD-2 avec le diluant. Bien mélanger.
- STD-4 :
- Dilution 1 pour 1 de la solution STD-3 avec le diluant. Bien mélanger.
- STD-5 :
- Dilution 2 pour 3 de la solution STD-4 avec le diluant. Bien mélanger.
- STD-6 :
- Dilution 1 pour 1 de la solution STD-5 avec le diluant. Bien mélanger.
- STD-7 :
- Dilution 1 pour 1 de la solution STD-6 avec le diluant. Bien mélanger.
- STD-8 :
- Dilution 2 pour 3 de la solution STD-7 avec le diluant. Bien mélanger.
- STD-9 :
- Dilution 3 pour 1 de la solution STD-8 avec le diluant. Bien mélanger (LOD).
| Solutions-étalon d'étalonnage | Concentration en NDMA (ng/mL) |
|---|---|
| STD-1 | 200 |
| STD-2 | 100 |
| STD-3 | 50 |
| STD-4 | 25 |
| STD-5 | 10 |
| STD-6 | 5 |
| STD-7 | 2,5 |
| STD-8 | 1 |
| STD-9 | 0,75 |
Le R2 de la courbe d'étalonnage devrait être inférieur à (NLT) 0,99.
Préparation des échantillons
- Peser au moins 20 comprimés et calculer le poids moyen par comprimé.
- Moudre et homogénéiser les 20 comprimés pesés en une fine poudre à l'aide d'un mortier et d'un pilon.
Méthode suggérée pour la préparation des échantillons :
- Préparer trois réplicats par échantillon.
- Peser précisément l'équivalent de 150 mg d'ingrédient pharmaceutique actif de la poudre d'échantillon homogénéisée, dans différents tubes en verre pour centrifugeuse.
- Ajouter 5,0 mL de diluant dans chaque tube d'échantillon. Bien refermer les tubes, soniquer pendant 10 minutes, puis vortexer pendant 5 minutes à 2 500 rpm.
- Transférer 2,0 mL de la solution dans un tube à centrifugeuse de 2 mL, puis centrifuger à 12 000 rpm pendant 5 minutes. Délicatement retirer les tubes de la centrifugeuse.
- Filtrer le surnageant à l'aide d'un filtre à seringue PTFE 0,2 µm, jeter le premier 0,5 mL de filtrat. Recueillir et transférer la solution de l'échantillon dans un flacon HPLC de 2 mL et fermer le bouchon.
La concentration des échantillons (poids et/ou volume) peut être modifiée au besoin.
Récupération suggérée pour les échantillons enrichis :
Échantillons enrichis : enrichir les solutions des échantillons avec la solution étalon, en triplicatas, puis vérifier la récupération.
5. Paramètres instrumentales
Paramètres suggérés pour l'UPLC :
- Débit :
- 0,4 mL/min
- Volume d'injection :
- 10,0 µL
- Durée :
- 12,5 min
| Temps (minutes) | % de la phase mobile A | % de la phase mobile B |
|---|---|---|
| 0 | 95 | 5 |
| 5 | 95 | 5 |
| 7 | 0 | 100 |
| 10 | 0 | 100 |
| 10,1 | 95 | 5 |
| 12,5 | 95 | 5 |
Paramètres suggérés pour le détecteur MS :
- Température de la sonde APCI :
- 450 °C
- Température de la source :
- 150 °C
- Corona :
- 4,0 kV
- Type :
- MRM
- Mode ionique :
- Positif
- Étendue (Da) :
- 0,3
- Temps de début :
- 3,3 min
- Temps de fin :
- 5,0 min
Programmation :
- Programmation 1 :
- 0,00 min : déchet
- Programmation 2 :
- 3,30 min : LC
- Programmation 3 :
- 5,00 min : déchet
Remarque : Le débit peut être ajusté selon le système pour dévier la ranitidine au déchet.
| Nom | Ion mère (m/z) | Ion fille (m/z) | Temporisation (s) | Cône (V) | Cellule de collision (eV) |
|---|---|---|---|---|---|
| NDMA | 75,1 | 42,9 | 0,3 | 22 | 10 |
| NDMA | 75,1 | 58,1 | 0,3 | 22 | 10 |
Remarque : La transition 75,1 → 58,1 est utilisée pour la quantification; un bruit de fond plus élevé est normalement observé pour la transition 75,1 → 42,9. Il est possible d'effectuer la quantification à l'aide d'une autre paire d'ions (ion mère et d'un ion fille).
6. Calcul
Les résultats, en ppm par rapport à la quantité déclarée d'une substance dans un produit, sont calculés de la façon suivante :
NDMA (ppm) = [(y-b)÷m] x AVGwt x V ÷ Wtspl ÷ LC
Où :
- y =
- surface du pic de NDMA
- b =
- ordonée à l'origine de la courbe d'étalonnage
- m =
- pente de la courbe d'étalonnage
- AVGwt =
- poids moyen d'un comprimé (mg)
- V =
- 5 mL (volume)
- Wtspl =
- poids de l'échantillon (mg)
- LC =
- quantité déclarée sur l'étiquette de l'échantillon (mg)
Description textuel
NDMA en parties par million est égale à y moins b sur m, qui représente la différence entre la surface du pic d'impureté moins l'ordonnée à l'origine de la courbe d'étalonnage sur la pente de la courbe d'étalonnage. Cette valeur est multipliée par le poids moyen d'un comprimé, ensuite multipliée par le volume, divisée par le poids de l'échantillon et ensuite divisée par la quantité déclarée sur l'étiquette de l'échantillon.
7. Plage, limite de détection (LOD) et limite de quantification (LOQ)
| S/O | NDMA (ng/mL) | NDMA (ppm)Tableau 3 Note de bas de page * |
|---|---|---|
| LOQ | 1 | 0,033 |
| LOD | 0,75 | 0,025 |
| Plage | 1 – 200 | 0,03 – 6,7 |
|
||
8. Exemples de courbe d'étalonnage et chromatogrammes
Figure 1 : Courbe d'étalonnage (disponible en anglais seulement)

Description texte
La figure montre une courbe d'étalonnage avec la concentration des solutions étalons de référence de NDMA sur l'axe x et le signal (unités arbitraires) sur l'axe y. Il y a un point de donnée pour chacun des neufs concentrations des solutions étalons de référence, reliées par une ligne droite. Le coefficient de corrélation est R2 = 0,999761, et l'équation de la courbe est y = 257,934 x – 15,8397.
Figure 2 : Chromatogrammes de solutions-étalon à 200 ppb : MRM et UV (disponibles en anglais seulement)
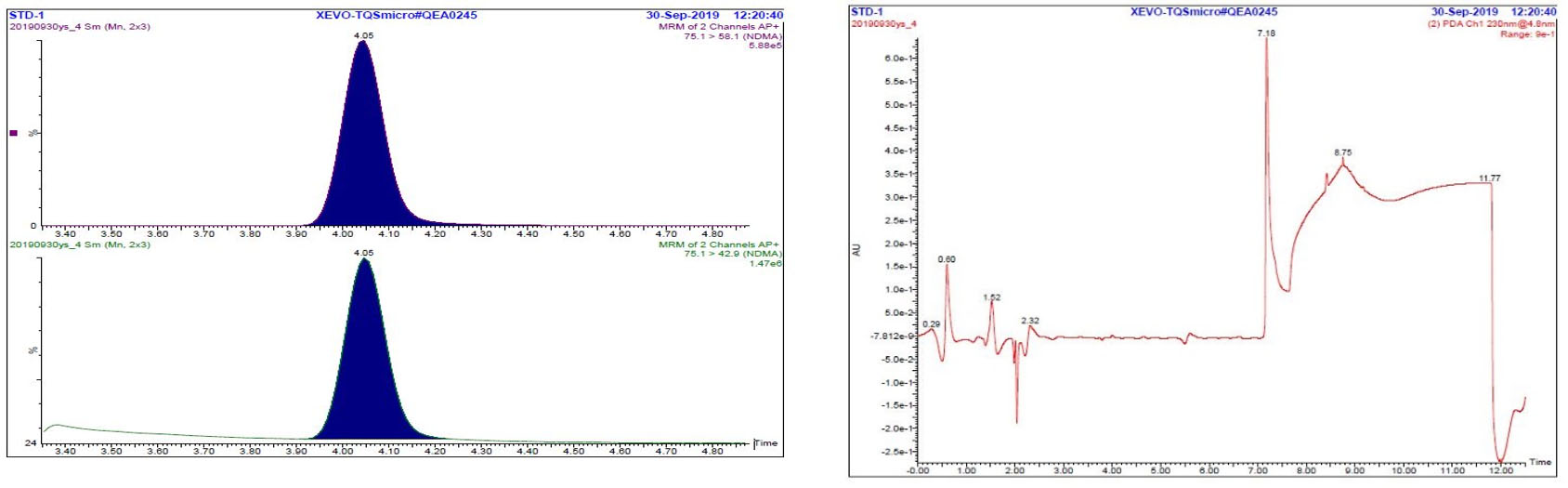
Description texte
La figure comprend deux panneaux. Le panneau à la gauche montre deux chromatogrammes MRM (m/z 75,1 → 58,1 et m/z 75,1 → 42,9) de la solution étalon STD-1, chacun avec un seul pic à 4,05 minutes pour la NDMA. Le panneau à la droite montre le chromatogramme UV de la solution étalon STD-1. La section du chromatogramme entre 3,3 et 5,0 minutes (correspondant au moment où le débit est acheminé au détecteur MS) est relativement plate, tandis que le reste du chromatogramme contient plusieurs pics et décalages de la ligne de base.
Figure 3 : Chromatogrammes d'un échantillon : MRM et UV (disponibles en anglais seulement)
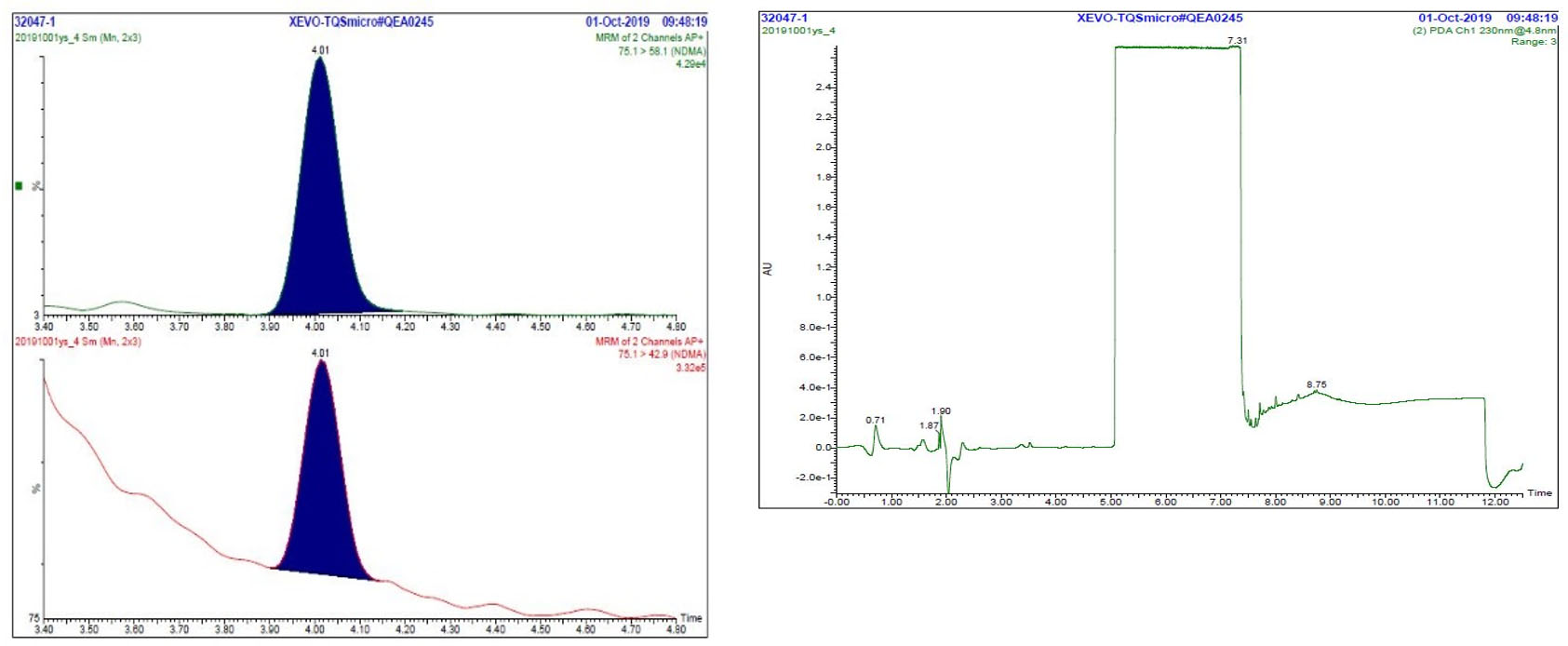
Description texte
La figure comprend deux panneaux. Le panneau à la gauche montre deux chromatogrammes MRM (m/z 75,1 → 58,1 et m/z 75,1 → 42,9) d'une solution d'échantillon typique, chacun avec un seul pic à 4,01 minutes pour la NDMA. Le panneau à la droite montre le chromatogramme UV d'une solution d'échantillon typique. La section du chromatogramme entre 3,3 et 5,0 minutes (correspondant au moment où le débit est acheminé au détecteur MS) est relativement plate, tandis que le reste du chromatogramme contient plusieurs pics et décalages de la ligne de base.
Méthodes d'analyse pour les produits contenant de la metformin
Détermination des impuretés de nitrosamines dans les médicaments contenant de la metformine
1. Principe et portée
La présente méthode a été développée afin de détecter et de quantifier les impuretés de nitrosamine suivantes dans les médicaments contenant de la metformine à l'aide de la chromatographie liquide haute performance couplée à un spectromètre de masse en tandem (UPLC-MS/MS) : N-nitrosodiméthylamine (NDMA), N-nitrosodiéthylamine (NDEA), N-nitrosodiisopropylamine (NDIPA), N-éthyl-N-nitroso-isopropylamine (NEIPA), N-nitroso-di-n-butylamine (NDBA) et l'acide N-nitroso-N-méthyl-4-aminobutyrique (NMBA)
2. Réactifs et étalons de références
- NDMA, solution de N-nitrosodiméthylamine (200 ppm), CAS # 62-75-9
- NDEA, solution de N-nitrosodiéthylamine (100 ppm), CAS # 55-18-5
- NEIPA, solution de N-éthyl-N-nitroso-isopropylamine (100 ppm), CAS # 16339-04-01
- NDIPA, solution de N-nitrosodiisopropylamine (100 ppm), CAS # 601-77-4
- NDBA, solution de N-nitroso-di-n-butylamine (100 ppm), CAS # 924-16-3
- NMBA, acide N-nitroso-N-méthyl-4-aminobutyrique, CAS # 61445-55-4
- Méthanol, grade LC-MS, CAS # 67-56-1
- Acide formique, grade LC-MS, CAS # 64-18-6
- Eau déionizée
3. Instruments et équipements
- UPLC-TQ-S avec source APCI de Waters ou l'équivalent
- Colonne ACQUITY UPLC HSS T3, 100 Å, 1,8 µm, 3 mm X 150 mm ou l'équivalent
- Tubes en verre de 16 x 125 mm avec bouchons vissables
- Microtubes 2,0 mL pour centrifugeuse
- Pipettes Eppendorf, volumes variés, ou l'équivalent
- Balance analytique
- Ballons volumétriques (catégorie A), volumes variés, ou l'équivalent
- Mélangeur Vortex, à un et à plusieurs tubes
- Mortier et pilon
- Bain à ultrason
- Vials pour HPLC
- Centrifugeuses
4. Préparation des solutions
4.1 Entreposage
Les solution d'étalonnage et d'échantillons sont conservées au réfrigérateur.
4.2 Préparation des phases mobile
- Phase mobile A : 0,1% d'acide formique dans l'eau
- Préparation: Mélanger de l'acide formique et de l'eau dans un ratio volumétrique de 1:1000.
- Phase mobile B : 0,1% d'acide formique dans du méthanol
- Préparation: Mélanger de l'acide formique et du méthanol dans un ratio volumétrique de 1:1000.
4.3 Préparation du diluant
- Diluant : 5% méthanol dans l'eau
- Préparation : Mélanger du méthanol et de l'eau dans un ratio volumétrique de 5:95.
4.4 Solutions étalons
Solutions étalons de référence (telles qu'achetées)
- Solution étalon de NDMA dans du méthanol (200 ppm)
- Solution étalon de NDEA dans du méthanol (100 ppm)
- Solution étalon de NEIPA dans du méthanol (100 ppm)
- Solution étalon de NDIPA dans du méthanol (100 ppm)
- Solution étalon de NDBA dans du méthanol (100 ppm)
Méthode suggérée pour la préparation de la solution étalon mère de NMBA (100 ppm)
Peser précisément 2,0 mg de NMBA dans un ballon volumétrique de 20 mL. Dissoudre et diluer au volume avec du méthanol.
Remarque: La concentration de la solution étalon mère de NMBA peut variée. La dilution pour la préparation des solutions étalons intermédiares -1 et -2 peut être calculée et ajustée selon le cas pour s'assurer que la concentration finale soit approximativement de 200 ppb et 5 ppb.
Préparation de la solution étalon intermédiare-1 (200 ppb)
Transférer 100 µL de solution étalon de référence de NDMA (200 ppm), 200 µL des autres solutions étalons de référence de nitrosamine (100 ppm) et 200 µL de la solution étalon mère de NMBA (100 ppm) dans un ballon volumétrique, diluer au volume avec le diluant. Bien mélanger.
Préparation de la solution étalon intermédiare-2 (5 ppb) (STD-4)
Transférer 500 µL de la solution étalon intermédiare-1 (200 ppb) dans un ballon volumétrique de 20 mL, diluer au volume avec le diluant. Bien mélanger.
| Solution STD |
Solution de travail | Concentration de la solution de travail (ppb) | Volume de la solution de travail (mL) | Volume total (mL) | Concentration en nitrosamine (ppb) |
|---|---|---|---|---|---|
| LOD | Solution étalon Intermédiaire-2 | 5 | 0,5 | 5 | 0,5 |
| LOQ | Solution étalon Intermédiaire-2 | 5 | 0,75 | 5 | 0,75 |
| STD-1 | Solution étalon Intermédiaire-2 | 5 | 1 | 5 | 1 |
| STD-2 | Solution étalon Intermédiaire-2 | 5 | 2 | 5 | 2 |
| STD-3 | Solution étalon Intermédiaire-2 | 5 | 3 | 5 | 3 |
| STD-4 | Solution étalon Intermédiaire-2 | 5 | - | - | 5 |
| STD-5 | Solution étalon Intermédiaire-1 | 200 | 0,25 | 5 | 10 |
| STD-6 | Solution étalon Intermédiaire-1 | 200 | 0,375 | 5 | 15 |
| STD-7 | Solution étalon Intermédiaire-1 | 200 | 0,5 | 5 | 20 |
| STD-8 | Solution étalon Intermédiaire-1 | 200 | 0,625 | 5 | 25 |
| STD-9 | Solution étalon Intermédiaire-1 | 200 | 1,25 | 5 | 50 |
Le R2 de la courbe d'étalonnage ne devrait pas être inférieur à (NLT) 0,995.
La solution STD-9 servira à effectuer l'évaluation de la performance du système ainsi que la dérive du système.
4.5 Préparation des échantillons
- Peser au minimum 20 comprimés et calculer le poids moyen par comprimé.
- Moudre soigneusement les comprimés pesés en une fine poudre à l'aide d'un mortier et d'un pilon.
Méthode suggérée pour la préparation des échantillons :
- Préparer trois réplicats par échantillon.
- Peser précisément l'équivalent de 500 mg d'ingrédient pharmaceutique actif (Metformine) de la poudre d'échantillon homogénéisée, dans différents tubes en verre pour centrifugeuse.
- Ajouter 10,0 mL de diluant dans chaque tube d'échantillon. Bien refermer les tubes, soniquer pendant 20 minutes, puis vortexer pendant 10 minutes à 2 500 rpm.
- Centrifuger les échantillons pendant 10 minutes à 2500 rpm.
- Transférer 2,0 mL du surnageant dans un tube pour centrifugeuse de 2 mL, centrifuger pendant 5 minutes à 12 000 rpm. Délicatement retirer les tubes de la centrifugeuse.
- Transférer la solution de l'échantillon dans un vial pour HPLC et soumettre pour analyse.
La concentration des échantillons (poids et/ou volume) peut être modifiée au besoin.
4.6 Préparation suggérée pour les échantillons enrichis :
- Si aucun nitrosamine n'a été détecté dans l'échantillon, préparer un échantillon enrichi et vérifier le ratio signal/bruit. Sinon, préparer trois réplicats d'échantillons enrichis.
- Peser précisément l'équivalent de 500 mg d'ingrédient pharmaceutique actif (Metformine) de la poudre d'échantillon homogénéisée, dans différents tubes en verre pour centrifugeuse.
- Dans chaque tube d'échantillon, ajouter 10,0 mL de diluant puis 125 µL de la solution étalon intermédiare-1 (200 ppb). Bien refermer les tubes, soniquer pendant 20 minutes, puis vortexer pendant 10 minutes à 2 500 rpm.
- Centrifuger les échantillons pendant 10 minutes à 2500 rpm.
- Transférer 2,0 mL de solution dans un tube pour centrifugeuse de 2 mL, centrifuger pendant 5 minutes à 12 000 rpm. Délicatement retirer les tubes de la centrifugeuse.
- Transférer la solution de l'échantillon dans un vial HPCL et soumettre pour analyse.
5. Paramètres instrumentales
5.1 Paramètres suggérés pour l'UPLC:
- Débit :
- 0,4 mL/min
- Volume d'injection :
- 10,0 µL
- Durée :
- 30 min
| Temps (minutes) | % de la phase mobile A | % de la phase mobile B |
|---|---|---|
| 0 | 95 | 5 |
| 5 | 95 | 5 |
| 22 | 0 | 100 |
| 27 | 0 | 100 |
| 28 | 95 | 5 |
| 30 | 95 | 5 |
5.2 Paramètre suggérés pour le détecteur MS :
- Température de la sonde APCI :
- 400°C
- Température de la source :
- 150°C
- Corona :
- 4,0 kV
- Type :
- MRM
- Mode ionique :
- Positive
- Span (Da) :
- 0
- Temps de début :
- 3.5 min
- Temps d'arrêt :
- 21 min
Programmation:
- Programmation 1 : 0,00 min
- Flow State: déchet
- Programmation 2 : 3,5 min
- Flow State: LC
- Programmation 3 : 21 min
- Flow State: déchet
Remarque : Le débit peut être ajusté, si nécessaire, pour permettre au système de détourner la metformine vers les déchets.
5.3 Paramètres pour MRM « Multiple Reaction Monitoring » :
| Nom | Période de temps (minutes) |
Ion mère (m/z) | Ion fille (m/z) | Temporisation (s) | Cône (V) | Cellule de collision (eV) |
|---|---|---|---|---|---|---|
| NDMA | 3,5 – 6,0 | 75,0 | 43,1 | 0,1 | 30 | 10 |
| 75,0 | 58,0* | 0,1 | 30 | 8 | ||
| NMBA | 6,0 – 10,0 | 146,9 | 44,0 | 0,1 | 22 | 12 |
| 146,9 | 117,0* | 0,1 | 22 | 4 | ||
| NDEA | 10,0 – 13,0 | 103,0 | 47,1 | 0,1 | 30 | 12 |
| 103,0 | 75,0* | 0,1 | 30 | 10 | ||
| NEIPA | 12,8 – 15,0 | 117,0 | 47,0 | 0,1 | 26 | 14 |
| 117,0 | 75,0* | 0,1 | 26 | 10 | ||
| NDIPA | 14,6 – 17,0 | 131,0 | 43,1 | 0,1 | 26 | 10 |
| 131,0 | 89,0* | 0,1 | 26 | 6 | ||
| NDBA | 17,0 – 21,0 | 159,0 | 57,1 | 0,1 | 32 | 12 |
| 159,0 | 103,0* | 0,1 | 32 | 10 | ||
| *Ions cible utilisés pour les calculs. | ||||||
6. Calculs
Les résultats, en ppm par rapport à la quantité déclarée d'une substance dans un produit, sont calculés de la façon suivante :
Impureté de nitrosamine (ppm) = [(y-b)÷m] × AVGwt × V ÷ Wtspl ÷ LC
Où:
Impureté de nitrosamine réfère à la NDMA, NDEA, NEIPA, NDIPA NDBA ou la NMBA
- y =
- surface du pic de l'impureté de nitrosamine
- b =
- ordonnée à l'origine de la courbe d'étalonnage
- m =
- pente de la courbe d'étalonnage
- AVGwt =
- poids moyen d'un comprimé (mg)
- V =
- 10 mL (volume)
- Wtspl =
- poids de l'échantillon (mg)
- LC =
- quantité déclarée sur l'étiquette de l'échantillon (mg)
Équation - Description textuel
La concentration d'impureté de nitrosamine en parties par million (ppm) est égale à y moins b divisé par m, ce qui représente la différence entre la surface du pic d'impureté moins l'ordonnée à l'origine de la courbe d'étalonnage, le tout divisé par la pente de la courbe d'étalonnage. Cette valeur est multipliée par le poids moyen d'un comprimé, qui est ensuite multipliée par le volume, divisée par le poids de l'échantillon et pour terminer, divisée par la quantité déclarée sur l'étiquette de l'échantillon.
7. Plage, limite de détection (LOD) et limite of quantification (LOQ)
| Nom du composé | Concentration (ng/mL) | Concentration (ppm*) | ||||
|---|---|---|---|---|---|---|
| LOD | LOQ | Plage | LOD | LOQ | Plage | |
| NDMA | 0,5 | 0,75 | 0,75 – 50 | 0,010 | 0,015 | 0,015 – 1,0 |
| NDEA | 0,1 | 0,5 | 0,5 – 50 | 0,002 | 0,010 | 0,010 – 1,0 |
| NEIPA | 0,1 | 0,5 | 0,5 – 50 | 0,002 | 0,010 | 0,010 – 1,0 |
| NDIPA | 0,1 | 0,5 | 0,5 – 50 | 0,002 | 0,010 | 0,010 – 1,0 |
| NDBA | 0,1 | 0,5 | 0,5 – 50 | 0,002 | 0,010 | 0,010 – 1,0 |
| NMBA | 0,25 | 0,5 | 0,5 – 50 | 0,005 | 0,010 | 0,010 – 1,0 |
| * ppm (ng/g) par rapport à la quantité déclarée de Metformine dans le produit | ||||||
8. Example de chromatogrammes
Figure 1. Chromatogramme MRM de l'étalon de NDMA à 5 ppb
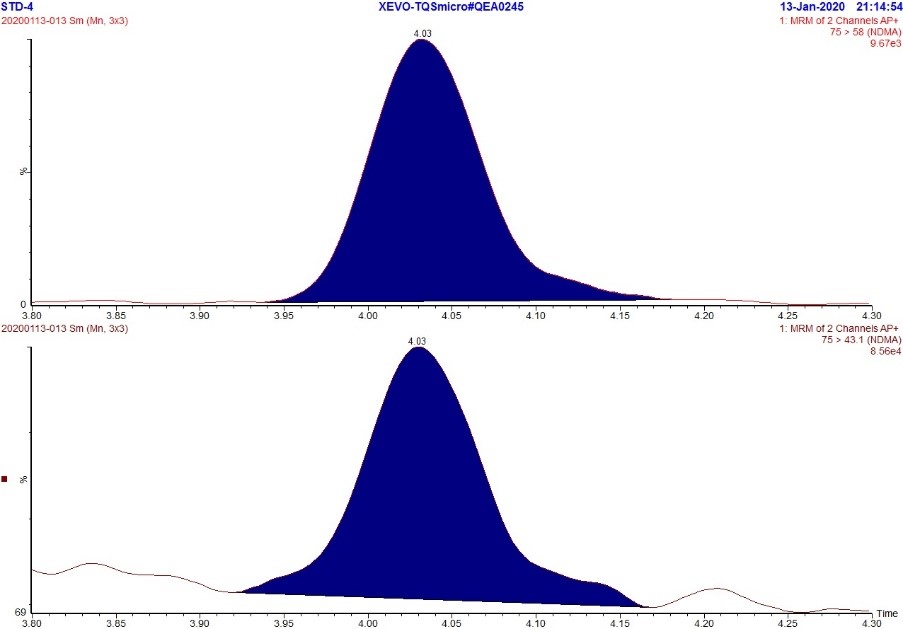
Description textuel
La figure montre deux rangées. La rangée du haut montre un chromatogramme MRM (m/z 75,0 → 58,0) de la solution étalon de NDMA à 5 ppb tandis que la rangée du bas montre un chromatogramme MRM (m/z 75,0 → 43,1) de la solution étalon de NDMA à 5 ppb. Chaque chromatogramme montre un seul pic à environ 4.03 minutes.
Figure 2. Chromatogramme MRM de l'étalon de NBMA à 5 ppb
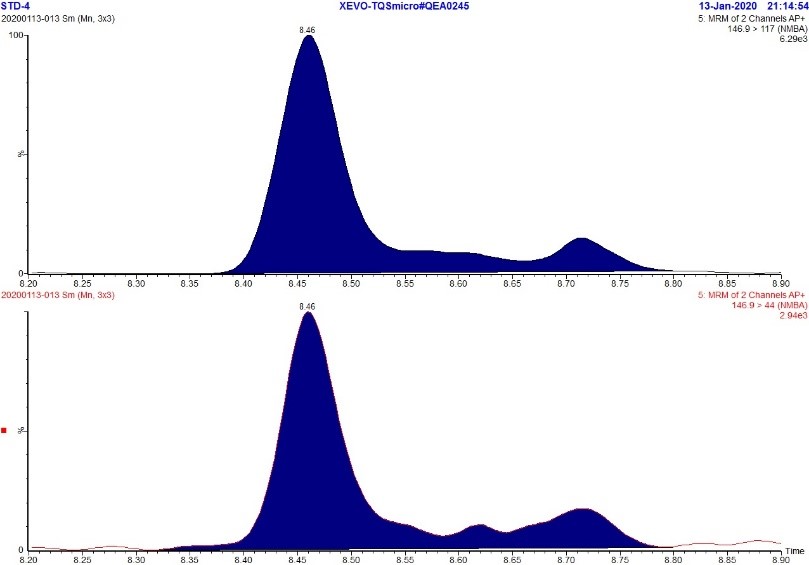
Description textuel
La figure montre deux rangées. La rangée du haut montre un chromatogramme MRM (m/z 146,9 → 117,0) de la solution étalon de NBMA à 5 ppb tandis que la rangée du bas montre un chromatogramme MRM (m/z 146,9 → 44,0) de la solution étalon de NBMA à 5 ppb. Chaque chromatogramme montre un grand pic à environ 8,5 minutes et deux pics plus petits à environ 8,6 et 8,7 minutes. La présence des deux derniers pics est probablement dû à la structure asymétrique du NBMA.
Figure 3. Chromatogramme MRM de l'étalon de NDEA à 5 ppb
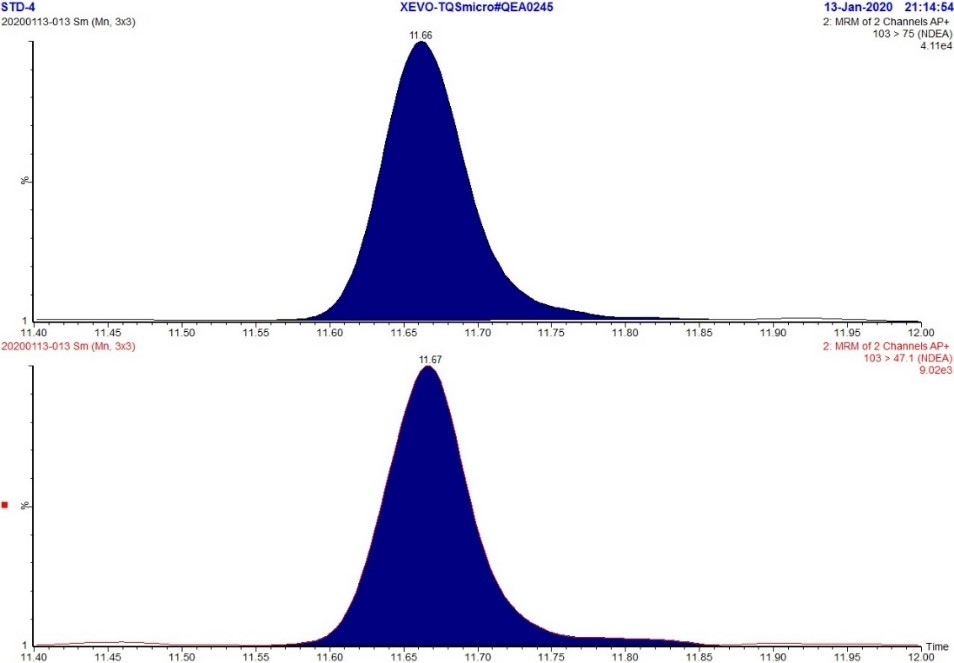
Description textuel
La figure montre deux rangées. La rangée du haut montre un chromatogramme MRM (m/z 103,0 → 75,0) de la solution étalon de NDEA à 5 ppb tandis que la rangée du bas montre un chromatogramme MRM (m/z 103,0 → 47,1) de la solution étalon de NDEA à 5 ppb. Chaque chromatogramme montre un seul pic à environ 11.7 minutes.
Figure 4. Chromatogramme MRM de l'étalon de NEIPA à 5 ppb

Description textuel
La figure montre deux rangées. La rangée du haut montre un chromatogramme MRM (m/z 117,0 → 75,0) de la solution étalon de NEIPA à 5 ppb tandis que la rangée du bas montre un chromatogramme MRM (m/z 117,0 → 47,0) de la solution étalon de NEIPA à 5 ppb. Chaque chromatogramme montre un grand pic à environ 13,8 minutes et l'épaulement d'un petit pic à environ 14,0 minutes. La présence de ce dernier est probablement dû à la structure asymétrique de la NEIPA.
Figure 5. Chromatogramme MRM de l'étalon de NDIPA à 5 ppb
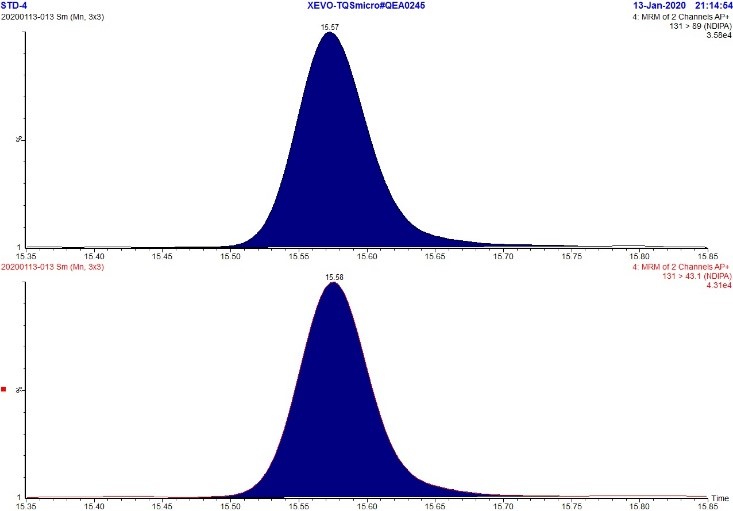
Description textuel
La figure montre deux rangées. La rangée du haut montre un chromatogramme MRM (m/z 131,0 → 89,0) de la solution étalon de NDIPA à 5 ppb tandis que la rangée du bas montre un chromatogramme MRM (m/z 131,0 → 43,1) de la solution étalon de NDIPA à 5 ppb. Chaque chromatogramme montre un seul pic à environ 15.6 minutes.
Figure 6. Chromatogramme MRM de l'étalon de NDBA à 5 ppb
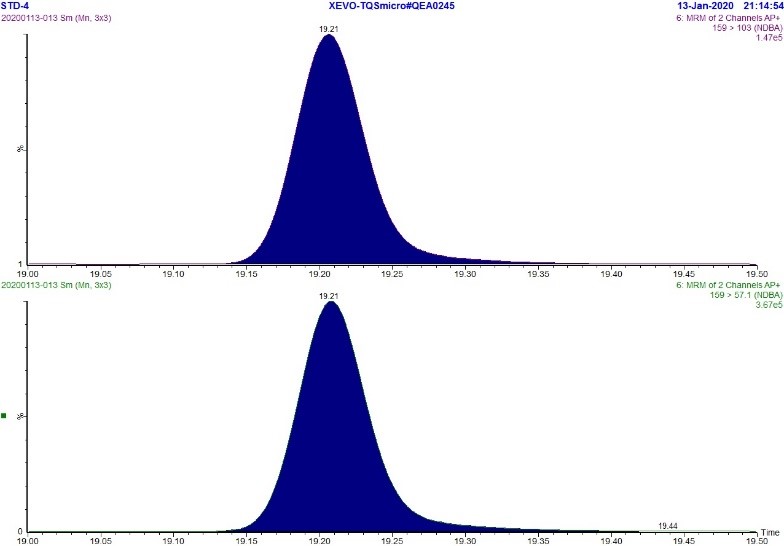
Description textuel
La figure montre deux rangées. La rangée du haut montre un chromatogramme MRM (m/z 159,0 → 103,0) de la solution étalon de NDBA à 5 ppb tandis que la rangée du bas montre un chromatogramme MRM (m/z 159,0 → 57,1) de la solution étalon de NDBA à 5 ppb. Chaque chromatogramme montre un seul pic à environ 19.2 minutes.
Détermination des impuretés de N-nitrosodiméthylamine dans les produits de metformine par GC-MS/MS
1. Principe et portée
La méthode ci-dessous a été mise au point pour déceler et quantifier les impuretés de N-nitrosodiméthylamine (NDMA) dans les produits de metformine par GC-MS/MS.
2. Réactifs et normes de référence
- NDMA, solution de N-Nitrosodiméthylamine (200 ppm), no CAS 62-75-9
- NDMA-d6, solution de N-nitrosodiméthylamine-d6 (1 000 ppm), no CAS 17829-05-9
- Dichlorométhane, qualité GC, no CAS 75-09-2
3. Instruments et équipements
- Agilent GC 7890A avec MSMS 7000 avec source EI ou l'équivalent
- Colonne : Agilent DB-624 30m x 0,32 µm x 1,8 µm ou l'équivalent
- Tubes de verre filetés de 16 x 125 mm avec bouchons vissables
- Microtubes pour centrifugeuse de 2,0 mL
- Pipettes Eppendorf, volumes variés, ou l'équivalent
- Balance analytique
- Ballons volumétriques (catégorie A), volumes variés, ou l'équivalent
- Mélangeur Vortex, mono ou multitubes
- Mortier et pilon
- Bain à ultrasons
- Fioles pour CG
- Centrifugeuses
4. Préparation des solutions
4.1 Entreposage
Les solutions d'étalonnage et d'échantillons sont conservées au réfrigérateur.
4.2 Solutions étalons
Solutions étalons de référence (telles qu'achetées)
- Solution-étalon de NDMA dans du méthanol (200 ppm)
- Solution-étalon de NDMA-d6 dans du méthanol (1 000 ppm)
Préparation de la solution-étalon de NDMA-1 (1 ppm)
Transférer 125 µL de la solution-étalon mère de NDMA (200 ppm) dans un ballon volumétrique de 25 mL, diluer au volume avec le dichlorométhane. Bien mélanger.
Préparation de la solution-étalon interne-1 (2 ppm)
Transférer 100 µL de la solution-étalon mère de NDMA-d6 (1 000 ppm) dans un ballon volumétrique de 50 mL, diluer au volume avec du dichlorométhane. Bien mélanger.
Préparation de la solution-étalon interne-2 (10 ppb)
Transférer 2,5 mL de la solution-étalon interne-1 (2 ppm) dans un ballon volumétrique de 500 mL, diluer au volume avec du dichlorométhane. Bien mélanger.
| Solution-étalon | Volume de solution-étalon enrichie (uL) |
Volume de l'étalon interne-1 (uL) |
Diluant | Ballon volumétrique (mL) |
Concentration de NDMA dans solution STD (ppb) |
Concentration étalon interne (ppb) |
|---|---|---|---|---|---|---|
| Étalon-1 | 500 (Solution-étalon de référence-1 NDMA) | 50 | Dichlorométhane | 10 | 50 | 10 |
| Étalon-2 | 250 (Solution-étalon de référence-1 NDMA) | 50 | Dichlorométhane | 10 | 25 | 10 |
| Étalon-3 | 100 (Solution-étalon de référence-1 NDMA) | 50 | Dichlorométhane | 10 | 10 | 10 |
| Étalon-4 | 50 (Solution-étalon de référence-1 NDMA) | 50 | Dichlorométhane | 10 | 5 | 10 |
| Étalon-5 | 25 (Solution-étalon de référence-1 NDMA) | 50 | Dichlorométhane | 10 | 2.5 | 10 |
| Étalon-6 | 50 (Solution-étalon de référence-1 NDMA) | 250 | Dichlorométhane | 50 | 1 | 10 |
| Étalon-7(LOQ) | 5 000(étalon-6) | 0 | Étalon interne-2 | 10 | 0.5 | 10 |
| LOD | 1 000(étalon-6) | 0 | Étalon interne-2 | 10 | 0.1 | 10 |
- R2 pour la courbe d'étalonnage devrait être au moins 0,995.
- La solution STD-1 servira à effectuer l'évaluation de la performance du système et la vérification de la dérive du système.
4.3 Préparation des échantillons
- Peser au moins 20 comprimés et calculer le poids moyen par comprimé.
- Moudre les comprimés pesés en une poudre fine à l'aide du mortier et du pilon.
Méthode pour la préparation des échantillons :
- Préparer trois réplicats par échantillon.
- Peser précisément l'équivalent d'environ 500 mg d'ingrédients pharmaceutiques actifs de la poudre d'échantillon homogénéisée dans différents tubes en verre pour centrifugeuse.
- Ajouter à chaque tube d'échantillon 10 mL de la solution-étalon interne-2. Bien refermer les tubes, soniquer pendant 20 minutes et ensuite, vortexer pendant 10 minutes à 2 500 rpm.
- Centrifuger l'échantillon à 2 500 rpm pendant 15 minutes.
- Transférer 2 mL du surnageant dans un tube à centrifugeuse de 2 mL, centrifuger à 12 000 rpm pendant 5 minutes. Retirer délicatement les tubes de la centrifugeuse.
- Transférer la solution-échantillon dans des fioles pour CG pour analyse.
4.4 Récupération pour les échantillons enrichis :
- Si aucune impureté de nitrosamine n'est décelée dans l'échantillon, préparer une solution de l'échantillon enrichi et vérifier le ratio signal/bruit. Sinon, préparer trois réplicats d'échantillons enrichis.
- Peser précisément l'équivalent de 500 mg d'ingrédients pharmaceutiques actifs (metformine) de la poudre d'échantillon homogénéisée, dans différents tubes en verre pour centrifugeuse.
- Ajouter 10 mL de la solution-étalon interne-2. Ajouter 25 µL de la solution-étalon NDMA-1 (1 ppm) à chaque tube d'échantillon. Bien refermer les tubes, soniquer pendant 20 minutes, ensuite vortexer pendant 10 minutes à 2 500 rpm.
- Centrifuger les échantillons à 2 500 rpm pendant 15 minutes.
- Transférer 2 mL de la solution dans un tube à centrifugeuse de 2 mL, centrifuger à 12 000 rpm pendant 5 minutes. Retirer délicatement les tubes de la centrifugeuse.
- Transférer la solution de l'échantillon dans des fioles pour CG et soumettre pour analyse.
5. Paramètres de fonctionnement des instruments
5.1 Paramètres pour le GC :
Paramètres de l'injecteur :
- Mode d'injection :
- Injecteur « Pulsed Splitless »
- Température de l'injecteur :
- 240 °C
- Débit :
- 1,3 mL/min.
- Débit de vidange de la membrane
- (Septum): 10 mL/min.
- Débit de vidange :
- 50 mL/min. après 1 minute
- Volume d'injection :
- 2,0 µL
- Programme du four
Température initiale : - 60 °C; attente : 2 minutes
| No d'échelle température | Débit (°C /min.) | Température finale (°C)(ºC) | Durée d'attente (min.) |
|---|---|---|---|
| 1 | 20 | 220 | 2 |
| 2 | 60 | 240 | 3 |
5.2 Paramètres pour le détecteur MS :
- Ligne de transfert de la MS (température auxiliaire)
- 240°C
- Source d'ion Source :
- EI
- Température de la source :
- 250°C
- Délai du solvant :
- 4 min
- Temps d'arrêt :
- 7 min
- Gaz d'injection :
- Hélium à 2,5 mL/min.
- Gaz de collision :
- Azote à 1,5 mL/min.
5.3 Paramètres pour la « surveillance de réactions multiples » (MRM) :
| Nom | Temps de rétention (min.) |
Ion précurseur (m/z) |
Ion produit (m/z) |
Delta gauche (TR) |
Delta droit (TR) |
Résolution (MS1 et MS2) |
CE | Tempo-risation (ms) |
|---|---|---|---|---|---|---|---|---|
| NDMA | 5,8 | 74 | 42 | 1.0 | 1.2 | Unité/étendue | 7 | 165,8 |
| 74 | 44Note de bas du tableau * | 1,0 | 1,2 | Unité/étendue | 4 | 165,8 | ||
| NDMA-d6 | 5,8 | 80,1 | 50,1 | 1,0 | 1,2 | Unité/étendue | 5 | 165,8 |
Notes de bas du tableau
|
||||||||
6. Calcul
Les résultats, en ppm par rapport à la quantité déclarée d'une substance dans un produit, sont calculés de la façon suivante :
Où :
Impureté de nitrosamine, NDMA, (ppm) = [(y-b)÷m] x AVGwt x V ÷ Wtspl ÷ LC
- y =
- Rapport de la surface du pic de NDMA à la surface du pic de NDMA-d6
- b =
- Ordonnée à l'origine de la courbe d'étalonnage
- m =
- Pente de la courbe d'étalonnage
- AVGwt =
- Poids de l'échantillon (mg)
- V =
- 10 mL (volume)
- Wtspl =
- Sample Weight (mg)
- LC =
- Quantité déclarée sur l'étiquette de l'échantillon (mg)
Équation – Description textuelle
La concentration d'impuretés de nitrosamine en parties par million (ppm) est égale à y moins b divisé par m, ce qui représente la différence entre la surface du pic d'impureté, moins l'ordonnée à l'origine de la courbe d'étalonnage, le tout divisé par la pente de la courbe d'étalonnage. Cette valeur est multipliée par le poids moyen d'un comprimé, ensuite multipliée par le volume, divisée par le poids de l'échantillon et pour terminer, divisée par la quantité déclarée sur l'étiquette de l'échantillon.
7. Plage, limite de détection (LOD) et limite de quantification (LOQ)
| Nom du composé | Concentration (ng/mL) | Concentration (ppmNote Tableaux x *) | ||||
|---|---|---|---|---|---|---|
| LOD | LOQ | Plage | LOD | LOQ | Plage | |
| NDMA | 0,1 | 0,5 | 0,5-50 | 0,002 | 0,01 | 0,01-1,00 |
|
||||||
8. Exemple de chromatogrammes
Figure 1. Chromatogramme de la solution STD-4 (solution-étalon de NDMA de 1ppb)

Description textuelle
pics typiques de la NDMA et de la NDMA-d6. Les chromatogrammes sont organisés en trois rangées.
- La première rangée montre un chromatogramme de courant total ionique de 5,6 à 6,25 minutes. Il y a un pic prononcé à 5,853 minutes (NDMA-d6) et un autre pic prononcé à 5,872 minutes (NDMA).
- La deuxième rangée montre un chromatogramme de surveillance de réactions multiples (m/z 74,0 → 44,0) avec un pic à 5,872 minutes pour la NDMA.
- • La troisième rangée illustre un chromatogramme de surveillance de réactions multiples (m/z 80,1 → 50,1) avec un seul pic à 5,853 minutes pour l'étalon interne NDMA-d6.
Figure 2. Chromatogramme des échantillons
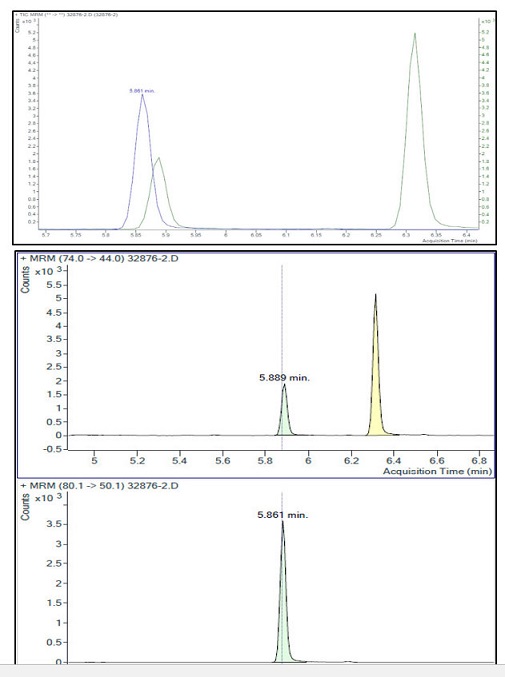
Description textuelle
La figure 2 illustre les chromatogrammes d'un échantillon montrant les pics typiques de la NDMA et de la NDMA-d6. Les chromatogrammes sont organisés en trois rangées :
- La première rangée illustre le chromatogramme ionique total de 5,7 à 6,4 minutes. Il y a un pic prononcé à 5,861 minutes (NDMA-d6), un pic léger à 5,889 minutes (NDMA) et un pic lié à la matrice à 6,32 minutes.
- La deuxième rangée illustre des chromatogrammes de surveillance de réactions multiples (m/z 74,0 → 44,0) avec un pic à 5,889 minutes pour la NDMA et un pic prononcé lié à la matrice à 6,3 minutes.
- La troisième rangée illustre un chromatogramme de surveillance de réactions multiples (m/z 80,1 → 50,1) avec un pic unique à 5,861 minutes pour l'étalon interne NDMA-d6.
Résultats des analyses pour les sartans ou récepteurs angiotensine II (ARB)
Santé Canada a analysé des échantillons d'ARA offerts sur le marché canadien pour vérifier la présence de NDMA ou de NDEA. Les résultats, présentés dans le tableau ci-dessous, indiquent :
- niveaux de NDMA ou de NDEA, si détectés
- si ces concentrations dépassent les limites acceptables, en fonction d'une exposition à vie
- si le produit a été rappelé
Nous continuerons d'évaluer les nouveaux développements afin de déterminer si des analyses additionnelles sont nécessaires.
| Nomme de la compagnie détenteur de l'autorisation de mise en marché | Nomme du produit et DIN | Force (mg) |
Numéro du lot | Date d'expiration | Résultats de NDMA ng / comprimé |
Résultats de NDEA ng / comprimé |
Rappelé au Canada | Date Ajoutée |
|---|---|---|---|---|---|---|---|---|
| Accel Pharma Inc. | ACCEL-CANDESARTAN DIN 02463784 |
32 | 1805003937 | 2020-02-29 | Non- détecté | Non- détecté | Non | 20 decembre 2018 |
| Actavis Pharma Company | ACT VALSARTAN DIN 02337517 |
320 | K44166 | 2018-07-31 | 15242.72Tableau 1 Note de bas de page 1 | 12.78 | Oui | 20 decembre 2018 |
| Actavis Pharma Company | ACT VALSARTAN DIN 02337517 |
320 | K45371 | 2018-10-31 | 10770.86Tableau 1 Note de bas de page 1 | 186.67Tableau 1 Note de bas de page 1 | Oui | 20 decembre 2018 |
| Actavis Pharma Company | ACT- OLMESARTAN DIN 02442205 |
40 | F83746 | 2020-03-31 | Non- détecté | Non- détecté | Non | 20 decembre 2018 |
| Angita Pharma Inc. | AG-IRBESARTAN DIN 02474417 |
300 | IE317017AR | 2019-10-31 | Non- détecté | Non- détecté | Non | 20 decembre 2018 |
| Apotex Inc. | APO-OLMESARTAN/HCTZ DIN 02453614 |
40/12.5 | NF7704 | 2019-02-28 | Non- détecté | Non- détecté | Non | 20 decembre 2018 |
| Apotex Inc. | APO-OLMESARTAN/HCTZ DIN 02453614 |
40/12.5 | NN7635 | 2019-12-31 | Non- détecté | Non- détecté | Non | 20 decembre 2018 |
| Apotex Inc. | APO-LOSARTAN/HCTZ DIN 02371235 |
50/12.5 | NL1445 | 2019-08-31 | Non- détecté | Non- détecté | Non | 20 decembre 2018 |
| Apotex Inc. | APO-LOSARTAN DIN 02353512 |
100 | NL1461 | 2019-08-31 | Non- détecté | Non- détecté | Non | 20 decembre 2018 |
| AstraZeneca Inc. | ATACAND – CANDESARTAN DIN 02311658 |
32 | KL0275 | 2021-04-30 | Non- détecté | Non- détecté | Non | 20 decembre 2018 |
| Auro Pharma Inc. | AURO-CANDESARTAN HCT DIN 02421046 |
32/12.5 | WKSA18004-A | 2020-07-29 | Non- détecté | Non- détecté | Non | 20 decembre 2018 |
| Auro Pharma Inc. | AURO-IRBESARTAN DIN 02406098 |
75 | IA7517001-A | 2020-06-30 | Non- détecté | 4.7 | Non | 29 avril 2019 |
| Auro Pharma Inc. | AURO-IRBESARTAN DIN 02406098 |
75 | IA7517002-A | 2020-11-05 | Non- détecté | 4.44 | Non | 29 avril 2019 |
| Auro Pharma Inc. | AURO-IRBESARTAN DIN 02406098 |
75 | IA7517003-A | 2020-11-05 | Non- détecté | 4.61 | Non | 29 avril 2019 |
| Auro Pharma Inc. | AURO-IRBESARTAN DIN 02406101 |
150 | IA1517002-A | 2020-10-31 | Non- détecté | 9.77 | Non | 29 avril 2019 |
| Auro Pharma Inc. | AURO-IRBESARTAN DIN 02406101 |
150 | IA1517001-A | 2020-06-30 | Non- détecté | 13.63Tableau 1 Note de bas de page 2 | NonTableau 1 Note de bas de page 2 | 29 avril 2019 |
| Auro Pharma Inc. | AURO-IRBESARTAN DIN 02406101 |
150 | IA1517003-A | 2020-10-31 | Non- détecté | 8.97 | Non | 29 avril 2019 |
| Auro Pharma Inc. | AURO-IRBESARTAN DIN 02406128 |
300 | IA3017001-A | 2020-06-30 | Non- détecté | 27.81Tableau 1 Note de bas de page 2 | NonTableau 1 Note de bas de page 2 | 29 avril 2019 |
| Auro Pharma Inc. | AURO-IRBESARTAN DIN 02406128 |
300 | IA3017003-A | 2020-10-31 | Non- détecté | 17.47 | Non | 29 avril 2019 |
| Auro Pharma Inc. | AURO-IRBESARTAN DIN 02406128 |
300 | IA3017002-A | 2020-10-31 | Non- détecté | 19.6 | Non | 29 avril 2019 |
| Auro Pharma Inc. | AURO-IRBESARTAN HCT DIN 02447894 |
300/25 | IN3018001-A | 2020-04-06 | Non- détecté | 26.78Tableau 1 Note de bas de page 2 | NonTableau 1 Note de bas de page 2 | 29 avril 2019 |
| Auro Pharma Inc. | AURO-IRBESARTAN HCT DIN 02447886 |
300/12.5 | IR3018001-A | 2020-04-06 | Non- détecté | 30.29 | Le lot n'a jamais été distribué | 29 avril 2019 |
| Auro Pharma Inc. | AURO-IRBESARTAN HCT DIN 02447878 |
150/12.5 | IN1518001-A | 2020-04-06 | Non- détecté | 15.82Tableau 1 Note de bas de page 1 | Oui | 29 avril 2019 |
| Auro Pharma Inc. | AURO-OLMESARTAN DIN 02443872 |
40 | WOSB18004-A | 2020-01-12 | Non- détecté | Non- détecté | Non | 20 decembre 2018 |
| Auro Pharma Inc. | AURO-LOSARTAN DIN 02403358 |
100 | WB1018003-A | 2021-03-15 | Non- détecté | Non- détecté | Non | 20 decembre 2018 |
| Auro Pharma Inc. | AURO-VALSARTAN DIN 02414201 |
40 | VWSA17003-A | 2019-10-31 | Non- détecté | 1.41 | Non | 16 janvier 2019 |
| Auro Pharma Inc. | AURO-VALSARTAN DIN 02414201 |
40 | VWSA18007-A | 2020-08-24 | Non- détecté | 1.07 | Non | 16 janvier 2019 |
| Auro Pharma Inc. | AURO-VALSARTAN DIN 02414201 |
40 | VWSA18003-A | 2020-08-23 | Non- détecté | 1.04 | Non | 16 janvier 2019 |
| Auro Pharma Inc. | AURO-VALSARTAN DIN 02414228 |
80 | VWSB17010-A | 2019-07-31 | Non- détecté | Non- détecté | Non | 16 janvier 2019 |
| Auro Pharma Inc. | AURO-VALSARTAN DIN 02414228 |
80 | VWSB17011-A | 2019-07-31 | Non- détecté | Non- détecté | Non | 16 janvier 2019 |
| Auro Pharma Inc. | AURO-VALSARTAN DIN 02414236 |
160 | VWSC17001-A | 2018-12-31 | Non- détecté | < 3.20 | Non | 16 janvier 2019 |
| Auro Pharma Inc. | AURO-VALSARTAN DIN 02414236 |
160 | VWSC17005-A | 2019-05-31 | Non- détecté | < 3.20 | Non | 16 janvier 2019 |
| Auro Pharma Inc. | AURO-VALSARTAN DIN 02414236 |
160 | VWSC18002-A | 2020-01-19 | Non- détecté | 4.58 | Non | 16 janvier 2019 |
| Auro Pharma Inc. | AURO-VALSARTAN DIN 02414236 |
160 | VWSC18001-A | 2020-01-19 | < 6.40 | 4.39 | Non | 16 janvier 2019 |
| Auro Pharma Inc. | AURO-VALSARTAN DIN 02414236 |
160 | VWSC18016-A | 2020-08-24 | Non- détecté | 4.7 | Non | 16 janvier 2019 |
| Auro Pharma Inc. | AURO-VALSARTAN DIN 02414244 |
320 | VWSD17001-B | 2019-05-31 | Non- détecté | Non- détecté | Non | 16 janvier 2019 |
| Auro Pharma Inc. | AURO-VALSARTAN DIN 02414244 |
320 | VWSD18005-A | 2020-08-25 | Non- détecté | 12.14 | Non | 16 janvier 2019 |
| Auro Pharma Inc. | AURO-VALSARTAN DIN 02414244 |
320 | VWSD18001-A | 2020-04-15 | Non- détecté | 8.56 | Non | 16 janvier 2019 |
| Auro Pharma Inc. | AURO-VALSARTAN DIN 02414244 |
320 | VWSD18001-A | 2020-04-15 | Non- détecté | 8.61 | Non | 20 decembre 2018 |
| Auro Pharma Inc. | AURO-VALSARTAN HCT DIN 02408112 |
80/12.5 | HHSA18001-A | 2021-08-02 | Non- détecté | 1.88 | Non | 16 janvier 2019 |
| Jamp Pharma Corp | JAMP-OLMESARTAN DIN 02461668 |
40 | MC218002A | 2020-04-30 | Non- détecté | Non- détecté | Non | 20 decembre 2018 |
| Jamp Pharma Corp | JAMP-LOSARTAN-HCTZ DIN 02408252 |
100/25 | LY218001A | 2019-06-30 | Non- détecté | Non- détecté | Non | 20 decembre 2018 |
| Jamp Pharma Corp | JAMP-IRBESARTAN DIN 02418215 |
300 | IE318005A | 2020-03-31 | Non- détecté | Non- détecté | Non | 20 decembre 2018 |
| Merck Canada Inc. | OLMETEC – OLMESARTAN DIN 02318679 |
40 | N021852 | 2020-04-30 | Non- détecté | Non- détecté | Non | 20 decembre 2018 |
| Mint Pharmaceuticals Inc. | MINT-LOSARTAN/HCTZ DS DIN 02389673 |
100/25 | 1805009844 | 2021-07-31 | Non- détecté | Non- détecté | Non | 20 decembre 2018 |
| Mylan Pharmaceuticals ULC | MYLAN-VALSARTAN DIN 02383527 |
40 | 3048813 | 2017-11-30 | < 1.60 | 8.32 | Oui | 16 janvier 2019 |
| Mylan Pharmaceuticals ULC | MYLAN-VALSARTAN DIN 02383535 |
80 | 3056368 | 2019-06-30 | < 3.20 | 22.43 | Oui | 16 janvier 2019 |
| Mylan Pharmaceuticals ULC | MYLAN-VALSARTAN DIN 02383543 |
160 | 3056371 | 2019-06-30 | Non- détecté | 62.76 | Oui | 16 janvier 2019 |
| Mylan Pharmaceuticals ULC | MYLAN-VALSARTAN DIN 02383551 |
320 | 3048815 | 2017-11-30 | Non- détecté | 132.77 | Oui | 16 janvier 2019 |
| Nonvartis Pharmaceuticals Canada Inc. | DIOVAN DIN 02289504 |
320 | BEK32 | 2021-07-31 | Non- détecté | Non- détecté | Non | 20 decembre 2018 |
| Pharmascience Inc. | PMS-CANDESARTAN HCTZ DIN 02391295 |
16 | 615170 | 2020-04-30 | Non- détecté | Non- détecté | Non | 20 decembre 2018 |
| Pharmascience Inc. | PMS-LOSARTAN DIN 02309777 |
100 | 613936 | 2021-03-31 | Non- détecté | 10.41 | Non | 20 decembre 2018 |
| Pharmascience Inc. | PMS-LOSARTAN-HCTZ DIN 02392232 |
100/12.5 | 0803847 | 2020-06-30 | Non- détecté | Non- détecté | Non | 20 decembre 2018 |
| Pharmascience Inc. | PMS-IRBESARTAN DIN 02317087 |
300 | 615908 | 2021-03-31 | Non- détecté | Non- détecté | Non | 20 decembre 2018 |
| Pharmascience Inc. | PMS-IRBESARTAN-HCTZ DIN 02328526 |
300/12.5 | 606524 | 2018-11-30 | Non- détecté | Non- détecté | Non | 20 decembre 2018 |
| Pharmascience Inc. | PMS-IRBESARTAN-HCTZ DIN 02328526 |
300/12.5 | 611016 | 2019-11-30 | Non- détecté | Non- détecté | Non | 20 decembre 2018 |
| Ranbaxy Pharmaceuticals Canada Inc. | RAN-VALSARTAN DIN 02363119 |
160 | 2884804 | 2019-05-31 | Non- détecté | Non- détecté | Non | 20 decembre 2018 |
| Sandoz Canada Inc. | SANDOZ CANDESARTAN DIN 02417340 |
32 | JC3223 | 2020-06-30 | Non- détecté | Non- détecté | Non | 20 decembre 2018 |
| Sandoz Canada Inc. | SANDOZ CANDESARTAN PLUS DIN 02420732 |
32 | HY8217 | 2020-04-30 | Non- détecté | Non- détecté | Non | 20 decembre 2018 |
| Sandoz Canada Inc. | SANDOZ OLMESARTAN DIN 02443422 |
40 | HX2039 | 2020-02-28 | Non- détecté | Non- détecté | Non | 20 decembre 2018 |
| Sandoz Canada Inc. | SANDOZ LOSARTAN DIN 02313359 |
100 | JD6746 | 2020-04-30 | Non- détecté | Non- détecté | Non | 20 decembre 2018 |
| Sandoz Canada Inc. | SANDOZ VALSARTAN DIN 02356775 |
320 | HW4965 | 2020-12-31 | 2703.76Tableau 1 Note de bas de page 1 | Non- détecté | Oui | 20 decembre 2018 |
| Sandoz Canada Inc. | SANDOZ IRBESARTAN DIN 02328496 |
300 | HX4282 | 2020-01-31 | Non- détecté | Non- détecté | Non | 20 decembre 2018 |
| Sandoz Canada Inc. | SANDOZ IRBESARTAN DIN 02328496 |
300 | JD1818 | 2020-05-31 | Non- détecté | Non- détecté | Non | 20 decembre 2018 |
| Sanis Health Inc. | IRBESARTAN DIN 02372398 |
300 | 35213058A | 2019-12-31 | Non- détecté | Non- détecté | Non | 20 decembre 2018 |
| SaNonfi-Aventis Canada Inc. | AVAPRO – IRBESARTAN DIN 02237925 |
300 | KC001 | 2020-01-31 | Non- détecté | Non- détecté | Non | 20 decembre 2018 |
| Septa Pharmaceuticals Inc. | SEPTA-LOSARTAN DIN 02424983 |
100 | LR318004A | 2020-03-31 | Non- détecté | Non- détecté | Non | 20 decembre 2018 |
| Sivem Pharmaceuticals Inc. | LOSARTAN HCT DIN 02388987 |
100/25 | QX1018005-B | 2021-06-08 | Non- détecté | Non- détecté | Non | 20 decembre 2018 |
| Sivem Pharmaceuticals Inc. | IRBESARTAN DIN 02385309 |
300 | HX7687 | 2019-12-31 | Non- détecté | Non- détecté | Non | 20 decembre 2018 |
| Sivem Pharmaceuticals Inc. | IRBESARTAN HCT DIN 02385325 |
300/12.5 | HY7380 | 2020-11-30 | Non- détecté | Non- détecté | Non | 20 decembre 2018 |
| Teva Canada Limited | TEVA-CANDESARTAN DIN 02366339 |
32 | 2537058 | 2020-05-31 | Non- détecté | Non- détecté | Non | 20 decembre 2018 |
| Teva Canada Limited | TEVA-LOSARTAN DIN 02357976 |
100 | 2070318 | 2021-03-31 | Non- détecté | Non- détecté | Non | 20 decembre 2018 |
| Teva Canada Limited | TEVA-LOSARTAN/HCTZ DIN 02358263 |
50/12.5 | 35349397A | 2020-09-30 | Non- détecté | 10.3 | Non | 20 decembre 2018 |
| Teva Canada Limited | TEVA-IRBESARTAN DIN 02316412 |
300 | 35213086A | 2019-12-31 | Non- détecté | Non- détecté | Non | 20 decembre 2018 |
| Teva Canada Limited | TEVA-VALSARTAN DIN 02356686 |
320 | 35211729R | 2019-03-31 | Non- détecté | Non- détecté | Non | 20 decembre 2018 |
| Teva Canada Limited | TEVA-VALSARTAN/HCTZ DIN 02357038 |
320/12.5 | 35212732 | 2019-10-31 | 14538.35Tableau 1 Note de bas de page 1 | Non- détecté | Le lot n'a jamais été distribué | 20 decembre 2018 |
| Teva Canada Limited | TEVA-VALSARTAN/HCTZ DIN 02357038 |
320/12.5 | 35211546R | 2019-01-31 | 258.19Tableau 1 Note de bas de page 1 | 1770.87 | Oui | 20 decembre 2018 |
| Teva Canada Limited | TEVA-VALSARTAN/HCTZ DIN 02357046 |
320/25 | 35212731R | 2019-11-30 | 13367.64Tableau 1 Note de bas de page 1 | Non- détecté | Oui | 20 decembre 2018 |
|
||||||||
Résulats des analyses pour les produits de ranitidine
Santé Canada a testé des échantillons de produits de ranitidine sur le marché canadien pour la NDMA. Nous avons établi une limite de concentration provisoire acceptable de 0,32 ppm pour la NDMA en fonction d'une dose quotidienne maximale recommandée de 300 mg.
Les résultats, présentés dans le tableau ci-dessous, indiquent :
- le niveau de NDMA détecté
- si le produit a été rappelé
Nous continuerons d'évaluer les nouveaux développements afin de déterminer si d'autres analyses sont nécessaires.
| Nom du détenteur d'autorisation de mise en marché (nom de la compagnie) | Nom du produit et DIN | Force (mg) | Numéro du lot | Date d'expiration | NDMA (ppm)Tableau 2 Note de bas de page 1 |
Produit rappelé |
|---|---|---|---|---|---|---|
| Laboratoire Riva Inc | OPTION+ Acid Reducer (75 mg) DIN 02452464 | 75 | 612043-B | 2020-05-30 | 0.1099 | Oui |
| Pharmascience Inc | LIFE BRAND Acid Reducer (150 mg) DIN 02400103 | 150 | 617496 | 2020-10-31 | 0.0816 | Oui |
| Pharmascience Inc | REXALL Acid Reducer 02247551 |
75 | 611186D | 2020-04-30 | 0.4779Tableau 2 Note de bas de page 2 | Oui |
| Pharmascience Inc | Equate Acid Reducer 02293471 | 150 | 618318 | 2020-10-31 | 0.0707 | Oui |
| Sanofi Consumer Health Inc Sanofi Sante Grand Public Inc | ZANTAC 02230287 | 75 | AK4388 | 2021-11-30 | 0.2452 | Oui |
| Sanofi Consumer Health Inc Sanofi Sante Grand Public Inc | ZANTAC 02277301 | 150 | AK6951 | 2021-01-31 | 0.0904 | Oui |
| Vita Health Products Inc | Equate Acid Reducer 02298740 | 75 | 8E228B4RKB | 2020-06-30 | 0.1246 | Oui |
| Vita Health Products Inc | Equate Acid Reducer 02298902 | 150 | 6152524N3J | 2020-12-31 | 0.0526 | Oui |
|
||||||
Résulats des analyses pour les produits de metformine
Santé Canada a testé des échantillons de produits de metformine sur le marché canadien pour la NDMA. Nous avons établi une limite de concentration provisoire acceptable de 0,0376 ppm pour la NDMA pour les produits pharmaceutiques avec une dose quotidienne maximale de 2,55 g/jour et de 0,048 ppm pour les produits pharmaceutiques avec une dose quotidienne maximale de 2 g/jour.
Les résultats, présentés dans le tableau ci-dessous, indiquent :
- le niveau de NDMA détecté
- si le produit a été rappelé
Nous continuerons d'évaluer les nouveaux développements afin de déterminer si d'autres analyses sont nécessaires.
| Nom du détenteur d'autorisation de mise en marché (nom de la compagnie) | Nom du produit et DIN | Force (mg) | Numéro du lot | Date d'expiration | NDMA (ppm)Tableau 3 Note de bas de page 1 |
Produit rappelé |
|---|---|---|---|---|---|---|
| Apotex Inc | Apo-Metformin ER 02305062 | 500 | PK3968 | 2020-09-30 | 0.044 ppm | Oui |
| Apotex Inc | Apo-Metformin ER 02460653 | 1000 | PY5749 | 2021-03-31 | NDTableau 3 Note de bas de page 2 | Non |
| Astrazeneca Canada Inc | Xigduo 02449943 | 5/1000 | X1032A | 2022-07-31 | ND | Non |
| Astrazeneca Canada Inc | Komboglyze 02389185 | 2.5/1000 | RB696 | 2022-04-30 | ND | Non |
| Auro Pharma Inc | Auro-Metformin 02438283 | 850 | MR19008-85A | 2022-04-15 | ND | Non |
| Auro Pharma Inc | Auro-Metformin 02438275 | 500 | MR19054-50A | 2022-04-28 | ND | Non |
| Boehringer Ingelheim (Canada) Ltd Ltee | Jentadueto 02403250 | 2.5/500 | 960201 | 2021-11-05 | ND | Non |
| Boehringer Ingelheim (Canada) Ltd Ltee | Jentadueto 02403277 | 2.5/1000 | 960205 | 2022-05-19 | ND | Non |
| Boehringer Ingelheim (Canada) Ltd Ltee | Jentadueto 02403269 | 2.5/850 | 958144 | 2022-03-26 | ND | Non |
| Boehringer Ingelheim (Canada) Ltd Ltee | Synjardy 02456591 | 5/1000 | 960496 | 2022-04-13 | ND | Non |
| Dominion Pharmacal | Dom-Metformin [Metformin 850] 02242726 | 850 | 624624 | 2021-09-30 | ND | Non |
| Jamp Pharma Corporation | Jamp-Metformin 02380218 | 850 | X20386 | 2020-07-31 | ND | Oui |
| Janssen Inc | Invokamet 02455455 | 150/1000 | JIL0T01 | 2022-04-30 | ND | Non |
| Laboratoire Riva Inc | Riva-Metformin 02242783 | 850 | C8385 | 2020-12-31 | ND | Non |
| Merck Canada Inc | Janumet Xr 02416786 | 50/500 | R017925 | 2020-04-22 | Detected; < LOQTableau 3 Note de bas de page 3 | Non |
| Merck Canada Inc | Janumet 02333872 | 50/1000 | R017774 | 2020-04-20 | ND | Non |
| Merck Canada Inc | Janumet 02333864 | 50/850 | R031038 | 2020-08-12 | ND | Non |
| Merck Canada Inc | Janumet 02333856 | 50/500 | N020597 | 2020-04-30 | ND | Non |
| Merck Canada Inc | Janumet Xr 02416794 | 50/1000 | R015954 | 2020-04-21 | Detected; < LOQ | Non |
| Merck Canada Inc | Janumet Xr 02416808 | 100/1000 | R019378 | 2020-04-28 | Detected; < LOQ | Non |
| Mint Pharmaceuticals Inc | Mint-Metformin 02388774 | 850 | XB10217 | 2020-05-31 | Detected; < LOQ | Non |
| Mylan Pharmaceuticals Ulc | Mylan-Metformin [Metformin 850] 02229656 | 850 | 4680005A | 2020-08-31 | ND | Non |
| Pharmascience Inc | Pms-Metformin [Metformin 850] 02242589 | 850 | 624407 | 2021-08-31 | ND | Non |
| Pharmascience Inc | Pms-Metformin -Tab 500mg [Metformin 500] 02223562 | 500 | 624584 | 2021-08-31 | ND | Non |
| Pro Doc Limitee | Pro-Metformin 02314894 | 850 | 624623 | 2021-09-30 | ND | Non |
| Ranbaxy Pharmaceuticals Canada Inc. | Ran-Metformin 02269058 | 850 | AJZ8003A | 2020-04-30 | Detected; < LOQ | Non |
| Sandoz Canada Incorporated | Sandoz Metformin Fc 02246820 | 500 | HZ0133 | 2020-11-30 | ND | Non |
| Sandoz Canada Incorporated | Sandoz Metformin Fc 02246820 | 500 | HT4634 | 2020-07-31 | ND | Non |
| Sandoz Canada Incorporated | Sandoz Metformin Fc 02246820 | 500 | JD7946 | 2021-06-30 | ND | Non |
| Sandoz Canada Incorporated | Sandoz Metformin Fc 02246820 | 500 | HL3031 | 2020-08-31 | ND | Non |
| Sandoz Canada Incorporated | Sandoz Metformin Fc 02246821 | 850 | JR3918 | 2022-01-31 | ND | Non |
| Sanis Health Inc | Metformin 02353385 | 850 | JJ1245 | 2021-05-31 | ND | Non |
| Sanis Health Inc | Metformin 02353385 | 850 | JD0660 | 2021-05-31 | ND | Non |
| Sanis Health Inc | Metformin 02353377 | 500 | JN3158 | 2021-10-31 | ND | Non |
| Sanofi-Aventis Canada Inc | Glucophage 02162849 | 850 | 8123285 | 2022-08-31 | ND | Non |
| Sivem Pharmaceuticals Ulc | Metformin Fc 02385341 | 500 | JW5467 | 2022-04-30 | ND | Non |
| Sivem Pharmaceuticals Ulc | Metformin Fc 02385368 | 850 | JR3921 | 2022-01-31 | ND | Non |
| Sivem Pharmaceuticals Ulc | Metformin Fc 02385368 | 850 | JW8773 | 2022-05-31 | ND | Non |
| Takeda Canada Inc | Kazano 02417235 | 12.5/1000 | 11616020 | 2021-05-31 | ND | Non |
| Teva Canada Limited | Ratio-Metformin 02242931 | 850 | 35212386A | 2020-03-31 | ND | Non |
| Teva Canada Limited | Act Metformin 02257726 | 500 | 4770082F | 2021-05-31 | ND | Non |
| Teva Canada Limited | Act Metformin 02257734 | 850 | 4780009F | 2020-10-31 | ND | Non |
| Valeant Canada Lp/Valeant Canada S.E.C. | Glumetza 02300451 | 1000 | 19L031P | 2022-10-31 | 0.032 ppm | Non |
|
||||||
Détails de la page
- Date de modification :