ARCHIVÉE - Liste des substances d'intérêt prioritaire - Rapport d'évaluation pour les sels de voirie
Environnement Canada
Santé Canada
2001
ISBN : 0-662-86219-8
No de catalogue : En40-215/63F
Loi canadienne sur la protection de l'environnement 1999
Table des matières
- Liste des abréviations
- Synopsis
- 1.0 Introduction
- 2.0 Résumé de l'information essentielle à l'évaluation des sels de voirie
- 2.1 Identité, propriétés, production et sources
- 2.2 Charges de sels de voirie
- 2.3 Élimination de la neige
- 2.4 Entrepôts de sels
- 2.5 Devenir et pénétration dans l'environnement
- 2.6 Concentrations de chlorure dans les eaux de surface au Canada
- 2.6.1 Carte des concentrations de chlorure dans les bassins versants du Canada
- 2.6.2 Concentrations dans l'environnement : lacs et rivières
- 2.6.2.1 Région de l'Atlantique (Terre-Neuve, Nouvelle-Écosse, Nouveau-Brunswick et Île-du-Prince-Édouard)
- 2.6.2.2 Région du centre (Ontario et Québec)
- 2.6.2.3 Région des Prairies (Manitoba, Saskatchewan, Alberta)
- 2.6.2.4 Région du Pacifique (Colombie-Britannique)
- 2.6.2.5 Yukon, Territoires du Nord-Ouest et Nunavut
- 2.6.3 Concentrations dans l'environnement : sédiments benthiques
- 2.6.4 Concentrations dans l'environnement : terres humides
- 2.6.5 Concentrations dans l'environnement : lacs et étangs urbains
- 2.6.6 Concentrations de chlorure basées sur le bilan massique
- 2.6.7 Sommaire
- 3.0 Évaluation du caractère " toxique " au sens de la LCPE 1999
- 3.1 Évaluation en vertu des alinéas 64a) - Environnement et 64b Environnement essentiel pour la vie de la LCPE de 1999
- 3.2 Eaux souterraines
- 3.3 Écosystèmes aquatiques
- 3.3.1 Méthode d'évaluation et d'établissement de la portée
- 3.3.2 Études en laboratoire
- 3.3.3 Évaluation de la toxicité pour les écosystèmes aquatiques
- 3.3.3.1 Caractérisation du risque selon le quotient
- 3.3.3.2 Évaluations de niveaux 1 et 2
- 3.3.3.3 Évaluations de niveau 3 avec validation sur le terrain
- 3.3.3.3.1 Étude de cas no 1 : Effets du ruissellement des sels de voirie sur les ruisseaux, cours d'eau et petites rivières de régions urbaines densément peuplées
- 3.3.3.3.2 Étude de cas no 2 : Effets du ruissellement des sels de voirie sur les ruisseaux, cours d'eau et rivières de régions moins densément peuplées
- 3.3.3.3.3 Étude de cas no 3 : Effets du ruissellement des sels de voirie sur les étangs et les lacs en milieux urbains
- 3.3.3.3.4 Étude de cas no 4 : Effets du ruissellement routier sur les lacs et étangs en milieux ruraux
- 3.3.3.3.5 Étude de cas no 5 : Lieux d'entreposage de sels et écosystèmes aquatiques
- 3.3.3.3.6 Cas no 6 : Lieux d'élimination de la neige
- 3.3.3.4 Autres effets
- 3.3.3.5 Conclusions pour les écosystèmes aquatiques
- 3.4 Sols
- 3.5 Végétation terrestre
- 3.5.1 Évaluation environnementale prudente
- 3.5.2 Évaluation environnementale détaillée - Analyse basée sur les valeurs-seuils
- 3.5.2.1 Réaction à la présence de sodium dans le sol
- 3.5.2.2 Réaction à la présence de chlorure dans le sol
- 3.5.2.3 Réaction à la présence de chlorure de sodium dans le sol
- 3.5.2.4 Réaction au sodium et au chlorure par dispersion aérienne
- 3.5.2.5 Évaluation environnementale détaillée - résumé de l'analyse basée sur les valeurs-seuils
- 3.5.3 Évaluation environnementale détaillée - analyse des lieux de référence
- 3.5.3.1 Propagation d'espèces végétales halophiles
- 3.5.3.2 Changements dans les communautés d'un marais perturbé par les sels de voirie
- 3.5.3.3 Effets de la dispersion de sels provenant d'une autoroute à quatre voies sur des vergers de pêches et de prunes de Grimsby (Ontario)
- 3.5.3.4 Effets de la dispersion de sels provenant d'une autoroute à quatre voies sur des vergers de pêches et de prunes situés près de St. Catharines (Ontario)
- 3.5.3.5 Effets de la dispersion de sels provenant d'une autoroute à deux voies sur des bleuets, dans l'ouest de la Nouvelle-Écosse
- 3.5.3.6 Concentrations dans le sol et les plantes ligneuses aux abords d'autoroutes dans l'intérieur de la Colombie-Britannique
- 3.5.3.7 Concentrations dans le sol et le feuillage de plantes ligneuses le long d'une autoroute à deux voies de la Colombie-Britannique
- 3.5.3.8 Concentrations dans le feuillage de plantes ligneuses longeant une autoroute à deux voies du Connecticut
- 3.5.3.9 Concentrations dans le sol et le feuillage de plantes ligneuses et herbacées, le long de routes du Massachusetts
- 3.5.3.10 Concentrations dans le sol et les plantes ligneuses, en aval d'une autoroute à quatre voies de la Colombie-Britannique
- 3.5.3.11 Concentrations dans le sol et le feuillage d'espèces ligneuses, à proximité d'un entrepôt de sels
- 3.5.4 Modifications des taux d'épandage et dommages actuellement observés au Canada
- 3.5.5 Estimation de la superficie à risque
- 3.5.6 Résumé de l'évaluation des risques et conclusions
- 3.6 Faune terrestre
- 3.7 Ferrocyanures
- 3.7.1 Caractérisation de l'exposition
- 3.7.2 Concentrations mesurées et estimées dans l'environnement
- 3.7.3 Caractérisation des effets
- 3.7.4 Caractérisation du risque
- 3.7.5 Conclusion pour les ferrocyanures
- 3.8 Conclusions globales
- 3.9 Considérations pour le suivi (mesures à prendre)
- 4.0 Références
Annexes
Liste des tableaux
- Tableau 1 Propriétés physico-chimiques des sels de voirie
- Tableau 2 Charges totales de chlorure de sodium sur les routes, hiver 1997-1998 (d'après Morin et Perchanok, 2000)
- Tableau 3 Quantités estimatives de chlorure de calcium épandues sur les routes, au cours d'une année normale (d'après Morin et Perchanok, 2000)
- Tableau 4 Charges totales de chlorure (d'après Morin et Perchanok, 2000)
- Tableau 5 Volume total de neige usée et quantité de sels utilisée dans certaines villes canadiennes, durant l'hiver 1997-1998 (d'après Delisle et Dériger, 2000)
- Tableau 6 Méthodes d'élimination de la neige utilisées dans certaines villes canadiennes, durant l'hiver 1997-1998 (d'après Delisle et Dériger, 2000)
- Tableau 7 Nombre d'entrepôts provinciaux de sels et quantité de chlorure de sodium et d'abrasifs utilisée, par province (d'après Snodgrass et Morin, 2000)
- Tableau 8 Estimation de l'importance des pertes de sels provenant des entrepôts (d'après Snodgrass et Morin, 2000)
- Tableau 9 Concentrations de chlorure dans divers cours d'eau du bassin visés par le Plan d'assainissement de la Communauté urbaine de Toronto, entre 1990 et 1996 (d'après la Toronto and Region Conservation Authority, 1998)
- Tableau 10 Réactions des organismes à la toxicité du chlorure de sodium, après une exposition de moins d'une journée (d'après Evans et Frick, 2001)
- Tableau 11 Réactions des organismes à la toxicité du chlorure de sodium, après une exposition d'une journée (d'après Evans et Frick, 2001)
- Tableau 12 Valeurs de la CL50 après 4 jours pour divers taxons exposés au chlorure de sodium (d'après Evans et Frick, 2001)
- Tableau 13 Valeurs de la CL50 et de la CE50 pour divers taxons, après une exposition de 7 à 10 jours au chlorure de sodium1 (d'après Evans et Frick, 2001)
- Tableau 14 Résumé des évaluations de niveau 2 (d'après Evans et Frick, 2001)
- Tableau 15 Valeurs optimales du pH, du phosphore total et du chlorure pour certaines espèces de diatomées dans le nord-est des États-Unis (d'après Dixit et al., 1999)
- Tableau 16 Tolérance de certaines espèces végétales au chlorure de sodium dans une section du lit du marais Pinhook (Indiana), qui avait été perturbée par les sels (d'après Wilcox, 1982)
- Tableau 17 Pourcentage cumulatif prévu d'espèces touchées par une exposition chronique au chlorure (d'après Evans et Frick, 2001)
- Tableau 18 Valeurs modélisées de la conductivité électrique et des concentrations de chlorure dans le ruisseau Corbett, en aval de l'entrepôt de sels de voirie de Fredericton
- Tableau 19 Liste d'espèces d'arbres et d'arbustes évalués en fonction de leur résistance aux sels de voirie aéroportés (d'après Lumis et al., 1983)
- Tableau 20 Liste des essences forestières indigènes, en fonction de leur résistance aux sels de voirie aéroportés
- Tableau 21 Intervalle des valeurs-seuils estimées dans le sol et l'eau, pour divers types de végétaux (d'après Cain et al., 2001)
- Tableau 22 Intervalle des valeurs-seuils estimées dans les tissus de plantes herbacées, après une exposition en solution du sol ou solution aqueuse (d'après Cain et al., 2001)
- Tableau 23 Intervalle des valeurs-seuils estimées dans les tissus de plantes ligneuses, après une exposition atmosphérique (d'après Cain et al., 2001)
- Tableau 24 Calcul du nombre de particules de sel qu'un oiseau doit ingérer pour atteindre la VCT, sur la base d'un moineau domestique de 28 g consommant des particules dont la taille se situe à l'extrémité supérieure de ses préférences connues
- Tableau 25 Calcul du nombre de particules de sel devant être ingérées pour atteindre la VCT, chez un moineau domestique de 28 g consommant des particules de taille moyenne
- Tableau 26 Résultats du calcul des quotients pour le biote aquatique - Niveau 1 (d'après Letts, 2000a)
- Tableau 27 Résultats du calcul des quotients pour le biote terrestre - Niveau 1 (d'après Letts, 2000a)
Liste des figures
- Figure 1 Segment régional du réseau routier provincial (d'après Morin et Perchanok, 2000)
- Figure 2 Taux d'épandage de sel de voirie (chlorure de sodium) par agence provinciale en 1998 (d'après Morin et Perchanok, 2000)
- Figure 3 Taux d'épandage moyen de sels de voirie (chlorure de sodium) par municipalité en 1998 (d'après Morin et Perchanok, 2000)
- Figure 4 Quantités totales de chlorure de sodium utilisées par district d'entretien (d'après Morin et Perchanok, 2000)
- Figure 5 Historique de l'utilisation de sel de voirie par les agences provinciales (fondée sur les enquêtes du « Salt Institute 1964-1983 » et Morin et Perchanok, 2000)
- Figure 6 Concentration moyenne quotidienne en 1975-1976 des lixiviats provenant d'un d'un amas d'abrasif mélangé avec du sel (d'après ME et MT NB, 1978)
- Figure 7 Concentration de chlorure dans deux puits d'approvisionnement de Heffley Creek (d'après AGRA, 1999)
- Figure 8 Le transport du sel de voirie à partir des routes
- Figure 9 Les concentrations de chlorure observées dans les bassins versants canadiens (d'après Mayer et al., 2000)
- Figure 10 Estimation de la concentration de chlorure à partir de la charge annuelle moyenne de sels de voirie (NaCl) et du ruissellement (d'après Mayer et al., 2000)
- Figure 11 Estimation de la concentration de chlorure dans le ruissellement provenant des routes provinciales au Canada
- Figure 12 Estimation de la concentration de chlorure dans les eaux souterraines à divers taux d'épandage et à un taux d'alimentation des eaux souterraines de 10 cm/an (d'après Johnston et al., 2000)
- Figure 13 Estimation de la concentration de chlorure dans les eaux souterraines à divers taux d'épandage et à un taux d'alimentation des eaux souterraines de 20 cm/an (d'après Johnston et al., 2000)
- Figure 14 Estimation de la concentration de chlorure dans les eaux souterraines à divers taux d'épandage et à un taux d'alimentation des eaux souterraines de 40 cm/an (d'après Johnston et al., 2000)
- Figure 15 Concentration de chlorure dans les eaux souterraines des puits d'approvisionnement municipaux dans le Sud de l'Ontario (d'après Johnston et al., 2000)
- Figure 16 Diversité des espèces dans différents gradients de salinité et de chlorure (d'après Wetzel, 1983)
- Figure 17 La toxicité aiguë expérimentale et toxicité chronique prévue pour les taxons aquatiques (d'après Evans et Frick, 2001)
- Figure 18 La contamination par les sels de voirie causant des effets biologiques défavorables à partir d'une brève exposition à des concentrations de chlorure dans l'environnement aquatique canadien
- Figure 19 La contamination par les sels de voirie causant des effets biologiques défavorables à partir d'une longue exposition à des concentrations de chlorure dans l'environnement aquatique canadien
- Figure 20 Régions où l'épandage de sels de voirie pose un danger faible, moyen ou élevée selon la teneur en argile du sol et du coefficient de sodium échangeable (d'après Morin et al., 2000)
- Figure 21 Le diagramme représente la conductivité électrique et les concentrations de chlorure dans l'eau de fossé longeant les deux routes près du dépôt de sel de voirie de Frédéricton pour les mois de juin, juillet et octobre 1999 et janvier 2000. Le diagramme démontre les données du 10e, 25e, 50e, 75e et 90e percentile ainsi que les données inférieures et supérieures aux 10e et 90e percentile (cercles). Les mots « bien-drainé », « écoulement croisé » et « stagnant » se réfèrent à trois conditions : crête à partir de laquelle l'eau est bien drainée; croisement d'un cours d'eau; et fossé sans écoulement (d'après Arp, 2001)
- Figure 22 Estimation par bassin versant et par municipalité des solides dissous totaux (SDT) et de la conductivité électrique (CE) moyenne des eaux du sol et de surface en Ontario et au Québec (d'après Morin et al., 2000)
- Figure 23 Pourcentage de sodium échangeable (PSE) le long des routes par district d'entretien provincial (d'après Morin et al., 2000)
- Figure 24 La tolérance au sel et le rendement des récoltes en fonction de la salinité du sol (conductivité électrique, CE) et le pourcentage estimé d'emprises routières ayant un niveau correspondant de CE (d'après Bresler et al., 1982)
Liste des Acronymes et des abréviations
CAS
Chemical Abstracts Service
CE
conductivité électrique
CE50
concentration efficace moyenne
CL50
concentration létale moyenne
CMEO
concentration minimale avec effet observé
CSEO
concentration sans effet observé
DL50
dose létale médiane
EES
évaluation environnementale d'un site
kg-p.c.
kilogramme de poids corporel
LCPE
Loi canadienne sur la protection de l'environnement
LCPE 1999
Loi canadienne sur la protection de l'environnement (1999)
LSIP
Liste des substances d'intérêt prioritaire
NMEO
niveau minimal avec effet observé
NSEO
niveau sans effet observé
VCT
valeur critique de la toxicité
VEE
valeur estimée de l'exposition
VESEO
valeur estimée sans effet observé
Synopsis
Les sels de voirie servent en hiver à l'entretien des routes (déglaçage et anti-glaçage) et, en été, à la réduction de la poussière. Les sels inorganiques de chlorure examinés dans la présente évaluation incluent le chlorure de sodium, le chlorure de calcium, le chlorure de potassium et le chlorure de magnésium. Dans l'environnement, ces sels se dissocient en un anion chlorure et son cation correspondant. On a en outre évalué les ferrocyanures, des additifs antiagglomérants ajoutés à certains sels de voirie. On estime qu'environ 4 750 000 tonnes de fondants au chlorure de sodium ont été épandues pendant l'hiver 1997-1998 et que 110 000 tonnes de chlorure de calcium sont utilisées sur les routes chaque année. On n'utilise que de très petites quantités des autres sels. D'après ces estimations, environ 4,9 millions de tonnes de sels de voirie peuvent être rejetées dans l'environnement au Canada chaque année, soit environ 3,0 millions de tonnes de chlorure. Les charges annuelles en sels de voirie sont les plus fortes en Ontario et au Québec, moyennes dans les provinces de l'Atlantique, et les plus faibles dans les provinces de l'Ouest.
Les sels de voirie pénètrent dans l'environnement canadien à la suite de leur entreposage et de leur utilisation, et de l'élimination de la neige enlevée des routes. Ils pénètrent dans les eaux de surface, dans le sol et dans les eaux souterraines après la fonte des neiges, et sont dispersés dans l'atmosphère par les éclaboussures et la pulvérisation d'eau causées par les véhicules et par la poussière transportée par le vent. Les ions chlorure sont très conservatifs, c'est-à-dire qu'ils suivent le cycle de l'eau sans retard et sans perte. Par conséquent, presque tous les ions chlorure qui pénètrent dans le sol et les eaux souterraines atteindront éventuellement les eaux de surface : quelques années à quelques décennies ou plus peuvent être nécessaires pour que les concentrations dans les eaux souterraines atteignent l'état d'équilibre. Les préoccupations qui concernent les sels de voirie touchent tous les milieux environnementaux à cause de leur dispersion générale dans l'environnement.
Les concentrations de fond naturelles de chlorure dans l'eau sont généralement de quelques mg/L, avec quelques instances locales ou régionales de plus forte salinité naturelle, par exemple dans certaines régions des Prairies et de la Colombie-Britannique. On a mesuré de fortes concentrations de chlorure liées à l'épandage des sels de voirie sur les routes ou rejetés des entrepôts de sels ou des lieux d'entreposage de la neige. Par exemple, on rapporte des concentrations de chlorure supérieures à plus de 18 000 mg/L dans les eaux de ruissellement des routes. On a aussi observé des concentrations allant jusqu'à 82 000 mg/L dans les eaux de ruissellement des amas non recouverts de mélanges d'abrasifs et de sels d'un entrepôt de sel. Les concentrations de chlorure de la neige déblayée des rues des villes peuvent varier considérablement. Par exemple, les concentrations moyennes de chlorure de la neige provenant des rues de Montréal allaient de 3 000 à 5 000 mg/L respectivement pour les rues secondaires et primaires. Les eaux provenant des routes, des entrepôts de sels ou des lieux d'entreposage de la neige peuvent se diluer à divers degrés lorsqu'elles pénètrent dans l'environnement, où on a mesuré des concentrations de chlorure allant jusqu'à 2 800 mg/L dans les eaux souterraines de zones adjacentes à des entrepôts de sels, jusqu'à 4 000 mg/L dans des étangs et des milieux humides, jusqu'à 4 300 mg/L dans des cours d'eau, jusqu'à 2 000 à 5 000 mg/L dans des étangs urbains endigués et jusqu'à 150 à 300 mg/L dans des lacs ruraux. Alors que les plus fortes concentrations sont habituellement associées au dégel hivernal ou printanier, on peut également mesurer de fortes concentrations en été, en raison du temps que prennent les ions à parvenir aux eaux de surface et des débits réduits en été. Les plans d'eau les plus sujets aux impacts des sels de voirie sont les petits étangs et les cours d'eau qui drainent les grandes zones urbanisées, ainsi que les cours d'eau, les milieux humides ou les lacs qui drainent les grandes routes. Des mesures sur le terrain révèlent que l'épandage sur les routes dans les régions rurales peut augmenter les concentrations de chlorure même dans des lacs à quelques centaines de mètres des routes.
On a évalué la possibilité d'impacts sur les réseaux régionaux d'eaux souterraines à l'aide d'une technique de bilan massique qui donne une indication des concentrations de chlorure possibles en aval d'un réseau routier sur lequel il y a épandage de sel. Le modèle de bilan massique et les mesures sur le terrain ont indiqué qu'on pourrait voir des concentrations de chlorure supérieures à 250 mg/L dans les eaux souterraines régionales sous un réseau routier à forte densité sujet à des charges annuelles de plus de 20 tonnes de chlorure de sodium par kilomètre de route à 2 voies. D'après les données sur les charges de sels de voirie, les zones urbaines du sud de l'Ontario et du Québec et les provinces de l'Atlantique sont les plus menacées par les impacts sur les eaux souterraines régionales. Les eaux souterraines aboutissent dans les eaux de surface ou émergent sous forme d'infiltration et de sources. Des recherches ont montré que 10 à 60 % du sel épandu pénètre dans les eaux souterraines peu profondes et s'accumule jusqu'à ce qu'on atteigne des concentrations stabilisées. On a décelé des concentrations élevées de chlorure dans les sources d'eaux souterraines émergeant à la surface.
On observe habituellement des effets toxiques aigus sur les organismes aquatiques à des concentrations de chlorure relativement élevées. Par exemple, la concentration létale moyenne de 4 jours (CL50) pour le cladocère Ceriodaphnia dubia est de 1 400 mg/L. L'exposition à de telles concentrations est possible dans les petits cours d'eau situés dans les zones urbaines très peuplées, où le réseau routier est dense et la charge en sel de voirie très élevée, dans les étangs et les milieux humides adjacents aux routes, près des entrepôts de sels mal gérés, et à certains lieux d'entreposage de la neige.
On observe une toxicité chronique à de plus faibles concentrations. Les effets toxiques pour le biote aquatique sont associés à l'exposition à des concentrations de chlorure aussi faibles que 870, 990 et 1 070 mg/L pour les effets létaux moyens (embryons de têtes-de-boule, oeufs/embryons de truite arc-en-ciel, daphnies, respectivement). La concentration sans effet observé (CSEO) pour le test sur la survie du premier stade de 33 jours de la tête-de-boule était de 252 mg/L de chlorure. De plus, on estime qu'environ 5 % des espèces aquatiques seraient touchées (concentration létale moyenne) à des concentrations de chlorure d'environ 210 mg/L, alors que 10 % pourraient l'être à environ 240 mg/L. Des concentrations encore plus faibles peuvent provoquer des changements à la structure des populations ou des communautés. Chaque espèce d'algue ayant sa concentration optimale de chlorure pour sa croissance et sa reproduction, on a associé des changements de populations dans les lacs à des concentrations de 12 à 235 mg/L. Les fortes concentrations de chlorure dans les lacs peuvent mener à une stratification qui, en retardant ou empêchant le mélange saisonnier des eaux, peut avoir des répercussions sur la distribution de l'oxygène et des éléments nutritifs. On a observé des concentrations de chlorure entre 100 et 1 000 mg/L ou plus dans divers cours d'eau et lacs urbains. Par exemple, les concentrations maximales de chlorure dans des échantillons d'eau prélevés dans quatre ruisseaux de la région de Toronto variaient de 1 390 à 4 310 mg/L. On a signalé des concentrations de chlorure supérieures à environ 230 mg/L, correspondant à celles qui ont des effets chroniques sur les organismes sensibles, dans ces quatre cours d'eau durant une grande partie de l'année. Dans les zones où on utilise beaucoup de sels de voirie, particulièrement dans le sud de l'Ontario et du Québec et dans les Maritimes, les concentrations de chlorure dans les eaux souterraines et les eaux de surface atteignent souvent des niveaux pouvant affecter le biote, comme l'ont démontré des études faites en laboratoire et sur le terrain.
L'épandage de sels de voirie sur les routes peut également avoir des effets nocifs sur les propriétés physiques et chimiques des sols, particulièrement dans les zones de piètre gestion des sels, sols et végétation. Les effets sont associés aux zones adjacentes aux entrepôts de sels et aux routes, principalement dans les zones de dépression mal drainées. Ces effets sur les sols incluent les impacts sur la structure, la dispersion, la perméabilité, le gonflement et l'encroûtement, la conductivité électrique et le potentiel osmotique du sol, qui peuvent, à leur tour, avoir des impacts abiotiques et biotiques sur l'environnement local. Le principal impact abiotique est la perte de stabilité du sol durant les cycles d'humidification et de séchage, et durant les périodes de fort ruissellement de surface et de vents violents. Les impacts biologiques sont principalement liés au stress osmotique imposé à la macro- et microflore et à la macro- et microfaune du sol, ainsi qu'à la mobilisation des macro- et micronutriments causée par le sel et qui affecte la flore et la faune.
De nombreuses études sur le terrain ont documenté les dommages causés à la végétation et les changements dans la structure des communautés végétales dans les zones touchées par le ruissellement de sels de voirie et la dispersion aérienne. Les espèces halophytes, comme les quenouilles et le roseau commun, envahissent facilement les zones touchées par les sels, modifiant ainsi la présence et la diversité des espèces sensibles au sel. Les teneurs élevées du sol en sodium et en chlorure ou l'exposition aérienne à ces ions entraînent une réduction du nombre de fleurs et de fruits chez les espèces végétales sensibles; des lésions au feuillage, aux pousses et aux racines; une réduction de la croissance; et une réduction de l'établissement des jeunes plants. Les plantes terrestres sensibles peuvent être affectées par des concentrations dans le sol supérieures à 68 mg/L de sodium et à 215 mg/L de chlorure. Les zones ayant ce genre de concentrations longent les routes et les autoroutes et les autres endroits où des sels de voirie sont épandus pour le déglaçage ou la réduction de la poussière. L'impact de la dispersion aérienne se fait sentir jusqu'à 200 m de la bordure des autoroutes à voies multiples et jusqu'à 35 m des routes à deux voies où du sel de déglaçage est utilisé. Le sel nuit aussi à la végétation le long des cours d'eau qui drainent les routes et les installations de manipulation des sels de voirie.
Chez la faune mammifère et aviaire, l'exposition aux sels de voirie provoque des effets sur le comportement ainsi que des effets toxicologiques. L'ingestion de sels de voirie augmente la susceptibilité des oiseaux à être frappés par les automobiles. De plus, le calcul de l'apport en sels de voirie suppose que ces derniers peuvent empoisonner directement certains oiseaux, particulièrement lorsqu'il n'y a pas d'eau libre durant les hivers rigoureux. Les sels de voirie peuvent aussi toucher la faune par leurs effets sur l'habitat : la réduction de la couverture végétale ou les déplacements de populations peuvent avoir des répercussions sur la faune qui dépend de ces plantes pour son alimentation ou son abri. Les données disponibles supposent qu'on aurait sous-estimé la sévérité des mortalités sur la route d'espèces d'oiseaux migrateurs protégées par le fédéral (p. ex. les pinsons de la sous-famille des carduélinés) et la contribution des sels de voirie à cette mortalité.
Les ferrocyanures sont très persistants mais peu toxiques. Toutefois, en solution et en présence de lumière, ils peuvent se dissocier pour former des cyanures. À leur tour, les ions de cyanure peuvent se volatiliser et se dissiper assez rapidement. Les effets ultimes des ferrocyanures dépendent donc de l'équilibre complexe de la photolyse et de la volatilisation qui, elles, dépendent des facteurs environnementaux. Des modèles venant appuyer cette évaluation révèlent qu'il est possible que certains organismes aquatiques subissent des effets du cyanure dans les régions où l'on utilise de grandes quantités de sels de voirie.
À la lumière des données disponibles, on conclut que les sels de voirie qui contiennent des sels inorganiques de chlorure avec ou sans sels de ferrocyanure pénètrent dans l'environnement en une quantité ou en une concentration ou dans des conditions de nature à avoir, immédiatement ou à long terme, un effet nocif sur l'environnement ou sur la diversité biologique, ou de nature à mettre en danger l'environnement essentiel pour la vie. En conséquence, on conclut que les sels de voirie qui contiennent des sels inorganiques de chlorure avec ou sans sels de ferrocyanure sont considérés comme « toxiques » au sens de l'article 64 de la Loi canadienne sur la protection de l'environnement (1999) (LCPE 1999).
Le recours aux fondants est une composante importante des stratégies visant à maintenir les routes ouvertes et sûres durant l'hiver et à réduire les accidents routiers, les blessures et la mortalité associés aux périodes de neige et de verglas. La Commission consultative d'experts auprès des ministres sur la deuxième liste de substances d'intérêt prioritaire (LSIP) reconnut ces avantages dans sa recommandation d'évaluer leurs effets potentiels sur l'environnement. Toute mesure élaborée à la suite de la présente évaluation ne devra pas compromettre la sécurité routière; le choix d'options devra être fondé sur l'optimisation des pratiques d'entretien des routes en hiver afin de ne pas compromettre la sécurité routière tout en minimisant les effets nocifs possibles sur l'environnement. Toute mesure prise pour diminuer les effets sur l'environnement réduira probablement aussi la contamination des sources souterraines d'eau potable, ce qui est assurément désirable.
Les activités futures de gestion devraient se concentrer sur les principales préoccupations que l'évaluation a mises en lumière, c'est-à-dire les entrepôts de sels, l'épandage sur les routes, les lieux d'entreposage de la neige et les ferrocyanures.
- Entrepôts de sels : Les principales préoccupations touchent à la contamination des eaux souterraines dans les entrepôts de sels et aux rejets dans les eaux de surface. En outre, le ruissellement des eaux salées de la fonte des neiges peut avoir des effets directs sur les eaux de surface et sur la végétation adjacente aux entrepôts. À la lumière des sondages et des recensions, les pertes de sels des entrepôts de sels se produisent à partir des amas (ce qui inclut les amas de sels ainsi que les amas de sable et de gravier auxquels on a ajouté des sels) et pendant la manutention du sel, tant lors de son entreposage que pour le chargement et le déchargement des camions. Le rejet des eaux de lavage des véhicules constitue lui aussi une source potentielle de pertes de sels. On devrait donc considérer prendre des mesures et des pratiques pour s'assurer que les sels et les abrasifs sont entreposés de manière à réduire les pertes en les protégeant des intempéries, pour réduire les pertes pendant les déplacements et pour améliorer la gestion des eaux de ruissellement et de lavage afin de réduire les rejets.
- Épandage sur les routes : Les principales préoccupations écologiques sont liées aux régions à forte densité routière où le recours aux sels de voirie est élevé. Les régions du sud de l'Ontario et du Québec et les provinces de l'Atlantique ont les plus hauts taux d'épandage par superficie et ont donc le plus fort potentiel de contamination des sols et des eaux de surface et souterraines par les sels de voirie due à l'épandage sur les routes. En outre, des régions urbaines d'autres parties du Canada où de grandes quantités de sels sont épandues peuvent causer des problèmes, en particulier pour les ruisseaux et les aquifères complètement entourés par la région urbaine. Dans les régions rurales, les eaux de surface réceptrices du ruissellement des routes sont aussi susceptibles de contamination. Les zones où des éclaboussures ou des gouttelettes d'eau salées provenant des routes peuvent être transportées dans l'atmosphère vers la végétation sensible doit retenir l'attention. Les terres humides directement adjacentes aux fossés des routes et qui reçoivent le ruissellement sous forme d'eaux salées de la fonte des neiges doivent aussi retenir l'attention pour la gestion. En conséquence, on devrait considérer prendre des mesures en vue de réduire l'utilisation globale des sels de voirie dans ces régions. On devrait penser à choisir des produits de remplacement ou des techniques appropriées permettant de réduire l'utilisation des sels tout en assurant le maintien de la sécurité des routes.
- Lieux d'entreposage de la neige : Les principales préoccupations écologiques touchent l'écoulement des eaux de la fonte des neiges dans les eaux de surface, dans le sol et les eaux souterraines dans les lieux d'entreposage de la neige. Des mesures devraient être considérées pour minimiser la percolation dans le sol et les eaux souterraines, et pourraient diriger les rejets des eaux salées de la fonte des neiges vers des eaux de surface dont la sensibilité environnementale est faible ou vers les systèmes d'évacuation des eaux pluviales. Des mesures devraient aussi être considérées pour que les eaux soient suffisamment diluées avant d'être rejetées.
- Ferrocyanures : La présente évaluation indique que l'exposition aux ferrocyanures peut avoir des effets nocifs sur les vertébrés aquatiques les plus sensibles dans les régions à forte utilisation de sels de voirie. On pourrait diminuer les risques en réduisant la quantité de sels utilisée ou en réduisant la teneur en ferrocyanures des formules de sels de voirie. Les fabricants de sels de voirie devraient songer à réduire la teneur en ferrocyanures des sels de voirie afin de minimiser les possibilités d'exposition. Toute réduction de l'utilisation globale des sels de voirie entraînerait une réduction équivalente des rejets de ferrocyanures.
1.0 Introduction
La Loi canadienne sur la protection de l'environnement (1999) (LCPE 1999) exige des ministres fédéraux de l'Environnement et de la Santé qu'ils préparent et publient une liste des substances d'intérêt prioritaire (LSIP) identifiant les substances chimiques, les groupes de substances chimiques, les effluents et les déchets qui peuvent être nocifs pour l'environnement ou constituer un danger pour la santé humaine. La Loi exige également des deux ministres qu'ils évaluent ces substances et qu'ils déterminent si elles sont effectivement ou potentiellement « toxiques » au sens de l'article 64 de la Loi :
[...] est toxique toute substance qui pénètre ou peut pénétrer dans l'environnement en une quantité ou concentration ou dans des conditions de nature à :
- avoir, immédiatement ou à long terme, un effet nocif sur l'environnement ou sur la diversité biologique;
- mettre en danger l'environnement essentiel pour la vie;
- constituer un danger au Canada pour la vie ou la santé humaines.
Les substances dont l'évaluation révèle la toxicité au sens de l'article 64 peuvent être inscrites sur la Liste des substances toxiques, à l'annexe I de la Loi, et l'on peut envisager, à leur égard, d'éventuelles mesures de gestion du risque, par exemple un règlement, des lignes directrices, des plans de prévention de la pollution ou des codes de pratiques, pour en régir le cycle de vie (de la recherche-développement à l'élimination finale en passant par la fabrication, l'utilisation, l'entreposage et le transport).
S'appuyant sur l'analyse initiale de l'information facilement accessible, la Commission consultative d'experts auprès des ministres sur la deuxième Liste des substances d'intérêt prioritaire (Commission consultative, 1995) a invoqué les motifs suivants pour justifier l'évaluation des sels de voirie :
La Commission reconnaît les avantages associés à l'utilisation des sels de voirie. Ceux-ci sont toutefois nocifs pour l'environnement et leur épandage sur les routes provoque la libération de grandes quantités, notamment en Ontario, au Québec et dans les Maritimes. Des données indiquent que les sels de voirie ont, localement, des effets nocifs sur les eaux souterraines, la flore et la faune après exposition. On a observé que les algues et la faune benthique sont particulièrement sensibles aux fluctuations des concentrations de l'ion chlorure et qu'il en résulte une diminution des populations de poissons. La Commission est consciente des progrès sensibles qui ont été réalisés en vue d'améliorer les installations d'entreposage de ces sels. Toutefois, vu l'exposition générale à ces substances et leur rejet massif dans l'environnement canadien, elle croit qu'une évaluation est requise pour déterminer leurs effets écologiques.
Les motifs invoqués par la Commission consultative d'experts auprès des ministres sur la deuxième Liste des substances d'intérêt prioritaire pour inclure les sels de voirie se limitent aux effets sur l'environnement, et aucune préoccupation liée à la santé humaine n'a été soulevée. L'exposition des humains aux sels de voirie résulte principalement de la contamination de l'eau de puits situés en bordure des routes, dont la concentration de chlorure et en sodium peut augmenter au point d'altérer le goût de l'eau. On ne considère cependant pas ces ions comme toxiques aux humains. En fait, les directives canadiennes sur la qualité de l'eau potable, qui s'appliquent au chlorure et au sodium, sont basées sur l'altération du goût; or ce phénomène se produit à des concentrations bien inférieures à celles qui pourraient être toxiques (Santé Canada, 1996). D'autres substances composant les sels de voirie, incluant les composés de ferrocyanure et certains métaux, ne sont présents qu'à l'état de traces.
En ce qui a trait aux effets possibles sur la santé des sels de voirie à base de chlorure de sodium, une vaste recherche documentaire n'a révélé aucune étude qui pourrait servir de fondement à une évaluation des risques pour la santé. Dans une étude, l'exposition cutanée à des solutions concentrées de sels de voirie a causé une irritation cutanée, mais aucune sensibilisation (Cushman et al., 1991). Une seule étude corrélationnelle établit un lien statistique entre l'utilisation des sels de voirie et la mortalité due à un certain nombre de cancers aux États-Unis (Foster, 1993). Il convient toutefois de noter que, dans cette étude, l'utilisation des sels de voirie a varié en fonction d'un certain nombre d'autres facteurs, les quantités utilisées étant notamment plus élevées dans les centres urbains, là où l'exposition à la pollution atmosphérique est également plus forte. Il aurait également fallu tenir compte des différences entre les États quant au tabagisme, au régime alimentaire et à une gamme d'autres facteurs. Cependant, la structure de cette étude préliminaire ne permet pas de corriger les données en fonction de ces autres facteurs, dont bon nombre sont des causes plus plausibles de cancer que les sels de voirie.
Comme la Commission consultative d'experts auprès des ministres a déterminé que l'évaluation devait porter sur les effets environnementaux, et étant donné le peu de données pertinentes pour évaluer les effets possibles des sels de voirie sur la santé humaine, la présente évaluation porte uniquement sur les effets de ces substances sur l'environnement et ne vise donc qu'à établir leur caractère « toxique », ou non, au sens des alinéas 64a) et 64b) de la LCPE 1999.
Les méthodes utilisées pour évaluer les effets des substances d'intérêt prioritaire sur l'environnement sont décrites dans un document connexe, intitulé « Évaluation environnementale des substances d'intérêt prioritaire conformément à la Loi canadienne sur la protection de l'environnement, Guide, version 1.0, mars 1997 » (Environnement Canada, 1997a). Ce document vise à servir de guide à l'évaluation environnementale des substances d'intérêt prioritaire au Canada; on peut l'acheter en le commandant des :
- Publications sur la protection de l'environnement
Direction générale de l'avancement des technologies environnementales
Environnement Canada
Ottawa (Ontario)
K1A 0H3
On peut également l'obtenir à partir du site Web de la Direction des substances existantes, à l'adresse www.ec.gc.ca/cceb1/fre/psap.htm, sous la rubrique « Guide technique ». Il est à noter que la démarche décrite ici a été modifiée pour tenir compte des changements apportés à la Loi canadienne sur la protection de l'environnement et des récents progrès réalisés dans les méthodes d'évaluation du risque, et ceux-ci seront mentionnés dans les futures versions du guide d'évaluation des effets des substances d'intérêt prioritaire sur l'environnement.
Les stratégies de recherche employées pour trouver les données utiles à l'évaluation des effets potentiels sur l'environnement (avant mai 2001) sont présentées à l'annexe A. Des articles de synthèse ont aussi été consultés, au besoin. Cependant, toutes les études originales ayant servi de fondement à la détermination du caractère « toxique » des sels de voirie au sens de la LCPE 1999 ont été soumises à une évaluation critique.
Les sections du présent rapport qui ont trait à l'évaluation des incidences environnementales ont été préparées par B. Elliott, sous la direction de R. Chénier. Une vaste documentation complémentaire (annexe B) sur l'évaluation environnementale des sels de voirie a été préparée et révisée par le Groupe-ressource environnemental, qui a été mis sur pied en juin 1997 par Environnement Canada pour appuyer l'évaluation environnementale, et qui est composé des membres suivants :
- P. Arp, Université du Nouveau-Brunswick
- M. Barre, Environnement Canada (jusqu'à décembre 1999)
- Y. Bourassa, Environnement Canada (depuis décembre 1999)
- L. Brownlee, Environnement Canada (jusqu'à avril 2000)
- B. Butler, Université de Waterloo
- N. Cain, Cain Vegetation Inc.
- R. Chénier, Environnement Canada
- C. Delisle, École Polytechnique de Montréal
- M. Eggleton, Environnement Canada (jusqu'à février 2000)
- B. Elliott, Environnement Canada
- M. Evans, Environnement Canada
- K. Hansen, Ministère de l'Environnement et de l'Énergie de l'Ontario
- J. Haskill, Environment Canada
- K. Howard, Université de Toronto (jusqu'à janvier 2000)
- A. Letts, Morton International Inc.
- B. Mander, Environnement Canada
- T. Mayer, Environnement Canada
- P. Mineau, Environnement Canada (depuis avril 2000)
- D. Morin, Environnement Canada
- M. Perchanok, Ministère des Transports de l'Ontario
- R. Smith, Association des transports du Canada
- W. Snodgrass, Snodgrass Consultants
- K. Taylor, Environnement Canada
- M. Weese, Ministère des Transports de l'Ontario (jusqu'en janvier 1999)
Le Groupe-ressource environnemental a également passé en revue le Rapport d'évaluation préparé par Environnement Canada. Les conclusions et les interprétations formulées dans ce rapport sont celles d'Environnement Canada et ne sont pas nécessairement partagées par tous les membres du Groupe-ressource environnemental.
La documentation complémentaire sur l'évaluation environnementale a aussi été révisée par les personnes suivantes :
- K. Adare, Environnement Canada
- J. Addison, Royal Roads University
- J. Van Barneveld, Ministère de l'Environnement, des Terres et des Parcs de la Colombie-Britannique
- Y. Bédard, Ministère des Transports du Québec
- D. Belluck, Minnesota Department of Transport
- Y. Blouin, Ville de Cap-de-la-Madeleine
- R. Brecher, Global Tox
- C. Chong, Université de Guelph
- A. Decréon, Ministère des Transports du Québec
- R. Delisle, Ministère des Transports du Québec
- G. Duval, Ministère des Transports du Québec
- A. El-Shaarawi, Environment Canada
- A. Fraser, Environnement Canada
- M. Frénette, Ville de Montréal
- D. Gutzman, Environnement Canada
- G. Haines, Ministère des Transports du Nouveau-Brunswick
- R. Hodgins, Ecoplans Limited
- M. Kent, Ministère des Transports et de la Voirie de la Colombie-Britannique
- C. MacQuarrie, Ministère des Transports du Nouveau-Brunswick
- B. Mason, Ville de Toronto
- L. McCarty, L.S. McCarty Consulting
- G. McRae, Ministère des Transports de l'Ontario
- T. Pollock, Environnement Canada
- M. Roberts, Université du Nouveau-Brunswick
- D. Rushton, Ministère des Transports et des Travaux publics de la Nouvelle-Écosse
- K. Solomon, Université de Guelph
- R. Stemberger, Dartmouth College, New Hampshire, États-Unis
- T. Young, Clarkson University, New York, États-Unis
Enfin, le Rapport d'évaluation a été révisé et approuvé par le Comité mixte de gestion de la LCPE formé de représentants d'Environnement Canada et de Santé Canada.
En août 2000, le rapport d'évaluation sur les sels de voirie a été mis à la disposition de tous ceux interessés à faire des commentaires pour une période de 60 jours. Après avoir reçu les commentaires, le rapport d'évaluation a été révisé. Un sommaire des commentaires du public et des réponses qui leurs furent adressées par Environnement Canada et Santé Canada peut être obtenu de la Direction des substances existantes ou au site internet suivant :
On peut obtenir un exemplaire du présent Rapport d'évaluation, sur demande, à :
- L'Informathèque Environnement Canada
Rez-de-chaussée, Place Vincent-Massey
351, boul. St-Joseph
Hull(Québec)
K1A 0H3
ou sur Internet, à l'adresse suivante :
Pour obtenir la documentation complémentaire inédite qui renferme des renseignements supplémentaires, s'adresser à la :
- Direction des substances existantes
Environnement Canada
14e étage, Place Vincent-Massey
351, boul. St-Joseph
Hull (Québec)
K1A 0H3
2.0 Résumé de l'information essentielle à l'évaluation du caractère « toxique » au sens de la LCPE 1999
2.1 Identité, propriétés, production et sources
2.1.1 Caractérisation
Les sels de voirie font référence à tout sel épandu sur les routes pour en assurer l'entretien. Comme on l'explique dans les sections qui suivent, les sels de voirie au Canada sont utilisés principalement comme agents de déglaçage et d'anti-givrage des routes durant l'hiver mais sont également utilisés - en plus faibles quantités -comme abat-poussière. « Sel » fait référence à tout composé formé du cation d'une base et de l'anion d'un acide, qui se dissocie facilement dans l'eau. Bien que le chlorure de sodium (NaCl) soit de loin le sel de voirie le plus utilisé au Canada, d'autres sels inorganiques - dont le chlorure de calcium (CaCl2), le chlorure de magnésium (MgCl2) et le chlorure de potassium (KCl) - le sont également. Au Canada, peu d'additifs sont ajoutés aux préparations de sels de voirie, le ferrocyanure de sodium (Na4Fe(CN)6·10H2O) étant le seul anti-agglomérant couramment utilisé. Des sels organiques et quelques autres produits sont également utilisés au Canada, mais ceux-ci servent essentiellement à l'entretien des aéroports et au dégivrage des avions ainsi qu'à des essais limités sur route. Enfin, on fait aussi usage d'abrasifs, comme le sable, pour l'entretien des routes en hiver et, bien que ces produits ne soient pas des sels, on y ajoute souvent des chlorures; ces abrasifs mélangés à des sels peuvent donc constituer une source de chlorure dans l'environnement.
Il a été décidé d'axer la présente évaluation sur les sels inorganiques de chlorure utilisés pour l'entretien des routes, car :
- dans ses recommandations initiales, la Commission consultative d'experts auprès des ministres a demandé qu'une évaluation environnementale soit faite des chlorures de déglaçage les plus couramment utilisés;
- le chlorure de sodium et, dans une moindre mesure, le chlorure de calcium sont de loin les sels les plus épandus sur les routes au Canada, et
- tous les sels inorganiques de chlorure ont à peu près le même comportement et les mêmes effets dans l'environnement. En fait, on peut considérer que les effets toxiques du chlorure dépendent de l'apport cumulatif de tous les sels qui en contiennent.
Des préoccupations publiques ont aussi été exprimées au sujet des ferrocyanures présents dans les sels de voirie, surtout parce que ces substances peuvent se dissocier par photolyse en solution et produire ainsi des ions cyanure libres, qui, eux, sont fortement toxiques pour les organismes aquatiques. De ce fait, et parce que les ferrocyanures sont couramment utilisés dans les préparations de sels de voirie, l'évaluation des sels de voirie portera également sur la pénétration des ferrocyanures dans l'environnement, sur l'exposition à ces substances et sur les effets qui en résultent.
Les sels organiques ne sont utilisés au Canada que dans des circonstances précises, entre autres dans les aéroports (plutôt que sur les routes), et ils ne sont pas évalués dans le présent rapport. De même, bien que les abrasifs soient utilisés en grande quantité au Canada, ces substances diffèrent des sels de voirie par leur nature et leurs effets potentiels sur l'environnement, et sont également exclus du présent rapport.
Enfin, même si l'on possède des données limitées sur l'usage de sels dans les aires de stationnement et sur les propriétés industrielles, commerciales et autres propriétés privées, la présente évaluation s'appuie essentiellement sur les utilisations et les rejets provenant de l'entrepôt de sels, de l'épandage sur les voies publiques et de l'enlèvement de la neige.
2.1.2 Propriétés physiques et chimiques
Le tableau 1 présente le numéro de registre du Chemical Abstracts Service (CAS) et les propriétés physico-chimiques de quatre sels inorganiques (soit le chlorure de sodium, le chlorure de calcium, le chlorure de magnésium et le chlorure de potassium) et des ferrocyanures utilisés comme sels de voirie.
Tableau 1 Propriétés physico-chimiques des sels de voirie
La température eutectique fait référence à la température de congélation minimale de l'eau à laquelle un sel a été ajouté. Plus la différence entre la température ambiante et la température eutectique est grande, plus le taux de fonte est grand (Groupe d'experts scientifiques de l'OCDE, 1989). Donc, de tous les sels présentés au tableau 1, le chlorure de calcium est celui qui aurait le taux de fonte le plus élevé. Les vitesses de réaction du chlorure de sodium et du chlorure de calcium sont comparables, à des températures entre -1 et 4 °C; cependant, à partir de -5 °C (en descendant), le chlorure de sodium agit plus lentement que le chlorure de calcium, à quantités épandues égales (Groupe d'experts scientifiques de l'OCDE, 1989).
On définit la salinité comme la teneur totale en matières dissoutes dans l'eau, lorsque tous les carbonates ont été convertis en oxydes, que tous les bromures et iodures ont été remplacés par des chlorures et que toute la matière organique a été oxydée (Stumm et Morgan, 1981). Comme les sels de voirie évalués ici sont des chlorures, le chlorure (Cl-) est l'anion qui contribue le plus à la salinité causée par l'épandage des sels de voirie. Cependant, d'autres anions présents dans l'environnement influent aussi sur la salinité; c'est le cas notamment du bicarbonate (HCO3-), du carbonate (CO32-) et du sulfate (SO42-). Parmi les cations qui contribuent sensiblement à la salinité, mentionnons le calcium (Ca2+), le magnésium (Mg2+), le sodium (Na+) et le potassium (K+). La salinité est par ailleurs étroitement liée à la concentration totale en halogénures, elle-même souvent désignée chlorinité. On décrit la relation entre les deux à l'aide de l'équation de Knudson déterminée empiriquement (Mayer et al., 1999).
Le ferrocyanure est un anion très complexe et peu soluble, composé d'un atome central de fer, entouré d'une configuration octaèdre de ligands cyanure (Letts, 2000a).
2.1.3 Production et utilisation
Au Canada, les sels de voirie (surtout le chlorure de sodium) sont utilisés comme agents de désintégration et de fonte de la glace depuis les années 1940 (Perchanok et al., 1991).
2.1.3.1 Chlorure de sodium
Le chlorure de sodium, qui est formé (en % de la masse) d'environ 40 % de sodium et 60 % de chlore, est le principal sel utilisé comme fondant en Amérique du Nord. Des éléments en traces, y compris des métaux en traces, peuvent constituer jusqu'à 5 % du poids total du sel. Les substances qui peuvent être présentes sont le phosphore (14-26 mg/L), le soufre (6,78-4 200 mg/L), l'azote (6,78-4 200 mg/L), le cuivre (0,14 mg/L) et le zinc (0,02-0,68 mg/L) (MDOT, 1993).
En 1995, la production mondiale de chlorure de sodium a totalisé 189 000 kilotonnes, les plus gros producteurs étant les États-Unis (21 %), la Chine (15 %), l'Allemagne (8 %) et le Canada (7 %) (Ressources naturelles Canada, 1998). L'industrie chimique constitue le principal marché mondial pour le chlorure de sodium (60 %); viennent ensuite la production de sel de table (20 %) et le déglaçage des routes (10 %) (CIS, 1994).
En 1993, le Canada comptait 12 fabricants de chlorure de sodium exploitant 24 usines réparties dans sept provinces, d'une capacité nominale totale de 13 645 kilotonnes par année; la production intérieure a atteint 10 895 kilotonnes et 1 010 kilotonnes ont été importées des États-Unis et du Mexique, pour un approvisionnement total de 11 905 kilotonnes. De cet approvisionnement total, le Canada a exporté 3 106 kilotonnes, surtout aux États-Unis, et la demande intérieure canadienne s'est chiffrée à 8 799 kilotonnes (CIS, 1994). Au Canada, le chlorure de sodium est utilisé principalement comme fondant, pour lutter contre la neige et le verglas, ce marché représentant environ la moitié de la demande intérieure (4 240 kilotonnes, en 1993). Les quantités totales utilisées pour le déglaçage varient d'une année à l'autre selon les conditions météorologiques (CIS, 1994).
2.1.3.2 Chlorure de calcium
Le chlorure de calcium (en % de la masse, 36 % calcium et 64 % chlore) est le deuxième sel de voirie le plus utilisé en Amérique du Nord et il est également le principal abat-poussière chimique en usage au Canada. Le chlorure de calcium liquide est surtout appliqué sur les routes de gravier pour consolider les agrégats et réduire la poussière. Il est également utilisé comme agent de pré-mouillage du sel et du sable pour l'entretien des routes en hiver et sert à stabiliser les mélanges de base après leur pulvérisation sur les routes. De ces trois utilisations, le contrôle de la poussière représente environ 97 % de l'utilisation totale (Morin et Perchanok, 2000). Les quantités de chlorure de calcium utilisées pour l'entretien des routes en hiver pourraient toutefois augmenter, car divers organismes commencent à faire l'essai des techniques de pré-mouillage.
En 1995, il y avait trois fabricants de chlorure de calcium au Canada, exploitant une usine en Ontario et quatre puits d'extraction de saumures en Alberta. Cette année-là, la capacité nominale totale pour le chlorure de calcium a atteint 629 kilotonnes au Canada; la production totale s'est chiffrée à 399 kilotonnes et 25 kilotonnes ont été importées, pour un approvisionnement total de 424 kilotonnes. De cet approvisionnement, 156 kilotonnes ont été exportées et la demande intérieure canadienne a été de 268 kilotonnes. Au total, 201 kilotonnes ont été utilisées comme abat-poussière et pour la construction de routes, en 1995 (CIS, 1996).
2.1.3.3 Mélange de chlorure de sodium et de chlorure de calcium
Le chlorure de sodium pré-mouillé par une saumure de chlorure de calcium est recommandé pour réduire l'épandage total de sel (Gooding et Bodnarchuk, 1994). La quantité totale utilisée sur les routes au Canada est incluse dans les estimations mentionnées plus haut pour le chlorure de sodium et le chlorure de calcium.
2.1.3.4 Chlorure de magnésium
Bien qu'on ne le recommande pas pour réduire la poussière sur les routes, le chlorure de magnésium (en % de la masse, 26 % magnésium et 74 % chlore) est un abat-poussière de remplacement utilisé sur les piles de matériel, l'accotement des routes ou les bassins servant au transfert de matériel (MEEO, 1993). À partir des données fournies par l'industrie, Morin et Perchanok (2000) ont estimé qu'entre 25 000 et 35 000 tonnes de chlorure de magnésium sont utilisées chaque année au Canada pour le déglaçage des routes. On n'a trouvé aucun renseignement sur le volume de production du chlorure de magnésium au Canada, mais il est sans doute très faible.
2.1.3.5 Mélange de chlorure de sodium et de chlorure de magnésium
Bien que des fondants à base de chlorure de sodium puissent contenir du chlorure de magnésium et certains additifs anticorrosifs (MDOT, 1993), aucune donnée n'indique que ces mélanges sont actuellement utilisés au Canada.
2.1.3.6 Chlorure de potassium
Le chlorure de potassium (en % de la masse, 52% potassium et 48% chlore) est peu utilisé comme fondant, mais des résidus miniers de potasse contenant entre 0,5 et 2 % de chlorure de potassium (le reste étant surtout du chlorure de sodium) sont épandus sur certaines routes du Canada comme agents de déglaçage (ICE, 1997). La quantité totale de chlorure de potassiumépandue chaque année sur les routes du Canada a été estimée à 2 000 tonnes, par Morin et Perchnok (2000), et à 3 300 tonnes par l'Institut canadien des engrais (1997). Il a par ailleurs été estimé que la production totale de chlorure de potassium a atteint 13,6 millions de tonnes en 1999, la capacité de production de l'industrie de la potasse étant alors exploitée à 61 % (Prud'homme, 2000). La majeure partie de la potasse produite a été destinée à des usages agricoles.
2.1.3.7 Saumures
La saumure extraite des champs pétrolifères est un abat-poussière classique, qui se compose de calcium, de magnésium, de sodium et de chlorure. On obtient cette saumure de l'eau de gisement produite durant l'exploration pétrolière, à plusieurs endroits du sud-ouest de l'Ontario (MEEO, 1993).
2.1.3.8 Ferrocyanure
Pour éviter l'agglutination des chlorures durant l'entreposage et les opérations de déglaçage, on peut y ajouter des ferrocyanures sodique et ferrique. Au Canada, de 30 à 124 mg/kg de ferrocyanure de sodium sont ajoutés au chlorure de sodium (Letts, 2000a).
Le Canada ne produit pas de ferrocyanure de sodium. Il en importe toutefois quelque 300 à 350 tonnes chaque année de fabricants européens et asiatiques, pour servir d'anti-agglomérant. Des sels de voirie contenant du ferrocyanure de sodium sont utilisés en Ontario, au Québec et dans les provinces de l'Atlantique. À partir du Manitoba jusqu'à l'intérieur de la Colombie-Britannique, le sel résiduaire provenant des mines de potasse de la Saskatchewan est utilisé comme fondant, sans être traité au ferrocyanure de sodium. Enfin, sur la côte ouest, le sel gemme importé du Chili est traité au ferrocyanure de sodium, à raison de 60 mg/kg. On peut estimer la quantité de ferrocyanures dans les diverses provinces à partir de la quantité de sel utilisée et de sa teneur moyenne en ferrocyanures.
2.1.4 Sources et rejets
2.1.4.1 Sources naturelles
Les sources naturelles de chlorure de sodium, de chlorure de calcium, de chlorure de magnésium et de chlorure de potassium dans l'environnement incluent la dégradation et l'érosion des roches et des sols, les précipitations atmosphériques, les infiltrations d'eaux souterraines et les évaporites ou saumures provenant de ces dépôts. La composition des roches, la topographie et le climat sont d'importants facteurs qui contrôlent en grande partie les taux d'altération et de dissolution. Dans les écosystèmes aquatiques, les cations comme le calcium, le magnésium et le potassium sont non seulement associés aux chlorures, mais peuvent aussi provenir de sources naturelles, comme les carbonates présents dans le sol et l'assise rocheuse du bassin versant (Mayer et al., 1999). Les roches ignées et les sols qui y sont associés ont en général une teneur en sels plus faible que le schiste et le calcaire (Pringle et al., 1981). La contribution des sources atmosphériques à la salinité est particulièrement importante dans les régions maritimes côtières. Dans les régions sèches à faibles précipitations, comme les Prairies canadiennes, les sels ont tendance à se concentrer à la surface du sol sous l'effet du taux élevé d'évapotranspiration nette. Evans et Frick (2001) passent en revue les diverses sources naturelles de sels dans les écosystèmes aquatiques.
La végétation emmagasine le sodium et le chlore, mais elle les perd aussi facilement sous l'effet de l'absorption d'ions, du lavage des feuilles et de la décomposition de la litière. Le chlorure est un important soluté inorganique de régulation osmotique. Les réactions chimiques ou biologiques n'influent pas sur la concentration de chlorure dans l'environnement et le chlorure ne se fixe pas aux particules. Le potassium a tendance à être l'ion en quantité la plus constante dans les cellules animales. Le calcium est l'ion le plus réactif de tous les principaux cations qui contribuent à la salinité; il est en outre un élément nutritif essentiel aux plantes supérieures et un des éléments inorganiques de base dans les algues.
Le magnésium joue un rôle important dans les transformations enzymatiques et il est essentiel aux plantes chlorophylliennes.
Enfin, bien que les ferrocyanures ne se trouvent pas à l'état naturel dans l'environnement, les composés de cyanure sont des substances présentes à l'état naturel dans plus de 2 000 espèces de végétaux (Conn, 1980). Le ferrocyanure de sodium et le ferrocyanure ferrique sont très stables et relativement immobiles dans l'environnement. Exposé au soleil, le complexe ferrocyanure se décompose et libère des ions cyanure (CN-) (Meeussen et al., 1992a). Dans des conditions naturelles, l'ion cyanure est hydrolysé en une molécule d'acide cyanhydrique (HCN) volatil (Shifrin et al., 1996).
2.1.4.2 Sources anthropiques
Parmi les sources anthropiques de chlorures inorganiques, mentionnons les eaux usées domestiques et les procédés industriels (Sonzogni et al., 1983), comme les effluents des industries chimique et pétrochimique (Johnson et Kauss, 1991), la production du gaz et les eaux d'exhaure acide (U.S. EPA, 1973; Pringle et al., 1981). Lorsque ces substances pénètrent dans l'environnement, elles restent en phase aqueuse jusqu'à ce que leur concentration dépasse leur produit de solubilité, auquel moment il peut y avoir cristallisation et sédimentation des sels minéraux.
Il peut y avoir rejet de sels dans l'environnement durant la production, l'extraction, le mélange, ainsi que le transport et l'entreposage en vrac de ces substances. Cependant, comme ces sources industrielles ne sont pas toutes destinées à l'épandage sur les routes, elles ne sont pas examinées plus à fond dans la présente évaluation.
Tous les sels de voirie finissent par pénétrer dans l'environnement à la suite de :
- l'entreposage dans les entrepôts de sels (y compris les pertes se produisant à partir des amas d'entreposage et durant la manutention)
- l'épandage sur les routes (au moment de l'épandage et du mouvement ultérieur des sels hors des routes), et
- l'élimination de la neige usée.
Les rejets sont donc associés à la fois à des sources ponctuelles (entreposage et élimination de la neige) et linéaires (épandage sur les routes). Les sections qui suivent passent en revue la documentation utile sur la pénétration des sels dans l'environnement, et plus particulièrement les charges (quantités épandues sur les routes), l'élimination de la neige usée et les entrepôts de sels.
2.2 Charges de sels de voirie
La présente section résume les résultats d'un rapport préparé par Morin et Perchanok (2000) qui caractérise l'utilisation des sels de voirie au Canada. On y présente des données sur les taux d'épandage et les charges massiques annuelles en fonction de la longueur du réseau routier et de la région géographique. Ces données géographiques détaillées ont servi à calculer l'exposition et à étayer des sections subséquentes de la présente évaluation. Les données de la présente section portent sur l'utilisation des sels à base de chlorure de sodium et de chlorure de calcium; les sels de chlorure de magnésium et de chlorure de potassium sont aussi utilisés, mais en moindre quantité. Les représentants de l'industrie estiment qu'environ 25 000 à 35 000 tonnes de chlorure de magnésium et 2 000 tonnes de chlorure de potassium sont utilisées chaque année au Canada pour le déglaçage des routes.
2.2.1 Enquêtes
On a obtenu des renseignements sur l'utilisation des sels de voirie au Canada au moyen d'enquêtes réalisées par l'Association des transports du Canada, le ministère des Transports de l'Ontario et Environnement Canada. L'enquête menée par Environnement Canada a permis de recueillir des données auprès des provinces, des municipalités et du secteur privé. Morin et Perchanok (2000) décrivent en détail la méthodologie utilisée pour ces enquêtes.
2.2.1.1 Provinces
Tous les ministères des Transports des provinces et des territoires ont fourni des données sur les charges de sels et sur la longueur du réseau routier. C'est pour l'hiver 1997-1998 que les données à l'échelle du pays sont les plus complètes et ce sont elles qui ont servi à estimer l'utilisation totale de sels. Une comparaison entre les données fournies par les fournisseurs de sels et celles obtenues des organismes provinciaux laisse croire que les quantités rapportées sont fiables (Morin et Perchanok, 2000).
2.2.1.2 Administrations municipales et régionales
Des données sur l'utilisation des sels de voirie et la longueur du réseau routier ont été obtenues de 104 municipalités du Canada. On a aussi obtenu des données sur l'utilisation de sels de tous les comtés et municipalités régionaux de l'Ontario. Certains répondants ont fourni des données sur l'usage de sels et la longueur du réseau routier pour chacune des cinq dernières années; d'autres n'ont fourni des données que sur l'utilisation de sels durant l'hiver 1997-1998.
2.2.1.3 Données de l'industrie du sel
Les fournisseurs de sels ont présenté des données sur les achats et les soumissions, pour 500 municipalités au Canada. Une comparaison entre les données sur les soumissions et les achats indique une forte concordance entre les deux.
2.2.1.4 Estimations municipales
Les renseignements sur l'utilisation de sels par type de route ne sont disponibles que pour 104 municipalités. Cependant, même en combinant les données des municipalités (104) à celles des fournisseurs de sels (500 municipalités), on n'arrive pas à la quantité totale utilisée par les municipalités. Des estimations ont donc été faites pour tenir compte de l'utilisation de sels par les municipalités n'ayant fourni aucune donnée.
Le nombre d'habitants est la variable qui a été choisie pour prévoir l'utilisation de sels à l'échelle municipale. Pour ce faire, on a calculé une charge annuelle moyenne par personne pour les municipalités ayant répondu à l'enquête ou fourni des données sur les achats et les soumissions, et on a multiplié cette charge par la population de toutes les autres municipalités d'un district d'entretien. On a ensuite fait la somme de l'utilisation connue et de l'utilisation estimée de sels par la municipalité pour estimer la quantité totale de sels utilisée par district d'entretien. À partir de ces estimations, une carte illustrant l'usage de sels par district d'entretien a été établie.
2.2.1.5 Utilisation provinciale et municipale de sels comme abat-poussière
Le principal producteur de chlorure de calcium a fourni des estimations sur l'épandage de chlorure de calcium sur les routes, par province, en précisant les taux d'épandage recommandés par l'industrie. Ces taux varient selon le type de route de gravier, la densité de la circulation et les politiques relatives à l'entretien des routes. Les charges minimale et maximale ont été calculées pour une route de gravier de 7,4 m de largeur.
2.2.2 Résultats
Des résultats détaillés sont présentés dans Morin et Perchanok (2000).
À partir des données recueillies lors de l'enquête, on a créé des cartes illustrant la distribution des routes provinciales. On a aussi calculé et cartographié une fraction de la superficie du réseau routier provincial (la figure 1 illustre la superficie des routes entretenues par les organismes provinciaux et sur lesquelles il peut y avoir épandage de sel, par district d'entretien). Cette carte peut servir à estimer les charges en sels dans les eaux de surface, dans les zones de drainage ayant une superficie et un profil similaires. Les districts affichant la plus forte proportion de routes sur lesquelles il peut y avoir épandage de sel sont situés dans certaines régions des provinces de l'Atlantique, le sud du Québec, le sud de l'Ontario et certaines parties de la Colombie-Britannique.
Figure 1 Segment régional du réseau routier provincial (d'après Morin et Perchanok, 2000)

2.2.2.1 Chlorure de sodium
La figure 2 montre les taux d'épandage provinciaux recommandés et la figure 3 présente ceux de certaines municipalités choisies. On ne peut toutefois pas utiliser les taux d'épandage pour quantifier les charges annuelles : ces taux renseignent sur la quantité de sel utilisée à chaque épandage, mais non sur le nombre d'épandages et sur la masse totale ainsi appliquée. Les charges font référence à la masse annuelle totale moyenne, et non aux taux d'épandage.
Les données détaillées ont été analysées séparément par administrations provinciales, municipales et régionales, incluant le calcul de la masse de sels en fonction de la longueur et de la superficie des routes à deux voies sur lesquelles il peut y avoir épandage de sels et de la superficie du district d'entretien (Morin et Perchanok, 2000). Les régions ayant les plus fortes charges sont situées dans le centre et le sud de l'Ontario et du Québec, suivies par les provinces de l'Atlantique et les Prairies, où les charges sont les plus faibles.
Les charges municipales ont été combinées aux charges provinciales et territoriales pour estimer l'utilisation totale de sels par district d'entretien, durant l'hiver 1997-1998 (figure 4); on estime que 4 418 462 tonnes de chlorure de sodium ont été utilisées pour le déglaçage des routes au Canada.
Figure 2 Taux d'épandage de sels de voirie (chlorure de sodium) par agence provinciale en 1998 (d'après Morin et Perchanok, 2000)

Cependant, cette estimation de la charge totale ne tient compte que de l'utilisation des sels de voirie par les administrations municipales, provinciales, territoriales et régionales. Les compagnies privées, les industries et les agences, comme les autorités portuaires et les sociétés de transport, utilisent elles aussi des sels de voirie. Cheminfo (1999) a estimé que l'utilisation totale par des clients commerciaux et industriels représente de 5 à 10 % du marché des sels de voirie. On a eu recours à une valeur médiane de 7,5 % pour estimer la quantité de sels de voirie utilisée par les sources commerciales et industrielles au Canada (tableau 2). Si on inclut cette quantité, on obtient alors une estimation de 4 749 847 tonnes de chlorure de sodium durant l'hiver 1997-1998.
2.2.2.2 Chlorure de calcium
Le tableau 3 indique la quantité de chlorure de calcium utilisée par les provinces et les territoires. Bien que l'Ontario soit la province qui utilise la plus grande quantité de chlorure de calcium sur ses routes, les analyses faites par Morin et Perchanok (2000) indiquent que la Nouvelle-Écosse est la province qui en consomme le plus, par unité de surface.
2.2.2.3 Charges totales de chlorure
Pour estimer l'utilisation totale de chlorures sur les routes par province, on a combiné les quantités estimatives de chlorure de sodium et de chlorure de calcium épandues sur les routes du Canada. Le tableau 4 présente l'utilisation totale de chlorures par province, d'après la charge totale de chlorure de sodium durant l'hiver 1997-1998 et l'utilisation estimée de chlorure de calcium au cours d'une année normale. La masse de chlorure utilisée par région d'une province a été calculée pour établir des comparaisons entre les charges. Ainsi, bien que l'Ontario et le Québec soient les provinces qui utilisent le plus de chlorures sur les routes, la Nouvelle-Écosse est celle où la charge par unité de surface est la plus élevée (Morin et Perchanok, 2000).
2.2.2.4 Tendances historiques
Les fluctuations, au fil des ans, des charges de sels de voirie ont été examinées, grâce aux données à long terme sur l'utilisation totale de sels obtenues de quelques organismes chargés de l'entretien des routes. Alors que ces données semblent indiquer que les charges totales de sels de voirie ont dans l'ensemble augmenté, elles indiquent également que ces charges fluctuent d'une année à l'autre. Il est en outre difficile de conclure qu'il y a eu augmentation des charges sans données sur la longueur du réseau routier à entretenir.
Figure 3 Taux d'épandage moyen de sels voirie (chlorure de sodium) par municipalité en 1998 (d'après Morin et Perchanok, 2000)

Figure 4 Quantités totales de chlorure de sodium utilisées par district d'entretien (d'après Morin et Perchanok, 2000)

- On suppose que l'usage commercial et industriel des sels de voirie correspond à 7,5 % de l'utilisation provinciale et municipale (d'après une estimation de Cheminfo, 1999).
- Incluant le Nunavut.
Un des moyens de déterminer, de façon approximative, si les charges annuelles de sels de voirie ont fluctué est de comparer les données d'enquête compilées par le Salt Institute, entre le milieu des années 1960 et le début des années 1980 (Salt Institute, 1964-1983), aux données recueillies dans le cadre de l'enquête quinquennale (de 1993-1994 à 1997-1998). Cette comparaison semble indiquer que les charges de sels de voirie, par kilomètre de route à deux voies, n'ont pas diminué. Ainsi, alors que certains organismes ont utilisé des quantités similaires de sels par kilomètre de routes à deux voies durant ces deux périodes, d'autres les ont légèrement augmentées entre le début des années 1980 et le milieu des années 1990. La figure 5 illustre les charges provinciales moyennes par kilomètre de route provinciale (à deux voies) pour l'Ontario, le Québec, le Nouveau-Brunswick et la Nouvelle-Écosse.
On a évalué la comparabilité et le regroupement des données obtenues des différentes sources, à différentes périodes, en comparant la concordance de divers ensembles de données obtenus d'organismes provinciaux de l'Ontario et de la Nouvelle-Écosse. Il a toutefois été impossible de faire cette comparaison pour les autres provinces, vu l'absence de chevauchement entre les données. Lorsqu'une comparaison a pu être établie, celle-ci a indiqué une concordance entre les quantités déclarées. À titre d'exemple, les données obtenues du Salt Institute indiquent que le ministère des Transports de l'Ontario a utilisé respectivement 418 997, 486 648 et 402 346 tonnes de chlorure de sodium durant les hivers 1978-1979, 1981-1982 et 1982-1983 (Salt Institute, 1964-1983), alors que les données fournies par le ministère des Transports de l'Ontario, pour ces mêmes années, font état respectivement de 415 381, 486 648 et 402 346 tonnes de chlorure de sodium. On note une même concordance entre les données du Salt Institute et celles du ministère des Transports et des Travaux publics de la Nouvelle-Écosse, toutes deux indiquant que 201 989 et 129 453 tonnes de chlorure de sodium ont été utilisées durant les hivers 1981-1982 et 1982-1983. Malgré le caractère limité de cette comparaison, celle-ci laisse croire que les données du Salt Institute et des organismes provinciaux concordent.
1 Incluant le Nunavut.
1 Incluant le Nunavut.
2.2.3 Fiabilité des données sur les charges
Malgré tous les efforts qui sont faits en vue d'obtenir des données auprès des sources les plus exactes qui soient, il se peut que des erreurs se glissent dans les données et les calculs. Il est possible, par exemple, que la quantité déclarée de sels épandus soit inexacte ou que certaines utilisations des sels ne soient pas rapportées. Il peut aussi y avoir manque de cohérence dans la déclaration des données. Ainsi, dans certaines provinces, les achats de sels de voirie destinés aux municipalités sont faits par les provinces ou celles-ci s'occupent de l'entretien des routes municipales; les données municipales peuvent donc être incluses dans les charges provinciales pour certains districts. Un autre problème tient au fait que les données de l'enquête portent sur le sel acheté et non sur le sel utilisé. Bien que tout le sel acheté finisse par être utilisé, il n'y a aucun moyen de déterminer la quantité de sel qui est épandue chaque année. On a évalué les erreurs possibles dans les données des fournisseurs de sels, en corrélant les appels d'offre et l'utilisation au niveau provincial. Dans l'ensemble, on note une forte corrélation entre les deux ensembles de données.
Une autre source potentielle d'erreurs pourrait être l'utilisation des données de 1997-1998 pour caractériser les charges de sels. En effet, même si ces quantités correspondent à la meilleure estimation, les données provinciales disponibles indiquent que les charges varient d'une année à l'autre. Une comparaison entre les données obtenues de tous les organismes ayant fourni des données sur les charges totales de sels par unité de longueur de route, pour les cinq années à l'étude, laisse croire toutefois que l'hiver 1997-1998 n'est pas anormal (figure 5). Aussi, pour valider l'hypothèse voulant que l'hiver 1997-1998 soit représentatif, deux analyses statistiques ont été faites (Collins, 2000). Les données ont d'abord été analysées selon l'analyse de la variance (ANOVA); comme ces données ne correspondaient pas à une distribution normale, une analyse a aussi été faite au moyen de la méthode non paramétrique à deux voies de Friedman, par rang. Chaque fois qu'une différence significative a été observée entre des années, la méthode de diminution graduelle de Ryan a été utilisée pour analyser les écarts entre les années. Les résultats obtenus par ces analyses indiquent des charges légèrement inférieures pour l'année 1997-1998 (Collins, 2000).
Une des limites potentielles de ces analyses pourrait être due au fait qu'une catégorie « route sur laquelle il peut y avoir épandage de sels » a servi à caractériser les charges de sels. Or, comme les autoroutes reçoivent généralement des charges plus fortes, on pourrait alléguer que l'utilisation d'une telle catégorie a pour effet de sous-estimer les charges de sels sur les routes où le volume de circulation est élevé. Une autre limite pourrait venir de l'utilisation du nombre d'habitants pour estimer les charges de sels dans les municipalités n'ayant pas fourni de données. En effet, même s'il existe une bonne corrélation entre la population des municipalités et l'utilisation de sels au niveau provincial, la rigueur de cette relation varie d'un district d'entretien à un autre.
En dépit de ces limites possibles, les données présentées sont de bons indicateurs des quantités de sels utilisées sur les routes au Canada, notamment lorsqu'on considère qu'il y a une différence de 9,4 % (417 501 tonnes) entre l'utilisation connue et l'utilisation estimée de chlorure de sodium par municipalité, comté et province, pour l'hiver 1997-1998.
2.2.4 Sommaire
L'utilisation annuelle de sels de voirie à base de chlorure de sodium et de chlorure de calcium au Canada a été estimée à partir d'enquêtes réalisées auprès d'agences provinciales, territoriales et municipales, des données obtenues de l'industrie et des estimations fondées sur la population. On estime ainsi qu'environ 4,75 millions de tonnes de chlorure de sodium ont servi au déglaçage des routes pendant l'hiver 1997-1998 et que 110 000 tonnes de chlorure de calcium sont épandues sur les routes durant une année normale. Si on les combine, on obtient 2,95 millions de tonnes de chlorure épandues sur les routes au Canada durant l'année 1997-1998. Il faut reconnaître toutefois que les quantités fluctuent d'une année à l'autre, notamment parce que les conditions climatiques varient.
Figure 5 Historique de l'utilisation de sels de voirie par les agences provinciales (fondée sur les enquêtes du « Salt Institute 1964-1983 » et Morin et Perchanok, 2000)

Les charges annuelles varient selon la région géographique, les charges les plus fortes (en fonction de la longueur du réseau routier) étant observées en Ontario et au Québec; les charges sont moyennes dans les provinces de l'Atlantique et elles sont les plus faibles dans les provinces de l'Ouest. Les données présentées dans cette section indiquent que, dans l'ensemble, les charges de sels de voirie n'ont pas diminué au cours des 20 dernières années et qu'elles auraient au contraire augmenté dans certaines provinces, depuis la fin des années 1970 (figure 5).
2.3 Élimination de la neige
Delisle et Dériger (2000) ont passé en revue les propriétés physico-chimiques et écotoxicologiques de la neige usée déblayée des routes, ainsi que les différentes méthodes utilisées pour l'enlèvement de la neige des routes et des trottoirs.
2.3.1 Caractérisation de la neige usée
Les sels de voirie contribuent à la présence d'ions sodium, chlorure et cyanure dans la neige. Parmi les autres principaux contaminants présents dans la neige en milieux urbains, mentionnons des débris, des matières en suspension, des huiles et des graisses et des métaux (plomb, manganèse, fer et chrome) (Gouvernement du Québec, 1997). Dans certaines municipalités du Québec, la concentration moyenne de chlorure dans la neige en bordure des routes ou dans l'eau de fonte qui en provient varie de 3,8 à 5 689 mg/L (voir Delisle et Dériger, 2000).
- Ces quantités sont approximatives et varient d'une année à l'autre en fonction des chutes de neige; n.d. = non disponible.
- Plus 100 000 tonnes d'un mélange de sable et de sel contenant 5 % de NaCl.
- Plus 39 000 tonnes d'un mélange de sable et de gravier (en proportions de 1:9 pour les trottoirs et de 5:5 pour les rues) en périodes de pluie verglaçante.
Chenevier (1997) a analysé les paramètres physico-chimiques de la neige prélevée en bordure de routes principales et secondaires de Montréal, en 1997. Pour tous les paramètres examinés, des concentrations plus élevées ont été observées dans la neige provenant des routes principales; dans le cas du chlorure, par exemple, la concentration moyenne a été de 3 115 mg/L pour les rues secondaires et de 5 066 mg/L pour les rues principales (Delisle et Dériger, 2000). Cette différence s'explique sans doute par une fréquence ou un taux d'épandage plus élevé des sels de voirie. Dans le cadre d'une étude similaire réalisée par Delisle et al. (1997), les propriétés physico-chimiques de la neige en bordure des routes ont été examinées lors de deux tempêtes en janvier 1997. La concentration moyenne de chlorure mesurée dans les échantillons prélevés durant la première et la deuxième tempêtes a été respectivement de 7 716 et 3 663 mg/L, la concentration dans les 24 échantillons prélevés durant les deux tempêtes variant entre 1 366 et 18 230 mg/L.
Un grand nombre de facteurs influent sur les caractéristiques de la neige en bordure des routes, notamment la taille de la collectivité, le facteur d'occupation des terres, la densité de la circulation, la quantité de sels de déneigement et d'abrasifs utilisés ainsi que la durée des activités de déneigement (Malmqvist, 1985; Delisle et al., 1995). En général, la teneur en contaminants varie aussi avec le temps : ainsi, 72 heures après le déneigement, des concentrations de chlorure de 530 mg/L et de 7 496 mg/L ont été mesurées dans la neige provenant respectivement de rues résidentielles et commerciales (Delisle et Leduc, 1987); après plus d'une semaine, ces concentrations avaient diminué à 590 mg/L, sans doute sous l'effet de la perte d'ions par l'eau de fonte.
2.3.2 Volumes de neige dans les villes canadiennes
Il est parfois nécessaire de procéder à l'enlèvement et à l'élimination de la neige, lorsque l'accumulation sur les routes ou le long des routes gêne la circulation ou nuit à la sécurité. La quantité de neige à enlever et à éliminer dépend du volume de neige et de l'ampleur de l'aménagement urbain (tableau 5). Étant donné l'importance des chutes de neige à Montréal (dans le sud du Québec, les chutes de neige varient annuellement entre 200 et 350 cm), ainsi que la superficie et la densité de la ville, quelque 11,258 millions de mètres cubes de neige ont été acheminés aux lieux d'élimination de la neige durant l'hiver 1997-1998, comparativement à 1,5 million de mètres cubes à Toronto (avant la fusion municipale) et à un total d'environ 30 millions de mètres cubes, pour l'ensemble des municipalités du Québec.
2.3.3 Méthodes d'enlèvement et d'élimination de la neige
Le déblaiement de la neige consiste habituellement à chasser la neige vers l'accotement de la route. Dans les villes, le déblaiement peut commencer lorsqu'il y a accumulation de 2,5 cm de neige au sol et celle-ci est alors repoussée sur les côtés des rues et sur les trottoirs. Lorsque l'accumulation est importante (plus de 10 cm) ou que les conditions l'exigent, on procède alors à l'enlèvement de la neige et à son transport dans divers lieux d'élimination (Ville de Montréal, 1998). Delisle et Dériger (2000) décrivent les diverses méthodes d'élimination de la neige qui sont regroupées ci-après en trois catégories.
2.3.3.1 Méthodes sans enlèvement de la neige
Les méthodes de déneigement sans enlèvement de la neige consistent habituellement à repousser la neige le long de la route au moyen de chasse-neige ou à la souffler sur les terrains adjacents. En général, ces méthodes ne sont pas efficaces dans les régions où le taux d'occupation des sols est élevé (Delisle, 1994). Elles sont par contre les méthodes les plus répandues pour dégager les routes dans les régions non urbaines. Ce type de méthode contribue aux impacts que peuvent causer les sels de voirie sur les sols, la végétation, les eaux de surface et les eaux souterraines en bordure des routes. Des données recueillies par Watson (2000) ont permis de déterminer les concentrations de chlorure dans les étangs et les terres humides situés à proximité de routes, dans le sud de l'Ontario. Les résultats de cette étude indiquent que les concentrations de chlorure varient, mais des concentrations supérieures à 4 000 mg/L ont été observées. Ils révèlent par ailleurs que le ruissellement provenant des routes peut avoir une incidence négative sur les milieux aquatiques adjacents.
Selon une étude menée par Delisle (1999), laquelle a établi un lien entre la présence de concentrations élevées de chlorure dans les puits municipaux et l'épandage de sels de voirie, des concentrations élevées de chlorure ont été observées dans une région où l'on a laissé l'eau des fossés s'infiltrer dans les sols. Les concentrations de chlorure dans trois puits municipaux de la région à l'étude ont ainsi augmenté de 102, 116 et 145 mg/L, entre 1983 et 1994.
2.3.3.2 Méthodes avec rejet dans les plans d'eau, après traitement de l'eau de fonte
La neige peut être transportée dans des lieux d'élimination, où la neige fond et où l'eau de fonte est traitée; cette méthode consiste habituellement à décharger la neige en surface ou dans des carrières où le ruissellement est acheminé vers des installations de traitement. En général, les lieux d'élimination de la neige sont aménagés sur des sols imperméables ou légèrement perméables, ou munis d'une membrane géotextile. Certains lieux sont également dotés d'installations de décantation ou sont conçus de manière à ce que l'eau de fonte soit acheminée vers des installations de traitement des eaux usées (Gouvernement du Québec, 1991). Ces sites ne doivent pas être aménagés à proximité de cours d'eau qui pourraient être dégradés par le ruissellement.
Pinard et al. (1989) ont déterminé les concentrations de chlorure dans le ruissellement provenant des lieux d'élimination de la neige. Cette étude a révélé que seulement 2 % du sel épandu sur les routes des villes se retrouvait dans l'eau de fonte s'écoulant des lieux d'élimination de la neige, la majeure partie du sel ayant probablement déjà pénétré dans l'environnement, à partir des routes ou des accotements. Ces données concordent avec celles de Delisle et Leduc (1987) qui ont constaté que la concentration de chlorure dans la neige en bordure des routes commence par augmenter, puis diminue avec le temps. Il convient toutefois de noter que la concentration de chlorure dans la neige usée varie selon le type de rue, la concentration mesurée dans la neige provenant de rues principales pouvant dépasser, d'un ordre de grandeur, la concentration mesurée dans la neige usée de routes secondaires.
Cependant, même si le pourcentage de sels dans la neige amenée aux lieux d'élimination peut être faible (p. ex., 2 %), la concentration de chlorure dans le ruissellement demeure élevée. Une étude réalisée par Péloquin (1993) fait ainsi état d'une concentration moyenne de chlorure de 414 mg/L dans l'eau de fonte d'un lieu d'élimination de la neige. Pour leur part, Pinard et al. (1989) ont évalué la concentration de chlorure dans l'eau de ruissellement provenant d'un lieu d'élimination de la neige situé à Québec, entre le 18 avril et la fin de juin 1988, et constaté que la concentration variait entre 100 et 1 100 mg/L. Les concentrations les plus élevées ont été observées au début de l'échantillonnage et ont diminué graduellement tout au long du printemps. On ignore toutefois si les concentrations de chlorure étaient plus élevées dans l'eau de ruissellement avant le début du programme de surveillance, ou si les concentrations ont augmenté tout au long de l'été à cause d'une diminution du volume d'eau de ruissellement.
Les effets potentiels de l'eau de fonte sur la qualité des eaux souterraines varient selon le lieu d'élimination. Selon une étude décrite dans Morin (2000), des concentrations de chlorure variant entre 233 et 1 820 mg/L ont été mesurées dans des puits de surveillance aménagés pour évaluer l'incidence d'un lieu d'élimination de la neige sur la qualité des eaux souterraines à faible profondeur.
Certains organismes (p. ex., la Ville de Montréal) déversent la neige dans des puits de descente reliés aux réseaux d'égouts municipaux (Godbout, 1996; Couture, 1997). D'autres ont recours à des fondeuses à neige, qui peuvent être fixes ou mobiles, et qui ont pour effet d'entraîner le déversement d'eau, plutôt que de neige, dans le réseau d'égouts. La neige est amenée par camion et versée dans des réservoirs d'eau préchauffée, munis de brûleurs au mazout ou au gaz. La Ville de Toronto utilise cette technique à l'occasion. Depuis janvier 1998, la ville de Cap-Rouge, au Québec, utilise une technique « géothermique » pour faire fondre la neige, laquelle consiste à utiliser des formations géologiques comme réservoirs naturels où l'eau est stockée durant l'été et maintenue à une température suffisamment élevée pour faire fondre la neige en hiver (Bilodeau, 1999).
2.3.3.3 Méthodes de rejet dans les eaux de surface sans traitement préalable
Cette méthode consiste à déverser la neige directement dans un cours d'eau ou sur ses rives, ou encore dans des puits de descente non reliés à une station d'épuration. Cette méthode entraîne le rejet direct de la neige usée et de tous les contaminants qu'elle renferme dans les eaux de surface (rivières ou océans), après l'élimination partielle des gros débris (rejet sur le rivage) ou dilution possible par les eaux pluviales (rejet dans des puits de descente non reliés à une usine d'épuration).
2.3.4 Méthodes d'élimination utilisées par les municipalités canadiennes
Le tableau 6 présente les méthodes d'élimination de la neige utilisées par certaines municipalités du Canada. La Ville de Montréal est celle qui utilise le plus large éventail de méthodes d'élimination; en 1997-1998, Montréal a ainsi eu recours à des décharges de surface (7), des puits de descente (11) et des carrières (2); la neige a aussi été déversée dans le fleuve Saint-Laurent à 3 endroits (Ville de Montréal, 1998).
Il est clair que les décharges de surface constituent la méthode d'élimination la plus courante au Canada. Regina, par exemple, en utilise de deux à cinq, selon l'année (Ville de Regina, 1997). Dans le cas de la municipalité régionale d'Ottawa-Carleton, plusieurs études ont été effectuées pour déterminer le nombre de décharges de surface nécessaires à l'élimination de la neige dans cette région (McNeely Engineering, 1990; McNeely-Tunnock Ltd., 1995). Dans quelques cas, comme St. John's, Halifax et Vancouver, la neige est déversée dans l'océan. Au Québec, le déversement direct de la neige dans les eaux douces de surface est restreint et sera interdit à compter de 2002.
Auparavant, des municipalités comme Montréal soufflaient la neige sur les propriétés privées et, à l'occasion, utilisaient des fondeuses à neige. Les pressions sociales et politiques ont toutefois forcé la Ville de Montréal à abandonner presque entièrement le soufflage de la neige sur les propriétés privées, et les fondeuses à neige se sont révélées trop coûteuses à exploiter, en raison du prix élevé du carburant (Ville de Montréal, 1998). Dans certaines villes comme Halifax, on a recours à de grandes quantités de sels de déneigement, mais l'enlèvement de la neige est très peu pratiqué, les eaux de fonte étant dirigées vers les réseaux d'égouts pluviaux (Delisle et Dériger, 2000).
2.3.5 Sommaire
Outre les ions inorganiques provenant des sels de voirie, la neige usée peut contenir une grande variété de contaminants physiques et chimiques. Les ions chlorure sont dissous puis transportés dans l'eau de fonte de la neige et échappent en grande partie aux procédés physiques ou biologiques de traitement de l'eau. Leurs effets dépendent des quantités et des concentrations totales d'ions au point de rejet de l'eau de fonte dans les eaux de surface, le sol et les eaux souterraines. Bien que les concentrations de chlorure dans la neige usée et son eau de fonte varient sensiblement, elles peuvent atteindre 18 000 mg/L. À Montréal, la concentration moyenne de chlorure dans la neige provenant d'artères principales et secondaires a été respectivement de 3 000 mg/L et de 5 000 mg/L. Les municipalités canadiennes utilisent diverses méthodes d'élimination de la neige, mais les décharges de surface sont les plus répandues. Enfin, malgré l'incertitude quant à la proportion de sels susceptible d'être transportée dans les lieux d'élimination de la neige, il ne fait aucun doute que l'eau de ruissellement qui s'écoule de ces lieux contient de fortes concentrations de chlorure.
1 Incluant le Nunavut.
2.4 Entrepôts de sels
Les entrepôts de sels (aussi appelés dépôts de voirie) servent à entreposer les produits d'entretien avant leur épandage sur les routes. Les sections qui suivent décrivent et caractérisent ces installations, indiquent les voies d'exposition environnementale et présentent les concentrations qui ont été mesurées à des endroits précis, autour de ces dépôts. La plupart des données sont basées sur les normes qui s'appliquaient avant 1998, relativement à la conception des entrepôts de sels et au stockage des sels de voirie. Bien que l'on fasse aujourd'hui la promotion de concepts plus efficaces pour réduire les pertes de sel (ATC, 1999), les normes actuelles en matière de conception et de gestion sont sensiblement les mêmes que celles examinées dans le présent rapport. Les données dans les sections qui suivent ont été résumées à partir d'un rapport préparé par Snodgrass et Morin (2000).
2.4.1 Nombre d'entrepôts de sels et quantités entreposées
Les données compilées par Morin et Perchanok (2000) ont servi à estimer le nombre d'entrepôts de sels provinciaux et territoriaux et les quantités de sels de voirie et d'abrasifs qui y sont entreposées. On ne possède pas d'information précise sur le nombre d'entrepôts de sels au Canada, mais on a estimé qu'il existe 1 300 entrepôts provinciaux. Les quantités moyennes dans chaque entrepôt de sels ont été estimées en supposant que la quantité totale de sels et d'abrasifs utilisée par les diverses instances était répartie également entre tous les entrepôts de sels (tableau 7). À noter toutefois que ce tableau n'inclut pas les dépôts des municipalités et des comtés, ni ceux des compagnies privées; le nombre de dépôts au Canada y est donc grandement sous-estimé. Au Canada, la quantité moyenne de sels et d'abrasifs entreposée varie considérablement d'un entrepôt à un autre. Selon le tableau 7, la quantité moyenne de sels dans les entrepôts du Québec, de l'Ontario et des Maritimes varie entre 1 300 et 3 800 tonnes, alors que la quantité moyenne d'abrasifs pour ces mêmes provinces varie entre 1 000 et 8 600 tonnes. Snodgrass et Morin (2000) présentent le nombre d'entrepôts de sels par district et les quantités moyennes (en tonnes) de chlorure de sodium et d'abrasifs par entrepôt, dans certaines provinces.
Selon les données obtenues pour 117 entrepôts administrés par le ministère des Transports de l'Ontario durant l'hiver 1997-1998, la quantité de chlorure de sodium stockée à ces endroits a varié de 45 à 21 400 tonnes par dépôt, alors que les quantités d'abrasifs ont varié entre 10 et 13 200 tonnes par dépôt.
2.4.2 Conception et gestion des entrepôts de sels
Les entrepôts de sels peuvent être aménagés à des endroits fort variés, et leur conception ainsi que les normes qui s'y appliquent varient considérablement d'un endroit à l'autre du pays. Par conséquent, le niveau de protection contre les intempéries varie lui aussi sensiblement. Les installations couvertes utilisées pour le stockage des sels de voirie incluent les dômes ou igloos, ainsi que les remises et les appentis, avec ou sans portes et murs. Certains organismes considèrent même que l'entreposage sous les ponts routiers correspond à un entrepôt couvert. Les sels peuvent être entreposés sur une plate-forme d'asphalte ou de béton, ou à l'extérieur sur une bâche de plastique épais et recouverts d'une autre bâche. Même si l'entreposage en installations couvertes offre une certaine protection contre les précipitations qui causent la lixiviation des sels, aucune norme universelle ne régit la conception des installations d'entreposage. L'utilisation des meilleures pratiques de gestion favorisant un bon entretien des entrepôts est tout aussi importante pour réduire les pertes de sels. L'efficacité de ces pratiques dépend cependant de la rigueur avec laquelle elles sont appliquées.
Les sels peuvent provenir aussi bien des piles d'abrasifs auxquels ils sont mélangés que des piles de sels. Les piles de sels et d'abrasifs consistent en du sel mélangé à du sable ou à du gravier pour éviter le gel ou l'agglomération des abrasifs (ministères de l'Environnement et des Transports du Nouveau-Brunswick, 1978). Le pourcentage de sel dans ces mélanges varie -la plupart des agences utilisent un mélange à 5 %, mais le pourcentage peut fluctuer entre 2,5 et 15 %. Une étude a été réalisée au Nouveau-Brunswick (ME et MT du N.-B., 1978) pour évaluer la quantité et la qualité du lixiviat provenant d'une pile d'abrasifs de 2 000 tonnes ayant une teneur en sel de 2,5 %. Durant la première année, 420 m3 de lixiviat ont été analysés grâce au système de surveillance. La figure 6 illustre les concentrations de sodium et de chlorure mesurées dans le lixiviat, les concentrations maximales ayant atteint respectivement 37 000 et 66 000 mg/L. On estime que la perte totale de sels par lixiviation durant la première année a été de 18,2 tonnes, soit plus du tiers de la quantité totale de sels ajoutée aux abrasifs, et ce même si 80 % de la pile d'abrasifs avait déjà été utilisée pour le sablage à la fin de janvier. Les résultats de la deuxième année indiquent aussi de fortes concentrations de chlorure dans les 255 m3 de lixiviat analysés, les concentrations maximales de sodium et de chlorure atteignant alors respectivement 49 000 et 82 000 mg/L. À la lumière de ces concentrations et des résultats d'une enquête révélant que peu d'organismes provinciaux couvrent les piles d'abrasifs et de sels (Snodgrass et Morin, 2000), on peut dire que les pertes potentielles de sels provenant des piles d'abrasifs et de sels sont élevées.
Les déversements pendant le stockage et le chargement des épandeuses sont une autre source importante de pertes de sels (ATC, 1999), comme le confirme un examen de levés électromagnétiques effectués dans les entrepôts de sels (Snodgrass et Morin, 2000). Ces levés, qui déterminent habituellement les matières et les eaux souterraines de la subsurface (à moins de 6 m de la surface) qui sont fortement conductrices (p. ex., les sols et les eaux souterraines à forte teneur en sels), ont révélé une grande conductivité dans les zones adjacentes aux voies d'accès aux installations d'entreposage de sels, ainsi qu'autour de ces installations.
Figure 6 Concentration moyenne quotidienne en 1975-1976 des lixiviats pouvenant d'un amas avec du sel (d'après ME et MT NB, 1978)

Les eaux usées provenant du lavage des véhicules d'entretien des routes durant l'hiver constituent une autre source potentielle de contamination. Dans les entrepôts de sels des régions urbaines, les eaux de lavage sont sans doute rejetées dans le réseau municipal d'égouts; dans les régions rurales, le rejet se fait probablement dans un puits sec où l'eau percole dans le sol. Une étude révèle que des échantillons d'eaux de lavage provenant de sept entrepôts de sels avaient une teneur en chlorure variant entre 3 500 et 37 000 mg/L, la concentration moyenne étant de 16 000 mg/L (Beck et al., 1994). La même étude a aussi révélé qu'entre le tiers et les deux tiers des entrepôts de sels de l'Ontario rejettent les eaux de lavage dans des puits secs. On peut aussi estimer les concentrations de chlorure dans les eaux de lavage en analysant les concentrations de chlorure dans les séparateurs huile-eau. Ces appareils sont installés dans certains garages des entrepôts de sels pour éliminer les huiles, les graisses et autres composés semblables présents dans les flux de déchets des eaux de lavage. Comme les séparateurs huile-eau n'éliminent pas le sel, les concentrations dans l'effluent sont identiques à celles de l'influent. Selon une étude effectuée par INTERA Consultants (1995), des concentrations de chlorure variant entre 1 100 et 35 400 mg/L ont été mesurées dans les séparateurs huiles/eau de trois entrepôts de sels , ces concentrations étant à peu près équivalentes à celles mesurées par Beck et al. (1994).
2.4.3 Estimation des rejets provenant des entrepôts de sels
Cette section présente une estimation des rejets de sels provenant des entrepôts de sels. Snodgrass et Morin (2000) définissent plus en détail les hypothèses qui ont servi à calculer ces rejets. Les rejets dans l'environnement ont été estimés à partir d'un scénario hypothétique sur les rejets de 190 dépôts en exploitation. Les rejets estimatifs totaux ont ensuite été comparés, en regard d'un épandage total de quelque 590 000 tonnes par année. Ce scénario hypothétique correspond à peu près à la quantité épandue dans une grande province ou dans plusieurs provinces plus petites et a servi de base globale de calcul.
Le tableau 8 présente trois estimations fondées sur les scénarios suivants : (1) un entrepôt de sels appliquant les meilleures pratiques de gestion, c'est-à-dire où les mélanges de sels et d'abrasifs sont entreposés à l'intérieur; (2) un entrepôt de sels où les sels sont entreposés à l'intérieur et les abrasifs, à l'extérieur et (3) un entrepôt de sels où tous les amas sont entreposés à l'extérieur. Des trois scénarios, les options 1 et 2 sont sans doute celles qui sont les plus représentatives des entrepôts de sels. La dernière colonne du tableau 8 présente une estimation du pourcentage de sels perdus dans les entrepôts de sels, par rapport à la quantité totale utilisée. Selon le type d'installation et le mode de gestion, les pertes de sels dans les entrepôts varient entre 0,2 et 20 % de la quantité totale utilisée.
2.4.4 Concentrations de sels à différents points autour des entrepôts
Les sections qui suivent donnent un aperçu des concentrations mesurées à différents endroits (en surface et subsurface), dans les entrepôts de sels.
2.4.4.1 Concentrations en surface autour des entrepôts de sels
On dispose d'une base de données limitée sur les systèmes de drainage de surface autour des entrepôts de sels; ces données proviennent d'évaluations environnementales des sites (EES) qui ont été faites à certains dépôts du ministère des Transports de l'Ontario (MTO, 1993-1999). Les concentrations de chlorure dans 29 dépôts où des échantillons ont été prélevés variaient de 4 à 4 880 mg/L, la concentration moyenne étant de 659 mg/L.
Une étude similaire a été réalisée dans un entrepôt de sels de l'Alberta. Un échantillon prélevé dans le bassin d'évaporation situé à cet endroit avait une concentration de chlorure de 32 100 mg/L (Alberta Infrastructure, 2000). Une autre étude, faite par le ministère des Transports et des Travaux publics de la Nouvelle-Écosse, a révélé que le ruissellement et les eaux souterraines peu profondes s'écoulant d'un entrepôt de sels vers un petit ruisseau ont eu pour effet d'accroître la concentration de chlorure dans un étang situé à environ 250 m en aval, cette concentration étant passée de moins de 75 mg/L à environ 1 000 mg/L (Rushton, 1999).
2.4.4.2 Concentrations dans l'eau de puits des entrepôts de sels
Une étude menée par le ministère des Transports de l'Ontario (MTO, 1997) a permis de dresser le graphique des concentrations de chlorure dans plus de 300 entrepôts de sels de l'Ontario, sur une période de 20 à 30 ans prenant fin en 1988. Une période de cinq ans (1983 à 1988) a été choisie pour caractériser la gamme de concentrations décelées dans les puits des entrepôts de sels. La plupart des dépôts examinés (229 dépôts, 74 %) avaient une concentration de chlorure inférieure à 200 mg/L. Un nombre moindre (82 dépôts, 26 %) avaient une concentration supérieure à 200 mg/L, dont 30 (9 %) affichaient une concentration supérieure à 500 mg/L et 14 (4 %), une concentration excédant 1 000 mg/L.
La qualité de l'eau des puits d'alimentation en eau potable a été testée, dans le cadre des évaluations environnementales des sites faites sur les entrepôts de sels de la région Est du ministère des Transports de l'Ontario (MTO, 1993-1999). Des concentrations de chlorure de 1,5 à 5 050 mg/L ont été mesurées dans les échantillons prélevés de 36 puits, pour une concentration moyenne de 722 mg/L. Soixante-quatre pour cent des échantillons avaient une concentration supérieure à 100 mg/L et 50 %, une concentration dépassant 250 mg/L. Dans 35 % des échantillons, la concentration a été supérieure à 500 mg/L. La profondeur des puits testés variait de 12 à 113 m, pour une moyenne de 39,2 m. Cependant, une concentration élevée de chlorure dans un puits ne signifie pas nécessairement que toute la nappe phréatique est contaminée; il peut arriver en effet que des défauts de construction entraînent l'infiltration de sels dans les eaux souterraines par le tubage du puits.
2.4.4.3 Concentrations dans les eaux souterraines de faible profondeur
La même série d'évaluations environnementales des sites (MTO, 1993-1999) a servi à évaluer la qualité des eaux souterraines peu profondes. Dans plusieurs entrepôts de sels, des puits de surveillance ont été aménagés à une profondeur variant entre 0,26 et 5,25 m et des échantillons d'eau souterraine y ont été prélevés. Les concentrations de chlorure dans les 102 échantillons ont varié de 1 à 24 000 mg/L, la concentration moyenne étant de 2 600 mg/L. Le résumé des données indique que 75 % des échantillons présentaient une concentration de chlorure supérieure à 100 mg/L, alors que 69 % avaient une concentration excédant 250 mg/L.
Des analyses similaires ont révélé que les concentrations de chlorure variaient de 26 à 26 400 mg/L dans l'eau souterraine prélevée de trois entrepôts de sels de l'Alberta (Alberta Infrastructure, 2000). En Nouvelle-Écosse, des concentrations de chlorure fluctuant entre 254 et 38 600 mg/L ont été mesurées dans les eaux souterraines peu profondes à trois entrepôts de sels gérés par le ministère des Transports et des Travaux publics de la province (Rushton, 1999).
2.4.4.4 Concentrations dans le sol aux entrepôts de sels
Dans plusieurs entrepôts de sels ayant fait l'objet d'évaluations environnementales, des puits d'essai et de forage ont été creusés et des échantillons de sol ont été analysés (MTO, 1993-1999). Les concentrations de chlorure dans 53 puits d'essai ont varié entre 5 et 14 500 µg/g de sol, alors que des concentrations de sodium de 39 à 13 100 µg/g de sol ont été décelées dans 46 échantillons. Les concentrations moyennes de chlorure et de sodium ont été respectivement de 2 100 et 2 600 µg/g de sol.
Figure 7 Concentration de chlorure dans deux puits d'approvisionnement de Heffley Creek (d'après AGRA, 1999)

Des concentrations de chlorure fluctuant entre 2 et 13 300 µg/g de sol ont été mesurées dans des échantillons de sol prélevés de 46 puits d'essai (concentration moyenne de 1 500 µg/g de sol). Dans le cas du sodium, les concentrations mesurées dans 98 échantillons ont varié de 86 à 6 720 g/g de sol, pour une moyenne de 870 µg/g.
Les puits d'essai avaient entre 0,1 et 5 m de profondeur (profondeur moyenne de 1,6 m).
2.0 Résumé de l'information essentielle à l'évaluation du caractère « toxique » au sens de la LCPE 1999
2.4.5 Concentrations à l'extérieur des entrepôts de sels
Un examen fait par Morin (2000) de certaines études de cas choisies a révélé la présence de fortes concentrations de sels hors des sites, à plusieurs entrepôts de sels de voirie, dont quelques-uns sont décrits dans les paragraphes qui suivent.
Arp (2001) a examiné le lien entre la présence d'un entrepôt de sels et la forte salinité des eaux de surface. Il a constaté que les concentrations de chlorure autour de l'entrepôt variaient selon le type d'eau (eau d'étang ou de cours d'eau), le lieu et la saison. Ainsi, les concentrations de chlorure ont été les plus élevées à l'entrepôt ou près de l'entrepôt, variant de 3 000 à plus de 10 000 mg/L. Les eaux de ruissellement et d'infiltration provenant des entrepôts ont été rapidement diluées par l'eau de surface près de l'entrepôt, les concentrations de chlorure diminuant entre 100 et 300 mg/L. Les concentrations de sels près de l'entrepôt ont aussi varié selon les saisons, atteignant leur plus bas niveau au moment de la fonte des neiges et durant la saison des pluies à l'automne et atteignant leur maximum durant l'été, alors que les précipitations sont moins abondantes et que la température de l'air augmente. Durant l'été, les concentrations plus élevées de sels autour de l'entrepôt se sont propagées à l'étang adjacent et causé une augmentation de la concentration de sels dans le principal ruisseau de drainage.
En Colombie-Britannique, des amas d'abrasifs et des réserves de sels entreposés à découvert, dans des remises offrant peu de protection contre les intempéries, ont causé la contamination du réseau municipal d'approvisionnement en eau de Heffley Creek (BC-MoTH, 1993). Des sels de voirie et des amas d'abrasifs non protégés ayant une teneur en sels de 3 % étaient entreposés à cet endroit depuis 1973 (AGRA, 1995). (Avant 1975, les concentrations de chlorure étaient inférieures à 5 mg/L.) En 1993, le ministère des Transports et de la Voirie de la Colombie-Britannique a reçu une plainte officielle de la municipalité de Heffley Creek, qui alléguait que la nappe phréatique alimentant un des deux puits municipaux avait été contaminée par les sels de voirie entreposés dans le dépôt de Heffley Creek. Des analyses de la qualité de l'eau ont révélé que les concentrations de chlorure à ce puits atteignaient près de 1 000 mg/L. En 1994, de fortes concentrations de chlorure ont été mesurées dans les deux puits municipaux situés à une distance de 175 à 200 m de l'entrepôt de sels de Heffley Creek (figure 7). Les concentrations de chlorure ont ensuite atteint un sommet d'environ 3 200 mg/L en 1995 et, bien qu'elles aient diminué depuis 1996, le puits no 1 affichait toujours des concentrations supérieures à 500 mg/L en 1998 (AGRA, 1999).
En 1996, des plaintes ont été déposées auprès du ministère des Transports et des Travaux publics et du ministère de l'Environnement de la Nouvelle-Écosse, au sujet de la contamination par le sel de puits résidentiels à Bible Hill (Nouvelle-Écosse) Des analyses effectuées dans trois puits alimentant six duplex ont révélé des concentrations de chlorure et de sodium fluctuant entre 130 et 640 mg/L (Rushton, 1999). On a établi que l'entrepôt de sels de Bible Hill, qui était situé assez près de ces résidences, était responsable de cette contamination au sel. Alors que les sels étaient entreposés sous un dôme, les mélanges d'abrasifs étaient habituellement entreposés à l'extérieur. Le ministère des Transports et des Travaux publics de la Nouvelle-Écosse a indiqué que ce genre de contamination des eaux souterraines était caractéristique des lieux où les amas d'abrasifs et de sels sont entreposés à découvert.
Une étude faite par Ohno (1990) sur des terres humides situées près d'entrepôts de sable et de sels dans le Maine a montré que les concentrations de chlorure et de sodium étaient supérieures à celles mesurées dans les sites témoins, de deux ou trois ordres de grandeur. Les concentrations aux sites témoins étaient de 6 mg de sodium/L et de 8 mg de chlorure/L, alors qu'elles ont atteint de 16 à 8 663 mg de sodium/L et de 14 à 12 463 mg de chlorure/L dans les lieux exposés aux sels.
Entre la fin des années 1960 et le début des années 1980, la tourbière Pinhook, dans le comté de LaPorte, en Indiana, a été contaminée par les sels provenant d'un entrepôt (Wilcox, 1982). En 1980 et 1981, des concentrations de chlorure de 5 à 6 mg/L ont été mesurées aux lieux témoins, alors que des concentrations maximales de 1 468 mg de chlorure/L, 982 mg de chlorure/L et 570 mg/L durant une seule journée ont été mesurées respectivement en 1979, 1980 et 1981, aux lieux contaminés. L'apport total de chlorure dans la tourbière pendant les dix années d'entreposage des sels a été estimé comme suit : 2,3 millions de kilogrammes provenant de la pile de sels, 0,4 million de kilogrammes provenant de l'épandage sur les routes et 0,012 million de kilogrammes, des précipitations directes.
2.5 Devenir et pénétration dans l'environnement
Les sels de voirie pénètrent et migrent dans l'environnement, sous forme de sels ou d'ions dissociés. En milieux aquatiques, les sels de chlorure sont présents sous forme dissociée, sous forme d'ions chlorure et de leurs cations correspondants (sodium, potassium, calcium, magnésium). Le mouvement du chlorure à travers le cycle de l'eau dépend essentiellement de processus physiques plutôt que chimiques. Les ions chlorure traversent facilement le sol, pénètrent dans les eaux souterraines et finissent par atteindre les eaux de surface. Comme les ions chlorure sont persistants et qu'ils entrent dans le cycle de l'eau, on peut s'attendre à ce que tous les ions chlorure - qui sont épandus sur les routes sous forme de sels de voirie ou qui s'échappent des entrepôts de sels ou des lieux d'élimination -finiront par atteindre les eaux de surface. Cette section traite du devenir et de la migration des sels de voirie dans l'environnement et de leurs voies de pénétration potentielles.
2.5.1 Devenir et transport
Une fois dans les eaux de surface, les sels de voirie restent en solution à moins que leur concentration ne soit très élevée et dépasse ainsi leur solubilité, auquel cas il peut y avoir cristallisation puis sédimentation des sels minéraux. Lorsque l'eau contenant des sels de voirie s'infiltre dans le sol, les ions de charge positive (c.-à-d. sodium, calcium, magnésium et potassium) sont attirés vers le sol de surface de charge négative inhérente et s'y lient. Le degré de liaison dépend du pouvoir d'échange cationique et du nombre de sites de charge négative dans le sol. L'ion sodium est très soluble et peut, une fois dissous, demeurer en solution; cependant, comme il se fixe facilement aux particules de sol, il est moins probable qu'il atteigne les eaux souterraines et les eaux de surface. Dans les cas toutefois où l'adsorption est limitée ou lorsqu'il se produit une lixiviation extrême dans le sol, l'ion sodium emprunte les voies de l'eau et finit par atteindre les eaux souterraines puis les eaux de surface (MDOT, 1993).
Il n'existe pas de mécanismes d'élimination majeurs, comme la volatilisation, la dégradation (photodégradation, biodégradation), la sorption (aux particules) ou l'oxydation, qui contribuerait à l'élimination des sels dans les eaux de surface. La dilution causée par le mélange avec des eaux de faible salinité diminuerait la concentration de sels en phase aqueuse. Les sels seront donc toujours présents en phase aqueuse plutôt que sous forme de particules (en suspension ou dans les sédiments benthiques). Dans le cas des sédiments benthiques, les sels peuvent s'accumuler dans l'eau interstitielle.
Les sels dissous peuvent altérer les propriétés physiques de l'eau en changeant sa densité, la densité augmentant de façon linéaire avec la salinité (Ruttner, 1963). Cette hausse de la densité associée à la salinité est importante lorsqu'on la compare aux fluctuations causées par la température. Ceci a des conséquences majeures sur les lacs, car les sels inorganiques peuvent s'accumuler de façon temporaire ou permanente dans les couches plus profondes et empêcher les eaux du lac de se mélanger (section 3.3.3).
Les sections qui suivent décrivent les comportements physiques et chimiques des principaux ions formant les quatre sels inorganiques, ainsi que des ferrocyanures utilisés comme anti-agglomérants, examinés dans le présent rapport.
2.5.1.1 Chlorure
Le chlorure est le principal anion provenant de l'épandage des sels de voirie, qui contribue à la salinité et influe sur l'équilibre osmotique général (Wetzel, 1975; Hammer, 1977). Le chlorure est un ion très soluble et mobile qui ne se volatilise pas et qui ne précipite pas facilement; il ne se fixe pas non plus à la surface des particules. Dans les écosystèmes dulcicoles, le chlorure a un comportement conservateur (c.-à-d. que ni les réactions chimiques, ni les réactions biologiques n'influent sur sa concentration dans l'eau) (Wetzel, 1975; Pringle et al., 1981). Les taux de chlorure dans les eaux de surface ne fluctuent essentiellement qu'en fonction de l'ajout de chlorure, de la dilution causée par les précipitations ou le débit ou de la concentration causée par l'évaporation de l'eau. Dans la majorité des eaux de surface intérieures, les concentrations de chlorure et de leurs cations correspondants atteignent rarement le produit de solubilité de leurs sels de chlorure respectifs, de sorte qu'il y a rarement précipitation.
2.5.1.2 Sodium et potassium
Dans les eaux de surface, les cations monovalents sodium et potassium ont un comportement relativement normal, pour ce qui est de leur réactivité chimique et de leurs faibles besoins biotiques. C'est ce qui explique que la distribution spatiale et temporelle du sodium et du potassium dans les systèmes dulcicoles non perturbés est uniforme et varie peu d'une saison à l'autre.
2.5.1.3 Calcium
De tous les principaux cations qui contribuent à la salinité, le calcium est le plus réactif et
sa concentration dans les eaux de surface varie en fonction des phénomènes chimiques et biologiques qui s'y produisent. Le calcium est un micronutriment essentiel aux végétaux supérieurs et un des éléments inorganiques de base des algues. Les concentrations de calcium dans les lacs d'eau dure fluctuent selon la saison : l'été, la concentration et l'alcalinité totale diminuent sous l'effet de la décalcification biogénétique qui élimine le calcium de la colonne d'eau. La diminution de la concentration de carbone inorganique dans l'épilimnion, causée par l'accroissement du taux de photosynthèse, provoque la précipitation du calcium avec le bicarbonate. Une partie du carbonate de calcium précipité se solubilise à nouveau dans l'hypolimnion et une autre est entraînée dans les sédiments. La décalcification dans la zone trophogène modifie le rapport entre les cations monovalent et divalent, ce qui influence la distribution et la dynamique des algues et des plantes aquatiques plus grosses dans les écosystèmes dulcicoles (Wetzel, 1975).
2.5.1.4 Magnésium
En général, les composés du magnésium sont plus solubles que les autres composés. Dans les systèmes d'eau dure, les carbonates de calcium précipitent avant les carbonates de magnésium, qui sont plus solubles. Il ne se produit une précipitation importante du carbonate et de l'hydroxyde de magnésium que lorsque le pH est très élevé (>10). Le magnésium sert de micronutriment dans la transformation enzymatique des organismes. Il est essentiel aux plantes à chlorophylle, où il agit comme porphyrine pour le magnésium des molécules de chlorophylle (Wetzel, 1975). Les besoins métaboliques en magnésium sont cependant faibles par rapport à sa disponibilité dans les systèmes dulcicoles.
2.5.1.5 Ferrocyanure de sodium
Le ferrocyanure de sodium se dissocie pour former des ions sodium et ferrocyanure. Dans l'ion ferrocyanure, la liaison chimique entre le groupe cyanure et le fer est très forte; dans l'eau, toutefois, ce composé peut libérer des ions cyanure par photolyse (Hsu, 1984). Selon des analyses en laboratoire, une solution contenant 15,5 mg/L de ferrocyanure libérerait 3,8 mg/L de cyanure après une exposition à la lumière du soleil pendant 30 minutes (U.S. EPA, 1971).
2.5.2 Voies de pénétration dans l'environnement
La figure 8 illustre les voies de pénétration des sels de voirie épandus sur les routes. Les sections qui suivent expliquent les différents milieux environnementaux qui peuvent être perturbés par la pénétration des sels de voirie provenant de l'épandage sur les routes, des lieux d'élimination de la neige et des lieux d'entreposage des sels.
2.5.2.1 Épandage sur les routes
Les sels de voirie épandus sur les routes peuvent pénétrer dans les eaux de surface par :
- le ruissellement chargé de sels qui s'écoule des routes vers les fossés de drainage, les cours d'eau ou les terres humides, peu après l'épandage;
- l'eau de fonte contaminée par les sels de voirie, qui s'écoule de la surface des routes ou de la neige déblayée en bordure des routes, après l'épandage de sels, et
- la dissémination des sels qui s'accumulent à la surface du sol (Scott, 1980).
Au nombre des facteurs qui influent sur le ruissellement des routes qui pénètre dans les écosystèmes aquatiques, mentionnons : a) la longueur des routes principales traitée et drainée; b) la quantité de sels épandue avant la période de dégel; c) le profil de drainage et la topographie des routes; d) le débit des eaux réceptrices; e) le niveau d'urbanisation; f) le rythme d'élévation de la température au-dessus du point de congélation et la durée de cette période de réchauffement, ainsi que g) les précipitations (Scott, 1981).
Les sels de voirie épandus sur les routes peuvent pénétrer dans le sol et les eaux souterraines par le ruissellement de l'eau de fonte de la neige déblayée en bordure des routes, ainsi que par le dépôt sec et humide des sels transportés par l'air.
Figure 8 Le transport du sel de voirie à partir des routes
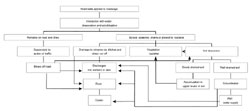
Les sels de voirie épandus sur les routes peuvent en effet pénétrer dans l'atmosphère, par les gouttelettes et les éclaboussures qui sont produites par les véhicules à leur passage et qui sont transportées par le vent, ainsi que par la poudre sèche provenant des résidus sur les routes. Le transport des éclaboussures et des gouttelettes des véhicules varie notamment en fonction de la vitesse des véhicules, du vent, de la déclivité des routes et des caractéristiques géométriques des routes (McBean et Al-Nassri, 1987).
2.5.2.2 Lieux d'élimination de la neige
Les sels de voirie rejetés par l'élimination de la neige pénètrent dans les eaux de surface :
- par rejet direct, lors du déversement de la neige usée dans les eaux de surface ou les eaux usées non traitées ou à la suite de la fonte de la neige déversée sur les rives des cours d'eau;
- par rejet indirect, depuis les stations d'épuration des eaux usées, là où la neige usée est éliminée dans les réseaux d'égouts pluviaux traités ou dans des lieux d'élimination de surface reliés à un système d'épuration;
- par le ruissellement des eaux pluviales et de l'eau de la fonte des neiges, et
- par les conduites des eaux pluviales qui drainent une partie du lieu d'élimination, vers un plan d'eau de surface.
Les sels de voirie provenant de l'élimination de la neige pénètrent dans le sol et les eaux souterraines par percolation directe des précipitations et de l'eau de fonte, depuis les lieux d'élimination de la neige.
2.5.2.3 Lieux d'entreposage des sels
Les sels de voirie provenant des entrepôts de sels pénètrent dans les eaux de surface :
- par le lixiviat chargé de sels qui s'écoule des amas de matériel non protégés;
- par le ruissellement des eaux pluviales qui contiennent des sels dissous et l'eau de fonte des neiges, et
- l'eau de lavage des véhicules.
Les sels de voirie provenant des entrepôts de sels pénètrent dans les eaux souterraines :
- par l'alimentation de la nappe souterraine par des eaux du sol et de surface chargées de sel;
- par le rejet des eaux de lavage des véhicules dans un puits sec, et
- par des puits ou le tubage des puits.
Enfin, les sels de voirie provenant des entrepôts de sels pénètrent dans le sol :
- par l'écoulement accidentel de sels dans les entrepôts, durant l'empilage ou le transfert des sels ou des mélanges d'abrasifs et de sels;
- par l'écoulement accidentel de sels ou de mélanges d'abrasifs et de sels, durant le chargement et le déchargement des véhicules d'entretien;
- par l'écoulement accidentel de sels dans le reste de l'entrepôt, au passage des camions d'entretien;
- sous l'effet de l'érosion éolienne des sels entassés en piles et stockés dans les véhicules d'entretien non couverts durant l'hiver;
- par le lixiviat chargé de sels, qui s'écoule des amas de sels ou de mélanges de sels et d'abrasifs à découvert;
- par les précipitations ou l'eau de fonte des neiges qui entraînent la dissolution des sels et leur infiltration dans le sol, et
- par les eaux de lavage des véhicules rejetées sur le sol.
2.6 Concentrations de chlorure dans les eaux de surface au Canada
Cette section présente des données sur les concentrations des constituants des sels de voirie dans les eaux de surface au Canada, ainsi que des estimations sur les concentrations de chlorure dans les eaux de surface au Canada; ces estimations ont été obtenues à l'aide de méthodes de modélisation basées sur le bilan massique. L'information présentée est résumée dans Mayer et al., (1999) et Evans et Frick (2001) et s'appuie sur un examen de nombreux rapports d'organismes, publications scientifiques et enquêtes de surveillance.
La présente évaluation porte à la fois sur les eaux de surface courantes (lotiques), comme les rivières et les ruisseaux, et stagnantes (lénitiques) comme les lacs, les étangs et les terres humides, en incluant les milieux pélagiques et benthiques. On y traite également des concentrations de fond et des concentrations mesurées dans des plans d'eau exposés aux rejets de sels de voirie. Des exemples décrivant les effets de l'entreposage des sels de voirie sur les plans d'eau ont été présentés dans la section sur les entrepôts de sels (voir la section 2.4). Les données recueillies laissent croire que les eaux de surface les plus sensibles aux effets des sels de voirie sont les milieux à faible dilution, comme les terres humides, les petits lacs et étangs en milieux urbains à long temps de séjour, ainsi que les petits cours d'eau drainant de grandes régions urbaines.
2.6.1 Carte des concentrations de chlorure dans les bassins versants du Canada
Une carte a été faite pour illustrer les concentrations de chlorure dans l'eau par bassin versant, dans tout le Canada; les concentrations observées sont présentées à la figure 9. Ces concentrations dans les eaux de surface sont basées sur les valeurs moyennes obtenues des stations fédérales et provinciales de surveillance de la qualité de l'eau au Canada. Les méthodes et la base de données qui ont servi à la production de la carte sont décrites dans Mayer et al. (1999). Essentiellement, les données de surveillance recueillies à proximité de l'embouchure de chaque bassin ont été combinées pour estimer la concentration dans l'ensemble du bassin. La quantité de données recueillies varie, d'un échantillonnage mensuel réalisé dans de nombreuses stations à un échantillonnage ponctuel intermittent. Les données illustrées à la figure 9 doivent donc être considérées comme une indication des variations relatives des concentrations de chlorure dans tout le Canada.
Les bassins versants qui drainent les principales régions urbaines et les régions à forte charge de sels de voirie, dans le sud du Québec, l'Ontario et les Maritimes, présentent des concentrations élevées de chlorure. À noter que ces concentrations correspondent à la moyenne pour un bassin et non à la concentration d'exposition réelle dans un bassin en particulier. La carte indique également que certains bassins des provinces des Prairies présentent des concentrations ambiantes élevées, qui s'expliquent par le climat aride des Prairies et la présence de lacs et de rivières salés dans la région.
Cependant, les concentrations représentées à la figure 9 ne sont pas imputables uniquement à l'utilisation des sels de voirie. En effet, les effluents de diverses industries (notamment des usines de pâtes et papiers), ainsi que les rejets provenant des installations septiques privées et des stations d'épuration municipales, peuvent aussi avoir une incidence sur les concentrations de chlorure. Dans les Grands Lacs inférieurs, par exemple, on estime que les sels de voirie sont responsables d'environ 20 % de la charge de chlorure, le reste provenant de sources naturelles et d'autres sources anthropiques (Jones et al., 1986).
2.6.2 Concentrations dans l'environnement : lacs et rivières
En l'absence de sources anthropiques, les caractéristiques des eaux de surface dépendent de la dissolution et des réactions chimiques qui se produisent avec les solides, les liquides et les gaz avec lesquels elles entrent en contact durant les différentes étapes du cycle de l'eau (Stumm et Morgan, 1981). Il est ainsi possible d'établir un lien entre, d'une part, la chimie de l'eau des ruisseaux et, d'autre part, la chimie de la roche d'origine et l'équilibre contrôlant la formation des phases solides (Feth et al., 1964; Garrels et Mackenzie, 1967). L'assise rocheuse du bassin versant et la géologie de surface jouent donc un rôle déterminant dans les concentrations de sels des eaux de surface. Le climat et la proximité de la mer sont d'autres importants facteurs dans la régulation des concentrations naturelles de sels dans les eaux de surface, et c'est ce qui explique la variation des concentrations de fond de sels (salinité) dans ces eaux.
Figure 9 Les concentrations de chlorure observées dans les bassins versants canadiens (d'après Mayer et al., 2000)

Les eaux de surface peuvent être douces, avec une salinité inférieure à 500 mg/L, ou salées, avec une salinité supérieure ou égale à 3 000 mg/L (Hammer, 1986). Alors que les lacs et les étangs intérieurs peuvent devenir salés, les ruisseaux et les rivières ont rarement une salinité naturelle suffisamment élevée pour être qualifiés de salés.
Dans le présent Rapport d'évaluation, la qualité des eaux de surface est évaluée par région géographique plutôt que par région hydrogéologique, afin de mieux cerner les effets des facteurs humains sur la qualité de ces eaux. On y présente à la fois les concentrations naturelles et les concentrations imputables à l'activité humaine. Bien que les diverses sources anthropiques, comme les sels de voirie, les eaux d'égout et les effluents industriels, puissent tous accroître la salinité, les effets sur les régions touchées sont examinés ici principalement en regard des rejets des sels de voirie.
2.6.2.1 Région de l'Atlantique (Terre-Neuve, Nouvelle-Écosse, Nouveau-Brunswick et Île-du-Prince-Édouard)
Jeffries (1997) a compilé les concentrations moyennes de chlorure et de calcium mesurées lors de relevés récents (1985 et après). Ces données portent sur 38 lacs du Labrador, 63 lacs de Terre-Neuve, 150 lacs de la Nouvelle-Écosse et 166 lacs du Nouveau-Brunswick. Les concentrations médianes de chlorure et de calcium dans les lacs des régions largement intactes se situent respectivement entre 0,3 et 4,5 mg/L et entre 0,82 et 1,10 mg/L.
Dans le cadre d'études détaillées, Kerekes et al. (1989), Kerekes et Freedman (1989) et Freedman et al. (1989) ont examiné la qualité de l'eau de plusieurs lacs et rivières du parc national Kejimkujik, en Nouvelle-Écosse. Ces chercheurs ont conclu que l'influence du sel de mer est significative en Nouvelle-Écosse. Des concentrations de 3,6 à 5,4 mg/L de chlorure, de 2,3 à 3,4 mg/L de sodium et de 0,36 à 0,96 mg/L de calcium ont en effet été observées, ces taux étant comparables à ceux mesurés dans d'autres eaux de surface de la région de l'Atlantique (Jeffries, 1997).
Des études sur les lacs Chain près de Halifax indiquent que les activités de déglaçage en hiver peuvent avoir une incidence sur la qualité de l'eau. Thirmurthi et Tan (1978) expliquent que, de juin à septembre 1975, la concentration de chlorure s'est maintenue à environ 19 mg/L; elle a commencé à augmenter en novembre pour atteindre un sommet de 43 mg/L en mai 1976. Elle a ensuite diminué rapidement durant le reste du mois de mai et en juin, pour atteindre 19 mg/L en juillet. L'augmentation des concentrations de chlorure dans les deux lacs correspond à l'ajout d'environ 19 440 kg de chlorure au premier lac Chain et de 7 920 kg au deuxième. On a continué d'étudier ces lacs jusqu'au début des années 1980 (Hart, 1985, 1988). Les concentrations de chlorure dans les deux lacs ont augmenté graduellement à partir de 1976 pour atteindre un sommet au milieu des années 1980, soit environ 120 mg/L dans le premier lac Chain et environ 170 mg/L dans le deuxième lac Chain. Les plus fortes concentrations de chlorure ont été observées au moment du ruissellement printanier.
Les sels de voirie ont également eu des effets sur le lac Chocolate en Nouvelle-Écosse.
Il s'agit d'un petit lac (82,7 ha) peu profond (profondeur moyenne de 3,9 m; profondeur maximale de 12,2 m), dont le volume est estimé à 350 000 m3 (Kelly et al., 1976). Le bassin versant est vaste (900 ha) et est environ 11 fois plus grand que la superficie du lac. Les concentrations de chlorure dans le lac ont été très élevées entre avril et août 1975, la concentration moyenne durant l'été atteignant 207,5 mg/L, comparativement à une concentration de fond estimée entre 15 et 20 mg/L dans les lacs intacts. Les concentrations de chlorure ont aussi varié en fonction de la profondeur, s'établissant entre 199 et 224 mg/L à la surface, entre 189 et 217 mg/L à une profondeur de 6,1 m et entre 225 et 330 mg/L à 12,1 m. À ces mêmes profondeurs, les concentrations de sodium ont varié respectivement de 108 à 125 mg/L, de 102 à 125 mg/L et de 116 à 183 mg/L. Le gradient de concentration de sels et la concentration absolue de sels dans les eaux profondes ont été assez importants pour empêcher le mélange vertical complet de la colonne d'eau au printemps et les eaux profondes sont devenues anoxiques en été. La principale source de chlorure a été attribuée au ruissellement d'eaux chargées de sels de voirie. Kelly et al. (1976) estiment que 58,4 tonnes (soit 35 409 kg de chlorure et 22 737 kg de sodium) ont été épandues dans le bassin versant du lac Chocolate durant l'hiver 1974-1975.
Une étude sur la qualité de l'eau dans 50 lacs de la région métropolitaine de Halifax/Dartmouth a révélé qu'il s'était produit une hausse très marquée des concentrations de sodium et de chlorure dans la plupart des lacs entre 1980 et 1991 (Keizer et al., 1993). De tous les lacs échantillonnés en 1980, 12 présentaient une concentration de chlorure supérieure à 50 mg/L et trois avaient une concentration supérieure à 100 mg/L (la concentration maximale étant de 125 mg/L). En 1991, 22 des 50 lacs échantillonnés présentaient une concentration de chlorure supérieure à 50 mg/L, 12 avaient une concentration excédant 100 mg/L et quatre, une concentration de plus de 150 mg/L (la concentration maximale étant alors de 197 mg/L). Les concentrations de sodium dans ces lacs ont fluctué de façon similaire. Ainsi, parmi les lacs échantillonnés en 1980, 9 présentaient des concentrations de sodium supérieures à 40 mg/L et trois, des concentrations de plus de 60 mg/L (concentration maximale de sodium de 73 mg/L). Onze ans plus tard, 21 lacs affichaient des concentrations de sodium supérieures à 40 mg/L, 12 avaient une concentration de plus de 60 mg/L et 7, une concentration excédant 80 mg/L (concentration maximale de 114 mg/L). Il convient de souligner que l'échantillonnage a été fait en surface, au milieu des lacs, et donc que les concentrations mesurées ne sont peut-être pas représentatives des conditions dans les baies, là où les concentrations peuvent être encore plus élevées. Qui plus est, comme l'eau chargée en sels est plus dense et a tendance à couler au fond, il est possible que les échantillons prélevés à la surface sous-estiment la concentration globale dans les lacs.
Keizer et al. (1993) ont également constaté que les concentrations de chlorure et de sodium étaient moins élevées dans les lacs situés dans les bassins de régions rurales. De plus, les concentrations de sels dans les lacs des régions moins urbanisées n'ont pas augmenté de façon marquée entre les deux périodes d'échantillonnage, contrairement aux lacs situés en régions urbaines. À titre d'exemple, 19 des lacs en régions rurales ont affiché une concentration de chlorure inférieure à 25 mg/L en 1980 et 1991 et 23 lacs avaient une concentration de sodium de moins de 20 mg/L en 1980 et 1991. Enfin, dans trois des lacs affichant les plus faibles concentrations, les concentrations de chlorure ont été de 5,1, 3,9 et 5 mg/L en 1980 et de 4,5, 3,4 et 5 mg/L en 1991; dans le cas du sodium, les concentrations ont été de 3,4, 2,5 et 3,2 mg/L en 1980 et de 2,9, 2,2 et 2,9, en 1991.
En général, les concentrations de chlorure dans les plans d'eau intacts de la région de l'Atlantique ne dépassent pas 20 mg/L et des concentrations plus faibles (<10 mg/L) sont habituellement observées dans les plans d'eau intérieurs, alors que des concentrations plus élevées se remarquent dans les régions côtières.
2.6.2.2 Région du centre (Ontario et Québec)
Les concentrations de chlorure, de sodium et de calcium dans les lacs et les rivières du Bouclier canadien, lequel couvre une grande partie du Québec et de l'Ontario, y compris le secteur supérieur des Grands Lacs, sont très faibles (de 1 à 10 mg de chlorure/L) (Jeffries, 1997). Selon Weiler et Chawla (1969), les concentrations annuelles de chlorure dans les lacs Érié et Ontario étaient respectivement de 24,6 et 27,5 mg/L et elle n'était que de 1,3 mg/L dans le lac Supérieur. Des études antérieures, ayant pour but d'examiner les tendances relatives à la qualité de l'eau dans les Grands Lacs, avaient fait état d'une augmentation rapide des concentrations de chlorure sous l'effet de l'activité humaine (Kramer, 1964; Beeton, 1965; Dobson, 1967). C'est dans le lac Ontario qu'on a observé la plus forte augmentation. Des données plus récentes (Williams et al., 1998) indiquent cependant une baisse des concentrations de chlorure, passant d'environ 22 mg/L en 1977 à quelque 16 mg/L plus récemment (1985-1993). La baisse dans les Grands Lacs inférieurs peut sans doute être attribuée à une diminution des charges provenant des sources industrielles et domestiques, elle-même imputable à l'amélioration des méthodes de contrôle et de traitement des effluents industriels et domestiques. Les affluents du lac Sainte-Claire (soit les rivières Sydenham et Thames) ont des concentrations de chlorure un peu plus élevées (environ 30-40 mg/L) que les autres rivières du sud de l'Ontario parce qu'ils drainent la roche sédimentaire paléozoïque adjacente au bassin du Michigan, lequel renferme des formations salées, comme les strates porteuses de sels (chlorure de sodium) et d'anhydrite (sulfate de calcium). Ces strates contribuent également à l'apport de sels (chlorure de sodium et sulfate de calcium) dans le lac Sainte-Claire et l'ouest du lac Érié.
Dans les régions urbaines, l'épandage de sels de déglaçage contribue de façon significative à la charge de chlorure. Des postes de surveillance à long terme dans la Région du Grand Toronto révèlent une hausse graduelle des concentrations de chlorure. Dans le ruisseau Highland, un cours d'eau urbain fortement dégradé, l'analyse statistique des tendances indique une hausse de la concentration de chlorure, laquelle est passée de 150 mg/L en 1972 (cours d'eau sans doute déjà altéré) à plus de 250 mg/L en 1995 (Bowen et Hinton, 1998). Dans le ruisseau Duffin, les concentrations moyennes de chlorure, qui étaient de 10 à 20 mg/L durant les années 1960, ont augmenté entre 30 et 40 mg/L au début des années 1990 (Bowen et Hinton, 1998). Dans les cours d'eau et les rivières urbains, comme la rivière Don à Toronto, les concentrations de chlorure ont augmenté à plus de 1 000 mg/L en hiver (Scott, 1980; Schroeder et Solomon, 1998), ces hausses semblant coïncider avec le dégel; à l'automne, les valeurs de base dans cette rivière se sont maintenues entre 100 et 150 mg de chlorure/L. Des concentrations de base similaires de chlorure (50 à 100 mg/L) ont été rapportées dans un autre cours d'eau de Toronto, le ruisseau Black (Scott, 1980), où on a mesuré des concentrations de chlorure 50 fois plus élevées que la valeur de base en périodes de dégel. Crowther et Hynes (1977) rapportent de fortes concentrations de chlorure (1 770 mg/L), de sodium (9 550 mg/L) et de calcium (4 890 mg/L) durant l'hiver, dans le ruisseau Laurel qui traverse la région urbaine de Waterloo, et Rodgers (1999) a observé des concentrations de chlorure élevées (4 355 mg/L) dans le ruisseau Red Hill, à Hamilton (Ontario).
Entre 1990 et 1996, le ministère de l'Environnement de l'Ontario a surveillé la qualité de l'eau dans plusieurs cours d'eau de la province, y compris ceux des bassins versants de la région de Toronto. Le tableau 9 présente les résultats pour quatre cours d'eau situés en régions urbaines. Les concentrations maximales ont été observées durant les mois d'hiver, soit la période où l'apport de sels de voirie est à son maximum. La concentration de chlorure a souvent dépassé 250 mg/L et très souvent, 500 mg/L (tableau 9).
Le lac Little Round, dans le centre de l'Ontario, a subi les effets de diverses perturbations, notamment l'urbanisation, l'aménagement de fosses septiques, le ruissellement des sels de voirie provenant des routes et les infiltrations provenant d'un entrepôt de sels (Smol et al., 1983). Ce petit lac (7,4 ha, profondeur maximale de 16,8 m) est devenu méromictique. Selon Smol et al. (1983), ces conditions méromictiques sont le résultat de l'apport de sels de voirie provenant du ruissellement et de l'entreposage du sel. Dans le monimolimnion, ou couche profonde, des concentrations de sels de 58,4 mg de sodium/L et de 103,7 mg de chlorure/L ont été observées, ce qui est bien supérieur aux taux pouvant être attribués à la géologie naturelle de la région. L'ajout de sels de voirie semble avoir contribué au développement de conditions méromictiques dans les 30 ans qui ont précédé l'étude réalisée en 1981.
Le ministère des Transports du Québec (1980, 1999) a étudié les effets des sels de voirie au lac à la Truite, près de Sainte-Agathe-des-Monts. Le bassin de drainage du lac, d'une superficie estimée à 728 ha, a été perturbé par un segment d'autoroute de 7 km (environ 30 kilomètres de voie). À certains endroits, le lac n'est qu'à 250 m de l'autoroute. Le lac a une superficie de 48,6 ha, une profondeur moyenne de 21,5 m et un volume estimé de 486 000 m3. En 1972, la concentration moyenne de chlorure dans le lac était de 12 mg/L. Elle a augmenté durant les années 1970 pour atteindre un maximum de 150 mg/L en 1979, ce qui correspond à l'ajout de 67 068 kg de chlorure dans le lac. Afin d'éviter toute autre hausse, les sels de voirie ont été remplacés par des abrasifs (contenant un peu de sel comme anti-agglomérant). La concentration de chlorure a baissé pendant les années 1980, pour atteindre 45 mg/L en 1990, et elle est demeurée stable depuis.
Aux États-Unis, des hausses significatives des concentrations de chlorure, attribuables à l'épandage de sels en hiver, ont été observées dans quatre cours d'eau des Adirondacks (Demers et Sage, 1990). On a par ailleurs observé une grande fluctuation de la concentration de chlorure entre les échantillons prélevés en amont et ceux prélevés en aval des routes, Demers (1992) ayant mesuré des concentrations de chlorure jusqu'à 66 fois plus élevées dans des échantillons prélevés en aval. Ainsi, la concentration globale moyenne de chlorure en amont a été de 0,61 mg/L, contre 5,23 mg/L en aval. Les caractéristiques du sol dans les cours d'eau des Adirondacks (New Hampshire) se comparent à celles des cours d'eau des Cantons de l'Est, au Québec. On a mesuré des concentrations de chlorure de 11 000 mg/L (Hawkins et Judd, 1972) durant l'hiver 1969 dans le Meadowbrook qui draine environ 10 km2 de la banlieue de Syracuse, New York (Hawkins et Judd, 1972). Toujours aux États-Unis, des concentrations de chlorure d'environ 400 mg/L ont été mesurées dans les eaux de fond de la baie Irodenquoit, une petite baie du lac Ontario située près de Rochester (New York) (Bubek et al., 1971, 1995).
Tableau 9 Concentrations de chlorure dans divers cours d'eau du bassin visés par le Plan d'assainissement de la Communauté urbaine de Toronto, entre 1990 et 1996 (d'après la Toronto and Region Conservation Authority, 1998)
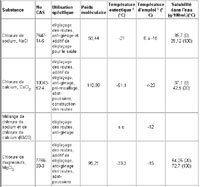
En résumé, les concentrations de chlorure dans les cours d'eau intacts du Bouclier canadien du centre du Canada sont parmi les plus faibles au pays et se situent entre <1 et 5 mg/L. Des concentrations de fond plus élevées (10 à 30 mg/L) sont observées dans les plans d'eau situés dans les basses terres du Saint-Laurent, laquelle région inclut le bassin des Grands Lacs inférieurs et du fleuve Saint-Laurent. Dans un grand nombre de petits lacs urbains et de cours d'eau de cette région, les concentrations de chlorure dépassent sensiblement les niveaux de fond, cette région étant la plus densément peuplée du Canada. Les fluctuations saisonnières et spatiales témoignent de l'importance des sels de voirie dans ces hausses.
2.6.2.3 Région des Prairies (Manitoba, Saskatchewan, Alberta)
Au Canada, les lacs salés naturels se trouvent pour la plupart dans deux régions. La première englobe plusieurs bassins hydrographiques endoréiques dans les Prairies canadiennes (Hammer, 1984). La région où les lacs salés sont les plus nombreux s'étend dans le sud de l'Alberta et de la Saskatchewan. Une assise rocheuse crétacée, composée surtout de schistes, de limon et de grès, sous-tend la région des lacs salés de l'Alberta et de la Saskatchewan (Hammer, 1984). À l'intérieur des provinces des Prairies, la Saskatchewan est de loin la province qui compte le plus grand nombre et le plus grand volume de lacs salés (Hammer, 1986). La proportion relative des cations dans la plupart des lacs des Prairies suit l'ordre suivant : Na>Mg>Ca. On ne connaît que deux lacs méromictiques dans les Prairies canadiennes, soit les lacs Waldsea et Deadmoose (Hammer, 1984). On trouve de nombreux lacs et étangs peu profonds, dont les eaux sont douces à salées, dans le sud des Prairies.
Il y a moins de lacs naturellement salés (environ 30) en Alberta (Hammer, 1984). La plupart sont situés dans les régions de Provost et Hanna, bien qu'on en trouve aussi plus au nord, jusqu'à Edmonton. Le Manitoba compte encore moins de lacs salés. Barica (1978) a étudié un groupe de plus de 100 petits étangs dont la salinité variait de douce à modérément salée, près de Erickson dans le sud-ouest du Manitoba. Les plages de concentrations variaient de 1 à 448 mg/L pour le chlorure, de 0,8 à 1 075 mg/L pour le sodium et de 27 à 380 mg/L pour le calcium. McKillop et al. (1992) ont étudié 23 sites le long de la rive ouest du lac Winnipegosis, où le sel dominant était le chlorure de sodium. Les gammes de concentrations pour le chlorure, le sodium et le calcium s'échelonnaient respectivement de 861 à 33 750 mg/L, de 587 à 21 313 mg/L et de 59 à 1 400 mg/L.
On rapporte (Jeffries, 1997) des concentrations beaucoup plus faibles de chlorure et de calcium pour 27 et 193 lacs situés respectivement dans la partie nord de la Saskatchewan et en Alberta, les concentrations médianes de chlorure s'établissant respectivement à 0,2 et 0,5 mg/L. Les concentrations de calcium des lacs de la Saskatchewan et de l'Alberta étaient de 2,0 et de 14,0 mg/L respectivement. Au Manitoba, les concentrations de chlorure et de calcium dans 26 lacs étaient respectivement de 2,0 et de 7,5 mg/L (Jeffries, 1997).
En résumé, bon nombre des cours d'eau salée du Canada sont situés dans les Plaines intérieures qui couvrent la partie sud des Prairies. En général, les concentrations de sels dissous, y compris de chlorure, sont plus élevées dans cette région géographique, en raison de sa géologie sous-jacente. On rapporte toutefois de faibles concentrations de chlorure (< 5 mg/L) dans les plans d'eau intacts situés dans le nord de ces provinces, à l'extérieur de la région des Plaines intérieures.
2.6.2.4 Région du Pacifique (Colombie-Britannique)
Le Plateau du sud de l'Intérieur de la Colombie-Britannique (Plateau du Fraser), exposé à l'ombre de pluie de la chaîne Côtière, est la deuxième région du Canada qui compte le plus de lacs salés naturels. Les lacs salés de la Colombie-Britannique sont petits et peu profonds (Topping et Scudder, 1977). Northcote et Halsey (1969) décrivent la limnologie de quatre de ces lacs et ont démontré que les concentrations de matières totales dissoutes diffèrent non seulement d'un lac à l'autre, mais aussi à l'intérieur d'un même lac (en surface ou près du fond). Des concentrations variant de 5,1 à 800 mg/L ont été rapportées. Dans trois de ces lacs, les conditions méromictiques ont été maintenues par les gradients de densité chimique alors que, dans le quatrième, les propriétés morphométriques ont empêché le mélange de l'eau. Dans les régions non salées, les concentrations médianes de chlorure et de calcium, dans six lacs sensibles aux acides situés dans le sud-ouest de la province, ont été respectivement de 2,5 et 3,7 mg/L (Phippen et al., 1996; Jeffries, 1997).
Un programme de surveillance a été mis en place afin d'étudier les effets des sels de voirie sur la qualité de l'eau de la rivière Serpentine, dans la vallée inférieure du Fraser (Colombie-Britannique). Des appareils électroniques enregistraient la température de l'eau, le pH, le niveau d'eau et la conductivité, toutes les 15 minutes. Durant le dégel faisant suite à une période de temps froid où il a fallu épandre du sel et du sable sur les routes, la conductivité a triplé sur une période de 10 à 20 heures (Whitfield et Wade, 1992). Ces périodes de forte conductivité ont été suivies d'une augmentation du niveau de l'eau, caractéristique de la fonte des neiges. Les résultats de cette étude indiquent que les organismes qui vivent dans certains cours d'eau, durant les mois d'hiver, peuvent être exposés aux fluctuations des concentrations de sels.
En résumé, il y a plusieurs lacs, dans le Plateau du sud de l'Intérieur de la Colombie-Britannique, où la concentration de chlorure est supérieure à 100 mg/ L, et plusieurs sont des lacs salés naturels. Dans le reste de la province, la concentration de chlorure dans les cours d'eau intacts est généralement inférieure à 5 mg/L.
2.6.2.5 Yukon, Territoires du Nord-Ouest et Nunavut
On a trouvé peu de données pour le Yukon, les Territoires du Nord-Ouest et le Nunavut.
2.6.3 Concentrations dans l'environnement : sédiments benthiques
Comme les sels de chlorure inorganiques utilisés pour l'entretien des routes sont très solubles et que leurs interactions avec les particules des sédiments sont minimes, on s'attend à ce qu'ils s'accumulent dans l'eau interstitielle des sédiments plutôt qu'en phase solide. L'étude (Mayer et al., 1999) d'un étang urbain (étang de la rivière Rouge) montre que l'eau interstitielle des sédiments, qui est en équilibre avec les eaux surjacentes enrichies de sels inorganiques, peut contenir de fortes concentrations de sels (voir la section 2.6.5). Or des concentrations élevées de sels dans l'eau interstitielle des sédiments peuvent non seulement causer un stress osmotique et des effets toxiques directs sur le biote benthique mais aussi, par la complexation des métaux avec le chlorure, accroître les concentrations de métaux lourds dissous (p. ex., le cadmium) qui sont toxiques pour les organismes benthiques.
2.6.4 Concentrations dans l'environnement : terres humides
Les terres humides sont d'importants éléments du paysage canadien, qui se caractérisent principalement par leur eau stagnante, des sols uniques, ainsi qu'une végétation qui est adaptée aux sols saturés ou qui les tolère (Mitsch et Gosselink, 1986). Le Canada dispose d'une grande variété de terres humides : on peut trouver une description détaillée des divers types de terres humides dans Mitsch et Gosselink (1986).
On possède peu de données sur les caractéristiques chimiques des terres humides d'eau douce (côtières et intérieures) en regard du chlorure, car la majeure partie des études sur ces milieux ont porté sur le cycle des substances nutritives, l'acidification ou la géochimie des métaux. Une étude effectuée en 1987 sur les terres humides du parc national Kejimkujik (Wood et Rubec, 1989) a évalué leurs caractéristiques chimiques. Les auteurs ont rapporté des différences significatives entre la chimie de la tourbe des tourbières hautes et basses, surtout au niveau des concentrations de sodium et de calcium. Les concentrations de calcium, de sodium et de chlorure dans les tourbières hautes ont été respectivement de 0,17, 0,8 et 0,15 mg/L, comparativement à des concentrations respectives de 0,32, 1,5 et 0,12 mg/L dans les tourbières basses. Aucune différence n'a toutefois été observée entre les deux types de tourbières, quant à la chimie des eaux de surface. De fait, les concentrations de calcium, de sodium et de chlorure dans l'eau des tourbières hautes ont été respectivement de 6 ´ 10-4, 3,0 ´ 10-3 et 3,5 ´ 10-3 mg/L, comparativement à des concentrations de 6 ´ 10-4, 2,8 ´ 10-3 et 3,9 ´ 10-3 mg/L dans les tourbières basses.
Bourbonniere (1995, 1998) a étudié la géochimie des terres humides de la Nouvelle-Écosse et de l'Ontario. Il a évalué la chimie des principaux ions dans l'eau interstitielle de la tourbière haute ombrotrophe du comté de Barrington en Nouvelle-Écosse. Les concentrations mesurées ont varié entre 9,6 et 24 mg/L pour le chlorure, entre 5,2 et 12,8 mg/L pour le sodium et entre 0,47 et 1,5 mg/Lpour le calcium. Dans le marais Beverly, en Ontario, des concentrations de calcium, de sodium et de chlorure fluctuant respectivement entre 58,1 et 95,3 mg/L, 5,1 et 20,0 mg/L et 8,7 et 41,2 mg/L ont été observées. La composition de l'eau des étangs décrits à la section 2.6.3.3 peut être qualifiée de caractéristique des terres humides des Prairies. On n'a trouvé aucune étude canadienne traitant des effets de l'épandage des sels de voirie sur la chimie des terres humides. Cependant, deux études décrites dans la section sur les entrepôts de sels (section 2.4) traitent des effets des entrepôts de sels sur les terres humides.
2.6.5 Concentrations dans l'environnement : lacs et étangs urbains
Dans les petits lacs et étangs urbains naturels qui reçoivent le ruissellement des routes, les concentrations d'ions peuvent fluctuer. On possède peu de données sur les concentrations de chlorure dans ces plans d'eau, mais les étangs faisant partie de réseaux municipaux de gestion des eaux pluviales constituent une source acceptable d'information. De nombreux étangs ont été construits et ceux-ci demeurent un ouvrage très répandu pour la gestion des bassins versants dans les régions urbaines. Bien que ces étangs soient des plans d'eau artificiels, conçus principalement pour la gestion de l'écoulement hydraulique et le traitement des eaux pluviales, une écologie aquatique semblable à celle des petits étangs urbains naturels s'y est développée. Et tout comme les systèmes aquatiques urbains naturels, ces étangs servent d'habitats aquatiques pour bon nombre d'espèces de flore et de faune. Ils constituent en outre de bons candidats pour illustrer les concentrations maximales de chlorure, puisqu'ils sont les plans d'eau les plus exposés aux charges de chlorure provenant des activités d'entretien durant l'hiver.
Une étude du lac Wabukayne, un petit lac artificiel situé à Mississauga (Ontario), fait état de concentrations de chlorure variant de 200 à 2 000 mg/L et de conditions méromictiques temporaires durant l'hiver et au début du printemps (Free et Mulamoottil, 1983). Des concentrations de chlorure de 1 100 à 2 000 mg/L (Vickers, 2000) ont été mesurées dans l'étang Harding à Richmond Hill dans la Région du Grand Toronto. Des relevés saisonniers des bassins de rétention des eaux pluviales de la Région du Grand Toronto (Mayer et al., 1996; Mayer, 2000) indiquent que les concentrations de chlorure augmentent durant les mois d'hiver. Des concentrations de chlorure de 380 et 800 mg/L ont été mesurées respectivement dans les étangs Heritage et Unionville situés en milieu résidentiel (Mayer, 2000), alors que des concentrations de chlorure atteignant 5 910 mg/L ont été observées en février 1999 dans le réservoir Col. S. Smith, lequel reçoit les eaux de ruissellement d'une autoroute à voies multiples (Autoroute Queen Elizabeth).
Une étude du bilan massique et une étude des sédiments ont été effectuées sur l'étang de la rivière Rouge, dans la vallée de la rivière Rouge à Scarborough (Ontario), près de l'autoroute 401 et du chemin Port Union. Cet étang est un bassin de gestion des eaux pluviales urbaines, aménagé pour traiter les eaux pluviales des autoroutes en y éliminant 70 % des matières en suspension. L'étude du bilan massique a été faite pour mesurer le taux d'élimination des polluants et évaluer la dynamique de plusieurs paramètres de la qualité de l'eau, entre 1995 et 1998 (Liang, 1998). Les premières études ont porté sur le bilan massique durant la saison sans glace, en 1995, 1996 et 1997. Elles ont révélé un déséquilibre du chlorure lié aux conditions méromictiques permanentes de l'étang, elles-mêmes dues sans doute à la conception de l'étang et aux fortes charges de sels de voirie. La concentration de sels, calculée en fonction du chlorure de sodium mesuré dans la couche de fond de l'étang, était de l'ordre de 5 000 mg/L. De fortes concentrations de métaux et d'ammoniac ont aussi été décelées dans la couche de fond. L'étude sur les sédiments (Mayer et al., 1999) a porté sur la chimie et la toxicité de l'eau interstitielle des sédiments et évalué la chimie des métaux en phase solide. Un modèle géochimique a été conçu pour évaluer les effets des sels sur la spéciation des métaux. Cette étude a révélé que l'eau interstitielle des sédiments, qui est en équilibre avec l'eau surjacente enrichie de sels inorganiques, peut elle aussi contenir de fortes concentrations de sels. Ainsi, à l'interface entre les sédiments et l'eau, des concentrations de chlorure et de sodium respectivement supérieures à 3 000 mg/L et 2 000 mg/L ont été mesurées dans l'eau interstitielle, la concentration des deux ions diminuant à mesure que la profondeur des sédiments augmentait. Cependant, même à une profondeur de 40 cm sous l'interface sédiments-eau, la concentration de chlorure était toujours d'environ 1 500 mg/L.
Une étude menée par Bishop et al. (2000) a porté sur la présence de contaminants dans six bassins de retenue des eaux pluviales de la Région du Grand Toronto et neuf bassins de retenue à Guelph (Ontario). Des 15 bassins analysés, quatre situés à Guelph ont été échantillonnés de 19 à 21 fois chacun, pour déterminer les concentrations de chlorure dans les eaux pluviales. Ces échantillons ont été prélevés à différentes périodes, durant les mois de septembre, octobre et novembre 1997, de même qu'en avril, mai, juin, juillet, août, septembre et novembre 1998. De plus, ces échantillons ont été recueillis le plus près possible des exutoires des étangs (Struger, 2000). Les concentrations moyennes de chlorure dans les échantillons d'eaux pluviales prélevés de ces quatre bassins ont varié entre 120 et 282 mg/L, les concentrations maximales s'établissant entre 416 et 1 230 mg/L (Struger, 2000). Bien qu'aucun échantillon n'ait été prélevé entre décembre et mars, les concentrations moyennes de chlorure dans les échantillons recueillis en novembre, avril et mai ont été supérieures aux concentrations moyennes mesurées les autres mois, dans chacun des bassins (336 contre 153 mg/L; 183 contre 79 mg/L; 469 contre 82 mg/L; 444 contre 188 mg/L).
Les échantillons ont été prélevés près des exutoires, car les concentrations mesurées à ces endroits sont probablement représentatives des concentrations rejetées dans les plans d'eau récepteurs. Les bassins de retenue des eaux pluviales servent au traitement des matières en suspension et autres composants liés; par contre, ils n'éliminent pas les sels dissous des eaux de ruissellement (MEO, 1991; Bishop et al., 2000). Selon le volume de ruissellement qui pénètre dans ces bassins, ceux-ci sont habituellement conçus pour retenir l'écoulement durant une période variant de 24 à 72 heures; il peut arriver toutefois que le temps de séjour soit à peine de dix heures, durant les périodes de débit de pointe.
Watson (2000) a évalué la qualité de l'eau dans 89 bassins de retenue situés à proximité de routes, dans le sud de l'Ontario. De multiples échantillons ont été prélevés au printemps et à l'été 2000, et les bassins ont été classés en fonction du nombre de voies de la route la plus près. La concentration moyenne de chlorure dans les bassins situés près de routes à deux voies a été de 95 mg/L (intervalle : 0 à 368 mg/L), comparativement à une concentration moyenne de 124 mg/L, pour les bassins situés près de routes de plus de deux voies mais de moins de six voies (intervalle : 0 à 620 mg/L). Enfin, la concentration moyenne de chlorure dans les bassins se trouvant près de routes à six voies et plus a été de 952 mg/L (intervalle : 49 à 3 950 mg/L). Watson (2000) ne précise pas les concentrations de fond, mais indique que les sels de voirie seraient la principale source de chlorures.
2.6.6 Concentrations de chlorure basées sur le bilan massique
2.6.6.1 Calcul des concentrations de chlorure dans les bassins versants provenant de l'utilisation des sels de voirie
Un modèle basé sur le bilan massique a été utilisé pour estimer les concentrations de chlorure dans les bassins versants du Canada, provenant de l'utilisation des sels de voirie. Les concentrations ainsi calculées ont ensuite été comparées aux concentrations observées, indiquées à la section 2.6.1. Mayer et al. (1999) traitent plus en détail de cette méthode de comparaison et d'analyse.
Bien que le modèle utilisé comporte certaines simplifications inhérentes (p. ex., hypothèse prévoyant un épandage similaire de sels de voirie et un volume de ruissellement comparable, d'une année à l'autre), il fournit néanmoins une estimation raisonnable des concentrations potentielles de chlorure résultant de l'usage des sels de voirie. Le modèle est également utile pour déterminer les concentrations relatives de chlorure dans différents bassins versants. Les calculs sont basés sur des sous-bassins; l'utilisation de cartes à plus petite échelle aurait permis de faire une comparaison plus précise des concentrations de chlorure calculées.
Figure 10 Estimation de la concentration de chlorure à partir de la charge annuelle moyenne de sels de voirie (NaCl) et du ruissellement (d'après Mayer et al., 2000)

Les résultats obtenus sont illustrés à la figure 10, laquelle montre que c'est sur l'Île de Montréal que la concentration modélisée de chlorure dans le ruissellement est la plus élevée. Cette figure montre également que les bassins versants situés sur la rive nord du lac Ontario, et plus particulièrement ceux largement exposés aux rejets provenant des municipalités de la région de Toronto, présentent eux aussi de fortes concentrations de chlorure attribuables à
l'utilisation de sels de voirie. C'est donc dans les bassins versants des régions urbaines, et plus particulièrement ceux situés dans le sud de l'Ontario, le sud du Québec, les Maritimes et les grands centres urbains des Prairies, que les concentrations (modélisées) de chlorure dans le ruissellement sont les plus élevées.
Il convient de rappeler que les concentrations illustrées à la figure 10 représentent des moyennes modélisées pour les bassins versants. Il ne s'agit pas de la concentration d'exposition réelle dans des cours d'eau ou des plans d'eau précis. Les données présentées à la figure 10 peuvent toutefois servir à déterminer les régions les plus susceptibles de subir les effets nocifs résultant de l'épandage des sels de voirie.
Figure 11 Estimation de la concentration de chlorure dans le ruissellement provenant des routes provinciales au Canada

2.6.6.2 Calcul des concentrations de chlorure dans le ruissellement des routes
Dans la section qui précède, les concentrations de chlorure imputables à l'utilisation des sels de voirie ont été évaluées pour l'ensemble du bassin versant. Or il se produit, au niveau du bassin versant, une dilution des concentrations (modélisées) sous l'effet du ruissellement qui ne provient pas uniquement des routes. Cette section présente une estimation de la concentration de chlorure provenant des routes, selon la méthode basée sur le bilan massique.
Ces estimations sont basées sur l'hypothèse voulant que la masse de sels utilisée par kilomètre de route provinciale à deux voies est dissoute et diluée par le volume de ruissellement annuel moyen qui s'accumulerait à la surface de la route (c.-à-d. sur 7 400 m2, d'après un kilomètre à deux voies d'une largeur de 7,4 m).
La figure 11 présente les concentrations estimatives de chlorure et la longueur des routes provinciales auxquelles s'appliquent ces concentrations - les concentrations de chlorure varient entre 30 et 31 000 mg/L. D'après ces estimations, la majorité des concentrations (85 %) se situe entre 1 000 et 10 000 mg/L. Ces estimations représentent les concentrations de chlorure dans le ruissellement provenant des routes. Divers coefficients peuvent être utilisés pour tenir compte de la dilution dans les plans d'eau récepteurs. L'exactitude des résultats dépend de la qualité des données utilisées pour calculer les concentrations. Une des limites de cette méthode tient au fait que le ruissellement annuel moyen a été estimé au moyen d'une carte d'une échelle de 1:7 500 000. Il est possible que l'utilisation de cartes plus détaillées (c.-à-d. 1:50 000) aurait donné des résultats légèrement différents. Qui plus est, ce sont des estimations du ruissellement annuel moyen qui ont été utilisées; or les valeurs calculées auraient pu être différentes si l'on s'était basé sur le ruissellement associé aux mois d'hiver ou encore au dégel du printemps.
Les concentrations de chlorure mesurées lors d'une étude récente (Mayer et al., 1998) sur le ruissellement routier à trois endroits, dans le sud de l'Ontario, concordent avec les concentrations estimées précédemment. L'étude fait état des concentrations de chlorure dans le ruissellement provenant des autoroutes, aux trois endroits suivants : a) le pont Burlington Skyway (route à quatre voies qu'empruntent quotidiennement 92 000 véhicules automobiles), b) route 2, à l'est de Brantford (route à deux voies, avec un achalandage quotidien de 31 100 véhicules) et c) le chemin Plains à Burlington (route à deux voies empruntée par 15 460 véhicules chaque jour). Les concentrations maximales de chlorure (jusqu'à 19 135 mg/L) ont été observées dans le ruissellement l'hiver provenant du pont Skyway, bien que des concentrations élevées aient aussi été observées au chemin Plains. Cette étude, qui portait sur la toxicité du ruissellement, a démontré que le ruissellement chargé de sels peut avoir des effets nocifs sur les organismes aquatiques, dans des milieux à faible dilution. Les concentrations élevées de chlorure dans cette étude sont caractéristiques des concentrations au point de rejet et représentent le pire des scénarios qui peut se produire dans des fossés longeant les routes ou dans de petites terres humides situées à proximité de routes principales.
2.6.7 Sommaire
Les données recueillies indiquent de grandes fluctuations dans les concentrations de fond de chlorure, dans les eaux de surface au Canada. Ces différences sont imputables aux variations dans l'assise rocheuse et la géologie de surface, le climat et la proximité de l'océan. Les données démontrent par ailleurs les effets manifestes résultant de l'utilisation de grandes quantités de sels de voirie, en particulier dans les régions fortement urbanisées. Les plans d'eau les plus sensibles aux rejets de sels de voirie sont les milieux à faible dilution, comme les petits lacs et étangs urbains à long temps de séjour, les bassins de retenue des eaux pluviales urbaines à court temps de séjour, les cours d'eau drainant de grandes régions urbanisées et les terres humides adjacentes aux routes principales.
En ce qui a trait aux concentrations naturelles partout au pays, voici les tendances régionales qui se dégagent :
- En général, les concentrations de chlorure dans les cours d'eau intacts des provinces de l'Atlantique ne dépassent pas 20 mg/L et des concentrations plus faibles (<10 mg/L) sont habituellement observées dans les plans d'eau intérieurs.
- Les concentrations de chlorure dans les cours d'eau intacts du Bouclier canadien, dans le centre du Canada, sont parmi les plus faibles au pays et varient entre <1 et 5 mg/L. On remarque par contre une hausse sensible des concentrations de chlorure dans bon nombre de petits lacs et cours d'eau urbains.
- Bon nombre des cours d'eau naturellement salés du Canada sont situés dans le sud des Prairies. On rapporte en revanche des concentrations naturellement faibles de chlorure (<5 mg/L) dans les cours d'eau intacts du nord de ces provinces.
- Plusieurs lacs naturellement salés se trouvent dans le Plateau du sud de l'Intérieur de la Colombie-Britannique (concentrations de chlorure supérieures à 100 mg/L); dans les cours d'eau intacts, les concentrations de chlorure sont généralement inférieures à 5 mg/L.
Une analyse spatiale des concentrations de chlorure a été faite, selon deux approches. Dans la première, les données de surveillance ont été regroupées au niveau du bassin versant; dans la deuxième, une méthode basée sur le bilan massique a été utilisée pour la modélisation des concentrations de chlorure au niveau du bassin versant. Cette dernière méthode a aussi été utilisée pour calculer les concentrations annuelles moyennes dans le ruissellement provenant de certaines autoroutes précises, au Canada. Les concentrations ainsi calculées atteignent jusqu'à 31 000 mg/L, mais se situent principalement entre 1 000 et 10 000 mg/L; ces estimations concordent avec les mesures du ruissellement non dilué provenant des routes.
Des concentrations élevées de chlorure ont aussi été mesurées dans des étangs et des terres humides adjacents aux routes. Des concentrations atteignant 4 300 mg/L ont ainsi été observées dans les cours d'eau et des concentrations variant entre 150 et 300 mg/L ont été mesurées dans des lacs situés en régions rurales et exposés aux effets de l'épandage des sels de voirie. Enfin, alors que les concentrations élevées s'observent habituellement durant l'hiver ou au moment du dégel printanier, de fortes concentrations peuvent aussi être mesurées durant l'été, sous l'effet du temps de parcours des ions vers les eaux de surface et de la réduction du débit, durant l'été.
3.0 Évaluation du caractère « toxique » au sens de la LCPE 1999 (Suite)
3.1 Évaluation en vertu des alinéas 64a) - Environnement et 64b) -Environnement essentiel pour la vie de la LCPE de 1999
La méthode d'évaluation environnementale d'une substance inscrite sur la LSIP consiste à caractériser l'exposition à cette substance, ses voies d'entrée dans l'environnement et ses effets, afin de pouvoir déterminer les risques qui y sont associés (Environnement Canada, 1997a). Cette démarche peut s'appuyer sur des données obtenues en laboratoire et sur le terrain; cependant, les données empiriques, recueillies sur le terrain et établissant un lien entre les effets environnementaux et la pénétration de la substance dans l'environnement, peuvent fournir une solide indication des risques réels.
On peut présumer que tous les sels de voirie finissent, tôt ou tard, par pénétrer dans l'environnement, que ce soit à la suite de fuites provenant des lieux d'entreposage de sels, de l'épandage des sels de voirie sur les routes ou de l'élimination de la neige usée. Cependant, même si tous les ions chlorure aboutiront dans les eaux de surface, les ions qui se dissocient des sels de voirie inorganiques à base de chlorures et de ferrocyanures peuvent être libérés ou se déplacer dans le sol, les eaux souterraines, les eaux de surface et l'atmosphère - les organismes peuvent donc y être exposés dans tous ces milieux. Aussi, l'évaluation des sels de voirie doit-elle tenir compte de tous les milieux environnementaux. De plus, les effets produits par ces substances dans l'environnement peuvent être de type biotique et abiotique. Les paramètres d'évaluation peuvent donc inclure des effets sur des organismes individuels, des populations ou des communautés et des effets abiotiques, comme la détérioration de la structure d'un sol ou encore la stratification d'un lac qui perturbe le mélange saisonnier des eaux.
Même s'il n'existe aucune évaluation systématique de l'exposition aux sels de voirie qui permettrait de caractériser d'une manière quantitative détaillée les risques au niveau national, dans quelque milieu écologique que ce soit, un grand nombre d'études individuelles permettent néanmoins d'établir des liens entre l'utilisation des sels de voirie et leurs répercussions sur les systèmes biotiques et abiotiques.
Les sections qui suivent visent à caractériser les risques associés aux rejets de sels de voirie dans l'environnement, à la lumière des données recueillies sur la pénétration et les effets des sels inorganiques de chlorure dans cinq milieux écologiques ou groupes biotiques et sur l'exposition à ces substances. Les données utiles à l'évaluation des ferrocyanures et des risques environnementaux qui y sont associés sont analysées dans une section distincte (section 3.7).
3.2 Eaux souterraines
3.2.1 Introduction
Cette section présente un résumé du devenir des sels de voirie dans les eaux souterraines et de leurs effets sur la qualité de ces eaux. Elle s'appuie sur un rapport préparé par Johnston et al. (2000); un résumé d'études de cas (Morin, 2000) y est aussi présenté.
Dans la documentation publiée et inédite, les concentrations de sels dans les eaux souterraines sont souvent examinées en fonction du dépassement des directives sur la qualité de l'eau potable, elles-mêmes fondées sur les seuils de gustation pour le sodium et le chlorure qui s'établissent respectivement à 200 mg/L et 250 mg/L (CCME, 1998). Bien que la présente évaluation ne porte pas sur les eaux souterraines comme source d'eau potable, il est néanmoins utile d'examiner les dépassements par rapport à la norme relative au chlorure (250 mg/L), pour évaluer les effets possibles de cette substance sur le biote aquatique. Comme l'indique la section 3.3, la concentration sans effet observé (CSEO), mesurée lors de l'essai de survie aux premiers stades de vie (33 jours) de la tête-de-boule, est de 252 mg/L de chlorure. De plus, les données sur la létalité obtenues par modélisation de l'exposition chronique indiquent que des concentrations de chlorure d'environ 240 mg/L auraient des effets sur 10 % des espèces aquatiques.
3.2.2 Principes reliés aux eaux souterraines
3.2.2.1 Cycle de l'eau
L'incidence des sels de voirie sur les eaux souterraines varie considérablement selon les charges de sels de voirie, les conditions climatiques, les conditions du sol en surface et subsurface, ainsi que l'emplacement du site à l'intérieur du milieu hydrogéologique global.
Les précipitations qui tombent sur une région, sous forme de pluie ou de neige, alimentent un certain nombre de processus hydrologiques. Une partie de ces précipitations s'écoulent sur les surfaces imperméables, comme les routes et les aires de stationnement, et sont acheminées par des fossés ouverts ou des canalisations en subsurface vers des ruisseaux, des terres humides, des lacs ou d'autres plans d'eau de surface. Habituellement quelques heures suffisent pour que ce ruissellement entraîne la migration directe des contaminants en surface, comme les sels de voirie, dans des plans d'eau de surface.
À certains endroits, une partie des précipitations s'infiltrent dans la zone peu profonde du sol et se déplacent latéralement à travers la zone non saturée au-dessus de la nappe phréatique, formant l'écoulement souterrain qui se dirige vers la source locale. Ce transport de contaminants vers les eaux de surface, par voie de l'écoulement souterrain, se produit généralement en une période de quelques heures à quelques jours.
Le reste des précipitations est éliminé par évapotranspiration ou s'infiltre et va alimenter la nappe souterraine. Les contaminants qui s'introduisent dans l'écoulement souterrain, au niveau local, intermédiaire ou régional, peuvent mettre plusieurs années ou plusieurs centaines d'années avant de se mêler au débit de base qui alimente les plans d'eau de surface.
3.2.2.2 Écoulement à travers un sol non saturé et alimentation de la nappe souterraine
La quantité de précipitations qui s'infiltrent dans la nappe phréatique dépend d'un certain nombre de facteurs, notamment de la durée et de l'intensité des précipitations, ainsi que du taux d'humidité initial et des conditions d'humidité du sol. Si l'on se base sur la température générale et le profil des précipitations au Canada, on peut s'attendre à ce que l'alimentation de la nappe souterraine se produise essentiellement vers la fin de l'hiver et au début du printemps, sous l'effet de la fonte des neiges et des pluies printanières (Geber et Howard, 1997; Singer et al., 1997).
Le temps de parcours vertical à travers la zone non saturée varie de moins de 0,5 m/an à plus de 20 m/an. Dans les régions où la zone non saturée est épaisse (de 20 à 30 m), les précipitations infiltrantes peuvent prendre de 5 à 20 ans avant d'atteindre la nappe souterraine, dans les sols sablonneux. Le temps de parcours est un paramètre important, lorsqu'on veut étudier les effets sur des récepteurs en aval ou évaluer le temps qu'il faudra pour que des mesures correctrices prises à la source produisent des effets notables.
3.2.2.3 Écoulement à travers un sol saturé et migration des contaminants
Sous la nappe phréatique, le mouvement de l'eau dépend du potentiel hydrique et de la perméabilité du matériau géologique. Cependant, plusieurs autres processus physiques et chimiques doivent être pris en considération pour évaluer la migration de solutés - comme les ions sodium, calcium et chlorure - dans les milieux souterrains. La dispersion mécanique, la diffusion moléculaire et les effets liés à la densité sont les principaux mécanismes de transport physique qui influent sur la migration des ions sodium, calcium et chlorure.
3.2.3 Effets des sels de voirie sur la qualité des eaux souterraines
3.2.3.1 Facteurs contrôlant la migration des sels de voirie
Une des principales préoccupations liées aux sels de voirie inorganiques à base de chlorure de sodium tient à la grande solubilité de ces substances dans l'eau. Les ions dissociés migrent vers la nappe phréatique avec les précipitations qui s'infiltrent; la migration du chlorure se fait au même rythme que la migration de l'eau, ce qui n'est pas le cas des cations comme le sodium, dont la vitesse de migration peut être influencée par les échanges de cations dans certains milieux géologiques. L'équation qui suit illustre la réaction d'échange ionique pour le sodium.
2Na+ +Ca(adsorbé) <> Ca2+ + 2Na(adsorbé)
Dans cette équation, il y a échange entre l'ion sodium et le calcium adsorbé aux matériaux riches en argile. Il en résulte une diminution de la concentration de sodium dans les eaux souterraines qui s'infiltrent, et le ratio Na:Cl devient inférieur à un. Howard et Beck (1993), de même que Pilon et Howard (1986), ont documenté cette réduction de la concentration des ions sodium dans les eaux souterraines exposées aux sels de voirie.
3.2.3.2 Concentrations prévues de sels de voirie dans les eaux souterraines
Pour bien comprendre les effets potentiels de l'épandage des sels de voirie sur la qualité des eaux souterraines, il faut estimer la quantité de sels pouvant être dissous dans les précipitations qui s'infiltrent. Un modèle simple du bilan massique sur chiffrier a été conçu pour estimer la concentration à l'équilibre de l'ion chlorure dans les eaux souterraines peu profondes (Johnston et al., 2000). Ce modèle est basé sur la dissolution du chlorure total retenu dans le sol par les précipitations de réalimentation et il ne tient pas compte du chlorure provenant d'autres sources. On peut donc considérer que les concentrations de chlorure ainsi calculées sont représentatives des concentrations régionales de chlorure à l'équilibre, en aval d'un réseau routier sur lequel il y a épandage de sels de voirie. Il est à noter que ce modèle ne fournit aucune indication des concentrations possibles de chlorure immédiatement en aval d'une source, par exemple une route particulière où il est possible que les concentrations de chlorure soient plus élevées.
Les paramètres d'entrée du modèle incluent le taux d'alimentation de la nappe souterraine, la charge de sels de voirie et la densité du réseau routier, caractéristique du sud de l'Ontario. Pour cette étude, des taux d'alimentation de 10 à 40 cm par année ont été choisis, en fonction d'un éventail de types de sol. Les volumes de chlorure sont fondés sur les charges annuelles épandues sur les réseaux routiers provinciaux et municipaux, indiqués précédemment à la section 2.2. La quantité de sels de voirie pouvant s'infiltrer dans la nappe phréatique a été estimée à partir des intervalles rapportés dans Wulkowicz et Saleem (1974), Scott (1980) et Howard et Haynes (1993). Enfin, on a choisi une densité routière de 1 à 15 km de route à deux voies par kilomètre carré, sur la base des données présentées dans Morin et Perchanok (2000) et Stantec Consulting Ltd. (2000). On suppose qu'un réseau routier d'une densité de 0,01 à 0,1 km de route à deux voies par kilomètre carré est caractéristique d'une région rurale à faible densité d'utilisation des sols, qu'une densité de 1 à 5 km de route à deux voies par kilomètre carré est représentative d'une région rurale de densité moyenne ou d'une région semi-rurale et enfin qu'un réseau d'une densité de 10 à 15 km de route à deux voies par kilomètre carré est représentatif d'une utilisation urbaine des sols.
Les concentrations prévues de chlorure, en regard d'un taux d'alimentation donné, augmentent proportionnellement à l'accroissement de la charge, de la densité du réseau routier et du pourcentage de chlorure retenu. À l'inverse, les concentrations de chlorure diminuent lorsque le taux d'alimentation de la nappe augmente, sous l'effet de dilution ainsi créé. La concentration de chlorure la plus élevée (3 600 mg/L) a été prévue pour un sol ayant un taux d'alimentation de 10 cm/an, une charge de 40 tonnes de chlorure par kilomètre de route à deux voies et un taux de rétention de 60 % du chlorure épandu pouvant être dilué par les précipitations. Par comparaison, la concentration de chlorure, à charge et pourcentage de rétention égaux, serait de 900 mg/L dans un sol où le taux d'alimentation de la nappe phréatique serait de 40 cm/an. On s'attend à ce que le pourcentage de chlorure retenu varie considérablement entre un site où le taux d'alimentation est de 10 cm/an et un autre où il serait de 40 cm/an, car le ruissellement sera plus important dans le premier cas et qu'il y aura donc moins de chlorure retenu dans le sol qui pourra ensuite être dissous par les précipitations.
Les figures 12 à 14 illustrent les concentrations régionales de chlorure dans les eaux souterraines, prévues en regard de divers charges de sels de voirie, densités routières et taux d'alimentation de la nappe. Chaque figure présente une courbe qui correspond aux concentrations maximale et minimale de chlorure, ainsi qu'une courbe illustrant la concentration moyenne de chlorure pour des réseaux routiers de densité moyenne et forte, en présumant un taux de rétention moyen de 30 % à 40 % de chlorure.
Les concentrations de chlorure dans les sols ayant un taux d'alimentation de 10 cm/an (lequel est caractéristique des sols riches en argile) peuvent dépasser 250 mg/L, lorsqu'il y a une charge d'environ cinq tonnes de chlorure par kilomètre de route à deux voies sur un réseau routier de forte densité (figure 12). Dans le cas de réseaux routiers de densité moyenne, on s'attend à ce que les concentrations de chlorure demeurent inférieures à 250 mg/L, lorsque les charges se situent entre 10 et 15 tonnes de chlorure par kilomètre de route à deux voies. Enfin, dans le cas des réseaux de faible densité, caractéristiques des régions rurales, les concentrations régionales de chlorure devraient se maintenir bien en deçà de 250 mg/L (Johnston et al., 2000).
La figure 13 présente une estimation des concentrations dans les eaux souterraines, pour un sol ayant un taux d'alimentation de 20 cm/an -ce qui est représentatif du sable. Un tel sol peut tolérer des charges légèrement plus élevés avant que la concentration de chlorure ne dépasse 250 mg/L, car il y a un effet de dilution causé par l'alimentation plus abondante. Ainsi, pour des réseaux routiers de densité moyenne et forte, des charges de chlorure, s'établissant respectivement à plus de 11 tonnes par kilomètre de route à deux voies et entre 25 et 34 tonnes par kilomètre de route à deux voies, pourraient donner lieu à des concentrations régionales de chlorure supérieures à 250 mg/L.
Enfin, dans les sols très perméables (comme le gravier ou l'assise rocheuse fragmentée) ayant un taux d'alimentation caractéristique, les concentrations de chlorure dans les eaux souterraines ne dépasseront 250 mg/L que dans le cas de réseaux routiers de forte densité. Des charges variant entre 16 et 22 tonnes de chlorure par kilomètre de route à deux voies pourraient alors entraîner des concentrations supérieures à 250 mg/L (figure 14).
Selon le modèle du bilan massique qui a été utilisé, des charges de plus de 15 tonnes de chlorure par kilomètre de route à deux voies, ou de 24 tonnes de chlorure de sodium par kilomètre de route à deux voies, donnera lieu à des concentrations régionales supérieures à 250 mg/L dans les eaux souterraines, et ce dans tous les types de sol des régions à forte densité d'utilisation des sols. Comme les charges de sels de voirie dans le sud de l'Ontario et du Québec et dans les Maritimes se situent entre 20 et 50 tonnes de chlorure de sodium par kilomètre de route à deux voies, c'est dans les régions fortement urbanisées de ces provinces que les eaux souterraines risquent le plus de subir les effets à grande échelle des sels de voirie. Or ces substances peuvent avoir un effet non seulement sur les eaux souterraines, mais également sur la qualité des eaux de surface dont le débit de base est alimenté par des eaux souterraines à fortes concentrations de sodium et de chlorure, surtout à la fin de l'été et à l'automne.
Figure 12 Estimation de la concentration de chlorure dans les eaux souterraines à divers taux d'épandage et à un taux d'alimentation des eaux souterraines de 10 cm/an (d'après Johnston et al., 2000)

Figure 13 Estimation de la concentration de chlorure dans les eaux souterraines à divers taux d'épandage et à un taux d'alimentation des eaux souterraines de 20 cm/an (d'après Johnston et al., 2000)

Figure 14 Estimation de la concentration de chlorure dans les eaux souterraines à divers taux d'épandage et à un taux d'alimentation des eaux souterraines de 40 cm/an (d'après Johnston et al., 2000)

Le modèle du bilan massique indique que, dans les régions à faible densité d'utilisation des sols, la concentration de chlorure demeurera bien en deçà de 250 mg/L et atteindra un maximum de 24 mg/L, à une charge de 40 tonnes de chlorure de sodium par kilomètre de route à deux voies. Il est à noter, cependant, que cette concentration constitue une moyenne régionale et que des concentrations plus élevées pourraient être observées immédiatement en aval de certaines routes.
3.2.3.3 Migration du panache et évaluation des effets
La section qui précède a présenté un aperçu des effets régionaux associés aux sources diffuses de sels de voirie provenant de l'épandage en régions urbaines et rurales. La présente section traite des effets sur la qualité des eaux souterraines et de la formation du panache à partir d'une source ponctuelle associée à l'épandage de sels de voirie le long d'une route particulière.
Pour estimer la concentration maximale de chlorure et les effets de la dispersion sur les concentrations dans le panache, un modèle numérique de transport des solutés a été élaboré pour un aquifère simple, libre de sable, à l'aide des programmes de modélisation en différences finies MODFLOW (McDonald et Harbaugh, 1988) et MT3D (Zheng, 1990). On a attribué à cet aquifère simplifié une conductivité hydraulique latérale de 1 ´ 10-4 m/s, une conductivité hydraulique verticale de 1 ´ 10-5 m/s, un débit spécifique de 0,25, une porosité efficace de 0,30, une dispersivité longitudinale de 10 m, ainsi que des dispersivités transversales latérale et verticale respectives de 1 m et 0,1 m. Des limites linéaires à charge constante ont été déterminées aux extensions amont (17,5 m) et aval (15 m) du modèle, pour simuler un gradient hydraulique latéral de 0,005 m/m sur les 500 m du modèle. Un taux d'alimentation de 30 cm/an a été appliqué à l'ensemble du domaine du modèle.
À l'intérieur du champ d'écoulement constant simulé, un terme source carré de concentration constante (1 000 mg/L) a été défini dans la nappe phréatique, pour représenter la charge de chlorure provenant d'un tronçon de route. Cette concentration se situe à l'intérieur de la gamme de concentrations (323 à 2 930 mg/L; moyenne de 923 mg/L) établie pour des eaux souterraines peu profondes, sous une autoroute à quatre voies de Kitchener (Ontario) (Stantec Consulting Ltd., 2000). On a simulé la formation et la migration d'un panache non freiné d'ions chlorure en phase dissoute, pendant 5 000 jours, puis la dissipation du panache après suppression du terme source.
Au terme d'une période de simulation de 100 jours, correspondant au début de l'été après que la nappe souterraine a été alimentée par de fortes concentrations de chlorure provenant de l'épandage de sels de voirie durant l'hiver, les concentrations dans les eaux souterraines parallèles au panache ont présenté la formation caractéristique d'un panache en « forme de cigare », illustrée par la courbe de niveau 10 mg/L. À 100 jours, la courbe de niveau 10 mg/L s'était déplacée à environ 40 m en aval de la source, alors que la courbe illustrant la concentration de 250 mg/L se limitait à moins de 10 m environ de la source. Après une période d'environ cinq ans, le panache a atteint l'état d'équilibre, comme l'indique la courbe de niveau 10 mg/L où il y a équilibre entre le flux en provenance de la source et le flux sortant des limites du panache. À l'équilibre, la courbe 10 mg/L se situe à 200 m environ en aval de la source, alors que la courbe correspondant à 250 mg/L s'est déplacée de 20 m en aval de la source.
Après une période de simulation d'environ cinq ans, la source de chlorure a été supprimée, pour estimer le temps nécessaire à la dissipation des concentrations. Les concentrations de chlorure ont diminué rapidement après 50 jours et aucune des concentrations simulées n'a dépassé alors 250 mg/L.
Les simulations qui précèdent montrent que l'étendue des effets associés à l'épandage de sels de voirie, le long d'une route donnée, peut être limitée par l'écoulement souterrain et les processus de transport, selon les propriétés de l'aquifère. Les résultats de la modélisation indiquent en outre que les puits peu profonds et les plans d'eau de surface situés à moins de 20 m des routes où il y a épandage sont les plus susceptibles de subir les effets du chlorure. Le modèle suggère enfin que si l'on suspend l'épandage des sels de voirie, les concentrations de chlorure dans l'aquifère peu profond peuvent diminuer considérablement, en une période de quelques mois à quelques années.
3.2.4 Études de cas
Cette section présente des mesures obtenues par modélisation et sur le terrain pour certaines régions du Canada. Morin (2000) examine d'autres études de cas portant sur les effets de l'épandage et de l'entreposage des sels sur la qualité des eaux souterraines.
Howard et Haynes (1993) ont évalué les effets de l'épandage de sels de voirie à l'échelle régionale, dans le bassin du ruisseau Highland situé près de Toronto (Ontario). Au moyen de mesures détaillées du débit du ruisseau et des concentrations de chlorure sur une période de trois ans, ces auteurs ont estimé que 45 % seulement du chlorure épandu sous forme de sels de voirie dans le bassin était éliminé par le ruissellement, le reste (55 %) étant stocké dans le réseau des eaux souterraines. Howard et Haynes (1993) ont en outre estimé à 426 ± 50mg/L la concentration moyenne de chlorure dans les eaux souterraines alimentant le débit de base du ruisseau Highland, aux taux d'épandage courants.
Bien qu'on ne précise pas le taux d'épandage de sels de voirie, on sait que la charge totale dans le bassin a été d'environ 200 g de chlorure de sodium/m2. Donc, si on suppose un réseau routier d'une densité caractéristique d'un milieu urbain, le taux d'épandage de sels de voirie dans la région à l'étude serait de l'ordre de 20 à 30 tonnes de chlorure de sodium par kilomètre de route à deux voies, ce qui se compare à la quantité prévue avec le modèle du bilan massique élaboré dans le cadre du présent rapport (section 3.2.3.2).
D'autres données sur les effets de l'épandage des sels de voirie en régions urbaines sur la qualité des eaux souterraines et sur les rejets dans les eaux de surface sont présentées dans Howard et Beck (1993) et Eyles et Howard (1988). Ainsi, des concentrations de chlorure d'environ 400 mg/L ont été mesurées dans les sources qui alimentent le lac Ontario, le long de Scarborough Bluffs près de Toronto, ce qui est comparable aux concentrations estimées par Howard et Beck (1993) pour le bassin versant du ruisseau Highland.
Les concentrations de chlorure à long terme mesurées dans les puits d'approvisionnement municipaux fournissent d'autres preuves des effets de l'épandage des sels de voirie en hiver sur la qualité des eaux souterraines (Johnston et al., 2000). La figure 15 présente les concentrations de chlorure dans les puits municipaux d'un centre urbain du sud de l'Ontario. Les données sur les taux actuels d'épandage de chlorure dans la région de l'étude, à proximité des puits, indiquent que les taux varient de 18 à 36 tonnes de chlorure de sodium par kilomètre de route à deux voies, pour un taux d'épandage moyen de 28 tonnes. Au début des années 1960, les concentrations de chlorure étaient inférieures à 50 mg/L, mais elles ont augmenté graduellement pour atteindre de 250 à 300 mg/L à la fin des années 90 (figure 15) (les données après 1998 ne sont pas représentées). Un des principaux problèmes qui ressort des tendances illustrées à la figure 15 est que la concentration de chlorure continue d'augmenter et n'a pas atteint l'état d'équilibre. De fait, depuis 1998, les concentrations de chlorure dans ces puits ont augmenté à un rythme comparable à celui observé depuis 1993 (et illustré sur la figure 15), et la concentration dans le puits no 3 dépasse maintenant 350 mg/L. Il convient toutefois de noter que les eaux souterraines qui alimentent ces puits représentent des précipitations qui ont alimenté la nappe phréatique entre le milieu et la fin des années 70, puisque le temps de parcours entre les eaux souterraines et les eaux de surface est de l'ordre de 30 ans. Donc, l'accroissement de la concentration de chlorure dans ces puits est imputable à l'épandage de sels de voirie qui s'est fait il y a 30 ans. Comme ces puits pompent en moyenne 3,3 millions de mètres cubes d'eau chaque année et que leur zone de captage sur 20 ans s'étend sur 12 km2, on considère que les concentrations prévues à ces puits sont représentatives des concentrations régionales de chlorure. Lorsqu'on compare les concentrations actuelles (environ 350 mg/L) aux concentrations prévues (300 à 450 mg/L), on constate que la modélisation basée sur le bilan massique, définie à la section précédente, offre une estimation raisonnable des concentrations de chlorure (Johnston et al., 2000).
Le temps nécessaire pour atteindre l'état d'équilibre (c.-à-d. le moment où il y a équilibre entre l'entrée et la sortie de sels) dépend des conditions hydrogéologiques locales et de la taille du bassin versant (Howard et al., 1993). Howard et al. (1993) ont utilisé deux modèles numériques pour illustrer les variations temporelles et spatiales de la qualité de l'eau. Le modèle FLOWPATH indique que les polluants chimiquement rémanents comme le chlorure, qui sont rejetés à quelques kilomètres des rivières et du lac Ontario, émergeront dans environ cinq ans. Dans le cas de contaminants rejetés dans des régions plus centrales, il faudra plus de 100 ans pour qu'ils soient éliminés des eaux souterraines. À l'aide du modèle FLOWPATH, Howard et al. (1993) ont démontré que, à l'intérieur d'une zone de 460 km2 représentative de la Région du Grand Toronto, les concentrations moyennes de chlorure atteindront l'état d'équilibre dans les 200 ans suivant l'épandage initial des sels répartis uniformément sur l'ensemble de cette zone. Au moyen d'un autre modèle (AQUA) appliqué à une région plus petite située près de Toronto, l'état d'équilibre a été atteint en 30 ans seulement. À l'état d'équilibre, les taux de chlorure à une distance de 200 m des autoroutes sur lesquelles il y a épandage de sels sont de deux à trois fois supérieurs aux concentrations de chlorure observées dans le débit de base.
Williams et al. (1997) ont étudié les concentrations de chlorure dans 20 sources du sud-est de l'Ontario; ces concentrations variaient entre 8,1 mg/L et 1 149 mg/L, les plus élevées provenant d'eaux souterraines susceptibles d'avoir été contaminées par les sels de voirie. Williams et al. (1999) ont poursuivi leur recherche et noté que la concentration moyenne de chlorure dans l'aire de conservation de Glen Majors était de 2,1 mg/L et qu'elle était d'environ 100 mg/L dans les régions rurales. Des concentrations de chlorure plus élevées (>200 mg/L) ont été observées dans des sources situées près de régions urbaines, la concentration maximale atteignant alors 1 345 mg/L et la concentration moyenne s'établissant à 1 092 mg/L. La source dans laquelle a été mesurée la concentration maximale était située à proximité d'une autoroute et d'un pont. De plus, les concentrations de chlorure dans ces sites urbains ont augmenté entre novembre 1996 et novembre 1997 et la contamination a été associée à l'usage des sels de voirie. Williams et al. (1999) ont également constaté qu'il était plus facile de déterminer le profil spatial de la contamination par les sels de voirie, en procédant à l'échantillonnage des sources plutôt que des ruisseaux, parce que les concentrations de chlorure dans l'eau de source (c.-à-d. rejet d'eaux souterraines) varient relativement peu selon la saison, alors que ces concentrations fluctuent considérablement dans les ruisseaux, d'une saison'a l'autre.
Howard et Taylor (1998) ont relevé de fortes concentrations de chlorure dans des sources alimentées par des aquifères le long de Scarborough Bluffs, un segment du rivage du lac Ontario à l'est de Toronto, de même que le long d'un transect urbain-rural qui s'étend de la moraine d'Oak Ridges à la région métropolitaine de Toronto. Dans cette dernière région, des concentrations de chlorure supérieures à 2 800 mg/L ont été mesurées dans des sources émergeant d'aquifères peu profonds; cette contamination par le chlorure a été attribuée principalement aux sels de déglaçage chimiques utilisés sur les routes (Howard et Beck, 1993).
En 1970, une autoroute a été construite à une distance de 50 à 200 m des puits utilisés par la municipalité de Trois-Rivières Ouest pour le captage des eaux souterraines. En 1976, on a noté une augmentation de la salinité (Gélinas et Locat, 1988) et, au début des années 1980, un panache d'eaux souterraines salées a été identifié. Des concentrations de chlorure variant de 3 à 1 500 mg/L ont été mesurées dans les échantillons prélevés des piézomètres. Des données recueillies en 1985 indiquent que la forme et l'étendue du panache ont varié selon la période de l'année et la quantité d'eau pompée à chacun des six puits municipaux. Les données pour 1985-1986 indiquent que la concentration a augmenté progressivement au printemps (pendant la fonte des neiges) pour atteindre un sommet en août et septembre; de plus, des concentrations plus élevées ont été observées dans une station de pompage municipale située en aval de l'autoroute. Ainsi, alors que les concentrations dans la plupart des puits en amont de l'autoroute ont été inférieures à 5 mg/L, la concentration moyenne de chlorure dans une station en aval (80 mg/L) a été environ six fois plus élevée que la concentration moyenne dans une station proche, située en amont (14 mg/L).
La municipalité de Cap-de-la-Madeleine pompe l'eau de 27 puits. Bien que l'on considérait que l'eau y était de très bonne qualité, la concentration de chlorure dans certains puits a augmenté graduellement depuis les années 1970 et cette hausse a été attribuée à l'utilisation des sels de déglaçage. Dans les régions où les fossés ne sont pas reliés à un réseau de drainage, le ruissellement s'infiltre de lui-même dans le sol (Delisle, 1999).
Figure 15 Concentration de chlorure dans les eaux souterraines des puits d'approvisionnement municipaux dans le Sud de l'Ontario (d'après Johnston et al., 2000)

3.2.5 Conclusions
Une méthode basée sur le bilan massique a été utilisée pour évaluer les effets potentiels des sels sur la qualité des eaux souterraines et des eaux de surface, cette méthode permettant d'estimer les concentrations potentielles de chlorure à l'échelle régionale, en aval des réseaux routiers sur lesquels il y a épandage. Ce modèle indique que les concentrations de chlorure dans les eaux souterraines régionales seront probablement supérieures à 250 mg/L, dans les régions où le taux d'épandage excède 20 tonnes de chlorure de sodium par kilomètre de route à deux voies, sur les réseaux routiers de forte densité caractéristiques des régions urbaines. Si l'on se base sur les taux d'épandage de sels de voirie au Canada, ce sont les eaux souterraines des régions urbaines du sud de l'Ontario et du Québec et des Maritimes qui sont les plus susceptibles de subir les effets à grande échelle des sels de voirie. Le modèle du bilan massique élaboré pour la présente évaluation indique par ailleurs que les régions rurales et semi-rurales risquent moins d'être exposées à des concentrations de chlorure supérieures à 250 mg/L, à l'échelle régionale. Des effets locaux le long de certaines routes ont toutefois été observés.
L'eau souterraine qui contient des sels de voirie finit par resurgir dans les eaux de surface ou dans les sources. Des recherches révèlent qu'une partie seulement des sels de voirie épandus sur les routes sont éliminés par le ruissellement et qu'une proportion importante peut être emmagasinée dans les eaux souterraines. Des concentrations élevées de chlorure ont ainsi été observées dans les eaux souterraines, ainsi que dans des sources alimentées par les eaux souterraines. En outre, les concentrations prévues et mesurées dans les eaux souterraines et les sources dépassent les seuils de létalité établis pour bon nombre d'organismes, comme on le verra à la section 3.3 (on peut s'attendre, par exemple, à ce que l'exposition à des concentrations supérieures à 240 mg/L produisent des effets chez 10 % des espèces).
3.3 Écosystèmes aquatiques
3.3.1 Méthode d'évaluation et d'établissement de la portée
Les sels de voirie peuvent avoir divers effets sur les écosystèmes aquatiques. Evans et Frick (2001) ont évalué ces impacts, en procédant a) à une recherche documentaire sur les effets de l'épandage des sels de voirie sur les écosystèmes aquatiques et b) à un examen des taux de chlorure de sodium et autres sels de chlorure produisant des effets létaux et sublétaux en laboratoire. Ces études ont ensuite servi à caractériser les risques associés aux sels de voirie. La présente section résume les faits saillants de ce rapport.
Les écosystèmes aquatiques examinés dans cette évaluation couvrent un large éventail d'habitats, incluant des cours d'eau, des rivières, des terres humides, des étangs et des lacs. Ces écosystèmes sont situés à divers endroits au Canada, dans des régions fort variées dont certaines sont exposées à des stress anthropiques minimes et d'autres à des stress intenses. Un grand nombre d'écosystèmes aquatiques sont situés dans des régions relativement inexploitées, où les impacts d'origine anthropique sont minimes. Cependant, même minimes, ces impacts sont préoccupants, car les habitats vierges sont sensibles à des stress anthropiques relativement mineurs. De faibles fluctuations dans la composition des espèces, en particulier des phytoplanctons, sont fortement représentatives de tels impacts, car les espèces présentes dans les milieux inexploités se composent en grande partie de taxons adaptés à des milieux non perturbés et que les espèces qui tolèrent la pollution n'y sont habituellement que des composantes mineures. Par conséquent, une augmentation même faible de la concentration de chlorure, imputable au ruissellement routier ou aux pertes des entrepôts de sels, pourrait avoir des impacts mesurables sur ces communautés.
D'autres écosystèmes aquatiques sont situés dans des régions rurales et agricoles, où les taxons sont exposés à une variété de stress liés à diverses activités humaines, notamment la perte de l'habitat et un apport accru de produits chimiques. Avec l'intensification du développement dans les régions rurales du Canada, incluant la conversion d'étangs et de terres humides naturels à des usages agricoles, les maigres dizaines de mètres longeant les routes peuvent devenir d'importants habitats pour des communautés végétales et fauniques déplacées. Ces zones peuvent aussi servir de corridors de migration entre des régions plus vastes, relativement non perturbées (Nadec, 2001).
Enfin, on trouve aussi des écosystèmes aquatiques en milieu urbain, bon nombre de ces écosystèmes étant peu à peu intégrés au paysage urbain, sous l'effet de l'étalement. Dans ces régions, diverses mesures sont prévues afin de protéger ces écosystèmes, en limitant le développement sur le littoral immédiat et en cherchant à réduire au minimum les impacts anthropiques dans le bassin immédiat. Il existe des exemples bien connus d'espaces ainsi intégrés, que l'on pense aux parcs aménagés autour des nombreux ruisseaux qui traversent la région métropolitaine de Toronto et aux parcs comme le parc Stanley, à Vancouver. Bien que ces écosystèmes aquatiques ne soient plus intacts, ils méritent néanmoins d'être protégés pour éviter qu'ils ne se dégradent davantage. De plus en plus, les plans d'aménagement urbain prévoient l'incorporation d'éléments propres aux régions rurales, comme des lacs et des ruisseaux. Bon nombre de ces écosystèmes artificiels sont aménagés dans le paysage naturel, à même des habitats aquatiques déjà existants (p. ex., des étangs, des terres humides, des marécages, des ruisseaux), lesquels sont rapidement colonisés de nouveau par des organismes aquatiques qui avaient temporairement été déplacés.
Les bassins de retenue des eaux pluviales, souvent aménagés à l'intérieur d'un écosystème aquatique naturel tel un ruisseau ou des terres humides, sont d'autres systèmes artificiels qui servent d'habitats à un large éventail d'organismes (Bishop et al., 2000). Malgré leur caractère manifestement non idéal, car ces habitats renferment une variété de contaminants et qu'ils perturbent le régime hydrologique, ces lieux procurent un habitat et des ressources aquatiques aux organismes et à la population (qui a besoin d'une aire critique pour assurer son autosuffisance), à l'intérieur d'un paysage urbain et rural de plus en plus fragmenté.
La présente évaluation porte sur toutes les composantes des écosystèmes aquatiques, incluant les bactéries, les champignons, les protozoaires, les zooplanctons, les invertébrés benthiques, les poissons et les amphibiens. Ces groupes n'ont toutefois pas tous été évalués également dans la documentation. Ainsi, les études en laboratoire sur la toxicité du chlorure portent principalement sur les poissons, les zooplanctons et les invertébrés benthiques et il s'agit, dans la plupart des cas, d'études sur l'exposition à court terme. De telles études visent essentiellement à évaluer la capacité d'une espèce de résister à un stress osmotique de courte durée, provoqué par l'élévation de la salinité. Peu d'études ont porté sur la toxicité chronique, laquelle a été estimée à l'aide de méthodes adoptées par la U.S. EPA (1988) pour définir les lignes directrices sur la qualité de l'eau qui s'appliquent au chlorure.
De même, relativement peu d'études sur le terrain ont porté expressément sur les effets des sels de voirie sur les écosystèmes aquatiques. Qui plus est, la majorité de ces études ont été réalisées durant les années 1970 et 1980, dont bon nombre aux États-Unis. Celles-ci peuvent néanmoins s'appliquer dans l'ensemble à l'environnement canadien.
Comme le prévoit la LCPE de 1999 et tel qu'indiqué dans un document publié par Environnement Canada (1997a), on utilise la méthode fondée sur le poids de la preuve -laquelle consiste à examiner plusieurs sources de données - pour accroître la confiance à l'égard des conclusions de l'évaluation. Ces données proviennent entre autres d'études sur la toxicité à court terme, d'estimations de la toxicité aiguë, d'études sur le terrain, de données nouvelles et de l'examen général des profils d'utilisation des sels de voirie dans l'environnement canadien. Enfin, une démarche par niveaux basée sur des quotients est aussi utilisée pour déterminer la probabilité que le rejet de sels de voirie dans l'environnement ait des effets nocifs sur les écosystèmes aquatiques.
3.3.2 Études en laboratoire
La recherche documentaire visant à relever les études en laboratoire examinant la toxicité du chlorure avait principalement pour but de recueillir de l'information sur la toxicité du chlorure de sodium, mais elle a aussi permis de relever des données sur la toxicité des chlorures de calcium, de potassium et de magnésium également présents dans divers sels de voirie. Les données sur la toxicité sont essentielles à l'évaluation des concentrations dans l'environnement et des durées d'exposition susceptibles d'êtres nocives. La toxicité à court terme (de quelques heures à quelques jours) et à long terme (semaines à mois) sont toutes deux préoccupantes. Les paragraphes qui suivent présentent un résumé de ces observations.
3.3.2.1 Études sur la toxicité à court terme ou toxicité aiguë
L'exposition à court terme (de quelques heures à quelques jours) à de fortes concentrations de chlorure est un des scénarios d'exposition préoccupants, en particulier lorsque la capacité de dilution du plan d'eau récepteur est faible. Le ruissellement routier, qui s'écoule directement dans les ruisseaux, les cours d'eau et autres plans d'eau qui longent les routes, est particulièrement préoccupant. Les organismes qui vivent dans des plans d'eau plus vastes ayant une plus grande capacité de dilution, comme les rivières et les lacs, risquent moins d'être exposés à des conditions de toxicité aiguë. En revanche, les organismes qui vivent dans les terres humides, qui sont des cours d'eau stationnaire relativement petits et à faible débit de renouvellement, peuvent subir des effets importants dus à une toxicité aiguë et chronique.
Une vaste recherche documentaire a permis de recenser plusieurs douzaines d'études sur la toxicité à court terme (aiguë) du chlorure de sodium pour les organismes aquatiques; moins d'études par contre ont été recensées sur les effets des sels de magnésium, de calcium et de potassium (Evans et Frick, 2001). Ces études sur la toxicité aiguë ont ensuite été réparties en quatre catégories basées sur l'intervalle de temps, pour estimer la toxicité résultant de diverses expositions à des concentrations élevées de chlorure.
- Moins de 24 heures : Quatre études ont été recensées sur les expositions de moins d'une journée, dont trois sur le poisson et une sur les organismes benthiques (tableau 10); les valeurs de la CL50 dans ces études varient de 6 063 à 30 330 mg de chlorure/L, la moyenne géométrique étant de 12 826 mg/L. Les salinités naturelles qui se situent dans cet intervalle s'observent dans les estuaires, les marais salés, les océans et les lacs intérieurs salés. Elles ont aussi été associées au ruissellement (et éclaboussures) provenant d'autoroutes à voies multiples, à la neige usée en milieux urbains, ainsi qu'au lixiviat et aux eaux souterraines s'écoulant d'entrepôts de sels. Enfin, des concentrations élevées de chlorure, se situant à l'extrémité inférieure de cet intervalle, ont été rapportées dans l'eau de puits, un cours d'eau ainsi qu'une terre humide située près d'un entrepôt de sels de voirie (voir les sections 2.3, 2.4, 2.6 et 3.4).
- 24 heures : Sept études ont été recensées sur des expositions de 24 heures, dont quatre sur le poisson et trois sur des cladocères (tableau 11); les valeurs de la CL50 qui y sont rapportées fluctuent entre 1 652 et 8 553 mg de chlorure/L, la moyenne géométrique étant de 3 746 mg/L. Les salinités dans cet intervalle sont caractéristiques des estuaires, des marais salés et des lacs intérieurs salés; elles ont aussi été observées dans l'eau de ruissellement (et les éclaboussures) d'autoroutes à voies multiples, dans la neige usée de régions urbaines et dans le lixiviat s'écoulant d'entrepôts de sels. Enfin, des concentrations élevées de chlorure, se situant à l'extrémité inférieure de cet intervalle, ont aussi été observées dans l'eau de puits, un cours d'eau et une terre humide située près d'un dépôt de sels de voirie (voir les sections 2.3, 2.4, 2.6 et 3.4).
- 3 à 4 jours : On a relevé plusieurs études examinant la toxicité après quatre jours d'exposition au chlorure de sodium pour une variété d'organismes et un nombre moindre d'études sur la toxicité après trois jours d'exposition. Les données sur l'exposition pendant trois jours ont été converties en estimations sur quatre jours, à l'aide d'un facteur de conversion décrit dans Evans et Frick (2001). Au total, 28 observations ont ainsi été obtenues, dont 13 sur le poisson, 7 sur des cladocères et 8 sur d'autres invertébrés (tableau 12). De plus, certaines espèces ont fait l'objet de plusieurs études; c'est le cas notamment de Daphnia magna et de la tête-de-boule (Pimephales promelas). Ces études font état de quelques différences dans la valeur de la CL50, attribuables sans doute aux variations dans les conditions d'essai (p. ex., utilisation d'eau reconstituée dans Birge et al., 1985) ou à des différences dans la tolérance physiologique des organismes d'essai, les poissons affichant généralement une plus grande tolérance que les invertébrés. Les valeurs de la CL50 varient ainsi de 1 400 à 13 085 mg de chlorure/L (moyenne géométrique de 4 033 mg/L). Cette tolérance plus élevée après quatre jours qu'après un jour s'explique, en grande partie, par l'inclusion du gambusie (Gambusia affinis, un poisson résistant qui est utilisé dans le monde entier pour lutter contre les moustiques) et de l'anguille (Anguilla rostrata, un poisson qui passe sa vie adulte dans l'océan) dans l'ensemble de données. Les salinités dans cet intervalle sont caractéristiques des estuaires, des marais salés et des lacs intérieurs salés; elles ont aussi été observées dans l'eau de ruissellement (et les éclaboussures) provenant d'autoroutes à voies multiples, dans la neige usée des villes et dans le lixiviat s'écoulant d'entrepôts de sels.
Enfin, des concentrations élevées de chlorure, se situant à l'extrémité inférieure de cet intervalle, ont été relevées dans l'eau d'un puits, un cours d'eau et une terre humide à proximité d'un dépôt de sels de voirie (voir les sections 2.3, 2.4, 2.6 et 3.4). Des salinités fluctuant entre 1 000 et 4 000 mg/L ont aussi été mesurées dans plusieurs ruisseaux de la région métropolitaine de Toronto.
- 7 à 10 jours : On a relevé 17 études estimant la toxicité du chlorure après une exposition de 7 à 10 jours (tableau 13). Les expositions de cette durée se situent à l'extrémité supérieure des durées d'exposition aiguë, sans pour autant être suffisamment longues pour être qualifiées d'expositions chroniques pour les organismes ayant une longue durée de vie, comme les amphibiens et les poissons. Différents paramètres ont été examinés dans le cadre de ces études, notamment la mortalité, la réduction de la croissance, la fécondité et l'échec du développement complet (c.-à-d. de l'oeuf à l'embryon). Cinq essais ont porté sur le poisson, deux sur des amphibiens, neuf sur des zooplanctons et un sur les algues. Les valeurs de la CL50 et de la CE50 varient de 874 à 3 660 mg de chlorure/L (moyenne géométrique de 1 840 mg/L); cet intervalle de salinité, qualifié de sous-salé (Hammer, 1986), est caractéristique de l'interface entre les milieux marins et dulcicoles, ainsi que des lacs intérieurs sous-salés. La diversité des espèces diminue rapidement à mesure qu'augmente la salinité dans cet intervalle (Wetzel, 1983). Pareilles salinités ont été observées dans l'eau de ruissellement (et les éclaboussures) des autoroutes, la neige usée, le lixiviat provenant d'entrepôts de sels, l'eau de puits, un cours d'eau, une terre humide située près d'un dépôt de sels de voirie, ainsi que dans des ruisseaux et rivières de la région métropolitaine de Toronto.
1Ratios CL50 /CE50 calculés pour les études où les deux paramètres ont été estimés (c.-à-d. Cowgill et Milazzo, 1990; Beak, 1999).
3.3.2.2 Toxicité chronique
La toxicité chronique (ou à long terme) du chlorure de sodium, qui peut se manifester après une exposition de plusieurs semaines à plusieurs mois, a été peu étudiée en laboratoire et seules deux études ont été relevées lors de la recherche documentaire.
Birge et al. (1985) ont estimé à 6 570 mg/L la valeur de la CL50 du chlorure après quatre jours, pour la tête-de-boule. La CSEO lors de l'essai de survie aux premiers stades de vie (à 33 jours) a été de 252 mg de chlorure/L et la concentration minimale avec effet observé (CMEO), de 352 mg/L, pour une moyenne géométrique de 298 mg/L. Cette dernière valeur a été utilisée comme valeur estimative de la toxicité chronique, ce qui donne un rapport entre la toxicité aiguë et chronique (RAC) de 22,1. Birge et al. (1985) ont également fait des essais sur Daphnia pulex et obtenu une CL50 après 4 jours de 1 470 mg/L. Lors de l'essai sur 21 jours visant à évaluer la toxicité chronique du chlorure pour cette espèce - la toxicité chronique correspondant à la moyenne géométrique entre la CSEO (314 mg/L) et la CMEO (441 mg/L) -ces auteurs ont obtenu une valeur de 372 mg/L, ce qui est comparable à celle calculée pour la tête-de-boule. Cependant, comme la valeur de toxicité aiguë est plus faible pour Daphnia, le rapport entre la toxicité aiguë et la toxicité chronique (RAC) est de 3,95. Birge et al. (1985) ont procédé à un deuxième essai de toxicité sur quatre jours avec D. pulex, cette fois-ci en utilisant de l'eau de ruisseau naturelle; ils ont obtenu alors une CE50 de 3 050 mg de chlorure/L, ce qui est deux fois supérieur à la tolérance calculée avec de l'eau reconstituée. (Si cette valeur était utilisée pour estimer le RAC, on obtiendrait un rapport de 8,20.) Birge et al. (1985) ont fait la moyenne géométrique des valeurs de toxicité chronique pour Daphnia et la tête-de-boule et estimé à 333 mg/L la valeur de toxicité chronique du chlorure; ils notent toutefois une certaine incertitude liée aux valeurs calculées pour D. pulex.
Dans le cadre d'une étude ultérieure, la U.S. EPA (1988) a défini des critères de qualité de l'eau pour le chlorure, en s'appuyant en grande partie sur les valeurs de toxicité aiguë et sur les rapports entre la toxicité aiguë et chronique estimés par Birge et al. (1985). Ainsi, l'agence américaine a utilisé les valeurs de toxicité et le RAC (3,95) établis par Birge et al. pour Daphnia pulex. Dans le cas toutefois de la tête-de-boule, la U.S. EPA a estimé à 433,1 mg/L la toxicité chronique (d'après la moyenne géométrique entre un taux de diminution de la survie de 9 % à 352 mg/L et un taux de diminution de 15 %, à 533 mg/L), pour un RAC de 15,17. Ces auteurs citent également une étude sur la truite arc-en-ciel (Salmo gairdneri, aujourd'hui désignée Oncorhynchus mykiss), qui a été réalisée par Spehar (1987) et qui fait état d'une valeur de toxicité aiguë de 6 743 mg de chlorure /L, d'une valeur de toxicité chronique de 922,7 mg de chlorure/L et d'un RAC de 7,31. La moyenne géométrique de ces trois rapports a été utilisée pour calculer le RAC final (7,59); ce rapport a ensuite été divisé par la valeur de toxicité aiguë finale pour l'ensemble du genre (1 720 mg/L), d'après le genre le plus sensible (Daphnia), pour déterminer la valeur de toxicité chronique finale (226,5 mg/L).
Une variante de la méthode basée sur le rapport entre la toxicité aiguë et la toxicité chronique a servi à estimer la toxicité chronique chez les organismes pour lesquels on possédait des données sur la toxicité aiguë à quatre jours. Deux méthodes auraient pu être utilisées à cette fin. La première aurait consisté à appliquer le RAC calculé pour Daphnia (3,95) par Birge et al. (1985), puis repris par l'Environmental Protection Agency des États-Unis (U.S. EPA, 1988), aux données sur les invertébrés et à utiliser la moyenne géométrique (10,53) du RAC pour le poisson, cité par l'EPA. Birge et al. (1985) ont toutefois estimé que la valeur de toxicité aiguë (et le RAC) étaient trop faibles. De plus, l'application de deux rapports différents modifie le classement général de la sensibilité des espèces d'après les données de toxicité aiguë à quatre jours, de sorte que le poisson semble maintenant plus sensible, alors que les invertébrés aquatiques semblent plus tolérants, à des expositions de longue durée à de fortes concentrations de chlorure - une hypothèse très peu plausible compte tenu du fait que les organismes aquatiques comme les cladocères et les larves d'insectes sont peu représentés dans les milieux marins et estuariens, alors que les taxons de poisson comme les salmonidés ont une grande affinité pour les milieux marins. Il est donc préférable de reprendre la démarche proposée par la U.S. EPA et d'utiliser le rapport moyen (7,59), lui-même basé sur la moyenne géométrique des trois rapports entre la toxicité aiguë et la toxicité chronique.
En utilisant un RAC moyen de 7,59, on a estimé que la valeur de toxicité aiguë du chlorure variait entre 184,5 mg/L (Ceriodaphnia dubia) et 1 724 mg/L (stade noir de l'anguille), pour une moyenne géométrique de 512,6 mg/L (Evans et Frick, 2001). La valeur inférieure de cet intervalle est environ 24 fois supérieure à la concentration moyenne de chlorure (8 mg/L) dans l'eau des rivières à l'échelle mondiale (Wetzel, 1983). La moyenne géométrique des valeurs de toxicité chronique (551,9 mg de chlorure/L) se situe à l'extrémité inférieure de l'intervalle (500 à 1 000 mg de chlorure/L) à l'intérieur duquel de nombreux chercheurs ont observé la disparition d'espèces dulcicoles avec l'accroissement de la salinité (Williams, 1987; Hart et al., 1990; Leland et Fend, 1998; Evans et Frick, 2001). De fait, on observe une diminution sensible de la diversité des espèces dans les écosystèmes dulcicoles lorsque la salinité passe d'environ 2 000 mg/L à 5 000 mg/L (figure 16; voir aussi Wetzel, 1983). En général, le nombre d'espèces dulcicoles diminue à mesure que la salinité augmente, les baisses les plus fortes et les plus rapides se produisant lorsque la concentration de chlorure se situe entre 1 000 et 3 000 mg/L. Or des salinités fluctuant entre 185 et 1 724 mg/L ont été mesurées dans l'eau de ruissellement (et les éclaboussures) provenant des autoroutes, la neige usée, le lixiviat s'écoulant d'entrepôts de sels et des ruisseaux de la région métropolitaine de Toronto. Les valeurs de salinité inférieures ont été associées à des lacs contaminés par du chlorure.
3.3.3 Évaluation de la toxicité pour les écosystèmes aquatiques
La toxicité des sels de voirie pour les milieux aquatiques a été évaluée au moyen des trois méthodes suivantes : a) caractérisation du risque basée sur les seuils de toxicité et les quotients, selon la procédure définie dans Environnement Canada (1997a); b) examen des données recueillies sur le terrain et démontrant des effets sur des populations ou des écosystèmes et c) examen des effets abiotiques. Les paragraphes qui suivent décrivent brièvement ces trois méthodes.
- Caractérisation du risque basée sur les seuils de toxicité et les quotients : Cette méthode basée sur le calcul de quotients détermine la probabilité que l'épandage de sels de voirie dans l'environnement ait des effets nocifs sur les écosystèmes aquatiques. Elle consiste à comparer les concentrations de chlorure dans le milieu aquatique, résultant du rejet de sels de voirie (d'après la documentation et les analyses préparées pour la présente évaluation), aux seuils de toxicité des sels de chlorure établis en laboratoire.
- Preuves sur le terrain d'effets sur des populations ou des écosystèmes : En général, la méthode du quotient s'appuie sur les seuils de toxicité. Il peut arriver toutefois que des conditions environnementales qui, sans nécessairement exposer les organismes à des concentrations de contaminants toxiques, procurent des avantages sélectifs pour certaines populations ou espèces et provoquent ainsi des modifications dans les populations et la structure des communautés. Les études sur le terrain conviennent donc tout particulièrement à l'examen des effets chroniques imputables à la présence de concentrations élevées de chlorure dans l'environnement. Cependant, comme il est impossible de tenir compte de toutes les variables dans des études de ce genre, il se peut que certains effets observés soient dus à l'effet combiné d'autres variables.
Figure 16 Diversité des espèces dans différents gradients de salinité et de chlorure (d'après Wetzel, 1983)

- Effets abiotiques : Les substances peuvent altérer l'environnement abiotique et, ainsi, avoir des effets sur les écosystèmes, par leurs interactions avec les composantes physiques, chimiques ou biologiques du milieu. Les sels de voirie peuvent, à cet égard, exercer leurs effets de deux manières importantes, d'abord en modifiant la densité de l'eau et donc ses propriétés de mélange. Ce phénomène est particulièrement important dans les plans d'eau relativement stationnaires comme les lacs, les étangs et les terres humides. Le chlorure peut aussi accroître la solubilité d'une variété de substances, y compris les métaux.
3.3.3.1 Caractérisation du risque selon le quotient
La méthode d'évaluation des risques environnementaux basée sur le quotient se fonde sur les procédures décrites dans Environnement Canada (1997a). À partir de scénarios d'exposition plausibles, on choisit une valeur estimée de l'exposition (VEE) prudente ou très prudente, puis on détermine la valeur estimée sans effet observé (VESEO) en divisant la valeur critique de la toxicité (VCT) expérimentale par un coefficient, afin de tenir compte des incertitudes dues à l'évaluation de l'exposition chronique ou intermittente par extrapolation, à l'extrapolation des conditions de laboratoire aux conditions sur le terrain, ainsi qu'aux variations de sensibilité observées entre les espèces de même qu'au sein d'une même espèce. La VCT peut être basée sur une vaste gamme d'effets toxiques, incluant la mortalité, la croissance, la reproduction, la fécondité, la longévité, la productivité, ainsi que la structure et la diversité des communautés.
Après avoir calculé la VESEO, on calcule un quotient très prudent (niveau 1) (VEE/VESEO) pour les taxons sensibles pertinents, afin de déterminer si le rejet de la substance présente des risques environnementaux potentiels. Si le quotient ainsi calculé est inférieur à un, on peut en conclure que la substance pose peu de risques pour l'environnement, et l'évaluation des risques prend fin. Par contre, si le quotient est supérieur à un pour un paramètre d'évaluation en particulier, il faut alors procéder, pour ce paramètre, à une évaluation de niveau 2 pour laquelle on calcule un quotient plus réaliste, mais toujours prudent, pour chaque taxon pertinent. Si ces quotients sont supérieurs à un, on procède à une évaluation de niveau 3, laquelle vise à évaluer la probabilité et l'ampleur des effets. Cette dernière méthode consiste en un examen plus approfondi des sources de variabilité et d'incertitude inhérentes à l'analyse du risque.
3.3.3.2 Évaluations de niveaux 1 et 2
3.3.3.2.1 Valeur estimée de l'exposition (VEE)
L'évaluation de niveau 1 est basée sur un scénario d'exposition très prudent, où l'on suppose généralement que la VEE correspond à la concentration maximale mesurée ou susceptible d'être observée dans l'environnement au Canada. Les plus fortes concentrations de chlorure de sodium en milieu aquatique ont été associées aux eaux de ruissellement des routes, à la neige contaminée par les sels et aux eaux contaminées près d'entrepôts de sels.
En Ontario, on a décelé des concentrations de chlorure atteignant 19 135 mg/L dans les eaux de ruissellement provenant du pont Skyway (Mayer et al., 1998). De leur côté, Delisle et al. (1995) ont évalué la concentration de chlorure dans la neige usée des rues de Montréal et font état d'une concentration moyenne de 3 851 mg/L et d'une concentration maximale de 10 000 mg/L; la concentration de chlorure s'est établie en moyenne à 3 115 mg/L dans la neige usée provenant des rues secondaires et à 5 066 mg/L pour la neige enlevée des rues principales (Delisle et Dériger, 2000; section 2.3.1). De plus, des concentrations de chlorure atteignant 66 000 mg/L ont été rapportées dans le lixiviat s'écoulant d'entrepôts de sels mal entretenus (section 2.4.2.1). Bien qu'on n'ait relevé aucune étude sur des terres humides au Canada, la concentration de chlorure dans les eaux de surface d'une tourbière située près d'un entrepôt de sels de voirie, dans le Maine, a atteint 13 500 mg/L et est demeurée élevée durant toute la période d'échantillonnage de mars à octobre (Ohno, 1990). Aux fins des évaluations de niveau 1, une VEE de 10 000 mg/L a été utilisée, cette valeur représentant la concentration maximale estimée de chlorure. Une telle concentration est représentative des eaux de fonte qui s'écoulent des routes et pénètrent dans les petits plans d'eau récepteurs, comme les ruisseaux et les terres humides en bordure des routes, et elle se rapproche des concentrations observées dans les terres humides situées près d'entrepôts de sels de voirie mal aménagés.
L'évaluation de niveau 2 consiste à faire une analyse plus poussée de l'exposition ou des effets (ou des deux), afin de calculer un quotient toujours prudent, mais plus réaliste que le quotient très prudent calculé pour l'évaluation de niveau 1 (Environnement Canada, 1997a). Au Canada, les données les plus complètes sur les effets des sels de voirie sur les concentrations de chlorure dans les eaux souterraines et autres systèmes aquatiques proviennent de la région métropolitaine de Toronto. Williams et al. (1997, 1999), par exemple, ont examiné les effets des sels de voirie sur les eaux souterraines et les communautés d'invertébrés dans des sources alimentées par des eaux souterraines. On possède également un vaste ensemble de données sur la qualité de l'eau pour un grand nombre de ruisseaux de la région métropolitaine de Toronto. Qui plus est, le sud de l'Ontario est une région où se fait l'épandage de fortes quantités de sels de voirie. C'est donc cet ensemble de données qui a été utilisé pour calculer la VEE de niveau 2.
Les concentrations de chlorure ont été mesurées dans plusieurs cours d'eau du bassin visé par le Plan d'assainissement de la Communauté urbaine de Toronto, entre 1990 et 1996 (voir Evans et Frick, 2001, tableau 9), les données étant recueillies sur une base saisonnière. Les concentrations maximales de chlorure rapportées aux diverses stations de surveillance s'établissent comme suit : de 2 140 à 3 780 mg/L à trois stations du ruisseau Etobicoke; 3 470 mg/L au ruisseau Mimico; 4 310 mg/L au ruisseau Black; de 96 à 4 310 mg/L aux cinq stations de la rivière Humber; de 960 à 2 610 mg/L aux trois stations de la rivière Don et 1 390 mg/L au ruisseau Highland. Les tracés saisonniers illustrant la fluctuation de la concentration de chlorure dans le ruisseau Highland, entre 1990 et 1993, montrent plusieurs périodes d'échantillonnage durant l'hiver où les concentrations de chlorure ont été supérieures à 1 000 mg/L, durant, semble-t-il, plusieurs périodes d'une semaine. Les concentrations moyennes de chlorure à ces endroits ont varié entre 278 et 553 mg/L, les concentrations durant l'hiver étant près de deux fois supérieures à celles observées durant l'été. Williams et al. (1999) rapportent également une concentration moyenne de chlorure de 1 092 mg/L dans une source située près d'une autoroute et d'un pont, en Ontario, ce résultat s'expliquant sans doute par la contamination des eaux souterraines par les sels de voirie. Bien que la concentration maximale de chlorure dans les ruisseaux et les rivières de la région de Toronto contaminés par les sels de voirie fluctue entre 2 000 et 4 000 mg/L, il est probable que la fréquence et la durée de ces épisodes varient. Par conséquent, une estimation moins prudente de 1 000 mg/L a été utilisée comme VEE pour les évaluations de niveau 2. Des concentrations de chlorure de cet ordre ont souvent été observées dans les ruisseaux et les rivières de la région de Toronto, dans une source contaminée de la région de Toronto et dans une tourbière contaminée par un entrepôt de sels de voirie (Wilcox, 1982). Pour ces scénarios, on présume que la durée d'exposition serait de l'ordre de quelques jours.
Les données utilisées pour calculer les VCT, aux fins des évaluations de niveaux 1 et 2, ont été obtenues dans le cadre de la recherche documentaire citée précédemment et décrite en détail dans Evans et Frick (2001). Il a toutefois été impossible de trouver des données pertinentes pour tous les groupes trophiques; les données les plus complètes proviennent d'études sur des périodes de deux à quatre jours. Par ailleurs, les paramètres les plus étudiés ont été la mortalité (zooplanctons et organismes benthiques), l'échec du développement de l'oeuf au stade larvaire (données sur la CE50) et la réduction de la croissance (phytoplanctons, macrophytes).
Pour calculer la VESEO, un coefficient de 100 a été appliqué aux données sur la toxicité basées sur les valeurs de la CL50 et de la CE50 , conformément aux directives énoncées dans le guide (Environnement Canada, 1997a); un coefficient de 10 a été utilisé pour les données de toxicité basées sur les valeurs de la CL25 et de la CE25.
L'évaluation de niveau 1 a révélé des quotients de risque supérieurs à un pour tous les taxons examinés. Une évaluation de niveau 2 a donc été faite pour tous ces taxons, en réduisant la VEE de 10 000 à 1 000 mg de chlorure/L. Le tableau 14 présente les résultats de l'évaluation de niveau 2 (si l'on tient compte des différences prévues dans les scénarios d'exposition, entre le niveau 1 et le niveau 2, tous les quotients de niveau 1 sont 10 fois supérieurs à ceux du niveau 2). Même en réduisant par un facteur de 10 les coefficients utilisés pour l'évaluation de niveau 2, la plupart des quotients demeurent supérieurs à un. On a donc effectué des évaluations de niveau 3 pour tous les groupes d'organismes examinés dans les évaluations de niveau 1 et de niveau 2.
3.3.3.3 Évaluations de niveau 3 avec validation sur le terrain
L'évaluation de niveau 3 consiste à examiner la distribution des expositions ou des effets (ou les deux) dans l'environnement (Environnement Canada, 1997a). C'est là une tâche considérable, étant donné la grande diversité des voies par lesquelles les sels de voirie peuvent s'introduire dans l'environnement canadien, que l'on pense au lixiviat s'écoulant des entrepôts de sels, au ruissellement (et éclaboussures) provenant des routes et des autoroutes et au transport de ces substances par l'intermédiaire des ruisseaux s'écoulant dans des écosystèmes aquatiques plus vastes, comme les terres humides, les rivières, les étangs et les lacs. Cette tâche est également complexe, car les plans d'eau varient considérablement quant à leur taille, à leur emplacement par rapport à une source potentielle de sels de voirie, à leur débit, etc.
Bien que des données sur les concentrations de chlorure soient recueillies dans le cadre des programmes réguliers de surveillance de la qualité de l'eau, la plupart de ces données n'ont pas fait l'objet d'une analyse rigoureuse quant à leur distribution spatiale et temporelle et aux facteurs de causalité. Donc, malgré la vaste recherche documentaire faite par Evans et Frick (2001), un nombre relativement faible d'études de cas ont été relevées, notamment sur l'environnement canadien. La situation pourrait toutefois commencer à changer, car les chercheurs et les organismes s'efforcent de mieux comprendre les effets des sels de voirie sur les concentrations de chlorure dans l'environnement.
L'évaluation de niveau 3 s'appuie sur des scénarios qui décrivent des situations diverses où les sels de voirie ont eu, ou pourraient avoir eu, des effets sur l'environnement aquatique au Canada. Cette démarche s'appuie sur les profils d'épandage des sels de voirie partout au Canada, les concentrations connues de chlorure dans l'environnement aquatique, les données de toxicité citées précédemment et les incidences environnementales rapportées ou les études de cas. Un grand nombre d'études de cas sont tirées d'ouvrages publiés aux États-Unis, où davantage d'études ont été réalisées; ces études sont néanmoins représentatives de l'usage au Canada.
3.3.3.3.1 Étude de cas no 1 : Effets du ruissellement des sels de voirie sur les ruisseaux, cours d'eau et petites rivières de régions urbaines densément peuplées
Sous l'effet de l'étalement urbain, les villes englobent un réseau de plus en plus vaste de ruisseaux, cours d'eau et rivières du paysage rural. À cela s'ajoute l'accroissement de la densité des routes à deux voies et, dans les villes plus grandes, la construction d'autoroutes à quatre voies et plus, qui ont pour effet de modifier sensiblement le bassin versant. Contrairement au milieu rural où une proportion appréciable du ruissellement peut être retenue relativement près des routes, la majeure partie du ruissellement, dans le paysage urbain largement recouvert d'asphalte, s'écoule de manière périodique dans les ruisseaux, cours d'eau et rivières. Le volume absolu de sels de voirie y est également plus élevé.
La région métropolitaine de Toronto nous offre l'exemple le plus manifeste de l'incidence d'un réseau routier de forte densité sur les nombreux ruisseaux, cours d'eau et, à la longue, rivières qui traversent cette région urbaine densément peuplée. À mesure qu'ils s'écoulent vers le sud en direction du lac Ontario, ces ruisseaux reçoivent de plus en plus de ruissellements urbains. Or comme nous l'avons mentionné précédemment, les concentrations de chlorure peuvent dépasser plusieurs centaines de milligrammes par litre durant la majeure partie de l'hiver, les concentrations maximales variant entre 1 000 et 4 000 mg/L. Les cours d'eau à fortes concentrations de chlorure incluent les ruisseaux Etobicoke, Mimico, Black et Highland. La rivière Don peut elle aussi présenter de fortes concentrations de chlorure durant la majeure partie de l'hiver.
Schroeder et Solomon (1998) ont effectué une étude rigoureuse des concentrations de chlorure et de la toxicité dans trois stations situées sur la rivière Don. De novembre 1995 à avril 1996, les concentrations de chlorure ont atteint environ 950 mg/L à la première station, jusqu'à 2 600 mg/L à la deuxième et 1 150 mg/L, à la troisième. Ces chercheurs ont également recueilli des données sur la toxicité aiguë (CL50 et CE50 ) pour treize taxons de poissons et sept d'invertébrés; ces valeurs ont varié de 1 000 à 30 000 mg/L. Ils ont ensuite appliqué les données cumulatives sur la toxicité aux données cumulatives sur la distribution du chlorure et estimé que 10 % des espèces seraient sensibles aux effets de la toxicité aiguë du chlorure, au moins 90 % du temps à deux des stations et au moins 85 % du temps, à la troisième.
Plusieurs études sur le terrain viennent corroborer l'hypothèse voulant que des concentrations de chlorure variant entre 500 et 1 000 mg/L peuvent avoir une incidence sur les écosystèmes des cours d'eau et des ruisseaux. Les paragraphes qui suivent résument certaines de ces études.
Williams et al. (1997) ont décelé des variations significatives dans la structure de la communauté des macroinvertébrés, liées à la fluctuation des concentrations de chlorure dans 20 sources alimentées par des eaux souterraines de la région métropolitaine de Toronto, dans le sud-est de l'Ontario. La teneur en chlorure de ces sources variait de 8,1 à 1 149 mg/L. La présence de tipules et de cératopogonidés a été associée aux sources à forte teneur en chlorure, tandis que les taxons comme Gammarus pseudolimnaeus (un amphipode) et les turbellariés (des plathelminthes) n'ont été observés que dans les sources à faible teneur en chlorure. Crowther et Hynes (1977) font état d'un taux de mortalité de 20 % dans une population d'essai de G. pseudolimnaeus exposée pendant une journée à une concentration de 4 121 mg de chlorure de sodium/L (2 500 mg de chlorure/L). Les concentrations plus élevées de chlorure dans certaines sources proviennent d'eaux souterraines apparemment contaminées par des sels de voirie.
Crowther et Hynes (1977) ont étudié expérimentalement les effets des concentrations de chlorure sur le déplacement des invertébrés benthiques dans le ruisseau Lutteral, un ruisseau à truites du sud de l'Ontario. Il s'agit d'un petit affluent de la rivière Speed, qui est alimenté par une source. Ils ont également étudié les concentrations de chlorure dans le ruisseau Laurel (débit annuel de 19 x 106 m3), un affluent de la rivière Grand qui traverse la région urbaine de Waterloo. Au moment de leur étude, la ville de Waterloo comptait 32 000 habitants. Les résultats de l'étude menée par Crowther et Hynes (1977) pourraient donc, dans l'ensemble, s'appliquer aux ruisseaux qui traversent les nombreuses petites villes des régions comme le sud de l'Ontario, le sud du Québec et les Maritimes, où l'on fait grand usage des sels de voirie. Les concentrations de chlorure dans le ruisseau Laurel ont varié d'une saison à l'autre, la concentration maximale (1 770 mg/L) ayant été mesurée durant une période de deux semaines entre le 5 janvier et le 6 février 1975.
En raison du taux élevé dans le ruisseau Laurel, une série d'expériences ont été réalisées dans le ruisseau Lutteral pour évaluer les effets de l'écoulement périodique d'eau chargée de chlorure de sodium, sur le déplacement des organismes benthiques. Pour cette étude, un segment de 15 m du ruisseau Lutteral a été divisé longitudinalement au moyen de feuilles d'acier ondulé, et le déplacement des organismes benthiques a été évalué des deux côtés de la séparation (zone témoin et zone d'analyse). Les faits saillants de cette étude sont présentés dans Evans et Frick (2001).
Crowther et Hynes (1977) concluent leur étude en notant que des effets sur le déplacement des organismes benthiques peuvent commencer à apparaître dans les cours d'eau lorsque le taux de chlorure se rapproche de 1 000 mg/L. Durant leur étude, ces chercheurs ont constaté que la plupart des effets devraient se produire durant l'hiver et au début du printemps. Ils ajoutent par ailleurs, que, comme les eaux souterraines continuent d'être contaminées par les sels de chlorure, il est possible que les cours d'eau soient contaminés par l'afflux d'eaux souterraines riches en chlorure durant les périodes d'étiage estivales.
Dickman et Gochnauer (1978) ont étudié les effets de l'exposition au chlorure de sodium sur la densité des bactéries et des algues dans le ruisseau Heyworth, près de Heyworth (Québec), entre le 24 juillet et le 1er octobre 1973. Du chlorure de sodium a été ajouté à un endroit le long du ruisseau, pour maintenir la concentration de chlorure à 1 000 mg/L (1 653 mg de chlorure de sodium/L). Cette concentration a été choisie pour simuler les effets des sels de voirie provenant des égouts pluviaux sur la microflore du plan d'eau récepteur. Cette concentration permet également de simuler les effets de concentrations élevées de chlorure dans des sources contaminées par des eaux souterraines. La concentration de chlorure de sodium au site témoin a varié de 2 à 3 mg/L. Le cours d'eau choisi pour l'étude est un ruisseau peu profond, densément ombragé et à débit rapide. Des substrats artificiels (tuiles) ont été placés dans le ruisseau, au site expérimental et à un site témoin en amont, et récupérés à intervalles d'une semaine. Le site traité a présenté une moins grande diversité d'algues et moins de cultures sur pied de périphytons ou d'algues photosynthétiques - un phénomène que l'on a attribué au stress osmotique. Au jour 28, on a observé la formation d'une auxospore (stade de repos) chez la diatomée Cocconeis placentula au site traité mais non au site témoin - l'auxospore est souvent déclenchée par une agression écologique. La densité des bactéries a également été plus élevée au site traité, un phénomène attribué à la réduction du broutage sur la population bactérienne, avec la diminution du nombre d'organismes brouteurs comme les flagellés, les ciliés et les rhizopodes. Enfin, l'incidence du parasitisme des diatomées a été plus faible dans le site traité qu'au site témoin, peut-être parce que le chlorure de sodium inhibe la croissance des champignons, comme l'ont indiqué d'autres chercheurs (Kszos et al., 1990; Rantamaki et al., 1992).
D'autres études ont porté sur les effets de la salinité sur la structure des communautés benthique et algale. Même si l'usage de sels de voirie n'était pas en cause dans ces études, celles-ci viennent néanmoins corroborer l'hypothèse voulant que la composition taxinomique des cours d'eau est sensible à la salinité, cette composition variant à mesure que la salinité se rapproche de 1 000 mg de chlorure/L.
Leland et Fend (1998) ont étudié la distribution des organismes benthiques dans la vallée de la rivière San Joaquin, en Californie, où les concentrations de matières totales dissoutes ont varié de 55 à 1 700 mg/L. Il y ont observé des assemblages différents selon que la salinité était faible ou élevée. Par ailleurs, la distribution de nombreux taxons indique des valeurs optimales de salinité, les éphéméroptères (larves d'éphémères), par exemple, étant rares à une salinité supérieure à 1 000 mg/L (600 mg de chlorure/L). Bien que ces effets aient pu être causés par d'autres facteurs, les auteurs notent que les profils observés n'étaient pas liés à la distribution des pesticides, ni au débit d'eau ou au régime d'irrigation.
Short et al. (1991) ont étudié les invertébrés benthiques dans un cours d'eau du Kentucky exposé à l'écoulement de chlorure provenant d'un champ de pétrole situé à proximité. Les éphéméroptères ont été le groupe le moins tolérant aux taux élevés de chlorure de sodium, ces organismes étant absents des régions d'une salinité supérieure à 2 000 mg de chlorure/L. Les poissons ont semblé mieux tolérer ces salinités élevées.
Enfin, Blinn et al. (1981) ont analysé la dynamique saisonnière des phytoplanctons à trois endroits le long du ruisseau Chevelon, en Arizona. Au premier endroit, la concentration de chlorure était de 88 mg/L au débit de base et elle a atteint de 900 à 1 100 mg/L au troisième endroit, situé à 10,8 km en aval du premier site et à 3,5 km en aval du deuxième (la concentration de chlorure au deuxième site n'est pas précisée). La forte concentration de chlorure au site 3 a été attribuée aux nombreuses infiltrations et sources provenant de la paroi du canyon. Des différences notables ont été observées entre les trois sites quant à la composition des phytoplanctons, les espèces présentes variant selon la fluctuation de la salinité.
Dans l'ensemble, ces études portent à croire que l'exposition continue à des concentrations de chlorure aussi faibles que 1 000 mg/L (1 653 mg de chlorure de sodium/L), pendant des périodes d'aussi peu qu'une semaine, peut provoquer des changements dans les communautés périphytoniques et benthiques d'un cours d'eau. De plus, si ces expositions persistent, la composition des communautés demeure différente de ce qu'elle est aux sites de salinité plus faible, situés en amont et en aval. Plusieurs cours d'eau et étangs, adjacents à des routes et fortement contaminés par le chlorure, ont été décelés dans la région métropolitaine de Toronto et les municipalités avoisinantes et il faut s'attendre à ce que le nombre de cours d'eau et de ruisseaux ainsi contaminés augmente avec la croissance démographique dans le sud de l'Ontario. On peut aussi observer des cours d'eau contaminés par le chlorure dans d'autres régions similaires où la densité du réseau routier est élevée et l'épandage de sels est abondant, au Québec et ailleurs. L'exposition continue (à long terme) au chlorure risque principalement de se produire dans les zones là où il y a infiltration provenant d'entrepôts de sels de voirie ou de sources contaminées par des eaux souterraines. Les données semblent indiquer que l'écoulement périodique d'eau chargée de chlorure de sodium, au moment de la fonte printanière, aura des effets marqués sur les communautés vivant dans les cours d'eau, tout comme le rejet continu de fortes concentrations de chlorure de sodium à partir des berges, durant l'été et l'automne. Dans bon nombre de ruisseaux, les périphytons forment la base du réseau trophique et servent d'alimentation aux invertébrés, eux-mêmes source d'alimentation des poissons. La réduction de la biomasse fongique, provoquée par l'accroissement de la concentration de chlorure de sodium, pourrait avoir une incidence sur les communautés d'invertébrés, de poissons proie et, en fin de compte, de poissons prédateurs.
3.3.3.3.2 Étude de cas no 2 : Effets du ruissellement des sels de voirie sur les ruisseaux, cours d'eau et rivières de régions moins densément peuplées
Des concentrations de chlorure sensiblement moins élevées ont été observées dans des ruisseaux de régions moins densément peuplées, traversées d'un réseau routier de moindre densité. Ces concentrations peu élevées, qui ne sont parfois que de 10 à 100 mg/L supérieures aux concentrations de fond, peuvent être attribuables à bon nombre d'activités humaines. Dans le bassin de la rivière Waterford (Terre-Neuve), par exemple, la concentration de chlorure a atteint en moyenne 70 mg/L à la station Donovans (située dans un parc industriel), alors qu'elle n'était que de 17 mg/L dans une région sans activité industrielle connue (Arsenault et al., 1985). Les concentrations élevées mesurées à la station Donovans ont été attribuées non seulement à l'activité industrielle, mais également à l'épandage de sels et à la contamination provenant de deux entrepôts de sels. Malheureusement, aucune étude n'a cherché précisément à étudier les concentrations de chlorure immédiatement après l'épandage de sels et la fonte des neiges.
De même, plusieurs études réalisées aux États-Unis font état de faibles concentrations de chlorure. Une étude montre comment des cours d'eau, dans l'ensemble peu perturbés, peuvent être exposés à des écoulements périodiques contenant des concentrations relativement élevées de chlorure. Boucher (1982) a étudié les effets du ruissellement des sels de voirie sur le ruisseau Penjajawoc, dans le Maine. Entre 1979 et 1982, les concentrations de chlorure en amont d'une zone commerciale ont varié en moyenne de 5 à 15 mg/L; à l'intérieur de cette zone, les concentrations ont été en moyenne de 10 à 50 mg/L, mais elles ont atteint 621 mg/L durant un épisode de ruissellement. D'autres études ont établi un lien entre l'épandage de sels de voirie et l'accroissement des concentrations de chlorure, lesquelles ont fluctué entre 10 et 150 mg/L dans de petits cours d'eau urbains et ruraux (Cherkauer et Ostenso, 1976; Gosz, 1977; Hoffman et al., 1981; Smith et Kaster, 1983; Prowse, 1987; August et Graupensperger, 1989; Demers et Sage, 1990; Mattson et Godfrey, 1994; Herlighy et al., 1998). Bien qu'il soit possible que d'autres facteurs aient également contribué à la hausse des concentrations moyennes de chlorure dans ces cours d'eau, les études ayant pour but d'évaluer les effets de la fonte des neiges sur les concentrations de chlorure ont nettement démontré une hausse périodique (Prowse, 1987). Prowse (1987) et Mattson et Godfrey (1994) ont en outre établi un lien entre, d'une part, la concentration de chlorure dans les cours d'eau et, d'autre part, la densité et la longueur du réseau routier dont les eaux de ruissellement s'écoulent directement dans ces cours d'eau (p. ex., lorsque la route longe un plan d'eau).
On ne connaît toutefois pas avec certitude l'impact de hausses relativement faibles de la concentration de chlorure sur les communautés vivant dans les cours d'eau et les ruisseaux, ni de hausses plus élevées sur une courte période (de quelques heures à quelques jours).
Demers (1992) a étudié les effets des taux élevés de chlorure sur les macro-invertébrés aquatiques, dans quatre cours d'eau situés près de la ville de Newcomb dans la région des Adirondacks, dans le nord de l'État de New York. Ces quatre cours d'eau longent un tronçon de deux kilomètres d'une autoroute nationale. Selon des mesures effectuées chaque semaine, la concentration moyenne de chlorure a varié de 0,61 mg/L en amont à 5,23 mg/L, en aval. Des substrats artificiels ont été placés dans des sections à débit rapide des ruisseaux, en amont et en aval de l'autoroute. Les dispositifs d'échantillonnage ont été placés à une distance de 50 à 100 m de la route et laissés en place du 22 avril au 3 juin 1988, auquel moment ils ont été récupérés pour caractériser les invertébrés colonisateurs de ces eaux. On a alors constaté que la diversité benthique était plus faible en aval qu'en amont. On a en outre observé une augmentation des moucherons en aval, mais une diminution des perlodidés (une famille de perles) et des Ephemerillidae (une famille d'éphémères communes) en aval. De même, une augmentation des moucherons et une diminution de la dominance des éphémères communes et des perles ont été observées dans la rivière Humber (Ontario), entre le mois de novembre alors qu'aucun sel n'avait encore été épandu et le mois de mars suivant, après l'épandage de sels de voirie (Kersey et Mackay, 1981).
D'autres études font état de variations dans les communautés benthiques, en amont et en aval d'autoroutes, fluctuations qui ont toutefois été attribuées à des différences plus marquées dans le régime d'écoulement, la charge de sédiments en suspension, l'habitat ou les contaminants inorganiques et organiques présents (Molles et Gosz, 1980; Kersey et Mackay, 1981; Smith et Kaster, 1983; Maltby et al., 1995). En l'absence d'études sur le terrain rigoureuses, il demeure impossible de déterminer avec certitude les effets de faibles hausses des concentrations de chlorure sur les écosystèmes des cours d'eau, des ruisseaux et des rivières. Cependant, une augmentation de la concentration moyenne de chlorure, d'environ 3 mg/L (moyenne mondiale pour les rivières) à 30 à 300 mg/L, pourrait avoir une incidence sur la succession des espèces dont les valeurs optimales de salinité diffèrent. De fait, des études paléolimnologiques récentes révèlent que la salinité optimale varie selon l'espèce d'algues et permettent de déduire les fluctuations de la salinité des lacs à partir des changements à long terme dans les communautés d'algues (Dixit et al., 1999).
Certains chercheurs commencent à s'intéresser au rôle de la chimie de l'eau dans la détermination de la structure des communautés des rivières. Rott et al. (1998), par exemple, ont étudié les assemblages de périphytons dans la rivière Grand, en Ontario, où la concentration de chlorure variait de 7,7 à 85,0 mg/L et la conductivité, de 180 à 540 µS/cm. Selon une analyse de corrélation canonique, la variabilité dans la composition des espèces ayant peuplé la rivière durant la période à l'étude pourrait s'expliquer en majeure partie par un gradient saisonnier lié à la température, ainsi que par les gradients latitudinaux dans les taux de nitrite et nitrate, la conductivité et la concentration de chlorure. La concentration de phosphore et d'ammoniac, le pH, la turbidité et le taux d'oxygène ont eu une importance moindre.
Chetelat et al. (1999) ont étudié la biomasse des périphytons et la composition des communautés de 13 rivières du sud de l'Ontario, dans lesquelles la concentration en éléments nutritifs et la conductivité différaient. Ils notent une forte corrélation entre la biomasse et le phosphore total (r2 = 0,56) et une corrélation encore plus grande avec la conductivité (r2 = 0,71). Ces auteurs attribuent la prédominance des cladophores, aux endroits de forte conductivité, aux concentrations plus élevées de calcium. Par ailleurs, des différences notables ont été observées au niveau de la composition des espèces, entre les endroits de faible conductivité et de conductivité élevée, laquelle a varié de 65 à 190 µS/cm.
On ne sait pas avec certitude si les phénomènes observés dans les communautés de périphytons sont en réaction directe au chlorure ou si le chlorure est un indicateur d'autres perturbations dans le bassin versant. Cependant, à la lumière d'études plus récentes sur la composition des communautés d'algues dans les lacs (p. ex., Dixit et al., 1999), il est probable qu'une partie au moins des réactions observées résultent directement des faibles différences dans les concentrations de sels.
3.3.3.3.3 Étude de cas no 3 : Effets du ruissellement des sels de voirie sur les étangs et les lacs en milieux urbains
Les étangs et les lacs diffèrent des ruisseaux, des cours d'eau et des rivières, sous trois aspects principaux. Premièrement, la vitesse d'écoulement de l'eau dans les étangs et les lacs ne présente pas les fortes fluctuations saisonnières qui sont caractéristiques des cours d'eau, des ruisseaux et des rivières. Deuxièmement, l'eau séjourne plus longtemps dans les étang et les lacs, le temps de séjour variant de quelques semaines à des années. Enfin, l'eau qui alimente les étangs et les lacs provient d'une variété de sources, de sorte que la capacité de dilution des contaminants peut y être plus grande que dans les ruisseaux et cours d'eau situés à proximité de sources de contamination similaires. Donc, la concentration de chlorure a tendance à être sensiblement moins élevée dans les étangs contaminés par des sels de voirie, même si la durée d'exposition y est en général beaucoup plus longue. Le degré de contamination dépend également du niveau de dilution possible, les plans d'eau plus vastes ayant en général une plus grande capacité de dilution.
L'effet des sels de voirie sur la concentration de chlorure dans les étangs et les lacs urbains varie considérablement. En général, toutefois, les impacts sur l'environnement au Canada ont été modestes, l'accroissement de la concentration de chlorure étant de l'ordre de dizaines à des centaines de milligrammes par litre et non de milliers de milligrammes par litre, comme on l'a constaté dans des ruisseaux de la région métropolitaine de Toronto.
À Terre-Neuve, Arsenault et al. (1985) ont étudié les concentrations de chlorure dans cinq étangs du bassin de la rivière Waterford et observé des concentrations moyennes variant de 6 à 24 mg de chlorure/L, les valeurs plus élevées étant associées au ruissellement routier et peut-être aussi au ruissellement s'écoulant d'un entrepôt de sels.
À Halifax, des hausses saisonnières des concentrations de chlorure ont été observées dans les premier et deuxième lacs Chain, ces augmentations étant apparemment liées à l'épandage de sels. À cet endroit, les concentrations de chlorure ont augmenté à partir du début des années 1980 pour atteindre un sommet (120 à 170 mg/L) au milieu des années 1980. Ces deux lacs, peu profonds (profondeur moyenne de 4,1 et 3,2 m respectivement), sont situés à l'intérieur d'un vaste bassin urbain. Plus récemment, Keizer et al. (1993) ont étudié la qualité de l'eau de 51 lacs de la région métropolitaine de Halifax-Dartmouth, en comparant les données recueillies en avril 1991 à celles d'avril 1980. Le changement le plus marqué se situe au niveau de la conductivité laquelle a presque doublé, la hausse étant due en majeure partie à un accroissement des concentrations de sodium et de chlorure. De fait, alors que seulement trois lacs présentaient une concentration de chlorure supérieure à 100 mg/L en 1980, 12 avaient une concentration supérieure à 100 mg/L en 1991 et la concentration a atteint 197 mg/L dans un de ces lacs.
Dans le sud-est de l'Ontario, il semble que le lac Little Round soit devenu méromictique (ou encore plus méromictique) durant les années 1950, par suite de l'introduction de sels de voirie provenant des eaux de ruissellement de deux autoroutes et des eaux d'infiltration d'un entrepôt de sels (Smol et al., 1983). Au début des années 1970, la concentration de chlorure dans le monimolimnion était de 104 mg/L; ces conditions méromictiques ont entraîné une diminution de l'échange saisonnier des éléments nutritifs entre les eaux profondes et les eaux de surface, ainsi qu'une réduction de la productivité du lac et des modifications dans la structure des communautés d'algues.
En Ontario, une étude en cours fait état d'une élévation de la concentration de chlorure dans des étangs situés à proximité d'autoroutes. La concentration de chlorure dans les étangs situés à moins de 10 m d'autoroutes à deux voies est en moyenne de 88 mg/L (5 à 150 mg/L), mais atteint 970 mg/L (84 à 2 630 mg/L) à proximité d'autoroutes à quatre voies (Watson, 2000). Des concentrations de chlorure toujours élevées ont été observées à 50 m de l'autoroute, les concentrations s'établissant en moyenne à 115 mg/L (35 à 368 mg/L) à proximité d'autoroutes à deux voies et à 1 219 mg/L (50 à 3 950 mg/L) pour les autoroutes à quatre voies. Free et Mulamoottil (1983) rapportent des concentrations de chlorure atteignant 282 mg/L dans le lac Wabekayne, un bassin de retenue des eaux pluviales situé à Mississauga.
Des données inédites du ministère des Transports de l'Ontario indiquent la concentration moyenne (mai à octobre 1995) de chlorure dans huit plans d'eau du bassin versant de la rivière Humber (Scanton, 1999) : ces concentrations s'établissent en moyenne à 10,6 mg/L au lac St. George, à 26,8 mg/L au lac Preston, à 47,0 mg/L au lac Wilcox, à 60,8 mg/L au lac Heart, à 107,9 mg/L au réservoir Claireville, à 110,3 mg/L au barrage G. Ross Lord, à 174,0 mg/L au lac Aquitanne et à 408,9 mg/L à l'étang Grenedier. La rivière Humber, comme le ruisseau Highland, est un important bassin hydrographique urbain. Il se pourrait que l'épandage de sels de voirie ait une incidence sur le bassin de la rivière Humber, comme on l'a constaté pour le bassin du ruisseau Highland (Howard et Haynes, 1997).
Des études américaines font état de hausses plus marquées des concentrations de chlorure dans des étangs et des ruisseaux de régions urbaines. Cherkauer et Ostenso (1976), par exemple, notent que les lacs Northridge à Milwaukee (Wisconsin) ont été perturbés par des concentrations élevées de chlorure durant les périodes de gel hivernal. Il s'agit de lacs artificiels peu profonds (9,2 m) qui sont reliés entre eux -les concentrations de chlorure y ont atteint 2 500 mg/L. La baie Irondequoit, un petit enfoncement situé sur la rive sud du lac Ontario, offre un autre exemple probant. Cette baie, d'une profondeur modérée (profondeur maximale de 23,8 m et profondeur moyenne de 6,8 m), est entourée d'un réseau routier de forte densité. Les concentrations de chlorure dans cette baie ont commencé à augmenter durant les années 1940 et la hausse s'est poursuivie jusqu'au début des années 1970. Les concentrations de chlorure dans les eaux profondes ont atteint plus de 400 mg/L, ce qui a freiné le mélange vertical de la colonne d'eau (Bubeck et al., 1971). Des mesures correctrices ont été apportées et, au début des années 1980, les concentrations maximales de chlorure à Ides Cove, à l'intérieur de la baie, avaient diminué entre 140 et 150 mg/L et le mélange vertical de l'eau s'était amélioré (Bubeck et al., 1995).
À Ann Arbor (Michigan), le lac Fonda a été fortement perturbé par le ruissellement routier entrant dans le lac par l'intermédiaire de deux canalisations d'évacuation. Au milieu des années 1960, les concentrations de chlorure ont atteint 177 mg/L et le mélange vertical des eaux a été perturbé (Judd, 1969). C'est ainsi que la ville a décidé de réduire l'épandage de sels dans la subdivision et de détourner le ruissellement. Les concentrations de chlorure ont toutefois continué d'augmenter sous l'effet d'un apport accru dû au plus grand nombre de routes et elles ont atteint 720 mg/L en eaux profondes (Judd et Stegall, 1982). Cependant, comme les sels dans le lac provenaient maintenant de sources diffuses, et non plus des deux canalisations d'évacuation, les sels se sont mêlés plus efficacement dans le lac et le mélange vertical n'a pas été perturbé.
Comme nous l'avons mentionné précédemment, peu d'études biologiques sont venues compléter ces études sur les étangs et les lacs en milieux urbains. Outre Smol et al. (1983), Free et Mulamoottil (1983) ont remarqué une diminution de la densité des invertébrés benthiques lorsque les eaux de fond deviennent anoxiques. Si l'on se fie aux estimations de la toxicité chronique, on peut s'attendre à ce que le chlorure ait des effets directs sur des espèces particulières, à des concentrations d'à peine 200 mg/L. Par ailleurs, des études récentes sur les phytoplanctons semblent indiquer que des effets pourraient survenir à des doses encore plus faibles, du moins chez les algues. C'est là l'objet de la prochaine section.
3.3.3.3.4 Étude de cas no 4 : Effets du ruissellement routier sur les lacs et étangs en milieux ruraux
Une augmentation de la concentration de chlorure imputable aux sels de voirie a aussi été observée dans des étangs et des lacs de régions rurales, la hausse étant ici aussi, comme en milieux urbains, liée à la taille de l'étang ou du lac et à la proximité du réseau routier.
Dans le parc national Terra-Nova, à Terre-Neuve, la concentration de chlorure dans l'étang Pine Hill a presque septuplé au printemps, passant d'une moyenne de 14 mg/L en décembre 1969 à 94 mg/L en avril (Kerekes, 1974); cette hausse a été associée à l'épandage de sels de voirie.
Underwood et al. (1986) ont étudié 234 lacs de la Nouvelle-Écosse, dans lesquels la concentration de fond de chlorure était de 8,1 mg/L et la concentration maximale a atteint 28,1 mg/L. Selon le ministère de l'Environnement de la Nouvelle-Écosse (Briggins et al., 1989), les concentrations de chlorure supérieures à 25 mg/L dans les plans d'eau sont dues à l'apport de chlorure de sources anthropiques. Or dans les bassins versants traversés de nombreuses autoroutes, les sels de voirie constitueraient la source probable de contamination.
Le ministère des Transports du Québec (1980, 1999) a étudié les effets des sels de voirie sur le lac à la Truite, situé près de l'autoroute 15 et de Sainte-Agathe-des-Monts. Le bassin versant de ce lac, d'une superficie estimée de 728 ha, est exposé à un tronçon de 7 km de l'autoroute, d'une déclivité maximale de 5 %. Ce lac, d'une superficie de 48,6 ha et d'une profondeur moyenne de 21,5 m, a un volume estimé de 486 000 m3. En 1972, la concentration moyenne de chlorure dans le lac était de 12 mg/L; cette concentration a augmenté tout au long des années 1970 pour atteindre 150 mg/L en 1979, ce qui correspond à l'ajout de quelque 67 068 kg de sels dans le lac. La quantité de sels épandus sur la route a donc été réduite et les concentrations de chlorure ont diminué tout au long des années 1980 pour atteindre 45 mg/L en 1990. Malgré cette baisse, les concentrations sont demeurées élevées, s'établissant à 42 mg/L à 3 m et à 49 mg/L, à 10 m.
Aux États-Unis, comme au Canada, des données de plus en plus abondantes font état d'un accroissement des taux de chlorure dans les lacs, ces hausses étant reliées, du moins en partie, à l'épandage des sels de voirie.
Plusieurs études réalisées aux États-Unis fournissent des données sur les effets probables des sels de voirie sur les lacs et les étangs en milieux ruraux, qui peuvent s'appliquer à l'environnement canadien. Ainsi, Hanes et al. (1970) discutent des effets des sels de voirie sur une variété d'écosystèmes aquatiques du Maine et notent que les étangs agricoles situés à proximité d'autoroutes présentent des concentrations de sodium variant de 1,4 à 115 mg/L et des concentrations de chlorure de <1 à 210 mg/L. De plus, les concentrations de sels ont été plus élevées en avril 1966 qu'en juillet 1965. En 1967, des concentrations de chlorure fluctuant entre 1,4 et 221 mg/L ont été mesurées, ceci laissant croire à une augmentation des taux de chlorure.
Une augmentation de la concentration de chlorure, attribuable à une contamination par les eaux souterraines chargées de sels de voirie, a aussi été observée dans le lac Sparkling situé dans le nord du district du lac Wisconsin (Bowser, 1992); la morphométrie du lac Sparkling n'a toutefois pas été précisée. Au départ, des sels de voirie avaient été appliqués sur les routes en amont du lac, et il semble que les sels se soient d'abord infiltrés dans les eaux souterraines, avant d'entrer dans le lac. Dans les lacs et les eaux souterraines non perturbés de la région, les concentrations de chlorure étaient de 0,3 à 0,5 mg/L, comparativement à 2,61 mg/L en 1982 et 3,68 mg/L en 1991, dans le lac Sparkling. Bowser (1982) a calculé qu'une charge de chlorure de 1 200 kg par année avait été nécessaire pour provoquer une telle élévation de la concentration de chlorure entre 1982 et 1991.
Eilers et Selle (1991) ont comparé les données sur la conductivité, l'alcalinité, le calcium et le pH de 149 lacs du nord du Wisconsin, qui avaient été recueillies entre 1925 et 1931, aux données obtenues entre 1973 et 1983; ils ont constaté que la valeur de tous les paramètres avait augmenté entre ces deux périodes, les plus fortes hausses étant associées à l'exploitation plus intensive des sols le long du littoral des lacs. Ainsi, la conductivité moyenne est passée de 31,5 µS/cm en 1925 à 44,3 µS/cm en 1983 dans les bassins versants aménagés, et de 14,3 µS/cm en 1925 à 14,7 mS/cm en 1983 dans les bassins non exploités. Cette hausse de la conductivité semble être associée à un ensemble de facteurs, y compris à l'épandage de sels de voirie, à l'eutrophisation due aux cultures ainsi qu'à des changements hydrologiques. Les hausses les plus marquées ont par ailleurs été observées dans les lacs situés à proximité d'autoroutes ou de routes asphaltées.
Aucune de ces études n'a examiné l'impact d'une faible augmentation de la concentration de chlorure provenant des sels de voirie sur les lacs et les étangs. Cependant, comme l'accroissement de la concentration de chlorures (et autres sels) était habituellement jugé préoccupant (Beeton, 1969; Pringle et al., 1981), des mesures ont été prises pour protéger les milieux aquatiques contre l'élévation des concentrations de sels.
Il est probable que de légères hausses des concentrations de chlorure influeront surtout sur la composition et la productivité des espèces. Des données nouvelles indiquent en effet que les microorganismes comme les champignons, les planctons et les macroinvertébrés ont des valeurs de salinité optimales. Il faut donc s'attendre à ce que des fluctuations de la salinité, qui modifient l'équilibre compétitif entre les espèces, entraînent des modifications dans la composition des espèces formant la base du réseau trophique. La productivité pourrait également augmenter. Evans et Frick (2001) se sont penchés sur cette question, en examinant les données sur les effets de la salinité et de la conductivité sur les écosystèmes dulcicoles en général.
L'introduction de sels de voirie dans les milieux aquatiques peut accroître la productivité de diverses manières. Les sels de voirie contiennent en effet des éléments nutritifs à l'état de traces, notamment du phosphore (14 à 26 mg/kg) et de l'azote (7 à 4 200 mg/kg); donc l'ajout de 100 mg de sels de chlorure/L pourrait entraîner une hausse de la concentration de phosphore de l'ordre de 1,4 à 2,6 µg/L et une augmentation de la concentration d'azote de 0,7 à 420 µg/L. Des métaux comme le cuivre et le zinc sont également des éléments essentiels et l'ajout de ces métaux dans les écosystèmes aquatiques pourrait accroître la productivité. Les écosystèmes à faible productivité seraient les plus sensibles à une eutrophisation stimulée par les sels de voirie. Des études paléolimnologiques dans les Grands Lacs font état d'un accroissement de la productivité dans la Baie de Quinte dès la fin des années 1600, cette hausse ayant été associée au défrichage et à l'apport accru en éléments nutritifs (et métaux en traces) provenant du bassin versant (Schelske et al., 1983, 1985; Stoermer et al., 1985).
Des études limnologiques plus récentes ont examiné la structure des communautés dans une grande variété de lacs, en fonction d'un certain nombre de variables limnologiques, comme la conductivité, la concentration en éléments nutritifs et les ions principaux. Ces
études ont été brièvement examinées aux fins de la présente évaluation, pour déterminer si elles contenaient des données additionnelles sur les réactions des organismes aquatiques à de faibles gradients de salinité, outre les réactions prévues aux fluctuations de la concentration de phosphore. Comme ces études ont été réalisées dans des lacs d'eau douce, la conductivité a varié principalement en fonction des carbonates de calcium. Voici ce qui en ressort.
Dixit et al. (1999) ont évalué les changements dans la qualité de l'eau dans le nord-est des États-Unis en se basant, comme indicateur de changement, sur les diatomées déposées dans les sédiments des lacs. Un lien a été établi entre la composition des diatomées dans les sédiments de surface et les paramètres actuels de qualité de l'eau, notamment le pH, la concentration de chlorure et la concentration de phosphore total. Les valeurs optimales du phosphore total et du chlorure ont été déterminées pour 235 espèces communes (tableau 15). Des modèles mathématiques ont ensuite été conçus pour prévoir le pH, la concentration de chlorure ou la concentration de phosphore total dans les lacs à l'étude, d'après l'assemblage de diatomées (et non de taxons individuels) dans les sédiments de surface. Puis des carottes ont été prélevées pour examiner l'assemblage de diatomées dans les sédiments à une profondeur de 30 cm et déterminer si la qualité de l'eau avait changé depuis la période ayant précédé les années 1850. Une détérioration appréciable de la qualité de l'eau a été observée dans des centaines de lacs, où les concentrations de phosphore et de chlorure sont nettement plus élevées aujourd'hui qu'elles ne l'étaient avant l'ère industrielle. On a aussi noté une hausse sensible du nombre de lacs eutrophes dans la région des terres basses et des plateaux côtiers; cet accroissement de l'état trophique des lacs a été associé à une augmentation, non seulement des concentrations de phosphore, mais aussi des concentrations d'ions chlorure. Dans ces lacs, une forte corrélation a été observée entre les concentrations de sodium et de chlorure, ce qui laisse croire à un lien entre l'accroissement de la concentration de chlorure et l'épandage de sels de voirie. Cependant, il a également été reconnu que l'agriculture, la sylviculture et l'urbanisation peuvent accroître la concentration de chlorure.
D'autres recherches, basées sur des études paléolimnologiques plus détaillées, permettront d'éclaircir ces questions. On peut toutefois déjà affirmer que les diatomées ont des concentrations optimales de chlorure et que tout écart par rapport à ces concentrations s'accompagne de changements dans la composition des espèces. Pareil phénomène doit aussi se produire pour d'autres organismes, comme d'autres groupes d'algues, des végétaux, des invertébrés benthiques et des zooplanctons.
Bien que peu nombreuses, les études portent fortement à croire qu'une faible augmentation de la concentration de chlorure entraînera des modifications dans la composition des communautés de phytoplanctons des étangs et des lacs. Il est en outre très probable que les stocks actuels de végétaux et d'animaux seront touchés. Enfin, la productivité augmentera probablement sous l'effet d'un apport accru de phosphore, d'azote et d'éléments traces.
.3.3.3.3.5 Étude de cas no 5 : Lieux d'entreposage de sels et écosystèmes aquatiques
On ignore le nombre exact d'entrepôts de sels de voirie au Canada. Morin et Perchanok (2000) ont estimé qu'il y avait plus de 1 300 entrepôts provinciaux, auxquels s'ajoutent un nombre inconnu d'entrepôts municipaux et privés. Snodgrass et Morin (2000) notent quant à eux que la conception de ces entrepôts varie considérablement, d'une région à l'autre du pays. Ainsi, certains sont bien conçus et le lessivage de sels durant l'hiver y est minime. D'autres, par contre, sont de piètre conception et les pertes de sels par lessivage peuvent atteindre 22 % et même davantage; les concentrations de sels dans ce lixiviat peuvent dépasser 80 000 mg/L (voir la section 2.4). Selon des études réalisées en Ontario par le ministère provincial des Transports (MTO, 1997), la concentration de sels a dépassé 500 mg/L dans l'eau de puits de 26 % des entrepôts de sels. Une autre étude a révélé que 69 % des échantillons d'eaux souterraines peu profondes avaient des concentrations de chlorure supérieures à 250 mg/L. Même si le lixiviat finit par être dilué dans le plan d'eau récepteur, les milieux aquatiques qui se trouvent dans la trajectoire de dilution peuvent subir des dommages considérables, un phénomène particulièrement préoccupant pour les terres humides et les petits cours d'eau, comme l'ont constaté Dickman et Gochnauer (1978). De plus, même après avoir été diluées, les concentrations de chlorure peuvent demeurer suffisamment élevées pour créer des conditions méromictiques dans les petits lacs ou accroître sensiblement leur salinité (ou les deux).
Les entrepôts de sels mal conçus ou mal entretenus constituent manifestement une menace pour l'environnement canadien. Une brève exposition (de quelques heures à quelques jours) au lixiviat non dilué se situe en effet dans l'intervalle de toxicité pour une variété d'organismes aquatiques. Et, dans les plans d'eau où l'eau salée s'accumule durant de longues périodes, comme les tourbières, les espèces végétales sensibles peuvent être détruites et remplacées par des espèces qui tolèrent mieux le sel (Wilcox, 1982). Dans un lac, l'écoulement d'eau salée peut perturber la circulation normale de la colonne d'eau et causer une plus grande stratification du lac. Des hausses relativement faibles de la salinité, même à des niveaux de 200 à 300 mg de chlorure/L, se situent dans l'intervalle de toxicité chronique d'un certain nombre d'organismes aquatiques.
Certaines études expliquent les concentrations de chlorure observées dans l'environnement canadien par la présence d'entrepôts de sels de voirie. Ainsi, Arsenault et al. (1985) ont établi un lien entre une faible augmentation de la concentration de chlorure à la station Donovans, sur la rivière Waterford (Terre-Neuve), et la proximité d'un entrepôt de sels et peut-être aussi l'épandage de sels de voirie. Arp (2001) (section 3.4.1.2) fait lui aussi état de concentrations élevées de sodium et de chlorure dans l'eau de ruisseaux et de fossés situés en aval d'un entrepôt de sels, les concentrations de chlorure les plus élevées ayant été observées durant l'été. Dans le sud-est de l'Ontario, Smol et al. (1983) ont procédé à une étude paléolimnologique du lac Little Round et noté que ce lac avait été oligotrophe avant l'arrivée des Européens, au milieu des années 1800. Cependant, avec l'intensification de l'exploitation forestière dans le bassin, le lac est devenu eutrophe, sans doute en raison de l'apport accru d'éléments nutritifs et de minéraux associé à la perturbation du sol. Une ligne de chemin de fer et deux autoroutes ont par la suite été construites à proximité du lac. Le lac est redevenu oligotrophe vers la fin des années 1960, sous l'effet, semble-t-il, des conditions méromictiques. Au début des années 1970, la concentration de chlorure en eau profonde a atteint 104 mg/L, dépassant alors largement le niveau de fond. Ces conditions méromictiques ont empêché les éléments nutritifs régénérés dans la couche profonde du lac de se mêler aux eaux de surface. Les concentrations élevées de chlorure (et les conditions méromictiques) ont été associées aux eaux de ruissellement routier et aux eaux d'infiltration provenant d'un entrepôt de sels. Malheureusement, très peu d'études ont été réalisées à proximité d'entrepôts de sels au Canada, même s'il en existe plus d'un millier au Canada et que, de toute évidence, bon nombre de ces installations contribuent à la contamination par le chlorure des eaux souterraines et de l'eau de puits.
Un plus grand nombre d'études limnologiques ont été réalisées à proximité d'entrepôts de sels aux États-Unis. Ces études ont révélé divers impacts laissant croire que la gestion de ces installations constitue une source de préoccupation environnementale. Les résultats de ces études ont de vastes applications pour l'environnement canadien, en particulier dans le cas des entrepôts de sels mal entretenus (selon qu'ils sont couverts et munis d'une plaque d'asphalte) et où la gestion des eaux de lavage ne se fait pas selon les meilleures pratiques.
Wilcox (1982) a étudié les effets de la contamination par le chlorure de sodium, imputable à la présence d'un dépôt de sels de voirie dans le marais Pinhook, en Indiana. En 1963, un dépôt non couvert de chlorure de sodium avait été aménagé à proximité du marais. Les eaux de ruissellement chargées de sels s'écoulant de l'entrepôt ont provoqué des changements en profondeur dans la végétation du marais à l'intérieur d'une zone de 2 ha, similaires à ceux produits par le ruissellement routier. L'amoncellement de sels a été recouvert en 1972 et les sels de voirie ont cessé d'être entreposés à cet endroit, après l'hiver 1980-1981. Les impacts ont été étudiés entre 1979 et 1983. Des concentrations de sodium atteignant 468 mg/L et des concentrations de chlorure de 1 215 mg/L ont été mesurées dans l'eau interstitielle du lit du marais, là où l'incidence des sels de voirie a été la plus forte (Wilcox, 1982,). Ces mesures ont été prises en 1979; il est donc possible que les concentrations aient été plus élevées durant les années précédentes. En 1980 et 1981, les concentrations de chlorure aux sites témoins ont varié de 5 à 6 mg/L. La concentration quotidienne maximale de chlorure qui a été mesurée aux endroits exposés aux sels a été de 1 468 mg/L en 1979, de 982 mg/L en 1980, de 570 mg/L en 1981 et de 610 mg/L en 1983. Ces données indiquent que la fermeture de cet entrepôt a entraîné une diminution des charges et des concentrations dans le marais; cependant, une grande partie du chlorure a par la suite été retenue dans cette terre humide.
Les espèces indigènes, comme Sphagnum spp. et Larix laricina, étaient absentes des sections perturbées du marais, lequel a par contre été envahi par des espèces halophiles comme Typha angustifolia. La tolérance à la salinité de diverses espèces végétales (Wilcox, 1982) a été déterminée et il a été démontré que les taxons étaient sensibles à des concentrations de chlorure de sodium dans l'eau du marais aussi faibles que 280 mg/L (170 mg de chlorure/L) (tableau 16). Les concentrations de sels ayant diminué de quelque 50 % entre 1980 et 1983, un grand nombre de plantes endémiques du marais, y compris Sphagnum, l'ont colonisé de nouveau (Wilcox, 1982). Sphagnum a recommencé à pousser sur de petits monticules, dans les sections où les concentrations de chlorure dans l'eau interstitielle avaient diminué à environ 300 mg/L.
Tuchman et al. (1984) ont utilisé des carottes prélevées des sédiments de lac pour étudier les effets historiques de la salinisation sur les diatomées du lac Fonda, au Michigan. Un entrepôt de sels était situé à proximité du lac Fonda depuis 1953; une plaque d'asphalte y a été ajoutée au début des années 1970 pour réduire les pertes de sels. La diversité des espèces d'algues a commencé à diminuer en 1960 et la diversité des diatomées a atteint son minimum en 1968, alors que l'abondance relative des taxons qui tolèrent le sel (ou halophiles) a atteint son maximum. Au cours des années qui ont suivi, la diversité a légèrement augmenté et l'abondance relative de certains taxons halophiles a diminué, ce qui laisse croire qu'il y a eu diminution de la charge de sels dans le lac. Malheureusement, la salinité du lac n'a pas été déterminée dans le cadre de cette étude. Zeeb et Smol (1991) ont élargi l'étude du lac Fonda aux chrysophytes recouverts d'écailles. Mallamonas caudata, un taxon insensible au chlorure, a dominé à toutes les profondeurs de la carotte. Mallamonas elongata, un taxon très répandu et présent surtout dans les eaux eutrophes et alcalines, de même que Mallamonas pseudocoronata, un taxon qui ne tolère pas le chlorure, ont dépéri durant la période où les concentrations de chlorure ont semblé être les plus fortes. À l'inverse, Mallamonas tonsurrata, présent surtout dans les lacs eutrophes, est devenu plus abondant durant cette période. Les changements importants dans les assemblages de diatomées et de chrysophytes ont été associés à des fluctuations relativement faibles de la salinité (c.-à-d. d'environ 12 à 235 mg de chlorure/L ou de 20 à 387 mg de chlorure de sodium/L).
Dans l'ensemble, ces études montrent que les entrepôts de sels mal conçus ou mal exploités peuvent avoir un certain nombre d'effets nocifs sur les milieux aquatiques, un aspect d'autant plus préoccupant qu'aucun programme de surveillance biologique n'a été mis en place à proximité de ces entrepôts pour assurer la protection des milieux aquatiques et terrestres locaux.
Des concentrations de chlorure variant entre 2 000 et 10 000 mg/L ont été mesurées dans la neige provenant de routes sur lesquelles il y avait eu épandage de sels. Or pareilles concentrations peuvent présenter une toxicité aiguë pour une variété d'organismes qui y sont exposés pendant une journée ou moins. La majorité des municipalités ont aujourd'hui recours à des décharges de surface comme lieux d'élimination de la neige (Delisle et Dériger, 2000). Cependant, l'emplacement de ces décharges varie considérablement, tout comme la réglementation environnementale qui régit ces installations. De plus, on ignore le nombre de décharges qui existent.
La neige déposée sur des terres basses peut entraîner une hausse de la concentration de chlorure dans les sols sous-jacents et les terres humides, au moment de la fonte des neiges. De même, la neige éliminée sur des terrains en hauteur finit par fondre et l'eau qui s'écoule transporte des sels dans les eaux souterraines et les écosystèmes aquatiques comme les cours d'eau, les terres humides et les étangs.
Peu d'études ont été réalisées à proximité de lieux d'élimination de la neige. Des concentrations élevées de chlorure (entre 233 et 994 mg/L) ont toutefois été observées dans des puits de surveillance aménagés pour évaluer l'impact de l'élimination de la neige sur les eaux souterraines peu profondes (Morin, 2000). Ces eaux souterraines chargées de sels peuvent à leur tour contaminer les sources qu'elles alimentent, comme l'ont constaté Williams et al. (1999).
En Colombie-Britannique, Warrington et Phelan (1998) ont remarqué que la composition ionique de deux lacs était passée d'un milieu dominé par les carbonates à un milieu dominé par le chlorure, à la suite du déversement de neige usée chargée de sels dans les lacs. Les eaux de ruissellement routier chargées de sels pourraient également avoir contribué à ce phénomène. Les effets biologiques n'ont pas été étudiés, mais certains pourraient être déduits des récentes études paléolimnologiques examinant l'impact de l'accroissement des concentrations de chlorure sur les communautés de phytoplanctons.
On n'a relevé aucune autre étude sur les effets nocifs de l'élimination de la neige en surface sur les écosystèmes aquatiques. Cependant, étant donné les milliers de décharges de neige qui existent probablement au Canada et compte tenu de la concentration élevée de chlorure dans les eaux de fonte, les risques potentiels pour les milieux aquatiques canadiens que présentent les décharges mal situées sont préoccupants, d'autant plus qu'il n'existe pas de réglementation uniforme régissant le fonctionnement de ces installations et que très peu de programmes de surveillance ont été mis en place pour assurer la protection de l'environnement contre les rejets de chlorure. Parmi les zones incompatibles avec l'implantation de lieux d'élimination de la neige, mentionnons les terres humides, les petits étangs et les petits lacs, de même que les secteurs surélevés d'où les eaux s'écoulent dans de petits ruisseaux. La contamination des eaux souterraines est un autre aspect dont il faut tenir compte.
3.3.3.4 Autres effets
En plus de leurs effets directs apparents sur la composition et l'abondance des espèces, les sels de voirie peuvent avoir des effets nocifs sur le milieu aquatique, par leurs interactions avec les composantes abiotiques du milieu. Plus particulièrement, les chlorures ont tendance à être plus solubles que les carbonates et ils peuvent, par diverses réactions, accroître la mobilité des métaux en traces dans les écosystèmes aquatiques. L'augmentation de la charge de sels peut aussi avoir des répercussions sur la densité de l'eau et gêner le mélange des eaux dans les lacs et ainsi perturber le fonctionnement écologique de cet écosystème.
L'augmentation de la concentration de sels de chlorure dans les eaux de surface peut entraîner la libération des métaux présents dans les sédiments et les particules en suspension. En faisant concurrence pour les sites de liaison des particules, le chlorure de sodium devient activateur des métaux en traces dissous et potentiellement biodisponibles, comme le cadmium, le cuivre et le zinc (Warren et Zimmerman, 1994). Or ces métaux présentent une toxicité aiguë pour les organismes aquatiques à des concentrations aussi faibles que 1 µg/L pour le cadmium (truite arc-en-ciel), 6,5 µg /L pour le cuivre (Daphnia magna) et 90 µg/L pour le zinc (truite arc-en-ciel) (CCME, 1991). De plus, comme les sels de voirie contiennent une variété de contaminants, incluant des métaux tels le cuivre (0 à 14 µg/g), le zinc (0,02 à 0,68 µg/g) et le cadmium (MDOT, 1993; Maltby et al., 1995), les eaux de fonte contenant des sels de voirie constituent une source potentielle de contamination des plans d'eau récepteurs par les métaux. Qui plus est, comme une variété de contaminants métalliques provenant des automobiles (plomb, cuivre, zinc et cadmium) sont présents à la surface des routes, les sels de voirie peuvent faciliter la mobilisation et le transport de ces contaminants dans les écosystèmes aquatiques (Maltby et al., 1995). Ces métaux peuvent ensuite s'accumuler dans divers tronçons des cours d'eau, sur les particules sédimentaires (Maltby et al., 1995) ou dans des eaux stationnaires, comme les étangs. Là, ils peuvent exercer leurs effets toxiques, notamment par des processus faisant intervenir les sédiments.
Il a été démontré que de fortes concentrations de sels dans l'eau interstitielle des sédiments augmentent les concentrations de métaux lourds dissous (le cadmium, par exemple) et la toxicité qui en résulte pour un invertébré benthique, Hyallela azteca (Mayer et al., 1999). Wang et al. (1991) ont constaté qu'une concentration de 709 mg de chlorure/L (ou 0,02 mol/L) augmente sensiblement la libération de mercure à partir des sédiments d'eau douce. Le mercure peut présenter une toxicité aiguë pour des espèces d'invertébrés et de poissons à des concentrations aussi faibles que 0,002 mg/L et 0,02 mg/L respectivement (CCME, 1991). De plus, sous sa forme méthylée, le mercure s'accumule dans les tissus des poissons. Le chlorure de sodium augmente aussi la mobilisation du mercure dans le sol (McLeod et al., 1996).
Les sels de voirie peuvent avoir une incidence sur les étangs et les lacs, en réduisant leur capacité de mélange vertical. Dans la plupart des lacs, il se produit un mélange vertical qui favorise l'échange entre les eaux de fond et les eaux de surface et qui est important pour le transfert de l'eau riche en oxygène, en surface, vers les sections plus profondes du lac - sans un tel échange, les eaux profondes peuvent devenir anoxiques. Ce mélange vertical est également important pour le transfert des éléments nutritifs qui se régénèrent dans les eaux plus profondes du lac et qui sont amenés en surface, où ils deviennent disponibles pour la communauté des phytoplanctons. Le mélange vertical dépend du vent qui mélange les eaux de surface jusqu'à diverses profondeurs, selon la vitesse du vent sur le lac, la topographie environnante et la température de l'eau. Le mélange vertical varie aussi en fonction des changements dans la température de l'eau qui influent sur la densité de l'eau. L'eau atteint sa densité maximale à 4 °C; ainsi, le réchauffement qui survient au printemps, alors que la température passe du point de congélation pour atteindre 4 °C, s'accompagne d'une augmentation de la densité qui favorise l'échange vertical entre les eaux de surface plus chaudes et les eaux profondes, plus froides et moins denses. Le refroidissement du lac à l'automne et le réchauffement (4 °C) au printemps ont donc pour effet de modifier la densité de l'eau qui influe sur le mélange vertical.
Un lac devient méromictique lorsque certaines conditions empêchent le mélange vertical entre les eaux de surface et les eaux profondes (Wetzel, 1983). Cela se produit lorsque le gradient de salinité est suffisant pour annuler les effets des fluctuations saisonnières de la température de l'eau sur la densité et le mélange de l'eau dans les lacs. Les sels de voirie, qui pénètrent dans les lacs par le débit de surface (ruissellement, fossés, cours d'eau) ou l'écoulement souterrain (infiltrations, sources), peuvent donc nuire à la circulation normale des lacs. Les petits lacs modérément profonds sont les plus susceptibles de présenter pareilles conditions méromictiques, en particulier dans les régions où on utilise de grandes quantités de sels de voirie. Les lacs plus grands sont moins vulnérables, parce que le panache d'eaux salées qui y pénètre subit une plus grande dilution, à mesure que l'eau plus dense chargée de sels s'écoule sur le fond vers les régions plus profondes du lac. En outre, les lacs plus grands ont un fetch plus long; les courants et autres échanges poussés par le vent y sont donc plus puissants.
La formation de conditions méromictiques peut avoir un certain nombre d'effets sur les lacs. La faible teneur en oxygène qui se développe sous la chimiocline peut provoquer la disparition de toutes les espèces benthiques en eaux profondes, sauf les espèces les plus résistantes. Les zooplanctons peuvent aussi être exclus de leur refuge diurne en eaux profondes et forcés de vivre dans les couches de surface plus claires, où ils risquent d'être plus sujets à la prédation par les poissons sélectifs quant à la taille de leur proie. Les poissons de la zone hypolimnique, comme le touladi, peuvent eux aussi être perturbés. L'apparition de conditions méromictiques aura également des répercussions sur les échanges entre les sédiments et l'eau. Le phosphore et divers métaux sont libérés plus facilement des sédiments mal oxygénés que des sédiments bien oxygénés (Wetzel, 1983). Cette libération accrue de phosphore peut augmenter la productivité et l'eutrophisation du lac, surtout si l'échange est suffisant au niveau de la chimiocline. À l'inverse, si l'échange y est limité, la production risque de diminuer et un lac eutrophe peut devenir oligotrophe (Smol et al., 1983).
1Les données sont tirées de la figure 17.
3.3.3.5 Conclusions pour les écosystèmes aquatiques
Des effets toxiques aigus (à court terme) ont été associés en laboratoire à de fortes concentrations de chlorure. Cependant, à mesure que la durée d'exposition augmente, la sensibilité au chlorure augmente elle aussi. Ainsi, la valeur de la CL50 pour Ceriodaphnia dubia (un cladocère) est de 1 400 mg/L après quatre jours d'exposition, mais de 1 261 mg/L après 9 jours (Cowgill et Milazzo, 1990). L'exposition à des concentrations létales aussi élevées serait fort probablement associée à des entrepôts de sels mal gérés, à des lieux d'élimination de la neige mal situés sur des terres humides, à des fossés longeant des routes à forte utilisation de sels, à des sources alimentées par des eaux souterraines contaminées et à des petits cours d'eau situés dans des régions urbaines très peuplées (p. ex., la région métropolitaine de Toronto) où le réseau routier est dense et sujet à l'épandage de grandes quantités de sels de voirie.
La toxicité à plus long terme se manifeste à des concentrations sensiblement moindres qui, selon les estimations, seraient aussi faibles que 210 mg/L. De telles concentrations de chlorure ont été observées dans une variété de ruisseaux, cours d'eau et lacs urbains, pour la plupart situés dans des régions très peuplées, ainsi que dans de petits cours d'eau situés près d'autoroutes fort achalandées. On peut également s'attendre à observer pareilles concentrations à proximité d'entrepôts de sels mal gérés et de lieux d'élimination de la neige mal situés comme sur des terres humides, dans de petits étangs ou encore à proximité de ruisseaux d'amont ou de sources alimentées par des eaux souterraines contaminées. On s'attend à ce que les écosystèmes aquatiques exposés à de tels niveaux de chlorure soient perturbés.
Un ensemble de courbes ont été préparées, à partir des données sur la toxicité du chlorure après des expositions de 4 jours, 7 jours et des expositions prévues à long terme (exposition chronique) (figure 17). Les données sur la toxicité qui ont servi à l'établissement de la figure 17 sont tirées de Evans et Frick (2001). Les données sur les expositions d'une journée et moins ont été exclues, car les études à l'appui étaient peu nombreuses. Les courbes sont définies sur une échelle log-linéaire, chacune selon un intervalle de confiance de 95 %. Un modèle log-logistique a été utilisé pour l'ajustement des courbes (Environnement Canada, 1997b). Sur la base des données prévues, on peut s'attendre à ce que 5 % des espèces soient touchées (concentration létale moyenne) à des concentrations de chlorure d'environ 210 mg/L (tableau 17) et que 10 % des espèces soient perturbées, à des concentrations d'environ 240 mg/L.
Les figures 18 et 19 illustrent diverses concentrations de chlorure dans des milieux aquatiques au Canada et les concentrations causant des effets biologiques néfastes. On présume que les concentrations de chlorure indiquées proviendraient de la contamination par les sels de voirie. À moins d'indications contraires, toutes les valeurs avec effets font référence à la létalité.
La figure 18 présente des données sur l'exposition à court terme, pour une période de cinq jours ou moins. Les concentrations indiquées s'appliquent à des rivières et des ruisseaux où les concentrations maximales de chlorure associées à des phénomènes tels le gel et le dégel ne devraient pas durer plus de quelques jours, à quelque point d'échantillonnage que ce soit. Les effets biologiques font référence à des essais de toxicité ayant pour paramètre de mesure une période de cinq jours ou moins (p. ex., CL50 après 4 jours).
Enfin, la figure 19 présente des données s'appliquant à des périodes d'exposition de plus de cinq jours. Les concentrations environnementales indiquées valent principalement pour des lacs et des étangs, où les taux de chlorure devraient en général demeurer stables durant une longue période. Les effets biologiques observés font référence à des essais de toxicité sur une durée de plus de cinq jours (p. ex., CL50 après 33 jours).
Comme nous l'avons indiqué précédemment, de plus en plus de données font état d'une hausse généralisée des concentrations de chlorure dans les rivières et les lacs du nord-est et du centre-ouest des États-Unis, incluant des lacs en milieux non urbains. Dixit et al. (1999), par exemple, ont étudié 257 lacs et réservoirs du nord-est des États-Unis et constaté que, alors que 34 % des réservoirs et 6 % des lacs affichaient une concentration de fond de chlorure supérieure à 8 mg/L avant les années 1850, ces proportions atteignent aujourd'hui respectivement 46 % et 18 %. Ces hausses sont liées en partie au nombre d'autoroutes dans la région, à la perturbation des sols et à l'utilisation de sels de voirie. Les chercheurs commencent également à observer des changements dans les communautés d'algues lorsque les concentrations de chlorure passent du niveau de fond (1,8 à 3,6 mg/L) à plus de 7 mg/L (Dixit et al., 1999). Bien que moins détaillées, des études menées au Canada semblent elles aussi indiquer une augmentation des concentrations de chlorure, lesquelles se situent dans les intervalles susceptibles de modifier la composition des algues dans les petits étangs et les petits lacs situés près de certaines autoroutes, ainsi que dans une variété de cours d'eau et de lacs en milieux urbains. Il importe toutefois de souligner que la grande majorité de ces études se limitent à des régions où l'on fait un grand usage des sels de voirie, situées pour la plupart dans le sud de l'Ontario, les Maritimes et le Québec.
La U.S. EPA (1988) a élaboré des lignes directrices sur la qualité de l'eau pour le chlorure et en est arrivée à la conclusion que, sauf peut-être dans les cas où une espèce localement importante est très sensible, les organismes dulcicoles et les utilisations qui y sont associées ne devraient pas être perturbés d'une manière inacceptable si :
- la concentration moyenne de chlorure (associé au sodium) sur quatre jours ne dépasse pas 230 mg/L, en moyenne plus d'une fois tous les trois ans;
- la concentration moyenne de chlorure pendant une heure ne dépasse pas 860 mg/L, en moyenne plus d'une fois tous les trois ans.
La U.S. EPA note cependant que ces critères n'assureront pas une protection suffisante lorsque le chlorure est associé au potassium, au calcium ou au magnésium et, comme l'intervalle de sensibilité aiguë au chlorure est restreint chez les animaux, le dépassement de cet intervalle pourrait avoir des incidences sur un nombre substantiel d'espèces. Evans et Frick (2001) ont également constaté que le chlorure de potassium et le chlorure de magnésium sont plus toxiques que le chlorure de sodium. De plus, le poisson semble moins sensible au chlorure de calcium qu'au chlorure de sodium, alors que l'inverse vaut pour les invertébrés; il convient toutefois de noter que ces observations s'appuient sur des ensembles limités de données. Enfin, bien que leur évaluation ait porté essentiellement sur le chlorure de sodium, le chlorure de potassium et le chlorure de magnésium semblent aussi, sinon plus, toxiques que le chlorure de sodium.
Figure 17 La toxicité aiguë expérimentale et toxicité chronique prévue pour les taxons aquatiques (d'après Evans et Frick, 2001)

Figure 18 La contamination par les sels de voirie causant des effets biologiques défavorables à partir d'une brève exposition à des concentrations de chlorure dans l'environnement aquatique canadien


Figure 19 La contamination par les sels de voirie causant des effets biologiques défavorables à partir d'une longue exposition à des concentrations de chlorure dans l'environnement aquatique canadien


À la lumière des données faisant état de plusieurs dépassements des seuils avec effets dans l'environnement et des données sur le terrain démontrant des effets sur les populations des écosystèmes, on en conclut que des concentrations élevées de chlorure associées à l'utilisation des sels de voirie peuvent avoir des effets nocifs immédiats ou à long terme sur les eaux de surface. Ces effets risquent surtout d'être observés à des entrepôts de sels mal gérés, des lieux d'élimination de la neige mal localisés et dans de petits cours d'eau longeant des réseaux routiers de forte densité. À des concentrations plus faibles, un accroissement des concentrations de chlorure peut avoir une incidence sur la structure, la diversité et la productivité des communautés. Il a en outre été démontré que des taux élevés de chlorure augmentent la biodisponibilité des métaux; de plus, en modifiant les gradients de densité dans les lacs, les sels de voirie peuvent avoir une incidence majeure sur les écosystèmes lacustres, en modifiant notamment la disponibilité de l'oxgène et des éléments nutritifs tributaire de la profondeur. Pareilles situations se produisent principalement dans les régions où l'on fait un grand usage des sels de voirie, lesquelles sont situées pour la plupart dans le sud de l'Ontario, le Québec et les Maritimes.
3.4 Sols
3.4.1 Salinisation des sols due à l'épandage de sels de voirie
Cette section résume l'information présentée dans le rapport préparé par Morin et al. (2000), sur l'étendue de la salinisation des sols due à l'épandage de sels de voirie. Ce rapport contient des cartes pédologiques pour toutes les provinces canadiennes, étayées de quelques études de cas qui visent à illustrer comment la salinité des solutions du sol varie de façon dynamique dans les zones touchées, y compris à de faibles distances de sources ponctuelles et linéaires de sels, et varie aussi en fonction de la saison. Les ions examinés sont le sodium, le calcium, le sulfate et le chlorure. On a peu tenu compte de la contribution des autres ions, comme le potassium et le magnésium, car ceux-ci influent habituellement peu sur la salinité globale du sol, et ce à la plupart des endroits.
Les cartes illustrant les apports (annuels) de sels de voirie et les concentrations de sels dans le sol sont basées sur les moyennes spatiales calculées pour des bassins versants de niveau 2, les moyennes spatiales au niveau municipal et les moyennes spatiales au niveau de la route (surtout des routes principales et des autoroutes). Ces trois niveaux d'analyse ont été choisis en raison du lien général entre la salinité du sol et la salinité des eaux de surface; la plupart des eaux de surface reçoivent en effet des apports directs du sol sous l'effet du ruissellement, de l'écoulement souterrain, de la percolation et du débit de base. De même, les sols situés dans le sens de la pente reçoivent souvent les eaux d'infiltration provenant de sources d'eau plus élevées. La dissolution graduelle des minéraux du sol et des roches facilement altérés augmente la salinisation des sols en aval, tout comme l'application d'engrais agricoles et horticoles et les eaux d'infiltration provenant des égouts domestiques et industriels. Dans les régions arides comme les Prairies canadiennes, l'évaporation à partir des sols arides contribue elle aussi à accroître la salinité du sol et mène, dans des conditions extrêmes, à l'accumulation de sels en surface et sous le sol, en particulier dans les dépressions du terrain et les infiltrations de la pente. Enfin, diverses activités industrielles, et plus particulièrement celles liées à l'extraction du sel et à l'utilisation de la soude caustique pour extraire les combustibles fossiles du goudron et des sables bitumineux, ne font qu'accroître la charge de sels dans l'environnement dans ces régions. La présente section porte toutefois sur les sels de voirie et vise à déterminer dans quelle mesure l'épandage de ces produits, combiné au dépôt atmosphérique, contribue à la salinité globale des sols à proximité des routes et dans quelle mesure ces épandages influent sur la salinité naturelle générale de l'eau qui refait surface, à divers endroits en aval. De façon générale, on s'attend à ce que les concentrations moyennes de sels provenant de l'épandage, dans les sols des bassins de niveau 2, soient inférieures aux concentrations municipales moyennes, elles-mêmes devant être inférieures aux moyennes dans le sol, aux abords des routes. Un travail de cartographie a donc été fait à trois niveaux pour estimer :
- les concentrations moyennes de sels prévues dans les solutions du sol, d'après l'apport total provenant de l'épandage et du dépôt atmosphérique, par bassin versant de niveau 2;
- les concentrations moyennes de sels prévues dans les solutions du sol, d'après l'apport total provenant de l'épandage et du dépôt atmosphérique, par région municipale, et
- les concentrations moyennes de sels prévues dans les solutions du sol, d'après l'apport total provenant de l'épandage et du dépôt atmosphérique, à proximité immédiate de la route.
Pour calculer ces moyennes, on a compilé les renseignements contenus dans diverses bases de données nationales, provinciales et municipales, afin de déterminer :
- l'épandage annuel moyen local de sels, par municipalité et comté;
- le dépôt atmosphérique annuel moyen, à l'échelle locale, lié aux précipitations et aux dépôts humides de sodium, de calcium, de chlorure et de sulfate (il n'existe pas encore de base de données sur les dépôts secs; or l'inclusion des dépôts secs augmenterait les charges globales de sels, surtout dans la région de l'Atlantique, à cause de l'embrun);
- le ruissellement annuel moyen, et
- la profondeur locale du sol, ainsi que sa teneur en argile et en matières organiques.
Les paramètres saisonniers n'ont pas été pris en considération pour ce travail de cartographie; il convient toutefois de noter que la salinité du sol varie en fonction de la charge de sels de voirie, des conditions météorologiques et de la topographie. Certains aspects saisonniers sont toutefois examinés dans cette section, au moyen d'études de cas spéciales qui portent sur la salinité du sol et des eaux de surface, à des endroits situés en aval d'un entrepôt de sels.
3.4.1.1 Définitions et équations
Les données compilées sur les charges atmosphériques d'ions sodium, calcium, chlorure et sulfate font référence aux concentrations d'ions, pondérées en fonction du volume (dépôt humide seulement) et sont exprimées en mg/L ou en meq/L. Les charges de sels, par contre, sont généralement exprimées en g/m2/an ou en kg/ha/an. Dans le présent rapport, les charges provenant du dépôt atmosphérique et de l'épandage de sels de voirie sont converties en concentrations de sels totaux dissous dans les solutions du sol, en divisant les charges combinées annuelles calculées, par le taux annuel prévu de percolation à travers le sol, où :
Pour simplifier les calculs, on estime que les taux annuels de percolation (mm/an) sont équivalents au débit d'un cours d'eau (mm/an), lequel débit est déterminé à partir d'observations hydrométriques spécifiques d'un bassin versant. Pour ce travail de cartographie, on considère donc que les taux de percolation prévus sont égaux au débit du cours d'eau. Les cartes présentées dans Morin et al. (2000) décrivent :
- le débit du cours d'eau (en millimètres) à l'échelle nationale, d'après les données de Ressources naturelles Canada, et
- le débit du cours d'eau (en mètres cubes) par bassin versant de niveau 2 (tiré de la carte nationale sur le débit).
Les bassins versants qui présentent les coefficients de ruissellement les plus élevés sont situés le long des côtes du Pacifique et de l'Atlantique. À l'opposé, c'est dans les bassins versants de la portion sud des Prairies que le ruissellement permettant de dissoudre et de diluer les sels est le plus faible. Il est important de déterminer les régions où le taux de ruissellement est faible, car ce ruissellement contient de fortes concentrations de sels de voirie.
Afin de représenter ces paramètres sur une carte, il a aussi fallu obtenir des données pédologiques nationales sur :
- la teneur en argile du sol (en % de la portion minérale du sol (particules < 2 mm),
- les matières organiques du sol (en %), et
- la capacité d'échange de cations (en meq/100 g de sol séché à l'étuve).
taux de percolation à travers le sol (mm/an) = taux de précipitation - taux réel d'évapotranspiration surface (mm/an) - ruissellement de surface (mm/an)
Les estimations des charges de sels totaux dissous et des concentrations d'ions correspondantes dans les solutions du sol ont servi à calculer :
- les cations totaux et les anions totaux (en meq/L);
- la conductivité électrique du sol (en mmho/cm ou mS/cm);
- le potentiel osmotique (en bars);
- le rapport d'absorption du sodium (sans dimension);
- le rapport de sodium échangeable (sans dimension);
- le pourcentage de sodium échangeable (en %);
- la teneur en sodium échangeable (en meq/100 g de sol séché à l'étuve);
- la dispersion de l'argile et du limon dans le sol (en % de la teneur en argile du sol), et
- les changements relatifs dans la conductivité hydraulique du sol (sans dimension).
Parmi les effets probables des sels sur les sols, mentionnons une réduction significative du potentiel osmotique du sol, une augmentation du gonflement du sol, une réduction de la stabilité (perte de la structure) et de la perméabilité du sol, un risque accru d'érosion, ainsi qu'une augmentation de la dispersion de l'argile et du limon et de la turbidité des eaux de surface. Tous ces effets sont en outre exacerbés par une augmentation de la teneur en sodium du sol, parce qu'une teneur accrue en ions sodium réduit l'affinité des particules du sol entre elles, étant donné la grande affinité entre les ions sodium et les molécules d'eau. Dans une certaine mesure, ces effets dus aux sels dépendent largement de la minéralogie de l'argile du sol (p. ex., le gonflement et la contraction dans les sols à forte teneur en montmorillonite). Sous d'autres aspects, toutefois, ces effets dus aux sels sont indépendants de la minéralogie du sol et dépendent uniquement de l'affinité qui s'exerce par l'action des électrolytes entre les diverses particules dans le sol ou en suspension. L'affinité dépend ainsi des forces électrolytiques entre les particules qui déterminent le degré de coagulation et de dispersion des particules (voir Ali et al., 1987). Lorsque la dispersion du sol augmente, par exemple lorsque des sols salinisés reçoivent de l'eau d'irrigation à faible teneur en électrolytes puis sont exposés à l'érosion hydrique et éolienne, non seulement y a-t-il dispersion de particules fines, mais ces particules peuvent aussi transporter des contaminants environnementaux tels des éléments nutritifs, des métaux lourds et des microbiotes sous l'effet de l'érosion hydrique et éolienne.
Les sols qui ont une teneur relativement élevée en argile et qui reçoivent, continuellement ou périodiquement, un apport élevé en sodium sont probablement ceux qui seront les plus perturbés à long terme (c.-à-d. ceux dont l'indice du risque de salinité devrait être élevé). Pour établir la carte des régions à indice élevé de risque de salinité, un indice simple du risque a été calculé comme suit :
Indice du risque de salinité = rapport de sodium échangeable x teneur en argile du sol (en %) Selon ces calculs, les régions qui présentent les risques les plus élevés sont situées dans le sud de l'Ontario, près de la Région du Grand Toronto, et dans le sud du Québec autour de l'île de Montréal (figure 20). L'indice est également élevé dans d'autres régions du sud de l'Ontario et du Québec, de même que dans certaines régions du sud des Prairies où la salinisation des sols par des phénomènes naturels constitue une préoccupation régionale majeure (voir Eilers et al., 1995).
3.4.1.2 Études de cas
Trois études de cas ont été faites, soit au parc national Kejimkujik (Nouvelle-Écosse), le long de certaines rues de Fredericton (Nouveau-Brunswick), ainsi que dans une région forestière située à proximité de l'entrepôt municipal de sels de Fredericton (boisé de l'Université du Nouveau-Brunswick). Ces études avaient pour but :
- de quantifier le taux général de renouvellement des ions sodium dans les sols des bassins supérieurs, au parc national Kejimkujik (un milieu essentiellement exempt de sels de voirie, mais exposé à l'embrun),
- d'évaluer la salinité du sol sous le gazon, près de la bordure de certaines routes de Fredericton, à l'automne;
- d'examiner la fluctuation de la salinité des eaux de surface en fonction de la distance par rapport à l'entrepôt de sels de Fredericton, par saison, et
- d'évaluer la salinité de l'eau dans les fossés longeant l'autoroute Fredericton-New Maryland.
Figure 20 Régions où l'épandage de sels de voirie pose un danger faible, moyen ou élevée selon la teneur en argile du sol et du coefficient de sodium échangeable (d'après Morin et al., 2000)
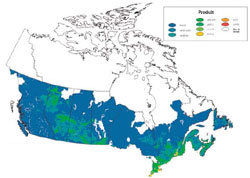
Les résultats de ces études de cas indiquent que les sols et les bassins versants du parc national Kejimkujik ont une très faible capacité de rétention des ions sodium et chlorure, les ions sodium et chlorure étant rapidement lessivés à travers les sols et les bassins versants. De plus, c'est au début de l'automne que les concentrations d'ions dans le sol et les cours d'eau sont les plus élevées, tandis qu'elles sont les plus faibles à la fonte des neiges.
Figure 21 Le diagramme représente la conductivité électrique et les concentrations de chlorure dans l'eau de fossé longeant les deux routes près du dépôt de sel de voirie de Frédéricton pour les mois de juin, juillet et octobre 1999 et janvier 2000. Le diagramme démontre les données du 10e, 25e, 50e, 75e et 90e percentile ainsi que les données inférieures et supérieures aux 10e et 90e percentile (cercles). Les mots « bien-drainé», « écoulement croisé» et « stagnant » se réfèrent à trois conditions : crête à partir de laquelle l'eau est bien drainée; croisement d'un cours d'eau; et fossé sans écoulement (d'après Arp, 2001)

Le long des rues de Fredericton, généralement peu de sodium est retenu sur les sites d'échange d'ions, dans les sols aux abords des routes, comme le démontrent les observations faites au début de l'automne. Les données indiquent en effet que le sodium échangeable est particulièrement faible à cette période de l'année, le long des routes les plus achalandées. Les concentrations de sodium échangeable sont en outre plus faibles près de la bordure des routes qu'à une distance de deux à trois mètres : c'est donc que l'éclaboussement et le ruissellement routier répétés et importants au printemps, à l'été et à l'automne éliminent le sodium des sols qui longent les routes.
Les concentrations de fond d'ions sodium et chlorure, dans les solutions du sol et les eaux de surface, sont légèrement plus faibles dans le boisé de l'Université du Nouveau-Brunswick (s'établissant respectivement à 2 mg/L et 3 mg/L) qu'elles le sont dans le parc national Kejimkujik; les concentrations de chlorure dans l'eau des fossés et des cours d'eau autour du boisé varient toutefois selon les endroits. Arp (2001) a mesuré
la conductivité électrique (qui est associée plus loin à la concentration de chlorure) de l'eau des fossés le long de l'autoroute Fredericton-New Maryland et le long de Bishop Drive, durant des journées représentatives de juin, juillet, octobre (1999) et janvier (2000). Les résultats de cette étude sont résumés à la figure 21, au moyen de tracés en boîte, en fonction des conditions hydrologiques à chaque point de mesure. Les fossés dans cette analyse ont été classés selon les trois caractéristiques d'emplacement suivantes :
- emplacements bien drainés, où les fossés ont tendance à s'assécher (crêtes);
- emplacements mal drainés, où l'eau s'accumule et devient stagnante, et
- emplacements exposés à un écoulement continu de l'eau, c.-à-d. sous un pont-ruisseau (ponceaux).
La figure 21 montre que la conductivité électrique de l'eau dans les fossés est à son maximum en juillet, en particulier dans les régions où l'eau n'est pas stagnante. Aux endroits où l'eau est stagnante, la conductivité électrique demeure relativement élevée en toute saison et elle tend à être à son maximum en juin et juillet, alors qu'elle est généralement minimale et plus stable à l'automne. Là où l'eau des ruisseaux, des cours d'eau ou des fossés se rencontre sous des autoroutes (sous des ponceaux), la conductivité est minimale, égale au niveau de fond ou s'en rapproche, à cause de l'écoulement continu; l'eau des fossés qui pénètre dans les ruisseaux et les cours d'eau est donc rapidement diluée toute l'année. En revanche, lorsque l'eau des fossés s'écoule dans des dépressions mal drainées, où l'eau s'accumule et où le taux de renouvellement de l'eau est faible, il n'y a pas de dilution et donc la conductivité électrique (et, partant, la salinité) demeure élevée toute l'année.
Tableau 18 Valeurs modélisées de la conductivité électrique et des concentrations de chlorure dans le ruisseau Corbett, en aval de l'entrepôt de sels de voirie de Fredericton

Les concentrations maximales de chlorure (de 300 à plus de 1 000 mg/L) ont été observées à l'entrepôt de sels et à proximité de cette installation. Le tableau 18 indique les concentrations de chlorure dans l'eau de cours d'eau et d'étangs, en fonction de l'accroissement de la superficie du bassin versant du ruisseau Corbett en aval de l'entrepôt de sels de Fredericton, à diverses périodes de l'année (mai, juin, juillet, octobre, janvier). Il se produit au départ une forte dilution, dans l'étang Larch Swale, qui est situé à proximité (0 km, tableau 18) et qui reçoit l'eau du cours supérieur de 172 ha. Au-delà de ce tronçon, la dilution se poursuit, graduellement ou brusquement, chaque hausse soudaine étant spécifique du bassin versant de chaque ruisseau contigu. À titre d'exemple, à 2 km environ de l'entrepôt de sels, le ruisseau O'Leary rejoint le ruisseau Corbett; là, la dilution augmente considérablement, mais toujours en proportion du bassin versant combiné des deux ruisseaux.
La saison influe considérablement sur la conductivité électrique et le facteur de dilution correspondant. En principe, les mesures de conductivité sont reliées au débit du cours d'eau : un débit élevé laisse supposer une dilution accrue et donc une diminution de la conductivité. À l'inverse, un débit faible laisse croire que la dilution est moindre et donc que la conductivité est plus élevée. Lorsque le débit est intermittent (comme cela peut se produire à l'été et au début de l'automne), l'influence globale de l'entrepôt de sels semble se limiter à la proximité de l'entrepôt, les régions plus éloignées recevant moins d'eau chargée de sels. Cette dilution « apparente » plus en aval, à mesure qu'augmente l'étendue du bassin versant, est plus marquée durant les périodes d'écoulement intermittent (par exemple, en juillet) qu'en périodes d'écoulement continu. En juillet, des concentrations supérieures à 250 mg/L ont été observées jusqu'à 500 m de l'entrepôt et elles étaient toujours de 100 mg/L à une distance de 1 250 m.
3.4.1.3 Discussion
Selon les calculs, les effets de l'épandage de sels de voirie sur les propriétés physiques et chimiques du sol - comme le potentiel osmotique, la conductivité électrique, la perméabilité, la dispersion et le rapport de sodium échangeable (voir Morin et al., 2000 pour de plus amples renseignements sur les autres propriétés physiques et chimiques) - sont à leur maximum à proximité des entrepôts de sels et des routes sur lesquelles il y a épandage de sels. Au niveau municipal, on peut s'attendre à ce que les effets de l'eau du sol sur les zones situées en aval varient considérablement en fonction de la densité du réseau routier, des conditions locales, des lieux où il y a épandage de sels et des caractéristiques physiques des entrepôts de sels. Ainsi, les concentrations de sels dans le sol et les eaux de surface, dues à l'épandage, devraient être plus élevées dans les régions urbaines où les routes sont en grande partie asphaltées que dans les régions moins exploitées. De fait, Williams et al. (1999) montrent que les concentrations de sels dans les sources, à l'intérieur de la région métropolitaine de Toronto, augmentent lorsque le principal mode d'utilisation des terres passe d'un mode rural à urbain. Ces auteurs ont également constaté :
- que les concentrations de sels atteignent leur maximum durant la période d'épandage;
- que, durant ces périodes de pointe, la concentration d'ions chlorure peut dépasser
1 000 mg/L, et - qu'une deuxième période de concentration maximale se produit au milieu de l'été (ce qui vient corroborer les résultats d'une des études de cas précitées), la concentration maximale de chlorure atteignant alors plus de 200 mg/L.
Donc, les concentrations de sels dans les eaux de surface, les eaux souterraines et les solutions du sol peuvent être élevées au moment de l'épandage des sels de voirie, mais des concentrations élevées peuvent aussi se produire plus tard l'été, durant des périodes de sécheresse alors que l'eau s'évapore et que l'eau salée provenant, par exemple, du sous-sol resurgit en aval. En périodes de précipitations abondantes, l'eau de faible conductivité électrique favorise l'élimination de l'eau saumâtre de ces régions. Le long des routes, les fréquentes éclaboussures en périodes de pluie peuvent accélérer le déplacement de l'eau saumâtre et favoriser un retour à un faible pourcentage de sodium à changeable dans le sol, bien qu'un tel phénomène ne puisse vraiment se produire que dans les sols de grande perméabilité, où l'eau ne s'accumule pas (c.-à-d. où l'eau n'est pas stagnante durant une longue période de l'année).
Il est possible que les sols sous les surfaces asphaltées (en régions urbaines) ne bénéficient pas de ce phénomène saisonnier de lessivage des sels. Il est donc probable que le sel à ces endroits reste concentré ou qu'il s'accumule encore davantage sous l'effet d'épandages accrus, parce que ces endroits sont situés, du moins en partie, en dehors des trajectoires qu'empruntent les eaux d'infiltration. Ces endroits deviennent donc une source de salinité du sol et des eaux de surface, cette salinité étant provoquée, soit par l'infiltration lente, soit par le lessivage rapide d'eau à forte teneur en sels au moment de la réparation de la chaussée ou par temps anormalement humide.
Les effets globaux du sel sur les sols doivent être évalués en fonction de l'emplacement de la source ou du puits, en tenant compte par exemple de l'emplacement de l'accotement par rapport à la route (est-il au même niveau que la route, plus bas ou plus haut, sous le vent ou exposé au vent) et des conditions du terrain aux abords de la route (s'agit-il d'un terrain découvert ou boisé, d'un sol bien ou mal drainé?). Habituellement, la dispersion des sels, depuis la route vers l'accotement, se fait par les éclaboussures, la poussière et le ruissellement soulevés au passage des véhicules. On peut donc s'attendre à ce que la salinité du sol augmente, des endroits surélevés (zones d'alimentation) vers les dépressions mal drainées.
Le processus de dilution des sels par les précipitations et les éclaboussures produites au passage des véhicules est un phénomène important, car il permet à la majeure partie des sols aux abords des routes de se remettre partiellement ou complètement des épandages saisonniers de sels de voirie. Il semble en effet que les éclaboussures des véhicules accélèrent le lessivage des sels qui se sont accumulés durant l'hiver le long des routes, comme l'indique une des études de cas précitées. Cependant, lorsque le pourcentage de sodium échangeable est élevé et que la conductivité électrique de l'eau d'éclaboussures est faible, ce phénomène peut au contraire avoir des effets nocifs sur l'agrégation du sol, notamment sur la dispersion de l'argile et du limon, ce qui peut réduire le taux d'infiltration dans le sol et de ce fait accroître l'érosion hydrique du sol et favoriser la dispersion des particules du sol par le vent. Un tel effet serait maximal en bordure des routes sans végétation.
La figure 22 illustre les valeurs moyennes prévues pour les matières totales dissoutes, le potentiel osmotique et la conductivité électrique des solutions du sol et des eaux de surface, à l'échelle du bassin versant de niveau 2 et de la municipalité. Un examen des teneurs en matières totales dissoutes indique que ces valeurs sont toutes supérieures aux niveaux de fond auxquels on peut s'attendre, sous l'effet uniquement des dépôts atmosphériques locaux et de l'évapotranspiration subséquente. Ces concentrations régionales moyennes sont toutefois loin d'être préoccupantes, sauf dans les régions fortement urbanisées. Comme prévu, les valeurs calculées pour la matières totales dissoutes, le potentiel osmotique et la conductivité électrique augmentent à mesure que la superficie moyenne diminue.
Les valeurs pour les matières totales dissoutes, le potentiel osmotique et la conductivité électrique dans les solutions du sol et les eaux de surface ont été calculées pour les sols des emprises routières. Ces valeurs sont basées sur les données provinciales sur les charges de sels de voirie, par district d'entretien. Dans l'ensemble, ces calculs indiquent que les zones en périphérie immédiate de l'emprise ont tendance à afficher des moyennes annuelles élevées, pour ce qui est des matières totales dissoutes, du potentiel osmotique et de la conductivité électrique. Évaluées sur une base saisonnière, ces valeurs seraient plus élevées durant les périodes d'épandage de sels de voirie alors qu'elles seraient nettement moindres en périodes de lessivage élevé. On peut toutefois s'attendre à observer le retour de valeurs élevées au milieu de l'été, dans les zones propices à l'accumulation d'eau; ces valeurs pourraient également demeurer élevées dans les bassins d'eau stagnante ou les dépressions à faible ruissellement de surface, comme nous l'avons indiqué précédemment.
La carte présentée à la figure 23 laisse croire que, dans certaines régions de l'Ontario et du Québec, le pourcentage de sodium échangeable est élevé sur certaines routes. Ces valeurs sont associées principalement aux régions à charges élevées de sels de voirie. Cette figure semble également indiquer que le pourcentage de sodium échangeable pourrait être élevé dans certaines régions des Prairies. Même si les routes des Prairies ont une faible charge de sels de voirie, lorsqu'on les compare à la plupart des municipalités du Québec et de l'Ontario, les précipitations permettant de diluer et de dissoudre les sels y sont moins abondantes. La situation est telle qu'un grand nombre de sols dans le sud de l'Alberta et le sud de la Saskatchewan, ainsi que certains sols du sud du Manitoba, sont déjà salés sous l'effet de phénomènes naturels, en particulier dans les dépressions et à proximité des terres humides et des voies de drainage. Là, les sels de voirie viendraient s'ajouter à la charge totale d'électrolytes dans le sol, car ils s'accumuleraient dans les dépressions à proximité des routes. En général, le profil spatial des concentrations de fond d'électrolytes dans les solutions du sol, basé uniquement sur les dépôts atmosphériques, correspond assez bien au profil spatial de la salinité du sol décrit par Eilers et al. (1995), ce qui vient corroborer le protocole du bilan massique simple qui sous-tend le modèle ayant servi à produire les cartes dans ce rapport.
La salinisation accrue des sols, due à l'épandage de sels de voirie, peut avoir des répercussions sur le biote du sol (macroflore, microflore, microfaune et macrofaune). La figure 24 présente un résumé simplifié de la sensibilité prévue de certains végétaux, ainsi que les seuils de tolérance correspondants spécifiques de l'espèce, en fonction d'une diminution du potentiel osmotique du sol. Cette figure établit un lien entre la sensibilité des cultures et la salinité du sol, en montrant dans quelle mesure le rendement des récoltes diminue à mesure que la conductivité électrique augmente. Les encadrés pointillés dans cette figure indiquent le pourcentage des routes provinciales auxquelles on associe certains niveaux de salinité. Les données de ce graphique suggèrent que la salinité de la solution du sol, le long de la majorité des routes provinciales, peut avoir des effets nocifs sur bon nombre d'espèces d'arbustes et d'arbres. Elles semblent en outre indiquer que le niveau de salinité du sol, en bordure de certaines routes, peut même avoir des effets néfastes sur des espèces halophiles comme l'agropyre. Les répercussions sur la végétation terrestre sont discutées plus en détail à la section 3.5.
On s'attend à ce que les effets des sels de voirie sur le sol dépendent fortement de l'étendue du couvert végétal. Ainsi, l'encroûtement, le ruissellement de surface et la dispersion de l'argile et du limon par le vent et l'eau devraient être les plus élevés sur les sols dénudés. Les sols couverts de végétation subiront eux aussi des effets lorsque le couvert végétal réagira négativement au potentiel osmotique négatif élevé dans le sol. Dans ce cas, la perte graduelle de la végétation de surface entraînera une augmentation de l'exposition du sol minéral et une diminution graduelle de la teneur en matières organiques du sol, ce qui aura pour effet d'accroître la dispersion et, de ce fait, de réduire la perméabilité du sol et d'en augmenter l'érosion. De toute évidence, l'application de bonnes pratiques en matière de gestion des végétaux, d'épandage de sels de voirie et d'entretien des routes contribuerait sensiblement à réduire ces effets. On trouvera d'autres renseignements sur la salinité du sol et bien d'autres aspects reliés à la gestion et à la conservation du sol, notamment dans Anon (1992), Holms et Henry (1982), Steppuhn et Curtin (1992) et Acton et Gregorich (1995).
D'autres effets des sels de voirie, qui ne sont pas examinés ici, ont trait à la libération de métaux lourds (p. ex., le zinc, le cuivre, le cobalt, la mercure et le cadmium) et de cations basiques (calcium, magnésium, potassium), en présence des sels. Tous ces phénomènes peuvent avoir des effets positifs ou négatifs sur la flore et la faune du sol, notamment :
- en favorisant la croissance de certaines espèces dans des écosystèmes par ailleurs pauvres en éléments nutritifs;
- en favorisant la perte d'éléments nutritifs comme le calcium, le magnésium et le potassium, sous l'effet de l'échange d'ions avec le sodium, et
- en mobilisant les métaux lourds dans le sol et les habitats aquatiques, selon les conditions locales.
Figure 22 Estimation par bassin versant et par municipalité des solides dissous totaux (SDT) et de la conductivité électrique (CE) moyenne des eaux du sol et de surface en Ontario et au Québec (d'après Morin et al., 2000)
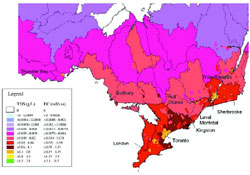
La mobilisation des métaux lourds résulte de la formation de complexes hydrosolubles entre le chlorure et un cation métallique, ce qui a pour effet d'accroître la phytodisponibilité d'un grand nombre de cations de métaux lourds, et de favoriser ainsi l'entrée des métaux lourds dans la chaîne alimentaire locale, qui sont assimilés par les plantes. Dans le pire des scénarios, les plantes pourraient elles-mêmes manifester des symptômes dus à la toxicité des métaux lourds. Pour un exemple des processus en cause, consulter Smolders et McLaughlin (1996) qui traitent de la mobilisation du cadmium favorisée par le chlorure et de l'assimilation subséquente de ce métal par les végétaux. Pour plus de renseignements sur les effets de la salinisation des sols, voir par exemple Bresler et al. (1982), Eilers et al. (1995), Butler et Addison (2000) et Cain et al. (2001).
Figure 23 Pourcentage de sodium échangeable (PSE) le long des routes par district d'entretien provincial (d'après Morin et al., 2000)
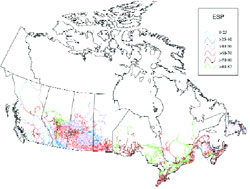
3.4.1.4 Conclusions
L'épandage de sels de voirie peut avoir des effets nocifs sur les paramètres physiques et chimiques du sol, en particulier dans les régions exposées aux sels où, par surcroît, les pratiques de gestion du sel, du sol et de la végétation sont déficientes. On estime que les effets les plus graves se produiraient dans les régions directement exposées au ruissellement provenant d'entrepôts de sels et celles situées le long des routes, en particulier dans les dépressions mal drainées. Les effets reliés aux électrolytes influent sur la stabilité structurale, la dispersion, la perméabilité, le gonflement, l'encroûtement, la conductivité électrique et le potentiel osmotique du sol. Les eaux de surface qui se trouvent dans la pente de sols perturbés par les sels subissent les effets de l'infiltration d'eaux saumâtres ou du ruissellement chargé de sédiments dispersés par les sels. Tous ces phénomènes ont, à leur tour, des effets abiotiques et biotiques sur l'environnement local. Les effets abiotiques ont trait principalement à la perte de stabilité du sol durant les cycles d'humidification et de dessication et durant les périodes de fort ruissellement de surface et de vent violent. Les effets biologiques, pour leur part, sont surtout liés au stress osmotique qui s'exerce sur la macroflore, la microflore, la microfaune et la macrofaune du sol, ainsi qu'à la mobilisation par le sel des micro-éléments et des macro-éléments, ce qui influe sur la flore et la faune in situ et dans les zones d'infiltration en aval.
3.0 Évaluation du caractère « toxique » au sens de la LCPE 1999
3.4 Sols
3.4.2 Effets biologiques des sels de voirie sur les sols
Butler et Addison (2000) font un examen exhaustif des effets du sel sur la microflore et la microfaune du sol. Il semble y avoir très peu de données sur l'exposition aux sels de voirie et sur les communautés microbiennes du sol ou leurs activités. Aux fins de la présente évaluation, on a examiné la documentation disponible sur les adaptations métaboliques requises pour que les microbes tolèrent le sel et sur les effets de la forte salinité du sol sur les processus essentiels à l'agriculture, même si ces études ont été menées dans une perspective très différente du présent rapport. Une autre difficulté tient aux diverses façons de rapporter l'exposition aux sels dans la documentation. En effet, les comparaisons entre les sols sont habituellement basées sur la conductivité électrique, le potentiel hydrique ou osmotique, et non sur l'augmentation de la concentration de sels, car la composition ionique des solutions du sol varie. Par contre, les concentrations de sels (masse/volume liquide) sont plus couramment rapportées dans la documentation sur la microbiologie. Enfin, les études sur la faune du sol rapportent habituellement les apports de sels exprimés en quantités par unité de surface.
3.4.2.1 Rôle écologique des communautés biotiques du sol
La dégradation et la minéralisation de la matière organique et le cycle des éléments (p. ex., du carbone, de l'azote, du phosphore et du soufre) dans le sol et les sédiments dépendent des communautés biologiques qui y sont présentes. Dans les systèmes terrestres, la contribution directe des microbes phototrophes et chimiolithotrophes à la production primaire est minime. Certaines expériences ont cependant démontré que la production primaire des végétaux supérieurs est grandement améliorée par l'activité des biotes microbiens et fauniques souterrains (Faber et Verhoef, 1991, Setälä et Huhta, 1991, Setälä et al., 1998). Les mycorhizes s'observent chez presque tous les végétaux terrestres; le partenaire fongique de cette association symbiotique plante-moisissure contribue à l'assimilation et à la translocation des éléments nutritifs (le phosphore en particulier) et à la protection potentielle contre les pathogènes, les nématodes et les produits toxiques des végétaux, comme les métaux lourds présents dans la zone des racines (Paul et Clark, 1996). Les capacités enzymatiques de la microfaune du sol (p. ex., les protozoaires et les nématodes) et de la mésofaune (p. ex., les acariens et les insectes aptères) sont plus limitées que celles des procaryotes et des micromycètes, de sorte que la plupart des transformations chimiques qui entrent en jeu dans la décomposition de la matière organique et le cycle des éléments nutritifs sont assurés par l'intermédiaire des microbes du sol. La contribution de la faune du sol à ces processus se fait au moyen de phénomènes plus indirects, comme la dégradation physique de la litière, la dispersion des propagules microbiens (y compris les mycorhizes et les pathogènes), le broutage sélectif des espèces microbiennes et, dans le cas de la macrofaune, la modification de la structure du sol. Les vers de terre, par exemple, peuvent avoir une influence énorme sur l'aération du sol, la structure des agrégats, la capacité de rétention de l'eau, la densité apparente du sol et le taux de minéralisation de l'azote (Lee, 1985).
Figure 24 La tolérance au sel et le rendement des récoltes en fonction de la salinité du sol (conductivité électrique, CE) et le pourcentage estimé d'emprises routières ayant un niveau correspondant de CE (d'après Bresler et al., 1982)

3.4.2.2 Effets sur le biote du sol
Butler et Addison (2000) présentent également des données sur les effets du chlorure de sodium sur les organismes du sol, une substance à laquelle les bactéries du sol peuvent être très sensibles. Hattori et Hattori (1980) ont étudié la croissance de 40 bactéries isolées de divers sols oligotrophes du Japon. La croissance de deux des 40 bactéries a été modérément inhibée à une concentration de 0,15 de chlorure de sodium/L (ce qui correspond à environ 60 mg de sodium/L et 90 mg de chlorure/L). La croissance d'une bactérie a été fortement inhibée par 1 g de chlorure de sodium/L (environ 400 mg de sodium/L et 600 mg de chlorure/L), alors que 17 ont été fortement inhibées par 5 g de chlorure de sodium/L (environ 2 000 mg de sodium/L et 3 000 mg de chlorure/L). Enfin, la croissance de 11 bactéries sur 40 a été fortement inhibée par 10 g de chlorure de sodium/L, alors que les 9 autres ont été modérément inhibées à 10 g/L. De leur côté, McCormick et Wolf (1980) ont observé une réduction sensible de la nitrification du sol en présence de 0,25 g de chlorure de sodium/kg (soit environ 100 mg de sodium/kg et 150 mg de chlorure/kg) ou plus, et il y a eu inhibition complète de la nitrification à 10 g de chlorure de sodium/kg. Certains rhizobiums - ces bactéries du sol qui forment des nodosités fixatrices d'azote avec les légumineuses (incluant des cultures importantes comme le soja, le pois et le trèfle) -ont tendance à être sensibles au sel. La durée de génération des souches Bradyrhizobia japonicum sensibles au sel a augmenté après une exposition à 2,6 g de chlorure de sodium/L, alors que peu d'effets ont été observés chez des variants insensibles au sel (Upchurch et Elkan, 1977). Les vers de terre peuvent eux aussi être assez sensibles au sel; les vers de l'espèce Eisenia fetida sont morts en moins de deux semaines, après avoir été exposés à≥5 g de chlorure de sodium/kg (Kaplan et al., 1980). McCormick et Wolfe (1980) rapportent une chute assez brusque du dégagement de dioxyde de carbone dans un loam sableux traité pendant 14 semaines au chlorure de sodium à raison de 10 g/kg (environ 4 000 mg de sodium/L et 6 000 mg de chlorure/kg). Aucune quantité décelable de dioxyde de carbone n'a été libérée d'un sol ayant reçu 100 g de chlorure de sodium/kg.
3.4.2.3 Exposition des organismes du sol aux sels de voirie
Cain et al. (2001) présentent les concentrations de sodium et de chlorure dans le sol. La concentration de chlorure la plus élevée dans le sol (1 050 mg/kg) a été mesurée dans un échantillon prélevé dans le terre-plein central d'une autoroute, alors que la plus forte concentration de sodium (890 mg/L) a été mesurée dans un échantillon prélevé à 10 m d'une autoroute, toutes deux mesurées dans une étude faite le long d'une autoroute à quatre voies de l'Ontario (Hofstra et Smith, 1984). Les concentrations de chlorure et de sodium ont diminué rapidement à mesure qu'a augmenté la distance par rapport à la route. À tous les sites canadiens rapportés, des concentrations de sodium inférieures à 100 mg/kg ont été observées à environ 20 m et plus, alors que les concentrations de chlorure étaient inférieures à 300 mg/kg à une distance supérieure à 30 m environ de la route.
Enfin, des concentrations de sodium et de chlorure atteignant respectivement 13 100 mg/kg et 14 500 mg/kg ont été mesurées dans le sol d'entrepôts de sels (section 2.4.4.2).
3.4.2.4 Évaluation environnementale
Des concentrations de chlorure de sodium aussi faibles que 150 mg/L (ce qui correspond environ à 60 mg de sodium/L et 90 mg de chlorure/L) peuvent inhiber modérément la croissance des bactéries sensibles dans le sol. Par ailleurs, la nitrification du sol peut être sensiblement réduite à une concentration de chlorure de sodium de 250 mg/kg (environ 100 mg de sodium/kg et 150 mg de chlorure/kg). Or des concentrations de sodium dans le sol supérieures à 60 mg/kg ont été observées à moins de 30 m environ des routes du Canada. On a aussi rapporté des concentrations de chlorure dans le sol supérieures à 200 mg/kg à moins de 200 m environ de routes du Canada.
Enfin, des concentrations suffisamment élevées pour nuire aux microorganismes et autres organismes du sol ont été mesurées dans le sol d'entrepôts de sels.
3.4.2.5 Conclusions
Les concentrations de sodium et de chlorure dans le sol, aux abords des routes du Canada et dans les entrepôts de sels, sont suffisamment élevées pour nuire aux organismes sensibles du sol. Il est cependant très difficile de déterminer à quel point ces effets peuvent nuire aux fonctions de l'écosystème édaphique. Il est possible que les micro-organismes aient une très grande capacité de s'adapter à l'augmentation de la salinité ou de se rétablir à partir des zones non perturbées. Par contre, le pouvoir de dispersion de la faune du sol, comme les vers de terre, est faible car la plupart des espèces sont adaptées à l'humidité relativement élevée du sol. Cependant, lorsque les zones perturbées sont assez petites et qu'elles se limitent par exemple aux bandes de terre qui longent les routes, le rétablissement des populations d'organismes du sol peut se faire assez rapidement, si les conditions salées défavorables sont éliminées.
3.5 Végétation terrestre
L'information présentée dans cette section est tirée de Cain et al. (2001).
Les concentrations élevées de sodium et de chlorure dans le substrat ou le sol influent sur les végétaux de diverses façons, notamment en :
- inhibant l'absorption d'eau et d'éléments nutritifs par les végétaux sous l'effet des déséquilibres osmotiques, ce qui entraîne une diminution de la croissance des pousses et des racines et la manifestation de symptômes apparentés à ceux d'une sécheresse;
- causant un déséquilibre nutritif chez certaines espèces, par la perturbation de l'assimilation d'autres éléments nutritifs;
- inhibant la croissance à long terme et, à de plus fortes concentrations, en ayant des effets toxiques directs sur les cellules des végétaux, ces effets se manifestant par des symptômes de brûlure des feuilles et la mort des tissus, et
- causant la détérioration de la structure du sol.
Une salinité excessive du sol détériore la structure du sol, sous l'effet de l'encroûtement et du colmatage des pores du sol par l'emprisonnement des particules d'argile et de limon dispersées (Morin et al., 2000). L'encroûtement du sol réduit à son tour la levée des pousses à partir des semences en subsurface, de même que la pénétration des racines des semences en surface et subsurface, réduisant de ce fait l'implantation des végétaux. Le colmatage des pores du sol réduit a) l'espace disponible dans le sol pour la rétention d'air et d'eau et b) la pénétration et la perméation de l'air et de l'eau. La diminution de l'aération du sol est préoccupante, car l'apport réduit d'oxygène qui en résulte nuit à la croissance des racines.
La hausse de la concentration de chlorure dans le sol, aux abords des routes, a également pour effet d'accroître la disponibilité des métaux lourds, car le chlorure forme des complexes avec les métaux lourds, ce qui rend bon nombre de ces métaux plus hydrosolubles et donc plus facilement assimilables par les racines des plantes. Il s'ensuit une absorption accrue de métaux par les végétaux qui peut avoir des effets toxiques, selon le type et la quantité de métaux présents dans le sol. Smolders et McLaughlin (1996) notent ainsi un accroissement de la mobilisation du cadmium dans le sol sous l'effet du chlorure, ainsi qu'une absorption accrue de ce métal par les plantes.
Des études en laboratoire et des études expérimentales sur le terrain (non réalisées aux abords des routes) ont démontré que l'application de chlorures de sodium et de calcium (dans le sol ou par pulvérisations) avait causé de graves dommages aux plantes et ces études ont cherché à caractériser les symptômes observés (Hall et al., 1972; Cordukes et Maclean, 1973; Dirr, 1975, 1978; Hofstra et Lumis, 1975; Paul et al., 1984; Headley et Bassuk, 1991; Dkhili et Anderson, 1992; Harrington et Meikle, 1994).
Parmi les symptômes observés après une exposition à des taux élevés de sodium et de chlorure dans le sol, mentionnons le déclin général de la plante, une réduction de la taille des feuilles et de la croissance de la plante, une chlorose des feuilles, la brûlure des feuilles et la mort des tissus. La germination des semences peut aussi être réduite ou retardée.
Le long des routes, les dommages causés aux plantes ligneuses exposées aux pulvérisations de sels résultent de la sécheresse ou du dessèchement des tissus et sont liés à la pénétration d'ions sodium et chlorure phytotoxiques dans les tissus des tiges, des bourgeons et des feuilles (Barrick et Davidson 1980; Chong et Lumis, 1990). La mort des tiges et la mort des bourgeons à feuilles et des bourgeons floraux, habituellement sur les pousses de la première année, sont les principaux symptômes qui se manifestent chez les plantes ligneuses à feuilles caduques. Les bourgeons floraux sont plus sensibles aux sels que les bourgeons à feuilles. Chez les conifères, on observe une perte prématurée des feuilles et un brunissement des aiguilles.
C'est habituellement au printemps que les taux de sels dans le sol ou les tissus végétaux sont les plus élevés, puis ils diminuent sous l'effet des précipitations (lessivage du sol) ou de la croissance des végétaux. Certains espèces peuvent même se rétablir ou repousser, après un traumatisme subi tôt au début de la saison de croissance. Cependant, pour bon nombre de plantes herbacées, la germination ou la repousse se fait à partir de propagules dormants au printemps, lorsque la photopériode, la température et l'humidité atteignent des niveaux précis. Donc, si la présence de fortes concentrations de sels à un endroit cause la destruction d'une banque de semences ou de propagules, il est possible que l'espèce touchée ne repousse pas et il en résultera des changements dans la phytocénose.
Dans le cas des espèces ligneuses, même si les lésions sont souvent pires au printemps et que certaines espèces se rétablissent plus tard durant la saison de croissance, des traumatismes qui se répètent d'année en année réduisent la vigueur et la croissance des végétaux. Et, si les concentrations dans le sol ou les tissus sont suffisamment élevées, il peut y avoir destruction totale de la plante ou un dépérissement marqué qui entraînera l'affaiblissement de la plante et sa mort après un certain nombre d'années (Sucoff, 1975; Lumis et al., 1976). Les plantes ligneuses affaiblies par une exposition répétée aux sels de voirie deviennent en outre plus sensibles aux maladies, aux insectes ou aux stress abiotiques comme la destruction par l'hiver (Sucoff et Hong, 1976) ou la sécheresse.
En ce qui a trait aux espèces ligneuses qui fleurissent au printemps, les bourgeons floraux détruits par le sel ne seront pas remplacés plus tard durant la saison de croissance. Donc si ces dommages se produisent année après année, il en résultera un impact négatif sur la capacité de reproduction des espèces qui fleurissent à cette période.
Dirr (1978) propose de se baser sur le profil des lésions observées chez les végétaux et sur les taux élevés de sels dans le sol ou les tissus pour confirmer que les dommages sont dus réellement aux sels de voirie. Voici les différents profils qui ont été associés aux sels de voirie (Lumis et al., 1973; Dirr, 1976) :
- manifestation de lésions selon un profil linéaire, le long des routes ou dans les régions où s'accumulent les eaux de ruissellement routier;
- manifestation de lésions plus marquées du côté de la plante faisant face à la route;
- diminution des lésions à mesure qu'augmente la distance par rapport à la route;
- aggravation des lésions sur le côté de la route qui est sous le vent;
- absence de symptômes sur les parties des plantes ligneuses protégées par la neige ou à l'abri des éclaboussures;
- absence de lésions, ou lésions moins graves, sur les parties des arbres qui se trouvent au-dessus de la zone exposée aux éclaboussures;
- présence de lésions dues aux éclaboussures de sels de voirie, sur une faible distance seulement dans la végétation dense;
- apparition des lésions sur les conifères à la fin de l'hiver et maintien de ces lésions durant la saison de croissance, et
- apparition des lésions sur les arbres à feuilles caduques au printemps, lorsque la croissance reprend, et maintien de ces lésions durant la saison de croissance.
Pour plus d'informations sur les lésions caractéristiques de l'exposition des végétaux aux sels de voirie, voir Cain et al. (2001).
De nombreuses compilations ont été faites sur les indices de sensibilité des plantes ligneuses, dans le cadre de diverses études expérimentales et études par observation. Une recherche documentaire sur les indices des plantes ligneuses (espèces ornementales et forestières) révèle que de 29,6 à 50,8 % des plantes citées dans chaque rapport ont été jugées sensibles au sel, selon au moins un critère (Sucoff, 1975; Dirr, 1976; Lumis et al., 1977; Thuet, 1977; Beckerson et al., 1980; Dobson, 1991).
Sur la base de leurs observations faites sur le terrain le long de routes de l'Ontario, Lumis et al. (1977) ont déterminé que 30 % des 73 espèces végétales étaient sensibles aux sels de voirie, 7 % d'entre elles ayant manifesté de graves symptômes susceptibles d'entraîner la mort de la plante. Un autre examen des indices de sensibilité des plantes ornementales couramment utilisées au Canada (Beckerson et al., 1980) a révélé que 40 % des 89 espèces étaient sensibles aux sels de voirie.
Selon une étude sur les indices de tolérance au sel de 32 cultivars ou variétés d'arbres fruitiers, de vignes ou d'arbustes, utilisés comme plantes commerciales ou ornementales (Annexe 2 dans Cain et al., 2001), 65 % ont été jugés sensibles aux sels de voirie sur la base d'au moins un critère.
1 Un indice de 1 indique l'absence de dépérissement terminal de la tige ou de brunissement des aiguilles chez les conifères et l'absence de dépérissement terminal, de formation de touffes et d'inhibition de la floraison chez les arbres et arbustes à feuilles caduques. À l'opposé, un indice de 5 indique un dépérissement terminal complet et un brunissement total des aiguilles des conifères, ainsi qu'un dépérissement terminal complet, des signes de formation antérieure de touffes et l'absence de floraison sur les arbres et arbustes à feuilles caduques.
Exposés à des conditions graves, les végétaux ayant un indice de 5 finiront par mourir. Les indices 2, 3 et 4 font référence respectivement à une intensification progressive légère, modérée et élevée des symptômes précités.
Selon Rowe (1972), il existe 15 principaux genres d'arbres (plus de 25 espèces) dans les régions forestières du Canada, dont 11 ont été jugés sensibles aux sels de voirie (section 4.5, dans Cain et al., 2001). Lorsqu'on examine les espèces natif, on constate que 19 des 27 espèces (73 %) ont été jugées sensibles aux sels de voirie selon au moins un critère par différents auteurs (Annexe 9 dans Cain et al., 2001).
Le tableau 19 présente une liste des arbres et arbustes en bordure des routes, en fonction de leur résistance aux sels de voirie véhiculés par les éclaboussures des voitures, d'après Lumis et al. (1983). Une liste des arbres forestiers indigènes, évalués en fonction de leur résistance aux sels de voirie aéroportés, est présentée au tableau 20.
Pour plus d'informations sur la sensibilité des divers types de végétaux, voir Cain et al. (2001).
3.5.1 Évaluation environnementale prudente
Les valeurs-seuils de la CE25 et de la VCT ont été estimées à partir de la documentation scientifique pour le chlorure, le sodium et le chlorure de sodium dans des milieux de croissance (sol, eau du sol ou eau); dans le cas du chlorure de sodium, elles ont aussi été déterminées dans des solutions foliaires et, pour le chlorure et le sodium, dans les tissus des plantes (Cain et al., 2001). Les niveaux minimaux avec effet observé (NMEO) ont été déterminés pour le chlorure et le chlorure de sodium dans les milieux de croissance, de même que les niveaux sans effet observé (NSEO) pour le chlorure de sodium.
3.5.1.1 Valeurs-seuils avec effet observé
Les tableaux 21, 22 et 23 présentent les valeurs-seuils, calculées à partir des données expérimentales ou d'études réalisées aux abords des routes (voir aussi la section 3.6 de Cain et al., 2001). Les espèces végétales présentées incluent des espèces de terres humides (comme les joncs, la sphaigne, les scirpes, les quenouilles et les lenticules), des espèces herbacées (comme les carex, les graminées et les betteraves), des espèces de conifères (comme le pin et l'épinette) et des espèces à feuilles caduques comme l'érable, le pêcher et le prunier. Les valeurs-seuils dans les milieux de croissance (solution du sol appliquée) varient de 67,5 à 300 ppm pour le sodium, de 215 à 1 500 ppm pour le chlorure et de 280 à 66 600 ppm pour le chlorure de sodium (tableau 21). Elles s'établissent entre < 280 et 17 800 ppm de sodium et à < 4 100 mg/L de chlorure dans les tissus de plantes herbacées, après une exposition dans une solution du sol ou une solution aqueuse (tableau 22) et varient de 200 à 16 100 ppm de sodium et de 800 à 70 700 ppm de chlorure dans les tissus de plantes ligneuses exposées par voie aérienne. Enfin, elle est de 7 140 ppm de chlorure de sodium, après pulvérisation foliaire (tableau 23).
Pour l'évaluation prudente, on a utilisé les concentrations minimales déterminées par l'analyse des valeurs-seuils (section 3.6 dans Cain et al., 2001) pour chaque type d'exposition décrite précédemment, d'après les évaluations expérimentales ou l'échantillonnage fait au-delà de l'emprise des routes ou des autoroutes.
3.5.1.2 Valeurs estimées de l'exposition
Les VEE utilisées pour l'évaluation prudente sont les valeurs maximales extraites de la documentation portant sur les concentrations environnementales de chlorure ou de sodium au Canada dans des milieux de culture (sol ou eau) d'après l'échantillonnage fait au-delà de l'emprise routière, ou les valeurs les plus élevées tirées de la documentation traitant des concentrations de chlorure et de sodium mesurées dans la végétation poussant en dehors de l'emprise routière au Canada.
La présente évaluation est basée sur des valeurs d'exposition de 240 ppm de chlorure et de 45 ppm de sodium dans le sol, lesquelles concentrations ont été mesurées dans des échantillons prélevés au-delà de l'emprise, à 40 m de l'autoroute, dans le cadre d'une étude réalisée le long d'une autoroute à quatre voies de l'Ontario (Hofstra et Smith, 1984). La plus forte concentration de chlorure dans le sol le long d'une autoroute (1 050 ppm) a été mesurée dans un échantillon prélevé dans le terre-plein central, tandis que la concentration maximale de sodium (890 ppm) a été mesurée dans un échantillon prélevé à 10 m de l'autoroute, dans le cadre de la même étude.
1 S - sensible, MS - modérément sensible, M - moyenne, MT - modérément tolérante, T - tolérante.
Aucune référence canadienne ne fait état des concentrations de chlorure de sodium dans le sol. Une valeur a donc été estimée à partir de la concentration de chlorure mesurée dans le sol, à 40 m de l'autoroute (240 ppm); cette valeur a été multipliée par un facteur de 1,6485, ce qui donne une valeur de 396 ppm de chlorure de sodium. Une deuxième valeur pour le chlorure de sodium dans le sol a été estimée à partir de la concentration de sodium dans le sol mesurée à 40 m de l'autoroute (45 ppm); cette concentration a été multipliée par un facteur de 2,542, pour une valeur de 114 ppm. La moyenne de ces deux valeurs (255 ppm) a été utilisée comme estimation prudente.
La documentation qui indiquait les concentrations de chlorure ou de sodium dans les tissus végétaux à certaines distances de routes ou d'autoroutes, après exposition aux sels de voirie aéroportés, a été analysée pour calculer les VEE des plantes au chlorure de sodium, par le biais de l'exposition aérienne aux sels de voirie (voir la section 2.3 dans Cain et al., 2001). Trois documents ont été consultés pour évaluer les concentrations de chlorure et de sodium dans les tissus; ces données portent sur des échantillons de tissus de végétaux prélevés à une distance de 10 m à 200 m de la route ou de l'autoroute et sont tirées d'études faites en Ontario sur des espèces de pêchers et de pruniers (Prunus) et d'autres végétaux non spécifiés.
Les concentrations tissulaires utilisées pour l'évaluation, soit 4 600 ppm de chlorure et 3 500 ppm de sodium, ont été mesurées dans des pêchers (Prunus persica) cultivés à 40 m d'une autoroute à quatre voies, en dehors de l'emprise routière, dans le sud de l'Ontario (Northover, 1987). Par comparaison, la plus forte concentration tissulaire de chlorure a été de 11 000 ppm, rapportée dans des végétaux non précisés poussant à 60 m d'une autoroute à quatre voies de l'Ontario (Hofstra et Smith, 1984).
Northover (1987) rapporte également une concentration de chlorure de 9 000 ppm dans des pêchers cultivés à 20 m d'une autoroute à quatre voies du sud de l'Ontario. La plus forte concentration de sodium dans les tissus a été de 6 900 ppm, celle-ci ayant été mesurée dans les tissus de branches de pêchers poussant à 20 m d'une autoroute à quatre voies du sud de l'Ontario (Northover, 1987).
3.5.1.3 Estimation des quotients
D'après l'information indiquée à la section 3.5.1.2, on constate que les concentrations de chlorure et de sodium mesurées dans les sols et les tissus végétaux, au Canada, en dehors de l'emprise routière, sont supérieures et, dans un cas, égales aux concentrations avec effets observés indiquées à la section 3.5.1.1 et à la section 3.6 dans Cain et al. (2001). Une évaluation détaillée des effets des sels de voirie sur la végétation terrestre est donc justifiée.
3.5.2 Évaluation environnementale détaillée - Analyse basée sur les valeurs-seuils
La caractérisation du risque consiste à passer en revue les concentrations de chlorure et de sodium dans le sol ou les tissus qui provoquent des effets biologiques pertinents sur la végétation, puis à établir un lien avec les concentrations décelées dans l'environnement canadien. Les données présentées sont tirées principalement d'études canadiennes et incluent les valeurs-seuils indiquées précédemment à la section 3.5.1.1, ainsi qu'à la section 3.6 de Cain et al. (2001).
3.5.2.1 Réaction à la présence de sodium dans le sol
Les valeurs-seuils pour le chlorure de sodium appliqué aux racines se situent entre 67,5 et 300 ppm de sodium (tableau 21 qui précède et section 3.6 dans Cain et al., 2001). Les végétaux les plus sensibles sont des jeunes plants de pin ponderosa de deux ans (Pinus ponderosa) dont la valeur-seuil a été établie à 67,5 ppm d'après les lésions foliaires observées après l'application dans le sol d'une solution de chlorure de sodium; la mortalité s'est produite à une concentration de 140 ppm de sodium (Bedunah et Trlica, 1979). Le taux de germination des semences de graminées et de fleurs sauvages à larges feuilles des Prairies a été réduit d'environ 60 à 70 % et la croissance des racines, dans une proportion atteignant 73 %, lorsque ces végétaux ont été exposés à un taux de 100 à 400 ppm de chlorure de sodium (environ 40 à 160 ppm de sodium) (Harrington et Meikle, 1994). Les valeurs-seuils de la CE25 dans le sol, qui ont été estimées à partir de cette étude, se situent entre 202 et 270 ppm.
Une concentration de sodium supérieure à l'intervalle des valeurs-seuils estimées (67,5 à 300 ppm) a été mesurée dans un certain nombre d'échantillons de sol prélevés au Canada à une distance d'environ 30 m ou moins des routes (figure 2.17 dans Cain et al., 2001). Une concentration de 890 ppm de sodium a ainsi été observée dans le sol, à 10 m d'une autoroute à quatre voies du sud de l'Ontario (Hofstra et Smith, 1984), et la même étude a révélé une concentration de 45 ppm de sodium à 40 m de l'autoroute, en dehors de l'emprise.
3.5.2.2 Réaction à la présence de chlorure dans le sol
L'intervalle des valeurs-seuils pour le chlorure de sodium appliqué aux racines se situe entre 215 et 1 500 ppm (tableau 21 qui précède et section 3.6 dans Cain et al., 2001). Les végétaux les plus sensibles sont des jeunes plants de pin ponderosa de deux ans, la valeur-seuil étant de 215 ppm de chlorure d'après les lésions foliaires observées après l'application dans le sol d'une solution de chlorure de sodium. La mortalité s'est produite à une concentration de 350 ppm de chlorure (Bedunah et Trlica, 1979).
Le NMEO, associé à une réduction de la croissance moyenne de la sphaigne (Sphagnum recurvum), a été estimé à 300 ppm de chlorure en solution hydroponique (Wilcox, 1984). Wilcox et Andrus (1987) ont observé des effets sur la reproduction (production réduite de gamétophores) chez Spagnum fimbriatum exposé à 300 ppm de chlorure.
Dans un certain nombre d'échantillons de sol prélevés au Canada, à une distance d'au plus 200 m des routes, la concentration de chlorure a dépassé le seuil minimal estimé (215 à 500 ppm) (figure 2.16 dans Cain et al., 2001).
Des concentrations de chlorure supérieures à 500 ppm n'ont été observées qu'à proximité des routes. Une concentration de chlorure de 240 ppm a été décelée dans des échantillons de sol recueillis à 40 m d'une autoroute à quatre voies, au-delà de l'emprise, dans le sud de l'Ontario (Hofstra et Smith, 1984) et une concentration de 1 200 ppm de chlorure a été rapportée dans le sol, derrière un entrepôt de sels situé près d'une autoroute, dans le nord-ouest de l'Ontario (Racette et Griffin, 1989).
3.5.2.3 Réaction à la présence de chlorure de sodium dans le sol
L'intervalle des valeurs-seuils pour le chlorure de sodium appliqué aux racines varie de 280 à 66 600 ppm (tableau 21 qui précède et section 3.6 dans Cain et al., 2001). Les espèces les plus sensibles sont deux espèces de terres humides, soit le carex trisperme (Carex trisperma) et le némopanthe mucroné (Nemopanthus mucronata [mucronatus]) dont les limites de tolérance au sel ont été établies à 280 ppm d'après les gradients de concentration du chlorure de sodium dans l'eau de marais (Wilcox, 1986a). La survie de l'épinette du Colorado (Picea pungens) et la croissance du pin sylvestre (Pinus sylvestris) ont été réduites par des concentrations de chlorure de sodium de 600 ppm (Werkhoven et al., 1966).
Schauffler (1993) a noté des effets sublétaux, une augmentation de la biomasse et un phénomène de tallage chez la linaigrette dense (Eriophorum vaginatum var. spissum) qui avait été exposée à une concentration de 400 ppm de chlorure de sodium en culture hydroponique, ainsi que des effets sur la reproduction (diminution de la production de fleurs), à une concentration de 1 600 ppm.
Aucune étude canadienne ne mentionne de concentrations de chlorure de sodium dans le sol; des valeurs ont donc été estimées à partir des concentrations rapportées de sodium et de chlorure. On a ainsi estimé à 1 978 ppm la concentration de chlorure de sodium dans le sol, en multipliant la concentration maximale de chlorure mesurée dans un sol adjacent à un entrepôt de sels (1 200 ppm) par un facteur de 1,6485. Une deuxième valeur (2 262 ppm) a été estimée en multipliant la concentration maximale de sodium mesurée dans le sol à 10 m de l'autoroute, soit 890 ppm, par un facteur de 2,542. La moyenne de ces deux valeurs (2 120 ppm) est environ 10 fois supérieure à la limite inférieure de l'intervalle des valeurs-seuils (280 ppm).
En utilisant la même méthode de calcul, on a estimé à 255 ppm la concentration de chlorure de sodium à l'extérieur de l'emprise routière, à partir de concentrations de chlorure (240 ppm) et de sodium (40 ppm) mesurées à 40 m d'une autoroute à quatre voies du sud de l'Ontario (Hofstra et Smith, 1984). Cette valeur se situe près de la valeur-seuil (280 ppm).
3.5.2.4 Réaction au sodium et au chlorure par dispersion aérienne
Les valeurs-seuils, liées à l'exposition aérienne au chlorure de sodium, se situent entre 800 et 70 700 ppm de chlorure et entre 200 et 16 100 ppm de sodium (tableau 23 qui précède et section 3.6 de Cain et al., 2001). Les espèces les plus sensibles dans l'environnement canadien sont le pêcher et le prunier (Prunus domestica), les valeurs-seuils pour ces espèces s'établissant à 800 ppm de chlorure et 650 ppm de sodium d'après le dépérissement terminal des branches (un effet sublétal) consécutif à une exposition atmosphérique (McLaughlin et Pearson, 1981). Pour bon nombre d'espèces de pin (Pinus spp.), les seuils de mortalité s'établissent à 13 000 ppm de chlorure et 8 000 ppm de sodium (Townsend et Kwolek, 1987). En ce qui a trait aux effets sur la reproduction évalués en fonction du rendement en fruits (pêches), les valeurs-seuils sont respectivement de 1 000 ppm et 1 700 ppm (Northover, 1987).
Des concentrations tissulaires supérieures aux valeurs-seuils minimales (soit 800 ppm de chlorure et 650 ppm de sodium), estimées pour les espèces végétales sensibles (section 3.6.2 de Cain et al., 2001), ont été observées à des distances atteignant jusqu'à 120 m de l'autoroute environ dans le cas du sodium et jusqu'à 200 m pour le chlorure. Des concentrations tissulaires de 4 600 ppm de chlorure et de 3 500 ppm de sodium ont été mesurées dans des pêchers cultivés à une distance de 40 m, en dehors de l'emprise d'une autoroute à quatre voies du sud de l'Ontario (Northover, 1987). Les plus fortes concentrations observées dans des plantes ligneuses poussant le long d'une route ont été de 9 000 ppm de chlorure et de 6 900 ppm de sodium, ces concentrations ayant été mesurées dans les tissus de branches de pêchers poussant à 20 m d'une autoroute à quatre voies du sud de l'Ontario (Northover, 1987).
3.5.2.5 Évaluation environnementale détaillée -résumé de l'analyse basée sur les valeurs-seuils
Des taux élevés de sodium et de chlorure dans le sol ont été enregistrés jusqu'à 30 m d'autoroutes à quatre voies (Hofstra et Smith, 1984; Davis et al.,1992) et jusqu'à 15 m d'autoroutes à deux voies (Davis et al., 1992; Soilcon Laboratories Ltd., 1995). Les concentrations pourraient dépasser les intervalles des valeurs-seuils établis pour le sodium (67,5 à 300 ppm) et le chlorure (215 à 500 ppm) sur une distance d'environ 30 m des autoroutes (figures 2.7 et 2.8 dans Cain et al., 2001) selon le type de route, les taux d'épandage, la topographie locale et le climat. On a aussi observé un dépassement des valeurs-seuils à des endroits où il y avait eu accumulation d'eaux de ruissellement salées (Racette et Griffin, 1989).
De même, on a rapporté de fortes concentrations tissulaires de sodium et de chlorure dans des végétaux poussant en bordure d'autoroutes du sud de l'Ontario. Ainsi, des concentrations dépassant les valeurs-seuils minimales estimées pour les espèces végétales sensibles (soit 650 ppm pour le sodium et 800 ppm pour le chlorure - section 3.6.2 de Cain et al., 2001) ont été mesurées sur une distance d'environ 120 m des autoroutes pour le sodium et jusqu'à 200 m, dans le cas du chlorure.
3.5.3 Évaluation environnementale détaillée - analyse des lieux de référence
Nous présentons dans cette section une analyse sur divers lieux de référence documentant les effets sur la végétation imputables à l'épandage de sels de voirie. Un certain nombre d'études canadiennes ont évalué les concentrations environnementales de sodium et de chlorure, ainsi que les effets sur les végétaux résultant de l'épandage de sels de voirie ou du ruissellement provenant d'entrepôts de sels servant à l'entretien des autoroutes. Certaines études américaines applicables au Canada sont aussi examinées. La section 4.4 de Cain et al. (2001) offre plus de détails sur ces études.
3.5.3.1 Propagation d'espèces végétales halophiles
On a constaté la propagation d'espèces halophiles, caractéristiques des zones côtières et des marais salés, le long de certaines routes de l'Ontario. Ainsi, Catling et McKay (1980) y ont observé la présence de 20 espèces de plantes halophiles, dont quatre signalées pour la première fois dans cette province et quatre autres dont l'aire de distribution s'était largement étendue. Les espèces mentionnées par Catling et McKay sont des espèces naturelles, et non des espèces qui avaient été plantées par les services d'entretien des routes pour la stabilisation ou l'aménagement du terrain. Ces espèces se sont propagées naturellement le long des autoroutes, en réponse à l'épandage de sels de voirie et au déclin de la végétation non adaptée. Les endroits étudiés avaient des concentrations de sodium de l'ordre de 1 000 ppm et les conditions de croissance variaient de milieux aquatiques à humides ou à de milieux périodiquement humides à secs. Ces endroits incluent des fossés, des terre-pleins centraux de routes et d'autoroutes, des zones adjacentes à des autoroutes exposées au ruissellement salé et des zones adjacentes à des entrepôts de sels et des lieux d'élimination de la neige, y compris des zones situées à l'intérieur et à l'extérieur des emprises routières aménagées ou vertes.
Parmi les espèces qui tolèrent des taux de sodium dans le sol variant de 500 à 1 000 ppm et qui sont souvent qualifiées d'espèces halophiles, mentionnons la quenouille à feuilles étroites (Typha angustifolia), le roseau commun (Phragmites australis) et les espèces adventices telles les espèces annuelles et vivaces de laiteron (Sonchus oleraceus, Sonchus arvensis, Sonchus uliginosus), la petite herbe à poux (Ambrosia artemisiifolia), la carotte sauvage (Daucus carota) et le kochia à balais (Kochia scoparia).
Reznicek et al. (1976) rapportent quant à eux une augmentation de la distribution de Carex praegracilis, une espèce de carex de l'ouest qui tolère les alcalis, depuis l'année (1973) où cette espèce a été observée pour la première fois en Ontario. Cette plante a ainsi été observée à 28 endroits le long des autoroutes de 14 comtés, en général à l'intérieur de l'emprise routière. D'autres rapports (Catling et MaKay, 1980) font état de la présence de cette espèce aux abords des routes et dans le terre-plein central des autoroutes.
Des observations similaires de la propagation d'espèces halophiles ont été faites au Michigan, un État dont le climat et la flore se comparent à ceux du sud de l'Ontario (Reznicek, 1980).
3.5.3.2 Changements dans les communautés d'un marais perturbé par les sels de voirie
Le marais Pinhook, situé dans le nord-ouest de l'Indiana, au sud-est de la ville de Michigan, a été choisi pour étudier les effets de la contamination par le sodium et le chlorure imputable au ruissellement des sels de voirie (Wilcox, 1982, 1986a,b). Cette étude prouve que des taux élevés de sels ont une incidence sur la phytocénose. Un grand nombre des espèces végétales prédominantes dans ce marais sont des espèces indigènes des terres humides, qui sont également présentes au Canada. Cette région de l'Indiana fait partie du bassin des Grands Lacs et de la même zone climatique que certaines parties du sud de l'Ontario, la région de Montréal, les provinces de l'Atlantique et la Colombie-Britannique.
De 1963 à 1972, des sels de voirie ont été entreposés à découvert, sur une berge adjacente au marais. Un dôme de protection a été placé sur le tas de sels en 1972 afin de limiter le ruissellement, et l'entreposage de sels à cet endroit a pris fin au milieu de 1981. Le marais recevait aussi les eaux de ruissellement provenant d'un tronçon d'un kilomètre d'une autoroute à quatre voies, où 11 300 kg/km de sels de voirie étaient épandus chaque année (5 650 kg par kilomètre de route à deux voies).
Dans la zone la plus perturbée, la concentration moyenne a atteint jusqu'à 486 ppm de sodium et 1 215 ppm de chlorure dans les eaux interstitielles du lit du marais. Une corrélation a été établie entre la distribution des concentrations élevées de sodium et de chlorure dans le marais et les zones où la végétation avait été perturbée. La concentration de sels dans la rhizosphère a diminué chaque année de 1979 à 1981.
De 1980 à 1983, des évaluations ont été faites de la végétation, dans les portions perturbées et non perturbées du marais. La contamination par le sel a provoqué une modification des espèces végétales dans les zones perturbées, presque toutes les plantes endémiques ayant disparu des sections du marais exposées à de fortes concentrations de sels. Elles avaient été remplacées par des espèces non spécifiques du marais, principalement la quenouille à feuilles étroites.
Sous l'effet d'une diminution de 50 % des concentrations de sels durant les quatre années de l'étude, bon nombre des espèces endémiques sont apparues de nouveau dans le marais. De plus, certaines espèces qui avaient envahi le marais au moment où les concentrations de sels étaient élevées ont décliné alors que d'autres, comme la quenouille à feuilles étroites et l'aronie à feuille de prunier (Pyrus floribunda), sont demeurées dominantes dans certaines autres parties perturbées. Cette étude montre que les communautés végétales des terres humides peuvent se rétablir après l'élimination de la source de sels, bien que certaines espèces envahissantes puissent persister et entraîner ainsi des changements permanents dans la composition de la phytocénose.
3.5.3.3 Effets de la dispersion de sels provenant d'une autoroute à quatre voies sur des vergers de pêches et de prunes de Grimsby (Ontario)
Une étude a été faite dans un certain nombre de vergers de pêches et de prunes situés le long de la Queen Elizabeth Way, une autoroute à quatre voies de la région de Grimsby et Beamsville, en Ontario (McLaughlin et Pearson, 1981), afin de déterminer dans quelle mesure les effets de la dispersion de sels varient en fonction de la distance. Ces plantations étaient situées sur des terrains privés, en dehors de l'emprise routière. On a étudié le dépérissement terminal des pêchers et des pruniers en avril 1980 et 1981 et les concentrations de chlorure et de sodium ont été mesurées dans des échantillons de branches.
Le contenu en chlorure et en sodium des branches, maximal à proximité de l'autoroute, a généralement diminué à mesure qu'on s'éloignait de l'autoroute (figures 4.15 et 4.16 dans Cain et al., 2001). La concentration de sodium dans les tissus des branches était de 2 030 ppm à 45 m de l'autoroute et la concentration de chlorure était de 2 300 ppm, à 40 m de l'autoroute.
C'est dans les arbres situés les plus près de l'autoroute que le dépérissement terminal a été le plus marqué, ce phénomène diminuant à mesure qu'on s'éloignait de l'autoroute (figure 4.17 dans Cain et al., 2001). Il convient toutefois de noter que le degré de dépérissement a varié d'une année à l'autre et d'une espèce à l'autre; des dommages plus importants ont ainsi été observés du côté sud de l'autoroute, en avril 1981, alors que le dépérissement terminal des pêchers a été de 288 mm à une distance de 22 m de l'autoroute, diminuant à 97 mm, à 82 m de l'autoroute. En avril 1980, le dépérissement terminal des pêchers du côté sud de l'autoroute est passé de 91 mm, à une distance de 36 m de l'autoroute, à 8 mm, à 82 m de l'autoroute. Une corrélation a été établie entre le dépérissement terminal et les concentrations de sodium et de chlorure dans les tissus. Les données combinées sur les pêchers et les pruniers indiquent un accroissement du dépérissement avec l'augmentation des concentrations de sodium et de chlorure (évaluation des valeurs-seuils, Annexe 8 dans Cain et al., 2001).
3.5.3.4 Effets de la dispersion de sels provenant d'une autoroute à quatre voies sur des vergers de pêches et de prunes situés près de St. Catharines (Ontario)
Les effets de la dispersion de sels ont aussi été étudiés sur des pêchers Loring durant l'hiver 1973-1974 (Northover, 1987). Les arbres étaient situés du côté sud d'une section est-ouest de la Queen Elizabeth Way, une autoroute à péage à quatre voies achalandée, près de St. Catharines (Ontario). Le verger était à la même élévation que l'autoroute, sur un terrain privé, à l'extérieur de l'emprise routière.
La concentration de sodium et de chlorure dans les tissus des pousses a diminué à mesure qu'a augmenté la distance par rapport à l'autoroute. La teneur en chlorure dans les tissus des branches de pêchers à 20 m de l'autoroute était ainsi quatre fois supérieure à celle observée à une distance de 120 m (9 000 ppm contre 1 900 ppm de chlorure). La teneur en sodium était quant à elle plus de sept fois le taux mesuré à 120 m de l'autoroute (6 900 ppm contre 900 ppm de sodium).
Le rendement fruitier a été réduit à des distances de moins de 80 m de l'autoroute, le nombre de pêches par pousse augmentant à mesure qu'on s'éloignait de l'autoroute. À 20 m de l'autoroute, 97 % des tiges de la cime étaient mortes, ce pourcentage diminuant à mesure qu'on s'éloignait de l'autoroute, pour atteindre 8 % à 80 m de l'autoroute et se situer à un niveau de fond (moins de 1 %), à 120 m de l'autoroute. Une corrélation positive a été observée entre la teneur en sodium et en chlorure des pousses et le pourcentage de bois mort dans la cime des arbres.
Les taux de sodium et de chlorure dans le sol n'étaient pas élevés dans ces vergers, ce qui signifie que la forte teneur dans les tissus et les effets sur les plantes ont été causés principalement par la dispersion atmosphérique de sels provenant de l'autoroute.
3.5.3.5 Effets de la dispersion de sels provenant d'une autoroute à deux voies sur des bleuets, dans l'ouest de la Nouvelle-Écosse
Eaton et al. (sans date) ont évalué les effets des sels de voirie provenant d'une autoroute à deux voies de la région de Folly Mountain, à l'ouest de Truro, entre les hivers 1993 à 1995, sur des peuplements naturels, mais aménagés, de bleuets nains situés sur des terrains adjacents. Durant les hivers 1993-1994 et 1994-1995, respectivement 33 et 40 tonnes de chlorure de sodium par kilomètre d'autoroute ont été épandues dans cette région.
À moins de 35 m de cette autoroute, le nombre de boutons à fleurs et le rendement fruitier ont été réduits, mais ils se rapprochaient des niveaux de fond, à plus de 50 m de l'autoroute. À moins de 10 m de l'autoroute, le nombre de boutons a été de 60 % à 90 % inférieur à celui observé dans des échantillons prélevés à 50 m de l'autoroute, alors que le rendement
a été réduit d'au moins 50 %. En 1994, le rendement obtenu sous une structure de protection faite d'une pellicule pour pépinière a été de 4 224 kg/ha de fruits frais, comparativement à moins de 2 000 kg/ha à 30 m et à moins de 200 kg/ha, à 5 m de l'autoroute. En 1995, le rendement sous la structure de protection a été de 8 092 kg/ha, comparativement à 3 000 kg/ha à 35 m et à moins de 1 500 kg/ha, à 5 m de l'autoroute.
En 1993-1994 et 1994-1995, les taux de sels dans les tissus de tiges prélevés de plants sous la structure de protection ont été respectivement de 0,53 g et de 0,3 g de chlorure de sodium pour 20 tiges, alors qu'ils ont atteint de 6 g à plus de 10 g, à 10 m de la route au printemps 1994 et de 3 g à plus de 8 g, au printemps 1995; des taux élevés dans les tissus ont été mesurés jusqu'à 45 ou 50 m de l'autoroute. Une corrélation négative a été observée entre la réduction du nombre de boutons et du rendement et la teneur élevée en sels dans les tiges de bleuets prélevées durant l'hiver et tôt au printemps.
3.5.3.6 Concentrations dans le sol et les plantes ligneuses aux abords d'autoroutes dans l'intérieur de la Colombie-Britannique
Davis et al. (1992) ont étudié les causes du dépérissement et des lésions observés sur des arbres de 17 sites forestiers du centre-sud et de l'est de la Colombie-Britannique, situés le long d'autoroutes à deux, trois et quatre voies.
À 15 de ces sites, il y avait épandage de chlorure de sodium sur les routes durant l'hiver, dans une proportion variant de 60 kg à 130 kg par kilomètre de voie, selon les besoins. Dans les deux autres sites situés le long de routes de gravier, le chlorure de sodium n'était pas utilisé comme agent de déglaçage, mais du sable contenant de 3 à 5 % de chlorure de sodium était épandu en hiver et, durant l'été, du chlorure de magnésium ou du chlorure de calcium était utilisé pour le traitement antipoussière, d'abord à raison de 2 L/m2 puis à un taux de 1,6 L/m2 au moment de l'étude.
Une évaluation détaillée sur le terrain a été faite de ces 17 sites. Pour ce faire, trois parcelles d'échantillonnage ont été définies, dont deux parcelles où les arbres présentaient des lésions de modérées à graves et une parcelle témoin, sans symptôme apparent. Une évaluation détaillée a été faite des symptômes de dommages à la végétation associés aux sels, ainsi que des lésions attribuables à d'autres facteurs notamment au stress abiotique, aux maladies, aux insectes ou au bris. Des échantillons de sol et de végétaux ont été analysés pour en déterminer la teneur en sodium et en chlorure et évaluer d'autres paramètres, et on a dressé un bilan détaillé de chaque site.
Dans 14 sites, les dommages subis par les conifères ont été similaires, les lésions diminuant à mesure qu'on s'éloignait de la route. Ces dommages étaient en outre caractéristiques des lésions causées par les sels de voirie chez les espèces ligneuses, incluant la pyrolyse, la chute des feuilles, le dégarnissement des cimes ainsi que la défoliation et le dépérissement terminal marqués chez les arbres gravement atteints. Dans la plupart des cas, ces dommages se sont manifestés à l'intérieur d'une bande étroite située à une distance de 5 à 15 m dans la pente de l'autoroute. Ailleurs, des dommages ont été observés à 2 m à peine de la route, dans un peuplement forestier situé près de la route. À un autre endroit où le peuplement recevait les eaux de ruissellement routier acheminées par un ponceau, des dommages ont été observés sur une distance de 40 m. Dans un autre site, des dommages mineurs attribués à la dispersion de sels provenant de la route ont été décelés à 50 m de l'autoroute. Dans bon nombre de ces endroits, les dommages se sont manifestés à l'intérieur de l'emprise routière car, dans cette province, l'emprise avec végétation s'étend habituellement sur une distance de 4,5 à 5 m en bordure des autoroutes à deux voies, mais peut atteindre jusqu'à 10 m sur certaines autoroutes. À d'autres endroits, les dommages se sont manifestés en dehors de l'emprise routière, à plus de 5 à 10 m de l'autoroute.
Dans les parcelles témoins, les concentrations de chlorure dans le sol à une profondeur de 0 à 10 cm ont varié entre < 1 et 12 ppm, alors qu'elles ont été de 0,9 à 230 ppm dans les parcelles qui avaient subi des dommages, dépassant 25 ppm à six sites. À deux endroits longeant une autoroute à quatre voies, les taux de chlorure dans le sol ont fluctué entre 3,0 et 198 ppm.
En ce qui a trait au sodium, les concentrations dans le sol à une profondeur de 0 à 10 cm ont été de < 1 à 8,5 ppm dans les parcelles témoins, mais de 0,02 à 50,2 ppm dans les parcelles endommagées. À 13 sites, les concentrations dans une ou les deux parcelles expérimentales ont été supérieures aux concentrations dans la parcelle témoin et elles ont dépassé 17 ppm, à sept sites. Dans deux de ces sites qui longeaient une autoroute à quatre voies, la concentration de sodium a atteint jusqu'à 43 ppm.
La teneur en chlorure des aiguilles provenant de parcelles perturbées a été jusqu'à 3,4 fois supérieure à la concentration mesurée dans les aiguilles de parcelles témoins, alors que leur teneur en sodium a été jusqu'à 206 fois supérieure à celle des aiguilles des parcelles témoins.
Aux deux endroits où il n'y avait pas d'épandage de chlorure de sodium durant l'hiver, le taux de sodium dans les tissus a été faible; par contre, la concentration tissulaire de chlorure dans les échantillons prélevés dans au moins une des deux parcelles endommagées a été de 2 à 2,4 fois supérieure au taux mesuré dans la parcelle témoin. À ces endroits, des lésions ont été observées sur des végétaux situés à moins de 10 m de la route, à l'intérieur et à l'extérieur de l'emprise. À un de ces endroits, la teneur en chlorure du sol a atteint 225 ppm, mais la teneur en sodium a été faible. Les lésions observées sur les arbres à ces deux endroits ont été attribuées à l'épandage de chlorure de calcium ou de chlorure de magnésium dans le cadre des programmes d'entretien des routes en vue d'éliminer la poussière durant l'été.
Cette étude montre que le chlorure de sodium utilisé comme agent de déglaçage et le chlorure de calcium ou de magnésium utilisé comme abat-poussière durant l'été ont fortement contribué aux lésions observées sur les arbres en bordure de la route, ainsi qu'au dépérissement de la végétation dans 16 de ces sites. Cette conclusion s'appuie sur les symptômes manifestés par les végétaux, le profil des lésions observées et les concentrations élevées de sodium et de chlorure mesurées dans le sol et la végétation.
3.5.3.7 Concentrations dans le sol et le feuillage de plantes ligneuses le long d'une route à deux voies de la Colombie-Britannique
Soilcon Laboratories Ltd. (1995) ont étudié les taux de sels dans le sol et dans les tissus de végétaux, en fonction des dommages observés le long d'un tronçon de 2 km de Loon Lake Road, une route à deux voies au nord-ouest de Kamloops (Colombie-Britannique). Le pin ponderosa et le Douglas taxifolié (Pseudotsuga menziesii) sont les deux essences forestières dominantes à cet endroit.
Le taux d'épandage de sel gemme était de 22, 88 ou 153 kg par kilomètre de route à deux voies, selon qu'il fallait procéder à un épandage faible, modéré ou élevé. La charge totale de sels durant l'hiver a été de 1 561 kg par kilomètre de route à deux voies, dont 1 031 kg de sel gemme et 530 kg de sable ayant une teneur en sels de 5 %. L'épandage de sels ou de sable s'est fait entre le 15 novembre 1993 et le 23 février 1994.
Neuf sites ont été évalués à l'intérieur de ce tronçon de 2 km de Loon Lake Road, à des endroits où les arbres manifestaient des symptômes légers, moyens ou graves causés par le sel. Les arbres présentant des lésions de modérées à graves étaient situés à une distance de 3 à 8,4 m de la route, à l'intérieur et à l'extérieur de l'emprise, alors que ceux présentant peu de dommages se trouvaient à une distance de 10 à 20 m de la route, en dehors de l'emprise.
Des échantillons de sol ont été prélevés aux neuf endroits, entre décembre 1993 et avril 1994, afin de déterminer les concentrations de chlorure et de sodium et de les comparer aux valeurs mesurées dans les échantillons témoins prélevés en avril 1991. Dans les sites où les arbres avaient subi des dommages de modérés à graves, la concentration de chlorure dans le sol à une profondeur de 0 à 10 cm a été de 31,3 ppm (intervalle : 4,1 à 84,5 ppm) en décembre, mais elle avait diminué à 5,12 ppm (intervalle : 1,6 à 12,6 ppm), en avril. Dans les sites présentant peu de dommages, la concentration de chlorure dans le sol, à une profondeur de 0 à 10 cm, a été de 7,2 ppm (intervalle : 1,4 à 23,5 ppm) en décembre, mais de 2,9 ppm en avril (intervalle : 1,3 à 4,5 ppm). La concentration de fond de chlorure était de 3,8 ppm (intervalle : 0,2 à 7,5 ppm).
Dans les sites affichant des dommages modérés et graves, la concentration de sodium mesurée à une profondeur de 0 à 10 cm du sol a été de 15,9 ppm (intervalle : 1,9 à 28,2 ppm) en décembre, mais est descendue à 9,1 ppm en avril (intervalle : 1,0 à 30,7 ppm). Dans les sites peu touchés, la concentration de sodium à une profondeur de 0 à 10 cm a été de 4,7 ppm (intervalle : 5,6 à 11,7 ppm) en décembre et de 1,2 ppm en avril (intervalle : 0,5 à 1,8 ppm). La concentration de fond de sodium était de 2,3 ppm (intervalle : 2,0 à 2,7 ppm).
Tant en décembre qu'en avril, les concentrations de chlorure et de sodium dans le sol ont été plus élevées aux endroits où les arbres avaient subi des dommages modérés ou graves qu'à ceux affichant des dommages légers. Par ailleurs, au moment de l'échantillonnage d'avril, les concentrations dans le sol avaient diminué à un niveau comparable aux concentrations de fond, probablement sous l'effet du lessivage par les précipitations, puisque le dernier épandage de sels a été fait en février.
Durant la période d'échantillonnage de décembre à avril, la concentration de chlorure a varié de 110 à 560 ppm dans le feuillage des arbres peu endommagés, de 110 à 3 180 ppm dans le feuillage des arbres ayant subi des dommages modérés et de 870 à 5 590 ppm dans le feuillage des arbres lourdement endommagés.
Durant la même période, les concentrations de sodium dans le feuillage ont varié respectivement de 0,5 à 70 ppm, de 0,5 à 190 ppm et de 30 à 920 ppm, selon que les arbres avaient subi des dommages légers, modérés ou graves.
3.5.3.8 Concentrations dans le feuillage de plantes ligneuses longeant une autoroute à deux voies du Connecticut
Button et Peaslee (1966) rapportent les concentrations de chlorure et de sodium mesurées dans le feuillage d'érables à sucre (Acer saccharum) à maturité (environ 70 ans). Ces arbres poussaient à proximité (de 1 à 4 m) de la Route 17 reliant Middletown et Durham, une route à deux voies du Connecticut, sans doute à l'intérieur de l'emprise routière. Cette étude est pertinente pour le Canada, puisque l'érable à sucre est une essence forestière indigène, qui est utilisée à la fois pour la production de sirop d'érable et comme essence ornementale. Cette étude illustre également le type de lésions résultant de l'exposition aux sels de voirie véhiculés par les eaux de ruissellement.
Bien que ces auteurs ne précisent pas la charge de sels, ils indiquent que 63 000 tonnes de sel gemme et 2 250 tonnes de chlorure de calcium ont été épandues chaque année sur les 7 180 km d'autoroutes du Connecticut, ce qui équivaut à un épandage annuel 9 850 kg de sel gemme et de 350 kg de chlorure de calcium par kilomètre.
Sur le côté ouest de l'autoroute, les arbres étaient exposés directement aux eaux de ruissellement routier. Sur le côté est, les eaux de ruissellement routier étaient détournées au moyen d'une bordure qui avait été aménagée durant l'été précédant l'étude. Sur le côté ouest, les concentrations de chlorure dans le feuillage, aux différentes périodes d'échantillonnage, ont varié en moyenne de 5 200 à 6 700 ppm, dépassant largement les concentrations mesurées du côté est (moyenne de 1 600 à 5 400 ppm). Par comparaison, les taux de chlorure dans des arbres témoins de la même essence et du même âge, mais situés loin de la route, ont fluctué entre 200 et 1 400 ppm. Dans le cas du sodium, les concentrations foliaires ont varié en moyenne de 1 100 à 1 600 ppm sur le côté ouest, comparativement à un taux de non décelable à 200 ppm sur le côté est et de 0 ppm dans les arbres témoins.
Une corrélation a été établie entre les concentrations plus élevées de chlorure et de sodium, mesurées dans le feuillage des arbres situés sur le côté ouest de l'autoroute et exposés aux eaux de ruissellement routier, et les symptômes modérés à graves observés dans les arbres du côté ouest. Du côté est, les symptômes ont été légers, voire absents, et ils ont également été absents chez les arbres témoins.
3.5.3.9 Concentrations dans le sol et le feuillage de plantes ligneuses et herbacées, le long de routes du Massachusetts
Des échantillons de sol et de végétaux ont été prélevés à différentes distances, le long de nombreuses autoroutes de l'intérieur (centre et ouest) du Massachusetts, en juin 2000 (Barker, 2000; Mills et Barker, 2001). Cette étude s'applique aux conditions canadiennes, car la majeure partie des essences échantillonnées sont des essences indigènes ou naturalisées du Canada et que les taux d'épandage au Massachusetts, en 1999, étaient comparables aux taux dans le centre et l'est du Canada. Les taux d'épandage au Massachusetts étaient en effet de 240 lb/mille linéaire (136 kg par kilomètre de route à deux voies), comparativement à des taux variant de 130 à 170 kg par kilomètre de route à deux voies, en Ontario.
Des échantillons de huit espèces ligneuses et d'un éventail d'espèces herbacées ont été prélevés à une distance de 1,5 à 12 m de différentes autoroutes et leurs concentrations de sodium ont été analysées. Des lésions ont été observées à une distance de 4 à 9 m des autoroutes et une corrélation a été établie entre ces lésions et l'accroissement de la concentration de sodium dans les tissus des végétaux de multiples essences de pins (Pinus spp.) et de sumacs (Rhus sp.). Chez le pin, la concentration foliaire moyenne de sodium a été de 2 139 ppm dans un arbre endommagé, comparativement à 28 ppm dans un échantillon prélevé d'un lieu hors des abords de la route. Chez le sumac, la concentration foliaire moyenne de sodium a été de 209 ppm dans le feuillage endommagé, comparativement à 177 ppm dans le feuillage en santé. Dans un échantillon unique de peuplier (Populus sp.), aucune différence significative n'a été observée entre les concentrations de sodium, celle-ci étant de 310 ppm dans le feuillage endommagé, comparativement à 338 ppm dans le feuillage d'arbres en santé.
Les concentrations de sodium dans le feuillage des végétaux sont demeurées élevées à une distance de 3 à 7,6 m de la route, puis ont diminué jusqu'à 12 m. À moins de 6,1 m de la route, la concentration de sodium extractible dans le sol a atteint jusqu'à 154 ppm, mais n'était plus que de 26 ppm à 12 m. Quant au pH du sol, il est demeuré élevé (au-dessus de 7) à moins de 3 m de la route, mais se situait à moins de 6,5 à plus de 6 m. Enfin, aucune tendance constante ne se dégage en ce qui a trait à la conductivité électrique, celle-ci ayant varié de 0,12 dS/m (à 9,1 m) à 0,30 dS/m à une distance de 12 m de la route.
3.5.3.10 Concentrations dans le sol et les plantes ligneuses, en aval d'une autoroute à quatre voies de la Colombie-Britannique
Une étude a été menée en 1989 dans le parc Boitanio, en Colombie-Britannique, afin de déterminer les causes du dépérissement et de la détérioration des arbres dans la section est du parc, située près de l'autoroute 97 (Van Barneveld et Louie, 1990). Le parc Boitanio est situé à Williams Lake, au sud-ouest d'un tronçon à quatre voies de cette autoroute. Le sapin bleu de Douglas (Pseudotsuga menziesii var. glauca) y est l'essence dominante.
Le secteur préoccupant se trouvait près de l'autoroute et descendait vers le sud-ouest, dans une pente de 5 à 15 %. Deux ponceaux aménagés le long de l'autoroute, et surplombant le parc, acheminaient l'eau à travers le parc. Chaque jour, quelque 12 000 véhicules empruntaient ce tronçon de l'autoroute sur lequel il y avait épandage de chlorure de sodium à raison de 60 à 130 kg de sels par kilomètre de voie.
De graves lésions et un dépérissement rapide ont été rapportés au printemps 1989 sur les arbres situés le long des canaux de drainage et de l'autoroute. Des échantillons préliminaires de sol ayant révélé la présence de taux élevés de sodium dans le sol, on a procédé à un échantillonnage exhaustif et à des analyses sur le terrain de la végétation et du sol à l'intérieur du parc, en juillet 1989. Les échantillons ont été prélevés selon une grille incomplète partant de l'autoroute, les postes d'échantillonnage étant situés tous les 50 m le long de la grille. Une évaluation a été faite de la végétation, afin de déceler la présence de symptômes dus à des lésions, à des insectes ou à des maladies. Le tissu des feuilles a été échantillonné et analysé pour en déterminer la teneur en chlorure et en sodium. Enfin, des échantillons de sol ont été prélevés dans des couches successives de 25 cm, jusqu'à une profondeur de 150 cm.
Les arbres ont été classés, selon qu'ils avaient subi des dommages légers, modérés ou graves. Sur les arbres peu endommagés, le taux de décoloration et de branches mortes avec des pousses apicales en santé était inférieur à 10 %. Les arbres modérément endommagés présentaient un taux de décoloration et de défoliation de 10 à 50 % et quelques branches mortes avec des pousses apicales en santé. Quant aux arbres lourdement endommagés, ils étaient morts ou présentaient un taux de décoloration, de défoliation et de dépérissement de la cime supérieur à 50 %.
Une association a été établie entre, d'une part, le type de dommages observés et, d'autre part, l'emplacement des arbres le long de la route et le régime d'écoulement de l'eau acheminée à travers le parc par les deux ponceaux. Les dommages les plus graves ont été observés le long de ces voies de drainage.
Des concentrations élevées de sodium et de chlorure ont été mesurées dans le sol des sites modérément et gravement endommagés, mais non dans les sites peu endommagés. La concentration moyenne de sodium dans le sol a ainsi été de 108,7 ppm dans les sites présentant de graves dommages, de 37,9 ppm aux sites modérément endommagés et de 29,0 ppm dans les sites peu endommagés. Quant au chlorure, la concentration moyenne s'est établie respectivement à 52,1 ppm, 50,0 ppm et 20,3 ppm, selon que les dommages étaient graves, modérés ou faibles. Par ailleurs, la concentration de sodium dans les sites lourdement endommagés était 3,7 fois supérieure à celle observée dans les sites peu endommagés, alors que la concentration de chlorure y était 2,6 fois plus élevée.
Des concentrations plus élevées de sodium et de chlorure ont été mesurées dans le feuillage des arbres ayant subi des dommages graves ou modérés que dans ceux légèrement atteints. De fait, la concentration moyenne de sodium dans les aiguilles d'arbres de 0 à 3 ans a été de 113 ppm dans les sites gravement perturbés, de 54,8 ppm dans les sites modérément perturbés et de 59,7 ppm dans les sites ayant subi de légers dommages; dans les aiguilles des arbres de 4 à 6 ans, les concentrations de sodium se sont établies à 208 ppm, 72,7 ppm et 47,9 ppm, respectivement dans les sites lourdement, modérément et peu endommagés.
Quant au chlorure, la concentration moyenne dans les aiguilles d'arbres de 0 à 3 ans a été respectivement de 3 560 ppm, 2 630 ppm et 572 ppm, dans les sites gravement, modérément et légèrement atteints; dans les aiguilles d'arbres de 4 à 6 ans, ces concentrations se sont établies respectivement à 4 180 ppm, 2 667 ppm et 1 060 ppm.
Il est possible que d'autres facteurs -comme une sécheresse récente, la présence d'autres contaminants dans les eaux de ruissellement, la présence d'insectes ou l'élimination récente des broussailles - aient contribué à aggraver le dépérissement des arbres. Il a toutefois été établi que ces autres facteurs n'avaient pas été la principale cause du dépérissement des arbres dans le parc. Ce parc évolue sous un climat sec, où les précipitations annuelles entre mai et août totalisent 158 mm. Ces précipitations peu abondantes, conjuguées à la récente sécheresse, auraient donc aggravé le problème, en empêchant le lessivage des taux élevés de sodium et de chlorure dans le sol par les précipitations.
Les symptômes des dommages sur les Douglas taxifoliés à cet endroit concordent avec les dommages causés par le sel et sont corroborés par la tendance voulant que les dommages plus graves aient été observés sur les arbres situés en bordure de la route et le long des voies de drainage dans le parc. À ces endroits, une corrélation a été établie entre les concentrations élevées de sodium et de chlorure dans le sol et les tissus et les symptômes les plus graves notés chez les arbres.
Kliejunas et al. (1989) font état des dommages causés par les eaux de ruissellement routier traversant des peuplements forestiers. Ces auteurs ont noté un dépérissement terminal des aiguilles des conifères, caractéristique de l'absorption de sels à partir du sol, dans des peuplements forestiers situés entre 91 et 122 m de l'autoroute 89 à Emerald Bay et de l'autoroute 80 à Donner Summit, dans la région de Lake Tahoe au Nevada. Des concentrations élevées de sodium et de chlorure (5 800 ppm de sodium et 13 700 ppm de chlorure) ont été décelées dans les aiguilles de sapins du Colorado (Abies concolor) et de pins de Jeffrey (Pinus jeffreyi) à Donner Summit, à l'intérieur d'un canal de drainage situé à 76 m en aval de l'autoroute 80.
3.5.3.11 Concentrations dans le sol et le feuillage d'espèces ligneuses, à proximité d'un entrepôt de sels
Racette et Griffin (1989) ont étudié les causes du dépérissement marqué des plantes ligneuses à proximité d'un entrepôt de sels de voirie, à l'est de Kenora (Ontario). Les arbres poussant derrière la sablière et le dépôt de sels, de même que le long du canal de drainage qui recevait les eaux de ruissellement de l'autoroute et de l'entrepôt de sels, ont manifesté de graves symptômes.
Une aire d'entreposage de sable et de gravier située à proximité avait servi, au moins une fois, au stockage de sable traité avec du sel. Dans cette zone, les pins gris (Pinus banksiana), les épinettes (Picea sp.), les sapins baumiers (Abies balsamea) et les peupliers (Populus sp.) étaient morts quelques années auparavant et la végétation existante présentait des dommages, le long d'une voie de drainage traversant cette zone. Les graminées avaient été détruites et les peupliers faux-tremble (Populus tremuloides) présentaient les symptômes d'une grave nécrose marginale.
Les taux de sodium et de chlorure dans les tissus des plantes ont été mesurés en septembre 1988, dans les zones où des dommages étaient apparents. Des concentrations de chlorure variant de 1 800 ppm (amélanchier, Amelanchier sp.) à 22 000 ppm (bouleau à papier, Betula papyrifera) ont été mesurées dans le feuillage, alors que les concentrations de sodium ont fluctué entre 10 ppm (épinette noire, Picea mariana) et 86 ppm (amélanchier). Les concentrations de fond de chlorure dans le feuillage ont varié de moins de 20 ppm (amélanchier et bouleau à papier) à 1 900 ppm (peuplier faux-tremble) et celles de sodium, de 7 ppm (épinette noire) à 19 ppm (amélanchier).
À ces endroits, on a aussi décelé de fortes concentrations de sodium et de chlorure dans les branches. De fait, les concentrations de chlorure ont varié de 900 ppm (peuplier faux-tremble) à 9 100 ppm (épinette noire), alors que la concentration de sodium a fluctué entre 9 ppm (peuplier faux-tremble) et 78 ppm (épinette noire). À titre de comparaison, les concentrations de fond de chlorure dans les branches ont varié de moins de 20 ppm (peuplier faux-tremble) à 200 ppm (épinette noire) et celles de sodium, de 7 ppm à 17 ppm (toutes deux mesurées dans l'épinette noire).
Des concentrations élevées de sodium et de chlorure dans le sol de surface ont aussi été observées à ces deux endroits, à une profondeur de 0 à 5 cm, mais non à un site témoin éloigné de la zone. La concentration de chlorure dans le sol a ainsi varié de 780 à 1 200 ppm et celle de sodium, de 370 à 680 ppm; les concentrations de fond étaient respectivement de 15 ppm et 91 ppm.
Durant l'hiver 1988-1989, des mesures ont été prises afin de réduire les pertes de sels à partir du dépôt. Dès août 1989, l'étendue et la gravité des dommages causés à la végétation avaient diminué. Les concentrations de sodium et de chlorure dans le feuillage avaient elles aussi diminué, mais demeuraient toujours élevées par rapport au site témoin.
3.5.4 Modifications des taux d'épandage et dommages actuellement observés au Canada
Les études sur le terrain, qui ont été réalisées au Canada et dont il est question à la section 3.5.3, de même que les concentrations dans l'environnement mentionnées à la section 3.5.1, s'appuient sur des données sur les concentrations de chlorure ou de sodium dans les végétaux ou le sol et sur les dommages causés aux végétaux, d'après un échantillonnage sur le terrain réalisé entre 1980 et 1995. Depuis les années 1980, les taux d'épandage de chlorure de sodium ont diminué de 20 à 30 % dans certaines provinces; en revanche, les charges annuelles totales n'ont pas diminué (Morin et Perchanok, 2000).
La quantité totale utilisée durant l'hiver (charge annuelle), ainsi que la quantité totale déposée dans le sol ou par voie atmosphérique, constituent les valeurs critiques pour les végétaux (Hofstra et Lumis, 1975). La quantité totale de sels épandus durant une saison sera plus élevée lorsque les épisodes de neige sont plus nombreux, que les précipitations de neige sont plus abondantes ou qu'il y a davantage d'épisodes de pluie verglaçante. Les végétaux sont également exposés à de plus grandes quantités de sels dispersés par voie atmosphérique au cours d'années où les quantités épandues sont plus abondantes, que davantage de tempêtes se produisent au début ou à la fin de la saison et que les conditions de gel qui exigent l'épandage de sels commencent plus tôt à l'automne et se prolongent plus tard au printemps.
Les données courantes obtenues de deux municipalités de l'Ontario et de l'Alberta indiquent la variation des quantités totales de sels épandus sur les routes durant l'hiver. Dans le district nord de la région de Peel, en Ontario, les quantités annuelles totales, par kilomètre de voie, ont augmenté de 22 % entre 1995 et 2000, passant de 22 à 27 tonnes (Zidar, 2000). Entre 1996-1997 et 1998-1999, la Ville d'Edmonton a préconisé un salage « judicieux » et l'application des « meilleures pratiques des gestion », afin de réduire au minimum les effets des sels de voirie sur l'environnement. La ville a constaté que la quantité totale de sels de voirie utilisée durant cette période a varié de 11 000 tonnes de chlorure de sodium et 69 400 L de chlorure de calcium à 21 300 tonnes de chlorure de sodium et 40 900 L de chlorure de calcium, ce qui représente un écart de plus de 90 % pour le chlorure de sodium et de 70 % pour le chlorure de calcium (Neehall, 2000).
D'autres facteurs entrent également en compte; ainsi, une plus grande quantité d'eaux de ruissellement salées pénétrera dans le sol autour des racines, lorsque les tempêtes se produisent au début ou à la fin de la saison et que le sol n'est plus gelé, que lorsque le ruissellement s'écoule sur un sol gelé (Headley et Bassuk, 1991). L'épandage de sels au printemps entraînera également le dépôt atmosphérique de sels sur les bourgeons des plantes ligneuses en formation et les jeunes pousses de plantes succulentes, en plus d'exposer les jeunes plants en période de germination dans le sol. Lorsque le printemps est sec, il peut arriver que les dépôts de sels sur les tiges et les feuilles des plantes ligneuses ne puissent être éliminés par les précipitations (Hofstra et al., 1979; Simini et Leone, 1986) et que les sels présents dans le sol ne soient pas éliminés autant que lorsque le temps est plus humide au printemps. Toutes ces variables signifient que l'exposition des plantes aux sels, qu'il s'agisse de dépôts dans le sol ou de dépôts atmosphériques, augmente ou diminue en fonction des conditions climatiques annuelles (Hofstra et al., 1979).
Au Canada, les végétaux en bordure des routes présentent toujours des dommages dus aux sels, tant en régions rurales qu'urbaines. La Ville d'Edmonton a constaté les effets négatifs causés par l'épandage de sels de voirie sur les graminées, les arbustes et les arbres qui poussent le long des routes, mais note qu'il y a peu de solutions de rechange pour assurer des conditions de conduite sécuritaires durant l'hiver (Neehall, 2000). Bien que les employés de la ville pratiquent un salage « judicieux » et recourent aux meilleures pratiques de gestion afin de réduire au minimum les effets des sels de voirie sur l'environnement, ils constatent que la sécheresse contribue à accroître les concentrations de chlorure dans le sol, car l'humidité du sol et le lessivage des sels solubles sont alors réduits. À Edmonton, la gravité des effets négatifs sur les arbres aux abords des routes varient d'une année à l'autre, ces effets étant plus graves en période de sécheresse.
Durant la saison de croissance 2000, des dommages causés par le sel ont été observés sur des arbres dans des régions rurales de l'Ontario, notamment le long de la route County Road 124 dans le comté de Dufferin (figure 3.4 dans Cain et al., 2001 et discussion connexe) et de l'autoroute 401. Dans la région de Peel (Ontario), les dommages causés par le sel ont été évalués sur les arbres se trouvant en bordure de routes situées dans la partie nord de la région et entretenues par la région de Peel et le ministère des Transports de l'Ontario (Thompson, 2000; Zidar, 2000). Les dommages ont semblé plus graves qu'à l'habitude après l'hiver 1999-2000. Les dommages causés par le sel ont été observés principalement sur des essences sensibles, comme le thuya (Thuja occidentalis), le pin rouge (Pinus resinosa) et le pin sylvestre (Pinus sylvestris). Parmi les autres facteurs ayant contribué à ces conditions, mentionnons la sécheresse durant les deux étés précédents qui a exercé un stress sur les arbres, ainsi que l'hiver doux durant la saison 1999-2000 qui pourrait avoir rendu la chaussée humide et propice aux éclaboussures. Les dommages varient également en fonction de la densité de la forêt le long des routes, de l'éloignement des arbres de la route, du type de sol et de sa pente, ainsi que de la vitesse des véhicules sur la route et du volume de la circulation.
3.5.5 Estimation de la superficie à risque
La zone d'impact des sels de voirie sur les végétaux sensibles s'étend généralement sur une distance de 80 m des autoroutes à voies multiples et jusqu'à 35 m des routes à deux voies. En se basant sur les données sur la longueur du réseau routier, il est possible d'estimer les régions du Canada où les sels de voirie pourraient avoir un impact sur les végétaux sensibles. À partir des données publiées par Transports Canada (2001), on a déterminé que la longueur des autoroutes au Canada, en 1995, équivalait à 16 571 kilomètres de route à deux voies. Ce chiffre peut être divisé en deux, pour obtenir la longueur linéaire approximative des autoroutes. La superficie où les végétaux sensibles pourraient être atteints, sur une distance de 80 m de la route, serait donc de 132 568 ha. Toujours en 1995, la longueur des routes asphaltées en régions urbaines et rurales au Canada a été évaluée à 301 348 équivalents de kilomètres de route à deux voies, en présumant une longueur linéaire similaire. Le long de ces routes, la superficie à l'intérieur de laquelle des dommages pourraient être causés aux végétaux à risque, sur une distance de 35 m de la route, serait de 2 109 436 ha.
À partir des données sur la longueur du réseau routier au Canada pour 1995, on estime que les sels de voirie pourraient avoir une incidence sur les végétaux sensibles, sur une superficie de 2 242 000 ha le long des routes du pays. Cependant, comme il n'y a pas épandage de sels de voirie sur toutes ces routes et autoroutes, la superficie réelle serait nettement moindre.
3.5.6 Résumé de l'évaluation des risques et conclusions
Le chlorure de sodium utilisé comme agent de déglaçage peut avoir des effets nocifs sur les végétaux qui poussent le long des routes ou dans les régions contaminées localement par le ruissellement d'eaux à forte teneur en sels. Les concentrations élevées de chlorure et de sodium dans le sol ou la dispersion atmosphérique de ces substances entraînent une diminution marquée du nombre de boutons à fleurs et du rendement fruitier des espèces sensibles ainsi que de graves dommages au feuillage, aux pousses et aux racines, et une réduction de la croissance, de la germination et de l'établissement des jeunes plants. Les plantes atteintes sont notamment des espèces indigènes de graminées, des espèces de terres humides comme la sphaigne et le carex, et des espèces ligneuses telles l'érable, le pin, le Douglas taxifolié, le cornouiller, le pêcher et le prunier.
Les effets graves peuvent entraîner la mort de la plante, alors que l'exposition répétée (chronique) des plantes vivaces à des taux élevés de sels, année après année, provoque une réduction de la croissance ainsi que la mort des tissus des pousses et du feuillage. De plus, le stress répété réduit la vigueur des plantes et leur capacité de se défendre contre les insectes, les maladies et le stress abiotique. Ces effets peuvent aussi provoquer la disparition de végétaux à l'intérieur d'une même communauté et avoir des répercussions sur d'autres organismes qui dépendent des plantes pour leur alimentation ou comme abri.
Des changements dans la phytocénose, en réponse aux taux élevés de sels, ont été observés dans les zones exposées au ruissellement routier et à la dispersion atmosphérique des sels de voirie. Les espèces halophiles, comme les quenouilles et les roseaux communs, envahissent facilement les zones perturbées par le sel, ce qui modifie l'incidence et la diversité des plantes sensibles au sel. Il s'ensuit une modification dans la composition des communautés qui ne tolèrent pas le sel, à cause de la disparition des espèces sensibles et leur remplacement par des espèces halophiles.
La zone d'impact est généralement linéaire et suit le tracé des routes et autoroutes ou des autres zones où il y a épandage de chlorure de sodium ou d'autres sels de chlorure, comme pour le déglaçage ou le traitement antipoussière. Des dommages surviennent également le long des voies de drainage qui transportent les eaux de ruissellement salées provenant des routes et des installations de manutention des sels de voirie. Il y a dispersion atmosphérique de sodium et de chlorure le long des routes durant la période d'épandage hivernal; cet effet, qui perturbe surtout les espèces ligneuses, s'exerce jusqu'à 80 m environ des autoroutes à voies multiples et jusqu'à 35 m des autoroutes à deux voies sur lesquelles il y a épandage de sels. L'étendue et la distance de la dispersion sont fonction de la charge de sels, du volume de la circulation et de sa vitesse, de la topographie locale et des vents dominants.
Les effets des sels de voirie sur les essences forestières aux abords des routes ont été étudiés dans le centre et le sud de la Colombie-Britannique. Ces études ont révélé que la zone d'impact s'étend sur une distance de 10 à 15 m d'une autoroute à deux voies mais a atteint 50 m, le long d'une autoroute à quatre voies de cette province. Au Canada, les régions de grande densité forestière, qui reçoivent des charges modérées à élevées de sels (selon les charges annuelles par district d'entretien), incluent l'île de Vancouver, le sud-ouest et le centre de l'Alberta, le centre et certaines parties du sud de l'Ontario, le sud et le centre du Québec ainsi que certaines régions du Nouveau-Brunswick et de la Nouvelle-Écosse. On a jugé que 53 % des essences forestières primaires du Canada sont sensibles aux sels de voirie.
Dans le cas des cultures fruitières, on note des dommages importants et une diminution marquée de la production de fruits, à l'intérieur d'une zone qui s'étend de 50 à 80 m d'une autoroute à quatre voies du sud de l'Ontario et jusqu'à 35 m environ d'une autoroute à deux voies de la Nouvelle-Écosse. Par ailleurs, 65 % des 32 cultivars ou variétés d'arbres fruitiers, de vignes ou d'arbustes ont été jugés sensibles au sel. La sensibilité de ces espèces donne une indication de la sensibilité des cultures fruitières indigènes qui forment la phytocénose, le long des routes.
Les effets graves et la mortalité observés sur les essences ornementales et les cultures de pépinières sensibles sont dus aux taux élevés de sels de voirie dans le sol ou aux sels dispersés par les éclaboussures. De 30 à 40 % des essences ornementales courantes utilisées en Ontario et dans l'ensemble du Canada sont sensibles aux sels de voirie.
3.6 Faune terrestre
Les effets, tant positifs que négatifs, de l'aménagement d'un réseau routier sur la faune vertébrée ont fait l'objet de nombreuses études scientifiques (p. ex., Bennett, 1991) et ces aspects ne seront pas examinés ici. Des effets spécifiques liés à l'usage des sels de voirie pourraient également résulter de la diminution du couvert végétal ou des changements dans la phytocénose décrits à la section 3.5. Dans certaines conditions, notamment lorsque l'habitat est limité, l'accotement des routes devient une zone précieuse qui sert à la fois d'habitat de reproduction pour la faune et de corridor entre des habitats mieux appropriés (p. ex., Oetting et Cassell, 1971; Drake et Kirchner, 1987; Bennett, 1991; Camp et Best, 1993a,b). Plusieurs administrations ont mis en oeuvre des initiatives en vue d'améliorer la gestion des zones en bordure de route et d'accroître ainsi la valeur de cet habitat. Les sels de voirie peuvent nuire à ces efforts de gestion. Les effets des sels de voirie sur des espèces ayant un stade de vie aquatique, comme les grenouilles et d'autres amphibiens, ont été examinés à la section 3.3. La présente section traite des effets toxicologiques directs des sels de voirie sur la faune terrestre, en l'occurrence les oiseaux et les mammifères.
3.6.1 Caractérisation de l'exposition
Le sodium est une composante essentielle des processus physiologiques chez tous les vertébrés qui devient toutefois toxique lorsqu'absorbé en trop grandes quantités. Normalement, le surplus de sodium est éliminé par une augmentation du taux de filtration glomérulaire et une réduction du pourcentage de sodium réabsorbé par les reins. Les oiseaux terrestres, surtout les espèces herbivores et granivores, sont plus susceptibles de souffrir d'une carence en sel, mais disposent de peu de mécanismes pour faire face à un excès de sodium. Tout animal qui cherche à satisfaire à sa « faim de sel » comble habituellement son déficit en le dépassant de beaucoup et cet excédent persiste pendant un certain temps (Schulkin, 1991). La surconsommation de sel est à son tour régulée par un mécanisme de rétroaction : la soif. L'absence d'une source d'eau augmente donc la toxicité du sel ingéré (voir la section 3.6.2.1). La faune qui souffre d'une carence en sel peut franchir de grandes distances pour trouver du sel et ainsi se retrouver sur les routes sur lesquelles il y a eu épandage (Schulkin, 1991). Une des préoccupations examinées dans le cadre de la présente évaluation tient à l'attrait qu'exercent les routes salées, les espèces sauvages très mobiles étant capables de parcourir de grandes distances pour y parvenir.
3.6.1.1 Mammifères
L'interaction la plus apparente entre les sels de voirie et la faune sauvage vient sans doute des grands ongulés, comme l'orignal (Alces alces), le cerf mulet (Odocoileus hemionus), le cerf de Virginie (Odocoileus virginianus), le wapiti (Cervus canadensis) et le mouflon d'Amérique (Ovis canadensis). Bien que d'autres facteurs puissent attirer les mammifères sur les routes, l'épandage de sels de voirie a souvent été largement mis en cause dans les collisions avec des voitures. En Ontario, par exemple, la période où survient le plus de collisions entre des orignaux et des voitures correspond à la période où les besoins en sodium des animaux sont les plus grands, et non à la période où la circulation automobile est la plus abondante (Fraser et Thomas, 1982). Par ailleurs, la plupart des orignaux sont aperçus là où se trouvent des mares de sels ou très près de ces lieux et c'est là que surviennent la moitié environ des collisions entre des orignaux et des voitures (Fraser et Thomas, 1982). Selon un rapport technique publié par le ministère des Transports de l'Ontario, les cerfs et les orignaux qui boivent de l'eau salée ont tendance à perdre leur crainte des humains et des véhicules et sont enclins à foncer, parfois même devant un véhicule, plutôt que de s'en éloigner comme ils le feraient normalement (Jones et al., 1986). Selon une autre étude, celle-ci menée au Québec, la présence des orignaux dans les étangs aux abords des routes augmentent proportionnellement aux taux de sodium et de calcium de ces eaux et le nombre de collisions est plus élevé à proximité des étangs plus fréquentés par ces animaux (Grenier, 1973). Dans l'ensemble, deux fois plus d'orignaux sont tués par kilomètre de route, lorsqu'il y une mare que lorsqu'il n'y en a pas. Miller et Litvaitis (1992) ont constaté que des orignaux porteurs d'un collier émetteur, dans le nord du New Hampshire, avaient élargi leur domaine vital pour y inclure des mares fortement contaminées par le sel, qui se trouvaient près de la route. De même, l'attrait des sels de voirie a été reconnu comme une des principales causes du décès de mouflons d'Amérique et une cause mineure de la mort de wapitis dans la parc national Jasper (Bradford, 1988). À notre connaissance, aucune étude officielle n'a porté sur la contribution des sels de voirie dans la mortalité d'autres espèces fauniques, comme les petits mammifères souvent tués par les véhicules automobiles, bien qu'un autre rapport du ministère des Transports de l'Ontario indique que la marmotte commune (Marmota monax), le lièvre d'Amérique (Lepus americanus) et le porc-épic (Erethizon dorsatum) sont souvent aperçus en train de se nourrir de sels de voirie (Hubbs et Boonstra, 1995).
Trainer et Karstad (1960) rapportent un cas d'intoxication par les sels de voirie chez le lapin à queue blanche (Sylvilagus floridanus).
3.6.1.2 Oiseaux
On a relevé douze rapports publiés établissant un lien entre les sels de voirie et des oiseaux morts (Brownlee et al., 2000). Deux incidents ont officiellement été diagnostiqués comme des intoxications par le sel (Trainer et Karstad, 1960; Martineau et Lair, 1995) et des comportements anormaux, évocateurs d'une toxicose, ont été observés dans plusieurs autres cas. Dans la plupart des cas, le chlorure de sodium est la substance à laquelle les oiseaux ont été exposés bien que, dans un cas, c'est du chlorure de calcium qui avait été épandu sur la route (Meade, 1942). Ces oiseaux morts ont été observés à plusieurs endroits à l'intérieur de la ceinture de neige canado-américaine, entre 1942 et 1999. Un autre rapport provient d'Allemagne et au moins deux des incidents signalés portent sur la mort de plus d'un millier d'oiseaux chacun. Compte tenu de la difficulté de retrouver les carcasses d'oiseaux (Mineau et Collins, 1988), en raison du nombre élevé de charognards aux endroits où des oiseaux sont fréquemment tués le long des routes (Benkman, 1998; Woods, 1998) et du peu de rapports sur la mortalité de la faune en général, le nombre de rapports sur les morts d'oiseaux associées à l'épandage de sels de voirie est significatif et suggère que ces décès sont sans doute plus répandus et plus fréquents que ne l'indiquent les cas documentés. Le fait que d'autres biologistes et chercheurs contactés ont dit être au courant de ces morts d'oiseaux sur les routes salées vient appuyer cette hypothèse, même si ces observations n'ont pas été publiées. À un endroit (parc Mount Revelstoke), la mortalité du tarin des aulnes et d'autres roselins (voir plus bas) a été observée assez souvent au cours des 25 dernières années pour que les habitants de la région les surnomment « oiseaux de radiateur », faisant ainsi référence à la tendance qu'ont ces oiseaux d'être frappés par l'avant des véhicules en mouvement (Woods, 1998). Ces morts surviennent souvent dans les courbes des autoroutes ou aux endroits où la chaussée présente de nombreuses fissures et crevasses propices à l'accumulation de sels, bien qu'elles puissent se produire n'importe où il y eu épandage de sable et de sels. Selon Baker (1965), les habitants d'une localité du Maine considèrent ce massacre d'oiseaux comme un phénomène quotidien naturel. Un autre chercheur rapporte avoir vu des centaines de becs-croisés des sapins morts après avoir été frappés par des véhicules alors qu'ils mangeaient du sel sur la route (Benkman, 1998).
Les roselins carduélinés (famille des Fringillidés, sous-famille des Carduélinés : becs-croisés des sapins, gros-becs et tarins des aulnes) sont en cause dans 11 des 12 incidents publiés. Tous les roselins carduélinés sont des espèces protégées qui figurent sur les listes établies en vertu de la Loi sur la Convention concernant les oiseaux migrateurs. L'aire de distribution de ce groupe d'oiseaux granivores couvre l'ensemble de la forêt boréale, ces oiseaux ne se déplaçant vers des latitudes plus au sud que lorsque le rendement grainier est faible. Les cartes animées produites par ordinateur, sur l'abondance de l'espèce, illustrent bien l'étendue de ce phénomène d'« invasion » (voir Cornell Laboratory of Ornithology, 2000a, b). Bien que les roselins se nourrissent de graines d'arbres à feuilles caduques, d'insectes et de baies, leur alimentation, surtout en hiver, se compose essentiellement de graines de conifères, et leur attrait pour le sel est bien connu. On utilise ainsi du sel pour piéger des becs-croisés des sapins (Loxia curvirostra) (Dawson et al., 1965) et on a constaté que les roselins carduélinés préfèrent le sodium à tout autre minéral, quelle que soit la grosseur du gravier (Bennetts et Hutto, 1985). Fraser et Thomas (1982) ont constaté que trois espèces de roselins, à savoir le gros-bec errant (Hesperiphona vespertina), le roselin pourpré (Carpodacus purpureus) et le tarin des pins (Carduelis pinus), étaient les principaux visiteurs des mares de sels aux abords des routes, dans le nord de l'Ontario.
Les renseignements sur les morts rapportées et sur les caractéristiques sociales et comportementales des roselins carduélinés laissent croire que ce groupe est le plus à risque de souffrir des effets de toxicité aiguë dus à l'ingestion de sels de voirie. Cependant, le fait que les oiseaux ont tendance à voyager et à s'alimenter en larges bandes en hiver introduit sans doute un biais qui explique la plus grande détectabilité de ces oiseaux et la déclaration d'un plus grand nombre d'oiseaux morts. Trainer et Karstad (1960) rapportent également des cas d'intoxication chez le colin de Virginie (Colinus virginianus), le faisan de Colchide (Phasianus colchicus), le pigeon biset (Columba livia) et le lapin à queue blanche.
On suppose souvent que l'ingestion de sel vise à satisfaire à un besoin physiologique associé à un régime essentiellement végétarien. Cependant, on ne peut écarter la possibilité que les cristaux de sel ingérés servent de gravier, lequel aide à broyer les aliments et constitue une source supplémentaire de minéraux pour les oiseaux dont le régime est faible en calcium (Gionfriddo et Best, 1995). La préférence quant à la taille du gravier varie de façon linéaire avec la taille de l'oiseau. La taille des particules de sels provenant d'une mine de l'Ontario a varié de 0,6 à 9,5 mm (Société canadienne de sel Ltée, 1991). Comme la taille des particules de sels épandus sur les routes diminue progressivement à mesure que cette substance fond (Letts, 1999), la taille des particules de sels finit par correspondre, à un moment ou à un autre après l'épandage sur les routes, à la taille du gravier qui convient à un oiseau donné. De plus, la grande fluctuation dans la taille des particules de sels de voirie au moment de leur épandage fait en sorte qu'un gravier de grosseur appropriée sera disponible pendant une longue période de temps.
3.6.2 Caractérisation des effets
3.6.2.1 Toxicité aiguë du chlorure de sodium
Les cas de toxicité du sel chez les vertébrés domestiques ou captifs se divisent en plusieurs catégories : surdose accidentelle dans l'alimentation qui peut être compensée par une consommation accrue d'eau (Sandals, 1978; Swayne et al., 1986; Howell et Grumbrell, 1992; Wages et al., 1995; Khanna et al., 1997); exposition à une eau potable salée (Franson et al., 1981); exposition à des lacs salés (Windingstad et al., 1987; Meteyer et al., 1997) ou apport de suppléments de sel avec privation d'eau (Trueman et Clague, 1978; Scarratt et al., 1985). Les toxicoses dues au sel, chez les vertébrés sauvages en liberté, ont été liées à une exposition aux sels de voirie, à la sécheresse, à la glace, à des lacs sursalés et à des étangs contenant les rejets de diverses industries (Baeten et Dein, 1996).
La DL50 du chlorure de sodium par voie orale est de 3 000 mg/kg-p.c. chez le rat et de 4 000 mg/kg-p.c. chez la souris (Bertram, 1997).
Le chlorure de sodium administré sous forme de solution aqueuse saturée (environ 2 100 mg/kg-p.c.) provoque généralement la mort en moins de 24 heures (Trainer et Karstad, 1960). De petites doses répétées de sels ne produisent aucune maladie si l'apport d'eau n'est pas limité.
Le Centre canadien coopératif de la santé de la faune de Saskatoon et le Centre national de la recherche faunique d'Environnement Canada ont récemment mené une étude conjointe sur les effets aigus du sel sur des moineaux domestiques capturés dans la nature (Passer domesticus) (Wickstrom et al., 2001). La méthode des charges croissantes et décroissantes a été utilisée dans le cadre d'une étude pilote ayant pour but d'estimer la dose létale orale approximative de chlorure de sodium granulaire chez des oiseaux qui n'étaient pas à jeun, mais qui ont été privés d'eau pendant six heures après l'administration de la dose. Les résultats indiquent une DL50 d'environ 3 000 à 3 500 mg/kg-p.c., ce qui se rapproche de la valeur déterminée pour les rongeurs. On a estimé, de façon provisoire, que le niveau sans effet observé (mortalité) était de 2 000 mg/kg-p.c. dans cette étude pilote, bien que la mort ait été observée à une dose de 1 500 mg/kg-p.c., lors d'une phase subséquente de l'étude.
3.6.2.2 Effets sublétaux dus à l'ingestion d'un excès de sels chez les oiseaux et les mammifères
Plusieurs auteurs, citant des incidents chez la faune associés aux sels de voirie, font état de comportements déficients chez les oiseaux exposés. L'observation la plus courante est que les oiseaux semblaient avoir perdu leur crainte naturelle et qu'on pouvait les approcher facilement (Meade, 1942; Trainer et Karstad, 1960; Baker, 1965; Thiel, 1980; Smith, 1981; Woods, 1999). D'autres ont indiqué que les oiseaux semblaient « faibles et lents » (Martineau et Lair, 1995) ou malades (Meade, 1942). Trainer et Karstad (1960) parlent de dépression, de tremblements, de torticolis, de rétropulsion et de paralysie partielle chez des oiseaux et des mammifères impliqués dans un incident.
Ces symptômes s'apparentent étroitement à ceux observés en laboratoire. Des faisans auxquels on a fait manger de fortes quantités de sodium dans leur pâtée ont manifesté des symptômes d'intoxication lorsque l'apport d'eau a été limité : dépression suivie d'excitation, tremblements, torticolis, opisthotonos, rétropulsion, incoordination totale et coma (Trainer et Karstad, 1960). Ces symptômes n'ont pas tous été constatés chez le même animal. Au nombre des signes fréquemment observés chez la volaille et le porc, mentionnons la salivation, la diarrhée, une démarche saccadée, des spasmes musculaires, des secousses musculaires et la prostration (Humphreys, 1978). À la suite de l'étude pilote mentionnée précédemment, Wickstrom et al. (2001) ont administré à des moineaux domestiques des doses orales de chlorure de sodium granulaire de 0, 500, 1 500, 2 500 et 3 500 mg/kg-p.c. Parmi les signes cliniques apparents observés à une dose de 1 500 mg/kg-p.c. et plus, mentionnons l'apparition rapide (< 30 minutes) de la dépression, de l'ataxie et de l'incapacité de voler ou de se percher, la mort survenant en moins de 45 minutes. En général, les oiseaux ayant survécu six heures se sont rétablis. Par ailleurs, des concentrations de sodium dans le plasma supérieures à 200 mmol/L ont régulièrement été associées à des signes cliniques patents. On a observé des lésions sous forme d'oedème du gésier après une heure chez la plupart des oiseaux ayant reçu une dose de 500 mg/kg-p.c. ou plus, ainsi qu'une vacuolisation du tronc cérébral, également compatible avec l'oedème, chez certains oiseaux manifestant des signes cliniques.
Il n'existe aucun relevé faisant état d'une toxicose due au sel chez l'orignal ou le cerf, bien que des observations isolées indiquent que les orignaux qui boivent de l'eau salée ont tendance à perdre leur crainte des humains et des véhicules (Jones et al., 1992), contrairement aux orignaux qui ne boivent pas d'eau salée et qui s'éloignent des humains. Le seul cas rapporté de petits mammifères manifestant des signes d'une toxicose au sel porte sur des lapins à queue blanche, durant un hiver rigoureux au Wisconsin (Trainer et Karstad, 1960).
3.6.3 Caractérisation du risque
Comme des cas de mortalité ont été documentés et que ces cas sont, de toute évidence, beaucoup plus fréquents et répandus que ne le laissent croire les rapports publiés, le risque pour les roselins carduélinés, pour le moins, est significatif. Et, localement, le risque pour les gros mammifères est également élevé. Il ne fait aucun doute que la simple présence des sels de voirie contribue à accroître les collisions, en augmentant l'attrait que présentent les routes. La principale incertitude liée à la présente caractérisation du risque est de savoir si la toxicité du sel rend certaines espèces plus vulnérables aux collisions. De même, s'il y a toxicité, il faut se demander si l'ingestion de sels pourrait entraîner la mort d'espèces fauniques, et plus particulièrement des roselins carduélinés, même en l'absence de collisions avec des véhicules.
3.6.3.1 Estimation du rôle de la toxicité du sel dans les collisions avec les véhicules
Les troubles de comportement graves (dépression, tremblements, torticolis, rétropulsion et paralysie partielle) observés à un site, ainsi que les taux élevés de sodium dans le cerveau à un autre, laissent croire fortement que la toxicité du sel contribuerait à la mort des oiseaux sur les routes. L'observation la plus répandue, quant à l'absence inhabituelle de crainte chez les oiseaux et les mammifères, pourrait être un symptôme précurseur de l'intoxication ou la manifestation d'une faim extrême de sel qui amène ces animaux à modifier leur comportement au risque de mettre leur vie en danger.
Bien que des signes patents d'intoxication aient été observés chez le moineau domestique, à une dose de 1 500 mg/kg-p.c. et plus, on ne connaît pas la dose susceptible de causer des troubles de comportement moins apparents. La limite inférieure pouvant causer des troubles a donc été estimée comme suit, en utilisant le moineau domestique comme modèle.
La distribution des concentrations normales de sodium dans le plasma des moineaux est très restreinte (moyenne : 163,2 mmol/L; intervalle : 158 à 168 mmol/L, n=12).
L'hypothèse posée est la suivante : des effets nocifs, par exemple une réduction de la coordination et une faiblesse, peuvent commencer à se manifester lorsque l'homéostasie du sodium est rompue et que les organes cibles sont exposés à des taux élevés de sodium. Pour le moineau domestique, ce taux a été établi à 266 mg/kg-p.c. (Brownlee et al., 2000).
Pour estimer l'exposition, on a présumé que les cristaux de sel seront fort probablement absorbés entiers, comme le sont les particules de gravier. Un roselin voulant étancher sa faim de sel pourrait ingérer une granule de la taille qui lui « convient ». La taille maximale du gravier pour le moineau domestique est de 2,4 mm (Gionfriddo et Best, 1995). Le tableau 24 indique le nombre de particules qu'un oiseau devrait ingérer pour atteindre une VCT précise; ce calcul laisse croire que des effets sublétaux pourraient se manifester chez les oiseaux après l'ingestion d'une grosse particule de sel et que l'ingestion de deux grosses particules pourrait entraîner la mort.
La taille moyenne du gravier ingéré par le moineau domestique est de 0,5 mm (Gionfriddo et Best, 1995). Donc, en présumant que les oiseaux chercheraient à ingérer des particules de sel de cette taille « préférée » pour favoriser la digestion, les calculs précités ont été refaits, cette fois-ci en fonction de la taille moyenne. En fait, cette taille moyenne est sans doute une sous-estimation car elle est basée sur des particules de gravier « usées », extraites du gésier de l'oiseau. Cette moyenne inclut également des particules très fines de minéraux qui ont probablement été ingérées accidentellement avec la nourriture. Le tableau 25 présente les résultats de ce calcul. Bien que le nombre de particules à ingérer pour atteindre la VCT soit beaucoup plus élevé que celui indiqué au tableau 24, un oiseau peut facilement en ingérer autant, si on compare ce nombre au compte moyen de particules de gravier. Par conséquent, les oiseaux qui doivent refaire leur provision de gravier pourraient facilement absorber des doses susceptibles d'avoir des effets toxiques significatifs.
3.6.3.2 Conclusions et discussion de l'incertitude
Les sels de voirie sont largement reconnus comme un important facteur qui contribue à attirer les gros mammifères sur les routes et ils semblent accroître la fréquence des collisions avec des véhicules.
Il est clair que, même en l'absence de sels de voirie, certains oiseaux viendraient sur les routes pour y trouver du gravier, de l'argile, des proies mortes, etc. Cependant, les observations faites aux abords des routes et, plus particulièrement, sur la biologie des roselins carduélinés laissent croire que les sels de voirie constituent un attrait important. De plus, les données compilées à ce jour semblent indiquer que les sels de voirie rendent les oiseaux plus vulnérables aux collisions, en modifiant leur comportement. Manifestement, les oiseaux qui, en bordure de la route, semblent faibles et lents (Martineau et Lair, 1995) ou malades (Meade, 1942), ou qui manifestent des signes de dépression, de tremblements, de torticolis, de rétropulsion et de paralysie partielle (Trainer et Karstad, 1960), sont moins en mesure de se déplacer pour éviter les automobiles en mouvement. Par ailleurs, les effets biologiques des sels de voirie diffèrent notamment de ceux du sable qui, on le sait, attire les oiseaux sur la route à la recherche de gravier mais ne cause pas de troubles de comportement. Qui plus est, les calculs sur les quantités ingérées laissent croire que les sels de voirie pourraient intoxiquer directement certains oiseaux, en particulier lorsque l'eau n'est pas facilement disponible durant les mois rigoureux de l'hiver. On a déjà vu des oiseaux manger de la neige, attraper des flocons de neige durant une tempête et briser de la glace pour obtenir de l'eau (Wolfe, 1996). Oeser (1977) note que des becs-croisés des sapins mangeaient de la neige durant l'incident rapporté en Allemagne. Or l'ingestion de neige en réaction à une surconsommation de sel pourrait avoir des conséquences énergétiques négatives. Enfin, la neige fondue sur les routes pourrait constituer la source d'eau la plus facilement accessible; cependant, selon la concentration de sels qu'elle renferme, sa consommation pourrait accroître la quantité de sels ingérée plutôt que d'atténuer la toxicose.
On ignore également si le moineau domestique est un modèle toxicologique qui convient aux roselins carduélinés et à d'autres oiseaux indigènes. Le moineau domestique vient en effet du Moyen-Orient et il pourrait donc être génétiquement prédisposé à mieux tolérer le sel que les roselins carduélinés. Il est possible également que le taux de consommation de gravier du moineau domestique soit élevé, par rapport à d'autres espèces d'oiseaux (Gionfriddo et Best, 1995). Les scénarios décrits précédemment sont basés sur une consommation de sels établie en fonction des besoins en gravier (tableau 25) et sur une optimisation de l'ingestion de sel par l'absorption de particules de sels plus larges dont la taille se situe à la limite de la taille de gravier tolérée par l'espèce (tableau 24). Cependant, quelle que soit la taille exacte des particules de sels ingérées, les oiseaux privés de sel pourraient ingérer des doses produisant des effets toxiques avant que les mécanismes de rétroaction ne réduisent le désir de consommer du sel.
La carte établie par Brownlee et al. (2000) montre un vaste recoupement entre l'aire de distribution des roselins durant l'hiver et les sections du réseau routier canadien sur lesquelles il y a épandage de sels de voirie. Ce phénomène est d'autant plus marqué durant les années où il y a « invasion », c'est-à-dire lorsque les roselins quittent la forêt boréale en direction sud. Il est raisonnable de présumer que les roselins seront davantage attirés par certains types de routes que d'autres. À titre d'exemple, un vol d'oiseaux aurait sans doute peu d'occasions de se poser sur une autoroute à voies multiples achalandée desservant une grande région métropolitaine, quelle que soit la quantité de sel qui s'y trouve. On ne possède pas les données nécessaires pour évaluer la probabilité qu'un vol d'oiseaux se pose sur une route donnée, ni la proportion de ces visites qui se solderont par la mort des oiseaux (que ce soit à la suite d'un attrait fatal, d'une collision avec un véhicule due à la toxicose ou de l'ingestion d'une dose létale). De même, il est difficile et hautement stochastique d'estimer la période durant laquelle les sels demeurent à la surface de la route ou à proximité (p. ex., dans le sol) et forment ainsi un « bloc à lécher » artificiel, attrayant pour les oiseaux et les mammifères même une fois les granules dissoutes; cependant, ce phénomène est sans aucun doute important.
Malgré ces incertitudes, les données scientifiques disponibles à ce jour laissent croire que le nombre d'oiseaux morts sur les routes appartenant à des espèces d'oiseaux migrateurs protégées par des lois fédérales (notamment les roselins carduélinés) et que la contribution des sels de voirie dans ces morts ont été sous-estimés par les gestionnaires de la faune et les autorités responsables des transports. Les responsables des transports reconnaissent toutefois depuis longtemps le rôle des sels de voirie dans l'augmentation du nombre de collisions entre de gros mammifères et des véhicules automobiles.
3.7 Ferrocyanures
La présente section est fondée sur un examen détaillé des ferrocyanures présenté dans Letts (2000a).
3.7.1 Caractérisation de l'exposition
Le ferrocyanure de sodium se dissout dans l'eau et libère l'anion ferrocyanure stable (Fe(CN)64-) qui n'est pas volatil et qui résiste à toute autre dégradation à moins d'être exposé à la lumière. L'anion est assez mobile dans les eaux souterraines, mais réagit rapidement avec le fer pour former un précipité de ferrocyanure ferrique, un composé très stable, non toxique et relativement immobile, qui constitue une importante voie d'élimination du ferrocyanure dans les eaux souterraines. Dans des conditions favorables, y compris en l'absence de lumière, la demi-vie du ferrocyanure est d'environ 2,5 ans (Higgs, 1992), alors que celle du ferrocyanure ferrique peut atteindre un millier d'années (Meeussen et al., 1992a).
Deux caractéristiques de l'anion ferrocyanure revêtent une importance considérable. Cet anion est extrêmement peu toxique lorsqu'il forme des complexes (Rader et al., 1993); cependant, en solution et sous la lumière directe, il se photodécompose et libère du cyanure libre qui réagit rapidement pour former de l'acide cyanhydrique (HCN), un composé hautement toxique et volatil. La photolyse du ferrocyanure est faible lorsque cette substance n'est pas en solution (American Cyanamid Company, 1953).
La photolyse de l'anion ferrocyanure est un phénomène qui a été bien étudié (Broderius, 1973; Broderius et Smith, 1980; Otake et al., 1982; Clark et al., 1984; Meeussen et al., 1992a) et qui peut donner lieu à la libération de cinq des six ions cyanure du composé d'origine. Cette réaction dépend notamment de la concentration initiale, de l'intensité de l'éclairage, du pH et de la température.
Un certain nombre de processus contribuent à l'atténuation du cyanure libre dans l'environnement. Ainsi, ce composé est rapidement chélaté avec de nombreux métaux de transition et forme des matériaux plus stables et moins toxiques (Chatwin, 1990). La présence d'argile ou de matière organique élimine le cyanure libre par adsorption en surface (Theis et West, 1986). Enfin, en présence de soufre, le cynaure libre est oxydé et forme des cyanates et des thiocyanates relativement inoffensifs.
3.7.1.1 Sol
La majeure partie des recherches sur le comportement des ferrocyanures dans le sol, en l'absence de lumière, ont porté sur les déchets provenant d'anciennes raffineries de gaz manufacturé. Ces études indiquent que la présence des ferrocyanures se limite aux alentours immédiats de la source (Effenberger, 1964; Parker et Mather, 1979). Cette faible mobilité est apparemment due à la présence de soufre et de métaux de transition dans le sol. À un pH variant entre 4 et 7, le fer se combine à l'anion ferrocyanure pour former le ferrocyanure ferrique peu soluble connu sous le nom de bleu de Prusse (Meeussen et al., 1992b). La présence de ce composé se remarque à la coloration bleue du sol dans plusieurs raffineries de gaz désaffectées. Dans les sols alcalins (pH supérieur à 7), le ferrocyanure en solution reste sous forme d'anion et est assez mobile. Dans des conditions fortement acides, toutefois, les anions ferrocyanure se dissocient et libèrent des ions cyanure (Belluck, 2000). Selon certains, de telles conditions s'observent en laboratoire, mais elles se produisent rarement, voire jamais, dans l'environnement (Chatwin, 1990).
La rétention et l'immobilisation dans le sol du ferrocyanure, sous sa forme peu toxique, sont les principales voies d'atténuation qui limitent la toxicité potentielle de cette substance. Les particules qui interviennent dans le processus d'adsorption, dans les sols argileux d'un pH modéré, peuvent en fait contenir des anions ferrocyanure. Ainsi, la géothite (a-FeOOH), un enduit de surface commun dans les particules du sol, élimine jusqu'à 95 % de l'anion ferrocyanure par adsorption à un pH de 4 (Theis et West, 1986). Ces méthodes d'élimination sont favorisées à un pH modéré. Au Canada, les sols sont acides dans les régions forestières, et plus particulièrement dans l'Est du Canada où l'épandage de sels est abondant. À l'opposé, les sols vont de neutres à alcalins dans les Prairies où ils sont naturellement enrichis de sels (Acton et Gregorich, 1995; voir aussi CANSIS à l'adresse http://sis.agr.gc.ca/cansis/ intro.html). Le ferrocyanure immobilisé est également sujet à la conversion chimique qui donne lieu à la libération de composés peu toxiques en présence de soufre; enfin, des microorganismes dégradant les cyanures liés à des métaux ont été identifiés (Mudder, 1991).
La photolyse du ferrocyanure est une réaction complexe qui a été largement étudiée (Broderius, 1973a; Broderius et Smith, 1980; Otake et al., 1982; Clark et al., 1984; Meeussen et al., 1992a). Parmi les facteurs qui influent sur ce processus, mentionnons le pH, la température, la concentration initiale, la saison et l'heure du jour. Dans leur étude sur la réaction photolytique, Miller et al. (1989) notent que la libération de cyanure libre dans le sol se limite à une profondeur de 1 mm, ce qui porte à conclure que seuls les anions ferrocyanure présents dans le premier millimètre du sol seront sujets à ce processus.
L'acide cyanhydrique produit dans le sol est légèrement persistant. Il a une demi-vie estimative de quatre semaines à six mois (Howard et al., 1991). Il est adsorbé par l'argile et la matière organique, à des taux respectifs de 0,05 mg/g et 0,5 mg/g (Chatwin, 1989). Il est également sujet à l'hydrolyse qui donne lieu à la formation d'acide formique jusqu'à un taux de 4 % dans les sols saturés (Chatwin, 1990). La volatilisation de l'acide cyanhydrique dans le sol représente jusqu'à 10 % des pertes, mais la saturation du sol retarde ce processus par un facteur de 104 (Chatwin, 1990). La dégradation biologique de divers cyanures par les microbes du sol (Towill et al., 1978; Dubey et Holmes, 1995) ou leur assimilation par les végétaux (Fuller, 1984; Knowles et Bunch, 1986) sont deux mécanismes d'élimination efficaces, qui sont fortement atténués en conditions anaérobies saturées (Strobel, 1967).
3.7.1.2 Eau
Le ferrocyanure se dissocie très lentement en l'absence de lumière. Dans ces conditions, la quantité de cyanure libre, qui est libérée à partir de concentrations de ferrocyanure fluctuant entre 1 et 100 000 mg/L, varie de 1,2 à 6µ g/L. En présence de lumière, toutefois, le ferrocyanure est rapidement converti en cyanure libre dans l'environnement (Ferguson, 1985; Singleton, 1986).
Dans l'eau, le cyanure libre est transformé en acide cyanhydrique, un acide faible, par la réaction d'équilibre H+ + CN- « HCN. La formation d'acide cyanhydrique est fortement favorisée à un pH inférieur à 6. L'acide cyanhydrique est très volatil et, dans des conditions ambiantes, se dissipe rapidement depuis les plans d'eau, son taux de volatilisation étant fonction de la concentration, de la température, du pH et du débit d'eau (Schmidt et al., 1981; Melis et al., 1987). Les processus secondaires d'élimination du cyanure incluent la complexation et la précipitation, la biodégradation, l'adsorption par la matière organique et l'assimilation par les végétaux. Enfin, un certain nombre d'organismes naturels produisent des cyanures (Knowles, 1976).
3.7.1.3 Air
Le ferrocyanure ne se volatilise pas. En revanche, l'acide cyanhydrique est très volatil et devrait se dissiper rapidement dans l'atmosphère, sa demi-vie estimée variant de 89 jours à 2,4 ans (Howard et al., 1991).
3.7.1.4 Bioamplification
Towill et al. (1978) n'ont trouvé aucune étude faisant état de la bioamplification du cyanure.
3.7.2 Concentrations mesurées et estimées dans l'environnement
Les concentrations de cyanure mesurées dans les eaux de ruissellement varient de 2,3 à 22 µg/L pour le cyanure libre et de 3 à 270 µg/L pour le cyanure total (Hsu, 1984; Ohno, 1989a; Novotny et al., 1997; Mayer et al., 1998). Comme les données réelles sont limitées, des concentrations ont aussi été estimées.
Morin et Perchanok (2000) ont documenté les activités d'épandage de sels de voirie au Canada. Le taux d'épandage le plus élevé est de 10 150 g de sels/m2 et le plus haut taux d'addition de ferrocyanure de sodium aux sels de voirie est de 124 mg/kg (Letts, 2000b). Ceci correspond à 86 mg de ferrocyanure/kg ou à une teneur stoechiométrique en cyanure de 63,7 mg/kg. À partir de ces valeurs, on calcule un taux de distribution de 877,8 mg de ferrocyanure/m2, soit 646,6 mg d'ions cyanure/m2. À l'aide des données sur les précipitations annuelles, il a été déterminé que la concentration d'anions ferrocyanure dans les eaux de ruissellement se situe entre 0,000142 et 1,42 mg/L, ce qui correspond à une teneur stoechiométrique de 0,000104 à 1,04 mg d'ions cyanure/L.
Comme la mobilité du ferrocyanure dans le sol varie en fonction des conditions locales, deux séries d'hypothèses sont formulées. Dans le premier cas, le ferrocyanure forme un précipité et les quantités annuelles épandues sont retenues dans les deux premiers centimètres du sol. Dans le deuxième cas, le ferrocyanure reste en solution et 20 % des quantités annuelles épandues sont retenues dans les 20 premiers centimètres du sol. Dans le premier cas, la concentration de ferrocyanure dans le sol fluctue entre 0,0043 et 43,8 mg/kg de sol, ce qui correspond à une teneur stoechiométrique en ions cyanure de 0,0032 à 32,3 mg/kg de sol. Dans le deuxième cas, la concentration se situe entre 0,000086 et 0,88 mg/kg de sol, pour une teneur stoechiométrique de 0,000064 à 0,64 mg/kg de sol.
3.7.3 Caractérisation des effets
L'évaluation préalable laisse croire que le plus grand danger inhérent à l'utilisation du ferrocyanure de sodium tient à la capacité de l'anion ferrocyanure de se photodécomposer et de libérer ainsi du cyanure libre. Les sections qui suivent résument les effets connus de ces deux composés sur les organismes terrestres et aquatiques. Il faut toutefois garder à l'esprit les limites de l'évaluation de la toxicité dans les conditions artificielles du laboratoire.
3.7.3.1 Biote aquatique
La concentration et la température de l'eau sont les principaux facteurs qui influent sur la toxicité dans l'eau. La toxicité est également fonction du taux d'oxygène dissous et de la salinité. La documentation propose un certain nombre d'examens exhaustifs sur la toxicité du cyanure pour les organismes dulcicoles (Doudoroff, 1966, 1976, 1980; Leduc et al., 1982; U.S. EPA, 1985). Certains organismes manifestent une acclimatation réversible aux effets toxiques.
Les effets du cyanure varient beaucoup d'une espèce microbienne à une autre. Un grand nombre d'espèces font preuve d'une résistance remarquable aux effets nocifs de ce composé, certaines espèces étant même utilisées dans les processus de détoxication des cyanures (Chatwin, 1990; Fallon et al., 1991). On a toutefois observé des effets nocifs chez Pseudomonas putida à une concentration de 1 µg/L (U.S. EPA,1985) - il s'agit de la plus faible concentration à laquelle des effets nocifs ont été signalés chez des micro-organismes aquatiques (Letts, 2000a).
Les données sur la toxicité des végétaux sont rares. L'espèce la plus sensible, Scenedesmus quadricauda, a présenté un début d'inhibition cellulaire après une exposition de 96 heures à 31 µg de cyanure libre/L (U.S. EPA, 1985).
Chez les invertébrés, la toxicité du ferrocyanure ne se manifeste généralement qu'à une concentration supérieure à 1 000 µg/L.
Cependant, la plus faible CL50 du cyanure libre (exposition de 96 heures) citée dans la documentation est de 83 µg/L, chez Daphnia magna (U.S. EPA, 1985; Eisler, 1991). L'écart de sensibilité au sein de groupes formés de diverses sous-espèces peut entraîner des modifications dans la structure d'une population, à la suite d'une exposition (Smith et al., 1979). Voir Letts (2000a) pour de plus amples détails.
La toxicité chez les vertébrés a été largement étudiée, que l'on pense aux travaux de Leduc et al. (1982). Les vertébrés sont moins sensibles au ferrocyanure (Schraufnagel, 1965) qu'au cyanure libre (Leduc et al., 1982). Cependant, les poissons semblent plus sensibles au cyanure libre que les invertébrés. La valeur estimative de la CL50 après 96 heures se situe entre 40 et 200 µg d'acide cyanhydrique/L (U.S. EPA, 1985) et on rapporte une grande variété d'effets physiologiques et comportementaux. Par ailleurs, les études sur les stades de vie semblent indiquer que le stade juvénile est le plus sensible, des effets négatifs sur la croissance étant couramment observés. Des effets négatifs sur la prédation, sur les comportements d'évitement et sur la capacité de nager ont aussi été signalés. Les effets nocifs sur la reproduction ont été retenus comme indicateurs cibles de la toxicité. Schraufnagel (1965) et Smith et al. (1979) ont observé une inhibition du frai à des concentrations respectives de 5,0 et 5,2 µg/L.
3.7.3.2 Biote terrestre
Le principal effet du cyanure est de nuire à la respiration, en perturbant une enzyme mitochondriale (Towill et al., 1978; Way et al., 1988). Cependant, si cet effet n'est pas rapidement fatal, le rétablissement est habituellement rapide.
Les microorganismes manifestent peu d'effets négatifs à la suite d'une exposition au cyanure. Certains s'adaptent, notamment en adoptant de nouvelles voies respiratoires. Les données recueillies laissent croire à l'existence d'un « microcycle du cyanure » qui permet aux microorganismes et aux végétaux d'utiliser l'acide cyanhydrique comme source d'azote et de carbone (Allen et Strobel, 1966).
Les végétaux terrestres sont dans l'ensemble assez insensibles au ferrocyanure et au cyanure libre. Il faut ainsi jusqu'à 10 g de ferrocyanure/kg de sol pour inhiber la croissance. Comme les microorganismes, certains végétaux utilisent des voies respiratoires de remplacement ou ont la capacité de métaboliser l'acide cyanhydrique, ou les deux. Certains végétaux manifestent toutefois des effets négatifs. On a ainsi observé une inhibition de 25 % de la levée des semis de radis, à des concentrations aussi faibles que 1,2 mg/kg (Environnement Canada, 1995) -cette concentration est la plus faible à laquelle des effets nocifs ont été observés chez les végétaux terrestres.
Bien que certains invertébrés résistent au cyanure ou en produisent pour se défendre, la plupart manifestent une certaine sensibilité. La plus faible concentration de cyanure libre (4 mg/kg) ayant causé des effets nuisibles chez les invertébrés terrestres a causé la mort de 25 % des vers de terre (Eisenia fetida) qui y avaient été exposés pendant 14 jours (Environnement Canada, 1995).
L'usage des ferrocyanures comme additifs alimentaires et à des fins thérapeutiques a été approuvé. Aucun effet n'a été observé chez des rats exposés à 3 200 mg/kg-p.c. par jour (Dvorak et al., 1971). Dans le cas de l'acide cyanhydrique, les normes actuelles établies en fonction d'une marge de sécurité de l'ordre de 7 à 8 fois limitent l'exposition à 5 mg/m3 (Klaassen, 1966). Se basant sur les études disponibles, la U.S. EPA a fixé la dose subchronique de référence à 0,08 mg/kg-p.c. par jour pour le cyanure libre. Toujours selon la documentation disponible, le mammifère le plus sensible aux effets nuisibles est le lapin (Oryctolagus spp.). Ballantyne (1987) a observé une DL50 de 0,6 mg/kg-p.c. Chez les oiseaux, le canard colvert (Anas platyrhynchos) semble le plus sensible, la DL50 orale s'établissant à 2,7 mg/kg-p.c., dans le cas du cyanure de sodium (Henny et al., 1994).
3.7.4 Caractérisation du risque
Comme on l'a mentionné précédemment, le principal danger environnemental lié à l'utilisation du ferrocyanure de sodium vient de la capacité de l'anion ferrocyanure en solution de se décomposer en présence de lumière pour libérer l'ion cyanure qui formera, par hydrolyse, de l'acide cyanhydrique. Ce processus a largement été étudié par Broderius et Smith (1980), qui notent que la vitesse de réaction est habituellement directement fonction de l'intensité de la lumière (elle-même tributaire de la période de l'année, de l'heure du jour et de la nébulosité), de la température et de la concentration et inversement liée au pH et à la latitude. Un maximum de cinq des six molécules de cyanure disponibles peuvent être libérées.
Pour les évaluations basées sur les hypothèses de niveau 1 et 2, on a calculé les valeurs du quotient pour le biote, en divisant la concentration maximale (mesurée ou estimée) de cyanure libre dans l'eau, l'air ou le sol, par la VESEO correspondante. Les VESEO utilisées correspondent aux VCT, c'est-à-dire aux plus faibles concentrations avec effet citées dans les études disponibles sur la toxicité, divisées par le coefficient approprié.
3.7.4.1 Caractérisation du risque de niveau 1
Pour l'évaluation de niveau 1, le taux de photolyse a été calculé à partir de facteurs de correction basés sur le pire des scénarios et de valeurs caractéristiques d'emplacements au Canada. On suppose ainsi que la réaction se produit à une latitude de 45 °N à midi, par une journée sans nuages, à une température de 4 °C. La vitesse de réaction dans ces conditions est de 28,5 % par heure. Au plus, cinq des six anions cyanure peuvent être libérés de la molécule de ferrocyanure, durant la photolyse. On considère en outre que la totalité du cyanure ainsi produit est retenue dans le milieu environnemental en question.
Si l'on se base sur les concentrations maximales annuelles moyennes de cyanure dans les eaux de ruissellement, qui ont été déterminées précédemment, on constate que la concentration maximale potentielle de cyanure, après libération du nombre maximal possible d'anions cyanure par photolyse, se situe entre 0,087 et 870 µg d'ions cyanure/L. Si on suppose une période de réaction d'une heure, la libération d'ions cyanure dans l'eau par photolyse donnerait lieu à une concentration variant entre 0,025 et 250 µg/L.
D'après le taux d'épandage maximal annuel de sels (c.-à-d. 10 150 g/m2) et les hypothèses de niveau 1 et du cas no I (sol), la concentration maximale potentielle de cyanure, après libération du nombre maximal possible d'anions cyanure par photolyse, serait de 1,35 mg d'ions cyanure/kg de sol. Après une période de réaction d'une heure, les ions cyanure libérés par photolyse donneraient lieu à une concentration de 0,39 mg/kg.
D'après le taux d'épandage maximal annuel de sels (c.-à-d. 10 150 g/m2) et les hypothèses de niveau 1 et du cas no II (sol), la concentration maximale potentielle de cyanure, après libération du nombre maximal possible d'anions cyanure par photolyse, serait de 0,027 mg d'ions cyanure/kg de sol. Après une période de réaction d'une heure, les ions cyanure libérés par photolyse donneraient lieu à une concentration de 0,0078 mg/kg.
Le taux de volatilisation du cyanure à des concentrations variant entre 0,1 et 0,5 mg/L est de 0,22 mg d'ions cyanure/m2 par heure (Higgs, 1992). Aux fins de l'évaluation de niveau 1, on a utilisé un modèle en boîte fermée qui correspond à une couche atmosphérique de 10 cm au-dessus de la route. Après une heure, la concentration maximale de cyanure dans cette couche serait de 2,2 mg d'ions cyanure/m3.
Les quotients ont été calculés en utilisant la concentration maximale estimée de cyanure libre et la concentration maximale mesurée de cyanure total (qu'on présume être du cyanure libre, aux fins de l'évaluation de niveau 1) dans l'eau (soit 250 et 270 µg/L ) (Novotny et al., 1997), comme suit : Quotient = VEE/VESEO.
Pour les organismes terrestres, les quotients ont été calculés en utilisant la concentration maximale estimée de cyanure libre dans le sol d'après les hypothèses de niveau 1 (c.-à-d. 0,39 mg/kg de sol). La documentation ne précise aucune concentration de cyanure libre mesurée dans le sol. Pour les oiseaux et les mammifères, les VEE ont été calculées à l'aide d'un modèle à voies multiples qui tient compte de l'apport provenant du sol, de l'air et de l'eau.
Tous les quotients sont supérieurs à un (tableaux 26 et 27), sauf ceux pour les vertébrés et les invertébrés terrestres, les organismes aquatiques paraissant particulièrement sensibles. Une évaluation de niveau 2 est donc justifiée.
3.7.4.2 Caractérisation du risque de niveau 2
L'évaluation de niveau 2, bien que toujours prudente, s'appuie sur des scénarios et des hypothèses plus représentatifs et sur des variables caractéristiques mesurées.
Le taux d'addition de ferrocyanure de sodium aux sels de voirie a diminué au cours des dernières années. Le taux d'addition en 1997, soit 80 mg de ferrocyanure de sodium/kg de sels (ce qui correspond à 55,8 mg d'ions ferrocyanure/kg et à 41,1 mg d'ions cyanure/kg de sels de voirie), étant plus représentatif de l'usage actuel, cette valeur sera utilisée pour l'évaluation de niveau 2.
Labadia et Buttle (1996) ont mesuré le profil de dispersion des sels de voirie le long d'un tronçon d'une autoroute du sud de l'Ontario. Leurs observations montrent qu'un peu plus de 50 % des sels épandus se retrouvent dans les bancs de neige adjacents, à l'intérieur d'une zone d'éclaboussures de 3,7 m. Cette donnée sera également utilisée pour l'évaluation de niveau 2.
Le calcul du taux de photolyse du ferrocyanure a été corrigé pour tenir compte d'une intensité lumineuse quotidienne moyenne et de conditions correspondant à un ciel dégagé à 70 %. Des corrections ont aussi été faites pour tenir compte des variations dans la concentration initiale de ferrocyanure. Dans l'ensemble, les hypothèses de niveau 2 donnent un taux de photolyse corrigé de 13,8 % par heure.
1 (m) = D'après la concentration mesurée dans l'eau; (e) = D'après la concentration estimée dans l'eau.
Selon les hypothèses de niveau 2 et les concentrations maximales annuelles moyennes d'ions chlorure compilées par Morin et Perchanok (2000), la concentration d'ions cyanure dans l'eau après une heure varie entre 0,0039 et 39 µg/L.
À partir du taux d'épandage maximal annuel de sels (c.-à-d. 10 150 g/m2) et des hypothèses de niveau 2 et du cas no I (sol), la concentration dans le sol après libération par photolyse des ions cyanure du ferrocyanure disponible serait de 0,12 mg d'ions cyanure/kg dans le sol, après une heure.
À partir du taux d'épandage maximal annuel de sels (c.-à-d. 10 150 g/m2) et des hypothèses de niveau 2 et du cas no II (sol), la concentration dans le sol après libération par photolyse des ions cyanure du ferrocyanure disponible serait de 0,0024 mg d'ions cyanure/kg dans le sol, après une heure.
Le taux de volatilisation du cyanure à des concentrations de 0,1 à 0,5 mg/L est de 0,22 mg d'ions cyanure/m2 par heure (Higgs, 1992). Aux fins de la présente évaluation, on suppose que la totalité du cyanure disponible est transférée dans l'air au-dessus de la route, sans aucune dispersion, et que le taux de diffusion gazeuse est identique au taux de diffusion interfaciale. Dans ces conditions, la concentration maximale de cyanure dans cette couche serait de 0,22 mg/m3, après une heure.
Pour calculer les quotients, on a utilisé la concentration maximale estimée de cyanure libre dans les eaux de ruissellement, selon les hypothèses de niveau 2 (c.-à-d. 39 µg/L), et la concentration maximale mesurée (41 µg/L), celle-ci correspondant à la moyenne géométrique des valeurs mesurées, citées dans la documentation. Les VCT ayant servi à l'évaluation de niveau 1 sont également utilisées pour l'évaluation de niveau 2, mais certains coefficients ont été modifiés pour offrir une analyse plus réaliste.
L'évaluation des organismes terrestres est basée sur la concentration maximale estimée de cyanure libre dans le sol, selon les hypothèses de niveau 2 (soit 0,12 mg/kg de sol). La documentation ne précise aucune concentration de cyanure libre mesurée dans le sol. La même méthode ayant servi à l'évaluation de niveau 1 a été utilisée pour calculer les VEE pour les oiseaux et les mammifères.
Selon les quotients calculés (tableaux 28 et 29), il faudrait procéder à une évaluation de niveau 3 pour les organismes aquatiques.
3.7.4.3 Caractérisation du risque de niveau 3
Les analyses de niveau 1 et 2 montrent que le ferrocyanure de sodium peut avoir des effets nocifs sur le milieu aquatique, à cause de la formation de cyanure. L'évaluation de niveau 3 vise à quantifier la probabilité que des effets nocifs se produisent en milieu aquatique.
Comme on l'a déjà mentionné, la libération de cyanure libre par photolyse du ferrocyanure demeure la principale préoccupation liée aux rejets de ferrocyanure dans l'environnement. La photolyse complète en fonction des longueurs d'onde qui s'appliquent et les taux de volatilisation peuvent être représentés au moyen de modèles mathématiques; à partir de ces modèles, on peut ensuite calculer la concentration de cyanure libre en solution, à n'importe quel moment après l'épandage des sels de voirie. Ces calculs ont fait partie de l'évaluation de niveau 3.
Aux fins de l'évaluation de niveau 3, on a utilisé les hypothèses et les facteurs de correction suivants pour estimer les taux de photolyse et de volatilisation du ferrocyanure. Comme la photolyse est fonction de la profondeur de l'eau et de sa limpidité, on a supposé que le ferrocyanure se situait dans les 20 premiers cm et on a utilisé les mesures de limpidité d'une variété de plans d'eau. De même, la vitesse de réaction est fonction de la période de l'année, de l'heure du jour, de la nébulosité et de la température. On a donc fait des calculs pour chaque heure du jour, le 1er janvier, le 1er avril, le 21 juin et le 21 septembre, selon un ciel dégagé à 70 %, la constante de la loi de Henry étant corrigée en fonction d'une température moyenne de 4 °C. Comme on l'a fait précédemment, on a tenu compte ici aussi des observations de Labadia et Buttle (1996), selon lesquelles environ 50 % de la quantité initiale des sels épandus se retrouve dans les bancs de neige adjacents. Le débit du cours d'eau et la vitesse du vent ont été estimés à partir de mesures directes provenant de sources canadiennes. Le débit moyen du cours d'eau a été établi à 0,52 m/s et la vitesse du vent a été fixée à 5,0, 4,7, 3,8 et 3,8 m/s, respectivement pour les mois de janvier, avril, juin et septembre. La concentration d'ions chlorure dans les eaux de ruissellement a été choisie parmi l'intervalle des valeurs compilées par Morin et Perchanok (2000), la probabilité de sélection d'une concentration donnée variant en fonction de la superficie de la zone pour laquelle cette concentration a été signalée. Enfin, les taux d'addition de ferrocyanure de sodium devant servir aux calculs ont été choisis en fonction là aussi d'une probabilité, celle-ci reflétant la part du marché détenue par la source correspondante de sels.
On a effectué les calculs en choisissant chaque variable au hasard à partir de la distribution statistique appropriée. Les variables incluent la concentration de chlorure dans les eaux de ruissellement, la concentration de ferrocyanure dans les sels, la vitesse du courant et du vent et le coefficient d'atténuation. Des courbes de la photodécomposition et de la volatilisation ont été créées pour chaque date à l'étude. On a ensuite enregistré la valeur maximale de cyanure libre ainsi produite. Cette démarche a été répétée 10 000 fois, puis les concentrations maximales observées de cyanure libre (VEEMax) ainsi calculées ont été triées par ordre ascendant. Les VCT pour chaque organisme aquatique ont ensuite été comparées à ces distributions obtenues de façon aléatoire et on a déterminé la probabilité qu'une exposition donnée soit égale ou supérieure à la VCT. Cette démarche a été exécutée en double, d'abord en utilisant des données calculées pour l'ensemble du Canada, puis en utilisant les données sur la région affichant le taux d'utilisation le plus élevé, en l'occurrence le corridor Québec-Windsor.
Comme on possède des données détaillées sur l'utilisation des sels de voirie par bon nombre de municipalités canadiennes, la démarche précitée a été répétée en utilisant les données sur l'épandage de sels de trois municipalités représentant les taux d'utilisation municipale maximal, moyen et minimal au Canada. Les municipalités choisies sont La Tuque (Québec), Newmarket (Ontario) et White River (Ontario). Un bref résumé des résultats obtenus est présenté ci-après. Les résultats complets sont décrits dans un document complémentaire préparé par Letts (2000a).
1) Microorganismes aquatiques
Les analyses indiquent que Pseudomonas putida subirait des effets nocifs dans 100 % des expositions modélisées. Dans la municipalité représentant le taux maximal d'utilisation, Microregma heterostoma subirait des effets nuisibles dans 60 % des cas. Il convient toutefois de préciser que le taux d'épandage de sels de voirie dans cette municipalité est au moins deux fois supérieur au taux déclaré par la totalité (sauf deux) des 90 autres villes canadiennes affichant les taux d'épandage les plus élevés. Dans les autres villes, des effets devraient se produire dans 10 à 20 % des cas. Aucun effet nocif n'a été signalé pour aucun des cinq autres microorganismes aquatiques étudiés. Donc, bien que le ferrocyanure présent dans les sels de voirie pose peu de risques pour cinq des sept microorganismes pour lesquels des données sont disponibles, des effets nocifs peuvent se manifester chez les espèces les plus sensibles.
2) Plantes aquatiques
Les résultats montrent que Scenedesmus quadricauda, qui est l'algue la plus sensible décelée, pourrait subir des effets nocifs dans 16 à 28 % des scénarios d'exposition possibles, cette proportion atteignant jusqu'à 82 % dans la municipalité ayant le taux d'épandage le plus élevé. Ces valeurs indiquent que des effets modérés pourraient se manifester à certaines périodes, chez certaines espèces sensibles, mais que le risque est moins élevé pour la plupart des plantes aquatiques, dans la plupart des lieux et des périodes.
3) Invertébrés aquatiques
Chlamys asperrimus pourrait subir des effets nocifs dans 34 % des expositions se produisant en avril, dans le corridor Québec-Windsor.
La probabilité d'effets négatifs sur cet organisme diminue à moins de 25 % des cas, dans d'autres lieux et à d'autres périodes. Dans la municipalité ayant le taux d'épandage le plus élevé, des effets nocifs ont été prévus dans 88 % des cas. Aucun autre organisme ne risque de subir des effets négatifs dans plus de 3,5 % des cas d'exposition. En général, on considère que les membres de ce groupe ne courent pas de risque grave, même si des expositions importantes peuvent se produire chez certaines espèces sensibles.
4) Vertébrés aquatiques
Ce sont les vertébrés aquatiques qui présentent le plus haut risque d'exposition importante. Parmi les études examinées par Letts (2000a), les valeurs de la CL50 après 96 heures pour la truite arc-en-ciel fluctuent entre 17 µg/L (Higgs, 1992), 27 µg/L (Smith et al., 1979) et 28 µg/L (Kovacs, 1979; Kovacs et Leduc, 1982). La probabilité que des concentrations supérieures ou égales à ces valeurs se produisent est respectivement de 52,6 %, 26,8 % et 25,2 % en janvier et de 67,2 %, 36,2 % et 33,8 % en avril, aux endroits situés dans le corridor Québec-Windsor. Il s'agit de la région où ont été enregistrées les concentrations les plus élevées, par les deux sources de données les plus complètes. Des concentrations de cet ordre sont plus susceptibles de se manifester dans les régions où la concentration maximale annuelle moyenne de chlorure issu des sels de voirie est supérieure à 1 000 mg/L dans les eaux de ruissellement (concentration modélisée pour 53 des 90 villes). Dans ces régions, le ferrocyanure dans les eaux de ruissellement non diluées pourrait avoir des effets sur les invertébrés aquatiques.
3.7.5 Conclusion pour les ferrocyanures
La présente évaluation indique qu'aux taux d'épandage actuels de sels de voirie les effets potentiellement négatifs associés au ferrocyanure de sodium se limitent au biote aquatique, certains effets négatifs pouvant se manifester chez les espèces sensibles de microorganismes, de végétaux et d'invertébrés aquatiques. Les vertébrés aquatiques les plus sensibles, présents dans les fossés et les cours d'eau qui longent les routes dans les régions de forte utilisation, seraient par ailleurs les plus vulnérables aux expositions nocives. D'une part, la modélisation de la probabilité que des effets se produisent a été basée sur les expositions prévues dans les fossés et n'a pas tenu compte de la dilution subséquente dans les plans d'eau récepteurs, ce qui aurait tendance à surestimer l'exposition. D'autre part, la modélisation a été basée sur la dilution des sels par les précipitations annuelles totales, ce qui sous-estimerait l'exposition à n'importe quelle période. L'effet ultime des ferrocyanures sur les populations de poissons varie en fonction d'un large éventail de paramètres, incluant des paramètres qui influent sur les quantités de ferrocyanure pénétrant dans les cours d'eau (p. ex., quantité de sels de voirie utilisée et période d'épandage, ruissellement), sur la photolyse des ferrocyanures en cyanure (p. ex., ensoleillement, turbidité de l'eau, température), sur la volatilisation du cyanure (p. ex., débit d'eau, température), sur l'état des populations de poissons et d'amphibiens dans les plans d'eau récepteurs, sur le taux de dilution dans les plans d'eau récepteurs, etc. Par conséquent, même si les données disponibles indiquent un risque d'effets négatifs, il est impossible de prévoir d'une manière fiable l'impact des ferrocyanures sur les populations de vertébrés dans les plans d'eau situés en bordure ou à proximité des routes.
3.8 Conclusions globales
3.8.1 Considérations
Comme le prévoit le paragraphe 76(1) de la LCPE 1999, les substances inscrites sur la LSIP doivent faire l'objet d'une évaluation afin de déterminer si elles sont « effectivement ou potentiellement toxiques ». Dans le cadre de la présente évaluation, les sels de voirie ont été évalués pour déterminer s'ils sont effectivement ou potentiellement toxiques au sens des alinéas 64a) et 64b) de la LCPE 1999, selon lesquels :
... est toxique toute substance qui pénètre ou peut pénétrer dans l'environnement en une quantité ou concentration ou dans des conditions de nature à : a) avoir, immédiatement ou à long terme, un effet nocif sur l'environnement ou sur la diversité biologique; b) mettre en danger l'environnement essentiel pour la vie.
3.8.1.1 Environnement
La LCPE 1999 propose une définition assez vaste d'« environnement », celui-ci incluant tous les composants biotiques et abiotiques de la biosphère (LCPE 1999, article 3) : « environnement » ensemble des conditions et des éléments naturels de la Terre, notamment
- l'air, l'eau et le sol;
- toutes les couches de l'atmosphère;
- toutes les matières organiques et inorganiques ainsi que les êtres vivants; d) les systèmes naturels en interaction qui comprennent les éléments visés aux alinéas a) à c).
Cette définition ne fait pas de distinction entre environnement « naturel » et « non naturel ». De fait, on peut considérer que tous les écosystèmes ont été exposés à des stress ou à des modifications résultant de l'activité humaine, que ce soit à l'échelle locale (p. ex., destruction de l'habitat, émission de polluants non persistants dans les effluents liquides), régionale (p. ex., dispersion de polluants atmosphériques) ou mondiale (polluants organiques persistants, effets atmosphériques mondiaux, etc.).
L'entreposage et l'épandage des sels de voirie, de même que l'élimination de la neige usée, se font dans des lieux aménagés - en l'occurrence les entrepôts de sels, le réseau routier et les lieux d'élimination de la neige. Cependant, le degré « d'aménagement » de ces lieux varie considérablement. Ainsi, les sels de voirie peuvent être entreposés dans des installations spécialement conçues à cette fin ou, au contraire, être temporairement empilés en bordure des routes ou dans des entrepôts de sels. Les routes peuvent faire partie de réseaux complexes avec emprises et fossés maçonnés ou longer des cours d'eau, des lacs ou des terres humides qui reçoivent directement les eaux de ruissellement routier. Enfin, les décharges de neige varient d'installations étanches dotées de dispositifs de rétention et de traitement des eaux de fonte à de simples décharges aménagées sur des terrains vacants. Donc, la quantité de sels de voirie qui s'échappent de ces lieux artificiels varie elle aussi sensiblement, tout comme le niveau de préoccupation que suscitent ces installations ou les mesures de protection qu'elles requièrent.
Dans certains cas, les composantes environnementales qui se trouvent à l'intérieur ou à proximité immédiate de ces systèmes artificiels peuvent revêtir une grande importance, sur le plan écologique (Nadec, 2001). Il a ainsi été démontré que les abords des routes servaient d'habitat à une grande diversité d'espèces (Perring et al., 1964; Oetting et Cassel, 1971; Way, 1977; Laursen, 1981; Adams et Geiss, 1983; Auestad et al., 1999; Bellamy et al., 2000). Les abords des routes jouent donc deux rôles écologiques importants :
- Ils contribuent à préserver la biodiversité en servant d'habitat à certaines espèces. En Grande-Bretagne, par exemple, 35 des 257 espèces végétales rares poussent le long des routes et ces endroits sont même devenus l'habitat principal de certaines de ces espèces (Way, 1977). Au Québec, 75 espèces d'oiseaux ont été observées dans les emprises routières, dont 29 espèces sont des oiseaux migrateurs qui parcourent de grandes distances et 10 sont des résidents locaux à l'année (Lacroix et Bélanger, 2000). Les oiseaux migrateurs sont des espèces protégées, en vertu des dispositions de la Loi sur la Convention concernant les oiseaux migrateurs. Dans certaines régions du Québec, les fossés en bordure des routes sont les seuls endroits où l'on a observé la reproduction de la grenouille Pseudacris triseriata - une espèce classée vulnérable parmi les espèces en péril de cette province (Saumure, 2001). Dans le sud-ouest de l'Ontario, de 0,5 à 3,8 % des prairies d'herbes hautes ou des savanes de chênes, recensées lors des relevés effectués durant les années 1700 et 1800, sont toujours présentes (Bakowsky et Riley, 1994). Au moins 35 espèces végétales indigènes des prairies d'herbes hautes sont toujours présentes en bordure des routes du sud et du centre de l'Ontario, là où les conditions rappellent celles des prairies (Woodliffe, 2001), et treize d'entre elles figurent sur la liste provinciale des espèces rares, menacées ou en péril (Argus et al., 1987; Woodliffe, 2001).
- Les abords des routes réduisent la probabilité que des espèces locales disparaissent à cause de la fragmentation de leur habitat. Bien qu'il ait été démontré que la fragmentation de l'habitat contribue à la disparition de l'espèce (Wilcox et Murphy, 1985), des recherches montrent également que, lorsqu'il y a fragmentation, le fait de relier les fragments au moyen de bandes d'habitat propice contribue au maintien de la biodiversité à l'intérieur de ces fragments (Noss, 1983; Lefkovitch et Fahrig, 1985; Bennett, 1990; Bélanger, 2000). Or il a été démontré que les bordures de route procurent des bandes d'habitat propice, qui relient divers fragments et qui assurent ainsi la continuité de l'habitat (Huey, 1941; Getz et al., 1978; Lewis, 1991; Andreassen et al., 1996).
Toute modification dans les habitats en bordure des routes, résultant de la contamination par les sels de voirie, pourrait donc nuire à la valeur écologique de ces zones.
3.8.1.2 Effets nocifs
Bien sûr, tout changement environnemental n'est pas forcément négatif. Ainsi, les changements qui se situent à l'intérieur des fluctuations normales ne sont pas forcément nocifs en soi, ni n'entraînent nécessairement des effets nocifs, mais les changements plus marqués peuvent l'être. Les dommages susceptibles de résulter d'une augmentation de la concentration de sels dans l'environnement dépendent, entre autres, de l'ampleur, de la durée et de la fréquence des changements.
Par ailleurs, les effets observés au niveau d'une population, d'une communauté ou d'un écosystème sont en général considérés plus dommageables, sur le plan environnemental, et plus préoccupants que ceux qui se manifestent à un niveau inférieur. Peu d'études ont cherché à déterminer directement les effets d'une substance inscrite sur la Liste des substances d'intérêt prioritaire sur une population, une communauté ou un écosystème. En effet, la plupart des études toxicologiques sont réalisées en laboratoire, sur des échantillons qui sont relativement petits lorsqu'on les compare à la taille des populations dans l'environnement naturel. Malgré ces limites, bon nombre des effets mesurés lors d'études en laboratoire et sur le terrain peuvent s'appliquer à des populations, communautés et écosystèmes. Les effets sur des processus tels que la croissance, la reproduction ou la survie sont étroitement liés à la viabilité des populations naturelles et servent d'indication des risques de dommage environnemental. Donc, bien qu'il soit souvent impossible de quantifier les effets probables sur l'écosystème, on peut présumer que, lorsque les concentrations ambiantes se rapprochent des concentrations associées à de graves effets sur des organismes particuliers (p. ex., la concentration létale moyenne), il en résultera également des effets nocifs sur l'environnement.
3.8.1.3 Poids de la preuve
En vertu de l'article 76.1 de la LCPE 1999, les ministres « appliquent la méthode du poids de la preuve et le principe de la prudence », durant l'examen et l'interprétation des résultats de l'évaluation visant à déterminer si une substance inscrite sur la LSIP est « effectivement ou potentiellement toxique ».
Il est impossible de déterminer le seuil précis où les effets sont considérés suffisamment étendus ou dommageables pour déclarer une substance « effectivement ou potentiellement toxique ». La méthode du poids de la preuve consiste à examiner plusieurs sources de données et paramètres, en tenant compte notamment de plusieurs sources de données pour un milieu environnemental particulier (p. ex., évaluation des eaux de surface en regard des seuils de toxicité pour un éventail d'organismes aquatiques, du risque de modification des populations d'algues dulcicoles, de la modification de la structure physique des lacs, de l'exposition due à la contamination des sources par des eaux souterraines). Les conclusions globales finales doivent tenir compte de l'éventail complet des sources de données, dont certaines ne permettent de tirer que des conclusions ténues alors que d'autres fournissent des preuves plus rigoureuses. En utilisant la méthode fondée sur le poids de la preuve, on peut réduire les biais et les incertitudes qui résultent de l'utilisation d'une seule méthode pour estimer les risques.
3.8.2 Résumé de l'évaluation
Les sels de voirie servent en hiver à l'entretien des routes (déglaçage et anti-glaçage) et, en été, à la réduction de la poussière. Les sels inorganiques de chlorure examinés dans la présente évaluation incluent le chlorure de sodium, le chlorure de calcium, le chlorure de potassium et le chlorure de magnésium. Dans l'environnement, ces sels se dissocient en un anion chlorure et son cation correspondant. On a en outre évalué les ferrocyanures, des additifs antiagglomérants ajoutés à certains sels de voirie. On estime qu'environ 4 750 000 tonnes de fondants au chlorure de sodium ont été épandues pendant l'hiver 1997-1998 et que 110 000 tonnes de chlorure de calcium sont utilisées sur les routes chaque année. On n'utilise que de très petites quantités des autres sels. D'après ces estimations, environ 4,9 millions de tonnes de sels de voirie peuvent être rejetées dans l'environnement au Canada chaque année, soit environ 3,0 millions de tonnes de chlorure. Les charges annuelles en sels de voirie sont les plus fortes en Ontario et au Québec, moyennes dans les provinces de l'Atlantique, et les plus faibles dans les provinces de l'Ouest.
Les sels de voirie pénètrent dans l'environnement canadien à la suite de leur entreposage et de leur utilisation, et de l'élimination de la neige enlevée des routes. Ils pénètrent dans les eaux de surface, dans le sol et dans les eaux souterraines après la fonte des neiges, et sont dispersés dans l'atmosphère par les éclaboussures et la pulvérisation d'eau causées par les véhicules et par la poussière transportée par le vent. Les ions chlorure sont très conservatifs, c'est-à-dire qu'ils suivent le cycle de l'eau sans retard et sans perte. Par conséquent, presque tous les ions chlorure qui pénètrent dans le sol et les eaux souterraines atteindront éventuellement les eaux de surface : quelques années à quelques décennies ou plus peuvent être nécessaires pour que les concentrations dans les eaux souterraines atteignent l'état d'équilibre. Les préoccupations qui concernent les sels de voirie touchent tous les milieux environnementaux à cause de leur dispersion générale dans l'environnement.
Les concentrations de fond naturelles de chlorure dans l'eau sont généralement de quelques mg/L, avec quelques instances locales ou régionales de plus forte salinité naturelle, par exemple dans certaines régions des Prairies et de la Colombie-Britannique. On a mesuré de fortes concentrations de chlorure liées à l'épandage des sels de voirie sur les routes ou rejetés des entrepôts de sels ou des lieux d'entreposage de la neige. Par exemple, on rapporte des concentrations de chlorure supérieures à plus de 18 000 mg/L dans les eaux de ruissellement des routes. On a aussi observé des concentrations allant jusqu'à 82 000 mg/L dans les eaux de ruissellement des amas non recouverts de mélanges d'abrasifs et de sels d'un entrepôt de sel. Les concentrations de chlorure de la neige déblayée des rues des villes peuvent varier considérablement. Par exemple, les concentrations moyennes de chlorure de la neige provenant des rues de Montréal allaient de 3 000 à 5 000 mg/L respectivement pour les rues secondaires et primaires. Les eaux provenant des routes, des entrepôts de sels ou des lieux d'entreposage de la neige peuvent se diluer à divers degrés lorsqu'elles pénètrent dans l'environnement, où on a mesuré des concentrations de chlorure allant jusqu'à 2 800 mg/L dans les eaux souterraines de zones adjacentes à des entrepôts de sels, jusqu'à 4 000 mg/L dans des étangs et des milieux humides, jusqu'à 4 300 mg/L dans des cours d'eau, jusqu'à 2 000 à 5 000 mg/L dans des étangs urbains endigués et jusqu'à 150 à 300 mg/L dans des lacs ruraux. Alors que les plus fortes concentrations sont habituellement associées au dégel hivernal ou printanier, on peut également mesurer de fortes concentrations en été, en raison du temps que prennent les ions à parvenir aux eaux de surface et des débits réduits en été. Les plans d'eau les plus sujets aux impacts des sels de voirie sont les petits étangs et les cours d'eau qui drainent les grandes zones urbanisées, ainsi que les cours d'eau, les milieux humides ou les lacs qui drainent les grandes routes. Des mesures sur le terrain révèlent que l'épandage sur les routes dans les régions rurales peut augmenter les concentrations de chlorure même dans des lacs à quelques centaines de mètres des routes.
On a évalué la possibilité d'impacts sur les réseaux régionaux d'eaux souterraines à l'aide d'une technique de bilan massique qui donne une indication des concentrations de chlorure possibles en aval d'un réseau routier sur lequel il y a épandage de sel. Le modèle de bilan massique et les mesures sur le terrain ont indiqué qu'on pourrait voir des concentrations de chlorure supérieures à 250 mg/L dans les eaux souterraines régionales sous un réseau routier à forte densité sujet à des charges annuelles de plus de 20 tonnes de chlorure de sodium par kilomètre de route à 2 voies. D'après les données sur les charges de sels de voirie, les zones urbaines du sud de l'Ontario et du Québec et les provinces de l'Atlantique sont les plus menacées par les impacts sur les eaux souterraines régionales. Les eaux souterraines aboutissent dans les eaux de surface ou émergent sous forme d'infiltration et de sources. Des recherches ont montré que 10 à 60 % du sel épandu pénètre dans les eaux souterraines peu profondes et s'accumule jusqu'à ce qu'on atteigne des concentrations stabilisées. On a décelé des concentrations élevées de chlorure dans les sources d'eaux souterraines émergeant à la surface.
On observe habituellement des effets toxiques aigus sur les organismes aquatiques à des concentrations de chlorure relativement élevées. Par exemple, la concentration létale moyenne de 4 jours (CL50) pour le cladocère Ceriodaphnia dubia est de 1 400 mg/L. L'exposition à de telles concentrations est possible dans les petits cours d'eau situés dans les zones urbaines très peuplées, où le réseau routier est dense et la charge en sel de voirie très élevée, dans les étangs et les milieux humides adjacents aux routes, près des entrepôts de sels mal gérés, et à certains lieux d'entreposage de la neige.
On observe une toxicité chronique à de plus faibles concentrations. Les effets toxiques pour le biote aquatique sont associés à l'exposition à des concentrations de chlorure aussi faibles que 870, 990 et 1 070 mg/L pour les effets létaux moyens (embryons de têtes-de-boule, oeufs/embryons de truite arc-en-ciel, daphnies, respectivement). La concentration sans effet observé (CSEO) pour le test sur la survie du premier stade de 33 jours de la tête-de-boule était de 252 mg/L de chlorure. De plus, on estime qu'environ 5 % des espèces aquatiques seraient touchées (concentration létale moyenne) à des concentrations de chlorure d'environ 210 mg/L, alors que 10 % pourraient l'être à environ 240 mg/L. Des concentrations encore plus faibles peuvent provoquer des changements à la structure des populations ou des communautés. Chaque espèce d'algue ayant sa concentration optimale de chlorure pour sa croissance et sa reproduction, on a associé des changements de populations dans les lacs à des concentrations de 12 à 235 mg/L. Les fortes concentrations de chlorure dans les lacs peuvent mener à une stratification qui, en retardant ou empêchant le mélange saisonnier des eaux, peut avoir des répercussions sur la distribution de l'oxygène et des éléments nutritifs. On a observé des concentrations de chlorure entre 100 et 1 000 mg/L ou plus dans divers cours d'eau et lacs urbains. Par exemple, les concentrations maximales de chlorure dans des échantillons d'eau prélevés dans quatre ruisseaux de la région de Toronto variaient de 1 390 à 4 310 mg/L. On a signalé des concentrations de chlorure supérieures à environ 230 mg/L, correspondant à celles qui ont des effets chroniques sur les organismes sensibles, dans ces quatre cours d'eau durant une grande partie de l'année. Dans les zones où on utilise beaucoup de sels de voirie, particulièrement dans le sud de l'Ontario et du Québec et dans les Maritimes, les concentrations de chlorure dans les eaux souterraines et les eaux de surface atteignent souvent des niveaux pouvant affecter le biote, comme l'ont démontré des études faites en laboratoire et sur le terrain.
L'épandage de sels de voirie sur les routes peut également avoir des effets nocifs sur les propriétés physiques et chimiques des sols, particulièrement dans les zones de piètre gestion des sels, sols et végétation. Les effets sont associés aux zones adjacentes aux entrepôts de sels et aux routes, principalement dans les zones de dépression mal drainées. Ces effets sur les sols incluent les impacts sur la structure, la dispersion, la perméabilité, le gonflement et l'encroûtement, la conductivité électrique et le potentiel osmotique du sol, qui peuvent, à leur tour, avoir des impacts abiotiques et biotiques sur l'environnement local. Le principal impact abiotique est la perte de stabilité du sol durant les cycles d'humidification et de séchage, et durant les périodes de fort ruissellement de surface et de vents violents. Les impacts biologiques sont principalement liés au stress osmotique imposé à la macro- et microflore et à la macro- et microfaune du sol, ainsi qu'à la mobilisation des macro- et micronutriments causée par le sel et qui affecte la flore et la faune.
De nombreuses études sur le terrain ont documenté les dommages causés à la végétation et les changements dans la structure des communautés végétales dans les zones touchées par le ruissellement de sels de voiries et la dispersion aérienne. Les espèces halophytes, comme les quenouilles et le roseau commun, envahissent facilement les zones touchées par les sels, modifiant ainsi la présence et la diversité des espèces sensibles au sel. Les teneurs élevées du sol en sodium et en chlorure ou l'exposition aérienne à ces ions entraînent une réduction du nombre de fleurs et de fruits chez les espèces végétales sensibles; des lésions au feuillage, aux pousses et aux racines; une réduction de la croissance; et une réduction de l'établissement des jeunes plants. Les plantes terrestres sensibles peuvent être affectées par des concentrations dans le sol supérieures à 68 mg/L de sodium et à 215 mg/L de chlorure. Les zones ayant ce genre de concentrations longent les routes et les autoroutes et les autres endroits où des sels de voirie sont épandus pour le déglaçage ou la réduction de la poussière. L'impact de la dispersion aérienne se fait sentir jusqu'à 200 m de la bordure des autoroutes à voies multiples et jusqu'à 35 m des routes à deux voies où du sel de déglaçage est utilisé. Le sel nuit aussi à la végétation le long des cours d'eau qui drainent les routes et les installations de manipulation des sels de voirie.
Chez la faune mammifère et aviaire, l'exposition aux sels de voirie provoque des effets sur le comportement ainsi que des effets toxicologiques. L'ingestion de sels de voirie augmente la susceptibilité des oiseaux à être frappés par les automobiles. De plus, le calcul de l'apport en sels de voirie suppose que ces derniers peuvent empoisonner directement certains oiseaux, particulièrement lorsqu'il n'y a pas d'eau libre durant les hivers rigoureux. Les sels de voirie peuvent aussi toucher la faune par leurs effets sur l'habitat : la réduction de la couverture végétale ou les déplacements de populations peuvent avoir des répercussions sur la faune qui dépend de ces plantes pour son alimentation ou son abri. Les données disponibles supposent qu'on aurait sous-estimé la sévérité des mortalités sur la route d'espèces d'oiseaux migrateurs protégées par le fédéral (p. ex. les pinsons de la sous-famille des carduélinés) et la contribution des sels de voirie à cette mortalité.
Les ferrocyanures sont très persistants mais peu toxiques. Toutefois, en solution et en présence de lumière, ils peuvent se dissocier pour former des cyanures. À leur tour, les ions de cyanure peuvent se volatiliser et se dissiper assez rapidement. Les effets ultimes des ferrocyanures dépendent donc de l'équilibre complexe de la photolyse et de la volatilisation qui, elles, dépendent des facteurs environnementaux. Des modèles venant appuyer cette évaluation révèlent qu'il est possible que certains organismes aquatiques subissent des effets du cyanure dans les régions où l'on utilise de grandes quantités de sels de voirie.
3.8.3 Incertitudes
La caractérisation des risques environnementaux associés aux sels de voirie, qui est présentée ici, comporte un certain nombre d'incertitudes et d'hypothèses. Ces incertitudes sont en général liées aux lacunes des données obtenues en laboratoire et sur le terrain, qui ont servi à caractériser l'utilisation des sels de voirie au Canada et à évaluer l'impact de ces sels sur différents paramètres environnementaux. Les paragraphes qui suivent traitent plus en détail des incertitudes inhérentes aux conclusions de la présente évaluation, qui viennent compléter les incertitudes soulevées dans les sections précédentes.
Les données sur les sels de voirie ont été obtenues, dans la mesure du possible, auprès des sources les plus exactes. Les données ont également été analysées, afin de déterminer si l'année de référence choisie pour déterminer les charges de sels de voirie était caractéristique. Les résultats de cette analyse révèlent que les charges durant l'hiver 1997-1998 ne sont pas élevées, lorsqu'on les compare à la période de cinq ans pour laquelle des données ont été recueillies. Cependant, une des limites des données vient de ce que celles-ci sont établies en fonction du district d'entretien provincial. Or bien que ces estimations soient fiables, on ignore la répartition exacte de l'utilisation des sels de voirie à l'intérieur d'un district d'entretien. On a présumé que les sels de voirie avaient été répartis également sur l'ensemble des districts d'entretien. Dans les faits, toutefois, certaines routes reçoivent des charges plus élevées et la densité du réseau routier varie à l'intérieur d'un même district. Des estimations ont également été faites pour tenir compte des municipalités qui n'avaient pas fourni de données et aussi des quantités de sels utilisées à des fins commerciales (p. ex., dans les aires de stationnement). Par contre, on n'a pas estimé le volume de sels utilisé par des particuliers ou d'autres organismes, comme les sociétés de transport ou les autorités portuaires.
La plupart des données présentées dans ce rapport portent sur l'épandage des sels de voirie sur les routes. Cependant, les sels de voirie sont également utilisés dans des aires de stationnement et dans d'autres terrains industriels et commerciaux. Le présent rapport ne fournit aucune donnée sur les concentrations de chlorure dans les eaux de ruissellement qui s'écoulent de ces endroits vers les plans d'eau récepteurs, même si ces rejets risquent d'avoir une incidence sur les eaux réceptrices.
De plus, on ignore le nombre exact de lieux d'entreposage des sels en exploitation au Canada. Selon les données obtenues des organismes provinciaux et territoriaux, ceux-ci géreraient quelque 1 300 entrepôts de sels. Cependant, si l'on considère que d'autres paliers de gouvernement (comme les comtés et les municipalités) et des organismes privés s'occupent également de l'entretien des routes, il est probable que le nombre réel d'entrepôts de sels au Canada ait été grandement sous-estimé. Une autre incertitude a trait à la quantité de sels entreposés dans ces lieux. Des données et des estimations sur la quantité de sels entreposés ont été présentées, mais il s'agit d'estimations approximatives. On a estimé, par exemple, que la quantité de sels entreposés dans ces lieux varie de 45 à 21 000 tonnes. D'autres incertitudes ont trait au type de structures servant à l'entreposage des sels de voirie, au nombre d'organismes qui entreposent des mélanges de sels et d'abrasifs à l'extérieur, au pourcentage de sels dans ces mélanges, au rejet des eaux de lavage ainsi qu'à l'éventail des pratiques utilisées pour réduire l'incidence de l'entreposage des sels de voirie sur l'environnement.
L'utilisation de données sur l'exposition en milieux artificiels, par exemple les fossés, les emprises routières et les bassins de retenue des eaux pluviales, pour estimer les effets environnementaux possibles, crée une autre incertitude. Les environnements modifiés peuvent avoir une importance écologique. Ainsi, dans les régions fortement urbanisées, industrialisées ou agricoles, les paysages modifiés tels que les emprises ou les bassins de retenue peuvent en fait être les seuls habitats disponibles pour bon nombre d'espèces, à l'échelle locale ou régionale, y compris des espèces sensibles et des organismes protégés comme les oiseaux migrateurs. À ce titre, l'examen des effets potentiels dans ces environnements modifiés peut être justifiable et, dans certains cas, les concentrations observées dans les milieux artificiels peuvent servir de valeurs substituts pour les concentrations susceptibles d'être présentes dans les régions adjacentes. Donc, les concentrations dans les fossés peuvent être représentatives des concentrations susceptibles d'être présentes dans les cours d'eau ou les terres humides adjacents aux routes, alors que les concentrations dans les eaux souterraines, sous les installations d'entreposage, peuvent être représentatives des concentrations dans les eaux souterraines, dans les alentours immédiats. Dans d'autres cas, toutefois, il pourrait être plus pertinent de considérer que les données sur des milieux artificiels offrent une estimation des concentrations susceptibles d'être rejetées dans l'environnement après une dilution faible ou importante.
Les modèles utilisés pour estimer l'impact des sels de voirie sur les sols, les eaux de surface et les eaux souterraines comportent eux aussi certaines incertitudes. Au départ, toutes les hypothèses formulées pour caractériser les charges de sels de voirie (p. ex., répartition égale sur l'ensemble du district d'entretien) ont été appliquées aux modèles. Qui plus est, ces modèles ont été conçus de manière à être les plus simples possibles, pour calculer des estimations approximatives raisonnables des effets spatiaux des sels de voirie sur divers paramètres environnementaux, à l'échelle nationale. En raison des variables nombreuses et souvent confusionnelles qui entrent en jeu dans l'environnement, il a été impossible d'élaborer un modèle fournissant des résultats propres à un lieu, et les calculs et les méthodes qui sous-tendent ces modèles s'appuient sur des hypothèses régionales. Or si les différentes variables incluses dans ces modèles avaient été mesurées en fonction de chaque lieu, il aurait été possible d'obtenir, par modélisation, des estimations plus précises de l'impact des sels de voirie sur ces différents paramètres environnementaux. Aussi, les estimations produites à partir de ces modèles doivent-elles être considérées comme étant caractéristiques de la gamme d'effets susceptibles de se produire à l'échelle nationale.
Certaines des données d'exposition présentées ici ont été recueillies dans le cadre des programmes réguliers de surveillance de la qualité de l'eau; les échantillons n'ont donc pas été nécessairement prélevés selon un protocole visant à évaluer les effets des sels de voirie sur la qualité de l'eau. Des études comme celle menée par Whitfield et Wade (1992) montrent l'importance de la surveillance continue pour caractériser les effets temporels des sels de voirie sur les cours d'eau, afin de préciser les fluctuations temporelles des concentrations et déterminer si les organismes sont exposés à des taux causant des effets aigus ou chroniques. Cependant, peu de données de surveillance continue étaient disponibles et les données de surveillance recueillies sur plusieurs années ont servi à caractériser les concentrations qui seraient caractéristiques dans certains lieux, à différentes périodes. De plus, quelques études basées sur un échantillonnage continu ou prolongé ont permis de corroborer les résultats d'autres études.
Faute de données de surveillance continue, il est difficile de déterminer si les échantillons prélevés au hasard sont représentatifs des concentrations maximales ou s'ils reflètent davantage les concentrations ambiantes propres à certaines périodes. Des données de surveillance récentes inédites, portant sur six cours d'eau de la région de Toronto entre septembre 2000 et avril 2001, laissent croire que les concentrations de chlorure demeurent élevées durant tous les mois d'hiver. Ainsi, la concentration de chlorure dans les échantillons prélevés entre le 30 octobre et la fin d'avril, dans le ruisseau Etobicoke, le ruisseau Mimico, la rivière Humber, la rivière Don, le ruisseau Highland et la rivière Rouge, a varié respectivement de 448 à 3 771, de 419 à 5 376, de 264 à 2 110, de 87 à 2 247, de 51 à 1 755 et de 101 à 434 mg/L (Ville de Toronto, 2001). Ces données concordent dans l'ensemble avec d'autres données qui ont servi à caractériser les concentrations de chlorure dans les cours d'eau de la Région du Grand Toronto. Ces données (et les données de surveillance présentées précédemment) semblent en outre indiquer que les organismes aquatiques dans ces cours d'eau seraient exposés à de fortes concentrations de chlorure tout au long de l'hiver et du printemps. D'autres études réalisées au Nouveau-Brunswick indiquent que les concentrations maximales sont atteintes durant l'été.
Une autre incertitude vient des espèces susceptibles d'être touchées par l'utilisation des sels de voirie. Dans les sections sur les écosystèmes aquatiques, la végétation, la faune et les ferrocyanures, les valeurs de toxicité ont été comparées aux concentrations d'exposition caractéristiques de la région en question. À l'intérieur d'une région, toutefois, la distribution des espèces et les concentrations d'exposition correspondantes peuvent varier. Malgré le degré certain d'incertitude, des études de cas ont permis de réduire le niveau d'incertitude et de mettre en lumière le type d'impact auquel on peut s'attendre.
Diverses études de cas, venant étayer les effets des sels de voirie sur des paramètres environnementaux, sont en effet présentées dans ce rapport d'évaluation et la documentation complémentaire. Cet examen des études de cas ne doit toutefois pas être considéré comme exhaustif et il est probable que ces études sous-estiment le nombre de cas où les concentrations de sels ont dépassé les niveaux préoccupants. Par ailleurs, la plupart des études de cas présentées ici ont été mises au premier plan en raison de l'altération du goût de l'eau potable dans des sources alimentées par les eaux souterraines, cette altération étant due à l'élévation de la concentration de sels par suite de l'épandage de sels de voirie. Il est probable que peu de cas de contamination seraient décelés ou déclarés dans les régions éloignées des sources d'eau potable.
Enfin, il est impossible de prévoir l'impact qu'auront les changements climatiques sur l'utilisation future de sels de voirie, cette utilisation étant notamment liée à la fréquence et à la durée des épisodes de précipitations durant lesquels la température de l'air se situe environ entre -10 °C et 0 °C. On peut s'attendre toutefois à ce que toute augmentation annuelle de l'évapotranspiration ou toute diminution des précipitations entraînent une hausse de la concentration de chlorure et d'autres solutés dans les eaux de surface et les eaux souterraines peu profondes. Des données sur le terrain recueillies dans la région des lacs expérimentaux, dans l'ouest de l'Ontario, indiquent qu'une augmentation de la température moyenne de l'air, de 14 °C à 16 °C, a entraîné une hausse de 30 % de l'évaporation (Schindler et al., 1996). Malgré l'accroissement prévu des précipitations dans certaines parties du bassin des Grands Lacs, on s'attend également à une forte hausse de l'évapotranspiration dans le bassin versant des Grands Lacs, ce qui se traduira par une réduction des terres humides (Mortsch et Quinn, 1996) et une hausse correspondante des concentrations de solutés.
3.8.4 Conclusions
Chaque année, près de cinq millions de tonnes de sels de voirie qui contiennent des sels inorganiques de chlorure avec ou sans sels de ferrocyanure sont utilisées au Canada. La presque totalité de ces sels se retrouve dans l'environnement, que ce soit à la suite de leur épandage sur le réseau routier ou de pertes provenant des entrepôts de sels ou des lieux d'élimination de la neige. Le présent rapport a défini les situations où les concentrations dans l'environnement sont supérieures ou comparables aux concentrations ayant des effets nocifs sur les propriétés physiques des sols ou des cours d'eau, ou sur les organismes associés à des habitats dulcicoles et terrestres, à de nombreux endroits au Canada.
La contamination locale et régionale des eaux souterraines peut donner lieu, parfois après plusieurs années ou décennies, à de fortes concentrations de chlorure, y compris à des concentrations supérieures aux valeurs de toxicité aiguë et chronique pour les organismes présents dans les sources d'eau.
Dans les eaux de surface associées à des routes ou des lieux d'entreposage, des épisodes de salinité ont été observés durant l'hiver et au printemps dans certains cours d'eau urbains, ces taux se situant dans l'intervalle des valeurs de toxicité aiguë mesurées en laboratoire. Les relevés faisant état de niveaux d'exposition plus faibles, variant d'un taux se rapprochant des niveaux de toxicité chronique calculés en laboratoire à des taux légèrement supérieurs aux taux de salinité de fond, sont plus fréquents et plus répandus. Certains changements mesurables dans le biote ou les communautés aquatiques, ou les deux, ont été observés en laboratoire et sur le terrain à ces concentrations plus faibles, y compris des effets possibles sur la stratification des lacs.
L'augmentation des charges de sels dans les sols peut modifier les propriétés essentielles au maintien d'un sol en santé. Un certain nombre d'études sur le terrain font état de dommages à la végétation et de modifications dans la structure de la phytocénose, dans les régions perturbées par les sels de voirie sous l'effet du ruissellement ou de la dispersion atmosphérique. En outre, des taux élevés de sodium et de chlorure dans le sol, ou l'exposition atmosphérique au sodium et au chlorure, ont souvent été rapportés, à des niveaux ayant un impact sur la croissance, la reproduction et la survie d'espèces végétales sensibles qui poussent le long des routes et des cours d'eau qui reçoivent les eaux de ruissellement des routes et des lieux d'entreposage des sels de voirie.
Des effets comportementaux et toxicologiques ont aussi été observés chez des mammifères et des oiseaux exposés aux sels de voirie, effets qui peuvent aussi se répercuter sur l'habitat de la faune en réduisant le couvert végétal ou en modifiant les communautés dont la faune dépend pour se nourrir ou s'abriter.
Comme les ferrocyanures peuvent se dissocier dans l'environnement pour former du cyanure, certains organismes aquatiques pourraient subir les effets nocifs du cyanure dans les régions où l'on fait un grand usage des sels de voirie.
Même s'il est impossible de quantifier l'importance écologique de bon nombre des effets potentiels décrits précédemment, il ne fait aucun doute, à la lumière des données disponibles, qu'il existe une probabilité raisonnable que les sels de voirie qui contiennent des sels inorganiques de chlorure avec ou sans sels de ferrocyanure aient, immédiatement ou à long terme, un effet nocif sur certains organismes des eaux de surface, certains végétaux terrestres et certaines espèces fauniques du Canada et qu'ils pourraient également mettre en danger l'environnement essentiel pour la vie à cause de leurs effets sur les systèmes aquatiques, les sols et les habitats terrestres. Par conséquent, les sels de voirie qui contiennent des sels inorganiques de chlorure avec ou sans sels de ferrocyanure devraient être considérés « toxiques » en vertu de la LCPE de 1999, en raison des menaces tangibles de dommages environnementaux graves ou irréversibles qui y sont associées.
LCPE 1999 64a) : À la lumière des données disponibles, on considère que les sels de voirie qui contiennent des sels inorganiques de chlorure avec ou sans sels de ferrocyanure pénètrent dans l'environnement en une quantité ou concentration ou dans des conditions de nature à avoir, immédiatement ou à long terme, un effet nocif sur l'environnement ou la diversité biologique. Par conséquent, on conclut que les sels de voirie qui contiennent des sels inorganiques de chlorure avec ou sans sels de ferrocyanure sont « toxiques » au sens de l'alinéa 64a) de la LCPE 1999.
LCPE 1999 64b) : À la lumière des données disponibles, on considère que les sels de voirie qui contiennent des sels inorganiques de chlorure avec ou sans sels de ferrocyanure pénètrent dans l'environnement en une quantité ou concentration ou dans des conditions de nature à mettre en danger l'environnement essentiel pour la vie. Par conséquent, on conclut que les sels de voirie qui contiennent des sels inorganiques de chlorure avec ou sans sels de ferrocyanure sont « toxiques » au sens de l'alinéa 64b) de la LCPE 1999.
Conclusion globale : Sur la base de l'évaluation critique des données pertinentes, les sels de voirie qui contiennent des sels inorganiques de chlorure avec ou sans sels de ferrocyanure sont considérés « toxiques » au sens de l'article 64 de la LCPE 1999.
3.9 Considérations pour le suivi (mesures à prendre)
Le recours aux fondants est une composante importante des stratégies visant à maintenir les routes ouvertes et sûres durant l'hiver et à réduire les accidents routiers, les blessures et la mortalité associés aux périodes de neige et de verglas. La Commission consultative d'experts auprès des ministres sur la deuxième liste de substances d'intérêt prioritaire (LSIP) reconnut ces avantages dans sa recommandation d'évaluer leurs effets potentiels sur l'environnement. Toute mesure élaborée à la suite de la présente évaluation ne devra pas compromettre la sécurité routière; le choix d'options devra être fondé sur l'optimisation des pratiques d'entretien des routes en hiver afin de ne pas compromettre la sécurité routière tout en minimisant les effets nocifs possibles sur l'environnement. Toute mesure prise pour diminuer les effets sur l'environnement réduira probablement aussi la contamination des sources souterraines d'eau potable, ce qui est assurément désirable.
Les activités futures de gestion devraient se concentrer sur les principales préoccupations que l'évaluation a mises en lumière, c'est-à-dire les entrepôts de sels, l'épandage sur les routes, les lieux d'entreposage de la neige et les ferrocyanures.
- Entrepôts de sels : Les principales préoccupations touchent à la contamination des eaux souterraines dans les entrepôts de sels et aux rejets dans les eaux de surface. En outre, le ruissellement des eaux salées de la fonte des neiges peut avoir des effets directs sur les eaux
de surface et sur la végétation adjacente aux entrepôts. À la lumière des sondages et des recensions, les pertes de sels des entrepôts de sels se produisent à partir des amas (ce qui inclut les amas de sels ainsi que les amas de sable et de gravier auxquels on a ajouté des sels) et pendant la manutention du sel, tant lors de son entreposage que pour le chargement et le déchargement des camions. Le rejet des eaux de lavage des véhicules constitue lui aussi une source potentielle de pertes de sels. On devrait donc considérer prendre des mesures et des pratiques pour s'assurer que les sels et les abrasifs sont entreposés de manière à réduire les pertes en les protégeant des intempéries, pour réduire les pertes pendant les déplacements et pour améliorer la gestion des eaux de ruissellement et de lavage afin de réduire les rejets. - Épandage sur les routes : Les principales préoccupations écologiques sont liées aux régions à forte densité routière où le recours aux sels de voirie est élevé. Les régions du sud de l'Ontario et du Québec et les provinces de l'Atlantique ont les plus hauts taux d'épandage par superficie et ont donc le plus fort potentiel de contamination des sols et des eaux de surface et souterraines par les sels de voirie due à l'épandage sur les routes. En outre, des régions urbaines d'autres parties du Canada où de grandes quantités de sels sont épandues peuvent causer des problèmes, en particulier pour les ruisseaux et les aquifères complètement entourés par la région urbaine. Dans les régions rurales, les eaux de surface réceptrices du ruissellement des routes sont aussi susceptibles de contamination. Les zones où des éclaboussures ou des gouttelettes d'eau salées provenant des routes peuvent être transportées dans l'atmosphère vers la végétation sensible doit retenir l'attention. Les terres humides directement adjacentes aux fossés des routes et qui reçoivent le ruissellement sous forme d'eaux salées de la fonte des neiges doivent aussi retenir l'attention pour la gestion. En conséquence, on devrait considérer prendre des mesures en vue de réduire l'utilisation globale des sels de voirie dans ces régions. On devrait penser à choisir des produits de remplacement ou des techniques appropriées permettant de réduire l'utilisation des sels tout en assurant le maintien de la sécurité des routes.
- Lieux d'entreposage de la neige : Les principales préoccupations écologiques touchent l'écoulement des eaux de la fonte des neiges dans les eaux de surface, dans le sol et les eaux souterraines dans les lieux d'entreposage de la neige. Des mesures devraient être considérées pour minimiser la percolation dans le sol et les eaux souterraines, et pourraient diriger les rejets des eaux salées de la fonte des neiges vers des eaux de surface dont la sensibilité environnementale est faible ou vers les systèmes d'évacuation des eaux pluviales. Des mesures devraient aussi être considérées pour que les eaux soient suffisamment diluées avant d'être rejetées.
- Ferrocyanures : La présente évaluation indique que l'exposition aux ferrocyanures peut avoir des effets nocifs sur les vertébrés aquatiques les plus sensibles dans les régions à forte utilisation de sels de voirie. On pourrait diminuer les risques en réduisant la quantité de sels utilisée ou en réduisant la teneur en ferrocyanures des formules de sels de voirie. Les fabricants de sels de voirie devraient songer à réduire la teneur en ferrocyanures des sels de voirie afin de minimiser les possibilités d'exposition. Toute réduction de l'utilisation globale des sels de voirie entraînerait une réduction équivalente des rejets de ferrocyanures.
4.0 Références
Acton, D.F. et L.J. Gregorich (éd.). 1995. La santé de nos sols : vers une agriculture durable au Canada, Centre de recherches sur les terres et les ressources biologiques, Direction générale de la recherche, Agriculture et Agroalimentaire Canada, publication no 1906/F.
Adams, L.W. et A.D. Geiss. 1983. Effects of roads on small mammals, J. Appl. Ecol., 20: 403-415.
Adelman, I.R., L.L.J. Smith et G.D. Siesennop. 1976. Acute toxicity of sodium chloride, pentachlorophenol, guthion and hexavalent chromium to fathead minnows (Pimephales promelas) and goldfish (Carassius auratus), J. Fish. Res. Board Can., 33: 203-208 [cité dans U.S. EPA, 1988].
AGRA. 1995. Phase 1 of groundwater flow and contaminant assessment, Heffley Creek, British Columbia. Rapport préparé par AGRA Earth and Environmental pour le ministère des Transports et de la Voirie de la Colombie-Britannique, Kamloops (Colombie-Britannique) (projet no KX11322).
AGRA. 1999. Chloride plume monitoring -October 1998 and February 1999, Heffley Creek, British Columbia. Rapport préparé par AGRA Earth and Environmental, pour le ministère des Transports et de la Voirie de la Colombie-Britannique, Kamloops (Colombie-Britannique) (projet no KX11538).
Alberta Infrastructure. 2000. Draft Phase 3 environmental site assessments for the Worsley Satellite Yard, Obed Satellite Yard, and 25th Baseline Satellite Yard. Rapport préparé par Green Plan Limited pour Alberta Infrastructure, Civil Projects Branch, Edmonton (Alberta).
Ali, O.M., M. Yousaf et J.D. Rhoades. 1987. Effect of exchangeable cation and electrolyte concentration on mineralogy of clay dispersed from aggregates, Soil Sci. Soc. Am. J., 51: 896-900.
Allen, J. et G.A. Strobel. 1966. The assimilation of H14CN by a variety of fungi, Can J. Microbiol., 12: 414-416 [cité dans Towill et al., 1978].
American Cyanamid Company. 1953. The chemistry of the ferrocyanides, The Beacon Press, Inc., New York (N.Y.).
Anderson, B.G. 1948. The apparent thresholds of toxicity to Daphnia magna for chlorides of various metals when added to Lake Erie water, Am. Fish. Soc., 78: 96-113.
Andreassen, H.P., R.A. Ims et O.K. Steinset. 1996. Discontinuous habitat corridors: effects on male root vole movements, J. Appl. Ecol., 33: 555-560.
Anon. 1992. Dryland salinity investigations procedures manual, Conservation and Development Branch, ministère de l'Agriculture de l'Alberta et Administration du rétablissement agricole des Prairies, Agriculture et Agroalimentaire Canada, 110 p.
Arambasic, M.B., S. Bjelic et G. Subakov. 1995.
Acute toxicity of heavy metals (copper, lead, zinc), phenol and sodium on Allium cepa L., Lepidium sativum L. and Daphnia magna St.: comparative investigations and the practical applications, Water Res., 29: 497-503.
Argus, G.W., K.M. Pryer, D.J. White et C.J. Keddy (éd.). 1987. Atlas des plantes vasculaires rares de l'Ontario, 1982-1987, Musée canadien de la nature, Ottawa (Ontario).
Arp, P.A. 2001. Electrical conductivity and chloride contents of stream, pond and ditchwater locations near a salt depot: a case study, Faculté de foresterie et de gestion environnementale, Université du Nouveau-Brunswick, Fredericton (Nouveau-Brunswick), 14 p.
Arsenault, R.A., T.L. Pollock, S. Ratnam et D. Hansen. 1985. Surface water quality study in the Waterford River Basin, Urban Hydrology Study of the Waterford River Basin, 91 p. (rapport technique no UHS-WRB1.4).
ATC (Association des transports du Canada). 1999. Salt management guide, Ottawa (Ontario).
Auestad, I., A. Norderhaug et I. Auestad. 1999. Road verges - Species rich habitats, Aspects Appl. Biol., 54: 269-275.
August, L.L. et T.A. Graupensperger. 1989. « Impacts of highway deicing programs on groundwater and surface water in Maryland », dans Groundwater issues and solutions in the Potomac River Basin, Chesapeake Bay Region, National Water Well Association Conference, du 14 au 16 mai 1989, Washington (D.C.), p. 37-394.
Baeten, L.A. et F.J. Dein. 1996. Salt toxicosis in wild birds, Am. Assoc. Zoo Vet. Annu. Proc., 1996: 296-297.
Baker, K.D. 1965. An observation of bird mortality on highways, Blue Jay, 23(2): 79-80.
Bakowsky, W. et J.L. Riley. 1994. « A survey of the prairies and savannas of southern Ontario », dans R.G. Wickett, P.D. Lewis, A. Woodliffe et P. Pratt (éd.), Proceedings of the 13th North American Prairie Conference, 1992, Department of Parks and Recreation, Windsor (Ontario).
Ballantyne, B. 1987. « Clinical and experimental toxicology of cyanides », dans B. Ballantyne et T.C. Marrs (éd.), Clinical and experimental toxicology of cyanides, John Wright, Bristol (R.-U.), p. 41-126.
Barica, J. 1978. Variability in ionic composition and phytoplankton biomass of saline eutrophic lakes within a small geographic area, Arch. Hydrobiol., 81(3): 304-326.
Barker, A.V. 2000. Search of literature and planning of research on salt damage along highways in Massachusetts, Massachusetts Highway Department and University of Massachusetts Cooperative Transportation Research Program, 44 p. (rapport trimestriel de recherche).
Barrick, W.E. et H. Davidson. 1980. Deicing salt spray injury in Norway maple as influenced by temperature and humidity treatments, HortScience, 15(2): 203-205.
BC-MoTH (ministère des Transports et de la Voirie de la Colombie-Britannique). 1993. Groundwater contamination study: Heffley Creek Pit, Thompson-Okanagan Region. Rapport préparé par R. Buchanan, Geotechnical and Materials Engineering, Victoria (Colombie-Britannique).
Beak. 1999. Ecotoxicity test results. Données inédites présentées à M.S. Evans, Beak International Inc., Brampton (Ontario).
Beck, P., S. Kok et W.J. Snodgrass. 1994. Technology assessment - removal of total dissolved solids from salty washwaters generated from vehicle washing operations. Rapport préparé pour le ministère des Transports de l'Ontario, Toronto (Ontario).
Beckerson, D.W., N.P. Cain, G. Hofstra, D.P. Ormrod et P.A. Campbell. 1980. A guide to: plant sensitivity to environmental stress, Landscape Archit., mai: 299-303.
Bedunah, D. et M.J. Trlica. 1979. Sodium chloride effects on carbon dioxide exchange rates and other plant and soil variables of ponderosa pine, Can. J. For. Res., 9(3): 349-353.
Beeton, A.M. 1965. Eutrophication of the St. Lawrence Great Lakes, Limnol. Oceanogr., 10: 240-254.
Beeton, A.M. 1969. « Changes in the environment and the biota of the Great Lakes ». In : Eutrophication: Causes, consequences, correctives, Printing and Publishing Office, National Academy of Sciences, Washington (D.C.), p. 150-187.
Bélanger, L. 2000. Communication personnelle, Section Faune et Habitats, Environnement Canada, Sainte-Foy (Québec).
Bellamy, P.E., R.F. Shore, D. Ardeshir, J.R. Treweek et T.H. Sparks. 2000. Road verges as habitat for small mammals in Britain, Mammal Rev., 30(2): 131-139.
Belluck, D.A. 2000. Communication personnelle, Minnesota Department of Transport, St. Paul (Minnesota).
Benkman, C.W. 1998. [Crossbills hit by vehicles while eating salts]. Communication personnelle de C.W. Benkman, Dept. of Biology, New Mexico State University, Las Cruces (Nouveau-Mexique) à Lorna Brownlee, Service canadien de la faune, Centre national de la recherche faunique, Ottawa, courriel en date du 18 février 1998.
Benkman, C.W. 1998. [The scavenging of finches killed at roadside in Algonquin Park]. Communication personnelle de Craig W. Benkman, Dept. of Biology, New Mexico State University, Las Cruces (Nouveau-Mexique) à P. Mineau, Service canadien de la faune, Centre national de la recherche faunique, Ottawa, courriel en date du 11 mai 2000.
Bennett, A.F. 1990. Habitat corridors and the conservation of small mammals in a fragmented forest environment, Landscape Ecol., 4: 109-122.
Bennett, A.F. 1991. « Roads, roadsides and wildlife conservation: a review », dans D.A. Saunders et R.J. Hobbs (éd.), Nature conservation 2: The role of corridors, Surrey Beatty and Sons, Victoria (Australie), p. 99-118.
Bennetts, R.E. et R.L. Hutto. 1985. Attraction of social fringillids to mineral salts: An experimental study, J. Field Ornithol., 56(2): 187-189.
Bertram, B.M. 1997. « Sodium chloride », dans J. I. Kroschwitz (éd. exéc.), M. Howe-Grant (éd.), Kirk-Othmer encyclopedia of chemical technology, 4e éd., vol. 22, John Wiley & Sons, New York (N.Y.), p. 371.
Bilodeau, S. 1999. La fondeuse à neige de Cap-Rouge, un an après son démarrage, Vecteur Environnement, 32(2): 70-73.
Birge, W. J., J.A. Black, A.G. Westerman, T.M. Short, S.B. Taylor, D.M. Bruser et E.D. Wallingford. 1985. Recommendations on numerical values for regulating iron and chloride concentrations for the purpose of protecting warmwater species of aquatic life in the Commonwealth of Kentucky, Kentucky Natural Resources and Environmental Protection Cabinet, Lexington (Kentucky) (protocole d'entente no 5429).
Bishop, C.A., J. Struger, L.J. Shirose, L. Dunn et G.D. Campbell. 2000. Contamination and wildlife communities in stormwater detention ponds in Guelph and the Greater Toronto Area, Ontario, 1997 and 1998. Part 2 -Contamination and biological effects of contamination, Water Qual. Res. J. Can., 35(3): 437-474.
Blinn, D.W., M. Hurley et L. Brokaw. 1981. The effects of saline seeps and restricted light upon the seasonal dynamics of phytoplankton communities within a southwestern (USA) desert canyon stream, Archiv. Hydrobiol., 92: 287-305.
Boucher, R.J. 1982. Penjajawoc Stream Salt Study, Materials and Research Division, Maine Department of Transportation, 15 p. (rapport technique no 82-85).
Bourbonnière, R.A. 1985. Données inédites, Institut national de recherche sur les eaux, Burlington (Ontario).
Bourbonnière, R.A. 1998. Données inédites, Institut national de recherche sur les eaux, Burlington (Ontario).
Bowen, G.S. et M.J. Hinton. 1998. « The temporal and spatial impacts of road salt on streams draining the Greater Toronto Area », dans Groundwater in a watershed context: proceedings, ministère de l'Environnement de l'Ontario et Commission géologique du Canada, Burlington (Ontario), p. 303-309.
Bowser, C.J. 1992. « Groundwater pathways for chloride pollution of lakes », dans F.M. D'Itri (éd.), Chemical deicers and the environment, Lewis Publishers, Boca Raton (Floride), p. 283-301.
Bradford, W. 1988. A plan to reduce wildlife mortality on transportation corridors in Jasper National Park. Plan de gestion inédit, Natural Resources Conservation, Parc national Jasper, Jasper (Alberta).
Bresler, E., B.L. McNeil et D.L. Carter. 1982. Saline and sodic soils, Advanced Series in Agriculture Sciences 10, Springer-Verlag, Berlin, 236 p.
Briggins, D., J. Walsh, C.L. Lin, K.A. Macdermid et R.H. Johnson (éd.). 1989. The environmental implications of road salting in Nova Scotia. Publication conjointe du ministère de l'Environnement et du ministère des Transports et des Communications de la Nouvelle-Écosse, 40 p.
Broderius, S.J. 1973. Determination of molecular hydrocyanic acid in water and studies of the chemistry and toxicity to fish of metal cyanide complexes. Thèse de doctorat, Oregon State University, Corvallis (Oregon) [cité dans Doudoroff, 1976; U.S. EPA, 1985].
Broderius, S.J. et L.L. Smith, Jr. 1980. Direct photolysis of hexacyanoferrate complexes: proposed applications to the aquatic environment, Environmental Research Laboratory, U.S. Environmental Protection Agency, Duluth (Minnesota) (rapport technique EPA-600/3-80-003).
Brownlee, L., P. Mineau et A. Baril. 2000. Risk characterization for wildlife. Rapport présenté au Groupe-ressource environnemental d'Environnement Canada chargé d'évaluer les sels de voirie inscrits sur la Liste des substances d'intérêt prioritaire de la LCPE, mai 2000, Direction de l'évaluation des produits chimiques commerciaux, Environnement Canada, Hull (Québec).
Bubeck, R.C., W.H. Diment, B.L. Deck, A.L. Baldwin et S.D. Lipton. 1971. Runoff of deicing salt: Effect on Irodequoit Bay, Rochester, New York, Science, 172: 1128-1132.
Bubeck, R.C., W.W. Staubitz, A.D. Weidemann et L.P. Spittal. 1995. Physical and chemical limnology of Ides Cove near Rochester, New York, 1970-1982, U.S. Geological Survey, Ithaca (N.Y.), 44 p. (Water-Resources Investigations Report 92-4052).
Butler, B.J. et J. Addison. 2000. Biological effects of road salts on soils. Rapport présenté au Groupe-ressource environnemental d'Environnement Canada chargé d'évaluer les sels de voirie inscrits sur la Liste des substances d'intérêt prioritaire de la LCPE, mars 2000, Direction de l'évaluation des produits chimiques commerciaux, Environnement Canada, Hull (Québec).
Button, E. F. et D. E. Peaslee. 1966. The effect of rock salt upon roadside sugar maples in Connecticut, Highw. Res. Rec., 161: 121-131. Cain, N.P., B. Hale, E. Berkelaar et D. Morin. 2001. Critical review of effects of NaCl and other road salts on terrestrial vegetation in Canada. Rapport présenté au Groupe-ressource environnemental d'Environnement Canada chargé d'évaluer les sels de voirie inscrits sur la Liste des substances d'intérêt prioritaire de la LCPE, juillet 2001, Direction des substances existantes, Environnement Canada, Hull (Québec).
Camp, M. et L.B. Best. 1993a. Nest density and nesting success of birds in roadsides adjacent to rowcrop fields, Am. Midl. Nat., 131: 347-358.
Camp, M. et L.B. Best. 1993b. Bird abundance and species richness in roadsides adjacent to Iowa rowcrop fields, Wildl. Soc. Bull., 21: 315-325.
Catling, P.M. et S.M. McKay. 1980. Halophytic plants in southern Ontario, Can. Field-Nat ., 94(3): 248-258.
CCME (Conseil canadien des ministres de l'Environnement). 1991. Recommandations pour la qualité des eaux au Canada, Environnement Canada, Ottawa (Ontario).
CCME (Conseil canadien des ministres de l'Environnement). 1998. Recommandations pour la qualité de l'eau potable au Canada, Environnement Canada, Ottawa (Ontario).
Chang, N.-Y., W. Pearson, J.I.J. Chang, A. Gross, M. Meyer, M. Jolly, B. Vang et H. Samour. 1994. Environmentally sensitive sanding and deicing practices, Colorado Transportation Institute et Colorado Department of Transportation, Denver (Colorado), 116 p.
Chatwin, T.D. 1989. Cyanide attenuation/ degradation in soil (final report), Resource Recovery and Conservation Company (R2C2), Salt Lake City (Utah).
Chatwin, T.D. 1990. Cyanide attenuation/ degradation in soil (Appendix), Resource Recovery and Conservation Company (R2C2), Salt Lake City (Utah).
Cheminfo. 1999. Socio-economic background and options study on the Canadian salt industry. Rapport préparé par Cheminfo, Toronto (Ontario) pour la Direction de la réglementation et de l'évaluation, Environnement Canada, Hull (Québec).
Chenevier, C. (1997). Synthèse des données physico-chimiques sur les neiges usées au Québec et leurs impacts environnementaux. M.Sc.A., Département des génies civil, géologique et des mines, École polytechnique de Montréal, Montréal (Québec).
Cherkauer, D.S. et N.A. Ostenso. 1976. The effect of salt on small artificial lakes, Water Res. Bull., 12(6): 1259-1266.
Chetelat, J., F.R. Pick, A. Morin et P.B. Hamilton. 1999. Periphyton biomass and community composition in rivers of different nutrient status, Can. J. Fish. Aquat. Sci., 56: 560-569.
Chong, C. et G.P. Lumis. 1990. Reduction of salt build-up and twig injury in roadside peach trees with film-forming sprays, Transp. Res. Rec., 1279: 45-53.
CIS (Camford Information Services). 1994. Sodium chloride, CPI Product Profiles, Don Mills (Ontario), 3 p.
CIS (Camford Information Services). 1996.
Calcium chloride, CPI Product Profiles, Don Mills (Ontario), 3 p.
Clark, M.J.R., H. Hanssen, G. Van Aggelen et S. Horvath. 1984. « Acute toxicity of iron cyanide species to rainbow trout and to Daphnia magna under exposure to different light intensities », dans Proceedings of the 11th Annual Aquatic Toxicity Workshop, ministère de l'Environnement de la Colombie-Britannique, Vancouver (Colombie-Britannique) [cité dans Higgs, 1992].
Collins, B. 2000. Comparison of salt use among years. Note de service en date du 3 novembre 2000, Division des populations d'oiseaux migrateurs, Centre national de la recherche faunique, Environnement Canada.
Commission consultative auprès des ministres. 1995. Rapport de la Commission consultative sur la deuxième liste de substances d'intérêt prioritaire dans le cadre de la Loi canadienne sur la protection de l'environnement (LCPE), Gouvernement du Canada, Ottawa (Ontario), 26 p.
Conn, E.E. 1980. Cyanogenic compounds, Annu. Rev. Plant Physiol., 31: 433 [cité dans Knowles et Bunch, 1986].
Cordukes, A.J. et W.E. Maclean. 1973. Tolerance of some turfgrass species to different concentrations of salt in soils, Can. J. Plant Sci., 53: 69-73.
Cornell Laboratory of Ornithology. 2000a. Biennial irruptions of pine siskins across North America, http://birdsource.cornell.edu/results/irruptions.htm
Cornell Laboratory of Ornithology. 2000b. Population trends in evening grosbeak, http://birdsource.cornell.edu/features/evegro
Couture, P. 1997. La gestion des neiges usées : Dilemmes et contradictions, Vecteur Environnement, 30(6): 18-20.
Cowgill, U. M. et D. P. Milazzo. 1990. The sensitivity of two cladocerans to water quality variables: Salinity and hardness, Arch. Hydrobiol., 120(2): 185-196.
Crowther, R.A. et H.B.N. Hynes. 1977. The effect of road deicing salt on the drift of stream benthos, Environ Pollut., 14: 113-126.
Cushman, J.R., V.A. Duff, G.H. Buteau, L.B. Aust, N. Caldwell et W. Lazer. 1991. Evaluation of calcium magnesium acetate and road salt for contact hypersensitivity potential and dermal irritancy in humans, Contact Dermatitis, 24: 289-292.
Davis, G., S. Krannitz et M. Goldstein. 1992. Phase II: A reconnaissance study of roadside tree injury and decline at 17 sites in interior British Columbia for the Roadside Tree Injury Committee, ministère de l'Environnement, des Terres et des Parcs de la Colombie-Britannique, Victoria (Colombie-Britannique), 98 p. et annexes.
Dawson, W.R., V.H. Shoemaker, H.B. Tordoff et A. Borut. 1965. Observations on metabolism of sodium chloride in the red crossbill, Auk, 82: 606-623.
Delisle, C.E. 1994. La gestion des neiges usées, Routes et transports, 24(4): 20-27.
Delisle, C.E. et L. Dériger. 2000. Caractérisation et élimination des neiges usées : impacts sur l'environnement. Rapport présenté au Groupe-ressource environnemental d'Environnement Canada chargé d'évaluer les sels de voirie inscrits sur la Liste des substances d'intérêt prioritaire de la LCPE, Direction de l'évaluation des produits chimiques commerciaux, Environnement Canada, Hull (Québec).
Delisle, C.E. et A. Leduc. 1987. Évolution dans le temps et dans l'espace de la qualité de la neige usée et de l'eau de ruissellement de pluie du territoire de la Ville de Montréal, Centre de développement technologique de l'École polytechnique de Montréal, rapport final, 155 p. et annexes.
Delisle, C.E., J.-F. Paradis et P. André. 1995. « The Montréal, Quebec experience in used snow disposal and treatment », dans Ecological reclamation in Canada at century's turn, Proceedings of the 35th Annual Meeting of the Canadian Society of Environmental Biologists, Canadian Plains Research Center, Regina (Saskatchewan), p. 10-18.
Delisle, C.E., C. Chenevier et P. André. 1997. Synthèse des données physico-chimiques sur les neiges usées au Québec et leurs répercussions environnementales, Vecteur Environnement, 30(6): 33-44.
Delisle, R. 1999. Autoroute 40 - Cap-de-la-Madeleine : Étude de la contamination de la nappe aquifère par les sels déglaçants, ministère des Transports du Québec (projet no 20-6373-9501).
Demers, C. L. 1992. « Effects of road deicing salt on aquatic invertebrates in four Adirondack streams », dans F.M. D'Itri (éd.), Chemical deicers and the environment, Lewis Publishers, Boca Raton (Floride), p. 245-252.
Demers, C.L. et R.W. Sage, Jr. 1990. Effects of road deicing salt on chloride levels in four Adirondack streams, Water Air Soil Pollut., 49: 369-373.
Dickman, M.D. et M.B. Gochnauer. 1978. Impact of sodium chloride on the microbiota of a small stream, Environ. Pollut., 17: 109-126.
Dirr, M.A. 1975. Effets of salts and application methods on English ivy, HortScience, 10(2): 182-184.
Dirr, M.A. 1976. Selection of trees for tolerance to salt injury, J. Arboric., 2(11): 209-216.
Dirr, M.A. 1978. Tolerance of seven woody ornamentals to soil-applied sodium chloride, J. Arboric., 4(7): 162-165.
Dixit, S. S., J.P. Smol, D.F. Charles, R.M. Hughes, S.G. Paulsen et G.B. Collins. 1999. Assessing water quality changes in the lakes of the northeastern United States using sediment diatoms, Can. J. Fish. Aquat. Sci., 56: 131-152.
Dkhili, M. et B. Anderson. 1992. « Salt effects on seedling growth of switchgrass and big bluestem », dans D. Smith et C.C. Jacobs (éd.), Proceedings of the 12th North American Prairie Conference 1990, University of Northern Iowa, Cedar Falls (Iowa), p. 13-16.
Dobson, H.H. 1967. « Principal ions and dissolved oxygen in Lake Ontario », dans Proceedings of the 10th Conference on Great Lakes Research , Association internationale de recherche sur les Grands Lacs, Ann Arbor (Michigan), Braun-Brumfield, Inc., Ann Arbor (Michigan), p. 337-356.
Dobson, M.C. 1991. De-icing salt damage to trees and shrubs, Forestry Commission, Surrey (Colombie-Britannique), 64 p. (bulletin no 101).
Doudoroff, P. 1966. Some experiments on the toxicity of complex cyanides to fish, Sewage Ind. Wastes, 28(8): 1020.
Doudoroff, P. 1976. Toxicity to fish of cyanides and related compounds. A Review, Environmental Research Laboratory, Office of Research and Development, U.S. Environmental Protection Agency, Duluth (Minnesota) (EPA-600/3-76-038).
Doudoroff, P. 1980. A critical review of recent literature on the toxicity of cyanides to fish, American Petroleum Institute, Washington (D.C.).
Doudoroff, P. et M. Katz. 1953. Critical review of literature on the toxicity of industrial wastes and their components to fish, Sewage Ind. Wastes , 25: 802-839 [cité dans Evans et Frick, 2001].
Dowden, B.F. et H.J. Bennett. 1965. Toxicity of selected chemicals to certain animals, J. Water Pollut. Control Fed., 37: 1308-1316 [cité dans Evans et Frick, 2001].
Drake, L. et B. Kirchner, 1987. Protecting remnant natural communities along rural roadsides, Nat. Areas J., 7(2): 79-80.
Dubey, S.K. et D.S. Holmes. 1995. Biological cyanide destruction mediated by microorganisms, World J. Microbiol. Biotechnol. 11: 257. Dvorak, P., M. Gunther, U. Zorn et A. Catsch. 1971. Metabolisches verhalten von kolloidalem ferrihexacyanoferrat(II), Naunyn-Schmiedebergs Arch. Pharmakol., 269: 48-56 [cité dans Shifrin et al., 1996].
Eaton, L.J., J. Hoyle et A. King. Sans date. The impact of road salt on lowbush blueberries, Nova Scotia Agricultural College et ministère de l'Agriculture et de la Commercialisation de la Nouvelle-Écosse, Truro (Nouvelle-Écosse).
Effenberger, E. 1964. Verunreinigunen eiyes grund-wasser durch cyanide, Arch. Hyg. Bakteriol., 148(4-5): 271-278 [cité dans Chatwin, 1990].
Eilers, J.M. et A.R. Selle. 1991. Changes in the conductivity, alkalinity, calcium, and pH during a 50-year period in selected Wisconsin lakes, Can. J. Fish. Aquat. Sci., 46: 1929-1944.
Eilers, R.G., W.D. Eilers, W.W. Pettapiece et G. Lelyk. 1995. « Salinisation du sol », dans D.F. Acton et L.J. Gregorich (éd.), La santé de nos sols, Agriculture et Agroalimentaire Canada, p. 77-86 (publication 1906/F).
Eisler, R. 1991. Cyanide hazards to fish, wildlife, and invertebrates: A synoptic review, U.S. Fish and Wildlife Service (FWS Biol. Rep., 85(1.23); NTIS no PB94-120144).
Environnement Canada. 1995. Toxicity testing of National Contaminated Sites Remediation Program priority substances for the development of soil quality criteria for contaminated sites, Retesting Volatile Substances Guidelines Division, Direction de l'évaluation et de l'interprétation, Service de conservation des écosystèmes.
Environnement Canada. 1997a. Évaluation environnementale des substances d'intérêt prioritaire conformément à la Loi canadienne sur la protection de l'environnement. Guide, version 1.0 - mars 1997, Série de la protection de l'environnement, Direction de l'évaluation des produits chimiques commerciaux, Environnement Canada (EPS/2/CC/3F).
Environnement Canada. 1997b. Canadian Environmental Protection Act - Problem formulation for the environmental assessment of the priority substance road salts, Gouvernement du Canada.
Evans, M. et C. Frick. 2001. The effects of road salts in stream, lake and wetland ecosystems. Institut national de recherche sur les eaux, Saskatoon (Saskatchewan).
Eyles, N, et K.W.F. Howard 1988. Urban landsliding caused by heavy rains: Geochemical identification of recharge waters along the Scarborough Bluffs, Toronto, Ontario, Can. Geotech. J., 25: 455-466.
Faber, J.H. et H.A. Verhoef. 1991. Functional differences between closely-related soil arthropods with respect to decomposition processes in the presence or absence of pine roots, Soil Biol. Biochem. 23(1): 15-23.
Fallon, R.D., D.A. Cooper, R. Speece et M. Henson. 1991. Anaerobic biodegradation of cyanide under methanogenic conditions, Appl. Environ. Microbiol., 57(6): 1656-1662.
Ferguson, K.D. 1985. The photolysis of iron-cyanide in a stream receiving effluent from a gold cyanidation mill, Service de la protection de l'environnement, région du Pacifique, Environnement Canada.
Feth, J.H., C.E. Robertson, et W.L. Polzer. 1964. Sources of mineral constituents in water from granitic rocks, Sierra Nevada, California and Nevada, U.S. Geological Survey, Washington (D.C.) (Water Supply Papers no 1535-I).
Foster, H.D. 1993. Road de-icing salt and cancer: the need for further study, J. Natl. Cancer Inst., 85(19): 1603-1605.
Franson, J.C., L. Sileo et W.J. Flemming. 1981. Iatrogenic salt poisoning in captive sandhill cranes, J. Am. Vet. Med. Assoc., 179(11): 1211-1213.
Fraser, D. et E.R. Thomas. 1982. Moose-vehicle accidents in Ontario: Relation to highway salt, Wildl. Soc. Bull., 10(3): 261-265.
Free, B.M. et G.G. Mulamoottil. 1983. The limnology of Lake Wabukayne, a storm-water impoundment, Water Res. Bull.,19(5): 821-827.
Freedman, B., J. Kerekes et G. Howell. 1989. Patterns of water chemistry among twenty-seven oligotrophic lakes in Kejimkujik National Park, Nova Scotia, Water Air Soil Pollut., 46: 119-130.
Fuller, W.H. 1984. « Cyanides in the environment with particular attention to soil », dans D. Van Zyl (éd.), Cyanide and the environment, vol. 1, Geochemical Engineering Program, Colorado State University, Fort Collins (Colorado), p. 19-46.
Garrels, R.M. et F.T. Mackenzie. 1967. « Origin of the chemical compositions of some springs and lakes », dans Equilibrium concepts in natural water systems, American Chemical Society, Washington (D.C.), p. 222-242 (Advances in Chemistry Series no 67).
Gélinas, P. et J. Locat. 1988. Effets des sels déglaçants sur la qualité de l'eau de l'aquifère de Trois-Rivières Ouest, ministère des Transports du Québec (rapport no RTQ-87-05).
Gerber, R.E. et K.W.F. Howard.1997. « Ground-water to the Oak Ridges Moraine », dans N. Eyles (éd.), Environmental geology of urban areas, Association géologique du Canada, St. John's (Terre-Neuve), p. 173-192.
Getz, L.L., F.R. Cole et D.L. Gates. 1978. Interstate roadsides as dispersal routes for Microtus pennsylvannicus, J. Mammal., 59: 208-212.
Gionfriddo, J.P. et L.B. Best. 1995. Grit use by house sparrows: Effects of diet and grit size, The Condor, 97: 57-67.
Godbout, P. 1996. Chute à neige à l'égout motorisée et asservie - Une innovation québécoise unique en Amérique du Nord, Les consultants BGH-Planning Inc, symposium tenu à l'hôtel Le Méridien, du 19 au 21 novembre 1996, Montréal (Québec), 27 p.
Gonzalez-Moreno, S., J. Gomez-Barrera, H. Perales et R. Moreno-Sanchez. 1997. Multiple effects of salinity on photosynthesis of the protist Euglena gracilis, Physiol. Plant., 101: 777-786.
Gooding, D. et A.J. Bodnarchuck. 1994. Field trials of prewetting salt and sand with MgCl2 and CaCl2 brines: Efficiency and effects, Highway Environmental Branch, ministère des Transports et de la Voirie de la Colombie-Britannique, 7 p. (MoTH-ENV-94-01).
Gosh, A.K. et R.N. Pal. 1969. Toxicity of four therapeutic compounds to fry of Indian major carps, Fish. Technol., 6: 120-123 [cité dans Hammer, 1977].
Gosz, J.R. 1977. Effects of ski area development and use in stream water quality on the Santa Fe Basin, New Mexico, For. Sci., 23(2): 167-179.
Gouvernement du Québec. 1991. Guide pour l'aménagement des lieux d'élimination des neiges usées, ministère de l'Environnement du Québec, 95 p.
Gouvernement du Québec. 1997. Gestion des neiges usées, Guide pour l'aménagement des lieux d'élimination de neige et mise en oeuvre du Règlement sur les lieux d'élimination de neige, ministère de l'Environnement du Québec, 56 p.
Gouvernement du Québec. 2001. Guide d'aménagement des lieux d'élimination de neige et mise en oeuvre du Règlement sur les lieux d'élimination de neige, ministère de l'Environnement du Québec, document téléchargé le 13 juin 2001, à partir du site www.menv.gouv.qc.ca/matieres/neiges_usees/index.htm
Grenier, P. 1973. Moose killed on the highway in the Laurentides Park, Quebec, 1962 to 1972, Proc. N. Am. Moose Conf. Workshop, 9: 155-193.
Hall, R., G. Hofstra et G.P. Lumis. 1972. Effects of deicing salt on eastern white pine: foliar injury, growth suppression, and seasonal changes in foliar concentrations of sodium and chloride, Can. J. For. Res., 2: 224-249.
Hamilton, R.W., J.K. Buttner et R.G. Brunetti. 1975. Lethal levels of sodium chloride and potassium chloride for an oligochaete, a chironomid midge, and a caddisfly of Lake Michigan, Environ. Entomol., 4: 1003-1006.
Hammer, U.T. 1977. « The effects of alkali halides on fish and other aquatic fauna », dans The effects of alkali halides in the Canadian environment, Comité associé des critères scientifiques concernant l'état de l'environnement, Conseil national de recherches du Canada, Ottawa (Ontario), p. 99-115 (publication no 15019 du CNRC).
Hammer, U.T. 1984. « The saline lakes of Canada », dans F.B. Taub (éd.), Lakes and reservoirs, Elsevier Scientific Publishing Company, Amsterdam, p. 521-540.
Hammer, U.T. 1986. Saline lake resources of the Canadian Prairies, Revue canadienne des ressources en eau, 11(1): 43-57.
Hanes, R.E., L.W. Zelazny et R.E. Blaser. 1970. Effects of deicing salts on water quality and biota: Literature review and recommended research, Highway Research Board, National Academy of Sciences/National Academy of Engineering, Washington (D.C.), 70 p.
Harrington, J.A. et T. Meikle. 1994. « Road salt effects on the germination of eight select prairie species », dans R.G. Wickett, P.D. Lewis, A. Woodliffe et P. Pratt (éd.), Proceedings of the 13th North American Prairie Conference, 1992, Department of Parks and Recreation, Windsor (Ontario), p. 183-192.
Hart, W.C. 1985. Effects on the chemistry of water supply lakes due to chloride inputs, Centre for Water Resources Research, Technical University of Nova Scotia, Halifax (Nouvelle-Écosse), 16 p. [cité dans Briggins et al., 1989].
Hart, W.C.. 1988. Chloride measured in the vicinity of Second Chain Lake, 1987-1988, Centre for Water Resources Research, Technical University of Nova Scotia, Halifax (Nouvelle-Écosse) [cité dans Briggins et al., 1989].
Hart, B.T., P. Bailey, R. Edwards, K. Hortle, K. James, A. McMahon, C. Meredith et K. Swadling. 1990. Effects of salinity on river, stream, and wetland ecosystems in Victoria, Australia, Water Res., 24: 1103-1107.
Hattori, R. et T. Hattori. 1980. Sensitivity to salts and organic compounds of soil bacteria isolated on diluted media, J. Gen. Microbiol., 26: 1-14.
Hawkins, R.H. et J.H. Judd. 1972. Water pollution as affected by street salting, Water Resour. Bull ., 8: 1246-1252.
Headley, D.B. et N. Bassuk. 1991. Effect of time and application of sodium chloride in the dormant season on selected tree seedlings, J. Environ. Hortic., 9(3): 130-136.
Henny, C.J., R.J. Hallock et E.F. Hill. 1994. Cyanide and migratory birds at gold mines in Nevada, USA, Ecotoxicology, 3: 45-58.
Herlihy, A.T., J.L. Stoddard et C.B. Johnson. 1998. The relationship between stream chemistry and watershed cover data in the mid-Atlantic region, U.S. Water Air Soil Pollut., 105: 377-386.
Higgs, T.W. 1992. Technical guide for the environmental management of cyanide in mining. Préparé pour le Cyanide Subcommittee, British Columbia Technical and Research Committee on Reclamation, par T.W. Higgs Associates Ltd., Vancouver (Colombie-Britannique).
Hinton, M.J. et A.G. Eversole. 1978. Toxicity of ten commonly used chemicals to American eels, Agricultural Experiment Station, U.S. Department of Agriculture (Technical Contribution 1595).
Hoffman, R.W., C.R. Goldman, S. Paulson et G.R. Winters. 1981. Aquatic impacts of deicing salts in the central Sierra Nevada Mountains, California, Water Res. Bull., 17: 280-285.
Hofstra, G. et G.P. Lumis. 1975. Levels of deicing salt producing injury on apple trees, Can. J. Plant Sci., 55(1): 113-115.
Hofstra, G. et D.W. Smith. 1984. The effects of road deicing salt on the levels of ions in roadside soils in southern Ontario, J. Environ. Manage., 19: 261-271.
Hofstra, G., R. Hall et G.P. Lumis. 1979. Studies of salt-induced damage to roadside plants in Ontario, J. Arboric., 5: 25-31.
Holms, H.M. et J.L. Henry. 1982. Understanding salt-affected soils, Plant Industry Branch, ministère de l'Agriculture de la Saskatchewan, 14 p. Howard, K.W.F. et P.J. Beck. 1993.
Hydrogeochemical implications of groundwater contamination by road de-icing chemicals, J. Contam. Hydrol., 12: 245-268.
Howard, K.W.F. et J. Haynes. 1993. Groundwater contamination due to road de-icing chemicals - salt balance implications, Geosci. Can., 20(1): 1-8.
Howard, K.W.F. et J. Haynes. 1997. « Contamination of urban groundwater by road de-icing chemicals », dans N. Eyles (éd.), Environmental geology of urban areas, Association géologique du Canada, St. John's (Terre-Neuve). Howard, K.W.F. et L.C. Taylor. 1998.
« Hydrogeochemistry of springs in urban Toronto, Canada », dans J. Van Brahana, Y. Eckstein, L.K. Ongley, R. Scheinder et J.E. Moore (éd.), Gambling with groundwater - physical, chemical, and biological aspects of aquifer-stream relations, American Institute of Hydrology, St. Paul (Minnesota), p. 639-644.
Howard, K.W.F., J.I. Boyce, S.J. Livingstone et S.L. Salvatori. 1993. Road salt impacts on ground-water quality - the worst is still to come, GSA Today, 3(12): 301-321.
Howard, P.H., R.S. Boethling, W.F. Jarvis, W.M. Meylan, et E.M. Michalenko. 1991.
Handbook of environmental degradation rates, Lewis Publishers, New York (N.Y.), p. 132-133.
Howell, J. et R.C. Gumbrell. 1992. Salt poisoning in broiler chickens, N. Z. Vet. J., 40: 85.
Hsu, M. 1984. Anticaking agents in deicing salt, Materials and Research Division, Maine Department of Transportation, 18 p. (rapport technique no 84-4).
Hubbs, A.H. et R. Boonstra. 1995. Study design to assess the effects of highway median barriers on wildlife, Direction de la recherche et du développement, ministère des Transports de l'Ontario (MAT-94-03).
Huey, L.M. 1941. Mammalian invasion via the highway, J. Mammal., 22: 383-385.
Humphreys, D.J. 1978. A review of recent trends in animal poisoning, Br. Vet. J., 134: 128-141.
ICE (Institut canadien des engrais). 1997. [Concernant la présence de chlorure de potassium dans les résidus des mines de potasse utilisés pour le salage des routes]. Communication personnelle de J. Farrell, directeur des affaires techniques, ICE à R. Chénier, Division de l'évaluation des produits chimiques, Environnement Canada, Hull, lettre datée du 18 avril 1997.
INTERA Consultants. 1996. Application guidelines for installation of oil/water separators at existing MTO patrol yards. Rapport soumis au Bureau de l'environnement, ministère des Transports de l'Ontario, Toronto (Ontario).
Jeffries, D.S. 1997. 1997 Canadian acid rain assessment: The effects on Canada's lakes, rivers and wetlands, vol. 3, Aquatic effects, Environnement Canada, Ottawa (Ontario).
Johnson, G.D. et P.B. Krauss. 1991. Tributary contaminant inputs on the St. Clair and Detroit rivers and Lake St. Clair 1984-1985, Direction des ressources en eau, ministère de l'Environnement de l'Ontario, Toronto (Ontario).
Johnston, C.T., R.C. Sydor et C.L.S. Bourne. 2000. Impact of winter road salting on the hydrogeologic environment - an overview. Projet de rapport, Stantec Consulting Ltd., Kitchener (Ontario).
Jones, P.H., B.A. Jeffrey, P.K. Watler et H. Hutchon. 1986. Environmental impact of road salting - State of the art, ministère des Transports et des Communications de l'Ontario (MTC no RR237).
Jones, P.H., B.A. Jeffery, P.M. Watler et H. Hutchon. 1992. « Environmental impact of road salting », dans F.M. D'Itri (éd.), Chemical deicers and the environment, Lewis Publishers, Chelsea (Michigan).
Judd, J.H. 1969. Lake stratification caused by runoff from street deicing, Milwaukee (Wisconsin), Center for Great Lakes Studies, 25 p.
Judd, J.H. et J.W. Stegall. 1982. Reevaluation of the effects of deicing salt runoff on a small lake, National Technical Information Service, Springfield (Virginie), 28 p. (A-114-MICH).
Kaplan, D.L., R. Hartenstein, E.F. Heuhauser et M.R. Malecki. 1980. Physicochemical requirements in the environment of the earthworm (Eisenia Foetida), Soil Biol. Biochem., 12: 347-352.
Keizer, P.D., D.C. Gordon, J.W. Rowell, R. McCurdy, D. Borgal, T.A. Clair, D. Taylor, J.D. Ogden et G.E.M. Hall. 1993. Synoptic water quality survey of Halifax/Dartmouth Metro Area lakes on April 16, 1991, Direction des services biologiques, région Scotia -Fundy, ministère des Pêches et des Océans.
Kelly, D., J. Underwood et J. Hansen. 1976. Influence of highway deicing salts upon water quality in Chocolate Lake, Halifax, Nova Scotia, ministère de l'Environnement de la Nouvelle-Écosse, Halifax (Nouvelle-Écosse), 118 p.
Kerekes, J.J. 1974. Limnological conditions in five small oligotrophic lakes in Terra Nova National Park, Newfoundland, J. Fish. Res. Board Can., 31: 555-583.
Kerekes, J. et B. Freedman 1989. Seasonal variation of water chemistry in oligotrophic streams and rivers in Kejimkujik National Park, NS, Water Air Soil Pollut., 46(1-4): 131-144.
Kerekes, J., B. Freedman, S. Beauchamp et R. Tordon. 1989. Physical and chemical characteristics of three acidic oligotrophic lakes and their watersheds in Kejimkujik Park, Nova Scotia, Water Air Soil Pollut., 46: 99-117.
Kersey, K. et R.J. Mackay. 1981. Laboratory and field studies on the effects of road de-icing salt on stream invertebrates SIC-9, Snow and Ice Control Working Group, Institute for Environmental Studies, Université de Toronto, Toronto (Ontario).
Khanna, C., H.J. Boermans et B. Wilcock. 1997. Fatal hypernatremia in a dog from salt ingestion, J. Am. Anim. Hosp. Assoc., 33: 113-117.
Klaassen, C.D. (éd.). 1996. Casarett and Doull's toxicology, The basic science of poisons, 5e édition, McGraw-Hill, New York (N.Y.).
Kliejunas, J., M. Marosy et J. Pronos. 1989. Conifer damage and mortality associated with highway de-icing and snow removal in the Lake Tahoe area, Forest Pest Management, U.S. Department of Agriculture Forest Service, 18 p. (rapport no 89-11).
Knowles, C.J. 1976. Microorganisms and cyanide, Bacteriol. Rev., 40: 652-680.
Knowles, C.J. et A.W. Bunch. 1986. Microbial cyanide metabolism, Adv. Microbial Physiol., 27: 73-111.
Kovacs, T.G. 1979. The effect of temperature on the cyanide toxicity to rainbow trout: I, Acute effects. II, Chronic effects. Thèse de maîtrise, Université Concordia, Montréal (Québec), 69 p. [cité dans Leduc et al., 1982].
Kovacs, T.G. et G. Leduc. 1982. Sublethal toxicity of cyanide to rainbow trout (Salmo gairdneri) at different temperatures, Can. J. Fish. Aquat. Sci., 39: 1389-1395.
Kramer, J.R. 1964. « Theoretical model for the chemical composition of fresh water with application to the Great Lakes », dans Proceedings of the 7th Conference on Great Lakes Research, Great Lakes Research Division, Institute of Science and Technology, University of Michigan, Ann Arbor (Michigan), p. 147-160 (publication no 11).
Kszos, L. A., J. D. Winter et T. A. Storch. 1990. Toxicity of Chautauqua Lake bridge runoff to young-of-the-year sunfish (Lepomis macrochirus), Bull. Environ. Contam. Toxicol., 45: 923-930.
Labadia, C.F. et J.M. Buttle. 1996. Road salt accumulation in highway snow banks and transport though the unsaturated zone of the Oak Ridges Moraine, southern Ontario, Hydrol. Processes, 10: 1575-1589.
Lacroix, G. et L. Bélanger. 2000. Suivi écologique du projet-pilote de gestion différenciée des emprises autoroutières : volet avifaune et mortalité par collision. Préparé pour le Département de chimie biologique de l'Université du Québec à Trois-Rivières et le ministère des Transports du Québec par le Service canadien de la faune, Environnement Canada, Sainte-Foy (Québec).
Laursen, K. 1981. Birds on roadside verges and the effect of mowing on frequency and distribution, Biol. Conserv., 20: 59-68.
Leduc, G., R.C. Pierce et I.R. McCracken. 1982. The effects of cyanides on aquatic organisms with emphasis on freshwater fishes, Comité associé des critères scientifiques concernant l'état de l'environnement, Conseil national de recherches du Canada, Ottawa (Ontario) (CNRC no 19246).
Lee, K. 1985. Earthworms: Their ecology and relationships with soils and land use, Academic Press, New York (N.Y.).
Lefkovitch, L.P. et I. Fahrig. 1985. Spatial characteristics of habitat patches and population survival, Ecol. Model., 30: 297-308.
Leland, H.V. et S.V. Fend. 1998. Benthic invertebrate distributions in the San Joaquin River, California, in relation to physical and chemical factors, Can. J. Fish. Aquat. Sci., 55: 1051-1067.
Letts, A. 1999. [The melting of salt applied to roads]. Communication personnelle de A. Letts, directeur technique, Morton International Inc., Chicago (Illinois) durant un entretien avec L. Brownlee, Service canadien de la faune, Centre national de la recherche faunique, Ottawa.
Letts, A.D. 2000a. Effects of sodium ferrocyanide derived from road salting on the ecosystem, Morton Salt, Morton International Inc., Chicago (Illinois).
Letts, A.D. 2000b. A model to predict chloride concentrations in meltwater runoff from road salt, Morton Salt, Morton International Inc., Chicago (Illinois).
Lewis, S.A. 1991. « The conservation and management of roadside vegetation in South Australia », dans D.A. Saunders et R.J. Hobbs (éd.), Nature conservation 2: The role of corridors, Beatty & Sons, Surrey, p. 314-318.
Liang, W. 1998. Performance monitoring of the Rouge River stormwater management facility. Projet de rapport, Stormwater Assessment Monitoring and Performance Program, ministère de l'Environnement de l'Ontario, Etobicoke (Ontario).
Lumis, G.P., G. Hofstra et R. Hall. 1973. Sensitivity of roadside trees and shrubs to aerial drift of deicing salt, Can. J. Plant Sci., 8(6): 475-477.
Lumis, G.P., G. Hofstra et R. Hall. 1976. Roadside woody plant susceptibility to sodium and chloride accumulation during winter and spring, Can. J. Plant Sci., 56: 853-859.
Lumis, G.P., G. Hofstra et R. Hall. 1977. Salt damage to roadside plants, fiche technique du ministère de l'Agriculture et de l'Alimentation de l'Ontario, 3 p. (no 77-063, déc. 1977).
Lumis, G.P., G. Hofstra et R. Hall. 1983. Salt damage to roadside plants, fiche technique du ministère de l'Agriculture et de l'Alimentation de l'Ontario, 3 p. MacLeod, C.L., M.P. Borcsik et P.R. Jaffe. 1996. Effect of infiltrating solutions on the desorption of mercury from aquifer sediments, Environ. Technol., 17: 465-475.
Malmqvist, P.-A. (1985). Environmental effects of snow disposal in Sweden, Molndalsvagen, Göteborg (Suède), 10 p.
Maltby, L., D.M. Farrow, A.B.A. Boxall, P. Calow et C.I. Betton. 1995. The effects of motorway runoff on freshwater ecosystems: 1.Field study, Environ. Toxicol. Chem., 14:1079-1092.
Martineau, D. et S. Lair. 1995. Nécropsie, Centre canadien coopératif de la santé de la faune, Saint-Hyacinthe (Québec) (rapport de pathologie inédit no 95-1893).
Mattson, M.D. et P.J. Godfrey. 1994. Identification of road salts contamination using multiple regression and GIS, J. Environ. Manage., 18: 767-773.
Mayer, T. 2000. Données inédites, Institut national de recherche sur les eaux, Burlington (Ontario).
Mayer, T., J. Marsalek et E. Delos Reyes. 1996. Nutrients and metal contaminants status of urban stormwater detention ponds, Lake Reserv. Manage., 12 (3): 348-368.
Mayer, T., Q. Rochfort, J. Marsalek, M. Servos, A. Jurkovic et R. McKinnis. 1998. Effects of de-icing salts on the chemistry and toxicology of highway runoff, Institut national de recherche sur les eaux, Burlington (Ontario).
Mayer, T., W.J. Snodgrass et D. Morin. 1999. Spatial characterization of the occurrence of road salts and their environmental concentrations as chlorides in Canadian surface waters and benthic sediments, Water Qual. Res. J. Can., 34(4): 545-574. Voir aussi Mayer, T., W.J. Snodgrass et D. Morin. 1999. Spatial characterization of the occurrence of road salts and their environmental concentrations as chlorides in Canadian surface waters and benthic sediments, Environnement Canada, collection de l'INRE no 99-097 (révisée en 2001), 44 p.
McBean, E. et S. Al-Nassri. 1987. Migration pattern of de-icing salts from roads, J. Environ. Manage., 25: 231-238.
McCormick, R.W. et D.C. Wolf. 1980. Effects of sodium chloride on CO2 evolution, ammonification and nitrification in a sassafras sandy loam, Soil Biol. Biochem., 12: 153-157.
McDonald, M.G. et A.W. Harbaugh. 1988. A modular three-dimensional finite-difference ground-water flow model, U.S. Geological Survey, Washington (D.C.), 586 p. (Techniques of Water Resources Investigations, Book 6).
McKee, J.E. et H.W. Wolf. 1963. Water quality criteria , 2e éd., California State Water Resources Control Board, 542 p.
McKillop, W.B., R.T. Patterson, L.D. Delorme et T. Nogrady. 1992. The origin, physico-chemistry and biotics of sodium chloride dominated saline waters on the western shore of Lake Winnipegosis, Man., Can. Field-Nat., 106(4): 454-473.
McLaughlin, D.L. et R.G. Pearson. 1981. Effectiveness of snow fence barriers in reducing salt spray injury to fruit orchards adjacent to the Queen Elizabeth Highway: 1978-1981, Section de phytotoxicologie, Direction des ressources atmosphériques, ministère de l'Environnement de l'Ontario, Brampton (Ontario).
McNeely Engineering. 1990. Snow disposal study for the designated growth centres. Rapport présenté au Service des transports de la Municipalité régionale d'Ottawa-Carleton, Ottawa (Ontario).
McNeely-Tunnock Ltd. 1995. Strategic plan for snow disposal inside the Greenbelt. Rapport final présenté à la Municipalité régionale d'Ottawa-Carleton, Ottawa (Ontario).
MDOT (Michigan Department of Transportation). 1993. The use of selected de-icing materials on Michigan roads: Environmental and economic impacts, 105 p.
ME et MT du N.-B. (ministère de l'Environnement et ministère des Transports du Nouveau-Brunsiwck). 1978. An investigation of the quantity and quality of leachate from a highway salt treated sand pile under normal operating conditions. Préparé conjointement par le ministère de l'Environnement (Direction des ressources en eau) et le ministère des Transports du Nouveau-Brunswick, pour le ministère des Transports.
Meade, G.M. 1942. Calcium chloride - a death lure for crossbills, Auk, 59: 439-440.
Meeussen, J.C.L., M.G. Keizer et F.A.M. DeHaan. 1992a. Chemical stability and decomposition rate of iron cyanide complexes in soil solutions, Environ. Sci. Technol., 26(3): 511-516.
Meeussen, J.C.L., M.G. Keizer, W.H. van Riemsdijk et F.A.M. de Haan. 1992b. Dissolution behavior of iron cyanide (prussian blue) in contaminated soils, Environ. Sci. Technol., 26(9): 1832-1838.
MEO (Ministère de l'Environnement de l'Ontario). 1991. Stormwater Quality Best Management Practices, Division des normes et des sciences de l'environnement, Direction des ressources en eau, ministère de l'Environnement de l'Ontario, juin (ISBN 0-7729-8478-6).
MEEO (Ministère de l'Environnement et de l'Énergie de l'Ontario). 1993. A study of dust suppressants in Ontario. Final Report. Préparé par CH2M Hill Engineering Ltd. pour la Direction de la gestion des déchets, ministère de l'Environnement et de l'Énergie de l'Ontario, Toronto (Ontario).
Melis. L.A., P.I. Tones et S.M. Swanson. 1987. Identification and evaluation of impacts resulting from the discharge of gold mill effluents. Rapport préparé pour Environnement Canada, 121 p. (projet no 52SS.KE145-6-095) [cité dans Higgs, 1992].
Meteyer, C.U., R.R. Dubielzig, F.J. Dein, L.A. Baeten, M.K. Moore, J.R. Jehl, Jr. et K. Wesenberg. 1997. Sodium toxicity and pathology associated with exposure of waterfowl to hypersaline playa lakes of southeast New Mexico, J. Vet. Diagn. Invest., 9: 269-280.
Miller, B.K. et J.A. Litvaitis. 1992. Use of roadside salt licks by moose, Alces alces, in northern New Hampshire, Can. Field-Nat., 106: 112-117.
Miller, G.C., V.R. Hebert et W.W. Miller. 1989. Effect of sunlight on organic contaminants at the atmosphere-soil interface, Soil Science Society of America, Madison (Wisconsin) p. 99-110 (SSSA Special Publication no 22).
Mills, G.E. et A.V. Barker. 2001. « Sodium accumulation in soils and plants along Massachusetts roadsides », dans Proceedings of the Annual Meeting of Northeast Region American Society for Horticultural Science (Abstract).
Mineau, P. et B.T. Collins. 1988. « Avian mortality in agro-ecosystems 2. Methods of detection », dans M.P. Greaves, B.D. Smith et P.W. Greig-Smith (éd.), Field methods for the study of environmental effects of pesticides, British Crop Protection Council, Croydon (R.-U.), p. 13-27.
Ministère des Transports du Québec. 1980. Prévention contre la pollution du lac à la Truite en hiver. Document préparé par François Berard, Office des autoroutes du Québec. Document obtenue du Centre de documentation du Ministère des Transports du Québec.
Ministère des Transports du Québec. 1999. Communication personnelle de G. D'Astous (Direction des Laurentides-Lanaudière), et A. Décréon (Service de l'aménagement des infrastructures et de l'environnement) à D. Morin (Environment Canada) à-propos du lac à la Truite.
Mitsch, W.J. et J.G. Gosselink. 1986. Wetlands, Van Nostrand Reinhold Company, New York (N.Y.), 539 p.
Molles, M.C. et J.R. Gosz. 1980. Effects of ski area on the water quality and invertebrates of a mountain stream, Water Air Soil Pollut., 14: 187-205.
Morin, D. 2000. Environmental impacts from the spreading and storage of road salts: Case Studies. Documentation complémentaire pour l'évaluation des sels de voirie inscrits sur la LSIP. Rapport présenté au Groupe-ressource environnemental sur les sels de voirie, Direction de l'évaluation des produits chimiques commerciaux, Environnement Canada, mai 2000, 84 p.
Morin, D. et M. Perchanok. 2000. Road salt loadings in Canada. Documentation complémentaire pour l'évaluation des sels de voirie inscrits sur la LSIP. Rapport présenté au Groupe-ressource environnemental d'Environnement Canada chargé d'évaluer les sels de voirie inscrits sur la Liste des substances d'intérêt prioritaire de la LCPE, Direction de l'évaluation des produits chimiques commerciaux, Environnement Canada, Hull (Québec), 85 p.
Morin, D., W. Snodgrass, J. Brown et P.A. Arp. 2000. Impacts evaluation of road salt loadings on soils and surface waters. Documentation complémentaire pour l'évaluation des sels de voirie inscrits sur la LSIP. Rapport présenté au Groupe-ressource environnemental d'Environnement Canada chargé d'évaluer les sels de voirie inscrits sur la Liste des substances d'intérêt prioritaire de la LCPE, juin 2000, Direction de l'évaluation des produits chimiques commerciaux, Environnement Canada, Hull (Québec), 76 p.
Mortsch, L.D. et F.H. Quinn. 1996. Climate change scenarios for Great Lakes Basin ecosystem studies, Limnol. Oceanogr., 41: 903-911.
MTO (Ministère des Transports de l'Ontario). 1993-1999. Phase 1 et/ou phase 2 des évaluations environnementales des sites effectuées par DST Consulting Engineers, Oliver Mangione McCalla & Associates, NAR Environmental Consultants, Conestoga-Rovers & Associates ou Ecoplans, pour les entrepôts de sel suivants appartenant au ministère des Transports de l'Ontario et exploités par ce Ministère : Alexandria, Almonte, Apsley, Barriefield, Belleville Sub PY, Bloomfield, Bobcaygeon, Brighton, Calabogie, Camden East, Carlsbad Springs, Cloyne, Coboconk, Crystal Beach, Denbigh, Eganville, Erinsville, Grafton, Greely, Hawkesbury, Johnstown, Kemptville, Lansdowne, Lorneville, Madawaska, Madoc, Marysville, Morrisburg, Navan, Norwood, Pembroke, Roseneath, Sharbot Lake, Summerstown, Toledo, Tory Hill, Trenton Sub PY, Vankleek Hill, Verona, Winchester, Wolf Island, Youngs Point.
MTO (Ministère des Transports de l'Ontario). 1997. Graphical compilation of chloride concentrations in patrol yards managed by the Ontario Ministry of Transportation, Toronto (Ontario).
Mudder, T. 1991. Communication personnelle, Steffen Robertson and Kristen, Seattle (Washington) [cité dans Higgs, 1992].
Nadec (Nadec Experts & Consultants Inc.). 2001. The ecological significance of roadside habitat - Revised final draft. Rapport présenté à la Direction de l'évaluation des produits chimiques commerciaux, Environnement Canada, Hull (Québec), mars.
Neehall, R. 2000. Comments on the draft assessment report on salts, Ville d'Edmonton, Office of the Environment, en date du 11 octobre 2000.
Northcote, T.G. et T.G. Halsey. 1969. Seasonal changes in the limnology of some meromictic lakes in southern British Columbia, J. Fish. Res. Board Can., 26: 1763-1787.
Northover, J. 1987. NaCl injury to dormant roadside peach trees and its effect on the incidence of infections by Leucostoma spp., Phytopathology, 77(6): 835-840.
Noss, R.F. 1983. A regional landscape approach to maintain diversity, Bioscience, 33: 700-706.
Novotny, V., D. Muehring, D.W. Smith, D.H. Zitomer et R. Facey. 1997. « Impact of nonpoint source snowmelt on receiving waters », dans Proceedings of the Water Environmental Federation 70th Annual Conference, 19 octobre, Chicago (Illinois) (atelier no 118). OCDE. Groupe d'experts scientifiques. 1989. Réduction de l'utilisation des fondants dans l'entretien hivernal, Organisation de coopération et de développement économiques, Paris (France).
Oeser, R. Jr. 1977. The crossbill (Loxia curvirostra) - Highway mortalities in the Fichtelbers area, Beitr. Vogelkd., 23(5): 278-280.
Oetting, R.B. et J.F. Cassell, 1971. Waterfowl nesting on interstate highway right-of-way in North Dakota, J. Wildl. Manage., 35(4): 774-781.
Ohno, T. 1989. Determination of levels of free cyanide in surface and in ground waters affected by MDOT salt storage facilities, Technical Services Division, Maine Department of Transportation, Orono (Maine) (rapport technique 86C: 16-17).
Ohno, T. 1990. Levels of total cyanide and NaCl in surface waters adjacent to road salt storage facilities, Environ. Pollut., 67: 123-132.
Otake, T., S. Tone, I. Komasawa, et M. Kawashima. 1982. Mécanisme et cinétique de la décomposition des cyanoferrates hydrosolubles par les rayonnements ultraviolets, Université d'Osaka, Osaka (Japon) [traduction].
Parker, A. et J.D. Mather. 1979. An investigation into pollution from a disused gasworks site near Ladybank, Fife, Atomic Energy Research Establishment, Harwell, Berkshire, 19 p. (AERE-R 9213) [cité dans Chatwin, 1990].
Patrick, R., J.J. Cairns et A. Scheier. 1968. The relative sensitivity of diatoms, snails and fish to twenty common constituents of industrial wastes, Prog. Fish-Cult., 30: 137-140.
Paul, E.A. et F.E. Clark. 1996. Soil microbiology and biochemistry, 2e éd., Academic Press, San Diego (Californie).
Paul, R., M. Rocher et R. Impens. 1984. [Influence of winter deicing with CaCl2 on mountain ash, maple, lime and plane], Bull. Soc. R. Bot. Belg., 117: 277-284 (en français).
Péloquin, Y. 1993. Qualité des eaux de fonte provenant d'un site de surface pour l'élimination des neiges usées à la Ville de Laval, Université du Québec à Montréal, Montréal (Québec), 91 p.
Perchanok, M.S., D.G. Manning et J.J. Armstrong. 1991. Highway deicers: Standards, practice and research in the Province of Ontario, Direction de la recherche et du développement, ministère des Transports de l'Ontario, Downsview (Ontario), 53 p. (MAT-91-13).
Perring, F.H., P.D. Sell, S.M. Walters et H.L.K. Whitehouse. 1964. A flora of Cambridgeshire, Cambridge University Press, Cambridge (R.-U.).
Phillips, A.M.J. 1944. The physiological effect of sodium chloride upon brook trout, Trans. Am. Fish. Soc., 74: 297-309.
Phippen, B.W., D.C. Parks, L.G. Swain, R. Nordin, C.J.P. McKean, J.B. Holms, P.D. Warrington, R. Nijman, J. Deniseger et L. Erickson. 1996. A ten year assessment of water quality in six acid-rain sensitive British Columbia lakes (1984-1994), ministère de l'Environnement, des Terres et des Parcs de la Colombie-Britannique, 250 p.
Pilon, P. et K.W.F. Howard. 1987. Origins of elevated chloride concentrations in groundwater systems, ministère de l'Environnement de l'Ontario, Congrès sur le transfert des techniques no 7, Toronto, décembre, Part C - Liquid and Solid Waste Research, p. 376-398 (ISSN 0-825-4591).
Pinard, D., J.B. Sérodes et P.A. Côté. 1989. Caractérisation des eaux de fonte d'un dépôt à neiges usées, Sci. Tech. Eau, 22(3): 211-215.
Pringle, C.M., D.S. White, C.P. Rice et M.L. Tuchman. 1981. The biological effects of chloride and sulfate with the special emphasis on the Laurentian Great Lakes, University of Michigan, Ann Arbor (Michigan), p. 1-51.
Prowse, C.W. 1987. The impact of urbanization on major ion flux through catchments: a case study in southern England, Water Air Soil Pollut., 32: 277-292.
Prud'homme, M. 2000. « Potasse », dans Annuaire des minéraux du Canada, 1999, Secteur des minéraux et des métaux, Ressources naturelles Canada, téléchargé le 10 novembre 2000 du site www.nrcan.gc.ca/mms/cmy/1999CMY_F2.html
Racette, D.J. et H.D. Griffin. 1989. Vegetation assessment surveys near the Ministry of Transportation's Longbow Lake Patrol Yard 1988-1989, ministère de l'Environnement de l'Ontario, Section du soutien technique, région du Nord-Ouest, 9 p.
Rader, W.S., L. Solujic, E.B. Milosavljevic et J.L. Hendrix. 1993. Sunlight-induced photochemistry of aqueous solutions of hexaferrocyanate (II) and (III) ions, Environ. Sci. Technol., 27(9): 1875-1879.
Rantamaki, J., L. Cerenius et K. Soderhall. 1992. Prevention of transmission of the crayfish plague fungus (Aphanomyces astaci) to the freshwater crayfish (Astacus astacus) by treatment with MgCl2, Aquaculture, 104: 11-18.
Ressources naturelles Canada. 1998. « Articles sur divers produits minéraux et métalliques -sel », dans Annuaire des minéraux du Canada, 1998, Secteur des minéraux et des métaux, Ressources naturelles Canada.
Reznicek, A.A. 1980. Halophytes along a Michigan roadside with comments on the occurrence of halophytes in Michigan, Mich. Bot., 19: 23-30.
Reznicek, A.A., P.M. Catling et S.M. McKay. 1976. Carex praegracilis W. Boott, recently adventive in southern Ontario, Can. Field-Nat., 90: 180-183.
Rodgers, G.K. 1998. Winter stratification in Hamilton Harbour, Institut national de recherche sur les eaux, Burlington (Ontario) (collection de l'INRE no 98-231).
Rodgers, G.K. 1999. Communication personnelle au sujet des données publiées dans la collection de l'INRE no 98-231 [voir Rodgers, 1998], Institut national de recherche sur les eaux, Burlington (Ontario).
Rott, E., H.C. Duthie et E. Pipp. 1998. Monitoring organic pollution and eutrophication in the Grand River, Ontario, by means of diatoms, Can. J. Fish. Aquat. Sci., 55: 1443-1453.
Rowe, J.S. 1972. Les régions forestières du Canada, Service canadien des forêts, ministère de l'Environnement, Ottawa (Ontario), 172 p.
Rushton D. 1999. [Données au sujet des entrepôts de sel de Bible Hill, Saulnierville et Oxford]. Communication personnelle de D. Rushton, Services environnementaux, ministère des Transports et des Travaux publics de la Nouvelle-Écosse à D. Morin, Division de l'évaluation des produits chimiques, Environnement Canada, octobre et novembre 1999.
Rushton D. 2000. [Données au sujet des entrepôts de sel de Bible Hill, Saulnierville et Oxford]. Communication personnelle de D. Rushton, Services environnementaux, ministère des Transports et des Travaux publics de la Nouvelle-Écosse à D. Morin, Division de l'évaluation des produits chimiques, Environnement Canada, hiver 2000.
Ruttner, F. 1963. Fundamentals of Limnology, traduit par D.G. Frey et F.E.J. Fry, University of Toronto Press, Toronto (Ontario), 295 p.
Salt Institute. 1964-1983. Survey of salt, calcium chloride, and abrasives use in the United States and Canada for 1964-65, 1966-67, 1969-70, 1973-74, 1978-79, 1982-83, Alexandria (Virginie).
Sandals, W.C.D. 1978. Acute salt poisoning in cattle, Can. Vet. J., 19: 136-137.
Santé Canada. 1996. Recommandations pour la qualité de l'eau potable au Canada, 6e éd., Ottawa (Ontario).
Saumure, R.A. 2001. Communication personnelle, Shark Reef at Mandalay Bay, Las Vegas (Nevada).
Scanton, D. 1999. Communication personnelle (lettre datée du 19 mai 1999), ministère des Transports de l'Ontario, Toronto (Ontario).
Scarratt, W.K., T.J. Collins et D.P. Sponenberg. 1985. Water deprivation-sodium chloride intoxication in a group of feeder lambs, J. Am. Vet. Med. Assoc., 186(9): 977-978.
Schauffler, M. 1993. Capture of road-salt aerosols in an acidic peatland in central Maine. Thèse de maîtrise, University of Maine, 41 p.
Schelske, C.L., E.F. Stoermer, D.J. Conley, J.A. Robbins et R.M. Glover. 1983. Early eutrophication in the lower Great Lakes: new evidence from biogenic silica in sediments, Science, Washington (D.C.), 222: 320-322.
Schelske, C.L., D.J. Conley et W.F. Warwick. 1985. Historical relationships between phosphorous loading and biogenic silica accumulation in Bay of Quinte sediments, Can. J. Fish. Aquat. Sci., 42: 1401-1409.
Schindler, D.W., S.E. Bayley, B.R. Parker, K.G. Beaty, D.R. Cruikshank, E.J. Fee, E.U. Schindler et M.P. Stainton. 1996. The effects of climatic warming on the properties of boreal lakes and streams at the Experimental Lakes Area, northwestern Ontario, Limnol. Oceanogr., 41: 1004-1017.
Schmidt, J.W., L. Simovic et E. Shannon. 1981. Natural degradation of cyanide in gold mill effluents. Présenté au séminaire sur le cyanure dans les mines d'or, janvier 1981, Ottawa (Ontario) [cité dans Higgs, 1992].
Schraufnagel, F.H., 1965. Chlorides. Committee on Water Pollution, Wisconsin Public Health Service, Madison (Wisconsin), p. 1-13 et annexe.
Schroeder, J.E. et K.R. Solomon. 1998. Impact of road salts on an urban watershed. Affiche présentée dans le cadre de la 19e assemblée annuelle de la Society of Environmental Toxicology and Chemistry (SETAC), Charlotte (Caroline du Nord).
Schulkin, J. 1991. Sodium hunger: The search for a salty taste, Cambridge University Press, Cambridge (R.-U.), p. 458-499.
Scott, W. S. 1980. Road salt movement into two Toronto streams, J. Environ. Eng. Div., EE3: 547-560.
Scott, W. S. 1981. An analysis of factors influencing de-icing salt levels in streams, J. Environ. Manage., 13: 269-287.
Setälä, H. et V. Huhta. 1991. Soil fauna increase Betula pendula growth - Laboratory experiments with coniferous forest floor, Ecology, 72(2): 665-671.
Setälä, H., J. Laakso, J. Mikola et V. Huhta. 1998. Functional diversity of decomposer organisms in relation to primary production, Appl. Soil Ecol., 9: 25-31.
Shifrin, N.S., B.D. Beck, T.D. Gauthier, S.D. Chapnick et G. Goodman. 1996. Chemistry, toxicology, and human health risk of cyanide compounds in soil at former manufactured gas plant sites, Regul. Toxicol. Pharmacol., 23: 106-116.
Short, T.M., J.A. Black et W.J. Birge. 1991. Ecology of a saline stream: community responses to spatial gradients of environmental conditions, Hydrobiologia 226: 167-178.
Simini, M. et I.A. Leone. 1986. The response of dormant Norway and sugar maples to simulated de-icing salt spray, J. Arboric., 12(1): 1-5.
Singer, S.N., C.K. Cheng et M.G. Scafe. 1997. The hydrogeology of southern Ontario, vol. 1, ministère de l'Environnement et de l'Énergie de l'Ontario, Toronto (Ontario), 80 p.
Singleton, H.J. 1986. Water quality criteria for cyanide. Rapport et annnexe technique, Water Management Division, ministère de l'Environnement de la Colombie-Britannique, Victoria (Colombie-Britannique), 84 p.
Smith, L.L., Jr., S.J. Broderius, D.M. Oseid, G.L. Kimball, W.M. Koenst, et D.T. Lind. 1979. Acute and chronic toxicity of HCN to fish and invertebrates, U.S. Environmental Protection Agency, 129 p. (EPA-600/3-79-009).
Smith, M.E. et J.L. Kaster. 1983. Effect of rural highway runoff on stream benthic macroinvertebrates, Environ. Pollut. Ser., A 32: 157-170.
Smith, W.G. 1981. Observations on a large highway kill of Evening Grosbeacks in British Columbia, Syesis, 14: 163.
Smol, J.P., S.R. Brown et R.N. McNeely. 1983. Cultural disturbances and trophic history of a small meromictic lake from Central Canada, Hydrobiologia, 103: 125-130.
Smolders, E. et M.J. McLaughlin. 1996. Chloride increases cadmium uptake in Swiss chard in a resin-buffered nutrient solution, Soil Sci. Soc. Am. J., 60: 1443-1447.
Snodgrass, W.J. et D. Morin. 2000. Patrol (maintenance/works) yard. Documentation complémentaire pour l'évaluation des sels de voirie inscrits sur la LSIP. Rapport présenté au Groupe-ressource environnemental d'Environnement Canada chargé d'évaluer les sels de voirie inscrits sur la Liste des substances d'intérêt prioritaire de la LCPE, juillet 2000, Direction de l'évaluation des produits chimiques commerciaux, Environnement Canada.
Société canadienne de sel Ltée. 1991. Windsor Safe-T-Salt, Coarse - Highway, Pointe-Claire (Québec) (PDS VIII-3 5/91).
Soilcon Laboratories Ltd. 1995. Detailed study of de-icing salt in the Loon Lake environment. Projet de rapport préparé pour la Highway Environmental Branch, ministère des Transports et de la Voirie de la Colombie-Britannique, Victoria (Colombie-Britannique), 97 p.
Sonzogni, W.C., W. Richardson, P. Rodgers et T.J. Monteith. 1983. Chloride pollution of the Great Lakes, J. Water Pollut. Control Fed,. 55: 513-521.
Spehar, R. L. 1987. Note de service à C. Stephan, U.S. Environmental Protection Agency, Duluth (Minnesota), 24 juin [cité dans U. S. EPA, 1988].
Sridhar, K.R. et F. Barlocher. 1997. Water chemistry and sporulation by aquatic hyphomycetes, Mycol. Res., 101(5): 591-596.
Stantec Consulting Ltd. 2000. Calculation of historical road densities within well field capture zones, Kitchener (Ontario).
Steppuhn, H. et D. Curtin (éd). 1992. Salinity and sustainable agriculture, Station de recherches de Swift Current, Direction générale de la recherche, Agriculture Canada, Swift Current (Saskatchewan), 192 p. (Prairie Salinity Publication no 1).
Stoermer, E.F., J.A. Wolin, C.L. Schelske et D.J. Conley. 1985. Postsettlement diatom succession in the Bay of Quinte, Lake Ontario, Can. J. Fish. Aquat. Sci., 42: 754-767.
Strobel, G.A. 1967. Cyanide utilization in soil, Soil Sci., 103(4): 299-302 [cité dans Chatwin, 1990].
Struger, J. 2000. Data on Cl concentrations in the outfall from water detention ponds, Données envoyées par courriel le 15 décembre 2000.
Stumm, W. et J.J. Morgan. 1981. Aquatic chemistry, John Wiley & Sons, New York (N.Y.), 780 p.
Sucoff, E. 1975. Effect of deicing salts on woody vegetation along Minnesota Roads, Minn. Agric. Exp. Stn. Tech. Bull. 303, For. Ser. 20. 49 p.
Sucoff, E. et S.G. Hong. 1976. Effect of NaCl on cold hardiness of Malus spp. and Syringa vulgaris, Can. J. Bot., 54: 2816-2819.
Sutcliffe, D.W. 1961. Studies on salt and water balance in caddis larvae (Trichoptera): II. Osmotic and ionic regulation of body fluids in Limnephilus stigma Curtis and Anabolia nervosa Leach, J. Exp. Biol., 38: 521-530.
Swayne, D.E., A. Shlosberg et R.B. Davis. 1986.
Salt poisoning in turkey poults, Avian Dis., 39(4): 847-852. Theis, T.L. et M.J. West. 1986. Effects of cyanide complexation on adsorption of trace metals at the surface of geothite, Environ. Technol. Lett., 7: 309-318 [cité dans Shifrin et al., 1996].
Thiel, R.P. 1980. Unusual vehicle caused mortality in red crossbills, Passenger Pigeon, 42(1): 23-24.
Thirmurti, D. et K.-H. Tan. 1978. Establishing baseline data for management of Halifax, N.S., lake Watersheds, J. Am. Water Works Assoc., 70(8): 436-445.
Thompson, P. 2000. Salt damage to trees along roads in the Regional Municipality of Peel. Rapport présenté à la municipalité régionale de Peel, 10 juillet 2000.
Thorton, K.W. et J.R. Sauer. 1972. Physiological effects of NaCl on Chironomus attenuatus (Diptera: Chironomidae), Ann. Entomol. Soc. Am., 65: 872-875.
Thuet, J.H. 1977. « Environment », dans Economic impact of highway snow and ice control: state of the art, Federal Highway Administration, Washington (D.C.), p. 146-168, 231-247 (rapport no FHWARD-77-20).
Topping, M.S. et G.G.E. Scudder. 1977. Some physical and chemical features of saline lakes in Central British Columbia, Syesis, 10: 145-166.
Toronto and Region Conservation Authority. 1998. 1990 to 1996 Water Quality Data From the Toronto RAP Watershed; d'après des données obtenues dans le cadre du réseau provincial de surveillance de la qualité de l'eau du ministère de l'Environnement de l'Ontario, Toronto (Ontario).
Towill, L.E., J.S. Drury, B.L. Whitfield, E.B. Lewis, E.L. Galyan, et A.S. Hammons.1978. Reviews of the environmental effects of pollutants: V. Cyanide, 190 p. (ORNL/EIS-81; US EPA-600/1-78-027).
Townsend, A.M. et W.F. Kwolek, 1987. Relative susceptibility of thirteen pine species to sodium chloride spray, J. Arboric., 13(9): 225-228.
Trainer, D.O. et L. Karstad. 1960. Salt poisoning in Wisconsin wildlife, J. Am. Vet. Med. Assoc., 13: 614-617.
Trama, F.B. 1954. The acute toxicity of some common salts of sodium, potassium, and calcium to the common bluegill (Lepomis macrochirus), Proc. Acad. Nat. Sci. Philadelphia, 196: 1885 [cité dans McKee et Wolf, 1963].
Transports Canada. 2001. Longueur du réseau routier, tableau présenté sur le site Web www.tc.gc.ca/pol/fr/ExcelSpreadsheets2/main.asp, le 28 mai 2001.
Trueman K.F. et D.C. Clague. 1978. Sodium chloride poisoning in cattle, Aust. Vet. J., 54: 89-91.
Tuchman, M.L., E.F. Stoermer et H.J. Carney. 1984. Effects of increased salinity on the diatom assemblage in Fonda Lake, Michigan, Hydrobiologia, 109: 179-188.
Underwood, J.K., J.G. Ogden et D.L. Smith. 1986. Contemporary chemistry of Nova Scotian lakes, Water Air Soil Pollut., 30: 991-999.
Upchurch, R.G. et G.H. Elkan. 1977. Comparison of colony morphology, salt tolerance, and effectiveness in Rhizobium japonicum, Can. J. Microbiol., 23: 1118-1122.
U.S. EPA (United States Environmental Protection Agency). 1971. Water quality research, Environmental impact of highway deicing, Edison Water Quality Laboratory, Edison (New Jersey) (NJ 11040 GKK).
U.S. EPA (United States Environmental Protection Agency). 1973. Water quality criteria, 1972, National Academy of Science et National Academy of Engineering, Washington (D.C.) (EPA-R3-73-03) [cité dans Singleton, 1986].
U.S. EPA (United States Environmental Protection Agency). 1985. Ambient water quality criteria for cyanide, 1984, Criteria and Standards Division, U.S. Environmental Protection Agency, Washington (D.C.) (EPA/440/5-84-028).
U.S. EPA (United States Environmental Protection Agency). 1988. Ambient water quality criteria for chloride, U.S. Environmental Protection Agency, Washington (D.C.)
Van Barneveld, J.W. et R.H. Louie. 1990. Boitanio Park, causes of tree decline, soil and vegetation analysis. Document de travail, ministère de l'Environnement de la Colombie-Britannique, Victoria (Colombie-Britannique), 34 p. et annexes.
Vickers, S. 2000. Metal accumulation and sediment-water exchange in an urban wet detention pond. Thèse de maîtrise présentée au Département de géographie, Université de Toronto, Toronto (Ontario).
Ville de Montréal. 1998. Actualisation et complément d'information relatifs au programme d'assainissement des lieux d'élimination de neige de la Ville de Montréal, Montréal (Québec), 28 p.
Ville de Regina. 1997. Soil investigation at city snow dump sites 1996-1997, City of Regina Municipal Engineering Department, Regina (Saskatchewan), 11 p. et annexes.
Ville de Toronto. 2001. [Données de surveillance inédites sur les cours d'eau de la région de Toronto]. Communication personnelle de G. Gris, Works and Emergency Services, Ville de Toronto à D. Morin, Division de l'évaluation des produits chimiques, Environnement Canada, avril et mai 2001.
Wages, D.P., M.D. Ficken, M.E. Cook et J. Mitchell. 1995. Salt toxicosis in commercial turkeys, Avian Dis., 39: 158-161.
Wallen, I.E., W.C. Greer et R. Lasater. 1957. Toxicity to Gambusia affinis of certain pure chemicals in turbid waters, Environ. Future, 29: 695 [cité dans McKee et Wolf, 1963].
Waller, D.L., S.W. Fisher et H. Dabrowska. 1996. Prevention of zebra mussel infestation and dispersal during aquaculture operations, Prog. Fish Cult., 58(2): 77-84.
Wang, J.S., P.M. Huang, W.K. Liaw et U.T. Hammer. 1991. Kinetics of the desorption of mercury from selected freshwater sediments as influenced by chloride, Water Air Soil Pollut., 56: 533-542.
Warren, L.A. et A.P. Zimmerman. 1994. The influence of temperature and NaCl on cadmium, copper and zinc partitioning among suspended particulate and dissolved phases in an urban river, Water Res., 28(9): 1921.
Warrington, P. et C. Phelan. 1998. Road salts and winter maintenance - a best management practices guide to protecting water quality, Water Management Section, ministère de l'Environnement, des Terres et des Parcs de la Colombie-Britannique, Victoria (Colombie-Britannique).
Watson, T. [Données sur les concentrations de chlorure dans des étangs adjacents aux routes, dans le sud de l'Ontario]. Communication personnelle de T. Watson, Université de Toronto, Département de biologie à D. Morin, Division de l'évaluation des produits chimiques, Environnement Canada, entre octobre 2000 et janvier 2001.
Way, J.L., P. Leung, E. Cannon, R. Morgan, C. Tamulinas, J. Leong-Way, L. Baxter, A. Nagi et C. Chui. 1988. « The mechanism of cyanide intoxication and its antagonism », dans Proceedings of the Symposium on Cyanide Compounds in Biology, 15-17 mars, Fondation CIBA, Londres (R.-U.), p. 233-243.
Way, J.M. 1977. Roadside verges and conservation in Britain: a review, Biol. Conserv., 12: 65-74.
Weast, R.C., D.R. Lide, M.J. Astle et W. Beyer (éd.). 1989. CRC handbook of chemistry and physics, 1989-1990, 70e éd., CRC Press, Boca Raton (Floride).
Weiler, R.R. et V.K. Chawla. 1969. « Dissolved mineral quality of Great Lakes waters », dans Proceedings of the 12th Conference on Great Lakes Research. Vol. 1, Association internationale de recherche sur les Grands Lacs, Ann Arbor (Michigan), Braun-Brumfield, Inc., Ann Arbor (Michigan), p. 801-818.
Werkhoven, C.H.E., P.J. Salisbury et W.H. Cram. 1966. Germination and survival of Colorado spruce, Scots pine, caragana, and Siberian elm at four salinity and two moisture levels, Can. J. Plant Sci., 46(1): 1-7.
Wetzel, R.G. 1975. Limnology, W.B. Saunders Co., Philadelphie (Pennsylvanie), 743 p.
Wetzel, R.G. 1983. Limnology, 2e édition, Saunders College Publishing, Toronto (Ontario).
Whitfield, P.H. et N.L. Wade. 1992. Monitoring transient water quality events electronically,
Water Resour. Bull., 28(4): 703-711.
Wickstrom, M.L., P. Mineau, L.J. Brownlee et T.K. Bollinger. 2001. Toxicity of road salt to house sparrows. Projet de rapport, Université de la Saskatchewan, Saskatoon (Saskatchewan).
Wilcox, B.A. et D.D. Murphy. 1985. Conservation strategy: the effects of fragmentation on extinction, Am. Nat., 125: 879-887.
Wilcox, D.A. 1982. The effects of deicing salts on water chemistry and vegetation in Pinhook Bog, Indiana Dunes National Lakeshore. Thèse de doctorat, Purdue University, West Lafayette (Indiana), 134 p.
Wilcox, D.A. 1984. The effects of NaCl deicing salt on Sphagnum recurvum, P. Beauv. Environ. Exp. Bot., 24(4): 295-304.
Wilcox, D.A. 1986a. The effects of deicing salts on vegetation in Pinhook Bog, Indiana, Can. J. Bot., 64(4): 865-874.
Wilcox, D.A. 1986b. The effects of deicing salt on water chemistry in Pinhook Bog, Indiana,
Water Resour. Bull., 22(1): 57-64.
Wilcox, D.A. et R.E. Andrus. 1987. The role of Sphagnum fimbriatum in secondary succession in a road salt impacted bog, Can. J. Bot., 65: 2270-2275.
Williams, D.D., N.E. Williams et Y. Cao. 1997. Spatial differences in macroinvertebrate community structure in springs in southeastern Ontario in relation to their chemical and physical environment, Can. J. Zool., 75: 1404-1414.
Williams, D.D., N.E. Williams et Y. Cao. 1999. Road salt contamination of groundwater in a major metropolitan area and development of a biological index to monitor its impact, Water Res., 34(1): 127-138.
Williams, D.J., K.W. Kuntz, S. L'Italien et V. Richardson. 1998. Lake Ontario Surveillance Program. Spatial and temporal trends of selected parameters, with emphasis on 1992-1993 results. Direction de la conservation de l'environnement - Région de l'Ontario, Division de la santé des écosystèmes, Environnement Canada, 24 p. (rapport no EHD/ECB-OR/98-04/l).
Williams, W.D. 1987. Salinity as a determinant of salt lake fauna: a question of scale, Hydrobiologia, 210: 151-160.
Windingstad, R.M., F.X. Kartch, R.K. Stroud et M.R. Smith. 1987. Salt toxicosis in waterfowl in North Dakota, J. Wildl. Dis., 23(3): 443-446.
WISLOH (Wisconsin State Laboratory of Hygiene). 1995. Données inédites sur la toxicité du chlorure pour les espèces aquatiques, communiquées par A. Letts, directeur technique, Morton International Inc., Chicago (Illinois) à M.S. Evans, Institut national de recherches hydrologiques, Environnement Canada, le 11 août 1998.
Wolfe, D.F.G. 1996. Opportunistic winter water acquisition by pine grosbeaks, Wilson Bull., 108(1): 186-187.
Wood, J.A. et C.D.A. Rubec. 1989. Chemical characterization of several wetlands in Kejimkujik National Park, Nova Scotia, Water Air Soil Pollut., 46: 177-186.
Woodliffe, P.A. 2001. Communication personnelle, ministère des Richesses naturelles de l'Ontario - District d'Aylmer, Chatham (Ontario).
Woods, J. 1998. [The recurrent kills of pine siskins witnessed by local inhabitants in Revelstoke National Park]. Communication personnelle de John Woods, Parcs Canada, Parc national du Mont Revelstoke et Parc national des Glaciers, Revelstoke (Colombie-Britannique) à P. Mineau et G. Fox, Service canadien de la faune, Centre national de la recherche faunique, Ottawa, lors d'une réunion tenue le 4 décembre 1998.
Wulkowicz, G.M. et Z.A. Saleem. 1974. Chloride balance of an urban basin in the Chicago area, Water Resour. Res., 10(5): 974-982.
Zeeb, B.A. et J.P. Smol. 1991. Paleolimnological investigation of the effects of road salt seepage on scaled chrysophytes in Fonda Lake, Michigan, J. Paleolimnol., 5: 263-266.
Zheng, C. 1990. MT3D: A modular three-dimensional transport model for simulation of advection, dispersion and chemical reactions of contaminant in groundwater systems. Rapport présenté à la U.S. Environmental Protection Agency, Ada (Oklahoma), 170 p.
Zidar, L. 2000. Commentaire du public. Salt damage to trees in North District of the Region of Peel. Lettre datée du 11 octobre 2000 adressée à J. Buccini, System Operations, région de Peel, Brampton (Ontario).
Annexe A Stratégies de recherche utilisées pour relever les données pertinentes
Les données utiles à l'évaluation du caractère « toxique » ou non des sels de voirie pour l'environnement, au sens de la LCPE 1999, ont été trouvées dans des documents de synthèse et des documents de recherche publiés ainsi qu'à partir de recherches en ligne effectuées entre janvier et mai 1996 dans les bases de données suivantes : Aqualine (1990-1996), ASFA (Aquatic Sciences and Fisheries Abstracts, Cambridge Scientific Abstracts, 1996), BIOSIS (Biosciences Information Services, 1990-1996), CAB (Bureaux agricoles du Commonwealth, 1990-1996), CESARS (Chemical Evaluation Search and Retrieval System, ministère de l'Environnement de l'Ontario et Michigan Department of Natural Resources, 1996), Chemical Abstracts (Chemical Abstracts Service, Columbus (Ohio), 1990-1996), CHRIS (Chemical Hazard Release Information System, 1964-1985), Current Contents (Institute for Scientific Information, 1990-1992, 1996), ELIAS (Système automatisé intégré des bibliothèques de l'environnement, Bibliothèque d'Environnement Canada, janvier 1996), Enviroline (R.R. Bowker Publishing Co., novembre 1995 - juin 1996), Environmental Abstracts (1975 - février1996), Environmental Bibliography (Environmental Studies Institute, International Academy at Santa Barbara, 1990-1996), GEOREF (Geo Reference Information System, American Geological Institute, 1990-1996), HSDB (Hazardous Substances Data Bank, U.S. National Library of Medicine, 1990-1996), Life Sciences (Cambridge Scientific Abstracts, 1990-1996), NTIS (National Technical Information Service, U.S. Department of Commerce, 1990-1996), Pollution Abstracts (Cambridge Scientific Abstracts, U.S. National Library of Medicine, 1990-1996), POLTOX (Cambridge Scientific Abstracts, U.S. National Library of Medicine, 1990-1995), RTECS (Registry of Toxic Effects of Chemical Substances, U.S. National Institute for Occupational Safety and Health, 1996), Toxline (U.S. National Library of Medicine, 1990-1996), TRI93 (Toxic Chemical Release Inventory, U.S. Environmental Protection Agency, Office of Toxic Substances, 1993), US EPA-ASTER (Assessment Tools for the Evaluation of Risk, U.S. Environmental Protection Agency, jusqu'au 21 décembre 1994), WASTEINFO (Waste Management Information Bureau of the American Energy Agency, 1973 -septembre 1995) et Water Resources Abstracts (Geological Survey, U.S. Department of the Interior, 1990-1996). On a eu recours à Reveal Alert pour maintenir un dossier continu de la documentation scientifique actuelle relative aux effets environnementaux potentiels des sels de voirie.
De plus, l'Association des transports du Canada a révisé l'information sur les sels de voirie à base de sodium et de calcium, dans le cadre de son programme sur la gestion des sels de voirie (ATC, 1999).
Enfin, des groupes de travail individuels ont effectué des recherches en vue d'étayer différentes parties de la documentation complémentaire. Les stratégies de recherche et les sources de données utilisées sont définies dans chacun de ces rapports.
On n'a pas tenu compte des données obtenues après mai 2001 dans la présente évaluation.
Annexe B Documentation complémentaire préparée pour l'évaluation des sels de voirie inscrits sur ls LSIP
Brownlee, L., P. Mineau et A. Baril. 2000. Risk characterization for wildlife. Rapport présenté au Groupe-ressource environnemental d'Environnement Canada chargé d'évaluer les sels de voirie inscrits sur la Liste des substances d'intérêt prioritaire de la LCPE, mai 2000, Direction de l'évaluation des produits chimiques commerciaux, Environnement Canada, Hull (Québec).
Butler, B.J. et J. Addison. 2000. Biological effects of road salts on soils. Rapport présenté au Groupe-ressource environnemental d'Environnement Canada chargé d'évaluer les sels de voirie inscrits sur la Liste des substances d'intérêt prioritaire de la LCPE, mars 2000, Direction de l'évaluation des produits chimiques commerciaux, Environnement Canada, Hull (Québec).
Cain, N.P., B. Hale, E. Berkelaar et D. Morin. 2001. Critical review of effects of NaCl and other road salts on terrestrial vegetation in Canada. Rapport présenté au Groupe-ressource environnemental d'Environnement Canada chargé d'évaluer les sels de voirie inscrits sur la Liste des substances d'intérêt prioritaire de la LCPE, juillet 2001, Direction des substances existantes, Environnement Canada, Hull (Québec).
Delisle, C.E. et L. Dériger. 2000. Caractérisation et élimination des neiges usées : impacts sur l'environnement. Rapport présenté au Grouperessource environnemental d'Environnement Canada chargé d'évaluer les sels de voirie inscrits sur la Liste des substances d'intérêt prioritaire de la LCPE, Direction de l'évaluation des produits chimiques commerciaux, Environnement Canada, Hull (Québec).
Environnement Canada. 1997. Canadian Environmental Protection Act - Problem formulation for the environmental assessment of the Priority Substance road salts, background document, draft. Direction de l'évaluation des produits chimiques commerciaux, Environnement Canada, Hull (Québec).
Evans, M. et C. Frick. 2001. The effects of road salts on aquatic ecosystems. Projet de rapport, Institut national de recherche sur les eaux, Saskatoon (Saskatchewan). Rapport présenté au Groupe-ressource environnemental d'Environnement Canada chargé d'évaluer les sels de voirie inscrits sur la Liste des substances d'intérêt prioritaire de la LCPE, juillet 2001, Direction des substances existantes, Environnement Canada, Hull (Québec).
Johnston, C.T., R.C. Sydor et C.L.S. Bourne. 2000. Impact of winter road salting on the hydrogeologic environment - an overview. Projet de rapport, Stantec Consulting Ltd., Kitchener (Ontario).
Letts, A.D. 2000. Effects of sodium ferrocyanide derived from road salting on the ecosystem, Morton Salt, Morton International Inc., Chicago (Illinois). Rapport présenté au Groupe-ressource environnemental d'Environnement Canada chargé d'évaluer les sels de voirie inscrits sur la Liste des substances d'intérêt prioritaire de la LCPE, mai 2000, Direction de l'évaluation des produits chimiques commerciaux, Environnement Canada, Hull (Québec)
Mayer, T., W.J. Snodgrass et D. Morin. 1999. Spatial characterization of the occurrence of road salts and their environmental concentrations as chlorides in Canadian surface waters and benthic sediments, Environnement Canada. Rapport INRE 99-097 (révisé 20010. 44pp..
Morin, D. 2000. Environmental impacts from the spreading and storage of road salts: Case studies. Documentation complémentaire pour l'évaluation des sels de voirie inscrits sur la LSIP. Rapport présenté au Groupe-ressource environnemental sur les sels de voirie, Direction de l'évaluation des produits chimiques commerciaux, Environnement Canada, mai 2000, 84 p.
Morin, D. et M. Perchanok. 2000. Road salt loadings in Canada. Documentation complémentaire pour l'évaluation des sels de voirie inscrits sur la LSIP. Rapport présenté au Groupe-ressource environnemental d'Environnement Canada chargé d'évaluer les sels de voirie inscrits sur la Liste des substances d'intérêt prioritaire de la LCPE, mai 2000, Direction de l'évaluation des produits chimiques commerciaux, Environnement Canada, Hull (Québec), 85 p.
Morin, D.,W. Snodgrass, J. Brown et P.A. Arp. 2000. Impacts evaluation of road salt loadings on soils and surface waters. Documentation complémentaire pour l'évaluation des sels de voirie inscrits sur la LSIP. Rapport présenté au Groupe-ressource environnemental d'Environnement Canada chargé d'évaluer les sels de voirie inscrits sur la Liste des substances d'intérêt prioritaire de la LCPE, juin 2000, Direction de l'évaluation des produits chimiques commerciaux, Environnement Canada, Hull (Québec), 76 p.
Snodgrass,W.J. et D. Morin. 2000. Patrol (maintenance/works) yards. Documentation complémentaire pour l'évaluation des sels de voirie inscrits sur la LSIP. Rapport présenté au Groupe-ressource environnemental d'Environnement Canada chargé d'évaluer les sels de voirie inscrits sur la Liste des substances d'intérêt prioritaire de la LCPE, juillet 2000, Direction de l'évaluation des produits chimiques commerciaux, Environnement Canada, Hull (Québec).
Détails de la page
- Date de modification :