Ligne directrice canadienne sur la biosécurité - Le double usage dans la recherche en sciences de la vie
Avis au lecteur :
La période de consultation en ligne est maintenant terminée.

Télécharger le format de rechange
(Format PDF, 1,35 Mo, 47 pages)
Organisation : Agence de la santé publique du Canada
Date publiée : 2018-06-29
Tables des matières
- Préface
- Abréviations et sigles
- Chapitre 1 - Introduction
- Chapitre 2 - La gouvernance de la recherche à possibilité de double usage au Canada
- Chapitre 3 - Évaluation des risques liés à la recherche à possibilité de double usage
- Chapitre 4 - La gouvernance internationale de la recherche à possibilité de double usage
- Chapitre 5 - Glossaire
- Chapitre 6 - Références et ressources
Préface
Au Canada, les installations où sont manipulés et entreposés les agents pathogènes humains ou les toxines des groupes de risque 2, 3 et 4 sont réglementées par l’Agence de la santé publique du Canada (ASPC) en vertu de la Loi sur les agents pathogènes humains et les toxines (LAPHT) et du Règlement sur les agents pathogènes humains et les toxines (RAPHT). L’importation d’agents zoopathogènes, d’animaux infectés, de produits d’animaux, de sous-produits d’animaux (p. ex. des tissus ou du sérum), ou d’autres substances qui pourraient être porteurs d’un agent zoopathogène ou d’une partie de celui-ci (p. ex. une toxine) est réglementée par l’ASPC ou l’Agence canadienne d’inspection des aliments (ACIA) en vertu de la Loi sur la santé des animaux (LSA) et du Règlement sur la santé des animaux (RSA).
La figure suivante illustre la hiérarchie des documents qu’utilisent l’ASPC et l’ACIA pour surveiller les activités de biosécurité et de biosûreté. Chaque niveau de la pyramide correspond à un type de document. Les documents sont placés en ordre de priorité du haut de la pyramide vers le bas. Les lois et les règlements se trouvent au sommet de la pyramide, car ce sont ces documents qui transmettent l’autorité légale à l’ASPC et à l’ACIA. Le matériel d’orientation et les éléments techniques se trouvent au bas de la pyramide, car ils sont destinés à résumer les recommandations et les informations scientifiques uniquement.
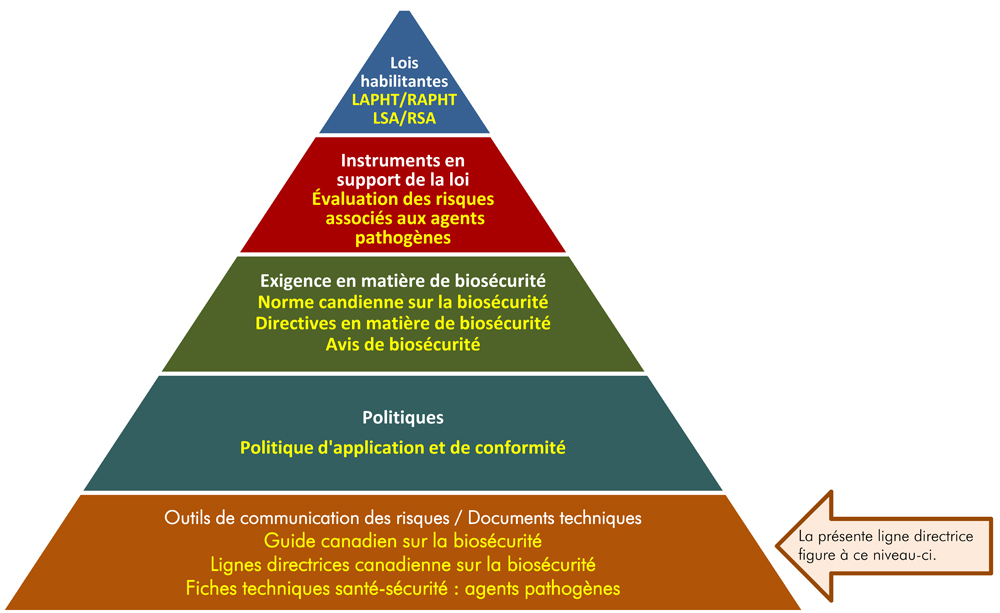
Figure 1 - Équivalent textuel
Figure sous la forme d'une pyramide représentant la hiérarchie des documents utilisés par l'ASPC pour superviser les opérations de biosécurité et de biosûreté. Chacun des cinq niveaux de la pyramide correspond à un type de document, dont l'ordre de préséance augmente du bas vers le haut.
Au sommet, se trouve la législation habilitante, c'est-à-dire la LAPHT, le RAPHT, la LSA et RSA, qui transmet les autorités légales à l'ASPC. Au-dessous des lois et des règlements figurent les Instrument à l'appui de la législation, et ceux-ci sont les évaluations des risques liés aux agents pathogènes. La prochaine étape est intitulée les Exigences en matière de biosécurité, notamment la Norme canadienne sur la biosécurité, les Directives en matière de biosécurité et les Avis de biosécurité. Le deuxième niveau du bas est Documents de politique, soit la Politique de conformité et d'application de la loi. Le matériel d'orientation et les pièces techniques trouvés au bas de la pyramide, sous l'en-tête des Outils de communication des risques et documents techniques, visent seulement à résumer les recommandations et les informations scientifiques. Il s'agit notamment du Guide canadien sur la biosécurité, des Lignes directrices canadiennes sur la biosécurité et des Fiches techniques santé-sécurité : agents pathogènes.
La ligne directrice Le double usage dans la recherche en sciences de la vie a été élaborée par l’ASPC et l’ACIA dans le cadre d’une série de publications électroniques qui s’étendent sur les concepts liés à la biosécurité et la biosûreté présentés dans l’édition actuelle du Guide canadien sur la biosécurité (GCB), soit le document complémentaire à la Norme canadienne sur la biosécurité (NCB). Cette ligne directrice donne des indications sur la façon d’identifier et d’atténuer la possibilité de double usage dans la recherche impliquant des agents pathogènes, des toxines ou d’autres matières infectieuses. De plus, ce document traite de la gouvernance de la recherche ayant une possibilité de double usage au Canada et dans d’autres pays. L’information présentée dans cette ligne directrice n’existe qu’à titre indicatif pour aider les parties réglementées à satisfaire aux exigences énoncées dans la NCB et ne devrait pas être interprétée comme des exigences. Les parties réglementées peuvent choisir d’autres approches pour satisfaire aux exigences énoncées dans la NCB.
Cette ligne directrice est un document en constante évolution et fait l’objet d’une amélioration continue. L’ASPC et l’ACIA accueillent avec intérêt les commentaires, les clarifications et les suggestions visant l’amélioration des versions subséquentes de ce document. Veuillez envoyer toute information ou suggestion, y compris les références, le cas échéant, à l’adresse suivante :
Adresse de courriel de l’ASPC : PHAC.pathogens-pathogenes.ASPC@canada.ca
Abréviations et sigles
- ABCSE
- Agents biologiques à cote de sécurité élevée
- ACIA
- Agence canadienne d’inspection des aliments
- ASB
- Agent de la sécurité biologique
- ASPC
- Agence de la santé publique du Canada
- CIB
- Comité institutionnel de biosécurité
- DURC
- Recherche à double usage préoccupante (Dual-use research of concern)
- GCB
- Guide canadien sur la biosécurité
- GR
- Groupe de risque (c.-à-d. GR1, GR2, GR3, GR4)
- LAPHT
- Loi sur les agents pathogènes humains et les toxines
- NCB
- Norme canadienne sur la biosécurité
- OMS
- Organisation mondiale de la Santé
- PSA
- Plan de surveillance administrative
- RAPHT
- Règlement sur les agents pathogènes humains et les toxines
Chapitre 1 - Introduction
Les termes en caractères gras sont définis dans le glossaire du chapitre 4.
Au cours des dernières décennies, les recherches en sciences de la vie et en biotechnologie ont entraîné d’incroyables améliorations pour la santé publique, pour la santé animale, pour l’environnement et pour l’approvisionnement alimentaire. Cependant, des avancées dans certains domaines comme la recherche sur les maladies infectieuses, les modifications génétiques (y compris les organismes et les aliments génétiquement modifiés), la génomique, la biologie de synthèse et les cellules souches ont soulevé bon nombre de questions sociales, juridiques et éthiquesNote de bas de page 1,Note de bas de page 2. La crainte est que certains types d’organismes, de recherche et de technologies pourraient avoir le potentiel d’avoir des conséquences néfastes sur la santé et la sécurité publiques, la population animale, l’environnement ou la sécurité nationale. En raison des craintes à l’égard de ces conséquences, les gouvernements de partout dans le monde débattent toujours à propos d’une surveillance officielle de la recherche sur le double usage et l’ont mise en œuvre dans bien des cas.
1.1 Qu’est-ce que le double usage dans la recherche en sciences de la vie?
Bien qu’il existe plusieurs définitions du double usage, l’Agence de la santé publique du Canada (ASPC) définit la possibilité de double usage comme les propriétés d’un agent pathogène ou d’une toxine qui lui permettent d’être utilisé autant pour mener des activités scientifiques légitimes (p. ex. à des fins commerciales ou médicales et à des fins de recherche) que pour être utilisé sciemment comme arme biologique pour causer du tort (p. ex. le bioterrorisme).
La définition de la possibilité de double usage comprend aussi toute ressource associée à un agent biologique pouvant être utilisés à des fins malveillantes, y compris les connaissances, les technologies ou les produits qui contribuent à la transformation d’un agent pathogène ou d’une toxine en arme. Par exemple :
- La création d’un agent pathogène ou d’une toxine à risque élevé, le développement d’une méthode de dispersion ou l’augmentation du risque que pose un agent pathogène ou une toxine.
- Les connaissances acquises au cours de recherches sur des organismes résistants aux médicaments. Alors qu’une meilleure compréhension des mécanismes de résistance pourrait donner lieu à des traitements améliorés, cette même information pourrait cependant être utilisée dans l’élaboration d’organismes capables de déjouer les médicaments.
Au Canada, les agents pathogènes et les toxines qui ont été identifiées comme ayant une possibilité de double usage sont appelés des agents biologiques à cote de sécurité élevée (ABCSE) et sont décrits comme des « agents pathogènes humains et toxines prescrits » dans le Règlement sur les agents pathogènes humains et les toxines (RAPHT)Note de bas de page 3.
1.1.1 L’histoire du double usage dans la recherche en sciences de la vie
Le domaine de la biologie moléculaire s’est développé très rapidement depuis la fin des années 1970, grâce à la découverte des vecteurs de clonage, des endonucléases de restriction et des ligases, et grâce à l’introduction du séquençage par la méthode « dideoxy » de Sanger et de la réaction en chaîne par polymérase (PCR). De même, il est devenu beaucoup plus facile d’analyser, de modifier, de synthétiser et de combiner les acides nucléiques. Des génomes entiers peuvent être séquencés en quelques heures, un génome peut être construit et des modifications génétiques précises peuvent être effectuées (p. ex. en utilisant la technologie CRISPR). L’essor de telles technologies et la capacité à créer ou à modifier des organismes vivants ont aussi entraîné des craintes à l’égard de leur possibilité de double usage, comme le démontrent les exemples mentionnés ci-dessous.
La nécessité d’une meilleure gouvernance en matière de recherche sur les agents biologiques a été mise à l’avant-scène en 2001, pour faire suite à l’incident où des lettres contenant des spores de Bacillus anthracis (l’agent causal de la maladie du charbon) ont été envoyées à deux sénateurs américains et aux bureaux de plusieurs médias d’information, tuant cinq personnes et en infectant 17 autres. Une enquête subséquente a dévoilé que les spores provenaient d’un centre de biodéfense et que les lettres avaient été envoyées par un scientifique qui avait accès aux spores et qui avait les compétences nécessaires pour les produireNote de bas de page 4.
Au cours des années suivantes, des avancées en sciences ont aussi suscité des craintes à l’égard de la recherche à possibilité de double usage. Le tableau 1-1 présente des exemples de telles recherches qui soulignent la crainte à l’égard du mésusage intentionnel d’agents pathogènes et de toxines ou de technologies et qui ont déclenché une discussion internationale sur la surveillance de la recherche à possibilité de double usage.
| Année | Recherche | Possibilité de double usage |
|---|---|---|
| 2001 | La création d’un virus mousepox génétiquement modifié pour agir comme type de contrôle des animaux nuisibles a donné de façon inattendue un virus mousepox beaucoup plus virulentNote de bas de page 5. | Une procédure semblable pourrait augmenter la virulence du virus de la variole ou d’autres poxvirus qui infectent les humains et engendrer un virus résistant aux vaccins. |
| 2002 | La synthèse d’un poliovirus infectieux par la manipulation biochimique in vitro de la structure et de la séquence nucléotide publiées du génome du poliovirusNote de bas de page 6. | Un virus pourrait être ressuscité par l’assemblage d’oligonucléotides fondé sur l’information génomique. |
| 2002 | L’ingénierie moléculaire d’une protéine du virus de la variole dans le but d’étudier la virulence du virus de la variole et de la vaccine a engendré un virus de la vaccine à virulence accrueNote de bas de page 7. | L’information de la recherche pourrait être utilisée pour augmenter la virulence du virus de la vaccine ou pour réduire l’efficacité des vaccins contre le virus de la variole. |
| 2005 | La reconstruction du virus grippal A (H1N1) responsable de la pandémie de grippe espagnole en 1918 dans le but de mieux comprendre la virulence du virus grippal afin d’évaluer les interventions actuelles et prochaines en santé publiqueNote de bas de page 8. | Le virus reconstruit et l’information de la recherche pourraient être utilisés pour causer du tort. |
| 2011 | La création de souches de virus grippal aviaire A/H5N1 hautement pathogènes à transmissibilité accrue chez les mammifères pour que la transmissibilité dans l’air entre mammifères puisse être étudiée et puisse conscientiser la population sur l’importante menace du H5N1 envers la santé publique et pour faciliter le développement de vaccins contre le virus grippalNote de bas de page 9,Note de bas de page 10. | L’information dans les manuscrits pourrait être utilisée à mauvais escient dans le but de mettre la santé publique ou la sécurité nationale en danger et le risque augmenté d’une libération accidentelle d’un virus pathogène d’un laboratoire. |
1.2 Portée
La ligne directrice Le double usage dans la recherche en sciences de la vie offre des directives exhaustives sur la manière d’identifier les recherches à possibilité de double usage et sur la manière d’atténuer les risques. Au Canada, toute personne manipulant et entreposant des agents pathogènes humains et des toxines a la responsabilité d’être consciente des risques potentiels en biosécurité et en biosûreté inhérents à ses activités. Il est donc exigé que ces personnes prennent toutes les précautions raisonnables afin d’atténuer les risques associés aux agents pathogènes humains et aux toxines manipulés ou entreposés (LAPHT 6). Cette ligne directrice a pour objectif d’accroître la sensibilisation au sujet du double usage et de promouvoir la conduite responsable de la recherche chez les scientifiques, les éducateurs, la haute direction, les agents de la sécurité biologique (ASB), les organismes de financement, les responsables des politiques et les décideurs ainsi que le grand public. Elle doit être utilisée conjointement avec la Norme canadienne sur la biosécurité (NCB) et le Guide canadien sur la biosécurité (GCB)Note de bas de page 11,Note de bas de page 12.
Les informations et les recommandations offertes dans la ligne directrice Le double usage dans la recherche en sciences de la vie n’existent qu’à titre indicatif et ne devraient pas être interprétées comme des exigences.
1.3 Comment utiliser la Ligne directrice canadienne sur la biosécurité : Le double usage dans la recherche en sciences de la vie
Au début de ce document figure une liste détaillée de tous les abréviations et sigles employés dans cette ligne directrice. Chacun est écrit au long lors de sa première occurrence et l’abréviation ou l’acronyme suit immédiatement entre parenthèses. Suite à la première définition, seules les abréviations sont utilisées pour le reste du document. Un glossaire exhaustif où sont définis les termes techniques se trouve au chapitre 5 de ce document. Les termes qui y figurent sont inscrits en caractères gras lors de leur première occurrence. Aux endroits où les lignes directrices renvoient à une exigence provenant de la loi (c.-à-d. de la LAPHT, du RAPHT), l’article concerné, ainsi que le ou les paragraphes concernés seront cités en référence (p. ex. LAPHT 33). Une liste de ressources est fournie au chapitre 6.
Afin de faciliter la lecture du présent texte, nous avons employé le masculin comme genre neutre pour désigner aussi bien les femmes que les hommes.
Chapitre 2 - La gouvernance de la recherche à possibilité de double usage au Canada
Les risques potentiels pouvant être occasionnés par la recherche à double usage peuvent être atténués grâce aux programmes de biosécurité et de biosûreté. La biosécurité décrit l’ensemble des principes, des technologies et des pratiques liés au confinement mis en œuvre pour prévenir l’exposition involontaire à des matières infectieuses et à des toxines, ou leur libération accidentelle. En comparaison, la biosûreté désigne l’ensemble des mesures visant à prévenir la perte, le vol, le mésusage, le détournement ou la libération intentionnelle non autorisée d’agents pathogènes, de toxines ou d’autres biens liés à l’installation (p. ex. le personnel, l’équipement, les matières non infectieuses et les animaux). Ces concepts ne s’excluent pas mutuellement et sont même intrinsèquement complémentaires, puisque la réalisation de bonnes pratiques en matière de biosécurité sert à renforcer le programme de biosûreté et vice-versa.
Comme la recherche à double usage revêt un intérêt accru à l’échelle internationale, un appel à la mobilisation s’est fait afin de vérifier la pertinence et l’efficacité des mesures actuelles en matière de biosécurité et de biosûreté concernant la protection contre les risques de la recherche à double usage. Plusieurs pays ont mis des mécanismes en place pour assurer la gouvernance de la recherche à double usage et ainsi équilibrer le besoin d’encourager la recherche scientifique tout en protégeant la santé et la sécurité nationales et mondiales contre d’éventuels préjudices. Ce chapitre fournit un résumé des mécanismes de surveillance en vigueur au Canada, des occasions de surveillance tout au long du continuum de recherche, ainsi que des considérations éthiques qui devraient être abordées lors de l’évaluation de la recherche à possibilité de double usage.
2.1 Canada
La surveillance des agents pathogènes et toxines à double usage, des marchandises et des technologies est partagée, au Canada, par divers départements et agences, dont :
- l’Agence de la santé publique du Canada;
- l’Agence canadienne d’inspection des aliments;
- Affaires mondiales Canada;
- l’Agence des services frontaliers du Canada.
2.1.1 Réglementation des agents pathogènes et des toxines au Canada
Au Canada, les installations où sont menées des activités réglementées comportant des agents pathogènes humains, y compris des agents pathogènes zoonotiques (c.-à-d. qui infectent autant les humains que les animaux) ou des toxines sont réglementées par l’ASPC en vertu de la LAPHT et du RAPHT, à moins qu’elles répondent aux critères d’exclusion spécifiés à l’article 4 de la LAPHT. Les installations qui ne sont pas exclues de la LAPHT ou exemptées par le RAPHT, se doivent d’avoir en leur possession un permis d’agents pathogènes et de toxines pour mener des activités réglementées avec des agents pathogènes humains ou des toxines. Ils doivent également se conformer aux exigences applicables énoncées dans la NCBNote de bas de page 11. L’importation d’agents zoopathogènes est régie par l’ASPC ou l’Agence canadienne d’inspection des aliments (ACIA) en vertu de la Loi sur la santé des animaux (LSA) et du Règlement sur la santé des animaux (RSA)Note de bas de page 13,Note de bas de page 14.
La LAPHT, le RAPHT et la NCB ont des exigences spécifiques concernant les ABCSE et la recherche à possibilité de double usage qui comporte des agents pathogènes humains et des toxinesNote de bas de page 3,Note de bas de page 11,Note de bas de page 15. Les agents zoopathogènes non indigènes (c.-à-d. qui causent des maladies animales étrangères) et les agents pathogènes causant des maladies animales émergentes font également l’objet d’exigences spécifiques conformément à la NBC, la LSA et au RSA.
Quelques-uns des principaux éléments de la LAPHT et du RAPHT qui visent à atténuer les risques de double usage sont les suivants :
- l’obligation de détenir une habilitation de sécurité en vertu de la LAPHT afin de pouvoir travailler avec ou avoir accès à des ABCSE (RAPHT 10[1]).
- la liste des quantités seuils de toxines de type ABCSE (RAPHT 10[2]).
- la déclaration obligatoire à l’ASPC de toute libération ou production accidentelle d’agents pathogènes humains ou de toxines et de leur vol ou de leur disparition, ainsi que la déclaration obligatoire si un ABCSE n’est pas reçu au maximum 24 heures après la date et l’heure de réception prévues. (RAPHT 4[2], 9[1]).
- l’interdiction de manipuler ou d’entreposer certains agents pathogènes humains et certaines toxines (LAPHT 8).
- la déclaration obligatoire au titulaire de permis ou à l’ASB de chaque activité qui pourrait entraîner la création d’un agent pathogène humain à virulence, pathogénécité ou transmissibilité accrues, résistant aux traitements préventifs et thérapeutiques ou qui produit une toxine à toxicité accrue (RAPHT 5). Cette exigence s’applique aussi aux travaux qui ne sont pas considérés comme étant à double usage. Si les modifications devaient engendrer un agent pathogène à groupe de risque plus élevé (p. ex. un agent pathogène de groupe de risque 2 [GR2] modifié est maintenant classifié comme GR3), une déclaration de cas de possession involontaire à l’ASPC pourrait s’avérer nécessaire ou un amendement au permis pourrait être soumis à l’ASPC.
- l’exigence que les demandeurs de permis d’agent pathogène et de toxine qui ont l’intention de mener des recherches scientifiques doivent inclure à leur demande un plan de surveillance administrative (PSA) à l’égard des agents pathogènes et des toxines dans un contexte de recherche (RAPHT 3) Note de bas de page 16. Les dix éléments administratifs communs doivent être inclus dans un PSA et comprennent les éléments spécifiques suivants liés au risque de double usage :
- Un aperçu décrivant de quelles façons les risques de biosécurité et de biosûreté, incluant ceux provenant de la recherche à possibilité de double usage, sont identifiés par l’établissement ou l’organisation.
- Un aperçu décrivant de quelles façons les risques de biosécurité et de biosûreté, incluant ceux provenant de la recherche à possibilité de double usage, sont évalués une fois identifiés par l’établissement ou l’organisation.
- Un aperçu décrivant de quelles façons les risques de biosécurité et de biosûreté, incluant ceux provenant de la recherche à possibilité de double usage, sont gérés ou contrôlés par l’établissement ou l’organisation.
Le PSA donne un aperçu de la façon dont les risques de biosécurité et de biosûreté, y compris ceux de la recherche à possibilité de double usage, sont évalués et atténués lorsqu’ils sont identifiés au niveau de l’organisation. Le but du PSA est de démontrer que les organisations ont des structures de responsabilisation internes en place afin d’assurer la surveillance reliée à la recherche impliquant des agents pathogènes et des toxines. Celles-ci incluent des mesures de gestion et de contrôle des risques de biosécurité et de biosûreté ainsi que pour l’identification, l’évaluation et la gestion des activités de recherche à possibilité de double usageNote de bas de page 16.
2.1.2 Exportation du Canada
La Loi sur les licences d’exportation et d’importation (LLEI) met en œuvre des contrôles d’exportation au moyen de la Liste des marchandises d’exportation contrôlée (LMEC) et est administrée par Affaires mondiales Canada (AMC) et l’Agence des services frontaliers du CanadaNote de bas de page 17,Note de bas de page 18. Les résidents du Canada souhaitant exporter un produit inclus dans la LMEC ou vers un pays inclus dans la Liste des pays visés doivent d’abord obtenir un permis d’exportation de la Division des contrôles à l’exportation de l’AMCNote de bas de page 19. La LMEC en vertu de la Loi sur les licences d’exportation et d’importation comprend :
- La liste des marchandises et des technologies à double usage, laquelle respecte l’entente du Canada concernant l’Accord de Wassenaar
- La liste de la non-prolifération des armes chimiques et biologiques, laquelle respecte l’entente du Canada avec le Groupe d’Australie
Le Canada a aussi mis en place des contrôles qui traitent de l’exportation d’éléments qui ne figurent nulle part sur la LMEC. Cette liste entraîne l’obligation de détenir un permis afin d’exporter ces éléments s’il est raisonnable de croire qu’ils seront utilisés par le destinataire final pour le développement, la production, la manutention, l’exploitation, l’entretien, l’entreposage, la détection, l’identification ou la dissémination d’armes chimiques ou biologiques, de dispositifs nucléaires explosifs ou de dispersion radiologique ou de leurs vecteurs. Avant d’exporter quelques produits que ce soient, l’exportateur doit s’assurer qu’ils ne seront pas transférés, directement ou indirectement, à un tel utilisateur final ou pour servir à de telles fins.
2.2 Moments opportuns pour exercer une surveillance lors du continuum de recherche
Tout au long du continuum de recherche se trouvent des moments pour augmenter la prise de conscience à propos du double usage, identifier la recherche à possibilité de double usage, évaluer le risque et, lorsque c’est possible, appliquer les mesures d’atténuation. Les étapes du continuum de recherche identifiées à la figure 2-1 ne sont pas exhaustives. Ce sont plutôt des exemples de cas où l’orientation, la surveillance et le contrôle de la recherche en sciences de la vie peuvent être appliqués.
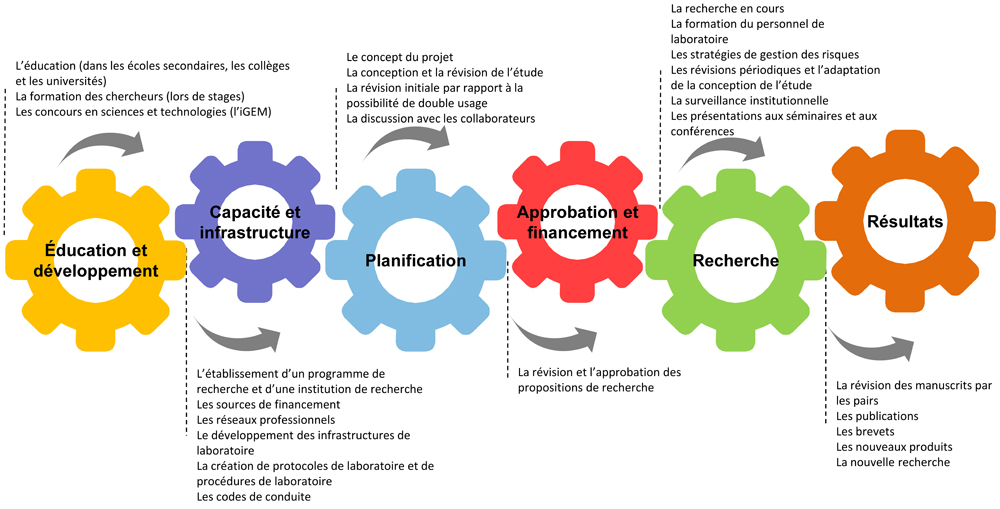
Figure 2-1 - Équivalent textuel
Figure illustrant 6 roues d’engrenage, chacune représentant un moment opportun pour la surveillance le long du continuum de recherche qui évolue de la gauche vers la droite dans la figure. La première roue à la gauche représente l’éducation et le développement, plus spécifiquement l’éducation formelle (dans les écoles secondaires, les collèges et les universités), les formations offertes aux chercheurs (par exemple lors de stages) et les concours en sciences et technologies (comme l’iGEM). La roue pour l’éducation et le développement tourne dans le sens des aiguilles d’une montre et s’emboîte dans la seconde roue qui représente la capacité et l’infrastructure pour la recherche. La roue pour la capacité et l’infrastructure représente l’établissement d’un programme de recherche et d’une institution de recherche, les sources de financement, les réseaux professionnels, le développement des infrastructures de laboratoire, la création de protocoles de laboratoire et de procédures de laboratoire et les codes de conduite. Cette roue tourne dans le sens inverse des aiguilles d’une montre et s’emboîte dans la troisième roue qui représente la planification de la recherche. La planification comprend le concept du projet, la conception et la révision de l’étude, la révision initiale par rapport à la possibilité de double usage et la discussion avec les collaborateurs. La roue pour la planification tourne dans le sens des aiguilles d’une montre vers la quatrième roue qui représente l’approbation et le financement, plus précisément la révision et l’approbation des propositions de recherche. Cette roue tourne dans le sens inverse des aiguilles d’une montre dans la cinquième roue qui représente la recherche elle-même. La recherche comprend la recherche en cours, la formation du personnel de laboratoire, les stratégies de gestion des risques, les révisions périodiques et l’adaptation de la conception de l’étude, la surveillance institutionnelle, et les présentations aux séminaires et aux conférences. La roue pour la recherche tourne dans le sens des aiguilles d’une montre vers la sixième et dernière roue de la figure qui représente les résultats de recherche. Les résultats incluent les manuscrits préparés pour la révision par les pairs, les publications, les brevets, les nouveaux produits et la nouvelle recherche.
2.2.1 Éducation et développement
En recherche, la possibilité de double usage existe dès qu’une hypothèse scientifique est conçue et jusqu’à ce que les résultats expérimentaux soient publiés. Une conduite sécuritaire et responsable de la recherche peut être encouragée à plusieurs étapes à travers ce processus, mais les occasions sont également présentes avant. Le fait d’obtenir des compétences nécessaires pour évaluer les risques et les avantages d’une recherche ainsi que les enjeux éthiques liés à ce travail le plus tôt possible permettra aux individus d’appliquer les connaissances dans leurs plans de recherche. Étant donné la nature complémentaire de la recherche et de l’innovation, le fait d’étendre la portée au-delà des domaines des sciences de la vie (p. ex. les ingénieurs, les informaticiens, les biochimistes, les sociologues) et en dehors des contextes classiques de recherche (p. ex. la biologie participative) permettra de sensibiliser toutes les personnes dont le travail pourrait potentiellement entraîner un double usage. La promotion peut, par exemple, se faire dans les écoles secondaires, les collèges, les universités et dans les concours en sciences et en ingénierie, et ainsi former les futurs scientifiques à faire preuve d’une conscience éthique et à être judicieux dès le début de leurs carrières.
Les scientifiques peuvent apprendre la conduite responsable de recherches scientifiques et les normes professionnelles pendant leurs études au premier cycle ainsi que pendant leurs études supérieures ou par le mentorat par des chercheurs chevronnés. Les établissements et les organisations devraient également décider si des formations supplémentaires ou une sensibilisation sur le double usage sont nécessaires pour leur personnel, selon les résultats de l’évaluation globale des risques et de l’évaluation des besoins en matière de formation (Matrice 4.1 de la NCB).
2.2.2 Capacité et infrastructure
Au sein d’une organisation ou d’un établissement d’enseignement, il existe des occasions de mettre en place des mécanismes de surveillance du double usage et de les faire respecter (p. ex. processus d’approbation internes pour obtenir l’autorisation de travailler avec des agents biologiques pouvant être liés aux fonds de recherche). Les approches varient et peuvent aller de la conception et la mise en œuvre de programmes de formation, des codes de conduite ou des plans de communication stratégique des risques. Les comités institutionnels formés en gestion de risques pourraient offrir des conseils aux chercheurs et apporter un niveau de surveillance supplémentaire.
2.2.3 Planification
Avant que la recherche n’ait lieu, la possibilité de double usage et les facteurs pour atténuer le risque d’utilisation malveillante par rapport aux bienfaits de la recherche doivent être évalués dès la conception du projet. C’est au cours de cette étape que la conception globale de la proposition de recherche est révisée afin d’évaluer les effets indésirables potentiels et que l’ajout de mesures d’atténuation est considéré ou, lorsque c’est possible, que la modification de la recherche proposée peut être envisagée afin de diminuer le risque. Les discussions entre les chercheurs principaux, le personnel de recherche et de laboratoire, les collaborateurs, la haute direction, les comités institutionnels de biosécurité (CIB), les organismes de réglementation pertinents et les organismes de financement sont encouragés et devraient être itératifs afin de faciliter l’élaboration d’un plan de gestion des risques appropriés.
2.2.4 Approbation et financement
Les politiques et les lignes directrices qui régissent l’administration, l’attribution de financement et l’utilisation des fonds varient, de la surveillance complète des projets subventionnés jusqu’à l’autogestion par les institutions ou les organisations financées. Néanmoins, les organisations ont la capacité de contrôler les travaux effectués sous leur sphère d’influence, soit par la révision éthique ou par une révision en matière de biosécurité de la recherche, par le contrôle du financement ou tous autres mécanismes (p. ex. la participation à une formation obligatoire, le suivi d’une norme particulière). Quelle que soit l’approche, l’atténuation des risques est toujours plus efficace lorsque tous les intervenants concernés y prennent part et le fait que toutes les parties participent au dialogue peut éviter d’entraver inutilement une recherche conduite de façon responsable. Ces intervenants peuvent être des organismes de financement, la haute direction, des chercheurs, le CIB et des organismes de réglementation.
2.3 Considérations éthiques
Historiquement, les considérations éthiques dans le cadre de la recherche en sciences de la vie portaient sur la protection des sujets humains et animaux de recherche, plutôt que sur les enjeux liés à la biosécurité et à la biosûreté. Plusieurs organismes de subvention ont mis en œuvre des politiques de conduite sur l’intégrité scientifique, sans tenir compte des enjeux éthiques comme la recherche à possibilité de double usage. L’historique de double usage démontre l’importance d’une évaluation éthique approfondie de toute proposition de recherche effectuée dans une organisation.
Une évaluation éthique d’une recherche scientifique devrait impliquer plusieurs acteurs dans une organisation. Les chercheurs connaissent mieux leur recherche que quiconque et sont donc les mieux placés pour évaluer les inconvénients et les avantages de leurs travaux, mais l’évaluation éthique ne devrait pas être effectuée seulement par le chercheur. Les ASB, le CIB, les collaborateurs de recherche, les organismes de financement, les organismes de réglementation gouvernementaux pertinents, et, lorsque c’est approprié, le public peuvent aussi contribuer à l’évaluation. L’évaluation éthique devrait prendre en considération à la fois les avantages potentiels du travail, comme le progrès de recherches scientifiques innovantes, et la protection de la santé, la sécurité et la sûreté publiques. Le but de l’évaluation est d’atteindre un accord sur un profil de risque acceptable pour l’organisation, compte tenu des avantages potentiels pour la science.
L’Organisation mondiale de la Santé (OMS), dans sa ligne directrice « Responsible Life Sciences Research For Global Health Security », énumère plusieurs questions éthiques fondamentales à considérer lors de l’évaluation d’une telle rechercheNote de bas de page 20. Ces questions peuvent être utilisées par les organisations comme principes directeurs lors d’une évaluation éthique d’une recherche :
- Comment compare-t-on les avantages de la recherche par rapport aux risques de mésusage? Sur quels critères doit-on se baser pour faire cette évaluation?
- Comment compare-t-on les intérêts des chercheurs par rapport aux bénéfices pour la santé publique? Qui devrait prendre ces décisions? Comment les tensions entre les chercheurs individuels et les institutions ou la société pourraient-elles être mieux gérées?
- Comment les risques associés à la recherche peuvent-ils être mieux gérés sans entraver les retombées bénéfiques pour la santé publique?
- Quelles sont les responsabilités des chercheurs individuels et celles de la communauté scientifique dans son ensemble?
Chapitre 3 - Évaluation des risques liés à la recherche à possibilité de double usage
En recherche, un équilibre doit être atteint entre la quête d’innovation et la protection de la santé publique par le biais de la réglementation. Au Canada, une approche axée sur les risques est utilisée afin d’appuyer les recherches avec des agents pathogènes humains ou des toxines qui soient innovantes, tout en préservant la santé et la sécurité des Canadiens. Les installations où on effectue des recherches scientifiques doivent présenter un plan (c.-à-d. le PSA) qui décrit la façon dont elles gèrent et contrôlent les risques relatifs à la biosécurité et à la biosûreté, dont les risques issus de la recherche à possibilité de double usageNote de bas de page 16. Ce plan repose sur ces différentes méthodes d’évaluation des risques :
- L’évaluation globale des risques : Une vaste évaluation de la fonction du programme et des activités prévues au niveau de l’organisation ou de l’installation. L’évaluation contribue au développement du programme de biosécurité, lequel pourrait inclure des politiques en matière de biosécurité et de biosûreté, un plan de gestion des risques, une méthode de gestion du personnel, le manuel de biosécurité, un programme de surveillance médicale, un plan d’intervention d’urgence, un programme d’entretien de l’installation et un programme de formation.
- L’évaluation des risques associés à l’agent pathogène : L’évaluation des propriétés intrinsèques de l’agent biologique ou de la toxine. Elle peut être utilisée afin d’évaluer les modifications proposées et les effets possibles sur l’organisme parental.
- L’évaluation locale des risques : L’évaluation des risques propre au site pour déterminer les risques liés à la matière infectieuse ou aux toxines utilisées et aux activités menées.
- L’évaluation des risques de biosûreté : L’évaluation des risques liés à la perte, au vol, au détournement ou à la libération intentionnelle non autorisée d’agents pathogènes, de toxines et de toute ressource connexe.
Bien que les évaluations des risques ainsi que le développement de stratégies d’atténuation des risques puissent inclure la contribution d’un large éventail d’individus (p. ex. une équipe multidisciplinaire comprenant l’ASB, le chercheur principal, le CIB et le personnel), ce sont les chercheurs principaux qui connaissent le mieux leurs travaux et devraient être les premiers à reconnaître la possibilité de double usage, dès l’étape de la planification et jusqu’à la fin du projet. Simultanément, la surveillance assurée par l’organisation, les organismes de subvention et même par les pairs peuvent jouer un rôle. Si le CIB est impliqué, les membres devraient avoir des connaissances, des compétences et de l’expertise dans une grande variété de domaines afin de s’assurer qu’une évaluation complète peut être effectuée sans limiter indûment la recherche.
Ce chapitre présente des considérations liées à l’identification et à l’évaluation de la recherche avec une possibilité de double usage ainsi qu’aux mesures d’atténuation qui pourraient être mises en œuvre pour assurer la sécurité du personnel, du public, de la population animale et de l’environnement.
3.1 Identifier la recherche avec une possibilité de double usage
Un élément important servant à atténuer les risques est l’identification rapide des activités liées à la recherche qui pourraient être intentionnellement utilisées au détriment des gens, des animaux, de l’environnement et de la sécurité nationale. Chaque projet de recherche devrait faire l’objet d’une évaluation sur la possibilité de double usage lors de l’étape de la planification, pendant toute la durée du travail (même lorsqu’il y a des résultats inattendus) et avant d’utiliser les résultats ou les diffuser (p. ex. la publication). La responsabilité du processus d’évaluation continu devrait être partagée entre les individus impliqués dans la conception et la conduite de la recherche ainsi qu’entre les membres de l’organisation qui supervisent les pratiques en matière de biosécurité et de biosûreté de l’installation.
L’identification comprend une évaluation de la recherche proposée et des organismes. Puisque la possibilité de double usage peut se présenter à tout moment, et souvent par inadvertance, les agents pathogènes manipulés et les tâches à exécuter sont évalués dès le début des étapes de la planification et jusqu’à ce que le travail soit complété et les résultats analysés. Plusieurs considérations peuvent guider la prise de décisions afin de savoir si le travail comporte une possibilité de double usage. Les questions portant sur la toxine ou l’organisme manipulé comprennent les suivantes :
- Est-ce que l’organisme ou la toxine est un ABCSE?
- Quels microorganismes, toxines ou composantes (dont les acides nucléiques) sont impliqués dans ce travail? Sont-ils dangereux pour les humains, pour les animaux ou pour l’environnement?
- Est-ce que des parties d’agents pathogènes ou d’organismes différents seront combinées?
- S’agit-il d’un nouvel agent pathogène ou d’une nouvelle toxine?
- Est-ce que l’agent pathogène a été éradiqué ou est-il éteint?
Voici quelques-unes des questions liées aux tâches prévues :
- Est-ce qu’un agent pathogène ou une toxine sera modifié et est-ce que le résultat de cette modification pourrait engendrer un agent pathogène ou une toxine à risque plus élevé?
- Est-ce qu’un agent pathogène sera créé ou recréé et est-ce que le résultat pourrait entraîner un risque plus élevé que celui présenté par ses composantes?
- Est-il possible que des conséquences imprévues se produisent si la toxine ou l’agent pathogène est libéré du confinement?
- Est-ce que la recherche contient ou produit de nouveaux renseignements qui pourraient être utilisés pour menacer la santé publique, la santé animale ou l’environnement, est-ce qu’elle évalue les méthodes de dispersion (p. ex. la projection d’aérosols, l’augmentation de la transmissibilité) ou est-ce que la recherche met en évidence une vulnérabilité dans le domaine de la santé publique ou dans le domaine des interventions de sûreté auprès du public? Est-ce que la recherche souligne une lacune dans le système de surveillance réglementaire?
- Y a-t-il un potentiel de mésusage des connaissances ou de la technologie? À quel point serait-il facile pour un individu d’utiliser l’information de la recherche envisagée pour causer du tort?
En tenant compte des facteurs reliés à l’organisme ou la toxine manipulés et de ceux reliés aux tâches prévues, l’arbre décisionnel présenté à la figure 3-1 peut servir de guide afin d’identifier s’il s’agit d’une recherche à possibilité de double usage.
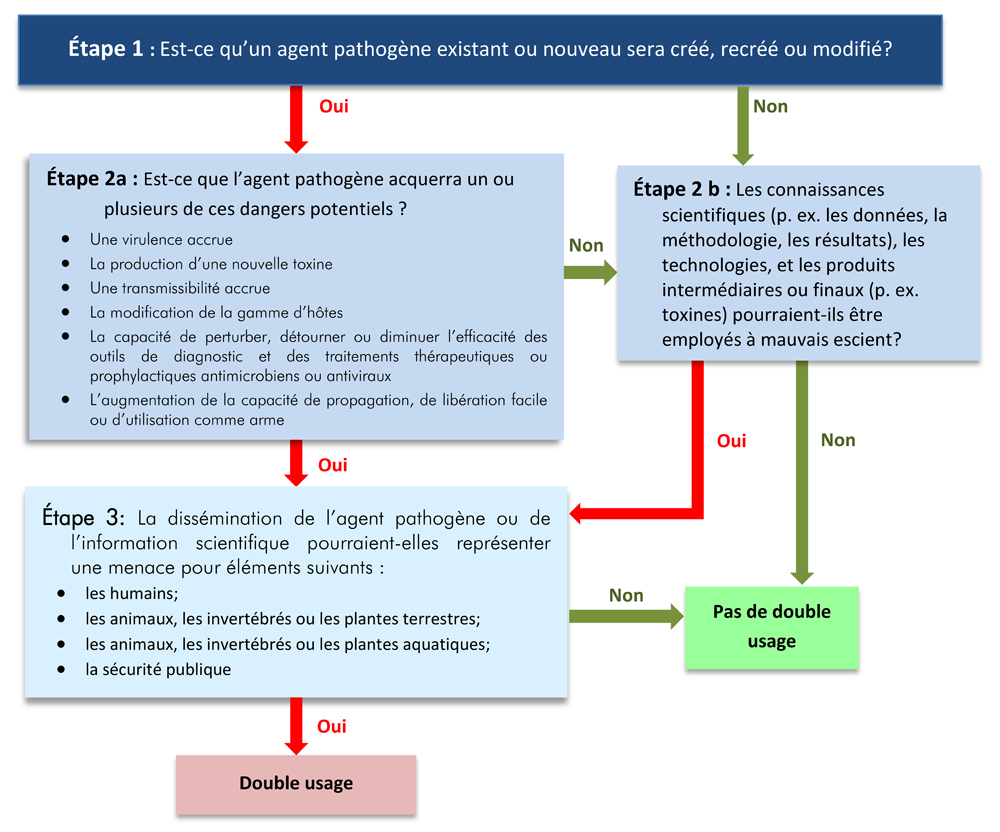
Figure 3-1 - Équivalent textuel
Figure illustrant un arbre décisionnel comprenant trois étapes (trois questions), qui mènent à deux conclusions au bas de la figure, soit un potentiel de double usage ou pas de potentiel de double usage de la recherche. La première question de cet arbre décisionnel (Étape 1), qui est dans un rectangle au haut de la figure, est: Est-ce qu’un agent pathogène existant ou nouveau sera créé, recréé ou modifié? Une réponse Oui correspond à une flèche menant vers la deuxième étape à la gauche (Étape 2a), alors que la réponse Non correspond à une flèche qui mène à la deuxième étape vers la droite (Étape 2b). À l’Étape 2a, la question est: Est-ce que l’agent pathogène acquerra un ou plusieurs des dangers potentiels suivants : une virulence accrue, la production d’une nouvelle toxine, une transmissibilité accrue, la modification de la gamme d’hôtes, la capacité de perturber, détourner ou diminuer l’efficacité des outils de diagnostic et des traitements thérapeutiques ou prophylactiques antimicrobiens ou antiviraux, et l’augmentation de la capacité de propagation, de libération facile ou d’utilisation comme arme? Une réponse affirmative mène à l’étape suivante en dessous (Étape 3), alors qu’une réponse négative correspond à une flèche menant à l’Étape 2b. La question à l’Étape 2b est: Est-ce que les connaissances scientifiques (p. ex. les données, la méthodologie, les résultats), les technologies, et les produits intermédiaires ou finaux (p. ex. toxines) pourraient être employés à mauvais escient? La réponse Non correspond à une flèche qui mène à une boîte verte au bas de la figure à droite concluant qu’il n’y a pas de potentiel de double usage. Si la réponse est oui, la flèche correspondante ramène alors à l’Étape 3. À l’Étape 3, la question est la suivante : La dissémination de l’agent pathogène ou de l’information scientifique pourraient-elle représenter une menace pour: les humains, les animaux, les invertébrés ou les plantes terrestres, les animaux, les invertébrés ou les plantes aquatiques, et/ou; la sécurité publique? En répondant Non à cette réponse, la flèche correspondante mène à la conclusion qu’il n’y a aucun potentiel de double-usage. La réponse Oui par contre correspond à une flèche qui mène à la conclusion qu’il y a effectivement un potentiel de double-usage pour la recherche.
Étape 1 : Est-ce qu’un agent pathogène existant ou éteint ou un nouvel agent pathogène sera créé, recréé ou modifié?
La première étape consiste à déterminer si la recherche créera, recréera ou modifiera un agent pathogène existant ou un nouvel agent pathogène. Il faut tenir compte des procédures suivantes : l’ajout de l’information génétique (p. ex. des plasmides pharmacorésistants), la modification du génome d’organismes existants, la combinaison de l’information génétique de deux organismes différents ou l’assemblage de l’information génétique dans un même génome (p. ex. la combinaison d’oligonucléotides produite synthétiquement).
Étape 2a : Est-ce que l’agent pathogène acquerra un ou plusieurs dangers potentiels?
La deuxième étape permet d’évaluer de manière critique les répercussions possibles suite aux procédures expérimentales et aux manipulations effectuées sur les caractéristiques d’un agent pathogène ou d’une toxine qui sera produite. Une revue de la littérature scientifique peut être effectuée afin de vérifier si des résultats imprévus ont déjà été répertoriés lors d’études semblables. Les facteurs suivants devraient être pris en considération :
- La transmissibilité augmentée (c.-à-d. le pouvoir de transmission d’un agent pathogène d’un hôte à un autre)
- La pathogénicité augmentée (c.-à-d. le pouvoir qu’a un agent pathogène de causer une maladie)
- L’augmentation de la capacité d’un agent pathogène à survivre et se propager dans l’environnement
- La capacité d’échapper aux défenses immunitaires
- La production d’une nouvelle toxine ou d’une toxine ayant une toxicité accrue
- Un changement dans les espèces hôtes que l’agent pathogène a la capacité d’infecter
- La résistance ou l’augmentation de la résistance d’un agent pathogène aux traitements antimicrobiens ou antiviraux existants
- Un changement par rapport à l’efficacité des traitements prophylactiques (c.-à-d. préventifs)
- Une diminution de la capacité à détecter les agents pathogènes avec les outils diagnostiques standards
- Une augmentation de la capacité de propagation, de transmission ou de la facilité de libération (c.-à-d. la facilité avec laquelle il peut être utilisé comme une arme)
Les propriétés intrinsèques de l’agent biologique ou de la toxine ou les composantes utilisées sont inclues dans l’évaluation des risques associés à l’agent pathogène qui tient compte des modifications proposées et des répercussions potentielles sur l’organisme parental. Le risque d’un nouvel agent pathogène ayant une pathogénicité inconnue pourrait être évalué à partir des données de substitution provenant d’agents pathogènes génétiquement reliés. Il en va de même pour les nouvelles toxines ayant un niveau de toxicité inconnu; les données de substitution obtenues à partir d’une toxine de structure semblable pourraient être utilisées.
Étape 2b : Les connaissances scientifiques, les technologies et les produits intermédiaires ou finaux pourraient-ils être employés à mauvais escient?
Dans le cas où aucune création, recréation ou modification d’un agent pathogène existant ou d’un nouvel agent pathogène n’est prévue, il faut tenir compte du risque lié au mésusage des connaissances acquises par la recherche (p. ex. les données, la méthodologie, les résultats), les technologies et les produits intermédiaires et finaux (p. ex. les toxines). Ceux-ci pourraient comprendre des séquences d’acide nucléique d’agents pathogènes ABCSE ou de gènes clés pour la virulence, des méthodes ou des technologies de vecteurs ou de dispersion (p. ex. projection d’aérosols, études de transmissibilité), la conception et les spécifications de l’ingénierie pour les installations, le manuel de biosûreté et les procédures opérationnelles normalisées, les nouvelles techniques (p. ex. pour la dispersion d’agents biologiques ou pour modifier leur sensibilité aux médicaments) et la bio-informatique (p. ex. afin de modifier la résistance aux médicaments ou la pathogénicité).
Étape 3 : Quels secteurs seraient menacés si l’agent pathogène était libéré ou si les connaissances acquises par la recherche étaient publiées?
La dernière étape se concentre sur l’évaluation des menaces que pourrait avoir la libération d’agents pathogènes, de toxines ou de connaissances, sur la santé humaine et animale, l’environnement et la sécurité publique. Cette étape a pour but d’examiner si les résultats de la recherche pourraient être utilisés à mauvais escient dans le but de causer des infections, des maladies ou des décès largement répandus ou qui progressent rapidement, ou d’entraver la surveillance des maladies, la détection, le diagnostic et le confinement de l’agent pathogène. Cette étape sert aussi à évaluer le potentiel que ces résultats de recherche soient intentionnellement utilisés pour altérer les écosystèmes, provoquer un déplacement des espèces ou nuire à l’usage durable de la diversité biologique, plus particulièrement dans les secteurs des ressources comme l’agriculture, la pêche et la foresterie. De tels principes tiennent compte de la possibilité que la recherche représente une menace à la sécurité nationale résultant du mésusage direct ou indirect des renseignements scientifiques publiés portant sur les agents pathogènes ou les toxines ou sur l’usage d’un agent pathogène ou d’une toxine dans le but de planifier une attaque contre les individus, les animaux ou l’environnement.
La réaction du public si la recherche venait à être complétée et publiée, soit telle quelle, soit dans une version abrégée, est un autre aspect à considérer. Cela pourrait-il entraîner de l’anxiété ou des préoccupations répandues à propos de la santé publique, la santé animale ou toute autre préoccupation au sujet de la sûreté et la sécurité publique? Serait-il possible que le public puisse mal comprendre et si cela se produisait, quelles en seraient les conséquences? Est-ce que cela pourrait donner lieu à du sensationnalisme (p. ex. l’exagération des avantages, des risques et des conséquences potentiels) de la part des auteurs d’articles scientifiques et des médias?
3.2 Évaluation des risques associés à la recherche avec une possibilité de double usage
Lorsqu’une recherche à possibilité de double usage est identifiée, il est nécessaire d’évaluer le risque qui lui est associé. La détermination du risque tient compte des dangers identifiés, la probabilité qu’un événement survienne et les conséquences possibles suite à un tel événement. Une évaluation en bonne et due forme guidera la sélection de stratégies d’atténuation appropriées afin de protéger les matériaux de recherche, les outils ainsi que l’information contre la perte, le vol, le mésusage, le détournement ou la publication ou libération intentionnelle non autorisée.
Certains des facteurs qui pourraient influencer la probabilité qu’un incident lié à la recherche à double usage puisse se produire incluent les suivants :
- Les conditions de laboratoire : Quelles sont les conditions de laboratoire nécessaires pour répéter l’expérience ou la reproduire à plus grande échelle? Les conditions de laboratoire nécessaires sont évaluées pour déterminer si l’expérience peut seulement être effectuée dans un laboratoire universitaire tout équipé ou s’il est possible de la répéter dans un laboratoire rudimentaire.
- Les compétences techniques : Quelles sont les compétences techniques essentielles afin de répéter l’expérience ou la reproduire à plus grande échelle? Les compétences techniques sont évaluées afin de déterminer si l’expérience pourrait seulement être répétée par du personnel hautement qualifié ou si elle pouvait être reproduite par du personnel n’ayant pas ces compétences techniques.
- La facilité à acquérir des ressources : À quel point est-ce facile d’acquérir des matériaux, des outils et de l’équipement pour répéter l’expérience ou pour la reproduire à plus grande échelle? Est-ce nécessaire d’utiliser des matériaux et un équipement coûteux ou hautement spécialisés?
- Le délai : Quel est le délai requis pour que le travail puisse être utilisé dans le but de causer du tort (p. ex. dans l’immédiat, à court terme)? L’évaluation du délai permet de voir si la recherche pourrait être utilisée immédiatement pour causer du tort ou si du travail supplémentaire est requis pour que les résultats de recherche deviennent préjudiciables.
- L’historique d’incidents : Est-ce qu’un événement semblable de mésusage d’un agent pathogène, d’une information ou d’une technologie s’est déjà produit auparavant dans l’organisation, la région, le pays ou ailleurs à l’échelle mondiale? S’il y a eu de tels incidents, combien de fois se sont-ils produits?
- La connaissance des menaces internes et externes : Existe-t-il des preuves qu’un groupe ou qu’un individu désire obtenir l’agent pathogène, l’information ou la technologie par malveillance?
Le deuxième facteur à considérer lors de l’évaluation du risque est la conséquence d’un incident, si un tel événement venait à se produire. C’est-à-dire la conséquence possible sur l’environnement, la santé publique, la population animale, l’économie ou la sécurité nationale si l’agent pathogène, la toxine, le matériel ou les renseignements étaient libérés. La gravité de l’effet préjudiciable devrait être évaluée (c.-à-d. éclosion ou épidémie, maladie légère ou modérée, décès, conséquence sur l’économie, peur du public et interruption mineure).
Le résultat d’une évaluation de la recherche à possibilité de double usage ou de toute évaluation des risques est constitué du niveau de risque et de la nécessité ou non de l’atténuer. Le risque est regroupé dans une catégorie de risque qui peut varier de « très bas » à « très élevé ». Les organisations peuvent décider de l’échelle qui est la plus appropriée à leur situation. Il existe différents exemples d’échelles, dont l’échelle de trois niveaux (p. ex. bas, modéré, élevé), l’échelle de cinq niveaux (p. ex. très bas, bas, modéré, élevé et très élevé) et l’échelle numérique (p. ex. de 1 à 10, de 1 à 100) où les chiffres les plus bas indiquent un risque plus faible.
3.2.1 L’analyse des risques et des avantages
Le dernier élément du processus d’évaluation des risques est l’évaluation des avantages potentiels de la recherche. Cette évaluation inclura les avantages possibles pour la santé publique, la santé animale et la sécurité de la recherche, ainsi que la portée des avantages possibles et la période de réalisation de ces avantages (p. ex. immédiat, court terme, long terme). Une recherche qui offre une possibilité de solution à une vulnérabilité touchant la santé publique, les animaux, l’agriculture, les plantes, l’environnement ou le matériel pourrait être vu comme un avantage significatif. Un des éléments essentiels à la communication entourant la recherche à possibilité de double usage est la discussion à propos des avantages des résultats de la recherche. Si les risques associés à la recherche sont jugés trop élevés par rapport aux avantages anticipés, le projet pourrait devoir être modifié ou annulé.
3.3 L’atténuation des risques
L’atténuation des risques est un processus dans lequel des mesures spécifiques sont mises en place afin de réduire au minimum la probabilité d’un incident ou de ses conséquences s’il se produisait. Les mesures d’atténuation appropriées sont proportionnelles au niveau de risque et comprennent les mesures physiques et opérationnelles ainsi que les mesures de sécurité à instaurer et qui devraient être imposées et surveillées par les organisations (p. ex. les ASB, la haute direction, le CIB, les organismes de financement, l’autorité de réglementation).
Il est important de garder en tête qu’une stratégie d’atténuation des risques ne peut réduire le risque à zéro sauf si le travail est complètement évité. L’objectif devrait être de gérer les risques identifiés de façon appropriée et adéquate afin de les maintenir à un niveau acceptable (c.-à-d. le seuil de risque de tolérance, lequel est déterminé par la haute direction). La recherche qui présente des risques qui ne peuvent être atténués à des niveaux acceptables pourrait devoir être modifiée ou annulée ou le travail pourrait devoir être effectué dans une installation ayant un niveau de mesures d’atténuation approprié.
Les stratégies d’atténuation de base pour la recherche avec possibilité de double usage devraient inclure :
- L’adhésion aux exigences physiques en matière de confinement, aux exigences opérationnelles et aux exigences relatives aux essais de vérification et de performance applicables énoncées dans la NCB, ainsi que dans tous les accords nationaux ou internationaux, les lois ou les règlements concernant les agents biologiques et la technologie à double usage (p. ex. les exigences de biosécurité et de biosûreté, les contrôles d’exportation et les traités sur la prolifération des armes biologiques)Note de bas de page 11.
- La création d’un plan de biosûreté complet pour résoudre des problèmes potentiels reliés à l’accès aux agents pathogènes ou aux toxines, aux connaissances, à l’information, à la technologie et aux produits.
Dans les établissements réglementés en vertu de la LAPHT, les chercheurs principaux et le personnel de laboratoire et de recherche sont encouragés à discuter de leurs plans spécifiques de projet avec l’ASB ou avec le titulaire de permis afin d’évaluer la pertinence du plan de gestion des risques existantNote de bas de page 15.
La possibilité d’utiliser une méthode ou un plan expérimental modifié, une toxine ou un agent pathogène alternatif devrait être considérée pour réduire le risque, si un tel changement pouvait fournir des renseignements équivalents. Par exemple, une souche atténuée d’un agent pathogène ou une souche à capacité de réplication réduite à l’extérieur du laboratoire ou dans différents hôtes (p. ex. les humains) pourrait être utilisée. S’il n’y a pas de contre-mesures existantes (c.-à.-d. des traitements prophylactiques ou thérapeutiques) disponibles pour l’agent pathogène ou la souche, la possibilité d’atteindre les objectifs globaux de la recherche en utilisant une souche ou une toxine susceptible aux contre-mesures peut être prise en considération.
3.3.1 Les mesures de biosécurité et de biosûreté
À la suite de l’identification d’une recherche à possibilité de double usage, une évaluation des risques indiquera si les mesures d’atténuation actuelles de biosécurité et de biosûreté sont adéquates. Il se pourrait que des mesures additionnelles soient nécessaires afin de gérer efficacement les risques associés à la recherche à double usage. Ces mesures peuvent comprendre des précautions précises additionnelles comme des mesures de contrôle administratives (p. ex. l’usage d’équipements de protection individuelle additionnelle ou un filtrage du personnel plus strict) ou des exigences physiques (p. ex. effectuer le travail à un niveau de confinement plus élevé ou avec une sécurité physique accrue). Dans les cas où la possibilité d’accroître les risques associés au microorganisme est incertaine, il serait prudent de travailler à un niveau de confinement plus élevé avec une sécurité accrue jusqu’à ce qu’il soit déterminé que l’organisme peut être manipulé de façon sécuritaire à un niveau de confinement moins élevé. Les discussions avec les collaborateurs, la haute direction, le CIB, les agences de réglementation pertinentes et les organismes de financement peuvent aider à la élaboration de stratégies d’atténuation du risque appropriées.
3.3.2 La formation et la sensibilisation
La formation est la pierre angulaire de la biosécurité et de la biosûreté et est exigée pour toutes les installations réglementées où sont manipulés et entreposés des agents pathogènes et des toxines. En ce qui concerne la possibilité de double usage, la formation offre à tout le personnel, dont les chercheurs principaux, les techniciens, les étudiants, les membres du CIB et la haute direction, une compréhension de ce qu'est la possibilité de double usage et comment l'identifier. La sensibilisation de ces individus permet l'identification de la possibilité de double usage pendant le processus de recherche et permet que les risques qui y sont associés soient portées à l'attention de la haute direction et qu'ainsi des stratégies d'atténuation soient créées et implantées au besoin.
Dans une organisation, la formation offre une occasion d’établir un mécanisme qui est applicable pour la surveillance du double usage (p. ex. l’accès à une installation n’est autorisé qu’une fois la formation complétée). Les organisations peuvent créer leurs propres programmes de formation sur le double usage et sur la biosûreté ou peuvent utiliser du matériel de formation provenant de sources externes. Le portail d’apprentissage en ligne de l’ASPC offre plusieurs cours de formation en ligne gratuits, notamment l’Introduction au double usage dans les recherches en science de la vie. L’Université Bradford, l’American Biological Safety Association, le National Science Advisory Board for Biosecurity et la Federation of American Scientists ont aussi des matériels de formation disponibles.
3.3.3 La recherche
Pendant la recherche, les mesures d’atténuation des risques devraient comprendre un contrôle périodique de la recherche et des données préliminaires reliées à la possibilité de double usage. Si une possibilité de double usage est identifiée, une évaluation des risques devrait être menée en tenant compte des nouveaux renseignements. C’est à cette étape du processus de recherche qu’il est important de réévaluer et, s’il y a lieu, de modifier ou d’arrêter la recherche et d’ajuster les plans de communication et les mesures d’atténuation des risques en place. Par exemple, selon le risque identifié, il se peut que l’amélioration des mesures de biosécurité et de biosûreté en laboratoire reliée au niveau de risque correspondant soit nécessaire. Les discussions avec les principaux intervenants (p. ex. les ASB, la haute direction, le CIB) sont aussi importantes afin de réévaluer les risques et les avantages de la recherche et afin de déterminer si celle-ci devrait se poursuivre ou nonNote de bas de page 20.
3.3.4 Le plan de communication
Un élément intégral de l’atténuation des risques liés à la recherche à possibilité de double usage est la création d’un plan organisationnel qui établit les informations (p. ex. les données de la recherche et les protocoles d’expérimentation) qui seront rendues publiques et la façon dont les informations de nature délicates sont communiquées.
Dans certains cas, il peut sembler que la science puisse mener à la libération d’agents pathogènes dangereux. Cette crainte fait parfois objet de récits sensationnalistes dans les médias. Puisque la confiance du public est essentielle à la poursuite de recherches pertinentes en sciences de la vie, il faut prendre en considération les préoccupations, les malentendus et le sensationnalisme potentiels au sein du public. Il est de la responsabilité des scientifiques de faire mieux comprendre leur science en prenant régulièrement part aux efforts de sensibilisation sur l’importance de la recherche et sur l’importance d’une gestion responsable. Un plan de communication peut aider à guider les individus à connaître le moment et la façon de communiquer avantageusement les données ou les renseignements.
Des considérations potentielles en matière de sécurité peuvent avoir des répercussions sur la façon de communiquer, le moment de la communication et ce qui est communiqué. Restreindre la communication a l’avantage d’éviter que les adversaires aient accès à l’information, mais comporte le risque de ralentir les progrès scientifiques et accroît la peur du public face à la science. Inversement, la communication franche et ouverte permet la validation rapide des découvertes et des progrès scientifiques, mais comporte aussi le désavantage de permettre un libre accès au public et aux adversaires. La décision de censurer la publication ne devrait jamais être prise à la légère et les résultats liés à la recherche en sciences de la vie devraient être communiqués autant que possible.
Il y a plusieurs aspects importants à se rappeler lors d’une discussion sur la communication des résultats d’une recherche à double usage. Le premier étant que la décision de communiquer l’information est rarement une réponse binaire « oui ou non ». De plus, les plans de recherche et les découvertes sont typiquement communiqués à plusieurs reprises pendant le processus de recherche, soit pendant : (1) la conception du projet, (2) la demande de financement, (3) l’approbation par le comité d’éthique institutionnel, (4) la recherche comme telle, (5) la création de publications ou d’autres méthodes de communication des résultats de la recherche et (6) lors de la publication du manuscrit de la recherche ou des autres produits de communication. La communication responsable devrait être prise en considération tout au long du processus.
3.3.4.1 La création d’un plan de communication
La création d’un plan de communication est essentielle et indique le contenu qui sera communiqué, le public visé par cette communication ainsi que la façon de communiquer et le moment de la communication. Un plan de communication devrait être créé en concertation avec la haute direction, le CIB, les organismes de financement et les agences de réglementation pertinentes et devrait comprendre les éléments et considérations suivants :
- Contenu à communiquer
- Les mesures physiques et opérationnelles en matière de biosécurité mises en place pendant la recherche et la conformité aux réglementations et aux normes nationales.
- L’importance de la recherche (c.-à-d. les avantages pour la santé publique et la sécurité nationale). Il est aussi important de rassurer le public sur la façon dont la recherche est menée. Les avantages peuvent inclure une discussion sur les façons dont la recherche pourrait mener ou a mené à la création de contre-mesures (p. ex. des vaccins, des antibiotiques et des antitoxines) ou l’amélioration de la surveillance des maladies, de la préparation et de l’intervention en cas de maladiesNote de bas de page 21.
- L’information contextuelle afin de réduire au minimum les inquiétudes et les incompréhensions du public ainsi que le sensationnalisme, en soulignant les avantages, l’importance et l’utilité de la recherche pour la communauté scientifique et le public.
- Les considérations de biosûreté et la conformité avec les lois fédérales et les accords internationaux.
- Public visé
- La communauté scientifique est-elle ciblée, ou est-ce plutôt le grand public qui l’est? Le contenu sera-t-il largement diffusé ou demeurera-t-il confidentiel (p. ex. le contenu sera limité à certains individus selon les besoins)?
- La possibilité que des renseignements à double usage pourraient engendrer des inquiétudes reliées à la biosûreté, non seulement auprès de la communauté scientifique, mais aussi auprès du grand public devrait être prise en considération.
- Choix du temps et la méthode de communication
- Comment la recherche sera-t-elle présentée dans les éditoriaux, les communiqués de presse, les questions et réponses, les points de discussion et les autres méthodes? Comment l’analyse des risques et des bénéfices sera-t-elle présentée?
- Comment la divulgation en temps opportun et le niveau de précision seront-ils utilisés lors de la présentation du contenu de la recherche? Les options peuvent varier entre la communication complète immédiate, la communication retardée, la communication restreinte ou la non-communication.
- Un mécanisme de révision à l’interne avant la publication ou la communication doit être créé
3.3.4.2 Le rôle des scientifiques et des revues scientifiques
Il y a eu plusieurs discussions à propos du rôle des scientifiques et des revues scientifiques dans la publication des recherches qui pourraient mener à l’utilisation malveillante de l’information. Bien qu’il n’y ait eu aucun consensus sur une approche à privilégier, plusieurs positions ont été émises sur cette question.
En 2003, un éditorial publié dans la revue Nature, intitulé the Statement on the Considerations of Biodefence and Biosecurity, a reconnu le statut particulier de l’information scientifique émise dans les revues de recherche scientifique révisées par les pairsNote de bas de page 22. Certains des principaux messages écrits dans cette déclaration figurent ci-dessous :
- L’équilibre entre la publication en temps opportun et d’excellents modèles afin de régir la conception des recherches est essentiel pour s’assurer que les documents sont efficacement évalués par les pairs.
- Si le danger potentiel de la publication dépasse le potentiel des avantages sociaux, le document doit être modifié ou non publié. Les possibilités pour d’autres types de communication scientifique sont disponibles afin de diffuser de l’information qui maximise les bénéfices publics, mais qui réduit au minimum les risques d’utilisation malveillante.
Le Committee on Publication Ethics (COPE) est une organisation à but non lucratif responsable de la mise au point d’un code de conduite pour les rédacteurs et les éditeurs internationaux qui soutient l’indépendance éditorialeNote de bas de page 23. Selon le COPE, les éditeurs sont responsables du contenu de leurs revues et ils devraient s’efforcer de répondre aux besoins des lecteurs et des rédacteurs, de produire des publications de qualité, de bien représenter la liberté d’expression et de maintenir l’intégrité des documents scientifiques.
3.4 La surveillance et la révision
Les risques peuvent évoluer selon les nouvelles découvertes ou les nouveaux développements technologiques. Tout comme l’évaluation des risques associés à l’agent pathogène et l’évaluation des risques de biosûreté, l’évaluation de la possibilité de double usage est révisée régulièrement et mise à jour au besoin. La révision régulière de la possibilité de double usage peut aider l’organisation, l’organisme de financement, l’ASPC et l’ACIA à confirmer la gestion appropriée et adéquate des risques au fil du temps. Si une possibilité de double usage est découverte, l’évaluation des risques associés à l’agent pathogène et l’évaluation des risques de biosûreté pourraient devoir être réexaminées. De même, si les risques associés au travail diminuent (p. ex. à la suite du développement d’un vaccin) les mesures d’atténuation pourraient être proportionnellement réduites.
Chapitre 4 - La gouvernance internationale de la recherche à possibilité de double usage
Le Canada est signataire d'un certain nombre d'instruments internationaux, qui sont tout reflétés dans la législation, les règlements et les politiques du Canada. Ce chapitre décrit les initiatives internationales qui s'efforcent d'identifier et d'atténuer les risques associés à la recherche biologique, et fournit le contexte mondial actuel sur le double usage dans la recherche en sciences de la vie.
4.1.1 La Convention sur les armes biologiques ou à toxines
À l’échelle internationale, l’élaboration délibérée d’agents microbiens dans le but de fabriquer une arme biologique est interdite depuis 1975 en vertu de la Convention sur l’interdiction de la mise au point, de la fabrication et du stockage des armes bactériologiques (biologiques) ou à toxines et sur leur destruction. Il est spécifiquement déclaré dans l’article I que : « Chaque État parti de cette Convention ne doit entreprendre sous aucune circonstance l’élaboration, la production, le stockage, ou sinon l’acquisition ou la rétention : (1) d’agents microbiens ou d’autres agents biologiques ou de toxines, peu importe leur origine ou leur méthode de production, dont les types et les quantités ne sont pas destinés à des fins prophylactiques, de protection ou à d’autres fins pacifiques; (2) d’armes, d’équipement et de vecteurs destinés à l’utilisation de tels agents pathogènes ou de toxines à des fins hostiles ou dans un conflit armé »Note de bas de page 24. Cette convention est un élément clé régissant les efforts fournis par la communauté internationale afin de résoudre la problématique de la prolifération des armes de destruction massive. Cette communauté regroupe environ 180 États membres, dont le Canada.
4.1.2 L’Accord de Wassenaar
L’Accord de Wassenaar relatif au contrôle des exportations des armes conventionnelles et des biens et technologies à double usage, connu sous le nom de l’Accord de Wassenaar, a été conclu en 1996 dans le but de contribuer à la sécurité et la stabilité régionales et internationales, de promouvoir la transparence volontaire, la responsabilisation accrue dans les transferts d’armes conventionnelles ainsi que des marchandises et technologies à possibilité de double usage, et donc d’empêcher les accumulations déstabilisantesNote de bas de page 25. Les États participants visent à assurer, à l’aide de leurs politiques internes, que les transferts de ces éléments ne contribuent pas au développement ou au renforcement des capacités militaires qui compromettent les objectifs de l’Accord et qu’ils ne soient pas détournés pour soutenir de telles capacités. Il y a présentement 41 États participants, dont le Canada.
4.1.3 Le Groupe d’Australie
Le Groupe d’Australie est un regroupement informel qui a pour objectif d’harmoniser le contrôle des exportations de façon à ce que ces dernières ne contribuent pas au développement et à la prolifération d’armes chimiques et biologiques. Il a été créé en 1985 et regroupe 43 pays membres, dont le Canada. Dans les années 90, les agents biologiques avec une possibilité de double usage ont été inclus dans les listes de contrôle des exportations. Le Canada met en application la Liste des agents pathogènes humains et animaux et des toxines réglementés à l’exportation, une « liste de contrôle commune » du Groupe d’Australie au moyen de la Loi sur les licences d’exportation et d’importation pour l’équipement biologique, les technologies et les logiciels connexes à possibilité de double usage, les agents pathogènes humains, les agents zoopathogènes, les toxines et les agents pathogènes pour les plantesNote de bas de page 17. De plus, la liste de contrôle commune du Groupe d’Australie est incorporée dans le RAPHT en tant que critère des agents pathogènes humains et des toxines prescrits (c.-à-d. ABCSE) au CanadaNote de bas de page 26. Pour qu'un agent pathogène humain soit considéré comme un ABCSE, il doit être un agent pathogène du GR3 ou GR4 et être inclus sur la liste de contrôle commune. Les toxines qui se trouvent dans l'annexe 1 de la LAPHT et sur la liste de contrôle commune sont également des ABCSE.
4.1.4 La Résolution 1540 du Conseil de sécurité des Nations unies
La Résolution 1540 du Conseil de sécurité des Nations unies a été adoptée en 2004 afin d’empêcher le développement d’armes biologiques et d’autres genres d’armes, ainsi que leurs matériaux connexesNote de bas de page 27. En vertu de la résolution, tous les États doivent adopter les lois appropriées à cet effet et les mettre en vigueur, ainsi que d’autres mesures efficaces pour empêcher la prolifération de ces armes et leurs vecteurs afin d’éviter que des acteurs non étatiques y ont accès, en particulier à des fins terroristes. Tous les membres des Nations unies, entre autres le Canada, doivent faire une déclaration de conformité.
4.1.5 L’Organisation mondiale de la Santé
En 2009, l’OMS a tenu un atelier sur la recherche responsable en sciences de la vie qui a engendré une publication qui résumait les connaissances actuelles au moment de la publication et qui a mis de l’avant trois concepts de gestion des risques biologiques afin d’assurer un contrôle sur la recherche en sciences de la vie : (1) l’excellence en recherche, (2) la bioéthique et (3) la biosécurité et la biosûreté en laboratoireNote de bas de page 20. En 2013, l’OMS a tenu une conférence informelle au sujet de la recherche à double usage préoccupante (DURC) afin d'identifier les enjeux principaux du DURC et ainsi, explorer les mesures possibles pour combler les lacunes dans les approches de gestion existantes qui abordent le DURCNote de bas de page 28. Alors que d'autres discussions internationales sur la recherche biologique se sont concentrées sur l'armement et la sécurité, l'OMS a fait des efforts de sensibilisation aux conséquences de la recherche à double usage sur la santé publique tout en promouvant une recherche scientifique responsable et innovante au niveau mondial.
4.1.6 Les États-Unis
À l’exception des quelques agents prescrits (Select Agents), la surveillance aux États-Unis se limite aux institutions nationales ou étrangères qui reçoivent un financement de la part du gouvernement fédéral des États-Unis (p. ex. les « National Institutes of Health » [NIH]).
Les établissements financés par le NIH qui souhaitent modifier des acides nucléiques ou des organismes doivent respecter les « NIH Guidelines for Research Involving Recombinant or Synthetic Nucleic Acid Molecules »Note de bas de page 29. Les recherches qui ne correspondent pas clairement aux définitions de la ligne directrice sont transmises au « Recombinant DNA Advisory Committee » du NIH. Si l’agent en question est un agent prescrit, le NIH s’en remettra à l’agence fédérale appropriée (p. ex. l’« U.S. Department of Health and Human Services » ou l’« U.S. Department of Agriculture Select Agents Division »).
L’outil du NIH, le « NIH Tool for the Identification Assessment, Management, and Responsible Communication of DURC », se voulait un guide d’accompagnement pour les institutions et pour les chercheurs principaux contribuant à la mise en œuvre du « U.S government’s Policy for Institutional Oversight of Life Sciences Dual Use Research of Concern » de 2012Note de bas de page 30. La politique et l’outil ne s’appliquent qu’aux recherches menées ou financées par le gouvernement fédéral, mais peuvent aussi servir de guide aux institutions qui ne sont pas directement assujetties à ce mécanisme de surveillance.
Chapitre 5 - Glossaire
ll est important de souligner que, bien que certaines des définitions fournies dans le glossaire soient universellement reconnues, plusieurs d’entre elles ont été établies expressément pour la NCB ou le GCB et certaines ont été modifiées pour pouvoir être appliquées au contexte de la ligne directrice sur le double usage en sciences de la vie.
- Agents biologiques à cote de sécurité élevée (ABCSE)
- Sous-ensemble d’agents pathogènes humains et de toxines qui présentent un risque accru en matière de biosûreté en raison de la possibilité qu’on les utilise comme arme biologique. Au paragraphe 10 (1) du Règlement sur les agents pathogènes humains et les toxines, les ABCSE sont identifiés comme des agents pathogènes et des toxines prescrits. Les ABCSE comprennent donc tous les agents pathogènes du groupe de risque 3 et du groupe de risque 4 qui se retrouvent sur la Liste des agents pathogènes humains et animaux et des toxines réglementés à l’exportation, publiée par le Groupe d’Australie et sujette à modifications, à l’exception du virus Duvenhage, du virus rabique et de tous les autres du genre Lyssavirus, ainsi que du virus de la stomatite vésiculaire. Les ABCSE comprennent aussi toutes les toxines qui se trouvent à la fois à l’annexe 1 de la Loi sur les agents pathogènes humains et les toxines et sur la Liste des agents pathogènes humains et animaux et des toxines réglementés à l’exportation et qui sont présentes en quantités supérieures aux quantités seuils énoncées au paragraphe 10 (2) du Règlement sur les agents pathogènes humains et les toxines.
- Agent de la sécurité biologique (ASB)
- Personne désignée pour superviser les pratiques en matière de biosécurité et de biosûreté dans une installation.
- Agent pathogène
- Microorganisme, acide nucléique ou protéine ayant la capacité de causer une maladie ou une infection chez l’humain ou l’animal. Des exemples d’agents pathogènes humains figurent aux annexes 2 à 4 et à la partie 2 de l’annexe 5 de la Loi sur les agents pathogènes humains et les toxines, mais ils ne constituent pas une liste exhaustive; des exemples d’agents zoopathogènes peuvent être trouvés à l’aide du Système automatisé de référence à l’importation offerte par l’Agence canadienne d’inspection des aliments.
- Biosécurité
- Ensemble des principes, des technologies et des pratiques liées au confinement mis en œuvre pour prévenir l’exposition involontaire à des matières infectieuses et à des toxines, ou à leur libération accidentelle.
- Biosûreté
- Ensemble des mesures visant à prévenir la perte, le vol, le mésusage, le détournement ou la libération intentionnelle d’agents pathogènes, de toxines ou d’autres biens liés à l’installation (p. ex. le personnel, l’équipement, les matières non infectieuses, les animaux).
- Confinement
- Ensemble de paramètres de conception physique et de pratiques opérationnelles visant à protéger le personnel, le milieu de travail immédiat et la communauté contre toute exposition à des matières biologiques. Dans le même contexte, on utilise aussi le terme « bioconfinement ».
- Exposition
- Contact ou proximité étroits avec des matières infectieuses ou des toxines pouvant respectivement causer une infection ou une intoxication. Les voies d’exposition sont l’inhalation, l’ingestion, l’inoculation et l’absorption.
- Groupe de risque (GR)
- Groupe dans lequel les matières biologiques sont classées en fonction de leurs caractéristiques inhérentes, comme la pathogénicité, la virulence, le risque de propagation et l’existence d’un traitement prophylactique ou thérapeutique efficace. Le groupe de risque énonce le risque pour la santé du personnel et du public ainsi que la santé des animaux et des populations animales.
- Incident
- Événement ou situation pouvant causer une blessure, du mal, une infection, une intoxication, une maladie ou un dommage. Les incidents peuvent mettre en cause des matières infectieuses, des animaux infectés ou des toxines. Le déversement, la libération et la perte de matières infectieuses ou de toxines ainsi que l’exposition à celles-ci, la fuite d’un animal, les cas où un employé se blesse ou développe une maladie, l’accès non autorisé à la zone de confinement, une panne de courant, un incendie, une explosion, une inondation ainsi que toutes les autres situations de crise (p. ex. séisme, ouragan) sont des exemples d’incidents. Les accidents et ceux évités de justesse sont considérés comme des incidents.
- Libération
- Rejet de matières infectieuses ou de toxines hors du système de confinement.
- Microorganisme
- Entité microbiologique cellulaire ou non cellulaire capable de se répliquer ou de transférer son matériel génétique, et ne pouvant pas raisonnablement être décelable à l’œil nu. Les microorganismes comprennent les bactéries, les champignons, les virus et les parasites, qu’ils soient pathogènes ou non.
- Niveau de confinement (NC)
- Exigences minimales liées au confinement physique et aux pratiques opérationnelles visant la manipulation sécuritaire de matières infectieuses et de toxines dans les laboratoires, les zones de production à grande échelle et les environnements de travail avec des animaux. Il existe quatre niveaux de confinement, allant du niveau de base (niveau de confinement 1 [NC1]) au niveau le plus élevé (niveau de confinement 4 [NC4]).
- Pathogénicité
- Capacité d’un agent pathogène de causer une maladie chez un hôte humain ou animal.
- Permis d’agent pathogène et de toxine
- Autorisation délivrée par l’Agence de la santé publique du Canada en vertu de l’article 18 de la Loi sur les agents pathogènes humains et les toxines, permettant de mener une ou plusieurs activités réglementées comportant des agents pathogènes humains ou des toxines.
- Possibilité de double usage
- Propriété d’un agent pathogène ou d’une toxine de pouvoir être utilisés autant pour mener des activités scientifiques légitimes (p. ex. à des fins commerciales ou médicales, aux fins de recherche) que pour créer sciemment une arme biologique ayant la capacité de causer une maladie (p. ex. le bioterrorisme).
- Recherche scientifique
- Selon la définition de l’article 1 du Règlement sur les agents pathogènes humains et les toxines, il s’agit d’une enquête ou d’une recherche systématique dans laquelle on étudie un domaine de la science ou de la technologie au moyen d’activités réglementées. Il y a trois types de recherche scientifique :
- la recherche fondamentale, qui consiste en la pratique d’activités réglementées dans le but de faire avancer la connaissance scientifique, sans toutefois viser une application pratique précise;
- la recherche appliquée, qui consiste en la pratique d’activités réglementées dans le but de faire avancer la connaissance scientifique par l’étude d’une application pratique précise;
- le développement expérimental, qui consiste à faire avancer la science ou la technologie par la pratique d’activités réglementées dans le but de créer ou d’améliorer des matériaux, des produits, des procédés ou des dispositifs.
- Risque
- Probabilité qu’un événement indésirable (p. ex. accident, incident, bris de confinement) survienne et conséquences de cet événement.
- Toxine (microbienne)
- Substance toxique produite par un microorganisme, ou dérivée de celui-ci, qui peut avoir des effets graves sur la santé humaine ou animale. Les toxines sont énumérées à l’annexe 1 et à la partie 1 de l’annexe 5 de la Loi sur les agents pathogènes humains et les toxines.
- Virulence
- Gravité ou sévérité d’une maladie causée par un agent pathogène.
Chapitre 6 - Références et ressources
Détails de la page
- Date de modification :