Recommandation sur la vaccination répétée contre la grippe saisonnière
Télécharger en format PDF
(1.40 Mo, 44 pages)
Organisation : Agence de la santé publique du Canada
Publiée : 2023-02-21
Une déclaration du comité consultatif (DCC)
Comité consultatif national de l'immunisation (CCNI)
Préambule
Le Comité consultatif national de l'immunisation (CCNI) et un organisme consultatif externe qui donne à l'Agence de la santé publique du Canada (ASPC) des conseils indépendants, continus et à jour dans le domaine de la médecine, des sciences et de la santé publique liés aux questions de l'ASPC concernant l'immunisation.
L'ASPC a élargi le mandat du CCNI de façon à inclure, en plus de l'impact des maladies et des caractéristiques vaccinales, l'étude systématique des facteurs liés aux programmes dans la formulation de ses recommandations fondées sur les données probantes afin de favoriser la prise de décisions opportunes concernant les programmes de vaccination financés par le secteur public à l'échelle provinciale et territoriale. Cette initiative devrait aider le CCNI à prendre des décisions en temps opportun en ce qui a trait aux programmes de vaccination financés par les fonds publics à échelle provinciale et territoriale.
Les nouveaux facteurs que le CCNI devra examiner de façon systématique sont les suivants : économie, équité, éthique, acceptabilité et faisabilité. Les déclarations du CCNI ne nécessiteront pas toutes une analyse approfondie de l'ensemble des facteurs programmatiques. Même si l'étude systématique des facteurs liés aux programmes sera effectuée à l'aide d'outils fondés sur des données probantes afin de cerner les problèmes distincts susceptibles d'avoir une incidence sur la prise de décision pour l'élaboration des recommandations, seuls les problèmes distincts considérés comme étant propres au vaccin ou à la maladie pouvant être prévenue par un vaccin seront inclus.
La présente déclaration contient les conseils indépendants et les recommandations du CCNI, qui reposent sur les connaissances scientifiques les plus récentes et diffuse ce document à des fins d'information. Les personnes qui administrent le vaccin devraient également connaître le contenu de la monographie de produit pertinente. Les recommandations d'utilisation et les autres renseignements qui figurent dans le présent document peuvent différer du contenu de la monographie de produit rédigée par le fabricant du vaccin au Canada. Les fabricants ont fait homologuer les vaccins et ont démontré leur innocuité et leur efficacité potentielle lorsqu'ils sont utilisés conformément à la monographie de produit uniquement. Les membres du CCNI et les membres de liaison doivent se conformer à la politique de l'ASPC régissant les conflits d'intérêts, notamment déclarer chaque année les conflits d'intérêts possibles.
Table des matières
- Résumé de l'information contenue dans la présente déclaration du CCNI
- I. Introduction
- II. Méthodologie
- III. Résultats
- III.1 Caractéristiques de l'étude
- III.2 Données probantes sur l'efficacité potentielle et l'efficacité réelle de la vaccination répétée par rapport à la vaccination limitée à la saison en cours
- III.3 Données probantes sur l'efficacité réelle de la vaccination répétée par rapport à la vaccination limitée à la saison précédente
- III.4 Données probantes sur l'efficacité réelle de la vaccination répétée par rapport à l'absence de vaccination
- IV. Discussion
- V. Recommandations
- VI. Priorités de recherche
- Tableaux supplémentaires
- Liste des abréviations
- Remerciements
- Annexe A : Stratégie et résultats de recherche
- Annexe B : Organigramme
- Références
Résumé de l'information contenue dans la présente déclaration du CCNI
Le texte suivant résume les renseignements importants pour les vaccinateurs. Voir le reste de la Déclaration pour des précisions.
1. Quoi
La grippe est une maladie respiratoire causée principalement par les virus A et B de l'influenza. La charge grippale varie d'une année à l'autre. Avant la pandémie de COVID-19, la grippe était responsable d'environ 12 200 hospitalisations et 3 500 décès par année au Canada. La vaccination antigrippale est répétée chaque année en raison de la baisse de l'immunité et de la tendance des virus de la grippe à muter fréquemment, ce qui nécessite des changements dans la formulation du vaccin.
Certaines études portant sur différentes saisons grippales ont suggéré que l'administration du vaccin contre la grippe saisonnière au cours d'une ou plusieurs saisons précédentes pourrait réduire l'efficacité réelle (ER) du vaccin contre les souches circulant pendant la saison en cours, contrairement à d'autres études.
2. Qui
La présente déclaration s'applique à toutes les personnes de 6 mois et plus chez qui le vaccin contre la grippe n'est pas contre-indiqué.
3. Comment
Le vaccin contre la grippe saisonnière doit être proposé chaque année à toutes les personnes de 6 mois et plus, qu'elles aient reçu ou non un vaccin contre la grippe saisonnière au cours des saisons précédentes.
4. Pourquoi
La vaccination annuelle contre la grippe réduit la morbidité et la mortalité associées à l'infection grippale. Dans l'ensemble, les données probantes ne montrent aucune différence d'ER entre la vaccination répétée contre la grippe et la vaccination limitée à la saison en cours. Parmi toutes les saisons examinées dans le cadre de nombreuses études, la vaccination répétée sur plusieurs saisons n'a été associée à une ER du vaccin réduite contre l'influenza A (H3N2) que pendant deux saisons grippales, par rapport à la vaccination limitée à la saison en cours. Il est nécessaire de poursuivre l'évaluation des effets de la vaccination répétée contre la grippe sur l'ER, car il n'existe actuellement aucune association prévisible qui pourrait éclairer les décisions concernant les programmes de vaccination d'une année à l'autre. En outre, la vaccination répétée, y compris pendant la saison en cours, est systématiquement plus efficace que l'absence de vaccination pendant la saison en cours.
I. Introduction
La grippe est une maladie respiratoire causée principalement par les virus A et B de l'influenza. Avant la pandémie de COVID-19, on estimait que la grippe provoquait chaque année au Canada environ 12 200 hospitalisationsNote de bas de page 1 et 3 500 décèsNote de bas de page 2. Bien que l'épidémiologie de la grippe ait changé au cours de la pandémie de COVID-19, la grippe saisonnière représente une charge de morbidité permanente au Canada pendant les mois d'automne et d'hiver, qui varie d'une année à l'autre. Pour réduire la morbidité et la mortalité associées à la grippe, le Comité consultatif national de l'immunisation (CCNI) recommande une vaccination annuelle contre la grippe pour toute personne âgée de 6 mois et plus qui ne présente aucune contre-indication au vaccinNote de bas de page 3. La vaccination antigrippale doit être répétée chaque année en raison de la diminution de l'immunité induite par le vaccin et l'infection contre la grippe au fil du temps et parce que les virus de la grippe subissent fréquemment une dérive antigénique. En conséquence, l'Organisation mondiale de la Santé (OMS) se réunit deux fois par année pour évaluer les souches grippales actuellement en circulation et recommander les souches à utiliser dans le vaccin antigrippal pour les prochaines saisons grippales des hémisphères Nord et SudNote de bas de page 4.
Toutefois, un nombre croissant de données probantes explorent les effets négatifs potentiels d'une vaccination répétée contre la grippe saisonnière sur l'ER du vaccin de la saison en cours. Cette question a été étudiée pour la première fois dans les années 1970Note de bas de page 5, et depuis lors, plusieurs études ont indiqué un impact négatif potentiel d'une vaccination précédente contre la grippe sur l'ER du vaccin de la saison en coursNote de bas de page 6Note de bas de page 7Note de bas de page 8Note de bas de page 9Note de bas de page 10. La théorie la plus importante expliquant ce phénomène est l'hypothèse de la distance antigéniqueNote de bas de page 7Note de bas de page 11. Selon cette hypothèse, la vaccination antigrippale de la saison précédente peut nuire à l'ER du vaccin de la saison en cours si la distance (différence) antigénique entre la souche vaccinale de la saison précédente et celle de la saison en cours est faible, et si la distance antigénique entre la souche vaccinale de la saison précédente et la souche circulante de la saison en cours est importanteNote de bas de page 7. En outre, d'autres observations et théories suggèrent que « l'empreinte » immunitaire des réponses à la grippe peut être liée à la cohorte de naissance et influencée par des expositions précoces survenues au cours des saisons précédentes, notamment la première exposition de la vie au virus de la grippeNote de bas de page 12Note de bas de page 13. On ne sait pas encore très bien comment la vaccination répétée peut avoir une incidence sur la réponse immunitaire du vaccin antigrippal. Le présent aperçu n'a pas pour objectif d'aborder les théories sur la façon dont les différences d'ER attribuables à la vaccination répétée contre la grippe peuvent se produire, mais plutôt de déterminer les répercussions globales de ce phénomène et de fournir une base de données probantes pour faciliter les décisions au niveau populationnel et individuel concernant la vaccination annuelle contre la grippe.
L'objectif principal de cet aperçu des examens est le suivant:
- Résumer les données probantes issues des examens systématiques concernant les effets de la vaccination répétée contre la grippe saisonnière sur l'ER du vaccin, l'efficacité potentielle (EP) et l'immunogénicité.
II. Méthodologie
II.1 Question de recherche
Quels sont les effets de la vaccination répétée contre la grippe saisonnière sur l'ER du vaccin, l'EP et l'immunogénicité?
P (population) : Adultes et enfants
I (intervention) : Vaccination contre la grippe saisonnière pendant la (des) saison(s) précédente(s) et la saison en cours
C (comparaison) : Vaccination contre la grippe saisonnière pendant la (des) saison(s) précédente(s) seulement OU pendant la saison en cours seulement OU non vacciné pendant l'une des saisons incluses dans l'étude
O (outcome/résultat) : ER du vaccin, EP ou immunogénicité pendant la saison en cours
S (plan d'étude) : Examen systématique et méta-analyse
Une stratégie de recherche a priori a été élaborée en collaboration avec un bibliothécaire de référence fédéral de la Bibliothèque de la santé de Santé Canada et de l'Agence de la santé publique du Canada (ASPC). Cette stratégie comprenait les termes de recherche suivants : « influenza », « vaccination répétée », « examen systématique » et « méta-analyse ». La stratégie de recherche complète se trouve à l'Annexe A. La recherche a été limitée aux études publiées en langue anglaise ou française et à une date de publication de 2016 à juin 2019. Le CCNI avait déjà connaissance de deux examens systématiques publiés en 2017Note de bas de page 14Note de bas de page 15; par conséquent, la recherche a été limitée aux examens systématiques et aux méta-analyses (ES/MA) publiés en 2016 ou après, afin de s'assurer que tout autre ES/MA récent et pertinent soit saisi. Aucune limite n'a été imposée aux types de plans d'études primaires inclus dans l'ES/MA.
Critères d'inclusion :
- L'étude est un ES/MA;
- L'étude évalue les effets de la vaccination répétée contre la grippe sur l'ER du vaccin, l'EP ou l'immunogénicité.
Critères d'exclusion :
- L'étude ne présente que des recherches primaires;
- L'étude est réalisée dans une langue autre que l'anglais ou le français;
- L'étude n'inclut que les études non humaines;
- La date de publication de l'étude est antérieure à 2016.
Les résumés et les titres des enregistrements récupérés par la recherche dans les bases de données ont été chargés dans DistillerSR (Evidence Partners, Ottawa, Canada) pour être examinés. Si le résumé et le titre répondaient aux critères d'inclusion, ou s'il n'était pas possible de déterminer l'admissibilité sur la base du résumé et du titre seuls, le texte intégral était évalué pour l'admissibilité. Deux examinateurs ont indépendamment passé en revue les titres, les résumés et les textes intégraux pour vérifier leur admissibilité. Les textes intégraux qui répondaient à tous les critères d'inclusion ont été évalués davantage en fonction de la pertinence du PICO de l'ES/MA, par rapport au PICO formulé a priori par le groupe de travail du CCNI sur la grippe (décrit ci-dessus) et de la qualité. Les ES/MA qui n'ont pas été jugés suffisamment pertinents aux objectifs du CCNI ou dont la qualité n'était pas convenable ont été exclus de la synthèse. Cette approche de l'inclusion des examens systématiques dans les directives de santé publique est basée sur la méthodologie proposée dans le cadre du Project on a Framework for Rating Evidence in Public Health (PRECEPT)Note de bas de page 16 et a été initialement élaborée par l'Agency for Healthcare Research and Quality (AHRQ) des États-UnisNote de bas de page 17. La qualité des ES/MA a été évaluée à l'aide d'AMSTAR 2Note de bas de page 18, un outil spécialement conçu pour examiner la qualité des ES/MA. Les ES/MA pour lesquels les examinateurs avaient de nombreuses préoccupations sérieuses dans les domaines d'AMSTAR 2 seraient exclus.
Les données des ES/MA inclus ont été extraits en utilisant un modèle ayant des variables définies a priori. Les estimations de l'effet regroupées extraites des ES/MA étaient supposées représenter des estimations regroupées non ajustées, sauf indication contraire. L'évaluation de la qualité et l'extraction des données ont été effectuées indépendamment par deux examinateurs. Tout désaccord au cours de l'évaluation de l'admissibilité, de l'évaluation de la qualité ou de l'extraction des données a été discuté jusqu'à ce qu'un consensus soit atteint. Les résultats des analyses de sous-groupes qui ne comprenaient qu'une seule étude n'ont pas été extraits. Les données probantes ont été synthétisées de manière narrative et les estimations de tous les ES/MA inclus ont été discutées, sans tenir compte du chevauchement des études primaires.
III. Résultats
III.1 Caractéristiques de l'étude
Grâce à une recherche documentaire exhaustive effectuée le 27 octobre 2017 et mise à jour le 3 juin 2019, 5 ES/MA ont été déterminés comme pouvant être inclus dans la synthèse des données probantes; 2 par MedlineNote de bas de page 19Note de bas de page 20, une par PROSPERONote de bas de page 21 et 2 qui avaient déjà été établis par des expertsNote de bas de page 14Note de bas de page 15. Les 5 ES/MA relevés s'alignent suffisamment sur le PICO de cet aperçu (Tableau 1). Aucun ES/MA nouveau ou en cours admissible à l'inclusion n'a été relevé par des mises à jour supplémentaires de la recherche dans PROSPERO effectuées jusqu'en mars 2022. Un organigramme complet de PRISMA se trouve à l'Annexe B et une liste complète des études exclues et des raisons de l'exclusion est disponible sur demande. Aucun des ES/MA ne comportait d'études primaires évaluant l'immunogénicité. Les critères d'inclusion et d'exclusion supplémentaires définis pour chaque ES/MA qui n'étaient pas spécifiés par le PICO de cet aperçu sont détaillés dans le Tableau 2.
| PICO | Critères | Ramsay et al. 2019Note de bas de page 15 | Bartoszko et al. 2018Note de bas de page 21 | Morimoto et al. 2018Note de bas de page 20 | Belongia et al. 2017Note de bas de page 14 | Caspard et al. 2016Note de bas de page 19 |
|---|---|---|---|---|---|---|
| Population | Tous les âges sont inclus | Oui | Oui | Oui | Oui | Partielle (les études sur les adultes de 18 ans et plus ont été exclues) |
| Intervention/ Comparaison | Vaccination contre la grippe saisonnière pendant la saison grippale précédente et la saison en cours | Oui | Oui | Oui | Oui | Oui |
| Vaccination contre la grippe saisonnière limitée à la saison grippale précédente | Oui | Oui | Oui | Oui | Oui | |
| Vaccination contre la grippe saisonnière limitée à la saison grippale en cours | Oui | Oui | Oui | Oui | Oui | |
| Non vacciné contre la grippe à la fois pendant la saison grippale précédente et la saison en cours | Oui | Oui | Non | Oui | Oui | |
| Tout vaccin contre la grippe saisonnière utilisé pour la vaccination | Oui | Oui | Oui | Oui | Non (seules les études sur le vaccin antigrippal vivant atténué ont été incluses) | |
| Résultats | Études sur l'ER du vaccin ou l'EP | Oui | Oui | Oui | Oui | Oui |
| Études sur l'immunogénicité | Non | Non | Non | Non | Non | |
|
||||||
Les résultats de l'évaluation de la qualité d'AMSTAR 2 sont présentés dans le Tableau 3. Pour cet examen, aucun des domaines d'AMSTAR 2 n'a été considéré comme étant « critique ». Les ES/MA menés par Bartoszko et al., Morimoto et al. et Ramsay et al. étaient de qualité similaire et présentaient des différences mineures entre les domaines. Il est important de noter que l'ES/MA réalisé par Belongia et al. a été jugé de qualité inférieure, principalement en raison de l'absence d'une évaluation documentée du risque de biais (RdB) des études incluses. Aucun des ES/MA ne comprenait une liste d'études exclues ou ne mentionnait les sources de financement des études primaires incluses. En outre, aucun des ES/MA n'a fourni une enquête complète sur l'hétérogénéité des résultats; toutefois, la plupart des études ont abordé des facteurs importants et non mesurés qui pourraient avoir un impact sur l'ER du vaccin dans la discussion (p. ex., l'histoire de l'infection naturelle). Deux des examens ont effectué des recherches dans la littérature grise (c.-à-d. dans les registres d'essais)Note de bas de page 14Note de bas de page 21, trois ont évalué la qualité des études inclusesNote de bas de page 15Note de bas de page 20Note de bas de page 21 et deux ont évalué la probabilité d'un biais de publicationNote de bas de page 20Note de bas de page 21. L'ES/MA mené par Caspard et al. présentait un grand nombre de préoccupations sérieuses dans presque tous les domaines d'AMSTAR 2. Il convient de noter qu'aucune donnée probante d'une conception a priori n'a été fournie, que la sélection des études et l'extraction des données n'ont pas été effectuées en double, qu'aucune évaluation de la qualité n'a été spécifiée et que l'hétérogénéité n'a pas été évaluée. En outre, un modèle à effets fixes a été utilisé pour estimer l'EP des vaccins antigrippaux, ce qui, étant donné les différences attendues dans les estimations d'une saison à l'autre, ne serait pas approprié; un modèle à effets aléatoires serait favorisé et a été utilisé dans tous les autres ES/MA inclus. En raison des limites des ES/MA de l'étude de Caspard et al. concernant ces domaines AMSTAR 2, cet ES/MA a été exclus de la synthèse des données probantes.
| PICO (T) | Critères | Ramsay et al. 2019Note de bas de page 15 | Bartoszko et al. 2018Note de bas de page 21 | Morimoto et al. 2018Note de bas de page 20 | Belongia et al. 2017Note de bas de page 14 | Caspard et al. 2016Note de bas de page 19 |
|---|---|---|---|---|---|---|
| Intervention/ Comparaison |
Ont également été incluses les études portant sur la vaccination au cours de deux saisons grippales précédentes ou plus | Inclus (Exclus de la MA) |
Inclus | Inclus | Exclus | Inconnu (non exclus) |
| Vaccination avec un vaccin monovalent contre la grippe pandémique | Inconnu (non exclus) |
Non exclus explicitement | Exclus | Exclus | Inconnu (non exclus) |
|
| Résultats | Infection grippale définie comme nécessitant des soins médicaux et confirmée en laboratoire par des tests moléculaires de réaction en chaîne de la polymérase par transcription inverse (RT-PCR) | Inclus | Inclus | Inclus | Inclus | Inconnu (non exclus) |
| Infection grippale définie comme nécessitant des soins médicaux et confirmée en laboratoire par toute méthode | Inconnu (Non inclus) |
Inclus | Inclus | Inconnu (Non inclus) |
Peu clair (la méthode de confirmation en laboratoire n'est pas indiquée) |
|
| Plan de l'étude | ECR | Inconnu (Non inclus) |
Inclus | Inclus | Inclus | Inclus |
| Études d'observation | Inclus | Inclus | Inconnu (Non inclus) |
Partiellement inclus (comprend seulement les cas-témoins négatifs, les cas-témoins et la cohorte, les autres ne sont pas inclus) | Exclus | |
| Études coût-efficacité, articles de synthèse | Inconnu (Non inclus) |
Inconnu (Non inclus) |
Inconnu (Non inclus) |
Exclus | Exclus | |
| Résumé ou compte rendu de conférence | Exclus | Inconnu (Non exclus) |
Inconnu (Non inclus) |
Inconnu (Non exclus) |
Inconnu (Non exclus) |
|
| L'article est un rapport intermédiaire d'ER du vaccin, qui a été remplacé par un rapport de fin de saison | Exclus | Inconnu (Non exclus) |
Inconnu (Non inclus) |
Inconnu (Non exclus) |
Inconnu (Non exclus) |
|
| L'étude n'a pas appliqué les critères standards de symptômes pour l'enrôlement | Inconnu (Non exclus) |
Inconnu (Non exclus) |
Inconnu (Non exclus) |
Exclus | Inconnu (Non exclus) |
|
| L'étude a utilisé un échantillon de commodité de tests de diagnostic clinique plutôt que des critères de dépistage prédéfinis | Inconnu (Non exclus) |
Inconnu (Non exclus) |
Inconnu (Non exclus) |
Exclus | Inconnu (Non exclus) |
|
| Calendrier | L'étude a fait état d'une ER du vaccin pour la saison en cours en lien avec la grippe saisonnière pré-2009 | Inconnu (Non exclus) |
Inconnu (Non exclus) |
Inconnu (Non exclus) |
Exclus | Inconnu (Non inclus) |
|
||||||
Les deux études qui ont évalué la qualité des études d'observation incluses ont constaté que le RdB de ces dernières était faible selon l'échelle de Newcastle-OttawaNote de bas de page 15Note de bas de page 21. Les données probantes sur l'infection grippale confirmée en laboratoire provenant d'essais contrôlés randomisés (ECR) inclus par Bartoszko et al. ont été jugées par les auteurs comme présentant un RdB sérieux, selon l'outil de RdB de Cochrane pour les ECR, en raison d'une mauvaise dissimulation de la répartition, d'une perte de suivi et d'un financement privé ou peu clairNote de bas de page 21. Parmi les études ECR incluses par Morimoto et al., les auteurs ont considéré que 3 d'entre elles avaient un RdB élevé, 2 un RdB faible et 3 un RdB peu clairNote de bas de page 20. Belongia et al. n'ont pas procédé à une évaluation de la qualité des études qu'ils ont incluses; toutefois, la qualité de toutes les études incluses a été examinée dans au moins un autre ES/MANote de bas de page 14 (voir Figure 1).
Les 4 ES/MA retenus contenaient un examen systématique (ES) et une MA des effets de la vaccination répétée contre la grippe sur l'EP ou l'ER du vaccin, et ont analysé les résultats de 24 études primaires uniques. Il y avait un chevauchement important des études primaires incluses dans les ES/MA, les résultats de 24 des 48 études primaires (50 %) ayant été évalués dans plus d'un ES/MA. Les détails sur le chevauchement des études primaires parmi les ES/MA inclus sont présentés dans la Figure 1.
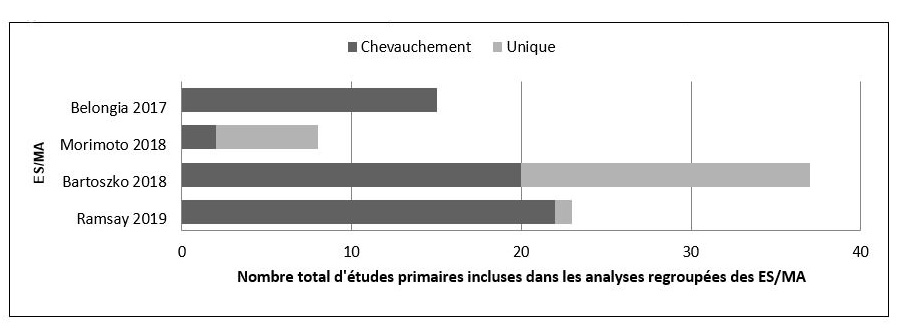
Figure 1 : Texte descriptif
Figure 1 montre un graphique à barres horizontales empilées fournissant des détails sur le degré de chevauchement des études primaires parmi les revues systématiques et les méta-analyses incluses. Les informations suivantes sont représentées :
| Ramsay 2019 | Bartoszko 2018 | Morimoto 2018 | Belongia 2017 | |
|---|---|---|---|---|
| Chevauchement | 20 | 21 | 2 | 17 |
| Unique | 0 | 18 | 6 | 0 |
| Total incluses dans les MA | 20 | 39 | 8 | 17 |
| Critères d'AMSTAR 2 | Ramsay et al. 2019Note de bas de page 15 | Bartoszko et al. 2018Note de bas de page 21 | Morimoto et al. 2018Note de bas de page 20 | Belongia et al. 2017Note de bas de page 14 | Caspard et al. 2016Note de bas de page 19 |
|---|---|---|---|---|---|
| 1. Les questions de recherche et les critères d'inclusion de l'examen comprenaient-ils les composantes du PICO? | Oui | Oui | Oui | Oui | Oui |
| 2. Le rapport de l'examen contient-il une déclaration explicite selon laquelle les méthodes d'examen ont été établies avant sa réalisation et le rapport justifie-t-il toute dérogation importante au protocole? | Oui | Oui | Non | Non | Non |
| 3. Les auteurs de l'examen ont-ils expliqué leur sélection des plans d'étude à inclure dans l'examen? | Non | Non | Oui | Non | Non |
| 4. Les auteurs de l'examen ont-ils utilisé une stratégie de recherche documentaire complète? | Oui partiel | Oui partiel | Non | Non | Non |
| 5. Les auteurs de l'examen ont-ils effectué la sélection des études en double? | Oui | Oui | Oui | Non | Non |
| 6. Les auteurs de l'examen ont-ils effectué l'extraction des données en double? | Oui | Oui | Oui | Oui | Non |
| 7. Les auteurs de l'examen ont-ils fourni une liste des études exclues et justifié les exclusions? | Non | Non | Non | Non | Non |
| 8. Les auteurs de l'examen ont-ils décrit les études incluses de manière suffisamment détaillée? | Oui | Oui | Oui | Oui | Oui |
| 9. Les auteurs de l'examen ont-ils utilisé une technique satisfaisante pour évaluer le RdB dans les études individuelles qui ont été incluses dans l'examen? | Oui | Oui | Oui | Non | Non |
| 10. Les auteurs de l'examen ont-ils indiqué les sources de financement des études incluses dans l'examen? | Non | Non | Non | Non | Non |
| 11. Si une MA a été réalisée, les auteurs de l'examen ont-ils utilisé des méthodes appropriées pour la combinaison statistique des résultats? | Oui | Oui | Oui | Oui | Non |
| 12. Si une MA a été réalisée, les auteurs de l'examen ont-ils évalué l'impact potentiel des RdB dans les études individuelles sur les résultats de la MA ou d'une autre synthèse de données probantes? | OuiTableau 3 Note de bas de page a | Non | Oui | Non | Non |
| 13. Les auteurs de l'examen ont-ils tenu compte des RdB dans les études individuelles lors de l'interprétation/discussion des résultats de l'examen? | Oui | Oui | Non | Non | Non |
| 14. Les auteurs de l'examen ont-ils fourni une explication et une discussion satisfaisantes de toute hétérogénéité observée dans les résultats de l'examen? | Non | Non | Non | Non | Non |
| 15. S'ils ont réalisé une synthèse quantitative, les auteurs de l'examen ont-ils effectué une enquête adéquate sur le biais de publication (biais des petites études) et discuté de son impact probable sur les résultats de l'examen? | Non | Oui | Oui | Non | Non |
| 16. Les auteurs de l'examen ont-ils signalé toute source potentielle de conflit d'intérêts, y compris tout financement reçu pour la réalisation de l'examen? | Oui | Oui | Oui | Oui | Oui |
| Total (sur 16) | 10,5 | 10,5 | 10 | 5 | 3 |
|
|||||
Deux des ES/MA comprenaient des études primaires avec des plans d'ECR et d'observationNote de bas de page 14Note de bas de page 21, un ne comprenait que des ECRNote de bas de page 20 et un autre ne comprenait que des études d'observationNote de bas de page 15. Le modèle cas-témoin à test négatif était le type de plan d'étude d'observation (études d'observation) le plus courant parmi les études primaires incluses. L'ES/MA mené par Bartoszko et al. avait les critères de sélection des études les moins restrictifs et comprenait le plus grand nombre d'études. Deux ES/MA n'ont inclus que des études primaires ayant confirmé l'infection grippale par RT-PCRNote de bas de page 14Note de bas de page 15. Bartoszko et al. ont inclus des études qui ont confirmé l'infection grippale par RT-PCR ou par culture virale comme résultat primaire, et par toute méthode de laboratoire comme résultat secondaire. Une analyse de sensibilité effectuée par les auteurs a indiqué que l'inclusion des études qui ne confirmaient pas l'infection grippale par RT-PCR ou par culture virale ne modifiait pas de manière significative les estimations de l'effet; les auteurs ont donc choisi d'inclure ces études dans leur MA finale. Morimoto et al. ont également inclus des études qui définissaient la grippe confirmée en laboratoire (GCL) comme étant confirmée par RT-PCR et sérologie et (ou) culture; toutefois, aucune analyse de sensibilité pour la méthode de confirmation en laboratoire n'a été réalisée.
Les 4 ES/MANote de bas de page 14Note de bas de page 15 Note de bas de page 20Note de bas de page 21 ont rapporté des estimations d'effets regroupées pour l'EP ou l'ER de la vaccination répétée contre la grippe à l'aide d'un modèle à effets aléatoires; toutefois, chacun a utilisé une méthode différente pour combiner les données des études primaires. Belongia et al. ont calculé séparément l'ER regroupée et non ajustée de la vaccination pendant deux saisons consécutives (c.-à-d. la saison en cours et la saison précédente), de la vaccination limitée à la saison en cours et de la vaccination limitée à la saison précédente, l'absence de vaccination pendant la saison en cours et la saison précédente servant de référence. Ramsay et al. ont regroupé les différences dans les estimations ajustées de l'ER pour les différents scénarios afin de contrôler les facteurs de confusion au sein de l'étude. Bartoszko et al. ont calculé les rapports de cote (RC) non ajustés de la GCL nécessitant des soins médicaux, en comparant les personnes vaccinées pendant deux saisons consécutives aux personnes vaccinées seulement pendant la saison en cours. Morimoto et al. ont calculé le rapport de risque (RR) pour la GCL nécessitant des soins médicaux chez les personnes ayant été vaccinées pendant deux saisons consécutives par rapport à celles ayant été vaccinées seulement pendant la saison en cours.
III.2 Données probantes sur l'efficacité potentielle et l'efficacité réelle de la vaccination répétée par rapport à la vaccination limitée à la saison en cours
En général, la vaccination antigrippale pendant deux saisons consécutives n'a pas eu d'effet négatif ou positif sur l'ER par rapport à la vaccination limitée à la saison en cours; toutefois, dans deux circonstances, un effet négatif potentiel a été constaté. Un ES/MA a démontré un effet négatif regroupé de la vaccination pendant deux saisons consécutives pour l'ER du vaccin contre l'influenza A(H3N2) lors de la saison grippale 2010-2011Note de bas de page 21 et un autre ES/MA a révélé un effet négatif regroupé pour l'ER du vaccin contre l'influenza A(H3N2) lors de la saison grippale 2014-2015Note de bas de page 15.
De plus, la probabilité de contracter une GCL nécessitant des soins médicaux était statistiquement plus élevée lorsque le vaccin contre la grippe saisonnière a été administré sur plusieurs saisons consécutives (trois ou plus), par rapport à la saison en cours seulement; toutefois, les données sur cette exposition étaient limitées (voir Section III.2.3 pour de plus amples renseignements).
III.2.1 Efficacité réelle du vaccin par type et sous-type de grippe
Trois ES/MA ont rapporté une ER du vaccin regroupée stratifiée par type et sous-type de grippe où l'on a comparé les participants vaccinés pendant la saison précédente et la saison en cours avec ceux qui ont été vaccinés seulement pendant la saison en coursNote de bas de page 14Note de bas de page 15Note de bas de page 21.
Influenza A (H1N1) : Les 3 ES/MA ont évalué l'effet de la vaccination répétée sur l'ER du vaccin contre l'influenza A(H1N1). Belongia et al. ont exclu les études qui faisaient état d'une ER de la saison en cours pour la grippe saisonnière antérieure à 2009; par conséquent, les estimations représentent l'ER du vaccin contre l'influenza A(H1N1) pdm09 spécifiquement, tandis que Ramsay et al. et Bartoszko et al. ont regroupé les estimations de l'ER du vaccin contre l'influenza A(H1N1) pendant n'importe quelle saison. Les MA réalisées par Belongia et al. et Ramsay et al. ont évalué l'effet de l'administration du vaccin contre la grippe saisonnière pendant la saison en cours et la saison précédente, tandis que les estimations regroupées rapportées par Bartoszko et al. comprenaient des estimations provenant d'études ayant évalué l'effet de l'administration du vaccin contre la grippe saisonnière pendant la saison en cours et du vaccin saisonnier ou monovalent contre la pandémie pendant la saison précédente. Aucun des ES/MA n'a montré de différence d'ER entre les personnes vaccinées pendant deux saisons consécutives et celles vaccinées seulement pendant la saison en cours pour l'influenza A(H1N1).
Bartoszko et al.Note de bas de page 21 ont constaté que les probabilités non ajustées d'influenza A (H1N1) confirmée en laboratoire nécessitant des soins médicaux étaient statistiquement similaires chez les participants vaccinés pendant deux saisons consécutives et chez ceux qui ont été vaccinés seulement pendant la saison en cours. Ce résultat était cohérent lorsque le RC était calculé à partir des estimations des ECR [RC : 0,86, intervalle de confiance (IC) à 95 % : 0,38 à 1,96 %, I2 : 0 %] et des études d'observation [RC : 0,87, IC à 95 % : 0,67 à 1,12 %, I2 : 46 %]. Ramsay et al.Note de bas de page 15 n'ont trouvé aucune différence statistiquement significative dans l'ER du vaccin ajustée contre l'influenza A(H1N1) lorsque la vaccination antigrippale pendant deux saisons consécutives était comparée à la vaccination limitée à la saison en cours (différence de l'ER du vaccin regroupée : 3 %, IC 95 % : -8 à 13 %, I2 : 0 %). Belongia et al.Note de bas de page 14 n'ont pas directement comparé l'ER entre les deux groupes; toutefois, ils ont rapporté des estimations regroupées similaires (c.-à-d. des IC à 95 % se chevauchant largement) de l'ER du vaccin non ajustée contre l'influenza A(H1N1) pdm09 pour les participants ayant reçu le vaccin antigrippal pendant deux saisons consécutives (ER du vaccin regroupée : 67 %, IC 95 % : 53 à 78 %, I2 : 69 %) et pour les ceux ayant reçu le vaccin antigrippal limité à la saison en cours (ER du vaccin regroupée : 58 %, IC à 95 % : 48 à 67 %, I2 : 0 %).
Influenza A (H3N2) : Les 3 ES/MA ont évalué l'effet de la vaccination saisonnière répétée sur l'ER du vaccin contre l'influenza A(H3N2). Toutefois, les résultats des ES/MA étaient incohérents.
Comme dans le cas de l'influenza A(H1N1), Bartoszko et al. n'ont pas constaté de différence statistiquement significative dans les probabilités non ajustées regroupées de contracter l'influenza A(H3N2) confirmée en laboratoire nécessitant des soins médicaux entre les participants ayant reçu un vaccin antigrippal pendant la saison en cours et la saison précédente et ceux ayant reçu le vaccin limité à la saison en cours [RC (ECR)] : 0,71, IC à 95 % : 0,37 à 1,34 %, I2 : 0 %; RC (observationnel) : 1,09, IC à 95 % : 0,86 à 1,38 %, I2 : 70 %]. Les résultats de l'ER du vaccin regroupée rapportés par Belongia et al. ont montré que si la vaccination antigrippal pendant la saison en cours n'a produit qu'une ER du vaccin statistiquement significative contre l'infection par l'influenza A(H3N2) (ER du vaccin regroupée : 39 %, IC à 95 % : 16 à 55 %, I2 : 73 %), la vaccination antigrippale pendant deux saisons consécutives ne l'a pas produit (ER du vaccin regroupée : 17 %, IC à 95 % : -10 à 37 %, I2 : 86 %). Ramsay et al. ont également constaté une différence statistiquement significative dans l'ER du vaccin ajustée regroupée contre l'influenza A(H3N2) lorsque la vaccination pendant deux saisons consécutives était comparée à la vaccination limitée à la saison en cours (différence d'ER du vaccin regroupée : -20 %, IC à 95 % : -36 à -4 %, I2 : 35 %). Les auteurs ont noté que cela semblait être attribuable aux estimations de la saison grippale 2014-2015 dont les résultats sont examinés plus en détail à la Section III.2.2.
Influenza B : Les 3 ES/MA ont évalué l'effet de la vaccination saisonnière répétée sur l'ER du vaccin contre l'influenza B. Les ES/MA ont obtenu des résultats concordants, ne démontrant aucune différence apparente entre la vaccination pendant deux saisons consécutives et la vaccination limitée à la saison en cours pour l'influenza B. Il n'y avait pas de différence statistiquement significative dans les estimations saisonnières de l'ER du vaccin ajustée contre l'influenza B entre la vaccination pendant deux saisons consécutives et la vaccination limitée à la saison en cours, uniquement dans l'analyse de Ramsay et al., sauf pour l'estimation de l'ER regroupée pour l'ensemble des saisons où la limite supérieure de l'IC était proche de la valeur nulle. (différence d'ER du vaccin regroupée : -11 %, IC à 95 % : -20 à -2 %, I2 : 0 %). De la même façon, Bartoszko et al. n'ont pas trouvé de différence statistique dans les RC regroupés de l'infection par le virus de l'influenza B, comparant la vaccination pendant deux saisons consécutives à la vaccination limitée à la saison en cours, à partir d'ECR ou de plans d'études d'observation [RC (ECR) : 0,85, IC à 95 % : 0,36 à 2,02 %, I2 : 15 %; RC (observationnel) : 1,13, IC à 95 % : 0,85 à 1,50 %, I2 : 52 %]. Belongia et al. ont également signalé une ER du vaccin similaire contre l'influenza B entre la vaccination au cours de saisons consécutives [ER du vaccin regroupée : 55 %, IC à 95 % : 38 à 67 %, I2 : non indiqué (NI)] et la vaccination limitée à la saison en cours (ER du vaccin regroupée : 61 %, IC à 95 % : 43 à 74 %, I2 : NI). Belongia et al. sont les seuls à avoir un ES/MA qui a rapporté une ER du vaccin contre les différentes lignées de l'influenza B; les auteurs ont trouvé une ER du vaccin non ajustée regroupée similaire entre les deux groupes contre l'influenza B/Yamagata [ER du vaccin regroupée (saisons consécutives) : 57 %, IC à 95 % : 47 à 65 %, I2 : NI; ER du vaccin regroupée (saison en cours seulement) : 62 %, IC à 95 % : 46 à 73 %, I2 : NI] et contre B/Victoria [ER du vaccin regroupée (saisons consécutives) : 62 %, IC à 95 % : 45 à 74 %, I2 : NI; ER du vaccin regroupée (saison en cours seulement) : 67 %, IC à 95 % : 41 à 81 %, I2 : NI].
III.2.2 Efficacité réelle du vaccin par saison grippale où des effets répétés ont été observés
Trois des 4 ES/MA ont examiné l'ER du vaccin stratifiée par saison grippale. Belongia et al. ont évalué une ER du vaccin regroupée contre l'influenza A(H1N1) pdm09 en 2010-2011 et en 2013-2014 et contre l'influenza A(H3N2) en 2014-2015. Ramsay et al. ont évalué l'ER du vaccin contre l'influenza A(H1N1) et B de 2010-2011 à 2014-2015, et contre l'influenza A(H3N2) en 2007-2008, 2011-2012, 2012-2013 et 2014-2015; toutefois, toutes les analyses ne comprenaient pas de données provenant de plus d'une étude primaire. Bartoszko et al. ont évalué l'effet de la vaccination répétée sur l'ER du vaccin contre l'influenza A(H3N2) au cours de neuf saisons grippales différentes (2008-2009 à 2016-2017) mais n'ont rapporté une estimation de l'effet que pour la saison 2010-2011 et ont décrit de manière narrative les résultats des autres saisons. Toutes les estimations ont comparé la vaccination pendant deux saisons consécutives à la vaccination limitée à la saison en cours.
Aucun des ES/MA n'a mis en évidence de différences statistiquement significatives en termes d'ER entre la vaccination pendant la saison en cours et la saison précédente et la vaccination limitée à la saison en cours pour l'influenza A(H1N1), A (H3N2) ou B pendant une saison grippale spécifique, à l'exception des deux énumérées ci-dessousNote de bas de page 14Note de bas de page 15Note de bas de page 21 (données non présentées, voir les études originales pour de plus amples renseignements).
2010-2011 : Bartoszko et al. ont réalisé une MA de sous-groupe post-hoc des estimations non ajustées par saison et ont constaté que pendant la saison grippale 2010-2011, la probabilité de contracter l'influenza A(H3N2) confirmée en laboratoire nécessitant des soins médicaux était statistiquement plus élevée chez les personnes vaccinées contre la grippe saisonnière pendant deux saisons consécutives que chez celles vaccinées seulement pendant la saison en cours (RC : 1,98, IC à 95 % : 1,32 à 2,97 %, I2 : 0 %) (estimation I2 reçue sur demande). Belongia et al. et Ramsay et al. n'avaient pas d'estimation de l'ER du vaccin contre l'influenza A(H3N2) pour la saison 2010-2011.
2014-2015 : Ramsay et al. ont constaté que la vaccination répétée était statistiquement et significativement moins efficace contre l'influenza A(H3N2) pendant la saison 2014-2015 que la vaccination limitée à la saison en cours (différence ER du vaccin ajustée regroupée : -54 %, IC à 95 % : -88 à -20 %, I2 : 29 %). Dans Belongia et al., bien que la direction des estimations ponctuelles pour la vaccination pendant deux saisons consécutives et pour la vaccination limitée à la saison en cours diffère, les IC pour les deux estimations se chevauchent largement, au point que l'IC d'une estimation englobe complètement celui de l'autre [ER du vaccin regroupée (consécutive)] : -9 %, IC à 95 % : -26 à 6 %, I2 : NI; ER du vaccin regroupée (en cours seulement) : 36 %, IC à 95 % : -32 à 69 %, I2 : NI]. De plus, les deux IC s'approchaient du zéro, ce qui indique qu'aucun des deux n'a démontré une ER du vaccin statistiquement significative contre l'influenza A(H3N2) nécessitant des soins médicaux au cours de la saison 2014-2015. Bartoszko et al. ont noté dans leur ES/MA qu'ils n'ont pas observé de différence statistiquement significative dans l'ER du vaccin non ajustée regroupée au cours de l'année 2014-2015 chez les vaccinés répétés par rapport à ceux de la saison en cours seulement (RC : 1,34, IC à 95 % : 0,97 à 1,83 %, I2 : 70 %) (estimation de l'effet reçue sur demande); toutefois, la tendance semble suivre celle observée dans les autres ES/MA.
III.2.3 Efficacité réelle chez les personnes vaccinées pendant trois saisons consécutives ou plus
Seul l'ES/MA de Bartoszko et al. a évalué l'ER du vaccin contre la grippe pendant trois saisons consécutives ou plus. Les auteurs ont comparé l'ER du vaccin de la saison en cours des personnes vaccinées consécutivement pendant trois, quatre ou plus, et cinq saisons grippales ou plus, par rapport à celles vaccinées seulement pendant la saison en cours, en regroupant les données de 2 ECR (cinq estimations) et de 3 ou 4 études d'observation (3 à 6 estimations). Dans les études d'observation, les probabilités non ajustées regroupées de GCL nécessitant des soins médicaux chez les personnes vaccinées pendant trois (RC : 1,97, IC à 95 % : 1,14 à 3,39 %, I2 : 60 %), quatre ou plus (RC : 1,40, IC à 95 % : 1,03 à 1,88 %, I2 : 54 %), et cinq ou plus (RC : 1,57, IC à 95 % : 1,23 à 2,02 %, I2 : 5 %) saisons consécutives étaient plus élevées par rapport à celles vaccinées seulement pendant la saison en cours. L'estimation regroupée des 2 ECR n'a pas révélé de différence statistiquement significative dans les probabilités non ajustées de contracter une GCL nécessitant des soins médicaux parmi les personnes ayant été vaccinées pendant trois saisons consécutives par rapport à celles ayant été vaccinées seulement pendant la saison en cours (RC : 1,06, IC à 95 % : 0,65 à 1,75 %, I2 : 0 %).
III.2.4 Efficacité potentielle et efficacité réelle par type de vaccin
Deux études ont examiné l'EP ou l'ER stratifiée selon le type de vaccin contre la grippe saisonnièreNote de bas de page 20Note de bas de page 21. Bartoszko et al. ont regroupé séparément les données de 4 ECR (huit estimations) et de 27 études d'observation (40 estimations) pour évaluer l'ER non ajustée de la vaccination répétée par rapport à la vaccination limitée à la saison en cours pour les vaccins antigrippaux inactivés (VAI). Les auteurs ont constaté que la probabilité de contracter une GCL nécessitant des soins médicaux n'était pas statistiquement différente entre les participants ayant reçu une vaccination répétée par le VAI pendant deux saisons consécutives et ceux qui ont été immunisés par le VAI limité à la saison en cours [RC (ECR) : 0,87, IC à 95 % : 0,59 à 1,30 %, I2 : 28 %; RC (observationnel) : 1,14, IC à 95 % : 0,98 à 1,33 %, I2 : 63 %].
Les auteurs ont également effectué une MA de sous-groupe de 2 ECR (deux estimations) sur l'ER comparative pour le vaccin antigrippal vivant atténué (VAVA) et n'ont pas trouvé de différence statistiquement significative dans les risques de contracter une GCL nécessitant des soins médicaux entre les deux scénarios de vaccination (RC : 1,16, IC à 95 % : 0,58 à 2,32 %, I2 : 69 %).
Morimoto et al. ont évalué l'EP par type de vaccin contre l'infection grippale chez les enfants nécessitant des soins médicaux (six estimations). Les auteurs ont constaté que le risque de contracter une GCL nécessitant des soins médicaux n'était pas significativement différent sur le plan statistique chez les enfants ayant reçu un VAI pendant deux saisons consécutives par rapport à la saison en cours seulement (cas appariés : RR : 1,16, IC à 95 % : 0,28 à 4,76 %, I2 : 0 %; cas non appariés : RR : 1,08, IC à 95 % : 0,27 à 4,37 %, I2 : 0 %). Voir la Section III.2.8 pour la définition de Morimoto et al. des cas appariés et non appariés. Il en était de même pour les cas appariés d'enfants ayant reçu le VAVA (RR : 0,61, IC à 95 % : 0,24 à 1,57 %, I2 : 46,3 %); toutefois, les enfants qui ont reçu des VAVA au cours de deux saisons consécutives et qui avaient une grippe non concordante présentaient un risque significativement plus élevé de GCL nécessitant des soins médicaux (RR : 2,03, IC à 95 % : 1,20 à 3,41 %, I2 : 0 %).
III.2.5 Vaccination de la saison précédente avec un produit monovalent contre la grippe pandémique
Un ES/MA a rapporté des estimations comprenant une immunisation préalable avec un vaccin monovalent contre la grippe pandémiqueNote de bas de page 21. Bartoszko et al. ont regroupé les données de 7 études d'observation (le nombre d'estimations n'a pas été communiqué) pour examiner la probabilité de contracter une GCL saisonnière nécessitant des soins médicaux en comparant les participants ayant reçu le vaccin monovalent contre la grippe pandémique pendant la saison précédente et le vaccin contre la grippe saisonnière pendant la saison en cours par rapport à ceux ayant reçu le vaccin contre la grippe saisonnière limitée à la saison en cours. Aucune différence n'a été détectée entre les deux groupes en ce qui concerne les probabilités non ajustées regroupées (RC : 0,97, IC à 95 % : 0,59 à 1,60 %, I2 : NI). Les auteurs n'ont pas précisé si l'estimation regroupée comprenait les études pour lesquelles les participants avaient reçu un vaccin pandémique monovalent avec ou sans adjuvant.
III.2.6 Efficacité potentielle et efficacité réelle du vaccin par groupe d'âge
Deux ES/MA ont évalué l'EP ou l'ER du vaccin par groupe d'âgeNote de bas de page 20Note de bas de page 21. Dans l'ensemble, il ne semble pas y avoir de différence significative dans l'ER du vaccin en fonction du groupe d'âge.
Deux MA de sous-groupes distinctes comparant l'ER du vaccin par groupe d'âge ont été réalisées par Bartoszko et al. qui représentait le seul ES/MA à signaler l'ER du vaccin stratifiée par âge. L'une d'entre elles était une MA de sous-groupe de 14 études d'observation (20 estimations) qui comparait les ER non ajustées de la vaccination au cours de saisons consécutives et de la vaccination limitée à la saison en cours pour les enfants (de 17 ans ou moins), les adultes (de 18 à 64 ans) et les adultes âgés (de 65 ans et plus) [RC (enfants) : 0,93, IC à 95 % : 0,51 à 1,69 %, I2 : 78 %; RC (adultes) : 0,95, IC à 95 % : 0,75 à 1,21 %, I2 : 34 %; RC (adultes âgés) : 0,78, IC à 95 % : 0,61 à 1,01 %, I2 : 0 %], tandis que l'autre MA de sous-groupe portant sur 4 ECR (huit estimations) a comparé l'ER du vaccin non ajustée pour les deux scénarios de vaccination chez les enfants et les adultes [RC (enfants) : 1,07, IC à 95 % : 0,63 à 1,80 %, I2 : 59 %; RC (adultes) : 0,79, IC à 95 % : 0,50 à 1,24 %, I2 : 0 %]. Les résultats de ces MA de sous-groupes ont montré que la probabilité d'une GCL nécessitant des soins médicaux n'était pas significativement différente sur le plan statistique entre les deux scénarios de vaccination pour toutes les tranches d'âge évaluées par les estimations regroupées des ECR ou des études d'observation.
Morimoto et al. ont évalué l'EP contre toute forme grippale nécessitant des soins médicaux constatée chez les enfants (six études, six estimations) et chez les adultes de 30 à 60 ans (une étude, trois estimations). Les auteurs ont constaté que le risque de contracter une GCL nécessitant des soins médicaux n'était pas significativement différent sur le plan statistique chez les enfants ou les adultes qui avaient été vaccinés contre la grippe pendant deux saisons consécutives par rapport à ceux qui avaient été vaccinés seulement pendant la saison en cours (enfants : RR : 1,31, IC à 95 % : 0,79 à 2,16 %, I2 : 37,6 %; adultes : RR : 1,12, IC à 95 % : 0,65 à 1,92 %, I2 : 19,1 %).
III.2.7 Efficacité réelle du vaccin selon la comorbidité sous-jacente
Une MA d'un sous-groupe de 11 études d'observation (12 estimations) réalisée par Bartoszko et al. a révélé qu'il n'y avait pas de différence statistiquement significative dans les probabilités non ajustées de contracter une GCL nécessitant des soins médicaux entre la vaccination pendant deux saisons consécutives et la vaccination limitée à la saison en cours dans les sous-groupes sans comorbidités signalées (RC : 1,06, IC à 95 % : 0,59 à 1,93 %, I2 : 81 %) ou dans les sous-groupes présentant une ou plusieurs comorbidités déclarées (RC : 0,95, IC à 95 % : 0,69 à 1,54 %, I2 : 63 %). Il y avait une hétérogénéité importante dans les deux estimations. Aucun autre ES/MA n'a évalué l'EP ou l'ER du vaccin par comorbidité sous-jacente.
III.2.8 Efficacité potentielle et efficacité réelle selon l'appariement du vaccin
Bartoszko et al. ont réalisé une MA d'un sous-groupe de 5 ECR (neuf estimations) et une MA d'un sous-groupe de 27 études d'observation (39 estimations) pour évaluer l'ER comparative de la vaccination répétée contre la grippe dans des scénarios où les souches grippales en circulation pendant la saison grippale en cours correspondaient aux souches vaccinales, et dans des scénarios où elles ne correspondaient pas aux souches vaccinales. La probabilité de contracter une GCL nécessitant des soins médicaux ne différait pas significativement entre les personnes vaccinées pendant des saisons consécutives et celles vaccinées seulement pendant la saison en cours, pour les saisons grippales où le vaccin correspondait aux souches en circulation [RC (ECR)] : 0,73, IC à 95 % : 0,42 à 1,26 %, I2 : 0 %; RC (observationnel) : 1,00, IC à 95 % : 0,80 à 1,26 %, I2 : 46 %] ou lorsque le vaccin ne correspond pas aux souches en circulation [RC (ECR) : 0,96, IC à 95 % : 0,61 à 1,51 %, I2 : 50 %; RC (observationnel) : 1,26, IC à 95 % : 1,00 à 1,58 %, I2 : 73 %]. La concordance et la non-concordance des vaccins ont été déterminées sur la base de ce qui avait été rapporté dans l'étude primaire et, en l'absence de rapport, sur la base du jugement des auteurs des ES/MA. Toutefois, les auteurs n'ont pas indiqué la façon dont l'appariement et le non-appariement des vaccins ont été définis; ces résultats devraient donc être interprétés avec prudence.
Morimoto et al. ont évalué l'EP en fonction de l'appariement des vaccins chez les enfants et chez les adultes. Les auteurs ont défini les cas comme étant appariés ou non appariés à la souche vaccinale sur la base de la caractérisation antigénique par le test d'inhibition de l'hémagglutinine. On a considéré que le vaccin correspondait à la souche en circulation si elle était du même sous-type (influenza A) ou de la même lignée (influenza B) et si elle était antigéniquement similaire à la souche vaccinale. Les résultats d'une MA ont montré que le risque de contracter une GCL nécessitant des soins médicaux n'était pas statistiquement différent des cas appariés chez les enfants (RR : 0,64, IC à 95 % : 0,33 à 1,22 %, I2 : 17,3 %) ou des cas non appariés chez les adultes (RR : 1,35, IC à 95 % : 0,77 à 2,38 %, I2 : 0 %); toutefois, tel qu'indiqué à la Section III.2.4, les enfants qui avaient été vaccinés pendant deux saisons consécutives étaient davantage exposés au risque d'infection grippale causée par un virus grippal non contenu dans le vaccin que ceux qui avaient été vaccinés seulement pendant la saison en cours (RR : 2,04, IC à 95 % : 1,29 à 3,22 %, I2 : 0 %). Aucune MA n'a été réalisée pour les cas appariés chez les adultes, car une seule estimation était disponibleNote de bas de page 20.
III.3 Données probantes sur l'efficacité réelle de la vaccination répétée par rapport à la vaccination limitée à la saison précédente
Deux des 4 ES/MA ont évalué l'ER de la vaccination répétée par rapport à l'ER de la vaccination limitée à la saison précédente. Ramsay et al. ont réalisé 3 MA, stratifiées par type de grippe, pour examiner la différence de l'ER ajustée entre la vaccination pendant la saison en cours et les saisons précédentes et la vaccination limitée à la saison précédente. Pour l'influenza A(H1N1), les données regroupées de 13 études d'observation (16 estimations) ont montré une ER ajustée statistiquement plus élevée chez les personnes vaccinées au cours des deux saisons grippales les plus récentes par rapport à la vaccination limitée à la saison précédente (différence d'ER du vaccin regroupée : 25 %, IC à 95 % : 14 à 35 %, I2 : 0 %). Des résultats similaires ont également été présentés pour l'influenza B, sur la base des données regroupées de 10 études d'observation (13 estimations) (différence d'ER du vaccin regroupée : 18 %, IC à 95 % : 3 à 33 %, I2 : 26 %).
Toutefois, les données regroupées de 11 études d'observation (14 estimations) n'ont révélé aucune différence statistiquement significative dans l'ER du vaccin ajustée contre l'influenza A(H3N2) entre les deux scénarios de vaccination (différence d'ER du vaccin regroupée : 7 %, IC à 95 % : -7 à 21 %, I2 : 4 %). Les estimations de l'ER du vaccin issues des MA réalisées par Belongia et al. ont montré des estimations de l'ER similaires pour la vaccination au cours de saisons consécutives et pour la vaccination limitée à la saison précédente pour l'influenza A(H1N1) [ER du vaccin regroupée (consécutive) : 67 %, IC à 95 % : 53 à 78 %, I2 : 69 %; ER du vaccin regroupée (précédente seulement) : 46 %, IC à 95 % : 29 % à 59 %, I2 : 40 %], influenza A (H3N2) [ER du vaccin regroupée (consécutive) : 17 %, IC à 95 % : -10 % à 37 %, I2 : 86 %; ER du vaccin regroupée (précédente seulement) : 9 %, IC à 95 % : -10 à 25 %, I2 : 48 %], et l'influenza B [ER du vaccin regroupée (consécutive) : 55 %, IC à 95 % : 38 à 67 %, I2 : NI; ER du vaccin regroupée (précédente seulement) : 25 %, IC à 95 % : 4 à 42 %, I2 : NI].
III.4 Données probantes sur l'efficacité réelle de la vaccination répétée par rapport à l'absence de vaccination
Deux ES/MA ont rapporté une ER de la vaccination répétée par rapport à l'absence de vaccination. L'ES/MA mené par Belongia et al. a rapporté l'ER regroupée de la vaccination répétée contre la grippe en se reportant aux personnes qui n'ont pas été vaccinées à la fois pendant la saison en cours et la saison précédente. D'après une MA des estimations non ajustées, la vaccination pendant la saison en cours et la saison précédente a montré une ER du vaccin statistiquement significative contre l'influenza A(H1N1) (ER du vaccin regroupée : 67 %, IC à 95 % : 53 à 78 %, I2 : 69 %) et contre l'influenza B (ER du vaccin regroupée : 55 %, IC à 95 % : 38 à 67 %, I2 : NI). Toutefois, la vaccination pendant la saison en cours et la saison précédente n'a pas produit une ER du vaccin statistiquement significative contre l'influenza A(H3N2) (ER du vaccin regroupée : 17 %, IC à 95 % : -10 à 37 %, I2 : 86 %). Une MA distincte de trois études ayant évalué l'ER au cours de saisons grippales spécifiques a révélé que la vaccination répétée n'était inefficace qu'au cours de la saison grippale 2014-2015. Les auteurs ont donc conclu que la faible ER pendant cette saison était à l'origine de l'absence globale d'ER du vaccin statistiquement significative contre l'influenza A(H3N2).
Bartoszko et al. ont conclu que, sur la base des données regroupées de 5 ECR (neuf estimations) et de 28 études d'observation (40 estimations), la vaccination pendant deux saisons consécutives était statistiquement efficace contre toute souche grippale lorsque l'absence de vaccination au cours de l'une ou l'autre saison était utilisée comme référence [ECR regroupées (ECR)] : 71 %, IC à 95 % : 62 à 78 %, I2 : NI; ER du vaccin regroupée (observationnelle) : 41 %, IC à 95 % : 30 à 51 %, I2 : NI].
IV. Discussion
Pour la plupart des estimations incluses dans les ES/MA, il n'y avait pas de différence significative dans l'EP ou l'ER entre la vaccination pendant deux saisons consécutives et la vaccination limitée à la saison en cours. Lorsqu'elles sont stratifiées par saison, la majorité des estimations ont démontré qu'il n'y avait pas de différence significative dans l'ER pour la vaccination pendant deux saisons consécutives et la vaccination limitée à la saison en cours. Toutefois, il y avait deux exceptions. Notamment, deux ES/MA ont démontré que la vaccination répétée avait une ER statistiquement significative plus faible que la vaccination limitée à la saison en cours; l'un des ES/MA a trouvé une ER du vaccin plus faible contre l'influenza A(H3N2) en 2010-2011Note de bas de page 21, et l'autre ES/MA a trouvé une ER du vaccin plus faible contre l'influenza A(H3N2) en 2014-2015 et contre l'influenza B, mais seulement dans l'estimation globale regroupéeNote de bas de page 15. Au cours de la saison grippale 2014-2015 de l'hémisphère Nord, le composant du vaccin contre l'influenza A(H3N2) était inchangée par rapport à la saison 2013-2014Note de bas de page 22 et ne correspondait pas à la souche circulante, ce qui constitue une situation où la vaccination répétée est prédite par l'hypothèse selon laquelle la distance antigénique interfère négativement avec l'ER du vaccinNote de bas de page 7Note de bas de page 11. Toutefois, les auteurs de cette étude ont noté que leur estimation était largement déterminée par la saison 2014-2015. La saison grippale 2010-2011 a été la première saison pandémique post-2009 et contenait également un composant vaccinal contre l'influenza A(H3N2) différent de celui du vaccin de l'hémisphère Nord de 2009Note de bas de page 22. Par conséquent, il est important de considérer que des facteurs autres que les composants du virus vaccinal peuvent affecter les estimations de l'ER du vaccin.
La vaccination pendant la saison en cours semblait offrir la meilleure protection contre la grippe, indépendamment du statut vaccinal de la saison précédente, puisque la vaccination limitée à la saison en cours et la vaccination pendant deux saisons consécutives étaient systématiquement plus efficaces que la vaccination limitée à la saison précédente et l'absence de vaccination pendant l'une ou l'autre saison. Le seul cas où la vaccination pendant deux saisons consécutives n'a pas été significativement plus efficace que la vaccination limitée à la saison précédente a été en 2014-2015 contre l'influenza A(H3N2). Il n'a pas été possible de tirer des conclusions fermes sur la différence entre la vaccination au cours de saisons consécutives et la vaccination limitée à la saison précédente à partir des comparaisons indirectes, car bon nombre des IC à 95 % pour ces estimations de l'ER du vaccin se chevauchaient légèrementNote de bas de page 23.
Le seul ES/MA qui a évalué l'effet de la vaccination pendant trois saisons grippales consécutives ou plus a montré que, sur la base de MA d'études d'observation, la probabilité de contracter une GCL nécessitant des soins médicaux était plus élevée chez les personnes vaccinées pendant trois, quatre ou plus, et cinq saisons grippales consécutives ou plus, par rapport à celles vaccinées seulement pendant la saison en cours. Toutefois, ces estimations reposaient sur un petit nombre d'études et n'ont pas été ajustées pour tenir compte des facteurs de confusion, ce qui peut être important, car il pourrait y avoir d'importantes différences sous-jacentes entre les personnes qui reçoivent le vaccin antigrippal chaque année et celles qui ne le reçoivent pas régulièrement (p. ex., les personnes à haut risque d'infection grippale pourraient être plus susceptibles de recevoir le vaccin chaque année et de consulter un médecin pour un syndrome grippal). Par conséquent, les données probantes actuelles sont insuffisantes pour tirer des conclusions fermes sur l'effet de la vaccination pendant trois saisons consécutives ou plus.
Une étude récente de Kwong et al. qui n'a été prise en compte par aucun des ES/MA inclus en raison de la récence de la publication, a évalué l'effet de la vaccination répétée contre la grippe chez les adultes plus âgés au cours de 10 saisons précédentes au CanadaNote de bas de page 21. Les auteurs de cette étude ont constaté une tendance statistiquement significative à la diminution de l'ER du vaccin pour les personnes vaccinées pendant la saison en cours, à mesure que le nombre de vaccinations précédentes augmentait. Toutefois, le contraire est vrai pour les personnes non vaccinées pendant la saison en cours — plus le nombre de vaccinations précédentes augmentait, plus la protection pendant la saison en cours augmentait également, ce qui implique une protection résiduelle croissante des vaccinations précédentes. Toutefois, quel que soit le nombre de vaccinations précédentes, la vaccination pendant la saison en cours a apporté un certain bénéfice et s'est révélée supérieure à la non-vaccination. Cela correspond aux résultats présentés dans cet aperçu pour les études qui ont évalué l'ER du vaccin sur une période plus courte.
Une hétérogénéité notable a été constatée pour certaines mesures d'effet regroupées incluses dans cet aperçu, ce qui indique la présence de facteurs sous-jacents importants pouvant rendre la MA des données inappropriée. Ce résultat était attendu pour les estimations qui regroupaient les données de plusieurs saisons grippales, car l'ER du vaccin est très variable d'une année à l'autre. Cela a été démontré par de multiples ES/MA, car les estimations de tous les ES/MA pour des saisons grippales spécifiques avaient tendance à présenter peu ou pas d'hétérogénéité, ce qui suggère que les caractéristiques spécifiques à la saison peuvent expliquer la majeure partie de l'hétérogénéité dans d'autres sous-analyses. Toutefois, malgré les différences saisonnières qui expliquent une partie de l'hétérogénéité présente, une hétérogénéité accrue existe toujours. Cela pourrait s'expliquer en partie par des différences dans l'épidémiologie locale, d'autant plus que tous les ES/MA ont regroupé des estimations provenant de multiples pays. Les souches grippales en circulation peuvent différer d'un endroit à l'autre, et pas seulement d'un hémisphère à l'autre. Par conséquent, les estimations qui regroupent les données de nombreux pays différents pourraient présenter une hétérogénéité importante en raison des contextes variés.
De nombreux autres facteurs peuvent également avoir des répercussions sur l'ER du vaccin contre la grippe, notamment l'appariement des souches vaccinales aux souches en circulationNote de bas de page 24, l'exposition initiale au virus grippalNote de bas de page 25, les mutations des virus vaccinaux qui s'adaptent à l'œufNote de bas de page 26Note de bas de page 27 et possiblement d'autres facteurs inconnus à l'heure actuelle. De plus, ces facteurs ont probablement des interactions complexes entre eux, comme le suggère un article récent de Skowronski et al.Note de bas de page 28. La mesure dans laquelle la vaccination répétée et ces autres facteurs affectent l'ER n'est pas entièrement comprise et varie d'une saison à l'autre. Il est donc extrêmement difficile de prévoir suffisamment longtemps avant la prochaine saison grippale pour modifier la politique vaccinale ou les pratiques administratives. Par conséquent, une meilleure compréhension des mécanismes immunologiques sous-jacents et des facteurs affectant la réponse immunitaire à la vaccination antigrippale est nécessaire pour améliorer le développement et les programmes de vaccination antigrippale.
Enfin, il demeure important d'aborder les facteurs programmatiques tels que l'éthique, l'équité, la faisabilité et l'acceptabilitéNote de bas de page 29 au fur et à mesure que des données probantes émergeront sur ce sujet. Les directives sur la vaccination antigrippale maintiennent les dimensions éthiques fondamentales de la santé publique en visant à prévenir les maladies futures mais elles doivent être données dans le contexte difficile de paramètres qui varient d'une saison à l'autre et qui sont très problématiques à prévoir (comme l'appariement ou l'inadéquation entre le vaccin et la souche circulante et la sévérité clinique variable de la maladie). Il est également important de tenir compte du fait que l'ER peut avoir un impact significatif sur l'acceptabilité du vaccinNote de bas de page 30, ce qui peut à son tour affecter l'adoption et l'impact d'un programme de vaccination. Par conséquent, malgré l'interférence négative qui se produit de manière incohérente dans la littérature résumée, le potentiel de réduction de l'ER du vaccin est préoccupant. Au fur et à mesure que de nouveaux produits vaccinaux seront ajoutés et que des données probantes émergeront, y compris les nouvelles études examinant l'effet de l'immunité préexistante sur les réponses au vaccin antigrippaNote de bas de page 31Note de bas de page 32Note de bas de page 33, le CCNI continuera de surveiller les données probantes sur ce phénomène et publiera de nouvelles directives si nécessaire.
IV.1 Limites
Cet aperçu a été conçu pour évaluer les effets de la vaccination répétée contre la grippe sur l'ER, l'EP et l'immunogénicité du vaccin dans le but de fournir des conseils sur la vaccination annuelle contre la grippe. Tous les ES/MA inclus contenaient un ES et une MA des effets de la vaccination répétée contre la grippe sur l'EP ou l'ER, mais ne fournissaient pas d'évaluation de l'immunogénicité. Dans cette optique, des données probantes supplémentaires sont nécessaires pour que les résultats de cet aperçu déterminent l'effet de la vaccination répétée au fil du temps et au cours de plusieurs saisons grippales. Toutefois, le regroupement des données entre les saisons et les différents lieux géographiques, comme l'ont fait les ES/MA inclus dans cet aperçu, est insuffisant pour déterminer les causes potentielles et les mécanismes qui sous-tendent l'effet de la vaccination répétée sur l'ER, et devrait donner des estimations présentant une grande hétérogénéité, puisque l'ER du vaccin est affectée par des variables qui changent souvent d'une saison à l'autre (p. ex., la souche circulante, la concordance des vaccins, etc.).
Les ES/MA inclus dans l'examen comportaient tous des questions de recherche similaires, ainsi que des critères d'inclusion et d'exclusion; par conséquent, il y avait un chevauchement important (46 %) dans les études primaires incluses pour la synthèse des données probantes dans les ES/MA. Par conséquent, bien que les résultats semblent tirer des données de nombreuses études et populations, les ES/MA ont utilisé une grande partie des mêmes données pour produire les estimations regroupées. Malgré les différentes méthodes utilisées par les ES/MA pour regrouper les données entre les études (ER du vaccin, différence d'ER du vaccin, RR et RC), les résultats et les conclusions des ES/MA étaient généralement cohérents entre eux, ce qui renforce la fiabilité des conclusions tirées de cette synthèse des données probantes. Les ES/MA étaient de bonne qualité d'après AMSTAR 2. Les études primaires incluses dans les ES/MA étaient aussi généralement de bonne qualité; le RdB était faible pour les études d'observation qui constituaient la majorité de la base de données probantes. Toutefois, les auteurs ont noté un RdB élevé pour les ECR. Des MA distinctes ont été réalisées pour les estimations provenant des ECR et des études d'observation. Les conclusions pour la plupart des résultats étaient similaires; par conséquent, il ne semble pas que le RdB élevé des ECR inclus ait affecté de manière significative les résultats des MA.
Les ES/MA de Bartoszko et al. et de Morimoto et al. comprenaient des études confirmant l'infection par le virus de la grippe à l'aide de la RT-PCR, ce qui représente l'étalon de référence pour la détection du virus de la grippe en raison de sa sensibilité et de sa spécificité accruesNote de bas de page 34Note de bas de page 35 mais aussi des études portant sur une infection par le virus de la grippe confirmée par des méthodes de laboratoire autres que la RT-PCR. Bartoszko et al. ont inclus ces études après avoir déterminé que leur inclusion ne modifiait pas de manière significative les estimations de l'effet, ce qui atténue certaines des préoccupations liées à l'inclusion des études qui ont détecté le virus de la grippe par d'autres méthodes de laboratoire pour leur ES/MA. Il convient de noter que les études utilisant des méthodes de laboratoire autres que la RT-PCR représentaient une faible proportion du nombre total d'études incluses (14 %).
Cet aperçu comprenait les ES/MA qui présentaient des estimations de l'effet regroupées pour des comparaisons directes (différence regroupée d'ER du vaccin, RR, RC) et des comparaisons indirectes, comme la comparaison d'estimations d'ER du vaccin regroupées distinctes pour différents scénarios de vaccination qui utilisaient comme référence les personnes non vaccinées pendant l'une ou l'autre saison. Puisque l'objectif de cet aperçu était de déterminer les effets de la vaccination répétée par rapport à la vaccination limitée à la saison en cours, à la vaccination limitée à la saison précédente ou à l'absence de vaccination, une estimation de l'effet provenant d'une comparaison directe est plus appropriée pour répondre à la question de recherche de cet aperçu qu'une comparaison indirecte, car les estimations dont les IC se chevauchent légèrement pourraient encore être significativement différentesNote de bas de page 23.
La façon dont certains sous-groupes ont été évalués et le choix des sous-groupes qui n'ont pas été évalués ont tous deux présenté des limitations particulières. Bartoszko et al. ont évalué l'ER du vaccin antigrippal en fonction de la concordance ou de la non-concordance des vaccins mais n'ont pas précisé la façon dont la concordance ou la non-concordance avait été définie, ce qui présente des difficultés pour l'interprétation de ces résultats. De plus, aucun des ES/MA n'a évalué l'EP ou l'ER des produits antigrippaux avec adjuvant, à haute dose, à base de cellules ou d'œufs, qui sont tous des formulations différentes de vaccins antigrippaux dont l'utilisation est autorisée au Canada.
V. Recommandations
1. Le CCNI continue de recommander que le vaccin contre la grippe saisonnière soit offert chaque année à toute personne de 6 mois et plus qui ne présente aucune contre-indication au vaccin, quel que soit son statut vaccinal contre la grippe des saisons précédentes. (Forte recommandation du CCNI)
- Le CCNI conclut qu'il existe des données probantes suffisantes pour recommander la vaccination annuelle contre la grippe, qu'une personne ait reçu ou non le vaccin contre la grippe saisonnière au cours des saisons précédentes (données probantes de catégorie B).
Résumé des données probantes
- La vaccination répétée au fil des saisons, y compris la saison en cours, était systématiquement plus efficace que l'absence de vaccination pendant la saison en cours.
- En général, les données probantes ne montrent pas de différence significative ou de tendance prévisible dans l'EP ou l'ER entre la vaccination pendant deux saisons consécutives et la vaccination limitée à la saison en cours.
- Parmi toutes les saisons examinées dans de nombreuses études, seules deux saisons grippales ont indiqué que l'ER de la vaccination pendant des saisons consécutives était significativement plus faible sur le plan statistique que la vaccination limitée à la saison en cours. Ces saisons notables ont été l'influenza A(H3N2) en 2010-2011Note de bas de page 21 et l'influenza A(H3N2) en 2014-2015Note de bas de page 15. Ces résultats n'étaient pas statistiquement significatifs dans tous les ES/MA qui ont évalué l'ER du vaccin au cours de ces deux saisons; toutefois, une tendance à la baisse de l'ER pour la vaccination répétée était constante pour la saison 2014-2015 dans toutes les étudesNote de bas de page 14Note de bas de page 21.
- Les données probantes sur les effets de la vaccination répétée pendant trois saisons consécutives ou plus étaient limitées et sont insuffisantes pour tirer des conclusions fermes à l'heure actuelle.
- Compte tenu de l'interaction complexe entre l'empreinte immunitaire (telle que les expositions antérieures par la vaccination et l'infection naturelle), les types de virus en circulation et les caractéristiques individuelles, il n'est pas actuellement possible ni justifié de modifier les programmes annuels existants de vaccination antigrippale pour tenir compte des effets d'interférence négatifs ou positifs potentiels liés à la vaccination répétée contre la grippe au fil des saisons.
VI. Priorités de recherche
Il est recommandé de poursuivre la recherche afin d'éclaircir les points suivants :
Priorités de recherche nouvelles et émergents
Une évaluation plus poussée de l'ER du vaccin stratifiée par des caractéristiques en plus du type et du sous-type de souche grippale permettrait de mieux déterminer quand les effets de la vaccination répétée contre la grippe devraient être pris en compte et quelles populations spécifiques peuvent être touchées.
- Poursuite de l'évaluation des effets de la vaccination antigrippale répétée à long terme sur l'ER du vaccin pendant plus de deux saisons consécutives.
- Évaluation plus approfondie des effets de la vaccination répétée contre la grippe sur l'ER du vaccin stratifiée par groupe d'âge et type de vaccin.
- Étude des effets de la vaccination répétée contre la grippe sur les complications sévères liées à la grippe, comme l'hospitalisation et le décès.
- Évaluation des effets de la vaccination répétée contre la grippe qui tient compte de l'exposition antérieure à la grippe par la vaccination et (ou) l'infection naturelle.
- Études plus poussées des mécanismes immunologiques qui sous-tendent les effets de la vaccination répétée contre la grippe sur l'ER du vaccin, notamment l'hypothèse de la distance antigénique et l'empreinte immunologique.
Tableaux supplémentaires
| Force de la recommandation du CCNI D'après les facteurs ne se limitant pas à la force des données probantes (p. ex., besoins en matière de santé publique) |
Catégorie des données probantes Selon l'évaluation de l'ensemble des données probantes |
|---|---|
Forte
|
|
Discrétionnaire
|
|
| Détails de l'étude | Résumé | |||||
|---|---|---|---|---|---|---|
| Étude | Vaccin | Plan de l'étude | Participants | Résumé des principales conclusions | Niveau des données probantes | Qualité |
Bartoszko JJ, McNamara IF, Aras OA, Hylton DA, Zhang YB, Malhotra D, Hyett SL, Morassut RE, Rudziak P, Loeb M. Does consecutive influenza vaccination reduce protection against influenza: A systematic review and meta-analysis. Vaccine. Juin 2018 7;36(24):3434-44.Note de bas de page 21 |
Vaccin contre la grippe saisonnière |
ES/MA PICO : Voir les Tableaux 1 et 2 Inclus : ECR, quasi-ECR, études d'observation Saisons grippales : 23 saisons entre 1983-1994 et mi- 2016-2017 Financement : Subvention de la Fondation des Instituts de recherche en santé du Canada |
Nombre de participants (ECR) : 11 987 Nombre de participants (observationnel) : 28 627 Tranche d'âge : tous les âges |
Principales conclusions : Le RC a été évalué en déterminant les probabilités non ajustées de contracter une infection grippale, confirmée par un test de laboratoire quelconque, entre la vaccination au cours de saisons consécutives et la vaccination limitée à la saison actuelle. Toute souche (ECR) Toute souche (Obs) A(H1N1) (ECR) A(H1N1) (Obs) A(H3N2) (ECR) A(H3N2) (Obs) B (ECR) B (Obs) L'ER de la vaccination répétée a également été évaluée en regroupant l'ER du vaccin non ajustée contre l'infection grippale, confirmée par tout RT-PCR. La catégorie de référence était celle des personnes non vaccinées pendant la saison en cours et les saisons précédentes : Saison en cours et précédente (ECR) Saison en cours et précédente (Obs) Saison en cours seulement (ECR) Saison en cours seulement (Obs) MA de sous-groupes : Protection contre toute souche grippale par type de vaccin : VAI (ECR) VAI (Obs) VAVA (ECR) Probabilité non ajustée d'une infection grippale, confirmée par tout test de laboratoire, entre l'immunisation par le vaccin monovalent contre la grippe pandémique pendant la saison précédente et le vaccin contre la grippe saisonnière pendant la saison en cours, par rapport à la vaccination limitée à la saison en cours : Observation Protection contre toute souche grippale selon l'âge : Âge 17 ans ou moins (ECR) Âge 17 ans ou moins (Obs) Âge 18–64 ans (ECR) Âge 18–64 ans (Obs) Âge 65 ans ou plus (Obs) Protection contre toute souche grippale selon l'appariement des vaccins : Appariement (ECR) Appariement (Obs) Non-Appariement (ECR) Non-Appariement (Obs) Protection contre toute souche grippale selon la présence d'une comorbidité sous-jacente : Aucune comorbidité indiquée (Obs) Au moins 1 comorbidité indiquée (Obs) Protection contre toute souche grippale pour les personnes vaccinées pendant trois saisons consécutives par rapport à la saison en cours seulement: ECR Obs Protection contre toute souche grippale pour les personnes vaccinées pendant quatre saisons consécutives ou plus par rapport à la saison en cours seulement : Obs Protection contre toute souche grippale pour les personnes vaccinées pendant cinq saisons consécutives ou plus par rapport à la saison en cours seulement : Obs Protection contre l'influenza A(H3N2) en 2010-2011 : Obs Les risques d'infection par l'influenza A(H3N2) n'étaient pas significativement différents sur le plan statistique entre la vaccination répétée et la vaccination limitée à la saison en cours pour toute autre saison grippale spécifique. |
ES/MA |
Voir le Tableau 3. |
Morimoto N, Takeishi K Change in the efficacy of influenza vaccination after repeated inoculation under antigenic mismatch: A systematic review and meta-analysis. Vaccine. Février 2018 8;36 (7):949-57Note de bas de page 20 |
Vaccin contre la grippe saisonnière |
ES/MA PICO : Voir les Tableaux 1 et 2 Inclus : ECR Saisons grippales (ES) : 22 saisons entre 1972-1973 et 2010-2011 Saisons grippales (MA) : 9 saisons entre 1973-1974 et 2009-2010 Financement : L'étude n'a pas été financée |
Nombre d'observations (MA) : 4 541 Tranche d'âge : tous les âges |
Principales conclusions : L'EP a été évaluée en calculant le RR d'infection grippale nécessitant des soins médicaux pour la vaccination pendant deux saisons consécutives par rapport à la vaccination limitée à la saison en cours. La grippe nécessitant des soins médicaux a été définie comme une maladie respiratoire aiguë (définie par la présence de fièvre, de toux, de maux de tête, de myalgies, de maux de gorge ou d'autres symptômes respiratoires), en plus de la confirmation en laboratoire du virus de la grippe. L'infection grippale a été confirmée par RT-PCR ou par sérologie et (ou) culture. Efficacité potentielle contre toute forme grippale nécessitant des soins médicaux : Enfants Adultes MA de sous-groupes : Efficacité potentielle selon l'appariement des vaccins* contre toute grippe nécessitant des soins médicaux : Appariés (Enfants) Appariés (Adultes) Non appariés (Children) Non appariés (Adultes) *L'appariement antigénique est défini comme étant un vaccin correspondant à des souches circulantes du même sous-type et similaire sur le plan antigénique. Efficacité potentielle selon le type et l'appariement des vaccins* contre toute grippe nécessitant des soins médicaux chez les enfants** : Appariés (VAI) Appariés (VAVA) Non appariés (VAI) Non appariés (VAVA) * L'appariement antigénique est défini comme étant un vaccin correspondant à des souches circulantes du même sous-type et similaire sur le plan antigénique. ** Le nombre d'estimations incluses dans l'analyse n'a pas été communiqué pour cette mesure. |
ES/MA |
Voir le Tableau 3. |
Ramsay LC, Buchan SA, Stirling RG, Cowling BJ, Feng S, Kwong JC, Warshawsky BF. The impact of repeated vaccination on influenza vaccine effectiveness: A systematic review and meta-analysis. BMC Med, 2019;17(1):9. Retraction of: Ramsay LC, Buchan SA, Stirling RG. The Impact of Repeated Vaccination on Influenza Vaccine Effectiveness: A Systematic Review and Meta-Analysis. BMC Med. 2017;15(1):159Note de bas de page 15 |
Vaccin contre la grippe saisonnière |
ES/MA PICO : Voir les Tableaux 1 et 2 Inclus : Études d'observation Saisons grippales : 2004-2005 à 2014-2015 Financement : L'étude n'a pas été financée |
Nombre de participants : NI Tranche d'âge : tous les âges |
Principales conclusions : L'ER du vaccin a été évaluée en déterminant la différence de l'ER du vaccin ajustée contre l'infection grippale confirmée par tout RT-PCR, entre : L'ER pour la vaccination pendant deux saisons consécutives moins l'ER pour la vaccination limitée à la saison en cours : A(H1N1) A(H3N2) B L'ER pour la vaccination pendant deux saisons consécutives moins l'ER pour la vaccination limitée à la saison précédente : A(H1N1) A(H3N2) B Résultats des sous-groupes : L'ER du vaccin contre l'influenza A (H3N2) pour la vaccination pendant deux saisons consécutives moins l'ER pour la vaccination limitée à la saison en cours en 2014-2015 A(H3N2) La vaccination pendant deux saisons consécutives était aussi efficace que la vaccination limitée à la saison en cours dans toutes les autres analyses regroupées spécifiques à la saison. |
ES/MA |
Voir le Tableau 3. |
Belongia EA, Skowronski DM, McLean HQ, Chambers C, Sundaram ME, De Serres G. Repeated annual influenza vaccination and vaccine effectiveness: Review of evidence. Expert Rev Vaccines. 2017;16(7):723-36Note de bas de page 14 |
Vaccin contre la grippe saisonnière |
ES/MA PICO : Voir les Tableaux 1 et 2 Inclus : cas-témoins à test négatif, cas-témoins, cohorte, ECR Saisons grippales : Financement : L'étude n'a pas été financée |
Nombre de participants : NI Tranche d'âge : au moins 2 ans |
Principales conclusions : L'ER du vaccin a été évaluée en regroupant l'ER du vaccin non ajustée contre l'infection grippale confirmée par tout RT-PCR. La catégorie de référence pour tous les scénarios suivants était celle des personnes non vaccinées pendant la saison en cours et les saisons précédentes : L'ER pour la vaccination pendant deux saisons consécutives : A(H1N1)pdm09 A(H3N2) B B/Yam B/Vic L'ER pour la vaccination limitée à la saison en cours : A(H1N1)pdm09 A(H3N2) B B/Yam B/Vic L'ER pour la vaccination limitée à la saison précédente : A(H1N1)pdm09 A(H3N2) B B/Yam B/Vic |
ES/MA |
Voir le Tableau 3. |
Abréviations – IC : intervalle de confiance, VAI : vaccin antigrippal inactivé, VAVA : vaccin antigrippal inactivé, MA : méta-analyse, NI : non indiqué, obs. : étude d'observation, RC : rapport de cote, PICO : « population, intervention, comparator, and outcome » (population, intervention, comparateur et résultat), ECR : essai contrôlé randomisé, RR : risque relatif, RT-PCR : tests moléculaires de réaction en chaîne de la polymérase par transcription inverse, ES/MA : examen systématique et méta-analyse |
||||||
Liste des abréviations
- AMSTAR 2 systématiques
- Outil de mesure servant à évaluer les examens
- ASPC
- Agence de santé publique du Canada
- CCNI
- Comité consultatif national de l'immunisation
- ECR
- Essai contrôlé randomisé
- EP
- Efficacité potentielle
- ER
- Efficacité réelle
- ES/MA
- Examen systématique et méta-analyse
- ES
- Examen systématique
- GCL
- Grippe confirmée en laboratoire
- IC
- Intervalle de confiance
- MA
- Méta-analyse
- NI
- Non indiqué
- PICO
- Population, intervention, comparaison, and outcome (population, intervention, comparateur et résultat)
- RC
- Rapport de cote
- RdB
- Risque de biais
- RR
- Risque relatif
- RT-PCR
- Tests moléculaires de réaction en chaîne de la polymérase par transcription inverse
- VAI
- Vaccin antigrippal inactivé
- VAVA
- Vaccin antigrippal vivant atténué
Remerciements
Cette déclaration du CCNI a été préparée par : K Young, MK Doll, J Przepiorkowski, L Zhao, R Harrison, I Gemmill, J Papenburg et A Sinilaite au nom du CCNI.
Le CCNI tient à remercier les personnes suivantes pour leur contribution : P Doyon-Plourde, A Gil, L Glandon (Bibliothèque de la santé, Santé Canada), A House, SJ Ismail, M Laplante, R Stirling, C Tremblay, M Tunis et M Xi.
Groupe de travail du CCNI sur la grippe
Membres : J. Papenburg (président), P. De Wals, D Fell, I. Gemmill, R. Harrison, J. Langley, A. McGeer et D. Moore.
Anciens membres du groupe de travail : N. Dayneka, K. Klein, D. Kumar, M. Lavoie, J. McElhaney, S. Smith et B. Warshawsky.
Représentants de liaison : L. Grohskopf (Centers for Disease Control and Prevention [CDC], États-Unis).
Anciens représentants d'office : C. Bancej (Centre de l'immunisation et des maladies respiratoires infectieuses [CIMRI], ASPC), J. Reiter (Direction générale de la santé des Premières Nations et des Inuits [DGSPNI], Services aux Autochtones Canada [SAI]) et J Xiong (Direction des produits biologiques et des thérapies génétiques [DPBTG], Santé Canada [SC]).
CCNI
Membres : S. Deeks (président), R. Harrison (vice-président), M. Andrew, J. Bettinger, N. Brousseau, H. Decaluwe, P. De Wals, E. Dubé, V. Dubey, K. Hildebrand, K. Klein, J. Papenburg, A. Pham-Huy, B. Sander, S. Smith et S. Wilson.
Anciens membres du CCNI : M. Lavoie, C. Quach, C. Rotstein, M. Salvadori et N. Sicard.
Représentants de liaison : L. Bill/M. Nowgesic (Association des infirmières et infirmiers autochtones du Canada), L.M. Bucci (Association canadienne de santé publique), E. Castillo (Société des obstétriciens et gynécologues du Canada), A. Cohn (Centers for Disease Control and Prevention, États-Unis), L. Dupuis (Association des infirmières et infirmiers du Canada), D. Fell (Association canadienne de recherche et d'évaluation en matière de vaccination), S. Funnell (Indigenous Physicians Association of Canada), J. Hu (Collège des médecins de famille du Canada), M. Lavoie (Conseil des médecins hygiénistes en chef), D. Moore (Société canadienne de pédiatrie), M. Naus (Comité canadien sur l'immunisation) et A. Ung (Association des pharmaciens du Canada).
Anciens représentants de liaison : J. Brophy (Association canadienne de recherche et d'évaluation en matière de vaccination), A. Cohn (CDC, États-Unis), J. Emili (Collège des médecins de famille du Canada), K. Klein (Conseil des médecins hygiénistes en chef) et A. Pham-Huy (Association pour la microbiologie médicale et l'infectiologie Canada).
Anciens représentants d'office : V. Beswick-Escanlar (Défense nationale et Forces armées canadiennes), E. Henry (Centre de l'immunisation et des maladies respiratoires infectieuses (CIMRI), ASPC), M. Lacroix (Groupe consultatif d'éthique en santé publique, ASPC), C. Lourenco (Direction des médicaments biologiques et radiopharmaceutiques, Santé Canada), D. MacDonald (COVID-19 Épidémiologie et surveillance, ASPC), S. Ogunnaike-Cooke (CIMRI, ASPC), K. Robinson (Direction des produits de santé commercialisés, SC), G. Poliquin (Laboratoire national de microbiologie, ASPC), et T. Wong (Direction générale de la santé des Premières Nations et des Inuits, Services aux Autochtones Canada).
Anciens représentants d'office : K. Barnes (Défense nationale et Forces armées canadiennes), J. Gallivan (Direction des produits de santé commercialisés, SC), J. Pennock (CIMRI, ASPC), et R. Pless (DPBTG, SC).
Annexe A : Stratégie et résultats de recherche
Vous trouverez ci-dessous les termes de recherche formatés pour les bases de données respectives; cette liste a été élaborée en collaboration avec un bibliothécaire de la Bibliothèque fédérale de la santé. Voir le tableau de Medline pour une ventilation des concepts de recherche.
OvidMEDLINE
Base(s) de données : Ovid MEDLINE(R) Epub Ahead of Print, In-Process & Other Non-Indexed Citations, Ovid MEDLINE(R) Daily, Ovid MEDLINE et Versions(R)
| ID | Recherches | Résultats |
|---|---|---|
| 1 | influenza vaccines/or influenza, human/pc | 26844 |
| 2 | (influenza, human/ or exp influenzavirus a/or exp influenzavirus b/) and (exp vaccines/ or exp vaccination/) | 18873 |
| 3 | ((influenza* or flu or H?N?) adj5 (vaccin* or immuni* or inoculat*)).tw,kf,kw. | 31281 |
| 4 | 1 or 2 or 3 | 40820 |
| 5 | (repeat* or annual* or yearly or consecutive* or ((each or every) adj3 (year* or season*))).tw,kf,kw. | 1162272 |
| 6 | 4 and 5 | 4070 |
| 7 | limit 6 to (meta analysis or "review" or systematic reviews) | 763 |
| 8 | (meta analysis or "review" or systematic reviews). pt. | 2592121 |
| 9 | meta-analysis/ or systematic review/ or meta-analysis as topic/ or "meta analysis (topic)"/ or "systematic review (topic)"/ | 114346 |
| 10 | ((systematic* adj3 (review* or overview*)) or (methodologic* adj3 (review* or overview*)) or (quantitative adj3 (review* or overview* or synthes*)) or (integrative adj3 (review* or overview*)) or (collaborative adj3 (review* or overview*)) or meta analy* or metaanaly*). tw, kf, kw. | 231991 |
| 11 | 8 or 9 or 10 | 2660082 |
| 12 | 6 and 11 | 708 |
| 13 | 7 or 12 | 773 |
| 14 | limit 13 to yr="2016 -Current" | 87 |
| 15 | limit 14 to (anglais ou français) | 86 |
86 résultats
EMBASE
Base de données : EMBASE de 1974 à 27 octobre 2017
| ID | Recherches | Résultats |
|---|---|---|
| 1 | influenza vaccine/ or influenza vaccination/ or exp influenza/pc or exp influenza virus/pc | 42496 |
| 2 | (exp influenza/ or exp influenza virus/) and (vaccine/ or virus vaccine/ or inactivated virus vaccine/ or vaccination/) | 12988 |
| 3 | ((influenza* or flu or H?N?) adj5 (vaccin* or immuni* or inoculat*)).tw,kw. | 35784 |
| 4 | 1 or 2 or 3 | 56476 |
| 5 | (repeat* or annual* or yearly or consecutive* or ((each or every) adj3 (year* or season*))).tw,kw. | 1472575 |
| 6 | 4 and 5 | 5508 |
| 7 | limit 6 to (meta analysis or "systematic review" or "review") | 927 |
| 8 | (meta analysis or "systematic review" or "review").pt. | 2348984 |
| 9 | meta analysis/ or review/ or systematic review/ or "meta analysis (topic)"/ or "systematic review (topic)"/ | 2472401 |
| 10 | ((systematic* adj3 (review* or overview*)) or (methodologic* adj3 (review* or overview*)) or (quantitative adj3 (review* or overview* or synthes*)) or (integrative adj3 (review* or overview*)) or (collaborative adj3 (review* or overview*)) or meta analy* or metaanaly*).tw,kw. | 268815 |
| 11 | 8 or 9 or 10 | 2663316 |
| 12 | 6 and 11 | 964 |
| 13 | 7 or 12 | 964 |
| 14 | limit 13 to yr="2016 -Current" | 114 |
| 15 | limit 14 to (anglais ou français) | 110 |
110 résultats
Bibliothèque Cochrane (interface Wiley)
| ID | Recherches | Résultats |
|---|---|---|
| 1 | MeSH descriptor: [Influenza Vaccines] this term only | 1572 |
| 2 | MeSH descriptor: [Influenza, Human] this term only and with qualifier(s): [Prevention & control - PC] | 1198 |
| 3 | MeSH descriptor: [Influenza, Human] this term only | 1674 |
| 4 | MeSH descriptor: [Influenzavirus A] explode all trees | 895 |
| 5 | MeSH descriptor: [Influenzavirus B] explode all trees | 268 |
| 6 | MeSH descriptor: [Vaccines] explode all trees | 9061 |
| 7 | MeSH descriptor: [Vaccination] explode all trees | 2618 |
| 8 | (#3 or #4 or #5) and (#6 or #7) | 1298 |
| 9 | ((influenza* or flu or H?N?) and (vaccin* or immuni* or inoculat*)):ti,ab,kw (Word variations have been searched) | 3988 |
| 10 | #1 or #2 or #8 or #9 | 4145 |
| 11 | (repeat* or annual* or yearly or consecutive* or ((each or every) near/3 (year* or season*))):ti,ab,kw (Word variations have been searched) | 103447 |
| 12 | #10 and #11 Publication Year from 2016 to 2017 | 78 |
78 résultats
SCOPUS
( TITLE-ABS-KEY ( ( influenza* OR flu OR h?n ?) W/5 ( vaccin* ou immuni* ou inoculat*))) AND ( TITLE-ABS-KEY ( repeat* OR annual* OR yearly OR consecutive* OR ( each OR every) W/3 ( year* OR season*)))) AND ( TITLE-ABS-KEY ( ( systematic* W/3 ( review* OR overview*)) OU ( méthodologique* W/3 ( review* OR overview*)) OU ( quantitative W/3 ( review* OR overview* OR synthes*)) OU ( intégrative W/3 ( review* OU overview*)) OU ( collaborative W/3 ( review* OR overview*)) OR meta AND analy* OR metaanaly*)) ET ( LIMIT-TO ( PUBYEAR, 2017) OU LIMIT-TO ( PUBYEAR, 2016))
18 résultats
ProQUEST Santé publique
Base de données : Base de données de la santé publique, affinée par : Date de saisie : 2016 - 2017; type de source : Revues universitaires
TI, AB, SU ((influenza* or flu or H?N?) NEAR/5 (vaccin* or immuni* or inoculat*)) AND TI,AB,SU(repeat* or annual* or yearly or consecutive* or ((each or every) NEAR/3 (year* or season*))) AND ((systematic* NEAR/3 (review* or overview*)) or (methodologic* NEAR/3 (review* or overview*)) or (quantitative NEAR/3 (review* or overview* or synthes*)) or (integrative NEAR/3 (review* or overview*)) or (collaborative NEAR/3 (review* or overview*)) or meta analy* or metaanaly*)Limits applied
81 résultats
PROSPERO
(influenza* or flu) and (vaccin* or immuni* or inoculat*) and (repeat* or annual* or yearly or consecutive* or "each year" or "every year" or "each season" or "every season")
25 résultats
Annexe B : Organigramme
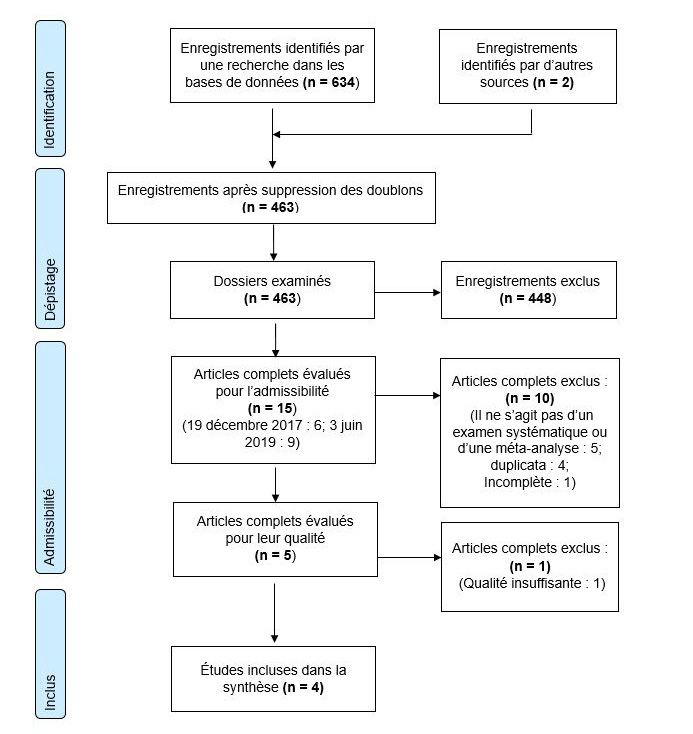
Texte descriptif
L'organigramme PRISMA décrit le processus par lequel les articles ont été sélectionnés pour la recherche documentaire. Le processus est décomposé en quatre étapes : Identification, Dépistage, Admissibilité et Inclus.
Étape 1 : Identification
- 634 enregistrements ont été identifiés par une recherche dans la base de données effectuée le 27 octobre 2017 et mise à jour le 3 juin 2019.
- 2 enregistrements avaient déjà été identifiés par d'autres sources.
- Il restait 463 enregistrements après la suppression des doublons.
Étape 2 : Dépistage
- 463 enregistrements ont ensuite été examinés.
- Sur ces 463 enregistrements, 448 enregistrements ont été exclus.
Étape 3 : Admissibilité
- L'admissibilité de 15 articles complets a été évaluée.
- Sur ces 15 articles complets, 10 ont été exclus. La répartition des exclusions est la suivante : 5 ne s'agissaient pas d'une revue systématique ou d'une méta-analyse; 4 étaient des doublons; 1 était incomplet.
- La qualité de 5 articles complets a été évaluée.
- Sur ces 5 articles complets, 1 a été exclu en raison de sa qualité insuffisante.
Étape 4: Inclus
- 4 articles ont été inclus dans la synthèse finale.
Références
- Note de bas de page 1
-
Schanzer DL, McGeer A, Morris K, Et. Al. Statistical estimates of respiratory admissions attributable to seasonal and pandemic influenza for Canada. Influenza Other Respir Viruses. 2013;7(5):799-808.
- Note de bas de page 2
-
Schanzer DL, Sevenhuysen C, Winchester B, Et. Al. Estimating Influenza Deaths in Canada, 1992–2009. PLoS ONE. 2013;8(11):e80481.
- Note de bas de page 3
-
Comité consultatif national de l'immunisation. Guide canadien d'immunisation et déclaration sur le vaccin contre la grippe saisonnière pour 2022-2023 — chapitre sur la grippe [Internet]. Agence de la santé publique du Canada. 2022. Tiré du site Chapitre sur la grippe du Guide canadien d'immunisation et Déclaration sur la vaccination antigrippale pour la saison 2022-2023 - Canada.ca. Disponible à: https://www.canada.ca/fr/sante-publique/services/publications/vaccins-immunisation/guide-canadien-immunisation-declaration-vaccination-antigrippale-2022-2023.html
- Note de bas de page 4
-
Organisation mondiale de la Santé. Influenza vaccine viruses and reagents. World Health Organization. [Internet]. Vol. 2017. [cité 28 nov 2017]. Disponible à: http://www.who.int/influenza/vaccines/virus/en/
- Note de bas de page 5
-
Hoskins TW, Davies JR, Smith AJ, Et. Al. Assessment of Inactivated Influenza-A Vaccine After Three Outbreaks of Influenza A at Christ's Hospital. The Lancet. 1979;313(8106):33-5.
- Note de bas de page 6
-
Sullivan SG, Kelly H. Stratified Estimates of Influenza Vaccine Effectiveness by Prior Vaccination: Caution Required. Clin Infect Dis. 2013;57(3):474-6.
- Note de bas de page 7
-
Skowronski DM, Chambers C, De Serres G, Et. Al. Serial Vaccination and the Antigenic Distance Hypothesis: Effects on Influenza Vaccine Effectiveness During A (H3N2) Epidemics in Canada, 2010–2011 to 2014–2015. J Infect Dis. 2017;215(7):1059-99.
- Note de bas de page 8
-
McLean HQ, Thompson MG, Sundaram ME, Et. Al. Influenza Vaccine Effectiveness in the United States During 2012-2013: Variable Protection by Age and Virus Type. J Infect Dis. 2015;211(10):1529-40.
- Note de bas de page 9
-
Puig-Barbera J, Burtseva E, Yu H, Et. Al. Influenza Epidemiology and Influenza Vaccine Effectiveness During the 2014-2015 Season: Annual Report from the Global Influenza Hospital Surveillance Network. BMC Public Health. 2016;16(Suppl 1):757.
- Note de bas de page 10
-
Thompson MG, Naleway A, Fry AM, Et. Al. Effects of Repeated Annual Inactivated Influenza Vaccination among Healthcare Personnel on Serum Hemagglutinin Inhibition Antibody Response to A/Perth/16/2009 (H3N2)-like virus during 2010-11. Vaccine. 2016;34(7):981-8.
- Note de bas de page 11
-
Smith DJ, Forrest S, Ackley DH, Et. Al. Variable Efficacy of Repeated Annual Influenza Vaccination. Proc Natl Acad Sci U S A. 1999;96(24):14001-6.
- Note de bas de page 12
-
Flannery B, Smith C, Garten RJ, Et. Al. Influence of Birth Cohort on Effectiveness of 2015–2016 Influenza Vaccine Against Medically Attended Illness Due to 2009 Pandemic Influenza A(H1N1) Virus in the United States. J Infect Dis. 2018;218(2):189-96.
- Note de bas de page 13
-
Gostic KM, Ambrose M, Worobey M, Et. Al. Potent Protection Against H5N1 and H7N9 Influenza via Childhood Hemagglutinin Imprinting. Science. 2016;354(6313):722-6.
- Note de bas de page 14
-
Belongia EA, Skowronski DM, McLean HQ, Et. Al. Repeated Annual Influenza Vaccination and Vaccine Effectiveness: Review of Evidence. Expert Rev Vaccines. 2017;16(7):1-14.
- Note de bas de page 15
-
Ramsay LC, Buchan SA, Stirling RG, Et. Al. The Impact of Repeated Vaccination on Influenza Vaccine Effectiveness: A Systematic Review and Meta-Analysis. BMC Med. 2019;17(1):9. Retraction de: Ramsay LC, Buchan SA, Stirling RG. The Impact of Repeated Vaccination on Influenza Vaccine Effectiveness: A Systematic Review and Meta-Analysis. BMC Med. 2017;15(1):159.
- Note de bas de page 16
-
Harder T, Remschmidt C, Haller S, Et. Al. Use of Existing Systematic Reviews for Evidence Assessments in Infectious Disease Prevention: A Comparative Case Study. Syst Rev. 2016;5(1):171.
- Note de bas de page 17
-
Robinson KA, Whitlock EP, Oneil ME, Et. Al. Integration of Existing Systematic Reviews into New Reviews: Identification of Guidance Needs. Syst Rev. 2014;3(1):60.
- Note de bas de page 18
-
Shea BJ, Reeves BC, Wells G, Et. Al. AMSTAR 2: A Critical Appraisal Tool for Systematic Reviews that Include Randomised or Non-Randomised Studies of Healthcare Interventions, or Both. BMJ. 2017;358:j4008.
- Note de bas de page 19
-
Caspard H., Heikkinen T., Belshe R.B., Et. Al. A Systematic Review of the Efficacy of Live Attenuated Influenza Vaccine upon Revaccination of Children. Hum Vaccines Immunother. 2016;12(7):1721-7.
- Note de bas de page 20
-
Morimoto N, Takeishi K. Change in the Efficacy of Influenza Vaccination After Repeated Inoculation Under Antigenic Mismatch: A Systematic Review and Meta-Analysis. Vaccine. 2018;36(7):949-57.
- Note de bas de page 21
-
Bartoszko JJ, McNamara IF, Aras OAZ, Et. Al. Does Consecutive Influenza Vaccination Reduce Protection Against Influenza: A Systematic Review and Meta-Analysis. Vaccine. 2018;36(24):3434-44.
- Note de bas de page 22
-
Organisation mondiale de la Santé. Recommended Composition of Influenza Virus Vaccines for Use in the 2021- 2022 Northern Hemisphere Influenza Season. Meet Rep. World Health Organization. [Internet]. 2021 [cité 13 mars 2018]; Disponible à: https://cdn.who.int/media/docs/default-source/influenza/202102_recommendation.pdf?sfvrsn=8639f6be_3&download=true
- Note de bas de page 23
-
Schenker N, Gentleman JF. On Judging the Significance of Differences by Examining the Overlap Between Confidence Intervals. Am Stat. 2001;55(3):182-6.
- Note de bas de page 24
-
Belongia EA, Simpson MD, King JP, Et. Al. Variable Influenza Vaccine Effectiveness by Subtype: A Systematic Review and Meta-Analysis of Test-Negative Design Studies. Lancet Infect Dis. 2016;16(8):942-51.
- Note de bas de page 25
-
Francis T. On the Doctrine of Original Antigenic Sin. Proc Am Philos Soc. 1960;104(6):572-8.
- Note de bas de page 26
-
Zost S, Parkhouse K, Et. Al. Contemporary H3N2 Influenza Viruses have a Glycosylation Site that Alters Binding of Antibodies Elicited by Egg-Adapted Vaccine Strains. Proc Natl Acad Sci U A. 2017;114(47):12578-83.
- Note de bas de page 27
-
Skowronski D, Janjua N, De Serres G. Low 2012-13 Influenza Vaccine Effectiveness Associated with Mutation in the Egg-Adapted H3N2 Vaccine Strain not Antigenic Drift in Circulating Viruses. PLoS One. 2014;9(3):e92153.
- Note de bas de page 28
-
Skowronski D, Sabaiduc S, Leir S. Paradoxical Clade- and Age-Specific Vaccine Effectiveness during the 2018/19 Influenza A(H3N2) Epidemic in Canada: Potential Imprint-Regulated Effect of Vaccine (I-REV). Euro Surveill. 2019;24(46):1900585.
- Note de bas de page 29
-
Ismail SJ, Hardy K, Tunis MC, Et. Al. A Framework for the Systematic Consideration of Ethics, Equity, Feasibility, and Acceptability in Vaccine Program Recommendations. Vaccine. 2020;38(36):5861-76.
- Note de bas de page 30
-
Gates A, Gates M, Rahman S. A Systematic Review of Factors that Influence the Acceptability of Vaccines among Canadians. Vaccine. 2021;39(2):222-36.
- Note de bas de page 31
-
Auladell M, Phuong H, Mai L. Influenza Virus Infection History Shapes Antibody Responses to Influenza Vaccination. Nat Med. 2022;28(2):363-372.
- Note de bas de page 32
-
Moritzky S, Richards K, Glover M. The Negative Effect of Pre-Existing Immunity on Influenza Vaccine Responses Transcends the Impact of Vaccine Formulation Type and Vaccination History [published online ahead of print, 2022 Feb 24]. J Infect Dis. 2022;jiac068.
- Note de bas de page 33
-
Snape N, Anderson G, Irving L. Vaccine Strain Affects Seroconversion after Influenza Vaccination in COPD Patients and Healthy Older People. NPJ Vaccines. 2022;7(1):8.
- Note de bas de page 34
-
Centers for Disease Control and Prevention. Information on Rapid Molecular Assays, RT-PCR, and other Molecular Assays for Diagnosis of Influenza Virus Infection. Centers for Disease control and Prevention [Internet]. [cité 13 mars 2018]. Disponible à: https://www.cdc.gov/flu/professionals/diagnosis/molecular-assays.htm
- Note de bas de page 35
-
Merckx J, Wali R, Schiller I. Accuracy of Novel and Traditional Rapid Tests for Influenza Infection Compared with Reverse Transcriptase Polymerase Chain Reaction: A Systematic Review and Meta-Analysis. Ann Intern Med. 2017;167(6):394-409.
Détails de la page
- Date de modification :
