Déclaration du CCNI : vaccin conjugué contre le pneumocoque -
13-valent chez les adultes


Téléchargez cet article en format PDF (0,98 Mo - 56 pages)
Publié par : L'Agence de la santé publique du Canada
Numéro : Volume 39 DCC-5
Date de publication : octobre 2013
ISSN : 1719-3109
Soumettre un article
À propos du RMTC
Naviguer
Volume 39 DCC-5, octobre 2013
Une déclaration d'un comité consultatif (DCC)
Comité consultatif national de l'immunisation (CCNI)†
Déclaration sur l’utilisation du vaccin conjugué contre le pneumocoque 13-valent chez l’adulte (PNEU-C-13)
Contributeurs
†Membres du CCNI : Dre B. Warshawsky (présidente), Dr I. Gemmill (vice-président), Dre N. Crowcroft, Dre B. Henry, Dre D. Kumar, Dre C. Quach-Thanh, Dre M. Salvadori, Dr B. Seifert, Dre N. Sicard, Dre W. Vaudry, Dr R. Warrington.
Agents de liaison : Dre J. Blake (Société des obstétriciens et gynécologues du Canada), Dr A. Corriveau (Conseil des médecins-hygiénistes en chef), Dre S. Deeks (Association canadienne de santé publique), Dre A. Mawle (U.S. Centers for Disease Control and Prevention), Dre D. Moore (Société canadienne de pédiatrie), Dre A. Pham-Huy (Canadian Association for Immunization Research and Evaluation).
Représentants d'office : Dre M. Carew (Direction générale de la santé des Premières nations et des Inuits, Santé Canada), Lt.-Col. Dr P. Eagan (Groupe des Services de santé des Forces canadiennes, ministère de la Défense nationale), Dre A. Klein (Direction des produits biologiques et des thérapies génétiques, Santé Canada), Dre B. Law (Centre de l'immunisation et des maladies respiratoires infectieuses, Agence de la santé publique du Canada), Dre B. Raymond (Centre de l'immunisation et des maladies respiratoires infectieuses, ASPC/Comité canadien d'immunisation), Dre E. Taylor (Direction des produits de santé commercialisés, Santé Canada), Mme M. St-Laurent (Centre de l'immunisation et des maladies respiratoires infectieuses, Agence de la santé publique du Canada).
†La présente déclaration a été rédigée par Dre C. Quach-Thanh et Mme H. Thomas, et approuvée par le CCNI.
Le CCNI tient à remercier la contribution des Lt-Col Dr J. Anderson, Dr J. Brophy, Dr P. DeWals, Dre E. Farzad, Mme M. Helferty, Dre J. Johnstone, Dr J. Kellner, Dre J. Laroche, Dre S. McNeil, Dre H. Morrison, Dre A. Opavsky, Dre S. Rechner, Mme L. Sherrard, Dr G. Tyrrell, Dr P. Van Buynder et Dre V. Senikas.
DOI
https://doi.org/10.14745/ccdr.v39i00a05f
Préambule
Le Comité consultatif national de l'immunisation (CCNI) donne à l'Agence de la santé publique du Canada (ASPC) des conseils constants et à jour liés à l'immunisation dans les domaines de la médecine, des sciences et de la santé publique. L'ASPC reconnaît que les conseils et les recommandations figurant dans la présente déclaration reposent sur les connaissances scientifiques les plus récentes et diffuse le document à des fins d'information. Les personnes qui administrent le vaccin doivent également connaître le contenu de la monographie de produit pertinente. Les recommandations d'utilisation et les autres renseignements qui figurent dans le présent document peuvent différer du contenu de la monographie de produit du fabricant du vaccin au Canada. Les fabricants ont fait approuver leur vaccin et démontré son innocuité et son efficacité uniquement lorsqu'il est utilisé conformément à la monographie de produit. Les membres du CCNI et les agents de liaison doivent se conformer à la politique de l'ASPC régissant les conflits d'intérêts, notamment déclaré chaque année les conflits d'intérêts possibles.
Table des matières
Sommaire de l'information contenue dans la présente déclaration du CCNI
Le tableau suivant résume l'information importante pour les vaccinateurs. Veuillez consulter le reste de la Déclaration pour obtenir plus de précisions.
1. Quoi Qu'est-ce qu'une infection à pneumocoque? Qu'est-ce que le vaccin contre le pneumocoque? Il existe deux formes de vaccins contre le pneumocoque : un vaccin conjugué (PNEU-C-13 et PNEU-C-10) et un vaccin polysaccharidique (PNEU-P-23). |
2. Qui Qui devrait recevoir le vaccin?
Les recommandations relatives aux enfants peuvent être consultées sur le site Web du CCNI. |
3. Comment Dose et calendrier Plus particulièrement :
Précautions/contre-indications Administration en concomitance Il est possible d'administrer le vaccin PNEU-C-13 en concomitance avec d'autres vaccins (en utilisant un autre site d'injection). |
4. Pourquoi Les données probantes actuelles appuient l'utilisation du vaccin PNEU-C-13 chez les adultes immunodéprimés, étant donné que ceux-ci présentent un risque accru de contracter une infection invasive à pneumocoque (IIP) et que les vaccins conjugués contre le pneumocoque se sont révélés plus efficaces chez certains groupes de sujets immunodéprimés. |
I. Introduction
La présente déclaration vise à compléter les déclarations antérieures sur les vaccins conjugués contre le pneumocoqueNote de bas de page commencer de1-à note de bas de page3 et à fournir de l'information sur une nouvelle indication qui a été approuvée concernant l'utilisation du vaccin conjugué contre le pneumocoque 13-valent, à savoir PrevnarMD 13 (PNEU-C-13). En janvier 2012, l'utilisation du vaccin PNEU-C-13 a été autorisée chez les adultes de 50 ans ou plus pour prévenir les infections invasives à pneumocoque (IIP), notamment la septicémie, la méningite, la bactériémie et la pneumonie (avec ou sans empyème) avec bactériémie. Lorsqu'on disposera de données supplémentaires sur l'utilisation du vaccin PNEU-C-13 chez l'adulte, le CCNI les examinera et formulera, le cas échéant, de nouvelles directives. Le vaccin polysaccharidique 23-valent (PNEU-P-23) ne sera pas abordé en détail dans la présente déclaration. Les recommandations relatives à son utilisation demeurent inchangées. Veuillez consulter le Guide canadien d'immunisation.
La présente déclaration:
- fait la mise à jour de l'épidémiologie des IIP au Canada en ce qui a trait à l'introduction du vaccin PNEU-C-13;
- présente une revue des articles portant sur l'utilisation de vaccins conjugués contre le pneumocoque dans des populations adultes (PNEU-C-7 et PNEU-C-13, lorsque disponibles);
- fournit des recommandations quant à l'utilisation du vaccin conjugué 13-valent chez l'adulte (PNEU-C-13) et à l'utilisation du PNEU-P-23 en plus du PNEU-C-13. Bien que le PNEU-C-13 ait été approuvé pour les adultes âgés de 50 ans et plus, cette déclaration se concentrera sur les adultes (tout âge) avec des conditions à haut risque d'IIP et les adultes en santé de 65 ans et plus à cause du fardeau de la maladie ayant mené à la recommandation d'utiliser le PNEU-P-23 dans ce groupe d'âge.
II. Méthodologie
Le CCNI a examinéNote de bas de page4 les éléments tels le fardeau de la maladie et la population cible, l'innocuité, l'immunogénicité, l'efficacité potentielle et réelle du (des) vaccin(s), les calendriers de vaccination et d'autres aspects de la stratégie globale d'immunisation. Suite à une évaluation critique de chacune des études, des tableaux sommaires avec cotes de qualité des preuves utilisant la hiérarchie méthodologique du CCNI (tableaux 6 et 7), des recommandations relatives à l'utilisation des vaccins ont été développées. Le président du groupe de travail a présenté les données probantes et proposé des recommandations au CCNI. Après un examen approfondi des preuves et une consultation des membres lors de réunions du CCNI, le Comité a adopté certaines recommandations. La présente déclaration présente une description des considérations pertinentes, les raisons sous-tendant certaines décisions et les lacunes dans les connaissances. L'ASPC a consigné les renseignements sur ces processus tout au long de la synthèse des connaissances et de l'élaboration des recommandations.
III. Épidemiologie des infections à pneumocoque au Canada
III.1 Description de la maladie
L'infection invasive à pneumocoque (IIP) est une maladie grave causée par la bactérie Streptococcus pneumoniae. Il existe actuellement 92 sérotypes de la bactérie connus à l'échelle mondiale, dont 15 sont à l'origine de la plupart des cas de maladie. Le S. pneumoniae peut se transmettre d'une personne à une autre par des gouttelettes projetées du nez ou de la bouche de la personne infectée lorsqu'elle éternue ou tousse. Les infections à S. pneumoniae sont une cause majeure de morbidité et de mortalité dans le monde. Il est estimé qu'environ un million d'enfants par année meurent d'infection à pneumocoque; la majorité de ces cas surviennent chez de jeunes enfants dans des pays en développement. Dans les pays développés, un lourd fardeau associé à la maladie existe également chez les personnes âgées. Chez les enfants et les adultes, les voies respiratoires supérieures et le rhinopharynx sont souvent colonisés par le S. pneumoniae, sans que cela provoque des symptômes. L'IIP est une infection grave qui survient lorsque la bactérie envahit des sites normalement stériles, comme le système sanguin et le système nerveux central. Les symptômes ou manifestations cliniques dépendent du site de l'infection. L'IIP peut donner lieu à plusieurs syndromes, comme la bactériémie, la méningite et/ou la pneumonie (avec ou sans empyème) avec bactériémie. Certains états pathologiques prédisposent les sujets à des complications secondaires à une infection pneumococcique, notamment l'anémie falciforme ou d'autres hémoglobinopathies, l'insuffisance rénale chronique, une hépatopathie chronique, un déficit immunitaire, une asplénie fonctionnelle ou anatomique, des fuites de liquide céphalorachidien, le diabète et l'infection à VIH. Les personnes plus âgées, en particulier celles de 65 ans et plus, courent également un risque accru d'IIPnote de bas de page5.
Les données épidémiologiques sur les IIP proviennent de deux sources canadiennes : le Système canadien de surveillance des maladies à déclaration obligatoire (SCSMDO) et le Laboratoire national de microbiologie (LNM).
III.2 Distribution de la maladie
Depuis que l'IIP est devenue une maladie à déclaration obligatoire au Canada en 2000, le nombre de cas déclarés et les taux d'incidence ont augmenté; ils se sont toutefois stabilisés au cours des cinq dernières années, le taux d'incidence se maintenant à 10 cas pour 100 000 habitants (figure 1). L'augmentation des taux d'incidence observée entre 2001 et 2004 était vraisemblablement attribuable, du moins en partie, à un biais de déclaration, le nombre de cas déclarés augmentant à mesure que le système de surveillance passive était mieux connu et compris.
Figure 1. Nombre de cas déclarés d'IIP et taux d'incidence, Canada, 2001-2011
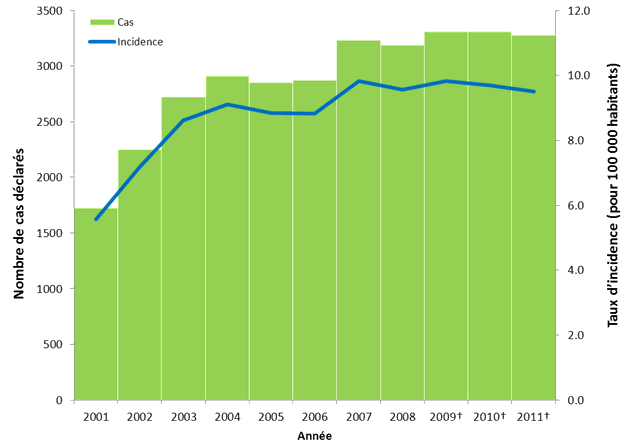
* Données tirées du Système canadien de surveillance des maladies à déclaration obligatoire.
† D'après des données provisoires.
Équivalent textuel pour la figure 1 Nombre de cas déclarés d'IIP et taux d'incidence, Canada, 2001-2011
| Année | Nombre de cas déclarés | Taux d'incidence (pour 100 000 habitants) |
|---|---|---|
| 2001 | 1 728 | 5,57 |
| 2002 | 2 251 | 7,18 |
| 2003 | 2 725 | 8,61 |
| 2004 | 2 910 | 9,11 |
| 2005 | 2 850 | 8,84 |
| 2006 | 2 875 | 8,83 |
| 2007 | 3 235 | 9,82 |
| 2008 | 3 186 | 9,56 |
| 2009note † | 3 311 | 9,82 |
| 2010note † | 3 309 | 9,70 |
| 2011note † | 3 274 | 9,49 |
note * Données tirées du Système canadien de surveillance des maladies à déclaration obligatoire. note † D'après des données provisoires. |
||
III.3 Distribution géographique
C'est en Ontario et au Québec que l'on observe le plus de cas déclarés, ce qui n'est pas étonnant puisqu'il s'agit de provinces populeuses. Dans les territoires, cependant, le taux d'incidence pour 100 000 habitants et la variabilité des résultats sont élevés, vraisemblablement en raison de la petite taille de la population (figure 2, tableaux 1 et 2). Fait à signaler, on attribue les taux d'incidence élevés observés en Colombie-Britannique (BC), en Alberta (AB), en Saskatchewan (SK) et au Manitoba (MB) aux éclosions importantes dues au sérotype 5 qui sont survenues dans ces provinces de 2006 à 2008. Aucune éclosion n'explique le taux d'incidence élevé observé au Québec.
Figure 2. Nombre moyen de cas et taux d'incidence moyens d'IIP (par 100 000 habitants), par province et territoire, Canada, 2007-2011
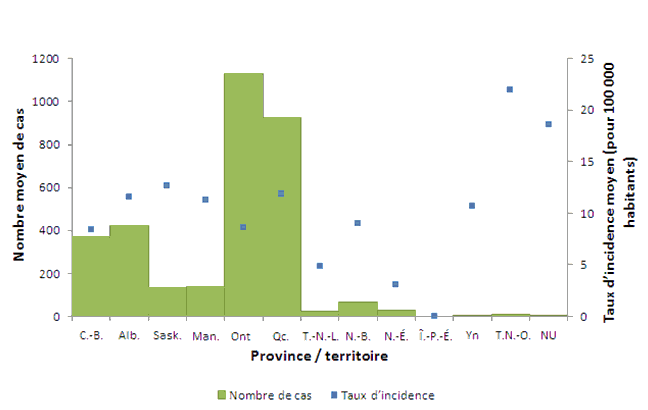
Équivalent textuel pour la figure 2 Nombre moyen de cas et taux d'incidence moyens d'IIP (par 100 000 habitants), par province et territoire, Canada, 2007-2011
| Province / Territoire | Nombre moyen de cas | Taux d'incidence moyen (pour 100 000 habitants) |
|---|---|---|
| C.-B. | 373 | 8,37 |
| Alb. | 425 | 11,62 |
| Sask. | 131 | 12,69 |
| Man. | 138 | 11,27 |
| Ont. | 1 130 | 8,64 |
| Qc. | 926 | 11,83 |
| T.-N.-L | 25 | 4,88 |
| N.-B. | 68 | 9,04 |
| N.-É. | 29 | 3,10 |
| Î.-P.-É. | 0 | 0,00 |
| Yn | 4 | 10,68 |
| T.N.-O. | 10 | 21,98 |
| NU | 6 | 18,60 |
| Année | Province / territoire | Canada | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| C.-B. | Alb. | Sask. | Man. | Ont. | Qc. | T.-N.-L. | N.-B. | N.-É. | Î.-P.-É. | Yn | T.N.-O. | NU | ||
| Moyenne pour 2001-2006 | 322 | 401 | 76 | 93 | 760 | 833 | 24 | 21 | 14 | 0 | 4 | 5 | 5 | 2557 |
| 2007 | 552 | 601 | 148 | 101 | 941 | 786 | 13 | 47 | 26 | 0 | 2 | 9 | 9 | 3235 |
| 2008 | 402 | 454 | 133 | 145 | 1065 | 877 | 35 | 46 | 14 | 0 | 1 | 7 | 7 | 3186 |
| 2009Tableau 1 Note de bas de page † | 324 | 371 | 112 | 138 | 1224 | 989 | 36 | 75 | 20 | 0 | 7 | 11 | 4 | 3311 |
| 2010Tableau 1 Note de bas de page † | 258 | 340 | 126 | 176 | 1185 | 1066 | 23 | 82 | 35 | 0 | 3 | 10 | 5 | 3309 |
| 2011Tableau 1 Note de bas de page † | 327 | 358 | 134 | 128 | 1235 | 914 | 17 | 89 | 51 | 0 | 5 | 11 | 5 | 3274 |
| Moyenne pour 2007-2011 | 373 | 425 | 131 | 138 | 1130 | 926 | 25 | 68 | 29 | 0 | 4 | 10 | 6 | 3263 |
|
||||||||||||||
| Année | Province / territoire | Canada | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| C.-B. | Alb. | Sask. | Man. | Ont. | Qc. | T.-N.-L. | N.-B. | N.-É. | Î.-P.-É. | Yn | T.N.-O. | NU | ||
| Moyenne pour 2001-2006 |
8,05 | 12,04 | 9,95 | 9,52 | 7,33 | 11,43 | 4,71 | 5,63 | 2,22 | 0,07 | 11,81 | 15,84 | 16,84 | 8,81 |
| 2007 | 12,81 | 17,11 | 14,80 | 8,46 | 7,36 | 10,22 | 2,57 | 6,30 | 2,78 | 0,00 | 6,14 | 20,67 | 28,78 | 9,82 |
| 2008 | 9,17 | 12,64 | 13,12 | 12,03 | 8,23 | 11,32 | 6,91 | 6,16 | 1,49 | 0,00 | 3,02 | 16,03 | 22,13 | 9,56 |
| 2009Tableau 2 Note de bas de page † | 7,26 | 10,10 | 10,88 | 11,32 | 9,36 | 12,64 | 7,07 | 10,00 | 2,13 | 0,00 | 20,78 | 25,21 | 12,41 | 9,82 |
| 2010Tableau 2 Note de bas de page † | 5,70 | 9,14 | 12,07 | 14,26 | 8,96 | 13,48 | 4,50 | 10,89 | 3,70 | 0,00 | 8,68 | 22,82 | 15,23 | 9,70 |
| 2011Tableau 2 Note de bas de page † | 7,15 | 9,47 | 12,67 | 10,24 | 9,24 | 11,45 | 3,33 | 11,78 | 5,39 | 0,00 | 14,42 | 25,19 | 15,01 | 9,49 |
| Moyenne pour 2007-2011 |
8,37 | 11,62 | 12,69 | 11,27 | 8,64 | 11,83 | 4,88 | 9,04 | 3,10 | 0,00 | 10,68 | 21,98 | 18,60 | 9,68 |
|
||||||||||||||
Le vaccin PNEU-C-7 a été intégré aux programmes de vaccination pédiatrique de l'ensemble des provinces et des territoires en 2006, et le vaccin PNEU-C-13, en 2011. La figure 3 montre le taux d'incidence moyen d'IIP par province et territoire, avant et après l'introduction du vaccin PNEU-C-7.
Figure 3. Taux d'incidence annuel moyen d'IIP par province et territoire – pour tous les groupes d'âge (par 100 000 habitants), avant et après l'introduction du vaccin PNEU-C-7, Canada, 2001-2011
| P/T | Année d'intoduction du VCP7 |
|---|---|
| C.-B. | 2003 |
| Alb. | 2002 |
| Sask. | 2005 |
| Man. | 2004 |
| Ont. | 2005 |
| Qc. | 2005 |
| T.-N.-L. | 2005 |
| N.-B. | 2005 |
| N.-É. | 2005 |
| Î.-P.-É. | 2005 |
| Yn | 2005 |
| T.N.-O. | 2006 |
| NU | 2002 |
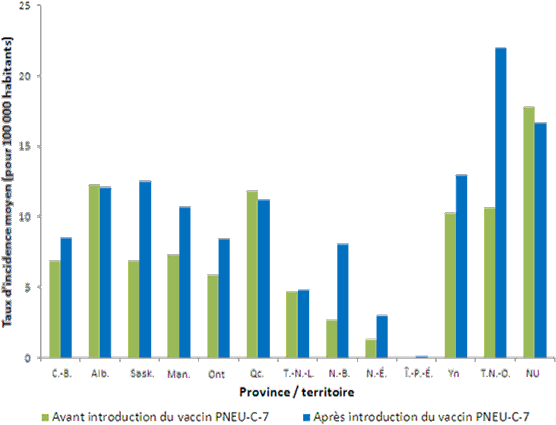
* Données tirées du Système canadien de surveillance des maladies à déclaration obligatoire (données provisoires de 2009-2011).
**L'année de mise en œuvre du programme est incluse dans la période « avant introduction ». Les données étaient disponibles de 2001 à 2011 pour l'ensemble des provinces et territoires.
Équivalent textuel pour la figure 3 Taux d'incidence annuel moyen d'IIP par province et territoire – pour tous les groupes d'âge (par 100 000 habitants), avant et après l'introduction du vaccin PNEU-C-7, Canada, 2001-2011
| Province / Territoire | Année d'introduction du VCP7 | Taux d'incidence moyen (pour 100 000 habitants) avant introduction du vaccin PNEU-C-7 | Taux d'incidence moyen (pour 100 000 habitants) après introduction du vaccin PNEU-C-7 |
|---|---|---|---|
| C.-B. | 2003 | 6,90 | 8,48 |
| Alb. | 2002 | 12,23 | 12,05 |
| Sask. | 2005 | 6,84 | 12,49 |
| Man. | 2004 | 7,32 | 10,70 |
| Ont. | 2005 | 5,87 | 8,43 |
| Qc. | 2004 | 11,79 | 11,22 |
| T.-N.-L | 2005 | 4,64 | 4,78 |
| N.-B. | 2005 | 2,67 | 8,08 |
| N.-É. | 2005 | 1,28 | 2,99 |
| Î.-P.-É. | 2005 | 0,00 | 0,12 |
| Yn | 2005 | 10,27 | 12,97 |
| T.N.-O. | 2006 | 10,62 | 21,98 |
| NU | 2002 | 17,77 | 16,66 |
note * Données tirées du Système canadien de surveillance des maladies à déclaration obligatoire (données provisoires de 2009–2011). note **L'année de mise en oeuvre du programme est incluse dans la période « avant introduction ». Les données étaient disponibles de 2001 à 2011 pour l'ensemble des provinces et territoires. |
|||
III.4 Répartition par âge
Les données sur les IIP par groupe d'âge révèlent que, jusqu'en 2005, les enfants de moins de cinq ans étaient les plus touchés (figure 4). Le vaccin PNEU-C-7 a été intégré aux programmes de vaccination de l'ensemble des provinces et des territoires en 2006, et les données nationales semblent indiquer que l'introduction du vaccin PNEU-C-7 a entraîné une diminution du taux d'incidence chez les enfants de moins de cinq ans. Bien que l'on ait observé une augmentation du taux d'incidence d'IIP de 2006 à 2008, ce taux était toujours inférieur à ceux enregistrés avant l'introduction du vaccin. On a observé une augmentation stable du taux d'incidence chez les adultes de 60 ans ou plus depuis 2006.
Figure 4. Taux d'incidence d'IIP chez les moins de 20 ans, par groupe d'âge et année, Canada, 2001-2011
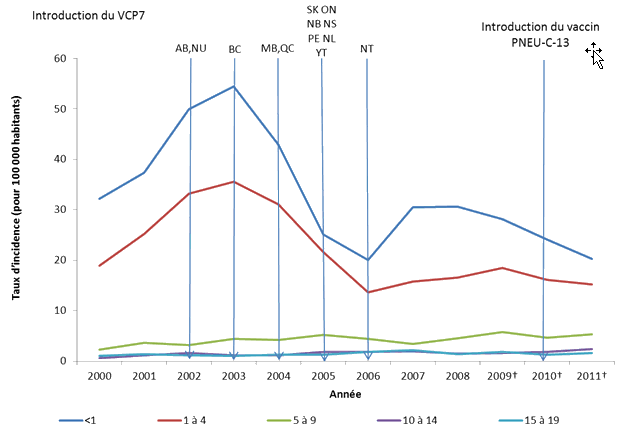
* Données tirées du Système canadien de surveillance des maladies à déclaration obligatoire.
† D'après des données provisoires.
Note : Certaines provinces et territoires canadiens avaient introduit le PNEU-C-10 dans leur programme en 2009.
Équivalent textuel pour la figure 4 Taux d'incidence d'IIP chez les moins de 20 ans, par groupe d'âge et année, Canada, 2001-2011
| Année | <1 ans | 1 à 4 ans | 5 à 9 ans | 10 à 14 ans | 15 à 19 ans |
|---|---|---|---|---|---|
| 2001 | 37,37 | 25,17 | 3,57 | 1,15 | 1,42 |
| 2002 | 50,00 | 33,24 | 3,12 | 1,56 | 1,18 |
| 2003 | 54,51 | 35,55 | 4,36 | 1,17 | 0,99 |
| 2004 | 42,90 | 31,04 | 4,20 | 1,17 | 1,31 |
| 2005 | 25,06 | 21,60 | 5,20 | 1,79 | 1,29 |
| 2006 | 19,99 | 13,58 | 4,44 | 1,81 | 1,81 |
| 2007 | 30,54 | 15,75 | 3,44 | 1,95 | 2,14 |
| 2008 | 30,56 | 16,56 | 4,52 | 1,44 | 1,33 |
| 2009note † | 28,16 | 18,51 | 5,78 | 1,57 | 1,82 |
| 2010note † | 24,03 | 16,10 | 4,60 | 1,86 | 1,30 |
| 2011note † | 20,26 | 15,17 | 5,26 | 2,42 | 1,64 |
note * Données tirées du Système canadien de surveillance des maladies à déclaration obligatoire. note † D'après des données provisoires. Remarque : Le vaccin PCV7 a été mis en marché en Alberta et au Nunavut en 2002, en Colombie-Britannique en 2003, au Manitoba et au Québec en 2004, en Saskatchewan, en Ontario, au Nouveau-Brunswick, en Nouvelle-Écosse, à l'Île-du-Prince-Édouard, à Terre-Neuve-et-Labrador et au Yukon en 2005 et dans les Territoires du Nord-Ouest en 2006. Certaines provinces et territoires canadiens avaient introduit le PNEU-C-10 dans leur programme en 2009. Le vaccin Pneu-C-13 a été mis en marché en 2010. |
|||||
Les taux d'incidence d'IIP chez l'adulte semblent augmenter en fonction de l'âge, les personnes de 60 ans ou plus étant les plus touchées (figure 5). Les taux d'incidence chez les personnes plus âgées ont augmenté dans le temps dans la quasi-totalité des groupes d'âge, la hausse la plus marquée étant survenue chez les 40 à 59 ans et les 60 ans ou plus.
Figure 5. Taux d'incidence d'IIP chez les 20 ans ou plus, par groupe d'âge et année, Canada, 2001-2011
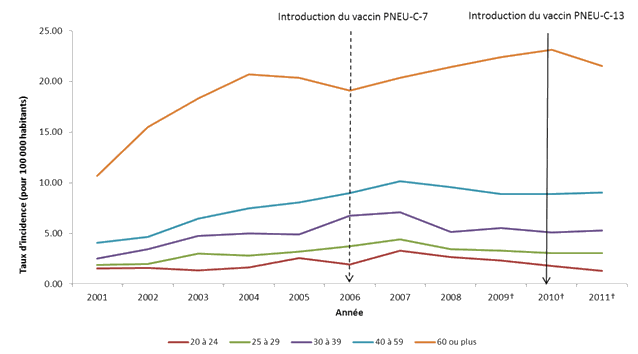
* Données tirées du Système canadien de surveillance des maladies à déclaration obligatoire.
† D'après des données provisoires.
Équivalent textuel pour la figure 5 Taux d'incidence d'IIP chez les 20 ans ou plus, par groupe d'âge et année, Canada, 2001-2011
| Année | 20 à 24 ans | 25 à 29 ans | 30 à 39 ans | 40 à 59 ans | 60+ ans |
|---|---|---|---|---|---|
| 2001 | 1,57 | 1,88 | 2,54 | 4,08 | 10,71 |
| 2002 | 1,59 | 2,02 | 3,45 | 4,66 | 15,53 |
| 2003 | 1,38 | 3,00 | 4,74 | 6,49 | 18,33 |
| 2004 | 1,63 | 2,83 | 5,00 | 7,50 | 20,70 |
| 2005 | 2,60 | 3,21 | 4,92 | 8,08 | 20,36 |
| 2006 | 1,95 | 3,75 | 6,74 | 9,00 | 19,11 |
| 2007 | 3,30 | 4,44 | 7,09 | 10,16 | 20,37 |
| 2008 | 2,67 | 3,45 | 5,17 | 9,58 | 21,43 |
| 2009Footnote † | 2,33 | 3,32 | 5,53 | 8,92 | 22,43 |
| 2010Footnote † | 1,78 | 3,05 | 5,11 | 8,89 | 23,15 |
| 2011Footnote † | 1,33 | 3,06 | 5,30 | 9,06 | 21,55 |
Footnote * Données tirées du Système canadien de surveillance des maladies à déclaration obligatoire. Footnote †D'après des données provisoires. Remarque : Le vaccin Pneu-C-7 avait été mis en marché dans l'ensemble des provinces et des territoires en 2006. Certaines provinces et territoires canadiens avaient introduit le PNEU-C-10 dans leur programme en 2009. Le vaccin Pneu-C-13 a été mis en marché en 2010. |
|||||
| Année | Groupes d'âge | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| <1 | 1 à 4 | 5 à 9 | 10 à 14 | 15 à 19 | 20 à 24 | 25 à 29 | 30 à 39 | 40 à 59 | 60 ou plus | |
| 2001 | 124 | 359 | 72 | 24 | 30 | 33 | 39 | 124 | 358 | 558 |
| 2002 | 164 | 465 | 62 | 33 | 25 | 34 | 42 | 166 | 421 | 828 |
| 2003 | 180 | 490 | 85 | 25 | 21 | 30 | 63 | 223 | 602 | 1002 |
| 2004 | 145 | 425 | 80 | 25 | 28 | 36 | 60 | 230 | 713 | 1161 |
| 2005 | 85 | 296 | 97 | 38 | 28 | 58 | 69 | 223 | 784 | 1171 |
| 2006 | 70 | 188 | 81 | 38 | 40 | 44 | 82 | 303 | 887 | 1133 |
| 2007 | 110 | 221 | 62 | 40 | 48 | 75 | 99 | 319 | 1008 | 1252 |
| 2008 | 114 | 237 | 81 | 29 | 30 | 61 | 79 | 234 | 957 | 1364 |
| 2009Tableau 3 Note de bas de page † | 107 | 271 | 104 | 31 | 41 | 54 | 78 | 252 | 897 | 1475 |
| 2010Tableau 3 Note de bas de page † | 92 | 242 | 83 | 36 | 29 | 42 | 73 | 235 | 900 | 1573 |
| 2011Tableau 3 Note de bas de page † | 78 | 233 | 96 | 46 | 36 | 32 | 74 | 246 | 921 | 1511 |
|
||||||||||
| Année | Groupes d'âge | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| <1 | 1 à 4 | 5 à 9 | 10 à 14 | 15 à 19 | 20 à 24 | 25 à 29 | 30 à 39 | 40 à 59 | 60 ou plus | |
| 2001 | 37,37 | 25,17 | 3,57 | 1,15 | 1,42 | 1,57 | 1,88 | 2,54 | 4,08 | 10,71 |
| 2002 | 50,00 | 33,24 | 3,12 | 1,56 | 1,18 | 1,59 | 2,02 | 3,45 | 4,66 | 15,53 |
| 2003 | 54,51 | 35,55 | 4,36 | 1,17 | 0,99 | 1,38 | 3,00 | 4,74 | 6,49 | 18,33 |
| 2004 | 42,90 | 31,04 | 4,20 | 1,17 | 1,31 | 1,63 | 2,83 | 5,00 | 7,50 | 20,70 |
| 2005 | 25,06 | 21,60 | 5,20 | 1,79 | 1,29 | 2,60 | 3,21 | 4,92 | 8,08 | 20,36 |
| 2006 | 19,99 | 13,58 | 4,44 | 1,81 | 1,81 | 1,95 | 3,75 | 6,74 | 9,00 | 19,11 |
| 2007 | 30,54 | 15,75 | 3,44 | 1,95 | 2,14 | 3,30 | 4,44 | 7,09 | 10,16 | 20,37 |
| 2008 | 30,56 | 16,56 | 4,52 | 1,44 | 1,33 | 2,67 | 3,45 | 5,17 | 9,58 | 21,43 |
| 2009Tableau 4 Note de bas de page † | 28,16 | 18,51 | 5,78 | 1,57 | 1,82 | 2,33 | 3,32 | 5,53 | 8,92 | 22,43 |
| 2010Tableau 4 Note de bas de page † | 24,03 | 16,10 | 4,60 | 1,86 | 1,30 | 1,78 | 3,05 | 5,11 | 8,89 | 23,15 |
| 2011Tableau 4 Note de bas de page † | 20,26 | 15,17 | 5,26 | 2,42 | 1,64 | 1,33 | 3,06 | 5,30 | 9,06 | 21,55 |
|
||||||||||
III.5 Distribution des sérotypes associés aux IIP au Canada
Le vaccin PNEU-C-7 contient les sérotypes 4, 6B, 9V, 14, 18C, 19F et 23F; le vaccin PNEU-C-13 contient, en plus des sérotypes inclus dans le PNEU-C-7, les sérotypes 1, 3, 5, 6A, 7F et 19A; et le vaccin PNEU-P-23 contient, en plus des sérotypes inclus dans le PNEU-C-13, les sérotypes 2, 8, 9N, 10A, 11A, 12F, 15B, 17F, 20, 22F et 33F, mais le PNEU-P-23 ne contient pas le sérotype 6A.
À l'échelle canadienne, la surveillance en laboratoire des sérotypes associés aux IIP s'effectue par l'entremise d'un système passif à participation volontaire : les souches sont envoyées au Laboratoire national de microbiologie (LNM), qui offre des services de diagnostic de référence. Ce système de surveillance passive est toutefois limité par les différences en matière de déclaration qui existent entre les provinces et les territoires; par la variabilité de la taille d'échantillonnage dans les petites administrations, où l'on se trouve à avoir de faibles nombres de cas mais de fortes proportions relatives; et par la disponibilité de souches bactériennes à envoyer pour fins d'analyse.
D'après les souches envoyées au LNM par les provinces et les territoires et d'après l'information additionnelle sur le sérotypage fournie par le Laboratoire de santé publique du Québec (LSPQ) et le Toronto Invasive Bacterial Disease Network (TIBDN), les sérotypes prédominants au Canada en 2011 étaient les sérotypes 19A, 7F et 3 (tous trois présents dans le vaccin PNEU-C-13 et le vaccin PNEU-P-23, mais non dans le vaccin PNEU-C-7), le sérotype 22F (présent dans le vaccin PNEU-P-23) et le sérotype 6C (présent dans aucun vaccin); ensemble, ces sérotypes représentaient 53 % (n = 1 252) des souches analysées associées à une IIP au Canada (figure 6). Le sérotype 19A demeure le sérotype prédominant en 2011 dans les isolats provenant des < 2 ans (23 %, n = 38), des 2 à 4 ans (41 %, n = 59), des 50 à 64 ans (16 %, n = 108) et des ≥ 65 ans (14 %, n = 126), tandis que le sérotype 7F demeure prédominant chez les 5 à 14 ans (28 %, n = 39) et les 15 à 49 ans (21 %, n = 134). Le sérotype 3 est relativement fréquent chez les 2 à 4 ans, les 50 à 64 ans et les ≥ 65 ans, représentant respectivement 11 % (n = 16), 8 % (n = 57) et 11 % (n = 99) des isolats dans ces groupes d'âge. Le sérotype 22F tend à être relativement fréquent chez les personnes plus âgées, à savoir les 15 à 49 ans (7 %, n = 46), les 50 à 64 ans (6 %, n = 43) et les ≥ 65 ans (10 %, n = 90), tandis que le sérotype 6C est fréquent chez les ≥ 65 ans, représentant 7 % (n = 60) des isolats analysés. La proportion de sérotypes contenus dans le vaccin PNEU-C-13 a diminué de 2010 à 2011 chez les < 2 ans : elle était de 63 % (n = 118) en 2010 et de 43 % (n = 70) en 2011. La proportion de sérotypes contenus dans le vaccin PNEU-P-23 est demeurée relativement constante dans tous les groupes d'âge au cours des deux ans (figures 7 à 9)note de bas de page6 - note de bas de page8
Figure 6. Distribution régionale des sérotypes de S. pneumoniae au Canada, 2011
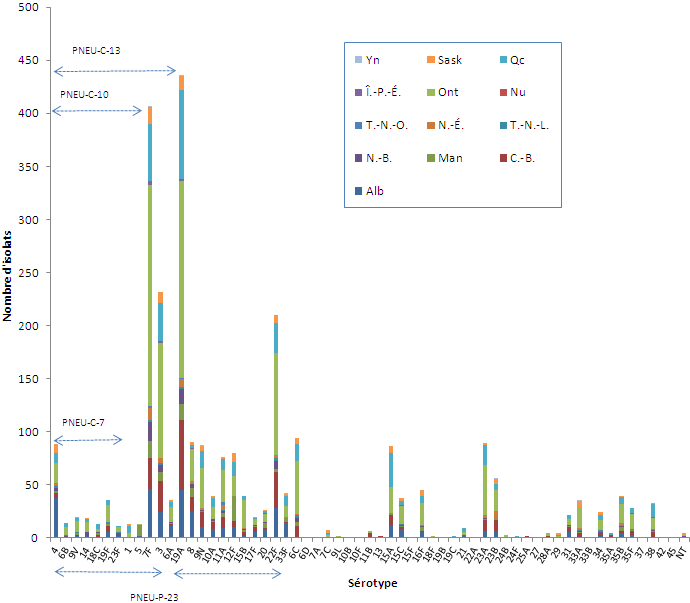
Équivalent textuel pour la figure 6 Distribution régionale des sérotypes de S. pneumoniae au Canada, 2011
Cette image est un graphique à barres empilées qui montre le nombre de cas déclarés de infection invasive à pneumocoque (IIP), par sérotype et par province ou territoire, au Canada en 2011. Les plus grands nombres de cas ont été observés en Ontario (n = 1 148), au Québec (n = 434), en Alberta (n = 354) et en Colombie-Britannique (n = 318). Le sérotype 19A a été le plus fréquemment signalé (n = 436), suivi des sérotypes 7F (n = 407), 3 (n = 232) et 22F (n = 210).
De ces sérotypes prédominants, seul le sérotype 22F n'est pas contenu dans le vaccin PCV-13. Toutefois, le vaccin Pneu-P-23, actuellement homologué au Canada, confère une protection contre ce sérotype. Notons que les sérotypes contenus dans le vaccin PCV7 n'ont pas été une cause prédominante de maladie au Canada en 2011.
La figure montre également quels sérotypes sont contenus dans différents vaccins :
- Le vaccin Pneu-C-7 contient les sérotypes 4, 9V, 6B, 14, 18C, 19F et 23F.
- Le vaccin Pneu-C-10 contient les mêmes sérotypes que le vaccin Pneu-C-7 ainsi que les sérotypes 1, 5 et 7F.
- Le vaccin Pneu-C-13 contient les mêmes sérotypes que les vaccins Pneu-C-7 et Pneu-C-10 ainsi que les sérotypes 3, 6A et 19A.
- Le vaccin Pneu-P-23 contient les mêmes sérotypes que les vaccins Pneu-C-7 et Pneu-C-10 ainsi que les sérotypes 3, 19A, 2, 8, 9N, 10A, 11A, 12F, 15B, 17F, 20, 22F et 33F.
Figure 7. Proportion des sérotypes contenus dans le vaccin PNEU-C-7 par groupe d'âge, 2010-2011
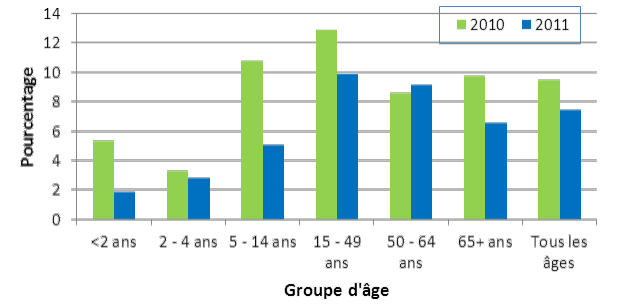
Équivalent textuel pour la figure 7 Proportion des sérotypes contenus dans le vaccin PNEU-C-7 par groupe d'âge, 2010-2011
| Année | <2 ans | 2 à 4 ans | 5 à 14 ans | 15 à 49 ans | 50 à 64 ans | 65+ ans | Tous les âges |
|---|---|---|---|---|---|---|---|
| 2010 | 5,35 | 3,29 | 10,74 | 12,84 | 8,58 | 9,72 | 9,50 |
| 2011 | 1,84 | 2,80 | 5,07 | 9,89 | 9,14 | 6,56 | 7.44 |
Figure 8. Proportion des sérotypes contenus dans le vaccin PNEU-C-13 par groupe d'âge, 2010-2011
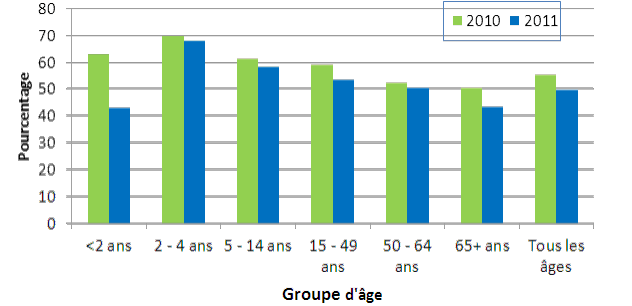
Équivalent textuel pour la figure 8 Proportion des sérotypes contenus dans le vaccin PNEU-C-13 par groupe d'âge, 2010-2011
| Année | <2 ans | 2 à 4 ans | 5 à 14 ans | 15 à 49 ans | 50 à 64 ans | 65+ ans | Tous les âges |
|---|---|---|---|---|---|---|---|
| 2010 | 63,10 | 69,74 | 61,16 | 58,73 | 52,03 | 50,36 | 55,01 |
| 2011 | 42,94 | 67,83 | 57,97 | 53,43 | 50,36 | 43,39 | 49,56 |
Figure 9. Proportion des sérotypes contenus dans le vaccin PNEU-P-23 par groupe d'âge, 2010-2011
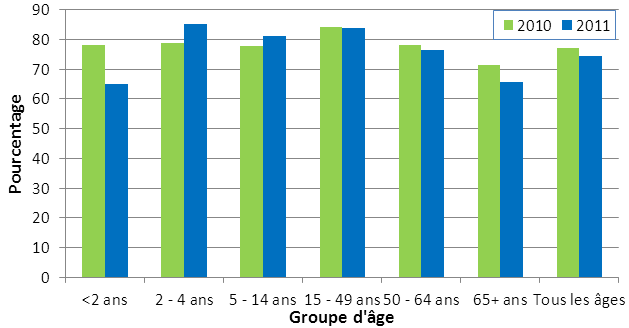
Équivalent textuel pour la figure 9 Proportion des sérotypes contenus dans le vaccin PNEU-P-23 par groupe d'âge, 2010-2011
| Année | <2 ans | 2 à 4 ans | 5 à 14 ans | 15 à 49 ans | 50 à 64 ans | 65+ ans | Tous les âges |
|---|---|---|---|---|---|---|---|
| 2010 | 78,07 | 78,95 | 77,69 | 84,08 | 78,34 | 71,35 | 77,08 |
| 2011 | 65,03 | 85,31 | 81,16 | 83,89 | 76,34 | 65,79 | 74,48 |
IV. Vaccin
IV.1 Préparation(s) autorisées au Canada
Deux formes de vaccin anti-pneumococcique sont présentement disponibles au Canada : un vaccin conjugué (PNEU-C-13 et PNEU-C-10) et un vaccin polysaccharidique (PNEU-P-23).
Prevnar13MD, un vaccin antipneumococcique conjugué, est une solution stérile contenant des antigènes capsulaires polysaccharidiques de 13 sérotypes de la bactérie Streptococcus pneumoniae (1, 3, 4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19A, 19F et 23F). Les polysaccharides sont conjugués séparément à une protéine diphtérique porteuse (CRM197) avant leur combinaison pour former un vaccin multivalent. La protéine porteuse CRM197 est adsorbée sur du phosphate d'aluminium en tant qu'adjuvant. Chaque dose de 0,5 ml de vaccin contient 4,4 µg de polysaccharide 6B et 2,2 µg des polysaccharides de chacun des autres sérotypes.
Le vaccin PNEU-C-13 est analogue au vaccin PNEU-C-7, mais contient six sérotypes supplémentaires, une modification de la conjugaison du sérotype 19F afin d'en accroître la stabilité, 0,02 % de polysorbate (Tween) 80 (un expédient) ainsi qu'un tampon succinate. Le bouchon de la seringue ne contient pas de latex.
Le vaccin PNEU-C-13 est commercialisé sous la forme d'une seringue unidose préremplie contenant 0,5 ml de vaccin.
IV.2 Efficacité potentielle - directe et indirecte (tableau 1)
Se reporter au tableau 1 pour une description détaillée des études
On ne dispose actuellement d'aucune donnée sur l'efficacité potentielle du vaccin PNEU-C-13 pour quelque indication que ce soit chez l'adulte. Des données sur l'efficacité potentielle du vaccin PNEU-C-13 pour la prévention de la pneumonie d'origine communautaire (POC) chez les adultes de 65 ans ou plus devraient être disponibles dans les prochaines années. Un examen approfondi de la littérature n'a révélé aucune étude sur l'efficacité potentielle du vaccin PNEU-C-7 ou PNEU-C-10 chez des adultes en bonne santé. Une étude de l'efficacité potentielle menée auprès d'adultes séropositifs pour le VIH a été trouvée et est résumée ci-après.
Le vaccin PNEU-C-7 présente une bonne efficacité potentielle chez les participants positifs pour le VIH. French et coll. ont réparti aléatoirement 439 Malawites positifs pour le VIH qui s'étaient remis d'une IIP confirmée dans des groupes recevant deux doses du vaccin PNEU-C-7 ou un placebo. Le critère de jugement utilisé était un nouvel épisode d'IIP, dû à l'un des sérotypes présents dans le vaccin, ou dû au sérotype 6A en raison de la possibilité d'une protection croisée. L'efficacité potentielle ajustée de deux doses du vaccin PNEU-C-7 par rapport au placebo était de 69 % (IC à 95 % 16 à 89)Note de bas de page9.
IV.3 Efficacité réelle (tableau 1)
On ne dispose actuellement d'aucune donnée sur l'efficacité du vaccin PNEU-C-13 chez l'adulte. Les seules études d'efficacité réelle existantes ont été menées avec le vaccin PNEU-P-23 auprès d'adultes séropositifs pour le VIH et auprès de personnes âgées; les résultats sont résumés ci-après.
Adultes séropositifs pour le VIH
Même avec des soins et des traitements appropriés, les IIP demeurent une affection sérieuse touchant les personnes vivant avec le VIH et le Sida (PVVIH). Siemieniuk et coll. ont récemment publié une étude canadienne dans laquelle ils décrivent 68 cas d'IIP survenus entre 2000 et 2010 parmi 1 946 PVVIH adultes vivant dans le Sud de l'Alberta. Dans cette étude, le taux d'incidence non-ajusté était de 342/100 000 années-personnes. Dans l'ensemble, 429 (22 %) PVVIH n'avaient jamais reçu le vaccin PNEU-P-23. Chez les personnes vaccinées, 34 % avaient reçu au moins deux doses de vaccin PNEU-P-23. L'administration du vaccin PNEU-P-23 était associée à une diminution du taux d'incidence d'IIP causées par les sérotypes vaccinaux (720 vs 189/100 000 personnes-années avant la vaccination et après la vaccination respectivement; p < 0,0001) et pour l'ensemble des sérotypes (768 vs 244/100 000 personnes-années; p < 0,001). La charge virale, ajustée pour la numération des lymphocytes CD4, était un prédicteur indépendant d'IIP chez les sujets vaccinés. Le rapport de cote (RC) ajusté pour le risque d'IIP était de 2,3 (IC à 95 % 1,0 à 5,4) pour les patients ayant reçu le vaccin PNEU-P-23 au moins une fois tous les cinq ans par rapport à ceux qui l'avaient reçu moins souvent, ce qui illustre à quel point l'efficacité réelle du vaccin PNEU-P-23 est limitée dans cette population, comme l'ont également indiqué d'autres chercheursnote de bas de page10 . Bien que 78 % de la population ait été vaccinée, 74 % des cas d'IIP étaient causés par un sérotype présent dans le vaccin PNEU-P-23; ces cas étaient répartis comme suit : 66 % des sérotypes détectés chez les personnes déjà immunisées étaient des sérotypes inclus dans le PNEU-P-23 contre 86 % des sérotypes détectés chez les personnes qui n'avaient pas été immunisées antérieurement.
Des études antérieures ont révélé le caractère sous-optimal de l'efficacité réelle du vaccin PNEU-P-23 chez les VVIH dans divers contextes. Dans le cadre d'une étude cas-témoins, Breiman et coll. ont observé une efficacité réelle ajustée du vaccin PNEU-P-23 de 49 % (IC à 95 % 12 à 70). Dans cette étude, la race jouait un rôle important dans l'efficacité réelle du vaccin : l'efficacité réelle ajustée était de 74 % (IC à 95 % 8 à 93 %) chez les personnes de race blanche et de 8 % (IC à 95 % -112 à 60 %) chez les personnes de race noirenote de bas de page11. Dans une étude d'observation prospective menée auprès de 507 VVIH (305 avaient reçu et 203 n'avaient pas reçu le vaccin PNEU-P-23), Hung et coll. rapportent un RC ajusté (RCa) de 0,22 (IC à 95 % 0,02 à 2,56) pour la bactériémie à pneumocoque, ce qui donne une efficacité réelle de 78 % (IC à 95 % -156 à 98), de même qu'un RCa de 0,09 (IC à 95 % 0,01 à 0,74) pour l'ensemble des infections à pneumocoque, ce qui donne une efficacité réelle de 91 % (IC à 95 % 26 à 99)note de bas de page12. French et coll. ont réparti aléatoirement 1 392 adultes ougandais infectés par le VIH dans des groupes devant recevoir le vaccin PNEU-P-23 (n = 697) ou un placebo; ils ont fait état d'un rapport de risque (RR) de 1,48 (IC à 95 % 0,7 à 3,3) pour un premier épisode d'IIP, d'un RR de 2,14 (IC à 95 % 0,86 à 5,31) pour une IIP due à un sérotype vaccinal, d'un RR de 2,02 (IC à 95 % 1,19 à 3,45) pour une pneumonie de tout type, et d'un RR de 1,46 (IC à 95 % 0,73 à 2,91) pour une infection pneumococcique de tout type. Les auteurs ont donc conclu que le vaccin PNEU-P-23 était incapable de protéger les VVIH des infections à pneumocoquenote de bas de page13.
Personnes âgées
Vila-Corcoles et coll. ont étudié l'efficacité réelle du vaccin PNEU-P-23 chez des adultes de 65 ans ou plus dans une étude de cohorte prospective (n = 4 986 sujets non vaccinés et n = 6 255 sujets vaccinés avant l'inscription à l'étude). L'efficacité réelle ajustée du vaccin en ce qui concerne la prévention des hospitalisations liées à une pneumonie était de 19 % (IC à 95 % -30 à 49 %). L'efficacité réelle du vaccin était de 15 % (IC à 95 % -31 à 44 %) contre les pneumonies, toutes causes confondues, de 72 % (IC à 95 % 20 à 91 %) contre les décès par pneumonie et de 33 % (IC à 95 % 17 à 46 %) contre la mortalité, toutes causes confonduesNote de bas de page14. Dans une deuxième étude, menée auprès de 11 241 adultes de 65 ans ou plus ayant reçu le vaccin PNEU-P-23, Vila-Corcoles et coll. ont montré que l'efficacité réelle ajustée du vaccin contre les IIP associées à un sérotype vaccinal était de 39 % (IC à 95 % -176 à 87 %). L'efficacité réelle pour la prévention de la pneumonie à pneumocoque était de 45 % (IC à 95 % 12 à 66 %), celle concernant la prévention des hospitalisations liées à une pneumonie était de 26 % (IC à 95 % 8 à 41 %) et celle concernant la prévention des pneumonies de tout type était de 21 % (IC à 95 % 2 à 36 %). Après stratification en fonction du statut vaccinal contre la grippe, les auteurs ont signalé une efficacité réelle de 35 % (IC à 95 % 1 à 57 %) du vaccin PNEU-P-23 concernant la réduction du risque d'hospitalisation liée à une pneumonie chez des sujets non vaccinés contre la grippeNote de bas de page15.
Mooney et coll. se sont également penchés sur l'efficacité réelle du vaccin PNEU-P-23 pour la prévention des IIP chez les adultes de 65 ans ou plus en Écosse au moyen d'une étude de cohorte rétrospective. L'efficacité réelle ajustée (excluant les patients à risque élevé) était de 61,7 % (IC à 95 % 45,1 à 73,2 %), ce qui donne un nombre de sujets à vacciner de 5 206 (IC à 95 % 4 388 à 7 122). L'efficacité réelle ajustée chez les adultes de 65 à 74 ans, excluant les patients à risque élevé, était de 54,4 % (IC à 95 % 20,1 à 74 %), et elle était de 68,8 % (IC à 95 % 52,0 à 79,8 %) chez les adultes de 75 ans ou plusNote de bas de page16.
Melegaro et coll. ont publié une méta-analyse de l'efficacité réelle du vaccin PNEU-P-23. Les estimations regroupées de l'efficacité réelle contre la pneumonie à pneumocoque (excluant les groupes à risque élevé), réalisées à l'aide de modèles à effets aléatoires, étaient de 16 % (IC à 95 % -50 à 50 %); lorsque les groupes à risque élevé étaient inclus, l'efficacité réelle était de -20 % (IC à 95 % -92 à 25 %). L'estimation groupée de l'efficacité réelle contre les IIP dans la population générale de personnes âgées était de 65 % (IC à 95 % -42 à 92 %), et chez les groupes à risque élevé, elle était de 20 % (IC à 95 % -187 à 78 %)note de bas de page17. Cette méta-analyse indique que le vaccin PNEU-P-23 avait une efficacité réelle très limitée chez les personnes âgées.
IV.4 Immunogénicité (tableau 1)
Les groupes à risque élevé suivants ont été examinés séparément : greffés (organe solide, et cellules souches hématopoïétiques), les sujets séropositifs pour le VIH et les personnes âgées (de 65 ans ou plus).
Greffés
A) Greffés d'organes solides
Kumar et coll. ont publié un essai comparatif randomisé (ECR), avec placebo, mené auprès de 130 participants qui avaient subi une greffe du foie au moins trois mois avant l'inscription à l'étude et, s'ils avaient déjà reçu le vaccin PNEU-P-23, l'avaient reçu au moins cinq ans avant l'inscription à l'étude. Soixante-cinq participants ont été répartis aléatoirement dans des groupes pour recevoir un placebo puis le vaccin PNEU-P-23 huit semaines plus tard, ou le vaccin PNEU-C-7 puis le vaccin PNEU-P-23 huit semaines plus tard. Il n'y avait aucune différence de proportion en ce qui concerne les patients qui avaient déjà reçu le vaccin PNEU-P-23 (8 % dans le groupe placebo et 14 % dans le groupe PNEU-C-7, p = 0,17), les patients qui recevaient de la prednisone (p = 0,09) ou les patients qui avaient déjà reçu un traitement par sérum antilymphocytaire (p = 0,06). Il n'y avait aucune différence dans la proportion de greffés qui avaient répondu à au moins un sérotype après 16 semaines (85,7 % vs 91,2 % dans le groupe placebo et le groupe PNEU-C-7, respectivement) ou dans le nombre moyen de sérotypes associés à une réponse (3,7 ± 2,3 vs 4,4 ± 2,2 dans le groupe placebo et le groupe PNEU-C-7, respectivement). Il n'y avait aucune différence dans le titre moyen géométrique (TMG – niveau d'anticorps) spécifique au sérotype, 16 semaines après l'administration de la première dose de vaccin ni dans l'activité opsonophagocytaire (OPA – reconnue comme la meilleure mesure fonctionnelle puisqu'elle représente le principal mécanisme de défense de l'hôte contre l'infection à pneumocoqueNote de bas de page18) lorsqu'on comparait le groupe placebo et le groupe PNEU-C-7, chacun suivi du PNEU-P-23 Note de bas de page19.
Kumar et coll. ont également publié un ECR à double insu mené auprès de 60 participants ayant subi une transplantation rénale de trois mois à trois ans avant l'inscription à l'étude. Les patients qui avaient subi une splénectomie ou qui avaient reçu le vaccin PNEU-P-23 au cours des cinq dernières années étaient exclus. La majorité des participants recevaient encore de la cyclosporine, des corticostéroïdes ou du mofétilmycophénolate (MMF) au moment de la vaccination. Dans chacun des groupes, 30 participants ont été aléatoirement reçus soit le vaccin PNEU-P-23 ou le vaccin PNEU-C-7. Les caractéristiques de base dans les deux groupes étaient similaires. Dans les deux groupes, il n'y avait aucune différence statistiquement significative dans l'augmentation moyenne des TMG spécifiques au sérotype après huit semaines par rapport aux valeurs de référence pour cinq des 7 sérotypes (4, 6B, 14, 18C, 19F). L'augmentation des TMG était plus importante après l'administration du vaccin PNEU-C-7 qu'après celle du vaccin PNEU-P-23 pour le sérotype 23F, et le taux de réponse semblait être meilleur dans le cas du sérotype 9 (p = 0,09). La proportion de patients ayant répondu (augmentation d'au moins un facteur de 2 des titres ELISA par rapport aux valeurs de référence, avec un titre absolu d'au moins 1 µg/ml) à au moins un sérotype était similaire dans les deux groupes (73,3 % vs 53,3 % dans le groupe PNEU-C-7 et le groupe PNEU-P-23, respectivement; p = 0,11). Le nombre médian de sérotypes associés à une réponse était de 2,5 (PNEU-C-7) et de 1,0 (PNEU-P-23); p = 0,069. Il n'y avait aucune différence entre les groupes en ce qui concerne le facteur d'augmentation des titres mesurés par l'OPA : une OPA contre un des sérotypes a été observée chez 80 % des participants après l'administration du vaccin PNEU-C-7 et chez 83,3 % des participants après l'administration du vaccin PNEU-P-23note de bas de page20. Un suivi effectué trois ans plus tard (PNEU-C-7 [n =23] ou PNEU-P-23 [n = 24]) a révélé qu'il n'y avait aucune différence quant à la proportion de participants ayant maintenu une réponse spécifique au sérotype après trois ans pour l'ensemble des sept sérotypes. Les TMG globaux après trois ans avaient chuté considérablement pour six des sept sérotypes en comparaison aux titres mesurés après huit semaines, sauf dans le cas du sérotype 19F (aucune différence). Toutefois, les titres après trois ans étaient nettement plus élevés dans les deux groupes que les titres mesurés avant la vaccination pour tous les sérotypes sauf le 14. Le taux de diminution du TMG était semblable dans les deux groupesnote de bas de page21.
Tobudic et coll.Note de bas de page22 ont mené une étude comparative randomisée à simple insu dans le but de déterminer l'utilité d'une dose initiale du vaccin PNEU-C-7 ou du vaccin PNEU-P-23 avant l'administration d'une dose de rappel du vaccin PNEU-P-23 une année plus tard chez des adultes ayant subi une transplantation rénale. La transplantation avait eu lieu au moins six mois avant l'inscription à l'étude. Les critères d'exclusion étaient les suivants : splénectomie, vaccination contre le pneumocoque au cours des cinq années précédant l'inscription à l'étude, traitement visant à prévenir le rejet d'une allogreffe, IGIV au cours des six semaines précédentes, maladie fébrile aiguë dans les deux semaines précédentes. Au total, 80 participants ont aléatoirement reçu le vaccin PNEU-C-7 ou le vaccin PNEU-P-23 puis une dose de rappel du vaccin PNEU-P-23 un an plus tard. Ces groupes ont été comparés entre eux puis avec le groupe initial, qui n'avait reçu que le vaccin PNEU-P-23. Les paramètres mesurés étaient une augmentation d'un facteur de 2 de la concentration d'anticorps par rapport aux valeurs de référence et une valeur absolue ≥ 1 µg/ml après la vaccination. Dans le groupe PNEU-C-7, 77,1 % des sujets avaient présenté une réponse à au moins un sérotype, comparativement à 93,1 % dans le groupe PNEU-P-23 (p = 0,046). Après l'administration de la dose de rappel (vaccin PNEU-P-23) un an plus tard, la réponse à au moins un sérotype était de 87,5 % dans le groupe PNEU-C-7/PNEU-P-23 et de 87,1 % dans le groupe PNEU-P-23/PNEU-P-23. Le nombre médian de sérotypes associés à une réponse n'était pas statistiquement différent entre les deux groupes. À la lumière de ces résultats, les auteurs ont conclu que l'administration d'une seule dose de vaccin PNEU-P-23 devrait demeurer la norme chez les patients adultes ayant subi une transplantation rénale.
B) Greffés de cellules souches hématopoïétiques (GCSH) Cordonnier et coll. ont publié un ECR multicentrique mené auprès de 158 GCSH allogéniques répartis aléatoirement dans des groupes pour recevoir le vaccin PNEU-C-7 3, 4 et 5 mois après la GCSH puis le vaccin PNEU-P-23 (groupe d'administration précoce; n = 75) 12 mois après la GCSH, ou le vaccin PNEU-C-7 9, 10 et 11 mois après la GCSH puis le vaccin PNEU-P-23 18 mois après la GCSH (groupe d'administration tardive; n = 83). Les caractéristiques de base étaient semblables dans les deux groupes, mais il y avait une différence significative en ce qui concerne la proportion de participants présentant des titres d'anticorps ≥ 0,15 µg/ml contre l'ensemble des sept sérotypes avant l'administration du vaccin PNEU-C-7 (44 % dans le groupe d'administration précoce vs 9 % dans le groupe d'administration tardive; p < 0,001). Un mois après l'administration de la troisième dose de vaccin PNEU-C-7, 79 % et 82 % des participants présentaient des titres d'anticorps ≥ 0,15 µg/ml contre l'ensemble des sept sérotypes, et 56 % vs 54 % présentaient une réponse à l'ensemble des sept sérotypes (TMG ≥ 0,5 µg/ml) dans le groupe d'administration précoce et le groupe d'administration tardive, respectivement. Vingt-quatre mois après la GCSH, 59 % vs 83 % (p = 0,013) des participants présentaient des titres d'anticorps ≥ 0,15 µg/ml contre l'ensemble des sept sérotypes, et 34 % vs 55 % présentaient une réponse à l'ensemble des sept sérotypes (TMG ≥ 0,5 µg/ml) dans le groupe d'administration précoce et le groupe d'administration tardive, respectivement. Un mois après l'administration de la troisième dose du vaccin PNEU-C-7, il n'y avait aucune différence concernant les TMG contre les sérotypes dans les deux groupes. Cependant, 24 mois après la GCSH, les TMG étaient significativement plus faibles contre tous les sérotypes, sauf pour le 23F, dans le groupe d'administration précocenote de bas de page23.
Molrine et coll. ont étudié l'immunisation des donneurs dans le cadre d'un ECR mené auprès de receveurs de GCSH allogéniques. Certains donneurs ont reçu le vaccin PNEU-C-7 10 jours avant le don de cellules souches, et d'autres, non. Tous les receveurs se sont vus administrer le vaccin PNEU-C-7 3, 6 et 12 mois après la GCSH. Les donneurs de 30 receveurs de GCSH avaient été immunisés, les donneurs de 35 autres receveurs n'avaient pas été immunisés, et 31 receveurs n'étaient pas évaluables (21 sont décédés peu avant ou peu après la greffe, 5 ont été exclus avant la greffe, 2 ont été exclus pour avoir violé le protocole expérimental, et 3 avaient subi une rechute). Il n'y avait aucune différence entre les deux groupes quant à la proportion de receveurs ayant un TMG ≥ 0,5 µg/ml 3, 12 et 13 mois après la GCSH. Les différences entre les TMG des greffés étaient considérablement plus élevées 6 et à 12 mois post-greffe pour les sérotypes 6B, 9V, 18C, 19F et 23F lorsque le donneur était immunisé. En dépit de difficultés d'interprétation, les chercheurs ont comparé les concentrations de TMG après l'administration du vaccin PNEU-C-7 dans cette étude avec les résultats obtenus lors d'une étude antérieure chez des receveurs de GCSH allogéniques à qui on avait administré le vaccin PNEU-P-23 12 mois après la greffe. On a constaté que les concentrations de TMG étaient significativement plus élevées pour les sept sérotypes communs aux deux vaccins avec le vaccin PNEU-C-7 plutôt qu'avec le vaccin PNEU-P-23Note de bas de page24.
Kumar et coll. ont réparti aléatoirement 64 paires donneur-receveur de GCSH allogénique (32 paires par groupe) dans des groupes devant recevoir le vaccin PNEU-P-23 ou le vaccin PNEU-C-7 : les donneurs avaient été vaccinés au moins deux semaines avant le don des cellules souches, et les receveurs de GCSH se sont vu administrer une dose du vaccin six mois après la GCSH. Les caractéristiques de base étaient semblables dans les deux groupes (donneurs et receveurs). Deux semaines après la vaccination, il n'y avait pas de différence entre les deux groupes en ce qui concerne les TMG des donneurs. Six mois après la GCSH, les TMG étaient semblables pour les sept sérotypes, sauf le 6B (plus élevé après le vaccin PNEU-C-7). Douze mois après la GCSH, les TMG étaient plus élevés après le vaccin PNEU-C-7 pour les sérotypes 14 et 18C. Une réponse à au moins un sérotype (≥ 0,35 µg/ml) a été observée chez 38,1 % et 0 % des receveurs de GCSH après le vaccin PNEU-C-7 et le vaccin PNEU-P-23 six mois après la GCSH, respectivement (p = 0,003). Douze mois après la GCSH, la proportion de sujets présentant une réponse était de 90,8 % vs 55,6 % dans le groupe PNEU-C-7 vs le groupe PNEU-P-23, respectivement (p = 0,02)Note de bas de page25.
Participants séropositifs pour le VIH
Feikin et coll. ont réparti aléatoirement 90 PVVIH (numération des CD4 d'au moins 200 cellules/µl) dans des groupes recevant deux doses d'une association de placebo, vaccin PNEU-C-7 et vaccin PNEU-P-23. Il y avait 67 patients évaluables. Les participants ayant reçu le vaccin PNEU-C-7 tendaient à présenter une meilleure réponse que ceux ayant reçu le vaccin PNEU-P-23 pour trois des cinq sérotypes à l'étude (23F, 4, 9V). Toutefois, la seconde dose de vaccin n'a entraîné aucun bénéfice additionnel: après la seconde dose, la concentration moyenne géométrique (CMG) était équivalente chez les participants ayant reçu les vaccins PNEU-C-7/PNEU-C-7 ou PNEU-C-7/PNEU-P-23. Les titres d'OPA étaient significativement meilleurs après le vaccin PNEU-C-7 qu'après le vaccin PNEU-P-23 pour les cinq sérotypes à l'étude. Une fois de plus, la seconde dose n'a provoqué aucune augmentation des titres d'OPANote de bas de page26.
Penaranda et coll. ont réparti aléatoirement 220 PVVIH (CD4 : 200 à 500 cellules/µl, charge virale < 5 log copies/ml) dans des groupes devant recevoir les vaccins PNEU-C-7/PNEU-P-23 ou le vaccin PNEU-P-23 (n = 110 dans chaque groupe). Les caractéristiques de base étaient semblables dans les deux groupes, et une forte proportion des patients recevait un traitement antirétroviral hautement actif (HAART) (98 % et 91 %). Il n'y avait aucune différence statistique dans la proportion de sujets ayant présenté une réponse après huit semaines (augmentation d'un facteur de 2 des IgG et titre minimum de 1 µg/ml) et il n'y avait aucune différence quant à l'avidité des IgGNote de bas de page27.
Crum-Cianflone et coll. ont réparti aléatoirement des patients de la façon suivante : 131 PVVIH dans un groupe devant être revacciné avec le vaccin PNEU-C-7 et 73 patients PVVIH dans un groupe devant être revacciné avec le vaccin PNEU-P-23 de trois à huit ans après la dernière dose du vaccin PNEU-P-23. Vingt-cinq participants négatifs pour le VIH qui n'avaient pas été vaccinés auparavant ont reçu le vaccin PNEU-C-7. Le nombre médian de lymphocytes CD4 était de 533 et de 513 cellules/mm3 dans le groupe PNEU-C-7 et le groupe PNEU-P-23, respectivement. Les participants du groupe PNEU-C-7 étaient plus nombreux à suivre un traitement HAART (84,7 % vs 56 %). La proportion de sujets ayant présenté une augmentation d'un facteur de 2 du titre des IgG au jour 60 pour deux des quatre sérotypes (4, 9V, 14, 19F) était plus élevée dans le groupe revacciné avec le vaccin PNEU-C-7 (57 %) que dans celui revacciné avec le vaccin PNEU-P-23 (36 %); p = 0,004. La proportion de sujets négatifs pour le VIH ayant présenté une réponse était de 88 %. Le RC (ajusté en fonction de la numération des lymphocytes CD4, de l'âge, de l'ethnicité, d'une pneumonie antérieure, du traitement HAART lors de la vaccination et de la charge virale du VIH) associé à une réponse à deux sérotypes sur quatre chez les patients infectés par le VIH était de 2,6 (IC à 95 % 1,4 à 5,0) lorsqu'on comparait le groupe PNEU-C-7 et le groupe PNEU-P-23note de bas de page28.
Lesprit et coll. ont réparti aléatoirement 212 PVVIH (CD4 : 200 à 500 cellules/µl) dans des groupes recevant les vaccins PNEU-C-7/PNEU-P-23 (n = 106) ou le vaccin PNEU-P-23 seul. Les titres de base en ce qui concerne les IgG, de même que les caractéristiques de base, étaient semblables dans les deux groupes. Quatre semaines après l'administration de la dernière dose de vaccin, les titres d'IgG étaient semblables dans les deux groupes; la réponse observée était toutefois meilleure après l'administration des vaccins PNEU-C-7/PNEU-P-23 dans le cas des sérotypes 18C et 23F. À la semaine 24, les titres d'IgG étaient plus élevés dans le groupe PNEU-C-7/PNEU-P-23 pour quatre des sept sérotypes. La proportion de sujets présentant une réponse (augmentation d'un facteur de 2 du titre d'IgG et titre minimum de 1 mg/L) à cinq des sept sérotypes était plus élevée dans le groupe PNEU-C-7/PNEU-P-23 (59 %) que dans le groupe n'ayant reçu que le vaccin PNEU-P-23 (40 %); p = 0,005. On a observé le même phénomène après 24 semaines : 30 % des sujets avaient présenté une réponse à cinq des sept sérotypes dans le groupe PNEU-C-7/PNEU-P-23, et seulement 10 % dans le groupe PNEU-P-23, respectivement (p = 0,003)note de bas de page29.
Personnes âgées
Deux études multicentriques ont porté sur l'immunogénicité associée à l'administration concomitante du vaccin trivalent contre l'influenza (VTI) et du vaccin PNEU-C-13 chez des participants en bonne santé n'ayant jamais reçu de vaccin contre le pneumocoque âgés de 50 à 59 ans (étude américaine)note de bas de page30 et de 65 ans ou plus (étude européenne)note de bas de page31. Dans ces études, les auteurs ont comparé l'administration des vaccins PNEU-C-13/VTI suivie, un mois plus tard, par l'administration d'un placebo et l'administration du VTI avec un placebo suivie, un mois plus tard, par le vaccin PNEU-C-13. Aucune comparaison n'a été effectuée avec le vaccin PNEU-P-23. Schwarz et coll. ont rapporté que les CMG pour 13 sérotypes se situaient entre 1,08 (sérotype 3) et 11,93 (19A) µg/ml dans le groupe d'administration concomitante et entre 1,15 (3) et 17,10 (19A) µg/ml lorsque le vaccin PNEU-C-13 était administré seul; les ratios des CMG (administration concomitante/PNEU-C-13 seul) étaient < 1,0, et outre le sérotype 19F, tous ont atteint le critère de non-infériorité prédéterminé. La réponse au VTI était similaire dans les deux groupesnote de bas de page31. De même, Frenck et coll. ont fait état de CMG se situant entre 1,15 (sérotype 3) et 16,80 (19A) µg/ml dans le groupe d'administration concomitante et entre 1,46 (3) et 18,84 (19A) µg/ml lorsque le vaccin PNEU-C-13 était administré seul. Les CMG mesurées par l'OPA se situaient entre 61 (sérotype 3) et 2 421 (6B) dans le groupe d'administration concomitante et entre 78 (3) et 3 215 (6B) lorsque le vaccin PNEU-C-13 était administré seul. Bien que, dans cette étude, les ratios des CMG aient tous été < 1, tous les sérotypes ont atteint le critère de non-infériorité. En ce qui concerne les ratios des TMG mesurés par l'OPA, bien qu'ils aient aussi tous été < 1, 5 des 13 sérotypes (1, 5, 7F, 9V et 19F) n'ont pas atteint le critère de non-infériorité (limite inférieure de l'IC à 95 % < 0,5)note de bas de page30.
Jackson et coll. ont réparti aléatoirement des adultes en bonne santé de 70 à 79 ans qui avaient reçu le vaccin PNEU-P-23 lorsqu'ils avaient 65 ans ou plus (au moins cinq ans avant l'étude) dans des groupes recevant une dose du vaccin PNEU-P-23 ou du vaccin PNEU-C-7, à raison de 0,5, 1 ou 2 ml. Les titres mesurés après la vaccination étaient significativement plus élevés chez les sujets ayant reçu la dose de 2 ml par rapport à ceux ayant reçu la dose de 0,5 ml pour trois des sept sérotypes (6B, 9V, 23F) et significativement plus élevés chez les sujets ayant reçu les doses de 1 ml et de 2 ml que chez ceux ayant reçu la dose de 0,5 ml pour les sérotypes 18C et 19. Un an après la vaccination, les CMG associées à tous les sérotypes étaient semblables aux titres mesurés avant la vaccination, pour tous les vaccins et pour toutes les doses. Il n'y avait aucune différence significative de la CMG entre le vaccin PNEU-C-7 (0,5 ml) et le vaccin PNEU-P-23; toutefois, après ajustement en fonction de la CMG de base, deux sérotypes répondaient au critère d'immunogénicité supérieure dans le groupe PNEU-C-7. Les TMG mesurés par l'OPA étaient considérablement plus élevés après le vaccin PNEU-C-7 (0,5 ml) qu'après le vaccin PNEU-P-23 pour les sérotypes 9V et 23F. Cependant, il n'y avait aucune différence significative entre les TMG mesurés par l'OPA un an après la vaccinationnote de bas de page32.
De Roux et coll. ont réparti aléatoirement 219 adultes de 70 ans ou plus dans des groupes devant recevoir une première dose de vaccin PNEU-C-7 (n = 110) ou de vaccin PNEU-P-23 (n = 109) suivi un an plus du vaccin PNEU-C-7 (PNEU-C-7/PNEU-C-7) ou PNEU-P-23 (PNEU-C-7/PNEU-P-23) pour les patients ayant d'abord reçu le vaccin PNEU-C-7, et le vaccin PNEU-C-7 (PNEU-P-23/PNEU-C-7) pour les patients ayant d'abord reçu le vaccin PNEU-P-23. Les titres d'IgG spécifiques étaient significativement plus élevés un mois après la première dose de vaccin PNEU-C-7 par rapport au vaccin PNEU-P-23. Les titres étaient considérablement plus faibles après un mois chez les sujets ayant reçu le vaccin PNEU-P-23 puis, un an plus tard, le vaccin PNEU-C-7 par rapport aux sujets ayant reçu une seule dose du vaccin PNEU-C-7. Aucun avantage additionnel n'a été observé après l'administration d'une seconde dose de vaccin PNEU-C-7 un an après l'administration d'une première dose de vaccin PNEU-C-7. Les TMG mesurés par l'OPA suivaient les mêmes tendances que les titres des IgGNote de bas de page33.
Miernyk et coll. ont réparti aléatoirement des Autochtones de l'Alaska de 55 à 70 ans qui n'avaient jamais reçu de vaccin contre le pneumocoque en trois groupes devant recevoir le vaccin PNEU-P-23 (n = 28), le vaccin PNEU-C-7 suivi du PNEU-P-23 deux mois plus tard (n = 29), ou le vaccin PNEU-C-7 suivi du vaccin PNEU-P-23 six mois plus tard (n = 29). Les caractéristiques de base des trois groupes étaient semblables. On a observé une augmentation significative des CMG pour tous les sérotypes vaccinaux par rapport aux valeurs de base dans les trois groupes (PNEU-P-23 [1 groupe] et PNEU-C-7 [2 groupes]), et l'augmentation était semblable dans les trois groupes, sauf en ce qui concerne le sérotype 1, qui était plus élevé après le vaccin PNEU-P-23. Deux mois après la dernière dose, il n'y avait aucune différence entre les trois groupes relativement aux CMG associées à tous les sérotypes. Les titres mesurés par l'OPA un mois après la première dose et deux mois après la dernière dose étaient semblables dans les trois groupesNote de bas de page34.
Goldblatt et coll. ont réparti aléatoirement des patients de 50 à 80 ans qui n'avaient pas reçu de vaccin contre le pneumocoque au cours des cinq dernières années dans des groupes devant recevoir le vaccin PNEU-C-7 suivi du PNEU-C-7 six mois plus tard (n = 133); le vaccin PNEU-C-7 suivi du PNEU-P-23 six mois plus tard (n = 171), le vaccin PNEU-P-23 seul (n = 159) ou le vaccin PNEU-C-7 seul (n = 136). Un mois après l'administration du vaccin PNEU-C-7 ou du vaccin PNEU-P-23, les CMG des sérotypes 4, 9 et 23F étaient plus élevées avec le vaccin PNEU-C-7; cependant, un an après la vaccination, il n'y avait plus de différence significative entre les deux groupes pour six des sept sérotypes (la CMG du sérotype 23F était plus élevée avec le vaccin PNEU-C-7). Un mois après la seconde dose, il n'y avait plus de différence sur le plan des CMG pour six des sept sérotypes (la CMG du sérotype 19F était plus élevée après les vaccins PNEU-C-7/PNEU-P-23 qu'après les vaccins PNEU-C-7/PNEU-C-7). Un an après l'administration des vaccins PNEU-C-7/PNEU-C-7 vs PNEU-P-23, la proportion de sujets présentant des concentrations d'anticorps > 1 µg/ml n'était pas différentenote de bas de page35.
Schenkein et coll. ont sélectionné aléatoirement 45 adultes de < 45 ans et 58 adultes de 65 ans ou plus pour leur administrer le vaccin PNEU-P-23. Il n'y avait aucune différence entre les deux groupes de sujets en ce qui concerne la CMG. On a toutefois démontré une activité anticorps (titres d'opsonisation) significativement plus importante contre tous les sérotypes chez les sujets plus jeunesNote de bas de page36.
Musher et coll. ont réparti aléatoirement des adultes de 50 à 65 ans et de 65 ans ou plus qui avaient déjà reçu le vaccin PNEU-P-23 (pas de minimum d'intervalle entre la dose antérieure du vaccin PNEU-P-23 et l'inscription à l'étude) ou non en deux groupes devant recevoir le vaccin PNEU-P-23 ou un placebo. Les chercheurs ont indiqué qu'il n'y avait aucune différence significative, à 30 jours et à 60 jours, entre les groupes qui recevaient le vaccin pour la première fois et le groupe revacciné en ce qui concerne les titres d'IgG pour tous les sérotypes, sauf pour les sérotypes 8 et 14 dans le groupe des 65 ans et plus et pour le sérotype 14 dans le groupe des 50 à 65 ansNote de bas de page37.
IV.5 Administration du vaccin et calendrier
La dose du vaccin PNEU-C-13 chez l'adulte est une injection de 0,5 ml par voie IM, laquelle devrait être suivie d'une dose de vaccin PNEU-P-23 deux mois plus tard dans le cas des patients à risque élevé d'IIP. Les greffés de cellules souches hématopoïétiques devraient recevoir une première série de trois doses de vaccin PNEU-C-13 administrées à un intervalle minimum de 4 semaines. Le moment exact auquel la série vaccinale devrait être amorcée sera à déterminer au cas par cas, en consultation avec un hémato-oncologue. Selon les articles publiés sur le sujet, la première série peut être amorcée de trois à neuf mois après la greffe. Cette série primaire devrait être suivie d'une injection de rappel du vaccin PNEU-P-23, administrée 6 à 12 mois plus tard.
IV.6 Épreuves sérologiques
Il n'y a aucune indication relativement à la réalisation d'épreuves sérologiques systématiques avant ou après l'immunisation.
IV.7 Exigences en matière d'entreposage
Le vaccin doit être réfrigéré à une température de 2 °C à 8 °C. S'il est soumis à des températures inférieures au point de congélation, le vaccin doit être jeté. En cas de rupture temporaire de la chaîne de froid, la stabilité du vaccin PNEU-C-13 est assurée jusqu'à 40 °C pendant un maximum de quatre joursNote de bas de page38. Les praticiens devraient toutefois se conformer aux normes provinciales usuelles pour déterminer la viabilité du vaccin en cas de rupture de la chaîne de froid.
IV.8 Administration en concomitance avec d'autres vaccins
Dans la population adulte, le vaccin PNEU-C-13 a été administré en concomitance avec le VTI uniquementNote de bas de page30,Note de bas de page31 , et la réponse immunitaire au VTI semble similaire que le VTI ait été administré seul ou en concomitance avec le vaccin PNEU-C-13. Dans la plupart des cas, les titres spécifiques d'anticorps n'étaient pas différents lorsque le vaccin PNEU-C-13 était administré seul ou en concomitance. Une étude a révélé une diminution des TMG mesurés par l'OPA lorsque le vaccin PNEU-C-13 était administré en concomitance avec le VTI, mais les implications cliniques de cette observation ne sont pas claires.
Le vaccin PNEU-C-13 a été étudié en administration concomitante avec un certain nombre d'antigènes utilisés dans le cadre d'un calendrier vaccinal pédiatrique canadien, et il n'y a eu aucun effet négatif sur l'immunogénicité ou le profil d'innocuité du vaccin. Les antigènes en question sont notamment ceux de la diphtérie, du tétanos, de la coqueluche (acellulaire), de l'Haemophilus influenzae de type b, de la poliomyélite (inactivé), de l'hépatite B, du méningocoques du sérogroupe C, de la rougeole, des oreillons, de la rubéole et de la varicelleNote de bas de page39. Comme le veulent les recommandations générales en matière de vaccination, il faut administrer le vaccin PNEU-C-13 en utilisant un site d'injection distinct de ceux utilisés pour les vaccins administrés en concomitance, en employant une seringue et une aiguille différentes.
IV.9 Évènements indésirables
Le vaccin PNEU-C-13 a été administré à 2 276 adultes de 50 ans ou plus dans deux études distinctes. Au total, 943 d'entre eux ont reçu le vaccin PNEU-C-13 seul : 453 âgés de 50-59 ans et 470 âgés de 65 ans et plus. Parmi ces participants, 607/926 (66 %) ont signalé une réaction localisée, le plus souvent de la douleur au site d'injection (chez 587/923 participants, soit 64 %). Des effets indésirables systémiques (de tous types) ont été signalés chez 562/912 (62 %) participants, les plus fréquents étant la fatigue (305/795; 38 %), les céphalées (283/787; 36 %) et les myalgies d'apparition récente (312/798; 39 %). Une fièvre (de 38 °C ou plus) a été signalée chez 21/663 (3 %) des participantsnote de bas de page30 note de bas de page31.
L'innocuité a été évaluée dans six essais cliniques (parmi lesquels figurent les deux essais décrits précédemment)note de bas de page38 : le vaccin PNEU-C-13 a été administré à 5 667 adultes; 2 616 adultes avaient entre 50 et 64 ans, et 3 051 adultes avaient 65 ans ou plus. Parmi les sujets ayant reçu le vaccin PNEU-C-13, 1 916 adultes avaient déjà reçu le vaccin PNEU-P-23 au moins trois ans plus tôt, et 3 751 adultes n'avaient jamais reçu le vaccin PNEU-P-23. Les résultats obtenus figurent ci-après.
Réactions localesNote de bas de page38
Chez les adultes de 50 à 59 ans n'ayant jamais reçu le vaccin PNEU-P-23, l'événement indésirable le plus fréquent était une douleur au site d'injection (88,8 %), mais celle-ci était légère dans la majorité des cas (85,9 %). Les autres événements locaux indésirables étaient une limitation de l'amplitude des mouvements du bras (40,7 % – légère dans la plupart des cas), un œdème (21,7 %) et des rougeurs (15,8 %). Chez les adultes de 60 à 64 ans n'ayant jamais reçu le vaccin PNEU-P-23, 80,1 % et 69,2 % des participants (deux études différentes) ont éprouvé de la douleur, ce qui était plus important qu'après le vaccin PNEU-P-23 (73,4 % et 58,3 %). La douleur était principalement de faible intensité. Les participants ont fait état d'une limitation de l'amplitude des mouvements du bras dans 28,5 % et 23,5 % des cas (moins fréquemment qu'après le PNEU-P-23), de rougeurs dans 20,2 % et 12,2 % des cas, et d'un œdème dans 19,3 % et 10 % des cas. Chez les adultes de 68 ans ou plus ayant déjà reçu le vaccin PNEU-P-23, 51 % ont éprouvé de la douleur, 16,2 % présentaient une limitation de l'amplitude des mouvements du bras, 14,3 % présentaient des rougeurs et 12,8 % avaient signalé un œdème. Chez les adultes de 70 ans ou plus ayant déjà reçu le vaccin PNEU-P-23, 51,7 % ont éprouvé de la douleur, 10,5 % présentaient une limitation de l'amplitude des mouvements du bras, 10,8 % présentaient des rougeurs et 10,4 % ont signalé un œdème, ce qui était considérablement moins important qu'après le vaccin PNEU-P-23 en ce qui concerne la limitation de l'amplitude des mouvements du bras (27,6 %), les rougeurs (22,2 %) et l'œdème (23,1 %).
Événements systémiquesNote de bas de page38
Chez les adultes de 50 à 59 ans n'ayant jamais reçu le vaccin PNEU-P-23, les événements les plus fréquents étaient les céphalées (65,9 %), puis la fatigue (63,3 %), la myalgie (61,8 %), l'arthralgie (31,5 %), l'anorexie (25,3 %), les frissons (19,6 %) et les éruptions cutanées (14,2 %).
Dans les deux études menées auprès d'adultes de 60 à 64 ans qui n'avaient jamais reçu le vaccin PNEU-P-23, 63,2 % et 50,5 % des sujets ont éprouvé de la fatigue, 54 % et 49,7 % ont eu des céphalées, 56,2% et 46,9 % ont décrit des symptômes de myalgie, 24,4 % et 15,5 % présentaient une arthralgie, 23,5 % et 19,9 % avaient des frissons, et 16,5 % et 8,6 % présentaient des éruptions cutanées. Dans une des études, la proportion d'événements indésirables déclarés après le vaccin PNEU-C-13 n'était pas différente de la proportion d'événements indésirables déclarés après le vaccin PNEU-P-23. Dans la deuxième étude, l'arthralgie (23,8 %) et l'anorexie (23 %) étaient signalées plus souvent après le vaccin PNEU-P-23 qu'après le vaccin PNEU-C-13.
Chez les adultes de 68 ans ou plus ayant déjà reçu le vaccin PNEU-P-23, les événements indésirables suivants ont été signalés par les sujets selon la proportion indiquée entre parenthèses : fatigue (34,4 %), céphalées (26,1 %), myalgie (25,3 %), diarrhée (14,5 %), arthralgie (12,8 %), anorexie (11,2 %), éruptions cutanées (8,4 %) et frissons (7,5 %). Chez les adultes de 70 ans ou plus ayant déjà reçu le vaccin PNEU-P-23, les événements indésirables suivants ont été signalés : myalgie (36,8 %), fatigue (34 %), céphalées (23,7 %), arthralgie (12,6 %), anorexie (10,4 %), frissons (7,9 %) et éruptions cutanées (7,3 %). Les événements indésirables sollicités suivants étaient considérablement plus fréquents après le vaccin PNEU-P-23 dans la même étude : fatigue (43,3 %), myalgie (44,7 %) et éruptions cutanées (16,4 %). La fièvre (de tout type) a été signalée par 1,1 % à 4,2 % des participants après le vaccin PNEU-C-13, et par 1,1 % à 2,3 % des participants après le vaccin PNEU-P-23. Dans la plupart des cas, la fièvre était caractérisée par une température de 38 °C à 38,5 °C.
IV.10 Contre-indications et précautions
Le vaccin PNEU-C-13 est contre-indiqué chez les personnes ayant des antécédents de réaction anaphylactique à un composant du vaccin, y compris l'anatoxine diphtérique.
V. Résumé
Les données passées en revue révèlent que la réponse immunitaire induite par les vaccins conjugués contre le pneumocoque est meilleure que celle provoquée par le vaccin PNEU-P-23 chez les adultes ayant reçu une GCSH. Dans le cas des greffés d'organes solides, les données ne sont pas aussi probantes. L'efficacité réelle du vaccin PNEU-P-23 chez les personnes vivant avec le VIH et le Sida est, au mieux, faible, mais elle est le plus souvent insuffisante pour que l'on puisse parler d'un véritable effet protecteur; le vaccin PNEU-C-7, toutefois, confère une meilleure protection. Aucune étude de l'efficacité potentielle ou de l'efficacité réelle des vaccins conjugués contre le pneumocoque n'a été menée chez les personnes âgées. Par ailleurs, les résultats découlant des études d'immunogénicité où l'on a comparé l'utilisation du vaccin PNEU-C-7 et celle du vaccin PNEU-P-23 ont fait état de titres d'anticorps semblables un an après l'administration de ces vaccins en ce qui a trait aux sept sérotypes communs. Du reste, on ne dispose pas actuellement d'études sur l'immunogénicité comparant l'utilisation du vaccin PNEU-C-13 et celle du vaccin PNEU-P-23 chez les personnes âgées; ni de corrélats de la protection définis qui permettraient d'interpréter les données d'immunogénicité dans ce segment de la population.
VI. Recommandations
Il est à noter que les provinces et les territoires doivent examiner les facteurs économiques et les autres facteurs programmatiques/opérationnels locaux lorsqu'ils envisagent d'inclure les recommandations suivantes aux programmes d'immunisation subventionnés par l'État.
Les recommandations suivantes seront réexaminées et mises à jour lorsque de nouvelles données seront disponibles.
Recommandation 1
Le CCNI a conclu qu'il existait des données probantes suffisantes pour recommander l'utilisation du vaccin PNEU-C-13 chez les greffés de cellules souches hématopoïétiques (GCSH), compte tenu de la meilleure immunogénicité associée aux vaccins conjugués contre le pneumocoque dans cette population par rapport au vaccin PNEU-P-23. Les GCSH devraient recevoir une série vaccinale primaire de trois doses de vaccin PNEU-C-13, trois à neuf mois après la greffe, après consultation avec un spécialiste en greffe. Les trois doses de la série primaire devraient être administrées à au moins quatre semaines d'intervalle et être suivies par une dose de rappel du vaccin PNEU-P-23 de 12 à 18 mois après la greffe (6 à 12 mois après la dernière dose du vaccin PNEU-C-13). (Recommandation du CCNI de catégorie A)
Recommandation 2
Le CCNI a conclu qu'il existait des données probantes suffisantes pour recommander l'utilisation du vaccin PNEU-C-13 chez les patients positifs pour le VIH, compte tenu des meilleures efficacités potentielle et réelle associées au vaccin conjugué contre le pneumocoque (PNEU-C-7) dans cette population. Les sujets positifs pour le VIH devraient recevoir une dose de vaccin PNEU-C-13, puis une dose de vaccin PNEU-P-23 huit semaines plus tard. Pour l'heure, aucune donnée probante n'indique que l'administration d'une dose de rappel du vaccin PNEU-C-13 confère un quelconque avantage. (Recommandation du CCNI de catégorie A)
La plupart des études publiées excluaient les participants qui avaient reçu une dose de vaccin PNEU-P-23 dans les cinq années précédant l'inscription à l'étude. Par conséquent, on ignore quel serait l'intervalle minimum à respecter entre la dernière dose de vaccin PNEU-P-23 reçue et le vaccin PNEU-C-13. Cependant, vu la possibilité d'une diminution des titres d'anticorps après l'administration du vaccin PNEU-P-23, vu la gravité de l'IIP chez les sujets immunodéprimés et vu les avantages associés au vaccin PNEU-C-13 dans cette population de patients, le CCNI recommande d'administrer le vaccin PNEU-C-13 au moins un an après la dernière dose de vaccin PNEU-P-23 (avis d'experts).
L'administration d'une dose de rappel à vie de PNEU-P-23 est recommandée pour les individus à haut risque d'IIP, entre autres les personnes vivant avec le VIH. Ceux ayant préalablement été vaccinés avec le PNEU-P-23 et qui nécessiteraient une dose supplémentaire de PNEU-P-23 devraient la recevoir au moins 8 semaines après la dose de PNEU-C-13 et au moins 5 ans après la dose la plus récente de PNEU-P-23 (avis d'experts).
Recommandation 3
Le CCNI a conclu qu'il existait des données probantes acceptables pour recommander l'utilisation du vaccin PNEU-C-13 chez les sujets immunodéprimés dont l'état est dû à l'une ou l'autre des raisons suivantes :
- asplénie (anatomique ou fonctionnelle);
- anémie falciforme ou autre hémoglobinopathie;
- déficit immunitaire congénital de tout type, touchant notamment l'immunité à médiation humorale (lymphocytes B) ou à médiation cellulaire (lymphocytes T), le système du complément (déficit en properdine ou en facteur D), ou l'activité phagocytaire;
- traitement immunosuppresseur comprenant l'utilisation de corticostéroïdes pendant une longue période, chimiothérapie, radiothérapie, traitement antirejet, biothérapie et autres immunosuppresseurs non-biologiques pour maladies inflammatoires rhumatologiques et autres.
- néoplasies malignes incluant la leucémie et le lymphome;
- greffe d'organe solide ou de cellules des îlots pancréatiques (candidat ou receveur).
Ces patients immunodéprimés devraient recevoir une dose de vaccin PNEU-C-13 suivie d'une dose de vaccin PNEU-P-23 huit semaines plus tard. On ne dispose actuellement d'aucune donnée indiquant que l'administration d'une dose de rappel de vaccin PNEU-C-13 offre un quelconque avantage. (Recommandation du CCNI de catégorie B)
Les études publiées excluaient les participants qui avaient reçu une dose de vaccin PNEU-P-23 dans les cinq années précédant l'inscription à l'étude. Par conséquent, on ignore quel serait l'intervalle minimum à respecter entre la dernière dose de vaccin PNEU-P-23 reçue et le vaccin PNEU-C-13. Cependant, vu la possibilité d'une diminution des titres d'anticorps après l'administration du vaccin PNEU-P-23, vu la gravité de l'IIP chez les sujets immunodéprimés et vu les avantages associés au vaccin PNEU-C-13 dans cette population de patients, le CCNI recommande d'administrer le vaccin PNEU-C-13 au moins un an après la dernière dose du vaccin PNEU-P-23 (avis d'experts).
L'administration d'une dose de rappel à vie de PNEU-P-23 est recommandée pour les individus à haut risque d'IIP, entre autres les personnes avec asplénie anatomique ou fonctionnelle, anémie falciforme, ou toute immunosuppression causée par une maladie ou un traitement, incluant les greffes d'organes solides. Les individus appartenant à ces groupes à haut risque, ayant préalablement été vaccinés avec le PNEU-P-23 et qui nécessiteraient une dose supplémentaire de PNEU-P-23 devraient la recevoir au moins 8 semaines après la dose de PNEU-C-13 et au moins 5 ans après la dose la plus récente de PNEU-P-23 (avis d'experts).
Il n'existe actuellement aucune étude portant sur l'ensemble des pathologies ou situations précédentes. Cependant, d'après les données dont on dispose sur les personnes ayant subi une greffe d'organe solide, la portée de la recommandation est élargie de façon à englober d'autres sujets immunodéprimés.
Recommandation 4
Le CCNI a conclu qu'il existait des données probantes insuffisantes pour recommander l'utilisation du vaccin PNEU-C-13 chez les patients présentant une affection chronique non associée à une immunodépression (voir la liste ci-dessous). Cependant, d'autres facteurs peuvent influer sur la prise de décisions. Les recommandations relatives à l'administration du vaccin PNEU-P-23 demeurent inchangées. (Recommandation du CCNI de catégorie I)
Les affections chroniques non associées à une immunodépression dont il est question sont les suivantes :
- fuite chronique de liquide céphalorachidien;
- implant cochléaire;
- atteinte neurologique chronique pouvant affecter la clairance des sécrétions orales;
- cardiopathie ou pneumopathie chronique;
- diabète sucré;
- néphropathie chronique, y compris le syndrome néphrotique;
- hépatopathie chronique (y compris l'hépatite B et l'hépatite C, ainsi qu'une cirrhose du foie, quelle qu'en soit la cause).
Recommandation 5
Le CCNI a conclu qu'il existait des données probantes insuffisantes pour recommander l'utilisation du vaccin PNEU-C-13 chez les adultes en bonne santé de 65 ans ou plus. Cependant, d'autres facteurs peuvent influer sur la prise de décisions. Les recommandations relatives à l'administration du vaccin PNEU-P-23 demeurent inchangées. (Recommandation du CCNI de catégorie I)
Comme on ne dispose pas de l'information critique suivante, le CCNI ne peut recommander l'utilisation du vaccin PNEU-C-13 chez des sujets en bonne santé de 65 ans ou plus :
- données sur l'efficacité potentielle ou réelle du vaccin PNEU-C-13 – en comparaison avec un placebo et, idéalement, avec le vaccin PNEU-P-23 – relativement à la prévention de l'IIP dans cette population;
- données sur l'efficacité potentielle ou réelle du vaccin PNEU-C-13 – en comparaison avec un placebo et, idéalement, avec le vaccin PNEU-P-23 – relativement à la prévention de la POC dans cette population;
- corrélats de protection qui permettraient d'interpréter les données d'immunogénicité dont on dispose actuellement pour le vaccin PNEU-C-13;
- protection indirecte des adultes contre les IIP causées par les sérotypes inclus dans le PNEU-C-13 attribuable au programme d'immunisation des nourrissons et des enfants avec le vaccin PNEU-C-13.
VII. Surveillance et priorités de recherche
L'épidémiologie des infections invasives à pneumocoque est en changement au Canada et ailleurs dans le monde, à la fois en raison de l'utilisation de vaccins contre le pneumocoque, mais également indépendamment de celle-ci. D'autres changements sont prévus en raison de l'utilisation du vaccin PNEU-C-13 dans le cadre des programmes de vaccination systématique des enfants. Il est essentiel d'effectuer une surveillance à l'échelle nationale pour détecter ces changements au fil du temps. La prise de décisions optimales concernant l'utilisation de vaccins contre le pneumocoque demande une surveillance continuelle des taux d'IIP spécifique à chaque sérotype ainsi que des taux d'autres syndromes causés par le pneumocoque, une estimation spécifique au sérotype de l'efficacité potentielle des différents vaccins et une évaluation continue de l'efficacité réelle et du coût-efficacité des divers calendriers de vaccination dans le temps.
Les activités de surveillance et de recherche qui visent à répondre aux questions en suspens suivantes sont particulièrement encouragées :
- Quelles sont l'efficacité potentielle et l'efficacité réelle du vaccin PNEU-C-13 chez l'adulte en ce qui concerne la prévention des IIP ou de la POC, par rapport au vaccin PNEU-P-23 ?
- Quelles sont les répercussions de l'utilisation de vaccins conjugués contre le pneumocoque sur les IIP chez les adultes de 65 ans ou plus, en particulier pour ce qui concerne les sérotypes en cause ?
- En ce qui concerne le vaccin PNEU-C-13, quelles en sont l'efficacité potentielle et l'efficacité réelle par sérotype ?
- Quelles concentrations d'anticorps ou d'autres marqueurs immunologiques sont le plus fortement corrélées avec une protection contre les IIP, la pneumonie à pneumocoque, l'otite moyenne aiguë et le portage rhinopharyngé?
- Le remplacement des sérotypes annulera-t-il les avantages associés à l'utilisation de vaccins conjugués contre le pneumocoque chez les enfants?
- Quels sont les déterminants de la protection indirecte conférée aux adultes par l'administration de vaccins aux enfants?
- Quels facteurs, autres que l'immunisation, modifient la fréquence des cas de maladie attribuables aux différents sérotypes au fil du temps?
- Chez l'adulte, le fait d'avoir reçu le vaccin PNEU-P-23 a-t-il une incidence sur l'efficacité réelle du vaccin PNEU-C-13?
- Une dose de rappel du vaccin PNEU-C-13 ou du vaccin PNEU-P-23 est-elle nécessaire chez l'adulte?
Tableaux
Tableau 5 – Sommaire des données à la base des recommandations du CCNI
- Données sur l'efficacité potentielle
- Données sur l'efficacité réelle
- Données sur l'immunogénicité
- Données sur l'innocuité
| Étude | DÉTAIL DE L'ÉTUDE | SOMMAIRE | ||||
|---|---|---|---|---|---|---|
| Vaccin | Devis de l'étude | Participants | Résumé des principales constatations sous forme de texte ou de données | Niveau de preuve | Qualité | |
| French, 2010 (9) |
PNEU-C-7 vs placebo Patients recrutés de l'hôpital central Queen Elizabeth au Malawi |
Essai comparatif randomisé, à double insu Durée du suivi : févr. 2003 – oct. 2007 (médiane : 1,2 an) Adolescents et adultes VIH+ rétablis d'un premier épisode de IIP |
496 patients, dont 439 étaient VIH+, ont été sélectionnés aléatoirement de manière à recevoir deux doses de vaccin ou de placebo à quatre semaines d'intervalle Groupe recevant le vaccin Suivi complet disponible pour 239 patients VIH+ |
Paramètre : Nouvel épisode de IIP dû à l'un des sérotypes du vaccin + 6A (compte tenu d'une éventuelle protection croisée) Paramètre principal (1er épisode de IIP dû à un sérotype du vaccin ou 6A) – IDT : RR (ajusté) = 0,31 (0,11-0,84)
|
Niveau I |
Bonne |
| Étude | DÉTAIL DE L'ÉTUDE | SOMMAIRE | ||||
|---|---|---|---|---|---|---|
| Vaccin | Devis de l'étude | Participants | Résumé des principales constatations sous forme de texte ou de données | Niveau de preuve | Qualité | |
Breiman, |
PNEU-P-23 Dose : n.d. |
Étude cas-témoins rétrospective Durée de l'étude : févr. 1992 - avril 1995 Détermination du statut vaccinal : communication avec les médecins et obtention des dossiers de vaccination |
N = 503 |
Efficacité réelle du vaccin (ERV) : 49 % (IC à 95 % 12, 70) ajustée pour toutes les variables, aucun terme d'interaction ERV avec terme d'interaction race*statut vaccinal : |
Niveau II-2
|
Bonne |
Hung, 2004 (12) |
PNEU-P-23 |
Étude d'observation prospective Durée du suivi : Période : 1er juin 2001 – 31 octobre 2002 |
N1 = 305 sujets infectés par le VIH vaccinés N2 = 203 sujets infectés par le VIH non vaccinés Lieu : National Taiwan University Hospital |
Incidence de la pneumococcie : Sujets vaccinés : 2,1/1 000 patients-années (IC à 95 % 1,7-2,5) Incidence de l'IBS : RC-A pour la pneumococcie : 0,085 (IC à 95 %, 0,01- 0,735) RC-A pour la bactériémie = 0,22 (IC à 95 %, 0,018- 2,561) ERV = 88 % (-156 %; 98,2 %) RC-A pour la pneumonie d'origine communautaire toutes causes confondues : 1,876 (IC à 95 %, 0,785-4,485) Nouvelle maladie opportuniste définissant le sida : 0,567 (IC à 95 % 0,217-1,484) Rapport de risque ajusté pour la mortalité : 0,733 (IC à 95 % 0,236 – 2,274) |
Niveau II-2 |
Bonne |
French, 2000 (13) |
PNEU-P-23 vs placebo |
Essai comparatif randomisé, avec placebo |
N = 1 392 |
Premier épisode de IIP : RR = 1,48; IC à 95 % 0,7- 3,3 |
Niveau I |
Bonne |
Vila-Corcoles, 2005 (14) |
PNEU-P-23 |
Étude de cohorte prospective Durée du suivi : 12 mois Cohorte de patients suivis dans des cliniques données. |
N = 11 241 Les caractéristiques de référence des sujets résidant dans la collectivité = 65 ans (vaccinés vs non vaccinés avant l'inscription) différaient significativement : l'âge, la comorbidité et le statut d'immunodéficience étaient significativement plus élevés dans le groupe des vaccinés que dans le groupe des non-vaccinés. Le pourcentage de fumeurs était significativement plus élevé dans le groupe des non-vaccinés. |
Rapports de risque ajustés selon les paramètres principaux : Taux d'hospitalisation pour pneumonie (ajusté selon le sexe, l'âge, l'obésité, la maladie pulmonaire chronique, le statut d'immunodéficience et le fait d'avoir été vacciné contre la grippe l'année précédente) : 0,81 (IC à 95 % 0,51- 1,30); p = 0,387
Taux global de pneumonie (ajusté selon le sexe, l'âge, la cardiopathie chronique, la maladie pulmonaire chronique, le statut d'immunodéficience et le fait d'avoir été vacciné contre la grippe l'année précédente) : 0,85 (IC à 95 % 0,56-1,31); p = 0,467 Mortalité par pneumonie (ajustée selon l'âge, le statut d'immunodéficience et le fait d'avoir été vacciné contre la grippe l'année précédente) : 0,28 (IC à 95 % 0,09- 0,80); p = 0,018 Mortalité toutes causes confondues (ajustée selon l'âge, le statut d'immunodéficience, le sexe, la maladie pulmonaire chronique, l'hypertension) : 0,67 (IC à 95 % 0,54- 0,83); p = 0,000 |
Niveau II-2 |
Moyenne |
Vila- Corcoles, 2006 (15) |
PNEU-P-23 : offert gratuitement aux 65 ans ou plus, sans campagne spécifique Vaccin : variable temporelle |
Étude de cohorte prospective Durée du suivi : 40 mois Incluait tous les sujets résidant dans la collectivité de 65 ans ou plus, répartis dans huit centres de soins primaires Résultats principaux : Évaluations diagnostiques Pneumonie Cas identifiés au moyen des codes de la CIM-9 (sommaires du congé) et des données de laboratoire |
Cohorte totale : 11 241 N (non-vaccinés avant l'étude) = 6 255 Tous les sujets étaient des résidents de la collectivité âgés de 65 ans ou plus Les caractéristiques de référence des deux groupes différaient considérablement. Ces différences ont été observées dans le groupe des 65-74 ans (46,2 % vs 62,4 % p < 0,001) : antécédents d'hospitalisation pour pneumonie les deux années précédentes (1,7 % vs 0,8 %; p < 0,01), taux de vaccination antigrippale l'année précédente, incidence de cardiopathie chronique, diabète sucré, maladie pulmonaire chronique, hypertension, hépatopathie chronique néphropathie, néoplasie active, prise d'un médicament immunodépresseur et statut d'immunodéficience significativement plus élevés dans le groupe des vaccinés que chez les non-vaccinés; p < 0,01. En général, la morbidité était supérieure dans la population des vaccinés. |
RR ajusté (IC à 95 %) - 1 . Incidence et risque de IIP due à des sérotypes présents dans le vaccin 0,61 (0,13-2,76); p = 0,517 (ajustés selon le statut immunitaire, le tabagisme, le fait d'avoir été vacciné contre la grippe l'année précédente) 2. Incidence pour tous les cas de IIP : 0,60 (0,22-1,65); p = 0,324 (ajustée selon l'âge, le tabagisme, l'immunocompétence, le fait d'avoir été vacciné contre la grippe l'année précédente) 3. Incidence de la pneumonie à pneumocoque avec bactériémie : 0,45 (0,15-1,40); p = 0,452 (ajustée selon l'âge, le tabagisme, l'immunocompétence, le fait d'avoir été vacciné contre la grippe l'année précédente) 4. Incidence de la pneumonie à pneumocoque sans bactériémie : RR ajusté : 0,61 (0,35-1,06); p = 0,81 (ajustée selon le sexe, l'âge, les antécédents d'hospitalisation pour pneumonie les deux années précédentes, le diabète sucré, l'hépatopathie chronique) 5. Incidence globale de la pneumonie à pneumocoque : 0,55 (0,34-0,88); p = 0,013 (ajustée selon l'âge, le sexe, l'hépatopathie chronique et le statut d'immunodéficience) 6. Risque d'hospitalisation due à la POC : 0,74 (0,59-0,92); p = 0,007 (ajusté selon l'âge, le sexe le nombre de consultations externes les deux années précédentes, les antécédents d'hospitalisation pour pneumonie les deux années précédentes, l'hépatopathie chronique, la cardiopathie chronique, l'immunocompétence) 7. Risque de POC chez les patients non hospitalisés : 0,90 (0,59-1,37); p = 0,619 (ajusté selon l'âge, le nombre de consultations externes les deux années précédentes, l'hépatopathie chronique, l'immunocompétence, le fait d'avoir été vacciné contre la grippe l'année précédente) 8. Risque global de POC : 0,79 (0,64-0,98); p = 0,032 (ajusté selon l'âge, le sexe, le nombre de consultations externes les deux années précédentes, les antécédents d'hospitalisation pour pneumonie les deux années précédentes, l'hépatopathie chronique, la cardiopathie chronique, l'immunocompétence, le fait ou non d'avoir été vacciné contre la grippe) 9. Mortalité due à l'infection à pneumocoque : 10. Mortalité due à la pneumonie : 0,41 (0,23-0,72); p = 0,002 ajustée selon les variables du no 9 et l'obésité) 11. Mortalité toutes causes confondues : 0,97 (0,86-1,09); p = 0,595 (ajustée selon le sexe, l'âge, l'hépatopathie chronique, l'immunocompétence, la cardiopathie chronique, la présence de diabète sucré, le tabagisme, l'hypertension, l'obésité et le fait d'avoir été vacciné contre la grippe Stratification selon le statut vaccinal antigrippal : Analyse limitée à la saison grippale : le vaccin PNEU-P-23 a réduit le risque de pneumonie à pneumocoque (RR 0,39; IC à 95 % 0,21-0,74) Hospitalisations pour pneumonie (RR 0,69; IC à 95 % 0,49-0,97) Mortalité due à la pneumonie (RR 0,44; IC à 95 % 0,20-0,98) |
Niveau II-2 |
Bonne |
Mooney, 2008 (16) |
PNEU-P-23 |
Étude de cohorte rétrospective Résultat principal : taux d'incidence de la IIP durant l'hiver 2003-2004 dans la population visée par le vaccin âgée de 65 ans ou plus Données extraites de la base de données nationale de la SPLI pour les cas de IIP Taux de vaccination par le PNEU-P-23 estimé à l'aide du réseau sentinelle (échantillon représentatif de 7 % de la population écossaise) Pour chaque cas de IIP : examen du dossier du patient (soins primaires) et questionnaire postal |
N (cas de IIP) : 396
Pas de différence significative dans l'incidence de IIP chez les sujets vaccinés de = 65 ans avec ou sans maladie respiratoire, maladie cardiovasculaire ou plus d'un facteur de risque % hommes (tous les cas de IIP) : 51,4 Taux de vaccination estimé : |
Âge 65+ ans : NSV : 5 :206 (IC à 95 % 4 388-7 122) Âge 65-74 ans : Âge 75+ ans : ERV (hommes) : 60,5 % (IC à 95 % 23,3-79,6) RR ajusté de mortalité |
Niveau II-2 |
Bonne |
Melagaro, 2004 (17) |
PNEU-P23 |
Méta-analyse Recherche dans Medline et PubMed pour trouver des études sur l'efficacité potentielle du PNEU-P-23 sans restriction d'année ou de langue Résultats évalués :
|
Études incluses :
Inclusion : Essais comparatifs randomisés ou quasi randomisés avec processus de randomisation ou quasi-randomisation bien défini; ciblant des sujets âgés de plus de 50 ans immunocompétents ou immunodéprimés, et évaluant la pneumonie à pneumocoque et/ou la IIP Deux examinateurs indépendants; utilisation des scores de Jadad |
ERV contre la pneumonie à pneumocoque N d'études analysées en fonction de ce paramètre : 7 Estimations regroupées de l'ERV au moyen d'un modèle à effets aléatoires incluant des essais sur des groupes non à risque élevé : 16 % (IC à 95 % : -50-53 %) Estimations regroupées de l'ERV au moyen d'un modèle à effets aléatoires incluant des essais sur des groupes à risque élevé (GRÉ) : -20 % (-92-25 %) Efficacité réelle du vaccin dans la réduction de la IIP Études incluses : 6 Estimation regroupée de l'ERV dans la réduction de la IIP chez les personnes âgées en général : 65 % (-42-92 %) Estimation regroupée de l'ERV dans la réduction de la IIP dans les GRÉ à l'exclusion des études quasi randomisées : 20 % (-187-78 %) Estimation regroupée de l'ERV dans la réduction de la IIP dans les GRÉ incluant les études quasi randomisées : 44 % (-45-79 %) |
Niveau I |
Bonne |
| Étude | DÉTAIL DE L'ÉTUDE | SOMMAIRE | ||||
|---|---|---|---|---|---|---|
| Vaccin | Devis | Participants | Résumé des principales constatations sous forme de texte ou de données | Niveau de preuve | Qualité | |
Kumar, 2008 (19) |
Placebo -PNEU-P-23 PNEU-C-7/
Voie : IM |
Essai comparatif randomisé, avec placebo et à double insu Durée du suivi : 16 semaines Puissance : 80 % pour détecter une différence de 25 % Réponse : augmentation d'un facteur de ≥ 2 et titre d'au moins 0,35 mg/l |
N = 130 Caractéristiques de référence – patients ayant subi une transplantation du foie ≥ 3 mois auparavant; PNEU-P-23 ≥ 5 ans auparavant PNEU-P-23 antérieur (%) : 8 %, 14 % p = 0,17
Dans les analyses multivariées et univariées, l'utilisation de corticostéroïdes a été associée significativement à une réponse anticorps inférieure (RC = 5,0; IC à 95 % 1,29–19,6; p = 0,02)
|
Immunogénicité Réponse à au moins 1 sérotype correspondant à une augmentation de ≥ 2 fois le titre de référence à la semaine 16 : 85,7 % vs 91,2 %; p = NS Nombre moyen de sérotypes pour lesquels on observe une réponse à la semaine 16 : Réponse à chaque sérotype à la semaine 16 (%) : TMG spécifique au sérotype à la semaine 16 (µg/ml) : Sérotype 4 : 0,67 vs 1,24; p = 0,25 Sérotype 6B : 1,8 vs 2,63; p = 0,56 Sérotype 9V : 2,37 vs 1,96; p = 0,28 Sérotype 14 : 12,42 vs 15,49; p = 0,84 Sérotype 18C : 4,34 vs 3,79 p = 0,46 Sérotype 19F : 4,95 vs 5,10; p = 0,78 Sérotype 23 F : 1,54 vs 2,57; p = 0,22 Activité opsonophagocytaire ≥ 4 fois la valeur de référence (%) : 16,7–45,8 vs 11,5–42,3 ( p = NS pour 6/7 sérotypes) |
Niveau I |
Bonne |
Kumar, 2003 (20) |
PNEU-C-7 Dose = 0,5 ml Période de l'étude : sept.-déc. 2001
|
Essai comparatif randomisé, avec placebo et à double insu Durée du suivi : 8 semaines Transplantation rénale : Exclusions : splénectomie ou PNEU-P-23 dans les 5 dernières années |
N = 60 – Transplantation rénale
Caractéristiques de référence : deux groupes présentant des caractéristiques démographiques et cliniques semblables, notamment sur le plan de la fonction rénale, du délai depuis la transplantation et de l'immuno-dépression Réponse : OPA : augmentation d'un facteur de ≥4, avec titre absolu >1:8 |
Immunogénicité (IgG) : Facteur d'augmentation moyen des TMG spécifiques au sérotype à 8 semaines comparativement aux valeurs de référence (PNEU-C-7 vs PNEU-P-23) : Sérotype 4, 6B, 14, 18C, 19F; p = NS Sérotype 23F : 16,8 (intervalle 0,8-160) vs 2,2 (intervalle 0,4-23,5); p = 0,046 Sérotype 9 : 17 vs 2,6, p = 0,09 Proportion de sujets qui ont présenté une réponse (PNEU-C-7 vs PNEU-P-23) : Sérotypes 4, 9V, 18C, 19F : PNEU-C-7 > PNEU-P-23; p = NS Sérotype 23F (%) : 40 vs 16,7; p = 0,046 Sérotype 6B : 33,7 vs 13,3; p = 0,067 ≥1 sérotype (%) : 53,3 vs 73,3 Nombre médian de sérotypes pour lesquels on a observé une réponse : 1,0 vs 2,5; p = 0,069 Facteur d'augmentation des titres d'OPA spécifiques au sérotype : Taux de réponses OPA spécifiques au sérotype : 83,3 vs 80; p = NS Nombre médian de réponses OPA spécifiques au sérotype : 2,0 vs 3,0; p = NS |
Niveau I |
Bonne |
Kumar, 2007 (21) |
PNEU-C-7 Dose de départ : 0,5ml
|
Étude de cohorte prospective constituant un suivi de trois ans d'un ECR auprès de patients ayant subi une transplantation rénale À 3 ans, la majorité des patients recevaient des inhibiteurs de la calcineurine (95,7 %) et du MMF (78, 7 %) |
60 cas sélectionnés aléatoirement |
Immunogénicité : Taux global de réponse spécifique au sérotype (PNEU-P-23 et PNEU-C-7) ( ≥ 0,35 µg/ml et augmentation d'un facteur de 2 par rapport à la valeur de référence) pour chacun des 7 sérotypes à 8 semaines : 12,8 % (sérotype 6B) -44,7 % (sérotype 9V) À 3 ans : 42,1 % (sérotype 4) -85,0 % (sérotype 14) des sujets ayant présenté une réponse initiale à 8 semaines. Le TMG global à 8 semaines après la vaccination était significativement plus élevé que la valeur de référence pour les 7 sérotypes; p < 0,001 Le TMG global à 3 ans a baissé significativement pour les sérotypes 4, 6B, 9V, 14, 18C, 23F par rapport aux titres à 8 semaines; p < 0,001 à l'exception du sérotype 19F; p = NS Significativement supérieur aux titres avant la vaccination ( p < 0,05) pour tous les sérotypes sauf le sérotype 14 Pas de différence significative dans la diminution des titres entre le groupe PNEU-C-7 et le groupe PNEU-P-23 à 3 ans, comparativement aux titres à 8 semaines; p = NS Facteur prédictif unique de la durabilité de la réponse par analyse de régression logistique – nombre de sérotypes pour lesquels le patient a présenté une réponse à 8 semaines (RC 2,63, IC à 95 % 1,49 – 4,76, p = 0,0007) À 13 mois : semblable pour les deux groupes à l'exception du sérotype 6B – 14,8 µg/ml vs 4,22 µg/ml; p = 0,046. |
Niveau I |
Bonne |
Tobudic, (22) |
PNEU-C-7 |
Essai comparatif randomisé, à simple insu, mené dans un seul centre |
N = 80 (receveurs de transplantation rénale) 9 se sont retirés; 9 ont été perdus de vue; 62 ont été analysés |
Immunogénicité Taux de réponse – un an après la vaccination initiale : (TMG) diminution pour tous les sérotypes dans le cas des deux vaccins Taux de réponse – 8 semaines après le rappel avec le PNEU-P-23 (TMG) Réponse au vaccin : augmentation du titre d'anticorps d'un facteur de ≥ 2 et valeur absolue > 1ug/ml. - Réponse à >1 sérotype après rappel avec le PNEU-P-23 : - Nombre médian de sérotypes associés à une réponse : |
Niveau I |
Bonne |
Cordonnier 2009 (23) |
PNEU-C-7 Calendrier : PNEU-P-23 à 12 mois (groupe de vaccination précoce) ou 18 mois (groupe de vaccination tardive) après la greffe |
Étude de non-infériorité randomisée multicentrique Marge de non-infériorité = -20 % Durée du suivi : 24 mois Réponse = titre d'au moins 0,15 mg/l 1 mois après 3e dose de PNEU-C-7 |
N = 158 ( GCSH allogéniques) Groupe précoce = 75 Caractéristiques de référence : Les deux groupes ont été équilibrés pour les facteurs suivants : maladie sous-jacente, statut GCSH, source des cellules souches, âge du donneur, sexe et type, vaccination antérieure du donneur, RGH aiguë ou chronique et délai entre la GCSH et la première dose de PNEU-C-7. Les deux groupes présentaient une différence significative dans le % de patients dont le titre d'anticorps était ≥ 0,15 µg/ml avant l'administration du PNEU-C-7. |
Immunogénicité Groupe de vaccination précoce vs groupe de vaccination tardive Taux de réponse (titres d'anticorps ≥ 0,15 µg/ml pour les 7 sérotypes du PNEU-C-7 à 1 mois après la 3e dose de vaccin) : 79 % vs 82 % (IC à 90 %, -15,6 à 8,6) Taux de réponse (TMG ≥ 0,5 µg/ml pour les 7 anticorps Taux de réponse (TMG ≥ 0,15 µg/ml pour les 7 sérotypes du PNEU-C-7 à 24 mois après la greffe) : 59 % vs 83 %; p = 0,013 Taux de réponse (TMG ≥ 0,5 µg/ml pour les 7 sérotypes à 24 mois après la greffe) : 34 % vs 55 %; p = 0,054 Les TMG pour les 7 anticorps à 1 mois après la 3e dose de PNEU-C-7 ne différaient pas significativement entre les deux groupes, à l'exception de 19F p < 0,001 Les TMG à 24 mois suivant la greffe, après la 3e dose de PNEU-C-7 et 1 dose de PNEU-P-23, étaient significativement plus bas dans le groupe de vaccination précoce que dans le groupe de vaccination tardive, pour les 7 sérotypes à l'exception de 23F; p = 0,12 |
Niveau I |
Bonne |
Molrine, 2003 (24) |
PNEU-C-7 Dose unique IM Calendrier Tous les receveurs de GCSH : PNEU-C-7 à 3, 6 et 12 mois après la GCSH Sérotypes analysés : 4, 6B, 9V, 14, 18C, 19F, 23F Greffons de cellules souches hémato-poïétiques allogéniques non appauvris en lymphocytes T |
Essai comparatif randomisé Durée du suivi : 13 mois Randomisation par strates selon l'âge Sujets ≥ 2 ans |
96 paires sélectionnées aléatoirement – GCSH allogéniques Donneurs immunisés évaluables = 30 Donneurs non immunisés évaluables = 35 Non évaluables = 31 Caractéristiques de référence : semblables dans les deux groupes sur les plans suivants : âge du receveur, âge du donneur, race, sexe, diagnostic, irradiation corporelle totale, présence d'une RGH et IgIV après la GCSH *Les donneurs ayant reçu une dose unique de PNEU-C-7 présentaient un TMG significativement plus élevé que celui des donneurs non immunisés, pour les 7 sérotypes du vaccin |
Immunogénicité Taux de réponse (%) – donneurs immunisés vs donneurs non immunisés (TMG ≥ 0,5 µg/ml pour les 7 sérotypes) à 3 mois : 57 vs 54 %; p = NS 6 mois : 67 vs 36 %; p = 0,05 12 mois : 60 vs 35 %; p = NS 13 mois : 75 vs 64 %; p = NS Différences dans le TMG entre les deux groupes à : 6 mois (après la 1re dose) : significative pour 5 des 7 sérotypes 12 mois (après la 2e dose) : significative pour 4 des 7 sérotypes *Les TMG du groupe ayant reçu le PNEU-C-7 à 3, 6 et 12 mois (n = 45) étaient significativement plus élevés pour les 7 sérotypes que ceux du groupe PNEU-P-23 d'une autre étude (n = 22) ayant reçu une première dose de PNEU-P-23 à 12 mois. Facteurs jouant un rôle indépendant dans le TMG à la suite d'une GCSH établis à l'aide d'une analyse de régression linéaire : |
Niveau I |
Moyenne |
Kumar, 2007 (25) |
PNEU-P-23 Dose : 0,5 ml Paires de donneurs et receveurs Donneurs : Receveurs : 1 dose de l'un ou l'autre des vaccins 6 mois après la GCSH Voie : IM Sérotypes analysés: 4, 6B, 14, 18C, 19F, 23F |
Essai comparatif randomisé, à double insu Paires sélectionnées aléatoirement Durée du suivi : 12 mois après la GCSH Réponse : augmentation d'un facteur de 2 du TMG et titre absolu ≥ 0,35 µ/ml |
N = 64 paires donneurs-receveurs ( GCSH allogéniques) Paires recevant le PNEU-C-7 = 32 Caractéristiques de référence : |
Immunogénicité TMG chez les donneurs : pas de différence entre le PNEU-P-23 et le PNEU-C-7 TMG à 12 mois après la GCSH : Réponse à au moins 1 sérotype (≥ 0,35 µg/ml à 6 mois après la GCSH) : PNEU-C-7 vs PNEU-P-23 = 38,1 vs 0 %; p = 0,003 Nombre moyen de sérotypes associés à une réponse à 6 mois après la GCSH : Réponse à au moins 1 sérotype (≥ 0,35 µg/ml à 12 mois) PNEU-C-7 vs PNEU-P-23 = 90,9 vs 55,6 %; p = 0,02 Le taux de réponse était généralement médiocre dans les deux groupes. *Facteurs dont on a établi qu'ils influaient sur la réponse au vaccin à 12 mois par une analyse multivariée : type de vaccin |
Niveau I |
Bonne |
Feikin, 2002 (26) |
Combinaison du PNEU-C-7, PNEU-P-23 ou placebo PNEU-C-7/PNEU-C-7 Voie : IM (deltoïde) |
Essai comparatif randomisé Durée du suivi : 24 semaines Sérotypes analysés : |
N = 90 Des adultes infectés par le VIH avec numération lymphocytaire CD4 ≥ 200/µl ont reçu 2 doses d'une combinaison de vaccins |
Immunogénicité IgG spécifiques au sérotype (ELISA) Sérotype 23F: PNEU-C-7/PNEU-C-7> placebo/PNEU-P-23; p = 0,024 Sérotype 4: PNEU-C-7/ PNEU-P-23> placebo/PNEU-P-23; p = 0,011 Sérotype 6B: PNEU-C-7/ PNEU-P-23> placebo/PNEU-P-23; p = 0,01 Sérotype 9V: PNEU-C-7/ PNEU-P-23> Placebo/PNEU-P-23; p = 0,024 *2e dose n'apportant pas d'avantages supplémentaires Après la 2e dose : CMG équivalentes pour le PNEU-C-7/PNEU-C-7 et le PNEU-C-7/ PNEU-P-23
Titres d'OPA Sérotype 9V: PNEU-C-7/ PNEU-P-23> placebo/PNEU-P-23; p = 0,034 Sérotype 23F: PNEU-C-7/ PNEU-P-23> placebo/PNEU-P-23; p = 0,028 Sérotype 4: PNEU-C-7/PNEU-C-7> placebo/PNEU-P-23; p <0,005 Sérotype 6B: PNEU-C-7/PNEU-C-7> placebo/PNEU-P-23; p = 0,012 Sérotype 9V: PNEU-C-7/PNEU-C-7> placebo/PNEU-P-23; p = 0,038 La proportion de sujets présentant une augmentation d'un facteur de 4 dans les titres après une 2e dose était plus élevée dans les groupes ayant reçu le PNEU-C-7 que dans le groupe placebo/PNEU-P-23 *2e dose n'apportant pas d'augmentation supplémentaire dans les titres d'OPA |
Niveau I |
Bonne |
Penaranda 2010 (27) |
PNEU-C-7 Calendrier Groupe 2 : PNEU-P-23 à 0 semaine |
Étude randomisée ouverte multicentrique Adultes non déjà immunisés infectés par le VIH avec numération CD4 entre 200 et 500 lymphocytes/µl et charge virale < 5 log copies/ml Durée du suivi : 8 semaines |
N = 220 (110 dans chaque groupe) Répartis aléatoirement entre deux groupes : Caractéristiques des patients : |
Paramètres principaux Pourcentage de répondeurs à 8 semaines selon les critères 1 et 2 : Pas de différence entre les deux groupes, à l'exception du sérotype 23F : 26 % de répondeurs (combinaison des 2 vaccins) vs 14 % de répondeurs (uniquement PNEU-P-23) RC = 2,2; IC à 95 % 1,07-4,56 Pas de différence sur le plan de l'avidité |
Niveau I |
Bonne |
Crum-Cianflone, 2010 (28) |
Revaccination avec le PNEU-C-7 ou le PNEU-P-23 Dose unique 3 à 8 années après administration antérieure du PNEU-P-23 |
Essai comparatif randomisé Sujets infectés par le VIH répartis aléatoirement selon un ratio 2:1 (PNEU-C-7: PNEU-P-23) Sujets non infectés par le VIH : Patients : 18-60 ans Durée du suivi : 180 jours Durée de l'étude : févr. 2006 - sept. 2008 |
N = 131 (PNEU-C-7) N = 73 (PNEU-P-23) Adultes infectés par le VIH ayant reçu le PNEU-P-23 de 3 à 8 ans auparavant N = 25 dans le groupe non infecté par le VIH au départ Caractéristiques de référence : semblables (nombre médian de CD4 > 500/mm3) à l'exception des sujets recevant le traitement HAART (%) = 84, 7, 56 |
Paramètre principal : Proportion de sujets présentant une réponse à 2 des 4 sérotypes à 60 jours : PNEU-C-7 = 57 % vs PNEU-P-23 = 36 %; p = 0,004 (sujets non infectés par le VIH = 88 %) Changements moyens dans le taux d'IgG par rapport à la valeur de référence à 60 jours: PNEU-C-7 > PNEU-P-23 pour les sérotypes 4, 9V, 19F ( p < 0,05), pas pour le sérotype 14 180 jours: PNEU-C-7 = PNEU-P-23 RC ajusté pour la réponse à 2 des 4 sérotypes |
Niveau I |
Bonne |
Lesprit, 2007 (29) |
PNEU-C-7/PNEU-P-23 (4 semaines plus tard) OU Dose – n.d. |
Essai comparatif randomisé Durée du suivi : 24 semaines Sujets inclus : infectés par le VIH1 avec numération CD4 de 200-500; CV : < 50 000 copies/ml; n'ayant jamais pris d'ARV ou schéma stable x au moins 3 mois; pas de pneumococcie les 5 dernières années Patients sélectionnés entre décembre 2002 et décembre 2003 |
N = 212 (patients infectés par le VIH) Caractéristiques de référence : |
Résultats sur le plan de l'immunogénicité Valeurs de référence : titres d'IgG semblables dans les deux groupes À 8 semaines (4 semaines après l'administration du PNEU-P-23 dans les deux groupes) : mêmes titres d'IgG dans les deux groupes, à l'exception de 18C et 23F (supérieur avec calendrier d'administration combinée) À 24 semaines : mêmes titres d'IgG dans les deux groupes, à l'exception de 18C, 23F, 14 et 19F Proportion de sujets répondant au critère b ci-dessus : Pas de différence entre les deux groupes à 8 semaines, à l'exception de la réponse à 5 des 7 sérotypes (59 % pour l'administration combinée vs 40 % pour le PNEU-P-23, p = 0,005) et identique pour les taux à 24 semaines, à l'exception de la réponse à 5 des 7 sérotypes (30 % pour l'administration combinée vs 10 % pour le PNEU-P-23, p = 0,003). |
Niveau I |
Bonne |
Frenck, 2012 (30) |
PNEU-C-13/VTG – placebo (1 mois plus tard) 0,5 ml IM |
Essai comparatif randomisé Population : sujets sains de 50-59 ans, n'ayant reçu pas déjà le vaccin contre le pneumocoque |
Multicentrique – É.-U. N = 1 158 sujets inscrits |
Réponse au PNEU-C-13 mesurée par les IgG spécifiques au sérotype (ELISA) 1 mois après la vaccination antipneumococcique
|
Niveau I |
Bonne |
Schwarz, 2011 (31) |
PNEU-C-13/VTG – placebo (1 mois plus tard) |
Essai comparatif randomisé Tous les sérotypes du PNEU-C-13 ont été analysés Sujets sains de 65 ans ou plus, Suivi jusqu'à 1 mois après la dernière administration de vaccin |
Multicentrique – Europe N = 1 190 parti-cipants inscrits; 1 160 répartis aléatoirement – 580 dans chaque groupe 1 096 évaluables |
CMG spécifiques aux IgG dans chaque groupe – rapport des CMG
|
Niveau I |
Bonne |
Jackson, 2007 (32) |
PNEU-C-7 Dose (PNEU-C-7) : *PNEU-C-7 homologué à la dose de 0,5 ml chez les enfants Dose (PNEU-P-23) : 0,5 ml IM Test de provocation de 0,1 ml avec la dose de PNEU-P-23 à 1 an |
Essai comparatif randomisé Durée du suivi : 1 an et 4 semaines Sérotypes analysés : 4, 6B, 9V, 14, 18C, 19F, 23F Population : sujets âgés de 70-79 ans qui avaient reçu le PNEU-P-23 à ou après leur 65e anniver-saire, au moins 5 années auparavant |
N = 220 N = 219 (sujets analysés après la 1re vaccination) N = 208 (avant le test de provocation du vaccin PNEU-P-23) N = 203 (sujets analysés après le test de provocation du vaccin) |
Immunogénicité CMG spécifiques au sérotype après la vaccination à l'inscription Les titres post-vaccination correspondant aux doses de 1 et 2 ml étaient supérieurs pour tous les sérotypes, à l'exception du sérotype 14 : 0,5 ml – 8,8 (5,8-13,2) vs Les titres post-vaccination étaient significativement plus élevés à la dose de 2 ml qu'à la dose de 0,5 ml pour : Sérotype 6B; p < 0,05 Les titres post-vaccination étaient significativement plus élevés aux doses de 1 ml et 2 ml qu'à la dose de 0,5 ml pour : Sérotype 18C; p < 0,05 Sérotype 19F; p < 0,05 Après 1 an (avant le test de provocation) : les CMG évaluées par ELISA étaient semblables à celles antérieures à la vaccination, peu importe le vaccin et la dose administrés Résultats ajustés selon les CMG de référence à la suite du VPC7 vs VPP23 Pas de différence significative entre le groupe PNEU-C-7 à 0,5 ml et le groupe PNEU-P-23 pour tous les sérotypes, mais après ajustement selon les CMG de référence, CMG pour les doses de 1 ml et 2 ml : Sérotype 4: TMG mesurés par l'OPA pour le PNEU-C-7 vs le PNEU-P-23 ; (IC à 95 %) Significativement supérieurs à la dose de 0,5 ml pour 2 des 7 sérotypes : Sérotype 9V: Sérotype 23F: 4 572 (2 674 – 7 818) vs 502 (207 -1 217) Significativement supérieurs aux doses de 1 ml et 2 ml pour les sérotypes 4, 6B, 9V, 18C et 23F Pas de différence significative entre les titres avant et après le test de provocation du vaccin pour tous les sérotypes des quatre groupes. |
Niveau I |
Bonne |
De Roux, 2008 (33) |
PNEU-C-7 suivi du PNEU-C-7 OU du PNEU-P-23 (un an plus tard OU |
Essai comparatif randomisé ouvert, de phase 2 Durée du suivi : 13 mois Population : sujets de 70 ans ou plus, n'ayant PAS déjà reçu le vaccin contre le pneumocoque |
N = 219 sujets de ≥ 70 années, ambulatoires 1re dose de PNEU-C-7 = 110 PNEU-C-7/ PNEU-C-7 = 43 Caractéristiques de référence : les titres d'anticorps pré-immunisation étaient semblables dans les deux groupes initiaux. L'âge moyen à l'inscription était de 75 ans. |
Immunogénicité Titres d'anticorps IgG (µg/ml) spécifiques au sérotype (mesurés 1 mois après la dernière dose) : Dose unique de PNEU-C-7 vs dose unique de PNEU-P-23 : Significativement supérieure ( p < 0,01) pour les sérotypes 4, 6B, 9V, 14, 18C et 23 F PNEU-P-23/ PNEU-C-7 vs dose unique de PNEU-C-7 : Significativement inférieure pour tous les sérotypes; p ≤ 0,05 PNEU-C-7/ PNEU-C-7 vs dose unique de PCV7 : Significativement inférieure pour le sérotype 9V; p = 0,02 Différence non significative pour les sérotypes 4, 6B, 9V, 14, 18C et 23F PNEU-C-7/PNEU-P-23 vs dose unique de PNEU-C-7 : Significativement supérieure pour les sérotypes 19F et 23 F. Pas de différence significative pour les sérotypes 4, 6B, 9V, 14, 18C TMG mesurés par l'OPA après la 1re et la 2e dose : PNEU-C-7 vs PNEU-P-23 : Significativement supérieure pour tous les sérotypes analysés; p < 0,01- à l'exception de 6B et 19F PNEU-P-23/ PNEU-C-7 vs dose unique de PNEU-C-7 : PNEU-C-7/ PNEU-C-7 vs dose unique de PNEU-C-7 : Pas de différence significative pour tous les sérotypes à l'exception de 23F; p < 0,01 PNEU-C-7/PNEU-P-23 vs dose unique de PNEU-P-23 : Significativement supérieure pour les sérotypes 4, 9V, 14, 18C, 19F, 23F; p < 0,01 Différence non significative dans le cas du sérotype 6B |
Niveau I |
Bonne |
Miernyk, 2009 (34) |
PNEU-P-23 Dose : 0,5ml IM Groupe 1 : PNEU-P- 23 Groupe 2 : PNEU-C-7/PNEU-P-23 (2 mois plus tard) Groupe 3 : PNEU-C-7/PNEU-P-23 (6 mois plus tard)
Sérotypes analysés : 1, 4, 6B, 14, 19F |
Essai comparatif randomisé Population :
|
PNEU-P-23 = 28 PNEU-C-7/PNEU-P-23 (2 mois plus tard) = 29 PNEU-C-7/PNEU-P-23 (6 mois plus tard) = 29 Caractéristiques de référence : pas de différence significative entre les groupes d'étude sur le plan de l'âge et du sexe |
Immunogénicité Titres d'IgG spécifiques au sérotype (CMG µg/ml) (IC à 95 %) Pas de différence dans les CMG des IgG de référence pour les sérotypes 1, 4, 6B, 14 et 19F entre les groupes 1, 2 et 3; p > 0,3
* 2 mois après la 1re dose (groupe 1 = PNEU-P-23 vs groupe 2 et 3 = PNEU-C-7) Dans tous les groupes à l'étude, on a observé des augmentations significatives des CMG en réponse à tous les sérotypes spécifiques du vaccin par rapport aux valeurs de référence, augmentations qui étaient semblables dans tous les groupes sauf dans les cas suivants : Sérotype 1: 1,95 (1,21-3,15) après PNEU-P-23 vs 0,43 (0,31-0,59) après PNEU-C-7; p < 0,001 Pas de différence significative entre les groupes 1, 2 et 3 pour les sérotypes 4, 6B, 14, 19F; p > 0,2 *2 mois après la dernière dose : Pas de différence significative entre les groupes 1, 2 et 3 pour tous les sérotypes analysés; p > 0,3 OPA médian (intervalle) Au départ, les valeurs d'OPA contre tous les sérotypes analysés étaient semblables dans les trois groupes à l'étude; p > 0,05
*2 mois après la 1re dose (groupe 1 vs groupes 2 et 3) Dans tous les groupes à l'étude, on a observé des augmentations significatives des CMG contre les sérotypes spécifiques du vaccin, à l'exception des suivants : Sérotype 1 : aucune augmentation dans les trois groupes Sérotype 4 : augmentation non significative dans le groupe 3; p = 0,122 Pas de différence significative entre les groupes 1, 2 et 3 pour tous les sérotypes analysés; p > 0,15 *2 mois après la dernière dose: Pas de différence significative entre les groupes 1, 2 et 3 pour tous les sérotypes analysés; p > 0,2 |
Niveau I |
Bonne |
Goldblatt, 2009 (35) |
PNEU-C-7 Groupe 1 : PNEU-C-7/PNEU-C-7 (6 mois plus tard) Groupe 2 : Groupe 3 : PNEU-P-23 Groupe 4 : PNEU-C-7 |
Essai comparatif randomisé, ouvert Durée du suivi : 12 mois Seuil pour les titres d'IgG : 0,35ug/ml |
Groupe 1 = 133 Sujets âgés de 50-80 ans, n'ayant reçu aucun des vaccins contre le pneumocoque dans les 3 à 5 années précédant le recrutement Même nombre de sujets dans chaque groupe d'âge, soit 50-59, 60-69, 70-79 Caractéristiques de référence non fournies |
Immunogénicité CMG (IgG spécifiques au sérotype) à 4-6 semaines après la vaccination (PNEU-C-7 vs PNEU-P-23) : CMG à 1 an (PNEU-C-7 vs PNEU-P-23) Pas de différence significative pour les sérotypes 4, 6B, 9V, 14, 18C, 19F Sérotype 23F : 4,11 (PNEU-C-7; IC à 95 %, 3,19-5,29) vs 2,3 (PNEU-P-23; IC à 95 %1,81- 2,92) CMG à 4-6 semaines après la 2e dose : Sérotype 19F : 9,9 (PNEU-C-7/PNEU-P-23; IC à 95 % 8,27-11,85) > 6,74 (PNEU-C-7/PNEU-C-7; IC à 95 % 5,76 – 7,19) Pas de différence entre le PNEU-C-7/PNEU-P-23 et le PNEU-C-7/PNEU-C-7 pour les 6 sérotypes restants Proportion de sujets associés à une concentration d'IgG spécifique au sérotype > 1,0 µg/ml à 12 mois après l'administration de PNEU-C-7/PNEU-C-7 vs PNEU-P-23 seul pour les sérotypes : Globalement, PNEU-C-7/PNEU-C-7 = PNEU-P-23 ( p = NS) |
Niveau I |
Bonne |
Schenkein, 2008 (36) |
PNEU-P-23 0,5 ml x1 Sérotypes analysés : 4, 6B, 9V, 14, 18C, 19F, 23F, analysés 28 jours après la vaccination |
Essai comparatif randomisé
Étude comparative de la réponse immunitaire chez des sujets âgés de 65 ans ou plus vs sujets âgés de 45 ans et moins |
<45 ans = 45
Les adultes âgés étaient des résidents de la collectivité venant d'un groupe témoin d'une étude déjà publiée, soit un essai comparatif contre placebo, randomisé et à double insu Les sujets jeunes étaient des volontaires en santé recrutés parmi le personnel de recherche d'un laboratoire rattaché à un grand centre médical universitaire
|
Immunogénicité CMG d'IgG spécifiques au sérotype : Pas de différence dans les CMG entre les sujets âgés et les sujets jeunes pour les sérotypes 4, 6B, 9V, 14, 18C et 23F. Sérotype 19F : 9,14 vs 5, 24; p = 0,001 Titres d'OPA spécifiques au sérotype (IC à 95 %) Sérotype 4: 1 735 (1 074-2 804) vs 453 (250-821); p < 0,01 Sérotype 6B: 1 707(1 046-2 787) vs 377(188-756); p < 0,01 Sérotype 9V: 3 957(1 921-8 151) vs 411(203-832); p < 0,001 Sérotype 14: 3 715 (1 888-7 309) vs 1 250 (717-2 179); p < 0,01 Sérotype 18C: 1 344 (721-2 505) vs 933 (500-1 740); p = 0,09 Sérotype 19F: 1 254 (707-2 223) vs 266 (133-532) p < 0,01 Sérotype 23F: 766 (377-1 554) vs 147 (76-285); p < 0,001 Activité anticorps (titres d'opsonisation/IgG) : Significativement plus élevée chez les sujets jeunes que chez les sujets âgés, pour tous les sérotypes; p < 0,05 pour tous les sérotypes. |
Niveau I |
Bonne |
Musher, 2010 (37) |
PNEU-P-23 Suivi 30 jours plus tard par l'administration d'un autre produit dans l'autre groupe d'étude Voie : IM Suivi : 5 ans – prélèvements sanguins annuels par la suite |
Essai comparatif randomisé Exclusion : IIP antérieure, splénectomie, déficit immunitaire Groupe stratifié selon l'âge et les antécédents de vaccination antipneu-mococcique (au moins 3 ans auparavant pour les sujets de 50-64 ans et de 3 à 5 ans auparavant pour ceux de 65 ans ou plus) |
50-65 ans, primovaccination = 222 50-65 ans, revaccination = 157 ≥ 65, primovaccination = 222 ≥ 65 revaccination = 407 Total n = 1 008; 721 ont persisté pendant une période allant jusqu'à 5 ans (moyenne de 3,9 ans) Caractéristiques de référence semblables dans les quatre groupes, sauf que les sujets revaccinés dans chaque groupe d'âge étaient plus nombreux à signaler des facteurs de risque de IIP Titres d'IgG de référence semblables entre les sujets jeunes et les sujets âgés qui n'avaient pas déjà reçu le PNEU-P-23, et entre les sujets jeunes et les sujets âgés qui avaient déjà été vaccinés Les titres d'IgG de référence étaient de 2-3 fois plus élevés chez les sujets déjà vaccinés que chez les sujets non vaccinés. |
Immunogénicité IgG spécifiques au sérotype au jour 30 : Titres d'IgG au jour 30, primovaccination vs revaccination 50-65 ans : Mêmes dans les deux groupes pour tous les sérotypes à l'exception du sérotype 14 : 36,1 vs 24,6 (p < 0,5) Pour tous les autres sérotypes, pas de différence significative entre le groupe de primovaccination et de revaccination dans les deux groupes d'âge, à part un titre légèrement supérieur dans le groupe de primvaccination IgG spécifiques au sérotype au jour 60 : Titres plus élevés qu'au jour 30 dans les groupes âgés de revaccination et de primovaccination ainsi que dans le groupe jeune de revaccination pour tous les sérotypes; p = NS Supérieurs dans le groupe jeune de revaccination pour les sérotypes 4, 6B, 14, 23F; p = NS IgG spécifiques au sérotype à 5 ans : Patients revaccinés : Patients primovaccinés : Chez les 50-65 ans, les titres étaient plus élevés que les valeurs de référence pour les sérotypes 4, 6B, 8, 9V, 12F, 14 et 23F; p = NS Chez les sujets de ≥ 65 ans, sérotypes 4, 6B, 9V, 12F, 14 et 23F; p = NS |
Niveau I |
Bonne |
| Étude | DÉTAIL DE L'ÉTUDE | SOMMAIRE | ||||
|---|---|---|---|---|---|---|
| Vaccin | Devis de l'étude | Nombre de participants | Résumé des principales constatations sous forme de texte ou de données | Niveau de preuve | Qualité | |
| Frenck, 2012 (30) |
PNEU-C-13/ VTG – placebo (1 mois plus tard) 0,5 ml IM |
Essai comparatif randomisé Population : Sujets sains de 50-59 ans, n'ayant pas déjà reçu le vaccin contre le pneumocoque |
Multicentrique – É.-U. N = 1 158 sujets inscrits |
Innocuité :
|
Niveau I |
Bonne |
| Schwarz, 2011 (31) |
PNEU-C-13/VTG – placebo (1 mois plus tard) |
Essai comparatif randomisé Tous les sérotypes du PNEU-C-13 analysés Sujets sains de 65 ans ou plus, n'ayant pas déjà reçu le vaccin contre le pneumocoque Suivi jusqu'à 1 mois après la dernière administration de vaccin |
Multicentrique – Europe N = 1 190 sujets inscrits; 1 160 sujets répartis aléatoirement – 580 dans chaque groupe 1 096 sujets évaluables |
Innocuité :
|
Niveau I |
Bonne |
I |
Données probantes provenant d'un ou de plusieurs essais cliniques comparatifs randomisés. |
II-1 |
Données probantes provenant d'un ou de plusieurs essais cliniques comparatifs sans randomisation. |
II-2 |
Données probantes provenant d'études analytiques de cohortes ou cas/témoins, de préférence de plus d'un centre ou groupe de recherche utilisant des indicateurs cliniques de résultats de l'efficacité d'un vaccin. |
II-3 |
Données probantes provenant d'études de plusieurs séries chronologiques avec ou sans intervention. Les résultats spectaculaires obtenus dans un contexte non contrôlé (comme les résultats de l'introduction de la pénicilline dans les années 1940) pourraient aussi être considérés comme faisant partie de ce type de données probantes. |
III |
Opinions d'experts reconnus se basant sur des expériences cliniques, des études descriptives et des études de cas ou des rapports de comités d'experts. |
Bonne |
Étude (notamment les méta-analyses ou les recensions systématiques) répondant bien à tous les critères propres à la méthodologieNote de bas *. |
Moyenne |
Étude (notamment les méta-analyses ou les recensions systématiques) ne répondant pas (ou du moins pas clairement) à au moins un critère propre à la méthodologieNote de bas *, mais n'ayant pas de « lacune majeure » connue. |
Mauvaise |
Étude (notamment les méta-analyses ou les recensions systématiques) ayant au moins une « lacune majeure » propre à la méthodologieNote de bas * ou une accumulation de lacunes moins importantes ne permettant pas de formuler des recommandations à partir des résultats de l'étude. |
note * Les critères spécifiques de la méthodologie générale sont décrits dans Haris et coll., 2001 .Note en bas de page1. note 1 Harris RP, Helfand M, Woolf SH, et al. Current methods of the US Preventive Services Task Force: a review of the process. Am J Prev Med 2001;20:21-35. |
|
A |
Le CCNI a conclu qu'il existait des données probantes suffisantes pour recommander l'immunisation. |
B |
Le CCNI a conclu qu'il existait des données probantes acceptables pour recommander l'immunisation. |
C |
Le CCNI a conclu qu'il existait des données probantes contradictoires qui ne permettent pas de faire une recommandation pour ou contre l'immunisation; cependant, d'autres facteurs peuvent influer sur la prise de décisions. |
D |
Le CCNI a conclu qu'il existait des données probantes acceptables pour déconseiller l'immunisation. |
E |
Le CCNI a conclu qu'il existait des données probantes suffisantes pour déconseiller l'immunisation. |
I |
Le CCNI a conclu qu'il existait des données probantes insuffisantes (en quantité ou en qualité) pour formuler une recommandation; cependant, d'autres facteurs peuvent influer sur la prise de décisions. |
Liste des abréviations
- ARV
- Antirétroviraux (traitement antirétroviral)
- CMG
- Concentration moyenne géométrique
- ECR
- Essai comparatif randomisé
- ERV
- Efficacité réelle du vaccin
- GCSH
- Greffe de cellules souches hématopoïétiques
- GRÉ
- Groupe à risque élevé
- HAART
- Traitement antirétroviral hautement actif
- IB
- Infection buccale
- IIP
- Infection invasive à pneumocoque
- IM
- Intramusculaire (voie)
- LNM
- Laboratoire national de microbiologie
- LSPQ
- Laboratoire de santé publique du Québec
- MMF
- Mofétilmycophénolate
- OP
- Organe plein (greffe d')
- OPA
- Activité opsonophagocytaire
- PNEU-C-13
- Vaccin conjugué contre le pneumocoque – 13-valent
- PNEU-P-23
- Vaccin polysaccharidique contre le pneumocoque – 23-valent
- POC
- Pneumonie d'origine communautaire
- PC
- Rapport de cotes
- RR
- Rapport de risque
- SCSMDO
- Système canadien de surveillance des maladies à déclaration obligatoire
- TIBDN
- Toronto Invasive Bacterial Disease Network
- TMG
- Titre moyen géométrique
- VTG
- Vaccin trivalent contre la grippe
Rechercher sur RMTC
Détails de la page
- Date de modification :