Programme intégré canadien de surveillance de la résistance aux antimicrobiens (PICRA) 2018 : Résultats intégrés
Télécharger la version PDF, 2727 Ko
Promouvoir et protéger la santé des canadiens grâce au leadership, aux partenariats, à l'innovation et aux interventions en matière de santé publique, Agence de la santé publique du Canada.
Préserver l'efficacité des antimicrobiens utilisés chez les humains et les animaux, Programme intégré canadien de surveillance de la résistance aux antimicrobiens.
Also available in English under the title:
Canadian Integrated Program for Antimicrobial Resistance Surveillance (CIPARS) 2018: Integrated Findings
Pour obtenir plus d'information, veuillez communiquer avec :
Dolly Kambo
Adjointe exécutive
Agence de la Santé Publique du Canada
370 Speedvale Avenue Ouest, Guelph, ON N1H 7M7
Téléphone : 519-826-2174
Télécopieur : 519-826-2255
Courriel : phac.cipars-picra.aspc@canada.ca
On peut obtenir, sur demande, la présente publication en formats de substitution.
©Sa Majesté la Reine du chef du Canada, représentée par la ministre de la Santé, 2020
Date de publication : décembre 2020
La présente publication peut être reproduite sans autorisation pour usage personnel ou interne seulement, dans la mesure où la source est indiquée en entier.
Cat. : HP2-4/2018F-2-1-PDF
ISBN : 978-0-660-36796-5
Pub. : 200322
Citation suggérée :
Gouvernement du Canada. Programme intégré canadien de surveillance de la résistance aux antimicrobiens 2018 : Résultats intégrés. Agence de la santé publique du Canada, Guelph (Ontario), 2020.
Sur la page
- Aperçu des activités du PICRA
- Faits saillants de 2018
- Résultats intégrés et discussion
- Quoi de neuf pour le PICRA en 2018
- Glossaire
Des questions?
Aperçu des activités du PICRA
Figure 1. Le PICRA réunit diverses sources de données d'une manière robuste et fiable
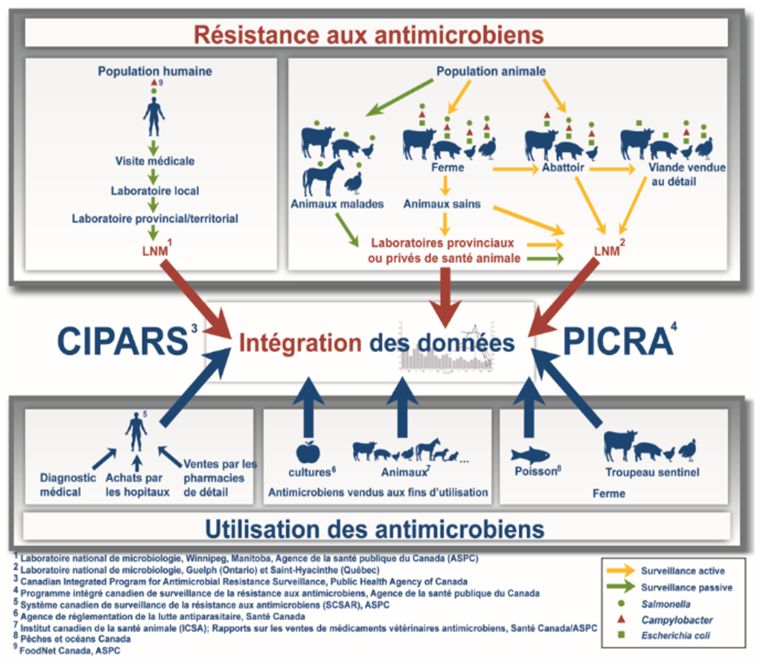
Figure 1 - Équivalent textuel
Le PICRA réunit diverses sources de données d'une manière robuste et fiable
Ce schéma représente l'ensemble des composantes de surveillance qui contribuent au Programme intégré canadien de surveillance de la résistance aux antimicrobiens (PICRA).
La moitié supérieure de la figure regroupe les composantes de surveillance relatives à la résistance aux antimicrobiens. À la gauche, on retrouve la composante de surveillance passive (flèches vertes) associée aux échantillons cliniques de Salmonella (cercle vert) et de Campylobacter (triangle rouge) d'origine humaine. Ces échantillons d'origine humaine sont prélevés lors de la visite médicale et sont acheminés à un laboratoire local, puis à un laboratoire provincial/territorial et enfin, au Laboratoire national de microbiologie de l'Agence de la santé publique du canada (ASPC) à Winnipeg. À la droite, on retrouve la composante de surveillance passive (flèches vertes) et les trois composantes de surveillance active (flèches jaunes) provenant du secteur agroalimentaire. La composante de surveillance passive (flèches vertes) comporte des échantillons cliniques provenant d'animaux malades (bovins, porcs, poulet, chevaux et dindons) qui sont soumis aux laboratoires provinciaux ou privés de santé animale pour l'isolement de Salmonella (cercle vert). Plus à droite, on retrouve les composantes de surveillance active (flèches jaunes) qui comportent des échantillons d'origine animale provenant de la ferme (bovins, porcs, poulets et dindons), de l'abattoir (bovins de boucherie, poulets et porcs) et aussi, des échantillons de viandes vendues au détail (bœuf, porc, poulet et dindon). En général, les échantillons provenant d'animaux malades sont acheminés au Laboratoire national de microbiologie de l'ASPC à Guelph par l'entremise des laboratoires provinciaux ou privés de santé animale. En ce qui concerne les autres échantillons du secteur agroalimentaire, la plupart seront acheminés directement au Laboratoire national de microbiologie de l'ASPC à Saint-Hyacinthe pour l'isolement de Salmonella (cercle vert), de Campylobacter (triangle rouge) et d'Escherichia coli (carré vert).
Le bas de la figure regroupe les composantes de surveillance relatives à l'utilisation des antimicrobiens. Parmi celles-ci, on retrouve à gauche, les trois composantes en lien avec l'utilisation d'antimicrobiens chez les humains qui reposent sur des données de diagnostic médical, d'achats faits par les hôpitaux et des ventes provenant des pharmacies de détail. Ces données d'origine humaine sont analysées par le Système canadien de surveillance de la résistance aux antimicrobiens de l'ASPC et sont intégrées aux autres données du PICRA. Au centre, on retrouve une composante qui repose sur la surveillance d'antimicrobiens vendus pour leur utilisation dans les cultures. Ces données sont traitées par l'Agence de réglementation de la lutte antiparasitaire de Santé Canada et sont aussi intégrées à certaines données du PICRA. Il y a également une autre composante qui surveille les antimicrobiens distribués aux animaux. Celle-ci comporte les antimicrobiens distribués pour la vente aux fins d'utilisation chez les animaux de production (bovins, porcs, poulets, dindons, etc.) et les animaux de compagnie (chiens, chats, chevaux, etc.). Les données issues de cette composante sont traitées par l'Institut canadien de santé animale puis sont envoyées au PICRA pour une intégration plus poussée. À droite, on retrouve les deux composantes de surveillance ciblant l'utilisation à la ferme, les données d'utilisation d'antimicrobiens chez les poissons (traitées par Pêches et Océans Canada) et les données d'utilisation des antimicrobiens des troupeaux sentinelles (bovins, porcs, poulets et dindons).
La section centrale de ce schéma illustre la collecte de toutes les données relatives à la résistance aux antimicrobiens et à l'utilisation d'antimicrobiens au sein du programme du PICRA. Toutes les données recueillies sont intégrées de manière à dresser un portrait de l'évolution des tendances et du statut de la résistance et de l'utilisation d'antimicrobiens chez les humains et le secteur agroalimentaire au canada.
Faits saillants de 2018
Utilisation des antimicrobiens
- Les ventes d'antimicrobiens ont augmenté entre 2017 et 2018.
- La surveillance à la ferme a démontré une diminution dans l'utilisation d'antimicrobiens chez les poulets de chair en 2018 comparativement à 2017, abstraction faite de certaines variations provinciales.
- Chez les porcs, l'UAM a significativement diminué dans l'ensemble et a considérablement diminué dans certaines provinces.
- Chez les dindons, l'UAM a augmenté dans l'ensemble, abstraction faite de certaines variations provinciales.
Résistance aux antimicrobiens
Salmonella enteritidis résistants aux quinolones
La résistance aux quinolones (acide nalidixique) chez S. Enteritidis provenant de sources agroalimentaires est extrêmement rare, surtout lorsqu'elle provient des poulets.
En 2018, on a détecté de la résistance à l'acide nalidixique chez S. Enteritidis provenant de poulets et de la viande de poulet à des niveaux jamais observés auparavant par le PICRA.
Salmonella hautement résistants aux médicaments
C'est en 2018 que nous avons observé le nombre le plus élevé d'isolats de Salmonella hautement résistants en provenance de toutes les sources humaines, animales et alimentaires.
De plus, c'est la première fois que nous avons détecté un isolat de Salmonella hautement résistant (sérotype Infantis) provenant de viande de poulet.
Données intégrées sur l'utilisation des antimicrobiens et la résistance aux antimicrobiens
Pour les poulets et les personnes
L'intervention de l'industrie de la volaille visant à éliminer l'utilisation des antimicrobiens de catégorie I (y compris les céphalosporines de 3e génération et les fluoroquinolones) pour prévenir les maladies semble avoir réduit la résistance aux antimicrobiens dans la plupart des cas.
Utilisation du ceftiofur et résistance à la ceftriaxone
- Depuis 2015, il n'y a eu aucun cas déclaré d'utilisation de ceftiofur parmi les poulets de chair.
- Dans la plupart des cas, on a constaté une réduction de la résistance à la ceftriaxone (une céphalosporine de 3e génération) dans les isolats d'E. coli et de Salmonella provenant de poulets et dans les isolats de Salmonella d'origine humaine.
- On a par contre observé une augmentation de la résistance à la ceftriaxone dans les isolats de Salmonella détectés chez des poulets d'élevage.
Campylobacter résistants aux fluoroquinolones
- En 2018, on a déclaré avoir utilisé des fluoroquinolones pour traiter des poulets malades provenant du même troupeau en Colombie-Britannique.
- Comme par le passé, on a observé des différences régionales dans la prévalence de Campylobacter résistants aux fluoroquinolones provenant de poulets et de la viande de poulet.
- La résistance à la ciprofloxacine (une fluoroquinolone) a surtout été observée dans les isolats humains de Campylobacter et dans le poulet vendu au détail de la Colombie-Britannique comparativement à l'Alberta et l'Ontario.
Résultats intégrés et discussion
Données intégrées sur l'utilisation des antimicrobiens
Les antimicrobiens sont regroupés en des catégories fondées sur leur importance pour la médecine humaine et les conséquences potentielles de la résistance à ces médicaments :
- Catégorie I : Très haute importance
Exemples : céphalosporines (3e et 4e générations), carbapénèmes, fluoroquinolones. - Catégorie II : Haute importance
Exemples : macrolides, pénicillines. - Catégorie III : Importance moyenne
Exemples : tétracyclines. - Catégorie IV : Faible importance
Exemples : ionophores, flavophospholipides.
Les antimicrobiens médicalement importants incluent les Catégories I à III. On a retiré des rapports intégrés sur l'utilisation des antimicrobiens ceux qui sont de Faible importance (catégorie IV, à l'exception des flavophospholipides). Les données seront fournies dans d'autres produits de communication du PICRA.
Remarque : les anticoccidiens de synthèse sont considérés comme des antimicrobiens non catégorisés.
Nous utilisons différentes mesures et approches pour présenter les données sur les antimicrobiens utilisés chez les animaux.
Pourquoi utilisons-nous différentes mesures ?
- Il y a plusieurs façons de recueillir, d'analyser et de présenter les données sur l'utilisation des antimicrobiens.
- Aucune approche ne peut, à elle seule, convenir à tous les usages.
- Certaines mesures conviennent mieux pour suivre les tendances au fil du temps, tandis que d'autres permettent de mieux comparer différentes régions ou différentes espèces-hôtes; d'autres, encore, aident à mieux comprendre les relations entre l'utilisation et la résistance.
Comparaisons entre les humains, les animaux et les cultures végétales
Figure 2. Estimations de la taille de la population humaine et animale comparées avec la quantité totale en kilogrammes des antimicrobiens distribués et/ou vendus en 2018
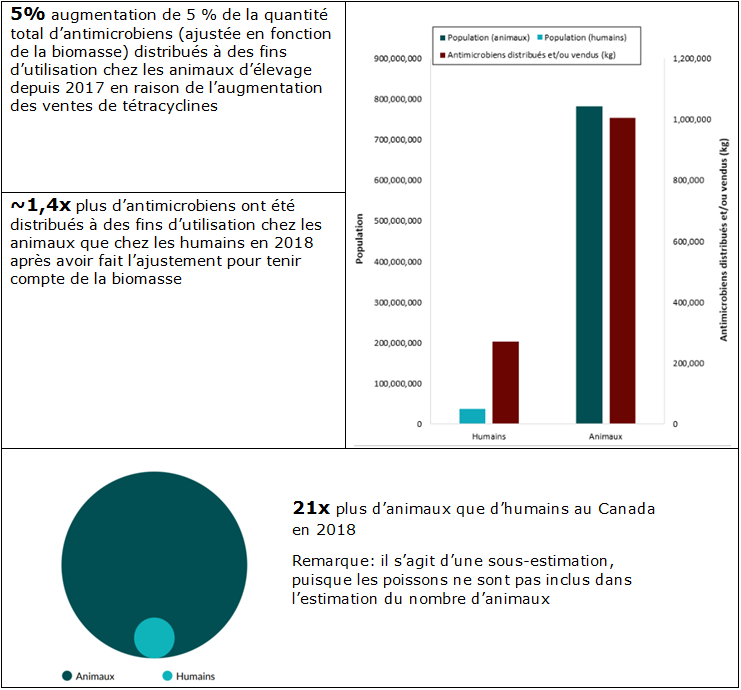
Figure 2 - Équivalent textuel
| Population | Population (animaux) | Antimicrobiens distribués et/ou vendus (kg) | Ratio (%) |
|---|---|---|---|
| Humains | 37 058 856 | 270 635 | 1 (4, 55 %) |
| Animaux | 782 985 707 | 1 004 392 | 21 (95,45 %) |
Des antimicrobiens distribués ou vendus* en 2018 :
- 78 % étaient destinés aux animaux d'élevage
- 21 % étaient destinés aux humains
- 1 % étaient destinés aux animaux de compagnie
- < 1 % étaient destinés aux cultures
*Les données actuelles sur la distribution chez les animaux ne tiennent pas compte des quantités importées pour une utilisation à des fins personnelles ou comme ingrédients actifs dans les préparations pharmaceutiques, d'où les sous-estimations des quantités totales utilisées.
Tant pour les humains que les animaux, les β-lactamines (pénicillines) étaient l'une des principales classes d'antimicrobiens distribuées ou vendues par kilogramme.
Bien que des antimicrobiens semblables soient autorisés chez les humains et les animaux, certaines classes d'antimicrobiens ont été vendues ou distribuées plus souvent aux fins d'utilisation chez les humains que les animaux (et vice-versa).
La quantité relative de céphalosporines et de fluoroquinolones (catégorie I) destinée aux humains est plus élevée que celle qu'on destine aux animaux (respectivement, environ 7 fois et 25 fois plus élevée).
Les tétracyclines (catégorie III) servent sont principalement utilisées par les animaux de production.
Remarques :
- Même si les céphalosporines sont des ß-lactamines, nous les présentons séparément pour faciliter la visualisation.
- Les pourcentages sont le poids total (en kilogrammes) des ingrédients actifs utilisés pour l'espèce hôte en question.
- Autres antimicrobiens destinés aux animaux : avilamycine, bacitracines, bambermycine, chloramphénicol, gluconate de chlorhexidine, florfénicol, acide fusidique, novobiocine, polymyxine B, tiamuline, virginiamycine.
- Autres antimicrobiens destinés aux humains : bacitracine, chloramphénicol, colistiméthate, colistine, daptomycine, fidaxomicine, fosfomycine, acide fusidique, linézolide, hippurate de méthénamine, mandélate de méthénamine, métronidazole, nitrofurantoïne, polymyxine B, quinupristine-dalfopristine et vancomycine.
Figure 3. Proportion de la quantité totale en kilogrammes des classes d'antimicrobiens distribuées et/ou vendues en 2018 chez les humains, les animaux de production et les animaux de compagnie
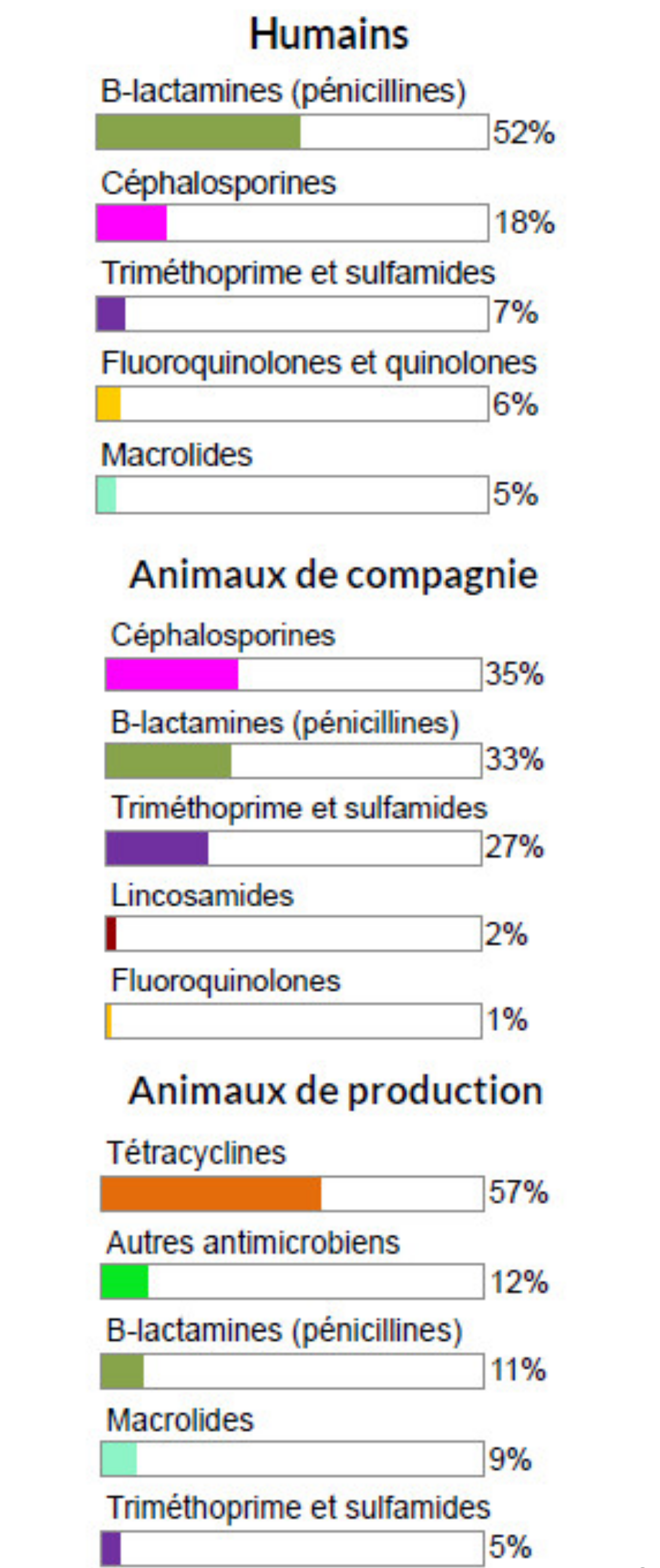
Figure 3 - Équivalent textuel
| Humains | Animaux de compagnie | Animaux de production | |||
|---|---|---|---|---|---|
| Classes d'antimicrobiens | % | Classes d'antimicrobiens | % | Classes d'antimicrobiens | % |
| B-lactamines (pénicillines) | 52% | Céphalosporines | 35% | Tétracyclines | 57% |
| Céphalosporines | 18% | B-lactamines (pénicillines) | 33% | Autre antimicrobiens | 12% |
| Triméthoprime et sulfamides | 7% | Triméthoprime et sulfamides | 27% | B-lactamines (pénicillines) | 11% |
| Fluoroquinolones et quinolones | 6% | Lincosamides | 2% | Macrolides | 9% |
| Macrolides | 5% | Fluoroquinolones | 1% | Triméthoprime et sulfamides | 5% |
On a observé une augmentation des quantités totales d'antimicrobiens vendus à des fins d'utilisation chez des animaux d'élevage. Mesuré en kilogrammes, la quantité totale distribuée a augmenté de 6 % depuis 2017. Suite à l'ajustement en fonction de la biomasse (mg/PCU), cette augmentation s'élève à 5 % depuis 2017.
Figure 4. Quantités d'antimicrobiens distribués pour une utilisation chez les animaux
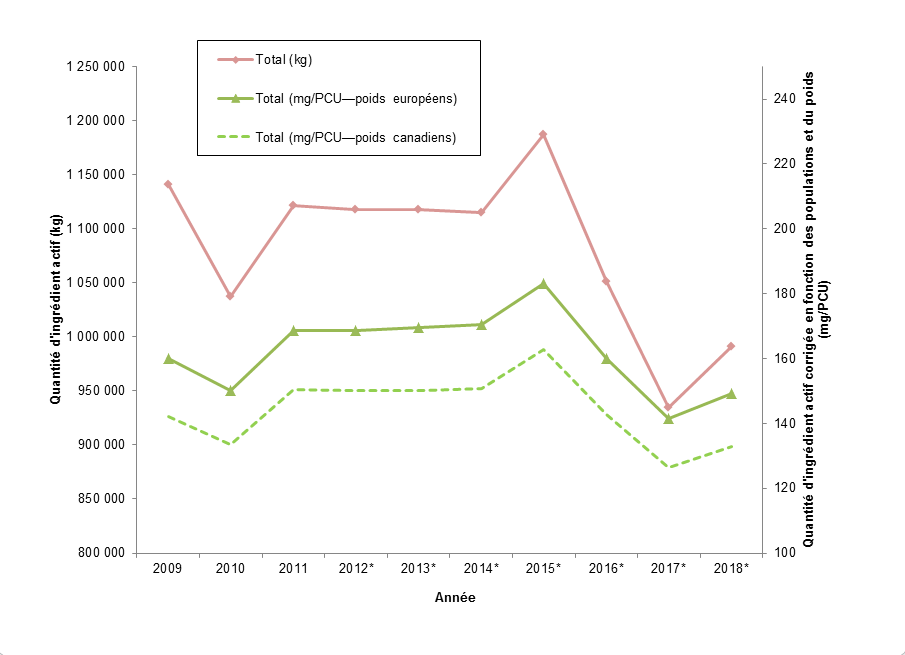
Figure 4 - Équivalent textuel
| Année | Total (kg) | Total (mg/PCU poids européens) | Total (mg/PCU poids canadiens) |
|---|---|---|---|
| 2008 | 1 143 187 | 150 | 128 |
| 2009 | 1 141 213 | 160 | 137 |
| 2010 | 1 037 313 | 150 | 129 |
| 2011 | 1 121 715 | 168 | 145 |
| 2012Note de bas de tableau 4 - * | 1 117 457 | 169 | 145 |
| 2013Note de bas de tableau 4 - * | 1 118 097 | 170 | 145 |
| 2014Note de bas de tableau 4 - * | 1 114 837 | 170 | 146 |
| 2015Note de bas de tableau 4 - * | 1 187 136 | 183 | 157 |
| 2016Note de bas de tableau 4 - * | 1 051 010 | 160 | 138 |
| 2017Note de bas de tableau 4 - * | 934 873 | 141 | 122 |
| 2018Note de bas de tableau 4 - * | 991 150 | 149 | 133 |
Le Canada se trouve au 6e rang (par rapport à l'Europe) pour ce qui est des quantités d'antimicrobiens vendus (mg/PCU).
Figure 5. Quantités d'antimicrobiens utilisés (mg/PCU) au Canada (2018) et dans les pays membres du réseau European Surveillance of Veterinary Antimicrobial Consumption (ESVAC) (2017)
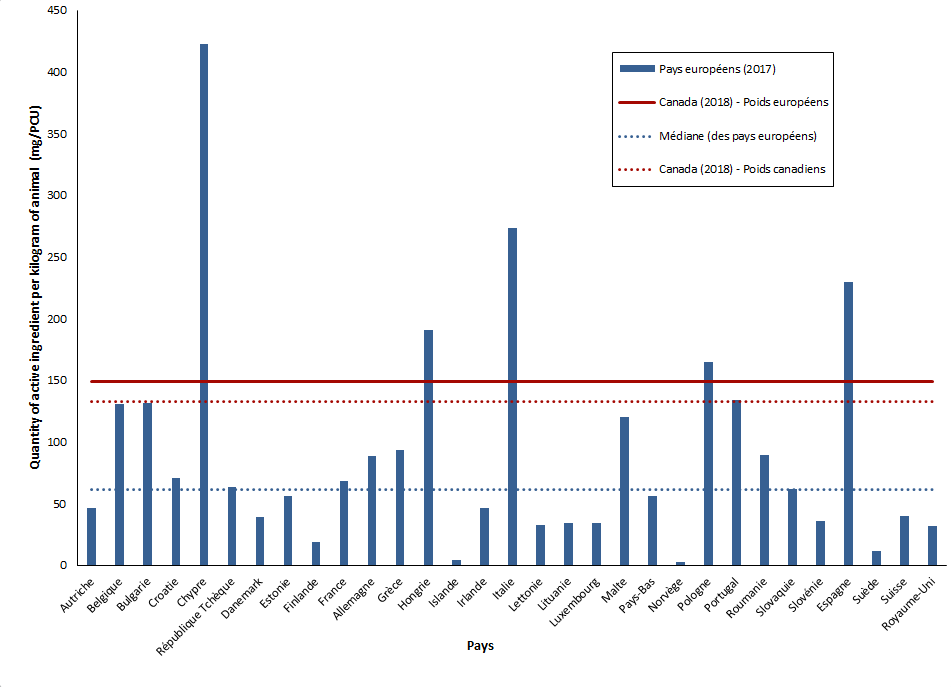
Figure 5 - Équivalent textuel
| Pays européens (2017) | mg/PCU | Canada (2018) Poids européens | Médiane (des pays européens) | Canada (2018) - Poids canadiens |
|---|---|---|---|---|
| Autriche | 47 | 149 | 62 | 133 |
| Belgique | 131 | 149 | 62 | 133 |
| Bulgarie | 132 | 149 | 62 | 133 |
| Croatie | 72 | 149 | 62 | 133 |
| Chypre | 423 | 149 | 62 | 133 |
| République Tchèque | 64 | 149 | 62 | 133 |
| Danemark | 39 | 149 | 62 | 133 |
| Estonie | 57 | 149 | 62 | 133 |
| Finlande | 19 | 149 | 62 | 133 |
| France | 69 | 149 | 62 | 133 |
| Allemagne | 89 | 149 | 62 | 133 |
| Grèce | 94 | 149 | 62 | 133 |
| Hongrie | 191 | 149 | 62 | 133 |
| Islande | 5 | 149 | 62 | 133 |
| Irlande | 47 | 149 | 62 | 133 |
| Italie | 274 | 149 | 62 | 133 |
| Lettonie | 33 | 149 | 62 | 133 |
| Lituanie | 35 | 149 | 62 | 133 |
| Luxembourg | 35 | 149 | 62 | 133 |
| Malte | 121 | 149 | 62 | 133 |
| Pays-Bas | 56 | 149 | 62 | 133 |
| Norvège | 3 | 149 | 62 | 133 |
| Pologne | 165 | 149 | 62 | 133 |
| Portugal | 135 | 149 | 62 | 133 |
| Roumanie | 90 | 149 | 62 | 133 |
| Slovaquie | 62 | 149 | 62 | 133 |
| Slovénie | 37 | 149 | 62 | 133 |
| Espagne | 230 | 149 | 62 | 133 |
| Suède | 12 | 149 | 62 | 133 |
| Suisse | 40 | 149 | 62 | 133 |
| Royaume-Uni | 33 | 149 | 62 | 133 |
*Les poids utilisés dans le calcul de la biomasse sont les poids standards européens au moment du traitement
**Dans cette figure, on présume que les données sont comparables.
Sources des données : Institut canadien de la santé animale (ICSA), European Surveillance of Veterinary Antimicrobial Consumption (ESVAC), Pêches et Océans Canada, Agence de réglementation de la lutte antiparasitaire, données d'origine humaine d'IQVIA fournies par les pharmacies et les hôpitaux, Système canadien de surveillance de la résistance aux antimicrobiens, Statistique Canada, Agriculture et Agroalimentaire Canada et Canada Équestre.
Comparaison des données sur l'utilisation des antimicrobiens à la ferme
Comparaison des classes d'antimicrobiens*
Il y a d'importantes différences dans les types et les quantités relatives d'antimicrobiens utilisés chez les animaux destinés à la consommation; c'est pourquoi nous avons besoin d'une surveillance continue pour ces espèces animales.
*Les pourcentages sont fondés sur le poids total (en kilogrammes) des ingrédients actifs utilisés pour l'espèce hôte en question.
Figure 6.1 Quantités relatives des classes d'antimicrobiens pour lesquelles on a signalé une utilisation (mg/PCU) chez les animaux en 2018 : poulets de chair
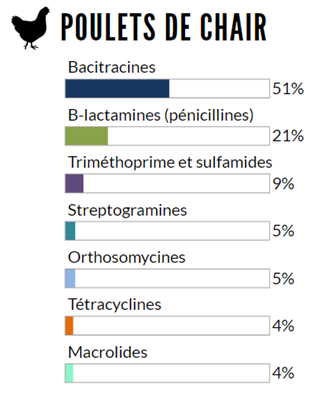
Non représenté : aminoglycosides (1%), lincosamides-aminocyclitols (moins de 1%).
Figure 6.2 Quantités relatives des classes d'antimicrobiens pour lesquelles on a signalé une utilisation (mg/PCU) chez les animaux en 2018 : porcs en croissance-finition
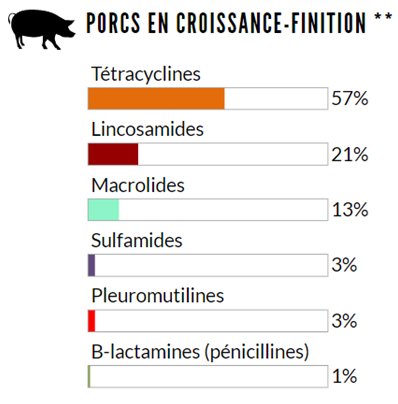
Non représenté : streptogramines (1%)
**utilisation dans les aliments seulement.
Figure 6.3 Quantités relatives des classes d'antimicrobiens pour lesquelles on a signalé une utilisation (mg/PCU) chez les animaux en 2018 : dindons

Non représenté : B-lactamines (pénicillines) (3%), orthomycines (1%), fluoroquinolones (moins de 1%).
Figure 6.1, 6.2, 6.3 - Équivalent textuel
| Poulets de chair | Porcs en croissance-finition | Dindons | |||
|---|---|---|---|---|---|
| Classes d'antimicrobiens | % | Classes d'antimicrobiens | % | Classes d'antimicrobiens | % |
| Bacitracines | 51% | Tétracyclines | 57% | Bacitracines | 53% |
| B-lactamines (pénicillines) | 21% | Lincosamides | 21% | Streptogramines | 26% |
| Triméthoprime et sulfamides | 9% | Macrolides | 13% | Triméthoprime et sulfamides | 7% |
| Streptogramines | 5% | Sulfamides | 3% | Tétracyclines | 6% |
| Orthosomycines | 5% | Pleuromutilines | 3% | Aminoglycosides | 4% |
| Tétracyclines | 4% | B-lactamines (pénicillines) | 1% | aucune donnée disponible | aucune donnée disponible |
| Macrolides | 4% | no data | no data | no data | no data |
Tendance temporelles de l'utilisation d'antimicrobiens
Poulets de chair
Dans l'ensemble (au plan national), la surveillance à la ferme a révélé une diminution de l'utilisation d'antimicrobiens chez les poulets de chair en 2018 comparativement à 2017. Les deux classes d'antimicrobiens les plus fréquemment employés chez les poulets de chair étaient les bacitracines (catégorie III) et les pénicillines (catégorie II).
On a constaté des différences régionales dans le nombre de doses d'antimicrobiens administrées. Depuis 2017, on note :
- Dans l'ensemble, les Prairies et l'Ontario ont diminué leur utilisation d'antimicrobiens.
- Dans l'ensemble, la Colombie-Britannique et le Québec ont augmenté leur utilisation d'antimicrobiens.
Figure 7. Tendances temporelles en nDDDvetCA/1000 poulets-jours à risque, de 2013 à 2018
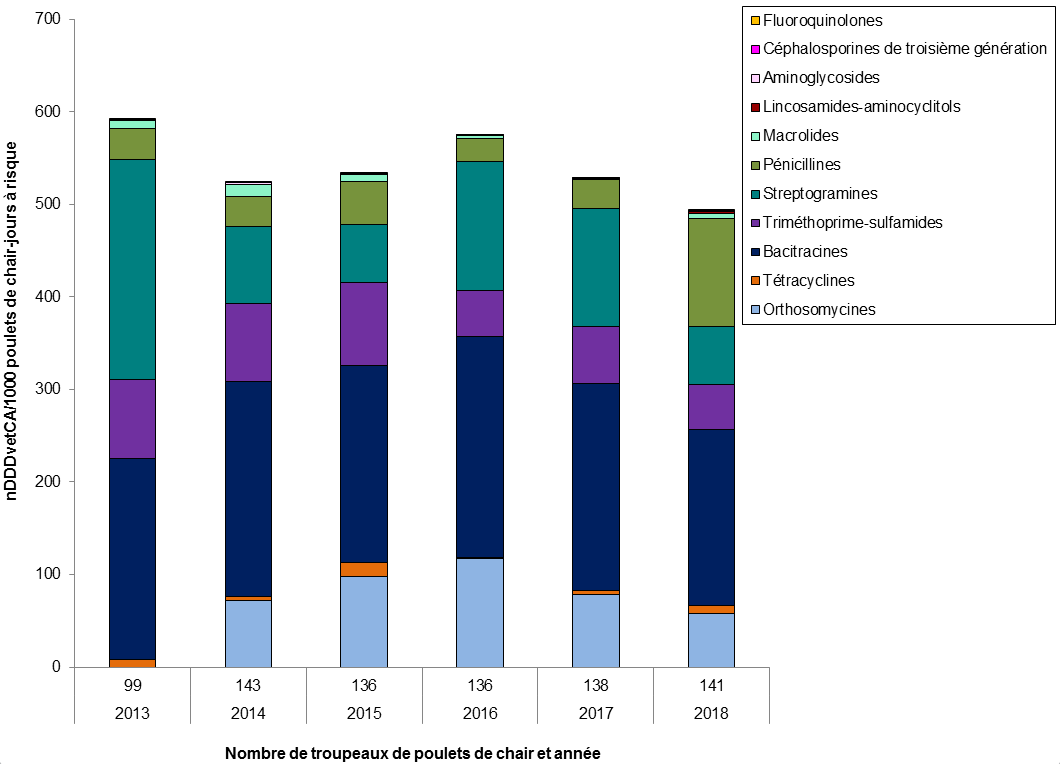
Figure 7 - Équivalent textuel
| Année | 2013 | 2014 | 2015 | 2016 | 2017 | 2018 | |
|---|---|---|---|---|---|---|---|
| Nombre de troupeaux | 99 | 143 | 136 | 136 | 138 | 141 | |
| Classe d'antimicrobiens | |||||||
| I | Fluoroquinolones | < 0,1 | 0 | 0 | 0 | 0 | < 0,1 |
| Céphalosporines de troisième génération | 1 | 0,1 | 0 | 0 | 0 | 0 | |
| II | Aminoglycosides | < 0,1 | 2 | 2 | 1 | 1 | 1 |
| Lincosamides-aminocyclitols | 1 | 1 | 1 | 0,5 | 0,5 | 2 | |
| Macrolides | 8 | 12 | 7 | 3 | 1 | 6 | |
| Pénicillines | 34 | 33 | 47 | 25 | 31 | 116 | |
| Streptogramines | 237 | 83 | 63 | 139 | 128 | 63 | |
| Triméthoprime-sulfamides | 85 | 85 | 89 | 50 | 61 | 49 | |
| III | Bacitracines | 217 | 232 | 213 | 239 | 224 | 190 |
| Tétracyclines | 9 | 4 | 15 | 1 | 4 | 8 | |
| Sans objet | Orthosomycines | 0 | 72 | 98 | 117 | 79 | 58 |
| Total | 591 | 524 | 535 | 576 | 529 | 493 | |
Figure 8. Tendances temporelles en nDDDvetCA/1000 poulets-jours à risque, par province/région, de 2014 à 2018
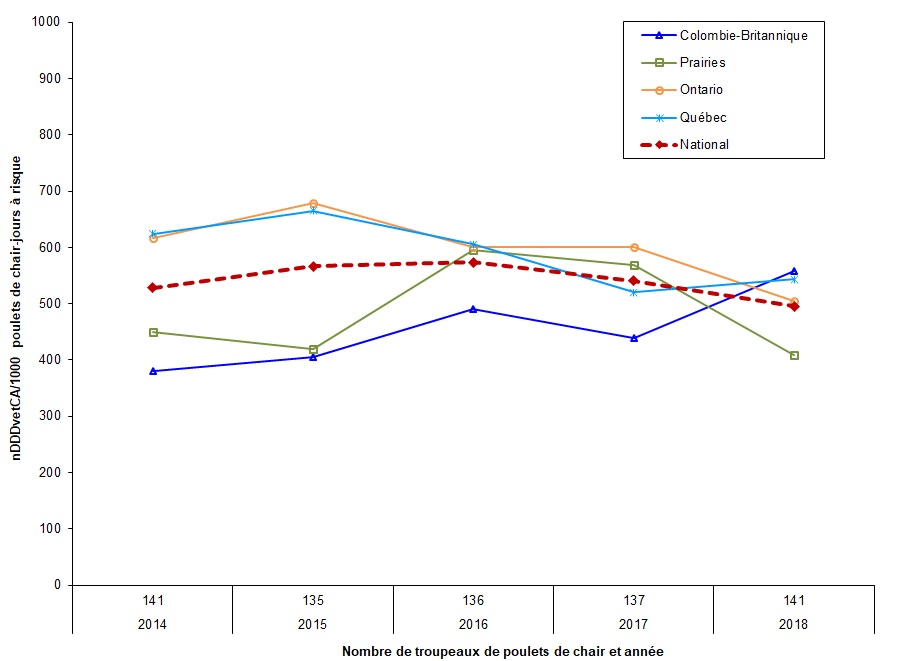
Figure 8 - Équivalent textuel
| Année | 2014 | 2015 | 2016 | 2017 | 2018 |
|---|---|---|---|---|---|
| Nombre de troupeaux de poulets de chair | 141 | 135 | 136 | 137 | 141 |
| Province/région | |||||
| Colombie-Britannique | 380 | 405 | 491 | 439 | 558 |
| Prairies | 450 | 419 | 595 | 568 | 410 |
| Ontario | 616 | 679 | 601 | 601 | 504 |
| Québec | 624 | 665 | 606 | 521 | 544 |
| National | 528 | 566 | 573 | 541 | 495 |
Porcs en croissance-finition
La surveillance à la ferme a montré une diminution de l'usage d'antimicrobiens dans les aliments (nDDDvetCA/1000 porcs-jours à risque) entre 2014 et 2018. Les classes d'antimicrobiens les plus fréquemment administrés aux porcs étaient les tétracyclines (catégorie III), les lincosamides (catégorie II) et les macrolides (catégorie II).
On a constaté des différences régionales dans la quantité et le nombre de doses administrées dans les aliments pendant une période d'engraissement des porcs en croissance-finition. Depuis 2017, on note :
- Dans l'ensemble, une diminution de l'utilisation des antimicrobiens a été notée pour les troupeaux du Québec et de l'Ontario.
- Dans l'ensemble, une augmentation de l'utilisation des antimicrobiens a été notée pour les troupeaux des Prairies.
Figure 9. Tendances temporelles en nDDDvetCA/1000 porcs-jours à risque, de 2009 à 2018
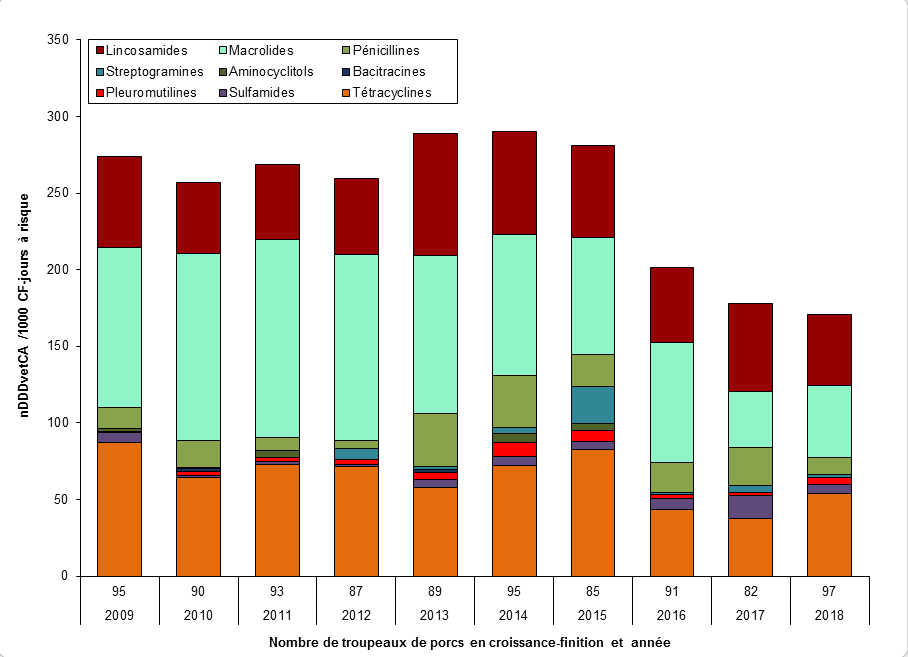
Figure 9 - Équivalent textuel
| Année | 2009 | 2010 | 2011 | 2012 | 2013 | 2014 | 2015 | 2016 | 2017 | 2018 | |
|---|---|---|---|---|---|---|---|---|---|---|---|
| Nombre de troupeaux de porcs en croissance-finition | 95 | 90 | 93 | 87 | 89 | 95 | 85 | 91 | 82 | 97 | |
| Classe d'antimicrobiens | |||||||||||
| II | Lincosamides | 59 | 47 | 49 | 49 | 79 | 68 | 60 | 49 | 57 | 46 |
| Macrolides | 104 | 122 | 129 | 122 | 103 | 92 | 76 | 78 | 37 | 47 | |
| Pénicillines | 14 | 17 | 8 | 5 | 35 | 34 | 21 | 20 | 25 | 11 | |
| Streptogramines | 0 | 0 | 0 | 7 | 2 | 4 | 24 | 1 | 4 | 2 | |
| III | Aminocyclitols | 2 | 1 | 4 | 0 | 0 | 6 | 4 | 0 | 0 | 0 |
| Bacitracines | 0 | 2 | 0 | 0 | 2 | 0 | 0 | 0 | 0 | 0 | |
| Pleuromutilines | 0 | 3 | 3 | 3 | 5 | 9 | 7 | 3 | 2 | 4 | |
| Sulfanamides | 7 | 2 | 2 | 1 | 5 | 5 | 5 | 7 | 15 | 6 | |
| Tétracyclines | 87 | 64 | 73 | 72 | 58 | 72 | 82 | 44 | 38 | 54 | |
| Total | 274 | 257 | 269 | 259 | 289 | 290 | 281 | 202 | 178 | 171 | |
Figure 10. Tendances temporelles en nDDDvetCA/1000 porcs-jours à risque, pour les antimicrobiens administrés dans les aliments, de 2014 à 2018
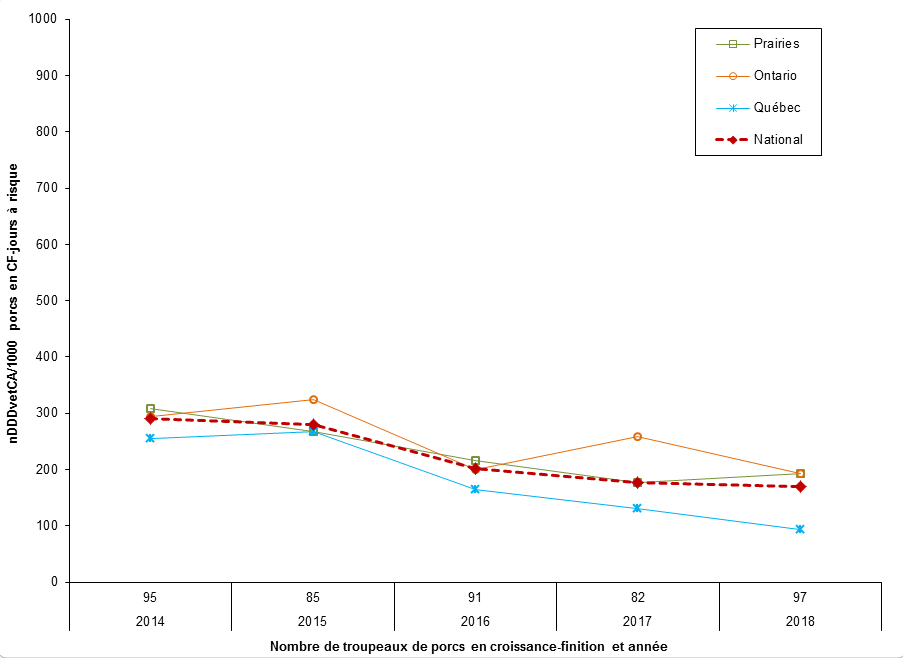
Figure 10 - Équivalent textuel
| Année | 2014 | 2015 | 2016 | 2017 | 2018 |
|---|---|---|---|---|---|
| Nombre de troupeaux de porcs en croissance-finition | 95 | 85 | 91 | 82 | 97 |
| Province/région | |||||
| Prairies | 308 | 268 | 217 | 177 | 193 |
| Ontario | 294 | 325 | 200 | 259 | 192 |
| Québec | 255 | 268 | 164 | 130 | 94 |
| National | 290 | 281 | 202 | 178 | 171 |
Dindons
Dans l'ensemble, le recours aux antimicrobiens chez les dindons a augmenté en 2018. Les deux classes d'antimicrobiens les plus fréquemment administrés chez les dindons étaient les streptogramines (catégorie II) et les bacitracines (catégorie III). Depuis 2017, on note :
- Dans l'ensemble, une diminution de l'utilisation des antimicrobiens a été notée pour les troupeaux de l'Ontario et du Québec.
- Dans l'ensemble, une augmentation de l'utilisation des antimicrobiens a été notée pour les troupeaux de la Colombie-Britannique.
Figure 11. Tendances temporelles en nDDDvet par 1000 dindons-jours à risque, de 2016 à 2018
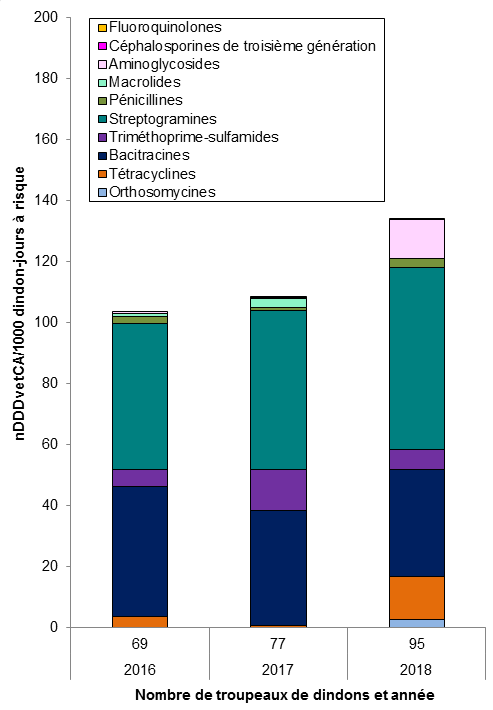
Figure 11 - Équivalent textuel
| Année | 2016 | 2017 | 2018 | |
|---|---|---|---|---|
| Nombre de troupeaux de dindons | 69 | 77 | 95 | |
| Classe d'antimicrobiens | ||||
| I | Fluoroquinolones | 0 | < 0,1 | 0,1 |
| Céphalosporines de troisième génération | 0 | 0 | 0 | |
| II | Aminoglycosides | 1 | 0,3 | 13 |
| Macrolides | 1 | 3 | 0 | |
| Pénicillines | 2 | 1 | 3 | |
| Streptogramines | 48 | 52 | 60 | |
| Triméthoprime-sulfamides | 5 | 13 | 7 | |
| III | Bacitracines | 43 | 38 | 35 |
| Tétracyclines | 4 | 0,4 | 14 | |
| Sans objet | Orthosomycines | 0 | 0 | 2 |
| Total | 104 | 108 | 134 | |
Figure 12. Tendances temporelles en nDDDvet par 1000 dindons-jours à risque, par province/région, de 2016 à 2018
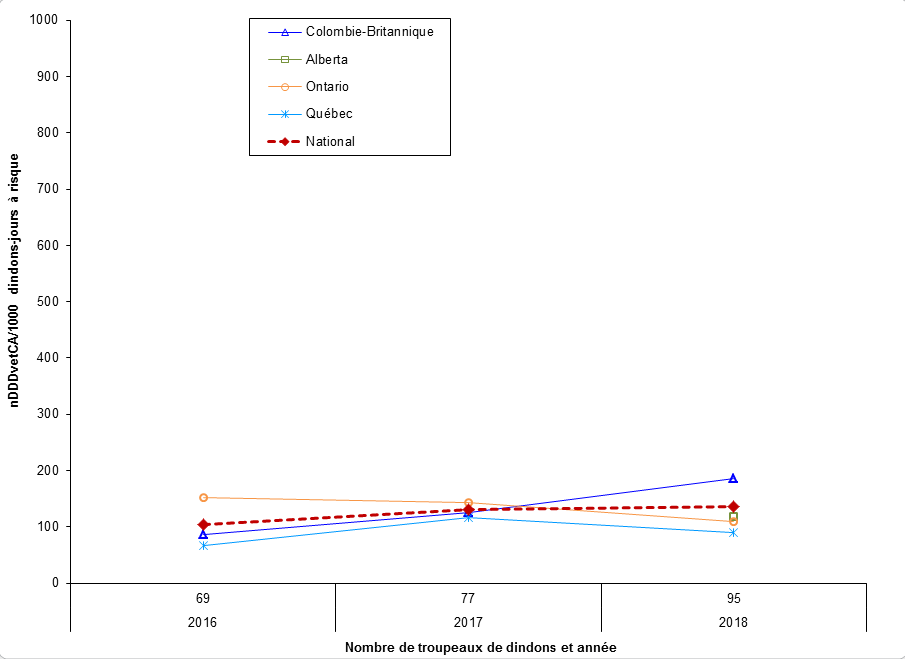
Figure 12 - Équivalent textuel
| Année | 2016 | 2017 | 2018 |
|---|---|---|---|
| Nombre de troupeaux de dindons | 69 | 77 | 95 |
| Province | |||
| Colombie-Britannique | 86 | 125 | 186 |
| Alberta | Sans objet | Sans objet | 119 |
| Ontario | 152 | 143 | 110 |
| Québec | 66 | 117 | 89 |
| National | 104 | 131 | 137 |
Raisons de l'utilisation d'antimicrobiens
- Chez les poulets de chair, les dindons et les porcs en croissance-finition (C-F), la principale raison évoquée pour administrer des antimicrobiens était la prévention de maladies.
- Chez les porcs en croissance-finition, on continue de signaler l'utilisation d'antimicrobiens pour stimuler la croissance de ces derniers.
Figure 13. Quantité d'antimicrobiens utilisés (mg/PCU) par raison d'utilisation; PICRA à la ferme, de 2014 à 2018
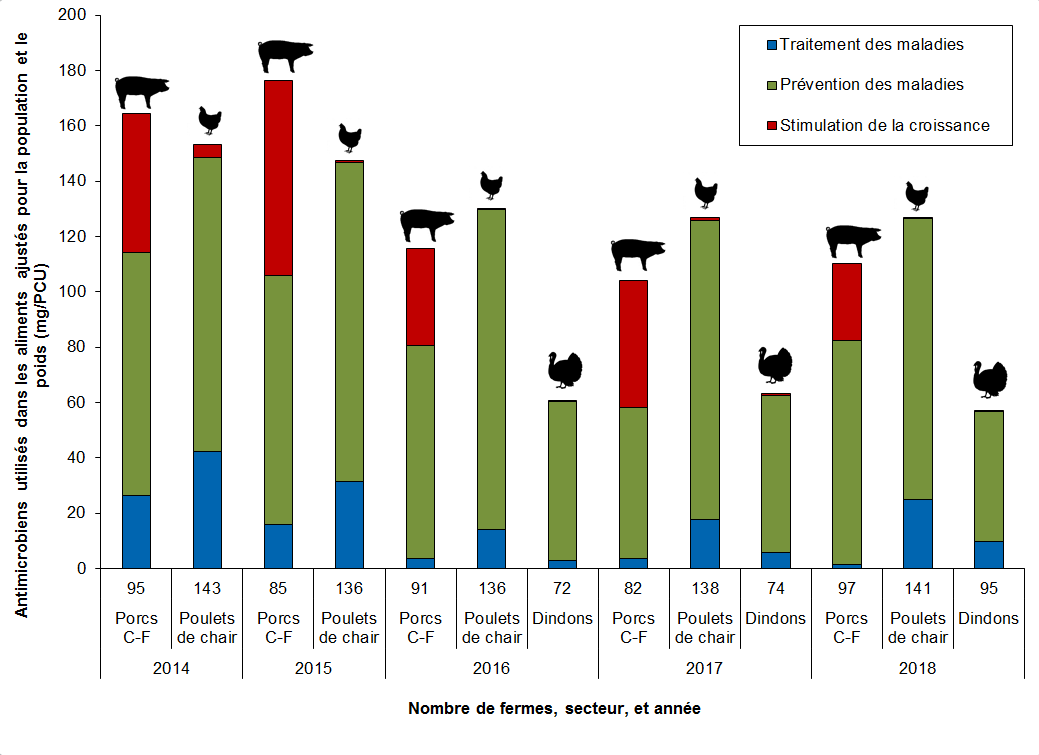
Figure 13 - Équivalent textuel
| Année | 2014 | 2015 | 2016 | 2017 | 2018 | ||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Secteur | Porcs C-F | Poulets de chair | Porcs C-F | Poulets de chair | Porcs C-F | Poulets de chair | Dindons | Porcs C-F | Poulets de chair | Dindons | Porcs C-F | Poulets de chair | Dindons |
| Nombre de fermes | 95 | 143 | 85 | 136 | 91 | 136 | 72 | 82 | 138 | 74 | 97 | 141 | 95 |
| Traitement des maladies | 26 | 43 | 16 | 31 | 4 | 14 | 3 | 4 | 18 | 6 | 2 | 25 | 10 |
| Prévention des maladies | 88 | 106 | 90 | 116 | 77 | 115 | 58 | 54 | 108 | 56 | 81 | 101 | 47 |
| Stimulation de la croissance | 50 | 5 | 70 | 1 | 35 | 0 | 0 | 46 | 1 | 1 | 28 | 0 | 0 |
| Total | 164 | 153 | 176 | 148 | 116 | 130 | 61 | 104 | 127 | 63 | 110 | 126 | 57 |
Remarque : Les données sur les porcs ont trait uniquement aux antimicrobiens administrés dans les aliments; les données sur les poulets et les dindons incluent toutes les voies d'administration.
Données intégrées sur la résistance aux antimicrobiens
Dans cette section, nous mettrons l'accent sur deux histoires portant sur la résistance en 2018 :
- La détection de Salmonella Enteritidis résistants aux quinolones chez le poulet.
- L'augmentation de Salmonella hautement résistants provenant de sources humaines et agroalimentaires.
En 2018, le PICRA a effectué des tests de résistance pour 7 classes d'antimicrobiens.
Bien qu'il n'existe aucune norme internationale définissant les isolats hautement résistants, le PICRA considère que les isolats résistants à au moins 6 classes d'antimicrobiens sont hautement résistants.
Détection de Salmonella Enteritidis résistants aux quinolones chez le poulet
En 2018, on a clairement observé une augmentation de la résistance à l'acide nalidixique (une quinolone) dans des isolats de S. Enteritidis provenant de poulets dans plusieurs composantes de surveillance et dans plusieurs provinces.
Détail
- 1 isolat provenant d'un hamburger au poulet en Colombie-Britannique (FoodNet Canada)
Détail
- 1 isolat de l'Alberta
- Jamais observé auparavant
Abattoir
- 2 isolats de l'Ontario et du Québec
- Jamais observé auparavant
Cas cliniques
- 2 isolats de l'Ontario (poulet malade)
- Observé en 2010, un seul isolat du Manitoba
La plupart des isolats de S. Enteritidis provenant de sources animales et alimentaires étaient susceptibles à tous les antimicrobiens testés.
De 2003 à 2018, la résistance à l'acide nalidixique a seulement été observée en 2010 pour un seul isolat qui provenait d'un poulet malade du Manitoba (isolat clinique).
La majorité des isolats de S. Enteritidis prélevés sur des humains étaient susceptibles à tous les antimicrobiens testés. Lorsqu'il y avait de la résistance, il s'agissait le plus souvent de résistance à l'acide nalidixique et ces cas humains peuvent être reliés à des voyages effectués à l'extérieur du Canada.
Les S. Enteritidis resistants à l'acide nalidixique pourraient représenter une nouvelle source d'exposition humaine au Canada. Le PICRA suivra de près cette augmentation soudaine et sans précédent de la résistance en provenance de poulets et de la viande de poulet.
Des Salmonella hautement résistants aux médicaments
- Depuis 2008, le nombre d'isolats de Salmonella hautement résistants a augmenté sensiblement chez les êtres humains et les animaux.
- C'est en 2018 qu'on a détecté pour la première fois des isolats de Salmonella hautement résistants qui provenaient de poulet.
- Malgré la légère diminution enregistrée en 2017, on a constaté en 2018 une augmentation considérable du nombre d'isolats de Salmonella hautement résistants, un niveau jamais observé auparavant par le PICRA.
En 2018, 132 isolats de Salmonella, identifiés comme hautements résistants aux médicaments, provenaient des sources suivantes :
Poulets
- Tous les isolats hautement résistants associés au poulet provenaient d'échantillons de viande vendue au détail (de hamburgers de poulet) prélevés en Colombie-Britannique, dans les Prairies et en Ontario.
- Tous étaient des isolats de S. Infantis.
Bovins
- Bovins malades (isolats cliniques).
- La plupart étaient des isolats de S. Dublin.
Porcs
- Porcs malades (isolats cliniques)
- Certains isolats affichent de la résistance aux 7 classes d'antimicrobiens testés.
- On a détecté quatre sérotypes.
Humains
- On n'a testé que des isolats cliniques.
- La plupart étaient des isolats de S. Infantis, de S. Newport et de S. Typhimurium.
Figure 14. Nombre d'isolats de Salmonella résistants à au moins 6 classes d'antimicrobiens de 2008 à 2018
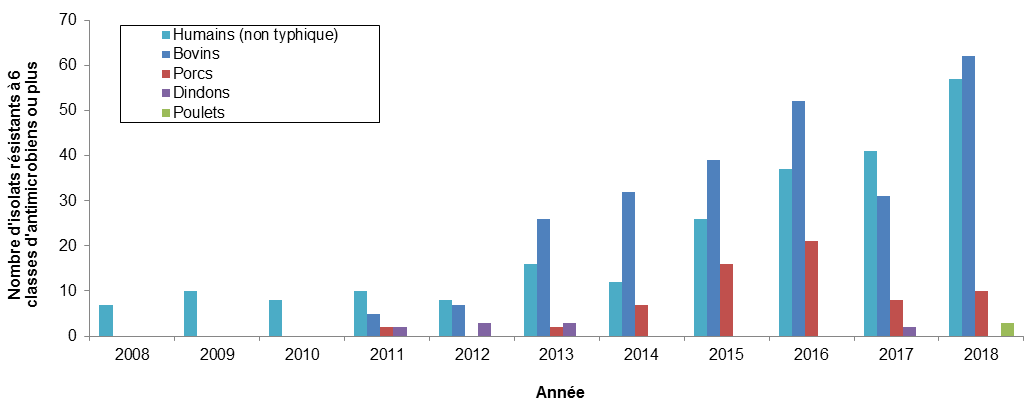
Figure 14 - Équivalent textuel
| Année | Bovins | Porcs | Poulets | Dindons | Humains (non typhique) |
|---|---|---|---|---|---|
| 2008 | 0 | 0 | 0 | 0 | 7 |
| 2009 | 0 | 0 | 0 | 0 | 10 |
| 2010 | 0 | 0 | 0 | 0 | 8 |
| 2011 | 5 | 2 | 0 | 2 | 10 |
| 2012 | 7 | 0 | 0 | 3 | 8 |
| 2013 | 26 | 2 | 0 | 3 | 16 |
| 2014 | 32 | 7 | 0 | 0 | 12 |
| 2015 | 39 | 16 | 0 | 0 | 26 |
| 2016 | 52 | 21 | 0 | 0 | 37 |
| 2017 | 31 | 8 | 0 | 1 | 41 |
| 2018 | 62 | 10 | 3 | 0 | 57 |
Données intégrées relatives à l'utilisation d'antimicrobiens et à la résistance aux antimicrobiens
Dans cette section, nous mettrons l'accent sur deux histoires portant sur les données intégrées relatives à l'utilisation d'antimicrobiens et à la résistance aux antimicrobiens en 2018 :
- Des Campylobacter résistants aux fluoroquinolones
- Résistance à la ceftriaxone chez des Salmonella non typhiques et des E. coli génériques
Des Campylobacter résistants aux fluoroquinolones
- En 2018, on a signalé l'utilisation d'une fluoroquinolone pour traiter un troupeau malade en Colombie-Britannique. On n'avait pas signalé l'utilisation de fluoroquinolones dans les fermes sentinelles de poulets de chair depuis 2014.
- En général, la proportion la plus élevée de Campylobacter résistants à la ciprofloxacine se situe encore en Colombie-Britannique. La résistance de Campylobacter chez les poulets continuait toutefois de varier au fil du temps et d'une région à l'autre.
- En Colombie-Britannique, le nombre d'isolats de Campylobacter résistants à la ciprofloxacine, qui provenaient d'élevages de poulets, a diminué pour atteindre 17 % (8 des 46 isolats étaient résistants).
- Au Québec, le nombre d'isolats de Campylobacter résistants à la ciprofloxacine, qui provenaient des élevages de poulets, a augmenté pour atteindre 50 % (8 des 16 isolats étaient résistants).
Figure 15. Résistance à la ciprofloxacine dans les isolats de Campylobacter provenant de poulet au fil du temps et selon la région; PICRA, de 2011 à 2018
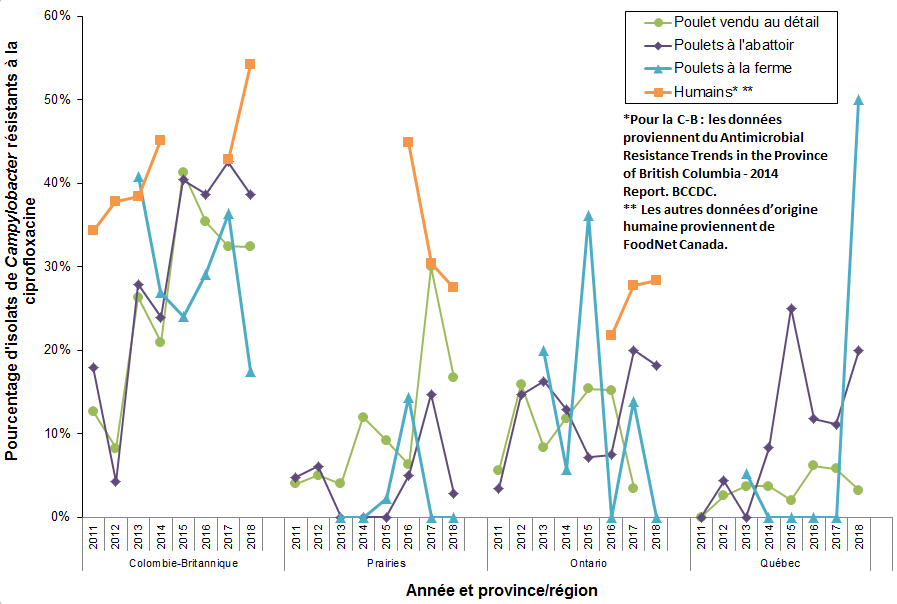
Figure 15 - Text Description
Les variations temporelles du pourcentage d'isolats de Campylobacter résistants à la ciprofloxacine sont représentées dans cette figure par année (2011 à 2018) et par province (Colombie-Britannique, Ontario et Québec) ou région (Prairies). Pour chaque province ou région, les variations temporelles sont représentées par 4 séries qui correspondent aux 4 sources de données de Campylobacter répertoriées ici :
- poulet provenant de la vente au détail (ligne verte et marqueur rond)
- poulet provenant de l'abattoir (ligne violette et marqueur losange)
- poulet provenant de la ferme (ligne bleue et marqueur triangle)
- d'origine humaine * / ** (ligne orange et marqueur carré).
* Pour la Colombie-Britannique: les données proviennent du « Antimicrobial Resistance Trends in the province of British Columbia - 2014 Report » du British Columbia Centre for Disease Control (BCCDC).
** Les autres données d'origine humaine proviennent de FoodNet Canada.
Résistance à la ceftriaxone chez des Salmonella non typhiques et des E. coli génériques
Depuis 2015, on n'a révélé aucune utilisation de ceftiofur dans les troupeaux de poulets de chair des fermes sentinelles et dans la plupart des cas, on a constaté une diminution de la résistance à la ceftriaxone chez les bactéries E. coli et Salmonella provenant de poulets et de viande de poulet.
Auparavant, les isolats de Salmonella résistants à la ceftriaxone d'origine humaine étaient surtout des isolats associés au sérotype Heidelberg. Cependant, en 2018, la plupart des isolats résistants étaient des isolats associés au sérotype Infantis ainsi qu'au sérotype Heidelberg.
En 2018, la résistance à la ceftriaxone de S. Infantis a diminué depuis 2017 en passant de 17% à 15%. De même, la résistance à la ceftriaxone de S. Heidelberg a diminué depuis 2017 en passant de 12% à 7%.
Dans l'ensemble, la résistance à la ceftriaxone observée parmi les isolats de Salmonella et d'E. coli provenant de différentes sources de poulet est demeurée relativement stable ou a diminué suite à l'intervention de 2014 qui consistant à éliminer le recours aux antimicrobiens de catégorie I pour la prévention des maladies. La majorité des isolats de Salmonella étaient des isolats de S. Kentucky, suivis de S. Heidelberg et de S. Infantis.
De 2017 à 2018, on a toutefois constaté des augmentations de la résistance à la ceftriaxone. Ce fait a été principalement observé parmi des isolats Salmonella provenant de poulets d'élevage.
Figure 16. Diminution du signalement de l'utilisation du ceftiofur dans les fermes sentinelles et changement de la résistance à la ceftriaxone parmi les Salmonella non typhiques provenant d'humains et de poulets entre 2013 et 2018
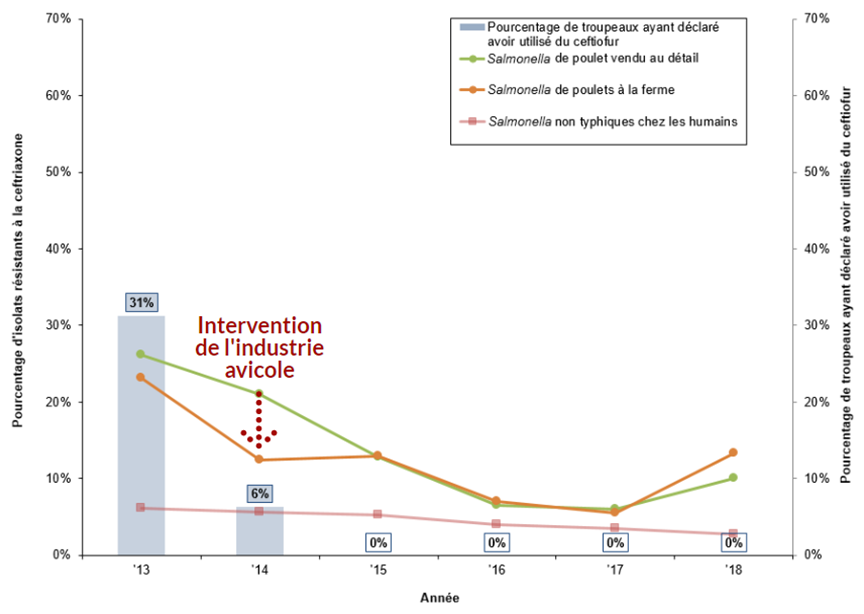
Figure 16 - Équivalent textuel
| Année | 2013 | 2014 | 2015 | 2016 | 2017 | 2018 |
|---|---|---|---|---|---|---|
| Composante | ||||||
| Pourcentage d'isolats résistants à la ceftriaxone | ||||||
| Salmonella de poulets à la ferme | 23% | 12% | 13% | 7% | 6% | 13% |
| Salmonella de poulet vendu au détail | 26% | 21% | 13% | 7% | 6% | 10% |
| Salmonella non typhiques chez les humains | 6% | 6% | 5% | 4% | 4% | 3% |
| Pourcentage de troupeaux ayant déclaré avoir utilisé du ceftiofur | ||||||
| Troupeaux de poulets de chair à la ferme | 31% | 6% | 0% | 0% | 0% | 0% |
La réduction dans l'utilisation de ceftiofur et la baisse connexe de la résistance à la ceftriaxone chez les poulets et les humains comparativement aux données d'avant 2014 est un bon exemple d'une intervention fructueuse visant à limiter la résistance aux antimicrobiens.
Quoi de neuf pour le PICRA en 2018
Nous modernisons la manière dont nous diffusons de l'information à différents publics et nous adoptons de nouveaux outils et formats de communication. Entre-temps, le PICRA continuera de fournir les mêmes renseignements, mais d'une manière différente.
Pour les données de 2018, nous publierons 4 documents :
- Sommaire
- Figures et tableaux (information résumée mais peu de texte qui l'accompagne)
- Design et méthodes
- Résultats intégrés
Utilisation des antimicrobiens
- Les données recueillies, en vertu de la loi, par Santé Canada auprès des distributeurs de produits pharmaceutiques pour usage vétérinaire, des importateurs et des fabricants pour l'année de 2018 sont en cours d'analyse. Les résultats seront publiés dans un rapport distinct au printemps de 2020.
- En 2018, les mesures quantitatives sur l'utilisation des antimicrobiens dans l'eau et par injection seront présentées pour la première fois pour les porcs en croissance-finition.
- La mesure nDDDvet/PCU, pour quantifier l'utilisation des antimicrobiens, ne sera plus présentée à partir de 2018.
Résistance aux antimicrobiens
- En 2018, il n'y aura plus d'échantillonnages effectués chez les poulets de chair lors du placement des poussins.
- Pour la surveillance à la ferme, l'échantillonnage des dindons a été amorcé en Alberta.
- Nous avons effectué dans le cadre de la vente au détail, des échantillonnages en Ontario et dans les Prairies pour une partie de l'année seulement et aucun échantillonnage n'a été effectué dans la région de l'Atlantique; ainsi les données temporelles de la vente au détail ne seront pas présentées pour ces régions en 2018.
En plus des changements décrits ci-dessus, en collaboration avec nos intervenants, nous avons lancé deux projets de surveillance de fermes sentinelles de bovins en parc d'engraissement et de bovins laitiers.
Glossaire
| Classe d'antimicrobiens | Les antimicrobiens sont regroupés dans la même classe s'ils ont une structure chimique commune et s'ils éliminent les bactéries ou freinent leur croissance de la même manière. Le PICRA utilise les données du Clinical and Laboratory Standards Institute pour définir les classes d'antimicrobiens. |
| Biomasse et Population Correction Unit (PCU) | Le PCU tient compte de la taille de la population, y compris le nombre et le poids (biomasse) des animaux ou des personnes qui la composent. Le PICRA ajuste (ou corrige) selon la « taille » des populations en vue d'interpréter les données sur l'utilisation, la consommation ou la vente d'antimicrobiens en utilisant les méthodes déclarées par l'European Surveillance of Veterinary Antimicrobial Consumption (surveillance européenne de la consommation d'antimicrobiens). |
| DDDvet | Sigle signifiant « Defined Daily Dose for animals » (dose quotidienne définie pour les animaux). La quantité d'antimicrobiens administrée pendant un traitement (dose) variera selon l'antimicrobien, la manière dont il est administré (par ex., par injection, dans l'eau ou les aliments) et la population traitée (bovins, volaille, porcs). Le PICRA utilise cette mesure pour tenir compte de cette variation et interpréter les données sur l'utilisation des antimicrobiens. |
| mg/PCU | Mesure de l'utilisation des antimicrobiens qui ajuste la quantité (milligramme/mg) d'antimicrobiens utilisés, consommés ou distribués selon la taille de la population. |
| DDDvet/1000 animaux-jours | Mesure de l'utilisation des antimicrobiens qui tient compte à la fois des variations dans la quantité d'antimicrobiens administrés pendant un traitement (DDDvet) et de la période de temps pendant laquelle un animal ou un groupe d'animaux est traité afin d'aider à interpréter les données sur l'utilisation des antimicrobiens. |
| Porc en croissance finition | Un porc dont le poids est approximativement à 25 kilogrammes du poids de marché. |
| Antimicrobiens médicalement importants | Antimicrobiens considérés comme étant de très haute importance (catégorie I), de haute importance (catégorie II) ou d'importance moyenne (catégorie III) en médecine humaine. |
| Salmonella non typhiques | Tous les sérotypes de Salmonella, à l'exception de S. Typhi et Paratyphi A et B. |
Le PICRA continuera de surveiller et de communiquer l'effet de l'évolution des pratiques de l'utilisation des antimicrobiens sur la résistance aux antimicrobiens afin de préserver leur efficacité chez les animaux et les humains.
Les analystes du PICRA travaillent en vue d'élaborer de nouvelles façons de déceler les problèmes émergents et d'intégrer les données relatives à différentes espèces hôtes, espèces de bactéries et régions.