Mise à jour des recommandations concernant l’utilisation du vaccin contre l’hépatite B
Une déclaration du comité consultatif (DCC) Comité consultatif national de l'immunisation (CCNI)
Préambule
Le Comité consultatif national de l'immunisation (CCNI) donne à l'Agence de la santé publique du Canada (ASPC) des conseils continus et à jour liés à l'immunisation dans le domaine de la médecine, des sciences et de la santé publique. L'ASPC confirme que les conseils et les recommandations figurant dans la présente déclaration reposent sur les connaissances scientifiques les plus récentes et diffuse ce document à des fins d'information. Les personnes qui administrent le vaccin doivent également connaître le contenu de la monographie de produit pertinente. Les recommandations d'utilisation et les autres renseignements qui figurent dans le présent document peuvent différer du contenu de la monographie de produit rédigée par le fabricant du vaccin au Canada. Les fabricants ont fait homologuer les vaccins et ont démontré leur innocuité et leur efficacité lorsqu'ils sont utilisés conformément à la monographie de produit uniquement. Les membres du CCNI et les agents de liaison doivent se conformer à la politique de l'ASPC régissant les conflits d'intérêts, notamment déclarer chaque année les conflits d'intérêts possibles.
Table des matières
- Sommaire de l'information contenue dans la présente déclaration du CCNI
- I. Introduction
- II. Méthodologie
- III. Épidémiologie de l'hépatite B
- IV. Vaccins
- V. Recommandations
- VI. Priorités en matière de surveillance et de recherche
- Tableaux
- Liste des abréviations
- Remerciements
- References
Sommaire de l'information contenue dans la présente déclaration du CCNI
Les faits saillants suivants mettent en relief des informations clés pour les vaccinateurs. Veuillez consulter le reste de la déclaration pour obtenir plus de précisions.
1. Quoi
Le virus de l'hépatite B (VHB) est à l'origine de l'infection du foie. Bien que la plupart des personnes élimineront l'infection spontanément, le risque de devenir un porteur chronique chez les personnes non vaccinées varie en fonction de l'âge auquel l'infection survient : jusqu'à 95 % des nourrissons, 50 % des enfants de moins de cinq ans et 10 % des adolescents et adultes développeront une infection chronique.

Télécharger le format de rechange
(Format PDF, 1912 Ko, 65 pages)
Organisation : Agence de la santé publique du Canada
Publiée : février 2017
Cat. : HP40-174/2017F-PDF
ISBN : 978-0-660-07209-8
Pub. : 160292
Sujets connexes
La mise en œuvre de programmes d'immunisation des nourrissons et des adolescents est un succès dans l’ensemble des provinces et territoires (PT) canadiens depuis 1990. On pense que la protection après un calendrier de primovaccination terminé est de longue durée et aucune dose de rappel systématique n'est indiquée à l'heure actuelle pour les personnes immunocompétentes.
2. Responsables
La présente déclaration aborde la question de savoir s’il est nécessaire de procéder à une revaccination contre l'hépatite B (HB) chez les adolescents ayant reçu une immunisation systématique durant la petite enfance, s'il existe un risque d'infection au virus de l'HB chez les personnes souffrant de diabète et quel est le moment approprié pour revacciner les personnes atteintes d'affections liées à l'immunodépression.
3. Comment
Bien qu'une baisse des niveaux d'anticorps puisse être observée au fil du temps, la prévention ainsi que la protection à long terme contre une infection chronique dépendent de la présence de lymphocytes T et B à mémoire. La réponse anamnestique à une dose d'amorce du vaccin contre l'HB est considérée comme une mesure fiable de la mémoire immunologique préservée et comme un corrélat de protection chez les personnes ayant déjà été vaccinées.
4. Pourquoi
La plupart des cas aigus se déclarent chez les membres du même foyer non vaccinés d'un porteur de l'hépatite B et chez les personnes d'au moins 30 ans qui contractent l'infection à la suite de rapports sexuels non protégés, du partage de matériel d'injection de drogues ou d'interventions donnant lieu à une exposition percutanée.
On considère que les personnes en bonne santé et immunocompétentes qui ont reçu un vaccin contre l'HB selon les calendriers recommandés ont acquis une immunité à l'infection par le VHB. La présence d'une réponse anamnestique chez la plupart des personnes vaccinées durant la petite enfance est révélatrice d'une protection à long terme.
I. Introduction
La présente déclaration viendra s'ajouter aux déclarations précédentes du Comité consultatif national de l'immunisation (CCNI) sur l'hépatite B (HB) en :
- offrant un aperçu de l'épidémiologie actuelle de l'hépatite B au Canada et des sources nationales de surveillance liée à l'hépatite B;
- examinant les preuves relatives à la primovaccination et à l'immunisation de rappel chez les personnes vaccinées durant la petite enfance et chez celles souffrant de diabète et d'affections liées à l'immunodépression;
- examinant des données probantes concernant les indications liées aux immunoglobulines contre l'hépatite B(IgHB);
- formulant des recommandations concernant les calendriers d'immunisation contre l'hépatite B, les tests sérologiques de sujets immunodéprimés et les priorités en matière de surveillance et de recherche.
Le principal objectif de cette déclaration est de fournir des directives supplémentaires sur la nécessité d'une revaccination des adolescents ayant reçu durant la petite enfance une immunisation systématique au moyen d'un vaccin contenant le virus de l'hépatite B.
II. Méthodologie
Le groupe de travail sur l'hépatite du CCNI (GTH) a étudié des éléments tels que l'épidémiologie, les populations cibles, l'innocuité, l'immunogénicité, l'efficacité potentielle, l'efficacité réelle des vaccins, les calendriers de vaccination et d'autres aspects de la stratégie globale d'immunisation. Les recherches, l'examen et la synthèse des données probantes ont été effectués par des conseillers médicaux de l'Agence de la santé publique du Canada (ASPC) sous la supervision du GTH. Après l’évaluation critique des études pertinentes, des tableaux récapitulatifs comprenant des cotes de qualité des données probantes ont été préparés à l’aide de la hiérarchie méthodologique du CCNI (Tableaux 4 et 5).
L'infection au virus de l'HB est une maladie à déclaration obligatoire au Canada depuis 1969. Les cas diagnostiqués cliniquement et en laboratoire sont signalés aux autorités sanitaires provinciales et territoriales qui, à leur tour, fournissent des données agrégées au Système de surveillance des maladies à déclaration obligatoire du Canada (SSMDOC) de l’ASPC. Les données de surveillance nationales obtenues auprès des autorités sanitaires sont notamment l'âge, le sexe, le territoire de compétence et l'année des cas signalés.
Il a été possible d’obtenir des données probantes sur l'efficacité et l'immunogénicité à long terme du vaccin, y compris la mémoire immunitaire et la réponse anamnestique après l'administration d'une dose de rappel du vaccin contre l'hépatite B grâce à l'examen documentaire d'études publiées et non publiées.
La vaste recherche documentaire des principales études publiées en anglais et en français au moyen des mots clés « hépatite B » ET « vaccin OU vaccination OU immunisation » a été menée à l'aide de Medline, d'Embase et de la bibliothèque Cochrane sur les essais cliniques. Les études d'immunogénicité étaient incluses si les résultats contenaient des données sur les enfants et les adolescents s'étant fait vacciner contre l'hépatite B avant l'âge d'un an et ayant reçu une dose de rappel du vaccin au moins dix ans après avoir terminé une série de primovaccination. Le GTH n'a pas tenu compte des études qui déclaraient les résultats de cohortes dans lesquelles des personnes avaient reçu une immunisation de rappel à des intervalles plus courts, en raison de biais de sélection possibles.
La recherche initiale a été menée en avril 2015 et une mise à jour de la recherche a été effectuée en avril 2016. Deux examinateurs indépendants ont aussi effectué une recherche manuelle dans les listes de référence des articles déterminés au moyen de la recherche documentaire. Au total, 41 articles pertinents ont été examinés et soumis à une évaluation critique par le GTH et le CCNI (Tableau 1). Le GTH a aussi pris note des résultats d'un examen d'études publiées en juin 2016 de la bibliothèque CochraneNote de bas de page 1 qui s'est penché sur les avantages et les inconvénients liés à une dose de rappel du vaccin contre l'hépatite B administrée plus de cinq ans après avoir rempli le calendrier de primovaccination recommandé. L'examen n'a pas permis de trouver des essais cliniques randomisés qui fourniraient des preuves appuyant ou rejetant la nécessité d'une dose de rappel du vaccin contre l'hépatite B chez les personnes en bonne santé, dont les niveaux d'anticorps sont inférieurs à 10 UI/L.
Le président du GTH a présenté les données et les recommandations proposées au CCNI le 1er août 2016. Après l'examen des données probantes et la tenue de consultations lors de la réunion du CCNI le 5 octobre 2016, les membres de ce dernier ont voté des recommandations précises. On trouvera dans le texte de la présente mise à jour une description des considérations pertinentes, des justifications des décisions et des lacunes dans les connaissances.
III. Épidémiologie de l'hépatite B
Le virus de l'hépatite B (VHB) provoque une infection aiguë et chronique du foie. Les symptômes typiques d'une infection aiguë sont notamment des nausées, des douleurs abdominales, de la fièvre et des signes de trouble hépatique comme la jaunisse, une urine foncée, une modification de la couleur des selles et l'hépatomégalie. Une infection aiguë par le VHB peut être asymptomatique chez jusqu'à 50 % des adultes et 90 % des enfants, et une hépatite fulminante peut se produire dans 1 à 2 % des cas.
Bien que la plupart des personnes aient éliminé l'infection spontanément après quatre à huit semaines, le risque de devenir un porteur chronique (pouvant entraîner une cirrhose et un carcinome hépatocellulaire) est inversement proportionnel à l'âge auquel survient l'infection. Les nourrissons ont de 90 à 95 % de risques, les enfants de plus d'un an et de moins de cinq ans ont de 25 à 50 % de risques et les adolescents et les adultes ont de 3 à 10 % de risques d'être atteints d'une infection chronique. Les adultes souffrant de diabète pourraient courir un risque plus important de progression d'une infection chronique et de maladie plus graveNote de bas de page 2 Note de bas de page 3 Note de bas de page 4 Note de bas de page 5
Après l'immunisation, la durée de séroprotection (communément considérée comme étant des anticorps anti-HBs [anticorps contre l'antigène de surface de l'HB] ≥ 10 UI/L) et la présence d'une réponse anamnestique ont été associées à l'état sérologique de la mèreNote de bas de page 6, à l'âge auquel une primovaccination est amorcée et à la puissance des doses utilisées dans le calendrier de vaccination primaireNote de bas de page 7 Note de bas de page 8 Note de bas de page 9 Bien que l'on pense que le niveau d'anticorps dirigés contre l'antigène de surface de l'hépatite B (anticorps anti-HBs) soit important pour prévenir une infection aiguë, la présence d'une mémoire immunologique est nécessaire pour une protection à long termeNote de bas de page 10 Note de bas de page 11 Note de bas de page 12 Note de bas de page 13 Note de bas de page 14 Note de bas de page 15.
En raison de la longue période d'incubation de 60 à 90 jours (en moyenne), même en l'absence de niveaux d'anticorps protecteurs, on pense que la stimulation de cellules mémoire par la vaccination après une exposition au VHB donne lieu à une réponse anticorps qui est adéquate pour la prévention d'une infection aiguë. Les preuves laissent également entendre que chez les personnes ayant déjà été vaccinées et présentant des lymphocytes T et B à mémoire, l'infection post-vaccination (c.-à-d. détection d'anticorps dirigés contre l'antigène capsidique de l'hépatite B [anticorps anti-HBc], l'antigène de surface de l'hépatite B [antigène HBs] ou l'ADN du VHB) n'entraîne pas le développement d'une maladie chroniqueNote de bas de page 16 Note de bas de page 17 Note de bas de page 18
Au cours de la décennie précédant l'introduction de programmes d'immunisation systématiques des adolescents et des nourrissons dans les années 1990, l'ensemble des PT a connu une augmentation graduelle des taux d'infection aiguë par le VHB, un pic de 13 cas pour 100 000 habitants ayant été signalé en 1989Note de bas de page 19 Note de bas de page 20 Note de bas de page 21 Depuis, les données du SSMDOC ont révélé une tendance à la baisse continue de l'incidence de l'hépatite B dans l'ensemble du Canada. Une analyse publiée récemmentNote de bas de page 22 a confirmé cette tendance, en faisant observer une diminution des taux de cas déclarés d'hépatite B aiguë, qui sont passés de 1 cas pour 100 000 habitants en 2005 à 0,5 cas pour 100 000 habitants en 2013. Les taux d'hépatite B chronique sont passés de 13,6 cas pour 100 000 à 12 cas pour 100 000 habitants entre 2009 et 2013.
Depuis 2005, les taux de cas déclarés d'infection aiguë par le VHB sont demeurés inférieurs à 1 cas pour 100 000 habitants chez les personnes de moins de 20 ans qui auraient été admissibles à une immunisation systématique contre l'hépatite B durant la petite enfance ou l'adolescence. Une diminution importante des taux d'hépatite B aiguë déclarée a également été constatée chez les personnes de 30 à 39 ans et dont l'admissibilité au vaccin aurait augmenté durant cette périodeNote de bas de page 23. On observe que les taux d'infection aiguë et chronique par le VHB sont plus élevés chez les hommes que chez les femmes. Cependant, l'absence de données explicatives (p. ex. renseignements sur les facteurs de risque ou l'état vaccinal), la variation dans les pratiques de déclaration entre les PT, le retard de déclaration et le faible nombre global de cas d'hépatite B aiguë ont limité la disponibilité d'analyses plus détaillées effectuées à l'aide du SSMDOC.
Les données permettant l'estimation de la prévalence de l'infection par le VHB à l'échelle nationale, d'après les échantillons de sang, sont aussi recueillies par l'intermédiaire de l'Enquête canadienne sur les mesures de la santé (ECMS).Note de bas de page 24 Les données recueillies entre 2007 et 2011 pour la population de 14 à 79 ans indiquent une prévalence de l'infection actuelle par le VHB de 0,4 % (IC à 95 % : 0,2 à 0,8), le taux d'infection déclaré étant le plus élevé chez les populations qui ne sont pas de race blanche (1,8 %, IC à 95 % : 0,9 à 3,4) et qui sont nées à l'étranger (1,6 %, IC à 95 % : 0,9 à 2,9).Note de bas de page 25
Depuis 1994, l’ASPC surveille systématiquement la couverture vaccinale au moyen de l'Enquête nationale sur la vaccination (ENV). Dans les PT offrant des programmes d'immunisation infantile universelle, l'ENV de 2013 a estimé que la couverture vaccinale contre l'hépatite B par l'administration d'au moins trois doses chez les enfants de 7 ans était de 74,5 % (IC à 95 % : 70,8; 77,9) et que celle par l'administration d'au moins une dose chez les adolescents de 17 ans représentait 87,9 % (IC à 95 % : 86,6; 89,1).Note de bas de page 26
Des renseignements détaillés sur les programmes d'immunisation systématique et les calendriers de vaccination PT sont disponibles sur le site Web du gouvernement du Canada et dans le Guide canadien d'immunisation (GCI).Note de bas de page 4
Infection par le virus de l'hépatite B chez les adultes atteints de diabète
La proportion d'adultes ayant reçu un diagnostic de diabète augmente avec l'âge, la plus forte augmentation de la prévalence survenant après 45 ans. En 2014, 6,7 % des Canadiens d'au moins 12 ans (environ deux millions de personnes) ont signalé qu'ils souffraient de diabèteNote de bas de page 27 En moyenne, entre 2012 et 2014, on comptait environ 65 000 personnes de 20 à 34 ans, 130 000 personnes de 35 à 44 ans, 845 000 personnes de 35 à 64 ans et 915 000 personnes d'au moins 65 ans souffrant de diabète au CanadaNote de bas de page 28 En raison de la mise en œuvre de programmes d'immunisation universelle des nourrissons et des adolescents, la plupart des personnes de moins de 30 ans et nées au Canada sont susceptibles d'avoir été vaccinées contre l'hépatite B.
Figure 1 : Prévalence du diabète chez les adultes, selon le groupe d'âge, 2012-2014 (population ayant déclaré qu'elles avaient reçu un diagnostic de diabète de type 1 ou 2 par un professionnel de la santé, Enquête sur la santé dans les collectivités canadiennes [ESCC])
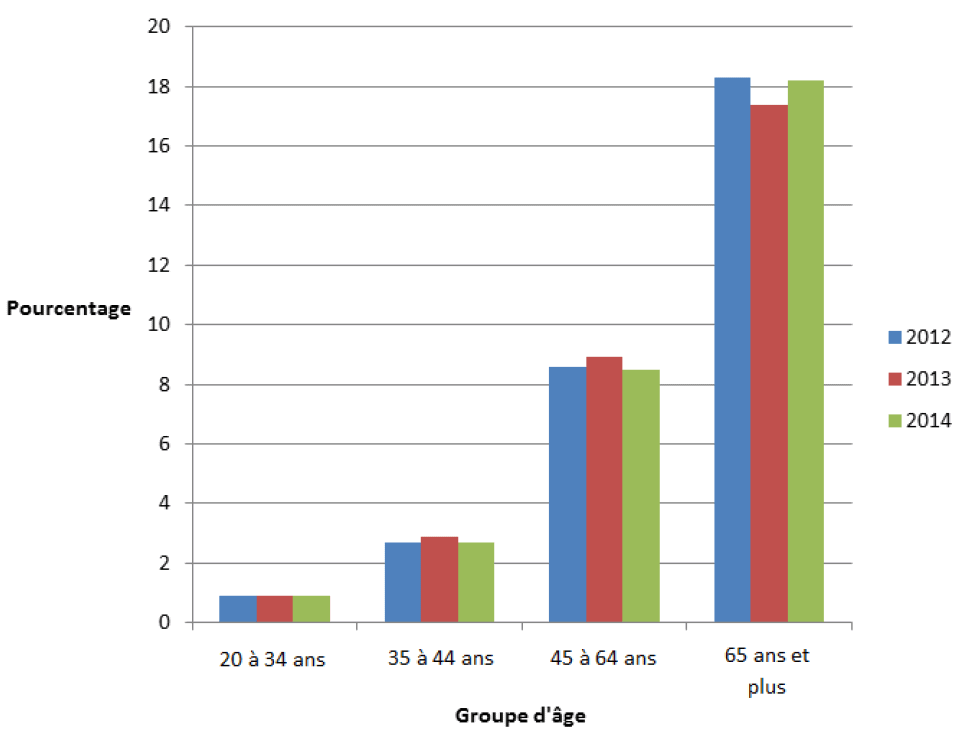
Équivalent textuel - Figure 1
Il s’agit d’un graphique à colonnes illustrant la concentration de cas.
L’axe horizontal compte quatre catégories au total. L’axe vertical est gradué par paliers de deux unités allant de 0 à 20.
Le graphique compte trois séries.
L’axe vertical est nommé « Pourcentage ».
L’axe horizontal est nommé « Groupes d’âge (ans) ».
Le titre de la série 1 est « 2012 ».
La valeur minimale est de 0,9E et correspond au groupe « 20-34 ».
La valeur maximale est de 18,3 et correspond au groupe « 65 et plus ».
Le titre de la série 2 est « 2013 ».
La valeur minimale est de 0,9 et correspond au groupe « 20-34 ».
La valeur maximale est de 17,4 et correspond au groupe « 65 et plus ».
Le titre de la série 3 est « 2014 ».
La valeur minimale est de 0,9 et correspond au groupe « 20-34 ».
La valeur maximale est de 18,2 et correspond au groupe « 65 et plus ».
En 2011, l'Advisory Committee on Immunization Practices (ACIP) des Centers for Disease Control and Prevention (CDC) des États-Unis a publié des données sur le risque d'infection par le virus de l'hépatite B chez les adultes souffrant de diabèteNote de bas de page 29 Ce risque d'infection à l'échelle de la population chez ces personnes a été estimé à partir de 865 cas confirmés d'infection aiguë par le VHB signalés durant la période 2009-2010 à partir de huit sites de l'Emerging Infections Program (EIP) représentant environ 17 % de la population aux États-Unis.
D'après des analyses multivariées, les adultes de 23 à 59 ans et atteints de diabète sont 2,1 fois (IC à 95 % : 1,6 à 2,8) plus à risque de développer une HB aiguë comparativement aux adultes du même âge qui ne souffrent pas de diabète. Les probabilités étaient 1,5 fois (IC à 95% : 0,9 à 2,5) plus élevées pour les personnes d'au moins 60 ansNote de bas de page 30 Une autre analyse des données du National Health and Nutrition Examination Survey (NHANES), effectuée par l'ACIP pour la période allant de 1999 à 2010, a indiqué une séroprévalence des anticorps contre l'antigène capsidique de l'hépatite B (anticorps anti-HBc) 60 % (p < 0,001) plus élevée chez les adultes ayant reçu un diagnostic de diabète par rapport à ceux ne souffrant pas de diabète.
Aux États-Unis, la couverture déclarée d'adultes d'au moins 19 ans ayant reçu au moins trois doses de vaccin contre l'hépatite B représentait 24,5 % (32,2 % chez les adultes de 19 à 49 ans et 15,7 % chez les adultes d'au moins 50 ans)Note de bas de page 31
Des données épidémiologiques similaires qui permettraient l'estimation du fardeau de l'hépatite B et du risque d'infection chez les personnes atteintes de diabète ne sont pas disponibles à l'heure actuelle au Canada.
IV. Vaccins
Des renseignements supplémentaires sur les types de vaccins à composant anti-hépatite B autorisés au Canada et leur contenu sont fournis dans le GCINote de bas de page 4
IV.1 Efficacité potentielle et efficacité réelle
Pré-exposition
L'évaluation des données probantes sur l'efficacité potentielle et l'efficacité réelle des vaccins contre l'hépatite B, effectuée par le GTH, chez les personnes immunocompétentes, et plus particulièrement les personnes immunisées durant la petite enfance et les travailleurs de la santé, reposait sur un triple fondement : les résultats d'une conférence conjointe du Viral Hepatitis Prevention Board (VHPB) et de l'OMSNote de bas de page 32 Note de bas de page 33, l’examen à jour des données probantes concernant la protection à long terme de la vaccination contre le VHB du Groupe stratégique consultatif d'experts (SAGE) de l’OMSNote de bas de page 32 Note de bas de page 33 Note de bas de page 34 et les résultats d'une méta-analyse menée par Poorolajal et al. Une recherche documentaire supplémentaire sur des études publiées depuis novembre 2011 et une demande de données supplémentaires auprès des fabricants de vaccins contre l'hépatite B n'ont pas permis de recenser des données probantes qui laisseraient supposer une efficacité à long terme réduite des vaccins après une immunisation durant la petite enfance ou parmi les travailleurs de la santé.
Deux examens complets d’études, l’un réalisé en novembre 2011 et l’autre en octobre 2015, renfermant jusqu'à 30 années de données de suivi, ont été présentés à l'OMS. Leurs données sur les échecs d'immunisation ont démontré que ces événements étaient rares et n'entraînaient pas de nouveaux cas cliniques parmi la population vaccinée. Ces examens n'ont donc pas permis de démontrer la nécessité d'une dose de rappel du vaccin contre l'hépatite B dans les programmes d'immunisation systématique.
Une méta-analyse des effets protecteurs à long terme de l'immunisation contre l'hépatite B chez plus de 9 300 personnes qui a été publiée en 2010 a signalé des résultats similaires. Menée par Poorolajal et al.Note de bas de page 35, l'étude a permis de constater que l'incidence cumulative globale de l'infection post-vaccination (en utilisant l'anticorps anti-HBc comme marqueur d'infection) jusqu'à 20 ans après avoir reçu trois doses de vaccin était de 0,007 (IC à 95 % : 0,005 à 0,010).
Les différences entre les études incluses dans la méta-analyse variaient de 0 à 0,094 (incidence cumulative de 0,006 [IC à 95 % : 0,002 à 0,010] après 11 à 15 ans et de 0,010 [IC à 95 % : 0 à 0,019] après 16 à 20 ans). On a déterminé que l'incidence cumulative d'infection était de 0,009 (IC à 95 % : 0 à 0,019) chez les participants recevant le vaccin recombinant et de 0,020 (IC à 95 % : 0,010 à 0,030) chez les participants recevant le vaccin dérivé du plasma (p = 0,003).
Dans les études portant sur une période de 20 ans, seules huit séroconversions transitoires de l'antigène HBs ont été enregistrées et aucune personne n'est devenue un porteur chronique. L'incidence cumulative d'infection était de 0,001 (IC à 95 % : 0,000 à 0,005) dans les régions à faible endémicité; de 0,061 (IC à 95 % : 0,000 à 0,177) dans les régions d'endémicité intermédiaire et de 0,017 (IC à 95 % : 0,008 à 0,025) dans les régions à endémicité élevée (p < 0,001).
Post-exposition
On estime que l'immunisation par immunoglobulines contre le virus de l'hépatite B (IgHB) et par le vaccin HB dans les 24 heures suivant la naissance permet de prévenir l'infection par le virus de l'hépatite B chez 85 à 95 % des nouveau-nés exposésNote de bas de page 2 Note de bas de page 4 Note de bas de page 36 Note de bas de page 37 On a démontré que l'administration de la prophylaxie avec le vaccin anti-HB dans la semaine suivant une exposition par voie percutanée ou muqueuse à du sang contaminé par le VHB et dans les deux semaines suivant une exposition par contact sexuel avec des personnes positives pour le VHB était hautement efficace dans la prévention de l'infection par le VHBNote de bas de page 4 Une recherche documentaire, un examen des recommandations d'autres administrations publiques et une demande de données inédites auprès de fabricants de vaccins n'ont pas permis de fournir de nouvelles preuves concernant l'efficacité de la prophylaxie post-exposition (PPE) avec le vaccin HB et les immunoglobulines contre l'hépatite B (IgHB).
IV.2 Immunogénicité
Au total, le GTH a examiné 39 publications dont les données déclarées portaient sur la réponse immunitaire après l'administration d'une dose de rappel du vaccin contre l'hépatite B chez les personnes qui avaient été immunisées durant la petite enfance. Dans la plupart de ces études, avant le vaccin de rappel, la séroprotection (définie par un titre d'anticorps anti-HBs ≥10 UI/L) était présente chez environ 60 à 85 % des personnes et chez 30 à 40 % des personnes 10 ans et 15 ans après, respectivement, la primovaccination durant la petite enfance.
Après un vaccin de rappel, la réponse anamnestique était présente chez 95 à 100 % des personnes et chez 65 à 100 % des personnes 10 ans et 15 ans après, respectivement, l'achèvement d'une série de primovaccination contre l'hépatite B. D'après la présence d'anticorps anti-HBs ≥ 10 UI/L, on peut donc s'attendre à ce que la protection contre l'infection par le VHB varie de 95 à 100 % et de 85 à 100 % 10 ans et 15 ans, respectivement, après l'immunisation contre l'hépatite B durant la petite enfance. Chez les adultes ayant reçu une primovaccination durant la petite enfance, on a constaté des niveaux d'anticorps séroprotecteurs chez environ un tiers des personnes avant l'immunisation de rappel et chez 75 à 90 % des personnes après l'immunisation de rappel. Dans toutes les études, chez pratiquement toutes les personnes qui n'avaient pas atteint des titres séroprotecteurs après une dose de rappel, aucun niveau d'anticorps n'a pu être détecté au début de l'étude.
Il convient de noter que, bien que certaines des études examinées faisaient état d'un seuil de séroprotection à 12 UI/L, les membres du CCNI ont généralement considéré que ces niveaux étaient dus à des différences dans les essais biologiques utilisés en laboratoire et qu'ils n'étaient pas pertinents pour les conclusions générales ayant trait à l'immunogénicité du vaccin.
Une analyse des données provenant de 21 étudesNote de bas de page 38 Note de bas de page 39 Note de bas de page 40 Note de bas de page 41 Note de bas de page 42 Note de bas de page 43 Note de bas de page 44 Note de bas de page 45 Note de bas de page 46 Note de bas de page 47 Note de bas de page 48 Note de bas de page 49 Note de bas de page 50 Note de bas de page 51 Note de bas de page 52 Note de bas de page 53 Note de bas de page 54 Note de bas de page 55 Note de bas de page 56 Note de bas de page 57 Note de bas de page 58 dans le cadre desquelles la réponse anamnestique a été mesurée de 10 à 23 ans après une primovaccination durant la petite enfance, menée par Hu et al. (non publiée)Note de bas de page 59 pour le ministère de la Santé de la Colombie-Britannique a été présentée au GTH. Les auteurs des études ont constaté que, dans la plupart des études examinées, une réponse anamnestique (définie par un titre d'anticorps anti-HBs ≥10 UI/L une à quatre semaines après le vaccin de rappel) était présente chez plus de 95 % des personnes et chez environ 75 % des personnes 10 ans et 20 ans, respectivement, après la primovaccination. Des tendances à la baisse similaires concernant les niveaux d'anticorps après l'immunisation de rappel ont aussi été signalées dans une méta-analyse menée par Shonberger et al. de 29 études(Note de bas de page 12, Note de bas de page 39, Note de bas de page 40, Note de bas de page 42 Note de bas de page 43 Note de bas de page 44, Note de bas de page 48, Note de bas de page 49, Note de bas de page 53 Note de bas de page 54 Note de bas de page 55, Note de bas de page 57, Note de bas de page 58, Note de bas de page 60 Note de bas de page 61 Note de bas de page 62 Note de bas de page 63 Note de bas de page 64 Note de bas de page 65 Note de bas de page 66 Note de bas de page 67 Note de bas de page 68 Note de bas de page 69 Note de bas de page 70 Note de bas de page 71 Note de bas de page 72 Note de bas de page 73 Note de bas de page 74 Note de bas de page 75) auxquelles ont participé plus de 2 600 personnesNote de bas de page 8.
D'après les données analysées, les auteurs des études ont développé un modèle pronostique d'estimation de la protection contre l'infection par le VHB jusqu'à 17 ans après l'immunisation contre l'hépatite durant la petite enfance. Selon le modèle, lorsque trois doses d'au moins 5 μg d'antigène HBs étaient administrées (dernière dose et dose précédente administrées à au moins six mois d'intervalle), un niveau d'anticorps anti-HBs ≥ 10 UI/L était observé chez 92 % (IC à 95 % : 82 à 100) des personnes 15 ans après la primovaccination. La proportion de personnes susceptibles d'être protégées diminuerait légèrement (90 %, IC à 95 % : 78 à 100) dans le cas d'un intervalle plus court (moins de six mois) entre la dernière dose et la dose précédente et serait considérablement réduite (61 %, IC à 95 % : 33 à 88) chez les personnes ayant reçu des doses contenant moins de 5 μg d'antigène HBs.
L'étude n'a pas révélé d'association entre l'âge à la première dose et les niveaux d'anticorps après l'immunisation de rappel. Outre ces résultats, le GTH a aussi examiné les résultats d'études publiées par la suite (depuis septembre 2011) qui rendaient compte de la réponse immunitaire après la dose de rappel suivant l'immunisation durant la petite enfance, ainsi que les données inédites provenant d'un essai canadien pertinent.
Les résultats non publiésNote de bas de page 76 d'un essai mené en Colombie-Britannique qui vérifiait la persistance de la réponse immunitaire chez les adolescents de 10 à 16 ans après une immunisation durant la petite enfance, selon un calendrier à 2, 4 et 6 mois, ont également été communiqués au GTH. Chez 215 adolescents de 15 à 16 ans ayant reçu une série de doses de 5 μg du vaccin Recombivax contre l'hépatite B, on a établi que 64 % (138/215) étaient séronégatifs (titre d'anticorps anti-HBs < 12 UI/L) et on leur a administré une dose d'amorce du vaccin pour évaluer la mémoire immunitaire. Dans ce groupe d'âge, 1,4 % (3/215) des personnes étaient des non-répondants primaires et 4,2 % (9/215) nécessitaient deux doses de vaccin supplémentaires pour atteindre une séroprotection.
Dans le groupe de 10 à 11 ans qui a reçu une série de doses de 2,5 μg du vaccin Recombivax contre l'hépatite B durant la petite enfance, 78,6 % (107/136) des personnes étaient séronégatives et ont reçu une dose d'amorce du vaccin. Dans ce groupe, 97,1 % (133/136) ont répondu à une dose d'amorce. Par contre, les autres, soit 2,9 % (3/136), ont atteint des titres séroprotecteurs après avoir reçu deux doses de vaccin supplémentaires. Aucun non-répondant primaire n'a été observé dans cette cohorte. Les chercheurs ont conclu que le vaccin contre l'hépatite B offre une protection adéquate tout au long de la petite enfance, mais il est moins certain que cette protection persiste à l'âge adulte, par rapport à une immunisation à l'adolescence.
Une étude menée par Middleman A. et al.Note de bas de page 77 a révélé une réponse anticorps après le vaccin de rappel chez 420 personnes de 16 à 19 ans qui avaient déjà reçu trois doses (2,5 μg/dose) de vaccin recombiné à 12 mois. Malgré une faible prévalence (24 %) de la séroprotection, 92 % des personnes ont présenté des niveaux d'anticorps protecteurs indépendants de la dose d'amorce utilisée (dose de 10 ou 20 μg). Même si la séroprotection était similaire entre les personnes dont la primovaccination avait été amorcée dans les sept jours suivant leur naissance et celles immunisées au moins quatre semaines après leur naissance, un âge plus avancé au moment de la première dose était associé à des niveaux du titre moyen géométrique des anticorps (TMG) beaucoup plus élevés (487,84 [IC : 319,65; 744,54] p/r à 1 745,77 [IC : 1 065,45; 2860,49]).
Dans une autre étude, Bagheri-Jamebozorgi et al.Note de bas de page 78 ont mesuré la réponse immunitaire chez 300 personnes, 20 ans après avoir reçu trois doses du vaccin Engerix®-B (10 μg) administré à la naissance, à 1,5 et à 9 mois. Parmi les 189 (63 %) personnes qui n'avaient pas atteint un niveau d'anticorps protecteurs (anticorps anti-HBs < 10 UI/L) au début de l'étude, 138 ont reçu une dose de rappel qui a donné lieu à un taux de réponse de 97 % (134/138).
La réponse anamnestique parmi les adolescents de 12 à 13 ans qui avaient déjà reçu trois doses (0, 1, 6 mois) du vaccin Engerix®-B (10 μg) avant leurs 18 mois a également été évaluée par Behre et alNote de bas de page 79. Les auteurs de l'étude ont constaté que des titres séroprotecteurs étaient présents chez 78,3 % (IC à 95 % : 73,1; 83) des participants de l'étude, la proportion des personnes présentant des titres séroprotecteurs augmentant jusqu'à 98,9 % (IC à 95 % : 96,9; 99,8) après l'administration d'une dose de rappel. Dans la même population, Van Der Meeren et al.Note de bas de page 80 ont signalé qu'un titre d'anti-HBs établi à au moins 10 UI/L était présent chez 65 % des personnes, 15 à 16 ans après la primovaccination. Après réception d’une dose de rappel de 10 μg, des titres d'anticorps protecteurs ont été observés chez tous les sujets sauf 6 % d’entre eux.
Hudu et al.Note de bas de page 81 ont évalué l'immunité contre l'hépatite B chez 402 étudiants de premier cycle 23 ans après que ces derniers ont reçu une à trois doses du vaccin contre l'HB à la naissance, à un et à cinq mois. L'étude a révélé la présence de titres séroprotecteurs chez 252 personnes, dont 68 % ont reçu trois doses, 19 % ont reçu deux doses et 13 % ont reçu une dose du vaccin.
Bien que la plupart des personnes séronégatives (85/150) aient reçu uniquement une dose de vaccin durant la petite enfance, après l'administration d'une dose de rappel, 94 % (141/150) ont atteint un niveau d'anticorps protecteurs d'au moins 10 UI/L. De même, Chan et al.Note de bas de page 82 ont évalué la réponse immunitaire à une immunisation de rappel dans une cohorte de 212 étudiants, dont 80 % étaient dépourvus d'une séroprotection 19 ans après la primovaccination consistant en trois doses (0, 1, 6) du vaccin dérivé du plasma. Parmi les 69 étudiants ayant reçu l'immunisation de rappel, 10 (14,5 %) sont demeurés séronégatifs un mois après la première dose de rappel. Après avoir reçu trois doses de rappel, tous les étudiants ont atteint des titres séroprotecteurs.
Chen et al.Note de bas de page 83 ont mesuré la réponse immunitaire chez 1 142 personnes après l'administration de deux doses de rappel différentes à 10 et à 15 ans, respectivement après la primovaccination (0, 1, 6). Bien que chez environ 50 % des personnes des deux groupes, leurs titres d'anticorps n'aient pas été détectables (anticorps anti-HBs < 1 UI/L), après l'administration de la première dose de rappel, une séroprotection a été observée chez 86,7 % (449/518) du groupe recevant une dose de vaccin de 5 μg et chez 91,2 % (569/624) du groupe recevant une dose de vaccin de 10 μg.
Dans les deux groupes, après l'administration de trois doses de rappel, plus de 99 % des personnes ont atteint des titres séroprotecteurs. Une étude européenne de plus petite envergure menée par Teoharov et al. a révélé un taux de réponse de 100 % à une dose de rappel du vaccin contre l'HB chez 30 enfants de 10 à 15 ans ayant reçu trois doses du vaccin contre l'HB à l'âge de 6 moisNote de bas de page 84 Dans une autre étude menée par Chen et al.Note de bas de page 83 qui utilisait un vaccin combiné contre l'hépatite A et l'hépatite B (HAHB) pour l'immunisation de rappel, on a signalé des taux de séroréaction similaires à ceux observés chez des enfants ayant reçu une dose de rappel du vaccin contre l'HB. Après la première dose de rappel du vaccin HAHB, 75 % des enfants ont atteint des titres séroprotecteurs et après la troisième dose, des titres séroprotecteurs ont été observés chez 98 % des personnes vaccinées.
Dans une autre étude menée à Taïwan par Chang et al.Note de bas de page 85 92,5 % des adolescents séronégatifs qui avaient été vaccinés durant la petite enfance et à qui l'on avait administré une dose de rappel du vaccin contre l'HB à l'âge de 15 ans ont atteint des titres séroprotecteurs six semaines après leur vaccination. Dans une semblable étude de cohorte représentative de la population menée par Katoonizadeh et al,Note de bas de page 86, une dose de rappel a été administrée à 275 jeunes de 10 à 18 ans qui étaient nés dans une famille composée d'au moins un parent positif pour l'antigène HBs et qui avaient été vaccinés durant la petite enfance à l'aide de trois doses du vaccin contre l'HB. Une réponse immunitaire anamnestique a été observée chez 96 % des enfants de 10 à 11 ans, chez 86 % des enfants de 12 à 14 ans et chez 75 % des enfants de 15 à 18 ans.
Outre ces études, le GTH a également examiné les données sur l'immunité à long terme après l'utilisation d'un vaccin combiné (Infanrix hexa; DCaT-HB-VPI-Hib) administré durant la petite enfance. Un rapport d'évaluation publié par l'Agence européenne des médicamentsNote de bas de page 87 a fourni des données sur l'immunogénicité du vaccin après l'administration d'une seule dose de 10 μg du vaccin contre l'HB à 12 ou 13 ans, chez les personnes ayant reçu trois doses du vaccin DCaT-HB-VPI-Hib à l'âge de 9 mois et une dose de ce vaccin entre 11 et 18 mois.
Quatre semaines après avoir reçu la dose de rappel du vaccin contre l'HB, 97,6 % (IC à 95 % : 95,1; 99) ont atteint des niveaux d'anticorps séroprotecteurs (anticorps anti-HBs ≥ 10 UI/L) et 94 % (IC à 95 % : 90,7; 96,5) ont atteint une concentration d'anti-HBs supérieure à 100 UI/L. Les concentrations moyennes géométriques (CMG) d'anticorps anti-HBs étaient 160 fois plus élevées et ont atteint 3 502,6 UI/L (IC à 95 % : 2 672; 4 591,5) après l'immunisation par le vaccin contre l'HB. Une autre étude menée par Avdicova et al. a révélé la persistance de la mémoire immunitaire 10 à 11 ans après la primovaccination durant la petite enfance avec le vaccin DCat-VHP-VPI-Hib ou le vaccin monovalent HB administré conjointement au vaccin DCaT-VPI-Hib.
Après la dose d'amorce du vaccin contre l'HB, 97 % des membres du groupe ayant reçu le vaccin DCat-VHP-VPI-Hib et 99 % des enfants du groupe à qui l'on a administré les vaccins en association ont atteint des titres séroprotecteurs. Des niveaux d'anticorps anti-HBs égaux ou supérieurs à 100 UI/L étaient présents chez plus de 93,5 % des personnes des deux groupes. Les CMG d'anticorps anti-HBs étaient au moins 180 fois plus élevées après la dose de rappel du vaccin contre l'HBNote de bas de page 88.
Le GTH a examiné deux étudesNote de bas de page 89 Note de bas de page 90 fournissant des renseignements sur la séroprotection chez les personnes immunodéprimées. Une étude menée par Inaba et al. a mesuré les niveaux d'anticorps à long terme chez 141 enfants ayant reçu le vaccin contre l'HB selon un calendrier de trois doses 12, 15 et 18 mois après la greffe de cellules souches hématopoïétiques (GCSH) allogénique. Avant l'immunisation, seuls 51,8 % des participants à l'étude avaient des niveaux séroprotecteurs (anticorps anti-HBs ≥ 10 UI/L). Cette proportion a augmenté pour atteindre 77,1 % après l'administration de trois doses du vaccin contre l'HB après la greffe.
Plus de cinq ans après l'immunisation effectuée après la GCSH, 72,9 % des participants ont conservé leurs titres séroprotecteurs (43/59). Une autre méta-analyse de 12 études mesurant les réponses immunitaires à long terme à la vaccination chez les patients infectés par le VIH (suivi variant de 12 à 115 mois) a été menée par Kerneis et al. Elle a révélé une diminution de la protection au fil du temps, 71 % des répondants primaires conservant leurs titres séroprotecteurs au bout d'un an, de 33 à 61 % au bout de deux ans et 40 % cinq ans après avoir reçu trois doses de vaccin, chacune d'entre elles contenant 40 μg d'antigènes HBs.
Chez les enfants dont la mère est infectée par le VIH et positive pour l'AgHBs, la conservation des titres d'anticorps séroprotecteurs représentait 24 % après 5,5 ans. La méta-analyse a révélé que parmi les répondants primaires, 38 % (IC à 95 % : 23 à 54 %) des adultes et 61 % (IC à 95 % : 27 à 90 %) des enfants conservaient leurs titres d'anticorps protecteurs deux ans après leur immunisation; et 8 % (IC à 95 % : 2 à 19 %) des adultes et 30 % (IC à 95 % : 0 à 76 %) des enfants les conservaient cinq ans après l'immunisation.
Le GTH a également examiné les renseignements concernant l'immunogénicité du vaccin contre l'HB chez les personnes atteintes de diabète. Un examen systématique de la documentation(Note de bas de page 29, Note de bas de page 91, Note de bas de page 92) mené par Schillie et al. a révélé une réponse similaire en fonction de l’âge chez les personnes atteintes de diabète et les non-diabétiques, lorsque le vaccin contre l'HB était administré selon les calendriers recommandés. La proportion de sujets protégés était généralement plus élevée chez les enfants, variant de 54,2 à 100 % (protection médiane, 93,9 %) chez ceux atteints de diabète et de 98 à 100 % (protection médiane, 100 %) chez les enfants non diabétiques. Chez les adultes, en particulier ceux qui étaient plus âgés, la séroprotection médiane était plus faible chez les diabétiques (31,3 à 94,4 % [médiane, 88,2 %]), comparativement aux non-diabétiques (35,2 à 96,9 % [médiane, 93,6 %]). Comme pour les adultes en bonne santé, les taux de séroprotection dans le cadre de ces études ont été déclarés chez les adultes diabétiques atteints de néphropathie chronique (variant de 41,8 à 85,3 % [séroprotection médiane, 60,1 %]).
IV.3 Innocuité
Les vaccins à composant anti-hépatite B sont bien tolérés, les effets indésirables tels que l'irritabilité, les céphalées, la fatigue et les réactions au point d'injection (p. ex. douleur et érythème) étant souvent légers et transitoires Note de bas de page 4
En octobre 2011, l'ACIP a publié l'examen de 12 études en vue d'évaluer les résultats en matière d'innocuité chez les personnes souffrant de diabète après l'administration du vaccin contre l'HBNote de bas de page 93. Aucune des études examinées n'a fait état d'événements indésirables graves liés au vaccin, bien que l'ACIP ait observé la manifestation très rare d'une réaction anaphylactique chez les personnes sensibles aux levures qui a été signalée par l'Institute of Medicine (IOM).Note de bas de page 94
V. Recommandations
Veuillez consulter le Tableau 6 pour avoir une explication sur les catégories de données probantes du CCNI.
Recommandation 1 : Le CCNI ne recommande pas l'administration de doses de rappel systématiques du vaccin contre l'HB chez les personnes immunocompétentes après l'achèvement d'un calendrier d'immunisation contre l'HB recommandé attribué durant la petite enfance. (Recommandation du CCNI selon les données probantes de catégorie B)
Le CCNI conclut qu'il existe des données probantes acceptables pour formuler cette recommandation, d'après le peu de renseignements disponibles au moyen des examens épidémiologiques et de la documentation résumés dans la présente déclaration. Avant la révision des recommandations actuelles, il sera nécessaire de procéder à une évaluation continue et à long terme des données épidémiologiques améliorées concernant l'apparition de maladies aiguës ou l'état de portage de l'antigène HBs dans les populations immunisées (population générale et groupes à risque). Les systèmes nationaux de surveillance améliorée doivent au minimum inclure les renseignements suivants : âge, sexe, comorbidités, vaccination et statut d'immigration.
Recommandation 2 : Le CCNI recommande que les adultes atteints de diabète ne soient pas considérés comme un groupe à risque élevé distinct pour l'immunisation par le vaccin contre l'HB. (Recommandation du CCNI selon les données probantes de catégorie I)
Le CCNI recommande le vaccin contre l'HB pour toutes les personnes ne présentant pas de contre-indications et qui souhaitent réduire leur risque d'HB, y compris les personnes atteintes d'un diabète de type 1 et 2. Les données américaines semblent indiquer une prévalence plus élevée de l'infection par le VHB antérieure ou actuelle chez les adultes atteints de diabète par rapport aux adultes non diabétiques, mais on ne dispose pas de données épidémiologiques canadiennes similaires. Compte tenu des différences notables entre les systèmes de soins de santé aux États-Unis et au Canada et de l'absence actuelle d'indication de risque plus élevé d'infection pour les personnes atteintes de diabète dans la population canadienne générale, le CCNI ne dispose pas de suffisamment de données probantes pour considérer ces personnes comme un groupe à risque élevé distinct pour l'immunisation par le vaccin à composant anti-hépatite B. Il continuera toutefois à surveiller les données probantes au fil de leur évolution.
Recommandation 3 : Pour les personnes immunodéprimées, on pourrait envisager une surveillance annuelle initiale des niveaux d'anticorps contre le VHB après une immunisation contre l'HB. (Recommandation du CCNI selon les données probantes de catégorie B)
Le moment optimal et la fréquence des tests sérologiques supplémentaires devraient être déterminés en se fondant sur la gravité de l'état d'immunodéficience et selon qu'il existe encore un risque d'HB. Si les titres d'anticorps anti-HBs sont inférieurs à 10 UI/L, les sujets immunodéprimés qui ont répondu au départ au vaccin contre l'HB pourraient avoir besoin de doses de rappel.
Cette recommandation concorde avec des recommandations similaires formulées par l'Advisory Committee on Immunization Practices (ACIP) des États-Unis, l'OMS et le groupe consultatif technique national sur l’immunisation de l'Australie. Le CCNI a déjà recommandé l'évaluation annuelle des niveaux d'anticorps contre le VHB chez les personnes atteintes d'une néphropathie chronique et sous dialyse et qui répondent de façon sous-optimale au vaccin contre l'hépatite B et chez qui les concentrations d'anti-HBs déclinent rapidement.
Recommandation 4 : L'immunisation par le vaccin à composant anti-hépatite B devrait être offerte selon des calendriers provinciaux et territoriaux déterminés. (Recommandation du CCNI selon les données probantes de catégorie I)
Il existe plusieurs calendriers autorisés pour l’administration des vaccins contre l'HB au Canada. Au cours des deux dernières décennies, l'ensemble des PT a mis en œuvre efficacement les programmes de dépistage prénatal de l'HB et d'immunisation des nourrissons à risque
Une réduction marquée de l'incidence de l'hépatite B ayant été observée dans l'ensemble du Canada et compte tenu de l'absence de donnée démontrant l'avantage évident de l'un ou l’autre des calendriers utilisés, le moment optimal de la primovaccination contre l'HB continue d'être subordonné aux considérations liées à des programmes précis et d'épidémiologie des PT. Afin de modifier selon les besoins les programmes d'immunisation contre l'HB existants, on devrait recueillir et analyser de façon continue les renseignements épidémiologiques démontrant l'échec des programmes de dépistage prénatal universel et d'immunisation systématique (c.-à-d. détection d'une infection par le VHB chez les nourrissons et les enfants en attente d'un vaccin).
VI. Priorités en matière de surveillance et de recherche
- Surveillance continue de l'épidémiologie de l'hépatite B au Canada, y compris l'incidence et les tendances des maladies aiguës et chroniques;
- Élaboration et entretien de systèmes de surveillance améliorée qui ont la capacité de saisir les cas d'échec du vaccin et d'infection post-vaccination, en particulier chez les sujets à risque élevé;
- Études visant à déterminer la durée des corrélats de protection immunitaire et à long terme, et plus particulièrement dans les pays dont l'incidence de l'HB est faible;
- Études visant à déterminer le niveau de réponse anamnestique humorale et/ou cellulaire nécessaire pour prévenir l'infection chronique et le moment d'administration de doses de rappel en fonction de la réponse anamnestique préservée;
- Études visant à évaluer l'efficacité potentielle et réelle des programmes contre l'hépatite B dans les établissements de soins de longue durée.
Tableaux
| Détails de l'étude | Résumé | |||||
|---|---|---|---|---|---|---|
| Étude | Vaccin | Modèle de l’étude | Participants | Résumé des principales conclusions et des données sur les résultats | Niveau des données probantes | Qualité |
| Samandari T., Fiore A.E., Negus S. et al. Differences in response to a hepatitis B vaccine booster dose among Alaska children and adolescents vaccinated during infancy. Pediatrics 2007; 120: e373-381.Note de bas de page 46 | Primovaccination :
Trois doses du vaccin recombiné (formulation à dose de 2,5-; 5- ou 10 μg) ou du vaccin dérivé du plasma (dose de 10 μg)
Immunisation de rappel : Recombivax; Merck & Co, dose de 5 μg |
États-Unis, Alaska
Étude de comparaison non randomisée Réponse anamnestique définie par ce qui suit : augmentation par un facteur de quatre ou plus des anticorps anti-HBs si les niveaux d'anticorps au départ ≥ 10 UI/L ou anticorps anti-HBs ≥ 10 UI/L si les niveaux au départ < 10 UI/L. Sérologie à la 4e semaine après la dose de rappel |
N = 212
Autochtones d'Alaska Groupe 1 : 138 enfants de 10 à 14,7 ans déjà immunisés par un vaccin recombiné Groupe 2 : 74 enfants de 11,7 à 14,9 ans déjà immunisés par un vaccin dérivé du plasma |
Groupe 1 :
Aucun participant ne présente des preuves probantes d'infection chronique par le virus de l'hépatite B. |
II-1 | Passable |
| Hammitt L.L., Hennessy T.W., Fiore A.E. et al. Hepatitis B immunity in children vaccinated with recombinant hepatitis B vaccine beginning at birth: a follow-up study at 15 years. Vaccine, 2007; 25(39-40): 6958-64.Note de bas de page 58 | Primovaccination :
Recombivax, Merck & Co, dose de 2,5 μg à la naissance, à l'âge de 1 à 3 mois et à l'âge de 6 à 9 mois
Immunisation de rappel : Recombivax; Merck & Co, dose de 5 μg |
États-Unis, Alaska
Étude sérologique Sérologie entre le 10e et 14e jour et 1 mois après la dose de rappel Réponse anamnestique définie par une augmentation des anticorps dans les 15 jours suivant la dose de rappel chez les personnes dont les anticorps anti-HBs < 10 UI/L ou chez les enfants dont les anticorps anti-HBs ≥ 5 UI/L, par une augmentation des anticorps par un facteur de 4 |
N = 37
Âge médian des sujets : 14,6 ans (tranche d'âge : de 13,7 à 15,6) nés d'une mère séronégative; tous les sujets ayant des anticorps anti-HBs ≥ 10 UI/L à l'âge de 18 mois |
% (2/37) des enfants ayant des anticorps anti-HBs ≥ 10 au moment de l'inscription à l'étude; tous les enfants sont négatifs pour l'AgHBc(-)
51 % (18/35) des participants ont une réponse anamnestique deux semaines après la dose de rappel; 60 % (21/35) atteignent un niveau d'anticorps protecteurs un mois après la dose de rappel Augmentation par un facteur de 16 et de 23 de la CMG observée 13 et 28 jours après la dose de rappel, respectivement |
III | Mauvaise |
| Petersen K.M., Bulkow L.R., McMahon B.J., Zanis C., Getty M., Peters H. et Parkinson A.J. Duration of hepatitis B immunity in low risk children receiving hepatitis B vaccinations from birth. Pediatr Infect Dis J. Juil. 2004;23(7):650-5.Note de bas de page 73 | Primovaccination : Dose de 10 μg du vaccin dérivé du plasma (Heptavax-B,
Merck Sharp & Dohme) administrée dans les sept jours suivant la naissance, entre la 4e et 6e semaine et à l'âge de six mois.
Dose de rappel : Recombivax (dose de 5 μg) |
États-Unis, Alaska
Étude sérologique |
Groupe 1 : 17 enfants, âge moyen de 12,6 ans, nés d'une mère négative pour l'AgHBs(-) et immunisés par un vaccin dérivé du plasma; tous avec des titres d'anti-HBs ≥ 10 UI/L après la primovaccination
Groupe 2 : 16 enfants, âge moyen de 12,1 ans, nés d'une mère positive pour l'AgHBs(+) et immunisés par un vaccin dérivé du plasma; tous avec des titres d'anti-HBs ≥ 10 UI/L après la primovaccination |
Groupe 1 :
|
II | Mauvaise |
| West D.J., Watson B., Lichtman J., Hesley T.M. et Hedberg K. Persistence of immunologic memory for twelve years in children given hepatitis B vaccine in infancy. Pediatr Infect Dis J. Août 1994;13(8):745-7Note de bas de page 95 | Primovaccination :
Deux doses de 5 μg du vaccin dérivé du plasma (Heptavax-B, Merck & Co) administrées à l'âge de 3 et 11 mois
Immunisation de rappel : Recombivax; Merck & Co, dose de 5 μg |
É.-U.
Étude sérologique Sérologie 7 jours et 1 mois après la dose de rappel Réponse anamnestique définie par une augmentation des anticorps par un facteur de deux dans un délai de sept jours ou par un titre d'anticorps ≥ 10 UI/L chez les personnes dont les anticorps anti-HBs < 10 UI/L |
N = 14
Enfants, 12 ans après la primovaccination durant la petite enfance, qui ont été initialement recrutés pour participer à une étude sur l'immunogénicité et l'innocuité du vaccin Heptavax-B |
Aucun enfant n'était positif pour l'AgHBs(+) ou l'anti-HBc(+); tous les enfants avaient un titre d'anti-HBs ≥ 10 UI/L
Une semaine après l'administration de la dose de rappel, tous ont présenté une augmentation du titre par un facteur de 2 à 42; tous avaient des titres supérieurs à ceux atteints après la primovaccination, 4 semaines après l'immunisation de rappel |
II | Mauvaise |
| Middleman A. et al. Duration of Protection After Infant Hepatitis B Vaccination Series. Pediatrics 2014; 133:6 e1500 -e1507Note de bas de page 77 |
Primovaccination :
Trois doses de 5 μg; primovaccination achevée à l'âge de 12 mois
Immunisation de rappel : ENGERIX®-B, GlaxoSmithKline, dose de 10 ou 20 μg |
É.-U.
Étude sérologique de comparaison non randomisée |
N = 420
Groupe 1 : 240 sujets de 16 à 19 ans chez qui une immunisation a été amorcée dans les sept jours suivant la naissance Groupe 2 : 180 sujets de 16 à 19 ans chez qui une immunisation a été amorcée à l'âge de 4 semaines ou plus |
Groupe 1 :
|
II | Bonne |
| Bialek S.R., Bower W.A., Novak R. et al. Persistence of protection against hepatitis B virus infection among adolescents vaccinated with recombinant hepatitis B vaccine beginning at birth: a 15-year follow-up study. Pediatr Infect Dis J, 2008; 27(10): 881-5.Note de bas de page 48 | Primovaccination :
Recombivax, Merck & Co, dose de 5 μg à la naissance, 2,5 μg à l'âge de 2 et 6 mois
Immunisation de rappel : Recombivax; Merck & Co, dose de 5 μg |
Micronésie
Étude sérologique Réponse anamnestique définie par ce qui suit : anticorps anti-HBs ≥ 10 UI/L si au départ < 10 UI/L. Sérologie à la 2e semaine après la dose de rappel |
N = 105
Sujets immunisés durant la petite enfance en moyenne 15,1 ans avant leur participation à l'étude (âge médian des participants : 15,8 ans) et sans donnée probante d'infection par le VHB à l'âge de 2 à 3 ans |
60 % (63/105) des participants avaient des niveaux d'anticorps protecteurs 35 mois après l'immunisation initiale
7 % (7/97) avaient des anticorps anti-HBs ≥ 10 UI/L et étaient négatifs à l'anticorps anti-HBc(-) au départ; aucun sujet n'était positif pour l'AgHBs(+); 7,6 % (8/105) étaient positifs pour l'AgHBc(+); 3/8 étaient positifs à l'anticorps anti-HBc(+) avec des anticorps anti-HBs ≥ 10 UI/L Après l'administration d'une dose de rappel, 48 % (46/97) des participants ont atteint des titres séroprotecteurs après une dose de rappel; proportion plus élevée de séroprotection (64,3 % p/r à 35,2 %) chez les sujets qui avaient des titres séroprotecteurs 35 mois après la primovaccination |
III | Passable |
| Chaves S.S., Groeger J., Helgenberger L. et al. Improved anamnestic response among adolescents boosted with a higher dose of the hepatitis B vaccine. Vaccine, 2010; 28(16): 2860-4.Note de bas de page 57 | Primovaccination :
Recombivax, Merck & Co, dose de 5 μg à la naissance et de 2,5 μg à l'âge de 2 et 6 mois
Immunisation de rappel : Recombivax, Merck & Co, dose de 5 ou 10 μg |
Micronésie
Étude de comparaison sérologique, non randomisée Sérologie 14 jours après la dose de rappel Titre d'anticorps ≥ 10 UI/L considéré comme protecteur Réponse anamnestique définie par une augmentation par un facteur de 4 des anticorps anti-HBs et par un titre ≥ 10 UI/L |
Groupe 1 : 89 sujets dont l'âge médian est 17,7 ans (IC à 95 % : 16,7; 18,7) auxquels on a administré une dose de 10 μg
Groupe 2 : 105 sujets dont l'âge médian est 15,7 ans (IC à 95 % : 14,9; 16,8) auxquels on a administré une dose de 5 μg |
Aucun des participants de l'étude n'était positif pour l'antigène HBs(+)
Groupe 1 :
|
III | Mauvaise |
| Chaves S.S., Fischer G., Groeger J., Patel P.R., Thompson N.D., Teshale E.H., Stevenson K., Yano V.M., Armstrong G.L., Samandari T., Kamili S., Drobeniuc J. et Hu D.J. Persistence of long-term immunity to hepatitis B among adolescents immunized at birth. Vaccine. 21 févr. 2012;30(9): 1644-9.Note de bas de page 96 | Primovaccination :
Recombivax, Merck & Co, dose de 5 μg à la naissance et dose de 2,5 μg à l'âge de 2 et de 6 mois (première dose administrée avant les sept jours suivant la naissance et troisième dose administrée avant l'âge d'un an)
Immunisation de rappel : Recombivax, Merck & Co, dose de 5 ou 10 μg |
Palaos
Étude de comparaison sérologique, non randomisée Sérologie 14 jours après la dose de rappel Titre d'anticorps ≥ 10 UI/L considéré comme protecteur Réponse anamnestique définie par une augmentation par un facteur de 4 des anticorps anti-HBs et par un titre ≥ 10 mUI |
Groupe 1 : 172 sujets dont l'âge médian est 11 ans (IC à 95 % : 10,3; 11,7)
Groupe 2 : 60 adolescents dont l'âge médian est 15,8 ans (IC à 95 % : 15,1; 16,5) Tous les participants étaient négatifs pour l'antigène HBs et aux anticorps anti-HBc(-) et présentaient des titres d'anticorps anti-HBs protecteurs à l'âge de 12 mois; plus de 70 % avaient des anticorps anti-HBs ≥ 100 UI/L à l'âge de 12 mois |
5 % (9/190) étaient positifs aux anticorps contre l'antigène HBc(+)
Groupe 1 :
|
III | Mauvaise |
| Salama I.I., Sami S.M., Salama S.I., Rabah T.M., El-Etreby L.A., Abdel-Hamid A.T., Elmosalami D., El-Hariri H. et Said Z.N. Immune response to second vaccination series of hepatitis B virus among booster dose non-responders. Vaccine. 27 févr. 2016Note de bas de page 97 | Primovaccination : non indiquée
Immunisation de rappel : Dose de 10 μg du vaccin recombiné contre l'HB Euvax |
Égypte
Étude de comparaison sérologique, non randomisée Titre d'anticorps ≥ 10 UI/L considéré comme protecteur Réponse anamnestique définie par un titre d'anticorps anti-HBs ≥ 10 UI/L 4 semaines après avoir reçu la dose de rappel |
1 026 sujets entre l'âge de 10 et 15 ans
Groupe 2 : 821 sujets ≥ 15 ans Tous les participants ont reçu 3 doses du vaccin durant la petite enfance |
Groupe 1 :
|
III | Mauvaise |
| Boxall E.H., A. Sira J., El-Shuhkri N. et al. Long-term persistence of immunity to hepatitis B after vaccination during infancy in a country where endemicity is low. J Infect Dis, 2004; 190(7): 1264-9Note de bas de page 51 | Primovaccination :
Dose de 10 μg Note de bas de page 98 du vaccin recombiné (HBVax, Merck Sharp & Dohme) administrée à la naissance, à 1, 2 et 6 mois; certains enfants ont aussi reçu des IgHB à la naissance
Immunisation de rappel : vaccin recombiné HBVax II, Aventis Pasteur, dose de 5 μg |
Royaume-Uni
Étude sérologique Sérologie à la 4e semaine après la dose de rappel Titre d'anticorps ≥ 10 UI/L considéré comme protecteur |
N = 116
Enfants ayant reçu 3 doses du vaccin contre l'HB avec ou sans IgHB à la naissance Groupe 1 : 64 enfants dont l'âge moyen est 14,5 ans (7,7 à 17,3), nés de mère antigène HBs(+) positif et déjà recrutés pour participer à une étude sur l'efficacité du vaccin contre l'HB Groupe 2 : 52 fratries parmi les enfants recrutés initialement, âge moyen de 11,7 ans (6 à 18,4 ans) |
Aucun enfant dans les groupes n'était positif pour l'antigène HBs(+); 1 enfant dans chaque groupe était positif aux anticorps contre l'antigène HBc(+)
Groupe 1 :
|
III | Passable |
| Behre U., Bleckmann G., Crasta P.D., Leyssen M., Messier M., Jacquet J.M. et Hardt K. Long-term anti-HBs antibody persistence and immune memory in children and adolescents who received routine childhood hepatitis B vaccination. Hum Vaccin Immunother. Juin 2012;8(6):813-8.Note de bas de page 79 | Primovaccination : Calendrier à trois doses (0, 1 et 6 mois) du vaccin ENGERIX®-B, GlaxoSmithKline (dose de 10 μg); deux premières doses administrées avant l'âge de 9 mois et troisième dose avant l'âge de 18 mois
Dose de rappel : ENGERIX®-B, GlaxoSmithKline (dose de 10 μg) |
Allemagne
Étude sérologique Sérologie 4 semaines après la dose de rappel Réponse anamnestique définie par des anticorps anti-HBs ≥ 10 UI/L chez les sujets séronégatifs avant l'administration de la dose de rappel ou une augmentation par au moins un facteur de 4 du niveau d'anticorps anti-HBs chez les sujets qui étaient séropositifs avant l'immunisation de rappel |
N = 282
Âge moyen des enfants immunisés à la naissance : 12,4 ans (ÉT : 0,48) |
78 % (220/282; IC à 95 % : 73,1 à 83) présentaient des anticorps anti-HBs ≥ 10 UI/L avant l'immunisation de rappel; 8 % (23/282) des enfants n'avaient pas de niveaux d'anticorps détectables (< 3,3 UI/mL)
97,2 % (IC à 95 % : 94,5 à 98,8) des enfants produisaient une réponse anamnestique à la dose d'amorce; 98,9 % (IC à 95 % : 96,9 à 99,8) étaient séropositifs après l'immunisation de rappel 91,3 % (IC à 95 % : 72 à 98,9) enfants sans anticorps anti-HBs détectables atteignaient des anticorps anti-HBs ≥ 10 UI/L après la dose de rappel; 93,6 % (IC à 95 % : 90,1 à 96,2) avaient des anticorps anti-HBs ≥ 100 UI/L |
III | Bonne |
| Van Der Meeren O., Behre U. et Crasta P. Immunity to hepatitis B persists in adolescents 15-16 years of age vaccinated in infancy with three doses of hepatitis B vaccine. Vaccine. 16 avr. 2016. pii: S0264-410X(16)30142-6.Note de bas de page 80 | Primovaccination : Calendrier à trois doses (0, 1 et 6 mois) du vaccin ENGERIX®-B, GlaxoSmithKline (dose de 10 μg); deux premières doses administrées avant l'âge de 9 mois et troisième dose avant l'âge de 18 mois
Dose de rappel : ENGERIX®-B, GlaxoSmithKline (dose de 10 μg) |
Allemagne
Étude sérologique Sérologie 4 semaines après la dose de rappel Séropositivité définie par des anticorps anti-HBs de 6,2 à 10 UI/L et séroprotection définie par des anticorps anti-HBs ≥ 10 UI/L Réponse anamnestique définie par des anticorps anti-HBs ≥ 10 UI/L chez les sujets séronégatifs avant l'administration de la dose de rappel ou une augmentation par au moins un facteur de 4 du niveau d'anticorps anti-HBs chez les sujets qui étaient séropositifs avant l'immunisation de rappel |
N = 292
Âge moyen des enfants immunisés à la naissance : 15,3 ans (ÉT : 0,5) |
65 % (190/292; IC à 95 % : 59,6 à 70,9) avaient des anticorps anti-HBs ≥ 10 UI/L avant l'immunisation de rappel
97,9 % (IC à 95 % : 95,6 à 99,2) avaient des anticorps anti-HBs ≥ 10 UI/L après la dose de rappel; 90,8 % (IC à 95 % : 86,8 à 93,8) avaient des anticorps anti-HBs ≥ 100 UI/L 6 % (6/102) des sujets ayant des niveaux d'anticorps < 10 UI/L demeuraient sans séroprotection après la dose de rappel; tous les sujets séropositifs ont atteint une séroprotection, ce qui a donné lieu à une réponse anamnestique dans l'ensemble observée chez 96,9 % (IC à 95 %: 94,2 à 98,6) des participants Augmentation médiane par un facteur de 150 de la CMG après l'immunisation de rappel (4 134,9 UI/L; IC à 95 % : 3 114,2 à 5 490,1) |
III | Bonne |
| Kao J.T., Wang J.H., Hung C.H. et al. Long-term efficacy of plasma-derived and recombinant hepatitis B vaccines in a rural township of Central Taiwan. Vaccine 2009; 27(12): 1858-62.Note de bas de page 56 | Primovaccination : 5 μg du vaccin dérivé du plasma (HEVAC-BMD; Institut Pasteur, Marnesla-Coquette, France ou LGVAC-BMD; Lifeguard Pharmaceutical Inc.,
Taipei, Taïwan) ou dose de 2,5 μg du vaccin recombiné (Recombivax HBMD; Merck Sharp & Dohme)
Immunisation de rappel : ENGERIX®-B, GlaxoSmithKline, dose de 2,5 μg |
Taïwan
Étude sérologique Titre d'anticorps ≥ 10 UI/L jugé protecteur; réponse anamnestique définie par une augmentation des anticorps anti-HBs ≥ 10 UI/L Sérologie 3 semaines après la dose de rappel |
Groupe 1 : 437 enfants entre 12 et 15 ans nés de mère antigène HBs(+) positif et déjà immunisés par un vaccin dérivé du plasma à 0, 1, 2 et 12 mois
Groupe 2 : 1 101 enfants entre 12 et 15 ans, déjà immunisés par un vaccin dérivé du plasma à 0, 1, 2 et 12 mois Groupe 3 : 250 enfants entre 12 et 15 ans, déjà immunisés par un vaccin recombiné à 0, 1 et 6 mois Les nourrissons nés de mère antigène HBe(+) positif ont aussi reçu des IgHB à la naissance Dose de rappel administrée à des sujets dont le titre d'anticorps < 10 UI/L |
Groupe 1 :
|
III | Passable |
| Chang Y.C., Wang J.H., Chen Y.S., Lin J.S., Cheng C.F. et Chu C.H. Hepatitis B virus vaccination booster does not provide additional protection in adolescents: a cross-sectional school-based study. BMC Public Health. 23 sept. 2014;14:991.Note de bas de page 85 | Primovaccination : 5 μg du vaccin dérivé du plasma (HEVAC-BMD; Institut Pasteur, Marnesla-Coquette, France ou LGVAC-BMD; Lifeguard Pharmaceutical Inc.,
Taipei, Taïwan) ou dose de 5 ou 20 μg du vaccin recombiné (Recombivax HBMD; Merck Sharp & Dohme ou ENGERIX®; GlaxoSmithKline)
Immunisation de rappel : ENGERIX®-B, GlaxoSmithKline, dose de 20 μg |
Taïwan
Étude sérologique Titre d'anticorps ≥ 10 UI/L jugé protecteur; réponse anamnestique définie par une augmentation des anticorps anti-HBs ≥ 10 UI/L Sérologie 6 semaines après la dose de rappel |
N = 1 054
Adolescents de 15 ans ayant reçu une immunisation durant la petite enfance |
|
III | Passable |
| Su F.H., Cheng S.H., Li C.Y. et al. Hepatitis B seroprevalence and anamnestic response amongst Taiwanese young adults with full vaccination in infancy, 20 years subsequent to national hepatitis B vaccination. Vaccine, 2007; 25(47): 8085-90.Note de bas de page 43 | Primovaccination :
Dose de 5 μg du vaccin dérivé du plasma (Hevac B, Pasteur-Mérieux ou Lifeguard, Hsin-Chu) administré à la naissance, à 1, 2 et 12 mois
Immunisation de rappel : ENGERIX®-B, GlaxoSmithKline, dose de 20 μg |
Taïwan
Étude sérologique Sérologie 4 semaines après la dose de rappel Titre d'anticorps entre 10 et 100 UI/L considéré comme étant un cas limite de titre d'anticorps protecteur; ≥ 100 UI/L considéré comme étant un titre d'anticorps protecteur; réponse anamnestique définie par une augmentation du titre d'anticorps anti-HBs ≥ 10 UI/L | N = 843
Âge moyen des étudiants immunisés durant la petite enfance : 18,7±0,4 ans |
34 % (283/843) avaient des titres séroprotecteurs au départ; 44 % des sujets séronégatifs sans titres détectables (anticorps contre l'antigène HBs < 0,1 UI/L)
2,7 % (23/843) étaient positifs aux anticorps contre l'antigène HBc(+)/négatifs aux anticorps contre l'antigène HBs et 1,4 % (12/843) étaient positifs aux anticorps contre l'antigène HBc/HBs; 75 % (8/12) des sujets positifs aux anticorps contre l'antigène HBc(+)/HBs(+) ont reçu des IgHB à la naissance 75 % (238/316) des sujets ont atteint des anticorps anti-HBs ≥ 10 UI/L après avoir reçu la dose de rappel 81,3 % (70/78) des sujets qui n'ont pas présenté une réponse anamnestique avaient un niveau d'anticorps anti-HBs < 0,1 UI/L avant le sérum de rappel |
III | Passable |
| Jan C.F., Huang K.C., Chien Y.C. et al. Determination of immune memory to hepatitis B vaccination through early booster response in college students. Hepatology, 2010; 51(5): 1547-54.Note de bas de page 44 | Primovaccination :
Au moins trois doses de 5 μg du vaccin dérivé du plasma (première dose administrée à la naissance)
Immunisation de rappel : ENGERIX®-B, GlaxoSmithKline, dose de 20 μg |
Taïwan
Étude sérologique Sérologie 7 à 10 jours et 4 semaines après la dose de rappel Titre séroprotecteur défini par des anticorps anti-HBs ≥ 10 UI/L |
N = 127
Étudiants négatifs pour l'antigène HBs(-), négatifs aux anticorps anti-HBc(-) et anti-HBs(-) entre 18 et 23 ans immunisés durant la petite enfance |
76 % (96/127) avaient des anticorps anti-HBs ≥ 10 UI/L 4 semaines après la dose de rappel; les niveaux d'anticorps protecteurs ont été atteints par 20,5 % (26/127) 7 à 10 jours après la dose de rappel
Parmi les 101 participants qui étaient séronégatifs 7 à 10 jours après la dose de rappel, 70 % (70/101) ont développé des titres d'anticorps protecteurs 4 semaines après l'immunisation |
II-3 | Passable |
| Lin C.C., Yang C.Y., Shih C.T., Chen B.H. et Huang Y.L. Waning immunity and booster responses in nursing and medical technology students who had received plasma-derived or recombinant hepatitis B vaccine during infancy. Am J Infect Control. Juin 2011;39(5):408-14.Note de bas de page 74 | Primovaccination : Dose de 5 μg du vaccin dérivé du plasma (Hevac B; Pasteur-Mérieux, Lyon, France ou
vaccin contre l'hépatite B de Lifeguard, Hsin-
Chu, Taïwan) à 0, 1, 2 et 12 mois ou
vaccin recombiné à 0, 1 et 6 mois
Dose de rappel : ENGERIX®-B, GlaxoSmithKline, dose de 20 μg |
Taïwan
Étude sérologique Séroprotection définie par des anticorps anti-HBs ≥ 10 UI/L |
Groupe 1 : 1 133 étudiants de 16 ans ayant reçu un vaccin dérivé du plasma durant la petite enfance
Groupe 2 : 674 étudiants de 16 ans ayant reçu un vaccin recombiné durant la petite enfance La plupart (93 %) des participants étaient de sexe féminin |
Groupe 1 :
|
III | Passable |
| Wang L.U. et Lin H.H. Ethnicity, substance use, and response to booster hepatitis B vaccination in anti-HBs-seronegative adolescents who had received primary infantile vaccination. J Hepatol, 2007; 46(6): 1018-25Note de bas de page 41 | Primovaccination : Vaccin contre l'hépatite dérivé du plasma,
dose de 5 μgNote de bas de page 99 à la naissance, à 1, 2 et 12 mois
Immunisation de rappel : ENGERIX®-B, GlaxoSmithKline, dose de 20 μg |
Taïwan
Étude sérologique Les répondants définis comme les sujets recevant une dose de rappel présentaient un titre d'anticorps anti-HBs ≥ 10 UI/L après la dose de rappel. |
N = 386
Moyenne d'âge des adolescents ayant des titres d'anticorps anti-HBs < 10 UI/L et ayant été immunisés durant la petite enfance : 15,9 ± 0,5 ans |
49 % (190/386) avaient des niveaux d'anticorps indétectables (< 0,1 UI/L) au départ
77,2 % (298/386) des participants atteignaient une séroprotection 4 semaines après la dose de rappel; 59 % (112/190) des sujets ayant des niveaux d'anticorps indétectables et 95 % (186/196) de ceux dont les niveaux d'anticorps étaient compris entre 0,1 et 9,9 UI/L répondaient à l'immunisation de rappel (rapport de cotes [RC] de 13,97; IC à 95 % : 6,63; 29,44) |
III | Passable |
| Lu C.Y., Ni Y.H., Chiang B.L. et al. Humoral and cellular immune responses to a hepatitis B vaccine booster 15-18 years after neonatal immunization. J Infect Dis, 2008; 197(10): 1419-26.Note de bas de page 40 | Primovaccination : Quatre doses de 10 μg du vaccin dérivé du plasma (Hevac B;
Pasteur-Mérieux)
Vaccin administré à la naissance, à 1, 2 et 12 mois; les nourrissons nés de mère antigène HBe(+) positif ont aussi reçu des IgHB
Immunisation de rappel : ENGERIX®-B, GlaxoSmithKline, dose de 20 μg |
Taïwan
Étude sérologique Sérologie à la 4e semaine après la dose de rappel Concentrations d'anticorps anti-HBs ≥ 10 UI/L définies comme étant protectrices Dose de rappel administrée uniquement aux sujets du groupe 2 |
Groupe 1 : 175 sujets entre 18 et 21 ans, immunisés lorsqu'ils étaient nourrissons et nés de mère antigène HBs(+) positif
Groupe 2 : 5 981 sujets entre 15 et 17 ans immunisés lorsqu'ils étaient nourrissons |
Groupe 1 :
|
III | Bonne |
| Lu S.N., Chen C.H., Chen T.M. et al. Hepatitis B virus infection in adolescents in a rural township--15 years subsequent to mass hepatitis B vaccination in Taiwan. Vaccine, 2006; 24(6): 759-65.Note de bas de page 38 | Primovaccination : Vaccin dérivé du plasma (Hevac B;
Pasteur-Mérieux),
dose de 10 μg à la naissance, à 1, 2 et 12 mois; les enfants nés de mère antigène HBe(+) positif ont aussi reçu des IgHB
Immunisation de rappel : ENGERIX®-B, GlaxoSmithKline, dose de 20 μg |
Taïwan
Étude sérologique Sérologie à la 4e semaine après la dose de rappel Réponse anamnestique définie par le développement d'un titre d'anticorps anti-HBs ≥ 10 mUI/mL |
Groupe 1 : 440 sujets entre 14 et 15 ans nés de mère antigène HBs(+) positif
Groupe 2 : 1 014 sujets entre 13 et 15 ans immunisés lorsqu'ils étaient nourrissons |
Groupe 1 :
|
III | Bonne |
| Lu C.Y., Chiang B.L., Chi W.K. et al. Waning immunity to plasma-derived hepatitis B vaccine and the need for boosters 15 years after neonatal vaccination. Hepatology, 2004; 40(6): 1415-20.Note de bas de page 39 | Primovaccination : Vaccin dérivé du plasma (Hevac B;
Pasteur-Mérieux),
dose de 5 μg à la naissance, à 1, 2 et 12 mois; les enfants nés de mère antigène HBe(+) positif ont aussi reçu des IgHB
Immunisation de rappel : ENGERIX®-B, GlaxoSmithKline, dose de 20 μg |
Taïwan
Étude sérologique Sérologie à la 4e semaine après la dose de rappel Réponse définie par le développement d'un titre d'anticorps anti-HBs ≥ 10 mUI/mL |
Groupe 1 : 78 adolescents de 15 ans nés de mère AgHBs(+)/AgHBe(+) positif et immunisés durant la petite enfance; tous les sujets étaient négatifs pour l'antigène HBs(-)/positifs aux anticorps anti-HBs(+) à 18 mois
Groupe 2 : 113 adolescents de 15 ans immunisés durant la petite enfance |
Groupe 1 :
|
III | Passable |
| Wang L.Y. et Lin H.H. Short-term response to a booster dose of hepatitis B vaccine in anti-HBs negative adolescents who had received primary vaccination 16 years ago. Vaccine. 10 oct. 2007;25(41) :7160-7Note de bas de page 64 | Primovaccination : Dose de 5 μg du vaccin dérivé du plasma (Hevac B; Pasteur-Mérieux, Lyon, France ou
son dérivé équivalent, le vaccin contre l'hépatite B de Lifeguard, Hsin-
Chu, Taïwan) administré à 0, 1, 2 et 12 mois
Dose de rappel : ENGERIX®-B, GlaxoSmithKline, dose de 20 μg |
Taïwan
Étude séro-épidémiologique |
N = 395
Adolescents séronégatifs (âge moyen : 15,9±0,6 ans) immunisés durant la petite enfance Le taux de séropositivité de la cohorte à partir de laquelle le sous-groupe a été sélectionné était de 45 % |
Deux mois après l'immunisation de rappel, 77 % (298/386) des sujets ont atteint des titres séroprotecteurs
Parmi les sujets qui avaient des titres indétectables avant la dose de rappel (< 0,1 UI/L), environ 35 % avaient des titres après la dose de rappel ≥ 10 UI/L; chez les adolescents qui avaient des titres avant la dose de rappel compris entre 0,1 et 9,9 UI/L, 95 % ont développé des titres protecteurs après la dose de rappel Parmi les 283 étudiants dont le titre ≥ 10 UI/L deux mois après l'immunisation de rappel, plus de 25 % ont perdu leur protection au 12e mois Dans le cas de la cohorte de principe à partir de laquelle des sujets séronégatifs ont été sélectionnés pour l'immunisation de rappel, on a estimé que 87 % des sujets avaient des titres séroprotecteurs après avoir reçu une dose de rappel. |
II | Mauvaise |
| Teoharov P., Kevorkyan A., Petrova N., Baltadzhiev I. et Van Damme P. Immune memory and immune response in children from Bulgaria 5-15 years after primary hepatitis B vaccination. Pediatr Infect Dis J. Janv. 2013;32(1):51-3. | Primovaccination :
ENGERIX®-B,
GlaxoSmithKline
Dose de rappel : ENGERIX®-B, GlaxoSmithKline |
Bulgarie
Étude séro-épidémiologique |
Groupe 1 : 52 enfants dont l'âge moyen est 10,46 (±1,21) ans déjà immunisés à la naissance, à 1 et 6 mois
Groupe 2 : 36 enfants dont l'âge moyen est 14,91 (±1,29) ans déjà immunisés à la naissance, à 1 et 6 mois |
Groupe 1 :
|
III | Mauvaise |
| Avdicova M., Crasta P.D., Hardt K. et Kovac M. Lasting immune memory against hepatitis B following challenge 10-11 years after primary vaccination with either three doses of hexavalent DTPa-HBV-IPV/Hib or monovalent hepatitis B vaccine at 3, 5 and 11-12 months of age. Vaccine. 28 mai 2015;33(23):2727-33. | Primovaccination : DCaT-VHB-VIP/Hib (Infanrix-hexa, GlaxoSmithKline) contenant 10 μg d'antigène HBs administré à 3, 5 et 11 mois
ENGERIX®-B, GlaxoSmithKline, dose de 10 μg Dose de rappel : ENGERIX®-B, GlaxoSmithKline, dose de 10 μg |
Slovaquie
Suivi de l'essai randomisé contrôlé déjà effectué |
Groupe 1 : 95 enfants âgés en moyenne de 11,3 ans et ayant déjà reçu trois doses du vaccin combiné hexavalent durant la petite enfance
Groupe 2 : 89 enfants entre 10 et 11 ans ayant déjà reçu trois doses du vaccin monovalent HB administré conjointement au vaccin pentavalent |
Groupe 1 :
|
II | Passable |
| Da Villa G., Peluso F., Picciotto L., Bencivenga M., Elia S. et Pelliccia Μ.G. Persistence of anti-HBs in children vaccinated against viral hepatitis B in the first year of life: follow-up at 5 and 10 years. Vaccine. Nov. 1996; 14(16):1503-5.Note de bas de page 49 | Primovaccination :
Dose de 5 μg du vaccin dérivé du plasma (Hevac B de Pasteur-Merieux)
Dose de rappel : Dose de 20 μg du vaccin recombiné ENGERIX®-B, GlaxoSmithKline |
Italie
Étude sérologique |
Groupe 1 : 214 enfants ayant
reçu trois doses du vaccin dérivé du plasma à l'âge de 3, 5 et 11 mois, 10 ans avant l'étude
Groupe 2 : 260 enfants ayant reçu quatre doses du vaccin dérivé du plasma à l'âge de 1, 2, 3 et 12 mois, 10 ans avant l'étude |
Groupe 1 :
|
II | Passable |
| Da Villa G., Pelliccia Μ.G., Peluso F., Ricciardi E. et Sepe A. Anti-HBs responses in children vaccinated with different schedules of either plasma-derived or HBV DNA recombinant vaccine. Res Virol. Mars-avr. 1997; 148(2):109-14.Note de bas de page 70 | Primovaccination :
Dose de 5 μgNote de bas de page 100 du vaccin dérivé du plasma (Hevac B de Pasteur-Merieux)
Dose de rappel : Dose de 20 μg du vaccin ENGERIX®-B, GlaxoSmithKline |
Italie
Étude sérologique de comparaison non randomisée |
Groupe 1 : 69 enfants immunisés par 3 doses durant la petite enfance (1er, 2e, 3e mois) 10 ans avant la participation à l'étude
Groupe 2 : 53 enfants immunisés par 3 doses durant la petite enfance (3e, 5e et 11e mois) 10 ans avant la participation Groupe 3 : 50 enfants immunisés par 2 doses durant la petite enfance (3e et 5e mois) 10 ans avant la participation |
Groupe 1 :
|
II | Passable |
| Resti M., Azzari C., Mannelli F. et al. Ten-year follow-up study of neonatal hepatitis B immunization: are booster injections indicated? Vaccine, 1997; 15(12-13): 1338-40.Note de bas de page 54 | Primovaccination :
Vaccin dérivé du plasma Hevac B
(Pasteur), dose de 5 μg; tous avaient reçu des immunoglobulines contre l'hépatite B (IgHB) à la naissance, à l'âge de 2 et 12 mois
Immunisation de rappel : ENGERIX®-B, GlaxoSmithKline, dose de 10 μg |
Italie
Étude sérologique Séroprotection : anticorps anti-HBs ≥ 10 mUI/ml |
N = 53
Enfants nés de mère antigène HBs positif dix ans après la primovaccination |
68 % (36/53) présentaient des titres d'anticorps protecteurs à l'âge de 10 ans; 26 % (14/53) avaient des niveaux d'anticorps indétectables
100 % (17/17) des participants ont atteint une séroprotection après la dose de rappel Marqueurs de l'infection par le VHB négatifs chez tous les enfants |
II-3 | Mauvaise |
| Zanetti A.R., Mariano A., Romanò L., D'Amelio R., Chironna M., Coppola R.C., Cuccia M., Mangione R., Marrone F., Negrone F.S., Parlato A., Zamparo E., Zotti C., Stroffolini T. et Mele A. Study Group. Long-term immunogenicity of hepatitis B vaccination and policy for booster: an Italian multicentre study. Lancet. 15-21 oct. 2005; 366(9494): 1379-84Note de bas de page 67 | Primovaccination : ENGERIX®-B, GlaxoSmithKline (dose de 10 μg) à l'âge de 3, 5 et 11 mois
Immunisation de rappel : ENGERIX®-B, GlaxoSmithKline (dose de 10 μg) |
Italie
Étude sérologique Séroprotection : anticorps anti-HBs ≥ 10 mUI/ml Tests sérologiques menés 2 semaines après l'administration de la dose de rappel |
N = 1 212
Enfants immunisés 10,6 ± 0,3 ans avant d'être recrutés pour l'étude |
64 % (779/1 212; IC à 95 % : 61,6; 67) étaient séropositifs; anticorps indétectables (< 1 UI/L) chez 9 % (106/1 212; IC à 95 % : 7,2; 10,3) 97 % (332/342) étaient séropositifs après une immunisation de rappel; 11 % (10/88) des sujets ayant des niveaux d'anticorps indétectables avant l'immunisation de rappel sont demeurés séronégatifs après l'administration d'une dose de rappel (7 % [6/88] avaient des niveaux d'anticorps indétectables) | II | Bonne |
| Chan P.K., Ngai K.L., Lao T.T., Wong M.C., Cheung T., Yeung A.C., Chan M.C. et Luk S.W. Response to booster doses of hepatitis B vaccine among young adults who had received neonatal vaccination. PLoS One. 8 sept. 2014;9(9):e107163.Note de bas de page 82 | Primovaccination : Vaccin dérivé du plasma à l'âge de 0, 1 et 6 mois
Dose de rappel : ENGERIX®-B, GlaxoSmithKline, dose de 20 μg |
Chine (Hong Kong)
Tests sérologiques menés 4 semaines après l'administration de la dose de rappel |
N = 212
Étudiants en soins infirmiers et en médecine inscrits ayant déjà (âge moyen : 19 ans) reçu une primovaccination durant la petite enfance |
19 % (40/212) étaient positifs aux anticorps dirigés contre l'antigène HBs(+), 80 % (170/212) étaient négatifs aux anticorps dirigés contre l'antigène HBs(-); 1 % (2/212) étaient positifs à l'antigène HBs(+)
86 % (59/69) avaient des anticorps anti-HBs ≥ 10 mUI/ml après la première dose de rappel; le reste des sujets avaient des niveaux d'anticorps anti-HBs qui variaient de 0,11 à 6,29 UI/L; après avoir reçu trois doses du vaccin de rappel, tous les étudiants présentaient des titres séroprotecteurs |
III | Passable |
| Chen Y., Lv H., Gu H., Cui F., Wang F., Yao J., Xia S. et Liang X. The effects of different dosage levels of hepatitis B vaccine as booster on anti-HBs-negative children 5-15 y after primary immunization; China, 2009-2010. Hum Vaccin Immunother. 2014;10(2):498-504 Note de bas de page 101 | Primovaccination : Vaccin recombiné (5 μg) administré à l'âge de 0, 1 et 6 mois
Dose de rappel : vaccin recombiné à trois doses de (0, 1 et 6 mois) 5 μg (Shenzhenkangtai Biotechnology Co) ou de 10 μg (Dalianhanxin Biotechnology Co) |
Chine | Sujets de 10 à 15 ans et immunisés lorsqu'ils étaient nourrissons et dont les anticorps anti-HBs < 10 UI/L
Groupe 1 : 518 sujets ayant reçu une dose de rappel de 5 μg Groupe 2 : 624 sujets ayant reçu une dose de rappel de 10 μg |
Groupe 1 :
|
III | Passable |
| Zhu C.L., Liu P., Chen T., Ni Z., Lu L.L., Huang F., Lu J., Sun Z. et Qu C. Presence of immune memory and immunity to hepatitis B virus in adults after neonatal hepatitis B vaccination. Vaccine. 13 oct. 2011;29(44): 7835-41.Note de bas de page 69 | Primovaccination : Vaccin dérivé du plasma Hep-B Vax (5 μg) administré à l'âge de 0, 1 et 6 mois
Immunisation de rappel : Dose de 10 μg du vaccin recombiné Vecon (Shenzhen Kangtai Biological Products Co.) administré à 0 et 1 mois |
Chine
Étude sérologique Séroprotection : anticorps anti-HBs ≥ 10 mUI/ml Sérologie 2 et 4 semaines et 6 mois après l'immunisation de rappel Réponse anamnestique définie par l'atteinte des niveaux séroprotecteurs deux semaines après l'administration de la dose de rappel |
N = 404
Adultes de 24 ans déjà immunisés durant la petite enfance |
30 % (121/404) présentaient des titres séroprotecteurs; 1 % (4/404) était positif pour l'AgHBs, 7 % (27/404) étaient négatifs pour l'AgHBs(-) et positifs aux anticorps dirigés contre l'antigène HBc(+)
84 % (87/103) des sujets séronégatifs présentaient des titres protecteurs 4 semaines après la première dose de rappel; 65 % (68/103) avaient une réponse anamnestique 6 % (6/103) des sujets séronégatifs sont demeurés séronégatifs 6 mois après la deuxième dose de rappel 80 % (32/40) des sujets qui ne présentaient pas de titres protecteurs lorsqu'ils avaient subi un test de dépistage à l'âge de 5 ans ont atteint une séroprotection un mois après la dose de rappel |
III | Passable |
| Yao J., Ren J., Shen L., Chen Y., Liang X., Cui F., Li Q., Jiang Z. et Wang F. The effects of booster vaccination of hepatitis B vaccine on anti-HBV surface antigen negative children 11-15 years after primary vaccination. Hum Vaccin. Oct. 2011; 7(10):1055-9.Note de bas de page 66 | Primovaccination : Vaccin recombiné (5 μg) administré à l'âge de 0, 1 et 6 mois
Dose de rappel : Trois doses de 20 μg du vaccin recombiné (NCPC GeneTech Biotechnology Pharmaceutical Co) administré à 0, 1 et 6 mois |
Chine
Étude sérologique Séropositivité définie par des anticorps contre l'antigène HBs ≥ 10 UI/L |
N = 841
Enfants de 11 à 15 ans (âge moyen : 13 ± 1,5 ans) |
47 % (393/841) étaient séropositifs au moment de leur participation à l'étude
85 % (378/444) des enfants ont développé des titres d'anticorps protecteurs après la première immunisation de rappel. Après l'administration de deux doses de rappel supplémentaires (enfants qui demeuraient séronégatifs après la première dose de rappel), 1,5 % (6/429) ont été désignés comme des non-répondants primaires et 13,5 % (57/426) ont été désignés comme des non-répondants secondaires (perte de la mémoire immunitaire) |
II | Bonne |
| Chen Y., Gu H., Cheng S., Shen L., Cui F., Wang F., Yao J., Xia S., Lv H. et Liang X. The effects of booster vaccination on combined hepatitis A and hepatitis B vaccine in both anti-HBs and anti-HAV negative children 5-15 years after hepatitis B vaccine primary immunization. Hum Vaccin Immunother. Avr. 2013;9(4):898-902.Note de bas de page 83 | Primovaccination : Vaccin recombiné (5 μg) administré à l'âge de 0, 1 et 6 mois
Dose de rappel : Trois doses du vaccin combiné contre l'hépatite A et l'hépatite B administré à 0, 1 et 6 mois |
Chine | N = 151
Sujets avec un titre d'anticorps contre le VHB < 10 UI/L immunisés 10 à 15 ans avant leur recrutement pour l'étude |
75,5 % (114/151) enfants ont atteint des titres séroprotecteurs après 1 dose et 98 % (148/151) après 3 doses d'immunisation de rappel | III | Passable |
| van der Sande M.A., Waight P.A., Mendy M., Zaman S., Kaye S., Sam O., Kahn A., Jeffries D., Akum A.A., Hall A.J., Bah E., McConkey S.J., Hainaut P. et Whittle H.C. Long-term protection against HBV chronic carriage of Gambian adolescents vaccinated in infancy and immune response in HBV booster trial in adolescence. PLoS One. 15 août 2007;2(8):e753 | Primovaccination :Note de bas de page 103 Quatre doses de 5 μg du vaccin dérivé du plasma
contre l'hépatite B (HBVvaxH; Merck, Sharpe & Dohme) administré à la naissance, à l'âge de 1, 4 et 9 mois.
Immunisation de rappel : EuvaxH |
Gambie
Séropositivité définie par des anticorps anti-HBs ≥ 10 UI/L Réponse anamnestique définie par une augmentation d'un facteur de 4 ou plus des anticorps anti-HBs dans les deux semaines suivant l'administration de la dose de rappel ou niveau d'anticorps anti-HBs ≥ 10 UI/L dans les deux semaines suivant la dose de rappel si le sujet est séronégatif avant l'immunisation de rappel 60 % ont été choisis de manière aléatoire parmi les groupes 1 et 2 pour recevoir une immunisation de rappel |
Participants à l'étude Gambia Hepatitis Intervention Study (GHIS) ayant au moins 2 doses de vaccin attestées durant la petite enfance
Groupe 1 : 492 sujets de 15 ans immunisés par 3 ou 4 doses Groupe 2 : 84 sujets de 15 ans immunisés par 1 ou 2 doses Groupe 3 : 424 sujets de 15 ans non immunisés |
Groupe 1 :
|
III | Passable |
| Saffar M.J. et Rezai M.S. Long-term antibody response and immunologic memory in children immunized with hepatitis B vaccine at birth. Indian Pediatr, 2004; 41(12): 1232-7Note de bas de page 55 | Primovaccination : Vaccin recombiné ENGERIX®-B GlaxoSmithKline, dose de 10 μg
Immunisation de rappel : Vaccin recombiné, dose de 10 μg (intra-musculaire [IM]), de 5 μg (IM) ou de 2,5 μg (voie intradermique [ID]) |
Iran
Étude de comparaison sérologique, non randomisée Sérologie 10 à 14 jours après la dose de rappel Titre d'anticorps ≥ 10 UI/L jugé protecteur; réponse anamnestique définie par une augmentation des anticorps anti-HBs ≥ 10 UI/L |
N = 453
Tous les enfants de 10 à 11 ans Enfants ayant reçu une primovaccination à la naissance, à l'âge de 1,5 et de 9 mois Groupe 1 : 57 enfants auxquels on a administré une dose de rappel par voie IM de 10 μg Groupe 2 : 52 enfants auxquels on a administré une dose de rappel par voie IM de 5 μg Groupe 3 : 56 enfants ayant reçu une dose par voie ID de 2,5 μg |
58 % (262/453) avaient des niveaux d'anticorps séroprotecteurs au départ; 18,6 % (84/453) avaient des titres d'anticorps indétectables (<2 UI/L)
Groupe 1 :
|
III | Mauvaise |
| Jafarzadeh A., Montazerifar S.J. Persistence of anti-HBs antibody and immunological memory in children vaccinated with hepatitis B vaccine at birth. J Ayub Med Coll Abbottabad. Oct.-déc. 2006;18(4):4-9Note de bas de page 60 | Primovaccination : ENGERIX®-B, GlaxoSmithKline (dose de 10 μg) à la naissance, à l'âge de 1,5 et 9 mois
Dose de rappel : ENGERIX®-B, GlaxoSmithKline (dose de 10 μg) |
Iran
Séroprotection définie par des anticorps anti-HBs ≥ 10 UI/L |
N = 146
Enfants en bonne santé de 10 à 11 ans immunisés durant la petite enfance |
48 % (70/146) des participants avaient des titres d'anticorps anti-HBs protecteurs; tous les enfants étaient négatifs pour l'AgHBs(-) et 7,5 % (11/146) étaient positifs aux anticorps contre l'antigène HBc(+)
95 % (72/76) étaient séropositifs après l'immunisation de rappel |
III | Passable |
| Katoonizadeh A., Sharafkhah M., Ostovaneh M.R., Norouzi A., Khoshbakht N., Mohamadkhani A., Eslami L., Gharravi A., Shayanrad A., Khoshnia M., Esmaili S., George J., Poustchi H. et Malekzadeh R. Immune responses to hepatitis B immunization 10-18 years after primary vaccination: a population-based cohort study. J Viral Hepat. 29 avr. 2016Note de bas de page 86 | Primovaccination : Dose de 10 μg du vaccin recombiné contre le VHB à la naissance, à l'âge de 1 et 6 mois; les immunoglobulines contre l'hépatite B (IgHB) ont été administrées immédiatement après la naissance aux enfants nés de mère antigène HBs positif
Dose de rappel : non indiquée |
Iran
Séroprotection définie par des anticorps anti-HBs ≥ 10 UI/L; réponse anamnestique définie par des anticorps anti-HBs ≥ 10 UI/L 4 semaines après l'administration de la dose de rappel |
N = 275
Groupe 1 : 25 enfants entre 10 et 11 ans Groupe 2 : 85 enfants entre 12 et 14 ans Groupe 3 : 163 enfants entre 15 et 18 ans |
Groupe 1 :
Un participant (2 %, 1/41) n'a pas présenté de réponse après avoir reçu 3 doses de rappel |
III | Passable |
| Bagheri-Jamebozorgi M., Keshavarz J., Nemati M., Mohammadi-Hossainabad S., Rezayati M.T., Nejad-Ghaderi M., Jamalizadeh A., Shokri F. et Jafarzadeh A. The persistence of anti-HBs antibody and anamnestic response 20 years after primary vaccination with recombinant hepatitis B vaccine at infancy. Hum Vaccin Immunother. 2014;10(12):3731-6.Note de bas de page 78 | Primovaccination : Vaccin ENGERIX®-B, GlaxoSmithKline (dose de 10 μg) administré à la naissance, à l'âge de 1,5 et 9 mois
Dose de rappel : Heberbiovac, Heberbiotec Co, Cuba (dose de 20 μg) |
Iran
Étude sérologique Réponse anamnestique définie par des anticorps anti-HBs ≥ 10 UI/L chez les sujets séronégatifs avant l'administration de la dose de rappel ou une augmentation par au moins un facteur de 4 du niveau d'anticorps anti-HBs chez les sujets qui étaient séropositifs avant l'immunisation de rappel Séropositivité et séroprotection définies par des concentrations d'anticorps anti-HBs ≥ 1,0 UI/L et ≥ 10 UI/L, respectivement. |
N = 300
Sujets en bonne santé qui ont reçu une primovaccination 20 ans avant d'être recrutés pour l'étude |
37 % (111/300) avaient des titres séroprotecteurs; tous les sujets étaient négatifs pour l'antigène HBs et aux anticorps contre l'antigène HBc; 12 % (35/300) étaient séronégatifs
Après la dose de rappel, 97 % (134/138) présentaient des titres séroprotecteurs; 91 % (125/138) ont produit une réponse anamnestique |
III | Mauvaise |
| Hudu S.A., Malik Y.A., Niazlin M.T., Harmal N.S., Adnan A., Alshrari A.S. et Sekawi Z. Antibody and immune memory persistence post infant hepatitis B vaccination. Patient Prefer Adherence. 27 sept. 2013;7:981-6. doi: 10.2147/PPA.S49776. eCollection 2013.Note de bas de page 81 | Primovaccination : Trois doses du vaccin recombiné administré à la naissance, à l'âge de 1 mois et de 5 mois
Dose de rappel : Vaccin recombiné contre l'hépatite B, Euvax B; Sanofi S.A., Paris (France) (20 μg) |
Malaisie | N = 402
Sujets ayant reçu trois doses (240, 60 %), deux doses (69, 17 %) ou une dose (93, 23 %) du vaccin recombiné contre l'HB 23 ans après avoir reçu la primovaccination |
63 % (252/402) avaient des niveaux d'anticorps séroprotecteurs au départ; parmi les sujets présentant des titres séroprotecteurs, 71 % (171/240) ont reçu trois doses, 68 % (47/69) ont reçu deux doses et 37 % (34/93) ont reçu une dose du vaccin contre l'hépatite A
5 % (20/402) étaient positifs aux anticorps anti-HBc(+); aucun sujet n'était positif pour l'antigène HBs(+) La plupart (85/150) des sujets séronégatifs n'ont reçu qu'une dose de vaccin 94 % (141/150) des sujets vaccinés produisaient une réponse anamnestique 4 semaines après la dose de rappel |
II | Mauvaise |
| Poovorawan Y., Chongsrisawat V., Theamboonlers A. et al. Persistence of antibodies and immune memory to hepatitis B vaccine 20 years after infant vaccination in Thailand. Vaccine, 2010; 28(3): 730-6Note de bas de page 42 | Primovaccination :
ENGERIX®-B, dose de 10 μg à la naissance, à 1, 2 et 12 mois
Immunisation de rappel : ENGERIX®-B, GlaxoSmithKline, dose de 20 μg |
Thaïlande
Étude sérologique de comparaison non randomisée Réponse anamnestique définie par un titre de l'antigène HBs ≥ 10 UI/L chez les sujets dont le titre < 3,3 UI/L ou par une augmentation par un facteur de 4 chez les sujets dont le titre ≥ 3,3 UI/L |
N = 36
Sujets ayant reçu une immunisation néonatale 20 ans avant l'étude; la plupart d'entre eux sont nés de mère antigène HBs(+) positif; la moitié aussi sont nés de mère antigène HBe(+) positif |
60,5 % (IC à 95 % : 43,4; 76) avaient un titre d'anticorps ≥ 10 UI/L et 86,8 % (IC à 95 % : 71,9; 95,6) avaient un titre d'anticorps ≥ 3,3 UI/L
4 semaines après la dose de rappel, tous les participants (IC à 95 % : 90,3; 100) ont atteint un titre d'anticorps ≥ 10 UI/L Des réponses anamnestiques similaires ont également été observées dans un second groupe de participants (n = 36) ayant reçu une dose de vaccin supplémentaire à l'âge de 5 ans |
III | Passable |
| Détails de l'étude | Résumé | |||||
|---|---|---|---|---|---|---|
| Étude | Vaccin | Modèle de l’étude | Participants | Résumé des principales conclusions et des données sur les résultats | Niveau des données probantes | Qualité |
| Inaba H. et al. Longitudinal analysis of antibody response to immunization in paediatric survivors after allogeneic haematopoietic stem cell transplantation. Br J Haematol. Janv. 2012;156(1):109-17Note de bas de page 89 | ENGERIX®-B, GlaxoSmithKline | Étude de suivi prospective à long terme
Immunisation à 12, 15 et 18 mois après une GCSH Sérologie menée pendant au moins 10 ans après une GCSH allogénique ou jusqu'à l'âge de 18 ans, selon la plus longue de ces deux périodes Séroprotection définie par des anticorps anti-HBs ≥ 10 UI/L |
N = 141 (n = 59 après la 5e année) survivants un an après avoir reçu une GCSH allogénique
âge médian au moment de la GCSH allogénique : 8,5 ans (variation entre 0,1 et 21,6 ans) âge médian au moment de l'immunisation : 9,5 ans (variation entre 1,6 et 25,1 ans) |
51,8 % des sujets bénéficiaient d'une séroprotection avant l'immunisation
77,1 % bénéficiaient d'une séroprotection 2 ans après l'immunisation 72,9 % présentaient des niveaux d'anticorps protecteurs à plus de 5 ans Les titres négatifs étaient associés de manière significative à des baisses de numérations des lymphocytes T-CD4 (p = 0,005) et à des antécédents de maladie du greffon contre l'hôte aiguë de grade 2 à 4 (p = 0,036); l'âge plus avancé au moment de l'immunisation était associé de façon marginale à des titres négatifs (p = 0,053). Des titres continuellement négatifs ont été observés chez 11 % des sujets, et une perte des niveaux d'anticorps protecteurs a été constatée chez 20 % des participants. |
III | Passable |
| Kerneis S., Launay O., Turbelin C., Batteux F., Hanslik T. et Boelle P.Y. Long-term immune responses to vaccination in HIV-infected patients: a systematic review and meta-analysis. Clin Infect Dis 2014, 58(8):1130–1139Note de bas de page 90. | Vaccin contre l'HB : dose de 10 et de 40 μg | Douze études incluses dans une méta-analyse, la durée du suivi variant entre 12 et 115 mois. | La séroprotection diminuait généralement au fil du temps : après 3 doses de 40 μg d'antigène HBs, 71 % des répondants primaires ont conservé leurs titres d'anticorps protecteurs la 1re année, 33 à 61 % la 2e année et 40 % la 5e année; la séroprotection était particulièrement faible chez les enfants nés de mère antigène HBs positif infectée par le VIH après 3 doses de 10 μg d'antigène HBs (24 % présentaient un niveau d'anticorps protecteurs après 5,5 ans).
Moins de la moitié des répondants primaires ont conservé leurs titres d'anticorps protecteurs deux ans après l'immunisation (38 % [IC à 95 % = 23 %, 54 %] chez les adultes et 61 % [27 %, 90 %] chez les enfants) et seuls 17 % (IC à 95 % : 3 %, 36 %) après cinq ans. Les calendriers de vaccination à deux doses, par rapport à ceux à dose normale, n'ont pas amélioré le maintien de la séroprotection après deux ans (respectivement 41 % [IC à 95 % : 14 à 71] et 50 % [IC à 95 % : 24 à 77 %]) Le titre d'anticorps anti-HBs protecteur diminuait plus rapidement chez les sujets dont l'anticorps anti-HBs était compris entre 10 et 100 UI/L |
II-2 | Passable | |
| Détails de l'étude | Résumé | |||||
|---|---|---|---|---|---|---|
| Étude | Vaccin | Modèle de l’étude | Participants | Résumé des principales conclusions et des données sur les résultats | Niveau des données probantes | Qualité |
| Schillie S.F., Spradling P.R. et Murphy T.V. Immune response of hepatitis B vaccine among persons with diabetes: a systematic review of the literature. Diabetes Care 2012; 35:2690 - 7Note de bas de page 92 | Vaccin recombiné (16 études) et dérivé du plasma (2 études), dose de l'antigène HBs variant de 3 à 40 μg | Examen systématique
Essai randomisé, contrôlé, publié, évalué par les pairs ou études d'observation évaluant la réponse au vaccin contre l'HB chez les personnes atteintes de diabète de type 1 ou 2 17 études comprenaient : 2 essais randomisés, contrôlés; 12 études prospectives et 3 études rétrospectives, publiées entre 1989 et 2012 |
Séroprotection contre l'infection par le virus de l'HB évaluée chez 1 764 sujets de 8,4 à 79,5 ans (633 atteints de diabète) | Les taux de séroprotection variaient de 31,3 à 100 % (médiane, 73,4 %) chez les personnes atteintes de diabète et de 35,2 à 100 % (médiane, 87,1 %) chez celles ne souffrant pas de diabète.
La proportion protégée était généralement plus élevée chez les enfants : 54,2 à 100 % (médiane, 93,9 %) chez les sujets atteints de diabète et 98 à 100 % chez les sujets non diabétiques; chez les adultes, la séroprotection médiane était plus faible chez les personnes atteintes de diabète (31,3 à 94,4 % [médiane, 88,2 %]) par rapport à celles qui n'étaient pas diabétiques (35,2 à 96,9 % [médiane, 93,6 %]). Les taux de séroprotection les plus faibles ont été déclarés chez les adultes diabétiques atteintes d'une néphropathie chronique (41,8 à 85,3 % [médiane, 60,1 %]). |
II-2 | Bonne |
| Niveau | Description |
|---|---|
| I | Données probantes provenant d’un ou de plusieurs essais cliniques comparatifs randomisés. |
| II-1 | Données probantes provenant d’un ou de plusieurs essais cliniques contrôlés sans randomisation. |
| II-2 | Données probantes obtenues dans le cadre d’études analytiques de cohortes ou cas-témoins, réalisées de préférence dans plus d’un centre ou par plus d’un groupe de recherche utilisant des indicateurs cliniques de résultats de l’efficacité d’un vaccin. |
| II-3 | Données probantes obtenues à partir de plusieurs séries chronologiques avec ou sans intervention. Les résultats spectaculaires obtenus dans un contexte non contrôlé (comme les résultats de l’introduction de la pénicilline dans les années 1940) pourraient aussi être considérés comme faisant partie de ce type de données probantes. |
| III | Opinions d’autorités respectées fondées sur des expériences cliniques, études descriptives et rapports de cas ou rapports de comités d’experts. |
| Cote de qualité | Description |
|---|---|
| Bonne | Une étude (comprenant les méta-analyses ou les examens systématiques) qui répond bien à tous les critères relatifs à la conceptionTable 5 - Note de bas de page * well. |
| Passable | Une étude (comprenant les méta-analyses ou les examens systématiques) qui ne répond pas (ou ne répond pas clairement) à au moins un des critères relatifs à la conceptionTable 5 - Note de bas de page *, mais ne comporte aucune « lacune fatale ». |
| Mauvaise | Étude (notamment les méta-analyses ou les recensions systématiques) ayant au moins une « lacune majeure » propre à la méthodologie ou une accumulation de lacunes moins importantes ne permettant pas de formuler des recommandations à partir des résultats de l’étude. |
|
|
| Catégorie | Recommandation |
|---|---|
| A | Le CCNI a conclu qu'il existait des données probantes suffisantes pour recommander l'immunisation. |
| B | Le CCNI a conclu qu'il existait des données probantes acceptables pour recommander l'immunisation. |
| C | Le CCNI conclut que les données existantes sont contradictoires et ne permettent pas de faire une recommandation pour ou contre l'immunisation; cependant, d'autres facteurs peuvent influer sur la prise de décisions. |
| D | Le CCNI a conclu qu'il existait des données probantes acceptables pour déconseiller l'immunisation. |
| E | Le CCNI a conclu qu'il existait des données probantes suffisantes pour déconseiller l'immunisation. |
| I | Le CCNI a conclu qu'il existait des données probantes insuffisantes (en quantité ou en qualité) pour formuler une recommandation; cependant, d'autres facteurs peuvent influer sur la prise de décisions. |
Liste des abréviations
- ACIP
- Advisory Committee on Immunization Practices
- Anticorps anti-HBc
- Anticorps contre l'antigène capsidique de l'HB
- Anticorps anti-HBs
- Anticorps contre l'antigène de surface de l'HB
- Antigène HBs
- Antigène de surface de l'HB
- ASPC
- Agence de la santé publique du Canada
- CCNI
- Comité consultatif national de l’immunisation
- CDC
- Centers for Disease Control and Prevention des États-Unis
- CMG
- Concentration moyenne géométrique d’anticorps
- ECMS
- Enquête canadienne sur les mesures de la santé
- EIP
- Emerging Infections Program
- ENV
- Enquête nationale sur la vaccination
- ÉT
- Écart-type
- GCI
- Guide canadien d’immunisation
- GCSH
- Greffe de cellules souches hématopoïétiques
- GTH
- Groupe de travail sur l’hépatite du CCNI
- HAHB
- Hépatites A et B
- HB
- Hépatite B
- IgHB
- Immunoglobuline contre l'hépatite B
- NHANES
- National Health and Nutrition Examination Survey des États-Unis
- OMS
- Organisation mondiale de la Santé
- PT
- Provinces et territoires, provinciaux et territoriaux
- REC
- Rapport d’étude clinique
- SAGE
- Groupe stratégique consultatif d'experts (de l’OMS)
- SSMDOC
- Système de surveillance des maladies à déclaration obligatoire du Canada
- TMG
- Titre moyen géométrique
- VHB
- Virus de l'hépatite B
- VHPB
- Viral Hepatitis Prevention Board
Remerciements
La présente déclaration a été préparée par : Dr O. Baclic (Centre de l'immunisation et des maladies respiratoires infectieuses [CIMRI], Agence de la santé publique du Canada [ASPC]), Dr Y. Choudhri (Centre de la lutte contre les maladies transmissibles et les infections [CLCMTI], ASPC), Dre S. Ismail (CIMRI, ASPC), Dre B. Henry (CCNI), Mme V. Morton (Centre des maladies infectieuses d’origine alimentaire, environnementale et zoonotique [CMIOAEZ], ASPC), et approuvée par le CCNI.
Membres du groupe de travail sur l’hépatite : Dre B. Henry (présidente), Dr J. Brophy, Dr Y. Choudhri (CLCMTI, ASPC), Dre G. Coleman, Mme M. Gale-Rowe (CLCMTI, ASPC), Dr V. Gilca (Institut national de santé publique du Québec), Mme C. Jensen (CIMRI, ASPC), Mme S. Marchant-Short, Dre A. Pham-Huy, Dre M. Salvadori, Dr R. Warrington.
Membres du CCNI : Dr I. Gemmill (président), Dre C. Quach (vice-présidente), Dre N. Dayneka, Dre S. Deeks, Dre B. Henry, Mme S. Marchant-Short, Dre M. Salvadori, Dre N. Sicard, Dre W. Vaudry, Dr D. Vinh, Dr R. Warrington.
Anciens membres du CCNI : Dre B. Warshawsky, Dre D. Kumar, Dr B. Seifert.
Représentants de liaison : Dre J. Blake (Société des obstétriciens et gynécologues du Canada), Dr J. Brophy (Association canadienne pour la recherche et l'évaluation en immunisation [CAIRE]), Dre A. Cohn (Centers for Disease Control and Prevention, États-Unis), Mme Teri Cole (Comité canadien sur l'immunisation), Dre J. Emili (Collège des médecins de famille du Canada), Dr M. Lavoie (Conseil des médecins hygiénistes en chef), Dre C. Mah (Association canadienne de santé publique), Dre D. Moore (Société canadienne de pédiatrie), Dre A. Pham-Huy (Association pour la microbiologie médicale et l'infectiologie [AMMI] Canada).
Anciens représentants de liaison : Dre A. Mawle (Centers for Disease Control and Prevention, États-Unis), Dr S. Rechner (Collège des médecins de famille du Canada), Mme E. Sartison (Comité canadien sur l'immunisation).
Représentants d'office : Dre (Capc) K. Barnes (Défense nationale et les Forces armées canadiennes), Mme G. Charos (CIMRI, ASPC), Dre G. Coleman (Direction des produits biologiques et des thérapies génétiques [DPBTG], Santé Canada [SC]), Dr J. Gallivan (Direction des produits de santé commercialisés [DPSC], SC), Mme J. Pennock (CIMRI, ASPC), Dr T. Wong (Direction générale de la santé des Premières nations et des Inuits [DGSPNI], SC).
Anciens représentants d’office : Dr (Lcol) P. Eagan (Défense nationale et les Forces armées canadiennes), Dre A. Klein (Direction des produits biologiques et des thérapies génétiques, Santé Canada), Dre B. Law CIMRI, ASPC), Dre B. Raymond (ASPC/Comité canadien sur l'immunisation), Dre E. Taylor (Direction des produits de santé commercialisés, Santé Canada).