PICRA 2019 : Résultats intégrés
Sur cette page
- Activités du PICRA
- Faits saillants de 2019
- Résultats intégrés sur l'utilisation des antimicrobiens
- Résultats intégrés sur l'utilisation des antimicrobiens et la résistance aux antimicrobiens - Données de la ferme
- Résultats intégrés sur la résistance aux antimicrobiens
- Glossaire
Informations supplémentaires
cipars-picra@phac-aspc.gc.ca
PICRA 2019 : Sommaire
PICRA 2019 : Figures et tableaux
PICRA 2019 : Design et méthodes
Activités du PICRA
Le Programme intégré canadien de surveillance de la résistance aux antimicrobiens (PICRA) réunit diverses sources de données d’une manière robuste et fiable.
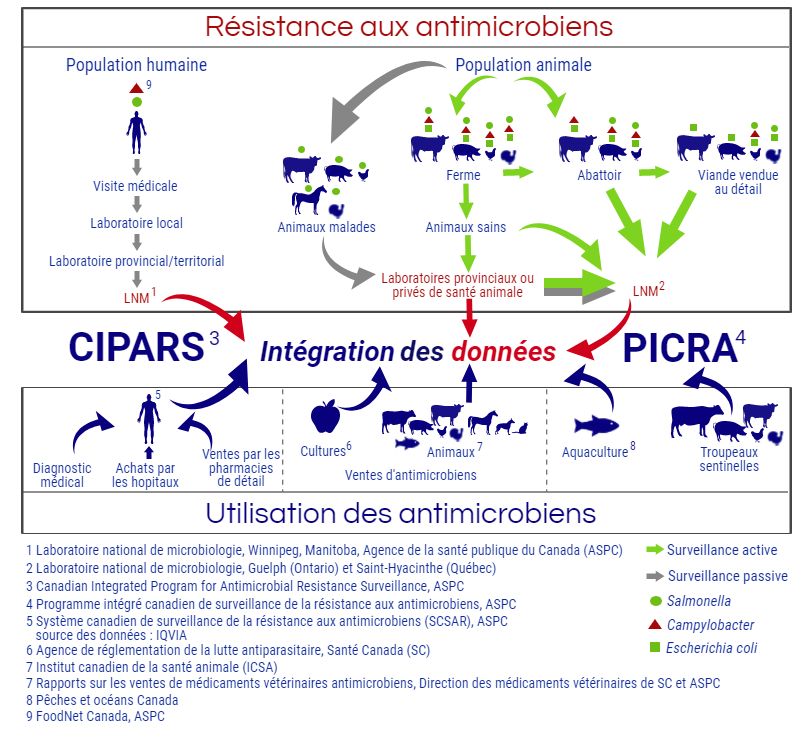
Diagramme 1 - Équivalent textuel
Le PICRA réunit des données sur la résistance aux antimicrobiens et l'utilisation des antimicrobiens provenant de diverses activités chez les humains, les animaux et les cultures.
Le PICRA exerce des activités de surveillance passive et active chez les humains et les animaux (y compris les bovins, les porcs, les poulets, les dindons et les chevaux). Les données de surveillance de la résistance humaine aux antimicrobiens sont obtenues à partir de cas humains d'infection à Salmonella et Campylobacter. Les données de surveillance de la résistance aux antimicrobiens chez les animaux comprennent des données provenant d’échantillons d'animaux d’élevage en santé échantillonnés à la ferme et à l’abattoir, ainsi que des données provenant de viandes vendues au détail. Le PICRA exerce également des activités de surveillance pour l'utilisation d'antimicrobiens à la ferme par les fermes sentinelles, et rapporte des données sur les ventes et la distribution d'antimicrobiens à partir de plusieurs sources de données. Les analystes du PICRA et les épidémiologistes analysent et rapportent les résultats de la résistance aux antimicrobiens et de l'utilisation des antimicrobiens pour chaque année de surveillance, y compris l'intégration des résultats des diverses activités de surveillance et sources de données.
Les sources de données comprennent :
- Le Laboratoire national de microbiologie (LNM), Agence de la santé publique du Canada (ASPC) à Winnipeg, Manitoba (1), à Guelph, Ontario (2) et à Saint-Hyacinthe, Québec (2)
- Canadian Integrated Program for Antimicrobial Resistance Surveillance, ASPC (3), Programme intégré canadien de surveillance de la résistance aux antimicrobiens, ASPC (4)
- Le Système canadien de surveillance de la résistance aux antimicrobiens (SCSRA), ASPC. Source des données : IQVIA (5)
- Agence de réglementation de la lutte antiparasitaire de Santé Canada (SC) (6)
- Institut canadien de la santé animale (ICSA) (7)
- Rapports sur les ventes de médicaments vétérinaires antimicrobiens, Direction des médicaments vétérinaires de SC et ASPC (7)
- Pêches et Océans Canada (8)
- FoodNet Canada, ASPC (9)
Faits saillants de 2019
Résultats intégrés sur l’utilisation des antimicrobiens
- Les ventes d'antimicrobiens (en kg) ont diminué de 10 % entre 2018 et 2019.
- Les ventes associées aux animaux de production (bétail, aquaculture, chevaux) ont diminué de 11 % (kg) et ont diminué de 12 % (après ajustement pour tenir compte de la biomasse en mg/PCU).
- Comparativement à 2018, les ventes destinées à une utilisation chez les porcs, la volaille et en aquaculture ont diminué; les ventes destinées à une utilisation chez les bovins, les chevaux, les chats et les chiens, et les petits ruminants ont augmenté en 2019.
Résultats intégrés sur l’utilisation des antimicrobiens et la résistance aux antimicrobiens
- Des données intégrées de surveillance à la ferme sont présentées pour les poulets de chair, les porcs en croissance-finition et les dindons.
- La surveillance à la ferme a révélé que l’UAM est restée stable ou a diminué parmi ces espèces animales.
- Pour les porcs en en croissance-finition, les données indiquent le signalement de l’utilisation d’antimicrobiens importants sur le plan médical pour la stimulation de la croissance (pour une ferme sentinelle en 2019).
- Pour les dindons, le nombre d’isolats de Campylobacter résistants à ≥ 1 classe d’antimicrobiens a diminué.
- Le nombre d’isolats de Salmonella résistants à ≥ 1 classe d’antimicrobiens provenant de poulets de chair a augmenté.
- Le pourcentage d’isolats résistants à ≥ 3 classes d’antimicrobiens est resté relativement inchangé pour ces espèces animales, hormis une diminution des Salmonella résistantes à ≥ 3 classes d’antimicrobiens chez les dindons.
- La mortalité parmi les troupeaux est restée inchangée.
Résultats intégrés sur la résistance aux antimicrobiens
Nouveauté: Salmonella Enteritidis et la résistance aux quinolones chez les humains
Salmonella Enteritidis, qui est le sérotype le plus courant chez les personnes malades, est en baisse.
Toutefois, la résistance à l’acide nalidixique des isolats de S. Enteritidis a augmenté.
La résistance à l’acide nalidixique de S. Enteritidis est plus courante dans les cas de voyages hors du Canada.
Détection de Salmonella Enteritidis résistants aux quinolones chez des poulets
Avant 2018, la résistance aux quinolones (acide nalidixique) a été observée une seule fois parmi les isolats de S. Enteritidis d'origine agroalimentaire.
Bien que les chiffres soient encore bas, de la résistance à l’acide nalidixique a été détectée parmi des isolats de S. Enteritidis provenant de poulets et de viande de poulet et parmi plusieurs provinces et composantes de surveillance en 2018 et 2019
Salmonella résistants à 6 ou 7 classes d’antimicrobiens
Bien que les nombres soient encore bas, nous continuons de constater une augmentation des isolats de Salmonella d’origine humaine, animale et alimentaire qui sont résistants à 6 ou 7 des 7 classes d’antimicrobiens testés en 2019.
Salmonella Heidelberg chez les bovins
En 2019, il s'agissait notamment de Salmonella Heidelberg résistants aux antimicrobiens provenant de bovins en santé; cela a été observée pour la première fois.
Résultats intégrés sur l'utilisation des antimicrobiens
Catégories des antimicrobiens
Les antimicrobiens sont regroupés en des catégories fondées sur leur importance pour la médecine humaine et les conséquences potentielles de la résistance à ces médicaments :
- Catégorie I : Très haute importance
Exemples : céphalosporines de 3e génération, fluoroquinolones - Catégorie II : Haute importance
Exemple : macrolides - Catégorie III : Importance moyenne
Exemples : tétracyclines, sulfamides - Catégorie IV : Faible importance
Exemples : ionophores, flavophospholipides
Les antimicrobiens médicalement importants incluent les Catégories I à III. On a retiré des rapports intégrés sur l'utilisation des antimicrobiens, les antimicrobiens de faible importance (catégorie IV, à l'exception des flavophospholipides). Ces données seront fournies dans d'autres produits de communication du PICRA.
Système de classement défini par la Direction des médicaments vétérinaires de Santé Canada. Les anticoccidiens de synthèse sont considérés comme des antimicrobiens non catégorisés.
Utilisation des antimicrobiens : Comparaison entre les humains, les animaux et les cultures
Nouveauté : Le système de Rapports sur les ventes de médicaments vétérinaires antimicrobiens (RVMVA)
- Les nouveaux règlements de Santé Canada exigent que les fabricants, les importateurs et les préparateurs de médicaments déclarent les ventes annuelles d’antimicrobiens importants sur le plan médical qui sont destinés à être utilisés chez les animaux.
- Pour répondre à ces exigences, l’Agence de la santé publique du Canada et Santé Canada ont conçu et développé l’outil de déclaration en ligne RVMVA.
- Le système de RVMVA recueille les données sur les quantités d’antimicrobiens vendus ou préparés par espèce animale et par province ou par territoire.
- La majorité des données sur les ventes figurant dans ce rapport comprennent des renseignements provenant des fabricants et des importateurs et n’incluent pas les données des préparateurs de médicaments.
Ventes globales de 2019
- Diminution de 12 % (depuis 2018)
- Antimicrobiens vendus (les kg ajustés en fonction de la biomasse) pour les animaux de production (baisse des ventes de tétracyclines, de sulfamides, de pénicillines et de macrolides).
- Près de 1,4 fois
- Plus d’antimicrobiens ont été vendus pour être utilisés chez les animaux de production que chez les humains, après ajustement en fonction de la biomasse.
- Près de 23 fois
- Plus d’animaux que de personnes au Canada.
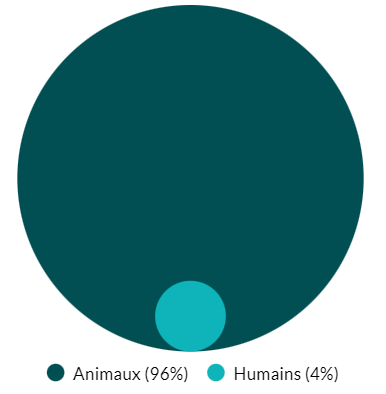
Diagramme 2 - Équivalent textuel
| Population | Proportion (%) |
|---|---|
| Animaux | 96 % |
| Humains | 4 % |
La population animale est sous-estimée, car les poissons ne sont pas inclus.
- De tous les antimicrobiens vendus en 2019 :
- 78 % étaient destinés aux animaux de production
- 22 % étaient destinés aux humains
- <1 % était destiné aux chats et aux chiens
- <1 % était destiné aux cultures
- 1 % des antimicrobiens vendus chez les animaux appartenaient à la catégorie I.
- Les tétracyclines représentaient environ 51 % des ventes totales.
Ventes d’antimicrobiens (2019) par espèce*
(comparaison entre 2018 et 2019)
- Volaille
- Les classes les plus vendues: NSI**, pénicillines et tétracyclines
- Diminution de 9 % en kg vendus
- De faibles quantités (<1 kg) de fluoroquinolones et de céphalosporines de 3e génération ont été fabriquées ou préparées pour être utilisées chez les volailles entre 2018 et 2019
- Bovins de boucherie
- Les classes les plus vendues: tétracyclines, macrolides et amphénicols
- Augmentation de 13 % en kg vendus
- Augmentation de 6 % (74 kg) des ventes d’antimicrobiens de catégorie I
- Porcs
- Les classes les plus vendues : tétracyclines, macrolides et pénicillines
- Diminution de 21 % en kg vendus
- Diminution de 24 % (123 kg) des ventes d’antimicrobiens de catégorie I
- Bovins laitiers
- Les classes les plus vendues : tétracyclines, combinaison de diaminopyrimidine-sulfamide et pénicillines
- Augmentation de 15 % en kg vendus
- Diminution de 25 % (112 kg) des ventes d’antimicrobiens de catégorie I
- Aquaculture
- Les seuls antimicrobiens vendus en 2019 étaient des tétracyclines et des amphénicols
- Diminution de 29 % en kg vendus
- Chats et chiens
- Les classes les plus vendues : pénicillines, céphalosporines de 1re ou 2e génération et inhibiteurs de bêta-lactamase
- Augmentation de 17 % en kg vendus
- Augmentation de 24 % (711 kg) des ventes d’antimicrobiens de catégorie I
*Pour de plus amples renseignements sur les veaux de boucherie, les chevaux, les petits ruminants et autres animaux, veuillez vous reporter aux Figures et tableaux du PICRA pour l’année 2019.
**NSI = Non signalées de manière indépendante.
Comparaison entre les espèces
La majorité (kg) des antimicrobiens vendus étaient destinés à être utilisés pour les porcs, les bovins et la volaille.
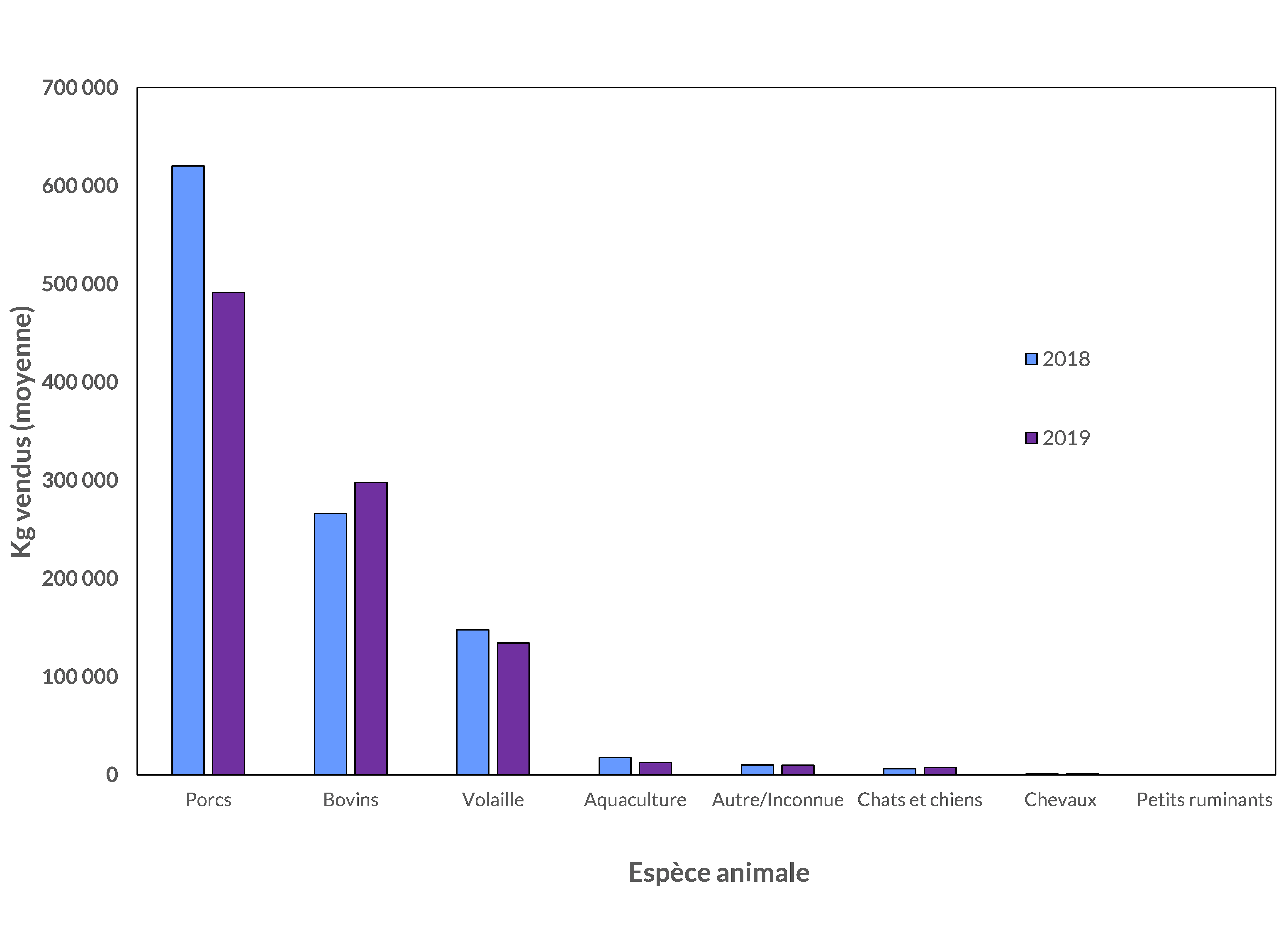
Figure 1 - Équivalent textuel
| Espèce animale | 2018 Moyenne des kg | 2019 Moyenne des kg |
|---|---|---|
| Aquaculture | 17 596 | 12 507 |
| Bovins de boucherie | 233 488 | 264 673 |
| Chats et chiens | 6 373 | 7 526 |
| Bovins laitiers | 16 511 | 18 964 |
| Chevaux | 1 236 | 1 504 |
| Autre/Inconnue | 10 274 | 10 093 |
| Porcs | 620 355 | 491 640 |
| Volaille | 147 853 | 134 351 |
| Petits ruminants | 43 | 68 |
| Veaux de boucherie | 16 344 | 14 173 |
Si l’on tient compte du nombre d’animaux et de leur poids (c’est-à-dire en mg/PCU, où 1 PCU = 1 kg d’animal), la majorité des ventes en 2019 étaient destinées aux porcs, à la volaille, aux bovins et à l’aquaculture.
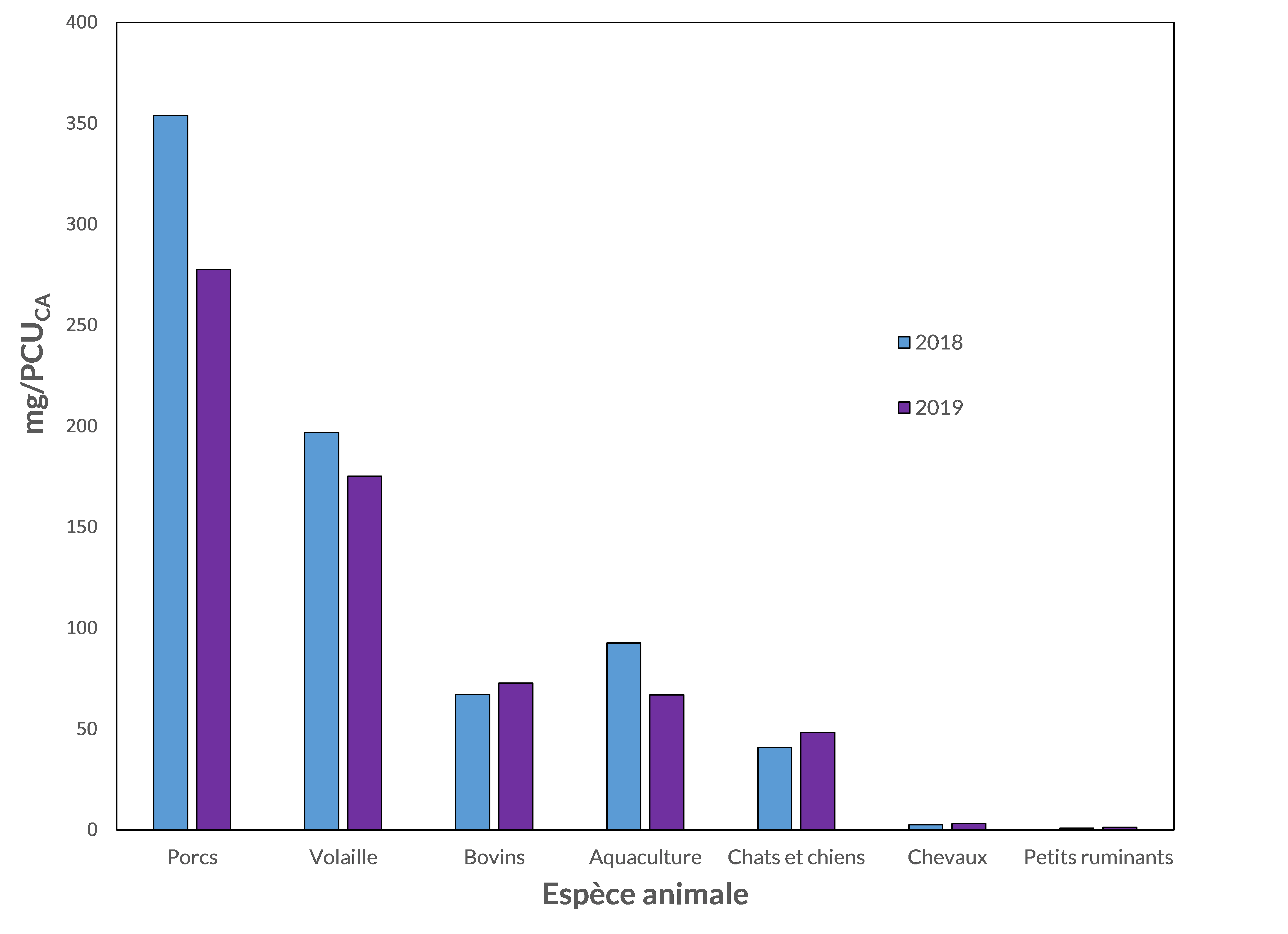
Figure 2 - Équivalent textuel
| Espèce animale | 2018 mg/PCUCA | 2019 mg/PCUCA |
|---|---|---|
| Aquaculture | 93 | 67 |
| Bovins | 67 | 73 |
| Chats et chiens | 41 | 48 |
| Chevaux | 2,57 | 3 |
| Porcs | 354 | 278 |
| Volaille | 197 | 175 |
| Petits ruminants | 0,79 | 1 |
Les quantités totales d’antimicrobiens vendues par les fabricants et les importateurs pour être utilisées chez les animaux de production ont diminué de 11 % entre 2018 et 2019. Lorsque les quantités totales ont été ajustées en fonction de la biomasse (mg/PCU), on observe que la diminution était de 12 % par rapport à 2018.
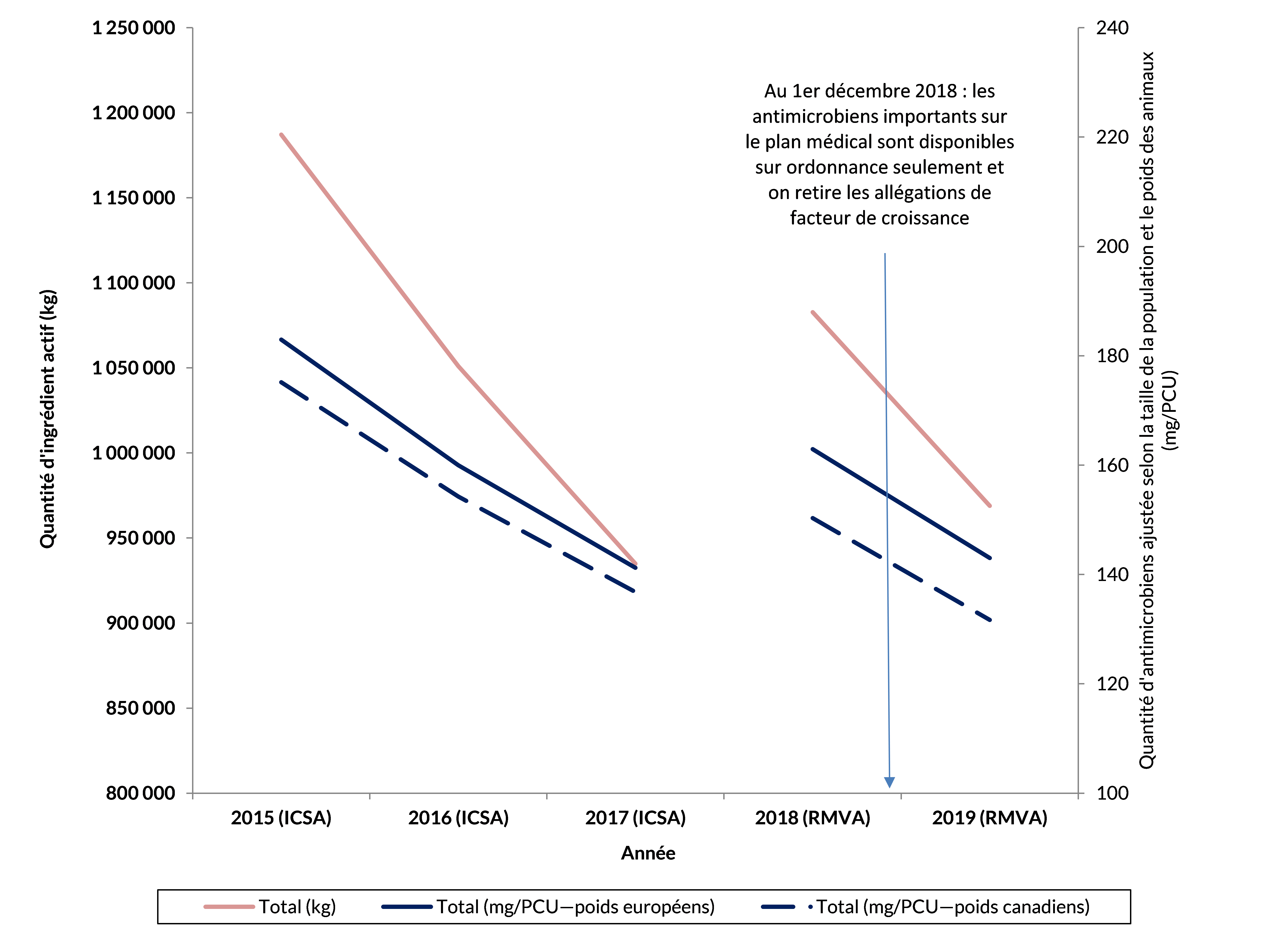
Figure 3 - Équivalent textuel
| Année | Total (kg) | Total (mg/PCU poids européens) | Total (mg/PCU poids canadiens) |
|---|---|---|---|
| 2015 (ICSA) | 1 187 136 | 183 | 175 |
| 2016 (ICSA) | 1 051 010 | 160 | 154 |
| 2017 (ICSA) | 934 873 | 141 | 137 |
| 2018 (RMVA) | 1 082 768 | 163 | 150 |
| 2019 (RMVA) | 968 985 | 143 | 132 |
Les données de 2015 à 2017 ont été fournies volontairement par l’Institut canadien de la santé animale (ICSA) et découlent des renseignements mis à disposition par ses membres. Les données pour 2018 et 2019 proviennent du RVMVA et incluent les importateurs, ainsi que plus de fabricants que l’ICSA. Il convient de faire preuve de prudence lors de la comparaison des renseignements entre ces deux ensembles de données.
Le Canada se classe au 8e rang (par rapport à l’Europe) pour ce qui est des quantités d’antimicrobiens vendues (mg/PCU).
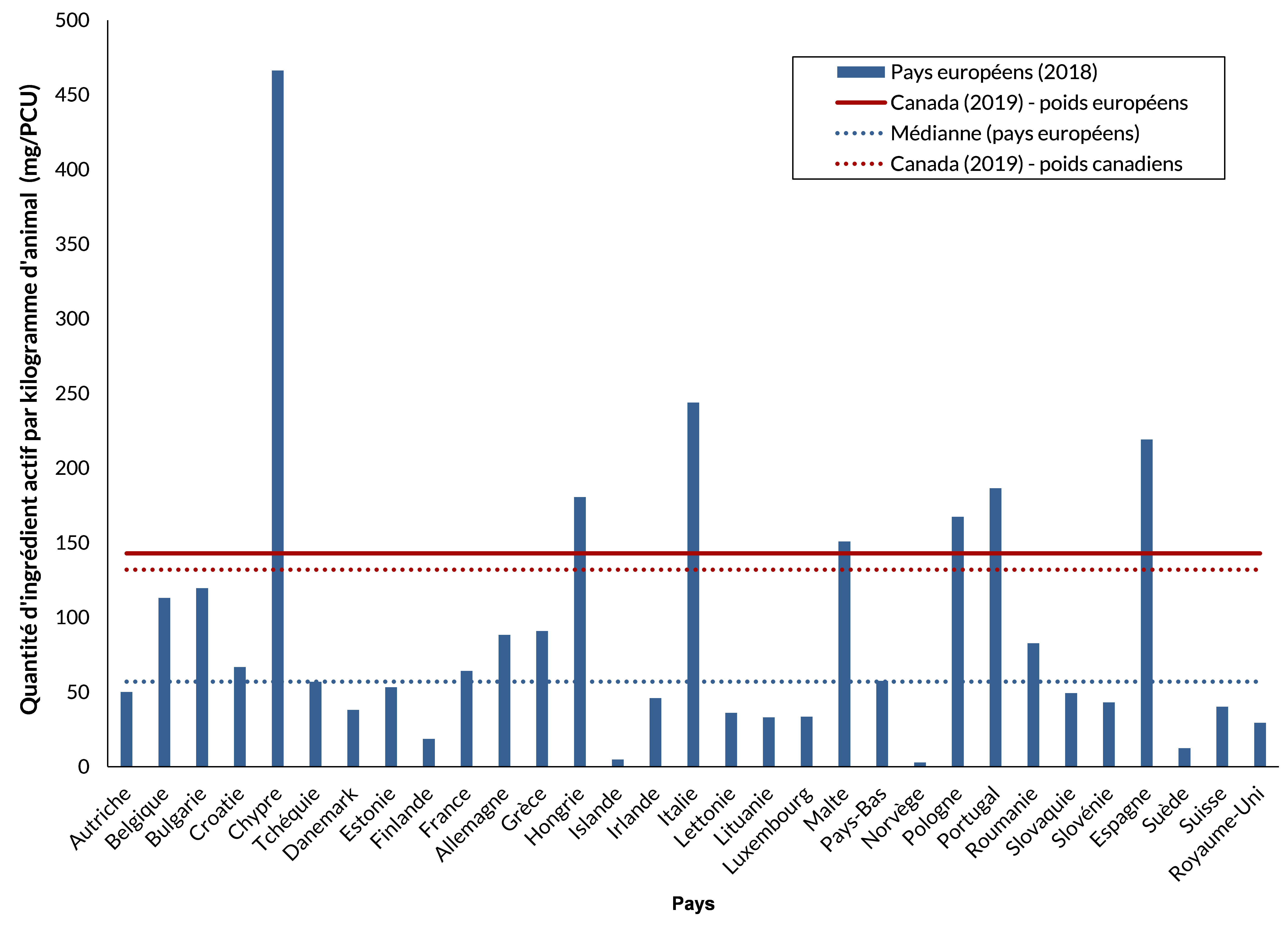
Figure 4 - Équivalent textuel
| Pays européens (2018) | mg/PCU | Canada (2019) poids européens | Médianne (pays européens) | Canada (2019) poids canadiens |
|---|---|---|---|---|
| Autriche | 50 | 143 | 57 | 132 |
| Belgique | 113 | 143 | 57 | 132 |
| Bulgarie | 120 | 143 | 57 | 132 |
| Croatie | 67 | 143 | 57 | 132 |
| Chypre | 466 | 143 | 57 | 132 |
| Tchéquie | 57 | 143 | 57 | 132 |
| Danemark | 38 | 143 | 57 | 132 |
| Estonie | 53 | 143 | 57 | 132 |
| Finlande | 19 | 143 | 57 | 132 |
| France | 64 | 143 | 57 | 132 |
| Allemagne | 88 | 143 | 57 | 132 |
| Grèce | 91 | 143 | 57 | 132 |
| Hongrie | 181 | 143 | 57 | 132 |
| Islande | 5 | 143 | 57 | 132 |
| Irlande | 46 | 143 | 57 | 132 |
| Italie | 244 | 143 | 57 | 132 |
| Lettonie | 36 | 143 | 57 | 132 |
| Lituanie | 33 | 143 | 57 | 132 |
| Luxembourg | 34 | 143 | 57 | 132 |
| Malte | 151 | 143 | 57 | 132 |
| Pays-Bas | 58 | 143 | 57 | 132 |
| Norvège | 3 | 143 | 57 | 132 |
| Pologne | 167 | 143 | 57 | 132 |
| Portugal | 187 | 143 | 57 | 132 |
| Roumanie | 83 | 143 | 57 | 132 |
| Slovaquie | 49 | 143 | 57 | 132 |
| Slovénie | 43 | 143 | 57 | 132 |
| Espagne | 219 | 143 | 57 | 132 |
| Suède | 13 | 143 | 57 | 132 |
| Suisse | 40 | 143 | 57 | 132 |
| Royaume-Uni | 30 | 143 | 57 | 132 |
Cette figure présume que les données sont comparables entre les pays.
Le dénominateur de l’ESVAC n’inclut pas les vaches de boucherie, alors qu’au Canada, elles représentent une population importante et sont incluses.
PCU = unité corrigée de la population.
Sources des données : Agence de réglementation de la lutte antiparasitaire de Santé Canada, Agriculture et Agroalimentaire Canada, données d’origine humaine d'IQVIA fournies par les pharmacies et les hôpitaux, Canada Équestre, Canfax, ESVAC, Institut canadien de la santé animale (ICSA), Les producteurs de poulet du Canada, Les producteurs d’œufs d’incubation du Canada, Les producteurs d'oeufs du Canada, Pêches et Océans Canada, RVMVA, Statistique Canada et le Système canadien de surveillance de la résistance aux antimicrobiens.
Bien que des antimicrobiens semblables aient été autorisés pour une utilisation chez les humains et les animaux, certaines classes d’antimicrobiens étaient vendues pour être utilisées plus souvent chez les humains que chez les animaux et inversement.
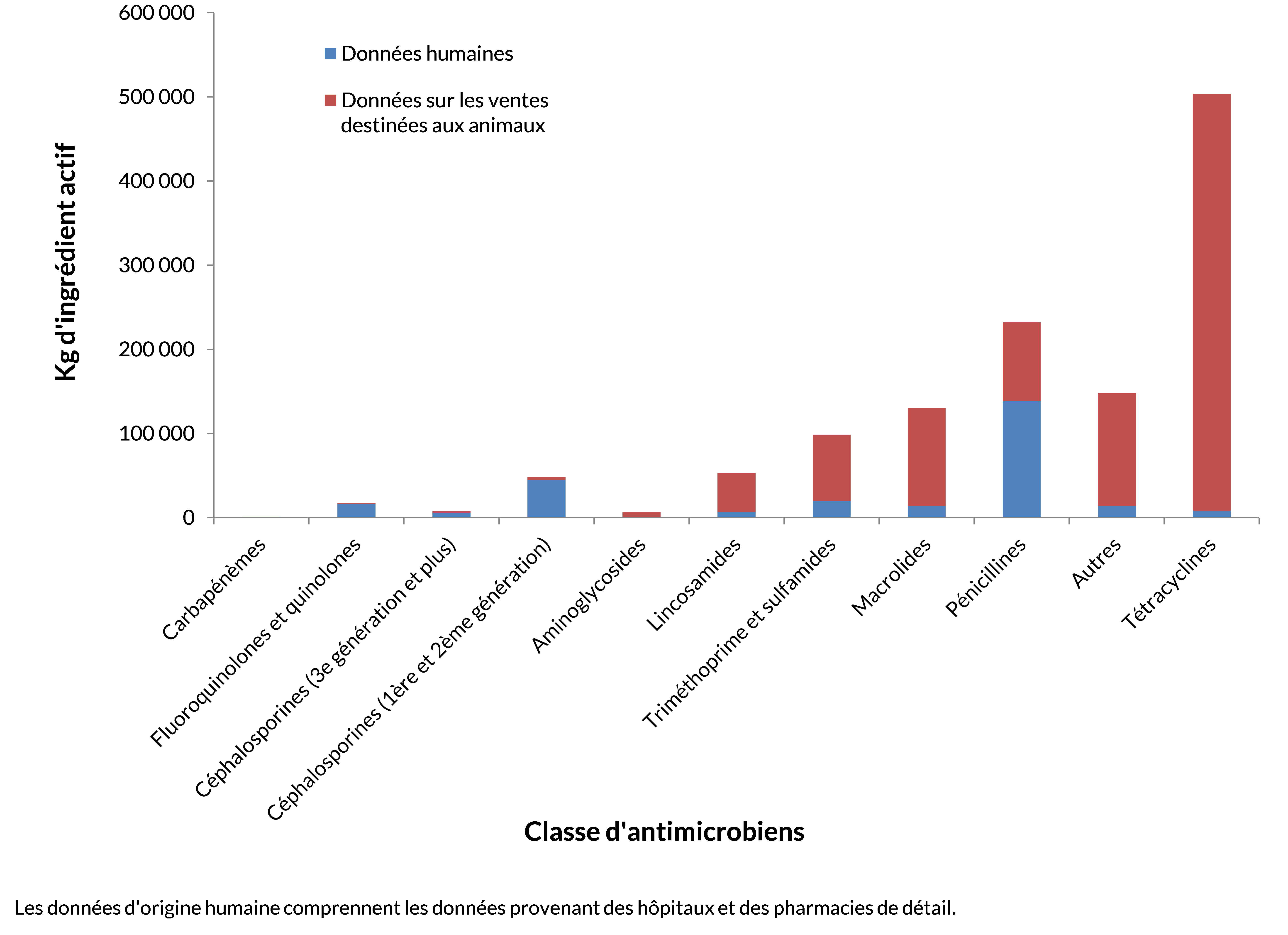
Figure 5 - Équivalent textuel
| Classe d'antimicrobiens | Données humaines (Kg d’ingrédient actif) | Données sur les ventes destinées aux animaux (Kg d’ingrédient actif) |
|---|---|---|
| Carbapénèmes | 1 096 | 0 |
| Fluoroquinolones et quinolones | 16 577 | 937 |
| Céphalosporines (3e génération et plus) | 5 864 | 1 676 |
| Céphalosporines (1ère et 2ème génération) | 44 894 | 3 234 |
| Aminoglycosides | 168 | 6 487 |
| Lincosamides | 6 514 | 46 390 |
| Triméthoprime et sulfamides | 19 827 | 78 962 |
| Macrolides | 14 074 | 115 822 |
| Pénicillines | 138 391 | 93 843 |
| Autres | 14 108 | 134 044 |
| Tétracyclines | 8 328 | 495 116 |
Remarques :
- Les céphalosporines sont des antimicrobiens bêta-lactamines, mais nous les affichons séparément à des fins de visualisation.
- Les autres antimicrobiens destinés aux humains comprennent : la bacitracine, le ceftobiprole médocaril, le ceftolozane-tazobactam, le chloramphénicol, la colistine, la daptomycine, la fidaxomicine, la fosfomycine, l’acide fusidique, le linézolide, le métronidazole, la nitrofurantoïne et la vancomycine.
- Les autres produits destinés aux animaux comprennent : les aminocoumarines, les aminocyclitols, les amphénicols, les polypeptides cycliques, l’acide fusidique, les glycopeptides, les nitrofurantoïnes, les nitroimidazoles, les orthosomycines, les dérivés de l’acide phosphonique, les pleuromutilines, les polymyxines, les acides pseudomoniques, les streptogramines et les agents thérapeutiques pour le traitement de la tuberculose.
Utilisation des antimicrobiens : Comparaison des données de la ferme
Comparaison entre les classes d'antimicrobiens*
Il existe des différences importantes dans les types et les quantités relatives d’antimicrobiens signalés pour l’utilisation entre les espèces animales destinées à l’alimentation, c’est pourquoi nous avons besoin d’une surveillance continue des espèces animales destinées à l’alimentation.
*Les pourcentages sont basés sur le nombre total de kilogrammes d'ingrédients actifs qui étaient destinés à être utilisés par une espèce hôte.
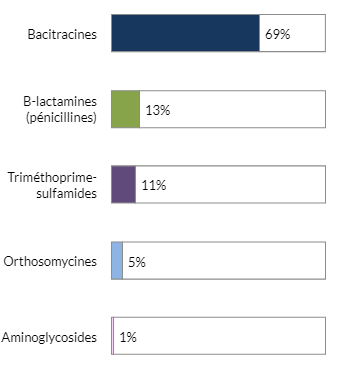
Figure 6 - Équivalent textuel
| poulets de chair | |
|---|---|
| Classe d'antimicrobiens | % |
| Bacitracines | 69 % |
| B-lactamines (pénicillines) | 13 % |
| Triméthoprime-sulfamides | 11 % |
| Orthosomycines | 5 % |
| Aminoglycosides | 1 % |
Non indiqués : flavophospholipides (<1 %), lincosamides-aminocyclitols (<1 %), streptogramines (1 %).
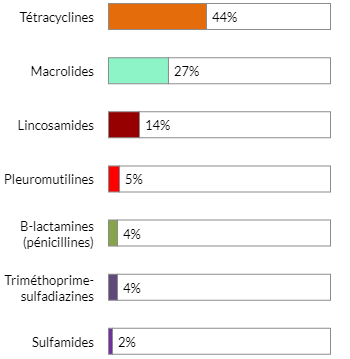
Figure 7 - Équivalent textuel
| porcs en croissance-finition | |
|---|---|
| Classe d'antimicrobiens | % |
| Tétracyclines | 44 % |
| Macrolides | 27 % |
| Lincosamides | 14 % |
| Pleuromutilines | 5 % |
| B-lactamines (pénicillines) | 4 % |
| Triméthoprime-sulfadiazines | 4 % |
| Sulfamides | 2 % |
Non indiqués : céphalosporines de 3e génération (< 1%), streptogramines (1%), flavophospholipides (< 1%).
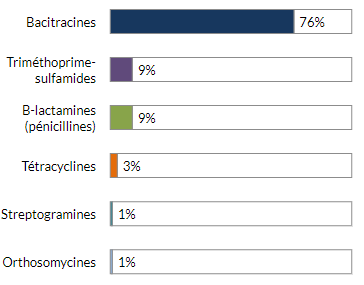
Figure 8 - Équivalent textuel
| dindons | |
|---|---|
| Classe d'antimicrobiens | % |
| Bacitracines | 76 % |
| Triméthoprime-sulfamides | 9 % |
| B-lactamines (pénicillines) | 9 % |
| Tétracyclines | 3 % |
| Streptogramines | 1 % |
| Orthosomycines | 1 % |
Non indiqués : fluoroquinolones (< 1%), aminoglycosides (< 1%), flavophospholipides (< 1%).
Résultats intégrés sur l’utilisation des antimicrobiens et sur la résistance aux antimicrobiens - Données de la ferme
Dans cette section, nous mettons en évidence les résultats intégrés sur l'utilisation et la résistance aux antimicrobiens à la ferme pour 2019 :
- Raisons de l'utilisation des antimicrobiens
- Poulets de chair
- Porcs en croissance-finition
- Dindons
Raisons de l'utilisation des antimicrobiens
- En majeure partie, les antimicrobiens étaient utilisés pour la prévention des maladies lorsque la dose, le nombre ou le poids des animaux étaient ajustés (≥ 74 %).
- Pour les 3 espèces, les antimicrobiens étaient principalement utilisés pour la prévention des maladies entériques.
- Les antimicrobiens ont été principalement administrés dans les aliments (≥ 90 %).
- La proportion d’antimicrobiens utilisés pour le traitement des maladies a augmenté parmi les 3 espèces.
- Volaille : Cette utilisation était principalement destinée aux maladies des jeunes poussins/dindonneaux et aux maladies respiratoires (traitement par la voie des aliments et par l’eau).
- Porcs en croissance-finition : Cette utilisation était principalement destinée à traiter les maladies respiratoires (traitement administré dans l’eau).
- En 2019, les bambermycines ont été utilisées pour la prévention de l’entérite nécrotique dans 4 à 5 % des troupeaux sentinelles de volailles. Le taux d’inclusion déclaré dans les aliments pour animaux était stable et similaire aux allégations concernant la stimulation de la croissance qui figuraient sur l’étiquette.
- Porcs en croissance-finition : L'utilisation d’antimicrobiens importants sur le plan médical pour la stimulation de la croissance est encore déclarée; toutefois, la quantité utilisée a nettement diminué par rapport à 2018 (1 ferme d'élevage).
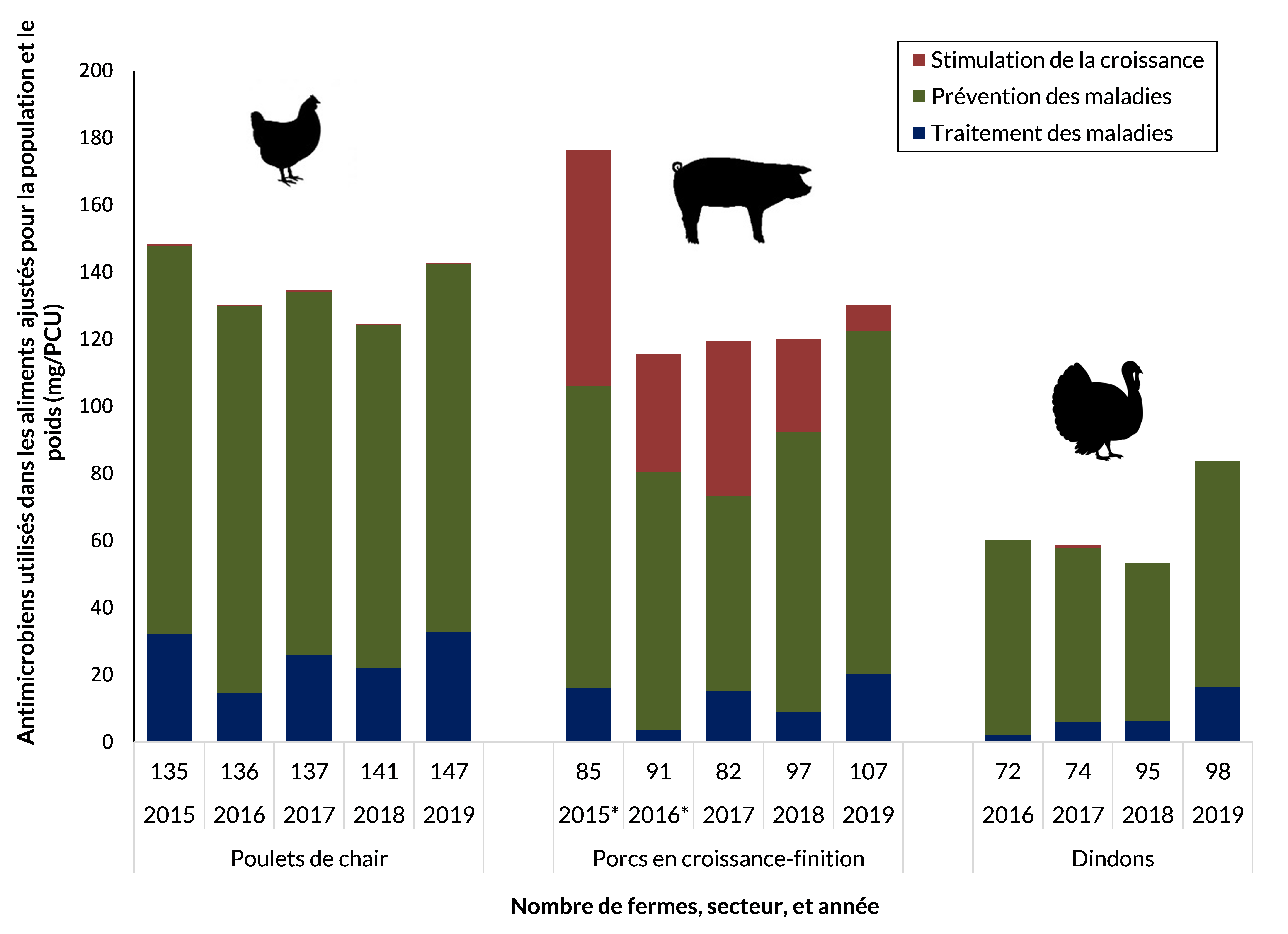
Figure 9 - Équivalent textuel
| Espèce | Poulets de chair | Porcs en croissance-finition | Dindons | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Année | 2015 | 2016 | 2017 | 2018 | 2019 | 2015* | 2016* | 2017 | 2018 | 2019 | 2016 | 2017 | 2018 | 2019 |
| Nombre de fermes | 135 | 136 | 137 | 141 | 147 | 85 | 91 | 82 | 97 | 107 | 72 | 74 | 95 | 98 |
| Prévention des maladies | 32 | 15 | 26 | 22 | 33 | 16 | 4 | 15 | 9 | 20 | 2 | 6 | 6 | 16 |
| Stimulation de la croissance | 115 | 115 | 108 | 102 | 110 | 90 | 77 | 58 | 84 | 102 | 58 | 52 | 47 | 67 |
| Prévention des maladies | 1 | 0 | 0 | 0 | 0 | 70 | 35 | 46 | 28 | 8 | 0 | 1 | 0 | 0 |
*Porcs en croissance-finition : Les données de 2015 et 2016 concernaient l'utilisation d'antimicrobiens dans les aliments seulement.
Poulets de chair
- À l’échelle nationale, l’utilisation des antimicrobiens (UAM)* a diminué en 2019** par rapport à 2018.
- Augmentation notable des isolats de Salmonella résistants à ≥ 1 classe d’antimicrobiens testés.
- Aucun changement notable de la résistance aux antimicrobiens (RAM) à la ceftriaxone ou à l’acide nalidixique, mais on observe une augmentation de la résistance à la ciprofloxacine.
- La résistance à ≥ 3 classes d’antimicrobiens variait.
- L’UAM a diminué alors que la RAM variait; cependant, la mortalité dans les troupeaux est demeurée inchangée.
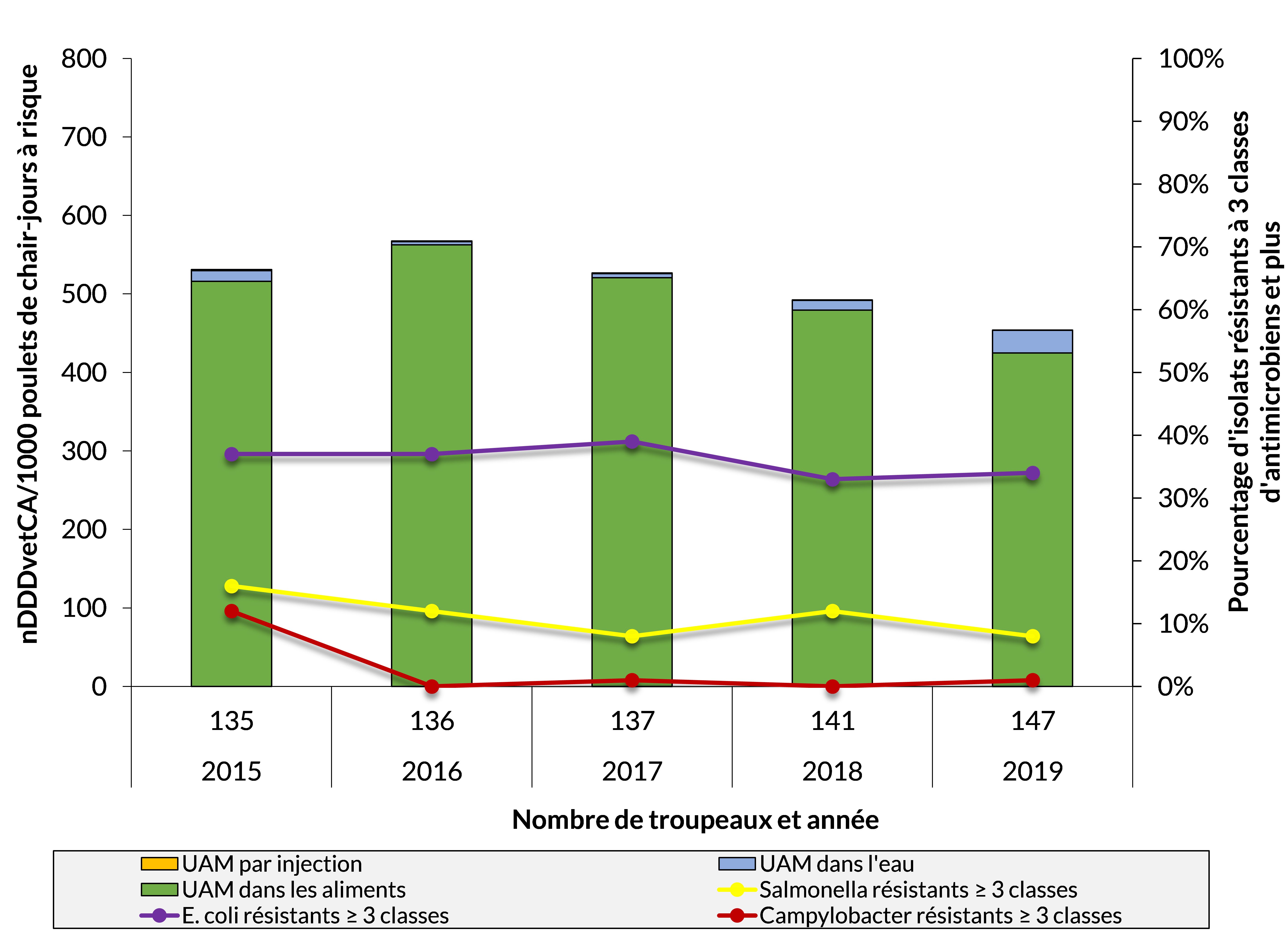
Figure 10 - Équivalent textuel
| Année | 2015 | 2016 | 2017 | 2018 | 2019 |
|---|---|---|---|---|---|
| Nombre de troupeaux | 135 | 136 | 137 | 141 | 147 |
| UAM dans les aliments | 516 | 563 | 521 | 479 | 425 |
| UAM dans l’eau | 14 | 4 | 5 | 13 | 29 |
| UAM par injection | 1 | 1 | 1 | 1 | 0 |
| Salmonella résistants to ≥ 3 classes | 16 % | 12 % | 8 % | 12 % | 8 % |
| E. coli résistant to ≥ 3 classes | 37 % | 37 % | 39 % | 33 % | 34 % |
| Campylobacter résistant to ≥ 3 classes | 12 % | 0 % | 1 % | 0 % | 1 % |
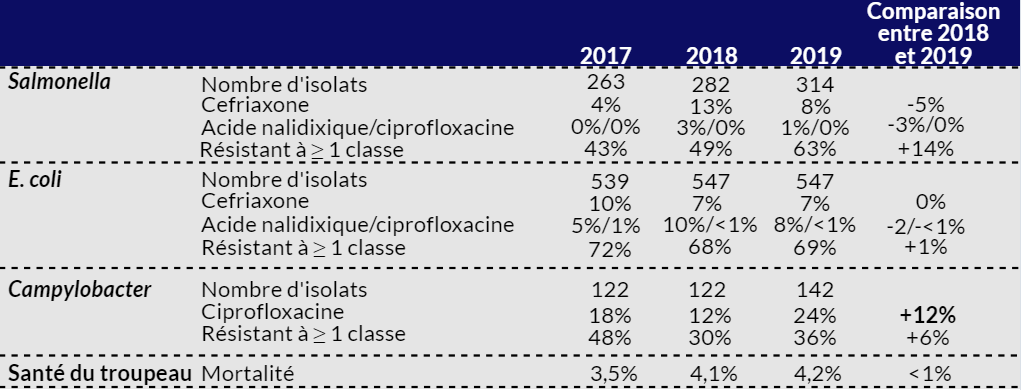
Tableau 1 - Équivalent textuel
| Bactéries ou indicateur de santé | Informations sur la résistance | 2017 | 2018 | 2019 | Comparaison entre 2018 et 2019 |
|---|---|---|---|---|---|
| Salmonella | Nombre d’isolats | 263 | 282 | 314 | aucune donnée |
| Ceftriaxone | 4 % | 13 % | 8 % | -5 % | |
| Acide nalidixique/ciprofloxacine | 0 %/0 % | 3 %/0 % | 1 %/0 % | -3 %/0 % | |
| Résistant à ≥ 1 classe | 43 % | 49 % | 63 % | +14 % | |
| E. coli | Nombre d’isolats | 539 | 547 | 547 | aucune donnée |
| Ceftriaxone | 10 % | 7 % | 7 % | 0 % | |
| Acide nalidixique/ciprofloxacine | 5 %/1 % | 10 %/<1 % | 8 %/<1 % | -2 %/-<1 % | |
| Résistant à ≥ 1 classe | 72 % | 68 % | 69 % | +1 % | |
| Campylobacter | Nombre d’isolats | 122 | 122 | 142 | aucune donnée |
| Ciprofloxacine | 18 % | 12 % | 24 % | +12 % | |
| Résistant à ≥ 1 classe | 48 % | 30 % | 36 % | +6 % | |
| Santé du troupeau | Mortalité | 3,5 % | 4,1 % | 4,2 % | <1 % |
Les chiffres en gras sont statistiquement significatifs.
*Ajusté pour les doses quotidiennes.
** Première année de la mise en œuvre de la stratégie de réduction de l’utilisation des antimicrobiens (étape 2) pour le secteur des poulets de chair.
Porcs en croissance-finition
- Au niveau national, l’utilisation des antimicrobiens (UAM)* est demeurée stable en 2019** par rapport à 2018.
- La proportion d’isolats résistant à ≥ 1 classe d’antimicrobiens est stable ou a légèrement augmenté.
- La résistance à l’acide nalidixique/ciprofloxacine est stable ou a légèrement augmenté.
- La résistance à ≥ 3 classes d’antimicrobiens a augmenté pour Salmonella mais a diminué pour E. coli et Campylobacter.
- UAM est demeurée inchangée, la RAM a généralement diminué et la mortalité dans les troupeaux est demeurée inchangée.
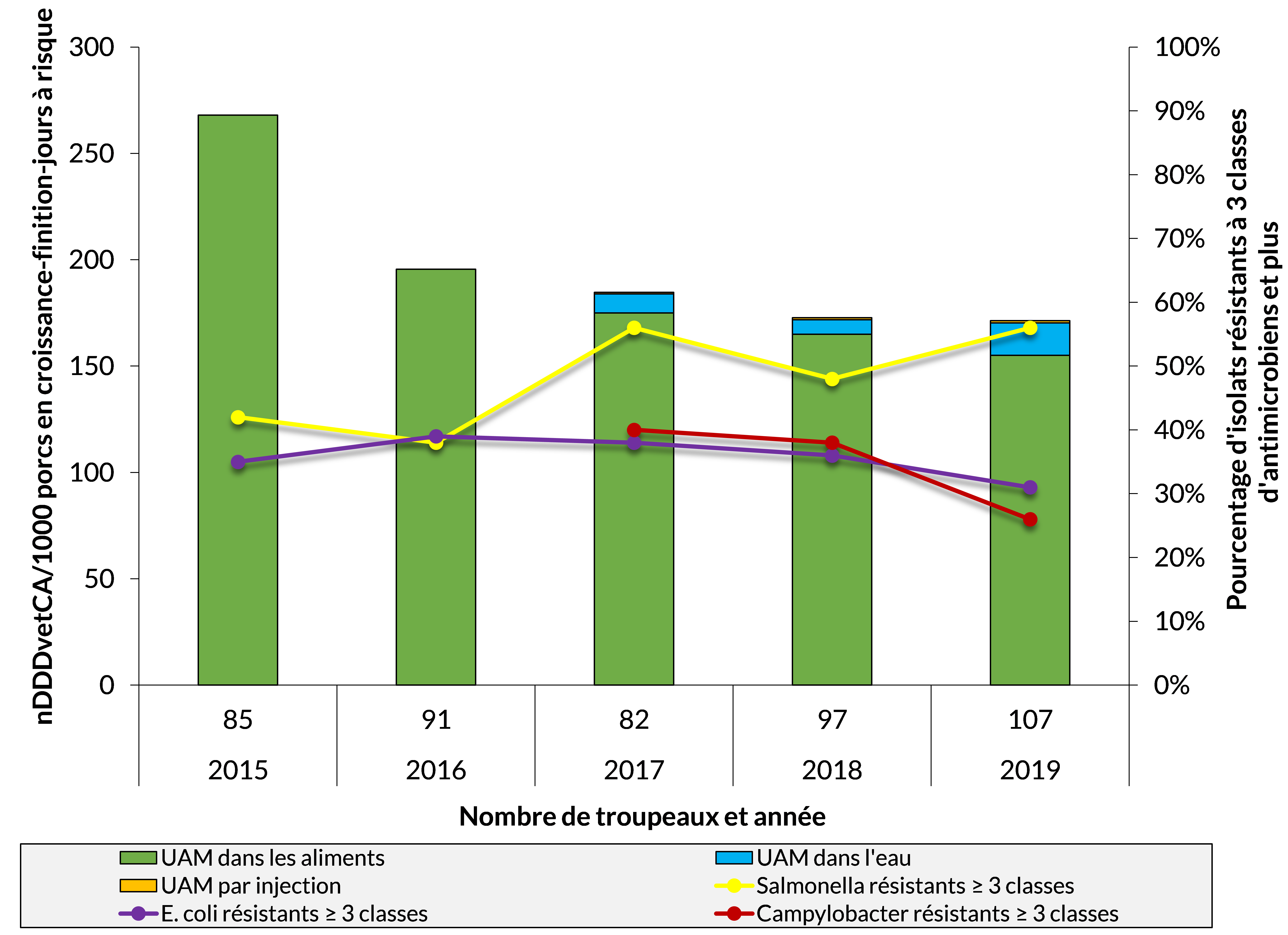
Figure 11 - Équivalent textuel
| Année | 2015 | 2016 | 2017 | 2018 | 2019 |
|---|---|---|---|---|---|
| Nombre de troupeaux | 85 | 91 | 82 | 97 | 107 |
| UAM dans les aliments | 268 | 196 | 175 | 165 | 155 |
| UAM dans l’eau | aucune donnée | aucune donnée | 9 | 7 | 15 |
| UAM par injection | aucune donnée | aucune donnée | 1 | 1 | 1 |
| Salmonella résistants to ≥ 3 classes | 42 % | 38 % | 56 % | 48 % | 56 % |
| E. coli résistant to ≥ 3 classes | 35 % | 39 % | 38 % | 36 % | 31 % |
| Campylobacter résistant to ≥ 3 classes | aucune donnée | aucune donnée | 40 % | 38 % | 26 % |
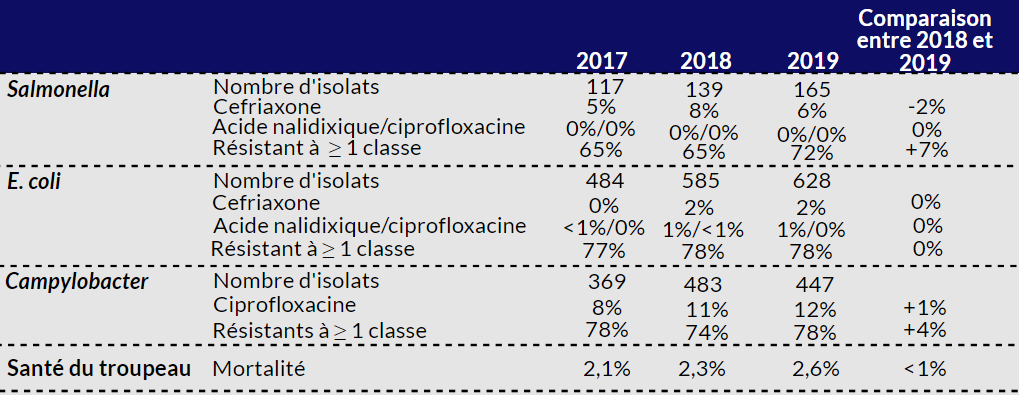
Tableau 2 - Équivalent textuel
| Bactéries ou indicateur de santé | Informations sur la résistance | 2017 | 2018 | 2019 | Comparaison entre 2018 et 2019 |
|---|---|---|---|---|---|
| Salmonella | Nombre d’isolats | 117 | 139 | 165 | aucune donnée |
| Ceftriaxone | 5 % | 8 % | 6 % | -2 % | |
| Acide nalidixique/ciprofloxacine | 0 %/0 % | 0 %/0 % | 0 %/0 % | 0 % | |
| Résistant à ≥ 1 classe | 65 % | 65 % | 72 % | +7 % | |
| E. coli | Nombre d’isolats | 484 | 585 | 628 | aucune donnée |
| Ceftriaxone | 0 % | 2 % | 2 % | 0 % | |
| Acide nalidixique/ciprofloxacine | <1 %/0 % | 1 %/<1 % | 1 %/0 % | 0 %/0 % | |
| Résistant à ≥ 1 classe | 77 % | 78 % | 78 % | 0 % | |
| Campylobacter | Nombre d’isolats | 369 | 483 | 447 | aucune donnée |
| Ciprofloxacine | 8 % | 11 % | 12 % | +1 % | |
| Résistant à ≥ 1 classe | 78 % | 74 % | 78 % | +4 % | |
| Santé du troupeau | Mortalité | 2,1 % | 2,3 % | 2,6 % | <1 % |
* Ajusté pour les doses quotidiennes.
**Première année de la mise en œuvre de la stratégie de réduction de l’utilisation des antimicrobiens au Canada.
Dindons
- À l’échelle nationale, l’UAM* a diminué en 2019** par rapport à 2018.
- Diminution notable des isolats de Campylobacter résistants à ≥ 1 classe d’antimicrobiens testés et de Salmonella résistants à ≥ 3 classes d’antimicrobiens testés.
- Pas de changement notable dans la RAM à la ceftriaxone, à l’acide nalidixique ou à la ciprofloxacine.
- La résistance à ≥ 3 classes d’antimicrobiens était stable ou légèrement en hausse pour E. coli et la Campylobacter.
- L’UAM a diminué alors que la RAM variait; cependant, la mortalité dans les élevages est demeurée inchangée.
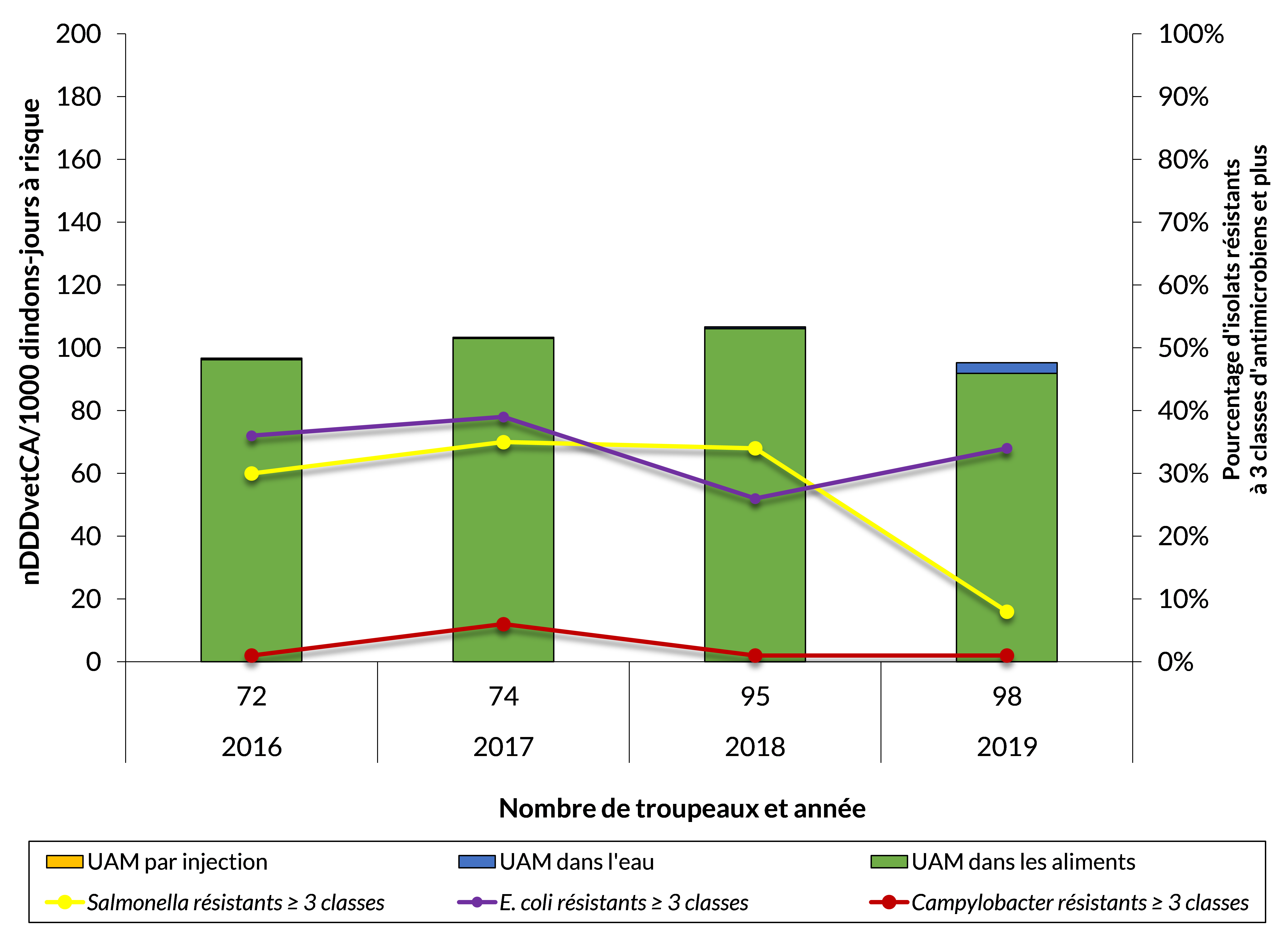
Figure 12 - Équivalent textuel
| Année | 2016 | 2017 | 2018 | 2019 |
|---|---|---|---|---|
| Nombre de troupeaux | 72 | 74 | 95 | 98 |
| UAM dans les aliments | 96 | 103 | 106 | 92 |
| UAM dans l’eau | 0 | 0 | 1 | 3 |
| UAM par injection | 0,1 | 0,1 | 0,0 | 0,0 |
| Salmonella résistants to ≥ 3 classes | 30 % | 35 % | 34 % | 8 % |
| E. coli résistant to ≥ 3 classes | 36 % | 39 % | 26 % | 34 % |
| Campylobacter resistant to ≥ 3 antimicrobial classes | 1% | 6% | 1% | 1% |
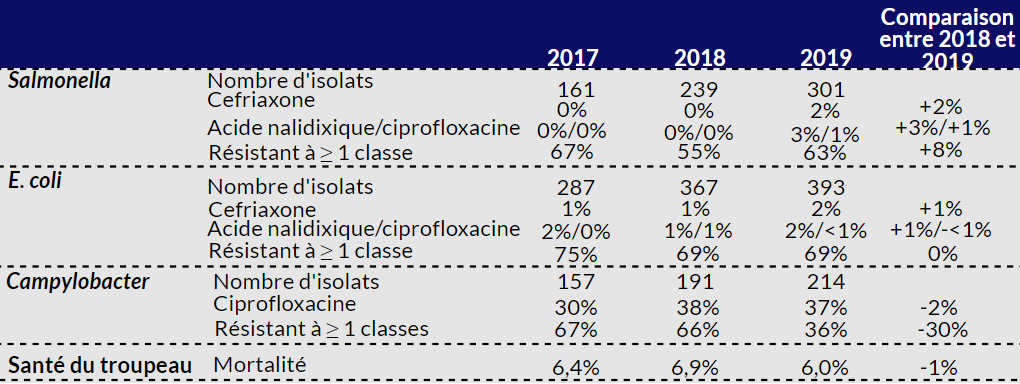
Tableau 3 - Équivalent textuel
| Bactéries ou indicateur de santé | Informations sur la résistance | 2017 | 2018 | 2019 | Comparaison entre 2018 et 2019 |
|---|---|---|---|---|---|
| Salmonella | Nombre d’isolats | 161 | 239 | 301 | aucune donnée |
| Ceftriaxone | 0 % | 0 % | 2 % | +2 % | |
| Acide nalidixique/ciprofloxacine | 0 %/0 % | 0 %/0 % | 3 %/1 % | +3 %/+1 % | |
| Résistant à ≥ 1 classe | 67 % | 55 % | 63 % | +8 % | |
| E. coli | Nombre d’isolats | 287 | 367 | 393 | aucune donnée |
| Ceftriaxone | 1 % | 1 % | 2 % | +1 % | |
| Acide nalidixique/ciprofloxacine | 2 %/0 % | 1 %/1 % | 2 %/<1 % | +1 %/-<1 % | |
| Résistant à ≥ 1 classe | 75 % | 69 % | 69 % | 0 % | |
| Campylobacter | Nombre d’isolats | 157 | 191 | 214 | aucune donnée |
| Ciprofloxacine | 30 % | 38 % | 37 % | -2 % | |
| Résistant à ≥ 1 classe | 67 % | 66 % | 36 % | -30 % | |
| Santé du troupeau | Mortalité | 6,4 % | 6,9 % | 6,0 % | <1 % |
* Ajusté pour les doses quotidiennes.
**Première année de la mise en œuvre de la stratégie de réduction de l’utilisation des antimicrobiens (étape 2) pour le secteur des dindons.
Résultats intégrés sur la résistance aux antimicrobiens
Dans cette partie, 4 récits sur la résistance en 2019 sont présentés :
- Salmonella Enteritidis résistants à l'acide nalidixique chez les humains et associés à des voyages.
- Détection de résistance aux quinolones parmi des Salmonella Enteritidis provenant de poulet(s).
- Augmentation du nombre de Salmonella provenant de sources humaines et agroalimentaires et résistants à 6 ou 7 classes d’antimicrobiens.
- Détection de Salmonella Heidelberg chez des bovins en santé.
Résistance aux quinolones parmi des Salmonella Enteritidis d'origine humaine
- La salmonellose est une maladie à déclaration obligatoire dans toutes les provinces et tous les territoires.
- S. Enteritidis est le sérotype le plus communément identifié chez les personnes atteintes de salmonellose.
- La plupart des infections à S. Enteritidis se produisent dans les intestins, mais peuvent provoquer des maladies graves si elles atteignent le flux sanguin, d’autres organes ou les articulations.
En 2018 et 2019, la détection de S. Enteritidis a diminué, ce qui a entraîné une réduction globale des cas de salmonellose.
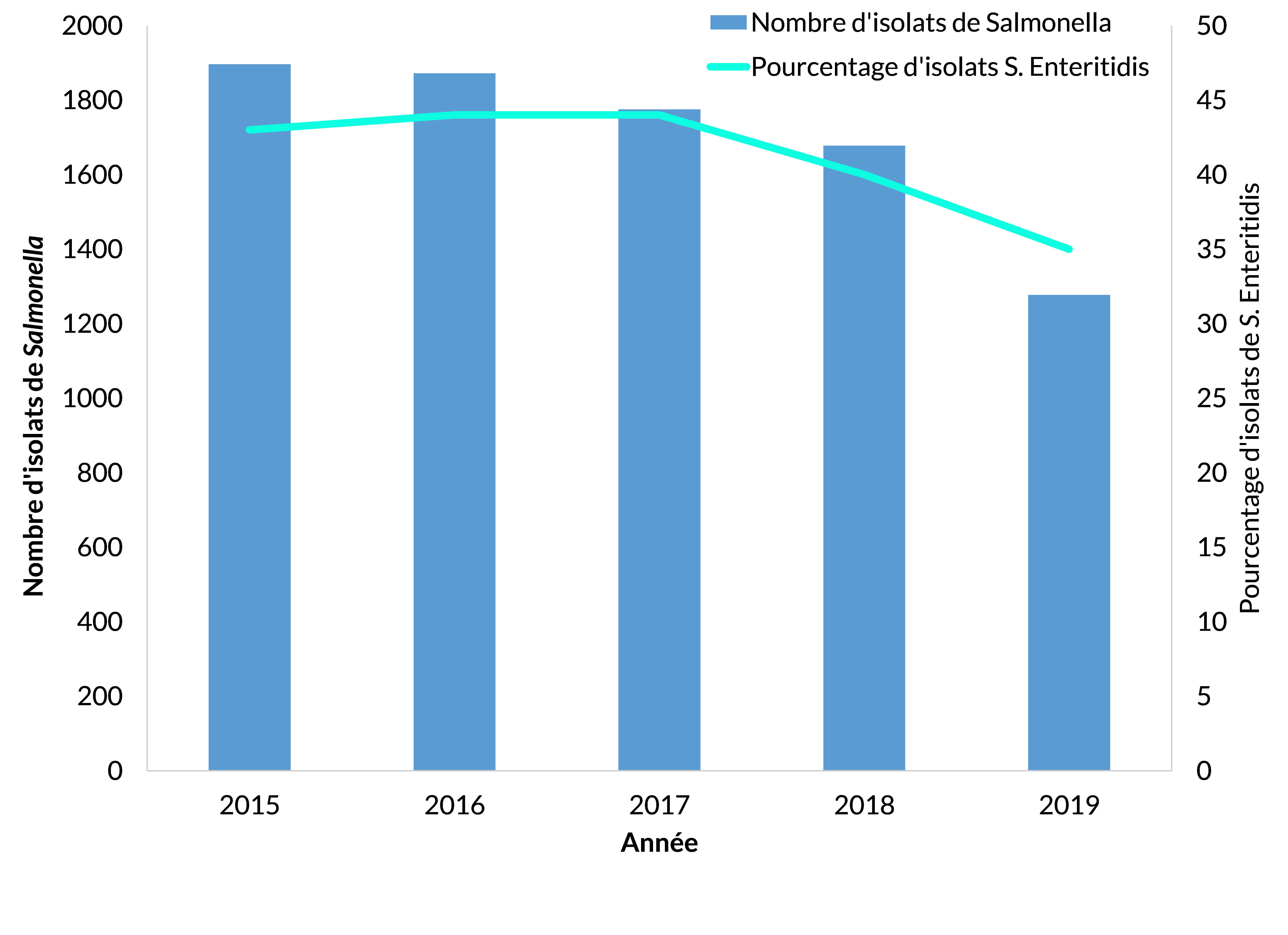
Figure 13 - Équivalent textuel
| Année | Nombre d'isolats de Salmonella | Pourcentage d'isolats de S. Enteritidis |
|---|---|---|
| 2015 | 1896 | 43 |
| 2016 | 1872 | 44 |
| 2017 | 1775 | 44 |
| 2018 | 1678 | 40 |
| 2019 | 1277 | 35 |
- La résistance est peu commune parmi les isolats de S. Enteritidis.
- Pour les antimicrobiens autres que l’acide nalidixique, généralement < 5 % des isolats sont résistants à un antimicrobien donné.
- Sauf pour la résistance à l’acide nalidixique; une quinolone et un antimicrobien de catégorie II.
Résistance aux quinolones parmi des Salmonella Enteritidis d'origine humaine
La résistance à l’acide nalidixique des isolats de S. Enteritidis d’origine humaine augmente depuis 2010.
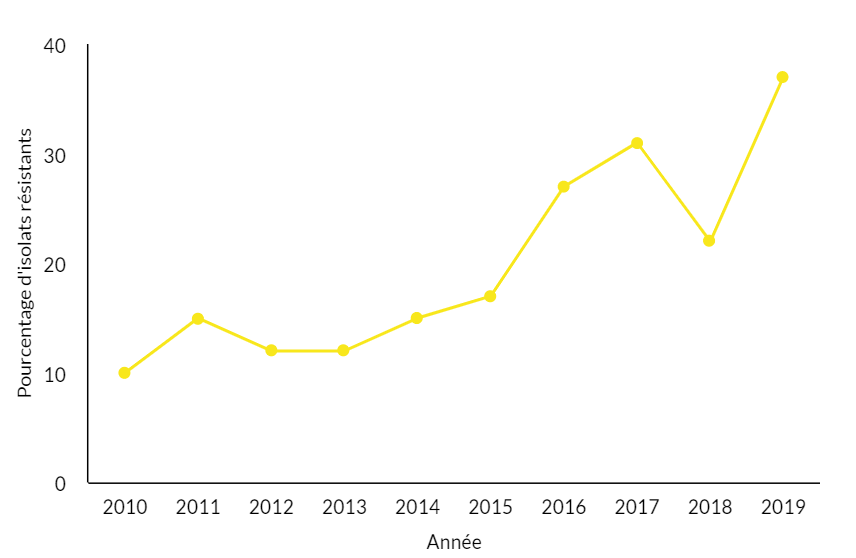
Figure 14 - Équivalent textuel
| Année | Pourcentage (%) de résistance – acide nalidixique |
|---|---|
| 2010 | 10 % |
| 2011 | 15 % |
| 2012 | 12 % |
| 2013 | 12 % |
| 2014 | 15 % |
| 2015 | 17 % |
| 2016 | 27 % |
| 2017 | 31 % |
| 2018 | 22 % |
| 2019 | 37 % |
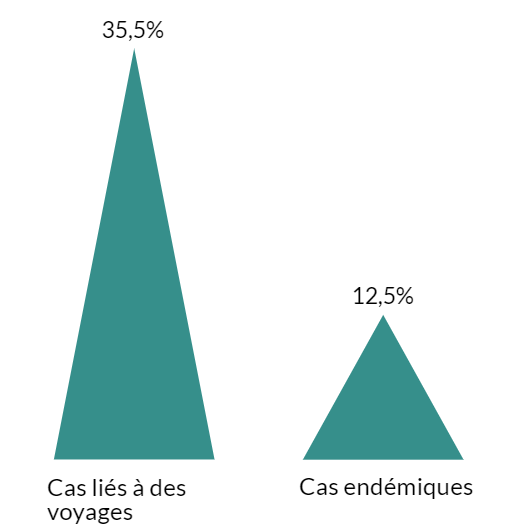
Figure 15 - Équivalent textuel
| Pourcentage (%) de résistance à l’acide nalidixique | |
|---|---|
| Cas liés à des voyages | 35,5 % |
| Cas endémiques | 12,5 % |
Les données* indiquent que la résistance à l’acide nalidixique de S. Enteritidis est plus fréquente lorsqu’il y a eu un voyage hors du Canada que lorsqu’il n’y en a pas eu (cas endémiques).
*Données provenant de FoodNet Canada
Les analyses génétiques en cours permettront de mieux expliquer le lien potentiel entre les voyages hors du Canada et les infections causées par des S. Enteritidis résistants à l’acide nalidixique.
Détection de résistance aux quinolones parmi des Salmonella Enteritidis provenant de poulets
En 2018, une nette augmentation (bien que les chiffres soient bas) de la détection de S. Enteritidis résistants à l’acide nalidixique a été observée dans plusieurs composantes de surveillance et dans plusieurs provinces. En 2019, cette tendance se poursuit.
Vente au détail
- 1 isolat provenant de l'Alberta (FoodNet Canada)
Vente au détail
- 1 isolat provenant du Québec
Abattoir
- 2 isolats provenant de la Nouvelle-Écosse et de l’Île-du-Prince-Édouard
La plupart des S. Enteritidis provenant de sources animales et alimentaires étaient sensibles à tous les antimicrobiens testés.
En 2019, en plus des isolats provenant d'échantillons de viande et d’échantillons d'abattoir, de la résistance à l’acide nalidixique a été détectée dans 8 isolats cliniques provenant de poulets de chair. (Remarque : les poulets malades n’entrent pas dans la chaîne alimentaire)
Les raisons de la détection d’une nouvelle résistance peuvent différer entre les isolats trouvés dans la chaîne agroalimentaire et les isolats cliniques.
Étant donné que le nombre d’isolats détectés est bas, le PICRA continuera de surveiller si les poulets domestiques peuvent constituer une nouvelle source d’exposition humaine à S. Enteritidis résistants à l’acide nalidixique.
Salmonella résistants à 6 ou 7 classes d’antimicrobiens
- Le nombre d’isolats de Salmonella résistants à 6 ou 7 des 7 classes d’antimicrobiens testés a continué d’augmenter (de sources humaines et animales).
- Il y a également eu une nouvelle détection de Salmonella Heidelberg provenant de fermes d'élevage de bovins et qui étaient résistants à 6 ou 7 classes d’antimicrobiens.
En 2019, 159 isolats de Salmonella ont été identifiés comme étant hautement résistants et provenaient des sources suivantes :
Humains
- Seuls les isolats cliniques ont été testés.
- La plupart des isolats étaient des Salmonella Newport, Infantis et Typhimurium.
Bovins
- Première détection d'isolats hautement résistants dans les fermes d'élevage de bovins (n = 2).
- Tous ces isolats provenant de bovins en santé étaient des S. Heidelberg.
- Toutefois, la plupart des isolats, provenant de bovins malades, qui avaient de la résistance à 6 ou 7 classes d’antimicrobiens étaient des S. Dublin (isolats cliniques).
Poulets
- La détection de S. Infantis hautement résistants se poursuit.
- Il a été détecté dans un échantillon de vente au détail en Ontario.
Porcs
- La résistance à 6 ou 7 classes d’antimicrobiens a été détectée parmi 8 sérotypes.
- La plupart provenaient de porcs malades (échantillons cliniques) (n = 18).
- 4, [5], 12:i:- était le sérotype prédominant (n = 8).
- Un isolat 4, [5], 12:i :- était résistant aux 7 classes (échantillon clinique).
Dindons
- Tous les isolats étaient des S. Infantis.
- La plupart des isolats (n = 3) provenaient de fermes d’élevage de l’Ontario.
Remarque : Les animaux malades n’entrent pas dans la chaîne alimentaire
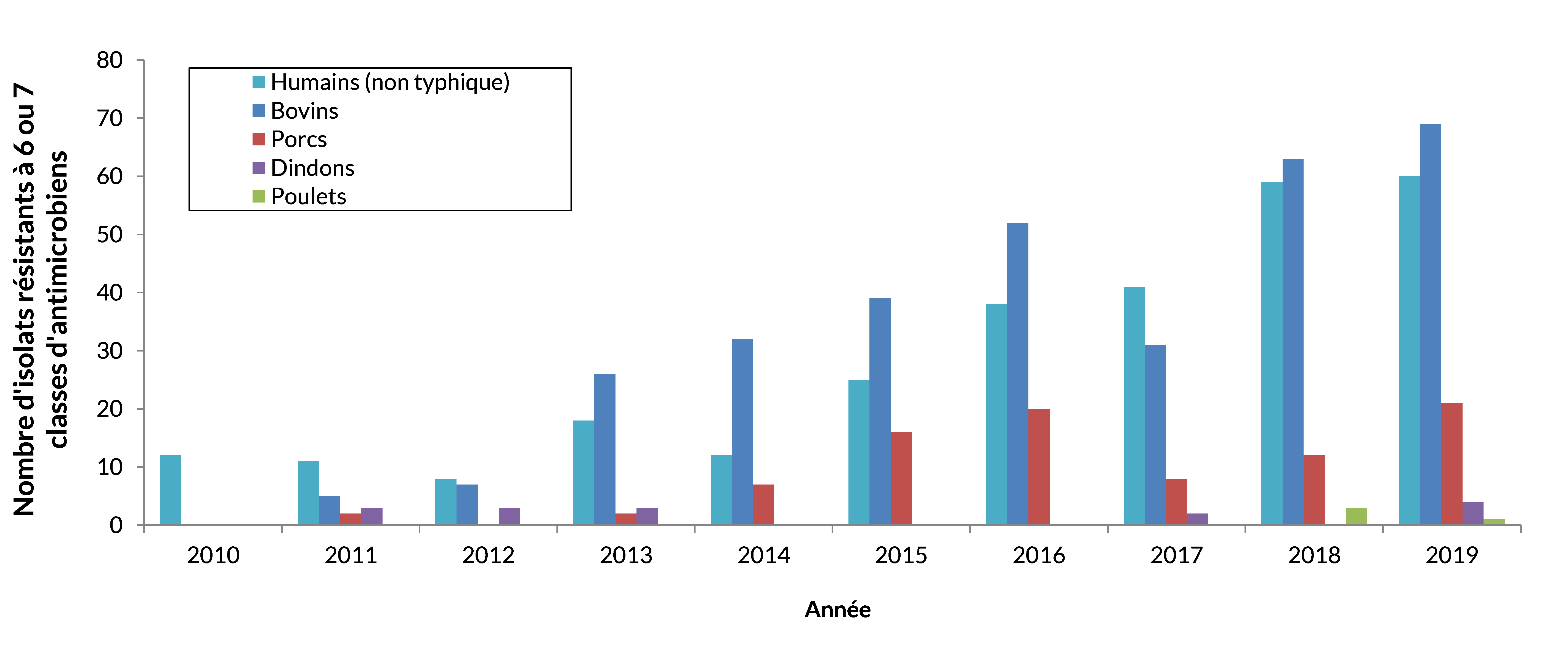
Figure 16 - Équivalent textuel
| Année | Bovins | Porcs | Poulets | Dindons | Humains (non typhique) |
|---|---|---|---|---|---|
| 2010 | 0 | 0 | 0 | 0 | 12 |
| 2011 | 5 | 2 | 0 | 3 | 11 |
| 2012 | 7 | 0 | 0 | 3 | 8 |
| 2013 | 26 | 2 | 0 | 3 | 18 |
| 2014 | 32 | 7 | 0 | 0 | 12 |
| 2015 | 39 | 16 | 0 | 0 | 25 |
| 2016 | 52 | 20 | 0 | 0 | 38 |
| 2017 | 31 | 8 | 0 | 2 | 41 |
| 2018 | 63 | 12 | 3 | 0 | 59 |
| 2019 | 69 | 21 | 1 | 4 | 60 |
Remarque : Les données sur les animaux malades (qui n’entrent pas dans la chaîne alimentaire) sont combinées aux données sur les viandes et animaux en santé. Ces données illustrent différents niveaux d’exposition préoccupants pour les humains.
Salmonella Heidelberg chez les bovins
- En 2019, des isolats de Salmonella Heidelberg résistants à 6 classes d’antimicrobiens ont été identifiés chez des bovins en santé provenant de parcs d’engraissement en Alberta.
- Il y avait 6 isolats résistants à 6 classes et un isolat supplémentaire qui était résistant à 5 classes (près de 25 %).
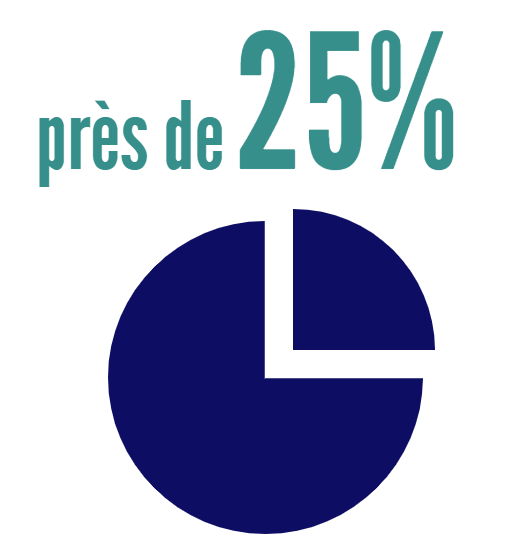
Diagram 3 - Équivalent textuel
| Isolat de Salmonella résistants à | Proportion (%) |
|---|---|
| 5 ou 6 classes d’antimicrobiens | 25 % |
| Moins de 5 classes d’antimicrobiens | 75 % |
- Ces isolats provenaient d'enclos dans lesquels il y avait des bovins Holstein (d'origine laitière) des États-Unis.
- Auparavant, les Salmonella d'origine bovine présentant de la résistance à 6 ou 7 classes d’antimicrobiens n’étaient identifiés que chez des animaux malades (principalement des isolats de S. Typhimurium ou de S. Dublin).
- Dans le passé, la prévalence de Salmonella provenant de bovins élevés dans des parcs d'engraissement canadiens (données de recherche et historiques du PICRA sur la RAM dans les parcs d’engraissement) était très faible (1 à 2 %) et de la résistance aux antimicrobiens testés était non détectée parmi ces isolats de Salmonella.
Salmonella Heidelberg chez les bovins
- Le PICRA ne teste pas les Salmonella chez les bovins de boucherie dans d’autres composantes de surveillance liés à la chaîne alimentaire (abattoir et vente au détail) en raison des très faibles taux de détection.
- Au Canada, l’engraissement de bovins Holstein en provenance des États-Unis est pratiqué depuis peu dans l’Ouest canadien et constitue dorénavant une activité importante de l’industrie du bovin de boucherie.
- Le séquençage du génome entier a indiqué qu’il n’y avait aucun lien entre ces isolats de S. Heidelberg détectés chez les bovins et les isolats humains.
Glossaire
Classe d'antimicrobiens
Les antimicrobiens sont regroupés dans la même classe s'ils ont une structure chimique commune et s'ils éliminent les bactéries ou freinent leur croissance de la même manière. Le PICRA utilise les données du Clinical and Laboratory Standards Institute pour définir les classes d'antimicrobiens.
Biomasse et Population Correction Unit (PCU)
Le PCU représente la taille de la population. Il comprend à la fois le nombre et le poids (biomasse) des animaux ou des personnes dans la population. Le PICRA utilise le PCU pour interpréter les données sur l'utilisation et les ventes d'antimicrobiens, en utilisant la même approche que le projet de l'European Surveillance of Veterinary Antimicrobial Consumption (projet de surveillance européen de la consommation d'antimicrobiens par les animaux).
DDDvet
Sigle signifiant « Defined Daily Dose for animals » (dose quotidienne définie pour les animaux). La quantité d'antimicrobiens administrée pendant un traitement (dose) variera selon l'antimicrobien, la manière dont il est administré (par exemple : par une injection, dans l'eau ou les aliments) et la population traitée (bovins, poulets, porcs). Le PICRA utilise cette mesure pour tenir compte de cette variation et faciliter l'interprétation des données sur l'utilisation des antimicrobiens.
Porc en croissance finition
Un porc dont le poids est approximativement à 25 kilogrammes du poids de marché.
Antimicrobiens hautement résistant
Résistance à 6 ou 7 classes d'antimicrobiens. Aucune norme internationale formelle n'existe pour définir les isolats hautement résistants.
Antimicrobiens médicalement importants
Antimicrobiens considérés comme étant de très haute importance (catégorie I), de haute importance (catégorie II) ou d'importance moyenne (catégorie III) en médecine humaine.
mg/PCU
Mesure de l'utilisation des antimicrobiens qui ajuste la quantité (milligramme/mg) d'antimicrobiens utilisés, consommés ou distribués selon la taille de la population.
nDDDvet/1000 animaux-jours
Mesure de l'utilisation des antimicrobiens qui tient compte à la fois des variations dans la quantité d'antimicrobiens administrés pendant un traitement (DDDvet) et de la période de temps pendant laquelle un animal ou un groupe d'animaux est traité afin d'aider à interpréter les données sur l'utilisation des antimicrobiens.
Sensible
Sensible à toutes les classes d'antimicrobiens testées. En 2019, le PICRA a testé la résistance à 7 classes d'antimicrobiens.
Les analystes du PICRA travaillent en vue d'élaborer de nouvelles façons de déceler les problèmes émergents et d'intégrer les données relatives à différentes espèces hôtes, espèces de bactéries et régions.
Le PICRA continuera de surveiller et de communiquer l'effet de l'évolution des pratiques d'utilisation des antimicrobiens sur l'apparition de la résistance aux antimicrobiens afin de préserver leur efficacité chez les animaux et les humains.