Rapport sur l'hépatite B et l'hépatite C au Canada : 2014
Télécharger le format de rechange
(format PDF, 567 ko, 47 pages)
Organization : Agence de la Santé Publique du Canada
Date publiée : 2017
Cat. : HP37-22F-PDF
ISBN : 2369-3835
Pub. : 170131
Table des matières
- Avant-propos
- Remerciements
- Résumé
- Abréviations
- 1.0 Méthodologie
- 2.0 Hépatite B
- 3.0 Hépatite C
- Références
- Annexe A: Définitions de cas
- Annexe B: Taux déclarés d'infection aiguë et chronique par le VHB au Canada, entre 2005 et 2014
- Annexe C: Déclaration des infections par le VHC au Canada: SCSMDO 2005 - 2014
Avant-propos
Le Centre de la lutte contre les maladies transmissibles et les infections de l'Agence de la santé publique du Canada (ASPC) a le plaisir de vous présenter le Rapport sur l'hépatite B et l'hépatite C au Canada : 2014. Le présent rapport vise à fournir de l'information sur les tendances relatives aux cas et aux taux de l'infection par le virus de l'hépatite B (VHB) et le virus de l'hépatite C (VHC) à tous ceux qui requièrent des données de surveillance, y compris des gestionnaires de programmes, des responsables des politiques et des chercheurs, entre autres.
L'hépatite virale est une inflammation du foie causée par l'un des cinq virus de l'hépatite; l'hépatite B et l'hépatite C sont les virus de l'hépatite à diffusion hématogène les plus courants et font l'objet du présent rapport. Bien qu'elles soient distinctes, l'infection par le VHB et l'infection par le VHC peuvent toutes les deux causer une infection aiguë asymptomatique ou symptomatique. L'infection par l'un de ces deux virus peut progresser jusqu'à une infection chronique, et elle peut entraîner une maladie grave et le décès prématuré Note de bas de page 1.
L'infection par le VHB et l'infection par le VHC sont des maladies à déclaration obligatoire au Canada. Le Rapport sur l'hépatite B et l'hépatite C au Canada : 2014 est fondé sur les données de surveillance déclarées au Système canadien de surveillance des maladies à déclaration obligatoire (SCSMDO) par les autorités sanitaires provinciales et territoriales.
Tous les commentaires et toutes les suggestions susceptibles d'améliorer les publications à venir sont appréciés. Nous vous invitons d'ailleurs à les adresser au personnel du Centre de la lutte contre les maladies transmissibles et les infections, Agence de la santé publique du Canada, à l'adresse ccdic-clmti@phac-aspc.gc.ca.
Remerciements
La publication du présent rapport n'aurait pas été possible sans la collaboration des unités épidémiologiques de toutes les provinces et de tous les territoires. Nous leurs sommes très reconnaissants de leur contribution continue à la surveillance nationale de l'infection par le virus de l'hépatite B (VHB) et de l'infection par le virus de l'hépatite C (VHC).
Ce rapport a été préparé par le Centre de la lutte contre les maladies transmissibles et les infections de la Direction générale de la prévention et du contrôle des maladies infectieuses de l'Agence de la santé publique du Canada.
Résumé
Le présent rapport résume les données de surveillance sur les cas et les taux de l'infection par le virus de l'hépatite B (VHB) et par l'infection par le virus de l'hépatite C (VHC) au Canada, de 2005 à 2014. Les cas sont déclarés au Système canadien de surveillance des maladies à déclaration obligatoire (SCSMDO) par les autorités sanitaires provinciales et territoriales. Alors que les données sur les infections aiguës et chroniques par le VHB sont résumées séparément dans la mesure du possible, il est impossible, à l'heure actuelle, de faire la distinction entre les cas d'infection aiguë et chronique de VHC pour toutes les provinces et tous les territoires en raison des différences dans leurs pratiques de déclaration. Les renseignements sur l'infection aiguë par le VHB donnent un aperçu des tendances et des profils actuels de transmission, tandis que les cas d'infection chronique par le VHB représentent le fardeau de la maladie au Canada. Les annexes B et C résument les différentes pratiques de déclaration sur l'hépatite B et C selon les différentes provinces et les différents territoires entre 2005 et 2014.
Hépatite B
En 2014, 178 cas au total d'hépatite B aiguë ont été signalés au Canada. L'analyse des données sur les infections aiguës par le VHB déclarées par l'entremise du SCSMDO montre que les taux d'infection aiguë par le VHB ont diminué; ils sont passés de 1,0 à 0,5 cas pour 100 000 personnes entre 2005 et 2014. En 2014, le taux le plus élevé de cas d'infection aiguë par le VHB a été observé chez les hommes de 30 à 59 ans (1,0 pour 100 000 personnes), suivis des hommes de 60 ans et plus (0,76 pour 100 000 personnes). Chez les hommes de plus de 30 ans, les taux étaient près de deux fois plus élevés que les taux des femmes, tandis que dans les groupes d'âge plus jeunes, les taux chez les hommes étaient semblables à celui des femmes. Au cours de cette période de dix ans, les taux d'infection aiguë par le VHB ont diminué chez les hommes de tous les groupes d'âge, où la diminution la plus importante a été observée dans les groupes d'âge de 30 à 39 ans et de 20 à 24 ans. Des résultats semblables ont été observés chez les femmes, où les taux des cas déclarés d'infection aiguë par le virus de l'hépatite B ont affiché une diminution dans tous les groupes d'âge, à l'exception des plus de 60 ans, avec la diminution la plus marquée observée dans le groupe d'âge de 20 à 24 ans. En 2014, des taux de cas déclarés supérieurs au taux national de 0,5 cas pour 100 000 personnes ont été observés en Saskatchewan, en Ontario, au Nouveau-Brunswick, en Nouvelle-Écosse et dans les Territoires du Nord-Ouest.
Pour l'hépatite B chronique, la déclaration faite par les différentes provinces a évolué avec le temps; en effet, les différentes provinces ont commencé à déclarer des cas d'infection chronique pour différentes années et ont parfois associé cette déclaration à des cas d'infection non précisée. En conséquence, les tendances liées aux taux doivent être interprétées avec prudence, en particulier au cours des premières années, et les tendances à plus court terme entre 2009 et 2014. Les tendances entre 2009 et 2014 sont généralement plus stables. En 2014, 4 058 cas d'infection chronique par le VHB ont été déclarés, ce qui équivaut à un taux de 12,0 pour 100 000 personnes. Les taux de cas déclarés d'infection chronique par le VHB ont varié de 10,9 (2008) à 13,6 (2012) pour 100 000 personnes, sans tendance définie à l'exception d'une diminution marginale dans les taux observés entre 2012 et 2014. Entre 2005 et 2014, le taux de VHB chronique est demeuré plus élevé chez les hommes que chez les femmes, sauf en 2007.
En 2014, les taux d'infection chronique par le VHB étaient plus élevés chez les hommes que chez les femmes de 30 ans et plus, tandis que les taux chez les femmes de moins de 30 ans étaient supérieurs ou égaux à ceux des hommes. En 2014, les femmes dans le groupe d'âge de 25 à 29 ans ont affiché le taux le plus élevé d'infection chronique par le VHB (25,7 pour 100 000 personnes); venaient ensuite les hommes dans le groupe d'âge de 30 à 39 ans (24,5 pour 100 000 personnes). La Colombie-Britannique, l'Alberta, l'Ontario et le Yukon ont déclaré des taux (20,8, 13,3, 13,6 et 16,2, respectivement) plus élevés que la moyenne nationale de 12,0 pour 100 000 personnes.
Divers facteurs peuvent expliquer les tendances décrites dans le présent rapport. Par exemple, le programme universel canadien de vaccination ciblant les bébés et les enfants d'âge scolaire et, dans certaines provinces et certains territoires, les populations à risque élevé, a probablement contribué à la baisse des taux d'infection aiguë par le VHB. D'autres interventions axées sur le contrôle des infections et interventions en matière de santé publique visant à prévenir la transmission des infections transmissibles sexuellement et par le sang peuvent aussi avoir eu une incidence sur les tendances observées.
Il convient de noter que les taux nationaux de VHB sont fortement influencés par les variations des pratiques de déclaration géographiques et temporelles, et devraient donc être interprétés avec prudence. Les provinces et les territoires n'ont pas la même capacité à distinguer les cas d'infection (aiguë et chronique) par VHB par état sérologique; par conséquent, la déclaration du VHB n'est pas uniforme dans l'ensemble du pays et un grand nombre de cas d'hépatite B sont déclarés comme étant non précisés (c.-à-d. état sérologique inconnu). En outre, les taux présentés dans le présent rapport sous-estiment probablement le véritable fardeau de l'infection au Canada étant donné que le VHB est asymptomatique chez la plupart des personnes qui, par conséquent, ne consultent probablement pas de professionnel de la santé pour subir un test de dépistage.
Hépatite C
Comme pour la surveillance de l'hépatite B au Canada, la surveillance de l'hépatite C continue à évoluer; la plupart des provinces et des territoires rapportent l'infection par le VHC sans différentiation entre les états aigus et chroniques. Seuls trois territoires ont commencé à faire une distinction entre la déclaration de cas d'infection aiguë et chronique (Alberta et Yukon depuis 2013) ou de cas d'infection aiguë et non précisée (Québec depuis 2012). Par conséquent, pour les besoins du présent rapport, une telle distinction n'est pas mise en évidence et tous les cas sont déclarés comme infections par le VHC qui incluent les cas aigus, chroniques et non spécifés. Il est à noter que les infections chroniques par le VHC représentent probablement la majorité des cas déclarés au SCSMDO, car les infections aiguës sont habituellement asymptomatiques et moins susceptibles d'être diagnostiquées.
Entre 2005 et 2014, le taux de cas déclarés d'hépatite C a constamment diminué; il est passé de 40,2 à 29,3 pour 100 000 personnes, et semble avoir atteint un plateau au cours des dernières années. Les taux ont diminué chez les hommes et les femmes de tous les groupes d'âge, à l'exception de faibles augmentations chez les hommes âgés de 20 à 24 ans, et de 60 ans et plus et les femmes de 25 à 29 ans. Au cours de la période de dix ans, les taux de cas déclarés de VHC ont été systématiquement plus élevés chez les hommes que chez les femmes âgées de 25 ans et plus. En 2014, le taux le plus élevé a été observé chez les hommes dans les groupes d'âge de 40 à 59 (58,2 pour 100 000 personnes) et de 25 à 29 ans (55 pour 100 000 personnes). La Colombie-Britannique, l'Alberta, la Saskatchewan, l'Ontario, la Nouvelle-Écosse, l'Île-du-Prince-Édouard, le Yukon et les Territoires du Nord-Ouest ont tous affiché des taux bien plus élevés que la moyenne nationale de 29,3 pour 100 000 personnes.
Les progrès réalisés dans le dépistage des dons de sang, les pratiques de contrôle des infections dans les milieux de soins de santé et les interventions médicales et de santé publique ont probablement contribué aux déclins observés dans les cas de VHC déclarés au Canada. Il est également possible que les interventions en matière de santé publique visant à prévenir la transmission de l'infection chez les utilisateurs de drogues injectables, aient eu une incidence importante sur ces tendances.
En raison des difficultés liées à la détermination de l'état sérologique (infection aiguë ou chronique par le VHC) et aux pratiques de déclaration, il est difficile de tirer des inférences sur les tendances dans la transmission de l'infection aiguë par le VHC ou le fardeau chronique de l'infection. De même, l'absence de données sur le facteur de risque pour les cas déclarés de VHC limite l'interprétation des résultats présentés dans le présent rapport.
Les statistiques et les tendances nationales en ce qui concerne le VHB et le VHC servent à documenter les programmes, les lignes directrices et les recommandations en matière de santé publique. Malgré les limites des données recueillies par le SCSMDO, les taux et les tendances observés de VHB et de VHC de 2005 à 2014 confirment la nécessité de poursuivre les efforts de prévention et de prise en charge au Canada. Étant donné que la déclaration des infections aiguës et chroniques par le VHB et le VHC devient plus harmonisée dans l'ensemble du pays, au fil du temps, les données disponibles seront plus représentatives du fardeau réel de l'hépatite virale au Canada.
Abréviations
- ADN
- Acide désoxyribonucléique
- ARN
- Acide ribonucléique
- ASPC
- Agence de la santé publique du Canada
- CDC
- Centers for Disease Control and Prevention des États-Unis
- CLMTI
- Centre de la lutte contre les maladies transmissibles et les infections
- É.-U.
- États-Unis
- ECMS
- Enquête canadienne sur les mesures de la santé
- EIA
- Épreuve immunoenzymatique
- RCITO
- Registre canadien des insuffisances et des transplantations d'organes
- SCS
- Société canadienne du sang
- SSMDOC
- Système de surveillance des maladies à déclaration obligatoire du Canada
- VHB
- Virus de l'hépatite B
- VHC
- Virus de l'hépatite C
- VIH
- Virus de l'immunodéficience humaine
1.0 Méthodologie
1.1 Définitions de cas
Les définitions de cas pour l'hépatite B et l'hépatite C utilisées au Canada à des fins de surveillance sont présentées à l'annexe A. L'infection par le virus de l'hépatite B (VHB) est à déclaration obligatoire au Canada depuis 1969, et la définition de cas nationale actuelle Note de bas de page 1 définit l'infection aiguë, chronique ou non précisée. L'infection par le virus de l'hépatite C (VHC) est à déclaration obligatoire à l'échelle nationale depuis 1991. La surveillance des cas d'hépatite C était graduelle au fil du temps par les provinces et les territoires, et l'ensemble des provinces et territoires déclaraient les cas en 1999. La définition des cas d'infection par le VHC actuellement utilisée pour la surveillance nationale Note de bas de page 2 définit l'état d'infection aiguë et non spécifiée (y compris l'infection chronique, résolue ou indéterminée).
1.2 Collecte de données
Au Canada, la surveillance des maladies infectieuses à déclaration obligatoire est menée par l'Agence de la santé publique du Canada (ASPC) en coordination avec les gouvernements provinciaux et territoriaux qui fournissent volontairement des données non nominatives à l'ASPC. La responsabilité de la collecte de données primaires sur les maladies à déclaration obligatoire relève des autorités de santé publique locales en vertu des lois provinciales et territoriales Note de bas de page 3 .
L'ASPC recueille et gère les données communiquées par les provinces et les territoires par l'intermédiaire du Système canadien de surveillance des maladies à déclaration obligatoire du Canada (SCSMDO). Le personnel du SCSMDO valide les données déclarées par une province ou un territoire au cours du traitement des données pour résoudre les erreurs ou les incohérences et maximiser l'exactitude des données. Les provinces et territoires fournissent des données sur les variables suivantes : âge au moment du diagnostic, année du diagnostic, province ou territoire où le diagnostic a été posé et sexe. Par conséquent, les rapports nationaux sont limités à l'analyse de ces variables. Les données extraites du SCSMDO servent de base aux rapports de surveillance nationale. Le présent rapport est fondé sur les données extraites en août 2016.
1.3 Analyse des données
Jusqu'à récemment, les données de surveillance déclarées au SCSMDO par la plupart des provinces et des territoires ne faisaient pas de distinction entre les cas d'infection aiguë et d'infection chronique par le VHB. Un certain nombre de provinces et de territoires ont commencé à déclarer les cas d'infections aiguës par le VHB en 2005; toutefois, la déclaration des infections chroniques par le VHB est devenue plus uniforme seulement en 2009. Afin d'examiner les tendances au fil du temps, seuls les provinces et territoires qui ont systématiquement déclaré des cas d'infection aiguë ou chronique par le VHB au cours de la période prise en compte ont été inclus dans le calcul des taux annuels. Les estimations de la population des provinces et territoires qui ne sont pas inclus dans une analyse précise (cas aigu ou chronique) ont été retirées du dénominateur d'ensemble utilisé pour calculer les taux nationaux. Par conséquent, les taux annuels d'infection aiguë par le VHB déclarés de 2005 à 2014 comprennent la Colombie-Britannique, l'Alberta, la Saskatchewan, l'Ontario, le Québec, le Nouveau-Brunswick, les Territoires du Nord-Ouest et les années choisies pour d'autres provinces et territoires tels que le Yukon (2008-2014), le Manitoba (2009-2014) et la Nouvelle-Écosse (2009-2014). Les taux annuels d'infection chronique par le VHB déclarés de 2005 à 2014 comprennent les données de l'Alberta, du Québec, du Nouveau-Brunswick et des années choisies pour d'autres provinces et territoires tels que la Saskatchewan (2005-2013), le Yukon (2008-2014), les Territoires du Nord-Ouest (2008-2014), la Colombie-Britannique (2009-2014), la Nouvelle-Écosse (2009-2014), l'Ontario (2012-2014) et le Manitoba (2009, 2010, 2012-2014). L'annexe B fournit des renseignements sur les années au cours desquelles les provinces et les territoires ont commencé à déclarer des cas en faisant la distinction entre l'infection aiguë et chronique par le VHB.
La plupart des provinces et des territoires diagnostiquent les cas de VHC en utilisant le dépistage des anticorps, ce qui ne permet pas de faire la distinction entre une infection aiguë et infection chronique par le VHC, ou entre une infection courante et une infection résolue; ces cas sont déclarés comme des cas non-spécifiques d'infections par le VHC (annexe C). Par conséquent, les données relatives au VHC présentées dans ce rapport sont des cas non-spécifiques d'infections et sont donc une compilation des cas d'infections aiguës, chroniques, résolues et indéterminées par le VHC.
Une analyse descriptive de l'infection par le VHB et de l'infection par le VHC par année, par groupe d'âge et par sexe a été menée à partir des données déclarées au SCSMDO. Les caractéristiques démographiques d'âge et de sexe ont été examinées pour les cas de VHB et de VHC déclarés en 2014 afin de fournir un aperçu plus détaillé des données accessibles les plus récentes. Les taux (indiqués pour 100 000 personnes), les pourcentages et le pourcentage de variation des taux ont été calculés à partir de valeurs non arrondies; par conséquent, les valeurs arrondies peuvent différer des calculs basés sur les valeurs arrondies et ne pas correspondre au total. Les données démographiques utilisées étaient des estimations d'octobre 2016 de Statistique Canada (Section des estimations démographiques de la Division de la démographie). Les taux calculés à l'aide de ces estimations à jour peuvent différer de celles indiquées dans les précédents rapports.
1.4 Limite des données
Les tendances observées au fil du temps doivent être interprétées avec prudence, car les taux basés sur de petits nombres de cas sont plus susceptibles de fluctuer au fil du temps. L'amélioration des capacités diagnostiques et de nettoyage et de validation des données (élimination des doublons), des délais de déclaration plus courts et des changements dans les pratiques de déclaration à l'échelle des provinces et des territoires peuvent entraîner des changements des tendances observées.
Une fois les données du présent rapport validées, les modifications apportées aux données des provinces et territoires après validation peuvent ne pas être prises en compte dans les données nationales de cette année, mais seront mises à jour pour les rapports ultérieurs. Par conséquent, on prévoit de petits écarts entre les chiffres de l'ASPC et ceux des provinces ou territoires en raison de la comparaison de bases de données dynamiques. Des écarts plus importants peuvent être constatés lorsque les provinces et les territoires utilisent une stratégie analytique différente de celle utilisée dans le présent rapport. Par exemple, certains territoires de compétence choisissent de déclarer des infections chroniques et non précisées par le VHB au sein d'une seule catégorie, tandis que les infections non précisées sont excluses de l'analyse à l'échelle nationale.
2.0 Hépatite B
2.1 Introduction
Le virus de l'hépatite B (VHB) est un virus à acide désoxyribonucléique (ADN) de la famille des hépadnavirus (Hepadnaviridae) qui infecte principalement les cellules du foie, mais que l'on trouve aussi dans une variété de tissus et d'organes, y compris les reins, le pancréas et les cellules mononucléaires Note de bas de page 4, Note de bas de page 5. Après avoir contracté l'infection par le VHB, moins de 10 % des enfants et 30 à 50 % des adultes vont exprimer des symptômes qui peuvent inclure la jaunisse, de la fatigue, une perte d'appétit, des nausées et des douleurs articulaires ou abdominales Note de bas de page 6. L'âge au moment de l'infection est un important déterminant de la probabilité de développement d'une infection chronique; elle survient chez environ 90 % des nourrissons infectés à la naissance et diminue avec l'augmentation de l'âge à moins de 5 % des adultes Note de bas de page 6. L'infection chronique par le VHB peut, au fil du temps, provoquer une cirrhose du foie, un carcinome hépatocellulaire, une hépatopathie décompensée et un décès prématuré Note de bas de page 6.
La transmission du VHB se produit par contact avec du sang et des liquides organiques infectés, le plus souvent lors de relations sexuelles ou d'un contact étroit avec une personne infectée, lors de l'utilisation d'équipement d'injection de drogues contaminé et de la transmission verticale (transmission de la mère à l'enfant) pendant la grossesse ou l'accouchement Note de bas de page 6. Les profils de transmission du VHB sont un peu différents entre les pays en développement et les pays développés; en effet, dans les pays en voie de développement, la transmission verticale et l'exposition par contact avec la famille proche sont d'une grande importance, tandis que la transmission sexuelle et l'utilisation de drogues injectables sont les profils prédominants dans les pays développés, comme le Canada Note de bas de page 7, Note de bas de page 8. Le VHB peut survivre à l'extérieur du corps jusqu'à sept jours et a été observé dans le cadre de la transmission nosocomiale (par l'entremise du matériel médical ou dentaire contaminé) et de l'exposition professionnelle chez les travailleurs de la santé Note de bas de page 9.
Le diagnostic de l'infection par le VHB doit être confirmé en laboratoire par l'analyse d'un échantillon de sang destiné à différencier l'infection par le VHB d'autres types d'hépatites. Les marqueurs de l'infection présents dans le sang peuvent également permettre de différencier les infections aiguës par le VHB des infections chroniques. L'infection aiguë par le VHB se caractérise par la présence de l'antigène de surface de l'hépatite B (antigène HBs) et des anticorps immunoglobine M de l'antigène capsidique de l'hépatite B (anticorps IgM anti-HBc) Note de bas de page 6. Une infection chronique se caractérise par la présence d'anticorps dirigés contre l'antigène capsidique de l'hépatite B (anticorps anti-HBc autre que l'anticorps IgM) et de l'antigène HBs pendant plus de six mois Note de bas de page 6. La présence de l'antigène HBe, un antigène caractéristique de la phase initiale de l'infection aiguë et qui peut être présent pendant une infection chronique, indique que la personne infectée est extrêmement contagieuse Note de bas de page 10, Note de bas de page 11. En revanche, l'anticorps anti-HBe apparaît au cours du rétablissement suivant une infection aiguë et sa présence durant une infection chronique indique généralement une réplication virale réduite et un faible niveau d'infectiosité Note de bas de page 11.
Un vaccin contre l'hépatite B est disponible à l'échelle mondiale depuis 1982 Note de bas de page 9. Au Canada, toutes les provinces et tous les territoires bénéficient d'un programme de vaccination universelle contre le VHB pour les nouveau-nés et les enfants depuis les années 1990, bien que ces programmes varient selon la province ou le territoire en ce qui concerne les doses et calendriers recommandés, ainsi que des groupes d'âge ciblés Note de bas de page 11, Note de bas de page 12. En outre, certaines provinces et certains territoires offrent un vaccin contre le VHB aux personnes à risque accru d'infection par le VHB (p. ex. les utilisateurs de drogues injectables ou les personnes ayant des relations sexuelles à haut risque) Note de bas de page 13. Le Comité consultatif national de l'immunisation recommande des tests de routine de dépistage de l'antigène HBs durant la grossesse et au moment de l'accouchement. Les bébés nés de mères infectées sont ajoutés sur un calendrier de vaccination immédiate afin de réduire le risque d'infection par le VHB Note de bas de page 14.
Il n'existe aucun traitement contre l'infection aiguë par le VHB; les soins sont axés sur les activités de soulagement des symptômes, la prévention des complications hépatiques et la réduction de la propagation de l'infection par l'intermédiaire de counseling Note de bas de page 9, Note de bas de page 11. Chez les personnes souffrant d'infection chronique par le VHB, les injections d'interférons et les médicaments antirétroviraux sont les traitements approuvés pour prévenir l'apparition de la cirrhose, de l'insuffisance hépatique et du cancer du foie. Toutefois, seules certaines personnes atteintes d'infection chronique par le VHB sont admissibles à un traitement, ce que l'on détermine en fonction de la personne, de l'âge, des concentrations d'aminotransférase sérique et d'ADN du VHB, et de la gravité de la maladie du foie, entre autres Note de bas de page 11.
2.2 Tendances nationales
2.2.1 Infection aiguë par le virus de l'hépatite B
Cette section du rapport présente les taux et les tendances de l'infection aiguë par le VHB au Canada entre 2005 et 2014. Afin de fournir des tendances uniformes au fil du temps, seuls les provinces et territoires ayant fourni des données sur l'infection aiguë par le VHB durant cette période sont inclus dans les taux nationaux d'infection aiguë par le VHB, et les dénominateurs ont été ajustés en conséquence.
2.2.1.1 Tendances au fil du temps
Le taux global des cas déclarés d'infection aiguë par le VHB a diminué régulièrement entre 2005 et 2014. En 2005, un total de 302 cas d'infection aiguë par le VHB ont été signalés, ce qui correspond à un taux d'incidence global de 1,0 cas pour 100 000 personnes, comparativement à 2014 où 178 cas ont été signalés, ce qui correspondait à un taux de 0,5 cas pour 100 000 personnes (figure 1).
Entre 2005 et 2014, le taux des cas déclarés d'infection aiguë par le VHB était constamment plus élevé chez les hommes que chez les femmes, malgré la réduction de l'écart entre les deux sexes observée au fil du temps; la baisse de ce taux était plus importante chez les hommes que chez les femmes (54,9 % par rapport à 38,2 %, respectivement) (figure 1).
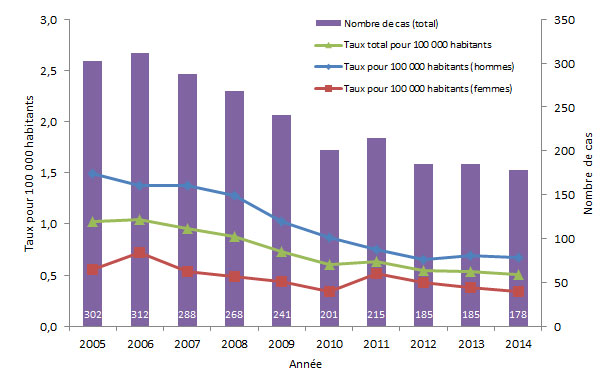
Figure 1 - Équivalent du texte
| Année | Nombre de cas (total) | Taux total pour 100 000 habitants | Taux pour 100 000 habitants (hommes) | Taux pour 100 000 habitants (femmes) |
|---|---|---|---|---|
| 2005 | 302 | 1,0 | 1,5 | 0,6 |
| 2006 | 312 | 1,0 | 1,4 | 0,7 |
| 2007 | 288 | 1,0 | 1,4 | 0,5 |
| 2008 | 268 | 0,9 | 1,3 | 0,5 |
| 2009 | 241 | 0,7 | 1,0 | 0,4 |
| 2010 | 201 | 0,6 | 0,9 | 0,3 |
| 2011 | 215 | 0,6 | 0,8 | 0,5 |
| 2012 | 185 | 0,5 | 0,7 | 0,4 |
| 2013 | 185 | 0,5 | 0,7 | 0,4 |
| 2014 | 178 | 0,5 | 0,7 | 0,3 |
- Note de bas de page 1
-
Comprend des données de la Colombie-Britannique, de l'Alberta, de la Saskatchewan, de l'Ontario, du Québec, du Nouveau-Brunswick, des Territoires du Nord-Ouest (données de 2005 à 2014), du Yukon (données de 2008 à 2014), du Manitoba et de la Nouvelle-Écosse (données de 2009 à 2014).
2.2.1.2 Tendances selon le groupe d'âge et le sexe
En 2014, le taux le plus élevé de cas d'hépatite C a été observé chez les hommes de 30 à 59 ans (1,0 pour 100 000 personnes), suivis des hommes de 60 ans et plus (0,76 pour 100 000 personnes). Chez les hommes de plus de 30 ans, les taux étaient près de deux fois plus élevés que ceux des femmes, tandis que dans les groupes d'âge plus jeunes, les taux chez les hommes étaient semblables à celui des femmes (figure 2).

Figure 2 - Équivalent du texte
| Groupe d'âge | Hommes | Femmes |
|---|---|---|
| 0-14 | 0,1 | 0,0 |
| 15-19 | 0,1 | 0,2 |
| 20-24 | 0,3 | 0,3 |
| 25-29 | 0,7 | 0,5 |
| 30-39 | 1,0 | 0,5 |
| 40-59 | 1,0 | 0,5 |
| 60+ | 0,8 | 0,3 |
- Note de bas de page 1
-
Comprend des données de la Colombie-Britannique, de l'Alberta, de la Saskatchewan, de l'Ontario, du Québec, du Nouveau-Brunswick, des Territoires du Nord-Ouest, du Yukon, du Manitoba et de la Nouvelle-Écosse.
Entre 2005 et 2014, le taux des cas déclarés d'infection aiguë par le VHB chez les hommes a diminué dans la plupart des groupes d'âge, la diminution la plus importante (réduction de 69 %, p < 0,05) étant dans le groupe d'âge 30 à 39 ans et la moins importante (réduction de 22 %; p < 0,05) chez les personnes de 60 ans et plus (figure 3).

Figure 3 - Équivalent du texte
| Année | 0 à 14 ans | 15 à 19 ans | 20 à 24 ans | 25 à 29 ans | 30 à 39 ans | 40 à 59 ans | 60 ans et plus |
|---|---|---|---|---|---|---|---|
| 2005 | 0,2 | 0,2 | 1,0 | 1,1 | 3,2 | 2,3 | 1,0 |
| 2006 | 0,1 | 0,4 | 0,5 | 1,9 | 2,5 | 2,2 | 0,8 |
| 2007 | 0,2 | 0,2 | 1,0 | 1,5 | 2,7 | 2,1 | 0,8 |
| 2008 | 0,2 | 0,7 | 0,9 | 1,2 | 1,9 | 2,0 | 1,0 |
| 2009 | 0,0 | 0,1 | 0,6 | 0,9 | 1,9 | 1,7 | 0,7 |
| 2010 | 0,1 | 0,1 | 0,3 | 0,7 | 1,2 | 1,5 | 0,8 |
| 2011 | 0,0 | 0,1 | 0,5 | 0,9 | 1,3 | 1,2 | 0,6 |
| 2012 | 0,1 | 0,1 | 0,0 | 1,0 | 1,4 | 0,9 | 0,5 |
| 2013 | 0,0 | 0,3 | 0,4 | 0,5 | 1,4 | 1,1 | 0,5 |
| 2014 | 0,1 | 0,1 | 0,3 | 0,7 | 1,0 | 1,0 | 0,8 |
- Note de bas de page 1
-
Comprend des données de la Colombie-Britannique, de l'Alberta, de la Saskatchewan, de l'Ontario, du Québec, du Nouveau-Brunswick, des Territoires du Nord-Ouest (données de 2005 à 2014), du Yukon (données de 2008 à 2014), du Manitoba et de la Nouvelle-Écosse (données de 2009 à 2014).
Chez les femmes, la tendance à la baisse la plus importante (p <0,05) des taux d'infection aiguë par le VHB est observée (figure 4) dans les groupes d'âge de 20 à 24 ans (de 1,3 à 0,3 pour 100 000 personnes; réduction de 80 %), de 25 à 29 ans (de 1,3 à 0,5 pour 100 000 personnes), de 30 à 39 ans (de 1,0 à 0,5 pour 100 000 personnes) et de 40 à 59 ans (de 0,7 à 0,5 pour 100 000 personnes). Dans d'autres groupes, on n'a observé aucun changement (de 0 à 14 ans) ou une légère augmentation (de 15 à 19 ans) et une augmentation de près de 50 % chez les femmes (60 ans et plus), tel que représenté dans la figure 4.
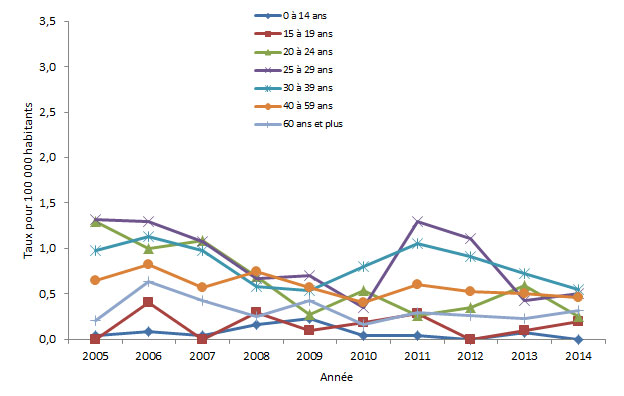
Figure 4 - Équivalent du texte
| Année | 0 à 14 ans | 15 à 19 ans | 20 à 24 ans | 25 à 29 ans | 30 à 39 ans | 40 à 59 ans | 60 ans et plus |
|---|---|---|---|---|---|---|---|
| 2005 | 0,0 | 0,0 | 1,3 | 1,3 | 1,0 | 0,7 | 0,2 |
| 2006 | 0,1 | 0,4 | 1,0 | 1,3 | 1,1 | 0,8 | 0,6 |
| 2007 | 0,0 | 0,0 | 1,1 | 1,1 | 1,0 | 0,6 | 0,4 |
| 2008 | 0,2 | 0,3 | 0,7 | 0,7 | 0,6 | 0,7 | 0,3 |
| 2009 | 0,2 | 0,1 | 0,3 | 0,7 | 0,5 | 0,6 | 0,4 |
| 2010 | 0,0 | 0,2 | 0,5 | 0,3 | 0,8 | 0,4 | 0,2 |
| 2011 | 0,0 | 0,3 | 0,3 | 1,3 | 1,1 | 0,6 | 0,3 |
| 2012 | 0,0 | 0,0 | 0,3 | 1,1 | 0,9 | 0,5 | 0,3 |
| 2013 | 0,1 | 0,1 | 0,6 | 0,4 | 0,7 | 0,5 | 0,2 |
| 2014 | 0,0 | 0,2 | 0,3 | 0,5 | 0,5 | 0,5 | 0,3 |
- Note de bas de page 1
-
Comprend des données de la Colombie-Britannique, de l'Alberta, de la Saskatchewan, de l'Ontario, du Québec, du Nouveau-Brunswick, des Territoires du Nord-Ouest (données de 2005 à 2014), du Yukon (données de 2008 à 2014), du Manitoba et de la Nouvelle-Écosse (données de 2009 à 2014).
2.2.1.3 Taux par province/territoire
En 2014, les taux de cas déclarés d'infection aiguë par le VHB étaient inférieurs dans tous les territoires de compétence participants. Toutefois, la Saskatchewan, l'Ontario, le Nouveau-Brunswick, la Nouvelle-Écosse et les Territoires du Nord-Ouest ont déclaré des taux d'infection aiguë par le VHB supérieurs à la moyenne nationale de 0,5 pour 100 000 personnes (0,8, 0,8, 1,2, 0,7 et 2,3 pour 100 000 personnes, respectivement). Dans toutes les provinces et tous les territoires, les taux chez les hommes étaient systématiquement supérieurs à ceux des femmes, sauf au Manitoba où le nombre de cas déclarés était trop bas pour permettre une comparaison valide (tableau 1).
| Province / territoire | Homme | Femme | Total | |||
|---|---|---|---|---|---|---|
| Nombre de cas | Taux pour 100 000 personnes | Nombre de cas | Taux pour 100 000 personnes | Nombre de cas | Taux pour 100 000 personnes | |
| Canada | 117 | 0,7 | 60 | 0,3 | 178 | 0,5 |
| C.-B. | 9 | 0,4 | 5 | 0,2 | 14 | 0,3 |
| Alb. | 9 | 0,4 | 1 | 0,0 | 10 | 0,2 |
| Sask. | 7 | 1,2 | 2 | 0,4 | 9 | 0,8 |
| Man. | 0 | 0,0 | 4 | 0,6 | 4 | 0,3 |
| Ont. | 60 | 0,9 | 43 | 0,6 | 104 | 0,8 |
| Qc | 17 | 0,4 | 3 | 0,1 | 20 | 0,2 |
| N.-B. | 8 | 2,1 | 1 | 0,3 | 9 | 1,2 |
| N.-É. | 6 | 1,3 | 1 | 0,2 | 7 | 0,7 |
| Î.-P.-É | S.O. | S.O. | S.O. | S.O. | S.O. | S.O. |
| T.-N.-L. | S.O. | S.O. | S.O. | S.O. | S.O. | S.O. |
| Yn | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| T.N.-O. | 1 | 4,4 | 0 | 0,0 | 1 | 2,3 |
| Nt | S.O. | S.O. | S.O. | S.O. | S.O. | S.O. |
|
||||||
2.2.2 Infection chronique par le virus de l'hépatite B
Les provinces et les territoires ont commencé à déclarer des infections chroniques par le VHB à des années différentes. Les statistiques relatives à l'infection chronique par le VHB présentées dans le rapport actuel ont été ajustées pour tenir compte des différences liées à la variation au cours de l'année durant laquelle chaque territoire de compétence a commencé à déclarer. En conséquence, une interprétation prudente de ces statistiques est recommandée vu que les données de différentes périodes peuvent représentées des groupes de provinces ou de territoires différents.
2.2.2.1 Tendances au fil du temps
On a observé une tendance variable, mais généralement en croissance, du taux de cas déclarés d'infection chronique par le VHB entre 2005 et 2014. Cela peut être en partie lié au fait que les années durant lesquelles les provinces ayant des taux différents participent aux systèmes de surveillance sont différentes. Malgré une tendance générale à la hausse dans le taux d'infection chronique par le VHB au fil des ans, il convient de noter que, depuis 2012, il a légèrement diminué de 13,6 à 12,0 en 2014 pour 100 000 personnes (figure 5). La diminution s'est produite chez les hommes et chez les femmes, mais était plus importante chez les hommes (diminution de 15,8 %) que chez les femmes (diminution de 6,5 %), tel que l'indique la figure 5.

Figure 5 - Équivalent du texte
| Année | Nombre de cas (total) | Taux total pour 100 000 habitants | Taux pour 100 000 habitants (hommes) | Taux pour 100 000 habitants (femmes) |
|---|---|---|---|---|
| 2005 | 752 | 5,9 | 6,5 | 5,3 |
| 2006 | 989 | 7,7 | 7,8 | 7,6 |
| 2007 | 923 | 7,1 | 6,5 | 7,7 |
| 2008 | 1 441 | 10,9 | 11,3 | 10,4 |
| 2009 | 2 644 | 13,2 | 14,5 | 11,9 |
| 2010 | 2 469 | 12,2 | 13,4 | 11,0 |
| 2011 | 1 993 | 10,4 | 11,5 | 9,2 |
| 2012 | 4 634 | 13,6 | 15,2 | 11,9 |
| 2013 | 4 483 | 13,0 | 14,5 | 11,4 |
| 2014 | 4 058 | 12,0 | 12,8 | 11,1 |
- Note de bas de page 1
-
Comprend des données de l'Alberta, du Québec, du Nouveau-Brunswick (données de 2005 à 2014), de la Saskatchewan (données de 2005 à 2013), du Yukon, des Territoires du Nord-Ouest (données de 2008 à 2014), de la Colombie-Britannique, de la Nouvelle-Écosse (données de 2009 à 2014), du Manitoba (données de 2009, 2010, et de 2012 à 2014), de l'Ontario (données de 2012 à 2014).
2.2.2.2 Tendances selon le groupe d'âge et le sexe
En 2014, les taux d'infection chronique par le VHB étaient plus élevés chez les hommes que chez les femmes de 30 ans et plus, tandis que pour les groupes d'âge plus jeunes (figure 6), les taux chez les femmes étaient supérieurs ou égaux à ceux des hommes. Sur l'ensemble des données de 2014, les taux de cas déclarés de VHB chronique les plus élevés ont été observés chez les femmes de 25 à 29 ans (25,7 pour 100 000 personnes) et chez les hommes de 30 à 39 (24,5 pour 100 000 personnes) (figure 6).
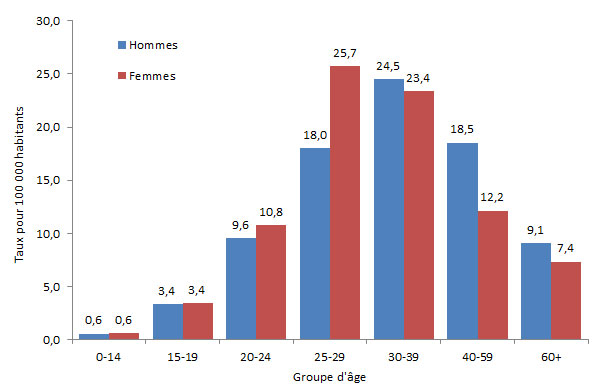
Figure 6 - Équivalent du texte
| Groupe d'âge | Hommes | Femmes |
|---|---|---|
| 0-14 | 0,6 | 0,6 |
| 15-19 | 3,4 | 3,4 |
| 20-24 | 9,6 | 10,8 |
| 25-29 | 18,0 | 25,7 |
| 30-39 | 24,5 | 23,4 |
| 40-59 | 18,5 | 12,2 |
| 60+ | 9,1 | 7,4 |
- Note de bas de page 1
-
Exemple de note de bas de page standard.
2.2.2.3 Tendances par province et par territoire
Le nombre de cas d'infection chronique par le VHB et les taux, selon le sexe et les provinces et territoires pour 2014, sont présentés dans le tableau 2. En 2014, l'Ontario a déclaré le nombre le plus élevé de cas (1 873), ce qui correspond à un taux de 13,6 pour 100 000 personnes; venait ensuite la Colombie-Britannique avec 971 cas, correspondant à un taux de 20,8 pour 100 000 personnes. Les provinces de l'Ontario, de la Colombie-Britannique, de l'Alberta et du Yukon ont déclaré des taux d'infection chronique par le VHB supérieurs à la moyenne nationale de 11,4 pour 100 000 personnes (13,6, 20,8, 13,3 et 16,2 pour 100 000 personnes, respectivement). À l'exception du Yukon et de la Colombie-Britannique, les taux étaient systématiquement plus élevés chez les hommes que chez les femmes.
| Province / territoire | Homme | Femme | Total | |||
|---|---|---|---|---|---|---|
| Nombre de cas | Taux pour 100 000 personnes | Nombre de cas | Taux pour 100 000 personnes | Nombre de cas | Taux pour 100 000 personnes | |
| Canada | 2 154 | 12,8 | 1 896 | 11,1 | 4 058 | 12,0 |
| C.-B. | 475 | 20,5 | 494 | 21,0 | 971 | 20,8 |
| Alb. | 301 | 14,3 | 249 | 12,3 | 550 | 13,3 |
| Sask. | S.O. | S.O. | S.O. | S.O. | S.O. | S.O. |
| Man. | 36 | 5,6 | 33 | 5,1 | 69 | 5,4 |
| Ont. | 992 | 14,7 | 875 | 12,5 | 1 873 | 13,6 |
| Qc | 319 | 7,8 | 223 | 5,4 | 542 | 6,6 |
| N.-B. | 18 | 4,8 | 12 | 3,1 | 30 | 4,0 |
| N.-É. | 11 | 2,4 | 6 | 1,2 | 17 | 1,8 |
| Î.-P.-É. | S.O. | S.O. | S.O. | S.O. | S.O. | S.O. |
| T.-N.-L. | S.O. | S.O. | S.O. | S.O. | S.O. | S.O. |
| Yn | 2 | 10,6 | 4 | 22,0 | 6 | 16,2 |
| T.N.-O. | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| Nt | S.O. | S.O. | S.O. | S.O. | S.O. | S.O. |
Notes de bas de page
|
||||||
2.3 Discussion
Dans l'ensemble, bien que le taux de cas déclarés d'infection par le VHB au Canada soit relativement faible, il s'agit toujours d'une cause importante et évitable de maladie et de décès. En 2013 (la plus récente année pour laquelle des données sur la mortalité étaient disponibles), l'infection aiguë par le VHB a été documentée comme la principale cause de 18 décès au Canada, et 50 autres décès ont été attribués à une infection chronique par le VHB Note de bas de page 15. Les premières observations sur les statistiques liées à la mortalité sont axées sur le fait que le nombre croissant de décès peut être attribué aux cas d'infection chronique par le VHB entre 2011 et 2013. En outre, la véritable ampleur des décès liés au VHB est probablement plus élevée et sous-estimée en raison d'une possible classification erronée sur les certificats de décès Note de bas de page 16.
Les cas d'infection aiguë par le VHB offrent de précieuses indications sur les tendances et les schémas actuels de transmission, car les cas diagnostiqués et déclarés comme une infection aiguë se rapprochent des cas incidents (c.-à-d. ceux qui ont été récemment contractés). Les données du SCSMDO indiquent une diminution du taux de cas déclarés d'infection aiguë par le VHB entre 2005 et 2014, au Canada, tant chez les hommes que chez les femmes, bien que les taux aient été constamment plus élevés chez les hommes que chez les femmes au cours de cette période. En 2014, les observations ont démontré que les taux de cas déclarés d'infection aiguë par le VHB étaient les plus élevés chez les hommes dans le groupe d'âge de 40 à 59 ans; viennent ensuite les hommes du groupe d'âge de 30 à 39 ans et les hommes de plus de 60 ans.
Ces taux d'infection aiguë par le VHB en diminution au Canada peuvent être attribuables à la mise en œuvre de programmes d'immunisation systématique dans toutes les provinces et tous les territoires à partir du début des années 1990. Ces programmes sont offerts aux nourrissons et aux enfants d'âge scolaire et, dans certaines provinces et certains territoires, aux populations à risque élevé Note de bas de page 13. On juge que les personnes ayant reçu le vaccin contre le VHB sont protégées d'une infection aiguë et chronique par le VHB. Étant donné qu'une proportion croissante de la population canadienne bénéficie d'une couverture vaccinale contre le VHB, on peut raisonnablement s'attendre à ce que les taux d'infection aiguë par le VHB continuent de baisser. En 2009, le taux de vaccination contre le VHB chez les enfants âgés de 2 ans était estimé à 69 % dans les provinces et les territoires bénéficiant d'un programme de vaccination des nourrissons en trois doses Note de bas de page 20. En 2011, la couverture vaccinale par l'administration d'au moins deux doses du vaccin contre le VHB était de 74,8 % chez les jeunes de 17 ans Note de bas de page 21. En 2012, la couverture vaccinale contre le VHB à l'échelle nationale était estimée à 39,7 % seulement parmi la population adulte ne résidant pas en établissement; par contre, près de 64,9 % des travailleurs de la santé en contact étroit avec des patients avaient reçu le vaccin Note de bas de page 21.
L'amélioration du dépistage dans le sang et l'amélioration des pratiques de prévention et de contrôle des infections dans les milieux de soins de santé ont probablement aussi contribué à la baisse des taux d'infection aiguë par le VHB au Canada. La surveillance des dons de sang reçus par la Société canadienne du sang en 2015 indique que le VHB a été détecté selon un taux de 42,6 cas pour 100 000 personnes faisant un don pour la première fois (ce qui représente moins de 10 % du total global des dons) et selon un taux de seulement 2,0 cas pour 100 000 personnes faisant un don répété (c.-à-d. des dons de personnes qui avaient déjà donné du sang). Tous les dons qui ont un résultat positif à un test de dépistage d'une maladie transmissible sont jetés Note de bas de page 22. En vertu du Programme de contributions pour la sûreté du sang (PCSS) de l'ASPC par l'entremise de ses systèmes de surveillance (Système de surveillance des incidents transfusionnels [SSIT], Système de surveillance des erreurs transfusionnelles [SSET]), aucun cas d'infection par le VHB liée à une transfusion sanguine n'a été déclaré.
Les comparaisons des taux d'infection aiguë par le VHB entre le Canada et d'autres pays sont limitées en raison des différences dans les définitions de cas, les sources de déclaration et les programmes de dépistage. Cependant, une diminution semblable des taux a été observée dans les pays avec une structure démographique, un état de santé et des infrastructures de santé publique comparables. Par exemple, les données issues de la surveillance systématique ou améliorée en Angleterre et aux États-Unis indiquent que les taux annuels d'infection aiguë par le VHB dans ces pays diminuent au fil du temps Note de bas de page 17 Note de bas de page 18 Note de bas de page 19. Selon le rapport le plus récent établi par les Centers for Disease Control and Prevention des États-Unis en 2014, les taux d'infection aiguë par le VHB diminuent aux États-Unis depuis 2010. En 2010, 3 350 cas d'infection aiguë par le VHB ont été déclarés, tandis qu'en 2014, le nombre de cas déclarés est tombé à 2 953 Note de bas de page 17. Comme aux États-Unis, l'Angleterre a connu une diminution du nombre de cas d'infection aiguë par le VHB, d'après le rapport le plus récent (2015) sur l'infection aiguë par le virus de l'hépatite B de la Public Health England. De 2014 à 2015, l'incidence annuelle des cas déclarés d'infection aiguë par le VHB est passé de 0,91 pour 100 000 personnes à 0,83 pour 100 000 personnes Note de bas de page 18.
Il est important de comprendre l'ampleur de l'infection chronique par le VHB au Canada, car elle représente le fardeau potentiel de la maladie au Canada en raison de l'incapacité prolongée à éliminer l'infection. Une infection chronique par le VHB peut entraîner des problèmes à long terme tels que la cirrhose et le cancer du foie Note de bas de page 6. Les données du Registre canadien des insuffisances et des transplantations d'organes (RCITO) indiquent que le VHB était le principal diagnostic de 4,2 % des receveurs de transplantation du foie au Canada de 2005 à 2014 Note de bas de page 23. Par rapport aux personnes atteintes d'une infection aiguë par le VHB, les personnes ayant une infection chronique par le VHB sont plus susceptibles de transmettre le virus à d'autres, car la période de transmissibilité est relativement brève pendant une infection aiguë Note de bas de page 24.
En raison de la déclaration variable de cas d'infection chronique par le VHB des provinces et des territoires entre 2005 et 2014, l'analyse des tendances d'infection chronique par le VHB au fil du temps doit être interprétée avec prudence. Les données du SCSMDO indiquent que les taux de cas déclarés d'infection chronique par le VHB ont légèrement diminué entre 2012 et 2014. En 2014, les taux les plus élevés ont été observés chez les femmes de 25 à 29 ans, et chez les hommes de 30 à 39 ans.
Les taux des cas déclarés d'infection chronique par le VHB sont plus élevés que celui des infections aiguës par le VHB pour diverses raisons, y compris le sous-diagnostic probable des cas d'infection aiguë en raison de leur nature en grande partie asymptomatique. L'infection chronique par le VHB est plus susceptible d'être diagnostiquée chez les personnes qui n'ont pas été vaccinées pendant leur enfance, comme en témoignent les taux plus élevés de cas déclarés chez les personnes de 30 ans et plus, qui auraient été plus vieilles que les personnes pour qui le vaccin était recommandé au moment de la mise en œuvre des programmes d'immunisation universelle.
Des données indiquent que l'immigration de pays où le VHB est endémique contribue aussi probablement à une augmentation du nombre de cas de VHB dans l'ensemble du Canada Note de bas de page 25. Selon une étude dirigée en 2011, on a estimé qu'environ 3 % des immigrants au Canada au début des années 2000 étaient touchés par le VHB, tandis que 0,5 % uniquement des personnes nées au Canada étaient infectées au cours de la même période Note de bas de page 26. Toutefois, le pourcentage de personnes touchées par une infection chronique par le VHB parmi les immigrants au Canada pourrait en fait être supérieur à 3 %, tel que l'indique une étude de 2012 de l'Université McGill, dans laquelle 6,7 % des immigrants étaient touchés par une infection chronique par le VHB Note de bas de page 27. Dans une étude en Colombie-Britannique, la majorité des cas d'infection chronique par le VHB décelés au cours des dernières années concernaient les personnes ayant immigré d'un pays où le VHB est endémique Note de bas de page 26.
Des études sur la séroprévalence des populations peuvent aider à fournir d'autres renseignements sur le fardeau de l'infection par le VHB au Canada. L'Enquête canadienne sur les mesures de la santé (ECMS) Note de bas de page 29 Note de bas de page 30 a révélé la séroprévalence des infections actuelles par le VHB, y compris les infections aiguës et chroniques, est de 0,4 % au cours d'une période de collecte de données qui s'étend de 2007 à 2011. Des signes sérologiques d'une infection antérieure par le VHB ont été décelés chez 4,2 % des participants. Chez les personnes déjà infectées par le VHB, 79 %, ont démontré une résolution complète et une immunité protectrice Note de bas de page 31. Ce genre d'enquêtes offre des renseignements utiles et complète le système de surveillance pour mieux caractériser le fardeau des maladies lié à l'infection par le VHB.
Bien que les taux d'infection par le VHB soient généralement faibles chez la population générale au Canada, des recherches antérieures ont démontré que certains facteurs sont fortement associés au risque d'infection, y compris l'activité sexuelle à risque élevé, l'utilisation de drogues injectables, le fait d'avoir un contact avec un membre de sa famille porteur de l'antigène HBs et des antécédents de transfusion sanguine, de tatouage et de perçage corporel Note de bas de page 32 Note de bas de page 33. En raison de tels facteurs de risque, certaines populations vulnérables connaissent des taux plus élevés que les taux moyens d'infection par le VHB, notamment les utilisateurs de drogues injectables et les jeunes de la rue qui pourraient ne pas avoir bénéficié des programmes d'immunisation provinciaux et territoriaux même s'ils y étaient admissibles Note de bas de page 34 Note de bas de page 35.
2.4 Limites
Il convient de mentionner qu'il existe des limites notables aux résultats présentés dans le présent rapport. Les pratiques de déclaration ne sont pas toujours demeurées uniformes au cours de la période incluse dans le présent rapport et, par conséquent, certaines provinces et certains territoires ont été exclus des analyses de données d'infections aiguës ou chroniques par le VHB. Contrairement à la déclaration des cas d'infection aiguë par le VHB qui était plus uniforme au cours de la période de 2005 à 2014, la déclaration des infections chroniques par le VHB dans l'ensemble des provinces et territoires au cours de la même période était plus variable. Par exemple, l'Île-du-Prince-Édouard et Terre-Neuve-et-Labrador n'ont pas précisé l'état sérologique pour les cas déclarés d'infection par le VHB au SCSMDO et ont toujours déclaré les cas d'hépatite B comme étant des cas non précisés. Parmi les provinces ayant déclaré des cas d'infection aiguë et chronique, certains de ces cas ont également été déclarés comme étant des cas non classés. En 2014, 712 des cas d'infections par le VHB ont été déclarés comme étant non précisés et ne sont donc pas présentés dans le présent rapport.
Les données ont été analysées uniquement en fonction de l'âge, du sexe et de l'état sérologique. Pour le moment, le SCSMDO ne dispose d'aucun autre élément de données pouvant aider à expliquer les tendances observées. Par conséquent, il est impossible d'établir avec certitude la proportion de cas déclarés d'infection par le VHB imputable aux cas importés des pays endémiques, à l'utilisation de drogues injectables ou à des pratiques sexuelles à risque élevé.
Les tendances observées au fil du temps peuvent également être représentatives de changements dans les pratiques de dépistage ou d'améliorations de la capacité diagnostique, entraînant ainsi une hausse de la détection des personnes atteintes du virus de l'hépatite B, dont beaucoup ont probablement contracté l'infection bien avant le moment du diagnostic. En outre, ces tendances peuvent être attribuables à la forte capacité à faire la distinction entre les infections aiguës et les infections chroniques, ainsi qu'à une amélioration de la surveillance et de la déclaration.
De même, les taux basés sur de petits nombres de cas sont davantage sujets à fluctuer au fil du temps, comme avec le virus de l'hépatite B, et doivent être interprétés avec prudence. Par exemple, la grande augmentation du taux observée d'infection aiguë par le VHB chez les femmes dans le groupe d'âge des 25 à 29 ans entre 2010 et 2011, et la diminution ultérieure observée au cours des années suivantes, peut s'expliquer en grande partie par le petit nombre de cas déclarés de ce groupe et le potentiel subséquent de fluctuation des taux.
Enfin, les taux d'infection par le VHB présentés dans le présent rapport sont sans doute une sous-estimation du fardeau réel des infections au Canada. Étant donné que l'infection aiguë par le VHB est asymptomatique chez plus de 90 % des enfants et chez 50 à 70 % des adultes, la majorité des personnes nouvellement infectées ne consulteront pas un professionnel de la santé pour subir un test de dépistage et, par conséquent, ne seront pas déclarées dans le SCSMDO en tant que cas d'infection aiguë par le VHB. Les résultats de l'Enquête canadienne sur les mesures de la santé de 2007 à 2009 et de 2009 à 2011 laissent penser que plus de la moitié des participants à l'enquête avec un virus de l'hépatite B confirmé en laboratoire n'étaient pas au courant de leur infection Note de bas de page 31. Le fardeau de l'infection chronique par le VHB au Canada est sous-estimé dans le présent rapport en raison de la non-disponibilité des données sur l'infection chronique par le VHB dans différentes provinces pour la période présentée. En outre, l'infection par le VHB survient souvent chez des populations difficiles à atteindre qui pourraient ne pas avoir accès à un fournisseur de soins de santé ou qui pourraient adopter un comportement insuffisant pour obtenir des soins de santé. Finalement, bien que, dans certains cas, un cas aigu déclaré puisse devenir un porteur plus tard, cela n'a pas été évalué dans le présent rapport et les données fournies à l'ASPC par les provinces et les territoires ont été considérées comme étant définitives pour l'année de déclaration respective.
2.5 Conclusion
Bien qu'il existe des limites aux données disponibles, les résultats présentés dans le présent rapport comblent une lacune importante en matière de connaissances, et ils sont utiles pour déceler les principales tendances liées aux infections aiguës et chroniques par le VHB au Canada. Le Canada continue d'afficher une tendance à la baisse dans les taux de VHB, plus particulièrement pour les cas d'infection aiguë par le VHB, et une tendance à la baisse dans les cas d'infection chronique par le VHB finira par découler des stratégies de vaccination, en particulier celles qui visent les populations à haut risque.
Compte tenu de la possibilité qu'une infection par le VHB entraîne de plus lourds problèmes, tels que la cirrhose, un carcinome hépatocellulaire et une décompensation hépatique, et du potentiel subséquent de fardeau qui pèse sur le système de soins de santé du Canada, une surveillance continue de l'infection par le VHB est requise. Les données de surveillance sont utilisées pour guider l'élaboration de lignes directrices, de recommandations et de programmes de santé publique. En 2013 Note de bas de page 11, l'ASPC a publié un guide de référence sur la prise en charge des soins primaires de l'hépatite B, et elle fournit des recommandations sur l'utilisation du vaccin contre le VHB dans le Guide canadien d'immunisation Note de bas de page 13. À l'avenir, le fait de renforcer la capacité à faire la distinction entre les cas d'infection aiguë et chronique de VHB et la déclaration normalisée permettront de générer davantage de données fiables, ce qui permettra de mieux cerner les tendances de la transmission de l'infection et le fardeau de la maladie au Canada, en plus de contribuer aux mesures de santé publique.
3.0 Hépatite C
3.1 Introduction
Le virus de l'hépatite C (VHC) est un virus enveloppé à acide ribonucléique (ARN) simple brin linéaire qui appartient à la famille des flavivirus Flaviviridae. On estime qu'environ 250 000 personnes vivent avec une infection par le VHC au Canada Note de bas de page 36. Six génotypes du virus de l'hépatite C ont été identifiés, et le génotype 1 est la souche prédominante au Canada et dans toute l'Amérique du Nord Note de bas de page 36 Note de bas de page 37. Les personnes atteintes d'une infection aiguë par le VHC sont souvent asymptomatiques, ce qui pose un défi pour l'identification de nouveaux cas. Environ 15 % à 50 % des personnes connaîtront une résolution spontanée et se rétabliront de l'infection Note de bas de page 6. Il a été démontré que la résolution spontanée survient plus souvent chez les personnes qui présentent une infection par le VHC symptomatique, ce qui semble indiquer une réponse immunitaire plus robuste Note de bas de page 38. Environ 50 % à 85 % des cas d'infection aiguë du VHC se transforment en infection chronique, mais demeurent asymptomatiques pendant des décennies Note de bas de page 39.
Le VHC est hautement transmissible; il se transmet par contact avec du sang contaminé. La majorité des infections par le VHC au Canada se produisent par le partage de matériel de préparation et d'injection de drogues (p. ex. cuiseur, eau, filtre) Note de bas de page 40. Dans le rapport de surveillance de 2011 sur le VHC au Canada, il était estimé qu'entre 54 % et 70 % des infections par le VHC déclarées entre 2005 et 2010 était dû à l'usage des drogues injectables Note de bas de page 40. Dans une étude dirigée par l'ASPC en 2009, 61 % des cas de VHC récemment diagnostiqués ont été associés à l'usage de drogues injectables Note de bas de page 41.
Aujourd'hui, le risque d'être infecté par le VHC à la suite de transfusions sanguines au Canada est extrêmement faible puisque tous les dons de sang sont soumis à un test de dépistage avant l'utilisation Note de bas de page 42. Dans son rapport de surveillance de 2015, la Société canadienne du sang a indiqué que le risque résiduel estimé de transmettre le VHC au Canada par le biais de transfusions sanguines était de 1 pour 12,6 millions de dons Note de bas de page 22. D'autres voies de transmission du VHC moins fréquentes comprennent la propagation par le partage de matériel d'hygiène personnelle et d'instruments pointus avec une personne infectée (p. ex. rasoirs, brosses à dents, ciseaux, coupe-ongles), de même que l'équipement pour renifler ou fumer des drogues (p. ex. pailles, pipes).
On croit que la transmission sexuelle est rare en général, bien que les hommes séropositifs ayant des relations sexuelles avec d'autres hommes semblent être à risque plus élevé de contracter le VHC par transmission sexuelle Note de bas de page 43. En outre, les couples qui ont des relations sexuelles non protégées au cours du cycle menstruel d'une femme risquent d'être infectés par le VHC Note de bas de page 42. La transmission verticale de la mère à l'enfant a également été documentée Note de bas de page 44 Note de bas de page 45.
3.2 Tendances nationales
3.2.1 Tendances au fil du temps
Entre 2005 et 2014, les taux de cas déclarés d'infection par le VHC ont constamment diminué chez les hommes et les femmes, et semblent s'être stabilisés au cours des dernières années (figure 7). En 2005, un total de 12 990 cas ont été signalés, ce qui correspond à un taux de 40,2 cas pour 100 000 personnes, comparativement à 2014, où un total de 10 458 cas d'hépatite C ont été déclarés, ce qui correspond à un taux de 29,3 cas pour 100 000 personnes et à une diminution de 27 % par rapport à 2005.
Au cours de cette période, les taux étaient constamment plus élevés chez les hommes que chez les femmes. Chez les hommes, de 2005 à 2014, le taux d'infection par le VHC a diminué de 29,7 % (de 52,9 à 37,2 pour 100 000 personnes), tandis que chez les femmes, au cours de la même période, ce taux a diminué de 22,6 % (de 27,4 à 21,2 pour 100 000 personnes) (figure 7).
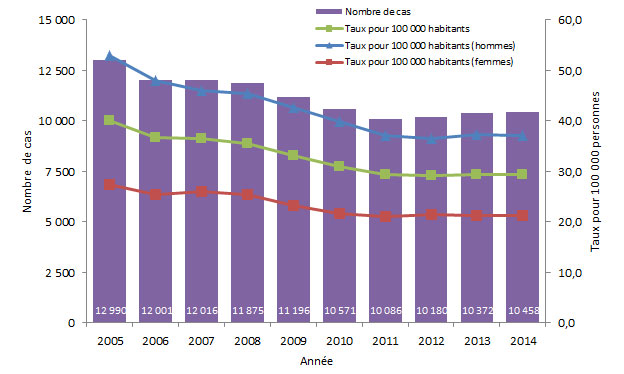
Figure 7 - Équivalent du texte
| Année | Nombre de cas | Taux pour 100 000 habitants | Taux pour 100 000 habitants (hommes) | Taux pour 100 000 habitants (femmes) |
|---|---|---|---|---|
| 2005 | 12 990 | 40,2 | 52,9 | 27,4 |
| 2006 | 12 001 | 36,7 | 47,9 | 25,4 |
| 2007 | 12 016 | 36,4 | 46,0 | 26,1 |
| 2008 | 11 875 | 35,6 | 45,4 | 25,4 |
| 2009 | 11 196 | 33,2 | 42,6 | 23,3 |
| 2010 | 10 571 | 31,0 | 40,0 | 21,5 |
| 2011 | 10 086 | 29,3 | 37,1 | 21,0 |
| 2012 | 10 180 | 29,2 | 36,6 | 21,4 |
| 2013 | 10 372 | 29,4 | 37,2 | 21,2 |
| 2014 | 10 458 | 29,3 | 37,2 | 21,2 |
3.2.2 Tendances selon le groupe d'âge et le sexe
Les taux les plus élevés d'infection par le VHC ont été observés chez les personnes âgées de 20 à 59 ans et variaient de 38,1 à 58,2 pour 100 000 personnes chez les hommes, par rapport à 27,2 à 42,1 pour 100 000 personnes chez les femmes (figure 8). Les jeunes, âgés de 0 à 19 ans, ont affiché les taux les plus bas : entre 0,6 et 6,5 pour 100 000 personnes chez les hommes et 1,0 à 13,2 pour 100 000 personnes chez les femmes (figure 8).

Figure 8 - Équivalent du texte
| Groupe d'âge | Hommes | Femmes |
|---|---|---|
| 0-14 | 0,6 | 1,0 |
| 15-19 | 6,5 | 13,2 |
| 20-24 | 38,1 | 35,2 |
| 25-29 | 55,0 | 42,1 |
| 30-39 | 51,0 | 30,6 |
| 40-59 | 58,2 | 27,2 |
| 60+ | 30,7 | 13,7 |
Entre 2005 et 2014, on a observé des baisses du taux de cas d'infection déclarés par le VHC chez les hommes de tous les groupes d'âge, à l'exception de ceux âgés de 60 ans et plus et de 20 à 24 ans, ces ceux groupes d'âge ayant connu une augmentation du taux de 21,6 pour 100 000 personnes à 30,7 pour 100 000 personnes, et de 33,0 pour 100 000 personnes à 38,1 pour 100 000 personnes, respectivement. Chez les hommes âgés de 25 à 29 ans, les taux d'infection par le VHC déclarée entre 2005 et 2014 sont restés stables. Les taux déclarés des hommes âgés de 40 à 59 ans étaient constamment plus élevés par rapport à d'autres groupes d'âge. En 2005, les hommes âgés de 40 à 59 ans détenaient le taux le plus élevé de cas déclarés d'infection par le VHC, soit 100,4 cas pour 100 000 personnes. À compter de 2014, ce taux a diminué à 58,2 pour 100 000 personnes (diminution de 42 % entre 2005 et 2014). Une importante diminution du taux a également été observée chez les hommes de 30 à 39 ans; de 2005 à 2014, les taux d'infection par le VHC ont diminué, passant de 83,7 à 51,0 cas pour 100 000 personnes (figure 9). Bien qu'il soit difficile de le prédire, à ce stade, les taux d'infection par le VHC chez les hommes âgés de 20 à 30 ans présentent une tendance à la hausse depuis 2012. Au cours de la période 2005 à 2014, une diminution importante du taux d'infection par le VHC déclarée a été observée uniquement dans deux groupes d'âge pour les hommes : De 30 à 39 ans, dont le taux est diminué de 83,7 à 51,0 pour 100 000 personnes (figure 9) et de 40 à 59 ans dont le taux de VHC est diminué de 100,4 à 58,2 pour 100 000 personnes, ce qui correspond à une diminution de 39,1 % et de 42,0 %, respectivement. Parmi tous les groupes d'âge pour les hommes, les taux étaient relativement stables au cours de la période précisée (figure 9).

Figure 9 - Équivalent du texte
| Année | 0 à 14 ans | 15 à 19 ans | 20 à 24 ans | 25 à 29 ans | 30 à 39 ans | 40 à 59 ans | 60 ans et plus |
|---|---|---|---|---|---|---|---|
| 2005 | 1,1 | 6,7 | 33,0 | 56,3 | 83,7 | 100,4 | 21,6 |
| 2006 | 0,8 | 5,8 | 28,7 | 50,5 | 72,6 | 92,7 | 20,6 |
| 2007 | 0,9 | 6,7 | 29,0 | 50,3 | 67,8 | 87,7 | 22,0 |
| 2008 | 1,1 | 5,7 | 30,8 | 50,6 | 61,7 | 88,3 | 22,1 |
| 2009 | 1,1 | 5,0 | 27,6 | 50,0 | 61,3 | 81,6 | 20,1 |
| 2010 | 0,8 | 5,8 | 26,6 | 42,0 | 54,8 | 76,6 | 22,6 |
| 2011 | 0,7 | 6,2 | 23,6 | 43,0 | 51,2 | 68,1 | 24,6 |
| 2012 | 0,8 | 5,8 | 30,6 | 41,3 | 51,3 | 64,2 | 26,0 |
| 2013 | 0,7 | 6,4 | 38,9 | 46,1 | 50,8 | 61,2 | 29,6 |
| 2014 | 0,6 | 6,5 | 38,1 | 55,0 | 51,0 | 58,2 | 30,7 |
Une tendance à la baisse du taux d'infection par le VHC a également été constatée chez les femmes âgées de 30 à 59 ans, mais de moindre ampleur que chez les hommes. Chez les personnes âgées entre 20 à 29 ans, les taux ont diminué de façon constante de 2005 à 2011 et ont depuis augmenté pour atteindre ou dépasser les niveaux de 2005. Le taux chez des personnes âgées de 60 ans et plus, a essentiellement été stable récemment tandis que celui des personnes de 15 à 19 ans a légèrement augmenté depuis 2011 (figure 10).

Figure 10 - Équivalent du texte
| Année | 0 à 14 ans | 15 à 19 ans | 20 à 24 ans | 25 à 29 ans | 30 à 39 ans | 40 à 59 ans | 60 ans et plus |
|---|---|---|---|---|---|---|---|
| 2005 | 1,4 | 13,2 | 36,5 | 35,4 | 45,6 | 40,5 | 15,8 |
| 2006 | 1,3 | 12,0 | 30,2 | 40,5 | 39,4 | 38,0 | 14,6 |
| 2007 | 1,2 | 11,7 | 31,4 | 39,5 | 39,8 | 40,7 | 14,1 |
| 2008 | 1,3 | 12,8 | 33,6 | 37,8 | 40,2 | 37,6 | 14,5 |
| 2009 | 1,0 | 12,9 | 29,9 | 36,0 | 34,8 | 35,3 | 13,0 |
| 2010 | 1,1 | 9,1 | 29,2 | 33,2 | 32,0 | 33,1 | 11,9 |
| 2011 | 1,0 | 8,2 | 27,1 | 32,5 | 31,5 | 32,0 | 12,5 |
| 2012 | 1,0 | 10,1 | 32,8 | 38,1 | 32,1 | 29,9 | 12,6 |
| 2013 | 0,7 | 12,1 | 33,0 | 40,9 | 30,6 | 28,1 | 13,7 |
| 2014 | 1,0 | 13,2 | 35,2 | 42,1 | 30,6 | 27,2 | 13,7 |
3.2.3 Tendances par province et par territoire
En 2014, les taux les plus élevés de cas déclarés d'hépatite C ont été observés en Saskatchewan (54,4 pour 100 000 personnes) au Yukon (54,0 pour 100 000 personnes), à l'Île-du-Prince-Édouard (49,9 pour 100 000 personnes), en Colombie-Britannique (42,5 pour 100 000 personnes), dans les Territoires du Nord-Ouest (40,9 pour 100 000 personnes), en Alberta (34,4 pour 100 00 personnes), en Nouvelle-Écosse (33,9 pour 100 000 personnes) et en Ontario (30,7 pour 100 000 personnes), dont les taux étaient tous supérieurs à la moyenne nationale de 29,3 pour 100 000 personnes (tableau 3). Dans toutes les provinces et tous les territoires, les taux chez les hommes étaient systématiquement supérieurs à ceux des femmes, sauf au Nunavut. L'inverse observé au Nunavut devrait être interprété avec prudence, étant donné le petit nombre de cas déclarés.
| Province / territoire | Homme | Femme | TotalNote de bas de page 1 | |||
|---|---|---|---|---|---|---|
| Nombre de cas | Taux pour 100 000 personnes | Nombre de cas | Taux pour 100 000 personnes | Nombre de cas | Taux pour 100 000 personnes | |
| Canada | 6 579 | 37,2 | 3 811 | 21,2 | 10 458 | 29,3 |
| C.-B. | 1 290 | 55,6 | 693 | 29,5 | 1 985 | 42,5 |
| Alb. | 890 | 42,3 | 531 | 26,1 | 1 423 | 34,4 |
| Sask. | 362 | 63,8 | 249 | 44,7 | 612 | 54,4 |
| Man. | 207 | 32,4 | 145 | 22,4 | 352 | 27,4 |
| Ont. | 2 623 | 38,9 | 1 579 | 22,6 | 4 214 | 30,7 |
| Qc | 724 | 17,7 | 352 | 8,5 | 1 127 | 13,7 |
| N.-B. | 123 | 33,0 | 57 | 14,9 | 180 | 23,8 |
| N.-É. | 205 | 44,3 | 115 | 23,9 | 320 | 33,9 |
| Î.-P.-É. | 46 | 64,5 | 27 | 36,0 | 73 | 49,9 |
| T.-N.-L. | 78 | 29,9 | 50 | 18,7 | 128 | 24,2 |
| Yn | 13 | 69,1 | 7 | 38,5 | 20 | 54,0 |
| T.N.-O. | 17 | 75,6 | 1 | 4,6 | 18 | 40,9 |
| Nt | 1 | 5,3 | 5 | 28,6 | 6 | 16,6 |
|
||||||
3.3 Discussion
L'infection par le VHC est un problème de santé publique important qui touche certains segments de la population canadienne, et qui a de nombreuses répercussions sur le traitement et les soins Note de bas de page 23. En 2013, aucun décès découlant d'une infection chronique par le VHC n'a été déclaré au Canada (par rapport à 33 en 2012); toutefois, 465 décès ont été attribués à une infection aiguë par le VHC Note de bas de page 15. Comme pour le VHB, le nombre de décès liés au VHC est probablement grandement sous-estimé en raison de la possible classification erronée sur les certificats de décès Note de bas de page 46.
Selon une étude menée en 2010, il a été estimé que, en Ontario, l'infection par le VHC représentait le plus important fardeau des maladies infectieuses en ce qui concerne le nombre d'années de vie perdues en raison d'un décès précoce, les années équivalentes de fonctionnement réduit et les années de vie ajustées en fonction de la santé, ce qui souligne l'impact de cette infection sur la santé des Canadiens Note de bas de page 47. Une étude de 2014 a estimé que d'ici 2035, 23 % des patients atteints d'hépatite C chronique éprouveront des complications graves. Entre 2013 et 2035, le taux de cirrhoses compensées devrait augmenter de 89 %, le taux de cirrhoses décompensées de 80 %, le taux de carcinomes hépatocellulaires de 205 % et le nombre de décès liés au foie de 160 % Note de bas de page 48. Une autre étude publiée en 2016 a indiqué qu'entre 1990 et 2013, les années de vie corrigées de l'incapacité dans les pays nord-américains à revenu élevé ont augmenté de 89,2 pour 100 000 personnes à 177,2 pour 100 000 personnes pour les infections par le VHC attribuables à l'utilisation de drogues injectables Note de bas de page 49.
Entre 2005 et 2014, les taux de cas déclarés de VHC ont diminué de 27 %. Bien que les hommes aient toujours représenté une plus grande proportion de cas déclarés de VHC, particulièrement chez le groupe d'âge des 30 ans et plus, les différences entre les taux de cas déclarés de VHC chez les hommes et les femmes se sont amenuisées depuis 2005 en raison d'une diminution plus importante dans le nombre de cas d'infection par le VHC déclarés chez les hommes (30 %) par rapport aux femmes (23 %).
Au Canada, le plus important mode de transmission du VHC est le partage de matériel d'injection de drogues contaminé. Parmi les nouveaux cas d'infection par le VHC au début des années 2000 pour lesquels on possède des renseignements en matière de facteurs de risque connus, 61 % avaient déclaré des antécédents d'utilisation de drogues injectables Note de bas de page 50. I-Track, système de surveillance comportementale et biologique à l'échelle nationale qui assure le suivi du VIH et de l'hépatite C et des comportements à risque associés parmi les utilisateurs de drogues injectables au Canada, a permis de révéler que l'exposition à vie à l'infection par le VHC (tel qu'il a été mesuré par la présence d'anticorps anti-VHC dans un échantillon de gouttes de sang séchées) était de 68 % au cours de la phase 3 de la collecte de données effectuée de 2010 à 2012 Note de bas de page 41. La majorité des participants au système I-Track (et la majorité des utilisateurs de drogues injectables en général) sont des hommes, ce qui peut en partie expliquer pourquoi les taux de cas déclarés de VHC sont plus élevés chez les hommes. Les différences entre les taux d'infections déclarées et d'infections non diagnostiquées chez les hommes et les femmes peuvent être le reflet des différents comportements liés aux tests, car les femmes sont plus susceptibles d'avoir recours à des soins de santé et de subir un test de dépistage Note de bas de page 51.
Les tendances dans les taux de VHC peuvent être touchées par les changements observés dans les pratiques de consommation de drogues. Par exemple, des études ont démontré que l'utilisation de drogues fumées ou reniflées comme le crack cocaïne au lieu de celles administrées principalement par injection peuvent réduire le risque de transmission du VHC et des autres infections à diffusion hématogène Note de bas de page 52. Les interventions de santé publique visant à prévenir les conséquences négatives de l'usage de substances psychoactives peuvent aussi avoir un effet important sur ces tendances et avoir une incidence sur les taux de transmission Note de bas de page 53.
Comme pour l'infection par le VHB, des changements dans les pratiques de dons de sang et de contrôle des infections peuvent avoir contribué à la baisse des taux de VHC au Canada. Les données de la Société canadienne du sang pour 2013 indiquent que le VHC a été détecté selon un taux de 56 cas pour 100 000 personnes faisant un don pour la première fois et de 0,5 cas pour 100 000 personnes faisant un don répété Note de bas de page 22. Le dépistage des dons de sang et l'élimination des dons positifs sont d'importantes protections pour la prévention de la transmission des infections à diffusion hématogène, y compris le VHC Note de bas de page 22. En vertu du Programme de contributions pour la sûreté du sang (PCSS) de l'ASPC par l'entremise de ses systèmes de surveillance (Système de surveillance des incidents transfusionnels [SSIT], Système de surveillance des erreurs transfusionnelles [SSET]), aucun cas d'infection par le VHC liée à une transfusion sanguine n'a été déclaré.
L'Enquête canadienne sur les mesures de la santé (ECMS) a estimé que la séroprévalence des anticorps contre le VHC (anti-VHC), un paramètre de l'exposition à vie au virus, était de 0,5 % parmi la population vivant dans un ménage au Canada durant une période de collecte de données s'étalant de 2007 à 2011 Note de bas de page 31. Toutefois, les estimations modélisées de la prévalence tenant compte des populations vulnérables non interrogées par l'ECMS (comme les sans-abri, les détenus et les personnes nées à l'étranger qui ne parlent pas l'anglais ou le français) indiquent que le taux de l'anti-VHC au sein de la population canadienne pourrait être plus près de 1 % (intervalle de plausibilité de 0,6 % à 1,3 %) et qu'a peu près 42 % à 45 % de ces personnes ne sont pas au courant de leur état. La prévalence de l'infection chronique par le VHC a été estimée à 0,6 % Note de bas de page 54.
Une autre source de cas d'infection par le VHC peut être l'immigration au Canada en provenance de pays où le virus est endémique , en particulier des régions où des mesures de contrôle visant à prévenir la transmission des infections transmissibles par le sang en milieu de soins de santé ne sont pas systématiquement mises en œuvre. En 2002, on a estimé que les immigrants représentaient 20 % des cas d'hépatite C dans l'ensemble du Canada Note de bas de page 55.
3.4 Limites
L'interprétation des résultats du présent rapport devrait tenir compte des diverses limites des données. Tout d'abord, la définition de cas d'infection par le VHC utilisée à des fins de surveillance nationale et de protocoles de production de rapports utilisés par les provinces et les territoires a évolué avec le temps, ce qui pourrait avoir eu une influence sur la déclaration de cas. La définition de cas a systématiquement permis de réaliser des tests de confirmation à l'aide d'un essai immunoenzymatique (EIA) d'un deuxième fabricant. Les plus faibles sensibilité et spécificité de la première et de la deuxième génération de ces essais de VHC ont pu avoir des répercussions sur l'exactitude des données de la surveillance du VHC Note de bas de page 56.
Ensuite, on ignore dans quelle mesure ces données reflètent l'incidence réelle du VHC. Les personnes atteintes d'une infection aiguë par le VHC sont souvent asymptomatiques et, par conséquent, elles pourraient ne pas avoir subi un test ou reçu un diagnostic. Les données du SCSMDO peuvent donc refléter principalement les cas d'infection chronique. Selon les résultats de l'ECMS, seulement 30 % des répondants canadiens dont les tests avaient révélé la présence actuelle d'une infection par le VHC ont indiqué qu'ils avaient reçu un diagnostic d'infection par le VHC Note de bas de page 29. De plus, en raison de la longue durée de l'infection et de la réinfection, il est possible qu'une personne ait subi un test de dépistage et reçu un diagnostic dans plus d'une province ou d'un territoire au fil du temps et, par conséquent, qu'elle ait été comptée plus d'une fois dans l'ensemble de données du SCSMDO.
D'autre part, les données accessibles depuis le SCSMDO ont été analysées uniquement en fonction de l'âge, du sexe et de la province ou du territoire. Pour le moment, le SCSMDO ne dispose d'aucun autre élément de données permettant d'expliquer les tendances observées. En conséquence, il est impossible d'établir avec certitude la proportion de cas déclarés d'infections par le VHC attribuables à la transmission par l'utilisation de drogues injectables, à d'autres comportements à risque ou si le virus affecte de façon disproportionnée d'autres groupes ou populations. Les données de surveillance doivent être interprétées en fonction d'autres renseignements disponibles pour établir l'épidémiologie du VHC au Canada.
Finalement, les renseignements sur le caractère aigu ou chronique des cas déclarés d'infection par le VHC n'étaient pas accessibles pour la plupart des provinces et des territoires. Par conséquent, les résultats ne permettent pas d'interpréter les tendances actuelles possibles en matière de transmission ou le fardeau potentiel de l'infection par le VHC au Canada. De même, les erreurs dans le classement des cas d'infection aiguë permettant de faire la distinction entre les infections chroniques ou non précisées ne peuvent être écartées.
3.5 Conclusion
Les taux de nouveaux diagnostics d'infection par le VHC semblent diminuer au Canada. Compte tenu de la possibilité qu'une infection par le VHC entraîne de plus lourds problèmes et du potentiel subséquent de fardeau sur le système de soins de santé du Canada, une surveillance continue du VHC est requise.
Pour améliorer la capacité des données de surveillance a évaluer les progrès en matière de prévention et de lutte contre l'infection par le VHC, des efforts supplémentaires sont en train d'être déployés pour harmoniser la déclaration des cas d'hépatite C par stade d'infection et pour améliorer la qualité des données sur le VHC recueillies par l'intermédiaire d'une surveillance de routine.
Références
- Note de bas de page 1
-
Agence de la santé publique du Canada. Définitions nosologiques des maladies transmissibles faisant l'objet d'une surveillance nationale. Mis à jour en 2011. Inédit.
- Note de bas de page 2
-
Agence de la santé publique du Canada. Système de surveillance des maladies à déclaration obligatoire, rapport canadien 2005-2008. 2012.
- Note de bas de page 3
-
Agence de la santé publique du Canada. Supplément : Définitions nosologiques des maladies transmissibles faisant l'objet d'une surveillance nationale. 2009. Relevé des maladies transmissibles au Canada 2009; 35(Supp 2).
- Note de bas de page 4
-
Gitlin N. Hepatitis B: diagnosis, prevention, and treatment. Clin Chem 1997; 43(8 Pt 2):1500-1506.
- Note de bas de page 5
-
Ganem D, Prince AM. Hepatitis B Virus Infection -- Natural History and Clinical Consequences. N Engl J Med 2004; 350(11):1118-1129.
- Note de bas de page 6
-
Heymann D (éd.). Control of communicable diseases manual. 19th ed. United States of America: American Public Health Association; 2008.
- Note de bas de page 7
-
Gray Davis L, Weber D, Lemon S. Horizontal transmission of hepatitis B virus. The Lancet 1989; 333(8643):889-893.
- Note de bas de page 8
-
Modi AA, Feld JJ. Viral Hepatitis and HIV in Africa. AIDS Reviews 2007; 9(1):25.
- Note de bas de page 9
-
Organisation mondiale de la Santé. Hépatite B (Aide-mémoire no 204). 2013. Accès : http://www.who.int/mediacentre/factsheets/fs204/fr/. Consulté le 8 août 2013.
- Note de bas de page 10
-
Organisation mondiale de la Santé. Vaccins anti-hépatite B. Relevé épidémiologique hebdomadaire. 2009; 84(40):405-420.
- Note de bas de page 11
-
Agence de la santé publique du Canada. Soins primaires de l'hépatite B - Aide-Mémoire. 2013.
- Note de bas de page 12
-
Comité consultatif national de l'immunisation (CCNI). Rapport national sur l'immunisation au Canada : mise à jour du programme. Paediatr Child Health 1999; 4(Supp C):30C.
- Note de bas de page 13
-
Agence de la santé publique du Canada. Guide canadien d'immunisation : Partie 4, Agents d'immunisation active - Vaccin contre l'hépatite B. Mars 2017. Accès : https://www.canada.ca/fr/sante-publique/services/publications/vie-saine/guide-canadien-immunisation-partie-4-agents-immunisation-active/page-7-vaccin-contre-hepatite-b.html. Consulté en mars 2017.
- Note de bas de page 14
-
Santé Canada. Guide canadien d'immunisation. 6e éd. 2002.
- Note de bas de page 15
-
Statistique Canada, Statistique de l'état civil, Base de données sur les décès. Tableau de CANSIM 102-0521. Décès, selon la cause, Chapitre I : Certaines maladies infectieuses et parasitaires (A00 à B99), le groupe d'âge et le sexe, Canada. 2014. Accès : http://www5.statcan.gc.ca/cansim/a05?id=1020521&retrLang=fra&lang=fra. Consulté le 11 avril 2017.
- Note de bas de page 16
-
Pohani G, Zou S, Tepper M. Trends of hepatitis B and hepatitis C mortality in Canada, 1979-1997. Can J Public Health 2001 Jul-Aug; 92(4):250-254.
- Note de bas de page 17
-
CDC. Viral Hepatitis Surveillance. CDC, CDC. Washington DC: Centers for Disease Control and Prevention. United States, 2014. Accès : https://www.cdc.gov/hepatitis/statistics/2014surveillance/index.htm. Consulté le 11 avril 2017.
- Note de bas de page 18
-
PHE. Acute hepatitis B (England): annual report for 2015. Public Health England, Public Health England. London:Public Health England, 2016. Pg. 1 - 6; Accès : https://www.gov.uk/government/uploads/system/uploads/attachment_data/file/549028/hpr2816_hepB.pdf. Consulté le 11 avril 2017.
- Note de bas de page 19
-
Agence de la santé publique du Canada. Mise à jour des recommandations concernant l'utilisation du vaccin contre l'hépatite B. Ottawa, ASPC, 2017. Accès : https://www.canada.ca/fr/sante-publique/services/publications/vie-saine/mise-a-jour-recommandations-utilisation-vaccin-hepatite-b.html. Consulté le 11 avril 2017.
- Note de bas de page 20
-
Laroche J, Frescura A, Belzak L. Résultats de l'Enquête sur la couverture vaccinale nationale des enfants de 2006 et 2009. Conférence canadienne sur l'immunisation, Québec (Québec). 2010.
- Note de bas de page 21
-
Agence de la santé publique du Canada. Couverture vaccinale des enfants canadiens : Résultats de l'Enquête sur la couverture vaccinale nationale des enfants de 2011. 2014. Accès : http://www.phac-aspc.gc.ca/im/nics-enva/vccc-cvec-fra.php. Consulté en mai 2014.
- Note de bas de page 22
-
Société canadienne du sang. Surveillance Report, 2015. Ottawa: SCS, 2015. Accès : https://www.blood.ca/sites/default/files/blood/blood-safety/External-Surveillance-Report-2014-fr.pdf. Consulté le 11 avril 2017.
- Note de bas de page 23
-
Institut canadien d'information sur la santé. Registre canadien des insuffisances et des transplantations d'organes 2016. Ottawa, Ontario. Accès : https://www.cihi.ca/fr/registre-canadien-des-insuffisances-et-des-transplantations-dorganes-2016
- Note de bas de page 24
-
Fondation canadienne du foie. Les maladies du foie au Canada : Une crise en devenir. 2013.
- Note de bas de page 25
-
Greenaway C, Narasiah L, Plourde P, Ueffing E, Pottie K, Deschenes M, et al. Appendix 5: Hepatitis B: evidence review for newly arriving immigrants and refugees. Can Med Assoc J 2011; 183(12).
- Note de bas de page 26
-
Pottie K, Greenaway C, Feightner J, Welch V, Swinkels H, Rashid M, Narasiah L,. Kirmayer LJ, Ueffing E, MacDonald NE, Hassan G, McNally M, Kahn K, Buhrmann R, Dunn S, Dominic A,. McCarthy AE, Gagnon AJ, Rousseau C, Tugwell P. Evidence-based clinical guidelines for immigrants and refugees. Can Med Assoc J 2011; 183(12).
- Note de bas de page 27
-
Rossi C, Shrier I, Marshall Lee, Cnossen S, Schartzman K, Kleing M, Scharzer G, Greenaway C. Seroprevalence of Chronic Hepatitis B Virus Infection and Prior Immunity in Immigrants and Refugees: A Systematic Review and Meta-Analysis. PLoS ONE: e44611, 2012. Accès : http://journals.plos.org/plosone/article/file?id=10.1371/journal.pone.0044611&type=printable. Consulté le 12 avril 2017.
- Note de bas de page 28
-
Centre de contrôle des maladies de la Colombie-Britannique. British Columbia Annual Summary of Reportable Diseases, 2013. 2014.
- Note de bas de page 29
-
Statistique Canada. Guide de l'utilisateur des données de l'Enquête canadienne sur les mesures de la santé (ECMS) : Cycle 1. 2011.
- Note de bas de page 30
-
Statistique Canada. Liste d'autres documents de l'Enquête canadienne sur les mesures de la santé (ECMS) disponibles. 2013. Accès : http://www23.statcan.gc.ca/imdb-bmdi/document/5071_D4_T9_V1-fra.htm. Consulté le 18 décembre 2013.
- Note de bas de page 31
-
Rotermann M, Langlois K, Andonov A, Trubnikov M. Séroprévalence des infections par le virus de l'hépatite B et par le virus de l'hépatite C : Résultats de l'Enquête canadienne sur les mesures de la santé, 2007 à 2009 et 2009 à 2011. Rapports sur la santé. 2013; 24(11):3-13.
- Note de bas de page 32
-
Jafari S, Buxton JA, Afshar K, Copes R, Baharlou S. Tattooing and Risk of Hepatitis B: A Systematic Review and Meta-analysis. Can J Public Health 2012 May-Jun; 103(3):207-212.
- Note de bas de page 33
-
Zhang J, Zou S, Giulivi A. Epidemiology of hepatitis B in Canada. Can J Infect Dis 2001; 12(6):345-350.
- Note de bas de page 34
-
Moses S, Mestery K, Kaita KD, Minuk GY. Viral hepatitis in a Canadian street-involved population. Can J Public Health 2002; 93(2):123-128.
- Note de bas de page 35
-
Huang L, Gilbert ML, Rossi MF, Haase D, Wright J, Sicard N, et al. Trends in Vaccine-induced Immunity to Hepatitis B among Canadian Street-involved Youth. J Urban Health 2010; 87(2):337-348.
- Note de bas de page 36
-
Nguyen T, Liang RH, Khudyakov Y, Olmstead A, et al. (2016, March 30). The spread of hepatitis C virus genotype 1a in North America:a retrospective phylogenetic study. Lancet Infect Dis 2016; 16(6):698-702.
- Note de bas de page 37
-
Messina JP, Humphreys I, Flaxman A, Brown A, Cooke GS, Pybus OG, et al. Global distribution and prevalence of hepatitis C virus genotypes. Hepatology 2015; 61(1):77-87.
- Note de bas de page 38
-
Micallef JM, Kaldor JM, Dore GJ. Spontaneous viral clearance following acute hepatitis C infection: a systematic review of longitudinal studies. J Viral Hepat 2006 Jan; 13(1):34-41.
- Note de bas de page 39
-
Wong T, Lee SS. Hepatitis C: a review for primary care physicians. Can Med Assoc J 2006 Feb 28; 174(5):649-659.
- Note de bas de page 40
-
Agence de la santé publique du Canada. L'hépatite C au Canada : Rapport de surveillance de 2005-2010. Ottawa : ASPC, 2011. Accès : http://publications.gc.ca/collections/collection_2012/aspc-phac/HP40-70-2012-fra.pdf. Consulté le 12 avril 2017.
- Note de bas de page 41
-
Ha S, Totten S, Pogany L, Wu J, Gale-Rowe M. L'hépatite C au Canada et l'importance du dépistage fondé sur les risques. Relevé des maladies transmissibles au Canada (RMTC) 2016; 42:57-62. Accès : http://www.phac-aspc.gc.ca/publicat/ccdr-rmtc/16vol42/dr-rm42-3/assets/pdf/16vol42_3-ar-02-fra.pdf. Consulté le 12 avril 2017.
- Note de bas de page 42
-
Fondation canadienne du foie. Hépatite C. 2016. Accès : http://www.liver.ca/fr/liver-disease/types/viral_hepatitis/Hepatitis_C.aspx. Consulté le 11 avril 2017.
- Note de bas de page 43
-
Totten S, McGuire M, Cox J, Lambert G, Fyfe M, Husbands W, et al. Hepatitis C virus in men who have sex with men with no history of injection drug use - evidence for sexual transmission? A Canadian perspective. Sex Transm Infec 2011 Jul; 87(Supp 1):A145.
- Note de bas de page 44
-
Bevilacqua E, Fabris A, Floreano P, Pembrey L, Newell ML, Tovo PA, et al. Genetic factors in mother-to-child transmission of HCV infection. Virol J 2009 Jul 20; 390(1):64-70.
- Note de bas de page 45
-
Ngo-Giang-Huong N, Jourdain G, Sirirungsi W, Decker L, Khamduang W, Le Coeur S, et al. Human immunodeficiency virus-hepatitis C virus co-infection in pregnant women and perinatal transmission to infants in Thailand. Int J Infect Dis 2010 Jul; 14(7):e602-7.
- Note de bas de page 46
-
Mahajan R, Xing J, Liu SJ, Ly KN, Moorman AC, Rupp L, et al. Mortality among persons in care with hepatitis C virus infection: the Chronic Hepatitis Cohort Study (CHeCS), 2006-2010. Clin Infect Dis 2014 Apr; 58(8):1055-1061.
- Note de bas de page 47
-
Kwong J, Crowcroft N, Campitelli M, Ratnasingham S, Daneman N, Deeks S, et al. Ontario Burden of Infectious Disease Study (ONBOIDS): An OAHPP/ICES Report 2010;Toronto: Ontario Agency for Health Protection and Promotion, Institute for Clinical Evaluative Sciences.
- Note de bas de page 48
-
Myers RP, Krajden M, Bilodeau M, Kaita K, Marotta P, Peltekian K, Ramji A, Estes C, Razavi H, Sherman M. Burden of disease and cost of chronic hepatitis C virus infection in Canada. Can J Gastroenterol Hepatol. 2014 May; 28(5):243-250.
- Note de bas de page 49
-
Degenhardt L, Charlson F, Stanaway J, Larney S, Alexander LT, Hickman M, Cowie B, Hall WD, Strang J, Whiteford H, Vos T.. Estimating the burden of disease attributable to injecting drug use as a risk factor for HIV, hepatitis C, and hepatitis B: findings from the Global Burden of Disease Study 2013. Lancet Infect Dis. 2016 Dec; 16(12):1385-1398.
- Note de bas de page 50
-
Agence de la santé publique du Canada, Section de la surveillance et de l'épidémiologie des ITS et de l'hépatite C. Épidémiologie de l'infection aiguë par le virus de l'hépatite C au Canada. Résultats du Système de surveillance accrue des souches de l'hépatite (SSASH). 2009.
- Note de bas de page 51
-
Galdas PM, Cheater F, Marshall P. Men and health help-seeking behaviour: literature review. J Adv Nurs 2005 Mar; 49(6):616-623.
- Note de bas de page 52
-
Strike C, Gohil H, Watson TM. La distribution de matériel plus sécuritaire pour fumer le crack (cocaïne) : lignes directrices exhaustives pour des pratiques exemplaires. Point de mire sur la prévention. Automne 2014. Accès : http://www.catie.ca/fr/pdm/automne-2014/distribution-materiel-plus-securitaire-fumer-crack-cocaine-lignes-directrices-exhau
- Note de bas de page 53
-
Grebely J, Lima VD, Marshall BD, Milloy MJ, DeBeck K, Montaner J, et al. Declining incidence of hepatitis C virus infection among people who inject drugs in a Canadian setting, 1996-2012. PLoS One 2014 Jun 4; 9(6):e97726.
- Note de bas de page 54
-
Trubnikov M, Yan P, Archibald C. Estimation de la prévalence de l'infection par le virus de l'hépatite C au Canada, 2011. Relevé des maladies transmissibles au Canada (RMTC) 2014; 40(19).
- Note de bas de page 55
-
Greenaway C, Thu Ma A, Kloda Lorie A, Klein M, Cnossen S, Guido S, Shrier Ian The Seroprevalence of Hepatitis C Antibodies in Immigrants and Refugees from Intermediate and High Endemic Countries: A Systematic Review and Meta-Analysis, 2015. Accès : http://journals.plos.org/plosone/article/file?id=10.1371/journal.pone.0141715&type=printable. Consulté le 12 avril 2017.
- Note de bas de page 56
-
Kesli R. Evaluation of assay methods and false positive results in the laboratory diagnosis of hepatitis C virus infection. Archives of Clinical Microbiology 2011; 2(4):1-4.
Annexe A: Définitions de cas
| Stade de l'infection | Définition des casNote de bas de page 3 |
|---|---|
| Infection aiguë par le VHB | Antigène HBs et anticorps IgM anti-HBc positifs, lorsqu'il existe des antécédents cliniques compatibles ou une probabilité d'exposition OU Élimination de l'antigène HBs chez un cas ayant été recensé comme positif pour l'antigène HBs au cours des six derniers mois, lorsqu'il existe des antécédents cliniques compatibles ou une probabilité d'exposition |
| Cas confirmé d'infection chronique par le VHB | Persistance de l'antigène HBs pendant plus de six mois OU Détection de l'antigène HBs en l'absence documentée d'anticorps IgM anti-HBc OU Détection de l'ADN du VHB pendant plus de six mois |
| Infection par le VHB non préciséeNote de bas de page 1 | Profil sérologique incompatible avec la définition de cas aigu ou chronique et antigène HBs détecté OU Détection de l'ADN du VHB |
|
|
| Stade de l'infection | Définition des cas Note de bas de page 4 |
|---|---|
| Cas confirmé, sans distinction entre l'infection aiguë ou l'infection récente | Détection d'anticorps dirigés contre le virus de l'hépatite C (anti-VHC) ou d'ARN du virus de l'hépatite C (ARN du VHC) chez un sujet présentant une apparition discrète de symptômes, quels qu'ils soient, ou des signes d'une hépatite virale aiguë au cours des six mois précédant le premier test positif pour le virus de l'hépatite C ET réaction négative aux anticorps IgM anti-VHA, et résultat négatif au test de détection des anticorps IgM anti-HBc ou des antigènes HBs ET taux sériques d'alanine-aminotransférase (ALT) 2,5 fois supérieurs à la limite supérieure de la normale OU Détection d'anticorps contre le virus de l'hépatite C (anti-VHC) chez un sujet pour lequel un résultat négatif a été documenté suite à un test de dépistage des anticorps anti-VHC au cours des 12 mois précédents OU Détection de l'ARN du virus de l'hépatite C (ARN du VHC) chez un sujet pour lequel un résultat négatif a été documenté suite à un test d'ARN du VHC au cours des 12 mois précédents. |
| Cas confirmé - Non spécifié (y compris une infection chronique ou résolue)Note de bas de page 1 | Détection d'anticorps dirigés contre le virus de l'hépatite C (anti-VHC) OU Détection de l'ARN du virus de l'hépatite C (ARN du VHC) |
NOTE :
|
|
Annexe B: Taux déclarés d'infection aiguë et chronique par le VHB au Canada, entre 2005 et 2014
| P/T | 2005 | 2006 | 2007 | 2008 | 2009 | 2010 | 2011 | 2012 | 2013 | 2014 |
|---|---|---|---|---|---|---|---|---|---|---|
| C.-B. | 1,38 | 0,99 | 0,95 | 0,66 | 0,59 | 0,25 | 0,33 | 0,28 | 0,24 | 0,30 |
| Alb. | 0,78 | 0,87 | 0,51 | 0,91 | 0,70 | 0,61 | 0,58 | 0,61 | 0,65 | 0,24 |
| Sask. | 1,11 | 1,31 | 0,69 | 1,37 | 0,77 | 1,04 | 1,21 | 0,82 | 0,63 | 0,80 |
| Man. | ND | ND | ND | ND | 0,33 | 0,16 | 0,48 | 0,16 | 0,39 | 0,31 |
| Ont. | 1,23 | 1,44 | 1,32 | 1,11 | 1,00 | 0,96 | 0,92 | 0,76 | 0,80 | 0,76 |
| Qc | 0,61 | 0,52 | 0,58 | 0,57 | 0,43 | 0,28 | 0,30 | 0,37 | 0,22 | 0,24 |
| N.-B. | 0,80 | 0,54 | 1,07 | 0,53 | 1,07 | 0,53 | 1,06 | 0,40 | 0,13 | 1,19 |
| N.-É. | ND | ND | ND | ND | 0,32 | 0,11 | 0,53 | 0,21 | 0,74 | 0,74 |
| Î.-P.-É. | ND | ND | ND | ND | ND | ND | ND | ND | ND | ND |
| T.-N.-L. | ND | ND | ND | ND | ND | ND | ND | ND | ND | ND |
| Yn | ND | ND | ND | 0,00 | 0,00 | 2,87 | 0,00 | 0,00 | 0,00 | 0,00 |
| T.N.-O. | 0,00 | 0,00 | 0,00 | 0,00 | 3,05 | 0,00 | 0,00 | 0,00 | 2,81 | 2,76 |
| Nt | ND | ND | ND | ND | ND | ND | ND | ND | ND | ND |
| P/T | 2005 | 2006 | 2007 | 2008 | 2009 | 2010 | 2011 | 2012 | 2013 | 2014 |
|---|---|---|---|---|---|---|---|---|---|---|
| C.-B. | ND | ND | ND | ND | 26,54 | 25,74 | 22,68 | 21,12 | 23,24 | 20,79 |
| Alb. | 0,03 | 4,31 | 5,83 | 19,70 | 16,57 | 15,32 | 12,84 | 16,96 | 15,16 | 13,31 |
| Sask. | 8,05 | 6,85 | 0,00 | 0,00 | 7,79 | 8,14 | 6,82 | 12,45 | 9,10 | S.O. |
| Man. | ND | ND | ND | ND | 8,42 | 10,70 | S.O. | 4,14 | 4,65 | 5,37 |
| Ont. | ND | ND | ND | ND | ND | ND | ND | 17,05 | 14,95 | 13,64 |
| Qc | 8,63 | 9,72 | 8,93 | 9,02 | 8,11 | 6,06 | 4,64 | 5,85 | 6,61 | 6,58 |
| N.-B. | 2,01 | 3,76 | 3,75 | 3,48 | 3,99 | 4,24 | 3,18 | 5,15 | 5,69 | 3,97 |
| N.-É. | ND | ND | ND | ND | 0,53 | 0,64 | 0,42 | 0,85 | 0,53 | 1,80 |
| Î.-P.-É. | ND | ND | ND | ND | ND | ND | ND | ND | ND | ND |
| T.-N.-L. | ND | ND | ND | ND | ND | ND | ND | ND | ND | ND |
| Yn | ND | ND | ND | 0,00 | 0,00 | 11,50 | 14,07 | 8,28 | 16,56 | 16,21 |
| T.N.-O. | ND | ND | ND | 0,00 | 0,00 | 0,00 | 0,00 | 0,00 | 0,00 | 0,00 |
| Nt | ND | ND | ND | ND | ND | ND | ND | ND | ND | ND |
ND : Les provinces et les territoires n'ont pas déclaré de cas classés en tant qu'infections aiguës et chroniques par le VHB
ND : Les données de l'année en question n'étaient pas disponibles.
Annexe C: Déclaration des infections par le VHC au Canada: SCSMDO 2005 - 2014
| 2005 | 2006 | 2007 | 2008 | 2009 | 2010 | 2011 | 2012 | 2013 | 2014 | |
| BC | Les infections VHC ont été classées en aiguë, chronique et non spécifié | |||||||||
| AB | Les infections VHC ont été classées en aiguë, chronique et non spécifié | Signalé comme infection VHC non spécifiée | ||||||||
| SK | Les infections VHC ont été classées en aiguë, chronique et non spécifié | |||||||||
| MB | Les infections VHC ont été classées en aiguë, chronique et non spécifié | |||||||||
| ON | Les infections VHC ont été classées en aiguë, chronique et non spécifié | |||||||||
| QC | Les infections VHC ont été classées en aiguë, chronique et non spécifié | Signalé comme infection VHC non spécifiée | ||||||||
| NB | Les infections VHC ont été classées en aiguë, chronique et non spécifié | |||||||||
| NS | Les infections VHC ont été classées en aiguë, chronique et non spécifié | |||||||||
| PE | Les infections VHC ont été classées en aiguë, chronique et non spécifié | |||||||||
| NL | Les infections VHC ont été classées en aiguë, chronique et non spécifié | |||||||||
| YT | Les infections VHC ont été classées en aiguë, chronique et non spécifié | Signalé comme infection VHC non spécifiée | ||||||||
| NT | Les infections VHC ont été classées en aiguë, chronique et non spécifié | |||||||||
| NU | Les infections VHC ont été classées en aiguë, chronique et non spécifié | |||||||||