Recommandations pour la qualité de l'eau potable au Canada : document technique – le manganèse
Télécharger au format PDF
(1,10 Mo, 132 pages)
Organisation : Santé Canada
Type : Recommandations
Date publiée : 2019-05-10
Table des matières
Partie I. Vue d'ensemble et application
Partie II. Science et considérations techniques
- 4.0 Propriétés, utilisation et sources dans l'environnement
- 5.0 Exposition
- 6.0 Méthodes d'analyse
- 7.0 Techniques de traitement et considérations liées au réseau de distribution
- 7.1 Chimie et traitement du manganèse
- 7.2 Traitement à l'échelle municipale
- 7.3 Réseau de distribution
- 7.4 Traitement dans les systèmes résidentiels
- 8.0 Cinétique et métabolisme
- 9.0 Effets sur la santé humaine
- 10.0 Effets sur la santé des animaux de laboratoire
- 11.0 Mode d'action
- 12.0 Classification et évaluation
- 13.0 Justification de la recommandation
- 14.0 Références
- Annexe A : Liste des acronymes
Partie I. Vue d'ensemble et application
1.0 Recommandation
Une concentration maximale acceptable (CMA) de 0,12 mg/L (120 µg/L) est établie pour le manganèse total dans l'eau potable. Un objectif d'ordre esthétique (OE) de 0,02 mg/L (20 µg/L) est également établi pour le manganèse total dans l'eau potable.
2.0 Sommaire
Le manganèse est présent naturellement dans l'environnement et il est très répandu dans l'air, l'eau et le sol. On ne le retrouve pas sous sa forme élémentaire dans l'environnement, mais il peut exister sous plusieurs états d'oxydation. Dans l'environnement, la présence de manganèse dans l'eau peut être de source naturelle (vieillissement climatique du sol et des roches) ou anthropique (exploitation minière, rejets industriels, relargage provenant des sites d'enfouissement, etc.). Le manganèse est utilisé dans diverses industries, notamment dans l'industrie de l'acier, ainsi que pour la fabrication de différents produits (p. ex. les feux d'artifice, les piles sèches, les fertilisants, les fongicides, les cosmétiques et les peintures). Le manganèse peut également être ajouté à l'eau comme oxydant (permanganate) ou peut s'y retrouver comme impureté dans les coagulants utilisés pour le traitement de l'eau potable.
Ce document technique passe en revue et évalue tous les risques connus pour la santé qui sont associés à la présence de manganèse dans l'eau potable. Il tient compte des nouvelles études et approches, ainsi que de la disponibilité de techniques de traitement appropriées. D'après cet examen, la recommandation pour le manganèse dans l'eau potable est une concentration maximale acceptable (CMA) de 0,12 mg/L (120 μg/L), établie en fonction des nourrissons, qui constituent la population la plus sensible. Bien que la CMA ait été calculée en fonction des nourrissons, elle est établie pour protéger la santé de tous les Canadiens.
2.1 Effets sur la santé
Le manganèse est un élément essentiel pour les humains. Le risque de carence en manganèse est jugé faible au Canada, puisque l'apport en manganèse provenant des aliments se révèle suffisant. Puisque les études dont on dispose ne permettent pas d'établir un lien entre le manganèse et le cancer, un effet autre que le cancer a été retenu dans le cadre de cette évaluation. Certaines études menées chez les humains semblent établir un lien entre le manganèse présent dans l'eau potable et certains effets neurologiques chez les enfants. Toutefois, ces études ne peuvent être utilisées que pour appuyer le choix du principal effet sur la santé. Les effets observés chez les enfants concordent avec les effets neurologiques constatés dans les études clés sur les animaux qui ont servi à établir la CMA.
2.2 Considérations esthétiques
Les préoccupations relatives à la présence de manganèse dans l'eau potable sont souvent liées à des plaintes de consommateurs au sujet de la couleur de l'eau. L'objectif d'ordre esthétique (OE) de 0,02 mg/L (20 µg/L) a pour but de réduire au minimum le nombre de plaintes concernant la couleur de l'eau en raison de la présence d'oxydes de manganèse et d'accroître la confiance des consommateurs envers la qualité de l'eau potable.
2.3 Exposition
Le manganèse est présent naturellement et est très répandu dans l'environnement. La population canadienne peut être exposée au manganèse par sa présence dans l'air, dans les aliments, dans les produits de consommation, dans le sol et dans l'eau potable. Bien que les aliments constituent la principale source d'exposition, le manganèse dans l'eau potable est plus facilement absorbé que le manganèse contenu dans les aliments. Au Canada, les concentrations de manganèse dans l'eau douce sont généralement inférieures à 0,1 mg/L, avec parfois des pics de quelques milligrammes par litre. Il est parfois possible d'observer des niveaux plus élevés dans des conditions acides ou réductrices, par exemple dans des eaux souterraines, des lacs et des réservoirs, ainsi qu'en raison de rejets industriels. En général, on retrouve davantage de manganèse dans les eaux souterraines que dans les eaux de surface. L'absorption du manganèse dans l'eau potable par contact cutané ou par inhalation est jugée improbable.
2.4 Analyse et traitement
Il existe plusieurs méthodes d'analyse du manganèse total dans l'eau potable à des concentrations bien inférieures à la CMA et à l'OE. Le manganèse total comprend les formes particulaires et dissoutes de manganèse présentes dans un échantillon d'eau. Par conséquent, si les deux formes sont mesurées séparément, les deux concentrations doivent être additionnées avant de comparer le taux de manganèse total à la CMA et à l'OE.
On dispose de différentes méthodes pour ramener le taux de manganèse dans l'eau potable en deçà de la CMA. Le choix de la méthode la mieux adaptée dépend de la forme de manganèse présente dans la source d'eau. Les usines de traitement de l'eau bien exploitées et optimisées peuvent obtenir un taux de manganèse inférieur ou égal à 0,015 mg/L dans l'eau traitée, réduisant ainsi au minimum l'accumulation de manganèse et le rejet potentiel de manganèse ou d'autres contaminants dans l'eau distribuée. Cela permettrait d'éviter la présence de manganèse dans l'eau du robinet des consommateurs à un taux supérieur à l'OE, et de réduire à la fois le nombre de plaintes liées à la couleur de l'eau et la possibilité que des concentrations plus élevées de manganèse (qui pourraient excéder la CMA) se retrouvent dans l'eau du robinet. On recommande aux services publics d'établir un taux cible de manganèse inférieur ou égal à 0,015 mg/L dans l'eau traitée pour la conception et l'exploitation d'usines de traitement appelées à enlever le manganèse. Plusieurs techniques de traitement permettent d'éliminer efficacement le manganèse à l'échelle résidentielle. Cependant, il n'existait, lors de la rédaction de ce rapport, aucun dispositif de traitement certifié pour cet usage précis.
2.5 Réseau de distribution
De faibles taux de manganèse dans l'eau brute ou dans l'eau traitée (présents ou passés) peuvent s'accumuler dans le réseau de distribution et provoquer périodiquement des taux élevés de manganèse dans l'eau du robinet. De plus, d'autres contaminants, comme les métaux lourds, qui se déposent avec les oxydes de manganèse dans le réseau de distribution, peuvent également être libérés dans l'eau et être acheminés aux robinets des consommateurs. On recommande aux services publics d'élaborer un plan de gestion du réseau de distribution pour réduire la probabilité d'événements de relargage du manganèse dans le réseau de distribution. Ce plan inclut généralement une réduction au minimum des taux de manganèse entrant dans le réseau de distribution, l'utilisation des meilleures pratiques de nettoyage des conduites principales afin de minimiser les dépôts d'oxydes de manganèse dans le réseau de distribution, une réduction des perturbations physiques et hydrauliques, et le maintien de la stabilité chimique de l'eau.
2.6 Considérations internationales
Les recommandations, normes ou directives relatives à la qualité de l'eau potable établies par des gouvernements étrangers ou des agences internationales peuvent varier en raison des connaissances scientifiques disponibles au moment de l'évaluation, ainsi que de l'utilisation de différentes politiques et approches.
L'U.S. EPA a publié un avis de santé non réglementaire de 0,3 mg/L et établi une concentration maximale de contaminants secondaire de 0,05 mg/L, en se fondant sur des considérations d'ordre esthétique, pour le manganèse dans l'eau potable. L'Organisation mondiale de la santé a établi une valeur basée sur la santé (VBS) de 0,4 mg/L, mais a déterminé qu'il n'était pas nécessaire d'établir une recommandation formelle pour l'eau potable pour le manganèse, car le VBS est bien au-dessus des concentrations normalement présentes dans l'eau potable. Les directives australiennes sur l'eau potable (Australian Drinking Water Guidelines) indiquent une recommandation pour la santé de 0,5 mg/L et une recommandation esthétique de 0,1 mg / L pour le manganèse dans l'eau potable. Dans l'Union européenne, la directive du Conseil de la Commission européenne mentionne le manganèse comme paramètre indicateur pour l'eau potable, avec une valeur paramétrique de 0,05 mg/L.
3.0 Application de la recommandation
Remarque : des conseils spécifiques concernant l'application des recommandations pour l'eau potable devraient être obtenus auprès de l'autorité appropriée en matière d'eau potable dans le secteur de compétence concerné.
Les préparations pour nourrissons reconstituées avec de lau du robinet peuvent être une source d'exposition au manganèse importante. Dans les régions où les niveau de manganèse dans l'eau potable se situe au-delà de la recommandation, l'utilisation d'une autre source d'eau est recommandée pour les préparations pour nourrissons.
Étant donné que les taux de manganèse peuvent varier considérablement dans l'eau prélevée à la source ainsi que dans les usines de traitement et les réseaux de distribution, il est nécessaire d'élaborer un programme de surveillance propre à chaque système pour permettre aux services publics de bien comprendre les taux de manganèse de la source au robinet. Les programmes de surveillance devraient être conçus en fonction des facteurs de risque qui contribuent à la possibilité que les taux de manganèse soient élevés dans le système d'eau potable, notamment les niveaux historiques de manganèse dans le système, le manque de traitement, un entretien réduit du réseau de distribution et une chimie variable de l'eau prélevée à la source ou dans le réseau de distribution. Les lieux de collecte, la fréquence et le genre d'échantillons à prélever varieront selon l'objectif désiré (p. ex. identification des sources de manganèse, vérification de la conformité, estimation de l'exposition au manganèse) et selon les considérations particulières au site. Divers emplacements pour la surveillance dans un système d'eau potable sont suggérés à la section 3.1.
3.1 Surveillance
3.1.1 Caractérisation de l'eau à la source
Il faut caractériser les sources d'eau afin de déterminer si elles contiennent du manganèse. Pour cette analyse, des échantillons doivent être prélevés pendant les périodes où le taux de manganèse est le plus susceptible d'être élevé dans les eaux de surface, par exemple au moment de la stratification thermique en été et du renouvellement de l'eau des lacs à l'automne. Bien qu'il soit moins probable que la concentration de manganèse dans les eaux souterraines varie avec les saisons, des variations importantes ont été observées entre des puits situés à proximité les uns des autres. Par conséquent, tous les puits d'un champ de captage doivent être caractérisés. La surveillance des eaux de surface doit être effectuée tous les trois mois, ainsi que chaque semaine pendant l'été et l'automne dans les lacs et les réservoirs qui subissent une stratification ou des variations importantes de la concentration en manganèse. Les sources d'eau souterraine doivent faire l'objet d'une surveillance semestrielle. Les autorités peuvent envisager de réduire l'échantillonnage lorsqu'il a été démontré que la concentration de manganèse dans l'eau d'une source est inférieure ou égale à 0,02 mg/L, ou que des mesures de traitement appropriées sont en place. Il est important de remarquer que le fer et le manganèse sont souvent présents en même temps dans une source d'eau et peuvent entraîner une coloration de l'eau. Il est donc conseillé aux services publics de déterminer si du fer est également présent dans la source d'eau.
3.1.2 Surveillance du traitement et des processus
Les services publics qui traitent l'eau pour en éliminer le manganèse doivent également effectuer des vérifications fréquentes de l'eau brute et de l'eau traitée, afin d'ajuster éventuellement les procédés et de s'assurer que les procédés de traitement utilisés permettent de maintenir les concentrations de manganèse en deçà de la CMA et de l'OE. La fréquence de la surveillance de l'eau traitée dépendra des données historiques sur les fluctuations du manganèse dans l'eau brute et des procédés de traitement en place. Par exemple, les usines de traitement des eaux de surface où les concentrations de manganèse varient et qui traitent l'eau par oxydation et par filtration peuvent avoir besoin d'effectuer une surveillance quotidienne. Si les services publics ont de la difficulté à contrôler les concentrations de manganèse dans l'eau traitée, il peut être nécessaire d'effectuer une surveillance à l'usine à chaque étape clé du traitement. Une partie des échantillons prélevés doit faire l'objet d'une filtration adaptée qui permettra d'en déterminer le contenu en manganèse particulaire et dissous. Cette étape est importante pour déterminer le type de traitement requis et pour évaluer le rendement de l'usine de traitement. Les services publics qui ont de la difficulté à contrôler le taux de manganèse dans l'eau traitée et qui oxydent directement le manganèse avec du permanganate de potassium, du dioxyde de chlore ou de l'ozone, peuvent également envisager de quantifier la fraction colloïdale du manganèse dans des échantillons recueillis dans la chaîne de traitement. Dans de nombreux cas, la surveillance des procédés d'une usine de traitement peut se faire par colorimétrie afin de réduire les coûts d'analyse.
3.1.3 Réseau de distribution
Puisque le manganèse peut s'accumuler et être libéré dans les réseaux de distribution, une surveillance de l'eau à plusieurs endroits du système de distribution doit être effectuée si du manganèse est présent ou a déjà été présent dans l'eau prélevée à la source. Cette procédure sert à vérifier que les opérations et l'entretien effectués permettent de maintenir les concentrations de manganèse dans le système de distribution sous l'OE. La libération de manganèse étant généralement sporadique, il est difficile d'établir un programme de surveillance régulier qui permette de détecter efficacement la présence de manganèse dans l'eau du robinet due à des rejets de cet élément dans le système de distribution. Toutefois, les facteurs de risques associés à l'accumulation et à la libération de manganèse dans le réseau de distribution peuvent servir d'indicateurs pour déterminer à quel moment (selon les occurrences) et à quel endroit surveiller les rejets de manganèse. Une surveillance fondée sur les événements peut être requise lorsque les risques de libération augmentent, notamment après toute perturbation hydraulique du système (p. ex. bris de canalisation ou purge des bornes-fontaines) ou toute variation des propriétés chimiques de l'eau (p. ex. changement de pH, de température ou de type de source d'eau, mélange de sources d'eau non contrôlé, concentration résiduelle de chlore ou mélange non contrôlé de désinfectants). Idéalement, les échantillons dans le système de distribution doivent être prélevés aux endroits associés à d'importants facteurs de risque d'accumulation de manganèse (p. ex. proximité de l'usine de traitement, matériaux de tuyauterie, biofilm) et de rejet de manganèse à la suite d'un événement. Une surveillance doit également être effectuée en cas de changement de couleur de l'eau, bien que l'absence d'un tel changement ne signifie pas nécessairement qu'il n'y a pas de libération de manganèse. La surveillance du manganèse doit être effectuée conjointement avec celle d'autres métaux susceptibles d'apparaître simultanément dans le réseau de distribution, et dont le relargage a déjà été observé concomitamment à celui du manganèse (p. ex. fer, arsenic, plomb). Les services publics qui ont mis en place des mesures préventives, qui possèdent des données de base démontrant l'absence de manganèse dans le réseau de distribution, et dont la qualité de l'eau et les conditions hydrauliques et physiques sont stables peuvent effectuer une surveillance moins fréquente.
3.1.4 Conformité
Dans le cas des systèmes où du manganèse est présent dans l'eau prélevée à la source, y compris ceux qui n'utilisent pas de traitement pour enlever le manganèse, la CMA s'applique à l'eau dans le réseau de distribution, y compris à l'entrée de ce dernier. Il faut donc que la conformité du taux de manganèse soit surveillée à l'entrée du réseau de distribution, ainsi qu'à plusieurs autres endroits dans celui-ci. Les échantillons prélevés doivent permettre d'évaluer globalement le taux de manganèse dans le réseau de distribution, et d'estimer notamment l'exposition possible des consommateurs au manganèse dans l'eau du robinet. Certains des échantillons du réseau de distribution doivent être prélevés à des endroits situés à proximité de l'usine de traitement, à des bornes-fontaines et des vannes, ainsi qu'à des robinets d'eau potable situés dans des édifices publics ou privés. Il est recommandé d'effectuer une surveillance au minimum tous les trois mois. On doit également procéder à une surveillance fondée sur les événements pendant les périodes où le risque de libération de manganèse est accru, ou lorsqu'une coloration de l'eau est signalée.
3.1.5 Surveillance résidentielle
Les particuliers qui possèdent un puits privé sont encouragés à faire analyser leur eau chaque année pour s'assurer que la concentration de manganèse y est inférieure à la CMA. Les propriétaires d'un puits privé qui utilisent un dispositif de traitement au point d'entrée ou au point d'utilisation doivent faire régulièrement analyser l'eau qui entre dans l'appareil de traitement ainsi que l'eau traitée, pour s'assurer de l'efficacité du dispositif. Il est important que ces particuliers sachent que l'exploitation et l'entretien inadéquats de filtres au sable vert ont été associés à une augmentation des taux de manganèse dans l'eau du robinet des maisons qui traitent l'eau de puits pour en enlever le manganèse.
3.1.6 Mesures correctives
Lorsque les taux de manganèse dépassent la CMA, il est nécessaire de mener une enquête et de prendre les mesures correctives appropriées. Selon l'endroit et la durée du dépassement, l'enquête pour en identifier la cause pourrait comprendre :
- continuer la surveillance du taux de manganèse à des emplacements appropriés, jusqu'à ce que les taux soient inférieurs à la CMA;
- confirmer les concentrations de manganèse dans l'eau prélevée à la source;
- vérifier le fonctionnement de l'usine de traitement et les concentrations dans l'eau traitée;
- examiner le fonctionnement du réseau de distribution et des activités d'entretien pour déterminer s'il y a eu une perte de charge hydraulique;
- vérifier la qualité de l'eau dans le réseau de distribution (p. ex. pH, potentiel d'oxydoréduction [Eh], concentration résiduelle de chlore, turbidité) pour déterminer s'il y a eu un rejet de produit chimique.
En fonction des résultats de l'enquête ainsi que de l'importance et de l'étendue de l'excès de manganèse, les mesures correctives appropriées pourraient comprendre :
- aviser les collectivités et autres autorités appropriées;
- émettre un avis de non-consommation;
- envisager d'effectuer des ajustements à l'usine de traitement;
- mener des activités d'entretien ciblées et sur mesure dans le réseau de distribution, selon les meilleures pratiques, par exemple un rinçage unidirectionnel, un ramonage des conduites avec glace ou un nettoyage hydraulique par torpille.
Partie II. Science et considérations techniques
4.0 Propriétés, utilisation et sources dans l'environnement
Le manganèse (numéro de registre du Chemical Abstracts Service : 7439-96-5) est un métal de transition du groupe VIIB qui coexiste souvent naturellement avec le fer dans les dépôts géologiques et les sols, et qui est corrodé par les conditions atmosphériques. Le manganèse possède un point d'ébullition de 1 962 °C et un point de fusion de 1 244 °C. Sa pression de vapeur est de 1 mm Hg à 1 292 °C (U.S. EPA, 2004; ATSDR, 2012). Le manganèse existe sous des formes organiques et inorganiques qui présentent des caractéristiques physico-chimiques différentes. Le manganèse est un élément essentiel pour un grand nombre d'organismes, y compris les humains, et il est présent dans de nombreux aliments (IOM, 2001).
Le manganèse est présent à l'état naturel dans l'environnement (il est largement répandu dans l'air, l'eau et le sol) et il forme 0,1 % de la croûte terrestre. On ne le retrouve toutefois pas sous sa forme élémentaire (Barceloux, 1999; Kohl et Medlar, 2006; OMS, 2011). La concentration de manganèse dans les différents milieux varie beaucoup selon les conditions de l'environnement et la proximité de sources anthropiques, telles que des installations industrielles de ferro-alliage (U.S. EPA, 2004). Le manganèse peut présenter différents états d'oxydation dans l'environnement (les plus courants étant le Mn(II) et le Mn(IV)) et il peut former une grande variété de complexes en se combinant avec d'autres éléments tels que l'oxygène, le soufre et le chlore, ainsi qu'avec des carbonates et des silicates (Stokes et coll., 1988; ATSDR, 2012).
Dans le sous-sol (sol et roches), le manganèse existe sous la forme d'oxydes de Mn(II) dissous et d'oxydes de Mn(III) et de Mn(IV) insolubles (Brandhuber et coll., 2013). Les minéraux que l'on retrouve le plus abondamment dans le sol sont la pyrolusite (dioxyde de manganèse), la rhodochrosite (carbonate de manganèse [MnCO3] et la rhodonite [silicate de manganèse]) (Stokes et coll., 1988; PISSC, 1999; Kohl et Medlar, 2006). La rétention du manganèse dans le sol résulte du pouvoir d'échange cationique du sol, qui forme des oxydes et des hydroxydes de manganèse insolubles, et de l'adsorption aux oxydes et aux hydroxydes (OMS, 2004). Le manganèse est présent à un taux variable dans les roches, et il est surtout présent dans les roches métamorphiques et sédimentaires (Stokes et coll., 1988). L'oxyde de Mn(IV) représente la forme la plus abondamment retrouvée dans les minerais de manganèse (Kohl et Medlar, 2006). Seulement une douzaine des quelques 300 minéraux contenant du manganèse sont considérés comme des gisements de minerai suffisamment importants pour appuyer l'extraction minière du manganèse (International Manganese Institute, 2014). La forme des composés de manganèse dans le sol dépend surtout du pH et de l'Eh du sol et de l'eau, mais la minéralogie du sol, l'activité microbienne oxydative et la teneur en matière organique représentent également des facteurs connexes importants (OMS, 2004, 2011). Par exemple, la formation de manganèse soluble est favorisée par un pH acide et des conditions de réduction, comme celles causées par les pluies acides ou la décomposition de matières organiques (Kohl et Medlar, 2006). La présence de manganèse dans les eaux souterraines ou de surface peut être d'origine naturelle (dissolution des oxydes, des carbonates et des silicates de manganèse dans le sol et les roches) ou anthropique (rejets industriels, activités minières et relargage provenant des sites d'enfouissement) (Stokes et coll., 1988; Kohl et Medlar, 2006; Llung et Vahter, 2007). Les propriétés physico-chimiques du milieu environnant (p. ex. teneur en carbone organique, pouvoir d'échange cationique, pH, activité des électrons [Eh] et teneur en particules et en minéraux) ont une incidence sur la spéciation et la solubilité dans l'eau du manganèse; le pH et les conditions d'oxydoréduction représentent les éléments les plus influents (Stokes et coll., 1988; Kohl et Medlar, 2006). Dans les eaux de surface, le manganèse existe sous forme particulaire, colloïdale et dissoute. Toutefois, dans les eaux souterraines, le manganèse est plus souvent présent sous la forme de Mn(II) dissous, en raison des faibles concentrations d'oxygène dissous qui découlent de la réduction du Mn(IV) en Mn(II) dissous. La plupart des sels de manganèse inorganiques sont, dans une certaine mesure, solubles dans l'eau. Le carbonate de manganèse est moins soluble (0,065 g/L) que le sel haloïde, mais il est à l'origine de la majorité du manganèse dissous présent dans l'eau (PISSC, 1999; Luo et Millero, 2003). Parmi les autres formes solubles, citons le chlorure de manganèse (MnCl2), le permanganate de potassium (KMnO4) et le sulfate de manganèse (MnSO4), qui ont respectivement une solubilité de 72,3 g/L, 6,38 g/L et 52 g/L (CRC, 1983). Dans l'eau, les états d'oxydation les plus courants sont le Mn(II) soluble et le Mn(IV) insoluble (Stokes et coll., 1988; ATSDR, 2012; Rumsby et coll., 2014). Le Mn(III), le Mn(V) et le Mn(VI) ne sont pas stables dans des solutions neutres. Les milieux acides et très réducteurs, ainsi que la présence de nitrates, de sulfates et de chlorures, favorisent la réduction des composés minéraux de Mn(III) et de Mn(IV) en Mn(II), une forme plus stable et plus soluble, de même que la formation de sulfate de manganèse et de chlorure de manganèse (Stokes et coll., 1988; OMS, 2004; Kohl et Medlar, 2006; ATSDR, 2012). Dans des conditions alcalines (pH > 8 à 9) et d'oxydation (en présence d'oxygène dissout [OD]), le Mn(II) est converti en Mn(IV), et le manganèse précipite et forme des minéraux insolubles de composés de Mn(IV) (OMS, 2004). Le Mn(IV) est donc insoluble, mais il peut se retrouver dans l'eau à l'état particulaire (Kohl et Medlar, 2006). Le cycle d'oxydation-réduction peut survenir de façon abiotique ou biotique (PISSC, 1999; OMS, 2004).
La chimie du manganèse est un élément important dont il faut tenir compte par rapport à l'acceptation de l'eau potable par les consommateurs, car les oxydes de manganèse particulaire sont visibles à de faibles concentrations, tandis que le manganèse dissous n'est pas visible. Cohen et coll. (1960) et Sain et coll. (2014) ont étudié les taux seuils de manganèse dans l'eau potable relatifs au goût et à l'aspect de cette dernière. Sain et coll. (2014) ont examiné les seuils relatifs à l'apparence et au goût pour le Mn(II) dissous et le Mn(IV) particulaire, en effectuant des tests un sur cinq, un sur trois et triangulaires avec des concentrations comprises entre 0,005 et 506 mg/L. Selon les résultats, la meilleure estimation du seuil relatif au goût, pour la population, est de 101 mg/L pour le Mn(II) provenant du sulfate de manganèse, bien que ce résultat dépende sans doute à la fois du sulfate et du Mn(II). La régression logistique des données a indiqué que le seuil relatif au goût pour le Mn(II) était de 75,4 mg/L pour 50 % de la population. Bien que les tests associés au seuil relatif au goût pour le Mn(IV) aient été limités par la coloration de l'eau, les résultats ont révélé qu'une eau contenant 0,05 mg/L de Mn(IV) ne pouvait être distinguée de l'eau distillée. Les études sur le seuil relatif à l'aspect ont révélé que le Mn(II) dissous était incolore et qu'il ne pouvait être détecté à l'œil nu à des concentrations aussi élevées que 506 mg/L. En revanche, le Mn(IV) particulaire a été détecté à l'œil nu par 100 % des participants à une concentration de 0,005 mg/L. Les auteurs ont conclu qu'une concentration de manganèse de 0,01 à 0,02 mg/L est une limite acceptable pour protéger contre la coloration de l'eau. Cette conclusion est appuyée par de nombreuses études menées sur les systèmes d'approvisionnement en eau potable, selon lesquelles les consommateurs se plaignent d'une coloration de l'eau ou de taches sur la lessive lorsque la concentration de manganèse est supérieure à 0,02 mg/L (Sly et coll., 1990; Casale et coll., 2002; Kohl et Medlar, 2006).
Les principales sources de manganèse particulaire dans l'atmosphère sont de nature industrielle : usines de production de fer et d'acier, centrales électriques, fours à coke et poussières produites par l'extraction minière. Les sources naturelles de manganèse, comme les éruptions volcaniques, les incendies de forêt, les embruns océaniques et l'érosion du sol, peuvent également faire augmenter les taux de manganèse dans l'atmosphère (Stokes et coll., 1988; PISSC, 1999; U.S. EPA, 2004). Les particules de manganèse rejetées dans l'atmosphère, notamment sous forme de dioxyde de manganèse (MnO2) et de tétraoxyde de manganèse (Mn3O4), sont de petite taille et peuvent être transportées sur de longues distances avant de se déposer sur le sol ou dans les eaux de surface.
Le manganèse est utilisé dans diverses industries en raison de ses propriétés d'oxydoréduction (Kohl et Medlar, 2006). Il est surtout employé en sidérurgie, principalement pour améliorer les propriétés mécaniques de l'acier inoxydable et des alliages d'aluminium et de ferromanganèse (Barceloux, 1999; U.S. EPA, 2004; ATSDR, 2012). Les industries utilisent le dioxyde et le chlorure de manganèse pour les piles sèches, les feux d'artifice, l'essence, l'agriculture, le cuir et les tissus, et comme agent de contraste en imagerie par résonnance magnétique (PISSC, 1999; International Manganese Institute, 2014). Le sulfate de manganèse est employé dans les fertilisants et dans certains fongicides. On utilise également le manganèse dans les cosmétiques et les peintures en raison de ses propriétés colorantes. Les usines de traitement de l'eau potable utilisent l'ion permanganate (MnO4-) comme agent oxydant pour éliminer le fer, le manganèse et d'autres contaminants. Le manganèse peut également être présent comme impureté dans les coagulants (p. ex. chlorure de ferrique) utilisés dans les procédés de traitement de l'eau potable. En 2004, l'utilisation du méthylcyclopentadiényl manganèse tricarbonyl (MMT) comme additif pour essence a diminué radicalement au Canada à la suite de mesures volontaires prises par les raffineries de pétrole du pays (Walsh, 2007).
5.0 Exposition
Les Canadiens peuvent être exposés au manganèse par l'air, les aliments, les produits de consommation, le sol et l'eau potable. Toutefois, l'alimentation représente la principale source d'exposition au manganèse (Barceloux, 1999). Le manganèse est un élément essentiel, car il agit comme cofacteur pour les enzymes participant aux mécanismes de défense antioxydants, à la croissance et au métabolisme. À ce titre, il fait l'objet d'un apport quotidien recommandé fixé par les organismes internationaux pertinents (PISSC, 1999; IOM, 2001). Diverses publications et autres évaluations des risques reconnaissent que la biodisponibilité du manganèse présent dans l'eau potable (prise à jeun) est supérieure à celle du manganèse provenant des aliments (Ruoff, 1995; U.S. EPA, 2002, 2004; Bouchard et coll., 2011).
5.1 Eau
La concentration de manganèse dans l'eau douce se situe habituellement entre 1 et 200 μg/L, sous forme de Mn(II) dissous ou sous forme de particules d'oxydes, d'hydroxydes et de carbonates de manganèse (Mn(IV)). Les concentrations de manganèse peuvent être plus élevées dans les eaux souterraines ou de surface qui sont acides, qui présentent un faible Eh ou qui sont touchées par des rejets industriels. Les données canadiennes montrent d'ailleurs que l'eau potable contient en général moins de 100 μg/L de manganèse, sauf dans quelques cas où la concentration peut atteindre des milliers de microgrammes par litre.
En général, le manganèse est plus répandu et est présent à des concentrations plus élevées dans les sources d'eaux souterraines que dans les sources d'eaux de surface, car les conditions réductrices ou anoxiques (manque d'oxygène) sont plus fréquentes dans les eaux souterraines que dans les eaux de surface (Kohl et Medlar, 2006; OMS, 2011). Kohl et Medlar (2006) ont relevé les concentrations annuelles moyennes de manganèse dans la source d'approvisionnement en eau de 179 usines de traitement situées un peu partout en Amérique du Nord (15 usines au Canada). La valeur moyenne maximale de manganèse était de 3 000 µg/L pour les eaux souterraines et de 500 µg/L pour les eaux de surface. Toutefois, les auteurs ont remarqué que les valeurs médianes du taux de manganèse dans les eaux souterraines et les eaux de surface étaient similaires et inférieures à 100 µg/L. Dans les fleuves et les cours d'eau, les concentrations de manganèse ont tendance à être plus faibles en raison de la présence d'oxygène dissous qui limite la quantité de manganèse dissous présent dans ces types de cours d'eau. Le taux de manganèse peut cependant être élevé dans des réserves d'eau de surface, comme les lacs et les réservoirs qui subissent une stratification selon les saisons (ce sujet est abordé plus en détail à la section 7.2.1). La stratification peut rendre les couches inférieures d'un lac ou d'un réservoir anoxiques, ce qui entraîne la libération d'oxydes de manganèse depuis les sédiments situés au fond du lac (Civardi et Tompeck, 2015). Plus rarement, des concentrations élevées de manganèse peuvent exister dans les cours d'eau, selon les sources d'eau qui les alimentent et les conditions d'écoulement (Brandhuber et coll., 2013).
L'Étude nationale sur l'eau potable a fait état de la concentration de manganèse dans l'eau potable à divers endroits au Canada (Santé Canada, 2014a). Dans toutes les provinces et dans tous les territoires, des échantillons ont été recueillis à divers points d'alimentation en eau potable des réseaux de distribution pour en mesurer le manganèse dissous (n = 65). En 2009, 39 % des échantillons se sont révélés en deçà de la limite de détection (2 μg/L). En 2010, ce pourcentage a atteint 63,2 %. Les concentrations moyennes étaient de 16,1 μg/L en 2009 et de 10,8 μg/L en 2010.
En Colombie-Britannique, une surveillance du taux de manganèse a été effectuée à divers endroits, autant dans les eaux souterraines que dans les eaux de surface, entre 1991 et 2014 (British Columbia Ministry of Health, 2014). La concentration en manganèse total (extraction chimique; 3 573 échantillons) affichait une moyenne de 593.6 μg/L, une médiane de 18 μg/L et une valeur maximale observée de 796 000 µg/L. Le taux de manganèse total était inférieur à 5 μg/L dans 893 échantillons (31%) et supérieur à 200 μg/L dans 411 échantillons (14%). La concentration en manganèse dissous (155 échantillons) affichait une moyenne de 388 μg/L, une médiane de 12 μg/L et une valeur maximale observée de 26 200 µg/L. Le taux de manganèse dissous était inférieur à 5 μg/L dans 41 échantillons (32%) et supérieur à 200 μg/L dans 20 échantillons (16 %).
En Alberta, les concentrations de manganèse ont été mesurées entre 2003 et 2013 dans deux usines de traitement de l'eau recevant de l'eau des rivières Elbow et Bow à Calgary, et dans quatre de leurs réseaux de distribution (extrémités nord et sud de Calgary) (Alberta Ministry of Environment and Sustainable Resource Development, 2014). Le taux de manganèse extractible ou total dans les échantillons d'eau brute non traitée (n = 2 748) affichait une moyenne de 6,2 μg/L, une médiane de 3,3 μg/L et une valeur maximale de 434,3 μg/L. Aucun manganèse dissous ou total n'a été détecté dans 17 échantillons (moins de 1 %; limite de détection : 0,5 à 1,0 μg/L) et 31 échantillons (1 %) affichaient une concentration supérieure à 50 μg/L. Le taux de manganèse extractible ou total dans les échantillons d'eau traitée sortant des usines de traitement (n = 2 120) affichait une moyenne de 86 μg/L, une médiane de 6 μg/L et une valeur maximale de 16,3 μg/L. Aucun manganèse dissous ou total n'a été détecté dans 1 544 échantillons (73 %). Le taux de manganèse extractible ou total dans les échantillons du réseau de distribution (n = 1 925) affichait une moyenne de 1,0 μg/L, une médiane de 7 μg/L et une valeur maximale de 12,6 μg/L. Aucun manganèse extractible ou total n'a été détecté dans 1 169 échantillons (61 %).
En Saskatchewan, des échantillons d'eau potable traitée ont été prélevés dans le réseau de distribution (95 % des échantillons) et dans des usines de traitement entre 2003 et 2014 (n = 4 024; limite de détection : 0,5 à 10 μg/L) (Saskatchewan Water Security Agency, 2014). Dans le réseau de distribution, le taux de manganèse affichait une moyenne de 200,5 μg/L, une médiane de 30 μg/L et une valeur maximale de 8 440 μg/L pour le manganèse total et dissous. Les échantillons d'eau traitée affichaient une moyenne de 244,7 μg/L, une médiane de 30 μg/L et une valeur maximale de 3 510 μg/L.
Au Manitoba, des échantillons d'eau brute (n = 1 670), d'eau traitée (n = 1 595) et d'eau du réseau de distribution (n = 17) ont été prélevés entre 2002 et 2012 (Conservation et Gestion des ressources hydriques Manitoba, 2015). Dans l'eau brute, le taux de manganèse affichait une moyenne de 202,34 μg/L, une médiane de 26 μg/L et une valeur maximale de 9 870 μg/L; 69 % des concentrations mesurées étaient inférieures à 100 μg/L et 23 % étaient supérieures à 200 μg/L. Dans l'eau traitée, le taux de manganèse affichait une moyenne de 66,4 μg/L, une médiane de 8,41 μg/L et une valeur maximale de 5 150 μg/L; 92 % des concentrations mesurées étaient inférieures à 100 μg/L et 6 % étaient supérieures à 200 μg/L. Les échantillons d'eau du réseau de distribution affichaient une moyenne de 544,06 μg/L, une médiane de 28 μg/L et une valeur maximale de 4 400 μg/L; 76 % des mesures ont été inférieures à 100 µg/L et 18 % ont été supérieures à 200 µg/L. Les limites de détection n'étaient pas fournies.
En Ontario, la concentration de manganèse dans l'eau potable a été mesurée dans des échantillons recueillis entre 2009 et 2014 (Ministère de l'Environnement et de l'Action en matière de changement climatique de l'Ontario, 2014). La limite de détection était de 0,05 μg/L. Dans l'eau brute (2 105 échantillons), le manganèse était détectable dans 2 047 échantillons. Le taux de manganèse affichait une moyenne de 24,11, une médiane de 7,32 μg/L et une valeur maximale de 838 μg/L. Cent huit (5%) résultats étaient supérieurs à 100 μg/L et 50 (2%) dépassaient 200 μg/L. Dans l'eau traitée (1 700 échantillons), le manganèse était détectable dans 1 628 échantillons. La concentration de manganèse affichait une moyenne de 6,1 μg/L, une médiane de 1,33 μg/L et une valeur maximale de 442 μg/L; douze échantillons (0.8%) avaient un taux supérieur à 100 μg/L et deux échantillons (0.15%) avaient un taux supérieur à 200 μg/L. Dans le réseau de distribution (1 730 échantillons), le manganèse était détectable dans 1 696 échantillons. La concentration de manganèse affichait une moyenne de 4,46 μg/L, une médiane de 1,5 μg/L et une valeur maximale de 187 μg/L; quatre échantillons (0.2%) avaient un taux supérieur à 100 μg/L et aucun échantillons avaient un taux supérieur à 200 μg/L.
Au Québec, la concentration en manganèse d'échantillons d'eau prélevés dans des usines de traitement et le réseau de distribution ayant des sources souterraines a été mesurée entre 2010 et 2014 (Ministère du Développement durable, de l'Environnement et de la Lutte contre les changements climatiques du Québec, 2014). La limite de détection était de 0,2 μg/L. Dans l'eau brute (n = 283), la concentration de manganèse affichait une moyenne de 97,7 μg/L, une médiane de 7,7 μg/L et une valeur maximale de 4 100 μg/L; 31 échantillons (12 %) présentaient un taux de manganèse égal ou supérieur à 200 μg/L. La concentration de manganèse dans l'eau traitée (n = 126) affichait une moyenne de 38,4 μg/L, une médiane de 3,45 μg/L et une valeur maximale de 470 μg/L; 6 échantillons (5 %) avaient un taux de manganèse égale ou supérieur à 200 μg/L. La seule concentration de manganèse mesurée dans le réseau de distribution était de 68 μg/L. Une étude menée dans le sud-ouest du Québec a révélé des concentrations allant de 0,5 à 71,1 μg/L (moyenne : 4,11 μg/L) dans des sources municipales (n = 262) (Baldwin et coll., 1999). Dans les puits, les concentrations mesurées étaient de 0,2 à 158,9 μg/L (n = 16; moyenne : 2,78 μg/L).
Au Nouveau-Brunswick, les taux de manganèse ont été mesurés dans des systèmes d'approvisionnement d'eau de la Couronne (puits d'eau souterraine) et municipaux (eaux souterraines et de surface) (Ministère de la Santé du Nouveau-Brunswick, 2014). Dans l'eau potable provenant des systèmes sur les terres de la Couronne (1 817 échantillons), la concentration en manganèse était égale ou inférieure à 5 μg/L dans 942 échantillons (52 %) et égale ou supérieure à 200 μg/L dans 310 échantillons (35 %). Le taux de manganèse affichait une moyenne de 178,7 μg/L, une médiane de 68 μg/L et une valeur maximale de 4 000 μg/L. Dans l'eau du réseau de distribution municipal (2 675 échantillons), la concentration de manganèse était égale ou inférieure à 5 μg/L dans 1 453 échantillons (54 %) et supérieure à 200 μg/L dans 154 échantillons (13 %). Le taux de manganèse affichait une moyenne de 144,1 μg/L, une médiane de 15 μg/L et une valeur maximale de 2 560 μg/L. Dans l'eau des systèmes municipaux alimentés par des sources souterraines (2 980 échantillons), la concentration en manganèse était égale ou inférieure à 10 μg/L dans 685 échantillons (29%) et supérieure à 200 μg/L dans 1 094 échantillons (52 %). Le taux de manganèse affichait une moyenne de 443 μg/L, une médiane de 170 μg/L et une valeur maximale de 4 400 μg/L. Dans l'eau des réseaux municipaux alimentés par des sources d'eau de surface (467 échantillons), la concentration en manganèse était égale ou inférieure à 5 μg/L dans 131 échantillons (28 %) et égale ou supérieure à 200 μg/L dans 69 échantillons (21 %). Le taux de manganèse affichait une moyenne de 196,7 μg/L, une médiane de 52 μg/L et une valeur maximale de 3 130 μg/L. L'usine de traitement de Sackville a déclaré une concentration habituelle de manganèse total allant de 1 500 à 2 500 μg/L dans l'eau brute, et inférieure à 50 μg/L dans l'eau traitée sortant de l'usine de traitement.
À Terre-Neuve-et-Labrador, la concentration en manganèse a été mesurée dans des échantillons d'eau potable recueillis entre 2011 et 2014 (Newfoundland and Labrador Department of Environment and Conservation, 2014). Toutes les valeurs obtenues se situaient au dessus de la limite de détection (10 μg/L). Le taux de manganèse dans l'eau du robinet (n = 253) affichait une moyenne de 170,9 μg/L, une médiane de 120 μg/L et une valeur maximale de 980 μg/L. Dans l'eau prélevée à la source (n = 88), le taux de manganèse affichait une moyenne de 240,8 μg/L, une médiane de 130 μg/L et une valeur maximale de 2 400 μg/L.
Au Yukon, on a mesuré la concentration en manganèse dans des échantillons d'eau potable provenant de 21 sources d'eau souterraine, prélevés en 2012, 2013 et 2014 (limite de détection : 1 à 50 μg/L) (Yukon Environmental Health Services, 2014). La concentration moyenne de manganèse dans l'eau brute (n = 34) et dans l'eau traitée (n = 12) était respectivement de 97,91 μg/L et de 20,7 μg/L, et la concentration médiane était respectivement de 105 μg/L et de 13,2 μg/L. Onze échantillons avaient une concentration de manganèse supérieure à 50 μg/L (24 %, tous des échantillons d'eau brute). La concentration maximale relevée était de 209 μg/L dans l'eau brute et 54 μg/L dans l'eau traitée.
Les données recueillies dans le cadre des programmes de surveillance des eaux souterraines et d'échantillonnage des puits à usage domestique dans plusieurs provinces ont démontré que les concentrations de manganèse peuvent être élevées dans les puits à usage domestique, selon la géochimie des eaux souterraines locales. Fitzgerald et coll. (2001) ont échantillonné 816 puits à usage domestique situés sur des exploitations agricoles en Alberta et y ont relevé des concentrations de manganèse variant de < 1 à 5 334 µg/L, pour une moyenne de 135 µg/L; 34 % des échantillons affichaient des concentrations supérieures à 50 µg/L. De même, Kennedy et Finlayson-Bourque (2001) ont constaté que les concentrations de manganèse dans des échantillons prélevés dans des aquifères du substratum rocheux en Nouvelle-Écosse variaient entre 12 et 12 000 µg/L, avec une valeur médiane de 20 µg/L et une moyenne de 220 µg/L; 37 % des échantillons affichaient une concentration supérieure à 50 µg/L. En outre, des renseignements sur la teneur en manganèse dans l'eau provenant de puits privés ont été relevés dans des échantillons géoréférencés dans l'Atlas de la composition chimique de l'eau souterraine du Nouveau-Brunswick 1994-2007 (Ministère de l'Environnement et des Gouvernements locaux du Nouveau-Brunswick, 2008). Sur les 10 751 échantillons recueillis, 7 811 (74 %) affichaient des concentrations en manganèse supérieures à 5 µg/L et 4 207 (40 %) avaient des concentrations supérieures à 50 µg/L; la concentration maximale observée était de 33 600 µg/L. Thompson et coll. (2003) ont prélevé des échantillons provenant de 283 puits privés en Saskatchewan et ont obtenu un taux de manganèse variant de 10 à 5 480 µg/L, avec une moyenne de 430 µg/L et une médiane de 240 µg/L. Un échantillonnage effectué sur 139 puits privés et à usage domestique dans la région de l'Outaouais, au Québec, a relevé des concentrations de manganèse variant de 0,2 à 630 µg/L, avec une médiane de 11 µg/L et une moyenne de 54 µg/L (Montcoudiol et coll., 2015). Ces données sont semblables aux résultats d'un vaste programme d'échantillonnage mené aux États-Unis, portant sur plus de 4 900 échantillons de puits municipaux, privés et de surveillance et analysés pour détecter la présence de métaux traces. Le taux de manganèse observé avait une valeur médiane de 7 µg/L, une valeur correspondant au 75e percentile de 84 µg/L et une valeur maximale de 28 000 µg/L (Ayotte et coll., 2011).
5.2 Aliments
Les aliments constituent la principale source d'exposition au manganèse et la majeure partie de l'apport provient des céréales, des noix et des légumes. Dans le cadre de l'Étude canadienne sur l'alimentation totale (ECAT), on a estimé la concentration moyenne de manganèse dans divers aliments (Santé Canada, 2009). De fortes concentrations de manganèse (supérieures à 1,0 μg/g) ont été observées dans les céréales (le pain [3,5 à 19,1 μg/g], la farine blanche [3,5 à 7,5 μg/g], le riz [3,0 à 4,9 μg/g], les céréales [1,0 à 25,9 μg/g], le maïs à éclater [7,2 à 10,6 μg/g]), les noix (28,5 μg/g), le beurre d'arachide (13,1 à 16,8 μg/g), les abats (3,1 à 4,0 μg/g), certains fruits (bleuets [8,3 à 10,0 μg/g], ananas en boîte [12,0 à 20,4 μg/g], bananes [1,7 à 4,6 μg/g]), les légumes (0,8 à 3,0 μg/g pour les betteraves, le brocoli, le chou, le chou-fleur, les carottes, le céleri, la laitue, le maïs, les concombres, les oignons et les pommes de terre, et 3,0 à 7,5 μg/g pour les épinards), le thé (2,3 à 5,1 μg/g) et les herbes et épices (71,0 à 123,6 μg/g). Des concentrations intermédiaires (0,5 à 1,0 μg/g) de manganèse ont été relevées dans le fromage (0,05 à 1,0 μg/g), les poivrons (0,6 à 0,8 μg/g), les raisins (0,5 à 0,8 μg/g) et les saucisses (0,4 à 1,0 μg/g). De faibles concentrations (0,02 à 0,5 μg/g) de manganèse ont été relevées dans la viande et le poisson (0,02 à 0,2 μg/g pour le bœuf, l'agneau, le poulet, le poisson et le veau), les champignons (0,4 à 0,6 μg/g), les pommes (0,2 à 0,3 μg/g), le café (0,2 à 0,3 μg/g), les œufs (0,3 à 0,4 μg/g) et le lait (0,01 à 0,04 μg/g).
L'ECAT a également mesuré l'apport alimentaire en différents éléments de la population canadienne, selon l'âge et le sexe (Santé Canada, 2009). L'apport quotidien moyen de manganèse a été estimé pour les groupes d'âge suivants : 0 à 1 mois, 2 à 3 mois, 4 à 6 mois, 7 à 9 mois, 10 à 12 mois, 1 à 4 ans, 5 à 11 ans, 12 à 19 ans, 20 à 39 ans, 40 à 64 ans, âge égal ou supérieur à 65 ans. L'apport alimentaire quotidien moyen de manganèse, pour l'ensemble des groupes d'âge, a été estimé à 61,3 μg/kg poids corporel (p.c.) par jour entre 1993 et 1999 (Montréal), à 59,0 μg/kg p.c. par jour en 2000 (Ottawa), à 51,0 μg/kg p.c. par jour en 2001 (St. John's), à 56,0 μg/kg p.c. par jour en 2002 (Vancouver), à 52,0 μg/kg p.c. par jour en 2003 (Montréal), à 50,0 μg/kg p.c. par jour en 2004 (Winnipeg), à 44,0 μg/kg p.c. par jour en 2005 (Toronto), à 53,0 μg/kg p.c. par jour en 2006 (Halifax) et à 54,0 μg/kg p.c. par jour en 2007 (Vancouver). Ces valeurs d'apport en manganèse concordent avec les estimations antérieures de 2 à 9 mg/jour pour les adultes (apport plus élevé chez les végétariens) (Schroeder et coll., 1966; Barceloux, 1999; IOM, 2001).
Les concentrations moyennes de manganèse dans le lait maternel ont été estimées à 3,7 μg/L (2,7 à 5,4 μg/L; n = 11 mères en santé) pendant le premier mois après la naissance, les concentrations les plus élevées ayant été mesurées au jour 1 (Casey et coll., 1985). Ces concentrations diminuaient ensuite à 1,9 μg/L trois mois après la naissance (Casey et coll., 1985; IOM, 2001). En se fondant sur des données préliminaires et d'après les mesures de l'ECAT, Santé Canada a estimé que la teneur médiane en manganèse du lait maternel était de 2,2 ng Mn/g (Santé Canada, 2014b). L'OMS a estimé que l'apport quotidien de manganèse pour les nourrissons allaités variait entre 2,6 et 11,1 μg/jour (OMS, 2011).
Aux États-Unis, l'apport quotidien provenant des aliments a été estimé à 2,7 mg pour les hommes et à 2,2 mg pour les femmes (NRC, 1989). Les apports ont été estimés à 1,1 mg/jour pour les nourrissons de 6 à 11 mois et à 1,5 mg/jour pour les enfants de deux ans. Au Royaume-Uni, l'apport moyen pour les adultes est estimé à 4,9 mg/jour, dont la moitié provient du thé (EVM, 2002).
En ce qui concerne le manganèse dans les préparations pour nourrissons, le Règlement sur les aliments et drogues du Canada prescrit un minimum de 5 μg de manganèse/100 kcal (3,33 μg/100 mL de préparation prête à l'emploi) (Gouvernement du Canada, 2014). Le règlement n'a pas établi de quantité maximale de manganèse dans les préparations pour nourrissons. Le groupe d'experts du Life Science Research Office (LSRO) et le comité du Codex de l'OMS et de l'Organisation des Nations Unies pour l'alimentation et l'agriculture (FAO) ont établi des lignes directrices pour la concentration de manganèse dans les préparations pour nourrissons (en poudre ou en liquide) vendues sur le marché comme substitut au lait maternel, soit un minimum de 1 μg manganèse/100 kcal, et un maximum de 100 μg manganèse/100 kcal (67 μg/100 mL, correspondant à la limite supérieure recommandée par l'OMS et la FAO), afin que ces préparations répondent aux besoins nutritionnels des nourrissons (Raiten et coll., 1998; OMS, 2007).
5.3 Air
L'air ambiant contient généralement de faibles taux de manganèse, étant donné que les composés de manganèse ont une faible pression de vapeur (Stokes et coll., 1988). De faibles concentrations ont également été mesurées dans les matières particulaires (PM) au Canada, où le Réseau national de surveillance de la pollution atmosphérique surveille le taux de manganèse dans l'air ambiant dans les aérosols atmosphériques (fins/grossiers). En 2013, les concentrations de manganèse mesurées étaient de 0,050 à 51,4 ng/m3 pour les PM 2,5 (la grande majorité des échantillons affichait un taux < 10 ng/m3) et de 1 à 43 ng/m3 (0,001 à 0,043 μg/m3) pour les PM10 (la grande majorité des échantillons affichait un taux < 0,010 μg/m3) (Environnement Canada, 2014). Ces résultats sont similaires à ceux obtenus en 2003 et en 2005, avec des taux de manganèse mesurés qui se situaient entre 0,002 et 0,025 μg/m3 (Santé Canada 2010). Les concentrations oscillaient entre 0,06 et 0,22 μg/m3 dans certaines parties des villes abritant d'importantes sources industrielles de manganèse (2003 et 2005). Les concentrations de manganèse (PM2,5 et PM10) ont chuté de 13 à 77 % entre la fin des années 1980 et le début des années 2000 (Santé Canada, 2010).
Des études portant sur l'exposition de la population dans différentes villes du Canada et des États-Unis (Toronto, Ontario, Riverside, Californie et Indianapolis,Indiana) ont également été menées en 1995 et en 1996, deux années pendant lesquelles l'utilisation de MMT dans l'essence était largement répandue (Wallace et Slonecker, 1997). Des échantillons provenant de points de surveillance personnels (population générale) et fixes ont révélé des valeurs médianes respectives de 0,015 μg/m3 et de 0,024 μg/m3 (limite de détection : 2 à 9 ng/m3). Aux États-Unis, la valeur médiane de l'exposition personnelle mesurée était de 0,003 μg/m3 à Indianapolis (où aucun MMT n'était ajouté à l'essence) et de 0,020 à 0,049 μg/m3 à Riverside, en Californie. Des concentrations estimatives de 1 à 2 ng/m3 ont été établies comme concentrations de référence dans les milieux non contaminés au Canada et aux États-Unis.
5.4 Produits de consommation
Il est possible de se procurer du manganèse comme supplément nutritif au Canada (Santé Canada, 2007a). Les doses recommandées par Santé Canada pour les produits de santé naturels sont de 0,13 à 9 mg/jour pour les adultes (aucune pour les moins de 19 ans), provenant de sources multiples de manganèse, comme le chlorure, le citrate et l'oxyde de manganèse.
5.5 Sol
Le manganèse est présent naturellement dans le sol à des concentrations estimatives de 40 à 900 mg/kg. Selon le type de roche, les concentrations peuvent parfois se situer en dehors de cette plage (plus élevées dans les minerais de fer et les roches mafiques et sédimentaires, moins élevées dans le grès) (Barceloux, 1999; PISSC, 1999; Michaelke et coll., 2007). Les enfants peuvent ingérer le manganèse présent dans le sol par leur tendance à tout porter à la bouche (PISSC, 1999).
Dans le cadre d'une étude exhaustive menée à l'échelle nationale et régionale, la concentration moyenne de référence (sans influence de l'activité humaine), pour les différents profils de sol de cinq principales régions géologiques (n = 173) du Canada, a été établie à 520 mg/kg, avec une plage allant de 100 à 1 200 mg/kg (McKeague et Wolynetz, 1980).
5.6 Concentrations de biomarqueurs dans la population canadienne
Statistique Canada, Santé Canada et l'Agence de la santé publique du Canada ont mis en œuvre le cycle 1 de l'Enquête canadienne sur les mesures de la santé, une étude de prévalence menée entre 2007 et 2009 dans 15 sites différents et qui a permis de recueillir des données sur la santé et de prélever des échantillons de matériel biologique auprès d'environ 5 600 Canadiens et Canadiennes âgés de 6 à 79 ans, répartis en cinq groupes d'âge (6 à 11 ans, 12 à 19 ans, 20 à 39 ans, 40 à 59 ans et 60 à 79 ans) (Santé Canada, 2010). Le cycle 2 de l'enquête, réalisé entre 2009 et 2011 selon un protocole similaire, portait sur les Canadiens et les Canadiennes âgés de 3 à 79 ans. La moyenne géométrique de la concentration de manganèse dans le sang total, tous âges confondus, était de 9,2 μg/L (intervalle de confiance [IC] à 95 % = 9,0-9,5 μg/L; n = 5 309) pour le cycle 1 et de 9,8 μg/L (IC à 95 % = 9,5-10,0 μg/L; n = 5 575) pour le cycle 2. La concentration moyenne de manganèse dans le sang total était de 11,0 μg/L (IC à 95 % = 11,0-12,0 μg/L) pour les trois à cinq ans (cycle 1 seulement; aucune donnée pour le cycle 2). Pour les autres groupes d'âge de plus de six ans, cette concentration variait de 8,8 à 10 μg/L pour le cycle 1 et de 9,4 à 11 μg/L pour le cycle 2. La concentration moyenne de manganèse dans le sang total, tous groupes d'âge confondus, variait de 8,6 à 9,5 μg/L pour le cycle 1 et de 9 à 10 μg/L pour le cycle 2 pour les hommes, et de 9,2 à 11 μg/L pour le cycle 1 et de 9,5 à 11 μg/L pour le cycle 2 pour les femmes. Les plus forts taux de manganèse dans le sang (10 à 12 µg/L) ont été relevés chez les 6 à 11 ans. La moyenne géométrique des concentrations de manganèse dans l'urine s'élevait à 0,081 μg/L (IC à 95 % = 0,072-0,092 μg/L; n = 5 431) pour l'ensemble de la population canadienne âgée de 6 à 79 ans pour le cycle 1 (aucune donnée n'est présentée pour le cycle 2, la plupart des mesures se situant en deçà de la limite de détection). Les concentrations de manganèse dans le sang total variaient entre 6,3 μg/L (10e percentile) et 15,0 μg/L (95e percentile). Aucune donnée n'a été fournie pour les enfants de moins de trois ans.
L'étude MIREC de Santé Canada (n = 1 415 à 1 938) a mesuré la moyenne géométrique des concentrations de manganèse dans le sang de femmes enceintes durant le premier trimestre (8,8 μg/L; IC à 95 % = 8,7-8,9 μg/L; maximum : 29,1 μg/L) et le troisième trimestre de grossesse (12,0 μg/L; IC à 95 % = 12,0-12,4 μg/L; maximum : 33,5 μg/L), dans le sang ombilical (30,9 μg/L; IC à 95 % = 30,9-32,0 μg/L; maximum : 98,9 μg/L) et dans le méconium (4,5 μg/L; IC à 95 % = 4,3-4,7 μg/L; maximum : 40,0 μg/L) (Santé Canada, 2015).
Au Québec, une enquête transversale menée en 2001 a permis de colliger des données sur les métaux traces chez des hommes et des femmes de 18 à 65 ans habitant dans la région de la ville de Québec (n = 500) (Leblanc et coll., 2004). Les données comprenaient les taux de manganèse dans le sang total (moyenne géométrique de 169,8 nmol/L [IC à 95 % = 164,9-174,8 nmol/L]; n = 427) et dans le sérum (moyenne géométrique de 12,0 nmol/L [IC à 95 % = 11,8-12,3 nmol/L]; n = 403). Une autre étude portant sur l'exposition au manganèse, menée dans le sud-ouest du Québec (Baldwin et coll., 1999), a notamment mesuré le taux de manganèse dans le sang (n = 306, personnes âgées de 20 à 69 ans). La moyenne géométrique du taux de manganèse dans le sang total était de 7,1 μg/L (intervalle : 2,5 à 15,9). Une autre étude a trouvé que la moyenne géométrique des concentrations de manganèse mesurées chez des ostréiculteurs (âgés de 33 à 64 ans; n = 61) de la Colombie-Britannique, était de 176,8 nmol/L pour les hommes et de 217,8 nmol/L pour les femmes dans le sang total, et de 16,5 nmol/L pour les hommes et de 12,9 nmol/L pour les femmes dans le sérum (Clark et coll., 2007). Bien que les concentrations de manganèse dans le sang étaient considérablement plus élevées chez les femmes que chez les hommes, elles étaient relativement les mêmes pour les deux sexes dans le sérum.
5.7 Apport quotidien total et exposition
L'estimation de l'apport quotidien provenant de l'eau potable peut varier considérablement selon les concentrations de manganèse dans l'eau (voir la section 5.1). Il faut tenir compte de plusieurs facteurs pour obtenir une estimation juste de l'exposition de la population canadienne, tels que des renseignements exacts concernant les concentrations dans l'eau, l'âge des personnes exposées et la durée d'exposition à une source d'eau donnée. En outre, il faut faire preuve de prudence en extrapolant les apports estimés provenant de différentes sources par rapport à l'absorption relative provenant de chaque source, puisque d'autres facteurs (dont la biodisponibilité et la forme ou la spéciation du manganèse) ont une incidence sur l'importance toxicologique de la dose estimée.
5.8 Exposition multivoies par l'eau potable
En raison de la faible volatilité du manganèse, l'exposition par inhalation au manganèse dans l'eau potable est probablement négligeable. L'évaluation habituelle de l'exposition par voies multiples, qui mesure l'exposition, par inhalation, aux produits chimiques volatils produits pendant la douche ou le bain, ne permettrait pas de rendre compte de façon exacte de l'inhalation de manganèse sous forme d'aérosol pendant une douche. Il est également peu probable que l'exposition par voie cutanée pendant la douche ou le bain soit importante : il existe peu de rapports sur la toxicité du manganèse par voie cutanée, et les rapports de risque calculés et recensés dans la documentation scientifique sont faibles (< 1) (IPCS, 1999; Karim, 2011).
6.0 Méthodes d'analyse
L'United States Environmental Protection Agency (U.S. EPA) recommande actuellement quatre méthodes d'analyse (méthode 200.5 révision 4.2, méthode 200.7 révision 4.4, méthode 200.8 révision 5.4 et méthode 200.9 révision 2.2) pour mesurer la concentration de manganèse total dans l'eau potable (U.S. EPA, 2014). Elle recommande également plusieurs méthodes (SM 3111B, SM 3113B et SM 3120B) mises au point par un organisme d'élaboration de normes volontaires consensuelles.
Le manganèse total est défini comme étant la somme des concentrations des fractions dissoute et particulaire (en suspension) d'un échantillon d'eau. On le mesure à l'aide de méthodes qui permettent de déterminer la concentration de manganèse total récupérable. L'analyse du manganèse total est nécessaire pour effectuer une comparaison avec la CMA. Il est toutefois essentiel de connaître la concentration de chaque fraction (dissoute et particulaire) pour pouvoir déterminer la méthode de traitement appropriée et pour vérifier si le traitement élimine efficacement le manganèse. Cette question est abordée en détail aux sections 6.2 et 7.2.
La limite de détection de la méthode (LDM) associée à chaque méthode recommandée est indiquée ci-dessous. Toutefois, il importe de préciser que les LDM dépendent de la matrice de l'échantillon, des instruments utilisés et des conditions d'exploitation choisies, et qu'elles varieront d'un laboratoire à l'autre.
- La méthode EPA 200.5 Rév. 4.2 fait appel à la spectrométrie d'émission atomique avec plasma induit par haute fréquence (ICP-AES) avec visée axiale, qui présente une LDM de 0,06 µg/L (U.S. EPA, 2003).
- La méthode EPA 200.7 Rév. 4.4 utilise une méthode d'ICP-AES, qui présente une LDM de 1,4 µg/L (U.S. EPA, 1994a).
- La méthode EPA 200.8 Rév. 5.4 utilise une méthode de spectrométrie de masse avec plasma induit par haute fréquence (ICP-MS), qui présente une LDM de 0,02 µg/L pour le manganèse total récupérable et de 0,04 µg/L pour une injection aqueuse directe (U.S. EPA, 1994b).
- La méthode EPA 200.9 Rév. 2.2 utilise une méthode de spectrométrie d'absorption atomique en four au graphite (GFAA), qui présente une LDM de 0,3 µg/L (U.S. EPA, 1994c).
- La méthode SM (standard method) 3111B utilise une méthode de spectrométrie d'absorption atomique directe avec flamme air-acétylène, qui présente une LDM de 0,01 mg/L (10 µg/L) (APHA et coll., 1992, 1995, 2005, 2012).
- La méthode SM 3113B utilise une méthode de spectrométrie d'absorption atomique électrothermique, qui présente une LDM de 0,2 µg/L (APHA et coll., 1992, 1995, 2005, 2012).
- La méthode SM 3120B utilise une méthode d'ICP-AES, qui présente une LDM de 2 µg/L (APHA et coll., 1992, 1995, 1998, 2005, 2012).
- Les versions en ligne des méthodes SM 3113B-04, 99 et SM 3120B-99 sont également des méthodes recommandées.
Il existe une autre méthode d'analyse normalisée qui ne fait pas partie des méthodes recommandées par l'U.S. EPA. Il s'agit de la méthode SM 3125, qui est bien établie et jugée acceptable pour l'analyse du manganèse dans l'eau potable.
- La méthode SM 3125B utilise une méthode d'ICP-MS, qui présente une LDM de 0,002 µg/L (APHA et coll., 1992, 1995, 2005, 2012).
6.1 Méthodes
Les méthodes EPA 200.5 révision 4.2, EPA 200.7 révision 4.4 et SM 3120B sont fondées sur des analyses multi-élémentaires réalisées par signaux d'émission atomique avec plasma induit par haute fréquence (ICP-AES), à l'aide d'instruments séquentiels ou simultanés. Les instruments mesurent les spectres linéaires d'émission atomique par spectrométrie optique. Les spectres d'émission propres aux éléments sont produits à l'aide d'une torche à plasma induit par haute radio-fréquence radiofréquence (ICP). Les spectres sont dispersés par un spectromètre à grille de réflexion et un appareil photosensible vérifie l'intensité des spectres linéaires à des longueurs d'onde précises. Une variation de la méthode EPA 200.5 consiste à utiliser des signaux d'émission atomique à plasma vus en direction axiale pour analyser tous les analytes. Des effets de matrice peuvent se produire avec la méthode EPA 200.5 lorsque les concentrations totales de calcium, de magnésium et de sodium dépassent 125 mg/L et que la concentration en silice dépasse 250 mg/L. Des interférences peuvent survenir avec les méthodes EPA 200.7 et SM 3120B lorsque la concentration de matières dissoutes totales est supérieure respectivement à 0,2 % (p/v) et 1 500 mg/L.
Dans les méthodes EPA 200.8 révision 5.4 et SM 3125 B, les échantillons sont atomisés et ionisés dans un plasma induit par radiofréquence. Les ions sont extraits du plasma par une interface à pression négative et séparés par un spectromètre de masse en fonction de leur rapport masse/charge. Un multiplicateur d'électrons ou un détecteur de Faraday détecte ensuite les ions séparés. Des effets de matrice peuvent se produire avec les méthodes EPA 200.8 et SM 3125B lorsque la concentration de matières dissoutes totales est supérieure respectivement à 0,2 % et 0,5 % (p/v).
Les méthodes EPA 200.9 révision 2.2 et SM 3113B font appel à la spectrométrie d'absorption atomique en four au graphite avec une plateforme maintenue à température constante. Cette technique comprend une série de trois étapes de chauffage visant à sécher, à carboniser (afin de réduire les interférences causées par d'autres ions) et à atomiser les analytes sur la surface en graphite pyrolytique. L'atomisation élève les analytes dans une atmosphère d'argon de grande pureté. On fait ensuite passer une lumière d'une longueur d'onde donnée à travers le nuage atomique et on mesure la diminution de l'intensité de la lumière. Aucune interférence de matrice liée au manganèse n'a été relevée dans ces méthodes.
La méthode SM 3111B est une méthode d'absorption atomique directe par flamme air-acétylène, dans laquelle l'échantillon est aspiré dans la flamme et atomisé. Elle consiste à envoyer un faisceau de lumière vers un détecteur en le faisant passer d'abord à travers la flamme puis dans un monochromateur. Le détecteur mesure alors la quantité de lumière absorbée par l'élément atomisé dans la flamme. Comme chaque métal possède une longueur d'onde d'absorption qui lui est propre, la méthode utilise une lampe source composée de l'élément concerné.
L'U.S. EPA n'a pas fixé de seuil pratique d'évaluation quantitative (SPEQ) pour le manganèse. Un rapport publié par cet organisme en 2010 indique cependant que l'utilisation des SPEQ pour la détermination des capacités d'analyse peut être problématique en raison des différentes méthodes utilisées pour établir ces SPEQ. Le rapport souligne que le seuil minimal de niveau à rapporter (SMNR) peut être utile pour remplacer le SPEQ. Le SMNR d'un analyte est mesuré à l'aide d'une méthode analytique particulière et on le définit comme une estimation du seuil minimal de niveau à rapporter de la plus faible concentration qu'il est possible d'obtenir avec un degré de confiance de 95 % dans au moins 75 % des cas (U.S. EPA, 2010). Aucun SMNR n'a été fourni pour les méthodes citées plus haut, à l'exception de la méthode EPA 200.5 pour laquelle un SMNR de 0,2 µg/L. À l'exception de la méthode EPA 3111B, les SMNR ou les LDM des méthodes précitées sont bien inférieurs aux concentrations de manganèse nécessaires pour effectuer une analyse quantitative précise du manganèse en deçà de la CMA et de l'OE.
6.2 Conservation et préparation des échantillons
Pour effectuer une évaluation quantitative du manganèse dissous, particulaire et total, certaines étapes de préparation et de conservation des échantillons doivent être respectées. La méthode SM 3030B fournit des directives sur les procédures de filtration et de conservation à effectuer pour le dosage des métaux dissous ou particulaires (APHA et coll., 2012). Pour le dosage des métaux dissous, les échantillons doivent être filtrés au moment du prélèvement à l'aide d'un dispositif de filtration en plastique prétraité, sous vide ou sous pression. Pour fractionner le manganèse dissous et le manganèse particulaire, il est recommandé d'utiliser des membranes filtrantes dont le diamètre des pores est de 0,22 à 0,45 µm (Kohl et Medlar, 2006; Brandhuber et coll., 2013). Le filtrat doit être acidifié à un pH < 2 avec de l'acide nitrique concentré. Pour la détermination du manganèse particulaire, le filtre doit être conservé et les particules qu'il contient doivent être digérées en laboratoire par une méthode appropriée (APHA et coll., 2012).
À l'heure actuelle, pour les méthodes EPA 200.7, EPA 200.8, EPA 200.9, SM 3111B, SM 3113B, SM 3120B et SM 3125B, la digestion acide des échantillons n'est nécessaire que si la turbidité d'un échantillon préservé dans l'acide est supérieure à une (1) unité de turbidité néphélométrique (UTN). Dans le cas des méthodes EPA, la digestion est réalisée en transférant une aliquote de l'échantillon dans une solution d'acide nitrique et d'acide chlorhydrique, puis en chauffant doucement la solution à une température d'environ 85 °C (digestion thermique) (U.S. EPA, 1994a, 1994b, 1994c). Il est recommandé d'effectuer une digestion par micro-ondes (SM 3030K) lorsque l'analyse du manganèse total récupérable est effectuée à l'aide d'une méthode SM qui fait appel à l'ICP-MS. Bien que les méthodes énoncées ci-dessus ne requièrent pas de digestion thermique en milieu acide pour l'analyse du manganèse total à moins que la turbidité ne dépasse 1 UTN, des recherches menées sur d'autres métaux, comme le plomb et le chrome, ont indiqué que cela ne permettait pas de quantifier avec précision la concentration totale d'un métal dans un échantillon. Par exemple, les exigences en matière d'analyse de la Third Unregulated Contaminant Monitoring Rule (UCMR3) prescrivent de solubiliser l'échantillon préservé dans l'acide par chauffage léger à l'aide d'acide nitrique, quelle que soit la turbidité de l'échantillon ou la méthode utilisée (U.S. EPA, 2012). De même, APHA et coll. (2012) recommandent de vérifier si les métaux ont été récupérés de manière adéquate dans les différentes matrices d'échantillon, en comparant les résultats obtenus avec et sans la digestion.
Dans certains cas, les services publics peuvent vouloir mesurer la fraction de manganèse colloïdal présente dans l'usine de traitement ou dans l'eau traitée. Cette mesure peut se révéler particulièrement importante lorsque l'on tente de déterminer la cause d'un problème touchant le fonctionnement d'une usine de traitement. Du manganèse colloïdal peut être présent dans les échantillons d'eau prélevés après l'application d'un oxydant fort comme l'ozone, le permanganate ou le dioxyde de chlore, avant la coagulation, ou dans les usines de traitement ayant recours à l'ozonisation intermédiaire (c.-à-d. les usines de biofiltration). Il est également plus probable de trouver ces solides colloïdaux dans les eaux douces, puisque les ions calcium et magnésium contribuent à déstabiliser et à agréger les particules d'oxyde de manganèse. En règle générale, on définit le manganèse colloïdal comme les particules d'oxyde de manganèse qui sont < 0,20 µm et > 30 000 daltons. Si du manganèse colloïdal est présent, il traversera les filtres de 0,20 µm et sera faussement quantifié en tant que manganèse dissous. Par conséquent, pour mesurer le manganèse colloïdal, il faudra faire passer l'échantillon sur un filtre possédant un seuil de coupure de 30 000 daltons, après la filtration initiale sur filtre de 0,20 µm.
6.3 Méthodes colorimétriques
Plusieurs méthodes colorimétriques permettent de mesurer le manganèse dissous dans l'eau potable. Ces méthodes sont fondées sur une réaction entre le manganèse dissous et d'autres composés, qui produit du permanganate, lequel est alors mesuré par colorimétrie. D'autres métaux ou composés organiques en solution peuvent provoquer des interférences au cours de ces réactions, qui peuvent avoir une incidence sur l'exactitude des résultats. Ces méthodes conviennent donc mieux à la surveillance de l'efficacité du traitement dans les usines de traitement qu'à la surveillance de la conformité. L'avantage des méthodes colorimétriques est qu'il existe des trousses sur le marché permettant de détecter rapidement les changements de concentration de manganèse, ce qui peut faciliter la surveillance des procédés dans une usine de traitement (Brandhuber et coll., 2013).
La méthode SM 3500 Mn B est une méthode colorimétrique basée sur l'oxydation au persulfate du manganèse dissous en présence de nitrate d'argent. Les échantillons contenant des oxydes de manganèse particulaire doivent être traités avec une série de composés réducteurs pour dissoudre ces oxydes. Il est possible d'effectuer des mesures photométriques en préparant des solutions étalons et en comparant l'absorbance de l'échantillon à celle des étalons. La concentration minimale détectable associée à cette méthode est de 42 µg/L (APHA et coll., 2012). Il existe également une méthode colorimétrique brevetée qui utilise de l'acide ascorbique, du cyanure alcalin et une solution indicatrice. L'intervalle de détection de cette méthode est de 0,01 à 0,7 mg/L (Brandhuber et coll., 2013).
7.0 Techniques de traitement et considérations liées au réseau de distribution
7.1 Chimie et traitement du manganèse
Il est important de connaître la chimie et la microbiologie du manganèse dans les systèmes d'approvisionnement en eau potable pour déterminer le système de traitement le plus approprié ou pour évaluer et optimiser les systèmes déjà utilisés pour l'élimination du manganèse. Comme il en a été question à la section 4.0, le manganèse existe sous différents états d'oxydation dans les systèmes d'approvisionnement en eau. Les quatre états d'oxydation les plus importants, dans le contexte du traitement de l'eau potable, sont les suivants : le Mn(II), un cation métallique divalent libre soluble et transparent dans l'eau; le Mn(III), un état transitoire qui existe sous la forme d'oxyde de manganèse (Mn2O3), lequel est un solide brun foncé/noir; le Mn(IV), un solide noir sous forme de MnO2(S); le Mn(VII), sous forme de MnO4-, un ion permanganate dissous qui est violet dans l'eau et qu'on ajoute à l'eau comme agent oxydant au cours du traitement de l'eau potable. Un bref aperçu de la chimie du manganèse pertinente au traitement de l'eau potable est présenté ci-dessous. Pour obtenir des renseignements plus détaillés, veuillez consulter Sommerfield (1999), Kohl et Medlar (2006), et Brandhuber et coll. (2013).
Les réactions chimiques qui dictent quelles espèces de manganèse sont présentes dans le cadre d'un traitement de l'eau potable sont les réactions d'oxydation/réduction, de précipitation/dissolution et de sorption/désorption. Dans une usine de traitement de l'eau potable, les trois réactions peuvent se produire au cours d'un même traitement. Les espèces de manganèse présentes varient en fonction du potentiel d'oxydation/réduction et du pH de l'eau, ainsi que d'autres paramètres présents dans l'eau qui peuvent se combiner au manganèse pour former des composés de manganèse. Dans des conditions de pH élevé ou de forte oxydation, le Mn(II) dissous, à l'équilibre, va former des oxydes, des hydroxydes ou des carbonates solides insolubles.
Les procédés de traitement du manganèse sont conçus de façon à tirer parti des différences de solubilité entre les espèces de manganèse. La solubilité du Mn(II) réduit est de plusieurs fois supérieure à celle du Mn(IV). Par conséquent, l'oxydation du Mn(II) en Mn(IV) entraîne la formation d'un précipité d'oxydes de manganèse solides. Étant donné que ces solides peuvent exister dans plusieurs états d'oxydation (p. ex. Mn(III) et Mn(IV)), on utilise souvent l'appellation MnOx(s) pour les désigner (Brandhuber et coll., 2013). La tendance du manganèse à précipiter ou à se dissoudre peut être contrôlée par la modification des conditions d'oxydation/réduction et de pH dans une usine de traitement de l'eau potable. Il convient de souligner que le fer et le manganèse se retrouvent fréquemment ensemble dans les sources d'approvisionnement en eau potable et que la présence de fer dans celles-ci peut avoir une incidence sur le traitement du manganèse. Pour en apprendre davantage sur ce sujet, veuillez consulter l'étude de Brandhuber et coll. (2013).
L'adsorption/désorption est le troisième procédé utilisé pour contrôler l'enlèvement du manganèse dans les usines de traitement de l'eau potable. Les particules de MnOx(s) ont une charge électrique qui varie avec le pH, mais dans la plupart des cas ces particules sont chargées négativement et ont la capacité d'adsorber les ions Mn(II) des solutions. Une fois le Mn(II) adsorbé sur les particules de MnOx(s), la surface catalyse l'oxydation du Mn(II) adsorbé en Mn(IV), ce qui accroît la vitesse d'oxydation du Mn(II) en Mn(IV).
Dans la pratique, le manganèse peut passer de la forme soluble à la forme particulaire et le taux de manganèse peut être difficile à gérer à des concentrations faibles (c.-à-d. < 0,015 mg/L) dans les usines de traitement et les réseaux de distribution (Brandhuber et coll., 2013). Il importe également de souligner que le MnOx (s) peut exister sous forme particulaire et colloïdale. La forme particulaire est composée de solides oxydés volumineux (> 0,20 à 0,45 µm) tandis que la forme colloïdale est formée de particules oxydées plus petites (< 0,20 µm et > 30 000 daltons). Dans certaines conditions, de grandes quantités de manganèse colloïdal peuvent se former lorsque du Mn(II) est oxydé directement avec un oxydant fort tel que l'ozone. Les particules colloïdales peuvent être difficiles à déstabiliser et l'ajout d'un coagulant doit être optimisé pour éliminer efficacement ces particules lors de la sédimentation et de la filtration (Casale et coll., 2002; Brandhuber et coll., 2013).
7.2 Traitement à l'échelle municipale
Pour choisir le système de traitement approprié pour enlever le manganèse ou pour optimiser un système existant, il est nécessaire de bien connaître les formes de manganèse (dissous, colloïdal ou particulaire) présentes dans l'eau prélevée à la source. Lorsque l'eau prélevée à la source doit être traitée pour en éliminer le manganèse, le Mn(II) sous forme dissoute est généralement la principale espèce présente (c.-à-d. dans les lacs ou les eaux souterraines anoxiques). Toutefois, selon le pH et la teneur en oxygène dissous (OD) de l'eau, le manganèse peut être présent sous formes dissoute et particulaire. Les méthodes de traitement utilisées font généralement appel à une combinaison de procédés (p. ex. oxydation, adsorption et (ou) filtration) permettant d'éliminer à la fois le manganèse dissous et particulaire. Si le manganèse n'est présent que sous forme colloïdale ou particulaire (Mn(IV)), il peut être éliminé par des procédés courants d'élimination des particules, tels que la filtration conventionnelle ou la filtration membranaire à basse pression (microfiltration ou ultrafiltration).
Le Mn(II) dissous peut être éliminé ou contrôlé de différentes façons : pratiques relatives à l'eau de à la source, oxydation/séparation physique, adsorption/oxydation, filtration biologique et adoucissement par précipitation. L'une des techniques les plus couramment utilisées pour réduire efficacement les concentrations de manganèse dans l'eau potable consiste à effectuer une oxydation directe du Mn(II) dissous pour former du MnOx (s) particulaire, puis à éliminer ce dernier par un procédé physique, comme la clarification et la filtration sur milieu granulaire ou la filtration membranaire à basse pression. Ces méthodes permettent habituellement d'éliminer 80 à 99 % du manganèse et d'atteindre une concentration inférieure à 0,04 mg/L dans l'eau traitée. Une autre technique de traitement courante pour enlever le manganèse est l'utilisation d'un milieu filtrant enrobé de MnOx(s) qui adsorbe le Mn(II) dissous pour l'oxyder ensuite à la surface en présence d'un oxydant approprié, tel que du chlore libre ou du permanganate de potassium. Cette technique de traitement conduit généralement à un taux d'élimination très élevé et permet d'atteindre des concentrations de manganèse inférieures à 0,020 mg/L dans l'eau traitée. La filtration biologique et l'adoucissement se sont également révélés efficaces pour éliminer le manganèse, et permettent d'atteindre des concentrations inférieures à 0,03 mg/L dans l'eau traitée (Casale et coll., 2002; Kohl et Medlar, 2006; Tobiason et coll., 2008; Kohl et Dixon, 2012; Brandhuber et coll., 2013). Beaucoup de ces technologies, en particulier le milieu filtrant enrobé de MnOx(s), peuvent être utilisées avec efficacité pour éliminer le manganèse de l'eau potable dans les systèmes à petite échelle. Les services publics peuvent réussir à atteindre des concentrations de manganèse encore plus faibles que celles mentionnées plus haut, selon le fonctionnement et la conception des installations de l'usine de traitement. En particulier, il a été démontré que l'optimisation d'usines de traitement existantes pouvait permettre de réduire avec efficacité les concentrations de manganèse en deçà de 0,02 mg/L (Brandhuber et coll., 2013).
Le type de traitement qui sera le plus efficace pour éliminer le manganèse dépend du type et du taux de manganèse présent dans l'eau prélevée à la source, de la chimie générale de l'eau, du procédé de traitement choisi, et des objectifs relatifs à la qualité de l'eau. Les services publics devraient effectuer des activités de surveillance dans les usines de traitement, notamment un dosage périodique des différentes formes de manganèse (p. ex. dissous et particulaire), pour s'assurer que les procédés de traitement utilisés éliminent adéquatement le manganèse. Brandhuber et coll. (2013) fournissent des directives détaillées sur le traitement du manganèse dans l'eau potable.
Par le passé, les limites fixées pour le manganèse dans l'eau potable étaient fondées sur des considérations esthétiques et sur la faisabilité des traitements (U.S. EPA, 1979). Plus récemment, des études ont révélé que les particules de MnOx(s) présentes dans l'eau potable entraînaient une coloration de l'eau et qu'elles étaient visibles à l'œil nu à des concentrations aussi faibles que 0,005 à 0,02 mg/L (Sly et coll., 1990; Sain et coll., 2014). En outre, des enquêtes approfondies ont démontré qu'une concentration de manganèse de 0,05 mg/L dans l'eau traitée n'était pas assez faible pour maintenir au minimum le nombre de plaintes de consommateurs (Sly et coll., 1990; Casale et coll., 2002; Kohl et Medlar, 2006). Selon Kohl et Medlar (2006), les résultats d'études détaillées concernant les services publics indiquent qu'une majorité de consommateurs a régulièrement des problèmes de coloration de l'eau lorsque les concentrations de manganèse sont de 0,05 mg/L au robinet. De nombreuses études ont révélé que la concentration de manganèse dans l'eau traitée pouvait être réduite à moins de 0,02 mg/L en optimisant la conception et le fonctionnement d'une usine de traitement nouvelle ou existante (Kohl et Medlar, 2006; Tobiason et coll., 2008; Brandhuber et coll., 2013). Kohl et Medlar (2006) ont publié des données tirées d'une enquête effectuée dans 189 usines de traitement éliminant le manganèse des sources d'eau souterraine et de surface à l'aide de diverses technologies de traitement. La moyenne géométrique des concentrations moyennes de manganèse relevées dans l'eau traitée par ces usines était de 0,010 mg/L. De même, Casale et coll. (2002) ont indiqué qu'environ 80 % des usines de traitement des eaux souterraines et 70 % des usines de traitement des eaux de surface (193 usines de traitement) atteignaient des concentrations de manganèse de 0,01 mg/L dans l'eau traitée. Ces données montrent que les services publics peuvent obtenir des concentrations plus faibles dans l'eau traitée que celles indiquées précédemment et que la plupart des usines de traitement sont capables d'atteindre une concentration de manganèse inférieure à 0,02 mg/L dans l'eau traitée (Casale et coll., 2002; Kohl et Medlar; 2006; Tobiason et coll., 2008; Brandhuber et coll., 2013).
Les répercussions de l'accumulation et de la libération de manganèse et de métaux coexistants dans les réseaux de distribution ont également fait l'objet de recherches approfondies (U.S. EPA, 2006; Friedman et coll., 2010; Ginige et coll., 2011; Brandhuber et coll., 2015). Des concentrations élevées de manganèse au robinet peuvent être liées à l'accumulation et à la libération de manganèse dans le réseau de distribution plutôt qu'à une concentration élevée de manganèse dans l'eau prélevée à la source ou dans l'eau traitée (Brandhuber et coll., 2015).
À la lumière de ce qui précède, il est recommandé que les usines de traitement établissent un objectif de manganèse total dans l'eau traitée ≤ 0,015 mg/L (Brandhuber et coll., 2013), ce qui représente un objectif atteignable pour la plupart des usines de traitement optimisées et exploitées de façon adéquate. L'établissement d'un tel objectif permettra de minimiser l'accumulation de manganèse dans le réseau de distribution et la libération subséquente de manganèse dans l'eau distribuée, et d'éviter ainsi autant les plaintes de clients à l'égard de la couleur de l'eau que l'augmentation des concentrations de manganèse dans l'eau du robinet (qui pourraient être supérieures à la CMA).
7.2.1 Élimination dans les sources d'eau
Dans certains cas, il peut être possible de réduire les concentrations de manganèse dans l'eau qui entre dans une usine de traitement en gérant le taux de manganèse présent dans l'eau prélevée à la source. Les concentrations de manganèse varient généralement moins dans le temps (d'une journée ou d'une saison à l'autre), dans les eaux souterraines d'un puits individuel, que dans les eaux de surface (Barbeau et coll., 2011). Des variations importantes de la concentration de manganèse ont toutefois été observées entre différents puits d'un même champ de captage situés à proximité les uns des autres. Les services publics qui disposent de plusieurs puits peuvent donc pomper de façon sélective une combinaison de puits à différents débits pour diminuer la concentration de manganèse dans l'eau qui entre dans l'usine de traitement (Brandhuber et coll., 2013). Une autre solution pour contrôler la concentration de manganèse dans l'eau souterraine consiste à oxyder le Mn(II) dissous in situ en augmentant le potentiel redox dans l'aquifère entourant les puits. Pour ce faire, on injecte de l'eau aérée dans l'aquifère par des puits de recharge. Cette technologie est rarement utilisée en raison des préoccupations liées à l'altération des propriétés géochimiques de l'aquifère et du risque de colmatage des puits d'extraction (Mettler et coll., 2001). Malgré ces préoccupations, cette technologie est utilisée à grande échelle avec succès en Suisse et aux États-Unis (AWWA, 1984; Mettler et coll., 2001).
Des techniques d'aération peuvent également être employées comme solution pour réduire la concentration de manganèse dans les eaux de surface. L'oxygène dissous (OD) présent dans l'hypolimnion des réservoirs et des lacs peut disparaître entièrement au cours de la stratification thermique. Ce phénomène peut entraîner une augmentation de la concentration de Mn(II) dissous dans la colonne d'eau, causée par les rejets provenant des sédiments dans des conditions anoxiques. L'oxygénation et l'aération hypolimnique peuvent être utilisées pour ajouter de l'OD dans les réservoirs tout en maintenant la stratification (Brandhuber et coll., 2013). Il existe plusieurs types d'aérateurs qui génèrent un flux de gaz au contact de l'eau. L'eau reçoit ainsi de l'oxygène, qui est ensuite transporté dans l'hypolimnion. La quantité d'oxygène requise pour aérer adéquatement une partie ou la totalité de l'hypolimnion dépend du volume d'eau, du profil d'OD dans le lac et de la demande en oxygène des sédiments. L'aération doit être soigneusement contrôlée pour éviter la déstratification du réservoir, qui pourrait entraîner d'autres problèmes liés à la qualité de l'eau (Kohl et Medlar, 2006). Brandhuber et coll. (2013) ont présenté des données tirées d'une étude de cas portant sur un système d'aération hypolimnique à grande échelle installé dans un réservoir en période de stratification thermique. La concentration de Mn(II) mesurée à l'entrée d'eau de l'usine était de 1,7 mg/L. Après avoir considéré plusieurs options de traitement, le service public a décidé d'installer un système d'oxygène liquide constitué de deux conduits de diffusion d'oxygène gazeux placés au fond du réservoir. On a fait fonctionner le système d'avril à octobre en réglant le flux d'oxygène de façon à maintenir la concentration d'OD au-dessus de 5 mg/L. Ce système a permis de réduire au minimum la quantité de Mn(II) dissous libéré par les sédiments et d'abaisser la concentration de manganèse dans l'eau prélevée à la source à une moyenne annuelle inférieure à 0,05 mg/L (la valeur maximale était inférieure à 0,2 mg/L).
Les usines de traitement des eaux de surface qui possèdent des réservoirs profonds et un système de prise d'eau à plusieurs niveaux peuvent également puiser l'eau à des profondeurs variables. Ces systèmes permettent de prendre l'eau à la profondeur choisie du réservoir en fonction de la qualité de l'eau aux différentes profondeurs. Lorsque le principal objectif est de réduire au minimum le taux de manganèse, les usines de traitement peuvent surveiller la concentration d'OD et de Mn(II) dissous à chaque prise d'eau, et tirer l'eau là où la concentration est la moins élevée (généralement à de faibles profondeurs une fois que l'hypolimnion devient anoxique dans un réservoir). Habituellement, dans la pratique, on détermine à quel niveau prendre l'eau en tenant compte de divers facteurs liés à la qualité de l'eau, puisque tirer l'eau à de faibles profondeurs risque d'entraîner d'autres problèmes, comme une augmentation de la quantité de cellules algales ou des problèmes liés au goût et à l'odeur (Benskin et coll., 2004; Brandhuber et coll., 2013).
7.2.2 Oxydation chimique/séparation physique
Lorsque la principale forme de manganèse présente dans l'eau prélevée à la source est le Mn(II) dissous, effectuer une oxydation directe pour convertir le Mn(II) en précipités de MnOx(s) avant d'effectuer une séparation physique peut être un moyen efficace d'éliminer le manganèse dans l'eau potable. L'efficacité de ces procédés repose en grande partie sur la capacité du ou des agents oxydants à convertir entièrement le Mn(II) dissous en MnOx(s) solide(s). L'efficacité de l'oxydation du manganèse dépend de plusieurs facteurs, dont le pH, l'Eh, la température, le temps de réaction, l'alcalinité et la demande totale en oxydant dans l'eau (p. ex. présence de fer, de sulfure, de nitrate, d'ammoniac et de composés organiques) (Casale et coll., 2002; Brandhuber et coll., 2013). Une fois que le Mn(II) dissous est converti en particules de MnOx(s), il peut être retiré par coagulation/floculation, par sédimentation, ou par flottation à l'air dissous et filtration sur milieu granulaire. La filtration membranaire à basse pression (ultra et microfiltration) peut également être utilisée. Pour que les procédés d'élimination physiques soient efficaces, il faut s'assurer que le manganèse qui entre dans le filtre est particulaire (Tobiason et coll., 2008). En outre, selon Brandhuber et coll. (2013), la taille des particules et l'endroit où elles sont générées dans la chaîne de traitement sont des facteurs clés de l'élimination efficace du manganèse. Par exemple, les particules colloïdales doivent être déstabilisées par coagulation/floculation avant d'être filtrées.
L'oxydation du manganèse dans l'eau est une réaction autocatalytique en trois étapes ayant différentes cinétiques de réactions, ce qui entraîne d'importantes répercussions sur le traitement de l'eau potable. La première étape est l'oxydation du Mn(II) en solution par l'oxydant (réaction relativement lente), la deuxième phase est l'adsorption du Mn(II) sur les solides de MnOx(s) (réaction rapide) et la troisième réaction est l'oxydation catalysée en surface de l'ion Mn(II) sorbé par l'ajout d'un oxydant (réaction moyennement rapide). Il convient de noter que la deuxième étape est également importante dans les processus de filtration, car les couches de MnOx(s) présentes sur le matériau filtrant adsorbent rapidement le Mn(II) dissous, qui peut alors être oxydé. Cette question est abordée plus en détail à la section 7.2.3.
Les agents oxydants généralement utilisés pour convertir le Mn(II) dissous en précipités de MnOx(s) sont notamment le permanganate (MnO4-), le dioxyde de chlore (ClO2) et l'ozone (O3). Dans des conditions de pH élevé, le chlore et l'oxygène peuvent également être efficaces. Des études menées par Knocke et coll. (1990a) et Gregory et Carlson (2003) ont indiqué que la cinétique des réactions de ces oxydants avec le Mn(II) est suffisamment rapide, dans la plupart des conditions de pH, de température, de quantités de carbone organique dissous (COD) et de concentrations initiales de Mn(II), pour être utilisée dans les procédés de traitement de l'eau potable. L'oxydation au chlore et l'oxydation à l'oxygène ne sont efficaces que si le pH est supérieur respectivement à 9 et à 9,5 (Knocke et coll., 1990a; Brandhuber et coll., 2013). Des renseignements détaillés sur l'efficacité de différents oxydants pour l'élimination du manganèse dans l'eau potable sont donnés dans Knocke et coll. (1990a), Casale et coll. (2002), Gregory et Carlson (2003), Kohl et Medlar (2006), Tobiason et coll. (2008), et Brandhuber et coll. (2013).
Brandhuber et coll. (2013) se sont penchés sur les principaux facteurs ayant un effet sur l'efficience de l'oxydation chimique du Mn(II), notamment le choix de l'oxydant, la dose appliquée, la cinétique de réaction, le temps de réaction, le lieu de l'ajout de l'oxydant, et la surveillance. Sur le plan opérationnel, le point le plus important est de laisser suffisamment de temps de réaction, dans l'usine de traitement, pour obtenir une oxydation complète et efficace du Mn(II). En général, dans une usine de traitement, l'utilisation d'un oxydant fort ayant un pH approprié est nécessaire pour pouvoir obtenir une réaction d'oxydation suffisamment rapide pour être efficace (Brandhuber et coll., 2013). De plus, les doses d'oxydant doivent être supérieures aux rapports stœchiométriques pour répondre à la demande en oxydant de l'eau prélevée à la source et pour obtenir une oxydation adéquate du manganèse (Kohl et Medlar, 2006). La présence de fer, qui accompagne souvent celle du manganèse dans l'eau prélevée à la source, peut notamment avoir un effet sur l'efficacité de l'oxydation du manganèse. Comme le fer s'oxyde plus facilement que le manganèse à n'importe quel pH, la demande en oxydant du fer doit être comblée avant qu'une oxydation significative du manganèse ne puisse se produire (Brandhuber et coll., 2013). Avant de choisir un agent oxydant, les services publics doivent effectuer des essais de floculation afin de déterminer quels oxydants seraient efficaces pour leur source d'eau et leur usine de traitement.
L'utilisation de permanganate, de dioxyde de chlore et d'ozone pour oxyder le Mn(II) peut entraîner la formation de particules colloïdales de MnOx(s) d'une taille inférieure à un (1) µm (Knocke et coll., 1990a; Brandhuber et coll., 2013). La formation de ces particules MnOx(s) colloïdales se produit plus souvent dans une eau de faible dureté, puisque la présence d'ions calcium et magnésium dissous aide à la déstabilisation et à l'agrégation de ces colloïdes. On recommande généralement d'ajouter ces oxydants avant les étapes de coagulation/floculation afin que les particules colloïdales puissent être déstabilisées et retirées au moyen de procédés de sédimentation et de filtration conventionnels (Brandhuber et coll., 2013).
Plusieurs combinaisons différentes d'oxydation et de séparation physique sont utilisées pour réduire le taux de manganèse dans l'eau : emploi de multiples oxydants, variation dans le site d'ajout de l'oxydant, recours à diverses méthodes de séparation physique, etc. Les sections qui suivent abordent les considérations relatives à chaque agent oxydant et à chaque technologie de filtration. Ces sections présentent également les capacités d'élimination du manganèse dissous de ces technologies et offrent des exemples d'usines de traitement qui ont utilisé ces techniques à grande échelle ou dans le cadre d'essais-pilotes, tout en reconnaissant que l'efficacité de tout procédé de traitement est propre à chaque site, et qu'elle varie en fonction de la qualité de l'eau prélevée à la source, et de la conception et du fonctionnement de chaque installation de traitement.
7.2.2.1 Permanganate
Du permanganate MnO4-), obtenu sous forme de permanganate de sodium (NaMnO4) ou de permanganate de potassium (KMnO4), permet d'oxyder le Mn(II) dissous. Par le passé, le KMnO4 était la forme de permanganate la plus utilisée pour l'oxydation du Mn(II). Brandhuber et coll. (2013) ont toutefois noté que de plus en plus de services publics ont recours au NaMnO4, car celui-ci est disponible sous forme de solution très concentrée, ce qui leur évite d'avoir à se procurer le matériel nécessaire pour dissoudre le produit sec à l'usine de traitement.
Les données sur l'oxydation du Mn(II) par le permanganate indiquent que cette réaction se produit très rapidement dans toute une gamme de pH et de température de l'eau, lorsque l'eau a une faible teneur en COD (< 3 mg/L) (Knocke et coll., 1987, 1990a). La dose stœchiométrique de permanganate requise pour oxyder le Mn(II) en Mn(IV) est de 1,9 mg de KMnO4 par mg de Mn(II). Cependant, comme pour toutes les réactions d'oxydation, la demande provenant des autres éléments présents dans l'eau prélevée à la source peut faire augmenter la dose totale nécessaire. Knocke et coll. (1990a) ont démontré que pour un pH situé entre 5,5 et 9,0, l'oxydation de 0,25 mg/L de Mn(II) avec une quantité de permanganate équivalente à 105 % de la valeur stœchiométrique se produisait en 60 secondes (T = 25 °C, COD < 1 mg/L). L'augmentation de la teneur en COD à 10 mg/L a fait grimper le temps d'oxydation du Mn(II) à 1 à 2 minutes (T = 25 °C, pH = 7,0). À une température de 5 °C et à un pH de 5,5, l'oxydation n'a pas permis de réduire efficacement la concentration finale de résidus de Mn(II) en deçà de 0,05 mg/L. Les auteurs ont fait observer que l'utilisation du permanganate pour oxyder le Mn(II) constitue une solution peu pratique lorsque l'eau prélevée à la source contient beaucoup de matière organique, en raison du coût élevé en produits chimiques (Knocke et coll., 1987). Les résultats des travaux de Gregory et Carlson (2003) ont montré que plus la concentration initiale de Mn(II) était faible, plus la durée de la réaction d'oxydation du Mn(II) par le permanganate était longue. Pour une concentration initiale de Mn(II) de 60 µg/L et une dose de KMnO4 correspondant à 300 % de la valeur stœchiométrique, il a fallu 1 200 secondes pour atteindre une concentration résiduelle de Mn(II) inférieure à 20 µg/L (objectif de l'étude pour l'eau traitée). En comparaison, le taux d'oxydation avec une concentration initiale 1 000 µg/L était beaucoup plus rapide, et a permis d'atteindre une concentration de Mn(II) inférieure à 10 µg/L en moins de 200 secondes. Pour ces tests, les paramètres de qualité de l'eau étaient les suivants : pH = 7,0; COT = 3,4 mg/L; T = 9 °C.
Dans la pratique, le dosage du permanganate pour oxyder le Mn(II) doit être optimisé avec précision de façon à oxyder complètement le Mn(II) sans laisser d'excédent de permanganate dans l'eau traitée. Un excédent de permanganate pourrait colorer en rose l'eau qui sort de l'usine de traitement ou produire un précipité de MnOx(s) dans le réseau de distribution, ce qui entraînerait une augmentation du nombre de plaintes de consommateurs à propos de la couleur de l'eau. Il est donc important de porter une attention particulière au temps de contact et à la dose de permanganate utilisée. Brandhuber et coll. (2013) ont indiqué que pour la plupart des usines de traitement, un temps de réaction de 2 à 4 minutes est suffisant lorsque la concentration initiale de Mn(II) ou le pH sont plus faibles (p. ex. pH de 6 à 6,5), mais que le temps de réaction peut souvent être plus court dans des conditions de pH plus élevé.
De nombreuses études ont démontré qu'il est possible d'éliminer efficacement le Mn(II) dissous dans des usines de traitement de l'eau potable à grande échelle en utilisant l'oxydation au permanganate suivie d'une séparation physique (Carlson et coll., 1997; Kohl et Medlar, 2006; Brandhuber et coll., 2013). Kohl et Medlar (2006) ont publié des données provenant de sept usines de traitement à grande échelle qui éliminaient le manganèse par l'ajout de KMnO4 suivi d'une filtration. Dans tous les cas, ces usines ont réussi à éliminer plus de 80 % du manganèse et à atteindre une concentration moyenne de manganèse inférieure à 0,045 mg/L dans l'eau traitée. Deux de ces usines ont réussi à éliminer entre 80 et 86 % du manganèse présent dans l'influent en effectuant une oxydation au KMnO4 suivie d'une filtration conventionnelle (mélange, floculation, décantation et filtration sur média granulaire) : les concentrations moyennes de manganèse, qui étaient de 0,090 et 0,111 mg/L à l'entrée de l'usine, étaient respectivement de 0,019 mg/L et 0,021 mg/L à la sortie. Les installations qui ont couplé l'ajout de KMnO4 à une autre méthode d'oxydation ont obtenu un taux d'élimination du manganèse plus élevé. Deux usines ayant combiné l'aération à l'ajout de KMnO4 et à la filtration conventionnelle ont réussi à éliminer respectivement 92 et 97 % du manganèse, et à atteindre des concentrations moyennes de 0,019 mg/L et de 0,045 mg/L dans l'eau traitée. La méthode de flottation à l'air dissous a également été utilisée pour éliminer le manganèse oxydé. En Australie, une usine de traitement a réussi à éliminer avec succès le manganèse en utilisant un prétraitement combiné avec du permanganate de potassium, suivi de l'ajout de chlorhydrate de polyaluminium, d'une floculation et d'une flottation à l'air dissous (Kohl et Medlar, 2006). La concentration de manganèse a été réduite de 0,08 mg/L dans l'eau brute à moins de 0,02 mg/L dans l'eau traitée. Aucune donnée opérationnelle n'était disponible pour les usines de traitement mentionnées ci-dessus.
La documentation consultée contient plusieurs études de cas portant sur des techniques visant l'optimisation des systèmes utilisant la méthode d'oxydation par KMnO4 suivie d'une filtration conventionnelle (Brandhuber et coll., 2013). Une installation municipale qui traitait l'eau brute d'un lac dont la concentration en Mn(II) variait considérablement (fluctuations horaires de 0,2 à 1,0 mg/L) a été optimisée en utilisant la mesure du Eh pour contrôler la dose de permanganate ajoutée. L'usine est passée de l'ajout de substances chimiques par débit contrôlé à un dosage déterminé par l'Eh. Avec cette méthode, la concentration de manganèse dans l'eau traitée était inférieure à 0,01 mg/L 90 % du temps et inférieure à 0,02 mg/L 95 % du temps.
Une méthode combinant la filtration membranaire à basse pression et l'oxydation du Mn(II) par KMnO4 a également été utilisée pour l'élimination du manganèse dans des usines de traitement de l'eau potable à grande échelle. Le permanganate est l'oxydant de choix pour les installations qui utilisent des membranes qui résistent aux oxydants. Dans ces cas, il est important que les réactions d'oxydation soient terminées avant que l'eau n'atteigne les membranes, car la formation d'un précipité dans les pores de la membrane pourrait endommager la structure de cette dernière. Une usine à grande échelle utilisant l'ultrafiltration/le permanganate de potassium a réussi à traiter de l'eau brute contenant 0,62 mg/L de manganèse et 0,4 mg/L de fer, pour atteindre des concentrations inférieures à la limite de détection (non précisée) (AWWA, 2005). L'usine, qui fonctionne à un flux net de 25 gfd, ajoute d'abord du KMnO4 à l'eau, laquelle est ensuite soumise à un mélange statique avant d'être envoyée dans une chambre d'oxydation, puis dans trois réservoirs à membrane immergés placés parallèlement. Un réservoir de récupération reçoit les eaux rejetées et le surnageant est recyclé et réacheminé au début du procédé, ce qui permet un taux de récupération total du système de 99 %. Kohl et Medlar (2006) mentionnent également une usine de traitement de l'eau potable à grande échelle qui obtient un taux élevé d'élimination du manganèse en utilisant le KMnO4 suivi d'une microfiltration. L'usine a déclaré avoir atteint un taux d'élimination du manganèse de 99 %, en obtenant une concentration de 0,005 mg/L à partir d'une concentration moyenne de 0,811 mg/L dans l'influent. On ne dispose d'aucune donnée opérationnelle sur cette usine de traitement (AWWA, 2005).
7.2.2.2 Dioxyde de chlore
Le dioxyde de chlore (ClO2) peut oxyder efficacement le Mn(II) dissous en Mn(IV), mais il convient davantage pour les sources d'eau où la demande en oxydant des matières organiques n'est pas très élevée (Tobiason et coll., 2008). La réaction entre le ClO2 et le Mn(II) dissous est rapide, habituellement 1 à 2 minutes au maximum; la durée varie avec la dose de ClO2 et la concentration initiale de Mn(II) dissous (Brandhuber et coll., 2013). Comme pour le permanganate, l'efficacité de l'oxydant est fortement réduite à basse température (5 °C) et à pH faible (5,5) (Knocke et coll., 1990a). La dose stœchiométrique de ClO2 pour l'oxydation du Mn(II) est de 2,45 mg ClO2 par mg de Mn(II). Toutefois, en présence de Mn(II), le ClO2 n'est pas complètement réduit en ion chlorure (Cl-), mais seulement en ion chlorite (ClO2-) (Knocke et coll., 1990a). Il est également important de souligner que si le dioxyde de chlore et l'ion chlorite ne sont pas éliminés avant la deuxième désinfection au chlore, ils réagiront avec le chlore libre pour former un ion chlorate. Lorsqu'un ion chlorate est présent dans l'eau, il est très persistant et extrêmement difficile à éliminer. Au Canada, la recommandation basée sur la santé pour l'eau potable est de 1 mg/L pour le chlorite et le chlorate. Toutefois, pour être en mesure de respecter cette recommandation, on conseille aux usines de traitement qui utilisent le ClO2 comme désinfectant principal de ne pas en ajouter plus de 1,2 mg/L (Santé Canada, 2008).
Knocke et coll. (1987) ont démontré qu'une dose de 1 à 1,5 mg/L de ClO2 oxydait efficacement des concentrations initiales de Mn(II) d'environ 0,25 mg/L sur une large gamme de pH lorsque le COD était inférieur à 2,5 mg/L. Par opposition, l'eau contenant entre 8 et 10 mg/L de COD nécessitait plus de 3 mg/L de ClO2. Gregory et Carlson (2003) ont comparé l'oxydation du Mn(II) au dioxyde de chlore, au permanganate de potassium et à l'ozone en utilisant des concentrations initiales de Mn(II) plus faibles (60 µg/L). Ils ont découvert que le dioxyde de chlore était le plus efficace pour obtenir des concentrations de manganèse < 10 µg/L dans l'eau traitée. Avec du ClO2 à la dose stœchiométrique relative de 200 %, l'oxydation a fait passer la concentration de manganèse dans l'eau de 60 µg/L à moins de 10 µg/L en 300 secondes (T = 9 °C; pH = 7,0; COT = 3,4 mg/L). À une concentration initiale de Mn(II) de 200 µg/L, le processus a pris moins de 75 secondes.
Étant donné que la dose de dioxyde de chlore ne doit pas dépasser 1,2 mg/L, plusieurs auteurs ont indiqué que l'utilisation du dioxyde de chlore seul pour l'oxydation du Mn(II) se limite à l'eau qui présente une faible teneur en COD et en Mn(II) dissous, et qui nécessite un traitement par oxydation. Dans certains cas, l'ajout de permanganate en plus du dioxyde de chlore peut se révéler efficace pour l'eau ayant une teneur en COD plus élevée (Knocke et coll., 1987; Casale et coll., 2002; Brandhuber et coll., 2013). Il faut également tenir compte du fait que le dioxyde de chlore doit être produit sur place en raison de son haut degré de réactivité.
Malgré ces restrictions, plusieurs usines de traitement à grande échelle ont déclaré avoir recours à l'oxydation au dioxyde de chlore puis à la séparation physique pour éliminer le manganèse. Kohl et Medlar (2006) ont présenté des données provenant de plusieurs usines qui réussissaient à éliminer 81 à 95 % du manganèse et à atteindre des concentrations aussi faibles que 0,001 mg/L dans l'eau traitée en utilisant du dioxyde de chlore avant une filtration conventionnelle. Dans une étude de cas présentée par Brandhuber et coll. (2013), une usine de traitement à grande échelle qui recevait des plaintes au sujet de la couleur de l'eau a obtenu des résultats concluants en remplaçant le permanganate de potassium par le dioxyde de chlore pour l'oxydation du Mn(II) dans l'eau brute, dont la concentration variait entre 0,07 et 0,2 mg/L. On y a découvert que le ClO2 était plus efficace pour contrôler les concentrations à moins de 0,02 mg/L. De même, des études visant à déterminer quel était l'oxydant le plus efficace pour l'élimination du Mn(II) ont montré que le ClO2 était plus efficace que le permanganate de potassium et l'ozone pour obtenir des concentrations faibles de Mn(II). Des doses de dioxyde de chlore allant de 0,44 à 1,5 mg/L ont permis d'oxyder efficacement le Mn(II) et d'en abaisser la concentration à 0,005 mg/L sans produire des taux inacceptables de chlorite (Carlson et Gregory, 2003).
Une méthode consistant à combiner l'oxydation au ClO2 et la microfiltration est également efficace pour enlever le manganèse de l'eau potable. Tobiason et coll. (2008) ont fait état d'un système pilote capable de faire passer la concentration de manganèse dans l'influent de 0,094 mg/L à 0,001 mg/L en utilisant 0,5 mg/L de dioxyde de chlore comme oxydant de préfiltration, suivi d'une microfiltration.
7.2.2.3 Ozone
L'ozone est un puissant oxydant qui peut oxyder efficacement le Mn(II), mais il est considéré comme moins efficace que les autres oxydants pour obtenir des concentrations de manganèse inférieures à 0,02 mg/L dans l'eau potable (Brandhuber et coll., 2013). L'oxydation à l'ozone, dans les procédés de traitement de l'eau potable, met habituellement en jeu de l'O3 moléculaire et le radical hydroxyle HO neutre. Dans le cas de l'oxydation du Mn(II) dissous, des études ont démontré que c'est l'O3 moléculaire qui réagit directement avec le Mn(II) et que les radicaux hydroxyles sont relativement inefficaces (Nowell et Hoigne, 1987). La dose stœchiométrique d'ozone nécessaire à l'oxydation du Mn(II) est de 0,87 mg O3 par mg Mn(II) (Knocke et coll., 1990a). Dans la pratique, la dose requise est généralement deux à cinq fois supérieure, selon l'alcalinité et la teneur en COD de l'eau prélevée à la source. La présence de COD dans l'eau prélevée à la source inhibe considérablement l'oxydation du Mn(II) par l'ozone en raison de la demande en oxydant concurrentielle provenant du COD (Knocke et coll., 1990a). Cet effet peut être atténué par l'augmentation de l'alcalinité, qui favorise l'oxydation directe du Mn(II) par l'O3 en diminuant la formation de radicaux hydroxyles (Paillard et coll., 1989). La cinétique de l'oxydation du Mn(II) par l'ozone est similaire à celle observée avec le permanganate et le dioxyde de chlore à un pH et à une température similaires, bien que le taux de manganèse résiduel soit habituellement plus élevé. Selon Knocke et coll. (1990a) et Carlson et Gregory (2003), l'oxydation du Mn(II) par l'ozone se produit rapidement (30 à 60 secondes) avec diverses doses d'ozone (0,5 à 2,0 mg/L) et dans des conditions variées de pH (5,63 à 7,0), de teneurs en COD (1 et 3,4 mg/L), et de températures (9 et 25 °C), mais ces expériences n'ont pas révélé de faibles concentrations (< 0,02 mg/L) de manganèse résiduel.
De nombreux auteurs ont souligné qu'il peut être difficile d'obtenir un dosage optimal de l'ozone en raison des demandes concurrentes en oxydant (Kohl et Medlar, 2006; Tobiason et coll., 2008; Brandhuber et coll., 2013). Non seulement l'ozone oxyde le Mn(II) dissous, mais à des doses suffisamment élevées il peut également oxyder des particules d'oxyde de Mn(III) et de Mn(IV) à l'état d'oxydation du Mn(VII) et produire du permanganate, ce qui peut provoquer une coloration rose de l'eau. Gregory et Carlson (2003) ont indiqué qu'en raison de la demande de base provenant de la matière organique naturelle (MON), l'élimination efficace du Mn(II) avec l'ozone nécessitait des doses d'ozone suffisamment élevées pour entraîner la production de Mn(VII) et une coloration de l'eau traitée.
Quelques études pilotes ont été menées pour évaluer une méthode d'élimination du manganèse consistant à effectuer une ozonation suivie d'une filtration (McKnight et coll., 1993; Wilczak et coll., 1993). McKnight et coll. (1993) ont réalisé des études pilotes visant à déterminer s'il était possible de remplacer le chlore par l'ozone pour oxyder le manganèse dans une usine de filtration conventionnelle. L'eau brute, à cet endroit, avait une teneur en COT de 6 à 8 mg/L, un pH de 6,5 à 7,2 et une alcalinité de 30 à 40 mg/L sous forme de CaCO3. Les auteurs ont découvert qu'il fallait des doses élevées d'ozone pour oxyder le Mn(II) dans l'eau brute et que les particules oxydées formaient de petits flocs à tête d'épingle difficiles à sédimenter et à filtrer. L'ozone était alors utilisé sur l'eau décantée. L'application d'une dose d'ozone de 2,5 mg/L à l'eau décantée, suivie d'une filtration, a permis d'éliminer 95 % du Mn(II) dissous, dont les concentrations initiales se situaient entre 0,6 et 1,0 mg/L. D'autres auteurs ont indiqué que l'oxydation du Mn(II) produisait des particules de MnOx(s) colloïdales difficiles à retirer après la sédimentation, et que des adjuvants de filtration étaient nécessaires pour capter les solides à l'étape de la filtration (O'Brien et coll., 1996; Tobiason et coll., 2008). En outre, on ajoute rarement du chlore avant la filtration lorsqu'une ozonation est effectuée à cette étape, ce qui élimine la possibilité de réactions d'adsorption ou d'oxydation dans le filtre. Ces facteurs font en sorte qu'un traitement à l'ozone permet difficilement d'obtenir des concentrations de Mn(II) dissous résiduel inférieures à 0,025 mg/L (Tobiason et coll., 2008).
7.2.2.4 Chlore et oxygène
Les usines de traitement de l'eau potable font rarement appel à l'oxydation chimique directe du Mn(II) avec du chlore et de l'oxygène, parce que la cinétique réactionnelle est lente et le temps de contact insuffisant, sauf dans des conditions de pH alcalin (pH > 8 à 9) (Kohl et Medlar, 2006; Brandhuber et coll., 2013). La dose stœchiométrique de chlore libre requise pour oxyder le Mn(II) en Mn(IV) est de 1,3 mg HOCl par mg Mn(II); toutefois, Knocke et coll. (1990a) ont indiqué que des doses quatre fois plus élevées que la dose stœchiométrique et un temps de contact minimal de trois heures avaient été nécessaires pour abaisser une concentration initiale de Mn(II) de 1,0 mg/L à 0,7 mg/L à un pH de 7,0 et une température de 25 °C. Lorsque le pH a été augmenté à 9,0, le Mn(II) a été oxydé et son taux réduit à moins de 0,05 mg/L en une heure. Des températures moins élevées (14 °C) et la présence de COD ont aussi réduit de façon importante le temps de réaction. Avec le chlore, il faut également tenir compte du fait que si l'eau sortant de l'usine de traitement contient un taux élevé de Mn(II) dissous, celui-ci peut être oxydé par les résidus de chlore libre présents dans le réseau de distribution, en raison des temps de contact prolongés, ce qui produit des MnOx(s). Ce phénomène pourrait donner lieu à des plaintes de consommateurs à l'égard de la couleur de l'eau (Kohl et Medlar, 2006; Brandhuber et coll., 2013). Comme il en a été mentionné précédemment, même si le chlore n'est pas efficace pour oxyder directement le Mn(II) dissous dans les conditions normales d'exploitation des usines de traitement, cet élément reste essentiel à l'efficacité de certains procédés d'adsorption ou d'oxydation abordés à la section 7.2.3 (Brandhuber et coll., 2013).
L'OD peut oxyder le Mn(II) dissous à la dose stœchiométrique requise de 0,29 O2(aq) par mg Mn(II). Toutefois, comme dans le cas du chlore, la cinétique de la réaction est lente, à moins que le pH ne soit d'au moins 9,0 à 9,5. Ces conditions alcalines sont absentes de la plupart des procédés de traitement de l'eau potable, sauf dans les usines de traitement qui utilisent un procédé d'adoucissement chaux-soude ou à la chaux.
7.2.3 Adsorption/oxydation
Le traitement du Mn(II) dissous par adsorption et oxydation est fondé sur la présence des MnOx(s) recouvrant le matériau filtrant, qui ont la capacité d'adsorber le Mn(II) dissous dans l'eau d'alimentation et de le retenir dans le lit filtrant. La surface de ces oxydes agit alors comme catalyseur pour l'oxydation du Mn(II) adsorbé par les oxydants (p. ex. chlore ou permanganate) ajoutés à l'eau, pour produire encore plus d'oxydes. Plusieurs types de matériaux filtrants peuvent adsorber le Mn(II) dissous. Citons notamment le sable vert de manganèse, la pyrolusite et les matériaux filtrants conventionnels recouverts d'un enrobage de MnOx(s) appliqué commercialement par le fournisseur du matériau filtrant. L'ajout continu ou intermittent d'oxydant à l'eau brute avant son contact avec le matériau filtrant est nécessaire au maintien des sites d'adsorption des MnOx(s) (Knocke et coll., 1990b; Tobiason et coll., 2008; Islam et coll., 2010). Le lieu où est effectuée cette procédure dans l'usine de traitement peut varier. Dans les usines de traitement des eaux de surface qui effectuent une chloration avant la filtration, cette étape fait souvent partie du procédé de filtration utilisé pour éliminer les particules. Si aucune chloration de préfiltration n'est effectuée, un contacteur d'adsorption peut être placé après la filtration (Knocke et coll., 2010). Dans les usines de traitement des eaux souterraines, le procédé d'adsorption/de filtration est souvent utilisé expressément pour l'élimination du manganèse ou du fer. L'un des principaux avantages de la présence d'un milieu de filtration enrobé de MnOx(s) dans la chaîne de traitement est qu'elle permet d'obtenir des concentrations de manganèse uniformément faibles (< 0,015 mg/L) dans l'eau traitée (Brandhuber et coll., 2013).
7.2.3.1 Sable vert de manganèse
Le sable vert de manganèse conventionnel est un matériau filtrant granulaire constitué de sable glauconieux. La glauconite est enrobée artificiellement d'une fine couche de matière à base de manganèse (ions manganeux), qui est ensuite transformée en une couche de MnOx(s) par le traitement du sable vert à l'aide d'une solution de permanganate de potassium ou de chlore (Knocke et coll., 1990b; Sommerfield, 1999). Ce matériau possède une grande capacité d'adsorption pour éliminer le Mn(II) dissous (1,5 kg/m3). Le matériau filtrant en sable vert est généralement plus petit (taille effective de 0,30 à 0,35 mm) que celui en sable siliceux, et il capte donc bien les petites particules. Puisque le sable vert entraîne une perte de charge générée supérieure à celle d'un lit filtrant de même profondeur en sable siliceux, il est le plus souvent utilisé avec la filtration sous pression (Brandhuber et coll., 2013). De plus, les filtres au sable vert conviennent davantage aux réseaux d'eaux souterraines où la concentration en fer et en manganèse est inférieure à 5 mg/L (Kohl et Medlar, 2006).
Deux méthodes normalisées peuvent être utilisées pour éliminer le manganèse par filtration sur sable vert : la régénération continue et la régénération intermittente. La régénération continue nécessite d'ajouter à l'eau brute un oxydant (permanganate de potassium ou chlore) ou une combinaison de deux oxydants avant que cette eau n'entre en contact avec le sable vert. Lorsque l'oxydant utilisé est le permanganate de potassium, la majorité du Mn(II) dissous dans l'eau prélevée à la source sera directement oxydée en MnOx(s) et le sable vert agira essentiellement comme un système d'élimination physique. Si toutefois du Mn(II) atteint le sable vert, il peut être éliminé par adsorption sur l'enrobage de MnOx(s). Dans ces cas, la capacité d'adsorption du sable vert diminue plus lentement, puisque le manganèse qui entre dans le filtre est déjà oxydé. Lorsque la perte de charge a atteint un niveau donné, on effectue un lavage à contre-courant pour retirer les particules de MnOx (Knocke et coll., 1990b). Un excès d'oxydant est nécessaire pour assurer la régénération des sites d'adsorption du MnOx(s). Les services publics doivent savoir que l'ajout continu de permanganate de potassium au sable vert crée un excédent de permanganate et peut donc entraîner une coloration de l'eau traitée (Brandhuber et coll., 2013). Du chlore, ou de faibles doses de permanganate de potassium combinées à du chlore, peuvent également être utilisés pour la régénération continue du milieu filtrant en sable vert. Le maintien d'une concentration de chlore libre allant de 0,5 à 1,0 mg/L dans l'ensemble du milieu filtrant permet la régénération de son enrobage de MnOx(s) en oxydant le Mn(II) adsorbé. Selon Brandhuber et coll. (2013), l'utilisation de chlore libre constitue une solution convenable pour la régénération du milieu filtrant au sable vert, en raison de son coût peu élevé en produits chimiques, de la quantité plus faible de solides qui se retrouve dans le filtre, et de l'absence de risque de coloration de l'eau attribuable à un excès de permanganate. Le chlore libre peut régénérer l'enrobage de MnOx(s) du milieu filtrant en oxydant le Mn(II) adsorbé. Lorsque la concentration de Mn(II) dans l'eau prélevée à la source dépasse 1 mg/L ou qu'il faut diminuer la formation de sous-produits de désinfection (SPD), le permanganate de potassium peut alors être l'oxydant de choix ou à privilégier, en utilisant des concentrations moins élevées de chlore libre.
Dans un procédé de régénération intermittente, le Mn(II) dissous est éliminé par le milieu filtrant en étant adsorbé sur l'enrobage de MnOx(s) du sable vert. À mesure que les sites d'adsorption se remplissent, le milieu filtrant commence à perdre sa capacité à éliminer le Mn(II) dissous. Le milieu filtrant doit alors être retiré de la chaîne afin qu'un oxydant puisse être appliqué pour oxyder le Mn(II) adsorbé et créer de nouveaux sites d'adsorption. Cette méthode exige une surveillance minutieuse du Mn(II) dans l'eau traitée, car le milieu filtrant au sable vert doit être retiré et régénéré avant qu'une quantité importante de Mn(II) dissous ne traverse le filtre et se retrouve dans l'eau traitée.
Kohl et Medlar (2006) ont présenté des données provenant de quatre usines de traitement des eaux souterraines ayant recours à la filtration sur sable vert de manganèse. Ces usines ont atteint un taux d'élimination du manganèse de 86 % à 100 %, en obtenant une concentration moyenne inférieure à 0,020 mg/L dans l'eau traitée alors qu'elle se situait entre 0,35 mg/L et 0,52 mg/L dans l'influent.
Outre les milieux filtrants granulaires faits avec de la glauconite, plusieurs fabricants produisent également des milieux filtrants en charbon anthraciteux et en sable siliceux recouverts d'une couche de MnOx(s) appliquée par traitement chimique. Ces milieux filtrants éliminent le Mn(II) par le même mécanisme que le sable vert. Losqu'il y a des quantités limitées de glauconite, ces autres milieux constituent une solution viable pour les usines de traitement de l'eau qui utilisent une technique de traitement fondée sur l'adsorption/l'oxydation.
7.2.3.2 Couches de MnOx(s) sur un milieu filtrant conventionnel
Une méthode d'élimination du Mn(II) importante, mais souvent oubliée, est l'adsorption de Mn(II) sur une couche de MnOx(s) qui se crée sur les milieux filtrants en charbon anthraciteux ou en sable siliceux dans une usine de traitement, en raison de la présence de Mn(II) dissous et de chlore libre dans le lit filtrant (Knocke et coll., 1988, 1990b). Dans ce procédé, le Mn(II) adsorbé est par la suite oxydé par la présence de chlore libre dans tout le filtre, ce qui permet de créer de nouveaux sites d'adsorption sur les MnOx(s) (régénération continue). En outre, seule une partie des MnOx(s) est éliminée lors du lavage à contre-courant, ce qui permet une augmentation nette du nombre de sites d'adsorption pendant la durée d'opération (Hargette et Knocke, 2001). Ce processus a été nomé effet naturel du sable vert par Knocke et coll. (1988) et effet du milieu filtrant artificiellement enrobé d'oxydes par Kohl et Medlar (2006). Dans beaucoup d'usines de traitement, ce processus s'amorce et se maintient de lui-même sans que les ingénieurs de procédé et les opérateurs ne s'en aperçoivent (Kohl et Melar, 2006; Brandhuber et coll., 2013).
Plusieurs recherches ont été menées pour mieux comprendre les facteurs qui contribuent à l'élimination efficace du Mn(II) dans les usines de traitement qui utilisent un milieu filtrant enrobé de MnOx(s). L'efficacité de la filtration par milieu filtrant enrobé de MnOx(s) dépend du nombre de sites d'adsorption et de l'état d'oxydation du milieu filtrant, du pH de l'eau, et de la concentration de chlore libre dans le filtre (Knocke et coll., 1988, 1990b, 1991; Hargette et Knocke, 2001; Tobiason et coll., 2008). Brandhuber et coll. (2013) ont résumé les principales conditions opérationnelles propices au bon fonctionnement de ce procédé. Ces conditions comprennent une concentration en chlore libre de 0,5 à 1,0 mg/L dans l'eau filtrée (pour assurer une régénération efficace du revêtement de MnOx(s)), ainsi que l'application au filtre d'un pH supérieur ou égal à 6,0, étant donné qu'un pH plus faible créerait une concurrence entre le Mn(II) et les ions H+ pour les sites d'adsorption. Enfin, le manganèse doit entrer dans le filtre sous forme de Mn(II) dissous, puisque les particules de Mn(IV) ne sont pas adsorbées sur le milieu filtrant. Brandhuber et coll. (2013) ont noté que dans ces conditions, les usines de production d'eau potable réussissent régulièrement à obtenir des concentrations en manganèse très faibles dans l'eau traitée (< 0,015 mg/L), même lorsque les concentrations de manganèse avant la filtration sont aussi élevées que 0,5 mg/L.
Tobiason et coll. (2008) ont réalisé des recherches sur des milieux filtrants en charbon anthraciteux et en sable siliceux enrobés de MnOx(s) provenant d'usines de traitement d'eau à grande échelle. Les résultats de leurs recherches indiquent que le niveau d'enrobage est plus élevé sur les milieux filtrants qui sont exposés en premier au chlore libre et au Mn(II) lorsque l'eau traverse le filtre (p. ex. la couche supérieure d'un filtre à deux couches), quel que soit le type de matériau (anthracite et sable). L'adsorption du Mn(II) se produit donc dans la partie supérieure d'un lit filtrant. Cette étude a également révélé que même si les résidus normaux de chlore libre utilisés dans une usine de traitement peuvent régénérer partiellement les sites d'adsorption de MnOx(s), la capacité d'élimination du manganèse diminue avec le temps. Il a été suggéré que les installations aient occasionnellement recours à la régénération intermittente hors ligne du milieu filtrant, en utilisant des solutions concentrées de chlore ou de permanganate de potassium pour améliorer la capacité d'adsorption du milieu.
Le potentiel de formation de SPD est l'un des principaux éléments à prendre en compte avec la filtration sur milieu filtrant enrobé de MnOx(s). Tobiason et coll. (2008) ont démontré que le contrôle du manganèse par chloration de préfiltration, réalisée de façon continue et avec un milieu filtrant enrobé de MnOx(s), peut faire augmenter de 10 à 50 % les concentrations de SPD (trihalométhanes et acides haloacétiques) dans le réseau de distribution, comparativement à une chloration après la filtration.
Beaucoup de gouvernements ont modifié les règlements relatifs aux SPD dans l'eau potable, ce qui a poussé les usines de traitement à déplacer le point d'application du chlore en aval des filtres. Avec ce changement, il n'y a pas de résidus de chlore libre dans le filtre, ce qui exclut ainsi la possibilité d'utiliser la filtration sur milieu enrobé de MnOx(s) pour éliminer le manganèse. Plusieurs auteurs ont démontré que le manganèse qui s'était accumulé sur un milieu filtrant enrobé de MnOx(s) se libère durant la transition vers la filtration biologique, ce qui entraîne des concentrations élevées de manganèse dans l'eau traitée (Gabelich et coll., 2006; Tobiason et coll., 2008; Kohl et Dixon, 2012). Les usines qui songent à déplacer le point d'application du chlore après la filtration devraient évaluer le potentiel de rejet de manganèse du milieu filtrant. La libération de manganèse provenant du milieu filtrant a été observée dans divers systèmes possédant différentes concentrations et sources de manganèse (et non seulement dans des systèmes où l'eau prélevée à la source contient une forte concentration de manganèse). Citons, par exemple, les systèmes dont l'eau prélevée à la source présente une concentration en manganèse faible mais constante, et les systèmes qui utilisent des coagulants (p. ex. chlorure de fer(III)) contenant des impuretés de manganèse. Kohl et Dixon (2012) ont réalisé des essais pilotes avec un système de filtration conventionnel de 23 L/min en utilisant un milieu filtrant provenant d'une usine de traitement à grande échelle et recouvert d'un enrobage uniforme et bien établi de MnOx(s). Lorsque les filtres ont été utilisés sans chlore, ils ont commencé à relarguer du manganèse, ce qui a provoqué une augmentation de la concentration de manganèse dans l'eau filtrée allant jusqu'à 0,03 mg/L, pendant une période allant jusqu'à 30 jours. De même, Gabelich et coll. (2006) ont fait état d'un milieu filtrant, dans une usine à grande échelle, qui a commencé à relarguer du manganèse dans les heures suivant l'élimination du chlore dans les filtres (p. ex. en cas de conversion à la filtration biologique). Il a été établi que le manganèse était attribuable aux impuretés présentes dans le coagulant en chlorure de fer(III) utilisé à l'usine et à la présence de chlore libre dans les filtres, qui ont causé une accumulation de MnOx(s) dans le milieu filtrant. L'installation en question a signalé une augmentation de 70 à 110 µg/L du manganèse total à la sortie de l'usine suite à l'élimination du chlore des filtres. Des essais plus approfondis ont révélé que la dissolution du manganèse provenant du milieu filtrant est un processus complexe au cours duquel se produisent des échanges entre trois formes chimiques de manganèse dans la partie supérieure (premier mètre) du milieu filtrant. Il semble également que le choix du coagulant et le pH de la solution aient une grande incidence sur la mobilité du manganèse dans le milieu filtrant.
Dans les cas où il faut limiter la quantité de chlore ajoutée avant la filtration pour prévenir la formation de SPD, l'utilisation de contacteurs sur milieu filtrant de MnOx(s) après la filtration peut constituer un traitement approprié du manganèse (Tobiason et coll., 2008; Knocke et coll., 2010; Bierlein et coll., 2015). Knocke et coll. (2010) ont démontré qu'un contacteur d'adsorption sur milieu enrobé de MnOx(s) constitue un moyen efficace d'éliminer le Mn(II) dissous pour toute une gamme de pH (6,3 à 8,0), de doses de chlore libre (> 1,0 mg/L), de concentrations initiales de Mn(II) (0,03 à 0,3 mg/L) et de taux de charge hydraulique (jusqu'à 24 gpm/pi2).
Comme il est mentionné plus haut, plusieurs études ont démontré l'efficacité de la filtration sur milieu filtrant enrobé de MnOx(s) dans les usines à grande échelle (Charlton et coll., 2002; Kohl et coll., 2002; Herzner et coll., 2003; Angara et coll., 2004; Kohl et Medlar, 2006; Tobiason et coll., 2007, 2008). Les résultats d'une enquête menée auprès de plusieurs usines utilisant la filtration sur milieu filtrant enrobé de MnOx(s) donnent une concentration moyenne de manganèse de 0,007 mg/L dans l'eau traitée, pour l'ensemble des usines. Le taux d'élimination dans ces usines allait de 98 à 99 % et chaque usine présentait une concentration moyenne de manganèse allant de 0,001 mg/L à 0,014 mg/L dans l'eau traitée (Kohl et Medlar, 2006). Selon Jeffcoat et coll. (2007), déplacer le point d'injection de chlore du mélangeur rapide à l'influent du filtre (où se crée le milieu filtrant enrobé de MnOx(s)) dans une usine conventionnelle à grande échelle est une méthode efficace pour éliminer le manganèse. Ce procédé a permis d'abaisser des concentrations de manganèse d'environ 0,05 mg/L dans l'influent à moins de 0,01 mg/L.
Tobiason et coll. (2008) et Brandhuber et coll. (2013) ont publié des données tirées d'études de cas portant sur des installations utilisant la filtration sur milieu filtrant enrobé de MnOx(s) pour éliminer le Mn(II) dissous. Tobiason et coll. (2008) ont démontré qu'une usine d'un débit de 25 mgd utilisant la coagulation à l'alun, la floculation, la décantation, la filtration sur milieu filtrant double et la désinfection au chlore libre avait pu diminuer la concentration de chlore avant la filtration sans nuire à l'élimination du Mn(II). La dose de chlore avant la filtration est passée de 2,8 à 1,6 mg/L, ce qui a entraîné une baisse de la concentration des résiduels de chlore après la filtration, qui est passée de 0,9 à 0,2 mg/L. Les concentrations de Mn(II) dans l'eau traitée sont demeurées inférieures à 0,020 mg/L pendant toute cette transition, malgré des concentrations dans l'eau brute allant de 0,1 à 0,7 mg/L.
7.2.3.3 Pyrolusite
Il est possible d'éliminer le manganèse d'une solution par adsorption sur une tour de filtration composée de pyrolusite granulaire, qui est la forme minérale du MnO2(s) (aucun enrobage nécessaire). Les filtres de pyrolusite utilisés pour le traitement de l'eau potable sont généralement constitués d'un mélange de sable et de pyrolusite. Le rapport sable/pyrolusite dépend de la concentration de manganèse dans l'eau prélevée à la source. Il arrive souvent que du chlore soit ajouté à l'eau en amont du filtre pour assurer la régénération continue du milieu filtrant en pyrolusite. Cependant, une régénération intermittente effectuée avec de l'eau de lavage à contre-courant chlorée peut également s'avérer efficace. L'un des avantages du milieu filtrant en pyrolusite est qu'il peut permettre d'obtenir des taux de filtration plus élevés qu'avec le sable vert, et de réduire ainsi la grosseur des filtres utilisés ainsi que les coûts de construction (Sommerfield, 1999, Casale et coll., 2002). Toutefois, comme les milieux en pyrolusite possèdent une très forte densité (> 4,0), ils nécessitent des taux de charge hydraulique plus élevés pour fluidiser le lit filtrant au cours des lavages à contre-courant.
Peu de données sont disponibles sur l'efficacité de la pyrolusite pour l'élimination du manganèse. Les données publiées par Kohl et Medlar (2006) indiquent que la pyrolusite a permis d'éliminer de 81 à 99 % du manganèse dans trois usines de traitement des eaux souterraines. Ces usines ont réussi à obtenir, dans l'eau traitée, des concentrations moyennes de manganèse allant de 0,001 mg/L à 0,024 mg/L.
Kenari et Barbeau (2014) ont présenté une utilisation différente de la pyrolusite pour l'élimination du Mn(II) dissous. Ils ont utilisé un réacteur à lit fluidisé comme moyen de contact entre l'eau et le milieu filtrant en pyrusite. Les résultats de leurs essais indiquent qu'après une minute ou moins de temps de contact, presque 100 % du Mn(II) dissous avait été éliminé (avec des concentrations initiales de manganèse allant jusqu'à 0,3 mg/L). Du chlore libre a été utilisé comme oxydant pour régénérer la surface du milieu filtrant en pyrolusite dans le lit fluidisé. Des charges hydrauliques de 24 à 63 m/h appliquées au lit filtrant ont permis d'éliminer le Mn(II) dissous de façon extrêmement efficace (pH entre 6,2 et 7,8).
7.2.4 Filtration biologique
L'élimination du manganèse par filtration biologique repose sur la capacité des bactéries oxydant le manganèse (BOM), naturellement présentes dans les films biologiques recouvrant les milieux filtrants, à adsorber et à oxyder le Mn(II) dissous et à former du Mn(IV) particulaire, qui peut être ensuite éliminé par lavage à contre-courant. La documentation scientifique a recensé de nombreuses souches de bactéries ayant la capacité d'oxyder le Mn(II), comme Leptothrix, Sphaerotilus, Crenothrix et Metallogenium (Mouchet, 1992). Les recherches ont révélé que pour éliminer le Mn(II), les BOM font appel à divers mécanismes, comme l'oxydation intercellulaire par action enzymatique, l'adsorption à la surface de la membrane cellulaire et l'oxydation extracellulaire par l'action catalytique des polymères excrétés. L'adsorption sur les particules de MnOx(s) qui s'accumulent dans le filtre pendant le processus d'oxydation contribue également de façon importante à l'élimination du Mn(II) dans les procédés de biofiltration (Casale et coll., 2002; Burger et coll., 2008a; Sahabi et coll., 2009; Kohl et Dixon, 2012; Brandhuber et coll., 2013; Bruins et coll., 2015).
Plusieurs facteurs biologiques et physico-chimiques influent sur l'efficacité des filtres biologiques pour l'élimination du manganèse. Les facteurs biologiques sont notamment la présence et la diversité des BOM dans l'eau prélevée à la source, la capacité des BOM à former un biofilm actif dans les conditions d'utilisation du filtre, la période d'acclimatation de la population de BOM, et le maintien de l'activité biologique après un lavage à contre-courant ou d'autres contraintes exercées sur le filtre. La période d'acclimatation des BOM varie de 14 à 100 jours, les périodes les plus courtes étant observées après l'ensemencement des filtres et lorsque la température se situe entre 20 et 30 °C (Mouchet et coll., 1992; Holst, 2004).
Les facteurs physico-chimiques importants sont le pH, le potentiel redox, la concentration initiale de Mn(II) et le taux de charge du filtre (Kohl et Dixon, 2012). Les conditions opérationnelles requises pour établir une population adéquate de BOM dans les filtres consistent notamment à maintenir des conditions aérobies avec une concentration minimale en oxygène dissous (OD) de 5 mg/L, un potentiel redox de 300 à 400 mV, et un pH égal ou supérieur à 6,3 (Mouchet coll., 1992; Burger et coll., 2008a; Hoyland et coll., 2014). La présence d'ammoniac, de nitrite et de sulfure dans l'eau prélevée à la source nuit à la capacité des BOM à oxyder le manganèse. On a également constaté que l'élimination du manganèse par biofiltration convenait généralement mieux aux eaux souterraines, car la concentration en manganèse, la température et le pH de ces eaux sont relativement stables. À l'inverse, dans les eaux de surface, la concentration de manganèse et la température varient beaucoup et il n'est pas certain que les BOM puissent longtemps survivre dans un biofiltre dans de telles conditions (Brandhuber et coll., 2013).
La documentation scientifique fait état de nombreuses usines de traitement par biofiltration qui ont réussi à éliminer le manganèse dans les eaux souterraines (Mouchet et coll., 1992; Li et coll., 2005; Burger et coll., 2008b; Kohl et Dixon, 2012). Kohl et Dixon (2012) ont publié des données provenant de huit usines de traitement du Canada, de l'Europe et de la Chine qui utilisent des biofiltres à sable monocouches à courant descendant. Ces usines de traitement étaient capables d'éliminer plus de 93 % du manganèse et d'atteindre des concentrations de manganèse inférieures à la limite de détection de la méthode, établie à 0,03 mg/L. Plusieurs de ces usines sont situées au Nouveau-Brunswick et figurent dans les travaux de Burger et coll. (2008b). Dans la chaîne de traitement de ces usines, l'eau est pompée d'un aquifère vers un filtre à courant descendant ayant une capacité nominale de 1 325 L/min, une unité de filtration de 2,1 m de diamètre, un lit filtrant de 1,8 m de profondeur et une surface de 3,4 m2. De l'air comprimé est pompé dans les filtres pour assurer un Eh élevé. Les filtres sont soumis à un lavage à contre-courant d'une vitesse de 20 m/h après chaque tranche d'environ 300 heures d'exploitation. Après le lavage à contre-courant, les usines laissent maturer les filtres pendant cinq minutes avant de les remettre en service. Ces usines ont réussi à éliminer plus de 99 % du manganèse, passant d'une concentration de manganèse dans l'influent allant de 0,86 à 1,39 mg/L à une concentration inférieure à 0,03 mg/L dans l'eau traitée. L'eau prélevée à la source présentait un pH variant de 6,46 à 7,63 et une température comprise entre 9 et 10 °C.
La majorité des usines de filtration biologique du manganèse ont été mises en place pour traiter les eaux souterraines. Des recherches ont été menées afin d'examiner la possibilité d'utiliser la biofiltration pour éliminer le manganèse dans les eaux de surface (Kohl et Dixon, 2012; Granger et coll., 2014; Hoyland et coll., 2014). Hoyland et coll. (2014) ont mené des études à l'échelle de banc d'essai visant à évaluer s'il était possible d'éliminer à la fois les MON et le Mn(II) par biofiltration dans des conditions représentatives des usines de traitement de l'eau de surface utilisant la coagulation et l'ozonation avant la filtration. L'étude a révélé que les BOM pouvaient éliminer plus de 98 % du Mn(II) dans un biofiltre avec un pH aussi faible que 6,3. Des essais marginaux ont de plus révélé que des BOM bien acclimatées (50 jours) pouvaient éliminer efficacement le Mn(II) dans diverses conditions de concentrations de manganèse dans l'influent (0,1 à 0,2 mg/L), de charge hydraulique (1,3 × 10-3 à 2,72 × 10-3 m/s) et de températures (7 à 22 °C) pendant une période de 1 à 2 jours. Kohl et Dixon (2012) ont publié des données sur l'élimination du manganèse dans une usine de traitement des eaux de surface d'un débit de 454 ML/jour qui utilisait l'ozonation intermédiaire ainsi que 14 filtres à double couche composés de 180 cm de charbon actif en grains (CAG) sur 25 cm de sable. L'ozone était appliqué après la sédimentation et avant la filtration, à une dose de 1,5 à 2,0 mg/L, et le pH à l'entrée des filtres était de 7,2 à 7,6. La concentration de manganèse total dans l'influent variait de 0,032 à 0,089 mg/L. Dans l'eau traitée, la concentration de manganèse était inférieure à 0,002 mg/L (LDM) dans tous les échantillons, ce qui signifie que plus de 94 % du manganèse a pu être éliminé. En revanche, un taux d'élimination beaucoup moins élevé a été constaté dans une usine de traitement de 190 ML/jour utilisant l'ozonation intermédiaire et des filtres à CAG de 6 pieds (1,83 m) de profondeur. La concentration de manganèse total dans l'influent variait cette fois de 0,018 à 0,071 mg/L. Les filtres ont éliminé en moyenne 40 % du manganèse total, mais de grandes variations (21 à 76 %) ont été observées pour différentes dates d'échantillonnage. Les auteurs n'ont pas cherché à déterminer l'origine de cette différence de rendement entre les deux usines de traitement.
Tel que mentionné à la section 7.2.3.2, il est important que les services publics qui envisagent de passer de la filtration sur milieu enrobé de MnOx(s) à la filtration biologique tiennent compte du manganèse accumulé sur le milieu filtrant, qui pourrait être libéré dans l'eau une fois le chlore libre résiduel épuisé (Gabelich et coll., 2006; Kohl et Dixon, 2012). On recommande aux installations qui ont l'intention de convertir un filtre existant contenant un milieu filtrant enrobé de MnOx(s) de retirer ce dernier et de le nettoyer ou de le remplacer avant d'entreprendre la filtration biologique (Kohl et Dixon, 2012).
7.2.5 Adoucissement et échange d'ions
Les usines de traitement qui utilisent l'adoucissement à la chaux ou à la soude peuvent également éliminer le manganèse en augmentant le pH de l'eau (p. ex. > 9,5 à 10) au-dessus de la valeur de solubilité de diverses phases solides d'hydroxyde et de carbonate de manganèse. De même, le pH élevé associé à l'adoucissement à la chaux ou à la chaux-soude augmentera considérablement la vitesse d'oxydation du Mn(II) dissous en présence d'OD. La présence d'OD entraînera la formation de solides de MnOx(s). L'augmentation du pH de l'eau prélevée à la source ne constitue pas en elle-même un moyen rentable d'éliminer le Mn(II) dissous. Il s'agit plutôt d'une méthode que l'on utilise habituellement quand l'eau prélevée à la source doit être adoucie. Dans beaucoup d'installations faisant appel à l'adoucissement à la chaux ou à la soude, le taux élevé d'élimination du manganèse (ou du fer) obtenu découle des réactions chimiques liées à l'adoucissement. De plus, bien souvent, le personnel de l'usine n'utilise pas le système de traitement dans le but d'éliminer le manganèse. Dans les usines qui adoucissent l'eau, il peut arriver que le manganèse soit éliminé à l'insu de l'opérateur du système de traitement, en particulier lorsque le taux de manganèse dans l'eau prélevée à la source et dans l'eau traitée ne fait pas l'objet d'une surveillance régulière. Une usine d'adoucissement à la chaux à grande échelle a déclaré avoir obtenu une concentration moyenne de manganèse de 0,001 mg/L dans l'eau traitée à partir d'une concentration moyenne dans l'eau prélevée à la source de 0,520 mg/L (Kohl et Medlar, 2006).
Le Mn(II) dissous peut également être éliminé par échange de cations dans les procédés d'adoucissement à la zéolite. Comme c'est le cas pour d'autres procédés reposant sur l'échange cationique, le lavage à contre-courant de la zéolite, généralement effectué à l'aide d'une solution hypersaline, permet d'éliminer le manganèse (tout comme le fer, le calcium et le magnésium) accumulé sur la résine. L'adoucissement à la zéolite comme moyen d'élimination du Mn(II) dissous pose toutefois le problème de la présence d'oxygène ou d'autres oxydants. De telles conditions peuvent entraîner l'oxydation des ions Mn(II) échangés en MnOx(s) à la surface de la zéolite, ce qui fera diminuer le pouvoir global d'échange cationique de la résine de zéolite avec le temps (Sommerfield, 1999).
7.2.6 Séquestration
La séquestration est une mesure de contrôle qui vise à limiter les problèmes de qualité de l'eau d'ordre esthétique associés à l'oxydation du Mn(II) dissous, qui entraîne la formation de particules de MnOx(s) dans le réseau de distribution. Dans le cas du manganèse, la séquestration est généralement considérée comme une mesure de contrôle temporaire, étant donné que l'effet de l'agent séquestrant est d'une durée limitée (Kohl et Medlar, 2006). Puisque la séquestration n'élimine pas le manganèse de l'eau, elle ne réduit pas l'exposition au manganèse liée à l'eau potable. C'est pourquoi cette solution ne devrait être envisagée, comme mesure de contrôle visant à réduire le risque de coloration de l'eau, que pour les systèmes d'approvisionnement dont l'eau prélevée à la source ou l'eau traitée contient une concentration de manganèse inférieure à la CMA. Il convient toutefois de noter qu'une dose constante doit être maintenue à long terme. Dans la plupart des cas, la méthode la plus appropriée pour réduire les concentrations de Mn(II) dissous au robinet consiste à installer ou à optimiser un système de traitement du manganèse qui permettra de maintenir la concentration bien en deçà de la CMA et de l'OE, de façon à limiter la quantité de manganèse qui s'accumule dans le réseau de distribution. L'utilisation d'un agent séquestrant peut constituer la solution la plus pratique pour éviter la coloration de l'eau dans les très petits systèmes alimentés en eau souterraine qui présentent de faibles concentrations en Mn(II) dissous dans l'eau prélevée à la source et dont les ressources sont limitées (AWWA, 1993). Une attention particulière devra toutefois être portée au risque d'accumulation et de libération subséquente de manganèse dans le réseau de distribution.
Une séquestration chimique utilise un agent chimique qui se liera au manganèse dissous afin de créer un complexe en solution dans lequel le manganèse ne peut être oxydé ou précipité. L'ajout de polyphosphates seuls ou en conjonction avec du chlore est la méthode la plus couramment utilisée pour la séquestration du manganèse (Sommerfield, 1999; Kohl et Medlar, 2006). La dose adéquate d'agent chimique séquestrant à utiliser dépend des caractéristiques de la qualité de l'eau et des recommandations du fabricant. Il est souvent difficile de déterminer la combinaison chimique à appliquer en raison des fluctuations de la qualité de l'eau (c.-à-d. variation des concentrations de manganèse et d'autres cations) et des conditions dans le réseau de distribution (c.-à-d. variation du temps de rétention et de la température) (Kohl et Medlar, 2006). De plus, les polyphosphates s'hydrolysent avec le temps et peuvent entraîner la libération de Mn(II) dissous séquestré antérieurement. La vitesse d'hydrolyse augmente à pH faible ou élevé, et avec la température de l'eau (Brandhuber et coll., 2013). Si la séquestration est utilisée comme stratégie de gestion, des échantillons doivent être prélevés périodiquement dans l'eau traitée et dans le réseau de distribution pour mesurer la concentration de manganèse total et s'assurer qu'elle demeure sous la CMA. Même si la séquestration peut aider à gérer le problème de particules ou de coloration, elle n'exclut pas la possibilité que le manganèse s'accumule dans le réseau de distribution.
7.2.7 Autres facteurs à prendre en compte
Le taux de manganèse présent dans l'eau prélevée à la source, l'ajout de produits chimiques et les procédés utilisés par l'usine de traitement peuvent influer sur la quantité de manganèse qu'une usine de traitement doit gérer. Les trois principales sources de manganèse résultant des opérations d'une usine de traitement sont : 1) la présence d'impuretés de manganèse dans les coagulants (principalement des coagulants ferriques) utilisés pour la déstabilisation des particules; 2) la resolubilisation du Mn(II) par la réduction de solides de MnOx(s) stockés dans les bassins de sédimentation, en raison des conditions anoxiques de ces bassins; 3) la présence de manganèse dissous dans les flux de recyclage qui découle des opérations de traitement des solides (Tobiason et coll., 2008). Kohl et Medlar (2006) ont résumé les études publiées sur les risques de contamination de l'eau potable par les sels ferriques susceptibles de contenir du manganèse. Dans le cas des coagulants certifiés conformes à la norme 60 de la NSF/ANSI, la concentration maximale de manganèse à laquelle un produit seul peut contribuer (c.-à-d. la concentration permissible par produit individuel ou CPPI) est de 0,03 mg/L (NSF/ANSI, 2015a). Toutefois, selon le dosage et les conditions opérationnelles d'une usine de traitement, cela peut donner lieu à des concentrations élevées de manganèse dans l'usine de traitement. Certaines études ont révélé que dans les usines qui utilisent la coagulation améliorée, la contamination au manganèse du chlorure de fer(III) peut faire augmenter la concentration de manganèse soluble jusqu'à 0,5 mg/L. Les taux de manganèse attribuables à l'ajout d'un coagulant dans l'eau de surface varient généralement entre 0,025 et 0,055 mg/L. Les rejets provenant des solides présents dans les bassins de sédimentation contiennent habituellement des concentrations de manganèse allant de 0,01 à 0,10 mg/L, avec quelques variations saisonnières, et le taux de manganèse provenant des flux de recyclage se situe entre 0,01 et 1 mg/L (Tobiason et coll., 2008). Par conséquent, bien que le débit total des flux secondaires découlant du traitement des résidus puisse être relativement faible en comparaison à celui de l'eau qui entre dans l'usine de traitement, la charge totale de Mn(II) dissous provenant de ces flux secondaires peut être considérable. Il est fortement recommandé d'effectuer un échantillonnage rigoureux des flux secondaires provenant des installations de traitement des résidus pour y mesurer la concentration en Mn(II) dissous. Le traitement de ces flux secondaires pour en éliminer le Mn(II) dissous devrait également être envisagé. Brandhuber et coll. (2013) ont fait état d'un cas où une usine a fabriqué un milieu filtre à grande échelle enrobé de MnOx(s) pour traiter les flux secondaires provenant des installations de traitement des résidus avant qu'ils n'atteignent le réservoir terminal de l'usine (c.-à-d. la source d'eau d'alimentation de l'installation). La concentration de Mn(II) dissous dans l'eau non traitée des flux secondaires variait de 0,02 mg/L à plus de 1 mg/L. En faisant passer ces flux secondaires à travers le lit filtrant enrobé de MnOx(s), l'usine a réussi à éliminer plus de 90 % du Mn(II) dissous. Avec le temps, cette usine a pu démontrer que le fait de traiter les flux secondaires provenant du traitement des résidus avant qu'ils n'atteignent le réservoir terminal permettait de diminuer considérablement la concentration de Mn(II) dissous dans l'influent de l'usine de traitement. Cette approche a permis de faciliter la gestion des problèmes de manganèse sur le plan opérationnel, et de faire des économies en réduisant la quantité d'oxydants chimiques (p. ex. le permanganate) nécessaire pour traiter l'eau prélevée à la source.
7.3 Réseau de distribution
Le réseau de distribution est un système dynamique sur le plan hydraulique, physique, chimique et biologique, ce qui entraîne des répercussions importantes pour l'atteinte de l'OE ainsi que de la CMA au robinet des consommateurs. Des concentrations de manganèse supérieures à 0,02 mg/L peuvent donner lieu à des plaintes relatives à la coloration de l'eau et à l'apparition de taches sur la plomberie et la lessive, et entraîner l'insatisfaction des consommateurs envers la qualité de l'eau (Sommerfield, 1999; Casale et coll., 2002; Kohl et Medlar, 2006; Tobiason et coll., 2008). Un examen approfondi de la documentation scientifique, effectué par Kohl et Medlar (2006), a révélé que des dépôts de manganèse peuvent se créer dans les réseaux de distribution même lorsque la concentration de manganèse dans l'eau qui sort de l'usine de traitement est aussi faible que 0,02 mg/L. Par conséquent, un objectif de traitement ≤ 0,015 mg/L est recommandé pour le manganèse dans l'eau traitée (Brandhuber et coll., 2013). Dans le cadre d'une étude communautaire, Barbeau et coll. (2011) ont remarqué que la concentration de manganèse entrant dans le réseau de distribution était habituellement plus élevée que celle mesurée aux domiciles des consommateurs, et que l'entrée du réseau de distribution serait un endroit raisonnablement prudent pour estimer l'exposition au manganèse. Cependant, dans certains cas, les problèmes de manganèse dans l'eau du robinet ne sont pas associés à des concentrations élevées de manganèse dans l'eau brute, et ne peuvent donc pas être estimés en évaluant les niveaux de manganèse à l'entrée du réseau de distribution. Ces expositions au manganèse résultent plutôt de la libération de manganèse accumulé dans le réseau de distribution en raison de la présence constante de manganèse, même en faible concentration, dans l'eau prélevée à la source ou dans l'eau traitée. De temps à autre, une instabilité chimique de l'eau ou des perturbations physiques ou hydrauliques peuvent libérer des dépôts de manganèse dans le réseau de distribution, et entraîner une exposition au manganèse ainsi que des plaintes sur la coloration de l'eau.
En plus de ces préoccupations d'ordres esthétique et sanitaire liées à l'exposition au manganèse, le manganèse peut agir comme capteur et comme puits pour les métaux indésirables comme le baryum, le plomb, le nickel, le vanadium, l'arsenic, le radium, le chrome et l'uranium (Friedman et coll., 2010) et inhiber la formation d'incrustations stables de Pb(IV) dans les tuyaux en plomb (Schock et coll., 2014). Il entraîne donc d'autres risques pour la santé, puisque d'autres contaminants inorganiques concomitants peuvent ainsi être libérés dans le réseau (Schock et Holm, 2003; Schock, 2005). Dans de nombreux cas, la stratégie la plus efficace consiste à réduire au maximum la concentration de manganèse dans l'eau avant distribution. Les services publics doivent veiller à ce que les mesures de contrôle et de traitement du manganèse mises en œuvre tiennent compte des dépôts et des éventuels rejets de manganèse dans le réseau de distribution. Les pratiques de gestion des réseaux de distribution et toute modification concernant la source d'approvisionnement en eau ou les procédés de traitement auront une incidence sur d'autres objectifs en matière de traitement des eaux. Schock et coll. (2014) ont constaté que la présence de dépôts de manganèse permettait l'accumulation de plomb et empêchait la formation des incrustations de corrosion plus stables de Pb(IV), ce qui augmente ainsi le risque de libération de plomb en raison d'incrustations plus facilement solubles. Les auteurs ont conclus que le contrôle de l'accumulation de manganèse permettrait de mieux contrôler la libération de plomb dans les résidences. Dans un autre exemple, la salubrité de l'eau a été compromise par des pratiques de traitement inadéquates mises en place pour tenter de répondre aux préoccupations des consommateurs concernant le goût et les taches. À la suite de l'éclosion d'un foyer épidémique de Cryptosporidium survenue en 2001 à North Battleford, Saskatchewan, les analyses ont montré qu'on avait conservé la concentration de chlore résiduel délibérément basse (en dessous du 0,5 mg/L requis) pour tenter de minimiser le nombre de plaintes des consommateurs concernant le goût (chlore) et la lessive tachée (à cause du manganèse oxydé) (Hrudey et Hrudey, 2014).
Les services publics cherchent à gérer le manganèse et d'autres objectifs de traitement par des changements à la source d'eau, aux procédés de traitement, à la qualité de l'eau et aux pratiques de gestion des réseaux de distribution; toutefois, des tests effectués en laboratoire, à l'échelle pilote et sur le terrain (en particulier pour l'élaboration d'une stratégie d'entretien des conduites principales) sont nécessaires pour pouvoir déterminer certaines conséquences inattendues de ces changements apportés au réseau.
7.3.1 Accumulation et rejet de manganèse dans les réseaux de distribution
Les dépôts de manganèse peuvent découler d'un processus physique résultant de la sédimentation de particules (U.S. EPA, 2006), d'une sorption physico-chimique (Friedman et coll., 2010) ou d'une accumulation biologique (Sly et coll., 1990; Cerrato et coll., 2010; Ginige et coll., 2011). Le manganèse s'accumule dans les dépôts meubles de matériaux qui composent les tuyaux des réseaux de distribution, comme le fer (Zacheus et coll., 2001; Cerrato et coll., 2006; Peng et Korshin, 2011), le polyéthylène (Zacheus et coll., 2001), le polychlorure de vinyle (Cerrato et coll., 2006) et le plomb (Schock et coll., 2014). Cerrato et coll. (2006) ont découvert que le manganèse s'accumulait moins dans les incrustations de surface des tuyaux en fer (3,48 % en poids) que dans les tuyaux en polychlorure de vinyle (PVC) (6.12 % en poids). Ils ont aussi découvert que dans les tuyaux en fer, le manganèse était associé à des dépôts sous forme de pustules, alors que dans les tuyaux en PVC, il s'agissait de dépôts de surface facilement éliminés/libérés. La concentration en manganèse de l'eau, dans les réseaux de distribution, diminue à mesure que l'eau s'éloigne de l'usine de traitement (Kohl et Medlar, 2006). Par ailleurs, Barbeau et coll. (2011) ont constaté que la concentration de manganèse dans l'eau était inversement proportionnelle à son âge, une diminution de 37 % du taux de manganèse ayant été observée après un temps de rétention de l'eau de 24 heures. Notamment, Brandhuber et coll. (2015) ont estimé la quantité de manganèse emmagasinée dans les conduites d'un système de distribution, d'après les données de Friedman et coll. (2010). Les dépôts de manganèse variaient de 0,1 mg/pi2 à 10 000 mg/pi2, avec une médiane estimée à 210 mg/pi2, ce qui équivaut à environ 3,8 lb Mn/mille (pour un tuyau de 6 pouces de diamètre) ou à 7,7 lb Mn/mille (pour un tuyau de 12 pouces de diamètre). Brandhuber et coll. (2015) ont également noté que la libération de seulement 1,5 % des dépôts de manganèse suffirait pour que le niveau de manganèse dépasse les valeurs des avis pour la santé de l'U.S. EPA, soit 1 mg Mn/L pour un jour et dix jours. Peng et Korshin (2011) ont découvert que le manganèse était fortement lié aux fractions organiques et mobiles des incrustations de corrosion, et que la majorité du manganèse se trouvait sous forme dissoute. Les auteurs ont également découvert que 9 % du manganèse faisait partie de la fraction échangeable, laquelle est susceptible d'être remplacée par des ions concurrents, ce qui rend les dépôts de manganèse vulnérables aux fluctuations de la qualité de l'eau.
Il existe très peu d'études portant sur l'accumulation du manganèse dans la plomberie des bâtiments; toutefois, les travaux de Barbeau et coll. (2001) semblent indiquer que le manganèse peut s'y accumuler et être libéré par la suite. Selon les auteurs, les concentrations de manganèse étaient stables tout au long de la journée dans cinq des six échantillons de ménages. De façon générale, le rinçage par écoulement de l'eau pendant cinq minutes n'a pas changé les concentrations de manganèse, même si, dans certains cas, cela s'est traduit par une légère hausse du taux de manganèse total (11 % maximum) ou dissous (16 % maximum). Des pics de libération du manganèse total ont également été observés dans le tout premier échantillon d'eau du robinet (premier jet) ainsi que dans un échantillon recueilli après cinq minutes d'écoulement. Par contre, dans un site d'échantillonnage de ménage, la concentration de manganèse avait diminué au cours de la journée, et le rinçage par écoulement durant cinq minutes a permis de diminuer le taux de manganèse particulaire dans l'eau comparativement au taux relevé dans l'échantillon d'eau prélevé au premier jet. Les concentrations de manganèse dissous sur ce site étaient plus faibles dans l'échantillon d'eau prélevé au premier jet que dans celui prélevé après cinq minutes d'écoulement; selon les auteurs, cela pourrait être lié à une diminution de l'âge de l'eau. Ces données limitées sur les ménages semblent indiquer que la plomberie des bâtiments constituerait également un important site d'échantillonnage pour mieux comprendre l'exposition au manganèse. Il est nécessaire d'effectuer d'autres recherches et de recueillir plus de données d'échantillonnage sur le terrain concernant les conditions d'accumulation et de libération du manganèse dans la plomberie des bâtiments pour pouvoir élaborer des stratégies d'intervention et d'atténuation propres à cet environnement.
Les perturbations physiques qui touchent le réseau de distribution peuvent également provoquer la libération d'incrustations contenant du manganèse. Par exemple, Del Toral et coll. (2003) ont fait état d'un lien entre la libération accrue de plomb et divers événements perturbateurs, tels que l'installation ou le remplacement d'un compteur, l'installation d'un compteur automatisé, la réparation d'une fuite, la réparation ou le remplacement du robinet d'arrêt de la conduite externe, ou d'importants travaux d'excavation dans la rue. Lakin et Bryan (2007) ont signalé un cas de coloration par le manganèse qui avait engendré plus de 11 000 plaintes de consommateurs dans les trois premiers jours. La libération de manganèse était liée à l'utilisation d'un rouleau vibrant de 10 tonnes utilisé pour des travaux routiers.
Le manganèse peut également s'accumuler dans les biofilms du réseau de distribution (Ginige et coll., 2011; Cerrato et coll., 2010; Sly et coll., 1990). Il existe des bactéries qui oxydent (Cerrato et coll., 2010; Sly et coll., 1990) et qui réduisent (Cerrato et coll., 2010) le manganèse. Il a été démontré que le manganèse emprisonné et accumulé dans les biofilms de l'eau potable pouvait être libéré lors de l'inactivation de ces biofilms (Ginige et coll., 2011). Dans le cadre d'études à l'échelle du banc d'essai réalisées par Ginige et coll. (2011), des réacteurs à biofilm exposés à des influents contenant une concentration faible (0,02 mg/L) ou élevée (0,04 mg/L) de manganèse ont été soumis pendant 14 jours à un traitement de désactivation du biofilm à l'aide de 3 mg/L de chlore. Dans les deux réacteurs (concentration faible et élevée de manganèse), la concentration d'ATP dans le biofilm a diminué d'un facteur de 10 environ en 2 jours. Pendant l'inactivation, la turbidité et le taux de manganèse ont tous les deux augmenté dans les deux réacteurs. Dans le réacteur exposé à l'influent contenant une faible concentration de manganèse, la libération de manganèse a atteint son apogée (0,07 mg/L) au jour 4, puis a diminué pour atteindre le niveau de référence de 0,01 mg/L au jour 8. Dans le réacteur exposé à une concentration élevée de manganèse (0,06 mg/L à l'origine), la libération de manganèse a culminé (0,08 mg/L) au jour 4, et le taux de manganèse dans l'effluent a diminué graduellement pour tomber à 0,03 mg/L au jour 12. Les auteurs avancent que les substances exopolymériques et la couche d'oxyde/hydroxyde métallique pourraient jouer un rôle dans le rythme auquel le manganèse se détache des biofilms. Les travaux de Friedman et coll. (2016) ont démontré que le manganèse était capable de s'accumuler dans les biofilms dans diverses conditions de qualité de l'eau (chlore à 0 ou à 2 mg/L, COD à 0 ou à 2 mg/L, température de 7 ou de 15 °C). L'ajout de chlore (2 mg/L) a diminué le taux de manganèse dans l'effluent, mais a accru l'accumulation de manganèse dans les biofilms. D'autres détails de l'étude de Friedman et coll. (2016) fournis par Kent (2016) ont montré que le manganèse s'accumulait dans les biofilms à une densité moyenne de 1 962 µg/g ± 431 µg/g. Contrairement aux résultats décrits par Ginige et coll. (2011), Friedman et coll. (2016) et Kent (2016) ont constaté que les matières accumulées étaient résistantes aux déversements de produits chimiques, bien que les auteurs aient mis en lumière la possibilité de perturbations hydrauliques en cas d'événements de rejet. La documentation scientifique existante donne à penser que le biofilm peut agir comme un réservoir important et complexe aussi bien pour le manganèse que pour les composés inorganiques à l'état de traces. Les services publics devraient tenir compte du rôle du biofilm au moment d'élaborer des stratégies de gestion du manganèse et d'entretien des réseaux de distribution.
Les événements de rejet du manganèse sont généralement des changements de couleur de l'eau, qui cessent lorsque l'eau qui s'écoule devient claire. Toutefois, des données probantes ont montré que des concentrations élevées de manganèse peuvent subsister plusieurs jours au robinet des consommateurs après un événement de coloration de l'eau. Les résultats ont montré que la majorité du manganèse détecté durant et après un changement de couleur de l'eau se trouvait sous forme dissoute (c.-à-d. non visible) (Brandhuber et coll., 2015).
Étant donné que les concentrations de manganèse peuvent varier tout le long du réseau de distribution, il est recommandé qu'un programme d'échantillonnage inclut des sites à divers emplacements le long du réseau de distribution pour permettre la caractérisation des concentrations types de manganèse de même que des concentrations de manganèse après traitement. L'échantillonnage du réseau de distribution ne doit pas être vu comme une sentinelle efficace contre les événements de rejet. Il est difficile de détecter les événements de rejet (particulièrement ceux qui n'entraînent pas un changement de couleur), même en présence d'un grand nombre d'échantillons (Friedman et coll., 2016).
7.3.2 Répercussions de l'accumulation de manganèse sur les autres sources de préoccupation dans les réseaux de distribution
La présence de manganèse dans les réseaux de distribution a également des répercussions sur d'autres métaux préoccupants. L'accumulation de manganèse dans les tuyaux de plomb peut entraver la formation d'incrustations de Pb(IV) plus stables, ce qui accroît le risque de libération de plomb en raison d'incrustations plus facilement solubles (Schock et coll., 2014). Les MnOx(s) se sont révélés efficaces pour capter toute une variété de métaux lourds, y compris le plomb (Dong et coll., 2003) et l'arsenic (Ouvrard et coll., 2002). Friedman et coll. (2010) ont montré que les dépôts de MnOx(s) dans les matériaux de la tuyauterie du réseau de distribution étaient associés à la présence d'éléments comme le baryum, le plomb, le nickel, le vanadium, l'arsenic, le radium, le chrome et l'uranium. Les dépôts de manganèse constituent des puits potentiels pour l'accumulation et la libération subséquente de ces métaux. Schock et coll. (2014) ont découvert que dans les réseaux de distribution où le manganèse était contrôlé au moyen d'un programme de rinçage unidirectionnel, les taux de plomb étaient eux aussi inférieurs, la quantité de plomb accumulée étant moins importante en l'absence de manganèse.
De plus, un lien a pu être établi entre la présence de particules dans le réseau de distribution et une teneur accrue en matières organiques (Vreeburg, 2010). Les résultats d'une étude dans laquelle un traitement supplémentaire avait permis d'éliminer la totalité des particules (> 0,1 µm) entrant dans le réseau de distribution ont montré que la teneur en matières organiques était six fois moins élevée dans ce réseau que dans les réseaux de distribution conventionnels contenant des particules. Selon Vreeburg (2010), il se pourrait que les particules augmentent la surface disponible pour la régénération biologique.
7.3.3 Gestion du manganèse dans les réseaux de distribution
Dans un article de synthèse portant sur la coloration de l'eau dans les réseaux de distribution, Vreeburg et Boxall (2007) mentionnent deux méthodes pour gérer les risques de coloration : 1) adopter un seuil de nettoyage pour éviter l'accumulation de matière; 2) limiter ou empêcher la pénétration ou la génération de particules dans le réseau de distribution. De même, Brandhuber et coll. (2015) ont recommandé une méthode de gestion qui réduit au minimum la quantité de manganèse entrant dans le réseau de distribution, qui réduit au minimum la quantité de manganèse emmagasinée dans le réseau de distribution par des pratiques exemplaires de nettoyage des conduites principales, qui réduit au minimum les perturbations physiques et hydrauliques, et qui stabilise les propriétés chimiques de l'eau.
Des réseaux à grande vitesse d'écoulement peuvent être utilisés comme méthode d'autonettoyage afin de minimiser l'accumulation de sédiments (Vreeburg, 2010). Les particules qui s'accumulent pendant les périodes où la demande en eau est faible peuvent être remises en suspension en augmentant suffisamment la vitesse d'écoulement de l'eau, ce qui empêche ainsi les problèmes d'accumulation à long terme. La mise en pratique de cette technique peut être limitée, car la conception des réseaux de distribution doit s'y prêter (système ramifié par rapport à système en boucle).
Les sédiments peuvent également être enlevés par ramonage, mais cette technique doit être utilisée avec précaution, car elle ne convient pas à tous les types de tuyaux et de qualité d'eau (FCM, 2003). Par exemple, le ramonage de canalisations en fonte sans revêtement a été associé à une libération accrue de fer et de rejets de plomb en aval, comparativement à ce qui est observé dans les canalisations en fonte dotées d'un revêtement et ayant été raclées, et dans les canalisations dépourvues de revêtement et n'ayant pas été raclées (Camara et coll., 2013). Zacheus et coll. (2001) ont constaté qu'avant un prélèvement au moyen d'un écouvillon en polyuréthane, le manganèse représentait 3,7 % (en poids) des dépôts dans les conduites du réseau de distribution, tandis que, un an après l'écouvillonnage, le manganèse ne représentait plus que 0,58 % (en poids) des dépôts.
Barbeau et coll. (2005) ont découvert que les dépôts meubles retrouvés dans les canalisations de réseaux de distribution en fonte ductile recouverte de ciment, ainsi que dans celles en fonte grise sans revêtement, étaient constitués à 5,9 % (en poids) de manganèse. Un an après le rinçage de cul-se-sacs, le contenu en manganèse était tombé à 0,35 %. On considère que le rinçage unidirectionnel est une pratique exemplaire pour la gestion des particules dans un réseau de distribution (FCM, 2003; Brandhuber et coll. (2015). Dans une étude sur le terrain réalisée par Carrière et coll. (2005), le rinçage unidirectionnel s'est révélé efficace, dans certains cas, pour l'enlèvement des dépôts meubles dans le réseau de distribution. Les auteurs ont tenu à souligner que cette méthode devait être appliquée selon les particularités de chaque site. Vreeburg (2010) a également recommandé l'approche du « réservoir d'eau propre », qui nécessite que l'eau en amont utilisée pour le rinçage des canalisations provienne de tuyaux ne contenant aucune matière pouvant être remise en suspension, afin d'empêcher l'introduction de sédiments dans les canalisations rincées.
Friedman et coll. (2016) ont réalisé une étude de cas portant sur les considérations liées à l'efficacité et aux coûts de diverses techniques de nettoyage pour éliminer l'accumulation de contaminants inorganiques à l'état de traces dans les conduites. Les auteurs ont constaté que sur deux sites différents, le nettoyage avec glace et par torpille (deux méthodes plus efficaces que le rinçage unidirectionnel à une vitesse de 3 ou de 6 pieds par seconde [pps]) enlevaient, avec différents degrés d'efficacité, les sédiments de manganèse et les contaminants inorganiques à l'état de traces associés. Les résultats ont mis en lumière la nécessité d'adopter une approche sur mesure et ciblée en fonction du site. Les auteurs ont également mis au point une approche qualitative de caractérisation et de priorisation des risques pour le nettoyage des conduites, que les services publics pourraient adapter en fonction de leurs besoins.
Le rinçage classique des conduites principales n'est pas considéré comme une stratégie efficace pour gérer l'accumulation de manganèse. Il s'agit plutôt d'une stratégie qui devrait être appliquée pour diminuer l'âge de l'eau et qui devrait être menée selon les pratiques exemplaires, notamment le rinçage à une vitesse assez faible pour ne pas perturber les sédiments (FCM, 2003). Par ailleurs, le nettoyage des conduites principales fait partie d'une stratégie efficace de gestion des dépôts de manganèse dans les réseaux de distribution. Toutefois, la stratégie de nettoyage doit être ciblée et adaptée aux matériaux des tuyaux ainsi qu'aux caractéristiques des sédiments, et les pratiques exemplaires doivent également être appliquées afin de minimiser l'exposition aux sédiments perturbés. Dans les cas extrêmes, le remplacement des tuyaux pourrait constituer une solution de dernier recours contre le manganèse accumulé dans les réseaux de distribution (Brandhuber et coll., 2015).
La stabilité des conditions de qualité de l'eau est importante pour minimiser la libération de manganèse accumulé dans les réseaux de distribution. Friedman et coll. (2010) ont relevé plusieurs paramètres liés à la qualité de l'eau (pH, Eh et pouvoir corrosif) qui doivent être contrôlés afin de maintenir la stabilité de l'eau pour les dépôts de matière inorganique. Le mélange non contrôlé des eaux de surface et des eaux souterraines, ainsi que le mélange non contrôlé d'eau chlorée et d'eau chloraminée sont à éviter. Les services publics peuvent fixer une base de référence pour la qualité de l'eau afin d'établir des valeurs limites en dehors desquelles une excursion pourrait déclencher un événement de rejet (Friedman et coll., 2016).
La gestion de l'accumulation et de la libération de manganèse peut représenter un défi de taille pour les services publics, car même si une installation réussit à atteindre les OE, il se peut que les canalisations du réseau de distribution contiennent une quantité de manganèse accumulée avec le temps. Afin de découvrir les zones du réseau de distribution qui présentent un risque élevé, il faut d'abord connaître les facteurs qui ont une incidence sur le risque d'accumulation (p. ex. présence de manganèse dans l'eau prélevée à la source ou dans l'eau traitée, proximité de l'usine de traitement, matériau de fabrication des tuyaux, biofilm) et sur le risque de libération (p. ex. instabilité des conditions liées à la qualité de l'eau, perturbations hydrauliques ou physiques). Un cadre d'auto-évaluation, comme celui présenté dans l'étude de Brandhuber et coll. (2015), peut aider les services publics à cerner les risques liés au manganèse qui entre dans leur réseau, qui s'y accumule et qui s'en échappe. En comprenant ces risques, ils peuvent mettre en œuvre des stratégies d'atténuation du manganèse plus efficaces et ciblées. En outre, les zones du réseau de distribution qui ont été reconnues comme étant fortement susceptibles d'accumuler et de rejeter du manganèse peuvent constituer des emplacements de choix pour effectuer une surveillance accrue fondée sur les événements.
7.4 Traitement dans les systèmes résidentiels
Dans les cas où l'on souhaite éliminer le manganèse à l'échelle résidentielle, par exemple lorsque l'eau potable d'une résidence provient d'un puits privé, un dispositif résidentiel de traitement de l'eau potable peut être employé pour réduire les concentrations de manganèse dans l'eau potable. Avant d'installer un dispositif de traitement, il convient de faire analyser l'eau par un laboratoire accrédité afin d'en caractériser la chimie générale et de vérifier la présence et la concentration de manganèse dans l'eau prélevée à la source. Il faut faire analyser régulièrement l'eau pénétrant dans l'appareil de traitement, de même que l'eau traitée, par un laboratoire accrédité pour vérifier l'efficacité du dispositif. Les dispositifs de traitement deviennent moins efficaces avec l'usage et avec le temps et doivent donc être entretenus ou remplacés. Les consommateurs doivent suivre les instructions du fabricant en ce qui concerne la durée de vie prévue des composants de leur dispositif de traitement, et faire réviser le dispositif quand il le faut.
Santé Canada ne recommande pas de dispositifs de traitement de marques particulières, mais conseille fortement aux consommateurs d'utiliser un dispositif qu'un organisme de certification accrédité a certifié conforme aux normes applicables aux unités de traitement de l'eau de NSF International (NSF) et de l'American National Standards Institute (ANSI). Ces normes visent à préserver la qualité de l'eau potable en aidant à assurer l'innocuité des matériaux et l'efficacité des produits qui entrent en contact avec elle. La norme NSF/ANSI 42 Drinking Water Treatment Units – Aesthetic Effects contient des exigences relatives à la réduction du taux de manganèse. Pour qu'un dispositif puisse être certifié conforme à la norme 42 pour la réduction du taux de manganèse, il doit pouvoir réduire une concentration initiale de 1 à 2 mg/L de manganèse dissous (Mn(II)) à une concentration maximale de 0,05 mg/L dans l'eau traitée (NSF/ANSI, 2015b).
Les organismes de certification garantissent qu'un produit est conforme aux normes en vigueur et doivent être accrédités par le Conseil canadien des normes (CCN). Au Canada, les organismes suivants ont été accrédités par le CCN pour la certification des dispositifs de traitement de l'eau potable comme étant conformes aux normes de la NSF/ANSI (CCN, 2016)) :
- Groupe CSA (www.csagroup.org);
- NSF International (www.nsf.org);
- Water Quality Association (http://www.wqa.org);
- UL LLC (www.ul.com);
- Bureau de Normalisation du Québec (www.bnq.qc.ca);
- International Association of Plumbing and Mechanical Officials (www.iapmo.org).
On peut obtenir une liste à jour des organismes de certification accrédités en s'adressant au CCN (www.ccn.ca).
Bien qu'il n'existe actuellement aucune unité de traitement certifiée expressément pour la réduction du manganèse, plusieurs technologies de traitement peuvent être efficaces pour éliminer le manganèse à l'échelle résidentielle. Les systèmes de traitement du manganèse sont habituellement installés au point d'entrée (PE) dans la maison pour réduire la possibilité de coloration de l'eau et de taches sur la lessive (considérations d'ordre esthétique). Ces systèmes sont généralement conçus et fabriqués pour un usage résidentiel par des fournisseurs ou des détaillants de systèmes de traitement de l'eau potable. Les technologies de traitement qui peuvent être employées au point d'entrée dans la maison pour réduire le risque de coloration de l'eau et de taches sont l'échange d'ions (c.-à-d. un adoucisseur d'eau) et la filtration sur sable vert. Il existe également des dispositifs de traitement de l'eau potable qui réduisent les concentrations de manganèse au point d'utilisation (PU) dans la maison (p. ex. au robinet de l'évier de cuisine), ainsi que des filtres de type déversoir (p. ex. carafe munie d'un filtre). Les technologies d'élimination du manganèse appropriées pour un traitement résidentiel sont l'osmose inverse, l'échange d'ions (y compris les adoucisseurs d'eau et autres systèmes d'échange cationique), et les filtres oxydants (p. ex. filtres au sable vert).
Santé Canada recommande fortement que tout composant et produit chimique utilisés dans ces systèmes de traitement soient certifiés conformes aux normes NSF/ANSI pertinentes, à savoir la norme 60 (Drinking Water Treatment Chemicals – Health Effects) (NSF/ANSI, 2015a), la norme 61 (Drinking Water System Components – Health Effects) (NSF/ANSI, 2016a) et la norme 372 (Drinking Water System Components – Lead Content) (NSF/ANSI, 2016b). Les systèmes d'osmose inverse sont visés par la norme 58 (Reverse Osmosis Drinking Water Treatment Systems) (NSF/ANSI, 2015c) et les adoucisseurs d'eau par la norme 44 (Cation exchange water softeners) (NSF/ANSI, 2015d).
Le choix du système de traitement le plus efficace pour un foyer dépendra de divers facteurs, dont la concentration et la forme (dissoute ou particulaire) de manganèse, ainsi que d'autres paramètres de l'eau prélevée à la source, comme la dureté et l'alcalinité, ainsi que le taux de fer, de sulfure, d'ammoniac et de carbone organique dissous.
Il a été démontré que le système de traitement par osmose inverse (OI) est la technique de traitement au PU la plus efficace et la plus fiable pour éliminer le manganèse de l'eau potable dans les habitations dont l'alimentation en eau contient des concentrations élevées de manganèse (Barbeau et coll., 2011; Brodeur et Barbeau, 2015; Santé Canada, 2015). Barbeau et coll. (2011) ont constaté que huit systèmes d'OI installés dans des habitations alimentées en eau de puits éliminaient 100 % du manganèse, même lorsque la concentration initiale était élevée (> 1 mg/L). Dans un rapport plus détaillé produit à partir des mêmes données, Brodeur et Barbeau (2015) ont indiqué que les systèmes d'OI installés au PU pouvaient abaisser la concentration en manganèse à moins de 1,0 µg/L dans l'eau traitée lorsque la concentration de manganèse dans l'eau du puits se situait entre 141 et 3,9 µg/L (taux d'élimination de 86 à 100 %). Les systèmes d'OI au PU ont également fait l'objet d'essais contrôlés en laboratoire afin d'évaluer leur capacité à réduire les concentrations de manganèse au robinet (Santé Canada, 2015). Cette étude a testé trois systèmes différents de ce type, certifiés selon la norme 58 de NSF/ANSI pour l'élimination d'autres métaux (c.-à-d. l'arsenic, le baryum, le chrome, le cuivre et le plomb). Les essais ont été effectués conformément aux exigences énoncées dans la norme 58 de NSF/ANSI concernant les allégations liées à la réduction des produits chimiques inorganiques. Deux séries d'essais ont été menées avec différentes concentrations de manganèse dans l'influent. Dans la première série, la concentration médiane de manganèse dans l'influent était de 100 µg/L pour les deux systèmes d'OI (une valeur représentative de la concentration moyenne de manganèse dans l'eau de puits). Deux des systèmes ont obtenu un taux d'élimination médian supérieur à 95 %, avec des concentrations de manganèse inférieures à 4 µg/L dans l'eau traitée. Le troisième système, qui a été testé après retrait du réservoir de stockage, a montré un taux d'élimination médian de 88 %, avec des concentrations inférieures à 24 µg/L dans l'eau traitée. Dans la deuxième série d'essais, les concentrations de manganèse dans l'influent se situaient entre 1,5 et 3,5 mg/L pour les deux systèmes d'OI (une valeur représentative des concentrations maximales de manganèse dans l'eau de puits). Les résultats obtenus avec les deux systèmes étaient similaires à ceux de la première série, avec des taux d'élimination médians allant de 95 à 97 % et des concentrations médianes de manganèse comprises entre 63 et 100 µg/L dans l'eau traitée. Le système sans réservoir de stockage a obtenu un taux d'élimination plus faible, soit une médiane de 91 %, et une concentration médiane de manganèse de 140 µg/L dans l'eau traitée. Dans l'ensemble, dans la plupart des conditions, les systèmes d'OI installés au PU sont capables d'abaisser la concentration de manganèse sous la CMA. Les propriétaires de puits dont l'eau contient une concentration élevée en manganèse (> 2 mg/L) devront peut-être utiliser une combinaison de deux technologies de traitement, comme l'échange d'ions au PE suivi de l'OI au PU, pour obtenir des concentrations de manganèse inférieures à 100 µg/L dans l'eau traitée.
Il convient de souligner que les systèmes d'OI sont conçus pour être installés au PU, car de grandes quantités d'eau d'arrivée sont nécessaires pour obtenir le volume requis d'eau traitée, ce qui n'est généralement pas pratique pour des systèmes de traitement résidentiels destinés au PE. Les systèmes d'OI certifiés conformes à la norme 58 de la NSF/ANSI sont conçus pour une installation au PU, car l'eau traitée par ces systèmes peut avoir un effet corrosif sur la plomberie. Il peut être nécessaire de prétraiter l'eau d'arrivée afin de réduire l'encrassement de la membrane et de prolonger sa durée de vie utile.
Il existe également des dispositifs au PU pourvus d'un milieu d'échange cationique qui sont efficaces pour éliminer le manganèse. Carrière et coll. (2011) ont découvert que les filtres de type déversoir contenant un milieu d'échange cationique (et de CAG) pouvaient réduire un taux de manganèse de 1 mg/L dans l'eau d'un influent, avec une efficacité supérieure à plus de 60 % à 100 % de leur capacité estimée. Ces filtres ont même souvent atteint un taux d'élimination de 100 % lors de leurs premières utilisations. Les dispositifs d'échange cationique conçus pour être installés sous l'évier se sont également révélés efficaces pour éliminer le manganèse dissous (jusqu'à 100 %), mais dans certains cas leur efficacité a diminué après avoir atteint seulement 50 % de leur capacité de traitement prévue. Il est également important de noter que les concentrations de manganèse dans l'eau traitée augmentaient lorsque les dispositifs étaient utilisés au-delà de leur capacité estimée. Puisque la plupart des milieux d'échange cationique utilisés dans les dispositifs de traitement de l'eau potable ont une affinité plus faible pour le manganèse que pour le calcium, le magnésium et d'autres métaux comme le fer, les ions manganèse sont plus facilement séparés de la résine, ce qui réduit la capacité d'élimination du manganèse et peut augmenter la quantité de manganèse dans l'eau traitée (Carrière et coll., 2011). Par conséquent, ces dispositifs doivent être utilisés avec beaucoup de précautions et faire l'objet d'une étroite surveillance.
Les adoucisseurs d'eau classiques conçus pour l'enlèvement des ions de dureté (Ca2+ et Mg2+) qui sont utilisés pour traiter l'eau à l'entrée des habitations font également appel à l'échange d'ions et peuvent permettre d'éliminer de faibles concentrations de manganèse. Si l'eau prélevée à la source contient du manganèse particulaire, ce dernier peut endommager la résine et réduire l'efficacité du système. Comme il a été mentionné précédemment, les systèmes fondés sur l'échange d'ions peuvent présenter un taux d'élimination varié en raison de la sélectivité de la résine envers les cations responsables de la dureté de l'eau (calcium et magnésium). Par conséquent, un adoucisseur d'eau sera moins efficace pour éliminer le manganèse si l'eau prélevée à la source est très dure ou contient beaucoup de fer. Brodeur et Barbeau (2015) et Barbeau et coll. (2011) ont constaté que l'efficacité des systèmes à échange d'ions utilisés pour traiter les eaux souterraines à l'échelle résidentielle variait beaucoup (-48 % à 99 %). Malgré l'écart important observé entre les différents taux d'élimination du manganèse dans cette étude, les systèmes se sont globalement révélés efficaces. Soixante-quinze pour cent des systèmes ont réussi à éliminer 99 % du manganèse (concentrations dans l'influent allant jusqu'à 211 µg/L) et à atteindre une concentration de manganèse inférieure à 19 µg/L dans l'eau traitée.
L'adoucissement de l'eau repose sur l'échange d'ions de dureté, de même que d'autres cations comme le manganèse, avec des ions sodium ou potassium. Toutefois, les propriétaires qui utilisent des adoucisseurs d'eau résidentiels doivent savoir que ces systèmes augmentent la concentration de sodium ou de potassium dans l'eau traitée, et qu'il est recommandé qu'une partie de l'eau (c.-à-d. l'eau du robinet de la cuisine) contourne complètement l'adoucisseur pour limiter ces intrants.
Les filtres oxydants au PE, comme les filtres au sable vert, peuvent être utilisés pour l'élimination du manganèse à l'échelle résidentielle. Ces systèmes contiennent un milieu filtrant traité avec du permanganate de potassium pour produire un enrobage qui absorbe puis oxyde le manganèse dissous. Ces filtres sont souvent appelés filtres au sable vert de manganèse. Les filtres au sable vert demandent beaucoup d'entretien, y compris une régénération fréquente avec un oxydant et des lavages à contre-courant réguliers pour retirer les particules de manganèse oxydées. L'oxydant de choix est le chlore, bien que le permanganate de potassium puisse également être efficace. Une utilisation et un entretien déficients des filtres au sable vert ont été associés à une augmentation des concentrations de manganèse dans l'eau du robinet des maisons qui traitaient l'eau de puits en raison de la présence de manganèse (Barbeau et coll., 2011). Brodeur et Barbeau (2015) ont publié des données sur trois filtres au sable vert installés dans des résidences pour l'élimination du manganèse. Aucun de ces systèmes n'a permis de réduire la concentration de manganèse en deçà de 100 µg/L. On a de plus constaté que dans deux des systèmes, les filtres libéraient du manganèse, ce qui a fait augmenter de 17 à 199 % la concentration de manganèse dans l'eau traitée. Pour cette raison, les propriétaires qui veulent utiliser ce type de système de traitement pour l'élimination du manganèse doivent porter une attention particulière au choix du système et à son fonctionnement. De plus, il est important de surveiller régulièrement la concentration de manganèse dans l'eau traitée par filtration sur sable vert afin de s'assurer que le système élimine efficacement le manganèse et que le filtre n'en libère pas.
Selon la concentration de manganèse dans l'eau prélevée à la source et le type de traitement choisi, les propriétaires qui possèdent un puits pourraient décider de traiter l'eau au PE afin de réduire le risque de coloration de l'eau et de taches sur la lessive, en plus de traiter l'eau au PU pour s'assurer que la concentration de manganèse dans l'eau potable de la résidence est systématiquement en deçà de la CMA.
8.0 Cinétique et métabolisme
La section qui suit résume les données présentées dans plusieurs synthèses (Aschner et coll., 2005; Dorman et coll., 2006; Santé Canada, 2010) et dans des articles scientifiques publiés plus récemment. Le lecteur est invité à consulter ces documents pour obtenir des renseignements plus détaillés.
8.1 Absorption
Le manganèse est un nutriment essentiel qui est soumis à un contrôle homéostatique par la régulation aussi bien de son absorption dans le tractus gastrointestinal (GI) que de son excrétion hépatobiliaire (effet de premier passage) après son ingestion. En revanche, le manganèse inhalé lors d'une exposition en milieu professionnel peut être transporté au cerveau par l'appareil olfactif ou les voies respiratoires sans être soumis à cette régulation homéostatique de l'absorption intestinale et du premier passage hépatique (Aschner et coll., 2005; Roth, 2006). L'absorption de manganèse par inhalation diffère donc considérablement de l'absorption par ingestion d'eau potable.
L'ingestion par voie alimentaire est la plus importante source d'exposition au manganèse par voie orale pour les humains. L'absorption, régulée de façon homéostatique, dépend également de divers facteurs tels que la biodisponibilité ou la bioaccessibilité du manganèse dans le tractus GI, sa forme chimique, la quantité de manganèse ingérée, le bilan en fer, ainsi que le sexe et l'âge de la personne. Le tractus GI des adultes absorbe habituellement moins de manganèse provenant des aliments et de l'eau que celui des nourrissons (Davidsson et coll., 1988; Johnson et coll., 1991; Finley et coll., 1994; IOM, 2000; Santé Canada, 2010). Des études menées sur l'exposition par voie orale sur des animaux ont donné des résultats similaires sur le plan de l'absorption (Pollack et coll., 1965; Davis et coll., 1993; Finley et coll., 1997; Zheng et coll., 2000). Le taux d'absorption du manganèse ingéré est plus élevé pendant la période néonatale, et il semblerait que la biodisponibilité du manganèse soit également plus élevée pendant cette période (Dorothy Klimis-Zacas, 1993). Les nouveau-nés auraient un taux plus élevé de rétention du manganèse, un taux de rétention de 20 % de l'apport oral ayant été mesuré chez des nourrissons nourris d'une préparation pour nourrissons (Aschner et Aschner, 2005).
Un examen de 13 études publiées portant sur une large gamme de scénarios d'exposition chez les humains (sans égard à l'état de jeûne) n'a révélé aucune différence statistiquement significative en ce qui concerne la biodisponibilité (définie dans l'examen comme étant la fraction qui pénètre dans la circulation générale, c.-à-d. excluant la partie excrétée dans la bile après l'effet de premier passage hépatique) du manganèse selon qu'il est ingéré avec l'eau ou les aliments (rapport aliment:eau = 0,7) (Ruoff, 1995). Dans le cas des aliments, la disponibilité dans le tractus GI était la même que le manganèse ait été présent naturellement dans les aliments ou qu'il y ait été ajouté. Cependant, une réévaluation des données qui tenait compte des personnes à jeun a montré que la biodisponibilité du manganèse provenant de l'eau était environ deux fois plus élevée que celle du manganèse provenant des aliments (rapport aliment:eau = 0,5) (Ruoff, 1995). Dans l'ensemble, ces données indiquent que la biodisponibilité du manganèse dans le tractus GI des humains pourrait dépendre en partie des interactions entre le manganèse et les matières présentes dans le tube digestif (fibres, protéines et autres substances inorganiques), plutôt que de sa biodisponibilité dans chaque matière ingérée. Les recherches ont révélé que l'absorption nette du manganèse par voie alimentaire était influencée par la présence d'autres métaux traces, de cellulose, de pectine, de phytate, d'acide ascorbique et d'autres composants alimentaires (Aschner et coll., 2005), ainsi que par la bioaccessibilité du manganèse dans les matrices solides (c.-à-d. la proportion de manganèse, dans une matrice solide, qui est potentiellement biologiquement disponible pour absorption). La bioaccessibilité estimée était de 55 à 95 % dans une variété d'aliments d'origine animale (Lei et coll., 2013) et de 12 à 41 % dans 20 sols en milieu urbain (Sialelli et coll., 2010). La biodisponibilité s'est révélée similaire pour des rats adultes ayant été soumis pendant 61 jours à des expositions équivalentes au manganèse dans l'eau potable et dans les aliments (Foster et coll., 2015). Il convient toutefois de noter que les changements adaptatifs qui se produisent chez les adultes pour réguler le taux de manganèse après une forte exposition (notamment la diminution de l'absorption gastrointestinale et l'augmentation de l'excrétion) ne sont pas établis chez les nourrissons, qui ne possèdent pas encore ces mécanismes de régulation homéostatique (Aschner et coll., 2005; Foster et coll., 2015).
La forme chimique (c.-à-d. l'espèce) et l'état de valence du manganèse ont une incidence sur son absorption. Le manganèse soluble (p. ex. le chlorure de manganèse) est plus facilement absorbé (Roels et coll., 1997) que le complexe de manganèse à l'état d'oxydation trivalent présent dans le lait maternel humain. Cette forme trivalente se lie à la lactoferrine et son absorption depuis le tractus GI est régulée par les récepteurs de la lactoferrine présents dans la membrane (bordure en brosse) des cellules épithéliales sur toute la longueur de l'intestin grêle. Les préparations pour nourrissons contiennent du manganèse à l'état d'oxydation divalent qui ne se lie pas à la lactoferrine, ce qui signifie que les récepteurs de la lactoferrine ne peuvent pas réguler son absorption intestinale (Erikson et coll., 2007b). Dans certaines des études consultées, un apport élevé en manganèse dans l'alimentation d'adultes en santé était accompagné d'une diminution du pourcentage d'absorption ainsi que d'une augmentation du métabolisme hépatique et de l'élimination biliaire et pancréatique du manganèse (Finley et coll., 2003; Aschner et coll., 2005).
Autant chez les humains que chez les animaux, un faible bilan en fer augmente l'absorption du manganèse, quelles que soient les réserves en manganèse de l'organisme (Mena et coll., 1969; Chandra et Shukla, 1976; Shukla et coll., 1976; Finley et Davis, 1999; Arnich et coll., 2004). L'absorption du fer et l'absorption du manganèse dans le tube digestif font appel au même système de transport, ce qui crée une compétition entre le manganèse et le fer non héminique pour le transporteur de métaux divalent 1 (DMT-1, également appelé DCT-1 ou nramp-2) (Davis et coll., 1992a). Le taux d'expression du DMT-1 (taux d'ARNm) augmente considérablement dans le duodénum en présence d'une déplétion martiale (Gunshin et coll., 2001).
L'absorption gastrointestinale est également influencée par des facteurs liés à la personne, comme le sexe et l'âge. Chez les humains, le manganèse est davantage absorbé dans le tractus GI des femmes que des hommes (Finley et coll., 1994), probablement en raison du bilan en fer moins élevé des femmes et de leur besoin accru en fer. Une augmentation de l'absorption et de la rétention de manganèse a été observée chez les nouveau-nés et les nourrissons, jusqu'à un âge non déterminé pour les humains et jusqu'à 17 à 18 jours pour les rongeurs (Gruden, 1977; Keen et coll., 1986; Dörner et coll., 1989; Kostial et coll., 1989; Zlotkin et coll., 1995; Aschner et coll., 2005). Les nourrissons peuvent absorber jusqu'à 40 % du manganèse ingéré (comparativement à 3 % environ pour les adultes), ce qui les rend particulièrement vulnérables aux effets d'une forte exposition au manganèse (Neal et Guilarte, 2013). La rétention biliaire accrue du manganèse observée chez les nouveau-nés peut s'expliquer par l'immaturité du système hépatobiliaire (excrétion réduite) (Miller et coll., 1975; Cotzias et coll., 1976) et par une absorption accrue dans le tractus GI (Cahill et coll., 1980). L'absorption accrue observée chez les très jeunes enfants pourrait également être un mécanisme compensatoire résultant des besoins métaboliques des nourrissons, qui sont plus élevés que ceux des adultes étant donné que le manganèse est essentiel à une minéralisation adéquate des os et à la synthèse des tissus conjonctifs (Santamaria, 2008). La rétention de manganèse semble varier considérablement entre les individus : des adultes humains ayant reçu une dose de manganèse radiomarqué dans une préparation pour nourrissons montrent une absorption moyenne mesurée de 5,9 ± 4,8 %, avec un intervalle de 0,8 à 16 %, ce qui représente une différence d'un facteur vingt. Le taux de rétention mesuré au dixième jour (0,6 à 9,2 %) montrait également les différences considérables entre les individus (Davidsson et coll., 1989a).
On connaît mal l'absorption du manganèse par voie cutanée, mais on s'attend à ce qu'elle soit extrêmement limitée (Aschner et coll., 2005). Aucune donnée expérimentale concernant l'absorption du manganèse par voie cutanée n'a été recensée.
8.2 Distribution
Deux synthèses (Aschner et coll., 2005; 2007) et un rapport de Santé Canada (2010) résument en détail les renseignements relatifs à la distribution du manganèse.
8.2.1 Distribution dans les tissus
Le manganèse est distribué dans tout le corps par la circulation générale. Dans le sang, le manganèse est présent dans le plasma (où le Mn(II) se lie à l'albumine), dans les globules rouges (où il se lie principalement à l'hémoglobine [Gibbons et coll., 1976; Saric, 1986; Davidsson et coll., 1989b]) et dans les globules blancs.
La distribution du manganèse dépend de sa forme chimique (valence et solubilité). Dans une étude de toxicité par voie alimentaire, les taux de manganèse dans le foie et les reins se sont révélés beaucoup plus élevés chez les souris mâles exposées à l'acétate de manganèse ou au carbonate de manganèse que chez celles exposées au chlorure de manganèse ou au dioxyde de manganèse (Komura et Sakamoto, 1991). Dans une étude portant sur des rats ayant reçu des doses identiques de Mn(II) ou de Mn(III) par voie intrapéritonéale, les concentrations dans le cerveau et dans le sang se sont révélées plus élevées chez les rats ayant reçu du Mn(III) (Reaney et coll., 2006).
Dans la plupart des tissus humains, la concentration de manganèse varie entre 0,1 et 1 µg/g de poids humide, mais des valeurs plus élevées ont été recensées dans le foie, le bulbe olfactif, les reins et certaines parties du cerveau d'adultes présumés normaux (Aschner et coll., 2005). On trouve généralement les concentrations les plus élevées de manganèse dans les tissus riches en mitochondries, tels que le foie, le pancréas, les reins, l'hypophyse et les intestins. Les concentrations les plus faibles sont observées dans les muscles, les os et la graisse (Merian et coll., 2004; Santé Canada, 2010). C'est dans les os qu'est stockée la plus grande quantité de manganèse, ces tissus représentant 25 à 40 % de la charge corporelle de manganèse en raison de la masse osseuse et non de la concentration nette (Aschner et coll., 2005; Roth, 2006). La gestation a été associée à des concentrations élevées de manganèse dans le foie des rates (Jarvinen et Ahlström, 1975).
Dans le lait humain, les concentrations de manganèse sont généralement inférieures à 30 µg/L, mais des valeurs atteignant 60 µg/L ont été signalées (Santé Canada, 2010). Les concentrations de manganèse mesurées dans le lait diminuaient à partir de la naissance jusqu'à plus de sept jours post-partum (Arnaud et Favier, 1995). Les ratios des concentrations de manganèse dans le sang total par rapport au lait maternel ont été estimés pour des femmes soumises à une exposition professionnelle ou environnementale à différents métaux dans une région de l'Inde fortement touchée par l'industrie sidérurgique, ainsi que pour des femmes (témoins) vivant à 100 km de là (Sharma et Pervez, 2005). Les ratios moyens étaient de 2,8 à 4,1 pour les femmes exposées, et de 1,7 à 2,5 pour les femmes témoins. Dans les deux groupes exposés, il existait une corrélation entre la concentration de manganèse dans le sang et dans le lait maternel. Une étude menée au Bangladesh sur des mères exposées à des concentrations élevées de manganèse et d'autres métaux dans l'eau potable a révélé des taux élevés de manganèse dans l'urine, mais aucune corrélation n'a été établie entre une forte concentration de manganèse dans l'eau potable et des taux élevés dans le lait maternel ou le sang (Ljung et coll., 2009).
Les fœtus, les nouveau-nés et les petits sont exposés au manganèse (maternel), étant donné qu'il traverse la barrière placentaire et qu'il est présent dans le lait. Après que des rates mères aient été exposées par voie orale à du chlorure de manganèse dans l'eau potable (2 000 ppm) pendant la période de gestation (272 mg Mn/kg p.c. par jour) et de lactation (480 mg Mn/kg p.c. par jour), la charge corporelle de manganèse (mesurée par spectrométrie d'absorption atomique) des nouveau-nés et des petits âgés de 11 jours a augmenté d'un facteur six à huit. Cette augmentation était indépendante de l'âge et de la durée d'exposition; la même hausse a été observée que l'exposition ait eu lieu uniquement pendant la gestation, uniquement pendant l'allaitement, ou pendant la gestation et l'allaitement (Kostial et coll., 2005). Des concentrations accrues de manganèse ont également été observées dans le prosencéphale et le rhombencéphale de rats nouveau-nés après une exposition in utero (Kontur et Fechter, 1985).
8.2.2 Distribution dans le cerveau
Le cerveau absorbe facilement le manganèse de la circulation, et les taux de manganèse peuvent augmenter dans le cerveau après de fortes expositions. La demi-vie estimative du manganèse dans le cerveau est de 51 à 74 jours pour le rat, de 53 jours pour le macaque et de 53 jours pour l'humain (Cotzias et coll., 1968; Newland et coll., 1987; Takeda et coll., 1995).
Des recherches portant sur l'absorption du manganèse dans le cerveau ont mené à la conclusion que le manganèse peut pénétrer dans le cerveau par différentes voies, notamment à partir du sang en traversant les cellules endothéliales capillaires de la barrière hémato-encéphalique (BHE) ou en passant du sang au liquide céphalorachidien (LCR) par l'intermédiaire des plexus choroïdes; en cas d'exposition par inhalation, le manganèse peut passer de la muqueuse nasale au bulbe olfactif par l'entremise des connexions neuronales du système olfactif. Toutefois, dans le dernier cas, l'absorption ne serait importante que si le sujet est soumis à une forte exposition respiratoire par voie nasale (Aschner et coll., 2005; Crossgrove et Yokel, 2005; Bock et coll., 2008). On ne sait pas avec certitude si l'une de ces voies en particulier prédomine dans les cas graves de manganisme ou dans les cas de troubles neurologiques légers chez les humains, ni quels sont les principaux mécanismes de transport moléculaire de ces voies (Aschner et coll., 2005).
De nombreuses études animales font état d'une augmentation des concentrations de manganèse dans le cerveau après une exposition aiguë ou chronique par voie orale (Holbrook et coll., 1975; Rehnberg et coll., 1982; Kristensson et coll., 1986; Newland et coll., 1989; Chan et coll., 1992; Davis et coll., 1992b; Malecki et coll., 1996; Lai et coll., 1999). Par exemple, une augmentation du taux de manganèse a été constatée dans certaines parties du cerveau de rats exposés au manganèse dans l'eau potable (10 mg MnCl2•4H2O/mL) pendant cinq jours, les concentrations les plus élevées ayant été observées dans le striatum et les plus faibles, dans le cortex cérébral. Après dix jours, les concentrations les plus élevées ont été relevées dans la protubérance et le bulbe rachidien, et les concentrations les plus faibles dans l'hypothalamus. Les variations du taux de manganèse entre les différentes parties du cerveau étaient plus marquées chez les nouveau-nés que chez les rats sevrés ou adultes (Chan et coll., 1992). Chez les descendants femelles matures (jour postnatal [JPN] 120) de rats Wistar ayant été exposés directement au manganèse dans l'eau potable (280, 2 800 ou 5 600 mg Mn/L) pendant toute la période de gestation et de lactation ainsi qu'à partir du sevrage, une augmentation de la concentration de manganèse liée à la dose a été observée dans toutes les parties du cerveau (soit le mésencéphale, la protubérance, le bulbe rachidien, le cervelet, le cortex cérébral et, de façon plus importante, l'hypothalamus, le striatum et l'hippocampe), sauf dans le cortex cérébral et l'hippocampe des rats ayant reçu la dose la plus faible (Lai et coll., 1999).
Une étude de Dorman et coll. (2000) a mis en évidence une distribution différente du manganèse dans le cerveau des rats nouveau-nés et des rats adultes exposés à des doses similaires de chlorure de manganèse par voie orale (25 ou 50 mg/kg p.c. par jour). Une augmentation de la concentration de manganèse n'a été observée que dans le striatum et le cervelet des rats adultes du groupe ayant reçu la dose la plus élevée, alors que l'exposition des nouveau-nés a entraîné une augmentation de la concentration de manganèse dans le striatum, l'hippocampe, le rhombencéphale et le cortex cérébral pour tous les groupes exposés. Ces résultats indiquent qu'une exposition à de fortes concentrations de manganèse par voie orale serait plus susceptible d'entraîner une neurotoxicité chez les nouveau-nés que chez les adultes.
La toxicité induite par le manganèse est associée à des taux élevés de manganèse dans le cerveau après une forte exposition, et les régions du cerveau les plus particulièrement sensibles seraient le striatum (noyau caudé et putamen), le globus pallidus et le noyau sous-thalamique (appelés collectivement « ganglions de la base »), ainsi que les zones frontales du cortex (Dobson et coll., 2004). Chez les humains, le noyau caudé/le putamen et le globus pallidus ont été caractérisés comme étant les principaux organes cibles de neurotoxicité après une exposition au manganèse (Pal et coll., 1999; Aschner et coll., 2005).
8.2.3 Absorption et relargage cellulaires
Le Mn(II) et le Mn(III) peuvent tous les deux traverser la BHE (Aschner et coll., 1999). Le Mn(II) utilise divers transporteurs de cations divalents, alors que le Mn(III) associé à la transferrine est absorbé par le biais du récepteur de la transferrine (TfR) (Santé Canada, 2010). L'absorption du Mn(II) non lié aux protéines semble se faire beaucoup plus rapidement que celle du complexe Mn(III)-transferrine (Tf); le Mn(II) serait donc l'espèce prédominante de manganèse qui pénètre dans le cerveau à partir du plasma, tandis que l'absorption du complexe Mn(III)-Tf participerait moins à l'absorption du manganèse dans le cerveau (Yokel et coll., 2006). On connaît mal les mécanismes de transport du manganèse dans le cerveau au cours du développement. Le DMT-1 et le TfR sont présents dans le cerveau en développement, comme en témoigne l'expression des protéines DMT-1 et TfR chez les ratons Sprague-Dawley dès le JPN 5, avec des concentrations augmentant jusqu'au JPN 15 dans toutes les parties du cerveau examinées (cortex, hippocampe, striatum) (Siddappa et coll., 2002; Garcia et coll., 2006).
Il a été établi que le SLC30A10, un transporteur présent à la surface des cellules, joue un rôle important dans la sortie du manganèse hors du cerveau (Leyva-Illades et coll., 2014). Ce transporteur réduit le taux de Mn dans les cellules, et des mutations de ce transporteur provoquent une toxicité du manganèse. D'autres transporteurs contribuent également à maintenir l'homéostasie du manganèse dans la cellule (Chen et coll., 2015).
8.3 Métabolisme
Dans sa forme élémentaire, le manganèse n'est pas métabolisé et il est absorbé et excrété sans modification. Le manganèse est généralement ingéré sous forme de sels ionisés, et son état de valence peut changer pendant ou après son absorption. Bien que la forme divalente du manganèse prédomine dans les systèmes biologiques, le manganèse peut également être présent à l'état trivalent dans la plupart des enzymes, lié à la transferrine (Tf) et, dans le lait humain, lié à la lactoferrine (Aschner et coll., 2005).
Dans le foie et la circulation, une partie du manganèse divalent est oxydée en manganèse trivalent et stabilisée en se liant à des ligands protéiques tels que la Tf (Aschner et coll., 2005). La Tf se lie au Mn(III) — ou au Fe(III) —, mais pas au Mn(II) (Aisen et coll., 1969; Critchfield et Keen, 1992; Ueda et coll., 1993). Le Mn(II) peut également s'oxyder en Mn(III) à l'intérieur des cellules, en réagissant avec des espèces de radicaux libres tels que des anions superoxydes (Archibald et Tyree, 1987). Il a été avancé que la céruloplasmine présente dans le plasma sanguin catalyserait l'oxydation du Mn(II) en Mn(III), provoquant un changement in vitro conduisant le manganèse à se lier davantage à la Tf qu'à l'α2-macroglobuline (Gibbons et coll., 1976). Cependant, des études menées sur des souris n'exprimant pas la céruloplasmine ont clairement démontré que cette dernière n'était pas nécessaire à l'oxydation du manganèse dans le plasma ni à sa liaison à la Tf plasmatique (Jursa et Smith, 2009). De plus, il est possible que de petites quantités de Mn(II) soient spontanément oxydées et forment de petites quantités de Mn(III) qui, même à l'état de traces, peuvent entraîner la formation de radicaux libres réactifs (HaMai et coll., 2001). Certaines études laissent entendre que la majorité du manganèse présent dans les cellules de mammifère existerait sous forme de Mn(II) (Reaney et coll., 2002). Toutefois, la détection précise de l'état de valence du manganèse in vivo est limitée par diverses contraintes d'ordre technologique.
Les données semblent indiquer que l'état de valence du manganèse joue un rôle important dans la rétention et la toxicité de ce dernier (Yokel et coll., 2006). Chez les vaches, le Mn(II)-α2-macroglobuline a été éliminé plus rapidement que le Mn(III)-Tf (Gibbons et coll., 1976). Des études in vitro ont révélé que le Mn(III) était plus susceptible que le Mn(II) d'engendrer une cytotoxicité et une neurotoxicité, vraisemblablement en raison du potentiel de réduction plus élevé du Mn(III), et de sa capacité à produire un stress oxydatif (Ali et coll., 1985; Archibald et Tyree, 1987; Chen et coll., 2001; Reaney et coll., 2002; Reaney et Smith, 2005).
8.4 Excrétion
Le manganèse est essentiellement éliminé du sang par le foie et excrété dans la bile jusque dans l'intestin (Miller et coll., 1967). Une grande partie du manganèse biliaire présente dans l'intestin est éliminée dans les selles, tandis qu'une petite partie est réabsorbée (Schroeder et coll., 1966; Davis et coll., 1993). Le manganèse est également présent dans les excrétions pancréatiques, et une quantité minime est éliminée dans l'urine (Lee, 2009).
La demi-vie de la clairance du manganèse dans le corps est d'environ quatre jours durant la phase rapide et de 39 jours durant la phase lente, pendant laquelle s'effectuent environ les deux tiers de l'élimination (OMS, 1981). Les demi-vies estimatives de la rétention de manganèse dans le corps sont de 13 à 37 jours pour des humains ayant ingéré du manganèse radiomarqué (sous forme de chlorure de manganèse) (Mena et coll., 1969; Sandstrom et coll., 1986; Davidsson et coll., 1989a). Dans le cerveau, les demi-vies étaient de 50 à 220 jours pour les rats et les primates non humains (Takeda et coll., 1995; Santé Canada, 2010). L'absorption du manganèse dans le cerveau s'effectue par transport facilité. Il en sortirait toutefois plus lentement et par diffusion, ce qui pourrait entraîner une accumulation avec le temps (Yokel et Crossgrove, 2004).
Le transport direct du manganèse présent dans le sérum à travers la paroi intestinale peut contribuer à l'excrétion dans les selles (Bertinchamps et coll., 1965; Garcia-Aranda et coll., 1984). De petites quantités de manganèse sont excrétées dans l'urine, la sueur, le lait maternel, les cheveux et les ongles (Merian et coll., 2004; Santé Canada, 2010). La concentration de manganèse dans l'urine est généralement faible (Alessio et coll., 1989; Minoia et coll., 1990; Park et coll., 2003), et l'excrétion urinaire est considérée comme un mauvais biomarqueur de la charge corporelle après une exposition par voie orale ou par inhalation (Andersen et coll., 1999). Plusieurs études ont également utilisé les cheveux comme biomarqueurs de la charge corporelle et de l'exposition au manganèse dans l'environnement, bien qu'ils nécessitent un nettoyage approprié pour éliminer toute contamination au manganèse de nature exogène, de façon à pouvoir examiner uniquement le manganèse incorporé par métabolisme (Eastman et coll., 2013).
Les nourrissons, en particulier les nouveau-nés, font preuve d'une moins grande capacité d'excrétion biliaire que les adultes (Cotzias et coll., 1976). Il en résulte qu'après une exposition donnée, la charge corporelle de manganèse sera plus élevée pour les nouveau-nés et les jeunes enfants que pour les adultes; cette augmentation de la charge corporelle, associée aux processus neurodéveloppementaux importants qui se produisent chez les nouveau-nés, rend ces derniers particulièrement sensibles aux effets toxiques du manganèse (Neal et Guilarte, 2013).
8.5 Modèles pharmacocinétiques à base physiologique
Des modèles pharmacocinétiques à base physiologique (PBPK) pour le manganèse ont été élaborés pour les rats (Teeguarden et coll., 2007a; 2007b; 2007c; Na et coll., 2008; Nong et coll., 2008; 2009; Yoon et coll., 2009a; 2009b), les singes (Nong et coll., 2009; Schroeter et coll., 2011; 2012) et les humains (Schroeter et coll., 2011; Yoon et coll., 2011). Les modèles PBPK publiés depuis 2008 comprennent la voie orale et l'inhalation. Diverses voies d'injection (intrapéritonéale, sous-cutanée et intraveineuse) sont également utilisées dans les modèles humains et simiens (Schroeter et coll., 2011), pour permettre l'évaluation des données expérimentales obtenues avec du manganèse radiomarqué (54Mn). Il est possible d'estimer la quantité de manganèse qui passe dans le lait maternel chez le rat (Yoon et coll., 2009a), ainsi que la dose reçue par le fœtus et l'élimination du manganèse chez le rat (Yoon et coll., 2009b) et l'humain (Yoon et coll., 2011) (mère et fœtus). Un modèle PBPK a également été élaboré pour le transport du manganèse inhalé de la muqueuse olfactive au striatum chez le rat (Leavens et coll., 2007). Taylor et coll. (2012) présentent un aperçu de ces modèles.
Les plus récents modèles humains et simiens (Schroeter et coll., 2011; 2012) permettent d'estimer les concentrations de manganèse dans les tissus cibles du cerveau (globus pallidus). Ces modèles peuvent estimer la concentration tissulaire de manganèse après une exposition par ingestion, par inhalation ou par injection (intraveineuse, intrapéritonéale, sous-cutanée). Brièvement, les modèles comportent des compartiments pour le foie, les poumons, la cavité nasale, les os, le sang, le bulbe olfactifNote de bas de page 1, le cerveletNote de bas de page 1, le globus pallidusNote de bas de page 2, l'hypophyseNote de bas de page 2 et d'autres tissus de l'organisme. Ces modèles tiennent compte des capacités de liaison aux tissus du manganèse saturable, des flux préférentiels du manganèse dans des tissus précis (du cerveau), et des mécanismes de régulation homéostatique (c.-à-d. diminution de l'absorption intestinale et induction de la sécrétion biliaire en cas d'exposition à de fortes concentrations).
Les modèles humains et simiens ont tous les deux été validés par comparaison avec des données sur le manganèse obtenues à l'aide d'un traceur. La validation du modèle simien comprenait l'excrétion fécale (après injection sous-cutanée ou inhalation), la rétention dans tout le corps (après injection intrapéritonéale ou intraveineuse, ou exposition par voie orale) et la concentration dans le tissu cérébral (après une exposition par inhalation). Le modèle humain a réussi à intégrer les caractéristiques, liées à la dose, de l'élimination du manganèse (rétention dans tout le corps, rétention dans le plasma) pour diverses voies d'exposition. Selon les auteurs, les modèles utilisés pour estimer les concentrations d'exposition susceptibles d'accroître les concentrations tissulaires de manganèse pourraient également servir dans le cadre d'une évaluation des risques fondée sur la dosimétrie (Shroeter et coll., 2011). Bien que le modèle puisse être utilisé pour estimer la concentration de manganèse dans le tissu cérébral, ces types de simulations n'ont pas été validés pour les humains.
9.0 Effets sur la santé humaine
Un grand nombre d'études épidémiologiques ont étudié les effets d'une exposition au manganèse sur la santé humaine. Une forte exposition au manganèse, notamment en milieu de travail, peut provoquer une maladie neurologique clinique appelée « manganisme ». Cette affection est caractérisée par des troubles cognitifs et moteurs généralisés, tels qu'une bradykinésie, une rigidité généralisée, une démarche anormale, des chutes, une dystonie, une difficulté à marcher à reculons et des troubles d'élocution. En outre, de nombreuses études ont démontré qu'une faible exposition au manganèse, en particulier par inhalation, pouvait entraîner des déficits sur le plan des paramètres neurofonctionnels, dont une détérioration de la motricité fine, de la coordination œil-main et du temps de réaction. De études épidémiologiques semblent également indiquer un lien entre l'exposition au manganèse dans l'eau potable et certains effets neurologiques observés chez les enfants (Bouchard et coll., 2011; Khan et coll., 2011; Roehls et coll., 2012; Oulhote et coll., 2014).
9.1 Caractère essentiel
Santé Canada et d'autres organismes internationaux considèrent le manganèse comme un élément essentiel (CNRC, 1989; IOM, 2001; Expert Group on Vitamins and Minerals [EVM], 2002; National Institutes of Health, 2011; OMS, 2011). Le manganèse est un cofacteur essentiel pour certains enzymes (pyruvate carboxylase, superoxyde dismutase à manganèse) (CNRC, 1989; IOM, 2001). Il peut également agir comme cofacteur pour des enzymes (décarboxylases, hydrolases, kinases, etc.) qui sont aussi activés par d'autres cations divalents similaires, et qui ne sont pas altérés par une carence en manganèse (EVM, 2002). Les enzymes nécessitant du manganèse assurent plusieurs fonctions, dont la défense antioxydante, la formation des os, le métabolisme des hydrates de carbone, du cholestérol et des protéines, et utilisent d'autres nutriments comme les vitamines biotine et acide ascorbique (Saudin et coll., 1988; IOM, 2001).
Les carences en manganèse sont extrêmement rares et leurs symptômes ne sont pas clairement définis (Dupont et Tanaka, 1985; IOM, 2001). Chez les animaux, de telles carences entraînent des malformations des os et des cartilages, des retards de croissance, des perturbations neurologiques, des anomalies de la fonction reproductrice, ainsi que des troubles du métabolisme du glucose, des hydrates de carbone (symptômes pseudo-diabétiques) et des lipides (EVM, 2002). Chez les humains, une alimentation pauvre en manganèse (environ 0,01 à 0,34 mg/jour) est associée à des anomalies cutanées telles qu'un rash érythémateux, une croissance lente des ongles, une diminution de la densité osseuse, une dépigmentation des cheveux et une hypocholestérolémie.
Santé Canada a adopté les apports nutritionnels de référence fixés par l'IOM pour le manganèse. Faute de données suffisantes sur la dose et la réponse, aucun besoin moyen estimatif (BME) n'a été établi. Des apports suffisants (AS) ont été calculés d'après les données sur l'apport alimentaire moyen de personnes en santé. Les AS ont été établis à 0,003 mg/jour pour les nourrissons de 0 à 6 mois, 0,6 mg/jour pour les nourrissons de 6 à 12 mois, 1,2 mg/jour pour les enfants de 1 à 3 ans, 1,5 mg/jour pour les enfants de 4 à 8 ans, 2,3 mg/jour pour les hommes adultes, 1,8 mg/jour pour les femmes adultes, 2,0 mg/jour pour les femmes enceintes et 2,6 mg/jour pour les femmes qui allaitent. Ils ont été calculés à partir des données sur l'apport médian de l'étude de la Food and Drug Administration sur l'alimentation totale des enfants, des adolescents et des adultes, et d'après la concentration de manganèse dans le lait maternel pour les nourrissons (IOM 2001; Santé Canada 2007b).
L'apport maximal tolérable (AMT) a été fixé à 2 à 6 mg/jour pour les enfants de 1 à 18 ans, 11 mg/jour pour les adultes, et 9 à 11 mg/jour pour les femmes enceintes ou allaitantes (IOM, 2001). Comme les données sur la toxicité sont insuffisantes et que l'on ne sait pas exactement à quel âge les nourrissons acquièrent les mécanismes nécessaires pour maintenir l'homéostasie du manganèse, aucun AMT n'a été fixé pour les nourrissons (IOM, 2001). La cinquième édition du manuel Pediatric Nutrition Handbook de l'American Academy of Pediatrics ainsi que le rapport de l'American Society for Parenteral and Enteral Nutrition recommandent tous les deux un apport de 1 µg Mn/kg p.c. par jour pour les nouveau-nés nourris par voie parentérale (3 à 10 kg), même si le taux de rétention du manganèse administré par voie intraveineuse atteint presque 100 % (comparativement à 8 % pour l'ingestion par le lait maternel) (Committee on Nutrition, 2003; Mirtallo et coll., 2004; Aschner et Aschner, 2005).
L'AMT pour les adultes est fondé sur l'absence d'effets observés pour les adultes en santé ayant un régime alimentaire occidental contenant jusqu'à 10,9 mg/jour de manganèse (NOAEL de 11 mg/jour dans Greger, 1999), et d'après les données d'une étude portant sur une alimentation végétarienne riche en manganèse, contenant possiblement 13 à 20 mg/jour de manganèse (Schroeder et coll., 1966). Davis et Greger (1992), pour leur part, indiquent une LOAEL de 15 mg/jour. Une augmentation de l'activité de la superoxyde dismutase à manganèse dans les lymphocytes a été observée après l'application de cette dose en supplément pendant 90 jours. Chez les humains, il n'existe aucune étude de toxicité par l'alimentation visant à évaluer les effets neurologiques du manganèse à un taux correspondant à l'AMT.
Le Comité scientifique de l'alimentation humaine de la Commission européenne a fixé la concentration maximale de manganèse dans le lait maternisé à 100 μg/100 kcal (SCF 2003). Le calcul de cette valeur n'est pas clairement expliqué, mais la Commission a indiqué que la neurotoxicité du manganèse était une source de préoccupation grandissante.
Les carences en manganèse sont peu probables au Canada, l'alimentation étant la principale source de manganèse. En outre, selon l'ECAT (Santé Canada, 2009), la population atteint les valeurs d'AS établies par l'IOM. Les produits de santé naturels (c.-à-d. les suppléments contenant du manganèse) peuvent également contribuer de façon importante à l'apport quotidien, soit jusqu'à 9 mg/jour au Canada.
9.2 Toxicité aiguë
Un homme de 66 ans ayant ingéré accidentellement de faibles doses de permanganate de potassium (environ 1,8 mg Mn/kg p.c./jour) pendant quatre semaines a manifesté une faiblesse musculaire, ainsi que des perturbations neurologiques telles qu'une altération des capacités mentales (Holzgraefe et coll., 1986). Toutefois, étant donné qu'il a été exposé à d'autres substances, il n'est pas possible d'affirmer avec certitude que les effets observés chez cet homme étaient dus au manganèse. Dans une autre étude de cas portant sur un homme de 50 ans ayant ingéré du sulfate de manganèse hydraté (trois cuillérées à table par jour, pendant une durée indéterminée), les symptômes suivants ont été observés : léthargie, vomissements, douleurs abdominales diffuses, diarrhée abondante, insuffisance hépatique, atteinte rénale aiguë, détresse respiratoire aiguë, dysfonction du myocarde et choc avec acidose lactique. Le patient est décédé en 72 heures. Il est important de souligner que cet homme suivait un régime alimentaire sans protéines et qu'il consommait beaucoup de tisanes dans le cadre d'un nettoyage hépatique (Sanchez et coll., 2012).
9.3 Épidémiologie
L'exposition chronique au manganèse en suspension dans l'air a été associée à plusieurs reprises à des effets neurologiques nocifs (Santé Canada, 2010). Des études de cohortes, des études transversales et des études de rapports de cas portant sur les effets de l'exposition au manganèse en suspension dans l'air ont été menées auprès de soudeurs, de travailleurs et de populations vivant à proximité d'usines de ferro-alliage (Roels et coll., 1992; Lucchini et coll., 1999; Mergler et coll., 1999; Bowler et coll., 2006; Bouchard et coll., 2007b; Lees-Haley et coll., 2007; Myers et coll., 2009; Riojas-Rodríguez et coll., 2010; Criswell et coll., 2011; Menezes-Filho et coll., 2011; Meyer-Baron et coll., 2013; Michalke et Fernsebner, 2014; Yoon et Ahn, 2015).
Le lien entre l'exposition professionnelle au manganèse et des résultats subcliniques aux tests neuropsychologiques est équivoque, mais des modifications du temps de réaction visuelle, de la coordination œil-main, de la stabilité des mains et des résultats aux tests de performance motrice ont été observés. Des cas de manganisme ont été relevés dans les groupes les plus exposés, avec des symptômes tels qu'une bradykinésie, des troubles d'élocution, une démarche anormale, une rigidité généralisée, une dystonie, une tendance à tomber vers l'arrière et une démarche caractéristique consistant à marcher sur les orteils avec la colonne droite et les coudes fléchis. On ne sait pas exactement si les effets associés à l'exposition par inhalation peuvent être induits par voie orale. Il est difficile d'extrapoler les effets d'une voie d'exposition à une autre, en raison des différences observées, sur le plan de la toxicocinétique, entre les diverses voies d'exposition et les divers états d'oxydation (Aschner et coll., 2005; Roels et coll., 2012).
De nombreuses études épidémiologiques transversales ont observé une association entre d'une part l'exposition accrue au manganèse, et d'autre part des effets neurologiques chez les nourrissons et les enfants, notamment une désinhibition comportementale ainsi que de faibles résultats aux tests portant sur les fonctions exécutives, la lecture et l'aptitude numérique (Kawamura et coll., 1941; Kondakis et coll., 1989; He et coll., 1994; Woolf et coll., 2002; Wright et coll., 2006; Ericson et coll., 2007; Wasserman et coll., 2011; Khan et coll., 2012; Bhang et coll., 2013; Chen et coll., 2014; Yu et coll., 2014; Haynes et coll., 2015).
Une étude épidémiologique transversale réalisée au Québec et menée auprès d'enfants d'âge scolaire a étudié le lien éventuel entre le manganèse présent dans l'eau potable et la déficience intellectuelle (Bouchard et coll., 2011). Cette étude portait sur 362 enfants âgés de 6 à 13 ans vivant dans des collectivités alimentées par des eaux souterraines contenant des concentrations variées de manganèse (plage de 1 µg/L à 2 700 µg/L, avec une valeur médiane de 34 µg/L). Les auteurs de l'étude ont mesuré les concentrations de manganèse dans l'eau du robinet des résidences (MnW) ainsi que dans les cheveux des enfants (MnH), et ont évalué le rendement des enfants (QI) sur l'Échelle abrégée d'intelligence de Wechsler. Une différence de 6,2 points a été observée entre le QI des enfants des quintiles inférieur (concentration médiane de 1 µg/L) et supérieur (concentration médiane de 216 µg/L) d'exposition au manganèse dans l'eau. Les fortes MnW ont été associées à des QI et des résultats globaux de rendement plus faibles, après neutralisation des covariables (c.-à-d. scolarité et intelligence non verbale de la mère, revenu familial, niveau de stimulation à la maison et structure familiale). Les fortes MnH ont été associées à des résultats globaux de QI plus faibles, après neutralisation des mêmes covariables. La MnH augmentait avec la consommation de manganèse dans l'eau, mais pas avec la consommation de manganèse dans les aliments (questionnaire semi-quantitatif sur la fréquence de consommation des aliments), et les auteurs expliquent que cela pourrait indiquer une variation de la biodisponibilité du manganèse entre celui contenu dans l'eau et celui contenu dans les aliments.
Dans une deuxième publication de ce groupe, un rapport inverse a également été observé entre les fonctions neurocomportementales (mémoire, attention, fonction motrice, hyperactivité) et l'exposition au manganèse chez les mêmes enfants (n = 375) (Oulhote et coll., 2014). Les auteurs ont fait état d'une association inverse entre la MnW ou la MnH normalisées (transformées en log10) et la mémoire, l'attention ou la fonction motrice, après neutralisation des facteurs de confusion (c.-à-d., sexe et âge de l'enfant, scolarité de la mère, intelligence non verbale de la mère, revenu familial, dépression maternelle, concentrations de plomb dans l'eau). Pour le manganèse présent dans les cheveux, une augmentation d'un écart-type de la MnH en log10 était associée à une baisse de 24 % de l'écart-type des résultats relatifs à la mémoire (IC à 95 % : -36, -12 %) et à une baisse de 25 % de l'écart-type des résultats relatifs à l'attention (IC à 95 % : -41, -9 %), après neutralisation des facteurs de confusion. Aucune association importante n'a été observée entre la MnH et la fonction motrice. Pour le manganèse présent dans l'eau, l'augmentation d'un écart-type de la MnW en log10 (plage non précisée par les auteurs) était associée à une baisse de 14 % de l'écart-type des résultats relatifs à la mémoire (IC à 95 % : -24, -4 %). Une faible association négative avec la fonction motrice a été observée (baisse de 11 % de l'écart-type, IC à 95 % : -21, -0,4 %). Une détérioration importante de la mémoire et de la fonction motrice a été observée à des MnW supérieures, respectivement, à 100 µg/L et à 180 µg/L. L'étude n'a révélé aucune association importante entre la MnW et l'hyperactivité ou l'attention.
Une étude menée auprès de 262 enfants au Nouveau-Brunswick a tenté d'examiner le lien entre la cognition et l'exposition au manganèse par l'eau potable (Bouchard et coll., 2016). Les concentrations de manganèse signalées dans l'eau potable étaient généralement faibles : 48 % des enfants avaient consommé une eau contenant moins de 5 µg/L de manganèse, 25 % avaient consommé une eau contenant plus de 50 µg/L de manganèse, et seulement 4 % d'entre eux avaient été exposés à des concentrations de manganèse supérieures à 400 µg/L. Les auteurs ont évalué la cognition des enfants au moyen de l'échelle d'intelligence de Wechsler pour enfants (WISC-IV). Étant donné que les concentrations de manganèse dans l'eau potable étaient considérablement plus faibles que dans des études antérieures ayant relevé des effets, les auteurs ont été incapables de détecter un effet significatif.
Les contaminants non métalliques dans l'eau potable n'étaient pas évalués dans le cadre de ces études, mais celles-ci tenaient compte de plusieurs covariables présentes dans l'eau (p. ex. le plomb et l'arsenic), du statut socioéconomique, et de divers facteurs liés à la mère susceptibles d'influer sur l'association entre le manganèse et les capacités cognitives. Le risque de biais dans ces études ne peut toutefois pas être écarté. Peu de renseignements ont été fournis sur les critères d'admissibilité des sujets et sur les caractéristiques des sujets « perdus de vue ». Une classification erronée de l'exposition est possible, pour diverses raisons : la MnW n'a été mesurée qu'une seule fois, les sujets n'avaient pas besoin d'avoir habité la maison plus de trois mois pour participer à l'étude (les expositions antérieures au manganèse n'étaient pas prises en compte), l'utilisation de cheveux comme biomarqueur pouvait fausser les données d'exposition, aucune information sur la concentration de manganèse dans l'alimentation ou dans le sol n'a été fournie, et le moment ainsi que la durée associés aux niveaux d'exposition pendant les périodes cruciales du développement ne sont pas indiqués. Il n'est pas indiqué si le niveau d'exposition des participants était connu ou non des chercheurs. Enfin, les intervalles de confiance étaient grands et bon nombre des effets observés se situaient à la limite de la signification.
En Ohio, une étude transversale (Communities Actively Researching Exposure Study) a été menée auprès d'enfants âgés de 7 à 9 ans (n = 404) entre octobre 2008 et mars 2013 (Haynes et coll., 2015). Dans cette étude, les auteurs ont évalué les variables dépendantes (développement cognitif évalué avec le WISC-IV) ainsi que les covariables, comme le taux de manganèse dans le sang et les cheveux, au cours de la première visite. Des concentrations élevées de manganèse dans le sang (> 11,2 μg/L) et dans les cheveux (> 747 ng/g) ont été associées de façon significative à un QI global plus faible, comparativement aux groupes témoins (sang : 8,2 à 11,2 μg/L; cheveux : 207 à 747 ng/g), après neutralisation des facteurs de confusion (les plus importants étant le taux de créatinine, la plombémie, la communauté, le sexe, ainsi que le QI et la scolarité des parents). Les auteurs ne se sont penchés que sur l'association entre les variables prédictives et les effets, sans interpréter leurs résultats du point de vue des risques. Les associations mesurées peuvent être biaisées, étant donné le peu de renseignements fournis sur les participants et sur l'exposition. Par exemple, les auteurs ont exclu les participants pour lesquels il manquait des données pour n'importe quel modèle de covariables, ainsi que ceux qui présentaient des concentrations de manganèse plus élevées, ce qui peut créer un biais dans la relation observée (p. ex. si des participants pour lesquels il manquait des données présentaient une faible concentration de manganèse et avaient un QI peu élevé, ou si des participants ayant un QI élevé présentaient une concentration élevée de manganèse, l'exclusion de ces participants entraînerait un biais de résultats par rapport à la valeur nulle dans les deux scénarios, et causerait une surévaluation des effets). Comme les caractéristiques des participants exclus n'étaient pas présentées, on ne sait pas dans quelle mesure les sujets pris en compte dans l'étude sont représentatifs de la population. L'exposition peut avoir fait l'objet d'une classification erronée, puisque les expositions antérieures et les variations dans le temps ont mal été évaluées (les cheveux et le sang sont des bioindicateurs limités; il n'y avait aucune estimation de l'apport total en manganèse ou de l'apport provenant de l'eau potable; les bioindicateurs du manganèse et les autres covariables n'ont été mesurés qu'une seule fois). Il existe également un risque de confusion, car les caractéristiques de base n'ont pas été réparties selon les groupes d'exposition (impossible d'évaluer les différences autres que celles touchant le manganèse par rapport aux valeurs de référence) et les modèles statistiques n'ont pas été construits de façon à inclure tous les facteurs de confusion importants (le choix des covariables devrait être fondé sur les changements touchant les variables dépendantes, et non sur les variables d'exposition). De plus, le manganèse a été corrélé avec d'autres covariables considérées, ce qui réduit la confiance à l'égard du modèle. Les participants pourraient également être classés dans différents quartiles d'exposition, en fonction du bioindicateur choisi comme principale variable indépendante (Mn dans les cheveux ou dans le sang). Il existe aussi un risque de coïncidence, et comme les résultats n'étaient pas précis (large IC à 95 % incluant presque la valeur nulle), il aurait été utile d'indiquer la signification (valeurs p) des résultats provenant des modèles à multiples variables.
Plusieurs études transversales réalisées au Bangladesh ont établi des liens entre les concentrations de manganèse dans l'eau potable et le rendement cognitif chez les enfants d'âge scolaire. Wasserman et coll. (2011) ont étudié l'association entre l'exposition au manganèse et à l'arsenic et la fonction intellectuelle pour 304 enfants âgés de 8 à 11 ans, en utilisant des sous-tests adaptés du WISC-IV. Les auteurs ont classé les enfants en fonction des concentrations de manganèse (inférieures ou supérieures à 500 µg/L) et d'arsenic (inférieures ou supérieures à 10 µg/L) présentes dans l'eau de puits. Après avoir fait les ajustements nécessaires (scolarité et intelligence de la mère, type de logement, fait que la famille possède une télévision, taille de l'enfant et circonférence de sa tête), les auteurs ont trouvé que l'augmentation de la concentration de manganèse dans le sang (MnB) était associée à des indices de mémoire de travail et de raisonnement perceptif plus faibles. Cette étude présente certaines faiblesses, notamment le fait qu'elle visait à l'origine un autre objectif et que d'autres contaminants présents dans l'eau potable pourraient être la cause des effets observés. Ensuite, aucune autre source de manganèse n'a été prise en compte, et aucune tentative n'a été faite pour vérifier s'il y avait un lien entre la MnW et la MnB. En outre, les résultats neurologiques ont été mesurés à l'aide d'une échelle modifiée qui n'était ni validée, ni normalisée. De plus, les quartiles d'exposition utilisés dans l'étude n'ayant pas été quantifiés, les données ne peuvent pas être utilisées pour une évaluation quantitative des risques. Enfin, seules les erreurs-types des coefficients de régression ont été présentées.
Les limites de l'étude de Wasserman et coll. (2011) s'appliquent également à une publication antérieure des mêmes auteurs (Wasserman et coll., 2006). Dans cette étude antérieure, les auteurs ont observé une diminution liée à la dose des résultats bruts obtenus pour l'échelle globale, le rendement et les compétences verbales, après avoir tenu compte des facteurs de confusion (identiques à ceux de l'étude de 2011). Contrairement à l'étude de 2011 (dans laquelle l'association avec la MnB était significative), seule l'association avec la MnW était significative dans l'étude de 2006.
Khan et coll. (2012) ont examiné les associations entre l'exposition au manganèse et à l'arsenic dans l'eau potable et le rendement scolaire de 840 enfants au Bangladesh. La fonction intellectuelle a été évaluée sur le plan des langues et des mathématiques. L'étude a révélé une association marquée entre une MnW > 400 µg/L et la diminution des résultats au test de mathématiques ajustés en fonction des facteurs de confusion (arsenic, année scolaire, scolarité de la mère, scolarité du père, circonférence de la tête, corrélation dans les façons dont les enfants sont notés par les enseignants). Dans une étude précédente menée par les mêmes auteurs avec un protocole similaire, l'augmentation de la MnW a été associée à des comportements négatifs en classe après un ajustement en fonction des facteurs de confusion (arsenic, sexe, indice de masse corporelle, scolarité de la mère, circonférence des bras) (Khan et coll., 2011). Les conclusions de ces deux études peuvent être confondues par le fait que l'exposition possible à d'autres substances neurotoxiques n'a pas été prise en compte (p. ex. l'ajustement pour l'exposition à l'arsenic et au plomb est incomplet), que la caractérisation de l'exposition n'est pas exhaustive (absence de prise en compte des autres sources de manganèse, comme l'air et les poussières), que les résultats sont très variables (large IC à 95 %) et qu'il existe un risque lié à la partialité de l'enseignant.
Une étude prospective menée auprès d'une vaste cohorte de mères et de leurs enfants dans des régions rurales du Bangladesh a porté sur une période d'exposition au manganèse dans l'eau potable allant de la grossesse à dix ans (Rahman et coll., 2017). Les capacités cognitives et le comportement de 1 265 enfants âgés de un an ont été respectivement évalués au moyen du WISC-IV et du Questionnaire sur les forces et les difficultés. Les concentrations médianes correspondant à l'exposition au manganèse dans l'eau potable étaient de 0,2 mg/L durant la grossesse et de 0,34 mg/L à dix ans. Les auteurs ont constaté que l'exposition au manganèse en début de vie semblait nuire au comportement des enfants, en augmentant le risque de troubles de comportement, surtout chez les garçons. Toutefois, une exposition prénatale élevée au manganèse a été positivement corrélée aux capacités cognitives chez les filles, tandis qu'aucun effet n'a été observé chez les garçons. À l'instar des nombreuses études résumées ci-dessus, cette étude comporte certaines limites. Pour étudier les effets neurologiques, elle utilise notamment un test non validé ni uniformisé pour la population à l'étude. L'étude ne fournit pas non plus d'estimations précises des expositions (aucun biomarqueur d'exposition n'a été utilisé pour le manganèse, l'âge auquel les nourrissons ont consommé pour la première fois de l'eau potable variait vraisemblablement et il n'y avait pas assez d'échantillons provenant des écoles des enfants).
L'association entre les concentrations de manganèse dans le sang ombilical et les sous-échelles de psychomotricité a été évaluée dans le cadre d'une étude de cohortes réalisée à Paris auprès de personnes favorisées sur le plan social (n = 247 femmes enceintes et leurs enfants) (Takser et coll., 2003). Les enfants ont été évalués au moyen de trois tests psychologiques (à 9 mois, à 3 ans et à 6 ans). L'attention, la mémoire non verbale et les aptitudes manuelles ont été associées négativement à l'exposition au manganèse, après ajustement pour tenir compte des facteurs de confusion (sexe de l'enfant, niveau de scolarité de la mère). L'étude n'a toutefois révélé aucun lien entre l'exposition au manganèse à la naissance et les indices psychomoteurs généraux, le quotient de développement à 9 mois sur l'échelle de Brunet–Lézine ou l'indice de cognition générale (ICG) de McCarthy à 3 et à 6 ans. La contribution de l'exposition au manganèse par l'eau potable n'était pas claire. Les auteurs n'ont fait mention d'aucune méthode pour prendre en compte la corrélation intra-individuelle (mesures prises plusieurs fois sur la même personne au fil du temps) dans l'analyse statistique, ce qui augmente le risque d'erreurs de type I. Bien que les auteurs aient précisé avoir ajusté tous les modèles de régression pour tenir compte des concentrations de plomb dans le sang maternel et ombilical, ils ont utilisé différents ensembles de covariables sans indiquer clairement lesquels ils ont choisis pour chaque modèle.
Une étude de cohortes longitudinale et multicentrique réalisée à Shanghaï, en Chine, a examiné les effets d'une exposition prénatale aux taux de manganèse présent dans l'environnement, en étudiant les concentrations de manganèse dans le sérum ombilical (MnUmbi) et en effectuant une évaluation comportementale et neurologique des nouveaux-nés (test NBNA), c'est-à-dire des évaluations comportementales et neurologiques des nouveau-nés (Yu et coll., 2014). Les auteurs ont examiné 933 couples mère-enfant en mesurant la MnUmbi et en évaluant le développement comportemental des nouveau-nés (réflexes, capacités fonctionnelles et état comportemental) à l'aide du test NBNA. Les résultats montrent que le fait d'être dans le quartile supérieur pour la MnUmbi est associé à une note plus faible au test NBNA (signification statistique du coefficient de régression) après ajustement en fonction des facteurs de confusion (âge, scolarité, revenu, emploi et tabagisme des parents; âge gestationnel; sexe, poids à la naissance, taux de plomb et de mercure). Toutefois, le faible taux de participation (70 % des sujets recrutés) pourrait avoir entraîné un biais de sélection. Aucune analyse du taux de manganèse dans le sérum maternel n'a été effectuée pendant la grossesse pour déterminer s'il pourrait y avoir une relation avec le développement intra-utérin. Aucun suivi à long terme n'a été effectué pour évaluer les effets sur le développement des enfants. Aucun ajustement n'a été effectué pour tenir compte de facteurs de confusion importants tels que d'autres sources d'exposition, des facteurs de risques environnementaux et une exposition aux métaux. De plus, le risque d'effet de confusion résiduel est grand en raison des importantes différences de statut socioéconomique entre les groupes d'exposition. Les auteurs n'ont pas expliqué la signification clinique des changements (l'importance d'une diminution de 1,1 du coefficient de régression), et on ne sait pas exactement pourquoi ils ont décrit la relation comme étant non linéaire, puisqu'aucun effet dose-réponse clair n'était observé. Les covariables considérées étaient plus probablement colinéaires (p. ex. scolarité et emploi de la mère), mais les auteurs n'ont pas justifié l'inclusion de ces covariables dans le modèle.
L'association entre l'exposition aux contaminants environnementaux et le neurodéveloppement à l'âge de deux ans a été examinée dans le cadre de l'étude intitulée Taiwan Birth Panel Study (n = 230 couples formés de mères non fumeuses et de leurs enfants) (Lin et coll., 2013). L'étude a trouvé que l'exposition in utero à des concentrations de manganèse supérieures au 75e percentile (c.-à-d. 59,3 µg/L) dans le sang ombilical était associée aux faibles quotients cognitifs et langagiers obtenus à l'inventaire CDIIT (Comprehensive Developmental Inventory for Infants and Toddlers) comparativement aux concentrations inférieures au 75e percentile (signification statistique du coefficient de régression), après ajustement en fonction de l'âge maternel, du sexe, du tabagisme, du soutien et de la stimulation offerts à la maison, et des taux d'arsenic et de mercure dans le sang ombilical. Les quotients globaux, moteurs, sociaux et d'autonomie n'ont pas été associés au modèle. Aucune explication n'a été donnée pour justifier l'inclusion de moins de 50 % des participants sélectionnés, qui se distinguaient de la population générale par un niveau de scolarité de la mère plus élevé, des taux de mercure et de plomb dans le sang ombilical plus élevés, et un plus grand poids à la naissance. De plus, les auteurs n'ont effectué qu'une seule mesure des contaminants (plomb, mercure, manganèse, arsenic). Enfin, l'étude était axée sur les effets d'une co-exposition et les auteurs n'ont pas indiqué s'ils avaient fait des ajustements en fonction du plomb dans le modèle pour le manganèse.
Sahni et coll. (2007) et Brna et coll. (2011) ont présenté des études de cas portant sur deux fillettes (six et dix ans) qui buvaient de l'eau de puits contenant des concentrations élevées de manganèse (jusqu'à 2,4 mg/L dans les deux cas). Des taux sériques élevés de manganèse et des symptômes neurologiques, tels que le pica, des changements de comportement, des troubles d'élocution, un manque de coordination, des difficultés à marcher et un retrait social, ont été observés chez les deux fillettes. Dans les deux cas, les autres membres de la famille ne présentaient aucun symptôme. Les auteurs ont avancé qu'un trouble métabolique lié aux métaux divalents pourrait être associé à l'apparition des symptômes.
Une autre étude de cas portait sur un garçon de dix ans du Massachusetts ayant bu pendant cinq ans de l'eau de puits turbide contenant du manganèse à une concentration de 1 210 µg/L (Woolf et coll., 2002). L'enfant ne présentait aucun trouble cognitif ou neurologique, et sa motricité fine, son équilibre, son rendement scolaire, son QI et les résultats de l'examen d'imagerie par résonance magnétique étaient normaux. Toutefois, son rendement se situait sous la moyenne pour l'indice de mémoire général (17e percentile), la mémoire verbale (19e percentile), la mémoire visuelle (14e percentile) et l'indice d'apprentissage (19e percentile). Ses enseignants ont remarqué qu'il manquait de concentration en classe. La causalité est incertaine, parce que l'eau bue par le garçon avait une forte teneur en fer (1 570 µg/L) et que les déchets toxiques constituaient une source de préoccupation pour les résidents du quartier fortement industrialisé où il habitait. Un seul échantillon d'eau a été recueilli à la fin de la période d'exposition de cinq ans.
Plusieurs études transversales (Zota et coll., 2009; Chen et coll., 2014; Eum et coll., 2014; Guan et coll., 2014) ainsi qu'une étude de cohortes (Yu et coll., 2013) ont examiné l'association entre l'exposition au manganèse et le poids corporel à la naissance. Seules quelques-unes de ces études (études transversales menées en Asie) ont observé un lien entre l'exposition au manganèse et un faible poids corporel. Toutes les études ayant mis en lumière une association positive présentaient plusieurs limites, notamment une conception ne permettant pas de déterminer la temporalité (direction de l'effet), un biais de sélection et l'absence d'ajustement pour tenir compte des covariables importantes, ce qui limite l'établissement d'un lien causal entre le manganèse et les effets observés sur la santé.
Les autres études, en revanche, n'ont relevé aucune association entre une forte exposition environnementale au manganèse et quelconques effets neurologiques (Vieregge et coll., 1995; Torrente et coll., 2005a; Hernandez-Bonilla et coll., 2011). L'étude exploratoire de Torrente et coll. (2005a) n'a révélé aucune corrélation entre la concentration de différents éléments dans les cheveux (taux moyen de manganèse : 0,18 à 0,26 µg/g) et l'état cognitif d'enfants âgés de 12 à 14 ans (n ± 100) habitant à proximité de zones industrielles de la Catalogne, en Espagne. L'étude transversale de Vieregge et coll. (1995) n'a relevé aucune différence de résultats, relatifs aux affections neurologiques et à la maladie de Parkinson, entre deux cohortes composées d'adultes de plus de 40 ans (homogènes sur le plan de l'âge [âge moyen de 57 ans], du sexe, de la nutrition et des médicaments) exposés pendant au moins dix ans à différents taux de manganèse dans l'eau potable provenant de puits dans une région rurale de l'Allemagne (groupe A : taux de manganèse < 50 µg/L, n= 74; groupe B : taux de manganèse > 300 µg/L, n = 41). Les taux de manganèse dans le sang n'étaient pas statistiquement différents entre les deux groupes. Dans leur étude transversale, Hernandez-Bonilla et coll. (2011) n'ont observé aucune différence significative de résultats neuromoteurs entre des enfants de sept et onze ans habitant dans des collectivités rurales et présentant des taux faibles ou élevés de biomarqueurs de l'exposition au manganèse (sang : 9,7 comparativement à 8,2 µg/L; cheveux : 12 comparativement à 0,57 µg/g) après neutralisation des covariables (taux de plomb dans le sang, taux de mercure, sexe, âge, scolarité de la mère), à l'exception d'une faible association entre le test de tapotement des doigts et le taux de manganèse dans le sang. Dans l'ensemble, les résultats ont révélé l'absence d'une association et n'ont pas été interprétés du point de vue des risques par les auteurs. L'association marginale avec la capacité de tapoter des doigts n'est pas concluante, car les auteurs n'ont pas neutralisé les autres covariables (tabagisme des parents; différences du point de vue de la nutrition; présence de 13 enfants ayant un surpoids dans le groupe ayant une faible exposition comparativement à un seul dans le groupe ayant une forte exposition, possiblement un indicateur d'autres facteurs socioéconomiques). En outre, les expositions antérieures n'ont pas été évaluées. Les conclusions tirées de ces trois études n'indiquant aucun effet sont limitées, en raison du modèle d'étude utilisé (étude transversale), de la possibilité que seuls les sujets en santé sont demeurés dans les zones où la concentration en manganèse était élevée (effet du malade survivant), de l'existence éventuelle d'autres sources d'exposition ou de variations antérieures non répertoriées, et du fait que des covariables importantes (p. ex. l'état nutritionnel) n'ont pas été neutralisées.
Bien que le manganèse soit essentiel à la santé humaine, plusieurs rapports de cas, études transversales et études de cohortes corroborent l'existence d'une association entre l'exposition à des taux élevés de manganèse dans l'eau potable et divers problèmes neuropsychologiques observés chez les nourrissons et les enfants, tels qu'un changement de comportement, un QI plus faible, des troubles du langage et de la mémoire, ainsi qu'un manque de coordination et de contrôle des mouvements. Des études transversales et des études de rapports de cas ont fait état de liens entre divers effets neuropsychologiques et des concentrations élevées de manganèse (centaines de µg/L) dans l'eau potable, tandis que des études de cohortes ont démontré de telles associations avec les taux prénataux, révélés par les concentrations de manganèse dans le sang ombilical. La plupart des études n'ont pas permis de déterminer la temporalité (c.-à-d. que l'effet survient après la cause) de l'association. Le risque d'établir de fausses associations a été jugé élevé, et les mesures de l'exposition étaient généralement rudimentaires et reposaient sur une seule mesure prise sur un seul échantillon. Une meilleure compréhension du mode d'action neurotoxique du manganèse permettrait d'identifier des biomarqueurs neurologiques précis des effets et de mesurer les premiers signes de toxicité.
Des cas de manganisme subséquents à l'inhalation de manganèse en milieu de travail ont été observés. Toutefois, on ne sait pas si cet effet peut être extrapolé à l'exposition par voie orale, car il existe des différences toxicocinétiques majeures entre l'absorption par inhalation et l'absorption par voie orale, et la sensibilité des personnes varie également entre la période de développement et l'âge adulte. Afin de pouvoir effectuer une analyse dose-réponse pour les effets examinés, il faudrait disposer de mesures d'exposition plus fiables qui permettraient d'établir un point de départ précis, sur le plan toxicologique, pour les effets neurologiques. Il convient toutefois de noter que les études épidémiologiques appuient, sur le plan qualitatif, l'utilisation des effets neurotoxiques comme un effet critique possible.
10.0 Effets sur la santé des animaux de laboratoire
Le manganèse est facilement absorbé dans le système nerveux central (SNC), mais son absorption dans de nombreux autres tissus comme les poumons, les reins et les testicules a également été décrite. Plusieurs études réalisées sur des modèles animaux ont démontré qu'après une exposition au manganèse par voie orale, le SNC est la principale cible de la toxicité, suivi de l'appareil reproducteur. Les sections qui suivent présentent des données toxicologiques relatives à une exposition à des sels de manganèse solubles par voie orale.
Il est important de noter que les études menées avec des sels de manganèse auprès d'animaux de laboratoire ne précisent souvent pas clairement si la dose indiquée fait référence à du manganèse ou à un complexe du manganèse (p. ex. MnCl2, MnCl2·4H2O). Santé Canada a donc exprimé la dose dans les mêmes mots que ceux utilisés par les auteurs de ces études. Lorsque cela était possible, Santé Canada a communiqué avec les auteurs des études considérées comme étant possiblement essentielles à l'évaluation, afin de confirmer que les doses avaient été correctement interprétées. Dans l'ensemble, les doses indiquées dans la majorité des études faisaient référence au manganèse ionique.
10.1 Toxicité aiguë
Le taux de létalité aiguë du manganèse par voie orale varie selon l'espèce chimique et la voie d'exposition (gavage ou voie alimentaire). Les composés de manganèse semblent présenter une plus faible toxicité aiguë lorsqu'ils sont donnés dans les aliments que lorsqu'ils sont administrés par gavage (Finley et Johnson, 1996; U.S. EPA, 2003; Santé Canada, 2010). Les doses létales moyennes (DL50), pour la voie orale, variaient approximativement entre 250 mg Mn/kg p.c. (sous forme de chlorure de manganèse) et 1 082 mg Mn/kg p.c. (sous forme d'acétate de manganèse) pour des rats adultes exposés par gavage (Hazaradze, 1961; Smyth et coll., 1969; Kostial et coll., 1989; OMS, 2011). En comparaison, une exposition répétée à une dose similaire de manganèse (50 000 ppm) sous forme de sulfate de manganèse ajoutée aux aliments n'a entraîné aucun décès de rats ayant subi cette exposition pendant 14 jours (NTP, 1993).
Un certain nombre d'effets neurologiques ont été constatés chez des rats ayant été exposés par gavage à une seule dose de MnCl2 aqueux (50 mg/kg MnCl2·H2O). Ces effets étaient notamment une diminution importante et réversible de l'activité générale, un retard dans l'acquisition de réactions d'évitement en réponse à des stimulus conditionnés et non conditionnés, une augmentation de la période de latence des réflexes conditionnés, et une dégradation temporaire du processus d'apprentissage (Shukakidze et coll., 2003).
10.2 Exposition à court terme et exposition chronique
10.2.1 Neurotoxicité
La neurotoxicité est considérée dans plusieurs études comme un effet particulièrement sensible après une exposition au manganèse. Les effets neurotoxiques causés par une exposition au manganèse peuvent être classés selon qu'ils touchent des paramètres comportementaux (altération des réflexes, de l'activité motrice, de l'apprentissage, de la mémoire ou des sens), des paramètres structuraux (gliose, neuroinflammation, altérations neurostructurales) ou des paramètres neurochimiques (altération des systèmes de neurotransmetteurs). La présente section traite des effets neurotoxiques résultant d'une exposition au manganèse pendant le développement et à l'âge adulte.
10.2.1.1 Effets neurocomportementaux chez les nouveau-nés et les jeunes
Des effets neurocomportementaux ont été observés chez des rats et des souris (petits ou nouveau-nés) ayant été exposés au manganèse pendant les périodes de gestation ou de lactation, ou de façon directe après le sevrage (alimentation, eau potable ou gavage). Des effets neurocomportementaux ont également été observés chez des primates non humains exposés au manganèse par l'intermédiaire de préparations pour nourrissons.
Des souris exposées au manganèse par le lait maternel du JPN 2 au JPN 24 (mères exposées à 5 mg Mn/mL [dose équivalant à 5 000 ppm Mn] dans l'eau potable) et par l'eau potable du JPN 25 au JPN 180 (3 µg/mL ou 3 ppm Mn dans l'eau potable) ont fait preuve d'une augmentation passagère de leur activité motrice. La dose d'exposition réelle des mères (en mg/kg p.c.) n'est pas précisée, et celle des petits pendant la période de lactation n'est pas connue. L'activité locomotrice (mesurée à des intervalles de 30 jours) était accrue aux JPN 60 et 90 seulement, et non aux JPN 30, 120, 150 ou 180 (Chandra et coll., 1979a). Des doses plus fortes de manganèse ont entraîné des effets sur les mouvements des souris dans une étude sur trois générations murines : deux nouveau-nés de la portée de la troisième génération exposée à 25 mg Mn/kg p.c. par jour (Ishizuka et coll., 1991) ont fait preuve d'une démarche anormale. De même, une augmentation de l'activité motrice spontanée a été observée chez des rats nouveau-nés exposés par voie orale (per os) pendant 50 jours (du JPN 1 au JPN 49) à la dose d'essai la plus élevée (50 mg MnCl2/kg p.c. par jour) d'une solution aqueuse de chlorure de manganèse (Brenneman et coll., 1999). Une dose d'exposition journalière de 25 mg MnCl2/kg p.c n'a entraîné aucun effet observé.
Des troubles ont été observés lors de tests en espace ouvert (évaluation du comportement et locomotion) chez des souris mâles exposées quotidiennement durant deux semaines, par gavage, à 10 ou à 30 mg Mn/kg p.c. de chlorure de manganèse dans une solution saline, pendant la période juvénile uniquement ou pendant la période juvénile (JPN 20 à JPN 34) et la période adulte (SPN 12 à SPN 20). L'étude a révélé que les souris en développement étaient plus sensibles aux effets du Mn, et qu'une exposition en début de vie augmentait la sensibilité au manganèse à l'âge adulte. Aucun effet n'a été observé chez les souris femelles (Moreno et coll., 2009b). Une NOAEL de 250 µg Mn/jour a été établie après l'administration de manganèse dans une solution de sucrose à 10 % par micropipette (LOAEL : 750 µg Mn/jour), pour les effets sur le comportement neurologique (résultats aux épreuves de géotaxie négative et de distance parcourue pour des rats provoqués avec de la cocaïne). Les rats étaient exposés pendant 21 jours (du JPN 1 au JPN 21; Reichel et coll., 2006).
L'exposition au manganèse entraîne divers effets sensoriels chez les jeunes animaux. Les effets sur l'orientation ont été évalués par le réflexe de redressement en situation de chute chez des rats ayant été exposés in utero et par le lait maternel (du JG 10 au JPN 21), dont la mère avait reçu une dose de 32, 160 ou 800 ppm MnCl2•4H2O par voie alimentaire. Les petits mâles exposés à une dose maternelle de manganèse ≥ 160 ppm et les petits femelles exposés à une dose maternelle de manganèse de 800 ppm faisaient preuve d'une importante diminution du réflexe de redressement en situation de chute (Ohishi et coll., 2012).
Des rats exposés quotidiennement par voie orale, du JPN 1 au JPN 20, à 500 µg Mn (MnCl2 dans une solution de sucrose à 10 %) ont montré une diminution de la perception des odeurs. Les résultats au test du fouisseur et au tests d'évitement passif semblent également indiquer une diminution de la mémoire et de la capacité d'apprentissage (Tran et coll., 2002a; Tran et coll., 2002b). Des rats nouveau-nés exposés quotidiennement par voie orale pendant 21 jours (du JPN 1 au JPN 21) à 25 ou à 50 mg MnCl2/kg p.c. (administré par micropipette sous forme de MnCl2.4H2O) ont présenté une réaction de sursaut prononcée à des stimulus acoustiques sous forme d'impulsions (on présume que la dose indiquée par les auteurs fait référence au Mn) (Dorman et coll., 2000).
Les effets neurocomportementaux résultant d'un excès de manganèse dans les préparations pour nourrissons à base de soja ont été évalués dans le cadre d'une étude menée auprès de bébés singes rhésus nourris pendant quatre mois après leur naissance avec une préparation commerciale à base de lait de vache (50 μg Mn/L), une préparation commerciale à base de protéines de soja (300 μg Mn/L) ou une préparation à base de soja enrichie en manganèse (1 000 μg Mn/L) (Golub et coll., 2005). Les doses journalières correspondantes indiquées par les auteurs étaient respectivement de 0,018, 0,106 et 0,323 mg Mn/kg p.c. (notées dans un erratum : Golub, 2012). Les auteurs ont effectué un ensemble complet de tests comportementaux (dimensions motrice, cognitive et sociale, et tests visant spécialement le système de dopamine)Note de bas de page 3 sur une période de 18 mois (ce qui équivaut à environ l'âge de six ans chez les humains). Il est important de noter qu'en plus de ne pas contenir la même quantité de manganèse, les préparations à base de lait de vache et celles à base de soja différaient à d'autres égards sur le plan nutritionnel, notamment en ce qui concerne les taux de protéines, de glucides, de matières grasses et d'autres composants susceptibles de contribuer aux différences de réponses comportementales observées (Golub et coll., 2005). Ainsi, le groupe nourri avec la préparation à base de lait de vache ne constitue pas un témoin adéquat pour évaluer l'effet du manganèse dans le groupe nourri avec la préparation à base de soja ou dans le groupe nourri avec la préparation de soja enrichie en manganèse, dans le cadre d'une évaluation quantitative des risques. La comparaison du groupe nourri avec la préparation à base de soja enrichie en manganèse et du groupe nourri avec la préparation à base de soja seul permettrait de mieux évaluer l'effet du manganèse; toutefois, aucune analyse statistique permettant de comparer ces deux groupes n'a été fournie. Néanmoins, des modifications du cycle activité/sommeil et des interactions sociales (moins de jeu et tendance accrue à s'accrocher à l'autre dans les interactions sociales dyadiques) ont été observées chez les singes des deux groupes nourris avec une préparation à base de soja, comparativement à ceux du groupe nourri avec la préparation à base de lait de vache. Les deux groupes nourris avec une préparation à base de soja ont également présenté des cycles de veille plus courts et des périodes d'inactivité diurnes plus brèves que le groupe nourri avec une préparation à base de lait de vache. Toutefois, aucune différence apparente n'a été relevée entre les deux groupes nourris avec une préparation à base de soja (soja seul ou soja + Mn; analyse statistique non disponible). Les trois groupes ne faisaient preuve d'aucune différence importante en ce qui concerne la concentration des métabolites de la dopamine et de la sérotonine (acide homovanillique [HVA] et acide 5-hydroxy-indolacétique [5HIAA]) dans le LCR, la stéréotypie et les tests de rendement continu. Cette étude pourrait indiquer l'existence d'une sensibilité des comportements sociaux et des systèmes de la dopamine à une exposition au manganèse par voie alimentaire en début de la vie. Il faut toutefois souligner que les différences nutritionnelles entre les préparations à base de lait de vache et les préparations à base de soja pourraient contribuer aux variations de réactions comportementales. Dans l'ensemble, les résultats n'ont révélé aucune différence entre les groupes dans les situations d'essai les plus structuréesNote de bas de page 4 utilisées pour évaluer des fonctions cognitives précises telles que l'apprentissage, la mémoire et l'attention. Cependant, les auteurs ont noté que les nourrissons participaient peu aux tests formels visant les fonctions cognitives, aux âges testés; la réalisation d'autres tests à un âge plus avancé pourrait permettre d'en apprendre davantage (Golub et coll., 2005; Golub, 2012).
McDougall et coll. (2008) ont étudié les effets d'une exposition postnatale au manganèse sur les comportements associatifs et non associatifs de rats nouveau-nés auxquels on a donné des suppléments de manganèse par voie orale (750 μg/jour) du JPN 1 au JPN 21 (voir également la section sur les effets neurochimiques pour connaître les résultats relatifs à la fonction présynaptique de la dopamine). Les effets d'une exposition postnatale au manganèse sur le fonctionnement du système nigro-strié ont été évalués au moyen d'un test de la tige tournante et par l'induction d'une stéréotypie par amphétamine à l'âge adulte. Les auteurs ont trouvé que le manganèse n'avait aucun effet sur la performance au test de la tige tournante, mais que les rats exposés au manganèse faisaient preuve de stéréotypies induites par amphétamine beaucoup plus importantes que les rats témoins. En ce qui concerne les processus associatifs, l'exposition au manganèse n'a altéré la performance des rats dans aucun des aspects du test de préférence de place conditionnée à la cocaïne (préférence, extinction ou réinstallation), et n'a eu aucun effet sur les réponses lors des séances de ratio progressif (réponse opérante renforcée avec du sucrose, une mesure de la motivation). Dans le régime de ratio fixe, toutefois, l'acquisition du comportement s'est révélée déficiente, ce qui indique un éventuel déficit dans l'apprentissage procédural.
Des rats nouveau-nés ayant reçu de plus fortes doses de manganèse par voie orale (dose minimale estimée à 8,8 mg Mn/kg p.c. par jour [à partir de 500 µg/jour]) ont montré d'autres troubles du comportement, notamment une diminution des perceptions olfactives (Tran et coll., 2002a). En outre, à des doses ≥ 25 mg/kg p.c. par jour, on a observé des effets neurocomportementaux reflétant une anxiété accrue et des troubles d'autres comportements émotionnels, une diminution des capacités d'apprentissage et de mémorisation, une augmentation des signes d'hypoactivité ou d'hyperactivité, et une baisse de l'activité motrice (Kristensson et coll., 1986; Pappas et coll., 1997; Brenneman et coll., 1999; Liu et coll., 2006; McDougall et coll., 2008; Kern et coll., 2010; Kern et Smith, 2011; Molina et coll., 2011; Nowak et coll., 2011; Peneder et coll., 2011; Betharia et Maher, 2012; Ohishi et coll., 2012; Beaudin et coll., 2013).
Kern et coll. (2010) ont présenté une évaluation détaillée des effets neurodéveloppementaux d'une exposition au manganèse chez les rats. Les auteurs ont exposé des nouveau-nés Sprague-Dawley à des doses journalières de 25 ou de 50 mg Mn/kg p.c. (solution de sucrose administrée par voie orale à l'aide d'une micropipette) pendant 21 jours après leur naissance. Ils ont soumis les rats (15 à 20 mâles/traitement) à une batterie de tests neurologiques (espace ouvert, labyrinthe en croix surélevé, labyrinthe radial à huit branches) afin d'évaluer les effets d'une exposition au manganèse par voie orale pendant une période correspondant au développement des voies dopaminergiques dans les parties du cerveau qui sont importantes pour la régulation des comportements liés aux fonctions exécutives (qui font appel à l'attention, à l'apprentissage et à la mémoire). En plus d'effectuer des tests comportementaux, les auteurs ont également mesuré le taux de récepteurs et de transporteurs de la dopamine dans le cerveau (décrits dans la présente section sous « effets neurochimiques »). Les résultats de cette étude ont permis d'établir une LOAEL de 25 mg Mn/kg p.c. par jour, d'après l'ampleur des stéréotypies observées pendant un nombre accru de jours de séances au cours des tests du labyrinthe radial à huit branches (modification du comportement orienté vers un but, indicatrice d'une mémoire spatiale déficiente) et la diminution du taux de récepteurs de type D1 dans le striatum dorsal. Les résultats n'ont pas permis de définir une NOAEL. À la dose d'essai la plus forte (50 mg Mn/kg p.c. par jour), les auteurs ont également observé des troubles de l'activité locomotrice et une désinhibition des comportements au cours du test en espace ouvert au JPN 23, une altération de l'apprentissage et un nombre accru d'erreurs dans le labyrinthe radial au JPN 23, et des difficultés d'apprentissage et de mémorisation (retard/échec dans l'atteinte du critère relatif à l'apprentissage et nombre accru d'erreurs dans le test du labyrinthe radial à huit branches) du JPN 33 au JPN 46. D'après les résultats au test du labyrinthe en croix surélevé, l'exposition au manganèse (jusqu'à une dose de 50 mg Mn/kg p.c. par jour) n'a pas eu d'effet apparent sur la peur ou l'anxiété (Kern et coll., 2010).
Une étude subséquente visait à établir si une exposition au manganèse tôt dans la vie entraîne des effets neurocomportementaux et neurochimiques qui persistent jusqu'à l'âge adulte. Dans cette étude, les auteurs ont exposé des rats à des doses orales de manganèse identiques à celles de l'étude précédente, pendant les 21 jours suivant leur naissance et sans autre exposition, puis les ont examinés plus tard au cours de leur vie. Les résultats obtenus ont révélé que l'exposition néonatale au manganèse provoquait une modification des taux de récepteurs de la dopamine ainsi qu'une astrogliose (indiquée par la protéine acide fibrillaire gliale [GFAP]) à l'âge adulte. Bien que les auteurs n'aient observé aucune désinhibition comportementale ni trouble de l'activité motrice chez les adultes, une évaluation du rendement comportemental (mesuré par l'activité dans la zone centrale de l'espace ouvert) réalisée sans (JPN 97) et avec (JPN 98) provocation par D-amphétamine a révélé que les animaux exposés présentaient une réponse locomotrice accrue avec la provocation par D-amphétamine (Kern et Smith, 2011). L'ensemble de ces résultats indique qu'une exposition au manganèse en début de vie pourrait avoir des effets de longue durée sur le système dopaminergique.
Beaudin et coll. (2013) ont utilisé le même modèle (nouveau-nés) et le même régime d'administration des doses pour explorer davantage les effets chroniques de l'exposition au manganèse sur le développement sensori-moteur. Dans cette étude, les auteurs ont comparé les effets d'une exposition au manganèse en début de vie et ceux d'une exposition pendant la vie entière sur la fonction sensori-motrice fine de rats Long-Evans mâles. Le test de l'escalier a servi à mesurer objectivement les effets sur la motricité qui sont pertinents pour les effets moteurs étudiés en recherche pédiatrique. Les auteurs ont exposé les animaux (n = 11/groupe) à une dose orale quotidienne de 25 mg Mn/kg p.c. ou de 50 mg Mn/kg p.c., soit pendant une courte période postnatale de 21 jours, soit pendant toute leur vie (même à l'âge adulte). Les tests menés à l'âge adulte ont révélé un déficit de rendement (test de l'escalier, capacité à saisir et à manger les granules) à la dose de 25 mg Mn/kg p.c. par jour, et le rendement était pire pour les rats ayant subi l'exposition toute leur vie que pour ceux ayant été exposés pendant une courte période de 21 jours après leur naissance. Ces résultats corroborent ceux des études épidémiologiques ayant fait état d'un déficit de la fonction sensori-motrice fine chez des enfants exposés au manganèse (Beaudin et coll., 2013; Zoni et Lucchini, 2013).
On a également constaté que l'exposition postnatale précoce de rats au manganèse entraînait des déficits sur le plan de l'attention et de la maîtrise des impulsions, qui subsistent à l'âge adulte (Beaudin et coll., 2016). Les auteurs ont exposé 115 rats mâles Long-Evans nouveau-nés à une dose orale de 0, 25 ou 50 mg Mn/kg/jour, du JPN 1 au JPN 21 ou du JPN 1 jusqu'à la fin de l'étude (~JPN 192). Le manganèse était administré au moyen d'une micropipette pour la période JPN 1-JPN 21, et dans l'eau potable après le sevrage (JPN 22) (il est à noter que les concentrations de manganèse dans l'eau ont été ajustées pour assurer des niveaux d'exposition adéquats). Les auteurs ont fait appel à une tâche de temps de réaction en série à cinq choix pour évaluer l'apprentissage et l'attention des animaux. Ils ont constaté que l'exposition au manganèse durant le développement avait entraîné une atteinte durable de la régulation de l'attention et de la stimulation, et que certains déficits d'attention observés chez les adultes dépendaient de la dose et de la durée de l'exposition prénatale au manganèse de façon « non monotone ».
10.2.1.2 Effets neurocomportementaux observés chez les adultes
Plusieurs études font état d'altérations du comportement neurologique consécutives à une exposition au manganèse à l'âge adulte. Des rats exposés au manganèse par l'eau potable (1 mg MnCl2•4H2O/mL) ont montré des signes d'hyperactivité et d'hypoactivité, tels qu'une augmentation ou une réduction de l'activité motrice spontanée, une altération de la réponse au test de provocation par D-amphétamine, une diminution de la distance parcourue, et une baisse de l'activité dans l'espace ouvert (Nachtman et coll., 1986).
Des rats femelles albinos matures ayant reçu du chlorure de manganèse par gavage (0,357 et 0,714 mg Mn/kg p.c. par jour, dans l'eau distillée) pendant 15 ou 30 jours ont présenté une augmentation des taux de manganèse et de cholestérol dans le cerveau (hippocampe, cervelet et cortex) accompagnée de difficultés d'apprentissage aux deux doses (après une période d'entraînement au jour 29, les rats exposés mettaient 3,7 fois plus de temps que les rats témoins pour atteindre la sortie d'un labyrinthe en T). Le retard manifesté par les rats exposés a été entièrement corrigé par une administration simultanée de mevinolin (un inhibiteur de la biosynthèse du cholestérol) avec le manganèse ou par la suppression du manganèse (Öner et Sentürk, 1995; Sentürk et Öner, 1996).
L'acquisition de réactions d'évitement conditionnées et non conditionnées, ainsi que la dynamique des difficultés d'apprentissage et de mémorisation, ont été étudiées chez des rats adultes exposés à du manganèse avant ou après l'apprentissage d'un labyrinthe à voies multiples. Pendant 30 jours, les rats ont reçu du chlorure de manganèse (doses de 20 ou de 50 mg MnCl2•4H2O/kg) dans leurs aliments. Des tests ont été effectués immédiatement ou 90 jours après l'apprentissage. Les animaux exposés à la dose la plus forte étaient plus agressifs, tombaient souvent de la plateforme et ont échoué aux tests en labyrinthe. Une dégradation irréversible du processus d'apprentissage a été observée après une exposition au manganèse. Toutefois, aux deux doses, le manganèse n'a pas modifié de façon importante la capacité des animaux à reproduire un comportement acquis antérieurement (réussir à traverser le labyrinthe), mais a plutôt ralentit leur mouvement à travers le labyrinthe (Shukakidze et coll., 2003).
Des jeunes rats Wistar adultes (16 animaux/dose) ont été exposés à du chlorure de manganèse par gavage (14,84 ou 59,36 mg MnCl2•4H2O/kg p.c. par jour, cinq jours par semaine, dans l'eau distillée) pendant dix semaines, puis soumis à une période de récupération de 12 semaines. Les deux doses étaient associées à une diminution statistiquement significative du rendement relatif à la mémoire spatiale à court et à long terme au cours du test du labyrinthe à huit branches, ainsi que de l'activité locomotrice spontanée durant le test en espace ouvert. Sept semaines après la fin de l'exposition, l'activité motrice est redevenue normale. Une diminution du nombre de réactions de sursaut aux stimuli acoustiques et de l'inhibition avant l'impulsion qui y est associée a été observée. Une augmentation du temps de latence et une diminution de la durée des potentiels évoqués sensoriels ont été observées aux deux doses après les 10 semaines d'exposition, et ont persisté pendant la période de récupération uniquement chez les rats ayant reçu la dose élevée. Une densité accrue de la protéine acide fibrillaire gliale immunoréactive (GFAP-IR) a été observée aux deux doses dans le gyrus denté de l'hippocampe, mais pas dans la couche radiée ni le stratum oriens (Vezer et coll., 2005). Dans une étude antérieure portant sur les effets du manganèse sur l'activité motrice, des rats exposés de façon chronique au manganèse dans l'eau potable (1 mg MnCl2•4H2O/mL) ont présenté des signes d'hyperactivité et d'hypoactivité, tels qu'une augmentation (à partir des semaines 5 à 7) ou une baisse (à partir de la semaine 8) de l'activité motrice spontanée, une modification de la réponse au test de provocation par D-amphétamine (réponse accrue de la semaine 14 à 29, disparaissant aux semaines 41 et 65), une diminution de la distance parcourue, et une diminution de l'activité au cours des tests en espace ouvert (Nachtman et coll., 1986).
Des troubles de l'apprentissage spatial ont été observés chez des rats femelles Sprague-Dawley gravides soumises au test de la piscine de Morris après avoir reçu pendant 43 semaines une alimentation pauvre en fer (3 mg Fe/kg) et enrichie en manganèse (100 mg Mn/kg), comparativement à des rats femelles gravides soumises à un régime témoin (35 mg Fe/kg, 10 mg Mn/kg) (Fitsanakis et coll., 2009). Dans cette étude, l'exposition au manganèse par voie alimentaire a révélé qu'une carence en fer (particulièrement fréquente pendant la gestation) peut accroître les effets du manganèse sur le système cognitif (Fitsanakis et coll., 2009).
Des rats mâles adultes exposés pendant huit mois à 0,1 ou à 5,0 mg Mn/mL sous forme de chlorure de manganèse dans l'eau potable ont fait preuve d'une augmentation de l'activité motrice spontanée (mesurée de façon hebdomadaire pendant 60 sessions de une minute chacune) pendant le premier mois d'exposition (Bonilla, 1984a). Une exposition supplémentaire allant jusqu'à six mois n'a pas eu d'incidence sur cet effet, mais une diminution importante de l'activité motrice a été observée après sept et huit mois chez les animaux exposés comparativement aux témoins. Une étude a examiné le développement de la motricité fine de rats exposés au manganèse (soit de la naissance à 21 jours, soit toute leur vie), à l'aide du test de l'escalier (Beaudin et coll., 2013). Les résultats ont montré une altération de la régulation de la motricité fine chez les adultes ayant été exposés par gavage à 50 mg Mn/kg p.c. par jour au début de leur vie seulement. De plus, les adultes exposés pendant toute la vie ont présenté des difficultés supplémentaires généralisées à atteindre et à saisir des objets (Beaudin et coll., 2013).
Des signes de faiblesse musculaire et de rigidité des membres inférieurs ont été observés chez quatre singes rhésus (Macaca mulatta) mâles adultes ayant reçu une dose quotidienne de 25 mg MnCl2•4H2O/kg p.c. (correspondant à 6,94 mg Mn/kg p.c. par jourNote de bas de page 5) par voie orale pendant 18 mois (Gupta et coll., 1980).
Des effets neurocomportementaux ont été relevés chez des rats et des souris (petits, jeunes ou adultes) exposés au manganèse (doses estimatives de 43,7 à 910 mg Mn/kg p.c. par jour, sous forme de chlorure de manganèse) par voie orale (aliments, eau potable ou gavage) pendant une durée variable (de 14 jours à 21 semaines) (Gray et Laskey, 1980; Ali et coll., 1983; Chandra, 1983; Kristensson et coll., 1986; Pappas et coll., 1997; Calabresi et coll., 2001; Torrente et coll., 2005b; Liu et coll., 2006; Vezer et coll. 2007; Avila et coll., 2008; Molina et coll., 2011; Nowak et coll., 2011; Betharia et Maher, 2012; Fordahl et coll., 2012; Shi et coll., 2012; Takacs et coll., 2012; Krishna et coll., 2014). Les chercheurs ont noté les effets suivants : retard du réflexe de redressement; ataxie; déficits de l'apprentissage, de la mémoire et de l'activité motrice (faibles résultats au test de la piscine de Morris et au test de descente); signes d'hypoactivité ou d'hyperactivité; anxiété; mauvaise humeur; agressivité et impulsivité (au cours du test en espace ouvert, du test du nouvel objet, du test de nage forcée et du test du labyrinthe en croix surélevé).
10.2.1.3 Évaluation structurelle des tissus neuronaux
Plusieurs études ont décrit les effets délétères de l'exposition au manganèse sur l'ultrastructure des tissus cérébraux des rongeurs jeunes et adultes, comme une dégénérescence neuronale, une gliose (astrogliose)Note de bas de page 6 ou une neuroinflammation.
Une altération des tissus cérébraux a été observée chez des rats mâles juvéniles (JPN 21) exposés quotidiennement par gavage à de très faibles doses de MnCl2•4H2O dans l'eau (une seule dose de 50 µg MnCl2•4H2O par rat par jour) pendant une période d'une durée variée (15, 30, 45 ou 60 jours, c.-à-d. jusqu'au JPN 80; six rats par groupe). Même si les données n'indiquaient qu'une seule dose par jour, on peut s'attendre à ce que les doses réelles en mg/kg varient considérablement, puisque le poids des jeunes en croissance change tout au long de l'étude. Les modifications observées comprennent une dégénérescence neuronale dans le cortex cérébral (région frontale) et dans le cortex cérébelleux après 30, 45 et 60 jours d'exposition (aucun effet à 15 jours), une dégénérescence neuronale et une prolifération neurogliale dans le noyau caudé après 60 jours d'exposition, et la présence de déformations astrocytaires du type II d'Alzheimer (changement morphologique) dans la zone de dégénérescence neuronale (cortex cérébral) (Chandra et Shukla, 1978).
Quatre singes rhésus (Macaca mulatta) mâles adultes ayant reçu pendant 18 mois une dose quotidienne de 25 mg MnCl2•4H2O/kg p.c. par voie orale (les détails relatifs à l'administration de la dose n'ont pas été fournis) ont montré une dégénérescence neuronale marquée (gliose, perte neuronale et dépigmentation dans la région de la substance noire), comparativement à quatre singes témoins (Gupta et coll., 1980). Les autres régions du cerveau n'ont pas été examinées.
Une autre étude a exposé des ratons mâles et femelles à du chlorure de manganèse in utero et par le lait maternel. Les mères recevaient une solution aqueuse de chlorure de manganèse dans leur première portion de nourriture, ce qui donne une dose estimative de 10 ou de 20 mg MnCl2•4H2O/kg p.c. par jour. L'exposition des mères a duré 70 jours (soit 15 à 20 jours avant la gestation, pendant toute la gestation, et pendant un mois après la mise bas). Les résultats de l'étude ont révélé que les deux doses étaient associées à une gliose marquée et proportionnelle à la dose dans le noyau caudé, les noyaux septaux dorsal et ventral, le noyau accumbens et le cortex cérébral (Lazrishvili et coll., 2009).
Deux études qui exposaient par gavage de jeunes rats adultes à une dose quotidienne de manganèse (20 ou 50 mg MnCl2H2O/kg) pendant 30 jours ont signalé des changements dans l'ultrastructure des neurones, les contacts inter-neuronaux et les cellules gliales dans le noyau caudé, la substance noire et la région fronto-pariétale du cortex. Ces changements se sont accentués après trois mois (c.-à-d. après l'arrêt de l'exposition) et ont entraîné une dégénérescence cellulaire. Dans les deux études, les auteurs notent également la destruction de la majorité des mitochondries des neurones et des astrocytes (Bikashvili et coll., 2001; Shukakidze et coll., 2002). Les doses quotidiennes à l'essai étaient de 50 mg MnCl2•4H2O/kg (Bikashvili et coll., 2001) et de 20 ou 50 mg MnCl2•4H2O MnCl2/kg p.c. (Shukakidze et coll., 2002).
Les effets différentiels d'une exposition par gavage à du chlorure de manganèse dans une solution saline (10 ou 30 mg Mn/kg p.c. par jour) ont été examinés sur trois périodes de vie de la souris : juvénile (JPN 20 à 34); adulte (SPN 12 à 20); juvénile et adulte (Moreno et coll., 2009a). À une dose ≥ 10 mg Mn/kg p.c. par jour, le manganèse a augmenté l'expression de l'oxyde nitrique synthase 2 (NOS2)Note de bas de page 7 dans les cellules microgliales et entraîné une légère activation des astrocytes (non statistiquement significative) chez les souris juvéniles, tandis qu'il a provoqué une augmentation de l'astrogliose chez les souris adultes. Les souris ayant subi l'exposition pendant les deux périodes (juvénile et adulte) ont montré les mêmes changements, mais ces derniers étaient de plus grande ampleur; de plus, l'expression du NOS2 était accrue dans les astrocytes (Moreno et coll., 2009a).
Une activation des astrocytes (indiquée par un taux élevé de GFAP) ou une baisse de la neurogenèse (indiquée par un nombre accru de cellules exprimant la doublecortine et de cellules exprimant la reeline, et par une diminution de la concentration des hormones thyroïdiennes) ont été observées chez des rats exposés à du chlorure de manganèse par micropipette du JPN 1 au JPN 21 (25 ou 50 mg Mn/kg p.c. par jour, dans une solution de sucrose à 25 %; Kern et coll., 2011), ou in utero et dans le lait maternel du JG 10 au JPN 21 (concentration dans l'alimentation de la mère : 32, 160, 800 ou 1 600 ppm de MnCl2•4H2O) (Ohishi et coll., 2012). Une augmentation du taux de GFAP (dans le gyrus denté) a également été observée chez des rats mâles adultes ayant été exposés au manganèse par gavage pendant 10 semaines (15 et 59 mg MnCl2•4H2O/kg p.c. par jour dans l'eau distillée) (Vezer et coll., 2005; Vezer et coll., 2007). Une exposition au manganèse avant le sevrage a entraîné une expression accrue de la GFAP dans le cortex préfrontal des rats exposés à 25 ou à 50 mg Mn/kg p.c. par jour (JPN 24), et a mené également avec le temps à une activation accrue des astrocytes dans d'autres régions du cerveau qui contrôlent la fonction exécutive, soit le striatum médial et le noyau accumbens, à la dose de 50 mg Mn/kg p.c. par jour (JPN 107). Ces résultats indiquent un effet de l'exposition au manganèse sur l'astrogliose qui a persisté ou progressé dans d'autres régions du cerveau des animaux adultes, après que le taux de manganèse dans le sang soit revenu à la normale (Kern et Smith, 2011).
Une expression accrue de la GFAP, de l'ARNm de la GFAP, de l'oxygénase hémique-1 (un marqueur de stress oxydatif) et des NOS inductibles a été observée dans la substance noire de souris adultes mâles ayant été exposées pendant 8 semaines à 0,4 g Mn/L dans l'eau potable (Krishna et coll., 2014).
Après que des souris aient été exposées in utero et par le lait maternel (du JG 10 au JPN 21) à du manganèse dans les aliments (32, 160 ou 800 ppm Mn provenant de chlorure de manganèse), une augmentation du nombre de cellules exprimant la reeline a été constatée au JPN 21 pour les animaux ayant reçu une dose de manganèse égale ou supérieure à 160 ppm. D'autres altérations neuronales ont également été observées à la dose la plus élevée. Selon les auteurs, le manganèse pourrait cibler les cellules granulaires immatures et empêcher leur différentiation en cellules granulaires matures, entraînant une apoptose et une migration neuronale anormale (Wang et coll., 2012).
Les résultats d'une étude multigénérationnelle menée sur des souris exposées à 25 mg Mn/kg p.c. par jour (sous forme de chlorure de manganèse) dans l'eau potable ont montré que 2 nouveau-nés (3e génération) exhibaient une toxicité cellulaire, révélée par une démarche anormale. Le rapport fait état d'une perte d'aptitude à la coloration des cellules granulaires de la couche externe du cortex cérébral et des cellules de Purkinje dans le cortex cérébelleux, et d'une augmentation de l'aptitude à la coloration des fibres nerveuses dans la région médullaire du cervelet (Ishizuka et coll., 1991).
10.2.1.4 Effets neurochimiques
Une augmentation de l'activité de la monoamine oxydase (MAO) a été observée chez de jeunes rats mâles exposés à du manganèse de façon quotidienne au début de la période postnatale.
L'exposition a eu lieu par gavage avec du chlorure de manganèse tétrahydraté dans l'eau distillée (50 µg MnCl2•4H2O par jour par rat; une seule dose d'essai) pendant une durée variée (15, 30, 45 ou 60 jours). Le cerveau des animaux de tous les groupes exposés a montré une augmentation de l'activité de la MAO (Chandra et Shukla, 1978). Puisque la MAO sert à métaboliser (inactiver) les neurotransmetteurs monoaminergiques (norépinéphrine [NE], dopamine [DA], épinéphrine et sérotonine), cette observation concorde avec les résultats d'autres études faisant état d'une modification des taux de neurotransmetteurs comme la DA ou la sérotonine. Une diminution des taux de DA a été relevée dans le striatum et la région hypothalamique de jeunes rats et de jeunes souris ayant été exposés par gavage à une dose ≥ 10 mg Mn/kg p.c. par jour du JPN 1 au JPN 21 ou du JPN 1 au JPN 24Note de bas de page 8 (Deskin et coll., 1980; Moreno et coll., 2009b). Une diminution dose-réponse des taux de DA dans le striatum a également été observée chez de jeunes rats exposés par gavage à 0, 50, 250 ou 500 µg Mn/jour entre le JPN 1 et le JPN 20) (Tran et coll., 2002b). Cette baisse de la DA était accompagnée des troubles fonctionnels du développement moteur et du comportement, évalués selon le test de redressement (réflexe), le test de retour au gîte et le test d'évitement passif (Tran et coll., 2002b).
Une diminution du taux de DA dans le striatum a été observée chez des souris mâles et femelles exposées par gavage à des doses de 10 et de 30 mg Mn/kg p.c. par jour sous forme de chlorure de manganèse dans une solution saline, sur deux périodes (période juvénile du JPN 20 au JPN 34 et période adulte de la SPN 12 à la SPN 20) (Moreno et coll., 2009b). Une diminution des taux de DA a également été observée dans le tronc cérébral de rats adultes (âgés de trois mois) ayant été exposés par gavage à une dose de 20 mg MnCl2/kg p.c. par jour de chlorure de manganèse pendant 6,5 jours (Desole et coll., 1997). Une diminution à long terme de la libération de dopamine striatale induite par a cocaïne, mesurée par microdialyse in vivo au JPN 90, a également été notée chez des rats après leur exposition à 750 µg Mn/jour pendant la période néonatale (du JPN 1 au JPN 21) (McDougall et coll., 2008).
À de fortes doses (égales ou supérieures à environ 20 mg Mn/kg p.c. par jour), le striatum de souris et de rats juvéniles présentait des changements dans les taux d'autres neurotransmetteurs (p. ex. GABA, sérotonine, aspartate, Gln, Glu, taurine) ou dans l'activité enzymatique liée aux neurotransmetteurs (acétylcholinestérase [AChE]) (Deskin et coll., 1981; Lipe et coll., 1999; Garcia et coll., 2006), ainsi qu'une réduction des sites de fixation des transporteurs de la DA, des récepteurs de la DA de type D1 (Dorman et coll., 2000; Liu et coll., 2006; Reichel et coll., 2006; McDougall et coll., 2008; Kern et coll., 2010; Kern et Smith, 2011) et des aberrations touchant la neurogenèse (Wang et coll., 2012). Une étude menée auprès de souris suisses a révélé une diminution de l'activité du glutathion et de la glutathion-S-transférase après une exposition chronique à des doses faibles ou à des doses élevées de manganèse (Okada et coll., 2016). Les souris exposées pendant longtemps à de faibles doses de Mn (par la gestation et l'allaitement ou le gavage) ont également présenté une diminution de l'activité de l'acétylcholinestérase. Les doses déclarées étaient de 0,013, de 0,13 et de 1,3 mg/kg/jour de MnCl2 par gavage quotidien pour l'exposition des deux parents, et par gavage quotidien pour les petits.
Une étude menée sur des rats a montré que les effets d'une exposition précoce au manganèse sur la cognition et le comportement étaient associés à d'importantes modifications de la quantité de transporteurs de la dopamine (DAT) et des récepteurs D1 et D2 dans le striatum dorsal, le cortex préfrontal et le noyau accumbens (Kern et coll., 2010). Dans cette étude, des rats nouveau-nés ont reçu des doses quotidiennes de 25 et de 50 mg Mn/kg p.c. (sous forme de MnCl2), administrées par micropipette, du JPN 1 au JPN 21. Les animaux ont été soumis à une série de tests conçus pour évaluer divers comportements relevant de la fonction exécutive (n = 15 à 20 mâles/traitement) (les détails de cette expérience sont présentés dans la sous-section « effets comportementaux » ci-dessous), et une analyse immunohistochimique a été effectuée sur une cohorte d'animaux distincte afin de mesurer les taux de D1, de D2 et de DAT dans le cerveau (n = 4 à 7 rats/traitement). Le nombre de récepteurs D1 était significativement moins élevé dans le striatum dorsal des animaux exposés (pour les deux doses), tout comme le nombre DAT pour le groupe ayant reçu la dose la plus élevée. Le nombre de récepteurs D2 dans le striatum est resté inchangé. Une diminution du nombre de récepteurs D1 et du taux de DAT dans le noyau accumbens a également été observée à la dose élevée. Bien que le taux de récepteurs D2 n'ait pas changé de façon mesurable dans le striatum ou le noyau accumbens, une augmentation importante de ce taux a été observée dans le cortex préfrontal des animaux ayant reçu la dose élevée. Ces résultats indiquent que l'exposition au manganèse pendant le développement pourrait altérer l'environnement synaptique dopaminergique dans les cellules du cerveau.
Une étude subséquente, qui visait à déterminer si une exposition précoce au manganèse entraîne des effets neurocomportementaux et neurochimiques persistant jusqu'à l'âge adulte, a décrit des changements neurochimiques après une telle exposition (Kern et Smith, 2011). Dans cette étude, des rats nouveau-nés (JPN 1 à 21) ont reçu du MnCl2 (25 ou 50 mg Mn/kg p.c. par jour, dans une solution de sucrose à 25 %) par micropipette. Les auteurs ont effectué des analyses au JPN 24 (rats sevrés) et au JPN 107 (âge adulte) afin de mesurer la densité de DAT et de récepteurs de la dopamine de type D1 et D2 dans le cortex préfrontal, le striatum, et le noyau accumbens. Les résultats ont révélé que les rats exposés avant le sevrage à 25 mg Mn/kg p.c. par jour présentaient un nombre accru de récepteurs D1 dans le noyau accumbens au JPN 107. Toutefois, au JPN 24, le nombre de récepteurs D1 avait diminué dans ce tissu pour les rats ayant reçu la dose la plus élevée, et avait diminué dans le striatum dorsal pour tous les rats (quelle que soit la dose). Une augmentation significative du nombre de récepteurs D2 (environ 800 % de la valeur notée chez les témoins) a été observée au JPN 24 et au JPN 107 dans le cortex préfrontal des animaux ayant reçu la dose la plus forte. Le nombre de DAT était accru au JPN 24 dans le striatum dorsal et le noyau accumbens des animaux ayant reçu la dose la plus forte, mais les changements relatifs au nombre de transporteurs avaient disparu au JPN 107. Il est intéressant de noter que les concentrations de manganèse relevées dans le sang et le cerveau au JPN 107 (après une exposition des animaux avant sevrage, du JPN 1 au JPN 21) n'étaient pas statistiquement différentes de celles des animaux témoins (malgré l'augmentation observée au JPN 24) (Kern et Smith, 2011). Cette observation laisse à penser qu'une exposition précoce au manganèse entraînerait des effets sur le système dopaminergique qui persistent même après que les concentrations de manganèse soient revenues à leurs valeurs d'avant l'exposition. Dans le cadre d'une étude antérieure réalisée par un autre groupe de chercheurs, des souris nouveau-nés mâles ont reçu du manganèse dans l'eau potable (5 mg MnCl2/L) pendant une période allant jusqu'à 180 jours. Les résultats ont révélé une augmentation passagère de la teneur en DA, en NE, en HVA et en tyrosine dans le corps strié (Chandra et coll., 1979a). Les auteurs ont indiqué que cette augmentation temporaire des taux striataux de DA et de NE pourrait être liée à l'hyperactivité observée après 60 et 90 jours d'exposition (Chandra et coll., 1979a).
Une diminution des taux de DA a été observée dans le sérum, le cervelet, l'hypothalamus, le cortex, l'hippocampe, le mésencéphale ou le striatum de rats adultes exposés à une dose ≥ 22,5 mg Mn/kg p.c. par jour (sous forme de chlorure ou de sulfate de manganèse) dans l'eau potable. Une modification des quantités de neurotransmetteurs ou de métabolites de neurotransmetteurs (GABA, sérotonine, NE, DA, Glu, taurine), ainsi que des altérations des transporteurs de neurotransmetteurs et de l'activité enzymatique (tyrosine hydroxylase [TH]), ont également été notée chez des rats et des souris adultes ayant reçu des doses quotidiennes estimatives allant de 22,5 à 2 943,3 mg Mn/kg p.c. (sous forme de chlorure ou de sulfate de manganèse) dans l'eau potable ou par gavage pendant une période variant de 7 jours à 8 mois (Bonilla, 1978, 1980; Chandra, 1983; Eriksson et coll., 1987a; Subhash et Padmashree, 1991; Miele et coll., 2000; Ranasinghe et coll., 2000; Spadoni et coll., 2000; Calabresi et coll., 2001; Centonze et coll., 2001; Montes et coll., 2001; Anderson et coll., 2007, 2008, 2009; Fordahl et coll., 2010; Krishna et coll., 2014). Quatre singes rhésus mâles ayant reçu par gavage, pendant 18 mois, du chlorure de manganèse tétrahydraté (20 mg/kg p.c. par jour, dans de l'eau distillée) ont fait preuve d'une augmentation des concentrations tissulaires de manganèse et d'une diminution des taux de DA et de NE dans le diencéphale, le corps strié, le mésencéphale et la protubérance. Le taux de 5-hydroxytryptamine (5-HT) était réduit dans le mésencéphale. Une diminution des taux de DA et de 5-HT a été observée dans le bulbe rachidien, bien que la teneur en manganèse dans le cerveau des singes exposés était similaire à celle mesurée dans le cerveau des témoins (Chandra et coll., 1979b).
Une modification des taux de GABA et d'autres neurotransmetteurs a également été notée chez des rats sevrés âgés de 30 jours et des rats adultes âgés de 90 jours ayant reçu pendant 30 jours une dose de 10 ou de 20 mg Mn/kg p.c. par jour (sous forme de chlorure de manganèse dans l'eau), par gavage. À la dose de 20 mg Mn/kg p.c. par jour, les rats juvéniles présentaient une augmentation des taux de GABA dans le noyau caudé et les rats adultes, une augmentation des taux d'aspartate, de glutamate (Glu), de glutamine (Gln), de taurine et de GABA dans le cervelet. Aucun effet dose-réponse n'a été relevé dans les autres parties du cerveau examinées (cortex frontal et hippocampe) (Lipe et coll., 1999). Une modification des taux de GABA et d'autres neurotransmetteurs (c.-à-d. une augmentation des taux de sérotonine et de GABA, et une diminution du taux d'AChE) a été observée dans le striatum, l'hypothalamus et le cerveau en général des rats juvéniles des deux sexes exposés par gavage (sous forme de chlorure de manganèse dans une solution de sucrose à 5 %; doses d'essai : 10, 15 et 20 µg Mn/kg p.c. par jour) par gavage (Deskin et coll., 1981), ou par le lait maternel (petits exposés du JPN 4 au JPN 21, alors que leur mère recevait un supplément de manganèse de 100 ppm Mn par voie alimentaire) puis dans leurs aliments lorsqu'ils ont été capables de les consommer (c.-à-d. au JPN 11) (Garcia et coll., 2006).
Aux deux doses d'essai (0,1 et 1,0 mg Mn/mL), une diminution du taux d'acide 3,4-dihydroxyphénylacétique a été observée dans le striatum et l'hypothalamus de rats mâles ayant reçu du chlorure de manganèse dans l'eau potable pendant 8 mois. Les deux doses d'essai (ont également été associées à une augmentation du taux d'acide 5-hydroxy-indol-acétique dans l'hippocampe, et du taux de NE dans la protubérance (Bonilla, 1984b).
Il a été suggéré que les changements touchant les systèmes de neurotransmetteurs variaient en fonction de la durée d'exposition durant une intoxication au manganèse. De tels changements ont été observés dans des études menées par un groupe de chercheurs ayant exposé des souris
nouveau-nés mâles à du chlorure de manganèse par le lait maternelNote de bas de page 9 puis dans l'eau potable contenant 3 µg Mn/mL (3 mg/L) pendant une période allant jusqu'à 180 jours (Chandra et coll., 1979a), ou ayant exposé des souris mâles à du chlorure de manganèse dans l'eau potable (1 mg/mL ou 1 000 mg/L) pour une durée allant jusqu'à 360 jours (Chandra et Shukla, 1981). L'exposition au manganèse a fait augmenter les taux de DA, de NE, de HVA et de tyrosine dans le corps strié (Chandra et coll., 1979a; Chandra et Shukla, 1981). Il convient toutefois de noter que cette augmentation était passagère (les concentrations sont descendues sous les valeurs témoins après 300 ou 360 jours d'exposition) (Chandra et Shukla, 1981). Ces changements ne corrélaient pas avec le taux de manganèse dans le corps strié, qui a augmenté progressivement jusqu'au jour 120 pour les souris et jusqu'au jour 240 pour les rats, avant de se stabiliser (Chandra et coll., 1979a; Chandra et Shukla, 1981). Cependant, les changements notés dans les taux de neurotransmetteurs ont été associés à une activité accrue de la MAO dans le striatum des rats pendant les premières périodes d'exposition au manganèse (du 15e au 120e jour d'exposition). Selon les auteurs, l'augmentation initiale des taux de NE et de DA dans le striatum des souris pourrait être liée à l'hyperactivité observée après 60 et 90 jours d'exposition (Chandra et coll., 1979a). Des résultats similaires (augmentation temporaire des taux de DA dans le noyau caudé/le putamen) ont été constatés chez des rats ayant reçu une plus forte dose de manganèse (2,8 mg/L) sous forme de chlorure de manganèse tétrahydraté dans l'eau potable (Eriksson et coll., 1987a).
On a émis l'hypothèse que les changements — provoqués par le manganèse — d'absorption synaptosomale des amines dans le cerveau des rats varient avec l'âge. Dans leurs études, Lai et coll. (1982, 1984) ont exposé des rats in utero et durant toute leur vie à une dose de 1 mg MnCl2•4H2O/mL de chlorure de manganèse dans l'eau potable, ce qui correspond à une dose estimative de 33 mg Mn/kg p.c. par jour (Lai et coll., 1982)Note de bas de page 10, ou à 36,1 mg Mn/kg p.c. par jour (Lai et coll., 1984)Note de bas de page 11. Chez les rats âgés de 70 à 90 jours, les auteurs ont constaté une diminution passagère de l'absorption de DA par les synaptosomes isolés à partir de l'hypothalamus, du striatum et du mésencéphale, ainsi qu'une diminution de l'absorption synaptosomale de la choline dans l'hypothalamus. Chez les rats plus vieux (âgés de 90 à 120 jours), l'absorption synaptosomale de la choline était accrue dans le striatum et l'hypothalamus, mais aucun changement d'absorption de la DA n'a été noté.
10.2.2 Toxicité pour la reproduction
10.2.2.1 Appareil reproducteur des mâles adultes
Des études ont révélé que le manganèse altérait les fonctions des testicules et provoquait des lésions testiculaires après une exposition de courte ou de longue durée.
Chez des souris CD-1 mâles exposées pendant 43 jours à de l'acétate de manganèse (dose quotidienne de 7,5, de 15,0 et de 30,0 mg/kg p.c.), une diminution du nombre de spermatozoïdes dans les testicules (doses ≥ 7,5 mg/kg p.c. par jour) et une diminution de la motilité des spermatozoïdes (doses ≥ 15,0 mg/kg p.c. par jour) ont été observées. La capacité des mâles exposés au manganèse à féconder les femelles n'a toutefois pas diminué (Ponnapakkam et coll., 2003a). Une autre étude a relevé une augmentation des anomalies de la tête des spermatozoïdes et du pourcentage de spermatozoïdes anormaux chez des souris ayant reçu du permanganate de potassium (65 à 380 mg/kg p.c. par jour) ou du sulfate de manganèse (102,5 à 610 mg/kg p.c. par jour) pendant 21 jours par gavage (Joardar et Sharma, 1990).
Des lésions testiculaires ont été observées chez le singe et le rat. Les auteurs d'une étude portant sur des singes rhésus adultes exposés par voie oraleNote de bas de page 12 à du chlorure de manganèse (25 mg MnCl2•4H2O/kg p.c. par jour pendant 18 mois) ont observé une congestion et une enflure testiculaires, une augmentation marquée du poids des testicules, un œdème interstitiel et une dégénérescence des tubes séminifères. Les cellules de Leydig ne présentaient aucune anomalie. L'activité de plusieurs enzymes (déshydrogénase succinique, glucose-6-phosphate déshydrogénase et phosphatase acide) était fortement inhibée dans les tubes séminifères. Les auteurs de cette étude ont conclu qu'une exposition chronique au manganèse ne provoquait pas d'importants changements dégénératifs dans les testicules plus tôt que n'apparaissent les encéphalopathies causées par les métaux chez les primates (Murthy et coll., 1980).
Chez des rats Sprague-Dawley exposés à de l'acétate de manganèse pendant 63 jours, une dégénérescence segmentaire légère à modérée de l'épithélium germinal dans les tubes séminifères s'est produite à une dose ≥ 612 mg Mn/kg p.c. par jour (aucun effet à 306 mg Mn/kg p.c. par jour). Il semble que ces changements soient réversibles et disparaissent après l'arrêt de l'exposition (Ponnapakkam et coll., 2003c).
Une baisse de fertilité a été observée chez des souris mâles ayant reçu du chlorure de manganèse dans l'eau potable (8 000 mg MnCl2/L, correspondant à des doses de 706 mg MnCl2/kg p.c. par jour ou de 309 mg Mn/kg p.c. par jour si la dose indiquée par les auteurs fait référence au MnCl2 et non au Mn élémentaire) pendant 12 semaines avant leur accouplement avec des femelles non exposées (aucun effet observé à 1 000, 2 000 et 4 000 mg MnCl2/L) (Elbetieha et coll., 2001).
10.2.2.2 Appareil reproducteur des femelles adultes
Plusieurs études ont été menées chez le rat, la souris et le lapin afin d'évaluer la toxicité du manganèse sur l'appareil reproducteur des femelles. Certaines de ces études ont révélé une diminution de la fertilité, une augmentation des pertes après l'implantation et une baisse de la viabilité des fœtus à des doses d'exposition élevées.
Une diminution du nombre d'implantations et de fœtus viables a été observée chez des souris suisses femelles ayant reçu du chlorure de manganèse tétrahydraté dans l'eau potable (8 000 mg MnCl2/L) pendant 12 semaines avant d'être accouplées à des mâles non exposés (aucun effet à 1 000, 2 000 ou 4 000 mg MnCl2/L) (Elbetieha et coll., 2001). Les auteurs ont également noté une augmentation des pertes après l'implantation chez les femelles gravides ayant reçu de l'eau potable contenant 8 000 mg Mn/L (Elbetieha et coll., 2001). En revanche, une autre étude portant sur des lapines gravides ayant reçu des doses similaires de chlorure de manganèse entre le JG 6 et le JG 20 n'a mis en évidence aucun effet sur la reproduction (Szakmáry et coll., 1995).
Le manganèse n'a pas eu d'effets nocifs sur la santé des mères, la taille des portées ou la proportion mâles/femelles chez les petits lorsque des rats mères ont reçu du chlorure de manganèse dans l'eau potable (2 ou 10 mg MnCl2/mL) pendant la gestation; les auteurs de l'étude n'ont effectué aucune analyse plus poussée des organes reproducteurs des femelles (Pappas et coll., 1997). Dans une autre étude, une diminution du poids des portées a été constatée chez des rats femelles ayant reçu du chlorure de manganèse dans l'eau potable (20 mg MnCl2/mL) (Kontur et Fechter, 1985). À cette dose, la consommation d'eau et le gain de poids corporel des femelles ont diminué de façon très importante.
Le manganèse n'a eu aucun effet sur le gain de poids maternel, le nombre d'implantations, les résorptions ou le pourcentage de morts fœtales chez des rats femelles Sprague-Dawley ayant reçu des doses variées de sulfate de manganèse par voie alimentaire (4, 24, 54, 154, 504 et 1 004 mg Mn/kg d'aliments secs) du sevrage à l'accouplement, et jusqu'au JG 21 (Jarvinen et Ahlström, 1975).
10.2.3 Toxicité pour le développement
Plusieurs études portant sur la toxicité pour le développement d'une exposition au manganèse chez le rat, la souris ou le lapin ont été réalisées avec des périodes d'exposition comparables pendant la gestation et la période postnatale. Le manganèse traverse facilement la barrière placentaire et est libéré dans le lait maternel (Saric, 1986). Les nouveau-nés sont particulièrement sensibles à l'exposition au manganèse pendant le développement, car tout indique qu'ils absorbent et accumulent davantage le manganèse et qu'ils en excrètent moins, étant donné que leur capacité d'excrétion biliaire n'est pas encore développée (Deskin et coll., 1980; Dorman et coll., 2000; Keen et coll., 1986).
Des études ont révélé qu'une exposition au manganèse par voie orale ou par inhalation pendant la gestation, la lactation et la période postnatale a un effet sur la croissance ou la survie, altère le rendement reproducteur et entraîne des effets neurotoxiques. L'exposition au manganèse pendant la gestation a également été associée à un moindre gain de poids des petits. Cette évaluation porte principalement sur la toxicité pour le développement résultant d'une exposition au manganèse par voie orale. Un compte-rendu détaillé de la toxicité résultant d'une exposition par inhalation est présenté dans une autre publication (Santé Canada, 2010).
10.2.3.1 Effets sur la croissance et la survie
Deux études portant sur les effets de formes solubles du manganèse sur le développement n'ont mis en évidence aucun effet clair sur l'implantation ou sur la survie maternelle ou fœtale chez des rats, des souris, des hamsters et des lapins ayant reçu par gavage du sulfate de manganèse monohydraté pendant 5 à 13 jours de gestation consécutifs (souris et rats : JG 6 à 15; hamsters : JG 6 à 10; lapins : JG 6 à 18). Les doses quotidiennes variaient de 0,783 à 1,36 mg/kg p.c. (faible dose) et de 78,3 à 136,0 mg/kg p.c. (dose élevée), selon l'espèce visée (NTIS, 1973).
Dans une étude portant sur des souris exposées à du chlorure de manganèse par voie alimentaire (0, 32, 160 ou 800 ppm de Mn) du JG 10 au JPN 21, une diminution du poids corporel a été constatée pour les petits mâles ayant reçu une dose de 160 ppm (du JPN 21 au JPN 70) ou de 800 ppm (du JPN 17 au JPN 63). En revanche, aucune altération du poids corporel n'a été observée pour les femelles entre le JPN 2 et le JPN 77 (Wang et coll., 2012).
10.2.3.2 Altération du développement de l'appareil reproducteur
Un développement pubertaire précoce induit par le manganèse a été constaté chez des rats mâles et femelles exposés par gavage à des doses allant de 10 à 25 mg/kg MnCl2 au début de la période de développement postnatal (Pine et coll., 2005; Lee et coll., 2006; Hiney et coll., 2011).
Une étude fait état de mauvais résultats sur le plan du rendement reproducteur ainsi que de la croissance et de la survie des nouveau-nés pour des rats ayant été exposés au manganèseNote de bas de page 13 par voie alimentaire (aliments contenant à la base une dose de manganèse de 50 mg/kg p.c. par jour, plus un supplément de 0, 500 ou 1 000 mg Mn/kg p.c. par jour, sous forme sèche) pendant une période allant jusqu'à 7,5 mois. Des études histologiques décrites dans Gerber et coll. (2002) ont révélé une diminution de la spermatogénèse, une altération de l'épithélium, une atrésie (dégénérescence) des follicules ovariens ainsi qu'une persistance du corps jaune, ce qui est le signe d'un dysfonctionnement ovarien.
Des souris exposées par voie alimentaire à 1 050 ppm de manganèse sous forme de Mn3O4, tout en étant soumises à un régime alimentaire pauvre en fer, ont montré une diminution du développement sexuel mâle, révélée par une diminution du poids des testicules, des vésicules séminales et du prépuce (Gray et Laskey, 1980).
10.2.3.3 Tératogénicité
Seulement deux études ont examiné la tératogénicité des formes solubles du manganèse après une exposition par voie orale, et aucune d'elles n'a fait état d'un nombre accru d'anomalies dans les tissus mous ou squelettiques (NTIS, 1973; Grant et coll., 1997). Dans la première étude, des rats, des souris, des hamsters et des lapins ont reçu du sulfate de manganèse monohydraté par gavage, pendant 5 à 13 jours de gestation consécutifs (souris et rats : JG 6 à 15; hamsters : JG 6 à 10; lapins : JG 6 à 18; les doses quotidiennes variaient de 0,783 à 1,36 mg/kg p.c. [faible dose] et de 78,3 à 136,0 mg/kg p.c. [dose élevée], selon l'espèce; NTIS, 1973). Dans la deuxième étude, des rats ont reçu du chlorure de manganèse par gavage, du JG 6 au JG 17 (400 µmol/kg p.c. par jour; Grant et coll., 1997).
10.2.3.4 Neurotoxicité au stade du développement
L'exposition au manganèse pendant la gestation, la lactation ou la période postnatale peut causer plusieurs types d'effets neurotoxiques, y compris des effets sur le comportement qui sont révélés par une altération neurochimique et neurostructurale chez les animaux, comme il a été mentionné à la section 10.2.1. Les effets notés comprennent une altération des fonctions cognitives et comportementales, qui concorde avec les effets sur le développement observés dans les études épidémiologiques.
Les nouveau-nés sont particulièrement sensibles à l'exposition au manganèse pendant le développement postnatal. De nombreuses données probantes indiquent que les nouveau-nés absorbent et retiennent davantage le manganèse que les adultes, ce qui entraîne une augmentation du taux de manganèse dans le cerveau et de la neurotoxicité du manganèse durant cette période (Deskin et coll., 1980; Kontur et Fechter, 1985; Keen et coll., 1986; Kristensson et coll., 1986; Brenneman et coll., 1999; Dorman et coll., 2000; Weber et coll., 2002; Tran et coll., 2002a). Cette sensibilité accrue peut être attribuable à plusieurs facteurs, notamment une plus grande absorption du manganèse depuis le tube digestif, une barrière hémato-encéphalique incomplètement formée,
l'absence d'excrétion biliaire du manganèse jusqu'au sevrage, ainsi qu'une plus grande propension à présenter des perturbations de l'activité de divers enzymes et une déficience des systèmes de neurotransmetteurs (Kostial et coll., 1978; Shukla et coll., 1980; Kristensson et coll., 1986; Brenneman et coll., 1999; Dorman et coll., 2000; Moreno et coll., 2009b; Santé Canada, 2010). Cette dernière différence entre les animaux en cours de développement et les animaux adultes a été observée dans des études ayant comparé les effets d'une exposition au manganèse sur des animaux nouveau-nés et adultes (Kostial et coll., 1978; Shukla et coll., 1980; Dorman et coll., 2000; Moreno et coll., 2009b).
Les effets de doses plus élevées de manganèse sur les mouvements ont été observés dans une étude sur trois générations chez la souris : deux nouveau-nés de la portée de la troisième génération exposée à 25 mg Mn/kg p.c. par jour présentaient une démarche anormale (Ishizuka et coll., 1991).
10.2.4 Autres effets
Une étude menée par le NTP (1993) décrit les effets (à l'exception des effets neurotoxiques) d'une exposition au manganèse par voie alimentaire. L'étude examinait des rats et des souris ayant ingéré du sulfate de manganèse monohydraté dans les aliments pendant 14 jours, 13 semaines ou 2 ans. Dans l'étude ayant duré 2 ans, les souris ont reçu des doses de manganèse de 1 500 à 15 000 ppm par voie alimentaire. Les doses correspondant au niveau d'exposition le plus élevé n'ont pas été ajustées en fonction du poids corporel, ce qui signifie qu'elles variaient avec la croissance (gain de poids) des animaux. Les doses estimées, sur la durée de l'étude, variaient entre 1 171 mg/kg p.c. par jour (semaine 4) et 505 mg/kg p.c. par jour (semaine 104) pour les rats mâles (1 249 à 561 mg/kg p.c. par jour pour les rats femelles). De façon similaire, les doses correspondant au niveau d'exposition le plus élevé, chez les souris, allaient de 2 263 à 1 916 mg/kg p.c. par jour pour les mâles et de 3 449 à 1 983 mg/kg p.c. par jour pour les femelles.
Les auteurs de cette étude n'ont observé aucun effet important touchant l'appareil respiratoire, le système cardiovasculaire, le foie, les yeux, les muscles ou les os (lésions pathologiques) de l'une ou l'autre des espèces (NTP, 1993). Il est utile de mentionner que dans cette étude, l'exposition se faisait par les aliments et non par l'eau potable. Comme il est mentionné dans la section traitant de la cinétique, on s'attend à ce que la biodisponibilité du manganèse soit plus importante avec une exposition par l'eau potable (si l'eau est consommée à jeun) comparativement à une exposition par les aliments.
10.2.4.1 Effets sur le poids corporel
Plusieurs études menées dans des conditions variées ont fait état d'une diminution du poids corporel après une exposition au manganèse par voie orale chez les rongeurs. Des rats nouveau-nés ayant reçu 250 ou 750 µg Mn/jour (sous forme de chlorure de manganèse dans une solution de sucrose à 10 %) du JPN 1 au JPN 21 présentent un poids largement inférieur à JPN 21 (Reichel et coll., 2006). Une diminution de la croissance et du gain de poids a également été observée chez des rats nouveau-nés après une exposition par voie oraleNote de bas de page 14 à 25 ou à 50 mg/kg p.c. par jour de chlorure de manganèse, du JPN 1 au JPN 49 et du JPN 21 au JPN 49 (Brenneman et coll., 1999;
Dorman et coll., 2000). Des rats âgés de 90 jours exposés par gavage à 10 ou à 20 mg Mn/kg p.c. par jour (sous forme de chlorure de manganèse dans l'eau distillée) pendant 30 jours présentaient une diminution de leur poids corporel (Lipe et coll., 1999). Les plus fortes doses (≥ 120 mg Mn/kg p.c. par jour) de manganèse dans les aliments ou dans l'eau potable ont également provoqué une diminution du gain de poids corporel chez des rats et des souris (Komura et Sakamoto, 1991; NTP, 1993; Torrente et coll., 2005b; Avila et coll., 2008).
Dans l'étude du NTP (1993), le poids corporel moyen a diminué pour les souris femelles exposées à une dose ≥ 1 500 ppm de manganèse par voie alimentaire et pour les rats mâles exposés à une dose de 15 000 ppm de manganèse. Aucun effet sur le poids corporel des souris mâles ou des rats femelles n'a été observé (NTP, 1993).
10.2.4.2 Effets respiratoires
Il a été démontré que le manganèse entraînait des effets sur les voies respiratoires après une exposition par voie orale (réduction du poids des poumons) et par inhalation (inflammation nasale et pulmonaire). Une évaluation détaillée des effets toxicologiques associés à l'inhalation de manganèse est présentée dans le rapport Évaluation du risque pour la santé humaine du manganèse inhalé de Santé Canada (Santé Canada, 2010).
10.2.4.3 Effets gastro-intestinaux
Des cobayes ayant été exposés par gavage à 10 mg/kg de chlorure de manganèse pendant 30 jours ont présenté des foyers de nécrose dans l'estomac et dans l'intestin grêle, ainsi qu'une diminution de l'activité cellulaire de l'adénosine triphosphatase et de la glucose 6-phosphatase (Chandra et Imam, 1973). Toutefois, dans cette étude, il est possible que le gavage lui-même ait été entièrement ou en partie responsable des effets nocifs observés dans l'estomac et dans l'intestin grêle des animaux. Une hyperplasie de l'estomac antérieur, associée à des ulcères et une inflammation (principalement chez les mâles), a été observée chez des souris (mais pas chez les rats) ayant reçu 15 000 ppm de sulfate de manganèse par voie alimentaire pendant deux ans (NTP, 1993).
Chez des souris mâles exposées à du sulfate de manganèse monohydraté (jusqu'à 50 000 ppm) par voie alimentaire pendant 13 semaines, une hyperplasie et une hyperkératose légères de l'estomac antérieur ont touché trois animaux sur dix à la dose d'essai la plus élevée (1 950 mg Mn/kg p.c. par jour). Par contre, aucun effet gastro-intestinal n'a été observé chez les souris femelles soumises aux mêmes conditions, ni chez des rats ayant reçu une dose de manganèse allant jusqu'à 25 000 ppm (NTP, 1993).
10.2.4.4 Effets cardiovasculaires
Dans deux études menées sur des rats mâles Sprague-Dawley sevrés, une exposition au manganèse par voie alimentaire (45 à 50 ppm dans les aliments) pendant 15 semaines a entraîné une réduction de la contraction maximale des vaisseaux (Kalea et coll., 2005). Elle a également provoqué des altérations structurelles aortiques (augmentation du taux d'acide uronique et de la concentration de galactosaminoglycanes totaux, et diminution de la concentration d'hyaluronane et de sulfate d'héparane dans les aortes) (Kalea et coll., 2006).
10.2.4.5 Effets hématologiques
Chez les rats (en particulier chez les mâles), une augmentation de la numération globale des leucocytes et des neutrophiles survenait après une exposition par voie alimentaire à 50 000 ppm de sulfate de manganèse monohydraté pendant 14 jours. Des effets hématologiques ont également été signalés chez les rats après 13 semaines d'exposition (augmentation de la numération des neutrophiles à partir d'une dose de manganèse correspondant à 1 600 ppm pour les mâles et de 6 250 ppmNote de bas de page 15 pour les femelles) et chez les souris (pour les mâles et les femelles, diminution respective des taux d'hématocrite et d'hémoglobine à partir d'une dose de manganèse de 50 000 ppm) (NTP, 1993).
On n'a observé aucune différence notable dans l'hématologie des rats et des souris exposés à du manganèse dans leur alimentation pendant deux ans; à 15 mois (évaluation intermédiaire) les seuls effets hématologiques observés chez les souris mâles recevant une dose de manganèse de 15 000 ppm était une augmentation des taux d'hématocrite et d'hémoglobine, et un nombre accru d'érythrocytes (Er); cependant on ne connaît pas la signification de ces effets (NTP, 1993). Ces résultats contrastent avec ceux obtenus chez des souris ayant reçu une alimentation contenant 2 g de Mn/kg pendant 100 jours : les taux d'Er ont diminué après l'exposition à l'acétate et au chlorure de manganèse, et la numération leucocytaire a baissé sous l'effet de l'acétate, du chlorure et du dioxyde de manganèse (Komura et Sakamoto, 1991). Une baisse de l'hématocrite a été observée après l'exposition au carbonate de manganèse (Komura et Sakamoto, 1991).
10.2.4.6 Effets hépatiques
Les résultats d'une étude menée auprès de rats exposés à 16 mg de MnCl2•4H2O/kg pc/jour (dans une solution buvable de sucrose à 10 %) pendant 30 jours ont montré des modifications de plusieurs taux d'enzymes hépatiques et sériques (dans le foie : diminution de l'activité de la déshydrogénase succinique et de l'alcool déshydrogénase, et augmentation de l'activité de la MAO, de l'adénosine triphosphatase, de l'arginase, de l'alanine aminotransférase, de la ribonucléase et de la glucose-6-phosphatase; dans le sérum : augmentation de l'activité de l'α-amylase et diminution de l'activité de la β-amylase) (Shukla et coll., 1978). Dans une autre étude, les rats femelles exposés de la conception à l'âge de 60 jours à des doses plus élevées de manganèse dans l'eau potable, sous forme de chlorure de manganèse tétrahydraté (1 000, 10 000 ou 20 000 mg MnCl2/L), présentaient une nécrose hépatique et des modifications ultrastructurales (Leung et coll., 1982). L'étude du NTP (1993) signale que les rats mâles qui ont reçu une dose de sulfate de manganèse monohydraté supérieure ou égale à 12 500 ppm pendant 14 jours font preuve d'une baisse du poids relatif du foie. Après 13 semaines d'exposition, on signale également une baisse du poids du foie pour les rats mâles ayant reçu une dose supérieure ou égale à 35,8 mg Mn/kg pc/jour (dose supérieure ou égale à 1 600 ppm) et pour les rats femelles ayant reçu une dose de 650 mg Mn/kg pc/jour (dose de 25 000 ppm). Chez les souris, seuls les mâles présentaient une baisse relative et absolue du poids du foie, à une dose d'exposition de 2 410 mg Mn/kg pc/jour (50 000 ppm) (NTP, 1993).
10.2.4.7 Effets rénaux
Les rats Sprague-Dawley mâles qui ont reçu par voie orale (gavage) des doses élevées de manganèse (de 306 à 1 838 mg Mn/kg pc/jour sous forme d'acétate de manganèse) pendant 63 jours ont contracté des maladies rénales graves (glomérulosclérose, néphrite et urolithiase [calculs rénaux]; Ponnapakkam et coll., 2003b). Les femelles ne présentaient pas de différences significatives avec les groupes témoins en ce qui concerne les effets sur les tissus, ce qui donne à penser que les mâles sont plus sensibles à cet effet induit par le manganèse. Contrairement à ces
constatations, une autre étude n'a révélé aucun changement histopathologique rénal significatif chez les souris et les rats recevant pendant 13 semaines des doses élevées de sulfate de manganèse (doses respectives allant jusqu'à 2 410 et 650 mg Mn/kg pc/jour) (NTP, 1993), ni chez les souris et les rats recevant pendant 14 jours du sulfate de manganèse (jusqu'à 50 000 ppm par voie alimentaire) (NTP, 1993). Aucune augmentation du stress oxydatif n'a été observée dans les reins de rats exposés par l'eau potable pendant 30 jours à des doses de manganèse allant jusqu'à 25 000 ppm de MnCl2 (soit environ 861 mg Mn/kg pc/jour) (Avila et coll., 2008)Note de bas de page 16.
Une augmentation marginale de la gravité moyenne de la néphropathie (comparativement au groupe témoin) a été relevée chez les rats mâles ayant reçu du sulfate de manganèse monohydraté (15 000 ppm) pendant deux ans, alors qu'aucun changement histopathologique rénal significatif n'a été observé chez les rats femelles ou chez les souris des deux sexes soumises à une exposition similaire (NTP, 1993).
10.2.4.8 Effets endocriniens et neuroendocriniens
Un groupe de chercheurs a mené plusieurs études, suivant des méthodologies semblables, pour examiner l'effet du manganèse (chlorure de manganèse) sur l'état hormonal. Les effets signalés comprennent une augmentation des taux de gonadolibérine (GnRHNote de bas de page 17), d'hormone lutéinisante (LH), d'hormone folliculostimulante (FSH), d'estradiol ou de testostérone chez des rats Sprague-Dawley immatures exposés par gavage à du MnCl2 avant la puberté : des effets touchaient les femelles exposées à une dose de 10 mg MnCl2/kg pc/jour du JPN 12 au JPN 29 et les mâles exposés à une dose de 25 mg MnCl2/kg pc/jour du JPN 15 au JPN 48 ou du JPN 15 au JPN 55 (Pine et coll., 2005; Lee et coll., 2006). À ces doses, l'exposition continue au manganèse a également induit un avancement modéré mais significatif de l'âge de l'ouverture vaginale (1,5 jour) chez les femelles, ainsi qu'une augmentation de la production quotidienne de sperme et de l'efficacité de la spermatogénèse chez les mâles (Pine et coll., 2005; Lee et coll., 2006).
Dans une autre étude, le même groupe de chercheurs a étudié les effets de l'exposition au manganèse pendant la période prépubère sur des gènes précis liés à la puberté dérivés des cellules gliales et connus pour influer sur la libération neuronale de l'hormone de libération de l'hormone lutéinisante (LHRH) dans le segment basal médian de l'hypothalamus et dans l'aire préoptique et le noyau périventriculaire antéro-ventral (AVPV). Pour ce faire, les auteurs ont exposé des femelles à du manganèse par gavage (solution saline; 10 mg de MnCl2/kg pc) du JPN 12 au JPN 22 ou du JPN 12 au JPN 29. Les auteurs ont noté une augmentation de l'expression du facteur de croissance semblable à l'insuline 1 (IGF-1) et de la cyclooxygénase-2 (COX-2) dans le segment basal médian de l'hypothalamus au JPN 22 et au JPN 29, ainsi que de la LHRH dans l'aire préoptique et l'AVPV au JPN 29 (Hiney et coll., 2011).
La sensibilité des femelles au manganèse pendant la puberté est prouvée par les résultats d'études in vitro portant sur des coupes d'hypothalamus basal de rats mâles adultes et de rats mâles et femelles immatures (Pine et coll., 2005; Lee et coll., 2006; Prestifilippo et coll., 2007). Ces résultats ont montré que le taux de chlorure de manganèse nécessaire pour stimuler la libération
de LHRH était plus grand chez les mâles adultes (500 µM) que chez les femelles (50 µM) et les mâles (250 µM) immatures. Les femelles immatures sont donc plus sensibles à cet effet induit par le manganèse, que les mâles matures et immatures (Pine et coll., 2005; Lee et coll., 2006; Prestifilippo et coll., 2007).
Les résultats d'une étude du NTP de 1993 n'ont montré aucun effet endocrinien lié au manganèse (lésions histopathologiques) chez les souris et les rats recevant pendant 13 semaines du sulfate de manganèse monohydraté (jusqu'à 25 000 ppm pour les rats et jusqu'à 50 000 ppm pour les souris). Les souris mâles et femelles recevant du sulfate de manganèse monohydraté (15 000 ppm) pendant deux ans présentaient une augmentation de l'incidence de l'hyperplasie et de l'hypertrophie des cellules folliculaires thyroïdiennes; aucun effet endocrinien n'a été relevé chez les rats exposés à des conditions similaires (NTP, 1993).
10.2.4.9 Cancérogénicité
En 1996, l'U.S. EPA a déclaré que le manganèse était non classifiable parmi les agents cancérogènes pour les humains (groupe D), étant donné que les études existantes étaient considérées comme inadéquates pour en évaluer la cancérogénicité (U.S. EPA, 1996, 2014). À ce jour, le Centre International de Recherche sur le Cancer (CIRC) n'a pas encore évalué la cancérogénicité du manganèse.
Aucune donnée ne démontre clairement la cancérogénicité du manganèse (Assem et coll., 2011). Dans une étude du NTP, les chercheurs ont administré du sulfate de manganèse monohydraté à des souris et à des rats par voie alimentaire (0, 1 500, 5 000 ou 15 000 ppm) pendant deux ans (NTP, 1993). Les auteurs n'ont observé aucun signe d'activité cancérogène chez les rats des deux sexes (avec des doses d'exposition allant jusqu'à 615 mg/kg pc/jour pour les mâles et jusqu'à 715 mg/kg pc/jour pour les femelles). Chez les souris des deux sexes (doses d'exposition allant jusqu'à 1 800 mg/kg pc/jour pour les mâles et jusqu'à 2 250 mg/kg pc/jour pour les femelles), les résultats ont montré des signes équivoques de cancérogénicité en raison d'une augmentation marginale de l'incidence de l'adénome folliculaire de la thyroïde et d'une augmentation statistiquement significative de l'incidence d'hyperplasie des cellules folliculaires thyroïdiennes.
10.3 Génotoxicité
On ne connaît pas très bien le potentiel génotoxique du manganèse, et les résultats des tests de génotoxicité semblent dépendre du système d'essai et du protocole utilisés. Des études in vitro ont révélé qu'au moins quelques-unes des formes chimiques du manganèse (telles que le sulfate de manganèse) présentent un potentiel mutagène ou génotoxique. Cependant, aucune conclusion générale ne peut être tirée quant à la possibilité que les composés de manganèse posent un risque génotoxique pour les humains, étant donné que les résultats des études in vivo menées chez les mammifères sont contradictoires (Commission européenne, 2000; Santé Canada, 2010; Assem et coll., 2011).
10.3.1 Observations in vitro
10.3.1.1 Mutagénicité et transformation cellulaire
Les résultats d'essais de mutagénicité sur Salmonella (test d'Ames) effectués avec et sans activation métabolique ont montré que le sulfate de manganèse n'était pas mutagène pour les souches TA97, TA98, TA100, TA1535 et TA1537 de S. typhimurium (Mortelmans et coll., 1986); cependant, une autre étude a trouvé qu'il était mutagène pour la souche TA97 (Pagano et Zeiger, 1992). Dans d'autres études, le chlorure de manganèse n'était pas mutagène pour les souches TA98, TA100 et TA1535 de S. typhimurium, mais il l'était pour la souche TA1537 (Wong, 1988; de Méo et coll., 1991). Le sulfate et le chlorure de manganèse ont tous les deux donné un résultat positif lorsqu'ils ont été testés avec la souche TA102 sans activation métabolique (de Méo et coll., 1991). Il est possible que l'absence de mutagénicité du manganèse observée dans certains des tests d'Ames soit due à une faible biodisponibilité de l'ion métallique attribuable aux composants du milieu de culture, qui inhibent l'activité mutagénique des ions métalliques en les chélatant ou en leur faisant concurrence pour les sites de transport actif (NTP, 1993).
Le chlorure de manganèse a donné des résultats positifs, sans activation métabolique, au cours d'essais sur des cellules de lymphome de souris (80, 60 et 40 µg/mL) (Oberly et coll., 1982) et au cours d'un test des comètes réalisé sur des lymphocytes humains en culture (pouvoir mutagène de 2,4 révertants/nmole MnCl2) (de Méo et coll., 1991). Il a également provoqué des transformations cellulaires dans des cellules d'embryons de hamster de Syrie (0,13 mM MnCl2) (Casto et coll., 1979).
Le sulfate de manganèse a présenté une faible capacité de mutation et de conversion dans des essais de conversion génique et de mutation réverse mené sur la souche D7 de Saccharomyces cerevisiae (Singh, 1984). Il a donné des résultats négatifs aux essais de conversion génique dans deux autres études menées sur la levure (Baranowska et coll., 1977; Parry, 1977).
10.3.1.2 Échange de chromatides sœurs et aberrations chromosomiques
Le sulfate de manganèse (12 500 ppm) a provoqué un échange de chromatides sœurs sans activation métabolique dans des fibroblastes de souris (Andersen, 1983), des cellules ovariennes de hamster chinois (Galloway et coll., 1987) et des lymphocytes humains (Andersen, 1983), et avec activation métabolique dans des cellules ovariennes de hamster chinois (NTP, 1993). Le sulfate de manganèse a également provoqué des aberrations chromosomiques sans activation métabolique dans des cellules ovariennes de hamster chinois (Galloway et coll., 1987; NTP 1993).
En revanche, des tests effectués sans activation métabolique ont montré que le permanganate de potassium n'avait causé aucune aberration chromosomique dans une culture primaire de cellules provenant d'embryons de hamster de Syrie (Tsuda et Kato, 1977).
10.3.2 Observations in vivo
10.3.2.1 Mutagénicité
Le sulfate de manganèse n'a pas provoqué de mutations létales récessives liées au sexe chez Drosophila melanogaster (Valencia et coll., 1985; NTP, 1993). Le chlorure de manganèse n'a pas provoqué de mutations somatiques chez D. melanogaster (Rasmuson, 1985).
Aucune translocation héréditaire (chez la souris) ni mutation létale dominante (chez le rat) n'ont été détectées après l'administration de sulfate de manganèse à des souris par voie alimentaire pendant 7 semaines ou à des rats par gavage une fois par jour pendant 1 à 5 jours (Newell et coll., 1974 cités dans NTP, 1993).
10.3.2.2 Aberrations chromosomiques
Des souris albinos suisses exposées par voie orale à du sulfate de manganèse (doses allant de 33 à 132 mg Mn/kg p.c. par jour) pendant trois semaines ont présenté un nombre accru d'anomalies de la tête des spermatozoïdes et une plus grande fréquence d'aberrations chromosomiques et de la présence de micronoyaux dans les cellules de la moelle osseuse (Joardar et Sharma, 1990). Dans une étude similaire, des souris albinos suisses exposées par voie orale à une dose de 22,6, de 45,2 et de 132,1 mg Mn/kg p.c. par jour (sous forme de permanganate de potassium) pendant trois semaines ont présenté un nombre accru d'anomalies de la tête des spermatozoïdes et une plus grande fréquence d'aberrations chromosomiques dans la moelle osseuse (Joardar et Sharma, 1990).
Aucune altération chromosomique importante n'a été relevée dans la moelle osseuse ou les spermatogonies de rats mâles exposés à une dose quotidienne de 0,014 mg Mn/kg p.c. (sous forme de chlorure de manganèse) pendant 180 jours (Dikshith et Chandra, 1978).
10.3.3 Épigénétique
De plus en plus de données probantes indiquent que l'exposition à des substances toxiques, comme des métaux, en début de vie pourrait influer sur l'expression des gènes plus tard dans la vie, possiblement par des mécanismes épigénétiques (Wright et Baccarelli, 2007). Il semblerait que les changements dans l'expression des gènes, qui se produisent sans modification de la séquence d'ADN, finissent par altérer les protéines produites par ces gènes. On ne possède pas encore toutes les connaissances nécessaires pour déterminer si une forte exposition au manganèse provoque des modifications épigénétiques de l'ADN qui seraient susceptibles d'altérer
l'expression génique et d'entraîner les effets sur la santé qui ont été décrits. L'exposition au manganèse pendant le développement provoque des changements durables de l'expression de plusieurs protéines du système dopaminergique (D2, DAT et catécholamine méthyltransférase). Ces protéines sont régulées de façon épigénétique par la méthylation des îlots CpG par l'ADN méthyltransférase (DNMT) (Kern et coll. 2010, 2011; Shumay et coll., 2010; Day et coll., 2013). Une exposition à de fortes doses de manganèse entraîne un effet pro-oxydant, et il a été démontré que le stress oxydatif inhibait la DNMT ou entraînait une diminution des taux de DNMT (Han et coll., 2011). En outre, une altération de la fonction du système dopaminergique a été associée aux déficits comportementaux et cognitifs découlant d'une exposition au manganèse pendant le développement (Kern et coll., 2010, 2011; Beaudin et coll., 2013, 2015; Reichel et coll., 2006; McDougall et coll., 2008).
11.0 Mode d'action
Le système nerveux central est une cible cruciale de la toxicité du manganèse chez les humains, les primates non humains et les rongeurs. Comme les sections 9 et 10 du présent document le montrent, des études toxicologiques ont révélé que l'exposition au manganèse par voie orale (ou par inhalation) avait divers effets délétères sur le comportement (p. ex. réduction des capacités d'apprentissage et de mémorisation), sur la fonction motrice (p. ex. altération des réflexes et de l'activité) et sur l'ultrastructure du tissu cérébral.
Divers mécanismes ont été proposés pour expliquer la neurotoxicité du manganèse, mais les données indiquent qu'elle fait intervenir plusieurs processus interdépendants, tels qu'un dysfonctionnement mitochondrial (Gavin et coll., 1992; Zheng et coll., 1998), la formation de radicaux libres (Desole et coll., 1994, 1995; Hussain et coll., 1997; Taylor et coll., 2006) et une déficience des neurotransmetteurs (Chandra et coll., 1979a; Deskin et coll., 1980; Chandra et Shukla, 1981; Lai et coll., 1982, 1984; Subhash et Padmashree, 1991; Komura et Sakamoto, 1994; Ranasinghe et coll., 2000; Calabresi et coll., 2001; Montes et coll., 2001; Tran et coll., 2002a, 2002b; Fitsanakis et coll., 2006; McDougall et coll., 2008; Peneder et coll., 2011). Ces processus génèrent des radicaux, perturbent la phosphorylation oxydative et la synthèse de l'ATP, et entraînent un dysfonctionnement cellulaire, une apoptose ou une nécrose et la mort cellulaire. L'exposition au manganèse perturbe également la régulation du fer, ce qui pourrait contribuer au mécanisme de neurotoxicité du manganèse (Kwik-Uribe et coll., 2003; Kwik-Uribe et Smith, 2006; Reaney et coll., 2006; Crooks et coll., 2007).
Un taux élevé de manganèse peut perturber la régulation et l'interaction des neurotransmetteurs (DA, Glu et GABA) dans les noyaux gris centraux (Chandra et coll., 1979a; Deskin et coll.,1980; Chandra et Shukla, 1981; Lai et coll., 1982, 1984; Subhash et Padmashree, 1991; Komura et Sakamoto, 1994; Ranasinghe et coll., 2000; Calabresi et coll., 2001; Montes et coll., 2001; Tran et coll., 2002a, 2002b; Fitsanakis et coll., 2006; McDougall et coll., 2008; Burton et Guilarte, 2009; Peneder et coll., 2011).
La DA joue un rôle dans la régulation de la cognition, du comportement, de l'activité motrice et de la sécrétion neuroendocrine (Fitsanakis et coll., 2006; Farina et coll., 2013; Guilarte, 2013), tandis que les voies dopaminergiques participent à la régulation des comportements liés aux fonctions exécutives (p. ex. mémoire, apprentissage, attention) (Kern et coll., 2010). Environ 80 % de la DA extracellulaire est recyclée dans les neurones présynaptiques au moyen de son recaptage par les transporteurs de dopamine (DAT et TNE dépendants du Na+/Cl-) qui se trouvent principalement dans le noyau caudé, le putamen et le noyau accumbens. L'activité des DAT est essentielle à l'homéostasie cérébrale de la DA, car elle contribue au relargage cellulaire de la DA (Roth et coll., 2013) et aide à contrôler la durée et la dimension de la signalisation dopaminergique dans le cerveau.
Les déficits neurologiques relevés dans les études chez les animaux, notamment les rongeurs et les primates non humains, étaient accompagnés d'une altération du taux de DAT et du nombre de récepteurs de la DA, et d'une altération de la réponse aux antagonistes de la DA. Puisque le nombre de DAT augmente tout au long du développement pour culminer à l'âge adulte (Roth et coll., 2013), il a été avancé que les effets cognitifs et neurocomportementaux observés chez les enfants après une exposition au manganèse pourraient être liés à des effets sur le système dopaminergique pendant le développement (Neal et Guilarte, 2013).
Le glutamate (Glu) est le neurotransmetteur excitatoire le plus abondant dans le cerveau et il pourrait jouer un rôle dans le développement du SNC et dans diverses fonctions de ce dernier, telles que la cognition, l'apprentissage et la mémoire (Fitsanakis et coll., 2006). Un taux élevé de manganèse dans les astrocytes semble entraîner une neurotoxicité principalement par stress oxydatif et dysfonctionnement mitochondrial, mais il semble également nuire au cycle de couplage métabolique Gln-Glu entre les astrocytes et les neurones (c.-à-d. le cycle Gln/Glu-GABA), lequel joue un rôle crucial pour le fonctionnement normal du cerveau (Erikson et Aschner, 2003; Aschner et coll., 2009; Sidoryk-Wegrzynowicz et coll., 2009; Farina et coll., 2013; Karki et coll., 2013; Sidoryk-Wegrzynowicz et Aschner, 2013a; Sidoryk-Wegrzynowicz et Aschner, 2013b). Le cycle Gln/Glu-GABA est essentiel pour un fonctionnement optimal du SNC, parce qu'il produit les acides aminés neurotransmetteurs Glu (excitateur) et GABA (inhibiteur) par des interactions dynamiques entre les astrocytes et les neurones (Sidoryk-Wegrzynowicz et Aschner, 2013b). L'interruption de ce cycle provoque des changements dans les transmissions glutamatergiques ou GABAergiques ainsi que dans le métabolisme du Gln (Zwingmann et coll., 2003; Sidoryk-Wegrzynowicz et coll., 2009; Sidoryk-Wegrzynowicz et Aschner, 2013a; Sidoryk-Wegrzynowicz et Aschner, 2013b). De plus, la perturbation du métabolisme et de la fonction astrocytique pourrait empêcher les astrocytes de fournir les substrats utilisés par les neurones pour le métabolisme des neurotransmetteurs, ce qui entraîne une diminution de l'oxydation du glucose dans les neurones, une détérioration du métabolisme énergétique des neurones et une perturbation des processus de neurotransmission (Zwingmann et coll., 2003; Sidoryk-Wegrzynowicz et Aschner, 2013b).
L'exposition au manganèse peut accroître la fréquence et l'amplitude des potentiels postsynaptiques excitateurs dans le striatum, en raison de l'hyperactivité des neurones corticostriataux (Centonze et coll., 2001; Fitsanakis et coll., 2006), ou favoriser l'excitotoxicité par une suractivation des récepteurs post-synaptiques du Glu (Fitsanakis et coll., 2006). L'hyperactivité du récepteur au Glu N-méthyl-D-aspartate peut provoquer une augmentation de la consommation d'énergie, en raison de l'entrée d'ions Na+ et Ca2+ qui doivent être activement expulsés de la cellule. Les cellules affaiblies en énergie peuvent permettre une libération passive de Glu, causant ainsi une élévation de la concentration extracellulaire de Glu et, en conséquence, une excitation anormale des neurones striataux (excitotoxicité) (Erikson et Aschner, 2003; Fitsanakis et Aschner, 2005; Fitsanakis et coll., 2006).
Des données contradictoires ont été publiées au sujet du GABA, certains groupes de chercheurs faisant état d'une augmentation des taux de GABA striatal causée par le manganèse, alors que d'autres groupes n'ont constaté aucun effet lié au manganèse ou, au contraire, une diminution des taux de GABA dans le striatum ou le cortex frontal (Fitsanakis et coll., 2006; Racette et coll., 2012; Martinez-Finley et coll., 2013; Michalke et Fernsebner, 2014). Ces conclusions divergentes peuvent s'expliquer par des différences méthodologiques (p. ex. voie ou durée de l'exposition, âge au moment de l'exposition) ou par la contribution et l'altération d'autres systèmes de neurotransmetteurs (Martinez-Finley et coll., 2013).
12.0 Classification et évaluation
Bien que le manganèse soit un élément essentiel, les carences en manganèse sont très rares puisque les besoins nutritionnels sont facilement comblés par l'alimentation. Les préoccupations relatives aux effets toxiques du manganèse concernent principalement les expositions excessives, en particulier pour les nourrissons, puisqu'ils ne possèdent pas les mécanismes de régulation homéostatique nécessaires à la stabilisation des taux de manganèse dans les tissus (Costa et Aschner, 2014).
Les études existantes menées chez les humains et les animaux de laboratoire ne permettent pas de proposer la cancérogénicité comme effet préoccupant clé dans l'évaluation des risques associés au manganèse. L'U.S. EPA (1999) juge que les données sont insuffisantes pour évaluer le potentiel cancérogène du manganèse pour les humains. Le manganèse n'a pas été classé par le CIRC. Un effet autre que le cancer a donc été choisi pour l'évaluation des risques associés à la présence de manganèse dans l'eau potable.
Chez les mammifères, la principale cible de la toxicité du manganèse semble être le SNC, suivi de l'appareil reproducteur. Il a été établi que le manganèse était facilement absorbé dans le SNC après une exposition par voie orale, mais des concentrations élevées peuvent également se retrouver dans d'autres tissus comme les poumons, les reins et les testicules (Aschner et coll., 2005; Bock et coll., 2008).
Plusieurs études épidémiologiques indiquent une possible association entre l'exposition au manganèse dans l'eau potable et des effets neurologiques chez les enfants (Bouchard et coll., 2011; Khan et coll., 2011; Roels et coll., 2012; Oulhote et coll., 2014). Ces effets comprennent une déficience intellectuelle et de moins bonnes fonctions neurocomportementales (mémoire, attention, fonction motrice, hyperactivité) entre les quintiles inférieur et supérieur d'exposition au manganèse dans l'eau potable qui ont été observés, où les concentrations médianes variaient de 1 à 216 µg/L (Bouchard et coll., 2011; Oulhote et coll., 2014).
Ces études ne peuvent être utilisées pour effectuer une évaluation quantitative des risques en raison des limites qu'elles présentent, à savoir les facteurs de confusion potentiels, des estimations inadéquates de l'exposition, le risque de biais et l'absence de détermination de la temporalité des effets, et du fait qu'on ne dispose pas d'un point de départ clairement établi (nécessaire pour une analyse dose-réponse). Cependant, les résultats de ces études peuvent être utilisés pour appuyer qualitativement le choix du principal effet pour une évaluation quantitative menée chez les animaux, puisque des effets similaires représentant des comportements liés à la fonction exécutive ont été étudiés chez les rongeurs (p. ex. l'hyperactivité [mesurée par un test en espace ouvert] et des déficits d'apprentissage [mesurés à l'aide du labyrinthe radial à huit branches]; Kern et coll., 2010). En outre, d'après certaines études, les effets sur la cognition et le comportement neurologique observés chez les enfants après une exposition au manganèse pourraient être liés aux effets sur le système dopaminergique pendant le développement (Neal et Guilarte, 2013). De plus, les données mécanistes semblent révéler qu'il existe des éléments communs aux rongeurs et aux primates non humains quant au rôle du système dopaminergique dans la neurotoxicité induite par le manganèse (Neal et Guilarte, 2013). L'Organisation de coopération et de développement économiques (OCDE), (2007) recommande le rat comme modèle de choix à utiliser pour l'extrapolation de la neurotoxicité développementale aux humains.
Plusieurs études menées sur des animaux ont établi des LOAEL après une exposition au manganèse par voie orale. La documentation publiée soulève des préoccupations quant à la pertinence pour les humains de certains des effets étudiés, et bon nombre d'études portent uniquement sur les effets après une exposition de courte durée, sans offrir de suivi à long terme. Toutefois, trois études menées sur les animaux se démarquent par le fait qu'elles évaluent de près et quantifient les effets neurologiques qui concordent avec ceux relevés dans les études épidémiologiques, en tenant compte des effets observés à long terme (Kern et coll., 2010, 2011; Beaudin et coll., 2013).
Les études de Kern et de Beaudin ont été choisies comme fondement pour la présente évaluation des risques en raison de leur rigueur dans l'évaluation des effets neurodéveloppementaux en début de vie (les effets neurocomportementaux observés sont appuyés par les résultats neurochimiques correspondants) qui concordent avec les constatations des études épidémiologiques (Bouchard et coll., 2011; Khan et coll., 2011; Roehls et coll., 2012; Oulhote et coll., 2014). Ces études ont établi une LOAEL de 25 mg Mn/kg p.c. par jour pour différents effets neurologiques chez le rat. En plus d'apporter la preuve que l'exposition au manganèse en début de vie peut entraîner des effets comportementaux et sensori-moteurs, ces études ont fourni un appui mécaniste en démontrant l'existence des changements neurostructuraux et neurochimiques correspondants. De plus, Kern et coll. (2011) et Beaudin et coll. (2013) ont démontré que l'exposition au manganèse en début de vie entraîne des effets qui persistent tout au long de la vie adulte, après que les concentrations de manganèse dans le cerveau sont revenues à la normale.
Malgré les forces citées ci-dessus, il importe de préciser que les études clés choisies ne reflètent pas la LOAEL la plus faible relevée dans la documentation pour les effets neurologiques liés à une exposition au manganèse par voie orale, et qu'une analyse de la dose de référence n'a pas été possible puisque seules deux doses ont été testées. D'autres études ont fait état d'une neurotoxicité résultant de l'exposition au manganèse par voie orale chez des rats, des souris et des primates non humains, à des concentrations allant de 0,106 mg/kg p.c. par jour pour les primates non humains (Golub et coll., 2005) à 6,5 mg/kg p.c. par jour pour les jeunes rats adultes (Vezer et coll., 2005, 2007). Toutefois, on juge que ces études à elles seules ne suffisent pas pour effectuer une évaluation des risques (Chandra et Shukla, 1978; Chandra et coll., 1979a, 1979b; Deskin et coll., 1980; Gupta et coll., 1980; Oner et Senturk, 1995, 1996; Shukakidze et coll. 2002, 2003; Tran et coll., 2002b; Larishvili et coll., 2009; Moreno et coll., 2009a, 2009b). Ces études comportent de nombreuses limites, telles que des lacunes dans les données concernant les effets à long terme, un manque d'information sur la dose fournie aux animaux et des facteurs de confusion qui nuisent à l'interprétation des résultats. Néanmoins, ces études appuient le choix de la neurotoxicité comme principal effet préoccupant pour cette évaluation des risques.
Il faut garder à l'esprit que plusieurs facteurs peuvent avoir une incidence sur l'ampleur des effets toxiques associés à l'exposition au manganèse dans l'eau potable chez les nourrissons, notamment la biodisponibilité accrue du manganèse ingéré à jeun, la variabilité de la forme chimique et de l'état de valence du manganèse dans l'eau potable, et le fait que l'absorption et la rétention du manganèse sont plus importantes chez les nourrissons que chez les adultes (Dorothy Klimis-Zacas, 1993; Costa et coll., 2014; Aschner et Aschner, 2005; Keen et coll., 1986). Il convient également de noter que la présente évaluation des risques tient compte des études les plus appropriées dans le contexte de l'élaboration d'une recommandation pour le taux de manganèse dans l'eau potable. La documentation scientifique et les évaluations des risques antérieures reconnaissent que le manganèse ne présente pas la même biodisponibilité à jeun selon qu'il provient des aliments ou de l'eau potable (Ruoff, 1995; U.S. EPA, 2002, 2004; Bouchard et coll., 2011), et il n'existe aucune donnée quantitative sur la biodisponibilité du manganèse selon la source d'exposition chez les nourrissons. Les concentrations de manganèse dans les cheveux des enfants (un biomarqueur de l'exposition au manganèse) corrélaient avec l'exposition au manganèse par l'eau potable, mais non à l'exposition par les aliments (Bouchard et coll., 2011). Compte tenu des différences de biodisponibilité entre les diverses voies et sources d'exposition, et de la capacité limitée de la population vulnérable à maintenir l'homéostasie du manganèse, on a choisi avec soin les études ayant les voies et les sources d'exposition au manganèse les plus appropriées pour obtenir une valeur basée sur la santé pour le taux de manganèse dans l'eau potable.
Étant donné les défis posés par l'utilisation des études épidémiologiques existantes menées chez les humains pour l'évaluation quantitative des risques, des études chez les animaux qui étaient représentatives des effets constatés chez les humains ont été utilisées pour quantifier les risques dans la présente évaluation. Les études de Kern et coll. (2010, 2011) et de Beaudin et coll. (2013) ont été menées chez des rats nouveau-nés afin de refléter les risques pour les nourrissons (sous-population la plus sensible) sur le plan du développement. Les nourrissons (et les nouveau-nés) sont particulièrement sensibles aux effets du manganèse en raison de leur capacité accrue d'absorption et de leur faible capacité d'excrétion biliaire. Des éléments probants indiquent également qu'une exposition au manganèse en début de vie, pendant une période cruciale du développement du système dopaminergique, peut entraîner des effets neurotoxiques persistant à l'âge adulte.
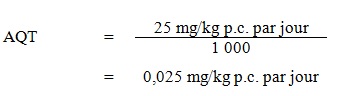
Figure 1 - Description textuel
L'AQT pour le manganèse est de 0,025 mg/kg de poids corporel par jour. Cet AQT est obtenu en divisant la LOAEL de 25 mg/kg poids corporel par jour par le facteur d'incertitude de 1000.
où :
- AQT est l'apport quotidien tolérable, c'est-à-dire la dose de manganèse provenant de l'eau potable qui ne devrait pas poser de risque pour la santé humaine. Il convient de noter que la biodisponibilité du manganèse varie de façon importante en fonction de la voie et de la source d'exposition (aliments, air et eau);
- 25 mg/kg p.c. par jour est la LOAEL tirée des études de Kern et coll. (2010, 2011) et de Beaudin et coll. (2013). Elle repose sur les effets neurologiques observés après une exposition postnatale au manganèse chez le rat;
- 1 000 représente le facteur d'incertitude, choisi pour tenir compte de l'extrapolation interspécifique (×10), de la variabilité intraspécifique (×10), et de l'utilisation d'une LOAEL plutôt que d'une NOAEL (×10).
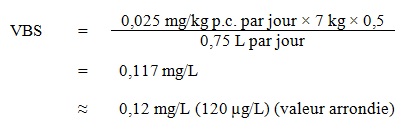
Figure 2 - Description textuel
La VBS pour le manganèse dans l'eau potable est de 0,12 mg/L (arrondie). Cette valeur est calculée en multipliant l'AQT de 0,025 mg/kg de poids corporel par jour par 7 kg, le poids corporel moyen d'un nourrisson puis par le facteur d'attribution de 0,5, qui tient compte de la contribution de l'eau potable à l'apport quotidien tolérable, et en divisant le résultat par 0,75 L, soit le volume moyen d'eau potable ingéré quotidiennement par un nourrisson (0 – 6 mois).
où :
- 0,025 mg/kg p.c. par jour est l'AQT calculé ci-dessus;
- 7 kg est le poids corporel moyen d'un nourrisson (0 à 6 mois) (Santé Canada, 1994);
- 0,5 est le facteur d'attribution estimé pour l'eau potable; étant donné que le lait maternisé constitue l'alimentation totale des nourrissons qui ne sont pas nourris au sein au cours des premiers mois de leur vie, les concentrations potentiellement élevées de manganèse présentes dans le lait maternisé et dans l'eau utilisée pour sa préparation sont considérées comme les principales sources d'exposition. Comme la quantité de manganèse contenue dans l'eau potable et le lait maternisé varie grandement, on suppose que la moitié de la quantité totale potentielle de manganèse consommée provient de l'eau potable, et que l'autre moitié provient du lait maternisé. On s'attend à ce que la quantité de manganèse provenant d'autres sources soit négligeable pour ce groupe d'âge;
- 0,75 L par jour est le volume estimé d'eau du robinet consommé par un nourrisson nourri au biberon dans le groupe des 0 à 6 mois (Santé Canada, 1994).
12.1 Considérations internationales
D'autres organismes ont fixé des limites pour la concentration de manganèse dans l'eau potable. En général, deux valeurs différentes sont établies : une pour les limites d'ordre esthétique ou opérationnel, et une fondée sur la santé humaine.
Le Minnesota Department of Health (département de la santé du Minnesota) a élaboré un document d'orientation par paliers fondé sur le même effet et la même étude clé (Kern et coll., 2010) que ceux utilisés par Santé Canada pour dériver sa VBS. Ce département a établi une concentration de manganèse dans l'eau potable de 0,1 mg/L pour les enfants de moins d'un an et de 0,3 mg/L pour les enfants ayant au moins un an et les adultes (MDH, 2012).
L'U.S. EPA a établi un niveau maximal secondaire de contaminant (secondary maximum contaminant level) de 0,05 mg/L pour le manganèse dans l'eau potable, en se fondant sur des considérations d'ordre esthétique. Il a en outre publié un avis sanitaire non réglementaire de 0,3 mg/L, en se fondant sur l'absence d'effets dans des études de toxicité du manganèse par voie alimentaire (U.S. EPA, 2004).
L'Organisation mondiale de la Santé a établi une valeur basée sur la santé de 0,4 mg/L, en se fondant sur l'absence d'effets dans un ensemble d'études de toxicité du manganèse par voie alimentaire (OMS, 2011). L'OMS a déterminé qu'il n'était pas nécessaire d'établir une ligne directrice officielle, puisque la valeur basée sur la santé est largement supérieure aux concentrations de manganèse habituellement présentes dans l'eau potable.
Les recommandations australiennes (Australian Drinking Water Guidelines) donnent une valeur guide basée sur la santé de 0,5 mg/L, calculée d'après un niveau d'exposition au manganèse jugé sécuritaire par l'OMS et valable quelle que soit la source d'exposition, ainsi qu'une recommandation d'ordre esthétique de 0,1 mg/L pour le manganèse dans l'eau potable, calculée d'après les expériences des usines de traitement concernant l'acceptation de l'eau par les consommateurs (NHMRC, 2011).
Dans l'Union européenne, la directive du Conseil sur la qualité des eaux destinées à la consommation humaine, annexe I, mentionne le manganèse dans la partie C en tant que paramètre indicateur, avec une valeur paramétrique de 0,05 mg / L (Union européenne, 1998).
13.0 Justification de la recommandation
Le manganèse est présent naturellement dans l'environnement sous plusieurs états d'oxydation. Le manganèse est largement répandu dans l'air, l'eau et le sol, et il peut se retrouver dans l'eau en provenance de sources naturelles, comme le vieillissement climatique des sols et des roches, ou du fait de l'activité humaine. En général, on retrouve davantage de manganèse dans les eaux souterraines que dans les eaux de surface.
Le manganèse est un élément essentiel pour les humains. Le risque de carence en manganèse est jugé faible au Canada, puisqu'on le retrouve en quantité suffisante dans les aliments. Les études dont on dispose actuellement ne permettent pas de déterminer si le manganèse pourrait être cancérogène, et il n'a pas été classé par le CIRC, ni par l'U.S. EPA pour ce qui a trait à la cancérogénicité. La biodisponibilité du manganèse est plus élevée lorsqu'il est consommé dans l'eau potable que lorsqu'il est ingéré avec les aliments. Les concentrations de manganèse observées dans les cheveux des enfants corrèlent avec l'exposition au manganèse par l'eau potable, mais non avec l'exposition au manganèse par les aliments.
Le système nerveux central semble être la principale cible des effets toxiques du manganèse aussi bien chez les humains que chez les animaux. Plusieurs études épidémiologiques indiquent un lien possible entre l'exposition au manganèse dans l'eau potable et certains effets neurologiques chez les enfants, tels qu'une diminution de la capacité intellectuelle et un moins bon comportement neurologique. Bien que ces études présentent des limites qui nous empêchent de les utiliser pour établir une concentration maximale acceptable (CMA), elles peuvent servir à appuyer qualitativement le choix des principaux effets dans les études menées sur des animaux. Les effets neurologiques relevés chez les enfants correspondent aux effets neurologiques observés dans les principales études menées sur les animaux qui ont servi de fondement au calcul de la valeur basée sur la santé (VBS).
Les nourrissons représentent la sous-population la plus sensible aux effets du manganèse sur la santé, car ils absorbent et retiennent davantage le manganèse que les adultes. Bien que la VBS ait été établie pour la sous-population la plus sensible, elle protège également les enfants et les adultes d'une exposition chronique. En outre, l'exposition au manganèse dans l'eau potable à des concentrations égales ou inférieures à la VBS ne devrait entraîner aucun autre type d'effet toxique associé à l'exposition au manganèse. Une VBS de 0,12 mg/L a été calculée pour le taux de manganèse dans l'eau potable.
Une CMA de 0,12 mg/L (120 µg/L) et un objectif esthétique (OE) de 0,02 mg/L (20 µg/L) sont établis pour le taux de manganèse total dans l'eau potable. La CMA sert à protéger la population la plus sensible, à savoir les nourrissons, contre les effets neurologiques. L'OE permettra de réduire le nombre de plaintes de consommateurs concernant la couleur de l'eau et les taches sur la lessive. La CMA et l'OE proposés pour le manganèse peuvent être mesurés à l'aide des méthodes analytiques existantes et peuvent être atteints avec les techniques de traitement utilisées aux échelles municipale et résidentielle. Dans son processus permanent de révision des recommandations, Santé Canada continuera à suivre les recherches dans ce domaine et recommandera au besoin toute modification de la recommandation qu'il juge appropriée.
14.0 Références
- Aisen, P., Aasa, R. et Redfield, A.G. (1969). The chromium, manganese, and cobalt complexes of transferrin. J. Biol. Chem., 244(17): 4628–4633. [tel que cité dans Santé Canada, 2010]
- Alberta Ministry of Environment and Sustainable Resource Development (2014). Communication personnelle de H. Li, J. Gawor, D. Reid et J. Benjamin.
- Alessio, L., Apostoli, P., Ferioli, A. et Lombardi, S. (1989). Interference of manganese on neuroendocrinal system in exposed workers. Biol. Trace Elem. Res., 21: 249–253. [tel que cité dans Santé Canada, 2010]
- Ali, M.M., Murthy, R.C., Saxena D.K., Srivastava, R.S. et Chandra, S.V. (1983). Effect of low protein diet on manganese neurotoxicity: I. Developmental and biochemical changes. Neurobehav. Toxicol.Teratol., 5(3): 377–383. [tel que cité dans Santé Canada, 2010]
- Ali, M.M., Murthy, R.C., Mandal, S.K. et Chandra, S.V. (1985). Effect of low protein diet on manganese neurotoxicity: III. Brain neurotransmitter levels. Neurobehav. Toxicol.Teratol., 7: 427–431. [tel que cité dans Santé Canada, 2010]
- Andersen, O. (1983). Effects of coal combustion products and metal compounds on sister chromatid exchange (SCE) in a macrophage-like cell line. Environ. Health Perspect., 47: 239–253. [tel que cité dans NTP, 1993]
- Andersen, M.E., Gearhart, J.M. et Clewell, H.J. 3rd (1999). Pharmacokinetic data needs to support risk assessments for inhaled and ingested manganese. Neurotoxicology, 20(2): 161–171. [tel que cité dans Santé Canada, 2010]
- Anderson, J.G., Cooney, P.T. et Erikson, K.M. (2007). Brain manganese accumulation is inversely related to gamma-amino butyric acid uptake in male and female rats. Toxicol. Sci., 95(1): 188–195.
- Anderson, J.G., Fordahl, S.C., Cooney, P.T., Weaver, T.L., Colyer, C.L. et Erikson, K.M. (2008). Manganese exposure alters extracellular GABA, GABA receptor and transporter protein and mRNA levels in the developing rat brain. Neurotoxicology, 29(6): 1044–1053.
- Anderson, J.G., Fordahl, S.C., Cooney, P.T., Weaver, T.L., Colyer, C.L. et Erikson, K.M. (2009). Extracellular norepinephrine, norepinephrine receptor and transporter protein and mRNA levels are differentially altered in the developing rat brain due to dietary iron deficiency and manganese exposure. Brain Res., 1281: 1–14.
- Angara, G., Cummings, L., Knocke, W.R. et Budd, G.C. (2004). Intermediate and long-term manganese control strategies during the upgrade of the Little Falls Water Treatment Plants. Proceedings of the American Water Works Association Water Quality Technology Conference.
- APHA, AWWA et WEF (1992). Standard methods for the examination of water and wastewater. 18e édition. American Public Health Association, American Water Works Association et Water Environment Federation, Washington, D.C.
- APHA, AWWA et WEF (1995). Standard methods for the examination of water and wastewater. 19e édition. American Public Health Association, American Water Works Association et Water Environment Federation, Washington, D.C.
- APHA, AWWA et WEF (1998). Standard methods for the examination of water and wastewater. 20e édition. American Public Health Association, American Water Works Association et Water Environment Federation, Washington, D.C.
- APHA, AWWA et WEF (2005). Standard methods for the examination of water and wastewater. 21e édition. American Public Health Association, American Water Works Association et Water Environment Federation, Washington, D.C.
- APHA, AWWA et WEF (2012). Standard methods for the examination of water and wastewater. 22e édition. American Public Health Association, American Water Works Association et Water Environment Federation, Washington, D.C.
- Archibald, F.S. et Tyree, C. (1987). Manganese poisoning and the attack of trivalent manganese upon catecholamines. Arch. Biochem. Biophys., 256(2): 638–650. [tel que cité dans Santé Canada, 2010]
- Arnaud, J. et Favier, A. (1995). Copper, iron, manganese and zinc contents in human colostrum and transitory milk of French women. Sci. Total Environ., 159(1): 9–15. [tel que cité dans Santé Canada, 2010]
- Arnich, N., Cunat, L., Lanhers, M.C. et Burnel, D. (2004). Comparative in situ study of the intestinal absorption of aluminum, manganese, nickel, and lead in rats. Biol. Trace Elem. Res., 99:(1–3): 157–171. [tel que cité dans Santé Canada, 2010]
- Aschner, J.L. et Aschner, M. (2005). Nutritional aspects of manganese homeostasis. Mol. Aspects Med. 26(4–5): 353–362.
- Aschner, M., Vrana, K.E. et Zheng, W. (1999). Manganese uptake and distribution in the central nervous system (CNS). Neurotoxicology, 20(2–3): 173–180. [tel que cité dans Santé Canada, 2010]
- Aschner, M., Erikson, K.M. et Dorman, D.C. (2005). Manganese dosimetry: Species differences and implications for neurotoxicity. Crit. Rev. Toxicol., 35(1): 1–32.
- Aschner, M., Guilarte, T.R., Schneider, J.S. et Zheng, W. (2007). Manganese: recent advances in understanding its transport and neurotoxicity. Toxicol. Appl. Pharmacol., 221(2): 131–147.
- Aschner, M., Erikson, K.M., Herrero Hernandez, E., Hernandez, E.H. et Tjalkens, R. (2009). Manganese and its role in Parkinson's disease: from transport to neuropathology. Neuromolecular Med., 11(4): 252–266.
- Assem, F.L., Holmes, P. et Levy, L.S. (2011). The mutagenicity and carcinogenicity of inorganic manganese compounds: a synthesis of the evidence. J. Toxicol. Env. Heal. B, 14(8): 537–570.
- ATSDR (2012). Toxicological profile for manganese. U.S. Department of Health and Human Services. Public Health Service. Atlanta, Georgia.
- Avila, D.S., Gubert, P., Fachinetto, R., Wagner, C., Aschner, M., Rocha, J.B. et coll. (2008). Involvement of striatal lipid peroxidation and inhibition of calcium influx into brain slices in neurobehavioral alterations in a rat model of short–term oral exposure to manganese. Neurotoxicology, 29(6): 1062–1068.
- AWWA (1984). Removing iron and manganese from groundwater. Confluence, 76(11): 67–69.
- AWWA (1993). Committee Report: Research needs for inorganic contaminants. J. Am. Water Works Assoc., 5: 106 –113.
- AWWA (2005). Microfiltration and ultrafiltration membranes for drinking water. M53 Manual of Water Supply Practices. American Water Works Association, Denver, Colorado.
- Ayotte, J.D., Gronberg, J.M. et Apodaca, L.E (2011). Trace elements and radon in groundwater across the United States. National Water Quality Assessment Program. United States Geological Survey. Scientific Investigations Report 2011-5059.
- Baldwin, M., Mergler, D., Larribe, F., Belanger, S., Tardif, R., Bilodeau, L. et Hudnell, K. (1999). Bioindicator and exposure data for a population based study of manganese. Neurotoxicology, 20(2–3): 343–353.
- Baranowska, H., Ejchart, A. et Putrament, A. (1977). Manganese mutagenesis in yeast. V. On mutation and conversion induction in nuclear DNA. Mutat. Res., 42: 343–348. [tel que cité dans NTP, 1993]
- Barbeau, B., Gauthier, V., Julienne, K. et Carrière, A. (2005). Dead-end flushing of a distribution system: Short and long-term effects on water quality. J. Water Supply Res. T., 54(6): 371–383.
- Barbeau, B., Carriere, A. et Bouchard, M. (2011). Spatial and temporal variations in manganese concentrations in drinking water. J. Environ. Sci. Health A Tox. Hazard. Subst. Environ. Eng., 46(6): 608–616.
- Barceloux, D.G. (1999). Manganese. J. Toxicol. Clin. Toxicol., 37(2): 293–307.
- Beaudin, S.A., Nisam, S. et Smith, D.R. (2013). Early life versus lifelong oral manganese exposure differently impairs skilled forelimb performance in adult rats. Neurotoxicol. Teratol., 38: 36–45.
- Beaudin, S.A., Strupp, B.J., Strawderman, M. et Smith, D.R. (2017). Early postnatal manganese exposure causes lasting impairment of selective and focused attention and arousal regulation in adult rats. Environ. Health Perspect., 125(2): 230–237.
- Benskin, P. et Linder, K. (2004). Hypoliminion withdrawal renews reservoir. Opflow, 5: 12–15.
- Bertinchamps, A.J., Miller, S.T. et Cotzias, G.C. (1965). Interdependence of routes excreting manganese. Am. J. Physiol., 211: 217–224.
- Betharia, S. et Maher, T.J. (2012). Neurobehavioral effects of lead and manganese individually and in combination in developmentally exposed rats. Neurotoxicology, 33(5): 1117–1127.
- Bhang, S., Cho, S., Kim, J., Hong, Y., Shin, M., Yoo, H.J., Cho, I.H., Kim, Y. et Kim, B. (2013). Relationship between blood manganese levels and children's attention, cognition, behavior, and academic performance: A nationwide cross-sectional study. Environ. Res., 126(0): 9–16.
- Bierlein, K.A., Knocke, W.R., Tobiason, J.E., Subramaniam, Pham, M. et Little, J.C. (2015). Modeling manganese removal in a pilot-scale postfiltration contractor. J. Am. Water Works Assoc., 107(2): 109–119.
- Bikashvili, T.Z., Shukakidze, A.A. et Kiknadze, G.I. (2001). Changes in the ultrastructure of the rat cerebral cortex after oral doses of manganese chloride. Neurosci. Behav. Physiol., 31(4): 385–389.
- Bock, N.A., Paiva, F.F., Nascimento, G.C., Newman, J.D. et Silva, A.C. (2008). Cerebrospinal fluid to brain transport of manganese in a non-human primate revealed by MRI. Brain Res., 1198: 160–170.
- Bonilla, E. (1978). Increased GABA content in caudate nucleus of rats after chronic manganese chloride administration. J. Neurochem., 31(2): 551–552.
- Bonilla, E. (1980). L-tyrosine hydroxylase activity in the rat brain after chronic oral administration of manganese chloride. Neurobehav. Toxicol., 2: 37–41. [tel que cité dans Newland, 1999]
- Bonilla, E. (1984a). Chronic manganese intake induces changes in the motor activity of rats. Exp. Neurol., 84(3): 696–700.
- Bonilla, E. (1984b). Effects of chronic manganese intake on the levels of biogenic amines in rat brain regions. Neurobeh. Toxicol. Teratol., 6: 341–344.
- Bouchard, M.F., Sauve, S., Barbeau, B., Legrand, M., Brodeur, M.E., Bouffard, T., Limoges, E., Bellinger, D.C. et Mergler, D. (2011). Intellectual impairment in school-age children exposed to manganese from drinking water. Environ. Health Perspect., 119(1): 138–143.
- Bouchard, M.F., Surette, C., Cormier, P. et Foucher, D. (2016). Exposure to manganese from drinking water and IQ in school-age children. International Society for Environmental Epidemiology, Enviro. Health Perspect. Numéro de résumé : P3-124 | ID: 4713.
- Bowler, R.M., Gysens, S., Diamond, E., Nakagawa, S., Drezgic, M. et Roels, H.A. (2006). Manganese exposure: Neuropsychological and neurological symptoms and effects in welders. Neurotoxicology, 27(3): 315–326.
- Bowman, A.B., Kwakye, G.F., Hernandez, E.H. et Aschner, M. (2011). Role of manganese in neurodegenerative diseases. J. Trace Elem. Med. Biol., 25(4): 191–203.
- Brandhuber, P., Clark, S., Knocke, W. et Tobiason, J. (2013). Guidance for the treatment of manganese. Water Research Foundation, Denver, Colorado.
- Brandhuber, P., Craig, S., Friedman, M.J., Hill, A., Booth, S. et Hanson, A. (2015). Legacy of manganese accumulation in water systems. Water Research Foundation, Denver, Colorado.
- Brenneman, K.A., Cattley, R.C., Ali, S.F. et Dorman, D.C. (1999). Manganese-induced developmental neurotoxicity in the CD rat: Is oxidative damage a mechanism of action? Neurotoxicology, 20(2–3): 477–488. [tel que cité dans Santé Canada, 2010]
- British Columbia Ministry of Health (2014). Communication personnelle de D. Fishwick.
- Brna, P., Gordon, K., Dooley, J.M. et Price, V. (2011). Manganese toxicity in a child with iron deficiency and polycythemia. J. Child Neurol., 26(7): 891–894.
- Brodeur, M.E. et Barbeau, B. (2015). Performance of point-of-use and point-of-entry technologies for the removal of manganese in drinking water: Summary of the EDU-MANGO Epidemiological Study. Rapport préparé pour Santé Canada.
- Bruins, J.H., Petrusevski, B., Slokar, Y.M., Huysman, K., Koen, J., Kruithof, J.C. et Kennedy, M.D. (2015). Biological and physico-chemical formation of Birnessite during the ripening of manganese removal filters. Water Res., 69: 154–161.
- Burger, M.S., Mercer, S.S., Shupe, G.D. et Gagnon, G.A. (2008a). Manganese removal during bench-scale biofiltration. Water Res., 42: 4733–4742.
- Burger, M.S., Krentz, C.A., Mercer, S.S. et Gagnon, G.A. (2008b). Manganese removal and occurrence of manganese-oxidizing bacteria in full-scale biofilters. J. Water Supply Res. T., 57(5): 351–359.
- Burton, N.C. et Guilarte, T.R. (2009). Manganese neurotoxicity: Lessons learned from longitudinal studies in nonhuman primates. Environ. Health Perspect., 117(3): 325–332.
- Cahill, D.F., Bercegeay, M.S., Haggerty, R.C., Gerding, J.E. et Gray, L.E. (1980). Age-related retention and distribution of ingested Mn3O4 in the rat. Toxicol. Appl. Pharmacol., 53(1): 83–91. [tel que cité dans Santé Canada, 2010]
- Calabresi, P., Ammassari-Teule, M., Gubellini, P., Sancesario, G., Morello, M., Centonze, D. et coll. (2001). A synaptic mechanism underlying the behavioral abnormalities induced by manganese intoxication. Neurobiol. Dis., 9: 419–432.
- Camara, E., Montreuil, K.R., Knowles, A.D. et Gagnon, G.A. (2013). Role of the water main in lead service line replacement: A case study. J. Am. Water Works Assoc., E423–E431.
- Carlson, K.H., Knocke, W.R. et Gertig, K.R. (1997). Optimizing treatment through Fe and Mn fractionations. J. Am. Water Works Assoc., 89(4): 162–171.
- Carrière, A., Gauthier, V., Desjardins, R., et Barbeau, B. (2005). Evaluation of loose deposits in distribution systems through unidirectional flushing. J. Am. Water Works Assoc., 97(9): 82–92.
- Carrière, A., Brouillon, M., Sauvé, S., Bouchard, M. et Barbeau, B. (2011). Performance of point-of-use devices to remove manganese from drinking water. J. Environ. Sci. Health A Tox. Hazard Subst. Environ. Eng., 46(6): 601–607.
- Casale, R.J., LeChevallier, M.W. et Pontius, F.W. (2002). Manganese control and related issues. American Water Works Research Foundation et American Water Works Association. Denver, Colorado.
- Casey, C.E., Hambidge, K.M. et Neville, M.C. (1985). Studies in human lactation: Zinc, copper, manganese and chromium in human milk in the first month of lactation. Am. J. Clin. Nutr., 41(6): 1193–1200.
- Casto, B.C., Meyers, J. et DiPaolo, J.A. (1979). Enhancement of viral transformation for evaluation of the carcinogenic or mutagenic potential of inorganic metal salts. Cancer Res., 39: 193–198.
- CCN (2018). Répertoire des organismes de certification accrédités de produits, de processus et de services.Conseils canadien des normes. Disponible à : www.scc.ca/fr/accreditation/certification-de-produits-procedes-et-services/repertoire-des-organismes-de-certification-accredites
- Centonze, D., Gubellini, P., Bernardi, G. et Calabresi, P. (2001). Impaired excitatory transmission in the striatum of rats chronically intoxicated with manganese. Exp. Neurol., 172(2): 469–476.
- Cerrato, J.M., Reyes, L.P., Alvarado, C.N. et Dietrich, A.M. (2006). Effect of PVC and iron materials on Mn(II) deposition in drinking water distribution systems, Water Res., 40: 2720–2726.
- Chan, A.W., Minski, M.J., Lim, L. et Lai, J.C. (1992). Changes in brain regional manganese and magnesium levels during postnatal development: modulations by chronic manganese administration. Résumé. Metab. Brain Dis., 7(1): 21–33.
- Chandra, S.V. (1983). Psychiatric illness due to manganese poisoning. Acta Psychiat. Scand., 67(Suppl 303): 49–54.
- Chandra, S.V. et Imam, Z. (1973). Manganese induced histochemical and histological alterations in gastrointestinal mucosa of guinea pigs. Résumé. Acta pharmacol. Toxicol., 33: 449–458.
- Chandra, S.V. et Shukla, G.S. (1976). Role of iron deficiency in inducing susceptibility to manganese toxicity. Arch. Toxicol., 35(4): 319–323. [tel que cité dans Santé Canada, 2010]
- Chandra, S.V. et Shukla, G.S. (1978). Manganese encephalopathy in growing rats. Environ. Res., 15: 28–37.
- Chandra, S.V. et Shukla, G.S. (1981). Concentrations of striatal catecholamines in rats given manganese chloride through drinking water. J. Neurochem., 36: 683–687.
- Chandra, S.V., Shukla, G.S. et Saxena, D.K. (1979a). Manganese-induced behavioral dysfunction and its neurochemical mechanism in growing mice. J. Neurochem., 33: 1217–1221.
- Chandra, S.V., Srivastava, R.S. et Shukla, G.S. (1979b). Regional distribution of metals and biogenic amines in the brain of monkeys exposed to manganese. Toxicol. Lett., 4(3): 189–192.
- Charlton, N., Tikos, E., Gaffney, L. et Kohl, P. (2002). Breakpoint breakdown: optimization of manganese removal to very low levels with oxide-coated filter media. Proceedings of the American Water Works Association Water Quality Technology Conference.
- Chen, P., Chakraborty, S., Mukhopadhyay, S., Lee, E., Paoliello, M.M., Bowman, A.B. et Aschner, M. (2015). Manganese homeostasis in the nervous system. J. Neurochem., 134(4): 601–610.
- Chen, J.Y., Tsao, G.C., Zhao, Q. et Zheng, H.S. (2001). Differential cytotoxicity of Mn(II) and Mn(III): Special reference to mitochondrial [Fe-S] containing enzymes. Toxicol. Appl. Pharmacol., 175(2): 160–168. [tel que cité dans Santé Canada, 2010]
- Chen, L., Ding, G., Gao, Y., Wang, P., Shi, R., Huang, H. et Tian, Y. (2014). Manganese concentrations in maternal-infant blood and birth weight. Environ. Sci. Pollut. Res. Int., 21(9): 6170–6175.
- Civardi, J. et Tompeck, M. (2015). Iron and manganese removal handbook. 2e édition. American Water Works Association, Denver, Colorado.
- Clark, N.A., Teschke, K., Rideout, K. et Copes, R. (2007). Trace element levels in adults from the west coast of Canada and associations with age, gender, diet, activities, and levels of other trace elements. Chemosphere, 70(1): 155–164.
- Cohen, J.M., Kamphake, L.J., Harris, E.K. et Woodward, R.L. (1960). Taste threshold concentrations of metals in drinking water. J. Am. Water Works Assoc., 52: 660.
- Commission européenne (2000). Opinion of the Scientific Committee on Food on the tolerable upper intake level of manganese. Rapport no SCF/CS/NUT/UPPLEV/21.
- Committee on Nutrition, American Academy of Pediatrics (2003). Dans : Kleinman, R.E. (éditeur), Pediatric Nutrition Handbook, 5e édition.
- Corella-Vargas, R. (1984). [High levels of manganese in the diet of rats (Rattus norvegicus albinicus). I. Effect on reproduction] (Spanish). Arch. Latinoam. Nutr., 34: 457–65. [tel que cité dans Gerber et coll., 2002]
- Corkal, D.R., Braul, L., Poon, D., Hicks, W. et Germin, G. (2005). Piloting small rural systems for Fe, Mn and TDS removal. Proceedings of the 57th Annual Conference of the Western Canada Water and Wastewater Association, Saskatoon, Saskatchewan.
- Costa, L. et Aschner, M., éditeurs (2014). Manganese in health and disease. RSC Publishing.
- Cotzias, G.C., Horiuchi, K., Fuenzalida, S. et Mena, I. (1968). Chronic manganese poisoning. Clearance of tissue manganese concentrations with persistence of the neurological picture. Neurology, 18(4): 376–382. [tel que cité dans Santé Canada, 2010]
- Cotzias, G.C., Miller, S.T., Papavasiliou, P.S. et Tang, L.C. (1976). Interactions between manganese and brain dopamine. Med. Clin. North Am., 60(4): 729–738. [tel que cité dans Santé Canada, 2010]
- CRC Handbook of Chemistry and Physics (1983). 64e édition. CRC Press.
- Criswell, S.R., Perlmutter, J.S., Videen, T.O., Moerlein, S.M., Flores, H.P., Birke, A.M. et Racette, B.A. (2011). Reduced uptake of [18F]FDOPA PET in asymptomatic welders with occupational manganese exposure. Neurology, 76(15): 1296–1301.
- Critchfield, J.W. et Keen, C.L. (1992). Manganese+2 exhibits dynamic binding to multiple ligands in human plasma. Metabolism 41(10): 1087–1092. [tel que cité dans Santé Canada, 2010]
- Crooks, D.R., Ghosh, M.C., Braun-Sommargren, M., Rouault, T.A. et Smith, D.R. (2007). Manganese targets m-aconitase and activates iron regulatory protein 2 in AF5 GABAergic cells. J. Neurosci. Res., 85(8): 1797–809.
- Crossgrove, J.S. et Yokel, R.A. (2004). Manganese distribution across the blood-brain barrier. III. The divalent metal transporter-1 is not the major mechanism mediating brain manganese uptake. Neurotoxicology, 25(3): 451–460. [tel que cité dans Santé Canada, 2010]
- Crossgrove, J.S. et Yokel, R.A. (2005). Manganese distribution across the blood-brain barrier. IV. Evidence for brain influx through store-operated calcium channels. Neurotoxicology, 26(3): 297–307. [tel que cité dans Santé Canada, 2010]
- Crossgrove, J.S., Allen, D.D., Bukaveckas, B.L., Rhineheimer, S.S. et Yokel, R.A. (2003). Manganese distribution across the blood-brain barrier I. Evidence for carrier-mediated influx of manganese citrate as well as manganese and manganese transferrin. Neurotoxicology, 24(1): 3–13. [tel que cité dans Michalke et coll., 2007]
- Davidsson, L., Cederblad, A., Hagebo, E., Lönnerdal, B. et Sandström, B. (1988). Intrinsic and extrinsic labeling for studies of manganese absorption in humans. J. Nutr., 118(12): 1517–1521.
- Davidsson, L., Cederblad, A., Lönnerdal, B. et Sandström, B. (1989a). Manganese retention in man: A method for estimating manganese absorption in man. Am. J. Clin. Nutr., 49(1): 170–179.
- Davidsson, L., Lönnerdal, B., Sandström, B., Kunz, C. et Keen, C.L. (1989b). Identification of transferrin as the major plasma carrier protein for manganese introduced orally or intravenously of after in vitro addition in the rat. J. Nutr., 119(10): 1461–1464.
- Davis, C.D., Malecki, E.A. et Greger, J.L. (1992a). Interactions among dietary manganese, heme iron and non-heme iron in women. Am. J. Clin. Nutr., 56: 926–932. [tel que cité dans Santé Canada, 2010]
- Davis, C.D., Wolf, T.L. et Greger, J.L. (1992b). Varying levels of manganese and iron affect absorption and gut endogenous losses of manganese by rats. J. Nutr., 122: 1300–1308.
- Davis, C.D., Zech, L. et Greger, J.L. (1993). Manganese metabolism in rats: An improved methodology for assessing gut endogenous losses. Proceedings of the Society for Experimental Biology and Medicine, 202(1): 103–108. [tel que cité dans Santé Canada, 2010]
- Day, J.J., Childs, D., Guzman-Karlsson, M.C., Kibe, M., Moulden, J., Song, E., Tahir, A. et Sweatt, J.D. (2013). DNA methylation regulates associative reward learning. Nat. Neurosci., 16(10): 1445–1452.
- Del Toral, M.A., Porter, A. et Schock, M.R. (2013). Detection and evaluation of elevated lead release from service lines: a field study. Environ. Sci. Tech., 47(16): 9300–9307.
- De Méo, M., Laget, M., Castegnaro, M. et Duménil, G. (1991). Genotoxic activity of potassium permanganate in acidic solutions. Mutat. Res., 260(3): 295–306. [tel que cité dans ATSDR 2008]
- Deskin, R., Bursian, S.J. et Edens, F.W. (1980). Neurochemical alterations induced by manganese chloride in neonatal rats. Neurotoxicology, 2: 65–73.
- Deskin, R., Bursian, S.J. et Edens, F.W. (1981). The effect of chronic manganese administration on some neurochemical and physiological variables in neonatal rats. Gen. Pharmacol., 12: 279–280.
- Desole, M.S., Miele, M., Esposito, G., Migheli, R., Fresu, L., De Natale, G. et coll. (1994). Dopaminergic system activity and cellular defense mechanisms in the striatum and striatal synaptosomes of the rat subchronically exposed to manganese. Résumé. Arch. Toxicol., 68(9): 566–570.
- Desole, M.S., Esposito, G., Migheli, R., Fresu, L., Sircana, S., Miele, M. et coll. (1995). Allopurinol protects against manganese-induced oxidative stress in the striatum and in the brainstem of the rat. Neurosci. Lett., 192(2): 73–76.
- Desole, M.S., Esposito, G., Migheli, R., Sircana, S., Delogu, M.R., Fresu, L. et coll. (1997). Glutathione deficiency potentiates manganese toxicity in rat striatum and brainstem and in PC12 cells. Pharmacol. Res, 36(4): 285–292.
- Dikshith, T.S. et Chandra, S.V. (1978). Cytological studies in albino rats after oral administration of manganese chloride. Bull. Environ. Contam. Toxicol., 19: 741–746. [tel que cité dans Santé Canada, 2010]
- Dobson, A.W., Weber, S., Dorman, D.C., Lash, L.K., Erikson, K.M. et Aschner, M. (2003). Oxidative stress is induced in the rat brain following repeated inhalation exposure to manganese sulfate. Biol. Trace Elem. Res., 93(1–3): 113–126.
- Dong, D., Derry, L.A., Lion, L.W. (2003). Pb scavenging from a freshwater lake by Mn oxides in heterogeneous surface coating materials. Water Res., 37: 1662–1666.
- Dorman, D.C., Struve, M.F., Vitarella, D., Byerly, F.L., Goetz, J. et Miller, R. (2000). Neurotoxicity of manganese chloride in neonatal and adult CD rats following subchronic (21-day) high-dose oral exposure. J. Appl. Toxicol., 20(3): 179–187.
- Dorman, D.C., Struve, M.F., Clewell, H.J., 3rd et Andersen, M.E. (2006). Application of pharmacokinetic data to the risk assessment of inhaled manganese. Neurotoxicology, 27(5): 752–764.
- Dörner, K., Dziadzka, S., Höhn, A., Sievers, E., Oldigs, H.D., Schulz-Lell, G. et coll. (1989). Longitudinal manganese and copper balances in young infants and preterm infants fed on breast-milk and adapted cow's milk formulas. British Journal of Nutrition, 61: 559–572. [tel que cité dans Santé Canada, 2010]
- Dupont, C.L. et Tanaka, Y. (1985). Blood manganese levels in children with convulsive disorder. Biochem. Med., 33(2): 246–255.
- Eastman, R.R., Jursa, T.P., Benedetti, C., Lucchini, R.G. et Smith, D.R. (2013). Hair as a biomarker of environmental manganese exposure. Environmental Science & Technology, 47(3), 1629–1637.
- Elbetieha, A., Bataineh, H., Darmani, H. et Al-Hamood, M.H. (2001). Effects of long-term exposure to manganese chloride on fertility of male and female mice. Toxicol. Lett., 119(3): 193–201.
- Environnement Canada (2014). Quality assured data, national air pollution surveillance (NAPS). Ottawa. Disponible à : http://maps-cartes.ec.gc.ca/rnspa-naps/data.aspx?lang=fr.
- Erikson, K.M. et Aschner, M. (2003). Manganese neurotoxicity and glutamate-GABA interaction. Neurochem. Int., 43: 475–480.
- Erikson, K.M., Dorman, D.C., Lash, L.H. et Aschner, M. (2007). Manganese inhalation by rhesus monkeys is associated with brain regional changes in biomarkers of neurotoxicity. Toxicol. Sci., 97(2): 459–466.
- Ericson, J.E., Crinella, F.M., Clarke-Stewart, K.A., Allhusen, V.D., Chan, T. et Robertson, R.T. (2007). Prenatal manganese levels linked to childhood behavioral disinhibition. Neurotoxicol. Teratol., 29(2): 181–187.
- Eum, J.H., Cheong, H.K., Ha, E.H., Ha, M., Kim, Y., Hong, Y.C., Park, H. et Chang, N. (2014). Maternal blood manganese level and birth weight: A MOCEH birth cohort study. Environ. Health, 13(1): 31-069X-13-31.
- Expert Group on Vitamins and Minerals Secretariat (EVM) (2002). Review of manganese – revised version. EVM/99/22.REVISEDAUG2002, United Kingdom.
- Farina, M., Avila, D.S., da Rocha, J.B.T. et Aschner, M. (2013). Metals, oxidative stress and neurodegeneration: A focus on iron, manganese and mercury. Neurochem. Int., 62: 575–594.
- FCM (2003). Qualité de l'eau dans les réseaux de distribution. Fédération canadienne des municipalités. Disponible à : www.fcm.ca/Documents/reports/Infraguide/Water_Quality_in%C2%A0Distribution_System_FR.pdf
- Finley, J.W. et Davis, C.D. (1999). Manganese deficiency and toxicity: Are high or low dietary amounts of manganese cause for concern? Biofactors, 10(1): 15–24. [tel que cité dans Santé Canada, 2010]
- Finley, J.W. et Johnson, P.E. (1996). Manganese deficiency and excess in rodents. Dans :Watson, R.R. (eds.). Trace elements in laboratory rodents. Florida, CRC Press: p. 85–102.
- Finley, J.W., Johnson, P.E. et Johnson, L.K. (1994). Sex affects manganese absorption and retention by humans from a diet adequate in manganese. Am. J. Clin. Nutr., 60(6): 949–955.
- Finley, J.W., Caton, J.S., Zhou, Z. et Davison, K.L. (1997). A surgical model for determination of true adsorption and biliary excretion of manganese in conscious swine fed commercial diets. J. Nutr., 127(12): 2334–2341.
- Finley, J.W., Penland, J.G., Pettit, R.E. et Davis, C.D. (2003). Dietary manganese intake and type of lipid do not affect clinical or neuropsychological measures in healthy young women. J. Nutr., 133(9): 2849–2856. [tel que cité dans Santé Canada 2007]
- Fitsanakis, V.A. et Aschner, M. (2005). The importance of glutamate, glycine, and gamma-aminobutyric acid transport and regulation in manganese, mercury and lead neurotoxicity. Toxicol. Appl. Pharmacol., 204(3): 343–354.
- Fitsanakis, V.A., Au, C., Erikson, K.M. et Aschner, M. (2006). The effects of manganese on glutamate, dopamine and gamma-aminobutyric acid regulation. Neurochem. Int, 48(6–7): 426–433.
- Fitsanakis, V.A., Piccola, G., Marreilha dos Santos, A.P., Aschner, J.L. et Aschner, M. (2007). Putative proteins involved in manganese transport across the blood-brain barrier. Hum. Exp. Toxicol., 26(4): 295–302.
- Fitsanakis, V.A., Thompson, K.N., Deery, S.E., Milatovic, D., Shihabi, Z.K., Erikson, K.M. et coll. (2009). A chronic iron-deficient/high-manganese diet in rodents results in increased brain oxidative stress and behavioral deficits in the Morris water maze. Neurotox. Res., 15(2): 167–178.
- Fitzgerald, D., Chanasky, D.S., Neilson, R.D., Kiely, D. et Audette, R. (2001). Farm well water quality in Alberta. Water Qual. Res. J. Canada, 36(3):565–588.
- Fordahl, S.C., Anderson, J.G., Cooney, P.T., Weaver, T.L., Colyer, C.L. et Erikson, K.M. (2010). Manganese exposure inhibits the clearance of extracellular GABA and influences taurine homeostasis in the striatum of developing rats. Neurotoxicology, 31(6): 639–646.
- Fordahl, S., Cooney, P., Qiu, Y., Xie, G., Jia, W. et Erikson, K.M. (2012). Waterborne manganese exposure alters plasma, brain, and liver metabolites accompanied by changes in stereotypic behaviors. Neurotoxicol. Teratol., 34(1): 27–36.
- Foster, M.L., Bartnikas, T.B., Johnson, L.C., Herrera, C., Pettiglio, M.A., Keene, A.M., Taylor, M.D. et Dorman, D.C. (2015). Pharmacokinetic evaluation of the equivalency of gavage, dietary, and drinking water exposure to manganese in f344 rats. Toxicol. Sci., 145(2): 244–251.
- Friedman, M.J., Hill, A.S., Reiber, S.H., Valentine, R.L., Larsen, G., Young, A., Korshin, G.V. et Peng, C-Y. (2010). Assessment of Inorganics Accumulation in Drinking Water system scales and sediments. Water Research Foundation and United States Environmental Protection Agency, Denver, Colorado.
- Friedman, M.J., Hill, A., Booth, S., Hallett, M., McNeill, L., McLean, J., Stevens, D., Sorensen, D., Hammer, T., Kent, W., De Haan, M., MacArthur, K. et Mitchell, K. (2016). Metals accumulation and release within the distribution system: evaluation and mitigation. Water Research Foundation and United States Environmental Protection Agency, Denver, Colorado.
- Furst, A. (1978). Tumorigenic effect of an organomanganese compound on F344 rats and Swiss albino mice: Brief communication. J. Natl. Cancer Inst., 60: 1171–1173. [tel que cité dans U.S. EPA, 2008; Santé Canada, 2010]
- Gabelich, C.J., Gerringer, F.W., Lee, C.C. et Knocke, W.R. (2006). Sequential manganese desorption and sequestration in anthracite coal and silica sand filter media. J. Am. Water Works Assoc., 98(5): 116–127.
- Galloway, S.M., Armstrong, M.J., Reuben, C., Colman, S., Brown, B., Cannon, C. et coll. (1987). Chromosome aberrations and sister chromatid exchanges in Chinese hamster ovary cells: Evaluations of 108 chemicals. Environ. Mol. Mutagen., 10(Suppl. 10): 1–175.
- Garcia, S.J., Gellein, K., Syversen, T. et Aschner, M. (2006). A manganese-enhanced diet alters brain metals and transporters in the developing rat. Toxicol. Sci., 92(2): 516–525.
- Garcia-Aranda, J.A., Lifshitz, F. et Wapnir, R.A. (1984). Intestinal absorption of manganese in experimental malnutrition. J. Pediatr. Gastroenterol. Nutr., 3: 602–607.
- Garrick, M.D., Dolan, K.G., Horbinski, C., Ghio, A.J., Higgins, D., Porubcin, M. et coll. (2003). DMT1: a mammalian transporter for multiple metals. BioMetals, 16: 41–54. [tel que cité dans Reany and Smith 2005]
- Gavin, C.E., Gunter, K.K. et Gunter, T.E. (1992). Mn2+ sequestration by mitochondria and inhibition of oxidative phosphorylation. Toxicol. Appl. Pharmacol., 115: 1–5. [tel que cité dans Santé Canada, 2010]
- Gerber, G.B., Léonard, A. et Hantson, P. (2002). Carcinogenicity, mutagenicity and teratogenicity of manganese compounds. Crit. Rev. Oncol. Hematol., 42: 25–34.
- Gibbons, R.A., Dixon, S.N., Hallis, K., Russell, A.M., Sansom, B.F. et Symonds, H.W. (1976). Manganese metabolism in cows and goats. Biochim. Biophys. Acta, 444(1): 1–10. [tel que cité dans Davidsson et coll., 1989b; Santé Canada, 2010]
- Gilani, S.H. et Alibhai, Y. (1990). Teratogenicity of metals to chick embryos. J. Toxicol. Environ. Health, 30: 23–31. [tel que cité dans Gerber et coll. 2002]
- Ginige, M.P., Wylie, J. et Plumb, J. (2011). Influence of biofilms on iron and manganese deposition in drinking water distribution systems. Biofouling, 27(2), 151–163.
- Golub, M.S. (2012). Erratum. Neurotoxicol. Teratol., 34(1): 220.
- Golub, M.S., Hogrefe, C.E., Germann, S.L., Tran, T.T., Beard, J.L., Crinella, F.M. et coll. (2005). Neurobehavioral evaluation of rhesus monkey infants fed cow's milk formula, soy formula, or soy formula with added manganese. Neurotoxicol. Teratol., 27(4): 615–627.
- Gonzalez, L.E., Juknat, A.A., Venosa, A.J., Verrengia, N. et Kotler, M.L. (2008). Manganese activates the mitochondrial apoptotic pathway in rat astrocytes by modulating the expression of proteins of the Bcl-2 family. Neurochem. Int., 53(6–8): 408–415.
- Gouvernement du Canada (2014). Règlement sur les aliments et drogues. Dernière modification 2014-01-29. C.R.C., ch. 870. Disponible à : http://laws.justice.gc.ca/fra/reglements/C.R.C.%2C_ch._870/
- Grant, D., Blazak, W.F. et Brown, G.L. (1997). The reproductive toxicology of intravenously administered MnDPDP in the rat and rabbit. Acta Radiologica, 38: 759–769. [tel que cité dans Santé Canada, 2010]
- Gray, E.L. et Laskey, J.W. (1980). Multivariate analysis of the effects of manganese on the reproductive physiology and behavior of the male house mouse. J. Toxicol. Environ. Health, 6: 861–867. [tel que cité dans Santé Canada, 2010]
- Greger, J.L. (1999). Nutrition versus toxicology of manganese in humans: Evaluation of potential biomarkers. Neurotoxicology, 20(2-3): 205–212.
- Gregory, D. et Carlson, K. (2003). Effect of soluble Mn concentration on oxidation kinetics. J. Am. Water Works Assoc., 95(1): 98–108.
- Gruden, N. (1977). Suppression of transduodenal manganese transport by milk diet supplemented with iron. Nutr. Metab. 21(5): 305–309. [tel que cité dans Santé Canada, 2010]
- Guan, H., Wang, M., Li, X., Piao, F., Li, Q., Xu, L., Kitamura, F. et Yokoyama, K. (2014). Manganese concentrations in maternal and umbilical cord blood: Related to birth size and environmental factors. Eur. J. Public Health, 24(1): 150–157.
- Guilarte, T.R. (2013). Manganese neurotoxicity: new perspectives from behavioral, neuroimaging, and neuropathological studies in humans and non-human primates. Front. Aging Neurosci., 5(23): 1–10.
- Gunshin, H., Allerson, C.R., Polycarpou-Schwarz, M., Rofts, A., Rogers, J.T., Kishi, F. et coll. (2001). Iron-dependent regulation of the divalent metal ion transporter. FEBS Letters 509(2): 309–316. [tel que cité dans Santé Canada, 2010]
- Gupta, S.K., Murthy, R.C. et Chandra, S.V. (1980). Neuromelanin in manganese-exposed primates. Toxicol. Lett., 6: 17–20.
- HaMai, D. et Bondy, S.C. (2004). Oxidative basis of manganese neurotoxicity. Ann. N. Y. Acad. Sci., 1012: 129–141.
- HaMai, D., Campbell, A. et Bondy, S.C. (2001). Modulation of oxidative events by multivalent manganese complexes in brain tissue. Free Radic. Biol. Med., 31(6): 763–768. [tel que cité dans Santé Canada, 2010]
- HaMai, D., Rinderknecht, A.L., Guo-Sharman, K., Kleinman, M.T. et Bondy, S.C. (2006). Decreased expression of inflammation-related genes following inhalation exposure to manganese. Neurotoxicology, 27(3): 395–401.
- Han, Z.J., Song, G., Cui, Y., Xia, H.F., Ma, X. (2011). Oxidative stress is implicated in arsenic-induced neural tube defects in chick embryos. Int. J. Dev. Neurosci., 29(7): 673–680.
- Hargette, A. et Knocke, W.R. (2001). Assessement of fate of manganese in oxide-coated filtration systems. J. Environ. Eng., 127(2): 1132–1138.
- Hauser, R.A., Zesiewicz, T.A., Rosemurgy, A.S., Martinez, C. et Olanow, C.W. (1994). Manganese intoxication and chronic liver failure. Ann. Neurol., 36(6): 871–875. [tel que cité dans IOM, 2004; Santé Canada, 2010]
- Haynes, E.H., Sucharew, H., Kuhnell, P., Alden, J., Barnas, M., Wright, R.O., Parsons, P.J., Aldous, K.M., Praamsma, M.L., Beidler, C. et Dietrich, K.N. (2015). Manganese exposure and neurocognitive outcomes in rural school-age children: The Communities Actively Researching Exposure Study (Ohio, USA). Environ. Health Perspect., 123(10): 1066–1071.
- Hazaradze, R.E. (1961). Hygienic background for determining the maximum permissible concentration of manganese in water basins. Gig. Sanit., 26(12): 8–14. [tel que cité dans OMS, 1981]
- He, P., Liu, D.H. et Zhang, G.Q. (1994). Effects of high-level-manganese sewage irrigation on children's neurobehavior. Zhonghua Yu Fang Yi Xue Za Zhi, 28(4): 216–218.
- Hejtmancik, M., Peters, A.C., Toft, J.D., Basaran, A., Sheridan, A. et Athey, P. (1987a). The chronic study of manganese sulfate monohydrate (CAS No. 10034-96-5) in F344 rats. Battelle's Columbus Laboratories, Columbus, Ohio. [tel que cité dans Santé Canada, 2010]
- Hejtmancik, M., Peters, A.C., Toft, J.D., Dersing, R., Basaran, A., Sheridan, A. et coll. (1987b). The chronic study of manganese sulfate monohydrate (CAS No. 10034-96-5) in B6C3F1 mice. Battelle's Columbus Laboratories, Columbus, Ohio. [tel que cité dans Santé Canada, 2010]
- Hernandez-Bonilla, D., Schilmann, A., Montes, S., Rodriguez-Agudelo, Y., Rodriguez-Dozal, S., Solis-Vivanco, R., Rios, C. et Riojas-Rodriguez, H. (2011). Environmental exposure to manganese and motor function of children in mexico. Neurotoxicology, 32(5): 615–621.
- Herzner, J.A., Parmenter, W., Page, J. et Heupler, S. (2003). Manganese control: a back to basics approach to stop customer complaints and works with unconventional processes. Proceedings of the American Water Works Association Water Quality and Technology Conference.
- Hiney, J.K., Srivastava, V.K. et Dees, W.L. (2011). Manganese induces IGF-1 and cyclooxygenase-2 gene expressions in the basal hypothalamus during prepubertal female development. Toxicol. Sci., 121(2): 389–96.
- Holbrook, D.J.J., Washington, M.E., Leake, H.B. et Brubaker, P.E. (1975). Studies on the evaluation of the toxicity of various salts of lead, manganese, platinum, and palladium. Environ. Health Perspect., 10: 95–101.
- Holst, T.C. (2004). Large-scale biological manganese removal: from pilot study to implementation. Proceedings of the American Water Works Association Water Quality and Technology Conference.
- Holzgraefe, M., Poser, W., Kijewski, H. et Beuche, W. (1986). Chronic enteral poisoning caused by potassium permanganate: A case report. J. Toxicol. Clin. Toxicol., 24(3): 235–244.
- Hoyland, V.W., Knocke, W.R., Falkinham III, J.O., Pruden, A. et Singh, G. (2014). Effect of drinking water treatment process parameters on biological removal of manganese from surface water. Water Res., 66: 31–39. Disponible à : www.epa.gov/waterscience/criteria/drinking/dwstandards2009.pdf
- Hussain, S., Lipe, G.W., Slikker, W. et coll. (1997). The effects of chronic exposure of manganese on antioxidant enzymes in different regions of rat brain. Neurosci. Res. Commun., 21: 135–144.
- International Manganese Institute (2014). Paris, France. Disponible à : www.manganese.org/index.php.
- IOM (2000). Dietary reference intakes for vitamin A, vitamin K, arsenic, boron, chromium, copper, iodine, iron, manganese, molybdenum, nickel, silicon, vanadium, and zinc. Institute of Medicine, National Academy of Sciences, National Academies Press, Washington, D.C.: p. 394–419.
- IOM (2001). Dietary reference intakes for vitamin A, vitamin K, arsenic, boron, chromium, copper, iodine, iron, manganese, molybdenum, nickel, silicon, vanadium, and zinc. Institute of Medicine, National Academy of Sciences, National Academies Press. Washington, D.C.: p. 285–324. Disponible à : www.nap.edu/catalog.php?record_id=10026.
- Ishihara, N., Koizumi, M. et Yoshida, A. (1987). Metal concentrations in human pancreatic juice. Archives of Environmental Health, 42(6): 356–360.
- Ishizuka, H., Nishida, M. et Kawada, J. (1991). Changes in stainability observed by light microscopy in the brains of ataxial mice subjected to three generations of manganese administration. Biochem. Int., 25: 677–687.
- Islam, A.A., Goodwill, J.E., Bouchard, R., Tobiason, J.E. et Knocke, W.R. (2010). Characterization of filter media Mn)x(s) surfaces and Mn removal capability. J. Am. Water Works Assoc., 102(9): 71–83.
- Itoh, K., Sakata, M., Watanabe, M., Aikawa, Y. et Fujii, H. (2008). The entry of manganese ions into the brain is accelerated by the activation of N-methyl-D-aspartate receptors. Abstract. Neuroscience, 154(2): 732–740.
- Jarvinen, R. et Ahlström, A. (1975). Effect of the dietary manganese level on tissue manganese, iron, copper and zinc concentrations in female rats and their fetuses. Med. Biol., 53: 93–99. [tel que cité dans ATSDR, 2012]
- Jeffcoat, S.B., Lavinder, S.R., Dye, D. et Sosebee, R. (2007). Techniques for simultaneous control of manganese and disinfection by-products at conventional water treatment facilities. Proceedings of the American Water Works Association Water Quality and Technology Conference.
- Joardar, M. et Sharma, A. (1990). Comparison of clastogenicity of inorganic manganese administered in cationic and anionic forms in vivo. Mutat. Res., 240: 159–163. [tel que cité dans Santé Canada, 2010]
- Johnson, P.E., Lykken, G.I. et Korynta, E.D. (1991). Absorption and biological half-life in humans of intrinsic and extrinsic 54Mn tracers from foods of plant origin. Mn. J. Nutr., 121: 711–717.
- Jursa, T. et Smith, D.R. (2009). Ceruloplasmin alters the tissue disposition and neurotoxicity of manganese, but not its loading onto transferrin. Toxicol. Sci., 107(1): 182–193.
- Kalea, A.Z., Harris, P.D. et Klimis-Zacas, D.J. (2005). Dietary manganese suppresses alpha1 adrenergic receptor-mediated vascular contraction. J. Nutr. Biochem., 16(1): 44–49.
- Kalea, A.Z., Lamari, F.N., Theocharis, A.D., Schuschke, D.A., Karamanos, N.K. et Klimis-Zacas, D.J. (2006). Dietary manganese affects the concentration, composition and sulfation pattern of heparan sulfate glycosaminoglycans in Sprague-Dawley rat aorta. BioMetals, 19(5): 535–546.
- Karim, Z. (2011). Risk assessment of dissolved trace metals in drinking water of Karachi, Pakistan. Bull. Environ. Contam. Toxicol. 86: 676–678.
- Karki, P., Lee, E. et Aschner, M. (2013). Manganese neurotoxicity: a focus on glutamate transporters. Ann. Occup. Environ. Med., 25(4).
- Kawamura, C.L., Ikuta, H., Fukuzimi, S., Yamada, R., Tsubaki, S., Kodama, T. et Kurata S. (1941). Intoxication by manganese in well water. Kitasato Arch. Exp. Med. 18: 145–169.
- Keen, C.L., Bell, J.G. et Lönnerdal, B. (1986). The effect of age on manganese uptake and retention from milk and infant formulas in rats. J. Nutr., 116: 395–402.
- Kenari, S.L.D. et Barbeau, B. (2014). Pyrolusite fluidized-bed reactor: A robust and compact process for removing manganese from groundwater. Water Res., 49: 475–483.
- Kennedy, G.W. et Finlayson-Bourque, D. (2011). Manganese in groundwater from bedrock aquifers in Nova Scotia; Nova Scotia Department of Natural Resources, Mineral Resources Branch, Open File Map ME 2011-024, scale 1:500 000.
- Kent, W.W. (2016). Accumulation and release of trace inorganic contaminants from biofilm matrices produced and challenged under drinking water distribution system conditions. Utah State University. Logan, Utah (mémoire de maîtrise).
- Kern, C. et Smith, D.R. (2011). Pre-weaning Mn exposure leads to prolonged astrocyte activation and lasting effects on the dopaminergic system in adult male rats. Synapse, 65(6): 532–544.
- Kern, C.H., Stanwood, G.D. et Smith, D.R. (2010). Preweaning manganese exposure causes hyperactivity, disinhibition, and spatial learning and memory deficits associated with altered dopamine receptor and transporter levels. Synapse, 64(5): 363–378.
- Khan, K., Factor-Litvak, P., Wasserman, G.A., Liu, X., Ahmed, E., Parvez, F., Slavkovich, V., Levy, D., Mey, J., van Geen, A. et Graziano, J.H. (2011). Manganese exposure from drinking water and children's classroom behavior in Bangladesh. Environ. Health Perspect., 119(10): 1501–1506.
- Khan, K., Wasserman, G.A., Liu, X., Ahmed, E., Parvez, F., Slavkovich, V., Levy, D., Mey, J., van Geen, A., Graziano, J.H. et Factor-Litvak, P. (2012). Manganese exposure from drinking water and children's academic achievement. Neurotoxicology, 33(1): 91–97.
- Klimis-Zacas, D. (1993). Manganese in health and disease. CRC Press: p. 54–55.
- Knocke, W.R., Hoehn, R.C. et Sinsabaugh, R.L. (1987). Using alternative oxidants to remove dissolved manganese from water laden with organics. J. Am. Water Works Assoc., 79(3): 75–79.
- Knocke, W.R., Hamon, J.R. et Thompson, C.P. (1988). Soluble manganese removal on oxide-coated filter media. J. Am. Water Works Assoc., 74(12): 65–70.
- Knocke, W.R., Van Benschoten, J.E., Kearney, M., Soborski, A. et Reckhow, D.A. (1990a). Alternative oxidants for the removal of soluble manganese. American Water Works Research Foundation and American Water Works Association, Denver, Colorado.
- Knocke, W.R., Occiano, S.C. et Hungate, R. (1990b). Removal of soluble manganese from water by oxide-coated filter media. American Water Works Research Foundation and American Water Works Association, Denver, Colorado.
- Knocke, W.R., Occiano, S.C. et Hungate, R. (1991). Removal of soluble manganese by oxide-coated filter media: sorption rate and removal mechanism issues. J. Am. Water Works Assoc., 83(8): 64–69.
- Knocke, W.R., Zuransky, L., Little, J.C. et Tobiason, J.E. (2010). Adsorptive contactors for removal of soluble manganese during drinking water treatment. J. Am. Water Works Assoc., 102(8): 64–75.
- Kohl, P., Kim, A. et Charlton, N. (2002). Limitations of ozone for removal of manganese to very low levels, a comparative study. Proceedings of the American Water Works Association Water Quality and Technology Conference.
- Kohl, P.M et Dixon, D. (2012). Occurrence, impacts and removal of manganese in biofiltration processes. Water Research Foundation, Denver, Colorado.
- Kohl, P.M. et Medlar, S.J. (2006). Occurrence of manganese in drinking water and manganese control. American Water Research Foundation, American Water Works Association and IWA Publishing. Denver, Colorado.
- Komura, J. et Sakamoto, M. (1991). Short-term oral administration of several manganese compounds in mice: Physiological and behavioral alterations caused by different forms of manganese. Bull. Environ. Contam. Toxicol., 46: 921–928. [tel que cité dans Santé Canada, 2010]
- Komura, J. et Sakamoto, M. (1994). Chronic oral administration of methylcyclopentadienyl manganese tricarbonyl altered brain biogenic amines in the mouse: comparison with inorganic manganese. Toxicol. Lett., 73: 65–73.
- Kondakis, X.G., Makris, N., Leotsinidis, M., Prinou, M. et Papapetropoulos, T. (1989). Possible health effects of high manganese concentration in drinking water. Arch. Environ. Health, 44(3): 175–178.
- Kontur, P. et Fechter, L.D. (1985). Brain manganese, catecholamine turnover, and the development of startle in rats prenatally exposed to manganese. Teratology, 32: 1–11.
- Kostial, K., Kello, D., Jugo, S., Rabar, I. et Maljković, T. (1978). Influence of age on metal metabolism and toxicity. Environ. Health Perspect., 25: 81–86.
- Kostial, K., Blanusa, M., Maljković, T., Kello, D., Rabar, I. et Stara, J.F. (1989). Effect of a metal mixture in diet on the toxicokinetics and toxicity of cadmium, mercury and manganese in rats. Toxicol. Ind. Health, 5(5): 685–698. [tel que cité dans U.S. EPA, 2004]
- Kostial, K., Blanusa, M. et Piasek, M. (2005). Regulation of manganese accumulation in perinatally exposed rat pups. J. Appl. Toxicol. 25(2): 89–93.
- Koudinov, A.R. et Koudinova, N.V. (2005). Cholesterol homeostatis failure as a unifying cause of synaptic degeneration. J. Neurol. Sci., 229–230: 233–240.
- Krishna, S., Dodd, C.A., Hekmatyar, S.K. et Filipov, N.M. (2014). Brain deposition and neurotoxicity of manganese in adult mice exposed via the drinking water. Arch. Toxicol., 88(1): 47–64.
- Kristensson, K., Eriksson, H., Lundh, B., Plantin, O., Wachmeister, L., el Azazi, M. et coll. (1986). Effects of manganese chloride on the rat developing nervous system. Acta Pharmacol. Toxicol., 59(5): 345–348. [tel que cité dans Santé Canada, 2010]
- Kwik-Uribe, C. et Smith, D.R. (2006). Temporal responses in the disruption of iron regulation by manganese. J. Neurosci. Res., 83(8): 1601–1610.
- Kwik-Uribe, C.L., Reaney, S., Zhu, Z. et Smith, D. (2003). Alterations in cellular IRP-dependentiron regulation by in vitro manganese exposure in undifferentiated PC12 cells. Brain Res., 973(1): 1–15.
- Lai, J.C., Leung, T.K., Guest, J.F., Davison, A.N. et Lim, L. (1982). The effects of chronic manganese chloride treatment expressed as age-dependent, transient changes in rat brain synaptosomal uptake of amines. Journal of Neurochemistry, 38(3): 844–847.
- Lai, J.C., Leung, T.K. et Lim, L. (1984). Differences in the neurotoxic effects of manganese during development and aging: Some observations on brain regional neurotransmitter and non-neurotransmitter metabolism in a developmental rat model of chronic manganese encephalopathy. Neurotoxicology, 5(1): 37–47.
- Lai, J.C., Minski, M.J., Chan, A.W., Leung, T.K. et Lim, L. (1999). Manganese mineral interactions in brain. Neurotoxicology, 20(2–3): 433–444. [tel que cité dans Santé Canada, 2010]
- Laitung, J.K. et Mercer, D.M. (1983). Manganese absorption through a burn. Burns Incl. Therm. Inj., 10(2): 145–146.
- Lakin, B. et Bryan, D. (2007). Investigation of sources and transport of manganese deposits in a Connecticut distribution system. AWWA 2007 Annual Technical Conference & Vendor Expo Proceedings, Cromwell, Connecticut.
- Laskey, J.W., Rehnberg, G.L., Hein, J.F. et Carter, S.D. (1982). Effects of chronic manganese (Mn3O4) exposure on selected reproductive parameters in rats. J. Toxicol. Environ. Health, 9(4): 677–687. [tel que cité dans Santé Canada, 2007b; ATSDR, 2008]
- Lauwerys, R., Roels, H., Genet, P., Toussaint, G., Bouckaert, A. et de Cooman, S. (1985). Fertility of male workers exposed to mercury vapor or to manganese dust: A questionnaire study. Am. J. Ind. Med., 7(2): 171–176. [tel que cité dans Santé Canada, 2007b; ATSDR, 2008]
- Lazrishvili, I.L., Shukakidze, A.A., Chkhartishvili, N.N. et Bikashvili, T.Z. (2009). Morphological changes and manganese content in the brains of rat pups subjected to subchronic poisoning with manganese chloride. Neurosci. Behav. Physiol., 39(1): 7–12.
- Leavens, T.L., Rao, D., Andersen, M.E. et Dorman, D.C. (2007). Evaluating transport of manganese from olfactory mucosa to striatum by pharmacokinetic modeling. Toxicol. Sci., 97(2): 265–278.
- Leblanc, A., Lapointe, S., Beaudet, A., Côté, I., Dumas, P., Labrecque, F., Lamy, C., Larochelle, J., Lepage, L., Pelletier, F. et Weber, J. (2004). Étude sur l'établissement de valeurs de référence d'éléments traces et de métaux dans le sang, le sérum et l'urine de la population de la grande région de québec. Direction toxicologie humaine, Direction risques biologiques, environnementaux et occupationnels, Institut national de santé publique du Québec. Disponible à : www.inspq.qc.ca/pdf/publications/289-ValeursReferenceMetaux.pdf.
- Lee, B., Pine, M., Johnson, L., Rettori, V., Hiney, J.K. et Dees, W.L. (2006). Manganese acts centrally to activate reproductive hormone secretion and pubertal development in male rats. Reprod. Toxicol., 22(4): 580–585.
- Lee, B., Hiney, J.K., Pine, M.D., Srivastava, V.K. et Dees, W.L. (2007). Manganese stimulates luteinizing hormone releasing hormone secretion in prepubertal female rats: hypothalamic site and mechanism of action J. Physiol., 578(3): 765–772.
- Lee, M. (2009). Basic Skills in Interpreting Laboratory Data, 4e édition. American Society of Health-System Pharmacists, Inc.
- Lees-Haley, P.R., Rohling, M.L. et Langhinrichsen-Rohling, J. (2006). A meta-analysis of the neuropsychological effects of occupational exposure to manganese. Clin. Neuropsychol., 20(1): 90–107.
- Lei, B., Chen, L., Hao, Y., Cao, T., Zhang, X., Yu, Y. et coll. (2013). Trace elements in animal-based food from Shanghai markets and associated human daily intake and uptake estimation considering bioaccessibility. Ecotoxicol. Environ. Saf., 96: 160–7.
- Leung, T.K., Lai, J.C. et Lim, L. (1982). The effects of chronic manganese feeding on the ctivity of monoamine oxidase in various organs of the developing rat. Comp. Biochem. Physiol. C, 71(2): 223–228. [tel que cité dans U.S. EPA, 2004]
- Leyva-Illades, D., Chen, P., Zogzas, C.E., Hutchens, S., Mercado, J.M., Swaim, C.D., Morrisett, R.A., Bowman, A.B., Aschner, M. et Mukhopadhyay, S. (2014). SLC30A10 is a cell surface-localized manganese efflux transporter, and parkinsonism-causing mutations block its intracellular trafficking and efflux activity. J. Neurosci., 34(42): 14079–14095.
- Lin, C.C., Chen, Y.C., Su, F.C., Lin, C.M., Liao, H.F., Hwang, Y.H., Hsieh, W.S., Jeng, S.F., Su, Y.N. et Chen, P.C. (2013). In utero exposure to environmental lead and manganese and neurodevelopment at 2 years of age. Environ. Res., 123: 52–57.
- Lipe, G.W., Duhart, H., Newport, G.D., Slikker, W.J. et Ali, S.F. (1999). Effect of manganese on the concentration of amino acids in different regions of the rat brain. J. Environ. Sci. Health B, 34(1): 119–132.
- Liu, X., Sullivan, K.A., Madl, J.E., Legare, M. et Tjalkens, R.B. (2006). Manganese-induced neurotoxicity: the role of astroglial-derived nitric oxide in striatal interneuron degeneration. Toxicol. Sci., 91(2): 521–531.
- Liu, J., Jin, L., Zhang, L., Li, Z., Wang, L., Ye, R., Zhang, Y. et Ren, A. (2013). Placental concentrations of manganese and the risk of fetal neural tube defects. J. Trace Elem. Med. Biol., 27(4): 322–325.
- Ljung, K. et Vahter, M. (2007). Time to re-evaluate the guideline value for manganese in drinking water? Environ. Health Perspect., 115(11): 1533–1538.
- Ljung, K.S., Kippler, M.J., Goessler, W., Grandér, G.M., Nermell, B.M. et Vahter, M.E. (2009). Maternal and early life exposure to manganese in rural Bangladesh. Environ. Sci. Technol., 43(7): 2595–2601.
- Lucchini, R., Apostoli, P., Perrone, C., Placidi, D., Albini, E., Migliorati, P., Mergler, D., Sassine, M.P., Palmi, S. et Alessio, L. (1999). Long-term exposure to "low levels" of manganese oxides and neurofunctional changes in ferroalloy workers. Neurotoxicology, 20(2–3): 287–297.
- Luo, Y. et Millero, F.J. (2003). Solubility of rhodochrosite (MnCO3) in NaCl solutions. J. Solution Chem., 32(5).
- Malecki, E.A., Radzanowski, G.M., Radzanowski, T.J., Gallaher, D.D. et Greger, J.L. (1996). Biliary manganese excretion in conscious rats is affected by acute and chronic manganese intake but not by dietary fat. J. Nutr., 126(2): 489–498. [tel que cité dans Santé Canada, 2010]
- Manitoba Conservation and Water Stewardship. (2015). Communication personnelle de J. Muenster.
- Mann, M.A., Thomson, D., Jabari, E. et Rohe, D. (2002). Microfiltration and ultrafiltration: novel pre-treatments for iron and manganese removal from a reverse osmosis feedwater. Proceedings of the Water Quality and Technology Conference. American Water Works Association.
- Martinez-Finley, E.J., Gavin, C.E., Aschner, M. et Gunter, T.E. (2013). Manganese neurotoxicity and the role of reactive oxygen species. Free Radic. Biol. Med., 62: 65–75.
- McDougall, S.A., Reichel, C.M., Farley, C.M., Flesher, M.M., Der-Ghazarian, T., Cortez, A.M. et coll. (2008). Postnatal manganese exposure alters dopamine transporter function in adult rats: Potential impact on nonassociative and associative processes. Neuroscience, 154(2): 848–860.
- McKnight, K.F., Carlson, M., Fortin, P. et Ziesmer, C. (1993). Comparison of ozone efficiency for manganese oxidation between raw and settled water. Ozone. Sci. Eng., 15(4): 331–341
- MDH (2012). Health based guidance for groundwater. Manganese. Minnesota Department of Health.
- Mena, I., Horiuchi, K., Burke, K. et Cotzias, G.C. (1969). Chronic manganese poisoning: Individual susceptibility and absorption of iron. Neurology, 19(10): 1000–1006. [tel que cité dans Santé Canada, 2010]
- Menezes-Filho, J.A., Novaes, C.O., Moreira, J.C., Sarcinelli, P.N. et Mergler, D. (2011). Elevated manganese and cognitive performance in school-aged children and their mothers. Environ. Res., 111(1): 156–163.
- Mergler, D., Baldwin, M., Belanger, S., Larribe, F., Beuter, A., Bowler, R., Panisset, M., Edwards, R., de Geoffroy, A., Sassine, M.P. et Hudnell, K. (1999). Manganese neurotoxicity, a continuum of dysfunction: Results from a community based study. Neurotoxicology, 20(2–3): 327–342.
- Merian, E., Anke, M., Ihnat, M. et Stoeppler, M. (2004). Elements and their compounds in the environment – occurence, analysis and biological relevance. 2e édition. Weinheim, Wiley – VCH Verlag
- Mettler, S., Abdelmoula, M., Hoehn, E., Schoenenberger, R., Weidler, P. et von Gunten, U. (2001). Characterization of iron and manganese precipitates from an in-situ ground water treatment plant. Groundwater, 39(6): 921–930.
- Meyer-Baron, M., Schaper, M., Knapp, G., Lucchini, R., Zoni, S., Bast-Pettersen, R., Ellingsen, D.G., Thomassen, Y., He, S., Yuan, H., Niu, Q., Wang, X.L., Yang, Y.J., Iregren, A., Sjogren, B., Blond, M., Laursen, P., Netterstrom, B., Mergler, D., Bowler, R. et van Thriel, C. (2013). The neurobehavioral impact of manganese: Results and challenges obtained by a meta-analysis of individual participant data. Neurotoxicology, 36: 1–9.
- Michalke, B. et Fernsebner, K. (2014). New insights into manganese toxicity and speciation. J. Trace Elem. Med. Bio., 28(2): 106–116.
- Michalke, B., Halbach, S. et Nischwitz, V. (2007). Speciation and toxicological relevance of manganese in humans. J. Environ. Monit., 9(7): 650–656.
- Miele, M., Serra, P.A., Esposito, G., Delogu, M.R., Migheli, R., Rocchitta, G. et coll. (2000). Glutamate and catabolites of high-energy phosphates in the striatum and brainstem of young and aged rats subchronically exposed to manganese. Aging (Milano), 12(5): 393–397. [tel que cité dans Santé Canada, 2010]
- Miller, E.B., Kanabrocki, E., Case, L., Graham, L., Fields, T., Oester, Y.T. et coll. (1967). Non-dialyzable manganese, copper and sodium in human bile. J. Nucl. Med., 8: 891–895. [tel que cité dans Santé Canada, 2010]
- Miller, S.T., Cotzias, G.C. et Evert, H.A. (1975). Control of tissue manganese: Initial absence and sudden emergence of excretion in the neonatal mouse. Am. J. Physiol., 229: 1080–1084.
- Ministère de l'Environnement et de l'Action en matière de changement climatique de l'Ontario (2014). Communication personnelle de S. Deshpande.
- Ministère du Développement durable, de l'Environnement et de la Lutte contre les changements climatiques du Québec (2014). Communication personnelle de C. Robert.
- Minoia, C., Sabbioni, E., Apostoli, P., Pietra, R., Pozzoli, L., Gallorini, M. et coll. (1990). Trace element reference values in tissues from inhabitants of the European community. I. A study of 46 elements in urine, blood and serum of Italian subjects. Sci. Tot. Environ., 95: 89–105. [tel que cité dans Santé Canada, 2010]
- Mirtallo, J., Canada, T., Johnson, D., Kumpf, V., Petersen, C., Sacks, G., Seres, D. et Guenter, P. (2004). Task Force for the Revision of Safe Practices for Parenteral Nutrition. Safe Practices for Parenteral. J. Parenter. Enteral. Nutr. 28, S39–S70.
- Moberly, A.H., Czarnecki, L.A., Pottackal, J., Rubinstein, T., Turkel, D.J., Kass, M.D. et coll. (2012). Intranasal exposure to manganese disrupts neurotransmitter release from glutamatergic synapses in the central nervous system in vivo. Neurotoxicology, 33(5): 996–1004.
- Molina, R.M., Phattanarudee, S., Kim, J., Thompson, K., Wessling-Resnick, M., Maher, T.J. et coll. (2011). Ingestion of Mn and Pb by rats during and after pregnancy alters iron metabolism and behavior in offspring. Neurotoxicology, 32(4): 413–422.
- Montcoudiol, N., Molson, J. et Lemieux, J.M. (2015). Groundwater geochemistry of the Outaouais region (Quebec, Canada) : a regional-scale study. Hydrogeol. J., 23:377–396.
- Montes, S., Alcaraz-Zubeldia, M., Muriel, P. et coll. (2001). Striatal manganese accumulation induces changes in dopamine metabolism in the cirrhotic rat. Brain Res., 891: 123–129.
- Moreno, J.A., Streifel, K.M., Sullivan, K.A., Legare, M.E. et Tjalkens, R.B. (2009a). Developmental exposure to manganese increases adult susceptibility to inflammatory activation of glia and neuronal protein nitration. Toxicol. Sci., 112(2): 405–415.
- Moreno, J.A., Yeomans, E.C., Streifel, K.M., Brattin, B.L., Taylor, R.J. et Tjalkens, R.B. (2009b). Age-dependent susceptibility to manganese-induced neurological dysfunction. Toxicol. Sci., 112(2): 394–404.
- Mortelmans, K., Haworth, S., Lawlor, T., Speck, W., Tainer, B. et Zeiger, E. (1986). Salmonella mutagenicity tests: II. Results from testing of 270 chemicals. Environmental Mutagenesis, 8(Suppl. 7): 1–119.
- Mouchet, P. (1992). From conventional to biological of iron and manganese in France. J. Am. Water Works Assoc., 84(4): 158–167,
- Murthy, R.C., Srivastava, R.S., Gupta, S.K. et Chandra, S.V. (1980). Manganese induced testicular changes in monkeys. Exp. Pathol., 18(4): 240–244. [tel que cité dans Santé Canada, 2010]
- Myers, J.E., Fine, J., Ormond-Brown, D., Fry, J., Thomson, A. et Thompson, M.L. (2009). Estimating the prevalence of clinical manganism using a cascaded screening process in a South African manganese smelter. 10th International Symposium on Neurobehavioral Methods and Effects in Environmental and Occupational Health. Neurotoxicology, 30(6): 934–940.
- Na, H.K., Kim, E.H., Jung, J.H., Lee, H.H., Hyun, J.W. et Surh, Y.J. (2008). (-)-Epigallocatechin gallate induces Nrf2-mediated antioxidant enzyme expression via activation of PI3K and ERK in human mammary epithelial cells. Arch. Biochem. Biophys., 476(2): 171–177.
- Nachtman, J.P., Tubben, R.E. et Commissaris, R.L. (1986). Behavioral effects of chronic manganese administration in rats: Locomotor activity studies. Neurobehav. Toxicol.Teratol., 8(6): 711–715.
- Nam, J. et Kim, K. (2008). Abnormal motor function and the expression of striatal dopamine D2 receptors in manganese-treated mice. Biol. Pharm. Bull., 31(10): 1894–7.
- Neal, A.P. et Guilarte, T.R. (2013). Mechanisms of lead and manganese neurotoxicity. Toxicol. Res. (Camb.), 2(2): 99–114.
- New Brunswick Department of Environment (2008). New Brunswick groundwater chemistry atlas: 1994–2007. Sciences and Reporting Branch, Sciences and Planning Division, Environmental Reporting Series T2008-01.
- New Brunswick Department of Health (2014). Communication personnelle de K. Gould et T. L. Arsenault.
- Newell, G.W., Jorgenson, T.A. et Simmon, V.F. (1974). Study of mutagenic effects of manganese sulfate (FDA No. 71-71). Compound Report No. 3. U.S. Food and Drug Administration, Rockville, MD. [tel que cité dans NTP, 1993]
- Newfoundland and Labrador Department of Environment and Conservation (2014). Communication personnelle de H. Khan et A. Tobin.
- Newland, M.C., Cox, C., Hamada, R., Oberdorster, G. et Weiss, B. (1987). The clearance of manganese chloride in the primate. Fundam.Appl. Toxicol., 9(2): 314–328. [tel que cité dans Santé Canada, 2010]
- Newland, M.C., Ceckler, T.L., Kordower, J.H. et Weiss, B. (1989). Visualizing manganese in the primate basal ganglia with magnetic resonance imaging. Experimental Neurology, 106(3): 251–258. [tel que cité dans Santé Canada, 2010]
- NHMRC (2011). Australian Drinking Water Guidelines. National Health and Medical Research Council: Version 3.5, updated August 2018. 727–729. Disponible à : www.nhmrc.gov.au/guidelines/publications/eh52
- Nieminski, E. et Evans, D. (1995). Pilot testing of trace metals removal with ozone at Snowbird Ski Resort. Ozone. Sci. Eng., 17: 297–309.
- Nong, A., Taylor, M.D., Clewell, H.J., 3rd, Dorman, D.C. et Andersen, M.E. (2009). Manganese tissue dosimetry in rats and monkeys: accounting for dietary and inhaled Mn with physiologically based pharmacokinetic modeling. Toxicol. Sci., 108(1): 22–34.
- Nong, A., Teeguarden, J.G., Clewell, H.J., 3rd, Dorman, D.C. et Andersen, M.E. (2008). Pharmacokinetic modeling of manganese in the rat IV: Assessing factors that contribute to brain accumulation during inhalation exposure. J. Toxicol. Environ. Health A, 71(7): 413–26.
- Nowak, P., Bojanek, K., Szkilnik, R., Josko, J., Boron, D., Adwent, M. et coll. (2011). Ontogenetic exposure of rats to pre- and post-natal manganese enhances behavioral impairments produced by perinatal 6-hydroxydopamine. Neurotox. Res., 19(4): 536–43.
- Nowell, L.H. et Hoigne, J. (1987). Interaction of iron (II) and other transition metals with aqueous ozone. Dans : Proceedings from 8th Ozone World Congress, International Ozone Association, Norwalk, CT.
- NRC (1989). Recommended dietary allowances. National Research Council (éd.). 10e édition. National Academies Press, Washington, D.C.
- NSF International (2015a). NSF/ANSI Standard 60: Drinking water treatment chemicals – health effects. NSF International, Ann Arbor, Michigan.
- NSF International (2015b). NSF/ANSI Standard 42: Drinking water treatment units – aesthetic effects. NSF International, Ann Arbor, Michigan.
- NSF International (2015c). NSF/ANSI Standard 58: Reverse osmosis drinking water treatment systems. NSF International, Ann Arbor, Michigan.
- NSF International (2015d). NSF/ANSI Standard 44: Cation exchange water softeners. NSF International, Ann Arbor, Michigan.
- NSF International (2016a). NSF/ANSI Standard 61: Drinking water system components – health effects. NSF International, Ann Arbor, Michigan.
- NSF International (2016b). NSF/ANSI Standard 372: Drinking water system components – lead content. NSF International, Ann Arbor, Michigan.
- NTIS (1973). Teratologic evaluation of FDA 71-71 (manganese sulfate, monohydrate). PB 223-813. U.S. Department of Commerce, Springfield, VA. [tel que cité dans NTP, 1993]
- NTP (1993). Toxicology and carcinogenesis studies of manganese (II) sulfate monohydrate (CAS No. 10034-96-5) in F344/N rats and B6C3F1 mice (feed studies). National Toxicology Program. Rapport no TR-428. Disponible à : http://ntp.niehs.nih.gov/?objectid=0709D83B-9FDB-28AC-789C940D7855E09C.
- O'Brien, W.J., Lee, E., Freeman, S., Shorney, H., Long, B. et Elder, D. (1996). Manganese oxidation and removal by ozone and polymer-assisted filtration. Proceedings 1996 AWWA Water Quality Technology Conference. Boston, MA.
- Oberly, T.J., Piper, C.E. et McDonald, D.S. (1982). Mutagenicity of metal salts in the L5178Y mouse lymphoma assay. J. Toxicol. Environ. Health, 9: 367–376. [tel que cité dans Santé Canada, 2010]
- OCDE (2007). Lignes directrices de l'OCDE pour les essais de produits chimiques, Section 4: Effets sur la santé. Essai no 426 : Étude de neurotoxicité pour le développement). Disponible à : http://www.oecd-ilibrary.org/environment/essai-n-426-etude-de-neurotoxicite-pour-le-developpement_9789264067400-fr;jsessionid=1eom9e2phc5q8.x-oecd-live-02.
- Ohishi, T., Wang, L., Akane, H., Shiraki, A., Goto, K., Ikarashi, Y. et coll. (2012). Reversible aberration of neurogenesis affecting late-stage differentiation in the hippocampal dentate gyrus of rat offspring after maternal exposure to manganese chloride. Reprod. Toxicol., 34(3): 408–419.
- Okada, M.A., Neto, F.F., Noso, C.H., Voigt, C.L., Campos, S.X. et Alberto de Oliveira Ribeiro, C. (2016). Brain effects of manganese exposure in mice pups during prenatal and breastfeeding periods. Neurochem Int; 97:109–116.
- OMS (2004). Concise international chemical assessment document 63: Manganese and its compounds: Environmental aspects. Organisation mondiale de la Santé, ISBN 92 4 153063 4.
- OMS/FAO (2007). Norme pour les préparations destinées aux nourrissons et les préparations données à des fins médicales spéciales aux nourrissons. CODEX STAN 72-1981. Organisation mondiale de la Santé et Organisation des Nations Unies pour l'alimentation et l'agriculture (éd.). Codex Alimentarius (publié en 1981 et révisé en 2007). Disponible à : http://www.fao.org/fao-who-codexalimentarius/home/fr/.
- OMS (2011). Manganese in drinking water. Background document for development of WHO Guidelines for Drinking-water Quality. Organisation mondiale de la Santé. Disponible à : www.who.int/water_sanitation_health/dwq/chemicals/manganese.pdf
- Öner, G. et Sentürk, U.K. (1995). Reversibility of manganese-induced learning defect in rats. Food Chemistry and Toxicology, 33(7): 559–563.
- Oszlanczi, G., Vezer, T., Sarközi, L., Horvath, E., Szabo, A., Konya, Z. et coll. (2010). Metal deposition and functional neurotoxicity in rats after 3-6 weeks nasal exposure by two physicochemical forms of manganese. Environ. Toxicol. Pharmacol., 30(2): 121–126.
- Oulhote, Y., Mergler, D., Barbeau, B., Bellinger, D.C., Bouffard, T., Brodeur, M.E., Saint-Amour, D., Legrand, M., Sauve, S. et Bouchard, M.F. (2014). Neurobehavioral function in school-age children exposed to manganese in drinking water. Environ. Health Perspect., 122(12): 1343–1350.
- Ouvrard, S., Simonnot, M-O. et Sardin, M. (2002). Reactive behavior of natural manganese oxides toward the adsorption of phosphate and arsenate. Ind. Eng. Chem. Res., 41, 2785–2791.
- Pagano, D.A. et Zeiger, E. (1992). Conditions for detecting the mutagenicity of divalent metals in Salmonella typhimurium. Environ. Mol. Mutagen., 19(2): 139–146. [tel que cité dans Santé Canada, 2010]
- Paillard, H., Legube, B., Bourbigot, M.M. et Lefebvre, E. (1989). Iron and manganese removal with ozonation in the presence of humic substances. Ozone-Sci. Eng., 11(1): 93–99.
- Pal, P.K., Samii, A. et Calne, D.B. (1999). Manganese neurotoxicity: A review of clinical features, imaging and pathology. Neurotoxicology, 20(2–3): 227–238. [tel que cité dans Santé Canada, 2010]
- Pappas, B.A., Zhang, D., Davidson, C.M., Crowder, T., Park, G.A. et Fortin, T. (1997). Perinatal manganese exposure: Behavioral, neurochemical, and histopathological effects in the rat. Neurotoxicol. Teratol., 19(1): 17–25.
- Park, N.H., Park, J.K., Choi, Y., Yoo, C.I., Lee, C.R., Lee, H. et coll. (2003). Whole blood manganese correlates with high signal intensities on T1-weighted MRI in patients with liver cirrhosis. Neurotoxicology, 24(6): 909–915. [tel que cité dans Santé Canada, 2010]
- Park, J.D., Chung, Y.H., Kim, C.Y., Ha, C.S., Yang, S.O., Khang, H.S. et coll. (2007). Comparison of high MRI T1 signals with manganese concentration in brains of cynomolgus monkeys after 8 months of stainless steel welding-fume exposure. Inhal. Toxicol., 19(11): 965–971.
- Parry, J.M. (1977). The use of yeast cultures for the detection of environmental mutagens using a fluctuation test. Mutat. Res., 46: 165–176. [tel que cité dans NTP, 1993]
- Peneder, T.M., Scholze, P., Berger, M.L., Reither, H., Heinze, G., Bertl, J. et coll. (2011). Chronic exposure to manganese decreases striatal dopamine turnover in human alpha-synuclein transgenic mice. Neuroscience, 180: 280–92.
- Peng, C-Y. et Korshin, G.V. (2011). Speciation of trace inorganic contaminants in corrosion scales and deposits formed in drinking water distribution systems. Water Res., 45: 5553–5563.
- Pine, M., Lee, B., Dearth, R., Hiney, J.K. et Dees, W.L. (2005). Manganese acts centrally to stimulate luteinizing hormone secretion: a potential influence on female pubertal development. Toxicol. Sci., 85: 880–885.
- PISSC (1999). Concise international chemical assessment document 12: Manganese and its compounds. Programme international sur la sécurité des substances chimiques, Organisation mondiale de la Santé.
- Pollack, S., George, J.N. et Reba, R.C. (1965). The absorption of nonferrous metals in iron deficiency. J. Clin. Invest., 44: 1470–1473.
- Ponnapakkam, T.P., Bailey, K.S., Graves, K.A. et Iszard, M.B. (2003a). Assessment of male reproductive system in the CD-1 mice following oral manganese exposure. Reprod. Toxicol., 17(5): 547–551. [tel que cité dans Santé Canada, 2010]
- Ponnapakkam, T., Iszard, M. et Henry-Sam, G. (2003b). Effects of oral administration of manganese on the kidneys and urinary bladder of Sprague-Dawley rats. Int. J. Toxicol., 22(3): 227–232. [tel que cité dans Santé Canada, 2010]
- Ponnapakkam, T.P., Sam, G.H. et Iszard, M.B. (2003c). Histopathological changes in the testis of the Sprague Dawley rat following orally administered manganese. Bull. Environ. Contam. Toxicol., 71(6): 1151–1157. [tel que cité dans Santé Canada, 2010]
- Prestifilippo, J.P., Fernandez-Solari, J., Mohn, C., De Laurentiis, A., McCann, S.M., Dees, W. et coll. (2007). Effect of manganese on luteinizing hormone-releasing hormone secretion in adult male rats. Toxicol. Sci., 97(1): 75–80.
- Prestifilippo, J.P., Fernandez-Solari, J., De Laurentiis, A., Mohn, C.E., de la Cal, C., Reynoso, R. et coll. (2008). Acute effect of manganese on hypothalamic luteinizing hormone releasing hormone secretion in adult male rats: involvement of specific neurotransmitter systems. Toxicol. Sci., 105(2): 295–302.
- Racette, B.A., Aschner, M., Guilarte, T.R., Dydak, U., Criswell, S.R. et Zheng, W. (2012). Pathophysiology of manganese-associated neurotoxicity. Neurotoxicology, 33(4): 881–886.
- Rahman, S.M., Kippler, M., Tofail, F., Bölte, S., Derakhshani Hamadani, J. et Vahter, M. (2017). Manganese in drinking water and cognitive abilities and behavior at 10 years of age: A prospective cohort study. Environ Health Perspect., 125(5):057003.
- Raiten, D.J., Talbot, J.M. et Waters, J.H. (1998). Assessment of nutrient requirements for infant formulas. Life Sciences Research Office, American Society for Nutritional Sciences (ed.). Volume 128 (No. 11S): 2059S–2294S, Bethesda, Maryland, http://jn.nutrition.org/content/128/11/suppl/DC1.
- Ranasinghe, J.G.S., Liu, M., Sakakibara, Y. et coll. (2000). Manganese administration induces the increased production of dopamine sulfate and depletion of dopamine in Sprague-Dawley rats. J. Biochem. (Tokyo), 128: 477–480.
- Rasmuson, A. (1985). Mutagenic effects of some water-soluble metal compounds in a somatic eye-color test system in Drosophila melanogaster. Mutat. Res., 157: 157–162. [tel que cité dans Assem et al., 2011]
- Reaney, S.H. et Smith, D.R. (2005). Manganese oxidation state mediates toxicity in PC12 cells. Toxicol. Appl. Pharmacol., 205(3): 271–281.
- Reaney, S.H., Bench, G. et Smith, D.R. (2006). Brain accumulation and toxicity of Mn(II) and Mn(III) exposures. Toxicol. Sci., 93(1): 114–124.
- Reaney, S.H., Kwik-Uribe, C.L. et Smith, D.R. (2002). Manganese oxidation state and its implications for toxicity. Chemical Research in Toxicology, 15(9): 1119–1126.
- Rehnberg, G.L., Hein, J.F., Carter, S.D., Linko, R.S. et Laskey, J.W. (1982). Chronic ingestion of Mn3O4 by young rats: Tissue accumulation and distribution of manganese in two generations:. J. Toxicol. Environ. Health, 9(2): 175–188. [tel que cité dans Santé Canada, 2010]
- Reichel, C.M., Wacan, J.J., Farley, C.M., Stanley, B.J., Crawford, C.A. et McDougall, S.A. (2006). Postnatal manganese exposure attenuates cocaine-induced locomotor activity and reduces dopamine transporters in adult male rats. Neurotoxicol. Teratol., 28(3): 323–332.
- Rink, S.M., Ardoino, G., Queirolo, E.I., Cicariello, D., Manay, N. et Kordas, K. (2014). Associations between hair manganese levels and cognitive, language, and motor development in preschool children from Montevideo, Uruguay. Arch. Environ. Occup. Health, 69(1): 46–54.
- Riojas-Rodriguez, H., Solis-Vivanco, R., Schilmann, A., Montes, S., Rodriguez, S., Rios, C. et Rodriguez-Agudelo, Y. (2010). Intellectual function in Mexican children living in a mining area and environmentally exposed to manganese. Environ. Health Perspect., 118(10): 1465–1470.
- Roels, H.A., Ghyselen, P., Buchet, J.P., Ceulemans, E. et Lauwerys, R.R. (1992). Assessment of the permissible exposure level to manganese in workers exposed to manganese dioxide dust. Br. J. Ind. Med., 49(1): 25–34.
- Roels, H.A., Meiers, G., Delos, M., Ortega, I., Lauwerys, R.R., Buchet, J.P. et coll. (1997). Influence of the route of administration and the chemical form (MnCl2, MnO2) on the absorption and cerebral distribution of manganese in rats. Arch. Toxicol., 71(4): 223–230.
- Roels, H.A., Bowler, R.M., Kim, Y., Claus Henn, B., Mergler, D., Hoet, P., Gocheva, V.V., Bellinger, D.C., Wright, R.O., Harris, M.G., Chang, Y., Bouchard, M.F., Riojas-Rodriguez, H., Menezes-Filho, J.A. et Tellez-Rojo, M.M. (2012). Manganese exposure and cognitive deficits: A growing concern for manganese neurotoxicity. Neurotoxicology, 33(4): 872–880.
- Roth, J.A. (2006). Homeostatic and toxic mechanisms regulating manganese uptake, retention, and elimination. Biol. Res., 39(1): 45–57.
- Roth, J.A., Li, Z., Sridhar, S. et Khoshbouei, H. (2013). The effect of manganese on dopamine toxicity and dopamine tranposter (DAT) in control and DAT transfected HEK cells. Neurotoxicology, 35: 121–8.
- Rumsby, P., Clegg, H., Jonsson, J., Benson, V., Harman, M., Doyle, T., Rushton, L., Warwick, P. et Wilkinson, D. (2014). Speciation of manganese in drinking water. National Centre for Environmental Toxicology, UC9780. Préparé pour le bureau d'inspection de l'eau potable.
- Ruoff, W.L. (1995). Relative bioavailability of manganese ingested in food or water. Dans :Proceedings of the Workshop on the Bioavailability and Oral Toxicity of Manganese. Sponsored by the U.S. Environmental Protection Agency, Cincinnati, OH, August 30-31, 1994. [tel que cité dans U.S. EPA, 2002]
- Sahabi, D.M., Takeda, M., Suzuki, I. et Koizumi, J. (2009). Removal of Mn2+ from water by "aged" biofilter media: The role of catalytic oxides layers. J. Biosci. Bioeng., 107(2): 151–157,
- Sahni, V., Léger, Y., Panaro, L., Allen, M., Giffin, S., Fury, D. et Hamm N. (2007). Case report: a metabolic disorder presenting as pediatric manganism. Environ. Health Perspect., 115(12): 1776–1779.
- Sain, A.E., Griffin, A. et Dietrich, A.M. (2014). Assessing taste and visual perception of Mn(II) and Mn(IV). J. Am. Water Works Assoc., 106(1): 32–40.
- Salehi, F., Krewski, D., Mergler, D., Normandin, L., Kennedy, G., Philippe, S. et coll. (2003). Bioaccumulation and locomotor effects of manganese phosphate/sulfate mixture in Sprague-Dawley rats following subchronic (90 day) inhalation exposure. Toxicol. Appl. Pharmacol., 191(3): 264–271.
- Salehi, F., Normandin, L., Krewski, D., Kennedy, G., Philippe, S. et Zayed, J. (2006). Neuropathology, tremor and electromyogram in rats exposed to manganese phosphate/sulfate mixture. J. Appl. Toxicol., 26(5): 419–426.
- Sanchez, B., Casalots-Casado, J., Quintana, S., Arroyo, A., Martin-Fumado, C. et Galtes, I. (2012). Fatal manganese intoxication due to an error in the elaboration of epsom salts for a liver cleansing diet. Forensic Sci. Int., 223(1–3): e1–4.
- Sánchez, D.J., Domingo, J.L., Llobet, J.M. et Keen, C.L. (1993). Maternal and developmental toxicity of manganese in the mouse. Toxicology Letters, 69(1): 45–52. [tel que cité dans Santé Canada, 2010]
- Sandstrom, B., Davidsson, L., Cederblad, A., Eriksson, R. et Lonnerdal, B. (1986). Manganese absorption and metabolism in man. Acta Pharmacol. Toxicol., 59(Suppl 7): 60–62. [tel que cité dans Santé Canada, 2010]
- Santamaria, A.B. (2008). Manganese exposure, essentiality & toxicity. Indian J. Med. Res., 128(4): 484–500.
- Santé Canada (1994). Loi canadienne sur la protection de l'environnement – L'évaluation du risque à la santé humaine des substances d'intérêt prioritaire. Ministre des Approvisionnements et Services Canada, Ottawa, Ontario. Disponible à : www.hc-sc.gc.ca/ewh-semt/alt_formats/hecs-sesc/pdf/pubs/contaminants/approach/approche-fra.pdf
- Santé Canada (2007a). Suppléments de multivitamines/minéraux. Base de données d'ingrédients de produits de santé naturels, Direction des produits de santé naturels, Santé Canada, Ottawa, Ontario. Disponible à : http://webprod.hc-sc.gc.ca/nhpid-bdipsn/atReq.do?atid=multi_vitmin_suppl&lang=fra.
- Santé Canada (2007b). Average dietary intakes (µg/kg bw/day) of trace elements for Canadians in different age/sex groups for Total Diet Study. Bureau d'innocuité des produits chimiques, Direction générale des produits de santé et des aliments, Santé Canada, Ottawa, Ontario.
- Santé Canada (2009). Étude canadienne sur l'alimentation totale. Direction générale des produits de santé et des aliments, Santé Canada, Ottawa, Ontario. Disponible à : www.hc-sc.gc.ca/fn-an/surveill/total-diet/index-fra.php.
- Santé Canada (2010). Évaluation du risque pour la santé humaine du manganèse inhalé. Bureau de l'eau, de l'air et des changements climatiques, Programme de la sécurité des milieux, Santé Canada. Disponible à : http://canadiensensante.gc.ca/publications/healthy-living-vie-saine/manganese/index-fra.php
- Santé Canada (2014a). Communication personnelle de A.-M. Tugulea.
- Santé Canada (2014b). Communication personnelle de R. Dabeka.
- Santé Canada (2015). Drinking water treatment system testing for manganese removal. Réalisé par NSF International sous contrat avec Santé Canada.
- Saric, M. (1986). Manganese. Dans : Frieberg, L., Nordberg, G.F. and Vouk, V.B. (éds). Handbook on the Toxicology of Metals. Volume II: Specific Metals. 2e édition. Amsterdam, Elsevier Science Publishers BV (354–386). [tel que cité dans Geber et coll., 2002; Merian et coll., 2004.]
- Saskatchewan Water Security Agency (2014). Communication personnelle de S. Ferris.
- Saudin, F., Gelas, P. et Bouletreau, P. (1988). Trace elements in artificial nutrition. art and practice. Ann. Fr. Anesth. Reanim., 7(4): 320–332.
- Schneider, C., Johns, P. et Huehmer, R. (2001). Microfiltration for removal of manganese from surface water. AWWA 2001 Annual Conference Proceedings, Washington, D.C.
- Schock, M.R. (2005). Distribution systems as reservoirs and reactors for inorganic contaminants. Chapitre 6 dans : Distribution system water quality challenges in the 21st century – a strategic guide. M.J. Macphee (éditeur.). American Water Works Association, Denver, Colorado.
- Schock, M.R. et Holm, T.R. (2003). Are we monitoring in the right places for metals and radionuclides? Journal of the New England Water Works Association, 141(2): 102.
- Schock, M.R., Cantor, A.F., Triantafyllidou, S., Desantis, M.K. et Scheckel, K.G. (2014). Importance of pipe deposits to Lead and Copper Rule compliance. J. Am. Water Works Assoc., 106(7), E336–E349.
- Schroeder, H.A., Balassa, J.J. et Tipton, I.H. (1966). Essential trace metals in man: Manganese. A study in homeostasis. J. Chronic Dis., 19(5): 545–571. [tel que cité dans Santé Canada, 2010]
- Schroeter, J.D., Nong, A., Yoon, M., Taylor, M.D., Dorman, D.C., Andersen, M.E. et coll. (2011). Analysis of manganese tracer kinetics and target tissue dosimetry in monkeys and humans with multi-route physiologically based pharmacokinetic models. Toxicol. Sci., 120(2): 481–498.
- Schroeter, J.D., Dorman, D.C., Yoon, M., Nong, A., Taylor, M.D., Andersen, M.E. et coll. (2012). Application of a multi-route physiologically based pharmacokinetic model for manganese to evaluate dose-dependent neurological effects in monkeys. Toxicol. Sci., 129(2): 432–446.
- SCF (2003). Report of the scientific committee on food on the revision of essential requirements of infant formulae and follow-on formulae. Scientific Committee on Food, Health and Consumers Directorate-General, European Commission, SCF/CS/NUT/IF/65 Final, Brusselles, Belgique.
- Seel, N.M. (2012). Basal Ganglia. Dans : Seel, N.M. (éd.) Encyclopedia of the Sciences of Learning. Springer US. Disponible à : http://dx.doi.org/10.1007/978-1-4419-1428-6_2043.
- Sentürk, U.K. et Öner, G. (1996). The effect of manganese-induced hypercholesterolemia on learning in rats. Biol. Trace Elem. Res., 51( 3): 249–257.
- Sharma, R. et Pervez, S. (2005). Toxic metals status in human blood and breast milk samples in an integrated steel plant environment in Central India. Environ. Geochem. Health, 27(1): 39–45.
- Shi, X.Q., Yan, W., Wang, K.Y., Fan, Q.Y. et Zou, Y. (2012). Protective effects of dietary fibre against manganese-induced neurobehavioral aberrations in rats. Arh. Hig. Rada. Toksikol., 63(3): 263–270.
- Shukakidze, A.A., Lazriev, I.L. et Mitagvariya, N. (2003). Behavioral impairments in acute and chronic manganese poisoning in white rats. Neurosci. Behav. Physiol., 33(3): 263–267.
- Shukakidze, A.A., Lazriev, I.L., Khetsuriani, R.G. et Bikashvili, T.Z. (2002). Changes in neuroglial ultrastructure in various parts of the rat brain during manganese chloride poisoning. Neurosci. Behav. Physiol., 32(6): 561–566.
- Shukla, G.S., Singh, S. et Chandra, S.V. (1978). The interaction between manganese and ethanol in rats. Acta Pharmacol. Toxicol., 43(5): 354–362.
- Shukla, G.S., Chandra, S.V. et Seth, P.K. (1976). Effect of manganese on the levels of DNA, RNA, DNase and RNase in cerebrum, cerebellum and rest of brain regions of rat. Acta Pharmacol. Toxicol., 39(5): 562–569. [tel que cité dans Santé Canada, 2010]
- Shukla, G.S., Dubey, M.P. et Chandra, S.V. (1980). Manganese-induced biochemical changes in growing versus adult rats. Arch. Environ. Contam. Toxicol., 9(4): 383–391. [tel que cité dans Santé Canada, 2010]
- Shumay, E., Fowler, J.S. et Volkow, N.D. (2010). Genomic features of the human dopamine transporter gene and its potential epigenetic states: Implications for phenotypic diversity. PLOS ONE, 5(6): e11067.
- Sialelli, J., Urquhart, G.J., Davidson, C.M. et Hursthouse, A.S. (2010). Use of a physiologically based extraction test to estimate the human bioaccessibility of potentially toxic elements in urban soils from the city of Glasgow, UK. Environ. Geochem. Health, 32(6): 517–527.
- Siddappa, A.J., Rao, R.B., Wobken, J.D., Leibold, E.A., Connor, J.R. et Georgieff, M.K. (2002). Developmental changes in the expression of iron regulatory proteins and iron transport proteins in the perinatal rat brain. J. Neurosci. Res., 68(6): 761–775.
- Sidoryk-Wegrzynowicz, M., Lee, E., Albrecht, J. et Aschner, M. (2009). Manganese disrupts astrocyte glutamine transporter expression and function. J. Neurochem., 110(3): 822–830.
- Sidoryk-Wegrzynowicz, M. et Aschner, M. (2013a). Role of astrocytes in manganese mediated neurotoxicity. BMC Pharmacol. Toxicol., 14(23).
- Sidoryk-Wegrzynowicz, M. et Aschner, M. (2013b). Manganese toxicity in the central nervous system: the glutamine/glutamate-gamma-aminobutyric acid cycle. J. Intern. Med., 273: 466–477.
- Singh, I. (1984). Induction of gene conversion and reverse mutation by manganese sulphate and nickel sulphate in Saccharomyces cerevisiae. Mutat. Res. 137(1): 47–49. [tel que cité dans Santé Canada, 2010]
- Sly, L.I., Hodgkinson, M.C., Arunpairojana, V. 1990. Deposition of manganese in drinking water distribution systems. Appl. Environ. Microbiol., 56(3), 628–639.
- Smyth, H.F., Carpenter, C.P., Weil, C.S., Pozzani, U.C., Striegal, J.A. et Nycum, J.S. (1969). Range-finding toxicity data: List VII. AIHA, 30: 470–476. [tel que cité dans U.S. EPA, 2004; OMS, 2011]
- Sommerfield, E.O. (1999). Iron and manganese removal handbook. American Water Works Association. Denver, Colorado.
- Spadoni, F., Stefani, A., Morello, M., Giacomini, P. et Sancesario, G. (2000). Selective vulnerability of pallidal neurons in the early phases of manganese intoxication. Exp. Brain Res., 135(4): 544–551.
- Stokes, P.M., Campbell, P.G.C., Schroeder, W.H., Trick, C., France, R.L., Puckett, K.J., LaZerte, B., Speyer, M., Hanna, J.E. et Donaldson, J. (1988). Manganese in the Canadian environment. NRCC (éd.).
- Subhash, M.N. et Padmashree, T.S. (1991). Effect of manganese on biogenic amine metabolism in regions of the rat brain. Food Chem. Toxicol., 29: 579–82.
- Szakmáry, E., Ungváry, G., Hudák, A., Naray, M., Tatrai, E., Szeberenyi, S. et coll. (1995). Developmental effect of manganese in rat and rabbit. Central European Journal of Occupational and Environmental Medicine, 1(2): 149–159. [tel que cité dans OMS, 1999]
- Takacs, S., Szabo, A., Oszlanczi, G., Paulik, E. et Papp, A. (2012). A pilot study with simultaneous recording of changes in motility and cortical electrical activity of rats during four weeks of oral manganese exposure. Int. J. Environ. Health Res., 22(4): 331–9.
- Takeda, A., Sawashita, J. et Okada, S. (1995). Biological half-lives of zinc and manganese in rat brain. Brain Research, 695(1): 53–58. [tel que cité dans Santé Canada, 2007]
- Takser, L., Mergler, D., Hellier, G., Sahuquillo, J. et Huel, G. (2003). Manganese, monoaminemetabolite levels at birth, and child psychomotor development. Neurotoxicology. 24(4–5):667–674.
- Tapin, D., Kennedy, G., Lambert, J. et Zayed, J. (2006). Bioaccumulation and locomotor effects of manganese sulfate in Sprague-Dawley rats following subchronic (90 days) inhalation exposure. Toxicol. Appl. Pharmacol., 211(2): 166–174.
- Taylor, M.D., Clewell, H.J. 3rd, Andersen, M.E., Schroeter, J.D., Yoon, M., Keene, A.M. et Dorman, D.C. (2012). Update on a pharmacokinetic-centric alternative tier II program for MMT-Part II: Physiologically based pharmacokinetic modeling and manganese risk assessment. J. Toxicol., article no 791431.
- Taylor, M.D., Erikson, K.M., Dobson, A.W., Fitsanakis, V.A., Dorman, D.C. et Aschner, M. (2006). Effects of inhaled manganese on biomarkers of oxidative stress in the rat brain. Neurotoxicology, 27(5): 788–797.
- Teeguarden, J.G., Dorman, D.C., Covington, T.R., Clewell, H.J. 3rd et Andersen, M.E. (2007a). Pharmacokinetic modeling of manganese. I. Dose dependencies of uptake and elimination. J. Toxicol. Environ. Health A., 70(18): 1493–1504.
- Teeguarden, J.G., Dorman, D.C., Nong, A., Covington, T.R., Clewell, H.J. 3rd et Andersen, M.E. (2010). Pharmacokinetic modeling of manganese. II. Hepatic processing after ingestion and inhalation. J. Toxicol. Environ. Health A., 70(18): 1505–1514.
- Teeguarden, J.G., Gearhart, J., Clewell, H.J. 3rd, Covington, T.R., Nong, A. et Andersen, M.E. (2007c). Pharmacokinetic modeling of manganese. III. Physiological approaches accounting for background and tracer kinetics. J. Toxicol. Environ. Health A., 70(18): 1515–1526.
- Thompson, T.S. (2003). General chemical water quality of private groundwater supplies in Saskatchewan, Canada. Bull. Environ. Contam. Toxicol., 70:447–454.
- Thompson, K.J., Molina, R.M. et Donaghey, T.E.A. (2011). Manganese uptake and distribution in the brain after methyl bromide-induced lesions in the olfactory epithelia. Toxicol. Sci., 120(1): 163–72.
- Tjalkens, R.B., Zoran, M.J., Mohl, B. et Barhoumi, R. (2006). Manganese suppresses ATP-dependent intercellular calcium waves in astrocyte networks through alteration of mitochondrial and endoplasmic reticulum calcium dynamics. Brain Res., 1113(1): 210–219.
- Tobiason, J.E., Knocke, W.R., Islam, A.A. et Goodwill, J.E. (2007). Control of periodically elevated raw water manganese with oxide coated media. Proceedings of the American Water Works Association Water Quality Technology Conference.
- Tobiason, J.E., Islam, A.A., Knocke, W.R., Goodwill, J.E., Hargette, P., Bouchard, R. et Zuravnsky, L. (2008). Characterization and performance of filter media for manganese control. American Water Works Research Foundation, Denver, Colorado.
- Torrente, M., Colomina, M.T. et Domingo, J.L. (2005a). Metal concentrations in hair and cognitive assessment in an adolescent population. Biol. Trace Elem. Res., 104(3): 215–221.
- Torrente, M., Colomina, M.T. et Domingo, J.L. (2005b). Behavioral effects of adult rats concurrently exposed to high doses of oral manganese and restraint stress. Toxicology, 211(1–2): 59–69.
- Torres-Agustin, R., Rodriguez-Agudelo, Y., Schilmann, A., Solis-Vivanco, R., Montes, S., Riojas-Rodriguez, H. et coll. (2013). Effect of environmental manganese exposure on verbal learning and memory in Mexican children. Environ. Res., 121: 39–44.
- Tran, T.T., Chowanadisai, W., Crinella, F.M., Chicz-Demet, A. et Lonnerdal, B. (2002a). Effect of high dietary manganese intake of neonatal rats on tissue mineral accumulation, striatal dopamine levels, and neurodevelopmental status. Neurotoxicology 23(4–5): 635–643.
- Tran, T.T., Chowanadisai, W., Lonnerdal, B., Le, L., Parker, M., Chicz-Demet, A. et coll. (2002b). Effects of neonatal dietary manganese exposure on brain dopamine levels and neurocognitive functions. Neurotoxicology 23(4–5): 645–651.
- Treinen, K.A., Gray, T.J.B. et Blazak, W.F. (1995). Developmental toxicity of mangafodipir trisodium and manganese chloride in Sprague-Dawley rats. Teratology, 52: 109–115. [tel que cité dans Santé Canada, 2010]
- Tsuda, H. et Kato, K. (1977). Chromosomal aberrations and morphological transformation in hamster embryonic cells treated with potassium dichromate in vitro. Mutat. Res., 46: 87–94. [tel que cité dans ATSDR, 2008]
- Tuschl, K., Mills, P.B. et Clayton, P.T. (2013). Manganese and the brain. Int. Rev. Neurobiol., 110: 277–312.
- Ueda, F., Raja, K.B., Simpson, R.J., Trowbridge, I.S. et Bradbury, M.W. (1993). Rate of 59Fe uptake into brain and cerebrospinal fluid and the influence thereon of antibodies against the transferrin receptor. J. Neurochem., 60(1): 106–113. [tel que cité dans Santé Canada, 2010]
- Union européenne (1998). Directive 98/83/CE du 3 novembre 1998 relative à la qualité des eaux destinées à la consommation humaine. Disponible a: https://eur-lex.europa.eu/legal-content/FR/TXT/HTML/?uri=CELEX:01998L0083-20151027
- U.S. EPA (1979). National Secondary Drinking Water Regulations; Final Rule. U.S. Environmental Protection Agency. Federal Register 44(140): 42195–42202.
- U.S. EPA (1986). Guidelines for the health risk assessment of chemical mixtures. U. S. Environmental Protection Agency. Federal Register 51(185): 34014–34025.
- U.S. EPA (1988). Recommendations for and documentation of biological values for use in risk assessment. U.S. Environmental Protection Agency. Office of Health and Environmental Assessment, Environmental Criteria and Assessment Office, Cincinnati, Ohio.
- U.S. EPA (1994a). Method 200.7: Determination of metals and trace elements in water and wastes by inductively coupled plasma-atomic emission spectrometry. Rev 4.4. U.S. Environmental Protection Agency. Environment Monitoring Systems Laboratories. Office of Research and Development, Cincinnati, Ohio 45268.
- U.S. EPA (1994b). Method 200.8, Revision 5.4: Determination of trace elements in waters and wastes by Inductively Coupled Plasma-Mass Spectrometry. U.S. Environmental Protection Agency. Environment Monitoring Systems Laboratories. Office of Research and Development, Cincinnati, Ohio 45268
- U.S. EPA (1994c). Method 200.9, Revision 2.2: Determination of trace elements by stabilized temperature graphite furnace atomic adsorption. U.S. Environmental Protection Agency. Environment Monitoring Systems Laboratories. Office of Research and Development, Cincinnati, Ohio 45268
- U.S. EPA (1994d). Method 218.6, Revision 3.3: Determination of dissolved hexavalent chromium in drinking water, groundwater and industrial wastewater effluents by ion chromatography. U.S. Environmental Protection Agency. Environment Monitoring Systems Laboratories. Office of Research and Development, Cincinnati, OH.
- U.S. EPA (1999). Guidelines for carcinogen risk assessment. National Center for Environmental Assessment, Risk Assessment Forum. U.S. Environmental Protection Agency, Washington, D.C. NCEA-F-0644. July 1999. Disponible à : www.epa.gov/ncea/raf/car2sab.htm
- U.S. EPA (2002). Manganese (CASRN 7439-96-5). Integrated Risk Information System (IRIS). Last revision: 1996 ed., National Center for Environmental Assessment (NCEA). U.S. Environmental Protection Agency. Disponible à : www.epa.gov/ncea/iris/subst/0373.htm. Dernière révision : 2002.
- U.S. EPA (2003). Method 200.5. Determination of trace elements in drinking water by axially viewed inductively coupled plasma – atomic emission spectrometry. U.S. Environmental Protection Agency. National exposure research laboratory. Office of research and development, Ohio 45268. EPA 600/R-06/115
- U.S. EPA (2004). Drinking water health advisory for manganese. Office of Water, Health and Ecological Criteria Division, EPA-822-R-04-003, U.S. Environmental Protection Agency, Washington, D.C. Disponible à : www.epa.gov/safewater/ccl/pdfs/reg_determine1/support_cc1_magnese_dwreport.pdf
- U.S. EPA (2006). Inorganic contaminant accumulation in potable water distribution systems. Office of Water, U.S. Environmental Protection Agency, U.S. Environmental Protection Agency, Washington, D.C. Disponible à : www.epa.gov/ogwdw/disinfection/tcr/pdfs/issuepaper_tcr_inorganiccontaminantaccumulation.pdf
- U.S. EPA (2009). 2009 edition of the drinking water standards and health advisories. United States EPA 822-R-09-011, Office of Water, U.S.Environmental Protection Agency, Washington, D.C. Disponible à : www.epa.gov/waterscience/criteria/drinking/dwstandards2009.pdf
- U.S. EPA (2010). Technical basis for the lowest concentration minimum reporting level (LCMRL) calculation. Office of Water (MLK 140) EPA 815-R-11-001 Décembre 2010 http://water.epa.gov/drink
- U.S. EPA (2012). Federal Registry Part II. Revisions of the Unregulated Contaminant Monitoring Regulation (UCMR 3) for public water systems; Final Rule. Vol 77, No 85. May 2, 2012. U.S.Environmental Protection Agency, Washington, D.C.
- Valencia, R., Mason, J.M., Woodruff, R.C. et Zimmering, S. (1985). Chemical mutagenesis testing in Drosophila. III. Results of 48 coded compounds tested for the National Toxicology Program. Environ. Mutagen., 7(3): 325–348.
- Vezer, T., Kurunczi, A., Naray, M., Papp, A. et Nagymajtényi, L. (2007). Behavioral effects of subchronic inorganic manganese exposure in rats. Am. J. Ind. Med., 50(11): 841–852.
- Vezer, T., Papp, A., Hoyk, Z., Varga, M., Naray, M. et Nagymajtényi, L. (2005). Behavioral and neurotoxicological effects of subchronic manganese exposure in rats. Environ. Toxicol. Pharmacol, 19: 797–810.
- Vieregge, P., Heinzow, B., Korf, G., Teichert, H.M., Schleifenbaum, P. et Mosinger, H.U. (1995). Long term exposure to manganese in rural well water has no neurological effects. Can. J. Neurol. Sci., 22: 286–289.
- Vreeburg, J. (2010). Discolouration in Drinking Water Systems: The Role of Particles Clarified. London: IWA Publishing.
- Vreeburg, J.H.G. et Boxall, J.B. (2007). Discolouration in potable water distribution systems: A review. Water Res., 41: 519–529.
- Vreeburg, J.H.G., Schippers, D., Verberk, J.Q.J.C. et van Dijk, J.C. (2008). Impact of particles on sediment accumulation in a drinking water distribution system. Water Res., 42, 4233–4242.
- Wallace, L. et Slonecker, T. (1997). Ambient air concentrations of fine (PM25) manganese in U.S. national parks and in California and Canadian cities: The possible impact of adding MMT to unleaded gasoline. J.Air Waste Manage. Assoc., 47(6): 642–652.
- Walsh, M.P. (2007). The global experience with lead in gasoline and the lessons we should apply to the use of MMT. Am. J. Ind. Med., 50(11): 853–860.
- Wang, L., Ohishi, T., Shiraki, A., Morita, R., Akane, H., Ikarashi, Y. et coll. (2012). Developmental exposure to manganese chloride induces sustained aberration of neurogenesis in the hippocampal dentate gyrus of mice. Toxicol. Sci., 127(2): 508–21.
- Ward, J.M. (1980). The carcinogenicity of ethylene dichloride in Osborne-Mendel rats and B6C3F1 mice. Dans : Ames, B., Infante, P. et Reitz, R. (éditeurs). Ethylene dichloride: A potential health risk? Banbury Rapport no 5. Cold Spring Harbor Laboratory, Cold Spring Harbor, New York, New York. p. 35–53.
- Wasserman, G.A., Liu, X., Parvez, F., Ahsan, H., Levy, D., Factor-Litvak, P., Kline, J., van Geen, A., Slavkovich, V., LoIacono, N.J., Cheng, Z., Zheng, Y. et Graziano, J.H. (2006). Water manganese exposure and children's intellectual function in Araihazar, Bangladesh. Environ. Health Perspect., 114(1): 124–129.
- Wasserman, G.A., Liu, X., Parvez, F., Factor-Litvak, P., Ahsan, H., Levy, D., Kline, J., van Geen, A., Mey, J., Slavkovich, V., Siddique, A.B., Islam, T. et Graziano, J.H. (2011). Arsenic and manganese exposure and children's intellectual function. Neurotoxicology, 32(4): 450–457.
- Weber, S., Dorman, D.C., Lash, L.H., Erikson, K., Vrana, K.E. et Aschner, M. (2002). Effects of manganese (Mn) on the developing rat brain: Oxidative-stress related endpoints. Neurotoxicology, 23(2): 169–175.
- Wong, P.K. (1988). Mutagenicity of heavy metals. Bull. Environ. Contam. Toxicol., 40: 597–603.
- Woolf, A., Wright, R., Amarasiriwardena, C. et Bellinger, D. (2002). A child with chronic manganese exposure from drinking water. Environ. Health Perspect., 110(6): 613–616.
- Wright, R.O. et Baccarelli, A. (2007). Metals and neurotoxicology. J. Nutr. 137(12): 2809–2813. Examen.
- Wright, R.O., Amarasiriwardena, C., Woolf, A.D., Jim, R. et Bellinger, D.C. (2006). Neuropsychological correlates of hair arsenic, manganese, and cadmium levels in school-age children residing near a hazardous waste site. Neurotoxicology, 27(2): 210–216.
- Yokel, R.A., Lasley, S.M. et Dorman, D.C. (2006). The speciation of metals in mammals influences their toxicokinetics and toxicodynamics and therefore human health risk assessment. J. Toxicol. Environ. Health B, 9(1): 63–85.
- Yoon, J.H. et Ahn, Y.S. (2015). A large, nationwide, longitudinal study of central nervous system diseases among Korean workers exposed to manganese. Parkinsonism Relat. Disord., 21(3): 194–198.
- Yoon, M., Nong, A., Clewell, H.J., 3rd, Taylor, M.D., Dorman, D.C. et Andersen, M.E. (2009a). Lactational transfer of manganese in rats: predicting manganese tissue concentration in the dam and pups from inhalation exposure with a pharmacokinetic model. Toxicol. Sci., 112(1): 23–43.
- Yoon, M., Nong, A., Clewell, H.J., 3rd, Taylor, M.D., Dorman, D.C. et Andersen, M.E. (2009b). Evaluating placental transfer and tissue concentrations of manganese in the pregnant rat and fetuses after inhalation exposures with a PBPK model. Toxicol. Sci., 112(1): 44–58.
- Yoon, M., Schroeter, J.D., Nong, A., Taylor, M.D., Dorman, D.C., Andersen, M.E. et coll. (2011). Physiologically based pharmacokinetic modeling of fetal and neonatal manganese exposure in humans: describing manganese homeostasis during development. Toxicol. Sci., 122(2): 297–316.
- Yu, X., Cao, L. et Yu, X. (2013). Elevated cord serum manganese level is associated with a neonatal high ponderal index. Environ. Res., 121(0): 79–83.
- Yu, X., Zhang, J., Yan, C. et Shen, X. (2014). Prenatal exposure to manganese at environment relevant level and neonatal neurobehavioral development. Environ. Res., 133(0): 232–238.
- Yukon Environmental Health Services (2014). Communication personnelle de P. Brooks.
- Zacheus, O.M., Lehtola, M.J., Korhonen, L.K. et Martikainen, P.J. (2001). Soft deposits, the key site for microbial growth in drinking water distribution networks, Water Res., 35(7): 1751–1765.
- Zhao, F., Cai, T., Liu, M., Zheng, G., Luo, W. et Chen, J. (2009). Manganese induces dopaminergic neurodegeneration via microglial activation in a rat model of manganism. Toxicol. Sci., 107(1): 156–64.
- Zheng, W., Kim, H. et Zhao, Q. (2000). Comparative toxicokinetics of manganese chloride and methylcyclopentadienyl manganese tricarbonyl (MMT) in Sprague-Dawley rats. Toxicol. Sci., 54: 295–301.
- Zheng, W., Ren, S. et Graziano, J.H. (1998). Manganese inhibits mitochondrial aconitase: A mechanism of manganese neurotoxicity. Brain Res., 799: 334–342. [tel que cité dans Santé Canada, 2010]
- Zlotkin, S.H., Atkinson, S. et Lockitch, G. (1995). Trace elements in nutrition for premature infants. Clin. Perinatol., 22(1): 223–240. [tel que cité dans Santé Canada, 2010]
- Zota, A.R. Ettinger, A.S., Bouchard, M., Amarasiriwardena, C.J., Schwartz, J., Hu, H. et Wright, R.O. (2009). Maternal blood manganese levels and infant birth weight. Epidemiology, 20(3): 367–373.
- Zwingmann, C., Leibfritz, D. et Hazell, A.S. (2003). Energy metabolism in astrocytes and neurons treated with manganese: relation among cell-specific energy failure, glucose metabolism, and intercellular trafficking using multinuclear NMR-spectroscopic analysis. J. Cereb. Blood Flow Metab., 23: 756–771.
Annexe A : Liste des acronymes
- AMT
- apport maximal tolérable
- ANSI
- American National Standards Institute
- AQT
- apport quotidien tolérable
- AS
- apport suffisant
- ATP
- adénosine triphosphate
- BOM
- bactérie oxydant le manganèse
- CAG
- charbon actif en grains
- CAS
- Chemical Abstracts Service
- CCN
- Conseil canadien des normes
- CIRC
- Centre International de Recherche sur le Cancer
- CMA
- concentration maximale acceptable
- COD
- carbone organique dissous
- COT
- carbone organique total
- DA
- dopamine
- ECAT
- Étude canadienne sur l'alimentation totale
- EPA
- Environmental Protection Agency (États Unis)
- GFAP
- protéine acide fibrillaire gliale
- IC
- intervalle de confiance
- ICP-AES
- spectrométrie d'émission atomique avec plasma induit par haute fréquence
- ICP-MS
- spectrométrie de masse avec plasma induit par haute fréquence
- JPN
- jour postnatal
- LCR
- liquide céphalorachidien
- LD
- limite de détection
- LDM
- limite de détection de la méthode
- LOAEL
- dose minimale avec effet nocif observé
- MAO
- monoamine oxydase
- MIREC
- Maternal-Infant Research on Environmental Chemicals
- MnB
- concentration de manganèse dans le sang
- MnH
- concentration de manganèse dans les cheveux
- MnW
- concentration de manganèse dans l'eau
- MON
- matière organique naturelle
- NOAEL
- dose sans effet nocif observé
- NSF
- NSF International
- OCDE
- Organisation de coopération et de développement économiques
- OD
- oxygène dissous
- OE
- objectif d'ordre esthétique
- OI
- osmose inverse
- OMS
- Organisation mondiale de la Santé
- p.c.
- poids corporel
- PBPK
- pharmacocinétique à base physiologique (modèle)
- PE
- point d'entrée
- PM
- matières particulaires
- PU
- point d'utilisation
- PVC
- polychlorure de vinyle
- QI
- quotient intellectuel
- SM
- méthode normalisée (standard method)
- SMNR
- seuil minimal de niveau à rapporter
- SNC
- système nerveux central
- SPD
- sous-produit de désinfection
- SPN
- semaine postnatale
- Tf
- transferrine
- UCMR3
- Third Unregulated Contaminant Monitoring Rule
- UTN
- unité de turbidité néphélémétrique
- VBS
- valeur basée sur la santé
