Comité consultatif national de l'immunisation (CCNI) : Lignes directrices pour l'évaluation économique des programmes de vaccination au Canada
1re édition : Avril 2023
[Format PDF : 1 826 Mo, 164 page]
Sur cette page
- Remerciements
- À la mémoire de Murray Krahn
- Déclaration de conflits d'intérêts
- Abréviations
- Glossaire
- Avant-propos
- Introduction
- Enoncés des lignes directrices
- Les lignes directrices en détail
- Annexe 1 : Tableau d'inventaire des effets
- Annexe 2 : Spécifications du cas de référence
- Références de l'avant-propos
- Références
Remerciements
Membres et agents de liaison du groupe de travail sur les lignes directrices économiques du CCNI
Les membres du groupe de travail étaient responsables de la sélection, de la détermination et de la discussion sur les principales questions liées à chaque chapitre, de la rédaction des sections, de l'examen de tous les chapitres provisoires, de l'examen du projet de rapport consolidé, de l'examen par les pairs et des commentaires des intervenants, ainsi que de l'examen et de l'approbation de la version finale des lignes directrices.
Membres du milieu universitaire :
Beate Sander, Ph. D.
Coprésidente du groupe de travail et membre du CCNI
Scientifique principale
Réseau universitaire de santé
Toronto (Ontario)
Murray Krahn, M.D.
Coprésident du groupe de travail (janvier 2019 - décembre 2021)
Professeur et directeur, Toronto Health Economics and Technology Assessment (THETA) Collaborative
Université de Toronto
Toronto (Ontario)
Stirling Bryan, Ph. D.
Professeur
Université de la Colombie-Britannique
Vancouver (Colombie-Britannique)
Werner Brouwer, Ph. D.
Professeur
Université Erasmus de Rotterdam
Rotterdam, Pays-Bas
Mark Jit, Ph. D.
Professeur
École d'hygiène et de médecine tropicale de Londres
Londres, Royaume-Uni
Sachiko Ozawa, Ph. D.
Professeur agrégée
Université de Caroline du Nord à Chapel Hill
Chapel Hill, Caroline du Nord
Lisa Prosser, Ph. D.
Professeur
Université du Michigan
Ann Arbor, Michigan
Agents de liaison :
Karen M. Lee, M.A.
Agente de liaison avec l'ACMTS
Directrice, Économie de la santé
Agence canadienne des médicaments et des technologies de la santé (ACMTS)
Ottawa (Ontario)
Monika Naus, M.D.
Agente de liaison provinciale-territoriale et agente de liaison avec le CCNI
Directrice médicale, Service des maladies transmissibles et de l'immunisation
Centre de contrôle des maladies de la Colombie-Britannique
Vancouver (Colombie-Britannique)
Membres de l'ASPC :
Man Wah Yeung, M. Sc.
Économiste principale de la santé
ASPC
Toronto (Ontario)
Austin Nam, Ph. D.
Économiste principale de la santé
ASPC
Toronto (Ontario)
Ashleigh Tuite, Ph. D.
Gestionnaire
ASPC
Toronto (Ontario)
Althea House, B. Sc. nat.
Gestionnaire
ASPC
Ottawa (Ontario)
Matthew Tunis, Ph. D.
Secrétaire général
ASPC
Ottawa (Ontario)
Entrepreneur :
Nina Lathia, Ph. D.
Économiste de la santé
Pas d'affiliation
Toronto (Ontario)
Examinateurs
L'ASPC tient à remercier les examinateurs universitaires et le groupe de travail sur l'économie du CCNI (groupe de travail jumeau) pour leur examen par les pairs des lignes directrices complètes. Le mandat du groupe de travail jumeau est d'élaborer des processus liés à l'économie de la santé pour le CCNI.
Examinateurs universitaires :
Lauren Cipriano, Ph. D.
Université Western
London (Ontario)
Kim Dalziel, Ph. D.
Université de Melbourne
Melbourne, Australie
David Fisman, M.D.
Université de Toronto
Toronto (Ontario)
Susan Griffin, Ph. D.
Université de York
York, Angleterre
Ava John-Baptiste, Ph. D.
Université Western
London (Ontario)
Christopher McCabe, Ph. D.
Kate Harback, Ph. D.
Erin Kirwin, M.A.
Ellen Rafferty, Ph. D.
Jeff Round, Ph. D.
Sasha van Katwyk, M. Sc.
au nom de
Institut d'économie de la santé
Edmonton (Alberta)
Bohdan Nosyk, Ph. D.
Université Simon Fraser
Burnaby (Colombie-Britannique)
Wendy Ungar, Ph. D.
Institut de recherche de l'Hôpital pour enfants
Toronto (Ontario)
Membres du groupe de travail sur l'économie du CCNI :
Beate Sander, Ph. D.
Réseau universitaire de santé
Toronto (Ontario)
Philippe De Wals, M.D., Ph. D.
Université Laval
Québec (Québec)
David Fisman, M.D.
Université de Toronto
Toronto (Ontario)
Kristin Klein, M.D.
Organisme de santé publique Alberta Health Services
Edmonton (Alberta)
Joanne Langley, M.D.
Université Dalhousie
Halifax (Nouvelle-Écosse)
Monika Naus, M.D.
Centre de contrôle des maladies de la Colombie-Britannique
Vancouver (Colombie-Britannique)
Ellen Rafferty, Ph. D.
Institut d'économie de la santé
Edmonton (Alberta)
Bernice Tsoi, Ph. D.
Agence canadienne des médicaments et des technologies de la santé (ACMTS)
Ottawa (Ontario)
Collaborateurs
L'ASPC tient à remercier les personnes suivantes pour leur contribution :
Collaborateurs du milieu universitaire :
- Lisa Schwartz, Ph. D. - a contribué à l'élaboration du chapitre sur l'équité
- Richard Cookson, Ph. D. - a contribué à l'élaboration du chapitre sur l'équité
- Pieter van Baal, Ph. D. - a contribué à l'élaboration du chapitre sur l'utilisation et les coûts des ressources
Collaborateurs de Services aux Autochtones Canada :
- Kendra Hardy, M.A. - a révisé l'avant-propos, le chapitre sur l'équité et le chapitre sur les types d'évaluation
- Melanie Knight, inf. aut. - a révisé le chapitre sur l'équité et le chapitre sur les types d'évaluation
- Andrea Monahan, inf. aut. - a révisé l'avant-propos
- Denise Hamilton, MPA - a révisé l'avant-propos
- Tom Wong, M.D. - a révisé l'avant-propos, le chapitre sur l'équité et le chapitre sur les types d'évaluation
- Kim Daly, M. Nurs. - a révisé l'avant-propos
- Pamela Wolfe-Roberge, B.A. - a révisé le chapitre sur l'équité et le chapitre sur les types d'évaluation
Collaborateurs du Groupe consultatif en matière d'éthique en santé publique :
- Diego Silva, Ph. D. - a révisé le chapitre sur l'équité
- Béatrice Godard, Ph. D. - a révisé le chapitre sur l'équité
- Boluwaji Ogunyemi, M.D. - a révisé le chapitre sur l'équité
- Cassandra Opikokew Wajuntah, Ph. D. (c) - a révisé le chapitre sur l'équité
- Maxwell J. Smith, Ph. D. - a révisé le chapitre sur l'équité
- A.M. Viens, Ph. D. - a révisé le chapitre sur l'équité
- Alice Virani, Ph. D. - a révisé le chapitre sur l'équité
Collaborateurs du CCNI :
- Sheela Ramanathan, Ph. D. - a révisé le chapitre sur l'efficacité
- Kyla Hildebrand, M.D. - a révisé le chapitre sur l'efficacité
- Matthew Miller, Ph. D. - a révisé le chapitre sur l'efficacité
Collaborateurs de l'ASPC :
- Alexandra Cernat, M. Sc. - a fourni un soutien en matière de référencement, de collecte des commentaires du public et de révision linguistique
- Erica Tice, M. Sc. - a révisé l'avant-propos
- Shainoor Ismail, M.D. - a révisé le chapitre sur l'équité
- Angela Sinilaite, MSP - a révisé le chapitre sur l'équité
- Amanda Sumner, M.A. - a fourni un soutien technique au début du projet
- Christine Mauviel, B.A. - a fourni un soutien à la gestion de projet
- Chantale Tremblay, B. Sc. - a fourni un soutien à la gestion de projet
- Jennifer Daniel - a fourni un soutien à la gestion de projet
- Siobhan Kelly, B.A. - a fourni un soutien à la gestion de projet
- Caroline Rodriguez-Charette, B.J. - a fourni un soutien à la gestion de projet
- L'ASPC tient à souligner les discussions qui ont eu lieu lors des réunions du CCNI avec les membres du CCNI, les agents de liaison et les membres d'office, ainsi que l'examen de ces derniers. Les membres du CCNI ont approuvé la version finale des lignes directrices.
Membres du CCNI :
- Shelley Deeks (présidente), M.D., Santé et Mieux-être (Nouvelle-Écosse)
- Robyn Harrison (vice-présidente), M.D., organisme de santé publique Alberta Health Services
- Melissa Andrew, M.D., Université Dalhousie
- Julie Bettinger, Ph. D., Institut de recherche de l'hôpital pour enfants de la Colombie-Britannique
- Nicholas Brousseau, M.D., Institut national de santé publique du Québec
- Philippe De Wals, M.D., Ph. D., Université Laval
- Hélène Decaluwe, M.D., Ph. D., Université de Montréal
- Ève Dubé, Ph. D., Université Laval
- Vinita Dubey, M.D., Université de Toronto
- Kyla Hildebrand, M.D., Hôpital pour enfants de la Colombie-Britannique
- Kristin Klein, M.D., organisme de santé publique Alberta Health Services
- Miranda O' Driscoll, inf. aut., spécialiste du contrôle des maladies de Terre-Neuve-et-Labrador
- Jesse Papenburg, M.D., Hôpital de Montréal pour enfants
- Anne Pham-Huy, M.D., Hôpital pour enfants de l'est de l'Ontario
- Beate Sander, Ph. D., Réseau universitaire de santé
- Sarah Wilson, M.D., Santé publique Ontario
Anciens membres du CCNI :
- Caroline Quach-Thanh (ancienne présidente), M.D., Université de Montréal
- Natalie Dayneka, PharmD, Hôpital pour enfants de l'est de l'Ontario
- Soren Gantt, M.D., Université de la Colombie-Britannique
- Coleman Rotstein, M.D., Université de Toronto
- Susan Smith, inf. aut., gouvernement de l'Alberta
- Wendy Vaudry, M.D., Université de l'Alberta
- Martin Lavoie, M.D., Autorité sanitaire de Fraser
- Nadine Sicard, M.D., ministère de la Santé et des Services sociaux
- Marina Salvadori, M.D., Hôpital pour enfants de l'ouest de l'Ontario
Agents de liaison avec le CCNI :
- Lea Bill, inf. aut., Association canadienne des infirmières et infirmiers autochtones
- Lucie Marisa Bucci, M.A., Association canadienne de santé publique
- Eliana Castillo, M.D., Société des obstétriciens et gynécologues du Canada
- Jeannette Comeau, M.D., Association pour la microbiologie médicale et l'infectiologie Canada
- Martin Lavoie, M.D., Conseil des médecins hygiénistes en chef
- Dorothy Moore, M.D., Société canadienne de pédiatrie
- Monika Naus, M.D., Comité canadien d'immunisation
- Amanda Ung, B. Sc. Pharm., Association des pharmaciens du Canada
- Melanie Osmack, M.A., Association des médecins autochtones du Canada
- Jessica MacNeil, MSP, Centers for Disease Control and Prevention
Anciens agents de liaison avec le CCNI :
- Evan Adams, M.D., Association des médecins autochtones du Canada
- Loretta Dupuis, inf. aut., Association des infirmières et infirmiers du Canada
- Jia Hu, M.D., Collège des médecins de famille du Canada
- Julie Emili, M.D., Collège des médecins de famille du Canada
- Reka Gustafson, M.D., Conseil des médecins hygiénistes en chef
- Amanda Cohn, M.D., Centers for Disease Control and Prevention
- Kathleen Dooling, M.D., Centers for Disease Control and Prevention
- Jason Brophy, M.D., Association canadienne pour la recherche et l'évaluation en immunisation
- Deshayne Fell, Ph. D., Association canadienne pour la recherche et l'évaluation en immunisation
- Philip Emberley, PharmD, Association des pharmaciens du Canada
- Sarah Funnell, M.D., Association des médecins autochtones du Canada
Représentants d'office :
- Erin E. Henry, B. Sc. Nat., Agence de la santé publique du Canada
- Vincent Beswick-Escanlar, M.D., Défense nationale et Forces armées canadiennes
- Mireille Lacroix, LL. M., Agence de la santé publique du Canada
- Celia Lourenco, Ph. D., Santé Canada
- Susanna Ogunnaike-Cooke, M. Sc., Agence de la santé publique du Canada
- Kelly Robinson, M. Sc., Santé Canada
- Michael Routledge, M.D., Laboratoire national de microbiologie
- Tom Wong, M.D., Services aux Autochtones du Canada
- Patrick Fandja, M. Sc., Santé Canada
- Diane MacDonald, M. Sc., Agence de la santé publique du Canada
Anciens représentants d'office :
- Gina Charos, Agence de la santé publique du Canada
- Celia Lourenco, Ph. D., Santé Canada
- Robert Pless, M.D., Santé Canada
- Kelly Robinson, M. Sc., Santé Canada
- Jim Gallivan, Ph. D., Santé Canada
- Guillaume Poliquin, M.D., Ph. D., Laboratoire national de microbiologie
- Jennifer Pennock, M. Sc., Agence de la santé publique du Canada
À la mémoire de Murray Krahn
Après le décès d'un ami, d'un collègue, d'un mentor et d'un géant du domaine
1957 - 2022
Le Dr Murray Krahn est décédé le 1er juillet 2022 à l'âge de 65 ans. Au moment de son décès, nous étions à six mois de la finalisation de la première édition de ces lignes directrices - un travail qui a commencé en janvier 2019. M. Murray a un long et brillant passé, non seulement en tant que médecin membre du personnel prenant soin de ses patients et formant les nouveaux médecins résidents, mais aussi en tant que chef de file mondial de l'évaluation des technologies de la santé.
Après avoir vécu dans sa jeunesse à Kodaikanal, en Inde, à Seattle, dans l'État de Washington, et à Fresno, en Californie, la formation de Murray l'a conduit à Winnipeg, au Manitoba, où il a obtenu des diplômes en philosophie et en médecine, et à Toronto où il a suivi une formation en médecine interne. Pendant sa résidence, il s'est intéressé à la prise de décision médicale et a obtenu une maîtrise en épidémiologie clinique à l'université McMaster, puis il a obtenu une bourse de recherche sur la prise de décision clinique à l'université Tufts.
M. Murray a occupé de nombreux postes de direction, notamment en tant que président de la Society for Medical Decision Making (SMDM) et en tant que fondateur du la collaboration Toronto Health Economics and Technology Assessment (THETA), dont il a été le directeur pendant 13 ans. Il a également été professeur à l'École de santé publique Dalla Lana et à la Faculté de médecine et la Faculté de pharmacie de l'Université de Toronto, scientifique principal au Toronto General Research Institute et scientifique auxiliaire à l'IRSS (anciennement Institut de recherche en services de santé). Dans ces fonctions, il s'est fait le champion des évaluations des technologies de la santé et des évaluations économiques. Son influence a été reconnue par un certain nombre de prix prestigieux, notamment par une chaire de recherche du Canada de niveau 1 en évaluation des technologies de la santé, le Prix de la SMDM pour une carrière exceptionnelle, le Prix de la SMDM pour services distingués, le Prix d'excellence Dr Jill M. Sanders en évaluation des technologies de la santé de l'Agence canadienne des médicaments et des technologies de la santé, le Prix du chercheur principal de l'Association des facultés de pharmacie du Canada, le prix David Sackett du chercheur chevronné de la Société canadienne de médecine interne, une bourse de recherche des les Instituts de recherche en santé du Canada et la bourse Arthur Bond en recherche sur les systèmes de santé novateurs de la Physicians' Service Incorporated.
Au cours de l'élaboration de ces lignes directrices, M. Murray a coprésidé le groupe de travail sur les lignes directrices économiques, a révisé les premières versions des chapitres au fur et à mesure de leur élaboration, et a participé à des débats philosophiques amicaux. Il a apporté de la bienveillance et de la gentillesse saupoudrées d'humour à nos réunions.
Il est évident que la carrière de Murray lui a procuré une joie immense et un sens à sa vie. Comme l'a souligné sa famille, Murray chérissait ses amitiés et ses collaborations avec ses collègues et ses étudiants. Il était passionné par le mentorat et par la formation de la prochaine génération de chercheuses et chercheurs et de personnel médical. Son départ laissera un grand vide.
Déclaration de conflits d'intérêts
Dans le cadre des procédures standards d'identification et de traitement des affiliations et des intérêts, les membres du groupe de travail sur les orientations économiques ont rempli des formulaires de divulgation individuels qui ont été évalués par l'ASPC afin de s'assurer de l'absence d'influence indue ou de conflit d'intérêts perçu.
- Beate Sander n'avait aucune déclaration d'intérêts et d'affiliations à faire.
- Murray Krahn n'avait aucune déclaration d'intérêts et d'affiliations à faire.
- Stirling Bryan n'a aucune déclaration d'intérêts et d'affiliations à faire.
- Werner Brouwer n'avait aucune déclaration d'intérêts et d'affiliations à faire.
- Mark Jit a déclaré recevoir des fonds de recherche d'organisations à but non lucratif (Commission européenne et Organisation mondiale de la santé).
- Karen M. Lee n'avait aucune déclaration d'intérêts et d'affiliations à faire.
- Monika Naus n'avait aucune déclaration d'intérêts et d'affiliations à faire.
- Sachiko Ozawa a déclaré avoir reçu des fonds de recherche de Merck Sharp & Dohme Corporation, de la Fondation Bill & Melinda Gates, du North Carolina Department of Health and Human Services et du National Cancer Institute.
- Lisa Prosser n'avait aucune déclaration d'intérêts et d'affiliations à faire.
Abréviations
- ACA
- Analyse coûts-avantages
- ACMTS
- Agence canadienne des médicaments et des technologies de la santé
- ACU
- Analyse coût-utilité
- ASD
- Analyse de sensibilité déterministe
- AVAQ
- Année de vie ajustée en fonction de la qualité
- CARCE
- Courbe d'acceptabilité du rapport coût-efficacité
- CCNI
- Comité consultatif national de l'immunisation
- CHEERS II
- Consolidated Health Economic Evaluation Reporting Standards II
- CHU9D
- Mesure de l'utilité reliée à la santé chez l'enfant
- CP
- Corrélat de protection
- ÉÉFA
- Éthique, équité, faisabilité et acceptabilité
- EQ-5D
- Instrument sur la santé EQ-5D
- EQ-5D-Y
- Instrument sur la santé EQ-5D (pour enfant)
- ERC
- Essai randomisé contrôlé
- Évaluation de la QDV
- Instrument d'évaluation de la qualité de vie
- FE
- Frontière d'acceptabilité du rapport coût-efficacité
- HUI
- Health Utilities Index
- IQ
- Inuit Qaujimajatuqangit
- PedsQL
- Pediatric Quality of Life Inventory
- QVLS
- Qualité de vie liée à la santé
- RCED
- Rapport coût-efficacité différentiel
- SF-6D
- Instrument Short Form 6- Dimensions
- SIR
- susceptible-infectieux-remis (immunisé)
- SIS
- Susceptible-infectieux-susceptible
- TB
- Tuberculose
- VPH
- Virus du papillome humain
- Administration des doses
- Accumulation du nombre requis de doses d'un schéma vaccinal pendant une période donnée pour les schémas à plusieurs doses.
- Agence canadienne des médicaments et des technologies de la santé (ACMTS)
- Organisme indépendant et sans but lucratif chargé de fournir aux responsables des politiques de santé du Canada des données probantes sur l'utilisation optimale des médicaments et des instruments médicaux dans le cadre du système public de soins de santé.
- Analyse coûts-avantages (ACA)
- Évaluation économique dans laquelle les coûts et les résultats sont exprimés en termes financiers.
- Analyse coûts-conséquence (ACC)
- Évaluation économique dans laquelle les résultats en matière de santé sont exprimés en unités naturelles (p. ex. les infections évitées).
- Analyse coûts-efficacité distributive
- Extension du cadre conventionnel de l'ACE qui quantifie les impacts distributifs des interventions sanitaires en fonction de différents critères d'équité tels que le statut socio-économique ou la gravité de la maladie.
- Analyse coûts-efficacité étendue
- Extension du cadre conventionnel de l'analyse coûts-efficacité (ACE) qui quantifie les impacts distributifs des interventions sanitaires en fonction de critères d'équité ainsi que de la protection contre les risques financiers. La protection contre les risques financiers fait référence à l'accès des ménages aux services de santé nécessaires sans qu'ils aient à subir de difficultés financières excessives.
- Analyse coûts-utilité (ACU)
- Évaluation économique dans laquelle les résultats en matière de santé sont exprimés en année de vie ajustée en fonction de la qualité (ou autre mesure générique de l'utilité reliée à la santé). On parle parfois d'une analyse coûts-efficacité (ACE) ou ACE avec AVAQ. Il s'agit de l'évaluation économique privilégiée par les responsables des politiques de santé publique au Canada.
- Analyse de la valeur de l'information
- Analyse utilisée pour estimer la valeur, en matière de coûts et de résultats pour la santé, de la collecte de davantage de données sur les paramètres clés influençant une décision de financement. Elle est particulièrement utile lorsque le résultat d'une évaluation économique est incertain, mais proche d'un seuil de décision et qu'un paramètre clé sur lequel repose le résultat est incertain. Voir les définitions de la valeur attendue de l'information parfaite (VAIP) et de la valeur attendue de l'information partielle parfaite (VAIPP).
- Analyse de scénario
- Analyse qui teste des scénarios de rechange de modèles sous-tendus par différentes hypothèses structurelles plausibles.
- Analyse de sensibilité déterministe (ASD)
- Méthode utilisée pour explorer l'incertitude des résultats d'une évaluation économique fondée sur un modèle, dans laquelle on fait varier un ou plusieurs paramètres dans une fourchette prédéfinie tout en maintenant les autres paramètres fixes, afin de déterminer l'influence de la variation sur les résultats de l'analyse.
- Analyse de sensibilité probabiliste (ASP)
- Voir la définition de l'analyse probabiliste.
- Analyse probabiliste
- Méthode utilisée pour quantifier l'incertitude relative aux paramètres dans une analyse économique où une distribution de probabilité est attribuée à chaque paramètre incertain et où les valeurs sont échantillonnées au hasard de manière répétée à partir de chaque distribution afin de générer une distribution de résultats qui peuvent être analysés.
- Année de vie ajustée en fonction de la qualité (AVAQ)
- Mesure de résultat sommaire utilisée pour quantifier les résultats en matière de santé associés à une intervention particulière. Les AVAQ combinent l'impact des avantages liés à la fois à la survie et à la qualité de vie liée à la santé exprimés en tant qu'utilités de la santé, et permettent de comparer les interventions entre les différents états pathologiques.
- Avantage financier net
- Statistique sommaire qui représente la valeur d'une intervention exprimée en termes financiers. Il estime le bénéfice tiré d'une intervention (monétisé sur la base d'un seuil de rentabilité) et le compare au coût de l'intervention. Un avantage financier net positif implique un avantage supérieur au coût (c'est-à-dire que l'intervention est rentable par rapport à l'autre stratégie).
- Avantage net pour la santé
- Statistique sommaire, exprimée en AVAQ, qui représente l'impact sur la santé de la population liée à une intervention donnée. Il estime la santé qui est perdue ailleurs lorsque les fonds sont déplacés pour payer l'intervention. Un avantage net positif pour la santé implique que la santé globale de la population augmente avec l'introduction de l'intervention.
- Biais confusionnel
- Estimation biaisée de la relation entre une exposition et un résultat dans une étude, résultant d'une troisième variable, la variable confusionnelle, qui est liée à la fois à l'exposition et au résultat.
- Comité consultatif national de l'immunisation (CCNI)
- Comité consultatif national formé d'experts dans les domaines de la pédiatrie, des maladies infectieuses, de l'immunologie, de la pharmacie, des soins infirmiers, de l'épidémiologie, de la pharmacoéconomie, des sciences sociales et de la santé publique. Le Comité formule des recommandations sur l'utilisation des vaccins dont l'administration chez l'homme est actuellement ou récemment approuvée au Canada, notamment en signalant les groupes à risque pour les maladies évitables par la vaccination qui devraient être la cible des campagnes de vaccination.
- Consommation
- Biens et services achetés par les individus.
- Corrélat de protection (CP)
- Biomarqueur immunitaire qui prédit l'efficacité potentielle d'un vaccin chez les personnes vaccinées et peut être utilisé comme critère de substitution dans les études sur l'efficacité potentielle ou réelle des vaccins.
- Courbe d'acceptabilité du rapport coût-efficacité (CARCE)
- Résumé graphique de l'incertitude des résultats d'une évaluation économique, où une gamme de seuils de coût-efficacité est représentée en fonction de la probabilité qu'une intervention soit rentable.
- Coûts différentiels
- Différence entre les coûts moyens attendus associés à l'utilisation d'une intervention par rapport à l'utilisation d'une option. Il s'agit d'un résultat clé d'une évaluation économique.
- Couverture
- Pourcentage estimé de personnes admissibles ayant reçu un vaccin particulier.
- Dominance étendue
- Il y a dominance étendue lorsqu'on compare trois stratégies ou plus et que le coût total de la stratégie (A) est supérieur à celui de la stratégie (B), laquelle est supérieure à la stratégie (C); et que le rapport coût-efficacité différentiel de la stratégie (A) par rapport à la stratégie (C) est inférieur à celui de la stratégie (B) par rapport à la stratégie (C). Par conséquent, le décideur doit éliminer la stratégie (B) de toute considération ultérieure. En effet, le fait d'offrir une stratégie plus efficace (A) à une fraction de la population et une stratégie inférieure au reste de la population domine l'offre d'une stratégie éliminée par la dominance étendue (B) à l'ensemble de la population.
- Dominance
- Désigne un scénario dans lequel une stratégie entraîne des avantages plus importants et des coûts moindres par rapport à une autre stratégie. On dit que la stratégie qui entraîne le plus d'avantages et le moindre coût domine l'autre stratégie.
- Efficacité potentielle
- Avantage d'une intervention produit dans un cadre expérimental et contrôlé, comme dans un essai randomisé contrôlé (ERC). À distinguer de l'efficacité réelle (voir définition ci-dessus).
- Efficacité réelle
- Mesure dans laquelle une intervention donne les résultats souhaités dans la population de patients concernée dans le monde réel.
- Efficience
- Mesure dans laquelle le plus grand avantage des interventions est maximisé en utilisant les ressources disponibles, ou dans laquelle un avantage donné est obtenu en utilisant le moins de ressources possible et en réduisant les coûts au minimum.
- Élimination de la maladie
- L'incidence locale d'une infection particulière a été réduite à un niveau inférieur à celui nécessaire pour maintenir une transmission continue dans une zone géographique donnée, mais des efforts continus sont nécessaires pour maintenir cette réduction.
- Équilibre épidémiologique
- Situation dans laquelle le taux de nouvelles infections circulant dans une population est égal au taux de guérison de l'infection, ce qui donne lieu à un état stable ou immuable.
- Équité en matière de santé
- Absence de différences injustes et évitables ou remédiables en matière de santé entre des groupes de population définis par toute caractéristique pertinente (p. ex. sociale, économique, démographique ou géographique). L'équité horizontale consiste à traiter de la même manière des individus présentant des caractéristiques similaires (d'une pertinence éthique), tandis que l'équité verticale permet de traiter différemment des individus présentant des caractéristiques différentes (d'une pertinence éthique) afin d'obtenir des résultats plus équitables.
- Équité intergénérationnelle
- Concept selon lequel les personnes de différentes générations devraient bénéficier équitablement des décisions politiques comme les dépenses liées aux programmes de vaccination.
- Équité
- Voir la définition de l'équité en matière de santé.
- Éradication de la maladie
- L'incidence d'une infection a été définitivement réduite à zéro dans le monde entier, l'organisme causal n'est plus présent dans la nature et des efforts ne sont plus nécessaires pour maintenir cette réduction.
- Essai randomisé contrôlé (ERC)
- Étude comparative, conçue pour vérifier l'efficacité potentielle d'une intervention dans le domaine de la santé, dans laquelle des unités comme les individus sont réparties au hasard entre le groupe d'intervention et le groupe témoin.
- Évaluation des technologies de la santé (ETS)
- Processus pluridisciplinaire qui utilise des méthodes explicites pour déterminer la valeur d'une technologie de santé à différents moments de son cycle de vie. L'objectif est d'éclairer la prise de décision afin de promouvoir un système de santé équitable, efficace et de haute qualité.
- Externalités
- Coûts et conséquences d'une intervention telle qu'un programme de vaccination qui retombent sur d'autres membres de la population que ceux qui subissent l'intervention (p. ex., immunité collective, déplacement de la maladie en fonction de l'âge).
- Force de l'infection
- Taux d'infection des individus réceptifs par unité de temps. C'est une fonction du nombre d'individus infectieux dans la population à un moment donné et de la transmissibilité de l'infection.
- Frontière d'efficience (FE)
- Résumé graphique de l'incertitude des résultats d'une évaluation économique, qui indique la stratégie économiquement préférable pour différentes valeurs seuils du rapport coût-efficacité et la probabilité que cette stratégie soit efficace par rapport au coût. À mesure de l'augmentation du seuil, le traitement économiquement privilégié peut changer (point de basculement). Les FARCE sont les plus utiles lorsque l'on compare au moins trois options, auquel cas il peut y avoir deux points de basculement ou plus à des valeurs seuils différentes.
- Hétérogénéité
- Différences entre les personnes qui peuvent, en partie, être expliquées. Cela diffère du hasard qui veut que des individus ayant les mêmes caractéristiques sous-jacentes connaissent un résultat différent.
- Horizon temporel
- Période sur laquelle les résultats et les coûts sont quantifiés dans une évaluation économique.
- Immunité collective
- État dans lequel une proportion suffisante de la population est immunisée contre une maladie infectieuse, soit par la vaccination, soit par une infection antérieure, ce qui empêche l'apparition d'épidémies et rend la propagation entre individus moins probable. Le terme est couramment utilisé pour désigner la protection indirecte dont bénéficient les personnes non vaccinées du fait de la présence d'individus immunisés dans une population.
- Immunité de groupe
- Voir la définition de l'immunité collective.
- Incertitude de premier ordre
- Incertitude liée à la variabilité aléatoire des résultats pour des personnes identiques. Ce type d'incertitude est également appelé incertitude stochastique.
- Incertitude de second ordre
- Voir la définition de l'incertitude des paramètres.
- Incertitude des paramètres
- Incertitude des estimations des paramètres qui sont utilisées pour alimenter un modèle. Ce type d'incertitude est également appelé incertitude de second ordre.
- Incertitude méthodologique
- Incertitude liée aux différentes méthodes qui peuvent être utilisées pour réaliser une évaluation économique.
- Incertitude structurelle
- Incertitude liée à la structure d'un modèle et autres sources d'incertitude non paramétrées. L'analyse de scénarios est une approche permettant d'évaluer ce type d'incertitude.
- Lutte contre la maladie
- L'état dans lequel l'incidence, la prévalence, la morbidité ou la mortalité d'une maladie donnée a été réduit au niveau local, mais des efforts continus sont nécessaires pour maintenir cette réduction.
- Microsimulation
- Voir la définition du modèle individuel.
- Modèle (de population) fermé
- Modèle qui suit une ou plusieurs tranches fixes de personnes. Les personnes ne sont pas en mesure d'entrer ou de sortir dans le modèle par l'intermédiaire de naissances, de décès ou de l'immigration au fil du temps.
- Modèle (de population) ouvert
- Modèle qui permet à de nouveaux individus d'entrer dans le modèle par des naissances ou par des migrations entrantes, ou de sortir du modèle par des décès ou par des migrations sortantes au fil du temps.
- Modèle (de temps) continu
- Modèle dans lequel les événements peuvent se produire à tout moment.
- Modèle (temporel) discret
- Modèle dans lequel les événements ne peuvent se produire qu'à des moments prédéterminés dans le temps.
- Modèle à base d'agents
- Voir la définition du modèle individuel.
- Modèle basé sur les populations (modèle agrégé)
- Modèle dans lequel des groupes d'individus sont assignés à des compartiments ou à des états de santé en fonction de leur état de santé ou d'autres caractéristiques. Les individus se déplacent d'un compartiment à l'autre en fonction des valeurs des paramètres définis au niveau agrégé et le modèle enregistre le nombre d'individus dans chaque compartiment au fil du temps.
- Modèle déterministe
- Un modèle qui décrit ce qui se passe en moyenne et dans lequel les événements ne peuvent pas se produire de manière aléatoire (par hasard). Pour un ensemble défini de paramètres et de conditions de départ, ces modèles génèrent toujours les mêmes résultats, chaque fois qu'ils sont exécutés.
- Modèle dynamique (de transmission)
- Modèle dans lequel la force de l'infection peut varier dans le temps. L'incidence est fonction du nombre (ou de la proportion) de personnes infectées et réceptives et de la transmissibilité du virus.
- Modèle individuel (inclut la microsimulation et le modèle multiagents)
- Modèle dans lequel l'individu, plutôt que le groupe, est l'unité qui est modélisée. Les modèles basés sur l'individu peuvent être avec ou sans interactions (par exemple, les interactions avec d'autres individus ou avec l'environnement, y compris la disponibilité des ressources). Les modèles basés sur l'individu comprennent les modèles d'échantillonnage individuel, les modèles d'historique des événements individuels et les simulations d'événements discrets. Dans les modèles d'analyse décisionnelle au niveau individuel, la probabilité de transition, le risque d'événements ou le délai avant événement s'appliquent à chaque individu. Chaque simulation représente un individu, ce qui introduit l'hétérogénéité et la stochasticité. Dans les modèles de maladies infectieuses basés sur l'individu, la structure biologique, les caractéristiques démographiques et les facteurs de risque sont appliqués au niveau individuel, de sorte que l'histoire naturelle, le niveau de risque et les contacts/interactions peuvent varier entre les personnes.
- Modèle statique
- Modèle dans lequel la force de l'infection est constante dans le temps ou dépend uniquement des caractéristiques de chaque individu, et non du nombre d'autres individus qui sont infectieux.
- Modèle stochastique
- Aux fins des présentes lignes directrices, modèle qui tient compte de l'incertitude de premier ordre où les événements sont programmés pour se produire de manière aléatoire.
- Paramètres
- Variables qui déterminent les taux de mouvement entre les états du modèle ou les probabilités d'événements dans un modèle.
- Période d'incubation
- Temps qui s'écoule entre l'infection et l'apparition de la maladie clinique.
- Période de latence
- Période entre le moment où un hôte acquiert une infection et celui où il peut la transmettre à un autre hôte. On l'appelle parfois la période préinfectieuse.
- Période infectieuse
- Période allant de la fin de la période de latence ou de la période préinfectieuse jusqu'à ce que l'hôte ne soit plus en mesure de transmettre l'infection à d'autres individus.
- Perspective
- Point de vue à partir duquel une évaluation économique sera menée. La perspective détermine les résultats et les coûts qui seront inclus dans l'analyse.
- Peuples autochtones
- Premiers groupes humains connus sur n'importe quelle terre dans le monde. Aux fins des présentes lignes directrices, l'expression « peuples autochtones » désigne les individus qui sont de Premières nations, des Inuits et des Métis.
- Préférence temporelle positive
- Préférence pour les avantages actuels par rapport aux avantages à venir.
- Preuve dans le monde réel
- Preuve utilisée pour la prise de décision, qui est recueillie au moyen d'études non expérimentales.
- Problème de décision
- Déclaration explicite des interventions, des populations étudiées, des mesures de résultats et de la perspective adoptée dans une évaluation économique, liée spécifiquement aux décisions que l'évaluation cherche à guider.
- Productivité
- Mesure de l'efficacité avec laquelle les facteurs de production, tels que le travail et le capital, sont utilisés dans une économie pour produire un niveau donné d'extrants.
- Qualité de vie liée à la santé (QVLS)
- Un concept multidimensionnel qui décrit les aspects physiques, le fonctionnement des rôles, les aspects sociaux et psychologiques du bien-être et du fonctionnement.
- Rapport coût-efficacité différentiel (RCED)
- Rapport calculé en divisant la différence entre les coûts moyens attendus et la différence entre les résultats ou effets moyens attendus sur la santé entre deux options comparées dans une évaluation économique. Le comparateur représente généralement la norme de soins actuelle.
- Référence
- Ensemble de méthodes permettant d'effectuer une évaluation économique spécifiée par le décideur. Le but de l'analyse de référence est d'assurer la cohérence entre les méthodes qui sous-tendent les analyses et le processus décisionnel qui est employé.
- Remplacement du sérotype
- Expansion des sérotypes non vaccinaux d'un agent pathogène résultant de l'élimination de la population des sérotypes propres au vaccin qui leur font concurrence pour la colonisation d'hôtes.
- Retombées
- Les effets non intentionnels de l'intervention sur les soignants, les membres de la famille, les membres du foyer et autres (c'est-à-dire le réseau social des patients). Les retombées sont un type d'externalité. Voir la définition des externalités.
- Santé publique
- Les efforts organisés de la société pour maintenir les personnes en santé et éviter les blessures, les maladies et les décès prématurés. Cette définition est celle de l'Association canadienne de santé publique. Dans ces lignes directrices, la Santé publique est stylisée en majuscules pour mieux la distinguer des « soins de santé publics », qui font référence aux soins de santé publics.
- Santé
- La santé est un état de complet bien-être physique, mental et social, et ne consiste pas seulement en une absence de maladie ou d'infirmité. Cette définition est tirée de la constitution de l'Organisation mondiale de la santé.
- Stratégie de rattrapage
- Stratégie consistant à vacciner les personnes qui n'ont pas reçu une vaccination particulière à l'âge recommandé. Cette stratégie peut être utilisée chez les personnes qui n'étaient pas admissibles à la vaccination, qui ont manqué une dose de vaccin prévue ou qui n'ont pas terminé une série de vaccins.
- Système de santé
- Aux fins des présentes lignes directrices, le terme « système de santé » désigne à la fois les services cliniques de soins de santé et la santé publique.
- Taux d'escompte
- Les coûts et les résultats en matière de santé qui se produiront à l'avenir généralement considérés comme ayant une valeur moindre que ceux qui se produisent aujourd'hui; on les actualise donc dans une évaluation économique pour déterminer leur valeur actuelle. Le facteur par lequel les coûts et les résultats en matière de santé sont actualisés est exprimé en tant que taux d'escompte.
- Taux de reproduction de base
- Le nombre moyen de cas secondaires infectés par une personne infectieuse dans une population complètement réceptive.
- Taux de reproduction effectif
- Nombre moyen de cas secondaires infectés par une personne infectieuse dans une population dont certains individus sont immunisés contre l'infection, en raison de la vaccination ou de l'infection.
- Technologie de la santé
- L'application de connaissances et de compétences organisées sous la forme de dispositifs, de médicaments, de vaccins, de procédures et de systèmes mis au point pour résoudre un problème de santé et améliorer la qualité de vie. Cette définition est celle de l'Organisation mondiale de la santé.
- Utilité de la santé
- Mesure de la qualité de vie liée à la santé qui représente les préférences que les personnes attachent à leur état de santé général. Par convention, les évaluations sont ancrées à 0 (représentant un état de santé équivalent à la mort) et à 1 (représentant un état de santé équivalent à une santé parfaite). Les utilités de la santé sont également appelées mesures de la qualité de vie liée à la santé fondées sur les préférences.
- Valeur attendue de l'information parfaite (VAIP)
- La valeur, en termes financiers, de l'élimination de toute incertitude sur les paramètres de l'analyse (c'est-à-dire de l'obtention d'informations parfaites sur tous les paramètres). Les estimations sont calculées en utilisant un seuil de rentabilité préspécifié, qui peut être modifié dans les analyses de sensibilité. Si la VAIP dépasse le coût d'une recherche plus poussée, on peut considérer qu'il est rentable de collecter davantage d'informations (données) pour éliminer l'incertitude des paramètres du modèle. La VAIP peut également être exprimée pour l'ensemble de la population susceptible de bénéficier de l'intervention pendant la durée de vie prévue de celle-ci (connu sous le nom de VAIP de la population). L'utilisation de la VAIP suppose que la décision de financement est entièrement basée sur la question de savoir si l'intervention est rentable à un seuil de rentabilité précis.
- Valeur attendue de l'information parfaite partielle (VAIPP)
- La valeur, en termes financiers, de l'élimination de l'incertitude d'une ou plusieurs entrées d'un modèle économique (c'est-à-dire de l'obtention d'une information parfaite sur un sous-ensemble de paramètres). Les estimations sont calculées en utilisant un seuil de rentabilité préspécifié, qui peut être modifié dans les analyses de sensibilité. Si la VAIPP dépasse le coût d'une recherche plus poussée, on peut considérer qu'il est rentable de recueillir davantage d'informations (données) pour éliminer l'incertitude du sous-ensemble de paramètres du modèle. L'utilisation de la VAIPP suppose que la décision de financement est entièrement basée sur la question de savoir si l'intervention est rentable à un seuil de rentabilité précis.
- Variation de l'âge d'infection
- Phénomène qui peut se produire lorsqu'une tranche d'âge particulière de la population est vaccinée, ce qui réduit la force d'infection dans cette tranche et déplace l'âge moyen de l'infection.
- Variations de l'agent pathogène
- Différences entre les souches d'un agent pathogène liées aux sérotypes, aux sérogroupes ou aux génotypes.
Avant-propos : Comment prendre en compte les perspectives des Premières Nations, des Inuits et des Métis dans l'évaluation économique des programmes de vaccination
Évaluations économiques et évaluations des technologies de la santé des programmes de vaccination
Dans ces lignes directrices, nous suggérons comment les évaluations économiques des programmes de vaccination devraient être menées au Canada. Les recommandations relatives aux programmes de vaccination fédéraux sont formulées par le Comité consultatif national de l'immunisation (CCNI) selon son cadre décisionnel, où le rapport coût-efficacité (obtenu par des évaluations économiques) est l'un des facteurs à prendre en considération. Le cadre décisionnel du CCNI est basé sur le cadre analytique d'Erickson et De Wals, qui a été élaboré pour « l'analyse et la comparaison de programmes de vaccination potentiels ».Note de bas de page a Le cadre d'Erickson et De Wals comprend 13 critères de décision, dont huit entrent dans le champ d'application du CCNI et sont donc inclus dans le cadre de décision du CCNI (en italique) : (i) le fardeau de la maladie, (ii) les caractéristiques du vaccin (par exemple, efficacité, innocuité), (iii) les questions de recherche, (iv) la stratégie et le programme d'immunisation, (v) le rapport coût-efficacité, (vi) les considérations éthiques, (vii) l'équité, (viii) la faisabilité, (viii) l'acceptabilité, (ix) la capacité d'évaluer les programmes, (xi) les considérations juridiques, (xii) la conformité du programme, et (xiii) les considérations politiques.
Les décideurs peuvent noter le chevauchement important entre les facteurs ci-dessus et les attributs de prise de décision souvent inclus dans les cadres d'évaluation des technologies de la santé (ETS). Les ETS déterminent la valeur des interventions en matière de santé, telles que les instruments médicaux, les médicaments, les vaccins, les procédures ou les systèmes. Bien qu'il existe plusieurs cadres d'ETS, le modèle de base de l'ETS (figure 1) représente un moyen utile d'identifier la gamme complète des attributs de décision utilisés au niveau international dans l'ETS. Le modèle de base a été élaboré par le Réseau européen d'ETS (EUneHTA), qui regroupe 70 institutions dans 32 pays. Ce cadre comprend neuf domaines distincts d'évaluation de la technologie, dont la description du problème de santé, les caractéristiques techniques, la sécurité, l'efficacité, les coûts et l'évaluation économique, l'analyse éthique, les aspects organisationnels, les aspects liés au patient et à la société, et les aspects juridiques, et est donc plus large que la plupart des conceptualisations d'ETS. Les auteurs affirment que le modèle de base de l'ETS, bien qu'élaboré en Europe, est générique et conçu pour une utilisation mondiale.Note de bas de page b Le modèle de base de l'ETS représente une vaste conceptualisation de la gamme potentielle d'applications de l'ETS, plutôt que des directives détaillées sur la façon dont chacun de ces domaines doit être défini et mis en œuvre dans un cadre décisionnel à attributs multiples. Que l'on utilise le cadre décisionnel du CCNI ou le modèle de base de l'ETS, de nombreux attributs de décision sont les mêmes, et l'objectif des deux approches est de soutenir la prise de décision pour les interventions financées par des fonds publics. Dans les deux approches, aucune distinction n'est faite entre les attributs qui sont descriptifs (par exemple, les caractéristiques du vaccin), les attributs qui sont normatifs (par exemple, les critères d'évaluation tels que l'efficacité, le rapport coût-efficacité) et les attributs liés à des considérations de faisabilité (par exemple, l'impact budgétaire, la faisabilité organisationnelle).

Abréviations : HTA, health technology assessment (évaluation des technologies de la santé); REA, relative effectiveness assessment (évaluation de l'efficacité relative) Extrait de « The HTA Core Model-10 Years of Developing an International Framework to Share Multidimensional Value Assessment », par BørlumKristensen et al., 2017, Value in Health, Volume 20, p. 244-50. 2017 Tous droits réservés par Elsevier. Reproduit avec autorisation. Cette image a été traduite de sa version originale en anglais et utilisée avec l'autorisation de l'auteur.
Figure 1 - Équivalent textuel
La figure 1 illustre le champ d'application du modèle de base du réseau européen d'évaluation des technologies de la santé (EUneHTA). Une évaluation complète des technologies de la santé comprend neuf domaines : (1) le problème de santé et l'utilisation actuelle de la technologie, (2) la description et les caractéristiques techniques, (3) la sécurité, (4) l'efficacité clinique, (5) les coûts et l'évaluation économique, (6) l'analyse éthique, (7) les aspects organisationnels, (8) les aspects sociaux et relatifs aux patients, et (9) les aspects juridiques. Une évaluation rapide de l'efficacité relative comprend les quatre premiers domaines (1 - 4).
Réflexions préliminaires sur la prise en compte et l'intégration des perspectives autochtones dans le processus d'évaluation des technologies
Aussi large soit-elle, cette approche « occidentale conventionnelle » est-elle adaptée à la situation? En d'autres termes, les approches actuelles de l'ETS, telles que décrites dans le cadre décisionnel du CCNI ou dans le modèle de base de l'ETS, sont-elles adéquates pour mener et évaluer les ETS d'une manière qui tienne compte des connaissances et des savoirs des Premières nations, des Inuits et des Métis en matière de santé et de bien-être? Les attributs, les règles de décision pour combiner les attributs et les processus de décision utilisant les approches conventionnelles d'ETS sont-ils appropriés? Comment pouvons-nous intégrer davantage les perspectives autochtones dans les décisions relatives à la santé?Note de bas de page cNote de bas de page dNote de bas de page e Qu'en est-il des mécanismes de financement?
Il s'agit de questions difficiles, pour lesquelles il existe peu de réponses à l'heure actuelle sur la base de notre revue de la littérature. Alors que la littérature relative à l'évaluation de la santé des peuples autochtones ne cesse de croître,Note de bas de page c peu de choses sont publiées concernant l'évaluation des technologies du point de vue des autochtones, y compris la façon précise dont l'évaluation des technologies devrait être informée par les perspectives autochtones. Nous n'essayons donc pas, dans les présentes lignes directrices, de rendre pleinement compte ou d'exposer les perspectives autochtones qui devraient être incluses dans l'ETS. Nous proposons plutôt quelques ressources et réflexions préliminaires, tout en reconnaissant que les perspectives autochtones varient, notamment en fonction de la distinction, de la région et de la nation, et qu'il y a beaucoup de travail à faire pour mieux comprendre comment intégrer de manière significative les perspectives autochtones dans l'ETS. Les ressources suivantes peuvent éclairer une analyse de la santé et du bien-être qui intègre les perspectives autochtones :
1) Cadres sur les déterminants sociaux de la santé
L'une de ces ressources est l'état des connaissances sur la santé des autochtones du Centre de collaboration nationale de la santé autochtone (CCNSA) : Examen de la santé publique autochtone au Canada.Note de bas de page f Le document du CCNSA conceptualise la santé autochtone de manière générale dans un cadre de déterminants sociaux de la santé. Les déterminants sociaux de la santé qui ont un impact sur les populations autochtones sont notamment le colonialisme (y compris la perte irrévocable des terres, de la langue, de la culture et des moyens de subsistance), la mondialisation, la migration, la continuité culturelle, le territoire, l'accès, la pauvreté, le racisme, l'exclusion sociale, l'autodétermination, la terre et la gestion de l'environnement. Ces déterminants ne sont pas des catégories discrètes, mais ont plutôt une relation complexe et interconnectée.
Le document fait également état de la grande diversité culturelle et géographique (notamment selon qu'il s'agit d'endroits urbains, éloignés, dans les réserves ou hors des réserves) des Premières nations, des Inuits et des Métis. Il existe des disparités au sein des populations en ce qui concerne le statut socio-économique (y compris l'emploi, le type de travail, le revenu, le niveau d'éducation et le développement économique), le développement précoce et les structures familiales saines, le bien-être des femmes (y compris la violence et la criminalisation), l'accès aux services de santé, les conditions de logement et la perte de la langue et de la culture.
Une autre ressource est le Framework for Understanding the Social Determinants of Health and Indigenous People du Dr Margo GreenwoodNote de bas de page g. Le cadre met également en évidence les contextes historiques et contemporains des relations et réalités sociales, culturelles, politiques et économiques. Il couvre les systèmes, les structures et les disciplines non autochtones, les communautés, les nations et la culture autochtones, ainsi que leur interface.
Il convient de noter que les travaux axés sur les déterminants sociaux de la santé peuvent ne pas s'aligner complètement, en matière de portée et d'intention, sur l'ETS traditionnelle. Les travaux sur les déterminants sociaux de la santé identifient les facteurs associés à la santé et au bien-être. L'évaluation des technologies se concentre généralement un peu plus étroitement sur la santé et reflète une plus grande concentration sur les questions économiques telles que le rapport coût-efficacité et l'accessibilité financièreNote de bas de page f. Néanmoins, des efforts récents ont été déployés pour appliquer les dimensions de l'équité (y compris les déterminants sociaux de la santé) à l'ETS,Note de bas de page h notamment dans le cadre décisionnel du CCNI (voir le cadre d'éthique, d'équité, de faisabilité et d'acceptabilité [ÉÉFA] du CCNI)Note de bas de page iet dans les présentes lignes directrices sur les évaluations économiques (voir le chapitre 14 sur l'équité).
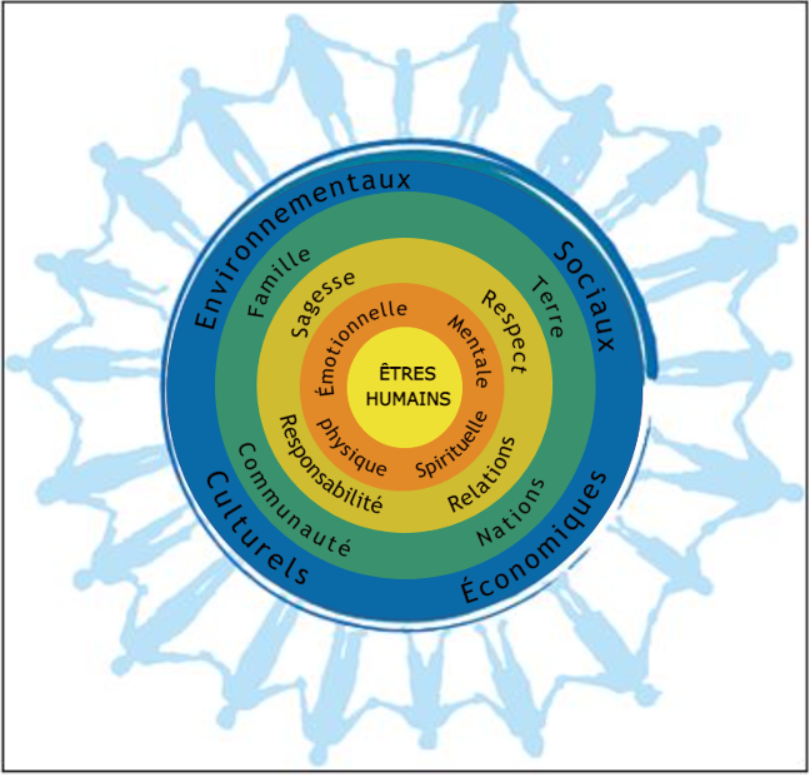
Tiré de « First Nations Perspective on Health and Wellness » par la Régie de la santé des Premières Nations, 2021. 2021, Tous droits réservés par la Régie de la santé des Premières Nations. Reproduit avec autorisation. Cette image a été traduite de sa version originale en anglais et utilisée avec l'autorisation de l'auteur.
Figure 2 - Équivalent textuel
La figure 2 est la représentation visuelle de la santé et du bien-être de la Régie de la santé des Premières Nations.Note de bas de page c Le cercle central représente les êtres humains individuels. Le bien-être commence par la prise en charge par les individus de leur propre santé. Le deuxième cercle illustre l'importance des facettes mentale, émotionnelle, spirituelle et physique d'une vie saine et équilibrée. Le troisième cercle représente les valeurs primordiales qui soutiennent et maintiennent le bien-être : le respect, la sagesse, la responsabilité et les relations. Le quatrième cercle dépeint les personnes qui nous entourent et les lieux d'où nous venons. La terre, la communauté, la famille et les nations sont toutes des composantes essentielles de notre expérience saine en tant qu'êtres humains. Le cinquième cercle représente les déterminants sociaux, environnementaux, culturels et économiques de la santé et du bien-être. Le document de la Régie de la santé des Premières Nations comporte une section particulière consacrée à l'économie, qui met l'accent sur la gestion, le partage et le maintien des ressources.
Les personnes qui forment le cercle externe représentent la vision de la Régie de la santé des Premières Nations : des enfants, des familles, des aînés et des personnes forts dans les communautés. Les personnes se tiennent la main pour démontrer l'unité, le respect et les relations, ce qui, selon les mots d'un aîné respecté de la Colombie-Britannique, peut se traduire par « un cœur, un esprit ».Note de bas de page c
2) Les perspectives inuites sur la santé et le bien-être
Une autre ressource du CCNSA décrit le rôle de l'Inuit Qaujimajatuqangit (IQ), le système de connaissances caractéristique de la culture inuite, dans le soutien du bien-être dans les communautés inuites du Nunavut.Note de bas de page j Tel que documenté par les aînés inuits du Nunavut, le cadre de l'IQ est fondé sur : (i) le travail pour le bien commun, (ii) le respect de tous les êtres vivants, (iii) le maintien de l'harmonie et l'équilibre, et (iv) la planification et la préparation continue de l'avenir. L'IQ est le fondement du bien-être social, émotionnel, spirituel, cognitif et physique, et favorise le bien-être personnel et culturel. La santé culturelle est « la base de toutes les autres formes de santé, car en elle réside le sentiment d'identité, les soutiens sociaux collectifs de l'individu et le sentiment d'appartenance ».Note de bas de page j Le document reconnaît la nécessité d'une approche culturelle de la santé pour la population inuite et reconnaît l'économie comme un aspect de l'environnement socioculturel à examiner.
Répercussions pour les lignes directrices économiques canadiennes des programmes de vaccination
Comme indiqué dans les ressources décrites ci-dessus, les conceptualisations de la santé et du bien-être sont vastes.Note de bas de page cNote de bas de page fNote de bas de page gNote de bas de page j L'accent mis sur les dimensions écologique, sociale et communautaire de la santé est remarquable. La santé individuelle n'est possible que si la communauté est en bonne santé. L'ETS utilise toute une série de définitions de la santé, dont certaines sont plus proches des conceptualisations autochtones de la santé et du bien-être, et d'autres non. Par exemple, les concepteurs du Health Utilities Index (HUI) et d'autres indices d'état de santé couramment utilisés adoptent délibérément une approche individuelle de la mesure de la santé.Note de bas de page kNote de bas de page lNote de bas de page mNote de bas de page n Ils excluent spécifiquement les dimensions sociales et culturelles de la santé. Cela contraste avec la définition plus large de la santé de l'Organisation mondiale de la santé (également utilisée par les lignes directrices ici), qui prend en compte le bien-être physique, mental et social.Note de bas de page o De plus, dans les ressources autochtones, il y a une reconnaissance explicite de l'importance du « territoire » dans le maintien de la vie individuelle et communautaire. Les considérations environnementales font l'objet d'une attention croissante dans la prise de décision en matière de santé en général. Les ressources de la Régie de la santé des Premières Nations de la Colombie-Britannique et du CCNSA soulignent la nécessité de prêter attention à la terre, à la nourriture, à l'air, à l'eau et au logement en tant que déterminants fondamentaux de la santé. Il est admis que les ressources sont limitées, mais ce problème est formulé différemment des approches économiques classiques. Plutôt que de considérer la prise de décision dans le contexte de ressources limitées comme un problème d'optimisation, les ressources ci-dessus présentent le problème des ressources limitées comme un défi de partage et de gestion des ressources disponibles. Le problème est le même, mais l'accent est mis sur le partage et la prise de décision en collaboration.
Nous n'avons pas l'intention de suggérer que nos nouvelles lignes directrices sur l'évaluation économique soient définitives. En particulier, nous reconnaissons que les futures versions de ces lignes directrices devront évoluer pour tenir compte plus globalement des perspectives des Premières nations, des Inuits et des Métis de manière. Toutefois, notre bref aperçu nous donne à penser que les attributs et les processus de décision utilisés dans l'ETS classique, bien qu'actuellement insuffisants, ne sont pas sans rapport avec la tâche consistant à éclairer les décisions publiques judicieuses concernant l'utilisation des vaccins. Bon nombre des thèmes abordés dans le document de l'EUneHTA sont également évoqués dans les ressources ci-dessus sur la santé et le bien-être des Autochtones. Nous reconnaissons également que les évaluations économiques ne sont pas indépendantes et qu'elles s'inscrivent dans des cadres décisionnels, notamment des attributs de décision, des règles de décision et des processus de décision précis.
Cet examen de haut niveau a révélé certaines des lacunes de la documentation sur l'ETS et nous donne à penser qu'il y a un travail important à entreprendre, en tant que comité et en tant que domaine d'étude, pour comprendre les perspectives autochtones sur la santé et la technologie. Pour cette version des lignes directrices, Services aux Autochtones Canada a révisé cet avant-propos, le chapitre 2 sur les types d'évaluation et le chapitre 14 sur l'équité. Les versions futures des lignes directrices, ainsi que le cadre décisionnel du CCNI de manière plus générale, nécessiteront une collaboration et un engagement avec, entre autres, les gouvernements, les organisations et les groupes universitaires autochtones. Les versions futures pourraient bénéficier de la prise en compte du cadre conceptuel Etuaptmumk (Mi'kmaq pour « approche à double perspective »), qui fournit des conseils sur la prise en compte des perspectives autochtones et occidentales en parallèle pour obtenir une compréhension enrichie et mutuelle. L'aîné mi'kmaq Albert Marshall, de la Première nation Eskasoni, définit la double perspective comme suit : « apprendre à voir d'un œil avec les forces des connaissances et des manières de savoirs autochtones, et de l'autre œil avec les forces des connaissances et des manières de savoir traditionnelles, et utiliser ces deux perspectives ensemble, pour que tous puissent en tirer avantage ».Note de bas de page p Dans la prochaine version des lignes directrices, nous prévoyons d'intégrer le savoir autochtone afin que les perspectives des peuples autochtones soient prises en compte dans le processus décisionnel des services de santé publique concernant les programmes de vaccination au Canada. Nous envisageons que ce travail sur les évaluations économiques influence et informe les développements futurs des cadres décisionnels de l'ETS.
Introduction
Le présent document constitue la première édition des Lignes directrices du Comité consultatif national de l'immunisation (CCNI) sur l'évaluation économique des programmes de vaccination au Canada; dans le texte qui suit, elles seront désignées par Lignes directrices. Les Lignes directrices ont été établies afin de définir les meilleures pratiques pour la réalisation et la communication des évaluations économiques des programmes de vaccination au Canada, au niveau régional, provincial ou national. L'adhésion à des pratiques exemplaires communes peut permettre aux décideurs du système de santé publique du Canada d'avoir accès à des renseignements cohérents et crédibles qui orienteront les décisions de financement relatives aux programmes de vaccination. Dans ses Lignes directrices de l'évaluation économique des technologies de la santé au CanadaNote de bas de page 1, l'Agence canadienne des médicaments et des technologies de la santé présente des renseignements plus généraux applicables aux technologies de la santé au Canada. Les technologies de la santé peuvent désigner des dispositifs, des médicaments, des procédures et des systèmes. Lorsque les énoncés des Lignes directrices de l'ACMTS peuvent s'appliquer aux évaluations économiques des programmes de vaccination, ils ont été repris dans les présentes Lignes directrices.
La principale caractéristique qui distingue les programmes de vaccination des autres technologies de la santé est leur effet au niveau de la population, qui résulte du fait qu'ils peuvent toucher à la fois les personnes vaccinées et celles qui ne le sont pas. Les Lignes directrices présentent des informations détaillées sur la manière d'intégrer ces effets au niveau de la population dans les évaluations économiques des programmes de vaccination, y compris les méthodes permettant de prendre en compte leurs impacts en dehors du secteur de la santé.
Processus de développement
Les recommandations formulées dans les Lignes directrices ont été préparées par le Groupe de travail sur les lignes directrices en matière d'économie du CCNI, composé d'experts canadiens et internationaux en maladies infectieuses et en économie de la santé. Pendant quatre ans, le groupe s'est engagé dans une série de discussions qui ont abouti à des décisions prises par consensus, lesquelles ont été étayées par des revues de la littérature pour certains sujets. Au cours du processus de développement, ce groupe a mené une série de discussions avec des intervenants, dont le Comité canadien d'immunisation (qui se concentre sur la planification des programmes d'immunisation) et le Conseil des médecins hygiénistes en chef, qui sont formés tous deux de représentants de chaque province et territoire. Pendant le processus d'examen, les partenaires du gouvernement fédéral, incluant Services aux Autochtones Canada et le Groupe consultatif en matière d'éthique en santé publique de l'Agence de la santé publique du Canada (ASPC) ont fournit leurs commentaires sur leur domaine de compétence. Un processus d'examen par les pairs et de consultation publique a été entrepris après l'achèvement de la première version des Lignes directrices et a permis de rédiger les recommandations et le texte définitifs du présent document. Un processus de consultation publique a permis de recueillir les commentaires des intervenants, notamment : l'industrie, les groupes de patients, les groupes d'orientation économique, les agences d'évaluation des technologies de la santé, les groupes consultatifs techniques nationaux sur la vaccination et le grand public. Ces consultations et examens ont permis de formuler les recommandations et le texte définitifs contenus du présent document. Les lignes directrices ont été approuvées par le Groupe de travail sur les lignes directrices économiques, le CCNI et l'ASPC.
Aperçu et structure des lignes directrices
Un cadre décisionnel social a été adopté pour les Lignes directrices. Il repose sur le fait que le responsable des politiques de santé agit au nom d'une autorité supérieure socialement légitime (p. ex. un gouvernement démocratiquement élu) pour atteindre un objectif politique explicite (p. ex. améliorer la santé globale de la population). Dans ce cadre, la fonction d'une évaluation économique est d'étayer les décisions sociales.Note de bas de page 2Note de bas de page 3Note de bas de page 4
Les Lignes directrices utilisent la définition de la santé de l'Organisation mondiale de la santé, selon laquelle « la santé est un état de complet bien-être physique, mental et social, et ne consiste pas seulement en une absence de maladie ou d'infirmité ».Note de bas de page 5 Les détracteurs de cette définition large affirment que le concept est irréalisable et difficile à mettre en œuvre en tant qu'objectif pour les services de santé. Les partisans d'une définition large affirment que les définitions biomédicales, souvent axées sur le handicap ou le déficit, sont inadéquates. Le groupe de travail est en phase avec la communauté de la santé publique qui voit l'intérêt d'inclure les domaines psychologique, social, spirituel et du bien-être. Le groupe de travail reconnaît également les besoins pragmatiques des chercheurs qui mesurent et évaluent la santé au moyen d'instruments génériques couramment utilisés. Par conséquent, les Lignes directrices recommandent aux chercheurs d'évaluer et de justifier les sources de données sur les valeurs d'utilité de l'état de santé en fonction de leur pertinence, de leur crédibilité et de leur cohérence. Il s'agit notamment d'évaluer dans quelle mesure les différents domaines de la santé sont pris en compte pour la maladie infectieuse en question, et si le fait de compléter les instruments génériques par des instruments spécifiques à la maladie peut permettre d'identifier les effets sur la santé qui ne sont pas pris en compte ou qui ne le sont pas de manière adéquate.
Les évaluations économiques se sont traditionnellement concentrées sur les compromis entre les coûts différentiels et les effets différentiels de différentes interventions en matière de santé afin de permettre aux décideurs de porter des jugements sur l'efficacité. Ces lignes directrices élargissent l'approche traditionnelle en encourageant l'intégration de considérations d'équité dans les évaluations économiques des programmes de vaccination. Cette intégration est conforme au cadre d'éthique, d'équitabilité, de faisabilité et d'acceptabilité (ÉÉFA) du CCNI, qui fournit un mécanisme permettant aux décideurs de prendre systématiquement en compte ces quatre facteurs, ainsi que l'efficacité et le rapport coût-efficacité, lorsqu'ils formulent des recommandations sur les programmes de vaccination.Note de bas de page 6
Des recommandations sont présentées pour les aspects suivants des évaluations économiques des programmes de vaccination : problème de décision, types d'évaluations, populations étudiées, comparateurs, perspectives, horizon temporel, actualisation, modélisation, efficacité, mesure et évaluation de la santé, utilisation et coût des ressources, analyse, incertitude, équité et rapports. Les conseils sur chacun de ces sujets sont donnés dans un chapitre distinct. Les énoncés des Lignes directrices sont présentés dans la section suivante de ce document et au début de chaque chapitre pour en faciliter l'utilisation, suivis d'une discussion détaillée sur les recommandations. Ces déclarations contiennent des recommandations pour deux analyses de cas de référence. Les cas de référence encouragent l'utilisation d'un ensemble standard de méthodes lors de l'évaluation économique des programmes de vaccination et permettent aux décideurs de comparer les résultats entre différents programmes de vaccination. Les cas de référence ne sont pas destinés à être une liste de vérification à suivre sans réserve. Par conséquent, les chercheurs qui ne peuvent pas (ou croient fermement qu'ils ne doivent pas) suivre une recommandation particulière doivent documenter cet écart, présenter une justification et discuter des implications probables sur les inférences de l'évaluation économique. En outre, tout écart doit être signalé de manière bien visible (par exemple, dans le résumé ou le sommaire) afin que les utilisateurs de l'étude qui ne lisent pas tous les détails ne se méprennent pas sur les principales conclusions.
Ces Lignes directrices sont rédigées à l'intention des chercheurs qui effectuent des évaluations économiques, ainsi que des utilisateurs finaux de données économiques tels que les décideurs - en d'autres termes, ceux qui maîtrisent techniquement les méthodes d'évaluation économique. Ainsi, le contexte des méthodes a été omis. Ces Lignes directrices ne sont pas destinées à servir d'introduction ou de traité méthodologique (par exemple, sur le choix de la structure du modèle, la construction du modèle, la classification des données probantes). De même, les Lignes directrices omettent les renseignements généraux détaillés relatives aux vaccins et à l'immunisation, car il est prévu que les chercheurs consultent des experts en la matière. Les références contenues dans ce document constituent des sources permettant aux chercheurs d'obtenir des renseignements supplémentaires si nécessaire.
Les conseils présentés dans ce document représentent les recommandations actuelles du CCNI pour la réalisation d'évaluations économiques des programmes de vaccination. Les Lignes directrices ont tenté de refléter les pratiques exemplaires actuelles, mais les recommandations qu'elles contiennent évolueront en fonction des progrès scientifiques et méthodologiques. Les sujets pour lesquels il n'existe pas de consensus actuel sur les pratiques exemplaires et qui nécessitent des recherches supplémentaires ont été déterminés. Ainsi, la fonction de ces Lignes directrices est non seulement de recommander les pratiques exemplaires actuelles pour l'évaluation économique des programmes de vaccination, mais aussi de suggérer des orientations pour les recherches futures. Les Lignes directrices ne sont pas destinées à être normatives pour ces sujets.
Le mandat de ces Lignes directrices est de spécifier les méthodes d'évaluation économique des programmes de vaccination, et non de fournir des conseils ou des réflexions sur le processus de prise de décision. Pour ceux qui s'intéressent au processus de prise de décision au niveau fédéral canadien, veuillez vous référer au « Processus d'intégration des données économiques dans les recommandations fédérales relatives aux vaccins » du CCNI.Note de bas de page 7
Justification pour deux cas de référence
Ces Lignes directrices recommandent l'adoption de deux analyses de cas de référence pour l'évaluation économique des programmes de vaccination : l'une menée du point de vue du système de santé publique et l'autre menée du point de vue de la société. Cette dernière consiste à prendre en compte l'ensemble des incidences associées aux programmes de vaccination, y compris ceux qui reviennent aux secteurs ne relevant pas de la santé et aux personnes qui ne sont pas directement vaccinées (c'est-à-dire par le biais des retombées et des externalités ne relevant pas de la santé). Certaines de ces incidences générales sont uniques ou exceptionnellement importantes dans le cadre des programmes de vaccination. Parmi les groupes universitaires ainsi que l'Organisation mondiale de la santé, on s'accorde de plus en plus à dire que les vaccins génèrent de la valeur par le biais d'incidence traditionnellement non pris en compte dans les évaluations des technologies de la santé.Note de bas de page 8Note de bas de page 9 Le fait de ne pas en tenir compte peut conduire à une sous-évaluation des programmes de vaccination, et par conséquent à des décisions de financement et d'allocation des ressources sous-optimales. Il convient de noter que les incidences générales ne concernent pas uniquement les avantages; par exemple, la mise en œuvre entraîne des coûts environnementaux que les Lignes directrices recommandent de prendre en compte dans une évaluation économique des programmes de vaccination.
Le groupe de travail a sérieusement envisagé l'adoption de deux perspectives, tout en reconnaissant qu'il existe des arguments contre l'utilisation de la perspective sociétale comme cas de référence (par exemple, l'absence d'un seuil de rentabilité sociétale estimé empiriquement; l'absence de méthodes établies pour quantifier en termes financiers certains des incidences plus larges). Le groupe de travail reconnaît que de nombreux arguments pour ou contre ce cas de référence impliquent un jugement normatif et des préférences sociales; il n'y a donc pas de « bon » choix. Au cours de la consultation, les décideurs de la santé publique canadienne ont exprimé l'intérêt de délibérer des résultats du point de vue de la société et du point de vue du système de santé publique. Les résultats obtenus tant du point de vue du système de santé publique que du point de vue de la société peuvent fournir aux décideurs un compte rendu plus complet des incidences du programme de vaccination.
Une note générale à l'intention des décideurs pour la prise en compte de deux perspectives
Les décideurs du CCNI n'utilisent pas de pondération explicite des différents déterminants de décision lorsqu'ils délibèrent sur les décisions au sujet de la vaccination à l'ordre fédéral. De même, ils n'utilisent pas de pondérations explicites lorsqu'ils interprètent les résultats des évaluations économiques du point de vue du système de santé publique par rapport au point de vue de la société. Pour les décideurs en général, cependant, certains peuvent choisir de mettre davantage l'accent sur les résultats d'une perspective plutôt qu'une autre, compte tenu de leur situation particulière. Par exemple, la perspective du système de santé peut être mise en avant lorsqu'il existe un budget de santé fixe à partir duquel les vaccins sont financés et que les autres technologies de santé de ce même budget sont évaluées uniquement du point de vue du système de santé. La perspective sociétale peut être mise en avant lorsque les vaccins sont financés par un budget général, ou lorsque les décideurs s'intéressent au bien-être général et pas seulement aux gains en santé. Les décideurs ne doivent pas ignorer les nombreux impacts des programmes de vaccination qui ne relèvent pas du secteur de la santé. Il en va de même pour d'autres technologies de la santé, même si leurs effets autres que sur la santé peuvent être moindres. À ce titre, le groupe de travail soutient même que les évaluations d'autres technologies de la santé au Canada pourraient bénéficier d'un cas de référence supplémentaire réalisé du point de vue de la société.
Là encore, des jugements normatifs et des préférences sociales entrent en jeu; il n'y a donc pas de « bonne » d'approche pour savoir comment ou si l'on doit pondérer les résultats des deux perspectives. Les recommandations sur les deux cas de référence et les multiples analyses de sensibilité trouvées dans ces Lignes directrices soutiennent la prise de décision fondée sur des données probantes pour le programme de vaccination.
Enoncés des lignes directrices
1. Problème de décision
- 1.1 « Énoncer clairement le problème de décision devant faire l'objet de l'évaluation économique. » [Énoncé des lignes directrices de l'ACMTS]
- 1.2 Dans l'énoncé du problème de décision, préciser les interventions à comparer, le cadre ou le contexte de la comparaison, la perspective de l'évaluation, la nature des coûts et des résultats ou des paramètres pris en considération (incluant les externalités), l'horizon temporel et la population cible de l'évaluation (incluant les populations directement ou indirectement ciblées par le programme de vaccination). [Énoncé des lignes directrices de l'ACMTS, modifié]
2. Types d'évaluations
- 2.1 L'analyse de référence dans l'évaluation économique est une analyse coût-utilité (ACU), dans laquelle les résultats sont exprimés en années de vie gagnées ajustées en fonction de la qualité (AVAQ). Justifier clairement tout autre choix. [Énoncé des lignes directrices de l'ACMTS, modifié]
- 2.2 Il est possible de recourir à une analyse coûts-avantages (ACA) en plus des ACU de référence lorsque le programme de vaccination peut être comparé à une intervention autre que de santé.
3. Populations étudiées
- 3.1 Les chercheurs doivent identifier les populations visées par le programme de vaccination, les populations à risque pour la maladie en question, et toutes les populations qui peuvent être indirectement affectées par le programme de vaccination, soit par des externalités, soit par des retombées.
- 3.2 Les chercheurs doivent présenter une analyse globale qui inclut les coûts et les résultats pour toutes les populations concernées. Le cas échéant, les chercheurs doivent également résumer les résultats séparément pour chaque groupe affecté (par exemple, la population visée, la population subissant des externalités ou des retombées) qui a été inclus dans l'analyse globale.
- 3.3 Lorsqu'il existe des facteurs susceptibles d'entraîner des différences de coûts et de résultats liés au programme de vaccination entre les sous-groupes, les chercheurs doivent réaliser des évaluations économiques distinctes pour chaque sous-groupe. Ces facteurs peuvent inclure des facteurs démographiques, des facteurs comportementaux, des facteurs liés à la maladie et l'efficacité du vaccin ou des interventions de comparaison.
4. Comparateurs
- 4.1 Choisir les comparateurs en fonction de la portée du problème de décision. Les comparateurs choisis doivent être adaptés à la population visée par le programme de vaccination et à la région où la décision s'appliquera. [Énoncé des lignes directrices de l'ACMTS, modifié]
- 4.2 Les chercheurs doivent prendre en compte les approches préventives et thérapeutiques lors de la sélection des comparateurs pour les évaluations économiques des programmes de vaccination. Les interventions préventives peuvent inclure des mesures basées sur des vaccins, des programmes de dépistage, des interventions préventives fondées sur des médicaments et des interventions préventives non médicales.
5. Perspectives
- 5.1 Il faut présenter deux analyses de cas de référence dans le cadre de l'évaluation économique des programmes de vaccination : l'une menée dans la perspective du système de santé financé par l'État, et l'autre dans la perspective sociétale.
- 5.2 « Veiller à ce que les coûts comme les résultats ou effets des interventions soient compatibles avec la perspective déterminée. » [Énoncé des lignes directrices de l'ACMTS]
6. Horizon temporel
- 6.1 Dans l'analyse de référence, l'horizon temporel doit être suffisamment long pour détecter toutes les différences pertinentes entre les interventions quant à leurs coûts et à leurs résultats (effets sur la santé) futurs connexes. Ainsi, l'horizon temporel doit être basé sur la maladie infectieuse et l'impact probable de l'intervention. [Énoncé des lignes directrices de l'ACMTS, modifié]
- 6.2 Les chercheurs doivent justifier leur choix d'horizon temporel. Lorsqu'il s'étend sur une longue période (c'est-à-dire sur plusieurs décennies), les chercheurs doivent estimer le RCED à partir de divers points dans le temps tout au long de l'horizon temporel.
7. Actualisation
- 7.1 Dans l'analyse de référence, actualiser les coûts et les résultats (effets) des interventions pour une période dépassant la première année afin de présenter les valeurs selon un taux de 1,5 % par an. [Énoncé des lignes directrices de l'ACMTS, modifié]
- 7.2 « Évaluer le retentissement de l'incertitude liée au taux d'escompte en comparant les résultats de l'analyse de référence à ceux d'analyses complémentaires à l'aide des taux de 0 % et de 3 % par an. » [Énoncé des lignes directrices de l'ACMTS]
8. Modélisation
- 8.1 Conceptualiser et élaborer le modèle en fonction du problème de décision [Énoncé des lignes directrices de l'ACMTS]
- 8.2 Dans la conceptualisation du modèle, prendre en considération tout modèle bien construit et validé qui incorpore adéquatement le cheminement clinique ou de soin dans la maladie infectieuse d'intérêt. [Énoncé des lignes directrices de l'ACMTS, modifié]
- 8.3 La structure du modèle doit refléter l'histoire naturelle de la maladie, le parcours clinique ou de soins, et tenir compte de la susceptibilité, de l'infectiosité, de l'immunité, de la morbidité et de la mortalité liées à l'infection.
- 8.4 Le cas échéant, il faut intégrer au modèle les dynamiques comportementales pertinentes, y compris les habitudes de contact entre les individus et les comportements liés à la prévention et au contrôle des infections.
- 8.5 Des modèles dynamiques doivent être pris en considération dans les évaluations économiques des vaccins et associés à des externalités comme la prévention de la transmission interhumaine de l'infection et le déplacement lié à l'âge de la maladie.
- 8.6 D'autres attributs du modèle, notamment le fait qu'il soit déterministe ou stochastique, basé sur les populations ou sur les individus, et ouvert ou fermé, doivent être considérés dans le contexte du problème de décision.
- 8.7 Les chercheurs doivent rendre compte de manière transparente des processus de calage et de validation du modèle qui ont été entrepris et de leurs résultats.
9. Efficacité
- 9.1 Effectuer une recherche documentaire exhaustive afin d'appuyer l'estimation de l'efficacité clinique et de l'innocuité des interventions à l'étude. Faire état des études retenues et des méthodes de sélection ou de regroupement des données. Les chercheurs doivent évaluer l'efficacité des sources utilisées en fonction de leur adéquation à l'objectif, de leur crédibilité et de leur cohérence. Décrire les compromis entre ces critères et justifier les sources sélectionnées. [Énoncé des lignes directrices de l'ACMTS, modifié]
- 9.2 Les critères suivants doivent être pris en compte lors de l'évaluation des estimations de l'efficacité des vaccins : l'efficacité du vaccin en fonction de la dose et du temps (par exemple, protection décroissante), l'efficacité spécifique à la variation de l'agent pathogène (c'est-à-dire les sérotypes, les sérogroupes, les souches), et les facteurs géographiques et liés à la personne vaccinée qui peuvent avoir une incidence sur l'efficacité.
- 9.3 Les chercheurs doivent s'assurer que les biomarqueurs immunitaires utilisés comme résultats de substitution dans les études sur l'efficacité potentielle ou réelle des vaccins répondent aux critères des corrélats de protection.
10. Mesure et évaluation de la santé
- 10.1 « Dans les deux analyses de référence, il convient d'utiliser la survie ajustée pour la qualité de vie (QALY) comme méthode pour évaluer les résultats en matière de santé.
- 10.2 Prendre en considération les préférences en matière de santé qui correspondent à celles de la population canadienne en général. » [Énoncé des lignes directrices de l'ACMTS]
- 10.3 Dans les analyses de référence, les chercheurs doivent utiliser les préférences en matière de santé qui sont obtenues par une méthode de mesure indirecte reposant sur un système de classification générique (p. ex. le questionnaire EuroQol 5-Dimensions [EQ-5D], le Health Utilities Index [HUI], le Short-Form 6-Dimensions [SF-6D], les Child Health Utility 9-Dimensions [CHU9D], l'évaluation de la qualité de vie [AQoL]). Les chercheurs doivent présenter une justification s'ils n'utilisent pas de méthode indirecte. [Énoncé des lignes directrices de l'ACMTS, modifié]
- 10.4. La sélection des sources de données à propos de la valeur d'utilité des états de santé est dictée par les motifs d'aptitude à l'emploi, de crédibilité et de cohérence. Faire état des études retenues et des méthodes de sélection ou de regroupement des données. Les chercheurs doivent évaluer les sources utilisées pour les valeurs d'utilité de l'état de santé en fonction de leur pertinence, de leur crédibilité et de leur cohérence. Décrire les compromis consentis entre ces critères et justifier les sources choisies. [Énoncé des lignes directrices de l'ACMTS, modifié]
11. Utilisation et coût des ressources
- 11.1 Pour chaque analyse de référence, les chercheurs doivent relever, mesurer et valoriser de manière systématique toutes les ressources pertinentes, consommées ou économisées à la suite de l'administration ou de l'exécution du programme de vaccination, et en faire état.
- 11.2 Dans la mesure du possible, les chercheurs doivent évaluer des ressources pertinentes relevées pour tous les secteurs, sur le plan pécuniaire. Lorsque ce n'est pas possible, les chercheurs doivent présenter aux décideurs les ressources pertinentes qui ont été relevées dans l'inventaire des effets à prendre en considération dans l'évaluation économique des stratégies de vaccination.
- 11.3 L'utilisation et les coûts des ressources doivent être basés sur des sources canadiennes et refléter la ou les administrations d'intérêts (comme il est précisé dans le problème de décision). [Énoncé des lignes directrices de l'ACMTS, modifié]
- 11.4 Dans la valorisation et la monétisation des ressources, les chercheurs doivent choisir les sources de données les plus exactes quant au coût de renonciation selon la perspective de l'analyse. [Énoncé des lignes directrices de l'ACMTS, modifié]
- 11.5 Les chercheurs doivent mener une recherche exhaustive des sources de données disponibles pour informer l'utilisation des ressources et la valeur des coûts. Faire état des études retenues et des méthodes de sélection ou de regroupement des données. Les chercheurs doivent évaluer les sources utilisées pour les coûts des ressources en fonction de leur aptitude à l'emploi, de leur crédibilité et de leur cohérence. Décrire les compromis consentis entre ces critères et justifier les sources choisies.
12. Analyse
- 12.1 Les rapports coûts-efficacité différentiels (RCED) et, lorsque cela est utile pour l'interprétation, les avantages financiers nets ou les avantages nets pour la santé, doivent être calculés pour les deux analyses de référence.
- 12.2 « Si l'analyse englobe plus de deux interventions, effectuer une analyse séquentielle du rapport coût-efficacité dans les règles standards de l'estimation du RCED, y compris l'exclusion des interventions dominées. » [Énoncé des lignes directrices de l'ACMTS]
- 12.3 Autant que possible, il faut générer les valeurs attendues des coûts et des résultats de manière probabiliste afin de refléter l'incertitude globale des paramètres du modèle.
13. Incertitude
- 13.1 Les chercheurs doivent aborder l'incertitude des paramètres en recourant à une analyse probabiliste de référence, si possible, ainsi qu'à des analyses de sensibilité déterministes.
- 13.2 « Étudier l'incertitude méthodologique en comparant les résultats de l'analyse de référence à ceux d'une analyse complémentaire fondée sur d'autres choix méthodologiques que ceux recommandés pour examiner l'incidence des différences d'ordre méthodologique. » [Énoncé des lignes directrices de l'ACMTS]
- 13.3 « Il convient d'utiliser les courbes d'acceptabilité du rapport coût-efficacité (CARCE) et les frontières d'efficience (FE) pour représenter l'incertitude des estimations des coûts et des résultats lorsque celles-ci ont été générées de manière probabiliste. » [Énoncé des lignes directrices de l'ACMTS, modifié]
- 13.4 « Lorsque le problème de décision comprend l'option de commander ou d'effectuer un projet de recherche, l'analyse de la valeur de l'information peut être utile dans l'attribution d'une valeur à ces options et dans la conception du projet de recherche; cette analyse doit alors être comprise dans l'analyse de référence. » [Énoncé des lignes directrices de l'ACMTS, modifié]
- 13.5. Évaluer l'incertitude structurelle par des analyses de scénarios. [Énoncé des lignes directrices de l'ACMTS, modifié]
14. Équité
- 14.1 Les chercheurs et les décideurs doivent travailler ensemble pour déterminer les dimensions et les objectifs d'équité à inclure dans l'évaluation économique du programme de vaccination envisagé. L'équité doit être considérée dans le contexte du cadre d'éthique, d'équité, de faisabilité et d'acceptabilité (ÉÉFA) du CCNI.
- 14.2 Les analyses qui intègrent les préoccupations pertinentes en matière d'équité doivent accompagner l'analyse de référence (par exemple, l'analyse coût-efficacité distributive, l'analyse coût-efficacité étendue ou d'autres méthodes émergentes) et être présentées avec les analyses de référence.
15. Production de rapports
- 15.1 « Présenter les résultats de l'évaluation économique de façon détaillée et transparente. Fournir suffisamment de renseignements pour que le lecteur ou l'utilisateur (le décideur, par exemple) puisse faire une analyse critique de l'évaluation. » [Énoncé des lignes directrices de l'ACMTS, modifié]
- 15.2 Prévoir un sommaire de l'évaluation dans un langage non technique. [Énoncé des lignes directrices de l'ACMTS]
- 15.3 « Présenter les résultats de l'évaluation économique à l'aide d'éléments graphiques ou visuels en plus de tableaux. » [Énoncé des lignes directrices de l'ACMTS]
- 15.4 « Inclure des renseignements ou des documents sur les processus d'assurance de la qualité et les résultats de l'évaluation économique dans le compte rendu. Fournir une copie du modèle par voie électronique aux fins d'examen ainsi que de la documentation connexe afin de faciliter la compréhension du modèle, de son déroulement et de son fonctionnement. » [Énoncé des lignes directrices de l'ACMTS]
- 15.5 « Préciser les sources de financement et les liens hiérarchiques dans le cadre de l'évaluation et mentionner tout conflit d'intérêts éventuel. » [Énoncé des lignes directrices de l'ACMTS]
- 15.6 Les chercheurs doivent utiliser les lignes directrices pour la présentation des évaluations économiques des programmes de vaccination au Canada du CCNI et remplir l'inventaire des effets à prendre en considération dans l'évaluation économique des stratégies de vaccination, qui se trouve à l'annexe 1.
Les lignes directrices en détail
1. Problème de décision
Énoncés des Lignes directrices
- 1.1 « Énoncer clairement le problème de décision devant faire l'objet de l'évaluation économique. » [Énoncé des lignes directrices de l'ACMTS]
- 1.2 Dans l'énoncé du problème de décision, préciser les interventions à mettre en œuvre, le cadre ou le contexte de la comparaison, la perspective de l'évaluation, la nature des coûts et des résultats ou des paramètres pris en considération (incluant les externalités), l'horizon temporel et la population cible de l'évaluation (incluant les populations directement ou indirectement ciblées par le programme de vaccination). [Énoncé des lignes directrices de l'ACMTS, modifié]
Le problème de décision visé par l'évaluation économique d'un programme de vaccination doit répondre aux préoccupations des décideurs et être clairement formulé dès le début de l'analyse. Le fait de suivre une approche normalisée peut garantir, dans la mesure du possible, la cohérence avec d'autres évaluations économiques de vaccins.
Au Canada, divers décideurs évaluent les évaluations économiques des programmes de vaccination. Au niveau fédéral, il s'agit du CCNI; à l'ordre provincial et territorial, il s'agit des ministères de la Santé et, selon l'administration, des groupes consultatifs techniques provinciaux sur l'immunisation. Le CCNI fournit des conseils non contraignants aux gouvernements provinciaux et territoriaux qui, à leur tour, prennent les décisions sur la mise en œuvre. Ces décisions portent notamment sur le financement public d'un nouveau programme de vaccination, sur la manière de déployer les programmes, et sur la manière de renforcer et de surveiller les programmes existants.
Le problème de décision doit fournir une description détaillée et une justification du programme de vaccination évalué, y compris : 1) les interventions à comparer; 2) les contextes dans lesquels elles doivent être comparées; 3) le type d'évaluation réalisée; 4) les perspectives à partir desquelles l'analyse est effectuée; 5) les coûts et les résultats à quantifier dans l'analyse; 6) l'horizon temporel sur lequel l'analyse doit être effectuée; 7) et les populations pour l'évaluation.
Il convient de fournir une description claire du vaccin évalué, y compris le dosage du vaccin, le nombre de doses requises, le calendrier des doses, la nécessité ou non de doses de rappel, l'administration prévue des doses, le traitement des pertes de vaccin, les hypothèses sur le déclin, les estimations de couverture et le lieu d'administration du vaccin, ainsi que des descriptions détaillées des comparateurs. Les comparateurs peuvent inclure d'autres vaccins préventifs existants, des approches préventives non vaccinales et les approches thérapeutiques actuelles, y compris les meilleurs soins de soutien.
Il convient de préciser et de justifier le type d'évaluation économique. Le type d'évaluation économique, ainsi que la perspective, détermineront quels coûts et résultats doivent être inclus (et comment). Les mesures de résultats incluses, qui doivent être les mêmes pour chaque comparateur, doivent être explicitement mentionnées dans le problème de décision et énumérées par domaine touché (par exemple, résultats en matière de santé, réussite scolaire). De même, les coûts inclus doivent être explicitement indiqués et répertoriés par domaine touché (par exemple, coûts des soins de santé, coûts liés à l'éducation, coûts liés à la productivité).
Les chercheurs doivent s'efforcer de s'entretenir avec un certain nombre de décideurs concernés et se mobiliser auprès d'eux afin de comprendre les préoccupations auxquelles ces derniers tentent de répondre en mettant en place le programme de vaccination. Certains aspects du problème de décision sont particulièrement pertinents pour les décideurs, notamment : 1) populations dans l'évaluation; 2) le contexte de l'administration du vaccin; 3) l'horizon temporel de l'évaluation; 4) les effets possibles du programme de vaccination au-delà du secteur de la santé; 5) les inégalités en matière de santé qui pourraient éventuellement être atténuées par l'introduction du programme de vaccination.
Les chercheurs, en collaboration avec les décideurs, doivent déterminer les populations à inclure dans l'évaluation. La population étudiée peut être l'ensemble de la population pour laquelle le vaccin est indiqué, un sous-ensemble de la population indiquée, ou une population différente pour l'utilisation non indiquée du vaccin, selon les besoins des décideurs. La population étudiée ne doit pas être limitée aux personnes pour lesquels le programme de vaccination est destiné. Le cas échéant, il convient d'inclure les personnes à risque pour la maladie en question et celles qui subissent des externalités et des retombées (par exemple, les aidants naturels). Lorsqu'il existe des hétérogénéités entre les groupes d'individus susceptibles d'affecter les résultats d'une évaluation économique (par exemple, les groupes d'âge, les groupes à risque clinique, la situation géographique), les chercheurs doivent identifier les sous-groupes et déterminer les différentes stratégies de vaccination susceptibles d'améliorer la couverture dans chacun des sous-groupes. Toutes les options présentant un intérêt pour le décideur doivent être évaluées ensemble en utilisant les principes de l'analyse différentielle complète. Le cas échéant, les analyses stratifiées et les rapports stratifiés doivent accompagner l'analyse complète.
Les chercheurs doivent s'assurer que les milieux d'administration du vaccin qui intéressent les décideurs sont pris en compte dans l'évaluation économique. Il s'agit par exemple de cliniques médicales, de pharmacies, d'écoles, de cliniques de santé publique et de lieux de travail. Le choix du cadre par les décideurs peut varier en fonction de la maladie et des facteurs liés au vaccin. En outre, ils peuvent choisir de mettre en œuvre le programme de vaccination dans plusieurs endroits.
Il est particulièrement important de s'assurer que l'horizon temporel est pertinent pour les décideurs lorsqu'un programme de vaccination permet de protéger les personnes non vaccinées grâce à l'immunité collective (de groupe), avec un potentiel d'élimination de la maladie. Il faut souvent un horizon temporel très long (parfois plusieurs décennies) pour que tous les coûts et les effets d'un programme de vaccination deviennent apparents. Dans ces cas, les chercheurs doivent s'assurer que les résultats d'une évaluation économique font l'objet de rapports selon plusieurs points dans le temps pour permettre aux décideurs de déterminer quand les gains du programme deviennent positifs.
Compte tenu des résultats plus généraux, non liés à la santé, qui sont associés à de nombreuses stratégies de vaccination, une perspective plus large que celle du système de santé sera généralement pertinente. Dans les présentes lignes directrices, le système de santé désigne à la fois les services de traitement des soins de santé et la santé publique. Les chercheurs doivent essayer de comprendre les coûts et les avantages plus vastes du programme de vaccination, qui ne concernent pas nécessairement le secteur de la santé, mais qui sont utiles au décideur. Par exemple, la prévention de la rougeole, une maladie qui peut entraîner des lésions neurologiques, par la vaccination des enfants, améliore les résultats scolaires. De même, la prévention de la grippe au sein de la population grâce à un programme de vaccination universelle procure des avantages liés à la productivité. Le chapitre 5, Perspectives, donne davantage de détails sur ce sujet.
Certains groupes sont vulnérables face aux maladies infectieuses et aux effets négatifs des politiques de contrôle des maladies infectieuses en raison de préjudices historiques et d'obstacles sociaux. Les vaccins ont été relevés comme étant une stratégie permettant de réduire potentiellement des inégalités spécifiques liées au risque d'infection ou au fardeau de la maladie en question. Les chercheurs, en collaboration avec les décideurs, doivent identifier les groupes précis qui pourraient particulièrement bénéficier du programme de vaccination. Par exemple, l'incidence du cancer du col de l'utérus et la mortalité liée à cette maladie sont plus élevées chez les personnes affichant un statut socio-économique inférieur et les membres de minorités. Ces résultats pourraient être évités grâce à un programme de vaccination contre le papillome humain (VPH).Note de bas de page 10 À l'inverse, les chercheurs et les décideurs doivent également se demander si le programme de vaccination peut ne pas profiter à certains groupes. Le chapitre 14, Équité, propose une discussion plus approfondie à ce sujet.
2. Types d'évaluations
Énoncés des Lignes directrices
- 2.1 L'analyse de référence dans l'évaluation économique est une analyse coût-utilité (ACU), dans laquelle les résultats sont exprimés en années de vie gagnées ajustées en fonction de la qualité (AVAQ). Justifier clairement tout autre choix. [Énoncé des lignes directrices de l'ACMTS, modifié]
- 2.2 Il est possible de recourir à une analyse coûts-avantages (ACA) en plus des ACU de référence lorsque le programme de vaccination peut être comparé à une intervention autre que de santé.
L'analyse de référence dans l'évaluation économique est une analyse coût-utilité (ACU), dans laquelle les résultats sont exprimés en années de vie gagnées ajustées en fonction de la qualité (AVAQ). Il est toutefois reconnu qu'il existe des populations au sein desquelles les ACU ne peuvent pas être menées de manière robuste parce qu'il n'existe pas d'instruments valides pour l'élicitation directe de l'utilité, comme chez les enfants de moins de 8 ans. Dans ces cas, des approches analytiques de rechange comme l'analyse coût-efficacité (ACE), avec une mesure de résultat pertinente en unités de santé naturelles, doivent être justifiées.
Outre les ACU de l'analyse de référence, une analyse coûts-avantages (ACA) peut être présentée dans les cas où des répercussions au-delà du secteur de la santé sont des facteurs importants pour les décideurs. L'ACA a été proposée comme méthode d'évaluation des programmes de vaccination associés à des conséquences qui ne relèvent pas du secteur de la santé.Note de bas de page 11Note de bas de page 12Note de bas de page 13 La recommandation du CCNI de réaliser une analyse coûts-utilité de référence dans la perspective sociétale devrait permettre aux chercheurs de tenir compte des avantages non liés au secteur de la santé en les monnayant et en les incluant dans le numérateur de l'estimation du rapport coût-efficacité différentiel (RCED). Cependant, cette approche ne permet pas aux décideurs de comparer les avantages non liés à la santé d'autres programmes ou de comparer des programmes de vaccination à des programmes autres que de santé puisque le dénominateur de l'estimation du rapport coût-efficacité différentiel est exprimé en années de vie ajustées par la qualité. Lorsqu'un décideur souhaite comparer l'attrait économique d'un programme de vaccination à une intervention non sanitaire (comme un programme de repas scolaires), les chercheurs pourraient présenter une analyse coûts-avantages parallèlement à l'analyse de référence menée dans la perspective sociétale afin de permettre une telle comparaison.Note de bas de page 11 Les chercheurs doivent être conscients du fait que différentes approches peuvent servir à monnayer les effets dans une analyse coûts-avantages et que cela peut donner de grandes variations dans les résultats d'une telle analyse.Note de bas de page 12 Par exemple, les chercheurs peuvent envisager l'approche du capital humain, l'approche du coût de friction, la valeur d'une vie statistique en utilisant les préférences révélées ou déclarées, ou la monétisation des AVAQ en utilisant un seuil de rentabilité. Le choix d'une approche particulière doit être précisé et justifié. Bien que ces Lignes directrices ne prescrivent pas d'approche particulière, les chercheurs peuvent souhaiter consulter les Reference Case Guidelines for Benefit-Cost Analysis in Global Health and DevelopmentNote de bas de page 14 ou d'autres lignes directrices en matière d'ACA en dehors du secteur de la santé.Note de bas de page 15Note de bas de page 16Note de bas de page 17
3. Populations étudiées
Énoncés des Lignes directrices
- 3.1 Les chercheurs doivent identifier les populations visées par le programme de vaccination, les populations à risque pour la maladie en question, et toutes les populations qui peuvent être indirectement affectées par le programme de vaccination, soit par des externalités, soit par des retombées.
- 3.2 Les chercheurs doivent présenter une analyse globale qui inclut les coûts et les résultats pour toutes les populations concernées. Le cas échéant, les chercheurs doivent également résumer les résultats séparément pour chaque groupe affecté (par exemple, la population visée, la population subissant des externalités ou des retombées) qui a été inclus dans l'analyse globale.
- 3.3 Lorsqu'il existe des facteurs susceptibles d'entraîner des différences de coûts et de résultats liés au programme de vaccination entre les sous-groupes, les chercheurs doivent réaliser des évaluations économiques distinctes pour chaque sous-groupe. Ces facteurs peuvent inclure des facteurs démographiques, des facteurs comportementaux, des facteurs liés à la maladie et l'efficacité du vaccin ou des interventions de comparaison.
Les résultats de toute évaluation économique d'un programme de vaccination dépendent de l'incidence du programme de vaccination sur trois populations : 1) les populations visées par le programme de vaccination; 2) les populations vulnérables face à la maladie en question; et 3) les populations qui peuvent subir des externalités ou des retombées. Le problème de décision doit inclure, au minimum, la première population étudiée et, le cas échéant, deux dernières populations. Les chercheurs doivent relever toutes les externalités associées aux programmes de vaccination (par exemple, l'immunité collective, le déplacement lié à l'âge de la maladie), et les populations qu'elles sont censées toucher. Par exemple, on peut s'attendre à ce qu'un programme de vaccination contre la rougeole destiné aux nourrissons et aux enfants entraîne une immunité collective susceptible d'éliminer la maladie à l'échelle de la population. Un autre exemple est le vaccin préventif contre la varicelle destiné aux jeunes enfants, qui pourrait accroître l'incidence du zona dans la population générale. De plus amples détails sur l'incorporation des externalités dans les évaluations économiques sont fournis au chapitre 8, Modélisation. En outre, les chercheurs doivent identifier les populations au sein desquelles le programme de vaccination pourrait avoir des retombées (p. ex. les aidants naturels).
Ils doivent fournir une description détaillée de chaque population prise en considération dans l'analyse, y compris l'âge, le sexe et l'emplacement géographique. Les chercheurs doivent également décrire tous les autres facteurs qui déterminent l'admissibilité au programme de vaccination évalué, ainsi que les facteurs susceptibles de toucher l'ampleur des externalités ressenties.
Les chercheurs doivent présenter une analyse globale qui inclut les coûts et les résultats pour toutes les populations concernées, y compris les groupes identifiés pour le programme de vaccination et tous les groupes qui pourraient subir des externalités ou des retombées. Cette analyse doit être présentée pour chaque stratégie de mise en œuvre envisagée (par exemple, vaccination universelle, vaccination des groupes à haut risque uniquement, vaccination des enfants uniquement). Le cas échéant, les chercheurs doivent également résumer les résultats séparément pour chaque groupe affecté (par exemple, la population visée, la population subissant des externalités ou des retombées) qui a été inclus dans l'analyse globale.
Cependant, dans les situations où des hétérogénéités susceptibles d'influer sur les résultats d'une évaluation économique ont été relevées entre des groupes d'individus, il convient d'envisager différentes stratégies qui améliorent la couverture au sein de chacun des sous-groupes et présenter des résultats stratifiés par sous-groupe. Les chercheurs doivent effectuer des analyses stratifiées et présenter des résultats par sous-groupes. Dans l'idéal, cela devrait reposer sur un modèle mathématique sous-jacent qui prenne en considération tous les sous-groupes et leurs interactions. Les hétérogénéités importantes concernant les programmes de vaccination peuvent être des facteurs démographiques (p. ex. l'âge, le genre, l'ethnicité, la profession, les groupes cliniques à risque, la fragilisation, les biomarqueurs, les profils génétiques, la situation géographique, la vie dans une habitation collective), des facteurs comportementaux (p. ex. l'adoption prévue du programme de vaccination, les comportements liés à la prise de risque), des facteurs liés à la maladie (p. ex. l'histoire naturelle de la maladie, le risque de transmission de la maladie), l'efficacité réelle du vaccin ou des interventions de comparaison ainsi que l'utilité pour la santé ou les coûts associés aux états pathologiques ou aux interventions inclus dans l'analyse. Certains de ces facteurs sont liés à l'équité. Certains sous-groupes supportent un fardeau de la maladie disproportionné ou un impact négatif des politiques de lutte contre les maladies infectieuses pour diverses raisons historiques, sociales et politiques. Le chapitre 14, Équité, propose une discussion plus approfondie à ce sujet.
4. Comparateurs
Énoncés des Lignes directrices
- 4.1 Choisir les comparateurs en fonction de la portée du problème de décision. Les comparateurs choisis doivent être adaptés à la population visée par le programme de vaccination et à la région où la décision s'appliquera. [Énoncé des lignes directrices de l'ACMTS, modifié]
- 4.2 Les chercheurs doivent prendre en compte les approches préventives et thérapeutiques lors de la sélection des comparateurs pour les évaluations économiques des programmes de vaccination. Les interventions préventives peuvent inclure des mesures basées sur des vaccins, des programmes de dépistage, des interventions préventives fondées sur des médicaments et des interventions préventives non médicales.
Lorsqu'ils choisissent les comparateurs pour les évaluations économiques des programmes de vaccination, les chercheurs doivent prendre en considération : 1) toutes les interventions actuelles, 2) celles qui pourraient devenir disponibles dans un avenir proche et 3) celles qui pourraient être déplacées en raison du programme de vaccination évalué. Les interventions utilisées à la fois pour la prévention et le traitement de la maladie en question doivent être prises en considération. Les interventions préventives peuvent inclure des mesures basées sur des vaccins, des programmes de dépistage, des interventions préventives fondées sur des médicaments et des interventions préventives non médicales. Souvent, plus d'un comparateur sera pertinent pour l'évaluation économique et, par conséquent, tous les comparateurs pertinents doivent être inclus. Les mesures des résultats inclus doivent être les mêmes pour chaque comparateur.
Les mesures fondées sur les vaccins pourraient inclure d'autres vaccins contre le même agent pathogène (par exemple, vaccin inactivé trivalent parentéral contre vaccin vivant atténué intranasal antigrippal, vaccins à cellules entières contre vaccins acellulaires contre la coqueluche, vaccins à ARNm contre vaccins à vecteur viral pour l'infection au coronavirus 2019 [COVID-19]). Elles peuvent inclure des vaccins avec des valences supplémentaires (par exemple, vaccins conjugués antipneumococciques 10-, 13-, 15- ou 20-valents). Les mesures fondées sur les vaccins pourraient également inclure une mise en œuvre ou une livraison différente avec le même produit vaccinal. Parmi les exemples figurent la vaccination universelle contre la vaccination des groupes à haut risque uniquement; la vaccination du groupe d'âge prévu sans stratégie de rattrapage contre la vaccination du groupe d'âge prévu avec une stratégie de rattrapage pour d'autres groupes d'âge; la stratégie de vaccination sans doses de rappel contre la stratégie avec doses de rappel; les stratégies de vaccination reposant sur un nombre de doses différent ou des calendriers d'administration différents; des milieux d'administration différents, comme une stratégie de vaccination dans les écoles, une stratégie de vaccination dans un centre de santé publique ou une stratégie de vaccination de masse.Note de bas de page 18Note de bas de page 19Note de bas de page 20Note de bas de page 21 Les mesures fondées sur les vaccins peuvent être affectées par la promotion de la santé, les campagnes de renseignements et d'autres efforts concomitants visant à instaurer la confiance de la communauté.
Les programmes de dépistage (également connus sous le nom de prévention secondaire) pourraient inclure des examens et des tests réguliers permettant de détecter la maladie à son stade le plus précoce. Ceux-ci pourraient être modifiés en raison de l'introduction des programmes de vaccination. Par exemple, la vaccination contre le VPH peut modifier la valeur et la nécessité des frottis cytologiques de routine pour le dépistage du cancer du col de l'utérus.
Les interventions préventives médicamenteuses peuvent nécessiter l'administration de médicaments avant ou après l'exposition. Il s'agit, par exemple, des médicaments antipaludéens destinés aux voyageurs canadiens se rendant dans des régions où le paludisme est endémique, et de la prophylaxie pré et post-exposition au virus de l'immunodéficience humaine (VIH).
Les interventions préventives non médicales pourraient inclure des mesures physiques comme les préservatifs pour prévenir les infections transmissibles sexuellement, les masques faciaux pour prévenir la transmission des infections respiratoires ou des modifications comportementales comme le respect de la distanciation physique et le lavage des mains pour prévenir les infections qui se transmettent par des contacts personnels étroits entre individus.
Lorsque des comparateurs fondés sur le traitement sont envisagés, les chercheurs doivent savoir que les soins de soutien optimaux doivent être considérés comme étant le comparateur pertinent dans les cas où il n'existe aucun traitement curatif pour la maladie en question.
Dans certains cas, l'objectif de ces interventions peut être différent et les données comparatives d'efficacité peuvent être limitées ou les critères d'évaluation utilisés dans les études cliniques différents. Les chercheurs doivent évaluer les sources en fonction de leur adéquation à l'objectif, de leur crédibilité et de leur cohérence, décrire les compromis entre ces critères et justifier la sélection des sources. Ce point est examiné plus en détail au chapitre 9, Efficacité, au chapitre 10, Mesure et l'évaluation de la santé, et au chapitre 11, Utilisation et coût des ressources.
5. Perspectives
Énoncés des Lignes directrices
- 5.1 Il faut présenter deux analyses de cas de référence dans le cadre de l'évaluation économique des programmes de vaccination : l'une menée dans la perspective du système de santé financé par l'État, et l'autre dans la perspective sociétale.
- 5.2 « Veiller à ce que les coûts comme les résultats ou effets des interventions soient compatibles avec la perspective déterminée. » [Énoncé des lignes directrices de l'ACMTS]
Il faut réaliser deux analyses de référence dans le cadre de l'évaluation économique des programmes de vaccination : l'une menée dans la perspective du système de santé financé par l'État et l'autre dans la perspective sociétale. Dans les présentes lignes directrices, le système de santé désigne à la fois les services de traitement des soins de santé et la santé publique. La Santé publique est stylisée en lettres majuscules pour mieux la distinguer des « soins de santé publics ». La Santé publique désigne « les efforts organisés de la société pour maintenir les personnes en santé et éviter les blessures, les maladies et les décès prématurés ».Note de bas de page 22 Il s'agit d'une combinaison de programmes, de services et de politiques qui protègent et favorisent la santé de la population (par opposition à la gestion clinique de patients individuels). Les soins de santé publics sont financés par l'État.
Perspective du système de santé financé à même les fonds publics
Le champ d'application de la perspective doit être défini de manière à inclure un seul système de santé provincial ou territorial à financement public, plusieurs systèmes de santé régionaux à financement public ou un système national. Les chercheurs doivent inclure : 1) les résultats en matière de santé expérimentés par les personnes vaccinées et leurs soignants informels; 2) les coûts encourus par le système de santé. Il faut reconnaître que, lorsque l'analyse de référence concerne plusieurs systèmes de santé financés par l'État, les éléments de coût financés par l'État peuvent varier d'une administration à l'autre (p. ex. les médicaments sur ordonnance), voire au sein d'une même administration (soins de longue durée). Les variations dans les éléments inclus entre les systèmes doivent être rendues transparentes.
Dans les cas où les vaccins sont associés à des externalités, les coûts et les résultats en matière de santé pris en considération dans l'analyse doivent inclure également les coûts et les résultats pour les personnes non vaccinées, car le vaccin joue un rôle essentiel dans la santé de la population.Note de bas de page 23 Les résultats en matière de santé à l'échelle de la population qui doivent être pris en considération sont les suivants : 1) l'incidence de l'infection et de la maladie chez les personnes vaccinées et non vaccinées (incluant l'élimination et l'éradication de la maladie); 2) les changements dans la répartition par âge des personnes infectées à la suite du déplacement lié à l'âge du programme de vaccination (lorsque cela a des conséquences sur le fardeau global de la maladie en raison de la dépendance à l'âge de la gravité de la maladie; 3) l'émergence de nouvelles maladies liées à des variations de l'agent pathogène (c.-à-d. sérotypes, sérogroupes, souches) ou à des agents pathogènes non apparentés qui peuvent remplacer ceux visés par le vaccin.
Les coûts du système de santé qui doivent être pris en considération selon cette perspective sont les suivants : 1) les services de soins de santé financés par l'État (p. ex., visites chez le médecin, hospitalisation); 2) les coûts futurs des soins de santé connexes et non connexes; 3) les coûts liés aux programmes financés par la Santé publique (p. ex., administration des vaccins, enquête et gestion des éclosions); et 4) les coûts liés aux interventions financés par la Santé publique (p. ex., doses de vaccin, administration). Le chapitre 11, Utilisation et coût des ressources, donne des conseils sur la quantification des coûts associés à ces résultats.
Perspective sociétale
Il est également recommandé de procéder à une analyse de référence supplémentaire dans une perspective sociétale, car bon nombre de vaccins préviennent des maladies qui ont des répercussions au-delà du secteur de la santé. Par exemple, le vaccin contre l'Haemophilus influenzae type b (Hib) administré aux nourrissons prévient les séquelles neurologiques (par exemple, la surdité, la cécité, les retards de développement), qui ont toutes une incidence sur la fréquentation scolaire de l'enfant, sa productivité et sa consommation futures, ainsi que sur son bien-être global.Note de bas de page 24Note de bas de page 25 Même des maladies relativement bénignes, comme la diarrhée infantile résultant d'une infection à rotavirus, peuvent avoir des répercussions au-delà du secteur de la santé. Dans bon nombre de cas, des soins médicaux ne sont pas nécessaires pour traiter ces infections; néanmoins, un parent doit s'absenter de son travail pour s'occuper de l'enfant malade.Note de bas de page 26Note de bas de page 27 Enfin, les maladies comme la COVID-19 ont des conséquences sanitaires et économiques considérables qui s'étendent à tous les domaines de l'économieNote de bas de page 28, et ces effets pourraient être atténués par des programmes de vaccination.Note de bas de page 29Note de bas de page 30 Ne pas prendre en considération l'ensemble des avantages associés aux vaccins revient à sous-estimer le rôle de la santé comme moteur de l'activité économique et du bien-être et pourrait conduire à une sous-évaluation des programmes de vaccination.Note de bas de page 23 Certains diront qu'un programme de vaccination peut être surévalué lorsqu'on compare un cas de référence mené du point de vue de la société à un cas de référence d'une technologie de santé non vaccinale, qui est normalement mené du point de vue du système de santé (selon la 4e édition actuelle des lignes directrices de l'ACMTS). Les présentes lignes directrices recommandent donc deux analyses de cas de référence utilisant les deux perspectives. La perspective du système de santé peut permettre la comparaison avec d'autres technologies de santé pour lesquelles il n'existe que des évaluations du point de vue des systèmes de santé, et la perspective sociétale peut mieux saisir les effets plus larges des programmes de vaccination.
La perspective sociétale englobe tous les résultats de santé et les coûts du système de santé du point de vue du système de santé. En outre, elle saisit les effets qui ne relèvent pas du système de santé publique, notamment les coûts des soins de santé non financés par le système de santé, les coûts directs pour les patients, les pertes de productivité, de consommation, d'éducation, de services sociaux et communautaires et l'environnement. Les effets à plus long terme, tels que l'effet des maladies infantiles sur les troubles du développement neurologique d'une personne, ses résultats scolaires et sa productivité (et sa consommation) à long terme, doivent être pris en compte lorsque cela est pertinent et possible. Les effets ci-dessus sont énumérés avec des exemples dans l'annexe I, Tableau 1 : Tableau d'inventaire des effets à prendre en considération dans l'évaluation économique des stratégies de vaccination. Le tableau a été adapté à partir de l'inventaire des effets publié par le 2e groupe d'experts sur le rapport coût-efficacitéNote de bas de page 31 afin d'inclure des effets plus larges qui n'avaient pas été prises en compte auparavant. Bon nombre de ces effets concernent les technologies de la santé en général, et certains sont spécifiques aux vaccins ou aux maladies infectieuses (par exemple, le déplacement de l'âge des maladies, l'éradication des maladies).Note de bas de page 8Note de bas de page 23Note de bas de page 31Note de bas de page 32Note de bas de page 33 Il convient de noter que des cadres de valeurs spécifiques aux vaccins ont été récemment publiés, soulignant les vastes effets des programmes de vaccination sur la société.Note de bas de page 34Note de bas de page 35Note de bas de page 36 Le tableau d'effets fournit une liste des effets sanitaires et non sanitaires qui pourraient résulter des programmes de vaccination. L'intention est de permettre aux chercheurs de prendre en considération de manières systématiques les effets lorsqu'ils planifient et réalisent des évaluations économiques des programmes de vaccination. Des conseils précis sur la quantification de ces effets et de leurs coûts connexes se trouvent au chapitre 11, Utilisation et coût des ressources.
Les chercheurs doivent remplir et présenter le tableau 1 dans le cadre de leur analyse afin d'indiquer de manière explicite quels effets sont inclus et exclus de l'évaluation économique pour chacune des deux analyses de référence. La colonne des commentaires peut être utilisée pour justifier l'inclusion ou l'exclusion de certains effets ou pour fournir des renseignements supplémentaires.
6. Horizon temporel
Énoncés des Lignes directrices
- 6.1 Dans l'analyse de référence, l'horizon temporel doit être suffisamment long pour détecter toutes les différences pertinentes entre les interventions quant à leurs coûts et à leurs résultats (effets sur la santé) futurs connexes. Ainsi, l'horizon temporel doit être basé sur la maladie infectieuse et l'impact probable de l'intervention. [Énoncé des lignes directrices de l'ACMTS, modifié]
- 6.2 Les chercheurs doivent justifier leur choix d'horizon temporel. Lorsqu'il s'étend sur une longue période (c'est-à-dire sur plusieurs décennies), les chercheurs doivent estimer le RCED à partir de divers points dans le temps tout au long de l'horizon temporel.
Les modèles utilisés pour estimer la rentabilité des programmes de vaccination peuvent être des modèles fermés ou ouverts. Les modèles fermés suivent une cohorte d'individus sur une période et ne permettent pas l'entrée de nouveaux individus dans le modèle. La plupart des modèles de Markov (transition entre des états de santé) sont des modèles fermés. Les modèles fermés sont généralement statiques, ce qui signifie qu'ils ne tiennent pas compte de la dynamique de transmission de la maladie entre les individus. Les modèles ouverts, en revanche, permettent l'entrée de nouveaux individus (par exemple, par le biais de nouvelles naissances, de l'immigration) dans le modèle au fil du temps, en particulier pour tenir compte de la dynamique de transmission de la maladie dans une population au fil du temps.Note de bas de page 37
Étant donné que les modèles fermés de programmes de vaccination suivent une seule groupe d'individus, ils doivent la suivre sur un horizon temporel suffisamment long pour saisir toutes les différences importantes dans les coûts et résultats futurs liés aux stratégies de vaccination comparées. Par exemple, une méningite B contractée pendant la petite enfance peut avoir des conséquences durables à l'âge adulte.
Les modèles ouverts peuvent avoir des horizons temporels qui s'étendent au-delà de la vie d'un individu vivant au début de la simulation. Cela est particulièrement vrai pour les vaccins qui assurent une protection au niveau de la population grâce à une immunité collective sur plusieurs générations. Par exemple, une cohorte d'individus vaccinés contre la rougeole aujourd'hui peut empêcher la transmission de cette infection à une autre génération des années plus tard. Les personnes qui ne sont pas vaccinées bénéficieraient de cette protection pour le reste de leur vie, et ne contamineraient pas les futures générations de rougeole qui en bénéficieraient également pour le reste de leur vie.Note de bas de page 38Note de bas de page 39 Dans les cas où les générations futures sont impliquées, il peut y avoir des considérations d'équité intergénérationnelle à prendre en compte dans l'évaluation économique. L'équité intergénérationnelle concerne les conséquences des décisions prises aujourd'hui pour les personnes qui ne sont pas encore nées. Vous trouverez de plus amples informations au chapitre 14, Équité.
Les modèles ouverts comportent généralement trois phases : 1) la phase de rodage, 2) la phase d'évaluation et 3) la phase de stabilité. La phase de rodage doit tenir compte des caractéristiques épidémiologiques de la maladie avant l'introduction du vaccin afin de prévoir de façon réaliste et précise l'adoption du vaccin. Les estimations épidémiologiques utilisées pendant la phase de rodage doivent être validées à partir des données historiques sur la maladie en question. Le chapitre 8, consacré à la modélisation, donne plus de précisions sur la validation. La phase d'évaluation commence lorsque le programme de vaccination est mis en œuvre dans la population visée et doit être suffisamment longue pour tenir compte des externalités associées au vaccin. La phase de stabilité commence lorsque la variation épidémiologique prend fin.Note de bas de page 40
Pour l'exemple de la rougeole ci-dessus, et pour des vaccins similaires, l'horizon temporel du modèle doit se poursuivre jusqu'à ce que les RCED non actualisés atteignent un état stable. C'est le moment où le rapport entre les coûts incrémentaux cumulatifs et les résultats de santé incrémentaux cumulatifs (AVAQ) entre les interventions comparées se stabilisent. Lorsque les estimations du RCED ne sont pas appropriées pour être calculées, comme dans le cas de la dominance, la stabilité des coûts incrémentaux et des résultats incrémentaux doit être vérifiée. Dans ces cas, il faut déterminer la durée appropriée de l'horizon temporel du modèle pendant l'analyse, plutôt qu'avant.Note de bas de page 13
La stabilité des estimations supplémentaires et du rapport coût-efficacité différentiel non actualisé en tant que critère devrait signifier que l'horizon temporel du modèle sera suffisamment long pour refléter l'ensemble des coûts et des avantages de l'immunité collective, ainsi que toutes les autres externalités (comme le déplacement de l'âge pour la maladie) associées à un programme de vaccination. Les chercheurs doivent noter que les modèles peuvent atteindre l'état de stabilité épidémiologique avant que les estimations supplémentaires et du rapport coût-efficacité différentiel se soient stabilisées. Par exemple, un programme peut continuer à accumuler des coûts ou des AVAQ par rapport à l'autre même après que l'équilibre épidémiologique a été atteint. Dans ces cas, l'horizon temporel du modèle doit être maintenu jusqu'à ce que l'estimation du rapport coût-efficacité différentiel se soit stabilisée. Pour certains programmes de vaccination, il peut être nécessaire de modéliser un très grand nombre de générations pour obtenir des estimations stables du rapport coût-efficacité différentiel. [39] Si le modèle n'est pas exécuté jusqu'à ce que les estimations différentielles et le rapport coût-efficacité se soient stabilisés, les chercheurs doivent en justifier la raison, et définir la durée d'exécution en matière d'horizon temporel ou de nombre de cohortes, et fournir une justification de ce choix.Note de bas de page 41
En justifiant l'horizon temporel et le nombre de cohortes, les chercheurs doivent être conscients des compromis à faire entre le biais et l'incertitude. Des horizons temporels plus courts peuvent introduire un biais dans les estimations du rapport coût-efficacité, car ils ne laissent pas suffisamment de temps pour tenir compte des changements épidémiologiques résultant du programme de vaccination. Des horizons temporels plus courts donnent plus de poids aux coûts anticipés liés au lancement du programme de vaccination par rapport aux coûts ultérieurs ou annuels, et réduisent les conséquences de l'actualisation sur les résultats mesurés. Des horizons temporels plus courts peuvent également ne pas permettre de quantifier tous les avantages obtenus par les générations finales vaccinées.
Pour les modèles à long terme, les chercheurs doivent tenir compte de la possibilité de changements futurs qui pourraient modifier les coûts et les avantages du vaccin (p. ex. changements technologiques, estimations à long terme de l'efficacité du vaccin, projections démographiques).Note de bas de page 18 Note de bas de page 42Note de bas de page 43 Bien qu'une partie de cette incertitude puisse être prise en compte dans le taux d'actualisation (en particulier pour le « risque catastrophique » - le risque qu'un événement imprévu fasse disparaître une grande partie de la valeur de l'intervention), les chercheurs peuvent souhaiter prendre en compte des incertitudes à long terme spécifiques au contexte, telles que l'émergence de maladies résistantes au traitement. Lorsque l'horizon temporel s'étend sur une longue période (c'est-à-dire plusieurs décennies), les chercheurs doivent présenter les estimations du rapport coût-efficacité à partir de divers points temporels tout au long de l'horizon temporel. Les points de repère temporels choisis devront peut-être être différents selon les évaluations économiques des différents programmes de vaccination. Le choix peut être spécifique au contexte, en fonction de la maladie infectieuse et du moment où les effets sur la santé se manifestent dans le modèle. Les chercheurs devraient envisager de s'engager avec les décideurs pour déterminer les points de temps intéressants à rapporter.
7. Actualisation
Énoncés des Lignes directrices
- 7.1 Dans l'analyse de référence, actualiser les coûts et les résultats (effets) des interventions pour une période dépassant la première année afin de présenter les valeurs selon un taux de 1,5 % par an. [Énoncé des lignes directrices de l'ACMTS, modifié]
- 7.2 « Évaluer le retentissement de l'incertitude liée au taux d'escompte en comparant les résultats de l'analyse de référence à ceux d'analyses complémentaires à l'aide des taux de 0 % et de 3 % par an. » [Énoncé des lignes directrices de l'ACMTS]
L'actualisation des coûts, des résultats sanitaires et non sanitaires dans les évaluations économiques reflète la préférence sociétale pour la consommation actuelle par rapport à la consommation future. En effet, l'actualisation réduit la valeur des coûts et des résultats futurs par rapport à leur valeur actuelle. Le taux d'escompte tient compte du taux social de préférence temporelle, des taux de croissance des ressources de santé et de la valeur de consommation de la santé, ainsi que de l'incertitude quant à la réalisation des résultats de santé futurs.Note de bas de page 44Note de bas de page 45
L'actualisation dans les évaluations économiques des programmes de vaccination peut avoir un effet profond sur la rentabilité des programmes, en particulier dans les situations où les avantages attendus du programme de vaccination peuvent ne pas se manifester avant des années, voire des générations (par exemple, la prévention du cancer du col de l'utérus par un programme de vaccination contre le VPH). Les populations pédiatriques sont particulièrement sensibles à ces effets. L'actualisation des résultats en matière ou non de santé qui s'accumulent dans un avenir lointain peut entraîner une réduction considérable de leur valeur actuelle. Par exemple, dans une analyse coûts-efficacité d'un programme de vaccination contre le VPH, les auteurs font état d'un rapport coût-efficacité non actualisé de 7 600 €/AVAQ, qui passe à 59 100 €/AVAQ lorsqu'on applique un taux d'escompte de 4 % aux coûts et aux avantages (3 462 AVAQ non actualisées contre 438 AVAQ actualisées).Note de bas de page 46
Les deux approches les plus courantes de l'actualisation dans les évaluations économiques des programmes de vaccination sont les suivantes : 1) l'actualisation constante, où le même taux d'escompte fixe est appliqué aux résultats et aux coûts; et 2) l'actualisation différentielle, où un taux d'escompte inférieur est appliqué aux résultats par rapport aux coûts.Note de bas de page 44Note de bas de page 45Note de bas de page 46Note de bas de page 47
Les chercheurs doivent utiliser l'actualisation constante dans les évaluations économiques des programmes de vaccination. Cette approche est plus couramment utilisée que l'actualisation différentielle dans les évaluations des interventions vaccinales et non vaccinales en matière de santé.Note de bas de page 45 Certaines lignes directrices des groupes consultatifs techniques nationaux sur la vaccination et certaines lignes directrices sur l'évaluation des technologies de la santé (ETS) recommandent des approches d'actualisation différentielle dans les analyses d'incertitude ou dans des circonstances particulières.Note de bas de page 48Note de bas de page 49
Les arguments en faveur de l'actualisation constante sont la cohérence et l'équité horizontale.Note de bas de page 45 L'argument de la cohérence part du postulat selon lequel les technologies de santé associées aux mêmes résultats et coûts sur le même horizon temporel analytique reçoivent la même priorité de la part des décideurs, quel que soit le moment où elles sont initiées.Note de bas de page 50 Cela s'explique par la valeur constante de la santé dans le temps. L'argument de l'équité horizontale part du postulat selon lequel tous les individus qui peuvent bénéficier d'un programme de vaccination, quel que soit le moment où ils en bénéficient par rapport au moment où le programme a été lancé, sont traités de la même manière. L'actualisation constante empêche de donner la préférence aux programmes de vaccination qui s'étendent sur plusieurs générations par rapport aux programmes qui durent moins longtemps.Note de bas de page 44 L'actualisation constante peut également empêcher l'utilisation stratégique des horizons temporels et du nombre de cohortes incluses pour modifier les estimations du rapport coût-efficacité. Par exemple, dans le cadre d'une stratégie d'actualisation différentielle, les rapports coût-efficacité peuvent être diminués en augmentant le nombre de cohortes de naissance incluses; cependant, cela ne se produit pas dans le cadre d'une stratégie d'actualisation constante.Note de bas de page 51Note de bas de page 52
Un argument en faveur d'une actualisation différentielle avec un taux d'actualisation plus faible pour les résultats sanitaires et non sanitaires par rapport aux coûts est d'accorder normativement plus de poids aux avantages futurs. Un autre argument principal en faveur de l'actualisation différentielle est la valeur croissante que représente la santé future, ou l'évolution des seuils de rapport coût-efficacité.Note de bas de page 53 Les taux d'actualisation pourraient être ajustés pour refléter ces changements, mais ils pourraient aussi être traités plus explicitement dans l'analyse d'incertitude. En ce qui concerne les programmes de vaccination, de longs horizons temporels - souvent plusieurs générations - peuvent être nécessaires pour obtenir des résultats liés aux effets indirects de l'immunité communautaire, qui profitent non seulement aux individus vaccinés, mais aussi aux cohortes futures par l'élimination ou l'éradication de la maladie.Note de bas de page 45 L'utilisation d'une actualisation constante, en particulier avec des taux d'actualisation plus élevés, peut rendre la valeur actuelle de ces programmes proche de zéro. Ce problème est moins préoccupant avec des taux d'actualisation plus faibles, comme le recommandent les présentes lignes directrices.
Les chercheurs doivent actualiser les résultats sanitaires, les résultats non sanitaires et les coûts survenant au-delà d'un an à un taux de 1,5 % par an dans les analyses du cas de référence. Cette valeur représente le coût réel des emprunts à long terme pour les provinces ou territoires canadiens, qui sont les autorités responsables du financement de la plus grande partie du système de santé canadienNote de bas de page 4, et se rapproche du taux auquel la société est prête à échanger la consommation actuelle contre la consommation future.Note de bas de page 45
Les analyses de sensibilité doivent être effectuées en utilisant des taux constants de 0 % et 3 % par an appliqués à la fois aux résultats et aux coûts pour tenir compte de toute incertitude dans le taux d'actualisation. Le faible taux d'actualisation dans les analyses du cas de référence atténue certaines des préoccupations concernant les valeurs actuelles des résultats attendus dans un avenir lointain. Dans les situations où les effets d'un programme de vaccination s'étendent sur plusieurs générations et peuvent être affectés par la stratégie ou le taux d'actualisation utilisés dans l'analyse, la présentation de résultats non actualisés aidera les décideurs à évaluer les effets intergénérationnels potentiels. Le chapitre 14, Équité, propose une discussion sur l'équité intergénérationnelle.
8. Modélisation
Énoncés des Lignes directrices
- 8.1 Conceptualiser et élaborer le modèle en fonction du problème de décision [Énoncé des lignes directrices de l'ACMTS]
- 8.2 Dans la conceptualisation du modèle, prendre en considération tout modèle bien construit et validé qui incorpore adéquatement le cheminement clinique ou de soin dans la maladie infectieuse d'intérêt. [Énoncé des lignes directrices de l'ACMTS, modifié]
- 8.3 La structure du modèle doit refléter l'histoire naturelle de la maladie, le parcours clinique ou de soins, et tenir compte de la susceptibilité, de l'infectiosité, de l'immunité, de la morbidité et de la mortalité liées à l'infection.
- 8.4 Le cas échéant, il faut intégrer au modèle les dynamiques comportementales pertinentes, y compris les habitudes de contact entre les individus et les comportements liés à la prévention et au contrôle des infections.
- 8.5 Des modèles dynamiques doivent être pris en considération dans les évaluations économiques des vaccins et associés à des externalités comme la prévention de la transmission interhumaine de l'infection et le déplacement lié à l'âge de la maladie.
- 8.6 D'autres attributs du modèle, notamment le fait qu'il soit déterministe ou stochastique, basé sur les populations ou sur les individus, et ouvert ou fermé, doivent être considérés dans le contexte du problème de décision.
- 8.7 Les chercheurs doivent rendre compte de manière transparente des processus de calage et de validation du modèle qui ont été entrepris et de leurs résultats.
Ce chapitre présente les considérations liées à la construction des modèles utilisés pour estimer la rentabilité des programmes de vaccination. Les modèles avec des hôtes non humains sont en dehors du champ d'application du CCNI et, par conséquent, du champ d'application des présentes lignes directrices. Un examen des modèles dynamiques et statiques dans le contexte de la modélisation des maladies infectieuses est présenté, suivi d'un aperçu des autres attributs des modèles. La section se termine par des recommandations sur le calage et la validation du modèle.
Structure et attributs du modèle
La structure et les attributs du modèle doivent refléter l'histoire naturelle de la maladie et inclure tous les états de santé pertinents et les transitions entre ces états. Deux considérations principales entrent en jeu lors de la conceptualisation d'un modèle utilisé pour estimer la rentabilité d'un programme de vaccination : la transmission de l'infection entre individus est-elle importante pour estimer les effets d'un programme de vaccination, et les comportements et caractéristiques individuels sont-ils importants pour comprendre les résultats liés à un programme de vaccination? Les chercheurs doivent se référer aux taxonomies de modèles plus détaillées dans Brennan et al.Note de bas de page 54, Kim et Goldie,Note de bas de page 37 Stahl et al.Note de bas de page 55 et Mac et al.Note de bas de page 56 pour obtenir des détails supplémentaires si nécessaire.
D'autres conseils sur la construction de modèles pour l'évaluation économique des programmes de vaccination figurent au chapitre 13 consacré à l'incertitude (par exemple, veiller à ce que la structure du modèle tienne compte des facteurs liés à la transmission de l'infection entre individus, de l'histoire naturelle de la maladie modélisée, ainsi que des effets directs et indirects du programme de vaccination).Note de bas de page 39Note de bas de page 57
Modèles dynamiques ou modèles statiques
Les modèles doivent tenir compte des externalités liées aux programmes de vaccination, comme l'immunité collective et la variation de l'âge de maladie. Dans ces lignes directrices, les termes « modèle dynamique » et « modèle statique » font référence à la nature du taux d'incidence qui est dynamique ou non (c'est-à-dire qui évolue dans le temps en fonction de la proportion de la population qui est infectieuse). Bien que certains puissent utiliser les termes « endogènes » ou « exogènes », les présentes lignes directrices suivent les conventions établies dans les directives d'évaluation économique de l'Organisation mondiale de la santé.Note de bas de page 58
Les modèles statiques, qui utilisent généralement un risque d'exposition constant, ne représentent pas explicitement la transmission dynamique de l'infection. Les modèles sont acceptables dans les évaluations économiques des programmes de vaccination lorsqu'il n'y a pas de transmission interhumaine (par exemple, le tétanos ou la rage).Note de bas de page 13 Ils sont également acceptables dans les situations où le groupe visé par la vaccination n'a pas d'influence épidémiologique sur la transmission (par exemple, la vaccination contre l'hépatite A du personnel de santé, la vaccination contre la grippe ou le pneumocoque chez les personnes âgées).Note de bas de page 13Note de bas de page 39 Les modèles statiques peuvent également être acceptables pour les infections où l'individu est déjà un « hôte » (par exemple, certaines souches de pneumocoques; le virus varicelle-zona où l'incidence de l'infection est plutôt un événement aléatoire dans la vie d'une personne après une colonisation de longue date à la suite d'une infection à la varicelle). Enfin, un modèle statique est acceptable dans les cas suivants : 1) il est démontré qu'un programme de vaccination est rentable, et un modèle dynamique ne servirait qu'à renforcer cette conclusion en comptabilisant les infections évitées par la protection indirecte ou la transmission secondaire; ou 2) il n'est pas démontré qu'un programme de vaccination est rentable, mais il existe des données épidémiologiques ou de modélisation qui permettront d'estimer l'ampleur de l'immunité collective ou de la transmission secondaire dans le même contexte ou un contexte très similaire.Note de bas de page 39Note de bas de page 59
Bien que les scénarios précédents décrivent des situations où les modèles statiques peuvent être acceptables pour estimer la rentabilité des programmes de vaccination, les chercheurs doivent être conscients de leurs limites. Tout d'abord, lorsqu'un modèle statique a démontré la rentabilité d'un vaccin sans tenir compte des effets de l'immunité collective ou de la transmission secondaire, la rentabilité réelle de l'intervention peut être sous-estimée, ce qui pourrait se traduire par des décisions d'allocation des ressources biaisées dans le cadre d'un budget fixe des soins de santé.Note de bas de page 39 Deuxièmement, lorsque des données épidémiologiques ou de modélisation sont utilisées pour estimer l'ampleur de l'immunité collective ou de la transmission secondaire dans le contexte de modèles statiques, les estimations du rapport coût-efficacité peuvent être biaisées lorsque les données utilisées proviennent d'une population différente de celle considérée dans le modèle et lorsqu'il existe d'autres différences importantes. De plus, si les données utilisées sont issues de l'équilibre épidémiologique, la fluctuation de la prévalence dans la période initiale post-vaccination ne sera pas prise en compte. Cette limitation est particulièrement importante pour les programmes de vaccination avec une préférence temporelle positive, étant donné que la période initiale est celle où la plupart des coûts et des avantages liés au vaccin sont accumulés.Note de bas de page 59 Les arbres de décision, les modèles de Markov fondés sur les cohortes et les simulations d'événements discrets sont des exemples de modèles statiques.
Les modèles dynamiques, qui représentent explicitement la transmission de l'infection, doivent être pris en compte dans les évaluations économiques des programmes de vaccination où la transmission interhumaine est un facteur important. Par exemple, il faut utiliser des modèles dynamiques lorsqu'un programme de vaccination à grande échelle est censé modifier la force de l'infection, ce qui permet de contrôler, d'éliminer ou d'éradiquer une maladie en empêchant sa transmission.
Les modèles dynamiques doivent également être utilisés lorsqu'un programme de vaccination peut entraîner le remplacement du sérotype et la variation de l'âge de maladie. Les vaccins qui sont spécifiques à une certaine variation de l'agent pathogène (c'est-à-dire un sérotype, un sérogroupe ou une souche) peuvent réduire une variation de la maladie, mais en présence de multiples variations, la prévalence de l'infection due à des variations non vaccinales peut encore augmenter.Note de bas de page 60Note de bas de page 61 Pour les maladies causées par de multiples variations d'un agent pathogène, les chercheurs doivent inclure chaque variation séparément dans le modèle afin de pouvoir tenir compte des infections et des maladies liées à l'émergence de nouvelles variations. Les situations où un programme de vaccination se traduit par une augmentation ou une diminution de l'âge moyen des individus touchés par une infection peuvent conduire à une augmentation correspondante de la gravité de la maladie, des coûts des traitements et de la mortalité, ce qui doit également être pris en compte dans une analyse coûts-efficacité.Note de bas de page 62Note de bas de page 63 Les modèles de cohorte dynamiques et les modèles de simulation individuels sont des exemples de modèles dynamiques.
Pour choisir entre un modèle dynamique ou statique, les chercheurs doivent tenir compte des compromis entre la nécessité de représenter la transmission et les complexités supplémentaires associées aux modèles dynamiques. Dans certaines situations, la décision de choisir un type de modèle plutôt qu'un autre n'est pas toujours simple à prendre. Les modèles dynamiques sont conceptuellement et informatiquement plus complexes que les modèles statiques. Les décideurs qui sont les utilisateurs finaux des résultats produits doivent être en mesure de comprendre et d'interpréter la structure du modèle. Ils doivent également être convaincus que les résultats sont une représentation raisonnable de ce qui devrait se produire dans le monde réel après la mise en œuvre du programme de vaccination. Il existe également un compromis entre la complexité (et le réalisme) d'un modèle et la facilité avec laquelle il peut être compris, communiqué et validé. Dans certains cas, la transmissibilité entre individus peut entraîner la propagation d'une infection, mais la représentation de la transmission dans un modèle économique peut être inutile du fait de la nature du programme de vaccination. Par exemple, un modèle statique peut être adéquat pour prédire les effets d'un programme de vaccination universelle qui devrait atteindre un niveau élevé de couverture dans la population. Pour obtenir des conseils supplémentaires sur l'utilisation d'un modèle statique ou dynamique lors de l'estimation de la rentabilité d'un programme de vaccination, les chercheurs peuvent consulter les schémas publiés par Jit et Brisson et l'Organisation mondiale de la santé, qui délimitent les considérations liées à ce choix (figure 4, tableau 8).Note de bas de page 58Note de bas de page 59
Il convient de noter qu'il existe des modèles « hybrides » entre les modèles dynamiques et statiques, dans lesquels les chercheurs ne tiennent pas entièrement compte de la transmission de l'infection. Ils estiment plutôt le nombre moyen d'infections secondaires évitées grâce à la prévention d'un cas et intègrent les coûts et les avantages de la prévention de ces cas dans l'analyse.
Autres attributs
Bien que le choix fondamental auquel sont confrontés les chercheurs qui modélisent la rentabilité des vaccins consiste à sélectionner des techniques de modélisation statique ou dynamique, ils doivent également tenir compte d'autres attributs liés à la structure du modèle.
Modèle déterministe ou modèle stochastique
Dans les modèles déterministes, les événements dépendent de paramètres préspécifiés et de la structure du modèle; autrement dit, l'incertitude de premier ordre n'est pas prise en compte puisque les événements ne peuvent pas se produire de manière aléatoire (par hasard). Dans les modèles stochastiques, en revanche, les événements sont programmés pour se produire de manière aléatoire, en tenant compte de l'incertitude de premier ordre.Note de bas de page 37Note de bas de page 64 Pour une discussion sur l'incertitude de second ordre (paramètres), les chercheurs se reporteront au chapitre 14 consacré à l'incertitude.
Les valeurs moyennes des paramètres utilisées dans les modèles déterministes peuvent se rapprocher de manière réaliste des processus modélisés si la population à risque est nombreuse et si l'infection n'est pas proche de l'élimination ou de l'éradication mondiale (par exemple, le VPH). Pour les petites populations (comme une éclosion d'infection à méningocoque B dans un collège) ou lors de la modélisation de l'augmentation d'une infection émergente ou rare qui est sur le point d'être éliminée (par exemple, la rougeole et la polio dans certains pays), les modèles qui intègrent la variabilité individuelle et l'incertitude de premier ordre (par exemple, les modèles individuels) sont plus appropriés car ils peuvent tenir compte des événements de transmission aléatoires qui sont importants dans ces situations.Note de bas de page 13Note de bas de page 39
Modèle agrégé ou individuel
Dans les modèles agrégés (également appelés modèles populationnels) tels que les modèles de cohorte de Markov et les modèles dynamiques à compartiments, les groupes d'individus sont agrégés en compartiments représentant les états de santé en fonction de leurs caractéristiques. Les changements dans le temps représentent l'évolution de la proportion de la population dans chaque état de santé en fonction des valeurs moyennes des paramètres.Note de bas de page 37Note de bas de page 65
Dans les modèles individuels, la progression de chaque individu avec différentes caractéristiques est simulée. Les modèles qui simulent la transmission entre les individus infectés et les individus sensibles sont dynamiques, en ce sens que le risque d'infection évolue au cours de la simulation.Note de bas de page 37 En revanche, ceux qui supposent un risque d'infection exogène indépendant de la présence ou non de personnes infectées dans la population sont statiques.Note de bas de page 37 Ce type de modèle est généralement plus complexe et nécessite plus de données qu'un modèle agrégé, et peut être programmé de manière stochastique afin que la probabilité d'événements futurs d'un individu tienne compte de l'incertitude liée au hasard.Note de bas de page 56
Le comportement des individus peut influencer les effets d'un programme de vaccination, et l'évaluation économique doit tenir compte de ces comportements lorsqu'ils sont pertinents. Ces modèles peuvent être programmés de telle sorte que les individus ont une mémoire et sont capables de modifier leurs comportements au fil du temps en fonction de leurs interactions précédentes.Note de bas de page 64
Les modèles individuels sont également appropriés lorsqu'il existe des hétérogénéités importantes entre les individus d'une population. Ces hétérogénéités peuvent être liées à des facteurs génétiques, au statut socio-économique, à l'âge, à l'accès aux services de santé et aux changements de comportement en réponse aux épidémies, pour n'en citer que quelques-uns. Voir le chapitre 14, Équité, pour plus de différences liées à l'équité. Les modèles basés sur les individus tiennent compte de ces caractéristiques et de l'effet qu'elles pourraient avoir sur les résultats liés à l'introduction d'un programme de vaccination.Note de bas de page 66
Les modèles agrégés, en revanche, sont appropriés pour les programmes de vaccination destinés à des groupes relativement homogènes d'individus (par exemple, un programme de vaccination contre le pneumocoque pour les personnes âgées dans une zone géographique donnée),Note de bas de page 67 car ils présentent des caractéristiques similaires qui pourraient être raisonnablement représentées par des valeurs moyennes lorsqu'ils passent d'un état de santé à l'autre. Il faut noter que les modèles populationnels peuvent néanmoins incorporer une certaine hétérogénéité en stratifiant par risque ou en intégrant un mélange assortatif par groupes d'âge et sur d'autres facteurs de risque.
Pour modéliser les hétérogénéités entre les groupes ou les individus (y compris les différences liées à l'équité), les chercheurs doivent déterminer le niveau de détail requis pour modéliser correctement la rentabilité d'un programme de vaccination, et prendre en compte les compromis entre les différents types de modèles qui pourraient être utilisés pour intégrer ces hétérogénéités.
Modèle ouvert ou modèle fermé
Les modèles peuvent représenter des populations ouvertes ou fermées. Les modèles ouverts permettent à de nouveaux individus réceptifs, par le biais des naissances et de l'immigration, d'entrer dans le modèle et d'en sortir au fil du temps, alors que les modèles fermés ne le permettent pas. Bien que les modèles ouverts puissent être plus complexes sur le plan informatique, ils permettent aux chercheurs d'estimer l'évolution de la population visée par la vaccination et de tenir compte de ses caractéristiques telles que l'exposition au risque, l'âge et la gravité de la maladie.Note de bas de page 37Note de bas de page 68
Les modèles ouverts doivent être utilisés lorsque les effets des programmes de vaccination dans une cohorte affecteront d'autres cohortes de population (par exemple, les programmes de vaccination des enfants contre des maladies comme la rougeole ou la polio). Les modèles fermés sont appropriés lorsqu'il s'agit d'examiner les programmes de vaccination de petits groupes d'individus qui ne sont pas susceptibles d'avoir une influence épidémiologique dans la population plus large (par exemple, le programme de vaccination contre l'hépatite A pour les travailleurs de la santé), ou lorsque les effets du vaccin sont de courte durée (par exemple, le programme d'immunisation antigrippale). Cependant, il faut noter que les modèles ouverts sont parfois nécessaires dans les petites populations relativement homogènes avec un fort renouvellement de la population, et que les modèles fermés peuvent être suffisants dans de nombreux cas lorsque le renouvellement de la population est approximativement neutre. Notez également que les modèles fermés avec de longs horizons temporels peuvent sous-estimer les coûts et les résultats potentiels.
Modèle discret ou modèle continu
Les modèles continus sont recommandés lorsqu'il faut modéliser plusieurs événements simultanément. Par exemple, dans le cas d'éclosions de maladie où la transmission de l'infection entre individus peut dépendre de multiples facteurs tels que les habitudes de contact entre les individus ou le nombre d'individus infectieux dans une population donnée.Note de bas de page 54 Bien que les modèles continus puissent fournir des résultats plus précis dans de telles situations, ces modèles sont plus complexes sur le plan informatique. Ils nécessitent l'utilisation d'équations différentielles ordinaires pour lesquelles les solutions peuvent être difficiles à obtenir. On peut déterminer approximativement les résultats des modèles continus en utilisant des modèles discrets avec un petit pas de temps et en redimensionnant les paramètres de manière appropriée.Note de bas de page 37Note de bas de page 54
Calage du modèle
Le calage du modèle désigne le processus qui sert à estimer les paramètres inconnus du modèle en les réglant et en veillant à ce que les données de sortie du modèle correspondent bien aux données observées (cibles du calage).Note de bas de page 69 Dans la modélisation des maladies infectieuses, de nombreux paramètres peuvent être inconnus ou ne peuvent pas être estimés directement à partir des données disponibles. Il peut s'agir de paramètres liés à la progression naturelle de l'infection ou de la maladie, de détails relatifs aux comportements sexuels dans le cas des infections transmissibles sexuellement et de données concernant l'adoption et la distribution des résultats des interventions de dépistage.Note de bas de page 70 Les cibles de calage sélectionnées doivent être des données indépendantes, rapportées avec précision et présentant un degré élevé de validité interne et externe. Le cas échéant, ces données doivent être stratifiées par sous-groupes pertinents afin de garantir une performance adéquate du modèle dans les principales strates de population.Note de bas de page 71 Les chercheurs pourraient également envisager de solliciter l'avis d'experts lors de la sélection des cibles de calage.
Les chercheurs doivent garder à l'esprit que comme des décisions subjectives sont nécessaires au cours du processus de calage, telles que la sélection des cibles de calage, les mesures de qualité de l'ajustement et la méthode de calage, une incertitude entoure les méthodes de calage utilisées. Ces incertitudes peuvent se traduire par des différences considérables dans les résultats des évaluations économiques. Bien que le calage soit souvent gourmand en ressources informatiques, les chercheurs devraient, dans la mesure du possible, envisager d'utiliser plus d'une approche pour le calage des modèles et plusieurs statistiques de qualité de l'ajustement.Note de bas de page 72Note de bas de page 73 Les chercheurs doivent conserver l'incertitude dans les paramètres estimés du calage, qui peuvent ensuite être utilisés dans une analyse probabiliste.
La difficulté à caler plusieurs paramètres du modèle peut indiquer que la structure du modèle ou ses hypothèses sous-jacentes sont incorrectes. Elle peut également suggérer une compréhension limitée de l'évolution naturelle de la maladie modélisée ou des comportements qui influencent sa transmissibilité, sa détection ou son traitement. Elle peut aussi révéler des biais, des incohérences ou des imprécisions dans les données utilisées comme cibles de calage. Ainsi, elle ne doit pas être réduite ou ignorée, mais plutôt utilisée pour aider à établir les futures priorités de recherche.Note de bas de page 39
Validation du modèle
La validation est le processus utilisé pour garantir l'exactitude des résultats générés par les modèles utilisés dans les évaluations économiques. La validité d'un modèle doit être examinée dans un contexte décisionnel pertinent afin que les décideurs soient en mesure de déterminer si le modèle considéré répond au problème de décision en question.Note de bas de page 74 Les chercheurs doivent évaluer les divers aspects de la validité du modèle grâce à différentes méthodes.
La validité apparente consiste à déterminer si un modèle reflète la compréhension actuelle et les preuves liées à la maladie et au programme de vaccination envisagé. Elle demande l'évaluation subjective de la structure, des hypothèses, des sources de données et des résultats d'un modèle. Il est préférable de confier cette tâche à des experts cliniques dans le domaine, et il est également possible de comparer la structure du modèle à normes de soins. La validité interne, souvent appelée vérification, consiste à déterminer si le modèle se comporte comme il le devrait. Il s'agit de vérifier que les équations mathématiques utilisées dans le modèle ont été programmées correctement. Cela permet de s'assurer que le modèle ne comporte pas d'erreurs de calcul. La validation croisée consiste à comparer les résultats générés par un modèle et à déterminer dans quelle mesure ils correspondent aux résultats d'autres modèles.Note de bas de page 75 La validité externe consiste à comparer les résultats générés par un modèle avec des données existantes provenant de sources indépendantes telles que des essais cliniques, des études épidémiologiques, des statistiques démographiques couramment disponibles, comme les données de mortalité, ou des dossiers médicaux électroniques. La validation externe n'est pas possible dans les situations où le modèle utilise toutes les données pertinentes connues. Elle peut être difficile dans les situations où ces types de données n'existent pas ou lorsqu'elles ne sont pas suffisamment détaillées pour permettre une comparaison appropriée.Note de bas de page 76 La validité prédictive consiste à déterminer si un modèle remplit l'objectif pour lequel il a été conçu, à savoir prédire les résultats d'un programme de vaccination. C'est également le type de validation le plus difficile à réaliser, car les résultats doivent se rapporter à des événements ou à des études qui auront lieu dans le futur. Ce type de validation n'est généralement pas applicable au processus décisionnel relatif à un nouveau programme de vaccination.Note de bas de page 76 Cependant, elle peut être pertinente lors de l'élaboration d'un modèle basé sur des modèles plus anciens. Les chercheurs peuvent évaluer les anciens modèles avant de les réutiliser. Comme pour le calage des modèles, les chercheurs pourraient envisager de solliciter l'avis d'experts lorsqu'ils entreprennent des processus de validation des modèles.
9. Efficacité
Énoncés des Lignes directrices
- 9.1. Effectuer une recherche documentaire exhaustive afin d'appuyer l'estimation de l'efficacité clinique et de l'innocuité des interventions à l'étude. Faire état des études retenues et des méthodes de sélection ou de regroupement des données. Les chercheurs doivent évaluer l'efficacité des sources utilisées en fonction de leur adéquation à l'objectif, de leur crédibilité et de leur cohérence. Décrire les compromis entre ces critères et justifier les sources sélectionnées. [Énoncé des lignes directrices de l'ACMTS, modifié]
- 9.2 Les critères suivants doivent être pris en compte lors de l'évaluation des estimations de l'efficacité des vaccins : l'efficacité du vaccin en fonction de la dose et du temps (par exemple, protection décroissante), l'efficacité spécifique à la variation de l'agent pathogène (c'est-à-dire les sérotypes, les sérogroupes, les souches), et les facteurs géographiques et liés à la personne vaccinée qui peuvent avoir une incidence sur l'efficacité.
- 9.3 Les chercheurs doivent s'assurer que les biomarqueurs immunitaires utilisés comme résultats de substitution dans les études sur l'efficacité potentielle ou réelle des vaccins répondent aux critères des corrélats de protection.
Ce chapitre décrit les facteurs à prendre en compte pour évaluer l'efficacité réelle des vaccins, ainsi que les considérations liées à la synthèse des données, à l'interprétation et à l'utilisation des résultats de substitution, ainsi qu'à l'extrapolation des estimations de l'efficacité réelle.
Évaluation des estimations de l'efficacité réelle des vaccins
Plusieurs facteurs particuliers aux vaccins doivent être pris en compte pour interpréter les données sur l'efficacité réelle. Ils sont examinés ci-après.
L'efficacité est établie par des essais contrôlés randomisés (ECR), qui évaluent les modifications des marqueurs immunitaires, la réduction de la gravité des maladies et l'amélioration de l'état de santé des personnes vaccinées. L'efficacité réelle des vaccins chez les individus est souvent différente de l'efficacité potentielle. Par exemple, les taux d'achèvement de la série vaccinale sont souvent plus élevés dans les ECR que dans le monde réel; le plan d'ECR présente des limites quant à la prise en compte de l'immunité communautaire; et il existe d'autres différences entre les populations des ECR et les populations du monde réel dans lesquelles le vaccin est utilisé.
L'achèvement de la série vaccinale est une considération importante pour les nombreux vaccins qui nécessitent l'administration de doses multiples à des intervalles de temps définis. Par exemple, le vaccin contre le VPH était initialement administré selon un calendrier à trois doses, mais on recommande désormais un calendrier à deux doses pour la plupart des personnes. Pour le calendrier à trois doses, la deuxième dose est administrée un à deux mois après la première, et la troisième dose six mois après la première.Note de bas de page 77 Les chercheurs doivent garder à l'esprit que chez les personnes qui ne reçoivent pas toutes les doses d'une série de vaccins recommandée, les taux d'efficacité réelle des vaccins peuvent être inférieurs à ceux observés chez les personnes qui reçoivent la série complète. Les chercheurs doivent évaluer à la fois les données des essais cliniques et les estimations de l'administration prévue des doses dans le monde réel, car les deux ont des points forts et des limites. Les données du monde réel peuvent provenir d'études d'acceptabilité sur l'achèvement de la série de vaccins ou de données sur l'achèvement d'autres séries de vaccins utilisées dans des populations similaires avec un nombre de doses similaire. Les chercheurs doivent garder à l'esprit que des facteurs de confusion résiduelle peuvent altérer les résultats des études d'observation qui examinent la relation entre les taux d'achèvement des doses et l'efficacité du vaccin. Plus précisément, les facteurs qui prédisent une probabilité moindre d'achèvement de la dose peuvent également augmenter le risque sous-jacent d'infection (p. ex. une exposition sexuelle plus précoce chez les filles qui reçoivent moins de trois doses de vaccin contre le VPH).Note de bas de page 21 Pour les analyses de cas de référence, les chercheurs doivent utiliser les estimations de l'administration prévue des doses dans le monde réel en fonction des régions concernées et de la population visée par le programme de vaccination.
En ce qui concerne l'immunité communautaire, les ECR peuvent sous-estimer les effets d'un vaccin dans la population. C'est-à-dire que l'immunité communautaire n'est pas observée chez les participants aux ECR puisqu'ils représentent une très faible proportion de la population. L'immunité collective dépend de la distribution de l'immunité conférée par le vaccin et de l'infection naturelle dans la population, de la transmissibilité de l'infection et des habitudes de contact des individus dans la population.Note de bas de page 78 L'efficacité au niveau de la population est généralement établie par des études d'observation, qui permettent normalement de saisir les effets indirects d'un vaccin. Les chercheurs ne doivent toutefois pas oublier que les études utilisant des données de surveillance sont soumises aux mêmes limites que les autres études d'observation et qu'il n'est peut-être pas approprié de les extrapoler à des milieux différents.Note de bas de page 39 Dans ces cas, il est possible d'utiliser des modèles dynamiques paramétrés grâce à des données épidémiologiques locales pour estimer les effets indirects des vaccins. Lorsqu'ils évaluent s'il convient d'inclure les estimations de l'efficacité potentielle ou de l'efficacité réelle des vaccins provenant d'ECR ou d'études d'observation dans les analyses de référence, les chercheurs doivent justifier quelles sources de données représentent le mieux les résultats obtenus dans les populations les plus semblables aux populations concernées par le programme de vaccination à mettre en œuvre.
Les variations géographiques doivent être prises en compte pour l'efficacité potentielle et l'efficacité réelle des vaccins. Plusieurs études ont montré que l'efficacité potentielle et l'efficacité réelle des vaccins peuvent varier selon les pays. On a envisagé divers facteurs pour expliquer ces différences, notamment : 1) les différences de prévalence des sérotypes ou des souches; 2) le rôle du climat et des températures moyennes quotidiennes; 3) les hétérogénéités de la population en ce qui concerne les facteurs sociaux et démographiques qui influencent l'efficacité potentielle du vaccin; 4) la co-administration d'autres vaccins (p. ex. la co-administration de vaccins oraux contre le rotavirus et la polio); et 5) les différences de prévalence d'autres infections endémiques.Note de bas de page 79Note de bas de page 80
Les facteurs liés à l'hôte doivent également être pris en compte dans l'évaluation de l'adéquation des données sur l'efficacité potentielle et l'efficacité réelle des vaccins. Ces facteurs sont notamment l'âge, la prédisposition génétique à l'infection, les déficiences immunitaires congénitales, l'effet de la nutrition sur les réponses de l'hôte, la sensibilisation antérieure à des organismes antigéniquement apparentés à l'agent pathogène, les comorbidités, en particulier celles qui peuvent toucher la réponse immunitaire, les immunodéficiences secondaires dues aux médicaments et les éventuelles différences génétiques dans la réaction à un vaccin particulier.Note de bas de page 81 Les essais randomisés contrôlés ont tendance à ne porter que sur des adultes en bonne santé, en particulier pour les essais essentiels et les essais tenus tôt dans le cycle de développement du produit. De leur côté, les études en situation réelle comprennent des populations vulnérables qui seraient autrement exclues des essais randomisés contrôlés, notamment les femmes enceintes, les enfants et les personnes immunodéprimées.
La couverture vaccinale peut varier selon les groupes d'individus ou les zones géographiques. Par exemple, la couverture vaccinale contre la diphtérie, le tétanos et la coqueluche de quatre doses ou plus chez les enfants de deux ans diffère entre les provinces canadiennes; elle est la plus élevée à Terre-Neuve-et-Labrador (89 %) et la plus faible au Manitoba (66 %), selon l'Enquête canadienne sur la couverture vaccinale de 2017.Note de bas de page 82 La couverture est un facteur important pour déterminer l'efficacité réelle au niveau de la population grâce à l'immunité collective. L'obtention de niveaux élevés de couverture vaccinale dépend de la stratégie de mise en œuvre adoptée lors de l'introduction d'un nouveau programme de vaccination, ainsi que des stratégies permanentes employées pour étendre et maintenir le programme. Par exemple, la promotion de la santé, les campagnes d'information et d'autres efforts visant à renforcer la confiance de la communauté peuvent contrer la réticence à l'égard de la vaccination. Le succès de ces stratégies dépendra de la capacité des ressources déployées, de la facilité d'accès aux doses de vaccins dans la population visée, de la préparation des fournisseurs de soins de santé et de l'attitude de ces derniers et du public. La prise en compte de ces facteurs dans les évaluations économiques peut permettre de mieux aligner ces évaluations sur les besoins pratiques des décideurs. Il est important de noter que l'inclusion de ces facteurs attire l'attention des décideurs sur des stratégies de mise en œuvre particulière, sur le temps et l'effort relatifs nécessaires à l'exécution de chacune d'elles, sur les compromis inhérents à ces autres plans d'action et sur leurs effets indépendants et conjoints sur la couverture de la population.Note de bas de page 83 Cela renforce l'importance d'impliquer les décideurs lors de la conceptualisation de l'évaluation économique.
Certains vaccins ne protègent que contre certaines variations d'un agent pathogène. Par exemple, le vaccin conjugué contre le pneumocoque 13-valent est actif contre 13 des plus de 90 sérotypes connus du pneumocoque,Note de bas de page 13Note de bas de page 84 et le vaccin polysaccharidique 23-valent contre le pneumocoque (VPSP23) est actif contre 23 sérotypes du pneumocoque.Note de bas de page 85 Les vaccins contre le VPH sont disponibles sous forme bivalente et quadrivalente, bien qu'il existe plus de 100 sérotypes du VPH.Note de bas de page 86 Pour ces types de vaccins, les chercheurs doivent s'assurer que les données d'efficacité potentielle et d'efficacité réelle envisagées sont particulières aux maladies causées par les variations de l'agent pathogène ciblé par les vaccins. Les chercheurs doivent également savoir que dans certains cas, les vaccins particuliers à certaines variations de l'agent pathogène peuvent également conférer un certain degré de protection contre des variations de l'agent pathogène non couvertes par le vaccin. Un exemple de cette protection croisée a été démontré avec les vaccins bivalents et quadrivalents contre le VPH, qui ont conféré une certaine protection contre les infections et les lésions associées aux VPH 31, 33 et 45, qui sont des sérotypes non vaccinaux.Note de bas de page 86
Synthèse des données
Les chercheurs doivent être attentifs aux considérations propres aux vaccins lorsqu'ils combinent des données provenant de différentes sources, notamment des facteurs potentiels géographiques et liés à l'hôte décrits précédemment, qui peuvent être différents entre les populations étudiées et la population visée dans une analyse économique réalisée dans le contexte canadien.
Résultats de substitution
Dans la mesure du possible, il faut déterminer l'efficacité potentielle ou l'efficacité réelle des vaccins par des études comparatives (essais randomisés contrôlés ou études d'observation) qui indiquent l'incidence de la maladie infectieuse ciblée par le vaccin, dans le groupe vacciné par rapport aux comparateurs pertinents.
Le critère d'évaluation primaire de ces études doit être défini comme une infection cliniquement apparente répondant aux critères de diagnostic clinique et en laboratoire. Dans certaines situations, il peut être impossible de mesurer les cas d'infection cliniquement apparente. Un exemple d'une telle situation se présente lorsque l'incidence de l'infection est trop faible pour être mesurée dans une étude, généralement limitée par sa période d'étude et la taille de la population étudiée. Cette situation se produit avec des maladies infectieuses rares (comme la méningite due à une infection à méningocoque du groupe B) ou celles qui touchent rarement la population parce que les vaccins actuels assurent une prévention efficace.Note de bas de page 87Note de bas de page 88 Un autre exemple est celui des vaccins antigrippaux saisonniers, dont beaucoup reçoivent une autorisation provisoire fondée sur la seule immunogénicité.Note de bas de page 89
Dans de tels cas, les corrélats de protection (CP), qui sont des biomarqueurs immunitaires (anticorps ou cellules T) permettant de prédire l'efficacité potentielle du vaccin chez les personnes vaccinées, peuvent être utilisés comme paramètres de substitution.Note de bas de page 87Note de bas de page 90Note de bas de page 91 Les chercheurs doivent savoir que plusieurs CP peuvent exister pour le même vaccinNote de bas de page 92Note de bas de page 93 et que différents types et formulations de vaccins contre la même maladie peuvent être associés à différents corrélats de protection.Note de bas de page 94Note de bas de page 95 Pour les vaccins multivalents qui protègent contre plusieurs variations d'un agent pathogène, des titres plus élevés du CP peuvent être nécessaires pour offrir une protection contre certaines variations par rapport à d'autres.Note de bas de page 96 Enfin, il est important que les chercheurs déterminent la dimension de la prévention (p. ex. la prévention de l'infection, la prévention de la maladie, la réduction de la gravité de la maladie) qui est liée à un CP puisque les corrélats peuvent différer quantitativement et qualitativement selon le résultat préventif considéré.Note de bas de page 97
Extrapolation
La durée des essais cliniques n'est souvent pas assez longue pour déterminer la durée de la protection conférée par un vaccin et les chercheurs doivent extrapoler des estimations de la durée de la protection à partir des données des essais cliniques.Note de bas de page 98Note de bas de page 99 Un certain nombre de techniques de modélisation différentes (p. ex. la décroissance logarithmique, la décroissance exponentielle) peuvent être utilisées pour générer des estimations de la durée de protection, qui peuvent varier considérablement en fonction de la technique choisie. Les estimations de la rentabilité peuvent donc être sensibles aux hypothèses sur la durée de la protection.Note de bas de page 98 Cela a été démontré par des analyses coûts-efficacité du vaccin contre le zona (Zostavax®) en Belgique, où les auteurs ont constaté que les estimations de la rentabilité variaient considérablement en fonction du modèle utilisé pour estimer l'efficacité potentielle du vaccin.Note de bas de page 42 Des conseils précis sur la manière d'aborder l'incertitude sur les estimations de la durée de la protection sont donnés dans le chapitre 13, Incertitude.
10. Mesure et évaluation de la santé
Énoncés des Lignes directrices
- 10.1 « Dans les deux analyses de référence, il convient d'utiliser la survie ajustée pour la qualité de vie (QALY) comme méthode pour évaluer les résultats en matière de santé.
- 10.2 Prendre en considération les préférences en matière de santé qui correspondent à celles de la population canadienne en général. » [Énoncé des lignes directrices de l'ACMTS]
- 10.3 Dans les analyses de référence, les chercheurs doivent utiliser les préférences en matière de santé qui sont obtenues par une méthode de mesure indirecte reposant sur un système de classification générique (p. ex. le questionnaire EuroQol 5-Dimensions [EQ-5D], le Health Utilities Index [HUI], le Short-Form 6-Dimensions [SF-6D], les Child Health Utility 9-Dimensions [CHU9D], l'évaluation de la qualité de vie [AQoL]). Les chercheurs doivent présenter une justification s'ils n'utilisent pas de méthode indirecte. [Énoncé des lignes directrices de l'ACMTS, modifié]
- 10.4 Il convient de faire une recherche exhaustive des sources de données disponibles pour déterminer les valeurs d'utilité de l'état de santé. Faire état des études retenues et des méthodes de sélection ou de regroupement des données. Les chercheurs doivent évaluer les sources utilisées pour les valeurs d'utilité de l'état de santé en fonction de leur pertinence, de leur crédibilité et de leur cohérence. Décrire les compromis consentis entre ces critères et justifier les sources choisies. [Énoncé des lignes directrices de l'ACMTS, modifié]
Les décideurs s'intéressent aux résultats en matière de santé, car ils constituent le principal résultat des interventions dans ce domaine. L'AVAQ est la mesure métrique utilisée pour quantifier les résultats en matière de santé dans une ACU. Les estimations de l'AVAQ sont générées en combinant les données sur la survie et la qualité de vie liée à la santé (QVLS). Pour pouvoir estimer l'AVAQ, il faut disposer de données sur la QVLS sous la forme d'une mesure sommaire, souvent appelée utilité en santé.
Données sur l'utilité en santé
Les coefficients d'utilité tirés des instruments de QVLS doivent représenter les préférences de la population canadienne en général, conformément au point de vue de la prise de décision sociale adopté par les présentes lignes directrices. Les préférences de la population pour les états de santé définis dans un instrument de QVLS sont normalement obtenues à partir d'un échantillon de la population générale selon des méthodes telles que le pari standard ou l'arbitrage temporel.
Bien qu'il soit possible d'obtenir les utilités en santé directement auprès des répondants, les instruments conçus pour saisir les utilités en santé indirectement constituent une méthode plus efficace et plus cohérente pour obtenir ces renseignements. Il existe des instruments de mesure de la QVLS propres à une maladie ou génériques permettant de mesurer indirectement l'utilité en santé. Les instruments génériques les plus couramment utilisés sont le questionnaire EuroQol 5-Dimensions (EQ-5D), le Health Utilities Index (HUI), le Short Form 6-Dimensions (SF-6D) et l'évaluation de la qualité de vie (AQoL). Les instruments de mesure de la QVLS des enfants comprennent le Child Health Utility 9-Dimensions (CHU9D), le questionnaire sur la qualité de vie KISCREEN, le Pediatric Quality of Life Inventory (PedsQL) Generic Cores Scales et l'EQ-5D-Youth (EQ-5D-Y). Les chercheurs doivent utiliser les données sur la QVLS provenant d'un instrument générique pour estimer l'AVAQ afin de garantir la comparabilité des programmes de vaccination envisagés par les responsables des politiques. Lorsque plusieurs estimations des utilités sont disponibles, les études sources doivent être soumises à une évaluation formelle de la qualité à l'aide d'un outil d'évaluation de la qualité approprié.Note de bas de page 100
Il faut reconnaître qu'il n'existe pas d'instruments valides pour mesurer directement l'utilité chez les nouveau-nés, les nourrissons ou les jeunes enfants, bien qu'il s'agisse d'un domaine actif de la recherche actuelle.Note de bas de page 101 De plus, le concept de QVLS pour les enfants diffère selon le groupe d'âge et est conceptuellement différent de celui des adultes.Note de bas de page 102 Bien que plusieurs mesures de la qualité de vie liée à la santé basées sur les préférences et particulières à l'enfant aient été développées récemment (p. ex. EQ-5D-Y, CHU-9D, A-QOL), toutes ont des limites d'âge inférieures et reposent généralement sur des ensembles de tarifs dérivés de populations adultes. La validité convergente des mesures de QVLS particulières à la pédiatrie et basées sur les préférences des adultes doit être étudiée. Malgré ces limites, les chercheurs devraient idéalement utiliser des utilités pour les états de santé des enfants provenant d'un instrument générique particulier à la pédiatrie, plutôt que d'utiliser des utilités pour adultes. Si un instrument générique particulier à la pédiatrie n'est pas utilisé pour un état de santé de l'enfant, il convient de le justifier et de tester son incidence dans une analyse de sensibilité. L'utilisation d'instruments génériques est encouragée en pédiatrie, bien que les méthodes d'élicitation directe soient fréquemment utilisées. Les utilités générées par l'élicitation directe pour les états de santé sont sensibles au cadrage. Dans les cas où les utilités peuvent manquer en raison du jeune âge de l'enfant (p. ex., moins de cinq ans), les hypothèses utilisées doivent être explicites et justifiées. Les préférences doivent provenir d'une population générale, complétées par des évaluations d'enfants si elles sont disponibles. Les enquêtés-substituts (p. ex. les parents ou les fournisseurs de soins de santé) sont souvent nécessaires en pédiatrie parce que les méthodes d'évaluation peuvent être difficiles sur le plan cognitif ou nécessiter une compréhension de la lecture. Cependant, les réponses des enquêtés-substituts peuvent systématiquement différer de l'autoévaluation de l'enfant, la direction de la divergence étant difficile à prévoir.Note de bas de page 103 Les chercheurs doivent utiliser les utilités des enfants à partir d'instruments autodéclarés lorsque cela est possible, et préciser si des substituts sont utilisés. Par ailleurs, de nombreux vaccins sont administrés pendant la petite enfance ou l'enfance, dont certains préviennent des maladies de l'enfance et d'autres des maladies qui apparaissent à l'âge adulte. Les chercheurs doivent indiquer explicitement quels états de santé d'un modèle sont liés aux états de santé de l'enfant et quels sont ceux qui concernent les futurs états de santé de l'adulte. Dans les évaluations économiques où les adultes et les enfants sont modélisés, la cohérence dans l'utilisation de l'instrument à travers les âges est encouragée. Dans les cas où les données ne sont pas disponibles, comme pour les vaccins qui préviennent les maladies rares, les chercheurs doivent justifier la manière dont ils gèrent les limitations de données.
Dans ces lignes directrices, le concept de santé est basé sur la définition de l'Organisation mondiale de la santé : « La santé est un état de complet bien-être physique, mental et social, et ne consiste pas seulement en une absence de maladie ou d'infirmité ».Note de bas de page 5 L'ampleur de la définition rend nécessairement difficile l'évaluation de cette conceptualisation de la santé. Par conséquent, pour des raisons pragmatiques, des instruments génériques qui se concentrent principalement sur les attributs physiques et parfois mentaux sont utilisés pour saisir la QVLS de nombreuses maladies. Les chercheurs doivent évaluer et justifier les sources de données en fonction de leur pertinence, de leur crédibilité et de leur cohérence. Il s'agit notamment d'évaluer dans quelle mesure le système descriptif de l'instrument permet de saisir ce que les individus et les décideurs veulent mesurer pour la maladie infectieuse en question. La santé mentale, la fatigue et les sens sont des exemples de domaines qui peuvent ne pas être bien saisis de manière cohérente dans différents instruments. Lorsque l'instrument est réputé omettre des domaines importants ou les capturer de manière inadéquate, les chercheurs doivent envisager de compléter les instruments génériques par un instrument particulier à la maladie. Cela permet d'identifier les éventuelles omissions et l'ampleur de la divergence dans la mesure de la perte de santé entre les instruments génériques et ceux particuliers à une maladie.
Les données sur l'utilité en santé utilisées pour alimenter un modèle économique sont souvent tirées de la littérature publiée. Pour garantir la cohérence au sein d'un modèle, dans la mesure du possible, les évaluations de l'utilité sanitaire de tous les états de santé inclus dans le modèle doivent être obtenues à partir du même instrument et utiliser des poids de préférence obtenus à partir de la même population.Note de bas de page 104 Lorsque cela n'est pas possible, les chercheurs doivent envisager des compromis entre l'adéquation à l'objectif, la crédibilité et la cohérence des données disponibles. Dans ces cas, les chercheurs peuvent également envisager de regrouper les données sur l'utilité en santé en utilisant des techniques telles que la méta-analyse ou la méta-régression, bien que l'utilité de ces méthodes puisse être limitée par l'hétérogénéité considérable des méthodes d'évaluation et des populations étudiées.Note de bas de page 105 Les chercheurs doivent explorer l'incertitude des utilités en santé dans les analyses de sensibilité.
En plus d'inclure des données sur l'utilité en santé de la population visée par le programme de vaccination et de toutes populations susceptibles de subir des externalités liées au programme, les chercheurs doivent inclure des données sur l'utilité sanitaire des aidants naturels dans les cas où des effets d'entraînement potentiels ont été identifiés qui pourraient affecter l'état de santé de cette population. Une discussion sur des questions méthodologiques des effets des retombées liés aux AVAQ et un catalogue des valeurs fondées sur les préférences pour les effets de débordement peut être trouvée ailleurs.Note de bas de page 106 L'analyse ne doit pas inclure les données sur l'utilité en santé des soignants professionnels afin d'éviter un double comptage de leurs coûts et AVAQ. Ce point est abordé plus en détail au chapitre 12 sur l'analyse.
Le chapitre 10, Mesure et évaluation de la santé du document de l'ACMTS intitulé Lignes directrices de l'évaluation économique des technologies de la santé au Canada, 4e édition, propose une discussion plus détaillée sur la mesure et les données de la QVLS.Note de bas de page 1
Année de vie ajustée en fonction de la qualité dans les évaluations économiques réalisées dans la perspective sociétale
Il n'est pas certain que l'AVAQ tient compte uniquement des avantages pour la santé ou qu'elle saisisse également, implicitement ou explicitement, les effets non liés à la santé. Cette incertitude est particulièrement importante pour les ACU réalisées dans une perspective sociétale, car ces analyses portent non seulement sur les coûts et les résultats pour le système de santé, mais aussi sur les coûts et les résultats qui concernent des secteurs autres que la santé. Plus précisément, des incertitudes entourent la manière d'inclure les effets de la productivité et de la consommation dans l'estimation du RCED.
Comme indiqué ci-dessus, l'AVAQ est estimée à partir des données de survie et des données sur la QVLS. Les données sur la QVLS sont souvent obtenues à partir de domaines de santé compris dans les instruments courants de QVLS. Cependant, il n'est pas clair si, ou dans quelle mesure, les répondants considèrent implicitement des facteurs non liés à la santé lorsqu'ils évaluent ces états de santé. En particulier, on s'est intéressé à la mesure dans laquelle les répondants considèrent comment les changements de productivité et de consommation peuvent influencer leur QVLS, et à la mesure dans laquelle ces considérations sont implicitement incorporées dans l'évaluation par les répondants de leur état de santé. Selon les preuves disponibles, leur influence est limitée.Note de bas de page 107Note de bas de page 108Note de bas de page 109Note de bas de page 110
Si les individus devaient tenir compte des effets économiques de la productivité lorsqu'ils évaluent leur état de santé, alors l'inclusion des estimations pécuniaires de la productivité dans le numérateur de l'estimation du RCED, avec les coûts des autres ressources, entraîne un double comptage de ces effets.Note de bas de page 109 Le consensus actuel est que les changements de productivité et de revenu ne sont pas susceptibles d'être pris en compte dans les estimations de l'AVAQ.Note de bas de page 111 Note de bas de page 112 Cela justifie l'inclusion des coûts de productivité dans le numérateur de l'estimation du RCED.
De même, des questions ont été posées pour savoir si les personnes interrogées dans le cadre des évaluations de l'état de santé prennent en compte et valorisent la consommation non médicale, comme les vêtements et le logement. L'un des arguments avancés est que si la valeur d'utilité de cette consommation n'est pas (implicitement) saisie dans l'AVAQ, il serait incohérent d'inclure les changements de cette consommation dans les coûts de l'évaluation et, par conséquent, ces coûts devraient être exclus.Note de bas de page 110 Un autre argument veut qu'une consommation non médicale (p. ex. l'apport alimentaire quotidien) soit nécessaire pour rester en vie. Même si les répondants n'en tiennent pas compte dans leur évaluation des états de santé, il faut néanmoins l'inclure comme un coût. Cela serait encore plus évident si les répondants supposaient des niveaux de consommation habituels dans leurs réponses aux questions d'évaluation de l'état de santé. Le même argument s'applique aux autres consommations non médicales qui, dans une certaine mesure, peuvent également contribuer à la QVLS d'un individu.Note de bas de page 108
Contrairement aux résultats liés à la prise en compte par les répondants des changements de productivité dans leur évaluation des états de santé, les preuves donnent à penser que les répondants intègrent l'utilité de la consommation lorsqu'ils évaluent les états de santé.Note de bas de page 113 On peut en déduire que les améliorations de la santé peuvent entraîner une augmentation de l'utilité marginale de la consommation non liée à la santé. Bien que des recherches supplémentaires soient nécessaires pour corroborer ces résultats, ils justifient l'inclusion des coûts de consommation dans le numérateur de l'estimation du RCED.
En résumé, pour l'analyse de référence dans une perspective sociétale, les changements liés à la productivité et les coûts de la consommation non liée à la santé doivent être compris dans le numérateur de l'estimation du RCED. Davantage de précisions sur la quantification des coûts de la productivité et de la consommation figurent dans le chapitre 11, Utilisation et coût des ressources.
11. Utilisation et coût des ressources
Énoncés des Lignes directrices
- 11.1 Pour chaque analyse de référence, les chercheurs doivent relever, mesurer et valoriser de manière systématique toutes les ressources pertinentes, consommées ou économisées à la suite de l'administration ou de l'exécution du programme de vaccination, et en faire état.
- 11.2 Dans la mesure du possible, les chercheurs doivent évaluer des ressources pertinentes relevées pour tous les secteurs, sur le plan pécuniaire. Lorsque ce n'est pas possible, les chercheurs doivent présenter aux décideurs les ressources pertinentes qui ont été relevées dans l'inventaire des effets à prendre en considération dans l'évaluation économique des stratégies de vaccination.
- 11.3 L'utilisation et les coûts des ressources doivent être basés sur des sources canadiennes et refléter la ou les administrations d'intérêts (comme il est précisé dans le problème de décision). [Énoncé des lignes directrices de l'ACMTS, modifié]
- 11.4 Dans la valorisation et la monétisation des ressources, les chercheurs doivent choisir les sources de données les plus exactes quant au coût de renonciation selon la perspective de l'analyse. [Énoncé des lignes directrices de l'ACMTS, modifié]
- 11.5 Les chercheurs doivent mener une recherche exhaustive des sources de données disponibles pour informer l'utilisation des ressources et la valeur des coûts. Faire état des études retenues et des méthodes de sélection ou de regroupement des données. Les chercheurs doivent évaluer les sources utilisées pour les coûts des ressources en fonction de leur aptitude à l'emploi, de leur crédibilité et de leur cohérence. Décrire les compromis consentis entre ces critères et justifier les sources choisies.
Les programmes de vaccination peuvent entraîner à la fois une augmentation et une diminution de la consommation de ressources et de services. Ils sont liés à la fois à la mise en œuvre du programme de vaccination et à son exécution continue, ainsi qu'aux effets en aval du programme. La consommation des ressources peut toucher les personnes vaccinées, la population vulnérable pour la maladie en question lorsque le programme de vaccination est associé à des externalités, et la population qui subit les retombées (comme les aidants naturels). Par ailleurs, les ressources consommées à la suite des programmes de vaccination peuvent relever du secteur du système de santé ou de l'extérieur de celui-ci. Les chercheurs doivent utiliser le tableau d'inventaire des effets à prendre en considération dans l'évaluation économique des stratégies de vaccination pour déterminer systématiquement toutes les ressources et tous les services potentiels associés au programme de vaccination envisagé. Une fois que l'éventail des ressources et des services résultant d'un programme de vaccination a été précisé, les chercheurs doivent déterminer lesquelles des ressources consommées peuvent être mesurées et évaluées sur le plan pécuniaire.Note de bas de page 114Note de bas de page 115 Lorsque les ressources ou les services ne sont pas liés à la production ou à la consommation, ils peuvent être considérés comme des coûts de transfert - c'est-à-dire le transfert financier d'une personne ou d'un groupe de personnes dans la société à une autre. Les coûts de transfert sont examinés à la fin du chapitre, après l'examen de l'utilisation et des coûts des ressources clés ci-dessous.
Coûts du système de santé
Pour l'analyse de cas de référence dans la perspective du système de santé, les chercheurs doivent déterminer et inclure toutes les ressources au sein du système de santé financé à même les fonds publics qui sont consommées par l'exécution du programme de vaccination, ainsi que les ressources qui sont consommées ou économisées grâce à sa mise en œuvre. Tous les coûts du système de santé encourus sur l'horizon temporel du modèle doivent être compris. Comme indiqué précédemment, aux fins des présentes lignes directrices, le terme « système de santé » désigne à la fois les services cliniques de soins de santé et la Santé publique; la Santé publique est en lettres majuscules pour mieux la distinguer des « soins de santé publics ».
Coûts des soins de santé
Lorsqu'ils attribuent des coûts unitaires locaux aux ressources qui ont été déterminées comme pertinentes pour le problème décisionnel modélisé, les chercheurs doivent consulter la deuxième édition du Guide pour l'évaluation des coûts des ressources en soins de santé dans le contexte canadien.Note de bas de page 116 Le document fournit des recommandations clés et des sources de données pour déterminer, évaluer et mesurer les coûts au sein du système de santé canadien. Pour les analyses menées au sein d'une province ou un territoire ou entre plusieurs provinces ou territoires, les variations dans le financement public de ressources et de services particuliers doivent être indiquées. Les chercheurs doivent indiquer si un seul ensemble de prix est utilisé ou si des ensembles de prix entre plusieurs provinces ou territoires sont appliqués et les méthodes utilisées pour attribuer des ensembles de prix aux données de plusieurs provinces ou territoires. Pour une analyse du point de vue du système de santé national, il faudrait idéalement utiliser des sources à l'échelle du Canada. Lorsque cette information n'est pas disponible, les chercheurs peuvent utiliser les coûts d'une province ou d'un territoire canadien représentatif ou une moyenne pondérée des coûts (coûts encourus par les administrations canadiennes pondérés par la proportion d'utilisation au Canada représentée par la province ou le territoire). Lorsque les données canadiennes ne sont pas disponibles, les chercheurs peuvent consulter des experts ou utiliser des estimations de coûts pour des interventions similaires ou nouvelles, et s'inspirer de sources internationales. Il convient de réaliser des analyses de scénarios pour tester la sensibilité de ces autres sources de données sur les résultats de l'évaluation économique.
Parmi les coûts des soins de santé énumérés dans le tableau d'inventaire des effets, les coûts des soins professionnels et les coûts des soins de santé futurs sont décrits plus en détail afin de compléter les directives canadiennes sur l'établissement des coûts.Note de bas de page 116
Soins professionnels
Les personnes qui ont besoin d'un soignant peuvent recevoir ces soins soit d'un soignant professionnel tel qu'une infirmière ou une infirmière auxiliaire qui est embauchée pour effectuer ces services, soit d'un aidant naturel, généralement un membre de la famille. Le temps des soignants professionnels doit être évalué au taux de salaire horaire qui serait versé à une personne qui effectue ce service. Les coûts des soins formels peuvent être ou non pris en charge par le système de santé financé à même les fonds publics, selon la nature précise de ces coûts et la province ou le territoire concerné. Par conséquent, les coûts des soins professionnels apparaissent dans le tableau de l'inventaire des impacts à la fois sous la colonne « coûts du système de santé financés par les pouvoirs publics » et sous la colonne « coûts des soins de santé non financés par le système de santé ». La question des soins informels est abordée plus loin dans le chapitre Productivité.
Coûts futurs des soins de santé
Pour les programmes de vaccination qui confèrent un avantage sur le plan de la survie par rapport aux comparateurs pris en compte dans l'évaluation économique, les chercheurs doivent inclure dans les analyses du cas de référence les coûts futurs des soins de santé, qu'ils soient liés ou non à l'infection et à la maladie en question. Cette recommandation est étayée par les considérations suivantes : 1) il y a un coût de renonciation associé aux interventions visant à prolonger la vie puisqu'elles augmentent les dépenses de santé futures de ces personnes, des dépenses qui auraient pu être utilisées pour répondre aux besoins de santé d'autres personnes 2) il est souvent difficile de distinguer les coûts liés des coûts non liés, comme dans le cas de différentes maladies dont les voies physiologiques se chevauchent (p. ex. le diabète et les coronaropathies), ce qui peut conduire à des décisions arbitraires quant aux coûts qui sont liés et non liés; et 3) la cohérence interne : les avantages liés aux dépenses médicales futures sont déjà compris dans les ACU par l'intermédiaire d'estimations de la survie et de la qualité de vie, et sont basés sur l'hypothèse que l'individu reçoive des soins médicaux futurs, qu'ils soient liés ou non à la maladie en question.Note de bas de page 108Note de bas de page 114Note de bas de page 117Note de bas de page 118
L'exclusion des coûts futurs conduit à des estimations de coûts différentiels et des estimations du RCED plus faibles pour les interventions qui prolongent la vie, et peut les faire paraître plus attrayantes économiquement que celles qui améliorent la qualité de vie. Cependant, l'inclusion des coûts futurs augmente les estimations de coûts différentiels et les RCED pour les interventions visant à prolonger la vie, ce qui conduit dans certains cas à ce qu'une option de non-intervention (c.-à-d. où les patients ne survivent pas) soit plus rentable que de fournir un traitement pour une maladie.Note de bas de page 119 Dans certains cas, même des interventions de maintien en vie relativement peu coûteuses chez des patients dont les coûts de soins continus sont élevés peuvent ne pas être rentables lorsque les coûts futurs sont pris en compte dans une évaluation économique.Note de bas de page 120 Les chercheurs doivent présenter les résultats et les coûts de manière désagrégée afin que les décideurs sachent comment les différents éléments compris dans l'analyse contribuent au rapport coût-efficacité global du programme de vaccination. Les chercheurs doivent présenter : 1) les résultats sanitaires attendus du programme de vaccination et des comparateurs; 2) les coûts directs du système de santé résultant du programme de vaccination et des comparateurs, mais à l'exclusion des coûts des soins futurs; et 3) l'augmentation attendue des coûts des soins continus résultant de l'amélioration de la survie pour le programme de vaccination et les comparateurs.Note de bas de page 120
Les estimations des coûts futurs des soins de santé peuvent être obtenues à partir des données publiées par les Tendances des dépenses nationales de santé de l'Institut canadien d'information sur la santé.Note de bas de page 121 Dans les situations où des estimations de coûts sont nécessaires pour des populations dont les coûts de soins continus sont élevés (p. ex. les patients sous dialyse, les receveurs de transplantation d'organe plein),Note de bas de page 122Note de bas de page 123 les chercheurs devront peut-être consulter les ouvrages médicaux publiés pour obtenir ces estimations.
Coûts de santé publique
Les coûts de santé publique peuvent représenter une part importante des coûts des programmes de vaccination et de gestion des maladies infectieuses. Il est nécessaire de les quantifier précisément pour garantir que les résultats des évaluations économiques des programmes de vaccination sont valides et conduisent à des décisions de financement optimales. Les coûts de santé publique peuvent être classés en deux catégories : les coûts liés aux programmes et les coûts liés aux interventions. Les coûts liés au programme sont les coûts de mise en œuvre, d'exécution et de maintien du programme. Ils comprennent les coûts des campagnes de santé publique et des activités de promotion de la santé, les coûts de transaction liés à l'introduction de nouveaux vaccins ou au passage d'un vaccin à un autre, et les coûts liés au dépistage dans la population, à la surveillance épidémiologique, à la recherche des contacts, aux enquêtes sur les cas et aux enquêtes sur les épidémies. Les éléments précis à prendre en compte dans la quantification de ces coûts sont les coûts de personnel, les frais généraux, les frais de déplacement et les autres coûts administratifs et coûts liés au service.Note de bas de page 116Note de bas de page 124 Les éléments précis à prendre en compte dans la quantification des coûts des éclosions de maladie comprennent les tests sérologiques en laboratoire; le temps du personnel consacré à la recherche des contacts, au dépistage des symptômes, aux déplacements, à la surveillance et au suivi; les vaccins ou les doses d'immunoglobulines pour la prophylaxie post-exposition et les coûts administratifs correspondants.Note de bas de page 125Note de bas de page 126Note de bas de page 127Note de bas de page 128 Les coûts liés aux interventions sont les coûts des doses de vaccin, de la distribution (p. ex. le transport et le stockage au froid) et de l'administration du vaccin, y compris les pertes et les fournitures auxiliaires nécessaires. Les chercheurs doivent présenter les coûts liés aux différents aspects de la mise en œuvre et de l'exécution continue du programme de vaccination de manière désagrégée. Par ailleurs, les chercheurs doivent préciser les différents niveaux d'intensité de la stratégie de mise en œuvre, ce qui est particulièrement pertinent pour les campagnes de santé publique et les activités de promotion de la santé par exemple, car elles peuvent produire différents niveaux d'avantages.
Étant donné la rareté des données publiées sur l'utilisation et les coûts de santé publique liés aux programmes dans le contexte canadien, les chercheurs devront peut-être faire appel aux données obtenues auprès des autorités en matière de santé publique locales ou des ministères provinciaux de la Santé par le biais de communications personnelles. Bien que les coûts des autorités en matière de Santé publique ou des ministères provinciaux soient propres à chaque province ou territoire, ils peuvent être généralisables à d'autres régions. Pour déterminer l'applicabilité des données d'un territoire de compétence à un autre, les chercheurs doivent tenir compte de facteurs tels que les similitudes géographiques, les caractéristiques de la population et les caractéristiques épidémiologiques.
On dispose de peu de données canadiennes sur l'utilisation et le coût des ressources de santé publique dans le cadre d'interventions. Certains organismes provinciaux de santé publique, comme l'Institut national de santé publique du Québec,Note de bas de page 129 publient en ligne les résultats de leurs travaux, qui peuvent inclure des données de surveillance épidémiologique et de coûts pertinentes pour l'évaluation économique d'un programme de vaccination. Le prix réel des doses de vaccin payé par les gouvernements est confidentiel. Les chercheurs doivent utiliser le prix courant du fabricant dans les analyses de cas de référence et effectuer des analyses de sensibilité déterministes en utilisant des prix réduits plausibles. Voir le chapitre 13, Incertitude, pour une discussion plus approfondie. Les chercheurs doivent également tenir compte des éléments de coût liés à l'administration des doses de vaccin, qui peuvent varier considérablement en fonction du lieu d'administration. Par exemple, en Alberta, l'administration communautaire du vaccin contre le VPH est considérablement plus coûteuse que l'administration en milieu scolaire.Note de bas de page 130 Les ressources et les services liés à la fourniture d'un accès culturellement sûr aux soins de santé et au matériel de communication du programme de vaccination doivent également être pris en compte lorsqu'ils sont applicables.
Coûts des soins de santé non financés par le système de santé
Certains services associés aux programmes de vaccination peuvent ne pas être remboursés ou financés par le système de santé publique. Les services qui sont exclus du système de santé publique peuvent varier selon les administrations ou les régions. Il s'agit notamment des services de soins de longue durée, des soins infirmiers privés, des traitements médicamenteux pour les personnes qui ne sont pas couvertes par un programme d'assurance médicaments financé par l'État, des médicaments sans ordonnance, ainsi que des frais accessoires liés à des éléments tels que les quotes-parts des assurances privées, les soins dentaires et ophtalmologiques, les appareils fonctionnels, la physiothérapie et autres. Ces coûts peuvent être assumés par des régimes d'assurance privés, par les particuliers ou par les deux à la fois. Quel que soit le mode de prise en charge de ces coûts, ils doivent être quantifiés et inclus dans les coûts différentiels et dans le rapport coût-efficacité différentiel (le cas échéant) pour l'analyse de cas de référence dans une perspective sociétale.
Coûts des systèmes autres que celui des soins de santé
Les chercheurs doivent également déterminer toutes les ressources consommées du fait de la mise en œuvre ou de l'exécution continue du programme de vaccination qui ne relèvent pas du système de santé publique, et quantifier les coûts correspondants. Par exemple, les secteurs autres que celui de la santé pertinents aux fins de l'analyse du cas de référence dans une perspective sociétale pourraient inclure : les coûts directs à la charge des patients (p. ex. les quotes-parts, les frais de transport, les frais associés aux soignants privés), les pertes de temps de travail rémunéré et non rémunéré, la consommation non médicale et les services non financés par d'autres secteurs, notamment l'éducation, les services sociaux et l'environnement. Des conseils sur la détermination des ressources et la quantification des coûts pour les secteurs autres que celui des soins de santé sont présentés ci-après.
Frais directs assumés de leur poche
Les évaluations économiques des programmes de vaccination doivent inclure des estimations des frais directs à la charge des patients (p. ex., les frais de transport et d'hébergement). Les coûts de transport comprennent les coûts liés aux transports en commun, y compris l'accès exempt d'obstacles à des transports entièrement accessibles si nécessaire, les taxis, l'utilisation de véhicules personnels et les frais de stationnement.Note de bas de page 131
Pertes de productivité
Les pertes de productivité (également appelées coûts de productivité) sont des pertes de production associées au temps productif consacré au travail rémunéré ou au travail non rémunéré (par exemple, le bénévolat, l'aide, le tutorat), y compris la production domestique (par exemple, la cuisine, le nettoyage, les courses, l'éducation des enfants).Note de bas de page 114
Les chercheurs doivent examiner les effets des programmes de vaccination sur la productivité des personnes et des soignants et, le cas échéant, sur les conséquences macroéconomiques. La vaccination peut améliorer la productivité par deux moyens distincts : 1) une augmentation de la productivité du travail rémunéré et non rémunéré liée soit à la prévention de la maladie, soit à la diminution de la gravité de la maladie chez les personnes vaccinées; et 2) une augmentation de la productivité des soignants liée à la diminution des besoins en soins des personnes malades.Note de bas de page 8Note de bas de page 11Note de bas de page 132 La productivité peut diminuer en raison des congés rémunérés et non rémunérés pour assister ou accompagner des personnes à des rendez-vous de vaccination. Lorsque les gains de productivité des interventions visant à prolonger la vie sont inclus dans une analyse du point de vue de la société, ils peuvent atténuer ou compenser l'augmentation des coûts différentiels due à l'augmentation de la consommation future de soins de santé chez les survivants. Chaque type de perte de productivité figurant dans le tableau d'inventaire des effets est décrit plus en détail ci-dessous.
Travail rémunéré et non rémunéré
Les deux principales méthodes d'évaluation du temps de travail rémunéré perdu sont celles du capital humain et du coût de friction. La méthode du capital humain est fondée sur le coût du temps productif perdu, tandis que l'approche du coût de friction tente d'estimer les pertes de production globales pour la société, en supposant le remplacement des travailleurs malades sur le marché du travail.Note de bas de page 114Note de bas de page 133Note de bas de page 134Note de bas de page 135
La méthode du capital humain est couramment utilisée pour évaluer la production perdue. Elle nécessite habituellement d'estimer le temps de travail rémunéré perdu et les taux de rémunération moyens des personnes concernées. On peut donc la considérer comme une estimation de la perte de production (ou de revenu) d'un point de vue individuel, due à une maladie, à une invalidité ou au décès. Comme la méthode du capital humain ne tient pas compte des mécanismes de remplacement sociétaux, en particulier pour les périodes d'absence plus longues (p. ex. en cas d'invalidité ou de décès prématuré), elle surestime probablement le coût réel de la perte de production d'un point de vue sociétal.Note de bas de page 136 Il s'agit d'une considération particulièrement importante dans les situations où un programme de vaccination pourrait permettre d'éviter le décès d'un enfant ou un handicap à vie.
L'approche du coût de friction, quant à elle, tente de quantifier la perte de productivité au niveau sociétal en partant du principe que l'absence d'un employé se limite à la période nécessaire à l'organisation pour le remplacer et retrouver le niveau de productivité initiale (p. ex. en cas de chômage) ou par du capital.Note de bas de page 133 Cela implique qu'après une certaine « période de friction », les pertes de production cessent de se produire d'un point de vue sociétal. On a estimé que les conséquences macroéconomiques des changements dans l'offre de main-d'œuvre et les prestations d'assurance-emploi sont faibles pour les programmes de soins de santé typiques. L'application de cette méthode nécessite des renseignements plus détaillés sur les périodes d'absence, le bassin de main-d'œuvre et la période de friction pertinente dans un pays ou une province.Note de bas de page 135
Bien que ces deux méthodes se concentrent principalement sur la valorisation de la production perdue dans le contexte du travail rémunéré, les changements de productivité liés au travail non rémunéré doivent également être pris en compte. La perte de productivité dans le contexte du travail non rémunéré peut être mesurée en évaluant les heures perdues avec une valeur appropriée. Les estimations du (changement de) temps productif dans le travail non rémunéré pour la population concernée peuvent être difficiles à obtenir dans certains cas.Note de bas de page 137 Outre l'utilisation d'estimations générales provenant de sources existantes, on peut avoir recours à des questionnaires pour estimer ces changements.Note de bas de page 138
Les chercheurs doivent mesurer la variation totale du temps productif découlant du programme de vaccination, qu'il s'agisse de travail rémunéré ou non rémunéré. Les chercheurs doivent tenir compte des pertes de temps productif d'un individu liées à l'obtention d'un vaccin, à la recherche d'un traitement, à la maladie, à l'invalidité et au décès des personnes vaccinées ou autrement touchées. Les changements dans la productivité associés aux programmes de vaccination devraient être quantifiés en utilisant la méthode du capital humain. C'est l'approche la plus couramment recommandée dans les directives pharmacoéconomiques de plusieurs pays du monde,Note de bas de page 139 et elle permet d'accroître la comparabilité entre les évaluations économiques des programmes de vaccination entreprises dans différentes régions.
Pour l'analyse de référence dans une perspective sociétale, les chercheurs doivent inclure la période complète au cours de laquelle les personnes touchées subiront des pertes de production rémunérées. Ces pertes doivent être évaluées en fonction du revenu moyen et du nombre d'heures travaillées selon l'âge, d'après les données de Statistique Canada (« Revenu des particuliers selon le groupe d'âge, le sexe et la source de revenu, Canada, provinces et certaines régions métropolitaines de recensement » et « Moyenne des heures habituellement et effectivement travaillées durant la semaine de référence selon le genre de travail [temps plein et temps partiel], données annuelles »),Note de bas de page 140Note de bas de page 141 combinés à la probabilité, selon la maladie, qu'une personne participe à la population active. L'utilisation du même taux de salaire pour les deux sexes est une correction du biais de mesure, car les femmes sont en moyenne moins bien payées que les hommes pour le même travail.Note de bas de page 142 Cette recommandation vise à éviter que les problèmes de discrimination existant dans la société ne se traduisent par des décisions en matière de politique de santé.
Dans la plupart des cas, des considérations d'équité se poseront pour savoir si et comment le temps productif est valorisé. S'il est valorisé de manière différentielle en fonction d'attributs tels que l'âge, le sexe ou l'état de santé, les résultats d'une évaluation économique pourraient favoriser les groupes ayant le plus grand potentiel de revenus et désavantager d'autres groupes tels que les enfants qui ne travaillent pas ou les personnes souffrant de handicaps ou de graves problèmes de santé qui les empêchent d'occuper des emplois à haut revenu.Note de bas de page 114 Dans ces situations, les chercheurs doivent effectuer une analyse de sensibilité supplémentaire en utilisant le revenu moyen et le nombre moyen d'heures travaillées à temps plein pour tous les Canadiens, selon les données de Statistique Canada.Note de bas de page 140Note de bas de page 141Bien que la mesure de ces pertes soit imparfaite et biaisée en faveur des hauts salaires, cette approche révèle les pertes d'efficience que les responsables des politiques doivent être prêts à accepter chaque fois qu'ils choisissent une option de production neutre par rapport aux caractéristiques individuelles.
Pour tenir compte de la surestimation probable des pertes de production associées à l'approche du capital humain, les chercheurs doivent inclure une analyse de sensibilité supplémentaire avec une approximation naïve des coûts de friction. L'analyse de sensibilité doit donc prendre en compte les changements de productivité pour une seule année. Après un an, les variations de production sont remises à zéro. Le revenu annuel moyen et le nombre annuel moyen d'heures travaillées pour l'ensemble des Canadiens devraient être utilisés pour cette analyse basée sur les données de Statistique Canada.Note de bas de page 140Note de bas de page 141 L'analyse de sensibilité permettra aux décideurs d'évaluer l'incidence de la méthode d'évaluation sur les résultats de l'évaluation économique.
Bien que les pertes de productivité puissent découler à la fois de l'absentéisme (temps d'arrêt de travail) et du présentéisme (continuer à travailler, mais en accusant une productivité réduite), les chercheurs ne sont pas tenus de tenir compte des effets du présentéisme dans leurs estimations de la perte de productivité dans l'analyse de référence. Il est souvent difficile de collecter ces informations étant donné qu'elles nécessitent des données d'enquête auprès des personnes concernées et que le souvenir peut être subjectif dans de nombreux cas.Note de bas de page 138Note de bas de page 143
La perte de production non rémunérée doit être évaluée en estimant les heures perdues de travail non rémunéré et en les évaluant selon la méthode du coût de remplacement (décrite ci-dessous). Bien que le travail non rémunéré puisse différer en matière de tâches effectuées et de compétences requises, pour l'analyse du cas de référence, les heures perdues doivent être évaluées en utilisant le taux de salaire d'un professionnel. Les chercheurs doivent exclure les coûts liés à la perte de temps de loisirs de l'évaluation économique des programmes de vaccination.
Productivité des aidants naturels
Les personnes qui ont besoin d'un aidant peuvent recevoir ces soins soit d'un aidant professionnel, soit d'un aidant naturel, généralement un membre de la famille. Deux approches ont été proposées pour évaluer le temps des aidants naturels : 1) l'approche du coût de remplacement et 2) l'approche du coût de renonciation. L'approche du coût de remplacement repose sur le coût estimé de l'embauche d'un aidant rémunéré si les soins ne peuvent pas être prodigués par un aidant naturel. L'approche du coût de renonciation est basée sur le coût du temps productif déplacé qui résulte du temps passé à fournir des soins informels.Note de bas de page 144 Étant donné que les personnes peuvent recevoir à la fois des soins formels et informels, les chercheurs doivent utiliser l'approche du coût de remplacement pour évaluer le temps des aidants pour l'analyse de référence de la perspective sociétale. Ces estimations peuvent être utilisées parallèlement aux estimations des retombées potentielles sur la santé des aux soins informels, exprimées en années de vie ajustées par la qualité (AVAQ) des aidants.Note de bas de page 145
Conséquences macroéconomiques
Bien qu'il soit peu probable que la plupart des programmes de vaccination aient des répercussions macroéconomiques importantes, ceux qui sont conçus pour prévenir les pandémies généralisées telles que la pandémie de COVID-19 de 2020 causée par le virus SRAS-CoV-2 pourraient atténuer les conséquences graves. L'incidence macroéconomique comprend les chocs de l'offre de main-d'œuvre et les fermetures généralisées d'entreprises, qui peuvent affecter les bassins de main-d'œuvre et les taux de participation à la population active, ainsi que les changements dans les préférences de consommation des ménages.Note de bas de page 146 Dans les cas où les coûts macroéconomiques sont importants, les chercheurs doivent discuter des effets de manière qualitative. Les chercheurs peuvent également envisager d'aborder les coûts de manière quantitative en faisant appel à des modélisateurs macroéconomiques et à d'autres experts.
Dans l'ensemble, les recommandations sur la productivité préconisent la transparence. La stratification des sous-groupes en plus d'une analyse globale peut révéler tout effet important dû à l'hétérogénéité. En outre, les recommandations visent à fournir aux décideurs plusieurs analyses de sensibilité et le choix de la manière de pondérer les gains d'efficacité dans divers sous-groupes (par exemple, les hauts salariés).
Consommation non médicale
La consommation non médicale représente les dépenses consacrées aux éléments non liés à la santé qui contribuent au bien-être global. Cela comprend les dépenses financières personnelles et la consommation de biens et services publics, comme l'accès à de l'eau potable et à des routes sécuritaires.Note de bas de page 108Note de bas de page 114 Les chercheurs doivent inclure les coûts de consommation chaque fois qu'ils sont modifiés par le programme de vaccination.
Ils doivent utiliser les données de Statistique Canada sur les dépenses des ménages comme source d'information pour la consommation non médicale (Tableau : 11-10-0222-01, auparavant CANSIM 203-0021, « Dépenses des ménages, Canada, régions et provinces »).Note de bas de page 147 Afin d'obtenir une estimation de la consommation non médicale, les chercheurs doivent exclure la consommation de santé de la consommation totale. Pour produire les estimations de la consommation individuelle, il faut ajuster les estimations de la consommation des ménages à l'aide d'une échelle d'équivalence d'Oxford modifiée, afin que la consommation reflète la taille du ménage.Note de bas de page 148 L'ajustement reflète le fait que les ménages d'une personne auraient une consommation par personne plus élevée que les ménages de plusieurs personnes. L'échelle d'équivalence Oxford modifiée attribue une valeur de 1 unité de consommation au premier adulte, de 0,5 à chaque adulte supplémentaire et de 0,3 à chaque enfant de moins de 14 ans. De plus amples informations sur les échelles d'équivalence sont disponibles dans le Framework for Statistics on the Distribution of Household Income, Consumption and Wealth de l'OCDE (pages 67 à 68).Note de bas de page 149 Pour les programmes de vaccination qui entraînent des changements dans la consommation, les chercheurs doivent soustraire les estimations individuelles de la consommation des estimations individuelles de la productivité pendant la période concernée. Pour assurer la cohérence entre les estimations de la productivité et de la consommation, les estimations de la consommation ne doivent pas être stratifiées par sexe pour les analyses du cas de référence.
Études
Les programmes de vaccination peuvent influer sur les résultats scolaires en prévenant les maladies qui entraînent des morbidités graves qui, à leur tour, pourraient se répercuter sur le niveau de réussite scolaire d'un individu. Par exemple, une étude danoise a révélé que les enfants ayant souffert d'une méningite bactérienne présentaient des niveaux inférieurs de réussite scolaire et d'autosuffisance économique à l'âge adulte.Note de bas de page 150
Des niveaux d'éducation plus élevés sont associés à une plus grande probabilité de participation au marché du travail et à des revenus plus élevés sur le marché du travail.Note de bas de page 151Note de bas de page 152 Au Canada, on estime que chaque année supplémentaire de scolarité augmente les revenus à vie d'environ 11 à 12 %. En supposant que la diminution du niveau d'éducation d'un individu entraîne une diminution similaire des gains au cours de la vie, on estime que chaque mois de perte d'éducation se traduira par une baisse d'environ 1 % du revenu à vie.Note de bas de page 153 Les changements de revenus liés à la réussite scolaire doivent être pris en compte dans les estimations de la productivité perdue (ou gagnée) et les chercheurs doivent s'assurer que ces coûts ne sont pas comptés deux fois lorsqu'ils examinent les effets des programmes de vaccination sur l'éducation. Bien que l'on reconnaisse que les méthodes sont encore en émergences, il est utile de présenter aux décideurs les effets sur le secteur de l'éducation.
Outre les effets sur les résultats scolaires et la productivité du marché du travail, les programmes de vaccination peuvent avoir des effets directs sur le secteur de l'éducation. Par exemple, les enfants qui ont souffert d'une méningite bactérienne peuvent présenter des troubles cognitifs, une perte auditive, des crises d'épilepsie et des difficultés d'apprentissage,Note de bas de page 154 qui peuvent nécessiter des ressources en éducation spécialisée à l'école. Les commissions scolaires et les écoles peuvent également investir dans des programmes de vaccination ainsi que dans des programmes auxiliaires visant, par exemple, à améliorer la qualité de l'air intérieur pendant la pandémie de la COVID-19.
Les chercheurs doivent tenir compte des résultats potentiels liés à l'éducation et des effets directs sur le secteur de l'éducation qui pourraient résulter du programme de vaccination et des comparateurs envisagés. Dans la mesure du possible, ils doivent les monnayer pour les inclure dans l'estimation du rapport coût-efficacité différentiel (RCED). En ce qui concerne les résultats qui peuvent être difficiles à monétiser (comme les perturbations des résultats d'apprentissage découlant de l'administration du vaccin en milieu scolaire, les maladies et les handicaps pédiatriques ou le décès/le handicap d'un membre de la famille proche), les chercheurs doivent néanmoins les déterminer et les inclure dans l'inventaire des effets à prendre en considération dans l'évaluation économique des stratégies de vaccination, afin que les décideurs puissent en tenir compte.
Services sociaux et services communautaires
Les programmes de vaccination peuvent avoir une incidence sur les services sociaux, les services communautaires et les services à l'enfance et à la jeunesse en prévenant les maladies qui entraînent de graves morbidités. Les services sociaux incluent notamment le soutien aux personnes handicapées, les programmes de sensibilisation, le répit pour les familles et les programmes visant à améliorer l'accès aux programmes de vaccination. Les chercheurs doivent déterminer (et si possible monnayer) les conséquences des services sociaux.
Environnement
Les programmes de vaccination et les comparateurs pris en compte dans l'analyse peuvent avoir des impacts environnementaux liés à la fabrication ou à la distribution des doses de vaccin, ainsi qu'à la mise en œuvre du programme. Par exemple, il a été démontré que les vaccins réduisent l'utilisation des antibiotiques,Note de bas de page 155Note de bas de page 156 ce qui peut faire baisser la quantité de résidus d'antibiotiques provenant de sources telles que les ménages, l'industrie pharmaceutique et les hôpitaux dans les eaux usées, connues comme un réservoir d'organismes résistants aux antibiotiques.Note de bas de page 157
Les conséquences environnementales peuvent être déterminées et incluses dans l'inventaire des effets à prendre en considération dans l'évaluation économique des stratégies de vaccination afin que les décideurs puissent en tenir compte. Dans la mesure du possible, elles doivent être monnayées, bien que cela soit parfois difficile à faire. Par exemple, des recherches supplémentaires sont nécessaires pour déterminer la valeur sociale de la consommation d'antibiotiques et de la prévalence de la résistance aux antibiotiques. D'autre part, il existe d'autres coûts environnementaux pour la société qui peuvent être plus facilement évalués. Par exemple, dans les cas où l'intervention permet de prolonger la vie, la consommation de carbone ainsi que les déchets alimentaires et non alimentaires peuvent être inclus dans l'analyse du cas de référence de la perspective sociétale. Des données sur la consommation de carbone sont disponibles au Canada (notamment par l'intermédiaire du Hot or Cool Institute et de la Direction des indicateurs canadiens de durabilité de l'environnement du gouvernement du Canada).Note de bas de page 158Note de bas de page 159 Les données sur les déchets alimentaires et les coûts municipaux de la gestion des déchets sont disponibles au Canada (notamment par le biais de Community Research Connections Research et d'Environnement et Changement climatique Canada, respectivement) et peuvent être converties en coûts par kilogramme.Note de bas de page 160Note de bas de page 161
Autres domaines
Les chercheurs doivent tenir compte des autres secteurs susceptibles d'offrir des services ou des programmes pertinents pour des programmes de vaccination en particulier. Il peut s'agir, par exemple, du secteur du logement (p. ex. les changements de type de logement ou les adaptations du logement nécessaires en raison des handicaps fonctionnels résultant de l'infection, ou pour améliorer la ventilation/réduire l'encombrement afin de réduire la transmission de l'infection).
Coûts de transfert
De manière pragmatique, les chercheurs peuvent assimiler les coûts aux prix lorsqu'ils paramètrent les évaluations économiques des programmes de vaccination, à moins que des informations ne permettent de faire la distinction - auquel cas, les chercheurs doivent utiliser les coûts. Le coût est le montant requis pour produire, acquérir, distribuer ou vendre des ressources et des services, tandis que le prix est la somme d'argent attendue en échange des ressources ou des services. Les marges bénéficiaires proviennent de la différence entre le prix facturé aux payeurs et les coûts encourus, et représentent les coûts de transfert. Les coûts de transfert s'appliquent à la fois à la perspective du système de santé publique et à la perspective sociétale. Prenons l'exemple du prix d'un vaccin, qui doit normalement couvrir les coûts de recherche et de développement, les coûts de production marginaux ou moyens, les coûts de distribution et une marge bénéficiaire. Les composantes exactes du coût sont souvent inconnues des chercheurs et des décideurs; il est donc impossible de faire la distinction entre le coût et le prix. En outre, on ne sait pas comment les coûts de transfert peuvent être redistribués ou réinvestis. Par exemple, une partie du transfert financier des autorités sanitaires au fabricant pour l'achat de doses de vaccin (profit) peut être utilisée par le fabricant de n'importe quelle manière pour produire ultérieurement une utilité ou du bien-être. Le contrefactuel est que les autorités sanitaires conservent ce qui aurait été le bénéfice du fabricant pour l'utiliser ensuite, à nouveau, de n'importe quelle manière pour produire une utilité ou du bien-être. L'utilité générée par le réinvestissement du fabricant ou celui des autorités sanitaires est inconnue. Une discussion plus approfondie sur les coûts de transfert en relation avec la tarification des vaccins se trouve au chapitre 14 sur l'équité dans la mesure où ils sont liés aux perceptions de l'équité en matière de santé et de la justice sociale.
12. Analyse
Énoncés des Lignes directrices
- 12.1 Les rapports coûts-efficacité différentiels (RCED) et, lorsque cela est utile pour l'interprétation, les avantages financiers nets ou les avantages nets pour la santé, doivent être calculés pour les deux analyses de référence.
- 12.2 « Si l'analyse englobe plus de deux interventions, effectuer une analyse séquentielle du rapport coût-efficacité dans les règles standards de l'estimation du RCED, y compris l'exclusion des interventions dominées. » [Énoncé des lignes directrices de l'ACMTS]
- 12.3 Autant que possible, il faut générer les valeurs attendues des coûts et des résultats de manière probabiliste afin de refléter l'incertitude globale des paramètres du modèle.
Les chercheurs doivent générer deux séries d'estimations des valeurs attendues pour les coûts liés à chaque intervention considérée dans l'évaluation économique : l'une pour l'analyse de cas de référence de la perspective du système de santé financé par les fonds publics, et l'autre pour l'analyse de cas de référence de la perspective sociétale. Une estimation des valeurs prévues des résultats (c'est-à-dire les AVAQ) doit être générée pour servir aux deux analyses de cas de référence.
Les coûts et les résultats (c'est-à-dire les AVAQ), lorsque possible, doivent être produits de manière probabiliste afin que les valeurs attendues reflètent l'incertitude globale des paramètres du modèle. Dans la plupart des cas, l'analyse probabiliste prendra la forme d'une simulation de Monte-Carlo, qui consiste à appliquer à chaque paramètre une estimation ponctuelle, une étendue et une distribution de probabilité appropriées. Les chercheurs peuvent se référer à d'autres conseils sur les distributions de probabilité à utiliser.Note de bas de page 162 Chaque simulation doit produire des estimations des coûts moyens et de l'efficacité moyenne pour chaque comparateur, ainsi que des estimations des coûts différentiels et de l'efficacité différentielle. Toutes les valeurs, y compris les estimations différentielles, doivent être rapportées avec des intervalles de confiance ou crédibles à 95 % comme indicateurs de précision. Ces intervalles peuvent être obtenus à partir des limites de 2,5 % et 97,5 % des simulations générées. Il peut également être approprié d'utiliser des indicateurs de précision supplémentaires si la distribution des résultats incertains n'est pas approximativement gaussienne. Dans les cas où les analyses probabilistes ne sont pas possibles, les estimations de ces valeurs doivent être générées de manière déterministe. Ce scénario est le plus susceptible de se produire lorsque la puissance de calcul requise pour une analyse probabiliste est un facteur limitant, surtout pour les modèles axés sur les agents.
Les coûts et les résultats suivants doivent être intégrés dans l'analyse de référence du système de santé publique : tous les coûts directement encourus par le système de santé publique au Canada et les AVAQ pour les personnes vaccinées, les personnes qui subissent des externalités liées au programme de vaccination, ainsi que les AVAQ pour les aidants naturels. Pour les proches du patient (par exemple, les parents d'un enfant malade), il peut y avoir des pertes d'AVAQ dues à l'anxiété ou au deuil. Comme indiqué au chapitre 10 sur la mesure et l'évaluation de la santé, l'analyse ne doit pas inclure les AVAQ qui reviennent aux aidants professionnels. Ceci afin d'éviter une double comptabilisation de l'évaluation non financière des effets (c'est-à-dire la désutilité de la charge des soins professionnels) et de la valeur financière de leur temps (où le salaire devrait déjà être ajusté pour compenser les pertes d'AVAQ telles que l'épuisement et la pression émotionnelle de la prestation de soins). Les coûts des aidants professionnels sont comptabilisés et évalués au taux de salaire horaire qui serait payé à une personne qui fournit ce service, comme décrit au chapitre 11 sur l'utilisation et les coûts des ressources.
Pour l'analyse du cas de référence de la perspective sociétale, les coûts et les résultats du point de vue du système de santé public doivent être inclus, et au moins les éléments suivants : les coûts supportés par les patients, les coûts des soignants et les pertes de productivité. Les incidences non sanitaires telles que la consommation, les services sociaux, l'éducation et l'environnement doivent également être prises en compte, le cas échéant.
Les rapports coût-efficacité différentiels (RCED) doivent être rapportés pour chaque perspective des cas de référence. Toutefois, selon la position des scénarios dans le plan coût-efficacité, il peut ne pas être judicieux de calculer les RCED, par exemple en cas de domination de la stratégie de vaccination ou du comparateur. Dans tous les cas, cependant, les valeurs moyennes des coûts, de l'efficacité, des coûts différentiels et de l'efficacité différentielle doivent être rapportées avec des intervalles de confiance ou crédibles à 95 %. Lorsque les valeurs différentielles moyennes des coûts et de l'efficacité sont toutes deux positives, des RCED doivent être présentés. Cette approche consiste à comparer chaque intervention à l'intervention suivante la plus coûteuse et à exclure toutes les interventions qui sont soit dominées, soit sujettes à une dominance étendue. Graphiquement, les résultats doivent être présentés sous forme de fonctions de production de la santé ou de frontières coûts-efficacité réelle et prévue. Lorsque les avantages financiers nets ou les avantages nets pour la santé sont utiles à l'interprétation, ils doivent être calculés et présentés en utilisant une gamme de seuils de rentabilité couramment utilisés.
Dans les cas où des analyses de sous-groupes ont été réalisées (comme décrit au chapitre 3 sur les populations étudiées), les valeurs moyennes des coûts et des résultats ainsi que les RCED doivent être générés pour chaque sous-groupe pertinent conformément aux orientations présentées dans ce chapitre. Dans les cas où plusieurs perspectives de systèmes de santé publics régionaux ou provinciaux/territoriaux ont été analysées, les résultats doivent être rapportés pour chacune d'entre elles.
13. Incertitude
Énoncés des Lignes directrices
- 13.1 Les chercheurs doivent aborder l'incertitude des paramètres en recourant à une analyse probabiliste de référence, si possible, ainsi qu'à des analyses de sensibilité déterministes.
- 13.2 « Étudier l'incertitude méthodologique en comparant les résultats de l'analyse de référence à ceux d'une analyse complémentaire fondée sur d'autres choix méthodologiques que ceux recommandés pour examiner l'incidence des différences d'ordre méthodologique. » [Énoncé des lignes directrices de l'ACMTS]
- 13.3 « Il convient d'utiliser les courbes d'acceptabilité du rapport coût-efficacité (CARCE) et les frontières d'efficience (FE) pour représenter l'incertitude des estimations des coûts et des résultats lorsque celles-ci ont été générées de manière probabiliste. » [Énoncé des lignes directrices de l'ACMTS, modifié]
- 13.4 « Lorsque le problème de décision comprend l'option de commander ou d'effectuer un projet de recherche, l'analyse de la valeur de l'information peut être utile dans l'attribution d'une valeur à ces options et dans la conception du projet de recherche; cette analyse doit alors être comprise dans l'analyse de référence. » [Énoncé des lignes directrices de l'ACMTS, modifié]
- 13.5 Évaluer l'incertitude structurelle par des analyses de scénarios. [Énoncé des lignes directrices de l'ACMTS, modifié]
Les décideurs ont besoin d'informations sur l'incertitude liée aux résultats des évaluations économiques des programmes de vaccination afin d'éviter de prendre des décisions de financement moins qu'optimales. Plus précisément, ils doivent examiner et présenter trois types d'incertitude : l'incertitude liée aux paramètres, l'incertitude liée à la structure et l'incertitude liée à la méthodologie.
Incertitude des paramètres
L'incertitude des paramètres, également appelée incertitude de second ordre, fait référence à l'incertitude dans les estimations des paramètres qui sont utilisés pour alimenter un modèle.Note de bas de page 57Note de bas de page 163Note de bas de page 164] Elle diffère de la variabilité aléatoire, également appelée incertitude de premier ordre ou incertitude stochastique, ainsi que de l'hétérogénéité. La plupart des lignes directrices sur la réalisation des évaluations économiques d'interventions dans le domaine des soins de santé recommandent d'utiliser une analyse probabiliste de référence ou une analyse de sensibilité probabiliste pour explorer l'incertitude paramétrique, mais dans de rares situations, cette technique peut ne pas être réalisable avec des modèles dynamiques. De telles situations se présentent lorsque les modèles sont particulièrement complexes (p. ex. les simulations fondées sur des agents) ou lorsque la puissance de calcul disponible est limitée. Dans les modèles dynamiques, de nombreux paramètres liés à la transmission, tels que les habitudes de contact entre individus et les comportements liés à la prévention, peuvent être corrélés et il convient de préserver ces corrélations dans les modèles afin de générer des résultats sensés et adaptés aux données existantes (p. ex. données de surveillance épidémiologique). Dans certains cas, les corrélations entre les paramètres peuvent être inconnues,Note de bas de page 39Note de bas de page 64bien qu'on puisse parfois les établir à l'aide de méthodes bayésiennes d'inférence des paramètres.Note de bas de page 165Note de bas de page 166 Dans ces cas, les chercheurs peuvent être amenés à choisir entre une structure de modèle complexe qui ne permet pas de réaliser d'analyse probabiliste et une structure plus simple qui permet d'étudier les conséquences des incertitudes liées aux paramètres.
Lorsque cela est possible, il faut traiter l'incertitude paramétrique de manière probabiliste par des analyses probabilistes de référence. Les chercheurs doivent s'assurer que les résultats convergent si des algorithmes différentiels sont utilisés pour l'inférence des paramètres. Les fourchettes de paramètres choisies pour évaluer l'incertitude doivent, dans la mesure du possible, être fondées sur des estimations provenant d'études d'observation ou de données de surveillance. Les résultats de ces analyses doivent être présentés sous forme de CARCE ou sous forme de FE. Des diagrammes de dispersion peuvent être fournis pour présenter le plan coût-avantage avec les CARCE et les FE. Les CARCE résument l'incertitude en représentant graphiquement la probabilité qu'une intervention soit rentable en fonction des valeurs possibles des seuils de rentabilité. Les FE résument l'incertitude de plusieurs interventions (généralement trois ou plus) en traçant l'intervention qui est économiquement préférée à différents seuils de coût-efficacité. Des diagrammes de dispersion sur le plan coût-efficacité peuvent être fournis avec les CARCE et les FE. Les diagrammes de dispersion sont utiles pour observer la densité et la dispersion des itérations, et pour évaluer les points d'inflexion et la forme des ellipses produites.
En plus de quantifier l'incertitude de manière probabiliste dans la référence, les chercheurs doivent effectuer des analyses de sensibilité déterministes (ASD) sur les différents paramètres du modèle afin d'avoir un aperçu des effets isolés des variations de ces paramètres, lequel est fourni par les méthodes déterministes. Les résultats des ASD à sens unique (ou univariés) peuvent être présentés à l'aide d'un graphique en tornade, et les ASD bidirectionnelles peuvent être présentés à l'aide de graphiques de seuil bidirectionnels.Note de bas de page 164 Au minimum, il y a deux paramètres d'entrée clés à examiner par le biais de l'ASD. En particulier, les chercheurs doivent mener une ASD sur le prix des vaccins en utilisant un certain nombre de valeurs plausibles puisque le prix unitaire réel des doses de vaccin au Canada est souvent confidentiel. Pour le payeur public, le prix négocié peut être inférieur au prix catalogue du fabricant. Il convient également de réaliser des ASD sur les estimations de l'efficacité des vaccins, car ces paramètres présentent souvent un degré élevé d'incertitude. En outre, les chercheurs doivent effectuer une analyse de sensibilité bidirectionnelle évaluant le prix du vaccin et l'efficacité du vaccin. Les autres paramètres à tester dans l'ASD comprennent les estimations pour lesquelles les données canadiennes ne sont pas utilisées.
Lorsqu'ils effectuent des ASD, les chercheurs doivent déterminer les régions des paramètres associées à des comportements distincts du modèle, comme la propagation épidémique ou l'extinction de la maladie, et indiquer si l'analyse de sensibilité a été limitée à une seule région. Si l'analyse de sensibilité porte sur plus d'une région, ils doivent indiquer la probabilité d'atteindre différents états d'équilibre de la maladie lorsque les valeurs des paramètres varient.Note de bas de page 39
Lorsque les analyses probabilistes ne sont pas entreprises dans le contexte de modèles dynamiques non linéaires, les chercheurs doivent effectuer des ASD complètes sur les paramètres incertains. Ils peuvent alors envisager d'utiliser de nouvelles méthodes d'analyses de sensibilité déterministes telles que l'analyse de sensibilité déterministe par étapes et l'analyse de sensibilité déterministe distributionnelle.Note de bas de page 167
Les effets de l'incertitude paramétrique peuvent être particulièrement prononcés dans les modèles dynamiques par rapport aux modèles statiques, car leur non-linéarité peut entraîner un comportement plus variable du modèle de résultats pour la population dans différentes régions des paramètres. Par exemple, une légère modification des valeurs des paramètres peut faire passer le modèle d'un état sans maladie à un état d'équilibre endémique lorsque le taux de reproduction de base (R0) est proche de 1. Ces comportements modèles ont des répercussions sur l'efficacité réelle des programmes de vaccination. Les effets indirects d'un programme introduit près d'un état seuil (p. ex. le début d'une épidémie) peuvent être importants par rapport à ceux d'un programme introduit à l'équilibre de la maladie, où son efficacité réelle peut présenter une relation linéaire entre le nombre d'individus vaccinés et la prévention de la maladie en question.Note de bas de page 39
Il est souvent difficile d'obtenir des estimations précises des paramètres des modèles de maladies infectieuses, car les chercheurs doivent souvent s'appuyer sur des études d'observation ou des données de surveillance.Note de bas de page 39 Les valeurs des paramètres tirées des données de surveillance peuvent être biaisées, car la proportion de cas détectés est souvent faible et varie considérablement entre les différentes maladies, même pour les maladies infectieuses à déclaration obligatoire dans le cadre des exigences de surveillance de la santé publique.Note de bas de page 168 La gravité de la maladie infectieuse influe sur la détection. Par exemple, l'infection par la coqueluche peut être asymptomatique, associée à des symptômes légers, à une toux grave, voire à la mort.Note de bas de page 169 Ainsi, les systèmes de surveillance qui reposent sur la déclaration passive surestiment souvent la gravité de la maladie, la morbidité et la mortalité, tout en sous-estimant l'incidence réelle de l'infection dans la population.Note de bas de page 39Note de bas de page 169
L'incertitude des estimations de l'efficacité réelle des vaccins peut résulter des différences entre les données obtenues à partir des essais randomisés contrôlés et celles tirées de grandes études d'observation. Dans les ERC, la force de l'infection ne change pas et conduit à une sous-estimation de la véritable efficacité du vaccin dans la population puisque ces études ne tiennent pas compte des effets indirects de la vaccination (c'est-à-dire de l'effet de l'immunité collective). Par ailleurs, les grandes études d'observation de l'efficacité réelle des vaccins basées sur la population tiennent compte des effets indirects, mais elles sont limitées par le risque de biais de sélection et de la confusion non mesurée.Note de bas de page 39Note de bas de page 170 Le biais de sélection peut résulter de différences systématiques dans l'échantillonnage des individus vaccinés et ceux qui ne le sont pas, se traduisant par une distribution des expositions et des résultats qui n'est plus représentative de la population source. Il y a confusion lorsque l'association entre le programme de vaccination et les résultats (p. ex. les hospitalisations évitées et les décès évités) a des distorsions ou est faussée. Ces facteurs sont notamment le niveau d'accès aux services de soins de santé, le statut socio-économique et la prévalence de l'immunité naturelle.Note de bas de page 170 Les chercheurs doivent noter que les études d'observation de l'efficacité réelle des vaccins sont généralement difficiles à réaliser et ne peuvent être entreprises avant l'homologation du vaccin. De plus, l'efficacité des programmes de vaccination dans la prévention de la maladie chez les personnes vaccinées et non vaccinées dans la population (immunité communautaire) dépend de la couverture vaccinale et des taux d'achèvement des doses. L'incertitude de ces paramètres doit être prise en compte. Lorsqu'ils envisagent d'inclure des études d'observation de l'efficacité des vaccins dans des évaluations économiques, les chercheurs peuvent considérer de se référer aux directives publiées pour évaluer les preuves provenant d'études d'efficacité comparative.Note de bas de page 171Note de bas de page 172
L'incertitude des paramètres liés à la transmission de l'infection entre individus doit être reflétée dans une analyse d'incertitude. Ces paramètres comprennent les habitudes de contact entre les individus, ainsi que d'autres comportements qui peuvent influencer la prévention et le contrôle des maladies. Les chercheurs doivent tenir compte de toutes les différences dans ces paramètres entre les groupes. Par exemple, pour les maladies où les individus asymptomatiques ou légèrement symptomatiques peuvent transmettre l'infection à d'autres, ces individus sont moins susceptibles de modifier leurs comportements pour réduire la transmission que les individus dont les symptômes sont plus graves.Note de bas de page 39
Dans certains cas, les valeurs des paramètres sont estimées à l'aide de modèles, qui peuvent être considérés comme des sous-modèles du modèle primaire d'analyse décisionnelle.Note de bas de page 163 Par exemple, un modèle prédictif peut être nécessaire pour établir la relation entre les biomarqueurs immunitaires qui sont des corrélats de protection du vaccin et l'incidence de la maladie cliniquement apparente. Dans ce cas, il faut tenir compte de l'incertitude des valeurs liées aux corrélats de protection ainsi que de l'incertitude des méthodes utilisées pour modéliser la relation entre les corrélats de protection et la maladie clinique.
Lorsqu'on a recours au calage pour estimer les paramètres du modèle, il faut étudier l'incertitude des estimations dérivées du processus de calage.Note de bas de page 164 Il s'agit de comprendre si les méthodes de calage ont pu introduire un biais dans les résultats du rapport coût-efficacité au-delà de la prise en compte de la variabilité des paramètres calibrés (par exemple, statistique de qualité d'ajustement, algorithme de recherche de paramètres). Comme Taylor et ses collaborateurs l'ont démontré dans leur analyse coûts-efficacité du vaccin contre le VPH, le fait de ne pas tenir compte de l'incertitude liée aux paramètres calibrés du modèle sous-estime l'ampleur réelle de l'incertitude dans les estimations du rapport coût-efficacité.Note de bas de page 72
Incertitude structurelle
L'incertitude structurelle concerne le choix de la structure du modèle. Lorsqu'ils construisent des modèles pour l'évaluation économique des programmes de vaccination, les chercheurs doivent s'assurer que la structure du modèle tient compte des facteurs liés à la transmission de l'infection entre les individus, y compris le rôle des sous-groupes de la population qui peuvent présenter un risque élevé de transmission ou d'acquisition de l'infection, l'évolution naturelle de la maladie modélisée, ainsi que les effets directs et indirects du programme de vaccination.Note de bas de page 39Note de bas de page 57
L'incertitude structurelle liée à la transmission de l'infection peut dépendre de l'un des facteurs suivants : 1) le mode de transmission; 2) la relation entre la gravité des symptômes et la transmissibilité (c'est-à-dire la possibilité pour les individus asymptomatiques ou peu symptomatiques de transmettre l'infection); 3) les habitudes de mélange et de contact des individus dans les populations; et 4) les changements de comportement en réaction aux éclosions de maladie.Note de bas de page 39Note de bas de page 173Note de bas de page 174 Les chercheurs doivent tester d'autres hypothèses sur ces facteurs dans toutes les situations applicables afin de s'assurer que l'incertitude liée à la transmission a été examinée de manière adéquate.
Pour certaines maladies infectieuses, des sous-groupes de population peuvent être épidémiologiquement importants pour la transmission de la maladie ou le risque d'infection dans la population globale. Ces sous-groupes peuvent recouper des sous-groupes liés à l'équité, qui sont abordés au chapitre 14, Équité. Par exemple, dans le cas de l'hépatite A, les hommes ayant des relations sexuelles avec d'autres hommes et les utilisateurs de drogues injectables courent un risque plus élevé de transmettre et de contracter l'infection.Note de bas de page 175 Il faut mettre à l'essai les hypothèses du modèle sur le rôle de ces groupes à haut risque pour la transmission pour comprendre le degré d'incertitude qu'elles apportent.
L'incertitude relative à l'évolution naturelle d'une maladie infectieuse porte souvent sur le fait de savoir si elle conduit à une infection latente ou à une immunité naturelle. C'est le cas de certaines souches à haut risque du VPH. Des modèles d'analyse décisionnelle pour lesquels on a utilisé différentes hypothèses sur la latence et l'immunité naturelle à ces souches de VPH ont démontré que les résultats sont très sensibles à ces hypothèses.Note de bas de page 176 Les chercheurs doivent donc tenir compte de ces incertitudes dans la structure d'un modèle. Dans cet exemple du VPH, on pourrait examiner à la fois les cadres susceptible-infectieux-susceptible (SIS) et susceptible-infectieux-remis (immunisé) (SIR) pour évaluer comment les résultats varient avec différentes structures de modèle.Note de bas de page 39
Les aspects importants de l'incertitude structurelle liée aux programmes de vaccination sont le moment où les doses de vaccin sont administrées, la durée de la protection conférée par la vaccination et tous les effets indirects possibles du vaccin.Note de bas de page 39Note de bas de page 98 Le cas échéant, il convient d'évaluer également l'utilisation de doses de rappel du vaccin.
Lorsqu'on ne sait pas si la protection conférée par un vaccin s'estompe, les chercheurs doivent tester différentes hypothèses plausibles relatives à la durée de la protection. Ces hypothèses, lorsque cela est possible, doivent être fondées sur des données probantes immunologiques de la relation entre les corrélats immunitaires de la protection à long terme et l'apparition de la maladie clinique dans la période après la vaccination.Note de bas de page 98Note de bas de page 177 Les données épidémiologiques sur les éclosions de maladie, lorsqu'elles sont disponibles, peuvent également être utiles pour modéliser la durée de la protection conférée par les vaccins, comme l'ont montré les exemples des vaccins des enfants contre les oreillonsNote de bas de page 178 et des vaccins à cellules entières et acellulaires contre la coqueluche.Note de bas de page 20 Les fonctions linéaires, les fonctions logarithmiques et les fonctions exponentielles sont des exemples de méthodes utilisées pour prédire la durée de l'effet. Les fonctions constantes sont employées dans les modèles qui supposent l'absence de déclin de la protection.Note de bas de page 42Note de bas de page 98
L'une des décisions critiques pour les chercheurs qui effectuent des évaluations économiques de programmes de vaccination est de savoir s'il faut modéliser les effets indirects des vaccins à l'aide de modèles dynamiques. Voir le chapitre 8 sur la modélisation pour les situations où les modèles statiques peuvent être acceptables. Dans les cas où des effets indirects sont associés à un vaccin, comme le déplacement de la maladie en fonction de l'âge ou le remplacement du sérotype, la décision d'utiliser un modèle statique au lieu d'un modèle dynamique pourrait être faussée. Avec l'utilisation de modèles dynamiques, les chercheurs doivent envisager divers scénarios liés à l'évolution de l'épidémiologie de la maladie après l'introduction d'un programme de vaccination afin d'évaluer les effets du changement d'âge, de l'immunité communautaire ou du remplacement du sérotype sur les résultats d'une évaluation économique.
Les décisions sur la façon d'aborder l'incertitude liée aux différentes dimensions de l'efficacité réelle des vaccins (prévention de la maladie clinique, gravité de la maladie clinique, infection et infectiosité) peuvent être compliquées dans les cas où ces effets ne sont pas bien compris. Par exemple, on pense que les vaccins contre le méningocoque B ne confèrent pas une immunité collective en empêchant la transmission de la bactérie entre les individus, mais les données sur la véritable ampleur de l'efficacité réelle de ce vaccin sont limitées.Note de bas de page 179 Les chercheurs doivent utiliser différentes structures de modèles pour explorer ce type d'incertitude, le cas échéant.
L'incertitude structurelle influence les résultats des évaluations économiques au moins dans la même mesure que l'incertitude paramétrique, et souvent davantage.Note de bas de page 57Note de bas de page 164 Il est particulièrement important d'explorer l'incertitude structurelle dans les modèles dynamiques avec l'analyse d'incertitude en raison de leurs effets non linéaires, qui peuvent conduire à un comportement variable du modèle.Note de bas de page 39 On doit avoir recours à une analyse de scénarios pour explorer les incertitudes structurelles des modèles. Cette technique consiste à mettre à l'essai d'autres scénarios du modèle qui sont étayés par différentes hypothèses structurelles plausibles. Les résultats de chaque analyse de scénario doivent être présentés individuellement. On peut ensuite faire la moyenne des modèles pour synthétiser les résultats de tous les scénarios de modèles de rechange qui ont été mis à l'essai. Des conseils sur le calcul de la moyenne des résultats des analyses de scénarios sont disponibles ailleurs, comme sur l'utilisation de pondérations pour chaque modèle en fonction de la capacité de prédiction du modèle, en fonction des données disponibles (par exemple, des mesures d'applicabilité).Note de bas de page 180Note de bas de page 181 Lorsqu'il est impossible d'établir les pondérations à partir des données, le jugement des chercheurs et l'avis d'experts peuvent être requis.
La paramétrisation des sources d'incertitude (c'est-à-dire d'inclure un paramètre d'incertitude) est une méthode émergente pour traiter l'incertitude structurelle.Note de bas de page 180 Elle consiste à ajouter à un modèle des paramètres censés être les sources de l'incertitude structurelle et à leur attribuer une valeur unique, souvent extrême, de sorte que, dans certains cas, ils peuvent être complètement exclus du modèle alors que dans d'autres, ils en constituent une composante importante.Note de bas de page 180 Cette méthode permet d'internaliser l'incertitude structurelle dans le modèle et pourrait être utilisée pour orienter les décisions sur les recherches à venir visant à résoudre ces incertitudes.Note de bas de page 164Note de bas de page 180
Il convient de justifier toutes les incertitudes structurelles qui n'ont pas été abordées.Note de bas de page 164
Incertitude méthodologique
L'incertitude méthodologique est liée aux différentes méthodes qui peuvent être utilisées pour réaliser une évaluation économique. Lorsqu'ils procèdent à des évaluations économiques de programmes de vaccination, les chercheurs doivent faire des choix méthodologiques importants, notamment le type d'analyse, la perspective, l'approche et le taux d'actualisation, ainsi que l'horizon temporel.Note de bas de page 57Note de bas de page 163
Étant donné que les programmes de vaccination préviennent souvent des maladies qui pourraient avoir des conséquences catastrophiques (p. ex. la vaccination contre le méningocoque de type B pourrait empêcher la mort ou des séquelles neurologiques permanentes résultant d'une méningite due à la bactérie méningocoque de sérogroupe B), ils offrent des avantages liés à la santé et d'autres tels que des améliorations de l'éducation ou de la productivité tout au long de la vie. Les analyses coûts-avantages (ACA) peuvent rendre compte de l'ensemble de leurs incidences et, à ce titre, leur utilisation en tant que cas de non-référence peut être comparée aux cas de référence de l'analyse coûts-utilité (ACU) afin d'étudier l'effet des différences méthodologiques.Note de bas de page 12 Dans la pratique, cependant, l'incertitude liée au type d'évaluation réalisée est rarement examinée.Note de bas de page 57 En principe, les coûts autres que pour la santé des programmes de vaccination pourraient être pris en compte dans une analyse coûts-utilité si une perspective plus large (sociétale par exemple) est adoptée pour l'analyse, mais la prise en compte des avantages autres que pour la santé pourrait être plus difficile.Note de bas de page 12Note de bas de page 163 Les expériences de choix discret sont une option de plus en plus prisée pour capturer les compromis pertinents relatifs aux avantages autres que pour la santé des interventions dans le cadre des ACA et des ACU.
Les évaluations économiques des programmes de vaccination sont particulièrement sensibles à l'approche d'actualisation et à l'horizon temporel choisi pour l'analyse. Les coûts liés à la mise en place d'un programme de vaccination sont subits lors de l'introduction du programme, alors qu'il faut souvent attendre beaucoup plus longtemps, parfois plusieurs années ou décennies, pour que le programme produise tous ses effets.Note de bas de page 13Note de bas de page 57 Par conséquent, les chercheurs doivent examiner comment le fait de varier l'approche d'actualisation, ainsi que l'horizon temporel de l'analyse, affecte les résultats. Lorsque l'horizon temporel de l'analyse est très long (par exemple, plusieurs décennies), les résultats de l'évaluation économique doivent être rapportés pour une gamme d'horizons temporels afin de s'assurer que les décideurs considèrent les coûts et les résultats qui sont pertinents pour le problème de décision qu'ils traitent.
Les évaluations économiques des programmes de vaccination sont particulièrement sensibles à l'approche d'actualisation et à l'horizon temporel choisi pour l'analyse. Les coûts liés à la mise en place d'un programme de vaccination sont subits lors de l'introduction du programme, alors qu'il faut souvent attendre beaucoup plus longtemps, parfois plusieurs années ou décennies, pour que le programme produise tous ses effets.Note de bas de page 13Note de bas de page 57 Par conséquent, les chercheurs doivent examiner comment le fait de varier l'approche d'actualisation, ainsi que l'horizon temporel de l'analyse, affecte les résultats. Lorsque l'horizon temporel de l'analyse est très long (par exemple, plusieurs décennies), les résultats de l'évaluation économique doivent être rapportés pour une gamme d'horizons temporels afin de s'assurer que les décideurs considèrent les coûts et les résultats qui sont pertinents pour le problème de décision qu'ils traitent.
Pour examiner en profondeur de nombreux volets de l'incertitude méthodologique, il faudrait idéalement disposer de plusieurs modèles distincts, ce qui est souvent difficile en pratique. À ce titre, les chercheurs doivent, dans la mesure du possible, collaborer de manière transparente avec d'autres groupes qui se penchent sur des problèmes décisionnels semblables, afin de pouvoir explorer l'étendue de l'incertitude liée aux choix méthodologiques.
Valeur de l'information
S'il y a analyse de la valeur de l'information, illustrer la valeur de l'information supplémentaire par la valeur probable de l'information parfaite sur le paramètre et la valeur escomptée par la population de l'information parfaite sur le paramètre. Voir les lignes directrices de l'ACMTS pour obtenir des renseignements supplémentaires. Les chercheurs doivent appliquer une série de seuils de rentabilité couramment utilisés pour leur analyse de la valeur de l'information.
14. Équité
Énoncés des Lignes directrices
- 14.1 Les chercheurs et les décideurs doivent travailler ensemble pour déterminer les dimensions et les objectifs d'équité à inclure dans l'évaluation économique du programme de vaccination envisagé. L'équité doit être considérée dans le contexte du cadre d'éthique, d'équité, de faisabilité et d'acceptabilité (ÉÉFA) du CCNI.
- 14.2 Les analyses qui intègrent les préoccupations pertinentes en matière d'équité doivent accompagner l'analyse de référence (par exemple, l'analyse coût-efficacité distributive, l'analyse coût-efficacité étendue ou d'autres méthodes émergentes) et être présentées avec les analyses de référence.
Les évaluations économiques des interventions dans le domaine des soins de santé mettent traditionnellement l'accent sur l'efficience. Cet exercice s'inscrit dans le cadre décisionnel plus large de l'évaluation des technologies de la santé (ETS), qui synthétise et évalue principalement les données cliniques et économiques relatives à une nouvelle intervention ou technologie de la santé. Cependant, il est de plus en plus reconnu que les questions éthiques et morales liées à la manière dont une technologie est évaluée et utilisée doivent être abordées dans le cadre des décisions relatives à l'adoption de nouvelles technologies de la santé.Note de bas de page 182Note de bas de page 183
Le CCNI a mis en place le cadre d'éthique, d'équité, de faisabilité et d'acceptabilité (ÉÉFA) pour prendre systématiquement en compte ces facteurs dans le cadre d'une approche multicritère des recommandations sur les vaccins. Dans ce cadre, l'éthique et l'équité sont prises en compte avec la faisabilité et l'acceptabilité d'une recommandation, ainsi que l'efficacité clinique, l'immunogénicité, l'innocuité et la rentabilité d'un vaccin.Note de bas de page 6 L'éthique de la Santé publique est le domaine de l'éthique appliquée en vaccination. Elle s'intéresse principalement aux dimensions éthiques fondamentales suivantes : 1) le respect des personnes et des communautés; 2) la non-malfaisance et la bienfaisance; 3) la confiance; et 4) la justice.Note de bas de page 184
L'équité est considérée comme faisant partie de la dimension éthique fondamentale de la justice, et est définie comme « l'absence de différences injustes, évitables et remédiables dans la santé entre différents groupes de la population, définis selon des critères sociaux, économiques, démographiques ou géographiques ou par des moyens de stratification ».Note de bas de page 6Note de bas de page 185 Dans les évaluations économiques, l'équité est une approche de la justice distributive qui concerne les jugements sur l'équité dans la distribution des résultats et des expériences de santé dans une population, et elle est liée à l'allocation équitable des ressources et à la réalisation d'amélioration de la santé entre les individus ou les groupes.Note de bas de page 186 L'équité dans l'évaluation économique des technologies de la santé a fait l'objet d'une activité et d'un développement méthodologique considérables récemment.Note de bas de page 183Note de bas de page 187Note de bas de page 188Note de bas de page 189
Les conséquences distributives liées à l'adoption d'une nouvelle technologie de la santé deviennent particulièrement importantes dans les situations où les décideurs doivent faire des compromis entre le rendement l'équité en matière de santé. Ces situations se présentent lorsqu'une technologie est rentable, mais accroît les inégalités entre les groupes d'une population, parce que certains segments de la société peuvent tirer parti de la technologie plus que d'autres. En revanche, elles se présentent lorsqu'une technologie n'est pas rentable, mais que son adoption améliorerait l'équité entre les groupes en réduisant les disparités en matière de gains en matière de santé, ou lorsqu'une technologie augmenterait l'équité entre certains groupes (par exemple, les strates de revenus), mais diminuerait l'équité entre d'autres (par exemple, géographiques).Note de bas de page 190
La recherche qualitative dans le contexte de la Santé publique canadienne suggère que les décideurs perçoivent l'équité en matière de santé et la justice sociale comme étant différentes, bien que toutes deux se situent dans l'espace théorique de la justice.Note de bas de page 191 L'équité en matière de santé est décrite comme ayant une qualité neutre ou objective et se concentre sur des enjeux liés à la proximité, tels que l'accès aux ressources et aux services de Santé publique. Le concept est donc qualifié de « confortable » et de « quantifiable ». En revanche, la justice sociale est perçue comme étant sujette à des sensibilités politiques, exigeant une confrontation personnelle des préjugés et des privilèges, et étant « structurelle » et donc « inapplicable » en raison d'un manque de mécanismes institutionnels ou d'appétit. Les perceptions de l'équité en matière de santé et de la justice sociale sont particulièrement pertinentes dans les discussions sur l'équité en matière de coûts de transfert. Lorsque les biens et services ne sont pas liés à la consommation ou à la production de ressources et de services, les coûts de transfert sont fonctionnellement des transferts financiers d'une personne ou d'un groupe de personnes de la société à une autre. Ils s'appliquent aussi bien dans la perspective du système de santé publique que dans celle de la société. Voir le chapitre 11 sur l'utilisation et le coût des ressources pour l'exemple sur le prix du vaccin et ses composantes de coût. Compte tenu de la nature publique du système de santé canadien, des questions se posent quant à l'équité et à la durabilité de la tarification des vaccins lorsque les fonds publics sont transférés au secteur privé, notamment aux multinationales.Note de bas de page 192 Les payeurs de soins de santé, ainsi que le public, s'intéressent aux moyens de réduire les coûts de production marginaux et de faire en sorte que l'attribution des bénéfices soit alignée sur la création de valeur. En d'autres termes, il y a un intérêt à assurer l'équité entre les acheteurs et les vendeurs. Le profit ou la perception du profit peut influencer la prise de décision en matière de remboursement et d'approvisionnement, et peut être lié aux objectifs d'équité du programme de vaccination. À ce titre, les chercheurs doivent prendre en compte le cheminement des transferts financiers au sein de la société et les parties impliquées, y compris les secteurs privé et public, lorsqu'ils sont connus.
Les chercheurs et les décideurs doivent travailler en collaboration pour déterminer lequel des objectifs d'équité suivants le programme de vaccination vise à atteindre : 1) améliorer l'équité en matière d'accès au programme de vaccination pour les personnes admissibles; 2) améliorer l'équité en matière de participation au programme de vaccination pour les personnes admissibles; 3) améliorer l'équité en matière d'avantages pour la santé liés aux conditions de santé visées par le programme de vaccination; 4) réduire les inégalités en matière de santé au cours de la vie entre les groupes au moyen du programme de vaccination; ou 5) réduire les inégalités globales (c'est-à-dire liées et non liées à la santé) entre les groupes au moyen du programme de vaccination. Différentes approches peuvent être utilisées pour conceptualiser les objectifs d'équité (par exemple, l'universalisme proportionné, l'égalitarisme). Les chercheurs peuvent trouver utile de se référer à la littérature publiée sur ce sujet lorsqu'ils conceptualisent les objectifs d'équité à inclure dans une évaluation économique.Note de bas de page 193Note de bas de page 194Note de bas de page 195
Lors de l'établissement des objectifs d'équité, les chercheurs doivent se demander s'il existe des groupes clés d'individus souffrant d'inégalités en matière de santé et d'obstacles à la santé qui pourraient être réduits ou traités par le programme de vaccination. Parmi les groupes susceptibles d'être victimes d'iniquités en matière de santé au Canada, mentionnons les peuples autochtones (c.-à-d. les Premières nations, les Inuits et les Métis aux fins des présentes lignes directrices), les personnes de bas statut socio-économique, les personnes qui font partie de groupes minoritaires sur le plan ethnique, sexuel ou du genre, les populations vivant dans certaines régions géographiques (urbaines, rurales, éloignées ou isolées), les personnes handicapées et les groupes à risque élevé comme les enfants, les personnes âgées ou les personnes institutionnalisées.Note de bas de page 6Note de bas de page 130Note de bas de page 189Note de bas de page 196Note de bas de page 197
Les chercheurs doivent également prendre en compte les facteurs qui pourraient entraîner des différences dans les avantages pour la santé résultant du programme de vaccination entre les groupes présentant des inégalités en matière de santé. Les facteurs comprennent les conditions de santé sous-jacentes, le potentiel de bénéfice à vie, les comportements de recherche de la santé, l'utilisation du vaccin et le rôle de l'immunité communautaire dans la réduction ou l'augmentation des inégalités entre les groupes, les comportements à risque, les différents modèles de mélange ou de contact au sein des groupes, et l'accès à des soins de santé culturellement sûrs.Note de bas de page 10Note de bas de page 198
Les chercheurs doivent être conscients du fait que certains groupes peuvent bénéficier de manière disproportionnée du programme de vaccination, ce qui pourrait accroître les inégalités. Par exemple, un accès différentiel à un programme de vaccination contre le virus du papillome humain (VPH) peut aggraver l'inégalité en réduisant le taux de cancer du col de l'utérus dans une population qui présentait déjà un risque plus faible, augmentant ainsi la différence de résultats entre les groupes. Les interventions qui semblent réduire les inégalités doivent être examinées afin de déterminer comment les obstacles pertinents à l'accès rencontrés par la population seraient surmontés.
Une fois que les chercheurs ont établi les résultats d'intérêt en matière d'équité, ils doivent examiner les caractéristiques du programme de vaccination destinées à atteindre ces résultats. Par exemple, si l'objectif du programme est d'améliorer l'équité dans l'accès au vaccin pour toutes les personnes admissibles, il faudrait alors envisager un programme qui diminue les obstacles à l'accès. Un exemple d'un tel programme serait un programme de vaccination contre le VPH à l'école qui élimine les obstacles pour les individus tels que le besoin de transport vers une clinique ou un cabinet médical.Note de bas de page 130 Cependant, si l'objectif du programme est d'améliorer l'équité dans l'adoption du vaccin, les chercheurs pourraient envisager des scénarios dans lesquels les vaccins sont obligatoires ou qui traitent de la désinformation sur le vaccin. Un exemple d'un tel programme serait un programme scolaire légalement obligatoire pour la vaccination contre le VPH, avec une clause active de refus.Note de bas de page 199 Si l'objectif est de réduire les inégalités en matière de santé entre les groupes au cours de la vie grâce au programme de vaccination, il convient d'envisager un programme conforme au principe d'équité verticale, qui implique de traiter différemment les individus présentant différentes caractéristiques pertinentes sur le plan éthique.Note de bas de page 200 Un exemple serait un programme de vaccination qui atteint des niveaux élevés de couverture vaccinale parmi les populations autochtones. Au Canada, les populations autochtones sont plus touchées par les maladies évitables par la vaccination que les populations non autochtones (par exemple, le cancer du col de l'utérus, l'hépatite A) en raison d'inégalités systématiques telles que la pauvreté, la promiscuité des logements, le manque d'eau courante et un mauvais état de santé sous-jacent, qui augmentent le risque de contracter ces infections.Note de bas de page 201 Note de bas de page 202 De plus, les peuples autochtones vivant dans des réserves et des communautés éloignées peuvent également être victimes d'inégalités dans l'accès aux traitements lorsqu'ils tombent malades, ce qui augmente leur risque de morbidité et de mortalité liées aux infections.Note de bas de page 203 Les chercheurs doivent cependant être conscients que les programmes de vaccination limités à certains groupes à haut risque ou marginalisés peuvent stigmatiser davantage ces groupes. Il convient alors d'envisager d'autres approches, telles que des programmes universels. Enfin, si l'objectif est d'améliorer l'équité sanitaire et non sanitaire entre les groupes, les chercheurs pourraient envisager des programmes de vaccination qui contribuent à améliorer la santé ainsi que la productivité économique. Il s'agit par exemple des programmes de vaccination des enfants, qui permettent aux enfants de participer à l'éducation, ce qui leur permet de devenir des adultes en bonne santé et économiquement productifs.Note de bas de page 204 Lorsque la prise en compte des résultats pertinents pour l'équité concerne la sélection et la définition des comparateurs à inclure dans l'analyse, les chercheurs doivent se référer au chapitre 3, Comparateurs, des présentes lignes directrices.
Lorsqu'ils présentent les résultats des évaluations économiques par sous-groupes pertinents pour l'équité, les chercheurs doivent s'assurer que les critères d'établissement de ces sous-groupes ont été délimités et justifiés de manière transparente. Un examen récent des analyses coût-efficacité (ACE) tenant compte de l'équité a identifié onze critères différents qui ont été utilisés pour intégrer explicitement l'équité dans un cadre de coût-efficacité (le statut socio-économique et la race et l'ethnie étant les plus fréquemment utilisés).Note de bas de page 205 Les cadres de l'ACE distribuée et de l'ACE étendue fournissent des orientations et des méthodes pour mener des ACE tenant compte de l'équité.Note de bas de page 187 Note de bas de page 206
En plus de tenir compte des résultats liés à l'équité associés aux programmes de vaccination, les chercheurs doivent également tenir compte de la distribution des coûts de renonciation liés à la mise en œuvre de ces programmes.Note de bas de page 190 Cette redistribution des ressources pourrait, par exemple, entraîner une diminution des dépenses consacrées aux programmes de dépistage ou aux mesures préventives non vaccinales liées à l'infection visée par le programme de vaccination. Les coûts de renonciation peuvent également concerner d'autres secteurs que celui de la santé, par exemple, par une diminution du financement des programmes éducatifs ou sociaux.Note de bas de page 190 Bien que, dans de nombreux cas, il puisse être difficile de déterminer explicitement les coûts de renonciation liés à la mise en œuvre de programmes de vaccination, les chercheurs doivent, dans la mesure du possible, les quantifier d'une manière pertinente pour les décideurs. Dans certains cas, les interventions visant à améliorer l'équité peuvent ne pas avoir de coût de renonciation net, puisqu'il peut être efficace d'affecter des ressources aux groupes dont la charge sanitaire est plus élevée.
Le cas échéant, ils doivent tenir compte des conséquences des programmes de vaccination sur l'équité intergénérationnelle. Les programmes de vaccination qui entraînent des externalités ont des effets sur des cohortes d'individus autres que celle qui est vaccinée.Note de bas de page 45 Par exemple, un programme de vaccination contre la varicelle pendant l'enfance peut provoquer une augmentation des cas de zona chez les personnes plus âgées;Note de bas de page 207 inversement, un programme de vaccination contre le VPH peut conduire à l'éradication de la maladie pour les générations futures.Note de bas de page 208 Dans ces deux exemples, il faut intégrer les effets indirects sur des cohortes d'individus non visées par le programme de vaccination dans les modèles dynamiques utilisés pour générer des estimations de la rentabilité. Les chercheurs doivent alors tenir compte explicitement des conséquences de ces résultats sur le plan de l'équité. Dans le premier exemple, les chercheurs doivent recenser de manière qualitative des compromis entre l'amélioration de la santé des enfants et les résultats négatifs en matière de santé éventuels chez les personnes plus âgées. Quantitativement, le résumé des coûts et les résultats estimés dans le cadre de l'analyse tiennent compte des compromis. Dans le second exemple, ils doivent se demander comment évaluer en termes actuels les résultats en matière de santé obtenus par des cohortes dans un avenir lointain. À l'heure actuelle, un débat est en cours sur la question de savoir quelles vies futures doivent être prises en compte, ainsi que sur la manière dont elles doivent l'être, en particulier dans le cas de programmes d'éradication de maladies ou de programmes ayant d'importants effets intergénérationnels (par exemple, des programmes ayant un impact sur la résistance aux antimicrobiens ou sur la fertilité).Note de bas de page 209 Les vies futures font référence à des personnes futures qui n'existent pas encore, et peuvent être : 1) des générations futures qui naîtront indépendamment de l'existence du programme; ou 2) des générations futures qui naîtront en raison de l'impact de l'intervention sur l'augmentation de la fertilité, ou qui peuvent vivre en raison de son effet sur la réduction de la mortalité.
Une telle évaluation des résultats de santé dans des cohortes dans un avenir lointain dépend de la stratégie d'actualisation employée dans le cadre de l'évaluation économique. Un taux d'escompte égal se traduit par une plus grande valeur accordée aux résultats en matière de santé de la cohorte actuelle et des cohortes proches dans le temps, et une valeur moindre aux résultats en matière de santé des cohortes dans un avenir lointain, ce qui, selon certains auteurs, est une caractéristique injuste de cette stratégie.Note de bas de page 44 L'application de taux d'escompte plus faibles pourrait toutefois avoir pour conséquence d'accorder plus de poids aux résultats en matière de santé dans les cohortes susceptibles d'avoir des revenus plus élevés et accès à davantage d'interventions sanitaires, et donc d'avoir plus de chances d'améliorer la santé. Compte tenu des résultats variables liés aux effets intergénérationnels des programmes de vaccination qui peuvent résulter de différentes stratégies d'actualisation, les chercheurs doivent examiner et signaler les conséquences sur le plan de l'équité intergénérationnelle des programmes de vaccination qui se traduisent par des avantages sanitaires pour les cohortes dans un avenir lointain.Note de bas de page 44Note de bas de page 45Note de bas de page 210
15. Production de rapports
Énoncés des Lignes directrices
- 15.1 « Présenter les résultats de l'évaluation économique de façon détaillée et transparente. Fournir suffisamment de renseignements pour que le lecteur ou l'utilisateur (le décideur, par exemple) puisse faire une analyse critique de l'évaluation. » [Énoncé des lignes directrices de l'ACMTS, modifié]
- 15.2 Prévoir un sommaire de l'évaluation dans un langage non technique. [Énoncé des lignes directrices de l'ACMTS]
- 15.3 « Présenter les résultats de l'évaluation économique à l'aide d'éléments graphiques ou visuels en plus de tableaux. » [Énoncé des lignes directrices de l'ACMTS]
- 15.4 « Inclure des renseignements ou des documents sur les processus d'assurance de la qualité et les résultats de l'évaluation économique dans le compte rendu. Fournir une copie du modèle par voie électronique aux fins d'examen ainsi que de la documentation connexe afin de faciliter la compréhension du modèle, de son déroulement et de son fonctionnement. » [Énoncé des lignes directrices de l'ACMTS]
- 15.5 « Préciser les sources de financement et les liens hiérarchiques dans le cadre de l'évaluation et mentionner tout conflit d'intérêts éventuel. » [Énoncé des lignes directrices de l'ACMTS]
- 15.6 Les chercheurs doivent utiliser les lignes directrices pour la présentation des évaluations économiques des programmes de vaccination au Canada du CCNI et remplir l'inventaire des effets à prendre en considération dans l'évaluation économique des stratégies de vaccination, qui se trouve à l'annexe 1.
La présentation des résultats des évaluations économiques doit fournir aux décideurs des informations transparentes et crédibles qui leur permettent d'aborder le problème de décision qui les intéresse et de prendre une décision de financement optimale concernant le programme de vaccination envisagé.
Les considérations relatives aux rapports spécifiques aux vaccins incluent notamment l'horizon temporel de l'évaluation et les mécanismes par lesquels les vaccins exercent leurs effets. Dans les cas où l'horizon temporel du modèle d'une évaluation économique s'étend sur une longue période, il convient de présenter les résultats à partir de divers points temporels sur l'horizon temporel du modèle pour que les conclusions de l'analyse soient pertinentes pour l'horizon temporel considéré par les décideurs. Étant donné que les vaccins peuvent exercer leurs effets par le biais de divers mécanismes (p. ex. la prévention de la transmission d'une infection, la prévention d'une infection, la prévention d'une maladie ou la diminution de sa gravité), les chercheurs doivent rendre compte des résultats des programmes de vaccination non seulement en matière d'AVAQ, mais aussi en nombre de cas évités, en nombre d'unités d'utilisation des soins de santé pertinentes (p. ex. les hospitalisations) évitées, en nombre de décès évités et en nombre d'individus à vacciner, le cas échéant. La présentation de ces unités de mesure en plus des AVAQ améliore la crédibilité et la transparence de l'analyse pour les décideurs.
L'utilisation des ressources, les coûts et les résultats doivent être présentés de manière désagrégée pour chaque comparateur faisant l'objet d'un examen dans le cadre de l'analyse et pour les deux analyses de référence. Si les analyses sont effectuées du point de vue de plusieurs payeurs publics (par exemple, pour plusieurs provinces ou territoires), chacune d'elles doit être présentée séparément.
Toutes les hypothèses et règles de décision utilisées dans le cadre des analyses doivent être présentées de manière transparente. Les chercheurs doivent donner des détails sur les processus d'assurance qualité et les résultats obtenus dans le cadre du processus de vérification du modèle. Une copie électronique entièrement exécutable du modèle doit être mise à disposition, ainsi que les détails relatifs à la fonctionnalité du modèle, afin de permettre au décideur de vérifier les résultats de l'analyse ou de réaliser des analyses supplémentaires si nécessaire.
Les chercheurs doivent divulguer toutes les sources de financement de l'évaluation économique et indiquer le rôle des bailleurs de fonds dans l'identification, la conception, la réalisation et le compte rendu de l'analyse. Les sources non financières de soutien (par exemple, en nature) doivent également être divulguées.Note de bas de page 211
Les chercheurs doivent indiquer tous les conflits d'intérêts potentiels, d'ordre financier ou non. Les types d'affiliations et d'intérêts devant être divulgués comprennent : la participation à la recherche, la participation financière, la propriété intellectuelle, et tout autre intérêt que les lecteurs pourraient percevoir comme un intérêt concurrent. Note de bas de page 7Note de bas de page 212
Les « lignes directrices pour la présentation des évaluations économiques des programmes de vaccination au Canada du CCNI », se trouvant sur le site Web du CCNI, fournissent un format standard pour la présentation des résultats des évaluations économiques des programmes de vaccination.Note de bas de page 7 Le modèle fourni s'aligne sur les lignes directrices existantes en matière de rapports, notamment les Consolidated Health Economic Evaluation Reporting Standards II (CHEERS II).Note de bas de page 211 Les chercheurs doivent suivre la structure décrite dans ce document pour présenter leurs résultats.
Annexe 1 : Tableau d'inventaire des effets
Le tableau a été adapté à partir de l'inventaire des effets publié par le 2e groupe d'experts sur le rapport coût-efficacitéNote de bas de page 1 afin d'inclure des effets plus larges qui n'avaient pas été pris en compte auparavant. Bon nombre de ces effets concernent les technologies de la santé en général, et certains sont spécifiques aux vaccins ou aux maladies infectieuses (par exemple, le déplacement de l'âge des maladies, l'éradication des maladies).Footnote 1,Footnote 2,Footnote 3,Footnote 4,Footnote 5 Le tableau fournit une liste des effets sanitaires et non sanitaires qui pourraient résulter des programmes de vaccination. L'intention est de permettre aux chercheurs de prendre en considération de manières systématiques les effets lorsqu'ils planifient et réalisent des évaluations économiques des programmes de vaccination. Des conseils précis sur la quantification de ces effets et de leurs coûts connexes se trouvent au chapitre 11, Utilisation et coût des ressources.
Les chercheurs doivent remplir et présenter le tableau 1 dans le cadre de leur analyse afin d'indiquer de manière explicite quels effets sont inclus et exclus de l'évaluation économique pour chacune des deux analyses de référence. La colonne des commentaires peut être utilisée pour justifier l'inclusion ou l'exclusion de certains effets ou pour fournir des renseignements supplémentaires.
| Domaine touché | Définitions/Exemples | Inclus dans le cas de référence?Note de bas de page b | Commentaires | |
|---|---|---|---|---|
| Perspective du système de santé financé à même les fonds publics | Perspective sociétale | |||
| Santé | ||||
| Résultats en matière de santé | Résultats de santé individuels pour les personnes destinées à la vaccination |
|||
| Mortalité | O/N | O/N | pas de données | |
| Qualité de vie liée à la santé | O/N | O/N | ||
| Innocuité (c'est-à-dire, événements indésirables) | O/N | O/N | ||
| Effets sur la santé non pris en compte dans les AVAQ | O/N | O/N | ||
Résultats individuels en matière de santé pour les aidants naturels |
||||
| Qualité de vie liée à la santé | O/N | O/N | pas de données | |
| Résultats en matière de santé de la population | ||||
| Incidence de l'infection et de la maladie chez les personnes vaccinées et non vaccinées | O/N | O/N | pas de données | |
| Changements dans la répartition par âge des individus qui développent une infection ou une maladie | O/N | O/N | ||
| Émergence de nouvelles maladies liées à des variations de l'agent pathogène (c'est-à-dire des sérotypes, des sérogroupes, des souches) ou à des agents pathogènes non apparentés qui peuvent remplacer ceux visés par le vaccin | O/N | O/N | ||
| Éradication de la maladie | O/N | O/N | ||
| Coûts du système de santé financé par l'État | Coûts des soins de santé | |||
| Services de soins de santé financés par l'État (par exemple, visites chez le médecin, tests diagnostiques, traitement médicamenteux le cas échéant, hospitalisation, soins professionnels,Note de bas de page a réadaptation dans un établissement ou à domicile,Note de bas de page a soins à domicile,Note de bas de page a soins de longue durée en maison de reposNote de bas de page a) | O/N | O/N | pas de données | |
| Coûts futurs des soins de santé connexes et non connexes | O/N | O/N | ||
| Coûts de santé publique | ||||
| Coûts liés au programme (par exemple, coûts de mise en œuvre, d'exécution et coûts récurrents, y compris les campagnes de Santé publique et les activités de promotion de la santé; coûts de transaction liés à l'introduction de nouveaux vaccins ou au passage d'un vaccin à un autre; coûts liés au dépistage, au diagnostic et au traitement des maladies; surveillance épidémiologique, recherche des contacts, enquête et gestion des épidémies) | O/N | O/N | pas de données | |
| Coûts liés à l'intervention (par exemple, le coût des doses de vaccin, la distribution comme le transport et l'entreposage frigorifique, l'administration, y compris le personnel, les pertes et les fournitures auxiliaires) | O/N | O/N | ||
| Coûts des soins de santé NON financés par le système de santé | Médicaments sur ordonnance (dans certains cas) | S. O. | O/N | pas de données |
| Services de soins professionnels,a réadaptation dans un établissement ou à domicile,a soins à domicile,a soins de longue durée en maison de repos,a (dans certains cas) | S. O. | O/N | ||
| Frais divers à la charge des patients (par exemple, médicaments sans ordonnance) | S. O. | O/N | ||
| Les frais accessoires (par exemple, les quotes-parts des assurances privées, les soins dentaires, les soins de la vue, les appareils fonctionnels, la physiothérapie, etc.) | S. O. | O/N | ||
| Non lié à la santé | ||||
| Frais directs à la charge des patients | Frais de transport | S. O. | O/N | pas de données |
| Frais d'hébergement | S. O. | O/N | ||
| Pertes de productivité | Travail rémunéré |
|||
| Arrêt de travail résultant de l'administration du vaccin, du traitement, de la maladie, de l'invalidité ou du décès | S. O. | O/N | pas de données | |
| Présentéisme | S. O. | O/N | ||
| Conséquences des maladies infantiles sur la productivité tout au long de la vie | S. O. | O/N | ||
| Travail non rémunéré | ||||
| Temps d'arrêt de travail sur le marché du travail non organisé (par exemple, bénévolat, aide, mentorat) résultant de l'administration d'un vaccin, d'un traitement, d'une maladie, d'un handicap ou d'un décès | S. O. | O/N | pas de données | |
| Production à la maison non compensée (par exemple, cuisine, nettoyage, courses, éducation des enfants, autres tâches liées à la gestion du ménage) | S. O. | O/N | ||
| Productivité des aidants naturels | ||||
| Temps d'arrêt de travail résultant de la prise en charge de personnes malades, de l'accompagnement de personnes à des rendez-vous de vaccination | S. O. | O/N | pas de données | |
| Présentéisme des soignants | S. O. | O/N | ||
| Conséquences macroéconomiques | ||||
| Chocs de l'offre de main-d'œuvre, fermetures généralisées d'entreprises | S. O. | O/N | pas de données | |
| Consommation | Consommation future individuelle non médicale | S. O. | O/N | |
| Changements dans la consommation des ménages | S. O. | O/N | ||
| Incidences de la consommation sur la santé (par exemple, associés à la perte d'emploi) | S. O. | O/N | ||
| Études | Le niveau de réussite scolaire résultant de la santé physique, de la santé mentale et de la cognition | S. O. | O/N | pas de données |
| Coûts des besoins éducatifs spéciaux résultant d'une maladie ou d'un handicap | S. O. | O/N | ||
| Perturbations des résultats d'apprentissage (par exemple, à la suite de l'administration d'un vaccin à l'école, d'une maladie ou d'un handicap pédiatrique, ou du décès ou du handicap d'un membre de la famille proche) | S. O. | O/N | ||
| Services sociaux et services communautaires | Services sociaux et services communautaires (par exemple, soutien aux personnes handicapées, programmes visant à améliorer l'accès aux programmes de vaccination pour les adultes) | S. O. | O/N | pas de données |
| Services aux enfants et aux jeunes (par exemple, programmes de sensibilisation, répit pour les familles, programmes visant à améliorer l'accès aux programmes de vaccination pour les enfants et les jeunes) | S. O. | O/N | ||
| Environnement | Incidence environnementale des programmes de vaccination et des comparateurs au niveau de la fabrication, de la distribution et de la mise en œuvre (par exemple, utilisation d'antibiotiques) | S. O. | O/N | pas de données |
| Déchets alimentaires et non alimentaires | S. O. | O/N | ||
| Consommation de carbone | S. O. | O/N | ||
| Autres domaines | Prendre en compte des domaines tels que le logement, le cas échéant | S. O. | O/N | |
|
||||
Annexe 2 : Spécifications du cas de référence
Le tableau 2 présente les recommandations pour les analyses du cas de référence. Dans les cas où les analyses ne suivent pas les recommandations présentées ci-dessous, les chercheurs doivent identifier les déviations et fournir une justification basée sur le problème de décision.
| Section | Directives |
|---|---|
| Problème de décision | Précisez les détails concernant : 1) les interventions à comparer; 2) les contextes dans lesquels elles doivent être comparées; 3) le type d'évaluation réalisée; 4) les perspectives à partir desquelles l'analyse est effectuée; 5) les coûts et les résultats à quantifier dans l'analyse; 6) l'horizon temporel sur lequel l'analyse doit être effectuée; 7) et les populations pour l'évaluation. |
| Types d'évaluations | Réaliser une analyse coût-utilité (ACU) permettant de représenter les résultats sanitaires en matière d'année de vie ajustée en fonction de la qualité (AVAQ). |
| Populations étudiées | Identifiez les populations dans lesquelles le programme de vaccination sera utilisé et, le cas échéant, les populations qui pourraient subir des effets externes résultant du programme de vaccination. Stratifier les analyses et établir des rapports par sous-groupes lorsque les hétérogénéités entre les groupes d'individus peuvent affecter les résultats de l'évaluation économique. |
| Comparateurs | Comparer toutes les interventions pertinentes, y compris les autres programmes de vaccination, les interventions de dépistage, les interventions préventives médicales et non médicales, et les approches thérapeutiques actuellement utilisées dans un contexte canadien. |
| Perspective | Réaliser deux analyses de cas de référence, l'une de la perspective du système de santé financé à même les fonds publics et l'autre de la perspective sociétale. |
| Horizon temporel | Choisir un horizon temporel suffisamment long pour saisir toutes les différences pertinentes dans les coûts et résultats futurs associés aux interventions qui sont comparées. |
| Actualisation | Actualiser les coûts et les résultats à un taux de 1,5 % par an. |
| Mesure et évaluation de la santé | Identifier, mesurer et valoriser tous les résultats pertinents en matière de santé en tenant compte des perspectives du système de santé publique et de la société. Utiliser des préférences en matière de santé qui reflètent la population canadienne en général. Obtenir les préférences en matière de santé à partir d'une méthode de mesure indirecte qui repose sur un système de classification générique. |
| Utilisation et coût des ressources | Identifier, mesurer et évaluer toutes les ressources et tous les coûts pertinents de la perspective : i) du système de santé publique et ii) de la société. Estimer les ressources et les coûts canadiens en utilisant des données qui reflètent les administrations d'intérêt. |
| Analyse | Déterminer les valeurs attendues des coûts et des résultats de la perspective du système de santé publique et de la perspective sociétale pour chaque intervention par le biais d'une analyse probabiliste, en incorporant la corrélation potentielle entre les paramètres, chaque fois que cela est possible. Lorsque des sous-groupes distincts sont identifiés au sein de la population étudiée, stratifier les analyses et établir des rapports par sous-groupes. Calculer les coûts différentiels, l'efficacité différentielle et les rapports coût-efficacité différentiels (RCED) pour les analyses des perspectives du système de santé publique et sociétale. Pour les évaluations comportant plus de deux comparateurs, calculer les RCED de manière séquentielle. |
| Incertitude | Traiter l'incertitude méthodologique en comparant les résultats du cas de référence à ceux d'une analyse sans cas de référence. Résumer l'incertitude de la décision, en utilisant les courbes d'acceptabilité du rapport coût-efficacité (CARCE) et les frontières d'acceptabilité du rapport coût/efficacité (FE), si possible. Utiliser l'analyse de scénarios pour traiter l'incertitude structurelle. S'il y a analyse de la valeur de l'information, résumer la valeur de l'information supplémentaire par la valeur probable de l'information parfaite sur le paramètre et la valeur escomptée par la population de l'information parfaite sur le paramètre. |
| Équité | Déterminer s'il existe des inégalités dont souffrent certains groupes particuliers et qui pourraient être améliorées par le programme de vaccination. L'équité doit être étudiée à l'aide de méthodes telles que l'analyse coût-efficacité distributive et l'analyse coût-efficacité étendue. Toute analyse supplémentaire doit accompagner les analyses de cas de référence, le cas échéant. |
Références de l'avant-propos
- Note de bas de page 1
-
Erickson L.J., De Wals P., Farand L. An analytical framework for immunization programs in Canada. Vaccine. 2005; 23(19): 2470-6. doi:10.1016/j.vaccine.2004.10.029
- Note de bas de page 2
-
Kristensen F.B., Lampe K., Wild C., Cerbo M., Goettsch W., Becla L. The HTA Core Model(®)-10 Years of Developing an International Framework to Share Multidimensional Value Assessment. Value Health. 2017; 20(2): 244-50. doi:10.1016/j.jval.2016.12.010
- Note de bas de page 3
-
Régie de la santé des Premières Nations. First Nations perspective on health and wellness. n.d. Disponible en anglais : https://www.fnha.ca/wellness/wellness-for-first-nations/first-nations-perspective-on-health-and-wellness
- Note de bas de page 4
-
Gallagher J. Indigenous approaches to health and wellness leadership: A British Columbia First Nations perspective. Healthcare Management Forum. 2019; 32(1): 5-10. doi:10.1177/0840470418788090
- Note de bas de page 5
-
Gouvernement du Canada. Soins de santé pour les Autochtones au Canada. 2021. Disponible sur : https://www.sac-isc.gc.ca/fra/1626810177053/1626810219482
- Note de bas de page 6
-
Regard sur la santé des Premières Nations, des Inuits et des Métis : Une analyse environnementale des organisations, de la documentation et de la recherche, 3e édition 2014. Disponible sur : https://www.ccnsa.ca/fr/publicationsview.aspx?sortcode=1.8.21.0&id=134
- Note de bas de page 7
-
Greenwood M. Determinants of health and Indigenous Peoples. 2017. Disponible en anglais : https://cps.ca/uploads/imich/Plenary_Friday_PM_SDOH_Greenwood.pdf.
- Note de bas de page 8
-
Benkhalti M., Espinoza M., Cookson R., Welch V., Tugwell P., Dagenais P. Development of a checklist to guide equity considerations in health technology assessment. Int J Technol Assess Health Care. 2021; 37:e17. doi: 10,1017/S0266462320002275
- Note de bas de page 9
-
Ismail S.J., Hardy K., Tunis M.C., Young K., Sicard N., Quach C. A framework for the systematic consideration of ethics, equity, feasibility, and acceptability in vaccine program recommendations. Vaccine. 2020; 38(36): 5861-76. doi:10.1016/j.vaccine.2020.05.051
- Note de bas de page 10
-
Tagalik S. Inuit Qaujimajatuqangit : le rôle du savoir autochtone pour favoriser le bien-être des communautés inuites du Nunavut. Centre de collaboration nationale de la santé autochtone (CCNSA), 2012.
- Note de bas de page 11
-
Feeny D., Torrance G., Furlong W. Health utilities index. Quality of Life and Pharmacoeconomics in Clinical Trials. 2nd ed: Lippincourt-Raven Publishers; 1996. p. 239-52.
- Note de bas de page 12
-
Kopec J.A., Williams J.I., To T., Austin P.C. Cross-cultural comparisons of health status in Canada using the Health Utilities Index. Ethn Health. 2001; 6(1): 41-50. doi:10.1080/13557850125061
- Note de bas de page 13
-
Mittmann N., Trakas K., Risebrough N., Liu B.A. Utility scores for chronic conditions in a community-dwelling population. Pharmacoeconomics. 1999; 15(4): 369-76. doi:10.2165/00019053-199915040-00004
- Note de bas de page 14
-
Torrance G.W., Furlong W., Feeny D., Boyle M. Multi-attribute preference functions. Health Utilities Index. Pharmacoeconomics. 1995; 7(6): 503-20. doi:10.2165/00019053-199507060-00005
- Note de bas de page 15
-
Organisation mondiale de la santé (OMS). Documents fondamentaux : Quarante-neuvième édition. 2020.
- Note de bas de page 16
-
Bartlett C., Marshall M., Marshall A. Two-Eyed Seeing and other lessons learned within a co-learning journey of bringing together indigenous and mainstream knowledges and ways of knowing. J Environ Sci Stud. 2012; 2(4): 331-40. doi:10.1007/s13412-012-0086-8
Références
- Note de bas de page 1
-
CADTH. Guidelines for the Economic Evaluation of Health Technologies: Canada 4th edition. 2017.
- Note de bas de page 2
-
Baron J. A theory of social decisions. J Theory Soc Behav. 1995; 25.
- Note de bas de page 3
-
Claxton K., Paulden M., Gravelle H., Brouwer W., Culyer A.J. Discounting and decision making in the economic evaluation of health-care technologies. Health Econ. 2011; 20(1): 2-15. doi:10.1002/hec.1612
- Note de bas de page 4
-
Paulden M., Galvanni V., Ghakraborty S., Kudinga B., McCabe C. Discounting and the evaluation of health care programs. n.d.
- Note de bas de page 5
-
Organisation mondiale de la santé (OMS). Documents fondamentaux : Quarante-neuvième édition. 2020.
- Note de bas de page 6
-
Ismail S.J., Hardy K., Tunis M.C., Young K., Sicard N., Quach C. A framework for the systematic consideration of ethics, equity, feasibility, and acceptability in vaccine program recommendations. Vaccine. 2020; 38(36): 5861-76. doi:10.1016/j.vaccine.2020.05.051
- Note de bas de page 7
-
Comité consultatif national sur les vaccinations (CCNI). Processus d'intégration des données économiques dans les recommandations fédérales relatives aux vaccins Agence de la santé publique du Canada; 2022.
- Note de bas de page 8
-
Jit M., Hutubessy R., Png M.E., Sundaram N., Audimulam J., Salim S., et al. The broader economic impact of vaccination: reviewing and appraising the strength of evidence. BMC Med. 2015; 13: 209. doi:10.1186/s12916-015-0446-9
- Note de bas de page 9
-
Gessner B.D., Kaslow D., Louis J., Neuzil K., O'Brien K.L., Picot V., et al. Estimating the full public health value of vaccination. Vaccine. 2017; 35(46): 6255-63. doi:https://doi.org/10.1016/j.vaccine.2017.09.048
- Note de bas de page 10
-
Brisson M., Drolet M., Malagón T. Inequalities in Human Papillomavirus (HPV)-associated cancers: implications for the success of HPV vaccination. J Natl Cancer Inst. 2013; 105(3): 158-61. doi:10.1093/jnci/djs638
- Note de bas de page 11
-
Brisson M., Drolet M., Malagón T. Inequalities in Human Papillomavirus (HPV)-associated cancers: implications for the success of HPV vaccination. J Natl Cancer Inst. 2013; 105(3): 158-61. doi:10.1093/jnci/djs638
- Note de bas de page 12
-
Park M., Jit M., Wu J.T. Cost-benefit analysis of vaccination: a comparative analysis of eight approaches for valuing changes to mortality and morbidity risks. BMC Med. 2018; 16(1): 139. doi:10.1186/s12916-018-1130-7
- Note de bas de page 13
-
Walker D.G., Hutubessy R., Beutels P. World Health Organization (WHO) Guide for standardisation of economic evaluations of immunization programmes. Vaccine. 2019; 28(11): 2356-9. doi:10.1016/j.vaccine.2009.06.035
- Note de bas de page 14
-
Robinson L., Hammitt J., Cecchini M., Chalkidou K., Claxton K., Cropper M., et al. Reference Case Guidelines for Benefit-Cost Analysis in Global Health and Development. 2019.
- Note de bas de page 15
-
HM Treasury. The Green Book: Central Government Guidance on Appraisal and Evaluation. 2022.
- Note de bas de page 16
-
US Department of Health and Human Services. Guidelines for Regulatory Impact Analysis. 2016.
- Note de bas de page 17
-
US Environmental Protection Agency. Guidelines for Preparing Economic Analyses. 2010.
- Note de bas de page 18
-
Brisson M., Edmunds W.J. The cost-effectiveness of varicella vaccination in Canada. Vaccine. 2002; 20(7-8): 1113-25. doi:10.1016/s0264-410x(01)00437-6
- Note de bas de page 19
-
Christensen H., Hickman M., Edmunds W.J., Trotter C.L. Introducing vaccination against serogroup B meningococcal disease: an economic and mathematical modelling study of potential impact. Vaccine. 2013; 31(23): 2638-46. doi:10.1016/j.vaccine.2013.03.034
- Note de bas de page 20
-
Gambhir M., Clark T.A., Cauchemez S., Tartof S.Y., Swerdlow D.L., Ferguson N.M. A change in vaccine efficacy and duration of protection explains recent rises in pertussis incidence in the United States. PLoS Comput Biol. 2015; 11(4): e1004138. doi:10.1371/journal.pcbi.1004138
- Note de bas de page 21
-
Markowitz L.E., Drolet M., Perez N., Jit M., Brisson M. Human papillomavirus vaccine effectiveness by number of doses: Systematic review of data from national immunization programs. Vaccine. 2018; 36(32 Pt A): 4806-15. doi:10.1016/j.vaccine.2018.01.057
- Note de bas de page 22
-
Agence de la santé publique du Canada (ASPC). Chapitre 2 : Rapport de l'administrateur en chef de la santé publique sur l'état de la santé publique au Canada 2008 - Qu'est-ce que la santé publique? 2008.
- Note de bas de page 23
-
Bärnighausen T., Bloom D.E., Cafiero-Fonseca E.T., O'Brien J.C. Valuing vaccination. Proc Natl Acad Sci U S A. 2014; 111(34): 12313-9. doi:10.1073/pnas.1400475111
- Note de bas de page 24
-
Bärnighausen T., Bloom D.E., Cafiero-Fonseca E.T., O'Brien J.C. Valuing vaccination. Proc Natl Acad Sci U S A. 2014; 111(34): 12313-9. doi:10.1073/pnas.1400475111
- Note de bas de page 25
-
Grimwood K., Anderson P., Anderson V., Tan L., Nolan T. Twelve year outcomes following bacterial meningitis: further evidence for persisting effects. Arch Dis Child. 2000; 83(2): 111-6. doi:10.1136/adc.83.2.111
- Note de bas de page 26
-
Soriano-Gabarró M., Mrukowicz J., Vesikari T., Verstraeten T. Burden of rotavirus disease in European Union countries. Pediatr Infect Dis J. 2006; 25(1 Suppl): S7-s11. doi:10.1097/01.inf.0000197622.98559.01
- Note de bas de page 27
-
Standaert B., Van de Mieroop E., Nelen V. Exploring the potential impact of rotavirus vaccination on work absenteeism among female administrative personnel of the City of Antwerp through a retrospective database analysis. BMJ Open. 2015; 5(6): e007453. doi:10.1136/bmjopen-2014-007453
- Note de bas de page 28
-
Kim D.D., Neumann P.J. Analyzing the Cost Effectiveness of Policy Responses for COVID-19: The Importance of Capturing Social Consequences. Med Decis Making. 2020; 40(3): 251-3. doi:10.1177/0272989x20922987
- Note de bas de page 29
-
Kim D.D., Neumann P.J. Analyzing the Cost Effectiveness of Policy Responses for COVID-19: The Importance of Capturing Social Consequences. Med Decis Making. 2020; 40(3): 251-3. doi:10.1177/0272989x20922987
- Note de bas de page 30
-
Zhu F.-C., Guan X.-H., Li Y.-H., Huang J.-Y., Jiang T., Hou L.-H., et al. Immunogenicity and safety of a recombinant adenovirus type-5-vectored COVID-19 vaccine in healthy adults aged 18 years or older: a randomised, double-blind, placebo-controlled, phase 2 trial. The Lancet. 2020; 396(10249): 479-88. doi:10.1016/S0140-6736(20)31605-6
- Note de bas de page 31
-
Sanders G.D., Neumann P.J., Basu A., Brock D.W., Feeny D., Krahn M., et al. Recommendations for Conduct, Methodological Practices, and Reporting of Cost-effectiveness Analyses: Second Panel on Cost-Effectiveness in Health and Medicine. JAMA. 2016; 316(10): 1093-103. doi:10.1001/jama.2016.12195
- Note de bas de page 32
-
Bärnighausen T., Bloom D.E., Canning D., O'Brien J. Accounting for the full benefits of childhood vaccination in South Africa. S Afr Med J. 2008; 98(11): 842, 4-6.
- Note de bas de page 33
-
Bloom B.S., Bruno D.J., Maman D.Y., Jayadevappa R. Usefulness of US cost-of-illness studies in healthcare decision making. Pharmacoeconomics. 2001; 19(2): 207-13. doi:10.2165/00019053-200119020-00007
- Note de bas de page 34
-
Beck E., Biundo E., Devlin N., Doherty T.M., Garcia-Ruiz A.J., Postma M., et al. Capturing the value of vaccination within health technology assessment and health economics: Literature review and novel conceptual framework. Vaccine. 2022; 40(30): 4008-16. doi:10.1016/j.vaccine.2022.04.050
- Note de bas de page 35
-
Postma M., Biundo E., Chicoye A., Devlin N., Mark Doherty T., Garcia-Ruiz A.J., et al. Capturing the value of vaccination within health technology assessment and health economics: Country analysis and priority value concepts. Vaccine. 2022; 40(30): 3999-4007. doi:https://doi.org/10.1016/j.vaccine.2022.04.026
- Note de bas de page 36
-
Brassel S., Neri M., O'Neill P., Steuten L. Realising the Broader Value of Vaccines in the UK. OHE Consulting Report. 2020.
- Note de bas de page 37
-
Kim S.Y., Goldie S.J. Cost-effectiveness analyses of vaccination programmes : a focused review of modelling approaches. Pharmacoeconomics. 2008; 26(3): 191-215. doi:10.2165/00019053-200826030-00004
- Note de bas de page 38
-
Kim S.Y., Goldie S.J. Cost-effectiveness analyses of vaccination programmes : a focused review of modelling approaches. Pharmacoeconomics. 2008; 26(3): 191-215. doi:10.2165/00019053-200826030-00004
- Note de bas de page 39
-
Pitman R., Fisman D., Zaric G.S., Postma M., Kretzschmar M., Edmunds J., et al. Dynamic transmission modeling: a report of the ISPOR-SMDM Modeling Good Research Practices Task Force--5. Value Health. 2012; 15(6): 828-34. doi:10.1016/j.jval.2012.06.011
- Note de bas de page 40
-
Ultsch B., Damm O., Beutels P., Bilcke J., Brüggenjürgen B., Gerber-Grote A., et al. Methods for Health Economic Evaluation of Vaccines and Immunization Decision Frameworks: A Consensus Framework from a European Vaccine Economics Community. Pharmacoeconomics. 2016; 34(3): 227-44. doi:10.1007/s40273-015-0335-2
- Note de bas de page 41
-
Mauskopf J., Talbird S., Standaert B. Categorization of methods used in cost-effectiveness analyses of vaccination programs based on outcomes from dynamic transmission models. Expert Rev Pharmacoecon Outcomes Res. 2012; 12(3): 357-71. doi:10.1586/erp.12.11
- Note de bas de page 42
-
Mauskopf J., Talbird S., Standaert B. Categorization of methods used in cost-effectiveness analyses of vaccination programs based on outcomes from dynamic transmission models. Expert Rev Pharmacoecon Outcomes Res. 2012; 12(3): 357-71. doi:10.1586/erp.12.11
- Note de bas de page 43
-
Zechmeister I., Blasio B.F., Garnett G., Neilson A.R., Siebert U. Cost-effectiveness analysis of human papillomavirus-vaccination programs to prevent cervical cancer in Austria. Vaccine. 2009; 27(37): 5133-41. doi:10.1016/j.vaccine.2009.06.039
- Note de bas de page 44
-
Attema A.E., Brouwer W.B.F., Claxton K. Discounting in Economic Evaluations. Pharmacoeconomics. 2018; 36(7): 745-58. doi:10.1007/s40273-018-0672-z
- Note de bas de page 45
-
Jit M., Mibei W. Discounting in the evaluation of the cost-effectiveness of a vaccination programme: A critical review. Vaccine. 2015; 33(32): 3788-94. doi:10.1016/j.vaccine.2015.06.084
- Note de bas de page 46
-
Jit M., Mibei W. Discounting in the evaluation of the cost-effectiveness of a vaccination programme: A critical review. Vaccine. 2015; 33(32): 3788-94. doi:10.1016/j.vaccine.2015.06.084
- Note de bas de page 47
-
OECD. Economic Valuation of Environmental Health Risks to Children: OECD Publishing; 2006.
- Note de bas de page 48
-
National Institute for Health and Care Excellence (NICE). Discounting of health benefits in special circumstances. 2011.
- Note de bas de page 49
-
STIKO. Modelling methods for predicting epidemiological and health economic effects of vaccinations - guidance for analyses to be presented to the German Standing Committee on Vaccination (STIKO). 2016.
- Note de bas de page 50
-
Weinstein M.C., Stason W.B. Foundations of cost-effectiveness analysis for health and medical practices. N Engl J Med. 1977; 296(13): 716-21. doi:10.1056/nejm197703312961304
- Note de bas de page 51
-
Gravelle H., Smith D. Discounting for health effects in cost-benefit and cost-effectiveness analysis. Health Econ. 2001; 10(7): 587-99. doi:10.1002/hec.618
- Note de bas de page 52
-
O'Mahony J.F., Postma M.J., Boersma C., Van Rosmalen J., Jit M. Correcting for Multiple Future Cohorts When Applying Differential Discounting of Costs and Health Effects. Society for Medical Decision Making 14th Bienniel European Meeting; 2012.
- Note de bas de page 53
-
O'Mahony J.F., de Kok I.M., van Rosmalen J., Habbema J.D., Brouwer W., van Ballegooijen M. Practical implications of differential discounting in cost-effectiveness analyses with varying numbers of cohorts. Value Health. 2011; 14(4): 438-42. doi:10.1016/j.jval.2010.09.009
- Note de bas de page 54
-
Brennan A., Chick S.E., Davies R. A taxonomy of model structures for economic evaluation of health technologies. Health Econ. 2006; 15(12): 1295-310. doi:10.1002/hec.1148
- Note de bas de page 55
-
Stahl J.E. Modelling methods for pharmacoeconomics and health technology assessment: an overview and guide. Pharmacoeconomics. 2008; 26(2): 131-48. doi:10.2165/00019053-200826020-00004
- Note de bas de page 56
-
Stahl J.E. Modelling methods for pharmacoeconomics and health technology assessment: an overview and guide. Pharmacoeconomics. 2008; 26(2): 131-48. doi:10.2165/00019053-200826020-00004
- Note de bas de page 57
-
Brisson M., Edmunds W.J. Impact of model, methodological, and parameter uncertainty in the economic analysis of vaccination programs. Med Decis Making. 2006; 26(5): 434-46. doi:10.1177/0272989x06290485
- Note de bas de page 58
-
Brisson M., Edmunds W.J. Impact of model, methodological, and parameter uncertainty in the economic analysis of vaccination programs. Med Decis Making. 2006; 26(5): 434-46. doi:10.1177/0272989x06290485
- Note de bas de page 59
-
Brisson M., Edmunds W.J. Impact of model, methodological, and parameter uncertainty in the economic analysis of vaccination programs. Med Decis Making. 2006; 26(5): 434-46. doi:10.1177/0272989x06290485
- Note de bas de page 60
-
Brisson M., Edmunds W.J. Impact of model, methodological, and parameter uncertainty in the economic analysis of vaccination programs. Med Decis Making. 2006; 26(5): 434-46. doi:10.1177/0272989x06290485
- Note de bas de page 61
-
Weinberger D.M., Malley R., Lipsitch M. Serotype replacement in disease after pneumococcal vaccination. Lancet (Londre, Angleterre). 2011; 378(9807): 1962-73. doi:10.1016/S0140-6736(10)62225-8
- Note de bas de page 62
-
Berge J.J., Drennan D.P., Jacobs R.J., Jakins A., Meyerhoff A.S., Stubblefield W., et al. The cost of hepatitis A infections in American adolescents and adults in 1997. Hepatology. 2000; 31(2): 469-73. doi:10.1002/hep.510310229
- Note de bas de page 63
-
Edmunds W.J., Brisson M. The effect of vaccination on the epidemiology of varicella zoster virus. J Infect. 2002; 44(4): 211-9. doi:10.1053/jinf.2002.0988
- Note de bas de page 64
-
Edmunds W.J., Brisson M. The effect of vaccination on the epidemiology of varicella zoster virus. J Infect. 2002; 44(4): 211-9. doi:10.1053/jinf.2002.0988
- Note de bas de page 65
-
Marshall D.A., Burgos-Liz L., MJ I. J., Crown W., Padula W.V., Wong P.K., et al. Selecting a dynamic simulation modeling method for health care delivery research-part 2: report of the ISPOR Dynamic Simulation Modeling Emerging Good Practices Task Force. Value Health. 2015; 18(2): 147-60. doi:10.1016/j.jval.2015.01.006
- Note de bas de page 66
-
Grefenstette J.J., Brown S.T., Rosenfeld R., DePasse J., Stone N.T.B., Cooley P.C., et al. FRED (A Framework for Reconstructing Epidemic Dynamics): an open-source software system for modeling infectious diseases and control strategies using census-based populations. BMC Public Health. 2013; 13(1): 940. doi:10.1186/1471-2458-13-940
- Note de bas de page 67
-
Wolff E., Storsaeter J., Örtqvist Å., Naucler P., Larsson S., Lepp T., et al. Cost-effectiveness of pneumococcal vaccination for elderly in Sweden. Vaccine. 2020; 38(32): 4988-95. doi:10.1016/j.vaccine.2020.05.072
- Note de bas de page 68
-
Ethgen O., Standaert B. Population- versus cohort-based modelling approaches. Pharmacoeconomics. 2012; 30(3): 171-81. doi:10.2165/11593050-000000000-00000
- Note de bas de page 69
-
Vanni T., Karnon J., Madan J., White R.G., Edmunds W.J., Foss A.M., et al. Calibrating models in economic evaluation: a seven-step approach. Pharmacoeconomics. 2011; 29(1): 35-49. doi:10.2165/11584600-000000000-00000
- Note de bas de page 70
-
Vanni T., Karnon J., Madan J., White R.G., Edmunds W.J., Foss A.M., et al. Calibrating models in economic evaluation: a seven-step approach. Pharmacoeconomics. 2011; 29(1): 35-49. doi:10.2165/11584600-000000000-00000
- Note de bas de page 71
-
Vanni T., Karnon J., Madan J., White R.G., Edmunds W.J., Foss A.M., et al. Calibrating models in economic evaluation: a seven-step approach. Pharmacoeconomics. 2011; 29(1): 35-49. doi:10.2165/11584600-000000000-00000
- Note de bas de page 72
-
Taylor D.C., Pawar V., Kruzikas D.T., Gilmore K.E., Sanon M., Weinstein M.C. Incorporating calibrated model parameters into sensitivity analyses: deterministic and probabilistic approaches. Pharmacoeconomics. 2012; 30(2): 119-26. doi:10.2165/11593360-000000000-00000
- Note de bas de page 73
-
van der Steen A., van Rosmalen J., Kroep S., van Hees F., Steyerberg E.W., de Koning H.J., et al. Calibrating Parameters for Microsimulation Disease Models: A Review and Comparison of Different Goodness-of-Fit Criteria. Med Decis Making. 2016; 36(5): 652-65. doi:10.1177/0272989x16636851
- Note de bas de page 74
-
Eddy D.M., Hollingworth W., Caro J.J., Tsevat J., McDonald K.M., Wong J.B. Model transparency and validation: a report of the ISPOR-SMDM Modeling Good Research Practices Task Force--7. Value Health. 2012; 15(6): 843-50. doi:10.1016/j.jval.2012.04.012
- Note de bas de page 75
-
Van de Velde N., Brisson M., Boily M.C. Modeling human papillomavirus vaccine effectiveness: quantifying the impact of parameter uncertainty. Am J Epidemiol. 2007; 165(7): 762-75. doi:10.1093/aje/kwk059
- Note de bas de page 76
-
Ghabri S., Stevenson M., Möller J., Caro J.J. Trusting the Results of Model-Based Economic Analyses: Is there a Pragmatic Validation Solution? Pharmacoeconomics. 2019; 37(1): 1-6. doi:10.1007/s40273-018-0711-9
- Note de bas de page 77
-
Gouvernement du Canada. Calendriers d'immunisation recommandés : Guide canadien d'immunisation. 2020. Disponible sur : https://www.canada.ca/fr/sante-publique/services/publications/vie-saine/guide-canadien-immunisation-partie-1-information-cle-immunisation/page-13-calendriers-immunisation-recommandes.html
- Note de bas de page 78
-
Fine P., Eames K., Heymann D.L. "Herd immunity": a rough guide. Clin Infect Dis. 2011; 52(7): 911-6. doi:10.1093/cid/cir007
- Note de bas de page 79
-
Czerkinsky C., Holmgren J. Vaccines against enteric infections for the developing world. Philos Trans R Soc Lond B Biol Sci. 2015; 370(1671). doi:10.1098/rstb.2015.0142
- Note de bas de page 80
-
Gjini E. Geographic variation in pneumococcal vaccine efficacy estimated from dynamic modeling of epidemiological data post-PCV7. Sci Rep. 2017; 7(1): 3049. doi:10.1038/s41598-017-02955-y
- Note de bas de page 81
-
Plotkin S.A. Complex correlates of protection after vaccination. Clin Infect Dis. 2013; 56(10): 1458-65. doi:10.1093/cid/cit048
- Note de bas de page 82
-
Plotkin S.A. Complex correlates of protection after vaccination. Clin Infect Dis. 2013; 56(10): 1458-65. doi:10.1093/cid/cit048
- Note de bas de page 83
-
Krebs E., Nosyk B. Cost-Effectiveness Analysis in Implementation Science: a Research Agenda and Call for Wider Application. Curr HIV/AIDS Rep. 2021; 18(3): 176-85. doi:10.1007/s11904-021-00550-5
- Note de bas de page 84
-
Andrews N.J., Waight P. A., Burbidge P., Pearce E., Roalfe L., Zancolli M., et al. Serotype-specific effectiveness and correlates of protection for the 13-valent pneumococcal conjugate vaccine: a postlicensure indirect cohort study. Lancet Infect Dis. 2014; 14(9): 839-46. doi:10.1016/s1473-3099(14)70822-9
- Note de bas de page 85
-
Daniels C.C., Rogers P.D., Shelton C.M. A Review of Pneumococcal Vaccines: Current Polysaccharide Vaccine Recommendations and Future Protein Antigens. J Pediatr Pharmacol Ther. 2016; 21(1): 27-35. doi:10.5863/1551-6776-21.1.27
- Note de bas de page 86
-
Malagón T., Drolet M., Boily M.C., Franco E.L., Jit M., Brisson J., et al. Cross-protective efficacy of two human papillomavirus vaccines: a systematic review and meta-analysis. Lancet Infect Dis. 2012; 12(10): 781-9. doi:10.1016/s1473-3099(12)70187-1
- Note de bas de page 87
-
Malagón T., Drolet M., Boily M.C., Franco E.L., Jit M., Brisson J., et al. Cross-protective efficacy of two human papillomavirus vaccines: a systematic review and meta-analysis. Lancet Infect Dis. 2012; 12(10): 781-9. doi:10.1016/s1473-3099(12)70187-1
- Note de bas de page 88
-
Malagón T., Drolet M., Boily M.C., Franco E.L., Jit M., Brisson J., et al. Cross-protective efficacy of two human papillomavirus vaccines: a systematic review and meta-analysis. Lancet Infect Dis. 2012; 12(10): 781-9. doi:10.1016/s1473-3099(12)70187-1
- Note de bas de page 89
-
Malagón T., Drolet M., Boily M.C., Franco E.L., Jit M., Brisson J., et al. Cross-protective efficacy of two human papillomavirus vaccines: a systematic review and meta-analysis. Lancet Infect Dis. 2012; 12(10): 781-9. doi:10.1016/s1473-3099(12)70187-1
- Note de bas de page 90
-
Malagón T., Drolet M., Boily M.C., Franco E.L., Jit M., Brisson J., et al. Cross-protective efficacy of two human papillomavirus vaccines: a systematic review and meta-analysis. Lancet Infect Dis. 2012; 12(10): 781-9. doi:10.1016/s1473-3099(12)70187-1
- Note de bas de page 91
-
Malagón T., Drolet M., Boily M.C., Franco E.L., Jit M., Brisson J., et al. Cross-protective efficacy of two human papillomavirus vaccines: a systematic review and meta-analysis. Lancet Infect Dis. 2012; 12(10): 781-9. doi:10.1016/s1473-3099(12)70187-1
- Note de bas de page 92
-
Cowling B.J., Lim W.W., Perera R., Fang V.J., Leung G. M., Peiris J.S.M., et al. Influenza Hemagglutination-inhibition Antibody Titer as a Mediator of Vaccine-induced Protection for Influenza B. Clin Infect Dis. 2019; 68(10): 1713-17. doi:10.1093/cid/ciy759
- Note de bas de page 93
-
Gilbert P.B., Luedtke A.R. Statistical Learning Methods to Determine Immune Correlates of Herpes Zoster in Vaccine Efficacy Trials. J Infect Dis. 2018; 218(suppl_2): S99-s101. doi:10.1093/infdis/jiy421
- Note de bas de page 94
-
Belshe R.B., Gruber W.C., Mendelman P.M., Mehta H.B., Mahmood K., Reisinger K., et al. Correlates of immune protection induced by live, attenuated, cold-adapted, trivalent, intranasal influenza virus vaccine. J Infect Dis. 2000; 181(3): 1133-7. doi:10.1086/315323
- Note de bas de page 95
-
Bentebibel S.E., Lopez S., Obermoser G., Schmitt N., Mueller C., Harrod C., et al. Induction of ICOS+CXCR3+CXCR5+ TH cells correlates with antibody responses to influenza vaccination. Sci Transl Med. 2013; 5(176): 176ra32. doi:10.1126/scitranslmed.3005191
- Note de bas de page 96
-
Cooper L.V., Boukary R.M., Aseffa A., Mihret W., Collard J.M., Daugla D., et al. Investigation of correlates of protection against pharyngeal carriage of Neisseria meningitidis genogroups W and Y in the African meningitis belt. PLoS One. 2017; 12(8): e0182575. doi:10.1371/journal.pone.0182575
- Note de bas de page 97
-
Plotkin S.A. Correlates of protection induced by vaccination. Clin Vaccine Immunol. 2010; 17(7): 1055-65. doi:10.1128/cvi.00131-10
- Note de bas de page 98
-
Bilcke J., Ogunjimi B., Hulstaert F., Van Damme P., Hens N., Beutels P. Estimating the age-specific duration of herpes zoster vaccine protection: a matter of model choice? Vaccine. 2012; 30(17): 2795-800. doi:10.1016/j.vaccine.2011.09.079
- Note de bas de page 99
-
Bilcke J., Ogunjimi B., Hulstaert F., Van Damme P., Hens N., Beutels P. Estimating the age-specific duration of herpes zoster vaccine protection: a matter of model choice? Vaccine. 2012; 30(17): 2795-800. doi:10.1016/j.vaccine.2011.09.079
- Note de bas de page 100
-
Zoratti M.J., Pickard A.S., Stalmeier P.F.M., Ollendorf D., Lloyd A., Chan K.K.W., et al. Evaluating the conduct and application of health utility studies: a review of critical appraisal tools and reporting checklists. Eur J Health Econ. 2021; 22(5): 723-33. doi:10.1007/s10198-021-01286-0
- Note de bas de page 101
-
Ungar W.J. Challenges in Health State Valuation in Paediatric Economic Evaluation. PharmacoEconomics. 2011; 29(8): 641-52. doi:10.2165/11591570-000000000-00000
- Note de bas de page 102
-
Oliveira C., de Silva N.T., Ungar W.J., Bayoumi A.M., Avitzur Y., Hoch J.S., et al. Health-related quality of life in neonates and infants: a conceptual framework. Quality of Life Research. 2020; 29(5): 1159-68. doi:10.1007/s11136-020-02432-6
- Note de bas de page 103
-
Ungar W.J., editor. Economic evaluation in child health: Oxford University Press; 2019.
- Note de bas de page 104
-
Brazier J., Ara R., Azzabi I., Busschbach J., Chevrou-Séverac H., Crawford B., et al. Identification, Review, and Use of Health State Utilities in Cost-Effectiveness Models: An ISPOR Good Practices for Outcomes Research Task Force Report. Value Health. 2019; 22(3): 267-75. doi:10.1016/j.jval.2019.01.004
- Note de bas de page 105
-
Peasgood T., Brazier J. Is Meta-Analysis for Utility Values Appropriate Given the Potential Impact Different Elicitation Methods Have on Values? PharmacoEconomics. 2015; 33(11): 1101-5. doi:10.1007/s40273-015-0310-y
- Note de bas de page 106
-
Wittenberg E., James L.P., Prosser L.A. Spillover Effects on Caregivers' and Family Members' Utility: A Systematic Review of the Literature. Pharmacoeconomics. 2019; 37(4): 475-99. doi:10.1007/s40273-019-00768-7
- Note de bas de page 107
-
Wittenberg E., James L.P., Prosser L.A. Spillover Effects on Caregivers' and Family Members' Utility: A Systematic Review of the Literature. Pharmacoeconomics. 2019; 37(4): 475-99. doi:10.1007/s40273-019-00768-7
- Note de bas de page 108
-
Wittenberg E., James L.P., Prosser L.A. Spillover Effects on Caregivers' and Family Members' Utility: A Systematic Review of the Literature. Pharmacoeconomics. 2019; 37(4): 475-99. doi:10.1007/s40273-019-00768-7
- Note de bas de page 109
-
Feeny D., Krahn M., Prosser L.A., Salomon J.A. Valuing Health Outcomes. Cost-Effectiveness in Health and Medicine. 2 ed. New York: Oxford University Press; 2016.
- Note de bas de page 110
-
Feeny D., Krahn M., Prosser L.A., Salomon J.A. Valuing Health Outcomes. Cost-Effectiveness in Health and Medicine. 2 ed. New York: Oxford University Press; 2016.
- Note de bas de page 111
-
Shiroiwa T., Fukuda T., Ikeda S., Shimozuma K. QALY and productivity loss: empirical evidence for "double counting". Value Health. 2013; 16(4): 581-7. doi:10.1016/j.jval.2013.02.009
- Note de bas de page 112
-
Shiroiwa T., Fukuda T., Ikeda S., Shimozuma K. QALY and productivity loss: empirical evidence for "double counting". Value Health. 2013; 16(4): 581-7. doi:10.1016/j.jval.2013.02.009
- Note de bas de page 113
-
Shiroiwa T., Fukuda T., Ikeda S., Shimozuma K. QALY and productivity loss: empirical evidence for "double counting". Value Health. 2013; 16(4): 581-7. doi:10.1016/j.jval.2013.02.009
- Note de bas de page 114
-
Basu A. Estimating Costs and Valuations of Non-Health Benefits in Cost-Effectiveness Analysis. Cost-Effectiveness in Health and Medicine. 2 ed. New York: Oxford University Press; 2016.
- Note de bas de page 115
-
Basu A. Estimating Costs and Valuations of Non-Health Benefits in Cost-Effectiveness Analysis. Cost-Effectiveness in Health and Medicine. 2 ed. New York: Oxford University Press; 2016.
- Note de bas de page 116
-
Jacobs P., Budden A., Lee K.M. Guidance document fo rthe costing of health care resources in the Canadian setting. 2nd edition. 2016.
- Note de bas de page 117
-
Feenstra T.L., van Baal P.H., Gandjour A., Brouwer W.B. Future costs in economic evaluation. A comment on Lee. J Health Econ. 2008; 27(6): 1645-9; discussion 50-1. doi:10.1016/j.jhealeco.2008.07.007
- Note de bas de page 118
-
Morton A., Adler A.I., Bell D., Briggs A., Brouwer W., Claxton K., et al. Unrelated Future Costs and Unrelated Future Benefits: Reflections on NICE Guide to the Methods of Technology Appraisal. Health Econ. 2016; 25(8): 933-8. doi:10.1002/hec.3366
- Note de bas de page 119
-
Meltzer D. Accounting for future costs in medical cost-effectiveness analysis. J Health Econ. 1997; 16(1): 33-64. doi:10.1016/s0167-6296(96)00507-3
- Note de bas de page 120
-
Manns B., Meltzer D., Taub K., Donaldson C. Illustrating the impact of including future costs in economic evaluations: an application to end-stage renal disease care. Health Econ. 2003; 12(11): 949-58. doi:10.1002/hec.790
- Note de bas de page 121
-
ICIS. Tendances des dépenses nationales de santé. 2021. Disponible sur : https://www.cihi.ca/fr/tendances-des-depenses-nationales-de-sante.
- Note de bas de page 122
-
Levy A.R., Sobolev B., James D., Barrable W., Clarke-Richardson P., Sullivan S.D., et al. The costs of change: direct medical costs of solid organ transplantation in British Columbia, Canada, 1995-2003. Value Health. 2009; 12(2): 282-92. doi:10.1111/j.1524-4733.2008.00445.x
- Note de bas de page 123
-
Manns B.J., Mendelssohn D.C., Taub K.J. The economics of end-stage renal disease care in Canada: incentives and impact on delivery of care. Int J Health Care Finance Econ. 2007; 7(2-3): 149-69. doi:10.1007/s10754-007-9022-y
- Note de bas de page 124
-
CDC. Guidelines for Evaluating Surveillance Systems. 1988. Available from: https://www.cdc.gov/mmwr/preview/mmwrhtml/00001769.htm.
- Note de bas de page 125
-
Coleman M.S., Garbat-Welch L., Burke H., Weinberg M., Humbaugh K., Tindall A., et al. Direct costs of a single case of refugee-imported measles in Kentucky. Vaccine. 2012; 30(2): 317-21. doi:10.1016/j.vaccine.2011.10.091
- Note de bas de page 126
-
Dalton C.B., Haddix A., Hoffman R.E., Mast E.E. The cost of a food-borne outbreak of hepatitis A in Denver, Colo. Arch Intern Med. 1996; 156(9): 1013-6.
- Note de bas de page 127
-
Dayan G.H., Ortega-Sánchez I.R., LeBaron C.W., Quinlisk M.P. The cost of containing one case of measles: the economic impact on the public health infrastructure--Iowa, 2004. Pediatrics. 2005; 116(1): e1-4. doi:10.1542/peds.2004-2512
- Note de bas de page 128
-
Parker A.A., Staggs W., Dayan G.H., Ortega-Sánchez I.R., Rota P.A., Lowe L., et al. Implications of a 2005 measles outbreak in Indiana for sustained elimination of measles in the United States. N Engl J Med. 2006; 355(5): 447-55. doi:10.1056/NEJMoa060775
- Note de bas de page 129
-
Institut national de sante publique du Québec. Publications. n.d. Disponible sur : https://www.inspq.qc.ca/en/publications/.
- Note de bas de page 130
-
Institut national de sante publique du Québec. Publications. n.d. Disponible sur : https://www.inspq.qc.ca/en/publications/.
- Note de bas de page 131
-
Workplace Safety and Insurance Board. Operational policy manual: travel and related expenses. 2017.
- Note de bas de page 132
-
Doherty M., Buchy P., Standaert B., Giaquinto C., Prado-Cohrs D. Vaccine impact: Benefits for human health. Vaccine. 2016; 34(52): 6707-14. doi:10.1016/j.vaccine.2016.10.025
- Note de bas de page 133
-
Koopmanschap M.A., Rutten F.F., van Ineveld B.M., van Roijen L. The friction cost method for measuring indirect costs of disease. J Health Econ. 1995; 14(2): 171-89. doi:10.1016/0167-6296(94)00044-5
- Note de bas de page 134
-
Krol M., Brouwer W. How to estimate productivity costs in economic evaluations. Pharmacoeconomics. 2014; 32(4): 335-44. doi:10.1007/s40273-014-0132-3
- Note de bas de page 135
-
Pike J., Grosse S.D. Friction Cost Estimates of Productivity Costs in Cost-of-Illness Studies in Comparison with Human Capital Estimates: A Review. Appl Health Econ Health Policy. 2018; 16(6): 765-78. doi:10.1007/s40258-018-0416-4
- Note de bas de page 136
-
Goeree R., O'Brien B.J., Blackhouse G., Agro K., Goering P. The valuation of productivity costs due to premature mortality: a comparison of the human-capital and friction-cost methods for schizophrenia. Can J Psychiatry. 1999; 44(5): 455-63. doi:10.1177/070674379904400505
- Note de bas de page 137
-
Hank K., Stuck S. Volunteer work, informal help, and care among the 50+ in Europe: further evidence for 'linked' productive activities at older ages. Soc Sci Res. 2008; 37(4): 1280-91. doi:10.1016/j.ssresearch.2008.03.001
- Note de bas de page 138
-
Bouwmans C., Krol M., Severens H., Koopmanschap M., Brouwer W., Hakkaart-van Roijen L. The iMTA Productivity Cost Questionnaire: A Standardized Instrument for Measuring and Valuing Health-Related Productivity Losses. Value Health. 2015; 18(6): 753-8. doi:10.1016/j.jval.2015.05.009
- Note de bas de page 139
-
Pearce A. Productivity losses and how they are calculated. In: (CHERE) C.f.H.E.R.a.E., editor. 2016.
- Note de bas de page 140
-
Statistique Canada. Moyenne des heures habituellement et effectivement travaillées durant la semaine de référence selon le genre de travail (temps plein et temps partiel), données annuelles 2021. Disponible sur : https://www150.statcan.gc.ca/t1/tbl1/fr/tv.action?pid=1410004301&request_locale=fr.
- Note de bas de page 141
-
Statistique Canada. Revenu des particuliers selon le groupe d'âge, le sexe et la source de revenu, Canada, provinces et certaines régions métropolitaines de recensement 2021. Disponible sur : https://www150.statcan.gc.ca/t1/tbl1/fr/tv.action?pid=1110023901&request_locale=fr.
- Note de bas de page 142
-
Prosser L.A. SMDM President's Column: Gender bias and cost-effectiveness analysis. 2020. Disponible sur : https://myemail.constantcontact.com/SMDM-Newsletter---Issue-4--September-2020.html?soid=1116971938232&aid=ywAYbDuCkUY.
- Note de bas de page 143
-
Zhang W., Bansback N., Boonen A., Severens J.L., Anis A.H. Development of a composite questionnaire, the valuation of lost productivity, to value productivity losses: application in rheumatoid arthritis. Value Health. 2012; 15(1): 46-54. doi:10.1016/j.jval.2011.07.009
- Note de bas de page 144
-
Grosse S.D., Pike J., Soelaeman R., Tilford J.M. Quantifying Family Spillover Effects in Economic Evaluations: Measurement and Valuation of Informal Care Time. Pharmacoeconomics. 2019; 37(4): 461-73. doi:10.1007/s40273-019-00782-9
- Note de bas de page 145
-
Hoefman R.J., van Exel J., Brouwer W. How to include informal care in economic evaluations. Pharmacoeconomics. 2013; 31(12): 1105-19. doi:10.1007/s40273-013-0104-z
- Note de bas de page 146
-
McKibbin W.J., Fernando R. Global macroeconomic scenarios of the COVID-19 pandemic. CAMA Working Papers. 2020.
- Note de bas de page 147
-
Statistique Canada Dépenses des ménages, Canada, régions et provinces 2021. Disponible sur : https://www150.statcan.gc.ca/t1/tbl1/fr/tv.action?pid=1110022201&request_locale=fr.
- Note de bas de page 148
-
Statistique Canada Le ménage comme unité d'analyse 2020. Disponible sur : https://www150.statcan.gc.ca/n1/pub/13-607-x/2016001/952-fra.htm.
- Note de bas de page 149
-
Statistique Canada Le ménage comme unité d'analyse 2020. Disponible sur : https://www150.statcan.gc.ca/n1/pub/13-607-x/2016001/952-fra.htm.
- Note de bas de page 150
-
Statistique Canada Le ménage comme unité d'analyse 2020. Disponible sur : https://www150.statcan.gc.ca/n1/pub/13-607-x/2016001/952-fra.htm.
- Note de bas de page 151
-
Federal Reserve Bank of Cleveland. Educational attainment and employment. 2011. Disponible sur : https://www.clevelandfed.org/en/newsroom-and-events/publications/economic-trends/2011-economic-trends/et-20110302-educational-attainment-and-employment.aspx.
- Note de bas de page 152
-
US Bureau of Labor Statistics. Earnings and unemployment rates by educational attainment, 2020. 2021.
- Note de bas de page 153
-
Gallagher-Mackay K., Srivastava P., Underwood K., Dhuey E., McCready L., Born K.B., et al. COVID-19 and education disruption in Ontario: emerging evidence on impacts. 2021.
- Note de bas de page 154
-
Grimwood K., Anderson V.A., Bond L., Catroppa C., Hore R.L., Keir E.H., et al. Adverse outcomes of bacterial meningitis in school-age survivors. Pediatrics. 1995; 95(5): 646-56.
- Note de bas de page 155
-
Klein E.Y., Schueller E., Tseng K.K., Morgan D.J., Laxminarayan R., Nandi A. The Impact of Influenza Vaccination on Antibiotic Use in the United States, 2010-2017. Open Forum Infect Dis. 2020; 7(7): ofaa223. doi:10.1093/ofid/ofaa223
- Note de bas de page 156
-
Klugman K.P., Black S. Impact of existing vaccines in reducing antibiotic resistance: Primary and secondary effects. Proc Natl Acad Sci U S A. 2018; 115(51): 12896-901. doi:10.1073/pnas.1721095115
- Note de bas de page 157
-
Pruden A., Larsson D.G.J., Amézquita A., Collignon P., Brandt K.K., Graham D.W., et al. Management options for reducing the release of antibiotics and antibiotic resistance genes to the environment. Environ Health Perspect. 2013; 121(8): 878-85. doi:10.1289/ehp.1206446
- Note de bas de page 158
-
Akenji L., Bengtsson V.T., Lettenmeier M., Fawcett T., YParag Y., Saheb Y., et al. 1.5-degree lifestyles: twoards a cair consumption space for all. Berlin: Hot or Cool Institute, 2021.
- Note de bas de page 159
-
Gouvernement du Canada. Émissions de gaz à effet de serre à l'échelle mondiale. 2022. Disponible sur : https://www.canada.ca/fr/environnement-changement-climatique/services/indicateurs-environnementaux/emissions-gaz-effet-serre-echelle-mondiale.html.
- Note de bas de page 160
-
Gouvernement du Canada. Émissions de gaz à effet de serre à l'échelle mondiale. 2022. Disponible sur : https://www.canada.ca/fr/environnement-changement-climatique/services/indicateurs-environnementaux/emissions-gaz-effet-serre-echelle-mondiale.html.
- Note de bas de page 161
-
Gouvernement du Canada. Déchets solides municipaux : statistiques et tendances. 2020. Disponible sur : https://www.canada.ca/fr/environnement-changement-climatique/services/gestion-reduction-dechets/solides-municipaux/statistiques-tendances.html.
- Note de bas de page 162
-
Briggs A.H., Claxton K., Sculpher M.J. Decision Modelling for Health Economic Evaluation: Oxford University Press; 2006.
- Note de bas de page 163
-
Briggs A.H., Claxton K., Sculpher M.J. Decision Modelling for Health Economic Evaluation: Oxford University Press; 2006.
- Note de bas de page 164
-
Briggs A.H., Weinstein M.C., Fenwick E.A., Karnon J., Sculpher M.J., Paltiel A.D. Model parameter estimation and uncertainty: a report of the ISPOR-SMDM Modeling Good Research Practices Task Force--6. Value Health. 2012; 15(6): 835-42. doi:10.1016/j.jval.2012.04.014
- Note de bas de page 165
-
Mahsin M.D., Deardon R., Brown P. Geographically dependent individual-level models for infectious diseases transmission. Biostatistics. 2020. doi:10.1093/biostatistics/kxaa009
- Note de bas de page 166
-
Popinga A., Vaughan T., Stadler T., Drummond A.J. Inferring epidemiological dynamics with Bayesian coalescent inference: the merits of deterministic and stochastic models. Genetics. 2015; 199(2): 595-607. doi:10.1534/genetics.114.172791
- Note de bas de page 167
-
Vreman R.A., Geenen J.W., Knies S., Mantel-Teeuwisse A.K., Leufkens H.G.M., Goettsch W.G. The Application and Implications of Novel Deterministic Sensitivity Analysis Methods. Pharmacoeconomics. 2021; 39(1): 1-17. doi:10.1007/s40273-020-00979-3
- Note de bas de page 168
-
Sickbert-Bennett E.E., Weber D.J., Poole C., MacDonald P.D., Maillard J.M. Completeness of communicable disease reporting, North Carolina, USA, 1995-1997 and 2000-2006. Emerg Infect Dis. 2011; 17(1): 23-9. doi:10.3201/eid1701.100660
- Note de bas de page 169
-
Mattoo S., Cherry J.D. Molecular pathogenesis, epidemiology, and clinical manifestations of respiratory infections due to Bordetella pertussis and other Bordetella subspecies. Clin Microbiol Rev. 2005; 18(2): 326-82. doi:10.1128/cmr.18.2.326-382,2005
- Note de bas de page 170
-
Lipsitch M., Jha A., Simonsen L. Observational studies and the difficult quest for causality: lessons from vaccine effectiveness and impact studies. Int J Epidemiol. 2016; 45(6): 2060-74. doi:10.1093/ije/dyw124
- Note de bas de page 171
-
Lipsitch M., Jha A., Simonsen L. Observational studies and the difficult quest for causality: lessons from vaccine effectiveness and impact studies. Int J Epidemiol. 2016; 45(6): 2060-74. doi:10.1093/ije/dyw124
- Note de bas de page 172
-
Sterne J. A., Hernán M.A., Reeves B.C., Savović J., Berkman N.D., Viswanathan M., et al. ROBINS-I: a tool for assessing risk of bias in non-randomised studies of interventions. BMJ. 2016; 355: i4919. doi:10.1136/bmj.i4919
- Note de bas de page 173
-
Del Valle S.Y., Hyman J.M., Chitnis N. Mathematical models of contact patterns between age groups for predicting the spread of infectious diseases. Math Biosci Eng. 2013; 10(5-6): 1475-97. doi:10.3934/mbe.2013.10.1475
- Note de bas de page 174
-
Funk S., Bansal S., Bauch C.T., Eames K.T., Edmunds W.J., Galvani A.P., et al. Nine challenges in incorporating the dynamics of behaviour in infectious diseases models. Epidemics. 2015; 10: 21-5. doi:10.1016/j.epidem.2014.09.005
- Note de bas de page 175
-
CDC. Hepatitis A Questions and Answers for Health Professionals. 2020. Disponible sur : https://www.cdc.gov/hepatitis/hav/havfaq.htm.
- Note de bas de page 176
-
Gravitt P.E. The known unknowns of HPV natural history. J Clin Invest. 2011; 121(12): 4593-9. doi:10.1172/jci57149
- Note de bas de page 177
-
Campbell H., Andrews N., Borrow R., Trotter C., Miller E. Updated postlicensure surveillance of the meningococcal C conjugate vaccine in England and Wales: effectiveness, validation of serological correlates of protection, and modeling predictions of the duration of herd immunity. Clin Vaccine Immunol. 2010; 17(5): 840-7. doi:10.1128/cvi.00529-09
- Note de bas de page 178
-
Lewnard J.A., Grad Y.H. Vaccine waning and mumps re-emergence in the United States. Sci Transl Med. 2018; 10(433). doi:10.1126/scitranslmed.aao5945
- Note de bas de page 179
-
CDC. About Meningococcal Vaccines. 2021. Disponible sur : https://www.cdc.gov/vaccines/vpd/mening/hcp/about-vaccine.html.
- Note de bas de page 180
-
Bojke L., Claxton K., Sculpher M., Palmer S. Characterizing structural uncertainty in decision analytic models: a review and application of methods. Value Health. 2009; 12(5): 739-49. doi:10.1111/j.1524-4733.2008.00502.x
- Note de bas de page 181
-
Jackson C.H., Thompson S.G., Sharples L.D. Accounting for uncertainty in health economic decision models by using model averaging. J R Stat Soc Ser A Stat Soc. 2009; 172(2): 383-404. doi:10.1111/j.1467-985X.2008.00573.x
- Note de bas de page 182
-
Hofmann B. Toward a procedure for integrating moral issues in health technology assessment. Int J Technol Assess Health Care. 2005; 21(3): 312-8. doi:10.1017/s0266462305050415
- Note de bas de page 183
-
Krahn M.D., Bielecki J.M., Bremner K. E., de Oliveira C., Almeida N., Clement F., et al. Picturing ELSI+: a visual representation of ethical, legal, and social issues, and patient experiences in Health Technology Assessment in Canada. Int J Technol Assess Health Care. 2020; 36(1): 40-9. doi:10.1017/s0266462319000722
- Note de bas de page 184
-
Agence de la santé publique du Canada (ASPC). Cadre pour la réflexion et la prise de décisions fondées sur l'éthique en santé publique : un outil pour les praticiens de la santé publique, les responsables de l'élaboration de politique et les décideurs. Ottawa, Canada,2017.
- Note de bas de page 185
-
Organisation mondiale de la santé (OMS). Health equity. N.d. Disponible sur : https://www.who.int/health-topics/health-equity#tab=tab_1.
- Note de bas de page 186
-
Rawlins M., Barnett D., Stevens A. Pharmacoeconomics: NICE's approach to decision-making. Br J Clin Pharmacol. 2010; 70(3): 346-9. doi:10.1111/j.1365-2125.2009.03589.x
- Note de bas de page 187
-
Cookson R., Griffin S., Norheim O.F., Culyer A.J. Distributional Cost-Effectiveness Analysis: Quantifying Health Equity Impacts and Trade-Offs: Quantifying Health Equity Impacts and Trade-Offs. Oxford, UK: Oxford University Press; 2020 2020-10.
- Note de bas de page 188
-
Johri M., Norheim O.F. Can cost-effectiveness analysis integrate concerns for equity? Systematic review. Int J Technol Assess Health Care. 2012; 28(2): 125-32. doi:10.1017/s0266462312000050
- Note de bas de page 189
-
Norheim O.F., Baltussen R., Johri M., Chisholm D., Nord E., Brock D., et al. Guidance on priority setting in health care (GPS-Health): the inclusion of equity criteria not captured by cost-effectiveness analysis. Cost Eff Resour Alloc. 2014; 12: 18. doi:10.1186/1478-7547-12-18
- Note de bas de page 190
-
Cookson R., Mirelman A.J., Griffin S., Asaria M., Dawkins B., Norheim O.F., et al. Using Cost-Effectiveness Analysis to Address Health Equity Concerns. Value Health. 2017; 20(2): 206-12. doi:10.1016/j.jval.2016.11.027
- Note de bas de page 191
-
Smith M.J., Thompson A., Upshur R.E.G. Is 'health equity' bad for our health? A qualitative empirical ethics study of public health policy-makers' perspectives. Canadian Journal of Public Health. 2018; 109(5): 633-42. Doi:10.17269/s41997-018-0128-4
- Note de bas de page 192
-
Al M.J., Feenstra T., Brouwer W.B. Decision makers' views on health care objectives and budget constraints: results from a pilot study. Health Policy. 2004; 70(1): 33-48. doi:10.1016/j.healthpol.2004.01.009
- Note de bas de page 193
-
Converge3. Equity, values, and health decisions in Ontario: a Converge3 methods report. 2019.
- Note de bas de page 194
-
O'Neill J., Tabish H., Welch V., Petticrew M., Pottie K., Clarke M., et al. Applying an equity lens to interventions: using PROGRESS ensures consideration of socially stratifying factors to illuminate inequities in health. J Clin Epidemiol. 2014; 67(1): 56-64. doi:10.1016/j.jclinepi.2013.08.005
- Note de bas de page 195
-
Powers M., Powers A.P.P.M., Faden R.R., Faden R.R. Social Justice: The Moral Foundations of Public Health and Health Policy: Oxford University Press; 2006.
- Note de bas de page 196
-
Flannery B., Schrag S., Bennett N.M., Lynfield R., Harrison L.H., Reingold A., et al. Impact of childhood vaccination on racial disparities in invasive Streptococcus pneumoniae infections. Jama. 2004; 291(18): 2197-203. doi:10.1001/jama.291.18.2197
- Note de bas de page 197
-
Agence de la santé publique du Canada (ASPC). Les principales inégalités en santé au Canada. 2018.
- Note de bas de page 198
-
Castle P.E., Zhao F.-H. Population Effectiveness, Not Efficacy, Should Decide Who Gets Vaccinated Against Human Papillomavirus via Publicly Funded Programs. J Infect Dis. 2011; 204(3): 335-7. doi:10.1093/infdis/jir287
- Note de bas de page 199
-
Castle P.E., Zhao F.-H. Population Effectiveness, Not Efficacy, Should Decide Who Gets Vaccinated Against Human Papillomavirus via Publicly Funded Programs. J Infect Dis. 2011; 204(3): 335-7. doi:10.1093/infdis/jir287
- Note de bas de page 200
-
Culyer A.J. Equity of what in healthcare? Why the traditional answers don't help policy--and what to do in the future. Healthc Pap. 2007; 8 Spec No: 12-26. doi:10.12927/hcpap.2007.19216
- Note de bas de page 201
-
Culyer A.J. Equity of what in healthcare? Why the traditional answers don't help policy--and what to do in the future. Healthc Pap. 2007; 8 Spec No: 12-26. doi:10.12927/hcpap.2007.19216
- Note de bas de page 202
-
Veras M., Zakus D. Equity Aspects of Canadian Immunization Programs: Differences within and between countries. 2011. 2011 : 22. doi:10.5195/hcs.2011.45
- Note de bas de page 203
-
Brearley L., Eggers R., Steinglass R., Vandelaer J. Applying an equity lens in the Decade of Vaccines. Vaccine. 2013; 31 Suppl 2: B103-7. doi:10.1016/j.vaccine.2012.11.088
- Note de bas de page 204
-
Brearley L., Eggers R., Steinglass R., Vandelaer J. Applying an equity lens in the Decade of Vaccines. Vaccine. 2013; 31 Suppl 2: B103-7. doi:10.1016/j.vaccine.2012.11.088
- Note de bas de page 205
-
Brearley L., Eggers R., Steinglass R., Vandelaer J. Applying an equity lens in the Decade of Vaccines. Vaccine. 2013; 31 Suppl 2: B103-7. doi:10.1016/j.vaccine.2012.11.088
- Note de bas de page 206
-
Verguet S., Kim J.J., Jamison D.T. Extended Cost-Effectiveness Analysis for Health Policy Assessment: A Tutorial. Pharmacoeconomics. 2016; 34(9): 913-23. doi:10.1007/s40273-016-0414-z
- Note de bas de page 207
-
Verguet S., Kim J.J., Jamison D.T. Extended Cost-Effectiveness Analysis for Health Policy Assessment: A Tutorial. Pharmacoeconomics. 2016; 34(9): 913-23. doi:10.1007/s40273-016-0414-z
- Note de bas de page 208
-
Verguet S., Kim J.J., Jamison D.T. Extended Cost-Effectiveness Analysis for Health Policy Assessment: A Tutorial. Pharmacoeconomics. 2016; 34(9): 913-23. doi:10.1007/s40273-016-0414-z
- Note de bas de page 209
-
Verguet S., Kim J.J., Jamison D.T. Extended Cost-Effectiveness Analysis for Health Policy Assessment: A Tutorial. Pharmacoeconomics. 2016; 34(9): 913-23. doi:10.1007/s40273-016-0414-z
- Note de bas de page 210
-
Tinghög G. Discounting, preferences, and paternalism in cost-effectiveness analysis. Health Care Anal. 2012; 20(3): 297-318. Doi:10.1007/s10728-011-0188-6
- Note de bas de page 211
-
Husereau D., Drummond M., Augustovski F., de Bekker-Grob E., Briggs A.H., Carswell C., et al. Consolidated Health Economic Evaluation Reporting Standards (CHEERS) 2022 Explanation and Elaboration: A Report of the ISPOR CHEERS II Good Practices Task Force. Value Health. 2022; 25(1): 10-31. doi:10.1016/j.jval.2021.10.008
- Note de bas de page 212
-
Gouvernement du Canada. Comité consultatif national de l'immunisation (CCNI) : Composition et représentation 2021. Disponible sur : https://www.canada.ca/fr/sante-publique/services/immunisation/comite-consultatif-national-immunisation-ccni/composition-representation-ccni.html.