Évaluation locale des risques

Télécharger le format de rechange
(format PDF, 1 294 ko, 52 pages)
Organization : Agence de la Santé Publique du Canada
Date publiée : 2018-01-25
Table des matières
- Préface
- Abréviations et sigles
- Chapitre 1 - Introduction
- Chapitre 2 - Évaluations des risques
- Chapitre 3 - Évaluation locale des risques
- Chapitre 4 - Considérations supplémentaires
- Chapitre 5 - Glossaire
- Chapitre 6 - Références et ressources
Préface
Au Canada, les installations où sont manipulés et entreposés des agents pathogènes humains ou des toxines de groupe de risque 2, 3 et 4 sont réglementées par l'Agence de la santé publique du Canada (ASPC) en vertu de la Loi sur les agents pathogènes humains et les toxines (LAPHT) et du Règlement sur les agents pathogènes humains et les toxines (RAPHT). L'importation d'agents zoopathogènes, d'animaux infectés, de produits d'animaux, de sous-produits d'animaux (p. ex. du sang, du sérum), ou d'autres substances qui pourraient porter, en entier ou en partie, un agent zoopathogène ou une toxine est réglementée par l'ASPC ou l'Agence canadienne d'inspection des aliments (ACIA) en vertu de la Loi sur la santé des animaux (LSA) et du Règlement sur la santé des animaux (RSA).
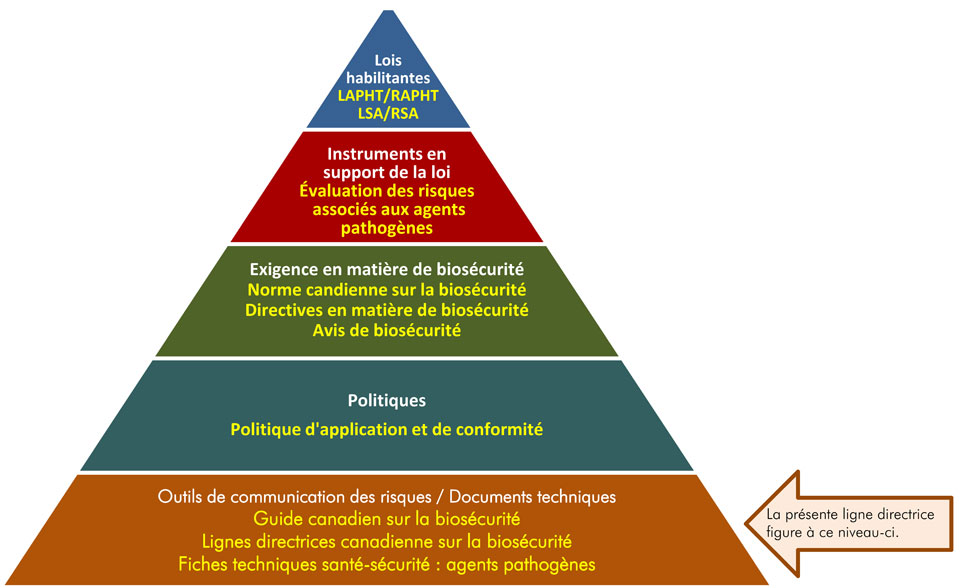
La figure suivante illustre la hiérarchie des documents qu'utilise l'ASPC pour surveiller les activités de biosécurité et de biosûreté.
Équivalent du texte
Figure sous la forme d'une pyramide représentant la hiérarchie des documents utilisée par l'ASPC pour superviser les opérations de biosécurité et de biosûreté. Chacun des cinq niveaux de la pyramide correspond à un type de document, dont l'ordre de préséance augmente du bas vers le haut.
Au sommet, se trouve la législation habilitante, c'est-à-dire la LAPHT, le RAPHT, la LSA et RSA, qui transmet les autorités légales à l'ASPC. Au-dessous des lois et des règlements figurent les Instrument à l'appui de la législation, et ceux-ci sont les évaluations des risques liés aux agents pathogènes. La prochaine étape est intitulée les Exigences en matière de biosécurité, notamment la Norme canadienne sur la biosécurité, les Directives en matière de biosécurité et les Avis de biosécurité. Le deuxième niveau du bas est Documents de politique, soit la Politique de conformité et d'application de la loi. Le matériel d'orientation et les pièces techniques trouvés au bas de la pyramide, sous l'en-tête des Outils de communication des risques et documents techniques, sont visent seulement à résumer les recommandations et les informations scientifiques. Il s'agit notamment du Guide canadien sur la biosécurité, des Lignes directrices canadiennes sur la biosécurité et des Fiches techniques santé-sécurité : agents pathogènes.
Chaque niveau de la pyramide correspond à un type de document. Les documents sont placés en ordre de priorité du haut de la pyramide vers le bas. La législation et les règlements se trouvent au sommet de la pyramide, car ce sont ces documents qui transmettent l'autorité légale à l'ASPC. Le matériel d'orientation et les éléments techniques se trouvent au bas de la pyramide, car ils sont uniquement destinés à résumer les recommandations et les informations scientifiques.
La ligne directrice Évaluation locale des risques a été élaborée par l'ASPC et l'ACIA dans le cadre d'une série de publications électroniques qui s'étendent sur les concepts liés à la biosécurité et la biosûreté présentés dans l'édition actuelle du Guide canadien sur la biosécurité (GCB), soit le document complémentaire à la Norme canadienne sur la biosécurité (NCB). Elle décrit les pratiques exemplaires pour réaliser une évaluation locale des risques dans une organisation où sont manipulés ou entreposés des agents pathogènes humains, des agents zoopathogènes, des toxines ou toute autre matière infectieuse réglementée. L'information présentée dans cette ligne directrice n'existe qu'à titre indicatif pour aider les parties réglementées à satisfaire aux exigences précisées dans la NCB, et ne devrait pas être interprétée comme des exigences. Les parties réglementées peuvent choisir d'autres approches pour satisfaire aux exigences précisées dans la NCB.
Cette ligne directrice est un document en constante évolution et fait continuellement l'objet d'améliorations. L'ASPC et l'ACIA sont ouvertes aux commentaires, aux demandes de clarification et aux suggestions visant l'amélioration des versions subséquentes de ce document. Veuillez envoyer toute information ou suggestion, y compris les références, le cas échéant, à l'adresse de l'ASPC.
Abréviations et sigles
- ACIA
- Agence canadienne d'inspection des aliments
- ASB
- Agent de la sécurité biologique
- ASPC
- Agence de la santé publique du Canada
- ELR
- Évaluation locale des risques
- EPI
- Équipement de protection individuel
- ESB
- Enceinte de sécurité biologique
- GCB
- Guide canadien sur la biosécurité
- GR
- Groupe de risque (c.-à-d. GR1, GR2, GR3, GR4)
- CIB
- Comité institutionnel de biosécurité
- NC
- Niveau de confinement (c.-à-d. NC1, NC2, NC3, NC4)
- NCB
- Norme canadienne sur la biosécurité
- PIU
- Plan d'intervention d'urgence
- PON
- Procédures opératoires normalisées
Chapitre 1 - Introduction
Les termes en caractères gras sont définis dans le glossaire du chapitre 5.
Les procédures nécessaires pour gérer la biosécurité et la biosûreté sont fondées sur une évaluation des risques associés aux dangers potentiels (p. ex. agents pathogènes, toxines, équipement, animaux et procédures) dans chaque installation. Le risque est une fonction de l'éventualité qu'un événement indésirable survienne et les conséquences de cet événement. Les risques associés à la manipulation et l'entreposage d'agents pathogènes et de toxines peuvent être réduits en appliquant les mesures d'atténuation des risques de biosécurité et de biosûreté appropriées établies au cours du processus d'évaluation des risques. Ces mesures d'atténuation peuvent varier des exigences de confinement pour la manipulation d'un agent pathogène particulier aux éléments du programme de biosécurité, tels le programme de formation et le programme de surveillance médicale.
1.1 Portée
La ligne directrice Évaluation locale des risques décrit les pratiques exemplaires pour réaliser une évaluation locale des risques (ELR) dans une organisation où sont manipulés ou entreposés des agents pathogènes humains, des agents zoopathogènes, des toxines ou toute autre matière infectieuse réglementée. Des renseignements sur l'évaluation des risques associés à l'agent pathogène, l'évaluation des risques de biosûreté et l'évaluation globale des risques ont été intégrés à ce document afin d'illustrer que les principes et les mécanismes utilisés pour réaliser des évaluations des risques sont les mêmes, peu importe le type d'évaluation. Néanmoins, les risques associés à l'agent pathogène (p. ex. pathogénicité, voie d'infection) sont toujours pris en compte dans la détermination des risques de biosécurité et de biosûreté. De plus amples renseignements sur l'évaluation des risques sont disponibles aux chapitres 4, 5 et 6 du Guide canadien sur la biosécurité (GCB); les exigences liées aux évaluations des risques sont décrites dans la matrice 4.1 de la Norme canadienne sur la biosécurité (NCB)Note de bas de page 5,Note de bas de page 6.
Bien que les ELR soient obligatoires dans les installations réglementées, l'information présentée dans ce document n'existe qu'à titre indicatif et ne devrait pas être interprétée comme des exigences. Les parties réglementées peuvent choisir d'autres approches pour satisfaire aux exigences précisées dans la NCB.
1.2 Comment utiliser la ligne directrice Évaluation locale des risques
Au début de ce document figure une liste détaillée des abréviations ou sigles utilisés dans cette ligne directrice, accompagnés de leur terme ou nom. Chaque terme et nom sont épelés en entier à leur première apparition dans la ligne directrice, suivi immédiatement de leur abréviation ou sigle entre parenthèses. Après cette définition initiale, leur abréviation ou sigle est utilisé exclusivement dans tout le reste du document. Un glossaire complet des définitions des termes techniques est présenté au chapitre 5 de ce document. Les termes définis dans le glossaire apparaissent en caractères gras à leur première apparition dans la ligne directrice. Une liste de références et d'autres ressources est présentée au chapitre 6.
Afin de faciliter la lecture du présent texte, nous avons employé le masculin comme genre neutre pour désigner aussi bien les femmes que les hommes.
Chapitre 2 - Évaluations des risques
Les évaluations des risques liés à la biosécurité et à la biosûreté visent à identifier et mesurer les dangers potentiels (p. ex. agents pathogènes, toxines, équipement, animaux et procédures) dans le but de réduire les risques identifiés. Elles servent aussi à déterminer si des mesures d'atténuation des risques existantes sont proportionnelles au risque et si elles peuvent être utilisées pour déterminer comment les exigences de la NCB sont appliquées. Le processus d'évaluation des risques déterminera le risque acceptable.
Les évaluations des risques font partie intégrante d'un programme de biosécurité et reposent sur une combinaison de science, de politique et de jugement d'experts. Elles sont effectuées pour plusieurs raisons, dont les suivantes :
- faire connaître les dangers et les risques biologiques;
- déterminer les personnes à risque;
- prioriser les risques et les mesures de contrôle;
- évaluer les exigences physiques en matière de confinement et les exigences opérationnelles applicables de la NCB;
- déterminer le plan de gestion des risques général qu'une organisation devrait élaborer;
- déterminer si les mesures d'atténuation existantes sont adéquates ou si des mesures supplémentaire sont nécessaires; et
- déterminer les besoins en matière de formation.
Différents types d'évaluations des risques sont utilisés pour évaluer les risques associés à la manipulation et à l'entreposage de matières infectieuses et de toxines, dont ceux associés à l'agent pathogène, aux travaux ou aux tâches spécifiques, à la biosûreté et au programme scientifique dans son ensemble. Les concepts et approches clés de l'évaluation des risques et de la gestion des risques peuvent être appliqués universellement à chaque type d'évaluation des risques. La relation entre les différentes évaluations des risques et les stratégies d'atténuation est présentée à la figure 2-1.

Équivalent du texte
Figure démontrant que les évaluations des risques de biosûreté, les évaluations des risques associés à l'agent pathogène et les ELR contribuent toutes au processus d'évaluation globale des risques. Bien que la surveillance médicale, les programmes de formation, les plans d'intervention d'urgence (PIU) et les procédures opératoires normalisées (PON) conformes aux pratiques de travail sécuritaires ne soient pas discutés dans cette ligne directrice, ils sont inclus dans la figure car leur élaboration est fondée sur l'évaluation globale des risques.
Les évaluations des risques de biosûreté, les évaluations des risques associés à l'agent pathogène et les ELR contribuent toutes au processus d'évaluation globale des risques. Bien que la surveillance médicale, les programmes de formation, les plans d'intervention d'urgence (PIU) et les procédures opératoires normalisées (PON) conformes aux pratiques de travail sécuritaires ne soient pas discutés dans cette ligne directrice, leur élaboration est fondée sur l'évaluation globale des risques.
2.1 Évaluation des risques associés à l'agent pathogène
L'évaluation des risques associés à l'agent pathogène caractérise les risques liés à l'agent pathogène en se fondant sur les caractéristiques inhérentes de l'agent pathogène qui contribuent aux risques qu'il pose pour les humains et les animaux. Elle est utilisée pour déterminer la probabilité qu'un agent pathogène ait des effets néfastes sur la santé et la gravité de ces effets. Le processus d'évaluation des risques associés à l'agent pathogène permet de déterminer le groupe de risque de l'agent pathogène et le niveau de confinement approprié pour sa manipulation sûre et sécuritaire. Des exemples d'agents pathogènes humains appartenant au groupe de risque 2 (GR2), au GR3 et au GR4 ainsi que d'agents pathogènes humains interdits sont offerts aux annexes 2, 3, 4 et 5 de la Loi sur les agents pathogènes humains et les toxines (LAPHT), respectivementNote de bas de page 10.
Pour les agents biologiques qui n'ont pas été classés par l'ASPC ou l'ACIA, les parties réglementées peuvent effectuer leur propre évaluation des risques associés à l'agent pathogène afin de déterminer le groupe de risque pour les humains ou les animaux. Le modèle modifiable pour créer une Évaluation des risques associés à l'agent pathogène est disponible en ligne et une fois complété, il peut être soumis à l'ASPC qui le validera en consultation avec l'ACIA. De plus amples renseignements sur l'évaluation des risques associés à l'agent pathogène et sur les groupes de risque sont disponibles au chapitre 4 du GCB.
2.2 Évaluation des risques de biosûreté
Une évaluation des risques de biosûreté sert à identifier, prioriser et atténuer les risques associés à la matière infectieuse et aux toxines manipulées ou entreposées dans une installation. Il s'agit d'une évaluation de la probabilité qu'une perte d'une ressource biologique (p. ex. agent pathogène, toxine, matière infectieuse, équipement, animaux, renseignements) ou qu'un événement intentionnel, tel que le vol, le mésusage, le détournement ou la libération non autorisée de ressources biologiques et connexes (p. ex. personnel, équipement, matière non infectieuse et animaux) se produise et des conséquences de cet événement (p. ex. l'incidence sur la santé de la communauté résultant de la libération non autorisée d'un agent pathogène ou le vol de renseignements exclusifs). L'évaluation des risques de biosûreté diffère de l'évaluation des risques de biosécurité (c.-à-d. les évaluations globale et locale des risques ainsi que les évaluations des risques associés à l'agent pathogène et à la toxine) dans la mesure où les personnes ou les groupes pouvant montrer un intérêt malveillant à l'égard d'une ressource (p. ex. des menaces) doivent également être pris en compte.
De plus, une évaluation des risques de biosûreté doit prendre en compte l'augmentation des exigences de sécurité pour les ressources à possibilité de double usage (c.-à-d. des ressources qui peuvent être utilisées dans le cadre d'activités scientifiques légitimes, mais qui posent aussi un risque de biosûreté accru en raison du potentiel inhérent qu'elles soient utilisées pour créer une arme biologique). Ce type de ressource comprend non seulement les agents biologiques à cote de sécurité élevée (ABCSE), mais aussi les ressources associées à leur manipulation et leur entreposage (p. ex. équipement, information). Des renseignements sur les ABCSE et les étapes pour mener une évaluation des risques de biosûreté sont disponibles au chapitre 6 du GCB.
2.3 Évaluation globale des risques
Une évaluation globale des risques est une évaluation générale de la fonction du programme et des activités prévues, au niveau de l'organisation ou de l'installation, qui permet d'orienter l'élaboration du programme de biosécurité dans son ensemble. Cela peut comprendre plusieurs zones de confinement d'un établissement ou d'une organisation. L'évaluation est effectuée afin d'identifier les dangers au sein de l'organisation ou de l'installation et de déterminer les stratégies de gestion de l'atténuation appropriées (matrice 4.1 de la NCB).
L'évaluation globale des risques est une révision systématique du type de matière biologique qui est ou qui sera manipulée et entreposée (p. ex. groupe[s] de risque des agents pathogènes et des toxines, échantillons primaires, agent pathogène purifié), l'endroit où elle sera manipulée et entreposée (p. ex. laboratoires, salles animalières, salles d'entreposage), le personnel la manipulant (p. ex. étudiants, techniciens subalternes, chercheurs, microbiologistes, boursiers de recherches postdoctorales), le type de travail prévu (p. ex. production à grande échelle, ou à l'échelle du laboratoire; petit ou gros animal; activités de recherche scientifique, d'enseignement ou diagnostiques) et les procédures et équipements divers qui seront utilisés.
L'évaluation globale des risques permet d'orienter l'élaboration des stratégies d'atténuation des risques du programme de biosécurité, notamment d'avoir en place un confinement physique approprié (p. ex. pour le niveau de confinement 2 [NC2], NC3, NC4, prion, zone de confinement de gros animaux, zone de confinement de petits animaux ou aire de production à grande échelle) ainsi que des mesures de contrôle administratives appropriées (p. ex. politiques, gestion du personnel, Manuel de biosécurité, programme de surveillance médicale, plan d'intervention d'urgence [PIU], entretien de l'installation et programme de formation). L'évaluation globale des risques permet de déterminer les enjeux clés au niveau du programme de biosécurité et de répartir les ressources (p. ex. personnel, temps, financement) là où elles sont nécessaires. L'évaluation peut être facilitée par des ELR, lesquelles sont axées sur des éléments particuliers du programme et qui sont décrites au chapitre 3.
Bien que les membres du personnel soient tenus informés au moyen du programme de formation, un plan de communication des risques peut aussi être compris dans les mesures d'atténuation des risques afin d'informer le public au sujet des risques associés à l'installation et ses opérations ainsi que, plus important encore, de l'acceptabilité des risques atténués. Un plan de communication des risques efficace est proactif, commence dès les premières étapes de planification de la construction d'une installation, continue après le début des opérations et peut comprendre le maintien d'un engagement et d'une communication avec le public, et ce, pendant la durée de vie entière de l'installation. La confiance, la transparence et la disponibilité de renseignements de nature non délicate sont des éléments essentiels d'un plan de communication des risques efficace.
2.4 Approche progressive pour effectuer toute évaluation des risques
Peu importe le type d'évaluation des risques, il y a une approche systématique à adopter. Les évaluations locales des risques suivent le cadre de « planifier, faire, vérifier, agir », un système de gestion de qualité utilisé dans le contrôle et l'amélioration continue de processus et de produits, afin de continuellement améliorer l'évaluation des risques et d'évaluer tout incident s'étant produit depuis la mise en œuvre des stratégies d'atténuation des risques. De plus, il est essentiel que ces stratégies n'aient pas introduit de nouveaux dangers. La méthodologie suivante s'applique à tous les types d'évaluations des risques associés à la matière biologique :
Étape 1 : Identification et caractérisation du danger - Reconnaître les dangers potentiels associés à la manipulation ou à l'entreposage d'agents pathogènes et de toxines. Voici des questions qui pourraient être posées :
- Quelle est la fonction du programme de l'organisation ?
- Quels travaux seront entrepris avec des agents pathogènes et des toxines ?
- Y a-t-il des aspects de sécurité associés aux travaux avec les agents pathogènes ou les toxines ?
La possibilité qu'une matière infectieuse ou qu'une toxine cause du mal au personnel, à la communauté et à l'environnement est prise en compte.
Étape 2 : Identification et évaluation des risques - Considérer la possibilité d'exposition, de libération ou de perte de matière infectieuse ou de toxine pour chaque danger, et les conséquence provoquées par un tel incident s'il se produisait. Par exemple :
- Quelle est la probabilité qu'un incident mène à l'infection ou l'intoxication du personnel ou de la communauté, ou à une libération dans l'environnement ?
- Quelles seraient les conséquences de l'incident ?
Déterminer le risque et s'il doit être atténué. Ceci n'est qu'une approximation des catégories de risque, qui peuvent varier de « très faible » à « très élevé ». Les installations peuvent choisir l'échelle qui convient le mieux à leur situation. Par exemple, il existe une échelle de trois niveaux (p. ex. faible, modéré, élevé), une autre de cinq niveaux (p. ex. très faible, faible, modéré, élevé, très élevé), et une échelle numérique (p. ex. 1 à 10, 1 à 100), dans laquelle les nombres plus petits indiquent un risque plus faible.
La matrice de l'évaluation des risques présentée à la figure 2-2 peut être utilisée pour déterminer le risque selon la probabilité qu'un évènement se produise et ses conséquences. Par exemple, le risque associé au pipetage d'un agent pathogène pouvant se transmettre dans l'air peut être évalué. La probabilité qu'il y ait une génération d'aérosols serait estimée de « modérée » à « élevée », selon certains facteurs tels l'appareil utilisé et la compétence de l'exploitant. La conséquence (exposition et infection subséquente) peut varier de « faible » à « très élevée », selon la gravité de la maladie résultant de l'infection. Si un technicien compétent effectuait le pipetage d'une souche de virus grippal saisonnier, le risque serait évalué au niveau « faible ». Si cette même personne effectuait le pipetage d'une souche d'un virus grippal hautement pathogène, le risque pourrait devenir de niveau « élevé ».

Équivalent du texte
Matrice d'évaluation des risques avec la probabilité sur l'axe y et les conséquences sur l'axe x allant de très bas à très élevé. La figure sert à démontrer que les conséquences passent de très bas à élevé lorsqu'un agent plus pathogène est utilisé, ce qui augmente le risque de bas à élevé, même si la probabilité ne change pas.
Le risque peut être évalué en fonction de la probabilité qu'un évènement survienne et les conséquences de ce dernier.
Étape 3 : Élaboration et mise en œuvre de stratégies d'atténuation des risques - Quelles stratégies d'atténuation peuvent être élaborées et mises en œuvre dans le but de réduire les risques à un niveau acceptable ? Dans certains cas, une seule mesure peut suffire, alors que dans d'autres, une combinaison de mesures peut être nécessaire. Cette étape peut aussi servir à évaluer les stratégies d'atténuation existantes afin de déterminer si elles sont suffisantes pour réduire le risque à un niveau acceptable et, dans le cas contraire, de déterminer le nouveau risque atténué. Les mesures d'atténuation à mettre en œuvre peuvent dépendre des ressources disponibles. Si un risque ne peut être suffisamment atténué, un remplacement (p. ex. avec un agent pathogène ou une procédure à plus faible risque) ou l'annulation du travail en question devraient être considérés.
Étape 4 : Révision et amélioration continuelle - La révision régulière de l'évaluation des risques peut permettre de révéler des lacunes et de déterminer si la mise en œuvre de mesures d'atténuation supplémentaires préviendrait qu'un incident se produit ou se reproduit. Tous changements, déficits ou points à améliorer devraient mener à la mise à jour de l'évaluation des risques et des mesures d'atténuation, lorsque requis.
Il n'y a aucune limite de temps particulière attribuée à la révision et la mise à jour des évaluations de risque puisqu'il s'agit d'un processus évolutif. Cependant, les évaluations devraient être révisées à la suite de tous changements ou incidents. Les organisations peuvent établir leurs propres calendriers de révision en adoptant une approche basée sur le risqueNote de bas de page 1.
Les exemples de situations qui pourraient susciter la révision ou la mise à jour d'une évaluation des risques comprennent, entre autres, les suivants :
- l'occurrence des incidents de biosécurité (p. ex. infections et intoxications contractées en laboratoire [ICL], incidents, accidents et ceux évités de justesse);
- l'ajout d'un nouveau danger biologique;
- l'initiation d'un nouveau projet;
- l'ajout d'une nouvelle zone de confinement;
- l'initiation d'une recherche impliquant la possibilité d'un gain de fonction ou de double usage;
- l'utilisation de nouvel équipement;
- la rénovation ou modification d'une installation ou d'équipement, ou une nouvelle construction;
- le changement de modèle, de type ou de fabricant d'équipement de protection individuel (EPI);
- la modification des besoins en personnel (p. ex. ajout d'entrepreneurs, de visiteurs, de bénévoles, d'étudiants);
- la modification des procédures opératoires normalisées (PON) ou des pratiques de travail pouvant affecter le confinement ou le risque d'exposition (p. ex. gestion de la décontamination et des déchets, utilisation et exigences relatives à l'EPI, procédures d'entrée et de sortie);
- la modification de la fonction du programme;
- la modification du déroulement ou de la quantité du travail (p. ex. augmentation du nombre de spécimens à traiter);
- l'identification d'une non-conformité véritable ou potentielle aux exigences internes ou externes (p. ex. registres, nouvelle législation ou nouvelles normes, accidents, expositions).
2.5 Risque acceptable
Le risque acceptable est le risque qu'une organisation accepte de tolérer. Il est fondé sur le postulat selon lequel le risque zéro est impossible. Le risque acceptable est le seuil de tolérance au risque, qui est déterminé par la haute direction. Ce seuil peut être défini tôt dans l'évaluation des risques et ajusté tout au long du processus.
Si le risque est estimé acceptable, les activités peuvent se poursuivre. Si le risque est estimé trop élevé, des stratégies d'atténuation des risques doivent être élaborées et mises en œuvre ou le travail doit être annulé.
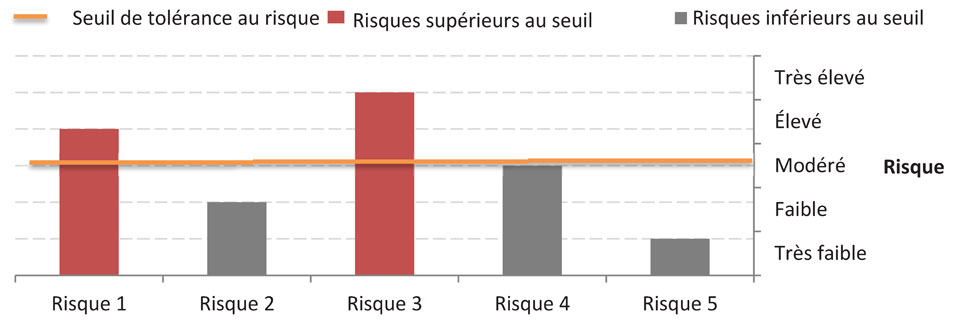
Équivalent du texte
Graphique à barres démontrant cinq risques variant de très bas à très élevé. Lorsque le seuil de tolérance est mis à modéré, les deux risques qui surpassent le seuil (ceux de niveau élevé et très élevé) prescrivent la mise en œuvre de mesures d'atténuation supplémentaires. Les autres risques sont acceptable.
Dans la figure 2-3, le seuil de tolérance au risque a été fixé à « modéré ». Les risques de types « élevé » et « très élevé » surpassent le seuil de tolérance au risque et prescrivent la mise en œuvre de mesures d'atténuation supplémentaires.
| Étape | Évaluation globale des risques | Évaluation des risques associés à l'agent pathogène | Évaluation locale des risques | Évaluation des risques de biosûreté |
|---|---|---|---|---|
| 1. Identification et caractérisation du danger |
|
|
|
|
| 2. Identification et évaluation du risque |
|
|
|
|
| 3. Élaboration et mise en œuvre des stratégies d'atténuation des risques |
|
|
|
|
| 4. Révision et amélioration continuelle |
|
|
|
|
Chapitre 3 - Évaluation locale des risques
Tandis qu'une évaluation des risques globales est une évaluation générale des risques au niveau de l'organisation, les ELR sont des évaluations des risques propres à un endroit particulier et portant sur des activités impliquant des agents pathogènes et des toxines. Elles servent à :
- identifier et caractériser les dangers associés à la matière infectieuse ou aux toxines utilisées ainsi qu'aux activités menées;
- évaluer les risques pour chaque danger et déterminer la probabilité que des incidents pouvant potentiellement causer une exposition, une libération ou une perte d'agents pathogènes et de toxines se produisent, ainsi que les conséquences de ces incidents;
- élaborer et mettre en œuvre des mesures d'atténuation.
Les ELR déterminent quelles stratégies d'atténuation des risques doivent être intégrées dans les procédures du programme et dans la conception de l'installation, selon les activités planifiées, pour la manipulation et l'entreposage sécuritaires de la matière infectieuse et des toxines. Par exemple, les mesures d'atténuation mises en œuvre pour la manipulation sécuritaire d'un agent pathogène au NC2 peuvent être très différentes si le travail ne comporte que quelques millilitres d'un échantillon diagnostique comparativement à la production de 20 litres de culture contenant le même agent pathogène. Par ailleurs, les mesures d'atténuation peuvent varier de façon significative si l'agent pathogène est utilisé lors d'études sur des animaux comparativement à sa manipulation dans un laboratoire.
Les ELR déterminent si les pratiques opérationnelles et le confinement physique existants sont suffisants pour atténuer les risques identifiés à des niveaux acceptables ou si des mesures additionnelles sont nécessaires, parfois dépassant les exigences minimales énoncées dans la NCB. De plus, puisque les exigences énoncées dans la NCB sont fondées sur les risques, les ELR sont utilisées pour déterminer la manière dont plusieurs des exigences sont mises en œuvre. Par exemple, la NCB exige que l'EPI approprié et spécifiquement destiné à chaque zone de confinement soit enfilé conformément aux procédures d'entrée; cependant, l'EPI utilisé et l'endroit où il est enfilé et retiré ainsi que la manière de le faire sont déterminés par une ELR.
Dans le cadre d'une ELR, il est possible qu'une installation réglementée identifie des exemptions relatives à des exigences précises de la NCB. Dans ce cas, les exemptions doivent être approuvées par l'Agence de la santé publique du Canada (ASPC) ou par l'Agence canadienne d'inspection des aliments (ACIA), et l'installation doit démontrer que le but de l'exigence en question a été atteint à l'aide d'un autre mécanisme. Vous pouvez communiquer avec l'ASPC et l'ACIA par courriel aux adresses suivantes : PHAC.pathogens-pathogenes.ASPC@canada.ca; et standardsnormes@inspection.gc.ca.
3.1 Effectuer une évaluation locale des risques
Les sections suivantes suivent les étapes générales d'une évaluation des risques décrites dans la section 2.4, mais elles ont été adaptées spécifiquement pour l'ELR. De plus, un modèle a été intégré à la présente ligne directrice comme exemple, avec des champs supplémentaires remplis étape par étape.
3.1.1 Étape 1 : Identifier et caractériser les dangers liés à la matière infectieuse ou la toxine utilisée et les activités menées
Les activités menées et les dangers propres aux activités sont identifiés et caractérisés. Il est important de diviser chaque activité en étapes afin de tenter de réduire la quantité de travail nécessaire pour chaque ELR. Si une étape est modifiée, seule celle-ci doit être réévaluée, et non la procédure en entier. Par exemple, l'activité d'« entreposage d'une culture souche d'un agent pathogène » pourrait impliquer les étapes suivantes : le pipetage, la centrifugation, l'élimination des déchets liquides et le déplacement d'une matière infectieuse de l'espace de travail au congélateur. Si une étape est commune à d'autres activités ou espaces (p. ex. centrifugation, pipetage), il se peut qu'il ne soit pas nécessaire de la réévaluer, à moins qu'elle ait été modifiée (p. ex. l'utilisation d'un type de centrifugeuse ou de dispositif de pipetage différent, ou l'introduction d'un agent pathogène au profil de risque différent).
Les points suivants sont à prendre en compte :
- Quelles sont la quantité et la concentration de la matière infectieuse ou de la toxine manipulée ou entreposée?
- Quelle est la possibilité qu'un équipement ou des activités génèrent des aérosols?
- Quel est l'état ou la forme de la matière infectieuse ou de la toxine (p. ex. liquide, solide, poudreuse)?
- Le travail implique-t-il des animaux?
- Utilise-t-on des objets pointus ou de verre? Les objets pointus sont-ils manipulés et éliminés de manière adéquate?
- Qui mènera l'activité? (p. ex. chercheur expérimenté, technicien subalterne, étudiant).
Bien que le groupe de risque de l'agent pathogène et le niveau de confinement auquel il doit être manipulé ou entreposé aient été déterminés par l'évaluation des risques associés à l'agent pathogène, certaines caractéristiques propres à l'agent pathogène pourraient devoir être prises en compte dans l'ELR, telles que :
- La façon dont l'agent pathogène pénètre dans les hôtes (c.-à-d. ingestion, inhalation, inoculation, contact avec la peau ou les muqueuses, ou voie génito-urinaire);
- La gamme d'hôtes;
- Le degré de stabilité de l'agent pathogène à l'extérieur de l'hôte. C'est-à-dire, les conditions environnementales dans lesquelles il peut survivre et pour combien de temps.
| Étape 1 : Identification des dangers | Étape 2 : Identification et évaluation des risques | Étape 3 : Élaboration et mise en œuvre de stratégies d'atténuation des risques | Étape 4 : Révision de l'évaluation des risques |
|---|---|---|---|
| Danger | |||
| Des cellules infectées d'un virus sont homogénéisées dans un homogénéisateur en verre. | ND | ND | ND |
3.1.2 Étape 2 : Évaluer le risque
Évaluer les risques potentiels associés à chaque danger propre à une activité. Lors de l'évaluation des risques, il faut prendre en compte la probabilité d'une exposition, d'une libération ou d'une perte d'un agent pathogène ou d'une toxine pour chaque étape et la gravité des conséquences (p. ex. infection, maladie, éclosion) en cas d'exposition, de libération ou de perte. Prioriser les dangers qui posent un risque inacceptable.
L'ELR doit prendre en compte tous les risques potentiels qui pourraient survenir à chaque étape ou tâche de l'activité. Ce faisant, les circonstances et la probabilité qu'un incident mène à une exposition, une libération ou une perte de matière infectieuse ou de toxines seront identifiées.
La personne menant l'activité pourrait aussi devoir être prise en compte, car la probabilité qu'un incident se produise peut dépendre d'elle. Par exemple, la probabilité qu'un incident survienne lorsqu'un étudiant mène une activité de laboratoire pour la première fois est beaucoup plus élevée que si cette même activité est menée par un technicien expérimenté. De la surveillance et des mesures d'atténuation supplémentaires pourraient être nécessaires pour l'étudiant.
| Étape 1 : Identification des dangers | Étape 2 : Identification et évaluation des risques | Étape 3 : Élaboration et mise en œuvre de stratégies d'atténuation des risques | Étape 4 : Révision de l'évaluation des risques | ||
|---|---|---|---|---|---|
| Danger | Scénarios de risque | RisqueNote de bas de page a | Atténuation nécessaire? (O ou N) | ||
| Des cellules infectées d'un virus sont homogénéisées dans un homogénéisateur en verre. | L'homogénéisateur en verre se casse si une trop grande force est exercée. Le travailleur se coupe et se retrouve exposé au virus par la peau endommagée, ce qui pourrait causer une infection. | Modéré à élevé | Oui | ND | ND |
|
|||||
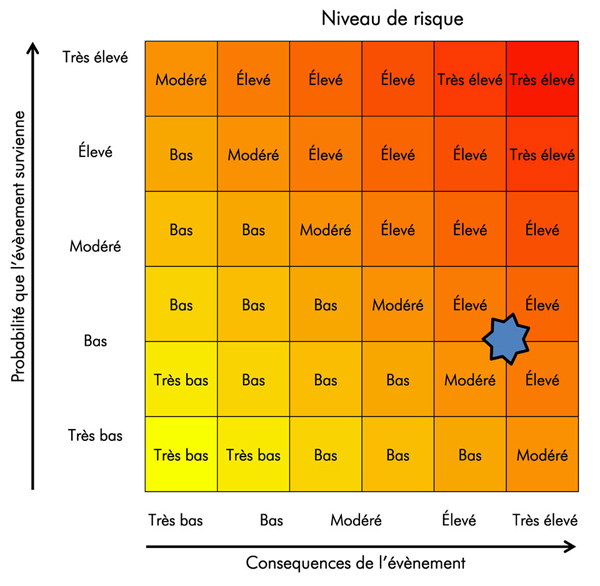
Équivalent du texte
La matrice d'évaluation des risques (présenté dans la figure 2-2) est utilisé pour démontrer graphiquement que le risque pour un opérateur expérimenté utilisant un homogénéisateur intact (probabilité « faible ») avec un agent pathogène très virulent transmissible par contact avec une lésion cutanée (conséquence « élevée » ou « très élevée ») serait de « modéré » à « élevé ».
3.1.3 Étape 3 : Élaborer et mettre en œuvre des stratégies d'atténuation des risques
Une fois les risques associés à chaque étape ou tâche évalués, des mesures d'atténuation abordant tout risque inacceptable (c.-à-d. supérieur au seuil de tolérance au risque) peuvent être mises en œuvre. Il se peut que les mesures d'atténuation en place réduisent les risques identifiés à des niveaux acceptables et qu'une mise en œuvre de mesures supplémentaires ne soit pas nécessaire. Dans l'éventualité où un risque est jugé acceptable ou que la décision de ne pas mettre en œuvre des stratégies d'atténuation est prise, une justification pour cette décision doit être clairement documentée, y compris les personnes impliquées dans le processus et celles ayant approuvé la décision. Si les stratégies d'atténuation ne peuvent pas réduire les risques à des niveaux acceptables, l'activité pourrait devoir être modifiée ou le travail pourrait devoir être annulé.
Il est préférable de mettre en œuvre des mesures afin d'éviter complètement qu'un incident ne se produise (c.-à-d. à la source du danger). Cependant, avoir un mécanisme en place pour contenir la matière infectieuse ou les toxines ou pour prévenir une exposition, une libération ou une perte dans le cas d'un incident (p. ex. contenant secondaire scellé, ESB, EPI) réduira les conséquences de l'incidentNote de bas de page 2. Il existe diverses stratégies pour atténuer les risques, dont les suivantes :
3.1.3.1 Confinement physique
Le confinement physique atténue les risques en respectant des barrières physiques spécifiques fournies par les mesures d'ingénierie et la conception de l'installation. Les mesures d'ingénierie appropriées (énoncées au chapitre 3 de la NCB) devraient déjà être en place, mais l'utilisation de certaines mesures (p. ex. cage de confinement primaire, ESB) peut être fondée sur une ELR. Des exemples de mesures d'ingénierie comprennent, entre autres :
- dispositif de confinement primaire (p. ex. ESB);
- confinement secondaire (p. ex. la barrière de confinement de la zone de confinement);
- ventilation (p. ex. courant d'air vers l'intérieur, filtres HEPA pour traiter l'air évacué);
- technologies de décontamination (p. ex. autoclave, système de décontamination des effluents).
3.1.3.2 Remplacement
Lorsque c'est possible, le remplacement par un agent pathogène à risque plus faible (p. ex. souche atténuée vs souche parentale), une toxine à risque plus faible ou de l'équipement à risque plus faible (p. ex. plastique vs verre) pourrait réduire la dépendance sur les mesures d'ingénierie. Dans certains cas, les mesures d'ingénierie existantes pourraient être suffisantes si l'agent pathogène, la toxine ou l'équipement était remplacé par une alternative à moindre risque.
3.1.3.3 Mesures de contrôle administratives
Les mesures de contrôle administratives sont des pratiques opérationnelles et des PON propres à la zone de confinement ou à la procédure. Des exemples de ces mesures comprennent, entre autres :
- des affiches;
- des PON;
- la sélection et l'utilisation d'EPI;
- des formations.
Afin de sélectionner les mesures d'atténuation appropriées, les avantages et les désavantages de chaque option devraient être comparés. La ou les mesures d'atténuation favorisées devraient toujours convenir au risque et être intégrées dans les PON. Les exigences opérationnelles pour les installations réglementées sont énoncées au chapitre 4 de la NCB.
| Étape 1 : Identification des dangers | Étape 2 : Identification et évaluation des risques | Étape 3 : Élaboration et mise en œuvre de stratégies d'atténuation des risques | Étape 4 : Révision de l'évaluation des risques | |||
|---|---|---|---|---|---|---|
| Danger | Scénarios de risque | Risque | Atténuation nécessaire? (O ou N) | Type(s) de stratégies | Description des stratégies | |
| Des cellules infectées d'un virus sont homogénéisées dans un homogénéisateur en verre. | L'homogénéisateur en verre se casse si une trop grande force est exercée. Le travailleur se coupe et se retrouve exposé au virus par la peau endommagée, ce qui pourrait causer une infection. | Modéré à élevé | Oui | Remplacement | Utiliser un homogénéisateur incassable en plastique ou en acier inoxydable. Utiliser une variante moins pathogène ou non pathogène du virus. |
ND |
| Mesures de contrôle administratives | Mettre en œuvre des pratiques de laboratoire spécifiques lors de l'homogénéisation de cellules infectées dans un homogénéisateur en verre (p. ex. mouvements lents et doux, force minimale et contrôlée). | |||||
| Fournir la formation nécessaire au personnel effectuant l'activité. | ||||||
| Effectuer l'homogénéisation avec des cellules non infectées d'abord jusqu'à ce que la procédure soit maîtrisée. | ||||||
| EPI | Utiliser un EPI propre à l'activité, tel que des gants résistants aux perforations. | |||||
3.1.4 Étape 4 : Réviser et continuellement améliorer l'évaluation des risques
Tout changement au sein de l'installation ou relatif à l'activité a le potentiel d'augmenter le risque. Par conséquent, l'ELR doit être révisée immédiatement après tout incident, y compris ceux évités de justesse, ou après toute modification de la procédure ou de l'équipement. La survenance d'un incident pourrait être une indication que l'ELR n'a pas tenu compte de la probabilité que cet incident se produise ou que les mesures d'atténuation appropriées n'étaient pas en place.
Une révision des ELR sert à confirmer ou réfuter que le risque reste inchangé, que les stratégies d'atténuation des risques mises en œuvre sont appropriées et que des mesures de contrôle supplémentaires ne sont pas nécessaires. Selon le résultat de la révision, une nouvelle ELR ou une mise à jour de celle en place pourrait être nécessaire.
| Étape 1 : Identification des dangers et des risques | Étape 2 : Identification et évaluation des risques | Étape 3 : Élaboration et mise en œuvre de stratégies d'atténuation des risques | Étape 4 : Révision de l'évaluation des risques | |||
|---|---|---|---|---|---|---|
| Danger | Scénarios de risque | Risque | Atténuation nécessaire? (O ou N) | Type(s) de stratégies | Description des stratégies | Révision des stratégies |
| Des cellules infectées d'un virus sont homogénéisées dans un homogénéisateur en verre. | L'homogénéisateur en verre se casse si une trop grande force est exercée. Le travailleur se coupe et se retrouve exposé au virus par la peau endommagée, ce qui pourrait causer une infection. | Modéré à élevé | Oui | Remplacement | Utiliser un homogénéisateur incassable en plastique ou en acier inoxydable. Utiliser une variante moins pathogène ou non pathogène du virus. |
Déterminer si le protocole ou l'équipement a changé. Déterminer si un incident s'est produit depuis la mise en œuvre de la procédure. Au besoin, faire la mise à jour de l'ELR ou en initier une nouvelle. Si aucun changement n'est nécessaire, l'inscrire ainsi. |
| Mesures de contrôle administratives | Mettre en œuvre des pratiques de laboratoire spécifiques lors de l'homogénéisation de cellules infectées dans un homogénéisateur en verre (p. ex. mouvements lents et doux, force minimale et contrôlée). | |||||
| Fournir la formation nécessaire au personnel effectuant l'activité. | ||||||
| Effectuer l'homogénéisation avec des cellules non infectées d'abord jusqu'à ce que la procédure soit maîtrisée. | ||||||
| EPI | Utiliser un EPI propre à l'activité, tel que des gants résistants aux perforations. | |||||
Chapitre 4 - Considérations supplémentaires
4.1 Rôles et responsabilités
Les rôles et responsabilités de toutes les personnes impliquées dans la réalisation d'une évaluation des risques devraient être clairement définis avant que l'évaluation soit amorcée afin que ces personnes sachent ce qui est attendu de leur part. Les rôles peuvent être délégués, mais la haute direction reste ultimement responsable des évaluations des risques et de la mise en œuvre des stratégies d'atténuation appropriées.
Afin d'aborder adéquatement tous les éléments, des personnes dont l'expertise et les responsabilités varient (p. ex. directeur de l'installation, chercheur principal, microbiologiste en chef, agent de la sécurité biologique [ASB], membres du comité institutionnel de biosécurité [CIB], travailleur de laboratoire) devraient être impliquées dans le processus d'évaluation des risques.
La ou les personnes responsables d'effectuer l'évaluation des risques devraient être déterminées tôt dans le processus afin d'aborder les préoccupations, les perceptions, les rôles, les responsabilités et les obligations qu'elles pourraient avoir. Tous les partis et leurs contributions potentielles devraient être pris en compte. Il faut noter que les rôles et les responsabilités diffèrent d'une organisation à l'autre et qu'il n'y a pas de façon universelle d'assigner les tâches et qu'une équipe d'évaluation des risques n'est pas toujours nécessaire ou disponible.
La haute direction et un éventail de membres du personnel pourraient participer dans la réalisation d'une évaluation globale des risques puisque cette dernière examine de manière générale le programme de biosécurité dans son ensemble. Inversement, ce sont souvent seulement celles et ceux qui sont plus étroitement impliqués dans les activités de laboratoire, tels le personnel de laboratoire, les superviseurs, les scientifiques et l'ASB, qui participeront aux ELR puisque les personnes à qui l'équipement, les activités et les procédures sont familiers peuvent mieux identifier les risques.
Le soutien et l'engagement de la haute direction en ce qui concerne l'évaluation et l'atténuation des risques encouragent largement la culture de biosécurité. Lorsque la haute direction démontre son dévouement à la biosécurité, elle donne le ton à toute l'organisation et motive le personnel à suive l'exemple.
4.2 Équipe d'évaluation des risques
Une équipe d'évaluation des risques peut comprendre un ASB, un CIB (au besoin), des directeurs de laboratoire, du personnel (ou un représentant) de laboratoire et la haute direction. Les connaissances et l'expérience de tous les membres de l'équipe devraient être prises en compte et les tâches devraient leur être assignées en conséquence. Bien que les membres participant à l'évaluation des risques puissent changer au cours de la progression vers l'atténuation des risques, une équipe de base devrait demeurer en place pour maintenir les progrès. Dans les installations réglementé par l'ASPC ou l'ACIA, l'ASB doit participer dans le processus d'évaluation des risques, qu'il soit membre de l'équipe ou qu'il travaille indépendamment, puisqu'il lui est exigé de surveiller l'élaboration et le maintien du Manuel de biosécurité et des PON.
Il est essentiel d'assigner les tâches de manière à ce que les membres de l'équipe comprennent la manière dont ils contribueront à l'évaluation des risques et quelle sera leur contribution. Tout manque de connaissances devrait être détecté et comblé par une formation ou par le recrutement de personnel ayant les connaissances adéquates dans les autres secteurs de l'organisation.
Une fois l'équipe d'évaluation des risques formée, une discussion et un accord sur le processus à suivre durant l'évaluation suivront immédiatement. Le processus devrait être adapté à la question et à son contexte tout en demeurant transparent. Une communication efficace assurera la clarté en ce qui concerne le processus suivi, l'information utilisée et les décisions prises. Le processus de documentation devrait être établi le plus tôt possible afin que chaque étape du processus soit documentée (c.-à-d. l'information amassée et les décisions prises à chaque étape).
Chapitre 5 - Glossaire
Il est important de noter que même si certaines des définitions fournies dans le glossaire sont universellement reconnues, beaucoup d'entre elles ont été établies expressément pour la NCB et le GCB et certaines ont été modifiées conformément au contexte de cette ligne directrice. Une liste complète des termes et de leurs définitions est offerte dans les glossaires de la NCB et du GCB.
- Aérosol
- Fines particules solides ou gouttelettes en suspension dans un milieu gazeux (p. ex. l'air); les aérosols peuvent se former lorsqu'une activité provoque un transfert d'énergie dans un liquide ou un semi-liquide.
- Agent de la sécurité biologique (ASB)
- Personne désignée pour superviser les pratiques en matière de biosécurité et de biosûreté dans une installation.
- Agent pathogène
- Microorganisme, acide nucléique ou protéine ayant la capacité de causer une maladie ou une infection chez l'humain ou l'animal. Des exemples d'agents pathogènes humains figurent aux annexes 2 à 4 et à la partie 2 de l'annexe 5 de la Loi sur les agents pathogènes humains et les toxines, mais ils ne constituent pas une liste exhaustive; des exemples d'agents zoopathogènes peuvent être trouvés sur le site Web de l'Agence canadienne d'inspection des aliments.
- Agent zoopathogène
- Agent qui cause des maladies chez les animaux, qu'il soit issu de la biotechnologie ou non. Dans la Norme canadienne sur la biosécurité, le Guide canadien sur la biosécurité, et les Lignes directrices canadiennes sur la biosécurité, le terme « agent zoopathogène » ne réfère qu'à un agent qui cause des maladies chez les animaux terrestres, y compris chez les oiseaux et les amphibiens; toutefois, ce terme ne s'applique pas aux agents qui causent des maladies chez les animaux aquatiques ou les invertébrés.
- Biosécurité
- Ensemble des principes, des technologies et des pratiques liés au confinement mis en œuvre pour prévenir l'exposition involontaire à des matières infectieuses et à des toxines, ou leur libération accidentelle.
- Biosûreté
- Ensemble des mesures visant à prévenir la perte, le vol, le mésusage, le détournement ou la libération intentionnelle d'agents pathogènes, de toxines ou d'autres biens liés à l'installation (p. ex. le personnel, l'équipement, les matières non infectieuses, les animaux).
- Confinement
- Ensemble de paramètres de conception physique et de pratiques opérationnelles visant à protéger le personnel, le milieu de travail immédiat et la communauté contre toute exposition à des matières biologiques. Dans le même contexte, on utilise aussi le terme « bioconfinement ».
- Communauté
- Englobe à la fois la communauté humaine (c.-à-d. le public) et la population animale.
- Danger
- Toute source (chose ou situation) ayant le potentiel de causer du dommage, du mal ou des effets néfastes sur la santé.
- Décontamination
- Procédé qui consiste à traiter des matières et des surfaces pour que leur manipulation soit sécuritaire et qu'elles soient relativement exemptes de microorganismes, de toxines ou de prions. La décontamination s'effectue par désinfection, inactivation ou stérilisation.
- Équipement de protection individuel (EPI)
- Équipement ou vêtement portés par le personnel à titre de barrière contre les matières infectieuses et les toxines afin de réduire le risque d'exposition à celles-ci. Sarraus, blouses, vêtements de protection couvrant toutes les parties du corps, gants, chaussures de sécurité, lunettes de sécurité, masques et appareils de protection respiratoire, tous sont des exemples d'EPI.
- Évaluation des risques associés à l'agent pathogène
- Détermination du groupe de risque et des exigences liées au confinement physique et aux pratiques opérationnelles nécessaires pour manipuler de façon sécuritaire les matières infectieuses ou les toxines concernées.
- Évaluation des risques de biosûreté
- Évaluation des risques qui consiste à répertorier et à classer par ordre de priorité les agents pathogènes, les toxines, les matières infectieuses et les autres ressources (p. ex. l'équipement, les animaux, les renseignements) présents dans une installation, à définir les menaces et les risques associés à ces matières, ainsi qu'à déterminer les stratégies d'atténuation appropriées afin de prévenir le vol, le mésusage, le détournement ou la libération intentionnelle de ces matières.
- Évaluation globale des risques
- Évaluation générale qui soutient le programme de biosécurité dans son ensemble et qui peut englober plusieurs zones de confinement au sein d'un établissement ou d'une organisation. Les stratégies d'atténuation et de gestion des risques tiennent compte du type de programme de biosécurité nécessaire pour prévenir l'exposition du personnel aux agents pathogènes et aux toxines ainsi que la libération de ceux-ci.
- Évaluation locale des risques (ELR)
- Évaluation propre à un endroit en particulier réalisée pour repérer les dangers associés aux activités menées ainsi qu'aux matières infectieuses ou aux toxines utilisées. Cette évaluation permet d'élaborer des stratégies d'atténuation des risques et des stratégies de gestion des risques sur lesquelles on se fondera pour apporter des modifications relativement au confinement physique et aux pratiques opérationnelles dans l'installation concernée.
- Exigence opérationnelle
- Mesure ou procédure administrative appliquées dans une zone de confinement pour protéger le personnel, l'environnement et, ultimement, la communauté contre les matières infectieuses et les toxines. Voir le chapitre 4 de la Norme canadienne sur la biosécurité.
- Exposition
- Contact ou proximité étroite avec des matières infectieuses ou des toxines pouvant respectivement causer une infection ou une intoxication. Les voies d'exposition sont l'inhalation, l'ingestion, l'inoculation et l'absorption.
- Groupe de risque (GR)
- Groupe dans lequel les matières biologiques sont classées en fonction de leurs caractéristiques inhérentes, comme la pathogénicité, la virulence, le risque de propagation et l'existence d'un traitement prophylactique ou thérapeutique efficace. Le groupe de risque énonce le risque pour la santé du personnel et du public ainsi que la santé des animaux et des populations animales.
- Haute direction
- Autorité ultimement responsable de la délégation des pouvoirs appropriés en matière de biosécurité. La haute direction est chargée de s'assurer que le programme de biosécurité dispose de ressources suffisantes, que les exigences légales sont respectées, que l'ordre de priorité des problèmes à l'égard de la biosécurité est bien établi et que ces problèmes sont corrigés adéquatement.
- Incident
- Événement ou situation pouvant causer une blessure, du mal, une infection, une intoxication, une maladie ou un dommage. Les incidents peuvent mettre en cause des matières infectieuses, des animaux infectés ou des toxines. Le déversement, la libération et la perte de matières infectieuses ou de toxines ainsi que l'exposition à celles-ci, la fuite d'un animal, les cas où un employé se blesse ou développe une maladie, l'accès non autorisé à la zone de confinement, une panne de courant, un incendie, une explosion, une inondation ainsi que toutes les autres situations de crise (p. ex. séisme, ouragan) sont des exemples d'incidents. Les accidents et ceux évités de justesse sont considérés comme des incidents.
- Installation
- Structure, bâtiment ou aire définie à l'intérieur d'une structure ou d'un bâtiment dans lesquels sont manipulées ou entreposées des matières infectieuses ou des toxines. Il peut s'agir d'un laboratoire de recherche, d'un laboratoire de diagnostic, d'une aire de production à grande échelle ou d'une zone où on héberge des animaux. Ce terme désigne également une succession de pièces ou un bâtiment contenant plusieurs de ces aires.
- Laboratoire
- Installation même ou aire située à l'intérieur d'une installation dans laquelle on manipule des matières biologiques à des fins scientifiques ou médicales.
- Libération
- Rejet de matières infectieuses ou de toxines hors du système de confinement.
- Manuel de biosécurité
- Manuel propre à une installation dans lequel on décrit les principaux éléments d'un programme de biosécurité (p. ex., plan de biosûreté, formation, équipement de protection individuel).
- Manipulation ou entreposage
- Englobent la possession, la manipulation, l'utilisation, la production, l'entreposage, le transfert, l'importation, l'exportation, la libération, l'élimination ou l'abandon de matières infectieuses ou de toxines, ainsi que le fait de permettre l'accès à de telles substances. La manipulation et l'entreposage englobent donc toutes les activités réglementées comportant des agents pathogènes humains ou des toxines énoncées au paragraphe 7(1) de la Loi sur les agents pathogènes humains et les toxines.
- Matière biologique
- Microorganisme pathogène ou non pathogène, protéine ou acides nucléiques, ou toute autre matière biologique pouvant contenir un de ces éléments, en partie ou en entier. Bactéries, virus, champignons, prions, toxines, organismes génétiquement modifiés, acides nucléiques, échantillons de tissus, échantillons de diagnostic, vaccins vivants et isolats d'un agent pathogène (p. ex. les cultures pures, les suspensions, les spores purifiées), tous sont des exemples de microorganismes.
- Matière infectieuse
- Tout isolat d'un agent pathogène ou toute matière biologique qui contient des agents pathogènes humains ou des agents zoopathogènes, et donc qui représente un risque pour la santé humaine ou animale.
- Niveau de confinement (NC)
- Exigences minimales liées au confinement physique et aux pratiques opérationnelles visant la manipulation sécuritaire de matières infectieuses et de toxines dans les laboratoires, les zones de production à grande échelle et les environnements de travail avec des animaux. Il existe quatre niveaux de confinement, allant du niveau de base (niveau de confinement 1 [NC1]) au niveau le plus élevé (niveau de confinement 4 [NC4]).
- Plan de gestion des risques
- Plan qui jette les bases de la gestion des risques grâce à des dispositions organisationnelles et qui permet de structurer, de mettre en pratique, de surveiller, de réviser et d'améliorer sans cesse les procédures de gestion des risques, et ce, dans toute l'organisation.
- Plan d'intervention d'urgence (PIU)
- Document énonçant les mesures à prendre et les parties responsables en cas d'urgence, par exemple en cas : de déversement, d'exposition ou de libération de matières infectieuses ou de toxines; de fuite d'un animal; de blessure ou de maladie chez un membre du personnel; de panne de courant; d'incendie; d'explosion; ou de toute autre situation d'urgence (p. ex. inondation, tremblement de terre, ouragan).
- Prion
- Petite particule protéique infectieuse généralement associée à la transmission d'un certain groupe de maladies neurodégénératives, à savoir les encéphalopathies spongiformes transmissibles, chez l'humain et l'animal.
- Procédure opératoire normalisée (PON)
- Document qui normalise, en fonction d'une évaluation locale des risques, les procédures et les pratiques de travail sécuritaires utilisées dans le cadre d'activités comportant des matières infectieuses ou des toxines.
- Production à grande échelle
- Activité comportant généralement l'utilisation de volumes de toxines ou de cultures in vitro de matières infectieuses de l'ordre de 10 litres ou plus. Ces activités peuvent se faire avec un seul récipient d'un volume de 10 litres ou plus, ou, selon le procédé et l'agent pathogène concernés, avec plusieurs récipients dont le volume cumulatif est de 10 litres ou plus. La décision d'exiger ou non la conformité aux exigences accrues ou particulières associées aux aires de production à grande échelle pour pouvoir effectuer des activités précises dans une zone de confinement est prise en fonction de chaque cas. La consultation menant à cette décision relève de l'Agence de la santé publique du Canada, de l'Agence canadienne d'inspection des aliments, ou des deux.
- Programme de surveillance médicale
- Programme conçu pour prévenir et déceler les maladies liées à une exposition à des matières infectieuses ou à des toxines chez le personnel. L'accent est principalement mis sur la prévention, mais le programme prévoit un mécanisme d'intervention par lequel une infection potentielle est décelée et traitée avant qu'il n'en résulte une blessure ou une maladie graves.
- Risque
- Probabilité qu'un événement indésirable (p. ex. accident, incident, bris de confinement) survienne et conséquences de cet événement.
- Ressources (biologiques)
- Ensemble des agents pathogènes, des matières infectieuses et des toxines que possède une installation. Les ressources comprennent aussi le matériel, l'équipement, les matières non infectieuses, les animaux, la connaissance et les renseignements (p. ex. les protocoles, les résultats de recherche) ainsi que le personnel d'une installation.
- Toxine (microbienne)
- Substance toxique produite par un microorganisme, ou dérivée de celui-ci, qui peut avoir des effets graves sur la santé humaine ou animale. Les toxines sont énumérées à l'annexe 1 et à la partie 1 de l'annexe 5 de la Loi sur les agents pathogènes humains et les toxines.
- Zone de confinement
- Espace physique qui répond aux exigences liées à un niveau de confinement donné. Il peut s'agir d'une salle unique (p. ex., laboratoire de niveau de confinement 2 [NC2]), d'une série de salles situées dans un même endroit (p. ex. plusieurs espaces de travail en laboratoire de NC2 non adjacents, mais verrouillables) ou d'une série de salles adjacentes (p. ex., salles de niveau de confinement 3 [NC3] comprenant des aires réservées au travail en laboratoire et des salles animalières ou des box séparés). La zone de confinement peut comprendre des zones réservées au soutien, notamment des sas équipés de douches, de vestiaires « propres » et de vestiaires « sales », le cas échéant.
Chapitre 6 - Références et ressources
Notes de bas de page
- Note de bas de page 1
-
Centers for Disease Control and Prevention des États-Unis. (2012) Guidelines for Safe Work Practices in Human and Animal Medical Diagnostic Laboratories. Consulté le 25 juillet 2017 à l'adresse http://www.cdc.gov/mmwr/pdf/other/su6101.pdf Retour à la référence de la note de bas de page13
- Note de bas de page 2
-
Centre canadien d'hygiène et de sécurité au travail. (2016) Fiches d'information Réponses SST. Consulté le 19 mai 2016 à l'adresse http://www.cchst.ca/oshanswers/hsprograms/hazard_control.html
- Note de bas de page 3
-
Department of Health and Human Services des États-Unis, Centers for Disease Control and Prevention des États-Unis et National Institutes of Health des États-Unis. (2009) Biosafety in Microbiological and Biomedical Laboratories, 5e éd., Washington, DC, États-Unis : United States Government Printing Office.
- Note de bas de page 4
-
Gouvernement du Canada. (2000) Cadre décisionnel de Santé Canada pour la détermination, l'évaluation et la gestion des risques pour la santé. Ottawa, ON, Canada : Gouvernement du Canada. Consulté le 25 juillet 2017 à l'adresse https://www.canada.ca/fr/sante-canada/organisation/a-propos-sante-canada/rapports-publications/direction-generale-produits-sante-aliments/cadre-decisionnel-sante-canada-determination-evaluation-gestion-risques-sante.html
- Note de bas de page 5
-
Gouvernement du Canada. (2015) Norme canadienne sur la biosécurité, 2e éd., Ottawa, ON, Canada : Gouvernement du Canada. Disponible à l'adresse https://www.canada.ca/fr/sante-publique/services/normes-lignes-directrices-canadiennes-biosecurite.html
- Note de bas de page 6
-
Gouvernement du Canada. (2016) Guide canadien sur la biosécurité, 2e éd., Ottawa, ON, Canada : Gouvernement du Canada. Disponible à l'adresse https://www.canada.ca/fr/sante-publique/services/normes-lignes-directrices-canadiennes-biosecurite.html
- Note de bas de page 7
-
Gouvernement du Canada. Fiches techniques santé-sécurité : agents pathogènes (FTSSP). Ottawa, ON, Canada : Gouvernement du Canada. Disponible à l'adresse https://www.canada.ca/fr/sante-publique/services/biosecurite-biosurete-laboratoire/fiches-techniques-sante-securite-agents-pathogenes-evaluation-risques.html
- Note de bas de page 8
-
Health and Safety Executive, Advisory Committee on Dangerous Pathogens. (2005). Biological Agents: Managing the risks in laboratories and health care premises. Consulté le 11 mai 2016 à l'adresse http://www.hse.gov.uk/biosafety/biologagents.pdf
- Note de bas de page 9
-
Loi sur la santé des animaux (L.C. 1990, ch. 21). (2015).
- Note de bas de page 10
-
Loi sur les agents pathogènes humains et les toxines (L.C. 2009, ch. 24). (2015).
- Note de bas de page 11
-
Portail d'apprentissage en ligne de l'Agence de la santé publique du Canada. Disponible à l'adresse https://training-formation.phac-aspc.gc.ca/?lang=fr
- Note de bas de page 12
-
Règlement sur la santé des animaux (C.R.C., c. 296). (2015).
- Note de bas de page 13
-
Règlement sur les agents pathogènes humains et les toxines (DORS/2015-44) (2015).
- Note de bas de page 14
-
Sandia National Laboratories, International Biological Threat Reduction. (2009) Risk Assessment for Biosecurity. Consulté le 25 juillet 2017 à l'adresse http://www.biosecurity.sandia.gov/ibtr/subpages/pastConf/20082009/brazil/riskassessment.pdf