Rapport sur le système de surveillance accrue de la résistance de la gonorrhée aux antimicrobiens (SARGA) - Résultats de 2014 et 2015

Télécharger le format de rechange
(Format PDF, 797 ko, 48 pages)
Organisation :
Agence de la santé publique du Canada
Date publiée : 2019-04-29
PROMOUVOIR ET PROTÉGER LA SANTÉ DES CANADIENS GRÂCE AU LEADERSHIP, AUX PARTENARIATS, À L’INNOVATION ET AUX INTERVENTIONS EN MATIÈRE DE SANTÉ PUBLIQUE.
— Agence de la santé publique du Canada
Also available in English under the title:
Report on the Enhanced Surveillance of Antimicrobial-Resistant Gonorrhea (ESAG): Results from 2014 and 2015
Pour obtenir plus d’information, veuillez communiquer avec :
Agence de la santé publique du Canada
Indice de l'adresse 0900C2
Ottawa (Ontario) K1A 0K9
Tél. : 613-957-2991
Sans frais : 1-866-225-0709
Téléc. : 613-941-5366
ATS : 1-800-465-7735
Courriel : publications@hc-sc.gc.ca
© Sa Majesté la Reine du chef du Canada, représentée par la ministre de la Santé, 2019
Date de publication : avril 2019
La présente publication peut être reproduite sans autorisation pour usage personnel ou interne seulement, dans la mesure où la source est indiquée en entier.
Cat. : HP40-206/1-2019F-PDF
ISBN : 978-0-660-30289-8
Pub. : 180944
Tables des matières
- Remerciements
- Principaux messages
- 1.0 Introduction
- 2.0 Méthodologie
- 3.0 Résultats
- 4.0 Discussion
- Références
- Annexe A
- Annexe B
- Annexe C
- Annexe D
Remerciements
L’élaboration et la poursuite du projet de surveillance accrue de la résistance de la gonorrhée aux antimicrobiens (SARGA) et la publication de ce rapport n’auraient pas été possibles sans la collaboration de l’organisme de santé publique Alberta Health Services, le laboratoire provincial de santé publique de l’Alberta, Aînés et Vie active du Manitoba, le laboratoire provincial Cadham, l’autorité sanitaire de la Nouvelle-Écosse – Zone centrale et le Réseau des laboratoires provinciaux de santé publique de la Nouvelle-Écosse. Les auteurs sont également reconnaissants de la contribution des sites sentinelles dans ces provinces.
Ce rapport a été préparé par le Centre de la lutte contre les maladies transmissibles et les infections et le Laboratoire national de microbiologie de la Direction générale de la prévention et du contrôle des maladies infectieuses de l’Agence de la santé publique du Canada (ASPC).
Principaux messages
- Actuellement, Neisseria gonorrhoeae (N. gonorrhoeae), la bactérie qui cause la gonorrhée, est considérée comme une grave menace pour la santé publique, car elle a développé une résistance accrue aux antimicrobiens recommandés pour le traiter.
- L’Agence de la santé publique du Canada a mis en œuvre le programme de surveillance accrue de la résistance de la gonorrhée aux antimicrobiens (SARGA) afin de mieux cerner les tendances actuelles de la résistance de la gonorrhée aux antimicrobiens et d’appuyer l’élaboration de lignes directrices sur le traitement et les interventions de santé publique pour réduire au minimum la propagation de la bactérie N. gonorrhoeae résistante aux antimicrobiens au Canada.
- En 2014 et 2015, des données ont été recueillies dans des sites sentinelles de quatre villes : Calgary, Edmonton, Winnipeg et Halifax. Ces sites sentinelles ont été choisis par les autorités sanitaires provinciales ou locales. Il s’agit de cliniques de santé sexuelle ou de dépistage des infections transmissibles sexuellement (ITS) ou de fournisseurs de soins de santé ayant la capacité de recueillir des cultures à des fins d’essais et de fournir des données épidémiologiques et cliniques améliorées. Elles ont recueilli des cultures à des fins d’essais, conformément aux lignes directrices de leur province.
- En 2014, le programme de SARGA a recueilli 534 cultures à partir de 458 cas. En 2015, 786 cultures ont été obtenues à partir de 660 cas. Une proportion presque égale des cas surveillés dans le cadre de SARGA en 2014 (17 %; 76/458) et en 2015 (16 %; 106/660) comportaient de multiples isolats provenant de différents foyers d’infection.
- La majorité des cas au cours des deux années étaient des hommes (84,5 % en 2014 et 81,7 % en 2015) et des personnes âgées de moins de 40 ans (85,6 % en 2014 et 83,8 % en 2015). La majorité des cas (60,3 %) concernaient des hommes gais, bisexuels et autres hommes ayant des rapports sexuels avec des hommes (gbHARSAHNote de bas de page a) en 2014, tandis qu’un peu moins de la moitié des cas (47,7 %) concernait des gbHARSAH en 2015. À chacune de ces années, presque tous les cas concernaient des femmes déclarant avoir eu des partenaires sexuels masculins.
- Dans l’ensemble, une proportion légèrement plus élevée d’isolats résistant à un ou plusieurs antimicrobiens a été déclarée en 2015 (60,0 %) qu’en 2014 (55,2 %).
- La diminution de la sensibilité au céfixime a diminué dans l’ensemble, passant de 3,5 % en 2014 à 0,8 % en 2015. La diminution de la sensibilité à la ceftriaxone est demeurée constante de 2014 (1,5 %) à 2015 (1,8 %); toutefois, parmi les isolats provenant des gbHARSAH, cette proportion est passée de 1,1 % en 2014 à 2,9 % en 2015. La proportion globale de la résistance à l’azithromycine a diminué, passant de 1,5 % en 2014 à 0,5 % en 2015.
- Chez les gbHARSAH, le traitement privilégié à l’échelle nationale de la ceftriaxone et à l’azithromycine a été systématiquement prescrite plus souvent pour traiter les infections pharyngées que pour traiter les infections anogénitales en 2014 (95,6 % contre 81,6 %) et en 2015 (90,8 % contre 87,2 %). Chez les autres adultes, les deux traitements d’association privilégiés ont été presque également prescrites (44 % pour la combinaison ceftriaxone et azithromycine; 42,7 % pour la combinaison céfixime et azithromycine) pour les infections anogénitales en 2014, tandis qu’en 2015, un changement a été noté de l’utilisation de ceftriaxone et azithromycine (9,1 %) à céfixime et azithromycine (81,9 %).
- En ce qui concerne l’identification moléculaire, ST7638 (20,9 %) était la séquence type (ST) la plus prévalent en 2015, tandis que ST5985 (12,6 %) était la ST le plus prévalent en 2014. ST7638 est la principale ST observée chez les femmes et les non gbHARSAH, et les isolats de ce groupe sont sensibles ou présentent une faible résistance à la tétracycline. ST5985, la ST primaire identifiée chez les gbHARSAH et ces isolats sont des bactéries Neisseria gonorrhoeae résistant à la tétracycline (NGRT) qui affichaient une résistance élevée, par médiation plasmidique.
- Des isolats gonococciques présentant une sensibilité réduite aux céphalosporines ont été identifiés chez des populations à risque élevé et des populations à transmission fréquente comme les gbHARSAH. Étant donné que la céftriaxone et le céfixime (en combinaison avec l’azithromycine) sont les options recommandées pour le traitement de la gonorrhée, la résistance accrue à ces antimicrobiens pourrait déclencher une ère de gonorrhée non traitable à l’aide de l’un ou l’autre de ces antimicrobiens dans le cadre d’un traitement par combinaison. Il est essentiel d’intensifier la surveillance de la résistance aux antimicrobiens (RAM) et d’étendre la couverture géographique de SARGA partout au Canada pour détecter et surveiller toute résistance accrue à ces antimicrobiens.
Introduction
Les taux d’infections transmises sexuellement (ITS) continuent d’augmenter à l’échelle mondiale, y compris au Canada. La gonorrhée est l’ITS résistante aux médicaments la plus fréquemment signalée et la deuxième infection bactérienne transmissible sexuellement en fréquence au Canada, avec plus de 19 000 cas déclarés en 2015Note de bas de page 1. On sait depuis longtemps que le micro-organisme responsable, Neisseria gonorrhoeae (N. gonorrhoeae), se développe rapidement et efficacement une résistance aux antimicrobiens (RAM) par diverses adaptations évolutivesNote de bas de page 2. En 2012, les augmentations de la sensibilité à la classe d’antibiotiques appelés les céphalosporines observées en laboratoire ont donné lieu à des nouvelles recommandations pour le traitement de la gonorrhée dans les Lignes directrices canadiennes sur les infections transmissibles sexuellement. Depuis, le traitement de première intention recommandé pour la gonorrhée anogénitale non compliquée chez les hommes gais, bisexuels et autres hommes ayant des rapports sexuels avec des hommes (gbHARSAH) et de la gonorrhée pharyngée chez tous les adultes est une thérapie par combinaison de 250 mg de ceftriaxone injectée par voie intramusculaire et de 1 g d’azithromycine ingérée par voie oraleNote de bas de page 3. En 2012, l’Organisation mondiale de la Santé (OMS) a qualifiée que la résistance aux médicaments de N. gonorrhoeae pourrait la faire évoluer en une « super bactérie »Note de bas de page 4 et que la gonorrhée pourrait devenir non traitable en raison de la résistance à toutes les classes d’antimicrobiensNote de bas de page 5. De plus, en 2013, le directeur des Centers for Disease Control and Prevention (CDC) des États-Unis l’a décrit comme étant l’une des trois principales menaces les plus graves pour la santé publique aux États-UnisNote de bas de page 6. Des échecs de traitement à double modalité ont également été signalés au CanadaNote de bas de page 7. La gestion de la résistance aux antimicrobiens a été définie comme étant une priorité dans le Rapport sur les plans et les priorités de 2017-2018 de l’Agence de la santé publique du Canada (ASPC)Note de bas de page 8, le Profil de risque du Ministère, le Plan opérationnel de l’ASPC, ainsi que dans l’étude du Comité permanent de la santé (HESA) sur l’état de la résistance aux antimicrobiens au Canada et les recommandations connexesNote de bas de page 9. Cela a également été mis en évidence dans les rapports du Système canadien de surveillance de la résistance aux antimicrobiens (SCSRA)Note de bas de page 10 de l’Agence ainsi que dans son Cadre d’action pancanadien sur les ITSS : réduction des répercussions sur la santé des infections transmissibles sexuellement et par le sang au Canada d’ici 2030Note de bas de page 11.
Les tests de résistance aux antimicrobiens sont un élément important de la surveillance des infections gonococciques (IG), car ils permettent 1) d’identifier et de caractériser les isolats résistants en circulation; et 2) de noter les changements dans la proportion des isolats résistants, ce qui est essentiel pour orienter les lignes directrices relatives au traitement clinique. À l’heure actuelle, les laboratoires régionaux des dix provinces ont recours aux cultures pour une proportion du nombre total de tests de dépistage de la gonorrhée réalisés sur leur territoire, mais le test d’amplification des acides nucléiques (TAAN) est la méthode de dépistage recommandée pour le diagnostic dans certaines de ces provinces. L’utilisation de cultures pour les tests de résistance aux antimicrobiens (RAM) est une pratique de laboratoire standard pour tous les isolats de gonorrhée positifs détectés par la mise en culture à l’échelle mondiale, y compris au Canada. Toutefois, comme la majorité des cas d’IG (70 %) ne sont pas consignés, les données sur la RAM ne sont pas disponibles pour ces casNote de bas de page 12. La plupart des provinces et des territoires disposant de laboratoires provinciaux qui font la mise en culture réalisent aussi des tests de résistance aux antimicrobiens sur toutes les cultures positives. Les isolats résistants ainsi que tous les isolats prélevés dans les provinces et les territoires qui ne réalisent pas de tests de résistance aux antimicrobiens sont envoyés par les laboratoires provinciaux au Laboratoire national de microbiologie (LNM) qui effectue une série normalisée de tests de résistance aux antimicrobiens sur les isolats. Cependant, les provinces et les territoires déterminent les isolats qui doivent être soumis au LNM, et les critères de sélection ne sont pas toujours uniformes, ce qui se traduit par un manque de représentativité. Le LNM procède aussi au typage NG-MAST de N. gonorrhoeae pour décrire les souches de gonorrhée en circulation dans l’ensemble du Canada. Les seules données épidémiologiques recueillies sur ces isolats sont le sexe et l’âge du patient, sa province de résidence et le siège anatomique de l’infection.
Bien que la gonorrhée soit une maladie à déclaration obligatoire au Canada depuis 1924, la quantité et la qualité des données recueillies et déclarées à l’ASPC dans le contexte de la surveillance de routine sont limitées. On ne dispose pas de données épidémiologiques exhaustives à l’échelle nationale sur les isolats de gonorrhée résistants, ce qui limite la capacité d’évaluer les facteurs de risque associés à la résistance aux antimicrobiens et d’orienter les recommandations nationales en matière de traitement. De plus, la recherche d’un dénominateur valide pour estimer la prévalence et les profils de résistance aux antimicrobiens au Canada présente des difficultés importantes. L’établissement d’une approche pancanadienne normalisée de la surveillance des gonocoques résistants aux antimicrobiens, combinant des données épidémiologiques et de laboratoire, assurerait une meilleure représentation à l’échelle du pays et une plus grande confiance dans l’estimation de la proportion d’isolats résistants aux médicaments. Conjuguée à la séquence NG-MAST et à l’amélioration de la qualité des données, cette approche permettrait également de détecter les grappes inhabituelles, de faciliter une intervention plus rapide en cas d’éclosion et de concevoir des lignes directrices de traitement fondées sur des données probantes.
En 2013, le Centre de lutte contre les maladies transmissibles et les infections (CLMTI), en partenariat avec le LNM et trois provinces (l’Alberta, le Manitoba et la Nouvelle-Écosse), a lancé la phase pilote de surveillance accrue de la résistance de la gonorrhée aux antimicrobiens (SARGA). L’Alberta, qui recueillait déjà des données sur la résistance aux antimicrobiens de N. gonorrhoeae (RAM-IG), a été la première province à prendre part à cette surveillance. Winnipeg et la Régie régionale de la santé Capital de la Nouvelle-Écosse (désormais l’autorité sanitaire de la Nouvelle-Écosse – Zone centrale) ont commencé à recueillir des données en 2014. Les autres provinces et territoires ont exprimé leur intérêt à participer à la SARGA et reconnaissent que la SARGA pourrait être intégrée à leurs activités de surveillance existantes.
1.1 Objectifs du projet
L’objectif global de ce système intégré de surveillance épidémiologique et de surveillance des laboratoires consiste à améliorer la compréhension des niveaux et des tendances actuels de résistance de la gonorrhée aux antimicrobiens au Canada et à fournir de meilleures preuves afin d’orienter l’élaboration de lignes directrices sur le traitement et les interventions de santé publique pour réduire au minimum la propagation de la bactérie N. gonorrhoeae résistante aux antimicrobiens.
1.2 Éléments livrables du projet
Les objectifs de ce système de surveillance sont :
- Augmenter le nombre de cultures pour la gonorrhée effectuées aux sites sentinelles participants afin d’améliorer la surveillance de la résistance de la gonorrhée aux antimicrobiens;
- Surveiller la sensibilité de N. gonorrhoeae aux antimicrobiens pour les cas récemment diagnostiqués par culture ainsi que les cas d’échec au traitement potentielNote de bas de page b;
- Recueillir des données supplémentaires épidémiologiques (caractéristiques démographiques et facteurs de risque) sur les personnes ayant fourni des échantillons aux fins d’une culture pour la gonorrhée, y compris les cas de gonorrhée nouvellement diagnostiquée par culture et les cas d’échec au traitement, afin de déterminer les facteurs de risque pour la résistance de la gonorrhée aux antimicrobiens au sein de cette population;
- Recueillir des données sur les médicaments prescrits pour traiter la gonorrhée; Déterminer les séquences types de N. gonorrhoeae résistantes aux antimicrobiens en circulation au moyen de la méthode NG-MAST.
2.0 Méthodologie
2.1 Définitions de cas
La définition nationale de cas de gonorrhée a été utilisée et comprend une preuve de laboratoire de détection de Neisseria gonorrhoeae par culture ou par test d’amplification des acides nucléiques (TAAN)Note de bas de page 13.
Un « cas de SARGA » fait référence à tout patient âgé de 16 ans et plus qui un échantillon ou tous les échantillons prélevés dans les 30 derniers jours correspondent à la définition nationale de cas de gonorrhée. Toutes les cultures positives des sites sentinelles participants ont été incluses dans la SARGA.
La définition pour un cas d’échec au traitement est l’absence de contact sexuel pendant la période suivant le traitement ET la présence de l’une des conditions suivantes: 1) des diplocoques intracellulaires gram négatifs pendant au moins 72 heures après le traitement; 2) une culture positive pour N. gonorrhoeae au moins 72 heures après le traitement; ou 3) un TANN positif pour N. gonorrhoeae au moins 2 à 3 semaines après le traitementNote de bas de page 3.
2.2 Collecte des données
Les données ont été recueillies dans les sites sentinelles de quatre villes : Calgary, Edmonton, Winnipeg et Halifax. Les sites sentinelles ont été choisis par les autorités sanitaires provinciales ou locales participantes et regroupaient des cliniques de santé sexuelle, des cliniques de traitement des infections transmissible sexuellement ou des fournisseurs de soins de santé qui étaient en mesure de recueillir des cultures aux fins d’analyse et de fournir des données épidémiologiques et cliniques améliorées. Les cultures ont été recueillies par les sites sentinelles conformément aux lignes directrices provinciales sur les tests de dépistage de la gonorrhée. Dans la mesure du possible, le nombre de cultures gonococciques a été augmenté afin d’améliorer la surveillance de la gonorrhée résistante aux antimicrobiens.
Les données ont été extraites des formulaires de déclaration de cas détectés par la surveillance accrue ou de routine des cas de gonorrhée admissibles à la SARGA signalés aux responsables de la santé publique par les sites sentinelles participants. Les éléments de données recueillis en tant que renseignements épidémiologiques comprenaient des renseignements sur les caractéristiques démographiques (p. ex. l’âge, le sexe, le foyer d’infection et la province), les partenaires sexuels, les comportements à risque, les raisons de la consultation et le traitement. Ces données ont ensuite été reliées aux données des analyses de laboratoire du LNM, comme les données sur la sensibilité aux antimicrobiens et le typage génomique, qui sont décrites plus en détail ci-dessous.
Les sites sentinelles ont envoyé des isolats aux laboratoires provinciaux de santé publique pour faire l’objet de tests de sensibilité aux antimicrobiens; ces isolats ont ensuite été acheminés au LNM qui a réalisé le typage génomique et les tests de sensibilité sur un large groupe d’antimicrobiens. Tous les isolats provenant des administrations comptant sur le LNM pour effectuer leurs tests de sensibilité ont été envoyés au LNM aux fins d’analyse. Les données sur les isolats répondant aux critères d’admissibilité ont été soumises au programme de SARGA. Des données épidémiologiques ont également été présentées pour tous les isolats sensibles; cependant, seulement environ la moitié des isolats sensibles ont été envoyés au LNM pour un nouveau test.
Les données épidémiologiques et les données de laboratoire ont été saisies ou téléchargées dans une base de données contenant des filtres sélectionnés par les villes, protégée par un mot de passe et accessible sur le Web, qui est hébergée sur la plateforme du Réseau canadien de renseignements sur la santé publique (RCRSP). Les mesures nécessaires ont été prises pour s’assurer de l’exactitude des liens entre les données épidémiologiques saisies par les sites sentinelles et les résultats de laboratoire saisis par le LNM dans cette base de données. Un numéro d’identification désigné au lieu du nom du patient a été utilisé pour corréler les données.
2.3 Méthodes de laboratoire
Tests de sensibilité aux antimicrobiens pour les isolats
La concentration minimale inhibitrice (CMI), soit la concentration minimale d’un antibiotique qui inhibe la croissance de l’organisme, a été déterminée pour la ceftriaxone, le céfixime, l’azithromycine, la ciprofloxacine, l’érythromycine, la pénicilline, la tétracycline et la spectinomycine pour ce qui est de tous les isolats de N. gonorrhoeae à l’aide de la dilution en gélose ou, pour les isolats sensibles de l’Alberta non envoyés au LNM, à l’aide d’Etest® (Biomerieux, Laval, Québec). Les interprétations étaient fondées sur les valeurs seuils du Clinical and Laboratory Standards Institute (CLSI)Note de bas de page 14 sauf dans les cas suivants : sensibilité réduite au céfixime (CMI ≥ 0,25 mg/L)Note de bas de page 4; sensibilité réduite à la ceftriaxone (CMI ≥ 0,125 mg/L)Note de bas de page 4 résistance à l’azithromycine (CMI ≥ 2,0 mg/L)Note de bas de page 15; la résistance à l’érythromycine (CMI ≥ 2,0 mg/L)Note de bas de page 16 (voir les annexes A et B pour plus de détails).
Typage génomique des isolats
Le typage génomique a été déterminé à l’aide de la méthode NG-MAST (N. gonorrhoeae multi-antigen sequence typing)Note de bas de page 17 qui allie l’amplification du gène de la porine (por) et du gène de la protéine B liant la transferrine (tbpB). Les séquences d’ADN des deux brins ont été modifiées, assemblées et comparées au moyen du logiciel de DNAStar Inc. (Madison, Wisconsin USA, https://www.dnastar.com). Les séquences obtenues ont été soumises au site Web NG-MAST (http://www.ng-mast.net/) en vue de la détermination des séquences types (ST). Les séquences concaténées des gènes porB et tbpB, qui avaient été identifiées à l’aide de la méthode NG-MAST, ont été alignées au moyen de ClustalWNote de bas de page 18, et un arbre phylogénétique a été construit par la méthode de vraisemblance maximale à l’aide de MEGA 6,06 (http://www.megasoftware.net) d’après le modèle Tamura-NeiNote de bas de page 19. Les tests à l’aide de la méthode NG-MAST n’ont pas été effectués sur les isolats sensibles dont les cultures n’ont pas été soumises au LNM.
2.4 Analyse des données
Bien que le programme de SARGA ait été lancé en 2013, l’analyse a été limitée aux données de 2014 et 2015 alors que les quatre sites participaient activement au programme. Les fréquences ont été calculées pour les cas associés à des cultures positives. Les cultures négatives (comme celles obtenues à la suite d’une visite de suivi ou d’un test de contrôle post-traitement) ont été exclues.
Aux fins des analyses, une seule culture par cas a été incluse. Lorsque plus d’une culture par cas a été soumise, le choix de la culture retenue aux fins des analyses était fondé sur une hiérarchie des foyers d’infection, la priorité étant accordée aux isolats provenant d’un foyer pharyngé, suivis de ceux prélevés dans un foyer rectal, urétral et cervical. Cette hiérarchie a été établie par un consensus avec les sites du programme SARGA et les intervenants. Cependant, toutes les cultures ont été retenues aux fins des analyses lorsque tous les foyers d’infection étaient mentionnés.
Afin d’améliorer la qualité des données, une variable dérivée du comportement sexuel a été créée pour compléter l’information sur le « sexe des partenaires sexuels » auto déclare. En plus d’inclure les hommes ayant indiqué que leurs partenaires sexuels étaient de sexe masculin ou de sexe masculin et de sexe féminin, la variable dérivée « gais, bisexuels, hommes ayant des relations sexuelles avec d’autres hommes (gbHARSAH) » comprenait les hommes qui n’avaient pas fourni d’information sur le sexe de leurs partenaires sexuels, mais qui étaient atteints d’une infection rectale. Les « non gbHARSAH » ont été définis comme étant des hommes qui avaient seulement des partenaires de sexe féminin ou des hommes qui n’ont déclaré aucun partenaire sexuel mâle et qui n’étaient pas atteints d’une infection rectale. La définition « hommes au comportement inconnu » s’appliquait aux hommes qui n’ont pas fourni de renseignements sur leurs partenaires sexuels et chez qui aucun isolat rectal n’a été prélevé. Les cas féminins et transgenres ont été regroupés aux fins des tests de sensibilité aux antimicrobiens, puisqu’un seul cas transgenre présentait un foyer infectieux vaginal. Dans la section sur le traitement, les cas sont catégorisés comme gbHARSAH (selon la même définition dérivée de gbHARSAH) et comme « Autres adultes », ce qui correspond aux catégories utilisées dans les Lignes directrices canadiennes sur les infections transmissibles sexuellementNote de bas de page 3 (les autres adultes comprennent les non gbHARSAH et les femmes, mais excluent les hommes ayant un comportement sexuel inconnu).
La figure 1 montre comment les données de la SARGA ont été classées par catégories pour obtenir le nombre total de cultures (y compris les multiples isolats par cas) et le nombre total de cas.
| Province/Territoire | Culture primaire | Cultures en double | Toutes les cultures | |||
|---|---|---|---|---|---|---|
| 2014 | 2015 | 2014 | 2015 | 2014 | 2015 | |
| Alberta | 420 | 638 | 75 | 124 | 495 | 762 |
| Manitoba | 25 | 12 | 0 | 2 | 25 | 14 |
| Nouvelle-Écosse | 13 | 10 | 1 | 0 | 14 | 10 |
| Total | 458 | 660 | 76 | 126 | 534 | 786 |
3.0 Résultats
3.1 Caractéristiques des cas
Il y a eu une forte diminution de la proportion de gbHARSAH par rapport aux non gbHARSAH, le ratio de 2,7:1 en 2014 passant à 2,4 :1 en 2015 (tableau 2).
| Sexe ou Comportement sexuel | Alberta | Manitoba | Nouvelle-Écosse | Tous | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 2014 | 2015 | 2014 | 2015 | 2014 | 2015 | 2014 | 2015 | |||||||||
| n | % | n | % | n | % | n | % | n | % | n | % | n | % | n | % | |
| gbHARSAH | 254 | 60,5 | 305 | 47,8 | 12 | 48,0 | 5 | 41,7 | 10 | 76,9 | 5 | 50,0 | 276 | 60,3 | 315 | 47,7 |
| Homme - Non gbHARSAH | 101 | 24,0 | 216 | 33,9 | 3 | 12,0 | 5 | 41,7 | 0 | 0,0 | 0 | 0,0 | 104 | 22,7 | 221 | 33,5 |
| Femme | 63 | 15,0 | 116 | 18,2 | 6 | 24,0 | 1 | 8,3 | 2 | 15,4 | 4 | 40,0 | 71 | 15,5 | 121 | 18,3 |
| Homme - Inconnu | 2 | 0,5 | 1 | 0,2 | 4 | 16,0 | 1 | 8,3 | 1 | 7,7 | 1 | 10,0 | 7 | 1,5 | 3 | 0,5 |
| Total | 420 | 100 | 638 | 100 | 25 | 100 | 12 | 100 | 13 | 100 | 10 | 100 | 458 | 100 | 660 | 100 |
En 2015, 786 cultures réalisées à partir des isolats prélevés chez 660 cas ont été soumises au programme de SARGA. Dans seize pour cent (n=126) de ces cas, plusieurs (deux ou trois) isolats positifs ont été prélevés de différents foyers d’infection. La répartition selon l’âge était très semblable pour les deux années. En 2014 et en 2015, la majorité des cas étaient âgés de moins de 40 ans (85,6 % et 83,8 % respectivement) et avaient un âge moyen de 31,8 ans et de 30,6 ans, respectivement.
À part de la diminution importante dans la proportion de cas de sexe masculin qui étaient des gbHARSAH, les comportements à risque pour les cas soumis au programme de SARGA en 2015 sont demeurés semblables à ceux de 2014, avec 2,6 % rapportant le travail sexuel au cours des 60 derniers jours et 0,6 % indiquant qu’il était probable qu’ils aient contracté l’infection pendant un voyage à l’extérieur de la province (tableau 3)
| Caractéristiques des cas | 2014 | 2015 | ||
|---|---|---|---|---|
| Âge | n | % | n | % |
| De 16 à 19 ans | 40 | 8,7 | 47 | 7,1 |
| De 20 à 29 ans | 215 | 46,9 | 329 | 49,8 |
| De 30 à 39 ans | 137 | 29,9 | 177 | 26,8 |
| De 40 à 49 ans | 38 | 8,3 | 64 | 9,7 |
| De 50 à 59 ans | 24 | 5,2 | 30 | 4,5 |
| 60 ans et plus | 4 | 0,9 | 13 | 2,0 |
| Total | 458 | 100 | 660 | 100 |
| Participer au travail du sexe | n | % | n | % |
| Oui | 12 | 2,6 | 17 | 2,6 |
| Non | 443 | 96,7 | 642 | 97,3 |
| Refus de répondre | 1 | 0,2 | 0 | 0,0 |
| Inconnu | 2 | 0,4 | 1 | 0,2 |
| Total | 458 | 100 | 660 | 100 |
| Infection contractée en voyage | n | % | n | % |
| Oui | 3 | 0,7 | 4 | 0,6 |
| Non | 32 | 7,0 | 655 | 99,2 |
| Refus de répondre | 1 | 0,2 | 0 | 0,0 |
| Inconnu | 422 | 92,1 | 1 | 0,2 |
| Total | 458 | 100 | 660 | 100 |
3.2 Motifs de la consultation
Parmi les gbHARSAH, la présence de signes/symptômes durant les deux années constituait le principal motif de la première consultation à la clinique au cours les deux années. Toutefois, cette proportion est passée de 45,7 % à 39,3 % de 2014 à 2015, ce qui correspond à une augmentation des consultations attribuables à des contacts du cas (17,4 % à 29,1 %, respectivement). Les gbHARSAH étaient le groupe chez qui le taux de dépistage des ITS était le plus élevé, représentant environ un cinquième des consultations au cours des deux années. Par ailleurs, les hommes non gbHARSAH ont rarement indiqué que le dépistage était le motif de consultation; les signes/symptômes sont demeurés le principal motif de consultation chez les hommes non gbHARSAH aux deux années, représentant environ 80 % des cas. Le principal motif de consultation chez les femmes était le contact du cas, et ce pour chacune des deux années. En 2015, on a observé une augmentation du nombre de consultations des femmes pour le motif des signes/symptômes (26,8 % à 35,0 %) et des contacts du cas (31,0 % à 41,0 %), et on a observé des diminutions correspondantes dans les catégories « inconnu » et « autres » (tableau 4).
| Motif de la première consultation | 2014 | 2015 | ||
|---|---|---|---|---|
| Hommes gbHARSAH | N | % | n | % |
| Symptômes | 126 | 45,7 | 123 | 39,3 |
| Contact du cas | 48 | 17,4 | 91 | 29,1 |
| Dépistage d’ITS | 52 | 18,8 | 73 | 23,3 |
| Inconnu | 19 | 6,9 | 13 | 4,2 |
| AutresNote de bas de page * | 31 | 11,2 | 13 | 4,2 |
| Total | 276 | 100 | 313 | 100 |
| Hommes non gbHARSAH | N | % | n | % |
| Symptômes | 82 | 78,8 | 173 | 78,3 |
| Contact du cas | 13 | 12,5 | 13 | 5,9 |
| Dépistage d’ITS | 0 | 0,0 | 5 | 2,3 |
| Inconnu | 3 | 2,9 | 5 | 2,3 |
| AutresNote de bas de page * | 6 | 5,8 | 25 | 11,3 |
| Total | 104 | 100 | 221 | 100 |
| Femme | N | % | n | % |
| Symptômes | 19 | 26,8 | 41 | 35,0 |
| Contact du cas | 22 | 31,0 | 48 | 41,0 |
| Dépistage d’ITS | 12 | 16,9 | 16 | 13,7 |
| Inconnu | 8 | 11,3 | 2 | 1,7 |
| AutresNote de bas de page * | 10 | 14,1 | 10 | 8,5 |
| Total | 71 | 100 | 117 | 100 |
| TousNote de bas de page ** | ||||
| Symptômes | 229 | 50,0 | 338 | 51,7 |
| Contact du cas | 83 | 18,1 | 153 | 23,4 |
| Dépistage d’ITS | 64 | 14,0 | 94 | 14,4 |
| Inconnu | 35 | 7,6 | 21 | 3,2 |
| AutresNote de bas de page * | 47 | 10,3 | 48 | 7,3 |
| Total généralNote de bas de page *** | 458 | 100 | 654 | 100 |
|
||||
3.3 Foyers d’infection
En 2015, 786 isolats ont été obtenus des 660 cas de gonorrhée confirmée par la culture. Des échantillons de sites anatomiques ont été prélevés en fonction des lignes directrices provinciales en matière de dépistage ou d’exposition. Les isolats prélevés chez les cas féminins provenaient principalement d’un foyer génitale (46,4 %), bien que ce pourcentage ait diminué par rapport à 55,8 % en 2014. La proportion d’infections rectales et pharyngiennes a augmenté chez les femmes. Chez les hommes non gbHARSAH, les infections étaient presque exclusivement génitales, tandis que chez les hommes gbHARSAH, elles étaient réparties à peu près également entre trois foyers : rectum (37,0 %), organes génitaux (32,7 %) et pharynx (30,4 %) (Tableau 5).
| Sexe ou comportement sexuel | 2014 | 2015 | ||
|---|---|---|---|---|
| Hommes gbHARSAH | N | % | n | % |
| Rectum | 124 | 37,8 | 145 | 37,0 |
| Pharynx | 92 | 28,0 | 119 | 30,4 |
| Génital | 112 | 34,1 | 128 | 32,7 |
| Total | 328 | 100 | 392 | 100 |
| Hommes non gbHARSAH | N | % | n | % |
| Pharynx | 2 | 1,9 | 3 | 1,3 |
| Génital | 102 | 98,1 | 220 | 98,7 |
| Total | 104 | 100 | 223 | 100 |
| Femme | N | % | n | % |
| Rectum | 18 | 18,9 | 38 | 22,6 |
| Pharynx | 24 | 25,3 | 52 | 31,0 |
| Génital | 53 | 55,8 | 78 | 46,4 |
| Total | 95 | 100 | 168 | 100 |
| TousNote de bas de page ** | N | % | n | % |
| Rectum | 142 | 26,6 | 183 | 23,3 |
| Pharynx | 120 | 22,5 | 176 | 22,4 |
| Génital | 272 | 50,9 | 427 | 54,3 |
| Total générale | 534 | 100 | 786 | 100 |
|
||||
3.4 Sensibilité aux antimicrobiens
Dans l’ensemble, 44,8 % (205/458) des isolats de 2014 et 40 % (264/660) des isolats de 2015 étaient sensibles à tous les antimicrobiens. La proportion d’isolats de 2014 et 2015 qui montraient une sensibilité réduite ou de la résistance à un seul antimicrobien était de 20,7 % (95/458) et de 24,4 % (161/660) respectivement. La proportion d’isolats de 2014 et 2015 qui montraient une sensibilité réduite ou de la résistance à deux antimicrobiens ou plus était de 34,5 % (158/458) et de 35,6 % (235/660), respectivement. En 2015, la proportion d’isolats présentant une sensibilité réduite ou de la résistance à deux antimicrobiens ou plus variait de 35,1 % à 60 % entre les villes participantes (tableau 6).
| Sensibilité | Alberta | Manitoba | Nouvelle-Écosse | Tous | ||||
|---|---|---|---|---|---|---|---|---|
| 2014 n (%) |
2015 n (%) |
2014 n (%) |
2015 n (%) |
2014 n (%) |
2015 n (%) |
2014 n (%) |
2015 n (%) |
|
| Sensibilité à tous les antimicrobiens sélectionnés | 192 (45,7) | 258 (40,4) | 8 (32,0) | 4 (33,3) | 3 (23,1) | 2 (20,0) | 205 (44,8) | 264 (40,0) |
| R/SRNote de bas de page * à 1 antimicrobien | 89 (21,2) | 156 (24,5) | 3 (12,0) | 3 (25,0) | 3 (23,1) | 2 (20,0) | 95 (20,7) | 161 (24,4) |
| R/SRNote de bas de page * à 2 antimicrobiens ou plus | 139 (33,1) | 224 (35,1) | 14 (56,0) | 5 (41,7) | 7 (53,8) | 6 (60,0) | 158 (34,5) | 235 (35,6) |
| Total | 420 (100) | 638 (100) | 25 (100) | 12 (100) | 13 (100) | 10 (100) | 458 (100) | 660 (100) |
|
||||||||
CéfiximeNote de bas de page c
Dans l’ensemble, 3,5 % (16/458) des isolats présentaient une sensibilité réduite au céfixime (CMI 0,25 mg/L) en 2014, passant à 0,8 % (5/660) en 2015 (annexe C). En 2014, 4,8 % (5/104) des isolats d’hommes non gbHARSAH et 7 % (5/71) des isolats provenant de femmes présentaient une sensibilité réduite au céfixime, passant à 0,5 % (1/221) et 0 % (0/121), respectivement, en 2015 (annexe C et figures 1a et 1b). Chez les hommes gbHARSAH, la sensibilité a également diminué, passant de 1,8 % (5/276) en 2014 à 0,6 % (2/315) en 2015, comme le montre le tableau 7.
Figure 1a. Distribution de la sensibilité réduite au céfixime selon le sexe ou le comportement sexuel, SARGA 2014 et 2015
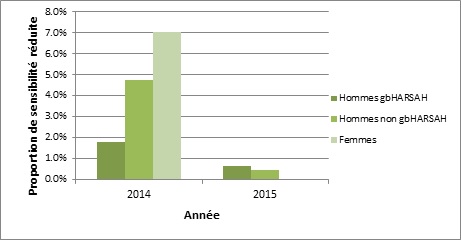
Distribution de la sensibilité réduite au céfixime selon le sexe ou le comportement sexuel, SARGA 2014 et 2015 - Description Textuel
L’histogramme présente le pourcentage d’isolats de SARGA qui présentant une sensibilité réduite au céfixime selon le sexe ou le comportement sexuel. L’axe horizontal représente l’année, et l’axe vertical la proportion de sensibilité réduite.
| Sexe ou Comportement sexuel | 2014 | 2015 |
|---|---|---|
| Hommes gbHARSAH | 1,8 | 0,6 |
| Hommes non gbHARSAH | 4,8 | 0,5 |
| Femmes | 7,0 | 0,0 |
Figure 1b. Distribution de la sensibilité réduite au céfixime selon le sexe et les foyers d’infection, SARGA, 2014 et 2015
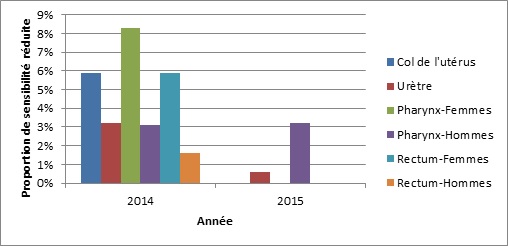
Note de bas de page a dénominateurs de 2014 : col de l’utérus =53; urètre=214; pharynx-femmes=24; pharynx-hommes=126; rectum- femmes =18; rectum-hommes =124
dénominateurs de 2015 : col de l’utérus=78; urètre =348; pharynx- femmes =52; pharynx-hommes =148; rectum- femmes =38; rectum-hommes =145
Distribution de la sensibilité réduite au céfixime selon le sexe et les foyers d’infection, SARGA, 2014 et 2015 - Description Textuel
L’histogramme présente le pourcentage d’isolats de SARGA qui présentant une sensibilité réduite au céfixime selon le sexe et les foyers d’infection. L’axe horizontal représente l’année, et l’axe vertical la proportion de sensibilité réduite.
| Sexe ou Comportement sexuel et Foyer d’Infection | 2014 | 2015 |
|---|---|---|
| Col de l’utérus | 5,9 | 0,0 |
| Urètre | 3,2 | 0,6 |
| Pharynx – Femmes | 8,3 | 0,0 |
| Pharynx – Hommes | 3,1 | 3,2 |
| Rectum – Femmes | 5,9 | 0,0 |
| Rectum – Hommes | 1,6 | 0,0 |
CeftriaxoneNote de bas de page d
Dans l’ensemble, 1,5 % (7/458) des isolats soumis au programme de SARGA présentaient une sensibilité réduite à la ceftriaxone en 2014; cette proportion a augmenté légèrement pour atteindre 1,8 % (12/660) en 2015. La fréquence de sensibilité réduite à la ceftriaxone dans les isolats prélevés chez des hommes gbHARSAH a augmenté, passant de 1,1 % (3/276) en 2014 à 2,9 % (9/315) en 2015, tandis qu’elle a diminué dans le cas des isolats d’hommes non gbHARSAH (1,9 % à 0,5 %) et des femmes (1,4 % à 0 %) au cours de la même période (annexe C et figures 2a et 2b), comme indiqué dans tableau 7.
Figure 2a. Distribution de la sensibilité réduite à la ceftriaxone selon le sexe ou le comportement sexuel, SARGA, 2014 et 2015
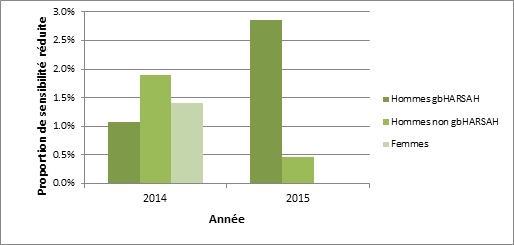
Distribution de la sensibilité réduite à la ceftriaxone selon le sexe ou le comportement sexuel, SARGA, 2014 et 2015 - Description Textuel
L’histogramme présente le pourcentage d’isolats de SARGA qui présentant une sensibilité réduite au ceftriaxone selon le sexe ou le comportement sexuel. L’axe horizontal représente l’année, et l’axe vertical la proportion de sensibilité réduite.
| Sexe ou Comportement sexuel et Foyer d’Infection | 2014 | 2015 |
|---|---|---|
| Hommes gbHARSAH | 1,1 | 2,9 |
| Hommes non gbHARSAH | 1,9 | 0,5 |
| Femmees | 1,4 | 0,0 |
Figure 2b. Distribution de la sensibilité réduite à la ceftriaxone selon le sexe et le foyer d’infection, SARGA, 2014 et 2015
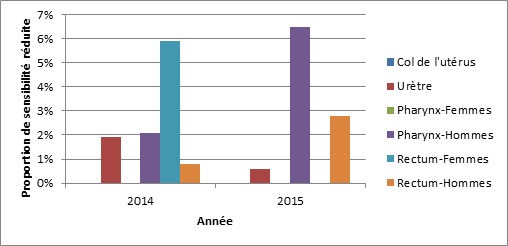
Note de bas de page a dénominateurs de 2014 : col de l’utérus =53; urètre=214; pharynx-femmes=24; pharynx-hommes=126; rectum- femmes =18; rectum-hommes =124 dénominateurs de 2015 : col de l’utérus=78; urètre =348; pharynx- femmes =52; pharynx-hommes =148; rectum- femmes =38; rectum-hommes =145
Distribution de la sensibilité réduite à la ceftriaxone selon le sexe et le foyer d’infection, SARGA, 2014 et 2015 - Description Textuel
L’histogramme présente le pourcentage d’isolats de SARGA qui présentant une sensibilité réduite au ceftriaxone selon le sexe et les foyers d’infection. L’axe horizontal représente l’année, et l’axe vertical la proportion de sensibilité réduite.
| Sexe ou Comportement sexuel et Foyer d’Infection | 2014 | 2015 |
|---|---|---|
| Col de l’utérus | 0,0 | 0,0 |
| Urètre | 1,9 | 0,6 |
| Pharynx – Femmes | 0,0 | 0,0 |
| Pharynx – Hommes | 2,1 | 6,5 |
| Rectum – Femmes | 5,9 | 0,0 |
| Rectum – Hommes | 0,8 | 2,8 |
AzithromycineNote de bas de page e
En 2014, 1,5 % (7/458) de tous les isolats obtenus à partir des cas soumis au programme de SARGA étaient résistants à l’azithromycine. Cette proportion a diminué à 0,5 % (3/660) en 2015 (annexe C). Tous les isolats résistant à l’azithromycine identifiés provenaient de l’Alberta. La proportion de résistance à l’azithromycine dans les isolats d’hommes gbHARSAH a diminué, passant de 2,2 % (6/276) en 2014 à 0,3 % (1/315) en 2015. Chez les isolats provenant d’hommes non gbHARSAH, la proportion augmenté légèrement, passant de 0 % (0/104) en 2014 à 0,5 % (1/221) en 2015, et la proportion d’isolats provenant de femmes a diminué légèrement, passant de 1,4 % (1/71) en 2014 à 0,8 % (1/121) en 2015 (annexe C et figures 3a et 3b), comme indiqué dans tableau 7.
Figure 3a. Distribution de la résistance à l’azithromycine selon le sexe ou le comportement sexuel, SARGA, 2014 et 2015
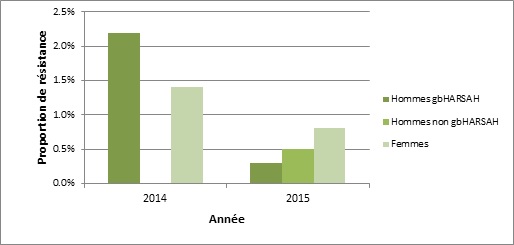
Distribution de la résistance à l’azithromycine selon le sexe ou le comportement sexuel, SARGA, 2014 et 2015 - Description Textuel
L’histogramme présente le pourcentage d’isolats de SARGA qui présentant une résistance à l’azithromycine selon le sexe ou le comportement sexuel. L’axe horizontal représente l’année, et l’axe vertical la proportion de sensibilité réduite.
| Sexe ou Comportement sexuel | 2014 | 2015 |
|---|---|---|
| Hommes gbHARSAH | 2,2 | 0,3 |
| Hommes non gbHARSAH | 0,0 | 0,5 |
| Femmes | 1,4 | 0,8 |
Figure 3b. Distribution de la résistance à l’azithromycine selon le sexe et le foyer d’infection, SARGA. 2014 et 2015
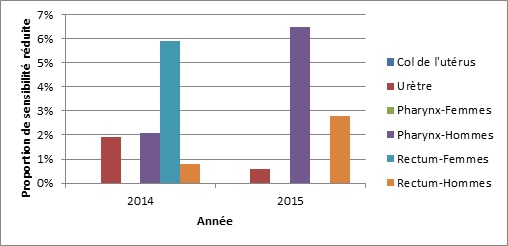
Note de bas de page a dénominateurs de 2014 : col de l’utérus =53; urètre=214; pharynx-femmes=24; pharynx-hommes=126; rectum- femmes =18; rectum-hommes =124
dénominateurs de 2015 : col de l’utérus=78; urètre =348; pharynx- femmes =52; pharynx-hommes =148; rectum- femmes =38; rectum-hommes =145
Distribution de la résistance à l’azithromycine selon le sexe et le foyer d’infection, SARGA. 2014 et 2015 - Description Textuel
L’histogramme présente le pourcentage d’isolats de SARGA qui présentant une résistance à l’azithromycine selon le sexe et les foyers d’infection. L’axe horizontal représente l’année, et l’axe vertical la proportion de sensibilité réduite.
| Sexe ou Comportement sexuel et Foyer d’Infection | 2014 | 2015 |
|---|---|---|
| Col de l’utérus | 0,0 | 0,0 |
| Urètre | 1,4 | 0,6 |
| Pharynx – Femmes | 4,2 | 1,9 |
| Pharynx – Hommes | 3,1 | 0,0 |
| Rectum – Femmes | 0,0 | 0,0 |
| Rectum – Hommes | 0,8 | 0,0 |
Ciprofloxacine
La prévalence de la résistance à la ciprofloxacine était de 27,1 % (124/458) en 2014, et a légèrement augmenté à 30,0 % en 2015 (198/660). Une forte augmentation a été observée dans les isolats obtenus des hommes gbHARSAH (30,4 % à 47,9 %) (annexe C).
Tétracycline
Environ 49,8 % (228/458) des isolats des cas de SARGA étaient résistants à la tétracycline en 2014, et ce pourcentage est passé à 56,2 % (371/660) en 2015. On a observé une forte augmentation de la résistance des isolats chez les hommes non gbHARSAH (27,9 % à 45,2 %) (annexe C).
Pénicilline
Environ 17,2 % (79/458) des isolats des cas de SARGA présentaient une résistance à la pénicilline en 2014, et ce pourcentage a diminué à 14,8 % (98/660) en 2015 (annexe C).
Érythromycine
La résistance à l’érythromycine est demeurée relativement constante de 2014 à 2015, 25,3 % (116/458) des isolats affichant une résistance en 2014 et 26,1 % (172/660) en 2015. Cette augmentation provenait principalement des isolats des cas de gbHARSAH, où une augmentation de 33,7 % à 44,1 % a été observée (annexe C).
Spectinomycine
Aucune résistance à la spectinomycine n’a été détectée dans les isolats soumis en 2014 et 2015.
Multi résistance aux médicaments
En 2014 et 2015, les isolats qui présentaient une sensibilité réduite au céfixime ou à la ceftriaxone étaient également résistants à un ou plusieurs autres antimicrobiens; cependant, aucun de ces isolats n’était résistant à l’azithromycine.
| Sexe et comportement sexuel | Alberta | Manitoba | Nouvelle-Écosse | Tous | ||||
|---|---|---|---|---|---|---|---|---|
| n (%) | n (%) | n (%) | n (%) | |||||
| CéfiximeSR | 2014 | 2015 | 2014 | 2015 | 2014 | 2015 | 2014 | 2015 |
| Hommes gbHARSAH | 5 (2,0) | 2 (0,7) | 0 (0,0) | 0 (0,0) | 0 (0,0) | 0 (0,0) | 5 (1,8) | 2 (0,6) |
| Hommes non gbHARSAH | 5 (5,0) | 1 (0,5) | 0 (0,0) | 0 (0,0) | 0 (0,0) | 0 (0,0) | 5 (4,8) | 1 (0,5) |
| Femmes/Transgenres | 5 (7,9) | 0 (0,0) | 0 (0,0) | 0 (0,0) | 0 (0,0) | 0 (0,0) | 5 (7,0) | 0 (0,0) |
| Hommes inconnu | 0 (0,0) | 0 (0,0) | 1 (25,0) | 1 (100) | 0 (0,0) | 1 (100) | 1 (14,3) | 2 (66,7) |
| Total | 15 (3,6) | 3 (0,5) | 1 (4,0) | 1 (8,3) | 0 (0,0) | 1 (10,0) | 16 (3,5) | 5 (0,8) |
| CeftriaxoneSR | 2014 | 2015 | 2014 | 2015 | 2014 | 2015 | 2014 | 2015 |
| Homme gbHARSAH | 3 (1,2) | 9 (3,0) | 0 (0,0) | 0 (0,0) | 0 (0,0) | 0 (0,0) | 3 (1,1) | 9 (2,9) |
| Hommes non gbHARSAH | 2 (2,0) | 0 (0,0) | 0 (0,0) | 1 (20,0) | 0 (0,0) | 0 (0,0) | 2 (1,9) | 1 (0,5) |
| Femmes/Transgenres | 1 (1,6) | 0 (0,0) | 0 (0,0) | 0 (0,0) | 0 (0,0) | 0 (0,0) | 1 (1,4) | 0 (0,0) |
| Hommes inconnu | 0 (0,0) | 0 (0,0) | 1 (25,0) | 1 (100) | 0 (0,0) | 1 (100) | 1 (14,3) | 2 (66,7) |
| Total | 6 (1,4) | 9 (1,4) | 1 (4,0) | 2 (16,7) | 0 (0,0) | 1 (10,0) | 7 (1,5) | 12 (1,8) |
| AzithromycineR | 2014 | 2015 | 2014 | 2015 | 2014 | 2015 | 2014 | 2015 |
| Hommes gbHARSAH | 6 (2,4) | 1 (0,3) | 0 (0,0) | 0 (0,0) | 0 (0,0) | 0 (0,0) | 6 (2,2) | 1 (0,3) |
| Hommes non gbHARSAH | 0 (0,0) | 1 (0,5) | 0 (0,0) | 0 (0,0) | 0 (0,0) | 0 (0,0) | 0 (0,0) | 1 (0,5) |
| Femmes/Transgenres | 1 (1,6) | 1 (0,9) | 0 (0,0) | 0 (0,0) | 0 (0,0) | 0 (0,0) | 1 (1,4) | 1 (0,8) |
| Homme inconnu | 0 (0,0) | 0 (0,0) | 0 (0,0) | 0 (0,0) | 0 (0,0) | 0 (0,0) | 0 (0,0) | 0 (0,0) |
| Total | 7 (1,7) | 3 (0,5) | 0 (0,0) | 0 (0,0) | 0 (0,0) | 0 (0,0) | 7 (1,5) | 3 (0,5) |
|
||||||||
3.5 Typage génomique
Le typage génomique au moyen de la méthode NG-MAST réalisé sur 778 isolats a permis d’identifier 197 séquences types différentes (ST). Les 20 ST les plus fréquentes en 2014 et 2015 sont représentés à la figure 4. En 2014, ST5985 (12,6 %, 42/334) était la ST la plus fréquente, suivie de ST10129 (6,0 %, 20/334) et de ST11299 (5,4 %, 18/334). En 2015, ST7638 (20,9 %, 93/444) était la ST la plus fréquente, suivie de ST11299 (10,4 %, 46/444) et de ST9663 (6,3 %, 28/444). Les trois séquences types les plus fréquentes en 2014 et 2015 combinées étaient ST7638 à 12,9 % (100/778), ST5985 à 9,1 % (71/778) et ST11299 à 8,2 % (64/778). La figure 5 représente la relation génétique entre 36 des ST les plus fréquentes selon la méthode de la probabilité maximale.
- ST7638 (n=100) a été identifié dans sept isolats en 2014 et 93 en 2015.
- ST12588 (n=4), qui diffère de ST7638 par seulement deux paires de base, n’a été identifié qu’en 2015.
- Les isolats de cette grappe étaient soit résistants soit sensibles à la tétracycline, et plus de 85 % (91/104) provenaient de non gbHARSAH, y compris de femmes (figure 5).
- ST5985 (n=71) a été identifié dans 42 isolats de 2014 et 29 isolats de 2015. Tous les isolats de ST5985 présentaient une résistance élevée à médiation plasmidique à la tétracycline N. gonorrhoeae (NGRT), et plus de 80 % (60/71) provenaient d’hommes gbHARSAH (figure 5). Tous les isolats de ST5985 soumis au programme de SARGA provenaient de l’Alberta, sauf un qui provenait du Manitoba. ST5985 était la ST la plus répandue au Canada en 2015, en Ontario, en Colombie-Britannique, en Alberta et en SaskatchewanNote de bas de page 20.
- ST11299 (n=64) a été identifié dans 18 isolats en 2014 et 46 isolats en 2015. ST11299 est répandu partout au Canada et est multi résistant aux antimicrobiens (NGRMC/ciprofloxacine – voir l’annexe B). Trois isolats de ST11299 soumis au programme de SARGA présentaient une sensibilité réduite aux céphalosporines. Plus de 85 % (56/64) de ces isolats provenaient d’hommes gbHARSAH (figure 5).
- ST2318 (n=17) diffère de ST11299 par seulement six paires de base et est également multi résistant (NGRMC/ciprofloxacine). Plus de 50 % (7/13) des isolats contenant cette ST en 2015 présentaient également une sensibilité réduite aux céphalosporines. L’un des isolats provenait de la Nouvelle-Écosse; les autres provenaient de l’Alberta. Tous les isolats de cette ST provenaient d’hommes gbHARSAH (figure 5).
- ST9663 (n=47) a été identifié dans 25 isolats en 2014 et 32 isolats en 2015. Les isolats étaient multi résistants aux antimicrobiens (NGRMC/ciprofloxacine) et 78,7 % (37/47) provenaient d’hommes gbHARSAH (figure 5). Tandis que la plupart des isolats ST9663 aient été identifiés en Alberta, cinq isolats du Manitoba présentaient la même résistance aux antimicrobiens.
- ST10129 (n=23) a été identifié en Alberta; 20 isolats en 2014 et seulement trois en 2015. Ces isolats étaient sensibles ou résistants à l’érythromycine et provenaient tous d’hommes gbHARSAH (figure 5).
- ST2400 (n=20) a été identifié dans huit isolats en 2014 et 12 isolats en 2015. L’un des isolats provenait de la Nouvelle-Écosse; les autres provenaient de l’Alberta. Les isolats étaient multi résistants aux antimicrobiens (NGRMC/ciprofloxacine) et provenaient tous d’hommes gbHARSAH. ST2400 était la deuxième ST la plus répandue au Canada en 2015Note de bas de page 20 selon les données courantes du LNM (figure 5).
- ST10451 (n=8) a été identifié dans un isolat de 2014 et sept de 2015. Les isolats étaient multi résistants (NGRMC/ciprofloxacine); deux étaient également résistants à l’azithromycine et un autre présentait une sensibilité réduite aux céphalosporines. Un des sept isolats de ST10451 identifiés en 2015 provenait du Manitoba et présentait une sensibilité réduite à la ceftriaxone; les six autres isolats provenaient de l’Alberta. ST10451 était la troisième ST la plus souvent observée au Canada en 2015 et elle est étroitement liée au clone identifié à l’échelle internationale, ST1407, qui a été décrit comme une super bactérie résistante aux céphalosporinesNote de bas de page 7Note de bas de page 21Note de bas de page 22 (figure 5).
- Les ST étroitement liées et qui sont groupées autour de ST21 sont toutes à l’intérieur de deux paires de base l’une de l’autre. Les 36 isolats de cette grappe sont tous résistants à la pénicilline, à la tétracycline et à l’érythromycine (NGRMC) et plus de 90 % (33/36) proviennent d’hommes gbHARSAH (figure 5).
Figure 4. Fréquence des séquences types établies au moyen de la méthode NG-MAST dans les isolats de N. gonorrhoeae, SARGA, 2014 et 2015
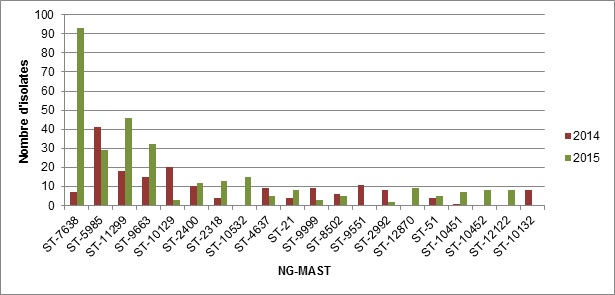
Fréquence des séquences types établies au moyen de la méthode NG-MAST dans les isolats de N. gonorrhoeae, SARGA, 2014 et 2015 - Description Textuel
L’histogramme présente le nombre d’isolats pour les 20 isolats fréquentes qui ont été testés utilisant la méthode NG-MAST. L’axe horizontal représente les différents types de séquences, et l’axe vertical le nombre d’isolats.
| Séquences types | 2014 | 2015 |
|---|---|---|
| ST-7638 | 7 | 93 |
| ST-5985 | 41 | 29 |
| ST-11299 | 18 | 46 |
| ST-9663 | 15 | 32 |
| ST-10129 | 20 | 3 |
| ST-2400 | 10 | 12 |
| ST-2318 | 4 | 13 |
| ST-10532 | 0 | 15 |
| ST-4637 | 9 | 5 |
| ST-21 | 4 | 8 |
| ST-9999 | 9 | 3 |
| ST-8502 | 6 | 5 |
| ST-9551 | 11 | 0 |
| ST-2992 | 8 | 2 |
| ST-12870 | 0 | 9 |
| ST-51 | 4 | 5 |
| ST-10451 | 1 | 7 |
| ST-10452 | 0 | 8 |
| ST-12122 | 0 | 8 |
| ST-10132 | 8 | 0 |
Figure 5. Relation génétique des séquences types prévalentes établies au moyen de la méthode NG-MAST de N. gonorrhoeae, SARGA, 2014 et 2015Note de bas de page **
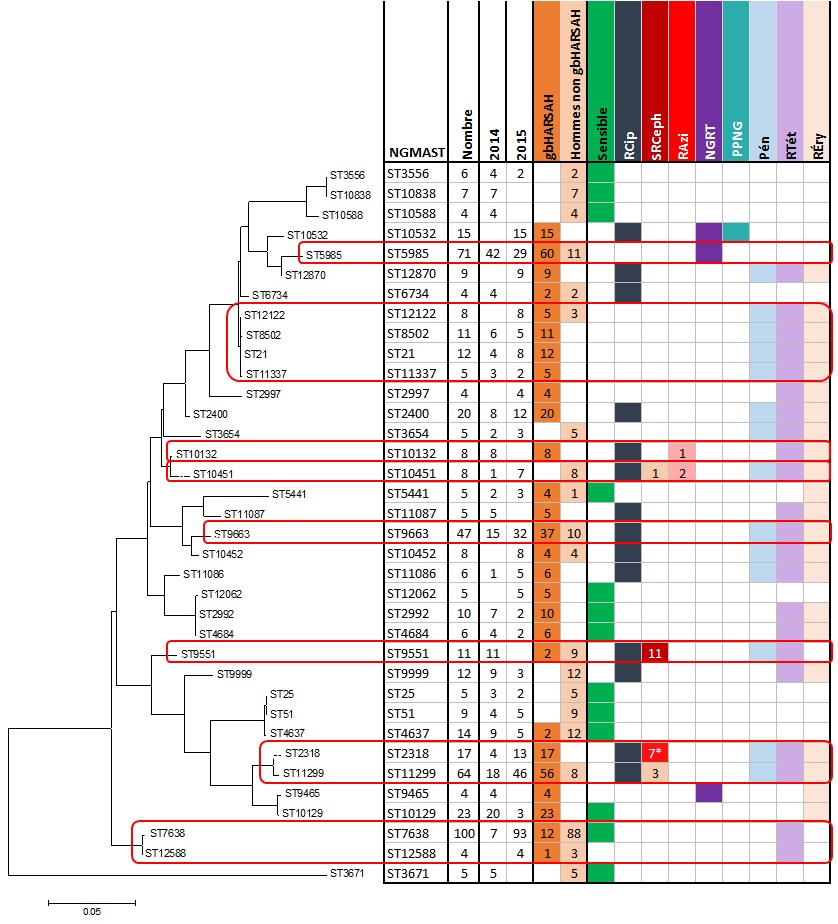
Relation génétique des séquences types prévalentes établies au moyen de la méthode NG-MAST de N. gonorrhoeae, SARGA, 2014 et 2015 - Description Textuel
La dendrogramme présente la relation génétique entre 36 des ST les plus fréquentes selon la méthode de la probabilité maximale. La partie la plus à gauche de la figure présente les relations phylogénétiques et la relativité de chaque ST – la longueur de branche de l’arbre représente le nombre de substitutions de paire de base par site. Le tableau correspondant à droit présente le NG-MAST dans les rangées, et le nombre de chaque ST, l’année, le sexe ou le comportement sexuel, et la caractérisation de la résistance (RCip, SRCeph, RAzi, NGRT, RPén, RTét, RÉry) comme étiquettes de colonne. Chaque variable de la colonne est colorée et la présence de la variable correspond à la couleur correspondante présente dans la ligne NG-MAST. Il y a huit groupes en surbrillance dans les cases rouges.
| ST-5985 | Cette ST, identifiée en 2014 et 2015, provenaient principalement dans la population de gbHARSAH, présente une résistance élevée à la tétracycline (NGRT) |
| ST-12122 ST-8502 ST-21 ST-1337 |
Les STs de cette grappe sont toutes étroitement liées (à l’intérieur de deux paires de base) et se trouvent principalement dans les gbHARSAH. Elles sont toutes NGRMC |
| ST-10132 | Cette ST a été identifiée en 2014 dans les gbHARSAH. Elle est résistante à la ciprofloxacine, à la tétracycline et à l’érythromycine. Un isolat avec cette ST était résistant à l’azithromycine |
| ST-10451 | Cette ST est multi résistante aux médicaments (NGRMC/RCip) et a été trouvée dans les hommes non gbHARSAH. Un des isolats identifies présentait une sensibilité réduite à la céphalosporine. Deux étaient aussi résistants à l’azithromycine |
| ST-9663 | Les isolats de cette ST sont NGRMC/RCip avec environ 75% identifiés dans la population gbHARSAH |
| ST-9551 | Cette ST a été identifiée en 2014 principalement dans la groupe hommes non gbHARSAH. Elle montre une résistance à la ciprofloxacine, à la pénicilline, à la tétracycline et une sensibilité réduites aux céphalosporines |
| ST-2318 ST-11299 |
Cette grappe se trouve principalement dans la population gbHARSAH, prévalent partout au Canada et multi résistant. Environ 10 % avaient une sensibilité réduite aux cephalosporins |
| ST-7638 ST-12588 |
Cette grappe se trouve principalement dans les hommes non gbHARSAH. Elle est sensible ou résistante à la tétracycline. Le ST-7638 était le ST le plus répandu en 2015 |
- Note de bas de page 1
-
2015 seulement
- Note de bas de page 2
-
Le dendrogramme représente 36 des séquences les plus prévalentes identifiées en 2014 et en 2015 (197 ST au total) et comprend les données de 557 des 1 118 isolats (2014 - 221/458; 2015 - 335/660).
- Note de bas de page 3
-
Les non gbHARSAH incluent les femmes dans cette figure.
3.6 Traitement
Les renseignements sur le traitement étaient disponibles pour 97,6 % (n=447) et 99,1 % (n=654) des patients atteints de gonorrhée en 2014 et 2015, respectivement. L’adhésion aux traitements recommandés dans les Lignes directrices canadiennes sur les infections transmissibles sexuellementNote de bas de page 3 (tableau 8) était supérieure à 80 % pour tous les groupes de traitement, à l’exception des autres adultes atteints d’infections pharyngées. Dans cette catégorie, 76 % des cas ont reçu un traitement privilégié en 2014; cette proportion est tombée à 20 % en 2015 (figure 6).
| Type d’infection | raitement | gbHARSAH | Autres adultes |
|---|---|---|---|
| Infections anogénitales | Thérapie privilégié | Ceftriaxone à raison de 250 mg + azithromycine à raison de 1 g | Ceftriaxone à raison de 250 mg + azithromycine à raison de 1 g |
| Thérapie privilégié | s/o | Céfixime à raison de 800 mg + azithromycine à raison de 1 g | |
| Autre traitement | Céfixime à raison de 800 mg + azithromycine à raison de 1 g OU Azithromycine à raison de 2 g OU Spectinomycine à raison de 2 g + azithromycine à raison de 1 g |
Spectinomycine à raison de 2 g + azithromycine à raison de 1 g OU Azithromycine à raison de 2 g |
|
| Infections pharyngées | Thérapie privilégié | Ceftriaxone à raison de 250 mg + azithromycine à raison de 1 g | Ceftriaxone à raison de 250 mg + azithromycine à raison de 1 g |
| Autre traitement | Céfixime à raison de 800 mg + azithromycine à raison de 1 g | Céfixime à raison de 800 mg + azithromycine à raison de 1 g OU Azithromycine à raison de 2 g |
La majorité des infections anogénitales chez les autres adultes ont été traitées au moyen d’un traitement privilégié en 2014 (86,7 %) et en 2015 (90,9 %). Les deux combinaisons préférées ont été prescrites de la même façon (44,0 % pour le traitement à la ceftriaxone et à l’azithromycine, 42,7 % pour le traitement au céfixime et à l’azithromycine) pour les infections anogénitales chez les autres adultes en 2014 (tableau 9). En 2015, cette tendance a changé et le traitement au céfixime et à l’azithromycine représentait 81,9 % des traitements contre les infections anogénitales chez les autres adultes, tandis que la combinaison avec la ceftriaxone a été utilisée dans seulement 9,1 % des cas. La même tendance a été observée chez d’autres adultes atteints d’infections pharyngées. En 2014, la proportion de cas associés à la combinaison ceftriaxone et céfixime était de 76,0 % et 16,0 %, respectivement. En 2015, elle est passée à 20 % et 50,9 %.
Figure 6. Adhésion aux lignes directrices canadiennes pour le traitement destine aux gbHARSAH et autres adultesNote de bas de page *, SARGA, 2014 et 2015

Adhésion aux lignes directrices canadiennes pour le traitement destine aux gbHARSAH et autres adultes, SARGA, 2014 et 2015 - Description Textuel
Ce diagramme est un graphique à barres empilées qui nous montre le pourcentage de gbHARSAH et autres adultes souffrant des infections anogénitales ou pharyngées qui ont été traités avec la thérapie privilégié, autre traitement, autre combinaison ou autre monothérapie selon les Lignes directrices canadienne pour le traitement. L’axe horizontal représente le pourcentage d’adhésion aux lignes directrices sur le traitement, et l’axe vertical représente le type d’infection (anogénitale or pharyngienne) chez les gbHARSAH et d’autres adultes.
| Traitement | Infection anogénitale – gbHARSAH | Infection anogénitale – Autres adultes | Infection pharyngée – gbHARSAH | Infection pharyngée – Autres adultes | ||||
|---|---|---|---|---|---|---|---|---|
| 2014 | 2015 | 2014 | 2015 | 2014 | 2015 | 2014 | 2015 | |
| Thérapie privilégié | 81,6 | 87,2 | 86,7 | 90,9 | 95,6 | 90,8 | 76,0 | 20,0 |
| Autre traitement | 8,1 | 8,2 | 4,7 | 2,4 | 0,0 | 1,7 | 16,0 | 56,4 |
| Autre combinaison | 5,9 | 3,1 | 5,3 | 4,5 | 2,2 | 4,2 | 0,0 | 14,5 |
| Autre monothérapie | 2,7 | 1,0 | 1,3 | 1,7 | 2,2 | 3,4 | 0,0 | 3,6 |
| Inconnu | 1,6 | 0,5 | 2,0 | 0,3 | 0,0 | 0,0 | 8,0 | 5,5 |
- Note de bas de page 1
-
Les autres adultes comprennent les hommes et les femmes non gbHARSAH. Ils n’incluent pas les hommes ayant un comportement sexuel inconnu.
| Type d’infection et Comportement sexuel | Traitement | 2014Note de bas de page * | 2015Note de bas de page ** | |||
|---|---|---|---|---|---|---|
| n | % | n | % | |||
| AnogénitaleNote de bas de page † | gbHARSAH | (P) Ceftriaxone 250 mg, Azithromycine 1 g | 151 | 81,6 | 171 | 87,2 |
| (A) Céfixime 800 mg, Azithromycine 1 g | 6 | 3,2 | 10 | 5,1 | ||
| (A) Azithromycine 2 g | 8 | 4,3 | 6 | 3,1 | ||
| (N) Ceftriaxone 250 mg, Azithromycine 1 g, Doxycycline 100 mg | 2 | 1,1 | 0 | 0,0 | ||
| Autre | 18 | 9,7 | 9 | 4,6 | ||
| Total | 185 | 100 | 196 | 100 | ||
| Autres adultes | (P) Ceftriaxone 250 mg, Azithromycine 1 g | 66 | 44,0 | 26 | 9,1 | |
| (P) Céfixime 800 mg, Azithromycine 1 g | 64 | 42,7 | 235 | 81,9 | ||
| (A) Azithromycine 2 g | 6 | 4,0 | 7 | 2,4 | ||
| (N) Céfixime 800 mg, Ceftriaxone 250 mg, Azithromycine 1 g | 3 | 2,0 | 6 | 2,1 | ||
| Autre | 11 | 7,3 | 13 | 4,5 | ||
| Total | 150 | 100 | 287 | 100 | ||
| Pharyngée | gbHARSAH | (P) Ceftriaxone 250 mg, Azithromycine 1 g | 87 | 95,6 | 108 | 90,8 |
| (A) Céfixime 800 mg, Azithromycine 1 g | 0 | 0,0 | 2 | 1,7 | ||
| (N) Azithromycine 2 g | 1 | 1,1 | 3 | 2,5 | ||
| (N) Ceftriaxone 250 mg, Doxycycline 100 mg | 1 | 1,1 | 1 | 0,8 | ||
| Autre | 2 | 2,2 | 5 | 4,2 | ||
| Total | 91 | 100 | 119 | 100 | ||
| Autres adultes | (P) Ceftriaxone 250 mg, Azithromycine 1 g | 19 | 76,0 | 11 | 20,0 | |
| (A) Céfixime 800 mg, Azithromycine 1 g | 4 | 16,0 | 28 | 50,9 | ||
| (A) Azithromycine 2 g | 0 | 0,0 | 3 | 5,5 | ||
| (N) Céfixime 800 mg, Ceftriaxone 250 mg, Azithromycine 1 g | 0 | 0,0 | 4 | 7,3 | ||
| Autre | 2 | 8,0 | 9 | 16,4 | ||
| Total | 25 | 100 | 55 | 100 | ||
(P) - Traitement privilégié dans les Lignes directrices canadiennes sur les infections transmises sexuellement – infections gonococciques, révisées en juillet 2013 (lignes directrices sur le traitement)Note de bas de page 3.
|
||||||
4.0 Discussion
Il s’agit du deuxième rapport du programme de SARGA qui résume les données sur la sensibilité gonococcique et décrit les répercussions sur la santé publique de la résistance accrue aux céphalosporines et à l’azithromycine.
Grâce à programme de SARGA, les laboratoires partenaires ont soumis un plus grand nombre d’isolats de gonorrhée aux fins d’amélioration des analyses et des données. En 2013, les deux sites participant au programme de SARGA ont fourni 124 cultures. En 2014, ces deux mêmes sites ont soumis 534 cultures et deux nouveaux sites ont commencé à participer. En 2015, 786 cultures ont été obtenues de quatre provinces/territoires. Bien que l’on ne puisse écarter la probabilité que le LNM ait pu analyser ces cultures au moyen de la surveillance de laboratoire de routine, le programme de SARGA permet d’obtenir des données épidémiologiques supplémentaires pour mieux comprendre les traitements, les populations et les facteurs de risque associés aux infections gonococciques.
Plus de 80 % des cas déclarés au programme de SARGA concernaient des hommes. Ce chiffre concorde avec les données historiques qui montrent que, en 2013, 60 % des cas signalés de gonorrhée au Canada concernaient les hommesNote de bas de page 1. Cela pourrait laisser entendre que les hommes, particulièrement les gbHARSAH ont été surreprésentés dans la SARGA parce qu’il est plus probable que ceux-ci se voient demander de fournir un échantillon aux fins de culture conformément aux Lignes directrices canadiennes sur les infections transmissibles sexuellement.
En moyenne, les cas féminins de SARGA étaient plus jeunes que leurs homologues masculins, et ce, dans les quatre villes concernées. En 2014, les taux nationaux de cas déclarés de gonorrhée étaient plus élevés chez les femmes que chez les hommes pour les personnes de moins de 20 ans; en revanche, pour les adultes de 20 ans et plus, les taux étaient plus élevés chez les hommesNote de bas de page 1. Même si les données de la SARGA semblaient refléter ces tendances, la taille de l’échantillon n’a pas permis d’effectuer des analyses par groupe d’âge et par sexe.
Environ la moitié des cas de SARGA qui avaient fourni des échantillons aux fins de culture ont cherché à obtenir des soins de santé en raison de symptômes, ce qui concorderait avec les Lignes directrices canadiennes sur les infections transmissibles sexuellement qui recommandent d’obtenir des cultures auprès des gbHARSAH symptomatiques, y compris auprès de la grande majorité de non gbHARSAH. Cependant, chez les gbHARSAH environ un tiers ont déclaré qu’ils avaient consulté un médecin parce qu’ils avaient été en contact avec un cas ou qu’ils souhaitaient se soumettre à un test de dépistage d’ITS. Même si les deux motifs de consultation médicale les plus souvent invoqués par les femmes étaient la présence de symptômes et un contact avec un cas, les motifs variaient selon les sites sentinelles. De plus, compte tenu du faible nombre de cas féminins de SARGA, il a été difficile de déceler une tendance cohérente.
De 2014 à 2015, la proportion des isolats résistants à l’azithromycine des cas soumis au programme de SARGA a diminué, passant de 1,5 % à 0,5 %, influencée par la diminution de la résistance observée dans les isolats obtenus de gbHARSAH et de femmes. On a observé une augmentation minimale de cette proportion dans les isolats obtenus de non gbHARSAH, qui est passée de 0 % en 2014 à 0,5 % en 2015.
La proportion d’isolats présentant une sensibilité réduite à la céfixime dans toutes les villes combinées participant à la programme de SARGA a diminué, passant de 3,5 % en 2014 à 0,8 % en 2015. Cette diminution est plus importante dans les isolats obtenus d’hommes non gbHARSAH (4,8 % en 2014 à 0,5 % en 2015) et de femmes (7,0 % en 2014 à 0 % en 2015) que dans le cas des gbHARSAH (1,8 % en 2014 à 0,6 % en 2015). Conformément aux recommandations de l’Organisation mondiale de la santé pour les cas où la proportion de souches résistantes se situe à un niveau de 5 % ou plus, ou lorsque toute augmentation inattendue de moins de 5 % est observée dans les populations clés (c.-à-d. gbHARSAH ou travailleurs du sexe), le Canada examine et modifie ses lignes directrices nationales pour le traitement et la gestionNote de bas de page 4.
Les données sur le traitement des isolats soumis au programme de SARGA indiquent que l’utilisation du céfixime (800 mg) et de l’azithromycine (1 g) chez les non gbHARSAH (y compris les femmes) est passée de 42,7 % en 2014 à 81,9 % en 2015 dans le cas des infections anogénitales, et de 16,0 % en 2014 à 56,4 % en 2015 dans le cas des infections pharyngées. La faible utilisation du céfixime en 2014 a probablement été causée par une pénurie survenue pendant cette période. Les cliniques participantes en Alberta ont ensuite adopté la ceftriaxone en juin 2014. Cette tendance s’est inversée en janvier 2015, et, par la suite, on a observé une augmentation du nombre de traitements au céfixime dans le cadre de la SARGA. La thérapie à l’aide du céfixime (800 mg) et de l’azithromycine (1 g) chez les gbHARSAH est demeurée faible pour les infections anogénitales et pharyngiennes. La pénurie de céfixime n’a pas semblé toucher les deux autres provinces/territoires de la même façon.
Bien que la proportion globale de sensibilité réduite à la ceftriaxone dans toutes les provinces/territoires participant à la SARGA ait augmenté légèrement (de 1,5 % à 1,8 %), la proportion d’isolats provenant d’hommes et de femmes qui ne sont pas des gbHARSAH a diminué entre 2014 et 2015. La proportion d’isolats d’hommes gbHARSAH ayant une sensibilité réduite à la ceftriaxone a augmenté, passant de 1,1 % en 2014 à 2,9 % en 2015.
Le traitement privilégié unique pour le traitement des infections anogénitales et pharyngées chez les gbHARSAH (céftriaxone (250 mg) et azithromycine (1 g)) est demeuré le traitement le prévalent pour ce type de cas. Toutefois, cette combinaison de thérapie pour le traitement des infections chez les non gbHARSAH (y compris les femmes) a diminué, passant de 44 % en 2014 à 9,1 % en 2015 dans le cas des infections anogénitales, et de 76 % en 2014 à 20 % en 2015 dans le cas des infections pharyngées. Dans le cas des infections anogénitales chez les non gbHARSAH, cela ne pose pas problème, car le recours à la deuxième thérapie privilégié, soit la combinaison céfixime (800 mg) et azithromycine (1 g), est passée de 42,7 % en 2014 à 81,9 % en 2015. Il peut toutefois y avoir lieu de s’inquiéter du fait que les infections pharyngées chez les non gbHARSAH (y compris les femmes) ont été traitées au moyen d’une autre thérapie (céfixime 800 mg et azithromycine 1 g) dans la moitié des cas (50,9 %), et que des thérapies de remplacement ont été utilisées plus souvent que les thérapies privilégié (29,2 % comparativement à 20 %, respectivement) en 2015. Cela peut être dû au fait que les infections pharyngées sont souvent asymptomatiques; le clinicien n’ayant obtenu un résultat positif qu’après que le traitement a été prescrit pour l’infection anogénitale.
En 2015, les proportions de la sensibilité réduite au céfixime et à la ceftriaxone et de la résistance à l’azithromycine observées dans les provinces/territoires combinées participant au programme de SARGA différaient des taux déterminés dans le système national de surveillance passive en laboratoire. À l’échelle nationale, la sensibilité réduite à l’heure fixe a été de 1,9 %, comparativement au taux de 0,8 % du SARGA. La sensibilité à la ceftriaxone a diminué de 3,5 % à l’échelle nationale et de seulement 1,8 % dans les provinces/territoires participant au programme de SARGA. De même, la résistance à l’azithromycine était beaucoup plus élevée à l’échelle nationale, soit 4,7 % que ce qui a été observé (0,5 %) dans les provinces/territoires participant à la SARGA, en raison d’une résistance accrue à l’azithromycine des isolats prélevés au Québec et en OntarioNote de bas de page 20.
Des isolats gonococciques présentant une sensibilité réduite aux céphalosporines ont été identifiés chez des populations à risque élevé et à transmissions fréquentes comme les gbHARSAH. Étant donné que la céftriaxone et le céfixime, en combinaison avec l’azithromycine, sont les options recommandées pour le traitement privilégié de la gonorrhée, la résistance accrue des infections gonococciques à ces antimicrobiens pourrait déclencher une ère de gonorrhée non traitable à l’aide de l’un ou l’autre de ces antimicrobiens en thérapie combinée. Il est essentiel d’intensifier la surveillance de la RAM et d’étendre la couverture géographique de la SARGA aux fins de l’identification et de la surveillance, partout au Canada, de la propagation des infections gonococciques résistantes à ces antimicrobiens.
Le typage génomique (ST) de la gonorrhée est une méthode de typage hautement discriminatoire qui aide à surveiller la propagation de clones résistants aux antimicrobiens et à cerner les modèles de transmission dans les réseaux sexuels. ST11299 et ST9663 étaient tous deux associés à une mut résistance aux antimicrobiens et ST5985 était associé à la résistance à la tétracycline. Ils ont tous été identifiés principalement dans la population de gbHARSAH. Dans l’ensemble, ST7638 était la ST la plus répandue en 2014 et 2015, à 12,9 %. Il s’agissait de loin de la ST la plus répandue en 2015, à 20,9 %; dix fois plus fréquentes qu’en 2014, à 2,1 %. ST7638 est la quatrième ST en importance à l’échelle nationale (5,69 %). Les isolats de ST7638 sont principalement résistants à la tétracycline (faible concentration) et environ 10 % y sont sensibles.
La majorité des cas dans les quatre sites participants se sont vu prescrire le traitement privilégié ou un autre traitement actuellement proposé dans les Lignes directrices canadiennes sur les infections transmissibles sexuellementNote de bas de page 3. Ce degré élevé de cohérence est probablement dû au fait que les médecins des cliniques de traitement des ITS connaissent bien les Lignes directrices canadiennes sur les infections transmissibles sexuellement, et il n’est pas forcément représentatif des comportements de prescription des omnipraticiens. Selon une étude récente sur la gestion des antibiotiques contre la gonorrhée en Ontario, au Canada, le taux d’observance au traitement de première intention recommandé a diminué à moins de 30 % à la suite de la publication des recommandations de 2011Note de bas de page 23. Après la publication des dernières lignes directrices de l’Ontario en 2013, environ 40 % des patients n’ont pas reçu de traitement de première intention, ce qui les expose à un risque d’échec de traitement et peut favoriser une résistance accrue aux médicamentsNote de bas de page 23. Les organisations de santé publique devraient envisager des façons d’améliorer l’adoption de nouvelles lignes directrices à mesure que les recommandations de traitement de la gonorrhée évoluent en fonction des tendances de la résistance aux antimicrobiens. Par conséquent, il devient de plus en plus souhaitable d’élaborer des stratégies actives de diffusion et de mise en œuvre des lignes directrices afin d’accélérer l’adoption par les cliniciens des nouvelles recommandations pour le traitement de la gonorrhée.
Il se peut aussi que les cliniciens de première ligne n’aient pas accès à de la ceftriaxone injectée par voie intramusculaire et qu’ils s’en remettent à l’utilisation du céfixime par voie orale, même dans les cas d’infection pharyngienne. En outre, les infections pharyngées sont souvent asymptomatiques; le clinicien n’ayant obtenu un résultat positif qu’après que le traitement a été prescrit pour l’infection anogénitale. Une autre possibilité est qu’un patient se présente avec des symptômes génito-urinaires et qu’il soit traité de façon empirique à l’aide de céfixime et d’azithromycine, le pharynx étant asymptomatique et le clinicien n’obtenant une confirmation d’un résultat positif qu’après la consultation. Il opte alors pour un test de contrôle post-traitement plutôt que pour un nouveau traitement, étant donné les faibles niveaux de sensibilité au céfixime. Étant donné que les indications posologiques n’étaient pas disponibles dans certains cas, il est possible que le respect des thérapies recommandées ait été encore plus élevé que ce qui a été observé dans les sites sentinelles de programme de SARGA. Un grand nombre d’autres thérapies combinées concernaient des cas où une thérapie privilégié semblait être fournie sans indication posologique, ou en combinaison avec un autre médicament.
4.1 Limites
Les résultats de l’initiative de SARGA ne sont pas représentatifs de tous les cas de gonorrhée ou des cas de gonorrhée confirmés par culture au Canada. De même, il est possible que les sites sentinelles ne soient pas représentatifs de leur province/territoire. En plus de la représentation géographique limitée, il est possible que les cas au programme de SARGA soient surreprésentés par les gbHARSAH. Étant donné que la majorité des cas de SARGA provenait de l’Alberta, les résultats agrégés doivent être interprétés avec prudence. En outre, certaines données sont difficiles à interpréter compte tenu du petit nombre de cas de SARGA recensés à Winnipeg et à Halifax.
La représentativité relative des gbHARSAH, des non gbHARSAH et des femmes peut varier selon ces sous-populations. Cette variation peut être associée à la proportion de participation par sous-population et au profil des personnes qui ont visité les sites de SARGA. Par exemple, les gbHARSAH participant pourraient représenter tous les cas de gbHARSAH de ces secteurs de compétence en termes de comportements à risque, tandis que les femmes participantes et les non gbHARSAH pourraient être plus à risque que leurs sous-populations sources.
La proportion de foyers d’infection des différents groupes formés selon le sexe et le comportement à risque peut être biaisée selon les lignes directrices en matière de dépistage de chaque site sentinelle ou compétence provinciale. En raison du faible nombre d’isolats présentant une sensibilité réduite aux céphalosporines et une diminution de la résistance à l’azithromycine, il a été difficile de cerner les augmentations et les diminutions significatives entre 2014 et 2015 ou les différences significatives entre les isolats des différents groupes que sont les foyers d’infection, le sexe et les comportements sexuels.
Les données sur les traitements privilégié et de remplacement dans les sites sentinelles reflétaient les pratiques de prescription dans les cliniques de dépistage des ITS participantes et ne devraient pas refléter les pratiques de traitement de la gonorrhée dans les cliniques de dépistage des ITS non participantes dans les trois administrations provinciales où la majorité des cas de gonorrhée ont été diagnostiqués en 2014 et en 2015. De plus, les lignes directrices provinciales sur le traitement et la disponibilité des antimicrobiens privilégiés peuvent avoir influencé les thérapies choisies; un client peut avoir reçu d’autres thérapies empiriques fondées sur des risques ou des présentations au cours d’une première consultation, avant de recevoir un diagnostic d’infection gonococcique.
Le taux d’achèvement de certaines variables était faible ou limité à certains sites sentinelles, et il s’agit d’une autre raison pour laquelle ces résultats ne refléteraient pas le contexte canadien général. En outre, certaines variables étaient fondées sur des données auto déclarées qui ne sont peut-être pas exactes et qui pourraient donner lieu à une sous-déclaration ou à une sur déclaration.
Tous les isolats provenant des cas de SARGA ont été prélevés à l’aide d’un écouvillon au cours de la première consultation ou des rappels après un Test d’amplification des acides nucléiques (TAAN) positif à la consultation initiale. Aucun échec de traitement connu n’a été signalé dans l’une ou l’autre des quatre villes participantes pendant la période à l’étude. Toutefois, il se peut que des personnes ne soient pas retournées à la clinique ou consulter un médecin participant pour un test de contrôle post-traitement. Comme aucune information clinique détaillée (p. ex. les allergies, les autres infections ou les contre-indications), n’a été recueillie pour les besoins de la SARGA, il n’a pas été possible de déterminer avec certitude pourquoi le traitement privilégié ou le traitement de remplacement n’a pas été prescrit. Les tests de contrôle post-traitement et les échecs de traitement peuvent être difficiles à mesurer à l’aide des données de surveillance parce qu’ils reposent sur la capacité de détecter les résultats négatifs.
4.2 Conclusion
L’initiative de surveillance accrue de la résistance de la gonorrhée aux antimicrobiens (SARGA) a surveillé la sensibilité de N. gonorrhoeae aux antimicrobiens en 2014 et 2015 dans les provinces/territoires participantes et a fourni des renseignements supplémentaires pour compléter la surveillance passive en laboratoire de la gonorrhée résistante aux antimicrobiens. Les données de l’initiative de SARGA pour 2014 et 2015 ont démontré une sensibilité réduite aux antimicrobiens recommandés pour les traitements privilégiés comme la ceftriaxone et au céfixime et une résistance à l’azithromycine. Cela suggère que la sensibilité réduite ou la résistance à ces antimicrobiens pourrait compliquer considérablement le traitement de la gonorrhée à l’avenir.
L’initiative de SARGA fournit des données épidémiologiques et de laboratoire intégrées utiles décrivant les comportements à risque, l’information clinique et les taux de sensibilité aux antimicrobiens des infections gonococciques qui n’auraient pas été disponibles autrement à l’échelle nationale. Ce projet a permis de déterminer qu’il est possible de surveiller la résistance de la gonorrhée dans les sites sentinelles partout au Canada en intégrant la surveillance locale, provinciale et territoriale existante. Toutefois, le nombre de sites capables de recueillir de telles données demeure limité et l’élargissement de la portée de la SARGA à l’échelle nationale demeure une priorité.
Étant donné que le Canada est aux prises avec un nombre croissant de cas de gonorrhée et de l’évolution continue ce cette infection, la résistance accrue et croissante aux antimicrobiens, des efforts sont déployés pour recruter d’autres sites pour l’initiative de SARGA afin de permettre la collecte de données plus représentatives qui, à leur tour, seraient plus utiles pour éclairer les lignes directrices sur le traitement, la pratique clinique et les interventions en santé publique. Le programme de SARGA a permis de surveiller la sensibilité aux antimicrobiens gonococciques malgré la diminution du recours à la culture dans la pratique clinique pour le diagnostic de la gonorrhée et les tests de sensibilité aux antimicrobiens. Le rapport récent d’une souche de N. gonorrhoeae résistante à la ceftriaxone au Québec, au Canada, constitue une menace potentielle pour la thérapie de combinaison actuellement utilisée pour traiter la gonorrhée au CanadaNote de bas de page 24. La surveillance continue des modèles de résistance aux antimicrobiens par le biais de la surveillance est d’une importance capitale pour assurer l’efficacité des antimicrobiens recommandés dans le traitement de l’infection gonococcique. La SARGA peut jouer un rôle important dans l’évaluation et la surveillance de l’efficacité des options de traitement de la gonorrhée et dans la réussite des initiatives canadiennes de lutte contre la RAM.
Références
- Note de bas de page 1
-
Agence de la santé publique du Canada. Maladies à déclaration obligatoire en direct. Centre de la lutte contre les maladies transmissibles et les infections. Direction générale de la prévention et du contrôle des maladies infectieuses. Agence de la santé publique du Canada; 2017.
- Note de bas de page 2
-
Barry PM, Klausner JD. The use of cephalosporins for gonorrhea: The impending problem of resistance. Expert Opin Pharmacother 2009;10:555-577.
- Note de bas de page 3
-
Agence de la santé publique du Canada. Lignes directrices canadiennes sur les infections transmissibles sexuellement. Section 5 – Prise en charge et traitement d’infections spécifiques. Infections gonococciques, Révisé : juillet 2013. [cité le 22 juillet 2014]. Accès : https://www.canada.ca/fr/sante-publique/services/maladies-infectieuses/sante-sexuelle-infections-transmissibles-sexuellement/lignes-directrices-canadiennes/infections-transmissibles-sexuellement/lignes-directrices-canadiennes-infections-transmissibles-sexuellement-34.html.
- Note de bas de page 4
-
Organisation mondiale de la santé. Global action plan to control the spread and impact of antimicrobial resistance in Neisseria gonorrhoeae. [cite le 12 June 2012]. Accès : http://www.who.int/reproductivehealth/publications/rtis/9789241503501/en/.
- Note de bas de page 5
-
Unemo M, Shafer WM. Antimicrobial resistance in Neisseria gonorrhoeae in the 21st Century: Past, evolution, and future. Clin Microbiol Rev 2014; 27(3): 587-613.
- Note de bas de page 6
-
Centers for Disease Control and Prevention. Antibiotic resistance threats in the United States, 2013.
- Note de bas de page 7
-
Allen VG, Mitterni L, Seah C, Rebbapragada A, Martin IE, Lee C, Siebert H, Towns L, Melano RG, Lowe DE. Neisseria gonorrhoeae treatment failure and susceptibility to cefixime in Toronto, Canada. JAMA 2013; 309: 163-170.
- Note de bas de page 8
-
Agence de la santé publique du Canada. Plan ministériel 2017-2018 : Agence de la santé. Accès : https://www.canada.ca/content/dam/phac-aspc/documents/corporate/transparency/corporate-management-reporting/reports-plans-priorities/2017-2018-report-plans-priorities-fra.pdf.
- Note de bas de page 9
-
Chambre des communes, Rapport du Comité permanent de la santé (HESA). Étude sur l’état de la résistance aux antimicrobiens au Canada et recommandations connexes 2018. Accès : https://www.ourcommons.ca/Content/Committee/421/HESA/Reports/RP9815159/hesarp16/hesarp16-f.pdf.
- Note de bas de page 10
-
Agence de la santé publique du Canada. Système canadien de surveillance de la résistance aux antimicrobiens – Rapport de 2017. Accès : https://www.canada.ca/content/dam/phac-aspc/documents/services/publications/drugs-health-products/canadian-antimicrobial-resistance-surveillance-system-2017-report-executive-summary/SCSRA-Rapport-2017-Fr.pdf.
- Note de bas de page 11
-
Agence de la santé publique du Canada. Un cadre d’action pancanadien sur les ITSS : réduction des répercussions sur la santé des infections transmissibles sexuellement et par le sang au Canada d’ici 2030. 2018. https://www.canada.ca/content/dam/phac-aspc/documents/services/infectious-diseases/sexual-health-sexually-transmitted-infections/reports-publications/sexually-transmitted-blood-borne-infections-action-framework/infections-transmissibles-sexuellement-sang-cadre-action.pdf
- Note de bas de page 12
-
Martin I, Sawatzky P, Liu G, and Mulvey MR. Antimicrobial resistance to Neisseria gonorrhoeae in Canada: 2009-2013. Canada Communicable Disease Report February 5, 2015; 41-02: 35-41.
- Note de bas de page 13
-
Agence de la santé publique du Canada. Définitions nosologiques des maladies transmissibles faisant l’objet d’une surveillance nationale. Relevé des maladies transmissibles au Canada (RMTC) 2009;3552: le 6 juin 2016.
- Note de bas de page 14
-
Clinical and Laboratory Standards Institute. Performance standards for antimicrobial susceptibility testing. Twenty-fifth international supplement. CLSI document, approved Standard M100-S25. Wayne, PA: Clinical and Laboratory Standards Institute; 2015.
- Note de bas de page 15
-
Centers for Disease Control and Prevention. Sexually Transmitted Disease Surveillance 2007 Supplement, Gonococcal Isolate Surveillance Project (GISP) Annual Report 2007. Atlanta, GA. [cited 30 November 2010]. http://www.cdc.gov/std/gisp2007/gispsurvsupp2007short.pdf.
- Note de bas de page 16
-
Ehret JM, Nims LJ, Judson FN. A clinical isolate of Neisseria gonorrhoeae with in vitro resistance to erythromycin and decreased susceptibility to azithromycin. Sex Transm Dis 1996; 23(4): 270-272.
- Note de bas de page 17
-
Martin IMC, Ison CA, Aanensen DM, et al. Rapid sequence-based identification of gonococcal transmission clusters in a large metropolitan area. J Infect Dis 2004; 189: 1497-1505.
- Note de bas de page 18
-
Larkin MA, Blackshields G, Brown NP, Chenna R, McGettigam PA, McWilliam H, Valentin F, Wallace IM, Wilm A, Lopez R, Thompson JD, Gibson TJ, Higgins DG. Clustal W and Clustal X version 2.0. Bioinformatics 2007; 23(21): 2947-2948.
- Note de bas de page 19
-
Tamura K, Nei M. Estimation of the number of nucleotide substitutions in the control region of mitochondrial DNA in humans and chimpanzees. Mol Biol Evol 1993;10:512-526.
- Note de bas de page 20
-
Agence de la santé publique du Canada. Laboratoire national de microbiologie. 2015. Surveillance nationale de la sensibilité aux antimicrobiens de Neisseria gonorrhoeae : Rapport sommaire annuel de 2015.
- Note de bas de page 21
-
Unemo M, Golparian D, Syversen G, Vestrheim DF, Mol H. Two cases of verified clinical failures using internationally recommended first-line cefixime for gonorrhoea treatment, Norway, 2010. Eurosurveillance 2010; 15(47) : pii=19721.
- Note de bas de page 22
-
Unemo M, Golparian D, Potočnik M, Jeverica S. Treatment failure of pharyngeal gonorrhoea with internationally recommended first-line ceftriaxone verified in Slovenia, September 2011. Eurosurveillance 2012; 17(25): pii=20200.
- Note de bas de page 23
-
Dickson C, Taljaard M, Friedman DS, Metz G, Wong T, Grimshaw JM. The antibiotic management of gonorrhoea in Ontario, Canada following multiple changes in guidelines: An interrupted time-series analysis. Sex Transm Infect Published Online First: 26-08-2017. doi:10.1136/sextrans-2017-053224, pp 1-6.
- Note de bas de page 24
-
Lefebvre B, Martin I, Demczuk W, Deshaies L, Michaud S, Labbé A-C, Beaudoin M-C, Longtin J. Ceftriaxone-resistant Neisseria gonorrhoeae, Canada, 2017. Emerging Infectious Diseases 2018; 24(2): 381-383.
Annexe A
| Antibiotique | Plages de concentrations recommandées pour les tests (mg/L) | Norme d’interprétation de la CMI (mg/L)Note de bas de page a | Source de l’antibiotique | |||
|---|---|---|---|---|---|---|
| SNote de bas de page b | SRNote de bas de page c | INote de bas de page d | RNote de bas de page e | |||
| Pénicilline | 0,032 à 128,0 | ≤ 0,06 | s/o | 0,12 à 1,0 | ≥ 2,0 | Sigma |
| Tétracycline | 0,064 à 64,0 | ≤ 0,25 | s/o | 0,5 à 1,0 | ≥ 2,0 | Sigma |
| Érythromycine | 0,032 à 32,0 | ≤ 1,0 | s/o | s/o | ≥ 2,0 | Sigma |
| Spectinomycine | 4,0 à 256,0 | ≤ 32,0 | s/o | 64 | ≥ 128,0 | Sigma |
| Ciprofloxacine | 0,001 à 64,0 | ≤ 0,06 | s/o | 0,12 à 0,5 | ≥ 1,0 | Bayer Health Care |
| Ceftriaxone | 0,001 à 2,0 | s/o | ≥ 0,125 | s/o | s/o | Sigma |
| Céfixime | 0,002 à 2,0 | s/o | ≥ 0,25 | s/o | s/o | Sigma |
| Azithromycine | 0,016 à 32,0 | ≤ 1,0 | s/o | s/o | ≥ 2.0 | Pfizer |
| Ertapénème | 0,002 à 2,0 | Norme d’interprétation non accessible | Sequoia | |||
| Gentamicine | 0,5 à 128,0 | Norme d’interprétation non accessible | MP Biomedicals | |||
|
||||||
Annexe B
| Caractérisation | Description | Définition |
|---|---|---|
| NGPP | Neisseria gonorrhoeae producteur de pénicillinase | CMI Pen ≥ 2,0 mg/L, positif pour β-lactamase, plasmide β-lactamase (plasmide de 3,05, 3,2 ou 4,5 Md) |
| NGRT | Neisseria gonorrhoeae résistant à la tétracycline | CMI Tét ≥ 16,0 mg/L, plasmide de 25,2 Md, positif pour réaction de polymérisations en chaîne de Tét M |
| NGRMC | Neisseria gonorrhoeae présentant une résistance à médiation chromosomique | CMI Pén MIC ≥ 2,0 mg/L, CMI Tét ≥ 2,0 mg/L mais ≤ 8,0 mg/L, et CMI Éry ≥ 2,0 mg/L |
| NGRMC probable | Neisseria gonorrhoeae présentant une résistance à médiation chromosomique probable | Une des valeurs de CMI de Pén, Tét, Éry = 1 mg/L, les deux autres ≥ 2,0 mg/L |
| RPén | Neisseria gonorrhoeae résistant à la pénicilline | CMI Pén ≥ 2,0 mg/L, négatif pour β-lactamase |
| RTét | Neisseria gonorrhoeae résistant à la tétracycline | CMI Tét ≥ 2,0 mg/L mais ≤ 8,0 mg/L |
| RÉry | Neisseria gonorrhoeae résistant à l’érythromycine | CMI Éry ≥ 2,0 mg/L |
| RCip | Neisseria gonorrhoeae résistant à la ciprofloxacine | Cip MIC ≥ 1.0 mg/L |
| RAzi | Neisseria gonorrhoeae résistant à l’azithromycine | CMI Az ≥ 2,0 mg/L |
| RSpec | Neisseria gonorrhoeae résistant à la spectinomycine | R Spec ≥ 128 mg/L |
| SRCx | Neisseria gonorrhoeae ayant une sensibilité réduite à la ceftriaxone | CMI Cx ≥ 0,125 mg/L |
| SRCe | Neisseria gonorrhoeae ayant une sensibilité réduite au céfixime | CMI Ce ≥ 0,25 mg/L |
Annexe C
| Résistance aux antimicrobiensNote de bas de page * | 2014 | 2015 | ||
|---|---|---|---|---|
| Hommes gbHARSAH | n | (%) | n | (%) |
| CéfiximeSRNote de bas de page * | 5 | 1,8 | 2 | 0,6 |
| CeftriaxoneSRNote de bas de page * | 3 | 1,1 | 9 | 2,9 |
| AzithromycineRNote de bas de page ** | 6 | 2,2 | 1 | 0,3 |
| CiprofloxacineRNote de bas de page ** | 84 | 30,4 | 151 | 47,9 |
| TétracyclineRNote de bas de page ** | 170 | 61,6 | 222 | 70,5 |
| PénicillineRNote de bas de page ** | 57 | 20,7 | 68 | 21,6 |
| ÉrythromycineRNote de bas de page ** | 93 | 33,7 | 139 | 44,1 |
| Sensibles à tous les antibiotiques testés | 94 | 34,1 | 75 | 23,8 |
| Total Hommes gbHARSAH | 276 | 100 | 315 | 100 |
| Hommes non gbHARSAH | n | (%) | n | (%) |
| CéfiximeSRNote de bas de page * | 5 | 4,8 | 1 | 0,5 |
| CeftriaxoneSRNote de bas de page * | 2 | 1,9 | 1 | 0,5 |
| AzithromycineRNote de bas de page ** | 0 | 0,0 | 1 | 0,5 |
| CiprofloxacineRNote de bas de page ** | 20 | 19,2 | 30 | 13,6 |
| TétracyclineRNote de bas de page ** | 29 | 27,9 | 100 | 45,2 |
| PénicillineRNote de bas de page ** | 10 | 9,6 | 21 | 9,5 |
| ÉrythromycinRNote de bas de page ** | 10 | 9,6 | 24 | 10,9 |
| Sensible à tous les antibiotiques testés | 66 | 63,5 | 117 | 52,9 |
| Total Hommes non gbHARSAH | 104 | 100 | 221 | 100 |
| Femmes | n | (%) | n | (%) |
| CéfiximeSRNote de bas de page * | 5 | 7,0 | 0 | 0,0 |
| CeftriaxoneSRNote de bas de page * | 1 | 1,4 | 0 | 0,0 |
| AzithromycineRNote de bas de page ** | 1 | 1,4 | 1 | 0,8 |
| CiprofloxacineRNote de bas de page ** | 17 | 23,9 | 15 | 12,4 |
| TétracyclineRNote de bas de page ** | 23 | 32,4 | 46 | 38,0 |
| PénicillineRNote de bas de page ** | 7 | 9,9 | 7 | 5,8 |
| ÉrythromycineRNote de bas de page ** | 9 | 12,7 | 7 | 5,8 |
| Sensible à tous les antibiotiques testés | 44 | 62,0 | 72 | 59,5 |
| Total Femmes | 71 | 100 | 121 | 100 |
| TousNote de bas de page *** | n | (%) | n | (%) |
| CéfiximeSRNote de bas de page * | 16 | 3,5 | 5 | 0,8 |
| CeftriaxoneSRNote de bas de page * | 7 | 1,5 | 12 | 1,8 |
| AzithromycineRNote de bas de page ** | 7 | 1,5 | 3 | 0,5 |
| CiprofloxacineRNote de bas de page ** | 124 | 27,1 | 198 | 30,0 |
| TétracyclineRNote de bas de page ** | 228 | 49,8 | 371 | 56,2 |
| PénicillineRNote de bas de page ** | 79 | 17,2 | 98 | 14,8 |
| ÉrythromycineRNote de bas de page ** | 116 | 25,3 | 172 | 26,1 |
| Sensibles à tous les antibiotiques testés | 205 | 44,8 | 264 | 40,0 |
| Total générale | 458 | 100 | 660 | 100 |
|
||||
| 2014 TotauxNote de bas de page ** | CéfiximeSRNote de bas de page * | CeftriaxoneSRNote de bas de page * | AzithromycineRNote de bas de page * | PénicillineRNote de bas de page * | TétracyclineRNote de bas de page * | ÉrythromycineRNote de bas de page * | CiprofloxacineRNote de bas de page * | ||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| n | % | n | % | n | % | n | % | n | % | n | % | n | % | ||
| Femmes | 93 | 6 | 6,5 | 1 | 1,1 | 1 | 1,1 | 11 | 11,8 | 30 | 32,3 | 13 | 14,0 | 23 | 24,7 |
| Col de l’utérus | 51 | 3 | 5,9 | 0 | 0,0 | 0 | 0,0 | 6 | 11,8 | 14 | 27,5 | 7 | 13,7 | 12 | 23,5 |
| Pharynx | 24 | 2 | 8,3 | 0 | 0,0 | 1 | 4,2 | 3 | 12,5 | 9 | 37,5 | 4 | 16,7 | 7 | 29,2 |
| Rectum | 17 | 1 | 5,9 | 1 | 5,9 | 0 | 0,0 | 2 | 11,8 | 7 | 41,2 | 2 | 11,8 | 4 | 23,5 |
| Hommes | 439 | 12 | 2,7 | 7 | 1,6 | 7 | 1,6 | 79 | 18,0 | 238 | 54,2 | 119 | 27,1 | 119 | 27,1 |
| Pharynx | 96 | 3 | 3,1 | 2 | 2,1 | 3 | 3,1 | 22 | 22,9 | 68 | 70,8 | 32 | 33,3 | 34 | 35,4 |
| Rectum | 124 | 2 | 1,6 | 1 | 0,8 | 1 | 0,8 | 24 | 19,4 | 81 | 65,3 | 39 | 31,5 | 33 | 26,6 |
| Urètre | 216 | 7 | 3,2 | 4 | 1,9 | 3 | 1,4 | 33 | 15,3 | 89 | 41,2 | 48 | 22,2 | 52 | 24,1 |
|
|||||||||||||||
| 2015 TotauxNote de bas de page ** | CéfiximeSRNote de bas de page * | CeftriaxoneSRNote de bas de page * | AzithromycineRNote de bas de page * | PénicillineRNote de bas de page * | TétracyclineRNote de bas de page * | ÉrythromycineRNote de bas de page * | CiprofloxacineRNote de bas de page * | ||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| n | % | n | % | n | % | n | % | n | % | n | % | n | % | ||
| Femmes | 168 | 0 | 0,0 | 0 | 0,0 | 1 | 0,6 | 8 | 4,8 | 70 | 41,7 | 13 | 7,7 | 22 | 13,1 |
| Col de l’utérus | 77 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 4 | 5,2 | 29 | 37,7 | 5 | 6,5 | 8 | 10,4 |
| Pharynx | 52 | 0 | 0,0 | 0 | 0,0 | 1 | 1,9 | 3 | 5,8 | 28 | 53,8 | 6 | 11,5 | 10 | 19,2 |
| Rectum | 38 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 2,6 | 13 | 34,2 | 2 | 5,3 | 4 | 10,5 |
| Hommes | 618 | 6 | 1,0 | 14 | 2,3 | 2 | 0,3 | 107 | 17,3 | 383 | 62,0 | 192 | 31,1 | 218 | 35,3 |
| Pharynx | 124 | 4 | 3,2 | 8 | 6,5 | 0 | 0,0 | 24 | 19,4 | 84 | 67,7 | 54 | 43,5 | 59 | 47,6 |
| Rectum | 145 | 0 | 0,0 | 4 | 2,8 | 0 | 0,0 | 37 | 25,5 | 106 | 73,1 | 66 | 45,5 | 70 | 48,3 |
| Urètre | 349 | 2 | 0,6 | 2 | 0,6 | 2 | 0,6 | 46 | 13,2 | 193 | 55,3 | 72 | 20,6 | 89 | 25,5 |
|
|||||||||||||||
Annexe D
| Infection anogénitale - gbHARSAH | 2014 | 2015 |
|---|---|---|
| (P) Ceftriaxone 250 mg, Azithromycine 1 g | 151 | 171 |
| (A) Céfixime 800 mg, Azithromycin 1 g | 6 | 10 |
| (A) Azithromycin 2 g | 8 | 6 |
| (N) Ceftriaxone 250 mg, Azithromycin 1 g, Doxycycline 100mg | 2 | 0 |
| (N) Céfixime/Azithromycine* | 3 | 0 |
| (N) Céfixime 800 mg, Ceftriaxone 250 mg, Azithromycine 1 g | 1 | 1 |
| (N) Azithromycine 1 g | 1 | 1 |
| (N) Céfixime 800 mg, Azithromycine 1 g, Bicilline 2,4 million unités | 1 | 0 |
| (N) Ceftriaxone 250 mg, Azithromycin 1 g, Ciprofloxacine 500 mg | 0 | 1 |
| (N) Spectinomycine 2 g (par l’entremise du PAS) | 1 | 0 |
| (N) Ciprofloxacine 500 mg | 0 | 1 |
| (N) Ceftriaxone 250 mg, Doxycycline 100 mg | 1 | 0 |
| (N) Ceftriaxone 250 mg, Azithromycin 2 g, Bicilline | 0 | 1 |
| (A) Spectinomycine 2 g (par l’entremise du PAS), Azithromycine 1 g | 1 | 0 |
| (N) Ceftriaxone 250 mg, Azithromycin 1 g, Doxycycline 100 mg bid x 14d | 1 | 0 |
| (N) Ceftriaxone 250 mg, Azithromycin 1 g, Benzathine pénicilline | 1 | 0 |
| (N) Céfixime 800 mg | 1 | 0 |
| (N) Ceftriaxone 250 mg, Azithromycine 1 g, Bicilline | 0 | 1 |
| (N) Ceftriaxone 250 mg | 1 | 0 |
| (N) Azithromycine 1 g, Ceftriaxone 500 mg | 1 | 0 |
| (N) Ceftriaxone | 1 | 0 |
| (N) Céfixime 400 mg, Azithromycine 1 g | 0 | 1 |
| (N) Ceftriaxone 125 mg, Azithromycine 1 g | 0 | 1 |
| Inconnu | 3 | 1 |
| Infection anogénitale – Autres adultes | 2014 | 2015 |
| (P) Céfixime 800 mg, Azithromycine 1 g | 64 | 235 |
| (P) Ceftriaxone 250 mg, Azithromycine 1 g | 66 | 26 |
| (A) Azithromycine 2 g | 6 | 7 |
| (N) Céfixime 800 mg, Ceftriaxone 250 mg, Azithromycine 1 g | 3 | 6 |
| (N) Azithromycine 1 g | 1 | 2 |
| (N) Céfixime 800 mg | 0 | 2 |
| (N) Céfixime 800 mg, Azithromycine 1 g, Azithromycine 2 g | 1 | 1 |
| (N) Ceftriaxone 250 mg, Doxycycline 100 mg | 2 | 0 |
| (N) Céfixime 400 mg, Céfixime 800 mg, Ceftriaxone 250 mg, Azithromycine 1 g | 0 | 1 |
| (N) Céfixime 400 mg, Céfixime 800 mg, Azithromycine 1 g | 1 | 0 |
| (A) Spectinomycine 2 g (par l’entremise du PAS), Azithromycine 1 g | 1 | 0 |
| (N) Ceftriaxone 250 mg | 1 | 0 |
| (N) Céfixime 400 mg, Azithromycine 1 g | 0 | 1 |
| (N) Ceftriaxone 250 mg, Azithromycine 1 g, Doxycycline 100 mg, Dox 14 jours | 0 | 1 |
| (N) Ceftriaxone 250 mg, Doxycycline 100 mg, Ciprofloxacin 500 mg, Dox 14 days | 0 | 1 |
| (N) Ceftriaxone 250 mg, Doxycycline 100 mg, Dox 14 jours | 1 | 0 |
| (N) Ceftriaxone 250 mg, Doxycycline 100 mg, Dox 14 jours | 0 | 1 |
| (N) Doxycycline 100 mg | 0 | 1 |
| (N) Céfixime 800 mg, Ceftriaxone 250 mg, Doxycycline 100 mg, Dox 14 jours | 0 | 1 |
| Inconnu | 3 | 1 |
| Infection pharyngée – gbHARSAH | 2014 | 2015 |
| (P) Ceftriaxone 250 mg, Azithromycin 1 g | 87 | 108 |
| (N) Azithromycine 2 g | 1 | 3 |
| (A) Céfixime 800 mg, Azithromycine 1 g | 0 | 2 |
| (N) Ceftriaxone 250 mg, Doxycycline 100 mg | 1 | 1 |
| (N) Azithromycine 1 g, Spectinomycine 2 g (par l’entremise du PAS) | 0 | 1 |
| (N) Ceftriaxone 250 mg | 1 | 0 |
| (N) Ceftriaxone 250 mg, Azithromycine 1 g, Benzathine pénicilline | 1 | 0 |
| (N) Ceftriaxone 250 mg, Bicilline | 0 | 1 |
| (N) Ceftriaxone 250 mg, Doxycycline 100 mg, Dox 14 jours | 0 | 1 |
| (N) Ciprofloxacine 500 mg | 0 | 1 |
| (N) Doxycycline 100 mg, Ciprofloxacine 500 mg, Dox 14 jours | 0 | 1 |
| Infection pharyngée – Autres adultes | 2014 | 2015 |
| (A) Céfixime 800 mg, Azithromycine 1 g | 4 | 28 |
| (P) Ceftriaxone 250 mg, Azithromycine 1 g | 19 | 11 |
| (N) Céfixime 800 mg, Ceftriaxone 250 mg, Azithromycine 1 g | 0 | 4 |
| (A) Azithromycine 2 g | 0 | 3 |
| (N) Azithromycine 1 g | 0 | 1 |
| (N) Céfixime 800 mg | 0 | 1 |
| (N) Céfixime 800 mg, Ceftriaxone 250 mg, Azithromycine 1 g, Doxycycline 100 mg | 0 | 1 |
| (N) Ceftriaxone 250 mg, Azithromycine 1 g, Azithromycine 2 g | 0 | 1 |
| (N) Ceftriaxone 250 mg, Doxycycline 100 mg, Dox 14 jours | 0 | 1 |
| (N) Spectinomycine 2 g (par l’entremise du PAS), Ciprofloxacine 500 mg | 0 | 1 |
| Inconnu | 2 | 3 |
- Note de bas de page 1
-
gbHARSAH : gais, bisexuels, hommes ayant des relations sexuelles avec des hommes
- Note de bas de page b
-
En l’absence d’un consensus pancanadien quant à la définition d’un échec au traitement, la définition propose pour un cas d’échec au traitement est l’absence de contact sexuel ET la présence de l’une des conditions suivantes: 1) des diplocoques intracellulaires gram négatifs pendant au moins 72 heures après le traitement; 2) une culture positive pour N. gonorrhoeae au moins 72 heures après le traitement; ou 3) un test d’amplification des acides nucléiques (TANN) positif pour N. gonorrhoeae au moins 2 à 3 semaines après le traitement(4).
- Note de bas de page c
-
Le céfixime, la ceftriaxone et l’azithromycine font partie des traitements préférés contre la gonorrhée au Canada(3).
- Note de bas de page d
-
Le céfixime, la ceftriaxone et l’azithromycine font partie des traitements préférés contre la gonorrhée au Canada(3).
- Note de bas de page e
-
Le céfixime, la ceftriaxone et l’azithromycine font partie des traitements préférés contre la gonorrhée au Canada(3).
- Note de bas de page f
-
Lignes directrices canadiennes sur les infections transmissibles sexuellement – infections gonococciques, révisées en juillet 2013 (3).