Système canadien de surveillance de la résistance aux antimicrobiens - Rapport de 2017

Télécharger le rapport complet (Format PDF, 657 ko, 139 pages)
Organisation : Agence de la Santé Publique du Canada
Publiée : 2017-11-06
Résumé
Message de l'administratrice en chef de la santé publique et de la présidente de l'Agence de la santé publique du Canada
À l'heure actuelle, la résistance aux antimicrobiens (RAM) demeure l'une des plus importantes menaces en matière de santé publique dans le monde. Les infections pharmacorésistantes constituent une menace à l'égard des soins de santé tels que nous les connaissons aujourd'hui, puisqu'elles diminuent notre capacité à prévenir et à traiter les infections. Au Canada, bien que les taux globaux de RAM soient restés stables au cours des dernières années, nous avons constaté qu'ils dépassent largement les taux observés au début des années 2000. Il est essentiel de déployer des efforts collectifs et continus pour diminuer le taux de RAM et préserver l'efficacité des antimicrobiens existants, et ainsi assurer notre capacité à combattre les maladies infectieuses.
Septembre 2017 a marqué la publication du document Lutter contre la résistance aux antimicrobiens et optimiser leur utilisation : un cadre d'action pancanadien (le Cadre). Le Cadre est issu d'efforts de collaboration de la part du gouvernement fédéral, des provinces et des territoires ainsi que d'autres partenaires clés dans les secteurs de la santé humaine et animale. Il a été conçu pour orienter les efforts de lutte contre la RAM et l'utilisation des antimicrobiens (UAM) dans l'ensemble de secteurs, en mettant l'accent sur les quatre éléments clés suivants : surveillance, gestion, prévention et contrôle des infections, et recherche et innovation. Le Système canadien de surveillance de la résistance aux antimicrobiens (SCSRA) fournit une base de données probantes à partir de laquelle il est possible de renforcer l'intégration.
Grâce à la synthèse et à l'analyse des renseignements provenant des systèmes de surveillance et des services de référence en laboratoire de l'Agence de la santé publique du Canada (ASPC), le SCSRA fournit un tableau exhaustif de la RAM et de l'UAM au Canada. Tentant de combler les lacunes déterminées dans le rapport de l'année dernière, le rapport de 2017 du SCSRA fournit plus de données de surveillance sur la RAM dans les organismes prioritaires et sur les infections survenant au sein de la communauté. Il présente également de nouveaux renseignements sur l'UAM auprès des prescripteurs non-médecins et la surveillance étendue de la RAM chez les animaux destinés à l'alimentation.
L'ASPC s'appuie sur les relations et les efforts collectifs de nombreux partenaires afin de fournir un tableau plus exhaustif de la RAM et de l'UAM au Canada dans le présent rapport. Nous remercions tous les contributeurs pour leur temps et leur soutien continu, et nous nous réjouissons à l'idée des collaborations nouvelles et continues qui visent à améliorer la surveillance de la RAM et de l'UAM au Canada.

Siddika Mithani
Présidente, Agence de santé publique du Canada

Dre Theresa Tam
Administratrice en chef de la santé publique
Introduction
Le Système canadien de surveillance de la résistance aux antimicrobiens (SCSRA) est le système de surveillance national pour la production de rapports sur la résistance aux antimicrobiens (RAM) et l'utilisation des antimicrobiens (UAM). Le SCSRA intègre et synthétise les renseignements provenant des systèmes de surveillance et des services de référence en laboratoire de l'Agence de la santé publique du Canada (ASPC), couvrant la population humaine et la population d'animaux destinés à l'alimentation. Le système a pour but de fournir des données probantes visant à appuyer l'élaboration des politiques et des programmes pour encourager une utilisation prudente des antimicrobiens et pour prévenir, limiter et contrôler la RAM au Canada. Il s'agit d'un élément essentiel du document Lutter contre la résistance aux antimicrobiens et optimiser leur utilisation : un cadre d'action pancanadienNote de bas de page 1.
Le rapport de 2017 du SCSRA fournit une analyse de la RAM et de l'UAM d'après les données de 2015 et 2016. En outre, il présente de nouveaux renseignements sur les infections résistantes aux antimicrobiens en milieu communautaire, les pratiques de prescription d'antimicrobiens chez les dentistes, la RAM dans les fermes sentinelles d'élevages de dindes, et l'utilisation des antimicrobiens chez les animaux de compagnie.
En 2014, le Comité directeur sur les maladies transmissibles et infectieuses (CDMTI) du Réseau pancanadien de santé publique et l'ASPC ont examiné une liste provisoire de microorganismes qui présentent une résistance aux antimicrobiens. À partir de cette liste, le groupe de travail sur la RAM du CDMTI a déterminé les microorganismes revêtant la plus grande importance pour la santé publique au Canada, et, par conséquent, prioritaires pour ce qui est de la surveillance nationaleNote de bas de page 2. Les renseignements techniques présentés sur les microorganismes prioritaires dans le cadre de chaque publication du SCSRA sont adaptés en fonction de mises à jour des données, de la disponibilité des données ainsi que des besoins changeants en matière d'information sur la RAM, lesquels sont établis grâce aux consultations continues avec les intervenants. Ainsi, le SCSRA s'engage à être flexible et à répondre aux problèmes liés à la RAM et à la surveillance de la RAM au Canada.
Il est possible d'effectuer des comparaisons à l'échelle internationale entre le Canada et les autres pays en ce qui a trait à la RAM uniquement lorsque les données sont présentées à l'échelle nationale et lorsqu'elles sont recueillies à l'aide de méthodes comparables. Bien que certaines données canadiennes sur les microorganismes résistants aux antimicrobiens soient recueillies et déclarées d'une façon permettant de faire des comparaisons à l'échelle internationale, ce n'est pas le cas de la plupart. Malgré ce défi, le rapport de 2017 du SCSRA vise à fournir une perspective internationale sur la RAM, le cas échéant, afin de fournir un plus vaste contexte pour les conclusions de la surveillance de la RAM au Canada.
Bien que le SCSRA fournisse des données utiles et fiables sur la résistance aux antimicrobiens et l'utilisation des antimicrobiens, des lacunes subsistent. Le rapport de 2017 du SCSRA décrit les limites actuelles de la surveillance de la RAM et de l'UAM au Canada, et fournit une mise à jour sur les efforts prévus ou en cours pour combler les lacunes existantes en matière de surveillance.
Le rapport de 2017 du SCSRA est divisé en deux parties. La première partie est un résumé qui met en évidence les conclusions de la surveillance de la RAM et de l'UAM au Canada. La deuxième partie est une annexe technique qui fournit un examen plus détaillé des données sur la surveillance de la RAM et de l'UAM. L'annexe technique comprend une section sur la RAM qui porte sur chaque microorganisme prioritaire et décrit les méthodes de surveillance et la situation au Canada. La section sur la RAM de l'annexe technique fournit des renseignements sur l'utilisation d'antimicrobiens chez les humains. Les données relatives à la population humaine portent sur la quantité d'antimicrobiens délivrés par les pharmacies communautaires, la répartition des spécialisations des prescripteurs, les achats d'antimicrobiens effectués par les hôpitaux et les indications relatives à l'utilisation des antimicrobiens.
Résumé
Résistance aux antimicrobiens et utilisation des antimicrobiens
De 2011 à 2016, le Canada a déclaré des taux de RAM semblables ou inférieurs à ceux déclarés par de nombreux autres pays développésNote de bas de page 3 Note de bas de page 4 Note de bas de page 5. Les infections causées par certains microorganismes résistants aux antimicrobiens ont augmenté dans certaines populations au cours des dernières années, tandis que les taux d'autres infections ont diminué. Par exemple, une tendance à la hausse a été observée pour les taux d'infection du sang à SARM dans les hôpitaux pédiatriques et les taux d'infections du sang aux entérocoques résistants à la vancomycine (ERV) dans les hôpitaux pour adultes. En outre, le taux de gonorrhée pharmacorésistante a augmenté entre 2014 et 2015. À l'inverse, les taux d'infections à Clostridium difficile (ICD) associées aux soins de santé ont diminué au fil du temps.
Si l'on examine l'utilisation des antimicrobiens au sein de la communauté au Canada, le taux d'ordonnances délivrées était relativement stable entre 2013 et 2016 et légèrement inférieur aux taux observés entre 2010 et 2012. Terre-Neuve-et-Labrador a enregistré le taux le plus élevé d'ordonnances délivrées au sein de la communauté en 2016, tandis que la Colombie-Britannique a enregistré le plus faible taux. En 2015, sur 31 pays, le Canada se classait au 13e rang en matière de consommation d'antimicrobiens, ce qui représente un reculement léger par rapport à 2014, où le Canada se classait au 12e rang parmi 31 paysNote de bas de page 5. On a observé une tendance à la baisse du taux de prescription d'antimicrobiens par les médecins, et un taux généralement stable du taux de prescription d'antimicrobiens par les dentistes, à la suite d'une augmentation de ce dernier entre 2010 et 2012. Pour ce qui est de l'utilisation des antimicrobiens en milieu hospitalier, les achats d'antimicrobiens sont demeurés stables entre 2010 et 2016. En 2016, le Manitoba, l'Île-du-Prince-Édouard et Terre-Neuve-et-Labrador enregistraient le plus fort taux d'achat d'antimicrobiens par habitant, alors que l'Ontario et l'Alberta enregistraient les plus faibles. En 2016, les hôpitaux ont acheté un plus grand nombre d'antimicrobiens considérés comme étant « de dernier recours » (p. ex. la daptomycine) que les années précédentes, ce qui est préoccupantNote de bas de page 6.
Les principaux résultats selon la surveillance de la RAM et de l'UAM sont présentés ci-dessous.
Résistance aux antimicrobiens
Promouvoir une formation normalisée en matière de prévention et lutte contre des infections en combinaison avec la gestion antimicrobienne contribue à réduire la propagation des infections, les prescriptions inappropriées et, par conséquent prévenir le développement de la RAM au Canada.
Même si le taux de RAM dans les isolats humains cliniques du Canada n'est pas aussi considérable que dans d'autres pays, il existe certaines préoccupationsNote de bas de page 7.
Bien que la bactérie Clostridium difficile ne soit habituellement pas considérée comme un microorganisme résistant aux antimicrobiens, l'infection à Clostridium difficile (ICD) peut être attribuable aux traitements médicamenteux standard couramment prescrits pour les infections non associées, parce que les bactéries sont naturellement résistantes à de nombreux antimicrobiens et se propagent rapidement dès que les microorganismes co-existants ont été éliminées par l'utilisation de ces médicamentsNote de bas de page 8. En 2016, les taux d'infection à Clostridium difficile (ICD) associée aux soins de santé ont continué à baisser au Canada. Le taux global d'ICD associée aux soins de santé a diminué, passant de 6,64 cas pour 10 000 jours-patients en 2011 à 4,05 cas pour 10 000 jours-patients en 2016 (figure 1). Lorsque les types d'hôpitaux sont comparés, le taux d'ICD associée aux soins de santé de 2016 a continué d'être plus élevé dans les hôpitaux pour adultes que dans les hôpitaux pédiatriques (4,50 et 3,25 pour 10 000 jours-patients, respectivement). La surveillance de l'ICD d'origine communautaire dans les hôpitaux sentinelles a commencé en 2015 et se poursuivra pendant trois ans. Les données de surveillance de la première année (2015) ont révélé que 37 % de toutes les ICD signalées chez des patients admis dans les hôpitaux sentinelles étaient d'origine communautaire. Cette proportion est similaire aux autres proportions d'ICD d'origine communautaire qui ont été déclarées dans la littératureNote de bas de page 5.
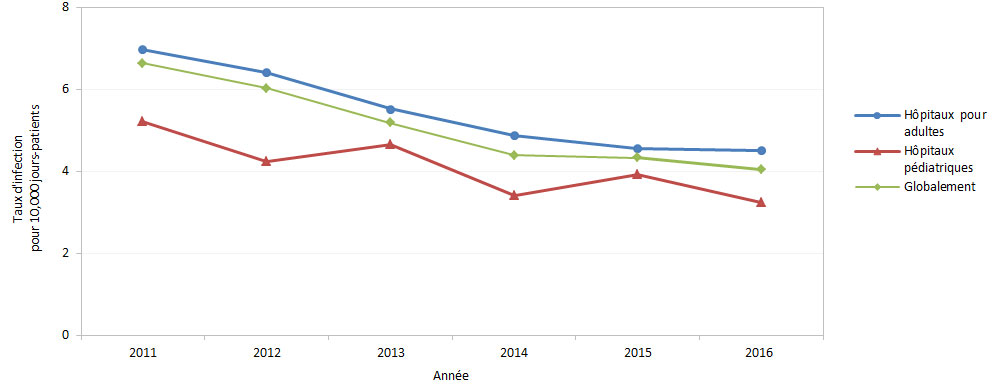
Figure 1 - Équivalent du texte
| 2011 | 2012 | 2013 | 2014 | 2015 | 2016 | |
|---|---|---|---|---|---|---|
| Hôpitaux pour adultes | 6.96 | 6.42 | 5.52 | 4.87 | 4.56 | 4.50 |
| Hôpitaux pédiatriques | 5.22 | 4.23 | 4.66 | 3.40 | 3.93 | 3.25 |
| Globalement | 6.64 | 6.03 | 5.19 | 4.39 | 4.33 | 4.25 |
Le présent graphique linéaire démontre le taux d'infection à C. difficile pour 10 000 jours-patients par type d'hôpital au Canada entre 2011 et 2016. L'axe horizontal réprésente l'année et l'axe vertical indique le taux d'infection.
La résistance aux antimicrobiens de la classe des carbapénèmes constitue un indicateur déterminant de résistance pour le groupe des entérobactéries. Pour les infections causées par desentérobactéries productrices de carbapénémase (EPC), les options thérapeutiques sont limitées et sont associées à de mauvais résultats de santé, ce qui en fait une préoccupation majeure en matière de santé publique dans le monde entierNote de bas de page 9. À l'échelle mondiale, les taux d'infection par EPC et d'autres organismes producteurs de carbapénémase ont augmenté au fil du tempsNote de bas de page 4,Note de bas de page 5, tandis que les taux d'EPC au Canada sont restés faibles et relativement stables. De 2011 à 2014, le taux national par d'EPC dans les hôpitaux sentinelles a diminué, passant de 0,13 cas à 0,07 cas pour 10 000 jours-patients. En 2015, ce taux a augmenté très légèrement pour atteindre 0,08 cas pour 10 000 jours-patients. En revanche, le nombre d'isolats d'EPC soumis volontairement aux laboratoires de santé provinciaux a augmenté passant de 4 en 2009 à 779 en 2016. La plus importante augmentation, selon un facteur de 1,8, a été observée entre 2015 et 2016. Cette différence est peut-être imputable à l'augmentation des cas d'infection par EPC dans la communauté ou dans les hôpitaux qui ne sont pas représentés dans le groupe des hôpitaux faisant l'objet d'une surveillance, à la sensibilisation accrue aux EPC et à la déclaration des EPC, ou à d'autres facteurs pas encore déterminés.
Décrit pour la première fois en 1961, leStaphylocoque aureus résistant à la méthicilline (SARM) est une bactérie Staphylococcus aureus qui a acquis une résistance aux antibiotiques de la classe des β-actamines anti-staphylococciques (p. ex. la méthicilline, l'oxacilline et la céfazoline). Même si le SARM était par le passé associé aux hôpitaux et à d'autres milieux de soins de santé (SARM associé aux soins de santé), le SARM d'origine communautaire fait également l'objet d'une surveillance et en cours d'observation deviennent une cause importante de la maladie au Canada et ailleursNote de bas de page 3 Note de bas de page 4 Note de bas de page 5. Le taux global d'infection au Staphylocoque aureus résistant à la méthicilline (SARM) dans les hôpitaux sentinelles au Canada a augmenté, passant de 2,84 cas à 3,13 cas par 10 000 jours-patients entre 2011 et 2016. Toutefois, ce taux est demeuré inférieur au taux de 2009, qui s'élevait à 3,78 cas pour 10 000 jours-patients. Lorsque les cas hospitalisés sont comparés selon le contexte, le taux global d'infection à SARM associée aux soins de santé a diminué entre 2011 et 2016 (passant de 1,93 cas à 1,69 cas pour 10 000 jours-patients, respectivement), tandis que le taux global d'infection à SARM d'origine communautaire a augmenté au cours de la même période (passant de 0,56 à 0,96 cas pour 10 000 jours-patients). Entre 2011 et 2016, le taux d'infection à SARM d'origine communautaire dans les hôpitaux pédiatriques était systématiquement plus élevé que le taux dans les hôpitaux mixtes et pour adultes (p. ex. 1,56, 1,02 et 0,75 cas pour 1 000 hospitalisations, respectivement). Le taux d'infection du sang à SARM associée aux soins dans les hôpitaux pour adultes était relativement stable de 2011 à 2016 (passant de 0,47 à 0,44 cas pour 10 000 jours-patients), tandis que le taux d'infection du sang à SARM associée aux soins de santé dans les hôpitaux pédiatriques a augmenté de plus de cinq fois (passant de 0,08 cas à 0,43 cas pour 10 000 jours-patients entre 2011 et 2016) (figure 2). Cette augmentation du taux d'infection du sang dans les hôpitaux pédiatriques est préoccupante et doit faire l'objet d'une surveillance plus étroite.
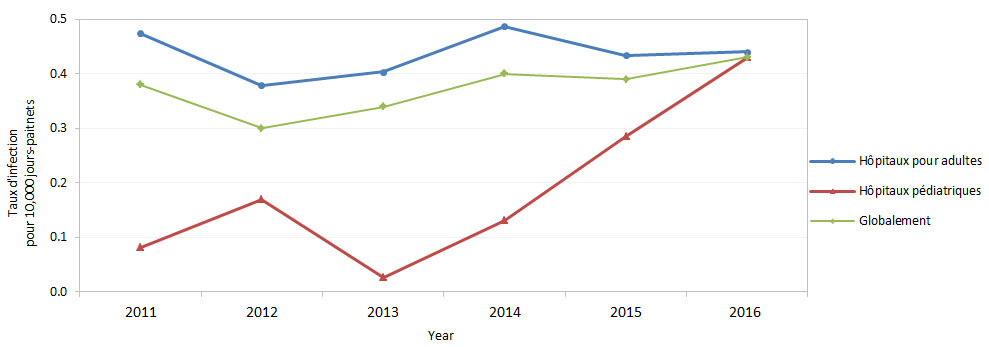
Figure 2 - Équivalent du texte
| 2011 | 2012 | 2013 | 2014 | 2015 | 2016 | |
|---|---|---|---|---|---|---|
| Hôpitaux pour adultes | 0.47 | 0.38 | 0.40 | 0.49 | 0.43 | 0.44 |
| Hôpitaux pédiatriques | 0.08 | 0.17 | 0.03 | 0.13 | 0.29 | 0.43 |
| Globalement | 0.38 | 0.30 | 0.34 | 0.40 | 0.39 | 0.43 |
Le présent graphique linéaire démontre le taux d'infection à SDRM pour 10 000 jours-patients par type d'hôpital au Canada entre 2011 et 2016. L'axe horizontal réprésente l'année et l'axe vertical indique le taux d'infection.
Les entérocoques résistant à la vancomycine (ERV) ont des options thérapeutiques limitées et font l'objet d'efforts de surveillance à l'échelle internationaleNote de bas de page 3 Note de bas de page 4 Note de bas de page 5,Note de bas de page 7. Au Canada, les ERV étaient par le passé associés aux établissements de soins de santé; le fardeau que représentent les infections à ERV dans la communauté est inconnu. Le taux global d'infection à ERV au Canada a fortement augmenté entre 2007 (0,10 cas pour 10 000 jours-patients) et 2012 (0,61 cas pour 10 000 jours-patients), et a diminué entre à 0,41 cas pour 10 000 jours-patients. Le taux d'infection a augmenté légèrement en 2016 à 0,44 cas pour10 000 jours-patients en 2015 (figure 3). Toutefois, lorsqu'on fait une comparaison par type d'hôpital et foyer d'infection, le taux d'infection du sang à ERV dans les hôpitaux pour adultes sentinelles a plus que doublé entre 2011 (0,12 cas pour 10 000 jours-patients) et 2016 (0,26 cas pour 10 000 jours-patients). Cela montre qu'il est nécessaire de procéder à une surveillance continue de ce microorganisme au Canada.
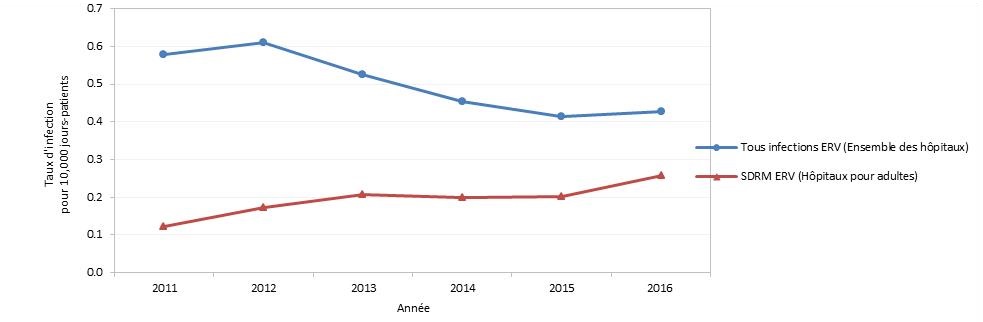
Figure 3 - Équivalent du texte
| 2011 | 2012 | 2013 | 2014 | 2015 | 2016 | |
|---|---|---|---|---|---|---|
| Tous infections ERV (Ensemble des hôpitaux) | 0.58 | 0.61 | 0.52 | 0.45 | 0.41 | 0.43 |
| SDRM ERV (Hôpitaux pour adultes) | 0.12 | 0.17 | 0.21 | 0.20 | 0.20 | 0.26 |
Ce graphique linéaire montrant le taux d'infection à ERV pour 10 000 cas enregistrées au Canada entre 2011 et 2016. L'axe horizontal réprésente l'année et l'axe vertical indique le taux d'infection pour 100 000 cas enregistrés.
La gonorrhée est une des infections bactériennes transmissibles sexuellement la plus couramment signalée au CanadaNote de bas de page 10. Le taux global de gonorrhée a plus que doublé, passant de 21,8 cas pour 100 000 personnes en 2001 à 55,4 cas pour 100 000 personnes en 2015. Le traitement et la prévention de la gonorrhée est un défi important en santé publique dans le monde entierNote de bas de page 7,Note de bas de page 11. Au Canada, la proportion d'isolats de Neisseria gonorrhoeae (N. gonorrhoeae) résistants à divers antimicrobiens a continué d'augmenter en 2015 (figure 4). Entre 2014 et 2015, la proportion d'isolats résistants à au moins un antimicrobien testé a augmenté, passant de 52% à 60 %. Entre 2010 et 2015, la proportion d'isolats de N. gonorrhoeae résistants à l'azithromycine a augmenté, passant de 1,3 % à 4,7 %. Lorsque la proportion de souches de N. gonorrhoeae résistantes aux antimicrobiens obtenues à partir d'isolats est de 5% ou plus, ou lorsqu'une augmentation inattendue de moins de 5% est observée dans les populations clés présentant des taux élevés d'infection gonococcique, l'Organisation mondiale de la Santé recommande les pays examinent et modifient leurs directives nationales pour le traitement et la gestion des ISTNote de bas de page 11, une pratique exemplaire que le Canada met en œuvre.Les isolats présentant une sensibilité réduite à la céfixime ou à la ceftriaxone, deux antimicrobiens de la classe des céphalosporines utilisés pour le traitement de la gonorrhée, ont également augmenté entre 2014 et 2015 (passant de 1,1 % à 1,9 % et de 2,7 % à 3,5 %, respectivement). Entre 2012 et 2014, une très petite proportion d'isolats au Canada présentait une résistance à l'azithromycine et avait une sensibilité réduite aux céphalosporines (la céfixime ou la ceftriaxone), le traitement à double modalité actuellement recommandé pour la gonorrhée (0,2 % en 2012, 0,3 % en 2013 et 0,03 % en 2014, respectivement). Le Royaume-Uni a signalé le premier échec de traitement à double modalité au monde en 2015Note de bas de page 12. Même si le Canada n'a pas signalé d'échec de traitement découlant de la résistance à l'azithromycine et d'une sensibilité réduite aux céphalosporines, ces observations indiquent qu'il est nécessaire de surveiller en continu la N. gonorrhoeae pharmacorésistante et l'utilisation appropriée des antimicrobiens pour aider à maintenir l'efficacité des schémas thérapeutiques actuels.
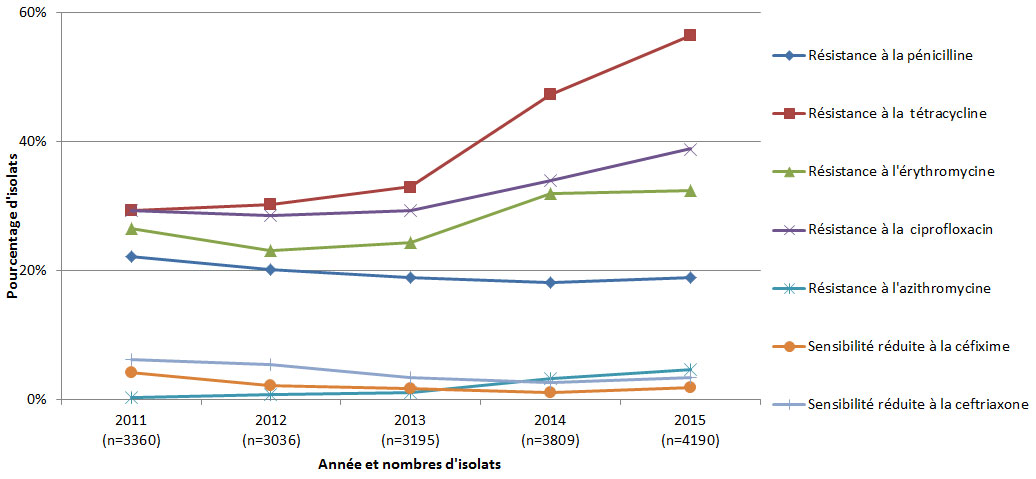
Figure 4 - Équivalent du texte
| 2011 (n=3360) |
2012 (n=3036) |
2013 (n=3195) |
2014 (n=3809) |
2015 (n=4190) |
|
|---|---|---|---|---|---|
| Résistance à la pénicilline | 22.2 | 20.26 | 18.94 | 18.22 | 18.93 |
| Résistance à la tétracycline | 29.4 | 30.3 | 32.99 | 47.34 | 56.42 |
| Résistance à l'érythromycine | 26.6 | 23.12 | 24.32 | 32 | 32.41 |
| Résistance à la ciprofloxacin | 29.3 | 28.52 | 29.33 | 34.02 | 38.88 |
| Résistance à l'azithromycine | 0.39 | 0.86 | 1.16 | 3.33 | 4.73 |
| Sensibilité réduite à la céfixime | 4.2 | 2.24 | 1.75 | 1.1 | 1.91 |
| Sensibilité réduite à la ceftriaxone | 6.2 | 5.53 | 3.51 | 2.65 | 3.46 |
Ce présent graphique linéaires montre le pourcentage des isolats de N. gonorrhée résistants à divers antimicrobiens au Canada entre 2011 et 2016 (représentés chacun par sa propre ligne). L'axe horizontal réprésente l'année et l'axe vertical indique le pourcentage des isolats de N. gonorrhée.
Utilisation des antimicrobiens chez les humains
L'utilisation généralisée des antimicrobiens est un facteur important de l'émergence et de la propagation des microorganismes résistants. L'UAM prudente est reconnue comme un élément de base de la gestion des risques de RAM pour préserver l'efficacité des antimicrobiens et ralentir le développement des organismes pharmacorésistants. Les programmes et politiques qui souligne l'éducation et la sensibilisation ainsi que la surveillance réglementaire et professionnels en matières de contrôle peut contribuer à favoriser la prescription, distribution et l'utilisation rationnelles et prudentes des agents antimicrobiens en médicine humaine. La surveillance de la RAM et l'UAM fournit des renseignements permettant d'orienter les efforts de gestion des antimicrobiensNote de bas de page 13.
Utilisation des antimicrobiens au sein de la communauté
Au Canada, la majorité des antimicrobiens destinés aux humains sont sur ordonnance seulement. En 2016, 92 % des doses d'antimicrobiens ont été délivrées dans la communauté, alors que le reste (8 %) a été acheté en vue d'un usage en milieu hospitalier (figure 5). La proportion des antimicrobiens délivrés dans la communauté était la même que les années précédentesNote de bas de page 14. En 2016, environ 22,6 millions d'ordonnances d'antimicrobiens ont été délivrées au Canada, représentant au total des dépenses d'environ 700 M$. Le taux d'ordonnances délivrées en milieu communautaire était relativement stable entre 2013 et 2016 (environ 625 ordonnances par 1 000 habitants) et était légèrement inférieur aux taux observés entre 2010 et 2012 (de 660 à 683 ordonnances par 1 000 habitants). En 2016, l'amoxicilline était l'antimicrobien le plus fréquemment prescrit (25 % des ordonnances), suivi de l'azithromycine (10 % des ordonnances). En 2016, le taux d'ordonnances délivrées chez les adultes âgés de 60 ans et plus était de 856 ordonnances par 1 000 habitants, ce qui représente un taux près de 1,5 fois plus élevé que le taux du groupe des 0 à 14 ans et des 15 à 59 ans (598 et 547 ordonnances par 1 000 habitants, respectivement). L'amoxicilline, la ciprofloxacine et la céfalexine étaient les antimicrobiens les plus couramment prescrits dans le groupe d'âge le plus âgé.
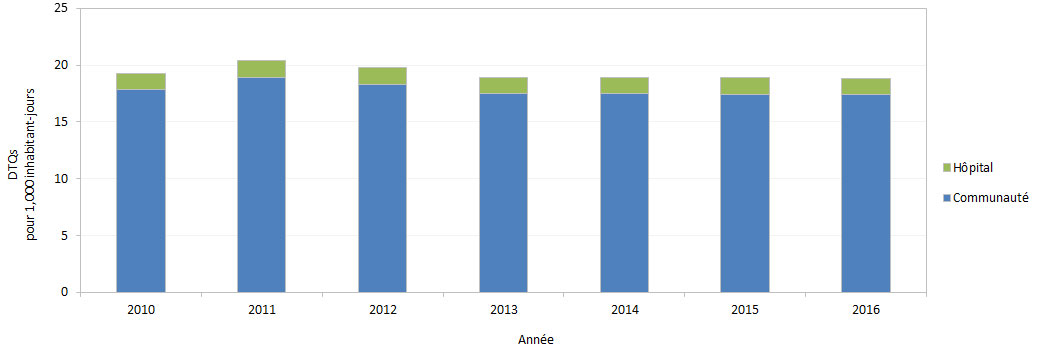
Figure 5 - Équivalent du texte
| Année | Communauté | Hôpital |
|---|---|---|
| 2010 | 17.8 | 1.4 |
| 2011 | 18.9 | 1.5 |
| 2012 | 18.3 | 1.5 |
| 2013 | 17.5 | 1.4 |
| 2014 | 17.5 | 1.4 |
| 2015 | 17.4 | 1.5 |
| 2016 | 17.4 | 1.4 |
Ce diagramme est un graphique à barres empilées qui nous montre la dose thérapeutiques quotidiennes (DTQ) par 1 000 habitants-jour à partir des données sur les achats hospitaliers et les ordonnances communautaires au Canada entre 2010 et 2016. L'axe horizontal réprésente l'année et l'axe vertical indique la dose thérapeutiques quotidienne par 1 000 habitants-jour.
En 2015, l'European Surveillance of Antimicrobial Consumption Network (ESAC-Net) signale la consommation globale d'antibactériens pour utilisation systémique (J01) dans les milieux hospitaliers et communautaires de pays européens participantsNote de bas de page 5. L'ESAC-Net est un bon moyen d'établir des comparaisons relatives à l'UAM chez les humains avec le Canada, étant donné que l'ESAC-Net représente l'une des plus grandes sources de données normalisées sur l'UAM à l'échelle internationale et utilise des méthodes comparables à celles du Canada. En comparant la consommation de 2015 en milieu extra-hospitalier en Europe avec la consommation communautaire canadienne de 2015 (exécution d'ordonnance par les pharmacies communautaires), le Canada se classait au 13e rang (classées des plus bas au plus élevées), sur 31 pays. Ce qui représente un reculement léger par rapport à 2014, lorsque le Canada se plaçait 12e sur 31 pays en matière de consommation communautaire d'antimicrobiens.
Par province au Canada, Terre-Neuve-et-Labrador avait le taux le plus élevé d'ordonnances (955 ordonnances par 1 000 habitants) en 2016, une constatation également faite au cours des années précédentes. Les taux d'ordonnances les plus faibles ont été observés en Colombie-Britannique ainsi qu'entre les personnes bénéficiaires du Programme des services de santé non-assurés (SSNA) (figure 6). Les raisons de ces différences provinciales sont actuellement examinées. Même si l'utilisation de la plupart des antimicrobiens était plus élevée à Terre-Neuve-et-Labrador que dans les autres provinces, l'amoxicilline a été prescrite à des taux particulièrement élevés (données non présentées).
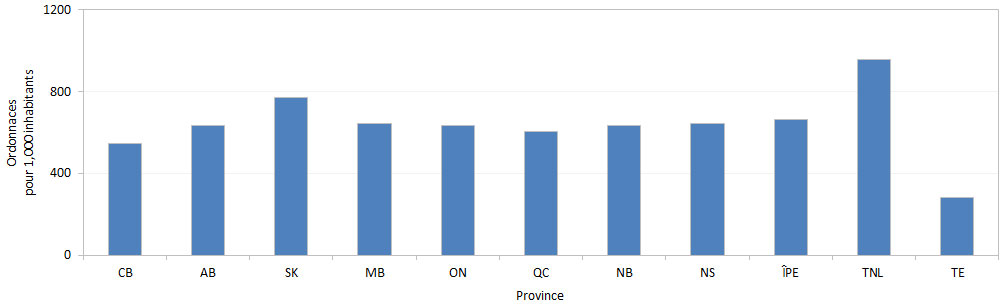
Figure 6 - Équivalent du texte
| Province | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| C.-B. | Alb. | Sask. | Man. | Ont. | Qc. | N.-B. | N.-É | Î.-P.-È. | T.-N.-L | Terr. | |
| Ordonnances /1,000 habitants | 546.0 | 634.6 | 771.5 | 643.0 | 636.8 | 602.8 | 632.1 | 643.9 | 665.6 | 955.2 | 279.7 |
Ce graphique à barres présente le taux d'ordonnances pour des médicaments antimicrobiens pour 1 000 personnes pur chaque province et territoire au Canada en 2016. L'axe horizontal énumère les provinces et territoire et l'axe vertical indique le taux d'ordonnances pour des médicaments antimicrobiens pour 1000 personnes.
Notes: CB = Columbie Britannique, AB = Alberta, SK = Saskatchewan, MB = Manitoba, ON = Ontario, QC = Québec, NB = Nouveau Brunswick, NE = Nouvelle Écosse, PEI = Île-du-Prince-Édouard, TN = Terre- Neuve- et- Labrador, TE = Territoires (Yukon, Territoires du Nord-ouest, et Nunavut)
En 2016, les omnipraticiens représentaient 65 % de l'ensemble des ordonnances exécutées par les pharmacies communautaires au Canada. Les antimicrobiens les plus couramment prescrits par les médecins en cabinet privé étaient l'amoxicilline, l'azithromycine et la céfalexine. Comme il a été observé au cours des années précédentes, les antimicrobiens étaient le plus souvent prescrits pour le traitement des infections respiratoires, suivies des infections du système génito-urinaire, et des infections de la peau et des tissus mous. En 2015, les médecins en cabinet privé ont rédigé 446 ordonnances d'antimicrobiens par 1 000 habitants, tandis que le taux pour les dentistes était 47 ordonnances par 1 000 habitants (figure 7). Les données de 2015 affichaient une tendance à la baisse des taux de prescription d'antimicrobiens par les médecins, et un taux généralement stable de prescription d'antimicrobiens par les dentistes, à la suite d'une augmentation de ce dernier entre 2010 et 2012.
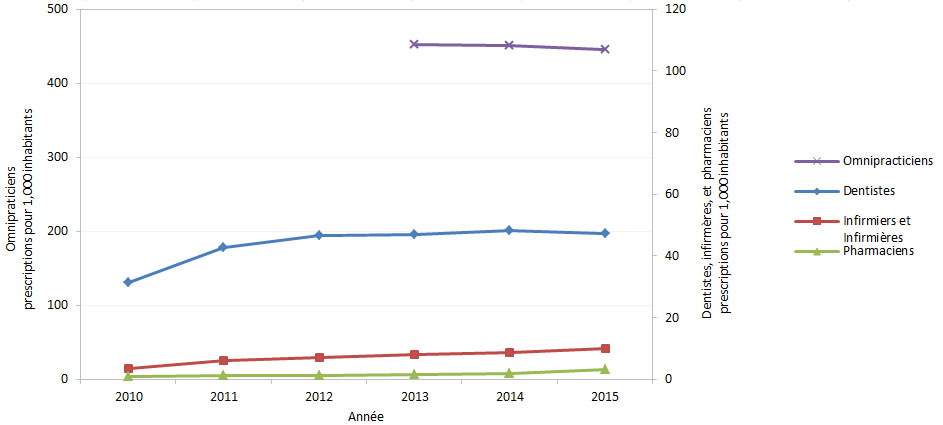
Figure 7 - Équivalent du texte
| Année | Dentistes | Infirmiers et Infirmières | Pharmaciens | Omnipraticiens et de médecins de famille |
|---|---|---|---|---|
| 2010 | 31.3 | 3.4 | 1.0 | N/A |
| 2011 | 42.7 | 6.0 | 1.3 | N/A |
| 2012 | 46.6 | 7.2 | 1.3 | N/A |
| 2013 | 46.9 | 8.1 | 1.6 | 452.2 |
| 2014 | 48.2 | 8.8 | 2.0 | 451.3 |
| 2015 | 47.4 | 10.0 | 3.3 | 445.7 |
Le graphique linéaire dans la figure 7 montre le taux d'ordonnances délivrées au sein de la communauté. Cette figure comportant deux axes verticaux.
Cette figure a recours a deux axes verticaux, l'un des axes a une fourchette de valeurs entre 0 et 120 afin de couvrir le taux d'ordonnances effectuées par les dentistes, infirmiers et infirmières et pharmaciens. Le deuxième axe a une fourchette de valeurs entre 0 et 500 afin de couvrir les ordonnances effectuées par les omnipracticiens par 1 000 habitants.
Utilisation des antimicrobiens en milieu hospitalier
En 2016, 8 % des doses d'antimicrobiens au Canada ont été achetées en vue d'un usage en milieu hospitalier (figure 5). Cette proportion était stable par rapport aux années précédentes. Le taux d'achat d'antimicrobiens par les hôpitaux était variable dans l'ensemble du Canada au cours de la période de surveillance. En 2016, le Manitoba, ainsi que l'Île-du-Prince-Édouard et Terre-Neuve-et-Labrador (combinés) enregistraient le taux d'achat d'antimicrobiens par habitant les plus élevés (2,7 et 2,3 doses thérapeutiques quotidiennes [DTQ] par 1 000 habitants-jour, respectivement). L'Ontario et de l'Alberta enregistraient les taux les plus faibles (1,01 et 1,32 dose thérapeutique quotidienne par 1 000 habitants-jour, respectivement).
Les céphalosporines étaient la classe de médicaments antimicrobiens la plus achetée par les hôpitaux au Canada en 2016, comme les années précédentes, suivies des fluoroquinolones. Même si le taux d'achat de céphalosporines est demeuré relativement stable entre 2010 et 2016, le taux d'achat de fluoroquinolones a diminué de 43 % au cours de la même période (passant de 0,25 à 0,17 dose thérapeutique quotidienne par 1 000 habitants-jour). De 2010 à 2016, le taux d'achat de deux classes de médicaments, les associations de pénicillines et les pénicillines sensibles aux β-lactamases (p. ex. pénicilline G), a augmenté de 41 % (passant de 0,09 à 0,15 dose thérapeutique quotidienne par 1 000 habitants-jour) et de 34 % (passant de 0,05 à 0,07 dose thérapeutique quotidienne par 1 000 habitants-jour), respectivement. Les achats de daptomycine effectués par les hôpitaux, l'un des antibiotiques « de dernier recours », ont augmenté en 2016, ce qui est préoccupant. La daptomycine est généralement réservée aux fins d'utilisation dans le traitement des infections à S. aureus et Enterococcus potentiellement mortellesNote de bas de page 6. La cause de cette hausse est inconnue.
Utilisation des antimicrobiens chez les animaux destinés à l'alimentation et les animaux de compagnie
Tout comme l'utilisation d'antimicrobiens chez les humains peut mener au développement et à la persistance de la résistance aux antimicrobiens (RAM), l'utilisation d'antimicrobiens chez les animaux destinés à l'alimentation et les animaux de compagnie peut aussi contribuer au développement de bactéries résistantes aux antimicrobiens. Ces bactéries peuvent ensuite être transmises aux humains par contact direct avec des animaux, de même que par les voies d'origine alimentaire ou hydrique. La surveillance de l'utilisation des antimicrobiens chez les animaux, dans les cultures et chez les humains fournit des données importantes permettant d'orienter les efforts en matière de gestion des antimicrobiens et de limiter la RAM au Canada.
En 2016, approximativement 1 million de kilogrammes d'antimicrobiens médicalement importants ont été distribués pour la vente à usage vétérinaire par les sociétés membres de l'Institut canadien de la santé animale (ICSA). Ce volume était d'environ 14 % de moins qu'en 2007 et 17 % de moins qu'en 2015. Ces quantités déclarées n'incluent pas les antimicrobiens importés pour «usage personnel» ou comme ingrédients pharmaceutiques actifs destinés à être recomposés davantage. En outre, 0,6 million de kilogrammes d'ionophores et d'anticoccidiens chimieues ont été distribués pour être administrés à des animaux (ces antimicrobiens ne sont pas considérés comme étant médicalement importants). En 2016, 99 % des antimicrobiens distribués visaient les animaux destinés à l'alimentation, et 1 % étaient destinés aux animaux de compagnie (selon le nombre de kilogrammes d'ingrédient actif).
La quantité globale de fluoroquinolones vendues pour utilisation chez les animaux a diminué d'environ 56 % entre 2015 et 2016. La Direction des médicaments vétérinaires de Santé Canada classe les fluoroquinolones dans la catégorie « de très haute importance en médecine humaine ». L'utilisation de fluoroquinolones est homologuée pour certaines espèces animales au Canada, et une mise en garde est inscrite sur leur étiquette contre une utilisation en dérogation des directives qui y sont prescrites en raison des préoccupations relatives à la RAM et les lignes directrices à utiliser seulement après l'échec d'un traitement initialNote de bas de page 15.
Entre 2012 et 2016, on a observé des différences interprovinciales relativement aux quantités d'antimicrobiens distribués pour la vente (selon le nombre de kilogrammes d'ingrédient actif) par les entreprises membres de l'ICSA, ainsi que des variations nettes d'une année sur l'autre des quantités distribuées. Les provinces ayant déclaré la plus grande baisse depuis 2015 (en pourcentages relatifs de la quantité totale [kg] pour 2015) ont été le Nouveau-Brunswick, le Manitoba, la Nouvelle-Écosse, Terre-Neuve-et-Labrador, la Saskatchewan et le Québec (diminution de > 15 % de la quantité totale [kg] pour chaque province)Note de bas de page 16. La seule province à avoir enregistré une augmentation de la quantité totale (kg) d'ingrédients actifs distribués pour la vente était l'Île-du-Prince-Édouard (augmentation d'environ 20 % de la quantité [kg]).
La Surveillance européenne de la consommation d'antibiotiques à usage vétérinaire (ESVAC) recueille des renseignements et fait rapport aux pays membres sur les agents antimicrobiens pour usage vétérinaire. L'ESVAC est un bon moyen d'établir des comparaisons relatives à l'UAM chez les animaux avec le Canada, puisqu'il représente la seule source internationale actuelle de données de surveillance quantitatives sur les agents antimicrobiens pour usage vétérinaire. Le Canada utilise des mesures pour la production de rapports qui sont semblables à celles de l'ESVAC, à l'exception notable de l'utilisation des vaches de boucherie dans le dénominateur au Canada. Selon les plus récentes données de l'ESVAC (2015) et du Canada (2016), sur 31 pays, le Canada a été le cinquième plus grand consommateur d'antimicrobiens, mesurés en milligrame de médicament par kilogramme d'animal (équivalant au milligramme par unité corrigée de la population)Note de bas de page 16. En 2016, le Canada avait une consommation supérieure à la moyenne signalée pour les pays participants européens. La quantité d'antimicrobiens par kg d'animal signalée par le Canada serait plus élevée si les quantités, actuellement inconnues, d'antimicrobiens importés pour « utilisation personnelle » ou comme ingrédients pharmaceutiques actifs destinés aux préparations étaient incluses.
L'Agence de la santé publique du Canada effectue une surveillance dans les fermes pour établir les tendances d'utilisation des antimicrobiens et de résistance à ces derniers dans les fermes, étudier les associations entre l'utilisation des antimicrobiens et la résistance à ces derniers dans les fermes et fournir des données solides pour l'évaluation des risques pour la santé humaine. La surveillance dans les fermes a montré qu'une modification des politiques d'utilisation d'antimicrobiens dans les fermes d'élevage de poulets à griller à l'échelle du Canada semblait avoir atteint l'objectif de réduction de l'utilisation des antimicrobiens dans les classes considérées comme extrêmement importantes, plus particulièrement de l'utilisation de l'antimicrobien ceftiofur (une céphalosporine de troisième génération).
Combler les lacunes en matière de données de surveillance
Le rapport de 2017 du SCSRA donne un bon aperçu de la situation actuelle de la RAM et de l'UAM au Canada. Les renseignements sur la RAM provenant de grands hôpitaux de soins tertiaires fournissent une bonne couverture. Un autre point fort est la représentation des données sur la RAM relatives aux bactéries d'origine alimentaire provenant d'animaux destinés à l'alimentation et d'aliments d'origine animale. En outre, les données sur l'UAM chez humains et les animaux se sont améliorées. Par exemple, l'ASPC a les données de références sur les fermes comprenant le comment et pourquoi les agents antimicrobiens sont utilisés et l'établissement de rapports et la présentation de rapports relatifs à l'utilisation antimicrobiennes parmi les populations autochtones au Canada. Cette question est maintenant à l'examen approfondi.
Il y a néanmoins des lacunes qui doivent être comblées afin d'augmenter le niveau de détail, l'ampleur et la qualité de la surveillance de la RAM et de l'UAM au Canada. Par exemple, il y a peu de données sur la RAM au sein de la communauté. Les données sur la RAM sont également limitées dans les petits hôpitaux non universitaires, et on a très peu ou pas de données pour les milieux de soins de santé et les populations autochtones et au grand Nord, et peu de données sur la RAM dans les établissements de soins de longue durée. Dans le domaine de l'UAM, on dispose de peu de données sur la covenance des agents antimicrobiens qui sont prescrits.
Les données relatives à la RAM tout au long de la chaine alimentaire pour des animaux que pour des humains sont limitées à certain organismes bactériens (p. ex. Salmonella). Les espèces d'animaux d'élevage pertinentes comprends le surtout des animaux produisants de la viande au Canada (p. ex. le bétail, le porc, les poulets de chair et les dindes), bien qu'aucune surveillance est actuellement en cours dans d'autres secteurs de production (p. ex. l'aquaculture, production de viande de veau et le mouton).Les données sur l'UAM à la ferme sont pour l'instant limitées à certaines fermes sentinelles avicoles et porcines pour déterminer les tendances et habitudes d'utilisation des antimicrobiens.
Depuis la publication du premier rapport du SCSRA en 2015, l'ASPC a collaboré avec un large éventail de partenaires représentant les secteurs de la santé publique, des soins de santé, de l'agriculture et d'autres secteurs, afin de combler les lacunes recensées et ainsi améliorer la surveillance de la RAM et de l'UAM au Canada. Voici des initiatives qui sont déjà en cours ou prévues et qui visent à recueillir de nouvelles données sur la RAM ou l'UAM ou à améliorer les données existantes sur la RAM ou l'UAM :
- l'étude de prévalence ponctuelle du SCSRA, qui vise à fournir des données hospitalières sur la RAM et l'UAM dans les petits hôpitaux communautaires ruraux et du Nord et dans les établissements de soins de longue durée;
- un module « Réponse rapide » sur l'UAM dans l'Enquête sur la santé dans les collectivités canadiennes (ESCC); L'objectif de la collecte de ces données est de fournir des réponses aux questions fréquentes sur l'UAM et des renseignements sur les pratiques de gestion des antibiotiques personnelles;
- une étude de trois ans de cas hospitalisés de Clostridium difficile d'origine communautaire;
- les études de surveillance de pépinière de porc et l'élevage de dindon pour examiner l'UAM et le RAM;
- un projet quinquennal qui permettra de mieux comprendre la façon dont les pratiques de production alimentaire contribue au développement de la RAM, qui représente une préoccupation pour la santé humaine.
Prochaines étapes/conclusion
L'évolution de l'épidémiologie de la RAM au Canada, et la menace croissante de la RAM à l'échelle mondiale, soulignent la nécessité d'une surveillance continue de cet événement de santé publique. L'ASPC continue de traiter les lacunes en matière de surveillance de la RAM et de l'UAM en partenariat avec d'autres ministères fédéraux, avec les provinces et territoires, avec les organisations non gouvernementales, avec des associations professionnelles, et avec le milieu universitaire. À cette fin, l'ASPC met en œuvre un certain nombre d'initiatives au cours des prochaines années afin d'améliorer les renseignements de surveillance dans le but d'améliorer la capacité du Canada à répondre aux menaces émergentes de la RAM, et soutient les efforts de gestion des antimicrobiens en fournissant de meilleures données probantes pour la prise de décisions.
Les problèmes mondiaux nécessitent des solutions à l'échelle mondiale. L'ASPC entreprend actuellement des travaux visant à harmoniser ses méthodes de surveillance pour participer aux programmes internationaux, tels que le Système mondial de surveillance de la résistance aux antimicrobiens (GLASS). L'ASPC a contribué au GLASS pour la toute première fois en 2017, en soumettant la base de données sur la bactérie Salmonella de 2015. Une participation complète est envisagée pour 2019. En outre, l'ASPC s'est engagée à collaborer avec ses partenaires internationaux relativement aux autres moyens de déterminer les approches communes et les pratiques exemplaires visant à prévenir, à limiter et à contrôler le développement et la propagation de la RAM au Canada et dans le monde entier.
Références
Notes de bas de page
- Note de bas de page 1
-
Public Health Agency of Canada. Tackling Antimicrobial resistance and antimicrobial use: A pan-Canadian framework for action. Infectious Disease Prevention and Control Branch. Ottawa: Public Health Agency of Canada; 2017. [Internet] Available from: https://www.canada.ca/en/health-canada/services/publications/drugs-health-products/tackling-antimicrobial-resistance-use-pan-canadian-framework-action.html
- Note de bas de page 2
-
Pan-Canadian Public Health Network. Antimicrobial resistance surveillance data requirements for priority organisms. The Communicable and Infectious Disease Steering Committee Antimicrobial Resistance Surveillance Task Group. Final Report to Public Health Network Council. Ottawa: April 2016. [Internet] Available from: http://www.phn-rsp.ca/pubs/arsdrpo-dsecrao/index-eng.php
- Note de bas de page 3
-
Australian Commission on Safety and Quality in Health Care (ACSQHC). AURA 2016: First Australian report on antimicrobial use and resistance in human health. Sydney: Australian Commission on Safety and Quality in Health Care; 2016. [Internet] Available from: https://www.safetyandquality.gov.au/wp-content/uploads/2017/01/AURA-2016-First-Austarlian-Reprot-on-Antimicrobial-use-and-resistance-in-human-health.pdf
- Note de bas de page 4
-
Centers for Disease Control and Prevention (CDC). Antibiotic resistance threats in the United States, Atlanta: U.S. Department of Health and Human Services, Centers for Disease Control and Prevention; 2013. [Internet] Available from: https://www.cdc.gov/drugresistance/threat-report-2013/pdf/ar-threats-2013-508.pdf#page-53
- Note de bas de page 5
-
European Centre for Disease Prevention and Control (ECDC). Summary of the latest data on antimicrobial resistance in EU. Stockholm: European Centre for Disease Prevention and Control; 2016. [Internet] Available from: https://ecdc.europa.eu/sites/portal/files/documents/antibiotics-EARS-Net-summary-2016_0.pdf
- Note de bas de page 6
-
World Health Organization. Critically important antimicrobials in human medicine, 5th edition. Geneva: World Health Organization. 2016. [Internet] Available from: http://www.who.int/foodsafety/publications/antimicrobials-fifth/en/
- Note de bas de page 7
-
World Health Organization. Antimicrobial resistance: Global report on surveillance. Geneva: World Health Organization; 2014. [Internet] Available from: http://apps.who.int/iris/bitstream/10665/112642/1/9789241564748_eng.pdf
- Note de bas de page 8
-
Bloomfield LE, Riley TV. Epidemiology and risk factors for community associated Clostridium difficile infection: a narrative review. Infect Dis Ther 2016 Sep: 5(3): 231-251. doi: 10.1007/s40121-016-0117-y
- Note de bas de page 9
-
van Duin D, Kaye KS, Neuner EA, Bonomo RA. Carbapenem-resistant Enterobacteriaceae: a review of treatment and outcomes. Diagn Microbiol Infect Dis. 2013 Feb;75(2):115-20 https://doi.org/10.1016/j.diagmicrobio.2012.11.009 [Internet] Available from: http://www.sciencedirect.com/science/article/pii/S0732889312004920
- Note de bas de page 10
-
Public Health Agency of Canada. Canadian Guidelines on sexually transmitted infections, Gonococcal infections. Infectious Disease Prevention and Control, [Directorate]. Ottawa: Public Health Agency of Canada; Revised July 2013. [Internet] Available from: https://www.canada.ca/en/public-health/services/infectious-diseases/sexual-health-sexually-transmitted-infections/canadian-guidelines/sexually-transmitted-infections/canadian-guidelines-sexually-transmitted-infections-34.html
- Note de bas de page 11
-
World Health Organization. Global action plan to control the spread and impact of antimicrobial resistance in Neisseria gonorrheaae. Geneva: World Health Organization; 2012. [Internet] Available from: http://apps.who.int/iris/bitstream/10665/44863/1/9789241503501_eng.pdf
- Note de bas de page 12
-
Fifer H, Natarajan U, Alexander S, Golparian D. Failure of dual antimicrobial therapy in treatment of Gonorrhea. N Engl J Med. 2016 Jun; 374:2504-2506. doi: 10.1056/NEJMc1512757
- Note de bas de page 13
-
Khan F, Arthur J, Maidment L, Blue D. Advancing antimicrobial stewardship: Summary of the 2015 CIDSC Report. CCDR. 2016 Dec; 42-12: 238-241. [Internet] Available from: https://www.canada.ca/content/dam/phac-aspc/migration/phac-aspc/publicat/ccdr-rmtc/16vol42/dr-rm42-11/assets/pdf/16vol42_11-eng.pdf
- Note de bas de page 14
-
Finley R, Glass-Kaastra SK, Hutchinson J, Patrick DM, Weiss K, Conly J. Declines in outpatient antimicrobial use in Canada (1995-2010). PLoS ONE 8(10): e76398. https://doi.org/10.1371/journal.pone.00763989
- Note de bas de page 15
-
Health Canada. Categorization of antimicrobial drugs based on importance in human medicine. [Branch], [Directorate]. Ottawa: Health Canada; (Version - April, 2009) [Internet] Available from: https://www.canada.ca/en/health-canada/services/drugs-health-products/veterinary-drugs/antimicrobial-resistance/categorization-antimicrobial-drugs-based-importance-human-medicine.html
- Note de bas de page 16
-
European Medicines Agency, European Surveillance of Veterinary Antimicrobial Consumption, 2017.'Sales of veterinary antimicrobial agents in 30 European countries in 2015'. (EMA/184855/2017). [Internet] Available from: http://www.ema.europa.eu/docs/en_GB/document_library/Report/2017/10/WC500236750.pdf. Accessed October 2017.