Mise à jour sur l'utilisation des vaccins quadrivalents contre le méningocoque au Canada
Une déclaration du comité consultatif (DCC) Comité consultatif national de l'immunisation (CCNI)
Préambule
Le Comité consultatif national de l'immunisation (CCNI) donne à l'Agence de la santé publique du Canada (ci-après appelée l'Agence) des conseils constants et à jour liés à l'immunisation dans le domaine de la médecine, des sciences et de la santé publique. L'Agence reconnaît que les conseils et les recommandations figurant dans la présente déclaration reposent sur les connaissances scientifiques les plus récentes et diffuse ce document à des fins d'information. Les personnes qui administrent le vaccin doivent également connaître le contenu de la monographie de produit pertinente. Les recommandations d'utilisation et les autres renseignements qui figurent dans le présent document peuvent différer du contenu de la monographie de produit rédigée par le fabricant du vaccin au Canada. Les fabricants ont fait approuver les vaccins et ont démontré leur innocuité et leur efficacité uniquement lorsqu'ils sont utilisés conformément à la monographie de produit. Les membres du CCNI et les agents de liaison doivent se conformer à la politique de l'Agence régissant les conflits d'intérêts, notamment déclaré chaque année les conflits d'intérêts possibles.
Table des matières
Sommaire de l'information contenue dans la présente déclaration du CCNI
Le tableau suivant résume l'information importante pour les vaccinateurs. Veuillez consulter le reste de la Déclaration pour obtenir plus de précisions.

Télécharger le format de rechange
(Format PDF, 1 985 ko, 92 pages)
Organisation : Agence de la santé publique du Canada
Date publiée : Avril 2015
Cat.: HP40-125/2014F-PDF
ISBN: 978-0-660-21972-1
Pub.: 140309
Sujets connexes
1. Quoi
La méningococcie invasive (MI) est une maladie potentiellement mortelle qui se caractérise habituellement par une maladie fébrile aiguë d'apparition soudaine associée à des caractéristiques de méningite ou de septicémie (méningococcémie), ou les deux, et à une éruption cutanée sans blancheur caractéristique.
NimenrixMC est un vaccin conjugué quadrivalent (sérogroupes A, C, Y et W135) contre le méningocoque à l'anatoxine tétanique (AT), qui a récemment été approuvé.
La présente déclaration fournit des renseignements sur l'immunogénicité, l'innocuité et l'utilisation recommandée de NimenrixMC, ainsi que des renseignements à jour sur l'immunogénicité et l'innocuité de MenactraMD (Men-C-ACYW-DT) liés à l'indication relative à l'âge.
2. Qui
Pour la vaccination systématique des adolescents, administrer le vaccin conjugué monovalent contre le méningocoque (sérogroupe C) ou le vaccin conjugué quadrivalent, en fonction de l'épidémiologie locale et d'autres considérations programmatiques. Si l'on administre un produit quadrivalent, opter pour l'un ou l'autre des trois produits offerts.
Pour les personnes à risque élevé de 2 ans ou plus et les voyageurs de 2 ans ou plus se rendant dans des régions où le vaccin contre le méningocoque est recommandé, utiliser l'un ou l'autre des produits quadrivalents offerts.
Pour les enfants à risque élevé âgés de 2 mois à moins de 2 ans ou les voyageurs de la même catégorie d'âge se rendant dans des régions où le vaccin contre le méningocoque est recommandé, MenveoMC (Men-C-ACYW-CRM) est le produit recommandé.
Pour les calendriers, voir le chapitre sur le méningocoque du Guide canadien d'immunisation.
3. Comment
NimenrixMC est approuvé pour l'immunisation des personnes âgées de 12 mois à 55 ans, mais il peut être utilisé chez les personnes de 56 ans et plus, moyennant indication. Il ne devrait pas être administré à des personnes présentant une hypersensibilité connue à l'un des composants du vaccin.
NimenrixMC peut être administré seul ou en association avec d'autres vaccins administrés systématiquement au Canada. Le Comité consultatif national de l'immunisation (CCNI) recommande des doses de rappel périodiques pour les personnes à risque élevé de méningococcie ou qui risquent fort d'y être exposées de façon continue. Pour plus de renseignements, consulter le chapitre sur le méningocoque du Guide canadien d'immunisation.
Le profil d'innocuité de NimenrixMC est semblable à celui d'autres vaccins conjugués monovalents et quadrivalents homologués au Canada.
4. Pourquoi
Le taux de mortalité associé à la MI est d'environ 10 %. Jusqu'à un tiers de ceux qui survivent à la maladie présenteront des séquelles à long terme.
Près du tiers de tous les cas de MI sont associés aux sérogroupes A, C, Y et W-135 de Neisseria meningitidis; l'immunisation contre la MI dont le sérogroupe est ciblé par la vaccination est importante, en particulier pour les personnes qui présentent un risque élevé d'infection.
I. Introduction
La présente déclaration vise à compléter plusieurs déclarations antérieuresNote de bas de page 1,Note de bas de page 2,Note de bas de page 3,Note de bas de page 4 qui ont décrit l'utilisation des vaccins conjugués monovalents contre le méningocoque du groupe C et des vaccins conjugués quadrivalents contre le méningocoque. La présente déclaration :
- examine les recommandations existantes du CCNI au sujet de l'utilisation des vaccins conjugués contre le méningocoque;
- met à jour l'épidémiologie de la méningococcie au Canada;
- examine et met à jour l'information sur les vaccins conjugués quadrivalents contre le méningocoque et les calendriers de vaccination utilisés au Canada à la suite de l'approbation d'un nouveau vaccin conjugué quadrivalent contre le méningocoque, NimenrixMC (GlaxoSmithKline [GSK]), et d'une nouvelle indication sur le plan de l'âge pour MenactraMD (Sanofi Pasteur).
Contexte :
Trois vaccins conjugués monovalents (utilisant la protéine CRM197 ou l'AT comme protéine porteuse) contre le méningocoque sont offerts au Canada; et par suite de l'homologation de NimenrixMC, trois vaccins conjugués quadrivalents (utilisant la protéine CRM197, l'anatoxine diphtérique [AD], ou l'AT, comme protéine porteuse) contre le méningocoque y sont également offerts. Chez les enfants en santé, le CCNI recommande l'utilisation systématique du vaccin monovalent conjugué contre le méningocoque du groupe C à 12 mois; toutefois, il est possible d'entamer plus tôt la vaccination, en fonction des calendriers des provinces/territoires. De plus, le CCNI recommande l'utilisation systématique d'un vaccin conjugué, monovalent ou quadrivalent (en fonction de l'épidémiologie locale et d'autres considérations programmatiques), pour une dose de rappel systématique chez les adolescents âgés d'environ 12 ans. Pour plus de précisions sur les recommandations vaccinales, voir le Guide canadien d'immunisation.
Le CCNI recommande l'utilisation du vaccin conjugué quadrivalent contre le méningocoque pour les sérogroupes A, C, W135 et Y pour immuniser les groupes suivants :
Personnes à haut risque dû à des problèmes médicaux sous-jacents :
- les personnes souffrant d'asplénie fonctionnelle ou anatomique (y compris une anémie falciforme);
- les personnes qui présentent un déficit congénital en complément ou en anticorps primaires, ou encore une carence congénitale en properdine ou en facteur D;
- les personnes qui présentent un déficit acquis en complément après avoir reçu de l'éculizumab (SolirisMC), un inhibiteur de la voie terminale du complément;
- de plus, l'administration du vaccin doit être envisagé pour les personnes infectées par le VIH, en particulier si la maladie est congénitale.
Personnes à risque accru d'exposition :
- les voyageurs chez qui un vaccin contre le méningocoque est recommandé ou requis, y compris les personnes se rendant en Afrique subsaharienne et les pèlerins participant au Hadj à La Mecque, en Arabie saoudite;
- les employés de laboratoires potentiellement exposés de façon régulière à N. meningitidis;
- le personnel militaire, lors de formations de recrutement ou lors de certains déploiements.
Pour les personnes à risque élevé dû à des problèmes médicaux sous-jacents, âgées de 2 ans et plus, il convient d'administrer Men-C-ACYW-CRM ou Men-C-ACYW-DT dans le cadre d'une série de 2 doses (à au moins 8 semaines d'intervalle). Quant aux vaccins Men-C-ACYW-135, même s'ils n'ont pas été approuvés pour les personnes de 56 ans et plus, on peut les administrer à ce groupe d'âge compte tenu de certaines données probantes et de l'avis d'experts. Chez les enfants à risque élevé âgés de 2 mois à moins de 2 ans, utiliser de préférence le vaccin Men-C-ACYW-CRM; chez les enfants âgés de 1 an à moins de 2 ans, une série de 2 doses est recommandée (à au moins 8 semaines d'intervalle). Enfin, chez les nourrissons âgés de 2 mois à moins de 1 an, il est recommandé d'appliquer un calendrier de 2 ou 3 doses, y compris une dose supplémentaire entre 12 et 23 mois.Note de bas de page 5
Les personnes à risque élevé d'une méningococcie due à des problèmes médicaux sous-jacents ont intérêt à recevoir des doses de rappel périodiques.Note de bas de page 5 Les personnes vaccinées à l'âge de 6 ans ou moins devraient recevoir une dose de rappel de 3 à 5 ans après la dernière dose, puis à tous les 5 ans par la suite. Celles vaccinées à l'âge de 7 ans ou après devraient recevoir une dose de rappel tous les 5 ans après la dernière dose. On trouvera les calendriers destinés aux personnes à risque élevé dû à des problèmes médicaux sous-jacents au tableau 3 du chapitre sur le méningocoque du Guide canadien d'immunisation.
Les personnes à risque accru d'expositions, notamment les voyageurs se rendant dans des régions où le vaccin contre le méningocoque est recommandé, ont tout intérêt à recevoir le vaccin conjugué quadrivalent contre le méningocoque, ainsi que des doses de rappel périodiques si elles demeurent dans de telles conditions de façon continue. Pour les calendriers destinés aux voyageurs, voir le tableau 1 du chapitre sur le méningocoque du Guide canadien d'immunisation. La revaccination contre le méningocoque est recommandée pour les contacts étroits d'un cas de MI, conformément au tableau 2 du chapitre sur le méningocoque du Guide canadien d'immunisation).
En décembre 2012, Santé Canada (SC) a approuvé l'administration de MenactraMD (Men-C-ACYW-DT) dès l'âge de 9 mois. En mars 2013, SC a autorisé l'utilisation d'un nouveau vaccin conjugué quadrivalent, NimenrixMC (Men-C-ACYW-TT), produit par GlaxoSmithKline (GSK), pour les personnes de 12 mois à 55 ans. La présente déclaration vise à formuler des recommandations liées au nouveau produit NimenrixMC et à la nouvelle indication relative à l'âge pour MenactraMD.
II. Méthodes
Le CCNI a examiné les principales questions dans le cadre de l'examen documentaire selon les propositions du groupe de travail sur le méningocoque, notamment le fardeau de la maladie qui peut être évité; la population cible, l'innocuité, l'immunogénicité, l'utilité et l'efficacité du vaccin; les calendriers de vaccination et d'autres aspects de la stratégie globale d'immunisation. La synthèse des connaissances a été effectuée par des médecins spécialistes à l'Agence et supervisée par le groupe de travail. Après une évaluation critique de chacune des études, des tableaux sommaires comprenant des cotes de qualité des données fondées sur la hiérarchie méthodologique du CCNI ont été préparés (Tableaux 4 et 5), et des recommandations relatives à l'utilisation des vaccins ont été proposées. Le président du groupe de travail et le médecin spécialiste de l'Agence ont présenté les données et les recommandations proposées au CCNI le 8 octobre 2013. Après un examen attentif des données et la tenue de consultations à la réunion du CCNI, les membres de ce dernier ont voté certaines recommandations. On trouvera dans le texte une description des considérations pertinentes, des justifications des décisions et des lacunes dans les connaissances.
III. Épidemiologie
N. meningitidis (méningocoque) est un pathogène potentiellement grave qui colonise jusqu'à 10 % des personnes en santé. On peut classer les méningocoques en fonction de la réactivité immunologique au polysaccharide capsulaire dans au moins 12 sérogroupes différents, parmi lesquels 5 (A, B, C, W-135 et Y) sont le plus souvent liés à la MI.
La MI se caractérise habituellement par une maladie fébrile aiguë d'apparition soudaine associée à des caractéristiques de méningite ou de septicémie (méningococcémie), ou les deux, et à une éruption cutanée sans blancheur caractéristique. Le taux de mortalité globale est d'environ 10 %, et jusqu'à un tiers des survivants conservent des séquelles durables, notamment une perte d'audition, diverses atteintes neurologiques et l'amputation de doigts ou de membres.Note de bas de page 4Note de bas de page 6Tous les cas probables et confirmés de MI sont signalés par les provinces et territoires à l'Agence par l'intermédiaire de son Système national de surveillance améliorée de la MI. Les laboratoires de santé publique ou d'hôpitaux à l'échelle provinciale et territoriale envoient tous les isolats de méningocoques au Laboratoire national de microbiologie de l'Agence aux fins de caractérisation des souches, notamment la confirmation du sérogroupe et l'établissement du sérotype, du sous-type sérologique et du type de séquence ou du complexe clonal.
On signale des cas de MI toute l'année. Cependant, il y a une grande différence d'incidence sur les plans géographique et temporel, la majorité des cas étant déclarés entre novembre et mars. L'incidence de la MI au Canada s'est étendue de 0,45 à 1,18 cas pour 100 000 habitants de 1995 à 2011. Entre 2007 et 2011, 193,8 cas de MI ont été signalés en moyenne chaque année au Canada, soit une incidence moyenne de 0,58 cas pour 100 000 habitants.
Figure 1. Incidence de la méningococcie invasive pour 100 000 Canadiens selon le sérogroupe et l’année, de 1995 à 2011
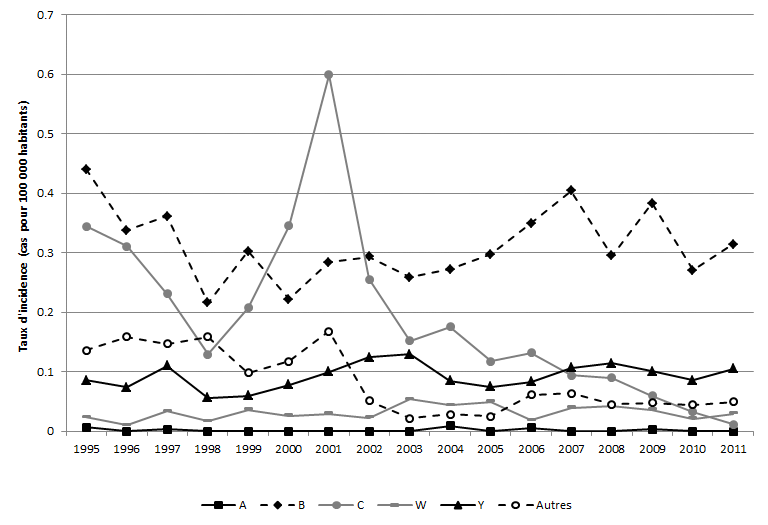
* « Autres » s'entend de tous les sérogroupes autres que ceux indiqués, ainsi que des sérogroupes ne pouvant être déterminés et des sérogroupes inconnus.
Figure 1. Incidence de la méningococcie invasive pour 100 000 Canadiens selon le sérogroupe et l’année, de 1995 à 2011 - Description textuel
La Figure 1 est un graphique linéaire illustrant le taux d’incidence annuel de cas signalés de méningococcie invasive (MI) au Canada pour 100 000 habitants selon le sérogroupe et l’année, de 1995 à 2011. L’axe des « x » présente les années de 1995 à 2011. L’axe des « y » à gauche présente les cas signalés pour 100 000 habitants, de 0 (partie inférieure) à 0,7 (partie supérieure). Les taux d’incidence annuels des sérogroupes A, B, C, W-135 et Y et des autres sérogroupes sont respectivement illustrés par une ligne. La catégorie des autres sérogroupes est formée des sérogroupes 29E, X et Z ainsi que des cas non sérogroupables et des cas pour lesquels le sérogroupe était inconnu.
Pour la majorité des années, le sérogroupe B a eu le taux d’incidence le plus élevé, allant de 0,22 à 0,44 cas pour 100 000 habitants. L’incidence du sérogroupe C diminue, passant de 0,35 cas à 0,13 cas pour 100 000 habitants de 1995 à 1998, puis augmente pour atteindre un sommet de 0,60 cas pour 100 000 habitants en 2001, pour encore diminuer au cours des dix années suivantes, atteignant son niveau le plus bas, soit de 0,01 cas pour 100 000 habitants en 2011. L’incidence des sérogroupes W-135 et Y est relativement stable, variant de 0,01 à 0,05 cas pour 100 000 habitants pour le sérogroupe W-135 et de 0,06 à 0,13 cas pour 100 000 habitants pour le sérogroupe Y. L’incidence du sérogroupe A est très faible pour toutes les années, soit 0,009 cas ou moins pour 100 000 habitants. De 1995 à 2001, les cas de MI attribuables aux autres sérogroupes, non sérogroupables et pour lesquels le sérogroupe était inconnu varient de 0,10 à 0,17 pour 100 000 habitants. Par la suite, les cas de MI attribuables aux autres sérogroupes diminuent, atteignant de 0,02 à 0,06 cas pour 100 000 habitants de 2002 à 2011.
Au Canada, le sérogroupe B est maintenant responsable de la majorité des cas de MI suivi du sérogroupe Y. À la suite d'éclosions localisées de cas imputables au sérogroupe C à la fin des années 1990 et au début des années 2000, on a mis en œuvre des programmes de vaccination par des vaccins conjugués contre le méningocoque du sérogroupe C dans l'ensemble des provinces et territoires canadiens entre 2002 et 2006 (Tableau 1), ce qui a entraîné une importante baisse de l'incidence de la MI du sérogroupe C dans tous les groupes d'âge et toutes les régions.Note de bas de page 6,Note de bas de page 7,Note de bas de page 8,Note de bas de page 9,Note de bas de page 10,Note de bas de page 11,Note de bas de page 12,Note de bas de page 13,Note de bas de page 14,Note de bas de page 15,Note de bas de page 16,Note de bas de page 17,Note de bas de page 18,Note de bas de page 19,Note de bas de page 20,Note de bas de page 21,Note de bas de page 22,Note de bas de page 23,Note de bas de page 24,Note de bas de page 25,Note de bas de page 26,Note de bas de page 27 Avec la baisse de l'incidence, les cas de MI du sérogroupe C sont maintenant rares et la part des cas de MI du sérogroupe B signalée est devenue la plus importante au Canada (62 % attribuables au sérogroupe B contre 2 % attribuables au sérogroupe C en 2011). La MI du sérogroupe A est extrêmement rare au Canada et a tendance à être associée aux voyages dans des régions du monde où elle demeure endémique (p. ex. la ceinture de méningite africaine).
| Province/ Territoire |
Année de mise en œuvre initiale du programme de vaccination systématique avec le vaccin conjugué contre le méningocoque C | Calendrier actuel de vaccination des nourrissons au moyen du vaccin conjugué contre le méningocoque C | Calendrier actuel de vaccination des adolescents au moyen du vaccin conjugué contre le méningocoque C (C) ou du vaccin conjugué contre le méningocoque ACYW-135 (Q) |
|---|---|---|---|
| C.-B. | 2003 | 2, 12 mois (depuis 2005) | (C) 6e année (depuis 2003) |
| Alb. | 2002 | 2, 4, 12 mois (depuis 2007) | (Q) 9e année (depuis 2011) |
| Sask. | 2004 | 12 mois (depuis 2004) | (Q) 6e année(depuis 2011) |
| Man. | 2004 | 12 mois (depuis 2009) | (C) 4e année (depuis 2004) |
| Ont. | 2004 | 12 mois (depuis 2004) | (Q) 7e année (depuis 2009) |
| Qc | 2002 | 12 mois (depuis 2002) | (C) 9e année (depuis 2013) |
| T.-N.-L. | 2005 | 12 mois (depuis 2005) | (Q) 4e année (depuis 2007) |
| N.-B. | 2004 | 12 mois (depuis 2004) | (Q) 9e année (depuis 2007) |
| N.-É. | 2005 | 12 mois (depuis 2005) | (C) 7e année (depuis 2010) |
| Î.-P.-É. | 2003 | 12 mois (depuis 2003) | (Q) 9e année (depuis 2006) |
| Yn | 2003 | 2, 12 mois (depuis 2009) | (C) 6e année (depuis 2006) |
| T.N.-O. | 2004 | 2, 12 mois (depuis 2004) | (C) 9e année (depuis 2008) |
| Nt | 2006 | 12 mois (depuis 2007) | (C) 6e année (depuis 2006) |
| Sérogroupe | Nombre moyen de cas par année (plage) |
Incidence moyenne par année (par 100 000 habitants) |
Âge médian | Taux de mortalité clinique |
|---|---|---|---|---|
| A | 0,2 (0 à 1) |
0,00 | 16 | 0.0 % |
| B | 112 (92 à 133) |
0,33 | 16 | 6,0 % |
| C | 19,2 (4 à 31) |
0,06 | 44,5 | 15,3 % |
| W-135 | 11,2 (7 à 14) |
0,03 | 38 | 8,5 % |
| Y | 34,4 (29 à 38) |
0,10 | 47 | 11,9 % |
| AutresNote de bas de tableau 2 - * « Autres » s'entend de tous les sérogroupes autres que ceux indiqués, ainsi que des sérogroupes ne pouvant être déterminés et des sérogroupes inconnus. | 16,8 (15 à 21) |
0,05 | 20 | 7,7 % |
| Tous les sérogroupes | 193,8 (154 à 233) |
0,58 | 20 | 8,2 % |
|
||||
Le Tableau 2 présente le nombre moyen et la plage de cas de MI et les taux d'incidence par année de 2007 à 2011. Il indique également l'âge médian et le taux de mortalité clinique de la maladie par sérogroupe de 2007 à 2011.
Figure 2. Distribution en pourcentage et nombre moyen de cas de méningococcie invasive au Canada de 2007 à 2011, par sérogroupe et par province/territoire
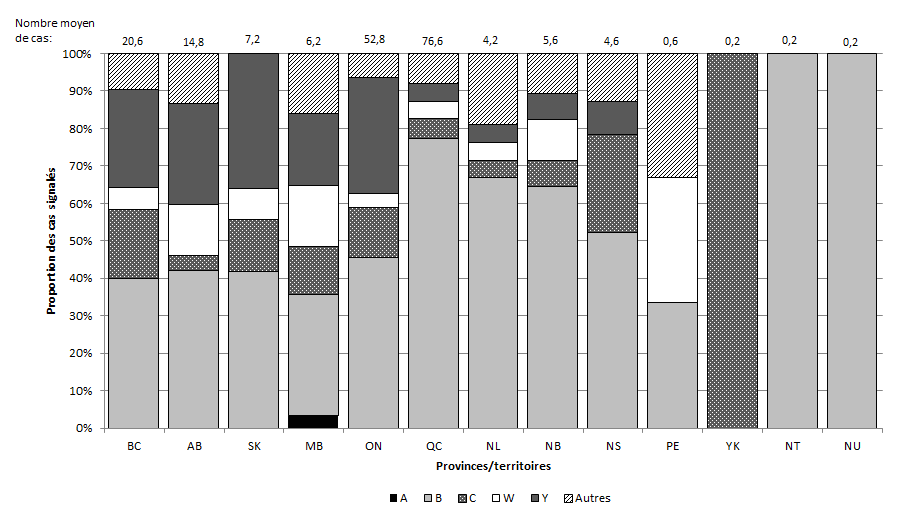
Figure 2. Distribution en pourcentage et nombre moyen de cas de méningococcie invasive au Canada de 2007 à 2011, par sérogroupe et par province/territoire - Description textuel
La Figure 2 est un graphe à barres empilées illustrant la distribution en pourcentage et le nombre moyen de cas de MI au Canada de 2007 à 2011, par sérogroupe et par province/territoire. L’axe des x présente chaque province/territoire, de la Colombie-Britannique au Nunavut. L’axe des y à gauche affiche la proportion globale des cas signalés au cours de la période de cinq ans s’échelonnant de 2007 à 2011. L’axe des y va de 0 % (partie inférieure) à 100 % (partie supérieure). Chaque barre empilée illustre la distribution en pourcentage des cas attribuables aux sérogroupes A, B, C, W-135 et Y et aux autres sérogroupes pour chaque province/territoire. La catégorie des autres sérogroupes est formée des sérogroupes 29E, X et Z ainsi que des cas non sérogroupables et des cas pour lesquels le sérogroupe était inconnu. Le nombre moyen de cas survenus au cours de cette période est exprimé en décimale au-dessus de la barre respective de chaque province/territoire.
Très peu de cas ont été signalés dans les trois territoires et à l’Île-du-Prince-Édouard (1 à 3 cas par année) de 2007 à 2011. Dans le territoire du Yukon, le sérogroupe C est à l’origine de 100 % des cas, tandis que 100 % des cas dans les Territoires du Nord-Ouest et le Nunavut sont attribuables au sérogroupe B. À l’Île-du-Prince-Édouard, les cas sont répartis de façon égale entre les sérogroupes B, W-135 et la catégorie des autres sérogroupes. Les nombres peu élevés signifient que les proportions varient grandement d’une année à l’autre; ils doivent donc être interprétés avec prudence.
Au sein des autres provinces, le sérogroupe B est à l’origine de la plus grande proportion de cas, qui se situe entre 32 % au Manitoba et 77 % au Québec. La proportion de cas attribuables au sérogroupe C s’échelonne de 4 % en Alberta à 26 % en Nouvelle-Écosse. La proportion de cas attribuables au sérogroupe Y va de 5 % au Québec et à Terre-Neuve-et-Labrador à 36 % en Saskatchewan. La proportion de cas attribuables au sérogroupe W-135 varie de 0 % en Nouvelle-Écosse à 16 % au Manitoba. La proportion de cas attribuables au sérogroupe A est de 0 % pour tous les groupes, à l’exception du Manitoba (3 %). La proportion de cas non sérogroupables, attribuables aux autres sérogroupes ou pour lesquels le sérogroupe était inconnu se situe entre 0 % en Saskatchewan et 19 % à Terre-Neuve-et-Labrador.
Le nombre moyen de cas dans chaque province/territoire était de 20,6 pour la Colombie-Britannique (distribution des sérogroupes : 40 % pour B, 18 % pour C, 6 % pour W-135, 26 % pour Y, 10 % pour tous les autres), 14,8 pour l’Alberta (distribution des sérogroupes : 42 % pour B, 4 % pour C, 14 % pour W-135, 27 % pour Y, 14 % pour tous les autres), 7,2 pour la Saskatchewan (distribution des sérogroupes : 42 % pour B, 14 % pour C, 8 % pour W-135, 36 % pour Y), 6,2 pour le Manitoba (distribution des sérogroupes : 3 % pour A, 32 % pour B, 13 % pour C, 16 % pour W-135, 19 % pour Y, 16 % pour tous les autres), 52,8 pour l’Ontario (distribution des sérogroupes : 45 % pour B, 13 % pour C, 4 % pour W-135, 31 % pour Y, 6 % pour tous les autres), 76,6 pour le Québec (distribution des sérogroupes : 77 % pour B, 5 % pour C, 4 % pour W-135, 5 % pour Y, 8 % pour tous les autres), 4,2 pour Terre-Neuve-et-Labrador (distribution des sérogroupes : 67 % pour B, 5 % pour C, 5 % pour W-135, 5 % pour Y, 19 % pour tous les autres), 5,6 pour le Nouveau-Brunswick (distribution des sérogroupes : 64 % pour B, 7 % pour C, 11 % pour W-135, 7 % pour Y, 11 % pour tous les autres), 4,6 pour la Nouvelle-Écosse (distribution des sérogroupes : 52 % pour B, 26 % pour C, 9 % pour Y, 13% pour tous les autres), 0,6 pour l’Île-du-Prince-Édouard (distribution des sérogroupes : 33 % pour B, 33 % pour W-135, 33 % pour tous les autres), 0,2 pour le Territoire du Yukon (100 % pour C), 0,2 pour les Territoires du Nord-Ouest (100 % pour B), et 0,2 pour le Nunavut (100 % pour B).
Comme l'indique la Figure 2, il existe des différences géographiques en matière de répartition des sérogroupes de la MI dans l'ensemble du Canada. L'incidence de MI la plus élevée et la MI propre au sérogroupe B sont visibles au Québec, où 77 % des cas en moyenne étaient attribuables au sérogroupe B de 2007 à 2011. Dans les autres provinces, la répartition des sérogroupes était variable. Le sérogroupe B représentait de 32 % à 67 % des cas entre 2007 et 2011, selon la province. Très peu de cas ont été signalés dans les trois territoires et à l'Île-du-Prince-Édouard (1 à 3 cas par année) de 2007 à 2011. Les nombres peu élevés signifient que les proportions peuvent varier grandement d'une année à l'autre; ils doivent donc être interprétés avec prudence.
Figure 3. Distribution en pourcentage et nombre moyen de cas de méningococcie invasive au Canada de 2007 à 2011, par sérogroupe et par groupe d’âge
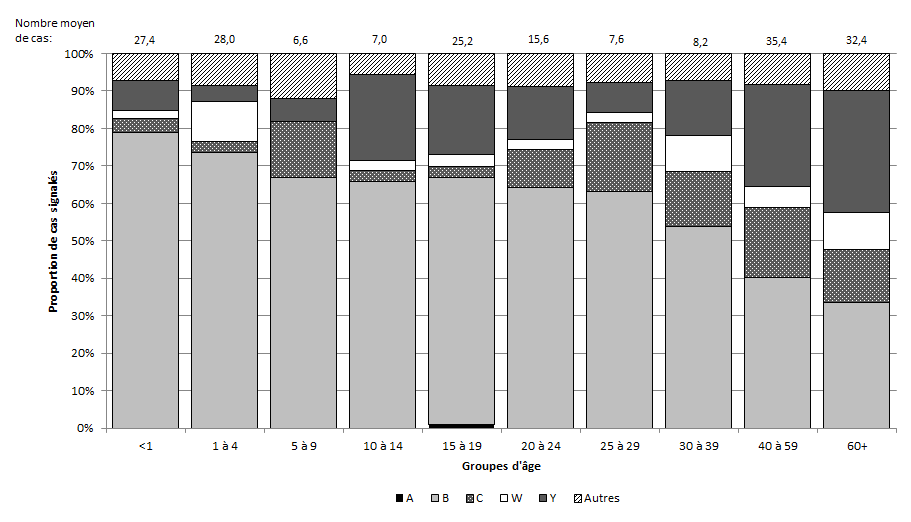
Figure 3. Distribution en pourcentage et nombre moyen de cas de méningococcie invasive au Canada de 2007 à 2011, par sérogroupe et par groupe d’âge - Description textuel
La Figure 3 est un graphe à barres empilées illustrant la distribution en pourcentage et le nombre moyen de cas de MI au Canada de 2007 à 2011, par sérogroupe et par groupe d’âge. L’axe des x présente les groupes d’âge, soit les nourrissons de moins d’un an, les tout-petits de 1 à 4 ans, les enfants de 5 à 9 ans, les adolescents de 10 à 14 ans et de 15 à 19 ans, les adultes de 20 à 24 ans, de 25 à 29 ans, de 30 à 39 ans, de 40 à 59 ans, ainsi que de 60 ans et plus. L’axe des y à gauche affiche la proportion globale des cas signalés au cours de la période de cinq ans s’échelonnant de 2007 à 2011. Cet axe va de 0 % (partie inférieure) à 100 % (partie supérieure). Chaque barre empilée illustre la distribution en pourcentage des cas attribuables aux sérogroupes A, B, C, W-135, Y et aux autres sérogroupes pour chaque groupe d’âge. La catégorie des autres sérogroupes est formée des sérogroupes 29E, X et Z ainsi que des cas non sérogroupables et des cas pour lesquels le sérogroupe était inconnu. Le nombre moyen de cas survenus au cours de cette période est exprimé en décimale au-dessus de la barre respective de chaque groupe d’âge.
Le sérogroupe B est à l’origine de la plus grande proportion de cas dans tous les groupes d’âge, bien que la proportion de cas attribuables à ce sérogroupe diminue avec l’âge, oscillant entre 33 % chez les personnes de 60 ans et plus et 79 % chez les nourrissons de moins d’un an. La proportion de cas attribuables aux sérogroupes C et Y a tendance à augmenter avec l’âge. La proportion de cas attribuables au sérogroupe C se situe entre 3 % pour le groupe des 10-14 ans et 19 % chez celui des 40-59 ans. La proportion de cas attribuables au sérogroupe Y varie de 4 % pour les enfants de 1 à 4 ans jusqu’à 33 % chez les adultes de 60 ans et plus. Dans chaque groupe, la proportion de cas attribuables au sérogroupe W-135 est faible, allant de 0 % chez les enfants de 5 à 9 ans à 11 % chez les enfants de 1 à 4 ans. La proportion de cas attribuables au sérogroupe A est de 0 % pour tous les groupes d’âge, à l’exception du groupe des 15-19 ans (1 %), et la proportion de cas non sérogroupables, attribuables aux autres sérogroupes ou pour lesquels le sérogroupe était inconnu varie de 6 % pour les 10-14 ans à 12 % pour les 5-9 ans.
Le nombre moyen de cas par groupe d’âge dans chaque province/territoire était de 27,4 pour les nourrissons de moins d’un an (distribution des sérogroupes : 79 % pour B, 4 % pour C, 2 % pour W-135, 8 % pour Y, 7 % pour tous les autres), 28,0 pour les enfants de 1 à 4 ans (distribution des sérogroupes : 74 % pour B, 3 % pour C, 11 % pour W-135, 4 % pour Y, 9 % pour tous les autres), 6,6 pour les 5 à 9 ans (distribution des sérogroupes : 67 % pour B, 15 % pour C, 6 % pour Y, 12 % pour tous les autres), 7,0 pour le groupe des 10 à 14 ans (distribution des sérogroupes : 66 % pour B, 3 % pour C, 3 % pour W-135, 23 % pour Y, 6 % pour tous les groupes), 25,2 pour les 15 à 19 ans (distribution des sérogroupes : 1 % pour A, 66 % pour B, 3 % pour C, 3 % pour W-135, 18 % pour Y, 9 % pour tous les groupes), 15,6 pour les 20 à 24 ans (distribution des sérogroupes : 64 % pour B, 10 % pour C, 3 % pour W-135, 14 % pour Y, 9 % pour tous les autres), 7,6 pour les 25 à 29 ans (distribution des sérogroupes : 63 % pour B, 18 % pour C, 3 % pour W-135, 8 % pour Y, 8 % pour tous les autres), 8,2 pour les 30 à 39 ans (distribution des sérogroupes : 54 % pour B, 15 % pour C, 10 % pour W-135, 15 % pour Y, 7 % pour tous les autres), 35,4 pour les 40 à 59 ans (distribution des sérogroupes : 40 % pour B, 19 % pour C, 6 % pour W-135, 27 % pour Y, 9 % pour tous les autres), 32,4 pour les personnes de 60 ans et plus (distribution des sérogroupes : 33 % pour B, 14 % pour C, 10 % pour W-135, 33 % pour Y, 10 % pour tous les autres).
La répartition des sérogroupes de MI varie également en fonction de l'âge. Les cas du sérogroupe Y possédaient l'âge médian le plus élevé de 2007 à 2011 (47 ans), suivis du sérogroupe C (44,5 ans) et du sérogroupe W-135 (38 ans). Comme l'indique la Figure 3, la part de cas attribuables au sérogroupe B baisse avec l'âge alors qu'à l'inverse, la part de cas attribuables aux sérogroupes C et Y a tendance à augmenter avec l'âge.
IV. Vaccin
| NimenrixMC | MenveoMC | MenactraMD | |
|---|---|---|---|
| Type de vaccin | Conjugué A, C, Y, W-135 (Men-C-ACYW-TT) |
Conjugué A, C, Y, W-135 (Men-C-ACYW- CRM) |
Conjugué A, C, Y, W-135 (Men-C-ACYW-DT) |
| Fabricant | GlaxoSmithKline | Novartis | Sanofi Pasteur |
| Concentration de polysaccharides | 5 µg de chaque sérogroupe | 10 µg du sérogroupe A 5 µg de chacun des sérogroupes C, Y, W-135 | 4 µg de chaque sérogroupe |
| Support protéique | 44 µg d'anatoxine tétanique (AT) Sérogroupes W-135 et Y directement conjugués à l'AT; sérogroupes A et C conjugués à un espaceur (dihydrazide adipique) et indirectement à l'AT |
Quantités variables de la protéine CRM197 conjuguée à chaque polysaccharide : 16,7 à 33,3 µg à A 7,1 à 12,5 µg à C 3,3 à 8,3 µg à W-135 5,6 à 10 µg à Y |
48 µg d'anatoxine diphtérique (AD) |
| Agent de conservation | S.O. | S.O. | S.O. |
| Adjuvant | S.O. | S.O. | S.O. |
| AdministrationNote de bas de tableau IV - * | 0,5 mL IM Doit être reconstitué |
0,5 mL IM Doit être reconstitué |
0,5 mL IM |
| Calendrier du fabricant | De 12 mois à 55 ans | De 2 ans à 55 ans | De 9 mois à 55 ans |
|
|||
Remarque sur les supports protéiques : Bien que les vaccins contenant la protéine CRM197 et l'AT montrent généralement une plus grande immunogénicité que ceux contenant l'AD, la supériorité comparative de ces deux protéines reste controversée.Note de bas de page 6,Note de bas de page 7,Note de bas de page 8,Note de bas de page 9,Note de bas de page 10,Note de bas de page 11
IV.2 Efficacité
Les essais cliniques préalables à l'autorisation sont difficiles à réaliser puisque la méningococcie est relativement rare. Par conséquent, l'activité bactéricide dépendante des anticorps et médiée par un complément est mesurée au moyen d'un essai bactéricide sérique et est utilisée comme corrélat immunologique de la protection.
L'efficacité des nouveaux vaccins conjugués contre le méningocoque peut être déduite de la démonstration de non-infériorité immunologique et permettre l'autorisation de ces vaccins. L'approbation réglementaire repose donc uniquement sur les données d'immunogénicité obtenues après la vaccination. L'efficacité des vaccins conjugués après leur homologation est fondée sur une méthode de dépistageNote de bas de page 28 qui nécessite des données exactes de couverture ainsi que l'état d'immunisation des patients. Au Canada, il y a peu de cas de méningococcie, il faudrait donc de nombreuses années pour disposer d'un nombre de cas suffisant pour être en mesure d'estimer l'efficacité des vaccins (EV). De plus, la qualité des données actuelles tirées de la surveillance de la couverture et des cas n'est pas assez élevée pour permettre la mesure de l'EV. L'immunogénicité constitue donc la meilleure méthode qui existe en ce moment.
IV.3 Immunogénicité (y compris les données pour les corrélats de la protection)
Les vaccins conjugués contre le méningocoque qui sont offerts au Canada sont homologués d'après l'induction d'une séroréaction, qui est mesurée par la présence d'anticorps bactéricides sériques en utilisant le sérum humain (ABSh) ou le sérum de lapereau (ABSl) comme source de complément exogène. Étant donné qu'il est difficile d'obtenir du sérum humain sans anticorps bactéricides contre le méningocoque, le sérum de lapereau, qui n'a pas d'activité bactéricide intrinsèque, est une source privilégiée de compléments pour évaluer les réponses bactéricides aux vaccins contre le méningocoque. Toutefois, l'évaluation de la réponse immunitaire aux vaccins conjugués contre le méningocoque mesurée par les ABSl donne lieu à des titres bactéricides beaucoup plus élevés et démontre divers niveaux de corrélation avec les ABSh pour différents sérotypes. La séroréaction aux fins d'homologation s'entend le plus souvent d'un titre d'ABSl ≥ 1:8 ou d'une augmentation du titre par un facteur de quatre chez les individus ayant un titre d'ABSl ≥ 1:4 au départ. Aux fins de l'homologation de NimenrixMC, la séroréaction a été définie comme suit :
- Sujets < 2 ans : Titre d'ABSl ≥ 1:8
- Sujets ≥ 2 ans : Titre d'ABSl ≥ 1:32 pour les sujets ayant un titre < 1:8 avant la vaccination, ou augmentation du titre par un facteur quatre pour ceux ayant un titre ≥ 1:8 avant la vaccination
Il n'y a pas de consensus en ce moment quant à l'utilisation préférentielle des ABSl ou des ABSh pour déterminer la protection à court terme contre la MI. En raison de l'apparition rapide de la maladie, la protection est mieux assurée par une circulation des anticorps que par la mémoire immunologique. À l'heure actuelle, on ne connaît pas le titre moyen géométrique (TMG) requis pour une protection à long terme.Note de bas de page 14 La quantification non fonctionnelle des anticorps IgG est mesurée à l'aide d'un dosage immuno-enzymatique (ELISA) standard et fournit des renseignements qui s'ajoutent aux résultats des ABS (anticorps bactéricides sériques). Toutefois, ils ne représentent pas une corrélation directe de la protection. Pour de plus amples renseignements sur les corrélats de la protection, veuillez consulter la précédente Mise à jour du CCNI sur l'utilisation des vaccins conjugués quadrivalents contre le méningocoque.
Bien que les résultats des essais sur les ABSh ou les ABSl conviennent à la comparaison des vaccins à l'intérieur d'une même étude, on ne peut s'en servir pour comparer les vaccins d'une étude à l'autre en raison des différences sur le plan de la méthodologie. De même, il faut user de prudence si l'on compare les résultats de différents laboratoires, car la méthodologie varie d'un laboratoire à l'autre.Note de bas de page 15,Note de bas de page 16,Note de bas de page 17 L'incidence de la vaccination sur le portage et l'immunité collective ne peut être prévue à l'aide des données tirées d'études d'immunogénicité.
IV.3.1 Immunogénicité de NimenrixMC
Immunogénicité de NimenrixMC chez les enfants de moins de 12 mois
L'immunogénicité d'une ou de deux doses (deuxième dose à 12 mois) de Men-C-ACYW-TT a été étudiée chez 149 nourrissons de 9 mois et comparée à celle d'une dose unique à 12 mois.Note de bas de page 18 À la suite de la vaccination initiale, un titre d'ABSl ≥ 1:8 a été obtenu chez tous les nourrissons pour tous les sérogroupes sauf le sérogroupe C; un nourrisson n'ayant pas atteint le niveau de séroprotection prédéfini. Bien que la proportion des patients présentant des titres d'ABSl ≥ 1:8 ait été comparable dans les groupes d'âge de 9 et 12 mois (personnes ayant reçu 1 dose de vaccin), la proportion d'ABSh ≥ 1:8 était significativement plus élevée dans le groupe d'âge de 12 mois (1 dose de vaccin) pour tous les sérogroupes sauf le sérogroupe C. De même, les TMG d'ABSl étaient significativement plus élevés après une seule dose à 12 mois qu'à 9 mois pour tous les sérogroupes sauf le sérogroupe A. L'étude ne comportait pas de vaccin de comparaison, car aucun vaccin contre le méningocoque n'était homologué pour ce groupe d'âge au moment de l'étude.
Immunogénicité de NimenrixMC chez les enfants âgés de 12 à 23 mois
L'immunogénicité de Men-C-ACYW-TT chez les tout-petits âgés de 12 à 23 mois a été évaluée chez environ 1 000 enfants dans le cadre de 5 essais cliniques de phase II et de phase III, de 4 à 6 semaines après la vaccination.Note de bas de page 18,Note de bas de page 19,Note de bas de page 20,Note de bas de page 21,Note de bas de page 22 Un titre d'ABSl ≥ 1:8 a été obtenu chez plus de 99 % des tout-petits pour les quatre groupes. Une non-inférioritéNote de bas de page 19Note de bas de page 20 a été démontrée dans toutes les études portant sur l'immunogénicité du vaccin Men-C-ACYW-TT par rapport à celle du vaccin Men-C-CRM197 monovalent. Dans le cadre de deux études qui mesuraient les ABSh à 4 et 6 semaines après la vaccination, les sujets à qui on avait administré le vaccin Men-C-ACYW-TT ont atteint des niveaux d'anticorps bactéricides significativement plus élevés, mesurés à l'aide du titre d'ABSh et du TMG, en comparaison de ceux obtenus à la suite de l'administration du vaccin Men-C-CRM197.
Immunogénicité de NimenrixMC chez les enfants de 2 à 10 ans
Au total, quatre études publiées portaient sur l'immunogénicité un mois après l'administration d'une dose unique de NimenrixMC chez 1 400 enfants de 2 à 10 ans. Dans la cohorte d'immunogénicité de l'essai comparatif randomisé (ECR) de Memish et al.,Note de bas de page 23 on a administré de façon aléatoire une dose unique de Men-C-ACYW-TT ou de Men-P-ACYW-135 à des enfants. La protection immunitaire, mesurée par la présence d'ABSl > 1:8, n'était pas inférieure dans le groupe ayant reçu le vaccin Men-C-ACYW-TT comparativement à celui ayant reçu le vaccin Men-P-ACYW-135. Les TMG étaient significativement plus élevés (sur le plan statistique) pour les quatre sérogroupes dans le groupe ayant reçu le vaccin Men-C-ACYW-TT. La séroréaction était également significativement plus élevée dans le groupe traité par Men-C-ACYW-TT que dans celui traité par Men-P-ACYW-135. De façon similaire, en utilisant le même vaccin de comparaison, Vesikari et al.Note de bas de page 24 ont démontré la non-infériorité (ABSl > 1:8) de Men-ACYW-TT pour les quatre sérogroupes. Par comparaison avec le vaccin Men-P-ACYW-135, les valeurs de TMG d'ABSl étaient plus élevées avec le vaccin Men-C-ACYW-TT pour chaque sérogroupe après ajustement pour les mesures prises avant la vaccination. Une analyse exploratoire a également démontré une séroréaction significativement plus élevée pour les sérogroupes A et C dans le groupe traité avec le vaccin Men-C-ACYW-TT que dans celui traité avec le vaccin Men-P-ACYW-135.
Dans le cadre d'un ECR effectué par Knuf et al.Note de bas de page 25, la non-infériorité de Men-C-ACYW-TT par rapport à Men-C-CRM197 a été démontrée. De fait, 99 % des sujets du groupe Men-C-ACYW-TT ont atteint des titres d'ABSl > 1:8. Les valeurs de TMG d'ABSl étaient significativement plus élevées dans le groupe traité par le vaccin Men-C-CRM197 monovalent pour le sérogroupe C, ce qui semble indiquer une réponse anticorps plus forte.
Baxter et al.Note de bas de page 26 ont évalué l'immunogénicité de Men-C-ACYW-TT chez 79 enfants en santé de 10 ans et ont comparé la réponse au vaccin par rapport à celle obtenue chez des adolescents et des adultes de 11 à 25 ans. La réponse immunitaire était similaire à l'exception des valeurs relativement élevées, mais non significatives sur le plan statistique, de TMG d'ABSh dans le groupe d'âge de 10 ans.
Immunogénicité de NimenrixMC chez les personnes de 11 à 19 ans
Plusieurs études ont porté sur l'immunogénicité de Men-C-ACYW-TT chez des personnes de plus de 10 ans, mais seulement 5 d'entre elles ont présenté des résultats pour le groupe des 11 à 19 ans. Dans une étude menée chez 115 sujets de 11 à 17 ans à qui on a administré le vaccin Men-C-ACYW-TT, Østergaard et al.Note de bas de page 27 ont observé un titre d'ABSl ≥ 1:8 chez tous les sujets 1 mois après la vaccination. Dans un autre ECR réalisé par Østergaard et al.,Note de bas de page 29Note de bas de page 30 50 sujets ont reçu le vaccin Men-C-ACYW-TT ou le vaccin Men-P-ACYW-135. Tous les sujets ont obtenu des titres d'ABSl ≥ 1:8 pour tous les sérogroupes, et il n'y avait pas de différence significative entre les groupes quant aux TMG d'ABSl, à l'exception de celle du sérogroupe W-135 à 42 mois qui était significativement plus élevé dans le groupe Men-C-ACYW-TT (n=19) que dans le groupe Men-P-ACYW-135 (n=17). Les taux de séroréaction dans le groupe Men-C-ACYW-TT étaient supérieurs à 90,2 % pour tous les sérogroupes. Dans les deux groupes, la plupart des sujets (58,8 % à 90,9 %) présentaient des titres d'ABSl élevés pour tous les sérogroupes avant la vaccination. De même, une étude menée par Bermal et al.Note de bas de page 31Note de bas de page 32 chez 1 025 sujets avec le même vaccin de comparaison a démontré la non-infériorité de Men-C-ACYW-TT par rapport à Men-P-ACYW-135. Avant la vaccination, le pourcentage de sujets de chaque groupe qui présentaient des titres d'ABSl ≥ 1:8 se situait entre 78,6 % et 90,9 % pour les sérogroupes A, W-135 et Y, et entre 58,6 % et 59,4 % pour le sérogroupe C. Un mois après la vaccination, au moins 99,6 % des sujets des deux groupes présentaient des titres d'ABSl ≥ 1:8 contre chaque sérogroupe visé par les vaccins contre le méningocoque. Les taux de séroréaction étaient significativement plus élevés dans le groupe Men-C-ACYW-TT pour les sérogroupes A, W-135 et Y, et non inférieurs pour le sérogroupe C en comparaison de ceux du groupe Men-P-ACYW-135. Après la vaccination, les TMG d'ABSl contre chaque sérogroupe étaient de 29,2 à 274,3 fois supérieurs chez les personnes ayant reçu le vaccin Men-C-ACYW-TT et de 16,4 à 185,9 fois supérieurs chez les personnes ayant reçu le vaccin Men-P-ACYW-135. Contrairement à l'étude menée par Østergaard et al., les TMG d'ABSl étaient significativement plus élevés après l'administration du vaccin Men-C-ACYW-TT qu'après celle du vaccin Men-P-ACYW-135 pour tous les sérogroupes; toutefois, l'étude de Østergaard était de bien moins grande envergure et son efficacité statistique n'était pas suffisante pour déceler les différences.
L'immunogénicité de Men-C-ACYW-TT a été comparée à celle d'un autre vaccin quadrivalent conjugué (Men-C-ACYW-DT, MenactraMD) dans le cadre de deux essais. Baxter et al.(26) ont réparti aléatoirement 784 sujets en santé de 11 à 25 ans. Les deux vaccins ont entraîné des réponses similaires quant aux ABSh > 1:4 pour le sérogroupe C après la vaccination. Dans le cas des sérogroupes A, W-135 et Y, le vaccin Men-C-ACYW-TT a provoqué une meilleure réponse que le vaccin Men-C-ACYW-DT. Les valeurs ajustées de TMG étaient plus élevées pour tous les sérogroupes chez les sujets ayant reçu le vaccin Men-C-ACYW-TT. Le pourcentage de sujets présentant une réponse à la vaccination était également plus élevé dans le groupe ayant reçu le vaccin Men-C-ACYW-TT. Halperin et al.Note de bas de page 33 ont administré de façon aléatoire une dose unique de l'un des deux lots (A ou B) du vaccin Men-C-ACYW‐TT ou bien d'un seul lot du vaccin Men-C-ACYW‐DT à 1 016 personnes en santé de 10 à 25 ans. Cette étude a révélé que le vaccin Men-C-ACYW‐TT entraînait une réponse immunitaire non inférieure à celle du vaccin Men-C-ACYW‐DT.
Immunogénicité de NimenrixMC chez les personnes de 19 à 55 ans
Dbaibo et al.Note de bas de page 34 ont comparé l'immunogénicité du vaccin Men-C-ACYW-TT à celle du vaccin Men-P-ACYW-135 dans le cadre d'une étude menée auprès de 1 100 personnes. Dans le groupe ayant reçu le vaccin Men-C-ACYW-TT, 99,3 % des personnes vaccinées présentaient des ABSl > 1:8, ce qui démontre une non-infériorité par rapport au vaccin Men-P-ACYW-135. Après l'administration du vaccin Men-C-ACYW-TT, les TMG d'ABSl ont augmenté d'un facteur 20 ou plus pour les sérogroupes A, W-135 et Y, et d'un facteur 109 pour le sérogroupe C. À la lumière des valeurs de TMG et de l'analyse exploratoire, on observe que les TMG étaient significativement supérieurs sur le plan statistique dans le groupe ayant reçu le vaccin Men-C-ACYW-TT pour tous les sérogroupes, sauf le sérogroupe C, pour lequel il n'y avait aucune différence statistique. Dans une étude menée par Borja-Tabora et al.Note de bas de page 35, un total de 500 personnes de 11 à 55 ans ont reçu le vaccin Men-C-ACYW-TT ou le vaccin Men-P-ACYW-135. Un mois après la vaccination, plus de 99,7 % des personnes ayant reçu le Men-C-ACYW-TT avaient un titre d'ABSl > 1:8. Compte tenu des titres d'ABSl, le vaccin Men-C-ACYW-TT n'était pas inférieur au vaccin Men-P-ACYW-135, et les valeurs de TMG un mois après la vaccination étaient plus élevées dans le groupe ayant reçu le vaccin Men-C-ACYW-TT pour chaque sérogroupe. Les taux de séroréaction variaient de 82,7 % à 96,3 % dans le groupe ayant reçu le vaccin Men-C-ACYW-TT et de 69,7 % à 91,7 % dans le groupe ayant reçu le vaccin Men-P-ACYW-135, la réponse étant statistiquement significative pour les sérogroupes A et Y à la suite de l'administration du vaccin Men-C-ACYW-TT.
Immunogénicité de NimenrixMC chez les personnes âgées de plus de 55 ans
Dbaibo et al.Note de bas de page 36 ont comparé l'immunogénicité du vaccin MenACWY-TT à celle du vaccin Men-P-ACYW-135 chez 369 adultes en santé âgés de 56 à 103 ans. Il n'y avait aucune différence significative quant aux ABSl > 1:8 un mois après la vaccination. Cependant, les personnes ayant reçu le vaccin Men-P-ACYW-135 présentaient une réaction au vaccin, des ABSl et un TMG significativement plus élevés pour le sérogroupe A que celles ayant reçu le vaccin conjugué. Ce phénomène est principalement attribuable à une plus faible réponse chez les personnes qui présentaient des titres très élevés (≥ 1:128) avant la vaccination.
Persistance de la réponse immunitaire
Cinq études (N = 1 306) ont porté sur la persistance de la réponse immunitaire après l'administration du vaccin Men-C-ACYW-TT, c'est-à-dire de 12 à 48 mois après l'immunisation. Toutes les études sont des ECRs de prolongation qui visent à évaluer la non-infériorité du vaccin Men-C-ACYW-TT par rapport à d'autres vaccins contre le méningocoque (Men-C-CRM197 ou Men-P-ACYW-135) parmi des comparateurs adaptés à l'âge. Dans toutes les études, la persistance des anticorps mesurée par la présence d'ABSl était semblable ou plus longue chez les sujets ayant reçu le vaccin Men-C-ACYW-TT que chez ceux ayant reçu l'un des autres vaccins, et ce, pour tous les sérogroupes.
L'étude menée par Knuf et al.Note de bas de page 37 a suivi pendant 15 mois des tout-petits âgés de 12 à 14 mois ainsi que des enfants de 3 à 5 ans afin de déterminer la persistance des anticorps. Le pourcentage de ceux présentant un titre d'ABSl ≥ 1:8 pour le sérogroupe C était plus élevé dans le groupe ayant reçu le vaccin Men-C-ACYW-TT que dans le groupe témoin ayant reçu le vaccin Men-C-CRM197 (groupe de sujets de 12 à 14 mois). Le groupe ayant reçu le vaccin Men-C-ACYW-TT avait également des titres d'ABSl plus élevés pour les sérogroupes C et Y que ceux du groupe témoin ayant reçu le vaccin Men-P-ACYW-135 (groupe de sujets de 3 à 5 ans). De plus, les valeurs de TMG étaient plus élevées.
Dans le cadre de deux études, Vesikari et al.Note de bas de page 19Note de bas de page 38 ont signalé des réponses immunitaires à la suite de l'administration du vaccin Men-C-ACYW-TT à des tout-petits âgés de 12 à 23 mois. Dans une étude portant sur 170 nourrissons à qui on a administré le vaccin Men-C-ACYW-TT, 90,8 % d'entre eux ont maintenu un titre d'ABSI ≥ 1:8 pour tous les sérogroupes, 73,6 % ont maintenu un titre d'ABSh ≥ 1:4 pour les sérogroupes C, W et Y, et seulement 28,1 % ont maintenu un titre d'ABSh ≥ 1:4 pour le sérogroupe A 3 ans après la vaccination. Il n'y avait aucune différence significative du titre d'ABSl 3 ans après la vaccination entre les sujets ayant reçu le vaccin Men-C-ACYW-TT et ceux ayant reçu le vaccin Men-C-CRM197. Au cours des deux premières années suivant la vaccination, les TMG étaient plus élevés dans le groupe immunisé à l'aide du vaccin Men-C-ACYW-TT que dans celui immunisé à l'aide du vaccin Men-C-CRM197, tandis qu'aucune différence significative n'a été observée au cours de la troisième année. De même, une étude portant sur 225 nourrissons a révélé que les titres d'ABSl et les valeurs de TMG étaient comparables pour le vaccin Men-C-ACYW-TT et le vaccin Men-C-CRM197, 4 ans après la vaccination initiale.Note de bas de page 38
Vesikari et al.Note de bas de page 24 ont également suivi des enfants de 2 à 10 ans pour un total de 3 ans après la vaccination. Les enfants du groupe Men-C-ACYW-TT présentaient des valeurs de TMG d'ABSl plus élevées pour tous les sérogroupes au cours des deux premières années après la vaccination par rapport à ceux du groupe Men-P-ACYW-135. Au cours de la troisième année, les valeurs de TMG étaient plus élevées dans le groupe ayant reçu le vaccin Men-C-ACYW-TT que dans celui ayant reçu le vaccin Men-P-ACYW-135 pour tous les sérogroupes sauf le sérogroupe C.
Dans l'étude réalisée par Østergaard et al.Note de bas de page 30, 36 adolescents ayant reçu le vaccin Men-C-ACYW-TT ou Men-P-ACYW-135 ont été suivis pendant un total de 42 mois. Dans les deux groupes, les titres d'ABSl ≥ 1:8 et les valeurs de TMG étaient similaires pour tous les sérogroupes à l'exception de celle du sérogroupe W-135 à 42 mois qui était significativement plus élevé dans le groupe Men-C-ACYW-TT.
Dans une étude de plus grande envergure menée auprès de 535 adolescents à l'aide du vaccin de comparaison Men-P-ACYW-135, Bermal et al.Note de bas de page 31 ainsi que Quiambao et al.Note de bas de page 32 ont signalé que les titres d'ABSl ≥ 1:8 et les valeurs de TMG étaient plus élevés 3 et 4 ans après la vaccination dans le groupe ayant reçu le vaccin Men-C-ACYW-TT que dans le groupe de comparaison ayant reçu le vaccin Men-P-ACYW-135, et ce, pour tous les sérogroupes sauf le sérogroupe C.
Dans une étude de persistance, Borja-Tabora et al.Note de bas de page 35 ont administré le vaccin Men-C-ACYW-TT ou le vaccin Men-P-ACYW-135 de façon aléatoire à 500 personnes de 11 à 55 ans. Les titres d'ABSl étaient plus élevés aux années 3 et 4 dans le groupe ayant reçu le vaccin Men-C-ACYW-TT que dans celui ayant reçu le vaccin Men-P-ACYW-135. Par ailleurs, plus de 82,8 % de ceux ayant reçu le vaccin Men-C-ACYW-TT présentaient encore des titres ≥ 1:8 pour tous les sérogroupes à l'année 4.
Dans la seule étude comportant des données sur les ABSh, Baxter et al.Note de bas de page 44 ont comparé la persistance de la réponse immunitaire chez 403 adolescents et jeunes adultes de 11 à 25 ans à la suite d'une immunisation à l'aide des vaccins Men-C-ACYW-TT et Men-C-ACYW-DT. Trois ans après la vaccination, la proportion des sujets du groupe Men-C-ACYW-TT qui présentaient des titres d'ABSh > 1:8 était légèrement supérieure pour les sérogroupes C et W-135, tandis que les valeurs de TMG étaient significativement plus élevées pour tous les sérogroupes sauf le sérogroupe A.
À la lumière des données existantes, le vaccin Men-C-ACYW-TT semble conférer une plus longue persistance immunitaire que les vaccins non conjugués, et n'est pas inférieur aux vaccins conjugués contre le méningocoque jusqu'à quatre ans après l'immunisation. Au moment de l'examen documentaire, il n'existait aucun article évalué par les pairs sur l'administration de doses de rappel à des sujets de plus d'un an. Aucune étude ne compare directement les trois vaccins conjugués quadrivalents contre le méningocoque, et MenveoMC n'a pas été comparé directement à NimenrixMC.
IV.3.2 Immunogénicité de MenactraMD
Pina et al.Note de bas de page 39 ont relevé des données sur l'immunogénicité après l'administration de MenactraMD à des nourrissons et des tout-petits âgés de 9 et de 12 mois, respectivement, dans deux études (A et B). Le vaccin a été administré à des sujets de 12 mois en deux doses sans autre vaccin ou bien avec un ou plusieurs autres vaccins homologués pour enfants (vaccin contre la rougeole, la rubéole, les oreilles et la varicelle [RORV], vaccin Haemophilus influenzae de type b [Hib], vaccin conjugué contre le pneumocoque [Pneu-C-7] et vaccin contre l'hépatite A). Dans toutes les études, la source de complément était le sérum humain (ABSh), et le principal paramètre d'immunogénicité était le pourcentage de participants qui présentaient un titre > 1:8, 30 jours après l'administration de la seconde dose.
L'immunogénicité a été évaluée chez 724 enfants. Après l'administration des deux doses du vaccin Men-C-ACYW-DT dans le cadre de l'étude A, le pourcentage d'enfants qui présentaient des titres d'ABSh ≥ 1:8 variait de 90,5 % à 100 % pour les sérogroupes A, C et Y, et de 81,2 % à 88,2 % pour le sérogroupe W-135. Dans le cas de l'administration du vaccin Men-C-ACYW-DT en association avec le vaccin RORV et le vaccin Pneu-C-7, l'immunogénicité n'était pas inférieure à celle observée pour l'administration du vaccin Men-C-ACYW-DT seul (la limite supérieure de l'intervalle de confiance [IC] à 95 % de la différence était < 10 %) pour tous les sérogroupes à l'exception du sérogroupe W-135 lorsque le vaccin Men-C-ACYW-DT était administré en même temps que la quatrième dose du vaccin Pneu-C-7. Dans l'étude B, les réponses aux antigènes des vaccins RORV et Hib étaient similaires, que les vaccins RORV et Hib aient été administrés seuls ou en association avec le vaccin Men-C-ACYW-DT. Dans le cas du vaccin Pneu-C-7, la non-infériorité statistique n'a pas été démontrée pour les sérotypes 4, 6B et 18C (la limite supérieure de l'IC à 95 % pour le rapport d'anticorps antipneumococciques était > 2) lorsqu'il était administré avec le vaccin Men-C-ACYW-DT. Toutefois, plus de 98 % des participants ont obtenu des titres ≥ 1:8 à l'essai multiplex d'opsonophagocytose du pneumocoque et une concentration d'anticorps ≥ 35 µg/mL selon le test ELISA pour tous les sérotypes. Avec un titre d'ABSh ≥ 1:4, une séroprotection a été observée chez plus de 91 % de ceux qui ont reçu le vaccin Men-C-ACYW-DT.
Sur une affiche présentée à la réunion de 2013 de l'European Society for Paediatric Infectious Diseases, Noya et al.Note de bas de page 40 faisait état d'un ECR et mené auprès de 122 enfants ayant reçu le vaccin Men-C-ACYW-DT ou un vaccin conjugué contre le méningocoque de sérogroupe C. Les titres d'ABSl à la suite de l'administration de deux doses ont été mesurés pour 55 enfants âgés de 18 ou de 19 mois. Un mois après la seconde dose (âgé de 19 mois), plus de 96 % de ceux qui avaient reçu le vaccin MenACYW-DT présentaient des titres d'ABSl ≥ 1:8 pour tous les sérogroupes (≥ 96 %).
IV.4 Administration du vaccin et calendrier de vaccination
Calendrier : L'utilisation de NimenrixMC a été approuvée chez les personnes de 12 mois à 55 ans.
Posologie : 0,5 mL du vaccin reconstitué doit être administré.
Voie d'administration : Injection intramusculaire. L'injection peut se faire dans le muscle deltoïde ou, pour les enfants âgés de 12 à 23 mois, dans la partie antérolatérale de la cuisse.
Doses de rappel : Le fabricant n'a pas encore établi la nécessité d'administrer une dose de rappel; toutefois, le CCNI recommande des doses de rappel périodiques pour les personnes à risque élevé de MI ou dont le risque d'exposition continue est élevé.
IV.5 Conditions d'entreposage
Conformément à la monographie de produit, NimenrixMC doit être conservé au réfrigérateur à une température de 2 ˚C à 8 ˚C. Le diluant peut être conservé à la température ambiante (25 ˚C). Ce produit ne doit pas être congelé et doit être à l'abri de la lumière.
IV.6 Administration simultanée avec d'autres vaccins
Le vaccin Men-C-ACYW-TT a été administré de façon simultanée avec un vaccin conjugué contre le pneumocoque 10-valent, un vaccin hexavalent pour nourrissons, un vaccin RORV, un vaccin contre la grippe saisonnière et un vaccin combiné contre l'hépatite A et l'hépatite B.
Dans une étude menée par Ruiz-Palacios et al.Note de bas de page 21, des nourrissons âgés de 12 à 23 mois ont reçu le vaccin Men-C-ACYW-TT et le vaccin Pneu-C-10. Une immunogénicité comparable a été démontrée lorsque ces produits étaient administrés de façon concomitante, à l'exception d'une réponse réduite pour le sérotype pneumococcique 18C, qui est conjugué à l'AT. Ces résultats semblent indiquer une interférence potentielle qui nécessite une recherche approfondie. Le vaccin Pneu-C-10 est homologué au Canada, mais à l'heure actuelle la totalité des provinces/territoires utilisent le vaccin Pneu-C-13.
Knuf et al.Note de bas de page 22 se sont penchés sur l'administration du vaccin Men-C-ACYW-TT en association avec DCaT-VHB-VIP/Hib. Des volets supplémentaires de l'étude comprenaient des patients qui ont reçu les deux vaccins à un mois d'intervalle et un groupe témoin qui a seulement reçu le vaccin Men-C-CRM197. Cette étude a révélé que l'administration séparée des vaccins Men-C-ACYW-TT et DCaT-VHB-VIP/Hib et leur administration en association donnaient des résultats similaires quant au profil d'innocuité et à la réponse immunitaire mesurée par les titres d'ABSl. Toutefois, les TMG d'ABSl pour les sérogroupes A, C et W-135 étaient significativement plus faibles dans le groupe ayant reçu le vaccin Men-C-ACYW-TT un mois après DCaT-VHB-VIP/Hib que dans celui ayant reçu le vaccin Men-C-ACYW-TT en premier. Ce résultat devrait avoir une signification clinique limitée, car plus de 97,3 % de ces sujets présentaient des titres d'ABSl ≥ 1:8.
Dans une étude finnoise réalisée par Vesikari et al.,Note de bas de page 20 on a administré le vaccin Men-C-ACYW-TT en association avec le vaccin RORV à des enfants âgés de 12 à 23 mois. Les groupes de comparaison étaient les suivants : vaccin Men-C-ACYW-TT seul, vaccin RORV seul et vaccin Men-C-CRM197 seul. Selon cette étude, l'administration concomitante de RORV et de Men-C-ACYW-TT entraînait des réponses immunitaires semblables à celles du vaccin RORV administré seul, sauf dans le cas de la rubéole pour laquelle les valeurs de TMG étaient plus faibles un mois après la vaccination dans le groupe à qui on a administré les vaccins en association. Toutefois, les enfants des deux groupes ont atteint le seuil de protection immunitaire de > 4 UI/mL. Le groupe Men-C-ACYW-TT + RORV et les groupes Men-C-ACYW-TT ont obtenu une réponse immunitaire similaire pour tous les sérogroupes du méningocoque. Un mois après la vaccination, les valeurs de TMG d'ABSl étaient plus élevées pour le sérogroupe C dans les deux groupes ayant reçu le Men-C-ACYW-TT que dans le groupe Men-C-CRM197. Cette information, fondée sur une étude, porte à croire que l'administration concomitante de ces deux vaccins est possible. Il faut toutefois garder à l'esprit que les TMG peuvent être plus faibles pour la rubéole.
Une étude menée par Østergaard et al.Note de bas de page 27 a porté sur l'administration du vaccin Men-C-ACYW-TT avec ceux contre les hépatites A et B à des adolescents. Elle a démontré que l'administration concomitante n'était pas inférieure sur le plan de l'immunogénicité et de l'innocuité.
Reyes et al.Note de bas de page 41 se sont penchés sur l'administration concomitante du vaccin Men-C-ACYW-TT et d'un vaccin antigrippal saisonnier sans adjuvant à des adultes de 18 à 55 ans. La non-infériorité a été démontrée en ce qui a trait aux rapports prédéfinis des TMG d'ABSl pour tous les sérogroupes à l'exception du sérogroupe C (le dépassement n'était que marginal, mais suffisant pour que le critère de non-infériorité ne soit pas respecté). Toutefois, plus de 99 % des sujets des deux groupes ont atteint des titres d'ABSl ≥ 1:8 pour tous les sérogroupes après la vaccination. Le profil d'innocuité était semblable pour l'administration individuelle et l'administration simultanée.
Le CCNI a passé en revue les données disponibles sur l'administration simultanée de Men-C-ACYW-TT avec les produits mentionnés. La monographie de produit, fournie par le fabricant, recommande son administration simultanée avec d'autres produits vaccinaux (vaccins contre l'hépatite A et l'hépatite B, vaccin ROR). Or, on ne dispose pas d'études cliniques portant sur l'administration simultanée de ces produits avec Men-C-ACYW-TT. Toutefois, selon l'avis d'experts, l'administration simultanée de Men-C-ACYW-TT avec des produits contenant un seul antigène ou moins d'antigènes que les produits cités dans les études déjà mentionnées ne devrait porter atteinte ni à l'innocuité ni à l'efficacité d'un produit ou de l'autre.
IV.7 Effets indésirables
IV.7.1 Innocuité de NimenrixMC
Innocuité de NimenrixMC chez les enfants de moins de 12 mois
Les deux profils d'innocuité dont ont fait état Klein et al.Note de bas de page 18 pour un groupe de 160 nourrissons ayant reçu le vaccin Men-C-ACYW-TT à l'âge de 9 mois étaient semblables à celui observé après l'administration du vaccin à des sujets de 12 mois.
Innocuité de NimenrixMC chez les enfants de 12 à 23 mois
L'innocuité du vaccin Men-C-ACYW-TT pour ce groupe d'âge a fait l'objet de quatre études. Dans le cadre d'un ECR mené auprès de 304 tout-petits en santé, Vesikari et al.Note de bas de page 19 ont signalé une réactogénicité et des profils d'innocuité similaires pour les vaccins Men-C-ACYW-TT et Men-C-CRM197. Des symptômes non sollicités ont été signalés par environ la moitié des participants, le plus fréquent étant la rhinite dans le groupe Men-C-ACYW-TT (8,3 %) et une pyrexie dans le groupe Men-C-CRM197 (13,3 %). Des symptômes locaux et généraux sollicités d'une intensité de catégorie 3 ont été signalés chez plus de 3,5 % des nourrissons dans les deux groupes, mais aucun effet indésirable grave qui semblait être lié à la vaccination n'a été rapporté. Par intensité de catégorie 3, on entend une rougeur et un œdème de plus de 30 mm de diamètre, des pleurs causés par le mouvement spontané d'un membre, une perte d'appétit allant jusqu'à l'absence d'alimentation, une fièvre de plus de 39,5 oC ou tout autre symptôme qui interfère avec les activités normales. Un autre ECR effectué par Vesikari et al.Note de bas de page 20 auprès de 749 tout-petits a donné des résultats similaires quant à l'innocuité pour le groupe ayant reçu seulement le vaccin Men-C-ACYW-TT.
Dans une étude menée par Ruiz-Palacios et al.Note de bas de page 21 auprès de 343 tout-petits ayant reçu de façon aléatoire le vaccin Pneu-C-10 ou le vaccin Men-C-ACYW-TT, la douleur au site d'injection et l'irritabilité étaient les symptômes sollicités les plus fréquents. Des symptômes d'une intensité de catégorie 3 ont été signalés chez moins de 2,2 % des tout-petits.
Selon l'étude de Klein et al.Note de bas de page 18 qui comparait l'innocuité d'une dose et deux doses du vaccin Men-C-ACYW-TT, le pourcentage de sujets qui présentaient des symptômes augmentait avec la fièvre et la perte d'appétit dans le groupe à 2 doses. Un pourcentage plus élevé de visites au service des urgences ainsi que de cas d'asthme et d'éruption cutanée a également été noté chez ceux ayant reçu deux doses.
Innocuité de NimenrixMC chez les enfants de 2 à 10 ans
Trois études ont été réalisées dans le but d'évaluer l'innocuité de NimenrixMC chez les enfants de 2 à 10 ans. Dans l'étude menée par Memish et al.Note de bas de page 23 auprès de 1 125 enfants, les profils d'innocuité étaient similaires pour les vaccins Men-C-ACYW-TT et Men-P-ACYW-135, des symptômes généraux sollicités et non sollicités de catégorie 3 ayant été observés chez moins de 1 % des sujets dans les deux groupes de traitement. Aucun effet indésirable grave attribuable à la vaccination n'a été observé dans cette étude. Dans l'ECR réalisé par Knuf et al.Note de bas de page 25 auprès de 414 enfants, on a observé moins d'effets indésirables de catégorie 3 chez les participants ayant reçu le vaccin Men-C-ACYW-TT (6,8 % des participants) que chez ceux ayant reçu le vaccin Men-C-CRM197 (15,1 %). Moins d'effets indésirables généraux de catégorie 3 ont été notés dans les deux groupes de cette étude. Parmi les 309 enfants visés par l'étude de Vesikari et al.Note de bas de page 24, l'effet indésirable le plus fréquent était la douleur au site d'injection (45,1 % pour le vaccin Men-C-ACYW-TT par rapport à 71,8 % pour le vaccin Men-P-ACYW-135). Des effets indésirables non sollicités de catégorie 3 se sont manifestés chez 6,5 % des personnes ayant reçu le vaccin Men-C-ACYW-TT par rapport à 5,1 % des personnes ayant reçu le vaccin Men-P-ACYW-135. Selon les chercheurs, un seul symptôme de catégorie 3 était associé à l'immunisation, soit un hématome observé chez un enfant ayant reçu le vaccin Men-C-ACYW-TT.
Innocuité de NimenrixMC chez les personnes de 11 à 17 ans
Dans l'étude menée par Østergaard et al.,Note de bas de page 12 auprès de seulement 50 personnes, l'effet indésirable le plus fréquent était la douleur pour la moitié des receveurs de Men-C-ACYW-TT et les maux de tête pour le tiers d'entre eux. Dans l'étude réalisée par Bermal et al.Note de bas de page 31 afin de comparer l'innocuité des vaccins Men-C-ACYW-TT et Men-P-ACYW-135 auprès de 1 025 sujets de 10 à 18 ans, des symptômes généraux de catégorie 3 ont respectivement été signalés par 1,6 % par rapport à 0,4 % des sujets vaccinés. L'effet indésirable le plus fréquent était la douleur au site d'injection (26,2 % par rapport à 26,8 %). Parmi les autres effets indésirables locaux, la rougeur au site d'injection a été signalée par 12,3 % par rapport à 9,6 % des sujets, respectivement (p = 0,0075). Il s'agissait du seul incident significatif sur le plan statistique. Parmi les symptômes généraux, la fatigue et les maux de tête étaient les plus fréquemment signalés (jusqu'à 14,3 % et 13,4 %, respectivement). Les différences entre les vaccins sur le plan des symptômes n'étaient pas statistiquement significatives. Aucun effet indésirable grave n'a été associé à l'administration de l'un ou l'autre des vaccins.
Innocuité de NimenrixMC chez les personnes de 18 à 55 ans
Trois études portaient sur l'innocuité du vaccin Men-C-ACYW-TT dans ce groupe d'âge. Selon Dbaibo et al.,Note de bas de page 34 la douleur et une rougeur au site d'injection (19,5 % [16,9 % à 22,1 %] et 13,5 % [9,9 % à 17,9 %]) étaient les effets indésirables les plus fréquents. Des symptômes généraux de catégorie 3 ont été signalés dans de rares cas (moins de 2 % des participants à l'étude), le plus fréquent étant les maux de tête. Les chercheurs estiment que seulement deux effets indésirables graves observés chez un sujet (0,6 %) étaient liés à la vaccination, soit une douleur abdominale et une gastrite 5 jours après la vaccination. Aucune apparition de maladie chronique n'a été signalée.
Dans une analyse groupée effectuée par Bermal et al.,Note de bas de page 31 qui consistait à comparer Men-C-ACYW-TT avec Men-P-ACYW, l'objectif principal prédéfini (non-infériorité sur le plan des symptômes sollicités et non sollicités de catégorie 3 dans un délai de 4 jours après la vaccination) n'a pas été atteint. Cela peut s'expliquer du fait d'une piètre estimation de l'incidence d'effets indésirables de catégorie III – la taille de l'échantillon s'est donc révélée inadéquate. Une analyse plus approfondie n'a pas permis de dégager des différences significatives quant au pourcentage de sujets manifestant l'un des symptômes généraux. Bien que cette étude ne comportait pas d'analyse distincte des sujets de 18 à 55 ans, il n'y avait pas de différence significative entre les taux de l'un ou l'autre des symptômes sollicités dans les cohortes de sujets de 11 à 17 ans et de 18 à 55 ans ni chez les receveurs de Men-C-ACYW-TT, ni chez les receveurs de Men-P-ACYW.
Les résultats de l'étude de Borja-TaboraNote de bas de page 35 étaient très semblables à ceux indiqués ci-dessus. Des symptômes généraux de catégorie 3 ont été signalés chez 1,3 % des participants ayant reçu le vaccin Men-C-ACYW-TT, mais chez aucun de ceux ayant reçu le vaccin Men-P-ACYW-135. Les symptômes les plus fréquents étaient de la douleur au site d'injection et des maux de tête. Les profils d'innocuité étaient comparables pour les deux vaccins, mais la rougeur et un œdème au site d'injection étaient plus fréquents chez les sujets ayant reçu le vaccin Men-C-ACYW-TT. Dans le cadre de la phase de suivi de six mois, un cas d'apparition de maladie chronique (allergie alimentaire) et deux effets indésirables graves (costochondrite et trouble mental) ont été signalés. Toutefois, les chercheurs jugent qu'ils ne sont pas liés à la vaccination.
Innocuité de NimenrixMC chez les personnes de plus de 55 ans
Dans l'étude menée par Dbaibo et al.,Note de bas de page 36 moins de 3,0 % des sujets ont signalé des effets indésirables et, selon les chercheurs, aucun effet indésirable grave n'était lié au vaccin.
Dans l'ensemble, peu d'effets indésirables ont été signalés dans les études disponibles, et la plupart d'entre eux étaient une douleur, une rougeur et un œdème localisés. Parmi les autres effets indésirables signalés, mentionnons l'irritabilité, la somnolence, les maux de tête, la perte d'appétit, la fatigue, des symptômes gastro-intestinaux et la fièvre. Aucun cas de purpura thrombocytopénique idiopathique, de syndrome de Guillain-Barré (SGB), de syndrome néphrotique ou de névrite brachiale n'a été signalé. Par comparaison avec les vaccins témoins, les effets indésirables étaient plus fréquents, bien que non pertinents sur le plan clinique, dans les groupes ayant reçu le vaccin Men-C-ACYW-TT. Ce résultat est probablement attribuable à la présence d'AT dans le vaccin, un composant qui est plus réactogène que d'autres supports protéiques.
IV.7.2 Innocuité de MenactraMD
Pina et al.Note de bas de page 39 ont regroupé des données sur l'innocuité provenant de trois études (A, B et C) menées auprès de nourrissons et de tout-petits âgés de 9 et 12 mois. Le vaccin Men-C-ACYW-DT a été administré une première fois à des sujets de 9 mois et une seconde fois, 3 mois plus tard, seul ou avec un ou plusieurs vaccins homologués (RORV, Hib, Pneu-C-7, hépatitis A) pour enfants. Les paramètres d'innocuité étudiés comprenaient les effets indésirables sollicités et non sollicités chez plus de 3 000 enfants jusqu'à 6 mois après la dernière vaccination.
La majorité des réactions sollicitées au site d'injection étaient similaires pour tous les groupes de l'étude et comprenaient de la sensibilité, un érythème et un œdème de catégorie 1. L'irritabilité était l'effet indésirable le plus souvent signalé. Des pleurs anormaux et de la somnolence ont été observés chez environ un tiers ou la moitié des participants. Des effets indésirables non sollicités ont été notés chez 40 à 50 % des enfants, mais ils étaient principalement de catégorie 1 ou 2 sur le plan de l'intensité et comparables dans l'ensemble des groupes. La fièvre a été plus fréquemment signalée chez les sujets à qui le vaccin Men-C-ACYW-DT était administré en association avec les vaccins RORV et Pneu-C-7 (20,7 % à 24,5 %) que chez ceux à qui il était administré seul (12,4 % à 13,7 %). Les taux de fièvre de catégorie 3 étaient similaires pour tous les groupes. Les effets indésirables graves étaient rares.
IV.8 Contre-indications et précautions
Conformément à la monographie de produit, NimenrixMC ne devrait pas être administré à des patients présentant une hypersensibilité connue à l'un des composants du vaccin.
IV.9 Autres considérations
Dans une étude réalisée par Dbaibo et al.Note de bas de page 42 auprès de 271 sujets, la réponse immunitaire à la suite de l'administration du vaccin Men-C-ACYW-TT a été évaluée chez des sujets de 4,5 à 34 ans qui avaient reçu le vaccin Men-P-ACYW-135 de 30 à 42 mois plus tôt; un autre groupe de témoins (qui n'avaient pas reçu le vaccin Men-P-ACYW-135 au cours des 10 dernières années) a également été recruté. Un mois après la vaccination, tous les participants à l'étude ont atteint des titres d'ABSl > 1:8 pour les quatre sérogroupes. Toutefois, les valeurs de TMG d'ABSl ainsi que les taux de réponse au vaccin étaient significativement plus élevés pour tous les sérogroupes chez ceux qui n'avaient pas reçu le vaccin Men-P-ACYW-135 antérieurement, ce qui indique une meilleure réponse immunitaire chez les sujets n'ayant jamais reçu un vaccin polysaccharidique. Dans le cadre de l'évaluation de l'innocuité, des symptômes de catégorie 3 ont été observés chez 11,5 % des sujets du groupe ayant reçu les vaccins Men-P-ACYW-135 et Men-C-ACYW-TT contre 3,8 % pour le groupe ayant seulement reçu le vaccin Men-P-ACYW-135 et Men-C-ACYW-TT. De la douleur, de la fièvre, des maux de tête et de la fatigue ont été signalés plus fréquemment dans le groupe ayant reçu les vaccins Men-P-ACYW-135 et Men-C-ACYW-TT (p < 0,05).
Knuf et al.Note de bas de page 37 ont évalué l'induction d'une mémoire immunitaire avec l'administration d'une dose d'amorce du vaccin Men-P-ACYW-135 (1/5 de la dose normale) à des enfants ayant subi une première immunisation au moyen du vaccin Men-C-ACYW-TT ou Men-C-CRM197 15 mois plus tôt. Un mois après l'administration du vaccin Men-P-ACYW-135, tous les participants à l'étude présentaient des titres d'ABSl > 1:8. Les valeurs de TMG d'ABSl étaient significativement plus élevées pour les sérogroupes A, W-135 et Y chez ceux ayant reçu le vaccin Men-C-ACYW-TT par rapport à ceux ayant reçu le vaccin Men-C-CRM197 et étaient comparables pour le sérogroupe C dans les deux groupes, ce qui semble indiquer que l'induction d'une mémoire immunitaire était similaire pour les deux vaccins. Les profils d'innocuité après l'administration du vaccin Men-P-ACYW-135 étaient similaires dans les deux groupes.
V. Recommandations
Veuillez noter que les provinces et les territoires doivent tenir compte des facteurs économiques et d'autres facteurs programmatiques/opérationnels locaux lorsqu'ils envisagent d'inclure les recommandations suivantes aux programmes d'immunisation subventionnés par l'État.
Recommandation no 1
Tout vaccin conjugué quadrivalent contre le méningocoque ou vaccin conjugué monovalent contre le méningocoque du groupe C peut être utilisé pour l'immunisation systématique des adolescents s'il est homologué au Canada. Le choix entre le vaccin conjugué quadrivalent ou monovalent (tous deux visant le groupe C) dépend de l'épidémiologie locale et d'autres considérations programmatiques. (Recommandation du CCNI de catégorie B)
Recommandation no 2
Tout vaccin conjugué quadrivalent contre le méningocoque peut être utilisé pour l'immunisation des personnes à risque élevé de deux ans ou plus s'il est homologué au Canada. (Recommandation du CCNI de catégorie B)
Recommandation no 3
Le vaccin Men-C-ACYW-CRM (MenveoMC) est le produit recommandé pour l'immunisation des personnes à risque élevé âgées de deux mois à moins de deux ans. On trouvera les calendriers pertinents au tableau 3 du chapitre sur le méningocoque du Guide canadien d'immunisation. (Recommandation du CCNI de catégorie B)
Recommandation no 4
N'importe quel vaccin conjugué quadrivalent contre le méningocoque peut être utilisé pour l'immunisation des personnes de 2 ans ou plus qui voyagent dans des régions où un vaccin contre le méningocoque est recommandé. (Recommandation du CCNI de catégorie B)
Men-C-ACYW-CRM (MenveoMC) est le vaccin recommandé chez les voyageurs de 2 mois à moins de 2 ans qui se rendent dans des régions où le vaccin contre le méningocoque est recommandé. À ce sujet, voir le tableau 1 du chapitre sur le méningocoque du Guide canadien d'immunisation.
Certains pays pourraient exiger l'authentification du vaccin contre le méningocoque. Par exemple, l'Arabie Saoudite exige une telle preuve pour les pèlerins participant au Hadj à La Mecque. Veuillez consulter les recommandations et exigences annuelles relatives au Hadj, publiées par l'Agence, pour vous assurer que tous les voyageurs concernés disposent de la documentation pertinente. De plus, on pourra trouver de l'information à jour concernant les pays aux prises avec des flambées de méningococcie sur l'un des sites de l'Organisation mondiale de la Santé.
Pour des recommandations supplémentaires à l'intention des voyageurs, veuillez consulter le site voyage.gc.ca, ainsi que la Déclaration sur la vaccination des voyageurs contre le méningocoque du Comité consultatif de la médecine tropicale et de la médecine des voyages.
VI. Priorités en matière de recherche
Il est recommandé de poursuivre la recherche afin d'éclaircir les points suivants :
- Durée de projection et d'innocuité de façon à permettre l'évaluation des recommandations relatives aux doses de rappel d'un vaccin quadrivalent.
- Étude comparative des trois vaccins conjugués quadrivalents sur le marché.
- Utilité, efficacité, immunogénicité et innocuité des vaccins quadrivalents dans les groupes à risque élevé, notamment les personnes splénectomisées.
- Immunogénicité et innocuité liées à l'administration concomitante de vaccins quadrivalents, de vaccins administrés systématiquement selon l'âge, y compris le vaccin contre le méningocoque B nouvellement autorisé.
VII. Questions liées à la surveillance
Il serait préférable de réaliser de la surveillance pour répondre aux questions en suspens suivantes :
- Incidence des programmes de vaccination contre le méningocoque sur l'épidémiologie de la MI au Canada.
- Couverture vaccinale de chacun des vaccins quadrivalents contre le méningocoque et incidence sur le portage et l'immunité collective.
- La survenue possible du remplacement de sérogroupe.
- Une détérioration possible de la niche écologique du méningocoque, ce qui permettrait à d'autres bactéries de remplacer ce dernier à mesure que décroît le portage de cet organisme.
- L'incidence sur la rubéole et la pneumococcie invasive à la suite de l'administration concomitante de NimenrixMC et d'un vaccin conjugué contre le pneumocoque ainsi que du vaccin ROR à des nourrissons.
Tableaux
| Niveau | Description |
|---|---|
| I | Données probantes provenant d'un ou de plusieurs essais cliniques comparatifs randomisés |
| II-1 | Données probantes provenant d'essais contrôlés sans randomisation. |
| II-2 | Données probantes provenant d'études de cohortes ou d'études analytiques cas-témoins, réalisées de préférence dans plus d'un centre ou groupe de recherche avec des mesures des résultats cliniques de l'efficacité des vaccins. |
| II-3 | Données probantes obtenues à partir de plusieurs séries chronologiques avec ou sans intervention. Les résultats spectaculaires d'expériences non comparatives (comme les résultats de l'introduction des traitements à la pénicilline dans les années 1940) peuvent également être considérés à titre de données probantes. |
| III | Opinions d'autorités respectées fondées sur des expériences cliniques, études descriptives et rapports de cas ou rapports de comités d'experts. |
| Cote de qualité | Description |
|---|---|
| Bonne | Une étude (comprenant les méta-analyses ou les examens systématiques) qui répond bien à tous les critères relatifs à la conceptionNote de bas de tableau 4 - *. |
| Passable | Une étude (comprenant les méta-analyses ou les examens systématiques) qui ne répond pas (ou ne répond pas clairement) à au moins un des critères relatifs à la conceptionNote de bas de tableau 4 - *, mais ne comporte aucune « lacune fatale ». |
| Médiocre | Une étude (comprenant les méta-analyses ou les examens systématiques) qui comporte au moins une « lacune fatale » relative à la conceptionNote de bas de tableau 4 - * ou une accumulation de lacunes moins importantes faisant en sorte que les résultats de l'étude sont jugés inadéquats en vue de l'élaboration des recommandations. |
|
|
| Catégorie | Recommandation |
|---|---|
| A | Le CCNI a conclu qu'il existait des données probantes suffisantes pour recommander l'immunisation |
| B | Le CCNI a conclu qu'il existait des données probantes acceptables pour recommander l'immunisation |
| C | Le CCNI a conclu qu'il existait des données probantes contradictoires qui ne permettent pas de faire une recommandation pour ou contre l'immunisation; cependant, d'autres facteurs peuvent influer sur la prise de décision |
| D | Le CCNI a conclu qu'il existait des données probantes acceptables pour déconseiller l'immunisation |
| E | Le CCNI a conclu qu'il existait des données probantes suffisantes pour déconseiller l'immunisation |
| I | Le CCNI a conclu qu'il existait des données probantes insuffisantes (en quantité ou en qualité) pour formuler une recommandation; cependant, d'autres facteurs peuvent influer sur la prise de décisions |
| Données probantes pour l'administration du vaccin conjugué après la réception du vaccin polysaccharidique | ||||||
|---|---|---|---|---|---|---|
| Détails des études | Sommaire | |||||
| Étude | Vaccin | Plan de l'étude | Participants | Résumé des principales conclusions | Niveau de données probantes | Qualité |
Dbaibo, G., et al., |
Men-C-ACWY-TT |
Essai comparatif ouvert Liban (prolongation de l'étude Men-P-ACYW menée en 2005) |
N = 271 personnes réparties en deux groupes en fonction de la réception de Men-P-ACYW dans les 30 à 42 mois précédant l'étude (groupes avec et sans Men-P-ACYW). Tous les sujets ont reçu une dose de Men-C-ACWY-TT. |
Titre d'ABSl > 1:8 utilisé comme mesure de l'immunité. Tous les sujets dans tous les groupes ont atteint une séroprotection (titre d'ABSl > 1:8) pour l'ensemble des sérogroupes, un mois après la vaccination. Tous les sujets dans le groupe sans Men-P-ACYW ont atteint des titres d'ABSl ≥ 1:128 pour tous les sérogroupes; la proportion de sujets présentant des titres d'ABSl ≥ 1:128 dans le groupe avec Men-P-ACYW S allait de 97,0 % à 100 %. La réponse immunitaire était significativement différente entre les deux groupes et variait de 41,1 % à 83 % dans le groupe avec Men-P-ACYW et de 76,9 % à 97,3 % dans le groupe sans Le facteur d'augmentation des TMG des ABSl, avant et après l'administration du vaccin, allait de 3,9 à 30,1 dans le groupe avec Men-P-ACYW, et de 11,8 à 246 dans le groupe sans Men-P-ACYW; après la vaccination, les titres d'ABSl et les TMG étaient significativement plus faibles dans le groupe avec Men-P-ACYW que dans le groupe sans Men-P-ACYW pour tous les sérogroupes. La CMG d'anti-PS après la vaccination, ajustée en fonction de l'âge, était significativement plus élevée dans le groupe avec Men-P-ACYW comparativement au groupe sans Men-P-ACYW et ce, pour tous les sérogroupes sauf le sérogroupe A. La liste ci-dessous contient les titres d'ABSl pour les sérogroupes de la méningococcie (≥ 1:8) un mois après l'administration du vaccin Men-C-ACWY-TT : Aucune dose précédente de Men-P-ACYW (IC à 95 %) |
Niveau I |
Bonne |
| Données probantes sur l'immunogénicité de NimenrixMC chez les enfants de moins de 12 mois | ||||||
|---|---|---|---|---|---|---|
| Détails des études | Sommaire | |||||
| Étude | Vaccin | Plan de l'étude | Participants | Résumé des principales conclusions | Niveau de données probantes | Qualité |
Klein, N.P., et al., 2013Note de bas de page 18 |
Autre schéma posologique du vaccin MenACWY-TT |
Essai ouvert comparatif randomisé Phase II |
N = 349 bébés de 9 mois Groupe ACWY-1 : vaccin MenACWY-TT à l'âge de 12 mois. Groupe ACWY-2 : |
La séroprotection a été définie par un titre d'ABSh ≥ 1:4 ou des titres d'ABSl ≥ 1:8 pour tous les sérotypes. Après une première vaccination, un titre d'ABSl ≥ 1:8 a été obtenu chez tous les nourrissons pour tous les sérogroupes, sauf le sérogroupe C où un nourrisson n'a pas atteint le niveau de séroprotection prédéfini. Bien que la proportion des patients avec titres d'ABSl ≥ 1:8 soit comparable dans les groupes d'âge de 9 et de 12 mois (ayant reçu une dose du vaccin), la proportion avec un titre d'ABSh ≥ 1:8 était significativement plus élevée dans le groupe d'âge de 12 mois (une dose de vaccin) pour tous les sérogroupes, sauf le sérogroupe C. De même, les titres moyens géométriques (TMG) d'ABSh étaient significativement plus élevés après une seule dose à 12 mois qu'à 9 mois pour tous les sérogroupes, sauf le sérogroupe A. L'étude ne comportait pas de vaccin de comparaison, car aucun vaccin contre le méningocoque n'était homologué pour ce groupe d'âge au moment de l'étude. La liste ci-dessous contient les % des titres d'ABSh ≥ 1:4 [IC de 95 %] pour tous les sérotypes, 1 mois après la vaccination avec une dose (ACWY-1) ou deux doses (ACWY-2). |
Niveau 1 |
Bonne |
| Données probantes sur l'innocuité de NimenrixMC chez les enfants de moins de 12 mois | ||||||
|---|---|---|---|---|---|---|
| Détails des études | Sommaire | |||||
| Étude | Vaccin | Plan de l'étude | Participants | Résumé des principales conclusions | Niveau de données probantes | Qualité |
Klein, N.P., et al., 2013Note de bas de page 18 |
Autre schéma posologique du vaccin MenACWY-TT |
Essai ouvert comparatif randomisé Phase II |
N = 349 bébés de 9 mois Groupe ACWY-1 : vaccin MenACWY-TT à l'âge de 12 mois. Groupe ACWY-2 : |
Après l'une ou l'autre dose, des symptômes sollicités (dans les 8 jours) d'une intensité de catégorie 3 ont été signalés par moins de 3,0 % des sujets. Fièvre signalée par 3,3 % des sujets vaccinés à l'âge de 9 mois et par 9,6 % et 10,8 % des sujets vaccinés à l'âge de 12 mois (groupes Men-ACWY-2 et Men-ACWY-1, respectivement). Aucune fièvre > 40 C n'a été signalée chez un enfant. La fièvre et la perte d'appétit ont été signalées plus souvent après la deuxième dose, par rapport à la première dose, dans le groupe Men-ACWY-2. Des EIG non sollicités (dans les six mois après la dernière dose) ont été déclarés par 3,1 % des sujets du groupe ACWY-1 et 1,1 % des sujets du groupe ACWY-2; aucun de ces effets n'a été considéré comme étant lié à la vaccination par les chercheurs. |
Niveau 1 |
Bonne |
| Données probantes sur l'immunogénicité de NimenrixMC chez les enfants de 12 à 23 mois | ||||||
|---|---|---|---|---|---|---|
| Détails des études | Sommaire | |||||
| Étude | Vaccin | Plan de l'étude | Participants | Résumé des principales conclusions | Niveau de données probantes | Qualité |
Knuf, M., et al., 2010Note de bas de page 13 |
NimenrixMC |
Essai comparatif à l'aveugle randomisé Sites multiple dans deux pays (Allemagne, Autriche) Phase II |
N = 240 enfants âgés de 12 à 14 mois |
Sommaire des résultats : Seules les données pour le groupe F3 du vaccin Men-ACWY-TT (de 12 à 14 mois) sont incluses, puisque c'est la seule formulation pertinente approuvée pour les tout-petits. La réponse immunitaire au vaccin a été définie par un titre d'ABSl ≥ 1:32 chez des sujets initialement séronégatifs et une augmentation des titres d'ABSl selon un facteur de ≥ 4 après la vaccination chez les sujets initialement séropositifs, 1 mois après la vaccination. Les taux de réponses aux vaccins pour le sérogroupe C chez les tout-petits étaient similaires dans chaque groupe Men- ACWY-TT (95,1 à 97,7 %) et le groupe témoin MenCCRM197 (91,1 %). Les taux de réponse pour le sérogroupe A et W-135 étaient > 95 % avec le vaccin Men-P-ACWY, et les taux de réponse pour le sérogroupe Y étaient de 87,5 %. Ces résultats dépassent significativement les taux de réponse au vaccin MenCCRM197 qui se situaient entre 9,7 et 13,6 % pour les sérogroupes A, W-135 et Y. Les titres étaient également évalués à ≥ 1:8 et ≥ 1:128. Les réponses de tous les sérogroupes au vaccin Men-P-ACWY (à l'exception du sérogroupe C) étaient significativement plus élevées que celles du groupe témoin ayant reçu le vaccin MenC-CRM197, pour les titres ≥ 1:8 et ≥ 1:128. Les pourcentages pour les titres d'ABSl ≥ 1:8 % [IC de 95 %] un mois après la vaccination sont énumérés ci-dessous : De 12 à 14 mois : Sérogroupe C : Sérogroupe W-135 : Sérogroupe Y : |
Niveau I |
Bonne |
Ruiz-Palacois, G.M., et al., 2013Note de bas de page 21 |
Vaccins MenACWY-TT et PHiD-CV |
Essai ouvert comparatif randomisé 2 centres au Mexique et 3 centres à Taïwan Phase IIIb |
N = 363 |
La séroprotection a été définie par un titre d'ABSl ≥ 1:8. Un mois après l'administration du vaccin MenACWY-TT, entre 97,5 % et 100 % des enfants affichaient des titres d'ABSl ≥ 128 pour chaque sérogroupe, et les TMG avaient augmenté entre la période précédant la vaccination et celle suivant la vaccination (augmentation selon un facteur allant de 75,4 à 439,1). La liste ci-dessous contient les résultats pour les sérotypes de vaccin méningocoque un mois après la vaccination contre le méningocoque : % d'ABSl ≥ 1:8 (IC à 95 %) Sérogroupe C Sérogroupe W-135 Sérogroupe Y TMG (IC à 95 %) Sérogroupe C Sérogroupe W-135 Sérogroupe Y |
Niveau I |
Bonne |
Knuf, M., et al., 2011Note de bas de page 22 |
MenACWY-TT et DCaT-VHB-VIP/Hib ou MenC (contre le méningo- |
Essai ouvert comparatif randomisé 72 centres en Autriche, en Allemagne et en Grèce Phase III |
N = 793 Enfants âgés de 12 à 23 mois |
La séroprotection a été définie par un titre d'ABSl ≥ 1:8. Les TMG des ABSl pour les sérogroupes A, C et W-135 étaient significativement plus faibles dans le groupe ayant reçu le vaccin Men-C-ACYW-TT un mois après DCaT-VHB-VIP/Hib que dans celui ayant reçu le vaccin Men-C-ACYW-TT en premier. La liste ci-dessous contient les % d'ABSl ≥ 1:8 (IC à 95 %) pour les sujets immunisés selon divers protocoles. Sérogroupe C Sérogroupe W-135 Sérogroupe Y TMG (IC à 95 %) Sérogroupe W-135 Sérogroupe Y |
Niveau I |
Bonne |
Vesikari, T., et al., 2011Note de bas de page 20 |
Administration conjointe |
Essai ouvert comparatif randomisé Phase III |
N = 1 000 enfants âgés de 12 à 23 mois |
La séroprotection a été définie par un titre d'ABSl ≥ 1:8. Non-infériorité démontrée pour Men-C-ACYW-TT par rapport au vaccin monovalent Men-C-CRM197. La liste ci-dessous contient les % d'ABSl ≥ 1:8 (IC à 95 %) pour chaque sérotype un mois après la vaccination. Sérotype A Sérotype C Sérotype W-135 Sérotype Y |
Niveau I |
Bonne |
| Données probantes sur l'innocuité de NimenrixMC chez les enfants de 12 à 23 mois | ||||||
|---|---|---|---|---|---|---|
| Détails des études | Sommaire | |||||
| Étude | Vaccin | Plan de l'étude | Participants | Résumé des principales conclusions | Niveau de données probantes | Qualité |
Vesikari, T., et al., 2012bNote de bas de page 19 |
MenACWY-TT |
Essai ouvert comparatif randomisé 11 centres en Finlande Phase II |
N = 304 enfants âgés de 12 à 23 mois |
Symptôme spontané de catégorie 3 si le vaccin est administré dans un membre. Douleur ou pleurs de l'enfant en bougeant le membre; rougeur et enflure au site d'injection si le diamètre > 30 mm; température rectale > 40,0 C; perte d'appétit ou refus de nourriture; pleurs de l'enfant et incapacité à le consoler; tout autre effet indésirable s'il empêche les activités normales. Les vaccins Men-ACYW-TT et Men-C-CRM ont donné des profils d'innocuité similaires, et aucun EIG semblant être causé par la vaccination n'a été rapporté pendant l'étude. Rougeurs au site d'injection le plus souvent mentionnées (dans les 4 jours suivant la vaccination) comme symptôme local sollicité dans les deux groupes (36,8 % et 32,9 % pour les vaccins Men-ACWY-TT et Men-C-CRM, respectivement). Irritabilité le plus souvent mentionnée comme symptôme général sollicité dans les deux groupes (38,6 % et 39,7 % pour les vaccins Men-ACWY-TT et Men-C-CRM, respectivement). Symptômes sollicités de catégorie 3 signalés chez moins de 3,5 % des enfants dans chaque groupe. Symptômes non sollicités (dans les 31 jours suivant la vaccination) signalés chez 52,8 % des enfants avec le vaccin MenACWY-TT et chez 50,7 % des enfants avec le vaccin MenC-CRM, dans un délai d'un mois après la vaccination; la rhinite a été le symptôme le plus fréquemment signalé (moins de 13,3 % dans les deux groupes). Des effets indésirables non sollicités d'une intensité de catégorie 3 ont été signalés pour 11,4 % des enfants avec le Men-ACWY-TT et pour 14,7 % des enfants dans le groupe ayant reçu le vaccin Men-PS. |
Niveau I |
Bonne |
Vesikari, T., et al., 2011Note de bas de page 20 |
Administration conjointe |
Essai ouvert comparatif randomisé Phase III |
N = 1 000 enfants âgés de 12 à 23 mois |
Symptôme spontané de catégorie 3 si le vaccin est administré dans un membre. Douleur ou pleurs de l'enfant en bougeant le membre; rougeur et enflure au site d'injection si le diamètre > 30 mm; température rectale > 40,0 °C; perte d'appétit ou refus de nourriture; pleurs de l'enfant et incapacité à le consoler; tout autre effet indésirable s'il empêche les activités normales. Rougeurs au site d'injection comme symptôme local le plus sollicité (dans un délai de 4 jours suivant la vaccination); symptômes locaux de catégorie 3 : groupe Men-ACWY-TT+RROV (4,1 %) et groupe Men-ACWY-TT (4,4 %). Symptômes généraux sollicités de catégorie 3 rarement signalés (moins de 1,6 % des sujets dans chaque groupe). Symptômes non sollicités (dans les 43 jours suivant la vaccination) signalés par 64,8 % des sujets du groupe Men-ACWY-TT+RROV, 60,2 % dans le groupe Men-ACWY-TT et 68,3 % dans le groupe RROV (30,7 %, 15,0 % et 28,6 %, respectivement, considérés comme liés à la vaccination). Irritabilité le plus souvent mentionnée comme symptôme sollicité et lié à la vaccination dans les groupes Men-ACWY-TT+RROV (8,8%) et RROV (7,9%). Aucun EIG non sollicité ne semblait être causé par la vaccination tout au long de l'étude. |
Niveau I |
Bonne |
Ruiz-Palacios, G.M., et al., 2013Note de bas de page 21 |
Vaccins MenACWY-TT et PHiD-CV |
Essai ouvert comparatif randomisé 2 centres au Mexique et 3 centres à Taïwan Phase IIIb |
N = 363 |
La douleur au point d'injection est le symptôme local sollicité le plus fréquemment signalé (dans un délai de 4 jours suivant la vaccination), chez 6,8 à 8,8 % des sujets du groupe PHiD-CV et 2,4 à 7,8 % des sujets du groupe Men-ACWY-TT, avec une intensité déclarée de catégorie 3. L'irritabilité est le symptôme général sollicité le plus courant, avec moins de 1,2 % des enfants dans les deux groupes signalant une intensité de catégorie 3 (chez un enfant du groupe Men-ACWY-TT, une fièvre ≥ 40,0 C a été signalée). Les symptômes non sollicités (dans un délai de 31 jours) après la première vaccination sont similaires entre les groupes (42,9 – 46,7 %); une intensité de catégorie 3 est signalée chez 6,0 % des sujets du groupe ayant reçu une administration conjointe du vaccin, et chez 2,2 % des sujets des groupes Men-ACWY-TT et PHiD-CV. Après la deuxième vaccination, des symptômes non sollicités ont été signalés chez 44,0 % et 34,4 % des enfants dans les groupes ayant reçu le vaccin MenACWY-TT et le vaccin PHiD-CV, respectivement; l'intensité des symptômes était de catégorie 3 chez 6,6 % des enfants du groupe Men-ACWY-TT et chez 3,3 % de ceux du groupe PHiD-CV. Aucun symptôme de catégorie 3 ne semblait être causé par la vaccination. Des EIG ont été signalés dans un délai d'un mois chez 2 enfants du groupe ayant reçu une vaccination conjointe, 3 du groupe Men-ACWY-TT et 1 du groupe PHiD-CV. Selon les chercheurs, aucun EIG n'était lié à la vaccination et tous les effets sont disparus sans séquelles. |
Niveau I |
Bonne |
Klein, N.P., et al., 2013Note de bas de page 18 |
Autre schéma posologique du vaccin MenACWY-TT |
Essai ouvert comparatif randomisé Phase II |
N = 349 bébés de 9 mois Groupe ACWY-1 : vaccin MenACWY-TT à l'âge de 12 mois. Groupe ACWY-2 : |
Après l'une ou l'autre dose, des symptômes sollicités (dans les 8 jours) d'une intensité de catégorie 3 ont été signalés par moins de 3,0 % des sujets. Fièvre signalée par 3,3 % des sujets vaccinés à l'âge de 9 mois et par 9,6 % et 10,8 % des sujets vaccinés à l'âge de 12 mois (groupes Men-ACWY-2 et Men-ACWY-1, respectivement). Aucune fièvre > 40 °C n'a été signalée chez un enfant. La fièvre et la perte d'appétit ont été signalées plus souvent après la deuxième dose, par rapport à la première dose, dans le groupe Men-ACWY-2. Des EIG non sollicités (dans les six mois après la dernière dose) ont été déclarés par 3,1 % des sujets du groupe ACWY-1 et 1,1 % des sujets du groupe ACWY-2; aucun de ces effets n'a été considéré comme étant lié à la vaccination par les chercheurs. |
Niveau 1 |
Bonne |
| Données probantes sur l'immunogénicité de NimenrixMC chez les enfants de 2 à 10 ans | ||||||
|---|---|---|---|---|---|---|
| Détails des études | Sommaire | |||||
| Étude | Vaccin | Plan de l'étude | Participants | Résumé des principales conclusions | Niveau de données probantes | Qualité |
Memish, Z.A., et al., 2011Note de bas de page 23 |
NimenrixMC (MenACWY-TT) comparé à Mencevax (Men-PS) |
Essai ouvert comparatif randomisé Arabie saoudite) |
N = 1 504 Les deux groupes ont reçu une dose du vaccin MenACWY-TT ou Men-PS. |
La séroprotection a été définie par un titre d'ABSl ≥ 1:8. La séroprotection était non inférieure dans le groupe Men-C-ACYW-TT, comparativement au groupe Men-P-ACYW-135. Les TMG étaient significativement plus élevés sur le plan statistique pour les quatre sérogroupes dans le groupe ayant reçu le vaccin Men-C-ACYW-TT. La séroréaction était aussi significativement plus élevée dans le groupe Men-C-ACYW-TT que dans le groupe Men-P-ACYW-135. Les niveaux d'ABSl sont énumérés ci-dessous pour les sérogroupes de la méningococcie (> 1:8) 1 mois après la vaccination : MenACWY-TT (IC à 95 %) Men-PS (IC à 95 %) TMG des ABSl : Men-PS (IC à 95 %) W-135 2 151 (1 824; 2 536) |
Niveau I |
Bonne |
Vesikari, T., et al., 2012aNote de bas de page 24 |
Vaccin MenACWY-TT comparé à MenACWY-PS |
Essai ouvert comparatif randomisé 11 centres en Finlande |
N = 309 enfants âgés de 2 à 5 ans Les deux groupes ont reçu le vaccin MenACWY-TT ou MenACYW-PS. |
La séroprotection a été définie par un titre d'ABSl ≥ 1:8. Un mois après la vaccination, les taux de séroréaction étaient d'au moins 94,3 % dans le groupe ACWY-TT et 81,2 % dans le groupe Men-PS. Le vaccin MenACWY-TT était non inférieur au vaccin MenACWY-PS. Selon l'analyse exploratoire, les TMG des ABSl étaient plus élevés chez les sujets ayant reçu le vaccin MenACWY-TT par rapport à MenACWY-PS pour les quatre sérotypes. La liste ci-dessous contient les titres d'ABSl ≥ 1:8 à 1 mois après la vaccination. MenACWY-TT (IC à 95 %) Men-PS (IC à 95 %) TMG des ABSl Men-PS (IC à 95 %) |
Niveau I |
Bonne |
Knuf, M., et al., 2013Note de bas de page 25 |
Vaccin MenACWY-TT comparé à |
Essai ouvert comparatif randomisé 31 centres dans deux pays (Allemagne et France) |
N = 414 enfants âgés de 2 à 5 ans Les deux groupes ont reçu le vaccin MenACWY-TT ou MenC-CRM197. |
La séroprotection a été définie par un titre d'ABSl ≥ 1:8. La réponse immunitaire au vaccin a été définie par un titre d'ABSl d'au moins 1:32 chez les enfants séronégatifs au départ (c.-à-d. un titre d'ABSl < 1:8) et une augmentation du titre selon un facteur de quatre, de la période précédant le vaccin à celle suivant le vaccin, chez les enfants initialement séropositifs (c.-à-d. un titre d'ABSl ≥ 1:8). Le vaccin MenACWY-TT ne s'est pas révélé inférieur au vaccin MenC-CRM197. Les taux de réponse immunitaire MenC-CRM197 TMG des ABSl MenC-CRM197 (IC à 95 %) |
Niveau I |
Bonne |
Baxter, R., et al., 2011Note de bas de page 26 |
MenACWY-TT comparé à MenACWY-DT |
Étude comparative randomisée avec groupes parallèles Phase II 10 centres aux États-Unis |
N = 827 sujets âgés de 10 à 25 ans (N = 587 MenACWY-TT; N = 197 MenACWY-DT; N = 88 MenACWY-TT/10 ans) |
Un titre de sérum ABSh ≥1:4 est considéré comme un facteur de protection contre la maladie causée par le sérogroupe C. La pratique courante consiste à appliquer le seuil de 1:4 seuil aux autres sérogroupes. La réponse immunitaire était similaire à l'exception de valeurs relativement élevées, mais non significatives sur le plan statistique, du TMG des ABSh-MenA dans le groupe d'âge de 10 ans. La liste ci-dessous contient les pourcentages des titres d'ABSh ≥ 1:4 [IC à 95 %] 1 mois après la vaccination pour chaque sérotype. Sérotype A Sérotype C Sérotype W-135 Sérotype Y |
Niveau II-1 |
Passable (faible taille de l'échanti-llon dans le groupe de 10 ans; aucun contrôle approprié) |
| Données probantes sur l'innocuité de NimenrixMC chez les enfants de 2 à 10 ans | ||||||
|---|---|---|---|---|---|---|
| Détails des études | Sommaire | |||||
| Étude | Vaccin | Plan de l'étude | Participants | Résumé des principales conclusions | Niveau de données probantes | Qualité |
Memish, Z.A., et al., 2011Note de bas de page 23 |
NimenrixMC (MenACWY-TT) comparé à Mencevax (Men-PS) |
Voir ci-dessus Les parents ont signalé des réactions locales et systématiques dans un délai de 4 jours après la vaccination. Des événements non sollicités survenus dans un délai de 31 jours ont également été consignés. Effets indésirables graves jusqu'à 6 mois après la vaccination |
N = 1 504 Les deux groupes ont reçu une dose du vaccin MenACWY-TT ou Men-PS. |
Les vaccins Men-C-ACYW-TT et Men-P-ACYW-135 ont donné des profils d'innocuité similaires, avec moins de 1 % de symptômes généraux sollicités et non sollicités de catégorie 3 dans les deux groupes de traitement. Il n'y a eu aucun EIG attribuable à la vaccination. Échantillonnage trop réduit pour atteindre l'objectif principal de non-infériorité de l'innocuité. Une comparaison exploratoire a démontré une incidence plus grande de douleur au site d'injection avec le vaccin Men-PS par rapport au vaccin MenACWY-TT chez les sujets ≥ 6 ans (p=0,0309). Aucun effet indésirable grave lié à l'injection, aucun décès. Fréquence des symptômes généraux de catégorie 3 : Enfants âgés de 2 à 5 ans : Enfants âgés de 6 à 10 ans : Effets indésirables graves : |
Niveau I |
Passable (échanti-llonnage trop réduit pour atteindre l'objectif principal de non-infériorité de l'innocuité) |
Vesikari, et al., 2012Note de bas de page 24 |
Vaccin MenACWY-TT comparé à Men-PS |
Essai ouvert comparatif randomisé 11 centres en Finlande |
N = 309 enfants âgés de 2 à 5 ans |
Dans les 4 jours suivant la vaccination, la douleur était le symptôme local sollicité le plus fréquent. Réaction locale la plus courante : douleur au site d'injection. Effets indésirables non sollicités de catégorie 3 (6,5 % par rapport à 5,1 % des enfants vaccinés). Un seul symptôme de catégorie 3 a été associé à la vaccination, soit un hématome observé chez un enfant ayant reçu le vaccin MenC-ACWY-TT. Événements sollicités : Événements non sollicités : Les EIG et les avis de conformité ont été consignés jusqu'à 6 mois après la vaccination. |
Niveau I |
Passable (La non-infériorité de l'innocuité n'a pas été évaluée.) |
Knuf, M., et al., 2013Note de bas de page 25 |
Vaccin MenACWY-TT comparé à |
Essai ouvert comparatif randomisé 31 centres dans deux pays (Allemagne et France) |
N = 414 enfants âgés de 2 à 5 ans |
La présence de symptômes locaux sollicités et de symptômes généraux sollicités a été consignée jusqu'à 4 jours après la vaccination. Des effets indésirables graves ont été signalés au cours des six mois suivant la vaccination. Chez les 6 à 10 ans, la fatigue était le symptôme général sollicité le plus fréquent (22,3 % pour ACWY-TT et 22,0 % pour MenC-CRM). Un moins grand nombre d'effets indésirables de catégorie 3 ont été observés chez les participants qui avaient reçu le vaccin Men-C-ACYW-TT (6,8 % des participants), comparativement au vaccin Men-C-CRM197 (15,1 %). Symptômes sollicités : Groupe de 6 à 10 ans Symptômes non sollicités : |
Niveau I |
Passable (La non-infériorité de l'innocuité n'a pas été évaluée.) |
| Données probantes sur l'immunogénicité de NimenrixMC chez les sujets de 11 à 19 ans | ||||||
|---|---|---|---|---|---|---|
| Détails des études | Sommaire | |||||
| Étude | Vaccin | Plan de l'étude | Participants | Résumé des principales conclusions | Niveau de données probantes | Qualité |
Ostergaard, L., et al., 2012Note de bas de page 27 |
Vaccins MenACWY-TT, HepA/B, ou administrés conjointement |
Étude ouverte comparative randomisée Phase III 5 centres en Suède et 1 centre au Danemark |
N = 611 participants âgés de 11 à 17 ans N = 122 MenACWY-TT |
La séroprotection a été définie par un titre d'ABSl ≥ 1:8. Le vaccin MenACWY-TT administré en association avec DCaT-VHB-VIP/Hib était non inférieur au vaccin MenACWY-TT administré seul. La liste ci-dessous contient les % des TMG des ABSl ≥ 1:8 à 1 mois après la vaccination [IC à 95 %]. Sérogroupe A Sérogroupe C Sérogroupe W-135 Sérogroupe Y |
Niveau I |
Bonne |
Ostergaard, L., et al., 2013Note de bas de page 30 |
Vaccin MenACWY-TT comparé à Men-PS |
Étude de prolongation Un seul centre au Danemark Phase II |
N = 50 – Persistance immunitaire 42 mois après la vaccination |
La séroprotection a été définie par un titre d'ABSl ≥ 1:8. Tous les sujets ont obtenu des titres d'ABSl ≥ 1:8 pour tous les sérogroupes; il n'y avait aucune différence significative entre les groupes quant aux TMG des ABSl, à l'exception de celles du sérogroupe W-135 qui étaient significativement plus élevées dans le groupe Men-C-ACYW-TT (n = 19) que dans le groupe Men-P-ACYW-135 (n = 17) après 42 mois. La liste des TMG des ABSl 42 mois après la vaccination pour le sérogroupe A est présentée ci-dessous. Sérogroupe C Sérogroupe W-135 Sérogroupe Y |
Niveau I |
Passable (IC à 95 % non fourni pour tous les titres d'ABSl; petite taille de l'échanti-llon) |
Bermal, N., et al., 2011Note de bas de page 31 |
Vaccin MenACWY-TT comparé à Men-PS |
Essai ouvert comparatif randomisé Plusieurs centres en Inde, aux Philippines et à Taïwan Phase III |
N = 1 025 Échantillons sanguins recueillis avant l'immunisation et un mois après. |
La séroprotection a été définie par un titre d'ABSl ≥ 1:8. Un mois après la vaccination, au moins 99,6 % des sujets des deux groupes présentaient des titres d'ABSl ≥ 1:8 pour chaque sérogroupe visé par les vaccins antiméningococciques; les taux de séroréaction étaient significativement plus élevés dans le groupe Men-C-ACYW-TT pour les sérogroupes A, W-135 et Y, et non inférieurs au sérogroupe C comparativement au groupe Men-P-ACYW-135. La liste ci-dessous contient les % des TMG des ABSl ≥ 1:8 à 1 mois après la vaccination [IC à 95 %]. Sérogroupe A Sérogroupe W-135 |
Niveau I |
Bonne |
Baxter, R., et al., 2011Note de bas de page 26 |
MenACWY-TT comparé à MenACWY-DT |
Étude comparative randomisée avec groupes parallèles Phase II Essai à simple insu pour les sujets de 11 à 25 ans, ouvert pour les sujets de 10 ans 10 centres aux États-Unis |
N = 827 sujets âgés de 10 à 25 ans (N = 587 MenACWY-TT; N = 197 MenACWY-DT; N = 88 MenACWY-TT/10 ans) |
Un titre de sérum ABSh ≥ 1:4 est considéré comme un facteur de protection contre la maladie causée par le sérogroupe C. La pratique courante consiste à appliquer le seuil de 1:4 seuil aux autres sérogroupes. La séroconversion est définie par des titres d'ABSh ≥ 1:8 un mois après la vaccination chez les sujets avec des titres < 1:4 avant la vaccination. La réponse immunitaire au vaccin est définie par un titre d'anticorps ABSh ≥ 1:16 après la vaccination, chez les sujets dont le titre d'ABSh était < 1:4 après la vaccination, ou par une augmentation selon un facteur ≥ 4 du titre d'anticorps ABSh après la vaccination, chez les sujets dont le titre d'ABSh était ≥ 1:4 avant la vaccination. La réponse immunitaire était similaire à l'exception de valeurs relativement élevées, mais non significatives sur le plan statistique, du TMG des ABSh-MenA dans le groupe d'âge de 10 ans. La liste ci-dessous contient les pourcentages des titres d'ABSh ≥ 1:4 [IC à 95 %] 1 mois après la vaccination pour chaque sérotype. Sérotype A Sérotype C Sérotype W-135 Sérotype Y |
Niveau I |
Bonne |
| Données probantes sur l'innocuité de NimenrixMC chez les sujets de 11 à 17 ans | ||||||
|---|---|---|---|---|---|---|
| Détails des études | Sommaire | |||||
| Étude | Vaccin | Plan de l'étude | Participants | Résumé des principales conclusions | Niveau de données probantes | Qualité |
Ostergaard, L., et al., 2009Note de bas de page 12 |
5 préparations vaccinales MenACWY-TT différentes |
Essai comparatif randomisé à double insu |
N = 50 jeunes de 18 à 25 ans |
Symptômes d'une intensité de catégorie 3 : rougeur et enflure > 50mm de diamètre, température corporelle axillaire/buccale > 39,5 C, ou tout autre événement entravant les activités quotidiennes normales La douleur au site d'injection est le symptôme sollicité le plus fréquemment signalé (dans les 8 jours). La fatigue et les maux de tête sont les symptômes systémiques les plus fréquemment signalés. Une fièvre a été signalée par six sujets (deux dans le groupe ayant reçu le vaccin MenACWY-TT 5c, un dans le groupe MenACWY-TT 2,5 et trois dans le groupe témoin); des symptômes sollicités locaux et généraux d'une intensité de catégorie 3 ont été signalés chez six et neuf sujets, respectivement; l'incidence des symptômes à la suite de l'administration du vaccin Men-ACWY-TT est semblable au vaccin témoin, sauf en ce qui concerne la douleur et l'enflure. Aucun symptôme non sollicité (dans un délai de 30 jours) après l'administration du vaccin MenACWY-TT n'a été considéré par les chercheurs comme étant lié à la vaccination; absence de symptômes de catégorie 3. Un EIG (urticaire) survenu huit jours après la vaccination semblait causé par la vaccination; les effets ont complètement disparu à la suite du traitement. |
Niveau I |
Passable (faible taille de l'échanti-llon pour l'évalua-tion de l'innocuité) |
Bermal, N., et al., 2011Note de bas de page 31 |
Vaccin MenACWY-TT comparé à Men-PS |
Essai ouvert comparatif randomisé Plusieurs centres en Inde, aux Philippines et à Taïwan Phase III |
N = 1 025 sujets âgés de 11 à 17 ans |
La douleur au site d'injection (dans les 4 jours suivant la vaccination) est le symptôme local sollicité le plus courant chez les adolescents (26,2 % avec Men-ACWY-TT et 26,8 % avec Men-PS). Des symptômes de rougeur et d'enflure ont été signalés par 12,3 % et 9,3 % des sujets (respectivement) dans le groupe ACWY-TT et par 6,3 % des sujets ayant reçu le vaccin Men-PS. Des symptômes locaux d'une intensité de catégorie 3 ont été signalés par moins de 1,2 % des sujets dans le groupe ACWY-TT et par aucun sujet dans le groupe Men-PS. Après la vaccination, des symptômes généraux sollicités de même intensité ont été signalés par les adolescents des deux groupes; moins de 0,9 % des sujets dans l'un ou l'autre des groupes de traitement ont signalé des symptômes généraux sollicités d'une intensité de catégorie 3 après la vaccination. Au moins un symptôme non sollicité (dans un délai de 31 jours) a été signalé par 9,4 % des participants dans le groupe Men-ACWY-TT et par 10,1 % des participants dans le groupe Men-PS. Des EI non sollicités ont été considérés comme causés par le vaccin chez 1,4 % et 1,2 % des sujets ayant reçu les vaccins Men-ACWY-TT et Men-PS, respectivement; aucun d'intensité de catégorie 3. Aucun cas d'apparition de maladie chronique n'a été signalé tout au long de la durée de l'étude. Cinq sujets ont signalé un ou plusieurs EIG, mais selon les chercheurs, aucun n'était causé par le vaccin. Dans une analyse groupée (adolescents et adultes), la non-infériorité en termes d'incidence des symptômes sollicités et non sollicités de catégorie 3 dans les quatre jours suivant la vaccination n'a pas été atteinte (la limite supérieure de l'IC à 95 % a dépassé légèrement [3,0024] la limite prédéfinie de 3). À l'examen de chaque étude prise séparément, les comparaisons exploratoires n'ont révélé aucune valeur de p < 0,05 pour les différences entre les groupes entre les taux signalés de symptômes généraux ou individuels de toute catégorie ou de catégorie 3. |
Niveau I |
Passable (échanti-llonnage insuffisant pour les analyses d'infério-rité) |
| Données probantes sur l'immunogénicité de NimenrixMC chez les sujets de 18 à 55 ans | ||||||
|---|---|---|---|---|---|---|
| Détails des études | Sommaire | |||||
| Étude | Vaccin | Plan de l'étude | Participants | Résumé des principales conclusions | Niveau de données probantes | Qualité |
Dbaibo, G., et al., 2012bNote de bas de page 34 |
Men-C-ACWY-TT Men-P-ACWY |
Essai ouvert comparatif randomisé Homogénéité des lots (3 lots) 4 centres au Liban et aux Philippines Phase III |
N = 1 247 sujets de 18 à 55 ans, répartis aléatoirement pour recevoir le vaccin Men-C-ACWY-TT (3 groupes) ou Tous les sujets ont reçu une dose de vaccin, soit Men-C-ACWY-TT, soit Men-P-ACWY. |
Titre d'ABSl > 1:8 utilisé comme mesure de l'immunité. L'homogénéité et la non-infériorité ont été démontrées entre les trois lots de vaccin ACWY-TT testés. Le pourcentage de sujets présentant des titres d'ABSl > 1:128 a augmenté, passant d'une plage de 48,8 % à 79 % à une plage de 98,9 % à 99,5 % après la vaccination avec Men-C-ACWY-TT pour tous les sérogroupes. La réponse au vaccin Men-C-ACWY-TT (combinée) a été > 80 % pour tous les sérogroupes; la non-infériorité a été démontrée dans la réponse immunitaire pour tous les sérogroupes (taux significativement plus élevés dans le groupe Men-C-ACWY-TT que dans le groupe Men-P-ACWY pour tous les sérogroupes, sauf le sérogroupe C). Les TMG des ABSl étaient significativement plus élevés dans le groupe Men-C-ACWY-TT que dans le groupe Men-P-ACWY pour tous les sérogroupes, sauf le sérogroupe C. |
Niveau I |
Bonne |
Borja-Tabora, C., et al., (2013)Note de bas de page 35 |
Men-C-ACWY-TT Men-P-ACWY |
Essai ouvert comparatif randomisé Trois centres aux Philippines et en Arabie saoudite Suivi sur une période de trois ans Phase IIb |
N = 500 sujets de 11 à 55 ans répartis aléatoirement pour recevoir le vaccin Men-C-ACWY-TT ou Men-P-ACWY Tous les sujets ont reçu une dose de vaccin, soit Men-C-ACWY-TT, soit Men-P-ACWY. Des échantillons sanguins ont été prélevés après 1 mois, 1 an, 2 ans et 3 ans. |
Titre d'ABSl > 1:8 utilisé comme mesure de l'immunité. Plus de 99,4 % des sujets ont obtenu des titres d'ABSl > 1:8 et > 1:128, avec une augmentation des TMG des ABSl, avant et après l'administration du vaccin, selon un facteur d'au moins 9 un mois suivant l'immunisation avec Men-C-ACWY-TT pour tous les sérogroupes. La réponse immunitaire dans le groupe Men-C-ACWY-TT variait de 82,7 % à 96,3 %; la non-infériorité a été démontrée dans la réponse immunitaire pour tous les sérogroupes (taux significativement plus élevés dans le groupe Men-C-ACWY-TT que dans le groupe Men-P-ACWY pour les sérogroupes A et Y). Après trois ans, ≥ 99,1 % et ≥ 92,9 % des participants dans le groupe Men-C-ACWY-TT ont conservé des titres d'ABSl ≥ 8 et ≥ 128 pour chacun des quatre sérogroupes; les TMG des ABSl après trois ans sont demeurés plus élevés que les valeurs de pré-vaccination et significativement plus élevés, d'un point de vue statistique, que dans le groupe Men-P-ACWY pour tous les sérogroupes. La liste ci-dessous contient les titres d'ABSl pour les sérogroupes de la méningococcie (≥ 1:8) un mois après l'administration du vaccin Men-C-ACWY-TT (IC à 95 %) : |
Niveau I |
Bonne |
Bermal, N., et al., 2011Note de bas de page 31 |
Vaccin MenACWY-TT comparé à Men-PS |
Essai ouvert comparatif randomisé Plusieurs centres en Inde, aux Philippines et à Taïwan Phase III |
N = 1 025 Échantillons sanguins recueillis avant l'immunisation et un mois après. |
La réponse immunitaire au vaccin a été définie par un titre d'ABSl d'au moins 1:32 chez les sujets initialement séronégatifs (c.-à-d. titre d'ABSl < 1:8) et une augmentation selon un facteur de quatre des titres chez les sujets initialement séropositifs (c.-à-d. titre d'ABSl ≥ 1:8). Un mois après la vaccination, ≥ 85,4 % – 97,1 % des sujets présentaient une réponse immunitaire au vaccin (post-titre ≥ 1:8 chez les sujets initialement séronégatifs et augmentation selon un facteur de 4 chez les sujets séropositifs au départ), comparativement à 78,0 % – 96,6 % après l'administration du vaccin Men-PS, pour chaque sérogroupe. Les TMG des ABSl dans chaque sérogroupe étaient de 29,2 à 274,3 fois supérieurs chez les sujets ayant reçu le vaccin ACWY-TT, et de 16,4 à 185,9 fois supérieurs chez ceux ayant reçu le vaccin Men-PS. Les comparaisons ont révélé que le pourcentage de sujets présentant une réponse immunitaire au vaccin pour les sérogroupes A, W-135 et Y était significativement plus élevé après le vaccin ACWY-TT qu'après le vaccin Men-PS, même en tenant compte des valeurs avant la vaccination. |
Niveau I |
Bonne |
| Innocuité de NimenrixMC chez les sujets de 19 à 55 ans | ||||||
|---|---|---|---|---|---|---|
| Détails des études | Sommaire | |||||
| Étude | Vaccin | Plan de l'étude | Participants | Résumé des principales conclusions | Niveau de données probantes | Qualité |
Bermal, N., et al., 2011Note de bas de page 31 |
Vaccin MenACWY-TT comparé à Men-PS |
Essai ouvert comparatif randomisé Plusieurs centres en Inde, aux Philippines et à Taïwan Phase III |
N = 1 247 Échantillons sanguins recueillis avant l'immunisation et un mois après. |
La non-infériorité du vaccin MenACWY-TT pour les symptômes sollicités et non sollicités de catégorie 3 n'a pas pu être démontrée. Sur le plan des symptômes de catégorie 3, le ratio du taux d'incidence dans le groupe ACWY-TT par rapport au groupe Men-PS était de 1,42 % [IC à 95 % : 0,67; 3,00]. Les deux vaccins ne présentaient pas de symptômes significativement différents. Les comparaisons exploratoires entre les groupes n'ont révélé aucune différence significative dans la fréquence des symptômes généraux (sollicités ou non sollicités). |
Niveau I |
Passable (taille insuffi-sante de l'échanti-llon pour le test de non-infériorité de l'innocuité) |
Dbaibo, G., et al., 2012bNote de bas de page 34 |
Vaccin MenACWY-TT comparé à Men-PS |
Essai comparatif à l'aveugle randomisé partiel Homogénéité des lots 4 centres au Liban et aux Philippines |
N = 1 025 |
Le pourcentage de sujets déclarant une douleur, une rougeur et une enflure au site d'injection était plus élevé chez les sujets ayant reçu le vaccin MenPS ACWY-TT, par rapport au vaccin MenPS, mais l'apparition de symptômes généraux était similaire dans les deux groupes. Au cours de la période de quatre jours suivant la vaccination, des symptômes généraux de catégorie 3 ont été signalés par cinq participants (1,3 %) dans le groupe ACWY-TT et par aucun participant dans le groupe Men-PS. Des symptômes non définis de catégorie 3 ont été signalés par 12 participants (3,2 %) dans le groupe ACWY-TT et par un participant (0,8 %) dans le groupe Men-PS. |
Niveau I |
Bonne |
Borja-Tabora, C., et al., 2013Note de bas de page 35 |
Voir ci-dessus |
Voir ci-dessus |
Voir ci-dessus |
La non-infériorité du vaccin MenACWY-TT par rapport au vaccin polysaccharidique MenACWY a été démontrée, en ce qui concerne les symptômes généraux de catégorie 3. La douleur comme symptôme local et les maux de tête comme symptôme général étaient les plus fréquents dans les deux groupes Au cours de la période de suivi de six mois pour vérifier l'innocuité, deux effets indésirables graves ont été signalés dans le groupe ayant reçu le vaccin ACWY-TT, mais les chercheurs considèrent que ces effets ne sont pas liés à la vaccination. |
Niveau I |
Bonne |
| Données probantes sur l'immunogénicité de NimenrixMC chez les sujets de plus de 55 ans | ||||||
|---|---|---|---|---|---|---|
| Détails des études | Sommaire | |||||
| Étude | Vaccin | Plan de l'étude | Participants | Résumé des principales conclusions | Niveau de données probantes | Qualité |
Dbaibo, G., et al., 2013Note de bas de page 36 |
NimenrixMC (MenACWY-TT) comparé à Mencevax (MenPS) |
Étude comparative, randomisée, ouverte, de phase IIIb Un seul centre au Liban |
N = 400 adultes en bonne santé de 56 à 103 ans |
La réponse immunitaire au vaccin est définie comme suit : titre d'ABSl C1:32 chez les sujets initialement séronégatifs; augmentation par facteur de quatre chez les sujets initialement séropositifs avec titres d'ABSl 1:8 et < 1:128; augmentation du double chez les sujets séropositifs au départ présentant un titre d'ABSl ≥ 1:128. Il n'y avait aucune différence significative quant aux ABSl > 1:8 un mois après la vaccination. Cependant, les personnes ayant reçu le vaccin Men-P-ACYW-135 présentaient une réponse immunitaire significativement plus élevée pour le sérogroupe A et les valeurs des ABSl et deTMG pour les sérogroupes A et C, que les sujets ayant reçu le vaccin conjugué. Une faible réponse immunitaire a été principalement observée chez les personnes recevant le vaccin MenACWY-TT qui présentaient des titres très élevés (≥ 1:128) avant la vaccination. La liste ci-dessous contient les pourcentages des titres d'ABSl ≥ 1:8 pour les sérogroupes de la méningococcie un mois après l'administration du vaccin Men-C-ACWY-TT (IC à 95 %) : Sérogroupe A : Sérogroupe C : Sérogroupe W-135 : Sérogroupe Y : |
Niveau I |
Bonne |
| Données probantes sur l'innocuité de NimenrixMC chez les sujets de plus de 55 ans | ||||||
|---|---|---|---|---|---|---|
| Détails des études | Sommaire | |||||
| Étude | Vaccin | Plan de l'étude | Participants | Résumé des principales conclusions | Niveau de données probantes | Qualité |
Dbaibo, G., et al., 2013Note de bas de page 36 |
NimenrixMC (MenACWY-TT) comparé à Mencevax (MenPS) |
Étude comparative, randomisée, ouverte, de phase IIIb (rapport de 3:1) Un seul centre au Liban |
N = 400 adultes en bonne santé de 56 à 103 ans |
Moins de 3,0 % des sujets ont signalé des effets indésirables; aucun effet indésirable grave n'était lié au vaccin. Dans le groupe ayant reçu le vaccin MenACWY-TT, une douleur a été signalée par six sujets (2,3 % [IC à 95 % : 0,8; 4,9]); des rougeurs et œdèmes ont été signalés par trois sujets (1,1 % [0,2; 3,3]). Pas de symptômes locaux signalés par les sujets du groupe MenPS. Aucun symptôme local d'une intensité de catégorie 3 n'a été signalé dans les deux groupes. |
Niveau 1 |
Bonne |
| Données probantes pour la persistance des anticorps | ||||||
|---|---|---|---|---|---|---|
| Détails des études | Sommaire | |||||
| Étude | Vaccin | Plan de l'étude | Participants | Résumé des principales conclusions | Niveau de données probantes | Qualité |
Vesikari, T. et al., 2012aNote de bas de page 24 |
Vaccin MenACWY-TT comparé à Men-PS |
Essai ouvert comparatif randomisé 11 centres en Finlande Phase II |
N = 309 enfants âgés de 2 à 5 ans Les deux groupes ont reçu le vaccin MenACWY-TT ou Men-P-ACYW. |
La réponse immunitaire au vaccin a été définie par un titre d'ABSl ≥ 1:32 pour les enfants séronégatifs au départ (titre d'ABSl < 1:8 avant la vaccination) et une augmentation par au moins un facteur de quatre des titres d'ABSl avant la vaccination pour les enfants initialement séropositifs TMG des ABSl Sérogroupe A Men-PS (IC à 95 %) Sérogroupe C Men-PS (IC à 95 %) Sérogroupe W-135 Men-PS (IC à 95 %) Sérogroupe Y Men-PS (IC à 95 %) La liste des titres d'ABSl ≥ 1:8 pour les sérogroupes méningococciques 3 ans après la vaccination est présentée ci-dessous : Men-PS (IC à 95 %) |
Niveau I |
Bonne |
Knuf, M., et al., (2012)Note de bas de page 37 |
MenACWY-TT comparé à MenC-CRM197 ou Men-PS |
Étude de prolongation de l'essai ouvert comparatif randomisé 35 centres en Allemagne et en Autriche |
N = 203 bébés âgés de 12 à 14 mois - les deux groupes testés pour la persistance 15 mois après la vaccination |
La séroprotection a été définie par un titre d'ABSl ≥ 1:8. La liste ci-dessous contient les titres d'ABSl ≥ 1:8 15 mois après la vaccination [IC à 95 %]. enfants âgés de 3 à 5 ans |
Niveau I |
Bonne |
Ostergaard et al., |
Vaccin MenACWY-TT comparé à Men-PS |
Étude de prolongation Un seul centre au Danemark Phase II |
N = 50 - Persistance immunitaire 42 mois après la vaccination |
La séroprotection a été définie par un titre d'ABSl ≥ 1:8. La liste ci-dessous contient les titres d'ABSl et les TMG ≥ 1:8 à 42 mois après la vaccination pour le sérogroupe A : Sérogroupe C Sérogroupe W-135 Sérogroupe Y |
Niveau I |
Passable (IC à 95 % non fourni pour tous les titres d'ABSl; petite taille de l'échanti-llon) |
Vesikari, T. et al., 2012bNote de bas de page 19 |
MenACWY-TT |
Essai ouvert comparatif randomisé |
N = 304 sujets de 12 à 23 mois : N = 177 (MenACWY-TT) + 37 (MenC-CRM197) |
La séroprotection a été définie par des titres d'ABSl ≥ 1:8 ou des titres d'ABSh ≥ 1:4. Trois ans après la vaccination, 90,8 % des sujets ayant reçu le vaccin Men-C-ACYW-TT ont maintenu des titres d'ABSI ≥ 1:8 pour tous les sérogroupes et 73,6 % ont conservé des titres d'ABSh ≥ 1:4 pour les sérogroupes C, W et Y; seuls 28,1 % avaient des titres d'ABSh ≥ 1:4 pour le sérogroupe A. Il n'y avait pas de différence significative entre les titres d'ABSI entre les sujets ayant reçu les vaccins Men-C-ACYW-TT ou Men-C-CRM197 3 ans après la vaccination. Au cours des deux premières années suivant la vaccination, les TMG étaient plus élevés dans le groupe immunisé à l'aide du vaccin Men-C-ACWY-TT que dans celui immunisé à l'aide du vaccin MenC-CRM197, tandis qu'aucune différence significative n'a été observée au cours de la troisième année. Les titres d'ABSl (≥ 1:8) et les titres d'ABSh (≥ 1:4 pour les sérogroupes méningocciques 3 ans après la vaccination sont présentés ci-dessous : Sérogroupe A (IC à 95 %) Sérogroupe C (IC à 95 %) Sérogroupe W-135 (IC à 95 %) Sérogroupe Y (IC à 95 %) |
Niveau I |
Bonne |
Borja-Tabora, C., et al., |
Men-C-ACWY-TT |
Essai ouvert comparatif randomisé Trois centres aux Philippines et en Arabie saoudite Phase IIb |
N = 500 sujets de 11 à 55 ans répartis aléatoirement pour recevoir le vaccin Men-C-ACWY-TT ou Men-P-ACWY Des échantillons sanguins ont été prélevés après 1 mois, 1 an, 2 ans et 3 ans. |
La séroprotection a été définie par un titre d'ABSl ≥ 1:8. La liste des titres d'ABSl ≥ 1:8 pour les sérogroupes méningococciques 3 ans après la vaccination est présentée ci-dessous : Men-PS (IC à 95 %) |
Niveau I |
Bonne |
Liste des abréviations
Remerciements
†Membres du CCNI : Dr I. Gemmill (président), Dre C. Quach-Thanh (vice-présidente) Dre S. Deeks, Dre B. Henry, Dre D. Kumar, Dre M. Salvadori, Dr B. Seifert, Dre N. Sicard, Dre W. Vaudry, Dr R. Warrington.
Anciens membres du CCNI : Dre N. Crowcroft, Dre B. Warshawsky (présidente).
Représentants chargés de la liaison : Dre J. Blake (Société des obstétriciens et gynécologues du Canada), Dr J. Brophy (Association canadienne pour la recherche et l'évaluation en immunisation), Dre J. Emili (Collège des médecins de famille du Canada), Dr M. Lavoie (Conseil des médecins hygiénistes en chef), Dre C. Mah (Association canadienne de santé publique), Dre D. Moore (Société canadienne de pédiatrie), Dre A. Pham-Huy (Association pour la microbiologie médicale et l'infectiologie), Mme E. Sartison (Comité canadien d'immunisation).
Ancien représentant de liaison : Dre A. Mawle (Centers for Disease Control and Prevention, États-Unis)
Représentants d'office : Mme G. Charos (Centre de l'immunisation et des maladies respiratoires infectieuses [CIMRI], Agence de la santé publique du Canada [ASPC]), Dre G. Coleman (Direction des produits biologiques et des thérapies génétiques [DPBTG], Santé Canada [SC]), Dr (LCol) P. Eagan (Défense nationale et les Forces armées canadiennes), Dr J. Gallivan (Direction générale des produits de santé commercialisées [DPSC], SC), Dre B. Law (CIMRI, ASPC), Mme M. St-Laurent (CIMRI, ASPC), Dr T. Wong (Direction générale de la santé des Premières nations et des Inuits [DGSPNI], SC).
Anciens représentants d'office : Dre M. Carew (DGSPNI, SC), Dr D. Garcia (DGSPNI, SC), Dre A. Klein (DPBTG, SC), Dre B. Raymond (CIMRI, ASPC), Dre E. Taylor, (DPSC, SC).
†Le présent document a été préparé par les Dre S. Desai, Dr O. Baclic, Dre N. Crowcoft, Dre B. Henry, Mme J. Rotondo, Dr M. Tunis, et approuvée par le CCNI.
Le CCNI tient également à souligner la contribution des Dre J. Bettinger, Dr. P. De Wals, Dre J. Embree.