Modélisation mathématique pour la préparation aux pandémies au Canada

 Téléchargez cet article en format PDF (176 ko)
Téléchargez cet article en format PDF (176 ko)Publié par : L'Agence de la santé publique du Canada
Numéro : RMTC : Volume 50-10, octobre 2024 : COVID-19 après la pandémie
Date de publication : octobre 2024
ISSN : 1719-3109
Soumettre un article
À propos du RMTC
Naviguer
Volume 50-10, octobre 2024 : COVID-19 après la pandémie
Science de la mise en œuvre
Modélisation mathématique pour la préparation aux pandémies au Canada : leçons de la COVID-19
Nicholas H Ogden1, Emily S Acheson1, Kevin Brown2,3, David Champredon1, Caroline Colijn4, Alan Diener5, Jonathan Dushoff6, David JD Earn7, Vanessa Gabriele-Rivet1, Marcellin Gangbè1, Steve Guillouzic8, Deirdre Hennessy9, Valerie Hongoh1, Amy Hurford10, Lisa Kanary1, Michael Li1, Victoria Ng1, Sarah P Otto11, Irena Papst1, Erin E Rees1, Ashleigh Tuite3,12, Matthew R MacLeod8, Carmen Lia Murall13, Lisa Waddell1, Rania Wasfi1, Michael Wolfson14
Affiliations
1 Division des sciences des risques pour la santé publique, Laboratoire national de microbiologie, Agence de la santé publique du Canada
2 Santé publique Ontario, Toronto, ON
3 École de santé publique Dalla Lana, Université de Toronto, Toronto, ON
4 Département de mathématiques, Université Simon Fraser, Burnaby, BC
5 Direction générale de la politique de la santé, Santé Canada, Ottawa, ON
6 Département de biologie et Michael G. DeGroote Institute for Infectious Disease Research, Université McMaster, Hamilton, ON
7 Département de mathématiques et de statistiques et Michael G. DeGroote Institute for Infectious Disease Research, Université McMaster, Hamilton, ON
8 Centre de recherche et d'analyse opérationnelle, Recherche et développement pour la défense Canada, ministère de la Défense nationale, Ottawa, ON
9 Division de l'analyse de la santé, Direction des études analytiques et de la modélisation et les collaborateurs, Statistique Canada, Ottawa, ON
10 Département de biologie et département de mathématiques et de statistiques, Université Memorial de Terre-Neuve, St. John's, NL
11 Département de zoologie et Centre de la recherche sur la biodiversité, Université de la Colombie-Britannique, Vancouver, BC
12 Centre des programmes d'immunisation, Agence de la santé publique du Canada, Ottawa, ON
13 Division de la génomique en santé publique, Laboratoire national de microbiologie, Agence de la santé publique du Canada
14 Faculté de médecine et Faculté de droit – Section de common law, Université d'Ottawa, Ottawa, ON
Correspondance
Citation proposée
Ogden NH, Acheson ES, Brown K, Champredon D, Colijn C, Diener A, Dushoff J, Earn DJD, Gabriele-Rivet V, Gangbè M, Guillouzic S, Hennessy D, Hongoh V, Hurford A, Kanary L, Li M, Ng V, Otto SP, Papst I, Rees EE, Tuite A, MacLeod MR, Murall CL, Waddell L, Wasfi R, Wolfson M. Modélisation mathématique pour la préparation aux pandémies au Canada : leçons de la COVID-19. Relevé des maladies transmissibles au Canada 2024;50(10):377–89. https://doi.org/10.14745/ccdr.v50i10a03f
Mots-clés : modélisation mathématique, préparation à une pandémie, maladies infectieuses, COVID-19
Résumé
Contexte : La pandémie de COVID-19 a mis en relief la nécessité d'une planification en cas de pandémie, mais a également mis en lumière l'utilisation de la modélisation mathématique pour soutenir les décisions en matière de santé publique. Les types de modèles qui furent nécessaires (à compartiments, à base d'agents, d'importation) sont décrits. Les meilleures pratiques concernant le réalisme biologique (y compris la nécessité de conseillers experts multidisciplinaires pour les modélisateurs), la complexité du modèle, la prise en compte de l'incertitude et la communication aux décideurs et au public sont décrites.
Méthodes : Les membres du Réseau externe en modélisation des maladies infectieuses de l'Agence de la santé publique du Canada (REM-MI ASPC), une communauté de pratique nationale sur la modélisation mathématique des maladies infectieuses pour la santé publique, ont élaboré une analyse narrative à partir de l'expérience de la COVID-19.
Résultats : La modélisation peut soutenir au mieux la préparation à la pandémie de deux manières : 1) en modélisant pour soutenir les décisions sur les besoins en ressources pour les pandémies futures probables en estimant le nombre d'infections, de cas hospitalisés et de cas nécessitant des soins intensifs, associés aux épidémies d'agents pathogènes pandémiques « hypothétiques, mais plausibles » au Canada; et 2) en disposant de méthodes de modélisation prêtes à l'emploi qui peuvent être facilement adaptées aux caractéristiques d'un agent pathogène pandémique émergent et utilisées pour les prévisions à long terme de l'épidémie au Canada, ainsi que pour explorer des scénarios afin de soutenir les décisions de santé publique sur l'utilisation d'interventions.
Conclusion : Les organismes de santé publique au Canada ont besoin d'une expertise en modélisation à l'interne, connectée avec les modélisateurs du milieu universitaire au sein d'une communauté de pratique, dans laquelle les relations établies en dehors des périodes de crise peuvent être utilisées pour améliorer la modélisation pendant les urgences de santé publique. Les difficultés majeures auxquelles fait face la modélisation dans la préparation à une pandémie incluent la disponibilité de données couplées de la santé publique, des hôpitaux et de la génomique au Canada.
Introduction
La pandémie de COVID-19, causée par le SRAS-CoV-2, a mis en relief la nécessité de planifier pour les futures pandémies. De nombreuses initiatives de préparation à la pandémie ont été lancées aux niveaux national et international Note de bas de page 1Note de bas de page 2. La modélisation a soutenu les plans de lutte contre les pandémies précédents, et l'Organisation mondiale de la Santé (OMS) a inclus la modélisation comme source de données probante pour soutenir la planification Note de bas de page 3. Au Canada, la modélisation a soutenu les décisions prises lors de la pandémie de grippe pH1N1 Note de bas de page 4Note de bas de page 5Note de bas de page 6 et la planification subséquente pour les pandémies de grippe Note de bas de page 7. Au cours de la pandémie de COVID-19, le rôle de la modélisation dans la prise de décision a été mis en évidence. Les modèles mathématiques synthétisent les informations relatives à la transmission de la maladie au sein de la population, à la gravité de la maladie dans différents groupes d'âge ou de population, à l'immunité de la population, à l'efficacité des interventions non pharmaceutiques (INP) et à l'efficacité des vaccins, entre autres aspects. Ce faisant, les modèles produisent un narratif qui peut être interprété par les décideurs et le public, et qui soutient la prise de décision fondée sur des données probantes, la transparence et la confiance du public.
L'objectif de cet article est de décrire comment les efforts de modélisation peuvent soutenir la préparation aux pandémies, y compris une description des types de modèles, de leurs rôles, des meilleures pratiques pour leur utilisation et de l'expertise requise, en se basant sur les pandémies passées et nos expériences récentes avec la COVID-19. Dans le cadre de cet article, la modélisation comprend les approches mathématiques et de simulation permettant de comprendre et de prévoir l'introduction, l'invasion, la propagation, l'évolution et le contrôle des agents pathogènes à l'origine d'une pandémie, ainsi que l'impact sur les capacités des services de soins de santé. L'accent est mis sur la préparation contre des agents pathogènes qui se répandent dans la population humaine par transmission de personne à personne, avec la capacité de se disperser à travers le réseau mondial de transport. Il est probable que ces agents pathogènes émergent des réservoirs animaux par transmission zoonotique. Si le retour vers les réservoirs animaux, comme cela s'est produit avec le SRAS-CoV-2, peut être une caractéristique de la transmission et de l'écologie de ces agents pathogènes, l'importance pour la préparation à la pandémie dépend de son impact sur la transmission de personnes à personnes (i.e., si le contact permanent entre l'animal et l'homme fait que le nombre de reproduction de base R0 est supérieur à un). L'OMS a établi une liste d'agents pathogènes prioritaires en fonction de leur importance pour la santé publique, mais ses critères sont généraux et vont au-delà de la capacité à provoquer une pandémie Note de bas de page 8, de sorte que cette liste est trop longue pour être prise en compte dans son intégralité dans le cadre de la planification en cas de pandémie. Par exemple, des zoonoses telles que le MERS-CoV, le Nipah, la fièvre hémorragique de Crimée-Congo et la fièvre de la vallée du Rift sont répertoriées, bien qu'elles aient souvent une transmission de personne à personne limitée, des cycles de transmission complexes et des voies de propagation dans les populations humaines impliquant des arthropodes vecteurs et des réservoirs d'animaux sauvages et domestiqués. Les flambées de ces maladies peuvent être définies par l'OMS comme des pandémies parce qu'elles touchent plusieurs pays. Toutefois, l'absence de transmission de personne à personne soutenue ou de conditions propices à la transmission zoonotique au Canada signifie que, sans évolution supplémentaire, il est peu probable qu'elles provoquent au Canada des épidémies de l'ampleur de la COVID-19 ou des pandémies de grippe de 1918 et 2009, auxquelles la planification des pandémies a pour but de nous préparer. La modélisation nous aide à comprendre le risque potentiel de ces maladies, en particulier dans le contexte du changement climatique Note de bas de page 9, mais cela n'entre pas dans le cadre de cet article.
Méthodes
Les membres du Réseau externe en modélisation des maladies infectieuses de l'Agence de la santé publique du Canada (REM-MI ASPC), une communauté de pratique nationale sur la modélisation mathématique des maladies infectieuses pour la santé publique, ont élaboré une analyse narrative de la manière dont la modélisation peut soutenir au mieux la préparation en cas de pandémie. Les auteurs ont recherché et examiné des articles scientifiques et de la littérature grise publiés au cours des 20 dernières années sur la préparation en cas de pandémie au Canada et l'utilisation de la modélisation pendant la pandémie de COVID-19. Comme la plupart des auteurs ont participé à la modélisation pour soutenir les décisions aux paliers fédéral, provincial et/ou territorial, leur avis d'expert et leurs expériences vécues sur la façon dont la modélisation a soutenu les décideurs en matière de santé publique pendant la pandémie ont été pris en compte.
Résultats
La modélisation de l'aide à la préparation à une pandémie comporte deux volets :
- La modélisation de la transmission d'agents pathogènes pandémiques « hypothétiques, mais plausibles » pour soutenir les décisions relatives aux activités préparatoires, telles que les réserves d'urgence
- La conception de méthodes et d'outils de modélisation validés qui sont maintenus, capables de s'adapter rapidement à la biologie des pathogènes émergents et qui sont donc « prêts à l'emploi » pour soutenir les décisions en cas d'émergence d'un pathogène à potentiel pandémique
Dans les deux cas, il faut tenir compte des bonnes pratiques en matière de méthodes de modélisation, de communication des résultats de la modélisation et des besoins en données pour la modélisation. Il est également essentiel de disposer de personnes formées à la reconnaissance et à la satisfaction des besoins en matière de modélisation, intégrées dans les organisations de santé publique et dans les cercles de décideurs, ou entretenant des relations étroites avec eux Note de bas de page 10. Bien qu'elle ne fasse pas explicitement partie de la planification en cas de pandémie, la modélisation peut également favoriser la résilience aux pandémies, ce qui est abordé à la fin de cet article.
Bonnes pratiques
Les modèles mathématiques actuellement utilisés pour soutenir les décisions en matière de santé publique et de politique de santé doivent concilier réalisme biologique et traçabilité Note de bas de page 11Note de bas de page 12. Si les modèles doivent être suffisamment simples pour être compris et mis en œuvre efficacement Note de bas de page 13, le réalisme utile implique d'intégrer les processus biologiques de l'infection et de la guérison, les conséquences de l'infection, le comportement humain qui sous-tend la transmission des agents pathogènes et l'efficacité des INP et des interventions pharmaceutiques (voir ci-dessous). Cependant, plus un modèle est complexe, plus il est sujet à des erreurs non détectées et à une paramétrisation imprécise Note de bas de page 13Note de bas de page 14Note de bas de page 15. La complexité excessive peut également limiter les méthodes standard d'évaluation des modèles, telles que les analyses de sensibilité Note de bas de page 16 et la possibilité de calibrer les modèles avec les données Note de bas de page 17. Toutefois, les progrès en matière de puissance de calcul, de disponibilité et de synthèse des données permettent de plus en plus une modélisation tractable basée sur la transmission avec un jumeau numérique de la société pour modéliser les contacts sociaux en détail Note de bas de page 18. Les résultats de modèles très simples peuvent également être utiles pour communiquer certains aspects d'une épidémie émergente à une audience profane, qui peut être le public ou des gestionnaires non experts, comme ce fut le cas lors de la pandémie de COVID-19 Note de bas de page 19. L'élaboration de critères universellement utilisables pour distinguer les « bons modèles » des « mauvais modèles », discutés en tant que vérification et validation de la modélisation dans la littérature de la simulation au sens large Note de bas de page 20Note de bas de page 21, reste un travail en cours Note de bas de page 11Note de bas de page 12Note de bas de page 22.
Types de modèles
Les principaux types de modèles pertinents pour la préparation à une pandémie sont 1) les modèles de transmission dynamique de la propagation d'un agent pathogène infectieux au sein d'une population, à la fois pour la prédiction, l'évaluation des alternatives de stratégies de réponses et l'incidence des changements évolutifs de l'agent pathogène; 2) les modèles d'importation qui explorent le risque estimé d'importation de maladies au Canada et à l'intérieur du pays, sur la base du réseau mondial de voyageurs aériens et terrestres et de la connaissance de la transmission dans les pays sources Note de bas de page 23; et 3) les modèles de propagation géographique qui sont capables d'identifier les voies spatiales de propagation des agents pathogènes à l'intérieur du Canada Note de bas de page 24.
Les modèles de transmission dynamique divisent généralement les populations humaines (ou animales) en « compartiments », tels que les modèles de type Susceptible-Exposé-Infectieux-Rétablis (SEIR). Les flux (ou transitions) entre ces compartiments reflètent les processus fondamentaux de la biologie de la transmission, de l'infection et de la guérison. Ils sont décrits par des taux d'événements, qui peuvent être utilisés pour définir des flux déterministes et continus entre les compartiments ou des transitions stochastiques.
Les modèles SEIR les plus simples supposent que la population se mélange de manière homogène. Par conséquent, ces modèles surestiment généralement la propagation des infections, y compris la taille maximale des épidémies. Les matrices de contact basées sur l'âge peuvent améliorer ces modèles en utilisant les résultats d'enquêtes de population Note de bas de page 25 ou des données démographiques Note de bas de page 26 pour estimer la fréquence des contacts quotidiens entre les individus. En outre, les modèles SEIR peuvent être construits avec une plus grande complexité pour modéliser différentes sections de la population Note de bas de page 27Note de bas de page 28 ou pour modéliser des variantes et des changements évolutifs Note de bas de page 29Note de bas de page 30.
Les modèles à base d'agents (MBA, également appelés modèles à base d'individus) peuvent intégrer encore plus d'hétérogénéité. Les MBA plus simples sont conceptuellement similaires aux modèles SEIR, mais modélisent explicitement les individus d'une population (i.e., les « agents ») qui existent dans des états de susceptibilité, d'exposition, d'infection ou de guérison. Les modèles à base d'agents permettent l'intégration de matrices de contact, la construction d'environnements quasi réalistes (e.g., le domicile, le lieu de travail, les écoles, les lieux de loisirs, les transports publics) à l'intérieur desquels et entre lesquels les agents se déplacent en fonction de leurs caractéristiques démographiques, et l'utilisation potentielle de données socio-économiques plus étendues. Cette structure permet d'explorer de manière plus réaliste des INP ciblées, telles que les fermetures limitées Note de bas de page 31 et les combinaisons d'INP avec la vaccination Note de bas de page 32. Les modèles compartimentaux et les modèles à base d'agents peuvent être utilisés pour étudier la propagation géographique d'une maladie infectieuse, auquel cas la transmission peut être modélisée de manière relativement simple dans chaque maille d'un paysage avec une propagation plausible de l'infection de cellule à cellule qui dépend de contraintes géographiques ou d'autres contraintes physiques Note de bas de page 24Note de bas de page 33, ou de manière plus élaborée sur la base d'une synthèse de données plus détaillée, y compris une estimation sur de petites zones.
Au début d'une pandémie apparue dans un autre pays, des modèles d'importation peuvent être utilisés pour estimer la probabilité d'importation et le nombre de cas susceptibles d'avoir été récemment introduits au Canada par des points d'entrée Note de bas de page 23. Les modèles d'importation prennent généralement en compte les volumes de voyage en provenance de différents pays et/ou provinces, ainsi que la prévalence de l'infection et l'immunité dans ces pays et/ou provinces. Les modèles d'importation peuvent également servir de base à des mesures relatives aux déplacements à l'intérieur d'un pays. Une fois que la transmission à l'intérieur du pays a commencé, les modèles d'importation peuvent fournir des données sur les cas importés aux modèles de transmission communautaire Note de bas de page 34Note de bas de page 35. Comme on l'a vu lors de la pandémie de COVID-19, pour les provinces et territoires plus petits, l'accent peut être mis sur l'importation plutôt que sur la transmission communautaire. Il peut y avoir relativement peu d'itinéraires de voyage dans les petites régions, qui peuvent être surveillés et gérés pour prévenir les éclosions communautaires, au début et pendant une pandémie.
Le couplage de l'analyse de la propagation géographique avec des analyses génomiques est de plus en plus utilisé pour modéliser la transmission et détecter les sources de nouveaux cas pour une variété d'agents pathogènes, notamment la COVID-19 Note de bas de page 36Note de bas de page 37Note de bas de page 38. Une utilisation pratique en temps réel de ces méthodes est Nextstrain Note de bas de page 39, une plateforme et un tableau de bord à code source ouvert qui permet aux décideurs, aux scientifiques et au grand public de suivre, en temps réel, l'évolution et la propagation du virus à l'échelle mondiale. Les méthodes phylogéographiques et phylodynamiques sous-jacentes sont des modèles mathématiques et statistiques qui s'appuient sur des modèles de génétique des populations, des modèles bayésiens et des modèles liés de type SEIR.
Il existe toute une série d'outils de modélisation et d'estimation permettant de fournir des informations pendant les éclosions. Il s'agit notamment de l'estimation du nombre instantané de reproduction, Rt Note de bas de page 40, des prévisions basées sur les signaux des eaux usées Note de bas de page 41Note de bas de page 42, des modèles de processus de ramification pour explorer les méthodes de contrôle à un stade précoce des éclosions Note de bas de page 43Note de bas de page 44Note de bas de page 45 et de l'analyse des arbres phylogénétiques des données de séquençage du génome entier pour obtenir des estimations du nombre de reproduction de base, R0, de l'agent pathogène et/ou des variants émergents à comparer avec les estimations des données de surveillance Note de bas de page 46.
Réalisme biologique
Au cours de la pandémie de COVID-19, l'importance des modèles pour la prise de décision en matière de santé publique a été renforcée, notamment parce qu'il a été reconnu que leurs résultats étaient biologiquement réalistes Note de bas de page 47. Pour ce faire, la structure des modèles (i.e., les compartiments/états et les flux/transitions entre les compartiments et les états) doit être réaliste en termes 1) de biologie de l'infection, probabilité liée à l'âge et au sexe des résultats cliniques et de la guérison (infections asymptomatiques, légères, nécessitant une hospitalisation ou des soins intensifs [i.e., en unité de soins intensifs]), en tenant compte de l'hétérogénéité des différents groupes de population lorsque ceux-ci jouent un rôle important dans la transmission, et des données disponibles; 2) de schémas de contacts entre les personnes infectées et non infectées, les vecteurs ou les hôtes réservoirs animaux, en fonction de l'âge et du genre Note de bas de page 48, et la manière dont ils sont susceptibles d'évoluer; 3) d'interventions de santé publique (INP et vaccinations); et 4) si possible, d'impacts directs réalistes sur les ressources de santé et impacts indirects, tels que l'annulation d'opérations chirurgicales et l'évitement de visites aux urgences (figure 1). Les valeurs des paramètres (e.g., la durée des périodes de latence et d'infection, le nombre de reproduction de base, R0, les schémas de contact au sein de la population) doivent être réalistes et obtenues à partir d'études prospectives ou déduites de la synthèse des données de type jumeaux numériques et de la littérature scientifique à l'aide de méthodes établies de synthèse des connaissances Note de bas de page 49. Elles peuvent également être obtenues en ajustant des modèles aux données de surveillance ou aux données hospitalières, en particulier pour les paramètres difficiles à mesurer dans les études, tels que la probabilité de transmission lorsque les personnes infectées entrent en contact avec des personnes susceptibles. La capacité d'ajuster des modèles aux données de surveillance (e.g., les cas humains, les hospitalisations et les données sur les eaux usées) dépend de la disponibilité de données fiables, ce qui a été une question problématique et largement non résolue pendant et après la pandémie de COVID-19 au Canada Note de bas de page 50. Pour atteindre un réalisme biologique (et idéalement un réalisme socio-économique) utile aux objectifs de santé publique, la modélisation doit être une entreprise multidisciplinaire, synthétisant les connaissances et les données d'un éventail de scientifiques et de cliniciens impliqués dans la santé publique. Grâce à ces principes, les données probantes fournies par les modèles seront plus fiables.
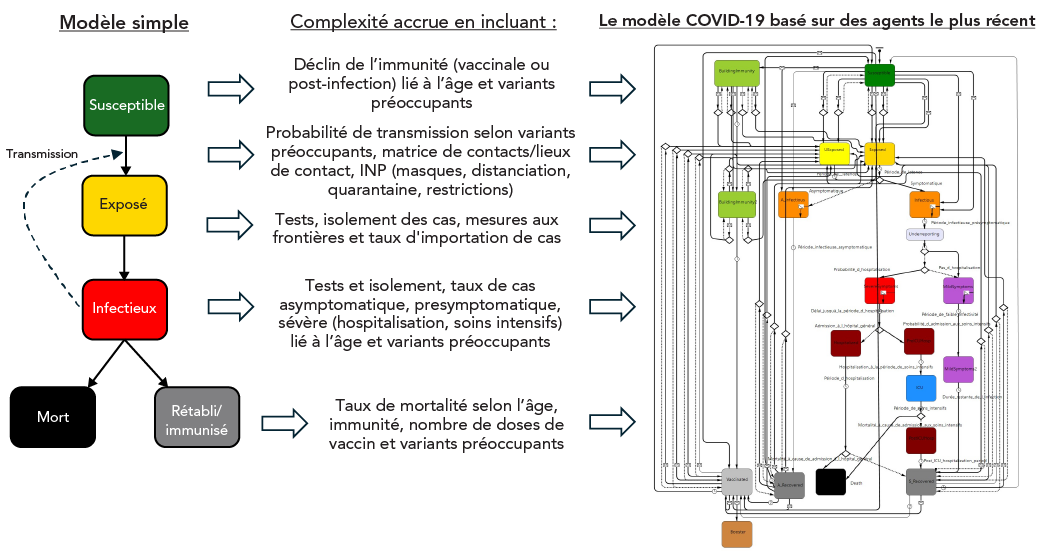
Figure 1 : Description textuelle
La figure comprend trois colonnes reliées par des flèches. La colonne de gauche est une image d'un modèle simple de maladie infectieuse (intitulé « Modèle simple ») dans lequel la population, lors d'une épidémie, est compartimentée en individus susceptibles (boîte verte), exposés (boîte jaune), infectieux (boîte rouge), rétabli/immunisé (boîte grise) et mort (boîte noire). Des flèches pleines relient les cases pour montrer la séquence des résultats de la maladie, tandis qu'une flèche en pointillé indique que les personnes du compartiment infecté sont responsables du passage des individus de la classe susceptible à la classe exposée. De chaque case, des flèches pointent vers le texte de la colonne centrale (avec un en-tête « Complexité accrue en incluant : ») qui identifie, pour chaque compartiment, comment plus de détails ont dû être ajoutés pour simuler la transmission et le contrôle de la COVID-19. Ce détail comprend, de haut en bas, pour le compartiment susceptible, « Déclin de l'immunité (vaccination ou post-infection) lié à l'âge et variants préoccupants »; pour la transition de susceptible à exposé, « Probabilité de selon variants préoccupants, matrice de contacts/lieux de contact, INP (masques, distanciation, quarantaine, restrictions) »; pour le compartiment exposé, « Tests, isolement des cas, mesures aux frontières et taux d'importation de cas »; pour le compartiment infectieux, « Tests et isolement, taux de cas asymptomatique, présymptomatique, sévère (hospitalisation, soins intensifs) lié à l'âge et variants préoccupants »; et pour les compartiments mort et rétabli/immunisé, « Taux de mortalité selon l'âge, immunité, nombre de doses de vaccin et variants préoccupants ». La colonne de droite (intitulée « Le modèle COVID-19 basé sur des agents le plus récent ») est une image des multiples compartiments et flux du modèle final très complexe pour la COVID-19 utilisé par l'Agence de la santé publique du Canada, qui ont été nécessaires pour inclure et modéliser les facteurs complexes identifiés dans la colonne centrale.
Abréviations : INP, interventions non pharmaceutiques; USI, unité de soins intensifs; VP, variant préoccupant
Notes de bas de page
- Footnote a
-
Le diagramme de gauche montre la structure d'un modèle simple Susceptible-Exposé-Infectieux-Rétabli (SEIR), à côté duquel figurent des exemples de facteurs qui ont dû être introduits pour modéliser de manière réaliste la transmission de la COVID-19 avec des VP émergents, et l'utilisation d'INP et de vaccinations, aboutissant à une structure de modèle complexe (diagramme de droite). Dans ce cas-ci, le modèle complexe est le modèle à base d'agents de l'Agence de la santé publique du Canada, tel que décrit, sous une forme antérieure, dans Ng et al., 2020 Note de bas de page 30
Incertitude
En général, les approches de modélisation doivent prendre en compte des plages et des distributions plausibles des valeurs des paramètres (e.g., la durée de l'infectivité) ou des probabilités d'occurrence des événements (e.g., les estimations de la probabilité de transmission) afin de permettre l'exploration et la quantification de l'incertitude. Il y a au moins trois types d'incertitude à prendre en compte :
- Incertitude des données due à l'erreur de mesure
- Incertitude due à des paramètres intrinsèquement variables
- Incertitude quant à la question de savoir si la structure du modèle représente pleinement le système réel
La comparaison des résultats initiaux du modèle avec les données observées peut suggérer que les résultats du modèle présentent une incertitude très élevée, et que le modèle n'est pas suffisamment robuste pour soutenir les décisions sans des modifications significatives de la structure du modèle, des paramètres ou de l'étalonnage du modèle, afin de terminer l'étape du développement. La validation peut indiquer que les résultats du modèle sont suffisamment robustes pour être utiles à la prise de décision de deux manières. Si l'incertitude est très faible, les modèles peuvent avoir une précision suffisante pour dire que « si l'effort de santé publique est modifié de X %, l'incidence changera de Y % » Cependant, les modèles peuvent aboutir à des résultats présentant un degré élevé d'incertitude, tout en étant suffisamment précis pour être utiles dans la réponse à des questions moins pointues, telles que « cela sera-t-il grand ou petit? » ou « vaut-il mieux faire X, Y ou ne rien faire? »
Types de projets de modélisation
Il existe deux types principaux de projets de modélisation prédictive : 1) la prévision et 2) l'exploration de scénarios. La prévision est l'utilisation de modèles mathématiques pour prédire la trajectoire d'une épidémie ou d'une éclosion dans un avenir proche ou lointain (e.g., la diapositive 7 dans Note de bas de page 51). La modélisation basée sur des scénarios consiste à utiliser des modèles pour répondre à des questions du type « que se passerait-il si? ». Les questions les plus courantes sont celles de l'impact épidémiologique potentiel (e.g., sur l'incidence, les hospitalisations, les décès) de diverses interventions (e.g., le traitement ou la vaccination, les INP) Note de bas de page 31Note de bas de page 52. La modélisation basée sur des scénarios évalue souvent les résultats sur plusieurs générations d'infections. Parfois, les prévisions peuvent également comporter des scénarios simplifiés. Par exemple, les prévisions en matière de COVID-19 de l'Agence comprenaient une prévision de la trajectoire actuelle de la maladie et des scénarios de ce qui pourrait se produire à court terme si les INP étaient renforcées ou assouplies.
Communiquer les résultats de la modélisation aux décideurs et au public
Il est essentiel de communiquer efficacement les résultats de la modélisation aux responsables de la santé publique et aux décideurs. Au-delà de la nécessité générale de disposer de bonnes méthodes de communication orale et visuelle utilisant un langage accessible, précis et sans jargon, il existe des exigences spécifiques à la modélisation. Premièrement, les objectifs de la modélisation doivent être clairs et placés dans le contexte des besoins des décideurs et, idéalement, les modélisateurs, les gestionnaires et les décideurs discutent et se mettent d'accord sur ce qui est nécessaire et possible dès le départ Note de bas de page 12. Les hypothèses et les limites des modèles, les résultats de la validation, ainsi que les sources et les degrés d'incertitude doivent être communiqués afin de préciser dans quelle mesure les résultats des modèles sont exploitables par les décideurs Note de bas de page 11Note de bas de page 53. La communication des résultats des modèles à un stade précoce de leur développement et des modèles dont les performances en matière de validation sont médiocres, ainsi que des résultats mal communiqués, seront probablement improductifs, voire contre-productifs, ce qui entraînera une perte de confiance dans la modélisation de la part des gestionnaires, des décideurs et des parties prenantes. La communication au public des résultats des modèles doit faire l'objet d'une attention particulière. Par exemple, la modélisation basée sur des scénarios réalisée au début de la pandémie de COVID-19 a été interprétée à tort par certains membres du public, de la presse et de la classe politique comme une prévision. Lorsque le scénario le plus pessimiste ne s'est pas produit (parce que des mesures de santé publique ont été mises en œuvre), on a eu l'impression que la modélisation était tout simplement erronée et que la COVID-19 était exagérée Note de bas de page 47.
Modélisation d'agents pathogènes pandémiques « hypothétiques, mais plausibles » avant que les pandémies ne surviennent
Objectif
La modélisation prépandémique vise à fournir une base pour les décisions relatives à la planification de la pandémie, y compris les ressources de soins de santé qui doivent être conservées dans les réserves nationales. Une modélisation basée sur des scénarios est nécessaire pour explorer l'ensemble des impacts potentiels sur les systèmes de santé canadiens d'agents pathogènes pandémiques « hypothétiques, mais plausibles » au Canada. Les résultats d'intérêt sont le nombre de cas, d'hospitalisations, de traitements en soins intensifs et de décès, ainsi que le taux auquel ils surviennent. Avec ces valeurs, on peut estimer les besoins en matière de soins de santé (capacité hospitalière, capacité des unités de soins intensifs, ventilateurs, équipements de protection individuelle, antiviraux) Note de bas de page 54 et évaluer les réserves pour les soins de santé (tels que la Réserve nationale stratégique d'urgence Note de bas de page 55) ainsi que les mesures INP nécessaires, en tenant compte de leurs incidences négatives sur la santé.
Modèles
Les modèles compartimentaux et les MBA peuvent être utilisés à cette fin. Les modèles basés sur des agents peuvent être particulièrement utiles pour étudier les impacts dans les communautés plus petites et/ou plus hétérogènes.
Agents pathogènes/types de maladies probables
Une hiérarchisation des agents pathogènes émergents probables de la pandémie reste à faire, mais les agents pathogènes zoonotiques qui deviennent transmissibles de personne à personne par contact ou par voie respiratoire (e.g., les grippes, les coronavirus, les fièvres hémorragiques) Note de bas de page 56Note de bas de page 57 sont considérés comme des candidats probables. Au moment de la rédaction du présent document, l'OMS a entrepris un processus qui vise plus spécifiquement à établir une liste d'agents pathogènes prioritaires à potentiel pandémique Note de bas de page 58.
Besoins en données
Les valeurs les « plus probables » des paramètres épidémiologiques peuvent être tirées de la littérature à l'aide de méthodes établies de synthèse des connaissances Note de bas de page 49.
Développement de méthodes de modélisation, d'outils et de personnel « prêts à l'emploi » face à une pandémie
Objectifs
Le développement de la modélisation face à une épidémie devrait garantir que les méthodes de modélisation et le personnel hautement qualifié (PHQ) nécessaire sont présents et prêts à répondre à une épidémie émergente au Canada.
Modèles
Des modèles compartimentaux et des MBA génériques, adaptables et de préférence validés doivent être développés à l'avance afin de pouvoir être adaptés à une pandémie émergente au Canada dans le but de faire des prévisions et de réaliser des modélisations basées sur des scénarios pour guider les interventions de santé publique. Les modèles fondés sur la modélisation des maladies respiratoires seraient probablement facilement adaptables à d'autres formes de transmission de personne à personne directe, mais il serait également utile de disposer de modèles plus explicitement conçus pour une variété de voies de transmission (e.g., la transmission sexuelle Note de bas de page 59). Les modèles d'importation doivent être prêts à estimer les taux et les voies d'importation des personnes infectieuses au Canada. Idéalement, les modèles de propagation géographique au Canada, permettant d'explorer les interventions qui limitent la propagation spatiale, seraient également prêts à être adaptés à un agent pathogène émergent. Il est également nécessaire de disposer de méthodes de modélisation et d'estimation qui améliorent l'analyse des données de surveillance, notamment l'estimation du nombre instantané de reproduction, Rt, la prévision à partir de la surveillance clinique et des données sur les eaux usées, et l'évaluation des données génomiques pour fournir des estimations des paramètres épidémiologiques clés, notamment R0 et l'avantage de sélection des variants émergents.
Besoins en données
Face à une pandémie émergente qui débute à l'extérieur du Canada, comme cela a été le cas lors de la pandémie de COVID-19, les valeurs de paramètres clés pour la modélisation apparaissent dans la littérature scientifique en constante évolution et des compétences en matière de synthèse des connaissances sont nécessaires pour être prêt à les trouver Note de bas de page 49. Idéalement, les estimations des valeurs des paramètres clés pour une série d'agents pathogènes tirées de la littérature actuelle permettraient d'alimenter les modèles avec les « meilleures estimations » au début d'une pandémie avant de quantifier les paramètres spécifiques à la pandémie émergente. Le Canada doit se préparer en matière de collecte, de partage et de couplage des données sur les cas avec les données d'hospitalisation et les données génomiques en tirant les leçons des difficultés rencontrées lors de la pandémie de COVID-19, ainsi que des succès dans l'obtention et le couplage des données sur les cas, les hospitalisations, les vaccinations et les données génomiques dans des pays tels que le Royaume-Uni Note de bas de page 50. En particulier, le Canada gagnerait à mettre en place un cadre d'accès aux données couplées pour les experts qualifiés, sous des conditions d'accès appropriées, bien avant que le besoin s'en fasse sentir.
Le besoin de personnel hautement qualifié (PHQ)
L'une des principales leçons apprises de la pandémie de COVID-19 est que les organismes de santé publique ont besoin de PHQ à l'interne pour pouvoir créer des modèles, réunir les compétences multidisciplinaires nécessaires et réaliser des modélisations utiles à des fins de santé publique. Les équipes de synthèse des connaissances sont essentielles pour intégrer dans les modèles des évidences qui évoluent rapidement; des géographes et des mathématiciens sont nécessaires pour la modélisation des importations, des réseaux et de la propagation; les épidémiologistes et les experts en médecine, microbiologie et immunologie sont requis pour garantir la réalité biologique; les experts en communication sont nécessaires pour expliquer au public les résultats de la modélisation technique; des méthodes sont nécessaires pour réunir ces compétences Note de bas de page 10. L'établissement d'un lien explicite entre ces PHQ et les modélisateurs du milieu universitaire permet à la modélisation au sein des organismes de santé publique de bénéficier des innovations en cours, de l'examen par les pairs, du renforcement des capacités de modélisation, du développement d'approches ensemble de modélisation et procure la transparence qui renforce la confiance du public dans la modélisation réalisée Note de bas de page 60. Sans expertise interne en matière de modélisation, la santé publique n'est pas préparée à répondre de manière adéquate aux épidémies et aux pandémies et doit se tourner vers des modélisateurs externes pour entreprendre le travail. La disponibilité et la capacité des modélisateurs externes ne seraient pas garanties et, en l'absence d'experts internes, la santé publique ne serait pas en mesure d'examiner ou d'adapter les modèles qui en résultent, ni de veiller à ce que les résultats soient communiqués avec précision aux décideurs, en raison de la perte de mémoire organisationnelle de la modélisation.
Le besoin d'une communauté nationale de praticiens de la modélisation
De nombreux pays ont reconnu l'importance de la contribution des modélisateurs universitaires à la prise de décision en matière de santé publique pendant la pandémie de COVID-19 Note de bas de page 47Note de bas de page 61. À la suite de la pandémie de SRAS-CoV-1 en 2003, une communauté de pratique de modélisateurs de maladies infectieuses s'est formée au Canada et s'est finalement fait connaître sous le nom de Pandemic Influenza Outbreak Research Modelling, ou Pan-InfORM, en 2008 Note de bas de page 62. Cette communauté vise à soutenir l'utilisation de la modélisation pour éclairer les décisions en cas de pandémie. Bien qu'elle ne soit pas spécifiquement axée sur la préparation à la pandémie, cette communauté de pratique a soutenu les décisions prises lors de la pandémie de grippe pH1N1 au Canada Note de bas de page 4Note de bas de page 63 et avait des liens avec des organisations de santé publique Note de bas de page 62. Bien que ce groupe ait poursuivi « en temps de paix » ses activités de modélisation de la transmission des maladies infectieuses en collaboration avec les organismes de santé publique jusqu'en 2018, entre cette date et le début de l'épidémie de COVID-19 au Canada en 2020, les liens avec la plupart des organismes de santé publique ont été perdus et de nouvelles communautés de pratique, telles que la Table scientifique de l'Ontario et le Groupe d'experts externes en modélisation de l'Agence Note de bas de page 64, ont dû être créées pour faire face à la pandémie. La perte de Pan-InfORM en tant que ressource reconnue pour la santé publique face à la COVID-19 souligne la nécessité pour les organisations de santé publique de disposer de PHQ à l'interne, capables de maintenir des communautés de pratique de modélisation en collaboration en dehors des périodes où nous répondons aux urgences liées aux maladies infectieuses.
La modélisation au service de la résilience face aux pandémies
Les études de modélisation peuvent contribuer à la résilience des organismes de santé publique face aux pandémies. Cette modélisation a une application générale pour la gestion des épidémies et la conception d'interventions utilisant des INP. Le tableau 1 présente une synthèse des moyens par lesquels la modélisation peut contribuer au développement de la résilience.
| Domaine d'intervention | Domaine d'intervention | Références |
|---|---|---|
| Conception des bâtiments | Améliorer la ventilation pour réduire la transmission des agents pathogènes respiratoires, en particulier dans les lieux où un grand nombre de personnes se rassemblent. | Note de bas de page 65Note de bas de page 66 |
Estimations à l'appui des décisions relatives aux capacités de santé publique |
Estimation de l'effort de surveillance nécessaire pour détecter les cas de pathogènes émergents. | Note de bas de page 67Note de bas de page 68 |
| Estimation de l'effort de test-et-traçage nécessaire pour contrôler la transmission, en l'absence de mesures restrictives, en fonction des différentes caractéristiques des agents pathogènes et des maladies qu'ils provoquent. | Note de bas de page 31Note de bas de page 69 | |
Outils pour les décisions stratégiques |
Critères permettant de déterminer si l'élimination d'un agent pathogène dans une juridiction donnée serait un succès ou si les mesures de santé publique devraient simplement viser à « aplanir la courbe » pour limiter les effets sur les soins de santé. | Note de bas de page 70 |
| Estimation de la probabilité de contrôle par test-et-traçage comparé au contrôle par des mesures restrictives, en fonction des caractéristiques des agents pathogènes et des maladies qu'ils provoquent (R0 et proportions de cas asymptomatiques, présymptomatiques ou présentant des manifestations graves). | Note de bas de page 71 | |
| Critères permettant de cibler les INP sur des groupes démographiques ou géographiques spécifiques de la population. | Note de bas de page 32Note de bas de page 72 | |
Pratiques exemplaires pour l'utilisation des mesures de santé publique |
Meilleures pratiques pour l'utilisation de mesures restrictives si celles-ci sont nécessaires pour contrôler la transmission. | Note de bas de page 52Note de bas de page 73 |
| Recommandations pour l'utilisation d'INP qui réduisent la probabilité ou l'impact de la transmission, telles que la distanciation, le port de masque et la cohorte lors de rassemblements. | Note de bas de page 73Note de bas de page 74Note de bas de page 78 | |
Abréviation : INP, interventions non pharmaceutiques |
||
Discussion
Principaux défis
La modélisation nécessite une infrastructure informatique, des logiciels et les mathématiques, mais aussi des équipes multidisciplinaires d'experts dans tous les aspects de la transmission des maladies et de la pratique de la santé publique pour que la modélisation soit ancrée dans la réalité biologique nécessaire à la prise de décision dans le domaine de la santé publique. De telles équipes ont été constituées au Canada lors de la pandémie de COVID-19, mais elles doivent être maintenues sous une forme ou une autre pour soutenir la préparation aux futures pandémies. Un problème persistant au Canada est la limitation de la collecte de données granulaires sur les cas de maladie, les cas hospitalisés, la caractérisation génomique des agents responsables et les métadonnées qui sont cruciales pour les analyses Note de bas de page 75Note de bas de page 76. Parallèlement, il est actuellement impossible de coupler les données de surveillance, les données hospitalières et les données génomiques entre les provinces et les territoires Note de bas de page 50. Ces problèmes de données font l'objet d'efforts considérables pour remédier aux problèmes de collecte, de couplage et de partage dans le cadre de la Stratégie pancanadienne de données sur la santé Note de bas de page 77 et, pour les données des systèmes de santé, dans la Feuille de route sur l'interopérabilité d'Inforoute Santé du Canada Note de bas de page 78, mais ils demeurent les défis les plus importants non résolus pour une modélisation efficace des maladies infectieuses au Canada.
Conclusion
La modélisation mathématique des maladies infectieuses est désormais reconnue comme une aide essentielle à la prise de décision en matière de préparation et de réponse de la santé publique aux éclosions, aux épidémies et aux pandémies. Une utilisation judicieuse de la modélisation peut soutenir la préparation à la pandémie en matière de stocks pour les services de santé et de planification nécessaires pour se préparer à une pandémie, tandis que des modèles prêts à l'emploi, des méthodes et du PHQ soutiendront la prise de décision tôt au début d'une pandémie. Les ressources de modélisation, en particulier le PHQ, doivent être maintenues dans les organisations de santé publique et dans les universités, ainsi que dans les réseaux de collaboration transdisciplinaires avec les scientifiques d'autres disciplines qui s'intéressent à la santé publique. L'un des principaux obstacles à une modélisation efficace des décisions de santé publique au Canada reste la question de la collecte et du partage des données de santé.
Déclaration des auteurs
NHO est à l'origine de l'article et a fourni un premier projet de cadre auquel tous les autres auteurs ont contribué. Il s'agit d'un projet du Réseau externe en modélisation des maladies infectieuses de l'Agence de la santé publique du Canada (REM-MI ASPC), une communauté de pratique nationale sur la modélisation mathématique des maladies infectieuses pour la santé publique, dont tous les auteurs sont membres. Les auteurs n'ont pas de conflits d'intérêts.
Références
- Notes de bas de page 1
-
Wu JT, Cowling BJ. The use of mathematical models to inform influenza pandemic preparedness and response. Exp Biol Med (Maywood) 2011;236(8):955–61. https://doi.org/10.1258/ebm.2010.010271
- Notes de bas de page 2
-
Viboud C, Sun K, Gaffey R, Ajelli M, Fumanelli L, Merler S, Zhang Q, Chowell G, Simonsen L, Vespignani A; RAPIDD Ebola Forecasting Challenge group. The RAPIDD ebola forecasting challenge: synthesis and lessons learnt. Epidemics 2018;22:13–21. https://doi.org/10.1016/j.epidem.2017.08.002
- Notes de bas de page 3
-
World Health Organization. Non-pharmaceutical public health measures for mitigating the risk and impact of epidemic and pandemic influenza. Geneva, CH: WHO; 2019. https://www.who.int/publications/i/item/non-pharmaceutical-public-health-measuresfor-mitigating-the-risk-and-impact-of-epidemic-and-pandemic-influenza
- Notes de bas de page 4
-
Fisman D. Pandemic Influenza Outbreak Research Modelling Team (Pan-InfORM). Modelling an influenza pandemic: A guide for the perplexed. CMAJ 2009;181(3-4):171–3. https://doi.org/10.1503/cmaj.090885
- Notes de bas de page 5
-
Tuite AR, Fisman DN, Kwong JC, Greer AL. Optimal pandemic influenza vaccine allocation strategies for the Canadian population. PLoS One 2010;5(5):e10520. https://doi.org/10.1371/journal.pone.0010520
- Notes de bas de page 6
-
Moghadas SM, Pizzi NJ, Wu J, Tamblyn SE, Fisman DN. Canada in the face of the 2009 H1N1 pandemic. Influenza Other Respir Viruses 2011;5(2):83–8. https://doi.org/10.1111/j.1750-2659.2010.00184.x
- Notes de bas de page 7
-
Greer AL, Schanzer D. Using a Dynamic Model to Consider Optimal Antiviral Stockpile Size in the Face of Pandemic Influenza Uncertainty. PLoS One 2013;8(6):e67253. https://doi.org/10.1371/journal.pone.0067253
- Notes de bas de page 8
-
World Health Organization. Prioritizing diseases for research and development in emergency contexts. Geneva, CH: WHO; 2024. https://www.who.int/activities/prioritizing-diseases-for-research-and-development-in-emergency-contexts
- Notes de bas de page 9
-
Ogden NH, Bouchard C, Brankston G, Brown E, Corrin T, Dibernardo A. La santé des Canadiens et des Canadiennes dans un climat en changement : faire progresser nos connaissances pour agir. Ottawa, ON : Santé Canada; 2022. [Consulté le 10 sept. 2024]. https://changingclimate.ca/health-in-a-changing-climate/fr/
- Notes de bas de page 10
-
Guillouzic S, MacLeod MR, Waller D, Bourdon S. How Flexible OR&A Teams Provided Decision Advantage through Pandemic Uncertainty. Proceedings of the 15th NATO Operational Research & Analysis Conference. 2021. https://cradpdf.drdc-rddc.gc.ca/PDFS/unc472/p815024_A1b.pdf#:~:text=How%20Flexible%20OR&A%20Teams%20Provided
- Notes de bas de page 11
-
Becker AD, Grantz KH, Hegde ST, Bérubé S, Cummings DA, Wesolowski A. Development and dissemination of infectious disease dynamic transmission models during the COVID-19 pandemic: what can we learn from other pathogens and how can we move forward? Lancet Digit Health 2021;3(1):e41–50. https://doi.org/10.1016/S2589-7500(20)30268-5
- Notes de bas de page 12
-
Thompson J, McClure R, Scott N, Hellard M, Abeysuriya R, Vidanaarachchi R, Thwaites J, Lazarus JV, Lavis J, Michie S, Bullen C, Prokopenko M, Chang SL, Cliff OM, Zachreson C, Blakely A, Wilson T, Ouakrim DA, Sundararajan V. A framework for considering the utility of models when facing tough decisions in public health: a guideline for policy-makers. Health Res Policy Syst 2022;20(1):107. https://doi.org/10.1186/s12961-022-00902-6
- Notes de bas de page 13
-
Brooks RJ, Tobias AM. Choosing the best model: level of detail complexity and model performance. Math Comput Model 1996;24(4):1–14. https://doi.org/10.1016/0895-7177(96)00103-3
- Notes de bas de page 14
-
Basu S, Andrews J. Complexity in mathematical models of public health policies: a guide for consumers of models. PLoS Med 2013;10(10):e1001540. https://doi.org/10.1371/journal.pmed.1001540
- Notes de bas de page 15
-
Li M, Dushoff J, Bolker BM. Fitting mechanistic epidemic models to data: A comparison of simple Markov chain Monte Carlo approaches. Stat Methods Med Res 2018;27(7):1956–67. https://doi.org/10.1177/0962280217747054
- Notes de bas de page 16
-
Vernon I, Owen J, Aylett-Bullock J, Cuesta-Lazaro C, Frawley J, Quera-Bofarull A, Sedgewick A, Shi D, Truong H, Turner M, Walker J, Caulfield T, Fong K, Krauss F. Bayesian emulation and history matching of JUNE. Philos Trans A Math Phys Eng Sci 2022;380(2233):20220039. https://doi.org/10.1098/rsta.2022.0039
- Notes de bas de page 17
-
Gallo L, Frasca M, Latora V, Russo G. Lack of practical identifiability may hamper reliable predictions in COVID-19 epidemic models. Sci Adv 2022;8(3):eabg5234. https://doi.org/10.1126/sciadv.abg5234
- Notes de bas de page 18
-
Bhattacharya P, Chen J, Hoops S, Machi D, Lewis B, Venkatramanan S, Wilson ML, Klahn B, Adiga A, Hurt B, Outten J, Adiga A, Warren A, Baek YY, Porebski P, Marathe A, Xie D, Swarup S, Vullikanti A, Mortveit H, Eubank S, Barrett CL, Marathe M. Data-driven scalable pipeline using national agent-based models for real-time pandemic response and decision support. Int J High Perform Comput Appl 2023;37(1):4–27. https://doi.org/10.1177/10943420221127034
- Notes de bas de page 19
-
Agence de la santé publique du Canada. La COVID-19 au Canada: Des données et une modélisation qui éclairent les mesures de la santé publique. Ottawa, ON : ASPC; 2020. https://www.canada.ca/fr/sante-publique/services/maladies/maladie-coronavirus-covid-19/recherches-donnees-epidemiologiques-economiques/modelisation-mathematique.html
- Notes de bas de page 20
-
Kleijnen JP. Verification and validation of simulation models. Eur J Oper Res 1995;82(1):145–62. https://doi.org/10.1016/0377-2217(94)00016-6
- Notes de bas de page 21
-
Balci O. Verification, Validation, and Testing. In Handbook of Simulation. Wiley Online Library 1998. https://doi.org/10.1002/9780470172445.ch10
- Notes de bas de page 22
-
Pollett S, Johansson MA, Reich NG, Brett-Major D, Del Valle SY, Venkatramanan S, Lowe R, Porco T, Berry IM, Deshpande A, Kraemer MU, Blazes DL, Pan-Ngum W, Vespigiani A, Mate SE, Silal SP, Kandula S, Sippy R, Quandelacy TM, Morgan JJ, Ball J, Morton LC, Althouse BM, Pavlin J, van Panhuis W, Riley S, Biggerstaff M, Viboud C, Brady O, Rivers C. Recommended reporting items for epidemic forecasting and prediction research: the EPIFORGE 2020 guidelines. PLoS Med 2021;18(10):e1003793. https://doi.org/10.1371/journal.pmed.1003793
- Notes de bas de page 23
-
Milwid RM, Gabriele-Rivet V, Ogden NH, Turgeon P, Fazil A, London D, de Montigny S, Rees EE. A methodology for estimating SARS-CoV-2 importation risk by air travel into Canada between July and November 2021. BMC Public Health 2024;24(1):1088. https://doi.org/10.1186/s12889-024-18563-1
- Notes de bas de page 24
-
Tardy O, Vincenot CE, Bouchard C, Ogden NH, Leighton PA. Context-dependent host dispersal and habitat fragmentation determine heterogeneity in infected tick burdens: an agent-based modelling study. R Soc Open Sci 2022;9(3):220245. https://doi.org/10.1098/rsos.220245
- Notes de bas de page 25
-
Prem K, Cook AR, Jit M. Projecting social contact matrices in 152 countries using contact surveys and demographic data. PLOS Comput Biol 2017;13(9):e1005697. https://doi.org/10.1371/journal.pcbi.1005697
- Notes de bas de page 26
-
Mistry D, Litvinova M, Pastore Y Piontti A, Chinazzi M, Fumanelli L, Gomes MF, Haque SA, Liu QH, Mu K, Xiong X, Halloran ME, Longini IM Jr, Merler S, Ajelli M, Vespignani A. Inferring high-resolution human mixing patterns for disease modeling. Nat Commun 2021;12(1):323. https://doi.org/10.1038/s41467-020-20544-y
- Notes de bas de page 27
-
van den Hoogen J, Okazawa S. A Stochastic Model of COVID-19 Infections During a Large-Scale Canadian Army Exercise. The 15th NATO Operations Research & Analysis (OR&A) Conference Proceedings: Emerging and Disruptive Technology NATO STO Review. Ottawa, ON: National Defence; 2022. https://cradpdf.drdc-rddc.gc.ca/PDFS/unc399/p814956_A1b.pdf
- Notes de bas de page 28
-
Okazawa S, van den Hoogen J, Guillouzic S. PyCoMod (Python Compartment Modelling) Programming Reference. Defence Research and Development Canada DRDC-RDDC-2023-D111. Ottawa, ON: Government of Canada; 2023. https://pubs.drdc-rddc.gc.ca/BASIS/pcandid/www/engpub/DDW?W%3DSYSNUM=817298&r=0
- Notes de bas de page 29
-
Day T, Kennedy DA, Read AF, Gandon S. Pathogen evolution during vaccination campaigns. PLoS Biol 2022;20(9):e3001804. https://doi.org/10.1371/journal.pbio.3001804
- Notes de bas de page 30
-
Otto SP, Day T, Arino J, Colijn C, Dushoff J, Li M, Mechai S, Van Domselaar G, Wu J, Earn DJ, Ogden NH. The origins and potential future of SARS-CoV-2 variants of concern in the evolving COVID-19 pandemic. Curr Biol 2021;31(14):R918–29. https://doi.org/10.1016/j.cub.2021.06.049
- Notes de bas de page 31
-
Ng V, Fazil A, Waddell LA, Bancej C, Turgeon P, Otten A, Atchessi N, Ogden NH. Projected effects of nonpharmaceutical public health interventions to prevent resurgence of SARS-CoV-2 transmission in Canada. CMAJ 2020;192(37):E1053–64. https://doi.org/10.1503/cmaj.200990
- Notes de bas de page 32
-
Gabriele-Rivet V, Spence KL, Ogden NH, Fazil A, Turgeon P, Otten A, Waddell LA, Ng V. Modelling the impact of age-stratified public health measures on SARS-CoV-2 transmission in Canada. R Soc Open Sci 2021;8(11):210834. https://doi.org/10.1098/rsos.210834
- Notes de bas de page 33
-
Tardy O, Bouchard C, Chamberland E, Fortin A, Lamirande P, Ogden NH, Leighton PA. Mechanistic movement models reveal ecological drivers of tick-borne pathogen spread. J R Soc Interface 2021;18(181):20210134. https://doi.org/10.1098/rsif.2021.0134
- Notes de bas de page 34
-
Mohammadi Z, Cojocaru M, Arino J, Hurford A. Importation models for travel-related SARS-CoV-2 cases reported in Newfoundland and Labrador during the COVID-19 pandemic. medRxiv 2023; 23291136. https://doi.org/10.1101/2023.06.08.23291136
- Notes de bas de page 35
-
Hurford A, Martignoni MM, Loredo-Osti JC, Anokye F, Arino J, Husain BS, Gaas B, Watmough J. Pandemic modelling for regions implementing an elimination strategy. J Theor Biol 2023;561:111378. https://doi.org/10.1016/j.jtbi.2022.111378
- Notes de bas de page 36
-
du Plessis L, McCrone JT, Zarebski AE, Hill V, Ruis C, Gutierrez B, Raghwani J, Ashworth J, Colquhoun R, Connor TR, Faria NR, Jackson B, Loman NJ, O'Toole Á, Nicholls SM, Parag KV, Scher E, Vasylyeva TI, Volz EM, Watts A, Bogoch II, Khan K, Aanensen DM, Kraemer MU, Rambaut A, Pybus OG; COVID-19 Genomics UK (COG-UK) Consortium. Establishment and lineage dynamics of the SARS-CoV-2 epidemic in the UK. Science 2021;371(6530):708–12. https://doi.org/10.1126/science.abf2946
- Notes de bas de page 37
-
Murall CL, Fournier E, Galvez JH, N'Guessan A, Reiling SJ, Quirion PO, Naderi S, Roy AM, Chen SH, Stretenowich P, Bourgey M, Bujold D, Gregoire R, Lepage P, St-Cyr J, Willet P, Dion R, Charest H, Lathrop M, Roger M, Bourque G, Ragoussis J, Shapiro BJ, Moreira S. A small number of early introductions seeded widespread transmission of SARS-CoV-2 in Québec, Canada. Genome Med 2021;13(1):169. https://doi.org/10.1186/s13073-021-00986-9
- Notes de bas de page 38
-
McLaughlin A, Montoya V, Miller RL, Mordecai GJ, Worobey M, Poon AF, Joy JB; Canadian COVID-19 Genomics Network (CanCOGen) Consortium. Genomic epidemiology of the first two waves of SARS-CoV-2 in Canada. eLife 2022;11:e73896. https://doi.org/10.7554/eLife.73896
- Notes de bas de page 39
-
Nextstrain: Real-time tracking of pathogen evolution. [Consulté le 27 août 2024]. https://nextstrain.org
- Notes de bas de page 40
-
Park SW, Sun K, Champredon D, Li M, Bolker BM, Earn DJ, Weitz JS, Grenfell BT, Dushoff J. Forward-looking serial intervals correctly link epidemic growth to reproduction numbers. Proc Natl Acad Sci USA 2021;118(2):e2011548118. https://doi.org/10.1073/pnas.2011548118
- Notes de bas de page 41
-
Dai X, Champredon D, Fazil A, Mangat CS, Peterson SW, Mejia EM, Lu X, Chekouo T. Statistical framework to support the epidemiological interpretation of SARS-CoV-2 concentration in municipal wastewater. Sci Rep 2022;12(1):13490. https://doi.org/10.1038/s41598-022-17543-y
- Notes de bas de page 42
-
Nourbakhsh S, Fazil A, Li M, Mangat CS, Peterson SW, Daigle J, Langner S, Shurgold J, D'Aoust P, Delatolla R, Mercier E, Pang X, Lee BE, Stuart R, Wijayasri S, Champredon D. A wastewater-based epidemic model for SARS-CoV-2 with application to three Canadian cities. Epidemics 2022;39:100560. https://doi.org/10.1016/j.epidem.2022.100560
- Notes de bas de page 43
-
Hellewell J, Abbott S, Gimma A, Bosse NI, Jarvis CI, Russell TW, Munday JD, Kucharski AJ, Edmunds WJ, Funk S, Eggo RM; Centre for the Mathematical Modelling of Infectious Diseases COVID-19 Working Group. Feasibility of controlling COVID-19 outbreaks by isolation of cases and contacts. Lancet Glob Health 2020;8(4):e488–96. https://doi.org/10.1016/S2214-109X(20)30074-7
- Notes de bas de page 44
-
Levesque J, Maybury DW, Shaw RH. A model of COVID-19 propagation based on a gamma subordinated negative binomial branching process. J Theor Biol 2021;512:110536. https://doi.org/10.1016/j.jtbi.2020.110536
- Notes de bas de page 45
-
Biron K, Drouin PL, Serre L. A branching process and simulation model to evaluate the spread of severe acute respiratory syndrome coronavirus 2 (SARS-Cov-2) in various environments: Enabling simultaneous mitigation strategies including social distancing masks symptomatic self isolation testing contact tracing and vaccination. Defence Research and Development Canada. Ottawa, ON: DRDC; 2023. https://pubs.drdc-rddc.gc.ca/BASIS/pcandid/www/engpub/DDW?W%3DSYSNUM=816419&r=0
- Notes de bas de page 46
-
Volz E, Mishra S, Chand M, Barrett JC, Johnson R, Geidelberg L, Hinsley WR, Laydon DJ, Dabrera G, O'Toole Á, Amato R, Ragonnet-Cronin M, Harrison I, Jackson B, Ariani CV, Boyd O, Loman NJ, McCrone JT, Gonçalves S, Jorgensen D, Myers R, Hill V, Jackson DK, Gaythorpe K, Groves N, Sillitoe J, Kwiatkowski DP, Flaxman S, Ratmann O, Bhatt S, Hopkins S, Gandy A, Rambaut A, Ferguson NM; COVID-19 Genomics UK (COG-UK) consortium. Assessing transmissibility of SARS-CoV-2 lineage B.1.1.7 in England. Nature 2021;593(7858):266–9. https://doi.org/10.1038/s41586-021-03470-x
- Notes de bas de page 47
-
Medley GF. A consensus of evidence: the role of SPI-M-O in the UK COVID-19 response. Adv Biol Regul 2022;86:100918. https://doi.org/10.1016/j.jbior.2022.100918
- Notes de bas de page 48
-
Yuan P, Tan Y, Yang L, Aruffo E, Ogden NH, Bélair J, Heffernan J, Arino J, Watmough J, Carabin H, Zhu H. Assessing transmission risks and control strategy for monkeypox as an emerging zoonosis in a metropolitan area. J Med Virol 2023;95(1):e28137. https://doi.org/10.1002/jmv.28137
- Notes de bas de page 49
-
Corrin T, Ayache D, Baumeister A, Young K, Pussegoda K, Ahmad R, Waddell L. Veille bibliographique de la COVID-19 – cadre pour gérer la littérature et appuyer la prise de décisions fondées sur des données probantes sur un sujet de santé publique en évolution rapide. Relevé des maladies transmissibles au Canada 2023;49(1):6–11. https://doi.org/10.14745/ccdr.v49i01a02f
- Notes de bas de page 50
-
Colijn C, Earn DJ, Dushoff J, Ogden NH, Li M, Knox N, Van Domselaar G, Franklin K, Jolly G, Otto SP. La nécessité d'une surveillance génomique liée du SRAS-CoV-2. Relevé des maladies transmissibles au Canada 2022;48(4):147–55. https://doi.org/10.14745/ccdr.v48i04a03f
- Notes de bas de page 51
-
Agence de la santé publique du Canada. Le point sur la COVID-19 au Canada : Épidémiologie et modélisation. Ottawa, ON : ASPC; 2021. https://www.canada.ca/content/dam/phac-aspc/documents/services/diseases-maladies/coronavirus-disease-covid-19/epidemiological-economic-research-data/update-covid-19-canada-epidemiology-modelling-20210903-fr.pdf
- Notes de bas de page 52
-
Ng V, Fazil A, Waddell LA, Turgeon P, Otten A, Ogden NH. Modelling the impact of shutdowns on resurging SARS-CoV-2 transmission in Canada. R Soc Open Sci 2021;8(5):210233. https://doi.org/10.1098/rsos.210233
- Notes de bas de page 53
-
McCabe R, Kont MD, Schmit N, Whittaker C, Løchen A, Walker PG, Ghani AC, Ferguson NM, White PJ, Donnelly CA, Watson OJ. Communicating uncertainty in epidemic models. Epidemics 2021;37:100520. https://doi.org/10.1016/j.epidem.2021.100520
- Notes de bas de page 54
-
Betti MI, Abouleish AH, Spofford V, Peddigrew C, Diener A, Heffernan JM. COVID-19 Vaccination and Healthcare Demand. Bull Math Biol 2023;85(5):32. https://doi.org/10.1007/s11538-023-01130-x
- Notes de bas de page 55
-
Agence de la santé publique du Canada. Réserve nationale stratégique d'urgence (RNSU). Ottawa, ON : ASPC; 2024. [Consulté le 10 sept. 2024]. https://canada.ca/fr/sante-publique/services/mesures-interventions-urgence/reserve-nationale-strategique-urgence.html
- Notes de bas de page 56
-
Meurens F, Dunoyer C, Fourichon C, Gerdts V, Haddad N, Kortekaas J, Lewandowska M, Monchatre-Leroy E, Summerfield A, Wichgers Schreur PJ, van der Poel WH, Zhu J. Animal board invited review: risks of zoonotic disease emergence at the interface of wildlife and livestock systems. Animal 2021;15(6):100241. https://doi.org/10.1016/j.animal.2021.100241
- Notes de bas de page 57
-
Mollentze N, Streicker DG. Predicting zoonotic potential of viruses: where are we? Curr Opin Virol 2023;61:101346. https://doi.org/10.1016/j.coviro.2023.101346
- Notes de bas de page 58
-
World Health Organization. WHO R&D Blueprint for Epidemics Updating the WHO list of pathogens with epidemic and PHEIC potential. Geneva, CH: WHO; 2022. [Consulté le 10 sept. 2024]. https://cdn.who.int/media/docs/default-source/blue-print/rd-blueprint_prioritization-2022_concept-note_v.1.pdf?sfvrsn=260e4e8f_3
- Notes de bas de page 59
-
Milwid RM, Li M, Fazil A, Maheu-Giroux M, Doyle CM, Xia Y, Cox J, Grace D, Dvorakova M, Walker SC, Mishra S, Ogden NH. Exploring the dynamics of the 2022 mpox outbreak in Canada. J Med Virol 2023;95(12):e29256. https://doi.org/10.1002/jmv.29256
- Notes de bas de page 60
-
Lewis MA, Brown P, Colijn C, Cowen L, Cotton C, Day T, Deardon R, Earn D, Haskell D, Heffernan J, Leighton P, Murty K, Otto S, Rafferty E, Hughes Tuohy C, Wu J, Zhu H. Charting a future for emerging infectious disease modelling in Canada. 2023. https://dspace.library.uvic.ca/server/api/core/bitstreams/5bd170ff-aa27-4fdf-af36-6e341c3749d8/content
- Notes de bas de page 61
-
Jit M, Cook AR. Informing Public Health Policies with Models for Disease Burden, Impact Evaluation, and Economic Evaluation. Annu Rev Public Health 2024;45(1):133–50. https://doi.org/10.1146/annurev-publhealth-060222-025149
- Notes de bas de page 62
-
Tariq M, Haworth-Brockman M, Moghadas SM. Ten years of Pan-InfORM: modelling research for public health in Canada. AIMS Public Health 2021;8(2):265–74. https://doi.org/10.3934/publichealth.2021020
- Notes de bas de page 63
-
Gojovic MZ, Sander B, Fisman D, Krahn MD, Bauch CT. Modelling mitigation strategies for pandemic (H1N1) 2009. CMAJ 2009;181(10):673–80. https://doi.org/10.1503/cmaj.091641
- Notes de bas de page 64
-
Bhatia D, Allin S, Di Ruggiero E. Mobilization of science advice by the Canadian federal government to support the COVID-19 pandemic response. Humanit Soc Sci Commun 2023;10(1):19. https://doi.org/10.1057/s41599-023-01501-8
- Notes de bas de page 65
-
Yan S, Wang L, Birnkrant MJ, Zhai Z, Miller SL. Multizone modeling of airborne SARS-CoV-2 quanta transmission and infection mitigation strategies in office hotel retail and school buildings. Buildings 2023;13(1):102. https://doi.org/10.3390/buildings13010102
- Notes de bas de page 66
-
World Health Organization. Airborne Risk Indoor Assessment. Geneva, CH: WHO; 2024. [Consulté le 10 sept. 2024]. https://partnersplatform.who.int/aria
- Notes de bas de page 67
-
Champredon D, Fazil A, Ogden NH. Méthodes simples de modélisation mathématique pour évaluer le risque de transmission du SRAS-CoV-2 pendant les rassemblements. Relevé des maladies transmissibles au Canada 2021;47(4):201–12. https://doi.org/10.14745/ccdr.v47i04a02f
- Notes de bas de page 68
-
Rees EE, Rodin R, Ogden NH. Approche de surveillance de la population afin de détecter les nouveaux agrégats de cas de COVID-19 et y répondre. Relevé des maladies transmissibles au Canada 2021;47(5/6):266–74. https://doi.org/10.14745/ccdr.v47i56a01f
- Notes de bas de page 69
-
Ludwig A, Berthiaume P, Orpana H, Nadeau C, Diasparra M, Barnes J, Hennessy D, Otten A, Ogden N. Évaluation de l'impact de divers niveaux de détection des cas et de recherche des contacts sur la transmission de la COVID-19 au Canada pendant la levée des fermetures imposées à l'aide d'un modèle à compartiments dynamique. Relevé des maladies transmissibles au Canada 2020;46(11/12):461–74. https://doi.org/10.14745/ccdr.v46i1112a08f
- Notes de bas de page 70
-
Martignoni MM, Arino J, Hurford A. Is SARS-CoV-2 elimination or mitigation best? Regional and disease characteristics determine the recommended strategy. R Soc Open Sci 2024;11(6):240186. https://doi.org/10.1098/rsos.240186
- Notes de bas de page 71
-
Tupper P, Otto SP, Colijn C. Fundamental limitations of contact tracing for COVID-19. Facets 2021;6:1993–2001. https://doi.org/10.1139/facets-2021-0016
- Notes de bas de page 72
-
Soucy JR, Ghasemi A, Sturrock SL, Berry I, Buchan SA, MacFadden DR, Brown KA. Trends in Interregional Travel to Shopping Malls and Restaurants Before and After Differential COVID-19 Restrictions in the Greater Toronto Area. JAMA Netw Open 2021;4(8):e2123139. https://doi.org/10.1001/jamanetworkopen.2021.23139
- Notes de bas de page 73
-
Hongoh V, Maybury D, Levesque J, Fazil A, Otten A, Turgeon P, Waddell L, Ogden NH. Aide multicritère à la décision pour l'évaluation du risque de transmission de la COVID-19 dans les lieux de rassemblement. Relevé des maladies transmissibles au Canada 2021;47(11):496–511. https://doi.org/10.14745/ccdr.v47i11a02f
- Notes de bas de page 74
-
Hoffman B, Gaas B, McPhee-Knowles S, Guillouzic S, Kanary L. Development of an age-adjusted activity-based contact probability model for infectious diseases. Facets 2024;9:1–11. https://doi.org/10.1139/facets-2023-0094
- Notes de bas de page 75
-
Wolfson M. COVID-19 data and modeling: we need to learn from and act on our experiences. Can J Public Health 2024;115(4):535–40. https://doi.org/10.17269/s41997-024-00917-2
- Notes de bas de page 76
-
Xia Y, Flores Anato JL, Colijn C, Janjua N, Irvine M, Williamson T, Varughese MB, Li M, Osgood N, Earn DJ, Sander B, Cipriano LE, Murty K, Xiu F, Godin A, Buckeridge D, Hurford A, Mishra S, Maheu-Giroux M. Canada's provincial COVID-19 pandemic modelling efforts: A review of mathematical models and their impacts on the responses. Can J Public Health 2024;115(4):541–57. https://doi.org/10.17269/s41997-024-00910-9
- Notes de bas de page 77
-
Agence de la santé publique du Canada. Collaboration avec des partenaires pour moderniser les données sur la santé publique. Ottawa, ON : ASPC; 2024. [Consulté le 10 sept. 2024]. https://www.canada.ca/fr/sante-publique/programmes/collaboration-avec-partenaires-moderniser-donnees-sante-publique.html
- Notes de bas de page 78
-
Inforoute Santé du Canada. Feuille de route commune de l'interopérabilité pancanadienne. 2023. [Consulté le 10 sept. 2024]. https://www.infoway-inforoute.ca/fr/component/edocman/6445-vous-connecter-a-des-soins-de-sante-modernes-feuille-de-route-commune-de-l-interoperabilite-pancanadienne/view-document?Itemid=107

Cette œuvre est mise à disposition selon les termes de la Licence Creative Commons Attribution 4.0 International