Résumé de l’éclosion de mpox au Canada, 28 avril au 31 décembre 2022

 Téléchargez cet article en format PDF (224 ko)
Téléchargez cet article en format PDF (224 ko)Publié par : L'Agence de la santé publique du Canada
Numéro : RMTC : Volume 51-2/3, février/mars 2025 : Économie de la santé en santé publique
Date de publication : février 2025
ISSN : 1719-3109
Soumettre un article
À propos du RMTC
Naviguer
Volume 51-2/3, février/mars 2025 : Économie de la santé en santé publique
Rapport d'éclosion
Résumé de l’éclosion de mpox au Canada, 28 avril au 31 décembre 2022
Meera Bhulabhai1, Jeyasakthi Venugopal2, Mireille Plamondon2, Geneviève Bergeron3, Geneviève Cadieux3, Jesse Kancir4, Mayank Singal5, Katherine Twohig5, Austin Zygmunt6, Erin Schillberg2, Rukshanda Ahmad7, Julia Paul2
Affiliations
1 Direction générale de la gestion des mesures d’urgence (DGGMU), Agence de la santé publique du Canada, Toronto, ON
2 Direction générale des programmes sur les maladies infectieuses et de la vaccination, Agence de la santé publique du Canada, Ottawa, ON
3 Direction régionale de santé publique de Montréal, Montréal, QC
4 Régie de la santé de la Nouvelle-Écosse, Halifax, NS
5 Centre de contrôle des maladies de la Colombie-Britannique, Vancouver, BC
6 Santé publique Ontario, Toronto, ON
7 Direction générale des données, de la surveillance et de la prospective, Agence de la santé publique du Canada, Ottawa, ON
Correspondance
Citation proposée
Bhulabhai M. Venugopal J, Plamondon M, Bergeron G, Cadieux G, Kancir J, Singal M, Twohig K, Zygmunt A, Schillberg E, Ahmad R, Paul J. Résumé de l’éclosion de mpox au Canada, 28 avril au 31 décembre 2022. Relevé des maladies transmissibles au Canada 2025;51(2/3):101–9. https://doi.org/10.14745/ccdr.v51i23a04f
Mots-clés : mpox, maladies transmissibles, zoonoses, orthopoxvirus, éclosions, hommes ayant des relations sexuelles avec d’autres hommes
Résumé
Contexte : La mpox est une maladie infectieuse causée par le virus de la variole simienne, étroitement lié au virus de la variole. En mai 2022, des cas de mpox ont été signalés dans des pays auparavant non endémiques, dont le Canada.
Objectif : Résumer l’épidémiologie de l’éclosion de mpox au Canada, ainsi que les principales activités de réponse de la santé publique, entre avril et décembre 2022.
Méthodes : L’Agence de la santé publique du Canada (l’Agence) a travaillé en étroite collaboration avec les autorités de santé publique locales, provinciales et territoriales, afin de mettre au point des outils nationaux d’enquête et de déclaration des cas, y compris des définitions nationales pour les cas confirmés et probables de mpox. Sur la base des données de cas anonymisées soumises à l’Agence, des modèles et des tendances ont été examinés, y compris la répartition des cas par facteurs sociodémographiques, cliniques et de transmission.
Résultats : Au total, 1 474 cas de mpox (1 396 confirmés, 78 probables) ont été signalés à l’Agence. Tous les cas signalés étaient associés au clade IIb du virus de la variole simienne. La mpox a touché de manière disproportionnée les personnes gays, bisexuels et les hommes ayant des relations sexuelles avec d’autres hommes (GBHARSAH) (80,0 %), ainsi que les personnes de 20 à 49 ans (86,0 %). Les données disponibles suggèrent que le mode d’acquisition le plus probable de la maladie est le contact sexuel, les données probantes concernant d’autres modes de transmission possibles étant limitées. Certains cas ont été hospitalisés (3,0 %), mais aucun décès lié à la mpox n’a été enregistré au Canada.
Conclusion : Des activités de coordination et de surveillance rapides ont permis de mettre en œuvre en temps utile des interventions adaptées, notamment l’approvisionnement et la distribution de vaccins. Ces mesures, associées à la vaccination et aux changements de comportement, ont contribué à réduire la transmission et les conséquences de la mpox sur la santé de la population canadienne.
Introduction
La mpox (anciennement variole simienne) est une maladie infectieuse virale causée par le virus de la variole simienne, qui fait partie du genre Orthopoxvirus. Découverte pour la première fois chez des primates non humains en 1958, cette maladie se manifeste chez l’humain par des symptômes semblables à ceux de la variole, mais avec un taux de létalité beaucoup plus faible Note de bas de page 1. Des années 1970 au début des années 2000, l’aire de répartition épidémiologique du virus de la variole simienne est restée principalement limitée à l’Afrique centrale et occidentale, en raison de la proximité de son réservoir animalier, notamment les rongeurs et autres petits mammifères Note de bas de page 1. La détection occasionnelle de cas en dehors de l’aire endémique traditionnelle du virus de la variole simienne était principalement due aux voyages et aux exportations d’animaux du réservoir Note de bas de page 2Note de bas de page 3Note de bas de page 4Note de bas de page 5Note de bas de page 6. Toutefois, une augmentation de la transmission chez l’humain a été observée au cours des deux dernières décennies, probablement en raison de changements à l’interface humain-environnement entraînant une augmentation des débordements zoonotiques, de la réduction de la protection croisée offerte par le vaccin contre la variole à la suite de la fin des programmes de vaccination mondiaux et de l’évolution génétique du virus de la variole simienne Note de bas de page 7.
Le 16 mai 2022, le Royaume-Uni a signalé un ensemble de cas de mpox chez des gays, bisexuels et hommes ayant des relations sexuelles avec d’autres hommes (GBHARSAH), sans antécédents de voyage dans une zone endémique Note de bas de page 8. Au Canada, la ville de Montréal au Québec a enquêté sur les premiers cas de mpox entre le 8 et le 13 mai 2022 Note de bas de page 9, et ce groupe de cas a ensuite été confirmé par le Laboratoire national de microbiologie de l’Agence de la santé publique du Canada (l’Agence) le 19 mai 2022 Note de bas de page 10. L’Agence a procédé à une évaluation préliminaire des risques, a fait passer son Centre des opérations du portefeuille de la santé au niveau 2 (vigilance accrue et préparation) le 21 mai 2022, et a activé un système de gestion des incidents, afin de répondre à l’émergence de la mpox et soutenir la coordination de l’enquête sur l’éclosion et des activités de réponse dans tout le pays, en collaboration avec les autorités de santé publique locales, provinciales et territoriales (LPT). Nous avons effectué une analyse descriptive des cas de mpox signalés au Canada entre avril et décembre 2022, et examiné les différences de caractéristiques sociodémographiques, cliniques et de transmission entre les sous-groupes GBHARSAH et non GBHARSAH.
Méthodes
Définition des cas, collecte des données et enquête
Après la déclaration initiale des cas de mpox au Canada, l'Agence a collaboré étroitement avec les services de santé publique locaux et provinciaux concernés, et a suivi les directives provisoires publiées par l'Organisation mondiale de la Santé Note de bas de page 11 pour élaborer des définitions de cas nationales (voir le tableau 1) Note de bas de page 12 et des outils d'investigation Note de bas de page 13. Ce travail s'est appuyé sur les observations épidémiologiques et cliniques effectuées par les unités de santé publique dans les régions concernées, ainsi que sur les données partagées par les partenaires internationaux. Cet échange rapide de connaissances entre les régions touchées a permis d'élaborer et d'harmoniser des outils normalisés pour les enquêtes de santé publique dans l'ensemble du pays. Les autorités de santé locales, provinciales et territoriales ont mené des enquêtes sur les cas, et les données ont été communiquées à l'Agence sur une base hebdomadaire. Par leurs enquêtes, les autorités de santé publique LPT ont recueilli des renseignements sur les caractéristiques démographiques, les symptômes et les manifestations cliniques, ainsi que sur les facteurs de risque pertinents, y compris les antécédents sexuels et de voyage récents. Elles ont effectué leurs propres tests moléculaires pour dépister ou confirmer les cas dans la mesure du possible, et ont bénéficié du soutien du Laboratoire national de microbiologie pour les tests de confirmation et le séquençage génomique, le cas échéant.
| Classification des cas | Définition |
|---|---|
| Confirmé | Une personne chez qui la présence du virus de la mpox simienne a été confirmée en laboratoire par la détection de séquences uniques d'ADN viral, par l'amplification en chaîne par polymérase en temps réel ou par séquençage |
| Probable | Toute personne, quel que soit son âge, qui présente une éruption ou une lésion aiguëNote de bas de page a inexpliquéeNote de bas de page b ET Qui présente une ou plusieurs des caractéristiques suivantes :
|
| Suspecté | Toute personne, quel que soit son âge, qui présente une ou plusieurs des caractéristiques suivantes :
|
|
|
Interventions
L'Agence de la santé publique du Canada a coordonné les différentes réponses à l'éclosion de mpox de 2022 au Canada. Un élément essentiel de la réponse de l'Agence a été le déploiement rapide de contre-mesures médicales à partir des stocks existants, principalement ImvamuneMD (Modified Vaccinia Ankara Bavarian Nordic), un vaccin approuvé à l'origine pour l'immunisation contre la variole. L'élargissement de l'indication du vaccin pour inclure l'immunisation contre tous les orthopoxvirus pour les adultes considérés comme présentant un risque élevé d'exposition avait été accordé par Santé Canada en 2020, ce qui a permis la mise en œuvre rapide d'un programme de vaccination en réponse à l'éclosion de mpox. Les autorités de santé LPT ont d'abord offert une dose du calendrier vaccinal à deux doses aux personnes admissibles, afin d'exploiter stratégiquement l'offre limitée de vaccins et de maximiser la participation à la vaccination. Suite aux premières recommandations émises par le Comité d'immunisation du Québec, la Direction régionale de santé publique de Montréal, au Québec, a lancé le premier programme de vaccination pour la prophylaxie postexposition contre la mpox le 30 mai 2022, qui a ensuite été élargi pour inclure la prophylaxie préexposition le 14 juin 2022 Note de bas de page 9. Le 8 juin 2022, le Comité consultatif national de l'immunisation a recommandé l'utilisation d'Imvamune pour la prophylaxie dans le contexte des éclosions de mpox au Canada Note de bas de page 14, favorisant la mise en œuvre rapide de programmes de vaccination contre la mpox dans toutes les autres administrations. L'Agence de la santé publique du Canada s'est approvisionnée en doses supplémentaires d'Imvamune pour soutenir l'expansion des activités de vaccination dans toutes les administrations. Elle a travaillé en étroite collaboration avec les autorités de santé LPT, afin d'établir des directives nationales harmonisées pour les professionnels de la santé Note de bas de page 13 ainsi que pour la gestion des cas et des contacts Note de bas de page 15. Elle a émis des directives de santé aux voyageurs et a diffusé une communication adaptée sur les risques par le biais de plateformes officielles, des journaux et des médias sociaux. L'activation de l'Agence de la santé publique du Canada a été ramenée à un niveau normal le 15 décembre 2022, à la suite d'une réduction soutenue du nombre de cas de mpox au Canada.
Analyse des données
Les personnes ayant une infection confirmée ou probable par la mpox et dont la maladie est apparue entre le 28 avril 2022 et le 31 décembre 2022 ont été incluses dans l'analyse. Une courbe épidémique a été élaborée pour résumer visuellement le nombre total de cas au fil du temps par date épidémiologique, définie comme la première date disponible dans la hiérarchie suivante : date d'apparition des symptômes, date de prélèvement des échantillons pour les tests de laboratoire et date de déclaration à l'unité locale de santé publique. Des statistiques descriptives ont été calculées pour résumer les schémas de cas en fonction des caractéristiques sociodémographiques, cliniques et de transmission. Les différences ont également été examinées entre les sous-groupes GBHARSAH et non GBHARSAH. Les différences statistiquement importantes dans les schémas de cas entre les GBHARSAH et les non GBHARSAH ont été déterminées sur la base d'un test t pour les variables continues et d'un test du chi carré ou d'un test exact de Fisher pour les variables catégorielles. Compte tenu du faible nombre de cas probables, les cas de mpox confirmés et probables ont été examinés ensemble pour toutes les analyses. Les renseignements sur les comportements sexuels n'ont pas été directement collectés à l'aide des formulaires de déclaration de cas, mais ont été déduits des données disponibles à partir des variables suivantes : sexe, genre et genre du ou des partenaires sexuels au cours des 21 jours précédant la date d'apparition des symptômes. Le lien épidémiologique fait référence au contact d'un cas connu avec un autre cas possible ou connu, ou au contact avec du matériel contaminé. Les données sont présentées sous forme de nombres et de pourcentages (%). Toutes les analyses ont été réalisées avec le logiciel statistique R Note de bas de page 16Note de bas de page 17.
Résultats
Au total, 1 474 cas de mpox ont été signalés à l'Agence en 2022 (1 396 confirmés; 78 probables). Les deux premiers cas de mpox ont été confirmés le 19 mai 2022, les symptômes du premier cas ayant débuté le 28 avril 2022. D'après les renseignements disponibles sur les tests de laboratoire et le séquençage génomique, tous les cas de mpox signalés en 2022 étaient associés au clade IIb du virus de la variole simienne. Comme le montre la figure 1, le nombre de cas a augmenté régulièrement, avec deux pointes au cours de l'été 2022. La majorité des cas ont été signalés en Ontario, au Québec et en Colombie-Britannique, représentant 96 % de l'ensemble des cas (tableau 2). Aucun cas n'a été signalé à l'Île-du-Prince-Édouard, au Nunavut et dans les Territoires du Nord-Ouest. Une diminution notable des cas a été observée à partir d'août 2022 et, en octobre 2022, les cas étaient plus sporadiques.
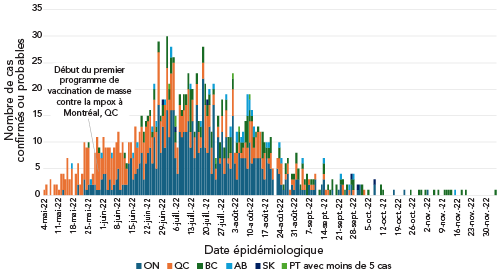
Figure 1 : Équivalent textuel
La figure 1 résume le nombre de cas confirmés ou probables signalés dans une province ou un territoire par jour entre le 28 avril 2022 et le 31 décembre 2022. Les cas sont résumés par date épidémiologique, c'est-à-dire la première date connue parmi les suivantes : date d'apparition des symptômes, date de prélèvement des échantillons pour des tests de laboratoire ou date de déclaration à l'unité locale de santé publique. Les cas des provinces ou territoires dont le nombre de cas cumulés est inférieur à cinq, c'est-à-dire le Manitoba, le Nouveau-Brunswick, la Nouvelle-Écosse, Terre-Neuve-et-Labrador et le Yukon, ont été regroupés et résumés ensemble. Les cas de l'Ontario sont représentés par des barres bleu foncé, ceux du Québec par des barres orange, ceux de la Colombie-Britannique par des barres vert foncé, ceux de l'Alberta par des barres bleu clair et ceux de la Saskatchewan par des barres violettes. Les provinces ou territoires dont le nombre de cas cumulés est inférieur à cinq sont représentés par des barres vert clair. Le début du premier programme de vaccination de masse à Montréal (Québec) est fixé au 30 mai 2022 dans la figure 1.
Notes de bas de page
Abréviations : AB, Alberta; BC, Colombie-Britannique; ON, Ontario; PT, provinces/territoires du Canada; QC, Québec; SK, Saskatchewan
| Caractéristiques | n (%) | Inconnu, n (%) |
|---|---|---|
| Nombre total de cas | 1 474 (100 %) | s.o. |
| Confirmé | 1 396 (94,7 %) | |
| Probable | 78 (5,3 %) | |
| Sexe | ||
| Masculin | 757 (98,7 %) | 707 (48,0 %) |
| Féminin | 9 (1,2 %) | |
| Genre | ||
| Femme | 11 (0,8 %) | 152 (10,3 %) |
| Homme | 1 296 (98,0 %) | |
| Transgenre | 4 (0,3 %) | |
| Non-binaire | 3 (0,2 %) | |
| Autre | 7 (0,5 %) | |
| Orientation sexuelle | ||
| GBHARSAH | 1 184 (80,3 %) | 244 (16,6 %) |
| Non GBHARSAH | 46 (3,1 %) | |
| Province | ||
| Ontario | 700 (47,5 %) | 0 (0,0 %) |
| Québec | 525 (35,6 %) | |
| Colombie-Britannique | 193 (13,1 %) | |
| Alberta | 43 (2,9 %) | |
| Saskatchewan | 6 (0,4 %) | |
| Terre-Neuve-et-Labrador | 2 (0,1 %) | |
| Yukon | 2 (0,1 %) | |
| Manitoba | 1 (0,1 %) | |
| Nouveau-Brunswick | 1 (0,1 %) | |
| Nouvelle-Écosse | 1 (0,1 %) | |
Abréviations : GBHARSAH, gays, bisexuels et hommes ayant des relations sexuelles avec d'autres hommes; non GBHARSAH, toutes les autres identités sexuelles, y compris celles pour lesquelles nous ne disposons pas de renseignements sur le sexe ou le genre et le genre du ou des partenaires sexuels; s.o., sans objet |
||
Les données disponibles sur le sexe et le genre étaient les suivantes : 99,0 % (n = 757/767) des cas étaient de sexe masculin (tableau 2) et 98,0 % (n = 1 296/1 322) s'identifiaient comme étant des hommes. Sur la base des renseignements disponibles concernant le sexe, le genre et le genre du ou des partenaires sexuels, 80,3 % (n = 1 184/1 474) ont été regroupés comme GBHARSAH, 3,1 % (n = 46/1 474) comme non GBHARSAH et l'information concernant le genre du ou des partenaires sexuels était inconnue pour 16,6 % (n = 244/1 474). La majorité des cas étaient âgés de 20 à 49 ans (86,1 %, n = 1 269/1 474), avec un âge moyen de 37 ans. Il n'y avait pas de différences importantes dans la répartition des cas par groupe d'âge entre les groupes GBHARSAH et non GBHARSAH (tableau 3). Près d'un tiers des cas pour lesquels des données sont disponibles (30,8 %, n = 299/972) ont déclaré vivre avec le VIH. Une proportion considérablement plus élevée de personnes ont déclaré vivre avec le VIH dans le groupe GBHARSAH (31,0 %, n = 246/793) par rapport au groupe non GBHARSAH (13,2 %, n = 5/38). De plus, 7,0 % (n = 48/244) des cas pour lesquels nous ne disposons pas de renseignements sur le genre du ou des partenaires sexuels ont déclaré vivre avec le VIH. Un diagnostic d'infection concomitante transmissible sexuellement ou par le sang a été rapporté dans 22,2 % (n = 209/941) des cas pour lesquels l'information était disponible, avec 22,7 % (n = 173/763) dans le groupe GBHARSAH et 20,6 % (n = 7/34) dans le groupe non GBHARSAH.
| Caractéristiques du cas | Global (N = 1 474) |
GBHARSAH (n = 1 184) |
Non GBHARSAH (n = 46) |
Valeur p |
|---|---|---|---|---|
| n (%) | ||||
| Groupe d'âge (années) | ||||
| Moins de 15 | 2 (0,1 %) | s.o. | s.o. | 0,281Note de bas de page b |
| 15 à 19 | 8 (0,5 %) | 6 (0,5 %) | 0 (0,0 %) | |
| 20 à 29 | 345 (23,4 %) | 271 (22,9 %) | 19 (41,3 %) | |
| 30 à 39 | 579 (39,3 %) | 475 (40,1 %) | 12 (26,1 %) | |
| 40 à 49 | 345 (23,4 %) | 276 (23,3 %) | 9 (19,6 %) | |
| 50 à 59 | 136 (9,2 %) | 111 (9,4 %) | 3 (6,5 %) | |
| 60 à 69 | 53 (3,6 %) | 41 (3,5 %) | 3 (6,5 %) | |
| 70 et plus | 5 (0,3 %) | 0 (0,0 %) | 0 (0,0 %) | |
| Hospitalisé | ||||
| Oui | 46 (3,4 %) | 35 (3,1 %) | 2 (4,3 %) | 0,651Note de bas de page c |
| Non | 1 319 (96,6 %) | 1 106 (96,9 %) | 44 (95,7 %) | |
| Admission en USI | ||||
| Oui | 3 (1,1 %) | 3 (1,2 %) | 0 (0,0 %) | 1,000Note de bas de page c |
| Non | 277 (98,9 %) | 244 (98,8 %) | 14 (100 %) | |
| Statut VIH | ||||
| Positif | 299 (30,8 %) | 246 (31,0 %) | 5 (13,2 %) | 0,019Note de bas de page a |
| Négative | 673 (69,2 %) | 547 (69,0 %) | 33 (86,8 %) | |
| ITSS concomitante | ||||
| Oui | 209 (22,2 %) | 173 (22,7 %) | 7 (20,6 %) | 0,776 |
| Non | 731 (77,8 %) | 590 (77,3 %) | 27 (79,4 %) | |
| Vacciné | ||||
| Oui | 307 (45,2 %) | 276 (47,4 %) | 2 (11,8 %) | 0,004Note de bas de page a |
| Non | 372 (54,8 %) | 306 (52,6 %) | 15 (88,2 %) | |
| Symptômes les plus fréquents | ||||
| Éruption cutanée ou lésion | 1 245 (89,1 %) | 1 061 (91,5 %) | 41 (89,1 %) | 0,588Note de bas de page c |
| Fièvre | 744 (76,2 %) | 634 (75,5 %) | 24 (85,7 %) | 0,213 |
| Frissons | 394 (75,2 %) | 331 (74,7 %) | 14 (82,4 %) | 0,580Note de bas de page c |
| Lymphadénopathie | 706 (73,2 %) | 610 (73,3 %) | 21 (65,6 %) | 0,336 |
| Fatigue ou épuisement | 699 (73,0 %) | 597 (72,0 %) | 23 (79,3 %) | 0,388 |
| Site de la lésion | ||||
| Anogénital | 483 (75,0 %) | 424 (76,4 %) | 14 (70,0 %) | 0,592Note de bas de page c |
| Visage | 197 (30,6 %) | 172 (31,0 %) | 7 (35,0 %) | 0,704 |
| Langue, bouche ou lèvre | 89 (13,8 %) | 78 (14,1 %) | 4 (20,0 %) | 0,510Note de bas de page c |
| Membres | 237 (36,8 %) | 199 (35,9 %) | 12 (60,0 %) | 0,028Note de bas de page a |
| Main | 153 (23,8 %) | 126 (22,7 %) | 6 (30,0 %) | 0,425Note de bas de page c |
| Pieds | 67 (10,4 %) | 52 (9,4 %) | 5 (25,0 %) | 0,039Note de bas de page aNote de bas de page b |
| Torse | 186 (28,9 %) | 161 (29,0 %) | 8 (40,0 %) | 0,289 |
| Nombre de lésions | ||||
| 1 ou moins | 33 (15,1 %) | 28 (15,0 %) | 1 (16,7 %) | 0,868Note de bas de page b |
| 2 à 9 | 126 (57,5 %) | 110 (58,8 %) | 3 (50,0 %) | |
| 10 à 49 | 53 (24,2 %) | 45 (24,1 %) | 2 (33,3 %) | |
| 50 à 99 | 5 (2,28 %) | 3 (1,6 %) | 0 (0,0 %) | |
| 100 ou plus | 2 (0,9 %) | 1 (0,5 %) | 0 (0,0 %) | |
| Expositions courantes et mode d'acquisition probable | ||||
| Contact avec un cas possible ou connu ou matériel contaminé | 191 (59,1 %) | 162 (57,9 %) | 3 (50,0 %) | 0,700Note de bas de page b |
| Transmission de personne à personne par contact sexuel | 717 (96,2 %) | 642 (97,1 %) | 16 (80,0 %) | 0,003Note de bas de page aNote de bas de page b |
| Antécédents de voyage dans les 21 jours précédant l'apparition des symptômes | 276 (22,1 %) | 241 (22,1 %) | 8 (17,8 %) | 0,489 |
Abréviations : GBHARSAH, gays, bisexuels et hommes ayant des rapports sexuels avec d'autres hommes; ITSS, infection transmise sexuellement ou par le sang; non GBHARSAH, toutes les autres identités sexuelles, y compris celles pour lesquelles nous ne disposons pas de renseignements sur le sexe ou le genre et le genre du ou des partenaires sexuels; s.o., sans objet; USI, unité de soins intensifs Note de bas de tableau 3
|
||||
Dans le groupe GBHARSAH, le contact sexuel était le mode d'acquisition le plus probable pour 97,1 % (n = 642/661) des cas, et 57,9 % (n = 162/280) des cas étaient liés d'un point de vue épidémiologique. Dans le groupe non GBHARSAH pour lesquels des données sont disponibles, le contact sexuel était le mode d'acquisition le plus probable pour 80,0 % (n = 16/20) des cas, alors que 50,0 % (n = 3/6) avaient un lien épidémiologique connu.
La majorité des cas ont fourni des renseignements sur leurs voyages récents au cours des 21 jours précédant l'apparition des symptômes (84,8 %, n = 1 250/1 474), 22,1 % (n = 276/1 250) ayant déclaré avoir voyagé à l'extérieur de leur province de résidence. Parmi ces derniers, 37,7 % (n = 104/276) ont déclaré des voyages internationaux, 36,6 % (n = 101/276) des voyages nationaux et 5,1 % (n = 14/276) des voyages à la fois internationaux et nationaux.
Parmi tous les cas pour lesquels des renseignements étaient disponibles, 45,2 % (n = 307/679) ont déclaré avoir reçu une vaccination pour un ou plusieurs des motifs suivants : vaccination antérieure contre la variole sans rapport avec l'éclosion actuelle; prophylaxie préexposition pour l'éclosion actuelle; ou prophylaxie postexposition pour l'éclosion actuelle. La proportion de personnes vaccinées était considérablement plus élevée chez les GBHARSAH (47,4 %, n = 276/582) que chez les non GBHARSAH (11,8 %, n = 2/17), ce qui reflète les critères d'admissibilité à la vaccination, fondés sur l'épidémiologie dans le contexte de l'éclosion au Canada.
Les cinq symptômes les plus fréquents signalés parmi les cas pour lesquels des données étaient disponibles étaient les suivants : éruption cutanée ou lésions (89,1 %, n = 1 245/1 398), fièvre (76,2 %, n = 744/977), frissons (75,2 %, n = 394/524), lymphadénopathie (73,2 %, n = 706/964) et fatigue ou épuisement (73,0 %, n = 699/958). Aucune différence importante n'a été observée dans la présentation des symptômes communs entre les groupes GBHARSAH et non GBHARSAH. La région anogénitale ou périanale était le site le plus souvent touché par l'éruption (75,0 %, n = 483/1 474). Une proportion considérablement plus élevée de cas dans le groupe non GBHARSAH a rapporté une éruption sur les membres (60,0 %, n = 12/20) et les pieds (25,0 %, n = 5/20) par rapport au groupe GBHARSAH (35,9 % et 9,4 %, respectivement). Parmi ceux qui ont fourni des renseignements sur le nombre de lésions, la majorité des cas ont fait état de deux à neuf lésions (57,5 %, n = 126/219).
Parmi tous les cas pour lesquels des renseignements étaient disponibles, 3,4 % (n = 46/1 365) ont été hospitalisés et 1,0 % (n = 3/300) ont été admis dans une unité de soins intensifs. Dans le groupe GBHARSAH, 3,1 % des cas (n = 35/1 141) ont été hospitalisés et 4,3 % (n = 2/46) des cas non GBHARSAH ont été hospitalisés. Aucune différence statistiquement importante n'a été observée entre les groupes GBHARSAH et non GBHARSAH en ce qui concerne les hospitalisations.
Discussion
Ce document décrit l'épidémiologie de l'éclosion multisectorielle de mpox au Canada entre avril et décembre 2022. L'éclosion de mpox de 2022 au Canada a principalement touché les personnes GBHARSAH dans les grandes villes métropolitaines (Toronto, Montréal et Vancouver) et le contact sexuel était la voie de transmission probable pour la plupart des cas Note de bas de page 9Note de bas de page 18Note de bas de page 19. Comme dans d'autres pays touchés par l'éclosion mondiale de mpox de 2022 Note de bas de page 20, la transmission initiale au sein de réseaux sexuels à fort contact a probablement été à l'origine de l'augmentation rapide du nombre de cas en juin 2022. Dans les groupes GBHARSAH et non GBHARSAH, les symptômes les plus fréquents étaient les suivants : éruption cutanée ou lésions, fièvre, frissons, lymphadénopathie et fatigue ou épuisement. Une proportion plus élevée de cas parmi les GBHARSAH vivaient avec le VIH, par rapport aux non GBHARSAH, ce qui concorde avec les résultats de l'éclosion mondiale de mpox de 2022 Note de bas de page 20. Cependant, aucune différence statistiquement importante n'a été observée dans le statut d'hospitalisation entre les deux groupes, et la majorité des cas n'ont pas nécessité d'hospitalisation, ce qui suggère une faible gravité de la maladie dans le contexte canadien. Aucun décès lié à la mpox n'a été signalé au Canada pendant toute la durée de l'éclosion.
Nos données montrent également que le pourcentage de cas associés à une transmission sexuelle est relativement plus faible dans le groupe non GBHARSAH que dans le groupe GBHARSAH. De plus, la présentation d'une éruption sur les membres et les pieds était considérablement plus fréquente chez les non GBHARSAH que chez les GBHARSAH, ce qui peut suggérer des sites d'inoculation et des schémas de lésions variables selon les sous-groupes. Une série de cas mondiaux examinant la transmission chez les femmes et les personnes non binaires dans 15 pays au cours de l'éclosion de mpox de 2022 a indiqué que l'acquisition par des contacts familiaux et professionnels étroits était plus fréquente dans ce groupe que par contact sexuel Note de bas de page 21. Au Canada, aucun cas de transmission professionnelle n'a été signalé et un nombre limité de cas ont été recensés parmi les contacts familiaux, y compris des enfants de moins de 15 ans. En raison du nombre limité de cas non GBHARSAH au Canada, il est difficile de tirer des conclusions sur d'autres modes de transmission possibles.
L'éclosion a été maîtrisée grâce à des approches à plusieurs niveaux, avec des efforts déployés à différents paliers de gouvernement, en s'appuyant fortement sur les liaisons existantes avec les unités de santé publique locales qui étaient les plus touchées par l'éclosion, ainsi que sur la mobilisation et la promotion des intérêts communautaires Au niveau fédéral, l'Agence : 1) a activé un système de gestion des incidents visant à coordonner et à répondre à l'éclosion émergente de mpox, 2) a effectué des évaluations des risques pour évaluer la situation nationale, 3) a recommandé des mesures fondées sur des données probantes et 4) a coordonné des réunions nationales pour partager des données et des renseignements, collaborer sur des produits et diffuser les meilleures pratiques afin de répondre efficacement à l'éclosion. Au niveau local, provincial et territorial, les stratégies réussies comprenaient des cliniques de vaccination de masse pour la prophylaxie préexposition, la gestion des cas et des contacts, les directives des professionnels de la santé et l'utilisation d'antiviraux pour les cas cliniquement graves Note de bas de page 9. Les autorités de santé publique LPT ont collaboré avec des organisations communautaires (e.g., l'Alliance pour la santé sexuelle des hommes gays en Ontario), pour aider à mobiliser les communautés touchées en leur transmettant des connaissances sur la mpox (e.g., les signes et les symptômes, la vaccination contre la mpox, les ressources de dépistage, les messages sur les pratiques sexuelles sûres, etc.) et encourager le dépistage en présence de symptômes compatibles par l'intermédiaire des médias sociaux et des applications de rencontres populaires.
Si la vaccination ciblée a joué un rôle important dans l'enrayement de l'éclosion de mpox Note de bas de page 22Note de bas de page 23, les données issues de modèles mathématiques calibrés sur les données canadiennes relatives aux cas et à la vaccination de 2022 ont mis en évidence l'importance de la modification des pratiques sexuelles comme facteur majeur de réduction de la transmission et de la durée de l'éclosion Note de bas de page 24.
La détection sporadique de cas de mpox continue de se produire dans le monde entier, avec de petites augmentations localisées de l'activité dans de nombreuses administrations, y compris au Canada, depuis 2022 Note de bas de page 25Note de bas de page 26. Il est donc important que les autorités poursuivent leurs efforts de surveillance de la mpox pour assurer la détection précoce d'une résurgence des cas, y compris de nouvelles éclosions liées à différentes lignées de virus de la variole simienne, et qu'elles continuent de proposer la vaccination contre la mpox aux personnes admissibles afin de réduire au minimum la transmission et la gravité de la maladie Note de bas de page 22Note de bas de page 23. La mpox est une maladie à déclaration obligatoire dans la plupart des provinces et territoires du Canada et, en août 2024, elle est devenue une maladie à déclaration obligatoire à l'échelle nationale, facilitant le travail de surveillance continue. L'Agence de la santé publique du Canada et les partenaires fédéraux et provinciaux collaborent et mènent des activités de surveillance, y compris la surveillance du virus de la variole simienne en laboratoire et dans les eaux usées Note de bas de page 27.
Limites
En raison de la complexité de la mise en place rapide d'une surveillance renforcée pour caractériser une infection émergente, plusieurs considérations sont à prendre en compte concernant la qualité et la cohérence des données communiquées. Tout d'abord, l'élaboration du formulaire national de rapport de cas a été itérative, certains renseignements maintenant jugés prioritaires pouvant être manquants dans les cas initiaux (e.g., la saisie de données élargies sur le genre). Ensuite, en raison de la diversité des systèmes de santé publique dans les LPT, certains renseignements n'ont pas pu être collectés ou étaient incomplets. Si les antécédents de vaccination contre la mpox ont pu atténuer l'étendue et la gravité de la présentation clinique globale des cas Note de bas de page 23, le nombre élevé de données manquantes concernant les antécédents de vaccination (54 %) dans l'ensemble de données nationales sur la mpox a empêché l'évaluation de cette variable dans le présent rapport. Certaines données, telles que les facteurs de risque et la source probable d'acquisition, ont également été déclarées sur une base volontaire et pourraient avoir été influencées par un biais de rappel ainsi que par la stigmatisation. Enfin, il est probable que le nombre de cas de mpox rapportés soit une sous-estimation du fardeau de la maladie réel, puisque les personnes présentant des symptômes bénins et qui n'ont pas consulté n'ont pas été testées pour le virus de la variole simienne.
Conclusion
Les schémas et les caractéristiques de l'éclosion de mpox au Canada étaient semblables à ceux d'autres pays impliqués dans l'éclosion mondiale de mpox de 2022, où les personnes GBHARSAH ont été touchées de manière disproportionnée. La modification des pratiques sexuelles et la vaccination ont permis de réduire rapidement la transmission de la mpox lors de l'éclosion de 2022 au Canada. Avec ses partenaires, l'Agence poursuivra sa surveillance attentive des cas et l'utilisation des pratiques fondées sur des données probantes pour soutenir la mise en œuvre en temps utile d'interventions de santé publique visant à réduire la transmission.
Déclaration des auteurs
- M. B. — Conceptualisation, enquête, méthodologie, analyse formelle, interprétation des données, rédaction de la version originale, rédaction–révision et édition
- J. V. — Conceptualisation, enquête, méthodologie, analyse formelle, interprétation des données, rédaction de la version originale, rédaction–révision et édition
- M. P. — Conceptualisation, méthodologie, interprétation des données, rédaction de la version originale, rédaction–révision et édition
- G. B. — Enquête, méthodologie, interprétation des données, rédaction–révision et édition
- G. C. — Enquête, méthodologie, interprétation des données, rédaction–révision et édition
- J. K. — Enquête, méthodologie, interprétation des données, rédaction–révision et édition
- M. S. — Enquête, méthodologie, interprétation des données, rédaction–révision et édition
- K. T. — Enquête, méthodologie, interprétation des données, rédaction–révision et édition
- A. Z. — Enquête, méthodologie, interprétation des données, rédaction–révision et édition
- E. S. — Enquête, méthodologie, interprétation des données, rédaction–révision et édition
- R. A. — Enquête, méthodologie, interprétation des données, rédaction–révision et édition
- J. P. — Conceptualisation, enquête, méthodologie, interprétation des données, rédaction–révision et édition
Intérêts concurrents
Aucun.
Identifiants ORCID
- Jeyasakthi Venugopal — 0000-0003-2233-5031
- Geneviève Bergeron — 0000-0001-9001-979X
- Katherine Twohig — 0000-0001-9514-0097
- Austin Zygmunt — 0000-0002-4219-6887
- Julia Paul — 0009-0000-9506-4311
Remerciements
Nous remercions les autorités de santé publique locales, provinciales et territoriales d'avoir mené des enquêtes de santé publique et d'avoir signalé et partagé des données sur les cas avec l'Agence. Nous tenons également à saluer le travail des partenaires fédéraux, notamment l'équipe du Système de gestion des incidents sur la mpox de l'Agence, qui a dirigé les activités d'intervention nationales, et le Centre de gestion, d'innovation et d'analyse des données, qui a géré la base de données nationale sur la mpox.
Financement
Ce travail a bénéficié du soutien de l'Agence de la santé publique du Canada, de Santé publique Ontario et du Centre de contrôle des maladies de la Colombie-Britannique.
Références
- Notes de bas de page 1
-
Jayswal S, Kakadiya J. A narrative review of pox: smallpox vs monkeypox. Egypt J Intern Med 2022;34(1):90–7. https://doi.org/10.1186/s43162-022-00174-0
- Notes de bas de page 2
-
Erez N, Achdout H, Milrot E, Schwartz Y, Wiener-Well Y, Paran N, Politi B, Tamir H, Israely T, Weiss S, Beth-Din A, Shifman O, Israeli O, Yitzhaki S, Shapira SC, Melamed S, Schwartz E. Diagnosis of Imported Monkeypox, Israel, 2018. Emerg Infect Dis 2019;25(5):980–3. https://doi.org/10.3201/eid2505.190076
- Notes de bas de page 3
-
Formenty P, Muntasir MO, Damon I, Chowdhary V, Opoka ML, Monimart C, Mutasim EM, Manuguerra JC, Davidson WB, Karem KL, Cabeza J, Wang S, Malik MR, Durand T, Khalid A, Rioton T, Kuong-Ruay A, Babiker AA, Karsani ME, Abdalla MS. Human monkeypox outbreak caused by novel virus belonging to Congo Basin clade, Sudan, 2005. Emerg Infect Dis 2010;16(10):1539–45. https://doi.org/10.3201/eid1610.100713
- Notes de bas de page 4
-
Yong SE, Ng OT, Ho ZJ, Mak TM, Marimuthu K, Vasoo S, Yeo TW, Ng YK, Cui L, Ferdous Z, Chia PY, Aw BJ, Manauis CM, Low CK, Chan G, Peh X, Lim PL, Chow LP, Chan M, Lee VJ, Lin RT, Heng MK, Leo YS. Imported Monkeypox, Singapore. Emerg Infect Dis 2020;26(8):1826–30. https://doi.org/10.3201/eid2608.191387
- Notes de bas de page 5
-
Vaughan A, Aarons E, Astbury J, Balasegaram S, Beadsworth M, Beck CR, Chand M, O’Connor C, Dunning J, Ghebrehewet S, Harper N, Howlett-Shipley R, Ihekweazu C, Jacobs M, Kaindama L, Katwa P, Khoo S, Lamb L, Mawdsley S, Morgan D, Palmer R, Phin N, Russell K, Said B, Simpson A, Vivancos R, Wade M, Walsh A, Wilburn J. Two cases of monkeypox imported to the United Kingdom, September 2018. Euro Surveill 2018;23(38):1800509. https://doi.org/10.2807/1560-7917.ES.2018.23.38.1800509
- Notes de bas de page 6
-
Centers for Disease Control and Prevention. Update: multistate outbreak of monkeypox--Illinois, Indiana, Kansas, Missouri, Ohio, and Wisconsin, 2003. MMWR Morbid Mortal Wkly Rep 2003;52(27):642–6. https://www.cdc.gov/mmwr/preview/mmwrhtml/mm5227a5.htm
- Notes de bas de page 7
-
Zebardast A, Latifi T, Shafiei-Jandaghi NZ, Gholami Barzoki M, Shatizadeh Malekshahi S. Plausible reasons for the resurgence of Mpox (formerly Monkeypox): an overview. Trop Dis Travel Med Vaccines 2023;9(1):23. https://doi.org/10.1186/s40794-023-00209-6
- Notes de bas de page 8
-
UK Health Security Agency. News story: Monkeypox cases confirmed in England – latest updates. London, UK: Government of the UK; 2022. [Consulté le 15 mars 2024]. https://www.gov.uk/government/news/monkeypox-cases-confirmed-in-england-latest-updates
- Notes de bas de page 9
-
Harrison LB, Bergeron G, Cadieux G, Charest H, Fafard J, Levade I, Blais AC, Huchet E, Trottier B, Vlad D, Szabo J, Thomas R, Poulin S, Greenaway C, Zaharatos GJ, Oughton M, Chakravarti A, Pilarski R, Bui-Nguyen A, Benomar K, Libman MD, Vinh DC, Duggan AT, Graham M, Klein MB, Barkati S. Monkeypox in Montréal: Epidemiology, Phylogenomics, and Public Health Response to a Large North American Outbreak. Ann Intern Med 2023;176(1):67–76. https://doi.org/10.7326/M22-2699
- Notes de bas de page 10
-
Agence de la santé publique du Canada. Dossier sur la variole simienne, juin 2022. Relevé des maladies transmissibles au Canada 2022;48(6):321. https://www.canada.ca/fr/sante-publique/services/rapports-publications/releve-maladies-transmissibles-canada-rmtc/numero-mensuel/2022-48/numero-6-juin-2022/variole-simienne-canada-2022.html
- Notes de bas de page 11
-
World Health Organization. Multi-country monkeypox outbreak in non-endemic countries 2022. Geneva, CH: WHO; 2022. [Consulté le 4 avril 2024]. https://www.who.int/emergencies/disease-outbreak-news/item/2022-DON385
- Notes de bas de page 12
-
Agence de la santé publique du Canada. Définition nationale de cas : Mpox (variole simienne). Ottawa, ON : ASPC; 2022. https://www.canada.ca/fr/sante-publique/services/maladies/mpox/professionnels-sante/definition-nationale-cas.html
- Notes de bas de page 13
-
Agence de la santé publique du Canada. Mpox (variole simienne) : Pour les professionnels de la santé. Ottawa, ON : ASPC; 2024. [Consulté le 4 avril 2024]. https://www.canada.ca/fr/sante-publique/services/maladies/mpox/professionnels-sante.html
- Notes de bas de page 14
-
Agence de la santé publique du Canada. Réponse rapide du CCNI : Orientations provisoires sur l’utilisation d’Imvamune dans le contexte des éclosions de variole simienne au Canada. Ottawa, ON : ASPC; 2024. https://www.canada.ca/fr/sante-publique/services/immunisation/comite-consultatif-national-immunisation-ccni/orientations-imvamune-variole-simienne.html
- Notes de bas de page 15
-
Agence de la santé publique du Canada. Mpox : Prise en charge par la santé publique des cas humains et des contacts qui y sont associés au Canada. Ottawa, ON : ASPC; 2024. [Consulté le 15 mars 2024]. https://www.canada.ca/fr/sante-publique/services/maladies/mpox/professionnels-sante/prise-charge-cas-contacts.html
- Notes de bas de page 16
-
R Core Team. R: A language and environment for statistical computing. R Core Team: Vienna, AT: GBIF; 2022. https://www.gbif.org/tool/81287/r-a-language-and-environment-for-statistical-computing
- Notes de bas de page 17
-
RStudio Team. RStudio: Integrated Development for R. Boston, MA: RStudio; 2022. https://www.r-project.org/conferences/useR-2011/abstracts/180111-allairejj.pdf
- Notes de bas de page 18
-
BC Centre for Disease Control. Mpox. Vancouver, BC: BCCDC. [Consulté le 15 mars 2024]. http://www.bccdc.ca/health-info/diseases-conditions/mpox#summary
- Notes de bas de page 19
-
Santé publique Ontario. Résumé épidémiologique amélioré : L’orthopoxvirose simienne en Ontario : du 1er mai 2022 au 31 juillet 2023. Toronto, ON : SPO; 2023. https://www.publichealthontario.ca/-/media/Documents/M/2022/monkeypox-episummary.pdf?rev=b056cead9ea246a0aa897baebc38872a&la=fr
- Notes de bas de page 20
-
World Health Organization. 2022-24 Mpox (Monkeypox) Outbreak: Global Trends. Geneva, CH: WHO; 2024. https://worldhealthorg.shinyapps.io/mpx_global/
- Notes de bas de page 21
-
Thornhill JP, Palich R, Ghosn J, Walmsley S, Moschese D, Cortes CP, Galliez RM, Garlin AB, Nozza S, Mitja O, Radix AE, Blanco JL, Crabtree-Ramirez B, Thompson M, Wiese L, Schulbin H, Levcovich A, Falcone M, Lucchini A, Sendagorta E, Treutiger CJ, Byrne R, Coyne K, Meyerowitz EA, Grahn AM, Hansen AE, Pourcher V, DellaPiazza M, Lee R, Stoeckle M, Hazra A, Apea V, Rubenstein E, Jones J, Wilkin A, Ganesan A, Henao-Martínez AF, Chow EJ, Titanji BK, Zucker JE, Ogoina D, Orkin CM; Share-Net writing group. Human monkeypox virus infection in women and non-binary individuals during the 2022 outbreaks: a global case series. Lancet 2022;400(10367):1953–65. https://doi.org/10.1016/S0140-6736(22)02187-0
- Notes de bas de page 22
-
Brousseau N, Carazo S, Febriani Y, Padet L, Hegg-Deloye S, Cadieux G, Bergeron G, Fafard J, Charest H, Lambert G, Talbot D, Longtin J, Dumont-Blais A, Bastien S, Dalpé V, Minot PH, De Serres G, Skowronski DM. Single-dose Effectiveness of Mpox Vaccine in Quebec, Canada: Test-negative Design With and Without Adjustment for Self-reported Exposure Risk. Clin Infect Dis 2024;78(2):461–9. https://doi.org/10.1093/cid/ciad584
- Notes de bas de page 23
-
Allard R, Leclerc P, Bergeron G, Cadieux G. Breakthrough cases of mpox: one-dose vaccination is associated with milder clinical manifestations. J Infect Public Health 2024;17(4):676–80. https://doi.org/10.1016/j.jiph.2024.02.015
- Notes de bas de page 24
-
Milwid RM, Li M, Fazil A, Maheu-Giroux M, Doyle CM, Xia Y, Cox J, Grace D, Dvorakova M, Walker SC, Mishra S, Ogden NH. Exploring the dynamics of the 2022 mpox outbreak in Canada. J Med Virol 2023;95(12):e29256. https://doi.org/10.1002/jmv.29256
- Notes de bas de page 25
-
Leonard CM, Poortinga K, Nguyen E, Karan A, Kulkarni S, Cohen R, Garrigues JM, Marutani AN, Green NM, Kim AA, Sey K, Pérez MJ. Mpox Outbreak - Los Angeles County, California, May 4–August 17, 2023. MMWR Morb Mortal Wkly Rep 2024;73(2):44–8. https://doi.org/10.15585/mmwr.mm7302a4
- Notes de bas de page 26
-
Pisano L, Magliulo M, Turco M, Farini J, Rapaccini AL, Lagi F, Bartoloni A, Pimpinelli N. The never-ending story of mpox epidemic: tracing a new cluster in Florence, Italy. Travel Med Infect Dis 2024;59:102704. https://doi.org/10.1016/j.tmaid.2024.102704
- Notes de bas de page 27
-
Sachdeva H, Shahin R, Ota S, Isabel S, Mangat CS, Stuart R, Padhi S, Chris A, Mishra S, Tan DH, Braukmann TW, Eshaghi A, Mejia EM, Hizon NA, Finkelstein M. Preparing for Mpox Resurgence: Surveillance Lessons From Outbreaks in Toronto, Canada. J Infect Dis 2024;229 Supplement_2:S305–12. https://doi.org/10.1093/infdis/jiad533
Appendice
Du matériel supplémentaire est disponible sur demande auprès de l'auteur : elissa.abrams@phac-aspc.gc.ca

Cette œuvre est mise à disposition selon les termes de la Licence Creative Commons Attribution 4.0 International