La vaccination antigrippale contribue-t-elle à la prévention des événements cardiovasculaires?

 Téléchargez cet article en format PDF (1.1 Mo)
Téléchargez cet article en format PDF (1.1 Mo)Publié par : L'Agence de la santé publique du Canada
Numéro : RMTC : Volume 51-9, septembre 2025 : Science de la mise en œuvre en santé publique
Date de publication : septembre 2025
ISSN : 1719-3109
Soumettre un article
À propos du RMTC
Naviguer
Volume 51-9, septembre 2025 : Science de la mise en œuvre en santé publique
Recherche
La vaccination antigrippale contribue-t-elle à la prévention des événements cardiovasculaires? Revue des données probantes
Fazia Tadount1,2, Nadine Sicard1, Winnie Siu1,3, Pamela Doyon-Plourde1, Angela Sinilaité1
Affiliations
1 Agence de la santé publique du Canada, Ottawa, ON
2 Département de microbiologie, infectiologie et immunologie, Université de Montréal, Montréal, QC
3 École d’épidémiologie et de santé publique, Université d’Ottawa, Ottawa, ON
Correspondance
Citation proposée
Tadount F, Sicard N, Siu W, Doyon-Plourde P, Sinilaité A. La vaccination antigrippale contribue-t-elle à la prévention des événements cardiovasculaires? Revue des données probantes. Relevé des maladies transmissibles au Canada 2025;51(9):360−73. https://doi.org/10.14745/ccdr.v51i09a02f
Mots-clés : vaccin antigrippal, événements cardiovasculaires, efficacité réelle du vaccin, infarctus du myocarde, accident vasculaire cérébral
Résumé
Contexte : Il existe de plus en plus de données probantes sur les avantages potentiels de la vaccination antigrippale sur la survenue d’événements cardiovasculaires.
Objectif : La présente revue d’examens systématiques et méta-analyses (ESMA) vise à résumer les données probantes disponibles sur le risque d’événements cardiovasculaires chez les adultes après la réception du vaccin antigrippal.
Méthodes : Quatre bases de données électroniques ont été consultées (CINAHL, PubMed, SYSVAC et la bibliothèque Cochrane) pour y retrouver des ESMA publiés en anglais ou en français entre le 1er janvier 2000 et le 14 janvier 2025. Les ESMA admissibles étaient ceux qui présentaient une synthèse quantitative des données examinant l’association entre la vaccination antigrippale et le risque d’événements cardiovasculaires chez les adultes. Les données des ESMA inclus ont été extraites à l’aide de variables prédéfinies. La qualité de chaque ESMA a été évaluée par deux examinateurs indépendants à l’aide de l’outil AMSTAR 2.
Résultats : La revue a porté sur 25 ESMA publiés entre 2012 et 2024. Dans l’ensemble, 15 ESMA ont été jugés de qualité moyenne ou élevée et ont fait l’objet d’un examen plus approfondi dans le cadre de la synthèse des données probantes. Les issues cliniques les plus fréquemment évaluées étaient l’infarctus du myocarde (IM), la mortalité toutes causes confondues et d’origine cardiovasculaire, ainsi que les événements cardiovasculaires indésirables majeurs (ECIM). Chez les personnes vaccinées présentant un risque élevé d’événements cardiovasculaires, le risque de décès d’origine cardiovasculaire a été réduit considérablement de 23 % à 47 %, le risque d’ECIM de 26 % à 37 %, le risque d’infarctus du myocarde de 29 % à 34 % et le risque d’accident vasculaire cérébral (AVC) de 13 % à 19 %, par rapport aux personnes non vaccinées.
Conclusion : Des données probantes de grande qualité issues de la littérature existante confirment que la vaccination antigrippale est une mesure préventive efficace pour réduire le fardeau de maladie cardiovasculaire. La mise en évidence de cet avantage pour les patients pourrait accroître le taux de vaccination et réduire les cas de grippe et de maladies cardiovasculaires, en particulier aux endroits où la couverture vaccinale reste sous-optimale.
Introduction
Les maladies cardiovasculaires (MCV) sont la principale cause de mortalité dans le monde Footnote 1. En 2021, les décès imputables aux cardiopathies ischémiques (CI) et aux AVC représentaient 23 % (~16 millions) des décès dans le monde Footnote 1. La surmortalité due aux MCV pendant les épidémies de grippe a été reconnue pour la première fois au début du XXe siècle Footnote 2. Depuis, des études ont montré une association importante au niveau clinique entre les infections respiratoires, en particulier la grippe, et les MCV Footnote 3Footnote 4Footnote 5Footnote 6Footnote 7Footnote 8. Le risque d’événements cardiovasculaires, tels que l’insuffisance cardiaque (IC), l’IM et l’AVC, est plusieurs fois plus élevé suite à une infection respiratoire qu’en l’absence d’infection et augmente proportionnellement à la gravité de l’infection Footnote 2Footnote 3Footnote 4Footnote 5Footnote 6.
Malgré la disponibilité du vaccin, la grippe saisonnière est à l’origine d’une morbidité et d’une mortalité importantes Footnote 9. Une partie de son fardeau de morbidité est liée aux événements cardiovasculaires, notamment l’IM, l’IC et l’AVC, en particulier chez les personnes souffrant de troubles cardiaques préexistants, tels que l’IC chronique ou la cardiomyopathie Footnote 10. Au niveau mondial, on estime que de 3 % à 5 % des décès dus aux CI peuvent être attribués à la grippe, ce qui correspond à 200 000 à 400 000 décès dus aux CI chaque année Footnote 11. Des études ont montré qu’une infection grippale peut provoquer des modifications cardiaques directes et que la réponse de l’hôte à l’infection par le virus de la grippe peut augmenter la circulation des médiateurs inflammatoires et activer les cellules immunitaires susceptibles de provoquer des lésions dans le système cardiovasculaire Footnote 8.
La vaccination contre la grippe saisonnière est un moyen de protection efficace contre la grippe grave et ses complications Footnote 12. En outre, les données probantes des effets cardioprotecteurs des vaccins antigrippaux s’accumulent Footnote 8Footnote 13. Au cours de la dernière décennie, de nombreux essais contrôlés randomisés (ECR) et études observationnelles ont été menés pour explorer cette association potentielle. Au Canada, le Comité consultatif national de l’immunisation (CCNI) identifie les personnes à haut risque de complications ou d’hospitalisations liées à la grippe, y compris les personnes souffrant de maladies chroniques, telles que des troubles cardiaques ou pulmonaires, comme une population pour laquelle la vaccination annuelle contre la grippe saisonnière est particulièrement importante Footnote 14. Toutefois, la couverture vaccinale contre la grippe saisonnière n’est pas optimale, y compris dans les populations à haut risque Footnote 15. Des recommandations similaires ont été formulées dans d’autres pays, tels que le Royaume-Uni, les États-Unis et l’Australie Footnote 16Footnote 17Footnote 18.
Plusieurs examens systématiques et méta-analyses (ESMA) évaluant la protection secondaire des vaccins antigrippaux contre les événements cardiovasculaires ont été publiés Footnote 13. L’objectif était donc de procéder à un examen des données probantes afin de fournir un résumé complet des ESMA publiés qui ont évalué l’effet de la vaccination contre la grippe saisonnière sur les événements cardiovasculaires.
Méthodes
La présente revue a été effectuée selon un protocole préétabli et conformément aux recommandations du groupe d’experts Systematic Reviews on Vaccines (SYSVAC) sur l’utilisation des examens systématiques existants pour élaborer des recommandations en matière de vaccination fondées sur des données probantes Footnote 19.
Stratégie de recherche et identification d’études
Une stratégie de recherche a priori a été élaborée pour identifier les études pertinentes dans PubMed, CINAHL, la bibliothèque Cochrane et le registre de SYSVAC. La stratégie de recherche détaillée se trouve dans l’appendice, matériel supplémentaire A. Dans un premier temps, nous avons recherché les études publiées entre le 1er janvier 2000 et le 27 mars 2024, en anglais ou en français. La recherche a été mise à jour le 14 janvier 2025 afin d’intégrer les dernières données probantes disponibles. Après les recherches dans les bases de données électroniques, les dossiers identifiés ont été téléchargés dans la plateforme DistillerSR pour le processus d’examen. Un évaluateur a procédé à la sélection des titres et des résumés, puis à la sélection des textes intégraux afin d’évaluer l’admissibilité des études. Pour être incluse dans l’examen, chaque étude devait être un ESMA; les examens systématiques ne contenant qu’un résumé narratif et aucune méta-analyse ont été exclus. En outre, la composante Population, Intervention, Comparaison et Résultat(s) (PICO) de chaque ESMA et la pertinence des questions de recherche ont été évaluées. Les ESMA pertinents étaient admissibles si chacune des définitions PICO suivantes était satisfaite, comme défini dans chaque ESMA :
- Population (P) : Adultes, avec ou sans MCV
- Intervention (I) : Vaccin contre la grippe saisonnière (toute formulation, dose ou type)
- Comparaison (C) : Pas de vaccination contre la grippe saisonnière ou placebo
- Résultats (O) : Incidence ou survenue d’événements cardiovasculaires
Extraction des données
Un formulaire électronique d’extraction de données a été mis au point pour cette revue. L’extraction des données a d’abord été effectuée par un évaluateur, puis validée ou corrigée par un second évaluateur. Dans l’ensemble, les données extraites étaient les caractéristiques générales de l’ESMA (auteur, date de publication, dates de recherche, objectif et éléments PICO) et un résumé des principales conclusions (c.-à-d., les caractéristiques des participants, les mesures des effets avec un intervalle de confiance [IC] à 95 % et le système GRADE [Grading of Recommendations Assessment, Development, and Evaluation] pour la qualité globale des données probantes), si elles étaient disponibles Footnote 20.
Évaluation méthodologique
La qualité de chaque ESMA a été évaluée à l’aide de l’outil AMSTAR 2 (A MeaSurement Tool to Assess Systematic Reviews), un outil spécialement conçu pour évaluer les ESMA d’études randomisées et non randomisées portant sur des interventions dans le domaine de la santé Footnote 21. Conformément aux recommandations, les domaines critiques de l’outil AMSTAR 2 ont été classés comme suit : 2, 4, 7, 9, 11, 13 et 15 (tableau S1) Footnote 21. Pour le présent examen, l’outil AMSTAR 2 a été adapté de manière à ce que tout élément ayant une réponse négative soit considéré comme un défaut critique, tandis que les éléments ayant une réponse partiellement positive ne sont pas considérés comme des défauts critiques. Le score global obtenu à l’aide de l’outil AMSTAR 2 a été utilisé pour classer la qualité de chaque ESMA inclus comme élevée (aucun défaut critique), modérée (un défaut critique), faible (deux à trois défauts critiques) ou très faible (plus de trois défauts critiques) Footnote 21. Cette évaluation a été réalisée par deux évaluateurs indépendants et les conflits ont été résolus par la discussion et le consensus.
Synthèse des données
Les caractéristiques et les principales conclusions des ESMA admissibles ont fait l’objet d’un résumé narratif. Conformément aux lignes directrices de SYSVAC concernant l’élaboration de recommandations sur la base d’examens systématiques existants, seuls les ESMA de qualité modérée ou élevée ont été inclus dans le résumé détaillé des conclusions Footnote 19. Les éléments PICO pour chaque ESMA ont été comparés afin d’évaluer l’hétérogénéité entre les ESMA sélectionnés. Une matrice a été créée pour présenter les études qui se chevauchent dans les ESMA. Les résultats concernant quatre événements cardiovasculaires principaux ont été synthétisés : mortalité cardiovasculaire, événements cardiovasculaires indésirables majeurs (ECIM), infarctus du myocarde et AVC. Les mesures des effets et les IC à 95 % pour ces résultats ont été présentés dans un graphique en forêt afin de présenter une vue d’ensemble visuelle des données probantes. Pour tenir compte de l’hétérogénéité potentielle due à la conception des études primaires (c.-à-d., des essais contrôlés randomisés [ECR], des études observationnelles ou les deux), les résultats stratifiés ont été présentés en fonction de la conception des études, dans la mesure du possible. Enfin, les résultats ont été présentés séparément pour les populations avec et sans MCV sous-jacentes afin de mieux évaluer l’effet de la vaccination antigrippale dans les populations à haut risque.
Résultats
Au total, 846 citations ont été identifiées et examinées au niveau du titre et du résumé. 151 études ont été évaluées pour déterminer leur admissibilité et examinées au niveau du texte intégral, et 25 ESMA ont finalement été inclus dans la revue (figure 1) Footnote 22Footnote 23Footnote 24Footnote 25Footnote 26Footnote 27Footnote 28Footnote 29Footnote 30Footnote 31Footnote 32Footnote 33Footnote 34Footnote 35Footnote 36Footnote 37Footnote 38Footnote 39Footnote 40Footnote 41Footnote 42Footnote 43Footnote 44Footnote 45Footnote 46.
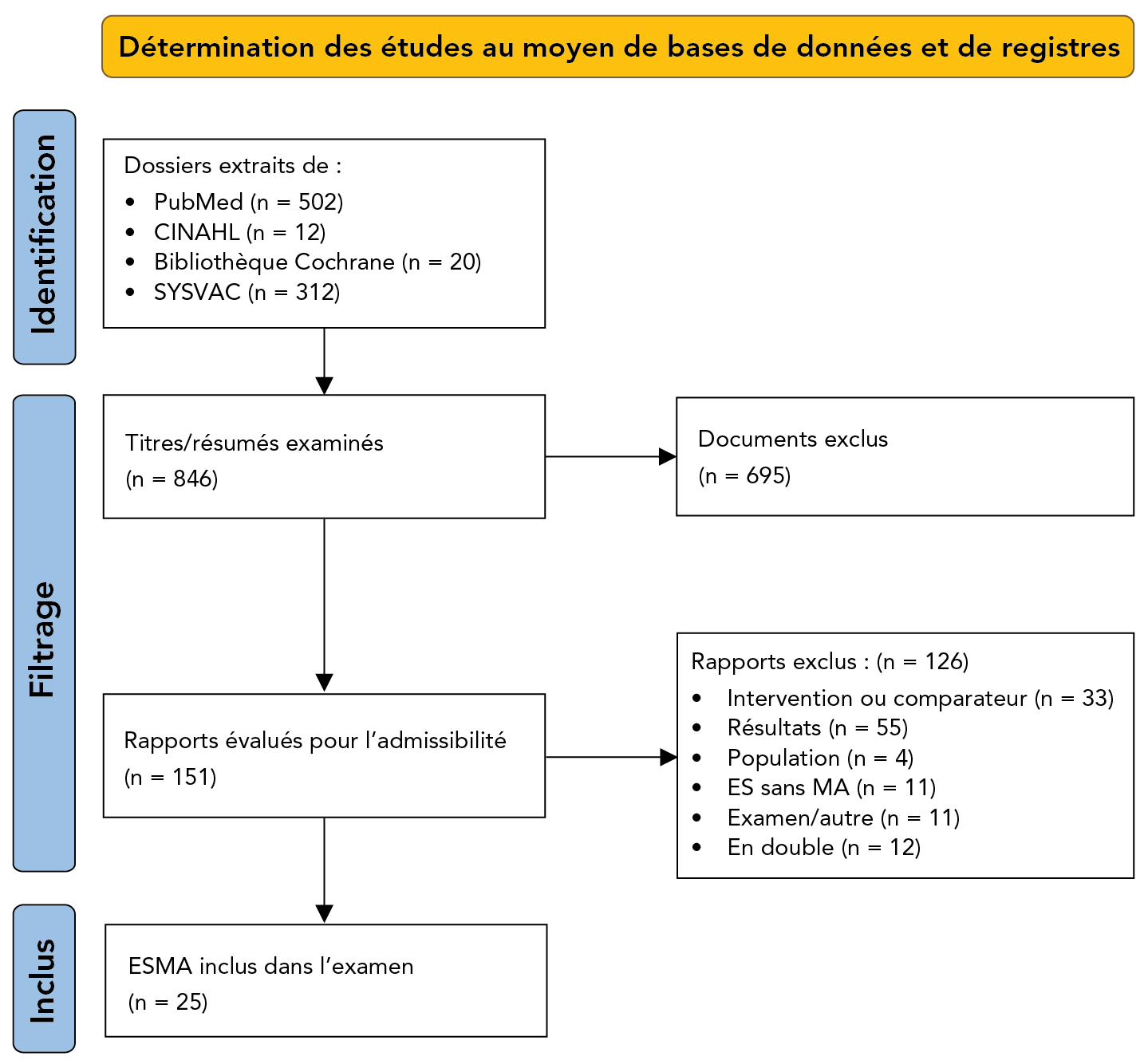
Figure 1 : Équivalent textuel
Le diagramme PRISMA montre le processus d’identification des études admissibles. Au total, 846 citations uniques ont été identifiées et examinées au niveau du titre et du résumé. En tout, 695 ont été exclues à ce niveau et les 151 restantes ont été évaluées pour leur admissibilité et examinés au niveau du texte intégral. Au total, 126 ont été jugées inadmissibles et 25 ESMA ont finalement été inclus dans l’examen général.
Description des études
Les ESMA inclus ont été publiés entre 2012 et 2024 et comprenaient de 5 à 22 études individuelles dans la synthèse quantitative (tableau 1). Dans l’ensemble, neuf (36 %) des études étaient des ESMA d’ECR Footnote 22Footnote 24Footnote 27Footnote 28Footnote 35Footnote 37Footnote 38Footnote 39Footnote 43, dix (40 %) étaient des ESMA d’ECR et d’études observationnelles Footnote 26Footnote 29Footnote 31Footnote 33Footnote 34Footnote 36Footnote 42Footnote 44Footnote 45Footnote 46, et six (24 %) ne comprenaient que des études observationnelles Footnote 23Footnote 25Footnote 30Footnote 32Footnote 40Footnote 41. Les populations d’intérêt de tous les ESMA étaient des adultes âgés de 18 ans et plus, bien que la plupart des ESMA (72 %) se soient concentrés sur les participants ayant reçu un diagnostic de MCV ou présentant un risque élevé d’événements cardiovasculaires, comme défini dans chaque ESMA (tableau 1) Footnote 22Footnote 23Footnote 24Footnote 25Footnote 28Footnote 29Footnote 31Footnote 32Footnote 34Footnote 35Footnote 36Footnote 37Footnote 38Footnote 39Footnote 40Footnote 42Footnote 43Footnote 44. En revanche, 28 % des ESMA incluaient une définition plus large de la population, englobant les adultes atteints ou non de MCV et les adultes plus âgés Footnote 26Footnote 27Footnote 30Footnote 33Footnote 41Footnote 45Footnote 46. En outre, les ESMA admissibles ont évalué plusieurs effets cardiovasculaires, l’IM, la mortalité toutes causes confondues ou cardiovasculaire et les ECIM étant les plus fréquemment évalués (figure 2).
| Auteur Année |
Conception de l’étude | PICO | Caractéristiques des participants | Définition détaillée des résultats | AMSTAR 2Footnote a |
|---|---|---|---|---|---|
| ESMA d’ECR | |||||
| Liu et al. 2024 |
N = 5 (ECR) Période couverte : Jusqu’en septembre 2024 |
P : Patients adultes atteints de CI I : Personnes vaccinées contre la grippe C : Personnes non vaccinées O : ECIM ou autres événements cliniques |
5 659 patients atteints de CI (2 838 vaccinés, 2 821 témoins) Âge médian : 57 à 66 ans 67,8 % d’hommes Suivi médian : 12 mois |
ECIM ou autres événements cliniques (y compris décès CV, mortalité toutes causes confondues, IM, hospitalisation pour IC et revascularisation) | Élevée |
| Omidi et al. 2023 |
N = 5 (ECR) Période couverte : Jusqu’au 1er août 2023 |
P : Patients ayant reçu un diagnostic de MCV I : Vaccin antigrippal C : Placebo O : Événements CV |
9 059 patients (4 529 vaccinés, 4 530 témoins) Âge moyen : 61,3 ans Suivi moyen : 9 mois |
ECIM Comprend : IM, AVC ou décès CV |
Faible |
| Barbetta et al. 2023 |
N = 5 (ECR) Période couverte : Jusqu’en septembre 2021 |
P : Patients atteints de coronaropathie I : Vaccin antigrippal C : Placebo ou absence de vaccin O : Au moins un des effets CV précisés signalé |
4 187 patients (2 098 vaccinés, 2 089 témoins) Groupe d’intervention : Âge moyen : 54,9 à 65 ans 61 % à 81,4 % d’hommes Groupe témoin : Âge moyen de 54,5 à 67 ans 52 % à 82,1 % d’hommes |
Résultats principaux : ECIM : Décès CV, IM non mortel, AVC non mortel Mortalité toutes causes confondues Mortalité CV Résultats secondaires : Hospitalisation pour IC, AVC ou AIT, revascularisation, SCA |
Modéré |
| Modin et al. 2023 |
N = 6 (ECR) Période couverte : Jusqu’en décembre 2022 |
P : Patients présentant un risque CV élevé (cardiopathie ischémique ou IC) I : Vaccin antigrippal C : Placebo O : Incidence des effets CV évalués en tant que résultats d’efficacité potentielle |
9 340 patients (4 670 vaccinés, 4 670 témoins) Âge moyen : 54,5 à 67 ans Suivi : 9,8 à 36 mois |
Critères d’évaluation primaires : Composite de décès CV, syndrome coronarien aigu, thrombose d’endoprothèse ou revascularisation coronarienne, AVC ou hospitalisation pour IC Critères d’évaluation secondaires : Décès CV, décès toutes causes confondues |
Modéré |
| Behrouzi et al. 2022 |
N = 6 (ECR) Période couverte : 2000 à 2021 |
P : Patients ayant des un historique cardiaque I : Vaccin antigrippal C : Placebo et absence de traitement O : Événements CV indésirables majeurs |
9 001 patients (4 510 vaccinés, 4 491 témoins) 42,5 % de femmes Âge moyen : 65,5 ans Historique cardiaque : 52,3 % Suivi moyen : 9 mois |
Résultat primaire : Composite d’ECIM (décès CV ou hospitalisation pour IM, angine instable, AVC, insuffisance cardiaque ou revascularisation coronarienne urgente) dans les 12 mois de suivi Résultat secondaire : Mortalité CV dans les 12 mois de suivi |
Très faible |
| Diaz-Arocutipa et al. 2022 |
N = 5 (ECR) Période couverte : Jusqu’en septembre 2021 |
P : Patients atteints de coronaropathie I : Vaccin antigrippal C : Placebo ou soins standard O : ECIM, mortalité toutes causes confondues, mortalité CV et IM |
4 175 patients (2 110 vaccinés, 2 065 témoins) 75 % d’hommes Âge moyen : 54,5 à 67 ans Suivi : 6 à 12 mois Comorbidités : hypertension (55 %), antécédents d’IM (23 %) et diabète (22 %) |
Résultat principal : ECIM Résultat secondaire : Mortalité toutes causes confondues, mortalité CV, IM |
Modéré |
| Maniar et al. 2022 |
N = 8 (ECR) Période couverte : Jusqu’en mai 2022 |
P : Patients hospitalisés pour IM ou IC aigu I : Vaccination antigrippale dans un délai précis après une hospitalisation pour IM ou IC C : Aucune vaccination antigrippale, placebo ou vaccination retardée O : Réduction des ECIM et de la mortalité CV |
14 420 patients Suivi : 6 à 36 mois |
ECIM, mortalité CV, mortalité toutes causes confondues, IM | Très faible |
| Clar et al. 2015 |
N = 8 (ECR) Période couverte : Jusqu’en février 2015 |
P : Patients âgés de 18 ans et plus ayant ou non des un historique de MCV I : Vaccination antigrippale C : Traitement témoin O : Décès CV ou événements CV non mortels |
12 029 patients (1 682 avec une MCV connue et 10 347 issus de la population générale ou personnes âgées) Suivi : 42 jours à 1 an |
Résultats principaux : Patients sans antécédent de MCV : premier IM, premier cas d’angine instable, décès d’origine CV Patients ayant déjà souffert d’une MCV : IM, angine instable, décès d’origine CV Résultats secondaires : Résultats cliniques composites |
Modéré |
| Udell et al. 2013 |
N = 6 (ECR) Période couverte : Jusqu’en août 2013 |
P : Patients présentant un risque CV élevé I : Vaccination antigrippale C : Placebo ou norme de soins O : Événements CV (événements liés à l’efficacité potentielle ou à la sécurité) |
6 735 patients 51,3 % de femmes Âge moyen : 67 ans Historique cardiaque : 36,2 % Durée moyenne du suivi : 7,9 mois |
ECIM, mortalité CV, mortalité toutes causes confondues, événements CV individuels non mortels (IM, AVC, IC, hospitalisation pour angine instable ou ischémie cardiaque, et revascularisation coronarienne urgente) | Modéré |
| ESMA d’ECR et d’études observationnelles | |||||
| Liu et al. 2024 |
N = 6 (ECR) N = 37 (Obs.) Période couverte : Jusqu’en septembre 2023 |
P : Adultes (18 ans et +) issus de la population générale ou atteints d’une MCV établie I : Vaccin antigrippal C : Placebo ou absence de vaccin O : Mortalité toutes causes confondues ou CV, hospitalisation toutes causes confondues ou pour MCV |
ECR : 12 662 participants Âge moyen, 62 ans; 45 % de femmes; 8 797 (69 %) avec une MCV préexistante Suivi : 6 à 12 mois Étude observationnelle : 6 311 703 participants Âge moyen : 49 ans; 50 % de femmes; 1 189 955 (19 %) avec une MCV préexistante |
Mortalité toutes causes confondues ou CV, hospitalisation toutes causes confondues ou pour une MCV (les MCV étaient définies comme incluant tout diagnostic d’IM, d’IC ou d’AVC) | Élevée |
| Zahhar et al. 2024 |
Jusqu’en décembre 2022 N = 3 (ECR) N = 23 (Obs.) |
P : Patients âgés de plus de 18 ans I : Vaccin antigrippal C : Pas de vaccin antigrippal O : Risque d’AVC ou d’hospitalisation pour AVC |
6 196 668 patients au total 42 % des études incluaient des patients de 65 ans et plus |
Incidence d’AVC ou hospitalisation due à un AVC (tout AVC, AVC ischémique, AVC hémorragique) et mortalité | Modéré |
| Liu et al. 2022 |
N = 1 (ECR) N = 6 (Obs.) Période couverte : Jusqu’en octobre 2021 |
P : Adultes (plus de 18 ans) I : Vaccin antigrippal C : Pas de vaccin antigrippal ou vaccin reçu hors de la période d’efficacité potentielle O : Risque d’arythmie |
ECR : 2 532 patients Âge moyen : 59,85 ans 80,51 % d’hommes Suivi moyen/médian : 1 an Étude observationnelle : 3 167 445 patients Âge : 18 à 73,3 ans 55,9 % à 85,29 % d’hommes Suivi moyen/médian : 9 mois à 3,7 ans |
Arythmie : comprend la FA, le flutter auriculaire, la fibrillation ventriculaire, le flutter ventriculaire et l’arrêt cardiaque | Modéré |
| Zangiabadian et al. 2020 |
N = 6 (ECR) N = 11 (Obs.) Période couverte : Janvier 2000 à novembre 2019 |
P : Patients âgés de plus de 18 ans I : Vaccin antigrippal C : Pas de vaccin antigrippal O : Événements CV |
Total : 180 043 cas et 276 898 témoins 47 % des études incluaient des patients de 65 ans et plus ECR : 3 677 cas, 3 681 témoins Âge : 18 ans et plus Cohorte : 78 522 cas, 127 833 témoins Âge : 31 ans et plus Cas-témoins : 97 844 cas, 145 384 témoins Âge : 40 ans et plus |
Survenue d’événements CV (décès CV, IM non mortel, AVC non mortel, hospitalisation pour IC, événements ischémiques coronariens, IC, décès vasculaire) | Faible |
| Gupta et al. 2023 |
N = 6 (ECR) N = 9 (Obs.) Période couverte : 2000 à 2021 |
P : Patients avec ou sans MCV I : Vaccination antigrippale C : Pas de vaccination antigrippale O : Résultats CV |
745 001 patients Âge moyen : 70,11 (vaccinés) et 64,55 (non vaccinés) ans Durée moyenne du suivi : 6 mois à 2 ans 50 % de femmes (vaccinées); 41 % de femmes (non vaccinées) |
Mortalité toutes causes confondues, décès CV, AVC, IM, hospitalisation pour IC | Très faible |
| Jaiswal et al. 2022 |
N = 5 (ECR) N = 13 (Obs.) Période couverte : Jusqu’en avril 2022 |
P : Patients présentant une MCV établie ou un risque CV élevé I : Vaccin antigrippal C : Pas de vaccination antigrippale ou placebo O : Mortalité toutes causes confondues, ECIM, IC, IM, mortalité CV, AVC |
22 532 165 patients au total 217 072 présentant un risque CV élevé ou une MCV établie (111 073 vaccinés, 105 999 non vaccinés) Âge moyen : 68 ans Suivi moyen : 1,5 an |
Résultats principaux : Mortalité toutes causes confondues, ECIM Résultats secondaires : IC, IM, mortalité CV, AVC |
Faible |
| Yedlapati et al. 2021 |
N = 4 (ECR) N = 12 (Obs.) Période couverte : Jusqu’en janvier 2020 |
P : Patients atteints de MCV (MCV athérosclérotique ou IC) I : Vaccin antigrippal C : Placebo O : Mortalité et effets CV |
237 058 patients au total (ECR : 1 667 patients, observationnelle : 235 391 patients) Âge moyen : 69,2 ± 7,01 ans 36,6 % de femmes Suivi médian : 19,5 mois |
Mortalité toutes causes confondues, mortalité CV, ECIM, IC, IM | Faible |
| Cheng et al. 2020 |
N = 6 (ECR) N = 69 (Obs.) Période couverte : Jusqu’en novembre 2018 |
P : Adultes I : Vaccin antigrippal C : Placebo O : Effets des maladies CV et respiratoires et mortalité toutes causes confondues |
4 419 467 patients au total Suivi : 4 mois à 9 ans |
MCV (y compris AVC, ECIM, IM, IC, cardiopathie ischémique, accident ischémique transitoire, syndrome coronarien aigu, arrêt cardiaque, mortalité CV, fibrillation auriculaire) et mortalité toutes causes confondues | Faible |
| Tsivgoulis et al. 2018 |
N = 5 (ECR ont tous inclus la grippe) N = 6 (Obs.) Période couverte : Jusqu’en mars 2017 |
P : Patients adultes présentant un risque d’ischémie cérébrovasculaire I : Vaccination antigrippale C : Pas de vaccination antigrippale ou différents types de vaccination O : AVC ischémique et autres effets CV |
431 937 patients au total Tranche d’âge moyen : 59,9 + 10,3 ans et plus 19,9 % à 59,7 % vaccinés 38,9 % à 72,5 % d’hommes Durée du suivi : 6 mois à 2 ans |
Résultats principaux : Ischémie cérébrovasculaire, en particulier AVC ischémique aigu Résultats secondaires : Événements ischémiques myocardiques, décès CV |
Élevée |
| Loomba et al. 2012 |
N = 3 (ECR) N = 2 (Obs.) Période couverte : 1998 à 2011 |
P : Patients atteints d’une maladie CV ou présentant un risque d’événement CV I : Vaccin antigrippal C : Pas de vaccin antigrippal O : Morbidité et mortalité CV |
292 383 patients au total (169 203 vaccinés et 123 481 non vaccinés) Âge moyen : 58 à 77 ans 42,6 % à 73,9 % d’hommes |
IM, mortalité toutes causes confondues et ECIM | Très faible |
| ESMA d’études observationnelles | |||||
| Tavabe et al. 2023 |
N = 14 (Obs.) Période couverte : 1980 à juillet 2021 |
P : Personnes âgées I : Vaccin antigrippal C : Pas de vaccin antigrippal O : AVC et hospitalisations |
3 198 646 patients Suivi moyen : 30 mois |
AVC ou hospitalisation due à un AVC | Modéré |
| Gupta et al. 2022 |
N = 7 (Obs.) Période couverte : Jusqu’en octobre 2021 |
P : Patients adultes souffrant d’insuffisance cardiaque I : Vaccin antigrippal C : Pas de vaccin antigrippal O : Mortalité toutes causes confondues, mortalité d’origine CV, hospitalisation toutes causes confondues, hospitalisation en raison d’une MCV, AVC non mortel et IM non mortel |
247 842 patients Âge moyen : 68 à 77 ans Ratio hommes/femmes proche de 50 % dans la plupart des études |
Mortalité et hospitalisation toutes causes confondues, mortalité et hospitalisation CV, AVC non mortel, IM non mortel dans les 12 mois suivant l’administration du vaccin antigrippal | Modéré |
| Rodrigues et al. 2020 |
N = 6 (Obs.) Période couverte : Jusqu’en décembre 2018 |
P : Patients adultes souffrant d’insuffisance cardiaque ou présentant une fraction d’éjection anormale/réduite (moins de 50 %) I : Vaccination antigrippale C : Pas de vaccination antigrippale O : Mortalité toutes causes confondues, mortalité à la suite d’une IC, mortalité d’origine CV, hospitalisations toutes causes confondues, taux d’hospitalisation CV, taux d’hospitalisation liés à l’IC, durée d’hospitalisation et arythmies ventriculaires |
179 158 patients Âge moyen : 62 à 75 ans Suivi : 3 mois à 8 ans |
Résultat primaire : Mortalité toutes causes confondues Résultats secondaires : Mortalité à la suite d’une IC, mortalité d’origine CV, hospitalisations toutes causes confondues, taux d’hospitalisation CV, taux d’hospitalisation liés à l’IC, durée d’hospitalisation et arythmies ventriculaires |
Élevée |
| Caldeira et al. 2019 |
N = 2 (SCCS) Période couverte : Jusqu’en septembre 2019 |
P : Patients adultes (plus de 18 ans) ayant subi un premier IAM au cours de la période d’étude et ayant été vaccinés contre la grippe I : Vaccination antigrippale C : Pas de vaccination antigrippale O : Taux d’incidence d’IAM |
32 676 patients Âge médian : 72,3 à 77 ans |
Rapport des taux d’incidence d’IM au cours du premier mois (1 à 28 jours) suivant la vaccination antigrippale | Faible |
| Lee et al. 2017 |
N = 11 (Obs.) Période couverte : Jusqu’en novembre 2016 |
P : Individus (plus de 18 ans) à risque d’AVC I : Vaccin antigrippal C : Pas de vaccin antigrippal O : Risque d’AVC (quelconque, premier, récurrent) |
593 513 patients 45 % des études incluaient des participants de 60 ans et plus |
Risque d’AVC (quelconque, premier, récurrent) | Modéré |
| Barnes et al. 2015 |
N = 7 (cas-témoins) Période couverte : Jusqu’en juin 2014 |
P : Patients adultes atteints d’IAM I : Vaccin antigrippal C : Patients sans IAM, y compris ceux qui ont reçu ou non le vaccin antigrippal O : IAM mortel ou non mortel, y compris le premier épisode ou les épisodes suivants |
17 695 cas d’IAM (9 428 vaccinés) et 65 343 témoins sans IAM (33 819 vaccinés) Âge moyen : 40 ans et plus |
Risque d’IAM (premier, récurrent). L’IAM a été défini comme une constellation de caractéristiques cliniques, y compris des symptômes ischémiques, des signes biochimiques ou électriques d’ischémie myocardique, des signes de sténose critique de l’artère à la coronarographie ou des signes d’IM à l’autopsie | Modéré |
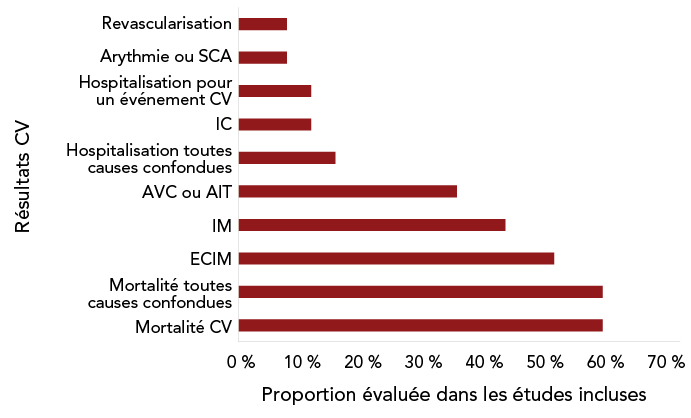
Figure 2 : Équivalent textuel
| Issues CV | Examen systématique et méta-analyse |
|---|---|
| Mortalité CV | 60 % |
| Mortalité toutes causes confondues | 60 % |
| ECIM | 52 % |
| IM | 44 % |
| AVC ou AIT | 36 % |
| Hospitalisation toutes causes confondues | 16 % |
| IC | 12 % |
| Hospitalisation pour un événement CV | 12 % |
| Arythmie ou SCA | 8 % |
| Revascularisation | 8 % |
Évaluation de la qualité et chevauchement des études primaires
L’évaluation de la qualité de chaque ESMA a été effectuée à l’aide d’AMSTAR 2. Cet outil a été adapté de façon à ce que tout élément ayant une réponse négative soit considéré comme un défaut critique, tandis que les éléments ayant une réponse partiellement positive ne sont pas considérés comme des défauts critiques. Dans l’ensemble, quatre ESMA ont été jugés de qualité « très faible », six de qualité « faible » et un total de 15 ESMA (60 %) ont été jugés de qualité « moyenne » ou « élevée ». Par conséquent, seuls les 15 ESMA de qualité « moyenne » ou « élevée » ont été inclus dans le résumé détaillé de la synthèse des résultats Footnote 22Footnote 23Footnote 27Footnote 28Footnote 29Footnote 32Footnote 33Footnote 34Footnote 35Footnote 38Footnote 40Footnote 41Footnote 42Footnote 43Footnote 45. Les principales raisons pour lesquelles la plupart des ESMA ont obtenu de mauvais scores sont : l’absence de liste complète des études exclues (élément 7); l’absence de technique satisfaisante pour évaluer le risque de biais dans les études individuelles incluses (élément 9); l’utilisation de méthodes appropriées dans les méta-analyses pour la combinaison statistique des résultats (élément 11); et le fait de ne pas tenir compte du risque de biais dans les études primaires lors de la discussion et de l’interprétation des résultats (élément 13) (tableau S1).
Enfin, le chevauchement entre les études primaires incluses dans chaque ESMA a fait l’objet d’une évaluation plus poussée, et seuls deux ESMA présentaient un chevauchement de 100 % entre leurs études primaires (tableau S2).
Résumé des résultats
L’examen général a abouti aux conclusions suivantes :
- Mortalité cardiovasculaire : Au total, neuf des 15 ESMA (67 %) ont évalué la mortalité d’origine cardiovasculaire, dont huit concernaient des patients atteints de MCV sous-jacentes ou présentant un risque élevé d’événements cardiovasculaires Footnote 22Footnote 28Footnote 29Footnote 34Footnote 35Footnote 38Footnote 40Footnote 43, tandis qu’une autre portait sur des adultes avec ou sans historique de MCV Footnote 28. Dans l’ensemble, six ESMA (67 %) ont montré une réduction considérable de la mortalité d’origine cardiovasculaire après la vaccination antigrippale (figure 3) Footnote 22Footnote 27Footnote 28Footnote 29Footnote 35Footnote 38. Chez les adultes présentant un risque plus élevé d’événements cardiovasculaires, le risque de décès dû à un événement cardiovasculaire a été réduit de 23 % (IC à 95 % : 19 %–27 %) à 47 % (IC à 95 % : 26 %–62 %) chez les personnes vaccinées par rapport à celles qui ne l’étaient pas. L’hétérogénéité de ces résultats était faible à modérée, allant de 0 % à 58 %. De même, les données regroupées de quatre ECR portant sur des adultes avec ou sans historique de MCV ont montré une réduction de 55 % (IC à 95 % : 24 %–74 %) du risque de mortalité d’origine cardiovasculaire, sans hétérogénéité (I2 : 0 %). En revanche, les résultats n’étaient pas importants dans trois ESMA, avec une hétérogénéité modérée à critique (I2 : 37 %–94 %) (figure 3) Footnote 34Footnote 40Footnote 43.
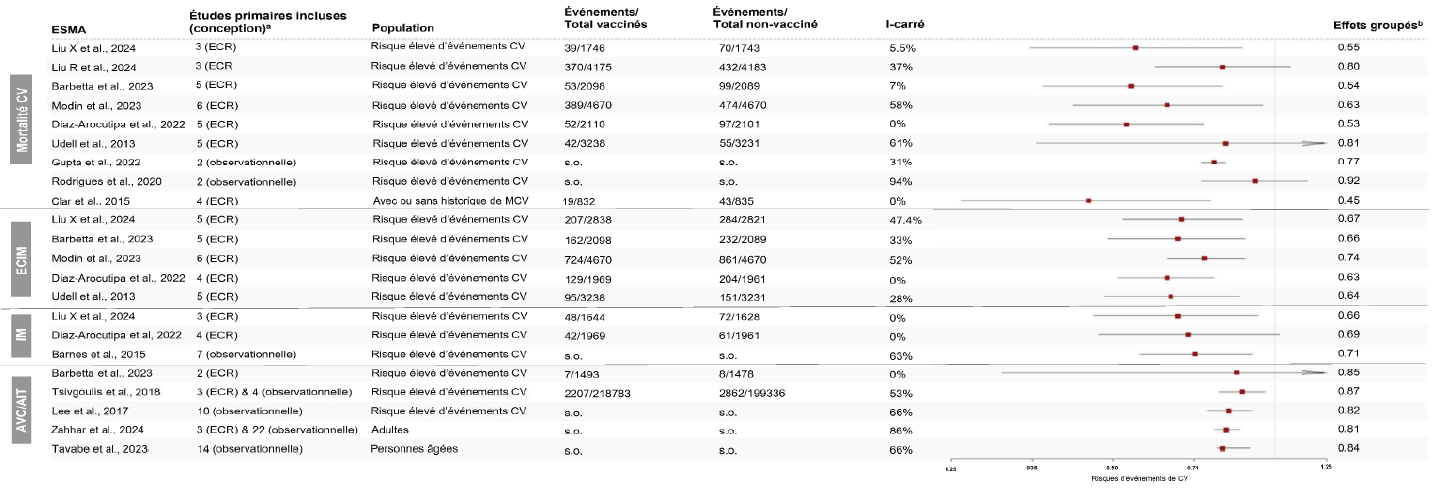
Figure 3 : Équivalent textuel
Ce graphique en forêt illustre les mesures d’effets regroupés d’examen systématique et méta-analyse examinant l’association entre la vaccination antigrippale et les événements cardiovasculaires. Il comprend des données probantes provenant de plusieurs études, principalement des ECR, portant sur des populations présentant un risque élevé d’événements cardiovasculaires. Chaque entrée indique le nombre d’événements cardiovasculaires chez les personnes vaccinées et non vaccinées, ainsi que les statistiques d’hétérogénéité (I2). Dans l’ensemble, le graphique résume visuellement la cohérence et la force des données probantes entre les études.
- Événements cardiaques indésirables majeurs : Les ECIM sont un critère d’évaluation composite qui comprend généralement : les décès d’origine cardiovasculaire, la mortalité toutes causes confondues, le syndrome coronarien aigu (SCA), l’IM, les hospitalisations pour des événements cardiovasculaires, la revascularisation, les AVC et l’insuffisance cardiaque. Dans l’ensemble, cinq ESMA (33 %) ont évalué l’effet de la vaccination antigrippale sur les ECIM chez les participants présentant un risque élevé d’événements cardiovasculaires. Il s’agissait dans tous les cas d’ESMA d’ECR, et leurs résultats globaux montraient systématiquement un taux de 26 % (IC à 95 % : 12 %–51 %) à 37 % (IC à 95 % : 23 %–49 %) de réduction importante du risque d’ECIM chez les personnes vaccinées. L’hétérogénéité de ces résultats était faible à modérée (I2 : 0 %–47 %) (figure 3) Footnote 22Footnote 28Footnote 35Footnote 38Footnote 43.
- Infarctus du myocarde : Le risque d’IM après la vaccination antigrippale a été évalué dans trois ESMA (20 %). Deux d’entre eux étaient des ESMA d’ECR, tandis qu’un autre incluait des études observationnelles. Les participants présentaient un risque élevé d’événement cardiovasculaire dans tous les ESMA. Les résultats ont montré une réduction importante du risque d’IM chez les personnes vaccinées, allant de 29 % (IC à 95 % : 9 %–44 %) à 34 % (IC à 95 % : 7 %–54 %) sans hétérogénéité (I2 : 0 %) Footnote 24Footnote 36, tandis qu’un autre ESMA a rapporté une réduction de 31 % des IM, bien qu’elle n’ait pas atteint la signification statistique et qu’elle ait présenté une hétérogénéité importante (I2 : 63 %) (figure 3) Footnote 28.
- AVC : Les AVC et les accidents ischémiques transitoires (AIT) chez les personnes vaccinées contre la grippe ont été évalués dans cinq (33 %) ESMA. Trois de ces ESMA concernaient des participants présentant un risque élevé d’événement cardiovasculaire Footnote 22Footnote 32Footnote 42, tandis que deux autres portaient sur des adultes et des personnes âgées Footnote 41Footnote 45. À l’exception d’un ESMA qui ne comportait que des ECR, les autres ESMA incluaient des études observationnelles ou des ECR et des études observationnelles en même temps. La réduction globale du risque d’AVC et d’AIT était d’entre 13 % (IC à 95 % : 4 %–21 %) et 19 % (IC à 95 % : 14 %–23 %), et était statistiquement importante dans quatre ESMA, avec une hétérogénéité importante (I2 : 53 %–86 %) (figure 3).
Discussion
Cette revue présente une synthèse complète des données probantes issues de plusieurs ESMA publiés et robustes qui ont évalué l’association entre la vaccination antigrippale et les événements cardiovasculaires. Des mesures détaillées d’effets regroupés ont été présentées pour quatre issues cardiovasculaires principales : mortalité d’origine cardiovasculaire, ECIM, IM et AVC/AIT. La plupart des ESMA ont fait état d’une réduction importante des événements cardiovasculaires à la suite de la vaccination antigrippale, en particulier chez les personnes souffrant de MCV sous-jacentes ou présentant un risque plus élevé d’événement cardiovasculaire. En effet, le risque de mortalité cardiovasculaire était jusqu’à 47 % plus faible chez les personnes vaccinées, tandis que le risque d’ECIM était réduit de 37 % et le risque d’IM de 34 % par rapport aux personnes non vaccinées. Enfin, le risque d’AVC ou d’AIT a été réduit de 19 % chez les personnes vaccinées.
Interprétations
La grippe est reconnue comme un facteur déclenchant des effets cardiovasculaires, en particulier dans les deux premières semaines suivant l’infection Footnote 8. Le risque d’exacerbation ou d’effets cardiovasculaires après une infection grippale est particulièrement élevé chez les personnes souffrant déjà de MCV Footnote 47. La vaccination antigrippale apparaît donc comme une intervention potentiellement efficace pour réduire le fardeau d’événements cardiovasculaires, en particulier dans les groupes à haut risque Footnote 8Footnote 13. Plusieurs mécanismes sous-tendent les effets cardioprotecteurs de la vaccination antigrippale. Alors que la grippe déclenche une inflammation systémique qui peut exacerber l’athérosclérose et les MCV, le vaccin active le système immunitaire, ce qui renforce la santé immunitaire globale et prévient les infections secondaires susceptibles d’aggraver les conditions maladies cardiovasculaires. En outre, il pourrait contribuer à stabiliser les plaques d’athérosclérose, réduisant ainsi le risque d’événements cardiovasculaires aigus, selon des résultats antérieurs Footnote 39.
Dans l’ensemble, les données probantes disponibles permettent de recommander la vaccination annuelle contre la grippe aux personnes à haut risque, en particulier celles qui souffrent de MCV sous-jacentes. Cette mesure préventive peut réduire considérablement le risque d’événements cardiovasculaires et améliorer l’état de santé général de ces populations.
Cependant, malgré les recommandations de vaccination des personnes atteintes de maladies chroniques au Canada Footnote 14, la couverture vaccinale contre la grippe reste sous-optimale dans ces groupes. Au cours de la saison 2023–2024, seuls 44,1 % des adultes âgés de 18 à 64 ans souffrant de maladies chroniques ont été vaccinés contre la grippe, alors que les objectifs nationaux pour la grippe saisonnière dans cette population étaient d’atteindre une couverture vaccinale de 80 % Footnote 48.
Implications
Une communication efficace sur les avantages du vaccin antigrippal par rapport à des issues précises pourrait contribuer à encourager la vaccination Footnote 49. Un vaste essai mené au Danemark, intitulé Nationwide Utilization of Danish Government Electronic Letter System for Increasing Influenza Vaccine Uptake (NUDGE-FLU), a étudié l’effet des incitations comportementales numériques sur l’acceptation du vaccin antigrippal chez les personnes âgées de 65 ans et plus, l’accent ayant été mis sur les maladies cardiovasculaires Footnote 50. Plus de 960 000 Danois ont été répartis au hasard entre les soins habituels et l’une de neuf lettres envoyées par voie électronique, conçues à partir de concepts comportementaux, avant la période de vaccination contre la grippe saisonnière 2022–2023. L’une de ces lettres mettait expressément l’accent sur les avantages cardiovasculaires potentiels de la vaccination antigrippale. Il est intéressant de noter que cette lettre sur les affections cardiovasculaires a eu le plus grand effet sur l’augmentation du taux de vaccination. L’effet était constant chez les personnes atteintes ou non de MCV, ainsi que dans les sous-groupes de MCV, ce qui suggère que la mise en avant des avantages cardiovasculaires peut être une stratégie efficace pour augmenter les taux de vaccination, même chez les personnes ne souffrant pas de MCV Footnote 50.
Ainsi, une communication claire sur les avantages cardiovasculaires potentiels associés à la vaccination antigrippale pourrait contribuer à sensibiliser les groupes à haut risque, déjà ciblés par la campagne de vaccination annuelle, à l’utilité des vaccins antigrippaux et à les motiver à se faire vacciner. Néanmoins, étant donné que les données sur les avantages cardiovasculaires ne sont généralement pas incluses dans les études analysant les avantages de la vaccination antigrippale et compte tenu de l’accumulation récente d’études sur le sujet, il serait intéressant de prendre en compte ce type d’effet dans les futures évaluations coût-efficacité des vaccins antigrippaux Footnote 13.
Limites
Malgré la force de cette synthèse de données probantes, la présente revue présente des limites propres aux études incluses. Premièrement, la qualité et l’hétérogénéité des études primaires incluses varient, ce qui peut influencer la précision des estimations groupées. L’hétérogénéité observée pourrait être attribuable aux différences entre les populations étudiées, la définition des effets cardiovasculaires, la durée du suivi et le moment de la vaccination. Deuxièmement, de nombreux ESMA comprenaient des études observationnelles, qui sont sujettes à des biais de confusion. Enfin, bien que les associations soient cohérentes, la causalité de l’effet ne peut être établie, et des ECR à grande échelle sont nécessaires pour explorer plus avant les effets cardioprotecteurs de la vaccination antigrippale.
Conclusion
En conclusion, le présent examen général fournit une synthèse de données probantes de haute qualité soutenant les avantages cardiovasculaires de la vaccination antigrippale. Les réductions importantes de la mortalité d’origine cardiovasculaire, des ECIM et des AVC soulignent l’importance de promouvoir la vaccination antigrippale, en particulier chez les personnes souffrant de maladies chroniques sous-jacentes, telles que des MCV. L’intégration de la vaccination antigrippale dans la pratique clinique courante et dans les stratégies de santé publique permet d’améliorer les résultats cardiovasculaires tout en réduisant le fardeau des MCV et de la grippe.
Déclaration des auteurs
- F. T. — Conceptualisation, conservation des données, visualisation, analyse formelle, rédaction de la version originale
- N. S. — Validation, rédaction–révision et édition
- W. S. — Validation, rédaction–révision et édition
- P. D. P. — Conceptualisation, validation, rédaction–révision et édition
- A. S. — Conceptualisation, supervision, validation, rédaction–révision et édition
Intérêts concurrents
Aucun.
Identifiants ORCID
Fazia Tadount — 0009-0001-4867-5942
Winnie Siu — 0009-0001-5772-1509
Remerciements
Nous remercions Katarina Gusic, Natalie Smith et Richard Huang pour leur aide dans la validation des données et l’évaluation de la qualité.
Financement
Ce travail a été soutenu par l’Agence de la santé publique du Canada.
Appendice
Du matériel supplémentaire est disponible sur demande auprès de l’auteur : naci-ccni@phac-aspc.gc.ca
Matériel supplémentaire A : Stratégie de recherche
Tableau S1 : Évaluation détaillée avec AMSTAR 2
Tableau S2 : Matrice de chevauchement entre les études primaires

Cette œuvre est mise à disposition selon les termes de la Licence Creative Commons Attribution 4.0 International