Document sur l'approche scientifique
Approche fondée sur le seuil de préoccupation toxicologique (SPT) pour certaines substances
Santé Canada
Septembre 2016
Table des matières
1.0 Sommaire
Conformément à l'article 68 de la Loi canadienne sur la protection de l'environnement, 1999 (LCPE) (Canada 1999), Santé Canada a évalué un sous-ensemble de 89 substances sur les quelque 1 500 substances d'intérêt prioritaire qu'il reste à évaluer dans le cadre de la phase 3 du Plan de gestion des produits chimiques (PGPC).
Ces 1 500 substances ont été déclarées d'intérêt prioritaire, car elles satisfaisaient aux critères de catégorisation du paragraphe 73(1) de la LCPE et/ou étaient considérées d'intérêt prioritaire en raison d'autres préoccupations relatives à la santé humaine. Un groupe de 237 substances candidates parmi les 1 500 substances d'intérêt prioritaire a été identifié par une caractérisation qualitative de leurs utilisations et de leur potentiel d'exposition. L'objectif était d'identifier les substances qui n'ont pas été évaluées lors des examens préalables rapides, et pour lesquelles l'exposition de la population générale devrait être limitée. Les substances candidates ont ensuite été évaluées selon l'approche dite du seuil de préoccupation toxicologique (SPT). Cette approche a permis d'identifier 89 substances peu susceptibles de présenter un risque pour la santé humaine, d'après les niveaux d'exposition actuels. Le numéro de registre du Chemical Abstracts Service (n° CASNote de bas de page1) de ces 89 substances est présenté dans ce document d'évaluation scientifique (DES).
Pour chaque substance candidate, les estimations d'exposition ont été comparées aux SPT assignés. D'après l'information présentée dans ce document, les estimations de l'exposition aux 89 substances identifiées selon l'approche SPT sont inférieures aux SPT assignés et sont donc considérées comme peu préoccupantes pour la santé humaine aux niveaux d'exposition actuels. Quant aux 148 substances restantes parmi les 237 substances candidates, elles ont été exclues ou leurs estimations d'exposition dépassaient le SPT. Ces substances feront l'objet d'une évaluation ultérieure dans le cadre d'initiatives distinctes.
L'évaluation de ces 89 substances, réalisée en vertu des articles 68 et/ou 74 de la LCPE, sera publiée ultérieurement.
2.0 Introduction
Au terme de la catégorisation des substances figurant sur la Liste intérieure des substances (LIS), terminée en 2006, environ 4 300 des quelque 23 000 substances inscrites sur la LIS ont été jugées d'intérêt prioritaire aux fins d'évaluation car elles répondent aux critères de catégorisation énoncés au paragraphe 73(1) de la LCPE, ou ont été jugées d'intérêt prioritaire en raison d'autres préoccupations touchant la santé humaine ou l'environnement. Selon cette approche, un groupe de 237 substances candidates a été identifié d'après la caractérisation qualitative de leurs utilisations et de leur potentiel d'exposition.
L'objectif était d'identifier les substances qui n'ont pas été évaluées lors des examens préalables rapides, et pour lesquelles l'exposition de la population générale devrait être limitée. Les substances candidates ont ensuite été évaluées selon l'approche dite du seuil de préoccupation toxicologique (SPT). Pour chaque substance candidate, les estimations de l'exposition ont été comparées aux valeurs du SPT assignées. Lorsque les expositions estimées étaient inférieures à ces valeurs, la substance était jugée peu préoccupante pour la santé humaine aux niveaux d'exposition actuels.
Le présent document décrit en détail l'approche utilisée pour assigner les valeurs du SPT, qui tient compte des résultats de travaux scientifiques récents (EFSA 2012; EFSA/WHO 2016), et l'élaboration d'estimations de l'exposition de la population générale aux substances d'intérêt prioritaire restantes considérées comme étant des substances candidates pour cette approche.
Ne constituant pas un examen exhaustif ou critique de toutes les données disponibles pour chacune de ces substances, le présent document fournit un résumé de l'approche suivie et des résultats obtenus. Des hypothèses et des modèles prudents ont été utilisés au besoin. Les 89 substances pour lesquelles on a estimé que l'exposition humaine était inférieure à leur SPT respectif ont été incluses dans un sommaire des données justificatives ou des prévisions. Dans le cas des substances jugées peu préoccupantes pour la santé humaine aux niveaux d'exposition actuels, les résultats de l'approche fondée sur le SPT sont destinés à former la base du volet santé humaine de l'évaluation préalable qui sera réalisée en vertu des articles 68 et/ou 74 de la LCPE et qui sera publiée ultérieurement.
Le présent document a été préparé par le personnel du Bureau de l'évaluation des risques pour les substances existantes (BERSE) de Santé Canada et il renferme des données et renseignements provenant d'autres programmes du ministère. Il a été soumis à un examen externe écrit réalisé par des pairs et à des consultations. Des commentaires sur l'approche technique ont été reçus de quatre examinateurs ayant une expertise et une perspective concernant l'approche fondée sur le SPT. Ces examinateurs étaient Susan Felter (Proctor & Gamble), Mitch Cheeseman (Steptoe & Johnson), Susan Barlow (consultante en toxicologie et en évaluation des risques) et Krul Lisette (TNO, l'Organisation néerlandaise de recherche scientifique appliquée). Les examinateurs experts proviennent d'entreprises, de sociétés d'experts-conseils et d'organisations de recherche indépendantes. Cependant, ces personnes ont travaillé à titre privé et se sont appuyées sur leurs propres opinions scientifiques pour effectuer cet examen. L'examen externe par les pairs et les consultations ont été administrés par le Toxicology Excellence for Risk Assessment Center (TERAC). Bien que les commentaires externes aient été pris en considération, Santé Canada demeurera responsable du contenu final et des résultats de l'approche fondée sur le SPT.
3.0 Application de l'approche fondée sur le SPT
3.1 Contexte
Seuil de préoccupation toxicologique
L'approche fondée sur le SPT vise à établir des valeurs seuils de l'exposition humaine à une substance chimique en deçà desquelles il est peu probable qu'il y ait un risque pour la santé humaine (Kroes et coll. 2004). Le concept de SPT est actuellement utilisé ou proposé dans plusieurs domaines de l'évaluation des risques chimiques à l'échelle internationale, notamment en ce qui concerne les substances utilisées dans les matières qui sont en contact avec les aliments (US FDA 1995), les agents aromatisants pour aliments étudiés par le Comité mixte FAO/OMS d'experts des additifs alimentaires (JECFA) (OMS 1995; OMS 1997) et les impuretés dans les produits pharmaceutiques (US FDA 2015). Le Comité scientifique de l'Autorité européenne de sécurité des aliments (EFSA) a recommandé l'approche fondée sur le SPT comme méthode scientifiquement valable de déterminer si l'exposition à une substance est faible au point que la probabilité d'effets nocifs sur la santé serait faible, auquel cas aucune évaluation additionnelle ne serait nécessaire (EFSA 2012).
Le concept de SPT a été appliqué pour la première fois par la Food and Drug Administration des États-Unis (FDA), comme seuil de réglementation pour les matières entrant en contact avec les aliments. Ce concept a évolué au fil du temps, et de nombreux SPT ont été élaborés d'après des analyses ayant porté sur des classes additionnelles de substances chimiques et sur des effets additionnels sur la santé, notamment des effets cancérogènes et non cancérogènes.
Munro et coll. (1996) ont compilé une base de données comportant 613 substances chimiques qui avaient fait l'objet d'analyses visant à en déterminer les effets non cancérogènes chez des rongeurs et des lapins dans le cadre d'essais de toxicité par voie orale, notamment des essais de toxicité subchronique, de toxicité chronique, de toxicité pour la reproduction et de toxicité pour le développement. Dans le cas des substances ayant uniquement fait l'objet d'études de toxicité subchronique, un facteur d'incertitude de trois a été appliqué à la dose sans effet observé (DSEO) obtenue dans ces études, afin de les regrouper avec les DSEO obtenues dans les études de toxicité chronique. Cependant, si une substance avait fait l'objet études de toxicité chronique et de toxicité subchronique mais que la DSEO la plus faible provenait de l'étude de toxicité subchronique, la DSEO subchronique était utilisée telle quelle. Chaque substance s'est vu assigner une classe de Cramer d'après un arbre décisionnel (Cramer et coll. 1978). Les substances de la classe I sont des substances ayant une structure simple indicative d'une faible toxicité; les substances de la classe II sont des substances moins nocives que celles de la classe I, mais pour lesquelles on ne dispose pas de preuves claires de toxicité; enfin, les substances de la classe III sont des substances dont la structure est indicative d'effets préoccupants potentiels sur la santé. Le 5e centile des répartitions cumulatives des DSEO selon une loi log-normale était de 3,0, 0,91 et 0,15 mg/kg p.c./j pour les substances des classes I, II et III, respectivement. Les valeurs seuils de l'exposition humaine ont été calculées en prenant le 5e centile de la distribution des DSEO pour chaque classe de Cramer, puis en le divisant par un facteur de sécurité de 100. Ces valeurs ont ensuite été ajustées en fonction du poids corporel afin d'exprimer les seuils pour les substances des classes I, II et III, soit 1 800, 540 et 90 µg/personne/j, respectivement.
En 1999, Cheeseman et coll. (1999) ont utilisé une base de données actualisée et élargie de données sur les substances chimiques et les effets sur la santé pour réaffirmer le seuil de réglementation de la FDA. S'appuyant sur les travaux de Cheeseman et coll. (1999), Kroes et coll. (2004) ont recommandé un SPT pour les substances chimiques présentant des alertes structurales associées à la génotoxicité. La détermination des seuils a été effectuée à la suite d'un examen des composés présentant des alertes structurales associées à la cancérogénicité et à la génotoxicité [d'après les alertes d'Ashby et Tennant (1991)] et d'un examen des données dose-réponse liées au cancer obtenues dans le cadre d'études menées sur des animaux. Pour ces substances chimiques, on a extrapolé la plage expérimentale à un niveau qui serait jugé négligeable. Kroes et coll. (2004) recommandent d'employer un SPT de 0,15 µg/personne/j pour les substances qui présentent des alertes structurales associées à la génotoxicité et qui ne font pas partie d'un groupe de substances exclues. En outre, le groupe de travail EFSA/OMS sur le SPT a recommandé d'incorporer les données sur la génotoxicité (si elles sont disponibles) et le poids de la preuve, en plus d'utiliser des alertes structurales, afin d'assigner des valeurs du SPT pour la génotoxicité aux substances chimiques (EFSA/OMS 2016).
Kroes et coll. (2004) ont également évalué l'incorporation de différents effets sur la santé, notamment la neurotoxicité et l'immunotoxicité, dans des applications possibles du concept de SPT. En raison de l'activité anti-acétylcholinestérase, un seuil distinct pour les composés organophosphorés a été proposé par Munro et coll. (1996) et discuté par Kroes et coll. (2004). Le Comité scientifique de l'EFSA a recommandé que ce seuil soit également utilisé pour les carbamates (EFSA 2012).
En combinant ces seuils aux seuils non cancérogènes calculés par Munro et coll. (1996), Kroes et coll. (2004) ont proposé un arbre décisionnel qui pourrait être utilisé comme guide pour l'application du concept de SPT (annexe A). Le Comité scientifique de l'EFSA et le groupe de travail EFSA/OMS ont recommandé que les valeurs du SPT soient exprimées en µg/kg p.c./j, afin qu'il soit possible d'appliquer l'approche fondée sur le SPT à différents groupes d'âge (EFSA 2012; EFSA/OMS 2016). Un résumé des valeurs du SPT établies pour les classes de Cramer, les composés organophosphorés et les composés présentant des alertes structurales associées à la génotoxicité est présenté au tableau 3-1.
Bien que les valeurs du SPT présentées ci-dessous aient été établies à l'aide d'anciens ensembles de données sur les effets des substances sur la santé, de nombreuses études utilisant cette approche avec des ensembles de données plus récents et dans lesquelles on obtenait des valeurs semblables à celles établies par Munro et coll. (1996) et Kroes et coll. (2004) ont été publiées après l'article de Kroes et coll. (2004) (Laufersweller 2012; Kalkhof et coll. 2011; Pinalli et coll. 2011; Tluczkiewicz et coll. 2011; Blackburn et coll. 2005; Feigenbaum et coll. 2015).
| Classe chimique | SPT (µg/personne/j)a |
SPT (µg/kg p.c./j) |
|---|---|---|
| Classe I de Cramer | 1 800 | 30 |
| Classe II de Cramer | 540 | 9,0 |
| Classe III de Cramer | 90 | 1,5 |
| Organophosphorés/carbamatesb | 18 | 0,3 |
| Seuil de réglementation de la FDAc | 1,5 | 0,025 |
| Composés génotoxiques | 0,15 | 0,0025 |
a Kroes et coll. (2004) – pour une personne d'un poids de 60 kg.
b Les carbamates ont été inclus dans ce seuil, à la suite d'une recommandation du Comité scientifique de l'EFSA.
c Valeurs historiques fondées sur les seuils de réglementation de la FDA et incorporées dans Kroes et coll. (2004). Ces valeurs ne sont pas prises en compte dans l'approche actuelle.
Exclusions
Un certain nombre de classes de substances chimiques ont été désignées comme faisant partie de la « cohorte préoccupante » (tableau 3-2). Cette cohorte consiste en des substances exclues et en des classes de substances chimiques non couvertes par l'actuelle approche fondée sur le SPT parce que 1) certaines substances pourraient être préoccupantes à des concentrations plus faibles que le SPT le plus faible, ou 2) très peu de substances de cette classe ont été incluses dans la base de données à partir de laquelle les SPT ont été calculés (Kroes et coll. 2004). Les exclusions additionnelles et subséquentes par l'EFSA (2012) et les comités de la Commission européenne qui se sont penchés sur les substances autres que les aliments (SCCS/SCHER/SCENIHR, 2012) incluent les benzidines et les hydrazines, car il s'agit de puissants cancérogènes génotoxiques. Ces exclusions sont prises en considération dans la présente approche fondée sur le SPT.
| Classe/groupe | Raison de l'exclusion | Références |
|---|---|---|
| Composés de type aflatoxine | Puissants cancérogènes génotoxiques | Kroes et coll. 2004; EFSA 2012; EFSA/OMS 2016 |
| Benzidines | Puissants cancérogènes génotoxiques | EFSA 2012; EFSA/OMS 2016 |
| Composés N-nitroso | Puissants cancérogènes génotoxiques | Kroes et coll. 2004; EFSA 2012; EFSA/OMS 2016 |
| Composés azoxy | Puissants cancérogènes génotoxiques | Kroes et coll. 2004; EFSA 2012; EFSA/OMS 2016 |
| Hydrazines | Puissants cancérogènes génotoxiques | EFSA 2012 |
| Stéroïdes | Puissants cancérogènes non génotoxiques | Kroes et coll. 2004; EFSA 2012; EFSA/OMS 2016 |
| Dibenzo-p-dioxines polyhalogénées, dibenzofuranes et PCB de type dioxine | Puissants cancérogènes non génotoxiques bioaccumulables, avec de très grandes différences cinétiques entre les animaux et les humains | Kroes et coll. 2004; EFSA 2012; EFSA/OMS 2016 |
| Protéines | Risque d'allergie, non inclus dans la base de données | EFSA 2012; EFSA/OMS 2016 |
| Substances organométalliques | Non inclus dans l'ensemble de données | Kroes et coll. 2004; EFSA 2012; EFSA/OMS 2016 |
| Composés organo-silicone | Non inclus dans l'ensemble de données | EFSA/OMS 2016 |
| Métaux | Non inclus dans l'ensemble de données; certaines substances sont bioaccumulables | Kroes et coll. 2004; EFSA 2012; EFSA/OMS 2016 |
| Substances à masse moléculaire élevée comme les polymères | Non inclus dans l'ensemble de données; structure non clairement définie | Kroes et coll. 2004 |
Kroes et coll. (2004) ont indiqué qu'il serait peut-être prématuré d'appliquer l'approche fondée sur le SPT aux substances chimiques ayant des effets endocriniens. Plus récemment, l'EFSA (2012) a indiqué que, s'il existait des données spécifiques pour ces substances indiquant une activité endocrinienne mais que leur pertinence n'était pas claire pour les humains, la décision de les inclure dans une approche fondée sur le SPT, ou de les en exclure, devrait être prise au cas par cas. Si les données indiquent des effets nocifs de nature endocrinienne, il faudrait alors procéder à la caractérisation des risques plutôt qu'utiliser l'approche fondée sur le SPT. Pour les autres substances, hormis les stéroïdes qui constituent une catégorie exclue, le Comité scientifique de l'EFSA a suggéré que l'on applique l'approche fondée sur le SPT (EFSA 2012); cette suggestion a également été adoptée dans la présente approche fondée sur le SPT.
Il a été recommandé d'exclure de l'approche fondée sur le SPT les mélanges de structures chimiques inconnues (EFSA 2012). Cependant, le Rapport du groupe de travail d'experts EFSA/OMS a présenté des suggestions pratiques pour les mélanges qui ne sont pas entièrement caractérisés. L'approche fondée sur le SPT pourrait être utilisée si l'on dispose de suffisamment de renseignements pour confirmer que le mélange ne contient pas de composés exclus et que les constituants pourraient être traités comme des substances potentiellement génotoxiques; le SPT de 0,0025 µg/kg p.c./j serait alors applicable. S'il est également possible de déterminer qu'il n'y a pas de préoccupation relative à la génotoxicité, la substance peut être placée directement dans la classe III de Cramer, pourvu qu'il ne s'agisse pas d'un organophosphoré ou d'un carbamate (EFSA/OMS 2016). L'approche utilisée pour traiter les mélanges dans le cadre de la présente évaluation est décrite à la section 3.2.
Il a été recommandé que les nanomatériaux, les substances radioactives et les substances bioaccumulables soient exclus de l'approche fondée sur le SPT (EFSA 2012; EFSA/OMS 2016). Ces types de substances ne font pas partie des substances candidates pour l'approche fondée sur le SPT envisagée par Santé Canada.
3.2 Assignation des SPT
Afin d'assigner un SPT aux substances candidates dans la présente approche, Santé Canada a intégré les recommandations pertinentes du Comité scientifique de l'EFSA et du Rapport du groupe de travail d'experts EFSA/OMS (EFSA 2012; EFSA/OMS 2016) en un arbre décisionnel général présenté à la figure 3-1. Ces recommandations comprenaient également la recommandation présentée dans les rapports de l'EFSA et du groupe de travail de l'OMS selon laquelle il faudrait tenir compte des données sur la génotoxicité propres à une substance chimique (p. ex. test d'Ames) dans l'utilisation de l'arbre décisionnel, si de telles données existent (EFSA/OMS 2016).
Par conséquent, Santé Canada, en collaboration avec le Laboratoire de chimie mathématique (LCM), a construit un flux de travail computationnel à l'aide du logiciel OASIS Pipeline (OASIS 2015) (figure 3-2), qui suit l'arbre décisionnel du SPT intégré (figure 3-1), mais qui est également relié à la boîte à outils QSAR de l'OCDE (v 3.3), ce qui permet de trouver les données empiriques pertinentes associées aux diverses substances et facilite la détermination d'un SPT pour chaque substance. Le flux de travail computationnel est également relié à OASIS TIMES, ce qui permet d'appliquer des modèles prédictifs de la génotoxicité des composés parents et des métabolites prévus; les modèles prédictifs sont décrits au tableau 3-3.
Longue description pour la figure 3-1
Cette figure représente un arbre décisonnel pour l'approche basée sur des SPT pour des composés de la LIS, d'intérêt prioritaire, restants, choisis. Elle a été adaptée des travaux de Kroes et al. (2004), du Comité scientifique de l'Autorité européenne de sécurité des aliments (EFSA 2012) et du Groupe de travail EFSA/OMS (EFSA/OMS 2016). La première question de l'arbre décisonnel est de savoir si la substance appartient à un membre d'une catégorie d'exclusion (on discute de ces catégories à la Section 3.1 du document). Si c'est le cas, la substance serait traitée en suivant une approche différente dans le cadre du PGPC. Si ce n'est pas le cas, la prochaine question est de savoir s'il existe des données spécifiques à la substance indiquant un potentiel de génotoxicité (p. ex. mutagénicité in vitro, clastogénicité in vitro et/ou épreuves in vivo). S'il existe peu ou pas de données disponibles, la prochiane question est de savoir s'il existe une alerte au niveau structurel liée à la génotoxicité (y compris pour les métabolites prédits). S'il y a potentiel de génotoxicité, les expositions estimées sont comparées une valeur de SPT de 0,0025 µg/kg-pc par jour. Si de telles expositions excédaient cette valeur, la substance serait traitée en suivant une approche différente dans le cadre du PGPC; autrement, la substance est considérée comme ne posant probablement pas de risque pour la santé humaine. Si aucun potentiel de génotoxicité n'a pu être identifié, la question est ensuite de savoir si la substance est un organophosphate ou un carbamate. Dans un tel cas, les expositions sont comparées à une valeur de SPT de 0,3 µg/kg-pc par jour. Si les expositions excédaient cette valeur, la substance serait traitée en suivant une approche différente dans le cadre du PGPC; autrement, la substance est considérée comme ne posant probablement pas de risque pour la santé humaine. Si la substance n'est pas un organophosphate ni un carbamate, la question est ensuite de savoir si elle est de la classe de Cramer III ou II. Si c'est le cas, les expositions sont comparées à une valeur de SPT de 1,5 µg/kg-pc par jour. Si les expositions excédaient cette valeur, la substance serait traitée en suivant une approche différente dans le cadre du PGPC; autrement, la substance est considérée comme ne posant probablement pas de risque pour la santé humaine. Finalement, si la substance n'appartient pas la la classe de Cramer III ou II, la question est de savoir si elle appartient à la classe de Cramer I. Pour de telles substances, les expositions sont comparées à une valeur de SPT de 30 µg/kg-pc par jour. Si les expositions excédaient cette valeur, la substance serait traitée en suivant une approche différente dans le cadre du PGPC; autrement, elle serait considérée comme ne posant probalement pas de risque pour la santé humaine.
Longue description pour la figure 3-2
Cette figure représente un flux informatique développé avec le logiciel OASIS Pipeline (OASIS 2015) qui correspond à l'arbre décisionnel pour l'approche basée sur des SPT, présenté à la figure 3-1. En tant que pré-étape, ce flux comprend le développement d'un inventaire de SMILES de substances de la LIS d'intérêt prioritaire, restantes, sélectionnées, qui ont subi un processus d'assurance de la qualité et de contrôle de la qualité (AQ/CQ). Une fois cet inventaire établi, l'étape A du flux consiste à déterminer si chaque substance est dans une catégorie d'exclusion, qui inclut les stéroïdes, les protéines, les compoés de type aflatoxine, les composés de type N-nitroso, les composés de type azoxy, les hydrazines, les benzidines, les dibenzodioxines polyhalogénées, les dibenzofuranes polyhalogénés, les biphényles polyhalogénés, les métaux et les composés organométalliques. Toutes ces substances qui font partie d'une catégorie d'exclusion, sont placées dans une case d'exclusion et le flux s'achève. On continue d'appliquer le flux à toutes les autres substances. Le flux fait ensuite intervenir un criblage des substances en fonction de deux types de données empiriques stockées dans la boîte à outils de l'OCDE, divisé en deux étapes B et C. Une vérification est d'abord faite pour déterminer s'il existe des données empiriques sur la carcinogénicité de ces substances (étape B), tel que souligné dans un résumé de la carcinogénicité et/ou une valeur de DT50 disponible. Les substances pour lesquelles il existe des données empiriques et pour lesquelles de telles données indiquent une carcinogénicité (c.-à-d. positive) seront traitées en suivant une approche différente lors de PGPC3. Pour toutes les autres substances, on passe à l'étape C du flux. Cette étape fait intervenir une vérification afin de déterminer s'il existe des données sur la génotoxicité de ces substances, tels que des résultats de tests de mutagénicité Ames, d'aberration chromosomique in vitro, de mutagénicité mammifère, de micronoyaux in vivo, de létalité dominante in vivo, d'épreuves COMET, d'épreuves UDS et d'échange de chromatides soeurs. Les substances pour lesquelles il existe des données empiriques et pour lesquelles de telles données indiquent un potentiel de génotoxicité (c.-à-d. positive) sont mises dans une boîte de SPT de génotoxicité, et le flux s'achève. Pour toutes les autres substances, on passe à l'étape D du flux. L'étape D fait intervenir l'utilisation de modèles OASIS TIMES pour faire des prédictions sur la génotoxicité (pour la substance parent et ses métabolites) lors de deux épreuves, à savoir une épreuve Ames avec S9 et une épreuve d'aberration chromosomale avec S9. Les résultats ont été analysés et une détermination manuelle de la génotoxicité a été faite pour chaque substance. Les substances déterminées comme génotoxiques sont ajoutées à la boîte de SPT de génotoxicité. Pour toutes les autres substances, on passe à l'étape E. À l'étape E, on demande si le composé est est un organophosphate ou un carbamate. Si c'est le cas, on place toutes ces substances dans une boîte à organophosphate/carbamate. Pour toutes les autres substances, on passe à l'étape F. À l'étape F, on demande si les substances sont de la classe de Cramer II ou III. Si c'est le cas, on les place dans une boîte de STP de classe II ou III. Toutes les autres substances sont placées dans une boîte de STP de classe I et le flux s'achève.
Considérations relatives à la structure chimique d'une substance
Afin d'assigner un SPT à une substance, il faut en établir une représentation structurale de qualité. Les logiciels utilisés dans le cadre de cette approche pour établir les SPT emploient la représentation dite Simplified Molecular-Input Line-entry System (SMILES). La représentation SMILES pour chaque composé a été extraite des bases de données et outils suivants :
- ensembles de données et inventaires de la boîte à outils QSAR de l'OCDE (OCDE 2015);
- ChemIDplus (ChemIDplus 1993); et/ou
- United States Environmental Protection Agency (US EPA) ACToR (ACToR 2013).
La préférence a été accordée aux représentations SMILES jugées de grande qualité d'après la boîte à outils QSAR. On a également employé les bases ChemIDPlus et ACToR de l'EPA pour vérifier les représentations SMILES pour chaque substance.
Les représentations structurales divergentes ont été résolues manuellement, à l'aide de connaissances spécialisées.
Un processus similaire de vérification de la structure des substances discrètes a été utilisé pour les substances apparentées à des mélanges. Un SPT était assigné aux mélanges lorsqu'il était possible de déterminer la structure représentative des constituants entrant dans leur composition. Pour ces substances, l'approche consistait à examiner les constituants représentatifs du mélange par rapport aux substances exclues. Si l'on estimait que les constituants représentatifs ne répondaient pas aux critères d'exclusion, un SPT leur était assigné. Ensuite, un SPT global était assigné au mélange entier. Si les valeurs du SPT étaient différentes pour les constituants individuels, la valeur globale était fondée sur la valeur associée au constituant ayant le seuil le plus bas.
Vérification des exclusions
Les substances ont été examinées par rapport aux exclusions précédemment établies, décrites par Kroes et coll. (2004), l'EFSA (2012) et l'EFSA/OMS (2016) (section 3.1). De plus, les mélanges de substances dont la structure chimique est inconnue ou de substances de type UVCB (substances de composition inconnue ou variable, produits de réaction complexes ou matières biologiques) n'ayant pas de structures représentatives jugées appropriées pour l'établissement d'un SPT n'ont pas été inclus dans l'approche. L'évaluation préalable des substances en vue de leur exclusion a été réalisée au moyen de profileurs structuraux incorporés dans le flux de travail computationnel OASIS Pipeline (figure 3-2 : ÉTAPE A).
Substances pour lesquelles on dispose de données empiriques sur la génotoxicité et la cancérogénicité
Une recherche a également été effectuée pour cibler les substances pour lesquelles il y avait des données empiriques sur la génotoxicité (figure 3-2 : ÉTAPE C). L'information sur la génotoxicité de nombreuses substances est toutefois limitée. Aux fins de l'approche fondée sur le SPT, une substance a été jugée potentiellement génotoxique :
- s'il existe des résultats positifs obtenus dans des essais in vivo de mutation génique ou d'aberrations chromosomiques (y compris des micronoyaux) dans des cellules de mammifères; et/ou
- b) s'il existe des résultats positifs dans des essais in vitro de mutation génique ou d'aberrations chromosomiques (y compris des micronoyaux) et qu'il n'y a pas de données contradictoires dans les essais in vivo menés sur des cellules de mammifères ayant porté sur le même critère d'effet qui avait donné un résultat positif à l'essai in vitro.
Lorsque plusieurs résultats pour un essai donné étaient disponibles dans la boîte à outils QSAR de l'OCDE, la réponse était assignée d'après le résultat le plus prudent.
On a assigné un SPT de 0,0025 µg/kg p.c./j aux substances jugées potentiellement génotoxiques selon les critères ci-dessus.
Substances présentant des alertes structurales associées à la génotoxicité
Les composés pour lesquels on ne dispose pas de données empiriques positives pour la génotoxicité ont fait l’objet d’une évaluation des alertes structurales associées à la génotoxicité, à l’aide des modèles computationnels décrits au tableau 3-3 (figure 3-2 : ÉTAPE D). Les détails de ces modèles sont présentés dans le format de rapport du modèle (Q)SAR (QMRF) (disponible sur demande).
| Nom du modèle (version) | Description | Référence |
|---|---|---|
| Simulateur métabolique de tissus LCM OASIS (TIMES) (v2.27.17) Sous-modèle : Test d'Ames de mutagénicité avec activation métabolique (S9) (v11.11) | Prédit quelles substances chimiques peuvent provoquer une mutagénicité à la suite d'interactions avec l'ADN des bactéries. Le modèle associe un simulateur métabolique pour les mammifères à une approche de groupe d'alertes structurales, combinée à un modèle de reconnaissance de formes pour prédire la réactivité d'une substance chimique avec l'ADN dans le cadre d'un mécanisme d'interaction donné. La prédiction de la mutagénicité des substances chimiques est établie pour les composés parents seulement, les composés parents et les métabolites, et les métabolites seulement. | TIMES 2015 |
| Simulateur métabolique de tissus LCM OASIS (TIMES) (v2.27.17) Sous-modèle : aberrations chromosomiques in vitro avec activation métabolique (S9) (v11.11) | Prédit quelles substances chimiques donnent lieu à des aberrations chromosomiques structurales dans les cellules pulmonaires du hamster chinois (CHL) ou les cellules ovariennes du hamster chinois (CHO). Le modèle associe un simulateur métabolique pour les mammifères à une approche de groupe d'alertes structurales, combinée à un modèle de reconnaissance de formes pour prédire la réactivité d'une substance chimique avec l'ADN dans le cadre d'un mécanisme d'interaction donné. Comprend l'interprétation mécaniste d'une liaison directe à l'ADN, ainsi que l'inhibition des topo-isomérases et l'interaction des substances chimiques avec des protéines nucléaires (p. ex. les histones) connues également pour causer des aberrations chromosomiques. Le simulateur métabolique a été entraîné pour reproduire des cartes documentées du métabolisme du foie chez les mammifères (surtout le rat). La prédiction de la mutagénicité des substances chimiques est établie pour les composés parents seulement, les composés parents et les métabolites, et les métabolites seulement. | TIMES 2015 |
Le système OASIS TIMES a été choisi comme outil prédictif pour l'approche fondée sur le SPT, car il utilise un simulateur métabolique et procède à une évaluation préliminaire des composés parents et de leurs métabolites prévus afin de détecter des alertes. Pour la plupart des alertes, on dispose d'une interprétation mécaniste et elles sont documentées de façon transparente. Ce modèle tient également compte des facteurs connus de modulation des alertes pour ces substances. De plus, le modèle procède à une analyse des domaines d'applicabilité pour chaque substance. Une substance chimique est jugée être dans le domaine si son log Koe et sa masse moléculaire sont situés à l'intérieur des plages spécifiées couvertes par l'ensemble d'entraînement. De plus, le modèle effectue une vérification des fragments centrés sur les atomes afin de déterminer si toutes les caractéristiques structurales sont représentées dans les substances chimiques qui font partie de l'ensemble d'entraînement. Le rendement des alertes, défini par les données empiriques dans l'ensemble d'apprentissage, est également pris en compte dans l'analyse des domaines. On estime qu'OASIS TIMES est plus avantageux que les autres logiciels d'évaluation préliminaire des alertes (p. ex. Toxtree), car c'est un modèle hybride qui combine des règles fondées sur les connaissances et un modèle établi sur des statistiques avec un simulateur métabolique et une analyse des domaines d'applicabilité.
Les prédictions données par les modèles ci-dessus sont également générées pour les composés pour lesquels on dispose de preuves empiriques montrant une absence de génotoxicité (p. ex., des prédictions ont été générées pour des substances pour lesquelles on avait fait uniquement un test d'Ames, qui s'était avéré négatif, et pour lesquelles il n'y avait aucune autre donnée empirique concernant d'autres critères d'effet génétiques, comme les aberrations chromosomiques). La raison sous-jacente est qu'il n'y a aucun test unique permettant de détecter tous les mécanismes génotoxiques pertinents. L'approche par modélisation reproduit deux critères d'effet de la batterie usuelle des essais de génotoxicité (c.-à-d. mutagénicité vs clastogénicité). Par conséquent, on peut avoir pour une substance des données négatives à un test d'Ames, qui décèle les mutations ponctuelles et les décalages (mutagénicité), mais prédire que cette même substance sera positive à l'aide du modèle d'aberrations chromosomiques in vitro, qui sert à déterminer la clastogénicité. Aux fins de l'approche fondée sur le SPT, les composés dont on prédit qu'ils seront positifs sont considérés comme présentant une alerte de génotoxicité.
Un processus manuel de vérification des prédictions du modèle par rapport aux données empiriques disponibles, sur une base test par test, a été réalisé lorsque les données le permettaient. Par exemple, lorsqu'un modèle prédisait qu'une substance chimique serait positive au test d'Ames mais qu'il existait des données empiriques indiquant le contraire, les résultats empiriques étaient privilégiés. Ce processus a également été utilisé pour les essais d'aberrations chromosomiques in vitro.
Les substances sont jugées potentiellement génotoxiques, comme il est décrit dans l'approche de modélisation ci-dessus, et un SPT de 0,0025 µg/kg p.c./j est assigné à ces substances.
Substances non génotoxiques
Lorsque les substances font l'objet d'une évaluation préliminaire du potentiel de génotoxicité, comme il est décrit ci-dessus, et qu'aucune donnée positive ou alerte pertinente n'est trouvée, on passe aux étapes suivantes dans l'arbre décisionnel pour ces substances.
La structure de chaque substance a été examinée au moyen d'un profileur de structure pour qu'il soit possible de déterminer si le composé est un organophosphoré ou un carbamate (figure 3-2 : ÉTAPE E). Cependant, aucune des substances candidates évaluées selon cette approche n'est un organophosphoré ou un carbamate (voir la section 6.0, Résultats).
Une classe de Cramer a été assignée aux substances selon l'arbre décisionnel de Cramer (figure 3-2 : ÉTAPE F). Le schéma de classification de Cramer a été intégré dans diverses solutions logicielles, afin de faciliter l'utilisation cohérente de ce schéma. Deux de ces programmes sont le logiciel Toxtree (Toxtree 2015) et la boîte à outils QSAR de l'OCDE (OCDE 2015). Pour implémenter le schéma de Cramer dans ces deux programmes, les programmeurs ont dû prendre certaines décisions, notamment concernant l'interprétation fondée sur les paramètres chimiques des règles originales et les « listes de consultation » prédéfinies des constituants normaux du corps et des constituants alimentaires courants. Par conséquent, il est possible d'obtenir des classifications différentes selon le logiciel utilisé. La classe de Cramer utilisée selon cette approche est d'abord fondée sur l'implémentation logicielle des 33 questions faisant partie de la boîte à outils QSAR de l'OCDE (v3.3). Toxtree a également été utilisé pour la vérification de la classe de Cramer de chaque substance à l'extérieur du flux de travail computationnel. Les écarts ont été examinés manuellement en tenant compte des points soulevés par Bhatia et coll. (2014) et Roberts et coll. (2015), afin d'accroître le degré de certitude à l'égard de la classification de Cramer pour l'ensemble des substances restantes du PGPC.
Plusieurs chercheurs ont fait état du faible nombre de substances qui appartiennent à la classe II de Cramer (Munro et coll. 1996; Tluczkiewicz et coll. 2011; Pinalli et coll. 2011; Feigenbaum et coll. 2015). Le Comité scientifique de l'EFSA a indiqué que la classe II de Cramer n'est pas suffisamment étayée par les bases de données existantes; sa recommandation a été de traiter comme des substances de la classe III les substances classées comme appartenant à la classe II de Cramer au moyen de l'arbre décisionnel de Cramer (EFSA 2012). Santé Canada a adopté cette façon de faire pour son approche fondée sur le SPT (figure 3-2 : ÉTAPE F).
3.3 Utilisation des SPT associés à une exposition orale avec d'autres voies d'exposition
Les valeurs du SPT existantes ont été obtenues à partir d'expériences dans lesquelles des animaux de laboratoire avaient été exposés à des substances chimiques à dose répétée par voie orale. Cependant, les expositions aux substances chimiques (évaluées dans le cadre du PGPC) se font souvent par voie cutanée ou par inhalation (p. ex. par l'utilisation de certains produits de consommation ou de cosmétiques, ou par l'environnement). Par conséquent, il faut faire preuve de circonspection lorsqu'on applique des SPT associés à une exposition orale à d'autres voies d'exposition.
L'EFSA (2012) a proposé deux méthodes pour calculer les SPT pour les voies d'exposition non orales : 1) utiliser les SPT pour la voie orale et effectuer une extrapolation « voie par voie »; 2) calculer des SPT distincts en utilisant les données obtenues dans le cadre d'études menées avec d'autres voies d'exposition. On a tenté d'établir des bases de données pour l'exposition par inhalation dans le cadre d'études de toxicité avec doses répétées (Carthew et coll. 2009, Escher et coll. 2010, Schüürmann et coll. 2016) et d'études de toxicité par voie cutanée avec doses répétées (William et coll. 2016) afin d'établir les SPT propres à ces voies, mais on estime généralement que le nombre d'études disponibles pour les autres voies d'exposition est faible par rapport à la base de données des études d'exposition par voie orale (Dewhurst et Renwick 2013). Ainsi, dans la majorité des travaux récents visant à adapter l'approche du SPT à d'autres voies d'exposition, on a tenté de mettre au point des méthodes d'extrapolation voie par voie en se fondant sur les études d'exposition par voie orale qui forment la base des SPT actuels.
Selon l'approche fondée sur le SPT, on applique les valeurs du SPT par voie orale à un petit sous-ensemble de substances associées à une exposition directe par voie cutanée (moins de 15 % des substances visées par la présente approche).
Une approche pragmatique pour appliquer les valeurs du SPT par voie orale à l'exposition cutanée consiste à quantifier l'estimation de l'exposition externe par voie cutanée et à comparer cette valeur au SPT associé à une exposition par voie orale. Cette approche présume que la biodisponibilité associée aux voies d'exposition est équivalente, peu importe les différences sur le plan toxicocinétique. Si l'estimation de l'exposition cutanée dépasse la valeur du SPT par voie orale établie, on examine alors les circonstances de l'exposition cutanée (p. ex. durée de l'exposition) et les caractéristiques de la substance qui peuvent influer sur le potentiel d'absorption cutanée. Le cas échéant, des ajustements sont apportés à l'estimation de l'exposition.
Les connaissances sont beaucoup plus limitées en ce qui concerne les différences en matière de biodisponibilité entre l'exposition par inhalation et l'exposition par le tractus gastro intestinal (GI), le métabolisme de premier passage différentiel et les processus de transport propres au tractus GI et aux poumons, de sorte que les substances associées à une exposition potentiellement importante par inhalation n'ont pas été incluses dans l'approche fondée sur le SPT. Cette façon de procéder est conforme à l'opinion de l'EFSA (2012), selon laquelle il semble peu judicieux de fonder l'approche du SPT sur l'ensemble de données de Munro et de réaliser une extrapolation voie par voie pour l'exposition par inhalation. De plus, l'EFSA (2012) a également indiqué qu'il serait souhaitable d'élargir la base de données associée à l'exposition par inhalation avant d'établir des SPT pour l'inhalation. Les substances étaient exclues de l'approche fondée sur le SPT en raison d'un risque d'exposition par inhalation si elles répondaient aux critères suivants :
- elles ont une pression de vapeur élevée et sont présentes dans des produits de consommation ou des cosmétiques;
- leur méthode d'application peut entraîner une exposition par inhalation (p. ex. assainisseurs d'air);
- elles ont été détectées dans le cadre d'activités de surveillance de la qualité de l'air intérieur au Canada.
Les données canadiennes sur la surveillance de la qualité de l'air intérieur sont tirées de deux rapports récents sur la surveillance de la qualité de l'air intérieur au Canada. Zhu et coll. (2013) ont réalisé une étude nationale exhaustive sur la qualité de l'air intérieur, basée sur la population générale, en 2009-2011, et Won et Lusztyk (2011) ont inclus l'information provenant de 115 résidences de Québec entre 2008 et 2010. Les substances répertoriées dont les concentrations mesurées étaient supérieures à la limite de détection dans l'air intérieur n'ont pas été incluses dans la présente approche fondée sur le SPT.
En ce qui concerne l'environnement, l'exposition par inhalation (fondée sur des rythmes de respiration sur 24 heures et sur les concentrations prévues dans l'air ambiant) a été regroupée avec l'exposition par voie orale, car la plupart des substances rejetées dans l'environnement devraient se retrouver dans l'air, à un certain degré. L'absorption par les tissus pulmonaires est potentiellement plus grande que l'absorption par les parois intestinales. On reconnaît que les lacunes dans les connaissances relatives à l'extrapolation voie par voie des valeurs du SPT oral aux expositions par inhalation décrites ci-dessus constituent des incertitudes en ce qui concerne cette approche.
4.0 Estimation des valeurs d'exposition
Pour chaque substance examinée dans la présente approche fondée sur le SPT, l'exposition potentielle de la population générale canadienne a été caractérisée et comparée à la valeur du SPT assignée à la substance.
Suivant les usages d'une substance donnée, l'exposition de la population générale peut s'effectuer de façon directe, p. ex. par contact avec des produits de consommation ou des cosmétiques, ou de façon indirecte, p. ex. par une exposition à l'environnement (eau, sol, air).
Des estimations prudentes de l'exposition ont été générées. Dans cette section, nous décrivons comment l'exposition indirecte et l'exposition directe ont été caractérisées pour permettre l'évaluation des substances qui demeurent prioritaires dans le cadre du PGPC au moyen de l'approche fondée sur le SPT.
4.1 Exposure from Environmental Media (Indirect Exposure)
La population générale peut être exposée à une substance qui est présente dans divers milieux de l'environnement. Une approche générale a été utilisée pour obtenir les concentrations environnementales par modélisation. Le modèle de fugacité environnementale canadien, ChemCAN v6.00 (ChemCAN 2003), a été sélectionné pour modéliser les concentrations environnementales dans l'air ambiant, l'eau de surface et le sol. Ces concentrations ont ensuite été utilisées pour estimer l'exposition de la population générale aux substances candidates par divers milieux de l'environnement selon l'approche fondée sur le SPT (voir le tableau B-3, qui présente les estimations de l'exposition par l'environnement).
Approche par modélisation de la fugacité (ChemCAN v6.00)
Le modèle ChemCAN v6.00, un modèle canadien de fugacité environnementale de niveau III, a été utilisé pour estimer les concentrations dans l'environnement. Ce modèle, qui comprend 24 régions du Canada préparamétrées, peut être utilisé pour estimer les concentrations de substances en régime stationnaire dans les milieux de l'environnement comme l'air ambiant, l'eau de surface et le sol. Comme le modèle estime les concentrations à l'échelle régionale, il convient très bien aux substances dont le rejet se fait de façon dispersée et aux substances qui ne se dégradent pas rapidement dans l'environnement. En outre, en estimant la moyenne de la masse d'une substance à l'échelle régionale, les concentrations environnementales peuvent convenir davantage aux compartiments « dynamiques » (comme l'air et l'eau) qu'aux compartiments « statiques » (comme le sol).
Le modèle ChemCAN v6.00 convient davantage aux substances qui sont de « type Mackay 1 ». Les substances de type Mackay 1 sont des substances organiques dont la pression de vapeur est supérieure à 10-7 Pa et dont la solubilité dans l'eau est supérieure à 10-6 g/m3 (Mackay et coll. 1996). Bien que l'on puisse utiliser le modèle ChemCAN v6.00 pour simuler quelques autres types de substances organiques, des coefficients de partage uniques peuvent s'avérer nécessaires, car il s'agit de données d'entrée difficiles à estimer. Environ 85 % des structures représentatives et organiques discrètes (dans le cas des mélanges ou des substances UVCB) évaluées selon l'approche fondée sur le SPT sont considérées comme des substances de type Mackay 1.
Pour les substances de type Mackay 1, six simulations ont été réalisées, soit deux pour chaque mode de pénétration (c. à d. 100 % de rejets dans l'air, l'eau ou le sol). Dans la première simulation pour chaque milieu, on a fait l'hypothèse selon laquelle il n'y avait aucune concentration entrante advective (provenant d'autres régions) dans l'air et dans l'eau dans la région d'intérêt. La deuxième simulation consistait à utiliser les concentrations obtenues pour l'air et l'eau à la première simulation comme concentrations entrantes advectives, et à utiliser les concentrations obtenues à la seconde simulation comme concentrations de points d'exposition pour estimer le taux d'absorption par les humains.
Le programme EPI Suite™ a été utilisé pour obtenir ou estimer les propriétés physico-chimiques et les demi-vies de dégradation dans l'environnement de chaque substance devant être soumise au modèle ChemCAN v6.00 (EPI Suite™ 2012). La préférence a été accordée aux données empiriques lorsqu'elles étaient disponibles; sinon, les propriétés obtenues par modélisation étaient utilisées. Dans chaque simulation par modélisation, on a utilisé la masse moléculaire, la constante de la loi d'Henry, le log Koe et les demi-vies de dégradation globales. Comme il fallait disposer de la demi-vie de dégradation globale pour chaque compartiment environnemental, les demi-vies ont été calculées comme étant la somme réciproque de chaque processus de dégradation individuel applicable à un milieu donné (lorsque ces renseignements étaient disponibles), soit :
1/(t½ globale) = [1/(t½ abiotique) + 1/(t½ biotique)]
Pour l'air, on a tenu compte de la réaction avec les radicaux hydroxyles et avec l'ozone. Pour l'eau, on a tenu compte de l'hydrolyse et de la biodégradation. On a estimé les demi-vies de biodégradation en convertissant les résultats numériques obtenus avec BIOWIN3 en une demi-vie fondée sur des facteurs de conversion par défaut donnés dans Aronson et coll. (2006). Pour le sol et les sédiments, seules les demi-vies de biodégradation ont été estimées, en fonction d'un facteur d'extrapolation présumé pour la biodégradation intermilieux « eau-sol-sédiments » de 1:1:4, d'après Boethling et coll. (1995).
Les volumes d'émissions utilisés pour les simulations avec ChemCAN v6.00 étaient les volumes totaux de substances commerciales (fabrication et importation) fondés sur les déclarations produites en vertu de l'article 71 qui avaient été reçues pour chaque substance dans le cadre des phases 1 et 2 de la mise à jour de l'inventaire de la Liste intérieure des substances (MJI LIS) (Canada 2014; Environnement Canada 2012). En outre, pour une substance, on a tenu compte des renseignements tirés des déclarations reçues en 2005 en réponse à une enquête distincte menée en vertu de l'article 71 (Canada 2006). Dans le cas des phases 1 et 2 de la MJI LIS, le seuil de déclaration était de 100 ou de 1 000 kg/an, et les années de déclaration étaient 2008 et 2011, respectivement (Canada 2009; 2012).
Si la substance avait été incluse dans l'enquête de la phase 1 ou de la phase 2 de la MJI LIS mais qu'aucune donnée sur les volumes n'avait été reçue, le seuil de déclaration de 100 kg pour la phase 1 de la MJI LIS et pour les substances de la partie 2 de la phase 2 de la MJI LIS était utilisé. On a également consulté l'Inventaire national des rejets de polluants (INRP) d'Environnement Canada pour vérifier s'il y avait des données sur les émissions (Environnement Canada 2013). De plus, les données sur les volumes de ventes pour les pharmacies de détail et les hôpitaux en 2011-2012, tirées de la base de données IMS MIDAS, ont été incluses dans les volumes des émissions des substances qui sont des matières pharmaceutiques actives (IMS 2013).
Pour chaque simulation à l'aide de ChemCAN v6.00, la région « Ontario, plaines boisées mixtes » a été sélectionnée comme région par défaut, car elle est représentative du Sud de l'Ontario, soit la région la plus peuplée et la plus industrialisée du Canada. Les paramètres d'entrée courants pour toutes les substances et structures de type Mackay 1 comprenaient les coefficients de dépendance à la température (ΔH) suivants : -20 000 J/mol (pour le Koe); +55 000 J/mol (pour le Kae); et -75 000 (pour le Koa) (Beyer et coll. 2002). De plus, la « méthode à un paramètre » a été utilisée pour calculer le paramètre de partage Kp(air-aérosol) fondé sur le Koa et une constante linéaire par défaut de 1,50E-12 pour toutes les substances (Finizio et coll. 1997).
Les concentrations environnementales dans l'air ambiant, l'eau de surface et le sol obtenues à l'aide ChemCAN v6.00 ont été utilisées pour estimer l'absorption par les humains pour deux groupes d'âge : les nourrissons alimentés avec des préparations (de 0 à 6 mois) et les tout-petits (7 mois à 4 ans). Ces deux groupes d'âge ont été sélectionnés, car ils représentent les groupes d'âge les plus exposés par rapport à leur poids corporel. Les concentrations dans l'air ambiant ont été utilisées pour représenter l'exposition à l'air ambiant et à l'air intérieur lorsqu'on ne trouvait pas de concentrations propres à la substance dans l'air intérieur mesurées récemment au Canada qui étaient supérieures à la limite de détection. Les concentrations dans l'eau de surface ont été utilisées pour représenter l'exposition par l'eau potable. Les concentrations dans le sol ont été utilisées pour représenter l'exposition au sol à l'extérieur et à la poussière intérieure (laquelle contient de la terre provenant de l'extérieur). Les facteurs d'exposition par défaut, nommément le taux de consommation d'eau, le taux d'inhalation, le poids corporel et le taux d'ingestion de poussière et de sol, ont été obtenus de Santé Canada (1998) et de Wilson et coll. (2013).
Pour chaque substance organique discrète de type Mackay 1, on a utilisé aux fins de comparaison avec la valeur du SPT l'estimation totale la plus élevée de l'absorption à partir de l'environnement parmi les trois modes de pénétration et les deux groupes d'âge. Pour les substances organiques discrètes qui n'étaient pas de type Mackay 1, on a calculé des estimations théoriques d'absorption à partir de l'environnement (voir la section suivante pour de plus amples renseignements sur ce sujet). Pour les substances qui sont des mélanges ou des UVCB, les taux d'absorption pour chacune des structures représentatives ont été comparés à la valeur du SPT de chaque structure.
Si une structure représentative d'une substance organique discrète ou d'une substance UVCB présentait un taux d'absorption supérieur à la valeur du SPT correspondante, un complément d'évaluation pour cette substance organique discrète ou cette substance UVCB serait habituellement justifié, au-delà de la présente approche fondée sur le SPT. Cependant, dans le cas des substances dont les taux d'absorption ont été jugés supérieurs à la valeur du SPT et pour lesquelles l'exposition directe ne dépassait pas le SPT (voir la section 4.2, qui traite de l'exposition directe), des ajustements ont été apportés aux hypothèses de modélisation prudentes utilisées dans ChemCAN v6.00 lorsque c'était possible. Ces ajustements comprenaient l'utilisation d'une fraction d'élimination par les usines de traitement des eaux usées et l'utilisation de demi-vies empiriques de dégradation relevées dans la littérature.
Estimation de l'exposition par l'environnement pour les substances autres que celles du type Mackay 1
Des estimations théoriques de l'absorption due à une exposition environnementale ont été produites pour les substances autres que celles du type Mackay 1. Tout d'abord, en utilisant les résultats obtenus avec ChemCAN v6.00, on a calculé le ratio entre les estimations totales les plus élevées pour l'absorption par les humains et les volumes d'émissions pour chaque substance de type Mackay 1 ou structure représentative, et on a effectué une évaluation en utilisant l'approche fondée sur le SPT. Ces ratios servent à déterminer la « sensibilité » de chaque estimation d'absorption par rapport aux volumes rejetés. Le ratio le plus élevé parmi toutes les structures et substances de type Mackay 1 a été sélectionné par prudence comme scénario de la pire éventualité, soit 3,42E-7 µg/kg p.c./j pour chaque kilogramme de substance rejetée par année. Le ratio de la pire éventualité représente la substance ou la structure représentative de ce groupe pour laquelle le risque d'exposition de la population générale par émission unitaire est le plus élevé, en l'occurrence la substance portant le numéro de registre CAS 68603-15-6.
On a utilisé le ratio ci-dessus pour calculer l'absorption théorique due à une exposition environnementale pour chaque structure ou substance autre que celles du type Mackay 1, en le multipliant par les volumes totaux vendus dans le commerce. Même si le ratio était fondé sur les substances de type Mackay 1, on l'a jugé suffisamment prudent pour être utilisé avec les substances autres que celles de type Mackay 1, car il s'agit d'un « ratio de la pire éventualité ». Cependant, ce ratio est fondé sur un sous-ensemble de toutes les substances de type Mackay 1 possibles dans l'univers chimique. Par conséquent, rien n'indique qu'il puisse exister des substances organiques de type Mackay 1 autres que celles qui ont été évaluées dans la présente approche fondée sur le SPT qui seraient associées à un ratio supérieur.
4.2 Exposition due à l'utilisation de produits
La population générale peut être exposée directement à diverses substances chimiques en utilisant des produits vendus ou mis à la disposition des Canadiens, soit directement, soit sous forme de mélange dans un produit ou un article fabriqué. Les substances examinées dans le cadre de cette approche étaient associées à une plage étroite d'utilisations. Il s'agissait notamment de substances utilisées dans des procédés industriels et de substances trouvées en faible concentration dans divers produits (p. ex. concentration inférieur(e) à 5 %), substances pour lesquelles on considère que le niveau d'exposition de la population générale est faible (p. ex. lubrifiants et emballages alimentaires).
Les principales utilisations examinées dans le cadre de la présente approche fondée sur le SPT comprennent celles associées aux cosmétiques (ingrédients parfumants), celles associées au secteur alimentaire (aromates pour aliments et emballages alimentaires) et celles associées aux produits de consommation (lubrifiants et adhésifs). Pour les scénarios étudiés, la principale voie d'exposition aux substances dans les produits de consommation et les cosmétiques était la voie cutanée. Des facteurs cutanés étaient appliqués lorsqu'un ajustement des estimations de l'exposition cutanée était jugé approprié (voir le tableau B-4 pour les estimations de l'exposition directe et les facteurs cutanés).
Substances utilisées comme ingrédients parfumants dans les produits cosmétiques
Dans la présente approche fondée sur le SPT, les utilisations dans les produits cosmétiques ont été limitées aux substances employées comme ingrédients parfumants. Les substances utilisées comme parfums sont présentes en faibles concentrations dans les produits cosmétiques, et les estimations de l'exposition sont pertinentes pour une comparaison avec les valeurs du SPT.
Les concentrations de mélanges parfumants (c. à d. des mélanges d'ingrédients parfumants individuels) dans les produits cosmétiques varient de 0,3 à 2 %, selon le type de produit. Des concentrations supérieures à 2 % ont été constatées dans les produits très parfumés, comme les extraits de parfum, les eaux de toilette et les crèmes parfumantes. Dans le cas des gels pour la douche et d'autres produits pour le bain, les concentrations étaient de l'ordre de supérieur(e) à 1 à 2 %, tandis que dans le cas des antisudorifiques, des fixatifs pour cheveux, des shampoings, des lotions pour le corps et des crèmes pour le visage, les concentrations de mélanges parfumants étaient de l'ordre de 1 % ou moins (Cadby et coll. 2002).
Les concentrations de substances individuelles dans les mélanges parfumants utilisés dans les produits cosmétiques ont été étudiées dans le cadre d'enquêtes menées par l'industrie. Cependant, ces données ne sont pas publiques. Afin d'estimer la concentration d'un ingrédient parfumant dans un produit cosmétique lorsqu'aucune information précise sur la substance n'était disponible, on a supposé que la concentration par défaut de chaque substance utilisée dans un mélange parfumant était de 10 %. Cette valeur par défaut de 10 % est fondée sur la concentration des ingrédients individuels entrant dans la composition des mélanges parfumants que l'on trouve dans les produits de nettoyage domestiques (Basketter et coll., 2015). Cependant, lorsque la concentration maximale recommandée d'un ingrédient parfumant dans un mélange parfumant était inférieure à 10 %, cette valeur recommandée était utilisée au lieu de la valeur par défaut. Pour calculer la quantité de substance dans un produit cosmétique donné, la concentration de la substance individuelle dans le mélange parfumant (10 % par défaut) est combinée à une valeur présumée de 1 % du mélange parfumant (ce qui devrait être représentatif d'un produit modérément parfumé, comme une lotion pour le corps). D'après ces hypothèses, on a estimé que la concentration d'une substance utilisée comme constituant d'un mélange parfumant est de 0,1 % dans les produits cosmétiques.
Les substances utilisées dans les mélanges parfumants peuvent ne pas être expressément indiquées sur les divers produits cosmétiques. Un scénario représentatif d'une exposition cutanée estimative élevée (p. ex. lotion pour le corps) a été utilisé avec la concentration de la substance parfumante pour estimer l'exposition cutanée associée aux substances censément utilisées comme ingrédients parfumants dans les produits cosmétiques. L'estimation de l'exposition cutanée à un ingrédient parfumant dans une lotion pour le corps (µg/kg p.c./j) était fondée sur l'algorithme suivant :
{quantité de produit appliquée (mg) x conc. de la substance (%) x fréq/jour x 1000 μg/mg}/p.c.(kg)
Les paramètres suivants ont été utilisés : une quantité de produit appliquée de 4 g/événement, une fréquence de 1,1 événement/j, une concentration par défaut de 0,1 % (substance utilisée comme ingrédient parfumant) et un poids corporel de 70,9 kg. Comme nous l'avons mentionné ci-dessus, l'exposition estimée a été ajustée au besoin à l'aide de facteurs cutanés.
Aliments
Les substances incluses dans cette approche étaient associées aux utilisations suivantes dans les aliments :
- aromates pour aliments;
- emballages alimentaires.
Au Canada, les aromates pour aliments sont homologués de façon analogue aux ingrédients alimentaires qui ne sont pas des additifs. En règle générale, les aromates peuvent être utilisés dans des aliments non normalisés, de même que dans les aliments normalisés qui suivent une norme de composition énoncée dans le Règlement sur les aliments et drogues (RAD) autorisant l'utilisation d'aromates. Dans certains cas, le RAD indique les aromates dont l'utilisation est permise ou non dans les aliments normalisés. Le RAD indique également les normes de composition pour diverses préparations aromatisantes.
Le Canada ne possède pas de liste d'agents aromatisants permis. Cependant, le RAD mentionne certaines substances dont l'utilisation est interdite dans les aliments, dont certaines substances qui pourraient être utilisées comme agents aromatisants. De plus, comme pour toute substance, l'utilisation de substances aromatisantes dans les aliments ne doit pas entraîner une violation de l'article 4 de la Loi sur les aliments et drogues (LAD), qui interdit la vente d'un aliment contenant une substance toxique ou délétère.
Des évaluations réalisées par le Comité mixte FAO/OMS d'experts des additifs alimentaires (JECFA) sont disponibles pour plusieurs de ces substances, et bon nombre de ces évaluations comportent des estimations des valeurs absorbées. Lorsqu'une évaluation du JECFA indiquait une valeur d'absorption représentative pour les États-Unis, cette valeur était utilisée pour caractériser l'exposition de la population générale canadienne et pour la comparaison avec la valeur du SPT.
Certains compendiums de substances aromatisantes indiquent qu'une substance pourrait être utilisée comme agent aromatisant dans des aliments sans qu'une évaluation ait été réalisée par le JECFA. Lorsqu'elles étaient disponibles, les estimations par habitant du taux d'absorption aux États-Unis étaient utilisées pour caractériser l'exposition potentielle et pour la comparaison avec les valeurs du SPT.
Dans le cas des substances utilisées dans les emballages alimentaires, les valeurs d'absorption ont été calculées pour les utilisations présentant une possibilité de contact direct avec les aliments. La dose journalière probable (DJP) est une estimation de la quantité d'une substance ou d'un produit chimique pouvant être ingérée par le régime alimentaire sur une base quotidienne. Pour calculer les DJP dues à l'exposition chimique à des matières entrant en contact avec les aliments, la Direction des aliments de Santé Canada tient compte des données analytiques sur la migration et de la distribution des types de matériaux d'emballage alimentaire, des parts de marché et des données disponibles sur la consommation des aliments. En l'absence de données analytiques sur la migration d'une substance chimique utilisée dans les matériaux d'emballage alimentaire, on utilise des hypothèses prudentes afin d'établir des limites supérieures dans un scénario d'exposition par le régime alimentaire.
Produits de consommation
Les produits de consommation examinés dans le cadre de la présente approche comprennent notamment des lubrifiants et des adhésifs. On a considéré que la voie cutanée était la principale voie d'exposition et qu'elle survenait au moment de l'application du produit; sa valeur estimative est donnée par l'algorithme suivant :
{quantité de produit contacting avec la peau (mg) x conc. de la substance (%) x 1000 μg/mg}/p.c.(kg)
Lorsque la concentration d'une substance dans un produit donné était inconnue, une hypothèse était formulée à partir des renseignements disponibles.
Pour les produits de consommation inclus dans la présente approche, l'exposition a été jugée comme étant intermittente (p. ex. lubrifiants et adhésifs). À l'heure actuelle, les SPT sont principalement utilisés dans les évaluations de l'exposition humaine à vie (EFSA/OMS 2016). Lorsqu'il n'y a pas d'alerte de génotoxicité pour une substance donnée, l'EFSA (2012) indique que les SPT pour les critères d'effet non cancérogènes sont tirés de bases de données ne tenant pas compte des effets découlant d'une l'exposition aiguë. L'EFSA (2012) recommande d'effectuer une évaluation au cas par cas avant d'appliquer ces SPT à des durées d'exposition plus courtes.
Dans la présente approche, les valeurs du SPT pour les substances classées selon le schéma de Cramer ont été comparées directement avec les estimations de l'exposition par événement pour des scénarios d'exposition intermittente (p. ex. lubrifiants utilisés quelques fois par année). Cette approche prudente permet de tenir compte des effets qui peuvent survenir à la suite d'une exposition pendant des périodes critiques du développement, et elle est fondée sur la conclusion de l'EFSA (2012) selon laquelle les valeurs du SPT pour les substances des classes I et III de Cramer sont jugées suffisamment protectrices contre les effets nocifs pour la reproduction et le développement.
Dans le cas des substances pour lesquelles il existe des alertes structurales associées à la génotoxicité et pour lesquelles l'exposition est intermittente, des doses journalières moyennes à vie (DJMV) ont été calculées d'après le nombre de jours d'utilisation prévue par année. Les critères d'effet non cancérogènes (p. ex. prise en compte des effets pouvant se produire à la suite d'expositions survenant pendant les périodes cruciales du développement) doivent également être pris en compte pour ces substances. Par conséquent, les estimations de l'exposition par événement ont été comparées aux SPT de ces substances selon la classe de Cramer.
5.0 Incertitudes associées à l'approche fondée sur le SPT
Assignation des valeurs du SPT
L'incertitude qui accompagne l'assignation des valeurs du SPT pour la génotoxicité est associée au degré de confiance à l'égard des modèles prédictifs de génotoxicité. Le degré de confiance à l'égard de la prédiction est tributaire du domaine d'applicabilité des modèles. Si la prédiction pour une paire modèle-substance donnée est classée à l'extérieur du domaine d'applicabilité par le modèle, cela ne veut pas nécessairement dire que la prédiction n'est pas valide ou qu'elle est incorrecte. Cela signifie que l'incertitude au sujet de la fiabilité du modèle est accrue, car les ensembles de données d'apprentissage et/ou de validation peuvent ne pas être applicables à la substance en cause.
Si une substance pour laquelle un résultat positif est prédit se trouve classée à l'extérieur du domaine des deux modèles de génotoxicité utilisés dans cette approche, l'incertitude associée à l'assignation d'un SPT relatif à la génotoxicité est accrue pour cette substance. Si la substance se trouve dans le domaine d'applicabilité d'au moins un modèle et qu'un résultat positif est prédit, la prédiction selon laquelle la substance pourrait être positive dans au moins un essai de modélisation est fiable. Dans ces cas, l'incertitude à l'égard de l'assignation d'un SPT relatif à la génotoxicité est moins grande. Dans le cas des substances pour lesquelles un résultat négatif est prédit dans les deux modèles, l'incertitude associée à la prédiction est accrue si la substance ne se situe pas dans le domaine d'applicabilité des deux modèles. Les détails au sujet des domaines d'applicabilité des modèles pour la détermination de la génotoxicité de chaque substance sont présentés à l'annexe B (tableau B-1).
La mesure dans laquelle une substance candidate particulière est bien représentée par rapport à l'espace chimique dans l'ensemble de données de Munro utilisé pour établir les seuils constitue une source d'incertitude en ce qui concerne l'application des SPT de substances non génotoxiques selon la classification de Cramer. Le Centre Commun de Recherche de la Commission européenne a étudié la question de l'espace chimique dans l'ensemble de données de Munro, et plus particulièrement la façon dont il est représentatif du « monde des substances chimiques » au sens large, en accordant une attention particulière aux produits chimiques cosmétiques. Le Centre a constaté que l'ensemble de données de Munro est largement représentatif de l'espace chimique des cosmétiques (EC 2012b). Le Rapport de l'atelier EFSA/OMS a également conclu que l'actuelle base de données sous-jacente à l'approche fondée sur le SPT a été évaluée et qu'il a été déterminé qu'elle couvre un éventail de substances chimiques suffisamment large (EFSA/OMS 2016).
Afin qu'il soit possible de déterminer dans quelle mesure une substance candidate est bien représentée dans l'espace chimique de l'ensemble de données de Munro, deux éléments de cet espace chimique ont été examinés.
1) Les propriétés physico-chimiques modélisées pour la substance candidate sont comparées à la plage des propriétés physico-chimiques modélisées pour les substances chimiques faisant partie de l'ensemble de données de Munro. Cet ensemble a été caractérisé (tableau 3-3) en termes de quelques propriétés physico-chimiques clés [semblables à celles qui sont décrites dans EC (2012b)], représentant la taille (masse moléculaire), la forme (diamètre, nombre de liens pouvant subir une rotation), le comportement de partage [log Koe / log D et surface polaire topologique (TPSA)] et la réactivité [énergie de l'orbitale la plus haute occupée (HOMO) et de l'orbitale vacante la plus basse (LUMO)] à l'aide de la plate-forme ACD Percepta et de la boîte à outils QSAR de l'OCDE (v3.3) (MOPAC 7 Stewart, J.J.P. Stewart Computational Chemistry; calculateur de diamètre OASIS) (ACD c1994-2015; OCDE 2015).
| Propriété | Min. | 5e centile | Median | 95e centile | Max. |
|---|---|---|---|---|---|
| Masse moléculaire (Da)b | 30 | 85 | 219 | 501 | 1135 |
| Diamètre – min. (Å)a | 2,9 | 3,2 | 4,9 | 6,7 | 8,1 |
| Diamètre – max. (Å)a | 4,68 | 6,96 | 11,9 | 20 | 52,5 |
| Log Koeb | -7,52 | -1,5 | 2,3 | 6,3 | 15,3 |
| Log D (à un pH de 7)b | -9,52 | -4,3 | 1,9 | 6,2 | 15,3 |
| Nombre de liens pouvant subir une rotationb | 0 | 0 | 3 | 11 | 39 |
| TPSAb | 0 | 0 | 49,3 | 179,2 | 554,1 |
| Énergie de la HOMO (eV)a | -17,8 | -11,6 | -9,6 | -8,1 | -2,3 |
| Énergie de la LUMO (eV)a | -9,4 | -1,8 | -0,3 | 1,5 | 3,8 |
a Valeur calculée à l'aide de la boîte à outils de l'OCDE (v3.3) (MOPAC 7 Module [Stewart, J.J.P. Stewart Computational Chemistry]; calculateur de diamètre OASIS)
b ACD Percepta (c1994-2015) – PhysChem Profiler
Si la substance candidate a des propriétés qui se situent à l'extérieur des plages maximale et minimale pour les substances chimiques dans l'ensemble de données de Munro, elle est jugée hors domaine (annexe B; tableau B-2). Pour 58 structures sur les 59 ayant reçu un SPT d'après la classification de Cramer, toutes les propriétés physico-chimiques décrites étaient situées à l'intérieur de l'ensemble de données de Munro.
2) Les substructures et caractéristiques chimiques (p. ex. les chémotypes) d'une substance candidate sont comparées avec celles de l'ensemble de données de Munro. Le logiciel ChemoTyper (Yang et coll. 2015), qui utilise des chémotypes ToxPrint accessibles au public, a été utilisé pour générer une empreinte moléculaire des substances chimiques candidates et des produits chimiques de l'ensemble de données de Munro afin de permettre une comparaison des caractéristiques chimiques dans les deux ensembles de substances. Les chémotypes ToxPrint contiennent un ensemble de caractéristiques chimiques et de règles établies d'après divers modèles prédictifs de toxicité et de lignes directrices en matière d'évaluation de l'innocuité élaborées par la FDA et d'autres organismes et industries (Yang et coll. 2015).
Lorsqu'un chémotype ToxPrint identifié pour une substance candidate ne figurait pas parmi les chémotypes ToxPrint des substances de l'ensemble de données de Munro, la substance était considérée comme étant hors domaine (annexe B; tableau B-2). Pour 50 structures sur les 59 ayant reçu un SPT d'après la classification de Cramer, tous les chémotypes identifiés étaient couverts par l'ensemble de données de Munro.
Lorsqu'une substance candidate est jugée hors domaine d'après l'une des deux comparaisons décrites ci dessus, il y a une plus grande incertitude rattachée à l'utilisation de l'approche fondée sur le SPT, car ces substances peuvent ne pas être bien représentées à l'intérieur de l'espace chimique de l'ensemble de données de Munro.
Une analyse complémentaire comparative a été réalisée afin d'examiner le voisin le plus proche dans l'ensemble de données de Munro pour chaque substance candidate pertinente, d'après les chémotypes ToxPrint observés. Les empreintes ToxPrint des substances candidates et dans l'ensemble de données de Munro ont été converties en un vecteur binaire pour représenter la substance (c. à d. une chaîne de 1 et de 0 selon la présence ou l'absence de chacun des chémotypes ToxPrint), à l'aide du nœud applicable dans le logiciel KNIME (version 2.11.2) (KNIME 2015). Le nœud de recherche de similarité (Similarity Search) dans KNIME a ensuite été utilisé pour chercher les substances chimiques les plus similaires dans l'ensemble de données de Munro pour chaque substance candidate, d'après la métrique de Tanimoto (calculée au moyen du vecteur binaire obtenu à l'aide de ToxPrint). Le voisin le plus proche pour chaque substance candidate dans l'ensemble de données de Munro, selon cette approche, est présenté à l'annexe B (tableau B-2).
Estimation de l'exposition
Les estimations de l'exposition associées à l'utilisation des produits sont fondées sur l'exposition cutanée, tandis que l'ensemble de données associées au SPT est fondé sur les expositions par voie orale. L'application de facteurs cutanés (décrits au tableau B 4) est considérée comme une mesure prudente, qui reflète quand même les principaux paramètres influant sur l'exposition cutanée.
Les estimations de l'exposition aux substances parfumantes utilisées dans les cosmétiques s'appuient sur des hypothèses concernant les concentrations de ces substances dans des produits et sur un scénario représentatif d'une exposition élevée par voie cutanée (lotion pour le corps). Cette approche est jugée prudente, particulièrement pour les substances parfumantes moins courantes.
Les estimations de l'exposition pour les substances aromatisantes tiennent compte des évaluations du JECFA datant d'avant 2009. Le JECFA a reconnu que la méthode d'estimation de l'absorption maximale calculée d'après les enquêtes (MSDI) qu'elle utilisait jusqu'en 2009 pouvait sous-estimer de façon importante l'exposition par le régime alimentaire à certains agents aromatisants, comme ceux qui sont consommés par moins de 10 % de la population, surtout s'ils sont utilisés dans quelques catégories d'aliments seulement, et aux agents aromatisants auxquels les consommateurs sont exposés de façon inégale par le régime alimentaire. Dans cette approche, l'utilisation d'une valeur d'absorption fondée sur la méthode MSDI a été limitée à un nombre très restreint de substances (à savoir 5). L'absorption estimée était bien inférieure au SPT.
6.0 Résultats
À l'aide de la méthode décrite ci-dessus, 89 substances sur les 237 évaluées dans le cadre de cette approche se sont révélées être associées à une exposition directe ou indirecte inférieure au SPT correspondant. Par conséquent, ces substances ne sont pas jugées préoccupantes pour la santé humaine aux niveaux d'exposition actuels.
En ce qui concerne les 148 autres substances, soit qu'elles ont été exclues de l'approche fondée sur le SPT (d'après les critères d'exclusion décrits à la section 3.1), soit que les estimations de l'exposition étaient supérieures au SPT assigné. Ces substances feront l'objet d'une évaluation ultérieure dans le cadre d'initiatives distinctes.
Une évaluation des 89 substances, réalisée en vertu des articles 68 et/ou 74 de la LCPE, sera publiée à une date ultérieure.
L'annexe B présente une liste de ces 89 substances, avec le SPT correspondant, ainsi que les estimations de l'exposition.
Références
ACD/Percepta [Prediction Module]. c1997-2015. Toronto (ON): Advanced Chemistry Development (en anglais seulement).
[ACToR] Aggregated Computational Toxicology Resource. 2013-. Washington (DC): US Environmental Protection Agency (en anglais seulement).
Aronson D, Boethling R, Howard P, Stiteler W. 2006. Estimating biodegradation half-lives for use in chemical screening. Chemosphere 63: 1953-1960.
Ashby J, Tennant R.W. 1991. Definitive relationships among chemicalstructure, carcinogenicity, and mutagenicity for 301 chemicals tested by the US NTP. Mutation Research 257: 229-306.
Barlow S. 2005. Threshold of toxicological concern (TTC). ILSI Europe Concise Monograph Series. p.1-31 (en anglais seulement).
Barlow SM, Kozianowski G, Wurtzen, Schlatter J. 2001. Threshold of toxicological concern for chemical substances present in diet. Report of a workshop held on 5-6 October 1999 in Paris, France organised by the ILSI Europe Threshold of Toxicological Concern Task Force. Food Chem Toxicol 39:893-905.
Basketter DA, Lemoine S, McFadden JP. Skin sensitisation to fragrance ingredients: is there a role for household cleaning/maintenance products? 2015. Eur J Dermatol 25(1):7-13.
Bernauer U, Heinemeyer G, Heinrich-Hirsch B, Ulbrich B, Gundert-Remy U. 2008. Exposure-triggered reproductive toxicity testing under the REACH legislation: a proposal to define significant/relevant exposure. Toxicology Letters 176:68-76.
Beyer A, Wania F, Gouin T, Mackay D, Matthies M. 2002. Selecting internally consistent physicochemical properties of organic compounds. Environ Toxicol Chem 21(5):941-953.
Bhatia S, Schultz T, Roberts D, Shen J, Kromidas L, Api AM. 2014. Comparison of cramer classification between Toxtree, the OECD QSAR Toolbox and expert judgment. Reg Tox Pharmacol 71:52-62.
Bitsch A, Jacobi S, Melber C, Wahnschaffe U, Simetska N, Mangelsdorf I. 2006. REPDOSE: a database on repeated dose toxicity studies of commercial chemicals-a multifunctional tool. Reg Toxicol Pharmacol 46:202-210.
Blackburn K, Stickney JA, Carlson-Lynch HL, McGinnis PM, Chappell L, Felter SP. 2005. Application of the threshold of toxicological concern approach to ingredients in personal and household care products. Reg Toxicol Pharmacol 43:249-259.
Boethling RS, Howard PH, Beauman JA, Larosche ME. 1995. Factors for intermedia extrapolations in biodegradability assessment. Chemosphere 30(4):741-752.
Burdock GA. 2009. Fenaroli's Handbook of Flavor Ingredients. Sixth Edition. CRC Press.
Cadby PA, Troy WR, Vey MGH. 2002. Consumer Exposure to Fragrance Ingredients: Providing Estimates for Safety Evaluation. Reg Toxicol Pharmacol 36:246-252.
Canada. 1999. Loi canadienne sur la protection de l'environnement (1999). L.C. 1999, ch. 33.
[Canada] Canada, Min. de l'Environnement, Min. de la Santé. 2006. Loi canadienne sur la protection de l'environnement (1999) : Avis concernant certaines substances considérées comme priorités pour suivi. Gazette du Canada, Partie I, vol. 140, no 9, p. 435-459.
Canada. 2009. Loi canadienne sur la protection de l'environnement (1999) : Avis concernant certaines substances inanimées (chimiques) inscrites sur la Liste intérieure, Gazette du Canada, Partie I, vol. 143, no 40, 3 oct. Disponible à : http://publications.gc.ca/gazette/archives/p1/2009/2009-10-03/pdf/g1-14340.pdf
Canada. 2012. Loi canadienne sur la protection de l'Environnement (1999) : Avis concernant certaines substances de la Liste intérieure. Gazette du Canada, Partie I, vol. 146, no 48, 1er décembre.
Canada. 2014. Draft results from Phase Two of the Domestic Substances List Inventory Update. Environnement Canada: Gatineau (QC).
Carthew P, Clapp C, Gutsell S. 2009. Exposure based waiving: the application of the toxicological threshold of concern (TTC) to inhalation exposure for aerosol ingredients in consumer products. Food Chem Toxicol 47:1287-1295.
Cheeseman MA, Machuga EJ, Bailey AB. 1999. A tiered approach to threshold of regulation. Food Chem Toxicol 37:387-412.
ChemIDplus. 1993. ChemIDplus Advanced. Bethesda (MD): National Library of Medicine (US) (en anglais seulement).
[ChemCAN]. 2003. ChemCAN: Level III fugacity model of regional fate of chemicals[Internet]. Version 6.00. Peterborough (ON): The Canadian Centre for Environmental Modelling and Chemistry, Trent University(en anglais seulement).
Cimino MC. 2006. Comparative overview of current international strategies and guidelines for genetic toxicology testing for regulatory purposes. Environ Mol Mutagen 47(5):362-390 (en anglais seulement).
[ConsExpo] Consumer Exposure Model. 2006. Version 4.1. Bilthoven (NL): Rijksinstituut voor Volksgezondheid en Milieu [National Institute for Public Health and the Environment] (en anglais seulement).
[CPCat] Chemical and Product Categories [database on the inventory]. 2014. U.S. Environmental Protection Agency (en anglais seulement).
[CPDB] The Carcinogenic Potency Database [database]. [modified 2007]. Berkley Lab, University of California (en anglais seulement).
Cramer GM, Ford RA, Hall RL. 1978. Estimation of toxic hazard - a decision tree approach. Food Cosmet Toxicol 16:255-276.
Danish Ministry of Environment - Environmental Protection Agency. 2011. The threshold of toxicological concern (TTC) concept: Development and regulatory applications. Environmental Project No. 1359 2011 (en anglais seulement).
Denmark. 2014. Danish surveys on chemicals in consumer products, Ministry of Environment and Food, The Danish Environment Protection Agency (en anglais seulement).
Dewhurst I, Renwick AG. 2013. Evaluation of the Threshold of Toxicological Concern (TTC) - Challenges and approaches, Regulatory Toxicology and Pharmacology 65(1):168-177.
Dolan DG, Naumann BD, Sargent EV, Maier A, Dourson M. 2005. Application of the threshold of toxicological concern concept to pharmaceutical manufacturing operations. Reg Toxicol Pharmacol 43:1-9.
Eastmond DA, Hartwig A, Anderson D, Anwar WA, Cimino MC, Dobrev I, Douglas GR, Nohmi T, Phillips DH, Vickers C. 2009. Mutagenicity testing for chemical risk assessment: update of the WHO/IPCS harmonized scheme. Mutagenesis 24(4): 341-349.
[EAFUS] Everything Added to Food in the United States[Internet]. 2013. U.S. Food and Drug Administration; [cité en 2015 November] (en anglais seulement).
[EC] European Commission. 2012. Opinion on use of the threshold of toxicological concern (TTC) approach for human safety assessment of chemical substances with focus on cosmetic and consumer products. Health and Consumer Directorate, Brussels (en anglais seulement).
[EC] European Commission. 2012b. Applicability of the threshold of toxicological concern (TTC) approach to cosmetics - preliminary analysis. Joint Research Council, Ispra, Italy (en anglais seulement).
[ECETOC] European Centre for Ecotoxicology and Toxicology of Chemicals. 2010. Guidance on Assessment Factors to Derive a DNEL. Brussels, Belgium (en anglais seulement).
[EFSA] European Food Safety Authority. 2012. Scientific opinion on exploring options for providing advice about possible human health risks based on the concept of Threshold of Toxicological Concern (TTC). EFSA Journal 10(7):2750 (en anglais seulement).
[EFSA] European Food Safety Authority/[WHO] World Health Organisation. 2016. Review Threshold of toxicological concern (TTC) and development of new TTC decision tree (en anglais seulement).
[EMA] European Medical Agency. 2006. Guideline on the Limits of Genotoxic Impurities. Committee for Medicinal Products for Human Use (CHMP). European Medicines Agency, EMEA/CHMP/QWP/251344/2006.
[EMA] European Medical Agency. 2008. Draft Guideline on the Assessment of Genotoxicity of Herbal Substances/Preparations. Committee on Herbal Medicinal Products (HMPC). European Medicines Agency, London, UK, EMEA/HMPC/107079/2007.
Environnement Canada. 2012. Final Results from Phase One of the Domestic Substances List Inventory Update Rapid Screening Assessment of Substances of Lower Ecological Concern - Detailed Spreadsheet. Gatineau (QC): Ecological Assessment Division, Environnement Canada.
Environnement Canada. 2013. Inventaire national des rejets de polluants [database on the Internet]. Gatineau (QC) : Environnement Canada.
[EPI Suite™] Estimation Programs Interface Suite for Microsoft Windows [Estimation Model]. 2012. Version 4.1. Office of Pollution Prevention and Toxics, U.S. Environmental Protection Agency: Washington DC; Syracuse Research Corporation: Syracuse (NY) (en anglais seulement).
Escher SE, Tluczkiewicz I, Batke M, Bitsch A, Melber C, Kroese, E.D., Buist, H.E, Mangelsdorf I. 2010. Evaluation of inhalation TTC values with the database RepDose. Reg Toxicol Pharmacol 58:259-274.
Feigenbaum A, Pinalli R, Giannetto M, Barlow S. Reliability of the TTC approach: Learning from inclusion of pesticide active substances in the supporting database. Food and Chemical Toxicology 75: 24-38.
Felter S, Lane RW, Latulippe ME, Llewellyn GC, Olin SS, Scimeca JA, Trautman TD. 2009. Refining the threshold of toxicological concern (TTC) for risk prioritization of trace chemicals in food. Food Chem Toxicol 47:2236-2245.
Finizio A, Mackay D, Bidleman T, Harners T. 1997. Octanol air-partition coefficient as a predictor of partitioning of semi-volatile organic chemicals to aerosol. Atmospheric Environment 31(15):2289-2296.
Geraets L, Bessems JG, Zeil MJ, Bos PM. (2014). Human risk assessment of dermal and inhalation exposures to chemicals assessed by route-to-route extrapolation: The necessity of kinetic data. Regulatory Toxicology and Pharmacology 70:54-64.
Gold LS, Sawyer CB, Magaw R, Backman GM, de Veciana M, Levinson R, Hooper NK, Havender WR, Bernstein L, Peto R, Pike M, Ames BN. 1984. A carcinogenesis potency database of the standardized results of animal bioassays. Environ Health Persp 58:9-319.
Gold LS, Slone TH, Bernstein L. 1989. Summary of carcinogenic potency and positivity for 492 rodent carcinogens in the carcinogenic potency database. Environ Health Persp 79:259-272.
Grant RL, Kadlubar BJ, Erraguntla NK, Honeycutt M. 2007. Evaluation of acute inhalation toxicity for chemicals with limited toxicity information. Reg Toxicol Pharmacol 47:261-273.
Health Canada. 1998. Exposure factors for assessing total daily intake of priority substances by the general population of Canada. Unpublished report. Ottawa (ON): Health Canada, Environmental Health Directorate.
Santé Canada. 2016. Ligne directrice - Directive sur l'évaluation de la génotoxicité des produits pharmaceutiques destinés à l'utilisation humaine et interprétation des données : ICH thème S2(R1). Ottawa (ON) : Santé Canada.
[ICH] International Conference on Harmonisation. 2012. Guidance for industry: S2(R1) Genotoxicity testing and data interpretation for pharmaceuticals intended for human use. International Conference on Harmonisation of Technical Requirements for Registration of Pharmaceuticals for human use.
[IMS] Intercontinental Marketing Services. 2013. Health Canada Sales Database 2011 & 2012[MIDAS database on CD]. IMS Brogan, Toronto (ON), IMS Brogan.
[IPCS] International Program on Chemical Safety. 2007. Mutagenicity testing for chemical risk assessment. Harmonization project draft document for public and peer review. World Health Organization (en anglais seulement).
[CMEAA] Comité mixte FAO/OMS d'experts des additifs alimentaires. 1993. Évaluation de certains additifs alimentaires et contaminants. Quarante et unième rapport du Comité mixte FAO/OMS d'experts des additifs alimentaires. OMS, Série de Rapports techniques, 837. Organisation mondiale de la Santé, Genève, Suisse (en anglais seulement).
[CMEAA] Comité mixte FAO/OMS d'experts des additifs alimentaires. 1995. Évaluation de certains additifs alimentaires et contaminants. Quarante-quatrième rapport du Comité mixte FAO/OMS d'experts des additifs alimentaires. OMS, Série de Rapports techniques, 859. Organisation mondiale de la Santé, Genève, Suissee (en anglais seulement).
[JECFA] Joint FAO/WHO Expert Committee on Food Additives. 1998. Safety Evaluation of Certain Food Additives and Contaminants. WHO Food Additives Series 40: Annex 5. World Health Organisation, Geneva, Switzerland. p. 497-532 (en anglais seulement).
[JECFA] Joint FAO/WHO Expert Committee on Food Additives. 2000. Evaluation of Certain Food Additives and Contaminants: Fifty-fifth Report of the Joint FAO/WHO Expert Committee, Geneva, Switzerland (en anglais seulement).
[JECFA] Joint FAO/WHO Expert Committee on Food Additives. 2003. Evaluation of Certain Food Additives and Contaminants: Sixty-First Report of the Joint FAO/WHO Expert Committee, Geneva, Switzerland (en anglais seulement).
[JECFA] Prepared by the Sixty-third meeting of the Joint FAO/WHO Expert Committee on Food Additives. 2006. Evaluation of Certain Food Additives. WHO Food Additive Series: 54. Geneva, Switzerland (en anglais seulement).
Kalkhof H, Herzler M, Stahlmann R, Gundert-Remy U. 2011. Threshold of toxicological concern values for non-genotoxic effects in industrial chemicals: re-evaluation of the Cramer classification. Archives of Toxicology 86: 17-25.KNIME [Computational workflow tool]. 2015. Version 2.11.2. Zurich (CH): KNIME.COM AG (en anglais seulement).
Kroes R, Galli CL, Munro I, Schilter B, Tran L.-A, Walker R, Wurtzen G. 2000. Threshold of toxicological concern for chemical substances present in the diet: a practical tool for assessing the need for toxicity testing. Food Chem Toxicol 38:255-312.
Kroes R, Muller D, Lambe J, Lowik MRH, van Klaveren J, Kleiner J, Massey R, Mayer S, Urieta I, Verger P, Visconti A. 2002. Assessment of intake from the diet. Food Chem Toxicol 40:327-385.
Kroes R, Renwick AG, Cheeseman M, Kleiner J, Mangelsdorf I, Piersma A, Schilter B, Schlatter J, van Schothorst F, Vos JG, Wurtzen G. 2004. Structure-based thresholds of toxicological concern (TTC): guidance for application to substances present at low levels in the diet. Food Chem Toxicol 42:65-83.
Kroes R, Renwick AG, Feron V, Galli CL, Gibney M, Greim H, Guy RH, L'Huguenot JC, van de Sandt JJM. 2007. Application of the threshold of toxicological concern (TTC) to the safety evaluation of cosmetic ingredients. Food Chem Toxicol 45:2533-2562.
Laufersweiler MC, Gadagbui B, Baskerville-Abraham IM, Maier A, Willis A, Scialli AR, Carr GJ, Felter SP, Blackburn K, Daston G, 2012. Correlation of chemical structure with reproductive and developmental toxicity as it relates to the use of the threshold of toxicological concern. Regulatory Toxicology and Pharmacology 62: 160-182.
Mackay D, Di Guardo A, Paterson S, Kicsi G, Cowan CE. 1996. Assessing the fate of new and existing chemicals: a five-stage process. Environ Toxicol Chem 15(9):1618-1626.
Muller L, Mauthe RJ, Riley CM, Andino MM, Antonis DD, Beels C, DeGeorge J, De Knaep AG, Ellison D, Fagerland JA, Frank R, Fritschel B, Galloway S, Harpur E, Humfrey CD, Jacks AS, Jagota N, Mackinnon J, Mohan G, Ness DK, O'Donovan MR, Smith MD, Vudathala G, Yotti L. 2006. A rationale for determining, testing, and controlling specific impurities in pharmaceuticals that possess potential for genotoxicity. Reg Toxicol Pharmacol 44:198-211.
Munro IC, Kennepohl E, Kroes R 1999. A procedure for the safety evaluation of flavouring substances. Food Chem Toxicol 37:207-232.
Munro IC, Ford RA, Kennepohl E, Sprenger JG. 1996. Correlation of structural class with no-observed effect levels: A proposal for establishing a threshold of concern. Food Chem Toxicol 34:829-867.
Munro IC. 1990. Safety assessment procedures for indirect food additives: An overview: Report of a workshop. Reg Toxicol Pharmacol 12:2-12.
[BDIPSN] Base de données d'ingrédients de produits de santé naturels[database on the internet]. 2016. Santé Canada, Gouvernement du Canada; [consultée en juillet 2016].
OASIS Pipeline Profiler [Computational workflow tool]. 2015. Version 1.0.52.1. Bourgas (BG): Bourgas Prof. Assen Zlatarov University, Laboratory of Mathematical Chemistry.
OCDE, Boîte à outils QSAR Toolbox. [Read across tool]. 2015. Version 3.3. Paris (FR) : Organisation de coopération et de développement économiques, Direction de l'Environnement.
Pinalli R, Croera C, Thebold A, Feigenbaum A. 2011. Threshold of toxicological concern approach for the risk assessment of substances used for the manufacture of plastic food contact materials. Trends in Food Sci 22:523-534.
Renwick AG.1993. Data-derived safety factors for the evaluation of food additives and environmental contaminants. Food Additives & Contaminants 10(3):275-305.
Roberts DW, Aptula A, Schultz TW, Shen J, Api AM, Bhatia S, Kromidas L. 2015. A practical guidance for cramer class determination. Reg Tox Pharmacol 1-14 (In press).
Rulis AM. 1989. Establishing a threshold of regulation. In: Bonin, J.J., Stevenson, D.E. (Eds.), Risk Assessment in Setting National Priorities. Plenum Publishing Corporation. p. 271-278.
Rulis AM. 1986. De minimis and the threshold of regulation. In: Felix, C.W. (Ed.), Food Protection Technology. Lewis Publishers. p. 29-37.
Safford RJ, Aptula AO, Gilmour N. 2011. Refinement of the dermal sensitisation threshold (DST) approach using a larger dataset and incorporating mechanistic chemistry domains. Reg Toxicol Pharmacol 60:218-224.
Safford RJ. 2008. The dermal sensitisation threshold--a TTC approach for allergic contact dermatitis. Reg Toxicol Pharmacol 51:195-200.
SCCS, SCHER, SCENIHR. 2012. Joint Opinion on the Use of the Threshold of Toxicological Concern (TTC) Approach for Human Safety Assessment of Chemical Substances with focus on Cosmetics and Consumer Products, 8 June 2012.
Schüümann G, Ebert R-U, Tluczkiewicz I, Escher S, Kühne R., 2016. Inhalation threshold of toxicological concern (TTC) - Structural alerts discriminate high from low repeated-dose inhalation toxicity. Environment International 88:123-132.
[TIMES] TIssue MEtabolism Simulator [Prediction module]. 2015. Version 2.27.17. Bourgas (BG): Bourgas Prof. Assen Zlatarov University, Laboratory of Mathematical Chemistry. [cited 2015 December 7] (en anglais seulement).
Tluczkiewicz I, Buist HE, Martin MT, Mangelsdorf I, Escher SE. 2011. Improvement of the Cramer classification for oral exposure using the database TTC RepDose - A strategy description Regulatory Toxicology and Pharmacology61: 340-350.
Toxtree [Prediction module]. 2015. Version 2.6.13. Bourgas (BG): IDEAconsult Ltd. (en anglais seulement).
[US FDA] Food and Drug Administration. 1995. Federal Register Food Additives; Threshold of Regulation for substances used in food contact articles. Department of Health and Human Services, Food and Drug Administration, 21 CFR Parts 5, 25, 170,171, and 174. Docket Nos 77P-0122, 92N-0181 (en anglais seulement).
[US FDA] Food and Drug Administration. 2001. 21 CFR, Ch.I, Subpart B. Food Additive Safety, 170.20, 170.22, 170.30 (en anglais seulement).
[US FDA] Food and Drug Administration. 2015. M7 Assessment and Control of DNA Reactive (Mutagenic) Impurities in Pharmaceuticals to Limit Potential Carcinogenic Risk Guidance for Industry (en anglais seulement).
Van Ravenzwaay B, Dammann M, Buesen R, Schneider S. 2011. The threshold of toxicological concern for prenatal developmental toxicity. Reg Toxicol Pharmacol 59:81-90.
[VKM] Norwegian Scientific Committee for Food Safety. 2006. Present and suggested use of the Threshold of Toxicological Concern (TTC) principle in areas of risk assessment relevant for the Norwegian Scientific Committee for Food Safety (VKM). Opinion of the Ad hoc working group for evaluation of the use of the Threshold of Toxicological Concern (TTC) principle in risk assessments performed by the Norwegian Scientific Committee for Food Safety.
[OMS] Organisation mondiale de la Santé. 1995. Évaluation de certains additifs alimentaires et contaminants (Quarante-quatrième rapport du Comité mixte FAO/OMS d'experts des additifs alimentaires). OMS, Série de Rapports techniques, 859. Genève, Suisse.
[OMS] Organisation mondiale de la Santé. 1997. Évaluation de certains additifs alimentaires et contaminants (Quarante-sixième rapport du Comité mixte FAO/OMS d'experts des additifs alimentaires). OMS, Série de Rapports techniques, 868. Genève, Suisse.
[WHO] World Health Organization. 2000. Evaluation of certain food additives. WHO Technical Report Series 891. Geneva, Switzerland (en anglais seulement).
Williams FM. 2008. Potential for metabolism locally in the skin of dermally absorbed compounds. Human Experimental Toxicology 27:277-280.
Williams FM, Rothe H, Barrett G, Whyte J, Chiodini A, Cronin MT, Monteiro-Riviere N, Plautx J, Roper C, Westerhout J, Yang C, Guy RH. 2016. Assessing the safety of cosmetic chemicals: considerations of a flux decision tree to predict dermally delivered systemic dose for comparison with oral TTC (Threshold of Toxicological Concern). Toxicology and Pharmacology. In press: accepted manuscript [not currently available online].
Wilson R, Jones-Otazo H, Petrovic S, Mitchell I, Bonvalot Y, Williams D, Richardson GM. 2013. Revisiting dust and soil ingestion rates based on hand-to-mouth transfer. Human and Ecological Risk Assessment19(1):158-188.
Won D, Lusztyk E. 2011. Data gathering on chemicals released to indoor air of residences from building materials and furnishings. NRC-Institute for Research in Construction Report no. B3332.2. Prepared for Health Canada, Ottawa, ON.
Yang C, Tarkhov A, Marusczyk J. 2015. New publicly available chemical query language, CSRML to support chemotype representations for application to data mining and modeling. J Chem Inf Model 55(3):510-528.
Zhu J, Wong S, Cakmak S. 2013. Nationally representative levels of selected volatile organic compounds in Canadian residential indoor air: population-based survey. Environ Sci Technol 47:13276-13283.
Annexes
Annexe A – Arbre décisionnel pour le SPT proposé par Kroes et coll. (2004)
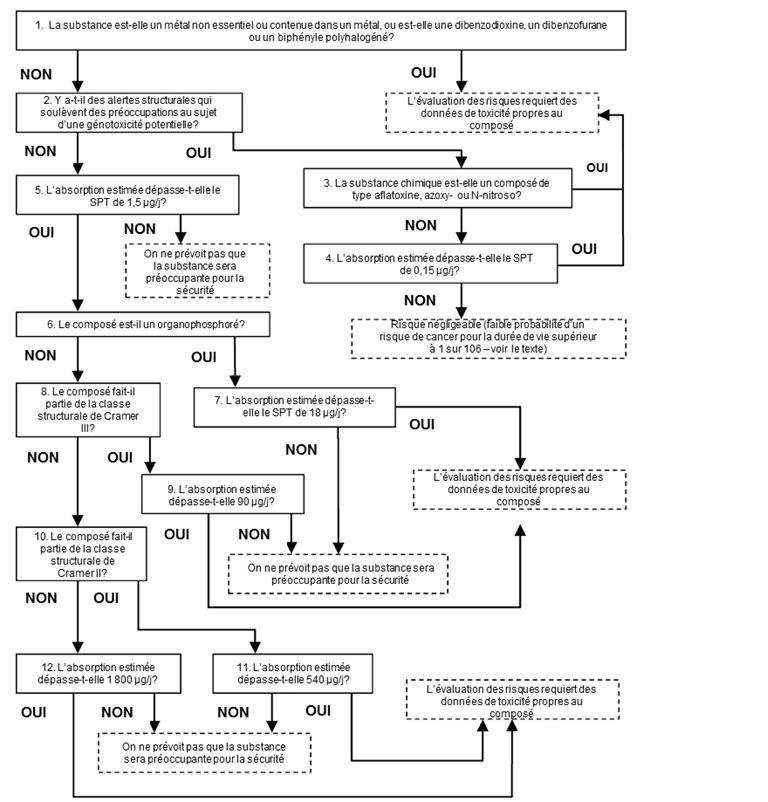
Longue description pour la figure Annexe A
Dans cette annexe, on présente l’arbre décisionnel de STP qui avait été proposé par Kroes et al. (2004). Cet arbre est présenté sous forme d’une série de questions permettant de traiter une substance donnée. À la question 1 de cet arbre, on demande si la substance est un métal non essentiel ou un composé contenant un métal ou si c’est une dibenzodioxine polyhalogénée, un dibenzofurane polyhalogéné ou un biphényle polyhalogéné. Si c’est le cas, l’évaluation des risques requérerait des données de toxicité spécifiques au composé et l’arbre serait clos. Dans le cas contraire, on demande à la question 2 s’il existe des alertes au niveau structurel qui soulèvent des inquiétudes au sujte du potentiel de génotoxicité. Si la substance est sujette à de telles alertes, on passe à la question 3. À cette question, on demande si le composé chimique est un composé de type aflatoxine, azoxy ou N-nitroso. Si c’est le cas, l’évaluation des risques requérerait des données spécifiques au composé et l’arbre serait clos. Sinon, on passe à la question 4. À cette question, on demande si l’absorption estimée de la substance excède une valeur de STP de 0,15 µg/jour. Si oui, l’évaluation des risques requérerait des données de toxicité spécifique au composé et l’arbre serait clos. Dans le cas contraire, le risque est considéré négligeable (c. à-d. faible probabilité d’un risque additionnel de cancer pendant la durée de vie supérieur à 1 en 106) et l’arbre serait donc clos. Si la substance ne présente pas d’alertes au niveau structurel ayant trait à la génotoxicité, on passe à la question 5. À cette question, on demande si l’absorption estimée excède une valeur de STP de 1,5 µg/jour. Si ce n’est pas le cas, la substance ne devrait pas être inquiétante au niveau de la sécurité, et l’arbre est clos. Dans le cas contraire, on passe à la question 6. À cette question on demande si la substance est un organophosphate. Dans l’affirmative, on passe à la question 7. À cette question, on demande si l’absorption estimée excède une valeur de STP de 18 µg/jour. Dans l’affirmative, l’évaluation des risques requérerait des données de toxicité spécifique au composé et l’arbre serait clos. Dans le cas contraire, la substance ne devrait pas être inquiétante au niveau de la sécurité et l’arbre serait de même clos. Si la substance n’est pas un organophosphate, on passe à la question 8. À cette question, on demande si elle fait partie de la classe structurelle III de Cramer. Si c’est le cas, on passe à la question 9. À cette question, on demande si l’absorption estimée excède 90 µg/jour. Si c’est le cas, l’évaluation des risques requérerait des données de toxicité spécifiques au composé et l’arbre serait clos. Dans le cas contraire, la substance ne devrait pas être inquiétante au niveau de la sécurité et l’arbre est de même clos. Si la substance n’appartient pas à la classe structurelle III de Cramer, on passe à la question 10. À cette question, on demande si elle fait partie de la classe structurelle II de Cramer. Si c’est le cas, on passe à la question 11. À cette question, on demande si l’absorption estimée excède 540 µg/jour. Si c’est le cas, l’évaluation des risques requérerait des données de toxicité spécifiques au composé et l’arbre serait clos. Dans le cas contraire, la substance ne devrait pas être inquiétante au niveau de la sécurité et l’arbree serait de même clos. Si la substance n’appartient pas à la classe structurelle II de Cramer, on passe à la question finale, à savoir la question 12. À cette question, on demande si l’absorption estimée excède 1800 µg/jour. Si c’est le cas, l’évlauation des risques requérerait des données de toxicité spécifiques au composé. Dans le cas contraire, la substance ne devrait pas être inquiétante au niveau de la sécurité.
Annexe B – Résultats de l'approche
| No CAS | SPT µg/kg p.c./j |
GT (Base) | GT SE1 | GT SE2 | GT SE3 | TIMES GT Ames avec S9 |
TIMES GT CA avec S9 |
CC |
|---|---|---|---|---|---|---|---|---|
| 50-48-6 | 0,0025 | P(M) | N | PD | PD | N(Ex) | P(Ex) | s.o. |
| 60-24-2 | 30 | N(E/M) | N | N | N | N(In) | N(In) | 1 |
| 64-86-8 | 0,0025 | P(E) | N | P | P | s.o. | s.o. | s.o. |
| 77-47-4 | 0,0025 | P(E) | N | P | Eq | s.o. | s.o. | s.o. |
| 78-67-1 | 1,5 | N(E/M) | N | N | PD | N(In) | N(In) | 3 |
| 79-74-3 | 30 | N(M) | PD | PD | PD | N(Ex)N | N(Ex)N | 1 |
| 85-42-7 | 1,5 | N(M) | PD | PD | PD | N(Ex)N | N(Ex)N | 2 |
| 87-66-1 | 0,0025 | P(E) | P | PD | P | s.o. | s.o. | s.o. |
| 92-70-6 | 1,5 | N(E) | N | P | N | s.o. | s.o. | 3 |
| 101-37-1 | 1,5 | N(E) | N | N | N | P(Ex)P | P(Ex)P | 3 |
| 103-24-2 | 30 | N(E/M) | N | N | PD | N(In)N | N(In)N | 1 |
| 111-55-7 | 0,0025 | P(M) | PD | PD | PD | P(I)P | P(I)P | s.o. |
| 111-96-6 | 30 | N(E/M) | N | PD | PD | N(In)N | N(In)N | 1 |
| 112-49-2 | 0,0025 | P(E) | P | PD | PD | s.o. | s.o. | s.o. |
| 118-96-7 | 0,0025 | P(E) | P | PD | N | s.o. | s.o. | s.o. |
| 120-11-6 | 1,5 | N(E) | N | PD | N | N(In) | P(Ex) | 3 |
| 120-24-1 | 30 | N(E) | N | PD | N | N(In) | P(Ex) | 1 |
| 120-54-7 | 1,5 | N(M) | PD | PD | PD | N(Ex)N | N(Ex)N | 3 |
| 121-91-5 | 30 | N(E/M) | N | N | PD | N(Ex)N | N(Ex)N | 1 |
| 122-68-9 | 30 | N(M) | PD | PD | PD | N(In)N | N(Ex)N | 1 |
| 122-79-2 | 0,0025 | P(M) | PD | PD | PD | P(Ex) | P(Ex) | s.o. |
| 126-33-0 | 0,0025 | P(E) | N | P | PD | s.o. | s.o. | s.o. |
| 132-65-0 | 0,0025 | P(M) | PD | PD | PD | N(Ex)N | P(Ex)P | s.o. |
| 133-14-2 | 0,0025 | P(E) | P | N | PD | s.o.s.o. | s.o.s.o. | s.o. |
| 288-88-0 | 1,5 | N(M) | PD | PD | PD | N(Ex)N | N(Ex)N | 3 |
| 614-45-9 | 0,0025 | P(E) | P | P | Eq | s.o.s.o. | s.o.s.o. | s.o. |
| 632-51-9 | 1,5 | N(M) | PD | PD | PD | N(Ex) | N(Ex) | 3 |
| 793-24-8 | 1,5 | N(E) | N | N | N | P(I)P | P(I)P | 3 |
| 2379-79-5 | 0,0025 | P(M) | PD | PD | PD | P(Ex)P | P(Ex)P | s.o. |
| 2398-96-1 | 0,0025 | P(M) | PD | PD | PD | N(Ex)N | P(Ex)P | s.o. |
| 3006-86-8 | 1,5 | N(E/M) | N | N | PD | N(In)N | N(In)N | 3 |
| 3081-14-9 | 1,5 | N(E/M) | N | N | PD | N(In)N | N(In)N | 3 |
| 3327-22-8 | 0,0025 | P(M) | PD | PD | PD | P(Ex)P | P(Ex)P | s.o. |
| 3851-87-4 | 30 | N(E/M) | N | N | PD | N(Ex)N | N(Ex)N | 1 |
| 4979-32-2 | 0,0025 | P(E) | N | P | PD | s.o.s.o. | s.o.s.o. | s.o. |
| 5285-60-9 | 1,5 | N(M) | PD | PD | PD | N(In)N | N(In)N | 3 |
| 6858-49-7 | 0,0025 | P(M) | PD | PD | PD | N(Ex)N | P(Ex)P | s.o. |
| 8001-04-5a | 1,5 | N(M) | PD | PD | PD | N(In)N | N(Ex)N | 2 |
| 8016-81-7a | 1,5 | N(E/M) | N | N | PD | N(Ex)N | N(Ex)N | 3 |
| 13082-47-8 | 0,0025 | P(M) | N | PD | PD | P(Ex)P | P(Ex)P | s.o. |
| 13472-08-7 | 1,5 | N(M) | PD | PD | PD | N(Ex)N | N(Ex)N | 3 |
| 15791-78-3 | 0,0025 | P(E) | P | PD | PD | s.o.s.o. | s.o.s.o. | s.o. |
| 19720-45-7 | 1,5 | N(M) | PD | PD | PD | N(In)N | N(Ex)N | 3 |
| 21652-27-7 | 1,5 | N(E/M) | N | N | PD | N(In)N | N(In)N | 3 |
| 26266-77-3 | 30 | N(M) | PD | PD | PD | N(Ex)N | N(Ex)N | 1 |
| 26544-38-7 | 1,5 | N(E/M) | N | PD | PD | N(Ex)N | N(Ex)N | 3 |
| 27193-86-8 | 0,0025 | P(M) | PD | PD | PD | N(In)N | P(Ex)P | s.o. |
| 28173-59-3 | 0,0025 | P(M) | PD | PD | PD | P(Ex)P | P(Ex)P | s.o. |
| 28777-98-2 | 1,5 | N(M) | PD | PD | PD | N(Ex) | N(Ex) | 3 |
| 28984-69-2 | 1,5 | N(M) | PD | PD | PD | N(Ex) | N(Ex) | 3 |
| 29036-02-0 | 0,0025 | P(M) | PD | PD | PD | N(Ex)N | P(Ex)P | s.o. |
| 29350-73-0 | 30 | N(E/M) | N | PD | PD | N(In)N | N(Ex)N | 1 |
| 32072-96-1 | 1,5 | N(M) | PD | PD | PD | N(Ex) | N(Ex) | 3 |
| 36437-37-3 | 0,0025 | P(M) | PD | PD | PD | N(Ex) | P(Ex) | s.o. |
| 38640-62-9 | 0,0025 | P(E) | N | P | PD | s.o. | s.o. | s.o. |
| 53894-23-8 | 30 | N(M) | PD | PD | PD | N(In) | N(In) | 1 |
| 61788-72-5 | 1,5 | N(M) | PD | PD | PD | N(In) | N(Ex) | 3 |
| 61789-01-3a | 1,5 | N(E/M) | N | PD | PD | N(In)N | N(Ex)N | 3 |
| 61790-28-1a | 0,0025 | P(M) | N | PD | PD | N(In)N | P(Ex)P | s.o. |
| 61790-29-2a | 0,0025 | P(M) | PD | PD | PD | N(In)N | P(Ex)P | s.o. |
| 61790-59-8 | 30 | N(E/M) | N | PD | PD | N(In)N | N(In)N | 1 |
| 61790-60-1a | 0,0025 | P(M) | PD | PD | PD | N(In)N | P(I)P | s.o. |
| 61791-55-7a | 1,5 | N(E) | N | N | PD | N(In)N | P(I)P | 3 |
| 64754-95-6 | 1,5 | N(M) | PD | PD | PD | N(Ex)N | N(Ex)N | 3 |
| 64800-83-5 | 0,0025 | P(M) | PD | PD | PD | P(Ex)P | P(Ex)P | s.o. |
| 65277-42-1 | 0,0025 | P(M) | PD | PD | PD | P(Ex)P | P(Ex)P | s.o. |
| 68082-35-9a | 1,5 | N(M) | PD | PD | PD | N(In)N | N(Ex)N | 3 |
| 68139-89-9a | 1,5 | N(M) | PD | PD | PD | N(In)N | N(In)N | 3 |
| 68140-48-7 | 1,5 | N(E/M) | N | PD | PD | N(Ex)N | N(Ex)N | 3 |
| 68398-19-6 | 1,5 | N(E) | N | N | PD | P(Ex)P | P(Ex)P | 3 |
| 68411-32-5a | 1,5 | N(E/M) | N | PD | PD | N(Ex)N | N(Ex)N | 2 |
| 68442-69-3a | 1,5 | N(M) | PD | PD | PD | N(In)N | N(Ex)N | 2 |
| 68515-60-6a | 30 | N(M) | PD | PD | PD | N(In)N | N(In)N | 1 |
| 68603-15-6a | 30 | N(E/M) | N | PD | PD | N(In)N | N(In)N | 1 |
| 68783-25-5a | 0,0025 | P(M) | PD | PD | PD | N(In)N | P(I)P | s.o. |
| 68783-36-8 | 1,5 | N(E/M) | N | PD | PD | N(Ex)N | N(Ex)N | 3 |
| 68784-12-3a | 1,5 | N(E/M) | N | PD | PD | N(In)N | N(Ex)N | 3 |
| 68784-26-9 | 1,5 | N(M) | PD | PD | PD | N(Ex)N | N(Ex)N | 3 |
| 68909-18-2a | 1,5 | N(E/M) | N | N | PD | N(In)N | N(Ex)N | 3 |
| 68916-97-2a | 0,0025 | P(E) | P | P | EQ | s.o. | s.o. | s.o. |
| 68955-53-3a | 30 | N(E/M) | N | PD | N | N(In)N | N(In)N | 1 |
| 70288-86-7a | 1,5 | N(M) | PD | PD | PD | N(Ex)N | N(Ex)N | 3 |
| 70955-34-9a | 1,5 | N(M) | PD | PD | PD | N(In)N | N(In)N | 3 |
| 71486-79-8a | 1,5 | N(M) | PD | PD | PD | N(Ex) | N(Ex) | 3 |
| 73984-93-7 | 1,5 | N(M) | PD | PD | PD | N(Ex)N | N(Ex)N | 3 |
| 80584-90-3 | 1,5 | N(M) | PD | PD | PD | N(Ex)N | N(Ex)N | 3 |
| 94270-86-7 | 1,5 | N(M) | PD | PD | PD | N(Ex)N | N(Ex)N | 3 |
| 125328-64-5a | 0,0025 | P(M) | PD | PD | PD | N(In)N | P(Ex)P | s.o. |
| 174333-80-3a | 1,5 | N(E) | N | N | PD | N(Ex)N | P(Ex)P | 3 |
a Mélange – Les résultats présentés sont fondés sur le constituant auquel est assignée la valeur du SPT la plus prudente ou sont associés à un mélange pouvant être représenté par une seule structure.
Abréviations : No CAS (numéro de registre du Chemical Abstract Services); SPT(seuil de préoccupation toxicologique); GT(génotoxicité); GT SE1(série usuelle d'essais 1 pour la génotoxicité – essai de mutation chez les bactéries); GT SE2 (série usuelle d'essais 2 pour la génotoxicité – essai cytogénétique pour lésions chromosomiques [p. ex. essai in vitro d'aberration chromosomique sur cellules en métaphase ou test du micronoyau in vitro], ou essai in vitro de mutation génique de la thymidine kinase du lymphome de la souris); GT SE3 (série usuelle d'essais 3 pour la génotoxicité – essai in vivo de génotoxicité [lésions chromosomiques avec cellules hématopoïétiques de rongeurs, soit pour des micronoyaux, soit pour des aberrations chromosomiques dans des cellules en métaphase]); TIMES GT Ames avec S9(LCM OASIS Tissue Metabolic Simulator [TIMES] [v2.27.17] – essai mutagène d'Ames avec prédiction modélisée de l'activation métabolique [S9] [v. 11.11]); TIMES GT CA avec S9 (LCM OASIS Tissue Metabolic Simulator [TIMES] [v. 2.27.17] – essai in vitro d'aberrations chromosomiques avec prédiction modélisée de l'activation métabolique [S9] [v. 11.11]); CC (classe de Cramer); P (positif); N (négatif); E (données empiriques); M(données modélisées); PD (pas de données); s.o. (sans objet); O (oui); Eq (équivoque); In (à l'intérieur du domaine d'applicabilité du modèle); Ex (à l'extérieur du domaine d'applicabilité du modèle
| No CAS | Structure représentative | PC | CT | Voisin Munro le plus proche d'après les chémotypes ToxPrint |
|---|---|---|---|---|
| 60-24-2 |  |
In | In |  |
| 78-67-1 |  |
In | In | 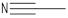 |
| 79-74-3 | 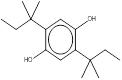 |
In | In | 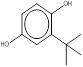 |
| 85-42-7 |  |
In | In |  |
| 92-70-6 |  |
In | In |  |
| 101-37-1 |  |
In | In |  |
| 103-24-2 |  |
In | In |  |
| 111-96-6 |  |
In | In |  |
| 120-11-6 |  |
In | In |  |
| 120-24-1 |  |
In | In |  |
| 120-54-7 |  |
In | Ex Chémotype non trouvé dans Munro : [(QQ(Q~0_S)_sulfure_di)] |
 |
| 121-91-5 |  |
In | In |  |
| 122-68-9 |  |
In | In |  |
| 288-88-0 |  |
In | In |  |
| 632-51-9 |  |
In | In |  |
| 793-24-8 |  |
In | In |  |
| 3006-86-8 |  |
In | Ex Chémotype non trouvé dans Munro : [OZ_oxyde_peroxy] |
 |
| 3081-14-9 |  |
In | In |  |
| 3851-87-4 |  |
In | Ex Chémotypes non trouvés dans Munro : [OZ_oxyde_peroxy]; [Branche alcane_isononyl_pentyl_1_1_1_3-méthyl] |
 |
| 5285-60-9 |  |
In | In |  |
| 8001-04-5a |  |
In | In |  |
| 8016-81-7a |  |
In | In |  |
| 8016-81-7a |  |
In | In | |
| 13472-08-7 |  |
In | In |  |
| 19720-45-7 |  |
In | In |  |
| 21652-27-7 |  |
In | In |  |
| 26266-77-3 |  |
In | In |  |
| 26544-38-7 |  |
In | In |  |
| 28777-98-2 |  |
In | In |  |
| 28984-69-2 |  |
In | In |  |
| 29350-73-0 |  |
In | In |  |
| 53894-23-8 |  |
In | Ex Chémotype non trouvé dans Munro : [alkaneBranch_isooctyl_hexyl_2-methyl] |
 |
| 61788-72-5 |  |
In | In |  |
| 61789-01-3a |  |
In | In |  |
| 61790-59-8a |  |
In | In |  |
| 61791-55-7a |  |
Ex | In |  |
| 61791-55-7a |  |
In | In |  |
| 64754-95-6 |  |
In | In |  |
| 68082-35-9a |  |
In | In |  |
| 68139-89-9a |  |
In | In |  |
| 68140-48-7a |  |
In | Ex Chémotypes non trouvés dans Munro : [fusion_[5_6]_indane] |
 |
| 68398-19-6 |  |
In | In |  |
| 68411-32-5a |  |
In | In |  |
| 68442-69-3a |  |
In | En Chémotypes non trouvés dans Munro : [chaîne : alcane aromatique_Ph-C10] |
 |
| 68515-60-6a |  |
In | In |  |
| 68603-15-6a |  |
In | In |  |
| 68783-36-8 |  |
In | In |  |
| 68784-12-3a |  |
In | In |  |
| 68784-26-9 |  |
In | Ex Chémotypes non trouvés dans Munro : [aromaticAlkane_Ph-C12] |
 |
| 68909-18-2a |  |
In | In |  |
| 68955-53-3a |  |
In | In |  |
| 70288-86-7a |  |
In | In |  |
| 70288-86-7a |  |
In | In |  |
| 70955-34-9a |  |
In | In |  |
| 71486-79-8 |  |
In | In |  |
| 73984-93-7 |  |
In | In |  |
| 80584-90-3 |  |
In | Ex Chémotypes non trouvés dans Munro : [cycle : hétéro [5]_N_triazole_(1_2_3-)] |
 |
| 94270-86-7 |  |
In | Ex Chémotypes non trouvés dans Munro : [cycle : hétéro _[5]_N_triazole_(1_2_3-)] |
 |
| 174333-80-3a |  |
In | In | 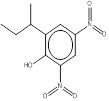 |
a Mélange – Tous les constituants représentés auxquels une classe de Cramer a été assignée, ou lorsque le mélange pouvait être représenté par une seule structure.
b Déterminé sur la base de la similarité de Tanimoto calculée à l'aide des empreintes ToxPrint (Yang et coll. 2015);
Abréviations : PGPC (Plan de gestion des produits chimiques); No CAS (numéro de registre du Chemical Abstract Service); PC (vérification des propriétés physico-chimiques de la substance chimique); CT (vérification du chémotype ToxPrint); NN (vérification de la similarité avec le plus proche voisin); In (la substance du PGPC se situe dans les plages respectives pour la comparaison de l'espace chimique d'une substance donnée, comme il est indiqué à la section 5); Ex (la substance du PGPC ne se situe pas dans les plages respectives pour la comparaison de l'espace chimique d'une substance donnée, comme il est indiqué à la section 5);
| Non CAS | Valeur du SPT (µg/kg p.c./j) | Type Mackay 1? | Volume total dans le commerce (kg/an)a | Estimation totale la plus élevée de l'absorption à partir de l'environnement (µg/kg p,c,/j)c |
|---|---|---|---|---|
| 50-48-6 | 0,0025 | Oui | 1 000-10 000d | 4,49E-4i |
| 60-24-2 | 30 | Oui | 10 000-100 000f | 1,04E-4l |
| 64-86-8 | 0,0025 | Non | 100-1 000e | 3,42E-4 |
| 77-47-4 | 0,0025 | Oui | inférieur(e) à 100g | 3,42E-5 |
| 78-67-1 | 1,5 | Oui | 10 000-100 000f | 5,32E-3i |
| 79-74-3 | 30 | Oui | inférieur(e) à 100f | 1,32E-6i |
| 85-42-7 | 1,5 | Oui | 10 000-100 000f | 6,86E-4i |
| 87-66-1 | 0,0025 | Oui | 1 000-10 000g | 6,92E-5i |
| 92-70-6 | 1,5 | Oui | 10 000-100 000f | 6,92E-4i |
| 101-37-1 | 1,5 | Oui | 10 000-100 000f | 3,86E-3i |
| 103-24-2 | 30 | Oui | 100 000-1,000 000f | 5,57E-3i |
| 111-55-7 | 0,0025 | Oui | 1 000-10 000f | 6,31E-5i |
| 111-96-6 | 30 | Oui | 1 000-10 000h | 6,92E-5i |
| 112-49-2 | 0,0025 | Oui | 10 000-100 000g | 6,92E-4i |
| 118-96-7 | 0,0025 | Oui | 100 000-1 000 000g | 8,09E-4j |
| 120-11-6 | 1,5 | Oui | inférieur(e) à 100f | 1,65E-6i |
| 120-24-1 | 30 | Oui | inférieur(e) à 100f | 8,12E-7i |
| 120-54-7 | 1,5 | Non | 100 000-1,000 000f | 3,42E-1 |
| 121-91-5 | 30 | Oui | 1 000 000-10 000 000f | 6,91E-2i |
| 122-68-9 | 30 | Oui | inférieur(e) à 100f | 1,57E-6i |
| 122-79-2 | 0,0025 | Oui | inférieur(e) à 100f | 8,98E-7j |
| 126-33-0 | 0,0025 | Oui | 10 000-100 000f | 6,91E-4i |
| 132-65-0 | 0,0025 | Oui | 130 000f | 8,76E-4i |
| 133-14-2 | 0,0025 | Oui | 100-1000f | 6,45E-6j |
| 288-88-0 | 1,5 | Oui | 1 000-10 000g | 1,18E-4j |
| 614-45-9 | 0,0025 | Oui | 1 000-10 000f | 8,68E-5j |
| 632-51-9 | 1,5 | Oui | inférieur(e) à 100f | 1,18E-6i |
| 793-24-8 | 1,5 | Oui | 1 000 000-10 000 000g | 1,65E-1i |
| 2379-79-5 | 0,0025 | Non | inférieur(e) à 100f | 3,42E-5 |
| 2398-96-1 | 0,0025 | Oui | 100-1000d | 1,33E-5i |
| 3006-86-8 | 1,5 | Oui | 100 000-1 000 000f | 1,95E-2i |
| 3081-14-9 | 1,5 | Oui | 1 000-10 000g | 1,20E-4i |
| 3327-22-8 | 0,0025 | Oui | 10 000-100 000f | 6,93E-4i |
| 3851-87-4 | 30 | Oui | 1 000-10 000f | 3,51E-5j |
| 4979-32-2 | 0,0025 | Oui | 100-1000f | 1,63E-5i |
| 5285-60-9 | 1,5 | Oui | 1 000-10 000f | 2,54E-4i |
| 6858-49-7 | 0,0025 | Non | inférieur(e) à 100f | 3,42E-5 |
| 8001-04-5 | 1,5 | Oui | inférieur(e) à 100f | 1,03E-6i |
| 8016-81-7 | 1,5 | Oui | 100 000-1 000 000f | 1,18E-2k |
| 13082-47-8 | 0,0025 | Non | inférieur(e) à 100f | 3,42E-5 |
| 13472-08-7 | 1,5 | Oui | 10 000-100 000f | 5,33E-3i |
| 15791-78-3 | 0,0025 | Non | 100-1000f | 3,42E-4 |
| 19720-45-7 | 1,5 | Oui | inférieur(e) à 100f | 2,08E-6i |
| 21652-27-7 | 1,5 | Non | 1 000-10 000f | 3,42E-3 |
| 26266-77-3 | 30 | Oui | inférieur(e) à 100f | 1,18E-6i |
| 26544-38-7 | 1,5 | Oui | 10 000-100 000g | 5,64E-4i |
| 27193-86-8 | 0,0025 | Oui | 1 000-10 000f | 5,68E-5i |
| 28173-59-3 | 0,0025 | Non | 100-1000f | 3,42E-4 |
| 28777-98-2 | 1,5 | Oui | 1 000 000-10 000 000g | 1,11E-1i |
| 28984-69-2 | 1,5 | Non | 100-1000f | 3,42E-4 |
| 29036-02-0 | 0,0025 | Oui | 10 000-100 000g | 1,12E-3i |
| 29350-73-0 | 30 | Oui | inférieur(e) à 100f | 9,17E-7i |
| 32072-96-1 | 1,5 | Oui | 100 000-1 000 000f | 1,11E-2i |
| 36437-37-3 | 0,0025 | Oui | 10 000-100 000g | 1,21E-3i |
| 38640-62-9 | 0,0025 | Oui | 10 000-100 000f | 9,99E-4i |
| 53894-23-8 | 30 | Non | 10 000-100 000g | 3,42E-2 |
| 61788-72-5 | 1,5 | Oui | inférieur(e) à 100f | 5,38E-6i |
| 61789-01-3 | 1,5 | Oui | 10 000-100 000f | 5,27E-4i |
| 61790-28-1b | 0,0025 | Oui | 100 000-1 000 000f | 3,38E-4i |
| 61790-29-2b | 0,0025 | Oui | 2,700 000f | 9,09E-4i |
| 61790-59-8 | 30 | Oui | 100 000-1 000 000f | 5,64E-3i |
| 61790-60-1 | 0,0025 | Oui | 10 000-100 000f | 5,63E-4i |
| 61791-55-7 | 1,5 | Oui | 100 000-1 000 000f | 5,68E-3i |
| 64754-95-6 | 1,5 | Non | 1 000-10 000f | 3,42E-3i |
| 64800-83-5 | 0,0025 | Oui | 1 000-10 000f | 1,02E-4i |
| 65277-42-1 | 0,0025 | Non | 1 000-10 000d | 1,78E-3 |
| 68082-35-9 | 1,5 | Oui | inférieur(e) à 100f | 6,11E-7i |
| 68139-89-9 | 1,5 | Oui | 10 000-100 000f | 5,66E-4i |
| 68140-48-7 | 1,5 | Oui | 1 000-10 000f | 2,30E-4i |
| 68398-19-6 | 1,5 | Oui | 1 000-10 000f | 1,05E-4i |
| 68411-32-5 | 1,5 | Oui | 100 000-1 000 000f | 1,67E-2i |
| 68442-69-3 | 1,5 | Oui | 1 000-10 000f | 5,60E-5i |
| 68515-60-6 | 30 | Oui | 1 000-10 000g | 1,05E-4i |
| 68603-15-6 | 30 | Oui | inférieur(e) à 100f | 3,42E-5i |
| 68783-25-5 | 0,0025 | Oui | 1 000-10 000f | 2,03E-4i |
| 68783-36-8 | 1,5 | Non | 10 000-100 000f | 3,42E-2 |
| 68784-12-3 | 1,5 | Oui | 1 000 000-10 000 000f | 1,11E-1i |
| 68784-26-9 | 1,5 | Non | 100 000-1 000 000f | 3,42E-1 |
| 68909-18-2 | 1,5 | Oui | 1 000 000-10 000 000f | 1,68E-1i |
| 68916-97-2 | 0,0025 | Oui | inférieur(e) à 100f | 1,08E-6i |
| 68955-53-3 | 30 | Oui | 1 000-10 000f | 1,11E-4i |
| 70288-86-7 | 1,5 | Non | 100-1000f | 3,42E-4 |
| 70955-34-9 | 1,5 | Non | 10 000-100 000f | 3,42E-2 |
| 71486-79-8 | 1,5 | Non | 10 000-100 000f | 3,42E-2 |
| 73984-93-7 | 1,5 | Non | inférieur(e) à 100f | 3,42E-5 |
| 80584-90-3 | 1,5 | Oui | 1 000-10 000f | 1,12E-4i |
| 94270-86-7 | 1,5 | Oui | 1 000-10 000f | 1,12E-4i |
| 125328-64-5 | 0,0025 | Oui | 180 000f | 1,99E-3k |
| 174333-80-3 | 1,5 | Oui | 10 000-100 000f | 1,34E-3i |
a Par prudence, un facteur d'émissions de 100 % (scénario de la pire éventualité) a été utilisé pour toutes les substances et les structures représentatives. Dans le cas des substances pour lesquelles une plage de volumes est présentée dans le tableau, les estimations du taux d'absorption par les humains ont été calculées en fonction de la limite supérieure de la plage.
b Un taux d'élimination modélisé total de 94,01 % pour le SPT a été utilisé pour les nos CAS 61790-28-1 et 61790-29-2, et un taux de 47,97 % a été utilisé pour le no CAS 65277-42-1 (EPI Suite™ 2012). Pour toutes les autres substances et structures représentatives, un taux d'élimination total de 0 % pour le SPT a été utilisé.
c Toutes les propriétés physico-chimiques et les demi-vies de dégradation ont été obtenues à l'aide du programme EPI Suite™ (2012), la préférence ayant été accordée aux valeurs empiriques lorsqu'elles étaient disponibles.
d Le volume total dans le commerce était la somme des volumes dans les bases de données de la Phase 2 de la Mise à jour de l'inventaire de la LIS et IMS MIDAS (Canada 2014; IMS 2013).
e Le volume total dans le commerce était la somme des volumes dans les bases de données de la Phase 1 de la Mise à jour de l'inventaire de la LIS et IMS MIDAS (Environnement Canada 2012, IMS 2013).
f Le volume total dans le commerce provenait de la Phase 2 de la Mise à jour de l'inventaire de la LIS (Canada 2014).
g Le volume total dans le commerce provenait de la Phase 1 de la Mise à jour de l'inventaire de la LIS (Environnement Canada 2012).
h Le volume total dans le commerce provenait d'une enquête sur des substances persistantes, bioaccumulables et intrinsèquement toxiques (PBiT), sur les polymères qui représentent le plus grand potentiel d'exposition pour les humains et sur les substances jugées dangereuses pour la santé humaine (Canada, 2006).
i Le mode de pénétration dans le scénario de la pire éventualité était par l'eau, et le groupe d'âge le plus exposé était celui des nourrissons alimentés avec des préparations (0 à 0,5 an).
j Le mode de pénétration dans le scénario de la pire éventualité était par l'air, et le groupe d'âge le plus exposé était celui des tout-petits (0,5 à 4 ans).
k Le mode de pénétration dans le scénario de la pire éventualité était par le sol, et le groupe d'âge le plus exposé était celui des tout-petits (0,5 à 4 ans).
l Le mode de pénétration dans le scénario de la pire éventualité était par le sol, et le groupe d'âge le plus exposé était celui des nourrissons alimentés avec des préparations (0 à 0,5 an).
| No CAS | Nom | SPT (µg/kg p.c./j) | Scénario(s) d'exposition directe | Estimation de l'exposition (µg/kg p.c./j)a,b |
|---|---|---|---|---|
| 60-24-2 | éthanol, 2-mercapto | 30 | Emballage alimentaire (usage répertorié pour la fabrication de différents types de matériaux d'emballages alimentaires au Canada) | 0,74 µg/kg p.c./j |
| 78-67-1 | propanenitrile, 2,2'-azobis[2-méthyl- | 1,5 | Emballage alimentaire (usage répertorié pour la fabrication de différents types de matériaux d'emballages alimentaires au Canada) | 0,0006 µg/kg p.c./j |
| 120-11-6 | benzène, 2-méthoxy-1-(phénylméthoxy)-4-(1-propényl)- | 1,5 | Agent aromatisant À noter que cette substance figure dans la Base de données sur les ingrédients de produits de santé naturels (BDIPSN) avec un rôle non médicinal pour un usage potentiel comme exhausteur de goût dans les produits de santé naturels; cependant, elle ne figure pas comme produit de santé naturel homologué dans la Base de données des produits de santé naturels homologués (BDPSNH) | 0,014 µg/kg p.c./j [d'après une valeur d'absorption aux États-Unis de 1 µg/j (d'après JECFA, 2003)] |
| 120-24-1 | acide benzèneacétique, ester méthoxy-4-(1-propényl)phénylique | 30 | Agent aromatisant À noter que cette substance figure dans la BDIPSN avec un rôle non médicinal pour un usage potentiel comme exhausteur de goût dans les produits de santé naturels; cependant, elle ne figure pas comme produit de santé naturel homologué dans la BDPSNH | 0,0042 µg/kg p.c./j [d'après une valeur d'absorption aux États-Unis de 0,3 µg/j (d'après JECFA, 2003)] |
| 121-91-5 | acide 1,3-benzènedicarboxylique | 30 | Emballage alimentaire (usage répertorié pour la fabrication de différents types de matériaux d'emballages alimentaires au Canada, y compris pour certains revêtements utilisés avec les préparations pour nourrissons) | 0,050 µg/kg p.c./j (adultes) 8,61 µg/kg p.c./j (nourrissons) |
| 122-68-9 | acide 2-propénoïque, 3-phényl, ester 3-phénylpropylique | 30 |
|
[d'après une valeur d'absorption aux États-Unis de 37 µg/j (d'après JECFA, 2000)] |
| 122-79-2 | acide acétique, ester phénylique | 0,0025 | Agent aromatisant À noter que cette substance figure dans la BDIPSN avec un rôle non médicinal pour un usage potentiel comme exhausteur de goût dans les produits de santé naturels; cependant, elle ne figure pas comme produit de santé naturel homologué dans la BDPSNH | 0,00014 µg/kg p.c./j [d'après une valeur d'absorption aux États-Unis de 0,01 µg/j (d'après JECFA, 2000)] |
| 288-88-0 | 1H-1,2,4-triazole | 1,5 | Produit de consommation, lubrifiant (concentration de 0,1 %) | 1,2 µg/kg p.c./j (d'après 1 184 µg/kg p.c./j * 0,001 * FC où 1 184 µg/kg p.c./j représente l'exposition cutanée au lubrifiant, concentration de 0,1 % de substance dans le produit, aucun facteur cutané appliqué) |
| 614-45-9 | acide benzènecarboperoxoïque, ester 1,1-diméthyléthylique | 0,0025 | Produit de consommation, adhésif en tube | Exposition « par événement » = 28 µg/kg p.c./j (par rapport au SPT de classe I assigné à cette substance de 30 µg/kg p.c./j) (d'après 1 128 µg/kg p.c./j * 0,05 * FC où 1 184 µg/kg p.c./j représente l'exposition cutanée à l'adhésif en tube, concentration de 5 % de substance dans le produit et un facteur cutané de 50 %) Exposition amortie = 0,005 µg/kg p.c./j [d'après (exposition par événement * 12 jours/année) ÷ (365 jours/année * 80 années)] |
| 3006-86-8 | peroxide, cyclohexylidènebis[(1,1-diméthyléthyle) | 1,5 | Emballage alimentaire(usage répertorié pour la fabrication de différents types de matériaux d'emballages alimentaires au Canada) | 0,0014 µg/kg p.c./j |
| 3327-22-8 | 1-propanaminium, 3-chloro-2-hydroxy-N,N,N-triméthyl, chlorure | 0,0025 | Emballage alimentaire (usage répertorié pour la fabrication de différents types de matériaux d'emballages alimentaires au Canada) | 0,0020 µg/kg p.c./j |
| 8001-04-5 | muscs (musc Tonkin) | 1,5 | Agent aromatisant | 0,00423 µg/kg p.c./j [d'après la valeur de consommation individuelle du musc du Tonkin (tiré de : Burdock, 2009 (Fenaroli's Handbook of Flavor Ingredients, Sixth Edition)] |
| 13472-08-7 | butanenitrile, 2,2'-azobis[2-méthyl- | 1,5 | Emballage alimentaire (usage répertorié pour la fabrication de différents types de matériaux d'emballages alimentaires au Canada) | 0,51 µg/kg p.c./j |
| 28777-98-2 | 2,5-furanedione, dihydro-3-(octadécényl)- | 1,5 | Emballage alimentaire (usage répertorié pour la fabrication de différents types de matériaux d'emballages alimentaires au Canada) | 0,15 µg/kg p.c./j |
| 28984-69-2 | 4,4(5H)-oxazolediméthanol, 2-(heptadécényl)- | 1,5 | Produit de consommation, antigel/ déglaçant (huile à moteur de rebut, scénario d'utilisation comme additif pour l'essence) | 1,1 µg/kg p.c./j (d'après 1214 µg/kg p.c./j * 0,00091 * FC où 1 184 µg/kg p.c./j représente l'exposition cutanée à l'additif pour l'essence [utilisée pour représenter les produits antigels], concentration de 0,091 % de la substance dans le produit, aucun facteur cutané appliqué) |
| 29350-73-0 | naphthalène, décahydro-1,6-diméthyl-4-(1-méthyléthyl)-, [1S-(1α,4α,4aα,6α,8aβ)]-, dérivé didéhydro | 30 | Agent aromatisant | 0,00071 µg/kg p.c./j [d'après une valeur d'absorption aux États-Unis de 0,05 µg/j (d'après JECFA, 2006)] |
| 32072-96-1 | 2,5-furanedione, 3-(hexadécényl)dihydro- | 1,5 | Emballage alimentaire (usage répertorié pour la fabrication de différents types de matériaux d'emballages alimentaires au Canada) | 0,55 µg/kg p.c./j |
| 68784-12-3 | 2,5-furanedione, dihydro-, dérivés mono-C15-20-alcényles | 1,5 | Emballage alimentaire usage répertorié pour la fabrication de différents types de matériaux d'emballages alimentaires au Canada) | 0,59 µg/kg p.c./j |
| 68784-26-9 | phénol, dodécyl-, sulfurisé, carbonates, sels de calcium, superbasiques | 1,5 | Produit de consommation, lubrifiant | 1,2 µg/kg p.c./j (D'après 1 184 µg/kg p.c./j * 0,01 * FC où 1 184 µg/kg p.c./j représente l'exposition cutanée au lubrifiant, concentration de 1 % de la substance dans produit, FC [facteur cutané] = 10 %) |
| 80584-90-3 | 1H-benzotriazole-1-méthanamine, N,N-bis(2-éthylhexyl)-4-méthyl- | 1,5 | Produit de consommation, lubrifiant | 0,9 µg/kg p.c./j (D'après 1 184 µg/kg p.c./j * 0,003 * FC où 1 184 µg/kg p.c./j représente l'exposition cutanée au lubrifiant, concentration de 0,3 % de la substance dans le produit, FC [facteur cutané] = 25 %) |
| 94270-86-7 | 1H-benzotriazole-1-méthanamine, N,N-bis(2-éthylhexyl)-ar-méthyl- | 1,5 | Produit de consommation, lubrifiant | 0,9 µg/kg p.c./j (D'après 1 184 µg/kg p.c./j * 0,003 * FC où 1 184 µg/kg p.c./j représente l'exposition cutanée au lubrifiant, concentration de 0,3 % de la substance dans le produit, FC [facteur cutané] = 25 %) |
a Des facteurs cutanés (FC) ont été appliqués lorsqu'il y avait lieu d'améliorer les estimations de l'exposition cutanée; ces facteurs cutanés ont été déterminés de la manière suivante :
- 10 % : substance ayant une masse moléculaire (MM) supérieur(e) à 500 g/mol et log Koe inférieur(e) à -1 ou supérieur(e) à 4;
- 25 % : durée d'exposition inférieur(e) à 1 heure (p. ex. utilisation de lubrifiant) et substance avec MM supérieur(e) à 300 g/mol ou log Koe (inférieur(e) à -1 ou supérieur(e) à 4);
- 50 % : durée d'exposition inférieur(e) à 1 heure (lorsque la substance n'a pas les caractéristiques physico-chimiques mentionnées ci-dessus);
- 75 % : la substance est un ingrédient dans un produit cosmétique (sauf dans les colorants capillaires).
b Exposition d'un adulte d'un poids corporel de 70,9 kg.