Ébauche d’évaluation préalable - Acide 4-méthylbenzènesulfonique ou acide toluène-4-sulfonique
Titre officiel : Ébauche d’évaluation préalable - Acide 4-méthylbenzènesulfonique ou acide toluène-4-sulfonique
Numéro de registre du Chemical Abstracts Service : 104-15-4
Environnement et Changement climatique Canada
Santé Canada
Octobre 2020
Sommaire
En vertu de l’article 74 de la Loi canadienne sur la protection de l’environnement (1999) [LCPE], les ministres de l’Environnement et de la Santé ont mené une évaluation préalable de l’acide toluène-4-sulfonique, ci-après appelé acide 4-méthylbenzènesulfonique. Le numéro de registre du Chemical Abstracts Service (no CASNote de bas de page 1) de l’acide 4-méthylbenzènesulfonique est 104-15-4. L’évaluation de cette substance a été désignée comme prioritaire, car elle satisfait aux critères de catégorisation énoncés au paragraphe 73(1) de la LCPE.
L’acide 4-méthylbenzènesulfonique n’est pas naturellement présent dans l’environnement. Selon l’information présentée en réponse à une enquête prévue à l’article 71 de la LCPE, 141 600 kg d’acide 4-méthylbenzènesulfonique ont été importés au Canada en 2011 et aucune quantité fabriquée n’a été déclarée.
Le risque pour l’environnement associé à l’acide 4-méthylbenzènesulfonique a été caractérisé à l’aide de l’Approche de classification des risques écologiques (CRE) des substances organiques, une approche fondée sur le risque qui tient compte des multiples paramètres liés au danger et à l’exposition et de la pondération de nombreuses données probantes pour catégoriser le risque. Les profils de danger sont principalement fondés sur les paramètres liés au mode d’action toxique, à la réactivité chimique, à des seuils de toxicité interne dérivés du réseau trophique, à la biodisponibilité et à l’activité chimique et biologique. Parmi les paramètres pris en compte pour les profils d’exposition, on retrouve les taux d’émission potentiels, la persistance globale et le potentiel de transport à grande distance. La méthode fait appel à une matrice du risque pour attribuer à ces substances un degré de préoccupation potentielle faible, modéré ou élevé, en fonction de leurs profils de danger et d’exposition. D’après les résultats de l’analyse de la CRE, il serait peu probable que la substance cause des effets nocifs pour l’environnement.
Compte tenu de tous les éléments de preuve contenus dans la présente ébauche d’évaluation préalable, l’acide 4-méthylbenzènesulfonique présente un risque faible de causer des effets nocifs pour l’environnement. Il est proposé de conclure que l’acide 4‑méthylbenzènesulfonique ne satisfait pas aux critères énoncés aux alinéas 64a) et b) de la LCPE, car il ne pénètre pas dans l’environnement en une quantité ou concentration ou dans des conditions de nature à avoir, immédiatement ou à long terme, un effet nocif sur l’environnement ou sur la diversité biologique, ou à mettre en danger l’environnement essentiel pour la vie.
Au Canada, l’acide 4-méthylbenzènesulfonique est principalement utilisé dans la fabrication de peintures, d’enduits ainsi que de matériaux en plastique et en caoutchouc. L’exposition de la population générale à l’acide 4-méthylbenzènesulfonique découle essentiellement de l’utilisation de cosmétiques (lotions pour le visage, colorants capillaires permanents et revitalisants), d’adhésifs pour la réparation de fissures et de vernis de couchage hors machine en pulvérisateur (enduit activé par un catalyseur pour l’ameublement d’intérieur en bois).
Bien que l’acide 4-méthylbenzènesulfonique n’ait pas été évalué à l’étranger, ses hydrotropes, dont les sels de l’acide 4-méthylbenzènesulfonique, l’ont été dans le cadre du Programme d’évaluation coopérative des produits chimiques de l’Organisation de coopération et de développement économiques (OCDE). Les évaluations de l'OCDE ont contribué à la caractérisation des effets sur la santé associés à l’acide 4-méthylbenzènesulfonique dans la présente évaluation préalable. D’après les renseignements relatifs aux effets sur la santé associés à l’acide 4-méthylbenzènesulfonique et aux analogues, et qui proviennent d’études en laboratoire, la substance ne présente ni effet génotoxique ou cancérogène, ni effet sur la reproduction ou le développement, et aucun effet nocif généralisé n’a été observé dans les études à doses répétées réalisées avec l’acide 4-méthylbenzènesulfonique ou ses analogues jusqu’à la dose limite de 1000 mg/kg p.c./jour. Étant donné le potentiel de danger faible que présente l’acide 4-méthylbenzènesulfonique, l’exposition de la population générale n’a pas été estimée, le risque pour la santé humaine étant considéré comme faible.
À la lumière des renseignements contenus dans la présente ébauche d’évaluation préalable, il est proposé de conclure que l’acide 4‑méthylbenzènesulfonique ne satisfait pas au critère énoncé à l’alinéa 64c) de la LCPE, car il ne pénètre pas dans l’environnement en une quantité ou concentration ou dans des conditions de nature à constituer un danger au Canada pour la vie ou la santé humaines.
Il est proposé de conclure que l’acide 4‑méthylbenzènesulfonique ne satisfait à aucun des critères énoncés à l’article 64 de la LCPE.
1. Introduction
En vertu de l’article 74 de la Loi canadienne sur la protection de l’environnement (1999) [LCPE] (Canada, 1999), les ministres de l’Environnement et de la Santé ont mené une évaluation préalable de l’acide toluène-4-sulfonique, ci-après appelé acide 4‑méthylbenzènesulfonique (AMBS) pour déterminer si cette substance présente ou peut présenter un risque pour l’environnement ou la santé humaine. L’évaluation de cette substance a été désignée comme prioritaire, car elle satisfait aux critères de catégorisation énoncés au paragraphe 73(1) de la LCPE(ECCC, SC [modifié en 2017]).
Le risque pour l’environnement associé à l’acide 4-méthylbenzènesulfonique a été caractérisé à l’aide de l’Approche de classification des risques écologiques (CRE) des substances organiques (ECCC 2016a). La CRE décrit les dangers associés à une substance à l’aide de paramètres liés au mode d’action toxique, à la réactivité chimique, à des seuils de toxicité interne dérivés du réseau trophique, à la biodisponibilité et à l’activité chimique et biologique et prend en compte l’exposition possible des organismes dans les milieux aquatiques et terrestres en se fondant sur des facteurs tels que les taux d’émission potentiels, la persistance globale et le potentiel de transport à grande distance dans l’atmosphère. Nous combinons les diverses données probantes pour déterminer quelles substances nécessitent une évaluation approfondie de leur potentiel à causer des effets nocifs pour l’environnement ou présentent une probabilité faible de causer de tels effets.
L’AMBS n’a pas été examinée à l’étranger. Cependant, les sels des acides sulfoniques aromatiques ou hydrotropes (comprenant les sels de l’acide 4‑méthylbenzènesulfonique) ont été examiné dans le cadre du Programme d’évaluation coopérative des produits chimiques de l’Organisation de coopération et de développement économiques (OCDE) et l’ensemble de données d’évaluation (SIDS) et les rapports d’évaluation initiale du SIDS (SIAR) sont accessibles : l’un pour plusieurs hydrotropes (OCDE, 2006) et un autre avec des données additionnelles pour le 4‑méthylbenzènesufonate de sodium, le sel de sodium de l’acide 4‑méthylbenzènesulfonique (OCDE, 2009). Ces évaluations sont soumises à un examen rigoureux (y compris à un examen par les pairs) et à des processus d’approbation par des autorités gouvernementales d’autres pays. Santé Canada and Environnement et Changement climatique Canada are active participants in this process and consider these assessments to be reliable. Ces évaluations de l’OCDE ont été utilisées pour éclairer la caractérisation des effets sur la santé associés à l’acide 4‑méthylbenzènesulfonique dans la présente évaluation préalable.
La présente évaluation préalable comprend l’examen des renseignements sur les propriétés chimiques, le devenir environnemental, les dangers, les utilisations et les expositions, y compris d’autres renseignements présentés par les intervenants. Les données pertinentes sur l’acide 4-méthylbenzènesulfonique ont été recensées jusqu’en mai 2019. Nous avons consulté les données empiriques des principales études ainsi que les résultats de modèles pour formuler les conclusions proposées.
La présente évaluation préalable a été préparée par le personnel du Programme d’évaluation des risques de la LCPE à Santé Canada et à Environnement et Changement climatique Canada et et elle comprend la contribution d’autres programmes de ces deux ministères. La partie de l’évaluation portant sur l’environnement repose sur le document de CRE (publié le 30 juillet 2016), lequel a fait l’objet d’un examen externe et d’une consultation publique de 60 jours.
La présente ébauche d’évaluation préalable repose sur les données essentielles pour déterminer si les substances satisfont aux critères énoncés à l’article 64 de la LCPE. À cette fin, des données scientifiques ont été examinées, et une approche de pondération des données probantes et le principe de prudence ont été adoptésNote de bas de page2. La présente évaluation préalable contient les renseignements et les considérations essentiels sur lesquels reposent les conclusions proposées.
2. Identité de la substance
Le numéro de registre du Chemical Abstracts Service (no CASNote de bas de page3), le nom sur la Liste intérieure des substances (LIS) et la structure moléculaire de l’acide 4‑méthylbenzènesulfonique sont présentés au tableau 2‑1.
| No CAS |
Nom sur la LIS (nom commun; abréviation) |
Structure et formule moléculaires | Poids moléculaire (g/mol) |
|---|---|---|---|
| 104-15-4 |
Acide toluène- 4‑sulfonique (acide 4‑méthylbenzène-sulfonique; AMBS) |
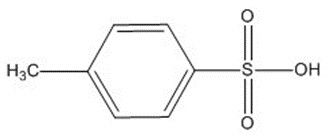 C7H8O3S
C7H8O3S
|
172,2 |
2.1 Sélection des analogues et utilisation des modèles (Q)SAR
Une approche par extrapolation faisant appel aux données d’analogues et aux résultats de modèles de relation (quantitative) structure-activité ([Q]SAR), s’il y a lieu, a été utilisée pour éclairer l’évaluation des effets sur la santé humaine où aucune donnée sur l’acide 4 méthylbenzènesulfonique n’a été trouvée. Des analogues dont la structure était semblable à celle de l’acide 4 méthylbenzènesulfonique (propriétés physicochimiques et toxicocinétique similaires) ont été choisis pour leurs données empiriques pertinentes pouvant être utilisées pour éclairer l’évaluation des effets de l’acide 4 méthylbenzènesulfonique sur la santé. L’applicabilité des modèles (Q)SAR a été déterminée au cas par cas. Les détails sur les données d’extrapolation employées pour l’évaluation des effets de l’acide 4-méthylbenzènesulfonique sur la santé humaine sont traités dans les sections pertinentes du présent rapport. Les données sur l’identité et la structure chimique des analogues qui ont servi à éclairer l’évaluation des effets de la substance sur la santé humaine sont présentées au tableau 2-2. Pour connaître les propriétés physicochimiques et toxicologiques de ces analogues, veuillez consulter l’annexe A.
| No CAS | Nom sur la LIS (nom commun) | Structure représentativea et formule moléculaire | Poids moléculaire (g/mol) |
|---|---|---|---|
| 657-84-1 |
Toluène-4-sulfonate de sodium (4-méthylbenzène-sulfonate de sodium) |
![[Na]OS(=O)(=O)c1ccc(cc1)C](/content/dam/eccc/images/pded/ptsa/20200923-Table2-2-1.jpg)
|
194,2 |
| 1300-72-7 |
Xylènesulfonate de sodium (3,4‑diméthyl-sulfonate de sodium) |
![[Na]OS(=O)(=O)c1ccc(cc1C)C](/content/dam/eccc/images/pded/ptsa/20200923-Table2-2-2.jpg)
|
208,2 |
| 28088-63-3 |
Ne s’applique pas (bis(2,3-diméthylbenzène-sulfonate) de calcium) |
![[Ca]OS(=O)(=O)c1ccc(cc1C)C](/content/dam/eccc/images/pded/ptsa/20200923-Table2-2-3.jpg)
|
410,5 |
| 28348-53-0 |
Cumènesulfonate de sodium ((4-(propane-2‑yl) benzènesulfonate de sodium) |
![[Na]OS(=O)(=O)c1ccc(cc1)C(C)C](/content/dam/eccc/images/pded/ptsa/20200923-Table2-2-4.jpg)
|
222,2 |
a Les formes commerciales des sulfonates aromatiques sont un mélange des isoformes ortho-, méta,- et/ou para- (OCDE, 2006), sauf lorsque l’isoforme est précisé dans le nom. Les structures représentatives présentées ici pour les molécules des nos CAS 1300-72-7, 28088-63-3 et 28348-53-0 sont celles des isoformes suivants : 1300-72-7, para, méta; 28088-63-3, ortho, méta; 28348-53-0, para.
La boîte à outil QSAR (version 4.2, 2018) de l’OCDE a permis de trouver l’hydrotrope 4‑méthylbenzènesufonate de sodium comme analogue possible de l’acide 4‑méthylbenzènesulfonique, avec trois acides sulfoniques aromatiques et un autre hydrotrope. De ceux-là, le 4-méthylbenzènesufonate de sodium a été retenu comme analogue pour ses données toxicologiques pertinentes (OCDE, 2009). Trois autres hydrotropes ont également été sélectionnés comme analogues pour l’acide 4‑méthylbenzènesulfonique, d’après ses similitudes structurales et fonctionnelles avec l’acide 4-méthylbenzènesulfonique et le 4-méthylbenzènesufonate de sodium, et pour ses données toxicologiques pertinentes (OCDE, 2006). Des hydrotropes ont également été trouvés comme analogues pour les acides sulfoniques aromatiques, dont l’acide 4‑méthylbenzènesulfonique dans un dossier d’homologation de l’Agence européenne des produits chimiques (ECHA, c2007-2019). Étant donné que le 4‑méthylbenzènesufonate de sodium est le sel de sodium de l’acide 4‑méthylbenzènesulfonique, il est considéré comme le meilleur analogue de cet examen.
À la différence des analogues (OCDE, 2006, 2009), l’acide 4‑méthylbenzènesulfonique est corrosif pour la peau à une concentration de 20 % et plus, et irritant pour la peau à une concentration inférieure (ECHA, c2007-2019). Il est donc possible que les données sur les effets sur la santé humaine sous-estiment les effets au point de contact après une exposition cutanée à l’acide 4-méthylbenzènesulfonique ou une inhalation des particules en aérosol contenant de l’acide 4‑méthylbenzènesulfonique. Cependant, puisque l’acide 4-méthylbenzènesulfonique est un acide fort qui devrait se dissocier complètement dans l’eau (HSDB, 1983-) et que les hydrotropes se dissocient également dans l’eau, nous nous attendons à ce que la toxicité généralisée de ces substances soit similaire par la voie orale.
3. Propriétés physiques et chimiques
Un résumé des propriétés physiques et chimiques de l’acide 4‑méthylbenzènesulfonique est présenté au tableau 3‑1. D’autres propriétés physicochimiques sont rapportées dans ECCC (2016b) et des données sur les propriétés des analogues le sont à l’annexe A.
| Propriétés | Valeura | Principales références |
|---|---|---|
| Poids moléculaire (g/mol) | 172,2 | (ChemID Plus, 1993-) |
| Pression de vapeur (mm Hg) | 2,7E-06b | (ChemID Plus, 1993-) |
| Solubilité dans l’eau (mg/L) | 6,2E+05 | (ChemID Plus, 1993-) |
| log Koe | -0,62b | (ChemID Plus, 1993-) |
| pKa | -1,34 | (HSDB, 1983-) |
Abréviations : Koe = coefficient de partage octanol-eau; pKa = constante de dissociation acide.
a Toutes les valeurs sont des valeurs mesurées sauf si indiqué autrement.
b Valeur obtenue par modélisation.
4. Sources et utilisations
L’acide 4‑méthylbenzènesulfonique n’est pas réputé être présent naturellement dans l’environnement. Cette substance a été visée par une enquête prévue à l’article 71 de la LCPE (Canada, 2012). Selon les données présentées en réponse à cette enquête, la quantité totale importée déclarée au Canada en 2011 était de 141 600 kg. Aucune quantité fabriquée au-dessus du seuil de 100 kg n’a été déclarée (Environnement Canada, 2013). Au Canada, l’acide 4-méthylbenzènesulfonique est principalement utilisé comme régulateur de procédé et additif dans la fabrication des peintures et des enduits, et comme agent technologique, régulateur de procédés, agent oxydant et réducteur, et intermédiaire dans la fabrication de matériaux en plastique et en caoutchouc (Environnement Canada, 2013). Même si l’utilisation de l’acide 4‑méthylbenzènesulfonique dans les tissus, les textiles et les articles en cuir avait initialement été déclarée dans l’enquête, elle n’est plus applicable d’après le suivi effectué auprès des industries (communication personnelle des industries adressée au Bureau de l’évaluation des risques pour les substances existantes [BERSE] de Santé Canada [SC], en juillet 2019; sans référence).
Un résumé d’autres utilisations de l’acide 4‑méthylbenzènesulfonique au Canada est présenté au tableau 4-1.
| Utilisation | Acide 4‑méthylbenzènesulfonique |
|---|---|
| Matériaux d’emballage des alimentsa | Oui |
| Présent dans des cosmétiques, d’après des déclarations présentées conformément au Règlement sur les cosmétiquesb, c | Oui |
| Formulant dans des produits antiparasitaires | Oui |
Abréviation : Oui = une utilisation de cette substance a été déclarée.
a Communication personnelle de la Direction des aliments de SC adressée au BERSE de SC, en février 2019; sans référence.
b Communication personnelle de la Direction de la sécurité des produits de consommation et des produits dangereux (DSPCPD) de SC adressée au BERSE de SC, en février 2019; sans référence.
c L’acide 4-méthylbenzènesulfonique est présent dans des cosmétiques tels que des lotions pour le visage, des colorants capillaires permanents et des revitalisants (Communication personnelle de la Direction de la sécurité des produits de consommation et des produits dangereux de SC adressée au BERSE de SC, en février 2019; sans référence).
d Communication personnelle de l’Agence de réglementation de la lutte antiparasitaire (ARLA) de SC adressée au BERSE de SC, en février 2019; sans référence.
Selon les données publiques,les fiches de données de sécurité (SDS) et les fiches techniques (TDS) sur les produits, l’acide 4-méthylbenzènesulfonique a été trouvé dans un adhésif pour la réparation des fissures (SDS, 2017) ainsi que dans des vernis de couchage hors machine (enduit activé par un catalyseur pour l’ameublement d’intérieur en bois) (TDS, 2010).
5. Potentiel à causer des effets nocifs pour l’environnement
Les risques pour l’environnement associés à l’acide 4‑méthylbenzènesulfonique a été caractérisé à l’aide de l’Approche de classification des risques écologiques (CRE) des substances organiques (ECCC, 2016a). La CRE est une approche axée sur la notion de risque; elle attribue un score de risque en tenant compte de nombreuses mesures du danger et de l’exposition, pondérées par différentes données probantes. Nous avons combiné les diverses données probantes pour distinguer les substances peu puissantes des moins puissantes ou celles dont le potentiel d’exposition dans divers milieux est plus élevé de celles dont le potentiel est moins élevé. Cette approche réduit l’incertitude globale de la caractérisation des risques comparativement à une approche de caractérisation fondée sur une seule mesure dans un seul milieu (p. ex., concentration létale médiane [CL50]).
Les données sur les propriétés physicochimiques, le devenir (les demi-vies chimiques dans divers milieux et biotes, les coefficients de partage et la bioconcentration dans les poissons), l’écotoxicité aiguë pour les poissons et le volume de produits chimiques importé ou fabriqué au Canada ont été extraits de la documentation scientifique, de bases de données empiriques accessibles (p. ex., boîte à outils QSAR de l’OCDE, 2014) et de réponses à une enquête prévue à l’article 71 de la LCPE, ou sont des données produites par modélisation de la relation (quantitative) structure-activité ([Q]SAR), du bilan massique ou de la bioaccumulation. Ces données ont servi à alimenter d’autres modèles de bilan massique ou à remplir les profils de risques et d’exposition des substances.
Les profils de danger reposent principalement sur des paramètres tels que le mode d’action toxique, la réactivité chimique, les seuils de toxicité interne dérivés du réseau trophique, la biodisponibilité et l’activité chimique et biologique. Les profils d’exposition sont également fondés sur plusieurs paramètres, dont le taux d’émission potentielle, la persistance globale et le potentiel de transport à grande distance. Nous avons comparé les profils de danger et d’exposition aux critères de décision afin de classer les potentiels de danger et d’exposition de chaque substance organique comme faibles, modérés ou élevés. Nous avons appliqué d’autres règles (p. ex., cohérence de la classification, marge d’exposition) pour préciser les classements préliminaires de danger et d’exposition.
Une matrice de risques a permis d’attribuer à chaque substance un risque potentiel faible, modéré ou élevé, en fonction du classement de son danger et de son exposition. Nous avons vérifié le classement du risque potentiel établi au moyen de la CRE en suivant une approche en deux étapes. La première étape consistait à faire passer le classement des risques de moyen ou élevé à faible, dans le cas des substances dont le taux d’émission estimé dans l’eau est faible après traitement des eaux usées, représentant un potentiel d’exposition faible. La deuxième étape consistait à réévaluer le classement du potentiel de risque faible à l’aide de scénarios de risque relativement prudents à échelle locale (c.-à-d., la zone entourant directement la source ponctuelle de rejet), conçus pour ne pas nuire à l’environnement, afin de déterminer si le classement du risque potentiel devrait être revu à la hausse.
La CRE est fondée sur une approche pondérée visant à réduire au minimum le potentiel de surclassement ou de sous-classement du danger et de l’exposition, et du risque subséquent. Une description détaillée des approches équilibrées de traitement des incertitudes est présentée dans ECCC (2016a). Voici une description de deux des domaines d’incertitude les plus importants. Une erreur dans les valeurs de toxicité aiguë empiriques ou modélisées pourrait modifier le classement du danger, surtout si les paramètres sont fondés sur les valeurs de résidus dans les tissus (c.-à-d. mode d’action toxique), dont bon nombre sont des valeurs estimées à l’aide de modèles QSAR (la boîte à outils QSAR de l’OCDE, 2014). L’incidence d’une telle erreur est toutefois atténuée par le fait qu’une surestimation de la létalité médiane générera une valeur prudente (protectrice) pour les résidus dans les tissus qui sera utilisée lors de l’analyse des résidus corporels critiques (RCC). Une erreur due à une sous-estimation de la toxicité aiguë sera atténuée par le recours à d’autres paramètres de danger, tels que le profilage structurel du mode d’action, la réactivité et/ou l’affinité de liaison à l’œstrogène. Les changements ou les erreurs touchant les quantités chimiques pourraient donner lieu à un classement de l’exposition différent, les classements de l’exposition et du risque étant très sensibles aux taux d’émission et aux quantités utilisées. Les classements obtenus au moyen de la CRE représentent donc l’exposition et le risque au Canada compte tenu des quantités utilisées actuellement (déterminées par estimations), mais pourraient ne pas rendre compte des tendances futures.
Les données critiques et les paramètres pris en compte pour mettre au point les profils propres à l’acide 4-méthylbenzènesulfonique, ainsi que les résultats de la classification du danger, de l’exposition et du risque sont présentés dans ECCC (2016b).
Étant donné le classement faible pour le danger et l’exposition, établi au moyen des données prises en compte dans la CRE, le potentiel de risque pour l’environnement associé à l’acide 4-méthylbenzènesulfonique est faible. Il est peu probable que cette substance suscite des préoccupations pour l’environnement au Canada.
6. Potentiel à causer des effets nocifs pour la santé humaine
6.1 Évaluation de l’exposition
Comme l’acide 4-méthylbenzènesulfonique est considéré présenter un potentiel de danger faible (voir l’évaluation des effets sur la santé ci-dessous), aucune valeur quantitative de l’exposition de la population générale n’a été estimée. La présente section fournit de l’information générale sur l’exposition à l’acide 4‑méthylbenzènesulfonique.
6.1.1 Milieux de l’environnement et aliments
Aucune donnée sur l’exposition n’a été trouvée pour l’acide 4-méthylbenzènesulfonique dans des milieux environnementaux pertinents ou des aliments au Canada ou à l’étranger. L’acide 4-méthylbenzènesulfonique présente une valeur élevée de solubilité dans l’eau et, s’il est rejeté dans l’eau, devrait rester dans la colonne d’eau. Il ne devrait pas se répartir dans le sol et les sédiments ni se volatiliser dans l’atmosphère (HSDB, 1983-, ECCC, 2016b). Le rejet d’acide 4-méthylbenzènesulfonique dans les eaux usées peut découler d’activités de formulation industrielles de la substance en produits disponibles aux consommateurs ou du rejet à l’égout consécutif à l’utilisation de ces produits. Il pourrait y avoir une exposition par voie orale de la population générale à l’acide 4‑méthylbenzènesulfonique par l’eau potable. Cependant, cette voie ne devrait pas être une source d’exposition importante de la population générale à l’acide 4‑méthylbenzènesulfonique.
L’acide 4‑méthylbenzènesulfonique pourrait également être utilisé comme composant dans certains matériaux d’emballage des aliments, comme l’encre d’imprimerie, la laque, les enduits de boîtes à conserve, les enduits pour papier et les adhésifs. Comme il n’existe aucun potentiel de contact direct avec des aliments associé à ces utilisations, il ne devrait pas y avoir d’exposition. Pour les utilisations dans lesquelles il pourrait y avoir un contact direct avec des aliments, l’exposition à l’acide 4‑méthylbenzènesulfonique est considérée comme négligeable (communication personnelle de la Direction des aliments de SC adressée au BERSE de SC, en février 2019; sans référence).
6.1.2 Produits disponibles aux consommateurs
Les produits disponibles aux consommateurs contenaient tous moins de 20 % d’acide 4‑méthylbenzènesulfonique. La population générale peut être exposée par voie cutanée à l’acide 4‑méthylbenzènesulfonique en utilisant des cosmétiques. L’acide 4‑méthylbenzènesulfonique est présent à des concentrations s’élevant jusqu’à 0,1 % dans les lotions pour le visage et jusqu’à 0,3 % dans les colorants capillaires permanents et les revitalisants (communication personnelle de la DSPCPD de SC adressée au BERSE de SC, en février 2019; sans référence). La population générale peut également être exposée par voie cutanée à l’acide 4‑méthylbenzènesulfonique en employant un adhésif pour la réparation des fissures dans des matériaux structuraux comme le béton, la maçonnerie, le bois et d’autres matériaux contenant jusqu’à 2 % d’acide 4‑méthylbenzènesulfonique (SDS, 2017). L’exposition par inhalation découlant de l’utilisation de ces produits devrait être minime.
L’acide 4‑méthylbenzènesulfonique est également présent dans les produits catalyseurs ajoutés aux vernis de couchage hors machine. Les vernis de couchage hors machine sont un type d’enduit utilisé pour l’ameublement intérieur en bois afin de lui procurer un fini protecteur clair. Ils nécessitent l’ajout d’un catalyseur pour être activés avant l’application et peuvent être appliqués au moyen d’un pistolet de pulvérisation (TDS, 2010). L’acide 4‑méthylbenzènesulfonique est présent à 15,6 % dans un produit catalyseur ajouté aux vernis de couchage hors machine applicables par pulvérisation (SDS, 2016). Le catalyseur est mélangé dans le vernis à une dilution allant jusqu’à 10 %, en volume (TDS, 2010), pour une concentration finale d’acide 4‑méthylbenzènesulfonique allant jusqu’à 1,6 %.
En raison de la faible volatilité de l’acide 4‑méthylbenzènesulfonique, l’exposition par inhalation devrait être minime pendant le mélange et le chargement du vernis de couchage hors machine dans le pulvérisateur. On peut être exposé par inhalation à une faible concentration d’acide 4‑méthylbenzènesulfonique dans le mélange final de vernis de couchage hors machine en pulvérisateur et de catalyseur pendant l’application par la formation d’aérosols. L’exposition par inhalation devrait être peu fréquente, car ce type de produit est conçu pour durer plusieurs années comme enduit protecteur durable appliqué sur de l’ameublement d’intérieur en bois.
6.2 Évaluation des effets sur la santé
Les principes généraux décrits dans le Document sur l’approche scientifique concernant les substances présentant un faible danger pour la santé humaine (Santé Canada 2017) ont été pris en compte dans la présente évaluation des effets sur la santé. Le potentiel de danger de l’AMBS est considéré comme faible en raison de l’absence d’effets cancérigènes, génotoxiques ou sur la reproduction ou le développement et d’autres effets nocifs pour la santé humaine, et ce jusqu’à 1000 mg/kg p.c./jour, d’après des études portant sur l’AMBS et des hydrotropes analogues décrits en détail ci-dessous. (ECHA c2007-2019, OCDE 2006, 2009).
Les données toxicologiques sur l’AMBS disponibles se limitent à celles relatives à la toxicocinétique, à une étude sur la toxicité orale menée sur 28 jours et à des études de génotoxicité in vitro. Ainsi, les effets de l’AMBS sur la santé ont été décrits en détail à partir d’hydrotropes analogues dans les rapports d’évaluation initiale des ensembles de données d’évaluation de l’OCDE et celle-ci a conclu qu’ils présentaient des profils de faible danger : le 4-méthylbenzènesufonate de sodium (OCDE, 2009), ainsi que le diméthylbenzènesulfonate de sodium et le (propane-2-yl)benzènesulfonate de sodium (OCDE, 2006). Un dossier d’enregistrement soumis à l’ECHA en vertu du REACH est disponible pour l’AMBS (ECHA c2007-2019). Une recherche dans la littérature a été effectuée à partir de l’année précédant la réunion du comité d’évaluation initiale des ensembles de données d’évaluation (SIDS) de l’OCDE (octobre 2005) jusqu’à février 2019 pour les hydrotropes examinés par l’OCDE.
Les données de toxicocinétique de l’AMBS chez les rats et les chiens montrent que celui-ci est rapidement absorbé, après administration par voie orale, et rapidement excrété, principalement par voie urinaire et dans les matières fécales, et présente une demi-vie plasmatique de 75 minutes (Dreyfuss et coll. 1985 dans ECHA c2007-2019, Ho et coll. 1982 dans ECHA c2007-2019, Kano et coll. 1985 dans ECHA c2007-2019). L’AMBS est corrosif sur la peau à des concentrations supérieures à 20 % et irritant sur la peau à des concentrations inférieures (ECHA c2007-2019). Il n’existe aucune étude disponible portant sur l’inhalation de l’AMBS par voie orale.
Dans une étude de toxicité avec doses répétées par voie orale menée sur 28 jours, aucun effet nocif n’a été observé chez des rats (10 ou plus/sexe/dose) s’étant vus administrer 0, 4, 20, 100 ou 500 mg/kg p.c./jour d’AMBS (mode d’administration orale non précisé) (ECHA c2007-2019). Il a été considéré que la dose sans effet nocif observé (DSENO) était de 500 mg/kg pc/jour, soit la dose maximale testée.
Dans une étude de toxicité avec doses répétées de 4-méthylbenzènesufonate de sodium par voie orale menée sur 28 jours, celui-ci étant considéré comme un analogue de l’AMBS, aucun effet nocif lié au traitement n’a été observé chez les rats (5 ou plus/sexe/dose) s’étant vue administrer 0, 100, 300 ou 1000 mg/kg p.c./jour par gavage. La DSENO a été considérée comme la dose maximale testée, soit 1000 mg/kg p.c./jour (OCDE, 2009).
Une étude de toxicité avec doses répétées de diméthylbenzènesulfonate de sodium par voie orale menée sur 90 jours a été considérée par l’OCDE comme une étude clé de la toxicité systémique du groupe des hydrotropes (OCDE, 2006). Cette substance est considérée comme analogue de l’AMBS. Des rats (15/sexe/dose) ont reçu un traitement par voie alimentaire pendant 90 jours (doses égales à 0, 130, 660 ou 3534 mg/kg p.c./jour chez les mâles et 0, 149, 763 ou 4092 mg/kg p.c./jour chez les femelles). Aucun effet n’a été observé chez les mâles. L’OCDE a considéré que la DSENO chez les femmes était égale à 763 mg/kg p.c./jour, en observant une diminution du poids relatif de la rate et des variations de chimie clinique et hématologiques non précisées pour une dose de 4092 mg/kg p.c./jour.
Dans plusieurs autres études de régime alimentaire menées sur 90 jours avec du diméthylbenzènesulfonate de sodium (chez les souris et les rats) et du (propane-2-yl)benzènesulfonate de sodium (chez les rats), aucun effet nocif n’a été observé chez les animaux traités (les doses maximales testées étaient 2439 et 2467, 1429 et 1561 mg/kg p.c./jour, respectivement chez les mâles et les femelles) (OCDE, 2006).
Dans des études de toxicité cutanée menées chez les rongeurs, aucun effet systémique nocif n’a été observé chez les animaux exposés à chacune des doses d'analogue du diméthylbenzènesulfonate de sodium. Ces études comportaient une étude avec doses répétées sur 17 jours (5/sexe/dose, dilution dans l’eau), une étude avec doses répétées sur 90 jours (10/sexe/dose, dilution dans l’éthanol) et une étude de toxicité chronique et de cancérogénicité sur 2 ans (50/sexe/dose, dilution dans l’éthanol). Dans l’étude menée sur 17 jours, l’OCDE a conclu qu’il n’y avait aucun effet nocif (systémique ou local) aux doses maximales de 1600 et 2000 mg/kg p.c./jour, respectivement chez les souris mâles et femelles, et de 800 et 1030 mg/kg p.c./jour, respectivement chez les rats mâles et femelles (OCDE, 2006). Dans l’étude de toxicité cutanée avec doses répétées menée sur 90 jours, l’OCDE n’a relevé aucun effet systémique, mais a considéré que les DSENO associées à des effets locaux étaient égales à 440 et 540 mg/kg p.c./jour chez les souris (respectivement mâles et femelles), en observant une hyperplasie épidermique au point d’application pour des doses supérieures et maximales de 1300 et 1620 mg/kg p.c./jour, respectivement chez les mâles et les femelles (NIH, 1998; OCDE, 2006). Aucun effet nocif n’a été observé chez les rats exposés à des doses atteignant 500 et 800 mg/kg p.c./jour, respectivement chez les mâles et les femelles. Aucun effet systémique (cancérigène ou non) n’a été observé chez les souris ou les rats, ayant respectivement reçu par application cutanée des doses atteignant 727 ou 240 mg/kg p.c./jour, pendant 2 ans. Une hyperplasie épidermique a été observée au point d’application chez les souris mâles, à des doses supérieures ou égales à 364 mg/kg p.c./jour, et chez les souris femelles (non liée à la dose) et les rats femelles, à des doses supérieures ou égales à 120 mg/kg p.c./jour (NIH, 1998; OECD, 2006).
L’AMBS ne s’est pas avéré génotoxique in vitro lors d’un test de mutagénicité bactérienne (Hoechst, 1988a, dans ECHA c2007-2019) et d’un test d’aberration chromosomique réalisé sur des cellules pulmonaires de hamster chinois (Hoechst, 1988b dans ECHA c2007-2019).
Des tests de génotoxicité in vivo avec des substances similaires se sont révélés négatifs. Le diméthylbenzènesulfoante de calcium a donné des résultats négatifs lors d’un test cytogénétique sur micronoyaux de cellules de souris par injection intrapéritonéale, de même que le (propane-2-yl)benzènesulfonate de sodium lors de deux tests cytogénétiques de micronoyaux de cellules de souris par gavage (OCDE, 2006).
Aucune étude des effets sur la reproduction ou le développement n’était disponible pour l’AMBS, mais des études étaient disponibles pour deux analogues. Dans le cadre du test 421 de l’OCDE, ou test d’évaluation de la toxicité pour la reproduction et le développement, le 4-méthylbenzènesufonate de sodium a été administré quotidiennement par gavage à des rats mâles et femelles (12/sexe/groupe) à des doses de 0, 300 ou 1000 mg/kg p.c./jour (ECHA c2007-2019). Les mâles ont été traités pendant 46 jours, entre le jour d’accouplement et le jour précédent leur mort (nécropsie le 47e jour). Les femelles ont été traitées 14 jours avant l’accouplement, pendant l’accouplement et la gestation et les mères et leurs petits ont été tués le 4e jour après la naissance de ces derniers (OCDE, 2009). Aucun effet sur la reproduction ou le développement n’a été observé à des doses de 300 ou 1000 mg/kg p.c./jour. L’OCDE a considéré que la DSENO associée à une toxicité générale était de 300 mg/kg p.c./jour chez les mâles et les femelles, en observant des diarrhées et des selles molles chez les deux sexes à 1000 mg/kg p.c./jour et une infiltration cellulaire inflammatoire modérée de la lamina propria, ainsi qu’une hyperplasie des cellules squameuses dans le repli séparant le préestomac et l’estomac glandulaire chez les mâles seulement, à 1000 mg/kg p.c./jour. L’OCDE (2009) a considéré que les diarrhées et les selles molles observées chez les deux sexes et les effets sur l’estomac des rats mâles à la dose maximale de 1000 mg/kg p.c./jour pourraient être une réponse à l’irritation répétée causée par le bolus administré par gavage. En effet, ces effets n’ont pas été observés chez les rats lors d’une étude menée sur 28 jours pour une dose de 1000 mg/kg p.c./jour de la même substance administrée par gavage.
Dans une étude des effets sur le développement menée chez les rats, des mères (30/dose) ont reçu par gavage, du 6e au 15e jour de gestation, des doses de diméthylbenzènesulfonate de calcium dilué dans l’eau égales à 0, 47, 468 ou 936 mg/kg p.c./jour. Un animal est mort durant l’étude à dose moyenne, ce que l’OCDE a attribué à une blessure due au gavage. Aucun effet nocif sur les mères ou sur le développement n’a été observé, quelle que soit la dose administrée. L’OCDE (2006) a déterminé que la DSENO associée à une toxicité maternelle et fœtale était égale à 936 mg/kg p.c./jour, soit la dose maximale testée (OCDE, 2006).
6.3 Caractérisation du risque pour la santé humaine
Les observations figurant dans le Document sur l’approche scientifique concernant les substances présentant un faible danger pour la santé humaine (Santé Canada, 2017) concernent l’évaluation des effets sur la santé de l’AMBS. D’après les données disponibles en ce qui a trait aux effets sur la santé, l’AMBS ne devrait être ni génotoxique ni cancérigène ni entrainer de toxicité pour la reproduction ou le développement. Aucun effet systémique n’a été observé chez les animaux après une exposition à des doses répétées d’AMBS ou d’analogues en dessous de la dose limite de 1000 mg/kg p.c./jour (ECHA c2007-2019; OCDE, 2006, 2009). Les effets observés étaient des irritations cutanées locales (hyperplasie épidermique), lesquels sont les effets liés au point d’application.
Étant donné le faible potentiel de danger de la substance, les estimations quantitatives d’exposition n’ont pas été calculées et son risque pour la santé humaine est considéré comme faible.
6.4 Incertitudes de l’évaluation des risques pour la santé humaine
Des incertitudes subsistent dans les bases de données relatives aux effets sur la santé (p. ex. la toxicité possiblement plus élevée de l’AMBS administrée par voie cutanée ou par inhalation que celle d’hydrotropes analogues, en raison de son plus grand potentiel irritant). Étant donné le faible potentiel de danger de l’AMBS, une approche qualitative de caractérisation des risques est considérée comme pertinente.
7. Conclusion
Compte tenu de tous les éléments de preuve contenus dans la présente ébauche d’évaluation préalable, le risque d’effets nocifs pour l’environnement de l’AMBS est faible. Il est proposé de conclure qu’il’ ne satisfait pas aux critères énoncés aux alinéas 64a) ou b) de la LCPE, car il ne pénètre pas dans l’environnement en une quantité ou concentration ou dans des conditions de nature à avoir, immédiatement ou à long terme, un effet nocif sur l’environnement ou sur la diversité biologique, ou à mettre en danger l’environnement essentiel pour la vie.
À la lumière des renseignements contenus dans la présente ébauche d’évaluation préalable, il est proposé de conclure que l’AMBS ne satisfait pas au critère énoncé à l’alinéa 64c) de la LCPE, car il ne pénètre pas dans l’environnement en une quantité ou concentration ou dans des conditions de nature à constituer un danger pour la vie ou la santé humaines au Canada.
Il est donc proposé de conclure que l’acide 4 méthylbenzènesulfonique ne satisfait à aucun des critères énoncés à l’article 64 de la LCPE.
Références
Boite à outils QSAR de l’OCDE [outil d’extrapolation]. 2018. Version 4.2. Paris (France) : Organisation de coopération et de développement économiques, Laboratoire de chimie mathématique.
Boite à outils QSAR de l’OCDE [outil d’extrapolation]. 2014. Version 3.3. Paris (France) : Organisation de coopération et de développement économiques, Laboratoire de chimie mathématique.
Canada, ministère de l’Environnement. 2012. Loi canadienne sur la protection de l’environnement (1999) : Avis concernant certaines substances de la Liste intérieure [PDF]. Gazette du Canada, partie I, vol. 146, no 48, supplément.
Canada. 1999. Loi canadienne sur la protection de l’environnement (1999). L.C. 1999, ch.33. Gazette du Canada, partie III, vol. 22, no 3.
ChemIDplus [database]. 1993-. Bethesda (MD): National Library of Medicine (États-Unis). [consulté le 10 juillet 2019]. (Disponible en anglais seulement)
[ECCC, SC] Environnement et Changement climatique Canada, Santé Canada [modifié le 12 mars 2017]. Catégorisation de substances chimiques. Ottawa (Ont.), gouvernement du Canada.
[ECCC] Environnement et Changement climatique Canada. 2016a. Document sur l’approche scientifique : Classification du risque écologique des substances organiques. Ottawa (Ont.), gouvernement du Canada.
[ECCC] Environnement et Changement climatique Canada. 2016b. Supporting documentation: data used to create substance-specific hazard and exposure profiles and assign risk classifications. Gatineau (Québec) : ECCC. Renseignements à l’appui du Document sur l’approche scientifique : Classification du risque écologique des substances organiques. Disponible à : substances@ec.gc.ca. (Disponible en anglais seulement)
[ECHA] Agence européenne des produits chimiques. c2007 -2019. Base de données des substances enregistrées; résultats de recherche pour le no CAS 104-15-4. Helsinki (Finlande) : ECHA. [Mis à jour le 16/07/2019; consulté le 12/08/2019]. (Disponible en anglais seulement)
Environnement Canada. 2013. Données sur la mise à jour de l’Inventaire de la LIS collectées en vertu de l’article 71 de la Loi canadienne sur la protection de l’environnement 1999 : Avis concernant certaines substances de la Liste intérieure. Données préparées par : Environnement Canada et Santé Canada; Programme des substances existantes.
Greim H, Ahlers J, Bias R, Broecker B, Hollander H, Gelbke HP, Klimisch HJ, Mangelsdorf I, Paetz A, Schon N, et al. 1994. Toxicity and ecotoxicity of sulfonic acids: structure-activity relationship. Chemosphere vol. 28 (No. 12) : 2203-2236. (Disponible en anglais seulement)
HSDB. Hazardous Substances Data Bank [database]. 1983-. Résultats de recherche pour le numéro CAS 104-15-4. Bethesda (Maryland) : National Library of Medicine (États-Unis). [Mis à jour le 14 février 2003; consulté en septembre 2020]. (Disponible en anglais seulement)
[NIH] National Institutes of Health. 1998. Department of Health and Human Services, Public Health Service, National Institutes of Health, Research Triangle Park, Caroline du Nord, États-Unis. Toxicology and carcinogenesis studies of technical grade sodium xylenesulfonate (CAS No. 1300-72-7) in F344/N Rats and B6C3F1 mice (dermal studies)/NIH no 98-3380. (Disponible en anglais seulement)
[OCDE] Organisation de coopération et de développement économiques. 2006. SIDS initial assessment report: Hydrotropes [PDF]. SIAM [SIDS Initial Assessment Meeting] 21; octobre 2005; Washington D.C., États-Unis. [Consulté en juillet 2019] (Disponible en anglais seulement)
[OCDE] Organisation de coopération et de développement économiques. 2009. SIDS initial assessment report: Sodium p-toluenesulfonate CAS RN 657-84-1 [PDF]. SIAM [SIDS Initial Assessment Meeting] 27; octobre 2008; Ottawa, Canada. [Consulté en juillet 2019] (Disponible en anglais seulement)
[PDS] Product Data Sheet. 2018. Sikadur Crack Fix [PDF]. Lyndhurst (New Jersey) : Sika Corporation [consulté en septembre 2020]. (Disponible en anglais seulement)
Santé Canada. 2015. Feuilles de calcul [format Excel] sur l’eau potable de l’Unité d’évaluation environnementale. Ottawa (Ont.), Santé Canada. [Cité le 6 mars 2019]
Santé Canada. 2017. Document sur l’approche scientifique concernant les substances présentant un faible danger pour la santé humaine. Ottawa (Ont.), gouvernement du Canada.
[SDS] Safety Data Sheet. 2016. Care Catalyst C1491 [PDF]. Cleveland (Ohio); M.L. Campbell [consulté en octobre 2019]. (Disponible en anglais seulement)
[SDS] Safety Data Sheet. 2017. Sikadur CrackFix Part B [PDF]. Lyndhurst (New Jersey) : Sika Corporation [consulté en mars 2019]. (Disponible en anglais seulement)
[TDS] Technical Data Sheet. 2010. Stealth Clear Base–Conversion Varnish [PDF]. Fort Érié (Ontario); M.L. Campbell [consulté en octobre 2019]. (Disponible en anglais seulement)
Annexe A. Extrapolation pour l’acide 4-méthylbenzènesulfonique (AMBS)
| Nom chimique | Paratoluènesulfonate de sodium | Diméthylbenzènesulfonate de sodium | Diméthylbenzènesulfoante de calcium | (Propane-2-yl)benzènesulfonate de sodium | Acide 4-méthylbenzènesulfonique (AMBS) |
|---|---|---|---|---|---|
| No de CAS | 657-84-1 | 1300-72-7 | 28088-63-3 | 28348-53-0 | 104-15-4 |
| Rôle | Substance similaire | Substance similaire | Substance similaire | Substance similaire | Cible |
| Référence | OECD 2009 | OECD 2006 | OECD 2006 | OECD 2006 | ECHA c2007-2019 (études des risques) et ChemIDplus 1993- (propriétés physicochimiques) |
| Structure représentativea | ![[Na]OS(=O)(=O)c1ccc(cc1)C](/content/dam/eccc/images/pded/ptsa/20200923-Table2-2-1.jpg) |
![[Na]OS(=O)(=O)c1ccc(cc1C)C](/content/dam/eccc/images/pded/ptsa/20200923-Table2-2-2.jpg) |
![[Ca]OS(=O)(=O)c1ccc(cc1C)C](/content/dam/eccc/images/pded/ptsa/20200923-Table2-2-3.jpg) |
![[Na]OS(=O)(=O)c1ccc(cc1)C(C)C](/content/dam/eccc/images/pded/ptsa/20200923-Table2-2-4.jpg) |
 |
| Hydrosolubilité (mg/l)b,d | > 2,5 x 105 | 4 x 105; | 5,5 x 105 | 3,3 x 105; 4 x 105; |
6,2 x 105 |
| Log Kowb | -2,4c | -1,9c | -2,7 | -1,5c | -0,62c |
| Pression de vapeur (mm Hg)b,e | 2,6 x 10-11 c | < 1,5 x 10-7 | 1,2 x 10-11 c | 8,2 x 10-12 c | 2,7 x 10-6 c |
| Toxicocinétique et ADME | Chez les rats et les chiens, absorption et excrétion rapides (principalement par l’urine et aussi par les selles) après administration orale. | N. d. (une évaluation qualitative met en évidence une absorption rapide par voie orale et une absorption limitée par voie cutanée) | N. d. (une évaluation qualitative met en évidence une absorption rapide par voie orale et une absorption limitée par voie cutanée) | N. d. (une évaluation qualitative met en évidence une absorption rapide par voie orale et une absorption limitée par voie cutanée) | Chez les rats et les chiens, absorption et excrétion rapides (principalement par l’urine et aussi par les selles) après administration orale; demi-vie de 75 minutes dans le plasma. |
| Toxicité aigüe (voie orale) | Rat : DL50 > 2000 mg/kg p.c./jour | Rat : DL50 = 6480 mg/kg p.c./jour | Rat : DL50 = 1044 mg/kg p.c./jour | Rat : DL50 > 7000 mg/kg p.c./jour | Rat : DL50 = 1410 mg/kg p.c./jour |
| Toxicité aigüe (voie cutanée) | Aucune donnée | N. d. | Lapin : > 624 mg/kg p.c./j | Lapin :> 624 mg/kg p.c./j | N. d. |
| Toxicité aigüe (inhalation) | N. f. | N. d. | N. d. | Rat : DL50 > 770 000 mg/m3 | N. f. |
| Irritation (voie cutanée) | N. f. | Non irritant | Non irritant | Non irritant | Corrosif pour la peau |
| Toxicité à doses répétées (voie orale) | 28 jours, rat, gavage : DSENO = 1000 mg/kg p.c./jour (DMT; aucun effet nocif lié au traitement chez les mâles et les femelles) 90 jours : N. d. |
90 jours, rat, voie alimentaire : DSENO pour les femelles = 763 mg/kg p.c./j (après observation d’une baisse du poids relatif de la rate, 17 % à la dose suivante de 4092 mg/kg p.c./j); aucun effet à la DMT pour les mâles (3534 mg/kg p.c./j) 90 jours, rongeurs, voie alimentaire : Aucun effet nocif jusqu’à la DMT de 2467 et 2439 mg/kg p.c./j, respectivement chez les souris mâles et femelles, et de 1429 et 1561 mg/kg p.c./j, respectivement chez les rats mâles et femelles |
N. d. | 90 jours, rat, voie alimentaire : Aucun effet nocif jusqu’à 114 et 159 mg/kg p.c./j, respectivement chez les mâles et les femelles (DMT) | 28 jours, rats, voie orale : Aucun effet nocif jusqu’à 500 mg/kg p.c./j (DMT) chez les rats (voie orale, alimentaire ou gavage non précisés); description d’étude limitée et contradictoire 90 jours : Extrapolation à partir du no de CAS 1300-72-7 |
| Toxicité à doses répétées (voie cutanée) | N. d. | 17 jours, rongeurs : Aucun effet nocif jusqu’à 1600 et 2000 mg/kg p.c./j, respectivement chez les souris mâles et femelles, et jusqu’à 800 et 1030 mg/kg p.c./j, respectivement chez les rats mâles et femelles (DMT) 90 jours, souris : DSENO (irritation locale) = 440 et 540 mg/kg p.c./j, respectivement chez les mâles et femelles (effet local sous la forme d’une hyperplasie épidermique au point d’application à la DMT (1300 et 1620 mg/kg p.c./j, respectivement chez les mâles et les femelles) 90 jours, rats : Aucun effet nocif jusqu’à 500 et 800 mg p.a./kg p.c./j (DMT), respectivement chez les mâles et les femelles |
N. d. | N. d. | Références croisées à partir du no de CAS 1300-72-7 |
| Toxicité à dose répétée (inhalation) | N. d. | N. d. | N. d. | N. d. | N. d. |
| Toxicité pour la reproduction ou le développement (voie orale) | Test d’évaluation de la toxicité pour la reproduction et le développement, rat, gavage : DSENO pour la reproduction = 1000 mg/kg p.c./j DSENO pour le développement et la croissance des petits = 1000 (mg p.a./kg p.c./j) DSENO de toxicité générale = 300 mg/kg p.c./j (pour les effets à 1000 mg/kg p.c./j (diarrhées ou selles molles chez les mâles et les femelles, effets sur l’estomac chez les mâles seulement) | N. d. | Effets sur le développement, rat, gavage : DSENO (pour les mères et le développement) = 936 mg/kg p.c./j (DMT) | N. d. | Extrapolation à partir des no de CAS 657-84-1 et 28088-63-3 |
| Toxicité génétique | In vitro : négatif(Test Ames et test d’aberration chromosomique) In vivo : N. d. |
In vitro : négatif In vivo : N. d. |
In vitro : Négatif In vivo : négatif(Test cytogénétique sur micronoyaux de cellules de souris, injection intrapéritonéale) |
In vitro : négatif In vivo : négatif(deux tests cytogénétiques sur micronoyaux de cellules de souris, gavage oral) |
In vitro : négatif (tests Ames et d’aberration chromosomique) In vivo : extrapolation à partir des no de CAS 28088-63-3 et 28348-53-0 |
| Cancérogénicité | N. d. | Aucun effet systémique observé chez les rats recevant jusqu’à 240 mg/kg p.c./j et les souris recevant jusqu’à 727 mg/kg p.c./j par voie cutanée (effet local sous la forme d’une hyperplasie épidermique au point d’application chez les souris mâles, à des doses supérieures ou égales à 364 mg/kg p.c./j, et chez les souris femelles (effet non lié à la dose) et les rats femelles à des doses supérieures ou égales à 120 mg/kg p.c./j. | N. d. | N. d. | Extrapolation à partir du no de CAS 1300-72-7 |
Abréviations : DMT, dose maximale testée; Kow, coefficient de partage octanol-eau; N. d., non disponible; S. o., sans objet; N. f., les études disponibles ne sont pas fiables.
a Les formes commerciales des sulfonates aromatiques contiennent un mélange d’isoformes ortho-, méta,- ou para- (OCDE, 2006), sauf si le nom mentionne une isoforme spécifique. Les structures représentatives montrées ici pour les no de CAS 1300-72-7, 28088-63-3, et 28348-53-0 sont celles des isoformes suivantes : no 1300-72-7, para, méta; no 28088-63-3, ortho, méta; no 28348-53-0, para.
b L’hydrosolubilité, le log Kow et la pression de vapeur sont des données mesurées, sauf indication contraire.
c Données modélisées
d Valeur à 20.
e Valeur à 25 sauf indication contraire.
