Ébauche d’évaluation préalable - coumarine 1
Title officiel : Ébauche d’évaluation préalable - 7-(Diéthylamino)-4-méthyl-2H-1-benzopyran-2-one (coumarine 1)
Numéro de registre du Chemical Abstracts Service
91-44-1
Environnement et Changement climatique Canada
Santé Canada
Octobre 2020
Sommaire
En vertu de l’article 74 de la Loi canadienne sur la protection de l’environnement 1999 (LCPE), les ministres de l’Environnement et de la Santé ont réalisé une évaluation préalable de la 7-(diéthylamino)-4-méthyl-2H-1-benzopyran-2-one, appelée ci-après coumarine 1. Le numéro de registre du Chemical Abstracts Service (no CASNote de bas de page 1 ) de cette substance est le 91-44-1. Cette substance a été jugée d’intérêt prioritaire, car elle satisfait aux critères de catégorisation du paragraphe 73(1) de la LCPE.
D’après les renseignements déclarés en réponse à une enquête menée en vertu de l’article 71 de la LCPE, aucune production de coumarine 1 supérieure au seuil de déclaration de 100 kg n’a été déclarée au Canada en 2011, et une quantité située entre 1000 et 10 000 kg y a été importée la même année. Les utilisations rapportées au Canada incluent des applications commerciales dans des articles en tissu, en textile ou en cuir. La coumarine 1 est aussi utilisée dans certains produits cosmétiques au Canada, tels que des colorants capillaires temporaires, des vernis à ongles et du maquillage pour le corps et le visage (y compris du maquillage pour les yeux et les lèvres). La coumarine 1 est aussi utilisée comme stabilisant dans des produits de nettoyage de tapis.
Le risque posé à l’environnement par la coumarine 1 a été caractérisé au moyen de la Classification du risque écologique (CRE) des substances organiques. La CRE est une approche basée sur le risque, qui tient compte de plusieurs paramètres liés au danger et à l’exposition et d’une pondération des éléments de preuve. Les profils de danger sont établis principalement en se basant sur des paramètres liés au mode d’action toxique, à la réactivité chimique, aux seuils de toxicité interne dérivés du réseau trophique, à la biodisponibilité et à l’activité chimique et biologique. Parmi les paramètres pris en compte pour les profils d’exposition, mentionnons la vitesse d’émission potentielle, la persistance globale et le potentiel de transport à grande distance. Une matrice de risque est utilisée pour assigner un niveau faible, modéré ou élevé de préoccupation potentielle, basé sur les profils de risque et d’exposition. D’après les résultats de la CRE, il est improbable que la coumarine 1 ait des effets nocifs sur l’environnement.
Compte tenu de tous les éléments de preuve avancés dans la présente ébauche d’évaluation préalable, le risque d’effet nocif sur l’environnement de la coumarine 1 est faible. Il est conclu que la coumarine 1 ne satisfait à aucun des critères des alinéas 64(a) et 64(b) de la LCPE, car elle ne pénètre pas dans l’environnement en une quantité ou concentration ni dans des conditions qui ont ou peuvent avoir un effet nocif immédiat ou à long terme sur l’environnement ou sa diversité biologique ou qui constituent ou peuvent constituer un danger pour l’environnement nécessaire à la vie.
L’ensemble des données sur les effets sur la santé de la coumarine 1 a été jugé limité. Pour tenir compte de cette limitation, nous avons suivi une approche de lecture croisée pour étayer l’évaluation des effets sur la santé. D’après les données disponibles sur des analogues, la toxicité pour le développement a été jugée l’effet critique sur la santé. La population générale du Canada est principalement exposée à la coumarine 1 lors de l’utilisation de certains produits cosmétiques, comme des colorants capillaires temporaires, des vernis à ongles et du maquillage pour le corps et le visage (y compris pour les yeux et les lèvres), ainsi que de certains produits de nettoyage. La comparaison des niveaux de coumarine 1 auxquels les Canadiens peuvent être exposés dans les milieux de l’environnement ou lors de l’utilisation de vernis à ongles, de colorants capillaires temporaires en poudre, de maquillage pour le visage, de rouge/brillant à lèvres ou de produits de nettoyage pour tapis avec les niveaux associés à des effets nocifs déterminés lors d’études en laboratoire a conduit à calculer des marges jugées adéquates pour tenir compte des incertitudes des bases de données sur les effets sur la santé et l’exposition. Toutefois, les marges entre l’exposition à la coumarine 1 due à une utilisation occasionnelle de maquillage spécial pour le corps et les niveaux d’effet critique de la coumarine 1 sont jugées potentiellement inadéquates pour tenir compte des incertitudes des bases de données sur les effets sur la santé et l’exposition.
En nous basant sur les renseignements présentés dans la présente ébauche d’évaluation préalable, nous concluons que la coumarine 1 satisfait aux critères de l’alinéa 64(c) de la LCPE, car elle pénètre dans l’environnement en une quantité ou concentration ou dans des conditions qui constituent ou peuvent constituer un danger au Canada pour la vie ou la santé humaine.
Nous concluons donc que la coumarine 1 satisfait à des critères de l’article 64 de la LCPE.
La coumarine 1 satisfait aussi aux critères de persistance, mais à ceux de bioaccumulation, du Règlement sur la persistance et la bioaccumulation de la LCPE.
1. Introduction
En vertu de l’article 74 de la Loi canadienne sur la protection de l’environnement 1999 (LCPE) (Canada 1999), les ministres de l’Environnement et de la Santé ont réalisé une évaluation préalable de la 7-(diéthylamino)-4-méthyl-2H-1-benzopyran-2-one, ci-après appelée coumarine 1. Cette substance a été jugée d’intérêt prioritaire pour une évaluation, car elle satisfait aux critères de catégorisation du pargraphe 73(1) de la LCPE (ECCC, SC [modifié en 2017]).
Le risque posé à l’environnement par la coumarine 1 a été caractérisé au moyen de la Classification du risque écologique (CRE) des substances organiques (ECCC 2016a). Pour la CRE, le danger d’une substance est décrit au moyen de paramètres liés au mode d’action toxique, à la réactivité chimique, aux seuils de toxicité interne dérivés du réseau trophique, à la biodisponibilité et à l’activité chimique et biologique. La CRE tient aussi compte de l’exposition possible des organismes dans des environnements aquatiques ou terrestres en se basant sur des facteurs tels que la vitesse d’émission potentielle, la persistance globale et le potentiel de transport atmosphérique à grande distance. Les divers éléments de preuve sont combinés afin d’identifier les substances nécessitant une évaluation plus poussée de leur potentiel d’effets nocifs sur l’environnement ou ayant une faible probablité d’effets nocifs sur l’environnement.
Pour la présente ébauche d’évaluation préalable, nous avons tenu compte de renseignements sur les propriétés chimiques, le devenir dans l’environnement, les dangers, les utilisations et les expositions, y compris des renseignements soumis par des parties intéressées. Des données pertinentes ont été identifiées jusqu’en avril 2019. Des données empiriques tirées d’études clés ainsi que des résultats de modélisation ont été utilisés pour tirer nos conclusions. Quand ils étaient pertinents, nous avons pris en compte des renseignements présentés dans des évalutions faites par d’autres juridictions (p. ex. le National Industrial Chemicals Notification and Assessment Scheme (NICNAS) de l’Australie, le Comité mixte d’experts FAO/OMS des additifs alimentaires (JECFA) et l’Autorité européenne de la sécurité des aliments (EFSA)).
La présente ébauche d’évaluation préalable a été préparée par le personnel du Programme d’évaluation du risque de la LCPE travaillant à Santé Canada et à Environnement et Changement climatique Canada. Elle comprend aussi des intrants provenant d’autres programmes de ces ministères. Les parties de la présente évaluation portant sur la santé humaine ont fait l’objet d’un examen externe et/ou de consultations. Des commentaires sur les parties techniques ayant trait à la santé humaine ont été faits par Tetra Tech Inc. (Theresa Lopez, Jennifer Flippin et Joan Garey). La partie portant sur l’environnement est basé sur le document de la CRE (publié le 30 juillet 2016), document qui a fait l’objet d’un examen externe ainsi que d’une période de commentaires du public de 60 jours. Bien que des commentaires externes aient été pris en compte, Santé Canada et Environnement et Changement climatique Canada restent responsables du contenu final et des conclusions de la présente ébauche d’évaluation préalable.
La présente ébauche d’évaluation préalable repose sur des renseignements critiques pour déterminer si la substance visée satisfait aux critères de l’article 64 de la LCPE. À cette fin, nous avons examiné des renseignements scientifiques et suivi une approche basée sur une pondération des éléments de preuve et le principe de précautionNote de bas de page 2 . Dans ce document, nous présentons les renseignements critiques et les éléments sur lesquels nos conclusions sont basées.
2. Identité de la substance
Nous donnons dans le tableau 2-1 le numéro de registre du Chemical Abstracts Service (no CASNote de bas de page 3 ), le nom de la substance visée sur la Liste intérieure des substances (LIS), son nom commun et sa structure moléculaire.
| No CAS | Nom sur la LIS (nom commun) | Structure chimique et formule moléculaire | Masse moléculaire (g/mol) | Référence |
|---|---|---|---|---|
| 91-44-1 | 7-(Diéthylamino)-4-méthylbenzopyr-2-one (coumarine 1) | 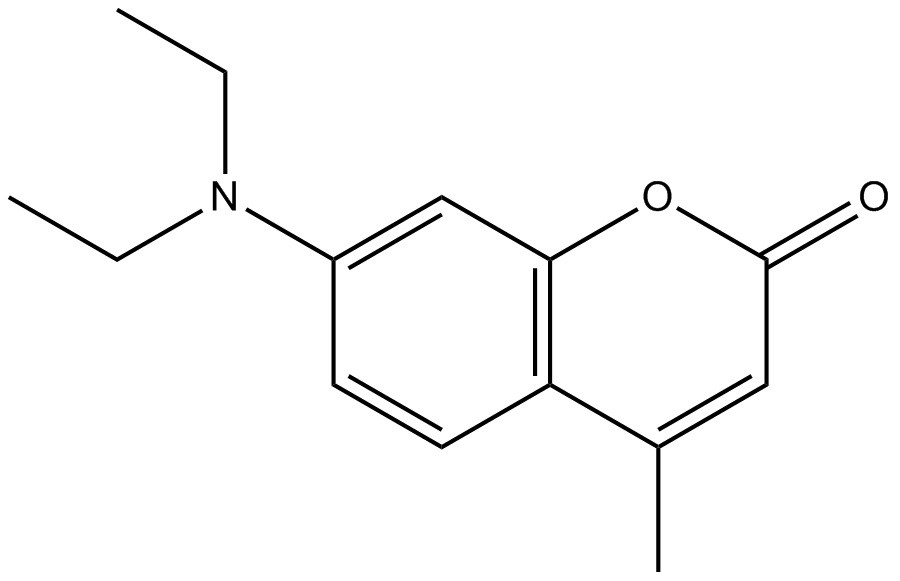 C14H17NO2 C14H17NO2 | 231,30 | ChemIDplus 1993- |
2.1 Sélection d’analogues
Nous avons suivi une approche de lecture croisée au moyen de données sur des analogues afin d’étayer l’évaluation ayant trait à la santé humaine. Nous avons choisi des analogues structurellement similaires à la substance visée (propriétés physico‑chimiques, métabolisme similaires) et sur lesquels il y avait des données empiriques pertinentes qui pouvaient être utilisées pour des paramètres pour lesquels les données empiriques sur la substance visée étaient limitées. Nous donnons dans le tableau 2-2 des renseignements sur l’identité et la structure chimique des analogues utilisés pour la présente évaluation. On trouvera à l’Annexe A d’autres détails sur des facteurs pris en compte pour l’identification des analogues. Pour plus de renseignements sur les propriétés physico-chimiques et les effets sur la santé de ces analogues, veuillez consulter l’Annexe B.
| No CAS | Nom sur la LIS (nom commun) | Structure chimique et formule moléculaire | Masse moléculaire (g/mol) | Référence |
|---|---|---|---|---|
| 92-48-8 | 6-Méthylcoumarine (6‑méthylcoumarine) | 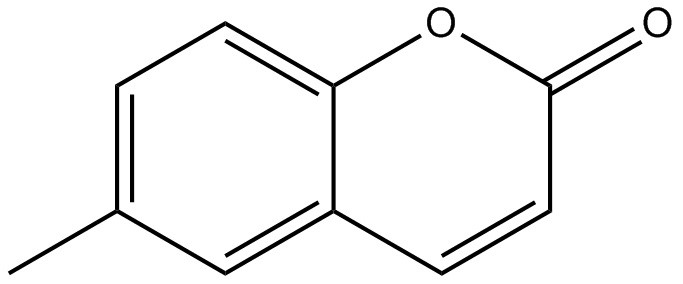 C10H8O2 C10H8O2 | 160,172 | ChemIDplus 1993- |
| 91-64-5 | Coumarine (coumarine) | 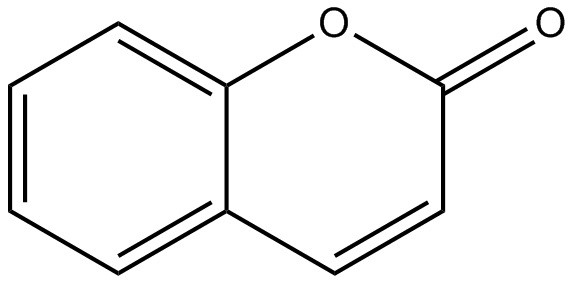 C9H6O2 C9H6O2 | 146,133 | ChemIDplus 1993- |
La 6-méthylcoumarine (no CAS 92-48-8) s’est avérée être l’analogue le plus proche de la coumarine 1, pour lequel des données sur la toxicité chronique ont été identifiées. Toutefois, aucune donnée sur la toxicité pour le développement/reproduction de la 6‑méthylcoumarine n’a été trouvée, et nous avons utilisé celles sur la coumarine pour ce paramètre.
3. Propriétés physiques et chimiques
Nous donnons dans le tableau 3-1 un résumé des données sur les propriétés physiques et chimiques de la coumarine 1. D’autres propriétés physiques et chimiques sont rapportées dans un document d’ECCC (2016b).
| Propriété | Valeur | Référence clé |
|---|---|---|
| État physique | Poudre cristalline, jaune pâle à brun | FSS 2019 |
| Point de fusion (°C) | 72–75 | Epi Suite c2000-2012 |
| Pression de vapeur (Pa) | 0,00257 à 25 °C | Epi Suite c2000-2012 |
| Constante de Henry (Pa·m3/mol) | 0,0309 | Epi Suite c2000-2012 |
| Solubilité dans l’eau (mg/L) | 53,28 at 25 °C | Epi Suite c2000-2012 |
| log Koe (sans dimension) | 3,22 | Epi Suite c2000-2012 |
Abréviation : Koe = coefficient de partage octanol-eau
4. Sources et utilisations
Lors d’une enquête menée en vertu de l’article 71 de la LCPE (Canada 2012), aucune production de coumarine 1 supérieure au seuil de déclaration de 100 kg n’a été rapportée au Canada en 2011. Pendant la même année, une quantité située entre 1000 et 10 000 kg a été importée au Canada (Environnement Canada 2013). Il a été rapporté lors de la même enquête, que la coumarine est utilisée au Canada comme colorant dans des articles commerciaux en tissu, textile ou cuir (Environnement Canada 2013).
D’après les déclarations faites en vertu du Règlement sur les cosmétiques, de la coumarine 1 est présente dans des produits cosmétiques vendus au Canada (communication personnelle, courriels de la Direction de la sécurité des produits de consommation et des produits dangereux (DSPCPD) de Santé Canada (SC) au Bureau d’évaluation du risque des substances existantes (BERSE) de SC, octobre 2018; non référencé). La coumarine 1 a aussi été identifiée comme stabilisant dans un produit de nettoyage pour tapis disponible au Canada (FSS 2015).
Au niveau international, la coumarine 1 a été identifiée dans des encres pour tatouage (Piccinini et al. 2015, Landeg et al. 2016), des produits de nettoyage (HCPA 2019, CPID c2001-2019, RB c2012-2019), des produits pour le traitement du cuir ou de textiles, des substances chimiques pour le papier et des colorants (ECHA c2007-2019).
5. Devenir et comportement dans l’environnement
5.1 Persistance dans l’environment
D’après les modèles utilisés pour la CRE (ECCC 2016b), la coumarine 1 devrait persister dans l’eau, les sédiments et les sols, mais pas dans l’air.
5.2 Potentiel de bioaccumulation
Étant donné son Koe faible et ses facteurs de bioconcentration faibles (ECCC 2016b), la coumarine 1 ne devrait pas subir de bioaccumulation significative dans des organismes.
6. Potentiel d’effets nocifs sur l’environnement
6.1 Caractérisation du risque pour l’environnement
Le risque posé à l’environnement par la coumarine 1 a été caractérisé en suivant l’approche de Classification du risque écologique des substances organiques (CRE) (ECCC 2016a). La CRE est une approche basée sur les risques qui tient compte de plusieurs paramètres liés au danger et à l’exposition et d’une pondération des éléments de preuve pour déterminer la classification du risque. Les divers éléments de preuve sont combinés pour différencier les substances plus ou moins dangereuses et les potentiels d’exposition plus ou moins grands dans divers milieux. Cette approche permet de réduire l’incertitude globale de la caractérisation du risque, comparativement à une approche basée sur un seul paramètre dans un seul milieu (p. ex. la concentration létale moyenne (CL50)). Nous avons résumé dans ce qui suit cette approche, qui est d’autre part décrite en détail dans un document d’ECCC (2016a).
Nous avons collecté des données sur les propriétés physico-chimiques, le devenir (demi-vie chimique dans divers milieux et biotes, coefficients de partition, bioconcentration dans les poissons), l’écotoxicité aiguë chez le poisson et les quantités importées ou produites au Canada, à partir de la littérature scientifique, des bases de données empiriques (p. ex. Boîte à outils (Q)RSA de l’OCDE 2014) et de renseignements soumis lors d’enquêtes menées en vertu de l’article 71 de la LCPE. D’autres données ont été obtenues à l’aide de modèles (Q)SAR (relation quantitative structure-activité) ou de devenir du bilan massique et de bioaccumulation. Nous avons utilisé ces données comme intrants dans d’autres modèles de bilan massique ou pour compléter les profils de danger et d’exposition de ces substances.
Les profils de danger ont été établis principalement à partir de paramètres liés au mode d’action toxique, à la réactivité chimique, aux seuils de toxicité interne dérivés du réseau trophique, à la biodisponibilité et à l’activité chimique et biologique. Les profils d’exposition ont aussi été basés sur plusieurs paramètres dont la vitesse d’émission potentielle, la persistance globale et le potentiel de transport à grande distance. Les profils de danger et d’exposition ont été comparés aux critères de décision afin de les classer comme faibles, moyens ou élevés. D’autres règles ont été appliquées (p. ex., constance de la classification, marge d’exposition) pour améliorer les classifications préliminaires du danger et de l’exposition.
Une matrice de risque a été utilisée pour assigner un risque potentiel faible, modéré ou élevé à chaque substance, en se basant sur la classification du danger et de l’exposition. Les classifications du risque potentiel au moyen de la CRE ont été vérifiées en suivant une approche en deux étapes. La première étape consistait à ajuster la classification du risque de modéré ou élevé à faible pour les substances dont la vitesse d’émission dans l’eau après le traitement des eaux usées était estimée faible, représentant un faible potentiel d’exposition. La deuxième étape consistait à revoir les résultats de classification de faible potentiel de risque en utilisant des scénarios de risque relativement prudents à l’échelle locale (c.‑à‑d. dans la zone à proximité du point de rejet) conçus pour protéger l’environnement, afin de déterminer si la classification du risque devrait passée à un niveau supérieur.
La CRE est basée sur une approche pondérée afin de réduire au minimum le potentiel de surclassification ou de sous-classification du danger et de l’exposition, et du risque subséquent. Les approches équilibrées suivies pour traiter les incertitudes sont décrites en détail dans un document d’ECCC (2016a). Dans ce qui suit, nous décrivons deux des domaines d’incertitude les plus importants. Les erreurs dans les valeurs de toxicité aiguë empiriques ou modélisées pourraient conduire à des changements de la classification du danger, en particulier en ce qui a trait aux paramètres reposant sur les concentrations de résidus dans les tissus (c.-à-d. mode d’action toxique), dont de nombreux sont des valeurs prédites à partir de modèles (Q)SAR (Boîte à outils QSAR de l’OCDE 2014). Cependant, l’impact d’une telle erreur est atténué par le fait qu’une surestimation de la létalité médiane donnera une valeur prudente (protectrice) pour les résidus dans les tissus aux fins d’analyse des résidus corporels critiques (RCC). Une erreur de sous-estimation de la toxicité aiguë sera atténuée par le recours à d’autres paramètres de danger, comme le profilage structural du mode d’action, la réactivité et/ou l’affinité de liaison aux œstrogènes. Les changements ou les erreurs dans les quantités chimiques pourraient entraîner des classifications différentes de l’exposition, la classification de l’exposition et du risque étant grandement dépendantes de la vitesse d’émission et des quantités utilisées. Les classifications obtenues à l’aide de la CRE reflètent donc l’exposition et le risque au Canada, sur la base de ce qui est connu au sujet des quantités actuellement utilisées, mais pourraient ne pas refléter de futures tendances.
Les données et éléments critiques utilisés pour développer les profils spécifiques à la coumarine 1, ainsi que les résultats de la classification du danger, de l’exposition et du risque, sont présentés dans un document d’ECCC (2016b).
En se basant sur les classifications de faible danger et de faible exposition obtenues au moyen de la CRE, la coumarine 1 a été classée comme ayant un faible potentiel de risque pour l’environnement. Il est improbable que cette substance soit préoccupante pour l’environnement au Canada.
7. Potentiel d’effets nocifs sur la santé humaine
7.1 Évaluation de l’exposition
Milieux de l’environnement et aliments
Nous n’avons trouvé aucune donnée de surveillance empirique de la coumarine 1 dans l’air, l’eau ou le sol, au Canada ou ailleurs. Étant donné les propriétés physiques et chimiques de cette substance, et en particulier le fait que c’est un solide à température ambiante, ainsi que ses utilisations identifiées au Canada, il ne devrait pas y avoir de rejets dispersés de coumarine 1 dans l’air. Il n’existe aucune indication de la présence de coumarine 1 dans des aliments. La coumarine 1 n’est pas autorisée comme additif alimentaire, tout comme son utilisation dans de l’emballage alimentaire ou comme additif alimentaire fortuit (communication personnelle, courriel de la Direction des aliments de SC au BERSE de SC, octobre 2018; non référencé). En conséquence, il ne devrait pas y avoir d’exposition à cette substance due aux aliments.
Étant donné l’absence de données de surveillance de la coumarine 1 dans l’eau potable ou des eaux de surface au Canada, nous avons utilisé un scénario de rejet industriel basé sur les Environmental Assessment Unit Drinking Water Spreadsheets (Santé Canada 2015a) pour estimer la concentration de coumarine 1 dans des eaux de surface, en remplacement de l’eau potable. Nous avons utilisé comme comme intrants l’utilisation annuelle totale correspondant à la quantité maximale importée rapportée lors d’une enquête menée en vertu de l’article 71 de la LCPE (10 000 kg), le taux d’élimination dans les usines de traitement des eaux usées de 16 % (ECCC 2016b) et un taux maximal de perte dans les rejets d’eaux usées de 1 % (Santé Canada 2015a). La concentration résultante dans les eaux de surface estimée de manière prudente était de 0,18 µg/L. Cette concentration a été utilisée pour estimer l’exposition de la population générale du Canada à la coumarine 1 due à l’eau potable.
L’absorption journalière potentielle de coumarine 1 estimée par la population générale du Canada due à l’eau potable allait de 0,003 µg/kg pc/jour pour les 14-18 ans à 0,02 µg/kg pc/jour pour les nourrissons nourris au lait maternisé (voir le tableau C-1 de l’Annexe C).
Produits disponibles pour les consommateurs
D’après les déclarations faites à Santé Canada en vertu du Règlement sur les cosmétiques, la coumarine 1 est utilisée dans certains produits cosmétiques au Canada, tels que des colorants capillaires temporaires, des vernis à ongles, du maquillage pour le corps et le visage (y compris pour les yeux et les lèvres), à des concentrations allant de 0,1 à 10 % (communication personnelle, courriels de la DSPCPD de SC au BERSE de SC, datés d’octobre 2018 à mai 2019; non référencé). De plus, la coumarine 1 peut être présente dans des produits de nettoyage pour tapis (CPID c2001-2019, RB c2012-2019, FSS 2015), avec des expositions potentielles pendant et après l’application.
Aucune donnée sur l’absorption dermique de la coumarine 1 n’a été trouvée. Il existe des études sur l’absorption dermique, in vitro et in vivo, de l’analogue coumarine. Elles indiquent que l’absorption se situe dans la gamme allant d’environ 45 à 98 %, selon le vecteur utilisé (Beckley-Kartey et al. 1997, Yourick et al. 1997, Minghetti et al. 2000, Ford et al. 2001). En se basant sur ces renseignements, il a été assumé que l’absorption dermique de la coumarine 1 était de 100 %. Des expositions par voie dermique et orale ont été calculées. Nous les présentons dans le tableau 7-1. Veuillez consulter l’Annexe D pour obtenir des détails sur les paramètres utilisés.
| Scénario d’exposition | Concentration maximale (%) | Exposition estimée |
|---|---|---|
| Vernis à ongles – 2 couches (dermique)b – 2-3 ans | 2a | 0,08 mg/kg pc/événement |
| Vernis à ongles – 2 couches (dermique)b – 14-18 ans | 2a | 0,052 mg/kg pc/événement |
| Vernis à ongles – 2 couches (dermique)b – 19 ans ou plus | 2a | 0,043 mg/kg pc/événement |
| Colorant capillaire temposraire en poudre (dermique)b – 2-3 ans | 0,5a | 0,06 mg/kg pc/événement |
| Colorant capillaire temposraire en poudre (dermique)b – 19 ans ou plus | 0,5a | 0,012 mg/kg pc/événement |
| Maquillage pour le visage (dermique)– 4-8 ans | 0,3a | 0,044 mg/kg pc/événement |
| Maquillage pour le visage (dermique)– 19 ans ou plus | 0,3a | 0,026 mg/kg pc/jour |
| Maquillage pour le corps (dermique)e – 4-8 ans | 0,3a | 0,27 mg/kg pc/événement |
| Maquillage pour le corps (dermique)e – 19 ans ou plus | 0,3a | 0,17 mg/kg pc/événement |
| Rouge/brillant à lèvres (orale)f – 2-3 ans | 1a | 0,015 mg/kg pc/événement |
| Rouge/brillant à lèvres (orale)f – 14‑18 ans | 1a | 0,0089 mg/kg pc/jour |
| Rouge/brillant à lèvres (orale)f – 19 ans ou plus | 1a | 0,0059 mg/kg pc/jour |
| Application de nettoyant pour tapis (dermique)b – 19 ans ou plus | 0,01d | 0,002 mg/kg pc/événement |
| Après application de nettoyant pour tapis (dermique due au fait e ramper sur le sol) – 6-11 mois | 0,01d | 0,0036 mg/kg pc/jour |
| Après application de nettoyant pour tapis (orale due à la mise en bouche d’objet) – 6-11 mois | 0,01d | 0,00077 mg/kg pc/jour |
| Après application de nettoyant pour tapis (orale et dermique combinées)– 6-11 mois | 0,01d | 0,00437 mg/kg pc/jour |
a Communication personnelle, courriels de la DSPCPD de SC au BERSE de SC, octobre 2018; non référencé.
b Les expositions par inhalation estimées n’étaient pas significatives en comparaison de celles par voie dermique.
c Absorption dermique de 100 % assumée.
d FSS 2015.
e Produit spécial qui serait utilisé occasionnelement sur le visage et/ou le corps.
f Produit spécialisé qui serait utilisé occasionnelement. On assume que le produit peut être réappliqué jusqu’à 2,5 fois par jour pour les 14-18 ans et jusqu’à 2 fois pour les adultes
7.2 Évalaution des effets sur la santé
Des données limitées sur le danger spécifique à la coumarine 1 ont été identifiées. Aucune étude sur la cancérogénicité ou la toxicité pour la reproduction/développement n’a été trouvée. Les données sur les effets sur la santé d’analogues ont donc été utilisées pour l’évaluation de la coumarine 1. Des analogues ont été retenus en fonction de la similarité de leurs propriétés physiques et chimiques, de leur métabolisme et de leur structure. Les données spécifiques de la substance seront présentées en premier, suivies de celles sur l’analogue utilisées pour éclairer la caractérisation des effets sur la santé de la coumarine 1.
La coumarine 1 a fait l’objet d’un examen dans le cadre de celui des coumarines réalisé par le National Industrial Chemicals Notification and Assessment Scheme (NICNAS) de l’Australie (2016). Un dossier d’enregistrement soumis à l’ECHA (ECHA c2007-2019) est également disponible pour la coumarine 1.
Lors d’une étude limitée, aucun signe de toxicité systémique n’a été observé suite à une application topique de coumarine 1 chez des lapins (Thomann et Krüger 1975).
Une étude limitée de 14 semaines par voie orale à dose répétée avec des rats est présentée dans le dossier de l’ECHA sur la coumarine 1. Toutefois, il est indiqué que les résultats de cette étude ne pouvaient pas être interprétés en raison des limites du rapport (ECHA c2007-2019).
En ce qui concerne la génotoxicité, la coumarine 1 a donné des résutats négatifs lors d’un test Ames avec ou sans activation métabolique (NICNAS 2016). Des résultats négatifs ont aussi été obtenus lors d’un test in vitro de mutation génétique de fibroblasts pulmonaires d’hamsters chinois (V79) avec l’hypoxanthine-guanine phosphoribosyltransférase (HPRT) (ECHA c2007-2019).
Aucune étude sur les effets de la coumarine 1 dus à une exposition chronique n’a été trouvée. La 6-méthylcoumarine (no CAS 92-48-8) est l’analogue le plus proche sur lequel nous avons trouvé des données sur la toxicité chronique.
La 6-méthylcoumarine et la coumarine 1 contiennent toutes deux un squelette de coumarine, constitué de deux cycles à 6 atomes fusionnés : un cycle benzénique et une lactone insaturé en positions α et β. La coumarine 1 comporte aussi un groupe méthyle en position 4 et un groupe diéthylamino en position 7. Pour ce qui est des propriétés physico-chimiques, la coumarine 1 et la 6-méthylcoumarine ont des masses moléculaires (respectivement de 231 et 160 g/mol), des points de fusion (72 à 75 et 76,5 ºC respectivement), des points d’ébullition (240 et 304 ºC respectivement) et des log Koe (3,22 et 2,06) similaires. Toutefois, la coumarine 1 et la 6-méthylcoumarine ont des solubilités dans l’eau (53,28 et 1189 mg/L respectivement) et des pressions de vapeur (0,00257 et 0,068 respectivement) qui diffèrent de plus ordres de grandeur (Annexe B).
D’après leur structure chimique, il est probable que la 6-méthylcoumarine et la coumarine 1 soient métabolisées en suivant une voie de 7-hydroxylation. La coumarine est quant à elle métabolisée en suivant une voie de 3,4-époxydation (Lake 1999). Bien que la coumarine ait aussi été prise en compte comme analogue quand il existait des lacunes dans les données, la 6-méthylcoumarine a été utilisée pour éclairer la caractérisation des effets sur la santé suite à des expositions à plus long terme, y compris pour la cancérogénicité.
La 6-méthylcoumarine a fait l’objet d’un examen au niveau international par le Comité mixte FAO/OMS d’experts des additifs alimentaires (JECFA 2004) et par l’Autorité européenne de la sécurité des aliments (EFSA 2019). Ces travaux ont été utilisés pour éclairer la section sur l’évaluation des effets sur la santé.
Lors d’une étude de 13 semaines à dose répétée, des souris B6C3F1 (10/sexe/dose) ont reçu par gavage de la 6-méthylcoumarine à raison de 0, 50, 100, 200, 400 ou 800 mg/kg pc/jour. Au cours de cette étude, une souris ayant reçu la dose 400 mg/kg pc/jour est morte. À la dose la plus élevée, 3 souris sont mortes et il a été rapporté une prostration, de la bradycardie, une bradypnée, une hypoactivité, une hypothermie et une perte du reflexe de préhension. Il n’a été observé aucune modification significative du poids du corps ou des organes ni aucun signe significatif lors d’examens cliniques, macroscopiques et microscopiques à aucune de autres doses testées (NTP 2002, cité dans JECFA 2004).
Lors d’une autre étude de 13 semaines à dose répétée, des rats F344/N (10/sexe/dose) ont reçu par gavage de la 6-méthylcoumarine à raison de 0, 75, 150, 300, 600 ou 1200 mg/kg pc/jour. Pendant la première semaine de l’étude, un rat ayant reçu la dose de 600 mg/kg pc/jour et tous les rats ayant reçu la dose la plus élevée sont morts. À la nécropsie, des lésions hépatiques microscopiques ont été observées, avec divers degrés de congestion, de dégénération, de nécrose et d’hépatite. Chez les mâles et les femelles ayant reçu 600 ou 1200 mg/kg pc/jour, des effets cliniques ont été observés, y compris une hypoactivité, un larmoiement, une ataxie, un reflexe de redressement perturbé et un tonus des membres moindre. À 600 mg/kg pc/jour, il y avait chez les mâles et les femelles une diminution statistiquement significative du poids corporel la semaine 13. À 300 et 600 mg/kg pc/jour, il y avait une augmentation du poids moyen relatif et absolu du foie chez les mâles et les femelles et une diminution significative de l’activité de la cholinestérase sérique chez les femelles. Aucune autre modification des paramètres hématologiques, biochimiques du sérum ou urinaires n’a été observé à n’importe quelle dose. À 150 mg/kg pc/jour, aucun effet lié au traitement n’a été observé (NTP 2002, cité dans JECFA 2004).
Lors d’Une étude de 13 semaines à dose répétée, des rats mâles Sprague-Dawley ont été exposés dans leur alimentation à la 6-méthylcoumarine, à raison de 0,82 % (695 mg/kg pc/jour). Une vacuolisation des hépatocytes et un poids relatif du foie accru ont été rapportés. Il n’y avait aucune augmentation de l’activité de l’aminotransférase plasmatique, aucune hyperplasie du canal biliaire ni aucune cholangiofibrose (Lake et al. 1994, cité dans JECFA 2004 et NICNAS 2016).
Pour une étude de 14 semaines à dose répétée, des rats Osborne-Mendel ont été exposés à la 6-méthylcoumarine dans leur alimentation, à une concentration de 0, 1000 ou 10 000 ppm (calculée équivalente à 0, 100 ou 1000 mg/kg pc/jour). Aucun effet lié au traitement sur la santé générale, le comportement, le poids corporel, la consommation alimentaire, le poids des organes et aucune modification macroscopique ou microscopique des tissus ou lors d’un examen hématologique n’ont été observés à aucune des doses (Hagan et al. 1967, cité dans JECFA 2004).
Pour une étude de 2 ans à dose répétée, des rats Osborne-Mendel (25/sexe/groupe) ont été exposés à la 6-méthylcoumarine dans leur alimentation, à des concentrations correspondant à environ 0, 25, 50, 175, 375 ou 750 mg/kg pc/jour. Chez les mâles, il y avait une diminution modérée de la croissance et de la consommation alimentaire à la dose de 375 mg/kg pc/jour et une sévère diminution de la croissance à la dose de 750 mg/kg pc/jour. À la dose la plus élevée testée, une métamorphose graisseuse, une télangiectasie focale et une prolifération de canaux bilaires dans le foie ont été observées. Une atrophie testiculaire a été observée à 750 mg/kg pc/jour. Aucun autre effet lié au traitement, y compris la cancérogénicité, n’a été observé aux doses testées (Hagan et al. 1967, cité dans EFSA 2019).
En ce qui concerne la génotoxicité, la 6-méthylcoumarine a donné des résultats négatifs lors de deux tests Ames (avec et sans activation métabolique), des résultats équivoques lors d’un test Ames avec Salmonella typhimurium TA100 (avec activation métabolique) et des résultats négatifs (avec activation métabolique) lors d’une épreuve de lymphome de la souris (ESFA 2019). Lors d’études limitées in vivo, la 6‑méthylcoumarine a donné des résultats négatifs lors d’un test létal récessif lié au sexe avec Drosophila melanogaster par alimentation, d’un test de micronoyaux de la moelle osseuse de souris par gavage et lors d’un test de 90 jours de micronoyaux du sang périphérique de souris par injection intrapéritonéale (EFSA 2019). Les données disponibles indiquent que la 6-méthylcoumarine ne devrait pas être génotoxique (EFSA 2019).
Nous n’acons trouvé aucune étude sur la toxicité pour la reproduction/développement de la coumarine 1 ni de la 6-méthylcoumarine. En tant qu’approche prudente, nous avons utilisé la coumarine pour éclairer la caractérisation de la toxicité pour la reproduction/développement de la coumarine 1. Lors d’une étude, des souris NMRI gravides ont reçu 0, 0,05, 0,10 ou 0,25 % de coumarine (équivalent à 0, 75, 150 ou 375 mg/kg pc/jour) dans leur alimentation pendant les jours 6 à 17 de la gestation. À 375 mg/kg pc/jour, une augmentation des résorptions tardives, une augmentation du nombre de mortinaissance et une ossification retardée ont été observées. À toutes les doses, une mortalité accrue des petits jusqu’à un âge de 3 semaines a été observée (NICNAS 2016). Aux doses de 75, 150 et 375 mg/kg pc/jour, il y avait une augmentation significative de la mortalité totale (nombre de mortinaissances et de petits morts avant 3 semaines (Roll et Bär 1967). La DMENO a été établie à 75 mg/kg pc/jour, basée sur la mortalité accrue chez les petits de moins de 3 semaines.
Nous n’avons trouvé aucune étude sur la cancérogénicité de la coumarine 1. Tel que susmentionné, lors d’une étude de 2 ans à dose répétée avec des rats Osborne-Mendel exposés à de la 6-méthylcoumarine, aucun effet cancérogène n’a été rapporté jusqu’à une dose de 750 mg/kg pc/jous (Hagan et al. 1967, cité dans EFSA 2019). Il existe des preuves de cancérogénicité de la coumarine observées lors de tests sur des animaux (NTP 1993, cité dans NICNAS 2016). Néanmoins, les effets cancérigènes de la coumarine ont été liés à son métabolisme par la voie de 3,4-époxydation (EFSA 2008), alors que, d’après leur structure chimique, il est probable que la 6-méthylcoumarine et la coumarine 1 sont métabolisées par la voie de 7-hydroxylation (Lake 1999). En se basant sur les données disponibles, il est probable que la coumarine 1 n’est pas cancérigène.
7.3 Caractérisation du risque pour la santé humaine
L’exposition de la population générale du Canada à la coumarine 1 peut être due à sa présence dans l’eau potable, résultant de rejets ponctuels dans les eaux. Les Canadiens peuvent être exposés à la coumarine 1 lors de l’utilisation de produits cosmétiques comme des colorants capillaires temporaires, des vernis à ongles, du maquillage pour le corps ou le visage (y compris pour les yeux et les lèvres). La présence de coumarine 1 a aussi été rapportée dans un produit de nettoyage pour tapis, avec des expositions potentielles pouvant avoir lieu pendant et après l’application du produit.
En se basant sur les données disponibles sur la coumarine 1 et sur l’analogue 6‑méthylcoumarine, il est probable que la coumarine 1 n’est pas génotoxique ni cancérigène (NICNAS 2016, ECHA c2007-2019, EFSA 2019).
Étant donné la gravité des effets observés et l’absence d’études sur la toxicité pour la reproduction/développement de la coumarine 1 et de la 6-méthylcoumarine, une DMENO de 75 mg/kg pc/jour a été établie comme niveau d’effet critique pour la caractérisation du risque, basée sur une mortalité accrue chez les petits de moins de 3 semaines observée lors d’une étude sur la toxicité pour la reproduction/développement réalisée avec la coumarine, un analogue de la coumarine 1.
Nous donnons dans le tableau 7‑2 toutes les valeurs pertinentes de l’exposition et du danger pour la coumarine 1, ainsi que les marges d’exposition correspondantes pour la détermination du risque.
| Scénario d’exposition | Exposition estimée | Niveau d’effet critique | ME |
|---|---|---|---|
| Eau potable | 2,4E-5 mg/kg pc/jour | DMENO = 75 mg/kg pc/jour | 3 125 000 |
| Vernis à ongles – 2 couches (dermique)– 2 à 19 ans et plus | 0,043–0,08 mg/kg pc/événement | DMENO = 75 mg/kg pc/jour | 937–1744 |
| Colorant capillaire temporaire en poudre (dermique)– 2 à 19 ans et plus | 0,012–0,06mg/kg pc/événement | DMENO = 75 mg/kg pc/jour | 1250–6250 |
| Maquillage pour le visage (dermique)– 4 à 19 ans et plus | 0,026–0,044 mg/kg pc/jour | DMENO = 75 mg/kg pc/jour | 1704–2884 |
| Maquillage pour le corps (dermique)a– 4 à 19 ans et plus | 0,17–0,27 mg/kg pc/événement | DMENO = 75 mg/kg pc/jour | 280–447 |
| Rouge/brillant à lèvres (orale)– 2 à 19 ans et plus | 0,0089–0,015 mg/kg pc/événement | DMENO = 75 mg/kg pc/jour | 5000–8427 |
| Pendant l’application de nettoyant pour tapis (dermique)– 19 ans et plus | 0,002 mg/kg pc/événement | DMENO = 75 mg/kg pc/jour | 37 500 |
| Après l’application de nettoyant pour tapis (orale et dermique combinées)– 6-11 mois | 0,00437 mg/kg pc/jour | DMENO = 75 mg/kg pc/jour | 17 162 |
a Préduit spécial qui serait utilisé occasionnellement sur le visage ou le corps
Les ME calculées pour les milieux de l’environnement, les vernis à ongles, les colorants capillaires temporaires en poudre, le maquillage pour le visage, le rouge/brillant à lèvres et le nettoyant pour tapis sont jugées adéquates pour tenir compte des incertitudes des bases de données sur les effets sur la santé et l’exposition. Toutefois, les ME pour le maquillage pour le corps sont jugées potentiellement inadéquates pour tenir compte des incertitudes des bases de données sur les effets sur la santé et l’exposition.
7.4 Incertitudes de l’évaluation du risque pour la santé humaine
Les sources clés d’incertitude sont présentées dans le tableau ci-après.
| Source clé d’incertitude | Impact |
|---|---|
| Les données sur l’absorption dermique de la coumarine 1 sont indisponibles. En conséquence, les données sur l’analogue coumarine ont été prises en compte et assumées équivalentes à l’absorption par voie orale. | + |
| Il n’existe aucune donnée de surveillance de la coumarine 1 dans l’environnement. | +/- |
| Il n’y a pas de donnée sur la toxicité chronique de la coumarine 1 et des renseignements limités sur l’analogue 6-méthylcoumarine. | +/- |
| Il existe une incertitude quant à l’utilisation d’une approche de lecture croisée et à l’extrapolation des données sur la coumarine pour la coumarine 1 pour la toxicité pour la reproduction/développement. | +/- |
+ = incertitude avec potentiel de surestimation de l’exposition/risque; - = incertitude avec potentiel de sous‑estimation de l’exposition/risque; +/- = potentiel inconnu de surestimation ou de sous‑estimation du risque.
8. Conclusion
Compte tenu de tous les éléments de preuve avancés dans la présente ébauche d’évaluation préalable, le risque d’effets nocifs de la coumarine 1 sur l’environnement est faible. Il est conclu que la coumarine 1 ne satisfait à aucun des critères de l’alinéa 64(a) ou 64(b) de la LCPE, car elle ne pénètre pas dans l’environnement en une quantité ou concentration ni dans des conditions qui ont ou peuvent avoir un effet nocif immédiat ou à long terme sur l’environnement ou sa diversité biologique ou qui constituent ou peuvent constituer un danger pour l’environnement essentiel à la vie.
En se basant sur les renseignements présentés dans la présente ébauche d’évaluation préalable, il est conclu que la coumarine 1 satisfait aux critères de l’alinéa 64(c) de la LCPE, car elle pénètre dans l’environnement en une quantité ou concentration ou dans des conditions qui constituent ou peuvent constituer un danger au Canada pour la santé ou la vie humaine.
Il est donc conclu que la coumarine 1 satisfait à un ou plusieurs des critères de l’article 64 de la LCPE.
Il est également conclu que la coumarine 1 satisfait aux critères de persistance, mais pas à ceux de bioaccumulation, du Règlement sur la persistance et la bioaccumulation de la LCPE.
Références
Beckley-Kartey S.A.J., Hotchkiss S.A.M. et Capel M.; 1997; Comparative in vitro skin absorption and metabolism of coumarin (1,2-benzopyrone) in human, rat and mouse; Toxicol. Appl. Pharmacol., 145, p. 34-42 (disponible en anglais seulement).
Boîte à outils QSAR de l’OCDE; 2014; version 3.3; Paris (France) : Organisation de coopération et de développement économiques, Laboratoire de chimie mathématique (disponible en anglais seulement).
Bremmer H.F., Prud’homme de Lodder L.C.H. et van Engelen J.G.M.; 2006; Cosmetics Fact Sheet [PDF]; RIVM Report 320104001/2006 (disponible en anglais seulement).
Canada; 1999; Loi canadienne sur la protection de l’environnement (1999), L.C. 1999, ch.33; Gazette du Canada, Partie III, vol. 22, no 3.
Canada, ministère de l’Environnement; 2012; Loi canadienne sur la protection de l’environnement (1999), Avis concernant certaines substances de la Liste intérieure [PDF]; Gazette du Canada, Partie I, vol. 146, no 48, Supplément.
ChemCAN [level III fugacity model of 24 regions of Canada]; 2003; version 6.00; Peterborough (ON) : Université Trent, Canadian Centre for Environmental Modelling and Chemistry (disponible en anglais seulement).
ChemIDplus [base de données]; 1993- ; Bethesda (MD) : US National Library of Medicine [consultée le 28 août 2018] (disponible en anglais seulement).
ChemSpider [base de données]; 2015; Search results for CAS RN 91-44-1; Londres (R.-U.) : Royal Society of Chemistry [consultée le 3 mai 2019] (disponible en anglais seulement).
[ConsExpo Web] Consumer Exposure Web Model; 2016; Bilthoven (Pays-Bas) : Rijksinstituut voor Volksgezondheid en Milieu [Institut nationalpour la santé publique et l’environnement] (disponible en anglais seulement).
[CPID] Consumer Product Information Database USA and Canada; c2001-2019; Resolve Professional Carpet Extraction Cleaner, Professional Use [consulté en mai 2019] (disponible en anglais seulement).
[ECCC] Environnement et Changement climatique Canada; 2016a; Document sur l’approche scientifique : classification du risque écologique des substances organiques; Ottawa (ON) : gouvernement du Canada.
[ECCC] Environnement et Changement climatique Canada; 2016b; Supporting documentation: data used to create substance-specific hazard and exposure profiles and assign risk classifications; Gatineau (QC) : ECCC; Information in support of the science approach document: ecological risk classification of organic substances; disponible à substances@ec.gc.ca (disponible en anglais seulement).
[ECCC, SC] Environnement et Changement climatique Canada, Santé Canada; [modifié le 12 mars 2017]; Catégorisation des substances chimiques; Ottawa (ON) : gouvernement du Canada [consulté le 30 avril 2019].
[ECHA] Agence européenne des produits chimiques; c2007-2019; Registered substances database; search results for CAS RN 91-44-1; Helsinki (Finlande) : ECHA [consulté le 30 avril 2019] (disponible en anglais seulement).
[EFSA] Autorité européenne pour la sécurité des aliments; 2008; Coumarin in flavourings and other food ingredients with flavouring properties - Scientific Opinion of the Panel on Food Additives, Flavourings, Processing Aids and Materials in Contact with Food (AFC) (disponible en anglais seulement).
[EFSA] Autorité européenne pour la sécurité des aliments; 2019; Scientific Opinion on Flavouring Group Evaluation 217 Revision 2 (FGE.217Rev2), consideration of genotoxic potential for α,β‐unsaturated ketones and precursors from chemical subgroup 4.1 of FGE.19: lactones; EFSA Journal, volume 17: Issue 1 (disponible en anglais seulement).
Environnement Canada; 2013; Données de la mise à jour de l’Inventaire de la LIS recueillies en vertu de l’article 71 de la Loi canadienne sur la protection de l’environnement 1999 : Avis concernant certaines substances de la Liste intérieure; Données préparées par : Environnement Canada, Santé Canada; Programme des substances existantes.
[EPA] Environmental Protection Agency des États-Unis; 2011; Chapter 6: Inhalation Rates. Exposure Factors Handbook 2011 Edition (Final); U.S. Environmental Protection Agency : Washington, DC; EPA/600/R-09/052F (disponible en anglais seulement).
[EPA] Environmental Protection Agency des États-Unis; 2012; Standard Operating Procedures for Residential Pesticide Exposure Assessment [PDF]; Washington (DC) : Health Effects Division, Office of Pesticide Programs, Office of Chemical Safety and Pollution Prevention (disponible en anglais seulement).
[EPI Suite] Estimation Program Interface Suite for Microsoft Windows [modèle d’estimation]; c2000-2012; ver. 4.11; Washington (DC) : US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY): Syracuse Research Corporation (disponible en anglais seulement).
Ficheux A.S., Morriset T., Chevillotte G., Postic C. et Roudot A.C.; 2014; Probabilistic assessment of exposure to nail cosmetics in French consumers; Food Chem. Toxicol., 66, p. 36-43 (disponible en anglais seulement).
Ficheux A.S., Chevillotte G., Wesolek N., Morisset T., Dornic N., Bernard A., Bertho A., Romanet A., Leroy L., Mercat A.C., Creusot T., Simon E. et Roudot A.C.; 2016; Consumption of cosmetic products by the French population second part: Amount data; Food Chem. Toxicol., 90, p. 130-141 (disponible en anglais seulement).
Ford R.A., Hawkins D.R., Mayo B.C. et Api A.M.; 2001; The in vivo dermal absorption and metabolism of [4-14C] coumarin by rats and by human volunteers under simulated conditions of use in fragrances; Food Chem. Toxicol., 39(2), p. 153-62 (disponible en anglais seulement).
[FSS] Fiche signalétique de sécurité; 2015; Electrolux Pet Stain & Odor W/BS2X with Baking Soda [PDF]; Michigan City (IN) : Fas-Pak [consulté en juin 2019] (disponible en anglais seulement).
[FSS] Fiche signalétique de sécurité; 2019; 7-Diethylamino-4-methylcoumarin [PDF]; Lancashire (R.-U.) : Thermo Fisher Scientific [consulté le 3 mai 2019] (disponible en anglais seulement).
Garcia-Hidalgo E., von Goetz N., Siegrist M. et Hungerbühle K.; 2017; Use-patterns of personal care and household cleaning products in Switzerland; Food Chem. Toxicol., 99, p. 24-39 (disponible en anglais seulement).
Hagan E.C., Hansen W.H., Fitzhugh O.G., Jenner P.M., Jones W.I., Taylor J.M., Long E.L., Nelson A.A. et Brouwer J.B.; 1967; Food flavourings and compounds of related structure. II.Subacute and chronic toxicity; Food Cosmet. Toxicol., 5(2), p. 141-57 (disponible en anglais seulement).
[HCPA] Household & Commercial Products Association; 2019; Consumer Product Ingredients Database: Diethylaminomethylcoumarin [Internet]; Washington (DC) : États-Unis (disponible en anglais seulement).
[JECFA] Comité mixte FAO/OMS d’experts des additifs alimentaires; 2004; Safety evaluation of certain food additives and contaminants prepared by the sixty-first meeting of the Joint FAO/WHO Expert Committee on Food Additives; WHO Food Additives Series No. 52 (disponible en anglais seulement).
Lake B.G.; 1999; Coumarin metabolism, toxicity and carcinogenicity: relevance for human risk assessment; Food Chem. Toxicol., 1999(4), p. 423-53 (disponible en anglais seulement).
Landeg S., Kirby A., Lee S., Bartlett F., Titmarsh K., Donovan E., Griffin C., Gothard L., Locke I. et McNair H.; 2016; A randomized control trial evaluating fluorescent ink versus dark ink tattoos for breast radiotherapy; Br. J. Radiol. [consulté en mai 2019] (disponible en anglais seulement).
Loretz L., Api A.M., Barraj L., Burdick J., Davis D.A., Dressler W., Gilberti E., Jarrett G., Mann S., Pan Y.H.L., Re T., Renskers K., Scrafford C. et Vater S.; 2006; Exposure data for personal care products: Hairspray, spray perfume, liquid foundation, shampoo, body wash, and solid antiperspirant; Food Chem. Toxicol., 44, p. 2008-2018 (disponible en anglais seulement).
Minghetti P., Casiraghi A., Cilurzo F. et Montanari L.; 2000; Development of local patches containing melilot extract and ex vivo–in vivo evaluation of skin permeation; Eur. J. Pharm. Sci., 10(2), p. 111-117 (disponible en anglais seulement).
[NICNAS] National Industrial Chemicals Notification and Assessment Scheme; 2016; Coumarins: Human health tier II assessment; gouvernement de l’Australie, ministère de la Santé [consulté en avril 2019] (disponible en anglais seulement).
Piccinini P., Contor L., Pakalin S., Raemaekers T. et Senaldi C.; 2015; Safety of tattoos and permanent make-up. State of play and trends in tattoo practices; Report on Work Package 2. Administrative Arrangement N. 2014-33617. Analysis conducted on behalf of DG JUST. Piccinini P, Contor L, Pakalin S, Raemaekers T, Senaldi C. JRC Technical Reports. Report EUR 27528. European Commission, 2015 (disponible en anglais seulement).
RB Professional Resolve Carpet Extraction Cleaner [Internet]; c2012-2019; [consulté en mai 2019] (disponible en anglais seulement).
[RIVM] Rijksinstituut voor Volksgezondheid en Milieu [Institut national pour la santé publique et l’environnement]; 2006; Cosmetics fact sheet: to assess the risks for the consumer: updated version for ConsExpo 4 [PDF]; Bilthoven (Pays-Bas) : RIVM, rapport no 320104001/2006 [consulté en mai 2019] (disponible en anglais seulement).
[RIVM] Rijksinstituut voor Volksgezondheid en Milieu [Institut national pour la santé publique et l’environnement]; 2018; Cleaning products fact sheet: default parameters for estimating consumer exposure – updated version 2018; Bilthoven (Pays-Bas) : RIVM, rapport no 2016-0179 [consulté en mai 2019] (disponible en anglais seulement).
Roll R. et Bär F.; 1967; Effect of coumarin (o-hydroxyeinnamic acid-lactone) on pregnant female mice; Arzneimittelforschung, 1, p. 97-100, en allemand.
Santé Canada; 1998; Exposure factors for assessing total daily intake of priority substances by the general population of Canada; rapport non publié; Ottawa (ON) : gouvernement du Canada (disponible en anglais seulement).
Santé Canada; 2015a; Environmental Assessment Unit Drinking Water Spreadsheets [Excel format]; Ottawa (ON) : Santé Canada (disponible en anglais seulement).
Santé Canada; 2015b; Food Consumption Table derived from Statistics Canada, Canadian Community Health Survey, Cycle 2.2, Nutrition (2004), Share file; Ottawa (disponible en anglais seulement).
Santé Canada; 2017; Water Consumption Table derived from Statistics Canada, Canadian Community Health Survey, Cycle 2.2, Nutrition (2004), Share file; Ottawa (disponible en anglais seulement).
Santé Canada; 2018; Draft backgrounder document on default values for breast milk and formula intakes; rapport non publié; Ottawa (ON) : gouvernement du Canada (disponible en anglais seulement).
Thomann P. et Krüger L.; 1975; Acute oral, dermal, and inhalation studies; Environ. Qual. Saf. Suppl., 4, p. 193-8 (disponible en anglais seulement).
Vocanson M., Valeyrie M., Rozières A., Hennino A., Floc'h F., Gard A. et Nicolas J.F.; 2007; Lack of evidence for allergenic properties of coumarin in a fragrance allergy mouse model; Contact Dermatitis, 6, p. 361-4 (disponible en anglais seulement).
Yourick J.J. et Bronaugh R.L.; 1997; Percutaneous absorption and metabolism of coumarin in human and rat skin; J. Appl. Toxicol., 13(3), p. 153-158 (disponible en anglais seulement).
Annexe A – Approche de lecture croisée
| Élément pris en compte | Justification |
|---|---|
1. Structure chimique. L’emphase est mis sur des analogues ayant un squelette de coumarine, squelette constitué de deux cycles à 6 atomes fusionnés : un cycle benzénique et une lactone insaturée en positions α et β. | Les analogues qui ont des structures chimiques similaires devraient avoir des profils de toxicité similaires. |
2. Métabolites similaires (prédits ou observés). | Les analogues qui sont métabolisés par des voies similaires en produits de dégradation similaires devraient avoir des profils de toxicité similaires. |
3. Alertes structurales communes. | Les analogues ayant des alertes structurales similaires devraient avoir une similarité plus grande en terme de toxicité. |
4. Propriétés physico-chimiques similaires. L’emplase a été placé sur les structures chimiques ayant une masse moléculaire, une solubilité dans l’eau, une pression de vapeur et un Koe similaires. | Les analogues ayant des propriétés physico-chimiques similaires peuvent potentiellement avoir des profils toxicologiques similaires. |
Annexe B – Résumé du danger de la coumarine 1 et de la 6‑méthylcoumarine
| Nom chimique | Coumarine 1 | 6-Méthylcoumarine | Coumarine |
|---|---|---|---|
| Rôle | Substance visée | Analogue | Analogue |
| No CAS | 91-44-1 | 92-48-8 | 91-64-5 |
| Structure chimique | 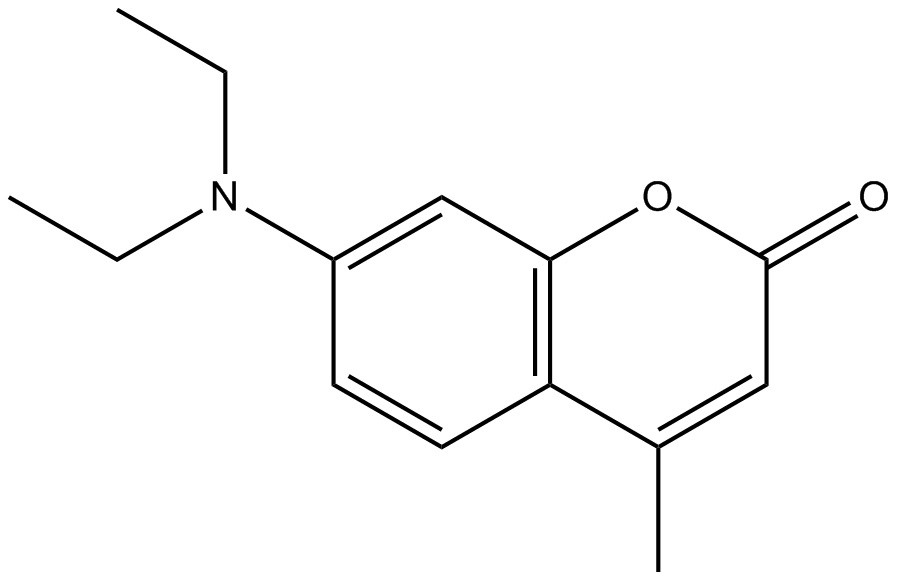 | 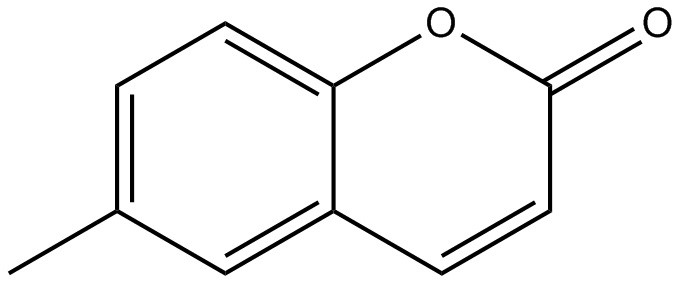 | 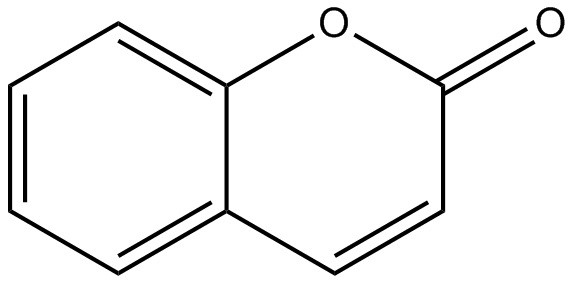 |
| Masse moléculaire (g/mol) | 231,290 (ChemIDplus 1993- ) | 160,172 (ChemIDplus 1993- ) | 146,144 (ChemIDplus 1993- ) |
| Point de fusion (ºC) | 72–75 (Epi Suite c2000-2012) | 76,5 (ChemIDplus 1993- ) | 71 (ChemIDplus 1993- ) |
| Point d’ébullition (ºC) | 240 (ChemSpider 2015) | 304 (ChemIDplus 1993- ) | 301,7 (ChemIDplus 1993- ) |
| Pression de vapeur (Pa) | 0,00257 (Epi Suite c2000-2012) | 0,068 (Epi Suite c2000-2012) | 0,087 (Epi Suite c2000-2012) |
| Solubilité dans l’eau (mg/L) | 53,28 à 25 °C (Epi Suite c2000-2012) | 1189 à 25 °C (Epi Suite c2000-2012) | 5126 à 25 °C (Epi Suite c2000-2012) |
| log Koe (sans dimension) | 3,22 (Epi Suite c2000-2012) | 2,060 (Epi Suite c2000-2012) | 1,51 (Epi Suite c2000-2012) |
| Toxicité aiguë (orale) | DL50 : 5000 mg/kg pc chez le rat et 1780 mg/kg pc chez la souris (NICNAS 2016) | DL50 : 1680 mg/kg pc chez le rat (NICNAS 2016) | DL50 : 290–680 mg/kg pc chez diverses souches de rat; 196‑780 mg/kg pc chez diverses souches de souris (NICNAS 2016) |
| Sensibilisation cutanée | Lors d’un test de maximisation sur des cobayes femelles, la coumarine s’est avérée non sensibilisante (ECHA c2007-2019).Lors d’un test épicutané limité chez des humains, il n’y a eu aucune réaction positive (ECHA c2007-2019). | Aucune preuve de potentiel photoallergène chez les cobayes et les humains (NIC NAS 2016).Lors d’un test de maximisation avec des humains, il n’y a eu aucune réaction cutanée après exposition des volontaires à de la 6‑méthylcoumarine à 4 % dans du pétrolatum (NICNAS 2006). | Aucun potentiel de sensibilisation cutanée (SCCP 2005, cité dans NICNAS 2016). La coumarine pure a de très faibles capacités de sensibilisation (Vocanson et al. 2007). |
| Toxicité sous-chronique à dose répétée (orale) | Étude par voie orale avec des rats (14 semaines) : Étude limitée décrite dans la section sur l’évaluation des effets sur la santé(ECHA c2007-2019) | Étude par gavage avec des rats (13 semaines) :DMENO = 150 mg/kg pc/jour, basée sur une diminution significative de l’activité de la cholinesterase sérique chez les femelles et une augmentation du poids moyen relatif ou absolu chez les deux sexes à la dose suivante (NTP 2002, cité dans JECFA 2004). Étude par voie orale avec des rats (13 semaines) :695 mg/kg pc = légère vacuolation des hépatocytes (Lake et al. 1994, cité dans JECFA 2004). Étude par voie orale avec des rats (14 semaines) : DMENO = 1000 mg/kg pc/jour (dose la plus élevée testée) (Hagan et al. 1967, cité dans JECFA 2004). | Étude par gavage avec des rats (13 semaines) : DMENO = 75 mg/kg pc/jour, basée sur une dégénération hépatocellulaire centrilobulaire et une nécrose accompagnée d’une inflammation active chronique et d’une hyperplasie des canaux bilaires à la dose suivante (150 mg/kg pc/jour) (NTP 1993, cité dans NICNAS 2016). |
| Étude sur la toxicité à long terme à dose répétée (orale) | ND | Étude par voie orale avec des rats (2 ans) : DMENo = 250 mg/kg pc/jour, basée sur une dépression modérée de la croissance à la dose suivante (Hagan et al. 1967). | Étude par gavage avec des rats (2 ans) :DMENO = 25 mg/kg pc/jour, basée sur des lésions au foie, aux reins et au préestomac (NTP 1993). |
| Toxicité pour la reproduction/développement (orale) | ND | Étude par voie orale avec des rats (2 ans) :Aucun effet lié au traitement observé sur les testicules (Hagan et al. 1967). | Étude par voie orale avec des souris (jours 6 à 17) :DMENO = 75 mg/kg pc/jour, basée sur une mortalité accrue jusqu’à 3 semaines d’âge (Roll et Bär 1967). |
| Toxicité génétique | Négative (NICNAS 2016) | Négative (EFSA 2019) | Négative (EFSA 2004) |
| Cancérogénicité (orale) | ND | Étude par voie orale avec des rats (2 ans) : Aucune cancérogénicité observée jusqu’à 750 mg/kg pc/jour (EFSA 2019). | Étude par gavage avec des rats et des souris (2 ans) :DMENO = 50 mg/kg pc/jour, basée sur des incidences accrues d’adénomes des tubules rénales chez les rats mâles; incidences accrues d’adénomes alvéolaires/bronchiolaires, de carcinomes alvéolaires/bronchiolaires et d’adénomes hépatocellulaires chez les souris femelles (NTP 1993, cité dans NICNAS 2016). |
Abréviation : ND = non disponible
Annexe C – Absoption journalière estimée pour divers groupes d’âge de la population générale du Canada
| Voie d’exposition | 0-5 moisa(nourris au sein)b | 0-5 moisa (nourris au lait maternisé)c | 6-11 moid | 1 ane | 2-3 ansf | 4-8 ansg | 9-13 ansh | 14-18 ansi | 19 ans et plusj |
|---|---|---|---|---|---|---|---|---|---|
| Eau potablek | N/A | 0,024 | 0,015 | 5,9E-3 | 5,2E-3 | 4,2E-3 | 3,2E-3 | 3,2E-3 | 3,7E-3 |
Abréviations : N/A = non applicable.
a En assumant peser 6,3 kg (Santé Canada 2015), respirer 3,7 m3 d.air par jour (EPA 2011 [modifié]), ingérer 21,6 mg de poussière par jour (Wilson et Meridian 2015 [modifié]). Il est assumé qu’il n’y a aucune ingestion de sol en raison des pratiques typiques des soignants.
b Exclusivement pour les nourrissons nourris au lait maternel, en assumant consommer 0,744 L de lait maternel par jour (Santé Canada 2018) et que le lait maternel est la seule source d’aliment.
c Exclusivement pour les nourrissons nourris avec du lait maternisé, en assumant boire 0,826 L d’eau par jour (Santé Canada 2018), cette eau étant utilisée pour reconstituer le lait. Voir la note de bas de page sur l’eau potable pour des détails.
d En assumant peser 9,1 kg (Santé Canada 2015), respirer 5,4 m3 d’air par jour (EPA 2011 [modifié]), boire 0 L d’eau par jour (Santé Canada 2017), ingérer 7,3 mg de sol par jour et 27,0 mg de poussière par jour (Wilson et Meridian 2015 [modifiéd]). Pour les bébés nourris au sein, assumant consommer 0,632 L de lait maternel par jour (Santé Canada 2018). Pour les bébés nourris au lait maternisé, en assumant boire 0,764 L d’eau par jour (Santé Canada 2018), cette eau étant utilisée pour reconstituer le lait. Voir la note de bas de page sur l’eau potable pour des détails.
e En assumant peser 11,0 kg (Santé Canada 2015), respirer 8,0 m3 d’air par jour (EPA 2011 [modifié]), boire 0,36 L d’eau par day (Santé Canada 2017), ingérer 8,8 mg de sol et 35,0 mg de poussière par jour (Wilson et Meridian 2015 [modifié]).
f En assumant peser 15 kg (Santé Canada 2015), respirer 9,2 m3 d’air par jour (EPA 2011 [modifié]), boire 0,43 L d’eau par jour (Santé Canada 2017), ingérer 6,2 mg de sol et 21,4 mg de poussière par jour (Wilson et Meridian 2015 [modifié]).
g En assumant peser 23 kg (Santé Canada 2015), respirer 11,1 m3 d’air par jour (EPA 2011 [modifié]), boire 0,53 L d’eau par jour (Santé Canada 2017), ingérer 8,7 mg de sol et 24,4 mg de poussière par jour (Wilson et Meridian 2015 [modifiéd]).
h En assumant peser 42 kg (Santé Canada 2015), respirer 13,9 m3 d’air par jour (EPA 2011 [modifié]), boire 0,74 L d’eau par jour (Santé Canada 2017), ingérer 6,9 mg de sol et 23,8 mg de poussière par jour (Wilson et Meridian 2015 [modifié]).
i En assumant peser 62 kg (Santé Canada 2015), respirer 15,9 m3 d’air par jour (EPA 2011 [modifié]), boire 1,09 L d’eau par jour (Santé Canada 2017), ingérer 1,4 mg de sol et 2,1 mg de poussière par jour (Wilson et Meridian 2015 [modifié]).
j En assumant peser 74 kg (Santé Canada 2015), respirer 15,1 m3 d’air par jour (EPA 2011 [modifié]), boire 1,53 L d’eau par jour (Santé Canada 2017), ingérer 1,6 mg de sol et 2,6 mg de poussière par jour (Wilson et Meridian 2015 [modifié]).
k Estimé à 0,18 µg/L en utilisant le NSACB EAU Drinking Water Spreadsheet (2003) et la limite supérieure des données sur les quantités (10 000 kg).
Annexe D – Paramètres utilisés pour estimer les expositions des humains dues aux produits disponibles pour les consommateurs
Les estimations d’exposition ont été faites en se basant sur des poids corporels par défaut de 6,3 kg (0-5 mois), 9,1 kg (6-11 mois), 11 kg (1 an), 15 kg (2-3 ans), 23 kg (4‑8 ans), 42 kg (9-13 ans), 62 kg (14-18 ans) et 74 kg (19 ans et plus) (Santé Canada 2015). Les expositions estimées par voie dermique et orale dues aux produits cosmétiques ainsi qu’au nettoyant pour tapis ont été faites en utilisant ConsExpo Web (2016). Les expositions à la coumarine 1 après l’application de nettoyant pour tapis ont été faites en utilisant la référence EPA 2012 pour les jeunes enfants. Les expositions estimées par inhalation pour tous les scénarios n’étaient pas significatives en comparaison de celles par voie dermique, elles n’ont donc pas été présentées. Les paramètres utilisés pour l’estimation des expositions sont décrits dans le tableau D-1.
| Scénario d’exposition | Hypothèsea,b |
|---|---|
Vernis à ongles (dermique) 2 couches de vernis appliquées sur les ongles des doigts et des orteils | Concentration maximale rapportée : 2 % (communication personnelle, courriels de la DSPCPD de SG au BERSE de SC, octobre 2018; non référencé) Quantité de produit sur la peau : 0,06 g/utilisation (2-3 ans), 0,16 g/utilisation (14-18 ans, 19 ans et plus) (modifié de Ficheux et al. 2014, ajusté par un facteur de 0,206 pour les adultes et de 0,205 pour les enfants pour tenir compte de la quantité de vernis qui finit sur la peau) |
Colorant cappilaire temposraire en poudre (dermique)c | Concentration maximale rapportée : 0,5 % (communication personnelle, courriels de la DSPCPD de SC au BERSE de SC, octobre 2018; non référencé) Charge : application instantanée Quantité de produit : 1,75 g (communication personnelle, courriels de la DSPCPD de SC au BERSE de SC, mai 2019; non référencé) Facteur de rétention : 0,1 |
Rouge/brillant à lèvresd (orale) | Concentration maximale rapportée : 1 % (communication personnelle, courriels de la DSPCPD de SC au BERSE de SC, octobre 2018; non référencé) Fréquence : 1/jour (2-3 ans), 2,5/jour (14-18 ans), 2/jour (19 ans et plus) Quantité ingérée : 0,022 g (Ficheux et al. 2016) |
Maquillage pour le visage (dermique) | Concentration maximale rapportée : 0,3 % (communication personnelle, courriels de la DSPCPD de SC au BERSE de SC, octobre 2018; non référencé) Scénario de maquillage pour le visage tiré de Cosmetic Fact Sheet (RIVM 2006), avec information supplémentaire sur la quantité appliquée Fréquence : < 1/jour (4-8 ans) (Garcia-Hidalgo et al. (2017) et jugement professionnel); 1,2/jour (19 ans et plus) (Loretz et al. 2006) Charge : application instantanée Quantité de produit : 0,34 g (4-8 ans), 0,54 g (19 ans et plus) (Loretz et al. (2006) |
Maquillage pour le corpse (dermique) | Concentration maximale rapportée : 0,3 % (communication personnelle de la DSPCPD de SC au BERSE de SC, octobre 2018; non référencé) Scénario d’hydratant pour le corps tiré de Cosmetics Fact Sheet (RIVM 2006), avec information supplémentaire sur la quantité appliquée Surface : 3393 cm2 (4-8 ans – pour le visage, les bras et 3/4 des jambes exposés), 7263 cm2 (19 ans et plus – pour le visage, les bras, 3/4 des jambes et la moitié du tronc exposés) Quantité de produit : 2,05 g (Ficheux et al. 2016, avec ajustement de la surface) (4-8 ans), 4,14 g (Ficheux et al. 2016, avec ajustement de la surface) (19 ans et plus) |
Application de nettoyant pour tapis (dermique) | Concentration : 0,01 % (FSS 2015) Groupe d’âges : 19 ans et plus Surface exposée : 2200 cm2 Charge : application instantanée Fraction massique de la substance : 0,01 % Quantité de produit : 1,5 g |
Après application de nettoyant pour tapis (dermique) | Concentration : 0,01 % (FSS 2015) Scénario basé sur EPA (2012), PEN résidentielles Absorption dermique = résidu en surface x concentration x efficacité du transfert sol-peau x coefficient de transfert x durée de l’exposition x (1 m2 / 10 000 cm2) x 1 000 000 µg/g / pc Groupe d’âge : 6-11 mois Résidu en surface : 9 g/m2 (basé sur la valeur par défaut de ConsExpo pour la quantité de nettoyant délogeable après l’application; RIVM 2018) Efficacité du transfert sol-peau : 0,06 (EPA 2012, valeur par défaut pour les tapis) Coefficient de transfert : 1528 cm2/h (EPA 2012, valeur par défaut de 1800 cm2/h pour les surfaces dures et les tapis ajustée pour la surface d’un enfant de 6-11 mois)f Durée de l’exposition : 4 h (EPA 2012, valeur par défaut pour les tapis) Facteurs de conversion : 1 m2 / 10 000 cm2, 1 000 000 µg/g |
Après application de nettoyant pour tapis (orale) | Concentration : 0,01 % (FSS 2015) Scénario basé sur EPA (2012) pour une absorption due au contact main-bouche Groupe d’âge : 6-11 mois Absorption due au contact main-bouche = charge de résidu sur les mains x surface mise en bouche x [durée de l’exposition x nombre d’intervales de recharge par heure] x [1- (1 – facteur d’extraction de la salive, 0.48)fréquence du contact main-bouche, 20 / nombre de recharges, 4] / pc Charge de résidu sur les mains (mg/cm2) : fraction de la substance sur les mains comparativement au résidu sur la surface totale tirée de l’étude de Jazzercise x dépôt dermique total calculé pour le scénario par voie dermique (mg/jour) / surface des deux mains. Il peut y avoir de légères différences dues aux arrondissements. Dépôt dermique : exposition dermique (mg/kg pc/jour) x pc =1,81 mg/kg pc/jour x 9,1 kg pc = 16,5 mg/jour Fraction de la substance sur les mains comparativement au résidu sur la surface totale tiré de l’étude de Jazzercise : 0,15 Surface des deux mains : 240 cm2 Surface mise en bouche : 22 cm2/événement Durée d’exposition : 4 h/jour Nombre d’intervlaes de recharge par heure : 4/h Facteur d’extraction de la salive : 0,48 Fréquence de la mise en bouche : 20/h Nombre de recharges : 4 |
a Les expositions aux cosmétiques ont été estimées en utilisant ConsExpo Web (2016).
b Sauf indication contraire, les valeurs par défaut proviennent du ConsExpo Fact Sheet pertinent pour le scénario présenté.
c Produit appliqué au moyen d’une éponge. Le scénario tient compte du produit qui se retrouve sur les mains durant l’application et qui est éliminé lors du lavage des mains. On assume que la moitié du contenant est utilisée.
d Produit spécial qui serait utilisé à l’occasion, probablement réappliqué au cours de la journée.
e Produit spécial qui serait utilisé à l’occasion.
f Coefficient de transfert = (1800 cm2 x 4500 cm2)/5300 cm2 = 1528 cm2/h.
