Évaluation préalable pour le Défi concernant l'acétate de 2-méthoxyéthyle
Numéro de registre du Chemical Abstracts Service 110-49-6
Environnement Canada
Santé Canada
Février 2009
Table des matières
- Synopsis
- Introduction
- Identité de la substance
- Propriétés physiques et chimiques
- Sources
- Utilisations
- Rejets dans l'environnement
- Devenir dans l'environnement
- Persistance et potentiel de bioaccumulation
- Potentiel d'effets nocifs sur l'environnement
- Potentiel d'effets nocifs sur la santé humaine
- Conclusion
- Références
- Annexe I. Sommaire des renseignements concernant les effets de l'acétate de 2-méthoxyéthyle sur la santé
Synopsis
Les ministres de l'Environnement et de la Santé ont effectué une évaluation préalable de l'acétate de 2-méthoxyéthyle, dont le numéro de registre du Chemical Abstracts Service (no CAS) est 110-49-6. Une priorité élevée a été accordée à la prise de mesures à l'égard de cette substance lors de la catégorisation visant la Liste intérieure dans le cadre du Défi, car on considère que l'acétate de 2-méthoxyéthyle présente un risque d'exposition intermédiaire pour les particuliers au Canada et il a été classé sur la base de sa toxicité sur le plan du développement et de la reproduction par la Commission européenne. La substance ne répondait pas aux critères environnementaux de la catégorisation relatifs à la persistance, au potentiel de bioaccumulation et à la toxicité intrinsèque pour les organismes aquatiques. Par conséquent, la présente évaluation de l'acétate de 2-méthoxyéthyle porte principalement sur les risques pour la santé humaine.
Selon les renseignements déclarés conformément à l'article 71 de la Loi canadienne sur la protection de l'environnement (1999) [LCPE (1999)], aucune entreprise n'a indiqué avoir fabriqué ou importé au Canada de l'acétate de 2-méthoxyéthyle en quantités supérieures au seuil de déclaration de 100 kg au cours de l'année civile 2006; toutefois, des importations en quantités inférieures à ce seuil ont été déclarées. D'après ces renseignements, l'exposition de la population générale au Canada devrait être très faible.
D'après les renseignements tirés des études toxicologiques sur des animaux de laboratoire ainsi que des enquêtes épidémiologiques menées auprès des populations exposées dans un cadre professionnel à l'acétate de 2-méthoxyéthyle et à son alcool correspondant, le 2-méthoxyéthanol (compte tenu du caractère limité de la base de données sur l'acétate de 2-méthoxyéthyle, de la conversion rapide de l'acétate en éthanol et du profil d'effets commun aux deux substances), les effets critiques sur la santé associés à l'exposition sont principalement des effets sur le plan du développement et de la reproduction (y compris des effets tératogènes graves et irréversibles); ces effets se produisent à des doses très faibles, souvent la plus faible dose à l'essai. En outre, certains signes indiquent que ces substances auraient la capacité d'interagir avec le matériel génétique dans les cellules germinales. Par conséquent, on ne peut ignorer qu'il existe une certaine probabilité que l'exposition, quel qu'en soit le degré, cause des effets nocifs.
Bien que l'exposition à l'acétate de 2-méthoxyéthyle soit vraisemblablement très faible au Canada, on conclut, principalement compte tenu du fait que le risque associé à l'acétate de 2-méthoxyéthyle est indiscernable de celui lié au 2-méthoxyéthanol (et que des effets sur le plan de la reproduction et du développement sont probables, quel que soit le degré d'exposition), de considérer que la conclusion du rapport d'évaluation du 2-méthoxyéthanol aux fins de la Liste des substances d'intérêt prioritaire (c'est-à-dire que, vu le risque élevé qu'il présente pour la santé, le 2-méthoxyéthanol est considéré comme un danger pour la vie ou la santé humaines au Canada) s'applique à l'analogue acétate de cette substance.
D'après les faibles risques pour l'environnement que présentent l'acétate de 2-méthoxyéthyle et ses faibles rejets attendus et compte tenu de la faible exposition escomptée de l'environnement à cette substance, on conclut que celle-ci ne pénètre pas dans l'environnement en une quantité ou concentration ou dans des conditions de nature à avoir, immédiatement ou à long terme, un effet nocif sur l'environnement ou sur la diversité biologique, ou encore à mettre en danger l'environnement essentiel pour la vie. L'acétate de 2-méthoxyéthyle ne remplit pas les critères de la persistance et du potentiel de bioaccumulation énoncés dans le Règlement sur la persistance et la bioaccumulation.
Cette substance s'inscrira dans la prochaine mise à jour de l'inventaire de la Liste intérieure (LIS). De plus, des activités de recherche et de surveillance viendront, s'il y a lieu, appuyer la vérification des hypothèses formulées au cours de l'évaluation préalable et, le cas échéant, l'efficacité des mesures de contrôle possibles définies à l'étape de la gestion des risques.
D'après les renseignements disponibles, l'acétate de 2-méthoxyéthyle remplit un ou plusieurs critères de l'article 64 de la LCPE (1999).
Introduction
La Loi canadienne sur la protection de l'environnement (1999) [LCPE (1999)] (Canada, 1999) exige que les ministres de l'Environnement et de la Santé procèdent à une évaluation préalable des substances qui répondent aux critères de catégorisation énoncés dans la Loi afin de déterminer si elles présentent ou sont susceptibles de présenter un risque pour l'environnement ou la santé humaines. Selon les résultats de cette évaluation, les ministres peuvent proposer de ne rien faire à l'égard de la substance, de l'inscrire sur la Liste des substances d'intérêt prioritaire en vue d'une évaluation plus détaillée, ou de recommander son inscription sur la Liste des substances toxiques de l'annexe 1 de la Loi et, s'il y a lieu, sa quasi-élimination.
En se fondant sur l'information obtenue dans le cadre de la catégorisation, les ministres ont jugé qu'une attention hautement prioritaire devait être accordée à un certain nombre de substances, à savoir :
- celles qui répondent à tous les critères environnementaux de la catégorisation, notamment la persistance (P), le potentiel de bioaccumulation (B) et la toxicité intrinsèque (Ti) pour les organismes aquatiques, et que l'on croit être commercialisées;
- celles qui répondent aux critères de la catégorisation pour le plus fort risque d'exposition (PFRE) ou qui présentent un risque d'exposition intermédiaire (REI) et qui ont été jugées particulièrement dangereuses pour la santé humaine, compte tenu du classement attribué par d'autres organismes nationaux ou internationaux quant à la cancérogénicité, à la génotoxicité ou à la toxicité sur le plan du développement ou de la reproduction.
Le 9 décembre 2006, les ministres ont donc publié un avis d'intention dans la Partie I de la Gazette du Canada(Canada, 2006) dans lequel ils priaient l'industrie et les autres parties intéressées de fournir, selon un calendrier déterminé, des renseignements précis qui pourraient servir à étayer l'évaluation des risques, ainsi qu'à élaborer et à évaluer les meilleures pratiques de gestion des risques et de bonne gestion des produits pour ces substances jugées hautement prioritaires.
L'acétate de 2-méthoxyéthyle est une substance dont l'évaluation des risques pour la santé humaine a été jugée hautement prioritaire, car on considère qu'il présente un REI et il a été classé par un autre organisme sur la base de sa toxicité sur le plan de la reproduction et du développement.
Le volet du Défi portant sur cette substance a été lancé le 18 août 2007 au moyen d'un avis paru dans la Gazette du Canada (Canada, 2007). En même temps a été publié le profil de cette substance (Canada, 2007b), qui présentait l'information technique (obtenue avant décembre 2005) sur laquelle a reposé sa catégorisation. Des renseignements sur la substance ont été communiqués en réponse au Défi (Environnement Canada, 2008).
Même si l'évaluation des risques que présente l'acétate de 2-méthoxyéthyle pour la santé humaine est jugée hautement prioritaire, cette substance ne répond pas aux critères relatifs à la persistance, au potentiel de bioaccumulation ou à la toxicité intrinsèque pour les organismes aquatiques. La présente évaluation est donc axée principalement sur les renseignements présentant de l'intérêt pour l'évaluation des risques touchant la santé humaine.
Les évaluations préalables effectuées aux termes de la LCPE (1999) mettent l'accent sur les renseignements jugés essentiels pour déterminer si une substance répond aux critères de « toxicité » des substances chimiques au sens de l'article 64 de la Loi :
« 64. [...] est toxique toute substance qui pénètre ou peut pénétrer dans l'environnement en une quantité ou concentration ou dans des conditions de nature à :
- avoir, immédiatement ou à long terme, un effet nocif sur l'environnement ou sur la diversité biologique;
- mettre en danger l'environnement essentiel pour la vie; ou
- constituer un danger au Canada pour la vie ou la santé humaines. »
Les évaluations préalables visent à examiner les renseignements scientifiques et à tirer des conclusions fondées sur la méthode du poids de la preuve et le principe de prudence, conformément aux dispositions de la LCPE (1999).
La présente évaluation préalable prend en considération les renseignements sur les propriétés chimiques, les dangers, les utilisations et l'exposition, y compris ceux fournis dans le cadre du Défi. Les données pertinentes pour l'évaluation préalable de cette substance ont été relevées dans des publications originales, des rapports de synthèse et d'évaluation, des rapports de recherche de parties intéressées et d'autres documents consultés lors de recherches documentaires menées récemment, jusqu'en juin 2008 (exposition) et jusqu'en juin 2007 (effets sur la santé). Les études importantes ont fait l'objet d'une évaluation critique; les résultats de la modélisation ont pu être utilisés dans la formulation des conclusions. L'évaluation des risques pour la santé humaine comprend l'examen de données pertinentes pour l'évaluation de l'exposition (non professionnelle) de la population dans son ensemble ainsi que de l'information sur les dangers pour la santé (surtout fondée sur des évaluations réalisées par d'autres organismes selon la méthode du poids de la preuve et ayant servi à déterminer le caractère prioritaire de la substance). Les décisions reposent sur la nature de l'effet critique retenu ou sur l'écart entre les valeurs prudentes donnant lieu à des effets et les estimations de l'exposition, en tenant compte de la confiance accordée au caractère exhaustif des bases de données sur l'exposition et les effets, cela dans le contexte d'une évaluation préalable. La présente évaluation préalable ne constitue pas un examen exhaustif ou critique de toutes les données disponibles. Il s'agit plutôt d'un sommaire des éléments d'information les plus importants pour appuyer la conclusion .
La présente évaluation préalable a été préparée par le personnel du Programme des substances existantes de Santé Canada et d'Environnement Canada et intègre les résultats d'autres programmes exécutés par ces ministères. Cette évaluation préalable a fait l'objet d'une consultation indépendante par des pairs. Des commentaires sur les portions techniques concernant la santé humaine ont été reçus de la part d'experts scientifiques désignés et dirigés par la Toxicology - Excellence for Risk Assessment (TERA), notamment Glenn Talaska (University of Cincinnati), Michael Jayjock (The Lifeline Group) et Joan Strawson (TERA). ToxEcology - Environmental Consulting Ltd. a aussi formulé des commentaires sur ces sections. De plus, une version provisoire de la présente évaluation préalable a fait l'objet d'une consultation publique de 60 jours. Bien que les commentaires externes aient été pris en considération, Santé Canada et Environnement Canada assument la responsabilité du contenu final et des résultats de l'évaluation préalable.
Les principales données et considérations sur lesquelles repose la présente évaluation sont résumées ci-après.
Identité de la substance
L'acétate de 2-méthoxyéthyle, aussi appelé acétate de l'éther monométhylique de l'éthylèneglycol (EMEG), est un ester organique comptant deux liaisons éther sur la même chaîne (tableau1). À la température ambiante, l'acétate de 2-méthoxyéthyle est un liquide incolore à l'odeur agréable (7 Budavari, 1996; OMS, 2003, Lewis, 2007). Il est combustible, soluble dans l'eau, et miscible avec les solvants organiques courants (Budavari, 1996). Le tableau 1 présente un résumé des autres données disponibles sur l'acétate de 2-méthoxyéthyle.
| No CAS | 110-49-6 |
|---|---|
| Nom dans la LIS | Acétate de 2-méthoxyéthyle |
| Noms relevés dans les National Chemical Inventories (NCI)Note de bas de tableaua |
Ethanol, 2-methoxy-, 1-acetate (TSCA, ENCS, AICS, SWISS, PICCS, ASIA-PAC) Acétate de 2-méthoxyéthyle (EINECS) Acetate, 2-Methoxyethyl (PICCS) Ethyl glygol monomethyl ether acetate (PICCS) |
| Autres noms | Acetate, 2-methoxyethyl; Acetic acid, 2-methoxyethyl ester; 1-Acetoxy-2-methoxyethane; Acetyl methyl cellosolve; Ethyl glycol, monomethyl ether acetate; Ethylene glycol acetate monomethyl ether; Ethylene glycol methyl ether acetate; Ethylene glycol monomethyl ether acetate; Glycol monomethyl ether acetate; 2-Methoxyethanol acetate; -Methoxyethyl acetate; Methyl cellosolve acetate; Methyl glycol acetate |
| Groupe chimique (Groupe de la LIS) |
Composés organiques |
| Sous-groupe chimique | Esters |
| Formule chimique | C5H10O3 |
| Structure chimique | 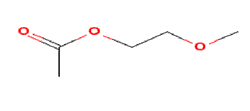 |
| Simplified Molecular Input Line Entry System (SMILES) | O=C(OCCOC)C |
| Masse moléculaire | 118,13 g/mol |
Propriétés physiques et chimiques
Le tableau 2 résume les propriétés physiques et chimiques (valeurs modélisées et expérimentales) de l'acétate de 2-méthoxyéthyle.
| Type | Valeur | Température (°C) | RéférencesNote de bas de tableaub | |
|---|---|---|---|---|
| Point de fusion (°C) | Expérimental | -65 à -70 | PhysProp, 2006; Verschueren, 2001 |
|
| Point d'ébullitions (°C) | Expérimental | 143; 144 | PhysProp, 2006; Verschueren, 2001 |
|
| Densité relative | 1,0 | 20 | Verschueren, 2001 | |
| Pression de vapeur (Pa) | Expérimental | 267 (2 mmHg)2 |
20 | PhysProp, 2006 |
| Constante de la loi de Henry (Pa·m3/mol) |
Modélisé | 2,54 × 10-2 - 2,77 × 10-1 (2,503 × 10-7 - 2,73 × 10-6 atm ·m3/mol)Note de bas de tableauc |
25 | EPIWIN, 2004 |
| Constante de la loi de Henry (Pa·m3/mol) |
Modélisé | 3,1 × 10-7 | 20 | PhysProp, 2006 |
| Log Koe (coefficient de partage octanol/eau) (sans dimension) |
Modélisé | 0.10 | 25 | KOWWIN, 2000; PhysProp, 2006 |
| Log Koe (sans dimension) |
Modélisé | -0.082 | 25 | ACD, 2007 |
| Log Kco (coefficient de partage carbone organique-eau) (sans dimension) |
Modélisé | 0.06; 1.33 | 25 | PCKOCWIN, 2000; ACD, 2007 |
| Solubilité dans l'eau (mg/L) | Expérimental | 1.00 × 106 | 20 | Yalkowsky et Dannenfelser, 1992 |
Sources
L'acétate de 2-méthoxyéthyle est un composé d'origine humaine dont on n'a trouvé aucune source naturelle (PISSC, 1990; NPI, 2005). Il est produit par estérification du 2 -méthoxyéthanol avec de l'acide acétique, un anhydrique d'acide ou du chlorure, en présence d'un catalyseur acide afin d'être utilisé dans des processus de fabrication (Kirk et Othmer, 1980).
D'après les renseignements fournis conformément à l'article 71 de la LCPE (1999), l'acétate de 2-méthoxyéthyle n'a pas été fabriqué au Canada pendant l'année civile 2006 en des quantités dépassant le seuil de déclaration de 100 kg . Des importations en quantités inférieures au seuil de déclaration ont été rapportées (Environnement Canada, a 2008).
Utilisations
Il était notamment utilisé dans des colles et des adhésifs pour les revêtements de sol et les surfaces imperméables à l'eau d'accessoires domestiques b . Il a également été utilisé comme solvant dans les revêtements de surface comme les peintures, les enduits, les vernis et les vernis-laques pour le papier et le cuir, et les adhésifs à base d'acétates (HSDB, 2005; NPI, 2005; HSDB 8 , 2008). Il a été employé comme solvant dans la nitrocellulose, l'acétate de cellulose, les gommes, les résines, les cires et les huiles (NPI, 2005). C'est aussi un composant des solvants utilisés dans l'impression textile et les films photographiques (Verschueren, 2001), ainsi que dans le vernis à ongles et les produits de nettoyage à sec (NPI, 2005).
Dans certaines publications, on signalait l'utilisation d'acétate de 2-méthoxyéthyle comme additif dans le carburant diesel, ceci afin de réduire les émissions produites par les véhicules (Guo et al., 2004; Yanfeng et al., 2007), mais rien n'indique que cette substance soit encore ou ne sera utilisée à cette fin dans le commerce, selon les recherches effectuées.
Aucune utilisation de l'acétate de 2-méthoxyéthyle dans les produits cosmétiques n'a été déclarée au Canada , alors que son alcool correspondant, le 2-méthoxyéthanol est actuellement interdit dans les produits cosmétiques et figure sur la Liste critique de Santé Canada concernant les cosmétiques (SDC, 2008). L'acétate de 2 -méthoxyéthyle a déjà été utilisé comme solvant et comme agent diminuant la viscosité dans les produits cosmétiques, et quelques fournisseurs actifs de cette substance sont toujours répertoriés par le Personal Care Products Council (anciennement The Cosmetic, Toiletry and Fragrance Association) (CTFA, 2008). Toutefois, l'utilisation d'acétate de 2-méthoxyéthyle comme de 2-méthoxyéthanol dans les produits cosmétiques est interdite au sein de l'Union européenne (CE, 1999).
Autrefois (c'est-à-dire il y a 15 ans), l'acétate de 2-méthoxyéthyle était employé comme solvant dans la fabrication de revêtements et d'adhésifs destinés aux emballages alimentaires. À l'heure actuelle, cependant, aucune utilisation de cette substance dans les emballages alimentaires n'est recensée au Canada (communication personnelle, Direction des aliments, Direction générale des produits de santé et des aliments, Santé Canada, 18 avril 2008 et 9 mai 2008, source non citée). L'acétate de 2-méthoxyéthyle entre dans la composition d'un nettoyant appliqué sur des surfaces en contact avec les aliments, qui sont ensuite rincées avec de l'eau potable, et il est employé pour le nettoyage des surfaces qui ne viennent pas en contact avec les aliments dans les usines de transformation des aliments, ceci sous bonne ventilation (communication personnelle, Direction des aliments, Direction générale des produits de santé et des aliments, Santé Canada, 27 juin 2008, source non citée).
L'utilisation d'éthers glycoliques à chaîne courte droite, dont l'acétate de 2-méthoxyéthyle et le 2-méthoxyéthanol, a progressivement diminuée au cours des 20 dernières années dans le monde (Johanson et Rick, 1996; De Kettenis, 2005; US EPA, 2005). La U.S. Environmental Protection Agency (EPA) a indiqué que l'acétate de 2-méthoxyéthyle et de 2-métoxyéthanol n'est pas utilisé à l'heure actuelle dans les produits de consommation aux États-Unis et que toute nouvelle utilisation importante de ces substances devrait faire l'objet d'un avis (U S EPA, 2005).
Rejets dans l'environnement
Les renseignements obtenus en vertu de l'article 71 de la LCPE (1999) n'indiquent aucun rejet considérable d'acétate de 2-méthoxyéthyle au cours de l'année civile 2006 (Environnement Canada, c 2008). De plus, aucune activité de fabrication ou d'importation de cette substance en une quantité supérieure au seuil de déclaration de 100 kg n'a été déclarée en réponse à cet avis (par contre, on a déclaré l'importation de quantités inférieures à ce seuil) [(Environnement Canada, c ]2008 . Les données de l'Inventaire national des rejets de polluants (INRP) d'Environnement Canada ne révèlent pas non plus de rejets d'acétate de 2-méthoxyéthyle pour la période de 1994 à 2006 (INRP, 2007). Par conséquent, on présume que les rejets industriels totaux de cette substance dans l'environnement sont négligeables.
À l'échelle internationale, l'acétate de 2-méthoxyéthyle ne figure pas dans le Toxics Release Inventory (TRI) de l'EPA des États-Unis (TRI, 2008), et un rapport du National Pollutant Inventory (NPI) de l'Australie indique qu'aucune émission de cette substance n'a été déclarée pour 2005 (NPI, 2005).
Devenir dans l'environnement
Les résultats de la modélisation de fugacité de niveau III obtenus pour l'acétate de 2-méthoxyéthyle sont résumés au tableau 3. Les résultats montrent que l'acétate de 2-méthoxyéthyle devrait se répartir principalement dans le sol lorsqu'il est rejeté dans l'air ou dans le sol. Si elle était rejetée dans l'eau, cette substance devrait se distribuer surtout dans cette phase, et seule une petite quantité devrait se retrouver dans les autres milieux. La faible affinité de l'acétate de 2-méthoxyéthyle pour les sédiments, quel que soit le milieu dans lequel ce produit est rejeté, concorde avec la très faible valeur estimée pour son Kco.
| Fraction de la substance se répartissant dans l'air (%) | Fraction de la substance se répartissant dans l'eau (%) | Fraction de la substance se répartissant dans le sol (%) | Fraction de la substance se répartissant dans les sédiments (%) | |
|---|---|---|---|---|
| Rejets de la substance dans l'air (100 %) | 20,8 | 24,1 | 55,0 | 0,04 |
| Rejets de la substance dans l'eau (100 %) | 0,001 | 99,8 | 0,012 | 0,17 |
| Rejets de la substance dans le sol (100 %) | 0,16 | 21,5 | 78,3 | 0,04 |
Persistance et potentiel de bioaccumulation
Persistance
Une fois libéré dans l'environnement, l'acétate de 2-méthoxyéthyle ne devrait pas être persistant dans l'air, l'eau, le sol ou les sédiments. Le tableau 4 résume les données modélisées et empiriques sur la persistance de l'acétate de 2-méthoxyéthyle. On a rapporté une forte réactivité photochimique pour cette substance en présence d'oxydes d'azote dans des essais en chambre à smog (Yanagihara et al., 1977).
| Processus du devenir | Type de données | Valeur pour la dégradation | Paramètres (unité) | Références |
|---|---|---|---|---|
| Biodégradation | Modélisées | 1,1 | t½ (jours) | AOPWIN, 2000 |
| Biodégradation dans l'eau | Modélisées | 15 | t½ (jours) | BIOWIN, 2000 (modèle d'enquête sur la dégradation ultime) |
| Biodégradation dans l'eau | Modélisées | 0,91 | Probabilité | BIOWIN, 2000 (modèle non linéaire Ministry of International Trade and Industry, Japon (MITI)) |
| Biodégradation dans l'eau | Empiriques | 97 | Biodégradation (%) | MITI, 1992 |
La solubilité élevée de l'acétate de 2-méthoxyéthyle indique également que, lorsque ce produit est rejeté dans l'eau, il est susceptible d'y demeurer. Il se dégrade rapidement dans l'eau et le sol (demi-vies de 15 jours). La demi-vie pour la réaction d'hydrolyse dans l'eau est de 391 jours à un pH 7 et 32 jours à un pH 8, ce qui laisse supposer que l'hydrolyse n'est pas susceptible d'être une voie de dégradation importante dans HSDB 8 l'eau à des pH pertinents du point de vue de l'environnement (HSDB, 2008).
D'après un ratio d'extrapolation 1:1:4 de la demi-vie de biodégradation dans l'eau, le sol et les sédiments (Boethling et al., 1995), la demi-vie dans le sol est inférieure à 182 jours, alors que celle dans les sédiments est inférieure à 365 jours. Cela indique que l'acétate de 2-méthoxyéthyle ne devrait pas être persistant dans le sol, ni dans les sédiments.
Si l'on applique la méthode du poids de la preuve aux données décrites ci-dessus, l'acétate de 2-méthoxyéthyle ne répond aux critères de la persistance ni pour l'air (demi-vie supérieur(e) ou égal(e) à 2 jours), ni pour l'eau ou le sol (demi-vie supérieur(e) ou égal(e) à 182 jours), ni pour les sédiments (demi-vie supérieur(e) ou égal(e) à 365 jours), tels qu'ils sont définis dans le Règlement sur la persistance et la bioaccumulation (Canada, 2000).
Potentiel de bioaccumulation
Les données modélisées sur le potentiel de bioaccumulation de l'acétate de 2-méthoxyéthyle dans les poissons (organisme d'essai) sont présentées au tableau 5. Les résultats montrent que cette substance ne devrait pas se bioaccumuler.
| Paramètre | Valeur en poids humide (L/kg) | Références |
|---|---|---|
| Facteur de bioaccumulation (FBA) | 1,02 | Arnot et Gobas, 2003 (Gobas BFA T2MTL) |
| Facteur de bioconcentration (FBC) | 1,01 | Arnot et Gobas, 2003 (Gobas FBC 5 % T2LTL) |
| FBC | 1,0 | ACD, 2007 |
| FBC | 11,7 | OASIS Forecast, 2005 |
| FBC | 3,16 | BCFWIN, 2000 |
Le modèle modifié du FBA de Gobas pour le niveau trophique intermédiaire chez le poisson a estimé le facteur de bioaccumulation à 1,02 L/kg en poids humide, ce qui indique que cette substance n'est pas susceptible de se bioconcentrer ou de se bioamplifier dans l'environnement. Le potentiel de bioconcentration de cette substance est aussi appuyé par les résultats des modèles du FBC selon la méthode du poids de la preuve.
Selon la méthode du poids de la preuve, l'acétate de 2-méthoxyéthyle ne répond pas aux critères de la bioaccumulation (FBC ou FBA supérieur(e) ou égal(e) à 5 000 L/kg) énoncés dans le Règlement sur la persistance et la bioaccumulation (Canada, 2000).
Potentiel d'effets nocifs sur l'environnement
Comme nous l'avons indiqué précédemment, l'acétate de 2-méthoxyéthyle ne répond pas aux critères de persistance et de bioaccumulation énoncés dans le Règlement sur la persistance et la bioaccumulation (Canada, 2000).
Une étude de la toxicité aiguë de l'acétate de 2-méthoxyéthyle pour le Carassius auratus (poisson) indique une concentration léthale médiane (CL50) de 160 mg/L (tableau 6). On considère que cette concentration reflète une toxicité aiguë faible à modérée, et que l'acétate de 2-méthoxyéthyle ne devrait pas entraîner d'effets nocifs chez les organismes aquatiques à des concentrations relativement faibles. Devillers et al. (2002) ont é une déclarent une valeur de reproduction chronique de 0,06 mg/L le pour Ceriodaphnia dubia t , c e qui semble indiquer que les invertébrés seraient plus sensibles à l'acétate de 2-méthoxyéthyle que les poissons et les amphibiens (Xenopus laevis) (tableau 6).
| Organisme d'essai | Type d'essai | Paramètre | Valeur (mg/L) | Références |
|---|---|---|---|---|
| Poisson | Aiguë | CL50 | 160 | Bridié et al., 1979 |
| Poisson | Aiguë | CL50 | 50 | Devillers et al,. 2002 |
| Ceriodaphnia dubia | Chronique | Reproduction | 0.06 | Devillers et al,. 2002 |
| Xenopus laevis | Chronique | Tératogénicité | 75 | Devillers et al,. 2002 |
Comme on l'a mentionné précédemment, aucun rejet d'acétate de 2-méthoxyéthyle dans l'environnement n'a été déclaré à l'Inventaire national des rejets de polluants (INRP) conformément à l'article 71 de la LCPE (1999) [INRP Environnement Canada, c ] 2008) ou dans le cadre de l'INPR (Canada, 2007c; NPRI, 2007). De plus, la quantité d'acétate de 2-méthoxyéthyle importée au Canada est très faible et cette substance n'y est pas fabriquée. Ainsi, d'après les données disponibles, les concentrations environnementales d'acétate de 2-méthoxyéthyle devraient être extrêmement faibles et la substance n'est pas susceptible de présenter un danger pour l'environnement au Canada.
Incertitudes dans l'évaluation es des risques pour l'environnement
L'emploi des modèles de relation quantitative structure-activité (RQSA) pour estimer la persistance et la bioaccumulation comporte des incertitudes. En outre, les données fournies aux modèles RQSA étaient fondées sur des valeurs estimées de certaines des propriétés physiques et chimiques fondamentales de la substance en question, entre autres la pression de vapeur, le Koe, le Kco et la constante de la loi de Henry.
Potentiel d'effets nocifs sur la santé humaine
Évaluation de l'exposition
Aucune mesure des concentrations d'acétate de 2-méthoxyéthyle dans les milieux naturels n'a été recensée. Selon l'INRP (2007 , aucun rejet important de ce produit n'a été déclaré au Canada depuis 1994. En outre, on ne fabrique pas d'acétate de 2-méthoxyéthyle au Canada, et on en importe seulement en de très faibles quantités, selon les déclarations fournies conformément à l'article 71. On ne s'attend donc pas à ce que cette substance soit présente en concentrations importantes dans l'environnement.
La concentration maximale d'acétate de 2-méthoxyéthyle mesurée dans 30 échantillons d'air intérieur prélevés entre 1988 et 1999 dans des lieux publics et privés en Allemagne était de 39 µg/m3 (concentration moyenne : 2 ± 7 µg/m3) [Schleibinger et al.., 2001]. Le produit a également été détecté dans 1 de 6 échantillons d'air intérieur recueillis en Italie, cette fois en concentration of 4 µg/m3 (De Bortoli et al..,1986); cependant, le produit n'a pas été détecté lors de l'analyse d'échantillons provenant de 200 appartements en Allemagne, analyse pour laquelle la limite de détection était de 1 µg/m3 (Plieninger et Marchl, 1999).
D'après les propriétés physiques et chimiques de l'acétate de 2-méthoxyéthyle et compte tenu qu'aucun rejet d'une quantité importante de cette substance n'a été signalé au Canada (Environnement Canada, c c2008), cette dernière ne devrait pas être présente en concentrations significatives dans l'air, l'eau, le sol ou les sédiments. L'acétate de 2-méthoxyéthyle ne devrait pas non plus être présent dans les aliments.
Aucune déclaration soumise en vertu de l'article 71 de la LCPE (1999) n'indique que l'acétate de 2-méthoxyéthyle est présent dans les produits de consommation au Canada (Environnement Canada, c c2008). Compte tenu que l'acétate de 2-méthoxyéthyle n'est utilisé ni aux États-Unis ni dans les pays de l'Union européenne, il est peu probable qu'il soit présent dans plusieurs produits de consommation au Canada . D'après les utilisations faites de l'acétate de 2-méthoxyéthyle dans le passé, une possible voie d'exposition à ce produit associée aux produits de consommation comprendrait l'inhalation d'air intérieur; cependant, selon les renseignements dont on dispose sur les utilisations actuelles, les expositions ne devraient pas être importantes. L'inhalation d'acétate de 2-méthoxyéthyle serait possible pendant l'utilisation de solvants domestiques renfermant cette substance (NPI, 2005); cependant, cette substance ne figurait pas dans la Household Products Database (base de données américaine , HPD, 2007).
Par conséquent, l'inhalation d'air intérieur constitue la plus importante source d'exposition à l'acétate de 2-méthoxyéthyle à laquelle la population du Canada dans son ensemble est susceptible d'être exposée, la concentration maximale signalée dans les études menées dans d'autres pays étant de 39 µg/m3. À la lumière du peu de données disponibles sur les concentrations de la substance dans les milieux naturels, la confiance dans cette estimation est très faible , bien qu'il soit probable que les expositions soient inférieures à cette concentration au Canada.
Évaluation des effets sur la santé
L'annexe 1 présente un résumé des renseignements dont on dispose au sujet des effets de l'acétate de 2-méthoxyéthyle sur la santé.
La Commission européenne a classé l'acétate de 2-méthoxyéthyle dans la catégorie 2, avec mentions de risque R60 (« risque d'altération de la fertilité ») et R61 (« risque d'effets néfastes pour l'enfant à naître ») [ESIS, 2007]. En outre, le Programme international sur la sécurité des substances chimiques a évalué la toxicité de cette substance en même temps que celle du 2-méthoxyéthanol ainsi que du 2--éthoxyéthanol et de son acétate, et a conclu que « les principaux effets préoccupants [de ces produits chimiques] pour l'humain sont leurs effets toxiques sur le plan du développement, sur les testicules et sur les paramètres hématologiques » (PISSC, 1990). Comme l'acétate de 2-méthoxyéthyle est rapidement hydrolysé par les estérases présentes dans divers tissus corporels pour donner du 2-méthoxyéthanol, les données sur la toxicité de ce dernier sont considérées comme pertinentes dans le cadre de l'évaluation de la toxicité de l'acétate. Dans l'évaluation du 2-méthoxyéthanol comme substance d'intérêt prioritaire, effectuée en application de la LCPE (1999), les effets critiques sur la santé ont également été définis comme étant la toxicité sur le plan de la reproduction et du développement, ainsi que les effets sur les systèmes hématologique, immunitaire et nerveux (Environnement Canada et Santé Canada, 2002). Note de bas de page1
Des effets sur les testicules, soit une diminution du poids absolu des testicules proportionnelle à la dose administrée, une atrophie au niveau de l'épithélium séminifère et une prolifération occasionnelle des cellules de Leydig, ont été observés chez des souris après administration par voie orale d'acétate de 2-méthoxyéthyle à raison de 500 mg/kg poids corporel par jour (kg-p.c.) dose minimale avec effet (nocif) observé [DSE(N)O]) ou à des doses plus élevées. Ces effets n'ont pas été enregistrés à 250 mg/kg-p.c. par jour (dose sans effet (nocif) observé [DSE(N)O]) Nagano et al., 1979, 1984]. En outre, le 2-méthoxyéthanol a invariablement exercé des effets toxiques sur le système reproducteur mâle chez diverses espèces d'animaux de laboratoire qui étaient exposés par voie orale, par voie cutanée ou par inhalation (Environnement Canada et Santé Canada, 2002). L'exposition à ce produit a également eu des effets sur le système reproducteur femelle, comme des modifications du cycle oestral et des concentrations hormonales ainsi qu'une atrophie des organes reproducteurs femelles (Environnement Canada et Santé Canada, 2002). Les DME(N)O les plus faibles pour le 2-méthoxyéthanol étaient de 25 mg/kg-p.c. par jour chez le lapin , avec une DSE(N)O de 12,5 mg/kg-p.c. par jour (Foote et al., 1995; Berndtson et Foote, 1997), de 625 mg/kg-p.c. par jour chez le rat (Feuston et al., 1989) et de 30 parties par million (ppm) (93 mg/m3) chez le lapin (Miller et al., 1983), respectivement, par voie orale, par voie cutanée et par inhalation.
On a enregistré des cas de mortalité foetale chez les souris traitées à l'acétate de 2 -méthoxyéthyle à raison de 1 225 mg/kg-p.c. par jour (seule dose à l'essai) par gavage aux jours de gestation 6 à 13 (Hardin et al., 1987). En outre, dans les études sur la toxicité par voie orale, par voie cutanée et par inhalation menées sur plusieurs espèces d'animaux de laboratoire, le 2-méthoxyéthanol a invariablement entraîné des effets toxiques sur le plan du développement, entre autres des malformations des ftus, principalement au niveau de l'appareil cardiovasculaire, de l'appareil rénal et du squelette (Environnement Canada et Santé Canada, 2002). La plus faible dose de 2-méthoxyéthanol par voie orale ayant entraîné un effet, soit 12 mg /kg -p.c la . par jour a été enregistrée dans une étude par gavage chez le singe (Scott et al., 1989) Par inhalation, la concentration minimale avec effet (nocif) observé (CME(N)O) était de 10 ppm de 2-méthoxyéthanol chez le lapin (31 mg/m3), avec une concentration sans effet (nocif) observé (CSE(N)O) de 3 ppm, soit 9 mg/m3) (Hanley et al., 1984a; id., 1984 b). Des effets ont été constatés après l'application d'environ 48 mg de 2-méthoxyéthanol/kg-p.c. par jour ou plus sur la peau chez les rats (Hellwig, 1993).
Des effets sur les paramètres hématologiques ont été constatés chez les animaux de laboratoire exposés par inhalation, notamment une hémolyse chez les rates après 4 heures d'exposition à une concentration de 32 ppm (154,6 mg/m3) d'acétate de 2-méthoxyéthyle (Carpenter et al., 1956) ainsi qu'une baisse des pigments sanguins et des corpuscules érythrocytaires chez les chats après 42 heures d'exposition à l'acétate de 2-méthoxyéthyle à raison de 1 100 mg/m3 (Gross, 1938). En outre, on a observé une leucopénie dans le cadre de l'étude sur la toxicité par voie orale chez les souris décrite précédemment (Nagano et al., 1979, 1984). Une altération de la réponse immunitaire a été notée chez les rats exposés par voie orale à une dose de 50 mg/kg-p.c. par jour ou plus (Smialowicz et al., 1992). On ne disposait d'aucune donnée sur la neurotoxicité de l'acétate de 2-méthoxyéthyle, mais on a constaté que le 2-méthoxyéthanol induisait des effets toxiques chez les rats et les souris exposés à des doses aiguës ou à court terme, par inhalation, à des concentrations de 25 ppm (78 mg/m3) ou plus (Goldberg et al.., 1962; Nelson et al.., 1984).
Il n'existe pas de données sur la cancérogénicité potentielle ou les effets chroniques de l'acétate de 2-méthoxyéthyle ou celle du 2-méthoxyéthanol. Des données limitées laissent supposer que ces produits auraient un faible potentiel de génotoxicité. Bien que ni l'acétate de 2 -méthoxyéthyle ni le 2-méthoxyéthanol n'aient induit de mutation génique chez les bactéries ou les levures, les deux substances ont eu des effets clastogènes in vitro dans les cellules des mammifères. L'acétate de 2-méthoxyéthyle a induit une aneuploïdie chez le Drosophila melanogaster et les levures, et certaines données indiquent que le 2 -méthoxyéthanol a causé des dommages à l'acide désoxyribonucléique (ADN) des cellules germinales mâles dans une étude sur la toxicité par gavage chez les rats. En outre, le 2-méthoxyacétaldehyde (MALD), métabolite initial de l'acétate de 2-méthoxyéthyle (après l'hydrolyse du 2-méthoxyéthanol) et du 2-méthoxyéthanol, a provoqué des mutations géniques dans les cellules de mammifères et il est davantage susceptible d'avoir des effets clastogènes dans ce type de cellules (Bootman et May, 1985; Zimmermann et al., 1985; Basler, 1986; Whittaker et al., 1989; Loveday et al., 1990; Sehgal et Osgood, 1990; Osgood et al., 1991; Zeiger et al., 1992; Environnement Canada et Santé Canada, 2002).
Chez les humains, certaines études épidémiologiques ont révélé un risque accru d'avortement spontané associé à l'exposition professionnelle, dans l'industrie des semi-conducteurs, à des mélanges d'éthers glycoliques renfermant notamment de l'acétate de 2-méthoxyéthyle et du 2 -méthoxyéthanol (Beaumont et al., 1995 ; Schenker et al., 1995; Swan et al., 1995; Schenker, 1996; Swan et Forest, 1996). Cependant, ces données ne sont pas concluantes en ce sens qu'elles ne permettent pas de déterminer la contribution relative de l'acétate de 2-méthoxyéthyle et du 2-méthoxyéthanol au risque d'avortement spontané. Les résultats de plusieurs études épidémiologiques semblaient également indiquer l'existence d'un risque accru de malformations congénitales associé à l'exposition maternelle à des mélanges d'éthers glycoliques (Gray et al., 1993; Ha et al., 1996; Cordier et al.., 1997; 2001). Toutefois, au terme d'un examen des données existantes, Maldonado et al.. (2003) ont estimé que les données ne suffisaient pas, dans l'état actuel des choses, pour établir si l'exposition professionnelle aux éthers glycoliques cause ou non des malformations congénitales. En outre, dans un rapport de cas, des malformations congénitales des organes reproducteurs ont été signalées chez deux garçons dont la mère avait été exposée dans un laboratoire industriel à l'acétate de 2-méthoxyéthyle (1 à 2 L/j) par inhalation et par contact cutané pendant ses grossesses (Bolt et Golka, 1990). Des effets sur le système reproducteur mâle, le système neuronal, le système hématologique et le système immunitaire ont aussi été observés chez des travailleurs exposés à l'acétate de 2-méthoxyéthyle et au 2-méthoxyéthanol; cependant, les données n'ont pas été jugées concluantes étant donné la présence de variables confusionnelles relatives à l'exposition, toutes les populations étudiées étant également exposées à d'autres produits chimiques (Environnement Canada et Santé Canada, 2002).
Une analyse approfondie du mode d'induction des effets enregistrés dépasse le cadre de la présente évaluation préalable, mais on sait que la génération du dérivé acide alkoxyacétique est une étape d'activation nécessaire pour le déclenchement des effets de l'acétate de 2-méthoxyéthyle et du 2-méthoxyéthanol sur les testicules et sur le plan du développement (PISSC, 1990). L'acétate de 2-méthoxyéthyle est rapidement hydrolysé en 2-méthoxyéthanol par les estérases, et cet alcool est oxydé par les déhydrogénases pour donner le MALD , puis l'acide 2-méthoxyacétique chez les humains et les animaux de laboratoire (ECETOC, 2005a). Par conséquent, comme la cinétique de réaction et la métabolisation sont similaires, d'un point de vue qualitatif, chez les animaux de laboratoire et les humains, on considère que les effets observés dans le cadre des études en laboratoire peuvent être transposés aux humains, avec des différences quantitatives possibles quant à la sensibilité.
Le degré de confiance associé à la base de données concernant la toxicité sur le plan de la reproduction et du développement et aux autres effets non néoplasiques associés à l'exposition à l'acétate de 2-méthoxyéthyle est jugé modéré. Les données limitées dont on dispose sur cette substance sont complétées par la base de données plus vaste qui existe sur l'alcool correspondant, le 2-méthoxyéthanol. Cependant, des incertitudes existent quant au potentiel néoplasique de l'acétate de 2-méthoxyéthyle, car on ne dispose d'aucune donnée sur l'exposition à long terme d'animaux de laboratoire à cette substance ou au 2-méthoxyéthanol, et certains signes indiquent l'existence d'un faible potentiel génotoxique.
Caractérisation des risques pour la santé humaine
Comme on n'a constaté aucune variation claire entre le profil toxicologique du 2-méthoxyéthanol et celui de l'acétate de 2-méthoxyéthyle, on considère que ces deux produits chimiques présentent le même risque intrinsèque et, étant donné le caractère limité de la base de données sur l'acétate de 2-méthoxyéthyle, on estime approprié d'utiliser les renseignements sur la toxicité du 2-méthoxyéthanol pour caractériser le risque que pose l'acétate de 2-méthoxyéthyle pour la santé humaine. Les effets sur la santé associés à l'exposition au 2-méthoxyéthanol et à l'acétate de 2-méthoxyéthyle sont principalement des effets de toxicité sur le plan du développement et de la reproduction (dont des effets tératogènes graves et irréversibles), certains étant observés à des doses très faibles, souvent la plus faible dose à l'essai dans l'étude. Bien que l'analyse du ou des mode(s) d'action à l'origine de ces effets dépasse la portée de la présente évaluation préalable dans le cadre du Défi, selon les observations des effets chez les animaux de laboratoire à de faibles niveau d'exposition (à des doses ou concentration les plus faibles testé dans certaines études) et, à la lumière du profil de génotoxicité de l'acétate de 2-méthoxyéthyle, du 2-méthoxyéthanol et de leurs métabolites (en particulier les effets génétiques induits dans les cellules germinales), écarter la possibilité d'un mode d'action faisant intervenir une interaction avec le matériel génétique, pour lequel il peut y avoir une probabilité de dommage à tout niveau d'exposition. De plus, d'autres effets, notamment sur les systèmes hématologique, immunitaire et nerveux, ont été constatés chez les animaux de laboratoire de même que chez les humains exposés au 2-méthoxyéthanol ou à l'acétate de 2-méthoxyéthyle en même temps qu'à d'autres substances chimiques dans leur milieu de travail.
Étant donné la rapide conversion de l'acétate de 2-méthoxyéthyle en 2-méthoxyéthanol et la similarité du profil d'effets critiques provoqués, il est jugé approprié de considérer que la conclusion du rapport d'évaluation du 2-méthoxyéthanol aux fins de la Liste des substances d'intérêt prioritaire (c'est-à-dire que, vu le risque élevé qu'il présente pour la santé, le 2-méthoxyéthanol est considéré comme un danger pour la vie ou la santé humaines au Canada [(Environnement Canada et Santé Canada, 2002)]) s'applique à l'acétate, même si l'exposition à ce dernier devrait être très faible au Canada.
Incertitudes dans l'évaluation des risques pour la santé humaine
La présente évaluation préalable de l'acétate de 2-méthoxyéthyle ne prend pas en compte la variabilité au sein de la population générale. En ce qui concerne les différences de sensibilité aux effets induits entre les humains et les animaux de laboratoire, même si les données expérimentales laissent supposer l'existence de telles variations , les données sont insuffisantes pour les quantifier. En outre, il existe une certaine incertitude quant à la capacité de l'acétate de 2-méthoxyéthyle à induire des effets néoplasiques.
Comme aucun rejet n'a été déclaré conformément à l'article 71 de la LCPE (1999), on s'attend à ce que les concentrations d'acétate de 2-méthoxyéthyle dans l'environnement soient négligeables. Cependant, il existe des incertitudes à ce chapitre à cause du manque de données de surveillance canadiennes adéquates. Comme des éléments indiquent que l'utilisation de l'acétate de 2-méthoxyéthyle a connu une nette diminution à l'étranger, il est probable que l'emploi de cette substance ait connu une baisse similaire au Canada. Toutefois, l'exposition potentielle par l'intermédiaire des produits demeure entourée d'incertitudes.
Conclusion
D'après les renseignements contenus dans ce rapport d'évaluation préalable, l'acétate de 2-méthoxyéthyle ne pénètre pas dans l'environnement en une quantité, à une concentration ou dans des conditions qui ont ou peuvent avoir un effet immédiat ou à long terme sur l'environnement ou sa diversité biologique, ou qui constituent ou peuvent constituer un danger pour l'environnement essentiel pour la vie.
D'après les renseignements présentés dans la présente ébauche d'évaluation préalable, l'acétate de 2-méthoxyéthyle ne pénètre pas dans l'environnement en une quantité ou concentration ou dans des conditions de nature à avoir, immédiatement ou à long terme, un effet sur l'environnement ou sur la diversité biologique, ou à mettre en danger l'environnement essentiel pour la vie.
On peut conclure, principalement compte tenu du fait que le risque intrinsèque associé à l'acétate de 2 -méthoxyéthyle est indistinguable du risque lié au 2 -méthoxyéthanol au chapitre des effets variés sur la santé humaine, dont ceux sur le plan de la reproduction et du développement pour lesquels il existe une probabilité quel que soit le degré d'exposition, que la conclusion formulée conformément à l'alinéa 64c) de la LCPE (1999) (Environnement Canada et Santé Canada, 2002) concernant le 2-méthoxyéthanol, s'applique à l'analogue acétate de cette substance, l'acétate de 2-méthoxyéthyle . En conséquence, on peut conclure que l'acétate de 2-méthoxyéthyle devrait être considéré comme une substance pouvant pénétrer dans l'environnement en une quantité ou concentration ou dans des conditions de nature à constituer un danger au Canada pour la vie ou la santé humaines.
Il est donc conclu que l'acétate de 2-méthoxyéthyle n'est pas « toxique » au sens des alinéas 64a) et 64b) de la LCPE (1999) mais qu'il répond aux critères énoncé à l'alinéa 64c) de la LCPE (1999). Par contre, cette substance ne répond pas aux critères de la persistance et de la bioaccumulation tels qu'ils sont définis dans le Règlement sur la persistance et la bioaccumulation (Canada, 2000).
Références
[ACD] Advances Chemistry Development. 2007. Valeurs calculées à l'aide du logiciel Advanced Chemistry Development (ACD/Labs), version 9.04 pour Solaris (c 1994-2007), présenté dans la base de données SciFinder. [consultée le 25 juillet 2007].
[AOPWIN] Atmospheric Oxidation Program for Windows [Modèle d'estimation]. 2000. Version 1.91. Washington (D.C.) : US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY): Syracuse Research Corporation. http://www.epa.gov/oppt/exposure/pubs/episuite.htm
Arnot, J.A., Gobas, F.A. 2003. A generic QSAR for assessing the bioaccumulation potential of organic chemicals in aquatic food webs. QSAR Comb. Sci.[Internet] 22(3):337 -345. [accès restreint]. http://www3.interscience.wiley.com/journal/104557877/home_
BASF. 1966. Methoxyglykolacetat : Unpublished data (XV/334). Abt. Toxikologie (1er mars 1966). Ludwigshafen (Allemagne) : BASF. [cité dans ECETOC, 2005b].
Basler, A. 1986. Aneuploidy-inducing chemicals in yeast evaluated by the micronucleus test. Mutat. Res. 174 11 : 11-13.
[BCFWIN] BioConcentration Factor Program for Windows [modèle d'estimation]. 2000. Version 2.15. Washington (DC) : U.S. Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY) : Syracuse Research Corporation. http://www.epa.gov/oppt/exposure/pubs/episuite.htm
Beaumont, J.J., Swan, S.H., Hammond, S.K., Samuels, S.J., Green, R.S., Hallock, M.F., Dominguez, C., Boyd, P., Schenker, M.B. 1995. Historical cohort investigation of spontaneous abortion in the semiconductor health study: epidemiologic methods and analysis of risk in fabrication overall and in fabrication work groups. Am J Ind Med 28(6): 735-750.
Berndtson, W.E., Foote, R.H. 1997. Disruption of spermatogenesis in rabbits consuming ethylene glycol monomethyl ether. Reprod. Toxicol. 11 1 9 36 11(1): 29-36.
Bridié, A., Wolff, C., Winter, M. 1979. The acute toxicity of some petrochemicals to goldfish, Water Res. 13: 623-626.
[BIOWIN] Biodegradation Probability Program for Windows [modèle d'estimation]. 2000. Version 4.02. Washington (DC) : U.S. Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY) : Syracuse Research Corporation. http://www.epa.gov/oppt/exposure/pubs/episuite.htm
Boethling, R.S., Howard, P.H., Beauman, J.A., Larosche, M.E. 1995. Factors for intermedia extrapolations in biodegradability assessment. Chemosphere 30(4): 741-752.
Bolt, H.M., Golka, K. 1990. Maternal exposure to ethylene glycol monoethylether acetate and hypospadia in offspring. A case report. Br J Ind Med 47: 352-353.
Bootman, J., May, K. 1985. Mutagenicity studies. Ames tests. Rapport inédit. Décembre 1985. Life Science Research, Royaume-Uni.
Budavari, S. (éd.). 1996. The Merck index -- An encyclopedia of chemicals, drugs, and biologicals 12e éd. Whitehouse Station (N.J.) : Merck and Co., Inc. p. 1032.
Canada. 1999. Loi canadienne sur la protection de l'environnement (1999). L.C. 1999, chap. 33. ois du Canada. Ottawa, Travaux publics et Services gouvernementaux Canada. Gazette du Canada, Partie III, vol. 22, no 3, ch. 33. http://canadagazette.gc.ca/partIII/1999/g3-02203.pdf
Canada. 1999. Loi canadienne sur la protection de l'environnement (1999). L.C., 1999, ch. 33. http://canadagazette.gc.ca/partIII/1999/g3-02203.pdf
Canada. 2000. Loi canadienne sur la protection de l'environnement (1999) : Règlement sur la persistance et la bioaccumulation, C.P. 2000-348, 23 mars 2000, DORS/2000-107, Gazette du Canada, Partie II, vol. 134, no 7, p. 607-612. http://canadagazette.gc.ca/partII/2000/20000329/pdf/g2-13407.pdf
Canada. 2002. Liste des substances d'intérêt prioritaire : Rapport d'évaluation : 2-Méthoxyéthanol. Ottawa (Ont.) : Environnement Canada, Santé Canada. http://www.hc-sc.gc.ca/ewh-semt/pubs/contaminants/psl2-lsp2/2_methoxyethanol/index-fra.php
Canada. Ministère de l'Environnement, ministère de Ministère de la Santé. 2006. Loi canadienne sur la protection de l'environnement l'environnement (1999) : Avis d'intention d'élaborer et de mettre en uvre des mesures d'évaluation et de gestion des risques que certaines substances présentent pour la santé des Canadiens et leur environnement. Gazette du Canada, Partie . Partie 1, vol. 140, no 49, p. 4109-4117. http://canadagazette.gc.ca/partI/2006/20061209/pdf/g1-14049.pdf
Canada. Ministère de l'Environnement, ministèreMinistère de la Santé. 2007a. Loi canadienne sur la protection de l'environnement (1999) : Avis de troisième divulgation d'information technique concernant les substances identifiées dans le Défi. Gazette du Canada, Partie 1, vol. 141, no 33, p. 2375-2379. http://gazetteducanada.gc.ca/partI/2007/20070818/pdf/g1-14133.pdf
Canada. Ministère de l'Environnement. 2007c. Loi canadienne sur la protection de l'environnement l'environnement (1999) : Avis concernant les substances du groupe 3 du Défi. Gazette du Canada, . Partie I, vol. 141, no 33, p. 2379-2394, 435 - 459. http://canadagazette.gc.ca/partI/2007/20070818/pdf/g1-14133.pdf
Ministère de l'Environnement, Ministère de la Santé. 2007a. Loi canadienne sur la protection de l'environnement (1999) : Avis de troisième divulgation d'information technique concernant les substances identifiées dans le Défi. Gazette du Canada. Partie I, vol. 141, no 33, p.2375-2379. http://gazetteducanada.gc.ca/partI/2007/20070818/pdf/g1-14133.pdf
Canada. Ministère de l'Environnement, Ministère de la Santé. Profil de substance pour le Défi aux intervenants : Acétate de 2-méthoxyéthyle, no CAS 110-49-6. /ese-ees/B333EB9D-7265-FF27-AC4A-FC6A06CAF1B7/batch3_110-49-6_fr.pdf
Canada. Ministère de l’Environnement, Ministère de la Santé. 2007c. Loi canadienne sur la protection de l’environnement (1999) : Avis concernant les substances du groupe 3 du Défi. Gazette du Canada. Partie I, vol. 141, no 33, p. 2379-2394. Accès : http://canadagazette.gc.ca/partI/2007/20070818/pdf/g1-14133.pdf#page=7
Carpenter, C.P., Pozzani , U.C., Weil, C.A., Weil , C.S., Nair , J.H., Keck , G.A., Smyth , H.F. 1956. The toxicity of butyl cellosolve solvent. AMA Arch. Ind. Health 14:114 -131.
Carpenter, C.P., Smyth, H.F. Jr, Pozzani, U. 1949. The assay of acute vapour toxicity, and the grading and interpretation of results on 96 chemical compounds. J. Ind. Hyg. Toxicol. 31: 343-346.
Carpenter, C.P., Smyth, H.F. 1946. Chemical burns of the rabbit cornea. Am. J. Ophthalmol. 29: 1363 -1372. [cité dans ECETOC, 2005b].
1999. The rules governing cosmetic products in the European Union, vol. 1, Cosmetics legislation, Cosmetic products. Council uncil Directive 76/768. Annex II. Commission européenne, Direction générale Entreprises et industrie, Produits pharmaceutiques et cosmétiques. http://www.leffingwell.com/cosmetics/vol_1en.pdf
Cordier, S., Bergeret, A., Goujard, J., Ha, M.C., Aymé, S., Bianchi, F., Calzolari, E., De Walle, H.E.K., Knill-Jones, R., Candela, S., Dale, I., Dananché, B., de Vigan, C., Fevotte, J., Kiel, G., Mandereau, L. 1997. Congenital malformations and maternal occupational exposure to glycol ethers. Epidemiology 8:355-63.
Cordier, S., Szabova, E., Fevotte, J., Bergeret, A., Plackova, S., Mandereau, L. 2001. Congenital malformations and maternal exposure to glycol ethers in the Slovak Republic. Epidemiology 12:592-3. 12e éd. Washington (DC) : CFTA.
[CTFA] The Cosmetic, Toiletry, and Fragrance Association, Inc. 2008. International cosmetic ingredient dictionary and handbook. 12e éd. Washington (D.C.) : CFTA.
De Bortoli, N., Knöppel, H., Pecchio, E., Peil, A., Rogora, L., Schauenburg, H., Schlitt, H., Vissers, H. 1986. Concentrations of selected organic pollutants in indoor and outdoor air in northern Italy. Environ.Int. 12: 343-350.
De Kettenis, P. 2005. The historic and current use of glycol ethers: a picture of change.Toxicol. Lett. 156: 5-11.
Devillers, J., Chezeau, A., Thybaud, E., Poulsen, V., Graff, L., Vasseur, P., Chenon, P., Mouchet, F., Ferrier, V., Quiniou, F. 2002. Ecotoxicity of ethylene glycol monomethyl ether and its acetate. Toxicol.Mech.Methods 12: 241 -254.
[ECETOC] European Centre for Ecotoxicology and Toxicology of Chemicals. 2005a. The toxicology of glycol ethers and its relevance to man. Rapport technique no 95, vol. I. Bruxelles (Belgique) : ECETOC.
[ECETOC] European Centre for Ecotoxicology and Toxicology of Chemicals. 2005b. The toxicology of glycol ethers and its relevance to man. Rapport technique no 95, vol. II. 4.2. Profil de la substance : EGMEA (no CAS 110-49-6). Bruxelles (Belgique) : ECETOC.
Environnement Canada. 2008. Données sur les substances du lot 3 recueillies en vertu de l'article 71 de la Loi canadienne sur la protection de l'environnement (1999) : Avis concernant les substances du lot 3 du Défi. Préparé par Environnement Canada et Santé Canada dans le cadre du Programme des substances existantes.
Environnement Canada et Santé Canada. 2002. Liste des substances d'intérêt prioritaire - Rapport d'évaluation du 2-Methoxyethanol [Internet]. Ottawa (Ont.) : Environnement Canada; Santé Canada. http://www.hc-sc.gc.ca/ewh-semt/pubs/contaminants/psl2-lsp2
[EQC] Equilibrium Criterion Model. 2003. Version 2.02 . Peterborough (Ont) : Trent University, Canadian Centre for Environmental Modelling Centre. and Chemistry. http://www.trentu.ca/academic/aminss/envmodel/models/EQC2.html
[ESIS] European Chemical Substances Information System [base de données sur Internet]. 2007. Version 5. 2-Me e anolMethoxyethanol acetate, no CAS No. 110-49-6. Bureau européen des substances chimiques (ECB). http://ecb.jrc.it/esis/
Feuston, M.H., Bodnar, K.R., Kerstetter, S.L., Grink, C.P., Belcak, M.H., Singer, J. 1989. Reproductive toxicity of 2- methoxyethanol applied dermally to occluded and nonoccluded sites in male rats. Toxicol. Appl. Pharmacol. 100: 145-61.
Foote, R.H., Farrel, P.B., Schlafer, D.H., McArdle, M.M., Trouern-Trend, V., Simkin, M.E., Brockett, C.C., Giles, J.R., Li, J. 1995. Ethylene glycol monomethyl ether effects on health and reproduction in male rabbits. Reprod. Toxicol. 9(6): 527-539.
Goldberg, M.E., Haun, C., Smyth, H.F. Jr. 1962. Toxicologic implication of altered behaviour induced by an industrial vapour. Toxicol. Appl. Pharmacol.4: 148-64. [cité dans Canada, 2002].
Gray, R.H., Corn, M., Cohen, R., Correa, A., Hapkim, R., Hou, W., Shah, F., Zauer, H. 1993. Final report. The Johns Hopkins University retrospective and prospective studies of reproductive health among IBM employees in semiconductor manufacturing. Baltimore (MD [États-Unis]): The Johns Hopkins University. [cité dans Maldonado et al., 2003].
Gross, E. 1938. Methyl glycol acetate. In Toxikologie und Hygiene der technischen Loesungsmittel. Lehmann, K.B , Flury, F. (éd.). Berlin (Allemagne) : Springer-Verlag. [version anglaise : Toxicology and hygiene of industrial solvents. King, E., Smyth, . (traducteurs) Williams and Wilkins Company, 1943
Guo, H., Huang, X., Wang, X., Zhang, Z. 2004. Research on a new type of oxygenate of 2-methoxyethyl acetate as a clean diesel fuel additive. Prepr. Pap.-Am. Chem. Soc. Div. Pet. Chem. 49(2) :): 232-235.
Ha, M.C., Cordier, S., Dananche, B., Bergeret, A., Mandereau, L., Bruno, F. 1996. Congenital malformations and occupational exposure to glycol ethers: a European collaborative case-control study. Occup. Hyg. 2: 417-421.
Hanley, T.R., Young, J.T. Jr., John, J.A., Rao, K.S. 1984a. Ethylene glycol monomethyl ether (EGME) and propylene glycol monomethyl ether (PGME): inhalation fertility and teratogenicity studies in rats, mice and rabbits. Environ. Health Perspect. 57: 7-12. [cité dans Canada, 2002].
Hanley, T.R., Yano, B.L., Jr., Nitschke, K.D., John, J.A. 1984b. Comparison of the teratogenic potential of inhaled ethylene glycol monomethyl ether in rats, mice, and rabbits. Toxicol. Appl. Pharmacol. 75: 409-22. [cité dans Canada, 2002].
Hardin, B.D., Schuler, R.L., Burg, J.R., Booth, G.M., Hazelden, K.P., Mackenzie, K.M., Piccirillo, V.J., Smith, K.N. 1987. Evaluation of 60 chemicals in a preliminary developmental toxicity test. Teratog. Carcinog. Mutagen. 7: 29-48.
Hellwig, J. 1993. Study of the prenatal toxicity of 2-methoxyethanol in rats after dermal application. Rapport inédit. Abt. Toxicologie. Ludwigshafen (Allemagne) : BASF AG (no OR53/89002). [cité dans Canada, 2002].
[HENRYWIN] Henry's Law Constant Program for Microsoft Windows [modèle d'estimation]. 2000. Version 3.10. Washington (D.C.) : US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY) : Syracuse Research Corporation. http://www.epa.gov/oppt/exposure/pubs/episuite.htm
[HPD] Household Products Database. [bade de données sur Internet]. 2007. 2-Methoxyethanol acetate. Bethesda (MD): U.S. Department of Health and Human Services, National Institutes of Health, National Library of Medicine, Toxicology Data Network [consulté en décembre 2007]. http://householdproducts.nlm.nih.gov/
[HSDB] Hazardous Substances Data Bank [base de données sur Internet]. 1983-Methyl cellosolve acetate. Bethesda (MD [États-Unis]) : National Library of Medicine (États-Unis). [. [mise à jour le 24 juin 2005; consultée le 21 août 2008]. http://toxnet.nlm.nih.gov/cgi-bin/sis/htmlgen?HSDB
[INRP] Inventaire national des rejets de polluants [base de données sur Internet]. 2007. Gatineau (Qc) :), Environnement Canada. [consultée le 6 janvier 2008]. http://www.ec.gc.ca/pdb/querysite/query_e.cfm
Johanson, G., Rick, U. 1996. Use and use patterns of glycol ethers in Sweden. Occupational Hygiene 2:. Hyg. 2: 105-110.
Kirk, R.E., ., Othmer, D.F. 1980. Encyclopaedia of chemical technology. 3eéd. V Vol. 11. New York (NY) : Wiley. Glycols (ethylene and propylene) : Wiley
[KOWWIN] Octanol-Water Partition Coefficient Program for Microsoft Windows [modèle d'estimation]. 2000. Version 1.67. Washington (D.C.) : U.S. Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY) : Syracuse Research Corporation. http://www.epa.gov/oppt/exposure/pubs/episuite.htm
Lewis, R.J Sr. 2007. Hawley's 15e condensed chemical dictionary. 15eéd.. Hoboken (N.J.) : Wiley . p. 530.
Loveday, K.S., Anderson, B.E., Resnick, M.A., Zeiger, E. 1990. Chromosome aberration and sister chromatid exchange tests in Chinese hamster ovary cells in vitro. V: Results with 46 chemicals. Environ. Mol. Mutagen. 16 4 7 303 16(4): 272-303.
Maldonado, G., Delzell, E., Tyl, R.W., Sever, L.E. 2003. Occupational exposure to glycol ethers and human congenital malformations. Int. Arch. Occup. Environ. Health 76 6 (6): 405-423.
Miller, R.R., Ayres, J.A., Young, J.T., McKenna, M.J. 1983. Ethylene glycol monomethyl ether. I. Subchronic vapor inhalation study with rats and rabbits. Fundam. Appl. Toxicol. 3: 49-54.
[MITI] Ministry of International Trade & Industry. 1992. Biodegradation and Bioaccumulation Data of Existing Chemicals Based on the CSCL Japan. (Japon), Basic Industries Bureau, Chemical Products Safety Division, Basic Industries Bureau, Ministry of International Trade & Industry. 1992. Biodegradation and bioaccumulation data of existing chemicals based on the CSCL Japan. Tokyo (Japon) : Chemicals Inspection & Testing Institute. Japan Chemical Industry Ecology-Toxicology & Information Centre.
Nagano, K., Nakayama, E., Koyano, M., Oobayashi, H., Adachi, H., Yamada, T. 1979. Testicular atrophy of mice induced by ethylene glycol mono alkyl ethers. Sanyo Igaku (revue japonaise sur la santé en milieu industriel) 21: 29-35 (en japonais, avec résumé et tableaux en anglais).
Nagano, K., Nakayama, E., Oobayashi, H., Nishizawa, T., Okuda, H., Yamazaki, K. 1984. Experimental studies on toxicity of ethylene glycol alkyl ethers in Japan. Environ. Health Perspect. 57: 75-84.
[NCI] National Chemical Inventories [base de données sur CD-ROM]. Issue 12006. Columbus (OH) : American Chemical Society. http://www.cas.org/products/cd/nci/index.html
Nelson, B.K., Brightwell, W.S., Burg, J.R., Massari, V.J. 1984. Behavioural and neurochemical alternations in the offspring of rats after maternal or paternal inhalation exposure to the industrial solvent 2-methoxyethanol. Pharmacol.Biochem.Behav. 20: 269-79.
[NPI] National Pollutant Inventory. 2005. Substance Fact Sheet. 2-Methoxyethanol Acetate. Parkes (Australie): Australian Government , Department of the Environment and Water Resources. [consulté le 2 mars 2007]. http://www.npi.gov.au/cgi-bin/npireport.pl?proc=substance;substance=37#Details
[OASIS Forecast] Optimized Approach based on Structural Indices Set [Internet]. 2005. Version 1.20. Bourgas (Bulgarie) : Université Prof. Assen Zlatarov de Bourgas, Laboratoire de chimie mathématique. http://oasis-lmc.org/?section=software
[OMS] Organisation mondiale de la santé. 2003. Fiches internationales de sécurité chimique : Acétate de 2-méthoxyéthyle. ICSC : 0476. http://www.cdc.gov/niosh/ipcsneng/neng0476.html
Osgood, C., Zimmering, S., Mason, J. 1991. Aneuploidy in Drosophila. II. Further validation of the FIX and ZESTE genetic test systems employing female Drosophila melanogaster. Mutat. Res. 259(2): 147-163.
[PCKOCWIN] Organic Carbon Partition Coefficient Program for Windows [modèle d'estimation]. 2000. Version 1.66. Washington (DC) : U.S. Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY) : Syracuse Research Corporation. http://www.epa.gov/oppt/exposure/pubs/episuite.htm
[PhysProp] Interactive PhysProp Database [base de données sur Internet]. 2006. Syracuse (NY) : Syracuse Research Corporation. [consulté en mars 2006]. http://www.syrres.com/esc/physdemo.htm
[PISSC] Programme international sur la sécurité des substances chimiques. 1990. 2 -Methoxyethanol, 2-ethoxyethanol, and their acetates. Genève (Suisse) : Organisation mondiale de la santé. (Critères d'hygiène de l'environnement no 115). Financé conjointemant par le Programme des Nations -Unies pour l'environnement, l'Organisation internationale du travail et l'Organisation mondiale de la santé. http://www.inchem.org/documents/ehc/ehc/ehc115.htm
Plieninger, P., Marchl, D. 1999. Proceedings of the 8th international conference on indoor air quality and climate, vol. 4, Edinburgh (Écosse). Du 8 au 13 août. Londres (Angleterre) : Construction Research Communications LTP.
Schenker, M.B. 1996. Reproductive health effects of glycol ether exposure in the semiconductor industry. Occup. Hyg. 2: 367-72.
Schenker, M.B., Gold, E.B., Beaumont, J.J., Eskenazi, B., Hammond, S.K., Lasley, B.L., McCurdy, S.A., Samuels, J.J., Saiki, C.L., Swan, S.H. 1995. The association of spontaneous abortion and other reproductive effects with work in the semiconductor industry. Am J Ind Med 28(6): 639-659.
Schleibinger, H., Hott, U., Marchl, D., Braun, P., Plieninger, P., Ruden, H. 2001. VOC-concentrations in Berlin indoor environments between 1988 and 1999. Gefahrstoffe Reinhaltung der Luft 61(1-2). 26-38.
Scott, W.J., Fradkin, R., Wittfoht, W., Nau, H. 1989. Teratologic potential of 2-methoxyethanol and transplacental distribution of its metabolite, 2-methoxyacetic acid, in non-human primates. Teratology 39(4): 363-73. [cité dans Canada, 2002].
[SDC] Système de déclaration des cosmétiques [base de données exclusive]. 2008. Ottawa (Ont.) : Santé Canada. [mis à jour en mars 2008].
Sehgal, A., Osgood, C. 1990. Rapid and efficient detection of chemically-induced aneuploidy using Drosophila females. Env. Mol. Mut. 15(suppl.N17): 53-4. [résumé].
Smialowicz, R.J., Williams, W.C., Riddle, M.M., Andrews, D.L., Luebke, R.W. Copeland, C.B. 1992. Comparative immunosuppression of various glycol ethers orally administered to Fischer 344 rats. Fundam. Appl. Toxicol. 18: 621-7.
Smyth, H., Seaton, J., Fisher, L. 1941. The single doses toxicity of some glycols and derivatives. J. Ind. Hyg. Toxicol. 23: 259-68.
Swan, S.H., Beaumont, J.J., Hammond, S.K., VonBehren, J., Green, R.S., Hallock, M.F., Woskie, S.R., Hines, C.J., Schenker, M.B. 1995. Historical cohort study of spontaneous abortion among fabrication workers in the semiconductor health study: agent-level analysis. Am J Ind Med28(6): 751-769.
Swan, S.H., Forest, W. 1996. Reproductive risks of glycol ethers and other agents used in semiconductor manufacturing. Occup. Hyg. 2: 373-385.
[TRI] Toxics base de données sur Internet. 2008 Washington (D.C.) : US Environmental Protection Agency. [consultée décembre] http://www.epa.gov/triexplorer/
[US EPA] U.S. Environmental Protection Agency. 2005. n 2-Ethoxyethanol, 2-ethoxyethanol acetate, 2-methoxyethanol, and 2-methoxyethanol acetate; Significant New Use Rule. Fed Regist 70(228):71401 -71406. [consulté le 5 juillet 2008]. http://www.epa.gov/EPA-TOX/2005/November/Day-29/t23421.htm
[US EPA] U.S. Environmental Protection Agency. 2008. Toxic Release Inventory [TRI]. TRI Explorer 4.7. [consulté en décembre 2007]. http://www.epa.gov/triexplorer/
Verschueren, K. 2001. Handbook of environmental data on organic chemicals. 4e éd . New York (NY) : Van Nostrand Reinhold Co. p. 1115.
Whittaker, S.G., Zimmermann, F.K., Dicus, B., Piegorsch, W.W., Fogel, S., Resnick, M.A. 1989. Detection of induced mitotic chromosome loss inSaccharomyces cerevisiae - an interlaboratory study. Mutat. Res. 224(1): 31-78.
Yalkowsky , S.H., Dannenfelser , R.M. 1992. The Aquasol database of 5e aqueous solubility. éd. Tucson (AZ) : University of Arizona, e of P y College of Pharmacy.
Yanagihara , S., Shimada , I., Shinoyama , E., Chisaka , P., Saito , K. 1977. Photochemical r h reactivities of hydrocarbons. In Proceedings of the Fourth International Clean Air Congress. Tokyo (Japon); Mai. Tokyo (Japon) : Clean Air Society. p. 472 -477.
Yanfeng, G., Shenghua, L., Hejun, G., Tiegang, H., Longbao, Z. 2007. A new diesel oxygenate additive and its effects on engine combustion and emissions. Applied Thermal Engineering 27(1): 202-207.
Zeiger, E., Anderson, B., Haworth, S., Lawlor, T., Mortelmans, K. 1988. Salmonellamutagenicity tests. V. Results from the testing of 311 chemicals. Environ. Mol. Mutagen. 19 S21 2 141 (s21): 2-141.
Zimmermann, F.K., Mayer, V.W., Scheel, I., Resnick, M.A. 1985. Acetone, methylethylketone, ethylacetate, acetonitrile and other polar aprotic solvents are strong inducers of aneuploidy in Saccharomyces cerevisiae. Mutat. Res. 149(3): 339-351.
Annexe I. Sommaire des renseignements concernant les effets de l'acétate de 2-méthoxyéthyle sur la santé
| Paramètre | Doses ou concentrations minimales avec effet/Résultats |
|---|---|
| Toxicité aiguë | DL50la plus faible, par voie orale(cobaye) = 1 250 mg/kg p.c./j (Smyth et al., 1941). [Autres études chez les rats : Smyth et al., 1941; BASF, 1966; Kirk et Othmer, 1980.] DL50 la plus faible par voie cutanée (lapin) = 5 250 à 5 560 mg/kg-p.c. (Kirk-Othmer, 1980). CLmin. la plus faible (cobaye et chat) = 22 000 mg/m3 (3 h) (Gross, 1938). CME(N)O la plus faible, par inhalation (rate) = 32 ppm, soit 154,6 mg/m3 (4 h), d'après l'hémolyse; CSE(N)O = 16 ppm (77,3 mg/m3) (Carpenter et al., 1956). |
| Toxicité à court terme, doses répétées | DME(N)O la plus faible, par voie orale (rat) = 50 mg/kg-p.c. par jour (plus faible dose à l'essai, 6 rats mâles/dose, 2 jours), d'après la suppression de la réponse des cellules à plaques formatrices d'anticorps au trinitrophényl-lipopolysaccharide, effet proportionnel à la dose; aux doses plus élevées, une diminution du titre hémagglutinant a été enregistrée (Smialowicz et al., 1992). CME(N)O la plus faible, par inhalation (chat) = 1 100 mg/m3 (total de 42 heures, pas d'autres précisions), d'après la baisse des pigments sanguins et des corpuscules érythrocitaires (Gross, 1938). Aucune étude à court terme à exposition répétée par voie cutanée n'a été recensée. |
| Toxicité subchronique | Aucune donnée recensée sur la toxicité subchronique. |
| Toxicité chronique et cancérogénicité | Aucune donnée recensée sur la toxicité chronique et la cancérogénicité. |
| Génotoxicté et paramètres connexes : in vivo |
Induction de micronoyaux Induction d'aneuploïdie Résultats négatifs : |
| Génotoxicté et paramètres connexes : in vitro |
Mutation génique les Saccharomyces cerevisiae D61.M, avec et sans activation (Zimmermann et al., 1985). Échange de chromatides soeurs Résultats négatifs : Aberrations chromosomiques Résultats négatifs : Induction de malségrégation et d'aneuploïdie Induction de recombinaison |
| Toxicité sur le plan de la reproduction | DME(N)O la plus faible, par voie orale (souris) = 500 mg/kg-p.c. par jour (5 souris mâles/dose, 5 semaines, gavage); DSE(N)O = 250 mg/kg-p.c. par jour, d'après la diminution du poids absolu des testicules proportionnelle à la dose administrée, l'atrophie au niveau de l'épithélium séminifère et la prolifération occasionnelle des cellules de Leydig (Nagano et al., 1979;id., 1984). [Aucune autre étude n'a été recensée.] |
| Toxicité sur le plan du développement | Effets à 1 225 mg/kg-p.c. par jour par gavage (seule dose à l'essai); souris gravides exposées aux jours de gestation 6 à 13; aucun foetus viable dans les 31 portées; les mères ne semblaient pas touchées par des effets (Hardin et al., 1987). [Aucune autre étude n'a été recensée.] |
| Sensibilisation | Aucune donnée sur la sensibilisation recensée. |
| Irritation | Irritation cutanée. Résultats négatifs ou légère irritation chez les lapins (Carpenter et Smyth, 1946; BASF, 1966). |
| Irritation | Irritation oculaire. Résultats négatifs chez les lapins (Carpenter et Smyth, 1946). Irritation des yeux chez les lapins (BASF, 1966). |
| Paramètre | Doses ou concentrations minimales avec effet/Résultats |
|---|---|
| Toxicité sur le plan de la reproduction et toxicité sur le plan du développement | Risque d'avortement spontané Malformations congénitales Trois études ont révélé qu'un risque accru de malformations congénitales était associé à l'exposition maternelle en milieu de travail à un mélange d'éthers glycoliques, soit une étude cas-témoin (984 cas pour 1 134 témoins) auprès de travailleurs de pays d'Europe de l'Ouest évoluant dans des milieux professionnels divers (Ha et al., 1996; Cordier et al., 1997); une étude de cohorte historique auprès de travailleurs de l'industrie américaine des semi-conducteurs (Gray et al., 1993) et une étude cas-témoin menée en Slovaquie (196 cas pour 196 témoins), semblable à l'étude signalée par Cordier et al. (1997) (Cordier et al., 2001). Aucun renseignement concernant le risque spécifiquement associé à l'acétate de 2 -méthoxyéthyle n'était fourni dans ces études. Rapport de cas On a signalé deux rapports de cas d'hypospadie pénienne et d'un scrotum de type bifide chez les enfants d'une femme exposée à l'acétate de 2-méthoxyéthyle (Bolt et Golka, 1990). |