Évaluation préalable pour le Défi concernant le
Archivée
1-[4-(phénylazo)phénylazo]-2-naphtol
Solvent Red 23
Numéro de registre du Chemical Abstracts Service
85-86-9
Environnement Canada
Santé Canada
Septembre 2011
Table des Matières
- Sommaire
- Introduction
- Identité de la substance
- Propriétés physiques et chimiques
- Sources
- Utilisations
- Rejets dans l'environnement
- Devenir dans l'environnement
- Persistance et potentiel de bioaccumulation
- Potentiel d'effets nocifs sur l'environnement
- Potentiel d'effets nocifs sur la santé humaine
- Conclusion
- Références
- Annexe 1 : Sommaires de rigueur d'étude pour les études clés
- Annexe 2 : Tableau sommaire des intrants des modèles de la persistance, de la bioaccumulation et de la toxicité
- Annexe 3 : Estimations de l'exposition de l'ensemble de la population au Solvent Red 23 dans les cosmétiques et les produits de soins personnels d'après ConsExpo, version 4.1 (ConsExpo, 2006; RIVM, 2006)
- Annexe 4 : Sommaire des renseignements relatifs aux effets sur la santé du Solvent Red 23 (n° CAS : 85-86-9)
- Annexe 5 : Sommaire des renseignements disponibles sur la cancérogénicité et la génotoxicité du Solvent Red 23 et des substances considérées comme analogues au Solvent Red 23 dans la présente évaluation
- Annexe 6 : Sommaire des renseignements disponibles sur la cancérogénicité et la génotoxicité des produits de rupture réductrice des liaisons azoïques potentiels du Solvent Red 23
- Annexe 7 : Sommaires des résultats des RQSA pour le Solvent Red 23 et ses métabolites prévus
Conformément à l’article 74 de la Loi canadienne sur la protection de l’environnement (1999) [LCPE (1999)], les ministres de l’Environnement et de la Santé ont effectué une évaluation préalable sur le 1-[4-(phénylazo)phénylazo)]-2-naphtol (ci-après appelé Solvent Red 23), dont le numéro de registre du Chemical Abstracts Service [1] est 85-86-9. Une priorité élevée a été accordée à l’évaluation préalable de cette substance inscrite au Défi, car elle répondait aux critères environnementaux de la catégorisation relatifs à la persistance, au potentiel de bioaccumulation et à la toxicité intrinsèque pour les organismes non humains et l’on croit qu’elle est commercialisée au Canada.
L’évaluation des risques que présente le Solvent Red 23 pour la santé humaine n’a pas été jugée hautement prioritaire à la lumière des résultats fournis par les outils simples de détermination du risque d’exposition et du risque pour la santé élaborés par Santé Canada aux fins de la catégorisation des substances de la Liste intérieure des substances.
Le Solvent Red 23 est une substance organique utilisée au Canada principalement dans des huiles, des graisses et des cires, mais aussi dans des solvants alcooliques, esters et hydrocarbonés, dans du polystyrène et des cosmétiques et comme indicateur. On l’utilise aussi comme colorant pour pesticides et il a déjà été utilisé comme teinture à textile. Cette substance n’est pas produite naturellement dans l’environnement. La fabrication du Solvent Red 23 n’a pas été déclarée au Canada. En 2006, du Solvent Red 23 a été importé ou utilisé au Canada. Toutefois, quatre entreprises ont déclaré avoir importé entre 100 et 1 000 kg de cette substance en produits au pays en 2005 pour répondre au sondage mené au Canada conformément à l’article 71 de la LCPE.
En se basant sur les profils d’utilisation déclarés au Canada dans les produits de soins personnels, on peut penser que tous les produits contenant du Solvent Red 23 pourraient être rejetés dans les égouts, les eaux de surface ou le sol au cours de leur utilisation. Les eaux d’égout pourraient recevoir la plus forte proportion de Solvent Red 23 au cours de l’utilisation des produits. On prévoit que la majeure partie de cette substance, fixée aux boues d’épuration des eaux usées venant des stations de traitement des eaux usées à la suite de rejets aux égouts de cosmétiques et de produits de soins personnels, sera entraînée dans les boues vers des sites d’enfouissement. En plus d’être mis en décharge, une partie des biosolides produits par les stations de traitement des eaux usées peuvent être épandus sur des terres en tant qu’engrais ou amendement synthétique à des fins agricoles, forestières ou de remise en état, et un petit pourcentage peut être incinéré.
On croit que le Solvent Red 23 n’est pas soluble dans l’eau et n’est pas volatil, mais qu’il sera adsorbé sur des particules en raison de sa nature hydrophobe. Pour ces raisons, le Solvent Red 23 se retrouvera sans doute principalement dans les sédiments et, peut-être dans une moindre mesure, dans les sols agricoles amendés avec des biosolides, après son rejet dans l’eau. On est d’avis que le Solvent Red 23 ne sera pas présent de manière significative dans d’autres milieux, et qu’il est peu probable qu’il fasse l’objet d’un transport atmosphérique à grande distance.
D’après ses propriétés physiques et chimiques, le Solvent Red 23 devrait être persistant dans l’eau, le sol et les sédiments. Toutefois, des données expérimentales sur le potentiel de bioaccumulation de deux analogues à la structure relativement similaire semblent indiquer que ce colorant a un faible potentiel d’accumulation dans les tissus adipeux des organismes. Cette substance répond donc aux critères de persistance, mais non à ceux de bioaccumulation énoncés dans leRèglement sur la persistance et la bioaccumulation. De plus, des données expérimentales sur la toxicité d’analogues chimiques amènent à penser que le Solvent Red 23 n’entraîne pas d’effets nocifs aigus chez les organismes aquatiques exposés à de faibles concentrations.
Pour la présente évaluation préalable finale, on a retenu un scénario d’exposition cumulative prudent, dans lequel une même station de traitement des eaux usées rejette, dans le milieu aquatique, la quantité maximale de Solvent Red 23 selon les données de 2005. De plus, étant donné que le Solvent Red 23 peut être utilisé dans les produits de consommation, un scénario de rejet prudent a été élaboré selon une estimation de la quantité de ce colorant sur le marché canadien. Les concentrations environnementales estimées étaient largement inférieures à la concentration estimée sans effet calculée pour les espèces aquatiques fragiles.
À la lumière des renseignements disponibles, on conclut que le Solvent Red 23 ne pénètre pas dans l’environnement en une quantité ou concentration ou dans des conditions de nature à avoir, immédiatement ou à long terme, un effet nocif sur l’environnement ou sur sa diversité biologique, ou à mettre en danger l’environnement essentiel pour la vie.
On est d’avis que l’exposition du public au Solvent Red 23 dans l’environnement est négligeable. Toutefois, il peut y être exposé lors de l’utilisation de cosmétiques et de produits de soins personnels contenant du Solvent Red 23. Les données empiriques sur les effets sur la santé pour cette substance sont limitées. Le Solvent Red 23 fait partie de la classe de composés caractérisés par la présence d’une liaison azoïque ou plus (-N=N-), ce qui peut donner lieu à un clivage réductif des azoïques causant le rejet d’amines aromatiques. Le clivage réductif des azoïques du Solvent Red 23 peut notamment causer le rejet de 4-aminoazobenzène, une substance qui a été classée par le Centre International de Recherche sur le Cancer (CIRC) et la commission européenne en fonction de sa cancérogénicité. La structure du Solvent Red 23 est également similaire à celle d’un colorant azoïque qui provoque un processus néoplasique du foie chez les rats mâles et femelles exposés oralement selon la dose administrée, et il est classé comme étant un agent mutagène et cancérogène par la commission européenne. Selon la considération du potentiel d’exposition de l’ensemble de la population découlant de l’utilisation de cosmétiques et de produits de soins personnels contenant du Solvent Red 23, et des données démontrant le potentiel de génotoxicité et de cancérogénicité pour lesquelles il peut y avoir une probabilité de préjudice à tous les niveaux d’exposition, on conclut que le Solvent Red 23 est rejeté dans l’environnement en quantité, à une concentration ou dans des conditions pouvant constituer un danger au Canada pour la vie et la santé humaine.
Des activités de recherche et de surveillance viendront, s’il y a lieu, appuyer la vérification des hypothèses formulées au cours de l’évaluation préalable et, le cas échéant, l’efficacité des mesures de contrôle possibles définies à l’étape de la gestion des risques.
D’après les renseignements disponibles, il est conclu que le 1-[4-(phénylazo)phénylazo)]-2-naphtol répond à un ou plusieurs des critères énoncés à l’article 64 de la LCPE (1999).
La Loi canadienne sur la protection de l’environnement (1999) [LCPE (1999)] (Canada, 1999) exige que les ministres de l’Environnement et de la Santé procèdent à une évaluation préalable des substances qui répondent aux critères de catégorisation énoncés dans la Loi afin de déterminer si elles présentent ou sont susceptibles de présenter un risque pour l’environnement ou la santé humaine.
En se fondant sur l’information obtenue dans le cadre de la catégorisation, les ministres ont jugé qu’une attention hautement prioritaire devait être accordée à un certain nombre de substances, à savoir :
- celles qui répondent à tous les critères environnementaux de catégorisation, notamment la persistance (P), le potentiel de bioaccumulation (B) et la toxicité intrinsèque pour les organismes aquatiques (Ti), et que l’on pense être commercialisées au Canada;
- celles qui répondent aux critères de catégorisation pour le plus fort risque d’exposition (PFRE) ou qui présentent un risque d’exposition intermédiaire (REI) et qui ont été jugées particulièrement dangereuses pour la santé humaine, compte tenu des classifications qui ont été établies par d’autres organismes nationaux ou internationaux concernant leur cancérogénicité, leur génotoxicité ou leur toxicité pour le développement ou la reproduction.
Le 9 décembre 2006, les ministres ont donc publié un avis d’intention dans la Partie I de la Gazette du Canada(Canada, 2006a), dans lequel ils priaient l’industrie et les autres parties intéressées de fournir, selon un calendrier déterminé, des renseignements précis qui pourraient servir à étayer l’évaluation des risques, ainsi qu’à élaborer et à évaluer les meilleures pratiques de gestion des risques et de bonne gestion des produits pour ces substances d’importance prioritaire.
La substance 1-[4-(phénylazo)phénylazo]-2-naphtol (qui sera appelée Solvent Red 23 dans le présent document) a été jugée hautement prioritaire pour l’évaluation des risques écologiques, car elle a été jugée persistante, bioaccumulable et intrinsèquement toxique pour les organismes aquatiques et l’on croit qu’elle est commercialisée au Canada. Le volet du Défi portant sur cette substance a été publié dans laGazette du Canada le 31 mai 2008 (Canada, 2008a, 2008b). En même temps a été publié le profil de cette substance qui présentait l’information technique (obtenue avant décembre 2005) sur laquelle a reposé sa catégorisation. Le Défi a permis d’obtenir des renseignements sur les utilisations du Solvent Red 23 et sur certains produits de formulation.
Même si l’évaluation des risques que présente le Solvent Red 23 pour l’environnement est jugée hautement prioritaire, cette substance ne répond pas aux critères pour le PFRE ou le REI ni aux critères définissant un grave risque pour la santé humaine, compte tenu du classement attribué par d’autres organismes nationaux ou internationaux quant à sa cancérogénicité, à sa génotoxicité ou à sa toxicité sur le plan du développement ou de la reproduction.
Les évaluations préalables mettent l’accent sur les renseignements jugés essentiels pour déterminer si une substance répond aux critères énoncés à l’article 64 de la LCPE (1999). Les évaluations préalables examinent les renseignements scientifiques et tirent des conclusions fondées sur la méthode du poids de la preuve et le principe de prudence[2].
La présente évaluation préalable finale prend en considération les renseignements sur les propriétés chimiques, les dangers, les utilisations et l’exposition, y compris ceux fournis dans le cadre du Défi. Les données pertinentes pour l’évaluation préalable de cette substance sont tirées de publications originales, de rapports de synthèse et d’évaluation, de rapports de recherche de parties intéressées et d’autres documents consultés lors de recherches documentaires menées récemment, jusqu’en juillet 2010. Les études importantes ont fait l’objet d’une évaluation critique; les résultats de la modélisation ont pu être utilisés dans la formulation des conclusions. Lorsqu’ils étaient disponibles et pertinents, les renseignements contenus dans les évaluations des dangers effectués par d’autres instances ont été utilisés. La présente évaluation préalable finale ne constitue pas un examen exhaustif ou critique de toutes les données disponibles. Il s’agit plutôt d’un sommaire des renseignements essentiels qui appuient la conclusion.
Cette évaluation préalable finale a été préparée par le personnel du Programme des substances existantes de Santé Canada et d’Environnement Canada et elle intègre les résultats d’autres programmes exécutés par ces ministères. Les portions de la présente évaluation portant sur l’écologie ont fait l’objet d’une étude consignée par des pairs ou d’une consultation de ces derniers. Des experts scientifiques choisis et dirigés par la Toxicology Excellence for Risk Assessment (TERA), notamment M. Larry Claxton (Ph.D.), M. Bernard Gadagbui (Ph.D.), M. Pertti Hakkinen (Ph.D.), M. Glenn Talaska (Ph.D.) et Mme Pam Williams (Ph.D.), ont formulé des commentaires sur les portions techniques touchant la santé humaine.
En outre, l’ébauche de la présente évaluation préalable a fait l’objet d’une période de commentaires du public de 60 jours. Bien que les commentaires venant de l’extérieur aient été pris en considération, Santé Canada et d’Environnement Canada sont seuls responsables du contenu final et des résultats de l’évaluation préalable. Les approches suivies lors évaluations préalables dans le cadre du Défi ont été examinées par un groupe indépendant, soit le Groupe consultatif du Défi.
Les considérations et renseignements importants qui sous-tendent la présente évaluation sont présentés ci-après.
Nom de la substance
Aux fins du présent document, 1-[4-(phénylazo)phénylazo]-2-naphtol sera appelé Solvent Red 23, conformément à son nom dans le Colour Index (n° du Colour Index : 26100; CII 2002). Les renseignements sur l’identité de la substance sont présentés au tableau 1 ci-dessous.
| Numéro de registre du Chemical Abstracts Service (n° CAS) | 85-86-9 |
|---|---|
| Nom dans la LIS | 1-[4-(phénylazo)phénylazo]-2-naphtol |
| Noms dans les inventaires[1] | 2-naphthalenol, 1-[[4-(phenylazo)phenyl]azo]- (TSCA, AICS, PICCS, ASIA-PAC, NZIoC) 1-(4-(phénylazo)phénylazo)-2-naphtol (EINECS) Solvent Red 23 (ENCS, PICCS) C.I. solvent red 02 (ECL) Sudan III (PICCS) naphth-2-ol, 1-((4-phenylazo)phenyl)azo)- (PICCS) |
| Autres noms | 1-(p-Phenylazophenylazo)-2-naphthol; 111440 Red; 2-Naphthol, 1-(p-phenylazophenylazo)-; Brasilazina Oil Scarlet; C.I. 26100; C.I. Solvent Red 23; Certiqual Oil Red; D and C Red No. 17; Fast Oil Scarlet III; Fat Red Bluish; Fat Red HRR; Fat Red R; Fat Red RS; Fat Scarlet LB; Fat Soluble Red Zh; FD And C Red No. 17; Grasal Brilliant Red G; Grasan Brilliant Red G; Japan Red 225; Japan Red No. 225; NSC 65825; NSC 8995; Oil Red 3G; Oil Red AS; Oil Red Extra; Oil Scarlet G; Organol Red BS; Organol Scarlet; Red No. 225; Red Zh; Silotras Scarlet TB; Somalia Red III; Stearix Scarlet; Sudan 3; Sudan P III; Sudan Red III; Tetrazobenzene-b-naphthol; Toney Red |
| Catégorie de la substance | Substances organiques définies |
| Classe chimique | Composés azoïques |
| Groupe chimique | Composés diazoïques |
| Formule chimique | C22H16N4O |
| Structure chimique |  |
| SMILES[2] | Oc(ccc(c1ccc2)c2)c1N=Nc(ccc(N=Nc(cccc3)c3)c4)c4 |
| Poids moléculaire | 352,40 g/mol |
[2] Simplified Molecular Input Line Entry System.
Solvent Red 23 est un colorant diazoïque. Les deux liens azoïques (–N=N–) de cette molécule sont des groupements fonctionnels qui produisent de la couleur (EPA du Danemark, 1999). Les colorants peuvent être classés selon leur structure chimique, mais aussi selon leurs applications industrielles et les méthodes de teinture du substrat considéré (ETAD, 1995). Leur classification, qui inclut les colorants acides et directs, tend à refléter les regroupements basés sur les propriétés physiques et chimiques des substances. Un bref exposé des usages de ce colorant est consultable à la partie « Utilisations » du présent document.
On dispose de peu de données expérimentales sur les propriétés physiques et chimiques du Solvent Red 23. À l’occasion de l’atelier sur les relations quantitatives structure-activité (RQSA) organisé par Environnement Canada en 1999 (Environnement Canada, 2000), des experts en modélisation ont classé de nombreuses catégories structurales de pigments et de teintures comme « difficiles à modéliser » à l’aide de RQSA. Les propriétés physiques ou chimiques de nombreuses classes structurales de teintures et de pigments se prêtent mal à la prévision modélisée, car on considère qu’elles « ne font pas partie du domaine d’applicabilité » (p. ex. domaines de la structure ou des paramètres des propriétés). Par conséquent, lorsqu’il s’agit de teintures et de pigments, on vérifie au cas par cas les domaines d’applicabilité des modèles RQSA pour déterminer leur utilité potentielle.
Pour la présente évaluation, on estime que certains modèles RQSA utilisés pour prévoir les propriétés physiques et chimiques qui n’ont pas de substances comparables au Solvent Red 23 dans leur domaine d’applicabilité peuvent produire des résultats ayant un degré d’incertitude élevé. Par conséquent, une méthode par analogie a été utilisée pour déterminer les propriétés physiques et chimiques approximatives au tableau 2. Ces propriétés ont été par la suite considérées lors de l’évaluation de diverses sources de données. Le tableau 2 présente certaines propriétés physiques et chimiques (valeurs calculées et extrapolées) du Solvent Red 23 et des analogues.
Un analogue est un produit chimique dont la structure est similaire à celle de la substance évaluée; il devrait donc avoir des propriétés physiques et chimiques, un comportement dans l’environnement et une toxicité semblables. Lorsque ce sont des données expérimentales pour un paramètre donné d’une substance analogue, celles-ci peuvent être directement utilisées ou avec un ajustement, comme estimation de cette valeur de paramètre pour la substance en cours d’évaluation.
Pour trouver des analogues acceptables, une revue des données pour plusieurs colorants azoïques dispersés a été effectuée (Anliker et al., 1981; Anliker et Moser, 1987; Baughman et Perenich; 1988, ETAD, 1995; Brown, 1992; Yen et al., 1989, Sijm et al., 1999). En plus de leurs similitudes structurelles avec le Solvent Red 23, ces composés partagent d’autres caractéristiques avec la substance, qui renforcent leur pertinence en tant qu’analogues. Cela comprend les propriétés influant sur leur devenir dans l’environnement comme des masses moléculaires élevées (généralement supérieures à 300 g/mol), un diamètre transversal élevé (entre 1,31 et 2,19 nm), des structures particulaires solides, un point de décomposition supérieur à 120 ºC et une « dispersabilité » dans l’eau (c’est-à-dire que ces composés ne sont pas entièrement « solubles »). De plus, leur pression de vapeur est négligeable et ils sont stables dans des conditions environnementales, car ils ont été conçus pour l’être. D’autres analogues ont été choisis aux fins de l’évaluation de la santé humaine, dans les cas où des données existent (voir la section Potentiel d’effets nocifs sur la santé humaine pour la justification et l’analyse).
Comme certaines des études concernant les colorants diazoïques ont été réalisées dans des conditions environnementales non pertinentes (à des températures élevées, par exemple) ou présentent peu de renseignements permettant d’évaluer leur fiabilité, des données sur les colorants dispersés monoazoïques et les colorants dispersés azoïques, en général, sont incluses dans le tableau 2.
| Propriété | Type[1] | Valeur | Température (°C) | Référence | |
|---|---|---|---|---|---|
| État physique | Analogue Disperse Orange 29 |
Poudre | Étude présentée, 2008a | ||
| Point de décomposition[2] (ºC) |
Solvent Red 23 | 195 | PhysProp, 2006 | ||
| Analogue Sudan IV (aussi appelé Solvent Red 24) | 185 | MITI, 1992 | |||
| Analogue Disperse Orange 29 |
223 | ETAD, 2005 | |||
| Analogue Disperse Yellow 23 |
158 178 | Odabasoglu et al., 2003; Datyner, 1978 | |||
| Analogue Disperse Orange 13 |
153 à 156,5 | NIshida et al., 1989 | |||
| Analogue Disperse Orange 30 | 126,9 à 128,5 | ETAD, 2005 | |||
| Analogue Disperse Blue 79 | 157 | PhysProp, 2006 | |||
| Analogue Disperse Blue 79:1 | 132 153 | Sijm et al., 1999; Yen et al., 1989 | |||
| Données déduites à partir d’analogues des colorants azoïques dispersés | 117 à 175 74 à 236 | Anliker et Moser, 1987; Baughman et Perenich, 1988 | |||
| Point d’ébullition[3] (ºC) |
Sans objet | ||||
| Masse volumique (kg/m3) |
Non disponible | ||||
| Pression de vapeur (Pa) |
Analogue Disperse Orange 13 |
0,18 à 0,42[4] | 191,5 à 211 | Nishida et al., 1989 | |
| Analogue Disperse Blue 79 |
4,53 x 10-7 | Clariant, 1996 | |||
| Données déduites à partir d’analogues des colorants azoïques dispersés | 5,3 x 10-12 à 5,3 x 10-5) (4 x 10-14 à 4 x 10-7 mm Hg) |
25 | Baughman et Perenich, 1988 | ||
| Constante de la loi de Henry (Pa·m3/mol) |
Données déduites à partir d’analogues des colorants azoïques | 10-8 à 10-1 (10-13 à 10-6atm·m3/mol)[5] |
Baughman et Perenich, 1988 | ||
| Log Koe (coefficient de partage octanol-eau) (sans dimension) |
Analogue Disperse Orange 29 |
4,6[6] | Étude présentée, 2008a | ||
| Analogue Disperse Blue 79 |
4,1; 4,3[7] | Clariant, 1996; Brown, 1992 | |||
| Analogue Disperse Blue 79:1 | 4,4; 4,8 | Sijm et al., 1999; Yen et al., 1989 | |||
| Analogue Disperse Orange 30 |
4,2[8] | Brown, 1992 | |||
| Données déduites à partir d’analogues des colorants azoïques dispersés | 1,79 à 5,1 | Baughman et Perenich, 1988 | |||
| > 2 à 5,1 | Anliker et al., 1981; Anliker et Moser, 1987 | ||||
| Log Kco (coefficient de partage carbone organique-eau) (sans dimension) |
Données déduites à partir d’analogues, calculées | 3,4 à 4,2[9] | Baughman et Perenich, 1988 | ||
| Solubilité dans l’eau (mg/L) |
Analogue Disperse Orange 13 |
0,345 | PhysProp, 2006 | ||
| Analogue Disperse Orange 29 |
42,9[6] | Étude présentée, 2008a | |||
| 0,0037 | 25 | Baughman et al., 1996 (estimé) | |||
| Analogue Disperse Yellow 23 |
0,00006 | 25 | Baughman et Perenich, 1988 | ||
| 0,00052 | Baughman et al., 1996 (estimé) | ||||
| 15,7 à 34,8[4] | 130 | Braun, 1991 | |||
| Analogue Disperse Yellow 68 |
16,6[4] | 125 | Prikryl et al., 1979 | ||
| Analogue Disperse Blue 79 | 0,0054 | 25 | Clariant, 1996 | ||
| 0,02[7] | Brown, 1992 | ||||
| Analogue Disperse Blue 79:1 | 0,02 | Sijm et al., 1999 | |||
| 0,0052 | Yen et al., 1989 | ||||
| 0,00063[4] | 100 à 125 | Baughman et Perenich, 1988 | |||
| Disperse Orange 30 | 0,07[8] | Brown, 1992 | |||
| Données analogues des colorants azoïques dispersés | < 0,01 | 20 | Anliker et Moser, 1987 | ||
| Très peu soluble dans l’eau | ETAD, 1995 | ||||
| 1,2 x 10-5 à 35,5 (4 x 10-11à 1,8 x 10-4 mol/L) | Baughman et Perenich, 1988 | ||||
| Solubilité dans le n-octanol (mg/L) | Analogue Disperse Orange 29 |
5 086 | ETAD, 2005 | ||
| Analogue Disperse Orange 30 | 576 | ETAD, 2005 | |||
| Analogue Disperse Blue 79:1 |
14 | Sijm et al., 1999 | |||
| Données analogues des colorants azoïques dispersés | 81 à 2100 | 20 | Anliker et Moser, 1987 | ||
| pKa (constante de dissociation) (sans dimension) |
Solvent Red 23 | 13,5 | ACD/pKa DB, 2005 | ||
| Disperse Yellow 23 | 8,1 | Haag et Mill, 1987 | |||
[2] On utilise l’expression « point de fusion », mais il serait plus exact de parler de point de décomposition; en effet, il est du domaine connu qu’à des températures élevées (supérieures à 200 °C) les colorants dispersés ne fondent pas, mais se carbonisent.
[3] En général, la notion de point d’ébullition ne s’applique pas aux colorants dispersés. Dans le cas des colorants en poudre, on observe, à température élevée, une carbonisation ou une décomposition de la substance plutôt qu’une ébullition. Pour ce qui est des liquides et des pâtes colorantes, on observe l’ébullition du solvant seulement, alors que le composant solide qui ne s’est pas évaporé se décompose ou se carbonise (ETAD, 1995).
[4] Il est à noter que les analyses de la solubilité de l’eau dans le cadre de ces études ont été menées à des températures très élevées; les valeurs sont donc plus élevées qu’on ne l’avait prévu à température ambiante.
[5] Les valeurs de solubilité de cinq colorants azoïques dispersés (Disperse Orange 3, Disperse Red 1, Solvent Yellow 2, Dis. A. 5, Dis. A. 7) à 25 et 80 °C ont été utilisées par Baughman et Perenich (1988) pour calculer les constantes de la loi de Henry de ces colorants. Nous donnons une plage de valeurs pour illustrer la constante de la loi de Henry prévue en ce qui concerne les colorants diazoïques.
[6] L’étude indique que le Disperse Orange 29 utilisé dans l’essai avait une dispersion du colorant à 20 % (eau 70 % et Reax 10 %).
[7] L’étude indique que le Disperse Blue 79 utilisé dans l’essai avait une pureté (de matières organiques) de 76 % et une dispersion du colorant à 20 %.
[8] L’étude indique que le Disperse Orange 30 utilisé dans l’essai avait une pureté (de matières organiques) de 73 % et une dispersion du colorant à 20 %.
[9] Les valeurs du log Kcosont fondées sur les calculs que Baughman et Perenich (1988) ont réalisés en utilisant une plage de valeurs de solubilité mesurées pour des colorants commerciaux, à un point de fusion supposé de 200 ºC.
En raison du peu de données empiriques sur le Solvent Red 23 et de l’erreur associée aux résultats de la modélisation portant sur les colorants dispersés, certaines données empiriques sur les propriétés physiques et chimiques (tableau 2), des données sur la bioaccumulation (tableaux 5a et 5b) et des données sur la toxicité aquatique (tableau 6) ont été utilisées pour étayer la preuve et les conclusions proposées dans cette évaluation préalable. Plus précisément, des données ont été obtenues sur un colorant solvant similaire (Sudan IV/Solvent Red 24), quatre colorants dispersés diazoïques ayant une structure similaire (Disperse Orange 29, Disperse Yellow 23, Disperse Yellow 68 et Disperse Orange 13) et six colorants monoazoïques ayant une structure similaire (Disperse Blue 79, Disperse Blue 79:1, Disperse Orange 30, Disperse Red 73, Disperse Orange 25 et Disperse Red 17). Des renseignements sur l’identité de la substance et des données empiriques sur les analogues utilisés dans le présent rapport sont présentés au tableau 3a, alors que les masses moléculaires et les diamètres transversaux sont présentés au tableau 3b.
| Nom commun (n° CAS) | Nom dans la LIS | Structure | Similarités et différences majeures avec le Solvent Red 23 | Données empiriques disponibles[1] |
|---|---|---|---|---|
| Solvent Red 23 (85-86-9) |
1-[4-(Phénylazo)phénylazo]-2-naphtol |  |
Sans objet (même substance). | Point de fusion |
| Sudan IV (aussi appelé Solvent Red 24) (85-83-6) |
1-({2-Méthyl-4-[(2-méthylphényl)azo]phényl}azo)-2-naphtalénol |  |
Similarités : Composé diazoïque aromatique avec un noyau napthtalène et un groupement hydroxyle. Même nombre de noyaux Différences : Deux groupements méthyle de plus – chacun attaché aux noyaux individuels. |
Point de fusion, toxicité, FBC |
| Disperse Orange 29 (19800-42-1) |
4-[[2-Méthoxy-4-[(4-nitrophényl) azo]phényl]azo)] phénol |
 |
Similarités : Composé diazoïque aromatique avec un groupement hydroxyle. Différences : Le Solvent Red 23 contient un noyau naphtalène et ne contient pas de groupement nitro terminal ni de groupement éthers |
État physique, point de fusion, log Koe, solubilité dans l’eau, solubilité dans le n-octanol |
| Disperse Yellow 23 (6250-23-3) |
p-[[p-(Phénylazo)phényl]azo]phénol |  |
Similarité : Composé diazoïque aromatique avec un groupement hydroxyle Différences : Disperse Yellow 23 ne contient pas de noyau naphtalène |
Point de fusion, solubilité dans l’eau, pKa et toxicité pour les organismes aquatiques |
| Disperse Yellow 68 (21811-64-3) |
Phénol, 4,4’-[1,4-phenylenebis(azo)]bis |  |
Similarité : Composé diazoïque aromatique avec un groupement hydroxyle Différence : Disperse Yellow 68 ne contient pas de noyau naphtalène et contient un groupement hydroxyle additionnel |
Solubilité dans l’eau |
| Disperse Orange 13 (6253-10-7) |
p-[[4-(Phénylazo)-1-naphtyl]azo]phénol |  |
Similarité : Composé diazoïque aromatique avec un noyau de naphtalène et un groupement hydroxyle Différence : Disperse Orange 13 contient un noyau naphtalène dans une position différente |
Point de fusion, hydrosolu-bilité, solubilité dans l’octanol |
| Disperse Orange 25 (31482-56-1) |
3-[Éthyl[4-[(4-nitrophényl)azo] phényl]amino] propiononitrile |
 |
Similarité : Composé diazoïque aromatique. Différence : Pas de second groupement azoïque, Disperse Orange 25 contient un nitrile, un groupement nitro et amine et n’a pas de noyau naphtalène |
Toxicité pour les organismes aquatiques |
| Disperse Orange 30 (5261-31-4) |
Acétate de 2-[N-(2-cyanoéthyl)-4-[2,6-dichloro-4-nitrophényl)azo]anilino]éthyle |  |
Similarité : Composé diazoïque aromatique. Différence : Pas de second groupement azoïque, Disperse Orange 30 contient des groupements fonctionnels nitrile, carboxylique, nitro et amine, et deux groupements chlore |
Bioaccumulation, toxicité pour les organismes aquatiques, log Koe |
| Disperse Blue 79 (12239-34-8) |
Diacétate de 2,2’-[[5-acétamide-4-[(2-bromo-4,6-dinitrophényl)azo]-2-éthoxyphényl] imino]diéthyle |
 |
Similarité : Composé diazoïque aromatique. Différence : Pas de second groupement azoïque, Disperse Blue 79 contient deux groupements carboxyliques, deux groupements fonctionnels nitro, une aniline ayant deux chaînes carbonées, un groupement fonctionnel amine et un groupement brome |
Point de fusion, pression de vapeur, log Koe, solubilité dans l’eau et toxicité de cette substance pour les organismes aquatiques |
| Disperse Blue 79:1 (3618-72-2) |
Diacétate de 2,2’-{[5-acétamido-4-(2-bromo-4,6-dinitrophénylazo)-2-méthoxyphényl] imino}diéthyle |
 |
Similarité : Composé diazoïque aromatique. Différence : Pas de second groupement azoïque, Disperse Blue 79:1 contient deux groupements carboxylique, deux groupements fonctionnels nitro, un groupement fonctionnel amine et une aniline avec deux courtes chaînes carbonées |
Point de fusion, log Koe, solubilité dans l’eau, bioaccumu lation et toxicité de cette substance pour les organismes aquatiques |
| Disperse Red 17 (3179-89-3) |
2,2'-[[3-méthyl-4-(4-nitrophénylazo) phényl]imino] diéthanol |
 |
Similarité : Composé diazoïque aromatique avec un groupement hydroxyle. Différence : Pas de second groupement azoïque, Disperse Red 17 contient un groupement hydroxyle additionnel et une aniline avec deux courtes chaînes carbonées |
Toxicité pour les organismes aquatiques |
| Disperse Red 73 (16889-10-4) |
2-({4-[(2-Cyanoéthyl)(2-phényléthyl)amino]phényl}azo)-5-nitrobenzonitrile |  |
Similarité : Composé diazoïque aromatique. Différence : Pas de second groupement azoïque, Disperse Red 73 contient deux groupements fonctionnels nitrile, des groupements nitro et aniline et deux courtes chaînes carbonées |
Toxicité pour les organismes aquatiques |
| Substance | N° CAS | Nom commun | Masse moléculaire (g/mol) | Dmax minimum–maximum (nm)[1] |
|---|---|---|---|---|
| Colorants solvants et colorants dispersés diazoïques | 85-86-9 | Solvent Red 23 | 352 | 1,50–2,03 |
| 85-83-6 | Sudan IV | 380 | 1,50–2,05 | |
| 19800-42-1 | Disperse Orange 29 | 377 | 1,56–2,19 | |
| 6250-23-3 | Disperse Yellow 23 | 302 | 1,50–2,07 | |
| 6253-10-7 | Disperse Orange 13 | 352 | 1,56–2,07 | |
| 21811-64-3 | Disperse Yellow 68 | 318 | 2,09–2,14 | |
| Colorants monoazoïques analogues | 12239-34-8 | Disperse Blue 79 | 639 | 1,69–2,05 |
| 3618-72-2 | Disperse Blue 79:1 | 625 | 1,43–2,03 | |
| 5261-31-4 | Disperse Orange 30 | 450 | 1,75–1,98 | |
| 16889-10-4 | Disperse Red 73 | 348 | 1,31–1,93 | |
| 31482-56-1 | Disperse Orange 25 | 323 | 1,37–1,95 | |
| 3179-89-3 | Disperse Red 17 | 344 | 1,41–1,86 |
Il faut noter qu’il existe plusieurs incertitudes associées à l’utilisation des données physiques, chimiques, toxicologiques et de bioaccumulation disponibles pour les substances. Toutes ces substances partagent le même groupe chimique, soit les composés azoïques (un sous-ensemble contient deux liaisons azoïques et un autre contient une liaison azoïque) – et sont utilisées à des fins industrielles similaires (c.-à-d. les colorants dispersés et un colorant solvant). Toutefois, ces substances présentent des différences liées à leur groupement fonctionnel propre (voir le tableau 3a). Malgré le fait que certains de ces colorants monoazoïques ont des masses moléculaires plus élevées que les colorants diazoïques, leur état physique, leurs points de fusion, leur solubilité dans l’eau, leur log Koe et leurs diamètres transversaux (tableau 3b) comparables offrent un fondement raisonnable permettant de conclure que les colorants monoazoïques auront un comportement similaire à celui des colorants diazoïques dans l’environnement et présenteront une biodisponibilité à peu près égale, et que leur utilisation comme analogues pour le Solvent Red 23 est donc acceptable.
Le Solvent Red 23 n’est pas produit naturellement dans l’environnement.
Des enquêtes menées récemment auprès de l’industrie en 2005 et 2006 par le truchement d’avis publiés dans laGazette du Canada conformément à l’article 71 de la LCPE (1999), ont permis de recueillir des renseignements récents (Canada, 2006b et 2008b). Ces avis demandaient que soient fournies des données sur la fabrication, l’importation et l’utilisation de Solvent Red 23 au Canada. Dans l’avis pour 2006, des données étaient également demandées sur les quantités utilisées de ce colorant. Dans le contexte de l’enquête susmentionnée pour 2005 et 2006, les entreprises qui n’étaient pas tenues de fournir des données selon les critères établis, mais qui avaient un intérêt commercial se rapportant au Solvent Red 23 ont été invitées à s’identifier en tant que parties intéressées.
Bien qu’elles ne répondent pas aux exigences obligatoires de déclaration, neuf entreprises ont manifesté un intérêt pour le Solvent Red 23 à l’aide du formulaire Déclaration des parties intéressées relatif à l’avis émis en application de l’article 71 pour 2006 (Environnement Canada, 2008a). Dans plus d’un cas, l’intérêt concernait l’importation ou l’utilisation courante de la substance au Canada en deçà du seuil. En 2005, quatre entreprises ont chacune déclaré avoir importé entre 100 et 1 000 kg de Solvent Red 23 (Environnement Canada, 2006). En 2005, huit entreprises ont déclaré avoir un intérêt en tant que partie intéressée pour le Solvent Red 23 (Environnement Canada, 2006).
Pendant l’élaboration de la Liste intérieure des substances (LIS), la quantité de Solvent Red 23 déclarée avoir été fabriquée, importée ou commercialisée en 1986 était de 2 200 kg (Environnement Canada, 1988).
Le Solvent Red 23 a été reconnu comme une substance chimique produite en faible quantité dans l’Union européenne (UE). Sa production au sein de l’Union européenne a été estimée entre 10 et 1 000 tonnes par an, environ (ESIS, 2008). Le Solvent Red 23 a également été utilisé en Suède de 1999 à 2006 et au Danemark de 2003 à 2006 (SPIN, 2008).
Les produits contenant du Solvent Red 23 peuvent entrer dans le pays même s’ils n’ont pas été recensés en tant que tels dans l’enquête menée en vertu de l’article 71, en raison de leur importation involontaire dans les articles manufacturés ou de leurs quantités inférieures au seuil de déclaration de 100 kg établi pour l’enquête.
Des renseignements relatifs aux utilisations pour les années civiles 2005 et 2006 ont été recueillis en réponse aux avis publiés en application de l’article 71 de la LCPE (1999) (Canada, 2006b, 2008b). En 2005, les importateurs du Solvent Red 23 ont indiqué qu’ils faisaient le commerce de détail de cosmétiques, de parfums, d’articles de toilette et de produits d’hygiène personnelle ou offraient des services de coiffure ou d’esthétique (Environnement Canada, 2006). En 2006, aucune des entreprises ayant déclaré qu’elles importaient ou utilisaient le Solvent Red 23 dans la Déclaration des parties intéressées n’a indiqué le type d’utilisation (Environnement Canada, 2008a). Au cours du processus d’inscription des substances sur la LIS (de 1984 à 1986), le code d’utilisation de la LIS pour les catégories « colorant / pigment / teinture / encre », « parfum / désodorisant / aromatisant », « cosmétiques », « santé et vétérinaire », « produits pharmaceutiques », « pigment, teinture et encre d’imprimerie » et « textile, produits » ont été employés pour le Solvent Red 23.
Le Solvent Red 23 est actuellement utilisé dans les cosmétiques de plusieurs pays dont le Canada, les États-Unis et l’Europe. Au Canada, le Solvent Red 23 figure dans la base de données du Système de déclaration des cosmétiques (SDC) de Santé Canada dans environ 300 cosmétiques et produits de soins personnels sous les noms « Solvent Red 23 », « D&C Red n° 17 » ou « CI 26100 » (SDC, 2009).
Le Solvent Red 23 est mentionné dans le Règlement sur les aliments et drogues à l’article C.01.040.2(4)(a) à titre de colorant autorisé dans les médicaments à usage externe sous le nom de Toney Red (D&C Red n° 17; C.I. n° 26100) (Canada, 1978). Le Solvent Red 23 figure également dans la base de données des ingrédients non médicinaux de la Direction des produits thérapeutiques à titre de colorant présent dans un désinfectant liquide utilisé dans les hôpitaux sur les lieux où de la nourriture est fabriquée, préparée ou conservée, mais il n’a pas été déclaré présent dans les médicaments pharmaceutiques ou vétérinaires (courriel de 2008 de la Direction des produits thérapeutiques de Santé Canada adressé au Bureau de gestion des risques; source non citée). Cette substance est également mentionnée dans la base de données sur les ingrédients des produits de santé naturels (BDIPSN) à titre d’ingrédient non médicinal autorisé utilise comme colorant pour les usages externes seulement (BDIPSN, 2010). Le Solvent Red 23 figure dans la Base de données des produits de santé naturels homologués; il est donc présent dans les produits de santé naturels homologués (BDPSNH, 2010). Bien que la présence de Solvent Red 23 dans les épices ait déjà été signalée, cette substance n’est pas un colorant alimentaire autorisé dans l’Union européenne, aux États-Unis ou au Canada (Union européenne, 1994; USFDA, 2007; Santé Canada, 2007). Le Solvent Red 23 ne figure pas parmi les additifs alimentaires autorisés en vertu du Règlement sur les aliments et drogues et n’est pas utilisé à des fins d’emballage alimentaire (Santé Canada, 2007).
Dans d’autres pays, le Solvent Red 23 est actuellement utilisé dans les cosmétiques et les médicaments. Cette substance est actuellement approuvée aux États-Unis sous le nom de D&C Red n° 17 pour être utilisée comme colorant dans des médicaments et cosmétiques à usage externe et dans les verres de contact (USFDA, 2009). En Europe, l’usage du Solvent Red 23 (appelé CI 26100) est également approuvé comme colorant dans les cosmétiques qui n’entrent pas en contact avec les membranes des muqueuses (Directive sur les cosmétiques, annexe IV). Le Solvent Red 23 a été retrouvé dans les teintures capillaires, mais cette utilisation est actuellement interdite en Europe (Directive sur les cosmétiques, annexe II) (Commission européenne, 2010).
Le Solvent Red 23 est inscrit au Canada comme produit de formulation dans les insecticides/herbicides (courriel de 2009 de l’ARLA adressé au Bureau de gestion des risques des substances existantes, Santé Canada; source non citée) et figure également sur la liste des ingrédients inertes autorisés dans les produits antiparasitaires appliqués sur des sites à usage non alimentaire comme les plantes ornementales et les emprises routières aux États-Unis (USEPA, 2008).
Les autres utilisations possibles du Solvent Red 23 comprennent les colorants biologiques (O’Neil, 2006; ProSciTech, 2006), les huiles, les gras, les cires et les matières plastiques (CII 2002-).
De plus, le règlement REACH (Registration,Evaluation, Authorisation and Restriction of Chemical substances, c.à-d. enregistrement, évaluation, autorisation et restrictions relatifs aux substances chimiques) de la Commission européenne (Commission européenne, 2006), particulièrement au point 43 de l’annexe XVII, restreint certains « colorants azoïques et teintures azoïques » dans certains textiles pouvant libérer l’un des 22 amines aromatiques par rupture des liaisons azoïques. En théorie, le Solvent Red 23 subit une rupture réductrice de ses liaisons azoïques, ce qui forme l’une des 22 amines aromatiques dérivées (c.-à-d. le 4-aminoazobenzène, n° CAS 60-09-3), mais, d’après les données disponibles, le profil d’utilisation actuel de cette substance n’indique pas qu’elle est présente dans les produits textiles et de cuir.
Dans le cas du Solvent Red 23, l’analyse du cycle de vie n’était pas applicable à cause de l’insuffisance des données. Toutefois, étant donné le profil d’utilisation de la substance dans les produits de soins personnels, on peut penser que tous les produits contenant du Solvent Red 23 pourraient être rejetés dans les égouts, les eaux de surface ou le sol au cours de leur utilisation. Une fois dans les eaux de surface ou les égouts, en raison de ses propriétés physiques et chimiques, le Solvent Red 23 devrait se lier aux sédiments dans les milieux aquatiques et aux boues dans les stations de traitement des eaux usées.
D’après ce qui précède, l’eau des égouts est le milieu qui reçoit la plus grande proportion de Solvent Red 23 rejeté pendant l’utilisation du produit. On prévoit que la majeure partie de la substance, fixée aux boues d’épuration à la suite de rejets aux égouts de produits de soins personnels aux usines de traitement des eaux usées, sera entraînée dans les sites d’enfouissement (décharges). En plus d’être mis en décharge, une partie des biosolides produits par les stations de traitement des eaux usées peuvent être épandus sur des terres en tant qu’engrais ou amendement synthétique à des fins agricoles, forestières ou de remise en état, et un petit pourcentage peut être incinéré.
Le Solvent Red 23 devrait être rejeté dans les effluents d’eaux usées par suite de traitements industriels et d’utilisations associées à des rejets dans les égouts. D’après la valeur élevée du log Koe déterminée par analogie (4,6) et les valeurs du log Kco (3,4 à 4,2) [voir le tableau 2], cette substance pourrait avoir une affinité pour les matières solides. Toutefois, les valeurs du log Kco sont calculées et non strictement expérimentales (voir la note 3 du tableau 2), et le potentiel d’adsorption des structures des colorants particulaires dispersés n’est généralement pas bien compris; par conséquent, l’importance de ce comportement particulier est incertaine.
Selon les modèles de biodégradation aérobie, il est attendu que la biodégradation du Solvent Red 23 soit lente (voir le tableau 4 ci-dessous). Cette substance peut être épandue comme engrais ou amendement synthétique à des fins agricoles, forestières et de remise en état, sous forme de composante de biosolides. Le Solvent Red 23 utilisé comme formulant de pesticide peut être déposé directement sur les sols.
Étant donné une valeur expérimentale du pKa de 8,1 pour l’analogue Disperse Yellow 23 et une valeur estimée de 13,5 pour le Solvent Red 23 (tableau 2), on peut s’attendre à ce que cette substance chimique se comporte comme un acide faible et soit partiellement ionisée dans l’eau aux valeurs élevées de la gamme normale du pH dans l’environnement (8 à 9). Toutefois, en raison de la faible solubilité dans l’eau attendue pour le Solvent Red 23 (tableau 2) et de son état particulaire, il est peu probable que l’ionisation à un pH élevé influe significativement sur la répartition de cette substance dans l’environnement ou sur sa solubilité dans l’eau. De ce fait, lorsqu’elle est rejetée dans l’eau, cette substance devrait se retrouver principalement sous forme solide ou être adsorbée sur les particules en suspension pour enfin se déposer sur les matériaux du lit où elle devrait demeurer sous une forme qui n’est relativement pas biodisponible. On affirme généralement que les colorants azoïques finissent par se retrouver dans des sédiments anaérobies, dans des aquifères et dans l’eau souterraine en raison de leur nature récalcitrante dans les milieux aérobies (Razo-Flores et al., 1997). Toutefois, puisque le Solvent Red 23 a une faible solubilité dans l’eau et une valeur de Kco relativement élevée, il est peu probable qu’il ne se lixivie à partir des sédiments et des sols.
La vitesse de volatilisation à partir de la surface de l’eau est proportionnelle à la constante de la loi de Henry (Baughman et Perenich, 1988). Baughman et Perenich (1988) mentionnent également que la volatilisation à partir de systèmes aquatiques devrait être un processus de perte peu important pour les colorants dispersés dont la valeur de la constante de la loi de Henry pour les analogues est de faible à négligeable (10-8 à 10-1 Pa·m3/mol, tableau 2). Le transport dans l’air qui résulte de la perte de cette substance des sols superficiels humides et secs n’est pas très important pour cette substance comme l’indiquent les très faibles pressions de vapeur obtenues par analogie (5,33 x (10-12 à 10-5) Pa; tableau 2). Ces données sont compatibles avec l’état physique (particule solide) des colorants diazoïques qui les rend peu sujets à la volatilisation. La valeur expérimentale de la pression de vapeur du Disperse Orange 13 n’est pas un indicateur utile de la volatilisation du Solvent Red 23 étant donné qu’elle a été obtenue à une température élevée.
Persistance dans l’environnement
Les colorants doivent avoir un haut degré de stabilité chimique et photolytique pour être utiles; c’est pourquoi la plupart d’entre eux sont généralement considérés comme non dégradables dans les conditions aérobies observées dans l’environnement (EPA du Danemark, 1999; ETAD, 1995). Des études appliquant des analyses de dépistage généralement reconnues (p. ex., les lignes directrices de l’OCDE) de la biodégradabilité rapide et intrinsèque ont confirmé ce fait (ETAD, 1992; Pagga et Brown, 1986). La dégradation abiotique, qui comprend la photolyse et l’hydrolyse, n’est pas réputée jouer un rôle important dans le devenir des colorants azoïques dans l’environnement (EPA du Danemark, 1999), même si une étude a montré une décomposition photolytique fortement accélérée de colorants azoïques en présence de matière humique naturelle (Brown et Anliker, 1988).
La dégradation biotique des colorants azoïques peut être relativement rapide en conditions anaérobies ou réductives (Baughman et Weber, 1994; EPA du Danemark, 1999; ETAD, 1995; Isik et Sponza, 2004; Yen et al., 1999). Il a été déterminé que la perméabilité de la paroi cellulaire des bactéries constitue l’étape limitante du processus de réduction (EPA du Danemark, 1999). Les colorants azoïques ont une forte tendance à la rupture de leur liaison azoïque avec la formation d’amines aromatiques (EPA du Danemark, 1999; Hunger, 2005). Le potentiel cancérogène des amines aromatiques varie considérablement en fonction de la structure moléculaire, les produits de dégradation cancérogènes étant associés aux groupements fonctionnels benzidine, aniline, toluène ou naphtalène. Toutefois, la formation de tels métabolites dans des sédiments anoxiques profonds n’entraînerait normalement pas l’exposition des organismes aquatiques. La minéralisation totale ou la dégradation avancée des métabolites pourrait avoir lieu si ces derniers sont transférés (p. ex. par resuspension des sédiments) dans des milieux aérobies (EPA du Danemark, 1999; Isik et Sponza, 2004). Des amines aromatiques peuvent également être présentes sous forme d’impuretés dans des colorants azoïque disponibles sur le marché, et ce, même si la principale source de ces composés est la rupture des liaisons azoïques des colorants lors du métabolime (EPA du Danemark, 1999).
Une étude sur la bioélimination dans l’eau présentée pour l’analogue Disperse Yellow 23 indique que cette substance subit une dégradation de 51 % en 14 jours (étude présentée, 2008b). Toutefois, cette valeur expérimentale n’a pas pu être utilisée pour soutenir l’évaluation de la persistance du Solvent Red 23, car l’étude a été considérée peu fiable en raison du manque de renseignements sur les conditions expérimentales (voir le sommaire de rigueur d’étude à l’annexe 1). Outre cette étude, aucune autre donnée expérimentale ou obtenue par analogie sur la dégradation du Solvent Red 23 ou ses analogues n’a été relevée. Aucune donnée de surveillance environnementale n’ayant trait à la présence de ces colorants dans l’environnement canadien (air, eau, sol et sédiments) n’a été relevée.
Comme on s’attend à ce que le Solvent Red 23 à titre de colorant soit rejeté dans les eaux usées, sa persistance a surtout été examinée à l’aide de modèles de prévision RQSA sur la biodégradation aérobie dans l’eau. Ces modèles sont jugés acceptables pour utiliser dans cette situation puisqu’ils sont fondés sur la structure chimique et que la structure diazoïque est représentée dans les ensembles d’apprentissage de tous les modèles BIOWIN utilisés, ce qui augmente la fiabilité des prévisions (Environnement Canada, 2007). L’analyse suivante concerne principalement la partie de cette substance actuellement dissoute dans l’environnement, tout en tenant compte du fait qu’il est probable qu’une grande partie de cette substance est dispersée sous la forme de particules solides. Le Solvent Red 23 et ses analogues ne contiennent pas de groupements fonctionnels susceptibles d’entreprendre une hydrolyse dans un milieu aérobie (les colorants sont connus pour être stables dans les milieux aqueux). Le tableau 4 résume les résultats des modèles RQSA disponibles sur la biodégradation aérobie dans l’eau.
| Processus du devenir | Modèle et base du modèle |
Résultat et prévision du modèle | Demi-vie extrapolée (jours) |
|---|---|---|---|
| Biodégradation (aérobie) | BIOWIN, 2008 Sous-modèle 4 : enquête d’expert (résultats qualitatifs) |
3,3[2] « se biodégrade lentement » |
≥ 182 |
| Processus du devenir | Modèle et base du modèle |
Résultat et prévision du modèle | Demi-vie extrapolée (jours) |
|---|---|---|---|
| Biodégradation (aérobie) | BIOWIN, 2008[1] Sous-modèle 3 : enquête d’expert (résultats qualitatifs) |
1,90[2] « se biodégrade très lentement » |
≥ 182 |
| Biodégradation (aérobie) | BIOWIN, 2008[1] Sous-modèle 5 : Probabilité linéaire MITI |
-0,24[3] « se biodégrade très lentement » |
≥ 182 |
| Biodégradation (aérobie) | BIOWIN, 2008[1] Sous-modèle 6 : Probabilité non linéaire MITI |
0[3] « se biodégrade lentement » |
≥ 182 |
| Biodégradation (aérobie) | TOPKAT, 2004 Probabilité |
s. o.[4] « se biodégrade lentement » |
≥ 182 |
| Biodégradation (aérobie) | CATABOL 2004-2008 % DBO[5] (demande biochimique en oxygène) |
% DBO = 0 « se biodégrade très lentement » |
≥ 182 |
[2] Le résultat s’exprime par une valeur numérique de 0 à 5.
[3] Le résultat s’exprime par un taux de probabilité.
[4] s. o. : sans objet (hors des champs d’application du modèle).
[5] DBO : demande biologique en oxygène.
Comme le montre le tableau 4, tous les modèles de biodégradation (BIOWIN 3, 5, 6 et CATABOL) portent à croire que la biodégradation du Solvent Red 23 se fait lentement de manière aérobie dans l’eau. En fait, les résultats de probabilité de BIOWIN 5 et 6 sont bien inférieurs à 0,3, ce qui est la limite suggérée par Aronson et al., (2006) pour trouver les substances qui ont une demi-vie de plus de 60 jours (selon les modèles de probabilité du MITI). En outre, les deux autres modèles de la dégradation ultime, BIOWIN 3 et CATABOL, prévoient que le Solvent Red 23 sera persistant dans l’eau. TOPKAT (2004) prévoit également une biodégradation lente, mais le résultat du modèle n’est pas fiable, car la structure se trouve en dehors du domaine d’applicabilité du modèle.
Lorsque les résultats de probabilité et les autres modèles de dégradation ultime sont pris en compte, il y a un important consensus qui suggère que la demi-vie de la biodégradation ultime dans l’eau est supérieure à 182 jours. Ce résultat correspond à ce qu’on s’attend de cette structure chimique (c.-à-d., peu de groupements fonctionnels dégradables, particules solides peu solubles).
Selon un ratio d’extrapolation de 1:1:4 pour la demi-vie associée à la biodégradation dans l’eau, le sol, les sédiments (Boethling et al., 1995), la demi-vie de biodégradation ultime dans le sol aérobie est égale ou supérieure à 182 jours, et la demi-vie dans les sédiments aérobie est égale ou supérieure à 365 jours. Ces résultats indiquent que le Solvent Red 23 devrait être persistant dans le sol et les sédiments.
D’après les données modélisées sur la dégradation ultime (tableau 4) et l’avis d’expert (EPA du Danemark, 1999; ETAD, 1995), le Solvent Red 23 répond aux critères de persistance dans l’eau, le sol (demi-vies dans le sol et dans l’eau en conditions aérobies ≥ 182 jours), les sédiments (demi-vie dans les sédiments en conditions aérobies de ≥ 365 jours) énoncés dans le Règlement sur la persistance et la bioaccumulation (Canada, 2000).
Potentiel de bioaccumulation
On ne dispose pas de données expérimentales sur la bioaccumulation du Solvent Red 23. Comme il est connu que les modèles de la bioaccumulation s’appliquent mal aux pigments et aux colorants, leurs prévisions ne sont pas considérées comme fiables pour les colorants diazoïques. La modélisation de la bioaccumulation n’a donc pas été employée pour évaluer le potentiel de bioaccumulation de ces substances.
Vu l’absence de données expérimentales et modélisées, les facteurs de bioconcentration (FBC) et de bioaccumulation (FBA) d’analogues structuraux, calculés à partir de données empiriques, ont été utilisés pour estimer le potentiel de bioaccumulation du Solvent Red 23. D’après des études présentées sur la bioconcentration des analogues structuraux relativement proches Sudan IV (MITI, 1992) et Disperse Orange 30 (Shen et Hu, 2008), l’accumulation du Solvent Red 23 dans les poissons serait peu probable.
Dans le cadre de l’essai effectué par le ministère du Commerce international et de l’industrie du Japon (MITI) avec le Solvent Red 23 (tableau 5a) sur des carpes, les facteurs de bioconcentration obtenus étaient faibles, soit inférieurs à 11 L/kg.
| Organisme d’essai | Concentration expérimentale (mg/L) et/ou source d’exposition | Paramètre (FBC, L/kg) | Référence |
|---|---|---|---|
| Carpe (Cyprinus carpio) |
0,35 | < 0,29-2,9 | MITI, 1992 |
| Carpe (Cyprinus carpio) |
0,035 | < 2,9-11 | MITI, 1992 |
Cet essai de bioconcentration de Shen et Hu (2008) a été réalisé conformément aux Directives de l’OCDE (OECD, 1996). La bioconcentration du Disperse Orange 30 chez le poisson zèbre (Brachydanio rerio) a été déterminée par un test semi-statique sur 28 jours, avec renouvellement du milieu de test tous les deux jours. Afin de vérifier le potentiel de bioconcentration de la substance d’essai, un essai en phase d’exposition à une concentration nominale de 20 mg/L (concentration moyenne mesurée entre 0,028 et 0,28 mg/L approximativement) a été mené en tenant compte du résultat obtenu lors de l’essai de toxicité aiguë pour le poisson. Des échantillons des deux solutions de test et des organismes d’essai ont été pris du 26e jour au 28ejour de la période de test d’exposition sur 28 jours. Les échantillons ont été préparés en extrayant le composant lipidique des poissons testés. La concentration mesurée de la substance d’essai, la teneur en lipides dans le poisson et le facteur de bioconcentration (FBC) figurent au tableau 5b.
| Traitements (20 mg/L) | Durée d’échantillonnage | ||
|---|---|---|---|
| 26e jour | 27e jour | 28e jour | |
| Concentration mesurée de la substance d’essai dans les solutions extraites (mg/L) | < 0,028 | < 0,028 | < 0,028 |
| Contenu de la substance test dans les lipides du poisson (mg) | < 1,68 | < 1,68 | < 1,68 |
| Poids total des poissons (g) | 2,07 | 2,13 | 2,53 |
| Concentration de la substance d’essai dans les poissons Cp (mg/kg) | < 0,81 | < 0,79 | < 0,66 |
| Concentration mesurée de la substance test dans le Ce de l’eau (mg/L) | 0,028 - 0,28 | 0,028 - 0,28 | 0,028 - 0,28 |
| Contenu lipidique du poisson (%) | 0,81 | 0,57 | 1,25 |
| FBC | < 100 | < 100 | < 100 |
| FBC moyen | < 100 | ||
L’étude de Shen et Hu (2008) a été révisée et considérée comme acceptable (voir l’annexe 1). Le niveau de détection très faible dans les extraits de poisson (< 0,028 mg/L) indiquerait une solubilité limitée dans les lipides ou un potentiel limité de répartition dans les tissus des poissons des systèmes aqueux. Toutefois, il existe une incertitude associée aux valeurs limites dans toute étude, car la « vraie » valeur n’est pas connue. Par contre, étant donné la structure et le comportement probable des colorants dispersés dans les systèmes aqueux, le faible résultat obtenu pour le FBC n’est pas inattendu. La plupart des colorants dispersés, ainsi que leur nom le laisse entendre, se présentent sous la forme de fines particules dispersibles avec des fractions réellement solubles limitées. Leur solubilité peut, toutefois, être augmentée en ajoutant à la molécule des groupements fonctionnels polarisés. Or, même si le Solvent Red 23 et ses analogues pertinents (tableau 2) comprennent certains groupements fonctionnels solubilisants (groupements phénols), les valeurs expérimentales disponibles sur la solubilité de cette substance et de ses analogues pertinents (qui varient de 0,000 06 à 0,345 mg/L) sont relativement faibles, soit inférieures ou comparables par moins d’un ordre de grandeur, à la solubilité dans l’eau du Disperse Orange30 (c.-à-d. 0,07 mg/L). Par conséquent, le Solvent Red 23 devrait avoir une biodisponibilité et un potentiel de bioconcentration similaires ou inférieurs à ceux du Disperse Orange 30.
Les études susmentionnées constituent un élément de preuve de première importance permettant de croire que le Solvent Red 23 ne serait pas bioaccumulable, et d’autres recherches viennent appuyer également cette conclusion. Anlikeret al., (1981) présentent des valeurs expérimentales sur la bioaccumulation dans les poissons pour 18 colorants monoazoïques dispersés, valeurs obtenues suivant les méthodes prescrites par le MITI. Le log des facteurs de bioaccumulation (FBC) variait entre 0,00 et 1,76 et est exprimé en fonction du poids humide total des poissons (Anliker et al., 1981). L’absence d’information sur les numéros de registre et la structure chimique précise des substances limite toutefois l’utilité de cette étude pour des déductions par analogie au sujet du Solvent Red 23. Néanmoins, des études complémentaires fournissant des précisions sur la structure chimique des colorants dispersés testés ont confirmé le faible potentiel de bioaccumulation de dix colorants azoïques nitrosubstitués pour lesquels les valeurs déterminées du log du facteur de bioaccumulation varient de 0,3 à 1,76 (Anliker et Moser, 1987; Anliker et al., 1988). Des études du MITI viennent également appuyer le faible potentiel de bioaccumulation des colorants azoïques dispersés. Les FBC publiés pour trois colorants azoïques dispersés (nos CAS 40690-89-9, 61968-52-3 et 71767-67-4) testés à une concentration de 0,01 mg/L varient de moins de 0,3 à 47 L/kg (MITI, 1992). Une étude sur l’accumulation d’une durée de huit semaines réalisée par Brown (1987) montre également qu’aucun des douze colorants dispersés ayant été testés ne s’accumulait chez la carpe.
Les valeurs élevées du log Koe déduites à partir d’analogues azoïques apparentés (tableau 2) sont les seules données indiquant que le Solvent Red 23 pourrait avoir un potentiel élevé de bioaccumulation. Malgré ces valeurs élevées du log Koe, la preuve de la bioaccumulation des colorants azoïques dispersés est insuffisante (Anliker et al., 1981; Anliker et Moser, 1987, MITI, 1992. 1988, MITI, 1992) Selon les auteurs qui ont mesuré des valeurs élevées du log Koe et de faibles facteurs de bioaccumulation concomitants pour les colorants azoïques dispersés, les facteurs d’accumulation faibles pourraient s’expliquer, dans certains cas, par leur faible liposolubilité absolue (Brown, 1987) ou leur poids moléculaire relativement élevé, ce qui pourrait rendre difficile le transport de ces substances à travers les membranes des poissons (Anliker et al., 1981; Anliker et Moser, 1987). Il se peut aussi que le manque de biodisponibilité et le comportement de répartition limité imposés par les conditions d’essai sur le FBC restreignent l’accumulation dans les tissus lipidiques des poissons.
De récentes études liées aux données sur le FBC chez les poissons et aux paramètres de la taille moléculaire (Dimitrovet al., (2002, 2005) laissent entendre que la probabilité qu’une molécule traverse des membranes cellulaires à la suite d’une diffusion passive diminue de façon importante avec l’augmentation du diamètre maximal (Dmax). La probabilité qu’une diffusion passive se produise diminue de façon notable lorsque le diamètre maximal est supérieur à environ 1,5 nm et diminue de façon encore plus significative dans le cas des molécules ayant un diamètre maximal supérieur à 1,7 nm. Sakuratani et al., (2008) ont également étudié l’effet du diamètre transversal sur la diffusion passive à l’aide d’un ensemble d’essais du FBC comptant environ 1 200 substances chimiques nouvelles et existantes. Ils ont observé que les substances qui n’ont pas un potentiel de bioconcentration très élevé (FBC < 5 000) ont souvent un Dmaxsupérieur à 2,0 nm et un diamètre effectif (Deff) supérieur à 1,1 nm.
Cependant, comme l’ont évoqué Arnot et al., (2010), il existe des incertitudes quant aux seuils proposés par Dimitrov et al. (2002, 2005) et Sakuratani et al. (2008), étant donné que les études sur le FBC utilisées pour calculer ces seuils n’ont pas fait l’objet d’évaluations critiques. Arnotet al. (2010), la taille moléculaire a un effet sur la solubilité et la capacité de diffusion dans l’eau et dans les phases organiques (membranes), et les plus grosses molécules peuvent avoir un taux d’absorption plus lent. Toutefois, ces mêmes contraintes liées aux facteurs cinétiques s’appliquent aux voies de diffusion de l’élimination chimique (c.-à-d., absorption lente = élimination lente). Un potentiel de bioaccumulation important peut donc s’appliquer aux substances qui sont soumises à un processus d’absorption lent, si elles sont biotransformées ou éliminées lentement par d’autres processus. Par conséquent, lorsqu’on évalue le potentiel de bioaccumulation, les données sur la taille moléculaire doivent être utilisées avec discernement et de pair avec des éléments de preuve pertinents dans le cadre d’une méthode du poids de la preuve.
Le Solvent Red 23 et ses analogues les plus proches (les colorants diazoïques) ont des poids moléculaires variant de 302 à 377 g/mol (voir le tableau 3b) et des structures moléculaires relativement peu compliquées; ces deux caractéristiques indiquent une capacité de bioaccumulation si le poids moléculaire est le seul indicateur utilisé. En revanche, Arnot et al. (2010) indiquent qu’il n’y a pas de rapports nets qui permettraient de fixer une valeur de taille moléculaire de démarcation pour l’évaluation du potentiel de bioaccumulation. Ce rapport ne met toutefois pas en cause la notion selon laquelle la réduction du taux d’absorption pourrait être associée à l’augmentation du diamètre transversal, comme cela a été démontré par Dimitrovet al. (2002, 2005). Le diamètre maximal du Solvent Red 23, de ses analogues les plus proches et de leurs conformères varie de 1,5 à 2,2 nm (BBM, 2008), ce qui indiquerait une possibilité de réduction significative de l’absorption à partir de l’eau et de la biodisponibilité in vivo pour ces colorants.
Étant donné l’absence d’accumulation observée dans les études sur la bioconcentration du Sudan IV, du Disperse Orange 30 et d’autres colorants azoïques dispersés apparentés ayant donné des résultats semblables, et compte tenu du grand diamètre transversal du Solvent Red 23 et de ses analogues qui restreint vraisemblablement leur comportement de partage, le Solvent Red 23 devrait présenter un faible potentiel de bioaccumulation. Par conséquent, en considérant les données disponibles, le Solvent Red 23 ne répond pas aux critères de bioaccumulation (FBC ou FBA ≥ 5 000) du Règlement sur la persistance et la bioaccumulation (Canada, 2000).
Évaluation des effets écologiques
A – Dans le milieu aquatique
Aucune étude sur la toxicité du Solvent Red 23 n’a été présentée. Toutefois, des données déduites à partir d’analogues ont été présentées pour plusieurs analogues du Solvent Red 23, dont le Disperse Yellow 23 et le Disperse Orange 29 (étude présentée, 2008a, 2000b). Elles indiquent que le Sudan IV a une CL50 sur 48 h de plus de 100 mg/L chez le médaka (Oryzias latipes), que le Disperse Yellow 23 a une CL50 sur 48 h de plus de 1 000 mg/L chez la truite arc-en-ciel (Oncorhynchus mykiss) et que le Disperse Orange 29 a une CL50 sur 96 h de 480 mg/L chez le poisson-zèbre (Brachydanio rerio) (tableau 6). Le Disperse Orange 29 a également une CE50 après 72 h de 6 mg/L pour l’algue Scenedesmus subspicatus et une CE50 après 48 h de 70 mg/L pour Daphnia magna. La fiabilité de ces études est toutefois considérée comme incertaine en raison de l’absence de certains détails sur leur réalisation (voir l’annexe 1). Néanmoins, il a été jugé que leurs données pouvaient être utilisées dans cette évaluation préalable aux fins de l’établissement du poids de la preuve.
Une étude présentée pour le compte de l’ETAD fournit des données écotoxicologiques aiguës pour les poissons, les invertébrés, les algues et les bactéries pour cinq colorants dispersés azoïques nitrosubstitués (Brown, 1992). La toxicité aiguë chez les poissons-zèbres, Daphnia magna etScenedesmus subspicatus, pour les cinq analogues variait de 17 à 710 mg/L, 4,5 à 110 mg/L et 6,7 à 54 mg/L, respectivement (tableau 6). De plus, tous les essais à l’aide de bactéries avaient une CI50 dépassant 100 mg/L. Le protocole expérimental détaillé de l’étude portant sur les colorants testés n’a pas été fourni, ce qui restreint grandement l’évaluation de ces études (Brown, 1992). Toutefois, on a jugé que ces données pouvaient être utilisées et elles sont comprises dans cette ébauche d’évaluation préalable en tant qu’élément du poids de la preuve.
Une autre étude de la toxicité aiguë d’un poisson a été présentée pour l’analogue Disperse Blue 79 (BASF, 1990). Elle a indiqué une CL50 après 96 h entre 100 et 220 mg/L pour l’ide dorée (tableau 6). Toutefois, sa fiabilité est aussi considérée comme incertaine en raison de l’absence de détails (annexe 1). On présente également dans le tableau 6 les résultats d’une étude sur la toxicité de l’analogue Sudan IV chez les poissons, soit une valeur dépassant 100 mg/L (MITI, 1992), pour contribuer au poids de la preuve; cette valeur n’est cependant pas la valeur critique puisque le paramètre n’a pas d’intervalle fini de valeurs.
Des données écotoxicologiques sur un autre colorant azoïque dispersé ont été reçues en vertu du Règlement sur les renseignements concernant les substances nouvelles(Environnement Canada, 1995). Une étude de la toxicité aiguë d’un poisson soumise afin de satisfaire les exigences en matière de déclaration a révélé que cette substance à une CL50 de 505 mg/L dans la truite arc-en-ciel après 96 heures (tableau 6). Cet essai a été mené en conformité avec les lignes directrices de l’OCDE n° 203. La fiche signalétique fournie avec cette déclaration contient également des renseignements sur les effets toxiques chez les bactéries. Les résultats indiquent une CE50 supérieure à 1 000 mg/L pour l’inhibition de la respiration de boues activées. À la lumière des données disponibles sur l’écotoxicité, les effets toxiques de la nouvelle substance pour les organismes aquatiques ont été considérés comme peu préoccupants. La fiabilité de cet essai a été évaluée à l’aide d’un sommaire de rigueur d’études et elle est jugée satisfaisante (annexe 1).
Enfin, une étude présentée sur la toxicité chronique de l’analogue Disperse Blue 79:1 a indiqué une concentration sans effet observé (CSEO) de 122 jours supérieure à 0,0048 mg/L chez la truite arc-en-ciel (tableau 6). Cette étude a été évaluée et jugée très fiable (annexe 1). Toutefois, comme la valeur susmentionnée est un résultat non lié (seuil d’effet incertain), elle n’a pas été utilisée pour calculer la concentration estimée sans effet).
À la lumière de toute l’information sur la toxicité des analogues structuraux et compte tenu des données sur la toxicité du Disperse Yellow 23 et du Disperse Orange 29, il y a lieu de croire que le Solvent Red 23 n’est pas très dangereux pour les organismes aquatiques (valeurs de la CL50 aiguë supérieures à 1 mg/L).
| Nom usuel ou n° CAS | Organisme d’essai | Gravité (durée) | Paramètre | Valeur (mg/L) | Référence |
|---|---|---|---|---|---|
| Sudan IV (85-83-6) |
Oryzias latipes | Aiguë ( 48 heures) |
CL50[1] | > 100 | MITI, 1992 |
| Disperse Orange 29 (19800-42-1) | Algues | Chronique (72 heures) |
CE50[2] | 6 | Étude présentée, 2008a |
| Daphnia | Aiguë (48 heures) |
CE50 | 70 | ||
| Poisson | Aiguë (96 heures) |
CL50 | 480 | ||
| Disperse Yellow 23 (6250-23-3) |
Poisson | Aiguë (48 heures) |
CL50 | > 1 000 | Étude présentée, 2008a |
| Disperse Blue 79[3] (12239-34-8) |
Ide dorée | Aiguë (96 heures) |
CL50 | 100 < CL50 < 220 | BASF, 1990 |
| Poisson-zèbre | Aiguë (96 heures) |
CL50 | 340 | Brown, 1992 | |
| Daphnia magna | Aiguë (48 heures) | CE50[3] | 4,5[*] | ||
| Scenedesmus subspicatus | Chronique - croissance (72 heures) |
CE50 | 9,5 | ||
| Bactérie | Non disponible | CI50[4] | > 100 | ||
| Disperse Red 73[5] (16889-10-4) |
Poisson-zèbre | Aiguë (96 heures) |
CL50 | 17 | |
| Daphnia magna | Aiguë (48 heures) |
CE50 | 23 | ||
| Scenedesmus subspicatus | Chronique - croissance (72 heures) |
CE50 | > 10 | ||
| Bactérie | Non disponible | CI50 | > 100 | ||
| Disperse Orange 30[6] (5261-31-4) |
Poisson-zèbre | Aiguë (96 heures) |
CL50 | 710 | |
| Daphnia magna | Aiguë (48 heures) |
CE50 | 5,8 | ||
| Scenedesmus subspicatus | Chronique - croissance (72 heures) |
CE50 | 6,7 | ||
| Bactérie | Non disponible | CI50 | > 100 | ||
| Disperse Orange 25[7] (31482-56-1) |
Poisson-zèbre | Aiguë (96 heures) |
CI50 | 268 | |
| Daphnia magna | Aiguë (48 heures) |
CL50 | 110 | ||
| Scenedesmus subspicatus | Chronique - croissance (72 heures) |
CE50 | 54 | ||
| Bactérie | Non disponible | CE50 | > 100 | ||
| Disperse Red 17 (3179-89-3)[8] |
Poisson-zèbre | Aiguë (96 heures) |
CL50 | 103 | |
| Daphnia magna | Aiguë (48 heures) |
CE50 | 98 | ||
| Scenedesmus subspicatus | Chronique - croissance (72 heures) |
CE50 | 7 | ||
| Bactérie | Non disponible | CI50 | > 100 | ||
| Colorant azoïque dispersé analogue (n° CAS confidentiel) |
Truite arc-en-ciel | Aiguë (96 heures) |
CL50 | 505 | Environnement Canada, 1995 |
| Disperse Blue 79:1 (3618-72-2) |
Truite arc-en-ciel | Chronique (122 jours) |
CSEO[9] | > 0,0048 | Cohle et Mihalik, 1991 |
[2] CE50 – La concentration d’une substance qui est jugée causer certains effets sublétaux toxiques chez 50 % des organismes d’essai.
[3] L’étude indique que le Disperse Blue 79 utilisé dans l’essai avait une pureté (de matières organiques) de 76 % et une dispersion du colorant à 20 %.
[4] CI50 – Concentration inhibitrice pour un pourcentage donné d’un effet. Estimation ponctuelle de la concentration d’une substance d’essai causant une réduction de 50 % d’une mesure biologique quantitative comme le taux de croissance.
[5] L’étude indique que le Disperse Red 73 utilisé dans l’essai avait une pureté de 96,6 %.
[6] L’étude indique que le Disperse Orange 30 utilisé dans l’essai avait une pureté (de matières organiques) de 73 % et une dispersion du colorant de 20 %.
[7] L’étude indique que le Disperse Orange 25 utilisé dans l’essai avait une pureté de 94 %.
[8] L’étude indique que le Disperse Red 17 utilisé dans l’essai avait une pureté de 98,8 %.
[9] CSEO – La concentration sans effet observé est la concentration la plus élevée, au cours d’un essai sur la toxicité, à laquelle on n’obtient pas d’effet statistiquement significatif, par comparaison aux témoins.
[*] La valeur de toxicité critique utilisée pour dériver une concentration sans effet probable.
En général, en raison de leur faible solubilité (soit < 1 mg/L), les colorants dispersés sont supposés avoir un impact écologique faiblement aigu (Hunger, 2003). Les résultats des études empiriques sur la toxicité portant sur des analogues du Solvent Red 23 concordent avec ces prévisions, indiquant des valeurs CL50 comprises entre 17 et 505 mg/L, laDaphnia étant l’organisme testé le plus sensible (CE50/CL50 allant de 4,5 à 110 mg/L). La valeur critique choisie pour dériver la concentration sans effet probable est réputée être la valeur de CE50 chezDaphnia magna, soit 4,5 mg/L (Brown, 1992).
L’interprétation des résultats de ces essais est compliquée par le fait que les valeurs obtenues (c.-à-d. CE50 et CL50) sont vraisemblablement nettement supérieures à la solubilité des substances d’essai. En effet, certaines des concentrations rapportées dans le tableau 6 peuvent représenter la charge de la substance à l’essai. Par conséquent, un sous-ensemble des valeurs réelles de CL50 ou de CE50 peuvent être inférieures aux concentrations rapportées puisque l’on ne connaît pas la concentration réelle dissoute dans l’eau qui peut causer un effet. Dans d’autres cas (voir les notes sous le tableau 6), les substances à l’essai se trouvaient dans des formulations et n’étaient donc pas pures à 100 %. Ainsi, d’autres substances chimiques dans la formulation peuvent avoir augmenté la solubilité et contribué à la toxicité totale. En dépit de ces incertitudes concernant la solubilité dans l’eau et la pureté de certains analogues, les données expérimentales et les données sur les analogues existantes indiquent clairement que la toxicité du Solvent Red 23 est probablement faible.
Une gamme de prévisions de la toxicité du Solvent Red 23 en milieu aquatique a également été obtenue à l’aide de modèles RQSA. Toutefois, tout comme pour la bioaccumulation, les estimations de l’écotoxicité fondées sur des RQSA ne sont pas jugées fiables à cause de l’erreur pouvant être associée aux paramètres d’entrée des modèles et de la nature particulière des colorants dispersés – état physique, caractéristiques structurales et/ou propriétés physiques et chimiques hors du domaine d’applicabilité des modèles.
L’information empirique disponible au sujet de l’écotoxicité du Solvent Red 23 indique donc que la substance n’est probablement pas très dangereuse pour les organismes aquatiques.
B – Dans d’autres milieux naturels
Comme le Solvent Red 23 devrait s’accumuler dans les sédiments et qu’il pourrait se retrouver dans les sols par suite de l’application directe de pesticides et de l’épandage de biosolides sur les sols, souvent utilisé pour enrichir les sols, et de la mise en décharge de produits qui les libèrent en se dégradant, il serait souhaitable de disposer de données sur la toxicité pour les organismes présents dans les sédiments et les sols. Cependant, on n’a trouvé aucune étude pertinente sur les effets écologiques de ces composés ou de leurs analogues dans d’autres milieux que l’eau. La toxicité pour les espèces vivant dans les sédiments et les sols devrait néanmoins aussi être faible, étant donné la biodisponibilité et le potentiel de bioaccumulation très faibles du Solvent Red 23 ainsi que ses propriétés physiques et chimiques, quoique cela ne puisse être confirmé faute de données acceptables sur la toxicité portant sur des organismes entiers. Cette hypothèse ne peut toutefois être corroborée en raison de l’absence de données globales valides sur la toxicité pour les organismes.
Évaluation de l’exposition écologique
Aucune donnée sur les concentrations de Solvent Red 23 dans l’eau au Canada n’a été retracée. On a donc évalué les concentrations dans l’environnement sur la base des renseignements disponibles, y compris les estimations relatives aux quantités de la substance, aux taux de rejets et aux cours d’eau récepteurs.
A – Rejets industriels
Les déclarations de l’industrie pour 2005 et 2006 n’indiquant aucune fabrication ou transformation du Solvent Red 23 au Canada, il ne devrait pas y avoir de rejets industriels de cette substance au pays.
B – Rejets par les consommateurs
Étant donné le profil d’utilisation de la substance dans les cosmétiques et certains produits de soins personnels, on peut penser que les produits contenant du Solvent Red 23 pourraient être rejetés dans les égouts ou les eaux de surface au cours de leur utilisation. Par conséquent, l’outil Mega Flush d’Environnement Canada qui sert à estimer les rejets à l’égout issus d’utilisations par les consommateurs a été utilisé pour estimer la concentration possible de la substance dans différents cours d’eau récepteurs d’effluents issus des stations de traitement des eaux usées dans lesquelles ont été rejetés par les consommateurs des produits contenant cette substance (Environnement Canada, 2008b). Le tableur fournit ces estimations pour environ 1 000 sites de rejet dans tout le Canada, et ce, d’après des hypothèses prudentes.
Ces hypothèses prudentes incluent :
- pertes dans les égouts à 100 %;
- un taux d’élimination dans les usines de traitement des eaux usées de 0,0 %,
- le nombre de jours de rejets annuels de 365 jours/an;
- facteur de dilution dans l’eau réceptrice sur une échelle de 1 à 10.
Les concentrations environnementales estimées (CEE) de Solvent Red 23 dans les cours d’eau récepteurs se situent dans la plage de 6,7 x 10-6 à 0,0061 mg/L. L’estimation est fondée sur un total de 4 000 kg/année pour la quantité de la substance d’après la limite supérieure de la fourchette des quantités déclarées de Solvent Red 23 qui auraient été importées au Canada en 2005 dans l’enquête menée en vertu de l’article 71 (Environnement Canada, 2006). L’équation et les entrées utilisées pour calculer les CEE sont décrites dans le rapport d’Environnement Canada (2010d).
Le Solvent Red 23 est également utilisé comme produit de formulation dans les pesticides agricoles (ARLA, 2010). Il figure sur la liste 2 de l’Agence de réglementation de la lutte antiparasitaire (ARLA), qui contient les produits de formulation considérés comme potentiellement toxiques d’après les similarités structurales avec les produits de formulation de la liste 1 (ceux, qui, selon l’ARLA, sont préoccupants), ou dans les données indicatrices de toxicité. On ne s’attend pas à ce que le Solvent Red 23 soit rejeté dans les égouts à la suite de son utilisation dans les pesticides. Le Solvent Red 23 pourrait toutefois être rejeté dans l’environnement par l’intermédiaire des applications agricoles. Cet usage n’est pas modélisé parmi les produits antiparasitaires et leurs produits de formulation sont réglementés par l’ARLA.
Caractérisation du risque écologique
La démarche utilisée pour cette évaluation écologique préalable examinait les renseignements scientifiques disponibles et dégageait des conclusions en appliquant la méthode du poids de la preuve et une approche préventive conformément à la LCPE (1999).
Si l’on se fonde sur les propriétés physiques et chimiques de substances analogues, le Solvent Red 23 devrait se dégrader lentement en milieu aérobie et devrait être persistant dans l’eau, le sol et les sédiments. Cette substance devrait présenter un faible potentiel de bioaccumulation. Bien que la proportion de Solvent Red 23 qui devrait être rejetée dans les égouts soit élevée, les faibles quantités importées de ce colorant au Canada ainsi que les données sur ses propriétés physiques et chimiques indiquent, dans l’ensemble, un faible potentiel de rejet dans l’environnement canadien. S’il est rejeté dans l’environnement, on s’attend à ce que le Solvent Red 23 soit principalement déversé dans les eaux usées, où il devrait finir par se déposer dans les sédiments et les sols. L’utilisation de données déduites à partir d’analogues a permis de démontrer que le Solvent Red 23 présente seulement un potentiel moyen de toxicité aiguë pour les organismes aquatiques.
La concentration estimée sans effet (CESE) a été évaluée en se fondant sur la CE50 de 48 h de 4,5 mg/L chez laDaphnia magna pour l’analogue Disperse Blue 79 (tableau 6). On a ensuite appliqué un facteur de 100 pour tenir compte de la toxicité aiguë à la toxicité chronique et des extrapolations au terrain des résultats en laboratoire et de l’utilisation d’une substance de remplacement. La CESE ainsi obtenue est de 0,045 mg/L.
Une analyse du quotient de risque, mettant en relation la CEE prudente avec une estimation prudente du potentiel d’effets nocifs ou une CESE, a été effectuée pour le milieu aquatique. Le quotient de risque (CEE/CESE) est une source de donnée importante à considérer dans l’évaluation du risque potentiel pour l’environnement.
Pour l’exposition résultant des rejets dans les égouts par suite des utilisations des consommateurs (scénario prudent), la CEE maximale pour le Solvent Red 23 tirées de Mega Flush était de 0,0061 mg/L. Lorsque la CEE maximale est comparée à la CESE de 0,045 mg/L, le quotient de risque (CEE/CESE) est de 0,136. Les quotients de risque étant inférieurs à 1 à tous les sites de Mega Flush, les rejets de Solvent Red 23 par les consommateurs dans le réseau d’égouts ne devraient pas être nocifs pour les organismes aquatiques.
Par conséquent, il est peu probable que le Solvent Red 23 nuise aux populations d’organismes aquatiques au Canada.
Incertitudes dans l’évaluation des risques pour l’environnement
L’évaluation de la persistance est limitée par le manque de données sur la biodégradation, ce qui a nécessité la production de prévisions modélisées. Bien que toutes les prévisions modélisées comportent un certain degré d’erreur, les résultats du modèle de biodégradation aérobie ont confirmé la persistance attendue du Solvent Red 23, compte tenu de ses utilisations et de ses caractéristiques structurales. De plus, l’évaluation de la persistance est limitée par les incertitudes quant à la vitesse de dégradation et à la mesure dans laquelle cette dégradation se produit dans des sédiments anaérobies ainsi qu’à la détermination de la biodisponibilité des produits de dégradation (p. ex. amines). On ne prévoit pas que les produits de dégradation soient biodisponibles étant donné qu’ils se forment seulement dans des sédiments anoxiques relativement profonds, mais il existe un risque de perturbation des sédiments. Par conséquent, ce point constitue une source d’incertitude dans l’évaluation de la toxicité du Solvent Red 23.
L’évaluation de la bioaccumulation de ces substances a été limitée par le manque de données empiriques sur le Solvent Red 23 et l’incapacité des modèles disponibles à estimer de façon fiable la bioaccumulation de colorants diazoïques. L’évaluation était plutôt fondée sur l’utilisation de données sur la bioaccumulation pour un analogue structural (Disperse Orange 30).
Il existe également des incertitudes en raison du manque de données sur les concentrations environnementales au Canada de Solvent Red 23. Cependant, l’absence de déclarations de fabrication au Canada, les faibles quantités importées et l’élimination prévue dans les effluents permettent de croire à un faible potentiel de rejet de ces substances dans l’environnement au Canada.
Les fractions de ces substances qui sont rejetées et de celles qui sont éliminées dans les usines de traitement des eaux usées constituent une autre source d’incertitude. Ces incertitudes ont été palliées par l’utilisation d’hypothèses prudentes dans la modélisation de l’exposition.
Les concentrations expérimentales, associées à la toxicité intrinsèque pour les organismes aquatiques, peuvent constituer une source additionnelle d’incertitude lorsqu’elles dépassent la solubilité du produit chimique dans l’eau (expérimentale ou prédite). Il existe également une incertitude liée à la pureté des substances utilisées dans les tests de solubilité et de toxicité. En raison de leur faible solubilité, les colorants sont souvent mélangés avec de l’eau et un agent solubilisant afin d’effectuer le test. Cette convention peut produire des valeurs de solubilité qui sont artificiellement élevées et qui peuvent également influer sur le résultat des tests de toxicité dans les milieux aquatiques. Toutefois, les efforts visant à rendre les colorants plus solubles augmenteront probablement de façon artificielle la biodisponibilité plutôt que de la diminuer. Par conséquent, malgré les incertitudes, les données disponibles indiquent que le Solvent Red 23 et ses analogues ne sont pas très dangereux pour les organismes aquatiques dans la colonne d’eau.
De plus, en ce qui a trait à l’écotoxicité, compte tenu du comportement prévu de répartition du Solvent Red 23 et de ses analogues, les données disponibles sur les effets ne rendent pas bien compte de l’importance du sol et des sédiments comme milieux d’exposition. En effet, les seules données sur les effets qui ont été trouvées s’appliquent principalement aux expositions aquatiques pélagiques, même si la colonne d’eau peut ne pas être le moyen le plus préoccupant à long terme d’après les estimations sur la répartition et les profils des rejets.
Étant donné que la substance est utilisée dans d’autres pays, il est possible qu’elle entre sur le marché canadien comme composant d’articles manufacturés ou de produits de consommation. Les renseignements obtenus dans le cadre de l’enquête menée en vertu de l’article 71 et d’autres sources de renseignements indiquent qu’elle est peut-être présente dans un certain nombre de ces produits au Canada. Les renseignements disponibles ne sont actuellement pas suffisants pour donner une estimation quantitative permettant de définir l’importance de cette source dans l’évaluation écologique. Cependant, on prévoit que les volumes de rejets de Solvent Red 23 dans les divers milieux naturels ne différeraient pas énormément des quantités estimées ici, bien que les quantités transférées au recyclage ou à l’élimination des déchets puissent être supérieures. On reconnaît également la possibilité que des rejets se dégagent des sites d’enfouissement, bien que cela soit peu probable et que les rejets éventuels soient faibles.
Évaluation de l’exposition
Aucune donnée empirique n’a été trouvée sur le Solvent Red 23 dans les milieux naturels. On ne disposait pas de suffisamment de données sur lesquelles fonder une analyse du cycle de vie permettant de prédire les pourcentages de perte aux fins de l’estimation des concentrations dans l’environnement. Par conséquent, on a estimé les concentrations du Solvent Red 23 en se fondant sur sa pression de vapeur et sa solubilité dans l’eau (valeurs les plus faibles de la fourchette de valeurs des analogues) et en présumant que la limite supérieure de la fourchette, soit 4 000 kg (1 000 kg provenant de chacune des quatre entreprises ayant fait une déclaration), a été entièrement rejetée dans les égouts, les eaux usées et les sols. Les concentrations environnementales estimées obtenues au moyen de la version 6 du logiciel ChemCAN sont négligeables (Environnement Canada, 2008a; ChemCAN, 2003).
On a estimé le potentiel d’exposition au Solvent Red 23 de l’ensemble de la population résultant de l’utilisation de cosmétiques et de certains produits de soins personnels à l’aide de ConsExpo 4.1 (ConsExpo, 2006; RIVM, 2006). On a calculé les estimations des expositions cutanées provenant de cosmétiques et de produits de soins personnels représentatifs contenant du Solvent Red 23, comme des préparations pour bains, des huiles à massage, des revitalisants, des colorants capillaires, des crèmes corporelles, des nettoyants pour le visage et des vernis à ongles. L’exposition orale a été estimée pour le brillant et le baume à lèvres contenant du Solvent Red 23.
L’estimation de l’exposition cutanée provenant de l’utilisation de produits de soins personnels va de 0,002 mg/kg p.c. par jour (huile de massage) à 0,18 mg/kg p.c. par jour (crème corporelle) avec une hypothèse prudente selon laquelle 26 % du produit appliqué est absorbé. On a estimé une exposition par voie orale de 0,01 mg/kg p.c. par jour pour les enfants âgés de 5 à 11 ans et de 0,006 mg/kg p.c. par jour pour la population générale provenant de l’utilisation de brillant et de baume à lèvres, en appliquant une hypothèse prudente selon laquelle 100 %[3] du produit appliqué est ingéré. Compte tenu de la nature prudente des hypothèses modélisées et en présumant prudemment une absorption par voies cutanée et orale de 26 et de 100 % respectivement, ces valeurs sont considérées comme les estimations des limites supérieures d’exposition. L’exposition aux produits de consommation par inhalation est considérée comme minime en raison de la faible volatilité de cette substance.
Évaluation des effets sur la santé
Le Solvent Red 23 est un membre de la famille des colorants azoïques, qui peuvent subir une rupture réductrice par l’intermédiaire des enzymes azoréductases trouvées dans les tissus des mammifères ainsi que par l’intermédiaire des bactéries de l’intestin et de la peau (p. ex. Chadwick et al., 1992; Platzek, 1999; Golka et al., 2004; Chen, 2006; Stingley et al., 2010). Par conséquent, des données sur les effets sur la santé des produits possibles de la rupture des liaisons azoïques ont été examinées dans le cadre de cette évaluation. Des données sur les analogues ont aussi été étudiées pour alimenter la base de données sur les effets sur la santé et pour préciser le potentiel de rupture réductrice des liaisons azoïques du Solvent Red 23. Les analogues ont été choisis en fonction de la disponibilité des données relatives aux effets sur la santé et de leur similarité avec le Solvent Red 23. Le tableau 7 présente les analogues considérés dans la présente évaluation ainsi que les produits potentiels résultant de la rupture des liaisons azoïques du Solvent Red 23.
Tableaux 7 : Analogues et produits possibles de la rupture des liaisons azoïques du Solvent Red 23 dans l’évaluation des effets sur la santé humaine
Solvent Red 23
| Composé d’origine : Solvent Red 23 (Sudan III) (85-86-9) 1-[4-(phénylazo)phénylazo]-2-naphtol - diazo, contient un noyau naphtalène hydroxylé |
 |
| Nom commun (n° CAS) |
Nom de la LIS | Structure | Principales similarités et différences structurales avec le Solvent Red 23 |
|---|---|---|---|
| Sudan I / C.I. Solvent Yellow 14 (842-07-9) |
1-phénylazo-2-naphtol |  |
Similarités : contient un noyau naphtalène hydroxylé et une liaison azoïque. Différences : monoazoïque, un seul groupement phényle. |
| Sudan II / Solvent Orange 7 (3118-97-6) |
1-(2,4-diméthylphénylazo) napht-2-ol |  |
Similarités : contient un noyau naphtalène hydroxylé et une liaison azoïque. Différences : monoazoïque, un seul groupement phényle, qui est diméthylé. |
| Sudan IV / Solvent Red 24 (85-83-6) |
1-(2-méthyl-4-(2-méthylphénylazo) phénylazo)-2-naphtol |  |
Similarités : diazoïque, contient un noyau naphtalène hydroxylé. Différences : les deux noyaux phényle ont chacun un groupement méthyle à la positionortho. |
| Produits possibles de la rupture des liaisons azoïques | Structure |
|---|---|
| 4-aminoazobenzène (60-09-3) |
 |
| 1-amino-2-naphtol (2834-92-6) |
 |
| p-phénylènediamine (106-50-3) |
 |
| Aniline (62-53-3) |
 |
Potentiel de rupture des liaisons azoïques
Des recherches sur la capacité des bactéries de l’intestin humain à métaboliser le Solvent Red 23, qui entraîne le rejet d’amines aromatiques, ont été effectuées en incubant du Solvent Red 23 avec des suspensions de selles humaines fraîches ou avec du Lactobacillus acidophilus et duLactobacillus fermentum. Les deux études ont permis d’identifier l’aniline en tant que métabolite du Solvent Red 23, ce qui indique que la microflore de l’intestin humain est capable de réduire la liaison azoïque du Solvent Red 23 (Xuet al., 2007; Chen et al., 2009). Des rats à qui l’on a injecté par voie intrapéritonale du Solvent Red 23 radioactif ont excrété 15,8 % de la radioactivité totale administrée dans l’urine, dont 80 % a été identifiée comme étant du 4-aminophénol, métabolite d’hydroxylation de l’aniline (Ryan et Welling, 1967), ce qui démontre que la rupture réductrice des liaisons azoïques du Solvent Red 23 a lieu in vivo.
Le Sudan I (n° CAS 842-07-9), un analogue monoazoïque du Solvent Red 23, a aussi été métabolisé en 4-aminophénol et ses conjugués dans des lapins exposés oralement, ce qui indique que les deux substances ont un devenir métabolique semblable qui entraîne le rejet d’aniline, qui est ensuite convertie en 4-aminophénol (EFSA, 2005). Sur ce fondement, l’EFSA juge prudent de supposer que la génotoxicité et la cancérogénicité associées au Sudan I peuvent aussi être associées au Solvent Red 23 (EFSA, 2005).
Le Sudan IV est un analogue méthylé diazoïque lipophile du Solvent Red 23, et sa capacité de subir une rupture des liaisons azoïques in vivo et in vitro a aussi été démontrée. Dans cette même étude, qui consistait à examiner la réduction azoïque du Solvent Red 23, on a observé que le Sudan IV subissait une rupture réductrice lorsqu’il était incubé avec des suspensions de selles humaines fraîchement isolées (Xu et al., 2007). Il a également été démontré que le Sudan IV était réduit de façon métaboliquein vivo à la suite d’une administration par voie trachéale chez les rats, alors qu’on a pu détecter dans l’urine du o-aminoazotoluène, l’analogue diméthyl du 4-aminoazobenzène (un produit potentiel de la rupture des liaisons azoïques du Solvent Red 23) (Parent et Dressler, 1977). Bien que l’administration par voie intratrachéale ne soit pas applicable à l’exposition humaine, l’étude susmentionnée démontre qu’un colorant lipophile avec solvant, le Sudan IV, peut subir une rupture in vivo et rejeter un amine aromatique cancérogène (o-aminoazotoluène) dont le profil de structure et de toxicité est très semblable à celui du 4-aminoazobenzène, un produit prévu de la rupture des liaisons azoïques du Solvent Red 23.
Collectivement, les données sur le Solvent Red 23 et ses analogues appuient le potentiel de rupture réductrice des liaisons azoïques, particulièrement lorsqu’ils sont administrés par voie orale, et par le fait même, le potentiel d’exposition aux amines aromatiques. Alors que l’aniline (n° CAS 62-53-3) a été le métabolite prédominant détecté dans les études visant à déterminer si les liaisons azoïques du Solvent Red 23 peuvent se rompre lors du métabolisme, la présence d’autres produits de rupture potentiels ne peut être évitée. Par conséquent, cette évaluation préalable considère aussi les données relatives aux effets sur la santé des produits potentiels de rupture des liaisons azoïques du Solvent Red 23 : 4-aminoazobenzène (n° CAS 60-09-3), 1-amino-2-naphtol (n° CAS 2834-92-6) etp-phénylénédiamine (n° CAS 106-50-3). Les renseignements sur les produits de rupture réductrice des liaisons azoïques potentiels sont présentés à l’annexe 6.
Solvent Red 23
Même s’il existe peu de données empiriques, les effets sur la santé du Solvent Red 23 ont déjà été évalués dans plusieurs études commandées par le Centre International de Recherche sur le Cancer (CIRC) (CIRC, 1975, 1987), le Comité scientifique des produits de consommation (CSPC) de l’Union européenne (CSPC, 2005, auparavant SCCNFP, 2002) et l’Autorité européenne de sécurité des aliments (EFSA) (EFSA, 2005). Un sommaire des données pertinentes issues de cette étude est présenté plus loin, de même que des renseignements additionnels (annexe 4). Des données pertinentes tirées de prévisions de modélisations du modèle de relation quantitative structure-activité (RQSA) sont présentés pour éclairer l’évaluation des effets sur la santé du Solvent Red 23 (annexe 7).
Génotoxicité et cancérogénicité
Plusieurs études sur des doses répétées orales et cutanées ont été relevées pour le Solvent Red 23. Le CIRC (1975) a cité deux études sur la toxicité chronique par voie alimentaire orale chez des souris et des rats. Les souris de « type B » (83 mâles, 54 femelles) provenant d’un croisement de multiples souches ont été exposées au Solvent Red 23 (appelées « Sudan G ») dans l’alimentation avec environ 67 mg/kg p.c. par jour[4] pendant 752 jours (Waterman et Lignac, 1958). À la fin de la période d’observation, les auteurs ont constaté des tumeurs aux poumons dans les groupes d’expositions mâles (9) et femelles (7), ce qui était statistiquement supérieur aux groupes témoins (0 chez les mâles, 1 chez les femelles). Les auteurs considéraient que l’incidence élevée de cancers du poumon chez les souris exposées était normale pour les souches de souris de type B, et que la faible incidence des tumeurs aux poumons dans les groupes témoins était attribuable à la distribution non uniforme des souris ayant des sensibilités différentes. Des incidences similaires de papillomes du secteur gastrique antérieur et des tumeurs mammaires ont été observées chez les animaux témoins et exposés. Un rapport sur les rats Wistar (5/sexe) nourris avec 4 % de Solvent Red 23 (sous le nom de Sudan III) dans leur alimentation pendant une période pouvant aller jusqu’à 18 mois (environ 2 000 mg/kg p.c. par jour[5]) n’a révélé aucun effet lié aux expositions; toutefois, l’examen sommaire et microscopique semblait être limité au tube digestif et au foie (Willheim et Ivy, 1953). Le CIRC a considéré ces données comme non pertinentes en raison des « doses administrées, du degré de déclaration ou du nombre d’animaux utilisés ». D’autres études orales non reconnues par le CIRC ont aussi été relevées. Dans une étude antérieure, le Solvent Red 23 a été administré à des rats par l’alimentation à une concentration de 0,04 % (environ 21 mg/kg p.c. par jour[6]) pendant onze mois. Des modifications non précisées aux reins ont été observées, mais aucune tumeur (Maruya, 1938). Aucune tumeur n’a été observée au foie ou ailleurs lorsque 16 rates Long-Evans ont été nourries avec 0,1 % Solvent Red 23 dans 1 mL d’huile de sésame (environ 3 mg/kg p.c. par jour[7]) par instillation gastrique pendant 25 semaines (5x/semaine) (Huggins et al., 1978). Les mêmes auteurs ont démontré que du Solvent Red 23, administré par voie orale à des rats aux mêmes doses, protégeait de la leucémie et des tumeurs de la glande mammaire induites par les substances hautement cancérogènes 7,12-di- et 7,8,12-tri-méthylbenz[a]anthracène) (DMBA et TMBA, respectivement) (Huggins et Pataki, 1965; Huggins et al., 1978). On a émis une hypothèse selon laquelle un mécanisme de cet effet protecteur est fondé sur une forte induction, par le Solvent Red 23, des systèmes d’enzymes en phases I et II qui peuvent agir pour éliminer efficacement le DMBA et le TMBA in vivo (Hatakeyama et al., 1996; Fujita et al., 1988). En raison de leurs limites, les études résumées ici ajoutent peu à l’évaluation des effets cancérogènes (p. ex. expositions par une seule dose, temps d’exposition court).
Des études sur des doses répétées par voie cutanée ont également été relevées pour le Solvent Red 23. Dans une étude non publiée, on a exposé des lapins à des concentrations allant jusqu’à 1 % (quotidiennement) de Solvent Red 23 dans un onguent blanc USP ou dans un onguent hydrophile USP pendant 21 ou 90 jours (CSPC, 1988). L’essai a été effectué à la fois sur la peau intacte et sur la peau éraflée. Les seuls effets déclarés étaient une inflammation de la peau, un épaississement et une hyperkératose, même si le CSPC (2005) considérait que l’étude n’était pas valable parce que sa méthode n’était pas décrite. Dans une étude sur l’exposition chronique par de la peinture sur la peau, des souris Webster suisses (50/sexe) étaient exposées une fois par semaine sur la peau rasée du dos à une concentration en une seule exposition de 1 % de Solvent Red 23, (D&C Red 17) dans 0,1 mL de laurylsulfate de sodium (dose hebdomadaire approximative de 33 mg/kg p.c.[8]) ou dans le véhicule seulement (Carson, 1984). Des observations cliniques ont été faites à tous les jours pendant la période d’exposition alors que des analyses histologiques de tous les tissus et des organes manifestement anormaux ont eu lieu à l’autopsie après 18 mois d’exposition ou dans le cadre de groupes provisoires sacrifiés. Les auteurs de l’étude n’ont déclaré aucune modification de pathologiques au lieu d’exposition ou dans les tissus examinés, qui pourraient être attribuables à l’exposition au D&C Red 17 à la concentration de l’essai étudiée (Carson, 1984).
D’après les évaluations du CSPC (2005, auparavant SCCNFP, 2002), les données disponibles sur la cancérogénicité du Solvent Red 23 ont été considérées comme non valables pour la caractérisation de la cancérogénicité de cette substance. Le CIRC a déterminé que la classification globale relative au cancer pour cette substance serait le Groupe 3 du CIRC (inclassable quant à sa cancérogénicité pour l’homme) en raison de données insuffisantes sur les animaux et de l’absence de données épidémiologiques sur les humains (CIRC, 1975, 1987). Même si les études disponibles sur les animaux concernant le Solvent Red 23, administré par voie orale et topique, n’ont démontré qu’il n’existe aucun signe de cancérogénicité aux doses uniques testées et que la substance peut avoir un effet protecteur contre la cancérogénicité des produits cancérogènes connus, soit le DMBA et le TMBA (Huggins et Pataki, 1965; Hugginset al., 1978), ces observations en elles-mêmes ne constituent pas une preuve suffisante que le Solvent Red 23 lui-même n’est pas cancérogène. En raison de l’insuffisance de détails sur les conditions de l’étude, du petit nombre d’animaux utilisés ou du nombre limité des doses testées, aucune conclusion ne peut être tirée concernant la cancérogénicité du Solvent Red 23 à partir de ces données.
Plusieurs études ont porté sur le potentiel génotoxique du Solvent Red 23. Les tests d’Ames, dans lesquels sont utilisées des souches Salmonella typhimurium TA98 et TA100, étaient négatifs lorsqu’un composé purifié a été testé. Toutefois, pour le Solvent Red 23, 3 des cinq préparations commerciales étaient mutagéniques en présence de l’activateur S9. Les auteurs ont attribué les résultats positifs à la présence de résidus de 4-aminoazobenzène (Miyagoshi et al., 1985; SCCNFP, 2002). La génotoxicité du Solvent Red 23 était également négative dans des essais de recombinaisons bactériologiques (Kada et al., 1972; Mamber et al., 1983). Il convient de noter que la réduction des liaisons azoïques s’est avérée nécessaire pour activer de nombreux colorants azoïques. Par conséquent, puisque les systèmes S9 standards ne sont pas des médiateurs efficaces de la rupture des liaisons azoïques, les résultats négatifs de ces études ne sont pas concluants, car la méthode d’activation négative pourrait ne pas convenir à ce groupe de composés (Prival et Mitchell, 1982; SCCNFP, 2002). Une incubation de cellules CHO en présence de Solvent Red 23, sans activation métabolique, a augmenté la fréquence des cassures chromosomiques comparativement aux témoins (Au et Hsu, 1979), alors qu’un autre essai d’aberrations chromosomiques effectué in vitrodans des lymphocytes humains a été négatif (CSPC, 2005). Le CSPC a jugé incomplètes les données sur la génotoxicité du Solvent Red 23 et qu’il était impossible de tirer une conclusion sur le potentiel de génotoxicité (SCCNFP, 2002; CSPC, 2005).
Les modèles RQSA CASETOX, DEREK et TOPKAT ont donné des résultats mitigés concernant le potentiel génotoxique et cancérogène du Solvent Red 23, lesquels sont résumés à l’annexe 7 (CASETOX, 2008; DEREK, 2008; TOPKAT, 2004).
Effets non cancérogènes
Le potentiel d’irritation et de sensibilisation du Solvent Red 23 a été résumé dans des rapports du CSPC. Le Solvent Red 23 a été considéré comme un irritant marginal, compte tenu de la preuve qu’il est légèrement irritant pour la peau et les membranes muqueuses des lapins (CSC, 1988, CSPC, 2005). Des recherches portant sur la sensibilisation de la peau ont montré que les individus à qui l’on a administré un ou plusieurs colorants azoïques n’étaient pas sensibles au Solvent Red 23 (Kozuka et Tashiro, 1980; CSPC, 2005). Toutefois, 3/6 et 1/6 des cobayes exposés à l’amine aromatiquep-phénylénédiamine ou 4-aminoazobenzène respectivement étaient sensibilisés au Solvent Red 23 (Xie et al., 2000; CSPC, 2005).
Les effets de l’exposition in utero sur la reproduction des mâles ont été examinés dans une étude de l’exposition par voie orale dans laquelle des souris enceintes étaient exposées par gavage au Solvent Red 23 (1 000 mg/kg p.c. par jour) ou par le véhicule seulement pendant les jours de gestation 8 à 12 (Gray et Ostby, 1993). Par la suite, les testicules des rejetons mâles (40 du groupe Solvent Red 23, 19 du groupe témoin) ont été examinés 48 à 50 jours après leur naissance. Aucune modification liée à l’exposition n’a été observée dans le poids corporel, le poids des testicules, le nombre de tubes séminifères, le pourcentage de tubules atrophiés ou le poids de la vésicule séminale. Les auteurs n’ont également relevé aucune toxicité des mères et aucune autre modification des paramètres néonataux. Ces données n’ont toutefois pas été mentionnées dans l’étude.
Analogues
Cancérogénicité et génotoxicité
Le potentiel génotoxique et cancérogène des colorants azoïques apparentés Sudan I, Sudan II et Sudan IV a également été étudié dans cette évaluation (voir le tableau 7 ci-dessus). Ces substances sont aussi des colorants lipophiles avec solvants du groupe Sudan et elles ont des propriétés physiques et chimiques, des amines aromatiques et un métabolisme semblables à ceux du Solvent Red 23 (voir aussi la section Absorption, distribution, métabolisme et excrétion). Par conséquent, le potentiel génotoxique et cancérogène de ces substances est examiné afin de mieux connaître le profil de toxicité du Solvent Red 23.
Le Sudan I est un analogue monoazoïque du même groupe de colorants Sudan que le Solvent Red 23 (Sudan III), et tous deux partagent deux composantes d’amines aromatiques identiques (aniline et 1-amino-2-naphtol). Dans des études de l’exposition chronique par l’alimentation réalisées par le National Toxicology Program (NTP) des États-Unis, la cancérogénicité orale du Sudan I était positive chez les rats mâles et femelles (mais pas chez les souris) d’après une augmentation de l’incidence de nodules néoplasiques au foie en fonction de la dose (NTP, 1982). Cette substance s’est avérée positive pour la mutagénicité dans l’analyse des mutations du lymphome de la souris et dans les tests d’Ames bactériologiques avec et sans activation métabolique par l’activateur S9 sur des rats et des hamsters, mais était négative pour les aberrations chromosomiquesin vitro et in vivo, et équivoque pour le micronoyau in vivo (NTP, 2010). Le Sudan I a été classé comme cancérogène et mutagène en Europe en vertu du règlement CLP[9] (Commission européenne, 2008). Par conséquent, compte tenu de l’absence de preuve de sécurité adéquate (CSPC, 2001, 2004), l’utilisation de cette substance dans les cosmétiques a été interdite en Europe par son inscription (sous l’appellation « CI Solvent Yellow 14 ») à l’annexe II de la Directive sur les cosmétiques (Commission européenne, 2010).
Le Sudan II, aussi appelé Solvent Orange 7, est un analogue monoazoïque dont la structure ressemble à celle du Sudan I. Contrairement au Sudan I, Sudan II a un groupement méthyle aux positions 2 et 4 du noyau phényle. Le Sudan II a fait l’objet d’essais dans un nombre limité d’études in vitro sur la mutagénicité bactérienne. Les résultats de ces études ont été considérés comme des preuves suffisantes de la mutagénicité du Sudan II chez les bactéries après activation métabolique (EFSA, 2005). Le seul essai in vitro portant sur la génotoxicité s chez les mammifères a donné des résultats négatifs. Plusieurs études sur la cancérogénicité ont été effectuées chez des souris ou des rats; toutefois, le CIRC a jugé que ces études étaient inadéquates pour évaluer la cancérogénicité du Sudan II (CIRC, 1975). L’EFSA, par contre, a déclaré l’incidence élevée de tumeurs de la vessie chez des souris ayant reçu des implants de Sudan II (directement dans la vessie) comme suffisante pour déclarer que cette substance présente une cancérogénicité possible, jusqu’à preuve du contraire (EFSA, 2005).
Le Sudan IV est un analogue diméthyle diazoïque lipophile du même groupe Sudan que le Solvent Red 23 (Sudan III) et tous deux partagent un composé d’amine aromatique similaire (o-aminoazotoluène)[10] et un composé d’amine aromatique identique (1-amino-2-naphthol)[11]. Le Sudan IV a été classé en fonction de sa cancérogénicité et de sa génotoxicité, bien que sa cancérogénicité ait été testée dans plusieurs essais dépassés évalués par le CIRC (1975). Vingt-quatre rats ont été exposés par voie sous-cutanée à 0,2 ml d’une solution contenant 2 % de Sudan IV, une fois par semaine, pendant 403 jours. Sur les huit rats qui ont survécu après 403 jours, quatre ont développé des sarcomes locaux; toutefois, cette étude ne comportait pas de groupes témoins (Umeda, 1957, 1958) véhicules (Tween 80). Les souris traitées oralement n’ont pas connu d’augmentation de l’incidence des tumeurs supérieure à celles des témoins, même si, chez une femelle traitée, on a observé de multiples adénomes hépatiques semblables aux tumeurs au foie observées chez des souris témoins positives exposées auo-aminoazotoluène (produit anticipé de la rupture des liaisons azoïques du Sudan IV) (Waterman et Lignac, 1958). Aucune tumeur n’a été observée chez des rats Wistar exposés à 4 % de Sudan IV dans leur alimentation (environ 2 000 mg/kg p.c. par jour) pendant 18 mois. Toutefois, le quart des rats exposés qui ont survécu après 18 mois avaient des modifications cirrhotiques au foie et de l’hyperplasie des conduits biliaires. Ces modifications n’ont pas été observées chez les 50 rats témoins (Willheim et Ivy, 1953). Des hyperplasies épithéliales, et non des tumeurs, ont été observées dans une étude sur des souris à la peau peinturée (CIRC, 1975). En raison des données inadéquates sur le cancer chez les animaux résumées plus haut et de l’absence de données épidémiologiques, le CIRC a classé le Sudan IV dans le Groupe 3 (inclassable quant à sa cancérogénicité pour l’homme) (CIRC, 1975, 1987). En ce qui concerne la génotoxicité, le Sudan IV était positif dans la souche de Salmonella typhimurium TA98 selon la méthode Prival modifiée afin de faciliter la réduction azoïque (Zhouet al., 1987). Des résultats positifs ont aussi été observés dans les souches TA 1537, 1538 et 98 ainsi qu’une réduction du dithionite (EFSA, 2005). Dans des études antérieures, effectuées sans réduction azoïque, il a été démontré que la mutagénicité des bactéries était attribuable à une impureté du colorant de grade commercial (Miyagoshi et al., 1985). Le Sudan IV était également positif pour la transformation cellulaire déclenchée de façon virale dans des cellules d’embryons de hamsters de Syrie (Heidelberger et al., 1983). Compte tenu de la preuve de génotoxicité limitée, de la capacité d’induction de la prolifération épithéliale et de la similarité structurale avec le cancérogène Sudan I, un comité scientifique de l’EFSA a déterminé que le Sudan IV était potentiellement génotoxique et possiblement cancérogène (EFSA, 2005). D’après un avis du Comité scientifique de cosmétologie (CSC) de la Commission européenne selon lequel il existe des indications de potentiel cancérogène du Sudan IV (sous l’appellation « CI 26105 », CSC, 1988), son utilisation comme colorant dans les cosmétiques est actuellement interdite en Europe en vertu de son inscription à l’annexe II de la Directive sur les cosmétiques (Commission européenne, 2010). L’utilisation du Sudan IV dans les cosmétiques est actuellement interdite au Canada (Santé Canada, 2009).
En résumé, les données d’essais empiriques sur la génotoxicité du Solvent Red 23 lui-même ne sont pas concluantes. Toutefois, compte tenu de la preuve de génotoxicité et de cancérogénicité de son analogue Sudan I, et du rejet prévu d’amines aromatiques par rupture réductrice des liaisons azoïques (en particulier le 4-aminobenzène), la génotoxicité et la cancérogénicité sont considérées comme des effets critiques pour la caractérisation des risques du Solvent Red 23.
Produits potentiels de la rupture réductrice de la liaison azoïque
Comme le Solvent Red 23 peut subir une rupture à l’exposition, puis rejeter des amines aromatiques potentiellement dangereuses (voir la section Potentiel de rupturedes liaisons azoïques), les effets sur la santé des produits potentiels de la rupture réductrice des liaisons azoïques du Solvent Red 23 sont examinés dans la présente évaluation.
Le 4-aminoazobenzène (n° CAS 60-09-3) est une substance cancérogène reconnue pour les animaux, qui cause des tumeurs au foie et à la peau chez les rats. Le CIRC l’a classé comme une substance cancérogène du Groupe 2B (CIRC, 1975; 1987). En Europe, le 4-aminoazobenzène est classé comme une substance cancérogène aux termes du règlement CLP européen (Commission européenne, 2008; ESIS, c1995-2009). Dans le règlement REACH, il figure parmi les 22 amines aromatiques préoccupantes, qui ne devraient pas être libérées des colorants azoïques utilisés dans les textiles et les articles de cuir pouvant entrer en contact direct et prolongé avec la peau humaine ou la cavité buccale (REACH, annexe XVII, appendice 8) (Commission européenne, 2006). En ce qui concerne la génotoxicité du 4-aminoazobenzène, plusieurs épreuves de génotoxicité in vivo et in vitro (références citées dans BfR, 2003; CIRC, 1987; BIBRA, 1989) ont donné des résultats positifs quant à la mutagénicité, la clastogénicité et les dommages subis par l’ADN. L’analogue diméthyle o-aminoazotoluène (n° CAS 97-56-3) est considéré comme cancérogène par le CIRC (1975, 1987), le NTP (2005) et la Commission européenne (2008), et figure parmi les 22 amines aromatiques réglementées dans les colorants azoïques du règlement REACH (Commission européenne, 2006).
L’aniline (n° CAS 62-53-3) a été évaluée précédemment comme une substance prioritaire par Santé Canada et Environnement Canada (Canada, 2010) et par l’Union européenne (UE, 2004). Dans des études sur l’exposition chronique par l’alimentation, des tumeurs à la rate propres aux espèces et aux sexes ont été observées chez des rats mâles (mais non chez les femelles) à la dose la plus élevée; ces tumeurs n’ont toutefois pas été observées chez les souris mâles ou femelles. Des résultats mitigés ont été obtenus dans des essais de génotoxicité, et aucune génotoxicité n’a été observée dans la rate. Des études sur l’exposition aiguë et à doses répétées chez des rats, des chiens et des volontaires humains ont également montré que l’aniline induit la formation de méthémoglobine (UE, 2004).
Le potentiel cancérogène du 1-amino-2-naphtol (n° CAS 2834-92-6) n’a pas été étudié, et aucune recherche pertinente avec doses répétées n’a été relevée (BfR, 2003). Toutefois, une augmentation du nombre de tumeurs à la vessie (10/36 comparativement à 2/56) et de métaplasies squameuses (18/36 comparativement à 9/56) a été observée lorsque du 1-amino-2-naphtol était implanté dans la vessie par l’intermédiaire de granulés de paraffine (Bonser et al., 1956). D’après des essais effectués sur la soucheSalmonella typhimurium TA100, le 1-amino-2-naphtol peut exercer une mutation bactérienne inverse (Dillon et al., 1994).
Le Comité scientifique des produits de consommation (CSPC) de la Commission européenne a examiné la toxicité dup-phénylénédiamine (n° CAS 106-50-3) dans le cadre d’une évaluation des risques (CSPC, 2006). Selon le CSPC, lep-phénylénédiamine présente une toxicité aiguë modérée par voie orale et une toxicité faible par voie cutanée. Par ailleurs, il est un sensibilisant cutané (CSPC, 2006). Lep-phénylénédiamine figure actuellement sur la Liste critique des ingrédients dont l’utilisation est interdite dans les cosmétiques de Santé Canada (Santé Canada, 2009) et ne peut être utilisé dans les produits devant être appliqués sur la peau. Les données sur la génotoxicité in vitro pour lep-phénylénédiamine sont mitigées : résultats positifs et négatifs dans le cadre du test d’Ames, de l’essai sur les lymphomes de souris et du test du micronoyau qui permettent d’évaluer la clastogénicité des cellules de mammifères. Une dose sans effet nocif observé (DSENO) de 4 mg/kg p.c. par jour a été calculée à partir d’une étude sur l’exposition subchronique par l’alimentation chez les souris fondée sur des gains de poids du foie et des reins. De nombreuses études sur la cancérogénicité du p-phénylénédiamine ont été trouvées, y compris une étude sur l’exposition chronique par l’alimentation chez des souris B6C3F1 et des rats F344 menée par le National Toxicology Program (NTP) des États-Unis en 1979. Cette étude a prouvé que le p-phénylénédiamine n’augmentait pas l’incidence des tumeurs chez les animaux exposés (CSPC, 2006).
Absorption, distribution, métabolisme et excrétion
Il existe peu de données permettant de caractériser l’absorption du Solvent Red 23 par voies orale et cutanée. Dans une étude sur l’exposition par voie orale réalisée sur des rats, du Solvent Red 23 intact a été éliminé principalement dans les selles (83,6 à 95 % selon le solvant), alors que le reste de la dose administrée n’a pas été pris en compte (Ryan et Welling, 1967). Plus récemment, des études sur des expositions répétées (doses de 3 à 900 mg/kg p.c. par jour) ont démontré que le Solvent Red 23 modifie considérablement le contenu en protéines et l’activité enzymatique (CYP1A, glutathion S-transférase, glutathion peroxydase, ménadione-réductase, etc.) dans le foie et le cerveau des hamsters, des souris et des rats exposés par la voie orale (Huggins et al., 1978; Hatakeyama et al., 1996; Romero et al., 2000). Les effets des modulateurs enzymatiques qui suivent une exposition orale indiquent fortement que le Solvent Red 23 ou les produits potentiels de la rupture des liaisons azoïques sont systématiquement absorbés et distribués par la voie orale. L’analogue monoazoïque du Solvent Red 23, le Sudan I, a été rapidement absorbé après une administration orale chez des rats et des lapins, et seulement de petites quantités ont été excrétées telles quelles (CIRC, 1975). Toutefois, en raison de la plus grande taille des molécules et de la solubilité moins élevée dans l’eau du Solvent Red 23 comparativement à celles du Sudan I (annexe 5), l’absorption orale de la structure fondamentale du Solvent Red 23 devrait être relativement moins importante. Dans l’ensemble, les données sur le Solvent Red 23 et son analogue Sudan I indiquent qu’il existe un potentiel d’absorption par la voie orale. Une fraction d’absorption orale par défaut prudente de 100 % a donc été utilisée pour calculer les estimations des expositions.
Dans une étude sur l’absorption cutanée in vitro, on a exposé de la peau de porc viable et de la peau d’humain non viable à un écran solaire contenant du Solvent Red 23 disponible sur le marché. Entre 12 et 15 % de la dose appliquée était retenue dans la peau (7,3 à 10,7% dans la couche cornée, 1,3 à 5,6 % dans le derme et l’épiderme combinés), et moins de 1 % de la radioactivité retrouvée dans le fluide récepteur (Youricket al., 2007). Une autre étude sur l’absorption par voie cutanée a également démontré des résidus de Solvent Red 23 liés à la peau après une application sur la peau excisée de glutathion peroxydase avec ou sans véhicules visant à accroître la pénétration chez des rats; toutefois, la substance n’a pas été détectée dans le fluide récepteur (Sasaki et al., 1990). Collier et al., (1993) ont démontré que l’analogue monoazoïque Sudan I (5 µg/cm2 dans de l’acétone) était conservé dans les couches de la peau à des niveaux semblables à ceux observés pour le Solvent Red 23. Mais, contrairement au Solvent Red 23, jusqu’à 30 % du Sudan I appliqué a été retrouvé dans le fluide récepteur, et environ 26 % était absorbé par la peau humaine en 24 heures. Collieret al., (1993) ont également rapporté que 50 % du marqueur du fluide récepteur détecté était causé par la présence de produits de la réduction des groupements azoïques, mesurés comme étant la somme de toutes les amines aromatiques (principalement l’aniline) présents, y compris leurs métabolites formés par N-oxydation etN-acétylation. Par conséquent, l’absence du Solvent Red 23 dans le fluide récepteur indiquée dans les études susmentionnées pourrait ne pas être une preuve certaine de la non-absorption cutanée, car il se peut que des amines aromatiques (ou leurs métabolites) non marquées générées par rupture réductrice des liaisons azoïques aient été présents mais non détectés. De plus, Yourick et al., (2007) ont lavé des échantillons de peau avec un détergent à 1 % avant l’exposition, ce qui a diminué le nombre de bactéries présentes sur la peau. Il a été démontré que les bactéries métabolisent les colorants azoïques jusqu’à 300 fois plus efficacement que les mammifères (Collier et al., 1993) et qu’elles peuvent ainsi rejeter des amines aromatiques susceptibles d'être plus facilement absorbées que leurs composés d’origine, qui ont un poids moléculaire plus élevé (Platzeket al., 1999). Par conséquent, on ignore si l’absorption des produits de la rupture des liaisons azoïques ou leurs métabolites subséquents est importante après une exposition cutanée au Solvent Red 23. En raison de ces incertitudes, on a utilisé une valeur d’absorption cutanée prudente de 26 % fondée sur les propriétés physiques et chimiques du Solvent Red 23, qui semblent indiquer une pénétration cutanée faible, ainsi que sur des données empiriques sur la pénétration cutanée pour l’analogue monoazoïque Sudan I (Collier et al., 1993). Toutefois, en raison de la plus grande taille des molécules et de la solubilité dans l’eau plus faible du Solvent Red 23 comparativement au Sudan I, l’absorption cutanée de la structure fondamentale du Solvent Red 23 devrait être relativement plus faible. Par conséquent, la valeur d’absorption cutanée choisie de 26 % est considérée comme prudente pour l’estimation de l’exposition cutanée du Solvent Red 23.
Caractérisation des risques pour la santé humaine
L’exposition de l’ensemble de la population au Solvent Red 23 dans les milieux naturels devrait être négligeable. Il ne devrait pas non plus y avoir d’exposition au Solvent Red 23 par la nourriture, car cette substance n’est pas autorisée dans les aliments destinés à être vendus au Canada en vertu du Titre 16 du Règlement sur les aliments et drogues, et son utilisation n’a pas été déclarée dans l’emballage alimentaire. Il peut toutefois y avoir une exposition par voie cutanée ou buccale provenant de l’utilisation de cosmétiques et de certains produits de soins personnels. L’estimation de la limite supérieure de l’exposition chronique par voie cutanée provenant de cosmétiques (y compris les préparations pour bain, les huiles à massage, les revitalisants, les colorants capillaires, les lotions corporelles, les nettoyants pour le visage et les vernis à ongles) est de 0,002 à 0,18 mg/kg p.c. par jour, en supposant une valeur d’absorption cutanée prudente de 26 %. L’exposition au Solvent Red 23 par voie orale peut aussi avoir lieu par l’utilisation de brillant ou de baume à lèvres dont l’estimation de la limite supérieure de l’exposition chronique est de 0,01 mg/kg p.c. par jour pour les enfants âgés de 5 à 11 ans et de 0,006 mg/kg p.c. par jour pour la population générale. L’exposition par inhalation provenant de ces sources devrait être minime.
Les données empiriques relatives aux effets sur la santé du Solvent Red 23 étaient limitées. Quant aux résultats des essais de génotoxicité, ils étaient mitigés. Le CIRC et le CSPC ont considéré comme inadéquates les études disponibles sur la cancérogénicité. Étant donné que les liaisons azoïque du Solvent Red 23 peuvent subir une rupture, les données relatives aux effets sur la santé des produits prévus de la rupture des liaisons azoïques, en particulier le 4-aminoazobenzène, ont été prises en considération dans la caractérisation des effets sur la santé du Solvent Red 23. Bien que le 4-aminoazobenzène n’ait pas été détecté dans des études du métabolisme in vitro avec du Solvent Red 23, un analogue étroitement lié, le Sudan IV, a bel et bien subi une rupture des liaisons azoïquesin vivo et rejeté du o-aminoazotoluène (analogue méthylé du 4-aminoazobenzène). Cela semble indiquer que le 4-aminoazobenzène peut aussi être libéré du Solvent Red 23 in vivo. Il a été démontré que le 4-aminoazobenzène induit des tumeurs chez les rats après une exposition par voie orale et cutanée, il a été classé cancérogène par le CIRC (1987) et la Commission européenne (2010), est s’est également avéré positif dans une gamme d’essais sur la génotoxicité in vivo et in vitro (références citées dans BfR, 2003; CIRC, 1987; BIBRA, 1989). De plus, il a été démontré que le colorant analogue monoazoïque Sudan I, classé cancérogène et mutagène en Europe, est métabolisé en certains amines aromatiques identiques à ceux du Solvent Red 23 in vitro et in vivo, soit l’aniline et le 1-amino-2-naphtol.
Compte tenu de la preuve de génotoxicité et de cancérogénicité du Sudan I, un analogue du Solvent Red 23, et des prévisions de rejet d’amines aromatiques par rupture réductrice des liaisons azoïques du Solvent Red 23 (c.-à-d. le 4-aminoazobenzène), la génotoxicité et la cancérogénicité sont considérées comme des effets critiques pour la caractérisation des risques du Solvent Red 23. Compte tenu du potentiel d’exposition de l’ensemble de la population provenant des cosmétiques et des produits de soins personnels contenant du Solvent Red 23 et du potentiel de génotoxicité et de cancérogénicité ayant une probabilité d’effets nocifs à tous les niveaux d’exposition, il est conclu que le Solvent Red 23 pénètre dans l’environnement en quantité, à des concentrations ou dans des conditions qui constituent ou peuvent constituer un danger pour la vie et la santé humaines au Canada.
Incertitudes de l’évaluation des risques pour la santé humaine
Comme il existe peu de données relatives aux effets sur la santé du Solvent Red 23 lui-même, le profil de risque est principalement fondé sur celui des produits potentiels de la rupture des liaisons azoïques et des colorants azoïques analogues. Bien que les données disponibles sur le métabolismein vitro du Solvent Red 23 dans lesquelles étaient utilisées des bactéries du tractus gastrointestinal semblent indiquer la probabilité d’une rupture réductrice des liaisons azoïques après une exposition orale, il existe une incertitude sur l’étendue de la rupture ainsi que la proportion et l’identité relatives des produits de rupture générés. Par conséquent, il existe une incertitude sur le degré d’exposition de l’ensemble de la population canadienne aux produits potentiels de la rupture des liaisons azoïques du Solvent Red 23 par voie orale.
Il existe une incertitude quant au potentiel d’absorption cutanée du Solvent Red 23 et à la possibilité que les amines aromatiques soient rejetés à l’exposition cutanée. Une valeur d’absorption cutanée de 26 % a été choisie d’après les propriétés physiques et chimiques du Solvent Red 23 et les données empiriques de l’analogue Sudan I. Cette valeur d’absorption cutanée est toutefois considérée comme prudente.
Le degré de confiance voulant que le Solvent Red 23 (ou ses produits de rupture prévus) soit absorbé par la voie orale en raison de l’induction d’enzymes observée chez de nombreuses espèces après une exposition est plus élevé par voie orale que par voie cutanée. Il existe également un degré de confiance élevé que le Solvent Red 23 subisse une rupture des liaisons azoïques, puis rejettent des amines aromatiques après une exposition par voie orale, comme l’a démontré la rupture des liaisons azoïques par des bactéries intestinales isolées. Donc, il existe une préoccupation relative plus importante pour la voie d’exposition orale (c.-à-d. le brillant et le baume à lèvres) dont le risque potentiel est soutenu par les données disponibles. Même si l’absence de données complémentaires n’empêche pas que des risques possibles augmentent suite à l’exposition par voie cutanée, les risques potentiels des effets sur la santé de l’exposition par voie cutanée sont considérés comme inférieurs à ceux posés suite à l’exposition par voie orale.
Les estimations des expositions au Solvent Red 23 par des cosmétiques et certains produits de soins personnels sont considérées comme des surestimations d’après plusieurs hypothèses prudentes telles que l’absorption cutanée de 26 % et l’utilisation de la limite supérieure de la fourchette des concentrations déclarées dans les produits de la base de données du SDC. Toutefois, il se peut que l’exposition totale au Solvent Red 23 soit sous-estimée, car ces estimations n’ont pas été calculées pour les usages simultanés des nombreux cosmétiques ou produits de soins personnels. Il demeure qu’on a confiance que l’exposition de l’ensemble de la population canadienne au Solvent Red 23 par ces produits ne dépasse pas les estimations présentées dans la présente évaluation.
D’après les renseignements contenus dans la présente évaluation préalable finale, le Solvent Red 23 ne pénètre pas dans l’environnement en une quantité, à une concentration ou dans des conditions de nature à avoir, immédiatement ou à long terme, un effet nocif sur l’environnement ou sur la diversité biologique, ou à mettre en danger l’environnement essentiel pour la vie. De plus, cette substance répond aux critères de persistance, mais ne répond pas aux critères relatifs au potentiel de bioaccumulation énoncés dans le Règlement sur la persistance et la bioaccumulation (Canada, 2000).
Compte tenu de l’exposition potentielle de l’ensemble de la population et de la preuve de génotoxicité et de cancérogénicité du 4-aminoazobenzène (produit potentiel de la rupture des liaisons azoïques) et du Sudan I (colorant azoïque analogue), il est conclu que le Solvent Red 23 pénètre dans l’environnement à une quantité, à une concentration ou dans des conditions de nature à constituer un danger au Canada pour la vie ou la santé humaines.
Par conséquent, il est conclu que le Solvent Red 23 satisfait à un ou plusieurs des critères établis dans l’article 64 de la LCPE (1999).
Considérations dans le cadre d’un suivi
Le Solvent Red 23 appartient à un groupe de substances azoïques pouvant être métabolisées et produire des amines aromatiques qui, en tant que classe, sont connues pour présenter des propriétés dangereuses, notamment en termes de cancérogénicité. Par conséquent, des activités supplémentaires (p. ex., recherche, évaluation, contrôle et surveillance) pourraient être entreprises afin de caractériser le risque présenté par ce vaste groupe de substances azoïques pour la santé humaine au Canada. Un avis d’intention décrivant la façon dont Santé Canada et Environnement Canada se pencheront sur ce groupe de substances se trouve à l’adresse Internet desSubstances chimiques.
ACD/pKaDB [module de prévision]. 2005. Version 9.04. Toronto (Ont.) : Advanced Chemistry Development. [réserve de consultation]
Anliker, R., Clarke, E.A., Moser, P. 1981. Use of the partition coefficient as an indicator of bioaccumulation tendency of dyestuffs in fish. Chemosphere 10(3):263-274.
Anliker, R., Moser, P. 1987. The limits of bioaccumulation of organic pigments in fish: their relation to the partition coefficient and the solubility in water and octanol.Ecotoxicol. and Environ. Safety 13:43-52.
Anliker, R., Moser, P., Poppinger, D. 1988. Bioaccumulation of dyestuffs and organic pigments in fish. Relationships to hydrophobicity and steric factors. Chemosphere17(8):1631-1644.
[ARLA] Agence de réglementation de la lutte antiparasitaire. 2010. Liste des produits de formulation de l’ARLA [en ligne]. Ottawa (Ont.) : Santé Canada, ARLA. [consulté le 13 janvier 2011].
Arnot, J.A., Arnot, M., Mackay, D., Couillard, Y., MacDonald, D., Bonnell, M., Doyle, P. 2010. Molecular size cut-off criteria for screening bioaccumulation potential: Fact or fiction?Integrated Environmental Assessment and Management6(2):210-224.
Aronson, D., Boethling, B., Howard, P., Stiteler, W. 2006. Estimating biodegradation half-lives for use in chemical screening.Chemosphere 63:1953-1960.
Au, W., Hsu, T.C. 1979. Studies on the clastogenic effects of biologic stains and dyes. Environ. Mutagen. 1:27-35.
BASF. 1990. Bericht uber die Prufung der akuten Toxizitit an der Goldorfe (Leuciscus idus L.,Goldvariante). Présenté par l’ETAD à Environnement Canada le 13 août 2008 par courriel.
Baughman, G.L., Perenich, T.A. 1988. Fate of dyes in aquatic systems: I. Solubility and partitioning of some hydrophobic dyes and related compounds. Environ. Toxicol. Chem.7(3):183-199.
Baughman, G.L., Weber, E.J. 1994. Transformation of dyes and related compounds in anoxic sediment: kinetics and products.Environ. Sci. Technol. 28(2):267-276.
Baughman, G.L., Bannerjee, S., Perenich, T.A. 1996. Dye Solubility. In: Physico-chemical Principles of Color Chemistry. Peters, A.T., Freeman, H.S. (éditeurs). Advances in Color Chemistry Series, Vol. 4. Glasgow (Écosse) : Blackie Academic and Professional Publishers. p. 145-195.
[BBM] Baseline Bioaccumulation Model. 2008. Gatineau (Qc) : Environnement Canada, Division des substances existantes. [modèle basé sur celui de Dimitrov et al., 2005]. Document disponible sur demande.
[BDIPSN] Base de données d’ingrédients de produits de santé naturels. 2010. Ottawa (Ont.) : Santé Canada. [consultée en juin 2010].
[BDPSNH] Base de données des produits de santé naturels homologués [en ligne]. 2010. Ottawa (Ont.) : Santé Canada. Accès : Qu'est-ce que l'extrait des données de la Base des données des produits de santé naturels homologués (BDPSNH)? [consultée en juin 2010]
[BfR] Institut fédéral allemand d’évaluation des risques (BfR Allemagne). 2003. Dyes Sudan I to IV in food : prise de position du BfR du 19 nov. 2003.
[BIBRA] Bibra Toxicology Advice and Consulting. 1989. Toxicity Profile: para-Aminoazobenzene. Surrey (Royaume-Uni).
[BIOWIN] Biodegradation Probability Program for Windows [modèle d’estimation]. 2008. Version 4.02. Washington (DC) : US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY) : Syracuse Research Corporation. Outils d'évaluation de l'exposition et des modèles.
Boethling, R.S., Howard, P.H., Beauman, J.A., Larosche, M.E. 1995. Factors for intermedia extrapolations in biodegradability assessment. Chemosphere 30(4):741-752.
Bonser, G.M., Bradshaw, L., Clayson, D.B., Jull, J.W. 1956. A further study of the carcinogenic properties of ortho hydroxy-amines and related compounds by bladder implantation in the mouse. Br. J. Canc. 10(3):539-546.
Braun, H. 1991. A new method for the determination of the solubility of disperse dyes. JSDC 107:77-83.
Brown, D. (ICI Group Environmental Laboratory, Brixham, Royaume-Uni). Environmental assessment of dyestuffs. Rédigé pour le compte de l’Ecological and Toxicological Association of the Dyes and Organic Pigments Manufacturers, Bâle (Suisse), ETAD ecological sub-committee project E3020, 1992. Présenté à Environnement Canada le 9 mai 2008.
Brown, D. 1987. Effects of colorants in the aquatic environment.Ecotox Environ. Safe 13:139-147.
Brown, D., Anliker, R. 1988. Dyestuffs and the environment – A risk assessment. Risk Assessment of Chemicals in the Environment. Richardson, M. (éd.). The Royal Society of Chemistry. P. 398−413. [comme cité dans : EPA du Danemark 1999].
Canada. 1978. Règlement sur les aliments et drogues. C.R.C., ch. 870.
Canada. 1999. Loi canadienne sur la protection de l’environnement (1999). L.C., 1999, ch. 33.
Canada. 2000. Loi canadienne sur la protection de l’environnement (1999) : Règlement sur la persistance et la bioaccumulation, C.P. 2000-348, 23 mars 2000, DORS/2000-107.Gazette du Canada, Partie II, vol. 134, n° 7.
Canada. Ministère de l’Environnement, ministère de la Santé. 1994. Liste des substances d’intérêt prioritaire, rapport d’évaluation : Aniline. Ministre des Approvisionnements et Services Canada, n° de cat. En 40-215/35E. Ottawa (Ont.) : Beauregard Printers, Ltd. 30 p.
Canada, Ministère de l’Environnement, Ministère de la Santé. 2006a. Loi canadienne sur la protection de l’environnement (1999) : Avis d’intention d’élaborer et de mettre en œuvre des mesures d’évaluation et de gestion des risques que certaines substances présentent pour la santé des Canadiens et leur environnement. Gazette du Canada, Partie I, vol. 140, n° 49.
Canada. Ministère de l’Environnement, ministère de la Santé. 2006b. Loi canadienne sur la protection de l’environnement (1999) : Avis concernant certaines substances considérées comme priorité pour suivi, Gazette du Canada, Partie I, vol. 140, n° 9.
Canada. Ministère de l’Environnement, ministère de la Santé. 2008a. Loi canadienne sur la protection de l’environnement (1999) : Avis de sixième divulgation d’information technique concernant les substances identifiées dans le Défi, Canada Gazette. Partie I, vol. 142, n° 22.
Canada. Ministère de l’Environnement. 2008b. Loi canadienne sur la protection de l’environnement (1999) : Avis concernant certaines substances identifiées dans le sixième lot du Défi. Canada Gazette. Partie I, vol. 142, n° 22.
Canada. Ministère de la Santé, ministère de l’Environnement. 2010. Loi canadienne sur la protection de l'environnement (1999) : Rapport de suivi : aniline.
Carson, S. 1984. Skin Painting Studies in Mice on 11 Fd&C and D&C Colors: Fd&C Green no. 3, Red No. 2, Red No. 4, Yellow No. 6, and External D&C No. 7, D&C Orange No. 4, Violet No. 2, Red No. 17, Red No. 34, and Yellow No. 7.Cutaneous and Ocular Toxicology 3(3):309-331. [cité dans CSPC, 2005].
CASETOX [module de prévision]. 2008. Version 2.0. Beachwood (OH) : MultiCASE Inc. CASETOX [réserve de consultation].
[CATABOL] Probabilistic assessment of biodegradability and metabolic pathways [modèle informatique]. c2004-2008. Version 5.10.2. Bourgas (Bulgarie) : Prof. Assen Zlatarov University, Laboratory of Mathematical Chemistry. CATALOGIC.
Chadwick, R.W., George, S.E., Claxton, L.D. 1992. Role of the gastrointestinal mucosa and microflora in the bioactivation of dietary and environmental mutagens or carcinogens. Drug Metab Rev 24(4):425-492.
ChemCAN [Level III fugacity model of 24 regions of Canada]. 2003. Version 6.00. Peterborough (Ont.): Trent University, Le centre canadien de modélisation et de chimie environnementales [consulté en janvier 2010].
Chen, H. 2006. Recent advances in azo dye degrading enzyme research. Curr. Protein Pept. Sci. 7(2):101-111.
Chen, H., Xu, H., Heinze, T.M., Cerniglia, C.E. 2009. Decolorization of water and oil-soluble azo dyes byLactobacillus acidophilus and Lactobacillus fermentum. J. Ind. Microbiol. Biotechnol. 36:1459-1466.
[CII] Color Index International [base de données sur Internet]. 2002- . 4e éd. Research Triangle Park (NC) : American Association of Textile Chemists and Colorists. Indice de couleur international [consultée le 3 février 2009].
[CIRC] Centre International de Recherche sur le Cancer. 1975.Monographies du CIRC sur l’évaluation des risques de cancérogénicité pour l’homme: Certains composés aromatiques azoïques, Volume 8. IARC Working Group on the Evaluation of the Risk of Chemicals to Man which met in Lyon, 26 novembre au 2 décembre 1974.
[CIRC] Centre International de Recherche sur le Cancer. 1987.Monographies sur l’évaluation des risques de cancérogénicité pour l’homme. Supplement 7 : Overall evaluations of carcinogenicity: an updating of IARC Monographs Volumes 1 to 42. Lyon (France) : CIRC.
Clariant. 1996. Ensemble de données IUCLID pour Disperse Blue 79 (N° CAS 12239-34-8). [base de données sur Internet]. [consultée le 28 octobre 2008].
Cohle, P., Mihalik, R. 1991. Early life stage toxicity of C.I. Disperse Blue 79:1 purified presscake to rainbow trout (Oncorhynchus mykiss) in a flow-through system. Final report. Columbia (MO) : ABC Laboratories Inc.
Collier, S.W., Storm, J.E., Bronaugh, R.L. 1993. Reduction of azo dyes during in vitro percutaneous absorption.Toxicol. Appl. Pharmacol. 118:73-79.
Commission européenne. 2006. Règlement (CE) n° 1907/2006 du Parlement européen et du Conseil (REACH).
Commission européenne. 2008. Règlement (CE) n° 1272/2008 relatif à la classification, à l’étiquetage et à l’emballage des substances et des mélanges.
Commission européenne. 2010. Directive 76/768/CEE du Conseil (Directive relative aux produits cosmétiques).
Communauté européenne. 1994. Directive du Conseil et du Parlement européen n° 94/36/CE du 30 juin 1994 sur les colorants aux fins d’utilisation dans les produits alimentaires. Journal officiel de l’Union européenne.
[ConsExpo] Consumer Exposure Model [en ligne]. 2006. Version 4.1. Bilthoven (Pays-Bas) : Rijksinstituut voor Volksgezondheid en Milieu (Institut national néérlandais de la santé publique et de l’environnement). ConsExpo 4.1.
[CPOP] Canadian POP Model. 2008. Gatineau (Qc) : Environnement Canada, Division des substances existantes; Bourgas (Bulgarie) : Prof. Assen Zlatarov University, Laboratory of Mathematical Chemistry. [Modèle élaboré à partir de celui de Mekenyan et al., 2005]. Disponible sur demande.
[CSC] Comité scientifique de cosmétologie.1988. Reports of the Scientific Committee on Cosmetology (Seventh Series). ISBN 92-825-8129-2. N° de catalogue CD-NA-11303-EN-C.
[CSPC] Comité scientifique des produits de consommation. 2001.Avis concernant les ingrédients chimiques dans les produits cosmétiques classés comme cancérogènes, mutagènes ou toxiques pour la reproduction selon la directive 67/548/EEC. SCCNFP/0474/01.
[CSPC] Comité scientifique des produits de consommation. 2004.Avis concernant les ingrédients chimiques dans les produits cosmétiques classés comme cancérogènes, mutagènes ou toxiques pour la reproduction selon la directive 67/548/EEC. SCCNFP/0825/04.
[CSPC] Comité scientifique des produits de consommation. 2005.Avis sur l'utilisation de CI26100 (CI Solvent Red 23) comme colorant dans les produits cosmétiques. SCCP/0902/05.
[CSPC] Comité scientifique des produits de consommation. 2006. Opinion on p-Phenylenediamine. SCCP/0989/06.
Datyner, A. 1978. The solubilisation of disperse dyes by dispersing agents at 127ºC. JSDC June 256-260.
[DEREK] Deductive Estimation of Risk from Existing Knowledge [module de prévision sur cédérom]. 2008. Version 10.0.2. Cambridge (MA) : Harvard University, LHASA Group. Prédiction de toxicologie [réserve de consultation].
Dillon, D., Combes, R., Zeiger, E. 1994. Activation by caecal reduction of the azo dye D and C red no. 9 to a bacterial mutagen.Mutagenesis 9(4):295-299.
Dimitrov, S, Dimitrova, N., Walker, J., Veith, G., Mekenyan, O. 2002. Predicting bioconcentration potential of highly hydrophobic chemicals. Effect of molecular size. Pure Appl. Chem. 74(10):1823-1830.
Dimitrov, S., Dimitrova, N., Parkerton, T., Comber, M., Bonnell, M., Mekenyan, O. 2005. Base-line model for identifying the bioaccumulation potential of chemicals. SAR QSAR Environ. Res. 16(6):531-554.
[EPA du Danemark] Danish Environmental Protection Agency. 1999.Enquête sur les colorants azoïques au Danemark. Consumption, use, health and environmental aspects. MiljØprojekt No. 509. Henriette, Danish Technological Institute, Environment, Ministry of Environment and Energy, Denmark, Danish Environmental Protection Agency, 1999. Rapport rédigé par Øllgaard, H., Frost, L., Galster, J., Hansen, O.C.
[EFSA] Autorité européenne de sécurité des aliments. 2005. Avis du groupe scientifique sur les additifs alimentaires, les arômes, les auxiliaires technologiques et les matériaux en contact avec les aliments [AFC] sur l’évaluation de la toxicologie d’un certain nombre de colorants illégalement présents dans l’alimentation au sein de l’UE. EFSA Journal (2005) 263:1-71. Article en anglais; résumé en français.
Environnement Canada. 1988. Données de la Liste intérieure des substances (LIS), 1984-1986, recueillies en vertu du paragraphe 25(1) de la LCPE (1988), et conformément à la Liste intérieure des substances : guide du déclarant. Données préparées par : Environnement Canada.
Environnement Canada. 1995. NSN submission. Données présentées à la Division des substances nouvelles d’Environnement Canada dans le cadre du Programme de renseignements concernant les substances nouvelles.
Environnement Canada. 2000. Environmental Categorization for Persistence Bioaccumulation and Inherent Toxicity of Substances on the Domestic Substances List Using QSARs. Rapport final. Division de l’évaluation des produits chimiques, Environnement Canada, juillet.
Environnement Canada. 2006. Données pour certaines substances recueillies en vertu de la Loi canadienne sur la protection de l’environnement (1999), article 71 : Avis concernant certaines substances considérées comme priorités pour suivi. Données préparées par Environnement Canada, Santé Canada, Programme des substances existantes.
Environnement Canada. 2007. QSARs: Reviewed Draft Working Document, Science Resource Technical Series, Guidance for Conducting Ecological Assessments under CEPA 1999. Division des substances existantes, Environnement Canada, Gatineau (Qc) : Environnement Canada, Division des substances existantes. Ottawa, K1A 0H3.
Environnement Canada. 2008a. Données sur les substances du lot 6 recueillies en vertu de l’article 71 de la Loi canadienne sur la protection de l’environnement (1999) : Avis concernant certaines substances identifiées dans le sixième lot du Défi. Données recueillies par Environment Canada, Programme des substances existantes.
Environnement Canada. 2008b. Guidance for conducting ecological assessments under CEPA, 1999: science resource technical series, technical guidance module: Mega Flush consumer release scenario. Document de travail préliminaire. Gatineau (Qc) : Environnement Canada, Division des substances existantes.
Environnement Canada. 2010. Rapport Mega Flush : Solvent Red 23 [consulté le 26 juillet 2010]. Rapport inédit. Gatineau (Qc) : Environnement Canada, Division des substances existantes.
[EPIsuite] Estimation Programs Interface Suite for Microsoft Windows [modèle d’estimation]. 2008. Version 4.0 Washington (DC) : US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY) : Syracuse Research Corporation. Outils d'évaluation de l'exposition et des modèles.
[ESIS] European Chemical Substances Information System [base de données sur Internet]. 2008. Version 5. Bureau Européen des Substances Chimiques (BESC). Système d'information des substances chimiques européenne [consulté le 13 février 2009].
[ESIS] European Chemical Substances Information System [base de données sur Internet]. c1995-2010. Ispra (Italie) : Commission européenne, Centre commun de recherche, Institut pour la santé et la protection des consommateurs, Bureau Européen des Substances Chimiques (BESC). [consultée en octobre 2009]. Système d'information des substances chimiques européenne (recherche dans l’onglet CLP Annex VI).
[ETAD] Ecological and Toxicological Association of Dyes and Organic Pigments Manufacturers. 1992. Draft Guidelines for the Assessment of Environmental Exposure to Dyestuffs.
[ETAD] Ecological and Toxicological Association of Dyes and Organic Pigments Canadian Affiliates, Dayan, J., Trebitz, H., consultants. 1995. Health and environmental information on dyes used in Canada. Rapport inédit présenté à Environnement Canada, Division des substances nouvelles. En page couverture : An overview to assist in the implementation of the New Substances Notification Regulations under the Canadian Environmental Protection Act.
[ETAD] Ecological and Toxicological Association of Dyes and Organic Pigments Manufacturers. 2005. Information received in support of DSL categorization for 12 disperse dyes. Courriel daté du 27 octobre 2005.
Fujita, S., Matsunaga, T., Masubunchi, Y., Suzuki, T. 1988. Possible mechanism of Sudan III-induced prevention of chemical carcinogenesis in rats. Canc. Res. 48:254-259.
Garner, R.C., Nutman, C.A.. 1977. Testing of some azo dyes and their reduction products for mutagenicity using salmonella typhimurium TA1538. Mutat Res 44:9-19.
Golka, K., Kopps, S., Myslak, Z.W. 2004. Carcinogenicity of azo colorants: influence of solubility and bioavailabilty. Toxicol. Lett. 151(1):203-210.
Gray, E.L., Ostby, J.S. 1993. The effects of prenatal administration of azo dyes on testicular development in the mouse: A structure activity profile of dyes dervived from benzidine, dimethylbenzidine, or dimethoxybenzidine. Fund. Appl. Toxicol. 20:177-183.
Haag, W.R., Mill, T. 1987. Direct and indirect photolysis of water-soluble azodyes: kinetic measurements and structure-activity relationships. Environ. Toxicol. Chem. 6:359-369.
Hatakeyama, S., Hayasaki, Y., Masuda, M., Kazusaka, A., Fujita, S. 1996. Mechanism for mouse strain differences in the protective effect of Sudan III against the in vivo genotoxicity of 7,12-dimethylbenz[a]anthracene. Toxicol. Lett.89(3):231-9.
Heidelberger, C., Freeman, A.E., Pienta, R.J., Sivak, A., Bertram, J.S., Casto, B.C., Dunkel, V.C., Francis, M.W., Kakunaga, T., Little, J.B., Schechtman, L.M. 1983. Cell transformation by chemical agents: a review and analysis of the literature: a report of the U.S. Environmental Protection Agency Gene-Tox program.Mutat. Res. 114:283-385.
Huggins, C.B., Pataki, J. 1965. Aromatic azo derivatives preventing mammary cancer and adrenal injury from 7,12-dimethylbenz[a]anthracene. Proc. Nat. Acad. Sci. 53:791-796.
Huggins, C.B., Ueda, N., Russo, A. 1978. Azo dyes prevent hydrocarbon-induced leukemia in the rat. Proc. Nat. Acad. Sci. 9:4524-4527.
Hunger, K. (éd). 2003. Industrial dyes; chemistry, properties, applications. Weinheim (Allemagne) : WILEY-VCH Verlag GmbH & Co. KGaA.
Isik, M., Sponza, D.T. 2004. Monitoring of toxicity and intermediates of C.I. Direct Black 38 azo dye through decolourization in an anaerobic/aerobic sequential reactor system.Journal of Hazardous Materials B114: 29−39.
Kada, T., Tutikawa, K., Sadaie, Y. 1972. In vitro and host-mediated ‘rec-assay’ procedures for screening chemical mutagens; and phloxine, a mutagenic red dye detected. Mutat. Res. 16:165-174.
Kier, L.D., Brusick, D.J., Auletta, A.E., Von Halle, E.S., Brown, M.M., Simmon, V.F., Dunkel, V., Mccann, J., Mortelmans, K., Prival, M., Rao, T.K., Ray, V. 1986. The salmonella typhimurium/mammaliam microsomal assay: a report of the U.S. Environmental Protection Agency Gene-Tox program. Mutat Res 168:69-240.
Kozuka, T., Tashiro, M. 1980. Pigmented contact dermatitis from azo-dyes. Cross sensitivity in humans. Contact Dermatitis6:330-336.
Liefer, Z., Kada, T., Mandel, M., Zeiger, E., Stafford, R., Rosenkranz, H.S. 1981. Evaluation of tests using DNA repair-deficient bacteria for predicting genotoxicity and carcinogenicity: report of the U.S. EPA’s gene-tox program.Mutat Res 87:211-297.
Mamber, S.W., Bryson, V., Katz, S.E. 1983. The Escherichia coli WP2/WP100 rec assay for detection of potential chemical carcinogens. Mutat. Res. 119:135-144.
Maruya, H. 1938. Renal changes in albino rats induced by the oral administration of various azo pigments and aromatic amino compounds. Trans. Soc. Path Jap. 28:541-547.
Mekenyan, G., Dimitrov, S.D., Pavlov, T.S., Veith, G.D. 2005. POPs: A QSAR system for creating PBT profiles of chemicals and their metabolites. SAR QSAR Environ. Res.16(1-2):103−133.
[MITI] Ministry of International Trade & Industry (Japon). 1992. Biodegradation and bioaccumulation data of existing chemicals based on the CSCL Japan, Basic Industries Bureau, Chemical Products Safety Division. Japan Chemical Industry Ecology-Toxicology & Information Centre,Tokyo (Japon).
Miyagoshi, M., Hayakawa, Y., Nagata, M., Nagayama, T. 1985. Mutagenic activities of commercial sudan III and scarlet red are due to impurities. Eisei Kagaku 31(2):79-86.
[NCI] National Chemical Inventories [base de données sur cédérom]. 2006. Columbus (OH) : American Chemical Society. [consultée le 11 décembre 2006]. Inventaire nationale des produits chimiques sur CD.
Nishida, K., Ando, Y., Ohwada, K., Mori, T., Koide, M., Koukitsu, A. 1989. Vapour pressures and heats of sublimation of some azo disperse dyes. JSDC 105:112-114.
[NTP] United States National Toxicology Program. 1982. TR 226: Cancérogenèse d'essais biologiques du C.I. Solvent Yellow 14 (N° CAS 842-07-9) dans le rat F344/N et la sourit B6C3F1 (Étude d'alimentation).
[NTP] United States National Toxicology Program. 2005. 11th Report on Carcinogens (RoC). U.S. Department of Health and Human Services, Public Health Service.
[NTP] United States National Toxicology Program. 2010. Status d'essai d'agents au programme national de toxicologie : CI Solvent yellow 14.
[OCDE] Organisation de coopération et de développement économiques. 1996. Lignes directrices de l’OCDE pour les essais de produits chimiques, n° 305B. Bioconcentration : Essai semi-statique chez le poisson. Paris : OCDE, adoptée en juin 1996.
Odabasoglu, M., Çakmak, S., Turgut, G., Içbudak, H. 2003. Preparation and characterization of chromophor group containing cyclotriphosphazenes: III bis-azo chromophor carrying some cyclotriphosphazenes. Phosphorus, Sulfur and Silicon178:549-558.
O’Neil, M.J. 2006. The Merck Index - An Encyclopedia of Chemicals, Drugs and Biologicals. Fourteenth Edition.Whitehouse Station (NJ) : Merck & Co., Inc. p. 1523-1524.
Pagga, U., Brown, D. 1986. The degradation of dyestuffs: Part II Behaviour of dyestuffs in aerobic biodegradation tests. Chemosphere. 15, 4, 479-491.
Parent, R.A., Dressler, I. 1977. Absorption and distribution of C.I. Solvent Red 24 in rats: intra-tracheal adminstration of labeled dye. Drug & Chemical Toxicology2(4):409-420.
[PhysProp] Interactive PhysProp Database [base de données sur Internet]. 2006. Syracuse (NY) : Syracuse Research Corporation.Démo de la base de données intéractives PhysProp [consulté le 16 février 2009].
Étude présentée. 2008a. Projet non publié et confidentiel présenté à la Division des substances existantes d’Environnement Canada dans le cadre du Plan de gestion des produits chimiques. Disponible en tant que Sommaire de rigueur d’étude, n° 11887Challenge006.
Étude présentée. 2008b. Projet non publié et confidentiel présenté à la Division des substances existantes d’Environnement Canada dans le cadre du Plan de gestion des produits chimiques. Disponible en tant que Sommaire de rigueur d’étude, n° 12890Challenge006.
Prikryl, J., Rusicka, Burgert, L. 1979. A new method of determining the solubility of disperse dyes. JSDC octobre: 349-351.
Platzek, T., Lang, C., Grohmann, G., Gi, U.S., Baltes, W. 1999. Formation of a carcinogenic aromatic amine from an azo dye by human skin bacteria in vitro. Hum. Exp. Toxicol. 18(9):552-559.
Prival, M.J., Mitchell, V.D. 1982. Analysis of a method for testing azo dyes for mutagenic activity in Salmonella typhimurium in the presence of flavin mononucleotide and hamster liver S9. Mutat. Res. 97(2):103-16.
ProSciTech. 2006. Fiche signalétique : Sudan III [en ligne].
Razo-Flores, E., Luijten, M., Donlon, B., Lettinga, G., Field, J. 1997. Biodegradation of selected azo dyes under methanogenic conditions. Wat. Sci. Technol. 36(6-7):65-72.
Romero, F.J., Romá , J., Bosch-Morell, F., Romero, B., Segura-Aguilar, J., Llombart-Bosch, A., Ernster, L. 2000. Reduction of brain antioxidant defense upon treatment with butylated hydroxyanisole (BHA) and Sudan III in Syrian golden hamster.Neurochem Res. 25(3):389-93.
[RIVM] Rijksinstituut voor Volksgezondheid en Milieu. 2006.Fiche cosmétiques. Pour évaluer les risques pour le consommateur.
Ryan, A.J., Welling, P.G. 1967. Some Observations on the Metabolism and Excretion of the Bisazo Dyes Sudan III and Sudan IV.Fd. Cosmet. Toxicol. 5:755-761.
Sakuratani, Y., Noguchi, Y., Kobayashi, K., Yamada, J., Nishihara, T. 2008. Molecular size as a limiting characteristic for bioconcentration in fish. J. Environ. Biol. 29(1):89-92.
Santé Canada. 1994. Loi canadienne sur la protection de l’environnement. L’évaluation du risque à la santé humaine des substances d’intérêt prioritaire. Ottawa (Ont.) : Ministre des Approvisionnements et Services Canada.
Santé Canada. 1995. Règlement sur les aliments et les drogues, partie C − Drogues.
Santé Canada 2007. Règlement sur les aliments et drogues, partie B − Aliments.
Santé Canada. 2009. Liste critique des ingrédients dont l’utilisation est restreinte ou interdite dans les cosmétiques − septembre 2009 [en ligne]. Ottawa (Ont.) : Santé Canada,Sécurité des produits de consommation [consultée le 6 janvier 2010].
Sasaki, H., Kojima, M., Nakamura, J., Shibasaki, J. 1990. Enhancing effect of pyrrolidone derivatives on the transdermal penetration of sulfaguanidine, aminopyrine and Sudan III.Journal of Pharmacobio-dynamics 13(3):200-205.
[SCCNFP] Safety Committee on Cosmetic Products and Non-Food Products Intended for Consumers. 2002. Le révision de sûreté de l'utilisation de certains colorants azoïques dans les produits cosmétiques. SCCNFP/0495/01.
Seifried, H.E., Seifried, R.M., Clarke, J.J., Junghans, T.B., San, R.H.C. 2006. A compilation of two decades of mutagenicity test results with the ames salmonella typhimurium and L5178Y mouse lymphoma cell mutation assays. Chem Res Toxicol19:627-644.
[SDC] Système de déclaration des cosmétiques [base de données exclusive]. 2009. Disponible auprès de Santé Canada, Division des cosmétiques.
Shen, G., Hu, S. 2008. Bioconcentration Test of C.I. Disperse Orange 30 in Fish. Préparé par Environmental Testing Laboratory, Shanghai Academy of Environmental Sciences, Shanghai (Chine) pour Dystar au nom de l’Ecological and Toxicological Association of the Dyes and Organic Pigments Manufacturers (ETAD), Bâle (Suisse). Rapport n° S-070-2007. Présenté à Environnement Canada en avril 2008. N° de déclaration dans le cadre du défi : 8351.
Sijm, D.T.H.M., Schuurmann, G., deVries, P.J., Opperhuizen, A. 1999. Aqueous solubility, octanol solubility, and octanol/water partition coefficient of nine hydrophobic dyes. Environ. Toxicol. Chem. 18(6):1109-1117.
[SPIN] Substances in Products in Nordic Countries [base de données sur Internet]. 2008. Projet financé par le Conseil des ministres des pays nordiques, Groupe chimique. Substances dans les produits dans les pays nordiques [consulté en décembre 2008].
Stingley, R.L., Zou, W., Heinze, T.M., Chen, H., Cerniglia, C.E. 2010. Metabolism of azo dyes by human skin microbiota. J. Med. Microbiol. 59(Pt.1):108-114.
[TOPKAT] TOxicity Prediction by Komputer Assisted Technology [en ligne]. 2004. Version 6.2. San Diego (CA) : Accelrys Software Inc. [consulté le 7 janvier 2009].
Tsuda, S., Matsusaka, N., Madarame, H., Ueno, S., Susa, N., Ishida, K., Kawamura, N., Sekihashi, K., Sasaki, Y.F. 2000. The comet assay in eight mouse organs: results with 24 azo compounds.Mutat. Res. 465:11-26.
[UE] Union européenne. 2004. . European Chemicals Bureau Risk Assessment Report. Rapport définitif : Aniline.
Umeda, M. 1957. Production of rat sarcoma by injections of Tween 80 solution of scarlet red. Gann 48:579-580.
Umeda, M. 1958. Prodution of rat sarcoma by injections of Tween 80 solution of scarlet re. Gann 49:27-31.
[USEPA] United States Environmental Protection Agency. 2008.Les ingrédients inertes autorisés pour utilisation dans des produits non alimentaires et utilisation des pesticides. [en ligne].
[USFDA] United States Food and Drug Administration. 2007. Color Additive Status List. [en ligne].
[USFDA] United States Food & Drugs Administration. 2009.Liste des statuts de couleurs additives.
Waterman, N., Lignac, G.O.E. 1958 The influence of the feeding of a number of food colours on the occurrence of tumours in mice.Acta. Physiol. Pharmacol. Neer. 7:35-55.
Willheim, R., Ivy, A.C. 1953. A preliminary study concerning the possibility of dietary carcinogenesis. Gastroenterology23:1-19.
Xie, Z., Hayakawa, R., Sugiura, M., Kojima, H., Konishi, H., Ichihara, G., Takeuschi, Y. 2000. Experimental study on skin sensitization potencies and cross-reactivities of hair-dye=related chemicals in guinea pigs. Contact Dermatitis42:270-275.
Xu, H., Heinze, T.M., Chen, S., Cerniglia, C.E., Chen, H. 2007. Anaerobic metabolism of 1-amino-2-napthol-based azo dyes (Sudan dyes) by human intestinal microflora. Appl. Environ. Microbiol. 73(23):7759-7762.
Yen, C.C., Perenich, T.A., Baughman, G.L. 1989. Fate of dyes in aquatic systems II. Solubility and octanol/water partition coefficients of disperse dyes. Environ. Toxicol. Chem.8(11):981-986.
Yen, C.C., Perenich, T.A., Baughman, G.L. 1991. Fate of commercial disperse dyes in sediments. Environ. Toxicol. Chem. 10:1009-1017.
Yourick, J.J., Sasik, C.T., Bronaugh, R.L. 2007. In vitro dermal absorption and metabolism of D&C red no. 17 in human and porcine skin. J. Cosmet. Sci. 58:255-266.
Zhou, Y., You, X., Ye, X. 1987. Mutgenicity of benzidines and their congener derivative dyes. Huanjing Kexue8(2):31-34.
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 1 | Référence : Bio-elimination study for CAS# 6250-23-3 (Disperse Yellow 23) Clariant dyestuff product = Foron Yellow E RGFL (Étude présentée, 2008b) | |||
| 2 | Identité de la substance : n° CAS | s.o.[1] | Oui | 6250-23-3 |
| 3 | Identité de la substance : nom(s) chimique(s) | s.o. | Oui | Disperse Yellow 23 |
| 4 | Composition chimique de la substance | 2 | Non | |
| 5 | Pureté chimique | 1 | Oui | 54 % Disperse Yellow 23 |
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 6 | Référence | 1 | Non | |
| 7 | Méthode normalisée (OCDE, UE, nationale, ou autre)? | 3 | Non | |
| 8 | Justification de la méthode ou du protocole si une méthode non normalisée a été utilisée | 2 | Non | |
| 9 | BPL (bonne pratique de laboratoire) | 3 | s.o. (étude réalisée en 1976) |
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 10 | Type d’essai (c.-à-d. hydrolyse, biodégradation) | s.o. | Oui | Biodégradation |
| 11 | Conditions d’essai (aérobie ou anaérobie) | s.o. | Non | Non indiqué |
| 12 | Milieu d’essai (eau, sédiments ou sol) | s.o. | Oui | Eau (par déduction d’après la concentration d’essai exprimée en mg/L) |
| 13 | Durée de l’essai | s.o. | Oui | 14 jours |
| 14 | Témoins négatifs ou positifs? | 1 | Non | |
| 15 | Nombre de répétitions (y compris les témoins) | 1 | Non | |
| 16 | Des concentrations mesurées sont-elles indiquées? | 3 | Non | |
| 17 | Méthode ou instrument analytique | 1 | Non |
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 18 | Type de biodégradation (immédiate ou intrinsèque) indiqué? | 2 | Non | Non indiqué |
| 19 | Lorsque le type de biodégradation (immédiate ou intrinsèque) n’est pas signalé, une information indirecte permet-elle l’identification du type de biodégradation? | 1 | Non | |
| 20 | Source de l’inoculum | 1 | Non | |
| 21 | Concentration dans l’inoculum ou nombre de microorganismes | 1 | Non | |
| 22 | Un préconditionnement et une préadaptation de l’inoculum ont-ils été signalés? | 1 | Non | |
| 23 | Le préconditionnement et la préadaptation de l’inoculum étaient-ils appropriés dans le cadre de la méthode utilisée? | s.o. | Non | |
| 24 | Température | 1 | Non | Non indiqué |
| 25 | Le pourcentage de dégradation du composé de référence a-t-il atteint les niveaux requis avant le 14ejour? | s.o. | Non | Pas de composé de référence testé |
| 26 | Sol : humidité du sol signalée? | 1 | ||
| 27 | Sol et sédiments : indication de la teneur de fond en MOS (matière organique du sol)? | 1 | ||
| 28 | Sol et sédiments : teneur en argile signalée? | 1 | ||
| 29 | Sol et sédiments : CEC (capacité d’échange cationique) signalée? | 1 |
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 30 | Valeurs du pH signalées? | 1 | ||
| 31 | Température | 1 | ||
| 32 | Les concentrations appropriées de la substance ont-elles été utilisées? | |||
| 33 | Si un solvant a été utilisé, l’a-t-il été de manière appropriée? |
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 34 | Température | 1 | ||
| 35 | Source lumineuse | 1 | ||
| 36 | Spectre lumineux (nm) | 1 | ||
| 37 | Intensité relative en fonction de l’intensité lumineuse du soleil | 1 | ||
| 38 | Spectre d’une substance | 1 | ||
| 39 | Photolyse indirecte : Sensibilisateur (type) | 1 | ||
| 40 | Photolyse indirecte : concentration du sensibilisateur | 1 |
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 41 | Paramètre et valeur | s.o. | s.o. | Biodégradation moyenne en 14 jours = 51 % |
| 42 | Produits de dégradation | s.o. | Non | |
| 43 | Note : ... % | 4,5 | ||
| 44 | Code de fiabilité d’Environnement Canada : | 4 | ||
| 45 | Catégorie de fiabilité (élevée, satisfaisante, basse) : | Non satisfaisante | ||
| 46 | Remarques | |||
| N° | Élément | Pondération | Oui/non | Précisions | |
|---|---|---|---|---|---|
| 1 | Référence : SHEN, G., HU, S. 2008. Bioconcentration Test of C.I. Disperse Orange 30 in Fish. Préparé par Environmental Testing Laboratory, Shanghai Academy of Environmental Sciences, Shanghai (Chine) pour Dystar au nom de l’Ecological and Toxicological Association of the Dyes and Organic Pigments Manufacturers (ETAD), Bâle (Suisse). Rapport n° S-070-2007. Présenté à Environnement Canada en avril 2008. N° de déclaration dans le cadre du défi 8351. |
||||
| 2 | Identité de la substance : n° CAS | s.o.[1] | Oui | 5261-31-4 | |
| 3 | Identité de la substance : nom(s) chimique(s) | s.o. | Oui | Acétate de 2-[N-(2-cyanoéthyl)-4-[2,6-dichloro-4-nitrophényl)azo]anilino]éthyle | |
| 4 | Composition chimique de la substance | 2 | Non | ||
| 5 | Pureté chimique | 1 | Non | ||
| 6 | Indication de la persistance/stabilité de la substance en milieu aqueux? | 1 | Non | ||
| 7 | Si le matériel d’essai est radiomarqué, est-ce que la ou les positions précises du ou des atomes marqués ainsi que le pourcentage de radioactivité associé aux impuretés ont été rapportés? | 2 | Non | ||
| N° | Élément | Pondération | Oui/non | Précisions | |
|---|---|---|---|---|---|
| 8 | Référence | 1 | Oui | Lignes directrices de l’OCDE pour les essais de produits chimiques n° 305B-1996 | |
| 9 | Méthode normalisée (OCDE, UE, nationale, ou autre)? | 3 | Oui | OCDE | |
| 10 | Justification de la méthode ou du protocole si une méthode non normalisée a été utilisée | 2 | Sans objet | ||
| 11 | BPL (bonne pratique de laboratoire) | 3 | Non | ||
| N° | Élément | Pondération | Oui/non | Précisions | |
|---|---|---|---|---|---|
| 12 | Identité de l’organisme : nom | s.o. | Oui | Poisson zèbre, Brachydanio rerio | |
| 13 | Indication du nom latin ou des deux noms (latin et commun)? | 1 | Oui | Les deux | |
| 14 | Âge ou stade biologique de l’organisme d’essai | 1 | Non | ||
| 15 | Longueur et/ou poids | 1 | Oui | Longueur moyenne du corps 3,91 +/- 0,18 cm et poids moyen du corps 0,32 +/- 0,06 g | |
| 16 | Sexe | 1 | Non | ||
| 17 | Nombre d’organismes par répétition | 1 | Oui | 7 | |
| 18 | Charge en organismes | 1 | Oui | 20 mg/L | |
| 19 | Type de nourriture et périodes d’alimentation pendant la période d’acclimatation | 1 | Oui | Mise au régime avec un poisson du commerce jusqu’à un jour avant le début du test | |
| N° | Élément | Pondération | Oui/non | Précisions | |
|---|---|---|---|---|---|
| 20 | Type d’expérience (en laboratoire ou sur le terrain) | s.o. | Oui | Laboratoire | |
| 21 | Voies d’exposition (nourriture, eau, les deux) | s.o. | Oui | Eau | |
| 22 | Durée de l’exposition | s.o. | Oui | 28 jours | |
| 23 | Nombre de répétitions (y compris les témoins) | 1 | Oui | ||
| 24 | Concentrations | 1 | Oui | 20 mg/L | |
| 25 | Type/composition de la nourriture et périodes d’alimentation (pendant l’essai) | 1 | Oui | Les poissons étaient nourris deux heures avant le renouvellement de l’eau | |
| 26 | Si le ratio FBC/FBA dérivait de la concentration chimique dans l’organisme et dans l’eau, la durée de l’expérience était-elle égale à ou supérieure au temps nécessaire pour que les concentrations chimiques atteignent un état stable? | 3 | Oui | 28 jours | |
| 27 | Si le rapport FBC/FBA a été déterminé comme correspondant au rapport de la concentration du produit chimique dans l’organisme sur sa concentration dans l’eau, est-ce que les concentrations mesurées dans l’organisme et dans l’eau étaient mentionnées? | 3 | Oui | ||
| 28 | Les concentrations dans les eaux d’essai ont-elles été mesurées périodiquement? | 1 | Oui | Sur trois jours distincts | |
| 29 | Les conditions du milieu d’exposition correspondaient-elles au produit chimique particulier signalé? (par exemple, pour la toxicité du métal : pH, DOC/TOC, dureté de l’eau, température) | 3 | Oui | Oui, tous les deux jours | |
| 30 | Photopériode et intensité de l’éclairage | 1 | Oui | 12:12 | |
| 31 | Préparation de solutions mères et de solutions d’essai | 1 | Oui | ||
| 32 | Intervalles des contrôles analytiques | 1 | Oui | Tous les deux jours pour l’oxygène dissous, le pH et la température | |
| 33 | Méthodes statistiques utilisées | 1 | Oui | ||
| 34 | Le solubilisant/émulsifiant a-t-il été utilisé si le produit chimique était faiblement soluble ou instable? | s.o. | Non | ||
| N° | Élément | Pondération | Oui/non | Précisions | |
|---|---|---|---|---|---|
| 35 | L’organisme d’essai correspondait-il à l’environnement au Canada? | 3 | Oui | ||
| 36 | Les conditions d’essai (pH, température, OD, etc.) sont-elles typiques pour l’organisme d’essai? | 1 | Oui | ||
| 37 | Le type et la conception du système (statique, semi-statique, dynamique; ouvert ou fermé; etc.) correspondent-ils aux propriétés de la substance et à la nature ou aux habitudes de l’organisme? | 2 | Oui | Semi-statique | |
| 38 | Le pH de l’eau se situait-il dans la plage des valeurs typiques de l’environnement au Canada (6 à 9)? | 1 | Oui | 7,22 à 7,84 | |
| 39 | La température de l’eau du test se situait-elle dans la plage des valeurs typiques de l’environnement au Canada (5 à 27 °C)? | 1 | Oui | 22 à 23 | |
| 40 | Le contenu lipidique (ou FBA/FBC lipidiquement normalisé) a-t-il été signalé? | 2 | Oui | ||
| 41 | Les concentrations mesurées d’un produit chimique dans l’eau d’essai étaient-elles inférieures à la solubilité dans l’eau du produit chimique? | 3 | Non | ||
| 42 | Si une substance radiomarquée a été utilisée, est-ce que le FBC a été déterminé d’après le composé d’origine (et non d’après les résidus radiomarqués)? | 3 | Non | ||
| N° | Élément | Pondération | Oui/non | Précisions | |
|---|---|---|---|---|---|
| 43 | Les paramètres déterminés (FBA, FBC) et leurs valeurs | s.o. | s.o. | FBC | |
| 44 | FBA ou FBC déterminés comme : 1) le rapport de la concentration en produit chimique produit dans l’organisme, ou 2) le rapport entre les constantes d’incorporation de produit chimique et du taux d’élimination | s.o. | s.o. | 1 | |
| 45 | Le FBA/FBC était-il issu 1) d’un échantillon de tissu ou 2) d’un organisme entier? | s.o. | s.o. | 2 | |
| 46 | Le FBA/FBC 1) moyen ou 2) maximal at-il été utilisé? | s.o. | s.o. | 1 | |
| 47 | Note : % | 67,9 | |||
| 48 | Code de fiabilité d’Environnement Canada : | 2 | |||
| 49 | Catégorie de fiabilité (élevée, satisfaisante, basse) : | Confiance satisfaisante | |||
| 50 | Remarques | La présente procédure est basée sur des conditions semi-statiques (renouvellement des solutions du test tous les deux jours). Par conséquent, les substances d’essai très peu solubles dans l’eau, comme les colorants diazoïques, peuvent aussi être caractérisées selon leur potentiel de bioconcentration sans l’ajout de solvants ou d’autres substances auxiliaires qui pourraient modifier les résultats. | |||
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 1 | Référence : Fish toxicity study for CAS# 6250-23-3 (Disperse Yellow 23) Clariant dyestuff product=Foron Yellow E RGFL (Étude présentée, 2008b) | |||
| 2 | Identité de la substance : n° CAS | s.o.[1] | Oui | 6250-23-3 |
| 3 | Identité de la substance : nom(s) chimique(s) | s.o. | Oui | Disperse Yellow 23 |
| 4 | Composition chimique de la substance | 2 | Non | |
| 5 | Pureté chimique | 1 | Oui | 54 % DY23 |
| 6 | Indication de la persistance/stabilité de la substance en milieu aqueux? | 1 | Non | |
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 7 | Référence | 1 | Non | |
| 8 | Méthode normalisée (OCDE, UE, nationale, ou autre)? | 3 | Non | |
| 9 | Justification de la méthode ou du protocole si une méthode non normalisée a été utilisée | 2 | Non | |
| 10 | BPL (bonne pratique de laboratoire) | 3 | s.o. (étude réalisée en 1974) |
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 11 | Identité de l’organisme : nom | s.o. | Oui | Truite arc-en-ciel |
| 12 | Indication du nom latin ou des deux noms (latin et commun)? | 1 | Non | |
| 13 | Âge ou stade biologique de l’organisme d’essai | 1 | Oui | |
| 14 | Longueur et/ou poids | 1 | Oui | Longueur : 11 cm; poids : 15 g |
| 15 | Sexe | 1 | Non | |
| 16 | Nombre d’organismes par répétition | 1 | Non | |
| 17 | Charge en organismes | 1 | Non | |
| 18 | Type de nourriture et périodes d’alimentation pendant la période d’acclimatation | 1 | Non |
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 19 | Type d’essai (toxicité aiguë ou chronique) | s.o. | Oui | Aiguë |
| 20 | Type d’expérience (en laboratoire ou sur le terrain) | s.o. | Oui | En laboratoire |
| 21 | Voies d’exposition (nourriture, eau, les deux) | s.o. | Oui | Eau |
| 22 | Durée de l’exposition | s.o. | Oui | 48 heures |
| 23 | Témoins négatifs ou positifs (préciser) | 1 | Non | |
| 24 | Nombre de répétitions (y compris les témoins) | 1 | Non | |
| 25 | Des concentrations nominales sont-elles indiquées? | 1 | Non | |
| 26 | Des concentrations mesurées sont-elles indiquées? | 3 | Non | |
| 27 | Type de nourriture et périodes d’alimentation durant les essais à long terme | 1 | Sans objet | |
| 28 | Les concentrations ont-elles été mesurées périodiquement (spécialement dans les essais de toxicité chronique)? | 1 | Non | |
| 29 | Les conditions du milieu d’exposition correspondaient-elles au produit chimique particulier signalé? (par exemple, pour la toxicité du métal : pH, DOC/TOC, dureté de l’eau, température) | 3 | Non | |
| 30 | Photopériode et intensité de l’éclairage | 1 | Non | |
| 31 | Préparation de solutions mères et de solutions d’essai | 1 | Non | |
| 32 | Un agent émulsionnant ou stabilisant a-t-il été employé si la substance était peu soluble ou instable? | 1 | Non | |
| 33 | Si un agent émulsionnant ou stabilisant a été employé, sa concentration est-elle indiquée? | 1 | ||
| 34 | Si un solubilisant/émulsifiant a été utilisé, son écotoxicité a-t-elle été signalée? | 1 | ||
| 35 | Intervalles des contrôles analytiques | 1 | Non | |
| 36 | Méthodes statistiques utilisées | 1 | Non |
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 37 | Le paramètre déterminé est-il directement attribuable à la toxicité de la substance, non à l’état de santé des organismes (p. ex., lorsque la mortalité des témoins est supérieure à 10 %) ou à des facteurs physiques (p. ex., « effet d’ombrage »)? | s.o. | Oui | |
| 38 | L’organisme d’essai correspondait-il à l’environnement au Canada? | 3 | Oui | |
| 39 | Les conditions d’essai (pH, température, OD, etc.) sont-elles typiques pour l’organisme d’essai? | 1 | Non | Seule la température est indiquée (typique pour l’organisme d’essai). |
| 40 | Le type et la conception du système (statique, semi-statique, dynamique; ouvert ou fermé; etc.) correspondent-ils aux propriétés de la substance et à la nature ou aux habitudes de l’organisme? | 2 | Impossible à évaluer | |
| 41 | Le pH de l’eau du test se situait-il dans la plage des valeurs typiques de l’environnement au Canada (6 à 9)? | 1 | pH non précisé | |
| 42 | La température de l’eau du test se situait-elle dans la plage des valeurs typiques de l’environnement au Canada (5 à 27 °C)? | 1 | Oui | 20 °C |
| 43 | La valeur de la toxicité était-elle inférieure à celle de la solubilité de la substance dans l’eau? | 3 | Non | La CL50 indiquée est supérieure de 8 ordres de grandeur à la solubilité dans l’eau mesurée par Baughman et Perenich (1989). |
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 44 | Valeurs de la toxicité (fournir paramètres et valeurs) | s.o. | s.o. | CL50 après 48 heures > 1 000 mg/L |
| 45 | Autres paramètres indiqués – p. ex., FBC/FBA, CMEO/CSEO (préciser)? | s.o. | Non | |
| 46 | Autres effets indésirables (par exemple, cancérogénicité, mutagénicité) signalés? | s.o. | Non | |
| 47 | Note : % | 17,5 | ||
| 48 | Code de fiabilité d’Environnement Canada : | 4 | ||
| 49 | Catégorie de fiabilité (élevée, satisfaisante, basse) : | Non satisfaisante | ||
| 50 | Remarques | |||
| N° | Élément | Pondération | Oui/non | Précisions | ||
|---|---|---|---|---|---|---|
| 1 | Référence: ETAD, Ecological and Toxicological Association of Dyes and Organic Pigments Manufacturers. 2005. Projet E 3020 : renseignements reçus à l’appui de la catégorisation de 12 colorants dispersés dans la LIS. (Courriel daté du 27 octobre 2005) | |||||
| 2 | Identité de la substance : n° CAS | s.o.[1] | Oui | 19800-42-1 | ||
| 3 | Identité de la substance : nom(s) chimique(s) | s.o. | Oui | Disperse Orange 29 | ||
| 4 | Composition chimique de la substance | 2 | Oui | Colorant : 20 %; Reax 85A : 10 %; Eau : 70 %. | ||
| 5 | Pureté chimique | 1 | Oui | Dispersion à 20 % du colorant | ||
| 6 | Indication de la persistance/stabilité de la substance en milieu aqueux? | 1 | Non | |||
| N° | Élément | Pondération | Oui/non | Précisions | ||
|---|---|---|---|---|---|---|
| 7 | Référence | 1 | Non | |||
| 8 | Méthode normalisée (OCDE, UE, nationale, ou autre)? | 3 | Oui | OCDE 203 | ||
| 9 | Justification de la méthode ou du protocole si une méthode non normalisée a été utilisée | 2 | Sans objet | |||
| 10 | BPL (bonne pratique de laboratoire) | 3 | s.o. (étude réalisée en 1990) | |||
| N° | Élément | Pondération | Oui/non | Précisions | ||
|---|---|---|---|---|---|---|
| 11 | Identité de l’organisme : nom | s.o. | Oui | Poisson-zèbre (Brachydanio rerio) | ||
| 12 | Indication du nom latin ou des deux noms (latin et commun)? | 1 | Oui | |||
| 13 | Âge ou stade biologique de l’organisme d’essai | 1 | Non | |||
| 14 | Longueur et/ou poids | 1 | Non | |||
| 15 | Sexe | 1 | Sans objet | |||
| 16 | Nombre d’organismes par répétition | 1 | Non | |||
| 17 | Charge en organismes | 1 | Non | |||
| 18 | Type de nourriture et périodes d’alimentation pendant la période d’acclimatation | 1 | Non | |||
| N° | Élément | Pondération | Oui/non | Précisions | ||
|---|---|---|---|---|---|---|
| 19 | Type d’essai (toxicité aiguë ou chronique) | s.o. | Oui | Aiguë | ||
| 20 | Type d’expérience (en laboratoire ou sur le terrain) | s.o. | Oui | En laboratoire | ||
| 21 | Voies d’exposition (nourriture, eau, les deux) | s.o. | Oui | Eau | ||
| 22 | Durée de l’exposition | s.o. | Oui | 48 heures | ||
| 23 | Témoins négatifs ou positifs (préciser) | 1 | Non | |||
| 24 | Nombre de répétitions (y compris les témoins) | 1 | Non | |||
| 25 | Des concentrations nominales sont-elles indiquées? | 1 | Non | |||
| 26 | Des concentrations mesurées sont-elles indiquées? | 3 | Non | |||
| 27 | Type de nourriture et périodes d’alimentation durant les essais à long terme | 1 | Sans objet | |||
| 28 | Les concentrations ont-elles été mesurées périodiquement (spécialement dans les essais de toxicité chronique)? | 1 | Non | |||
| 29 | Les conditions du milieu d’exposition correspondaient-elles au produit chimique particulier signalé? (par exemple, pour la toxicité du métal : pH, DOC/TOC, dureté de l’eau, température) | 3 | Non | |||
| 30 | Photopériode et intensité de l’éclairage | 1 | Non | |||
| 31 | Préparation de solutions mères et de solutions d’essai | 1 | Non | |||
| 32 | Un agent émulsionnant ou stabilisant a-t-il été employé si la substance était peu soluble ou instable? | 1 | Non | |||
| 33 | Si un agent émulsionnant ou stabilisant a été employé, sa concentration est-elle indiquée? | 1 | ||||
| 34 | Si un solubilisant/émulsifiant a été utilisé, son écotoxicité a-t-elle été signalée? | 1 | ||||
| 35 | Intervalles des contrôles analytiques | 1 | Non | |||
| 36 | Méthodes statistiques utilisées | 1 | Non | |||
| N° | Élément | Pondération | Oui/non | Précisions | ||
|---|---|---|---|---|---|---|
| 37 | Le critère d’évaluation a-t-il été directement causé par la toxicité du produit chimique et non par l’état de santé de l’organisme (par exemple, lorsque la mortalité lors du contrôle est supérieure à 10 %) ou des effets physiques (par exemple, « effet d’ombrage »)? | s.o. | Oui | |||
| 38 | L’organisme d’essai correspondait-il à l’environnement au Canada? | 3 | Non | |||
| 39 | Les conditions d’essai (pH, température, OD, etc.) sont-elles typiques pour l’organisme d’essai? | 1 | Non indiqué | |||
| 40 | Le type et la conception du système (statique, semi-statique, dynamique; ouvert ou fermé; etc.) correspondent-ils aux propriétés de la substance et à la nature ou aux habitudes de l’organisme? | 2 | Impossible à évaluer | |||
| 41 | Le pH de l’eau du test se situait-il dans la plage des valeurs typiques de l’environnement au Canada (6 à 9)? | 1 | pH non précisé | |||
| 42 | La température de l’eau du test se situait-elle dans la plage des valeurs typiques de l’environnement au Canada (5 à 27 °C)? | 1 | non précisé | |||
| 43 | La valeur de la toxicité était-elle inférieure à celle de la solubilité de la substance dans l’eau? | 3 | Oui | La CL50 et la solubilité dans l’eau déclarées sont à un ordre de grandeur l’une de l’autre. | ||
| N° | Élément | Pondération | Oui/non | Précisions | ||
|---|---|---|---|---|---|---|
| 44 | Valeurs de la toxicité (fournir paramètres et valeurs) | s.o. | s.o. | CL50 après 96 heures > 480 mg/L | ||
| 45 | Autres paramètres indiqués – p. ex., FBC/FBA, CMEO/CSEO (préciser)? | s.o. | Non | |||
| 46 | Autres effets indésirables (par exemple, cancérogénicité, mutagénicité) signalés? | s.o. | Non | |||
| 47 | Note : % | 28,6 | ||||
| 48 | Code de fiabilité d’Environnement Canada : | 4 | ||||
| 49 | Catégorie de fiabilité (élevée, satisfaisante, basse) : | Non satisfaisante | ||||
| 50 | Remarques | |||||
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 1 | Référence : [ETAD] Ecological and Toxicological Association of Dyes and Organic Pigments Manufacturers. 2005. Projet E 3020 : renseignements reçus à l’appui de la catégorisation de 12 colorants dispersés dans la LIS. (Courriel daté du 27 octobre 2005) (Étude présentée, 2008a) | |||
| 2 | Identité de la substance : n° CAS | s.o.[1] | Oui | 19800-42-1 |
| 3 | Identité de la substance : nom(s) chimique(s) | s.o. | Oui | Disperse Orange 29 |
| 4 | Composition chimique de la substance | 2 | Oui | Colorant : 20 %; Reax 85A : 10 %; Eau : 70 % |
| 5 | Pureté chimique | 1 | Oui | Dispersion à 20 % du colorant |
| 6 | Indication de la persistance/stabilité de la substance en milieu aqueux? | 1 | Non | |
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 7 | Référence | 1 | Non | |
| 8 | Méthode normalisée (OCDE, UE, nationale, ou autre)? | 3 | Oui | OCDE 201 |
| 9 | Justification de la méthode ou du protocole si une méthode non normalisée a été utilisée | 2 | Sans objet | |
| 10 | BPL (bonne pratique de laboratoire) | 3 | s.o. (étude réalisée en 1990) |
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 11 | Identité de l’organisme : nom | s.o. | Oui | Scenedesmus subspicatus |
| 12 | Indication du nom latin ou des deux noms (latin et commun)? | 1 | Oui | |
| 13 | Âge ou stade biologique de l’organisme d’essai | 1 | Non | |
| 14 | Longueur et/ou poids | 1 | Sans objet | |
| 15 | Sexe | 1 | Sans objet | |
| 16 | Nombre d’organismes par répétition | 1 | Non | |
| 17 | Charge en organismes | 1 | Non | |
| 18 | Type de nourriture et périodes d’alimentation pendant la période d’acclimatation | 1 | Non |
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 19 | Type d’essai (toxicité aiguë ou chronique) | s.o. | Oui | Aiguë |
| 20 | Type d’expérience (en laboratoire ou sur le terrain) | s.o. | Oui | En laboratoire |
| 21 | Voies d’exposition (nourriture, eau, les deux) | s.o. | Oui | Eau |
| 22 | Durée de l’exposition | s.o. | Oui | 72 heures |
| 23 | Témoins négatifs ou positifs (préciser) | 1 | Non | |
| 24 | Nombre de répétitions (y compris les témoins) | 1 | Non | |
| 25 | Des concentrations nominales sont-elles indiquées? | 1 | Non | |
| 26 | Des concentrations mesurées sont-elles indiquées? | 3 | Non | |
| 27 | Type de nourriture et périodes d’alimentation durant les essais à long terme | 1 | Sans objet | |
| 28 | Les concentrations ont-elles été mesurées périodiquement (spécialement dans les essais de toxicité chronique)? | 1 | Non | |
| 29 | Les conditions du milieu d’exposition correspondaient-elles au produit chimique particulier signalé? (par exemple, pour la toxicité du métal : pH, DOC/TOC, dureté de l’eau, température) | 3 | Non | |
| 30 | Photopériode et intensité de l’éclairage | 1 | Non | |
| 31 | Préparation de solutions mères et de solutions d’essai | 1 | Non | |
| 32 | Un agent émulsionnant ou stabilisant a-t-il été employé si la substance était peu soluble ou instable? | 1 | Non | |
| 33 | Si un agent émulsionnant ou stabilisant a été employé, sa concentration est-elle indiquée? | 1 | ||
| 34 | Si un solubilisant/émulsifiant a été utilisé, son écotoxicité a-t-elle été signalée? | 1 | ||
| 35 | Intervalles des contrôles analytiques | 1 | Non | |
| 36 | Méthodes statistiques utilisées | 1 | Non |
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 37 | Le critère d’évaluation a-t-il été directement causé par la toxicité du produit chimique et non par l’état de santé de l’organisme (par exemple, lorsque la mortalité lors du contrôle est supérieure à 10 %) ou des effets physiques (par exemple, « effet d’ombrage »)? | s.o. | Oui | |
| 38 | L’organisme d’essai correspondait-il à l’environnement canadien? | 3 | Oui | |
| 39 | Les conditions d’essai (pH, température, OD, etc.) sont-elles typiques pour l’organisme d’essai? | 1 | Non indiqué | |
| 40 | Le type et la conception du système (statique, semi-statique, dynamique; ouvert ou fermé; etc.) correspondent-ils aux propriétés de la substance et à la nature ou aux habitudes de l’organisme? | 2 | Impossible à évaluer | |
| 41 | Le pH de l’eau du test se situait-il dans la plage des valeurs typiques de l’environnement au Canada (6 à 9)? | 1 | pH non précisé | |
| 42 | La température de l’eau du test se situait-elle dans la plage des valeurs typiques de l’environnement au Canada (5 à 27 °C)? | 1 | non précisé | |
| 43 | La valeur de la toxicité était-elle inférieure à celle de la solubilité de la substance dans l’eau? | 3 | Oui | La différence entre la CE50 indiquée et la solubilité dans l’eau ne dépasse pas 1 ordre de grandeur. |
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 44 | Valeurs de la toxicité (fournir paramètres et valeurs) | s.o. | s.o. | CE50 après 72 h pour la biomasse = 6 mg/L |
| 45 | Autres paramètres indiqués – p. ex., FBC/FBA, CMEO/CSEO (préciser)? | s.o. | Oui | CE50 pour la croissance = 86 mg/L; CE10 pour la biomasse et la croissance = 1,7 et 5,4 mg/L |
| 46 | Autres effets indésirables (par exemple, cancérogénicité, mutagénicité) signalés? | s.o. | Non | |
| 47 | Note : | 38,2 | ||
| 48 | Code de fiabilité d’Environnement Canada : | 4 | ||
| 49 | Catégorie de fiabilité (élevée, satisfaisante, basse) : | Non satisfaisante | ||
| 50 | Remarques | |||
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 1 | Référence : [ETAD] Ecological and Toxicological Association of Dyes and Organic Pigments Manufacturers. 2005. Projet E 3020 : renseignements reçus à l’appui de la catégorisation de 12 colorants dispersés dans la LIS. Courriel daté du 27 octobre 2005) (Étude présentée, 2008a) | |||
| 2 | Identité de la substance : n° CAS | s.o.[1] | Oui | 19800-42-1 |
| 3 | Identité de la substance : nom(s) chimique(s) | s.o. | Oui | Disperse Orange 29 |
| 4 | Composition chimique de la substance | 2 | Oui | Colorant : 20 %; Reax 85A : 10 %; Eau : 70 %. |
| 5 | Pureté chimique | 1 | Oui | Dispersion à 20 % du colorant |
| 6 | Indication de la persistance/stabilité de la substance en milieu aqueux? | 1 | Non | |
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 7 | Référence | 1 | Non | |
| 8 | Méthode normalisée (OCDE, UE, nationale, ou autre)? | 3 | Oui | OCDE 202 |
| 9 | Justification de la méthode ou du protocole si une méthode non normalisée a été utilisée | 2 | Sans objet | |
| 10 | BPL (bonne pratique de laboratoire) | 3 | s.o. (étude réalisée en 1990) |
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 11 | Identité de l’organisme : nom | s.o. | Oui | Daphnia magna |
| 12 | Indication du nom latin ou des deux noms (latin et commun)? | 1 | Oui | |
| 13 | Âge ou stade biologique de l’organisme d’essai | 1 | Non | |
| 14 | Longueur et/ou poids | 1 | Sans objet | |
| 15 | Sexe | 1 | Sans objet | |
| 16 | Nombre d’organismes par répétition | 1 | Non | |
| 17 | Charge en organismes | 1 | Non | |
| 18 | Type de nourriture et périodes d’alimentation pendant la période d’acclimatation | 1 | Non |
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 19 | Type d’essai (toxicité aiguë ou chronique) | s.o. | Oui | Aiguë |
| 20 | Type d’expérience (en laboratoire ou sur le terrain) | s.o. | Oui | En laboratoire |
| 21 | Voies d’exposition (nourriture, eau, les deux) | s.o. | Oui | Eau |
| 22 | Durée de l’exposition | s.o. | Oui | 24 et 48 heures |
| 23 | Témoins négatifs ou positifs (préciser) | 1 | Non | |
| 24 | Nombre de répétitions (y compris les témoins) | 1 | Non | |
| 25 | Des concentrations nominales sont-elles indiquées? | 1 | Non | |
| 26 | Des concentrations mesurées sont-elles indiquées? | 3 | Non | |
| 27 | Type de nourriture et périodes d’alimentation durant les essais à long terme | 1 | Sans objet | |
| 28 | Les concentrations ont-elles été mesurées périodiquement (spécialement dans les essais de toxicité chronique)? | 1 | Non | |
| 29 | Les conditions du milieu d’exposition correspondaient-elles au produit chimique particulier signalé? (par exemple, pour la toxicité du métal : pH, DOC/TOC, dureté de l’eau, température) | 3 | Non | |
| 30 | Photopériode et intensité de l’éclairage | 1 | Non | |
| 31 | Préparation de solutions mères et de solutions d’essai | 1 | Non | |
| 32 | Un agent émulsionnant ou stabilisant a-t-il été employé si la substance était peu soluble ou instable? | 1 | Non | |
| 33 | Si un agent émulsionnant ou stabilisant a été employé, sa concentration est-elle indiquée? | 1 | ||
| 34 | Si un solubilisant/émulsifiant a été utilisé, son écotoxicité a-t-elle été signalée? | 1 | ||
| 35 | Intervalles des contrôles analytiques | 1 | Non | |
| 36 | Méthodes statistiques utilisées | 1 | Non |
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 37 | Le paramètre déterminé est-il directement attribuable à la toxicité de la substance, non à l’état de santé des organismes (p. ex., lorsque la mortalité des témoins est supérieure à 10 %) ou à des facteurs physiques (p. ex., « effet d’ombrage »)? | s.o. | Oui | |
| 38 | L’organisme d’essai correspondait-il à l’environnement au Canada? | 3 | Oui | |
| 39 | Les conditions d’essai (pH, température, OD, etc.) sont-elles typiques pour l’organisme d’essai? | 1 | Non indiqué | |
| 40 | Le type et la conception du système (statique, semi-statique, dynamique; ouvert ou fermé; etc.) correspondent-ils aux propriétés de la substance et à la nature ou aux habitudes de l’organisme? | 2 | Impossible à évaluer | |
| 41 | Le pH de l’eau du test se situait-il dans la plage habituelle pour l’environnement canadien (6 à 9)? | 1 | pH non précisé | |
| 42 | La température de l’eau du test se situait-elle dans la plage habituelle pour l’environnement canadien (5 à 27 °C)? | 1 | non précisé | |
| 43 | La valeur de la toxicité était-elle inférieure à celle de la solubilité de la substance dans l’eau? | 3 | Non | La CL50 indiquée est supérieure à la valeur fournie de la solubilité dans l’eau. |
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 44 | Valeurs de la toxicité (fournir paramètres et valeurs) | s.o. | s.o. | CE50 après 48 heures = 70 mg/L |
| 45 | Autres paramètres indiqués – p. ex., FBC/FBA, CMEO/CSEO (préciser)? | s.o. | Oui | CE50 après 24 heures > 100 mg/L |
| 46 | Autres effets indésirables (par exemple, cancérogénicité, mutagénicité) signalés? | s.o. | Non | |
| 47 | Note : % | 29,4 | ||
| 48 | Code de fiabilité d’Environnement Canada : | 4 | ||
| 49 | Catégorie de fiabilité (élevée, satisfaisante, basse) : | Non satisfaisante | ||
| 50 | Remarques | |||
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 1 | Référence : BASF. 1990. 1990. Bericht uber die Prufung der akuten Toxizitit an der Goldorfe (Leuciscus idus L., Goldvariante). Présenté à Environnement Canada par l’ETAD en août 2008. | |||
| 2 | Identité de la substance : n° CAS | s.o.[1] | ||
| 3 | Identité de la substance : nom(s) chimique(s) | s.o. | ||
| 4 | Composition chimique de la substance | 2 | Non | |
| 5 | Pureté chimique | 1 | Non | |
| 6 | Indication de la persistance/stabilité de la substance en milieu aqueux? | 1 | Non | |
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 7 | Référence | 1 | Non | |
| 8 | Méthode normalisée (OCDE, UE, nationale, ou autre)? | 3 | Non | |
| 9 | Justification de la méthode ou du protocole si une méthode non normalisée a été utilisée | 2 | Non | |
| 10 | BPL (bonne pratique de laboratoire) | 3 | ||
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 11 | Identité de l’organisme : nom | s.o. | Oui | Ide dorée |
| 12 | Indication du nom latin ou des deux noms (latin et commun)? | 1 | Oui | |
| 13 | Âge ou stade biologique de l’organisme d’essai | 1 | Non | |
| 14 | Longueur et/ou poids | 1 | Non | |
| 15 | Sexe | 1 | Non | |
| 16 | Nombre d’organismes par répétition | 1 | Non | |
| 17 | Charge en organismes | 1 | Non | |
| 18 | Type de nourriture et périodes d’alimentation pendant la période d’acclimatation | 1 | Non |
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 19 | Type d’essai (toxicité aiguë ou chronique) | s.o. | Oui | Aiguë |
| 20 | Type d’expérience (en laboratoire ou sur le terrain) | s.o. | Non | |
| 21 | Voies d’exposition (nourriture, eau, les deux) | s.o. | Non | |
| 22 | Durée de l’exposition | s.o. | Oui | 96 h |
| 23 | Témoins négatifs ou positifs (préciser) | 1 | Non | |
| 24 | Nombre de répétitions (y compris les témoins) | 1 | Non | |
| 25 | Des concentrations nominales sont-elles indiquées? | 1 | Non | |
| 26 | Des concentrations mesurées sont-elles indiquées? | 3 | Non | |
| 27 | Type de nourriture et périodes d’alimentation durant les essais à long terme | 1 | Sans objet | |
| 28 | Les concentrations ont-elles été mesurées périodiquement (spécialement dans les essais de toxicité chronique)? | 1 | Non | |
| 29 | Les conditions du milieu d’exposition correspondaient-elles au produit chimique particulier signalé? (par exemple, pour la toxicité du métal : pH, DOC/TOC, dureté de l’eau, température) | 3 | Non | |
| 30 | Photopériode et intensité de l’éclairage | 1 | Non | |
| 31 | Préparation de solutions mères et de solutions d’essai | 1 | Non | |
| 32 | Un agent émulsionnant ou stabilisant a-t-il été employé si la substance était peu soluble ou instable? | 1 | Non | |
| 33 | Si un agent émulsionnant ou stabilisant a été employé, sa concentration est-elle indiquée? | 1 | Non | |
| 34 | Si un solubilisant/émulsifiant a été utilisé, son écotoxicité a-t-elle été signalée? | 1 | Non | |
| 35 | Intervalles des contrôles analytiques | 1 | Non | |
| 36 | Méthodes statistiques utilisées | 1 | Non |
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 37 | Le critère d’évaluation a-t-il été directement causé par la toxicité du produit chimique et non par l’état de santé de l’organisme (par exemple, lorsque la mortalité lors du contrôle est supérieure à 10 %) ou des effets physiques (par exemple, « effet d’ombrage »)? | s.o. | Non | |
| 38 | L’organisme d’essai correspondait-il à l’environnement au Canada? | 3 | Oui | |
| 39 | Les conditions d’essai (pH, température, OD, etc.) sont-elles typiques pour l’organisme d’essai? | 1 | Non | |
| 40 | Le type et la conception du système (statique, semi-statique, dynamique; ouvert ou fermé; etc.) correspondent-ils aux propriétés de la substance et à la nature ou aux habitudes de l’organisme? | 2 | Non | |
| 41 | Le pH de l’eau du test se situait-il dans la plage des valeurs typiques de l’environnement au Canada (6 à 9)? | 1 | Non | |
| 42 | La température de l’eau du test se situait-elle dans la plage des valeurs typiques de l’environnement au Canada (5 à 27 °C)? | 1 | Non | |
| 43 | La valeur de la toxicité était-elle inférieure à celle de la solubilité de la substance dans l’eau? | 3 |
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 44 | Valeurs de la toxicité (fournir paramètres et valeurs) | s.o. | CL50 = 100 mg/L > < 220 mg/L | |
| 45 | Autres paramètres indiqués – p. ex., FBC/FBA, CMEO/CSEO (préciser)? | s.o. | CSEO = 100 mg/L | |
| 46 | Autres effets indésirables (par exemple, cancérogénicité, mutagénicité) signalés? | s.o. | ||
| 47 | Note : % | 9,5 | ||
| 48 | Code de fiabilité d’Environnement Canada : | 4 | ||
| 49 | Catégorie de fiabilité (élevée, satisfaisante, basse) : | Non satisfaisante | ||
| 50 | Remarques | Les données soumises ne sont pas suffisantes pour évaluer correctement la fiabilité de cette étude. | ||
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 1 | Référence : Environnement Canada, 1995. NSN submission. Données présentées à la Division des substances nouvelles d’Environnement Canada dans le cadre du Programme de déclaration des substances nouvelles. | |||
| 2 | Identité de la substance : n° CAS | s.o.[1] | Non | |
| 3 | Identité de la substance : nom(s) chimique(s) | s.o. | Oui | |
| 4 | Composition chimique de la substance | 2 | Non | |
| 5 | Pureté chimique | 1 | Non | |
| 6 | Indication de la persistance/stabilité de la substance en milieu aqueux? | 1 | Non | |
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 7 | Référence | 1 | Oui | OCDE 203 |
| 8 | Méthode normalisée (OCDE, UE, nationale, ou autre)? | 3 | Oui | |
| 9 | Justification de la méthode ou du protocole si une méthode non normalisée a été utilisée | 2 | Sans objet | |
| 10 | BPL (bonne pratique de laboratoire) | 3 | Oui |
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 11 | Identité de l’organisme : nom | s.o. | Oui | Truite arc-en-ciel |
| 12 | Indication du nom latin ou des deux noms (latin et commun)? | 1 | Oui | |
| 13 | Âge ou stade biologique de l’organisme d’essai | 1 | Oui | Longueur moyenne : 51 mm; poids moyen : 1,54 |
| 14 | Longueur et/ou poids | 1 | Oui | Voir ci-dessus |
| 15 | Sexe | 1 | Sans objet | |
| 16 | Nombre d’organismes par répétition | 1 | Oui | 10 |
| 17 | Charge en organismes | 1 | Oui | |
| 18 | Type de nourriture et périodes d’alimentation pendant la période d’acclimatation | 1 | Oui |
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 19 | Type d’essai (toxicité aiguë ou chronique) | s.o. | Oui | Aiguë |
| 20 | Type d’expérience (en laboratoire ou sur le terrain) | s.o. | Oui | En laboratoire |
| 21 | Voies d’exposition (nourriture, eau, les deux) | s.o. | Oui | Eau |
| 22 | Durée de l’exposition | s.o. | Oui | 96 h |
| 23 | Témoins négatifs ou positifs (préciser) | 1 | Oui | 3 |
| 24 | Nombre de répétitions (y compris les témoins) | 1 | Oui | 2 |
| 25 | Des concentrations nominales sont-elles indiquées? | 1 | Oui | 320 à 3 200 mg/L |
| 26 | Des concentrations mesurées sont-elles indiquées? | 3 | Non | |
| 27 | Type de nourriture et périodes d’alimentation durant les essais à long terme | 1 | Sans objet | |
| 28 | Les concentrations ont-elles été mesurées périodiquement (spécialement dans les essais de toxicité chronique)? | 1 | Non | |
| 29 | Les conditions du milieu d’exposition correspondaient-elles au produit chimique particulier signalé? (par exemple, pour la toxicité du métal : pH, DOC/TOC, dureté de l’eau, température) | 3 | Oui | |
| 30 | Photopériode et intensité de l’éclairage | 1 | Oui | |
| 31 | Préparation de solutions mères et de solutions d’essai | 1 | Oui | |
| 32 | Un agent émulsionnant ou stabilisant a-t-il été employé si la substance était peu soluble ou instable? | 1 | Non | |
| 33 | Si un agent émulsionnant ou stabilisant a été employé, sa concentration est-elle indiquée? | 1 | ||
| 34 | Si un solubilisant/émulsifiant a été utilisé, son écotoxicité a-t-elle été signalée? | 1 | ||
| 35 | Intervalles des contrôles analytiques | 1 | Oui | |
| 36 | Méthodes statistiques utilisées | 1 | Oui |
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 37 | Le paramètre déterminé était-il directement attribuable à la toxicité de la substance, non à l’état de santé des organismes (p. ex., lorsque la mortalité des témoins est supérieure à 10 %) ou à des facteurs physiques (p. ex., « effet d’ombrage »)? | s.o. | Oui | |
| 38 | L’organisme d’essai correspondait-il à l’environnement au Canada? | 3 | Oui | |
| 39 | Les conditions d’essai (pH, température, OD, etc.) sont-elles typiques pour l’organisme d’essai? | 1 | Oui | |
| 40 | Le type et la conception du système (statique, semi-statique, dynamique; ouvert ou fermé; etc.) correspondent-ils aux propriétés de la substance et à la nature ou aux habitudes de l’organisme? | 2 | Oui | |
| 41 | Le pH de l’eau du test se situait-il dans la plage des valeurs typiques de l’environnement au Canada (6 à 9)? | 1 | Oui | |
| 42 | La température de l’eau du test se situait-elle dans la plage des valeurs typiques de l’environnement au Canada (5 à 27 °C)? | 1 | Oui | |
| 43 | La valeur de la toxicité était-elle inférieure à celle de la solubilité de la substance dans l’eau? | 3 | Solubilité dans l’eau inconnue |
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 44 | Valeurs de la toxicité (fournir paramètres et valeurs) | s.o. | s.o. | CL50 après 96 h |
| 45 | Autres paramètres indiqués – p. ex., FBC/FBA, CMEO/CSEO (préciser)? | s.o. | Non | |
| 46 | Autres effets indésirables (par exemple, cancérogénicité, mutagénicité) signalés? | s.o. | Non | |
| 47 | Note : | 77,5 | ||
| 48 | Code de fiabilité d’Environnement Canada : | 2 | ||
| 49 | Catégorie de fiabilité (élevée, satisfaisante, basse) : | Confiance satisfaisante | ||
| 50 | Remarques | |||
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 1 | Référence : Cohle, P. et R. MIihalik. 1991. Early life stage toxicity of C.I. Disperse Blue 79:1 purified preecake to rainbow trout (Oncorhynchus mykiss) in a flow-through system. | |||
| 2 | Identité de la substance : n° CAS | s.o.[1] | ||
| 3 | Identité de la substance : nom(s) chimique(s) | s.o. | Disperse Blue 79:1 | |
| 4 | Composition chimique de la substance | 2 | Oui | |
| 5 | Pureté chimique | 1 | Oui | 96,61 |
| 6 | Indication de la persistance/stabilité de la substance en milieu aqueux? | 1 | Non | |
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 7 | Référence | 1 | Oui | |
| 8 | Méthode normalisée (OCDE, UE, nationale, ou autre)? | 3 | Oui | ASTM, 1983 |
| 9 | Justification de la méthode ou du protocole si une méthode non normalisée a été utilisée | 2 | Sans objet | |
| 10 | BPL (bonne pratique de laboratoire) | 3 | Oui |
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 11 | Identité de l’organisme : nom | s.o. | Truite arc-en-ciel | |
| 12 | Indication du nom latin ou des deux noms (latin et commun)? | 1 | Oui | |
| 13 | Âge ou stade biologique de l’organisme d’essai | 1 | Oui | |
| 14 | Longueur et/ou poids | 1 | Oui | |
| 15 | Sexe | 1 | Sans objet | |
| 16 | Nombre d’organismes par répétition | 1 | Oui | 20 |
| 17 | Charge en organismes | 1 | Oui | 0,36 à 4,8 µg/L |
| 18 | Type de nourriture et périodes d’alimentation pendant la période d’acclimatation | 1 | Oui |
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 19 | Type d’essai (toxicité aiguë ou chronique) | s.o. | Oui | Toxicité chronique |
| 20 | Type d’expérience (en laboratoire ou sur le terrain) | s.o. | Oui | En laboratoire |
| 21 | Voies d’exposition (nourriture, eau, les deux) | s.o. | Oui | Eau |
| 22 | Durée de l’exposition | s.o. | Oui | 122 jours |
| 23 | Témoins négatifs ou positifs (préciser) | 1 | Oui | Témoin et porteur non indiqués |
| 24 | Nombre de répétitions (y compris les témoins) | 1 | Oui | 2 |
| 25 | Des concentrations nominales sont-elles indiquées? | 1 | Oui | 5 |
| 26 | Des concentrations mesurées sont-elles indiquées? | 3 | Oui | |
| 27 | Type de nourriture et périodes d’alimentation durant les essais à long terme | 1 | Oui | |
| 28 | Les concentrations ont-elles été mesurées périodiquement (spécialement dans les essais de toxicité chronique)? | 1 | Oui | |
| 29 | Les conditions du milieu d’exposition correspondaient-elles au produit chimique particulier signalé? (par exemple, pour la toxicité du métal : pH, DOC/TOC, dureté de l’eau, température) | 3 | Oui | |
| 30 | Photopériode et intensité de l’éclairage | 1 | Oui | |
| 31 | Préparation de solutions mères et de solutions d’essai | 1 | Oui | |
| 32 | Un agent émulsionnant ou stabilisant a-t-il été employé si la substance était peu soluble ou instable? | 1 | Oui | |
| 33 | Si un agent émulsionnant ou stabilisant a été employé, sa concentration est-elle indiquée? | 1 | Oui | |
| 34 | Si un solubilisant/émulsifiant a été utilisé, son écotoxicité a-t-elle été signalée? | 1 | Oui | Pas de valeur pour la toxicité, mais l’agent a été utilisé comme témoin. |
| 35 | Intervalles des contrôles analytiques | 1 | Oui | |
| 36 | Méthodes statistiques utilisées | 1 | Oui |
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 37 | Le critère d’évaluation a-t-il été directement causé par la toxicité du produit chimique et non par l’état de santé de l’organisme (par exemple, lorsque la mortalité lors du contrôle est supérieure à 10 %) ou des effets physiques (par exemple, « effet d’ombrage »)? | s.o. | Oui | |
| 38 | L’organisme d’essai correspondait-il à l’environnement au Canada? | 3 | Oui | |
| 39 | Les conditions d’essai (pH, température, OD, etc.) sont-elles typiques pour l’organisme d’essai? | 1 | Oui | |
| 40 | Le type et la conception du système (statique, semi-statique, dynamique; ouvert ou fermé; etc.) correspondent-ils aux propriétés de la substance et à la nature ou aux habitudes de l’organisme? | 2 | Oui | Renouvellement continu |
| 41 | Le pH de l’eau du test se situait-il dans la plage des valeurs typiques de l’environnement au Canada (6 à 9)? | 1 | Oui | |
| 42 | La température de l’eau du test se situait-elle dans la plage des valeurs typiques de l’environnement au Canada (5 à 27 °C)? | 1 | Oui | |
| 43 | La valeur de la toxicité était-elle inférieure à celle de la solubilité de la substance dans l’eau? | 3 | Impossible à évaluer. Il y a lieu de croire que la plus forte dose d’essai correspond à la limite de solubilité. |
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 44 | Valeurs de la toxicité (fournir paramètres et valeurs) | s.o. | s.o. | CSEO = 0,005 mg/L |
| 45 | Autres paramètres indiqués – p. ex., FBC/FBA, CMEO/CSEO (préciser)? | s.o. | ||
| 46 | Autres effets indésirables (par exemple, cancérogénicité, mutagénicité) signalés? | s.o. | ||
| 47 | Note : | 97,7 | ||
| 48 | Code de fiabilité d’Environnement Canada : | 1 | ||
| 49 | Catégorie de fiabilité (élevée, satisfaisante, basse) : | Confiance élevée | ||
| 50 | Remarques | |||
| Paramètre | Propriétés physico-chimiques et devenir | Profils de persistance, bioaccumulation et toxicité | Écotoxicité |
|---|---|---|---|
| Paramètres d’entrée des modèles | EPI Suite (tous les modèles, notamment AOPWIN, KOCWIN, BCFWIN, BIOWIN et ECOSAR) |
Canadian POP Model (incluant : Catabol, modèle de facteurs d’atténuation du FBC, modèle de toxicité OASIS) |
Artificial Intelligence Expert System (AIES)/ TOPKAT/ ASTER |
| Code SMILES[1] | x | x | x |
| Scénario de cosmétiques et de produits de soins personnels | Hypothèses | Estimation de l’exposition |
|---|---|---|
| Brillant/ baume pour les lèvres[1] | Pourcentage du poids du Solvent Red 23: 1 % (SDC, 2009) Voie orale : Type d’exposition : absorption directe Quantité de produit ingérée : 0,01 g - en supposant que le produit entier est pris oralement (RIVM, 2006) Fréquence d’exposition : 1 460 fois/an (RIVM, 2006) |
Voie orale Dose aiguë (interne) : 0,001 mg/kg Dose chronique (interne) : 0,006 mg/kg p.c. par jour |
| Préparation pour bain – Savon liquide | Pourcentage du poids du Solvent Red 23: 0,1 % (SDC, 2009) Voie cutanée : Type d’exposition : application instantanée Partie exposée : corps – tête de 16 900 cm2(Santé Canada, 1995), Quantité de produit appliquée : 8,7 g (26,1g p/facteur de dilution 3) Fréquence d’exposition : 329 fois/an (RIVM, 2006) Fraction d’absorption : 0,26 (Collier et al., 1993) |
Voie cutanée Dose aiguë (interne) : 0,03 mg/kg Dose chronique (interne) : 0,03 mg/kg p.c. par jour |
| Huile de massage | Pourcentage du poids du Solvent Red 23 : 0,1 % (SDC, 2009) Voie cutanée : Type d’exposition : application instantanée Partie exposée : corps – tête de 16 900 cm2(Santé Canada, 1995) Quantité de produit appliquée : 8 g Fréquence : 24 fois/an (RIVM, 2006) Fraction d’absorption : 0,26 (Collier et al., 1993) |
Voie cutanée Dose aiguë (interne) 0,03 mg/kg Dose chronique (interne) 0,002 mg/kg p.c. par jour |
| Revitalisant capillaire | Pourcentage du poids du Solvent Red 23 : 0,1 % (SDC, 2009) Voie cutanée : Type d’exposition : application instantanée Partie exposée: mains + ½ de la tête, de 1 540 cm2 (Santé Canada, 1995), Quantité de produit appliquée : 14 g (54 g e/facteur de dilution 3,9) Fréquence d’exposition : 104 fois/an (RIVM, 2006) Fraction d’absorption : 0,26 (Collier etal.,1993) |
Voie cutanée Dose aiguë (interne) 0,05 mg/kg Dose chronique (interne) 0,0015 mg/kg p.c. par jour |
| Colorant capillaire | Pourcentage du poids du Solvent Red 23 : 0,1 % (SDC, 2009) Voie cutanée Type d’exposition : application instantanée Partie exposée : ½ de la tête, de 638 cm2(Santé Canada, 1995), Quantité de produit appliquée : 100 g, Fréquence d’exposition : 10 fois/an (RIVM, 2006) Fraction d’absorption : 0,26 (Collier et al., 1993) |
Voie cutanée Dose aiguë (interne) 3,67 mg/kg Dose chronique (interne) 0,10 mg/kg p.c. par jour |
| Crème corporelle | Pourcentage du poids du Solvent Red 23 : 0,3 % (SDC, 2009) Voie cutanée Type d’exposition : application instantanée Partie exposée : corps – tête 16 900 cm2(Santé Canada, 1995), Quantité de produit appliquée : 8 g Fréquence d’exposition : 730 fois/an (RIVM, 2006) Fraction d’absorption : 0,26 (Collier et al., 1993) |
Voie cutanée Dose aiguë (interne) 0,09 mg/kg Dose chronique (interne) 0,18 mg/kg p.c. par jour |
| Nettoyant pour le visage | Pourcentage du poids du Solvent Red 23 : 0,1 % (SDC, 2009) Voie cutanée : Type d’exposition : application instantanée Partie exposée : ½ de la tête, de 638 cm2(Santé Canada, 1995), Quantité de produit appliquée : 0,25 g (25 g avec un facteur de rétention de 10 %) Fréquence d’exposition : 730 fois/an (RIVM, 2006) Fraction d’absorption : 0,26 (Collier et al., 1993) |
Voie cutanée Dose aiguë (interne) 0,009 mg/kg Dose chronique (interne) 0,018 mg/kg p.c. par jour |
| Vernis à ongles | Pourcentage du poids du Solvent Red 23 : 10 % (SDC, 2009) Voie cutanée Type d’exposition : application instantanée Partie exposée : 4 cm2 (Santé Canada, 1995), Quantité de produit appliquée : 0,05 g Fréquence d’exposition : 156 fois/an (RIVM, 2006) Fraction d’absorption : 0,26 (Collier et al., 1993) |
Voie cutanée Dose aiguë (interne) 0,02 mg/kg Dose chronique (interne) 0,008 mg/kg p.c. par jour |
Annexe 4 : Sommaire des renseignements relatifs aux effets sur la santé du Solvent Red 23 (n° CAS : 85-86-9)
| Paramètre | Doses minimales avec effet[1] / Résultats |
|---|---|
| Toxicité aiguë | DL50 minimale (rat)>16 000 mg/kg p.c. Le CSPC a conclu que le Solvent Red 23 avait une faible toxicité par voie orale après une seule exposition (CSPC, 2005). |
| Toxicité de doses répétées à court terme | Aucune étude pertinente n’a été recensée. Une étude sur la toxicité cutanée sur 21 jours a été effectuée sur des lapins. La méthode n’étant pas décrite, le CSPC a considéré l’étude comme non pertinente (CSPC, 2005). |
| Toxicité subchronique | Aucune étude pertinente n’a été recensée. Une étude sur la toxicité cutanée sur 90 jours a été effectuée sur des lapins. La méthode n’étant pas décrite, le CSPC a considéré l’étude comme non pertinente (CSPC, 2005). |
| Toxicité chronique et cancérogénicité | Par voie orale : 83 souris mâles et 54 souris femelles ont été exposés par voie alimentaire à une concentration de 2 mg par jour de la substance sous forme de solution à 1 % dans l'huile (quel que soit le poids). Des tumeurs aux poumons étaient évidentes, mais n’étaient pas plus fréquentes que chez les témoins (CSPC, 2005). Des rats Wistar (5/sexe) ont été nourris de 40 000 mg/kg de nourriture pendant 18 mois. Aucune tumeur n’a été observée. Il n’existe aucune donnée sur le taux de survie (CSPC, 2005). Seize rats femelles ont été exposés par instillation gastrique à 1 mL d’une solution à 0,1 % (e/v) dans l’huile de sésame, 5 fois/semaine pendant 25 semaines. Aucune augmentation de l’incidence de tumeurs n’a été observée (CSPC, 2005). Par voie cutanée : Des souris Swiss-Webster (50/sexe) ont été exposées par l’intermédiaire de la peinture sur la peau. Une quantité de 0,1 mL d’une solution à 1 % a été appliquée sur de la peau épilée (6 cm2) (environ 40 mg/kg p.c. par jour) une fois par semaine pendant 18 mois. Aucune augmentation de l’incidence de tumeurs n’a été observée. Aucune modification du poids corporel ou du taux de survie n’a été observée (CSPC, 2005). Injection sous-cutanée : Deux groupes de 10 souris femelles ont reçu des doses répétées (nombre d’injections non précisé) de 0,25 mL d’une solution saturée de Solvent Red 23 ou de 5 mg de cristaux de Solvent Red 23. Aucune tumeur n’a été observée (CSPC, 2005). Injection intramusculaire : Des rats Long-Evans (8, âgés de 27 jours) ont reçu une injection de 0,5 mL d’une solution à 0,5 % (e/v) dans l’huile de sésame dans le muscle de la cuisse. Aucune tumeur n’a été observée à l’autopsie après 40 semaines (CSPC, 2005). REMARQUE : Le CIRC n’a considéré aucune de ces études comme pertinente pour la classification de la cancérogénicité du Solvent Red 23. |
| Toxicité sur le plan du développement | Du Solvent Red 23 a été administré à des souris gravides par voie orale du 8e au 12e jour de gestation. Les rejetons mâles âgés de 48 à 50 jours ont subi une autopsie, et on a recherché les anomalies du développement des testicules. Aucun effet lié au traitement n’a été observé. (Gray et Ostby, 1993). |
| Toxicité sur le plan de la reproduction | Aucune étude portant sur la toxicité potentielle du Solvent Red 23 sur le plan du développement n’a été recensée. |
| Génotoxicité et paramètres connexes : in vivo | Essai de Comet Résultats positifs : Des souris ddY mâles (4/groupe) ont reçu 2 000 mg/kg de substance par voie orale. Elles ont été sacrifiées à 0, 8, 3 ou 24 heures. Divers tissus ont été examinés par essai de Comet en vue d’y détecter des cassures de brin d’ADN. Une augmentation de la migration de l’ADN (indication de dommages à l’ADN) a été observée dans l’estomac, le côlon et la vessie des souris sacrifiées à 3 heures, mais non chez les souris des groupes de 0, 8 ou 24 heures (Tsuda et al., 2000). |
| Génotoxicité et paramètres connexes : in vitro | Mutagénicité Résultats négatifs : Test d’Ames effectué avec des composés d’essai purifiés dans les souches de contrôle de Salmonella typhimurium TA98 et TA100 en présence du mélange S9. Il se peut que le protocole ne soit pas approprié pour le groupe du composé (Miyagoshi et al., 1985). Résultats positifs : Test d’Ames effectué avec des préparations commerciales de colorants dans les souches de contrôle de Salmonella typhimurium TA98 et TA100 en présence du mélange S9. Les auteurs ont attribué l’activité à la contamination par des matières de synthèse (4-aminoazobenzène) (Miyagoshi et al., 1985). Résultats négatifs : Aucune augmentation de cellules mortes (indicateur de génotoxicité) n’a été observée dans les essais de recombinaison d’E. coliWP2/WP67 ou de B. subtilis 45T (Kada et al., 1972; Mamber et al., 1983). Aberrations chromosomiques Résultats positifs : Des cellules ovariennes (CHO) de hamsters de Chine ont été traitées au Solvent Red 23 sans activation. Un nombre accru de cassures par métaphase a été observé (Au et Hsu, 1979). Résultats négatifs : Des lymphocytes humains exposés in vitro à des doses allant jusqu’à 100 µg/ml n’ont subi aucune augmentation des aberrations chromosomiques (CSPC, 1988). |
| Irritation/sensibilisation | Des lapins exposés au Solvent Red 23 par voie cutanée n’ont montré que des signes d’irritation légers. La Loi sur les aliments et drogues a classé la substance comme légèrement irritante. Le CSC a conclu que le Solvent Red 23 a des propriétés irritantes marginales (CSPC, 2005). Des lapins ont été exposés au Solvent Red 23 par voie oculaire. La substance a été évaluée comme légèrement irritante. Le CSC a conclu que le Solvent Red 23 a des propriétés irritantes marginales (CSPC, 2005). Des groupes de six animaux exposés à 0,1 % (par voie intracutanée) ou à 1,0 % (par voie topique) n’ont pas réagi à des doses d’amorce de 0,001, de 0,01 et de 0,1 % de Solvent Red 23. Toutefois, un traitement initial avec plusieurs autres substances (p-phénylénédiamine,p-aminoazobenzène) n’a pas causé de sensibilisation croisée avec le Solvent Red 23 (CSPC, 2005). |
| Nom de la substance | Solvent Red 23 | Sudan I | Sudan IV | Sudan II |
|---|---|---|---|---|
| N° CAS | 85-86-9 | 842-07-9 | 85-83-6 | 3118-97-6 |
| Autres identifi- cateurs |
Sudan III, CI 26100 | Solvent Yellow 14, CI 12055 | Sudan IV, CI 26105 | C.I. Solvent Orange 7 |
| Formule | C22H16N4O | C16H12N2O | C24H20N4O | C18H16N2O |
| Poids molé- culaire |
352,39 | 248,28 | 380,45 | 276,3 |
| Solubi- lité dans l’eau |
2,60E-03 mg/L (estimée) | 0,67 mg/L (estimée) | 2,03E-04 mg/L (estimée) | 0,055 mg/L (estimée) |
| Log Koe | 7,63 (estimé) | 5,51 (estimé) | 8,72 (estimé) | 6,600 (estimé) |
| Structure |  |
 |
 |
 |
| Classifi- cations interna- tionales |
|
|
|
|
| Nom de la substance | Solvent Red 23 | Sudan I | Sudan IV | Sudan II | ||||
|---|---|---|---|---|---|---|---|---|
| Cancéro- génicité |
Par voie orale
Par voie cutanée
|
Par voie orale
* Autres études dépassées ou non pertinentes citées dans le CIRC, 1975. |
Par voie orale
Par voie cutanée
|
Par voie orale
Implantation
|
||||
Géno- in vivo |
Dommages à l’ADN :
|
Échange de chromatides sœurs
Aberration chromosomique
Essai du micronoyau :
Translocation réciproque
Mutation létale récessive associée au sexe
|
Aucune donnée. | Aucune donnée. | ||||
Géno- in vitro |
Mutagénicité bactérienne
Aberrations chromosomiques
|
Mutagénicité bactérienne
Mutagénicité des cellules mammaliennes
Échange de chromatides sœurs
Aberration chromosomique
|
Mutagénicité bactérienne
Transformation cellulaire
|
Mutagénicité bactérienne
Mutagénicité des cellules mammaliennes
|
||||
Annexe 6 : Sommaire des renseignements disponibles sur la cancérogénicité et la génotoxicité des produits de rupture réductrice des liaisons azoïques potentiels du Solvent Red 23[12],[13]
4-aminoazobenzène
Structure chimique :

- N° CAS : 60-09-3
- Formule :C12H11N3
- Poids moléculaire : 197,24
- Classifications : Groupe 2B du CIRC et Cancérogénicité : Catégorie 2 (UE)
Cancérogénicité
Par voie orale
Seize rats mâles ont été nourris d’environ 100 à 500 mg/kg p.c. par jour dans une alimentation faible en protéines (pour favoriser la formation de tumeurs au foie) jusqu’à leur mort. Sept tumeurs au foie ont été observées, dont deux étaient malignes. Huit rats mâles et huit rats femelles nourris avec la même alimentation, mais sans 4-aminoazobenzène, n’ont eu aucune anomalie au foie (BIBRA, 1989).
Huit rats mâles et huit rats femelles nourris de 75 mg/kg p.c. par jour dans une alimentation faible en protéines n’ont eu aucune tumeur au foie (BIBRA, 1989).
Quarante-quatre rats mâles ont été nourris de 40 à 90 mg/kg p.c. par jour dans une alimentation normale pendant 40 à 60 semaines. Aucune preuve de cancérogénicité n’a été observée (BIBRA, 1989).
Trente rats nourris d’environ 35 mg/kg p.c. par jour dans leur alimentation pendant 3 à 9 semaines n’ont connu aucune augmentation de l’incidence de tumeurs 18 mois plus tard, peu importe si leur traitement comportait ou non un stimulateur de tumeur (BIBRA, 1989).
Trente souris femelles ont été nourries de 52 mg/kg p.c. par jour dans leur alimentation pendant 10 mois. Des observations ont eu lieu pendant sept mois additionnels. Des tumeurs malignes ont été observées chez 22 des 30 souris. Des souris nourries de 27 mg/kg p.c. par jour dans la même étude n’ont montré aucune preuve de cancérogénicité (BIBRA, 1989).
Par voie cutanée
Six rats mâles ont été exposés par de la peinture sur la peau, deux fois par semaine jusqu’à leur mort. L’exposition était d’environ 5-20 mg/kg p.c. Les six rats ont développé des tumeurs bénignes ou malignes après 97 semaines d’exposition (BIBRA, 1989).
Injection sous-cutanée
Trente-six souris ont été nourries d’une alimentation normale ou faible en protéines, et ont reçu une injection sous-cutanée d’environ 250 mg/kg p.c. toutes les deux semaines pendant leur vie. Aucune augmentation de l’incidence de cancérogénicité n’a été observée (BIBRA, 1989).
Des souris (nombre et sexe non indiqués) ayant reçu quatre injections d’environ 200 mg/kg p.c. avant le sevrage ont été observées jusqu’à l’âge d’un an. Des tumeurs au foie ont été observées ainsi qu’une augmentation de l’incidence de tumeurs malignes du système lymphatique (BIBRA, 1989).
Injection intrapéritonale
Vingt rats femelles ont reçu 7,5 à 10 mg/kg p.c. trois fois par semaine pendant cinq semaines. Aucune preuve de cancérogénicité n’était présente après un an d’observation (BIBRA, 1989)
Deux cent quarante-deux souris ont reçu une ou quatre injections d’environ 3 mg/kg p.c. ou plus avant le sevrage. Un examen à l’âge de 9 à 12 mois a permis de détecter des tumeurs malignes au foie chez 190 des 242 souris (BIBRA, 1989).
Génotoxicité
In vivo
Dommages chromosomiques
Résultats positifs : Des rats traités avec une seule dose intrapéritonale (36 ou 143 mg/kg) on connu une augmentation considérable du nombre de cassures de l’ADN à double brin isolé du foie 4, 12 ou 24 heures après l’exposition (BIBRA, 1989).
Résultats positifs : Une augmentation de la fragmentation de l’ADN a été détectée lors d’un essai d’élution alcaline à l’ADN du foie des rats exposés à 1,42 mg/kg (BIBRA, 1989).
Échange de chromatides sœurs
Résultats positifs : Des souris Swiss mâles ont été exposées par voie intrapéritonale à 0, 31 ou 62 mg/kg. Une augmentation liée à la dose des échanges de chromatides sœurs a été observée dans les cellules de la moelle des os des souris (BIBRA, 1989).
In vitro
Mutagénicité bactérienne
Résultats positifs (mutation bactérienne inverse) : Test d’Ames dans diverses souches deSalmonella typhimurium avec activation métabolique seulement (examiné dans BIBRA, 1989).
Résultats positifs (essai par passage sur l’hôte) : Des souris ont reçu 125 mg/kg par injection intramusculaire après des injections intrapéritonales de bactéries. Une augmentation de la mutation inverse a été constatée dans une souche de S. typhimurium (BIBRA, 1989).
Résultats négatifs (essai par passage sur l’hôte) : Des souris exposées par voie orale à 500 mg/kg après une injection intrapéritonale d’une deuxième souche de S. tyhphimurium (non précisée dans la référence secondaire).
Résultats négatifs (mutation bactérienne inverse) : Test d’Ames utilisant des testeurs d’E. coli avec ou sans activation métabolique (BIBRA, 1989).
Mutagénicité des cellules mammaires
Résultats positifs (essai sur des souris L5178Y/TK) : Le taux de mutation directe a augmenté lorsque des cellules du lymphome de souris L5178Y/TK ont été exposées à la substance d’essai avec activation métabolique (BIBRA, 1989).
Synthèse d’ADN non programmée
Résultats positifs : Une incubation de cellules hépatiques de rats fraîchement isolées avec la substance d’essai a entraîné une augmentation de 124 % de la synthèse d’ADN non programmée comparativement à celle des témoins (BIBRA, 1989).
Transformation cellulaire
Résultats positifs : L’exposition a induit une transformation des divers types de cellules mammaliennes. Toutefois, elle n’a pas induit de transformation des cellules de poumons humains avec ou sans activation métabolique (BIBRA, 1989).
1-amino-2-naphtol
Structure chimique :

- N° CAS : 2834-92-6 1198-27-2 (sel Cl-)
- Formule : C10H9NO
- Poids moléculaire : 159,187
- Classifications : s.o.
Cancérogénicité
Implantation : Des granulés de paraffine contenant du 1-amino-2-naphtol dans la vessie des souris ont augmenté l’incidence de métaplasies pavimenteuses. Cette étude n’est pas considérée comme une preuve solide de cancérogénicité, car les granulés de paraffine mêmes peuvent induire la prolifération de cellules épithéliales dans le canal urinaire (BfG, 2003).
Génotoxicité
In vivo
Aucune donnée
In vitro
Mutagénicité bactérienne
Résultats positifs (mutation inverse bactérienne) : Une augmentation de l’incidence de mutation inverse a été observée dans des testeurs S. tyhphimurium TA100 et TA98 lorsque du 1-amino-2-naphtol a subi une réduction du caecum avant l’incubation avec des bactéries (Dillon et al., 1994).
p-phénylènediamine
Structure chimique :

- N° CAS : 106-50-3
- Formule :C6H8N2
- Poids moléculaire : 108,143
- Classifications : s.o.
Cancérogénicité
Par voie cutanée
Des groupes de 50 souris suisses femelles âgées de sept semaines ont reçu de 5 à 10 % d’acétone deux fois par semaine appliqué sur la peau rasée par voie interscapulaire. L’exposition a continué jusqu’à leur mort ou leur euthanasie ou à leur phase moribonde. Aucune augmentation de l’incidence n’a été observée (CSPC, 2006).
Des groupes de cinq lapins femelles ont été exposés à 5 ou 10 % dans l’acétone deux fois par semaine pendant 85 semaines. Aucune augmentation de l’incidence des tumeurs n’a été observée (CSPC, 2006).
Génotoxicité
In vivo
Essai du micronoyau
Résultats négatifs : Des rats exposés par gavage à deux doses de 300 mg/kg avec un intervalle de 24 heures n’ont pas eu d’augmentation de l’incidence d’érythrocytes polychromatiques micronucléés (Hossack et Richardson, 1977). Des résultats négatifs ont été obtenus lorsque des souris CD-1 ont été exposées à 25, 50 ou 100 mg/kg p.c. par injection IP (CSPC, 2006). Résultat négatif chez des rats Wistar exposés par voie orale à 25, 50 ou 100 mg/kg p.c. (CSPC, 2006).
Synthèse d’ADN non programmée
Résultats négatifs : Des rats Wistar exposés à 50 ou 100 mg/kg p.c. par voie orale n’ont pas eu d’augmentation de l’incidence de la synthèse d’ADN non programmée (CSPC, 2006).
In vitro
Mutagénicité bactériologique
Résultats négatifs (mutation inverse bactériologique) : Aucune augmentation de la fréquence de mutation n’a été observée dans les souches TA98, TA100, TA102 ou TA1538 de S. typhimurium avec activation (CSPC, 2006).
Résultats positifs (mutation inverse bactériologique) : Augmentation de la mutagénicité (100-fois) dans les souches de Salmonella typhimurium TA98 et TA98NR en présence d’activateur S9 dérivé du foie de rat (CSPC, 2006).
Mutagénicité mammalienne
Résultats positifs (essai sur des souris L5178Y/TK) : Cellules du lymphome de souris L5178Y exposées avec et sans activation. L’augmentation de la mutagénicité était liée à la dose (CSPC, 2006).
Résultats négatifs (souris L5178Y/hprt) : Des cellules du lymphome de souris L5178Y exposées avec et sans activation. Aucune augmentation de la mutation n’a été observée (CSPC, 2006).
Aberrations chromosomiques
Résultats positifs : Des cellules CHO-K1 exposées au 1,4’-diaminobenzène ont eu une légère augmentation du pourcentage de cellules aberrantes comparativement à celles des témoins (CSPC, 2006).
Aniline
Structure chimique :

- N° CAS : 62-53-3
- Formule : C6H7N
- Poids moléculaire : 93,1283
- Classifications : Groupe 3 du CIRC, Cancérogénicité : Catégorie 3 (UE) et Mutagénicité : Catégorie 3
Cancérogénicité
Par voie orale
Des rats F344 (130 par groupe/sexe) ont été nourris de chlorure d’anilinium à des doses de 0, 10, 30 ou 100 mg/kg p.c. par jour pendant 104 semaines. Il y a eu une augmentation de l’incidence de sarcomes spléniques primaires à la dose élevée (UE, 2004).
Des rats F344 (50/sexe/groupe) ont été nourris avec 0,3 ou 0,6 % de chlorure d’anilinium (174,4 ou 360,5 mg/kg p.c. par jour) pendant 103 semaines. Une augmentation de tumeurs à la rate liée à la dose a été observée. Il y a eu également une augmentation de l’incidence de tumeurs mésenchymateuses (hémangiosarcome, fibrosarcome, fibrome et sarcome) (UE, 2004).
Des souris B6C3F1 (50/groupe) ont reçu une nourriture contenant du chlorure d’anilinium à des concentrations de 0, 0,6 et 1,2 % (0, 737 ou 1 510 mg/kg p.c. par jour chez les mâles, 0, 733 ou 1 560 mg/kg p.c. par jour chez les femelles) pendant 103 semaines suivies de quatre semaines d’observation. Aucune tumeur n’a été liée à l’exposition à la substance d’essai (UE, 2004).
Génotoxicité
In vivo
Essai du micronoyau
Résultats équivoques : De nombreux essais du micronoyau ont été effectués par différents groupes. Quatre essais sur des souris ont donné des résultats positifs à la dose la plus élevée testée, alors que chez les rats, on a observé un résultat positif et un négatif (UE, 2004).
Aberration chromosomique
Résultats négatifs : Aucune augmentation des aberrations chromosomiques n’a été observée dans les cellules de la moelle osseuse des souris ayant reçu deux doses de 220, 300 ou 380 mg/kg par injections intrapéritonales à 24 heures d’intervalle. Des échantillons ont été pris 16, 20 et 24 heures après la seconde administration. Des symptômes cliniques ont été observés (UE, 2004).
Échange de chromatides sœurs
Résultats positifs : Une augmentation liée à une faible dose a été observée dans les cellules de la moelle osseuse chez des groupes de 3 à 9 souris exposées à des doses de 61 à 420 mg/kg par injection intrapéritonale (UE, 2004).
Cassures de brin
Résultats positifs : Des rats et des souris ont été exposées à de l’aniline par administration intrapéritonale. Les cassures ont augmenté dans le foie et les reins des rats, mais étaient négatives dans la rate des rats. Des résultats négatifs ont été obtenus pour le foie, les reins et la moelle osseuse des souris (UE, 2004).
Essai de létalité dominante
Résultats non concluants : Des groupes de 40 mâles ont été exposés à 47, 150 ou 200 mg/kg p.c. par jour par injection intrapéritonale pendant cinq jours. À dose élevée, le nombre d’implants vivants a légèrement diminué, mais était important d’un point de vue statistique. Le nombre de morts prématurées a également augmenté. Toutefois, les conclusions ont été confinées à un groupe de sept souris sur 40 ayant un nombre d’implants vivants manifestement réduit et un nombre élevé d’implants morts prématurément. Ces résultats ont été considérés comme non concluants par l’Union européenne (UE, 2004).
In vitro
Mutagénicité bactériologique
Résultats négatifs : Dans de nombreuses études qui ont utilisé des testeurs de Salmonella typhimurium TA98, TA100, TA1535 et TA1537 avec et sans activation métabolique (UE, 2004).
Résultats positifs (essai par passage sur hôte) : 10 ont reçu 300 mg/kg par voie orale. L’urine a été recueillie 24 heures plus tard et extraite avec de l’éther. Les extraits ont été testés sur des souches deSalmonella typhimurium TA98 et TA100. Une nette réaction dépendante de la dose a été observée dans la souche TA98 avec activation métabolique (UE, 2004).
Mutagénicité des cellules mammaliennes
Résultats équivoques : Cinq essais sur le lymphome de la souris ont été effectués par cinq groupes différents. Un résultat positif clair a été obtenu avec et sans activation métabolique. Trois résultats faiblement positifs ont été déclarés, tous à l’exposition la plus élevée. Un résultat négatif a été obtenu dans une étude comportant des essais seulement dans un système d’activation métabolique (UE, 2004).
Résultats positifs : Une augmentation de la fréquence de mutation a été observée dans un essai HPRT dans lequel étaient utilisées des cellules V79 en présence d’une activation métabolique. Sans activation, le test était négatif. Des résultats positifs n’ont été observés qu’aux doses extrêmement élevées. Cette étude était peu documentée (UE, 2004).
Aberration chromosomique
Résultats positifs : Dans des cellules CHO, des doses élevées d’aniline (1 600 et 5 000 µg/mL) ont causé une augmentation des aberrations chromosomiques en présence d’activation métabolique. Les doses se situant dans le même intervalle ont également augmenté le nombre d’aberrations chromosomiques dans les cellules CHL et V79 (UE, 2004).
Échange de chromatides sœurs
Résultats positifs : Un échange de chromatides sœurs a été induit dans les fibroblastes humains qui avaient un manque important de réductase cytochrome p450 et NADPH-cytochrome p450. Un échange de chromatides sœurs était également induit dans les lymphocytes T induisant de la concanavaline A de cultures de sang entier; toutefois, l’effet n’a pas été constaté dans les cultures comportant des lymphocytes purifiés alors qu’une augmentation marginale de l’échange de chromatides sœurs a été observée lorsque des lymphocytes purifiés étaient exposés à l’aniline en présence de 1 000 µg/mL d’hémoglobine. L’UE a noté que cette étude a démontré que les érythrocytes contribuaient à la transformation de l’aniline en intermédiaires génotoxiques (UE, 2004).
Synthèse d’ADN non programmée
Résultats négatifs : Aucune augmentation de la réparation de l’ADN n’a été observée dans les hépatocytes humains primaires ou dans ceux des rats (UE, 2004).
Cassures de brin
Résultats équivoques : Une dose très élevée (21,5 mM) a causé une augmentation des cassures de brin d’ADN dans les cellules du lymphome de souris avec activation métabolique. Les auteurs ont interprété ce résultat comme étant équivoque. Aucune augmentation n’a été observée sans activation métabolique (UE, 2004).
| N° CAS | DEREK1 | CASETOX (2008) | TOPKAT (2008) | |||||||
|---|---|---|---|---|---|---|---|---|---|---|
| Cancer | m-rat | f-rat | m-souris | f-souris | Rongeurs du NTP | NTP m-rat |
NTP f-rat |
NTP m-souris |
NTP f-souris |
|
| 85-86-9 (origine) | P | NC | NC | N | N | NC | P | HC | P | NC |
| 60-09-3 | P | NC | NC | N | N | P | P | NC | N | N |
| 62-53-3 | HC | P | P | N | N | P | P* | P* | N | N |
| 106-50-3 | P | N | N | N | N | N | N | N | P | N |
| 2834-92-6 | HC | N | N | N | N | P | P | N | N | N |
| N° CAS | Ames | ChrAb | Induction de micronoyaux | Mutation du lymphome de la souris | |||
|---|---|---|---|---|---|---|---|
| Derek | CT | TK | Derek | CT# | CT | CT | |
| 85-86-9 (origine) | P | N | NC | HC | NC | N | NC |
| 60-09-3 | P | N | P* | HC | P | NC | P |
| 62-53-3 | HC | N | N | HC | P | P | P |
| 106-50-3 | P | N | P* | P | P | N | P |
| 2834-92-6 | HC | N | P | HC | N | N | N |
Notes de bas de page
[2] La détermination de la conformité à l’un ou plusieurs des critères énoncés à l’article 64 repose sur l’évaluation des risques pour l’environnement ou la santé humaine associés aux expositions dans l’environnement en général. Pour les humains, ceci inclut, sans toutefois s’y limiter, les expositions à l’acrylate d’éthyle par l’air ambiant et intérieur, l’eau potable, les produits alimentaires et l’utilisation de produits de consommation. Une conclusion établie en vertu de la LCPE (1999) sur les substances des lots 1 à 12 du Défi, énumérées dans le Plan de gestion des produits chimiques, n’est pas pertinente, ni n’empêche une évaluation en fonction des critères de danger définis dans leRèglement sur les produits contrôlés qui fait partie du cadre réglementaire applicable au Système d’information sur les matières dangereuses utilisées au travail pour les produits destinés à être utilisés au travail.
[3] Voir la section Absorption et biodisponibilité pour des renseignements sur le fondement des valeurs d’absorption par voie orale et cutanée utilisées pour estimer l’exposition au Solvent Red 23.
[4] Dose approximative = 67 mg/kg p.c. par jour à 2 mg/animal par jour avec des souris ayant un poids corporel de 0,05 kg (Santé Canada, 1994).
[5] Dose approximative = 2 000 mg/kg p.c. par jour à partir de 40 000 ppm dans l’alimentation (4 %) et conversion de la dose de 0,05 pour les rats (Santé Canada, 1994).
[6] Expositions indiquées dans le pourcentage de l’alimentation. Converti en mg/kg p.c. par jour au moyen des valeurs de référence de Santé Canada (Santé Canada, 1994).
[7] Estimation de la dose basée sur : 1 mg/dose (0,1 % dans un volume de 1 mL) et un poids corporel de 0,35kg pour les rats (Santé Canada, 1994).
[8] La dose estimée est d’environ 33 mg/kg p.c. par dose hebdomadaire (l’équivalent de la dose amortie de 5 mg/kg p.c. par jour) d’après une dose de 1 mg appliquée hebdomadairement (1 % dans 0,1 mL appliqué) et un poids corporel de 0,03 kg pour les souris (Santé Canada, 1994).
[9] Classification actuelle de Cancérogène 2 et Mutagène 3, 2 dans (CLP, annexe VI, tableau 3.1), classification antérieure de Cancérogène Catégorie 3 et Mutagène Catégorie 3 (CLP, annexe VI, tableau 3.2) (Commission européenne, 2008; ESIS, 1995-2010).
[10] o-aminoazotoluène, le produit prévu de la rupture des liaisons azoïques du Sudan IV, est l’analogue diméthyle du 4-aminoazobenzène, un métabolite prévu du Solvent Red 23.
[11] elon les prévisions, le Solvent Red 23 et le Sudan IV génèrent du 1-amino-2-naphthol par rupture de ses liaisons azoïques.
[12] Les données relatives aux effets sur la santé des produits potentiels de rupture réductrice des liaisons azoïques ont été recueillies principalement de sources secondaires, qui sont citées ici.
[13] Le 1-((4-aminophényl)azo)-2-naphthalénol est également un produit de la rupture réductrice des liaisons azoïques du Solvent Red 23. Comme ce produit n’a pas de n° CAS ni de données relatives aux effets sur la santé, il n’a pas été présenté dans ce tableau.
Cette page Web a été archivée dans le Web
L'information dont il est indiqué qu'elle est archivée est fournie à des fins de référence, de recherche ou de tenue de documents. Elle n'est pas assujettie aux normes Web du gouvernement du Canada et elle n'a pas été modifiée ou mise à jour depuis son archivage. Pour obtenir cette information dans un autre format, veuillez communiquer avec nous.
Archivée
1-[4-(phénylazo)phénylazo]-2-naphtol
Solvent Red 23
Numéro de registre du Chemical Abstracts Service
85-86-9
Environnement Canada
Santé Canada
Septembre 2011
Table des Matières
- Sommaire
- Introduction
- Identité de la substance
- Propriétés physiques et chimiques
- Sources
- Utilisations
- Rejets dans l'environnement
- Devenir dans l'environnement
- Persistance et potentiel de bioaccumulation
- Potentiel d'effets nocifs sur l'environnement
- Potentiel d'effets nocifs sur la santé humaine
- Conclusion
- Références
- Annexe 1 : Sommaires de rigueur d'étude pour les études clés
- Annexe 2 : Tableau sommaire des intrants des modèles de la persistance, de la bioaccumulation et de la toxicité
- Annexe 3 : Estimations de l'exposition de l'ensemble de la population au Solvent Red 23 dans les cosmétiques et les produits de soins personnels d'après ConsExpo, version 4.1 (ConsExpo, 2006; RIVM, 2006)
- Annexe 4 : Sommaire des renseignements relatifs aux effets sur la santé du Solvent Red 23 (n° CAS : 85-86-9)
- Annexe 5 : Sommaire des renseignements disponibles sur la cancérogénicité et la génotoxicité du Solvent Red 23 et des substances considérées comme analogues au Solvent Red 23 dans la présente évaluation
- Annexe 6 : Sommaire des renseignements disponibles sur la cancérogénicité et la génotoxicité des produits de rupture réductrice des liaisons azoïques potentiels du Solvent Red 23
- Annexe 7 : Sommaires des résultats des RQSA pour le Solvent Red 23 et ses métabolites prévus
Conformément à l’article 74 de la Loi canadienne sur la protection de l’environnement (1999) [LCPE (1999)], les ministres de l’Environnement et de la Santé ont effectué une évaluation préalable sur le 1-[4-(phénylazo)phénylazo)]-2-naphtol (ci-après appelé Solvent Red 23), dont le numéro de registre du Chemical Abstracts Service [1] est 85-86-9. Une priorité élevée a été accordée à l’évaluation préalable de cette substance inscrite au Défi, car elle répondait aux critères environnementaux de la catégorisation relatifs à la persistance, au potentiel de bioaccumulation et à la toxicité intrinsèque pour les organismes non humains et l’on croit qu’elle est commercialisée au Canada.
L’évaluation des risques que présente le Solvent Red 23 pour la santé humaine n’a pas été jugée hautement prioritaire à la lumière des résultats fournis par les outils simples de détermination du risque d’exposition et du risque pour la santé élaborés par Santé Canada aux fins de la catégorisation des substances de la Liste intérieure des substances.
Le Solvent Red 23 est une substance organique utilisée au Canada principalement dans des huiles, des graisses et des cires, mais aussi dans des solvants alcooliques, esters et hydrocarbonés, dans du polystyrène et des cosmétiques et comme indicateur. On l’utilise aussi comme colorant pour pesticides et il a déjà été utilisé comme teinture à textile. Cette substance n’est pas produite naturellement dans l’environnement. La fabrication du Solvent Red 23 n’a pas été déclarée au Canada. En 2006, du Solvent Red 23 a été importé ou utilisé au Canada. Toutefois, quatre entreprises ont déclaré avoir importé entre 100 et 1 000 kg de cette substance en produits au pays en 2005 pour répondre au sondage mené au Canada conformément à l’article 71 de la LCPE.
En se basant sur les profils d’utilisation déclarés au Canada dans les produits de soins personnels, on peut penser que tous les produits contenant du Solvent Red 23 pourraient être rejetés dans les égouts, les eaux de surface ou le sol au cours de leur utilisation. Les eaux d’égout pourraient recevoir la plus forte proportion de Solvent Red 23 au cours de l’utilisation des produits. On prévoit que la majeure partie de cette substance, fixée aux boues d’épuration des eaux usées venant des stations de traitement des eaux usées à la suite de rejets aux égouts de cosmétiques et de produits de soins personnels, sera entraînée dans les boues vers des sites d’enfouissement. En plus d’être mis en décharge, une partie des biosolides produits par les stations de traitement des eaux usées peuvent être épandus sur des terres en tant qu’engrais ou amendement synthétique à des fins agricoles, forestières ou de remise en état, et un petit pourcentage peut être incinéré.
On croit que le Solvent Red 23 n’est pas soluble dans l’eau et n’est pas volatil, mais qu’il sera adsorbé sur des particules en raison de sa nature hydrophobe. Pour ces raisons, le Solvent Red 23 se retrouvera sans doute principalement dans les sédiments et, peut-être dans une moindre mesure, dans les sols agricoles amendés avec des biosolides, après son rejet dans l’eau. On est d’avis que le Solvent Red 23 ne sera pas présent de manière significative dans d’autres milieux, et qu’il est peu probable qu’il fasse l’objet d’un transport atmosphérique à grande distance.
D’après ses propriétés physiques et chimiques, le Solvent Red 23 devrait être persistant dans l’eau, le sol et les sédiments. Toutefois, des données expérimentales sur le potentiel de bioaccumulation de deux analogues à la structure relativement similaire semblent indiquer que ce colorant a un faible potentiel d’accumulation dans les tissus adipeux des organismes. Cette substance répond donc aux critères de persistance, mais non à ceux de bioaccumulation énoncés dans leRèglement sur la persistance et la bioaccumulation. De plus, des données expérimentales sur la toxicité d’analogues chimiques amènent à penser que le Solvent Red 23 n’entraîne pas d’effets nocifs aigus chez les organismes aquatiques exposés à de faibles concentrations.
Pour la présente évaluation préalable finale, on a retenu un scénario d’exposition cumulative prudent, dans lequel une même station de traitement des eaux usées rejette, dans le milieu aquatique, la quantité maximale de Solvent Red 23 selon les données de 2005. De plus, étant donné que le Solvent Red 23 peut être utilisé dans les produits de consommation, un scénario de rejet prudent a été élaboré selon une estimation de la quantité de ce colorant sur le marché canadien. Les concentrations environnementales estimées étaient largement inférieures à la concentration estimée sans effet calculée pour les espèces aquatiques fragiles.
À la lumière des renseignements disponibles, on conclut que le Solvent Red 23 ne pénètre pas dans l’environnement en une quantité ou concentration ou dans des conditions de nature à avoir, immédiatement ou à long terme, un effet nocif sur l’environnement ou sur sa diversité biologique, ou à mettre en danger l’environnement essentiel pour la vie.
On est d’avis que l’exposition du public au Solvent Red 23 dans l’environnement est négligeable. Toutefois, il peut y être exposé lors de l’utilisation de cosmétiques et de produits de soins personnels contenant du Solvent Red 23. Les données empiriques sur les effets sur la santé pour cette substance sont limitées. Le Solvent Red 23 fait partie de la classe de composés caractérisés par la présence d’une liaison azoïque ou plus (-N=N-), ce qui peut donner lieu à un clivage réductif des azoïques causant le rejet d’amines aromatiques. Le clivage réductif des azoïques du Solvent Red 23 peut notamment causer le rejet de 4-aminoazobenzène, une substance qui a été classée par le Centre International de Recherche sur le Cancer (CIRC) et la commission européenne en fonction de sa cancérogénicité. La structure du Solvent Red 23 est également similaire à celle d’un colorant azoïque qui provoque un processus néoplasique du foie chez les rats mâles et femelles exposés oralement selon la dose administrée, et il est classé comme étant un agent mutagène et cancérogène par la commission européenne. Selon la considération du potentiel d’exposition de l’ensemble de la population découlant de l’utilisation de cosmétiques et de produits de soins personnels contenant du Solvent Red 23, et des données démontrant le potentiel de génotoxicité et de cancérogénicité pour lesquelles il peut y avoir une probabilité de préjudice à tous les niveaux d’exposition, on conclut que le Solvent Red 23 est rejeté dans l’environnement en quantité, à une concentration ou dans des conditions pouvant constituer un danger au Canada pour la vie et la santé humaine.
Des activités de recherche et de surveillance viendront, s’il y a lieu, appuyer la vérification des hypothèses formulées au cours de l’évaluation préalable et, le cas échéant, l’efficacité des mesures de contrôle possibles définies à l’étape de la gestion des risques.
D’après les renseignements disponibles, il est conclu que le 1-[4-(phénylazo)phénylazo)]-2-naphtol répond à un ou plusieurs des critères énoncés à l’article 64 de la LCPE (1999).
La Loi canadienne sur la protection de l’environnement (1999) [LCPE (1999)] (Canada, 1999) exige que les ministres de l’Environnement et de la Santé procèdent à une évaluation préalable des substances qui répondent aux critères de catégorisation énoncés dans la Loi afin de déterminer si elles présentent ou sont susceptibles de présenter un risque pour l’environnement ou la santé humaine.
En se fondant sur l’information obtenue dans le cadre de la catégorisation, les ministres ont jugé qu’une attention hautement prioritaire devait être accordée à un certain nombre de substances, à savoir :
- celles qui répondent à tous les critères environnementaux de catégorisation, notamment la persistance (P), le potentiel de bioaccumulation (B) et la toxicité intrinsèque pour les organismes aquatiques (Ti), et que l’on pense être commercialisées au Canada;
- celles qui répondent aux critères de catégorisation pour le plus fort risque d’exposition (PFRE) ou qui présentent un risque d’exposition intermédiaire (REI) et qui ont été jugées particulièrement dangereuses pour la santé humaine, compte tenu des classifications qui ont été établies par d’autres organismes nationaux ou internationaux concernant leur cancérogénicité, leur génotoxicité ou leur toxicité pour le développement ou la reproduction.
Le 9 décembre 2006, les ministres ont donc publié un avis d’intention dans la Partie I de la Gazette du Canada(Canada, 2006a), dans lequel ils priaient l’industrie et les autres parties intéressées de fournir, selon un calendrier déterminé, des renseignements précis qui pourraient servir à étayer l’évaluation des risques, ainsi qu’à élaborer et à évaluer les meilleures pratiques de gestion des risques et de bonne gestion des produits pour ces substances d’importance prioritaire.
La substance 1-[4-(phénylazo)phénylazo]-2-naphtol (qui sera appelée Solvent Red 23 dans le présent document) a été jugée hautement prioritaire pour l’évaluation des risques écologiques, car elle a été jugée persistante, bioaccumulable et intrinsèquement toxique pour les organismes aquatiques et l’on croit qu’elle est commercialisée au Canada. Le volet du Défi portant sur cette substance a été publié dans laGazette du Canada le 31 mai 2008 (Canada, 2008a, 2008b). En même temps a été publié le profil de cette substance qui présentait l’information technique (obtenue avant décembre 2005) sur laquelle a reposé sa catégorisation. Le Défi a permis d’obtenir des renseignements sur les utilisations du Solvent Red 23 et sur certains produits de formulation.
Même si l’évaluation des risques que présente le Solvent Red 23 pour l’environnement est jugée hautement prioritaire, cette substance ne répond pas aux critères pour le PFRE ou le REI ni aux critères définissant un grave risque pour la santé humaine, compte tenu du classement attribué par d’autres organismes nationaux ou internationaux quant à sa cancérogénicité, à sa génotoxicité ou à sa toxicité sur le plan du développement ou de la reproduction.
Les évaluations préalables mettent l’accent sur les renseignements jugés essentiels pour déterminer si une substance répond aux critères énoncés à l’article 64 de la LCPE (1999). Les évaluations préalables examinent les renseignements scientifiques et tirent des conclusions fondées sur la méthode du poids de la preuve et le principe de prudence[2].
La présente évaluation préalable finale prend en considération les renseignements sur les propriétés chimiques, les dangers, les utilisations et l’exposition, y compris ceux fournis dans le cadre du Défi. Les données pertinentes pour l’évaluation préalable de cette substance sont tirées de publications originales, de rapports de synthèse et d’évaluation, de rapports de recherche de parties intéressées et d’autres documents consultés lors de recherches documentaires menées récemment, jusqu’en juillet 2010. Les études importantes ont fait l’objet d’une évaluation critique; les résultats de la modélisation ont pu être utilisés dans la formulation des conclusions. Lorsqu’ils étaient disponibles et pertinents, les renseignements contenus dans les évaluations des dangers effectués par d’autres instances ont été utilisés. La présente évaluation préalable finale ne constitue pas un examen exhaustif ou critique de toutes les données disponibles. Il s’agit plutôt d’un sommaire des renseignements essentiels qui appuient la conclusion.
Cette évaluation préalable finale a été préparée par le personnel du Programme des substances existantes de Santé Canada et d’Environnement Canada et elle intègre les résultats d’autres programmes exécutés par ces ministères. Les portions de la présente évaluation portant sur l’écologie ont fait l’objet d’une étude consignée par des pairs ou d’une consultation de ces derniers. Des experts scientifiques choisis et dirigés par la Toxicology Excellence for Risk Assessment (TERA), notamment M. Larry Claxton (Ph.D.), M. Bernard Gadagbui (Ph.D.), M. Pertti Hakkinen (Ph.D.), M. Glenn Talaska (Ph.D.) et Mme Pam Williams (Ph.D.), ont formulé des commentaires sur les portions techniques touchant la santé humaine.
En outre, l’ébauche de la présente évaluation préalable a fait l’objet d’une période de commentaires du public de 60 jours. Bien que les commentaires venant de l’extérieur aient été pris en considération, Santé Canada et d’Environnement Canada sont seuls responsables du contenu final et des résultats de l’évaluation préalable. Les approches suivies lors évaluations préalables dans le cadre du Défi ont été examinées par un groupe indépendant, soit le Groupe consultatif du Défi.
Les considérations et renseignements importants qui sous-tendent la présente évaluation sont présentés ci-après.
Nom de la substance
Aux fins du présent document, 1-[4-(phénylazo)phénylazo]-2-naphtol sera appelé Solvent Red 23, conformément à son nom dans le Colour Index (n° du Colour Index : 26100; CII 2002). Les renseignements sur l’identité de la substance sont présentés au tableau 1 ci-dessous.
| Numéro de registre du Chemical Abstracts Service (n° CAS) | 85-86-9 |
|---|---|
| Nom dans la LIS | 1-[4-(phénylazo)phénylazo]-2-naphtol |
| Noms dans les inventaires[1] | 2-naphthalenol, 1-[[4-(phenylazo)phenyl]azo]- (TSCA, AICS, PICCS, ASIA-PAC, NZIoC) 1-(4-(phénylazo)phénylazo)-2-naphtol (EINECS) Solvent Red 23 (ENCS, PICCS) C.I. solvent red 02 (ECL) Sudan III (PICCS) naphth-2-ol, 1-((4-phenylazo)phenyl)azo)- (PICCS) |
| Autres noms | 1-(p-Phenylazophenylazo)-2-naphthol; 111440 Red; 2-Naphthol, 1-(p-phenylazophenylazo)-; Brasilazina Oil Scarlet; C.I. 26100; C.I. Solvent Red 23; Certiqual Oil Red; D and C Red No. 17; Fast Oil Scarlet III; Fat Red Bluish; Fat Red HRR; Fat Red R; Fat Red RS; Fat Scarlet LB; Fat Soluble Red Zh; FD And C Red No. 17; Grasal Brilliant Red G; Grasan Brilliant Red G; Japan Red 225; Japan Red No. 225; NSC 65825; NSC 8995; Oil Red 3G; Oil Red AS; Oil Red Extra; Oil Scarlet G; Organol Red BS; Organol Scarlet; Red No. 225; Red Zh; Silotras Scarlet TB; Somalia Red III; Stearix Scarlet; Sudan 3; Sudan P III; Sudan Red III; Tetrazobenzene-b-naphthol; Toney Red |
| Catégorie de la substance | Substances organiques définies |
| Classe chimique | Composés azoïques |
| Groupe chimique | Composés diazoïques |
| Formule chimique | C22H16N4O |
| Structure chimique | 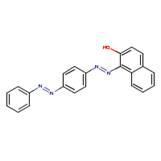 |
| SMILES[2] | Oc(ccc(c1ccc2)c2)c1N=Nc(ccc(N=Nc(cccc3)c3)c4)c4 |
| Poids moléculaire | 352,40 g/mol |
[2] Simplified Molecular Input Line Entry System.
Solvent Red 23 est un colorant diazoïque. Les deux liens azoïques (–N=N–) de cette molécule sont des groupements fonctionnels qui produisent de la couleur (EPA du Danemark, 1999). Les colorants peuvent être classés selon leur structure chimique, mais aussi selon leurs applications industrielles et les méthodes de teinture du substrat considéré (ETAD, 1995). Leur classification, qui inclut les colorants acides et directs, tend à refléter les regroupements basés sur les propriétés physiques et chimiques des substances. Un bref exposé des usages de ce colorant est consultable à la partie « Utilisations » du présent document.
On dispose de peu de données expérimentales sur les propriétés physiques et chimiques du Solvent Red 23. À l’occasion de l’atelier sur les relations quantitatives structure-activité (RQSA) organisé par Environnement Canada en 1999 (Environnement Canada, 2000), des experts en modélisation ont classé de nombreuses catégories structurales de pigments et de teintures comme « difficiles à modéliser » à l’aide de RQSA. Les propriétés physiques ou chimiques de nombreuses classes structurales de teintures et de pigments se prêtent mal à la prévision modélisée, car on considère qu’elles « ne font pas partie du domaine d’applicabilité » (p. ex. domaines de la structure ou des paramètres des propriétés). Par conséquent, lorsqu’il s’agit de teintures et de pigments, on vérifie au cas par cas les domaines d’applicabilité des modèles RQSA pour déterminer leur utilité potentielle.
Pour la présente évaluation, on estime que certains modèles RQSA utilisés pour prévoir les propriétés physiques et chimiques qui n’ont pas de substances comparables au Solvent Red 23 dans leur domaine d’applicabilité peuvent produire des résultats ayant un degré d’incertitude élevé. Par conséquent, une méthode par analogie a été utilisée pour déterminer les propriétés physiques et chimiques approximatives au tableau 2. Ces propriétés ont été par la suite considérées lors de l’évaluation de diverses sources de données. Le tableau 2 présente certaines propriétés physiques et chimiques (valeurs calculées et extrapolées) du Solvent Red 23 et des analogues.
Un analogue est un produit chimique dont la structure est similaire à celle de la substance évaluée; il devrait donc avoir des propriétés physiques et chimiques, un comportement dans l’environnement et une toxicité semblables. Lorsque ce sont des données expérimentales pour un paramètre donné d’une substance analogue, celles-ci peuvent être directement utilisées ou avec un ajustement, comme estimation de cette valeur de paramètre pour la substance en cours d’évaluation.
Pour trouver des analogues acceptables, une revue des données pour plusieurs colorants azoïques dispersés a été effectuée (Anliker et al., 1981; Anliker et Moser, 1987; Baughman et Perenich; 1988, ETAD, 1995; Brown, 1992; Yen et al., 1989, Sijm et al., 1999). En plus de leurs similitudes structurelles avec le Solvent Red 23, ces composés partagent d’autres caractéristiques avec la substance, qui renforcent leur pertinence en tant qu’analogues. Cela comprend les propriétés influant sur leur devenir dans l’environnement comme des masses moléculaires élevées (généralement supérieures à 300 g/mol), un diamètre transversal élevé (entre 1,31 et 2,19 nm), des structures particulaires solides, un point de décomposition supérieur à 120 ºC et une « dispersabilité » dans l’eau (c’est-à-dire que ces composés ne sont pas entièrement « solubles »). De plus, leur pression de vapeur est négligeable et ils sont stables dans des conditions environnementales, car ils ont été conçus pour l’être. D’autres analogues ont été choisis aux fins de l’évaluation de la santé humaine, dans les cas où des données existent (voir la section Potentiel d’effets nocifs sur la santé humaine pour la justification et l’analyse).
Comme certaines des études concernant les colorants diazoïques ont été réalisées dans des conditions environnementales non pertinentes (à des températures élevées, par exemple) ou présentent peu de renseignements permettant d’évaluer leur fiabilité, des données sur les colorants dispersés monoazoïques et les colorants dispersés azoïques, en général, sont incluses dans le tableau 2.
| Propriété | Type[1] | Valeur | Température (°C) | Référence | |
|---|---|---|---|---|---|
| État physique | Analogue Disperse Orange 29 |
Poudre | Étude présentée, 2008a | ||
| Point de décomposition[2] (ºC) |
Solvent Red 23 | 195 | PhysProp, 2006 | ||
| Analogue Sudan IV (aussi appelé Solvent Red 24) | 185 | MITI, 1992 | |||
| Analogue Disperse Orange 29 |
223 | ETAD, 2005 | |||
| Analogue Disperse Yellow 23 |
158 178 | Odabasoglu et al., 2003; Datyner, 1978 | |||
| Analogue Disperse Orange 13 |
153 à 156,5 | NIshida et al., 1989 | |||
| Analogue Disperse Orange 30 | 126,9 à 128,5 | ETAD, 2005 | |||
| Analogue Disperse Blue 79 | 157 | PhysProp, 2006 | |||
| Analogue Disperse Blue 79:1 | 132 153 | Sijm et al., 1999; Yen et al., 1989 | |||
| Données déduites à partir d’analogues des colorants azoïques dispersés | 117 à 175 74 à 236 | Anliker et Moser, 1987; Baughman et Perenich, 1988 | |||
| Point d’ébullition[3] (ºC) |
Sans objet | ||||
| Masse volumique (kg/m3) |
Non disponible | ||||
| Pression de vapeur (Pa) |
Analogue Disperse Orange 13 |
0,18 à 0,42[4] | 191,5 à 211 | Nishida et al., 1989 | |
| Analogue Disperse Blue 79 |
4,53 x 10-7 | Clariant, 1996 | |||
| Données déduites à partir d’analogues des colorants azoïques dispersés | 5,3 x 10-12 à 5,3 x 10-5) (4 x 10-14 à 4 x 10-7 mm Hg) |
25 | Baughman et Perenich, 1988 | ||
| Constante de la loi de Henry (Pa·m3/mol) |
Données déduites à partir d’analogues des colorants azoïques | 10-8 à 10-1 (10-13 à 10-6atm·m3/mol)[5] |
Baughman et Perenich, 1988 | ||
| Log Koe (coefficient de partage octanol-eau) (sans dimension) |
Analogue Disperse Orange 29 |
4,6[6] | Étude présentée, 2008a | ||
| Analogue Disperse Blue 79 |
4,1; 4,3[7] | Clariant, 1996; Brown, 1992 | |||
| Analogue Disperse Blue 79:1 | 4,4; 4,8 | Sijm et al., 1999; Yen et al., 1989 | |||
| Analogue Disperse Orange 30 |
4,2[8] | Brown, 1992 | |||
| Données déduites à partir d’analogues des colorants azoïques dispersés | 1,79 à 5,1 | Baughman et Perenich, 1988 | |||
| > 2 à 5,1 | Anliker et al., 1981; Anliker et Moser, 1987 | ||||
| Log Kco (coefficient de partage carbone organique-eau) (sans dimension) |
Données déduites à partir d’analogues, calculées | 3,4 à 4,2[9] | Baughman et Perenich, 1988 | ||
| Solubilité dans l’eau (mg/L) |
Analogue Disperse Orange 13 |
0,345 | PhysProp, 2006 | ||
| Analogue Disperse Orange 29 |
42,9[6] | Étude présentée, 2008a | |||
| 0,0037 | 25 | Baughman et al., 1996 (estimé) | |||
| Analogue Disperse Yellow 23 |
0,00006 | 25 | Baughman et Perenich, 1988 | ||
| 0,00052 | Baughman et al., 1996 (estimé) | ||||
| 15,7 à 34,8[4] | 130 | Braun, 1991 | |||
| Analogue Disperse Yellow 68 |
16,6[4] | 125 | Prikryl et al., 1979 | ||
| Analogue Disperse Blue 79 | 0,0054 | 25 | Clariant, 1996 | ||
| 0,02[7] | Brown, 1992 | ||||
| Analogue Disperse Blue 79:1 | 0,02 | Sijm et al., 1999 | |||
| 0,0052 | Yen et al., 1989 | ||||
| 0,00063[4] | 100 à 125 | Baughman et Perenich, 1988 | |||
| Disperse Orange 30 | 0,07[8] | Brown, 1992 | |||
| Données analogues des colorants azoïques dispersés | < 0,01 | 20 | Anliker et Moser, 1987 | ||
| Très peu soluble dans l’eau | ETAD, 1995 | ||||
| 1,2 x 10-5 à 35,5 (4 x 10-11à 1,8 x 10-4 mol/L) | Baughman et Perenich, 1988 | ||||
| Solubilité dans le n-octanol (mg/L) | Analogue Disperse Orange 29 |
5 086 | ETAD, 2005 | ||
| Analogue Disperse Orange 30 | 576 | ETAD, 2005 | |||
| Analogue Disperse Blue 79:1 |
14 | Sijm et al., 1999 | |||
| Données analogues des colorants azoïques dispersés | 81 à 2100 | 20 | Anliker et Moser, 1987 | ||
| pKa (constante de dissociation) (sans dimension) |
Solvent Red 23 | 13,5 | ACD/pKa DB, 2005 | ||
| Disperse Yellow 23 | 8,1 | Haag et Mill, 1987 | |||
[2] On utilise l’expression « point de fusion », mais il serait plus exact de parler de point de décomposition; en effet, il est du domaine connu qu’à des températures élevées (supérieures à 200 °C) les colorants dispersés ne fondent pas, mais se carbonisent.
[3] En général, la notion de point d’ébullition ne s’applique pas aux colorants dispersés. Dans le cas des colorants en poudre, on observe, à température élevée, une carbonisation ou une décomposition de la substance plutôt qu’une ébullition. Pour ce qui est des liquides et des pâtes colorantes, on observe l’ébullition du solvant seulement, alors que le composant solide qui ne s’est pas évaporé se décompose ou se carbonise (ETAD, 1995).
[4] Il est à noter que les analyses de la solubilité de l’eau dans le cadre de ces études ont été menées à des températures très élevées; les valeurs sont donc plus élevées qu’on ne l’avait prévu à température ambiante.
[5] Les valeurs de solubilité de cinq colorants azoïques dispersés (Disperse Orange 3, Disperse Red 1, Solvent Yellow 2, Dis. A. 5, Dis. A. 7) à 25 et 80 °C ont été utilisées par Baughman et Perenich (1988) pour calculer les constantes de la loi de Henry de ces colorants. Nous donnons une plage de valeurs pour illustrer la constante de la loi de Henry prévue en ce qui concerne les colorants diazoïques.
[6] L’étude indique que le Disperse Orange 29 utilisé dans l’essai avait une dispersion du colorant à 20 % (eau 70 % et Reax 10 %).
[7] L’étude indique que le Disperse Blue 79 utilisé dans l’essai avait une pureté (de matières organiques) de 76 % et une dispersion du colorant à 20 %.
[8] L’étude indique que le Disperse Orange 30 utilisé dans l’essai avait une pureté (de matières organiques) de 73 % et une dispersion du colorant à 20 %.
[9] Les valeurs du log Kcosont fondées sur les calculs que Baughman et Perenich (1988) ont réalisés en utilisant une plage de valeurs de solubilité mesurées pour des colorants commerciaux, à un point de fusion supposé de 200 ºC.
En raison du peu de données empiriques sur le Solvent Red 23 et de l’erreur associée aux résultats de la modélisation portant sur les colorants dispersés, certaines données empiriques sur les propriétés physiques et chimiques (tableau 2), des données sur la bioaccumulation (tableaux 5a et 5b) et des données sur la toxicité aquatique (tableau 6) ont été utilisées pour étayer la preuve et les conclusions proposées dans cette évaluation préalable. Plus précisément, des données ont été obtenues sur un colorant solvant similaire (Sudan IV/Solvent Red 24), quatre colorants dispersés diazoïques ayant une structure similaire (Disperse Orange 29, Disperse Yellow 23, Disperse Yellow 68 et Disperse Orange 13) et six colorants monoazoïques ayant une structure similaire (Disperse Blue 79, Disperse Blue 79:1, Disperse Orange 30, Disperse Red 73, Disperse Orange 25 et Disperse Red 17). Des renseignements sur l’identité de la substance et des données empiriques sur les analogues utilisés dans le présent rapport sont présentés au tableau 3a, alors que les masses moléculaires et les diamètres transversaux sont présentés au tableau 3b.
| Nom commun (n° CAS) | Nom dans la LIS | Structure | Similarités et différences majeures avec le Solvent Red 23 | Données empiriques disponibles[1] |
|---|---|---|---|---|
| Solvent Red 23 (85-86-9) |
1-[4-(Phénylazo)phénylazo]-2-naphtol | 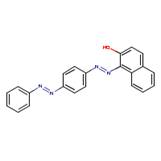 |
Sans objet (même substance). | Point de fusion |
| Sudan IV (aussi appelé Solvent Red 24) (85-83-6) |
1-({2-Méthyl-4-[(2-méthylphényl)azo]phényl}azo)-2-naphtalénol |  |
Similarités : Composé diazoïque aromatique avec un noyau napthtalène et un groupement hydroxyle. Même nombre de noyaux Différences : Deux groupements méthyle de plus – chacun attaché aux noyaux individuels. |
Point de fusion, toxicité, FBC |
| Disperse Orange 29 (19800-42-1) |
4-[[2-Méthoxy-4-[(4-nitrophényl) azo]phényl]azo)] phénol |
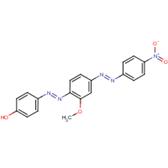 |
Similarités : Composé diazoïque aromatique avec un groupement hydroxyle. Différences : Le Solvent Red 23 contient un noyau naphtalène et ne contient pas de groupement nitro terminal ni de groupement éthers |
État physique, point de fusion, log Koe, solubilité dans l’eau, solubilité dans le n-octanol |
| Disperse Yellow 23 (6250-23-3) |
p-[[p-(Phénylazo)phényl]azo]phénol | 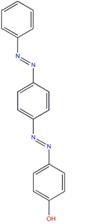 |
Similarité : Composé diazoïque aromatique avec un groupement hydroxyle Différences : Disperse Yellow 23 ne contient pas de noyau naphtalène |
Point de fusion, solubilité dans l’eau, pKa et toxicité pour les organismes aquatiques |
| Disperse Yellow 68 (21811-64-3) |
Phénol, 4,4’-[1,4-phenylenebis(azo)]bis | 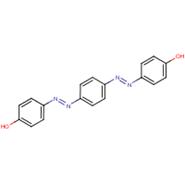 |
Similarité : Composé diazoïque aromatique avec un groupement hydroxyle Différence : Disperse Yellow 68 ne contient pas de noyau naphtalène et contient un groupement hydroxyle additionnel |
Solubilité dans l’eau |
| Disperse Orange 13 (6253-10-7) |
p-[[4-(Phénylazo)-1-naphtyl]azo]phénol | 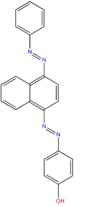 |
Similarité : Composé diazoïque aromatique avec un noyau de naphtalène et un groupement hydroxyle Différence : Disperse Orange 13 contient un noyau naphtalène dans une position différente |
Point de fusion, hydrosolu-bilité, solubilité dans l’octanol |
| Disperse Orange 25 (31482-56-1) |
3-[Éthyl[4-[(4-nitrophényl)azo] phényl]amino] propiononitrile |
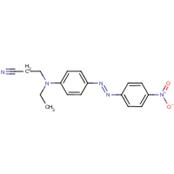 |
Similarité : Composé diazoïque aromatique. Différence : Pas de second groupement azoïque, Disperse Orange 25 contient un nitrile, un groupement nitro et amine et n’a pas de noyau naphtalène |
Toxicité pour les organismes aquatiques |
| Disperse Orange 30 (5261-31-4) |
Acétate de 2-[N-(2-cyanoéthyl)-4-[2,6-dichloro-4-nitrophényl)azo]anilino]éthyle | 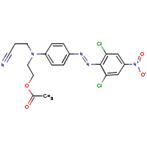 |
Similarité : Composé diazoïque aromatique. Différence : Pas de second groupement azoïque, Disperse Orange 30 contient des groupements fonctionnels nitrile, carboxylique, nitro et amine, et deux groupements chlore |
Bioaccumulation, toxicité pour les organismes aquatiques, log Koe |
| Disperse Blue 79 (12239-34-8) |
Diacétate de 2,2’-[[5-acétamide-4-[(2-bromo-4,6-dinitrophényl)azo]-2-éthoxyphényl] imino]diéthyle |
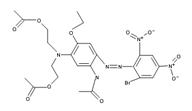 |
Similarité : Composé diazoïque aromatique. Différence : Pas de second groupement azoïque, Disperse Blue 79 contient deux groupements carboxyliques, deux groupements fonctionnels nitro, une aniline ayant deux chaînes carbonées, un groupement fonctionnel amine et un groupement brome |
Point de fusion, pression de vapeur, log Koe, solubilité dans l’eau et toxicité de cette substance pour les organismes aquatiques |
| Disperse Blue 79:1 (3618-72-2) |
Diacétate de 2,2’-{[5-acétamido-4-(2-bromo-4,6-dinitrophénylazo)-2-méthoxyphényl] imino}diéthyle |
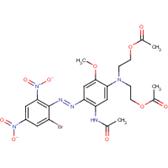 |
Similarité : Composé diazoïque aromatique. Différence : Pas de second groupement azoïque, Disperse Blue 79:1 contient deux groupements carboxylique, deux groupements fonctionnels nitro, un groupement fonctionnel amine et une aniline avec deux courtes chaînes carbonées |
Point de fusion, log Koe, solubilité dans l’eau, bioaccumu lation et toxicité de cette substance pour les organismes aquatiques |
| Disperse Red 17 (3179-89-3) |
2,2'-[[3-méthyl-4-(4-nitrophénylazo) phényl]imino] diéthanol |
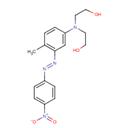 |
Similarité : Composé diazoïque aromatique avec un groupement hydroxyle. Différence : Pas de second groupement azoïque, Disperse Red 17 contient un groupement hydroxyle additionnel et une aniline avec deux courtes chaînes carbonées |
Toxicité pour les organismes aquatiques |
| Disperse Red 73 (16889-10-4) |
2-({4-[(2-Cyanoéthyl)(2-phényléthyl)amino]phényl}azo)-5-nitrobenzonitrile | 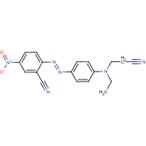 |
Similarité : Composé diazoïque aromatique. Différence : Pas de second groupement azoïque, Disperse Red 73 contient deux groupements fonctionnels nitrile, des groupements nitro et aniline et deux courtes chaînes carbonées |
Toxicité pour les organismes aquatiques |
| Substance | N° CAS | Nom commun | Masse moléculaire (g/mol) | Dmax minimum–maximum (nm)[1] |
|---|---|---|---|---|
| Colorants solvants et colorants dispersés diazoïques | 85-86-9 | Solvent Red 23 | 352 | 1,50–2,03 |
| 85-83-6 | Sudan IV | 380 | 1,50–2,05 | |
| 19800-42-1 | Disperse Orange 29 | 377 | 1,56–2,19 | |
| 6250-23-3 | Disperse Yellow 23 | 302 | 1,50–2,07 | |
| 6253-10-7 | Disperse Orange 13 | 352 | 1,56–2,07 | |
| 21811-64-3 | Disperse Yellow 68 | 318 | 2,09–2,14 | |
| Colorants monoazoïques analogues | 12239-34-8 | Disperse Blue 79 | 639 | 1,69–2,05 |
| 3618-72-2 | Disperse Blue 79:1 | 625 | 1,43–2,03 | |
| 5261-31-4 | Disperse Orange 30 | 450 | 1,75–1,98 | |
| 16889-10-4 | Disperse Red 73 | 348 | 1,31–1,93 | |
| 31482-56-1 | Disperse Orange 25 | 323 | 1,37–1,95 | |
| 3179-89-3 | Disperse Red 17 | 344 | 1,41–1,86 |
Il faut noter qu’il existe plusieurs incertitudes associées à l’utilisation des données physiques, chimiques, toxicologiques et de bioaccumulation disponibles pour les substances. Toutes ces substances partagent le même groupe chimique, soit les composés azoïques (un sous-ensemble contient deux liaisons azoïques et un autre contient une liaison azoïque) – et sont utilisées à des fins industrielles similaires (c.-à-d. les colorants dispersés et un colorant solvant). Toutefois, ces substances présentent des différences liées à leur groupement fonctionnel propre (voir le tableau 3a). Malgré le fait que certains de ces colorants monoazoïques ont des masses moléculaires plus élevées que les colorants diazoïques, leur état physique, leurs points de fusion, leur solubilité dans l’eau, leur log Koe et leurs diamètres transversaux (tableau 3b) comparables offrent un fondement raisonnable permettant de conclure que les colorants monoazoïques auront un comportement similaire à celui des colorants diazoïques dans l’environnement et présenteront une biodisponibilité à peu près égale, et que leur utilisation comme analogues pour le Solvent Red 23 est donc acceptable.
Le Solvent Red 23 n’est pas produit naturellement dans l’environnement.
Des enquêtes menées récemment auprès de l’industrie en 2005 et 2006 par le truchement d’avis publiés dans laGazette du Canada conformément à l’article 71 de la LCPE (1999), ont permis de recueillir des renseignements récents (Canada, 2006b et 2008b). Ces avis demandaient que soient fournies des données sur la fabrication, l’importation et l’utilisation de Solvent Red 23 au Canada. Dans l’avis pour 2006, des données étaient également demandées sur les quantités utilisées de ce colorant. Dans le contexte de l’enquête susmentionnée pour 2005 et 2006, les entreprises qui n’étaient pas tenues de fournir des données selon les critères établis, mais qui avaient un intérêt commercial se rapportant au Solvent Red 23 ont été invitées à s’identifier en tant que parties intéressées.
Bien qu’elles ne répondent pas aux exigences obligatoires de déclaration, neuf entreprises ont manifesté un intérêt pour le Solvent Red 23 à l’aide du formulaire Déclaration des parties intéressées relatif à l’avis émis en application de l’article 71 pour 2006 (Environnement Canada, 2008a). Dans plus d’un cas, l’intérêt concernait l’importation ou l’utilisation courante de la substance au Canada en deçà du seuil. En 2005, quatre entreprises ont chacune déclaré avoir importé entre 100 et 1 000 kg de Solvent Red 23 (Environnement Canada, 2006). En 2005, huit entreprises ont déclaré avoir un intérêt en tant que partie intéressée pour le Solvent Red 23 (Environnement Canada, 2006).
Pendant l’élaboration de la Liste intérieure des substances (LIS), la quantité de Solvent Red 23 déclarée avoir été fabriquée, importée ou commercialisée en 1986 était de 2 200 kg (Environnement Canada, 1988).
Le Solvent Red 23 a été reconnu comme une substance chimique produite en faible quantité dans l’Union européenne (UE). Sa production au sein de l’Union européenne a été estimée entre 10 et 1 000 tonnes par an, environ (ESIS, 2008). Le Solvent Red 23 a également été utilisé en Suède de 1999 à 2006 et au Danemark de 2003 à 2006 (SPIN, 2008).
Les produits contenant du Solvent Red 23 peuvent entrer dans le pays même s’ils n’ont pas été recensés en tant que tels dans l’enquête menée en vertu de l’article 71, en raison de leur importation involontaire dans les articles manufacturés ou de leurs quantités inférieures au seuil de déclaration de 100 kg établi pour l’enquête.
Des renseignements relatifs aux utilisations pour les années civiles 2005 et 2006 ont été recueillis en réponse aux avis publiés en application de l’article 71 de la LCPE (1999) (Canada, 2006b, 2008b). En 2005, les importateurs du Solvent Red 23 ont indiqué qu’ils faisaient le commerce de détail de cosmétiques, de parfums, d’articles de toilette et de produits d’hygiène personnelle ou offraient des services de coiffure ou d’esthétique (Environnement Canada, 2006). En 2006, aucune des entreprises ayant déclaré qu’elles importaient ou utilisaient le Solvent Red 23 dans la Déclaration des parties intéressées n’a indiqué le type d’utilisation (Environnement Canada, 2008a). Au cours du processus d’inscription des substances sur la LIS (de 1984 à 1986), le code d’utilisation de la LIS pour les catégories « colorant / pigment / teinture / encre », « parfum / désodorisant / aromatisant », « cosmétiques », « santé et vétérinaire », « produits pharmaceutiques », « pigment, teinture et encre d’imprimerie » et « textile, produits » ont été employés pour le Solvent Red 23.
Le Solvent Red 23 est actuellement utilisé dans les cosmétiques de plusieurs pays dont le Canada, les États-Unis et l’Europe. Au Canada, le Solvent Red 23 figure dans la base de données du Système de déclaration des cosmétiques (SDC) de Santé Canada dans environ 300 cosmétiques et produits de soins personnels sous les noms « Solvent Red 23 », « D&C Red n° 17 » ou « CI 26100 » (SDC, 2009).
Le Solvent Red 23 est mentionné dans le Règlement sur les aliments et drogues à l’article C.01.040.2(4)(a) à titre de colorant autorisé dans les médicaments à usage externe sous le nom de Toney Red (D&C Red n° 17; C.I. n° 26100) (Canada, 1978). Le Solvent Red 23 figure également dans la base de données des ingrédients non médicinaux de la Direction des produits thérapeutiques à titre de colorant présent dans un désinfectant liquide utilisé dans les hôpitaux sur les lieux où de la nourriture est fabriquée, préparée ou conservée, mais il n’a pas été déclaré présent dans les médicaments pharmaceutiques ou vétérinaires (courriel de 2008 de la Direction des produits thérapeutiques de Santé Canada adressé au Bureau de gestion des risques; source non citée). Cette substance est également mentionnée dans la base de données sur les ingrédients des produits de santé naturels (BDIPSN) à titre d’ingrédient non médicinal autorisé utilise comme colorant pour les usages externes seulement (BDIPSN, 2010). Le Solvent Red 23 figure dans la Base de données des produits de santé naturels homologués; il est donc présent dans les produits de santé naturels homologués (BDPSNH, 2010). Bien que la présence de Solvent Red 23 dans les épices ait déjà été signalée, cette substance n’est pas un colorant alimentaire autorisé dans l’Union européenne, aux États-Unis ou au Canada (Union européenne, 1994; USFDA, 2007; Santé Canada, 2007). Le Solvent Red 23 ne figure pas parmi les additifs alimentaires autorisés en vertu du Règlement sur les aliments et drogues et n’est pas utilisé à des fins d’emballage alimentaire (Santé Canada, 2007).
Dans d’autres pays, le Solvent Red 23 est actuellement utilisé dans les cosmétiques et les médicaments. Cette substance est actuellement approuvée aux États-Unis sous le nom de D&C Red n° 17 pour être utilisée comme colorant dans des médicaments et cosmétiques à usage externe et dans les verres de contact (USFDA, 2009). En Europe, l’usage du Solvent Red 23 (appelé CI 26100) est également approuvé comme colorant dans les cosmétiques qui n’entrent pas en contact avec les membranes des muqueuses (Directive sur les cosmétiques, annexe IV). Le Solvent Red 23 a été retrouvé dans les teintures capillaires, mais cette utilisation est actuellement interdite en Europe (Directive sur les cosmétiques, annexe II) (Commission européenne, 2010).
Le Solvent Red 23 est inscrit au Canada comme produit de formulation dans les insecticides/herbicides (courriel de 2009 de l’ARLA adressé au Bureau de gestion des risques des substances existantes, Santé Canada; source non citée) et figure également sur la liste des ingrédients inertes autorisés dans les produits antiparasitaires appliqués sur des sites à usage non alimentaire comme les plantes ornementales et les emprises routières aux États-Unis (USEPA, 2008).
Les autres utilisations possibles du Solvent Red 23 comprennent les colorants biologiques (O’Neil, 2006; ProSciTech, 2006), les huiles, les gras, les cires et les matières plastiques (CII 2002-).
De plus, le règlement REACH (Registration,Evaluation, Authorisation and Restriction of Chemical substances, c.à-d. enregistrement, évaluation, autorisation et restrictions relatifs aux substances chimiques) de la Commission européenne (Commission européenne, 2006), particulièrement au point 43 de l’annexe XVII, restreint certains « colorants azoïques et teintures azoïques » dans certains textiles pouvant libérer l’un des 22 amines aromatiques par rupture des liaisons azoïques. En théorie, le Solvent Red 23 subit une rupture réductrice de ses liaisons azoïques, ce qui forme l’une des 22 amines aromatiques dérivées (c.-à-d. le 4-aminoazobenzène, n° CAS 60-09-3), mais, d’après les données disponibles, le profil d’utilisation actuel de cette substance n’indique pas qu’elle est présente dans les produits textiles et de cuir.
Dans le cas du Solvent Red 23, l’analyse du cycle de vie n’était pas applicable à cause de l’insuffisance des données. Toutefois, étant donné le profil d’utilisation de la substance dans les produits de soins personnels, on peut penser que tous les produits contenant du Solvent Red 23 pourraient être rejetés dans les égouts, les eaux de surface ou le sol au cours de leur utilisation. Une fois dans les eaux de surface ou les égouts, en raison de ses propriétés physiques et chimiques, le Solvent Red 23 devrait se lier aux sédiments dans les milieux aquatiques et aux boues dans les stations de traitement des eaux usées.
D’après ce qui précède, l’eau des égouts est le milieu qui reçoit la plus grande proportion de Solvent Red 23 rejeté pendant l’utilisation du produit. On prévoit que la majeure partie de la substance, fixée aux boues d’épuration à la suite de rejets aux égouts de produits de soins personnels aux usines de traitement des eaux usées, sera entraînée dans les sites d’enfouissement (décharges). En plus d’être mis en décharge, une partie des biosolides produits par les stations de traitement des eaux usées peuvent être épandus sur des terres en tant qu’engrais ou amendement synthétique à des fins agricoles, forestières ou de remise en état, et un petit pourcentage peut être incinéré.
Le Solvent Red 23 devrait être rejeté dans les effluents d’eaux usées par suite de traitements industriels et d’utilisations associées à des rejets dans les égouts. D’après la valeur élevée du log Koe déterminée par analogie (4,6) et les valeurs du log Kco (3,4 à 4,2) [voir le tableau 2], cette substance pourrait avoir une affinité pour les matières solides. Toutefois, les valeurs du log Kco sont calculées et non strictement expérimentales (voir la note 3 du tableau 2), et le potentiel d’adsorption des structures des colorants particulaires dispersés n’est généralement pas bien compris; par conséquent, l’importance de ce comportement particulier est incertaine.
Selon les modèles de biodégradation aérobie, il est attendu que la biodégradation du Solvent Red 23 soit lente (voir le tableau 4 ci-dessous). Cette substance peut être épandue comme engrais ou amendement synthétique à des fins agricoles, forestières et de remise en état, sous forme de composante de biosolides. Le Solvent Red 23 utilisé comme formulant de pesticide peut être déposé directement sur les sols.
Étant donné une valeur expérimentale du pKa de 8,1 pour l’analogue Disperse Yellow 23 et une valeur estimée de 13,5 pour le Solvent Red 23 (tableau 2), on peut s’attendre à ce que cette substance chimique se comporte comme un acide faible et soit partiellement ionisée dans l’eau aux valeurs élevées de la gamme normale du pH dans l’environnement (8 à 9). Toutefois, en raison de la faible solubilité dans l’eau attendue pour le Solvent Red 23 (tableau 2) et de son état particulaire, il est peu probable que l’ionisation à un pH élevé influe significativement sur la répartition de cette substance dans l’environnement ou sur sa solubilité dans l’eau. De ce fait, lorsqu’elle est rejetée dans l’eau, cette substance devrait se retrouver principalement sous forme solide ou être adsorbée sur les particules en suspension pour enfin se déposer sur les matériaux du lit où elle devrait demeurer sous une forme qui n’est relativement pas biodisponible. On affirme généralement que les colorants azoïques finissent par se retrouver dans des sédiments anaérobies, dans des aquifères et dans l’eau souterraine en raison de leur nature récalcitrante dans les milieux aérobies (Razo-Flores et al., 1997). Toutefois, puisque le Solvent Red 23 a une faible solubilité dans l’eau et une valeur de Kco relativement élevée, il est peu probable qu’il ne se lixivie à partir des sédiments et des sols.
La vitesse de volatilisation à partir de la surface de l’eau est proportionnelle à la constante de la loi de Henry (Baughman et Perenich, 1988). Baughman et Perenich (1988) mentionnent également que la volatilisation à partir de systèmes aquatiques devrait être un processus de perte peu important pour les colorants dispersés dont la valeur de la constante de la loi de Henry pour les analogues est de faible à négligeable (10-8 à 10-1 Pa·m3/mol, tableau 2). Le transport dans l’air qui résulte de la perte de cette substance des sols superficiels humides et secs n’est pas très important pour cette substance comme l’indiquent les très faibles pressions de vapeur obtenues par analogie (5,33 x (10-12 à 10-5) Pa; tableau 2). Ces données sont compatibles avec l’état physique (particule solide) des colorants diazoïques qui les rend peu sujets à la volatilisation. La valeur expérimentale de la pression de vapeur du Disperse Orange 13 n’est pas un indicateur utile de la volatilisation du Solvent Red 23 étant donné qu’elle a été obtenue à une température élevée.
Persistance dans l’environnement
Les colorants doivent avoir un haut degré de stabilité chimique et photolytique pour être utiles; c’est pourquoi la plupart d’entre eux sont généralement considérés comme non dégradables dans les conditions aérobies observées dans l’environnement (EPA du Danemark, 1999; ETAD, 1995). Des études appliquant des analyses de dépistage généralement reconnues (p. ex., les lignes directrices de l’OCDE) de la biodégradabilité rapide et intrinsèque ont confirmé ce fait (ETAD, 1992; Pagga et Brown, 1986). La dégradation abiotique, qui comprend la photolyse et l’hydrolyse, n’est pas réputée jouer un rôle important dans le devenir des colorants azoïques dans l’environnement (EPA du Danemark, 1999), même si une étude a montré une décomposition photolytique fortement accélérée de colorants azoïques en présence de matière humique naturelle (Brown et Anliker, 1988).
La dégradation biotique des colorants azoïques peut être relativement rapide en conditions anaérobies ou réductives (Baughman et Weber, 1994; EPA du Danemark, 1999; ETAD, 1995; Isik et Sponza, 2004; Yen et al., 1999). Il a été déterminé que la perméabilité de la paroi cellulaire des bactéries constitue l’étape limitante du processus de réduction (EPA du Danemark, 1999). Les colorants azoïques ont une forte tendance à la rupture de leur liaison azoïque avec la formation d’amines aromatiques (EPA du Danemark, 1999; Hunger, 2005). Le potentiel cancérogène des amines aromatiques varie considérablement en fonction de la structure moléculaire, les produits de dégradation cancérogènes étant associés aux groupements fonctionnels benzidine, aniline, toluène ou naphtalène. Toutefois, la formation de tels métabolites dans des sédiments anoxiques profonds n’entraînerait normalement pas l’exposition des organismes aquatiques. La minéralisation totale ou la dégradation avancée des métabolites pourrait avoir lieu si ces derniers sont transférés (p. ex. par resuspension des sédiments) dans des milieux aérobies (EPA du Danemark, 1999; Isik et Sponza, 2004). Des amines aromatiques peuvent également être présentes sous forme d’impuretés dans des colorants azoïque disponibles sur le marché, et ce, même si la principale source de ces composés est la rupture des liaisons azoïques des colorants lors du métabolime (EPA du Danemark, 1999).
Une étude sur la bioélimination dans l’eau présentée pour l’analogue Disperse Yellow 23 indique que cette substance subit une dégradation de 51 % en 14 jours (étude présentée, 2008b). Toutefois, cette valeur expérimentale n’a pas pu être utilisée pour soutenir l’évaluation de la persistance du Solvent Red 23, car l’étude a été considérée peu fiable en raison du manque de renseignements sur les conditions expérimentales (voir le sommaire de rigueur d’étude à l’annexe 1). Outre cette étude, aucune autre donnée expérimentale ou obtenue par analogie sur la dégradation du Solvent Red 23 ou ses analogues n’a été relevée. Aucune donnée de surveillance environnementale n’ayant trait à la présence de ces colorants dans l’environnement canadien (air, eau, sol et sédiments) n’a été relevée.
Comme on s’attend à ce que le Solvent Red 23 à titre de colorant soit rejeté dans les eaux usées, sa persistance a surtout été examinée à l’aide de modèles de prévision RQSA sur la biodégradation aérobie dans l’eau. Ces modèles sont jugés acceptables pour utiliser dans cette situation puisqu’ils sont fondés sur la structure chimique et que la structure diazoïque est représentée dans les ensembles d’apprentissage de tous les modèles BIOWIN utilisés, ce qui augmente la fiabilité des prévisions (Environnement Canada, 2007). L’analyse suivante concerne principalement la partie de cette substance actuellement dissoute dans l’environnement, tout en tenant compte du fait qu’il est probable qu’une grande partie de cette substance est dispersée sous la forme de particules solides. Le Solvent Red 23 et ses analogues ne contiennent pas de groupements fonctionnels susceptibles d’entreprendre une hydrolyse dans un milieu aérobie (les colorants sont connus pour être stables dans les milieux aqueux). Le tableau 4 résume les résultats des modèles RQSA disponibles sur la biodégradation aérobie dans l’eau.
| Processus du devenir | Modèle et base du modèle |
Résultat et prévision du modèle | Demi-vie extrapolée (jours) |
|---|---|---|---|
| Biodégradation (aérobie) | BIOWIN, 2008 Sous-modèle 4 : enquête d’expert (résultats qualitatifs) |
3,3[2] « se biodégrade lentement » |
≥ 182 |
| Processus du devenir | Modèle et base du modèle |
Résultat et prévision du modèle | Demi-vie extrapolée (jours) |
|---|---|---|---|
| Biodégradation (aérobie) | BIOWIN, 2008[1] Sous-modèle 3 : enquête d’expert (résultats qualitatifs) |
1,90[2] « se biodégrade très lentement » |
≥ 182 |
| Biodégradation (aérobie) | BIOWIN, 2008[1] Sous-modèle 5 : Probabilité linéaire MITI |
-0,24[3] « se biodégrade très lentement » |
≥ 182 |
| Biodégradation (aérobie) | BIOWIN, 2008[1] Sous-modèle 6 : Probabilité non linéaire MITI |
0[3] « se biodégrade lentement » |
≥ 182 |
| Biodégradation (aérobie) | TOPKAT, 2004 Probabilité |
s. o.[4] « se biodégrade lentement » |
≥ 182 |
| Biodégradation (aérobie) | CATABOL 2004-2008 % DBO[5] (demande biochimique en oxygène) |
% DBO = 0 « se biodégrade très lentement » |
≥ 182 |
[2] Le résultat s’exprime par une valeur numérique de 0 à 5.
[3] Le résultat s’exprime par un taux de probabilité.
[4] s. o. : sans objet (hors des champs d’application du modèle).
[5] DBO : demande biologique en oxygène.
Comme le montre le tableau 4, tous les modèles de biodégradation (BIOWIN 3, 5, 6 et CATABOL) portent à croire que la biodégradation du Solvent Red 23 se fait lentement de manière aérobie dans l’eau. En fait, les résultats de probabilité de BIOWIN 5 et 6 sont bien inférieurs à 0,3, ce qui est la limite suggérée par Aronson et al., (2006) pour trouver les substances qui ont une demi-vie de plus de 60 jours (selon les modèles de probabilité du MITI). En outre, les deux autres modèles de la dégradation ultime, BIOWIN 3 et CATABOL, prévoient que le Solvent Red 23 sera persistant dans l’eau. TOPKAT (2004) prévoit également une biodégradation lente, mais le résultat du modèle n’est pas fiable, car la structure se trouve en dehors du domaine d’applicabilité du modèle.
Lorsque les résultats de probabilité et les autres modèles de dégradation ultime sont pris en compte, il y a un important consensus qui suggère que la demi-vie de la biodégradation ultime dans l’eau est supérieure à 182 jours. Ce résultat correspond à ce qu’on s’attend de cette structure chimique (c.-à-d., peu de groupements fonctionnels dégradables, particules solides peu solubles).
Selon un ratio d’extrapolation de 1:1:4 pour la demi-vie associée à la biodégradation dans l’eau, le sol, les sédiments (Boethling et al., 1995), la demi-vie de biodégradation ultime dans le sol aérobie est égale ou supérieure à 182 jours, et la demi-vie dans les sédiments aérobie est égale ou supérieure à 365 jours. Ces résultats indiquent que le Solvent Red 23 devrait être persistant dans le sol et les sédiments.
D’après les données modélisées sur la dégradation ultime (tableau 4) et l’avis d’expert (EPA du Danemark, 1999; ETAD, 1995), le Solvent Red 23 répond aux critères de persistance dans l’eau, le sol (demi-vies dans le sol et dans l’eau en conditions aérobies ≥ 182 jours), les sédiments (demi-vie dans les sédiments en conditions aérobies de ≥ 365 jours) énoncés dans le Règlement sur la persistance et la bioaccumulation (Canada, 2000).
Potentiel de bioaccumulation
On ne dispose pas de données expérimentales sur la bioaccumulation du Solvent Red 23. Comme il est connu que les modèles de la bioaccumulation s’appliquent mal aux pigments et aux colorants, leurs prévisions ne sont pas considérées comme fiables pour les colorants diazoïques. La modélisation de la bioaccumulation n’a donc pas été employée pour évaluer le potentiel de bioaccumulation de ces substances.
Vu l’absence de données expérimentales et modélisées, les facteurs de bioconcentration (FBC) et de bioaccumulation (FBA) d’analogues structuraux, calculés à partir de données empiriques, ont été utilisés pour estimer le potentiel de bioaccumulation du Solvent Red 23. D’après des études présentées sur la bioconcentration des analogues structuraux relativement proches Sudan IV (MITI, 1992) et Disperse Orange 30 (Shen et Hu, 2008), l’accumulation du Solvent Red 23 dans les poissons serait peu probable.
Dans le cadre de l’essai effectué par le ministère du Commerce international et de l’industrie du Japon (MITI) avec le Solvent Red 23 (tableau 5a) sur des carpes, les facteurs de bioconcentration obtenus étaient faibles, soit inférieurs à 11 L/kg.
| Organisme d’essai | Concentration expérimentale (mg/L) et/ou source d’exposition | Paramètre (FBC, L/kg) | Référence |
|---|---|---|---|
| Carpe (Cyprinus carpio) |
0,35 | < 0,29-2,9 | MITI, 1992 |
| Carpe (Cyprinus carpio) |
0,035 | < 2,9-11 | MITI, 1992 |
Cet essai de bioconcentration de Shen et Hu (2008) a été réalisé conformément aux Directives de l’OCDE (OECD, 1996). La bioconcentration du Disperse Orange 30 chez le poisson zèbre (Brachydanio rerio) a été déterminée par un test semi-statique sur 28 jours, avec renouvellement du milieu de test tous les deux jours. Afin de vérifier le potentiel de bioconcentration de la substance d’essai, un essai en phase d’exposition à une concentration nominale de 20 mg/L (concentration moyenne mesurée entre 0,028 et 0,28 mg/L approximativement) a été mené en tenant compte du résultat obtenu lors de l’essai de toxicité aiguë pour le poisson. Des échantillons des deux solutions de test et des organismes d’essai ont été pris du 26e jour au 28ejour de la période de test d’exposition sur 28 jours. Les échantillons ont été préparés en extrayant le composant lipidique des poissons testés. La concentration mesurée de la substance d’essai, la teneur en lipides dans le poisson et le facteur de bioconcentration (FBC) figurent au tableau 5b.
| Traitements (20 mg/L) | Durée d’échantillonnage | ||
|---|---|---|---|
| 26e jour | 27e jour | 28e jour | |
| Concentration mesurée de la substance d’essai dans les solutions extraites (mg/L) | < 0,028 | < 0,028 | < 0,028 |
| Contenu de la substance test dans les lipides du poisson (mg) | < 1,68 | < 1,68 | < 1,68 |
| Poids total des poissons (g) | 2,07 | 2,13 | 2,53 |
| Concentration de la substance d’essai dans les poissons Cp (mg/kg) | < 0,81 | < 0,79 | < 0,66 |
| Concentration mesurée de la substance test dans le Ce de l’eau (mg/L) | 0,028 - 0,28 | 0,028 - 0,28 | 0,028 - 0,28 |
| Contenu lipidique du poisson (%) | 0,81 | 0,57 | 1,25 |
| FBC | < 100 | < 100 | < 100 |
| FBC moyen | < 100 | ||
L’étude de Shen et Hu (2008) a été révisée et considérée comme acceptable (voir l’annexe 1). Le niveau de détection très faible dans les extraits de poisson (< 0,028 mg/L) indiquerait une solubilité limitée dans les lipides ou un potentiel limité de répartition dans les tissus des poissons des systèmes aqueux. Toutefois, il existe une incertitude associée aux valeurs limites dans toute étude, car la « vraie » valeur n’est pas connue. Par contre, étant donné la structure et le comportement probable des colorants dispersés dans les systèmes aqueux, le faible résultat obtenu pour le FBC n’est pas inattendu. La plupart des colorants dispersés, ainsi que leur nom le laisse entendre, se présentent sous la forme de fines particules dispersibles avec des fractions réellement solubles limitées. Leur solubilité peut, toutefois, être augmentée en ajoutant à la molécule des groupements fonctionnels polarisés. Or, même si le Solvent Red 23 et ses analogues pertinents (tableau 2) comprennent certains groupements fonctionnels solubilisants (groupements phénols), les valeurs expérimentales disponibles sur la solubilité de cette substance et de ses analogues pertinents (qui varient de 0,000 06 à 0,345 mg/L) sont relativement faibles, soit inférieures ou comparables par moins d’un ordre de grandeur, à la solubilité dans l’eau du Disperse Orange30 (c.-à-d. 0,07 mg/L). Par conséquent, le Solvent Red 23 devrait avoir une biodisponibilité et un potentiel de bioconcentration similaires ou inférieurs à ceux du Disperse Orange 30.
Les études susmentionnées constituent un élément de preuve de première importance permettant de croire que le Solvent Red 23 ne serait pas bioaccumulable, et d’autres recherches viennent appuyer également cette conclusion. Anlikeret al., (1981) présentent des valeurs expérimentales sur la bioaccumulation dans les poissons pour 18 colorants monoazoïques dispersés, valeurs obtenues suivant les méthodes prescrites par le MITI. Le log des facteurs de bioaccumulation (FBC) variait entre 0,00 et 1,76 et est exprimé en fonction du poids humide total des poissons (Anliker et al., 1981). L’absence d’information sur les numéros de registre et la structure chimique précise des substances limite toutefois l’utilité de cette étude pour des déductions par analogie au sujet du Solvent Red 23. Néanmoins, des études complémentaires fournissant des précisions sur la structure chimique des colorants dispersés testés ont confirmé le faible potentiel de bioaccumulation de dix colorants azoïques nitrosubstitués pour lesquels les valeurs déterminées du log du facteur de bioaccumulation varient de 0,3 à 1,76 (Anliker et Moser, 1987; Anliker et al., 1988). Des études du MITI viennent également appuyer le faible potentiel de bioaccumulation des colorants azoïques dispersés. Les FBC publiés pour trois colorants azoïques dispersés (nos CAS 40690-89-9, 61968-52-3 et 71767-67-4) testés à une concentration de 0,01 mg/L varient de moins de 0,3 à 47 L/kg (MITI, 1992). Une étude sur l’accumulation d’une durée de huit semaines réalisée par Brown (1987) montre également qu’aucun des douze colorants dispersés ayant été testés ne s’accumulait chez la carpe.
Les valeurs élevées du log Koe déduites à partir d’analogues azoïques apparentés (tableau 2) sont les seules données indiquant que le Solvent Red 23 pourrait avoir un potentiel élevé de bioaccumulation. Malgré ces valeurs élevées du log Koe, la preuve de la bioaccumulation des colorants azoïques dispersés est insuffisante (Anliker et al., 1981; Anliker et Moser, 1987, MITI, 1992. 1988, MITI, 1992) Selon les auteurs qui ont mesuré des valeurs élevées du log Koe et de faibles facteurs de bioaccumulation concomitants pour les colorants azoïques dispersés, les facteurs d’accumulation faibles pourraient s’expliquer, dans certains cas, par leur faible liposolubilité absolue (Brown, 1987) ou leur poids moléculaire relativement élevé, ce qui pourrait rendre difficile le transport de ces substances à travers les membranes des poissons (Anliker et al., 1981; Anliker et Moser, 1987). Il se peut aussi que le manque de biodisponibilité et le comportement de répartition limité imposés par les conditions d’essai sur le FBC restreignent l’accumulation dans les tissus lipidiques des poissons.
De récentes études liées aux données sur le FBC chez les poissons et aux paramètres de la taille moléculaire (Dimitrovet al., (2002, 2005) laissent entendre que la probabilité qu’une molécule traverse des membranes cellulaires à la suite d’une diffusion passive diminue de façon importante avec l’augmentation du diamètre maximal (Dmax). La probabilité qu’une diffusion passive se produise diminue de façon notable lorsque le diamètre maximal est supérieur à environ 1,5 nm et diminue de façon encore plus significative dans le cas des molécules ayant un diamètre maximal supérieur à 1,7 nm. Sakuratani et al., (2008) ont également étudié l’effet du diamètre transversal sur la diffusion passive à l’aide d’un ensemble d’essais du FBC comptant environ 1 200 substances chimiques nouvelles et existantes. Ils ont observé que les substances qui n’ont pas un potentiel de bioconcentration très élevé (FBC < 5 000) ont souvent un Dmaxsupérieur à 2,0 nm et un diamètre effectif (Deff) supérieur à 1,1 nm.
Cependant, comme l’ont évoqué Arnot et al., (2010), il existe des incertitudes quant aux seuils proposés par Dimitrov et al. (2002, 2005) et Sakuratani et al. (2008), étant donné que les études sur le FBC utilisées pour calculer ces seuils n’ont pas fait l’objet d’évaluations critiques. Arnotet al. (2010), la taille moléculaire a un effet sur la solubilité et la capacité de diffusion dans l’eau et dans les phases organiques (membranes), et les plus grosses molécules peuvent avoir un taux d’absorption plus lent. Toutefois, ces mêmes contraintes liées aux facteurs cinétiques s’appliquent aux voies de diffusion de l’élimination chimique (c.-à-d., absorption lente = élimination lente). Un potentiel de bioaccumulation important peut donc s’appliquer aux substances qui sont soumises à un processus d’absorption lent, si elles sont biotransformées ou éliminées lentement par d’autres processus. Par conséquent, lorsqu’on évalue le potentiel de bioaccumulation, les données sur la taille moléculaire doivent être utilisées avec discernement et de pair avec des éléments de preuve pertinents dans le cadre d’une méthode du poids de la preuve.
Le Solvent Red 23 et ses analogues les plus proches (les colorants diazoïques) ont des poids moléculaires variant de 302 à 377 g/mol (voir le tableau 3b) et des structures moléculaires relativement peu compliquées; ces deux caractéristiques indiquent une capacité de bioaccumulation si le poids moléculaire est le seul indicateur utilisé. En revanche, Arnot et al. (2010) indiquent qu’il n’y a pas de rapports nets qui permettraient de fixer une valeur de taille moléculaire de démarcation pour l’évaluation du potentiel de bioaccumulation. Ce rapport ne met toutefois pas en cause la notion selon laquelle la réduction du taux d’absorption pourrait être associée à l’augmentation du diamètre transversal, comme cela a été démontré par Dimitrovet al. (2002, 2005). Le diamètre maximal du Solvent Red 23, de ses analogues les plus proches et de leurs conformères varie de 1,5 à 2,2 nm (BBM, 2008), ce qui indiquerait une possibilité de réduction significative de l’absorption à partir de l’eau et de la biodisponibilité in vivo pour ces colorants.
Étant donné l’absence d’accumulation observée dans les études sur la bioconcentration du Sudan IV, du Disperse Orange 30 et d’autres colorants azoïques dispersés apparentés ayant donné des résultats semblables, et compte tenu du grand diamètre transversal du Solvent Red 23 et de ses analogues qui restreint vraisemblablement leur comportement de partage, le Solvent Red 23 devrait présenter un faible potentiel de bioaccumulation. Par conséquent, en considérant les données disponibles, le Solvent Red 23 ne répond pas aux critères de bioaccumulation (FBC ou FBA ≥ 5 000) du Règlement sur la persistance et la bioaccumulation (Canada, 2000).
Évaluation des effets écologiques
A – Dans le milieu aquatique
Aucune étude sur la toxicité du Solvent Red 23 n’a été présentée. Toutefois, des données déduites à partir d’analogues ont été présentées pour plusieurs analogues du Solvent Red 23, dont le Disperse Yellow 23 et le Disperse Orange 29 (étude présentée, 2008a, 2000b). Elles indiquent que le Sudan IV a une CL50 sur 48 h de plus de 100 mg/L chez le médaka (Oryzias latipes), que le Disperse Yellow 23 a une CL50 sur 48 h de plus de 1 000 mg/L chez la truite arc-en-ciel (Oncorhynchus mykiss) et que le Disperse Orange 29 a une CL50 sur 96 h de 480 mg/L chez le poisson-zèbre (Brachydanio rerio) (tableau 6). Le Disperse Orange 29 a également une CE50 après 72 h de 6 mg/L pour l’algue Scenedesmus subspicatus et une CE50 après 48 h de 70 mg/L pour Daphnia magna. La fiabilité de ces études est toutefois considérée comme incertaine en raison de l’absence de certains détails sur leur réalisation (voir l’annexe 1). Néanmoins, il a été jugé que leurs données pouvaient être utilisées dans cette évaluation préalable aux fins de l’établissement du poids de la preuve.
Une étude présentée pour le compte de l’ETAD fournit des données écotoxicologiques aiguës pour les poissons, les invertébrés, les algues et les bactéries pour cinq colorants dispersés azoïques nitrosubstitués (Brown, 1992). La toxicité aiguë chez les poissons-zèbres, Daphnia magna etScenedesmus subspicatus, pour les cinq analogues variait de 17 à 710 mg/L, 4,5 à 110 mg/L et 6,7 à 54 mg/L, respectivement (tableau 6). De plus, tous les essais à l’aide de bactéries avaient une CI50 dépassant 100 mg/L. Le protocole expérimental détaillé de l’étude portant sur les colorants testés n’a pas été fourni, ce qui restreint grandement l’évaluation de ces études (Brown, 1992). Toutefois, on a jugé que ces données pouvaient être utilisées et elles sont comprises dans cette ébauche d’évaluation préalable en tant qu’élément du poids de la preuve.
Une autre étude de la toxicité aiguë d’un poisson a été présentée pour l’analogue Disperse Blue 79 (BASF, 1990). Elle a indiqué une CL50 après 96 h entre 100 et 220 mg/L pour l’ide dorée (tableau 6). Toutefois, sa fiabilité est aussi considérée comme incertaine en raison de l’absence de détails (annexe 1). On présente également dans le tableau 6 les résultats d’une étude sur la toxicité de l’analogue Sudan IV chez les poissons, soit une valeur dépassant 100 mg/L (MITI, 1992), pour contribuer au poids de la preuve; cette valeur n’est cependant pas la valeur critique puisque le paramètre n’a pas d’intervalle fini de valeurs.
Des données écotoxicologiques sur un autre colorant azoïque dispersé ont été reçues en vertu du Règlement sur les renseignements concernant les substances nouvelles(Environnement Canada, 1995). Une étude de la toxicité aiguë d’un poisson soumise afin de satisfaire les exigences en matière de déclaration a révélé que cette substance à une CL50 de 505 mg/L dans la truite arc-en-ciel après 96 heures (tableau 6). Cet essai a été mené en conformité avec les lignes directrices de l’OCDE n° 203. La fiche signalétique fournie avec cette déclaration contient également des renseignements sur les effets toxiques chez les bactéries. Les résultats indiquent une CE50 supérieure à 1 000 mg/L pour l’inhibition de la respiration de boues activées. À la lumière des données disponibles sur l’écotoxicité, les effets toxiques de la nouvelle substance pour les organismes aquatiques ont été considérés comme peu préoccupants. La fiabilité de cet essai a été évaluée à l’aide d’un sommaire de rigueur d’études et elle est jugée satisfaisante (annexe 1).
Enfin, une étude présentée sur la toxicité chronique de l’analogue Disperse Blue 79:1 a indiqué une concentration sans effet observé (CSEO) de 122 jours supérieure à 0,0048 mg/L chez la truite arc-en-ciel (tableau 6). Cette étude a été évaluée et jugée très fiable (annexe 1). Toutefois, comme la valeur susmentionnée est un résultat non lié (seuil d’effet incertain), elle n’a pas été utilisée pour calculer la concentration estimée sans effet).
À la lumière de toute l’information sur la toxicité des analogues structuraux et compte tenu des données sur la toxicité du Disperse Yellow 23 et du Disperse Orange 29, il y a lieu de croire que le Solvent Red 23 n’est pas très dangereux pour les organismes aquatiques (valeurs de la CL50 aiguë supérieures à 1 mg/L).
| Nom usuel ou n° CAS | Organisme d’essai | Gravité (durée) | Paramètre | Valeur (mg/L) | Référence |
|---|---|---|---|---|---|
| Sudan IV (85-83-6) |
Oryzias latipes | Aiguë ( 48 heures) |
CL50[1] | > 100 | MITI, 1992 |
| Disperse Orange 29 (19800-42-1) | Algues | Chronique (72 heures) |
CE50[2] | 6 | Étude présentée, 2008a |
| Daphnia | Aiguë (48 heures) |
CE50 | 70 | ||
| Poisson | Aiguë (96 heures) |
CL50 | 480 | ||
| Disperse Yellow 23 (6250-23-3) |
Poisson | Aiguë (48 heures) |
CL50 | > 1 000 | Étude présentée, 2008a |
| Disperse Blue 79[3] (12239-34-8) |
Ide dorée | Aiguë (96 heures) |
CL50 | 100 < CL50 < 220 | BASF, 1990 |
| Poisson-zèbre | Aiguë (96 heures) |
CL50 | 340 | Brown, 1992 | |
| Daphnia magna | Aiguë (48 heures) | CE50[3] | 4,5[*] | ||
| Scenedesmus subspicatus | Chronique - croissance (72 heures) |
CE50 | 9,5 | ||
| Bactérie | Non disponible | CI50[4] | > 100 | ||
| Disperse Red 73[5] (16889-10-4) |
Poisson-zèbre | Aiguë (96 heures) |
CL50 | 17 | |
| Daphnia magna | Aiguë (48 heures) |
CE50 | 23 | ||
| Scenedesmus subspicatus | Chronique - croissance (72 heures) |
CE50 | > 10 | ||
| Bactérie | Non disponible | CI50 | > 100 | ||
| Disperse Orange 30[6] (5261-31-4) |
Poisson-zèbre | Aiguë (96 heures) |
CL50 | 710 | |
| Daphnia magna | Aiguë (48 heures) |
CE50 | 5,8 | ||
| Scenedesmus subspicatus | Chronique - croissance (72 heures) |
CE50 | 6,7 | ||
| Bactérie | Non disponible | CI50 | > 100 | ||
| Disperse Orange 25[7] (31482-56-1) |
Poisson-zèbre | Aiguë (96 heures) |
CI50 | 268 | |
| Daphnia magna | Aiguë (48 heures) |
CL50 | 110 | ||
| Scenedesmus subspicatus | Chronique - croissance (72 heures) |
CE50 | 54 | ||
| Bactérie | Non disponible | CE50 | > 100 | ||
| Disperse Red 17 (3179-89-3)[8] |
Poisson-zèbre | Aiguë (96 heures) |
CL50 | 103 | |
| Daphnia magna | Aiguë (48 heures) |
CE50 | 98 | ||
| Scenedesmus subspicatus | Chronique - croissance (72 heures) |
CE50 | 7 | ||
| Bactérie | Non disponible | CI50 | > 100 | ||
| Colorant azoïque dispersé analogue (n° CAS confidentiel) |
Truite arc-en-ciel | Aiguë (96 heures) |
CL50 | 505 | Environnement Canada, 1995 |
| Disperse Blue 79:1 (3618-72-2) |
Truite arc-en-ciel | Chronique (122 jours) |
CSEO[9] | > 0,0048 | Cohle et Mihalik, 1991 |
[2] CE50 – La concentration d’une substance qui est jugée causer certains effets sublétaux toxiques chez 50 % des organismes d’essai.
[3] L’étude indique que le Disperse Blue 79 utilisé dans l’essai avait une pureté (de matières organiques) de 76 % et une dispersion du colorant à 20 %.
[4] CI50 – Concentration inhibitrice pour un pourcentage donné d’un effet. Estimation ponctuelle de la concentration d’une substance d’essai causant une réduction de 50 % d’une mesure biologique quantitative comme le taux de croissance.
[5] L’étude indique que le Disperse Red 73 utilisé dans l’essai avait une pureté de 96,6 %.
[6] L’étude indique que le Disperse Orange 30 utilisé dans l’essai avait une pureté (de matières organiques) de 73 % et une dispersion du colorant de 20 %.
[7] L’étude indique que le Disperse Orange 25 utilisé dans l’essai avait une pureté de 94 %.
[8] L’étude indique que le Disperse Red 17 utilisé dans l’essai avait une pureté de 98,8 %.
[9] CSEO – La concentration sans effet observé est la concentration la plus élevée, au cours d’un essai sur la toxicité, à laquelle on n’obtient pas d’effet statistiquement significatif, par comparaison aux témoins.
[*] La valeur de toxicité critique utilisée pour dériver une concentration sans effet probable.
En général, en raison de leur faible solubilité (soit < 1 mg/L), les colorants dispersés sont supposés avoir un impact écologique faiblement aigu (Hunger, 2003). Les résultats des études empiriques sur la toxicité portant sur des analogues du Solvent Red 23 concordent avec ces prévisions, indiquant des valeurs CL50 comprises entre 17 et 505 mg/L, laDaphnia étant l’organisme testé le plus sensible (CE50/CL50 allant de 4,5 à 110 mg/L). La valeur critique choisie pour dériver la concentration sans effet probable est réputée être la valeur de CE50 chezDaphnia magna, soit 4,5 mg/L (Brown, 1992).
L’interprétation des résultats de ces essais est compliquée par le fait que les valeurs obtenues (c.-à-d. CE50 et CL50) sont vraisemblablement nettement supérieures à la solubilité des substances d’essai. En effet, certaines des concentrations rapportées dans le tableau 6 peuvent représenter la charge de la substance à l’essai. Par conséquent, un sous-ensemble des valeurs réelles de CL50 ou de CE50 peuvent être inférieures aux concentrations rapportées puisque l’on ne connaît pas la concentration réelle dissoute dans l’eau qui peut causer un effet. Dans d’autres cas (voir les notes sous le tableau 6), les substances à l’essai se trouvaient dans des formulations et n’étaient donc pas pures à 100 %. Ainsi, d’autres substances chimiques dans la formulation peuvent avoir augmenté la solubilité et contribué à la toxicité totale. En dépit de ces incertitudes concernant la solubilité dans l’eau et la pureté de certains analogues, les données expérimentales et les données sur les analogues existantes indiquent clairement que la toxicité du Solvent Red 23 est probablement faible.
Une gamme de prévisions de la toxicité du Solvent Red 23 en milieu aquatique a également été obtenue à l’aide de modèles RQSA. Toutefois, tout comme pour la bioaccumulation, les estimations de l’écotoxicité fondées sur des RQSA ne sont pas jugées fiables à cause de l’erreur pouvant être associée aux paramètres d’entrée des modèles et de la nature particulière des colorants dispersés – état physique, caractéristiques structurales et/ou propriétés physiques et chimiques hors du domaine d’applicabilité des modèles.
L’information empirique disponible au sujet de l’écotoxicité du Solvent Red 23 indique donc que la substance n’est probablement pas très dangereuse pour les organismes aquatiques.
B – Dans d’autres milieux naturels
Comme le Solvent Red 23 devrait s’accumuler dans les sédiments et qu’il pourrait se retrouver dans les sols par suite de l’application directe de pesticides et de l’épandage de biosolides sur les sols, souvent utilisé pour enrichir les sols, et de la mise en décharge de produits qui les libèrent en se dégradant, il serait souhaitable de disposer de données sur la toxicité pour les organismes présents dans les sédiments et les sols. Cependant, on n’a trouvé aucune étude pertinente sur les effets écologiques de ces composés ou de leurs analogues dans d’autres milieux que l’eau. La toxicité pour les espèces vivant dans les sédiments et les sols devrait néanmoins aussi être faible, étant donné la biodisponibilité et le potentiel de bioaccumulation très faibles du Solvent Red 23 ainsi que ses propriétés physiques et chimiques, quoique cela ne puisse être confirmé faute de données acceptables sur la toxicité portant sur des organismes entiers. Cette hypothèse ne peut toutefois être corroborée en raison de l’absence de données globales valides sur la toxicité pour les organismes.
Évaluation de l’exposition écologique
Aucune donnée sur les concentrations de Solvent Red 23 dans l’eau au Canada n’a été retracée. On a donc évalué les concentrations dans l’environnement sur la base des renseignements disponibles, y compris les estimations relatives aux quantités de la substance, aux taux de rejets et aux cours d’eau récepteurs.
A – Rejets industriels
Les déclarations de l’industrie pour 2005 et 2006 n’indiquant aucune fabrication ou transformation du Solvent Red 23 au Canada, il ne devrait pas y avoir de rejets industriels de cette substance au pays.
B – Rejets par les consommateurs
Étant donné le profil d’utilisation de la substance dans les cosmétiques et certains produits de soins personnels, on peut penser que les produits contenant du Solvent Red 23 pourraient être rejetés dans les égouts ou les eaux de surface au cours de leur utilisation. Par conséquent, l’outil Mega Flush d’Environnement Canada qui sert à estimer les rejets à l’égout issus d’utilisations par les consommateurs a été utilisé pour estimer la concentration possible de la substance dans différents cours d’eau récepteurs d’effluents issus des stations de traitement des eaux usées dans lesquelles ont été rejetés par les consommateurs des produits contenant cette substance (Environnement Canada, 2008b). Le tableur fournit ces estimations pour environ 1 000 sites de rejet dans tout le Canada, et ce, d’après des hypothèses prudentes.
Ces hypothèses prudentes incluent :
- pertes dans les égouts à 100 %;
- un taux d’élimination dans les usines de traitement des eaux usées de 0,0 %,
- le nombre de jours de rejets annuels de 365 jours/an;
- facteur de dilution dans l’eau réceptrice sur une échelle de 1 à 10.
Les concentrations environnementales estimées (CEE) de Solvent Red 23 dans les cours d’eau récepteurs se situent dans la plage de 6,7 x 10-6 à 0,0061 mg/L. L’estimation est fondée sur un total de 4 000 kg/année pour la quantité de la substance d’après la limite supérieure de la fourchette des quantités déclarées de Solvent Red 23 qui auraient été importées au Canada en 2005 dans l’enquête menée en vertu de l’article 71 (Environnement Canada, 2006). L’équation et les entrées utilisées pour calculer les CEE sont décrites dans le rapport d’Environnement Canada (2010d).
Le Solvent Red 23 est également utilisé comme produit de formulation dans les pesticides agricoles (ARLA, 2010). Il figure sur la liste 2 de l’Agence de réglementation de la lutte antiparasitaire (ARLA), qui contient les produits de formulation considérés comme potentiellement toxiques d’après les similarités structurales avec les produits de formulation de la liste 1 (ceux, qui, selon l’ARLA, sont préoccupants), ou dans les données indicatrices de toxicité. On ne s’attend pas à ce que le Solvent Red 23 soit rejeté dans les égouts à la suite de son utilisation dans les pesticides. Le Solvent Red 23 pourrait toutefois être rejeté dans l’environnement par l’intermédiaire des applications agricoles. Cet usage n’est pas modélisé parmi les produits antiparasitaires et leurs produits de formulation sont réglementés par l’ARLA.
Caractérisation du risque écologique
La démarche utilisée pour cette évaluation écologique préalable examinait les renseignements scientifiques disponibles et dégageait des conclusions en appliquant la méthode du poids de la preuve et une approche préventive conformément à la LCPE (1999).
Si l’on se fonde sur les propriétés physiques et chimiques de substances analogues, le Solvent Red 23 devrait se dégrader lentement en milieu aérobie et devrait être persistant dans l’eau, le sol et les sédiments. Cette substance devrait présenter un faible potentiel de bioaccumulation. Bien que la proportion de Solvent Red 23 qui devrait être rejetée dans les égouts soit élevée, les faibles quantités importées de ce colorant au Canada ainsi que les données sur ses propriétés physiques et chimiques indiquent, dans l’ensemble, un faible potentiel de rejet dans l’environnement canadien. S’il est rejeté dans l’environnement, on s’attend à ce que le Solvent Red 23 soit principalement déversé dans les eaux usées, où il devrait finir par se déposer dans les sédiments et les sols. L’utilisation de données déduites à partir d’analogues a permis de démontrer que le Solvent Red 23 présente seulement un potentiel moyen de toxicité aiguë pour les organismes aquatiques.
La concentration estimée sans effet (CESE) a été évaluée en se fondant sur la CE50 de 48 h de 4,5 mg/L chez laDaphnia magna pour l’analogue Disperse Blue 79 (tableau 6). On a ensuite appliqué un facteur de 100 pour tenir compte de la toxicité aiguë à la toxicité chronique et des extrapolations au terrain des résultats en laboratoire et de l’utilisation d’une substance de remplacement. La CESE ainsi obtenue est de 0,045 mg/L.
Une analyse du quotient de risque, mettant en relation la CEE prudente avec une estimation prudente du potentiel d’effets nocifs ou une CESE, a été effectuée pour le milieu aquatique. Le quotient de risque (CEE/CESE) est une source de donnée importante à considérer dans l’évaluation du risque potentiel pour l’environnement.
Pour l’exposition résultant des rejets dans les égouts par suite des utilisations des consommateurs (scénario prudent), la CEE maximale pour le Solvent Red 23 tirées de Mega Flush était de 0,0061 mg/L. Lorsque la CEE maximale est comparée à la CESE de 0,045 mg/L, le quotient de risque (CEE/CESE) est de 0,136. Les quotients de risque étant inférieurs à 1 à tous les sites de Mega Flush, les rejets de Solvent Red 23 par les consommateurs dans le réseau d’égouts ne devraient pas être nocifs pour les organismes aquatiques.
Par conséquent, il est peu probable que le Solvent Red 23 nuise aux populations d’organismes aquatiques au Canada.
Incertitudes dans l’évaluation des risques pour l’environnement
L’évaluation de la persistance est limitée par le manque de données sur la biodégradation, ce qui a nécessité la production de prévisions modélisées. Bien que toutes les prévisions modélisées comportent un certain degré d’erreur, les résultats du modèle de biodégradation aérobie ont confirmé la persistance attendue du Solvent Red 23, compte tenu de ses utilisations et de ses caractéristiques structurales. De plus, l’évaluation de la persistance est limitée par les incertitudes quant à la vitesse de dégradation et à la mesure dans laquelle cette dégradation se produit dans des sédiments anaérobies ainsi qu’à la détermination de la biodisponibilité des produits de dégradation (p. ex. amines). On ne prévoit pas que les produits de dégradation soient biodisponibles étant donné qu’ils se forment seulement dans des sédiments anoxiques relativement profonds, mais il existe un risque de perturbation des sédiments. Par conséquent, ce point constitue une source d’incertitude dans l’évaluation de la toxicité du Solvent Red 23.
L’évaluation de la bioaccumulation de ces substances a été limitée par le manque de données empiriques sur le Solvent Red 23 et l’incapacité des modèles disponibles à estimer de façon fiable la bioaccumulation de colorants diazoïques. L’évaluation était plutôt fondée sur l’utilisation de données sur la bioaccumulation pour un analogue structural (Disperse Orange 30).
Il existe également des incertitudes en raison du manque de données sur les concentrations environnementales au Canada de Solvent Red 23. Cependant, l’absence de déclarations de fabrication au Canada, les faibles quantités importées et l’élimination prévue dans les effluents permettent de croire à un faible potentiel de rejet de ces substances dans l’environnement au Canada.
Les fractions de ces substances qui sont rejetées et de celles qui sont éliminées dans les usines de traitement des eaux usées constituent une autre source d’incertitude. Ces incertitudes ont été palliées par l’utilisation d’hypothèses prudentes dans la modélisation de l’exposition.
Les concentrations expérimentales, associées à la toxicité intrinsèque pour les organismes aquatiques, peuvent constituer une source additionnelle d’incertitude lorsqu’elles dépassent la solubilité du produit chimique dans l’eau (expérimentale ou prédite). Il existe également une incertitude liée à la pureté des substances utilisées dans les tests de solubilité et de toxicité. En raison de leur faible solubilité, les colorants sont souvent mélangés avec de l’eau et un agent solubilisant afin d’effectuer le test. Cette convention peut produire des valeurs de solubilité qui sont artificiellement élevées et qui peuvent également influer sur le résultat des tests de toxicité dans les milieux aquatiques. Toutefois, les efforts visant à rendre les colorants plus solubles augmenteront probablement de façon artificielle la biodisponibilité plutôt que de la diminuer. Par conséquent, malgré les incertitudes, les données disponibles indiquent que le Solvent Red 23 et ses analogues ne sont pas très dangereux pour les organismes aquatiques dans la colonne d’eau.
De plus, en ce qui a trait à l’écotoxicité, compte tenu du comportement prévu de répartition du Solvent Red 23 et de ses analogues, les données disponibles sur les effets ne rendent pas bien compte de l’importance du sol et des sédiments comme milieux d’exposition. En effet, les seules données sur les effets qui ont été trouvées s’appliquent principalement aux expositions aquatiques pélagiques, même si la colonne d’eau peut ne pas être le moyen le plus préoccupant à long terme d’après les estimations sur la répartition et les profils des rejets.
Étant donné que la substance est utilisée dans d’autres pays, il est possible qu’elle entre sur le marché canadien comme composant d’articles manufacturés ou de produits de consommation. Les renseignements obtenus dans le cadre de l’enquête menée en vertu de l’article 71 et d’autres sources de renseignements indiquent qu’elle est peut-être présente dans un certain nombre de ces produits au Canada. Les renseignements disponibles ne sont actuellement pas suffisants pour donner une estimation quantitative permettant de définir l’importance de cette source dans l’évaluation écologique. Cependant, on prévoit que les volumes de rejets de Solvent Red 23 dans les divers milieux naturels ne différeraient pas énormément des quantités estimées ici, bien que les quantités transférées au recyclage ou à l’élimination des déchets puissent être supérieures. On reconnaît également la possibilité que des rejets se dégagent des sites d’enfouissement, bien que cela soit peu probable et que les rejets éventuels soient faibles.
Évaluation de l’exposition
Aucune donnée empirique n’a été trouvée sur le Solvent Red 23 dans les milieux naturels. On ne disposait pas de suffisamment de données sur lesquelles fonder une analyse du cycle de vie permettant de prédire les pourcentages de perte aux fins de l’estimation des concentrations dans l’environnement. Par conséquent, on a estimé les concentrations du Solvent Red 23 en se fondant sur sa pression de vapeur et sa solubilité dans l’eau (valeurs les plus faibles de la fourchette de valeurs des analogues) et en présumant que la limite supérieure de la fourchette, soit 4 000 kg (1 000 kg provenant de chacune des quatre entreprises ayant fait une déclaration), a été entièrement rejetée dans les égouts, les eaux usées et les sols. Les concentrations environnementales estimées obtenues au moyen de la version 6 du logiciel ChemCAN sont négligeables (Environnement Canada, 2008a; ChemCAN, 2003).
On a estimé le potentiel d’exposition au Solvent Red 23 de l’ensemble de la population résultant de l’utilisation de cosmétiques et de certains produits de soins personnels à l’aide de ConsExpo 4.1 (ConsExpo, 2006; RIVM, 2006). On a calculé les estimations des expositions cutanées provenant de cosmétiques et de produits de soins personnels représentatifs contenant du Solvent Red 23, comme des préparations pour bains, des huiles à massage, des revitalisants, des colorants capillaires, des crèmes corporelles, des nettoyants pour le visage et des vernis à ongles. L’exposition orale a été estimée pour le brillant et le baume à lèvres contenant du Solvent Red 23.
L’estimation de l’exposition cutanée provenant de l’utilisation de produits de soins personnels va de 0,002 mg/kg p.c. par jour (huile de massage) à 0,18 mg/kg p.c. par jour (crème corporelle) avec une hypothèse prudente selon laquelle 26 % du produit appliqué est absorbé. On a estimé une exposition par voie orale de 0,01 mg/kg p.c. par jour pour les enfants âgés de 5 à 11 ans et de 0,006 mg/kg p.c. par jour pour la population générale provenant de l’utilisation de brillant et de baume à lèvres, en appliquant une hypothèse prudente selon laquelle 100 %[3] du produit appliqué est ingéré. Compte tenu de la nature prudente des hypothèses modélisées et en présumant prudemment une absorption par voies cutanée et orale de 26 et de 100 % respectivement, ces valeurs sont considérées comme les estimations des limites supérieures d’exposition. L’exposition aux produits de consommation par inhalation est considérée comme minime en raison de la faible volatilité de cette substance.
Évaluation des effets sur la santé
Le Solvent Red 23 est un membre de la famille des colorants azoïques, qui peuvent subir une rupture réductrice par l’intermédiaire des enzymes azoréductases trouvées dans les tissus des mammifères ainsi que par l’intermédiaire des bactéries de l’intestin et de la peau (p. ex. Chadwick et al., 1992; Platzek, 1999; Golka et al., 2004; Chen, 2006; Stingley et al., 2010). Par conséquent, des données sur les effets sur la santé des produits possibles de la rupture des liaisons azoïques ont été examinées dans le cadre de cette évaluation. Des données sur les analogues ont aussi été étudiées pour alimenter la base de données sur les effets sur la santé et pour préciser le potentiel de rupture réductrice des liaisons azoïques du Solvent Red 23. Les analogues ont été choisis en fonction de la disponibilité des données relatives aux effets sur la santé et de leur similarité avec le Solvent Red 23. Le tableau 7 présente les analogues considérés dans la présente évaluation ainsi que les produits potentiels résultant de la rupture des liaisons azoïques du Solvent Red 23.
Tableaux 7 : Analogues et produits possibles de la rupture des liaisons azoïques du Solvent Red 23 dans l’évaluation des effets sur la santé humaine
Solvent Red 23
| Composé d’origine : Solvent Red 23 (Sudan III) (85-86-9) 1-[4-(phénylazo)phénylazo]-2-naphtol - diazo, contient un noyau naphtalène hydroxylé |
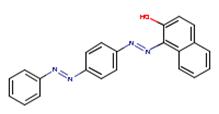 |
| Nom commun (n° CAS) |
Nom de la LIS | Structure | Principales similarités et différences structurales avec le Solvent Red 23 |
|---|---|---|---|
| Sudan I / C.I. Solvent Yellow 14 (842-07-9) |
1-phénylazo-2-naphtol |  |
Similarités : contient un noyau naphtalène hydroxylé et une liaison azoïque. Différences : monoazoïque, un seul groupement phényle. |
| Sudan II / Solvent Orange 7 (3118-97-6) |
1-(2,4-diméthylphénylazo) napht-2-ol |  |
Similarités : contient un noyau naphtalène hydroxylé et une liaison azoïque. Différences : monoazoïque, un seul groupement phényle, qui est diméthylé. |
| Sudan IV / Solvent Red 24 (85-83-6) |
1-(2-méthyl-4-(2-méthylphénylazo) phénylazo)-2-naphtol | 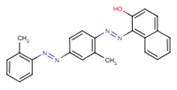 |
Similarités : diazoïque, contient un noyau naphtalène hydroxylé. Différences : les deux noyaux phényle ont chacun un groupement méthyle à la positionortho. |
| Produits possibles de la rupture des liaisons azoïques | Structure |
|---|---|
| 4-aminoazobenzène (60-09-3) |
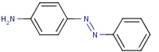 |
| 1-amino-2-naphtol (2834-92-6) |
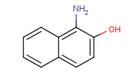 |
| p-phénylènediamine (106-50-3) |
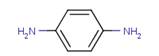 |
| Aniline (62-53-3) |
 |
Potentiel de rupture des liaisons azoïques
Des recherches sur la capacité des bactéries de l’intestin humain à métaboliser le Solvent Red 23, qui entraîne le rejet d’amines aromatiques, ont été effectuées en incubant du Solvent Red 23 avec des suspensions de selles humaines fraîches ou avec du Lactobacillus acidophilus et duLactobacillus fermentum. Les deux études ont permis d’identifier l’aniline en tant que métabolite du Solvent Red 23, ce qui indique que la microflore de l’intestin humain est capable de réduire la liaison azoïque du Solvent Red 23 (Xuet al., 2007; Chen et al., 2009). Des rats à qui l’on a injecté par voie intrapéritonale du Solvent Red 23 radioactif ont excrété 15,8 % de la radioactivité totale administrée dans l’urine, dont 80 % a été identifiée comme étant du 4-aminophénol, métabolite d’hydroxylation de l’aniline (Ryan et Welling, 1967), ce qui démontre que la rupture réductrice des liaisons azoïques du Solvent Red 23 a lieu in vivo.
Le Sudan I (n° CAS 842-07-9), un analogue monoazoïque du Solvent Red 23, a aussi été métabolisé en 4-aminophénol et ses conjugués dans des lapins exposés oralement, ce qui indique que les deux substances ont un devenir métabolique semblable qui entraîne le rejet d’aniline, qui est ensuite convertie en 4-aminophénol (EFSA, 2005). Sur ce fondement, l’EFSA juge prudent de supposer que la génotoxicité et la cancérogénicité associées au Sudan I peuvent aussi être associées au Solvent Red 23 (EFSA, 2005).
Le Sudan IV est un analogue méthylé diazoïque lipophile du Solvent Red 23, et sa capacité de subir une rupture des liaisons azoïques in vivo et in vitro a aussi été démontrée. Dans cette même étude, qui consistait à examiner la réduction azoïque du Solvent Red 23, on a observé que le Sudan IV subissait une rupture réductrice lorsqu’il était incubé avec des suspensions de selles humaines fraîchement isolées (Xu et al., 2007). Il a également été démontré que le Sudan IV était réduit de façon métaboliquein vivo à la suite d’une administration par voie trachéale chez les rats, alors qu’on a pu détecter dans l’urine du o-aminoazotoluène, l’analogue diméthyl du 4-aminoazobenzène (un produit potentiel de la rupture des liaisons azoïques du Solvent Red 23) (Parent et Dressler, 1977). Bien que l’administration par voie intratrachéale ne soit pas applicable à l’exposition humaine, l’étude susmentionnée démontre qu’un colorant lipophile avec solvant, le Sudan IV, peut subir une rupture in vivo et rejeter un amine aromatique cancérogène (o-aminoazotoluène) dont le profil de structure et de toxicité est très semblable à celui du 4-aminoazobenzène, un produit prévu de la rupture des liaisons azoïques du Solvent Red 23.
Collectivement, les données sur le Solvent Red 23 et ses analogues appuient le potentiel de rupture réductrice des liaisons azoïques, particulièrement lorsqu’ils sont administrés par voie orale, et par le fait même, le potentiel d’exposition aux amines aromatiques. Alors que l’aniline (n° CAS 62-53-3) a été le métabolite prédominant détecté dans les études visant à déterminer si les liaisons azoïques du Solvent Red 23 peuvent se rompre lors du métabolisme, la présence d’autres produits de rupture potentiels ne peut être évitée. Par conséquent, cette évaluation préalable considère aussi les données relatives aux effets sur la santé des produits potentiels de rupture des liaisons azoïques du Solvent Red 23 : 4-aminoazobenzène (n° CAS 60-09-3), 1-amino-2-naphtol (n° CAS 2834-92-6) etp-phénylénédiamine (n° CAS 106-50-3). Les renseignements sur les produits de rupture réductrice des liaisons azoïques potentiels sont présentés à l’annexe 6.
Solvent Red 23
Même s’il existe peu de données empiriques, les effets sur la santé du Solvent Red 23 ont déjà été évalués dans plusieurs études commandées par le Centre International de Recherche sur le Cancer (CIRC) (CIRC, 1975, 1987), le Comité scientifique des produits de consommation (CSPC) de l’Union européenne (CSPC, 2005, auparavant SCCNFP, 2002) et l’Autorité européenne de sécurité des aliments (EFSA) (EFSA, 2005). Un sommaire des données pertinentes issues de cette étude est présenté plus loin, de même que des renseignements additionnels (annexe 4). Des données pertinentes tirées de prévisions de modélisations du modèle de relation quantitative structure-activité (RQSA) sont présentés pour éclairer l’évaluation des effets sur la santé du Solvent Red 23 (annexe 7).
Génotoxicité et cancérogénicité
Plusieurs études sur des doses répétées orales et cutanées ont été relevées pour le Solvent Red 23. Le CIRC (1975) a cité deux études sur la toxicité chronique par voie alimentaire orale chez des souris et des rats. Les souris de « type B » (83 mâles, 54 femelles) provenant d’un croisement de multiples souches ont été exposées au Solvent Red 23 (appelées « Sudan G ») dans l’alimentation avec environ 67 mg/kg p.c. par jour[4] pendant 752 jours (Waterman et Lignac, 1958). À la fin de la période d’observation, les auteurs ont constaté des tumeurs aux poumons dans les groupes d’expositions mâles (9) et femelles (7), ce qui était statistiquement supérieur aux groupes témoins (0 chez les mâles, 1 chez les femelles). Les auteurs considéraient que l’incidence élevée de cancers du poumon chez les souris exposées était normale pour les souches de souris de type B, et que la faible incidence des tumeurs aux poumons dans les groupes témoins était attribuable à la distribution non uniforme des souris ayant des sensibilités différentes. Des incidences similaires de papillomes du secteur gastrique antérieur et des tumeurs mammaires ont été observées chez les animaux témoins et exposés. Un rapport sur les rats Wistar (5/sexe) nourris avec 4 % de Solvent Red 23 (sous le nom de Sudan III) dans leur alimentation pendant une période pouvant aller jusqu’à 18 mois (environ 2 000 mg/kg p.c. par jour[5]) n’a révélé aucun effet lié aux expositions; toutefois, l’examen sommaire et microscopique semblait être limité au tube digestif et au foie (Willheim et Ivy, 1953). Le CIRC a considéré ces données comme non pertinentes en raison des « doses administrées, du degré de déclaration ou du nombre d’animaux utilisés ». D’autres études orales non reconnues par le CIRC ont aussi été relevées. Dans une étude antérieure, le Solvent Red 23 a été administré à des rats par l’alimentation à une concentration de 0,04 % (environ 21 mg/kg p.c. par jour[6]) pendant onze mois. Des modifications non précisées aux reins ont été observées, mais aucune tumeur (Maruya, 1938). Aucune tumeur n’a été observée au foie ou ailleurs lorsque 16 rates Long-Evans ont été nourries avec 0,1 % Solvent Red 23 dans 1 mL d’huile de sésame (environ 3 mg/kg p.c. par jour[7]) par instillation gastrique pendant 25 semaines (5x/semaine) (Huggins et al., 1978). Les mêmes auteurs ont démontré que du Solvent Red 23, administré par voie orale à des rats aux mêmes doses, protégeait de la leucémie et des tumeurs de la glande mammaire induites par les substances hautement cancérogènes 7,12-di- et 7,8,12-tri-méthylbenz[a]anthracène) (DMBA et TMBA, respectivement) (Huggins et Pataki, 1965; Huggins et al., 1978). On a émis une hypothèse selon laquelle un mécanisme de cet effet protecteur est fondé sur une forte induction, par le Solvent Red 23, des systèmes d’enzymes en phases I et II qui peuvent agir pour éliminer efficacement le DMBA et le TMBA in vivo (Hatakeyama et al., 1996; Fujita et al., 1988). En raison de leurs limites, les études résumées ici ajoutent peu à l’évaluation des effets cancérogènes (p. ex. expositions par une seule dose, temps d’exposition court).
Des études sur des doses répétées par voie cutanée ont également été relevées pour le Solvent Red 23. Dans une étude non publiée, on a exposé des lapins à des concentrations allant jusqu’à 1 % (quotidiennement) de Solvent Red 23 dans un onguent blanc USP ou dans un onguent hydrophile USP pendant 21 ou 90 jours (CSPC, 1988). L’essai a été effectué à la fois sur la peau intacte et sur la peau éraflée. Les seuls effets déclarés étaient une inflammation de la peau, un épaississement et une hyperkératose, même si le CSPC (2005) considérait que l’étude n’était pas valable parce que sa méthode n’était pas décrite. Dans une étude sur l’exposition chronique par de la peinture sur la peau, des souris Webster suisses (50/sexe) étaient exposées une fois par semaine sur la peau rasée du dos à une concentration en une seule exposition de 1 % de Solvent Red 23, (D&C Red 17) dans 0,1 mL de laurylsulfate de sodium (dose hebdomadaire approximative de 33 mg/kg p.c.[8]) ou dans le véhicule seulement (Carson, 1984). Des observations cliniques ont été faites à tous les jours pendant la période d’exposition alors que des analyses histologiques de tous les tissus et des organes manifestement anormaux ont eu lieu à l’autopsie après 18 mois d’exposition ou dans le cadre de groupes provisoires sacrifiés. Les auteurs de l’étude n’ont déclaré aucune modification de pathologiques au lieu d’exposition ou dans les tissus examinés, qui pourraient être attribuables à l’exposition au D&C Red 17 à la concentration de l’essai étudiée (Carson, 1984).
D’après les évaluations du CSPC (2005, auparavant SCCNFP, 2002), les données disponibles sur la cancérogénicité du Solvent Red 23 ont été considérées comme non valables pour la caractérisation de la cancérogénicité de cette substance. Le CIRC a déterminé que la classification globale relative au cancer pour cette substance serait le Groupe 3 du CIRC (inclassable quant à sa cancérogénicité pour l’homme) en raison de données insuffisantes sur les animaux et de l’absence de données épidémiologiques sur les humains (CIRC, 1975, 1987). Même si les études disponibles sur les animaux concernant le Solvent Red 23, administré par voie orale et topique, n’ont démontré qu’il n’existe aucun signe de cancérogénicité aux doses uniques testées et que la substance peut avoir un effet protecteur contre la cancérogénicité des produits cancérogènes connus, soit le DMBA et le TMBA (Huggins et Pataki, 1965; Hugginset al., 1978), ces observations en elles-mêmes ne constituent pas une preuve suffisante que le Solvent Red 23 lui-même n’est pas cancérogène. En raison de l’insuffisance de détails sur les conditions de l’étude, du petit nombre d’animaux utilisés ou du nombre limité des doses testées, aucune conclusion ne peut être tirée concernant la cancérogénicité du Solvent Red 23 à partir de ces données.
Plusieurs études ont porté sur le potentiel génotoxique du Solvent Red 23. Les tests d’Ames, dans lesquels sont utilisées des souches Salmonella typhimurium TA98 et TA100, étaient négatifs lorsqu’un composé purifié a été testé. Toutefois, pour le Solvent Red 23, 3 des cinq préparations commerciales étaient mutagéniques en présence de l’activateur S9. Les auteurs ont attribué les résultats positifs à la présence de résidus de 4-aminoazobenzène (Miyagoshi et al., 1985; SCCNFP, 2002). La génotoxicité du Solvent Red 23 était également négative dans des essais de recombinaisons bactériologiques (Kada et al., 1972; Mamber et al., 1983). Il convient de noter que la réduction des liaisons azoïques s’est avérée nécessaire pour activer de nombreux colorants azoïques. Par conséquent, puisque les systèmes S9 standards ne sont pas des médiateurs efficaces de la rupture des liaisons azoïques, les résultats négatifs de ces études ne sont pas concluants, car la méthode d’activation négative pourrait ne pas convenir à ce groupe de composés (Prival et Mitchell, 1982; SCCNFP, 2002). Une incubation de cellules CHO en présence de Solvent Red 23, sans activation métabolique, a augmenté la fréquence des cassures chromosomiques comparativement aux témoins (Au et Hsu, 1979), alors qu’un autre essai d’aberrations chromosomiques effectué in vitrodans des lymphocytes humains a été négatif (CSPC, 2005). Le CSPC a jugé incomplètes les données sur la génotoxicité du Solvent Red 23 et qu’il était impossible de tirer une conclusion sur le potentiel de génotoxicité (SCCNFP, 2002; CSPC, 2005).
Les modèles RQSA CASETOX, DEREK et TOPKAT ont donné des résultats mitigés concernant le potentiel génotoxique et cancérogène du Solvent Red 23, lesquels sont résumés à l’annexe 7 (CASETOX, 2008; DEREK, 2008; TOPKAT, 2004).
Effets non cancérogènes
Le potentiel d’irritation et de sensibilisation du Solvent Red 23 a été résumé dans des rapports du CSPC. Le Solvent Red 23 a été considéré comme un irritant marginal, compte tenu de la preuve qu’il est légèrement irritant pour la peau et les membranes muqueuses des lapins (CSC, 1988, CSPC, 2005). Des recherches portant sur la sensibilisation de la peau ont montré que les individus à qui l’on a administré un ou plusieurs colorants azoïques n’étaient pas sensibles au Solvent Red 23 (Kozuka et Tashiro, 1980; CSPC, 2005). Toutefois, 3/6 et 1/6 des cobayes exposés à l’amine aromatiquep-phénylénédiamine ou 4-aminoazobenzène respectivement étaient sensibilisés au Solvent Red 23 (Xie et al., 2000; CSPC, 2005).
Les effets de l’exposition in utero sur la reproduction des mâles ont été examinés dans une étude de l’exposition par voie orale dans laquelle des souris enceintes étaient exposées par gavage au Solvent Red 23 (1 000 mg/kg p.c. par jour) ou par le véhicule seulement pendant les jours de gestation 8 à 12 (Gray et Ostby, 1993). Par la suite, les testicules des rejetons mâles (40 du groupe Solvent Red 23, 19 du groupe témoin) ont été examinés 48 à 50 jours après leur naissance. Aucune modification liée à l’exposition n’a été observée dans le poids corporel, le poids des testicules, le nombre de tubes séminifères, le pourcentage de tubules atrophiés ou le poids de la vésicule séminale. Les auteurs n’ont également relevé aucune toxicité des mères et aucune autre modification des paramètres néonataux. Ces données n’ont toutefois pas été mentionnées dans l’étude.
Analogues
Cancérogénicité et génotoxicité
Le potentiel génotoxique et cancérogène des colorants azoïques apparentés Sudan I, Sudan II et Sudan IV a également été étudié dans cette évaluation (voir le tableau 7 ci-dessus). Ces substances sont aussi des colorants lipophiles avec solvants du groupe Sudan et elles ont des propriétés physiques et chimiques, des amines aromatiques et un métabolisme semblables à ceux du Solvent Red 23 (voir aussi la section Absorption, distribution, métabolisme et excrétion). Par conséquent, le potentiel génotoxique et cancérogène de ces substances est examiné afin de mieux connaître le profil de toxicité du Solvent Red 23.
Le Sudan I est un analogue monoazoïque du même groupe de colorants Sudan que le Solvent Red 23 (Sudan III), et tous deux partagent deux composantes d’amines aromatiques identiques (aniline et 1-amino-2-naphtol). Dans des études de l’exposition chronique par l’alimentation réalisées par le National Toxicology Program (NTP) des États-Unis, la cancérogénicité orale du Sudan I était positive chez les rats mâles et femelles (mais pas chez les souris) d’après une augmentation de l’incidence de nodules néoplasiques au foie en fonction de la dose (NTP, 1982). Cette substance s’est avérée positive pour la mutagénicité dans l’analyse des mutations du lymphome de la souris et dans les tests d’Ames bactériologiques avec et sans activation métabolique par l’activateur S9 sur des rats et des hamsters, mais était négative pour les aberrations chromosomiquesin vitro et in vivo, et équivoque pour le micronoyau in vivo (NTP, 2010). Le Sudan I a été classé comme cancérogène et mutagène en Europe en vertu du règlement CLP[9] (Commission européenne, 2008). Par conséquent, compte tenu de l’absence de preuve de sécurité adéquate (CSPC, 2001, 2004), l’utilisation de cette substance dans les cosmétiques a été interdite en Europe par son inscription (sous l’appellation « CI Solvent Yellow 14 ») à l’annexe II de la Directive sur les cosmétiques (Commission européenne, 2010).
Le Sudan II, aussi appelé Solvent Orange 7, est un analogue monoazoïque dont la structure ressemble à celle du Sudan I. Contrairement au Sudan I, Sudan II a un groupement méthyle aux positions 2 et 4 du noyau phényle. Le Sudan II a fait l’objet d’essais dans un nombre limité d’études in vitro sur la mutagénicité bactérienne. Les résultats de ces études ont été considérés comme des preuves suffisantes de la mutagénicité du Sudan II chez les bactéries après activation métabolique (EFSA, 2005). Le seul essai in vitro portant sur la génotoxicité s chez les mammifères a donné des résultats négatifs. Plusieurs études sur la cancérogénicité ont été effectuées chez des souris ou des rats; toutefois, le CIRC a jugé que ces études étaient inadéquates pour évaluer la cancérogénicité du Sudan II (CIRC, 1975). L’EFSA, par contre, a déclaré l’incidence élevée de tumeurs de la vessie chez des souris ayant reçu des implants de Sudan II (directement dans la vessie) comme suffisante pour déclarer que cette substance présente une cancérogénicité possible, jusqu’à preuve du contraire (EFSA, 2005).
Le Sudan IV est un analogue diméthyle diazoïque lipophile du même groupe Sudan que le Solvent Red 23 (Sudan III) et tous deux partagent un composé d’amine aromatique similaire (o-aminoazotoluène)[10] et un composé d’amine aromatique identique (1-amino-2-naphthol)[11]. Le Sudan IV a été classé en fonction de sa cancérogénicité et de sa génotoxicité, bien que sa cancérogénicité ait été testée dans plusieurs essais dépassés évalués par le CIRC (1975). Vingt-quatre rats ont été exposés par voie sous-cutanée à 0,2 ml d’une solution contenant 2 % de Sudan IV, une fois par semaine, pendant 403 jours. Sur les huit rats qui ont survécu après 403 jours, quatre ont développé des sarcomes locaux; toutefois, cette étude ne comportait pas de groupes témoins (Umeda, 1957, 1958) véhicules (Tween 80). Les souris traitées oralement n’ont pas connu d’augmentation de l’incidence des tumeurs supérieure à celles des témoins, même si, chez une femelle traitée, on a observé de multiples adénomes hépatiques semblables aux tumeurs au foie observées chez des souris témoins positives exposées auo-aminoazotoluène (produit anticipé de la rupture des liaisons azoïques du Sudan IV) (Waterman et Lignac, 1958). Aucune tumeur n’a été observée chez des rats Wistar exposés à 4 % de Sudan IV dans leur alimentation (environ 2 000 mg/kg p.c. par jour) pendant 18 mois. Toutefois, le quart des rats exposés qui ont survécu après 18 mois avaient des modifications cirrhotiques au foie et de l’hyperplasie des conduits biliaires. Ces modifications n’ont pas été observées chez les 50 rats témoins (Willheim et Ivy, 1953). Des hyperplasies épithéliales, et non des tumeurs, ont été observées dans une étude sur des souris à la peau peinturée (CIRC, 1975). En raison des données inadéquates sur le cancer chez les animaux résumées plus haut et de l’absence de données épidémiologiques, le CIRC a classé le Sudan IV dans le Groupe 3 (inclassable quant à sa cancérogénicité pour l’homme) (CIRC, 1975, 1987). En ce qui concerne la génotoxicité, le Sudan IV était positif dans la souche de Salmonella typhimurium TA98 selon la méthode Prival modifiée afin de faciliter la réduction azoïque (Zhouet al., 1987). Des résultats positifs ont aussi été observés dans les souches TA 1537, 1538 et 98 ainsi qu’une réduction du dithionite (EFSA, 2005). Dans des études antérieures, effectuées sans réduction azoïque, il a été démontré que la mutagénicité des bactéries était attribuable à une impureté du colorant de grade commercial (Miyagoshi et al., 1985). Le Sudan IV était également positif pour la transformation cellulaire déclenchée de façon virale dans des cellules d’embryons de hamsters de Syrie (Heidelberger et al., 1983). Compte tenu de la preuve de génotoxicité limitée, de la capacité d’induction de la prolifération épithéliale et de la similarité structurale avec le cancérogène Sudan I, un comité scientifique de l’EFSA a déterminé que le Sudan IV était potentiellement génotoxique et possiblement cancérogène (EFSA, 2005). D’après un avis du Comité scientifique de cosmétologie (CSC) de la Commission européenne selon lequel il existe des indications de potentiel cancérogène du Sudan IV (sous l’appellation « CI 26105 », CSC, 1988), son utilisation comme colorant dans les cosmétiques est actuellement interdite en Europe en vertu de son inscription à l’annexe II de la Directive sur les cosmétiques (Commission européenne, 2010). L’utilisation du Sudan IV dans les cosmétiques est actuellement interdite au Canada (Santé Canada, 2009).
En résumé, les données d’essais empiriques sur la génotoxicité du Solvent Red 23 lui-même ne sont pas concluantes. Toutefois, compte tenu de la preuve de génotoxicité et de cancérogénicité de son analogue Sudan I, et du rejet prévu d’amines aromatiques par rupture réductrice des liaisons azoïques (en particulier le 4-aminobenzène), la génotoxicité et la cancérogénicité sont considérées comme des effets critiques pour la caractérisation des risques du Solvent Red 23.
Produits potentiels de la rupture réductrice de la liaison azoïque
Comme le Solvent Red 23 peut subir une rupture à l’exposition, puis rejeter des amines aromatiques potentiellement dangereuses (voir la section Potentiel de rupturedes liaisons azoïques), les effets sur la santé des produits potentiels de la rupture réductrice des liaisons azoïques du Solvent Red 23 sont examinés dans la présente évaluation.
Le 4-aminoazobenzène (n° CAS 60-09-3) est une substance cancérogène reconnue pour les animaux, qui cause des tumeurs au foie et à la peau chez les rats. Le CIRC l’a classé comme une substance cancérogène du Groupe 2B (CIRC, 1975; 1987). En Europe, le 4-aminoazobenzène est classé comme une substance cancérogène aux termes du règlement CLP européen (Commission européenne, 2008; ESIS, c1995-2009). Dans le règlement REACH, il figure parmi les 22 amines aromatiques préoccupantes, qui ne devraient pas être libérées des colorants azoïques utilisés dans les textiles et les articles de cuir pouvant entrer en contact direct et prolongé avec la peau humaine ou la cavité buccale (REACH, annexe XVII, appendice 8) (Commission européenne, 2006). En ce qui concerne la génotoxicité du 4-aminoazobenzène, plusieurs épreuves de génotoxicité in vivo et in vitro (références citées dans BfR, 2003; CIRC, 1987; BIBRA, 1989) ont donné des résultats positifs quant à la mutagénicité, la clastogénicité et les dommages subis par l’ADN. L’analogue diméthyle o-aminoazotoluène (n° CAS 97-56-3) est considéré comme cancérogène par le CIRC (1975, 1987), le NTP (2005) et la Commission européenne (2008), et figure parmi les 22 amines aromatiques réglementées dans les colorants azoïques du règlement REACH (Commission européenne, 2006).
L’aniline (n° CAS 62-53-3) a été évaluée précédemment comme une substance prioritaire par Santé Canada et Environnement Canada (Canada, 2010) et par l’Union européenne (UE, 2004). Dans des études sur l’exposition chronique par l’alimentation, des tumeurs à la rate propres aux espèces et aux sexes ont été observées chez des rats mâles (mais non chez les femelles) à la dose la plus élevée; ces tumeurs n’ont toutefois pas été observées chez les souris mâles ou femelles. Des résultats mitigés ont été obtenus dans des essais de génotoxicité, et aucune génotoxicité n’a été observée dans la rate. Des études sur l’exposition aiguë et à doses répétées chez des rats, des chiens et des volontaires humains ont également montré que l’aniline induit la formation de méthémoglobine (UE, 2004).
Le potentiel cancérogène du 1-amino-2-naphtol (n° CAS 2834-92-6) n’a pas été étudié, et aucune recherche pertinente avec doses répétées n’a été relevée (BfR, 2003). Toutefois, une augmentation du nombre de tumeurs à la vessie (10/36 comparativement à 2/56) et de métaplasies squameuses (18/36 comparativement à 9/56) a été observée lorsque du 1-amino-2-naphtol était implanté dans la vessie par l’intermédiaire de granulés de paraffine (Bonser et al., 1956). D’après des essais effectués sur la soucheSalmonella typhimurium TA100, le 1-amino-2-naphtol peut exercer une mutation bactérienne inverse (Dillon et al., 1994).
Le Comité scientifique des produits de consommation (CSPC) de la Commission européenne a examiné la toxicité dup-phénylénédiamine (n° CAS 106-50-3) dans le cadre d’une évaluation des risques (CSPC, 2006). Selon le CSPC, lep-phénylénédiamine présente une toxicité aiguë modérée par voie orale et une toxicité faible par voie cutanée. Par ailleurs, il est un sensibilisant cutané (CSPC, 2006). Lep-phénylénédiamine figure actuellement sur la Liste critique des ingrédients dont l’utilisation est interdite dans les cosmétiques de Santé Canada (Santé Canada, 2009) et ne peut être utilisé dans les produits devant être appliqués sur la peau. Les données sur la génotoxicité in vitro pour lep-phénylénédiamine sont mitigées : résultats positifs et négatifs dans le cadre du test d’Ames, de l’essai sur les lymphomes de souris et du test du micronoyau qui permettent d’évaluer la clastogénicité des cellules de mammifères. Une dose sans effet nocif observé (DSENO) de 4 mg/kg p.c. par jour a été calculée à partir d’une étude sur l’exposition subchronique par l’alimentation chez les souris fondée sur des gains de poids du foie et des reins. De nombreuses études sur la cancérogénicité du p-phénylénédiamine ont été trouvées, y compris une étude sur l’exposition chronique par l’alimentation chez des souris B6C3F1 et des rats F344 menée par le National Toxicology Program (NTP) des États-Unis en 1979. Cette étude a prouvé que le p-phénylénédiamine n’augmentait pas l’incidence des tumeurs chez les animaux exposés (CSPC, 2006).
Absorption, distribution, métabolisme et excrétion
Il existe peu de données permettant de caractériser l’absorption du Solvent Red 23 par voies orale et cutanée. Dans une étude sur l’exposition par voie orale réalisée sur des rats, du Solvent Red 23 intact a été éliminé principalement dans les selles (83,6 à 95 % selon le solvant), alors que le reste de la dose administrée n’a pas été pris en compte (Ryan et Welling, 1967). Plus récemment, des études sur des expositions répétées (doses de 3 à 900 mg/kg p.c. par jour) ont démontré que le Solvent Red 23 modifie considérablement le contenu en protéines et l’activité enzymatique (CYP1A, glutathion S-transférase, glutathion peroxydase, ménadione-réductase, etc.) dans le foie et le cerveau des hamsters, des souris et des rats exposés par la voie orale (Huggins et al., 1978; Hatakeyama et al., 1996; Romero et al., 2000). Les effets des modulateurs enzymatiques qui suivent une exposition orale indiquent fortement que le Solvent Red 23 ou les produits potentiels de la rupture des liaisons azoïques sont systématiquement absorbés et distribués par la voie orale. L’analogue monoazoïque du Solvent Red 23, le Sudan I, a été rapidement absorbé après une administration orale chez des rats et des lapins, et seulement de petites quantités ont été excrétées telles quelles (CIRC, 1975). Toutefois, en raison de la plus grande taille des molécules et de la solubilité moins élevée dans l’eau du Solvent Red 23 comparativement à celles du Sudan I (annexe 5), l’absorption orale de la structure fondamentale du Solvent Red 23 devrait être relativement moins importante. Dans l’ensemble, les données sur le Solvent Red 23 et son analogue Sudan I indiquent qu’il existe un potentiel d’absorption par la voie orale. Une fraction d’absorption orale par défaut prudente de 100 % a donc été utilisée pour calculer les estimations des expositions.
Dans une étude sur l’absorption cutanée in vitro, on a exposé de la peau de porc viable et de la peau d’humain non viable à un écran solaire contenant du Solvent Red 23 disponible sur le marché. Entre 12 et 15 % de la dose appliquée était retenue dans la peau (7,3 à 10,7% dans la couche cornée, 1,3 à 5,6 % dans le derme et l’épiderme combinés), et moins de 1 % de la radioactivité retrouvée dans le fluide récepteur (Youricket al., 2007). Une autre étude sur l’absorption par voie cutanée a également démontré des résidus de Solvent Red 23 liés à la peau après une application sur la peau excisée de glutathion peroxydase avec ou sans véhicules visant à accroître la pénétration chez des rats; toutefois, la substance n’a pas été détectée dans le fluide récepteur (Sasaki et al., 1990). Collier et al., (1993) ont démontré que l’analogue monoazoïque Sudan I (5 µg/cm2 dans de l’acétone) était conservé dans les couches de la peau à des niveaux semblables à ceux observés pour le Solvent Red 23. Mais, contrairement au Solvent Red 23, jusqu’à 30 % du Sudan I appliqué a été retrouvé dans le fluide récepteur, et environ 26 % était absorbé par la peau humaine en 24 heures. Collieret al., (1993) ont également rapporté que 50 % du marqueur du fluide récepteur détecté était causé par la présence de produits de la réduction des groupements azoïques, mesurés comme étant la somme de toutes les amines aromatiques (principalement l’aniline) présents, y compris leurs métabolites formés par N-oxydation etN-acétylation. Par conséquent, l’absence du Solvent Red 23 dans le fluide récepteur indiquée dans les études susmentionnées pourrait ne pas être une preuve certaine de la non-absorption cutanée, car il se peut que des amines aromatiques (ou leurs métabolites) non marquées générées par rupture réductrice des liaisons azoïques aient été présents mais non détectés. De plus, Yourick et al., (2007) ont lavé des échantillons de peau avec un détergent à 1 % avant l’exposition, ce qui a diminué le nombre de bactéries présentes sur la peau. Il a été démontré que les bactéries métabolisent les colorants azoïques jusqu’à 300 fois plus efficacement que les mammifères (Collier et al., 1993) et qu’elles peuvent ainsi rejeter des amines aromatiques susceptibles d'être plus facilement absorbées que leurs composés d’origine, qui ont un poids moléculaire plus élevé (Platzeket al., 1999). Par conséquent, on ignore si l’absorption des produits de la rupture des liaisons azoïques ou leurs métabolites subséquents est importante après une exposition cutanée au Solvent Red 23. En raison de ces incertitudes, on a utilisé une valeur d’absorption cutanée prudente de 26 % fondée sur les propriétés physiques et chimiques du Solvent Red 23, qui semblent indiquer une pénétration cutanée faible, ainsi que sur des données empiriques sur la pénétration cutanée pour l’analogue monoazoïque Sudan I (Collier et al., 1993). Toutefois, en raison de la plus grande taille des molécules et de la solubilité dans l’eau plus faible du Solvent Red 23 comparativement au Sudan I, l’absorption cutanée de la structure fondamentale du Solvent Red 23 devrait être relativement plus faible. Par conséquent, la valeur d’absorption cutanée choisie de 26 % est considérée comme prudente pour l’estimation de l’exposition cutanée du Solvent Red 23.
Caractérisation des risques pour la santé humaine
L’exposition de l’ensemble de la population au Solvent Red 23 dans les milieux naturels devrait être négligeable. Il ne devrait pas non plus y avoir d’exposition au Solvent Red 23 par la nourriture, car cette substance n’est pas autorisée dans les aliments destinés à être vendus au Canada en vertu du Titre 16 du Règlement sur les aliments et drogues, et son utilisation n’a pas été déclarée dans l’emballage alimentaire. Il peut toutefois y avoir une exposition par voie cutanée ou buccale provenant de l’utilisation de cosmétiques et de certains produits de soins personnels. L’estimation de la limite supérieure de l’exposition chronique par voie cutanée provenant de cosmétiques (y compris les préparations pour bain, les huiles à massage, les revitalisants, les colorants capillaires, les lotions corporelles, les nettoyants pour le visage et les vernis à ongles) est de 0,002 à 0,18 mg/kg p.c. par jour, en supposant une valeur d’absorption cutanée prudente de 26 %. L’exposition au Solvent Red 23 par voie orale peut aussi avoir lieu par l’utilisation de brillant ou de baume à lèvres dont l’estimation de la limite supérieure de l’exposition chronique est de 0,01 mg/kg p.c. par jour pour les enfants âgés de 5 à 11 ans et de 0,006 mg/kg p.c. par jour pour la population générale. L’exposition par inhalation provenant de ces sources devrait être minime.
Les données empiriques relatives aux effets sur la santé du Solvent Red 23 étaient limitées. Quant aux résultats des essais de génotoxicité, ils étaient mitigés. Le CIRC et le CSPC ont considéré comme inadéquates les études disponibles sur la cancérogénicité. Étant donné que les liaisons azoïque du Solvent Red 23 peuvent subir une rupture, les données relatives aux effets sur la santé des produits prévus de la rupture des liaisons azoïques, en particulier le 4-aminoazobenzène, ont été prises en considération dans la caractérisation des effets sur la santé du Solvent Red 23. Bien que le 4-aminoazobenzène n’ait pas été détecté dans des études du métabolisme in vitro avec du Solvent Red 23, un analogue étroitement lié, le Sudan IV, a bel et bien subi une rupture des liaisons azoïquesin vivo et rejeté du o-aminoazotoluène (analogue méthylé du 4-aminoazobenzène). Cela semble indiquer que le 4-aminoazobenzène peut aussi être libéré du Solvent Red 23 in vivo. Il a été démontré que le 4-aminoazobenzène induit des tumeurs chez les rats après une exposition par voie orale et cutanée, il a été classé cancérogène par le CIRC (1987) et la Commission européenne (2010), est s’est également avéré positif dans une gamme d’essais sur la génotoxicité in vivo et in vitro (références citées dans BfR, 2003; CIRC, 1987; BIBRA, 1989). De plus, il a été démontré que le colorant analogue monoazoïque Sudan I, classé cancérogène et mutagène en Europe, est métabolisé en certains amines aromatiques identiques à ceux du Solvent Red 23 in vitro et in vivo, soit l’aniline et le 1-amino-2-naphtol.
Compte tenu de la preuve de génotoxicité et de cancérogénicité du Sudan I, un analogue du Solvent Red 23, et des prévisions de rejet d’amines aromatiques par rupture réductrice des liaisons azoïques du Solvent Red 23 (c.-à-d. le 4-aminoazobenzène), la génotoxicité et la cancérogénicité sont considérées comme des effets critiques pour la caractérisation des risques du Solvent Red 23. Compte tenu du potentiel d’exposition de l’ensemble de la population provenant des cosmétiques et des produits de soins personnels contenant du Solvent Red 23 et du potentiel de génotoxicité et de cancérogénicité ayant une probabilité d’effets nocifs à tous les niveaux d’exposition, il est conclu que le Solvent Red 23 pénètre dans l’environnement en quantité, à des concentrations ou dans des conditions qui constituent ou peuvent constituer un danger pour la vie et la santé humaines au Canada.
Incertitudes de l’évaluation des risques pour la santé humaine
Comme il existe peu de données relatives aux effets sur la santé du Solvent Red 23 lui-même, le profil de risque est principalement fondé sur celui des produits potentiels de la rupture des liaisons azoïques et des colorants azoïques analogues. Bien que les données disponibles sur le métabolismein vitro du Solvent Red 23 dans lesquelles étaient utilisées des bactéries du tractus gastrointestinal semblent indiquer la probabilité d’une rupture réductrice des liaisons azoïques après une exposition orale, il existe une incertitude sur l’étendue de la rupture ainsi que la proportion et l’identité relatives des produits de rupture générés. Par conséquent, il existe une incertitude sur le degré d’exposition de l’ensemble de la population canadienne aux produits potentiels de la rupture des liaisons azoïques du Solvent Red 23 par voie orale.
Il existe une incertitude quant au potentiel d’absorption cutanée du Solvent Red 23 et à la possibilité que les amines aromatiques soient rejetés à l’exposition cutanée. Une valeur d’absorption cutanée de 26 % a été choisie d’après les propriétés physiques et chimiques du Solvent Red 23 et les données empiriques de l’analogue Sudan I. Cette valeur d’absorption cutanée est toutefois considérée comme prudente.
Le degré de confiance voulant que le Solvent Red 23 (ou ses produits de rupture prévus) soit absorbé par la voie orale en raison de l’induction d’enzymes observée chez de nombreuses espèces après une exposition est plus élevé par voie orale que par voie cutanée. Il existe également un degré de confiance élevé que le Solvent Red 23 subisse une rupture des liaisons azoïques, puis rejettent des amines aromatiques après une exposition par voie orale, comme l’a démontré la rupture des liaisons azoïques par des bactéries intestinales isolées. Donc, il existe une préoccupation relative plus importante pour la voie d’exposition orale (c.-à-d. le brillant et le baume à lèvres) dont le risque potentiel est soutenu par les données disponibles. Même si l’absence de données complémentaires n’empêche pas que des risques possibles augmentent suite à l’exposition par voie cutanée, les risques potentiels des effets sur la santé de l’exposition par voie cutanée sont considérés comme inférieurs à ceux posés suite à l’exposition par voie orale.
Les estimations des expositions au Solvent Red 23 par des cosmétiques et certains produits de soins personnels sont considérées comme des surestimations d’après plusieurs hypothèses prudentes telles que l’absorption cutanée de 26 % et l’utilisation de la limite supérieure de la fourchette des concentrations déclarées dans les produits de la base de données du SDC. Toutefois, il se peut que l’exposition totale au Solvent Red 23 soit sous-estimée, car ces estimations n’ont pas été calculées pour les usages simultanés des nombreux cosmétiques ou produits de soins personnels. Il demeure qu’on a confiance que l’exposition de l’ensemble de la population canadienne au Solvent Red 23 par ces produits ne dépasse pas les estimations présentées dans la présente évaluation.
D’après les renseignements contenus dans la présente évaluation préalable finale, le Solvent Red 23 ne pénètre pas dans l’environnement en une quantité, à une concentration ou dans des conditions de nature à avoir, immédiatement ou à long terme, un effet nocif sur l’environnement ou sur la diversité biologique, ou à mettre en danger l’environnement essentiel pour la vie. De plus, cette substance répond aux critères de persistance, mais ne répond pas aux critères relatifs au potentiel de bioaccumulation énoncés dans le Règlement sur la persistance et la bioaccumulation (Canada, 2000).
Compte tenu de l’exposition potentielle de l’ensemble de la population et de la preuve de génotoxicité et de cancérogénicité du 4-aminoazobenzène (produit potentiel de la rupture des liaisons azoïques) et du Sudan I (colorant azoïque analogue), il est conclu que le Solvent Red 23 pénètre dans l’environnement à une quantité, à une concentration ou dans des conditions de nature à constituer un danger au Canada pour la vie ou la santé humaines.
Par conséquent, il est conclu que le Solvent Red 23 satisfait à un ou plusieurs des critères établis dans l’article 64 de la LCPE (1999).
Considérations dans le cadre d’un suivi
Le Solvent Red 23 appartient à un groupe de substances azoïques pouvant être métabolisées et produire des amines aromatiques qui, en tant que classe, sont connues pour présenter des propriétés dangereuses, notamment en termes de cancérogénicité. Par conséquent, des activités supplémentaires (p. ex., recherche, évaluation, contrôle et surveillance) pourraient être entreprises afin de caractériser le risque présenté par ce vaste groupe de substances azoïques pour la santé humaine au Canada. Un avis d’intention décrivant la façon dont Santé Canada et Environnement Canada se pencheront sur ce groupe de substances se trouve à l’adresse Internet desSubstances chimiques.
ACD/pKaDB [module de prévision]. 2005. Version 9.04. Toronto (Ont.) : Advanced Chemistry Development. [réserve de consultation]
Anliker, R., Clarke, E.A., Moser, P. 1981. Use of the partition coefficient as an indicator of bioaccumulation tendency of dyestuffs in fish. Chemosphere 10(3):263-274.
Anliker, R., Moser, P. 1987. The limits of bioaccumulation of organic pigments in fish: their relation to the partition coefficient and the solubility in water and octanol.Ecotoxicol. and Environ. Safety 13:43-52.
Anliker, R., Moser, P., Poppinger, D. 1988. Bioaccumulation of dyestuffs and organic pigments in fish. Relationships to hydrophobicity and steric factors. Chemosphere17(8):1631-1644.
[ARLA] Agence de réglementation de la lutte antiparasitaire. 2010. Liste des produits de formulation de l’ARLA [en ligne]. Ottawa (Ont.) : Santé Canada, ARLA. [consulté le 13 janvier 2011].
Arnot, J.A., Arnot, M., Mackay, D., Couillard, Y., MacDonald, D., Bonnell, M., Doyle, P. 2010. Molecular size cut-off criteria for screening bioaccumulation potential: Fact or fiction?Integrated Environmental Assessment and Management6(2):210-224.
Aronson, D., Boethling, B., Howard, P., Stiteler, W. 2006. Estimating biodegradation half-lives for use in chemical screening.Chemosphere 63:1953-1960.
Au, W., Hsu, T.C. 1979. Studies on the clastogenic effects of biologic stains and dyes. Environ. Mutagen. 1:27-35.
BASF. 1990. Bericht uber die Prufung der akuten Toxizitit an der Goldorfe (Leuciscus idus L.,Goldvariante). Présenté par l’ETAD à Environnement Canada le 13 août 2008 par courriel.
Baughman, G.L., Perenich, T.A. 1988. Fate of dyes in aquatic systems: I. Solubility and partitioning of some hydrophobic dyes and related compounds. Environ. Toxicol. Chem.7(3):183-199.
Baughman, G.L., Weber, E.J. 1994. Transformation of dyes and related compounds in anoxic sediment: kinetics and products.Environ. Sci. Technol. 28(2):267-276.
Baughman, G.L., Bannerjee, S., Perenich, T.A. 1996. Dye Solubility. In: Physico-chemical Principles of Color Chemistry. Peters, A.T., Freeman, H.S. (éditeurs). Advances in Color Chemistry Series, Vol. 4. Glasgow (Écosse) : Blackie Academic and Professional Publishers. p. 145-195.
[BBM] Baseline Bioaccumulation Model. 2008. Gatineau (Qc) : Environnement Canada, Division des substances existantes. [modèle basé sur celui de Dimitrov et al., 2005]. Document disponible sur demande.
[BDIPSN] Base de données d’ingrédients de produits de santé naturels. 2010. Ottawa (Ont.) : Santé Canada. [consultée en juin 2010].
[BDPSNH] Base de données des produits de santé naturels homologués [en ligne]. 2010. Ottawa (Ont.) : Santé Canada. Accès : Qu'est-ce que l'extrait des données de la Base des données des produits de santé naturels homologués (BDPSNH)? [consultée en juin 2010]
[BfR] Institut fédéral allemand d’évaluation des risques (BfR Allemagne). 2003. Dyes Sudan I to IV in food : prise de position du BfR du 19 nov. 2003.
[BIBRA] Bibra Toxicology Advice and Consulting. 1989. Toxicity Profile: para-Aminoazobenzene. Surrey (Royaume-Uni).
[BIOWIN] Biodegradation Probability Program for Windows [modèle d’estimation]. 2008. Version 4.02. Washington (DC) : US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY) : Syracuse Research Corporation. Outils d'évaluation de l'exposition et des modèles.
Boethling, R.S., Howard, P.H., Beauman, J.A., Larosche, M.E. 1995. Factors for intermedia extrapolations in biodegradability assessment. Chemosphere 30(4):741-752.
Bonser, G.M., Bradshaw, L., Clayson, D.B., Jull, J.W. 1956. A further study of the carcinogenic properties of ortho hydroxy-amines and related compounds by bladder implantation in the mouse. Br. J. Canc. 10(3):539-546.
Braun, H. 1991. A new method for the determination of the solubility of disperse dyes. JSDC 107:77-83.
Brown, D. (ICI Group Environmental Laboratory, Brixham, Royaume-Uni). Environmental assessment of dyestuffs. Rédigé pour le compte de l’Ecological and Toxicological Association of the Dyes and Organic Pigments Manufacturers, Bâle (Suisse), ETAD ecological sub-committee project E3020, 1992. Présenté à Environnement Canada le 9 mai 2008.
Brown, D. 1987. Effects of colorants in the aquatic environment.Ecotox Environ. Safe 13:139-147.
Brown, D., Anliker, R. 1988. Dyestuffs and the environment – A risk assessment. Risk Assessment of Chemicals in the Environment. Richardson, M. (éd.). The Royal Society of Chemistry. P. 398−413. [comme cité dans : EPA du Danemark 1999].
Canada. 1978. Règlement sur les aliments et drogues. C.R.C., ch. 870.
Canada. 1999. Loi canadienne sur la protection de l’environnement (1999). L.C., 1999, ch. 33.
Canada. 2000. Loi canadienne sur la protection de l’environnement (1999) : Règlement sur la persistance et la bioaccumulation, C.P. 2000-348, 23 mars 2000, DORS/2000-107.Gazette du Canada, Partie II, vol. 134, n° 7.
Canada. Ministère de l’Environnement, ministère de la Santé. 1994. Liste des substances d’intérêt prioritaire, rapport d’évaluation : Aniline. Ministre des Approvisionnements et Services Canada, n° de cat. En 40-215/35E. Ottawa (Ont.) : Beauregard Printers, Ltd. 30 p.
Canada, Ministère de l’Environnement, Ministère de la Santé. 2006a. Loi canadienne sur la protection de l’environnement (1999) : Avis d’intention d’élaborer et de mettre en œuvre des mesures d’évaluation et de gestion des risques que certaines substances présentent pour la santé des Canadiens et leur environnement. Gazette du Canada, Partie I, vol. 140, n° 49.
Canada. Ministère de l’Environnement, ministère de la Santé. 2006b. Loi canadienne sur la protection de l’environnement (1999) : Avis concernant certaines substances considérées comme priorité pour suivi, Gazette du Canada, Partie I, vol. 140, n° 9.
Canada. Ministère de l’Environnement, ministère de la Santé. 2008a. Loi canadienne sur la protection de l’environnement (1999) : Avis de sixième divulgation d’information technique concernant les substances identifiées dans le Défi, Canada Gazette. Partie I, vol. 142, n° 22.
Canada. Ministère de l’Environnement. 2008b. Loi canadienne sur la protection de l’environnement (1999) : Avis concernant certaines substances identifiées dans le sixième lot du Défi. Canada Gazette. Partie I, vol. 142, n° 22.
Canada. Ministère de la Santé, ministère de l’Environnement. 2010. Loi canadienne sur la protection de l'environnement (1999) : Rapport de suivi : aniline.
Carson, S. 1984. Skin Painting Studies in Mice on 11 Fd&C and D&C Colors: Fd&C Green no. 3, Red No. 2, Red No. 4, Yellow No. 6, and External D&C No. 7, D&C Orange No. 4, Violet No. 2, Red No. 17, Red No. 34, and Yellow No. 7.Cutaneous and Ocular Toxicology 3(3):309-331. [cité dans CSPC, 2005].
CASETOX [module de prévision]. 2008. Version 2.0. Beachwood (OH) : MultiCASE Inc. CASETOX [réserve de consultation].
[CATABOL] Probabilistic assessment of biodegradability and metabolic pathways [modèle informatique]. c2004-2008. Version 5.10.2. Bourgas (Bulgarie) : Prof. Assen Zlatarov University, Laboratory of Mathematical Chemistry. CATALOGIC.
Chadwick, R.W., George, S.E., Claxton, L.D. 1992. Role of the gastrointestinal mucosa and microflora in the bioactivation of dietary and environmental mutagens or carcinogens. Drug Metab Rev 24(4):425-492.
ChemCAN [Level III fugacity model of 24 regions of Canada]. 2003. Version 6.00. Peterborough (Ont.): Trent University, Le centre canadien de modélisation et de chimie environnementales [consulté en janvier 2010].
Chen, H. 2006. Recent advances in azo dye degrading enzyme research. Curr. Protein Pept. Sci. 7(2):101-111.
Chen, H., Xu, H., Heinze, T.M., Cerniglia, C.E. 2009. Decolorization of water and oil-soluble azo dyes byLactobacillus acidophilus and Lactobacillus fermentum. J. Ind. Microbiol. Biotechnol. 36:1459-1466.
[CII] Color Index International [base de données sur Internet]. 2002- . 4e éd. Research Triangle Park (NC) : American Association of Textile Chemists and Colorists. Indice de couleur international [consultée le 3 février 2009].
[CIRC] Centre International de Recherche sur le Cancer. 1975.Monographies du CIRC sur l’évaluation des risques de cancérogénicité pour l’homme: Certains composés aromatiques azoïques, Volume 8. IARC Working Group on the Evaluation of the Risk of Chemicals to Man which met in Lyon, 26 novembre au 2 décembre 1974.
[CIRC] Centre International de Recherche sur le Cancer. 1987.Monographies sur l’évaluation des risques de cancérogénicité pour l’homme. Supplement 7 : Overall evaluations of carcinogenicity: an updating of IARC Monographs Volumes 1 to 42. Lyon (France) : CIRC.
Clariant. 1996. Ensemble de données IUCLID pour Disperse Blue 79 (N° CAS 12239-34-8). [base de données sur Internet]. [consultée le 28 octobre 2008].
Cohle, P., Mihalik, R. 1991. Early life stage toxicity of C.I. Disperse Blue 79:1 purified presscake to rainbow trout (Oncorhynchus mykiss) in a flow-through system. Final report. Columbia (MO) : ABC Laboratories Inc.
Collier, S.W., Storm, J.E., Bronaugh, R.L. 1993. Reduction of azo dyes during in vitro percutaneous absorption.Toxicol. Appl. Pharmacol. 118:73-79.
Commission européenne. 2006. Règlement (CE) n° 1907/2006 du Parlement européen et du Conseil (REACH).
Commission européenne. 2008. Règlement (CE) n° 1272/2008 relatif à la classification, à l’étiquetage et à l’emballage des substances et des mélanges.
Commission européenne. 2010. Directive 76/768/CEE du Conseil (Directive relative aux produits cosmétiques).
Communauté européenne. 1994. Directive du Conseil et du Parlement européen n° 94/36/CE du 30 juin 1994 sur les colorants aux fins d’utilisation dans les produits alimentaires. Journal officiel de l’Union européenne.
[ConsExpo] Consumer Exposure Model [en ligne]. 2006. Version 4.1. Bilthoven (Pays-Bas) : Rijksinstituut voor Volksgezondheid en Milieu (Institut national néérlandais de la santé publique et de l’environnement). ConsExpo 4.1.
[CPOP] Canadian POP Model. 2008. Gatineau (Qc) : Environnement Canada, Division des substances existantes; Bourgas (Bulgarie) : Prof. Assen Zlatarov University, Laboratory of Mathematical Chemistry. [Modèle élaboré à partir de celui de Mekenyan et al., 2005]. Disponible sur demande.
[CSC] Comité scientifique de cosmétologie.1988. Reports of the Scientific Committee on Cosmetology (Seventh Series). ISBN 92-825-8129-2. N° de catalogue CD-NA-11303-EN-C.
[CSPC] Comité scientifique des produits de consommation. 2001.Avis concernant les ingrédients chimiques dans les produits cosmétiques classés comme cancérogènes, mutagènes ou toxiques pour la reproduction selon la directive 67/548/EEC. SCCNFP/0474/01.
[CSPC] Comité scientifique des produits de consommation. 2004.Avis concernant les ingrédients chimiques dans les produits cosmétiques classés comme cancérogènes, mutagènes ou toxiques pour la reproduction selon la directive 67/548/EEC. SCCNFP/0825/04.
[CSPC] Comité scientifique des produits de consommation. 2005.Avis sur l'utilisation de CI26100 (CI Solvent Red 23) comme colorant dans les produits cosmétiques. SCCP/0902/05.
[CSPC] Comité scientifique des produits de consommation. 2006. Opinion on p-Phenylenediamine. SCCP/0989/06.
Datyner, A. 1978. The solubilisation of disperse dyes by dispersing agents at 127ºC. JSDC June 256-260.
[DEREK] Deductive Estimation of Risk from Existing Knowledge [module de prévision sur cédérom]. 2008. Version 10.0.2. Cambridge (MA) : Harvard University, LHASA Group. Prédiction de toxicologie [réserve de consultation].
Dillon, D., Combes, R., Zeiger, E. 1994. Activation by caecal reduction of the azo dye D and C red no. 9 to a bacterial mutagen.Mutagenesis 9(4):295-299.
Dimitrov, S, Dimitrova, N., Walker, J., Veith, G., Mekenyan, O. 2002. Predicting bioconcentration potential of highly hydrophobic chemicals. Effect of molecular size. Pure Appl. Chem. 74(10):1823-1830.
Dimitrov, S., Dimitrova, N., Parkerton, T., Comber, M., Bonnell, M., Mekenyan, O. 2005. Base-line model for identifying the bioaccumulation potential of chemicals. SAR QSAR Environ. Res. 16(6):531-554.
[EPA du Danemark] Danish Environmental Protection Agency. 1999.Enquête sur les colorants azoïques au Danemark. Consumption, use, health and environmental aspects. MiljØprojekt No. 509. Henriette, Danish Technological Institute, Environment, Ministry of Environment and Energy, Denmark, Danish Environmental Protection Agency, 1999. Rapport rédigé par Øllgaard, H., Frost, L., Galster, J., Hansen, O.C.
[EFSA] Autorité européenne de sécurité des aliments. 2005. Avis du groupe scientifique sur les additifs alimentaires, les arômes, les auxiliaires technologiques et les matériaux en contact avec les aliments [AFC] sur l’évaluation de la toxicologie d’un certain nombre de colorants illégalement présents dans l’alimentation au sein de l’UE. EFSA Journal (2005) 263:1-71. Article en anglais; résumé en français.
Environnement Canada. 1988. Données de la Liste intérieure des substances (LIS), 1984-1986, recueillies en vertu du paragraphe 25(1) de la LCPE (1988), et conformément à la Liste intérieure des substances : guide du déclarant. Données préparées par : Environnement Canada.
Environnement Canada. 1995. NSN submission. Données présentées à la Division des substances nouvelles d’Environnement Canada dans le cadre du Programme de renseignements concernant les substances nouvelles.
Environnement Canada. 2000. Environmental Categorization for Persistence Bioaccumulation and Inherent Toxicity of Substances on the Domestic Substances List Using QSARs. Rapport final. Division de l’évaluation des produits chimiques, Environnement Canada, juillet.
Environnement Canada. 2006. Données pour certaines substances recueillies en vertu de la Loi canadienne sur la protection de l’environnement (1999), article 71 : Avis concernant certaines substances considérées comme priorités pour suivi. Données préparées par Environnement Canada, Santé Canada, Programme des substances existantes.
Environnement Canada. 2007. QSARs: Reviewed Draft Working Document, Science Resource Technical Series, Guidance for Conducting Ecological Assessments under CEPA 1999. Division des substances existantes, Environnement Canada, Gatineau (Qc) : Environnement Canada, Division des substances existantes. Ottawa, K1A 0H3.
Environnement Canada. 2008a. Données sur les substances du lot 6 recueillies en vertu de l’article 71 de la Loi canadienne sur la protection de l’environnement (1999) : Avis concernant certaines substances identifiées dans le sixième lot du Défi. Données recueillies par Environment Canada, Programme des substances existantes.
Environnement Canada. 2008b. Guidance for conducting ecological assessments under CEPA, 1999: science resource technical series, technical guidance module: Mega Flush consumer release scenario. Document de travail préliminaire. Gatineau (Qc) : Environnement Canada, Division des substances existantes.
Environnement Canada. 2010. Rapport Mega Flush : Solvent Red 23 [consulté le 26 juillet 2010]. Rapport inédit. Gatineau (Qc) : Environnement Canada, Division des substances existantes.
[EPIsuite] Estimation Programs Interface Suite for Microsoft Windows [modèle d’estimation]. 2008. Version 4.0 Washington (DC) : US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY) : Syracuse Research Corporation. Outils d'évaluation de l'exposition et des modèles.
[ESIS] European Chemical Substances Information System [base de données sur Internet]. 2008. Version 5. Bureau Européen des Substances Chimiques (BESC). Système d'information des substances chimiques européenne [consulté le 13 février 2009].
[ESIS] European Chemical Substances Information System [base de données sur Internet]. c1995-2010. Ispra (Italie) : Commission européenne, Centre commun de recherche, Institut pour la santé et la protection des consommateurs, Bureau Européen des Substances Chimiques (BESC). [consultée en octobre 2009]. Système d'information des substances chimiques européenne (recherche dans l’onglet CLP Annex VI).
[ETAD] Ecological and Toxicological Association of Dyes and Organic Pigments Manufacturers. 1992. Draft Guidelines for the Assessment of Environmental Exposure to Dyestuffs.
[ETAD] Ecological and Toxicological Association of Dyes and Organic Pigments Canadian Affiliates, Dayan, J., Trebitz, H., consultants. 1995. Health and environmental information on dyes used in Canada. Rapport inédit présenté à Environnement Canada, Division des substances nouvelles. En page couverture : An overview to assist in the implementation of the New Substances Notification Regulations under the Canadian Environmental Protection Act.
[ETAD] Ecological and Toxicological Association of Dyes and Organic Pigments Manufacturers. 2005. Information received in support of DSL categorization for 12 disperse dyes. Courriel daté du 27 octobre 2005.
Fujita, S., Matsunaga, T., Masubunchi, Y., Suzuki, T. 1988. Possible mechanism of Sudan III-induced prevention of chemical carcinogenesis in rats. Canc. Res. 48:254-259.
Garner, R.C., Nutman, C.A.. 1977. Testing of some azo dyes and their reduction products for mutagenicity using salmonella typhimurium TA1538. Mutat Res 44:9-19.
Golka, K., Kopps, S., Myslak, Z.W. 2004. Carcinogenicity of azo colorants: influence of solubility and bioavailabilty. Toxicol. Lett. 151(1):203-210.
Gray, E.L., Ostby, J.S. 1993. The effects of prenatal administration of azo dyes on testicular development in the mouse: A structure activity profile of dyes dervived from benzidine, dimethylbenzidine, or dimethoxybenzidine. Fund. Appl. Toxicol. 20:177-183.
Haag, W.R., Mill, T. 1987. Direct and indirect photolysis of water-soluble azodyes: kinetic measurements and structure-activity relationships. Environ. Toxicol. Chem. 6:359-369.
Hatakeyama, S., Hayasaki, Y., Masuda, M., Kazusaka, A., Fujita, S. 1996. Mechanism for mouse strain differences in the protective effect of Sudan III against the in vivo genotoxicity of 7,12-dimethylbenz[a]anthracene. Toxicol. Lett.89(3):231-9.
Heidelberger, C., Freeman, A.E., Pienta, R.J., Sivak, A., Bertram, J.S., Casto, B.C., Dunkel, V.C., Francis, M.W., Kakunaga, T., Little, J.B., Schechtman, L.M. 1983. Cell transformation by chemical agents: a review and analysis of the literature: a report of the U.S. Environmental Protection Agency Gene-Tox program.Mutat. Res. 114:283-385.
Huggins, C.B., Pataki, J. 1965. Aromatic azo derivatives preventing mammary cancer and adrenal injury from 7,12-dimethylbenz[a]anthracene. Proc. Nat. Acad. Sci. 53:791-796.
Huggins, C.B., Ueda, N., Russo, A. 1978. Azo dyes prevent hydrocarbon-induced leukemia in the rat. Proc. Nat. Acad. Sci. 9:4524-4527.
Hunger, K. (éd). 2003. Industrial dyes; chemistry, properties, applications. Weinheim (Allemagne) : WILEY-VCH Verlag GmbH & Co. KGaA.
Isik, M., Sponza, D.T. 2004. Monitoring of toxicity and intermediates of C.I. Direct Black 38 azo dye through decolourization in an anaerobic/aerobic sequential reactor system.Journal of Hazardous Materials B114: 29−39.
Kada, T., Tutikawa, K., Sadaie, Y. 1972. In vitro and host-mediated ‘rec-assay’ procedures for screening chemical mutagens; and phloxine, a mutagenic red dye detected. Mutat. Res. 16:165-174.
Kier, L.D., Brusick, D.J., Auletta, A.E., Von Halle, E.S., Brown, M.M., Simmon, V.F., Dunkel, V., Mccann, J., Mortelmans, K., Prival, M., Rao, T.K., Ray, V. 1986. The salmonella typhimurium/mammaliam microsomal assay: a report of the U.S. Environmental Protection Agency Gene-Tox program. Mutat Res 168:69-240.
Kozuka, T., Tashiro, M. 1980. Pigmented contact dermatitis from azo-dyes. Cross sensitivity in humans. Contact Dermatitis6:330-336.
Liefer, Z., Kada, T., Mandel, M., Zeiger, E., Stafford, R., Rosenkranz, H.S. 1981. Evaluation of tests using DNA repair-deficient bacteria for predicting genotoxicity and carcinogenicity: report of the U.S. EPA’s gene-tox program.Mutat Res 87:211-297.
Mamber, S.W., Bryson, V., Katz, S.E. 1983. The Escherichia coli WP2/WP100 rec assay for detection of potential chemical carcinogens. Mutat. Res. 119:135-144.
Maruya, H. 1938. Renal changes in albino rats induced by the oral administration of various azo pigments and aromatic amino compounds. Trans. Soc. Path Jap. 28:541-547.
Mekenyan, G., Dimitrov, S.D., Pavlov, T.S., Veith, G.D. 2005. POPs: A QSAR system for creating PBT profiles of chemicals and their metabolites. SAR QSAR Environ. Res.16(1-2):103−133.
[MITI] Ministry of International Trade & Industry (Japon). 1992. Biodegradation and bioaccumulation data of existing chemicals based on the CSCL Japan, Basic Industries Bureau, Chemical Products Safety Division. Japan Chemical Industry Ecology-Toxicology & Information Centre,Tokyo (Japon).
Miyagoshi, M., Hayakawa, Y., Nagata, M., Nagayama, T. 1985. Mutagenic activities of commercial sudan III and scarlet red are due to impurities. Eisei Kagaku 31(2):79-86.
[NCI] National Chemical Inventories [base de données sur cédérom]. 2006. Columbus (OH) : American Chemical Society. [consultée le 11 décembre 2006]. Inventaire nationale des produits chimiques sur CD.
Nishida, K., Ando, Y., Ohwada, K., Mori, T., Koide, M., Koukitsu, A. 1989. Vapour pressures and heats of sublimation of some azo disperse dyes. JSDC 105:112-114.
[NTP] United States National Toxicology Program. 1982. TR 226: Cancérogenèse d'essais biologiques du C.I. Solvent Yellow 14 (N° CAS 842-07-9) dans le rat F344/N et la sourit B6C3F1 (Étude d'alimentation).
[NTP] United States National Toxicology Program. 2005. 11th Report on Carcinogens (RoC). U.S. Department of Health and Human Services, Public Health Service.
[NTP] United States National Toxicology Program. 2010. Status d'essai d'agents au programme national de toxicologie : CI Solvent yellow 14.
[OCDE] Organisation de coopération et de développement économiques. 1996. Lignes directrices de l’OCDE pour les essais de produits chimiques, n° 305B. Bioconcentration : Essai semi-statique chez le poisson. Paris : OCDE, adoptée en juin 1996.
Odabasoglu, M., Çakmak, S., Turgut, G., Içbudak, H. 2003. Preparation and characterization of chromophor group containing cyclotriphosphazenes: III bis-azo chromophor carrying some cyclotriphosphazenes. Phosphorus, Sulfur and Silicon178:549-558.
O’Neil, M.J. 2006. The Merck Index - An Encyclopedia of Chemicals, Drugs and Biologicals. Fourteenth Edition.Whitehouse Station (NJ) : Merck & Co., Inc. p. 1523-1524.
Pagga, U., Brown, D. 1986. The degradation of dyestuffs: Part II Behaviour of dyestuffs in aerobic biodegradation tests. Chemosphere. 15, 4, 479-491.
Parent, R.A., Dressler, I. 1977. Absorption and distribution of C.I. Solvent Red 24 in rats: intra-tracheal adminstration of labeled dye. Drug & Chemical Toxicology2(4):409-420.
[PhysProp] Interactive PhysProp Database [base de données sur Internet]. 2006. Syracuse (NY) : Syracuse Research Corporation.Démo de la base de données intéractives PhysProp [consulté le 16 février 2009].
Étude présentée. 2008a. Projet non publié et confidentiel présenté à la Division des substances existantes d’Environnement Canada dans le cadre du Plan de gestion des produits chimiques. Disponible en tant que Sommaire de rigueur d’étude, n° 11887Challenge006.
Étude présentée. 2008b. Projet non publié et confidentiel présenté à la Division des substances existantes d’Environnement Canada dans le cadre du Plan de gestion des produits chimiques. Disponible en tant que Sommaire de rigueur d’étude, n° 12890Challenge006.
Prikryl, J., Rusicka, Burgert, L. 1979. A new method of determining the solubility of disperse dyes. JSDC octobre: 349-351.
Platzek, T., Lang, C., Grohmann, G., Gi, U.S., Baltes, W. 1999. Formation of a carcinogenic aromatic amine from an azo dye by human skin bacteria in vitro. Hum. Exp. Toxicol. 18(9):552-559.
Prival, M.J., Mitchell, V.D. 1982. Analysis of a method for testing azo dyes for mutagenic activity in Salmonella typhimurium in the presence of flavin mononucleotide and hamster liver S9. Mutat. Res. 97(2):103-16.
ProSciTech. 2006. Fiche signalétique : Sudan III [en ligne].
Razo-Flores, E., Luijten, M., Donlon, B., Lettinga, G., Field, J. 1997. Biodegradation of selected azo dyes under methanogenic conditions. Wat. Sci. Technol. 36(6-7):65-72.
Romero, F.J., Romá , J., Bosch-Morell, F., Romero, B., Segura-Aguilar, J., Llombart-Bosch, A., Ernster, L. 2000. Reduction of brain antioxidant defense upon treatment with butylated hydroxyanisole (BHA) and Sudan III in Syrian golden hamster.Neurochem Res. 25(3):389-93.
[RIVM] Rijksinstituut voor Volksgezondheid en Milieu. 2006.Fiche cosmétiques. Pour évaluer les risques pour le consommateur.
Ryan, A.J., Welling, P.G. 1967. Some Observations on the Metabolism and Excretion of the Bisazo Dyes Sudan III and Sudan IV.Fd. Cosmet. Toxicol. 5:755-761.
Sakuratani, Y., Noguchi, Y., Kobayashi, K., Yamada, J., Nishihara, T. 2008. Molecular size as a limiting characteristic for bioconcentration in fish. J. Environ. Biol. 29(1):89-92.
Santé Canada. 1994. Loi canadienne sur la protection de l’environnement. L’évaluation du risque à la santé humaine des substances d’intérêt prioritaire. Ottawa (Ont.) : Ministre des Approvisionnements et Services Canada.
Santé Canada. 1995. Règlement sur les aliments et les drogues, partie C − Drogues.
Santé Canada 2007. Règlement sur les aliments et drogues, partie B − Aliments.
Santé Canada. 2009. Liste critique des ingrédients dont l’utilisation est restreinte ou interdite dans les cosmétiques − septembre 2009 [en ligne]. Ottawa (Ont.) : Santé Canada,Sécurité des produits de consommation [consultée le 6 janvier 2010].
Sasaki, H., Kojima, M., Nakamura, J., Shibasaki, J. 1990. Enhancing effect of pyrrolidone derivatives on the transdermal penetration of sulfaguanidine, aminopyrine and Sudan III.Journal of Pharmacobio-dynamics 13(3):200-205.
[SCCNFP] Safety Committee on Cosmetic Products and Non-Food Products Intended for Consumers. 2002. Le révision de sûreté de l'utilisation de certains colorants azoïques dans les produits cosmétiques. SCCNFP/0495/01.
Seifried, H.E., Seifried, R.M., Clarke, J.J., Junghans, T.B., San, R.H.C. 2006. A compilation of two decades of mutagenicity test results with the ames salmonella typhimurium and L5178Y mouse lymphoma cell mutation assays. Chem Res Toxicol19:627-644.
[SDC] Système de déclaration des cosmétiques [base de données exclusive]. 2009. Disponible auprès de Santé Canada, Division des cosmétiques.
Shen, G., Hu, S. 2008. Bioconcentration Test of C.I. Disperse Orange 30 in Fish. Préparé par Environmental Testing Laboratory, Shanghai Academy of Environmental Sciences, Shanghai (Chine) pour Dystar au nom de l’Ecological and Toxicological Association of the Dyes and Organic Pigments Manufacturers (ETAD), Bâle (Suisse). Rapport n° S-070-2007. Présenté à Environnement Canada en avril 2008. N° de déclaration dans le cadre du défi : 8351.
Sijm, D.T.H.M., Schuurmann, G., deVries, P.J., Opperhuizen, A. 1999. Aqueous solubility, octanol solubility, and octanol/water partition coefficient of nine hydrophobic dyes. Environ. Toxicol. Chem. 18(6):1109-1117.
[SPIN] Substances in Products in Nordic Countries [base de données sur Internet]. 2008. Projet financé par le Conseil des ministres des pays nordiques, Groupe chimique. Substances dans les produits dans les pays nordiques [consulté en décembre 2008].
Stingley, R.L., Zou, W., Heinze, T.M., Chen, H., Cerniglia, C.E. 2010. Metabolism of azo dyes by human skin microbiota. J. Med. Microbiol. 59(Pt.1):108-114.
[TOPKAT] TOxicity Prediction by Komputer Assisted Technology [en ligne]. 2004. Version 6.2. San Diego (CA) : Accelrys Software Inc. [consulté le 7 janvier 2009].
Tsuda, S., Matsusaka, N., Madarame, H., Ueno, S., Susa, N., Ishida, K., Kawamura, N., Sekihashi, K., Sasaki, Y.F. 2000. The comet assay in eight mouse organs: results with 24 azo compounds.Mutat. Res. 465:11-26.
[UE] Union européenne. 2004. . European Chemicals Bureau Risk Assessment Report. Rapport définitif : Aniline.
Umeda, M. 1957. Production of rat sarcoma by injections of Tween 80 solution of scarlet red. Gann 48:579-580.
Umeda, M. 1958. Prodution of rat sarcoma by injections of Tween 80 solution of scarlet re. Gann 49:27-31.
[USEPA] United States Environmental Protection Agency. 2008.Les ingrédients inertes autorisés pour utilisation dans des produits non alimentaires et utilisation des pesticides. [en ligne].
[USFDA] United States Food and Drug Administration. 2007. Color Additive Status List. [en ligne].
[USFDA] United States Food & Drugs Administration. 2009.Liste des statuts de couleurs additives.
Waterman, N., Lignac, G.O.E. 1958 The influence of the feeding of a number of food colours on the occurrence of tumours in mice.Acta. Physiol. Pharmacol. Neer. 7:35-55.
Willheim, R., Ivy, A.C. 1953. A preliminary study concerning the possibility of dietary carcinogenesis. Gastroenterology23:1-19.
Xie, Z., Hayakawa, R., Sugiura, M., Kojima, H., Konishi, H., Ichihara, G., Takeuschi, Y. 2000. Experimental study on skin sensitization potencies and cross-reactivities of hair-dye=related chemicals in guinea pigs. Contact Dermatitis42:270-275.
Xu, H., Heinze, T.M., Chen, S., Cerniglia, C.E., Chen, H. 2007. Anaerobic metabolism of 1-amino-2-napthol-based azo dyes (Sudan dyes) by human intestinal microflora. Appl. Environ. Microbiol. 73(23):7759-7762.
Yen, C.C., Perenich, T.A., Baughman, G.L. 1989. Fate of dyes in aquatic systems II. Solubility and octanol/water partition coefficients of disperse dyes. Environ. Toxicol. Chem.8(11):981-986.
Yen, C.C., Perenich, T.A., Baughman, G.L. 1991. Fate of commercial disperse dyes in sediments. Environ. Toxicol. Chem. 10:1009-1017.
Yourick, J.J., Sasik, C.T., Bronaugh, R.L. 2007. In vitro dermal absorption and metabolism of D&C red no. 17 in human and porcine skin. J. Cosmet. Sci. 58:255-266.
Zhou, Y., You, X., Ye, X. 1987. Mutgenicity of benzidines and their congener derivative dyes. Huanjing Kexue8(2):31-34.
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 1 | Référence : Bio-elimination study for CAS# 6250-23-3 (Disperse Yellow 23) Clariant dyestuff product = Foron Yellow E RGFL (Étude présentée, 2008b) | |||
| 2 | Identité de la substance : n° CAS | s.o.[1] | Oui | 6250-23-3 |
| 3 | Identité de la substance : nom(s) chimique(s) | s.o. | Oui | Disperse Yellow 23 |
| 4 | Composition chimique de la substance | 2 | Non | |
| 5 | Pureté chimique | 1 | Oui | 54 % Disperse Yellow 23 |
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 6 | Référence | 1 | Non | |
| 7 | Méthode normalisée (OCDE, UE, nationale, ou autre)? | 3 | Non | |
| 8 | Justification de la méthode ou du protocole si une méthode non normalisée a été utilisée | 2 | Non | |
| 9 | BPL (bonne pratique de laboratoire) | 3 | s.o. (étude réalisée en 1976) |
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 10 | Type d’essai (c.-à-d. hydrolyse, biodégradation) | s.o. | Oui | Biodégradation |
| 11 | Conditions d’essai (aérobie ou anaérobie) | s.o. | Non | Non indiqué |
| 12 | Milieu d’essai (eau, sédiments ou sol) | s.o. | Oui | Eau (par déduction d’après la concentration d’essai exprimée en mg/L) |
| 13 | Durée de l’essai | s.o. | Oui | 14 jours |
| 14 | Témoins négatifs ou positifs? | 1 | Non | |
| 15 | Nombre de répétitions (y compris les témoins) | 1 | Non | |
| 16 | Des concentrations mesurées sont-elles indiquées? | 3 | Non | |
| 17 | Méthode ou instrument analytique | 1 | Non |
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 18 | Type de biodégradation (immédiate ou intrinsèque) indiqué? | 2 | Non | Non indiqué |
| 19 | Lorsque le type de biodégradation (immédiate ou intrinsèque) n’est pas signalé, une information indirecte permet-elle l’identification du type de biodégradation? | 1 | Non | |
| 20 | Source de l’inoculum | 1 | Non | |
| 21 | Concentration dans l’inoculum ou nombre de microorganismes | 1 | Non | |
| 22 | Un préconditionnement et une préadaptation de l’inoculum ont-ils été signalés? | 1 | Non | |
| 23 | Le préconditionnement et la préadaptation de l’inoculum étaient-ils appropriés dans le cadre de la méthode utilisée? | s.o. | Non | |
| 24 | Température | 1 | Non | Non indiqué |
| 25 | Le pourcentage de dégradation du composé de référence a-t-il atteint les niveaux requis avant le 14ejour? | s.o. | Non | Pas de composé de référence testé |
| 26 | Sol : humidité du sol signalée? | 1 | ||
| 27 | Sol et sédiments : indication de la teneur de fond en MOS (matière organique du sol)? | 1 | ||
| 28 | Sol et sédiments : teneur en argile signalée? | 1 | ||
| 29 | Sol et sédiments : CEC (capacité d’échange cationique) signalée? | 1 |
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 30 | Valeurs du pH signalées? | 1 | ||
| 31 | Température | 1 | ||
| 32 | Les concentrations appropriées de la substance ont-elles été utilisées? | |||
| 33 | Si un solvant a été utilisé, l’a-t-il été de manière appropriée? |
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 34 | Température | 1 | ||
| 35 | Source lumineuse | 1 | ||
| 36 | Spectre lumineux (nm) | 1 | ||
| 37 | Intensité relative en fonction de l’intensité lumineuse du soleil | 1 | ||
| 38 | Spectre d’une substance | 1 | ||
| 39 | Photolyse indirecte : Sensibilisateur (type) | 1 | ||
| 40 | Photolyse indirecte : concentration du sensibilisateur | 1 |
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 41 | Paramètre et valeur | s.o. | s.o. | Biodégradation moyenne en 14 jours = 51 % |
| 42 | Produits de dégradation | s.o. | Non | |
| 43 | Note : ... % | 4,5 | ||
| 44 | Code de fiabilité d’Environnement Canada : | 4 | ||
| 45 | Catégorie de fiabilité (élevée, satisfaisante, basse) : | Non satisfaisante | ||
| 46 | Remarques | |||
| N° | Élément | Pondération | Oui/non | Précisions | |
|---|---|---|---|---|---|
| 1 | Référence : SHEN, G., HU, S. 2008. Bioconcentration Test of C.I. Disperse Orange 30 in Fish. Préparé par Environmental Testing Laboratory, Shanghai Academy of Environmental Sciences, Shanghai (Chine) pour Dystar au nom de l’Ecological and Toxicological Association of the Dyes and Organic Pigments Manufacturers (ETAD), Bâle (Suisse). Rapport n° S-070-2007. Présenté à Environnement Canada en avril 2008. N° de déclaration dans le cadre du défi 8351. |
||||
| 2 | Identité de la substance : n° CAS | s.o.[1] | Oui | 5261-31-4 | |
| 3 | Identité de la substance : nom(s) chimique(s) | s.o. | Oui | Acétate de 2-[N-(2-cyanoéthyl)-4-[2,6-dichloro-4-nitrophényl)azo]anilino]éthyle | |
| 4 | Composition chimique de la substance | 2 | Non | ||
| 5 | Pureté chimique | 1 | Non | ||
| 6 | Indication de la persistance/stabilité de la substance en milieu aqueux? | 1 | Non | ||
| 7 | Si le matériel d’essai est radiomarqué, est-ce que la ou les positions précises du ou des atomes marqués ainsi que le pourcentage de radioactivité associé aux impuretés ont été rapportés? | 2 | Non | ||
| N° | Élément | Pondération | Oui/non | Précisions | |
|---|---|---|---|---|---|
| 8 | Référence | 1 | Oui | Lignes directrices de l’OCDE pour les essais de produits chimiques n° 305B-1996 | |
| 9 | Méthode normalisée (OCDE, UE, nationale, ou autre)? | 3 | Oui | OCDE | |
| 10 | Justification de la méthode ou du protocole si une méthode non normalisée a été utilisée | 2 | Sans objet | ||
| 11 | BPL (bonne pratique de laboratoire) | 3 | Non | ||
| N° | Élément | Pondération | Oui/non | Précisions | |
|---|---|---|---|---|---|
| 12 | Identité de l’organisme : nom | s.o. | Oui | Poisson zèbre, Brachydanio rerio | |
| 13 | Indication du nom latin ou des deux noms (latin et commun)? | 1 | Oui | Les deux | |
| 14 | Âge ou stade biologique de l’organisme d’essai | 1 | Non | ||
| 15 | Longueur et/ou poids | 1 | Oui | Longueur moyenne du corps 3,91 +/- 0,18 cm et poids moyen du corps 0,32 +/- 0,06 g | |
| 16 | Sexe | 1 | Non | ||
| 17 | Nombre d’organismes par répétition | 1 | Oui | 7 | |
| 18 | Charge en organismes | 1 | Oui | 20 mg/L | |
| 19 | Type de nourriture et périodes d’alimentation pendant la période d’acclimatation | 1 | Oui | Mise au régime avec un poisson du commerce jusqu’à un jour avant le début du test | |
| N° | Élément | Pondération | Oui/non | Précisions | |
|---|---|---|---|---|---|
| 20 | Type d’expérience (en laboratoire ou sur le terrain) | s.o. | Oui | Laboratoire | |
| 21 | Voies d’exposition (nourriture, eau, les deux) | s.o. | Oui | Eau | |
| 22 | Durée de l’exposition | s.o. | Oui | 28 jours | |
| 23 | Nombre de répétitions (y compris les témoins) | 1 | Oui | ||
| 24 | Concentrations | 1 | Oui | 20 mg/L | |
| 25 | Type/composition de la nourriture et périodes d’alimentation (pendant l’essai) | 1 | Oui | Les poissons étaient nourris deux heures avant le renouvellement de l’eau | |
| 26 | Si le ratio FBC/FBA dérivait de la concentration chimique dans l’organisme et dans l’eau, la durée de l’expérience était-elle égale à ou supérieure au temps nécessaire pour que les concentrations chimiques atteignent un état stable? | 3 | Oui | 28 jours | |
| 27 | Si le rapport FBC/FBA a été déterminé comme correspondant au rapport de la concentration du produit chimique dans l’organisme sur sa concentration dans l’eau, est-ce que les concentrations mesurées dans l’organisme et dans l’eau étaient mentionnées? | 3 | Oui | ||
| 28 | Les concentrations dans les eaux d’essai ont-elles été mesurées périodiquement? | 1 | Oui | Sur trois jours distincts | |
| 29 | Les conditions du milieu d’exposition correspondaient-elles au produit chimique particulier signalé? (par exemple, pour la toxicité du métal : pH, DOC/TOC, dureté de l’eau, température) | 3 | Oui | Oui, tous les deux jours | |
| 30 | Photopériode et intensité de l’éclairage | 1 | Oui | 12:12 | |
| 31 | Préparation de solutions mères et de solutions d’essai | 1 | Oui | ||
| 32 | Intervalles des contrôles analytiques | 1 | Oui | Tous les deux jours pour l’oxygène dissous, le pH et la température | |
| 33 | Méthodes statistiques utilisées | 1 | Oui | ||
| 34 | Le solubilisant/émulsifiant a-t-il été utilisé si le produit chimique était faiblement soluble ou instable? | s.o. | Non | ||
| N° | Élément | Pondération | Oui/non | Précisions | |
|---|---|---|---|---|---|
| 35 | L’organisme d’essai correspondait-il à l’environnement au Canada? | 3 | Oui | ||
| 36 | Les conditions d’essai (pH, température, OD, etc.) sont-elles typiques pour l’organisme d’essai? | 1 | Oui | ||
| 37 | Le type et la conception du système (statique, semi-statique, dynamique; ouvert ou fermé; etc.) correspondent-ils aux propriétés de la substance et à la nature ou aux habitudes de l’organisme? | 2 | Oui | Semi-statique | |
| 38 | Le pH de l’eau se situait-il dans la plage des valeurs typiques de l’environnement au Canada (6 à 9)? | 1 | Oui | 7,22 à 7,84 | |
| 39 | La température de l’eau du test se situait-elle dans la plage des valeurs typiques de l’environnement au Canada (5 à 27 °C)? | 1 | Oui | 22 à 23 | |
| 40 | Le contenu lipidique (ou FBA/FBC lipidiquement normalisé) a-t-il été signalé? | 2 | Oui | ||
| 41 | Les concentrations mesurées d’un produit chimique dans l’eau d’essai étaient-elles inférieures à la solubilité dans l’eau du produit chimique? | 3 | Non | ||
| 42 | Si une substance radiomarquée a été utilisée, est-ce que le FBC a été déterminé d’après le composé d’origine (et non d’après les résidus radiomarqués)? | 3 | Non | ||
| N° | Élément | Pondération | Oui/non | Précisions | |
|---|---|---|---|---|---|
| 43 | Les paramètres déterminés (FBA, FBC) et leurs valeurs | s.o. | s.o. | FBC | |
| 44 | FBA ou FBC déterminés comme : 1) le rapport de la concentration en produit chimique produit dans l’organisme, ou 2) le rapport entre les constantes d’incorporation de produit chimique et du taux d’élimination | s.o. | s.o. | 1 | |
| 45 | Le FBA/FBC était-il issu 1) d’un échantillon de tissu ou 2) d’un organisme entier? | s.o. | s.o. | 2 | |
| 46 | Le FBA/FBC 1) moyen ou 2) maximal at-il été utilisé? | s.o. | s.o. | 1 | |
| 47 | Note : % | 67,9 | |||
| 48 | Code de fiabilité d’Environnement Canada : | 2 | |||
| 49 | Catégorie de fiabilité (élevée, satisfaisante, basse) : | Confiance satisfaisante | |||
| 50 | Remarques | La présente procédure est basée sur des conditions semi-statiques (renouvellement des solutions du test tous les deux jours). Par conséquent, les substances d’essai très peu solubles dans l’eau, comme les colorants diazoïques, peuvent aussi être caractérisées selon leur potentiel de bioconcentration sans l’ajout de solvants ou d’autres substances auxiliaires qui pourraient modifier les résultats. | |||
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 1 | Référence : Fish toxicity study for CAS# 6250-23-3 (Disperse Yellow 23) Clariant dyestuff product=Foron Yellow E RGFL (Étude présentée, 2008b) | |||
| 2 | Identité de la substance : n° CAS | s.o.[1] | Oui | 6250-23-3 |
| 3 | Identité de la substance : nom(s) chimique(s) | s.o. | Oui | Disperse Yellow 23 |
| 4 | Composition chimique de la substance | 2 | Non | |
| 5 | Pureté chimique | 1 | Oui | 54 % DY23 |
| 6 | Indication de la persistance/stabilité de la substance en milieu aqueux? | 1 | Non | |
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 7 | Référence | 1 | Non | |
| 8 | Méthode normalisée (OCDE, UE, nationale, ou autre)? | 3 | Non | |
| 9 | Justification de la méthode ou du protocole si une méthode non normalisée a été utilisée | 2 | Non | |
| 10 | BPL (bonne pratique de laboratoire) | 3 | s.o. (étude réalisée en 1974) |
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 11 | Identité de l’organisme : nom | s.o. | Oui | Truite arc-en-ciel |
| 12 | Indication du nom latin ou des deux noms (latin et commun)? | 1 | Non | |
| 13 | Âge ou stade biologique de l’organisme d’essai | 1 | Oui | |
| 14 | Longueur et/ou poids | 1 | Oui | Longueur : 11 cm; poids : 15 g |
| 15 | Sexe | 1 | Non | |
| 16 | Nombre d’organismes par répétition | 1 | Non | |
| 17 | Charge en organismes | 1 | Non | |
| 18 | Type de nourriture et périodes d’alimentation pendant la période d’acclimatation | 1 | Non |
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 19 | Type d’essai (toxicité aiguë ou chronique) | s.o. | Oui | Aiguë |
| 20 | Type d’expérience (en laboratoire ou sur le terrain) | s.o. | Oui | En laboratoire |
| 21 | Voies d’exposition (nourriture, eau, les deux) | s.o. | Oui | Eau |
| 22 | Durée de l’exposition | s.o. | Oui | 48 heures |
| 23 | Témoins négatifs ou positifs (préciser) | 1 | Non | |
| 24 | Nombre de répétitions (y compris les témoins) | 1 | Non | |
| 25 | Des concentrations nominales sont-elles indiquées? | 1 | Non | |
| 26 | Des concentrations mesurées sont-elles indiquées? | 3 | Non | |
| 27 | Type de nourriture et périodes d’alimentation durant les essais à long terme | 1 | Sans objet | |
| 28 | Les concentrations ont-elles été mesurées périodiquement (spécialement dans les essais de toxicité chronique)? | 1 | Non | |
| 29 | Les conditions du milieu d’exposition correspondaient-elles au produit chimique particulier signalé? (par exemple, pour la toxicité du métal : pH, DOC/TOC, dureté de l’eau, température) | 3 | Non | |
| 30 | Photopériode et intensité de l’éclairage | 1 | Non | |
| 31 | Préparation de solutions mères et de solutions d’essai | 1 | Non | |
| 32 | Un agent émulsionnant ou stabilisant a-t-il été employé si la substance était peu soluble ou instable? | 1 | Non | |
| 33 | Si un agent émulsionnant ou stabilisant a été employé, sa concentration est-elle indiquée? | 1 | ||
| 34 | Si un solubilisant/émulsifiant a été utilisé, son écotoxicité a-t-elle été signalée? | 1 | ||
| 35 | Intervalles des contrôles analytiques | 1 | Non | |
| 36 | Méthodes statistiques utilisées | 1 | Non |
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 37 | Le paramètre déterminé est-il directement attribuable à la toxicité de la substance, non à l’état de santé des organismes (p. ex., lorsque la mortalité des témoins est supérieure à 10 %) ou à des facteurs physiques (p. ex., « effet d’ombrage »)? | s.o. | Oui | |
| 38 | L’organisme d’essai correspondait-il à l’environnement au Canada? | 3 | Oui | |
| 39 | Les conditions d’essai (pH, température, OD, etc.) sont-elles typiques pour l’organisme d’essai? | 1 | Non | Seule la température est indiquée (typique pour l’organisme d’essai). |
| 40 | Le type et la conception du système (statique, semi-statique, dynamique; ouvert ou fermé; etc.) correspondent-ils aux propriétés de la substance et à la nature ou aux habitudes de l’organisme? | 2 | Impossible à évaluer | |
| 41 | Le pH de l’eau du test se situait-il dans la plage des valeurs typiques de l’environnement au Canada (6 à 9)? | 1 | pH non précisé | |
| 42 | La température de l’eau du test se situait-elle dans la plage des valeurs typiques de l’environnement au Canada (5 à 27 °C)? | 1 | Oui | 20 °C |
| 43 | La valeur de la toxicité était-elle inférieure à celle de la solubilité de la substance dans l’eau? | 3 | Non | La CL50 indiquée est supérieure de 8 ordres de grandeur à la solubilité dans l’eau mesurée par Baughman et Perenich (1989). |
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 44 | Valeurs de la toxicité (fournir paramètres et valeurs) | s.o. | s.o. | CL50 après 48 heures > 1 000 mg/L |
| 45 | Autres paramètres indiqués – p. ex., FBC/FBA, CMEO/CSEO (préciser)? | s.o. | Non | |
| 46 | Autres effets indésirables (par exemple, cancérogénicité, mutagénicité) signalés? | s.o. | Non | |
| 47 | Note : % | 17,5 | ||
| 48 | Code de fiabilité d’Environnement Canada : | 4 | ||
| 49 | Catégorie de fiabilité (élevée, satisfaisante, basse) : | Non satisfaisante | ||
| 50 | Remarques | |||
| N° | Élément | Pondération | Oui/non | Précisions | ||
|---|---|---|---|---|---|---|
| 1 | Référence: ETAD, Ecological and Toxicological Association of Dyes and Organic Pigments Manufacturers. 2005. Projet E 3020 : renseignements reçus à l’appui de la catégorisation de 12 colorants dispersés dans la LIS. (Courriel daté du 27 octobre 2005) | |||||
| 2 | Identité de la substance : n° CAS | s.o.[1] | Oui | 19800-42-1 | ||
| 3 | Identité de la substance : nom(s) chimique(s) | s.o. | Oui | Disperse Orange 29 | ||
| 4 | Composition chimique de la substance | 2 | Oui | Colorant : 20 %; Reax 85A : 10 %; Eau : 70 %. | ||
| 5 | Pureté chimique | 1 | Oui | Dispersion à 20 % du colorant | ||
| 6 | Indication de la persistance/stabilité de la substance en milieu aqueux? | 1 | Non | |||
| N° | Élément | Pondération | Oui/non | Précisions | ||
|---|---|---|---|---|---|---|
| 7 | Référence | 1 | Non | |||
| 8 | Méthode normalisée (OCDE, UE, nationale, ou autre)? | 3 | Oui | OCDE 203 | ||
| 9 | Justification de la méthode ou du protocole si une méthode non normalisée a été utilisée | 2 | Sans objet | |||
| 10 | BPL (bonne pratique de laboratoire) | 3 | s.o. (étude réalisée en 1990) | |||
| N° | Élément | Pondération | Oui/non | Précisions | ||
|---|---|---|---|---|---|---|
| 11 | Identité de l’organisme : nom | s.o. | Oui | Poisson-zèbre (Brachydanio rerio) | ||
| 12 | Indication du nom latin ou des deux noms (latin et commun)? | 1 | Oui | |||
| 13 | Âge ou stade biologique de l’organisme d’essai | 1 | Non | |||
| 14 | Longueur et/ou poids | 1 | Non | |||
| 15 | Sexe | 1 | Sans objet | |||
| 16 | Nombre d’organismes par répétition | 1 | Non | |||
| 17 | Charge en organismes | 1 | Non | |||
| 18 | Type de nourriture et périodes d’alimentation pendant la période d’acclimatation | 1 | Non | |||
| N° | Élément | Pondération | Oui/non | Précisions | ||
|---|---|---|---|---|---|---|
| 19 | Type d’essai (toxicité aiguë ou chronique) | s.o. | Oui | Aiguë | ||
| 20 | Type d’expérience (en laboratoire ou sur le terrain) | s.o. | Oui | En laboratoire | ||
| 21 | Voies d’exposition (nourriture, eau, les deux) | s.o. | Oui | Eau | ||
| 22 | Durée de l’exposition | s.o. | Oui | 48 heures | ||
| 23 | Témoins négatifs ou positifs (préciser) | 1 | Non | |||
| 24 | Nombre de répétitions (y compris les témoins) | 1 | Non | |||
| 25 | Des concentrations nominales sont-elles indiquées? | 1 | Non | |||
| 26 | Des concentrations mesurées sont-elles indiquées? | 3 | Non | |||
| 27 | Type de nourriture et périodes d’alimentation durant les essais à long terme | 1 | Sans objet | |||
| 28 | Les concentrations ont-elles été mesurées périodiquement (spécialement dans les essais de toxicité chronique)? | 1 | Non | |||
| 29 | Les conditions du milieu d’exposition correspondaient-elles au produit chimique particulier signalé? (par exemple, pour la toxicité du métal : pH, DOC/TOC, dureté de l’eau, température) | 3 | Non | |||
| 30 | Photopériode et intensité de l’éclairage | 1 | Non | |||
| 31 | Préparation de solutions mères et de solutions d’essai | 1 | Non | |||
| 32 | Un agent émulsionnant ou stabilisant a-t-il été employé si la substance était peu soluble ou instable? | 1 | Non | |||
| 33 | Si un agent émulsionnant ou stabilisant a été employé, sa concentration est-elle indiquée? | 1 | ||||
| 34 | Si un solubilisant/émulsifiant a été utilisé, son écotoxicité a-t-elle été signalée? | 1 | ||||
| 35 | Intervalles des contrôles analytiques | 1 | Non | |||
| 36 | Méthodes statistiques utilisées | 1 | Non | |||
| N° | Élément | Pondération | Oui/non | Précisions | ||
|---|---|---|---|---|---|---|
| 37 | Le critère d’évaluation a-t-il été directement causé par la toxicité du produit chimique et non par l’état de santé de l’organisme (par exemple, lorsque la mortalité lors du contrôle est supérieure à 10 %) ou des effets physiques (par exemple, « effet d’ombrage »)? | s.o. | Oui | |||
| 38 | L’organisme d’essai correspondait-il à l’environnement au Canada? | 3 | Non | |||
| 39 | Les conditions d’essai (pH, température, OD, etc.) sont-elles typiques pour l’organisme d’essai? | 1 | Non indiqué | |||
| 40 | Le type et la conception du système (statique, semi-statique, dynamique; ouvert ou fermé; etc.) correspondent-ils aux propriétés de la substance et à la nature ou aux habitudes de l’organisme? | 2 | Impossible à évaluer | |||
| 41 | Le pH de l’eau du test se situait-il dans la plage des valeurs typiques de l’environnement au Canada (6 à 9)? | 1 | pH non précisé | |||
| 42 | La température de l’eau du test se situait-elle dans la plage des valeurs typiques de l’environnement au Canada (5 à 27 °C)? | 1 | non précisé | |||
| 43 | La valeur de la toxicité était-elle inférieure à celle de la solubilité de la substance dans l’eau? | 3 | Oui | La CL50 et la solubilité dans l’eau déclarées sont à un ordre de grandeur l’une de l’autre. | ||
| N° | Élément | Pondération | Oui/non | Précisions | ||
|---|---|---|---|---|---|---|
| 44 | Valeurs de la toxicité (fournir paramètres et valeurs) | s.o. | s.o. | CL50 après 96 heures > 480 mg/L | ||
| 45 | Autres paramètres indiqués – p. ex., FBC/FBA, CMEO/CSEO (préciser)? | s.o. | Non | |||
| 46 | Autres effets indésirables (par exemple, cancérogénicité, mutagénicité) signalés? | s.o. | Non | |||
| 47 | Note : % | 28,6 | ||||
| 48 | Code de fiabilité d’Environnement Canada : | 4 | ||||
| 49 | Catégorie de fiabilité (élevée, satisfaisante, basse) : | Non satisfaisante | ||||
| 50 | Remarques | |||||
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 1 | Référence : [ETAD] Ecological and Toxicological Association of Dyes and Organic Pigments Manufacturers. 2005. Projet E 3020 : renseignements reçus à l’appui de la catégorisation de 12 colorants dispersés dans la LIS. (Courriel daté du 27 octobre 2005) (Étude présentée, 2008a) | |||
| 2 | Identité de la substance : n° CAS | s.o.[1] | Oui | 19800-42-1 |
| 3 | Identité de la substance : nom(s) chimique(s) | s.o. | Oui | Disperse Orange 29 |
| 4 | Composition chimique de la substance | 2 | Oui | Colorant : 20 %; Reax 85A : 10 %; Eau : 70 % |
| 5 | Pureté chimique | 1 | Oui | Dispersion à 20 % du colorant |
| 6 | Indication de la persistance/stabilité de la substance en milieu aqueux? | 1 | Non | |
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 7 | Référence | 1 | Non | |
| 8 | Méthode normalisée (OCDE, UE, nationale, ou autre)? | 3 | Oui | OCDE 201 |
| 9 | Justification de la méthode ou du protocole si une méthode non normalisée a été utilisée | 2 | Sans objet | |
| 10 | BPL (bonne pratique de laboratoire) | 3 | s.o. (étude réalisée en 1990) |
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 11 | Identité de l’organisme : nom | s.o. | Oui | Scenedesmus subspicatus |
| 12 | Indication du nom latin ou des deux noms (latin et commun)? | 1 | Oui | |
| 13 | Âge ou stade biologique de l’organisme d’essai | 1 | Non | |
| 14 | Longueur et/ou poids | 1 | Sans objet | |
| 15 | Sexe | 1 | Sans objet | |
| 16 | Nombre d’organismes par répétition | 1 | Non | |
| 17 | Charge en organismes | 1 | Non | |
| 18 | Type de nourriture et périodes d’alimentation pendant la période d’acclimatation | 1 | Non |
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 19 | Type d’essai (toxicité aiguë ou chronique) | s.o. | Oui | Aiguë |
| 20 | Type d’expérience (en laboratoire ou sur le terrain) | s.o. | Oui | En laboratoire |
| 21 | Voies d’exposition (nourriture, eau, les deux) | s.o. | Oui | Eau |
| 22 | Durée de l’exposition | s.o. | Oui | 72 heures |
| 23 | Témoins négatifs ou positifs (préciser) | 1 | Non | |
| 24 | Nombre de répétitions (y compris les témoins) | 1 | Non | |
| 25 | Des concentrations nominales sont-elles indiquées? | 1 | Non | |
| 26 | Des concentrations mesurées sont-elles indiquées? | 3 | Non | |
| 27 | Type de nourriture et périodes d’alimentation durant les essais à long terme | 1 | Sans objet | |
| 28 | Les concentrations ont-elles été mesurées périodiquement (spécialement dans les essais de toxicité chronique)? | 1 | Non | |
| 29 | Les conditions du milieu d’exposition correspondaient-elles au produit chimique particulier signalé? (par exemple, pour la toxicité du métal : pH, DOC/TOC, dureté de l’eau, température) | 3 | Non | |
| 30 | Photopériode et intensité de l’éclairage | 1 | Non | |
| 31 | Préparation de solutions mères et de solutions d’essai | 1 | Non | |
| 32 | Un agent émulsionnant ou stabilisant a-t-il été employé si la substance était peu soluble ou instable? | 1 | Non | |
| 33 | Si un agent émulsionnant ou stabilisant a été employé, sa concentration est-elle indiquée? | 1 | ||
| 34 | Si un solubilisant/émulsifiant a été utilisé, son écotoxicité a-t-elle été signalée? | 1 | ||
| 35 | Intervalles des contrôles analytiques | 1 | Non | |
| 36 | Méthodes statistiques utilisées | 1 | Non |
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 37 | Le critère d’évaluation a-t-il été directement causé par la toxicité du produit chimique et non par l’état de santé de l’organisme (par exemple, lorsque la mortalité lors du contrôle est supérieure à 10 %) ou des effets physiques (par exemple, « effet d’ombrage »)? | s.o. | Oui | |
| 38 | L’organisme d’essai correspondait-il à l’environnement canadien? | 3 | Oui | |
| 39 | Les conditions d’essai (pH, température, OD, etc.) sont-elles typiques pour l’organisme d’essai? | 1 | Non indiqué | |
| 40 | Le type et la conception du système (statique, semi-statique, dynamique; ouvert ou fermé; etc.) correspondent-ils aux propriétés de la substance et à la nature ou aux habitudes de l’organisme? | 2 | Impossible à évaluer | |
| 41 | Le pH de l’eau du test se situait-il dans la plage des valeurs typiques de l’environnement au Canada (6 à 9)? | 1 | pH non précisé | |
| 42 | La température de l’eau du test se situait-elle dans la plage des valeurs typiques de l’environnement au Canada (5 à 27 °C)? | 1 | non précisé | |
| 43 | La valeur de la toxicité était-elle inférieure à celle de la solubilité de la substance dans l’eau? | 3 | Oui | La différence entre la CE50 indiquée et la solubilité dans l’eau ne dépasse pas 1 ordre de grandeur. |
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 44 | Valeurs de la toxicité (fournir paramètres et valeurs) | s.o. | s.o. | CE50 après 72 h pour la biomasse = 6 mg/L |
| 45 | Autres paramètres indiqués – p. ex., FBC/FBA, CMEO/CSEO (préciser)? | s.o. | Oui | CE50 pour la croissance = 86 mg/L; CE10 pour la biomasse et la croissance = 1,7 et 5,4 mg/L |
| 46 | Autres effets indésirables (par exemple, cancérogénicité, mutagénicité) signalés? | s.o. | Non | |
| 47 | Note : | 38,2 | ||
| 48 | Code de fiabilité d’Environnement Canada : | 4 | ||
| 49 | Catégorie de fiabilité (élevée, satisfaisante, basse) : | Non satisfaisante | ||
| 50 | Remarques | |||
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 1 | Référence : [ETAD] Ecological and Toxicological Association of Dyes and Organic Pigments Manufacturers. 2005. Projet E 3020 : renseignements reçus à l’appui de la catégorisation de 12 colorants dispersés dans la LIS. Courriel daté du 27 octobre 2005) (Étude présentée, 2008a) | |||
| 2 | Identité de la substance : n° CAS | s.o.[1] | Oui | 19800-42-1 |
| 3 | Identité de la substance : nom(s) chimique(s) | s.o. | Oui | Disperse Orange 29 |
| 4 | Composition chimique de la substance | 2 | Oui | Colorant : 20 %; Reax 85A : 10 %; Eau : 70 %. |
| 5 | Pureté chimique | 1 | Oui | Dispersion à 20 % du colorant |
| 6 | Indication de la persistance/stabilité de la substance en milieu aqueux? | 1 | Non | |
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 7 | Référence | 1 | Non | |
| 8 | Méthode normalisée (OCDE, UE, nationale, ou autre)? | 3 | Oui | OCDE 202 |
| 9 | Justification de la méthode ou du protocole si une méthode non normalisée a été utilisée | 2 | Sans objet | |
| 10 | BPL (bonne pratique de laboratoire) | 3 | s.o. (étude réalisée en 1990) |
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 11 | Identité de l’organisme : nom | s.o. | Oui | Daphnia magna |
| 12 | Indication du nom latin ou des deux noms (latin et commun)? | 1 | Oui | |
| 13 | Âge ou stade biologique de l’organisme d’essai | 1 | Non | |
| 14 | Longueur et/ou poids | 1 | Sans objet | |
| 15 | Sexe | 1 | Sans objet | |
| 16 | Nombre d’organismes par répétition | 1 | Non | |
| 17 | Charge en organismes | 1 | Non | |
| 18 | Type de nourriture et périodes d’alimentation pendant la période d’acclimatation | 1 | Non |
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 19 | Type d’essai (toxicité aiguë ou chronique) | s.o. | Oui | Aiguë |
| 20 | Type d’expérience (en laboratoire ou sur le terrain) | s.o. | Oui | En laboratoire |
| 21 | Voies d’exposition (nourriture, eau, les deux) | s.o. | Oui | Eau |
| 22 | Durée de l’exposition | s.o. | Oui | 24 et 48 heures |
| 23 | Témoins négatifs ou positifs (préciser) | 1 | Non | |
| 24 | Nombre de répétitions (y compris les témoins) | 1 | Non | |
| 25 | Des concentrations nominales sont-elles indiquées? | 1 | Non | |
| 26 | Des concentrations mesurées sont-elles indiquées? | 3 | Non | |
| 27 | Type de nourriture et périodes d’alimentation durant les essais à long terme | 1 | Sans objet | |
| 28 | Les concentrations ont-elles été mesurées périodiquement (spécialement dans les essais de toxicité chronique)? | 1 | Non | |
| 29 | Les conditions du milieu d’exposition correspondaient-elles au produit chimique particulier signalé? (par exemple, pour la toxicité du métal : pH, DOC/TOC, dureté de l’eau, température) | 3 | Non | |
| 30 | Photopériode et intensité de l’éclairage | 1 | Non | |
| 31 | Préparation de solutions mères et de solutions d’essai | 1 | Non | |
| 32 | Un agent émulsionnant ou stabilisant a-t-il été employé si la substance était peu soluble ou instable? | 1 | Non | |
| 33 | Si un agent émulsionnant ou stabilisant a été employé, sa concentration est-elle indiquée? | 1 | ||
| 34 | Si un solubilisant/émulsifiant a été utilisé, son écotoxicité a-t-elle été signalée? | 1 | ||
| 35 | Intervalles des contrôles analytiques | 1 | Non | |
| 36 | Méthodes statistiques utilisées | 1 | Non |
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 37 | Le paramètre déterminé est-il directement attribuable à la toxicité de la substance, non à l’état de santé des organismes (p. ex., lorsque la mortalité des témoins est supérieure à 10 %) ou à des facteurs physiques (p. ex., « effet d’ombrage »)? | s.o. | Oui | |
| 38 | L’organisme d’essai correspondait-il à l’environnement au Canada? | 3 | Oui | |
| 39 | Les conditions d’essai (pH, température, OD, etc.) sont-elles typiques pour l’organisme d’essai? | 1 | Non indiqué | |
| 40 | Le type et la conception du système (statique, semi-statique, dynamique; ouvert ou fermé; etc.) correspondent-ils aux propriétés de la substance et à la nature ou aux habitudes de l’organisme? | 2 | Impossible à évaluer | |
| 41 | Le pH de l’eau du test se situait-il dans la plage habituelle pour l’environnement canadien (6 à 9)? | 1 | pH non précisé | |
| 42 | La température de l’eau du test se situait-elle dans la plage habituelle pour l’environnement canadien (5 à 27 °C)? | 1 | non précisé | |
| 43 | La valeur de la toxicité était-elle inférieure à celle de la solubilité de la substance dans l’eau? | 3 | Non | La CL50 indiquée est supérieure à la valeur fournie de la solubilité dans l’eau. |
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 44 | Valeurs de la toxicité (fournir paramètres et valeurs) | s.o. | s.o. | CE50 après 48 heures = 70 mg/L |
| 45 | Autres paramètres indiqués – p. ex., FBC/FBA, CMEO/CSEO (préciser)? | s.o. | Oui | CE50 après 24 heures > 100 mg/L |
| 46 | Autres effets indésirables (par exemple, cancérogénicité, mutagénicité) signalés? | s.o. | Non | |
| 47 | Note : % | 29,4 | ||
| 48 | Code de fiabilité d’Environnement Canada : | 4 | ||
| 49 | Catégorie de fiabilité (élevée, satisfaisante, basse) : | Non satisfaisante | ||
| 50 | Remarques | |||
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 1 | Référence : BASF. 1990. 1990. Bericht uber die Prufung der akuten Toxizitit an der Goldorfe (Leuciscus idus L., Goldvariante). Présenté à Environnement Canada par l’ETAD en août 2008. | |||
| 2 | Identité de la substance : n° CAS | s.o.[1] | ||
| 3 | Identité de la substance : nom(s) chimique(s) | s.o. | ||
| 4 | Composition chimique de la substance | 2 | Non | |
| 5 | Pureté chimique | 1 | Non | |
| 6 | Indication de la persistance/stabilité de la substance en milieu aqueux? | 1 | Non | |
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 7 | Référence | 1 | Non | |
| 8 | Méthode normalisée (OCDE, UE, nationale, ou autre)? | 3 | Non | |
| 9 | Justification de la méthode ou du protocole si une méthode non normalisée a été utilisée | 2 | Non | |
| 10 | BPL (bonne pratique de laboratoire) | 3 | ||
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 11 | Identité de l’organisme : nom | s.o. | Oui | Ide dorée |
| 12 | Indication du nom latin ou des deux noms (latin et commun)? | 1 | Oui | |
| 13 | Âge ou stade biologique de l’organisme d’essai | 1 | Non | |
| 14 | Longueur et/ou poids | 1 | Non | |
| 15 | Sexe | 1 | Non | |
| 16 | Nombre d’organismes par répétition | 1 | Non | |
| 17 | Charge en organismes | 1 | Non | |
| 18 | Type de nourriture et périodes d’alimentation pendant la période d’acclimatation | 1 | Non |
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 19 | Type d’essai (toxicité aiguë ou chronique) | s.o. | Oui | Aiguë |
| 20 | Type d’expérience (en laboratoire ou sur le terrain) | s.o. | Non | |
| 21 | Voies d’exposition (nourriture, eau, les deux) | s.o. | Non | |
| 22 | Durée de l’exposition | s.o. | Oui | 96 h |
| 23 | Témoins négatifs ou positifs (préciser) | 1 | Non | |
| 24 | Nombre de répétitions (y compris les témoins) | 1 | Non | |
| 25 | Des concentrations nominales sont-elles indiquées? | 1 | Non | |
| 26 | Des concentrations mesurées sont-elles indiquées? | 3 | Non | |
| 27 | Type de nourriture et périodes d’alimentation durant les essais à long terme | 1 | Sans objet | |
| 28 | Les concentrations ont-elles été mesurées périodiquement (spécialement dans les essais de toxicité chronique)? | 1 | Non | |
| 29 | Les conditions du milieu d’exposition correspondaient-elles au produit chimique particulier signalé? (par exemple, pour la toxicité du métal : pH, DOC/TOC, dureté de l’eau, température) | 3 | Non | |
| 30 | Photopériode et intensité de l’éclairage | 1 | Non | |
| 31 | Préparation de solutions mères et de solutions d’essai | 1 | Non | |
| 32 | Un agent émulsionnant ou stabilisant a-t-il été employé si la substance était peu soluble ou instable? | 1 | Non | |
| 33 | Si un agent émulsionnant ou stabilisant a été employé, sa concentration est-elle indiquée? | 1 | Non | |
| 34 | Si un solubilisant/émulsifiant a été utilisé, son écotoxicité a-t-elle été signalée? | 1 | Non | |
| 35 | Intervalles des contrôles analytiques | 1 | Non | |
| 36 | Méthodes statistiques utilisées | 1 | Non |
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 37 | Le critère d’évaluation a-t-il été directement causé par la toxicité du produit chimique et non par l’état de santé de l’organisme (par exemple, lorsque la mortalité lors du contrôle est supérieure à 10 %) ou des effets physiques (par exemple, « effet d’ombrage »)? | s.o. | Non | |
| 38 | L’organisme d’essai correspondait-il à l’environnement au Canada? | 3 | Oui | |
| 39 | Les conditions d’essai (pH, température, OD, etc.) sont-elles typiques pour l’organisme d’essai? | 1 | Non | |
| 40 | Le type et la conception du système (statique, semi-statique, dynamique; ouvert ou fermé; etc.) correspondent-ils aux propriétés de la substance et à la nature ou aux habitudes de l’organisme? | 2 | Non | |
| 41 | Le pH de l’eau du test se situait-il dans la plage des valeurs typiques de l’environnement au Canada (6 à 9)? | 1 | Non | |
| 42 | La température de l’eau du test se situait-elle dans la plage des valeurs typiques de l’environnement au Canada (5 à 27 °C)? | 1 | Non | |
| 43 | La valeur de la toxicité était-elle inférieure à celle de la solubilité de la substance dans l’eau? | 3 |
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 44 | Valeurs de la toxicité (fournir paramètres et valeurs) | s.o. | CL50 = 100 mg/L > < 220 mg/L | |
| 45 | Autres paramètres indiqués – p. ex., FBC/FBA, CMEO/CSEO (préciser)? | s.o. | CSEO = 100 mg/L | |
| 46 | Autres effets indésirables (par exemple, cancérogénicité, mutagénicité) signalés? | s.o. | ||
| 47 | Note : % | 9,5 | ||
| 48 | Code de fiabilité d’Environnement Canada : | 4 | ||
| 49 | Catégorie de fiabilité (élevée, satisfaisante, basse) : | Non satisfaisante | ||
| 50 | Remarques | Les données soumises ne sont pas suffisantes pour évaluer correctement la fiabilité de cette étude. | ||
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 1 | Référence : Environnement Canada, 1995. NSN submission. Données présentées à la Division des substances nouvelles d’Environnement Canada dans le cadre du Programme de déclaration des substances nouvelles. | |||
| 2 | Identité de la substance : n° CAS | s.o.[1] | Non | |
| 3 | Identité de la substance : nom(s) chimique(s) | s.o. | Oui | |
| 4 | Composition chimique de la substance | 2 | Non | |
| 5 | Pureté chimique | 1 | Non | |
| 6 | Indication de la persistance/stabilité de la substance en milieu aqueux? | 1 | Non | |
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 7 | Référence | 1 | Oui | OCDE 203 |
| 8 | Méthode normalisée (OCDE, UE, nationale, ou autre)? | 3 | Oui | |
| 9 | Justification de la méthode ou du protocole si une méthode non normalisée a été utilisée | 2 | Sans objet | |
| 10 | BPL (bonne pratique de laboratoire) | 3 | Oui |
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 11 | Identité de l’organisme : nom | s.o. | Oui | Truite arc-en-ciel |
| 12 | Indication du nom latin ou des deux noms (latin et commun)? | 1 | Oui | |
| 13 | Âge ou stade biologique de l’organisme d’essai | 1 | Oui | Longueur moyenne : 51 mm; poids moyen : 1,54 |
| 14 | Longueur et/ou poids | 1 | Oui | Voir ci-dessus |
| 15 | Sexe | 1 | Sans objet | |
| 16 | Nombre d’organismes par répétition | 1 | Oui | 10 |
| 17 | Charge en organismes | 1 | Oui | |
| 18 | Type de nourriture et périodes d’alimentation pendant la période d’acclimatation | 1 | Oui |
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 19 | Type d’essai (toxicité aiguë ou chronique) | s.o. | Oui | Aiguë |
| 20 | Type d’expérience (en laboratoire ou sur le terrain) | s.o. | Oui | En laboratoire |
| 21 | Voies d’exposition (nourriture, eau, les deux) | s.o. | Oui | Eau |
| 22 | Durée de l’exposition | s.o. | Oui | 96 h |
| 23 | Témoins négatifs ou positifs (préciser) | 1 | Oui | 3 |
| 24 | Nombre de répétitions (y compris les témoins) | 1 | Oui | 2 |
| 25 | Des concentrations nominales sont-elles indiquées? | 1 | Oui | 320 à 3 200 mg/L |
| 26 | Des concentrations mesurées sont-elles indiquées? | 3 | Non | |
| 27 | Type de nourriture et périodes d’alimentation durant les essais à long terme | 1 | Sans objet | |
| 28 | Les concentrations ont-elles été mesurées périodiquement (spécialement dans les essais de toxicité chronique)? | 1 | Non | |
| 29 | Les conditions du milieu d’exposition correspondaient-elles au produit chimique particulier signalé? (par exemple, pour la toxicité du métal : pH, DOC/TOC, dureté de l’eau, température) | 3 | Oui | |
| 30 | Photopériode et intensité de l’éclairage | 1 | Oui | |
| 31 | Préparation de solutions mères et de solutions d’essai | 1 | Oui | |
| 32 | Un agent émulsionnant ou stabilisant a-t-il été employé si la substance était peu soluble ou instable? | 1 | Non | |
| 33 | Si un agent émulsionnant ou stabilisant a été employé, sa concentration est-elle indiquée? | 1 | ||
| 34 | Si un solubilisant/émulsifiant a été utilisé, son écotoxicité a-t-elle été signalée? | 1 | ||
| 35 | Intervalles des contrôles analytiques | 1 | Oui | |
| 36 | Méthodes statistiques utilisées | 1 | Oui |
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 37 | Le paramètre déterminé était-il directement attribuable à la toxicité de la substance, non à l’état de santé des organismes (p. ex., lorsque la mortalité des témoins est supérieure à 10 %) ou à des facteurs physiques (p. ex., « effet d’ombrage »)? | s.o. | Oui | |
| 38 | L’organisme d’essai correspondait-il à l’environnement au Canada? | 3 | Oui | |
| 39 | Les conditions d’essai (pH, température, OD, etc.) sont-elles typiques pour l’organisme d’essai? | 1 | Oui | |
| 40 | Le type et la conception du système (statique, semi-statique, dynamique; ouvert ou fermé; etc.) correspondent-ils aux propriétés de la substance et à la nature ou aux habitudes de l’organisme? | 2 | Oui | |
| 41 | Le pH de l’eau du test se situait-il dans la plage des valeurs typiques de l’environnement au Canada (6 à 9)? | 1 | Oui | |
| 42 | La température de l’eau du test se situait-elle dans la plage des valeurs typiques de l’environnement au Canada (5 à 27 °C)? | 1 | Oui | |
| 43 | La valeur de la toxicité était-elle inférieure à celle de la solubilité de la substance dans l’eau? | 3 | Solubilité dans l’eau inconnue |
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 44 | Valeurs de la toxicité (fournir paramètres et valeurs) | s.o. | s.o. | CL50 après 96 h |
| 45 | Autres paramètres indiqués – p. ex., FBC/FBA, CMEO/CSEO (préciser)? | s.o. | Non | |
| 46 | Autres effets indésirables (par exemple, cancérogénicité, mutagénicité) signalés? | s.o. | Non | |
| 47 | Note : | 77,5 | ||
| 48 | Code de fiabilité d’Environnement Canada : | 2 | ||
| 49 | Catégorie de fiabilité (élevée, satisfaisante, basse) : | Confiance satisfaisante | ||
| 50 | Remarques | |||
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 1 | Référence : Cohle, P. et R. MIihalik. 1991. Early life stage toxicity of C.I. Disperse Blue 79:1 purified preecake to rainbow trout (Oncorhynchus mykiss) in a flow-through system. | |||
| 2 | Identité de la substance : n° CAS | s.o.[1] | ||
| 3 | Identité de la substance : nom(s) chimique(s) | s.o. | Disperse Blue 79:1 | |
| 4 | Composition chimique de la substance | 2 | Oui | |
| 5 | Pureté chimique | 1 | Oui | 96,61 |
| 6 | Indication de la persistance/stabilité de la substance en milieu aqueux? | 1 | Non | |
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 7 | Référence | 1 | Oui | |
| 8 | Méthode normalisée (OCDE, UE, nationale, ou autre)? | 3 | Oui | ASTM, 1983 |
| 9 | Justification de la méthode ou du protocole si une méthode non normalisée a été utilisée | 2 | Sans objet | |
| 10 | BPL (bonne pratique de laboratoire) | 3 | Oui |
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 11 | Identité de l’organisme : nom | s.o. | Truite arc-en-ciel | |
| 12 | Indication du nom latin ou des deux noms (latin et commun)? | 1 | Oui | |
| 13 | Âge ou stade biologique de l’organisme d’essai | 1 | Oui | |
| 14 | Longueur et/ou poids | 1 | Oui | |
| 15 | Sexe | 1 | Sans objet | |
| 16 | Nombre d’organismes par répétition | 1 | Oui | 20 |
| 17 | Charge en organismes | 1 | Oui | 0,36 à 4,8 µg/L |
| 18 | Type de nourriture et périodes d’alimentation pendant la période d’acclimatation | 1 | Oui |
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 19 | Type d’essai (toxicité aiguë ou chronique) | s.o. | Oui | Toxicité chronique |
| 20 | Type d’expérience (en laboratoire ou sur le terrain) | s.o. | Oui | En laboratoire |
| 21 | Voies d’exposition (nourriture, eau, les deux) | s.o. | Oui | Eau |
| 22 | Durée de l’exposition | s.o. | Oui | 122 jours |
| 23 | Témoins négatifs ou positifs (préciser) | 1 | Oui | Témoin et porteur non indiqués |
| 24 | Nombre de répétitions (y compris les témoins) | 1 | Oui | 2 |
| 25 | Des concentrations nominales sont-elles indiquées? | 1 | Oui | 5 |
| 26 | Des concentrations mesurées sont-elles indiquées? | 3 | Oui | |
| 27 | Type de nourriture et périodes d’alimentation durant les essais à long terme | 1 | Oui | |
| 28 | Les concentrations ont-elles été mesurées périodiquement (spécialement dans les essais de toxicité chronique)? | 1 | Oui | |
| 29 | Les conditions du milieu d’exposition correspondaient-elles au produit chimique particulier signalé? (par exemple, pour la toxicité du métal : pH, DOC/TOC, dureté de l’eau, température) | 3 | Oui | |
| 30 | Photopériode et intensité de l’éclairage | 1 | Oui | |
| 31 | Préparation de solutions mères et de solutions d’essai | 1 | Oui | |
| 32 | Un agent émulsionnant ou stabilisant a-t-il été employé si la substance était peu soluble ou instable? | 1 | Oui | |
| 33 | Si un agent émulsionnant ou stabilisant a été employé, sa concentration est-elle indiquée? | 1 | Oui | |
| 34 | Si un solubilisant/émulsifiant a été utilisé, son écotoxicité a-t-elle été signalée? | 1 | Oui | Pas de valeur pour la toxicité, mais l’agent a été utilisé comme témoin. |
| 35 | Intervalles des contrôles analytiques | 1 | Oui | |
| 36 | Méthodes statistiques utilisées | 1 | Oui |
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 37 | Le critère d’évaluation a-t-il été directement causé par la toxicité du produit chimique et non par l’état de santé de l’organisme (par exemple, lorsque la mortalité lors du contrôle est supérieure à 10 %) ou des effets physiques (par exemple, « effet d’ombrage »)? | s.o. | Oui | |
| 38 | L’organisme d’essai correspondait-il à l’environnement au Canada? | 3 | Oui | |
| 39 | Les conditions d’essai (pH, température, OD, etc.) sont-elles typiques pour l’organisme d’essai? | 1 | Oui | |
| 40 | Le type et la conception du système (statique, semi-statique, dynamique; ouvert ou fermé; etc.) correspondent-ils aux propriétés de la substance et à la nature ou aux habitudes de l’organisme? | 2 | Oui | Renouvellement continu |
| 41 | Le pH de l’eau du test se situait-il dans la plage des valeurs typiques de l’environnement au Canada (6 à 9)? | 1 | Oui | |
| 42 | La température de l’eau du test se situait-elle dans la plage des valeurs typiques de l’environnement au Canada (5 à 27 °C)? | 1 | Oui | |
| 43 | La valeur de la toxicité était-elle inférieure à celle de la solubilité de la substance dans l’eau? | 3 | Impossible à évaluer. Il y a lieu de croire que la plus forte dose d’essai correspond à la limite de solubilité. |
| N° | Élément | Pondération | Oui/non | Précisions |
|---|---|---|---|---|
| 44 | Valeurs de la toxicité (fournir paramètres et valeurs) | s.o. | s.o. | CSEO = 0,005 mg/L |
| 45 | Autres paramètres indiqués – p. ex., FBC/FBA, CMEO/CSEO (préciser)? | s.o. | ||
| 46 | Autres effets indésirables (par exemple, cancérogénicité, mutagénicité) signalés? | s.o. | ||
| 47 | Note : | 97,7 | ||
| 48 | Code de fiabilité d’Environnement Canada : | 1 | ||
| 49 | Catégorie de fiabilité (élevée, satisfaisante, basse) : | Confiance élevée | ||
| 50 | Remarques | |||
| Paramètre | Propriétés physico-chimiques et devenir | Profils de persistance, bioaccumulation et toxicité | Écotoxicité |
|---|---|---|---|
| Paramètres d’entrée des modèles | EPI Suite (tous les modèles, notamment AOPWIN, KOCWIN, BCFWIN, BIOWIN et ECOSAR) |
Canadian POP Model (incluant : Catabol, modèle de facteurs d’atténuation du FBC, modèle de toxicité OASIS) |
Artificial Intelligence Expert System (AIES)/ TOPKAT/ ASTER |
| Code SMILES[1] | x | x | x |
| Scénario de cosmétiques et de produits de soins personnels | Hypothèses | Estimation de l’exposition |
|---|---|---|
| Brillant/ baume pour les lèvres[1] | Pourcentage du poids du Solvent Red 23: 1 % (SDC, 2009) Voie orale : Type d’exposition : absorption directe Quantité de produit ingérée : 0,01 g - en supposant que le produit entier est pris oralement (RIVM, 2006) Fréquence d’exposition : 1 460 fois/an (RIVM, 2006) |
Voie orale Dose aiguë (interne) : 0,001 mg/kg Dose chronique (interne) : 0,006 mg/kg p.c. par jour |
| Préparation pour bain – Savon liquide | Pourcentage du poids du Solvent Red 23: 0,1 % (SDC, 2009) Voie cutanée : Type d’exposition : application instantanée Partie exposée : corps – tête de 16 900 cm2(Santé Canada, 1995), Quantité de produit appliquée : 8,7 g (26,1g p/facteur de dilution 3) Fréquence d’exposition : 329 fois/an (RIVM, 2006) Fraction d’absorption : 0,26 (Collier et al., 1993) |
Voie cutanée Dose aiguë (interne) : 0,03 mg/kg Dose chronique (interne) : 0,03 mg/kg p.c. par jour |
| Huile de massage | Pourcentage du poids du Solvent Red 23 : 0,1 % (SDC, 2009) Voie cutanée : Type d’exposition : application instantanée Partie exposée : corps – tête de 16 900 cm2(Santé Canada, 1995) Quantité de produit appliquée : 8 g Fréquence : 24 fois/an (RIVM, 2006) Fraction d’absorption : 0,26 (Collier et al., 1993) |
Voie cutanée Dose aiguë (interne) 0,03 mg/kg Dose chronique (interne) 0,002 mg/kg p.c. par jour |
| Revitalisant capillaire | Pourcentage du poids du Solvent Red 23 : 0,1 % (SDC, 2009) Voie cutanée : Type d’exposition : application instantanée Partie exposée: mains + ½ de la tête, de 1 540 cm2 (Santé Canada, 1995), Quantité de produit appliquée : 14 g (54 g e/facteur de dilution 3,9) Fréquence d’exposition : 104 fois/an (RIVM, 2006) Fraction d’absorption : 0,26 (Collier etal.,1993) |
Voie cutanée Dose aiguë (interne) 0,05 mg/kg Dose chronique (interne) 0,0015 mg/kg p.c. par jour |
| Colorant capillaire | Pourcentage du poids du Solvent Red 23 : 0,1 % (SDC, 2009) Voie cutanée Type d’exposition : application instantanée Partie exposée : ½ de la tête, de 638 cm2(Santé Canada, 1995), Quantité de produit appliquée : 100 g, Fréquence d’exposition : 10 fois/an (RIVM, 2006) Fraction d’absorption : 0,26 (Collier et al., 1993) |
Voie cutanée Dose aiguë (interne) 3,67 mg/kg Dose chronique (interne) 0,10 mg/kg p.c. par jour |
| Crème corporelle | Pourcentage du poids du Solvent Red 23 : 0,3 % (SDC, 2009) Voie cutanée Type d’exposition : application instantanée Partie exposée : corps – tête 16 900 cm2(Santé Canada, 1995), Quantité de produit appliquée : 8 g Fréquence d’exposition : 730 fois/an (RIVM, 2006) Fraction d’absorption : 0,26 (Collier et al., 1993) |
Voie cutanée Dose aiguë (interne) 0,09 mg/kg Dose chronique (interne) 0,18 mg/kg p.c. par jour |
| Nettoyant pour le visage | Pourcentage du poids du Solvent Red 23 : 0,1 % (SDC, 2009) Voie cutanée : Type d’exposition : application instantanée Partie exposée : ½ de la tête, de 638 cm2(Santé Canada, 1995), Quantité de produit appliquée : 0,25 g (25 g avec un facteur de rétention de 10 %) Fréquence d’exposition : 730 fois/an (RIVM, 2006) Fraction d’absorption : 0,26 (Collier et al., 1993) |
Voie cutanée Dose aiguë (interne) 0,009 mg/kg Dose chronique (interne) 0,018 mg/kg p.c. par jour |
| Vernis à ongles | Pourcentage du poids du Solvent Red 23 : 10 % (SDC, 2009) Voie cutanée Type d’exposition : application instantanée Partie exposée : 4 cm2 (Santé Canada, 1995), Quantité de produit appliquée : 0,05 g Fréquence d’exposition : 156 fois/an (RIVM, 2006) Fraction d’absorption : 0,26 (Collier et al., 1993) |
Voie cutanée Dose aiguë (interne) 0,02 mg/kg Dose chronique (interne) 0,008 mg/kg p.c. par jour |
Annexe 4 : Sommaire des renseignements relatifs aux effets sur la santé du Solvent Red 23 (n° CAS : 85-86-9)
| Paramètre | Doses minimales avec effet[1] / Résultats |
|---|---|
| Toxicité aiguë | DL50 minimale (rat)>16 000 mg/kg p.c. Le CSPC a conclu que le Solvent Red 23 avait une faible toxicité par voie orale après une seule exposition (CSPC, 2005). |
| Toxicité de doses répétées à court terme | Aucune étude pertinente n’a été recensée. Une étude sur la toxicité cutanée sur 21 jours a été effectuée sur des lapins. La méthode n’étant pas décrite, le CSPC a considéré l’étude comme non pertinente (CSPC, 2005). |
| Toxicité subchronique | Aucune étude pertinente n’a été recensée. Une étude sur la toxicité cutanée sur 90 jours a été effectuée sur des lapins. La méthode n’étant pas décrite, le CSPC a considéré l’étude comme non pertinente (CSPC, 2005). |
| Toxicité chronique et cancérogénicité | Par voie orale : 83 souris mâles et 54 souris femelles ont été exposés par voie alimentaire à une concentration de 2 mg par jour de la substance sous forme de solution à 1 % dans l'huile (quel que soit le poids). Des tumeurs aux poumons étaient évidentes, mais n’étaient pas plus fréquentes que chez les témoins (CSPC, 2005). Des rats Wistar (5/sexe) ont été nourris de 40 000 mg/kg de nourriture pendant 18 mois. Aucune tumeur n’a été observée. Il n’existe aucune donnée sur le taux de survie (CSPC, 2005). Seize rats femelles ont été exposés par instillation gastrique à 1 mL d’une solution à 0,1 % (e/v) dans l’huile de sésame, 5 fois/semaine pendant 25 semaines. Aucune augmentation de l’incidence de tumeurs n’a été observée (CSPC, 2005). Par voie cutanée : Des souris Swiss-Webster (50/sexe) ont été exposées par l’intermédiaire de la peinture sur la peau. Une quantité de 0,1 mL d’une solution à 1 % a été appliquée sur de la peau épilée (6 cm2) (environ 40 mg/kg p.c. par jour) une fois par semaine pendant 18 mois. Aucune augmentation de l’incidence de tumeurs n’a été observée. Aucune modification du poids corporel ou du taux de survie n’a été observée (CSPC, 2005). Injection sous-cutanée : Deux groupes de 10 souris femelles ont reçu des doses répétées (nombre d’injections non précisé) de 0,25 mL d’une solution saturée de Solvent Red 23 ou de 5 mg de cristaux de Solvent Red 23. Aucune tumeur n’a été observée (CSPC, 2005). Injection intramusculaire : Des rats Long-Evans (8, âgés de 27 jours) ont reçu une injection de 0,5 mL d’une solution à 0,5 % (e/v) dans l’huile de sésame dans le muscle de la cuisse. Aucune tumeur n’a été observée à l’autopsie après 40 semaines (CSPC, 2005). REMARQUE : Le CIRC n’a considéré aucune de ces études comme pertinente pour la classification de la cancérogénicité du Solvent Red 23. |
| Toxicité sur le plan du développement | Du Solvent Red 23 a été administré à des souris gravides par voie orale du 8e au 12e jour de gestation. Les rejetons mâles âgés de 48 à 50 jours ont subi une autopsie, et on a recherché les anomalies du développement des testicules. Aucun effet lié au traitement n’a été observé. (Gray et Ostby, 1993). |
| Toxicité sur le plan de la reproduction | Aucune étude portant sur la toxicité potentielle du Solvent Red 23 sur le plan du développement n’a été recensée. |
| Génotoxicité et paramètres connexes : in vivo | Essai de Comet Résultats positifs : Des souris ddY mâles (4/groupe) ont reçu 2 000 mg/kg de substance par voie orale. Elles ont été sacrifiées à 0, 8, 3 ou 24 heures. Divers tissus ont été examinés par essai de Comet en vue d’y détecter des cassures de brin d’ADN. Une augmentation de la migration de l’ADN (indication de dommages à l’ADN) a été observée dans l’estomac, le côlon et la vessie des souris sacrifiées à 3 heures, mais non chez les souris des groupes de 0, 8 ou 24 heures (Tsuda et al., 2000). |
| Génotoxicité et paramètres connexes : in vitro | Mutagénicité Résultats négatifs : Test d’Ames effectué avec des composés d’essai purifiés dans les souches de contrôle de Salmonella typhimurium TA98 et TA100 en présence du mélange S9. Il se peut que le protocole ne soit pas approprié pour le groupe du composé (Miyagoshi et al., 1985). Résultats positifs : Test d’Ames effectué avec des préparations commerciales de colorants dans les souches de contrôle de Salmonella typhimurium TA98 et TA100 en présence du mélange S9. Les auteurs ont attribué l’activité à la contamination par des matières de synthèse (4-aminoazobenzène) (Miyagoshi et al., 1985). Résultats négatifs : Aucune augmentation de cellules mortes (indicateur de génotoxicité) n’a été observée dans les essais de recombinaison d’E. coliWP2/WP67 ou de B. subtilis 45T (Kada et al., 1972; Mamber et al., 1983). Aberrations chromosomiques Résultats positifs : Des cellules ovariennes (CHO) de hamsters de Chine ont été traitées au Solvent Red 23 sans activation. Un nombre accru de cassures par métaphase a été observé (Au et Hsu, 1979). Résultats négatifs : Des lymphocytes humains exposés in vitro à des doses allant jusqu’à 100 µg/ml n’ont subi aucune augmentation des aberrations chromosomiques (CSPC, 1988). |
| Irritation/sensibilisation | Des lapins exposés au Solvent Red 23 par voie cutanée n’ont montré que des signes d’irritation légers. La Loi sur les aliments et drogues a classé la substance comme légèrement irritante. Le CSC a conclu que le Solvent Red 23 a des propriétés irritantes marginales (CSPC, 2005). Des lapins ont été exposés au Solvent Red 23 par voie oculaire. La substance a été évaluée comme légèrement irritante. Le CSC a conclu que le Solvent Red 23 a des propriétés irritantes marginales (CSPC, 2005). Des groupes de six animaux exposés à 0,1 % (par voie intracutanée) ou à 1,0 % (par voie topique) n’ont pas réagi à des doses d’amorce de 0,001, de 0,01 et de 0,1 % de Solvent Red 23. Toutefois, un traitement initial avec plusieurs autres substances (p-phénylénédiamine,p-aminoazobenzène) n’a pas causé de sensibilisation croisée avec le Solvent Red 23 (CSPC, 2005). |
| Nom de la substance | Solvent Red 23 | Sudan I | Sudan IV | Sudan II |
|---|---|---|---|---|
| N° CAS | 85-86-9 | 842-07-9 | 85-83-6 | 3118-97-6 |
| Autres identifi- cateurs |
Sudan III, CI 26100 | Solvent Yellow 14, CI 12055 | Sudan IV, CI 26105 | C.I. Solvent Orange 7 |
| Formule | C22H16N4O | C16H12N2O | C24H20N4O | C18H16N2O |
| Poids molé- culaire |
352,39 | 248,28 | 380,45 | 276,3 |
| Solubi- lité dans l’eau |
2,60E-03 mg/L (estimée) | 0,67 mg/L (estimée) | 2,03E-04 mg/L (estimée) | 0,055 mg/L (estimée) |
| Log Koe | 7,63 (estimé) | 5,51 (estimé) | 8,72 (estimé) | 6,600 (estimé) |
| Structure | 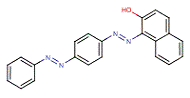 |
 |
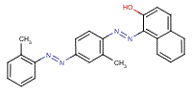 |
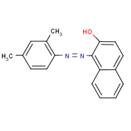 |
| Classifi- cations interna- tionales |
|
|
|
|
| Nom de la substance | Solvent Red 23 | Sudan I | Sudan IV | Sudan II | ||||
|---|---|---|---|---|---|---|---|---|
| Cancéro- génicité |
Par voie orale
Par voie cutanée
|
Par voie orale
* Autres études dépassées ou non pertinentes citées dans le CIRC, 1975. |
Par voie orale
Par voie cutanée
|
Par voie orale
Implantation
|
||||
Géno- in vivo |
Dommages à l’ADN :
|
Échange de chromatides sœurs
Aberration chromosomique
Essai du micronoyau :
Translocation réciproque
Mutation létale récessive associée au sexe
|
Aucune donnée. | Aucune donnée. | ||||
Géno- in vitro |
Mutagénicité bactérienne
Aberrations chromosomiques
|
Mutagénicité bactérienne
Mutagénicité des cellules mammaliennes
Échange de chromatides sœurs
Aberration chromosomique
|
Mutagénicité bactérienne
Transformation cellulaire
|
Mutagénicité bactérienne
Mutagénicité des cellules mammaliennes
|
||||
Annexe 6 : Sommaire des renseignements disponibles sur la cancérogénicité et la génotoxicité des produits de rupture réductrice des liaisons azoïques potentiels du Solvent Red 23[12],[13]
4-aminoazobenzène
Structure chimique :
- N° CAS : 60-09-3
- Formule :C12H11N3
- Poids moléculaire : 197,24
- Classifications : Groupe 2B du CIRC et Cancérogénicité : Catégorie 2 (UE)
Cancérogénicité
Par voie orale
Seize rats mâles ont été nourris d’environ 100 à 500 mg/kg p.c. par jour dans une alimentation faible en protéines (pour favoriser la formation de tumeurs au foie) jusqu’à leur mort. Sept tumeurs au foie ont été observées, dont deux étaient malignes. Huit rats mâles et huit rats femelles nourris avec la même alimentation, mais sans 4-aminoazobenzène, n’ont eu aucune anomalie au foie (BIBRA, 1989).
Huit rats mâles et huit rats femelles nourris de 75 mg/kg p.c. par jour dans une alimentation faible en protéines n’ont eu aucune tumeur au foie (BIBRA, 1989).
Quarante-quatre rats mâles ont été nourris de 40 à 90 mg/kg p.c. par jour dans une alimentation normale pendant 40 à 60 semaines. Aucune preuve de cancérogénicité n’a été observée (BIBRA, 1989).
Trente rats nourris d’environ 35 mg/kg p.c. par jour dans leur alimentation pendant 3 à 9 semaines n’ont connu aucune augmentation de l’incidence de tumeurs 18 mois plus tard, peu importe si leur traitement comportait ou non un stimulateur de tumeur (BIBRA, 1989).
Trente souris femelles ont été nourries de 52 mg/kg p.c. par jour dans leur alimentation pendant 10 mois. Des observations ont eu lieu pendant sept mois additionnels. Des tumeurs malignes ont été observées chez 22 des 30 souris. Des souris nourries de 27 mg/kg p.c. par jour dans la même étude n’ont montré aucune preuve de cancérogénicité (BIBRA, 1989).
Par voie cutanée
Six rats mâles ont été exposés par de la peinture sur la peau, deux fois par semaine jusqu’à leur mort. L’exposition était d’environ 5-20 mg/kg p.c. Les six rats ont développé des tumeurs bénignes ou malignes après 97 semaines d’exposition (BIBRA, 1989).
Injection sous-cutanée
Trente-six souris ont été nourries d’une alimentation normale ou faible en protéines, et ont reçu une injection sous-cutanée d’environ 250 mg/kg p.c. toutes les deux semaines pendant leur vie. Aucune augmentation de l’incidence de cancérogénicité n’a été observée (BIBRA, 1989).
Des souris (nombre et sexe non indiqués) ayant reçu quatre injections d’environ 200 mg/kg p.c. avant le sevrage ont été observées jusqu’à l’âge d’un an. Des tumeurs au foie ont été observées ainsi qu’une augmentation de l’incidence de tumeurs malignes du système lymphatique (BIBRA, 1989).
Injection intrapéritonale
Vingt rats femelles ont reçu 7,5 à 10 mg/kg p.c. trois fois par semaine pendant cinq semaines. Aucune preuve de cancérogénicité n’était présente après un an d’observation (BIBRA, 1989)
Deux cent quarante-deux souris ont reçu une ou quatre injections d’environ 3 mg/kg p.c. ou plus avant le sevrage. Un examen à l’âge de 9 à 12 mois a permis de détecter des tumeurs malignes au foie chez 190 des 242 souris (BIBRA, 1989).
Génotoxicité
In vivo
Dommages chromosomiques
Résultats positifs : Des rats traités avec une seule dose intrapéritonale (36 ou 143 mg/kg) on connu une augmentation considérable du nombre de cassures de l’ADN à double brin isolé du foie 4, 12 ou 24 heures après l’exposition (BIBRA, 1989).
Résultats positifs : Une augmentation de la fragmentation de l’ADN a été détectée lors d’un essai d’élution alcaline à l’ADN du foie des rats exposés à 1,42 mg/kg (BIBRA, 1989).
Échange de chromatides sœurs
Résultats positifs : Des souris Swiss mâles ont été exposées par voie intrapéritonale à 0, 31 ou 62 mg/kg. Une augmentation liée à la dose des échanges de chromatides sœurs a été observée dans les cellules de la moelle des os des souris (BIBRA, 1989).
In vitro
Mutagénicité bactérienne
Résultats positifs (mutation bactérienne inverse) : Test d’Ames dans diverses souches deSalmonella typhimurium avec activation métabolique seulement (examiné dans BIBRA, 1989).
Résultats positifs (essai par passage sur l’hôte) : Des souris ont reçu 125 mg/kg par injection intramusculaire après des injections intrapéritonales de bactéries. Une augmentation de la mutation inverse a été constatée dans une souche de S. typhimurium (BIBRA, 1989).
Résultats négatifs (essai par passage sur l’hôte) : Des souris exposées par voie orale à 500 mg/kg après une injection intrapéritonale d’une deuxième souche de S. tyhphimurium (non précisée dans la référence secondaire).
Résultats négatifs (mutation bactérienne inverse) : Test d’Ames utilisant des testeurs d’E. coli avec ou sans activation métabolique (BIBRA, 1989).
Mutagénicité des cellules mammaires
Résultats positifs (essai sur des souris L5178Y/TK) : Le taux de mutation directe a augmenté lorsque des cellules du lymphome de souris L5178Y/TK ont été exposées à la substance d’essai avec activation métabolique (BIBRA, 1989).
Synthèse d’ADN non programmée
Résultats positifs : Une incubation de cellules hépatiques de rats fraîchement isolées avec la substance d’essai a entraîné une augmentation de 124 % de la synthèse d’ADN non programmée comparativement à celle des témoins (BIBRA, 1989).
Transformation cellulaire
Résultats positifs : L’exposition a induit une transformation des divers types de cellules mammaliennes. Toutefois, elle n’a pas induit de transformation des cellules de poumons humains avec ou sans activation métabolique (BIBRA, 1989).
1-amino-2-naphtol
Structure chimique :

- N° CAS : 2834-92-6 1198-27-2 (sel Cl-)
- Formule : C10H9NO
- Poids moléculaire : 159,187
- Classifications : s.o.
Cancérogénicité
Implantation : Des granulés de paraffine contenant du 1-amino-2-naphtol dans la vessie des souris ont augmenté l’incidence de métaplasies pavimenteuses. Cette étude n’est pas considérée comme une preuve solide de cancérogénicité, car les granulés de paraffine mêmes peuvent induire la prolifération de cellules épithéliales dans le canal urinaire (BfG, 2003).
Génotoxicité
In vivo
Aucune donnée
In vitro
Mutagénicité bactérienne
Résultats positifs (mutation inverse bactérienne) : Une augmentation de l’incidence de mutation inverse a été observée dans des testeurs S. tyhphimurium TA100 et TA98 lorsque du 1-amino-2-naphtol a subi une réduction du caecum avant l’incubation avec des bactéries (Dillon et al., 1994).
p-phénylènediamine
Structure chimique :
- N° CAS : 106-50-3
- Formule :C6H8N2
- Poids moléculaire : 108,143
- Classifications : s.o.
Cancérogénicité
Par voie cutanée
Des groupes de 50 souris suisses femelles âgées de sept semaines ont reçu de 5 à 10 % d’acétone deux fois par semaine appliqué sur la peau rasée par voie interscapulaire. L’exposition a continué jusqu’à leur mort ou leur euthanasie ou à leur phase moribonde. Aucune augmentation de l’incidence n’a été observée (CSPC, 2006).
Des groupes de cinq lapins femelles ont été exposés à 5 ou 10 % dans l’acétone deux fois par semaine pendant 85 semaines. Aucune augmentation de l’incidence des tumeurs n’a été observée (CSPC, 2006).
Génotoxicité
In vivo
Essai du micronoyau
Résultats négatifs : Des rats exposés par gavage à deux doses de 300 mg/kg avec un intervalle de 24 heures n’ont pas eu d’augmentation de l’incidence d’érythrocytes polychromatiques micronucléés (Hossack et Richardson, 1977). Des résultats négatifs ont été obtenus lorsque des souris CD-1 ont été exposées à 25, 50 ou 100 mg/kg p.c. par injection IP (CSPC, 2006). Résultat négatif chez des rats Wistar exposés par voie orale à 25, 50 ou 100 mg/kg p.c. (CSPC, 2006).
Synthèse d’ADN non programmée
Résultats négatifs : Des rats Wistar exposés à 50 ou 100 mg/kg p.c. par voie orale n’ont pas eu d’augmentation de l’incidence de la synthèse d’ADN non programmée (CSPC, 2006).
In vitro
Mutagénicité bactériologique
Résultats négatifs (mutation inverse bactériologique) : Aucune augmentation de la fréquence de mutation n’a été observée dans les souches TA98, TA100, TA102 ou TA1538 de S. typhimurium avec activation (CSPC, 2006).
Résultats positifs (mutation inverse bactériologique) : Augmentation de la mutagénicité (100-fois) dans les souches de Salmonella typhimurium TA98 et TA98NR en présence d’activateur S9 dérivé du foie de rat (CSPC, 2006).
Mutagénicité mammalienne
Résultats positifs (essai sur des souris L5178Y/TK) : Cellules du lymphome de souris L5178Y exposées avec et sans activation. L’augmentation de la mutagénicité était liée à la dose (CSPC, 2006).
Résultats négatifs (souris L5178Y/hprt) : Des cellules du lymphome de souris L5178Y exposées avec et sans activation. Aucune augmentation de la mutation n’a été observée (CSPC, 2006).
Aberrations chromosomiques
Résultats positifs : Des cellules CHO-K1 exposées au 1,4’-diaminobenzène ont eu une légère augmentation du pourcentage de cellules aberrantes comparativement à celles des témoins (CSPC, 2006).
Aniline
Structure chimique :

- N° CAS : 62-53-3
- Formule : C6H7N
- Poids moléculaire : 93,1283
- Classifications : Groupe 3 du CIRC, Cancérogénicité : Catégorie 3 (UE) et Mutagénicité : Catégorie 3
Cancérogénicité
Par voie orale
Des rats F344 (130 par groupe/sexe) ont été nourris de chlorure d’anilinium à des doses de 0, 10, 30 ou 100 mg/kg p.c. par jour pendant 104 semaines. Il y a eu une augmentation de l’incidence de sarcomes spléniques primaires à la dose élevée (UE, 2004).
Des rats F344 (50/sexe/groupe) ont été nourris avec 0,3 ou 0,6 % de chlorure d’anilinium (174,4 ou 360,5 mg/kg p.c. par jour) pendant 103 semaines. Une augmentation de tumeurs à la rate liée à la dose a été observée. Il y a eu également une augmentation de l’incidence de tumeurs mésenchymateuses (hémangiosarcome, fibrosarcome, fibrome et sarcome) (UE, 2004).
Des souris B6C3F1 (50/groupe) ont reçu une nourriture contenant du chlorure d’anilinium à des concentrations de 0, 0,6 et 1,2 % (0, 737 ou 1 510 mg/kg p.c. par jour chez les mâles, 0, 733 ou 1 560 mg/kg p.c. par jour chez les femelles) pendant 103 semaines suivies de quatre semaines d’observation. Aucune tumeur n’a été liée à l’exposition à la substance d’essai (UE, 2004).
Génotoxicité
In vivo
Essai du micronoyau
Résultats équivoques : De nombreux essais du micronoyau ont été effectués par différents groupes. Quatre essais sur des souris ont donné des résultats positifs à la dose la plus élevée testée, alors que chez les rats, on a observé un résultat positif et un négatif (UE, 2004).
Aberration chromosomique
Résultats négatifs : Aucune augmentation des aberrations chromosomiques n’a été observée dans les cellules de la moelle osseuse des souris ayant reçu deux doses de 220, 300 ou 380 mg/kg par injections intrapéritonales à 24 heures d’intervalle. Des échantillons ont été pris 16, 20 et 24 heures après la seconde administration. Des symptômes cliniques ont été observés (UE, 2004).
Échange de chromatides sœurs
Résultats positifs : Une augmentation liée à une faible dose a été observée dans les cellules de la moelle osseuse chez des groupes de 3 à 9 souris exposées à des doses de 61 à 420 mg/kg par injection intrapéritonale (UE, 2004).
Cassures de brin
Résultats positifs : Des rats et des souris ont été exposées à de l’aniline par administration intrapéritonale. Les cassures ont augmenté dans le foie et les reins des rats, mais étaient négatives dans la rate des rats. Des résultats négatifs ont été obtenus pour le foie, les reins et la moelle osseuse des souris (UE, 2004).
Essai de létalité dominante
Résultats non concluants : Des groupes de 40 mâles ont été exposés à 47, 150 ou 200 mg/kg p.c. par jour par injection intrapéritonale pendant cinq jours. À dose élevée, le nombre d’implants vivants a légèrement diminué, mais était important d’un point de vue statistique. Le nombre de morts prématurées a également augmenté. Toutefois, les conclusions ont été confinées à un groupe de sept souris sur 40 ayant un nombre d’implants vivants manifestement réduit et un nombre élevé d’implants morts prématurément. Ces résultats ont été considérés comme non concluants par l’Union européenne (UE, 2004).
In vitro
Mutagénicité bactériologique
Résultats négatifs : Dans de nombreuses études qui ont utilisé des testeurs de Salmonella typhimurium TA98, TA100, TA1535 et TA1537 avec et sans activation métabolique (UE, 2004).
Résultats positifs (essai par passage sur hôte) : 10 ont reçu 300 mg/kg par voie orale. L’urine a été recueillie 24 heures plus tard et extraite avec de l’éther. Les extraits ont été testés sur des souches deSalmonella typhimurium TA98 et TA100. Une nette réaction dépendante de la dose a été observée dans la souche TA98 avec activation métabolique (UE, 2004).
Mutagénicité des cellules mammaliennes
Résultats équivoques : Cinq essais sur le lymphome de la souris ont été effectués par cinq groupes différents. Un résultat positif clair a été obtenu avec et sans activation métabolique. Trois résultats faiblement positifs ont été déclarés, tous à l’exposition la plus élevée. Un résultat négatif a été obtenu dans une étude comportant des essais seulement dans un système d’activation métabolique (UE, 2004).
Résultats positifs : Une augmentation de la fréquence de mutation a été observée dans un essai HPRT dans lequel étaient utilisées des cellules V79 en présence d’une activation métabolique. Sans activation, le test était négatif. Des résultats positifs n’ont été observés qu’aux doses extrêmement élevées. Cette étude était peu documentée (UE, 2004).
Aberration chromosomique
Résultats positifs : Dans des cellules CHO, des doses élevées d’aniline (1 600 et 5 000 µg/mL) ont causé une augmentation des aberrations chromosomiques en présence d’activation métabolique. Les doses se situant dans le même intervalle ont également augmenté le nombre d’aberrations chromosomiques dans les cellules CHL et V79 (UE, 2004).
Échange de chromatides sœurs
Résultats positifs : Un échange de chromatides sœurs a été induit dans les fibroblastes humains qui avaient un manque important de réductase cytochrome p450 et NADPH-cytochrome p450. Un échange de chromatides sœurs était également induit dans les lymphocytes T induisant de la concanavaline A de cultures de sang entier; toutefois, l’effet n’a pas été constaté dans les cultures comportant des lymphocytes purifiés alors qu’une augmentation marginale de l’échange de chromatides sœurs a été observée lorsque des lymphocytes purifiés étaient exposés à l’aniline en présence de 1 000 µg/mL d’hémoglobine. L’UE a noté que cette étude a démontré que les érythrocytes contribuaient à la transformation de l’aniline en intermédiaires génotoxiques (UE, 2004).
Synthèse d’ADN non programmée
Résultats négatifs : Aucune augmentation de la réparation de l’ADN n’a été observée dans les hépatocytes humains primaires ou dans ceux des rats (UE, 2004).
Cassures de brin
Résultats équivoques : Une dose très élevée (21,5 mM) a causé une augmentation des cassures de brin d’ADN dans les cellules du lymphome de souris avec activation métabolique. Les auteurs ont interprété ce résultat comme étant équivoque. Aucune augmentation n’a été observée sans activation métabolique (UE, 2004).
| N° CAS | DEREK1 | CASETOX (2008) | TOPKAT (2008) | |||||||
|---|---|---|---|---|---|---|---|---|---|---|
| Cancer | m-rat | f-rat | m-souris | f-souris | Rongeurs du NTP | NTP m-rat |
NTP f-rat |
NTP m-souris |
NTP f-souris |
|
| 85-86-9 (origine) | P | NC | NC | N | N | NC | P | HC | P | NC |
| 60-09-3 | P | NC | NC | N | N | P | P | NC | N | N |
| 62-53-3 | HC | P | P | N | N | P | P* | P* | N | N |
| 106-50-3 | P | N | N | N | N | N | N | N | P | N |
| 2834-92-6 | HC | N | N | N | N | P | P | N | N | N |
| N° CAS | Ames | ChrAb | Induction de micronoyaux | Mutation du lymphome de la souris | |||
|---|---|---|---|---|---|---|---|
| Derek | CT | TK | Derek | CT# | CT | CT | |
| 85-86-9 (origine) | P | N | NC | HC | NC | N | NC |
| 60-09-3 | P | N | P* | HC | P | NC | P |
| 62-53-3 | HC | N | N | HC | P | P | P |
| 106-50-3 | P | N | P* | P | P | N | P |
| 2834-92-6 | HC | N | P | HC | N | N | N |
Notes de bas de page
[2] La détermination de la conformité à l’un ou plusieurs des critères énoncés à l’article 64 repose sur l’évaluation des risques pour l’environnement ou la santé humaine associés aux expositions dans l’environnement en général. Pour les humains, ceci inclut, sans toutefois s’y limiter, les expositions à l’acrylate d’éthyle par l’air ambiant et intérieur, l’eau potable, les produits alimentaires et l’utilisation de produits de consommation. Une conclusion établie en vertu de la LCPE (1999) sur les substances des lots 1 à 12 du Défi, énumérées dans le Plan de gestion des produits chimiques, n’est pas pertinente, ni n’empêche une évaluation en fonction des critères de danger définis dans leRèglement sur les produits contrôlés qui fait partie du cadre réglementaire applicable au Système d’information sur les matières dangereuses utilisées au travail pour les produits destinés à être utilisés au travail.
[3] Voir la section Absorption et biodisponibilité pour des renseignements sur le fondement des valeurs d’absorption par voie orale et cutanée utilisées pour estimer l’exposition au Solvent Red 23.
[4] Dose approximative = 67 mg/kg p.c. par jour à 2 mg/animal par jour avec des souris ayant un poids corporel de 0,05 kg (Santé Canada, 1994).
[5] Dose approximative = 2 000 mg/kg p.c. par jour à partir de 40 000 ppm dans l’alimentation (4 %) et conversion de la dose de 0,05 pour les rats (Santé Canada, 1994).
[6] Expositions indiquées dans le pourcentage de l’alimentation. Converti en mg/kg p.c. par jour au moyen des valeurs de référence de Santé Canada (Santé Canada, 1994).
[7] Estimation de la dose basée sur : 1 mg/dose (0,1 % dans un volume de 1 mL) et un poids corporel de 0,35kg pour les rats (Santé Canada, 1994).
[8] La dose estimée est d’environ 33 mg/kg p.c. par dose hebdomadaire (l’équivalent de la dose amortie de 5 mg/kg p.c. par jour) d’après une dose de 1 mg appliquée hebdomadairement (1 % dans 0,1 mL appliqué) et un poids corporel de 0,03 kg pour les souris (Santé Canada, 1994).
[9] Classification actuelle de Cancérogène 2 et Mutagène 3, 2 dans (CLP, annexe VI, tableau 3.1), classification antérieure de Cancérogène Catégorie 3 et Mutagène Catégorie 3 (CLP, annexe VI, tableau 3.2) (Commission européenne, 2008; ESIS, 1995-2010).
[10] o-aminoazotoluène, le produit prévu de la rupture des liaisons azoïques du Sudan IV, est l’analogue diméthyle du 4-aminoazobenzène, un métabolite prévu du Solvent Red 23.
[11] elon les prévisions, le Solvent Red 23 et le Sudan IV génèrent du 1-amino-2-naphthol par rupture de ses liaisons azoïques.
[12] Les données relatives aux effets sur la santé des produits potentiels de rupture réductrice des liaisons azoïques ont été recueillies principalement de sources secondaires, qui sont citées ici.
[13] Le 1-((4-aminophényl)azo)-2-naphthalénol est également un produit de la rupture réductrice des liaisons azoïques du Solvent Red 23. Comme ce produit n’a pas de n° CAS ni de données relatives aux effets sur la santé, il n’a pas été présenté dans ce tableau.



