Évaluation préalable pour le Défi concernant le 1-(4-méthyl-2-nitrophénylazo)-2-naphtol (Pigment Red 3)
Numéro de registre du Chemical Abstracts Service 2425-85-6
Environnement Canada
Santé Canada
Février 2009
Table des matières
- Synopsis
- Introduction
- Identité de la substance
- Propriétés physiques et chimiques
- Sources
- Utilisations
- Rejets dans l'environnement
- Devenir dans l'environnement
- Persistance et potentiel de bioaccumulation
- Potentiel d'effets nocifs sur l'environnement
- Potentiel d'effets nocifs sur la santé humaine
- Conclusion
- Références
- Annexe 1. Sommaires de rigueur d'études
- Annexe 2 : Limites supérieures de l'exposition au Pigment Red 3 présent dans les produits de consommation, estimées à l'aide de la version 4.1 du modèle ConsExpo (RIVM, 2006a)
- Annexe 3 : Sommaire des renseignements concernant les effets du Pigment Red 3 sur la santé
Synopsis
Conformément à l'article 74 de la Loi canadienne sur la protection de l'environnement (1999) [LCPE (1999)], les ministres de l'Environnement et de la Santé ont effectué une évaluation préalable du 1-(4-Méthyl-2-nitrophénylazo)-2-naphtol (Pigment Red 3), dont le numéro de registre du Chemical Abstracts Service est 2425-85-6. Une priorité élevée a été accordée à l'évaluation préalable de cette substance inscrite au Défi, car elle répondait initialement aux critères environnementaux de la catégorisation relatifs à la persistance et à la toxicité intrinsèque pour les organismes non humains et l'on croit qu'elle est commercialisée au Canada.
Comme le Pigment Red 3 répondait aussi aux critères de la catégorisation pour le plus fort risque d'exposition, on a jugé prioritaire d'évaluer les risques qu'il peut présenter pour la santé humaine. Par conséquent, la présente évaluation est axée sur les renseignements utiles à l'évaluation des risques pour la santé et l'environnement.
Le Pigment Red 3 est un pigment azoïque organique utilisé principalement au Canada et dans d'autres pays comme pigment rouge dans les peintures. Il n'est pas produit naturellement dans l'environnement, Le Pigment Red 3 a été fabriqué dans une quantité de 100 000 à 1 000 000 kg au Canada en 2006. Après les exportations du produit, de 30 000 à 50 000 kg demeuraient au pays. Au total, sept entreprises ont déclaré avoir importé la substance entre 10 000 et 1 000 000 kg. Neuf entreprises ont indiqué avoir utilisé environ 40 000 kg de Pigment Red 3 au Canada.. Compte tenu de la quantité de Pigment Red 3 commercialisée au Canada et des utilisations susceptibles d'entraîner la dispersion de la substance, cette dernière pourrait être rejetée dans l'environnement au Canada.
Selon les profils d'utilisation déclarés et certaines hypothèses, la plus grande partie du Pigment Red 3 aboutit dans les décharges. De petites quantités seraient libérées dans l'eau (4,7 %) et le sol (1,6 %). Dans l'environnement, le Pigment Red 3 est présent sous forme particulaire; ainsi il n'est ni soluble dans l'eau ni volatil. Pour ces raisons, le Pigment Red 3 est susceptible, sous l'action de la gravité, de se déposer dans les sédiments s'il est rejeté dans l'eau et aura tendance à demeurer dans le sol s'il est rejeté en milieu terrestre. Il ne devrait pas être présent en quantité importante dans d'autres milieux. Il ne devrait pas non plus être transporté dans l'atmosphère sur de grandes distances.
D'après ses propriétés physiques et chimiques, le Pigment Red 3 devrait être persistant dans l'eau, le sol et les sédiments. De nouvelles données expérimentales sur sa solubilité dans l'octanol et dans l'eau semblent indiquer que ce pigment a un faible potentiel d'accumulation dans les tissus adipeux des organismes. La substance ne devrait donc pas répondre aux critères de la bioaccumulation tels qu'ils sont définis dans le Règlement sur la persistance et la bioaccumulation. En outre, de nouvelles données expérimentales sur la toxicité, de même que de nouvelles prévisions en matière de toxicité qui tiennent compte des estimations révisées du potentiel de bioaccumulation, semblent indiquer que la substance présente un potentiel de toxicité négligeable à faible pour les organismes aquatiques.
Dans le cadre de la présente évaluation préalable, un scénario d'exposition très prudent selon lequel on présume que toutes les activités industrielles (fabricants et utilisateurs du pigment) provoquent le rejet de Pigment Red 3 en un seul point de décharge en milieu aquatique a été conçu. La concentration environnementale estimée était inférieure à la concentration estimée sans effet chez une espèce aquatique sensible. En outre, puisque le Pigment Red 3 peut être utilisé dans des produits de consommation, un scénario de rejets domestiques prudent en fonction de la quantité de ce pigment sur le marché a également été élaboré. Selon ce scénario, les cours d'eau récepteurs canadiens modélisés obtenaient des concentrations environnementales estimées inférieures à la concentration estimée sans effet.
À la lumière des renseignements dont on dispose, il est conclu que le Pigment Red 3 ne pénètre pas dans l'environnement en une quantité ou une concentration, ou dans des conditions de nature à avoir, immédiatement ou à long terme, un effet nocif sur l'environnement ou sur la diversité biologique.
D'après les renseignements pertinents considérés, notamment le poids de la preuve basée sur des évaluations d'organismes nationaux et internationaux, la cancérogénicité constitue l'effet critique pour la caractérisation des risques que présente le Pigment Red 3 pour la santé humaine. Des tumeurs liées à l'exposition ont été observées à de nombreux endroits chez les rats mâles et femelles ainsi que chez les souris mâles. En conséquence, même si le mode d'induction tumorale n'a pas été élucidé, à la lumière des résultats équivoques concernant la génotoxicité, entre autres certains résultats positifs en matière de mutagénicité et des dommages à l'ADN relevés dans une base de données restreinte, on ne peut pas écarter la possibilité que les tumeurs observées résultent d'une interaction directe avec le matériel génétique.
Étant donné la cancérogénicité du Pigment Red 3, qui entraîne une probabilité d'effet nocif à tout degré d'exposition, il est conclu que le Pigment Red 3 est une substance pouvant pénétrer dans l'environnement en une quantité ou une concentration ou dans des conditions de nature à constituer un danger au Canada pour la vie ou la santé humaines.
Cette substance s'inscrira dans la prochaine mise à jour de l'inventaire de la Liste intérieure des substances (LIS). De plus, des activités de recherche et de surveillance viendront, s'il y a lieu, appuyer la vérification des hypothèses formulées au cours de l'évaluation préalable et, le cas échéant, l'efficacité des mesures de contrôle possibles définies à l'étape de la gestion des risques.
Compte tenu des renseignements disponibles, le Pigment Red 3 remplit un ou plusieurs critères de l'article 64 de la LCPE (1999).
Introduction
La Loi canadienne sur la protection de l'environnement (1999) [LCPE (1999)] (Canada, 1999) impose aux ministres de l'Environnement et de la Santé de procéder à une évaluation préalable des substances qui répondent aux critères de la catégorisation énoncés dans la Loi afin de déterminer si elles présentent ou sont susceptibles de présenter un risque pour l'environnement ou la santé humaine. Selon les résultats de cette évaluation, les ministres peuvent proposer de ne rien faire à l'égard de la substance, de l'inscrire sur la Liste des substances d'intérêt prioritaire en vue d'une évaluation plus détaillée, ou de recommander son inscription sur la Liste des substances toxiques de l'annexe 1 de la Loi et, s'il y a lieu, sa quasi-élimination'.
En se fondant sur l'information fournie dans le cadre de la catégorisation, les ministres ont jugé qu'une attention hautement prioritaire devait être accordée à un certain nombre de substances, à savoir :
- celles qui répondent à tous les critères environnementaux de la catégorisation, notamment la persistance (P), le potentiel de bioaccumulation (B) et la toxicité intrinsèque (Ti) pour les organismes aquatiques, et que l'on croit être commercialisées au Canada, ou;
- celles qui répondent aux critères de la catégorisation pour le plus fort risque d'exposition (PFRE) ou qui présentent un risque d'exposition intermédiaire (REI) et qui ont été jugées particulièrement dangereuses pour la santé humaine, compte tenu du classement attribué par d'autres organismes nationaux ou internationaux quant à la cancérogénicité, à la génotoxicité ou à la toxicité sur le plan du développement ou de la reproduction.
Le 9 décembre 2006, les ministres ont donc publié un avis d'intention dans la Partie I de la Gazette du Canada (Canada, 2006), dans lequel ils priaient l'industrie et les autres parties intéressées de fournir, selon un calendrier déterminé, des renseignements précis qui pourraient servir à étayer l'évaluation des risques ainsi qu'à élaborer et à évaluer les meilleures pratiques de gestion des risques et de bonne gestion des produits pour ces substances jugées hautement prioritaires.
Le 1-(4-méthyl-2-nitrophénylazo)-2-naphtol est une substance dont l'évaluation des risques pour l'environnement a été jugée hautement prioritaire, car elle est persistante, bioaccumulable et intrinsèquement toxique pour les organismes aquatiques et l'on croit qu'elle est commercialisée au Canada. Le volet du Défi portant sur cette substance a été publié dans la Gazette du Canada le 18 août 2007 (Canada, 2007a). En même temps a été publié le profil de cette substance, qui présentait l'information technique (obtenue avant décembre 2005) sur laquelle a reposé sa catégorisation. Des renseignements sur les propriétés chimiques, le potentiel de bioaccumulation les utilisations et les dangers inhérents à la substance ont été communiqués en réponse au Défi.
La substance 1-(4-méthyl-2-nitrophénylazo)-2-naphtol a également été considérée comme hautement prioritaire dans l'évaluation des risques potentiels encourus du point de vue de la santé humaine, car elle répond aux critères de classification du plus fort risque d'exposition (PFRE). La présente évaluation est donc axée principalement sur les renseignements d'intérêt pour l'évaluation des risques touchant à la fois l'environnement et la santé humaine.
Les évaluations préalables effectuées aux termes de la LCPE (1999) mettent l'accent sur les renseignements jugés essentiels pour déterminer si une substance répond aux critères de toxicité des substances chimiques énoncés à l'article 64 de la Loi :
« 64. [...] est toxique toute substance qui pénètre ou peut pénétrer dans l'environnement en une quantité ou concentration ou dans des conditions de nature à :
- avoir, immédiatement ou à long terme, un effet nocif sur l'environnement ou sur la diversité biologique;
- mettre en danger l'environnement essentiel pour la vie; ou
- constituer un danger au Canada pour la vie ou la santé humaines. »
Les évaluations préalables visent à examiner les renseignements scientifiques et à tirer des conclusions fondées sur la méthode du poids de la preuve et le principe de prudence, conformément aux dispositions de la LCPE (1999).
La présente évaluation préalable prend en considération les renseignements sur les propriétés chimiques, les dangers, les utilisations et l'exposition, y compris ceux fournis dans le cadre du Défi. Les données pertinentes pour l'évaluation préalable de cette substance ont été relevées dans des publications originales, des rapports de synthèse et d'évaluation, des rapports de recherche de parties intéressées et d'autres recherches documentaires menées récemment, jusqu'en juillet 2007 pour les sections traitant des aspects écologiques. Les études importantes ont fait l'objet d'une évaluation critique; les résultats de la modélisation ont pu être utilisés dans la formulation des conclusions. Lorsqu'ils étaient disponibles et pertinents, les renseignements contenus dans les évaluations des dangers effectuées par d'autres instances ont également été utilisés. L'évaluation des risques pour la santé humaine comprend l'examen des données pertinentes pour l'évaluation de l'exposition (non professionnelle) de la population dans son ensemble ainsi que de l'information sur les dangers pour la santé (surtout fondée sur des évaluations réalisées par d'autres organismes selon la méthode du poids de la preuve et ayant servi à déterminer le caractère hautement prioritaire de la substance). Les décisions concernant la santé humaine reposent sur la nature de l'effet critique retenu ou sur l'écart entre les valeurs prudentes donnant lieu à des effets et les estimations de l'exposition, en tenant compte de la confiance accordée au caractère exhaustif des bases de données sur l'exposition et les effets, cela dans le contexte d'une évaluation préalable. Cette évaluation préalable ne constitue pas un examen exhaustif ou critique de toutes les données disponibles. Elle fait plutôt état d'une synthèse des études et éléments d'information les plus importants venant appuyer la conclusion.
Cette évaluation préalable a fait l'objet d'une consultation indépendante par des pairs qui ont examiné la section traitant de la santé dans ce document. Des commentaires sur les parties techniques concernant la santé humaine ont été communiqués par des experts scientifiques qui ont été choisis et dirigés par Toxicology Excellence for Risk Assessment (TERA) et comprenaient Donna J.Vorhees (The Science Collaborative North Shore), Susan Griffin (U.S. Environmental Protection Agency), et Joan Strawson (TERA). Par ailleurs, l'ébauche de cette évaluation préalable a fait l'objet d'une période d'observation du public de 60 jours. Bien que des commentaires externes aient été pris en considération, Santé Canada et Environnement Canada assument la responsabilité du contenu final et des résultats de l'évaluation préalable. Les principales données et considérations sur lesquelles repose la présente évaluation sont résumées ci-après.
Identité de la substance
Aux fins du présent document, la substance dont il est question ici est appelée Pigment Red 3.
| Numéro de registre du Chemical Abstracts Service (no CAS) | 2425-85-6 |
|---|---|
| Nom dans la LIS | 1-(4-méthyl-2-nitrophénylazo) -2- naphtol |
| Noms relevés dans les National Chemical Inventories (NCI)Note de bas de tableau a | 2-Naphthalenol, 1-[2-(4-methyl-2-nitrophenyl)diazenyl]-(TSCA) 2-Naphthalenol, 1-[(4-methyl-2-nitrophenyl)azo]- (AICS, PICCS, ASIA-PAC, NZIoC) 1-(4-méthyl-2-nitrophénylazo)-2-naphtol (EINECS) Pigment Red 3 (ENCS) Pigment red 003(ECL) 2-Naphthalenol, 1-[(4-methyl-2-nitrophenyl)azo]-(toluidine red) (PICCS) C.I. Pigment Red 3, Naphth-2-ol, 1-[(4-methyl-2-nitrophenyl)azo](Toluidine Red) (PICCS) Toluidine Red (PICCS) |
| Autres noms | 1-(o-Nitro-p-tolylazo)-2-naphthol 1-[(2-Nitro-4-methylphenyl)azo]-2-naphthol 2-Nitro-p-toluidine-2-naphthol |
| Groupe chimique (groupe de la LIS) |
Produits chimiques organiques définis |
| Principale classe chimique ou utilisation | Dérivés azoïques; naphtalènes |
| Principale sous-classe chimique | Pigment du groupe du bêta-naphtol |
| Formule chimique | C17H13N3O3 |
| Structure chimique |  |
| Simplified Molecular Input Line Entry System (SMILES) | O=N(=O)c(c(N=Nc(c(c(ccc1)cc2)c1)c2O)ccc3C)c33 |
| Masse moléculaire | 307,31 g/mol |
Propriétés physiques et chimiques
L'industrie des pigments synthétise des pigments organiques qui sont peu ou même très peu solubles (moins de 1 mg/L à moins de 0,01 mg/L) dans presque tous les solvants, ceci parce que les fabricants veulent offrir' des produits qui conserveront leur couleur longtemps et dans n'importe quel type de matériau. Pour accentuer la faible solubilité, les fabricants conçoivent des produits caractérisés par des interactions intramoléculaires et intermoléculaires fortes. Dans le cas des dérivés du bêta-naphtol, il s'agit de ponts hydrogène intramoléculaires bifurqués. Même si la structure du Pigment Red 3 est souvent représentée sous la forme indiquée au tableau 1, il a été déterminé que le tautomère de cétohydrazone est favorisé d'après les longueurs de liaison mesurées. Le tautomère de cétohydrazone est différent pour ce qui concerne certaines liaisons. En l'occurrence, une cétone remplace le groupement hydroxyle sur le noyau naphtalénique, il y a une double liaison entre l'azote et le noyau naphtalénique, et la liaison azoïque est simple (figure 1). Cette structure permet la formation de ponts hydrogène bifurqués entre les substituants en position ortho sur le noyau phényle (comme -Cl ou -NO2), le groupement azoïque et l'oxygène de la cétone sur le groupement naphtalène. Ces molécules peuvent être liées par des forces de Van der Waals faibles et des forces de transfert de charge, ce qui provoque l'empilement de molécules en colonne dans un cristal (Herbst et Hunger, 2004; Whitaker, 1978; Lincke, 2003).

Figure 1. Structure du pigment de bêta-naphtol (Whitaker, 1978)
Comme dans le cas de la plupart des pigments organiques, les pigments de bêta-naphtol n'existent généralement pas en tant que molécules individuelles. Ils se présentent plutôt sous la forme de particules de taille submicronique. Ils forment des poudres typiquement composées de particules primaires (le réseau cristallin d'un pigment), d'agrégats et d'agglomérats. Les fabricants de pigments fournissent habituellement les spécifications physiques de leurs produits, dont la taille moyenne des particules dans la poudre (voir le tableau 2a). Les utilisateurs peuvent ainsi déterminer quel pigment convient le mieux pour colorer leurs produits, étant donné que la performance du pigment est principalement régie par la composition granulométrique (Herbst et Hunger, 2004).
Le tableau 2a présente les propriétés physiques et chimiques modélisées et expérimentales du Pigment Red 3 qui se rapportent à son devenir dans l'environnement. Des modèles de relations quantitatives structure-activité (RQSA) sont généralement utilisés pour estimer ces propriétés. Les prévisions générées par ces modèles sont quant à elles fondées sur les caractéristiques des molécules individuelles. On s'attend à ce que le Pigment Red 3 soit présent sous forme cristalline dans l'environnement; c'est pourquoi une incertitude est associée aux données physiques et chimiques modélisées. La valeur modélisée du log Koe, soit 6,45 (KOWWIN, 2000), qui a servi à la catégorisation, laisse supposer que la solubilité du Pigment Red 3 est beaucoup plus élevée dans l'octanol que dans l'eau. Les données expérimentales de solubilité, par contre, révèlent que la différence de solubilité dans les deux solvants est plutôt négligeable, et donc que le coefficient de partage modélisé est sans doute surestimé. Le logarithme du rapport Co/Ce a été calculé à partir des valeurs expérimentales de la solubilité du Pigment Red 3 dans l'octanol (Co) et dans l'eau (Ce), et ce rapport établi à l'aide des données expérimentales a été préféré au log Koe déterminé par modélisation. En conséquence, la valeur modélisée du log Koe n'a pas été prise en considération dans la présente évaluation. On a plutôt présenté le logarithme du rapport Co/Ce (tableau 2a).
Les valeurs expérimentales de solubilité indiquées au tableau 2a ont été déterminées selon une méthode dynamique comportant de longues périodes de contact entre les particules de pigment et le solvant, ainsi qu'une étape de filtration pour éliminer le plus de particules en suspension possible. Les résultats ont fait l'objet d'examens critiques et, bien que dans aucune de ces études on n'ait mentionné l'utilisation de substances de référence dont la solubilité était connue, ils ont été jugés suffisamment fiables aux fins de la présente évaluation des risques.
| Type | Valeur | Température (°C) | Références | |
|---|---|---|---|---|
| État physique | Expérimental | Poudre rouge | Fiche signalétique de BASF, 2004 | |
| Taille moyenne des particules (µm) | Expérimental | 255 à 370 | Clariant, 2007 | |
| Taille moyenne des particules (µm) | Expérimental | 260 à 530 | NPIRI, 2000 | |
| Point de fusion (°C) | Expérimental | 276 | APE du Danemark, 1998 | |
| Point de fusion (°C) | Modélisé | 200,3 | MPBPWIN, 2000. | |
| Point d'ébullition (°C) | Expérimental | Non disponible | ||
| Point d'ébullition (°C) | Modélisé | 473,67 | MPBPWIN, 2000. | |
| Masse volumique (kg/m3) | Expérimental | 1 400 (1,4 g/cm3) |
Fiche signalétique de BASF, 2004 | |
| Masse volumique (kg/m3) | Modélisé | Non disponible | ||
| Pression de vapeur (Pa) | Expérimental | Non disponible | ||
| Pression de vapeur (Pa) | Modélisé | 3,52 × 10-8 (2,64 × 10-10 mm Hg) |
25 | MPBPWIN, 2000. |
| Constante de la loi de Henry (Pa·m3/mol) |
Expérimental | Non disponible | ||
| Constante de la loi de Henry (Pa·m3/mol) |
Modélisé (méthode d'estimation fondée sur les liaisons) | 6,59 × 10-8 (6,5 × 10-13 atm·m3/mol) |
25 | HENRYWIN, 2000. |
| Constante de la loi de Henry (Pa·m3/mol) |
Modélisé (méthode d'estimation fondée sur les liaisons) | 1,19 × 10-7 (1,17 × 10-12 atm·m3/mol) |
25 | HENRYWIN, 2000. |
| Log Koe (coefficient de partage octanol/eau) [sans dimension] | Expérimental | Non disponible | ||
| Log Koe (sans dimension) | Modélisé | Non applicable | KOWWIN, 2000. | |
| Log (Co/Ce) (sans dimension) | Expérimental | 3,73 | Calculé à partir des données du tableau 2a | |
| Log Kco (coefficient de partage carbone organique/eau – L/kg) [sans dimension] | Expérimental | Non disponible | ||
| Log Kco (sans dimension) | Modélisé | Non disponible | ||
| Solubilité dans l'eau (mg/L) | Expérimental | 0,0033 | 23 à 24 | Étude présentée, 2007a |
| Solubilité dans l'eau (mg/L) | Modélisé | 0,49 | 25 | WSKOWWIN, 2000 |
| Solubilité dans d'autres solvants (mg/L) | Expérimental (octanol) | 17,9 | 23 à 24 | Étude présentée, 2007b |
| pKa (constante de dissociation acide) (sans dimension) | Modélisé | 13,5 | ACD, 2005. | |
| pKa (sans dimension) | Expérimental | Non disponible |
On a mené des études de solubilité dans l'octanol et dans l'eau sur deux substances ayant une structure semblable, soient le Pigment Red 4 et le Pigment Orange 5 (no CAS 2814-77-9 et 3468-63-1). Les résultats appuient la faible solubilité dans l'eau et l'octanol du Pigment Red 3. On a présenté le logarithme du rapport Co/Ce au lieu du log Koe (tableau 2b).
| Substance chimique | Structure | Notes |
|---|---|---|
| Analogue Pigment Red 4 (No CAS 2814-77-9) |
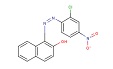 |
La structure du Pigment Red 4 diffère de celle du Pigment Red 3 à deux égards : elle comporte un Cl au lieu du NO2, et un NO2 au lieu du groupement méthyle sur le noyau benzénique terminal. |
| Analogue Pigment Orange 5 (No CAS 3468-63-1) |
 |
La structure du Pigment Orange 5 diffère de celle du Pigment Red 3 à un égard : elle comporte un NO2 au lieu du groupement méthyle sur le noyau benzénique terminal. |
| Propriété | Valeur | Température (°C) | Références |
|---|---|---|---|
| Point de fusion (°C) | 276 | NPIRI, 2000 | |
| Solubilité dans l'eau (mg/L) | 0,0033 | 22 à 23 | Étude présentée, 2007c |
| Solubilité dans l'octanol (mg/L) | 9,4 | 22 à 23 | Étude présentée, 2007d |
| Log du rapport Co/Ce (sans dimension) | 3,5 | Calculé |
| Propriété | Valeur | Température (°C) | Références |
|---|---|---|---|
| Point de fusion (°C) | 302 | EPA du Danemark,1998 | |
| Solubilité dans l'eau (mg/L) | 0,0068 | 26 à 27 | Étude présentée, 2007e |
| Solubilité dans l'octanol (mg/L) | 1,76 | 26 à 27 | Étude présentée, 2007f |
| Log du rapport Co/Ce (sans dimension) | 2,4 | Calculé |
Sources
Le Pigment Red 3 n'est pas produit naturellement dans l'environnement.
D'après les résultats d'une enquête menée auprès de l'industrie au cours de l'année civile 2006, à la suite de la publication d'un avis conformément à l'article 71 de la LCPE (1999) (Canada 2007b), douze (12) entreprises ont été identifiées comme ayant fabriqué, importé ou utilisé du Pigment Red 3 soit seul, dans un produit, dans un mélange ou dans un article manufacturé en une quantité d'au moins 100 kg, ou comme l'ayant utilisé en une quantité d'au moins 1 000 kg, à quelque concentration que ce soit (Environnement Canada, 2008a). Une seule entreprise a déclaré fabriquer du Pigment Red 3 au Canada en une quantité dépassant le seuil de déclaration de 100 kg (de 100 000 à 1 000,000 kg). Sur ces quantités fabriquées, 30 000 à 50 000 kg seulement étaient exportés du Canada. Par ailleurs, six entreprises ont déclaré avoir importé une quantité supérieure au seuil de 100 kg, tandis qu'une seule a déclaré en avoir importé une quantité inférieure, sachant que les importations déclarées dans l'ensemble se situent entre 10 000 et 100 000 kg. Sept entreprises ont déclaré avoir utilisé une quantité de Pigment Red 3 supérieure au seuil de déclaration de 1 000 kg, deux ayant indiqué en avoir utilisé une quantité inférieure. En 2006, la quantité totale utilisée était d'environ 40 000 kg.
Le Pigment Red 3 est l'un des vingt pigments organiques les plus produits (en volume) dans le monde (Herbst et Hunger, 2004). Des utilisations du Pigment Red 3 fluctuant entre 225 et 450 tonnes ont été déclarées aux États-Unis aux termes de l'Inventory Update Rule au cours des années 1990, 1994, 1998 et 2002. Le Pigment Red 3 est une substance chimique produite en faible quantité dans l'Union européenne (UE), ce qui signifie que sa production annuelle devrait y être de 10 à 1 000 tonnes. La base de données sur les substances dans les préparations dans les pays nordiques indique, pour 2004, des quantités utilisées totalisant environ 72,3 tonnes au Danemark, 18,4 tonnes en Norvège et 6 tonnes en Suède (SPIN, 2006).
Utilisations
Au Canada, le Pigment Red 3 est utilisé dans diverses applications industrielles et commerciales, soit principalement comme pigment organique dans la peinture-émail (brillante) alkyde (et dernièrement, dans la peinture acrylique) pour l'intérieur et pour l'extérieur, notamment dans les apprêts antirouille, dans les plastiques, et aussi dans les encres d'impression (poudres d'impression), dans les textiles et les revêtements au polyuréthane. (Environnement Canada, 2008a). L'unique fabricant de Pigment Red 3 au Canada utilise 95 % du pigment fabriqué pour des préparations commerciales de peinture. Parmi les applications industrielles, on compte la fabrication ou l'importation de peintures-émail industrielles destinées aux outils et au matériel en métal, mais aussi la formulation et la coloration des plastiques ainsi que la fabrication d'encres d'impression industrielles. Du côté commercial, on s'en sert dans les peintures-émail commerciales vendues pour utilisation à l'intérieur ou à l'extérieur, dans les peintures décoratives ou les revêtements et les agents d'étanchéité à base d'acrylique. L'exposition de la population canadienne dans son ensemble au Pigment Red 3 pourrait se limiter uniquement aux situations dans lesquelles des produits de consommation comportant cette substance sont utilisés. D'après l'enquête effectuée en vertu de l'article 71 de la LCPE(1999) et compte tenu des commentaires reçus de la part du public, de telles situations constitueraient les applications au pinceau, au rouleau et en aérosol de catégories de peinture contenant le Pigment Red 3.
Au Canada, il y a eu trois avis de déclaration en ce qui concerne des produits cosmétiques faisant état du Pigment Red 3 dans leur composition, à savoir un vernis à ongles et deux pains de savon à des concentrations inférieures à 0,1 % en poids (SDC, 2008). Il a été déclaré que l'un des deux savons était destiné à l'usage des enfants. Le Pigment Red 3 ne figure pas sur la Liste critique des ingrédients dont l'utilisation est restreinte ou interdite dans les cosmétiques de Santé Canada pour ce qui concerne les produits cosmétiques canadiens.
On sait que le Pigment Red 3 est utilisé dans certains autres pays comme agent de coloration dans les cosmétiques. En Europe, l'utilisation du Pigment Red 3 (CI 12120) est permise exclusivement dans les produits cosmétiques entrant brièvement en contact avec la peau, d'après l'annexe IV, Partie I, de la directive du Conseil 76/768/CEE, (Commission européenne, 1976). Contrairement au Canada, l'utilisation du Pigment Red 3 dans les cosmétiques n'a pas été approuvée aux États-Unis (CTFA, 2008).
Le Pigment Red 3 figure sur la liste des produits de formulation (liste 2) de l'Agence de réglementation de la lutte antiparasitaire qui regroupe les produits de formulation jugés potentiellement toxiques. (ARLA 2007, ARLA 2007a). Il est à noter que le Pigment Red 3 est utilisé dans deux produits antiparasitaires (peintures antisalissures) à des concentrations inférieures à 1 % de la quantité totale de produit (communication personnelle avec l'ARLA, 2008).
Aucune utilisation de Pigment Red 3 n'a été signalée dans les produits alimentaires (Environnement Canada, 2008a).
Rejets dans l'environnement
Les réponses à l'avis publié en application de l'article 71 de la LCPE (Environnement Canada, 2008a) indiquent que le Pigment Red 3 est principalement utilisé dans les peintures. Les quantités de Pigment Red 3 importées et fabriquées, ainsi que ses profils d'utilisation, tels qu'ils sont déclarés en 2006 au Canada, ont été utilisés pour estimer les rejets.
Outil de débit massique
Un outil basé sur le débit massique a été utilisé pour estimer les rejets potentiels de Pigment Red 3 dans l'environnement à différentes étapes de son cycle de vie (Environnement Canada, 2008b). On estime donc, pour chaque type d'utilisation connue, la proportion et la quantité des rejets de la substance dans les différents milieux naturels, ainsi que la proportion de la substance qui est transformée chimiquement ou envoyée dans des lieux d'élimination des déchets. Sauf s'il peut utiliser des données spécifiques sur le taux ou le potentiel de rejet de la substance à partir des décharges et des incinérateurs, l'outil de mesure du débit massique ne représente pas quantitativement les rejets dans l'environnement dus à l'élimination.
Les hypothèses et les paramètres employés pour effectuer ces estimations sont fondés sur les renseignements obtenus de diverses sources, notamment les réponses à des enquêtes menées conformément à la réglementation, les données de Statistique Canada, les sites Web des fabricants et les bases de données techniques. À cette fin, les facteurs d'émission sont très utiles; ils sont habituellement exprimés comme la fraction d'une substance rejetée dans l'environnement, notamment pendant sa fabrication, son traitement ou ses utilisations associées à des procédés industriels. Ces données découlent notamment de scénarios d'émissions, souvent élaborés sous les auspices de l'Organisation de coopération et de développement économiques (OCDE), et d'hypothèses par défaut utilisées par différents organismes internationaux de réglementation des produits chimiques. Il est à noter que le degré d'incertitude associé à la masse et à la quantité d'e substance rejetée dans l'environnement augmente généralement vers la fin du cycle de vie.
| Devenir | Proportion massique (%)Note de bas de tableau b | Principale étape du cycle de vieNote de bas de tableau c |
|---|---|---|
| Rejets dans le sol | 1,6 | Utilisation industrielle et utilisation des comsommateurs |
| Rejets dans l'air | 0,0 | - |
| Rejets à l'égoutNote de bas de tableau d | 4,7 | Production, formulation, utilisation industrielle et utilisation par les consommateurs |
| Transformation chimique | 0 | - |
| Envoi dans des lieux d'élimination des déchets (p. ex., les décharges, les incinérateurs) |
93,7 | Production, formulation, utilisation industrielle, utilisations par les consommateurs et élimination des déchets |
D'après les chiffres du tableau 4, on peut s'attendre à ce que le Pigment Red 3 se retrouve en grande partie dans les lieux d'élimination des déchets (94 %) en raison, majoritairement, des déchets produits lors de la fabrication du pigment ou des peintures, de l'utilisation de ces peintures et de l'élimination finale des produits qui en contiennent. Une petite fraction des déchets solides renfermant le pigment est incinérée, et on peut s'attendre à ce que la substance subisse alors une transformation. Si l'on se fonde surtout sur les renseignements fournis dans les documents de l'OCDE sur les scénarios d'émission concernant le traitement et les utilisations du Pigment Red 3, on estime qu'environ 1,6 % et 4,7 % du pigment pourrait être rejeté dans le sol et les eaux usées, respectivement. D'après les prévisions, les rejets de Pigment Red 3 dans le sol devraient être dus à l'effeuillage et à l'écaillage des peintures associés aux utilisations industrielles et aux utilisations par les consommateurs. Les rejets dans les eaux du Pigment Red 3 devraient être principalement attribuables aux rejets effectués pendant la fabrication du pigment (p. ex. nettoyage des canalisations de transfert), provenant des canalisations de transfert, des équipements de nettoyage, ou encore à des rejets au cours du transfert de la substance des cuves aux sacs pendant sa formulation (p. ex. fabrication de peintures). On s'attend également à ce que les résidus provenant des pinceaux (utilisations industrielles et utilisations par les consommateurs) provoquent des rejets dans les eaux.
Bien que l'on ne possède aucun renseignement sur la quantité des importations de produits de consommation renfermant du Pigment Red 3, on prévoit que les volumes de rejets dans les divers milieux naturels ne différeraient pas énormément des quantités estimées ici. Cependant, les quantités confiées à la gestion des déchets pourraient être plus élevées si on tenait compte de l'importation de produits finis.
Devenir dans l'environnement
La très faible valeur modélisée qu'on obtient pour la pression de vapeur de 3,52 × 10-8 Pa et la constante de la loi de Henry (environ 10-8Pa·m3/mol) du Pigment Red 3 sont compatibles avec le fait qu'il s'agit d'une grosse molécule complexe (Baughman et Perenich, 1988; APE du Danemark, 1998). Cette substance ne devrait pas se volatiliser à des températures réalistes sur le plan environnemental; elle ne sera donc pas sujette à un transport atmosphérique à grande distance.
Le fait que le Pigment Red 3 se présente sous la forme de particules devrait avoir une influence majeure sur son devenir dans l'environnement. La taille de ses particules, sa masse volumique, sa stabilité chimique et sa faible solubilité dans l'eau permettent de dire qu'il se déposera dans les sédiments, sous l'effet de la gravité, s'il est rejeté dans les eaux de surface, et qu'il tendra à demeurer dans le sol s'il est rejeté en milieu terrestre.
Persistance et potentiel de bioaccumulation
Persistance
En raison de sa très faible solubilité dans l'eau, on peut considérer que le Pigment Red 3 n'est pas touché par la biodégradation aérobie après avoir été rejeté dans l'eau par suite de sa fabrication. Selon Jaffe (1996), une fois qu'un pigment est intégré à une matrice (comme la peinture), on s'attend à ce qu'il soit durable et supporte les stress physiques et chimiques combinés des intempéries, du rayonnement solaire, de la chaleur, de l'eau et des polluants industriels. Par conséquent, le contact direct avec le biote est improbable quand le pigment est incorporé dans la peinture; de plus, le pigment ne devrait pas subir de dégradation abiotique.
Les fabricants de pigments reconnaissent que leurs produits sont persistants. Par exemple, la Color Pigments Manufacturers Association, Inc. (CPMA, 2003) a déclaré que l'on conçoit les pigments pour qu'ils soient durables ou persistants dans l'environnement afin de pouvoir colorer des revêtements finis, des encres et des peintures.
La persistance des pigments de bêta-naphtol, comme le Pigment Red 3, dans les milieux anoxiques demeure très incertaine. Les colorants azoïques seraient dégradés dans les eaux et les sédiments anoxiques par la réduction anaérobie de la liaison azoïque (-N=N-) (Weber et Wolfe, 1987). Leurs produits de dégradation, notamment les amines aromatiques, auraient un potentiel mutagène (Van der Zee, 2002). La structure des pigments du groupe du bêta-naphtol comporte aussi des chromophores azoïques. Toutefois, aucune source documentaire ne fait état d'une éventuelle dégradation de ces pigments en l'absence d'oxygène. En principe, il faudrait d'abord que le cristal se dissolve pour libérer les molécules qui le constituent. Ensuite, les liaisons azoïques de ces molécules pourraient être réduites. Toutefois, compte tenu de sa solubilité restreinte, on s'attend à ce qu'une très faible proportion seulement du pigment soit réduite de cette manière.
Il a été démontré que certains colorants azoïques dispersés connaissent une biodégradation aérobie dans les sédiments se trouvant en profondeur dans le sol, où les conditions anoxiques persistent (Yen et al., 1991; Baughman et Weber, 1994; Weber et Adams, 1995). Les pigments et les colorants dispersés devraient finalement se déposer dans les couches aérobies des sédiments de surface où ils vont s'accumuler jusqu'à ce que l'enfouissement des sédiments crée les conditions favorables à leur réduction. Le taux d'accumulation de sédiments et l'ampleur de la bioturbation varient d'un site à l'autre; il est donc très difficile de déterminer le temps passé par les colorants dans les couches de sédiments aérobies dépendant du processus d'enfouissement sédimentaire. Il est probable que ce temps dépasse de beaucoup 365 jours. Une fois dans un milieu aérobie ou réducteur, les colorants azoïques peuvent se dégrader en constituants amines aromatiques de substitution. En profondeur, on s'attend à ce que ces produits de biodégradation n'aient pas un niveau élevé d'exposition potentielle vis-à-vis de la plupart des organismes aquatiques, et qu'ils ne constituent donc pas un risque pour l'environnement. En outre, si le pigment azoïque est réduit, on s'attend à ce qu'il ne soit plus considéré comme présentant un risque potentiel pour l'environnement.
D'après le poids de la preuve qu'apportent les sources documentaires décrites ci-dessus, le Pigment Red 3 est considéré comme remplissant le critère de la persistance défini dans le Règlement sur la persistance et la bioaccumulation (Canada, 2000).
Potentiel de bioaccumulation
Il existe une relation prévisible entre le log Koe et le facteur de bioconcentration dans les lipides (Mackay, 1982). Le logarithme du rapport Co/Ce a été estimé d'après les valeurs expérimentales de la solubilité du Pigment Red 3 dans l'octanol (Co) et dans l'eau (Ce) (tableau 2a), et ce rapport de valeurs expérimentales est jugé préférable à la valeur du log Koe modélisée pour ce pigment. Cette approche s'appuie sur la constatation suivant laquelle l'affinité pour la phase octanol est un bon indice de l'aptitude d'une substance à se loger dans la phase lipidique chez le biote aquatique (Bertelsen et al., 1998) et, dans le cas des pigments, sur la constatation selon laquelle une solubilité réduite dans l'octanol se traduit par des valeurs également réduites du facteur de bioconcentration (FBC) et du facteur de bioaccumulation (FBA) dans un organisme aquatique (Banerjee et Baughman, 1991).
Une série de valeurs révisées de FBC et de FBA estimées pour le Pigment Red 3, différentes de celles employées lors de la catégorisation, a été produite au moyen de modèles de bioaccumulation fondés sur la relation quantitative structure-activité (RQSA) dans lesquels les valeurs expérimentales du log (Co/Ce) pour le Pigment Red 3 ont été utilisées au lieu de la valeur du log Koe estimée d'après la méthode RQSA. Le tableau 4 montre que la plupart des valeurs modélisées révisées du FBC et du FBA pour le Pigment Red 3 sont inférieures à 1 000, à l'exception d'une prévision générée par le modèle OASIS, qui est une valeur légèrement supérieure à 1 000. Des valeurs similaires de log (Co/Ce) ont été dérivées à partir des valeurs expérimentales de la solubilité concernant des analogues assez proches, le Pigment Red 4 et le Pigment Orange 5 (tableau 2b), ce qui confirme le faible potentiel de bioaccumulation du Pigment Red 3.
| Organisme d'essai | Paramètre | Valeur (L/kg) | Références |
|---|---|---|---|
| Poisson | FBA | 404 | Gobas BAF T2MTL (Arnot et Gobas, 2003) |
| Poisson | FBC | 299 | Gobas BCF T2LTL (Arnot et Gobas, 2003) |
| Poisson | FBC | 1 084 | OASIS Forecast, 2005 |
| Poisson | FBC | 10Note de bas de tableau e | BCFWIN, 2000 |
Ainsi, on s'attend à ce que le potentiel de bioaccumulation du Pigment Red 3 soit faible parce que ce pigment a une affinité très limitée pour la phase lipidique chez les organismes vivants. Cette conclusion concorde avec celles du rapport d'évaluation danois (APE du Danemark, 1998) selon lesquelles les pigments organiques ne sont généralement pas bioaccumulatifs.
Les résultats de la modélisation RQSA indiquent que le Pigment Red 3 ne répond pas au critère de bioaccumulation (FBC, FBA supérieure ou égale à 5000) tel qu'il est énoncé dans le Règlement sur la persistance et la bioaccumulation (Canada, 2000).
Potentiel d'effets nocifs sur l'environnement
Évaluation des effets sur l'environnement
A – Dans le milieu aquatique
Les données écotoxicologiques expérimentales indiquent que le Pigment Red 3 ne cause par d'effets nocifs aigus chez les organismes aquatiques à la concentration de saturation. De plus, des valeurs estimées de l'écotoxicité ont été déterminées au moyen du log (Co/Ce) du Pigment Red 3.
On a évalué l'effet d'une solution saturée de Pigment Red 3 sur l'immobilisation du Daphnia magna dans des conditions statiques pendant 48 heures (tableau 5a). On a exposé vingt organismes d'essai à la solution saturée et à une solution témoin. Les paramètres relatifs à la qualité de l'eau ont été mesurés au début et à la fin de l'essai. Le pH a été maintenu entre 7,80 et 7,88, et la teneur en oxygène dissous, entre 8,49 et 8,61 mg/L. La température a varié entre 18 et 22 ºC. On a atteint le point de saturation en agitant la solution mère pendant 24 heures et en en retirant les particules non dissoutes par centrifugation. La concentration du pigment dans la solution a été mesurée par analyse du carbone organique dissous (COD) au début et à la fin de l'essai. On a mesuré une concentration de COD de 0,6 mg/L au début de l'essai et à la fin de l'essai, ce qui indique que la concentration du pigment est demeurée constante tout au long de l'essai. Compte tenu de la concentration de COD, on estime que la concentration de pigment en conditions de saturation était d'environ 0,9 mg/L. Aucun effet biologiquement significatif (immobilisation) n'a été observé en conditions de saturation. On juge, aux fins de la présente évaluation, que cette étude est très fiable, étant donné le respect de bonnes pratiques de laboratoire (BPL), l'utilisation de substances témoins et de substances de référence et la mesure de la concentration de COD au début et à la fin de l'essai (annexe 1G). Toutefois, selon les recommandations de l'OCDE concernant les substances très peu solubles, lorsqu'une substance n'a aucun effet à la concentration de saturation, la concentration de saturation devrait être généralement inférieure à la valeur de solubilité dans l'eau obtenue en essai de solubilité dans l'eau (OCDE, 2000). La solubilité dans l'eau du Pigment Red 3 étant de 3,3 µg/L. Donc, il se peut que la concentration de COD mesurée dans cet essai ne soit pas seulement représentative de la concentration de la substance à l'état dissous, mais de celle des particules du pigment et, peut-être, d'une petite fraction de pigment dissous. La solubilité maximale pourrait ne pas avoir été atteinte par agitation de la solution mère pendant 24 heures. Lors de l'essai de solubilité, le pigment a été agité dans l'eau pendant 2 heures à 30 ºC, puis pendant 70 heures à 23 ou 24 ºC. Même pendant l'essai de solubilité, on a recueilli un résidu de colorant non dissous sur le filtre de 0,05 µm. On considère donc que des particules non dissoutes du pigment étaient également présentes lors de l'essai de toxicité. Cette hypothèse selon laquelle le COD n'était pas représentatif uniquement de la concentration dissoute est, de plus, corroborée par les résultats de l'essai sur la toxicité du Pigment Orange 5.
Dans un essai de toxicité semblable sur l'analogue Pigment Orange 5 (no CAS 3468 63 1), on a également constaté que la substance n'avait aucun effet biologiquement significatif sur le Daphnia magna à la concentration de saturation (tableau 5a). Cette étude est elle aussi jugée très fiable (annexe 1H). Plutôt que d'avoir recours à la centrifugation pour séparer la fraction non dissoute, on a utilisé une membrane filtrante de 0,45 µm. Cependant, la taille moyenne des particules de Pigment Red 3 n'est que de 0,285 µm; le filtre n'a donc pas pu retenir la plupart des particules. Le COD a également été mesuré dans le cadre de cet essai, et il a été établi que la valeur correspondait à une concentration de pigment de 1,6 mg/L. Comme les pores du filtre étaient trop grands pour retenir les particules de pigment, la concentration de 1,6 mg/L devrait représenter le pigment dissous et les particules. Comme les concentrations obtenues dans les essais sur la toxicité du Pigment Red 3 et du Pigment Orange 5 sont semblables et qu'elles excèdent toutes deux la solubilité dans l'eau, cette étude appuie la conclusion selon laquelle les résultats de l'essai sur le Pigment Red 3 reflètent la toxicité tant des particules de pigment que d'une petite fraction de pigment dissous. Par conséquent, les formes dissoute et particulaire du Pigment Red 3 devraient présenter une toxicité aiguë négligeable ou faible pour le Daphnia magna.
Des prévisions de la toxicité pour les organismes aquatiques recalculées en utilisant le log (Co/Ce) ont été fournies par le modèle ECOSAR (ECOSAR, 2004). On a supposé que le Pigment Red 3 avait un effet narcotique semblable à celui des phénols. Toutefois, le modèle ASTER (1999) prévoyait un mode d'action par découplage de la phosphorylation oxydative de ce pigment, en plus de la narcose. Un facteur de 100 a donc été appliqué à l'estimation du modèle ECOSAR pour extrapoler du mode d'action toxique de référence à ce mode d'action plus toxique. Il convient de faire remarquer que ces modes d'action sont prévus pour la molécule solubilisée, laquelle est probablement rejetée en très petites quantités en solution si l'on se fie sur les résultats de l'essai de solubilité dans l'eau. De plus, les ensembles d'étalonnage pour les phénols dans le modèle ECOSAR et pour le modèle ASTER ne contiennent pas de pigments, ce qui accentue l'incertitude entourant ces estimations. Au tableau 5b, on donne les résultats de la modélisation de l'écotoxicité, lesquels concordent avec les études empiriques indiquant qu'il n'y a aucun effet aigu à la concentration de saturation.
| Substance | Organisme | Type d'essai | Paramètre | Durée | Valeur | Références |
|---|---|---|---|---|---|---|
| Pigment Red 3 | Daphnie | Aiguë | CE50Note de bas de tableau f | 48 heures | Aucun effet en conditions de saturation (0,9 mg/L) | Étude présentée, 2007g |
| Pigment Orange 5 | Daphnie | Aiguë | CE50Note de bas de tableau f | 48 heures | Aucun effet en conditions de saturation(1,6mg /L) | Étude présentée, 2007h |
| Organisme | Paramètre | Durée | Valeur (mg/L) | Classe chimique/mode d'action | Références |
|---|---|---|---|---|---|
| Poisson | CL50 | 14 jours | 13,642Note de bas de tableau g | RSA pour composé organique neutre (toxicité de référence) | ECOSAR, 2004 |
| Poisson | CL50 | 14 jours | 0,1364 | Découplage de la phosphorylation oxydative | CalculéNote de bas de tableau h |
| Poisson | CL50 | 96 heures | 4,049Note de bas de tableau g | Phénols | ECOSAR, 2004 |
| Daphnie | CL50 | 48 heures | 3,336Note de bas de tableau g | Phénols | ECOSAR, 2004 |
| Algue verte | CE50 | 96 heures | 4,776Note de bas de tableau g | Phénols | ECOSAR, 2004 |
L'exposition chronique au Pigment Red 3 est susceptible d'être faible dans l'eau en raison de la faible solubilité de la substance, de son faible potentiel de bioaccumulation, de sa masse moléculaire élevée et de sa nature particulaire.
Dans l'ensemble, les données de toxicité expérimentales et modélisées indiquent que le Pigment Red 3 présente un risque de toxicité aiguë négligeable à faible chez les organismes aquatiques (CL50/CE50 supérieure à la concentration de saturation).
B – Dans autres milieux
Aucune donnée empirique ou prédite sur les effets chez les organismes non aquatiques n'a été trouvée pour ce composé chimique. On s'attend à ce que le Pigment Red 3 demeure dans les sédiments ou le sol; toutefois, on n'a pas déterminé les concentrations entraînant un effet dans ces milieux.
Évaluation de l'exposition de l'environnement
On n'a pas trouvé de données sur les concentrations du Pigment Red 3 dans l'environnement au Canada. D'après les estimations faites au moyen de l'outil de débit massique, environ 90 % de la masse de ce pigment aboutit dans les décharges. La migration du pigment à partir de ces installations est peu probable, ou est estimée minime, en raison de la mobilité géochimique négligeable que laisse prévoir sa très faible solubilité dans l'eau et les solvants organiques. Par conséquent, les rejets de cette substance à l'étape de la gestion des déchets devraient être négligeables.
Les rejets dans l'eau liés à l'utilisation du Pigment Red 3 pourraient atteindre environ 5 % de la masse totale du pigment pendant tout le cycle de vie de la substance, d'après les estimations fournies par l'outil de débit massique. Les données industrielles semblent indiquer que ces rejets proviendraient majoritairement de la production du pigment et de processus industriels employés pour fabriquer d'autres produits colorés à partir du pigment, p. ex. les peintures (Environnement Canada, 2007). On a utilisé un scénario prudent et propre au site pour obtenir une concentration environnementale estimée (CEE) au point de déversement de la substance par le fabricant du pigment (Environnement Canada, 2008c). On a choisi le site du fabricant parce que ce dernier manipule la plus grande quantité de Pigment Red 3 au Canada, selon les réponses à l'enquête menée en 2006 auprès des industries (Environnement Canada, 2008a). Par ailleurs, on a utilisé un scénario prudent selon lequel les rejets provenant du transport, de la manipulation, de la fabrication des peintures et des opérations de nettoyage des canalisations de transfert – activités associées aux importateurs du pigment – étaient également évacués vers l'usine de traitement utilisée par le fabricant. On a estimé à 78 % le taux d'élimination du Pigment Red 3 par cette usine de traitement (ASTreat, 2006). À partir de ces hypothèses, on a prévu que la CEE résultant de ces rejets combinés (en présumant une dilution instantanée) serait inférieure à 1 mg/L. Compte tenu de la nature confidentielle des quantités fabriquées et importées, il n'est pas possible de divulguer la CEE effective.
Le Pigment Red 3 est utilisé dans les peintures et les revêtements; c'est pourquoi l'utilisation de ces produits peut entraîner une exposition. On n'a trouvé aucune donnée sur les concentrations de Pigment Red 3 dans l'environnement au Canada. On a donc évalué les concentrations dans l'environnement sur la base des renseignements disponibles, y compris les estimations relatives aux quantités de la substance, aux taux de rejet et aux plans d'eau récepteurs. On a utilisé MegaFlush, outil mis au point par Environnement Canada, pour estimer les rejets à l'égout, afin de calculer la concentration potentielle de la substance dans de nombreux cours d'eau qui reçoivent des effluents de stations d'épuration des eaux usées (SEEU) susceptibles de contenir des produits de consommation renfermant la substance (Environnement Canada, 2008d). L'outil a été conçu pour fournir des estimations fondées sur des hypothèses prudentes de la quantité de la substance chimique utilisée et rejetée par les consommateurs. On a supposé que les taux d'élimination des usines de traitement des eaux d'égout en traitement primaire et secondaire étaient de 55,3 % et 78,1 % respectivement (ASTreat, 2006), que les pertes associées aux différentes utilisations étaient de 1,5 %, l'utilisation de la substance par les consommateurs étant de 365 jours par année et le débit à toutes les usines correspondant au 10e centile. Ces estimations visent quelque 1 000 points de rejet au Canada, lesquels représentent toutes les SEEU de grande taille au pays.
L'équation et les paramètres d'entrée utilisés pour calculer la CEE du Pigment Red 3 dans les cours d'eau récepteurs sont décrits dans Environnement Canada (2008d). Dans le scénario qui a été retenu, on a présumé que les consommateurs utilisaient 100 000 kg de Pigment Red 3/an au total, valeur dérivée de la limite supérieure de la plage des quantités totales fabriquées et importées, moins la quantité exportée. Selon ce scénario, l'outil a calculé que la CEE dans les cours d'eau récepteurs variait de 0 à 0,00095 mg/L.
Caractérisation des risques pour l'environnement
La démarche suivie dans cette évaluation écologique préalable a consisté à examiner les renseignements scientifiques disponibles et à tirer des conclusions en appliquant la méthode du poids de la preuve et en tenant compte du principe de prudence requis par la LCPE (1999). Une attention particulière a été accordée à l'analyse du quotient du risque, à la persistance, à la bioaccumulation, à la toxicité intrinsèque, aux sources et au devenir dans l'environnement.
D'après les données publiées et les commentaires de l'industrie, le Pigment Red 3 est une substance persistante. Toutefois, selon les observations faites sur sa très faible solubilité dans l'octanol et sur les faibles valeurs du FBC modélisées, on a déterminé qu'il n'est pas bioaccumulable suivant la définition qu'on donne de ce terme dans le Règlement sur la persistance et la bioaccumulation de la LCPE (1999) [Canada, 2000].
Dans une étude expérimentale sur la toxicité pour le Daphnia magna, on n'a constaté aucun effet à 0,9 mg/L. Considérant les modèles de toxicité pour les organismes aquatiques, on a obtenu une toxicité légèrement plus forte, avec une CL50 de 0,136 mg/L. On pense que ce résultat de modélisation concerne une valeur de seuil que les résultats expérimentaux actuels ne prennent pas en compte. Comme il est indiqué précédemment, les effets prévus du Pigment 3 en tant que substance organique neutre causant la narcose (CL50 de 13,6 mg/L) ont ensuite été extrapolés à l'aide d'un facteur d'application de 100, afin d'estimer le niveau auquel la substance est susceptible d'entraîner un découplage de la phosphorylation oxydative. On a pu ainsi obtenir une valeur critique de la toxicité (VCT) de 0,136 mg/L. On a utilisé un autre facteur d'application de 100 pour prendre en compte les incertitudes entourant l'extrapolation des effets aigus aux effets chroniques, des conditions de laboratoire aux conditions sur le terrain et de celles associées à l'utilisation de données de la substance analogue. La concentration environnementale estimée sans effet (CESE) est donc 0,0014 mg/L; elle est jugée très prudente en raison des facteurs d'application multiples appliqués à la prévision.
Si l'on applique cette CESE au scénario propre au site élaboré pour des rejets industriels et que l'on prend en compte les résultats de l'outil Mega Flush, le risque que présente l'exposition au Pigment Red 3 devrait être faible. Dans le premier cas, le scénario d'exposition propre au site a donné un quotient de risque inférieur à 1 au point de déversement du fabricant de ce pigment. Dans le second cas, en ce qui concerne l'exposition découlant des rejets domestiques à l'égout (scénario très prudent), les résultats de Mega Flush indiquent que la CESE ne devrait être dépassée dans aucun site (tous les quotients de risque sont inférieures à 1). Cela veut dire que les rejets domestiques de Pigment Red 3 à l'égout ne devraient pas nuire aux organismes aquatiques.
À la lumière de ces constatations, on peut conclure qu'il est improbable que le Pigment Red 3 ait des effets écologiques nuisibles au Canada
Incertitudes dans l'évaluation des risques pour l'environnement
Cette section résume les principales incertitudes liées à l'évaluation des risques du Pigment Red 3.
On s'attend à ce que le Pigment Red 3 se loge principalement dans les sédiments; cependant, les données sur le devenir et la toxicité de cette substance dans ce milieu sont insuffisantes. Plus précisément, on en connaît très peu sur la stabilité à long terme du Pigment Red 3 dans les sédiments anoxiques, de même que dans les couches anoxiques de la colonne de sol des lieux d'élimination des déchets. On a présumé que la structure cristalline du Pigment Red 3 demeurait intacte dans ces milieux; ainsi, elle est inaccessible pour les organismes des sédiments, et la réduction des liaisons azoïques, qui pourrait libérer des amines aromatiques biodisponibles, n'est pas possible. Bien que ne disposant d'aucune donnée sur la toxicité aiguë ou chronique dans les sédiments ou les organismes vivant dans le sol, on s'attend à ce que les données concernant les organismes aquatiques indiquent que la toxicité est faible.
Le spectre granulométrique des pigments organiques comme le Pigment Red 3 peut comprendre une certaine proportion de nanoparticules (p. ex. tableau 2a). Les nanomatériaux sont officieusement définis comme des substances dont au moins une dimension est inférieure à 100 nm. Les données sont de plus en plus nombreuses à indiquer que les nanoparticules peuvent être absorbées par des voies d'absorption biologique non spécifiques comme la pinocytose (Leroueil et al., 2007). Les mécanismes et le potentiel de bioaccumulation de ce genre de particules, sont actuellement mal compris, tout autant que la nature de la relation entre leur aptitude à la bioaccumulation et leur toxicité. Par surcroît, certains des processus qui déterminent le devenir de ce genre de substances da'ns l'environnement et qui sont moins souvent pris en compte pourraient avoir une influence importante sur la tendance des 'nanoparticules de pigment à être absorbées par le biote (p. ex. importance de l'agrégation en milieu naturel; Wiesner et al., 2006).
Potentiel d'effets nocifs sur la santé humaine
Évaluation de l'exposition
Comme il n'existe pas de données sur les concentrations du Pigment Red 3 dans les milieux naturels, il est impossible dans cette évaluation de calculer les limites supérieures de l'absorption journalière du Pigment Red 3 par l'ensemble de la population canadienne. Par conséquent, cette section ne présente que des estimations d'expositions concernant des produits de consommation dont les applications sont connues.
Pour mettre au point les scénarios d'exposition associés à trois types de peinture (à forte teneur en solvants, à haut extrait sec et en aérosol) et deux produits cosmétiques (vernis à ongles et pain de savon), on a utilisé la version 4.1 du logiciel ConsExpo 4.1 de modélisation des expositions visant des produits de consommation (RIVM, 2006a). Ces scénarios sont présentés plus en détail à l'annexe 2. En ce qui concerne le savon, les scénarios ont tenu compte d'un savon en pain utilisé par les adultes et les enfants pour le lavage des mains et la douche. Les expositions par inhalation et par voie cutanée ont été prises en compte dans les scénarios pour toutes les peintures; pour l'utilisation du savon, le scénario n'a pris en compte que l'exposition par voie cutanée.
En l'absence de données sur les taux d'absorption cutanée du Pigment Red 3, on a utilisé le Sudan I (Phénylazo-1 naphtol-2; CI 12055) comme analogue pour estimer le taux d'absorption. D'après les données d'étude disponibles, l'analyse de la perméabilité de la peau humaine à l'analogue au Pigment Red 3, Sudan I a donné un résultat de 26,4 ± 6,7 % pour une exposition à l'isotope radioactif marqué Sudan I pendant 24 heures au cours d'une étude in vitro de l'absorption percutanée (Collier et al., 1993). Par conséquent, on a utilisé un taux d'absorption percutanée (taux d'absorption) de 26,4 ± 6,7 % pour estimer l'exposition cutanée au Pigment Red 3.
D'après les données fournies en application de l'article 71 de la LCPE (1999), les concentrations de Pigment Red 3 dans les préparations de peinture varient normalement de 1 à 15 % en poids (Environnement Canada, 2008a). De ce fait, pour une estimation prudente de l'exposition pendant l'utilisation d'une préparation de peinture, on a utilisé une fraction massique de 15 % en poids. Dans le cas des peintures aérosol dont l'utilisation a été agréée au Canada, on utilise une concentration maximale de 10 % à titre d'estimation prudente (annexe 2).
Les valeurs estimées de l'exposition pendant l'utilisation de peintures à forte teneur en solvants et à haut extrait sec par inhalation étaient du même ordre de grandeur (1,4 × 10-8 et 2,2 × 10-8 mg/kg-p.c. respectivement par événement), alors que l'utilisation des peintures aérosol a donné une valeur estimée de l'exposition bien plus élevée, à savoir 0,1 mg/kg-p.c. par événement. Par contre, les expositions par voie cutanée ont été estimées à approximativement 2,0 mg/kg-p.c. par événement pour toutes les catégories de peinture, ce qui représente une valeur significativement plus élevée que celles estimées dans le cas de l'exposition par inhalation.
D'après les données fournies par l'enquête menée en application de l'article 71, lorsque le pigment est en dispersion dans une préparation de peinture (à base d'eau, de solvants ou de résines alkydes), le risque d'exposition au pigment est moindre puisque les particules de pigment sont emprisonnées dans la résine (Environnement Canada, 2008a). Les valeurs d'exposition faibles estimées au moyen de la version 4.1 du logiciel de modélisation ConsExpo sont concordantes en ce qui concerne les peintures à forte teneur en solvants et en extraits secs. Dans le cas des peintures aérosol, l'exposition au Pigment Red 3 par inhalation est estimée être bien plus élevée et résultant essentiellement de l'inhalation de gouttelettes de résines, lesquelles contiennent le pigment, en plus de l'exposition aux vapeurs dégagées par la peinture.
L'exposition pendant l'utilisation du vernis à ongles a donné lieu à une estimation par inhalation de 2,4 × 10-12 mg/kg-p.c. par événement et une estimation par voie cutanée de 1,8 × 10-4 mg/kg-p.c. par événement. L'exposition cutanée maximale résultant de l'utilisation du savon a été estimée à 4,4 × 10-3mg/kg-p.c. par jour, correspondant au lavage des mains par des adultes. L'utilisation par les enfants a donné des valeurs moindres. Pour les produits cosmétiques, l'exposition au Pigment Red 3 a été estimée bien moindre que celle résultant des préparations de peinture. En se fondant sur le nombre restreint de déclarations concernant les produits cosmétiques faites au Canada (CNS, 2008) et les valeurs faibles des estimations d'exposition, on peut dire que ces produits ne contribuent pas de manière significative à l'exposition des consommateurs.
Évaluation des effets sur la santé
L'annexe 3 présente un résumé des données disponibles sur les effets du Pigment Red 3 sur la santé.
Dans le cadre du U.S. National Toxicology Program (NTP), on a réalisé des études de deux ans sur la toxicité et la carcinogénèse associées au Pigment Red 3 chez des rats F344/N et des souris B6C3F1. D'après les résultats de ces études par voie orale, le NTP a conclu qu'il y avait certaines indications de cancérogénicité pour le Pigment Red 3 chez les rats et les rates F344/N et les souris mâles B6C3F1, mais aucune indication d'activité cancérogène chez les souris femelles (NTP, 1992). Le Centre international de recherche sur le cancer (CIRC) a évalué la cancérogénicité du Pigment Red 3 et a conclu que ce dernier ne pouvait être classifié quant à sa cancérogénicité pour l'homme (groupe 3) d'après les signes limités observés chez les animaux de laboratoire et en raison de l'insuffisance des preuves de cancérogénicité chez l'être humain (CIRC, 1993).
On a observé une incidence accrue de phéochromocytomes surrénaliens chez les rats et d'adénomes hépatocellulaires chez les rates. On a nourri des groupes de 50 rats et de 50 rates Fisher 344 avec des aliments contenant 0 ppm, 6 000 ppm, 12 500 ppm et 25 000 ppm (soit respectivement à 0, 325 à 378, 678 à 795 et 1 415 à 1 598 mg/kg p.c./j) de Pigment Red 3 pendant 2 ans. Chez les rats, l'incidence de phéochromocytomes surrénaliens bénins a connu une hausse significative dans les groupes traités à la dose moyenne ou élevée, comparativement au groupe témoin (22/50, 29/50, 35/50 et 34/50 pour les groupes à 0, 6 000, 12 500 et 25 000 ppm, respectivement; p = 0,001, analyse de régression logistique). On a aussi noté d'autres effets néoplasiques, dont des hausses marginalement significatives de l'incidence de papillomes spinocellulaires ou de carcinomes cutanés à la dose élevée (6/50 comparativement à 1/50 dans le groupe témoin, p = 0,051), ainsi qu'une hausse marginalement significative de l'incidence de carcinomes dans la glande de Zymbal (3/50 comparativement à 0/50 dans le groupe témoin) chez les rats (NTP, 1992).
Dans l'étude complémentaire sur la toxicité par voie alimentaire réalisée sur les souris, on a nourri des groupes de 50 souris B6C3F1 mâles et femelles avec des aliments contenant 0 ppm, 12 500 ppm, 25 000 ppm et 50 000 ppm (soit respectivement 0, 2 482 à 2 714, 4 710 à 5 491 et 9 933 à 12 461 mg/kg p.c./j) de Pigment Red 3. Chez les souris mâles auxquels on a administré une forte dose, on a observé une augmentation significative du nombre d'adénomes dans les tubules rénaux (0/50, 0/50, 0/50 et 6/50 à 0, 12 500, 25 000 et 50 000 ppm, respectivement; p = 0,017, analyse de régression logistique) et d'adénomes des cellules folliculaires dans la glande thyroïde (0/50, 0/49, 1/50, 5/50 à 0, 12 500, 25 000 et 50 000 ppm, respectivement; p = 0,027, analyse de régression logistique). Aucune tumeur associée au traitement n'a été observée chez les souris femelles (NTP, 1992).
Les résultats concernant la génotoxicité du Pigment Red 3 étaient équivoques dans les essais in vivo sur les animaux et négatifs dans les essais sur cellules de mammifères. Dans le cadre d'un essai Comet, on a mesuré une incidence significativement accrue de dommages à l'ADN dans les tissus du côlon chez des souris mâles ddY 24 heures après l'administration d'une dose orale de 2 000 mg/kg p.c. de Pigment Red 3. Toutefois, on n'a constaté aucun dommage à l'ADN dans les autres organes examinés (Tsuda et al., 2000), y compris dans ceux où des tumeurs avaient été observées lors de l'essai biologique de deux ans (NTP, 1992). Dans une autre étude, aucune hausse significative de l'induction de micronoyaux dans les cellules de la moelle osseuse et de la rate n'a été enregistrée après injection de Pigment Red 3 dans le péritoine (Barański et al., 1992; examiné dans Møller et Wallin, 2000; dose non mentionnée). Dans les études sur cellules de mammifères, le Pigment Red 3 n'a pas provoqué d'échanges de chromatides sœurs ni d'aberrations chromosomiques dans les cultures de cellules ovariennes de hamster chinois en présence ou en l'absence de S9 (NTP, 1992).
Les résultats concernant la mutagénicité du Pigment Red 3 obtenus dans l'essai biologique sur le genre Salmonella étaient équivoques. Le Pigment Red 3 était mutagène dans les souches de Salmonella typhimurium TA100 et TA98 en présence d'une fraction de S9 de foie de hamster avec induction. On a observé une relation dose-effet évidente, bien qu'un précipité se soit formé à la plus forte concentration à l'essai. Des résultats équivoques ont été observés en présence de S9 de foie de rat avec induction. Aucun accroissement des mutations géniques n'a été observé dans les souches TA100 et TA98 en l'absence de S9, ni dans les souches TA1535 et TA1537 avec ou sans S9 (Mortelmans et al., 1986; NTP, 1992). Dans d'autres études, on a aussi obtenu des résultats négatifs pour la mutagénicité dans des souches TA98 et TA100 de Salmonella avec activation métabolique (Miyagoshi et al., 1983; Baranski et al., 1992; examiné dans Møller et Wallin, 2000). Bien que, selon le CIRC, ces résultats indiquent que le Pigment Red 3 n'est pas mutagène pour le Salmonella typhimurium, sauf en présence d'un système métabolique exogène de foie de hamster (mais pas de rat), et faiblement mutagène à la concentration de précipitation, Mortelmans et al. (1986) ont conclu que les résultats sur la mutagénicité étaient positifs. Leur décision repose sur les critères d'évaluation de la mutagénicité définissant une réaction positive, c'est-à-dire une hausse reproductible, proportionnelle à la dose, du nombre de révertants par rapport à la valeur enregistrée en conditions naturelles, même si cette hausse est inférieure à un facteur de deux ».
Bien que les modes d'action à l'origine des tumeurs n'aient pas été complètement élucidés et que de telles analyses débordent le cadre de la présente évaluation préalable, le NTP a conclu, d'après la structure du Pigment Red 3, qui laisse supposer une réactivité avec l'ADN au niveau du groupement nitro aromatique et de la liaison diazoïque, et la mutagénicité positive observée chez le genre Salmonella en présence de S9 de hamster, que le Pigment Red 3 pouvait être considéré comme un cancérogène génotoxique (NTP, 1992).
En ce qui concerne le effets critiques autres que le cancer, on a enregistré des augmentations significatives de l'incidence de lésions non néoplasiques dans le foie des rats et des rates au cours des études de deux ans du NTP (0 ppm, 6 000 ppm, 12 500 ppm et 25 000 ppm dans l'alimentation, soit 0, 325 à 378, 678 à 795 et 1 415 à 1 598 mg/kg p.c./j, respectivement). À la plus faible dose, soit 6 000 ppm (c'est-à-dire 325 à 378 mg/kg-p.c./j), on a en effet observé chez les rats mâles une incidence significativement accrue des lésions hépatiques, dont des foyers éosinophiles (37/50 comparativement à 6/50 chez le groupe témoin, p inférieure à 0,01), des foyers de cellules mixtes (24/50 comparativement à 2/50 chez le groupe témoin, p inférieure à 0,01), une dégénérescence kystique (36/50 comparativement à 9/50 chez le groupe témoin, p inférieure à 0,01), et une angiectasie multifocale (dilatation chronique et souvent allongement des vaisseaux sanguins ou lymphatiques) (20/50 comparativement à 3/50 chez le groupe témoin, p inférieure à 0,01). Parmi les effets non néoplasiques observés chez les rates, on comptait des foyers éosinophiles, des foyers de cellules mixtes, des granulomes et une pigmentation cholestérolique. En outre, la hausse de l'incidence était plus significative aux doses les plus élevées. D'autres effets non néoplasiques ont également été observés à la plus faible dose, dont une augmentation proportionnelle à la dose de la gravité de la néphropathie tant chez les rats que chez les rates, et une incidence accrue d'hyperplasie dans l'épithélium transitionnel des papilles rénales chez les rats mâles (NTP, 1992). Dans l'étude de deux ans sur la toxicité par voie alimentaire réalisée sur les souris (0 ppm, 12 500 ppm, 25 000 ppm et 50 000 ppm dans l'alimentation, soit 0, 2 482 à 2 714, 4 710 à 5 491 et 9 933 à 12 461 mg/kg p.c./j, respectivement), on a noté une incidence accrue de cytomégalie au niveau de l'épithélium des tubules rénaux (0/50, 40/50, 47/50 et 46/50, respectivement) chez les souris mâles. De plus, on a observé une augmentation proportionnelle à la dose de la gravité de la néphropathie et une incidence accrue d'hyperplasie des cellules folliculaires thyroïdiennes chez les mâles comme chez les femelles (NTP, 1992).
En conséquence, en se basant sur les lésions hépatiques observées chez des rats au cours des études de deux ans sur la toxicité par voie alimentaire, la dose minimale avec effet (nocif) observé (DME(N)O) a été établie à 325 mg/kg-p.c./j (6 000 ppm dans les aliments étant la plus faible dose à l'essai).
Dans l'étude de toxicité subchronique, on a exposé des rats Fisher 344 au Pigment Red 3 par voie alimentaire (0 ppm, 3 000 ppm, 6 000 ppm, 12 500 ppm, 25 000 ppm et 50 000 ppm, soit 0,183 à 223, 408 à 478, 758 à 929, 1 474 à 1 704 et 3 183 à 3 736 mg/kg-p.c./j, respectivement) pendant 90 jours. On a observé des lésions histopathologiques associées au produit chimique tant chez les rats que chez les rates, dont une hyperplasie dans la moelle osseuse; une congestion, une prolifération des cellules hématopoïétiques et une pigmentation au niveau de la rate; une prolifération des cellules hématopoïétiques et une pigmentation au niveau du foie; une pigmentation des reins (Morgan et al., 1989; NTP, 1992). À la plus faible dose, soit 3 000 ppm dans les aliments (183 à 223 mg/kg p.c./j), on a observé une forte incidence (10/10 sujets par rapport à 0/10 chez le groupe témoin) d'hyperplasie légère dans la moelle osseuse et une congestion, une prolifération des cellules hématopoïétiques et la présence de pigment au niveau de la rate. On a enregistré d'autres effets à cette dose, dont une augmentation significative du rapport pondéral foie/corps (15 %, p inférieure à 0,05, n = 10), une augmentation significative du nombre de réticulocytes (p inférieure à 0,05, n = 10) et une baisse significative de l'hématocrite (p inférieure à 0,05, n = 10). Des relations dose-effet ont été notées dans le cas de l'augmentation du rapport pondéral foie/corps et de la gravité des lésions au niveau de la moelle osseuse et de la rate. Par conséquent, on a déterminé que la DME(N)O par voie orale était de 183 mg/kg p.c./j (3 000 ppm dans les aliments étant la plus faible dose à l'essai) d'après l'hyplerplasie constatée au niveau de la moelle osseuse, les lésions histopathologiques observées au niveau de la rate et l'augmentation significative du rapport pondéral foie/corps chez les rats mâles.
Dans une autre étude de toxicité subchronique, on a nourri des souris B6C3F1 avec des aliments contenant du Pigment Red 3 (0 ppm, 3 000 ppm, 6 000 ppm, 12 500 ppm, 25 000 ppm et 50 000 ppm, soit 0, 502 à 666, 1 048 à 1 540, 3 291 à 3 121, 6 298 à 6 306 et 10 177 à 12 520 mg/kg p.c./j, respectivement) pendant 90 jours. On a aussi observé des lésions histopathologiques associées au produit chimique chez les souris B6C3F1 mâles et femelles. Les effets histopathologiques comprenaient une augmentation significative de la prolifération des cellules hématopoïétiques dans la rate et dans le foie des souris mâles et femelles. On a aussi constaté une cytomégalie au niveau de l'épithélium des tubules rénaux chez les souris mâles, et plusieurs lésions graves aux concentrations élevées (Morgan et al., 1989; NTP, 1992). On a fixé entre 502 et 666 mg/kg p.c./j (3 000 ppm dans les aliments) la DME(N)O par voie orale pour le Pigment Red 3 chez les souris B6C3F1, ceci d'après l'augmentation significative de la prolifération des cellules hématopoïétiques dans la rate.
De plus, on a signalé des hausses significatives du rapport pondéral foie/corps chez les rats Osborne-Mendel mâles nourris avec des aliments contenant 0 ou 2 500 ppm de Pigment Red 3 pendant 90 jours; aucun effet n'a été observé sur la mortalité, la croissance ou les paramètres hématologiques (Graham et Davis, 1968). Par comparaison avec l'étude du NTP, une seule dose de traitement a été administrée dans cette étude. Cette dernière est donc considérée comme supplémentaire et ne permet d'établir aucune concentration entraînant un effet critique.
Dans une étude sur la toxicité par voie orale à court terme en doses répétées, des rats Fisher 344 et des souris B6C3F1 ont été exposés au Pigment Red 3 par les aliments (0 ppm, 3 000 ppm, 6 000 ppm, 12 500 ppm, 25 000 ppm, 50 000 ppm, 100 000 ppm) pendant 14 jours. Parmi les principaux effets toxiques observés, on compte une diminution proportionnelle à la dose du nombre d'érythrocytes et de la concentration d'hématocrite ainsi qu'une augmentation du nombre de réticulocytes chez les rats. On a établi la DME(N)O par voie orale à 738 mg/kg p.c./j (6 000 ppm dans les aliments étant la plus faible dose à l'essai) chez les femelles, ceci d'après les effets hématologiques observés (diminution de la concentration en hémoglobine) (Morgan et al., 1989). On a enregistré des diminutions significatives de l'hématocrite et de la concentration en hémoglobine et en érythrocytes chez les souris B6C3F1 mâles, sans toutefois pouvoir dégager une tendance dose-effet claire. La DME(N)O par voie orale pour la souris était de 1 048 mg/kg p.c./j (6 000 ppm dans l'alimentation étant la plus faible dose à l'essai), d'après les effets hématologiques (Morgan et al., 1986).
L'information disponible sur la biodisponibilité et le métabolisme du Pigment Red 3 était limitée. Seule une faible proportion du Pigment Red 3 a été décelée dans l'urine et différents échantillons de tissus (sang, foie, reins ou poumons) dans un délai de 48 heures au cours d'une étude sur l'absorption menée sur des rats Fischer 344 mâles auxquels on avait administré par gavage une dose unique de 11,8 mg/kg de Pigment Red 3 dans de l'huile de maïs, ce qui indique une faible absorption à partir du tractus gastro-intestinal (El Dareer et al., 1984, examiné dans CIRC, 1993 et dans BIBRA, 1996). On a mesuré un taux de récupération d'environ 72,4 % (dans les fèces) de la dose administrée au bout de 48 heures; cela laisse supposer que le composé pourrait être partiellement dégradé par les bactéries intestinales (El Dareer et al., 1984). On avance l'hypothèse que ce colorant azoïque puisse être réduit par la flore bactérienne présente dans les intestins et, dans une certaine mesure, par les enzymes présentes dans le foie, pour produire de la 4-méthyl-2-nitroaniline et de la 2-hydro-α-naphtylamine (Morgan et al., 1989). Dans cette étude sur l'absorption, seuls les composés d'origine et non les métabolites pertinents ont été mesurés et aucun traceur marqué n'a été utilisé pour ce composé. Dans une autre étude in vitro sur l'absorption percutanée de l'analogue au Pigment Red 3, Sudan I, une valeur pour la perméabilité cutanée de 26,4 ± 6,7 % a été déterminée pour de la peau humaine exposée pendant 24 heures au Sudan I radiomarqué (Collier et al.,1993).
Le Pigment Red 3 provoque une légère irritation cutanée chez l'humain. On a constaté un léger érythème ou un érythème avec œdème chez des patients souffrant d'une dermatite provoquée par des cosmétiques colorés au cours de tests épicutanés ou de photopatch-tests pendant lesquels du Pigment Red 3 était appliqué pendant 48 ou 72 heures. Le taux de réactions positives, en ce qui concerne l'irritation cutanée, était de 34,2 % (13/38) [Sugai et al., 1977]. On a observé une rougeur et une tuméfaction de la peau chez 5 des 155 patients souffrant d'une dermatite attribuable à un produit cosmétique au cours de tests épicutanés d'une durée de 48 heures utilisant une concentration de 5 % de Pigment Red 3 dans du polyéthylèneglycol. On a aussi observé une légère rougeur chez 25 autres patients (MJCDRG, 1978; cité dans BIBRA, 1996). Des tests épicutanés ont été effectués pour plusieurs colorants azoïques chez huit patients souffrant d'une dermite de contact causée par le Brilliant Lake Red R (no CAS 27757-79-5). On a observé des réactions négatives pour des tests épicutanés effectués avec une solution à 1 % de Pigment Red 3 dans de la gelée de pétrole, mais des réactions positives avec une solution à 1 % de Brilliant Lake Red R ou à 0,1 % de Sudan I dans cette gelée. De plus, on n'a observé aucune réaction cutanée chez 28 jeunes femmes en santé qui ont subi volontairement un test épicutané d'une durée de 48 heures utilisant une solution à 1 % de Pigment Red 3 dans de la gelée de pétrole (Kgzuka et al., 1980). Ces renseignements portent à croire que le Pigment Red 3 est un faible irritant dermique avec une concentration seuil supérieure à 1 % dans un solvant.
On accorde une confiance modérée à la base de données concernant la toxicité du Pigment Red 3 étant donné qu'elle comprend des études sur la toxicité subchronique, la toxicité chronique et la toxicité à court terme, mais seulement pour l'exposition par voie orale.
Caractérisation des risques pour la santé humaine
D'après les renseignements pertinents dont on dispose, notamment l'évaluation effectuée par un organisme international suivant la méthode du poids de la preuve, la cancérogénicité constitue l'effet critique pour la caractérisation des risques que présente le Pigment Red 3 pour la santé humaine. Des tumeurs liées à l'exposition ont été observées en de nombreux sièges chez les rats mâles et femelles ainsi que chez les souris mâles dans le cadre d'un essai biologique d'une durée de deux ans (NTP, 1992). Les effets néoplasiques observés comprenaient des tumeurs hépatiques chez les rates, ainsi que des tumeurs des glandes surrénales et de la peau et des tumeurs malignes de la glande de Zymbal chez les rats, de même que des tumeurs des reins et de la glande thyroïde chez les souris mâles. Aucune tumeur associée à l'exposition n'a été observée chez les souris femelles.
Bien que l'analyse du mode d'action à l'origine des tumeurs observées en de nombreux sièges chez les rats et les souris dépasse la portée de cette évaluation préalable du Défi, on ne peut pas, à la lumière des résultats équivoques concernant la génotoxicité tirés d'une base de données restreinte (dont des résultats positifs concernant la mutagénicité observés à de fortes doses dans certaines souches de Salmonella et certaines conditions d'activation métabolique, et l'induction de dommages à l'ADN observée dans le côlon chez les souris traitées par voie orale), écarter la possibilité d'un mode d'action faisant intervenir une interaction directe avec le matériel génétique.
\En ce qui concerne les effets critiques autres que le cancer dans le contexte d'une évaluation préalable, on se fonde sur la marge d'exposition pour caractériser les risques. Vu les utilisations du Pigment Red 3 et ses propriétés physiques et chimiques (pression de vapeur, constante de la loi de Henry et solubilité faible), l'exposition dans le milieu devrait être négligeable. Pour la population, l'exposition au Pigment Red 3 se produirait principalement par contact cutané pendant l'utilisation de produits de consommation contenant cette substance. En raison de l'absence d'études sur la toxicité associée à l'exposition par voie cutanée, on utilise les concentrations entraînant des effets critiques tirées des études par voie orale aux fins du calcul de la marge d'exposition, en supposant que le Pigment Red 3 exerce une toxicité semblable par voie orale et par voie cutanée. Dans les études de toxicité subchronique, de toxicité chronique et de toxicité à court terme réalisées sur les animaux de laboratoire, les effets toxicologiques identifiée on étés observés aux plus faibles doses à l'essai, la plus faible DMENO étant de 183 mg/kg p.c./j selon les effets histopathologiques et hématologiques observés chez les rats. En comparant cette concentration entraînant un effet critique et la limite supérieure des estimations de l'exposition par voie cutanée au Pigment Red 3 (soit 4,4 × 10-3 mg/kg p.c./j) pendant le lavage des mains avec un pain de savon par des adultes, on obtient une marge d'exposition d'environ 41 600. Si on compare la valeur estimée de l'exposition au Pigment Red 3 de 2,0 mg/kg pendant l'utilisation d'une peinture de ce genre, lors d'une exposition de 132 minutes, à la DMENO de 738 mg/kg/j tirée d'une étude sur la toxicité par voie orale à court terme (14 jours), on obtient une marge d'exposition d'environ 370. Toutefois, considérant la prudence de cette évaluation de l'exposition, l'exposition réelle pourrait être plus faible et résulterait alors dans une marge d'exposition plus élevée par rapport à ce résultat. Il peu être discuté que lors d'une évaluation de risque hautement précise, une marge d'exposition de 370 n'est pas adéquate pour traiter des incertitudes, surtout que puisque les effets non-cancérigènes ont étés observés à toutes les doses testées. Considérant la prudence de l'évaluation de l'exposition au Pigment Red 3 dans les peintures, une marge d'exposition de 370 ne cause pas de préoccupation en ce qui concerne des effets non-cancérogène à court terme.
Incertitudes dans l'évaluation des risques pour la santé humaine
Les résultats provenant d'études de génotoxicité du Pigment Red 3 sont équivoques, et les modes d'action à l'origine des tumeurs observées chez les rongeurs n'ont pas été élucidés. Il demeure une incertitude quant au potentiel de la substance à provoquer des effets à des doses plus faibles que celles testées, étant donné que des effets autres que le cancer ont été observés aux doses orales les plus faibles à l'essai, ce qui pourrait mener à sous-estimer les risques. Les études sur l'exposition chronique, l'exposition subchronique et l'exposition à court terme portent uniquement sur l'administration par voie orale. On suppose que le taux d'absorption du Pigment Red 3 est le même par voie orale et par voie cutanée et que l'exposition provoque des effets systémiques semblables. Cette hypothèse raisonnable se fonde sur le volume restreint de données étudiées concernant la biodisponibilité et donnerait une absorption orale potentielle maximale d'environ 28 %. Cette valeur est du même ordre de grandeur que celle de l'absorption par voie cutanée de son analogue.
Les données n'ont pas permis de quantifier l'exposition au Pigment Red 3 en milieu naturel au Canada. Une certaine incertitude est associée aux estimations quantitatives de l'exposition découlant de produits contenant du Pigment Red 3 du fait de l'utilisation de facteurs par défaut au degré de confiance variable pour la modélisation de produits de consommation à l'aide du logiciel ConsExpo. Ces incertitudes sont acceptées dans la mesure où en l'absence de taux d'absorption par voie cutanée propres au Pigment Red 3, on doit utiliser celui de son analogue. Pour ces raisons, la confiance à l'égard de l'évaluation de l'exposition au Pigment Red 3 par le biais des produits de consommation reste modérée; néanmoins, on considère que les valeurs d'exposition réelles restent inférieures aux valeurs prudentes de modélisation des expositions pour les produits de consommation.
Conclusion
D'après les renseignements présentés dans cette évaluation préalable, on en conclut que le Pigment Red 3 ne pénètre pas dans l'environnement en une quantité ou concentration ou dans des conditions de nature à avoir, immédiatement ou à long terme, un effet nocif sur l'environnement ou sur la diversité biologique, ou à mettre en danger l'environnement essentiel pour la vie.
Étant donné la cancérogénicité du Pigment Red 3, qui entraîne une probabilité d'effet nocif à toute concentration d'exposition, on en conclut que le Pigment Red 3 est une substance pouvant pénétrer dans l'environnement en une quantité ou concentration ou dans des conditions de nature à constituer un danger au Canada pour la vie ou la santé humaines.
On en conclut donc que le Pigment Red 3 répond au critère énoncé à l'alinéa 64c) de la LCPE (1999). De plus, cette substance répond aux critères de la persistance, mais non aux critères de la bioaccumulation tels qu'ils sont définis dans le Règlement sur la persistance et la bioaccumulation (Canada, 2000).
Références
ACD/pKaDB [module de prévision]. 2005. Version 9.04. Toronto (Ont.) : Advanced Chemistry Development. http://www.acdlabs.com/products/phys_chem_lab/pka/
[APE] Agence de protection de l'environnement du Danemark. 1998. Survey of azo-colorants in Denmark: Consumption, use, health and environmental aspects. Ministère de l'Environnement et de l'Énergie (Danemark).
[ARLA] Agence de réglementation de la lutte antiparasitaire. 2007. Note aux titulaires de pesticides - L'après-catégorisation des substances inscrites sur la Liste intérieure des substances : conséquences du Défi pour les titulaires de pesticides. Pièce jointe 1 : Matières actives, produits de formulation et impuretés contenues dans les produits de formulation inscrits sur la liste du Défi [Internet]. Ottawa (Ont.) : Santé Canada, Agence de réglementation de la lutte antiparasitaire. [consulté le 1er août 2008]. http://www.pmra-arla.gc.ca/english/pdf/appregis/Memo-Post-categorization-e.pdf
[ARLA] Agence de réglementation de la lutte antiparasitaire. 2007. Note aux titulaires de pesticides - L'après-catégorisation des substances inscrites sur la Liste intérieure des substances : conséquences du Défi pour les titulaires de pesticides. Pièce jointe 1 : Matières actives, produits de formulation et impuretés contenues dans les produits de formulation inscrits sur la liste du Défi [Internet]. Ottawa (Ont.) : Santé Canada, Agence de réglementation de la lutte antiparasitaire. [consulté le 1er août 2008]. http://www.pmra-arla.gc.ca/english/pdf/reg/reg2007-04-e.pdf
Arnot, J.A., Gobas, F.A.P.C. 2003. A generic QSAR for assessing the bioaccumulation potential of organic chemicals in aquatic food webs. QSAR Comb. Sci. 22(3):337-345.
[ASTER] Assessment Tools for the Evaluation of Risk [Internet]. 1999. Duluth (MN) : U.S. Environmental Protection Agency (U.S. EPA), Mid-Continent Ecology Division.
[ASTreat] Activated Sludge Treatment [CD-ROM]. 2006. Version 1.0. Cincinnati (OH) : Procter & Gamble. Modèle informatique de prévision des taux d'élimination des stations d'épuration des eaux usées. Disponible auprès de : P&G, P.O. Box 538707, Cincinnati (OH), 45253-8707, États-Unis.
Banerjee, S., Baughan, G.L. 1991. Bioconcentration factors and lipid solubility. Environ. Sci. Technol. 26:536-539.
Barański, B., Przybojewska, B., Spiechowicz, E., Wyszyńska, K., Zimnicki, J. 1992. Identification of potential carcinogenic dyes and intermediates on the basis of their genotoxicity. Med. Pr. 43:469-477 (en polonais; examiné dans Møller et Wallin, 2000).
Baughman, G.L., Perenich, T.A. 1988. Fate of dyes in aquatic systems: I. Solubility and partitioning of some hydrophobic dyes and related compounds. Environ. Toxicol. Chem. 14(1):79-91.
Baughman, G.L., Weber, E.J. 1994. Transformation of dyes and related compounds in anoxic sediment: kinetics and products. Environ. Sci. Technol. 28(2):267-276.
[BCFWIN] BioConcentration Factor Program for Windows [modèle d'estimation]. 2000. Version 2.15. Washington (DC) : U.S. Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY) : Syracuse Research Corporation. http://www.epa.gov/oppt/exposure/pubs/episuite.htm
Bertelsen, S.L., Hoffman, A.D., Gallinat, C.A., Elonen, C.M., Nichols, J.W. 1998. Evaluation of Log Kow and tissue lipid content as predictors of chemical partitioning in fish tissues. Environ Toxicol Chem. 17:1447-1455.
[BIBRA] British Industrial Biological Research Association. 1996. Toxicity Profile: Toluidine Red. Carshalton, Surrey (Royaume-Uni) : BIBRA.
Brooke, D.N., Crookes, M.J. 2007. Emission scenario document on transport and storage of chemicals [Internet]. Bristol (Royaume-Uni) : Environment Agency. Product code : SCHO0407BMLK-E-P. [consulté le 26 février 2008]. http://publications.environment-agency.gov.uk/pdf/SCHO0407BMLK-e-e.pdf
Canada. 1999. Loi canadienne sur la protection de l'environnement (1999). L.C., 1999, chap. 33. Gazette du Canada, Partie III, vol. 22, no 3. http://canadagazette.gc.ca/partIII/1999/g3-02203.pdf
Canada. 2000. Loi canadienne sur la protection de l'environnement (1999) : Règlement sur la persistance et la bioaccumulation, C.P. 2000-348, 23 mars 2000, DORS/2000-107. Gazette du Canada, Partie II, vol. 134, no 7, p. 607-612. http://canadagazette.gc.ca/partII/2000/20000329/pdf/g2-13407.pdf
Canada. Ministère de l'Environnement, ministère de la Santé. 2006. Loi canadienne sur la protection de l'environnement (1999) : Avis d'intention d'élaborer et de mettre en œuvre des mesures d'évaluation et de gestion des risques que certaines substances présentent pour la santé des Canadiens et leur environnement. Gazette du Canada, Partie I, vol. 140, no 49, p. 4109-4117. http://canadagazette.gc.ca/partI/2006/20061209/pdf/g1-14049.pdf
Canada. Ministère de l'Environnement. 2006b.
Ministère de la Santé. 2007a. Loi canadienne sur la protection de l'environnement (1999) : Avis de troisième divulgation d'information technique concernant les substances identifiées dans le Défi. Gazette du Canada, Partie I, vol. 141, no. 33, p. 2375-2379. http://canadagazette.gc.ca/partI/2007/20070818/pdf/g1-14133.pdf#page=7
Canada. Ministère de l'Environnement. 2007b. Loi canadienne sur la protection de l'environnement (1999) : Avis concernant les substances du groupe 3 du Défi. Gazette du Canada, Partie I, vol. 141, no 33, p. 2379-2394. http://canadagazette.gc.ca/partI/2007/20070818/pdf/g1-14133.pdf#page=7
[CIRC] Centre international de recherche sur le cancer. 1993. CI Pigment Red 3, IARC Monographs on the Evaluation of Carcinogenesis Risk of Chemicals to Man. Lyon (France) : IARC. Vol. 57:259-266.
Clariant. 2007. Colorants for the Paint Industry. [consulté le 3 juin 2007]. http://www.clariant.com/C1256C70004EEA54/vwLookupDownloads/DP8523ED.pdf/$File/DP8523ED.pdf
Collier, S.W., Storm, J.E., Bronaugh, R.L. 1993. Reduction of azo dyes in vitro percutaneous absorption. Toxicol. Appl. Pharmacol. 118:73-79.
Commission européenne. 1976. DIRECTIVE DU CONSEIL du 27 juillet 1976 concernant le rapprochement des législations des États membres relatives aux produits cosmétiques (76/768/CEE) (JO L 262 du 27.9.1976, p. 169). [consultée le 2 juin 2008]. http://ec.europa.eu/enterprise/cosmetics/html/consolidated_dir.htm
[CPMA] Color Pigments Manufacturers Association, Inc. 2003. Commentaires de la Color Pigments Manufacturers Association, Inc., sur l'ébauche du Document d'orientation sur la catégorisation des substances organiques et inorganiques inscrites sur la Liste intérieure des substances du Canada ainsi que sur les estimations calculées par Environnement Canada et les données empiriques concernant environ 12 000 produits chimiques organiques définis figurant sur la LIS. Lettre à Danie Dubé, Division des substances existantes, 30 septembre 2003.
[CSC] Comité scientifique de cosmétologie. 1988. Rapports du Comité scientifique de cosmétologie. 7e série, Commission des Communautés européennes. (Environnement et qualité de vie). [cité dans BIBRA, 1996].
[CTFA] Cosmetic, Toiletry and Fragrance Association. 2008. International Cosmetic Ingredient Dictionary and Handbook. The Cosmetic, Toiletry and Fragrance Association, Inc.
[ECOSAR] Ecological Structural Activity Relationships [Internet]. 2004. Version 0.99h. Washington (DC) : U.S. Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY) : Syracuse Research Corporation. http://www.epa.gov/oppt/exposure/pubs/episuite.htm
El Dareer, S.M., Tillery, K.F., Hill, D.L. 1984. Investigations on the disposition of oral doses of some water-insoluble pigments. Environ. Contam. Toxicol. 32(2): 171-174. Bull. Environ. Contam. Toxicol. 32(2): 171-174.
Environnement Canada. 2007. Assumptions, limitations and uncertainties of the Mass Flow Tool for SUBSTANCE NAME, CAS RN 79357-73-6. Document provisoire interne. Gatineau (Qc) : Environnement Canada, Division des substances existantes. Disponible sur demande.
Environnement Canada. 2008a. Données sur les substances du lot 3 recueillies en vertu de l'article 71 de la Loi canadienne sur la protection de l'environnement (1999). Avis concernant les substances du groupe 3 du Défi.Préparées par Environnement Canada et Santé Canada, Programme des substances existantes.
Environnement Canada. 2008b. Guidance for conducting ecological assessments under CEPA, 1999: science resource technical series, technical guidance module: Mass Flow Tool. Ébauche de document de travail préliminaire. Division des substances existantes d'Environnement Canada.
Environnement Canada. 2008c. Site-specific Exposure Scenario Report: CAS RN 2425-85-6. 2008-04-29. Rapport inédit. Gatineau (Qc) : Environnement Canada, Division des substances existantes.
Rapport : no CAS 2425-85-6. 2008-05-20. Rapport inédit. Gatineau (Qc) : Environnement Canada, Division des substances existantes.
Étude présentée. 2007a. Étude confidentielle inédite présentée à Environnement Canada, Division des substances existantes, dans le cadre du Défi du Plan de gestion des produits chimiques. Disponible sous la forme de sommaire de rigueur d'étude, numéro 13365Submission011. (voir l'annexe 1, A-1).
Étude présentée. 2007b. Étude confidentielle inédite présentée à Environnement Canada, Division des substances existantes, dans le cadre du Défi du Plan de gestion des produits chimiques. Disponible sous la forme de sommaire de rigueur d'étude, numéro 13365Submission012. (voir l'annexe 1, A-2).
Étude présentée. 2007c. Étude confidentielle inédite présentée à Environnement Canada, Division des substances existantes, dans le cadre du Défi du Plan de gestion des produits chimiques. Disponible sous la forme de sommaire de rigueur d'étude, numéro 13365Submission013. (voir l'annexe 1, A-3).
Étude présentée. 2007d. Étude confidentielle inédite présentée à Environnement Canada, Division des substances existantes, dans le cadre du Défi du Plan de gestion des produits chimiques. Disponible sous la forme de sommaire de rigueur d'étude, numéro 13365Submission014. (voir l'annexe 1, A-4).
Étude présentée. 2007e. Étude confidentielle inédite présentée à Environnement Canada, Division des substances existantes, dans le cadre du Défi du Plan de gestion des produits chimiques. Disponible sous la forme de sommaire de rigueur d'étude, numéro 13365Submission016. (voir l'annexe 1, A-5).
Étude présentée. 2007f. Étude confidentielle inédite présentée à Environnement Canada, Division des substances existantes, dans le cadre du Défi du Plan de gestion des produits chimiques. Disponible sous la forme de sommaire de rigueur d'étude, numéro 13365Submission017. (voir l'annexe 1, A-6).
Étude présentée. 2007g. Étude confidentielle inédite présentée à Environnement Canada, Division des substances existantes, dans le cadre du Défi du Plan de gestion des produits chimiques. Disponible sous la forme de sommaire de rigueur d'étude, numéro 13365Submission020. (voir l'annexe 1, A-7).
Étude présentée. 2007h. Étude confidentielle inédite présentée à Environnement Canada, Division des substances existantes, dans le cadre du Défi du Plan de gestion des produits chimiques. Disponible sous la forme de sommaire de rigueur d'étude, numéro 13365Submission015. (voir l'annexe 1, A-8).
Graham, S.L., Davis, K.J. 1968. Subacute toxicity of toluidine red. Toxicol. Appl. Pharmacol. 13:388-391.
[HENRYWIN] Henry's Law Constant Program for Microsoft Windows [modèle d'estimation]. 2000. Version 3.10. Washington (DC) : U.S. Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY) : Syracuse Research Corporation. http://www.epa.gov/oppt/exposure/pubs/episuite.htm
Herbst W, Hunger K. 2004. Industrial organic pigments, 3e éd. Weinheim (Allemagne) : Wiley-VCH, Verlag GmbH & Co. KGaA. 660 p.
Jaffe, E.E. 1996. Pigments (Organic). In: Kroschwitz, J.I., Howe-Grant, M. (éd.). Kirk-Othmer encyclopedia of chemical technology, 4e éd., New York (NY) : John Wiley and Sons. Vol. 19:41-78.
Kgzuka, T., Tashiro, M., Sano, S., Fujimoto, K., Nakamura, Y., Hashimoto, S., Nakaminami, G. 1980. Pigmented contact dermatitis from azo dyes. I. Cross-sensitivity in humans. Contact Dermatitis 6:330-336.
[KOWWIN] Octanol-Water Partition Coefficient Program for Microsoft Windows [modèle d'estimation]. 2000. Version 1.67. Washington (DC) : U.S. Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY) : Syracuse Research Corporation. http://www.epa.gov/oppt/exposure/pubs/episuite.htm
Leroueil, P.R., Hong, S., Mecke, A., Baker, J.R. Jr., Orr, B.G., Banaszak-Holl, M.M. 2007. Nanoparticle interaction with biological membranes: does nanotechnology present a Janus face? Acc. Chem. Res. 40:335-342.
Lincke G. 2003. Molecular stacks as a common characteristic in the crystal lattice of organic pigment dyes. A contribution to the "soluble-insoluble" dichotomy of dyes and pigments from the technological point of view. Dyes and Pigments. 59: 1-24.
Mackay, D. 1982. Correlation of bioconcentration factors. Environ. Sci. Technol. 16:274-278.
Miyagoshi, M., Hayakawa, Y., Nagayama, T. 1983. Studies on the mutagenicity of cosmetic azo-dyes. Eisei Kagaku 29:212-220 (examiné dans Møller et Wallin, 2000).
MJCDRG. 1978. Mid-Japan Contact Dermatitis Research Group. J. Dermaltol. 5:291 [cité dans BIBRA, 1996].
Møller P, Wallin H. 2000. Genotoxic hazards of azo pigments and other colorants related to 1-phenylazo-2-hydroxynaphthalene. Mutat. Res. 462:13-30.
Morgan, D.L., Jameson, C.W., Mennear, J.H., Prejean, D. 1989. 14-Day and 90-day toxicity studies of Pigment Red 3 in Fischer 344 rats and B6C3Fl mice. Food Chem. Toxicol. 26(3):255-61.
Mortelmans, K., Haworth, S., Lawlor, T., Speck, W., Tainer, B., Zeiger, E. 1986. Salmonella mutagenicity tests: II. Results from the testing of 270 chemicals. Environ. Mutagen. 8:1-119.
[MPBPWIN] Melting Point Boiling Point Program for Microsoft Windows [modèle d'estimation]. 2000. Version 1.41. Washington (DC) : U.S. Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY) : Syracuse Research Corporation. http://www.epa.gov/oppt/exposure/pubs/episuite.htm
[MSDS] Material Safety Data Sheet: Suco Red L 3750 [Internet]. 2004. Toronto (Ont.) : BASF Canada. [consultée le 27 décembre 2007]. [accès restreint]. http://www.msdsonline.com
[NCI] National Chemical Inventories [base de données sur CD-ROM]. 2006. Columbus (OH) : American Chemical Society, Chemical Abstracts Service. [consultée le 11 décembre 2006]. http://www.cas.org/products/cd/nci/index.html
[NPIRI] National Printing Ink Research Institute. 1983. Raw Materials Data Handbook. Volume 4. Pigments. Napim (NY). Page 21. [cité dans BIBRA, 1996].
[NPIRI] National Printing Ink Research Institute. 2000. Raw Materials Data Handbook. A reference guide to regulatory data and technical performance properties. Volume 4, Pigments, 2e éd. Woodbridge (NJ) : National Printing Research Institute. Page 62.
[NTP] National Toxicology Program. 1992. Toxicology and carcinogenesis studies of Pigment Red 3 (CAS No. 2425-85-6) in F344/N rats and B6C3F1 mice (feed studies). Natl Toxicol Program Tech Rep Ser. 407:1-289.
[OASIS Forecast] Optimized Approach based on Structural Indices Set [Internet]. 2005. Version 1.20. Bourgas (Bulgarie) : Laboratoire de chimie mathématique. http://oasis-lmc.org/?section=software
[OCDE] Organisation de coopération et de développement économiques. 2000. Guidance document on aquatic toxicity testing of difficult substances and mixtures. OECD Environmental Health and Safety Publications Series on Testing and Assessment. Paris (France) : Direction de l'environnement (OCDE). Number 23. [consulté le 28 février 2008]. http://www.epa.gov/oscpmont/oscpendo/pubs/ref-2_oecd_gd23_difficult_substances.pdf
OCDE] Organisation de coopération et de développement économiques. 2004. Emission Scenario Document on textile finishing industry [en ligne]. Paris (France) : Direction de l'environnement de l'OCDE, Division environnement, santé et sécurité. ENV/JM/MONO(2004)12, JT00166691. [Consulté en décembre 2008]. http://www.olis.oecd.org/olis/2004doc.nsf/LinkTo/NT0000452A/$FILE/JT00166691.PDF
[OCDE] Organisation de coopération et de développement économiques. 2006. Draft emission scenario document on coating industry (paints, lacquers and varnishes). Ébauche. Paris (France) : OCDE.
[OCDE] Organisation de coopération et de développement économiques. 2007. Emission scenario document on adhesive formulation [Internet]. Rapport final. Paris (France) : OCDE, Direction de l'environnement. (Series on Emission Scenario Documents). [consulté le 26 février 2008]. http://ascouncil.org/news/adhesives/docs/EPAFormulation.pdf
[RIVM] Rijksinstituut voor Volksgezondheid en Milieu. 2007. Paint Fact Sheet To Assess the risks for the Consumer. http://www.rivm.nl/cgi-bin/htsearch?config=zoek-en&words=fact+sheet&method=and&restrict=
[SPIN] Substances in Products in Nordic Countries [base de données sur Internet]. 2006. Copenhague (Danemark) : Conseil nordique des ministres. [consultée le 11 décembre 2006]. http://195.215.251.229/Dotnetnuke/Home/tabid/58/Default.aspx
Santé Canada. 1998. Exposure factors for assessing total daily intake of priority substances by the general population of Canada. Rapport inédit, décembre 1998. Ottawa (Ont.) : Santé Canada, Direction de l'hygiène du milieu.
[SDC] Système de déclaration des cosmétiques. Base de données exclusive. 2008. Ottawa (Ont.) : Santé Canada. Consultée en avril 2008.
Sugai, T., Takahashi, Y., Takagi, T. 1977. Pigmented cosmetic dermatitis and coal tar dyes. Contact Derm. 3:249-256 [cité dans CIRC, 1993].
Tsuda, S., Matsusaka, N., Madarame, H., Ueno, S., Susa, N., Ishida, K., Kawamura, N., Sekihashi, K., Sasaki, Y.F. 2000. The comet assay in eight mouse organs: results with 24 azo compounds. Mutat. Res. 465:11-26.
Van der Zee, F.P. 2002. Anaerobic azo dye reduction. Thèse de doctorat. Wageningen (Pays-Bas) : Université de Wageningen. Page 142.
Weber EJ, Adams RL. 1995. Chemical- and sediment-mediated reduction of the azo dye Disperse Blue 79. Environ. Sci. Technol. 29: 1163-1170.
Weber, E.J., Wolfe, N.L. 1987. Kinetic studies of the reduction of aromatic azo compounds in anaerobic sediment/water systems. Environ. Toxicol. Chem. 6:911-919.
Whitaker, A. 1978. Crystal structure analysis of azo pigments involving β-Naphthol: A review. J. Soc. Dyers Col. (Communications) 431-435.
Wiesner, M.R., Lowry, G.V., Alvarez, P., Dionysiou, D., Biswas, P. 2006. Assessing the risks of manufactured nanomaterials ». Environ. Sci. Technol. 40:4336-4345.
[WSKOWWIN] Water Solubility for Organic Compounds Program for Microsoft Windows [modèle d'estimation]. 2000. Version 1.41. Washington (DC) : U.S. Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY) : Syracuse Research Corporation. http://www.epa.gov/oppt/exposure/pubs/episuite.htm
Yen CC, Perenich TA, Baughman GL. 1991. Fate of commercial disperse dyes in sediments. Environ. Toxicol. Chem. 10:1009-1017.
Annexe 1. Sommaires de rigueur d’études
Évaluation des données expérimentales selon la méthode de Kollig
Kollig, H.P. 1988. Criteria for evaluating the reliability of literature data on environmental process constants. Toxicol. Environ. Chem. 17:287-311.
Tableau A-1. Évaluation des données expérimentales selon la méthode de Kollig pour 13365 projet 011
| Référence : | Présentation de projet, 2007a. 13365 projet 011. Water Solubility Following ETAD Method |
|---|---|
| Substance d'essai : | Pigment Red 3 (no CAS 2425-85-6) |
| Question | Pondération | Réponse | Note |
|---|---|---|---|
| Pourriez-vous répéter l'expérience avec les renseignements disponibles? | 5 | Oui | 5 |
| Un objectif clair est-il énoncé? | 1 | Oui | 1 |
| La qualité de l'eau est-elle caractérisée ou précise (distillée ou désionisée)? | 2 | Non | 2 |
| Les résultats sont-ils présentés de façon détaillée, claire et compréhensible? | 3 | Oui | 3 |
| Les données proviennent-elles d'une source primaire plutôt que d'un article cité? | 3 | Oui | 3 |
| La substance a-t-elle été testée à des concentrations inférieures à sa limite de solubilité dans l'eau? | 5 | s.o. | |
| Y avait-il absence de particules? | 2 | Oui | 2 |
| A-t-on fait un essai avec une substance de référence ayant une constante connue? | 3 | Non | 0 |
| D'autres processus intervenant dans le devenir ont-ils été pris en considération? | 5 | s.o. | |
| A-t-on fait un essai témoin (à blanc)? | 3 | Oui | 1.5 |
| La température a-t-elle été maintenue constante? | 5 | On présume que oui | 5 |
| L'expérience a-t-elle eu lieu à une température proche de la température ambiante (15 à 30 °C)? | 3 | Oui | 3 |
| La pureté de la substance est-elle précisée (supérieure à 98 %)? | 3 | Oui | 3 |
| L'identité de la substance a-t-elle été attestée? | 3 | Oui | 3 |
| La source de la substance est-elle indiquée? | 1 | Non | 0 |
| Résultats : | (X ± erreur-type) |
|---|---|
| Solubilité : | 3,3 µg/L |
| Note globale : | 31,5/37 = 85% |
| Degré de fiabilité (le code de fiabilité des études écotoxicologiques pour la catégorisation des substances de la LIS est utilisé) : |
Élevé |
| Commentaires : |
Tableau A-2. Évaluation des données expérimentales selon la méthode de Kollig pour 13365 projet 012
| Référence : | Présentation de projet, 2007b. 13365 projet 012. Octanol Solubility Following ETAD Method |
|---|---|
| Substance d'essai : | Pigment Red 3 (no CAS 2425-85-6) |
| Question | Pondération | Réponse | Note |
|---|---|---|---|
| Pourriez-vous répéter l'expérience avec l'information disponible? | 5 | Oui | 5 |
| Un objectif clair est-il énoncé? | 1 | Oui | 1 |
| La qualité de l'eau est-elle caractérisée ou précisée (distillée ou désionisée)? | 2 | Non | 2 |
| Les résultats sont-ils présentés de façon détaillée, claire et compréhensible? | 3 | Oui | 3 |
| Les données proviennent-elles d'une source primaire plutôt que d'un article cité? | 3 | Oui | 3 |
| La substance a-t-elle été testée à des concentrations inférieures à sa limite de solubilité dans l'eau? | 5 | s.o. | |
| Y avait-il absence de particules? | 2 | Oui | 2 |
| A-t-on fait un essai avec une substance de référence ayant une constante connue? | 3 | Non | 0 |
| D'autres processus intervenant dans le devenir ont-ils été pris en considération? | 5 | s.o. | |
| A-t-on fait un essai témoin (à blanc)? | 3 | Oui | 1,5 |
| La température a-t-elle été maintenue constante? | 5 | On présume que oui | 5 |
| L'expérience a-t-elle eu lieu à une température proche de la température ambiante (15 à 30 °C)? | 3 | Oui | 3 |
| La pureté de la substance d'essai est-elle précisée (supérieure à 98 %) | 3 | Oui | 3 |
| L'identité de la substance a-t-elle été attestée? | 3 | Oui | 3 |
| La source de la substance est-elle indiquée? | 1 | Non | 0 |
| Résultats : | (X ± erreur-type) |
|---|---|
| Solubilité : | 17,9 mg/L |
| Note globale : | 31,5/37 = 85% |
| Degré de fiabilité (le code de fiabilité des études écotoxicologiques pour la catégorisation des substances de la LIS est utilisé) : |
Élevé |
| Commentaires : |
Tableau A-3. Évaluation des données expérimentales selon la méthode de Kollig pour 13365 projet 013
| Référence : | Présentation de projet, 2007c. 13365 projet 013. Water Solubility Following ETAD Method |
|---|---|
| Substance d'essai : | Pigment Red 4 (no CAS 2814-77-9) |
| Question | Pondération | Réponse | Note |
|---|---|---|---|
| Pourriez-vous répéter l'expérience avec l'information disponible? | 5 | Oui | 5 |
| Un objectif clair est-il énoncé? | 1 | Oui | 1 |
| La qualité de l'eau est-elle caractérisée ou précisée (distillée ou désionisée)? | 2 | Non | 2 |
| Les résultats sont-ils présentés de façon détaillée, claire et compréhensible? | 3 | Oui | 3 |
| Les données proviennent-elles d'une source primaire plutôt que d'un article cité? | 3 | Oui | 3 |
| La substance a-t-elle été testée à des concentrations inférieures à sa limite de solubilité dans l'eau? | 5 | s.o. | |
| Y avait-il absence de particules? | 2 | Oui | 2 |
| A-t-on fait un essai avec une substance de référence ayant une constante connue? | 3 | Non | 0 |
| D'autres processus intervenant dans le devenir ont-ils été pris en considération? | 5 | s.o. | |
| A-t-on fait un essai témoin (à blanc)? | 3 | Oui | 1,5 |
| La température a-t-elle été maintenue constante? | 5 | On présume que oui | 5 |
| L'expérience a-t-elle eu lieu à une température proche de la température ambiante (15 à 30 °C)? | 3 | Oui | 3 |
| La pureté de la substance d'essai est-elle précisée (supérieure à 98 %) | 3 | Oui | 3 |
| L'identité de la substance a-t-elle été attestée? | 3 | Oui | 3 |
| La source de la substance est-elle indiquée? | 1 | Non | 0 |
| Résultats : | (X ± erreur-type) |
|---|---|
| Solubilité : | 3,3 µg/L |
| Note globale : | 31,5/37 = 85% |
| Degré de fiabilité (le code de fiabilité des études écotoxicologiques pour la catégorisation des substances de la LIS est utilisé) : |
Élevé |
| Commentaires : |
Tableau A-4. Évaluation des données expérimentales selon la méthode de Kollig pour 13365 projet 014
| Référence : | Présentation de projet, 2007d. 13365 projet 014. Octanol Solubility Following ETAD Method |
|---|---|
| Substance d'essai : | Pigment Red 4 (no CAS 2814-77-9) |
| Question | Pondération | Réponse | Note |
|---|---|---|---|
| Pourriez-vous répéter l'expérience avec l'information disponible? | 5 | Oui | 5 |
| Un objectif clair est-il énoncé? | 1 | Oui | 1 |
| La qualité de l'eau est-elle caractérisée ou précisée (distillée ou désionisée)? | 2 | Non | 2 |
| Les résultats sont-ils présentés de façon détaillée, claire et compréhensible? | 3 | Oui | 3 |
| Les données proviennent-elles d'une source primaire plutôt que d'un article cité? | 3 | Oui | 3 |
| La substance a-t-elle été testée à des concentrations inférieures à sa limite de solubilité dans l'eau? | 5 | s.o. | |
| Y avait-il absence de particules? | 2 | Oui | 2 |
| A-t-on fait un essai avec une substance de référence ayant une constante connue? | 3 | Non | 0 |
| D'autres processus intervenant dans le devenir ont-ils été pris en considération? | 5 | s.o. | |
| A-t-on fait un essai témoin (à blanc)? | 3 | Oui | 1,5 |
| La température a-t-elle été maintenue constante? | 5 | On présume que oui | 5 |
| L'expérience a-t-elle eu lieu à une température proche de la température ambiante (15 à 30 °C)? | 3 | Oui | 3 |
| La pureté de la substance d'essai est-elle précisée (supérieure à 98 %) | 3 | Oui | 3 |
| L'identité de la substance a-t-elle été attestée? | 3 | Oui | 3 |
| La source de la substance est-elle indiquée? | 1 | Non | 0 |
| Résultats : | (X ± erreur-type) |
|---|---|
| Solubilité : | 9,4 mg/L |
| Note globale : | 31,5/37 = 85% |
| Degré de fiabilité (le code de fiabilité des études écotoxicologiques pour la catégorisation des substances de la LIS est utilisé) : |
Élevé |
| Commentaires : |
Tableau A-5. Évaluation des données expérimentales selon la méthode de Kollig pour 13365 projet 016
| Référence : | Présentation de projet, 2007e. 13365 projet 016. Water Solubility Following ETAD Method. |
|---|---|
| Substance d'essai : | Pigment Orange 5 (no CAS 3468-63-1) |
| Question | Pondération | Réponse | Note |
|---|---|---|---|
| Pourriez-vous répéter l'expérience avec l'information disponible? | 5 | Oui | 5 |
| Un objectif clair est-il énoncé? | 1 | Oui | 1 |
| La qualité de l'eau est-elle caractérisée ou précisée (distillée ou désionisée)? | 2 | Non | 2 |
| Les résultats sont-ils présentés de façon détaillée, claire et compréhensible? | 3 | Oui | 3 |
| Les données proviennent-elles d'une source primaire plutôt que d'un article cité? | 3 | Oui | 3 |
| La substance a-t-elle été testée à des concentrations inférieures à sa limite de solubilité dans l'eau? | 5 | s.o. | |
| Y avait-il absence de particules? | 2 | Oui | 2 |
| A-t-on fait un essai avec une substance de référence ayant une constante connue? | 3 | Non | 0 |
| D'autres processus intervenant dans le devenir ont-ils été pris en considération? | 5 | s.o. | |
| A-t-on fait un essai témoin (à blanc)? | 3 | Oui | 1.5 |
| La température a-t-elle été maintenue constante? | 5 | On présume que oui | 5 |
| L'expérience a-t-elle eu lieu à une température proche de la température ambiante (15 à 30 °C)? | 3 | Oui | 3 |
| La pureté de la substance d'essai est-elle précisée (supérieure à 98 %) | 3 | Oui | 3 |
| L'identité de la substance a-t-elle été attestée? | 3 | Oui | 3 |
| La source de la substance est-elle indiquée? | 1 | Non | 0 |
| Résultats : | (X ± erreur-type) |
|---|---|
| Solubilité : | 6,8 µg/L |
| Note globale : | 31,5/37 = 85% |
| Degré de fiabilité (le code de fiabilité des études écotoxicologiques pour la catégorisation des substances de la LIS est utilisé) : |
Élevé |
| Commentaires : |
Tableau A-6. Évaluation de données expérimentales selon la méthode de Kollig pour 13365Submission017
| Référence : | Présentation de projet, 2007f. 13365Submission017. Octanol Solubility Following ETAD Method |
|---|---|
| Substance d'essai : | Pigment Orange 5 (no CAS 3468-63-1) |
| Item | Weight | Response | Mark |
|---|---|---|---|
| Pourriez-vous répéter l'expérience avec l'information disponible? | 5 | Oui | 5 |
| Un objectif clair est-il énoncé? | 1 | Oui | 1 |
| La qualité de l'eau est-elle caractérisée ou précisée (distillée ou désionisée)? | 2 | Non | 2 |
| Les résultats sont-ils présentés de façon détaillée, claire et compréhensible? | 3 | Oui | 3 |
| Les données proviennent-elles d'une source primaire plutôt que d'un article cité? | 3 | Oui | 3 |
| La substance a-t-elle été testée à des concentrations inférieures à sa limite de solubilité dans l'eau? | 5 | s.o. | |
| Y avait-il absence de particules? | 2 | Oui | 2 |
| A-t-on fait un essai avec une substance de référence ayant une constante connue? | 3 | Non | 0 |
| D'autres processus intervenant dans le devenir ont-ils été pris en considération? | 5 | s.o. | |
| A-t-on fait un essai témoin (à blanc)? | 3 | Oui | 1.5 |
| La température a-t-elle été maintenue constante? | 5 | On présume que oui | 5 |
| L'expérience a-t-elle eu lieu à une température proche de la température ambiante (15 à 30 °C)? | 3 | Oui | 3 |
| La pureté de la substance d'essai est-elle précisée (supérieure à 98 %) | 3 | Oui | 3 |
| L'identité de la substance a-t-elle été attestée? | 3 | Oui | 3 |
| La source de la substance est-elle indiquée? | 1 | Non | 0 |
| Résultats : | (X ± erreur type) |
|---|---|
| Solubilité : | 1,76 mg/L |
| Note globale : | 31,5/37 = 85 % |
| Degré de fiabilité (le code de fiabilité des études écotoxicologiques pour la catégorisation des substances de la LIS est utilisé) : |
Élevé |
| Commentaires : |
Formulaire pour sommaire de rigueur d'études : toxicité intrinsèque pour les organismes aquatiques
Tableau A-7. Formulaire pour sommaire de rigueur d'études pour 13365Submission020 : toxicité intrinsèque pour les organismes aquatiques
Référence : Présentation de projet, 2007g. 13365Submission020. Acute Immobilisation Test (Static, 48h) to Daphnia magna, Limit Test
| No | Point | Pondération | Oui/Non | Précisions |
|---|---|---|---|---|
| 2 | Identité de la substance : no CAS | s.o. | O | 2425-85-6 |
| 3 | Identité de la substance : Nom(s) chimique(s) | s.o. | O | Pigment Red 3 |
| 4 | Composition chimique de la substance | 2 | s.o. | |
| 5 | Pureté chimique | 1 | O | 98,20 % |
| 6 | Indication de la persistance/stabilité de la substance en milieu aqueux? | 1 | O |
| No | Point | Pondération | Oui/Non | Précisions |
|---|---|---|---|---|
| 7 | Références | 1 | O | |
| 8 | Méthode normalisée (OCDE, UE, nationale ou autre)? | 3 | O | OCDE 202 |
| 9 | Justification de la méthode ou du protocole non normalisé employé, le cas échéant | 2 | S.O. | |
| 10 | BPL (bonnes pratiques de laboratoire) | 3 | O |
| No | Point | Pondération | Oui/Non | Précisions |
|---|---|---|---|---|
| 11 | Identité de l'organisme : nom | S. O. | O | Daphnia magna STRAUS |
| 12 | Indication du nom latin ou des deux noms? (latin et commun?) | 1 | O | |
| 13 | Âge ou stade biologique de l'organisme d'essai | 1 | O | |
| 14 | Longueur et/ou poids | 1 | O | |
| 15 | Sexe | 1 | s.o. | |
| 16 | Nombre d'organismes par répétition | 1 | O | 5 |
| 17 | Charge en organismes | 1 | N | |
| 18 | Type de nourriture et périodes d'alimentation au cours de la période d'acclimatation | 1 | O |
| No | Point | Pondération | Oui/Non | Précisions |
|---|---|---|---|---|
| 19 | Type d'essai (toxicité aiguë ou chronique) | s.o. | O | Aiguë |
| 20 | Type d'expérience (en laboratoire ou sur le terrain) | s.o. | O | Laboratoire |
| 21 | Voies d'exposition (nourriture, eau, les deux) | s.o. | O | Eau |
| 22 | Durée de l'exposition | s.o. | O | 48 heures |
| 23 | Témoins négatifs ou positifs (préciser)? | 1 | O | Positifs et négatifs |
| 24 | Nombre de répétitions (y compris les témoins) | 1 | O | 4 |
| 25 | Des concentrations nominales sont-elles indiquées? | 1 | N | |
| 26 | Des concentrations mesurées sont-elles indiquées? | 3 | O | Indiquées en COD |
| 27 | Type de nourriture et périodes d'alimentation durant les essais à long terme | 1 | s.o. | |
| 28 | Les concentrations ont-elles été mesurées périodiquement (spécialement dans les essais de toxicité chronique)? | 1 | O | 2 mesures |
| 29 | Les conditions du milieu d'exposition pertinentes pour la substance sont-elles indiquées? (ex. : pour la toxicité des métaux - pH, COD/COT, dureté de l'eau, température) | 3 | O | |
| 30 | Photopériode et intensité de l'éclairage | 1 | O | |
| 31 | Préparation de solutions mères et de solutions d'essai | 1 | O | |
| 32 | Un agent émulsionnant ou stabilisant a-t-il été employé, si la substance était peu soluble ou instable? | 1 | N | |
| 33 | Si un agent émulsionnant ou stabilisant a été employé, sa concentration est-elle indiquée? | 1 | s.o. | |
| 34 | Si un agent émulsionnant ou stabilisant a été employé, des données sont-elles fournies sur son écotoxicité? | 1 | s.o. | |
| 35 | Intervalles des contrôles analytiques | 1 | O | |
| 36 | Méthodes statistiques utilisées | 1 | O |
| No | Point | Pondération | Oui/Non | Précisions |
|---|---|---|---|---|
| 37 | Le paramètre déterminé est-il directement attribuable à la toxicité de la substance, non à l'état de santé des organismes (p. ex. lorsque la mortalité des témoins est supérieure à 10 %) ou à des facteurs physiques (p. ex. effet d'ombrage)? | s.o. | O | |
| 38 | L'organisme d'essai convient-il à l'environnement au Canada? | 3 | O | |
| 39 | Les conditions d'essai (pH, température, OD, etc.) sont-elles typiques pour l'organisme d'essai? | 1 | O | |
| 40 | Le type et la conception du système (statique, semi-statique, dynamique; ouvert ou fermé, etc.) correspondent-ils aux propriétés de la substance et à la nature ou aux habitudes de l'organisme? | 2 | O | |
| 41 | Le pH de l'eau d'essai était-il dans la plage des valeurs typiques de l'environnement au Canada (6 à 9)? | 1 | O | |
| 42 | La température de l'eau d'essai était-elle dans la plage des valeurs typiques de l'environnement au Canada (5 à 27 °C)? | 1 | O | |
| 43 | La valeur de la toxicité était-elle inférieure à celle de la solubilité de la substance dans l'eau? | 3 | s.o. Testé à saturation, et aucun effet observé. |
| No | Point | Pondération | Oui/Non | Précisions |
|---|---|---|---|---|
| 44 | Valeurs de la toxicité (fournir paramètres et valeurs) | s.o. | s.o. | Aucun effet lorsque COD = 2,6 mg/L |
| 45 | Autres paramètres indiqués - p. ex. FBC/FBA, CMEO/CSEO (préciser)? | s.o. | N | |
| 46 | Autres effets nocifs indiqués (cancérogénicité, mutagénicité, etc.)? | s.o. | N |
| No | Point | Précisions |
|---|---|---|
| 47 | Note globale ... % | 92,1 |
| 48 | Code de fiabilité d'EC : | 1 |
| 49 | Catégorie de fiabilité (élevée, satisfaisante, faible) : | Confiance élevée |
| 50 | Commentaires | Le COD du pigment s’établit à 0,6 mg/L à t = 0 et à t = 48 h. Le COT du pigment, quant à lui, s’établit à 66,4 %. La concentration moyenne du pigment dans l’eau peut être calculée selon l’équation suivante : [COD] = [COD du pigment] × pureté du pigment/fraction de CO du pigment = 0,6 mg COD/L × 0,982/0,644 = 0,9 mg de pigment par litre. La solubilité du pigment dans l’eau est de 3,3 µg/L (valeur expérimentale) – la valeur en conditions de saturation est donc bien supérieure à la valeur de la solubilité dans l’eau; on présume donc que la valeur de 0,9 mg/L correspond à un mélange de particules et d’une petite fraction du pigment dissous. On a agité la solution mère pendant 24 heures, avant d’effectuer une centrifugation. On ignore si l’on a atteint une solubilité maximale puisque la solution n’a été agitée que pendant 24 heures et que la température n’a pas augmenté. Les recommandations de l’OCDE sur les essais de toxicité des substances difficiles à traiter pour les organismes aquatiques indiquent également que la concentration mesurée est généralement inférieure à la solubilité dans l’eau si la substance est en conditions de saturation. L’étude prouve que les particules et la fraction du pigment dissous n’ont causé aucun effet sur les daphnies. |
Tableau A-8. Formulaire pour sommaire de rigueur d'études pour 13365Submission015 : toxicité intrinsèque pour les organismes aquatiques
Référence : Présentation de projet, 2007h. 13365Submission015. Acute Immobilisation Test (Static, 48h) to Daphnia magna, Limit Test
| No | Point | Pondération | Oui/Non | Précisions |
|---|---|---|---|---|
| 2 | Identité de la substance : no CAS | s.o. | O | 3468-63-1 |
| 3 | Identité de la substance : Nom(s) chimique(s) | s.o. | O | Pigment Orange 5 |
| 4 | Composition chimique de la substance | 2 | s.o. | |
| 5 | Pureté chimique | 1 | O | 98,78 % |
| 6 | Indication de la persistance/stabilité de la substance en milieu aqueux? | 1 | O |
| No | Point | Pondération | Oui/Non | Précisions |
|---|---|---|---|---|
| 7 | Références | 1 | O | |
| 8 | Méthode normalisée (OCDE, UE, nationale ou autre)? | 3 | O | OCDE 202 |
| 9 | Justification de la méthode ou du protocole non normalisé employé, le cas échéant | 2 | s.o. | |
| 10 | BPL (bonnes pratiques de laboratoire) | 3 | O |
| No | Point | Pondération | Oui/Non | Précisions |
|---|---|---|---|---|
| 11 | Identité de l'organisme : nom | s.o. | O | Daphnia magna STRAUS |
| 12 | Indication du nom latin ou des deux noms (latin et commun)? | 1 | O | |
| 13 | Âge ou stade biologique de l'organisme d'essai | 1 | O | |
| 14 | Longueur et/ou poids | 1 | O | |
| 15 | Sexe | 1 | s.o. | |
| 16 | Nombre d'organismes par répétition | 1 | O | 5 |
| 17 | Charge en organismes | 1 | N | |
| 18 | Type de nourriture et périodes d'alimentation au cours de la période d'acclimatation | 1 | O |
| No | Point | Pondération | Oui/Non | Précisions |
|---|---|---|---|---|
| 19 | Type d'essai (toxicité aiguë ou chronique) | s.o. | O | Aiguë |
| 20 | Type d'expérience (en laboratoire ou sur le terrain) | s.o. | O | Laboratoire |
| 21 | Voies d'exposition (nourriture, eau, les deux) | s.o. | O | Eau |
| 22 | Durée de l'exposition | s.o. | O | 48 heures |
| 23 | Témoins négatifs ou positifs (préciser)? | 1 | O | Positifs et négatifs |
| 24 | Nombre de répétitions (y compris les témoins) | 1 | O | 4 |
| 25 | Des concentrations nominales sont-elles indiquées? | 1 | N | |
| 26 | Des concentrations mesurées sont-elles indiquées? | 3 | O | Indiquées en COD |
| 27 | Type de nourriture et périodes d'alimentation durant les essais à long terme | 1 | s.o. | |
| 28 | Les concentrations ont-elles été mesurées périodiquement (spécialement dans les essais de toxicité chronique)? | 1 | O | 2 mesures |
| 29 | Les conditions du milieu d'exposition pertinentes pour la substance sont-elles indiquées? (ex. : pour la toxicité des métaux - pH, COD/COT, dureté de l'eau, température) | 3 | O | |
| 30 | Photopériode et intensité de l'éclairage | 1 | O | |
| 31 | Préparation de solutions mères et de solutions d'essai | 1 | O | |
| 32 | Un agent émulsionnant ou stabilisant a-t-il été employé, si la substance était peu soluble ou instable? | 1 | N | |
| 33 | Si un agent émulsionnant ou stabilisant a été employé, sa concentration est-elle indiquée? | 1 | s.o. | |
| 34 | Si un agent émulsionnant ou stabilisant a été employé, des données sont-elles fournies sur son écotoxicité? | 1 | s.o. | |
| 35 | Intervalles des contrôles analytiques | 1 | O | |
| 36 | Méthodes statistiques utilisées | 1 | O |
| No | Point | Pondération | Oui/Non | Précisions |
|---|---|---|---|---|
| 37 | Le paramètre déterminé est-il directement attribuable à la toxicité de la substance, non à l'état de santé des organismes (p. ex. lorsque la mortalité des témoins est supérieure à 10 %) ou à des facteurs physiques (p. ex. effet d'ombrage)? | s.o. | O | |
| 38 | L'organisme d'essai convient-il à l'environnement au Canada? | 3 | O | |
| 39 | Les conditions d'essai (pH, température, OD, etc.) sont-elles typiques pour l'organisme d'essai? | 1 | O | |
| 40 | Le type et la conception du système (statique, semi-statique, dynamique; ouvert ou fermé, etc.) correspondent-ils aux propriétés de la substance et à la nature ou aux habitudes de l'organisme? | 2 | O | |
| 41 | Le pH de l'eau d'essai était-il dans la plage des valeurs typiques de l'environnement au Canada (6 à 9)? | 1 | O | |
| 42 | La température de l'eau d'essai était-elle dans la plage des valeurs typiques de l'environnement au Canada (5 à 27 °C)? | 1 | O | |
| 43 | La valeur de la toxicité était-elle inférieure à celle de la solubilité de la substance dans l'eau? | 3 | s.o. Testé à saturation, et aucun effet observé. |
| No | Point | Pondération | Oui/Non | Précisions |
|---|---|---|---|---|
| 44 | Valeurs de la toxicité (fournir paramètres et valeurs) | s.o. | s.o. | Aucun effet lorsque COD = 2,2 mg/L |
| 45 | Autres paramètres indiqués - p. ex. FBC/FBA, CMEO/CSEO (préciser)? | s.o. | N | |
| 46 | Autres effets nocifs indiqués (cancérogénicité, mutagénicité, etc.)? | s.o. | N |
| No | Point | Précisions |
|---|---|---|
| 47 | Note globale ... % | 92,1 |
| 48 | Code de fiabilité d'EC : | 1 |
| 49 | Catégorie de fiabilité (élevée, satisfaisante, faible) : | Confiance élevée |
| 50 | Commentaires | Le COD moyen du pigment s’établit à 0,9 mg/L. Le COT du pigment, quant à lui, s’établit 56,81 %. La concentration moyenne du pigment dans l’eau peut être calculée selon l’équation suivante : [COD]= [COD du pigment] × pureté du pigment/fraction de CO du pigment = 0,9 mg COD/L × 0,988/0,568 = 1,6 mg de pigment par litre. La solubilité du pigment dans l’eau n’est que de 6,8 µ g/L (valeur expérimentale) – la valeur en conditions de saturation est ainsi bien supérieure à la valeur de la solubilité dans l’eau; on présume donc que la valeur de 0,9 mg/L correspond à un mélange de particules et d’une petite fraction du pigment dissous. La solution mère a été agitée pendant 24 heures et filtrée à l’aide d’un filtre de 0,45 µ m. Toutefois, la taille moyenne des particules du Pigment Orange 5 n’est que de 285 nm. Cela indique que le filtre ne retient pas les particules, ce qui confirme la conclusion selon laquelle le pigment dans la solution d’essai comprend les particules et la fraction soluble dans l’eau de la substance. On ignore si l’on a atteint une solubilité maximale puisque la solution n’a été agitée que pendant 24 heures et que la température n’a pas augmenté. Les recommandations de l’OCDE sur les essais de toxicité des substances difficiles à traiter pour les organismes aquatiques indiquent également que la concentration mesurée est généralement inférieure à la solubilité dans l’eau si la substance est en conditions de saturation. L’étude prouve que les particules et la fraction du pigment dissous n’ont causé aucun effet sur les daphnies. |
Annexe 2 : Limites supérieures de l'exposition au Pigment Red 3 présent dans les produits de consommation, estimées à l'aide de la version 4.1 du modèle ConsExpo (RIVM, 2006a)
| Type de produits (% de Pigment Red 3) |
HypothèseNote de bas de tableau i : Poids corporel : 70,9 kg pour un adulte; taux d'inhalation de 16,2 m3/jour; température ambiante de 20 °C (RIVM, 2007); fraction absorbée par voie cutanée : 26 % (Collier et al., 1993). | Exposition estiméeNote de bas de tableauj (mg/kg-p.c.) |
|---|---|---|
Peinture à forte teneur en solvants (RIVM, 2007) (inférieure à 15 %)Note de bas de tableau k |
Inhalation : Exposition aux vapeurs par évaporation à partir d'une superficie croissante, pendant l'application au pinceau ou au rouleau. En supposant une fréquence de 1 événement/année, une durée d’exposition de 132 min, une quantité appliquée de 1 kg, une surface de rejets de 10 m2, une pièce d'un volume de 20 m3, un taux de renouvellement de l’air de 0,6 fois/h, une durée d’application de 120 min, une matrice d'une masse moléculaire de 300 g/mol, et un coefficient de transfert de masse de 2,15 × 103 m/min (méthode de Langmuir), et une fraction d'absorption de 1. Voie cutanée : Contact direct de peau avec le produit – taux constant Taux de contact de 30 mg/min et durée de rejet de 120 min. |
Inhalation : 1,36 × 10-8 Voie cutanée : Interne : 1,98 |
Peinture à haut extrait sec (RIVM, 2007) (inférieure à 15 %)Note de bas de tableau k |
Inhalation : Exposition aux vapeurs par évaporation à partir d'une superficie croissante, pendant l'application au pinceau ou au rouleau. Mêmes hypothèses que pour les peintures à forte teneur en solvants sauf pour les données d'hypothèse suivantes : une quantité appliquée de 1,3 kg, une matrice d'une masse moléculaire de 550 g/mol et un coefficient de transfert de masse de 2,15 × 103 m/min (méthode de Langmuir). Voie cutanée : Données identiques à celles des peintures à forte teneur en solvants. |
Inhalation : 2,23 × 10-8 Voie cutanée : Interne : 1,98 |
Peintures en aérosol (RIVM, 2007) (inférieure à 10 %)Note de bas de tableau l |
Inhalation : Exposition à la pulvérisation, aux émanations issues de la personne exposée Une durée d'exposition de 20 minutes, une pièce d'un volume de 34 m3, un taux de renouvellement de l'air de 1,5 fois/h1, un taux de production massique de 0,33 g/s, une durée de pulvérisation de 15 minutes, une fraction de particules en suspension de 1, une fraction massique non volatile de 0,3, une densité de non volatile de 1,5 g/cm3, une hauteur sous plafond de la pièce de 2,25 m, un diamètre minimum d'inhalation de 15 µm, et une fraction d'absorption non respirable de 1. Voie cutanée : Contact direct de peau avec le produit – taux constant |
Inhalation : 0,119 Voie cutanée : Interne : 0,55 |
Vernis à ongles (RIVM, 2006b) (inférieure à 0,1 %)Note de bas de tableau m |
Inhalation : Exposition aux vapeurs résultant de l'évaporation En supposant une fréquence de 156 événements/année, une durée d’exposition de 5 minutes, une quantité appliquée de 0,25 g, une surface de rejets de 19 cm2, une pièce d'un volume de 1 m3, un taux de renouvellement de l’air d'une fois/h1, une durée d’application de 5 minutes, une matrice d'une masse moléculaire de 124 g/mol, et un coefficient de transfert de masse de 2,15 × 103 m/min (méthode de Langmuir), et une fraction d'absorption de 1. Voie cutanée : Contact cutané direct avec le produit – taux constant |
Inhalation : 1,35 × 10-12 Voie cutanée : Interne : 1,83 × 10-4 |
Lavage des mains par un adulte avec un savon en pain (RIVM, 2006b) (inférieure à 0.1%)Note de bas de tableau m |
Voie cutanée : Contact cutané direct avec le produit – application instantanée Fréquence d'exposition de 1820/an (5 à 6/jour), surface exposée de 860 cm2, taux de contact de 30 mg/min, durée de rejet de 120 min, quantité appliquée de 0,8 gNote de bas de tableau m, et facteur de dilution estimé de 3 (rinçage des mains). |
Voie cutanée : 4,4 × 10-3 |
Annexe 3 : Sommaire des renseignements concernant les effets du Pigment Red 3 sur la santé
| Paramètre | Concentrations ou doses minimales avec effet/Résultats |
|---|---|
| Toxicité aiguë | Dose létale médiane (DL50) par voie orale (rat) supérieure à 5 g/kg p.c. chez le rat (souche non précisée) (NPIRI, 1983) Irritation cutanée : Aucune irritation manifeste n’a été observée sur la peau intacte ou abrasée de lapins après contact, à couvert, avec 500 mg de Pigment Red 3 non dilué (SCC, 1988). Aucune étude n’a été recensée sur la toxicité par inhalation. |
| Toxicité à court terme, doses répétées | Dose minimale avec effet nocif observé (DMENO) la plus faible, par voie orale : 738 mg/kg p.c./j (6 000 ppm dans la nourriture), d’après les effets hématologiques (diminution de la concentration d’hémoglobine) observés chez des rates Fisher 344 auxquelles on a administré du Pigment Red 3 par les aliments (0 ppm, 6 000 ppm, 12 500 ppm, 25 000 ppm, 50 000 ppm, 100 000 ppm) pendant 14 j (Morgan et al., 1989). Autres études sur la toxicité par voie orale : On a observé des diminutions significatives de l’hématocrite, de la concentration d’hémoglobine et du nombre d’érythrocytes à la plus faible dose de 1 048 mg/kg p.c./j (0,6 % dans la nourriture) chez les souris B6C3F1 mâles auxquelles on a administré du Pigment Red 3 par les aliments (0 ppm, 6 000 ppm, 12 500 ppm, 25 000 ppm, 50 000 ppm, 100 000 ppm) pendant 14 j (Morgan et al., 1989). Aucune étude n’a été recensée sur la toxicité par voie cutanée ou par inhalation. |
| Toxicité subchronique | DMENO la plus faible, par voie orale : 183 mg/kg p.c./j (3 000 ppm dans la nourriture), d’après l’augmentation du rapport pondéral foie/corps, les effets histopathologiques (hyperplasie dans la moelle osseuse, congestion, prolifération des cellules hématopoïétiques et pigmentation de la rate) et les effets hématologiques (diminution de l’hématocrite) observés chez les rats Fisher 344 (10 sujets/groupe) auxquels on a administré du Pigment Red 3 par les aliments (0 ppm, 3 000 ppm, 6 000 ppm, 12 500 ppm, 25 000 ppm, 50 000 ppm, 100 000 ppm) pendant 90 j. On a observé des relations dose-effet évidentes pour ces effets (Morgan et al., 1989; NTP, 1992). Autres études sur la toxicité par voie orale : On a observé une augmentation significative de la prolifération des cellules hématopoïétiques dans la rate à la plus faible dose de 502 à 666 mg/kg p.c./j (3 000 ppm dans la nourriture) chez les souris B6C3F1 (10 sujets/groupe) auxquelles on a administré du Pigment Red 3 par les aliments (0 ppm, 3 000 ppm, 6000 ppm, 12 500 ppm, 25 000 ppm, 50 000 ppm, 100 000 ppm) pendant 90 j. On a observé des lésions graves à des concentrations plus élevées (Morgan et al., 1989; NTP, 1992). On a observé une augmentation significative du rapport pondéral foie/corps chez les rats Osborne-Mendel mâles nourris avec des aliments contenant 0 ppm ou 2 500 ppm de Pigment Red 3 pendant 90 j. Aucun effet n’a été observé sur la mortalité, la croissance ou les paramètres hématologiques (Graham et Davis, 1968). Aucune étude n’a été recensée sur la toxicité par voie cutanée ou par inhalation. |
| Toxicité chronique et cancérogénicité | Cancérogénicité par voie orale chez les rats : On a nourri des groupes de 50 rats et de 50 rates Fisher 344 avec des aliments contenant 0 ppm, 6 000 ppm, 12 500 ppm et 25 000 ppm de Pigment Red 3 pendant 2 ans. Chez les mâles, l’incidence de phéochromocytomes surrénaliens bénins a connu une hausse significative, par rapport au groupe témoin, dans les groupes auxquels on a administré une dose moyenne ou élevée (22/50, 29/50, 35/50, 34/50 à 0, 6 000, 12 500 et 25 000 ppm, respectivement; p = 0,004, analyse de régression logistique). Chez les rates, on a observé une tendance positive quant aux adénomes hépatocellulaires, avec une incidence significativement accrue à la dose élevée (0/50, 0/50, 1/50, 10/50 à 0, 6 000, 12 500 et 25 000 ppm, respectivement; p = 0,001, analyse de régression logistique). On a aussi noté d’autres effets néoplasiques, dont des hausses marginalement significatives de l’incidence de papillomes spinocellulaires ou de carcinomes cutanés à la dose élevée (6/50 comparativement à 1/50 dans le groupe témoin, p = 0,051), ainsi qu’une hausse marginalement significative de l’incidence de carcinomes dans la glande de Zymbal (3/50 comparativement à 0/50 dans le groupe témoin) chez les rats (NTP, 1992). À la plus faible dose de 6 000 ppm (correspondant à une valeur de 215 à 275 mg/kg p.c./j chez les mâles), on a aussi observé une augmentation significative de l’incidence de papillomes spinocellulaires de la peau (NTP, 1992). Cancérogénicité par voie orale chez les souris : On a nourri des groupes de 50 souris mâles et de 50 souris femelles de souche B6C3F1 avec des aliments contenant 0 ppm, 12 500 ppm, 25 000 ppm et 50 000 ppm de Pigment Red 3 pendant 2 ans. Chez les souris mâles auxquels on a administré une forte dose, on a observé une augmentation significative du nombre d’adénomes dans les tubules rénaux (0/50, 0/50, 0/50 et 6/50 à 0, 12 500, 25 000 et 50 000 ppm, respectivement; p = 0,017,analyse de régression logistique) et d’adénomes des cellules folliculaires dans la glande thyroïde (0/50, 0/49, 1/50, 5/50 à 0, 12 500, 25 000 et 50 000 ppm, respectivement; p = 0,027, analyse de régression logistique). Aucune tumeur associée au traitement n’a été observée chez les souris femelles (NTP, 1992). DMENO la plus faible, par voie orale : 325 mg/kg p.c./j (6 000 ppm dans la nourriture), d’après l’augmentation significative de l’incidence des lésions hépatiques (foyers éosinophiles, foyers de cellules mixtes, dégénérescence kystique et angiectasie multifocale), la gravité accrue de la néphropathie et l’incidence accrue d’hyperplasie dans l’épithélium transitionnel des papilles rénales chez les rats exposés au Pigment Red 3 pendant 2 ans par les aliments (0 ppm, 6 000 ppm, 12 500 ppm, 25 000 ppm) [NTP, 1992]. Aucune étude n’a été recensée sur la cancérogénicité par inhalation ou par voie cutanée. |
| Toxicité sur le plan du développement et de la reproduction | Aucune donnée expérimentale disponible. |
| Génotoxicité et paramètres connexes in vivo | Essai Comet Formation de micronoyaux |
| Génotoxicité et paramètres connexes in vitro | Mutagénicité Aberrations chromosomiques Échange de chromatides sœurs Résultats négatifs dans les cellules ovariennes de hamster chinois avec ou sans activation par S9 de foie de rat avec induction (NTP, 1992). |
| Paramètre | Concentrations ou doses minimales avec effet/Résultats |
|---|---|
| Toxicité par voie cutanée | On a constaté un léger érythème ou un érythème avec œdème chez des patients souffrant d’une dermatite provoquée par des cosmétiques colorés au cours de tests épicutanés ou de photopatch-tests pendant lesquels du Pigment Red 3 était appliqué pendant 48 ou 72 heures. Le taux de réactions positives, en ce qui concerne l’irritation cutanée, était de 34,2 % (13/38) (Sugai et al., 1977). On a observé une rougeur et une tuméfaction de la peau chez 5/155 patients souffrant d’une dermatite attribuable à un produit cosmétique au cours de tests épicutanés d’une durée de 48 heures utilisant une concentration de 5 % de Pigment Red 3 dans du polyéthylèneglycol. On a aussi observé une légère rougeur chez 25 autres patients (MJCDRG, 1978). Lors d’un test épicutané, des réactions négatives furent observée avec 1% Pigment Red 3 (dans du pétrolatum) sur la peau de patients souffrant d’une dermite causée par Brilliant Lake Red R. Toutefois, on n’a observé aucune réaction cutanée chez 28 jeunes femmes en santé qui ont subi volontairement un test épicutané d’une durée de 48 heures utilisant une solution à 1 % de Pigment Red 3 dans de la gelée de pétrole (Kgzuka et al., 1980). |