Évaluation préalable pour le Défi concernant
Archivée
la thiourée
Numéro de registre du Chemical Abstracts Service
62-56-6
Environnement Canada
Santé Canada
Novembre 2008
Table des matières
- Synopsis
- Introduction
- Identité de la substance
- Propriété physiques et chimiques
- Sources
- Utilisations
- Rejets dans l'environnement
- Devenir dans l'environnement
- Persistance et potentiel de bioaccumulation
- Potentiel d'effets écologique nocifs
- Potentiel d'effets nocifs sur la santé humaine
- Conclusion
- Références
- Annexe 1 : Valeurs estimées de la limite supérieure de l'exposition à la thiourée à partir de produits de consommation
- Annexe 2 : Résumé des renseignements concernant les effets de la thiourée sur la santé
En application de l’article 74 de la Loi canadienne sur la protection de l’environnement (1999) [LCPE (1999)], les ministres de l’Environnement et de la Santé ont effectué une évaluation préalable de la thiourée, dont le numéro de registre du Chemical Abstracts Service Registry est le 62 -56 -6. Une priorité élevée a été accordée à la prise de mesures à l'égard de cette substance lors de la catégorisation visant la Liste intérieure des substances dans le cadre du Défi lancé par les ministres, car on considère qu’elle présente le plus fort risque d’exposition (PFRE) pour les particuliers au Canada et elle a été classée par d’autres organismes quant à la cancérogénicité, à la génotoxicité ou à la toxicité sur le plan du développement ou de la reproduction . Comme la thiourée satisfait aux critères environnementaux de la catégorisation pour la persistance dans l’eau, le sol et les sédiments et non à celui du potentiel de bioaccumulation ou de la toxicité intrinsèque pour les organismes aquatiques, la présente évaluation est surtout axée sur les aspects relatifs à la santé humaine.
Selon les renseignements déclarés conformément à l'article 71 de la LCPE (1999), entre 10 000 et 100 000 kg de thiourée ont été importés au Canada en 2006. Cette substance est utilisée dans les solutions de finition de métaux et pour le traitement par gravure des cartes de circuits imprimés, comme agent réducteur sous forme de dioxyde de thiourée, comme intermédiaire chimique, comme réactif dans l'industrie de l'affinage du cuivre et comme inhibiteur de corrosion. La thiourée peut également être utilisée dans les produits à polir l'argent, les produits antiternissures, les nettoyants de métaux, les produits pour la photographie noir et blanc et les papiers au ferrocyanure. Elle sert aussi à la synthèse de produits pharmaceutiques.
L'exposition à la thiourée à partir de l'environnement étant jugée négligeable, on prévoit que les produits de consommation contenant cette substance constitueront la principale source d'exposition de la population générale.
En se fondant principalement sur des évaluations reposant sur le poids de la preuve réalisées par plusieurs organismes nationaux et internationaux, il appert que la cancérogénicité est un effet critique pour la caractérisation du risque pour la santé humaine que présente la thiourée. Cette substance a provoqué l'apparition de tumeurs dans de nombreux organes de rats mâles et femelles ainsi que dans les glandes mammaires de souris. Bien que cette substance ne semble que très légèrement génotoxique, le mode d'induction des tumeurs n'a pas été complètement élucidé et on ne peut exclure la possibilité que les tumeurs observées chez les animaux de laboratoire résultent d'une interaction directe avec le matériel génétique. En outre, les marges entre les estimations de la limite supérieure de l'exposition par inhalation et par voie cutanée par suite de l'utilisation de produits de consommation contenant de la thiourée et les concentrations entraînant un effet critique pour les effets autres que le cancer, qui ont été relevées dans des études sur la toxicité à court terme et la toxicité pour la reproduction, ne seraient pas suffisantes pour tenir compte des incertitudes liées aux bases de données sur l'exposition et les effets, particulièrement en ce qui a trait aux incertitudes sur le mode d'induction des tumeurs.
Compte tenu de la cancérogénicité de la thiourée, pour laquelle il existe une probabilité d'effet nocif à toute valeur d'exposition, et de l’insuffisance possible de la marge d’exposition pour des effets autres que le cancer, il est conclu que la thiourée est une substance qui pourrait pénétrer dans l’environnement en une quantité ou une concentration ou dans des conditions de nature à constituer un danger au Canada pour la vie ou la santé humaines.
D'après le faible risque écologique que présentent la thiourée et ses rejets déclarés, il est conclu que cette substance ne pénètre pas dans l'environnement en une quantité ou concentration ou dans des conditions de nature à avoir, immédiatement ou à long terme, un effet nocif sur l'environnement ou sur la diversité biologique, ni à mettre en danger l'environnement essentiel pour la vie. La thiourée répond aux critères de la persistance, mais non à celui du potentiel de bioaccumulation, qui sont énoncés dans le Règlement sur la persistance et la bioaccumulation.
De plus, des activités de recherche et de surveillance viendront, s'il y a lieu, appuyer la vérification des hypothèses formulées au cours de l’évaluation préalable et, le cas échéant, l’efficacité des possibles mesures de contrôle définies à l’étape de la gestion des risques.
Compte tenu des renseignements disponibles, il est proposé de conclure que la thiourée satisfait à un ou à plusieurs critères de l’article 64 de la LCPE (1999).
La Loi canadienne sur la protection de l’environnement (1999) [LCPE (1999)] (Canada, 1999) impose aux ministres de l’Environnement et de la Santé de procéder à une évaluation préalable des substances qui répondent aux critères de la catégorisation énoncés dans la Loi pour déterminer si ces substances présentent ou pourraient présenter un risque pour l’environnement ou la santé humaine. Selon les résultats de cette évaluation, les ministres peuvent décider de ne rien faire à l'égard de la substance, l'inscrire sur la Liste des substances d'intérêt prioritaire en vue d'une évaluation plus détaillée, recommander son inscription sur la Liste des substances toxiques de l’annexe 1 de la Loi et, s’il y a lieu, la quasi-élimination de ses rejets dans l’environnement.
En se fondant sur l'information obtenue dans le cadre de la catégorisation, les ministres ont jugé qu'une attention hautement prioritaire devait être accordée à un certain nombre de substances, à savoir :
- celles qui répondent à tous les critères environnementaux de la catégorisation, notamment la persistance (P), le potentiel de bioaccumulation (B) et la toxicité intrinsèque (Ti) pour les organismes aquatiques, et que l’on croit être commercialisées ;
- celles qui répondent aux critères de la catégorisation pour le plus fort risque d'exposition (PFRE), ou qui présentent un risque d'exposition intermédiaire (REI), et qui ont été jugées particulièrement dangereuses pour la santé humaine à la lumière de leur classement par d'autres organismes nationaux ou internationaux quant à la cancérogénicité, à la génotoxicité ou à la toxicité pour le développement ou la reproduction.
Le 9 décembre 2006, les ministres ont donc publié un avis d'intention dans la Partie I de la Gazette du Canada(Canada, 2006), dans lequel ils ont mis au défi l'industrie et les autres intervenants intéressés de fournir, selon un calendrier déterminé, des renseignements précis qui pourraient servir à étayer l'évaluation des risques, ainsi qu'à élaborer et à évaluer comparativement les meilleures pratiques de gestion des risques et de gérance des produits pour ces substances jugées hautement prioritaires.
La thiourée est une substance dont l'évaluation des risques pour la santé humaine a été jugée hautement prioritaire, car on considère qu'elle présente un REI et elle a été classée par d'autres organismes quant à la cancérogénicité et à la toxicité sur le plan du développement ou de la reproduction. Le volet du Défi portant sur la thiourée a été lancé au moyen d’un avis paru dans la Gazette du Canada le 12 mai 2007 (Canada 2007). En même temps a été publié le profil de cette substance, qui présentait l’information technique (obtenue avant décembre 2005) sur laquelle a reposé sa catégorisation . De nouveaux renseignements sur la substance ont été communiqués en réponse au Défi.
Même si l’évaluation des risques que présente la thiourée pour la santé humaine a été jugée hautement prioritaire et que la substance remplit le critère de la catégorisation écologique de la persistance, elle ne remplit pas celui du potentiel de bioaccumulation ou de la toxicité intrinsèque pour les organismes aquatiques. Par conséquent, la présente évaluation est axée principalement sur les renseignements utiles à l'évaluation des risques pour la santé humaine.
Les évaluations préalables effectuées aux termes de la LCPE (1999) mettent l’accent sur les renseignements jugés essentiels pour déterminer si une substance répond aux critères de toxicité des substances chimiques au sens de l’article 64 de la Loi :
64. [...] Pour l'application de la présente partie et de la partie 6, mais non dans le contexte de l'expression « toxicité intrinsèque », est toxique toute substance qui pénètre ou peut pénétrer dans l'environnement en une quantité ou concentration ou dans des conditions de nature à :
a) avoir, immédiatement ou à long terme, un effet nocif sur l'environnement ou sur la diversité biologique;
b) mettre en danger l'environnement essentiel pour la vie;
c) constituer un danger au Canada pour la vie ou la santé humaine.
Les évaluations préalables visent à examiner des renseignements scientifiques et à tirer des conclusions fondées sur la méthode du poids de la preuve et le principe de prudence.
La présente ébauche d’évaluation préalable prend en considération les renseignements sur les propriétés chimiques, les dangers, les utilisations et l’exposition, y compris ceux fournis dans le cadre du Défi. Les données pertinentes pour l’évaluation préalable de cette substance ont été relevées dans des publications originales, des rapports de synthèse et d’évaluation, des rapports de recherche de parties intéressées et d’autres documents consultés lors de recherches documentaires menées récemment, jusqu’en mars 2008 (effets sur la santé humaine). Les études importantes ont fait l’objet d’une évaluation critique; les résultats de la modélisation ont pu être utilisés dans la formulation des conclusions. L’évaluation des risques pour la santé humaine comprend l’examen de données pertinentes pour l’évaluation de l’exposition (non professionnelle) de la population dans son ensemble ainsi que de l’information sur les dangers pour la santé (surtout fondée sur des évaluations réalisées par d’autres organismes selon la méthode du poids de la preuve et ayant servi à déterminer le caractère prioritaire de la substance). Les décisions reposent sur la nature de l’effet critique retenu ou sur l’écart entre les valeurs prudentes donnant lieu à des effets et les estimations de l’exposition, en tenant compte de la confiance accordée au caractère exhaustif des bases de données sur l’exposition et les effets, cela dans le contexte d’une évaluation préalable. L’évaluation préalable réalisée dans le cadre du Défi ne constitue pas un examen exhaustif ou critique de toutes les données disponibles. Il s’agit plutôt d’un sommaire des éléments d’information les plus importants pour appuyer la conclusion proposée.
La présente ébauche d’évaluation préalable a été préparée par le personnel du Programme des substances existantes de Santé Canada et d’Environnement Canada et intègre les résultats d’autres programmes exécutés par ces ministères. Cette évaluation préalable a fait l’objet d’une consultation indépendante par des pairs. Des commentaires sur les parties techniques touchant la santé humaine ont été formulés par des experts scientifiques choisis et dirigés par le Toxicology Excellence for Risk Assessment (TERA), notamment Michael Jayjock (The Lifeline Group), John Christopher (California Department of Toxic Substances Control) et Wendy Heiger-Bernays (Boston University School of Public Health & The Science Collaborative). Bien que les commentaires externes aient été pris en considération, Santé Canada et Environnement Canada assument la responsabilité du contenu final et des résultats de l’évaluation préalable. De plus, une version provisoire de la présente évaluation préalable a fait l’objet d’une consultation publique de 60 jours. Les principales données et considérations sur lesquelles repose la présente évaluation sont résumées ci-après.
Aux fins du présent document, le nom utilisé pour la substance est celui qui apparaît dans l'inventaire de la Liste intérieure des substances (LIS) : la thiourée.
| Numéro de registre du Chemical Abstracts Service (n° CAS) | 62-56-6 |
| Nom dans la LIS | thiourée |
| Autres noms | ß-thiopseudourée; 2-thiourée; isothiourée; NSC 5033; pseudothiourée; pseudourée (NH2·C(OH):NH), thio-; pseudourée, 2-thio-; thiocarbamide; THU; TsIZP 34; UN 2810; urée, 2-thio; urée, thio- |
| Formule chimique | CH4N2S |
| Groupe chimique (Groupe de la LIS) |  Organiques |
| Structure chimique | |
| SMILES | NC(=S)N |
| Masse moléculaire | 76,12 g/mole |
Un résumé des principales propriétés physiques et chimiques de la thiourée est présenté dans le tableau 2.
| Propriété | Type | Valeur / unités (unités SI)[1] |
Référence |
|---|---|---|---|
| Point de fusion (°C) |
expérimental | 177 | Sax, 1984 |
| 182 | PhysProp, 2003 | ||
| Point d'ébullition (°C) |
décomposition | Verschueren, 2001 | |
| modélisé | 157,8 | MPBPWIN, 2000 | |
| Pression de vapeur (Pa) à 25 ºC |
extrapolé | 0,37 (2,8 × 10-3 mm Hg) |
PhysProp, 2003 |
| estimé | 2,44 × 10-2 (1,83 × 10-4 mm Hg) |
CHEMFATE, 2007 | |
| Constante de la loi de Henry (Pa·m3/mole) |
expérimental | 1,29e-10atm·m3/mole (1,31e-05 Pa·m3/mole) |
Hine et Mookerjee, 1975 |
| Log Koe (coefficient de partage octanol/eau) |
expérimental | - 1,02 | Mackay et al., 2006 |
| expérimental | - 0,95 à - 2,38 | Mackay et al., 2006 | |
| Solubilité dans l'eau (kg/m3) |
mesuré | 91 800 -142 000g/L | ISHOW, 1992; Milleman et Ehrenberg, 1982 |
| Log Kco (coefficient de partage carbone organique/eau) |
modélisé | 0,44 (sans unité) | PCKOCWIN, 2000 |
[1] Lorsqu'elles diffèrent, les valeurs entre parenthèses sont celles indiquées par les auteurs ou estimées par les modèles.
Deux méthodes sont utilisées pour synthétiser la thiourée de façon industrielle. La première fait appel à une fusion à sec de thiocyanate d'ammonium qui est suivie d'une extraction à l'aide d'une solution concentrée de thiocyanate d'ammonium et d'une cristallisation (Lewis, 2001; O'Neil et al., 2001). La deuxième méthode, qui est la plus courante, consiste à traiter une cyanamide par le sulfure d'hydrogène (Lewis, 2001; O'Neilet al., 2001).
Selon une enquête réalisée en vertu de l’article 71 de la LCPE (1999), aucune entreprise canadienne n’a déclaré avoir fabriqué en 2006 de la thiourée en une quantité égale ou supérieure au seuil de déclaration de 100 kg. Par ailleurs, cette même enquête et des données communiquées de façon volontaire par l’industrie indiquaient que la quantité totale importée au Canada en 2006 se situait entre 10 000 et 100 000 kg (Environnement Canada, 2007a).
On trouve de la thiourée à l'état naturel dans des arbustes du genre Laburnum et sous forme de métabolite chezVerticillium albo-atrum et Bortrylio cinera (Verschueren, 2001).
Selon les déclarations présentées en vertu de l’article 71 de la LCPE (1999), la thiourée est utilisée dans les solutions de finition de métaux et pour le traitement par gravure des cartes de circuits imprimés (Environnement Canada, 2007a), comme agent réducteur sous forme de dioxyde de thiourée et comme intermédiaire chimique (Environnement Canada, 2007a; NTP, 2005; Raffaelli et al., 1997). Elle sert aussi de réactif dans l’industrie de l’affinage du cuivre (INRP, 2005). Elle est également un élément de produits utilisés dans les usines de pâtes et papiers pour la fabrication de papier et de carton d'emballages pour produits alimentaires, et sert de nettoyant et de produit antitartre dans les usines d'aliments; toutefois, comme les surfaces sont rincées, le transfert de la thiourée aux aliments n’est pas anticipé (selon le courriel des sections responsables de l’emballage des produits alimentaires et des additifs indirects, Direction générale des produits de santé et des aliments, Santé Canada, daté du 18 mars 2008, non cité). La thiourée est utilisée comme inhibiteur de corrosion (Hosein, 2005) et on en retrouve dans les produits à polir l’argent, les produits antiternissures et les nettoyants de métaux (HPD, 2005). Elle entre dans la production de résines ignifuges utilisées dans le nylon (PISSC, 2003; Calamari et Harper, 1994) et sert d’agent auxiliaire dans l’industrie du textile (BUA, 1995), de fixateur photographique et de détachant des négatifs photographiques (Lewis, 2001; Verschueren, 2001). On l’a aussi utilisée pour l’extraction de l’or et de l’argent par lessivage des minéraux (Laursen, 2002; Morrison, 1983; PISSC, 2003; Yen, 1992).
La thiourée peut aussi servir d'agent auxiliaire dans le papier diazo (papier pour bleus) et d'autres papiers de reproduction (PISSC, 2003), de liquéfiant dans les colles animales (BUA, 1998; O'Neil et al., 2001), d'additif dans les explosifs sous forme de bouillies et d'émulsions (BUA, 1998), d'intermédiaire dans des synthèses organiques, d'agent dans des colorants, de réactif analytique pour les ions bismuth et sélénite, d'agent pour les résines aminiques et d'accélérateur dans la fabrication du caoutchouc et la vulcanisation (Ash et Ash, 1998; Lewis, 2001; Verschueren, 2001; Winter, 2005). La thiourée peut aussi être utilisée comme agent de nettoyage à sec et pour le traitement des chaudières (NTP, 2005), comme inhibiteur de corrosion, comme agent dans des tensioactifs et pour la synthèse de produits pharmaceutiques (Ash et Ash, 1998; Lewis, 2001; Winter, 2005).
La thiourée et ses dérivés figurent maintenant sur la Liste critique des ingrédients dont l'utilisation est restreinte ou interdite dans les cosmétiques (Santé Canada, 2007). Cette substance peut cependant avoir été utilisée comme agent antimicrobien ou l'être encore (dans d'autres pays) et servir d'humectant dans des conditionneurs de la peau (Gottschalck et McEwen, 2004) et dans des préparations capillaires (Lewis, 2001; Winter, 2005).
On en retrouve aussi dans des insecticides (NTP, 2005) et des produits agrochimiques et elle sert d'inhibiteur de moisissures (Ash et Ash, 1998; Lewis, 2001), mais selon l'Agence de réglementation de la lutte antiparasitaire (ARLA), aucun pesticide homologué au Canada ne contient cette substance à titre d'ingrédient actif ou d'agent de formulation (ARLA, 2007a; ARLA, 2007b).
Sur la base des déclarations présentées en vertu de l’article 71 de la LCPE (1999), les rejets industriels de thiourée dans l’air, l’eau et le sol sont jugés négligeables, mais il a été déclaré qu’entre 100 et 1 000 kg de thiourée avaient été transférés dans une installation de traitement des déchets hors site (Environnement Canada, 2007a). Les déchets de fabrication ne devraient pas être une source d’exposition dans l’environnement, car ils sont incinérés, utilisés par l’industrie de la fabrication des briques ou du ciment ou sont éliminés dans des dépotoirs autorisés où le lixiviat est recueilli et réintroduit dans le procédé de traitement (PISSC, 2003). Aux États-Unis, certains déchets contenant de la thiourée sont éliminés par injection dans des puits de classe I (TRI, 2005).
Si l'on fait exception d'un rejet dans l'air en 2002 de 50 kg de thiourée sous forme d'émissions fugitives, il n'y a pas eu depuis 1994 de rejet sur place suffisamment important pour être déclaré à l'Inventaire national des rejets de polluants (INRP, 2007). Il a été noté, entre 1999 et 2002, une augmentation de 12 à 23,55 kg de la quantité déclarée de thiourée expédiée dans des usines de traitement des eaux usées municipales hors site avant l'élimination définitive (INRP, 2007). Il n'a pas été déclaré d'élimination hors site de thiourée depuis 2002. Les propriétés physiques et chimiques et le profil d'utilisation de la thiourée font que celle-ci devrait surtout de se retrouver dans l'eau (PISSC, 2003).
Comme on peut le voir dans le tableau 2, la thiourée a une pression de vapeur se situant entre faible et modérée (1,83 × 10-4 à 2,8 × 10-3 mm Hg) et une solubilité dans l'eau très élevée (91 800 à 142 000 g/L) qui portent à croire que cette substance serait éliminée de l'atmosphère par des dépôts humides. La valeur très faible de la constante de la loi de Henry (1,98 × 10-9atm·m3/mole) et du Log Kco (0,44) de la thiourée fait qu'elle devrait demeurer dans l'eau.
Les résultats de la modélisation de la fugacité de niveau III (tableau 3) montrent que la thiourée devrait surtout se retrouver dans l'eau ou le sol, selon le milieu de rejet.
| Rejet de la substance dans | Fraction de la substance répartie dans chaque milieu (%) |
|||
|---|---|---|---|---|
| Air | Eau | Sol | Sédiments | |
| Air (100 %) | 0,018 | 27,5 | 72,4 | 0,046 |
| Eau (100 %) | 1,7 × 10-8 | 99,8 | 6,8 × 10-5 | 0,17 |
| Sol (100 %) | 4,3 × 10-6 | 21,6 | 78,4 | 0,036 |
Persistance dans l'environnement
D'après ses propriétés physiques et chimiques (tableau 2) et les données empiriques et modélisées sur la dégradation présentées plus bas (tableaux 4a et 4b), la thiourée ne répond pas aux critères de la persistance dans l'eau, le sol et les sédiments (demi-vie dans le sol et l'eau ≥ 182 jours et demi-vie dans les sédiments ≥ 365 jours) énoncés dans le Règlement sur la persistance et la bioaccumulation(Canada, 2000).
| Milieu | Processus du devenir | Valeur pour la dégradation |
Paramètre et unité | Référence |
|---|---|---|---|---|
| Eau | biodégradation | 2,6 | biodégradation, DBO, % (14 jours) |
MITI, 1992 |
| Eau | hydrolyse | 54 750 | demi-vie (jours) | Ellington et al., 1988 |
| Milieu | Processus du devenir | Valeur pour la dégradation |
Paramètre pour la dégradation |
Référence |
|---|---|---|---|---|
| Air | oxydation atm. | 0,25 | demi-vie (jours) | AOPWIN, 2000 |
| Air | réaction avec l'ozone | non réactif | demi-vie (jours) | AOPWIN, 2000 |
| Eau | biodégradation | 15 | demi-vie (jours) | BIOWIN, 2000, Ultimate survey |
| Eau | biodégradation | 0,77 | probabilité | BIOWIN, 2000, MITI Non-linear Probability |
| Eau | biodégradation | 0,61 | probabilité | BIOWIN, 2000, MITI Linear Probability |
| Eau | biodégradation | 1 | probabilité | TOPKAT, 2004 |
| Eau | hydrolyse | n. d.[1] | demi-vie (jours) | HYDROWIN, 2000 |
| Sol | hydrolyse | ≥ 182 jours | demi-vie (jours) | fondé sur la demi-vie modélisée dans l'eau[2] |
| Sédiments | hydrolyse | ≥ 728 jours | demi-vie (jours) | fondé sur la demi-vie modélisée dans l'eau[2] |
[1] Une vitesse d'hydrolyse ne pouvait être estimée pour ce type de composé.
[2] Les valeurs ont été obtenues à partir de la demi-vie modélisée dans l'eau et en appliquant les facteurs d'extrapolation de Boethling et al. (1995), à savoir : t1/2 eau: t1/2 sol : t1/2 sédiments = 1: 1: 4.
Potentiel de bioaccumulation
Comme on ne disposait que de peu de données expérimentales sur le facteur de bioaccumulation (FBA) et le facteur de bioconcentration (FBC) de la thiourée (tableau 5a), une méthode du poids de la preuve fondée sur la relation quantitative structure-activité (RQSA) (Environnement Canada, 2007b) a aussi été appliquée en utilisant les modèles du FBA et du FBC présentés dans le tableau 5b. Selon cette méthode, la thiourée ne satisfait pas au critère de la bioaccumulation (FBC ou FBA ≥ 5 000) du Règlement sur la persistance et la bioaccumulation (Canada, 2000).
| Organisme d'essai | Paramètre | Valeur en L/kg (poids humide) |
Référence |
|---|---|---|---|
| Poisson (carpe) | FBC | 2,0 | MITI, 1992 |
| Poisson (carpe) | FBC | 0,2 | MITI, 1992 |
| Organisme d'essai | Paramètre | Valeur en L/kg (poids humide) |
Référence |
|---|---|---|---|
| Poisson | FBA | 0,93 | Gobas BAF T2MTL Arnot et Gobas, 2003 |
| Poisson | FBC | 9,12 | Gobas BCF T2LTL Arnot et Gobas, 2003 |
| Poisson | FBC | 3,16 | OASIS Forecast, 2005 |
| Poisson | FBC | 0,95 | BCFWIN, 2000 |
La thiourée satisfait aux critères de la persistance dans l'eau, le sol et les sédiments, mais non à celui du potentiel de bioaccumulation, qui sont énoncés dans le Règlement sur la persistance et la bioaccumulation (Canada, 2000).
Des données écotoxicologiques obtenues de façon expérimentale (base de données ECOTOX) indiquent que la thiourée n'a pas d'effets nocifs appréciables chez les organismes aquatiques quand elle est présente en faibles concentrations. Les valeurs de toxicité aiguë obtenues de façon expérimentale se situent dans la gamme des 4,8 à 600 g/L pour les algues et les poissons.
D'après les déclarations présentées en vertu de l'article 71 de la LCPE (1999) (Environnement Canada, 2007a), les rejets industriels de thiourée dans l'air, l'eau et le sol sont jugés négligeables, mais il a été déclaré qu'entre 100 et 1 000 kg de thiourée avaient été transférés dans une installation de traitement des déchets hors site. Depuis 2002, il n'y a pas eu de déclaration d'élimination hors site de thiourée sous l'inventaire national des rejets de polluants (INRP, 2007). Étant donné la quantité et la nature des rejets, il est peu probable qu'ils puissent donner lieu à une exposition appréciable des organismes présents dans l'environnement.
Sur la base des renseignements disponibles, il est peu probable que la thiourée ait des effets écologiques nocifs au Canada.
Évaluation de l'exposition
On n'a pas relevé de concentrations mesurées, tant au Canada qu'ailleurs, permettant d'établir des limites supérieures de l'absorption estimée de thiourée à partir d'un milieu naturel. La seule étude relevée, réalisée au Japon en 1977, portait sur l'analyse de six échantillons d'eau de mer et de six échantillons de sédiments pour la présence de thiourée (PISSC, 2003). La thiourée n'a pas été décelée dans l'eau de mer (seuil de détection de 0,011- 0,4 ug/L) ou les sédiments (seuil de détection de 0,055 et 1 ug/kg) (PISSC, 2003). Cette étude n'a pas été jugée acceptable pour l'estimation des limites supérieures de l'absorption car les échantillons ont été prélevés en mer et les résultats sont relativement anciens. Les renseignements disponibles ne permettaient pas d'estimer de limites supérieures de l'exposition à la thiourée à partir de l'environnement. Par ailleurs, selon les renseignements obtenus en vertu de l'avis émis conformément à l'article 71 de la LCPE (1999) (Environnement Canada, 2007a) et les données de l'Inventaire national des rejets de polluants (INRP, 2007), les rejets dans l'air, l'eau et le sol sont jugés négligeables.
Il existe une possibilité d'exposition de la population générale à la thiourée par l'utilisation de produits de consommation, notamment les produits à polir l'argent, les nettoyants de métaux, les papiers diazo (bleus), les textiles et divers produits pharmaceutiques. On ne dispose pas de suffisamment de données sur les quantités et la fréquence d'utilisation de ces produits pour estimer l'exposition. Des estimations n'ont donc été obtenues que pour l'exposition par inhalation ou par voie cutanée résultant de l'utilisation de produits à polir l'argent ou à nettoyer les métaux et de solutions de virage pour la photographie noir et blanc (annexe 1).
Le modèle ConsExpo (RIVM, 2006) a été appliqué à la prévision de valeurs prudentes de la concentration de thiourée dans l'air résultant de l'utilisation de nettoyants de métaux et de solutions de virage pour la photographie. Le modèle, qui supposait un rejet instantané et la saturation de vapeur, indiquait une dose aiguë de 0,11 mg/kg m.c. par événement, tant pour les nettoyants de métaux que pour la solution de virage. Ce même modèle a été appliqué à une estimation plus fine de l'exposition par inhalation (modèle par évaporation) à partir de ces deux produits en supposant que la totalité de la substance n'était pas émise par le produit au cours de son utilisation. Cela a donné une dose aiguë de 0,002 mg/kg m.c. par événement pour le nettoyant à métaux et de 0,001 mg/kg m.c. par événement pour la solution de virage photographique. Ackermann et Flynn (1987) ont obtenu un coefficient de perméabilité cutanée pour la thiourée (9,6 × 10-5 cm/h) en utilisant de la peau de souris dénudée de poils. Cette valeur est très semblable à la valeur Kp estimée par le modèle DERMWIN (2000) qui prend en compte le coefficient de partage octanol-eau. Si l'on tient compte de la valeur Kp d'Ackermann et Flynn (1987), on trouve que les doses résultant d'un seul événement d'exposition cutanée au nettoyant pour métaux et à la solution de virage sont respectivement de 0,02 et de 0,1 mg/kg m.c.
Le niveau de confiance à l'égard de la base de données sur l'exposition est jugé faible, car on ne disposait pas de données sur les concentrations de thiourée dans les milieux naturels ou les aliments. Par ailleurs, selon les renseignements disponibles, les rejets industriels dans l'environnement sont jugés négligeables. Le niveau de confiance à l'égard de l'estimation de l'exposition à partir des produits de consommation est aussi jugé faible. Selon les renseignements obtenus grâce à l'avis émis en vertu de l'article 71 de la LCPE (1999), les utilisations déclarées de la thiourée se limitaient surtout à des applications industrielles, ce qui ne devrait pas donner lieu à une exposition de la population générale. Par ailleurs, des renseignements obtenus d'autres sources indiquent que la thiourée se retrouve dans divers produits de consommation, mais l'absence de données sur sa concentration dans ces produits, la fréquence d'utilisation et les quantités utilisées interdisent d'obtenir des estimations plus exactes de l'exposition de la population générale.
Évaluation des effets sur la santé
Un aperçu des renseignements toxicologiques est présenté dans l'annexe 2.
La thiourée a été classée par le National Toxicology Program (NTP) comme une substance que l'on peut raisonnablement présumer cancérogène pour les humains (NTP, 2005) et par la Communauté européenne dans la catégorie 3 pour la cancérogénicité (substances préoccupantes pour l'humain en raison d'effets cancérogènes possibles) (Commission européenne, 1998a; ESIS, 2006). Ces classifications sont fondées sur l'observation d'adénomes et de carcinomes de la thyroïde chez des rats mâles et femelles auxquels on avait donné de l'eau contenant 0,25 % de thiourée (350 mg/kg m.c. par jour) pendant une période pouvant atteindre 24 mois (Purves et Griesbach, 1947). Des carcinomes des cellules pavimenteuses de la glande de Zymbal et des glandes de Meibomius ont été observés chez des rats mâles exposés par de l'eau contenant 0,2% de thiourée (280 g/kg m.c. par jour) ou par injection intrapéritonéale suivie d'une exposition par l'eau (0,2 % de thiourée) pendant une période pouvant atteindre 23 mois (Ungar et Rosin, 1957, 1960). L’administration de thiourée dans la diète de rats , à raison de 5 mg/kg de poids corporel par jour pendant 24 mois, a provoqué des adénomes hépatocellulaires (Fitzhugh et Nelson 1948). Une augmentation de l’incidence des tumeurs des glandes mammaires a aussi été signalée chez des souris femelles exposées à la thiourée (0,1 – 0,2 % ou 140 – 280 mg/kg m.c. par jour) dans l’eau potable pendant des périodes pouvant atteindre six mois (Vasquez-Lopez, 1949). Il est à noter que l’évaluation du NTP est fondée sur l’évaluation de la thiourée du Centre international de recherche sur le cancer (CIRC) réalisée en 1974 et qui concluait à l’existence de suffisamment de faits démontrant un effet cancérogène chez les animaux de laboratoire. Le CIRC a conclu, au moment de son évaluation la plus récente, que la thiourée ne pouvait être classée pour sa cancérogénicité (groupe 3) étant donné l’insuffisance de données probantes pour les humains et le peu de données probantes pour les animaux de laboratoire (CIRC, 2001). Aucune étude appropriée chez les humains n’a été signalée sur une relation possible entre l’exposition à la thiourée et le cancer (CIRC, 2001; PISSC, 2003; NTP, 2005).
La thiourée n'a pas fait l'objet d'essais détaillés pour sa génotoxicité in vivo. Des études chezDrosophila ont donné des résultats incertains. L'examen des données sur la génotoxicité in vitromontre que la thiourée n'est pas mutagène chez les bactéries. Les résultats obtenus avec des cellules de mammifères sont variables, mais on note de façon constante des résultats positifs pour la transformation cellulaire et la recombinaison chromosomique chez les levures (CIRC, 2001; PISSC, 2003).
Bien que le mode d'action de cette substance déborde le cadre de la présente évaluation préalable, il est à noter que le PISSC (2003) a indiqué que la thiourée n'était pas considérée comme une substance cancérogène génotoxique et que le développement de tumeurs de la thyroïde provoquées par la thiourée pouvait comporter une inhibition de la peroxydase dans la glande thyroïde qui provoquerait une diminution de la production d'hormones thyroïdiennes et une prolifération résultant d'un accroissement de l'hormone de stimulation de la thyroïde. Mais étant donné le caractère variable des résultats des essais de génotoxicité, il était impossible de tirer une conclusion définitive sur le mode d'action à l'origine de la cancérogénicité (CIRC, 2001; PISSC, 2003).
L'effet pondéral critique non néoplasique se produit dans la thyroïde. La dose minimale avec effet nocif observé, fondée sur une hypertrophie de la thyroïde et une réduction du gain pondéral, était de 27,5 mg/kg m.c. par jour chez des rats exposés par voie orale pendant des périodes pouvant atteindre trois ans (Hartzell, 1942 et 1945). Des effets sur la glande thyroïde ont aussi été observés à la dose de 50 mg/kg m.c. par jour au cours d'études de toxicité subchronique portant sur des moutons mâles (Sokkar et al., 2000) et femelles (Nasseri et Prassad, 1987a), les effets observés étant une hyperplasie de la glande thyroïde chez les mâles, une augmentation du volume de la glande thyroïde et une réduction significative de la T4 sérique chez les femelles. Une réduction des niveaux d'iode dans la glande thyroïde à été déclarée chez des rats ou l'on administrait par voie orale une dose en thiourée de 70 mg/kg m.c par jour pendant 10 jours (Astwooodet al., 1945)
La Commission européenne a aussi classé la thiourée dans la catégorie 3 pour les effets sur la reproduction en se fondant sur un risque possible de dommages pour l'enfant à naître (Commission européenne, 1998a; Commission européenne, 1998b; ESIS, 2006).
Les effets observés sur le développement sont une réduction des concentrations de testostérone, la présence de tubules séminifères petits ou vides et de testicules « mal développés » chez des moutons mâles, et des organes génitaux externes infantiles à développement interrompu de même que l'absence d'œstrus et un développement retardé des glandes mammaires chez les femelles, à la dose de 50 mg/kg m.c. par jour (Sokkar et al., 2000; Nasseri et Prassad, 1987). Les effets sur la reproduction observés chez les moutons mâles et femelles après administration par voie orale comprenaient des testicules « mal développés », des tubules séminifères petits et vides et une réduction non significative de la taille et de la masse des ovaires, des cornes de l'utérus et du vagin (Alavi Shoushtari et Safaii, 1993). L'administration par voie orale de plus de 35 mg/kg m.c. par jour de thiourée à des rats mâles a donné lieu à une réduction ou à l'interruption de la spermatogenèse (Fitzhugh et Nelson, 1948).
Des cas de dermatite par contact après exposition à la thiourée attribuable à l'utilisation de papier de reproduction diazo et d'autres types de papier de reproduction ou de l'utilisation de produit à polir l'argent ont été signalés et certains s'accompagnaient d'une sensibilité au rayonnement (Voir l'annexe 2). On a montré que des dérivés de la thiourée servant d'accélérateurs de réaction dans l'industrie du caoutchouc donnaient lieu à des dermatites par contact de type allergique
Le niveau de confiance à l'égard des renseignements sur la toxicité est jugé de modéré à faible. Il existe des données sur la toxicité aiguë et chronique, la toxicité par doses répétées, la toxicité pour le matériel génétique, la reproduction et le développement et la cancérogénicité, mais il manque d'essais de génotoxicité in vivo et bon nombre des études de la cancérogénicité sont anciennes et ne sont pas conformes aux standards des essais actuels.
Caractérisation du risque pour la santé humaine
À la lumière principalement des évaluations de plusieurs organismes internationaux et nationaux réalisées selon la méthode du poids de la preuve (CIRC, PISSC et NTP), la cancérogénicité constitue un effet critique pour la caractérisation du risque pour la santé humaine que pose la thiourée. Cette substance a provoqué l'apparition de tumeurs dans plusieurs organes de rats mâles et femelles ainsi que dans les glandes mammaires de souris. Comme la thiourée ne semble être que faiblement génotoxique, le PISSC (2003) a émis l'hypothèse qu'elle n'était pas une substance cancérogène génotoxique. Par ailleurs, les modes d'action à l'origine des divers types de tumeurs observés chez des rats et des souris n'ont pas été complètement élucidés et de telles analyses débordent le cadre de la présente évaluation préalable. On ne peut donc exclure la possibilité d'une interaction directe avec le matériel génétique.
En ce qui a trait aux effets autres que le cancer, les données étaient insuffisantes pour quantifier l'exposition à partir de l'environnement général, mais on prévoit qu'elle soit négligeable. Pour caractériser le risque des effets autres que le cancer, on a donc comparé l'exposition estimée par inhalation et par voie cutanée résultant de l'utilisation de produits de consommation, tels des nettoyants pour métaux (0.023 mg/kg m.c. par jour) et une solution de virage photographique (0.11 mg/kg m.c par jour), à la plus faible valeur de toxicité orale par exposition à court terme (DMEO de 70 mg/kg m.c. par jour). Les marges d'exposition (ME) pour le produit à polir l'argent étaient approximativement de 3000; dans le cas de la solution de virage photographique, les marges d'exposition étaient approximativement de 600. Bien qu'établies de façon prudente, ces marges pour les scénarios d'exposition à des produits de consommation pourraient ne pas tenir compte de façon adéquate des incertitudes des bases de données sur l'exposition et les effets, surtout dans le contexte des incertitudes liées au mode ou aux modes d'action à l'origine de la formation des tumeurs ainsi qu'a la variation de la relation entre la toxicité et la durée d'exposition (ex : DMEO pour une exposition a court-terme, subchronique et chronique étaient de 70, 50 et 27,5 mg/kg m.c. par jour, respectivement).
Incertitudes de l'évaluation des risques pour la santé humaine
La présente évaluation préalable réalisée dans le cadre du Défi ne prend pas en compte les écarts possibles entre les humains et les animaux de laboratoire pour ce qui est de la vulnérabilité aux effets de la substance, notamment à cause de l'absence d'études épidémiologiques pertinentes. Les études de la génotoxicité disponibles ne permettent pas de bien comprendre le potentiel de la thiourée de provoquer des dommages génétiques. En outre, le ou les modes d'induction des tumeurs observées chez les rongeurs n'ont pas été complètement élucidés, mais un mode autre que la génotoxicité a été proposé pour les tumeurs thyroïdiennes. Il demeure des incertitudes à l'égard de la quantification de la réponse à l'exposition, car la plus grande partie des données toxicologiques sont passablement anciennes, mais les quantités signalées donnant lieu à un effet se situent généralement dans la même gamme. De plus, les études par doses répétées se limitent à l'administration par voie orale. Des études réalisées par administration par inhalation et par voie cutanée permettraient d'accroître le degré de certitude à l'égard de la base de données.
Les données étaient insuffisantes pour permettre la quantification de l'exposition à la thiourée à partir des milieux naturels au Canada, mais si l'on se fonde sur les renseignements disponibles sur les rejets au Canada, les concentrations dans ces milieux devraient être négligeables. Les estimations de l'exposition à partir de l'utilisation de produits de consommation contenant de la thiourée reposent sur des hypothèses prudentes et pourraient surestimer l'exposition réelle, mais les données disponibles ne permettent pas d'obtenir d'estimations quantitatives de l'apport d'autres produits de consommation à l'exposition de la population générale du Canada.
À D'après les renseignements disponibles, on conclut que la thiourée ne pénètre pas dans l'environnement en une quantité ou concentration ou dans des conditions de nature à avoir, immédiatement ou à long terme, un effet nocif sur l'environnement ou sur la diversité biologique, ni à mettre en danger l'environnement essentiel pour la vie. En outre, la thiourée satisfait au critère de la persistance, mais non à celui du potentiel de bioaccumulation énoncés dans le Règlement sur la persistance et la bioaccumulation.
Compte tenu de la cancérogénicité de la thiourée, pour laquelle il existe une probabilité d'effet nocif à toute valeur d'exposition, et de l'insuffisance possible de la marge de l’exposition pour des effets autres que le cancer, la thiourée est considérée comme une substance pouvant pénétrer dans l'environnement en quantité , à des concentrations ou dans des conditions qui constituent ou peuvent constituer un danger au Canada pour la vie ou la santé humaines.
Il est par conséquent conclu que la thiourée ne répond pas aux critères des paragraphes 64a et 64b de la LCPE (1999), mais qu’elle répond aux critères du paragraphe 64c de la LCPE (1999).
Ackermann, C., et G. Flynn. 1987. Ether-water partitioning and permeability through nude mouse skin in vitro. I. Urea, thiourea, glycerol and glucose. Int. J. Pharm. 36:61-66.
Alavi Shoushrari, S.M. et M. Safaii. 1993. Effects of hypothyroidism on the reproductive system of female lambs. Journal of the Veterinary Faculty of the Univeristy of Tehran 48:40-35 [cité dans PISSC, 2003].
[AOPWIN] Atmospheric Oxidation Program for Windows [Modèle d’estimation]. 2000. Version 1.91. Washington (DC): U.S. Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY): Syracuse Research Corporation. [cité le 30 avril 2007]. Exposure Assessment Tools and Models.
[ARLA] Agence de réglementation de la lutte antiparasitaire. 2007a. Liste des produits de formulation de l’ARLA. Ottawa (Ont.). Santé Canada, Agence de réglementation de la lutte antiparasitaire. [cité le 17 octobre 2007].
[ARLA] Agence de réglementation de la lutte antiparasitaire. 2007b. Base de données de l’ARLA sur les étiquettes des produits[base de données sur Internet]. [cité le 17 octobre 2007].
Arnot, J.A., et F.A. Gobas. 2003. A generic QSAR for assessing the bioaccumulation potential of organic chemicals in aquatic food webs. QSAR Comb Sci[Internet]. [cité le 15 mars 2007]; 22(3): 337-345. [restricted access]
Ash, M., et I. Ash. 1998. Handbook of industrial chemical additives. Volume 2. 2nd Edition. Endicott (NY): Synapse Information Resources. p. 2025.
Astwood, E.B. 1943. The chemical nature of compounds which inhibit the function of the thyroid gland. J. Pharmacol. Exp. Ther. 78:79-89 [cité dans PISSC, 2003].
Astwood, E.B., A. Bissell et A.M. Hughes. 1945. Further studies on the chemical nature of compounds which inhibit the thyroid gland. Endocrinology 37:456-481 [cité dans PISSC, 2003].
Aubrecht, J., R. Rugo, R.H. Schiestl. 1995. Carcinogens induce intrachromosomal recombination in human cells. Carcinogenesis 16:2841-2846 [cité dans CIRC, 2001].
Bartels S., et S. Schauder. 1994. Photoallergic contact dermatitis and persistent light reaction from thiourea in blueprint paper. Aktuelle Derm 20:182–184 [cité dans PISSC, 2003].
Batiste-Alentorn, M., N. Xamena, A. Creus et R. Marcos. 1991. Genotoxicity studies with the unstable zeste-white (UZ) system of Drosophila melanogaster: results with ten carcinogenic compounds. Environ. Mol. Mutagen. 18:120–125 [cité dans CIRC, 2001; PISSC, 2003].
Batiste-Alentorn, M., N. Xamena, A. Creus et R. Marcos. 1994. Further studies with the somatic white-ivory system of Drosophila melanogaster:genotoxicity testing of ten carcinogens. Environ. Mol. Mutagen. 24:143–147 [cité dans CIRC, 2001; PISSC, 2003].
Batiste-Alentorn, M., N. Xamena, A. Creus et R. Marcos. 1995. Genotoxic evaluation of ten carcinogens in the Drosophila melanogaster wing spot test. Experientia 51:73-76 [cité dans CIRC, 2001].
[BCFWIN] BioConcentration Factor Program for Windows [Modèle d’estimation]. 2000. Version 2.15. Washington (DC): U.S. Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY): Syracuse Research Corporation. [cité le 30 avril 2007]. Exposure Assessment Tools and Models
[BIOWIN] Biodegradation Probability Program for Windows [Modèle d’estimation]. 2000. Version 4.02. Washington (DC): U.S. Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY): Syracuse Research Corporation. [cité le 30 avril 2007]. Exposure Assessment Tools and Models
Boethling, R.S., P.H. Howard, J.A. Beauman et M.E. Larosche. 1995. Factors for intermedia extrapolations in biodegradability assessment. Chemosphere. 30 (4): 741-752.
Bradley, M.O., S. Patterson et L.A. Zwelling. 1982. Thiourea prevents cytotoxicity and mutagenicity, but not sister-chromatid exchanges in V79 cells treated with cis-diaminedichloroplatinum(II). Mutat. Res. 96:67-74 [cité dans CIRC, 2001].
Brams, A., J.P. Buchet, M.C. Crutzen-Fayt, C. De Meester, R. Lauwerys et A. Leonard. 1987. A comparative study, with 40 chemicals, of the efficiency of the Salmonella assay and the SOS chromotest (kit procedure). Toxicol. Lett. 38:123-133 [cité dans CIRC, 2001; PISSC, 2003].
[BUA] Beratergremium fur Umwetrelevante Altstoffe (edited by the GDCh-Advisory Committee on Existing Chemicals of Environmental Relevance). 1998. Thiourea. BUA Report 179 (octobre 1995). Stuttgart: S. Hirzel: Wissenschaftliche Verlagsgesellschaft. Report No. 179.
Calamari Jr., T.A., et R.J. Harper Jr.1994. Flame Retardants for Textiles [Internet]. Kirk-Othmer Encyclopedia of Chemical Technology. John Wiley & Sons, Inc. [4 décembre 2000; 19 avril 2007].
Canada. 1999. Loi canadienne sur la protection de l’environnement (1999 ), L.C . 1999, c hap. 33. Gazette du Canada, Partie III, vol. 22, n° 3.
Canada. 2000. Loi canadienne sur la protection de l’environnement : Règlement sur la persistance et la bioaccumulation . C.P. 2000-348, 23 mars 2000, DORS/2000-107. Gazette du Canada, Partie II, vol. 134, n° 7.
Canada, ministère de l’Environnement et ministère de la Santé. 2006. Loi canadienne sur la protection de l’environnement (1999) : Avis d’intention d’élaborer et de mettre en œuvre des mesures d’évaluation et de gestion des risques que certaines substances présentent pour la santé des Canadiens et leur environnement. Gazette du Canada, Partie I, vol. 140, n° 49.
Canada . Ministère de l'Environnement. 2007.Loi canadienne sur la protection de l’environnement (1999) : Avis concernant certaines substances identifiées dans le groupe 2 du Défi. Gazette du Canada, Partie I, vol. 141, n° 19
Casas, C.B., et E. Koppisch. 1952. The thyroid and adrenal glands of the castrated C3H mice treated with thiourea. Endocrinology 51:322-328 [cité dans CIRC, 2001; PISSC, 2003].
[CHEMFATE] Chemical Fate Database [base de données sur Internet]. 2007. Syracuse (NY): Syracuse Research Corporation. [cité le 31 octobre 2007].
Crebelli, R., D. Bellincampi, G. Conti, L. Conti, G. Morpurgo et A. Carere. 1986. A comparative study on selected chemical carcinogens for chromosome malsegregation, mitotic crossing-over and forward mutation induction in Aspergillus nidulans. Mutat. Res. 172:138–149 [cité dans CIRC, 2001; PISSC, 2003].
Dalton, J., H.P. Morris et C.S. Durnik. 1948. Morphologic changes in the organs of female C3H mice after long-term ingestion of thiourea and thiouracil. J. Natl. Cancer Inst. 9:201-223 [cité dans CIRC, 2001; PISSC, 2003].
Deichmann, W.E., M. Keplinger, F. Sala et E. Glass. 1967. Synergism amoung oral carcinogens. IV. The simultaneous feeding of four tumorigens to rats. Toxicol. Appl. Pharmacol. 11:88-103 [cité dans CIRC, 2001; PISSC, 2003].
[DERMWIN] Dermal Permeability Coefficient Program [Modèle d’estimation]. 2000. Version 1.43. Washington (DC): U.S. Environmental Protection Agency. [cité en février 2008]. Exposure Assessment Tools and Models.
Dieke SH. Allen G.S., Richter C.P., 1947. The acute toxicity of thioureas and related compounds to wild and domestic Norway rats. J Pharmacol Exp Ther 90: 260-270. [cité en tant que Dieke, 1947 dans MAK, 1991].
Dooms-Goossens, A., M.T. Chrispeels, H. de Veylder, R. Roelandts, L. Willems et H. Degreef. 1987. Contact and photocontact sensitivity problems associated with thiourea and its derivatives: a review of the literature and case reports. Br. J. Derm. 116:573–579 [cité dans PISSC, 2003].
Dooms-Goossens, A., K. Debusschere, M. Morren, R. Roelandts et S. Coopman. 1988. Silver polish: another source of contact dermatitis reactions to thiourea. Contact Dermatitis 19:133–135 [cité dans CIRC, 2001; PISSC, 2003].
Dunkel, V.C., R.J. Pienta, A. Sivak et K.A. Traul. 1981. Comparative neoplastic transforation responses of Balb/3T3 cells, Syrian hamster embryo cells, and Rauscher murine leukemia virus-infected Fischer rat embryo cells to chemical carcinogens. J. Natl. Cancer Inst. 67:1303-1315 [cité dans CIRC, 2001].
Dunkel, V.C., E. Zeiger, D. Brusick, E. McCoy, D. McGregor, K. Mortelmans, H.S. Rosenkranz et V.F. Simmon. 1984. Reproducibility of microbial mutagenicity assays. I. Tests with Salmonella typhimurium and Escherichia coli using standardized protocol. Environ. Mutag. 6(Supp. 2):1-252 [cité dans CIRC, 2001].
[ECOTOX] ECOTOXicology Database[base de données sur Internet]. 2006. Washington (DC): U.S. Environmental Protection Agency, Office ofResearch and Development; U.S. Environmental Protection Agency, National Health and Environmental Effects Research Laboratory's, Mid-Continent Ecology Division. [cité Mar, 2006].
Egilsson, V., I.H. Evans et D. Wilkie. 1979. Toxic and mutagenic effects of carcinogens on the mitochondria of Saccharomyces cerevisiae. Mol. Gen. Genet. 174:39-46 [cité dans CIRC, 2001].
Ellington, J.J., F.E. Stancil, W.D. Payne et C.D. Trusty. 1988. Measurement of hydrolysis rate constants for evaluation of hazardous waste land disposal: Volume 3. Data on 70 Chemicals. NTISPB88-234 042/AS; EPA/600/S3-88/028.
Environnement Canada. 2007 a. Données pour certaines substances recueillies en vertu de la Loi canadienne sur la protection de l’environnement, 1999, article 71 : Avis concernant certaines substances identifiées dans le groupe 2 du Défi. Préparé par : Environnement Canada, Programme des substances existantes.
Environnement Canada. (2007b). QSARs: Reviewed Draft Working Document, Science Resource Technical Series, Guidance for Conducting Ecological Assessments under CEPA 1999. Gatineau (QC) : Division des substances existantes, Environnement Canada, Document provisoire interne disponible sur demande.
[EQC] [Estimation Model]. 2003. Version : Peterborough (Ont.) : Université Trent, The Canadian Centre for Environmental Modelling and Chemistry - TaPL3. [2008 Feb 14 ].
[ESIS] European Chemical Substances Information System [base de données sur Internet]. 2006. Thiourea. CAS No. 62-56-6. Version 4.50. Bureau européen des substances chimiques (BESC).
Commission européenne. 1998a. Thiourea. Summary Record Meeting of the Commission Working Group on the Classification and Labelling of Dangerous Substances. ECB Ispra 1-3 juillet 1998. ECBI/27/98 – Rev.2.17.12.
Commission européenne. 1998b. Thiourée. Directive de la Commission 98/98/EC du 15 décembre 1998. Annexe 1A. Journal officiel des Communautés européennes 30.12.1998.
Fautz, R., R. Forster, C.M.A. Hechenberger, W. von der Hude, G. Kaufmann, H. Madle, S. Madle, H.G. Miltenberger, L. Mueller, B.L. Pool-Zobel, E.C. Puri, P. Schmezer, A.H. Seeberg, R. Strobel, W. Suter et M. Baumeister. 1991. Report of a comparative study of DNA damage and repair assays in primary rat hepatocytes with five coded chemicals. Mutat. Res. 260:281–294 [cité dans CIRC. 2001; PISSC, 2003].
Fitzhugh, O.G., et A.A. Nelson. 1948. Liver tumors in rats fed thiourea or thioacetamide. Science 108: 626-628 [cité dans CIRC, 2001; PISSC, 2003].
Fritzenschaf, K., M. Kohlpoth, B. Rusche et D. Schiffmann 1993. Testing of known carcinogens and noncarcinogens in the Syrian hamster embryo (SHE) micronucleus test in vitro; correlations with in vivo micronucleus formation and cell transformation. Mutat. Res. 319:47-53 [cité dans CIRC, 2001].
Galli, A., et R.H. Schiestl. 1995. Salmonella test positive and negative carcinogens show different effects on intrachromosomal recombination in G2 cell cycle arrested yeast cell. Carcinogenesis 16:659-663 [cité dans CIRC, 2001].
Galli, A., et R.H. Schiestl. 1996. Effects of Salmonella assay negative and positive carcinogens on intrachromosomal recombination in G1-arrested yeast cells. Mutat. Res. 370:209–221 [cité dans CIRC, 2001; PISSC, 2003].
Galli, A., et R.H. Schiestl. 1998. Effect of Salmonella assay negative and positive carcinogens on intrachromosomal recombination in S-phase arrested yeast cells. Mutat. Res. 419:53-68 [cité dans CIRC, 2001].
Gargus, J.L., O.E. Paynter et W.H. Reese. 1969. Utilization of newborn mice in the bioassay of chemical carcinogens. Toxicol. Appl. Pharmacol. 15:552 [cité dans PISSC, 2003].
Gaudreault, R.A. 2007. Material Safety Data Sheet: Tarn-X Tarnish Remover. Skokie (IL): Jelmar. [Internet]. [2 novembre 2007].
Geier, J., et T. Fuchs.1993. Contact allergy due to 4-N,N-dimethylaminobenzene diazonium chloride and thiourea in diazo copy paper. Contact Dermatitis, 28:304–305 [cité dans PISSC, 2003].
Gorbman, A. 1947. Thyroidal and vascular changes in mice following chronic treatment with goitrogens and carcinogens. Cancer Res. 7: 746-758 [cité dans CIRC, 2001; PISSC, 2003].
Gottschalack, T.E. et G.N. McEwen, editors. 2004. International cosmetic ingredient dictionary and handbook. Volume 3. 10th Edition. Washington (DC): Cosmetic, Toiletry, and Fragrance Association. p. 1888.
Hartzell, A. 1942. Adult life span animal feeding experiments with thiourea (thioucarbamide). Contributions from the Boyce Thompson Institute 12:471-480 [cité dans PISSC, 2003].
Hartzell, A. 1945. Thiourea (thiocarbamide): adult life span animal feeding experiments with rats. Contributions from the Boyce Thompson Institute 13:501-513 [cité dans PISSC, 2003].
Hayes, S., A. Gordon, I. Sadowski et C. Hayes. 1984. RK bacterial test for independently measuring chemical toxicity and mutagenicity: short termforward selection assay. Mutat. Res. 130:97-106 [cité dans CIRC, 2001].
Hazelton. 1987. 13-week drinking water study in rats with thiourea. Hazelton Laboratories America Inc. for SKW Trostberg AC, Trostberg, p. 1-360 (HLA Study No. 2319-119) [cité dans PISSC, 2003].
Helleday, T., C. Arnaudeau et D. Jenssen. 1998. Effects of carcinogenic agents upon different mechanism for intragenic recombination in mammalian cells. Carcinogenesis. 19:973-978 [cité dans CIRC, 2001].
Hellmér, L., et G. Bolcsfoldi. 1992. An evaluation of theE. coli K-12 uvrB/recA DNA repair host-mediated assay. I. In vitro sensitivity of the bacteria to 61 compounds. Mutat. Res. 272:145-160 [cité dans CIRC, 2001; PISSC, 2003].
Hine, J., et P.K. Mookerjee. 1975. Structural effects on rates and equilibriums. XIX. Intrinsic hydrophilic character of organic compounds. Correlations in terms of structural contributions. Journal of Organic Chemistry, 40: 292-8.
[HPD] Household Products Database [base de données sur Internet]. 2005. Bethesda (MD): National Library of Medicine (US). [révisé le 12 mai 2005; cité le 13 octobre 2006].
Hosein, A.G. 2005. Material Safety Data Sheet: Liquid Rust Remover. Mississauga (Ont.). Dominion Sure Seal Ltd. [Internet]. [cité en septembre 2007].
[HYDROWIN] Hydrolysis Rates Program for Microsoft Windows [Modèle d’estimation]. 2000. Version 1.67. Washington (DC): U.S. Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY): Syracuse Research Corporation. [cité le 30 avril 2007]. Exposure Assessment Tools and Models
[CIRC] IARC Working Group on the Evaluation of Carcinogenic Risks to Humans. 2004. Some thyrotropic agents: Thiourea. IARC Monogr. Eval. Carcinog. Risks Hum. 79:703-725.
ISHOW ] Information System for Hazardous Organics in Water . 1992. Computerized database developed by U.S. EPA and University of Minnesota, Duluth)
[INRP] Inventaire national des rejets de polluants [base de données sur Internet]. 2005. Gatineau (Qc) : Environnement Canada. [cité le 10 octobre 2007].
[INRP] Inventaire national des rejets de polluants [base de données sur Internet]. 2007. Gatineau (Qc) : Environnement Canada. [Cité le 10 octobre 2007].
Japon, Gouvernement du Japon, Ministère de l’Environnement. 2004. Chemicals in the environment. Surveyed chemical substances and their detected levels in the environment (A cumulative list for fiscal year 1974-2003)[Internet]. [Cité en octobre 2007].
Jiang, Z., et al. 1989. Genotoxicity of 23 chemicals to S. cerevisiae. Environ. Mol. Mutagen. 14(Suppl. 15):95 [cité dans PISSC, 2003].
Jones, R.P. 1946. Studies on the effect of thiourea and allied substances on the thyroid gland and other organs in rats and mice. J. Pathol. Bacteriol. 58:483 [cité dans PISSC, 2003].
Kanerva, L., T. Estlander et R. Jolanki. 1994. Occupational allergic contact dermatitis caused by thiourea compounds. Contact Dermatitis 31(4):242–248 [cité dans PISSC, 2003].
Kanerva, L., T. Estlander et R. Jolanki. 2000. Occupational allergic contact dermatitis from trichlorozincates of 4-(dimethylamino)-benzendiazonium (Diazo A) and 3-methyl-4-(pyrrolidin-1-yl)-benzenediazonium (Diazo Y) and thiourea in diazo copy paper.
Contact Dermatitis 43(3):170–171 [cité dans PISSC, 2003].
Kellett, J.K., M.H. Beck et G. Auckland. 1984. Contact sensitivity to thiourea in photocopy paper. Contact Dermatitis 11:124 [cité dans PISSC, 2003].
Kern, M., Z. Tatar-Kiss, P. Kertai et I. Foldes. 1980. Teratogenic effect of 2’-thiourea in the rat. Acta Morphol. Acad. Sci. Hung. 18:259-267 [cité dans CIRC, 2001; PISSC, 2003].
Keston, A.S., E.D. Goldsmith, A.S. Gordon et H.A. Charipper. 1944. The effect of thiourea upon the metabolism of iodine by rat thyroid. J. Biol. Ch. 152:241-244 [cité dans PISSC, 2003].
Kevekordes, S., V. Mersch-Sundermann, C.M. Burghaus, J. Spielberger, H.H. Schmeiser, V.M. Arlt et H. Dunkelberg. 1999. SOS induction of selected naturally occuring substances inEscherichia coli (SOS induction chromo test). Mutat. Res. 445:81-91 [cité dans CIRC, 2001].
Kowalski, L.A., A.M. Laitinen, B. Mortazavi-Asl, R.K.-H. Wee, H.E. Erb, K.P. Assi et Z. Madden. 2000. In vitro determination of carcinogenicity of sixty-four compounds using a bovine papillomavirius DNA-carrying C3H/10T1/2 cell line. Environ. Mol. Mutag. 35:300-311 [cité dans CIRC, 2001].
Laursen, J. 2002. Cleaning materials and polishes for metal. Survey of chemical substances in consumer products [Internet]. Survey no. 16. Denmark: Danish Ministry of Environment. [2002; 17 octobre 2007].
Lewis RJ Sr. 2001. Hawley’s Condensed Chemical Dictionary. 14e édition. New York (NY): Wiley. p. 1098.
Liden, C. 1984. Contact allergy to the photographic chemical PBA-1. Contact Dermatitis 11:156 [cité dans PISSC, 2003].
Lonati-Galligani, M., P.H.M. Lohman et F. Berends. 1983. The validity of the autoradiographic method for detecting DNA repair synthesis in rat hepatocytes in primary culture. Mutat. Res. 113:145–160 [cité dans CIRC, 2001; PISSC, 2003].
Mackay, D., W.Y. Shiu, K.-C. Ma et S.L. Lee. 2006. Handbook of physical-chemical properties and environmental fate for organic chemicals. Volume 4. 2nd Edition. Boca Raton (FL): CRC/Taylor & Francis. p. 3423.
MacKenzie, C.G., et J.B. MacKenzie. 1943. Effect of sulfonamides and thioureas on the thyroid gland and basal metabolism. Endocrinology 32:185-209 [cité dans PISSC, 2003].
MAK. 1988. Thiourea. In: Henschler D, ed. Occupational toxicants: Critical data evaluation for MAK values and classification of carcinogens. Volume 1. Deutsche Forschungsgemeinschaft (DFG); Commission for the Investigation of Health Hazards of Chemical Compounds in the Work Area (MAK Commission). Weinheim, VCH, Verlagsgesellschaft mbH, p. 301–312 [cité dans PISSC, 2003].
MAK. 1991. Thiourea. In: Henschler D, ed. Occupational toxicants: Critical data evaluation for MAK values and classification of carcinogens. Volume 1. Deutsche Forschungsgemeinschaft (DFG); Commission for the Investigation of Health Hazards of Chemical Compounds in the Work Area (MAK Commission). Weinheim, VCH, Verlagsgesellschaft mbH, p. 301–314 [cité dans PISSC, 2003].
Malcom, J., W. Griesbach et F. Bielschowsky. 1949. Hyperplasia of the parathyroids associated with osteitis fivrosa in rats treated with thioureacil and related compounds. Br. J. Exp. Pathol. 30:17 [cité dans PISSC, 2003].
Mamber, S.W., V. Bryson et S.E. Katz. 1984. Evaluation of the Escherichia coli K12 inductest for detection of potential chemical carcinogens. Mutat. Res. 130:141-151 [cité dans CIRC, 2001].
McCarroll, N.E., C.E. Piper et B.H. Keech. 1981. An E. Coli microsuspension assay for the detection of DNA damage induced by direct-acting agents and promutagens. Environ. Mutag. 3:429-444 [cité dans CIRC, 2001].
McCleskey, P.E., et R.A. Swerlick. 2001. Clinical review: thioureas and allergic contact dermatitis. Cutis 68(6):387–396 [cité dans PISSC, 2003].
Milleman, R.E., et D.S. Ehrenberg. 1982. Chronic toxicity of the azaarene quinoline, a synthetic fuel component, to the pond snailPhysa gyrina. Environ. Technol. Lett. 3(5): 193- 8.
[MITI] Ministry of International Trade & Industry (Jpn), Basic Industries Bureau, Chemical Products Safety Division. 1992. Biodegradation and bioaccumulation data of existing chemicals based on the CSCL Japan. Tokyo (Jpn): Japan Chemical Industry Ecology-Toxicology & Information Centre.
Mitchell, A.D., C.J. Rudd et W.J. Caspary. 1988. Evaluation of the L5178Y mouse lymphoma cell mutagenesis assay: Intralaboratory results for sixty-three coded chemicals tested at SRI International. Environ. Mol. Mutag. 12(Suppl. 13):37-101 [cité dans CIRC, 2001].
Morris, H.P., A. Dubnik et A. Dalton. 1946. Effect of prolonged ingestion of thiourea on mammary glands and the appearance of mammary tumors in adult C3H mice. J. Natl. Cancer Inst. 7:159 [cité dans PISSC, 2003].
Morrison, R.M. 1983. Thiourea leaching of silver-bearing materials I. Literature survey. Ottawa (Ont.). Centre canadien de la technologie des minéraux et de l'énergie. Énergie, Mines et Ressources Canada. Rapport no : MRP-3.4.0.3.10.
Morita, T., Y. Iwamoto, T. Shimizu, T. Masuzawa et Y. Yanagihara. 1989. Mutagenicity tests with a permeable mutant of yeast on carcinogens showing false-negative in the Salmonella assay. Chem. Pharm. Bull. 37:407–409 [cité dans CIRC, 2001; PISSC, 2003].
[MPBPWIN] Melting Point Boiling Point Program for Microsoft Windows [Modèle d’estimation]. 2000. Version 1.41. Washington (DC): U.S. Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY): Syracuse Research Corporation. [cité le 30 avril 2007]. Exposure Assessment Tools and Models
Myhr, B.C., et W.J. Caspary. 1988. Evaluation of the L5178Y mouse lymphoma cell mutagenesis assay: Intralaboratory results for sixty-three coded chemicals tested at Litton Bionetics, Inc. Environ. Mol. Mutag. 12 (Suppl. 13): 103-194 [cité dans CIRC, 2001].
Nakamura, S., Y. Oda, T. Shimada, I. Oki et K. Sugimoto. 1987. SOS-inducing activity of chemical carcinogens and mutagens in Salmonella typhimurium TA1535/pSK1002: Examination with 151 chemicals. Mutat. Res. 192:239–246 [cité dans CIRC, 2001; PISSC, 2003].
Nasseri, A.A., et M.C. Prassad. 1987a. Experimental hydrothyroidism in lambs: clinicobiochemical studies. Indian J. Anim. Sci. 57:383-387 [cité dans PISSC, 2003].
Nasseri, A.A., et M.C. Prassad. 1987b. Effects of hypothyroidism on reproductive behaviour in female sheep: clinical studies. Indian Vet. J. 11:191-199 [cité dans PISSC, 2003].
Niinimäki, A. 1989. Photocontact allergy from photocopy paper: a report of two cases. In: Frosch PJ, Dooms-Goossens A, Lachapelle J-M, Rycroft RJG, Scheper RJ, eds. Current topics in contact dermatitis. Berlin, Springer 507–509.
[INRP] Inventaire national des rejets de polluants [base de données sur Internet]. 2007. Gatineau (QC): Environnement Canada. [cité le 10 octobre 2007].
National Toxicology Program (NTP); 2005. Report on Carcinogens. 11e édition. Substance Profile: Thiourea [Internet]. Research Triangle Park (NC): National Toxicology Program. [Consulté en décembre 2006].
Nurse, D. 1980. Sensitivity to thiourea in plain printing paper. Contact Dermatitis 6:153-154 [cité dans PISSC, 2003].
[OASIS Forecast] Optimized Approach based on Structural Indices Set [Internet]. Version 1.20 Bourgas (BG ) : Bourgas Prof. Assen Zlatarov University, Laboratory of Mathematical Chemistry.
[cited 2007 Apr 30]. OASIS Software.
O’Neil, M.J., et. al., editors. 2001. The Merck Index, 13th Edition. Whitehouse Station (NJ): Merck & Co., Inc. p. 1670.
Painter, R.B. 1977. Rapid test to detect agents that damage human DNA. Nature 265:650 [cité dans PISSC, 2003].
Pasche-Koo, F., et E. Grosshans. 1991. Contact dermatitis from thiourea. Nouvelles dermatologiques 10:694–696 [cité dans PISSC, 2003].
[PCKOCWIN] Organic Carbon Partition Coefficient Program for Windows [Modèle d’estimation]. 2000. Version 1.66. Washington (DC): U.S. Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY): Syracuse Research Corporation. [cité le 30 avril 2007]. Exposure Assessment Tools and Models
Photographers’ Formulary Inc. 2006. Formulary Thiourea Toner Bleach and Redevelopment [Internet]. [cité en février 2008].
[PhysProp] Interactive PhysProp Database [base de données sur Internet]. 2003. Syracuse (NY): Syracuse Research Corporation. [cité en mars 2006].
Pienta, R.J., J.A. Poiley et W.B. Lebherz III. 1977. Morphological transformation of early passage golden Syrian hamster embryo cells derived from cryopresserved primary cultures as a reliable in vitro bioassay for identifying diverse carcinogens. Int. J. Cancer 19:642-655 [cité dans CIRC, 2001].
[PISSC] Programme international sur la sécurité des substances chimiques. 2003. Thiourea. Geneva (CH): World Health Organization. (Concise International Chemical Assessment Document 49). Publication parrainée conjointement par le Programme des Nations Unies pour l’environnement, l’Organisation internationale du travail et l’Organisation mondiale de la santé et produite dans le cadre du Programme inter-organisations pour la gestion écologiquement rationnelle des produits chimiques.
Purves, H.D., et W.E.Griesbach. 1947. Studies on experimental goitre. VIII: Thyroid tumors in rats treated with thiourea. J. Exp. Pathol. 28:46 [cité dans CIRC, 2001; PISSC, 2003].
Raffaelli, A., S. Pucci, R. Lazzaroni et P. Salvadori. 1997. Rapid determination of thiourea in waste water by atmospheric pressure chemical ionization tandem mass spectrometry using selected-reaction monitoring. Rapid Communications in Mass Spectrometry 11(3): 259 – 264.
Randomski, J.L., W.B. Deichmann, W.E. MacDonald et E.M. Glass. 1965. Synergism amoung oral carcinogens. I. Results of the simultaneous feeding of four tumorigens to rats. Toxicol. Appl. Pharmacol. 7:652-656 [cité dans CIRC, 2001; PISSC, 2003].
[RIVM] Rijksinstituut voor Volksgezondheid en Milieu. 2006a. Consumer Exposure (ConsExpo 4.1) Model [Internet]. Version 4.1. The Netherlands: The National Institute for Public Health and the Environment (Rijksinstituut voor Volksgezondheid en Milieu).
[RIVM] Rijksinstituut voor Volksgezondheid en Milieu. 2006b. Cleaning Products Fact Sheet: To assess the risks for the consumer [Internet]. Report 320104003/2006. Bilthoven: RIVM. [cité en janvier 2008].
Rodrigues-Arnaiz, R. 1997. Genotoxic activation of hydrazine, two dialkylhydrazines, thiourea and ethylene thiourea in the somatic w/w+ assay of Drosphila melanogaster. Mutat. Res. 395:229-242 [cité dans CIRC, 2001].
Rosenkranz, H.S., et L.A. Poirier. 1979. Evaluation of the mutagenicity and DNA-modifying activity of carcinogens and noncarcinogens in microbial systems. J. Natl. Cancer Inst. 62: 873-892 [cité dans CIRC, 2001].
Rosin, A., et M. Rachmilewitz. 1954. The development of malignant tumors of the face in rats after prolonged treatment with thiourea. Cancer Res. 274:494-496 [cité dans PISSC, 2003].
Rosin, A., et H. Ungar. 1957. Malignant tumors in the eyelids and the auricular region of thiourea-treated rats. Cancer Res. 17:302-305 [cité dans CIRC, 2001; PISSC, 2003].
Ruddick, J.A., W.H. Newsome et L. Nash 1976. Correlation of teratogenicity and molecular structure: ethylenethiourea and related compounds. Teratology 13:263-266 [cité dans PISSC, 2003].
Santé Canada. 1998. Exposure factors for assessing total daily intake of priority substances by the general population of Canada. Rapport inédit. Ottawa (Ont.). Santé Canada, Direction de l’hygiène du milieu.
Santé Canada. 2007. Liste critique des ingrédients dont l'utilisation est restreinte ou interdite dans les cosmétiques (« liste critique ») - mars 2007 [Internet]. Ottawa (Ont.). Santé Canada, Sécurité des produits de consommation. [cité le 17 octobre 2007].
Sax, N.I. 1984. Dangerous properties of industrial materials. 6th Edition. New York (NY): Van Nostrand Reinhold Co.
Schiestl, R.H. 1989. Nonmutagenic carcinogens induce intrachromosomal recombination in yeast. Nature 337:285–288 [cité dans CIRC, 2001; PISSC, 2003].
Schiestl, R.H., R.D. Gietz, R.D. Mehta et P.J. Hastings. 1989. Carcinogens induce intra-chromosomal recombination in yeast. Carcinogenesis 10: 1445-1455 [cité dans CIRC, 2001].
Simmon, V.F. 1979a. In vitro mutagenicity assay of chemical carcinogens and related compounds with Salmonella typhimurium. J. Natl. Cancer Inst. 62:893-899 [cité dans CIRC, 2001].
Simmon, V.F. 1979b. In vitro assay for recombinogenic activity of chemical carcinogens and related compounds with Saccharomyces cerevisiae D3. J. Natl. Cancer Inst. 62:901-902 [cité dans CIRC, 2001].
Sina, J.F., C.L. Bean, G.L. Dysart, V.I. Taylor et M.O. Bradley. 1983. Evaluation of the alkaline elution/rat hepatocyte assay as a predictor of carcinogenic/mutagenic potential. Mutat. Res. 113:357–391 [cité dans CIRC, 2001; PISSC, 2003].
Smith, C.C. 1950. A short term chronic toxicity test. J. Pharmacol. Exp. Ther. 100:408-420 [cité dans PISSC, 2003].
Sokkar, S., A. Soror, Y. Ahmed, O. Ezzo et M. Hamouda. 2000. Pathological and biochemical studies on experimental hypothyroidism in growing lambs. Journal of Veterinary Medicine, Series B 47(9):641-652 [cité dans PISSC, 2003].
Teramoto, S., M. Kaneda, H. Aoyama et Y. Shiramu,1981. Correlation between the molecular structure of N-alkylureas adn N-alkylthioureas and their teratogenic properties. Teratology 23:335 [cité dans PISSC, 2003].
TNO. 1978. Acute dermal toxicity study with the product “Thioharnstoff” in albino rabbits. Central Institute for Nutrition and Food Research, Netherlands, for SKW Trostberg AG, Trostberg, 8 p. (Report No. R 5693) [cité dans PISSC, 2003].
TNO. 1979a Acute inhalation toxicity study of a 10% aqueous solution of « Thioharnstoff » with rats. Central Institute for Nutrition and Food Research, Netherlands, for SKW Trostberg AG, Trostberg, 5 p. (Report No. R 6264) [cité dans PISSC, 2003].
TNO. 1979b Evaluation of “Kalkstickstoff” and “Thioharnstoff” in the micronucleus test. Central Institute for Nutrition and Food Research, Netherlands, for SKW Trostberg AG, Trostberg (Report No. R 6012) [cité dans PISSC, 2003].
[TOPKAT] Toxicity Prediction Program [Internet]. 2004. Version 6.2. San Diego (CA): Accelrys Software Inc. [cité le 30 avril 2007].
Torres, V., J. Campos Lopes, L. Lobo et A. Pinto Soares. 1992. Occupational contact dermatitis to thiourea and dimethylthiourea from diazo copy paper. Am. J. Contact Dermat. 3:37–39 [cité dans PISSC, 2003].
[TRI] Toxic Release Inventory Program [Internet]. 2005. Washington (DC): US Environmental Protection Agency.
Ungar, H., et A. Rosin. 1960. The histogenesis of thiourea-induced carcinoma of the auditory duct sebaceous (Zymbal’s) glands in rats. Arch. De Vecchi. Anat. Patol. 31:419 [cité dans CIRC, 2001; PISSC, 2003].
Univar . 2007. Univar Canada Ltd. Composites, plastics & rubber industry: Raw materials for rubber [Internet]. [Cité le 17 mars 2008].
[US EPA] US Environmental Protection Agency. 1986. Standard scenarios for estimating exposure to chemical substances during use of consumer products, vol 1. Washington (DC): prepared for the US EPA, Office of Toxic Substances, Exposure Evaluation Division, by Versar, Inc. Contract no. 68-02-3968.
Van der Leun, J., E. De Kreek, H. Deenstra-van Leeuwen et H. van Weelden. 1977. Photosensitivity owing to thiourea. Arch. of Dermatol. 113:1611 [cité dans PISSC, 2003].
Van Gerwen H.J.L., Alkemade J.A.C., van der Valk P.G.M.. 1996. Photocontact allergy to thiourea as a component of photocopy paper: photocontact eczema of “airborne allergic contact dermatitis”. Nederlands Tijdschrift voor Dermatologie en Venereologie 6: 194-195 [En Hollandais, cité dans PISSC, 2003].
E. Vasquez-Lopez. 1949. The effects of thiourea on the development of spontaneous tumours on mice. Br. J. Cancer Research, 3:401 [cité dans CIRC, 2001; PISSC, 2003].
Verschueren, K. 2001. Handbook of Environmental Data on Organic Chemicals. Volume 2. 4th Edition. New York: Wiley. p.1997.
Vogel, E.W., et M.J.M. Nivard. 1993. Performance of 181 chemicals in a Drosophila assay predominantly monitoring interchromosomal mitotic recombination. Mutagenesis, 8:57–81 [cité dans CIRC, 2001; PISSC, 2003].
Wangenheim, J., et G. Bolcsfoldi. 1988. Mouse lymphoma L5178Y thymidine kinase locus assay of 50 compounds. Mutagenesis, 3:193–205 [cité dans CIRC, 2001; PISSC, 2003].
Wilkie, D., et S. Gooneskera. 1980. The yeast mitochondrial system in carcinogen testing. Chem. Ind. 21:847-850 [cité dans CIRC, 2001].
Winter R. 2005. A consumer’s dictionary of cosmetic ingredients: complete information about the harmful and desirable ingredients found in cosmetics and cosmeceuticals. 6e édition. New York (NY): Three Rivers Press. p. 516.
Yamaguchi, T. 1980. Mutagenicity of isothiocyanates, isocyanates and thioureas on Salmonella typhimurium. Agric. Biol. Chem. 44:3017–3018 [cité dans CIRC, 2001; PISSC, 2003].
Yen, W.T. 1992. Gold and silver elution from carbon loaded in thiourea leach solution. Rapport final. Kingston (Ont.). Ministère du Génie minier, Université Queen’s. No de contrat : 23440-0-9154/01-SS.
Zeiger, E., B. Anderson, S. Haworth, T. Lawlor et K. Mortelmans. 1988. Salmonella mutagenicity tests. IV. Results from the testing of 300 chemicals. Environ. Mol. Mutag. 11: (Suppl. 12)1-158 [cité dans CIRC, 2001].
Ziegler-Skylakakis, K., S. Nill, J.F. Pan et U. Andrae. 1998. S-Oxygenation of thiourea results in the formation of genotoxic products. Environ. Mol. Mutag. 31:362-373 [cité dans CIRC, 2001; PISSC, 2003].
Ziegler-Skylakakis, K., S. Rossberger et U. Andrae. 1985. Thiourea induces DNA repair synthesis in primary rat hepatocyte cultures and gene mutations in V79 Chinese hamster cells. Arch. Toxicol. 58:5-9 [cité dans CIRC, 2001; PISSC, 2003].
| Scénario d'exposition aux produits de consommation | Hypothèse | Exposition estimée |
|---|---|---|
| Produit à polir l'argent[1] | Inhalation (évaporation)
|
Concentration moyenne par événement = 0,204 Dose aiguë = 0,0019 mg/kg m.c. |
| Produit à polir l'argent[1] | Voie cutanée[2]
Dose estimée par événement
|
Dose estimée = 0,021 mg/kg m.c. par événement (par heure) |
| Tirage photographique (noir et blanc; virage sépia)[1] |
Inhalation (évaporation)
|
Concentration moyenne par événement = 0,144 Dose aiguë = 0,0014 |
| Tirage photographique (noir et blanc; virage sépia)[1] |
Voie cutanée
|
Dose aiguë = 0,11 mg/kg m.c. par événement |
[1]Possibilité d'exposition des adolescents (12-19 ans), des adultes (20-59 ans) et des personnes âgées (60 ans et plus), mais comme ces produits sont surtout utilisés par des adultes (20-59 ans), l'estimation de l'exposition s'est limitée à ce groupe d'âge.
[2] Les scénarios par voie cutanée ont aussi étés obtenus en utilisant le modèle ConsExpo, version 4.1. Des résultats similaires à ceux présentés ci-haut ont étés obtenus.
| Paramètre | Dose minimale produisant un effet - résultats |
|---|---|
| Toxicité aiguë | Plus faible DL50par voie orale (rat) = 125 mg/kg m.c. (Dieke, 1947) Plus faible CL50 par inhalation (rat) > 195g/m3 (TNO, 1979a) Plus faible DL50 par voie cutanée(lapin) > 2 500 mg/kg m.c. (TNO, 1978) |
| Toxicité à court terme par doses répétées | Plus faible DMEO par voie orale(rat) = 70 mg/kg m.c. par jour fondée sur la réduction de la concentration d'iode dans la glande thyroïde après 10 jours d'exposition (Astwood et al ., 1945) [Note : Une légère augmentation de la masse de la thyroïde a été observée chez des rats ayant reçu une dose plus faible (25 mg/kg m.c. par jour), mais aucune analyse statistique n'a été présentée. MacKenzie et MacKenzie, 1943] [Autres études : Astwood, 1943; Smith, 1950; Keston, 1944; MAK, 1988; Jones, 1946; Malcom et al ., 1949] Exposition par inhalation Aucune étude n'a été relevée. |
| Toxicité subchronique | Plus faible DMEO par voie orale (mouton) = 50 mg/kg m.c. par jour fondée sur une réduction significative de la masse corporelle, du nombre d'érythrocytes et de leucocytes et des concentrations de T3 et de testostérone, sur un mauvais développement des testicules et sur la présence de tubules séminifères petits et vides après administration quotidienne de la substance pendant 3,5 mois (Sokkaret al., 2000) [Autres études : Morris, 1946; Malcolm et al., 1949; Hazelton, 1987; Nasseri et Prassad, 1987a; Sokkar et al., 2000] Exposition par inhalation Aucune étude n'a été relevée. |
| Toxicité chronique /cancérogénicité | Essais de cancérogénicité par voie orale chez le rat Administration à des rats de 0,25 % de thiourée dans l'eau potable (350 mg/kg m.c. par jour) pendant 12 à 24 mois. Observation de tumeurs des cellules folliculaires thyroïdiennes chez 8 de 10 rats albinos mâles de la Nouvelle-Zélande (carcinomes de la thyroïde chez 4/10) et chez 8 de 10 rats albinos femelles de la Nouvelle-Zélande (carcinomes de la thyroïde chez 3/10) et chez 6 de 10 rats mâles Wistar (carcinomes de la thyroïde chez 0/10 [Purves et Griesbach, 1947). [Note : Aucun groupe témoin n'a été utilisé pour l'étude.] Administration à des rats de 0 ou 0,2 % de thiourée dans l'eau potable pendant une période pouvant atteindre 26 mois. Observation d'une augmentation des carcinomes épidermoïdes du canal auditif externe ou des glandes de Meibomius chez 17 de 19 rats albinos comparativement à 0 sur 12 chez les témoins (Rosin et Ungar, 1957). Administration à des rats de 0,2 % de thiourée dans l'eau potable. Observation de carcinomes des cellules pavimenteuses de la glande de Zymbal ou des glandes de Meibomius chez tous les sujets sauf un (Rosin et Ungar, 1960).[Note : Dans l'étude de Rosin et Ungar (1960) les rats utilisés étaient les survivants d'études de transplantation de tumeurs pour lesquels on avait jugé que l'implantation intrascapulaire avait été un échec.] Administration à des rats albinos (mâles et femelles) de 0, 0,01, 0,025, 0,05, 0,1, 0,25, 0,5 ou 1 % de thiourée dans la nourriture ( 0, 5, 12, 25, 50, 125, 250, 500 mg/kg m.c. par jour) pendant 24 mois. Observation d'une hyperplasie et d'une hypertrophie de la glande thyroïde allant de modérées à marquées aux doses de 0,25 % à 1 % (125-500 mg/kg m.c. par jour). Augmentation de l'incidence des tumeurs hépatiques (adénomes des cellules hépatiques) aux doses de 5 mg/kg m.c. par jour et plus (3/5, 4/8, 2/8 et 5/8 à 5 mg/kg m.c. par jour). Tous les animaux des deux groupes ayant reçu les doses les plus élevées sont morts avant 17 mois (Fitzhugh et Nelson, 1948; Deichmann et al., 1967). Administration à des souris femelles (R3) de 0,1 à 0,2 % (140-280 mg/kg m.c. par jour) de thiourée dans l'eau potable pendant 4 à 6 mois. Observation de tumeurs mammaires chez 54 % des souris exposées (dose non précisée dans la source secondaire) comparativement à 28 % chez les témoins (Vasquez-Lopez, 1949). Plus faible DMENO par voie orale (rat) = 27,5 mg/kg m.c. par jour pour une hypertrophie de la glande thyroïde et une réduction du gain pondéral chez des rats exposés tous les jours pendant deux ans dans l'eau potable (Hartzell, 1942 et 1945) Exposition par inhalation : Aucune étude n'a été recensée. [Autres études : Fitzhugh et Nelson, 1948; Gorbman, 1947; Daltonet al., 1948; Casas et Koppisch, 1952; Gargus et al., 1969; Purves et Griesbach, 1947; Rosin et Rachmilewitz, 1954; Rosin et Ungar, 1957; Rosin et Ungar, 1960; Randomski et al., 1965; Deichmann et al., 1967; Hartzell, 1942, 1945; Hazelton, 1987; Morris et al., 1946] |
| Toxicité pour le développement | Plus faible DMEO par voie orale (mouton) = 50 mg/kg m.c. par jour pour une hyperplasie de la glande thyroïde, une réduction significative de la masse corporelle et une réduction des concentrations d'érythrocytes, de leucocytes, de la T3 et de testostérone. Fondée sur la présence de tubules séminifères petits et vides et de testicules « mal développés » (Sokkar et al., 2000) et d'organes génitaux externes infantiles et non développés, l'absence d'œstrus et le développement retardé des glandes mammaires (Nasseri et Prassad, 1987) [Autres études : Sokkar et al ., 2000; Teramoto et al., 1981; Ruddick et al., 1976; Kern et al., 1980; Nasseri et Prassad, 1987b] |
| Toxicité pour la reproduction | Plus faible DMEO par voie orale (mouton) = L'administration à des moutons femelles d'une dose de thiourée pouvant atteindre 50 mg/kg m.c. par jour pendant 80 jours a donné lieu à une légère réduction, mais non statistiquement significative, de la taille et de la masse des ovaires, des cornes de l'utérus et du vagin. L'examen histologique a montré la présence de follicules atrétiques dans les ovaires et de cellules endométriales plus courtes.(Alavi Shoushtari et Safaii, 1993) Autres études :Le PISSC (2003) a signalé que des rats dont la nourriture contenait de la thiourée présentaient après une exposition de 24 mois une réduction ou un arrêt de la spermatogenèse aux doses supérieures à 35 mg/kg m.c. par jour (Fitzhugh et Nelson, 1948) |
| Paramètre | Résultats et référence | |||
|---|---|---|---|---|
| Espèce, souche | Résultat | Activation métabolique | Référence | |
| Mutation génétique | Salmonella typhimurium, TA 97 |
négatif | +/- | Brams et al., 1987 Zeiger et al., 1988 |
| Salmonella typhimurium, TA 98 |
négatif | +/- | Simmon, 1979a Dunkel et al., 1984 Brams et al., 1987 Zeiger et al., 1988 |
|
| Salmonella typhimurium, TA 100 |
négatif | +/- | Simmon, 1979a Yamaguchi, 1980 Dunkel et al., 1984 Brams et al., 1987 Zeiger et al., 1988 |
|
| Salmonella typhimurium, TA1535 |
négatif | +/- | Simmon, 1979a Rozenkranz et Poirier, 1979 Dunkel et al., 1984 Zeiger et al., 1988 |
|
| Salmonella typhimurium, TA1535/pSK1002, essai umu | négatif | +/- | Nakamura et al., 1987 |
|
| Salmonella typhimurium, TA1537 |
négatif | +/- | Simmon, 1979a Dunkel et al., 1984 |
|
| Salmonella typhimurium, TA1538 |
négatif | +/- | Rozenkranz et Poirier, 1979 Simmon, 1979a Dunkel et al., 1984 |
|
| Escherichia coli, réparation SOS |
négatif | +/- | Brams et al., 1987 Kevekordes et al., 1999 |
|
| Escherichia coli, WP2 uvr A | négatif | +/- | Dunkel et al., 1984 | |
| Escherichia coli, pol A | négatif | + | Rosenkranz et Poirier, 1979 McCarrol et al., 1981 |
|
| - | McCarrol et al., 1981 | |||
| Escherichia coli, souches uvr/rec |
positif | - | Hellmer et Bolscfoldi, 1992 | |
| négatif | + | Hellmer et Bolscfoldi, 1992 | ||
| Escherichia coli, K12 | négatif | + | Mamber et al., 1984 | |
| aucun essai | - | Mamber et al., 1984 | ||
| Escherichia coli, RK | négatif | +/- | Hayes et al., 1984 | |
| Aspergillus nidulans | négatif | - | Crebelli et al., 1986 | |
| Saccharamyces cerevisiae | positif | - | Schiestl, 1989 Schiestl et al., 1989 Galli et Schiestl, 1995, 1996, 1998 |
|
| + | Galli et Schiestl 1998 Egilsson et al., 1979 Wilkie et Gooneskera, 1980 |
|||
| Saccharamyces cerevisiae, locus trp | positif | + | Morita et al., 1989 | |
| négatif | - | Morita et al., 1989 | ||
| Saccharamyces cerevisiae, locus D7 trp | positif | non précisé | Jiang et al., 1989 | |
| Drosophila melanogaster | positif | - | Batiste-Alentorn et al., 1991 | |
| faiblement positif | - | Vogel et Nivard, 1993 | ||
| non concluant | - | Batiste-Alentorn et al., 1994, 1995 | ||
| négatif | - | Rodriguez-Arnaiz, 1997 | ||
| cellules de souris L5178Y | faiblement positif | + | Myhr et Caspary, 1988 Wangenheim et Bolscfoldi, 1988 |
|
| - | Wangenheim et Bolscfoldi, 1988 | |||
| négatif | + | Mitchell et al., 1988 | ||
| - | Mitchell et al., 1988 Myhr et Caspary, 1988 |
|||
| cellules ovariennes de hamsters chinois (V79), locus hprt | négatif | - | Bradley et al., 1982 | |
| positif | +/- | Ziegler-Skylakakis et al., 1985 | ||
| cellules ovariennes de hamsters chinois (V79), sous-lignée Sp5 | négatif | - | Helleday et al., 1998 | |
| Paramètre | Résultats et référence | |||
|---|---|---|---|---|
| Échange de chromatides sœurs | négatif : cellules de hamsters chinois - V79 (- activation) [Bradley et al., 1982] |
|||
| Synthèse non programmée de l'ADN | faiblement positif : cellules du foie du rat (Ziegler-Skylakakis et al., 1985) négatif : cellules du foie du rat (- activation, + activation non testée) [Lonati-Galligani et al., 1983; Fautz et al., 1991) |
|||
| Recombinaison mitotique | négatif : Saccharamyces cerevisiae D3 (+/- activation) [Simmon, 1979b] |
|||
| Recombinaison | positif : cellules lymphoblastoïdes humaines transformées GM6804 (Aubrechtet al., 1995) |
|||
| Formation de micronoyaux | positif : cellules d'embryons du hamster syrien (- activation, + non testé) [Fritzenschaf et al., 1993)faiblement positif : hamster chinois, V79 (Ziegler-Skylakakis et al., 1998) |
|||
| Bris de brins d'ADN | positif : hépatocytes de rat in vitro (-activation, non testé + activation) [Sina et al., 1983]négatif : hépatocytes de rat in vitro (-activation, non testé + activation) [Fautz et al., 1991] |
|||
| Transformation cellulaire | positif : cellules d'embryons du hamster syrien (-activation, + non testé) [Pienta et al., 1977] cellules d'embryons de rat infectées par le virus de Rauscher (-activation, + non testé) [Dunkel et al., 1981] faiblement positif : cellules C3H10T1/2 infectées par le virus à ADN modifié du papillome bovin (-activation, + non testé) [Kowalski et al., 2000] |
|||
| Inhibition de la synthèse de l'ADN | positif : cellules fibroblastiques humaines (Painter) |
|||
| Génotoxicité et paramètres connexes : in vivo | ||||
| Mutation génétique | positif ; Drosophila melanogaster (Batiste-Alentorn et al., 1991) faiblement positif : Drosophila melanogaster (Vogel et Nivard, 1993) négatif : Drosophila melanogaster (Rodriguez-Arnaiz, 1997) non concluant : Drosophila melanogaster (Batiste-Alentorn et al., 1994; Batiste-Alentorn et al., 1995) |
|||
| Essai des micronoyaux | négatif : rats traités par deux doses orales successives en 24 heures (TNO, 1979b) |
|||
| Effets chez les Humains | ||||
| Études de cas | Des cas individuels de dermatite par contact ont été signalés après exposition à de la thiourée résultant de l'utilisation de papier à reproduction diazo et de la plupart des autres types de papier à reproduction (Van der Leun et al ., 1977; Nurse, 1980; Kellet et al., 1984; Liden, 1984; Dooms-Goossens et al., 1987; Niinimaki, 1989; Pashe-Koo et Grosshans, 1991; Torres et al., 1992; Geier et Fuchs, 1993; Bartels et Schauder, 1994; van Gerwen et al., 1996; Kanerva et al., 2000). Une dermatite par contact due à la thiourée présente dans un produit à polir l'argent a été signalée (Dooms-Goossens et al., 1988). Il a été montré que des dérivés de la thiourée utilisés comme accélérateurs dans l'industrie du caoutchouc provoquaient une dermatite par contact de type allergique (Kanerva et al., 1994; McCleskey et Swerlick, 2001). |
|||
Cette page Web a été archivée dans le Web
L'information dont il est indiqué qu'elle est archivée est fournie à des fins de référence, de recherche ou de tenue de documents. Elle n'est pas assujettie aux normes Web du gouvernement du Canada et elle n'a pas été modifiée ou mise à jour depuis son archivage. Pour obtenir cette information dans un autre format, veuillez communiquer avec nous.
Archivée
la thiourée
Numéro de registre du Chemical Abstracts Service
62-56-6
Environnement Canada
Santé Canada
Novembre 2008
Table des matières
- Synopsis
- Introduction
- Identité de la substance
- Propriété physiques et chimiques
- Sources
- Utilisations
- Rejets dans l'environnement
- Devenir dans l'environnement
- Persistance et potentiel de bioaccumulation
- Potentiel d'effets écologique nocifs
- Potentiel d'effets nocifs sur la santé humaine
- Conclusion
- Références
- Annexe 1 : Valeurs estimées de la limite supérieure de l'exposition à la thiourée à partir de produits de consommation
- Annexe 2 : Résumé des renseignements concernant les effets de la thiourée sur la santé
En application de l’article 74 de la Loi canadienne sur la protection de l’environnement (1999) [LCPE (1999)], les ministres de l’Environnement et de la Santé ont effectué une évaluation préalable de la thiourée, dont le numéro de registre du Chemical Abstracts Service Registry est le 62 -56 -6. Une priorité élevée a été accordée à la prise de mesures à l'égard de cette substance lors de la catégorisation visant la Liste intérieure des substances dans le cadre du Défi lancé par les ministres, car on considère qu’elle présente le plus fort risque d’exposition (PFRE) pour les particuliers au Canada et elle a été classée par d’autres organismes quant à la cancérogénicité, à la génotoxicité ou à la toxicité sur le plan du développement ou de la reproduction . Comme la thiourée satisfait aux critères environnementaux de la catégorisation pour la persistance dans l’eau, le sol et les sédiments et non à celui du potentiel de bioaccumulation ou de la toxicité intrinsèque pour les organismes aquatiques, la présente évaluation est surtout axée sur les aspects relatifs à la santé humaine.
Selon les renseignements déclarés conformément à l'article 71 de la LCPE (1999), entre 10 000 et 100 000 kg de thiourée ont été importés au Canada en 2006. Cette substance est utilisée dans les solutions de finition de métaux et pour le traitement par gravure des cartes de circuits imprimés, comme agent réducteur sous forme de dioxyde de thiourée, comme intermédiaire chimique, comme réactif dans l'industrie de l'affinage du cuivre et comme inhibiteur de corrosion. La thiourée peut également être utilisée dans les produits à polir l'argent, les produits antiternissures, les nettoyants de métaux, les produits pour la photographie noir et blanc et les papiers au ferrocyanure. Elle sert aussi à la synthèse de produits pharmaceutiques.
L'exposition à la thiourée à partir de l'environnement étant jugée négligeable, on prévoit que les produits de consommation contenant cette substance constitueront la principale source d'exposition de la population générale.
En se fondant principalement sur des évaluations reposant sur le poids de la preuve réalisées par plusieurs organismes nationaux et internationaux, il appert que la cancérogénicité est un effet critique pour la caractérisation du risque pour la santé humaine que présente la thiourée. Cette substance a provoqué l'apparition de tumeurs dans de nombreux organes de rats mâles et femelles ainsi que dans les glandes mammaires de souris. Bien que cette substance ne semble que très légèrement génotoxique, le mode d'induction des tumeurs n'a pas été complètement élucidé et on ne peut exclure la possibilité que les tumeurs observées chez les animaux de laboratoire résultent d'une interaction directe avec le matériel génétique. En outre, les marges entre les estimations de la limite supérieure de l'exposition par inhalation et par voie cutanée par suite de l'utilisation de produits de consommation contenant de la thiourée et les concentrations entraînant un effet critique pour les effets autres que le cancer, qui ont été relevées dans des études sur la toxicité à court terme et la toxicité pour la reproduction, ne seraient pas suffisantes pour tenir compte des incertitudes liées aux bases de données sur l'exposition et les effets, particulièrement en ce qui a trait aux incertitudes sur le mode d'induction des tumeurs.
Compte tenu de la cancérogénicité de la thiourée, pour laquelle il existe une probabilité d'effet nocif à toute valeur d'exposition, et de l’insuffisance possible de la marge d’exposition pour des effets autres que le cancer, il est conclu que la thiourée est une substance qui pourrait pénétrer dans l’environnement en une quantité ou une concentration ou dans des conditions de nature à constituer un danger au Canada pour la vie ou la santé humaines.
D'après le faible risque écologique que présentent la thiourée et ses rejets déclarés, il est conclu que cette substance ne pénètre pas dans l'environnement en une quantité ou concentration ou dans des conditions de nature à avoir, immédiatement ou à long terme, un effet nocif sur l'environnement ou sur la diversité biologique, ni à mettre en danger l'environnement essentiel pour la vie. La thiourée répond aux critères de la persistance, mais non à celui du potentiel de bioaccumulation, qui sont énoncés dans le Règlement sur la persistance et la bioaccumulation.
De plus, des activités de recherche et de surveillance viendront, s'il y a lieu, appuyer la vérification des hypothèses formulées au cours de l’évaluation préalable et, le cas échéant, l’efficacité des possibles mesures de contrôle définies à l’étape de la gestion des risques.
Compte tenu des renseignements disponibles, il est proposé de conclure que la thiourée satisfait à un ou à plusieurs critères de l’article 64 de la LCPE (1999).
La Loi canadienne sur la protection de l’environnement (1999) [LCPE (1999)] (Canada, 1999) impose aux ministres de l’Environnement et de la Santé de procéder à une évaluation préalable des substances qui répondent aux critères de la catégorisation énoncés dans la Loi pour déterminer si ces substances présentent ou pourraient présenter un risque pour l’environnement ou la santé humaine. Selon les résultats de cette évaluation, les ministres peuvent décider de ne rien faire à l'égard de la substance, l'inscrire sur la Liste des substances d'intérêt prioritaire en vue d'une évaluation plus détaillée, recommander son inscription sur la Liste des substances toxiques de l’annexe 1 de la Loi et, s’il y a lieu, la quasi-élimination de ses rejets dans l’environnement.
En se fondant sur l'information obtenue dans le cadre de la catégorisation, les ministres ont jugé qu'une attention hautement prioritaire devait être accordée à un certain nombre de substances, à savoir :
- celles qui répondent à tous les critères environnementaux de la catégorisation, notamment la persistance (P), le potentiel de bioaccumulation (B) et la toxicité intrinsèque (Ti) pour les organismes aquatiques, et que l’on croit être commercialisées ;
- celles qui répondent aux critères de la catégorisation pour le plus fort risque d'exposition (PFRE), ou qui présentent un risque d'exposition intermédiaire (REI), et qui ont été jugées particulièrement dangereuses pour la santé humaine à la lumière de leur classement par d'autres organismes nationaux ou internationaux quant à la cancérogénicité, à la génotoxicité ou à la toxicité pour le développement ou la reproduction.
Le 9 décembre 2006, les ministres ont donc publié un avis d'intention dans la Partie I de la Gazette du Canada(Canada, 2006), dans lequel ils ont mis au défi l'industrie et les autres intervenants intéressés de fournir, selon un calendrier déterminé, des renseignements précis qui pourraient servir à étayer l'évaluation des risques, ainsi qu'à élaborer et à évaluer comparativement les meilleures pratiques de gestion des risques et de gérance des produits pour ces substances jugées hautement prioritaires.
La thiourée est une substance dont l'évaluation des risques pour la santé humaine a été jugée hautement prioritaire, car on considère qu'elle présente un REI et elle a été classée par d'autres organismes quant à la cancérogénicité et à la toxicité sur le plan du développement ou de la reproduction. Le volet du Défi portant sur la thiourée a été lancé au moyen d’un avis paru dans la Gazette du Canada le 12 mai 2007 (Canada 2007). En même temps a été publié le profil de cette substance, qui présentait l’information technique (obtenue avant décembre 2005) sur laquelle a reposé sa catégorisation . De nouveaux renseignements sur la substance ont été communiqués en réponse au Défi.
Même si l’évaluation des risques que présente la thiourée pour la santé humaine a été jugée hautement prioritaire et que la substance remplit le critère de la catégorisation écologique de la persistance, elle ne remplit pas celui du potentiel de bioaccumulation ou de la toxicité intrinsèque pour les organismes aquatiques. Par conséquent, la présente évaluation est axée principalement sur les renseignements utiles à l'évaluation des risques pour la santé humaine.
Les évaluations préalables effectuées aux termes de la LCPE (1999) mettent l’accent sur les renseignements jugés essentiels pour déterminer si une substance répond aux critères de toxicité des substances chimiques au sens de l’article 64 de la Loi :
64. [...] Pour l'application de la présente partie et de la partie 6, mais non dans le contexte de l'expression « toxicité intrinsèque », est toxique toute substance qui pénètre ou peut pénétrer dans l'environnement en une quantité ou concentration ou dans des conditions de nature à :
a) avoir, immédiatement ou à long terme, un effet nocif sur l'environnement ou sur la diversité biologique;
b) mettre en danger l'environnement essentiel pour la vie;
c) constituer un danger au Canada pour la vie ou la santé humaine.
Les évaluations préalables visent à examiner des renseignements scientifiques et à tirer des conclusions fondées sur la méthode du poids de la preuve et le principe de prudence.
La présente ébauche d’évaluation préalable prend en considération les renseignements sur les propriétés chimiques, les dangers, les utilisations et l’exposition, y compris ceux fournis dans le cadre du Défi. Les données pertinentes pour l’évaluation préalable de cette substance ont été relevées dans des publications originales, des rapports de synthèse et d’évaluation, des rapports de recherche de parties intéressées et d’autres documents consultés lors de recherches documentaires menées récemment, jusqu’en mars 2008 (effets sur la santé humaine). Les études importantes ont fait l’objet d’une évaluation critique; les résultats de la modélisation ont pu être utilisés dans la formulation des conclusions. L’évaluation des risques pour la santé humaine comprend l’examen de données pertinentes pour l’évaluation de l’exposition (non professionnelle) de la population dans son ensemble ainsi que de l’information sur les dangers pour la santé (surtout fondée sur des évaluations réalisées par d’autres organismes selon la méthode du poids de la preuve et ayant servi à déterminer le caractère prioritaire de la substance). Les décisions reposent sur la nature de l’effet critique retenu ou sur l’écart entre les valeurs prudentes donnant lieu à des effets et les estimations de l’exposition, en tenant compte de la confiance accordée au caractère exhaustif des bases de données sur l’exposition et les effets, cela dans le contexte d’une évaluation préalable. L’évaluation préalable réalisée dans le cadre du Défi ne constitue pas un examen exhaustif ou critique de toutes les données disponibles. Il s’agit plutôt d’un sommaire des éléments d’information les plus importants pour appuyer la conclusion proposée.
La présente ébauche d’évaluation préalable a été préparée par le personnel du Programme des substances existantes de Santé Canada et d’Environnement Canada et intègre les résultats d’autres programmes exécutés par ces ministères. Cette évaluation préalable a fait l’objet d’une consultation indépendante par des pairs. Des commentaires sur les parties techniques touchant la santé humaine ont été formulés par des experts scientifiques choisis et dirigés par le Toxicology Excellence for Risk Assessment (TERA), notamment Michael Jayjock (The Lifeline Group), John Christopher (California Department of Toxic Substances Control) et Wendy Heiger-Bernays (Boston University School of Public Health & The Science Collaborative). Bien que les commentaires externes aient été pris en considération, Santé Canada et Environnement Canada assument la responsabilité du contenu final et des résultats de l’évaluation préalable. De plus, une version provisoire de la présente évaluation préalable a fait l’objet d’une consultation publique de 60 jours. Les principales données et considérations sur lesquelles repose la présente évaluation sont résumées ci-après.
Aux fins du présent document, le nom utilisé pour la substance est celui qui apparaît dans l'inventaire de la Liste intérieure des substances (LIS) : la thiourée.
| Numéro de registre du Chemical Abstracts Service (n° CAS) | 62-56-6 |
| Nom dans la LIS | thiourée |
| Autres noms | ß-thiopseudourée; 2-thiourée; isothiourée; NSC 5033; pseudothiourée; pseudourée (NH2·C(OH):NH), thio-; pseudourée, 2-thio-; thiocarbamide; THU; TsIZP 34; UN 2810; urée, 2-thio; urée, thio- |
| Formule chimique | CH4N2S |
| Groupe chimique (Groupe de la LIS) | 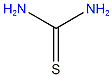 Organiques |
| Structure chimique | |
| SMILES | NC(=S)N |
| Masse moléculaire | 76,12 g/mole |
Un résumé des principales propriétés physiques et chimiques de la thiourée est présenté dans le tableau 2.
| Propriété | Type | Valeur / unités (unités SI)[1] |
Référence |
|---|---|---|---|
| Point de fusion (°C) |
expérimental | 177 | Sax, 1984 |
| 182 | PhysProp, 2003 | ||
| Point d'ébullition (°C) |
décomposition | Verschueren, 2001 | |
| modélisé | 157,8 | MPBPWIN, 2000 | |
| Pression de vapeur (Pa) à 25 ºC |
extrapolé | 0,37 (2,8 × 10-3 mm Hg) |
PhysProp, 2003 |
| estimé | 2,44 × 10-2 (1,83 × 10-4 mm Hg) |
CHEMFATE, 2007 | |
| Constante de la loi de Henry (Pa·m3/mole) |
expérimental | 1,29e-10atm·m3/mole (1,31e-05 Pa·m3/mole) |
Hine et Mookerjee, 1975 |
| Log Koe (coefficient de partage octanol/eau) |
expérimental | - 1,02 | Mackay et al., 2006 |
| expérimental | - 0,95 à - 2,38 | Mackay et al., 2006 | |
| Solubilité dans l'eau (kg/m3) |
mesuré | 91 800 -142 000g/L | ISHOW, 1992; Milleman et Ehrenberg, 1982 |
| Log Kco (coefficient de partage carbone organique/eau) |
modélisé | 0,44 (sans unité) | PCKOCWIN, 2000 |
[1] Lorsqu'elles diffèrent, les valeurs entre parenthèses sont celles indiquées par les auteurs ou estimées par les modèles.
Deux méthodes sont utilisées pour synthétiser la thiourée de façon industrielle. La première fait appel à une fusion à sec de thiocyanate d'ammonium qui est suivie d'une extraction à l'aide d'une solution concentrée de thiocyanate d'ammonium et d'une cristallisation (Lewis, 2001; O'Neil et al., 2001). La deuxième méthode, qui est la plus courante, consiste à traiter une cyanamide par le sulfure d'hydrogène (Lewis, 2001; O'Neilet al., 2001).
Selon une enquête réalisée en vertu de l’article 71 de la LCPE (1999), aucune entreprise canadienne n’a déclaré avoir fabriqué en 2006 de la thiourée en une quantité égale ou supérieure au seuil de déclaration de 100 kg. Par ailleurs, cette même enquête et des données communiquées de façon volontaire par l’industrie indiquaient que la quantité totale importée au Canada en 2006 se situait entre 10 000 et 100 000 kg (Environnement Canada, 2007a).
On trouve de la thiourée à l'état naturel dans des arbustes du genre Laburnum et sous forme de métabolite chezVerticillium albo-atrum et Bortrylio cinera (Verschueren, 2001).
Selon les déclarations présentées en vertu de l’article 71 de la LCPE (1999), la thiourée est utilisée dans les solutions de finition de métaux et pour le traitement par gravure des cartes de circuits imprimés (Environnement Canada, 2007a), comme agent réducteur sous forme de dioxyde de thiourée et comme intermédiaire chimique (Environnement Canada, 2007a; NTP, 2005; Raffaelli et al., 1997). Elle sert aussi de réactif dans l’industrie de l’affinage du cuivre (INRP, 2005). Elle est également un élément de produits utilisés dans les usines de pâtes et papiers pour la fabrication de papier et de carton d'emballages pour produits alimentaires, et sert de nettoyant et de produit antitartre dans les usines d'aliments; toutefois, comme les surfaces sont rincées, le transfert de la thiourée aux aliments n’est pas anticipé (selon le courriel des sections responsables de l’emballage des produits alimentaires et des additifs indirects, Direction générale des produits de santé et des aliments, Santé Canada, daté du 18 mars 2008, non cité). La thiourée est utilisée comme inhibiteur de corrosion (Hosein, 2005) et on en retrouve dans les produits à polir l’argent, les produits antiternissures et les nettoyants de métaux (HPD, 2005). Elle entre dans la production de résines ignifuges utilisées dans le nylon (PISSC, 2003; Calamari et Harper, 1994) et sert d’agent auxiliaire dans l’industrie du textile (BUA, 1995), de fixateur photographique et de détachant des négatifs photographiques (Lewis, 2001; Verschueren, 2001). On l’a aussi utilisée pour l’extraction de l’or et de l’argent par lessivage des minéraux (Laursen, 2002; Morrison, 1983; PISSC, 2003; Yen, 1992).
La thiourée peut aussi servir d'agent auxiliaire dans le papier diazo (papier pour bleus) et d'autres papiers de reproduction (PISSC, 2003), de liquéfiant dans les colles animales (BUA, 1998; O'Neil et al., 2001), d'additif dans les explosifs sous forme de bouillies et d'émulsions (BUA, 1998), d'intermédiaire dans des synthèses organiques, d'agent dans des colorants, de réactif analytique pour les ions bismuth et sélénite, d'agent pour les résines aminiques et d'accélérateur dans la fabrication du caoutchouc et la vulcanisation (Ash et Ash, 1998; Lewis, 2001; Verschueren, 2001; Winter, 2005). La thiourée peut aussi être utilisée comme agent de nettoyage à sec et pour le traitement des chaudières (NTP, 2005), comme inhibiteur de corrosion, comme agent dans des tensioactifs et pour la synthèse de produits pharmaceutiques (Ash et Ash, 1998; Lewis, 2001; Winter, 2005).
La thiourée et ses dérivés figurent maintenant sur la Liste critique des ingrédients dont l'utilisation est restreinte ou interdite dans les cosmétiques (Santé Canada, 2007). Cette substance peut cependant avoir été utilisée comme agent antimicrobien ou l'être encore (dans d'autres pays) et servir d'humectant dans des conditionneurs de la peau (Gottschalck et McEwen, 2004) et dans des préparations capillaires (Lewis, 2001; Winter, 2005).
On en retrouve aussi dans des insecticides (NTP, 2005) et des produits agrochimiques et elle sert d'inhibiteur de moisissures (Ash et Ash, 1998; Lewis, 2001), mais selon l'Agence de réglementation de la lutte antiparasitaire (ARLA), aucun pesticide homologué au Canada ne contient cette substance à titre d'ingrédient actif ou d'agent de formulation (ARLA, 2007a; ARLA, 2007b).
Sur la base des déclarations présentées en vertu de l’article 71 de la LCPE (1999), les rejets industriels de thiourée dans l’air, l’eau et le sol sont jugés négligeables, mais il a été déclaré qu’entre 100 et 1 000 kg de thiourée avaient été transférés dans une installation de traitement des déchets hors site (Environnement Canada, 2007a). Les déchets de fabrication ne devraient pas être une source d’exposition dans l’environnement, car ils sont incinérés, utilisés par l’industrie de la fabrication des briques ou du ciment ou sont éliminés dans des dépotoirs autorisés où le lixiviat est recueilli et réintroduit dans le procédé de traitement (PISSC, 2003). Aux États-Unis, certains déchets contenant de la thiourée sont éliminés par injection dans des puits de classe I (TRI, 2005).
Si l'on fait exception d'un rejet dans l'air en 2002 de 50 kg de thiourée sous forme d'émissions fugitives, il n'y a pas eu depuis 1994 de rejet sur place suffisamment important pour être déclaré à l'Inventaire national des rejets de polluants (INRP, 2007). Il a été noté, entre 1999 et 2002, une augmentation de 12 à 23,55 kg de la quantité déclarée de thiourée expédiée dans des usines de traitement des eaux usées municipales hors site avant l'élimination définitive (INRP, 2007). Il n'a pas été déclaré d'élimination hors site de thiourée depuis 2002. Les propriétés physiques et chimiques et le profil d'utilisation de la thiourée font que celle-ci devrait surtout de se retrouver dans l'eau (PISSC, 2003).
Comme on peut le voir dans le tableau 2, la thiourée a une pression de vapeur se situant entre faible et modérée (1,83 × 10-4 à 2,8 × 10-3 mm Hg) et une solubilité dans l'eau très élevée (91 800 à 142 000 g/L) qui portent à croire que cette substance serait éliminée de l'atmosphère par des dépôts humides. La valeur très faible de la constante de la loi de Henry (1,98 × 10-9atm·m3/mole) et du Log Kco (0,44) de la thiourée fait qu'elle devrait demeurer dans l'eau.
Les résultats de la modélisation de la fugacité de niveau III (tableau 3) montrent que la thiourée devrait surtout se retrouver dans l'eau ou le sol, selon le milieu de rejet.
| Rejet de la substance dans | Fraction de la substance répartie dans chaque milieu (%) |
|||
|---|---|---|---|---|
| Air | Eau | Sol | Sédiments | |
| Air (100 %) | 0,018 | 27,5 | 72,4 | 0,046 |
| Eau (100 %) | 1,7 × 10-8 | 99,8 | 6,8 × 10-5 | 0,17 |
| Sol (100 %) | 4,3 × 10-6 | 21,6 | 78,4 | 0,036 |
Persistance dans l'environnement
D'après ses propriétés physiques et chimiques (tableau 2) et les données empiriques et modélisées sur la dégradation présentées plus bas (tableaux 4a et 4b), la thiourée ne répond pas aux critères de la persistance dans l'eau, le sol et les sédiments (demi-vie dans le sol et l'eau ≥ 182 jours et demi-vie dans les sédiments ≥ 365 jours) énoncés dans le Règlement sur la persistance et la bioaccumulation(Canada, 2000).
| Milieu | Processus du devenir | Valeur pour la dégradation |
Paramètre et unité | Référence |
|---|---|---|---|---|
| Eau | biodégradation | 2,6 | biodégradation, DBO, % (14 jours) |
MITI, 1992 |
| Eau | hydrolyse | 54 750 | demi-vie (jours) | Ellington et al., 1988 |
| Milieu | Processus du devenir | Valeur pour la dégradation |
Paramètre pour la dégradation |
Référence |
|---|---|---|---|---|
| Air | oxydation atm. | 0,25 | demi-vie (jours) | AOPWIN, 2000 |
| Air | réaction avec l'ozone | non réactif | demi-vie (jours) | AOPWIN, 2000 |
| Eau | biodégradation | 15 | demi-vie (jours) | BIOWIN, 2000, Ultimate survey |
| Eau | biodégradation | 0,77 | probabilité | BIOWIN, 2000, MITI Non-linear Probability |
| Eau | biodégradation | 0,61 | probabilité | BIOWIN, 2000, MITI Linear Probability |
| Eau | biodégradation | 1 | probabilité | TOPKAT, 2004 |
| Eau | hydrolyse | n. d.[1] | demi-vie (jours) | HYDROWIN, 2000 |
| Sol | hydrolyse | ≥ 182 jours | demi-vie (jours) | fondé sur la demi-vie modélisée dans l'eau[2] |
| Sédiments | hydrolyse | ≥ 728 jours | demi-vie (jours) | fondé sur la demi-vie modélisée dans l'eau[2] |
[1] Une vitesse d'hydrolyse ne pouvait être estimée pour ce type de composé.
[2] Les valeurs ont été obtenues à partir de la demi-vie modélisée dans l'eau et en appliquant les facteurs d'extrapolation de Boethling et al. (1995), à savoir : t1/2 eau: t1/2 sol : t1/2 sédiments = 1: 1: 4.
Potentiel de bioaccumulation
Comme on ne disposait que de peu de données expérimentales sur le facteur de bioaccumulation (FBA) et le facteur de bioconcentration (FBC) de la thiourée (tableau 5a), une méthode du poids de la preuve fondée sur la relation quantitative structure-activité (RQSA) (Environnement Canada, 2007b) a aussi été appliquée en utilisant les modèles du FBA et du FBC présentés dans le tableau 5b. Selon cette méthode, la thiourée ne satisfait pas au critère de la bioaccumulation (FBC ou FBA ≥ 5 000) du Règlement sur la persistance et la bioaccumulation (Canada, 2000).
| Organisme d'essai | Paramètre | Valeur en L/kg (poids humide) |
Référence |
|---|---|---|---|
| Poisson (carpe) | FBC | 2,0 | MITI, 1992 |
| Poisson (carpe) | FBC | 0,2 | MITI, 1992 |
| Organisme d'essai | Paramètre | Valeur en L/kg (poids humide) |
Référence |
|---|---|---|---|
| Poisson | FBA | 0,93 | Gobas BAF T2MTL Arnot et Gobas, 2003 |
| Poisson | FBC | 9,12 | Gobas BCF T2LTL Arnot et Gobas, 2003 |
| Poisson | FBC | 3,16 | OASIS Forecast, 2005 |
| Poisson | FBC | 0,95 | BCFWIN, 2000 |
La thiourée satisfait aux critères de la persistance dans l'eau, le sol et les sédiments, mais non à celui du potentiel de bioaccumulation, qui sont énoncés dans le Règlement sur la persistance et la bioaccumulation (Canada, 2000).
Des données écotoxicologiques obtenues de façon expérimentale (base de données ECOTOX) indiquent que la thiourée n'a pas d'effets nocifs appréciables chez les organismes aquatiques quand elle est présente en faibles concentrations. Les valeurs de toxicité aiguë obtenues de façon expérimentale se situent dans la gamme des 4,8 à 600 g/L pour les algues et les poissons.
D'après les déclarations présentées en vertu de l'article 71 de la LCPE (1999) (Environnement Canada, 2007a), les rejets industriels de thiourée dans l'air, l'eau et le sol sont jugés négligeables, mais il a été déclaré qu'entre 100 et 1 000 kg de thiourée avaient été transférés dans une installation de traitement des déchets hors site. Depuis 2002, il n'y a pas eu de déclaration d'élimination hors site de thiourée sous l'inventaire national des rejets de polluants (INRP, 2007). Étant donné la quantité et la nature des rejets, il est peu probable qu'ils puissent donner lieu à une exposition appréciable des organismes présents dans l'environnement.
Sur la base des renseignements disponibles, il est peu probable que la thiourée ait des effets écologiques nocifs au Canada.
Évaluation de l'exposition
On n'a pas relevé de concentrations mesurées, tant au Canada qu'ailleurs, permettant d'établir des limites supérieures de l'absorption estimée de thiourée à partir d'un milieu naturel. La seule étude relevée, réalisée au Japon en 1977, portait sur l'analyse de six échantillons d'eau de mer et de six échantillons de sédiments pour la présence de thiourée (PISSC, 2003). La thiourée n'a pas été décelée dans l'eau de mer (seuil de détection de 0,011- 0,4 ug/L) ou les sédiments (seuil de détection de 0,055 et 1 ug/kg) (PISSC, 2003). Cette étude n'a pas été jugée acceptable pour l'estimation des limites supérieures de l'absorption car les échantillons ont été prélevés en mer et les résultats sont relativement anciens. Les renseignements disponibles ne permettaient pas d'estimer de limites supérieures de l'exposition à la thiourée à partir de l'environnement. Par ailleurs, selon les renseignements obtenus en vertu de l'avis émis conformément à l'article 71 de la LCPE (1999) (Environnement Canada, 2007a) et les données de l'Inventaire national des rejets de polluants (INRP, 2007), les rejets dans l'air, l'eau et le sol sont jugés négligeables.
Il existe une possibilité d'exposition de la population générale à la thiourée par l'utilisation de produits de consommation, notamment les produits à polir l'argent, les nettoyants de métaux, les papiers diazo (bleus), les textiles et divers produits pharmaceutiques. On ne dispose pas de suffisamment de données sur les quantités et la fréquence d'utilisation de ces produits pour estimer l'exposition. Des estimations n'ont donc été obtenues que pour l'exposition par inhalation ou par voie cutanée résultant de l'utilisation de produits à polir l'argent ou à nettoyer les métaux et de solutions de virage pour la photographie noir et blanc (annexe 1).
Le modèle ConsExpo (RIVM, 2006) a été appliqué à la prévision de valeurs prudentes de la concentration de thiourée dans l'air résultant de l'utilisation de nettoyants de métaux et de solutions de virage pour la photographie. Le modèle, qui supposait un rejet instantané et la saturation de vapeur, indiquait une dose aiguë de 0,11 mg/kg m.c. par événement, tant pour les nettoyants de métaux que pour la solution de virage. Ce même modèle a été appliqué à une estimation plus fine de l'exposition par inhalation (modèle par évaporation) à partir de ces deux produits en supposant que la totalité de la substance n'était pas émise par le produit au cours de son utilisation. Cela a donné une dose aiguë de 0,002 mg/kg m.c. par événement pour le nettoyant à métaux et de 0,001 mg/kg m.c. par événement pour la solution de virage photographique. Ackermann et Flynn (1987) ont obtenu un coefficient de perméabilité cutanée pour la thiourée (9,6 × 10-5 cm/h) en utilisant de la peau de souris dénudée de poils. Cette valeur est très semblable à la valeur Kp estimée par le modèle DERMWIN (2000) qui prend en compte le coefficient de partage octanol-eau. Si l'on tient compte de la valeur Kp d'Ackermann et Flynn (1987), on trouve que les doses résultant d'un seul événement d'exposition cutanée au nettoyant pour métaux et à la solution de virage sont respectivement de 0,02 et de 0,1 mg/kg m.c.
Le niveau de confiance à l'égard de la base de données sur l'exposition est jugé faible, car on ne disposait pas de données sur les concentrations de thiourée dans les milieux naturels ou les aliments. Par ailleurs, selon les renseignements disponibles, les rejets industriels dans l'environnement sont jugés négligeables. Le niveau de confiance à l'égard de l'estimation de l'exposition à partir des produits de consommation est aussi jugé faible. Selon les renseignements obtenus grâce à l'avis émis en vertu de l'article 71 de la LCPE (1999), les utilisations déclarées de la thiourée se limitaient surtout à des applications industrielles, ce qui ne devrait pas donner lieu à une exposition de la population générale. Par ailleurs, des renseignements obtenus d'autres sources indiquent que la thiourée se retrouve dans divers produits de consommation, mais l'absence de données sur sa concentration dans ces produits, la fréquence d'utilisation et les quantités utilisées interdisent d'obtenir des estimations plus exactes de l'exposition de la population générale.
Évaluation des effets sur la santé
Un aperçu des renseignements toxicologiques est présenté dans l'annexe 2.
La thiourée a été classée par le National Toxicology Program (NTP) comme une substance que l'on peut raisonnablement présumer cancérogène pour les humains (NTP, 2005) et par la Communauté européenne dans la catégorie 3 pour la cancérogénicité (substances préoccupantes pour l'humain en raison d'effets cancérogènes possibles) (Commission européenne, 1998a; ESIS, 2006). Ces classifications sont fondées sur l'observation d'adénomes et de carcinomes de la thyroïde chez des rats mâles et femelles auxquels on avait donné de l'eau contenant 0,25 % de thiourée (350 mg/kg m.c. par jour) pendant une période pouvant atteindre 24 mois (Purves et Griesbach, 1947). Des carcinomes des cellules pavimenteuses de la glande de Zymbal et des glandes de Meibomius ont été observés chez des rats mâles exposés par de l'eau contenant 0,2% de thiourée (280 g/kg m.c. par jour) ou par injection intrapéritonéale suivie d'une exposition par l'eau (0,2 % de thiourée) pendant une période pouvant atteindre 23 mois (Ungar et Rosin, 1957, 1960). L’administration de thiourée dans la diète de rats , à raison de 5 mg/kg de poids corporel par jour pendant 24 mois, a provoqué des adénomes hépatocellulaires (Fitzhugh et Nelson 1948). Une augmentation de l’incidence des tumeurs des glandes mammaires a aussi été signalée chez des souris femelles exposées à la thiourée (0,1 – 0,2 % ou 140 – 280 mg/kg m.c. par jour) dans l’eau potable pendant des périodes pouvant atteindre six mois (Vasquez-Lopez, 1949). Il est à noter que l’évaluation du NTP est fondée sur l’évaluation de la thiourée du Centre international de recherche sur le cancer (CIRC) réalisée en 1974 et qui concluait à l’existence de suffisamment de faits démontrant un effet cancérogène chez les animaux de laboratoire. Le CIRC a conclu, au moment de son évaluation la plus récente, que la thiourée ne pouvait être classée pour sa cancérogénicité (groupe 3) étant donné l’insuffisance de données probantes pour les humains et le peu de données probantes pour les animaux de laboratoire (CIRC, 2001). Aucune étude appropriée chez les humains n’a été signalée sur une relation possible entre l’exposition à la thiourée et le cancer (CIRC, 2001; PISSC, 2003; NTP, 2005).
La thiourée n'a pas fait l'objet d'essais détaillés pour sa génotoxicité in vivo. Des études chezDrosophila ont donné des résultats incertains. L'examen des données sur la génotoxicité in vitromontre que la thiourée n'est pas mutagène chez les bactéries. Les résultats obtenus avec des cellules de mammifères sont variables, mais on note de façon constante des résultats positifs pour la transformation cellulaire et la recombinaison chromosomique chez les levures (CIRC, 2001; PISSC, 2003).
Bien que le mode d'action de cette substance déborde le cadre de la présente évaluation préalable, il est à noter que le PISSC (2003) a indiqué que la thiourée n'était pas considérée comme une substance cancérogène génotoxique et que le développement de tumeurs de la thyroïde provoquées par la thiourée pouvait comporter une inhibition de la peroxydase dans la glande thyroïde qui provoquerait une diminution de la production d'hormones thyroïdiennes et une prolifération résultant d'un accroissement de l'hormone de stimulation de la thyroïde. Mais étant donné le caractère variable des résultats des essais de génotoxicité, il était impossible de tirer une conclusion définitive sur le mode d'action à l'origine de la cancérogénicité (CIRC, 2001; PISSC, 2003).
L'effet pondéral critique non néoplasique se produit dans la thyroïde. La dose minimale avec effet nocif observé, fondée sur une hypertrophie de la thyroïde et une réduction du gain pondéral, était de 27,5 mg/kg m.c. par jour chez des rats exposés par voie orale pendant des périodes pouvant atteindre trois ans (Hartzell, 1942 et 1945). Des effets sur la glande thyroïde ont aussi été observés à la dose de 50 mg/kg m.c. par jour au cours d'études de toxicité subchronique portant sur des moutons mâles (Sokkar et al., 2000) et femelles (Nasseri et Prassad, 1987a), les effets observés étant une hyperplasie de la glande thyroïde chez les mâles, une augmentation du volume de la glande thyroïde et une réduction significative de la T4 sérique chez les femelles. Une réduction des niveaux d'iode dans la glande thyroïde à été déclarée chez des rats ou l'on administrait par voie orale une dose en thiourée de 70 mg/kg m.c par jour pendant 10 jours (Astwooodet al., 1945)
La Commission européenne a aussi classé la thiourée dans la catégorie 3 pour les effets sur la reproduction en se fondant sur un risque possible de dommages pour l'enfant à naître (Commission européenne, 1998a; Commission européenne, 1998b; ESIS, 2006).
Les effets observés sur le développement sont une réduction des concentrations de testostérone, la présence de tubules séminifères petits ou vides et de testicules « mal développés » chez des moutons mâles, et des organes génitaux externes infantiles à développement interrompu de même que l'absence d'œstrus et un développement retardé des glandes mammaires chez les femelles, à la dose de 50 mg/kg m.c. par jour (Sokkar et al., 2000; Nasseri et Prassad, 1987). Les effets sur la reproduction observés chez les moutons mâles et femelles après administration par voie orale comprenaient des testicules « mal développés », des tubules séminifères petits et vides et une réduction non significative de la taille et de la masse des ovaires, des cornes de l'utérus et du vagin (Alavi Shoushtari et Safaii, 1993). L'administration par voie orale de plus de 35 mg/kg m.c. par jour de thiourée à des rats mâles a donné lieu à une réduction ou à l'interruption de la spermatogenèse (Fitzhugh et Nelson, 1948).
Des cas de dermatite par contact après exposition à la thiourée attribuable à l'utilisation de papier de reproduction diazo et d'autres types de papier de reproduction ou de l'utilisation de produit à polir l'argent ont été signalés et certains s'accompagnaient d'une sensibilité au rayonnement (Voir l'annexe 2). On a montré que des dérivés de la thiourée servant d'accélérateurs de réaction dans l'industrie du caoutchouc donnaient lieu à des dermatites par contact de type allergique
Le niveau de confiance à l'égard des renseignements sur la toxicité est jugé de modéré à faible. Il existe des données sur la toxicité aiguë et chronique, la toxicité par doses répétées, la toxicité pour le matériel génétique, la reproduction et le développement et la cancérogénicité, mais il manque d'essais de génotoxicité in vivo et bon nombre des études de la cancérogénicité sont anciennes et ne sont pas conformes aux standards des essais actuels.
Caractérisation du risque pour la santé humaine
À la lumière principalement des évaluations de plusieurs organismes internationaux et nationaux réalisées selon la méthode du poids de la preuve (CIRC, PISSC et NTP), la cancérogénicité constitue un effet critique pour la caractérisation du risque pour la santé humaine que pose la thiourée. Cette substance a provoqué l'apparition de tumeurs dans plusieurs organes de rats mâles et femelles ainsi que dans les glandes mammaires de souris. Comme la thiourée ne semble être que faiblement génotoxique, le PISSC (2003) a émis l'hypothèse qu'elle n'était pas une substance cancérogène génotoxique. Par ailleurs, les modes d'action à l'origine des divers types de tumeurs observés chez des rats et des souris n'ont pas été complètement élucidés et de telles analyses débordent le cadre de la présente évaluation préalable. On ne peut donc exclure la possibilité d'une interaction directe avec le matériel génétique.
En ce qui a trait aux effets autres que le cancer, les données étaient insuffisantes pour quantifier l'exposition à partir de l'environnement général, mais on prévoit qu'elle soit négligeable. Pour caractériser le risque des effets autres que le cancer, on a donc comparé l'exposition estimée par inhalation et par voie cutanée résultant de l'utilisation de produits de consommation, tels des nettoyants pour métaux (0.023 mg/kg m.c. par jour) et une solution de virage photographique (0.11 mg/kg m.c par jour), à la plus faible valeur de toxicité orale par exposition à court terme (DMEO de 70 mg/kg m.c. par jour). Les marges d'exposition (ME) pour le produit à polir l'argent étaient approximativement de 3000; dans le cas de la solution de virage photographique, les marges d'exposition étaient approximativement de 600. Bien qu'établies de façon prudente, ces marges pour les scénarios d'exposition à des produits de consommation pourraient ne pas tenir compte de façon adéquate des incertitudes des bases de données sur l'exposition et les effets, surtout dans le contexte des incertitudes liées au mode ou aux modes d'action à l'origine de la formation des tumeurs ainsi qu'a la variation de la relation entre la toxicité et la durée d'exposition (ex : DMEO pour une exposition a court-terme, subchronique et chronique étaient de 70, 50 et 27,5 mg/kg m.c. par jour, respectivement).
Incertitudes de l'évaluation des risques pour la santé humaine
La présente évaluation préalable réalisée dans le cadre du Défi ne prend pas en compte les écarts possibles entre les humains et les animaux de laboratoire pour ce qui est de la vulnérabilité aux effets de la substance, notamment à cause de l'absence d'études épidémiologiques pertinentes. Les études de la génotoxicité disponibles ne permettent pas de bien comprendre le potentiel de la thiourée de provoquer des dommages génétiques. En outre, le ou les modes d'induction des tumeurs observées chez les rongeurs n'ont pas été complètement élucidés, mais un mode autre que la génotoxicité a été proposé pour les tumeurs thyroïdiennes. Il demeure des incertitudes à l'égard de la quantification de la réponse à l'exposition, car la plus grande partie des données toxicologiques sont passablement anciennes, mais les quantités signalées donnant lieu à un effet se situent généralement dans la même gamme. De plus, les études par doses répétées se limitent à l'administration par voie orale. Des études réalisées par administration par inhalation et par voie cutanée permettraient d'accroître le degré de certitude à l'égard de la base de données.
Les données étaient insuffisantes pour permettre la quantification de l'exposition à la thiourée à partir des milieux naturels au Canada, mais si l'on se fonde sur les renseignements disponibles sur les rejets au Canada, les concentrations dans ces milieux devraient être négligeables. Les estimations de l'exposition à partir de l'utilisation de produits de consommation contenant de la thiourée reposent sur des hypothèses prudentes et pourraient surestimer l'exposition réelle, mais les données disponibles ne permettent pas d'obtenir d'estimations quantitatives de l'apport d'autres produits de consommation à l'exposition de la population générale du Canada.
À D'après les renseignements disponibles, on conclut que la thiourée ne pénètre pas dans l'environnement en une quantité ou concentration ou dans des conditions de nature à avoir, immédiatement ou à long terme, un effet nocif sur l'environnement ou sur la diversité biologique, ni à mettre en danger l'environnement essentiel pour la vie. En outre, la thiourée satisfait au critère de la persistance, mais non à celui du potentiel de bioaccumulation énoncés dans le Règlement sur la persistance et la bioaccumulation.
Compte tenu de la cancérogénicité de la thiourée, pour laquelle il existe une probabilité d'effet nocif à toute valeur d'exposition, et de l'insuffisance possible de la marge de l’exposition pour des effets autres que le cancer, la thiourée est considérée comme une substance pouvant pénétrer dans l'environnement en quantité , à des concentrations ou dans des conditions qui constituent ou peuvent constituer un danger au Canada pour la vie ou la santé humaines.
Il est par conséquent conclu que la thiourée ne répond pas aux critères des paragraphes 64a et 64b de la LCPE (1999), mais qu’elle répond aux critères du paragraphe 64c de la LCPE (1999).
Ackermann, C., et G. Flynn. 1987. Ether-water partitioning and permeability through nude mouse skin in vitro. I. Urea, thiourea, glycerol and glucose. Int. J. Pharm. 36:61-66.
Alavi Shoushrari, S.M. et M. Safaii. 1993. Effects of hypothyroidism on the reproductive system of female lambs. Journal of the Veterinary Faculty of the Univeristy of Tehran 48:40-35 [cité dans PISSC, 2003].
[AOPWIN] Atmospheric Oxidation Program for Windows [Modèle d’estimation]. 2000. Version 1.91. Washington (DC): U.S. Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY): Syracuse Research Corporation. [cité le 30 avril 2007]. Exposure Assessment Tools and Models.
[ARLA] Agence de réglementation de la lutte antiparasitaire. 2007a. Liste des produits de formulation de l’ARLA. Ottawa (Ont.). Santé Canada, Agence de réglementation de la lutte antiparasitaire. [cité le 17 octobre 2007].
[ARLA] Agence de réglementation de la lutte antiparasitaire. 2007b. Base de données de l’ARLA sur les étiquettes des produits[base de données sur Internet]. [cité le 17 octobre 2007].
Arnot, J.A., et F.A. Gobas. 2003. A generic QSAR for assessing the bioaccumulation potential of organic chemicals in aquatic food webs. QSAR Comb Sci[Internet]. [cité le 15 mars 2007]; 22(3): 337-345. [restricted access]
Ash, M., et I. Ash. 1998. Handbook of industrial chemical additives. Volume 2. 2nd Edition. Endicott (NY): Synapse Information Resources. p. 2025.
Astwood, E.B. 1943. The chemical nature of compounds which inhibit the function of the thyroid gland. J. Pharmacol. Exp. Ther. 78:79-89 [cité dans PISSC, 2003].
Astwood, E.B., A. Bissell et A.M. Hughes. 1945. Further studies on the chemical nature of compounds which inhibit the thyroid gland. Endocrinology 37:456-481 [cité dans PISSC, 2003].
Aubrecht, J., R. Rugo, R.H. Schiestl. 1995. Carcinogens induce intrachromosomal recombination in human cells. Carcinogenesis 16:2841-2846 [cité dans CIRC, 2001].
Bartels S., et S. Schauder. 1994. Photoallergic contact dermatitis and persistent light reaction from thiourea in blueprint paper. Aktuelle Derm 20:182–184 [cité dans PISSC, 2003].
Batiste-Alentorn, M., N. Xamena, A. Creus et R. Marcos. 1991. Genotoxicity studies with the unstable zeste-white (UZ) system of Drosophila melanogaster: results with ten carcinogenic compounds. Environ. Mol. Mutagen. 18:120–125 [cité dans CIRC, 2001; PISSC, 2003].
Batiste-Alentorn, M., N. Xamena, A. Creus et R. Marcos. 1994. Further studies with the somatic white-ivory system of Drosophila melanogaster:genotoxicity testing of ten carcinogens. Environ. Mol. Mutagen. 24:143–147 [cité dans CIRC, 2001; PISSC, 2003].
Batiste-Alentorn, M., N. Xamena, A. Creus et R. Marcos. 1995. Genotoxic evaluation of ten carcinogens in the Drosophila melanogaster wing spot test. Experientia 51:73-76 [cité dans CIRC, 2001].
[BCFWIN] BioConcentration Factor Program for Windows [Modèle d’estimation]. 2000. Version 2.15. Washington (DC): U.S. Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY): Syracuse Research Corporation. [cité le 30 avril 2007]. Exposure Assessment Tools and Models
[BIOWIN] Biodegradation Probability Program for Windows [Modèle d’estimation]. 2000. Version 4.02. Washington (DC): U.S. Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY): Syracuse Research Corporation. [cité le 30 avril 2007]. Exposure Assessment Tools and Models
Boethling, R.S., P.H. Howard, J.A. Beauman et M.E. Larosche. 1995. Factors for intermedia extrapolations in biodegradability assessment. Chemosphere. 30 (4): 741-752.
Bradley, M.O., S. Patterson et L.A. Zwelling. 1982. Thiourea prevents cytotoxicity and mutagenicity, but not sister-chromatid exchanges in V79 cells treated with cis-diaminedichloroplatinum(II). Mutat. Res. 96:67-74 [cité dans CIRC, 2001].
Brams, A., J.P. Buchet, M.C. Crutzen-Fayt, C. De Meester, R. Lauwerys et A. Leonard. 1987. A comparative study, with 40 chemicals, of the efficiency of the Salmonella assay and the SOS chromotest (kit procedure). Toxicol. Lett. 38:123-133 [cité dans CIRC, 2001; PISSC, 2003].
[BUA] Beratergremium fur Umwetrelevante Altstoffe (edited by the GDCh-Advisory Committee on Existing Chemicals of Environmental Relevance). 1998. Thiourea. BUA Report 179 (octobre 1995). Stuttgart: S. Hirzel: Wissenschaftliche Verlagsgesellschaft. Report No. 179.
Calamari Jr., T.A., et R.J. Harper Jr.1994. Flame Retardants for Textiles [Internet]. Kirk-Othmer Encyclopedia of Chemical Technology. John Wiley & Sons, Inc. [4 décembre 2000; 19 avril 2007].
Canada. 1999. Loi canadienne sur la protection de l’environnement (1999 ), L.C . 1999, c hap. 33. Gazette du Canada, Partie III, vol. 22, n° 3.
Canada. 2000. Loi canadienne sur la protection de l’environnement : Règlement sur la persistance et la bioaccumulation . C.P. 2000-348, 23 mars 2000, DORS/2000-107. Gazette du Canada, Partie II, vol. 134, n° 7.
Canada, ministère de l’Environnement et ministère de la Santé. 2006. Loi canadienne sur la protection de l’environnement (1999) : Avis d’intention d’élaborer et de mettre en œuvre des mesures d’évaluation et de gestion des risques que certaines substances présentent pour la santé des Canadiens et leur environnement. Gazette du Canada, Partie I, vol. 140, n° 49.
Canada . Ministère de l'Environnement. 2007.Loi canadienne sur la protection de l’environnement (1999) : Avis concernant certaines substances identifiées dans le groupe 2 du Défi. Gazette du Canada, Partie I, vol. 141, n° 19
Casas, C.B., et E. Koppisch. 1952. The thyroid and adrenal glands of the castrated C3H mice treated with thiourea. Endocrinology 51:322-328 [cité dans CIRC, 2001; PISSC, 2003].
[CHEMFATE] Chemical Fate Database [base de données sur Internet]. 2007. Syracuse (NY): Syracuse Research Corporation. [cité le 31 octobre 2007].
Crebelli, R., D. Bellincampi, G. Conti, L. Conti, G. Morpurgo et A. Carere. 1986. A comparative study on selected chemical carcinogens for chromosome malsegregation, mitotic crossing-over and forward mutation induction in Aspergillus nidulans. Mutat. Res. 172:138–149 [cité dans CIRC, 2001; PISSC, 2003].
Dalton, J., H.P. Morris et C.S. Durnik. 1948. Morphologic changes in the organs of female C3H mice after long-term ingestion of thiourea and thiouracil. J. Natl. Cancer Inst. 9:201-223 [cité dans CIRC, 2001; PISSC, 2003].
Deichmann, W.E., M. Keplinger, F. Sala et E. Glass. 1967. Synergism amoung oral carcinogens. IV. The simultaneous feeding of four tumorigens to rats. Toxicol. Appl. Pharmacol. 11:88-103 [cité dans CIRC, 2001; PISSC, 2003].
[DERMWIN] Dermal Permeability Coefficient Program [Modèle d’estimation]. 2000. Version 1.43. Washington (DC): U.S. Environmental Protection Agency. [cité en février 2008]. Exposure Assessment Tools and Models.
Dieke SH. Allen G.S., Richter C.P., 1947. The acute toxicity of thioureas and related compounds to wild and domestic Norway rats. J Pharmacol Exp Ther 90: 260-270. [cité en tant que Dieke, 1947 dans MAK, 1991].
Dooms-Goossens, A., M.T. Chrispeels, H. de Veylder, R. Roelandts, L. Willems et H. Degreef. 1987. Contact and photocontact sensitivity problems associated with thiourea and its derivatives: a review of the literature and case reports. Br. J. Derm. 116:573–579 [cité dans PISSC, 2003].
Dooms-Goossens, A., K. Debusschere, M. Morren, R. Roelandts et S. Coopman. 1988. Silver polish: another source of contact dermatitis reactions to thiourea. Contact Dermatitis 19:133–135 [cité dans CIRC, 2001; PISSC, 2003].
Dunkel, V.C., R.J. Pienta, A. Sivak et K.A. Traul. 1981. Comparative neoplastic transforation responses of Balb/3T3 cells, Syrian hamster embryo cells, and Rauscher murine leukemia virus-infected Fischer rat embryo cells to chemical carcinogens. J. Natl. Cancer Inst. 67:1303-1315 [cité dans CIRC, 2001].
Dunkel, V.C., E. Zeiger, D. Brusick, E. McCoy, D. McGregor, K. Mortelmans, H.S. Rosenkranz et V.F. Simmon. 1984. Reproducibility of microbial mutagenicity assays. I. Tests with Salmonella typhimurium and Escherichia coli using standardized protocol. Environ. Mutag. 6(Supp. 2):1-252 [cité dans CIRC, 2001].
[ECOTOX] ECOTOXicology Database[base de données sur Internet]. 2006. Washington (DC): U.S. Environmental Protection Agency, Office ofResearch and Development; U.S. Environmental Protection Agency, National Health and Environmental Effects Research Laboratory's, Mid-Continent Ecology Division. [cité Mar, 2006].
Egilsson, V., I.H. Evans et D. Wilkie. 1979. Toxic and mutagenic effects of carcinogens on the mitochondria of Saccharomyces cerevisiae. Mol. Gen. Genet. 174:39-46 [cité dans CIRC, 2001].
Ellington, J.J., F.E. Stancil, W.D. Payne et C.D. Trusty. 1988. Measurement of hydrolysis rate constants for evaluation of hazardous waste land disposal: Volume 3. Data on 70 Chemicals. NTISPB88-234 042/AS; EPA/600/S3-88/028.
Environnement Canada. 2007 a. Données pour certaines substances recueillies en vertu de la Loi canadienne sur la protection de l’environnement, 1999, article 71 : Avis concernant certaines substances identifiées dans le groupe 2 du Défi. Préparé par : Environnement Canada, Programme des substances existantes.
Environnement Canada. (2007b). QSARs: Reviewed Draft Working Document, Science Resource Technical Series, Guidance for Conducting Ecological Assessments under CEPA 1999. Gatineau (QC) : Division des substances existantes, Environnement Canada, Document provisoire interne disponible sur demande.
[EQC] [Estimation Model]. 2003. Version : Peterborough (Ont.) : Université Trent, The Canadian Centre for Environmental Modelling and Chemistry - TaPL3. [2008 Feb 14 ].
[ESIS] European Chemical Substances Information System [base de données sur Internet]. 2006. Thiourea. CAS No. 62-56-6. Version 4.50. Bureau européen des substances chimiques (BESC).
Commission européenne. 1998a. Thiourea. Summary Record Meeting of the Commission Working Group on the Classification and Labelling of Dangerous Substances. ECB Ispra 1-3 juillet 1998. ECBI/27/98 – Rev.2.17.12.
Commission européenne. 1998b. Thiourée. Directive de la Commission 98/98/EC du 15 décembre 1998. Annexe 1A. Journal officiel des Communautés européennes 30.12.1998.
Fautz, R., R. Forster, C.M.A. Hechenberger, W. von der Hude, G. Kaufmann, H. Madle, S. Madle, H.G. Miltenberger, L. Mueller, B.L. Pool-Zobel, E.C. Puri, P. Schmezer, A.H. Seeberg, R. Strobel, W. Suter et M. Baumeister. 1991. Report of a comparative study of DNA damage and repair assays in primary rat hepatocytes with five coded chemicals. Mutat. Res. 260:281–294 [cité dans CIRC. 2001; PISSC, 2003].
Fitzhugh, O.G., et A.A. Nelson. 1948. Liver tumors in rats fed thiourea or thioacetamide. Science 108: 626-628 [cité dans CIRC, 2001; PISSC, 2003].
Fritzenschaf, K., M. Kohlpoth, B. Rusche et D. Schiffmann 1993. Testing of known carcinogens and noncarcinogens in the Syrian hamster embryo (SHE) micronucleus test in vitro; correlations with in vivo micronucleus formation and cell transformation. Mutat. Res. 319:47-53 [cité dans CIRC, 2001].
Galli, A., et R.H. Schiestl. 1995. Salmonella test positive and negative carcinogens show different effects on intrachromosomal recombination in G2 cell cycle arrested yeast cell. Carcinogenesis 16:659-663 [cité dans CIRC, 2001].
Galli, A., et R.H. Schiestl. 1996. Effects of Salmonella assay negative and positive carcinogens on intrachromosomal recombination in G1-arrested yeast cells. Mutat. Res. 370:209–221 [cité dans CIRC, 2001; PISSC, 2003].
Galli, A., et R.H. Schiestl. 1998. Effect of Salmonella assay negative and positive carcinogens on intrachromosomal recombination in S-phase arrested yeast cells. Mutat. Res. 419:53-68 [cité dans CIRC, 2001].
Gargus, J.L., O.E. Paynter et W.H. Reese. 1969. Utilization of newborn mice in the bioassay of chemical carcinogens. Toxicol. Appl. Pharmacol. 15:552 [cité dans PISSC, 2003].
Gaudreault, R.A. 2007. Material Safety Data Sheet: Tarn-X Tarnish Remover. Skokie (IL): Jelmar. [Internet]. [2 novembre 2007].
Geier, J., et T. Fuchs.1993. Contact allergy due to 4-N,N-dimethylaminobenzene diazonium chloride and thiourea in diazo copy paper. Contact Dermatitis, 28:304–305 [cité dans PISSC, 2003].
Gorbman, A. 1947. Thyroidal and vascular changes in mice following chronic treatment with goitrogens and carcinogens. Cancer Res. 7: 746-758 [cité dans CIRC, 2001; PISSC, 2003].
Gottschalack, T.E. et G.N. McEwen, editors. 2004. International cosmetic ingredient dictionary and handbook. Volume 3. 10th Edition. Washington (DC): Cosmetic, Toiletry, and Fragrance Association. p. 1888.
Hartzell, A. 1942. Adult life span animal feeding experiments with thiourea (thioucarbamide). Contributions from the Boyce Thompson Institute 12:471-480 [cité dans PISSC, 2003].
Hartzell, A. 1945. Thiourea (thiocarbamide): adult life span animal feeding experiments with rats. Contributions from the Boyce Thompson Institute 13:501-513 [cité dans PISSC, 2003].
Hayes, S., A. Gordon, I. Sadowski et C. Hayes. 1984. RK bacterial test for independently measuring chemical toxicity and mutagenicity: short termforward selection assay. Mutat. Res. 130:97-106 [cité dans CIRC, 2001].
Hazelton. 1987. 13-week drinking water study in rats with thiourea. Hazelton Laboratories America Inc. for SKW Trostberg AC, Trostberg, p. 1-360 (HLA Study No. 2319-119) [cité dans PISSC, 2003].
Helleday, T., C. Arnaudeau et D. Jenssen. 1998. Effects of carcinogenic agents upon different mechanism for intragenic recombination in mammalian cells. Carcinogenesis. 19:973-978 [cité dans CIRC, 2001].
Hellmér, L., et G. Bolcsfoldi. 1992. An evaluation of theE. coli K-12 uvrB/recA DNA repair host-mediated assay. I. In vitro sensitivity of the bacteria to 61 compounds. Mutat. Res. 272:145-160 [cité dans CIRC, 2001; PISSC, 2003].
Hine, J., et P.K. Mookerjee. 1975. Structural effects on rates and equilibriums. XIX. Intrinsic hydrophilic character of organic compounds. Correlations in terms of structural contributions. Journal of Organic Chemistry, 40: 292-8.
[HPD] Household Products Database [base de données sur Internet]. 2005. Bethesda (MD): National Library of Medicine (US). [révisé le 12 mai 2005; cité le 13 octobre 2006].
Hosein, A.G. 2005. Material Safety Data Sheet: Liquid Rust Remover. Mississauga (Ont.). Dominion Sure Seal Ltd. [Internet]. [cité en septembre 2007].
[HYDROWIN] Hydrolysis Rates Program for Microsoft Windows [Modèle d’estimation]. 2000. Version 1.67. Washington (DC): U.S. Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY): Syracuse Research Corporation. [cité le 30 avril 2007]. Exposure Assessment Tools and Models
[CIRC] IARC Working Group on the Evaluation of Carcinogenic Risks to Humans. 2004. Some thyrotropic agents: Thiourea. IARC Monogr. Eval. Carcinog. Risks Hum. 79:703-725.
ISHOW ] Information System for Hazardous Organics in Water . 1992. Computerized database developed by U.S. EPA and University of Minnesota, Duluth)
[INRP] Inventaire national des rejets de polluants [base de données sur Internet]. 2005. Gatineau (Qc) : Environnement Canada. [cité le 10 octobre 2007].
[INRP] Inventaire national des rejets de polluants [base de données sur Internet]. 2007. Gatineau (Qc) : Environnement Canada. [Cité le 10 octobre 2007].
Japon, Gouvernement du Japon, Ministère de l’Environnement. 2004. Chemicals in the environment. Surveyed chemical substances and their detected levels in the environment (A cumulative list for fiscal year 1974-2003)[Internet]. [Cité en octobre 2007].
Jiang, Z., et al. 1989. Genotoxicity of 23 chemicals to S. cerevisiae. Environ. Mol. Mutagen. 14(Suppl. 15):95 [cité dans PISSC, 2003].
Jones, R.P. 1946. Studies on the effect of thiourea and allied substances on the thyroid gland and other organs in rats and mice. J. Pathol. Bacteriol. 58:483 [cité dans PISSC, 2003].
Kanerva, L., T. Estlander et R. Jolanki. 1994. Occupational allergic contact dermatitis caused by thiourea compounds. Contact Dermatitis 31(4):242–248 [cité dans PISSC, 2003].
Kanerva, L., T. Estlander et R. Jolanki. 2000. Occupational allergic contact dermatitis from trichlorozincates of 4-(dimethylamino)-benzendiazonium (Diazo A) and 3-methyl-4-(pyrrolidin-1-yl)-benzenediazonium (Diazo Y) and thiourea in diazo copy paper.
Contact Dermatitis 43(3):170–171 [cité dans PISSC, 2003].
Kellett, J.K., M.H. Beck et G. Auckland. 1984. Contact sensitivity to thiourea in photocopy paper. Contact Dermatitis 11:124 [cité dans PISSC, 2003].
Kern, M., Z. Tatar-Kiss, P. Kertai et I. Foldes. 1980. Teratogenic effect of 2’-thiourea in the rat. Acta Morphol. Acad. Sci. Hung. 18:259-267 [cité dans CIRC, 2001; PISSC, 2003].
Keston, A.S., E.D. Goldsmith, A.S. Gordon et H.A. Charipper. 1944. The effect of thiourea upon the metabolism of iodine by rat thyroid. J. Biol. Ch. 152:241-244 [cité dans PISSC, 2003].
Kevekordes, S., V. Mersch-Sundermann, C.M. Burghaus, J. Spielberger, H.H. Schmeiser, V.M. Arlt et H. Dunkelberg. 1999. SOS induction of selected naturally occuring substances inEscherichia coli (SOS induction chromo test). Mutat. Res. 445:81-91 [cité dans CIRC, 2001].
Kowalski, L.A., A.M. Laitinen, B. Mortazavi-Asl, R.K.-H. Wee, H.E. Erb, K.P. Assi et Z. Madden. 2000. In vitro determination of carcinogenicity of sixty-four compounds using a bovine papillomavirius DNA-carrying C3H/10T1/2 cell line. Environ. Mol. Mutag. 35:300-311 [cité dans CIRC, 2001].
Laursen, J. 2002. Cleaning materials and polishes for metal. Survey of chemical substances in consumer products [Internet]. Survey no. 16. Denmark: Danish Ministry of Environment. [2002; 17 octobre 2007].
Lewis RJ Sr. 2001. Hawley’s Condensed Chemical Dictionary. 14e édition. New York (NY): Wiley. p. 1098.
Liden, C. 1984. Contact allergy to the photographic chemical PBA-1. Contact Dermatitis 11:156 [cité dans PISSC, 2003].
Lonati-Galligani, M., P.H.M. Lohman et F. Berends. 1983. The validity of the autoradiographic method for detecting DNA repair synthesis in rat hepatocytes in primary culture. Mutat. Res. 113:145–160 [cité dans CIRC, 2001; PISSC, 2003].
Mackay, D., W.Y. Shiu, K.-C. Ma et S.L. Lee. 2006. Handbook of physical-chemical properties and environmental fate for organic chemicals. Volume 4. 2nd Edition. Boca Raton (FL): CRC/Taylor & Francis. p. 3423.
MacKenzie, C.G., et J.B. MacKenzie. 1943. Effect of sulfonamides and thioureas on the thyroid gland and basal metabolism. Endocrinology 32:185-209 [cité dans PISSC, 2003].
MAK. 1988. Thiourea. In: Henschler D, ed. Occupational toxicants: Critical data evaluation for MAK values and classification of carcinogens. Volume 1. Deutsche Forschungsgemeinschaft (DFG); Commission for the Investigation of Health Hazards of Chemical Compounds in the Work Area (MAK Commission). Weinheim, VCH, Verlagsgesellschaft mbH, p. 301–312 [cité dans PISSC, 2003].
MAK. 1991. Thiourea. In: Henschler D, ed. Occupational toxicants: Critical data evaluation for MAK values and classification of carcinogens. Volume 1. Deutsche Forschungsgemeinschaft (DFG); Commission for the Investigation of Health Hazards of Chemical Compounds in the Work Area (MAK Commission). Weinheim, VCH, Verlagsgesellschaft mbH, p. 301–314 [cité dans PISSC, 2003].
Malcom, J., W. Griesbach et F. Bielschowsky. 1949. Hyperplasia of the parathyroids associated with osteitis fivrosa in rats treated with thioureacil and related compounds. Br. J. Exp. Pathol. 30:17 [cité dans PISSC, 2003].
Mamber, S.W., V. Bryson et S.E. Katz. 1984. Evaluation of the Escherichia coli K12 inductest for detection of potential chemical carcinogens. Mutat. Res. 130:141-151 [cité dans CIRC, 2001].
McCarroll, N.E., C.E. Piper et B.H. Keech. 1981. An E. Coli microsuspension assay for the detection of DNA damage induced by direct-acting agents and promutagens. Environ. Mutag. 3:429-444 [cité dans CIRC, 2001].
McCleskey, P.E., et R.A. Swerlick. 2001. Clinical review: thioureas and allergic contact dermatitis. Cutis 68(6):387–396 [cité dans PISSC, 2003].
Milleman, R.E., et D.S. Ehrenberg. 1982. Chronic toxicity of the azaarene quinoline, a synthetic fuel component, to the pond snailPhysa gyrina. Environ. Technol. Lett. 3(5): 193- 8.
[MITI] Ministry of International Trade & Industry (Jpn), Basic Industries Bureau, Chemical Products Safety Division. 1992. Biodegradation and bioaccumulation data of existing chemicals based on the CSCL Japan. Tokyo (Jpn): Japan Chemical Industry Ecology-Toxicology & Information Centre.
Mitchell, A.D., C.J. Rudd et W.J. Caspary. 1988. Evaluation of the L5178Y mouse lymphoma cell mutagenesis assay: Intralaboratory results for sixty-three coded chemicals tested at SRI International. Environ. Mol. Mutag. 12(Suppl. 13):37-101 [cité dans CIRC, 2001].
Morris, H.P., A. Dubnik et A. Dalton. 1946. Effect of prolonged ingestion of thiourea on mammary glands and the appearance of mammary tumors in adult C3H mice. J. Natl. Cancer Inst. 7:159 [cité dans PISSC, 2003].
Morrison, R.M. 1983. Thiourea leaching of silver-bearing materials I. Literature survey. Ottawa (Ont.). Centre canadien de la technologie des minéraux et de l'énergie. Énergie, Mines et Ressources Canada. Rapport no : MRP-3.4.0.3.10.
Morita, T., Y. Iwamoto, T. Shimizu, T. Masuzawa et Y. Yanagihara. 1989. Mutagenicity tests with a permeable mutant of yeast on carcinogens showing false-negative in the Salmonella assay. Chem. Pharm. Bull. 37:407–409 [cité dans CIRC, 2001; PISSC, 2003].
[MPBPWIN] Melting Point Boiling Point Program for Microsoft Windows [Modèle d’estimation]. 2000. Version 1.41. Washington (DC): U.S. Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY): Syracuse Research Corporation. [cité le 30 avril 2007]. Exposure Assessment Tools and Models
Myhr, B.C., et W.J. Caspary. 1988. Evaluation of the L5178Y mouse lymphoma cell mutagenesis assay: Intralaboratory results for sixty-three coded chemicals tested at Litton Bionetics, Inc. Environ. Mol. Mutag. 12 (Suppl. 13): 103-194 [cité dans CIRC, 2001].
Nakamura, S., Y. Oda, T. Shimada, I. Oki et K. Sugimoto. 1987. SOS-inducing activity of chemical carcinogens and mutagens in Salmonella typhimurium TA1535/pSK1002: Examination with 151 chemicals. Mutat. Res. 192:239–246 [cité dans CIRC, 2001; PISSC, 2003].
Nasseri, A.A., et M.C. Prassad. 1987a. Experimental hydrothyroidism in lambs: clinicobiochemical studies. Indian J. Anim. Sci. 57:383-387 [cité dans PISSC, 2003].
Nasseri, A.A., et M.C. Prassad. 1987b. Effects of hypothyroidism on reproductive behaviour in female sheep: clinical studies. Indian Vet. J. 11:191-199 [cité dans PISSC, 2003].
Niinimäki, A. 1989. Photocontact allergy from photocopy paper: a report of two cases. In: Frosch PJ, Dooms-Goossens A, Lachapelle J-M, Rycroft RJG, Scheper RJ, eds. Current topics in contact dermatitis. Berlin, Springer 507–509.
[INRP] Inventaire national des rejets de polluants [base de données sur Internet]. 2007. Gatineau (QC): Environnement Canada. [cité le 10 octobre 2007].
National Toxicology Program (NTP); 2005. Report on Carcinogens. 11e édition. Substance Profile: Thiourea [Internet]. Research Triangle Park (NC): National Toxicology Program. [Consulté en décembre 2006].
Nurse, D. 1980. Sensitivity to thiourea in plain printing paper. Contact Dermatitis 6:153-154 [cité dans PISSC, 2003].
[OASIS Forecast] Optimized Approach based on Structural Indices Set [Internet]. Version 1.20 Bourgas (BG ) : Bourgas Prof. Assen Zlatarov University, Laboratory of Mathematical Chemistry.
[cited 2007 Apr 30]. OASIS Software.
O’Neil, M.J., et. al., editors. 2001. The Merck Index, 13th Edition. Whitehouse Station (NJ): Merck & Co., Inc. p. 1670.
Painter, R.B. 1977. Rapid test to detect agents that damage human DNA. Nature 265:650 [cité dans PISSC, 2003].
Pasche-Koo, F., et E. Grosshans. 1991. Contact dermatitis from thiourea. Nouvelles dermatologiques 10:694–696 [cité dans PISSC, 2003].
[PCKOCWIN] Organic Carbon Partition Coefficient Program for Windows [Modèle d’estimation]. 2000. Version 1.66. Washington (DC): U.S. Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY): Syracuse Research Corporation. [cité le 30 avril 2007]. Exposure Assessment Tools and Models
Photographers’ Formulary Inc. 2006. Formulary Thiourea Toner Bleach and Redevelopment [Internet]. [cité en février 2008].
[PhysProp] Interactive PhysProp Database [base de données sur Internet]. 2003. Syracuse (NY): Syracuse Research Corporation. [cité en mars 2006].
Pienta, R.J., J.A. Poiley et W.B. Lebherz III. 1977. Morphological transformation of early passage golden Syrian hamster embryo cells derived from cryopresserved primary cultures as a reliable in vitro bioassay for identifying diverse carcinogens. Int. J. Cancer 19:642-655 [cité dans CIRC, 2001].
[PISSC] Programme international sur la sécurité des substances chimiques. 2003. Thiourea. Geneva (CH): World Health Organization. (Concise International Chemical Assessment Document 49). Publication parrainée conjointement par le Programme des Nations Unies pour l’environnement, l’Organisation internationale du travail et l’Organisation mondiale de la santé et produite dans le cadre du Programme inter-organisations pour la gestion écologiquement rationnelle des produits chimiques.
Purves, H.D., et W.E.Griesbach. 1947. Studies on experimental goitre. VIII: Thyroid tumors in rats treated with thiourea. J. Exp. Pathol. 28:46 [cité dans CIRC, 2001; PISSC, 2003].
Raffaelli, A., S. Pucci, R. Lazzaroni et P. Salvadori. 1997. Rapid determination of thiourea in waste water by atmospheric pressure chemical ionization tandem mass spectrometry using selected-reaction monitoring. Rapid Communications in Mass Spectrometry 11(3): 259 – 264.
Randomski, J.L., W.B. Deichmann, W.E. MacDonald et E.M. Glass. 1965. Synergism amoung oral carcinogens. I. Results of the simultaneous feeding of four tumorigens to rats. Toxicol. Appl. Pharmacol. 7:652-656 [cité dans CIRC, 2001; PISSC, 2003].
[RIVM] Rijksinstituut voor Volksgezondheid en Milieu. 2006a. Consumer Exposure (ConsExpo 4.1) Model [Internet]. Version 4.1. The Netherlands: The National Institute for Public Health and the Environment (Rijksinstituut voor Volksgezondheid en Milieu).
[RIVM] Rijksinstituut voor Volksgezondheid en Milieu. 2006b. Cleaning Products Fact Sheet: To assess the risks for the consumer [Internet]. Report 320104003/2006. Bilthoven: RIVM. [cité en janvier 2008].
Rodrigues-Arnaiz, R. 1997. Genotoxic activation of hydrazine, two dialkylhydrazines, thiourea and ethylene thiourea in the somatic w/w+ assay of Drosphila melanogaster. Mutat. Res. 395:229-242 [cité dans CIRC, 2001].
Rosenkranz, H.S., et L.A. Poirier. 1979. Evaluation of the mutagenicity and DNA-modifying activity of carcinogens and noncarcinogens in microbial systems. J. Natl. Cancer Inst. 62: 873-892 [cité dans CIRC, 2001].
Rosin, A., et M. Rachmilewitz. 1954. The development of malignant tumors of the face in rats after prolonged treatment with thiourea. Cancer Res. 274:494-496 [cité dans PISSC, 2003].
Rosin, A., et H. Ungar. 1957. Malignant tumors in the eyelids and the auricular region of thiourea-treated rats. Cancer Res. 17:302-305 [cité dans CIRC, 2001; PISSC, 2003].
Ruddick, J.A., W.H. Newsome et L. Nash 1976. Correlation of teratogenicity and molecular structure: ethylenethiourea and related compounds. Teratology 13:263-266 [cité dans PISSC, 2003].
Santé Canada. 1998. Exposure factors for assessing total daily intake of priority substances by the general population of Canada. Rapport inédit. Ottawa (Ont.). Santé Canada, Direction de l’hygiène du milieu.
Santé Canada. 2007. Liste critique des ingrédients dont l'utilisation est restreinte ou interdite dans les cosmétiques (« liste critique ») - mars 2007 [Internet]. Ottawa (Ont.). Santé Canada, Sécurité des produits de consommation. [cité le 17 octobre 2007].
Sax, N.I. 1984. Dangerous properties of industrial materials. 6th Edition. New York (NY): Van Nostrand Reinhold Co.
Schiestl, R.H. 1989. Nonmutagenic carcinogens induce intrachromosomal recombination in yeast. Nature 337:285–288 [cité dans CIRC, 2001; PISSC, 2003].
Schiestl, R.H., R.D. Gietz, R.D. Mehta et P.J. Hastings. 1989. Carcinogens induce intra-chromosomal recombination in yeast. Carcinogenesis 10: 1445-1455 [cité dans CIRC, 2001].
Simmon, V.F. 1979a. In vitro mutagenicity assay of chemical carcinogens and related compounds with Salmonella typhimurium. J. Natl. Cancer Inst. 62:893-899 [cité dans CIRC, 2001].
Simmon, V.F. 1979b. In vitro assay for recombinogenic activity of chemical carcinogens and related compounds with Saccharomyces cerevisiae D3. J. Natl. Cancer Inst. 62:901-902 [cité dans CIRC, 2001].
Sina, J.F., C.L. Bean, G.L. Dysart, V.I. Taylor et M.O. Bradley. 1983. Evaluation of the alkaline elution/rat hepatocyte assay as a predictor of carcinogenic/mutagenic potential. Mutat. Res. 113:357–391 [cité dans CIRC, 2001; PISSC, 2003].
Smith, C.C. 1950. A short term chronic toxicity test. J. Pharmacol. Exp. Ther. 100:408-420 [cité dans PISSC, 2003].
Sokkar, S., A. Soror, Y. Ahmed, O. Ezzo et M. Hamouda. 2000. Pathological and biochemical studies on experimental hypothyroidism in growing lambs. Journal of Veterinary Medicine, Series B 47(9):641-652 [cité dans PISSC, 2003].
Teramoto, S., M. Kaneda, H. Aoyama et Y. Shiramu,1981. Correlation between the molecular structure of N-alkylureas adn N-alkylthioureas and their teratogenic properties. Teratology 23:335 [cité dans PISSC, 2003].
TNO. 1978. Acute dermal toxicity study with the product “Thioharnstoff” in albino rabbits. Central Institute for Nutrition and Food Research, Netherlands, for SKW Trostberg AG, Trostberg, 8 p. (Report No. R 5693) [cité dans PISSC, 2003].
TNO. 1979a Acute inhalation toxicity study of a 10% aqueous solution of « Thioharnstoff » with rats. Central Institute for Nutrition and Food Research, Netherlands, for SKW Trostberg AG, Trostberg, 5 p. (Report No. R 6264) [cité dans PISSC, 2003].
TNO. 1979b Evaluation of “Kalkstickstoff” and “Thioharnstoff” in the micronucleus test. Central Institute for Nutrition and Food Research, Netherlands, for SKW Trostberg AG, Trostberg (Report No. R 6012) [cité dans PISSC, 2003].
[TOPKAT] Toxicity Prediction Program [Internet]. 2004. Version 6.2. San Diego (CA): Accelrys Software Inc. [cité le 30 avril 2007].
Torres, V., J. Campos Lopes, L. Lobo et A. Pinto Soares. 1992. Occupational contact dermatitis to thiourea and dimethylthiourea from diazo copy paper. Am. J. Contact Dermat. 3:37–39 [cité dans PISSC, 2003].
[TRI] Toxic Release Inventory Program [Internet]. 2005. Washington (DC): US Environmental Protection Agency.
Ungar, H., et A. Rosin. 1960. The histogenesis of thiourea-induced carcinoma of the auditory duct sebaceous (Zymbal’s) glands in rats. Arch. De Vecchi. Anat. Patol. 31:419 [cité dans CIRC, 2001; PISSC, 2003].
Univar . 2007. Univar Canada Ltd. Composites, plastics & rubber industry: Raw materials for rubber [Internet]. [Cité le 17 mars 2008].
[US EPA] US Environmental Protection Agency. 1986. Standard scenarios for estimating exposure to chemical substances during use of consumer products, vol 1. Washington (DC): prepared for the US EPA, Office of Toxic Substances, Exposure Evaluation Division, by Versar, Inc. Contract no. 68-02-3968.
Van der Leun, J., E. De Kreek, H. Deenstra-van Leeuwen et H. van Weelden. 1977. Photosensitivity owing to thiourea. Arch. of Dermatol. 113:1611 [cité dans PISSC, 2003].
Van Gerwen H.J.L., Alkemade J.A.C., van der Valk P.G.M.. 1996. Photocontact allergy to thiourea as a component of photocopy paper: photocontact eczema of “airborne allergic contact dermatitis”. Nederlands Tijdschrift voor Dermatologie en Venereologie 6: 194-195 [En Hollandais, cité dans PISSC, 2003].
E. Vasquez-Lopez. 1949. The effects of thiourea on the development of spontaneous tumours on mice. Br. J. Cancer Research, 3:401 [cité dans CIRC, 2001; PISSC, 2003].
Verschueren, K. 2001. Handbook of Environmental Data on Organic Chemicals. Volume 2. 4th Edition. New York: Wiley. p.1997.
Vogel, E.W., et M.J.M. Nivard. 1993. Performance of 181 chemicals in a Drosophila assay predominantly monitoring interchromosomal mitotic recombination. Mutagenesis, 8:57–81 [cité dans CIRC, 2001; PISSC, 2003].
Wangenheim, J., et G. Bolcsfoldi. 1988. Mouse lymphoma L5178Y thymidine kinase locus assay of 50 compounds. Mutagenesis, 3:193–205 [cité dans CIRC, 2001; PISSC, 2003].
Wilkie, D., et S. Gooneskera. 1980. The yeast mitochondrial system in carcinogen testing. Chem. Ind. 21:847-850 [cité dans CIRC, 2001].
Winter R. 2005. A consumer’s dictionary of cosmetic ingredients: complete information about the harmful and desirable ingredients found in cosmetics and cosmeceuticals. 6e édition. New York (NY): Three Rivers Press. p. 516.
Yamaguchi, T. 1980. Mutagenicity of isothiocyanates, isocyanates and thioureas on Salmonella typhimurium. Agric. Biol. Chem. 44:3017–3018 [cité dans CIRC, 2001; PISSC, 2003].
Yen, W.T. 1992. Gold and silver elution from carbon loaded in thiourea leach solution. Rapport final. Kingston (Ont.). Ministère du Génie minier, Université Queen’s. No de contrat : 23440-0-9154/01-SS.
Zeiger, E., B. Anderson, S. Haworth, T. Lawlor et K. Mortelmans. 1988. Salmonella mutagenicity tests. IV. Results from the testing of 300 chemicals. Environ. Mol. Mutag. 11: (Suppl. 12)1-158 [cité dans CIRC, 2001].
Ziegler-Skylakakis, K., S. Nill, J.F. Pan et U. Andrae. 1998. S-Oxygenation of thiourea results in the formation of genotoxic products. Environ. Mol. Mutag. 31:362-373 [cité dans CIRC, 2001; PISSC, 2003].
Ziegler-Skylakakis, K., S. Rossberger et U. Andrae. 1985. Thiourea induces DNA repair synthesis in primary rat hepatocyte cultures and gene mutations in V79 Chinese hamster cells. Arch. Toxicol. 58:5-9 [cité dans CIRC, 2001; PISSC, 2003].
| Scénario d'exposition aux produits de consommation | Hypothèse | Exposition estimée |
|---|---|---|
| Produit à polir l'argent[1] | Inhalation (évaporation)
|
Concentration moyenne par événement = 0,204 Dose aiguë = 0,0019 mg/kg m.c. |
| Produit à polir l'argent[1] | Voie cutanée[2]
Dose estimée par événement
|
Dose estimée = 0,021 mg/kg m.c. par événement (par heure) |
| Tirage photographique (noir et blanc; virage sépia)[1] |
Inhalation (évaporation)
|
Concentration moyenne par événement = 0,144 Dose aiguë = 0,0014 |
| Tirage photographique (noir et blanc; virage sépia)[1] |
Voie cutanée
|
Dose aiguë = 0,11 mg/kg m.c. par événement |
[1]Possibilité d'exposition des adolescents (12-19 ans), des adultes (20-59 ans) et des personnes âgées (60 ans et plus), mais comme ces produits sont surtout utilisés par des adultes (20-59 ans), l'estimation de l'exposition s'est limitée à ce groupe d'âge.
[2] Les scénarios par voie cutanée ont aussi étés obtenus en utilisant le modèle ConsExpo, version 4.1. Des résultats similaires à ceux présentés ci-haut ont étés obtenus.
| Paramètre | Dose minimale produisant un effet - résultats |
|---|---|
| Toxicité aiguë | Plus faible DL50par voie orale (rat) = 125 mg/kg m.c. (Dieke, 1947) Plus faible CL50 par inhalation (rat) > 195g/m3 (TNO, 1979a) Plus faible DL50 par voie cutanée(lapin) > 2 500 mg/kg m.c. (TNO, 1978) |
| Toxicité à court terme par doses répétées | Plus faible DMEO par voie orale(rat) = 70 mg/kg m.c. par jour fondée sur la réduction de la concentration d'iode dans la glande thyroïde après 10 jours d'exposition (Astwood et al ., 1945) [Note : Une légère augmentation de la masse de la thyroïde a été observée chez des rats ayant reçu une dose plus faible (25 mg/kg m.c. par jour), mais aucune analyse statistique n'a été présentée. MacKenzie et MacKenzie, 1943] [Autres études : Astwood, 1943; Smith, 1950; Keston, 1944; MAK, 1988; Jones, 1946; Malcom et al ., 1949] Exposition par inhalation Aucune étude n'a été relevée. |
| Toxicité subchronique | Plus faible DMEO par voie orale (mouton) = 50 mg/kg m.c. par jour fondée sur une réduction significative de la masse corporelle, du nombre d'érythrocytes et de leucocytes et des concentrations de T3 et de testostérone, sur un mauvais développement des testicules et sur la présence de tubules séminifères petits et vides après administration quotidienne de la substance pendant 3,5 mois (Sokkaret al., 2000) [Autres études : Morris, 1946; Malcolm et al., 1949; Hazelton, 1987; Nasseri et Prassad, 1987a; Sokkar et al., 2000] Exposition par inhalation Aucune étude n'a été relevée. |
| Toxicité chronique /cancérogénicité | Essais de cancérogénicité par voie orale chez le rat Administration à des rats de 0,25 % de thiourée dans l'eau potable (350 mg/kg m.c. par jour) pendant 12 à 24 mois. Observation de tumeurs des cellules folliculaires thyroïdiennes chez 8 de 10 rats albinos mâles de la Nouvelle-Zélande (carcinomes de la thyroïde chez 4/10) et chez 8 de 10 rats albinos femelles de la Nouvelle-Zélande (carcinomes de la thyroïde chez 3/10) et chez 6 de 10 rats mâles Wistar (carcinomes de la thyroïde chez 0/10 [Purves et Griesbach, 1947). [Note : Aucun groupe témoin n'a été utilisé pour l'étude.] Administration à des rats de 0 ou 0,2 % de thiourée dans l'eau potable pendant une période pouvant atteindre 26 mois. Observation d'une augmentation des carcinomes épidermoïdes du canal auditif externe ou des glandes de Meibomius chez 17 de 19 rats albinos comparativement à 0 sur 12 chez les témoins (Rosin et Ungar, 1957). Administration à des rats de 0,2 % de thiourée dans l'eau potable. Observation de carcinomes des cellules pavimenteuses de la glande de Zymbal ou des glandes de Meibomius chez tous les sujets sauf un (Rosin et Ungar, 1960).[Note : Dans l'étude de Rosin et Ungar (1960) les rats utilisés étaient les survivants d'études de transplantation de tumeurs pour lesquels on avait jugé que l'implantation intrascapulaire avait été un échec.] Administration à des rats albinos (mâles et femelles) de 0, 0,01, 0,025, 0,05, 0,1, 0,25, 0,5 ou 1 % de thiourée dans la nourriture ( 0, 5, 12, 25, 50, 125, 250, 500 mg/kg m.c. par jour) pendant 24 mois. Observation d'une hyperplasie et d'une hypertrophie de la glande thyroïde allant de modérées à marquées aux doses de 0,25 % à 1 % (125-500 mg/kg m.c. par jour). Augmentation de l'incidence des tumeurs hépatiques (adénomes des cellules hépatiques) aux doses de 5 mg/kg m.c. par jour et plus (3/5, 4/8, 2/8 et 5/8 à 5 mg/kg m.c. par jour). Tous les animaux des deux groupes ayant reçu les doses les plus élevées sont morts avant 17 mois (Fitzhugh et Nelson, 1948; Deichmann et al., 1967). Administration à des souris femelles (R3) de 0,1 à 0,2 % (140-280 mg/kg m.c. par jour) de thiourée dans l'eau potable pendant 4 à 6 mois. Observation de tumeurs mammaires chez 54 % des souris exposées (dose non précisée dans la source secondaire) comparativement à 28 % chez les témoins (Vasquez-Lopez, 1949). Plus faible DMENO par voie orale (rat) = 27,5 mg/kg m.c. par jour pour une hypertrophie de la glande thyroïde et une réduction du gain pondéral chez des rats exposés tous les jours pendant deux ans dans l'eau potable (Hartzell, 1942 et 1945) Exposition par inhalation : Aucune étude n'a été recensée. [Autres études : Fitzhugh et Nelson, 1948; Gorbman, 1947; Daltonet al., 1948; Casas et Koppisch, 1952; Gargus et al., 1969; Purves et Griesbach, 1947; Rosin et Rachmilewitz, 1954; Rosin et Ungar, 1957; Rosin et Ungar, 1960; Randomski et al., 1965; Deichmann et al., 1967; Hartzell, 1942, 1945; Hazelton, 1987; Morris et al., 1946] |
| Toxicité pour le développement | Plus faible DMEO par voie orale (mouton) = 50 mg/kg m.c. par jour pour une hyperplasie de la glande thyroïde, une réduction significative de la masse corporelle et une réduction des concentrations d'érythrocytes, de leucocytes, de la T3 et de testostérone. Fondée sur la présence de tubules séminifères petits et vides et de testicules « mal développés » (Sokkar et al., 2000) et d'organes génitaux externes infantiles et non développés, l'absence d'œstrus et le développement retardé des glandes mammaires (Nasseri et Prassad, 1987) [Autres études : Sokkar et al ., 2000; Teramoto et al., 1981; Ruddick et al., 1976; Kern et al., 1980; Nasseri et Prassad, 1987b] |
| Toxicité pour la reproduction | Plus faible DMEO par voie orale (mouton) = L'administration à des moutons femelles d'une dose de thiourée pouvant atteindre 50 mg/kg m.c. par jour pendant 80 jours a donné lieu à une légère réduction, mais non statistiquement significative, de la taille et de la masse des ovaires, des cornes de l'utérus et du vagin. L'examen histologique a montré la présence de follicules atrétiques dans les ovaires et de cellules endométriales plus courtes.(Alavi Shoushtari et Safaii, 1993) Autres études :Le PISSC (2003) a signalé que des rats dont la nourriture contenait de la thiourée présentaient après une exposition de 24 mois une réduction ou un arrêt de la spermatogenèse aux doses supérieures à 35 mg/kg m.c. par jour (Fitzhugh et Nelson, 1948) |
| Paramètre | Résultats et référence | |||
|---|---|---|---|---|
| Espèce, souche | Résultat | Activation métabolique | Référence | |
| Mutation génétique | Salmonella typhimurium, TA 97 |
négatif | +/- | Brams et al., 1987 Zeiger et al., 1988 |
| Salmonella typhimurium, TA 98 |
négatif | +/- | Simmon, 1979a Dunkel et al., 1984 Brams et al., 1987 Zeiger et al., 1988 |
|
| Salmonella typhimurium, TA 100 |
négatif | +/- | Simmon, 1979a Yamaguchi, 1980 Dunkel et al., 1984 Brams et al., 1987 Zeiger et al., 1988 |
|
| Salmonella typhimurium, TA1535 |
négatif | +/- | Simmon, 1979a Rozenkranz et Poirier, 1979 Dunkel et al., 1984 Zeiger et al., 1988 |
|
| Salmonella typhimurium, TA1535/pSK1002, essai umu | négatif | +/- | Nakamura et al., 1987 |
|
| Salmonella typhimurium, TA1537 |
négatif | +/- | Simmon, 1979a Dunkel et al., 1984 |
|
| Salmonella typhimurium, TA1538 |
négatif | +/- | Rozenkranz et Poirier, 1979 Simmon, 1979a Dunkel et al., 1984 |
|
| Escherichia coli, réparation SOS |
négatif | +/- | Brams et al., 1987 Kevekordes et al., 1999 |
|
| Escherichia coli, WP2 uvr A | négatif | +/- | Dunkel et al., 1984 | |
| Escherichia coli, pol A | négatif | + | Rosenkranz et Poirier, 1979 McCarrol et al., 1981 |
|
| - | McCarrol et al., 1981 | |||
| Escherichia coli, souches uvr/rec |
positif | - | Hellmer et Bolscfoldi, 1992 | |
| négatif | + | Hellmer et Bolscfoldi, 1992 | ||
| Escherichia coli, K12 | négatif | + | Mamber et al., 1984 | |
| aucun essai | - | Mamber et al., 1984 | ||
| Escherichia coli, RK | négatif | +/- | Hayes et al., 1984 | |
| Aspergillus nidulans | négatif | - | Crebelli et al., 1986 | |
| Saccharamyces cerevisiae | positif | - | Schiestl, 1989 Schiestl et al., 1989 Galli et Schiestl, 1995, 1996, 1998 |
|
| + | Galli et Schiestl 1998 Egilsson et al., 1979 Wilkie et Gooneskera, 1980 |
|||
| Saccharamyces cerevisiae, locus trp | positif | + | Morita et al., 1989 | |
| négatif | - | Morita et al., 1989 | ||
| Saccharamyces cerevisiae, locus D7 trp | positif | non précisé | Jiang et al., 1989 | |
| Drosophila melanogaster | positif | - | Batiste-Alentorn et al., 1991 | |
| faiblement positif | - | Vogel et Nivard, 1993 | ||
| non concluant | - | Batiste-Alentorn et al., 1994, 1995 | ||
| négatif | - | Rodriguez-Arnaiz, 1997 | ||
| cellules de souris L5178Y | faiblement positif | + | Myhr et Caspary, 1988 Wangenheim et Bolscfoldi, 1988 |
|
| - | Wangenheim et Bolscfoldi, 1988 | |||
| négatif | + | Mitchell et al., 1988 | ||
| - | Mitchell et al., 1988 Myhr et Caspary, 1988 |
|||
| cellules ovariennes de hamsters chinois (V79), locus hprt | négatif | - | Bradley et al., 1982 | |
| positif | +/- | Ziegler-Skylakakis et al., 1985 | ||
| cellules ovariennes de hamsters chinois (V79), sous-lignée Sp5 | négatif | - | Helleday et al., 1998 | |
| Paramètre | Résultats et référence | |||
|---|---|---|---|---|
| Échange de chromatides sœurs | négatif : cellules de hamsters chinois - V79 (- activation) [Bradley et al., 1982] |
|||
| Synthèse non programmée de l'ADN | faiblement positif : cellules du foie du rat (Ziegler-Skylakakis et al., 1985) négatif : cellules du foie du rat (- activation, + activation non testée) [Lonati-Galligani et al., 1983; Fautz et al., 1991) |
|||
| Recombinaison mitotique | négatif : Saccharamyces cerevisiae D3 (+/- activation) [Simmon, 1979b] |
|||
| Recombinaison | positif : cellules lymphoblastoïdes humaines transformées GM6804 (Aubrechtet al., 1995) |
|||
| Formation de micronoyaux | positif : cellules d'embryons du hamster syrien (- activation, + non testé) [Fritzenschaf et al., 1993)faiblement positif : hamster chinois, V79 (Ziegler-Skylakakis et al., 1998) |
|||
| Bris de brins d'ADN | positif : hépatocytes de rat in vitro (-activation, non testé + activation) [Sina et al., 1983]négatif : hépatocytes de rat in vitro (-activation, non testé + activation) [Fautz et al., 1991] |
|||
| Transformation cellulaire | positif : cellules d'embryons du hamster syrien (-activation, + non testé) [Pienta et al., 1977] cellules d'embryons de rat infectées par le virus de Rauscher (-activation, + non testé) [Dunkel et al., 1981] faiblement positif : cellules C3H10T1/2 infectées par le virus à ADN modifié du papillome bovin (-activation, + non testé) [Kowalski et al., 2000] |
|||
| Inhibition de la synthèse de l'ADN | positif : cellules fibroblastiques humaines (Painter) |
|||
| Génotoxicité et paramètres connexes : in vivo | ||||
| Mutation génétique | positif ; Drosophila melanogaster (Batiste-Alentorn et al., 1991) faiblement positif : Drosophila melanogaster (Vogel et Nivard, 1993) négatif : Drosophila melanogaster (Rodriguez-Arnaiz, 1997) non concluant : Drosophila melanogaster (Batiste-Alentorn et al., 1994; Batiste-Alentorn et al., 1995) |
|||
| Essai des micronoyaux | négatif : rats traités par deux doses orales successives en 24 heures (TNO, 1979b) |
|||
| Effets chez les Humains | ||||
| Études de cas | Des cas individuels de dermatite par contact ont été signalés après exposition à de la thiourée résultant de l'utilisation de papier à reproduction diazo et de la plupart des autres types de papier à reproduction (Van der Leun et al ., 1977; Nurse, 1980; Kellet et al., 1984; Liden, 1984; Dooms-Goossens et al., 1987; Niinimaki, 1989; Pashe-Koo et Grosshans, 1991; Torres et al., 1992; Geier et Fuchs, 1993; Bartels et Schauder, 1994; van Gerwen et al., 1996; Kanerva et al., 2000). Une dermatite par contact due à la thiourée présente dans un produit à polir l'argent a été signalée (Dooms-Goossens et al., 1988). Il a été montré que des dérivés de la thiourée utilisés comme accélérateurs dans l'industrie du caoutchouc provoquaient une dermatite par contact de type allergique (Kanerva et al., 1994; McCleskey et Swerlick, 2001). |
|||