Évaluation préalable pour le Défi concernant le N-[2-[(2-Bromo-4,6-dinitrophényl)azo]-5-(diéthylamino)phényl]acétamide]-
Numéro de registre du Chemical Abstracts Service 52697-38-8
Environnement Canada
Santé Canada
Août 2009
Table des matières
- Synopsis
- Introduction
- Identité de la substance
- Propriétés physiques et chimiques
- Sources
- Utilisations
- Rejets dans l'environnement
- Devenir dans l'environnement
- Persistance et potentiel de bioaccumulation
- Potentiel d'effets nocifs sur l'environnement
- Conclusion
- Références
- Annexe I - Sommaires de rigueur d'étude pour les études clés
Synopsis
Conformément à l'article 74 de la Loi canadienne sur la protection de l'environnement (1999) [LCPE (1999)], les ministres de l'Environnement et de la Santé ont effectué une évaluation préalable duN-[2-[(2-bromo-4,6-dinitrophényl)azo]-5-(diéthylamino)phényl]acétamide (BDAP), dont le numéro de registre du Chemical Abstracts Service est le 52697-38-8. Une priorité élevée a été accordée à l'évaluation préalable de cette substance inscrite au Défi, parce qu'elle répondait aux critères environnementaux de la catégorisation écologique relatifs à la persistance, au potentiel de bioaccumulation et à la toxicité intrinsèque pour les organismes non humains et parce que l'on croit qu'elle est commercialisée au Canada.
L'évaluation des risques que présente le BDAP pour la santé humaine n'a pas été jugée hautement prioritaire à la lumière des résultats fournis par les outils simples de détermination du risque d'exposition et du risque pour la santé élaborés par Santé Canada aux fins de la catégorisation des substances figurant sur la Liste intérieure. Par conséquent, la présente évaluation est axée sur les renseignements utiles à l'évaluation des risques pour l'environnement.
Le BDAP est un composé organique utilisé au Canada principalement comme colorant noir dans l'industrie textile. Il n'est pas produit naturellement dans l'environnement. On n'a pas déclaré la fabrication de cette substance au Canada; toutefois, on en a importé entre 10 000 et 100 000 kg en 2006, destinés à l'industrie des textiles et du finissage des tissus.
Selon les modes d'utilisation signalés et certaines hypothèses, la plus grande partie de cette substance devrait être rejetée dans des sites d'élimination des déchets solides, mais on estime qu'une proportion significative est rejetée dans les eaux usées (14,8 %). On croit que le BDAP n'est ni soluble dans l'eau, ni volatil, mais qu'il devrait se déplacer vers les particules à cause de son caractère hydrophobe. Ainsi, après son rejet dans l'eau, cette substance devrait se répartir principalement dans les sédiments et, dans une moindre mesure, dans les sols agricoles amendés avec des boues d'égout. Le BDAP ne devrait pas se retrouver en quantités significatives dans d'autres milieux, et il est peu probable qu'il fasse l'objet de transport atmosphérique à grande distance.
Compte tenu de ses propriétés physiques et chimiques, on croit que le BDAP est persistant dans l'environnement (dans l'eau, les sédiments et le sol). Toutefois, selon de nouvelles données expérimentales sur le potentiel de bioaccumulation d'un composé analogue à structure relativement semblable, on croit que ce colorant présente un faible potentiel d'accumulation dans les tissus lipidiques des organismes. Il satisfait donc aux critères de persistance, mais non aux critères de bioaccumulation, établis dans le Règlement sur la persistance et la bioaccumulation. De plus, les données expérimentales sur la toxicité de composés analogues permettent de croire que de faibles concentrations de BDAP n'ont pas d'effets nocifs chez les organismes aquatiques.
Aux fins de la présente évaluation préalable, on a retenu un scénario d'exposition très prudent selon lequel une installation industrielle (le plus grand importateur de ce colorant) a rejeté du BDAP à un seul point de rejet dans un plan d'eau récepteur relativement petit. La concentration environnementale estimée pour l'eau était inférieure à la concentration sans effet estimée pour les espèces aquatique sensibles. De plus, étant donné que le BDAP peut être utilisé dans des produits de consommation, on a également élaboré un scénario pour leur rejet, fondé sur la quantité estimée de BDAP dans le commerce au Canada. Selon ce scénario, les concentrations environnementales estimées déterminées pour tous les cours d'eau modélisés devraient être inférieures à la concentration sans effet estimée établie pour les espèces aquatiques sensibles.
Cette substance s'inscrira dans la prochaine mise à jour de l'inventaire de la Liste intérieure. De plus, des activités de recherche et de surveillance viendront, le cas échéant, appuyer la vérification des hypothèses formulées au cours de l'évaluation préalable.
D'après les renseignements disponibles, le BDAP ne remplit aucun des critères de l'article 64 de la LCPE (1999).
Introduction
La Loi canadienne sur la protection de l'environnement, 1999 [LCPE (1999)] (Canada, 1999) exige que les ministres de l'Environnement et de la Santé procèdent à une évaluation préalable des substances qui répondent aux critères de la catégorisation énoncés dans la Loi, afin de déterminer si elles présentent ou sont susceptibles de présenter un risque pour l'environnement ou la santé humaine. Selon les résultats de cette évaluation, les ministres peuvent proposer de ne rien faire à l'égard de la substance, de l'inscrire sur la Liste des substances d'intérêt prioritaire en vue d'une évaluation plus détaillée ou de recommander son inscription sur la Liste des substances toxiques de l'annexe 1 de la Loi et, s'il y a lieu, sa quasi-élimination.
En se fondant sur l'information obtenue dans le cadre de la catégorisation, les ministres ont jugé qu'une attention hautement prioritaire devait être accordée à un certain nombre de substances, à savoir :
- celles qui répondent à tous les critères environnementaux de la catégorisation, notamment la persistance (P), le potentiel de bioaccumulation (B) et la toxicité intrinsèque pour les organismes aquatiques (Ti), et que l'on croit être commercialisées au Canada ou;
- celles qui répondent aux critères de la catégorisation pour le plus fort risque d'exposition (PFRE) ou qui présentent un risque d'exposition intermédiaire (REI) et qui ont été jugées particulièrement dangereuses pour la santé humaine, compte tenu des classifications qui ont été établies par d'autres organismes nationaux ou internationaux concernant leur cancérogénicité, leur génotoxicité ou leur toxicité pour le développement ou la reproduction.
Le 9 décembre 2006, les ministres ont donc publié un avis d'intention dans la Partie I de la Gazette du Canada (Canada, 2006a), dans lequel ils priaient l'industrie et les autres parties intéressées à fournir, dans des délais précis, des renseignements spécifiques qui pourraient servir à étayer l'évaluation des risques, à élaborer et à déterminer les meilleures pratiques en matière de gestion des risques et d'intendance des produits des substances jugées hautement prioritaires.
On a décidé d'accorder une attention hautement prioritaire à l'évaluation des risques pour l'environnement du N-[2-[(2-Bromo-4,6-dinitrophényl)azo]-5-(diéthylamino)phényl]acétamide (BDAP), car cette substance a été jugée persistante, bioaccumulable et intrinsèquement toxique pour les organismes aquatiques et il semble qu'elle est commercialisée au Canada. Le volet du Défi portant sur cette substance a été publié dans la Gazette du Canada le 16 février 2008 (Canada, 2008). En même temps a été publié le profil de cette substance, qui présentait l'information technique (obtenue avant décembre 2005) sur laquelle a reposé sa catégorisation. Des renseignements sur la toxicité et les utilisations de la substance ont été communiqués en réponse au Défi.
Même si l'évaluation des risques que présente le BDAP pour l'environnement est jugée hautement prioritaire, cette substance ne répond pas aux critères de la catégorisation pour le PFRE ou le REI ni aux critères définissant un grave risque pour la santé humaine, compte tenu du classement attribué par d'autres organismes nationaux ou internationaux quant à sa cancérogénicité, à sa génotoxicité ou à sa toxicité sur le plan du développement ou de la reproduction. La présente évaluation est donc axée principalement sur les renseignements présentant de l'intérêt pour l'évaluation des risques touchant l'environnement.
Les évaluations préalables effectuées aux termes de la LCPE (1999) mettent l'accent sur les renseignements jugés essentiels pour déterminer si une substance répond aux critères de toxicité des substances chimiques au sens de l'article 64 de la Loi :
« 64. [...] est toxique toute substance qui pénètre ou peut pénétrer dans l'environnement en une quantité ou concentration ou dans des conditions de nature à :
- avoir, immédiatement ou à long terme, un effet nocif sur l'environnement ou sur la diversité biologique;
- mettre en danger l'environnement essentiel pour la vie; ou
- constituer un danger au Canada pour la vie ou la santé humaines. »
Les évaluations préalables visent à examiner des renseignements scientifiques et à tirer des conclusions fondées sur la méthode du poids de la preuve et le principe de prudence.
La présente évaluation préalable prend en considération les renseignements sur les propriétés chimiques, les dangers, les utilisations et l'exposition, y compris ceux fournis dans le cadre du Défi. Les données pertinentes pour l'évaluation préalable de cette substance ont été trouvées dans des publications originales, des examens des documents, des rapports de recherche de parties intéressées et d'autres documents consultés lors de recherches documentaires menées récemment, jusqu'en août 2008. Les principales études ont fait l'objet d'une évaluation rigoureuse et en général, seuls les résultats des études de qualité élevée ont été utilisés dans la formulation des conclusions, même si les résultats des autres études et modélisations peuvent avoir été pris en compte dans l'établissement du poids de la preuve. Lorsqu'ils étaient disponibles et pertinents, les renseignements présentés dans l'évaluation des dangers provenant d'autres instances ont également été utilisés. L'évaluation préalable n'est pas un examen exhaustif ou critique de toutes les données disponibles. Elle fait plutôt état des études et des éléments d'information les plus importants pour appuyer la conclusion.
La présente évaluation préalable a été préparée par le personnel du Programme des substances existantes de Santé Canada et d'Environnement Canada et elle intègre les résultats d'autres programmes exécutés par ces ministères. Cette évaluation préalable a fait l'objet d'une étude consignée par des pairs. Bien que des commentaires externes aient été pris en considération, Santé Canada et Environnement Canada assument la responsabilité du contenu final et des résultats de l'évaluation préalable des risques. De plus, une version provisoire de la présente évaluation préalable a fait l'objet d'une consultation publique de 60 jours. Les principales données et considérations sur lesquelles repose la présente évaluation sont résumées ci-après.
Identité de la substance
Aux fins du présent document, la substance N-[2-[(2-Bromo-4,6-dinitrophényl)azo]-5-(diéthylamino)phényl]acétamide est appelée BDAP. Le tableau 1 présente des données sur l'identité de la substance.
| Numéro de registre du Chemical Abstracts Service (no CAS) | 52697-38-8 |
|---|---|
| Nom dans la LIS | N-[2-[(2-Bromo-4,6-dinitrophényl)azo]-5-(diéthylamino)phényl]acétamide]- |
| Noms dans les inventairesNote de bas de tableau a | Acetamide, N-[2-[(2-bromo-4,6-dinitrophenyl)azo]-5-(diethylamino)phenyl]- (TSCA, LIS, AICS, PICCS, ASIA-PAC, NZIoC); N-[2-[(2-Bromo-4,6-dinitrophényl)azo]-5-(diéthylamino)phényl]acétamide (LIS, EINECS, ECL); 2'-[(2-Bromo-4,6-dinitrophenyl)azo]-5'-(diethylamino)acetanilide (ENCS); Acetamide, N-[2-[(2-bromo-4,6-dinitrophenyl)azo]-5-(diethylamino)phenyl]- (PICCS); ACETAMIDE, N-(2-((2-BROMO-4,6-DINITROPHENYL)AZO) -5-(DIETHYLAMINO)PHENYL)- (PICCS) |
| Autres noms | 2-Bromo-4,6-dinitro-1-[[2-(acetylamino)-4-(diethylamino)phenyl]azo]benzene; Acetanilide, 2-(2,4-dinitro-6-bromophenylazo)-5-N,N-diethylamino-; Disperse Violet 93 |
| Groupe chimique | Composés azoïques |
| Sous-groupe chimique | Composés monoazoïques2 |
| Formule chimique | C18H19BrN6O5 |
| Structure chimique | 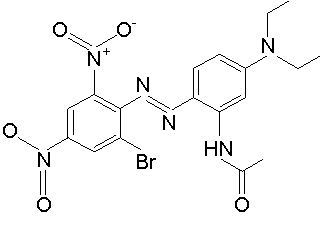 |
| Simplified Molecular Line Input Entry System (SMILES) | O=C(Nc(c(N=Nc(c(cc(N(=O)(=O))c1)Br)c1N(=O)(=O))ccc2N(CC)CC)c2)C |
| Masse moléculaire | 479,29 g/mol |
Propriétés physiques et chimiques
À l'exception des données sur le point de fusion, peu de données expérimentales sont disponibles sur le BDAP. Lors de l'atelier sur les modèles de relations quantitatives structure-activité (RQSA), parrainé par Environnement Canada en 1999 (Environnement Canada, 2000), des experts en modélisation ont reconnu qu'il est « difficile de modéliser » de nombreuses classes structurelles de pigments et de colorants avec le modèle RQSA. Les propriétés physiques et chimiques de nombreuses classes structurelles de teintures et de pigments (y compris les colorants acides et dispersés) se prêtent mal à la prévision modélisée, car on considère qu'elles « ne font pas partie du domaine d'applicabilité » (p. ex. domaines de la structure ou des paramètres des propriétés). Par conséquent, lorsqu'il s'agit de teintures et de pigments, on vérifie au cas par cas le domaine d'applicabilité des modèles RQSA pour déterminer leur utilité potentielle. En général, Environnement Canada considère que l'utilisation des modèles RQSA ne convient pas à la prévision des propriétés physiques et chimiques du BDAP. Par conséquent, des substances analogues ont été identifiées et l'on a utilisé des données déduites à partir d'analogues pour la détermination des propriétés physiques et chimiques approximatives données au tableau 2. Ces propriétés ont été utilisées par la suite pour d'autres modélisations et éléments d'information au cours de cette évaluation.
Un analogue est une substance chimique de structure similaire à la substance évaluée, qui devrait donc présenter des propriétés physiques et chimiques, un comportement dans l'environnement et/ou une toxicité similaires. Les données expérimentales pour un paramètre donné d'une substance analogue, lorsqu'elles existent, peuvent être utilisées directement ou après ajustement comme une estimation de la valeur du paramètre pour la substance en cours d'évaluation.
Pour trouver des analogues acceptables, un examen des données relatives à plusieurs colorants azoïques dispersés a été mené. (Anliker et al., 1981; Anliker et Moser, 1987; Baughman et Perenich, 1988, ETAD, 1995; Brown, 1992; Yen et al., 1989, Sijm et al., 1999). Ces composés conviennent comme analogues en raison de leurs analogies structurales avec le BDAP et d'autres caractéristiques importantes communes avec cette substance. Ces propriétés sont, entre autres, celles qui ont un effet sur leur devenir environnemental, comme un poids moléculaire élevé (généralement supérieur à 300 g/mol), un diamètre transversal similaire (1,31 à 2,05 nm), des structures particulaires solides, la décomposition à une température supérieure à 74 °C (jusqu'à 236 °C) et la « dispersibilité » dans l'eau (c'est-à-dire pas entièrement solubles). De plus, ils sont faiblement ou modérément solubles dans le n-octanol, leur pression de vapeur est négligeable et ils sont stables dans des conditions environnementales normales.
Le tableau 2 présente les substances analogues au BDAP ainsi que les valeurs expérimentales et modélisées des propriétés physiques et chimiques déduites à partir d'analogues du BDAP qui se rapportent à son devenir dans l'environnement.
| TypeNote de bas de tableau b | Valeur | Température (°C) | Références | |
|---|---|---|---|---|
| État physique | Poudre | Canada, 2008 | ||
| Point de fusionNote de bas de tableau c (°C) | expérimental | 184-186 | Thiel et al., 1986 | |
| Point de fusionNote de bas de tableau c (°C) | Disperse Blue 79 analogue | 157 | PhysProp, 2006 | |
| Point de fusionNote de bas de tableau c (°C) | Disperse Blue 79:1 analogue | 132 à 153 | Sijm et al., 1999; Yen et al., 1989 | |
| Point de fusionNote de bas de tableau c (°C) | Analogue au no CAS 68877-63-4 | 175 à 193 | Anliker et Moser, 1987; Yen et al., 1989 | |
| Point de fusionNote de bas de tableau c (°C) | Disperse Blue 165 analogue | 252 | Sijm et al., 1999 | |
| Point de fusionNote de bas de tableau c (°C) | données déduites à partir d'analogues des colorants azoïques dispersés | 117 à 175 74 à 236 |
Anliker et Moser, 1987 Baughman et Perenich, 1988 |
|
| Point d'ébullitionNote de bas de tableau d (°C) | sans objet | sans objet | sans objet | sans objet |
| Masse volumique (kg/m3) | non disponible | non disponible | non disponible | non disponible |
| Pression de vapeur (Pa) | Disperse Blue 79 analogue | 4,53 × 10-7 | Clariant, 1996 | |
| Pression de vapeur (Pa) | données déduites à partir d'analogues des colorants azoïques dispersés | 5,33× (10-12 à 10-5) (4 × 10-14 à 4 × 10-7 mm Hg) |
25 | Baughman et Perenich, 1988 |
| Constante de la loi de Henry (Pa·m3/mol) | données déduites à partir d'analoguesNote de bas de tableau e | 10-8 à 10-1 (10-13 à 10-6 atm·m3/mol) |
Baughman et Perenich, 1988 | |
| Log Koe (coefficient de partage octanol/eau) (sans dimension) | Disperse Blue 79 analogue | 4,1; 4,3 | Clariant, 1996, Brown, 1992 | |
| Log Koe (sans dimension) | Disperse Blue 79:1 analogue | 4,4; 4,8 | Sijm et al., 1999; Coughtrie et al., 1989 | |
| Log Koe (sans dimension) | analogue au no CAS 68877-63-4 | 2,5; 5,4 | Anliker et Moser, 1987; Yen et al., 1989 | |
| Log Koe (sans dimension) | Disperse Orange 30 analogue | 4,2 | Brown, 1992 | |
| Log Koe (sans dimension) | données déduites à partir d'analogues des colorants azoïques dispersés | 1,79 à 5,1 | Baughman et Perenich, 1988 | |
| Log Koe (sans dimension) | données déduites à partir d'analogues des colorants azoïques dispersés | supérieur(e) à 2 à 5,1 | Anliker et al., Anliker et Moser,1987 | |
| Log Kco (coefficient de partage carbone organique) (sans dimension) | données déduites à partir d'analogues, calculéesNote de bas de tableau f | 3,4 à 4,2 | Baughman et Perenich, 1988 | |
| Solubilité dans l'eau (mg/L) | Disperse Blue 79 analogue | 0,0054 | 25 | Clariant, 1996 |
| Solubilité dans l'eau (mg/L) | Disperse Blue 79 analogue | 0,02 | Brown, 1992 | |
| Solubilité dans l'eau (mg/L) | Disperse Blue 79:1 analogue | 0,02 | Sijm et al. 1999 | |
| Solubilité dans l'eau (mg/L) | Disperse Blue 79:1 analogue | 0,0052 | Yen et al., 1989 | |
| Solubilité dans l'eau (mg/L) | Disperse Blue 79:1 analogue | 0,00063 | 100-125 | Baughman et Perenich, 1988 |
| Solubilité dans l'eau (mg/L) | analogue au no CAS 68877-63-4 | 0,00069 | Yen et al., 1989 | |
| Solubilité dans l'eau (mg/L) | Disperse Blue 79 analogue | 0,0058 à 1,3 | Sijm et al. 1999 | |
| Solubilité dans l'eau (mg/L) | données déduites à partir d'analogues des colorants azoïques dispersés | inférieur(e) à 0,01 | 20 | Anliker et Moser, 1987 |
| Solubilité dans l'eau (mg/L) | données déduites à partir d'analogues des colorants azoïques dispersés | Hautement insoluble dans l'eau | ETAD, 1995 | |
| Solubilité dans l'eau (mg/L) | données déduites à partir d'analogues des colorants azoïques dispersés | 1,2 × 10-5 à 35,5 (4 × 10-11 à 1,8 × 10-4 mol/L) |
Baughman et Perenich, 1988 | |
| Solubilité dans le n-octanol (mg/L) | Disperse Blue 79:1 analogue | 14 | Sijm et al. 1999 | |
| Solubilité dans le n-octanol (mg/L) | Analogue au 68877-63-4 | 81 | 20 | Anliker et Moser,1987 |
| Solubilité dans le n-octanol (mg/L) | Disperse Blue 79 analogue | 225 | Sijm et al. 1999 | |
| Solubilité dans le n-octanol (mg/L) | données déduites à partir d'analogues des colorants azoïques dispersés | 81-2100 | 20 | Anliker et Moser,1987 |
| pKa (constante de dissociation) (sans dimension) | modélisé | 13,9 sous forme acide 1,85 sous forme de base |
ACD/pKaDB, 2005 |
Les colorants azoïques dispersés analogues du BDAP sont présentés dans le tableau 3a ci-après. Certaines des propriétés physiques et chimiques (tableau 2), les données empiriques sur la bioaccumulation (tableau 6) ainsi que les données empiriques sur la toxicité (tableau 7) de ces analogues ont été utilisées pour établir le poids de la preuve et pour appuyer les propositions de décision présentées dans cette évaluation préalable. Plus précisément, les données ont été obtenues pour les analogues structuraux suivants : le Disperse Orange 30, le Disperse Blue 79, le Disperse Blue 79:1, le no CAS 68877-63-4, le Disperse Blue 165, le Disperse Red 73, le Disperse Orange 25 et le Disperse Red 17.
| No CAS | Nom commun | Nom dans la LIS | Structure chimique de l'analogue | Données empiriques disponibles |
|---|---|---|---|---|
| 3618-72-2 | Disperse Blue 79:1 | Diacétate de 2,2'-{[5-acétamide-4-(2-bromo-4,6-dinitrophénylazo)-2-méthoxyphényl]imino}diéthyle | 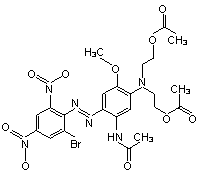 |
Point de fusion, log Koe, solubilité dans l'eau, toxicité pour les organismes aquatiques |
| 12239-34-8 | Disperse Blue 79 | Diacétate de 2,2'-[[5-acétamide-4-[(2-bromo-4,6-dinitrophényl)azo]-2-éthoxyphényl]imino]diéthyle | 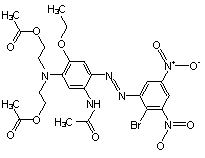 |
Point de fusion, pression de vapeur, log Koe, solubilité dans l'eau, toxicité de cette substance pour les organismes aquatiques |
| 68877-63-4 | s. o. | -[2-[(2-Bromo-4,6-dinitrophényl) azo]-5-[(2-cyanoéthyl)allylamino]-4-méthoxyphényl ]acétamide | 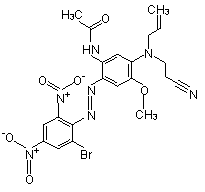 |
Point de fusion, log Koe, solubilité dans l'eau, solubilité dans l'octanol, bioaccumulation |
| 41642-51-7 | Disperse Blue 165 | -[(2,6-Dicyano-4-nitrophényl) azo]-5-(diéthylamino)phényl]acétamide | 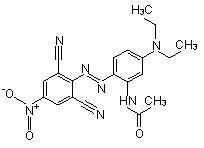 |
Point de fusion, solubilité dans l'eau, solubilité dans l'octanol |
| 5261-31-4 | (Disperse Orange 30) | Acétate de 2-[N-(2-cyanoéthyl)-4-[2,6-dichloro-4-nitrophényl)azo]anilino]éthyle | 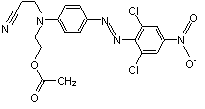 |
Bioaccumulation, toxicité de cette substance pour les organismes aquatiques, log Koe |
| 16889-10-4 | Disperse Red 73 | 2-[[4-[(2-Cyanoéthyl)éthylamino] phényl]azo]-5-nitrobenzonitrile | 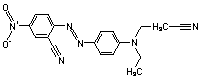 |
Toxicité de cette substance pour les organismes aquatiques |
| 31482-56-1 | Disperse Orange 25 | Propanenitrile, 3-[ethyl[4-[(4-nitrophenyl)azo]phenyl] amino]- | 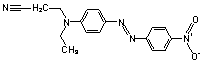 |
Toxicité de cette substance pour les organismes aquatiques |
| 3179-89-3 | Disperse Red 17 | 2,2'-{[3-Méthyl-4-(4-nitrophénylazo) phényl]imino}diéthanol |  |
Toxicité de cette substance pour les organismes aquatiques |
Il faut souligner que l'on dénombre diverses incertitudes liées à l'utilisation des données disponibles sur les propriétés physiques et chimiques, la toxicité et la bioaccumulation des substances qui apparaissent au tableau 3a. Toutes ces substances appartiennent à la même classe chimique, soit celle des colorants azoïques dispersés (caractérisés par une liaison azoïque) et sont utilisées à des fins industrielles similaires. Toutefois, ces substances présentent des différences liées à leur groupement fonctionnel propre (voir le tableau 3b ci-après). Par conséquent, les valeurs empiriques de solubilité dans l'eau de ces analogues varient de plus de quatre ordres de grandeur, soit de 10-4 à 1 mg/L et des valeurs empiriques de log Koe qui varient de deux ordres de grandeur, soit de 2,5 à 5,4 (tableau 2). En raison de cette variabilité, il faut être prudent lorsque l'on tire des conclusions à partir des valeurs des analogues, car il serait préférable d'utiliser des valeurs empiriques propres à la substance BDAP (tableau 2).
| No CAS | Nom commun | Masse moléculaire (g/mol) | % de similarité structuraleNote de bas de tableau g | Diamètre transversal minimum et maximum (nm)Note de bas de tableau h |
|---|---|---|---|---|
| 3618-72-2 | Disperse Blue 79:1 | 625,39 | 89,1 | 1,43-2,03 |
| 12239-34-8 | Disperse Blue 79 | 639,4 | 86,7 | 1,69-2,045 |
| 68877-63-4 | s. o. | 546,3 | 84,2 | 1,48-1,97 |
| 41642-51-7 | Disperse Blue 165 | 405,4 | 82,1 | 1,35-1,82 |
| 5261-31-4 | (Disperse Orange 30) | 450,28 | 68,9 | 1,75-1,98 |
| 16889-10-4 | Disperse Red 73 | 348,36 | 58,8 | 1,31-1,93 |
| 31482-56-1 | Disperse Orange 25 | 323,35 | - | 1,37-1,95 |
| 3179-89-3 | Disperse Red 17 | 344,36 | - | 1,41-1,86 |
Sources
Le BDAP n'est pas produit naturellement dans l'environnement.
Des enquêtes menées auprès de l'industrie en 2005 et 2006 par le truchement d'avis publiés dans la Gazette du Canada conformément à l'article 71 de la LCPE (1999) ont permis de recueillir des renseignements récents (Canada, 2006b et 2008). Comme le précisaient ces avis, les enquêtes visaient à recueillir des données sur la fabrication et l'importation de la substance au Canada. En 2006, on demandait également de fournir des données sur les quantités de BDAP utilisées.
En 2006, aucune entreprise n'a déclaré avoir fabriqué des quantités de BDAP supérieures au seuil de déclaration fixé à 100 kg/an au Canada. Moins de quatre entreprises ont déclaré avoir importé cette substance en 2006, qui ont totalisé entre 10 000 et 100 000 kg (Canada, 2008). Deux entreprises ont déclaré avoir utilisé entre 10 000 et 100 000 kg de cette substance en 2006 (Canada, 2008). Bien qu'elle ne réponde pas aux exigences obligatoires de déclaration, une entreprise a manifesté un intérêt pour la substance à l'aide du formulaire Déclaration des parties intéressées relatif à l'avis émis en application de l'article 71 pour 2006.
En 2005, moins de quatre entreprises ont déclaré avoir importé entre 100 et 1 000 kg par an de BDAP et aucune entreprise n'a manifesté son intérêt pour cette substance (Canada, 2006b).
Le BDAP a été reconnu comme substance chimique produite en faible quantité dans l'Union européenne (UE); sa production y est estimée entre 10 et 1 000 tonnes par an (ESIS, 2008). Le volume de production de production de BDAP aux États-Unis se situait entre 10 000 et 500 000 livres en 1986, 1990, 1994 et 2002, et entre 500 000 et 1 000 000 livres en 1998 (US EPA, 2007). Selon la base de données des pays nordiques sur les substances dans les préparations (SPIN), le BDAP été utilisé en Suède de 1999 à 2006 et en Finlande et au Danemark de 2000 à 2006 dont les quantités déclarées atteignaient de 0,2 à 10 tonnes (SPIN, 2008).
Utilisations
L'avis publié en application de l'article 71 de la LCPE (1999) a fourni des renseignements sur les utilisations de cette substance aux cours des années civiles 2005 et 2006 (Canada, 2008).
En 2006, quelques entreprises important du BDAP ont indiqué que leurs activités commerciales consistaient à fabriquer des produits chimiques ainsi que des colorants et des pigments synthétiques. Ensembles, des entreprises ont vendu du BDAP à 18 autres entreprises (Canada, 2008). Ces acheteurs teignent et veillent à la finition des tissus à des fins vestimentaire et industrielle (Industrie Canada, 2008a). Une recherche approfondie sur les noms commerciaux présentés par l'entreprise importatrice (Canada, 2008) indique que le BDAP est utilisé comme ingrédient dans une teinture de textile noire dont l'application aux mélanges de polyester et de polyester/cellulose. Cette teinture présente une bonne résistance à la transpiration et au lavage et se distingue par sa rentabilité et sa capacité à donner aux textiles des teintes très foncées. Les méthodes d'application de la teinture comprennent l'éjection, l'application continue et la teinture rapide et alcaline (All Business, 2000).
En 2005, une entreprise importatrice de BDAP était grossiste-distributrice de produits chimiques (Canada, 2006b).
Les codes d'utilisation suivants de la LIS ont été indiqués pour la substance dans le cadre de l'inscription sur la LIS (1984 à 1986) : « Colorant - pigment/teinture/encre », « Pigments, teintures et encre d'imprimerie » et « Produits textiles ».
Dans les pays nordiques, le BDAP sert d'agent colorant dans l'industrie du textile (SPIN, 2008).
Rejets dans l'environnement
Outil de débit massique
Pour estimer les rejets potentiels de la substance dans l'environnement à différentes étapes de son cycle de vie, l'outil de mesure du débit massique a été créé (Environnement Canada, 2008a). Les données empiriques sur les rejets de substances particulières dans l'environnement sont rarement disponibles. On estime donc, pour chaque type d'utilisation connue de la substance, la proportion et la quantité des rejets dans les différents milieux naturels, ainsi que la proportion de la substance qui est transformée chimiquement ou envoyée dans des lieux d'élimination des déchets. À moins de disposer de données précises sur le taux ou le potentiel de rejet de cette substance provenant des sites d'enfouissement et des incinérateurs, l'outil de débit massique ne permet pas de quantifier les rejets dans l'environnement à partir de ces sources.
Les hypothèses et les paramètres d'entrée utilisés pour estimer les rejets sont fondés sur des renseignements obtenus de diverses sources, dont les réponses aux enquêtes sur la réglementation, Statistique Canada, les sites Web des fabricants et les bases de données et documents techniques. Ce qui est particulièrement pertinent, ce sont les facteurs d'émission, généralement exprimés en fraction d'une substance rejetée dans l'environnement, notamment durant sa fabrication, sa transformation et son utilisation associées aux procédés industriels. Les sources de ces renseignements comprennent des documents sur des scénarios d'émission, souvent produits sous les auspices de l'Organisation de coopération et de développement économiques (OCDE), et les hypothèses par défaut utilisées par différents organismes internationaux de réglementation des produits chimiques. On a remarqué que le degré d'incertitude quant à la masse de la substance et à la quantité rejetée dans l'environnement augmente généralement vers la fin du cycle de vie.
Selon les données de Statistique Canada et une analyse réalisée par Industrie Canada (2008b), le BDAP pourrait être importé dans des articles manufacturés. Le rapport de textiles fabriqués au Canada et importés de 30/70 a été utilisé pour estimer la quantité de teinture importée dans les textiles (Environnement Canada, 2008b). Cette quantité importée a été incluse dans les calculs de l'outil de débit massique ainsi que dans les scénarios d'exposition plus détaillés.
| Devenir | Proportion massique (%)Note de bas de tableau i | Principale étape du cycle de vieNote de bas de tableau j |
|---|---|---|
| Rejets dans le sol | 0,0 | Sans objet |
| Rejets dans l'air | 0,0 | Sans objet |
| Rejets dans les égoutsNote de bas de tableau k | 14,8 | Formulation, utilisation par les consommateurs |
| Transformation chimique | 0,0 | Sans objet |
| Transfert vers les lieux d'élimination des déchets (p. ex. enfouissement, incinérateurs) | 85,2 | Formulation, élimination de déchets |
Les résultats indiquent que, comme les autres colorants azoïques dispersés, le BDAP pourrait être largement décelé dans les lieux d'élimination des déchets solides (85,2 %), en raison de l'élimination définitive des articles fabriqués qui en contiennent. Ces calculs sont fondés sur l'hypothèse que ces sites n'émettent aucun rejet de cette substance, bien que ce soit possible à long terme. Une faible fraction des déchets solides est incinérée, ce qui devrait donner lieu à une transformation chimique de cette substance. D'après les renseignements contenus dans les documents sur les scénarios d'émission de l'OCDE concernant la transformation et les utilisations associées à ce type de substance, on estime que 14,8 % du BDAP peut être rejeté dans les égouts (5,4 % découlant du traitement industriel et 9,4 % provenant des utilisations par les consommateurs).
D'après ce qui précède, l'eau (égouts) est le milieu qui reçoit la plus grande proportion du BDAP rejeté pendant la transformation des produits. On prévoit que la majeure partie de cette substance fixée dans les produits sera envoyée aux sites d'enfouissement aux fins d'élimination.
Devenir dans l'environnement
Selon les résultats obtenus à l'aide de l'outil de débit massique (tableau 4), la substance BDAP est susceptible d'être rejetée dans les effluents d'eaux usées pendant sa transformation industrielle et son utilisation. Les valeurs moyennes de log Koe (de 2,5 à 5,4) et les valeurs élevées de log Kco (données déduites à partir d'analogues de 3,4 à 4,2) [voir le tableau 2] indiquent que cette substance pourrait avoir une affinité pour les solides. Toutefois, le log Kco est une valeur calculée (voir la note 3 du tableau 2), et le potentiel d'adsorption des structures particulaires solides des colorants n'est généralement pas bien compris; par conséquent, le degré d'adsorption du BDAP est incertain.
Le BDAP devrait être le plus souvent trouvé dans les sédiments ou le sol. Il ne devrait pas être transporté dans l'atmosphère sur de grandes distances.
Selon les modèles de biodégradation aérobie, le BDAP ne devrait pas se biodégrader rapidement (voir le tableau 5 ci-dessous). Au Canada, il pourrait être répandu non intentionnellement sur des sols agricoles et des terres de pâturage comme composant des boues activées, couramment utilisées pour fertiliser les sols (Environnement Canada, 2006). De plus, la substance pourrait être libérée des textiles teints qui se retrouvent dans les sites d'enfouissement.
En solution, le BDAP se comporte comme une base, avec une valeur estimative de pKa jugée faible (1,85; voir le tableau 2). Par conséquent, les formes dissoutes de BDAP ne devraient pas s'ioniser dans l'eau à des pH pertinents au point de vue de l'environnement. D'après la solubilité dans l'eau de différents analogues (tableau 2), le BDAP ne devrait être que peu soluble et se comporter comme une dispersion colloïdale (Yenet al., 1991). De ce fait, lorsqu'elle est rejetée dans l'eau, cette substance devrait se retrouver principalement sous forme solide ou être adsorbée sur les particules en suspension pour enfin se déposer sur les couches de sédiments où elle devrait demeurer sous une forme qui n'est relativement pas biodisponible. Dans leur étude, Yen et al. (1989) ont conclu que les colorants dispersés ont tendance à s'accumuler abondamment dans les sédiments et le biote, sauf s'ils se dégradent aussi vite qu'ils sont absorbés. Razo-Flores et al. (1997), les colorants azoïques finissent par se retrouver dans des sédiments anaérobies, dans des aquifères et dans l'eau souterraine en raison de leur nature récalcitrante dans le milieu aérobie. Yenet al. (1991) ont observé que certains analogues de colorants à base d'azobenzène étaient transformés dans les sédiments, en anaérobie, par hydrolyse et réduction, et ont conclu que la plupart des colorants azoïques sont peu susceptibles de persister dans les systèmes sédimentaires anaérobies. Dans les sédiments enfouis, le BDAP peut subir une dégradation, comme cela est décrit dans la rubrique suivante sur la persistance.
La vitesse de volatilisation à partir de la surface de l'eau est proportionnelle à la constante de la loi de Henry (Baughman et Perenich, 1988). En outre, Baughman et Perenich (1988) mentionnent que la volatilisation à partir de systèmes aquatiques devrait être un processus de perte peu important pour les colorants dispersés, ce qui correspond à la valeur faible à négligeable de la constante de la loi de Henry (10-8 à 10-1 Pa m3/mol, données déduites à partir d'analogues du tableau 2). Le transport dans l'air qui résulte de la perte de cette substance des sols superficiels humides et secs n'est pas très important pour cette substance comme l'indique la très faible pression de vapeur du BDAP (5,33 × (10-12 à 10-5) Pa, données déduites à partir d'analogues du tableau 2). Ces données sont compatibles avec l'état physique (structure particulaire solide) du BDAP, état qui rend la substance peu sujette à la volatilisation.
Persistance et le potentiel de bioaccumulation
Persistance
Aucune donnée expérimentale sur la dégradation du BDAP n'a été trouvée. Aucune donnée de surveillance ayant trait à la présence de cette substance dans les milieux naturels (air, eau, sol et sédiments) n'a encore été relevée.
D'après l'Ecological and Toxicological Association of Dyes and Organic Pigments Manufacturers (ETAD, 1995), les teintures, à part quelques exceptions, sont considérées comme essentiellement non biodégradables dans des conditions aérobies. Des évaluations répétées de la biodégradabilité immédiate et intrinsèque à l'aide d'essais préliminaires acceptés (les Lignes directrices de l'OCDE pour les essais de produits chimiques) ont confirmé cette hypothèse (Pagga et Brown, 1986; ETAD, 1992). Étant donné la structure chimique du BDAP, rien ne permet de penser que sa biodégradation serait différente de celle des teintures généralement (ETAD, 1995).
Il a été démontré que certains colorants azoïques dispersés connaissent une biodégradation anaérobie relativement rapide dans les sédiments qui se trouvent en profondeur dans le sol, où les conditions anoxiques persistent (Yen et al., 1991; Baughman and Weber, 1994; Weber and Adams, 1995). Les colorants dispersés se répandent dans le système aquatique principalement par la dispersion de fines particules en suspension, s'accumulant ultérieurement dans les couches aérobies des sédiments de surface où ils resteront jusqu'à ce que l'enfouissement dans les sédiments crée un milieu réducteur. Le taux d'accumulation de sédiments et l'ampleur de la bioturbation varient d'un site à l'autre. Il est donc très difficile de déterminer le temps passé par les colorants sur les couches de sédiments aérobies. Cependant, il est probable que dans plusieurs cas ce taux soit supérieur à 365 jours. Une fois dans un milieu anaérobie ou réducteur, les colorants azoïques peuvent se dégrader rapidement en constituants amines aromatiques de substitution, comme l'ont démontré Yen et al. (1991) qui ont mesuré des valeurs de demi-vie de réduction de 2,9 heures à 2,0 jours pour les teintures à base d'azobenzène dans les sédiments compactés, à température ambiante. Toutefois, dans des sédiments anoxiques, le produit de la biodégradation ne devrait pas présenter un potentiel d'exposition élevé pour la majorité des organismes aquatiques, ni de préoccupation pour l'environnement.
Faute de données expérimentales sur la bioaccumulation du BDAP, une méthode du poids de la preuve reposant sur des RQSA (Environnement Canada, 2007) a été utilisée avec les modèles de dégradation indiqués dans le tableau 5 ci-dessous. Bien que l'on anticipe un rejet de BDAP dans les eaux usées, son temps de résidence dans la colonne d'eau peut être court avant qu'il s'écoule finalement dans le dépôt sédimentaire en raison de sa faible solubilité et de son comportement comme dispersion colloïdale. Cependant, faute de données à ce sujet, la persistance a surtout été examinée à l'aide de modèle de prédiction RQSA sur la biodégradation dans l'eau. L'analyse suivante concerne principalement la partie de cette substance actuellement dissoute dans l'environnement, tout en tenant compte du fait qu'il existe aussi une grande partie dispersée qui se présente sous la forme de particules solides. Le BDAP ne contient pas de groupements fonctionnels susceptibles d'entreprendre une hydrolyse en milieu anaérobie (les colorants sont connus pour être stables en milieu aqueux). Le tableau 5 résume les résultats des modèles RQSA disponibles sur la biodégradation dans l'eau.
| Processus du devenir | Modèle et base du modèle |
Résultat | Interprétation | Demi-vie extrapolée (jours) | Référence et/ou source d'extrapolation |
|---|---|---|---|---|---|
| Biodégradation (aérobique) | BIOWIN, 2000 Sous-modèle 1 : probabilité linéaire |
-0,44 | Ne se biodégrade pas rapidement dans l'eau | s. o. | s. o. |
| Biodégradation (aérobique) | BIOWIN, 2000 Sous-modèle 2 : probabilité non linéaire |
0,00 | Ne se biodégrade pas rapidement dans l'eau | s. o. | s. o. |
| Biodégradation (aérobique) | BIOWIN, 2000 Sous-modèle 3 : enquête d'expert (biodégradation ultime) |
1,05 | Récalcitrant | 182 | US EPA 2002 Aronson et al., 2006 |
| Biodégradation (aérobique) | BIOWIN, 2000 Sous-modèle 4 : enquête d'expert (biodégradation primaire) |
2,65 | Biodégradation primaire en semaines et en mois dans l'eau | 37,5 | US EPA 2002, Aronson et al., 2006 |
| Biodégradation (aérobique) | BIOWIN, 2000 Sous-modèle 5 : probabilité linéaire MITI |
-0,79 | Ne se biodégrade pas rapidement dans l'eau | supérieur(e) à 60 | Aronson et al., 2006 |
| Biodégradation (aérobique) | BIOWIN, 2000 Sous-modèle 6 : probabilité non linéaire MITI |
0,00 | Ne se biodégrade pas rapidement dans l'eau | supérieur(e) à 60 | Aronson et al., 2006 |
| biodégradation | BIOWIN, 2000 Conclusion générale |
No | Ne se biodégrade pas immédiatement dans l'eau | s. o. | s. o. |
| Biodégradation (aérobique) | CATABOL v. 5.10.2 % DBO (OCDE 301C) |
0 | Persistant dans l'eau | supérieur(e) à 182 | Calculé à partir de la DBO en supposant une cinétique de premier ordre |
Les résultats du tableau 5 montrent que la majorité des modèles de biodégradation (BIOWIN 1, 2, 3, 5, 6 et 7) indiquent que cette substance ne se biodégrade pas rapidement. Les probabilités sont en fait toutes inférieures à 0,3, seuil suggéré par Aronson et al. (2006) pour trouver les substances qui ont une demi-vie de plus de 60 jours (selon les modèles de probabilité du MITI). Le résultat de la demi-vie du modèle d'enquête primaire (BIOWIN 4) des « semaines-mois » pourrait signifier environ 37,5 jours (US EPA, 2002; Aronsonet al., 2006), bien que la nature du produit de dégradation soit inconnue. Le résultat du modèle d'enquête ultime (BIOWIN 3) de « récalcitrant » pourrait signifier plus de 182 jours, selon la US EPA (2002). Conclusion générale de BIOWIN : « pas immédiatement biodégradable ».
Selon un autre modèle de dégradation ultime, CATABOL, le BDAP sera persistant dans l'eau.
Lorsque les modèles de probabilité, la conclusion générale de BIOWIN et les modèles de dégradation ultime sont pris en compte, un plus grand consensus s'en dégage pour suggérer que la demi-vie de la biodégradation dans l'eau est supérieure à 182 jours. Ce résultat correspond à ce qu'on s'attend de cette structure chimique (c.-à-d., peu de groupements fonctionnels dégradables, particules solides peu solubles).
D'après un ratio d'extrapolation de 1:1:4 pour une demi-vie de biodégradation dans l'eau, le sol et les sédiments (Boethling, et al., 1995), la demi-vie de biodégradation dans le sol est aussi supérieure à 182 jours et la demi-vie dans les sédiments est supérieure à 365 jours. Cela indique que le BDAP devrait être persistant dans le sol et les sédiments.
D'après les données modélisées pour la dégradation ultime (voir tableau 5 ci-dessus) et l'avis d'expert (ETAD, 1995), le BDAP répond aux critères de la persistance dans l'eau, le sol (demi-vies dans le sol et dans l'eau 182 jours), les sédiments (demi-vie dans les sédiments de 365 jours) énoncés dans le Règlement sur la persistance et la bioaccumulation(Canada, 2000).
Potentiel de bioaccumulation
Aucune donnée expérimentale sur la bioaccumulation n'est disponible pour le BDAP. Les modèles de bioaccumulation disponibles étant inapplicables aux colorants azoïques, les prévisions fondées sur ces modèles ne sont pas jugées assez fiables pour ce lot de substances. De ce fait, la présente évaluation ne tient pas compte de ces modèles pour l'évaluation de la bioaccumulation du BDAP.
Face au manque de données expérimentales et modélisées, des facteurs de bioconcentration (FBC) et de bioaccumulation (FBA) pour analogues structuraux ont été utilisés pour estimer le potentiel de bioaccumulation du BDAP. Pour ce faire, les données relatives à la bioaccumulation du Disperse 79:1, de la substance 68877-63-4 et du Disperse Orange 30 ont été examinées pour vérifier leur pertinence quant au BDAP. Une étude sur la bioconcentration d'un analogue structural relativement similaire, le Disperse Orange 30, indique qu'il est peu probable qu'il s'accumule dans l'organisme des poissons (Shen et Hu, 2008). Cette étude a été menée en conformité avec les Lignes directrices de l'OCDE pour les essais de produits chimiques, no 305B-1996, « Bioconcentration: Semi-Static Fish Test ». L'effet de bioconcentration du Disperse Orange 30 chez le poisson-zèbre (Brachydanio rerio) été déterminé par un essai de 28 jours en régime semi-statique, avec renouvellement du milieu d'essai tous les deux jours. Afin de vérifier le potentiel de bioconcentration de la substance d'essai, un essai en phase d'exposition à une concentration nominale de 20 mg/L (concentration moyenne mesurée entre 0,028 et 0,28 mg/L) a été mené en tenant compte du résultat obtenu lors de l'essai de toxicité aiguë pour le poisson. Des échantillons ont été prélevés quotidiennement des milieux et des organismes d'essai, à partir du 26e jour jusqu'à la dernière journée de la période d'exposition de 28 jours. On a préparé les échantillons en extrayant le composant lipidique des poissons à l'étude. La concentration mesurée de la substance d'essai, la teneur en lipides des poissons et le facteur de bioconcentration (FBC) figurent au tableau 6.
| Traitements (20 mg/L) | 26e jour de l'échantillonnage | 27e jour de l'échantillonnage | 28e jour de l'échantillonnage |
|---|---|---|---|
| Concentration mesurée de la substance d'essai dans les solutions extraites (mg/L) | inférieur(e) à 0,028 | inférieur(e) à 0,028 | inférieur(e) à 0,028 |
| Quantité de la substance d'essai dans les lipides des poissons (mg) | inférieur(e) à 1,68 | inférieur(e) à 1,68 | inférieur(e) à 1,68 |
| Poids total des poissons (g) | 2,07 | 2,13 | 2,53 |
| Concentration de la substance d'essai dans les lipides des poissons CP (mg/kg) | inférieur(e) à 0,81 | inférieur(e) à 0,79 | inférieur(e) à 0,66 |
| Concentration mesurée de la substance d'essai dans l'eau CE (mg/L) | 0,028 ~ 0,28 | 0,028 ~ 0,28 | 0,028 ~ 0,28 |
| Teneur en lipides des poissons (%) | 0,81 | 0,57 | 1,25 |
| FBC | inférieur(e) à 100 | inférieur(e) à 100 | inférieur(e) à 100 |
| FBC moyen | inférieur(e) à 100 | inférieur(e) à 100 | inférieur(e) à 100 |
L'étude de Shen et Hu (2008) a été revue et jugée acceptable (voir l'annexe 1). La non-détection dans les extraits de poisson (inférieur(e) à 0,028 mg/L) indiquerait une solubilité limitée dans les lipides ou un potentiel limité de répartition dans les tissus des poissons des systèmes aqueux. Toutefois, dans toute étude, certaines incertitudes demeurent concernant les valeurs limites parce qu'on ne connaît pas la « vraie » valeur. Par contre, vu la structure et le comportement probable des colorants dispersés dans les systèmes aqueux, étant donné le faible résultat pour le FBC n'est pas inattendu. La plupart des colorants dispersés, ainsi que leur nom le laisse entendre, se présentent sous la forme de fines particules dispersibles aux fractions réellement solubles limitées. Leur solubilité peut, toutefois, être augmentée en ajoutant à la molécule des groupements fonctionnels polarisés. Alors que le BDAP contient certains des groupes fonctionnels solubilisants (groupements amide et nitro), les valeurs expérimentales de solubilité obtenues pour les analogues contenant plusieurs des mêmes groupes sont plutôt faibles.
Bien que l'étude mentionnée plus haut constitue la preuve principale du faible potentiel de bioaccumulation du BDAP, d'autres recherches viennent corroborer cette conclusion. Anliker et al., (1981) présentent des valeurs expérimentales sur la bioaccumulation dans les poissons pour 18 colorants monoazoïques dispersés, valeurs obtenues suivant les méthodes prescrites par le ministère du Commerce international et de l'Industrie du Japon (MITI). Le log des facteurs de bioaccumulation (FBC) variait entre 0,00 et 1,76 et est exprimé en fonction du poids humide total des poissons (Anliker et al., 1981). Vu l'absence de déclaration de numéros de registre de substances chimiques et de structures chimiques, l'utilité de cette étude était limitée en ce qui a trait aux données déduites à partir d'analogues du BDAP. Des études de suivi, qui faisaient état des structures chimiques des colorants dispersés à l'essai, ont toutefois confirmé le faible potentiel de bioaccumulation de dix colorants azoïques du groupe nitro et ont indiqué un log des facteurs de bioaccumulation variant entre 0,3 et 1,76 (Anliker et Moser, 1987; Anliker et al., 1988). Plus précisément, le log des facteurs de bioaccumulation pour un analogue très similaire au BDAP (no CAS : 68877-63-4) était de 10. Des études du MITI viennent également appuyer le faible potentiel de bioaccumulation des colorants azoïques dispersés. Les facteurs de bioconcentration déclarés de trois colorants azoïques dispersés (nos CAS 40690-89-9, 61968-52-3 et 71767-67-4) testés à une concentration de 0,01 mg/L variaient entre moins de 0,3 jusqu'à 47 (MITI, 1992). Une étude sur l'accumulation d'une durée de huit semaines réalisée par Brown (1987) montre également qu'aucun des douze colorants dispersés ayant été testés ne s'accumulait chez la carpe.
La seule source de données probantes indiquant que le BDAP pourrait avoir un potentiel élevé de bioaccumulation est une valeur médiane élevée calculée à partir d'une analogue du log Koe de 4,3 pour le BDAP (tableau 2). Malgré les valeurs élevées du log Koe déduites à partir d'analogues structuraux du BDAP, la preuve de la bioaccumulation des colorants azoïques dispersés est insuffisante (Anliker et al., 1981; Anliker et Moser, 1987; Anliker et al., 1988, MITI 1992). Selon les auteurs qui ont mesuré des valeurs élevées du log Koe et de faibles facteurs de bioaccumulation concomitants pour les colorants azoïques dispersés, les facteurs d'accumulation faibles pourraient s'expliquer, dans certains cas, par leur faible liposolubilité absolue (Brown, 1987) ou leur masse moléculaire relativement élevée (généralement entre 450 et 550 g/mol), ce qui pourrait rendre difficile le transport de ces substances à travers les membranes des poissons (Anliker et al., 1981; Anliker et Moser, 1987). Il se peut aussi que le manque de biodisponibilité et le comportement de répartition limité imposés par les conditions d'essai sur le FBC restreignent l'accumulation dans les tissus lipidiques des poissons.
Selon l'ETAD (1995), les caractéristiques moléculaires indiquant une absence de bioaccumulation sont une masse moléculaire supérieure à 450 g/mol et un diamètre transversal supérieur à 1,05 nm. D'après une étude récente menée par Dimitrov et al., 2002; Dimitrov et al., (2005) et le BBM (2008), la probabilité qu'une molécule traverse des membranes cellulaires à la suite d'une diffusion passive diminue de façon importante lorsque le diamètre transversal maximal (Dmax) augmente. La probabilité qu'une diffusion passive se produise diminue de façon notable lorsque le diamètre transversal est supérieur à environ 1,5 nm et de façon encore plus significative dans le cas des molécules ayant un diamètre transversal supérieur à 1,7 nm. Sakurataniet al., (2008) ont également étudié l'effet du diamètre transversal sur la diffusion passive à l'aide d'un ensemble d'essais comptant environ 1 200 substances chimiques nouvelles et existantes et ont aussi observé que les substances dont le potentiel de bioconcentration n'était pas très élevé avaient souvent un Dmax supérieur(e) à 2,0 nm ainsi qu'un diamètre effectif (Deff) supérieur(e) à 1,1 nm.
Le BDAP a une masse moléculaire de 479,3 g/mol (voir le tableau 1) et sa structure moléculaire est relativement simple; la seconde caractéristique, en particulier, indique une capacité de bioaccumulation potentielle. En outre, un rapport d'Environnement Canada (2007) indique qu'il n'y a pas de preuves évidentes qui permettraient de fixer une valeur de taille moléculaire de démarcation pour évaluer le potentiel de bioaccumulation. Ce rapport ne met toutefois pas en cause la notion selon laquelle la réduction du taux d'absorption pourrait être associée à l'augmentation du diamètre transversal, comme cela a été démontré par Dimitrov et al., (2002, 2005). Le diamètre maximal du BDAP et de ses conformères varie entre 1,43 jusqu'à 1,80 nm (BBM, 2008), ce qui indiquerait que, en ce qui concerne ce colorant, il y a une possibilité de réduction importante du taux d'absorption dans l'eau et de la biodisponibilité in vivo.
Toutefois, compte tenu de l'absence d'accumulation observée lors des essais de bioconcentration sur le BDAP et sur d'autres colorants azoïques dispersés apparentés, et de la grande taille de la molécule du BDAP, qui restreint vraisemblablement son comportement de répartition, le BDAP présenter un faible potentiel de bioaccumulation. Par conséquent, si l'on tient compte de la preuve du facteur de bioconcentration des analogues ainsi que des considérations sur la biodisponibilité et la structure, le BDAP ne répond pas au critère de bioaccumulation (FBC ou FBA 5 000) énoncé dans le Règlement sur la persistance et la bioaccumulation (Canada, 2000).
Potentiel d'effets nocifs sur l'environnement
Évaluation des effets sur l'environnement
A - Dans le milieu aquatique
Une seule étude empirique soutenant la toxicité du BDAP a été présentée (SafePharm, 1990). D'après cette étude, le BDAP présente une CL50 (96 h) supérieure à 100 mg/L chez la truite arc-en-ciel (Salmo gairdneri) (tableau 7a). Or, cette étude n'a pas été jugée fiable, car trop peu détaillée (voir l'annexe 1 pour connaître le sommaire de rigueur d'étude). En outre, l'ordre de grandeur de la CL50 présentée dans cette étude est quatre fois supérieur à la valeur prévue de la solubilité aqueuse du BDAP (c.-à-d. une médiane des données des analogues ~ 0,005 mg/L, au tableau 2).
| Organisme d'essai | Type d'essai | Durée (en heures) |
Paramètre | Fiabilité de l'étude | Valeur (mg/L) | Références |
|---|---|---|---|---|---|---|
| Salmo gairdneri | Tox. aiguë | 96 | La concentration médiane d'une substance qui serait létale pour 50 % des organismes de l'essai (CL50) | Peu fiable | supérieur(e) à 100 | SafePharm, 1990 |
Des données écotoxicologiques ont été trouvées pour plusieurs des analogues du BDAP (tableau 7b). Une étude présentée pour le compte de l'ETAD fournit des données écotoxicologiques aiguës pour les poissons, les invertébrés, les algues et les bactéries pour cinq colorants dispersés azoïques du groupe nitro, dont les analogues très similaires au Disperse Blue 79 (Brown, 1992) La toxicité aiguë chez les poissons zèbres, Daphnia magna et Scenedesmus subspicatus, pour les cinq analogues variait de 17 à 710 mg/L, 4,5 à 110 mg/L et 6,7 à 54 mg/L, respectivement (tableau 7b). De plus, tous les essais à l'aide de bactéries avaient une CI50 dépassant 100 mg/L. Le protocole expérimental détaillé de l'étude portant sur les colorants testés n'a pas été fourni, ce qui restreint grandement l'évaluation de ces études (Brown, 1992). Toutefois, on a jugé que ces données pouvaient être utilisées et elles sont comprises dans cette ébauche d'évaluation préalable en tant qu'élément dans l'établissement du poids de la preuve.
Une autre étude de la toxicité aiguë pour le poisson a été présentée pour le Disperse Blue 79 (BASF, 1990). Selon cette étude, le Disperse Blue 79 a une CL50 (96 h) comprise entre 100 et 220 mg/L pour l'ide dorée (Leuciscus idus). Cependant, la fiabilité de cette étude est incertaine étant donné le manque de détails fournis (annexe 1).
Environnement Canada a reçu des données écotoxicologiques sur un autre colorant azoïque dispersé présentant une structure similaire en vertu du Règlement sur les renseignements concernant les substances nouvelles (Environnement Canada, 1995). Une étude de la toxicité aiguë pour le poisson soumise en vue de satisfaire aux exigences en matière de déclaration a révélé que cette substance présentait une CL50 (96 h) de 505 mg/L chez la truite arc-en-ciel (Onchorhynchus mykiss) (tableau 7b). Cet essai a été mené en conformité avec les Lignes directrices de l'OCDE no 203. Les fiches techniques santé-sécurité (FTSS) sur la substance déclarée contiennent également de l'information relative aux effets toxiques bactériens. Les résultats de cet essai indiquent une CE50 supérieur(e) à 100 mg/L pour l'inhibition de respiration de boues activées. D'après les données disponibles sur l'écotoxicité, les effets toxiques de la substance déclarée devraient être peu préoccupants pour les organismes aquatiques. La fiabilité de cet essai a été évaluée à l'aide d'un sommaire de rigueur d'études et elle est jugée satisfaisante (annexe 1).
Enfin, une étude sur la toxicité chronique présentée pour le Disperse Blue 79:1 a révélé que la concentration estimée sans effet (CESE) chez la truite arc-en-ciel (Onchorhynchus mykiss) est supérieure à 0,0048 mg/L (tableau 7b). Cette étude a été évaluée et jugée très fiable (annexe 1). Toutefois, comme cette valeur est un résultat non borné fondé sur une hypothèse, elle n'a pas été utilisée pour calculer la concentration estimée sans effet (CESE). En tenant compte de toute l'information sur la toxicité des analogues structuraux et de la valeur de la toxicité expérimentale propre au BDAP, ces données suggèrent que cette substance n'est pas très dangereuse pour les organismes aquatiques (c.-à-d., des valeurs de CL50 aiguë supérieures à 1 mg/L).
| Nom commun ou no CAS | Organisme d'essai | Paramètre | Valeur (mg/L) | Références |
|---|---|---|---|---|
| Disperse Blue 79 | Ide dorée | CL50 | 100 inférieur(e) à CL50 inférieur(e) à 220 | BASF, 1990 |
| Disperse Blue 79 | Poisson-zèbre | CL50 | 340 | Brown, 1992 |
| Disperse Blue 79 | Daphnia magna | La concentration médiane d'une substance qui causerait des effets toxiques sublétaux chez 50 % des organismes de l'essai (CE50) | 4,5 | Brown, 1992 |
| Disperse Blue 79 | Scenedesmus subspicatus | CE50 | 9,5 | Brown, 1992 |
| Disperse Blue 79 | Bactérie | La concentration médiane d'une substance qui inhiberait la croissance pour 50 % des organismes de l'essai (CI50) | supérieur(e) à 100 | Brown, 1992 |
| Disperse Red 73 | Poisson-zèbre | CL50 | 17 | Brown, 1992 |
| Disperse Red 73 | Daphnia magna | CE50 | 23 | Brown, 1992 |
| Disperse Red 73 | Scenedesmus subspicatus | CE50 | supérieur(e) à 10 | Brown, 1992 |
| Disperse Red 73 | Bactérie | CI50 | supérieur(e) à 100 | Brown, 1992 |
| Disperse Orange 30 | Poisson-zèbre | CL50 | 710 | Brown, 1992 |
| Disperse Orange 30 | Daphnia magna | CE50 | 5,8 | Brown, 1992 |
| Disperse Orange 30 | Scenedesmus subspicatus | CE50 | 6,7 | Brown, 1992 |
| Disperse Orange 30 | Bactérie | CI50 | supérieur(e) à 100 | Brown, 1992 |
| Disperse Orange 25 | Poisson-zèbre | CI50 | 268 | Brown, 1992 |
| Disperse Orange 25 | Daphnia magna | CL50 | 110 | Brown, 1992 |
| Disperse Orange 25 | Scenedesmus subspicatus | CE50 | 54 | Brown, 1992 |
| Disperse Orange 25 | Bactérie | CE50 | supérieur(e) à 100 | Brown, 1992 |
| Disperse Red 17 | Poisson-zèbre | CL50 | 103 | Brown, 1992 |
| Disperse Red 17 | Daphnia magna | CE50 | 98 | Brown, 1992 |
| Disperse Red 17 | Scenedesmus subspicatus | CE50 | 7 | Brown, 1992 |
| Disperse Red 17 | Bactérie | CI50 | supérieur(e) à 100 | Brown, 1992 |
| Analogue de colorant azoïque dispersé | Truite arc-en-ciel | CL50 | 505 | Environnement Canada, 1995 |
| Disperse Blue 79:1 | Truite arc-en-ciel | CSEO (122 jours) | supérieur(e) à 0,0048 | Cohle et Mihalik, 1991 |
En général, en raison de leur faible solubilité (inférieur(e) à 1 mg/L), on s'attend à ce que les colorants dispersés aient peu d'effets écologiques aigus (Hunger, 2003). Les résultats des études empiriques sur la toxicité portant sur le BDAP et plusieurs de ses analogues concordent avec ces prévisions, indiquant des valeurs CL50 chez le poisson comprises entre 17 et 505 mg/L, la Daphnia étant l'organisme testé le plus sensible (CE50/CL50 allant de 4,5 à 110 mg/L). L'interprétation des résultats de ces tests est difficile du fait que ces valeurs avec effet (c.-à-d., CE50 et CL50) sont largement supérieures à la solubilité des substances testées et de le BDAP, mais les données disponibles déduites à partir d'analogues montrent effectivement que le BDAP est sans doute peu toxique.
Une gamme de prévisions de la toxicité du BDAP pour les organismes aquatiques a également été obtenue à l'aide de divers modèles RQSA. Toutefois, comme c'était le cas pour la bioaccumulation, ces prévisions des RQSA n'ont pas été jugées fiables à cause de l'erreur possible associée aux paramètres d'entrée et de la nature particulière des colorants dispersés, comme les propriétés structurales et/ou physicochimiques qui sont hors du domaine d'applicabilité des modèles.
Les informations empiriques disponibles au sujet de l'écotoxicité du BDAP et de plusieurs de ses analogues indiquent donc que la substance ne constitue pas un danger très élevé pour les organismes aquatiques.
B - Dans d'autres milieux naturels
Étant donné que le BDAP peut pénétrer dans le sol potentiellement à partir des boues activées communément utilisées pour amender les sols ou à partir de l'élimination de produits qui se dégradent et rejettent le BDAP, il est souhaitable d'obtenir les données de toxicité vis-à-vis des organismes dans le sol. Malgré l'absence d'étude appropriée sur les effets écologiques de ce composé sur le sol, l'examen des données de toxicité sur les organismes aquatiques ainsi que l'absence de potentiel de bioaccumulation et sa faible biodisponibilité indiquent que le potentiel de toxicité pour les organismes du sol est probablement faible. Pour les mêmes raisons, la toxicité potentielle est probablement faible pour les espèces vivant dans les sédiments, bien qu'aucune preuve ne puisse étayer cette assertion en raison de l'absence de données sur la toxicité du BDAP ou d'analogues appropriés pour les organismes entiers vivant dans les sédiments.
Évaluation de l'exposition de l'environnement
Aucune donnée sur les concentrations de cette substance dans l'eau au Canada n'a été retracée. On a donc évalué les concentrations dans l'environnement sur la base des renseignements disponibles, notamment les quantités de la substance sur le marché, les taux de rejet estimés et les caractéristiques des cours d'eau récepteurs. Pour examiner la question des rejets issus des activités industrielles, l'outil générique d'estimation de l'exposition attribuable à des rejets industriels en milieu aquatique (IGETA) d'Environnement Canada a servi à estimer la concentration (la pire éventualité) de la substance dans un cours d'eau générique qui reçoit des effluents industriels (Environnement Canada, 2008c). Le scénario générique vise à fournir des estimations fondées sur des hypothèses prudentes sur la quantité de la substance traitée et rejetée, le nombre de jours de traitement, le taux d'élimination de l'usine de traitement des eaux usées et la superficie du cours d'eau récepteur. Le scénario modélisé tient compte des données sur la charge obtenues de sources telles que des enquêtes industrielles, ainsi que des connaissances sur la distribution des rejets industriels au pays, et calcule la concentration environnementale estimée (CEE). L'équation et les entrées utilisées pour calculer la CEE dans les eaux réceptrices sont décrites dans le rapport d'Environnement Canada (2008d). La quantité maximale utilisée par une seule installation a servi à calculer la CEE dans l'environnement récepteur. Pour rendre ce scénario d'exposition plus concret, le taux moyen du traitement des eaux usées (0,282 m3/s) et 10e percentile du courant du cours d'eau récepteur pour la collectivité qui abrite cette installation (5,6 m3/s) ont été entrées dans le modèle IGETA pour remplacer les valeurs par défaut. Pour ajouter à la prudence de cette évaluation, on a présumé que le rendement d'élimination de l'usine de traitement des eaux usées (STP) était de 0 %, bien que l'usine de traitement des eaux usées de cette installation faisait bien le traitement secondaire. D'après ces hypothèses, le modèle IGETA a permis de calculer une valeur prudente de la CEE de 0,014 mg/L pour le cours d'eau récepteur (Environnement Canada, 2008d).
Pour évaluer les rejets issus d'une utilisation par les consommateurs vers le réseau d'égouts, on a utilisé l'outil Mega Flush d'Environnement Canada. Mega Flush a permis d'évaluer les concentrations possibles de la substance dans différents cours d'eau récepteurs d'effluents issus des usines de traitement des eaux usées dans lesquelles ont été rejetés par les consommateurs des produits contenant cette substance (Environnement Canada, 2008e). Ce modèle est conçu de manière à fournir des estimations sur la base d'hypothèses prudentes en ce qui concerne la quantité de produit chimique utilisé et rejeté par les consommateurs. Par défaut, les taux d'élimination primaire et secondaire de l'usine de traitement des eaux usées sont supposés être de 0 % - fraction rejetée pendant une utilisation de 100 %; l'utilisation de la substance par les consommateurs est fixée à plus de 365 jours par an et le débit retenu pour le rejet vers les cours d'eau récepteurs sur tous les sites est au 10e percentile de la valeur. Ces estimations sont réalisées pour 1 000 sites de rejet environ dans tout le Canada, prenant donc en compte les usines de traitement des eaux usées les plus importantes du pays. Les conséquences induites globalement par ces paramètres font que ce scénario est comparable à une situation réaliste de pire éventualité. Ces valeurs de paramètres sont estimées correspondre à un scénario très prudent.
L'équation et les entrées utilisées dans l'outil Mega Flush pour calculer la concentration environnementale estimée (CEE) dans les eaux réceptrices sont décrites dans le rapport d'Environnement Canada (2008f). L'outil de débit massique a été utilisé pour prévoir les rejets vers les eaux (égouts) provenant de l'utilisation de produits de formulation et de l'utilisation par les consommateurs de produits contenant cette substance. Dans le scénario qui a été retenu, on a présumé que les consommateurs utilisaient 30 184 kg/an de cette substance (Environnement Canada, 2008b). Cette quantité utilisée par les consommateurs a été évaluée de manière prudente en se basant sur la masse totale de la substance qui aurait été importée au Canada par moins de quatre entreprises, d'après les enquêtes menées en vertu de l'article 71, et en appliquant un rapport de 30/70 entre les textiles fabriqués au Canada et ceux d'importation. On prend l'hypothèse d'une perte de 10 % de teinture pour la quantité totale de substance utilisée par les consommateurs (Øllgaard et al., 1998). On a donc estimé que 3 018 kg de BDAP étaient rejetés dans l'eau à la suite de pertes se retrouvant dans les égouts, au cours du lavage d'articles manufacturés qui contiennent cette teinture, mais sont fabriqués dans un autre pays, ainsi que d'articles fabriqués au Canada qui contiennent cette teinture (Environnement Canada, 2008b).
Sur la base de ce scénario, les estimations de l'outil Mega Flush donnent des valeurs de CEE dans les cours d'eau récepteurs variant de 0,00038 à 0,0046 mg/L.
Caractérisation des risques pour l'environnement
La concentration estimée sans effet (CESE) a été évaluée en se fondant sur la CE50 de 48 h de 4,5 mg/L chez Daphnia magna pour un analogue du Disperse Blue 79 (Tableau 7b). On a ensuite appliqué un facteur de 100 pour tenir compte de la toxicité aiguë à la toxicité chronique et des extrapolations au terrain des résultats en laboratoire et de l'utilisation d'une substance de remplacement. La concentration estimée sans effet (CESE) ainsi obtenue est de 0,045 mg/L.
Quand on le compare à la CEE prudente calculée plus haut à l'aide de l'IGETA, le quotient de risque applicable aux rejets industriels (CEE/CESE) est de 0,014/0,045 = 0,3. Les concentrations de BDAP dans les eaux de surface provenant de rejets industriels au Canada ne semblent donc pas susceptibles d'avoir des effets nocifs sur les organismes aquatiques. Étant donné que l'IGETA fournit une estimation prudente de l'exposition et du risque, les résultats indiquent que l'exposition locale attribuable à une source ponctuelle de rejets industriels en milieu aquatique présente un faible potentiel de risques pour l'environnement.
Concernant l'exposition attribuable aux rejets à l'égout issus d'utilisations par les consommateurs (scénario très prudent), il est estimé d'après les résultats de Mega Flush que la CEE ne dépassera pas la CESE quel que soit le site (c.-à-d. tous les quotients de risque inférieur(e) à 1). Cela montre que les rejets des consommateurs dans le réseau d'égouts de BDAP ne devraient pas être nocifs pour les organismes aquatiques.
Compte tenu des renseignements disponibles, on s'attend à ce que le BDAP soit persistant dans l'eau, le sol et les sédiments, mais il devrait avoir un faible potentiel de bioaccumulation. Les quantités de BDAP relativement élevées importées au Canada ainsi que les renseignements sur ses propriétés physiques et chimiques et ses utilisations indiquent un potentiel faible à modéré de rejets dans l'environnement au Canada. S'il est rejeté dans l'environnement, on s'attend à ce que le BDAP soit principalement déversé dans les eaux de surface où il devrait finir par se déposer dans les sédiments. L'utilisation de données déduites à partir d'analogues a permis de démontrer que le BDAP présente seulement un potentiel faible à modéré de toxicité aiguë pour les organismes aquatiques. Les quotients de risque associés à l'exposition aquatique montrent que la concentration de BDAP ne dépasse probablement pas celle où se manifestent des effets, même lorsque des hypothèses et des scénarios prudents sont évoqués. Par conséquent, il est peu probable que le BDAP nuise aux populations d'organismes aquatiques au Canada.
Incertitudes dans l'évaluation des risques pour l'environnement
Une zone d'incertitude pour le BDAP tient à l'utilisation des données déduites à partir d'analogues pour déterminer ses propriétés physiques et chimiques, ainsi que des données sur la toxicité provenant d'analogues. Bien que les produits chimiques identifiés (Disperse Blue 79, Disperse Blue 79:1, Disperse Orange 30, Disperse Orange 25, Disperse Red 17 et Disperse Red 73) aient beaucoup de similitudes avec le BDAP, étant entre autres des colorants azoïques de poids moléculaire élevé, présentant un diamètre transversal similaire, ayant une structure particulaire solide qui se décompose au-delà de 74 °C et étant « dispersibles » dans l'eau (c'est-à-dire pas entièrement solubles), ils présentent des différences au niveau des groupes fonctionnels. Ces différences au niveau de la structure chimique ajoutent une part d'incertitude, car les propriétés et la toxicité du BDAP peuvent être quelque peu différentes. Toutefois, il a été estimé que les similitudes sont suffisantes pour inclure les données des analogues dans le poids de la preuve pour l'évaluation du BDAP.
L'évaluation de la persistance est limitée par le manque de données sur la biodégradation, ce qui a nécessité la production de prévisions modélisées. Bien que toutes les prévisions modélisées comportent un certain degré d'erreur, les résultats du modèle de biodégradation aérobique ont confirmé la persistance attendue du BDAP, compte tenu de ses utilisations et de ses caractéristiques structurales. De plus, l'évaluation de la persistance est limitée par les incertitudes quant à la vitesse de dégradation et à la mesure dans laquelle cette dégradation se produit dans des sédiments anaérobiques ainsi qu'à la détermination de la biodisponibilité des produits de dégradation (p. ex., amines). Néanmoins, il est clair que la dégradation anaérobie de la fraction biodisponible des colorants azoïques en amines constitutives dans les sédiments est beaucoup plus rapide (demi-vies de l'ordre de jours) que la dégradation aérobie. On ne prévoit pas une biodisponibilité des produits de dégradation aminés du fait qu'ils se forment uniquement dans les sédiments anoxiques relativement profonds et peuvent être liés de manière irréversible aux sédiments, par addition nucléophile et par couplage radicalaire oxydant (Colon et al., 2002; Weberet al., 2001), ce point constitue une source d'incertitude dans l'évaluation du BDAP.
L'évaluation de la bioaccumulation de cette substance a été limitée par le manque de données empiriques et l'incapacité des modèles disponibles à estimer de façon fiable la bioaccumulation de colorants azoïques. L'évaluation était plutôt fondée sur l'utilisation de données sur la bioaccumulation pour un analogue structural.
Il existe également des incertitudes liées au manque de données sur les concentrations de BDAP dans l'environnement canadien. Cependant, l'absence de rapports sur sa fabrication au Canada, son taux de fixation élevé sur les textiles et le taux d'élimination élevé prévu des usines de traitement des eaux usées suggèrent un faible risque de rejet de ce produit chimique dans l'environnement canadien.
Les concentrations expérimentales, associées à la toxicité intrinsèque pour les organismes aquatiques, peuvent constituer une source additionnelle d'incertitude lorsqu'elles dépassent la solubilité du produit chimique dans l'eau (expérimentale ou prédite). Malgré ce fait, les données dont on dispose indiquent que le BDAP n'est pas très dangereux pour les organismes aquatiques.
La fraction de la substance qui est rejetée pendant son utilisation et celle qui est éliminée dans les usines de traitement des eaux usées constituent une autre source d'incertitude. Ces incertitudes ont été atténuées par le recours à des hypothèses relativement prudentes dans la modélisation de l'exposition.
Quant à l'écotoxicité, le comportement de répartition prévu de ce produit chimique montre que les données disponibles sur les effets ne permettent pas d'évaluer comme il se doit l'importance du sol et des sédiments comme milieu d'exposition. En fait, les seules données qui ont été trouvées sur les effets portent principalement sur l'exposition des organismes pélagiques.
Conclusion
D'après les renseignements contenus dans ce rapport d'évaluation préalable, le BDAP ne pénètre pas dans l'environnement en une quantité, à une concentration ou dans des conditions qui ont ou peuvent avoir un effet nuisible immédiat ou à long terme sur l'environnement ou sa diversité biologique, ou qui constituent ou peuvent constituer un danger pour l'environnement essentiel pour la vie.
Par conséquent, il est proposé de conclure que le BADP ne correspond pas à la définition de « substance toxique » énoncée dans l'article 64 de la LCPE (1999). De plus, cette substance répond aux critères de potentiel de persistance, mais ne répond pas à ceux du potentiel de bioaccumulation énoncés dans le Règlement sur la persistance et la bioaccumulation (Canada, 2000).
Références
ACD/pKaDB [module prédictif]. 2005. Version 9.04. Toronto (Ont.) : Advanced Chemistry Development. http://www.acdlabs.com/products/phys_chem_lab/pka/
All Business. 2000. [Article sur Internet]. New products from Ciba Specialty chemicals. http://www.allbusiness.com/manufacturing/textile-product-mills/902357-1.html
Anliker, R., Clarke, E.A., Moser, P. 1981. Use of the partition coefficient as an indicator of bioaccumulation tendency of dyestuffs in fish. Chemosphere. 10(3):263-274.
Anliker, R., Moser, P. 1987. The limits of bioaccumulation of organic pigments in fish: their relation to the partition coefficient and the solubility in water and octanol. Ecotoxicol. Environ. Safety 13:43-52.
Anliker, R., Moser, P., Poppinger, D. 1988. Bioaccumulation of dyestuffs and organic pigments in fish. Relationships to hydrophobicity and steric factors. Chemosphere. 17(8):1631-1644.
Aronson D., Boethling B., Howard P., Stiteler W., 2006. Estimating biodegradation half-lives for use in chemical screening. Chemosphere. 63:1953-1960.
BASF. 1990. Bericht uber die Prufung der akuten Toxizitit an der Goldorfe (Leuciscus idus L., Goldvariante). Présenté par l'ETAD à Environnement Canada le 13 août 2008 par courriel.
Baughman, GL., Perenich, T.A. 1988. Fate of dyes in aquatic systems: I. Solubility and partitioning of some hydrophobic dyes and related compounds. Environ. Toxicol. Chem.7(3):183-199.
Baughman, G.L., Weber, E.J. 1994. Transformation of dyes and related compounds in anoxic sediment: kinetics and products. Environ. Sci. Technol. 28(2):267-276.
[BBM] Baseline Bioaccumulation Model. 2008. Gatineau (Qc) : Environnement Canada, Division des substances existantes. [modèle élaboré d'après Dimitrov et al., 2005]. [consulté le 21 novembre 2008]. Disponible sur demande.
[BIOWIN] Biodegradation Probability Program for Windows [modèle d'estimation]. 2000. Version 4.20. Washington (DC) : US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY) : Syracuse Research Corporation. http://www.epa.gov/oppt/exposure/pubs/episuite.htm
Boethling, R.S., Howard, P.H., Beauman, J.A., Larosche, M.E. 1995. Factors for intermedia extrapolations in biodegradability assessment. Chemosphere. 30(4):741-752.
Brown D., 1987. Effects of colorants in the aquatic environment. Ecotox. Environ. Safe. 13:139-47.
Brown, D. (ICI Group Environmental Laboratory, Brixham, UK). 1992. Environmental assessment of dyestuffs. Rédigé pour le compte de l'Ecological and Toxicological Association of the Dyes and Organic Pigments Manufacturers, Bâle, Suisse. ETAD ecological sub-committee project E3020. Présenté à Environnement Canada le 9 mai 2008.
Canada. 1999. Loi canadienne sur la protection de l'environnement (1999), L.C. 1999, chap. 33. Partie III. vol. 22, no 3. http://canadagazette.gc.ca/partIII/1999/g3-02203.pdf
Canada. 2000. Loi canadienne sur la protection de l'environnement (1999) : Règlement sur la persistance et la bioaccumulation, C.P. 2000-348, 23 mars 2000, DORS/2000-107, Gazette du Canada. Partie II, vol. 134, no 7, p. 607-612. http://canadagazette.gc.ca/partII/2000/20000329/pdf/g2-13407.pdf
Canada. Ministère de l'Environnement, ministère de la Santé. 2006a. Loi canadienne sur la protection de l'environnement (1999) : Avis d'intention d'élaborer et de mettre en uvre des mesures de gestion et d'évaluation des risques que certaines substances présentent pour la santé des Canadiens et leur environnement. Gazette du Canada. Partie I, vol. 140, no 49, p. 4109-4117. http://canadagazette.gc.ca/partI/2006/20061209/pdf/g1-14049.pdf
Canada. Ministère de l'Environnement, ministère de la Santé. 2006b. Loi canadienne sur la protection de l'environnement (1999) : Avis concernant certaines substances considérées comme priorités pour suivi. Gazette du Canada, Partie I, vol. 140, no 9, p. 435-459. http://canadagazette.gc.ca/partI/2006/20060304/pdf/g1-14009.pdf
Canada. Ministère de l'Environnement, ministère de la Santé. 2008. Loi canadienne sur la protection de l'environnement (1999) : Avis de quatrième divulgation d'information technique concernant les substances identifiées dans le Défi. Gazette du Canada. Partie I, vol. 147, no 7, p. 310-310. http://canadagazette.gc.ca/partI/2008/20080216/pdf/g1-14207.pdf
[CATABOL] Probabilistic assessment of biodegradability and metabolic pathways [modèle informatique]. c2004-2008. Version 5.10.2. Bourgas (BG) : Bourgas Prof. Assen Zlatarov University, Laboratory of Mathematical Chemistry. http://oasis-lmc.org/?section=software&swid=1
ChemID Plus. 2007 [base de données sur Internet]. 2008. [consulté le 1er octobre 2008] http://chem.sis.nlm.nih.gov/chemidplus/
Clariant. 1996. IUCLID dataset for C.I. Disperse Blue 79 (no CAS 12239-34-8). [base de données sur Internet]. [consulté le 21 octobre 2008] http://ecb.jrc.ec.europa.eu/esis/index.php?PGM=dat
Cohle P, R Mihalik R. 1991. Early life stage toxicity of C.I. Disperse Blue 79:1 purified preecake to rainbow trout (Oncorhynchus mykiss) in a flow-through system. Final report. ABC Laboratories Inc. Columbia, MO.
Colón D., Weber E.J. et Baughman G.L., 2002. Sediment-associated reactions of aromatic amines. 2. Développement des RQSA. Environ. Sci. Technol. 36:2443-2450.
[CPOPs] Canadian POPs Model. 2008. Gatineau (Qc) : Environnement Canada. Existing Substances Division; Bourgas (BG): Bourgas Prof. Assen Zlatarov University, Laboratory of Mathematical Chemistry. [Modèle mis au point par Dimitrov et al., 2005]. Disponible sur demande.
Dimitrov, S., Dimitrova, N., Parkerton, T., Comber, M., Bonnell, M., Mekenyan, O. 2005. Base-line model for identifying the bioaccumulation potential of chemicals. SAR QSAR Environ. Res. 16(6):531-554.
Dimitrov, S., N. Dimitrova, J. Walker. Gil Veith, and O. Mekenyan. 2002. Predicting bioconcentration potential of highly hydrophobic chemicals. Effect of molecular size. Pure Appl. Chem. 74(10):1823-1830.
Environnement Canada. 1995. Soumission d'essais sur la toxicité aiguë à l'égard du poisson en vertu du Règlement sur les renseignements concernant les substances nouvelles; soumission de déclaration de substances nouvelles (DSN). NSN submission. Données présentées à la Division des substances nouvelles d'Environnement Canada dans le cadre du Programme de renseignements concernant les substances nouvelles.
Environnement Canada. 2000. Division de l'évaluation des substances chimiques. Environmental Categorization for Persistence, Bioaccumulation and Inherent Toxicity of Substances on the Domestic Substances List Using QSARs. Rapport final. Environnement Canada. Juillet.
Environnement Canada. 2007. Review of the limitations and uncertainties associated with use for molecular size information when assessing bioaccumulation potential. Rapport final inédit. Gatineau (Qc) : Environnement Canada, Division des substances existantes. Disponible sur demande.
Environnement Canada. 2008a. Guidance for conducting ecological assessments under CEPA, 1999 : science resource technical series, technical guidance module: Mass Flow Tool. Document de travail préliminaire. Gatineau (Québec) : Environnement Canada, Division des substances existantes.
Environnement Canada. 2008b. Assumptions, limitations and uncertainties of the mass flow tool for BDAP, no CAS 52697-38-8. Document préliminaire interne. Gatineau (Qc) : Environnement Canada, Division des substances existantes. Disponible sur demande.
Environnement Canada. 2008c. Guidance for conducting ecological assessments under CEPA, 1999: Science resource technical series, Technical guidance module: the Industrial Generic Exposure Tool - Aquatic (IGETA). Document de travail. Gatineau (Qc) : Environnement Canada, Division des substances existantes.
Environnement Canada. 2008d. Rapport IGETA : no CAS 52697-38-8, [consulté le 21 novembre 2008]. Rapport inédit. Gatineau (Qc) : Environnement Canada, Division des substances existantes.
Environnement Canada. 2008e. Guidance for conducting ecological assessments under CEPA, 1999: science resource technical series, technical guidance module: Mega Flush consumer release scenario. Document de travail préliminaire. Gatineau (Qc) : Environnement Canada, Division des substances existantes.
Environnement Canada. 2008f. Rapport sur Mega Flush: no CAS 52697-38-8, [consulté le 23 octobre 2008]. Rapport inédit. Gatineau (Qc) : Environnement Canada, Division des substances existantes.
[ESIS] European Substances Information System [base de données sur Internet]. [date inconnue]. Version 5. European Chemical Bureau (ECB). [consultée en août 2008]. http://ecb.jrc.it/esis
[ETAD] Ecological and Toxicological Association of Dyes and Organic Pigments Canadian Affiliates, Dayan J, Trebitz H, consultants. 1995. Health and environmental information on dyes used in Canada. Rapport inédit présenté à Environnement Canada, Division des substances existantes. Sur la page couverture: An overview to assist in the implementation of the New Substances Notification Regulations under the Canadian Environmental Protection Act.
[ETAD] Ecological and Toxicological Association of Dyes and Organic Pigments Manufacturers. 1992. Draft Guidelines for the Assessment of Environmental Exposure to Dyestuffs.
Hunger K, éd.. 2003. Industrial dyes; chemistry, properties, applications. Weinheim (Allemagne) : WILEY-VCH Verlag GmbH & Co. kgaA.
Industrie Canada 2008a. Canadian Company Capabilities [base de données sur Internet]. [consultée en août 2008] http://strategis.ic.gc.ca/app/ccc/srch/cccBscSrch.do?lang=eng&prtl=1&app=1
Industrie Canada 2008b. Finissage de textiles et de tissus [SCIAN 31331] : 2004-2007 et Revêtement de tissus [SCIAN 31332] : 2004-2007, préparé par la Direction de l'habillement et des textiles, Direction générale des industries de services et des produits de consommation (DGISPC), Industrie Canada. Demandes de renseignements : B. John (Jazz) Szabo, 613-957-1242. Courriel: szabo.john@ic.gc.ca
[MITI] Ministry of International Trade & Industry (Jpn). 1992. Biodegradation and bioaccumulation data of existing chemicals based on the CSCL Japan, Basic Industries Bureau, Chemical Products Safety Division. Japan Chemical Industry Ecology-Toxicology & Information Centre, Tokyo (Japon).
[NCI] National Chemical Inventories [base de données sur CD-ROM]. 2006. Columbus, Ohio : American Chemical Society. [Consulté le 11 décembre 2006]. http://www.cas.org/products/cd/nci/index.html
OCDE - Organisation de coopération et de développement économiques 2007. Emission scenario document on plastics additives [Internet]. Rapport final. Paris (France) : OCDE, Direction de l'environnement. (Series on Emission Scenario Documents No.10). [consulté le 9 juillet 2008]. http://ascouncil.org/news/adhesives/docs/EPAFormulation.pdf
OCDE - Organisation de coopération et de développement économiques Draft emission scenario on textile manufacturing wool mills [Internet]. (France) : OCDE, Direction de l'environnement. Rapport no ENV/JM/MONO(2004)8, JT00166678. [consulté le 9 juillet 2008]. http://www.oecd.org/document/21/0,3343,en_2649_34379_1939669_1_1_1_1,00.html
Øllgaard, H., Frost, L., Galster J., Hansen, O. C. 1998. Survey of azo-colorants in Denmark - Consumption, use, health and environmental aspects. Miljøprojekt nr. 509. Miljøstyrelsen
Pagga, U., Brown, D. 1986. The degradation of dyestuffs: Part II Behaviour of dyestuffs in aerobic biodegradation tests. Chemosphere 15(4):479-491.
[PhysProp] Interactive PhysProp Database [base de données sur Internet]. 2006. Syracuse, N. Y. : Syracuse Research Corporation. [consultée en mars 2006]. http://www.syrres.com/esc/physdemo.htm
Razo-Flores, E., Luijten, M., Donlon, B., Lettinga, G., Field, J. 1997. Biodegradation of selected azo dyes under methanogenic conditions. Wat. Sci. Technol. 36(6-7):65-72.
SafePharm Laboratories Ltd. 1990. Acute toxicity to rainbow trout. Project number 47/918. Challenge submission ID#11347. Présenté à Environnement Canada le 30 juillet 2008.
Sakuratani, Y., Noguchi, Y., Kobayashi, K., Yamada, J., Nishihara, T. 2008. Molecular size as a limiting characteristic for bioconcentration in fish. J. Environ. Biol.29(1):89-92
Shen, G., Shuangqing, H. 2008. Bioconcentration Test of C.I. Disperse Orange 30 in Fish. Rédigé par Environmental Testing Laboratory, Shanghai Academy of Environmental Sciences, Shanghai (Chine) pour Dystar au nom de l'Ecological and Toxicological Association of the Dyes and Organic Pigments Manufacturers (ETAD) Bâle (Suisse). Rapport no S-070-2007. Présenté à Environnement Canada en avril 2008. No de déclaration dans le cadre du défi 8351.
Sijm, DTHM., Schuurmann, G., deVries, P.J., Opperhuizen, A. 1999. Aqueous solubility, octanol solubility, and octanol/water partition coefficient of nine hydrophobic dyes. Environ. Toxicol. Chem. 18(6):1109-1117.
[SPIN] Substances in Products in Nordic Countries [base de données sur Internet]. 2008. Copenhague (Danemark) : Conseils des ministres des pays nordiques. [consultée en août 2008] http://195.215.251.229/Dotnetnuke/Home/tabid/58/Default.aspx
Thiel, W., Mayer, R., Jauer, E.-A, Modrow, H., Dost, H. 1986. Synthese und spektrale Charakterisierung von blauen Benzenazofarbstoffen. Journal f prakt Chemie. 328(4):497-514.
[US EPA] US Environmental Protection Agency. 2002. PBT Profiler Methodology [Internet]. Washington (DC) : US EPA, Office of Pollution Prevention and Toxics. [consulté en août 2008]. http://www.pbtprofiler.net/methodology.asp
[US EPA] US Environmental Protection Agency. 2007. Inventory Update Reporting, Past IUR Data, Non-confidential Production Volume Information submitted by companies under the 1986, 1990, 1994, 1998, and 2002 Inventory Update Reporting Regulation, CAS No 52697-38-8 [Internet]. Washington (DC) : US EPA; [consulté le 28 février 2007]. http://www.epa.gov/oppt/iur/tools/data/2002-vol.htm
Weber, E.J., Adams, R.L. 1995. Chemical- and sediment-mediated reduction of the azo dye Disperse Blue 79. Environ. Sci. Technol. 29:1163-1170.
Weber E.J., Colón D. et G.L. Baughmann. 2001. Sediment-Associated Reactions of Aromatic Amines. 1. Elucidation of sorption mechanisms. Environ. Sci. Technol.35:2470-2475.
Yen, C.C., Perenich, T.A., Baughman, G.L. 1989. Fate of dyes in aquatic systems II. Solubility and octanol/water partition coefficients of disperse dyes. Environ. Toxicol. Chem.8(11):981-986.
Yen, C.C., Perenich, T.A., Baughman, G.L. 1991. Fate of commercial disperse dyes in sediments. Environ. Toxicol. Chem. 10:1009-1017.
Annexe I - Sommaires de rigueur d'étude pour les études clés
Tableau A-1. Formulaire pour sommaire de rigueur d'étude : organismes aquatiques B
Référence : SHEN, Genxiang et Hu SHUANGQING. 2008. Bioconcentration Test of C.I. Disperse Orange 30 in Fish. Rédigé par Environmental Testing Laboratory, Shanghai Academy of Environmental Sciences, Shanghai (Chine) pour Dystar au nom de l'Ecological and Toxicological Association of the Dyes and Organic Pigments Manufacturers (ETAD) Bâle (Suisse). Rapport No S-070-2007. Présenté à Environnement Canada en avril 2008. No de déclaration dans le cadre du défi 8351.
| No | Article | Pondération | Oui/Non | Précisions |
|---|---|---|---|---|
| 2 | Identité de la substance : no CAS | s. o. | O | 5261-31-4 |
| 3 | Identité de la substance : nom(s) chimique(s) | s. o. | O | Acétate de 2-[N-(2-cyanoéthyl)-4-[2,6-dichloro-4-nitrophényl)azo]anilino]éthyle |
| 4 | Composition chimique de la substance | 2 | N | |
| 5 | Pureté chimique | 1 | N | |
| 6 | Indication de la persistance/stabilité de la substance en milieu aqueux? | 1 | N | |
| 7 | Si le matériel d'examen est radiomarqué, est-ce que la ou les positions précises du ou des atomes marqués ainsi que le pourcentage de radioactivité associé avec les impuretés ont été rapportés? | 2 | s. o. |
| No | Article | Pondération | Oui/Non | Précisions |
|---|---|---|---|---|
| 8 | Références | 1 | O | Lignes directrices de l'OCDE pour les essais de produits chimiques no 305B-1996 |
| 9 | Méthode normalisée (OCDE, UE, nationale, ou autre)? | 3 | O | OCDE |
| 10 | Justification de la méthode ou du protocole non normalisé utilisé, le cas échéant | 2 | ||
| 11 | BPL (bonnes pratiques de laboratoire) | 3 | N |
| No | Article | Pondération | Oui/Non | Précisions |
|---|---|---|---|---|
| 12 | Identité de l'organisme : nom | s. o. | O | Poisson-zèbre (Brachydanio rerio) |
| 13 | Indication du nom latin ou des deux noms (latin et commun)? | 1 | O | Les deux |
| 14 | Âge ou stade biologique de l'organisme d'essai | 1 | N | |
| 15 | Longueur et/ou poids | 1 | O | Longueur moyenne du corps 3,91+/-0,18 cm et poids moyen 0,32+/-0,06 g |
| 16 | Sexe | 1 | N | |
| 17 | Nombre d'organismes par répétition | 1 | O | 7 |
| 18 | Charge en organismes | 1 | O | 20 mg/L |
| 19 | Type de nourriture et périodes d'alimentation au cours de la période d'acclimatation | 1 | O | Nourri avec du poisson acheté dans le commerce jusqu'à la veille du début de l'essai |
| No | Article | Pondération | Oui/Non | Précisions |
|---|---|---|---|---|
| 20 | Type d'expérience (en laboratoire ou sur le terrain) | s. o. | O | Laboratoire |
| 21 | Voies d'exposition (nourriture, eau, les deux) | s. o. | O | Eau |
| 22 | Durée de l'exposition | s. o. | O | 28 jours |
| 23 | Nombre de répétitions (y compris les témoins) | 1 | O | |
| 24 | Concentrations | 1 | O | 20 mg/L |
| 25 | Type/composition de la nourriture et périodes d'alimentation (pendant l'essai) | 1 | O | Les poissons étaient nourris deux heures avant le changement d'eau |
| 26 | Si le rapport FBC/FBA a été utilisé comme dérivé de la concentration du produit chimique dans l'organisme et dans l'eau, est-ce que la durée de l'expérimentation était égale ou plus longue que le temps requis pour que la concentration du produit chimique atteigne un état stable ? | 3 | O | 28 jours |
| 27 | Si le rapport FBC/FBA a été déterminé comme correspondant au rapport de la concentration du produit chimique dans l'organisme sur sa concentration dans l'eau, est-ce que les concentrations mesurées dans l'organisme et dans l'eau étaient mentionnées? | 3 | O | |
| 28 | Les concentrations dans les eaux d'essai ont-elles été mesurées périodiquement? | 1 | O | Trois jours distincts |
| 29 | Les conditions du milieu d'exposition pertinentes pour la substance sont-elles indiquées? (p. ex. : pour la toxicité des métaux - pH, COD/COT, dureté de l'eau, température) | 3 | O | Oui, tous les deux jours |
| 30 | Photopériode et intensité de l'éclairage | 1 | O | 12:12 |
| 31 | Préparation de solutions mères et de solutions d'essai | 1 | O | |
| 32 | Intervalles des contrôles analytiques | 1 | O | Tous les deux jours pour l'oxygène dissous, le pH et la température |
| 33 | Méthodes statistiques utilisées | 1 | O | |
| 34 | Un agent émulsionnant ou stabilisant a-t-il été employé, si la substance était peu soluble ou instable? | s. o. | N |
| No | Article | Pondération | Oui/Non | Précisions |
|---|---|---|---|---|
| 35 | L'organisme d'essai convient-il à l'environnement au Canada? | 3 | O | |
| 36 | Les conditions d'essai (pH, température, OD, etc.) sont-elles typiques pour l'organisme d'essai? | 1 | O | |
| 37 | Le type et la conception du système (statique, semi-statique, dynamique; ouvert ou fermé; etc.) correspondent-ils aux propriétés de la substance et à la nature ou aux habitudes de l'organisme? | 2 | O | Semi-statique |
| 38 | Le pH de l'eau d'essai était-il dans la plage des valeurs typiques de l'environnement au Canada (6 à 9)? | 1 | O | 7,22-7,84 |
| 39 | La température de l'eau d'essai était-elle dans la plage des valeurs typiques de l'environnement au Canada (5 à 27 °C)? | 1 | O | 22-23 |
| 40 | Est-ce que le contenu en lipides (ou FBA/FBC normalisé par rapport aux lipides) a été rapporté? | 2 | O | |
| 41 | Est-ce que les concentrations mesurées d'un produit chimique dans les eaux d'essai étaient plus basses que la solubilité du produit? | 3 | N | |
| 42 | Si une substance radiomarquée a été utilisée, est-ce que le FBC a été déterminé d'après le composé d'origine (et non d'après les résidus radiomarqués)? | 3 | s. o. |
| No | Article | Pondération | Oui/Non | Précisions |
|---|---|---|---|---|
| 43 | Les paramètres déterminés (FBA, FBC) et leurs valeurs | s. o. | s. o. | FBC inférieur(e) à 100 |
| 44 | FBA ou FBC déterminés comme : 1)le rapport de la concentration en produit chimique produit dans l'organisme, ou 2) le rapport entre les constantes d'incorporation de produit chimique et du taux d'élimination | s. o. | s. o. | 1 |
| 45 | Le FBA/FBC a t-il été déterminé d'après un 1) échantillon de tissu ou 2) l'organisme entier? | s. o. | s. o. | 2 |
| 46 | Le FBA/FBC utilisé était-elle la valeur 1) moyenne ou 2) maximale? | s. o. | s. o. | 1 |
| No | Article | Précisions |
|---|---|---|
| 47 | Note : ... % | 75.5 |
| 48 | Code de fiabilité d'EC : | 2 |
| 49 | Catégorie de fiabilité (élevée, satisfaisante, faible) : | Confiance satisfaisante |
| 50 | Commentaires | La présente procédure est réalisée en conditions semi-statiques (renouvellement des solutions d'essai tous les deux jours). Par conséquent, une substance d'essai très peu soluble dans l'eau, comme le Disperse Orange 61, peut aussi être caractérisée selon son potentiel de bioconcentration sans l'ajout de solvants ou d'autres substances auxiliaires qui pourraient modifier les résultats. |
Tableau A-2. Formulaire pour sommaire de rigueur d'étude : toxicité intrinsèque pour les organismes aquatiques
Référence : SafePharm Laboratories Ltd., Acute toxicity to Rainbow Trout for FORVI (CAS No 52697-38-8), 1990.
| No | Article | Pondération | Oui/Non | Précisions |
|---|---|---|---|---|
| 2 | Identité de la substance : no CAS | s. o. | O | 52697-38-8 |
| 3 | Identité de la substance : nom(s) chimique(s) | s. o. | O | FORVI |
| 4 | Composition chimique de la substance | 2 | N | |
| 5 | Pureté chimique | 1 | N | |
| 6 | Indication de la persistance/stabilité de la substance en milieu aqueux? | 1 | N |
| No | Article | Pondération | Oui/Non | Précisions |
|---|---|---|---|---|
| 7 | Références | 1 | N | |
| 8 | Méthode normalisée (OCDE, UE, nationale, ou autre)? | 3 | N | |
| 9 | Justification de la méthode ou du protocole non normalisé utilisé, le cas échéant | 2 | N | |
| 10 | BPL (bonnes pratiques de laboratoire) | 3 | N |
| No | Article | Pondération | Oui/Non | Précisions |
|---|---|---|---|---|
| 11 | Identité de l'organisme : nom | s. o. | O | Truite arc-en-ciel, Salmo gairdneri |
| 12 | Indication du nom latin ou des deux noms (latin et commun)? | 1 | O | |
| 13 | Âge ou stade biologique de l'organisme d'essai | 1 | N | |
| 14 | Longueur et/ou poids | 1 | O | 4,8 +/- 0,2 cm; 1,55 +/- 0,13 g |
| 15 | Sexe | 1 | N | |
| 16 | Nombre d'organismes par répétition | 1 | O | 2 |
| 17 | Charge en organismes | 1 | O | (g/L) |
| 18 | Type de nourriture et périodes d'alimentation au cours de la période d'acclimatation | 1 | N |
| No | Article | Pondération | Oui/Non | Précisions |
|---|---|---|---|---|
| 19 | Type d'essai (toxicité aigüe ou chronique) | s. o. | O | Aiguë |
| 20 | Type d'expérience (en laboratoire ou sur le terrain) | s. o. | O | Laboratoire |
| 21 | Voies d'exposition (nourriture, eau, les deux) | s. o. | O | Eau |
| 22 | Durée de l'exposition | s. o. | O | (96 h) |
| 23 | Témoins négatifs ou positifs (préciser) | 1 | N | |
| 24 | Nombre de répétitions (y compris les témoins) | 1 | O | 4 |
| 25 | Des concentrations nominales sont-elles indiquées? | 1 | O | 4 |
| 26 | Des concentrations mesurées sont-elles indiquées? | 3 | N | |
| 27 | Type de nourriture et périodes d'alimentation durant les essais à long terme | 1 | ||
| 28 | Les concentrations ont-elles été mesurées périodiquement (spécialement dans les essais de toxicité chronique)? | 1 | N | |
| 29 | Les conditions du milieu d'exposition pertinentes pour la substance sont-elles indiquées? (p. ex. : pour la toxicité des métaux - pH, COD/COT, dureté de l'eau, température) | 3 | O | conditions d'exposition limitées (température, dureté, aération) |
| 30 | Photopériode et intensité de l'éclairage | 1 | N | |
| 31 | Préparation de solutions mères et de solutions d'essai | 1 | O | |
| 32 | Un agent émulsionnant ou stabilisant a-t-il été employé, si la substance était peu soluble ou instable? | 1 | N | |
| 33 | Si un agent émulsionnant ou stabilisant a été employé, sa concentration est-elle indiquée? | 1 | ||
| 34 | Si un agent émulsionnant ou stabilisant a été employé, sa concentration est-elle indiquée? | 1 | ||
| 35 | Intervalles des contrôles analytiques | 1 | N | |
| 36 | Méthodes statistiques utilisées | 1 | N |
| No | Article | Pondération | Oui/Non | Précisions |
|---|---|---|---|---|
| 37 | Le paramètre déterminé est-il directement attribuable à la toxicité de la substance, non à l'état de santé des organismes (p. ex., lorsque la mortalité des témoins est supérieur(e) à 10 %) ou à des facteurs physiques (p. ex., « effet d'ombrage »)? | s. o. | O | |
| 38 | L'organisme d'essai convient-il à l'environnement au Canada? | 3 | O | |
| 39 | Les conditions d'essai (pH, température, OD, etc.) sont-elles typiques pour l'organisme d'essai? | 1 | O | |
| 40 | Le type et la conception du système (statique, semi-statique, dynamique; ouvert ou fermé; etc.) correspondent-ils aux propriétés de la substance et à la nature ou aux habitudes de l'organisme? | 2 | O | |
| 41 | Le pH de l'eau d'essai était-il dans la plage des valeurs typiques de l'environnement au Canada (6 à 9)? | 1 | pH non précisé | |
| 42 | La température de l'eau d'essai était-elle dans la plage des valeurs typiques de l'environnement au Canada (5 à 27 °C)? | 1 | O | 14 +/- 1 °C |
| 43 | La valeur de la toxicité était-elle inférieure à celle de la solubilité de la substance dans l'eau? | 3 | N | On ne dispose d'aucune donnée sur la solubilité dans l'eau du 52697-38-8, mais d'après sa similarité avec les divers colorants azoïques dispersés, les données disponibles (0,00063 à 1,3), sur sa solubilité devrait être inférieure à 0,01 mg/L. |
| No | Article | Pondération | Oui/Non | Précisions |
|---|---|---|---|---|
| 44 | Valeurs de la toxicité (fournir paramètres et valeurs) | s. o. | s. o. | CL50 (96 heures) supérieur(e) à 100 mg/L |
| 45 | Autres paramètres indiqués - p. ex., FBC/FBA, CMEO/CSEO (préciser)? | s. o. | N | |
| 46 | Autres effets nocifs indiqués (p. ex., cancérogénicité, mutagénicité)? | s. o. | N |
| No | Article | Précisions |
|---|---|---|
| 47 | Note : ... % | 37,8 |
| 48 | Code de fiabilité d'EC : | 4 |
| 49 | Catégorie de fiabilité (élevée, satisfaisante, faible) : | Non satisfaisante |
| 50 | Commentaires |
Tableau A-3. Formulaire pour sommaire de rigueur d'étude : toxicité intrinsèque pour les organismes aquatiques
Référence : BASF. 1990. Bericht uber die Prufung der akuten Toxizitit an der Goldorfe (Leuciscus idus L.,.Goldvariante). Présenté à Environnement Canada par l'ETAD en août 2008.
| No | Article | Pondération | Oui/Non | Précisions |
|---|---|---|---|---|
| 2 | Identité de la substance : no CAS | s. o. | ||
| 3 | Identité de la substance : nom(s) chimique(s) | s. o. | ||
| 4 | Composition chimique de la substance | 2 | N | |
| 5 | Pureté chimique | 1 | N | |
| 6 | Indication de la persistance/stabilité de la substance en milieu aqueux? | 1 | N |
| No | Article | Pondération | Oui/Non | Précisions |
|---|---|---|---|---|
| 7 | Références | 1 | N | |
| 8 | Méthode normalisée (OCDE, UE, nationale, ou autre)? | 3 | N | |
| 9 | Justification de la méthode ou du protocole non normalisé utilisé, le cas échéant | 2 | N | |
| 10 | BPL (bonnes pratiques de laboratoire) | 3 |
| No | Article | Pondération | Oui/Non | Précisions |
|---|---|---|---|---|
| 11 | Identité de l'organisme : nom | s. o. | O | Golden orfe |
| 12 | Indication du nom latin ou des deux noms (latin et commun)? | 1 | O | |
| 13 | Âge ou stade biologique de l'organisme d'essai | 1 | N | |
| 14 | Longueur et/ou poids | 1 | N | |
| 15 | Sexe | 1 | N | |
| 16 | Nombre d'organismes par répétition | 1 | N | |
| 17 | Charge en organismes | 1 | N | |
| 18 | Type de nourriture et périodes d'alimentation au cours de la période d'acclimatation | 1 | N |
| No | Article | Pondération | Oui/Non | Précisions |
|---|---|---|---|---|
| 19 | Type d'essai (toxicité aigüe ou chronique) | s. o. | O | tox. aiguë |
| 20 | Type d'expérience (en laboratoire ou sur le terrain) | s. o. | N | |
| 21 | Voies d'exposition (nourriture, eau, les deux) | s. o. | N | |
| 22 | Durée de l'exposition | s. o. | O | (96 heures) |
| 23 | Témoins négatifs ou positifs (préciser) | 1 | N | |
| 24 | Nombre de répétitions (y compris les témoins) | 1 | N | |
| 25 | Des concentrations nominales sont-elles indiquées? | 1 | N | |
| 26 | Des concentrations mesurées sont-elles indiquées? | 3 | N | |
| 27 | Type de nourriture et périodes d'alimentation durant les essais à long terme | 1 | s. o. | |
| 28 | Les concentrations ont-elles été mesurées périodiquement (spécialement dans les essais de toxicité chronique)? | 1 | N | |
| 29 | Les conditions du milieu d'exposition pertinentes pour la substance sont-elles indiquées? (p. ex. : pour la toxicité des métaux - pH, COD/COT, dureté de l'eau, température) | 3 | N | |
| 30 | Photopériode et intensité de l'éclairage | 1 | N | |
| 31 | Préparation de solutions mères et de solutions d'essai | 1 | N | |
| 32 | Un agent émulsionnant ou stabilisant a-t-il été employé, si la substance était peu soluble ou instable? | 1 | N | |
| 33 | Si un agent émulsionnant ou stabilisant a été employé, sa concentration est-elle indiquée? | 1 | N | |
| 34 | Si un agent émulsionnant ou stabilisant a été employé, des données sont-elles fournies sur son écotoxicité? | 1 | N | |
| 35 | Intervalles des contrôles analytiques | 1 | N | |
| 36 | Méthodes statistiques utilisées | 1 | N |
| No | Article | Pondération | Oui/Non | Précisions |
|---|---|---|---|---|
| 37 | Le paramètre déterminé est-il directement attribuable à la toxicité de la substance, non à l'état de santé des organismes (p. ex., lorsque la mortalité des témoins est supérieur(e) à 10 %) ou à des facteurs physiques (p. ex., « effet d'ombrage »)? | s. o. | N | |
| 38 | L'organisme d'essai convient-il à l'environnement au Canada? | 3 | O | |
| 39 | Les conditions d'essai (pH, température, OD, etc.) sont-elles typiques pour l'organisme d'essai? | 1 | N | |
| 40 | Le type et la conception du système (statique, semi-statique, dynamique; ouvert ou fermé; etc.) correspondent-ils aux propriétés de la substance et à la nature ou aux habitudes de l'organisme? | 2 | N | |
| 41 | Le pH de l'eau d'essai était-il dans la plage des valeurs typiques de l'environnement au Canada (6 à 9)? | 1 | N | |
| 42 | La température de l'eau d'essai était-elle dans la plage des valeurs typiques de l'environnement au Canada (5 à 27 °C)? | 1 | N | |
| 43 | La valeur de la toxicité était-elle inférieure à celle de la solubilité de la substance dans l'eau? | 3 |
| No | Article | Pondération | Oui/Non | Précisions |
|---|---|---|---|---|
| 44 | Valeurs de la toxicité (fournir paramètres et valeurs) | s. o. | CL50 = supérieur(e) à 100 inférieur(e) à 220 mg/L | |
| 45 | Autres paramètres indiqués - p. ex., FBC/FBA, CMEO/CSEO (préciser)? | s. o. | CSEO = 100 mg/L | |
| 46 | Autres effets nocifs indiqués (p. ex., cancérogénicité, mutagénicité)? |
s. o. |
| No | Article | Précisions |
|---|---|---|
| 47 | Note : ... % | 9,5 |
| 48 | Code de fiabilité d'EC : | 4 |
| 49 | Catégorie de fiabilité (élevée, satisfaisante, faible) : | Non satisfaisante |
| 50 | Commentaires | Les données soumises ne sont pas suffisantes pour évaluer correctement la fiabilité de cette étude. |
Tableau A-4. Formulaire pour sommaire de rigueur d'étude : toxicité intrinsèque pour les organismes aquatiques
Référence : Environnement Canada. 1995. Soumission d'essais sur la toxicité aiguë à l'égard du poisson en vertu du Règlement sur les renseignements concernant les substances nouvelles, auprès de la direction des substances nouvelles d'Environnement Canada, dans le cadre du programme de déclaration des substances nouvelles.
| No | Article | Pondération | Oui/Non | Précisions |
|---|---|---|---|---|
| 2 | Identité de la substance : no CAS | s. o. | N | |
| 3 | Identité de la substance : nom(s) chimique(s) | s. o. | O | |
| 4 | Composition chimique de la substance | 2 | N | |
| 5 | Pureté chimique | 1 | N | |
| 6 | Indication de la persistance/stabilité de la substance en milieu aqueux? | 1 | N |
| No | Article | Pondération | Oui/Non | Précisions |
|---|---|---|---|---|
| 7 | Références | 1 | O | OCDE 203 |
| 8 | Méthode normalisée (OCDE, UE, nationale, ou autre)? | 3 | O | |
| 9 | Justification de la méthode ou du protocole non normalisé utilisé, le cas échéant | 2 | sans objet | |
| 10 | BPL (bonnes pratiques de laboratoire) | 3 | O |
| No | Article | Pondération | Oui/Non | Précisions |
|---|---|---|---|---|
| 11 | Identité de l'organisme : nom | s. o. | O | Truite arc-en-ciel |
| 12 | Indication du nom latin ou des deux noms (latin et commun)? | 1 | O | |
| 13 | Âge ou stade biologique de l'organisme d'essai | 1 | O | Longueur moyenne 51 mm poids moyen 1,54 |
| 14 | Longueur et/ou poids | 1 | O | voir ci-dessus |
| 15 | Sexe | 1 | sans objet | |
| 16 | Nombre d'organismes par répétition | 1 | O | 10 |
| 17 | Charge en organismes | 1 | O | |
| 18 | Type de nourriture et périodes d'alimentation au cours de la période d'acclimatation | 1 | O |
| No | Article | Pondération | Oui/Non | Précisions |
|---|---|---|---|---|
| 19 | Type d'essai (toxicité aigüe ou chronique) | s. o. | O | Aiguë |
| 20 | Type d'expérience (en laboratoire ou sur le terrain) | s. o. | o | Laboratoire |
| 21 | Voies d'exposition (nourriture, eau, les deux) | s. o. | o | Eau |
| 22 | Durée de l'exposition | s. o. | o | 96 h |
| 23 | Témoins négatifs ou positifs (préciser) | 1 | O | 3 |
| 24 | Nombre de répétitions (y compris les témoins) | 1 | O | 2 |
| 25 | Des concentrations nominales sont-elles indiquées? | 1 | O | 320 à 3 200 mg/L |
| 26 | Des concentrations mesurées sont-elles indiquées? | 3 | N | |
| 27 | Type de nourriture et périodes d'alimentation durant les essais à long terme | 1 | sans objet | |
| 28 | Les concentrations ont-elles été mesurées périodiquement (spécialement dans les essais de toxicité chronique)? | 1 | N | |
| 29 | Les conditions du milieu d'exposition pertinentes pour la substance sont-elles indiquées? (p. ex. : pour la toxicité des métaux - pH, COD/COT, dureté de l'eau, température) | 3 | O | |
| 30 | Photopériode et intensité de l'éclairage | 1 | O | |
| 31 | Préparation de solutions mères et de solutions d'essai | 1 | O | |
| 32 | Un agent émulsionnant ou stabilisant a-t-il été employé, si la substance était peu soluble ou instable? | 1 | N | |
| 33 | Si un agent émulsionnant ou stabilisant a été employé, sa concentration est-elle indiquée? | 1 | ||
| 34 | Si un agent émulsionnant ou stabilisant a été employé, sa concentration est-elle indiquée? | 1 | ||
| 35 | Intervalles des contrôles analytiques | 1 | O | |
| 36 | Méthodes statistiques utilisées | 1 | O |
| No | Article | Pondération | Oui/Non | Précisions |
|---|---|---|---|---|
| 37 | Le paramètre déterminé est-il directement attribuable à la toxicité de la substance, non à l'état de santé des organismes (p. ex., lorsque la mortalité des témoins est supérieur(e) à 10 %) ou à des facteurs physiques (p. ex., « effet d'ombrage »)? | s. o. | O | |
| 38 | L'organisme d'essai convient-il à l'environnement au Canada? | 3 | O | |
| 39 | Les conditions d'essai (pH, température, OD, etc.) sont-elles typiques pour l'organisme d'essai? | 1 | O | |
| 40 | Le type et la conception du système (statique, semi-statique, dynamique; ouvert ou fermé; etc.) correspondent-ils aux propriétés de la substance et à la nature ou aux habitudes de l'organisme? | 2 | O | |
| 41 | Le pH de l'eau d'essai était-il dans la plage des valeurs typiques de l'environnement au Canada (6 à 9)? | 1 | O | |
| 42 | La température de l'eau d'essai était-elle dans la plage des valeurs typiques de l'environnement au Canada (5 à 27 °C)? | 1 | O | |
| 43 | La valeur de la toxicité était-elle inférieure à celle de la solubilité de la substance dans l'eau? | 3 | Solubilité dans l'eau inconnue |
| No | Article | Pondération | Oui/Non | Précisions |
|---|---|---|---|---|
| 44 | Valeurs de la toxicité (fournir paramètres et valeurs) | s. o. | s. o. | CL50 (96 heures) = 505 mg/L |
| 45 | Autres paramètres indiqués - p. ex., FBC/FBA, CMEO/CSEO (préciser)? | s. o. | N | |
| 46 | Autres effets nocifs indiqués (p. ex., cancérogénicité, mutagénicité)? | s. o. | N |
| No | Article | Précisions |
|---|---|---|
| 47 | Note : ? % | 77,5 |
| 48 | Code de fiabilité d'EC : | 2 |
| 49 | Catégorie de fiabilité (élevée, satisfaisante, faible) : | Confiance satisfaisante |
| 50 | Commentaires |
Tableau A-5. Formulaire pour sommaire de rigueur d'étude : toxicité intrinsèque pour les organismes aquatiques
Référence : Cohle P., R Mihalik R., 1991. Early life stage toxicity of C.I. Disperse Blue 79:1 purified preecake to rainbow trout (Oncorhynchus mykiss) in a flow-through system. Rapport final. ABC Laboratories Inc., Columbia, MO.
| No | Article | Pondération | Oui/Non | Précisions |
|---|---|---|---|---|
| 2 | Identité de la substance : no CAS | s. o. | ||
| 3 | Identité de la substance : nom(s) chimique(s) | s. o. | Disperse Blue 79:1 | |
| 4 | Composition chimique de la substance | 2 | s. o. | |
| 5 | Pureté chimique | 1 | O | 96,61 |
| 6 | Indication de la persistance/stabilité de la substance en milieu aqueux? | 1 | N |
| No | Article | Pondération | Oui/Non | Précisions |
|---|---|---|---|---|
| 7 | Références | 1 | O | |
| 8 | Méthode normalisée (OCDE, UE, nationale, ou autre)? | 3 | O | |
| 9 | Justification de la méthode ou du protocole non normalisé utilisé, le cas échéant | 2 | s. o. | |
| 10 | BPL (bonnes pratiques de laboratoire) | 3 | O |
| No | Article | Pondération | Oui/Non | Précisions |
|---|---|---|---|---|
| 11 | Identité de l'organisme : nom | s. o. | Truite arc-en-ciel | |
| 12 | Indication du nom latin ou des deux noms (latin et commun)? | 1 | O | |
| 13 | Âge ou stade biologique de l'organisme d'essai | 1 | O | |
| 14 | Longueur et/ou poids | 1 | O | |
| 15 | Sexe | 1 | s. o. | |
| 16 | Nombre d'organismes par répétition | 1 | O | 20 |
| 17 | Charge en organismes | 1 | O | 0,36 à 4,8 µg/L |
| 18 | Type de nourriture et périodes d'alimentation au cours de la période d'acclimatation | 1 | O |
| No | Article | Pondération | Oui/Non | Précisions |
|---|---|---|---|---|
| 19 | Type d'essai (toxicité aigüe ou chronique) | s. o. | O | chronique |
| 20 | Type d'expérience (en laboratoire ou sur le terrain) | s. o. | O | Laboratoire |
| 21 | Voies d'exposition (nourriture, eau, les deux) | s. o. | O | Eau |
| 22 | Durée de l'exposition | s. o. | O | 122 jours |
| 23 | Témoins négatifs ou positifs (préciser) | 1 | O | Témoin et porteur non indiqués |
| 24 | Nombre de répétitions (y compris les témoins) | 1 | O | 2 |
| 25 | Des concentrations nominales sont-elles indiquées? | 1 | O | 5 |
| 26 | Des concentrations mesurées sont-elles indiquées? | 3 | O | |
| 27 | Type de nourriture et périodes d'alimentation durant les essais à long terme | 1 | O | |
| 28 | Les concentrations ont-elles été mesurées périodiquement (spécialement dans les essais de toxicité chronique)? | 1 | O | |
| 29 | Les conditions du milieu d'exposition pertinentes pour la substance sont-elles indiquées? (p. ex. : pour la toxicité des métaux - pH, COD/COT, dureté de l'eau, température) | 3 | O | |
| 30 | Photopériode et intensité de l'éclairage | 1 | O | |
| 31 | Préparation de solutions mères et de solutions d'essai | 1 | O | |
| 32 | Un agent émulsionnant ou stabilisant a-t-il été employé, si la substance était peu soluble ou instable? | 1 | O | |
| 33 | Si un agent émulsionnant ou stabilisant a été employé, sa concentration est-elle indiquée? | 1 | O | |
| 34 | Si un agent émulsionnant ou stabilisant a été employé, des données sont-elles fournies sur son écotoxicité? | 1 | O | Aucune donnée sur la toxicité, mais a été utilisé comme témoin |
| 35 | Intervalles des contrôles analytiques | 1 | O | |
| 36 | Méthodes statistiques utilisées | 1 | O |
| No | Article | Pondération | Oui/Non | Précisions |
|---|---|---|---|---|
| 37 | Le paramètre déterminé est-il directement attribuable à la toxicité de la substance, non à l'état de santé des organismes (p. ex., lorsque la mortalité des témoins est supérieur(e) à 10 %) ou à des facteurs physiques (p. ex., « effet d'ombrage »)? | s. o. | O | |
| 38 | L'organisme d'essai convient-il à l'environnement au Canada? | 3 | O | |
| 39 | Les conditions d'essai (pH, température, OD, etc.) sont-elles typiques pour l'organisme d'essai? | 1 | O | |
| 40 | Le type et la conception du système (statique, semi-statique, dynamique; ouvert ou fermé; etc.) correspondent-ils aux propriétés de la substance et à la nature ou aux habitudes de l'organisme? | 2 | O | dynamique |
| 41 | Le pH de l'eau d'essai était-il dans la plage des valeurs typiques de l'environnement au Canada (6 à 9)? | 1 | O | |
| 42 | La température de l'eau d'essai était-elle dans la plage des valeurs typiques de l'environnement au Canada (5 à 27 °C)? | 1 | O | |
| 43 | La valeur de la toxicité était-elle inférieure à celle de la solubilité de la substance dans l'eau? | 3 | s. o. |
| No | Article | Pondération | Oui/Non | Précisions |
|---|---|---|---|---|
| 44 | Valeurs de la toxicité (fournir paramètres et valeurs) | s. o. | s. o. | CSEO supérieur(e) à 0,005 mg/L |
| 45 | Autres paramètres indiqués - p. ex., FBC/FBA, CMEO/CSEO (préciser)? | s. o. | ||
| 46 | Autres effets nocifs indiqués (p. ex., cancérogénicité, mutagénicité)? | s. o. |
| No | Article | Précisions |
|---|---|---|
| 47 | Note : ? % | 97,6 |
| 48 | Code de fiabilité d'EC : | 1 |
| 49 | Catégorie de fiabilité (élevée, satisfaisante, faible) : | Confiance élevée |
| 50 | Commentaires |