Évaluation et rapport de situation du COSEPAC sur le crapet sac-à-lait (Lepomis gulosus) au Canada - 2015

Illustration: © J. Tomelleri. Reproduction autorisée.
Description longue de la bannière
L'espèce a une grande bouche dont la mâchoire supérieure se prolonge bien au delà du bord antérieur de l'œil. De 3 à 5 barres foncées rayonnent de l'œil et du museau. Les nageoires pectorales sont généralement courtes, à bout arrondi. Le corps est de couleur olive jaune clair à vert olive foncé. On trouve de 6 à 11 bandes doubles semblables à des chaînes de couleur olive foncé sur le dos et les flancs, tandis que de 3 à 5 barres gris foncé, brunes ou lavande rayonnent de l'œil et du museau vers l'arrière. Les nageoires dorsale, caudale et anale molles sont fortement vermiculées, et les nageoires paires, non tachetées, sont transparentes ou olive.
Table des matières
- Table des matières
- Sommaire de l'évaluation
- Résumé
- Résumé technique
- Préface
- Description et importance de l'espèce sauvage
- Répartition
- Habitat
- Biologie
- Taille et tendances de la population
- Menaces et facteurs limitatifs
- Modifications des systèmes naturels (7.3 autres modifications de l'écosystème)
- Enlèvement de la végétation aquatique (1.1 zones résidentielles et urbaines; 1.3 zones touristiques et récréatives; 4.3 voies de transport par eau)
- Pollution (9.1 eaux usées domestiques et urbaines; 9.3 effluents agricoles et sylvicoles)
- Intrusions et perturbations humaines (6.3 travail et autres activités)
- Développement résidentiel et commercial (1.1 zones résidentielles et urbaines)
- Utilisation de ressources biologiques (5.4 pêche et récolte de ressources aquatiques)
- Espèces et gènes envahissants ou autrement problématiques (8.1 espèces exotiques [non indigènes] envahissantes)
- Changements climatiques et phénomènes météorologiques violents (11.1 déplacement et altération de l'habitat)
- Nombre de localités
- Protection, statuts et classements
- Remerciements et experts contactés
- Sources d'information
- Sommaire biographique du rédacteurs du rapport
- Collections examinées
Liste des figures
- Figure 1. Illustration d'un crapet sac à lait (Lepomis gulosus; vue latérale).
- Figure 2. Aire de répartition mondiale du crapet sac à lait (carte modifiée d'après Page et Burr [1991]).
- Figure 3(a). Répartition du crapet sac-à-lait (Lepomis gulosus) au Canada. Les cercles gris représentent les sites d'échantillonnage où aucun crapet sac-à-lait n'a été détecté.
- Figure 3(b). Répartition du crapet sac-à-lait (Lepomis gulosus)dans le parc national de Pointe-Pelée. Les cercles gris représentent les sites d'échantillonnage où aucun crapet sac-à-lait n'a été détecté.
- Figure 3(c). Répartition du crapet sac-à-lait (Lepomis gulosus) dans la baie Rondeau. Les cercles gris représentent les sites d'échantillonnage où aucun crapet sac-à-lait n'a été détecté.
- Figure 3(d). Répartition du crapet sac-à-lait (Lepomis gulosus) dans la baie Long Point et à proximité. Les cercles gris représentent les sites d'échantillonnage où aucun crapet sac-à-lait n'a été détecté.
- Figure 4. Zone d'occurrence du crapet sac-à-lait (Lepomis gulosus) calculée selon la méthode de l'enveloppe convexe pour une période actuelle (2004-2013) et deux périodes historiques (1994-2003; avant 2004).
- Figure 5(a). Indice de zone d'occupation du crapet sac-à-lait (Lepomis gulosus) au cours des 10 dernières années (2004-2013).
- Figure 5(b). Indice de zone d'occupation du crapet sac-à-lait (Lepomis gulosus) au cours de la décennie (1994-2003) précédant les 10 dernières années.
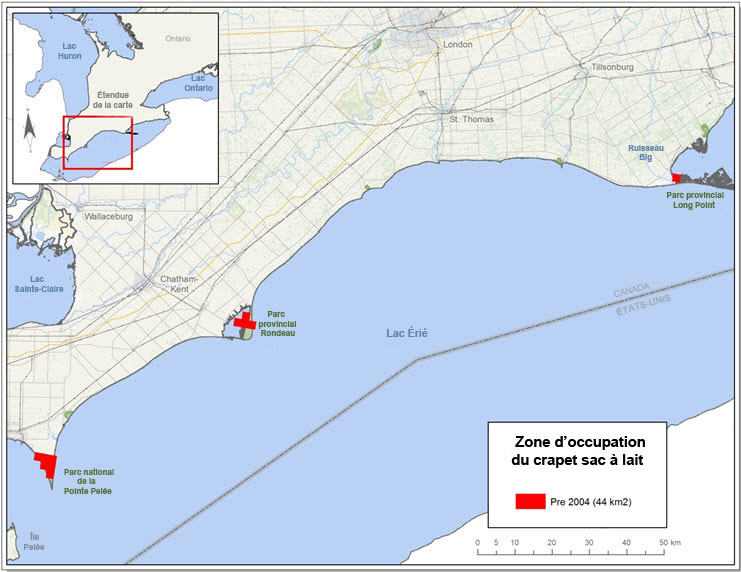
- Figure 5(c). Indice de zone d'occupation du crapet sac-à-lait (Lepomis gulosus) selon toutes les mentions historiques (avant 2004).
- Figure 6. Composition du substrat (en %) dans les sites où le crapet sac-à-lait (Lepomis gulosus) a été observé en 2005 (n = 11), en 2007 (n = 1) et en 2012 (n = 46) dans la baie Long Point.
- Figure 7. Histogramme illustrant la fréquence des tailles du crapet sac à lait (Lepomis gulosus) dans le parc national de la Pointe Pelée en 2002 et en 2003 (n = 332). Les flèches représentent les classes d'âge probables de 0 à 4 ans (H. Surette, University of Guelph, données inédites).
Liste des tableaux
- Tableau 1. résumé de l'effort d'échantillonnage passé et actuel dans l'aire de répartition connue du crapet sac-à-lait dans a) le parc échelle nationale de la pointe-pelée, b) la baie rondeau et c) la baie long point. les cellules grises représentent les sites où aucun crapet sac-à-lait (Lepomis gulosus) n'a été détecté.
- Tableau 2. Description des menaces qui peuvent avoir une incidence sur le crapet sac-à-lait (Lepomis gulosus) dans les zones d'occupation dont l'existence est connue au Canada. La classification des menaces est fondée sur le système de classification des menaces proposé par l'UICN et le Partenariat pour les mesures de conservation (Conservation Measures Partnership, ou CMP) (IUCN, 2014).
- Tableau 3. Classements et statuts du crapet sac-à-lait (Lepomis gulosus) à l'échelle mondiale (G), Échelle nationalee (N) et infraÉchelle nationalee (S; État ou province) (NatureServe, 2014).
Liste des annexes
COSEWIC
Committee on the Status
of Endangered Wildlife
in Canada

COSEPAC
Comité sur la situation
des espèces en péril
au Canada
Les rapports de situation du COSEPAC sont des documents de travail servant à déterminer le statut des espèces sauvages que l'on croit en péril. On peut citer le présent rapport de la façon suivante :
COSEPAC. 2015. Évaluation et Rapport de situation du COSEPAC sur lecrapet sac-à-lait (Lepomis gulosus) au Canada. Comité sur la situation des espèces en péril au Canada. Ottawa. x + 51 p. (Registre public des espèces en péril).
Rapport(s) précédent(s) :
COSEWIC 2005. COSEWIC assessment and update status report on the warmouth Lepomis gulosus in Canada. Committee on the Status of Endangered Wildlife in Canada. Ottawa. vi + 16 pp. (Registre public des espèces en péril).
COSEPAC. 2001. (Sous-presse). Évaluation et Rapport de situation du COSEPAC sur le crapet sac-à-lait (Lepomis gulosus) au Canada. Comité sur la situation des espèces en péril au Canada. Ottawa. ix + 14 p. (Registre public des espèces en péril).
Crossman, E.J., J. Houston et R.R. Campbell. 1994. Rapport de situation du COSEPAC sur la situation du crapet sac-à-lait (Lepomis gulosus) au Canada. Comité sur la situation des espèces en péril au Canada. Ottawa. Pages 1-14.
Le COSEPAC remercie Nick Mandrak (Ph. D.) et Lynn Bouvier d'avoir rédigé le rapport de situation sur le crapet sac-à-lait (Lepomis gulosus) auCanada, aux termes d'un marché conclu avec Environnement Canada. La supervision et la révision du rapport ont été assurées par John Post (Ph. D.), coprésident du Sous-comité de spécialistes des poissons d'eau douce du COSEPAC.
Pour obtenir des exemplaires supplémentaires, s'adresser au :
Secrétariat du COSEPAC
a/s Service canadien de la faune
Environnement Canada
Ottawa (Ontario)
K1A 0H3
Tél. : 819-938-4125
Téléc. : 819-938-3984
Courriel : COSEPAC courriel
Site web : COSEPAC
Also available in English under the title COSEWIC Assessment and Status Report on the Warmouth Lepomis gulosus in Canada.
Crapet sac-à-lait -- Illustration par J. Tomelleri. Reproduction autorisée.


Crapet sac-à-lait
Lepomis gulosus
Le crapet sac-à-lait (Lepomis gulosus) appartient à la famille des Centrarchidés. Il est l'un des onze membres de cette famille et l'un des six membres du genre Lepomis dans le bassin canadien des Grands Lacs. Il se distingue des autres Lepomis par la présence de dents sur la langue, une grande bouche et des bandes foncées rayonnant à partir de l'œil.
Le crapet sac-à-lait est largement réparti en Amérique du Nord, dans les bassins hydrographiques du Mississippi, de l'Atlantique et des Grands Lacs. L'espèce a également été introduite dans les bassins hydrographiques du Pacifique, aux États-Unis et au Mexique. Au Canada, on fait mention du crapet sac-à-lait dans trois localités, toutes dans le bassin du lac Érié.
Le crapet sac-à-lait est une espèce d'eau chaude qui préfère les échancrures très végétalisées des lacs, les cours d'eau à faible courant et les milieux humides. L'espèce conserve des préférences similaires en matière d'habitat tout au long de son cycle vital.
Le crapet sac-à-lait fraye dans un nid, et on pense qu'il peut frayer plusieurs fois par été. Il construit généralement un nid sur un substrat de limon et de sable couvert de brindilles et d'autres débris. Le mâle protège le nid et ventile activement les œufs fécondés. Le crapet sac-à-lait atteint la maturité à 2 ans ou lorsqu'il mesure 89 mm. La fécondité, très variable, est liée à la taille, comme c'est le cas chez de nombreux poissons d'eau douce. L'âge maximal connu est de 8 ans, et les taux de survie sont inconnus. On sait que l'espèce s'hybride avec d'autres membres de la famille des Centrarchidés.
La taille de la population canadienne de crapets sac-à-lait est actuellement inconnue. D'après les effectifs relativement élevés dans le parc national de la Pointe-Pelée (2002-2003) ainsi que dans la baie Long Point et à proximité de celle-ci (2003-2013), ces populations seraient bien établies. La population de la baie Rondeau est relativement moins grande, mais des observations régulières récentes (2003-2013) révèlent l'existence d'une population potentiellement bien établie dans cette localité. Des recherches additionnelles s'imposent dans les trois localités pour déterminer la taille et les tendances des populations.
Une grande variété de menaces ont des effets négatifs sur le crapet sac-à-lait dans l'ensemble de son aire de répartition. Les menaces les plus graves à la survie et à la persistance de l'espèce au Canada sont liées aux modifications des systèmes naturels résultant de l'élimination de la végétation aquatique et de la perte de milieux humides, et la pollution, attribuable aux pratiques agricoles et au développement. Aucune des preuves des menaces nuisant aux populations de crapets sac-à-lait qui existent n'est propre à l'espèce.
Le crapet sac-à-lait figure actuellement à titre d'espèce préoccupante dans la Loi sur les espèces en péril du Canada et la Loi de 2007 sur les espèces en voie de disparition de l'Ontario. Son habitat peut être indirectement protégé en vertu de la Loi sur les pêches du Canada puisque le crapet sac-à-lait cohabite avec des poissons ayant une valeur pour les pêches commerciale, récréative ou autochtone. L'espèce est non en péril à l'échelle mondiale (G5) et aux États-Unis (N5). Au Canada, elle est classée « gravement en péril » à l'échelle nationale (N1) et provinciale (S1).
Durée d'une génération
- ~ 3 ans
Y a-t-il un déclin continu [observé, inféré ou prévu] du nombre total d'individus matures?
- Inconnu
Pourcentage estimé de déclin continu du nombre total d'individus matures sur [cinq ans ou deux générations] (52-60 ans).
- Inconnu
Il est peu probable que le nombre d'individus ait diminué considérablement, car l'habitat de la grande sous-population du lac Carrigan (95 % de la population canadienne totale) n'a pas subi de modification importante.
- Inconnu
Pourcentage prévu de réduction du nombre total d'individus matures au cours des 100 prochaines années.
- Inconnu
Pourcentage [observé, estimé, inféré ou présumé] [de réduction ou d'augmentation] du nombre total d'individus matures au cours de toute période de [dix ans ou trois générations] commençant dans le passé et se terminant dans le futur. Voir ci-dessus.
- Inconnu
Est-ce que les causes du déclin sont clairement réversibles et comprises et ont effectivement cessé?
- Inconnu
Y a-t-il des fluctuations extrêmes du nombre d'individus matures?
- Inconnu
Superficie estimée de la zone d'occurrence
Avant 2004 = 1 628 km2
1994-2003 = 1 562 km2- 2 409 km2
Indice de zone d'occupation (IZO)
Avant 2004 = 44 km2
1994-2003 = 32 km2- 100 km2
La population totale est-elle gravement fragmentée?
- Non
Nombre de localités Table Footnotea
- Parc national de la Pointe-Pelée
- Baie Rondeau
- Baie Long Point/marais de la pointe Turkey/ruisseau Big
- 3
Y a-t-il un déclin continu [observé, inféré ou prévu] de la zone d'occurrence?
- Non
Y a-t-il un déclin continu [observé, inféré ou prévu] de l'indice de zone d'occupation?
- Non
Y a-t-il un déclin continu [observé, inféré ou prévu] du nombre de populations?
- Non
Y a-t-il un déclin continu [observé, inféré ou prévu] du nombre de localités Table Footnotea ?
- Non
Y a-t-il un déclin continu [observé, inféré ou prévu] de [la superficie, l'étendue ou la qualité] de l'habitat?
- Oui, de la qualité
Y a-t-il des fluctuations extrêmes du nombre de populations?
- Non
Y a-t-il des fluctuations extrêmes du nombre de localités Table Footnotea?
- Non
Y a-t-il des fluctuations extrêmes de la zone d'occurrence?
- Non
Y a-t-il des fluctuations extrêmes de l'indice de zone d'occupation?
- Non
Population:
Parc national de la Pointe-Pelée
- Nbre d'individus matures:
Inconnu
Baie Rondeau
- Nbre d'individus matures:
Inconnu
Baie Long Point/marais de la pointe Turkey/ruisseau Big
- Nbre d'individus matures:
Inconnu
- Nbre d'individus matures:
Total
Nbre d'individus matures:
Inconnu
La probabilité de disparition de l'espèce à l'état sauvage est d'au moins [20 % sur 20 ans ou 5 générations, ou 10 % sur 100 ans].
- Inconnu
- Les plus graves menaces à la survie et à la persistance du crapet sac-à-lait au Canada seraient liées aux modifications des systèmes naturels résultant de l'élimination de la végétation aquatique et de la perte de milieux humides, et la pollution, attribuable aux pratiques agricoles et au développement. De plus, des peuplements denses de roseaux communs envahissants éliminent l'habitat du crapet sac-à-lait.
- Situation des populations de l'extérieur?
Michigan (non en péril)
Ohio (apparemment non en péril)
État de New York (sans objet)
Pennsylvanie (vulnérable) Une immigration a-t-elle été constatée ou est-elle possible?
- Inconnu
Des individus immigrants seraient-ils adaptés pour survivre au Canada?
- Oui
Y a-t-il suffisamment d'habitat disponible au Canada pour les individus immigrants?
- Inconnu
La possibilité d'une immigration depuis des populations externes existe-t-elle?
- Non
L'information concernant l'espèce est elle de nature délicate?
- Non
COSEPAC : Espèce désignée « préoccupante » en avril 1994. Réexamen et confirmation du statut en novembre 2001 et en mai 2005. Réexamen du statut : l'espèce a été désignée « en voie de disparition » en mai 2015.
Le crapet sac-à-lait demeure une espèce peu surveillée et, quand il est détecté, c'est généralement dans le cadre d'activités de recherche ne le ciblant pas. Les résultats des activités d'échantillonnage dans les zones que l'on sait occupées par le crapet sac-à-lait au cours des 10 dernières années laissent croire que toutes les populations reliques se maintiennent actuellement. Des travaux d'échantillonnage d'envergure à proximité de site faisant l'objet de mentions historiques de l'espèce ont permis d'élargir l'aire de répartition connue de l'espèce dans la baie Long Point et la baie Rondeau. Le crapet sac-à-lait n'a pas été observé dans de nouveaux sites depuis le dernier rapport d'évaluation, malgré d'importants travaux d'échantillonnage dans des zones correspondant à son habitat préféré. Une comparaison de la zone d'occurrence actuelle (2004-2013) à celle de 2 périodes historiques (1994-2003 et avant 2004) indique une augmentation de la zone d'occurrence. En effet, la zone d'occurrence actuelle (2004-2013; 2 408,62 km2) a augmenté de 54,2 % par rapport à celle des 10 années précédentes (1994-2003; 1 561,70 km2) et de 47,9 % par rapport à toutes les données historiques (avant 2004; 1 628,36 km2). L'indice de zone d'occupation (IZO) montre une tendance semblable; en effet, on observe une hausse de l'IZO actuel (2004-2013) par rapport à celui des 2 périodes historiques (1994-2003 et avant 2004). L'IZO actuel (2004-2013; 100 km2) a plus que triplé comparativement à celui des 10 années précédentes (1994-2003; 32 km2) et a plus que doublé par rapport à toutes les données historiques (avant 2004; 44 km2). Il est difficile de déterminer la cause de ces augmentations de la zone d'occurrence et de l'IZO, l'effort d'échantillonnage n'étant pas uniforme et les données sur les tendances à long terme n'étant pas disponibles. Les hausses des 2 paramètres peuvent être attribuables en partie à l'augmentation des travaux d'échantillonnage dans les zones que l'ont sait occupées par le crapet sac-à-lait. Nos connaissances sur les conséquences des menaces qui pèsent sur les populations de crapets sac-à-lait se limitent à la documentation générale; cependant, les menaces les plus importantes à la survie et à la persistance de l'espèce au Canada seraient liées aux modifications des systèmes naturels, causées par l'élimination de la végétation aquatique et la perte de milieux humides, et la pollution, attribuable aux pratiques agricoles et au développement.
Le Comité sur la situation des espèces en péril au Canada (COSEPAC) a été créé en 1977, à la suite d'une recommandation faite en 1976 lors de la Conférence fédérale-provinciale sur la faune. Le Comité a été créé pour satisfaire au besoin d'une classification nationale des espèces sauvages en péril qui soit unique et officielle et qui repose sur un fondement scientifique solide. En 1978, le COSEPAC (alors appelé Comité sur le statut des espèces menacées de disparition au Canada) désignait ses premières espèces et produisait sa première liste des espèces en péril au Canada. En vertu de la Loi sur les espèces en péril (LEP) promulguée le 5 juin 2003, le COSEPAC est un comité consultatif qui doit faire en sorte que les espèces continuent d'être évaluées selon un processus scientifique rigoureux et indépendant.
Le Comité sur la situation des espèces en péril au Canada (COSEPAC) évalue la situation, au niveau national, des espèces, des sous-espèces, des variétés ou d'autres unités désignables qui sont considérées comme étant en péril au Canada. Les désignations peuvent être attribuées aux espèces indigènes comprises dans les groupes taxinomiques suivants : mammifères, oiseaux, reptiles, amphibiens, poissons, arthropodes, mollusques, plantes vasculaires, mousses et lichens.
Le COSEPAC est composé de membres de chacun des organismes responsables des espèces sauvages des gouvernements provinciaux et territoriaux, de quatre organismes fédéraux (le Service canadien de la faune, l'Agence Parcs Canada, le ministère des Pêches et des Océans et le Partenariat fédéral d'information sur la biodiversité, lequel est présidé par le Musée canadien de la nature), de trois membres scientifiques non gouvernementaux et des coprésidents des sous-comités de spécialistes des espèces et du sous-comité des connaissances traditionnelles autochtones. Le Comité se réunit au moins une fois par année pour étudier les rapports de situation des espèces candidates.
Le Service canadien de la faune d'Environnement Canada assure un appui administratif et financier complet au Secrétariat du COSEPAC.
Règne : Animaux
Phylum : Cordés
Classe : Actinoptérygiens
Ordre : Perciformes
Famille : Centrarchidés
Genre et espèce : Lepomis gulosus (Cuvier, 1829)
Nom commun français : crapet sac-à-lait (Page et al., 2013)
Nom commun anglais : warmouth (Page et al., 2013)
En raison des dents sur sa langue, le crapet sac-à-lait (Lepomis gulosus) a d'abord été classé dans son propre genre monotype, Chaenobryttus (Bailey et al., 1970). Ce dernier était considéré comme un synonyme du genre Lepomis. Malgré des efforts récents pour ressusciter le genre Chaenobryttus (Crossman et al.,1996), le crapet sac-à-lait est demeuré dans le genre Lepomis (Page et al., 2013).
Le crapet sac-à-lait appartient à la famille des Centrarchidés (Page et al., 2013). Il est caractérisé par une grande bouche dont la mâchoire supérieure se prolonge bien au-delà du bord antérieur de l'œil (voir la figure 1; Holm et al., 2010), parfois jusqu'au centre de l'œil ou plus loin chez les adultes (Trautman, 1981). De trois à cinq barres foncées rayonnent de l'œil et du museau (Trautman, 1981), et les nageoires pectorales sont généralement courtes, à bout arrondi (Holm et al., 2010). Le crapet sac-à-lait est également caractérisé par une bande de petites dents sur la langue (Holm et al.,2010).
Le crapet sac-à-lait est de couleur olive jaune clair à vert olive foncé (Holm et al., 2010). On trouve de 6 à 11 bandes doubles semblables à des chaînes de couleur olive foncé sur le dos et les flancs, tandis que de 3 à 5 barres gris foncé, brunes ou lavande rayonnent de l'œil et du museau vers l'arrière (Trautman, 1981). Les nageoires dorsale, caudale et anale molles sont fortement vermiculées, et les nageoires paires sont transparentes ou olive (Holm et al., 2010).
Le crapet sac-à-lait est l'une des 11 espèces de Centrarchidés que l'on trouve dans le bassin canadien des Grands Lacs (Holm et al., 2010). Il se distingue de l'achigan à grande bouche (Micropterus salmoides) et de l'achigan à petite bouche (M. dolomieu) par l'absence d'une nageoire dorsale encochée et par son corps trapu (Holm et al., 2010). Il a également moins d'épines anales (3) que le crapet de roche (Ambloplites rupestris; de 5 à 7 épines; Holm et al., 2010). Le crapet sac-à-lait se distingue de la marigane blanche (Pomoxis annularis) et de la marigane noire (P. nigromaculatus) par le nombre d'épines dorsales; il en a 10, tandis que les mariganes en possèdent de 6 à 8 (Holm et al., 2010). La grande bouche, les bandes foncées qui rayonnent de l'œil et la présence de dents sur la langue distinguent le crapet sac-à-lait des autres membres du genre Lepomis (Holm et al., 2010).

©J. Tomelleri, reproduction autorisée
Description longue pour la figure 1
L'espèce a une grande bouche dont la mâchoire supérieure se prolonge bien au delà du bord antérieur de l'œil. De 3 à 5 barres foncées rayonnent de l'œil et du museau. Les nageoires pectorales sont généralement courtes, à bout arrondi. Le corps est de couleur olive jaune clair à vert olive foncé. On trouve de 6 à 11 bandes doubles semblables à des chaînes de couleur olive foncé sur le dos et les flancs, tandis que de 3 à 5 barres gris foncé, brunes ou lavande rayonnent de l'œil et du museau vers l'arrière. Les nageoires dorsale, caudale et anale molles sont fortement vermiculées, et les nageoires paires, non tachetées, sont transparentes ou olive.
On ne possède actuellement aucune information sur les structures populationnelle et génétique des populations canadiennes de crapets sac-à-lait. Cependant, la structure populationnelle de l'espèce a été étudiée dans 14 bassins hydrographiques situés depuis la Caroline du Sud jusqu'à la Louisiane (Bermingham et Avise, 1986). On a utilisé l'ADN mitochondrial pour reconstituer les relations évolutives, et il a été conclu que les clones d'ADN qui étaient étroitement liés génétiquement étaient généralement contigus sur le plan géographique (Bermingham et Avise, 1986). En appliquant ces conclusions aux populations canadiennes de crapets sac-à-lait, on peut poser l'hypothèse que, puisque les 3 localités restantes de crapets sac-à-lait sont isolées les unes des autres par plus de 50 km et que de larges étendues de milieux non propices se trouvent entre ses localités (non géographiquement contigus), l'isolement génétique à cette échelle spatiale est probable.
Toutes les populations canadiennes de crapets sac-à-lait se trouvent dans une seule zone biogéographique nationale d'eau douce du COSEPAC (COSEWIC, 2011), c'est-à-dire la zone biogéographique des Grands Lacs et du haut Saint-Laurent. De ce fait, et puisqu'on ne possède pas assez d'information sur la viabilité des structures populationnelle et génétique, tous les crapets sac-à-lait devraient être considérés comme formant une seule unité désignable.
On trouve seulement le crapet sac-à-lait dans trois zones au Canada : le parc national de la Pointe-Pelée, la baie Rondeau et la baie Long Point. Ainsi, cette espèce et les zones qu'elle occupe sont d'importance nationale.
Le crapet sac-à-lait est indigène dans de nombreuses zones des bassins du Mississippi, de l'Atlantique et des Grands Lacs. Les populations indigènes sont très répandues dans la plus grande partie du centre et de l'est des États-Unis, du Texas jusqu'en Floride, au sud, et du Minnesota à l'État de New York, au nord (Page et Burr, 2011). Le crapet sac-à-lait a également été introduit à grande échelle dans les bassins versants du Pacifique, dans l'ouest des États-Unis (Nouveau-Mexique, Arizona, Californie, Nevada, Idaho, Oregon et État de Washington; Hubble, 1966; Page et Burr, 2011; NatureServe, 2014). L'espèce a aussi été introduite au Mexique (Page et al., 2013). Dans son aire de répartition naturelle de l'Illinois, elle a été introduite à grande échelle dans des bassins de retenue (Larimore, 1957). Malgré sa vaste répartition aux États-Unis, le crapet sac-à-lait se trouve seulement dans quelques zones isolées du sud-ouest de l'Ontario.
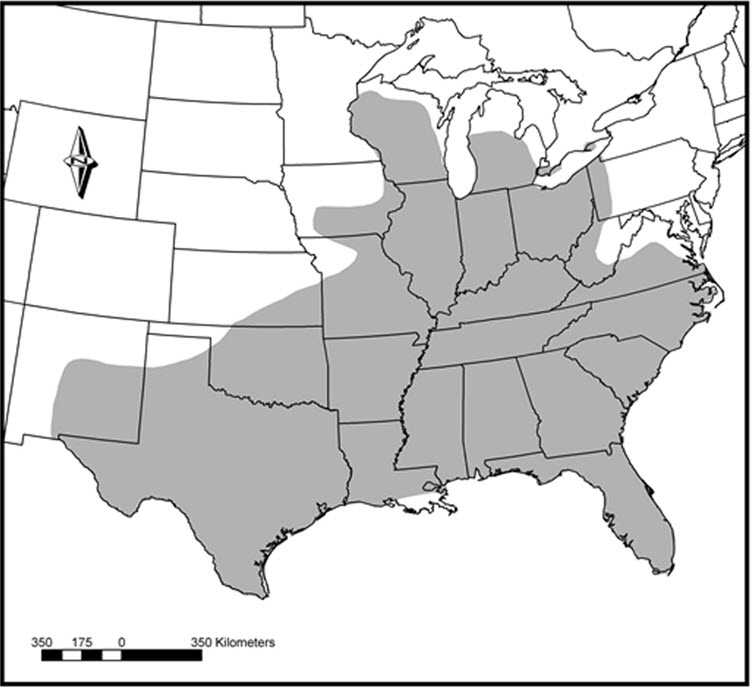
Carte modifiée d'après Page et Burr,1991
Description longue pour la figure 2
Carte montrant l'aire de répartition mondiale du crapet sac-à-lait. L'espèce est indigène dans de nombreuses zones des bassins du Mississippi, de l'Atlantique et des Grands Lacs. Les populations indigènes sont très répandues dans la plus grande partie du centre et de l'est des États-Unis, du Texas jusqu'en Floride, au sud, et du Minnesota à l'État de New York, au nord. Malgré sa vaste répartition aux États-Unis, le crapet sac-à-lait se trouve seulement dans quelques zones isolées du sud-ouest de l'Ontario.
La première observation du crapet sac-à-lait dans la baie Long Point et ses environs (ruisseau Big, marais du ruisseau Big et marais de la pointe Turkey) remonte à 2003, lorsqu'un jeune de l'année a été recueilli à l'intérieur de la baie Long Point.
Des mentions provenant de deux autres sites sont décrites dans la littérature. Un jeune de l'année du ruisseau Cedar (affluent du lac Érié) recueilli en 1994 (Leslie et al., 1999) s'est révélé être un crapet du Nord (L. peltastes) (E. Holm, Musée royal de l'Ontario, comm. pers., in COSEWIC, 2005). Un autre crapet sac-à-lait a été observé dans le ruisseau Duck (affluent du lac Sainte-Claire; Leslie et Timmins, 1998). Cependant, ce spécimen de référence n'a pas été récupéré ou vérifié; par conséquent, il est exclu du présent rapport. Des activités d'échantillonnage limitées ont été effectuées dans le ruisseau Duck en 2001 et en 2004, mais on n'y a pas détecté de crapets sac-à-lait. Il est toutefois improbable que le crapet sac-à-lait occupe ce système puisque les milieux ne semblent pas propices (DFO, données inédites; Essex Erie Conservation Authority, données inédites). De plus, les affluents canadiens du lac Sainte-Claire font l'objet d'échantillonnages à grande échelle depuis 2002 au moyen d'un équipement adéquat et selon un effort efficace favorisant la capture de crapets sac-à-lait; cependant, aucun individu n'a été trouvé (voir la figure 3a).
Selon Crossman et al. (1996), la colonisation des eaux canadiennes par le crapet sac-à-lait pourrait être plus récente que celle d'autres espèces de poissons d'eau douce indigènes, et pourrait être le résultat d'une période de réchauffement planétaire et/ou de l'expansion continue de l'aire de répartition après la dernière glaciation (COSEWIC, 2005). Il se pourrait également que le crapet sac-à-lait ait été récemment introduit dans ces systèmes par des actions humaines directes. Des introductions récentes, certaines fructueuses, ont en effet été rapportées dans les eaux états-uniennes (Van Meter et Trautman, 1970). Cependant, aucune population états-unienne qui aurait permis un transfert facile n'existe près des populations canadiennes, il n'y a aucune motivation pour un tel transfert, et il est improbable que l'on ait introduit des individus dans une aire hautement protégée, comme le parc national de Pointe-Pelée. L'hypothèse la plus probable est que le crapet sac-à-lait est présent au Canada depuis la dernière période glaciaire, mais qu'il n'a pas été repéré ou qu'il a été mal identifié jusqu'à la première mention de sa présence dans la baie Rondeau en 1966. Cette hypothèse est appuyée par une probabilité de détection généralement faible, malgré les échantillonnages à grande échelle dans l'aire de répartition connue au Canada (voir la section Activités de recherche).
De plus, si le crapet sac-à-lait a seulement colonisé l'aire de répartition canadienne récemment, on s'attendrait à ce qu'il soit présent dans d'autres milieux propices le long de la rive nord du lac Érié, qui aurait constitué le tracé de colonisation vers la population établie le plus à l'ouest, dans le parc national de la Pointe-Pelée. Parmi les milieux propices possibles figurent la rivière Canard, le complexe de la plage Holiday/ruisseau Big et le ruisseau Cedar, dans le comté d'Essex. Or, le crapet sac-à-lait n'a été détecté dans aucun de ces milieux. En effet, les efforts ont été vains dans la rivière Canard (années d'échantillonnage : 1980, 1985, 1990-91, 1994, 1996, 2002-2004, 2009, 2012-2014; sources variées), à la plage Holiday, qui a également fait l'objet d'activités d'échantillonnage intensives par verveux et par pêche électrique à partir d'un bateau en 2003 et en 2004 (L. Bouvier, données inédites), dans le ruisseau Big (affluent de la plage Holiday), échantillonné au moyen de verveux et de sennes en 2007 (N. Mandrak, données inédites) ainsi que dans le ruisseau Cedar, affluent du lac Érié situé entre la plage Holiday et Pointe-Pelée (neuf années d'échantillonnage de 1941 à 2013).
En outre, la connectivité entre les étangs du parc national de la Pointe-Pelée et le lac Érié est régulée par un cordon littoral sur le périmètre est du parc. Les brèches sont rares dans ce cordon littoral; on a noté seulement cinq cas de 1922 à 1983 (Surette, 2006). Les occasions de colonisation étaient donc limitées pour le crapet sac-à-lait durant la période précédant sa découverte en 1983.
Figure 3(a). Répartition du crapet sac-à-lait (Lepomis gulosus) au Canada. Les cercles gris représentent les sites d'échantillonnage où aucun crapet sac-à-lait n'a été détecté.
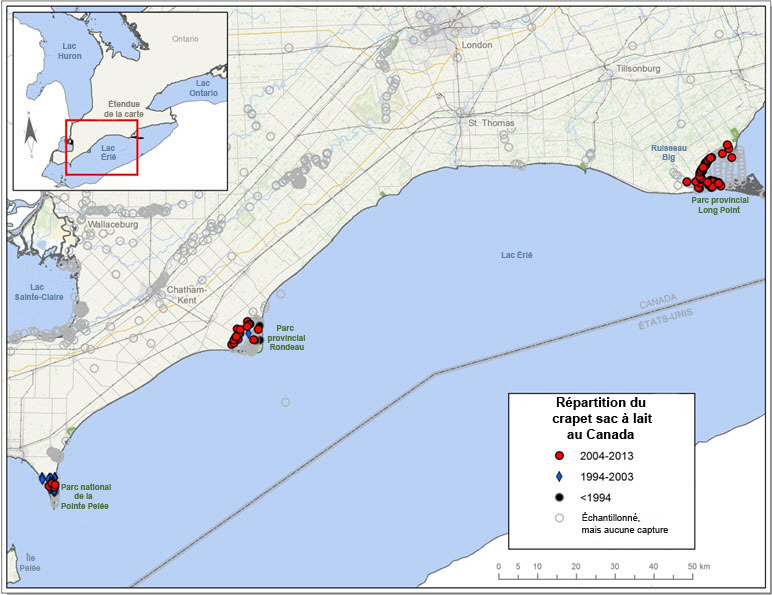
s.o.
Description longue pour la figure 3(a)
Carte montrant la répartition du crapet sac-à-lait au Canada, où l'espèce a été observée dans trois localités, toutes situées dans le bassin versant du lac Érié. Ces localités sont le parc provincial Rondeau, le parc national de la Pointe-Pelée et la baie Long Point. La répartition est indiquée pour trois périodes : avant 1994, 1994-2003 et 2004-2013.
Figure 3(b). Répartition du crapet sac-à-lait (Lepomis gulosus)dans le parc national de Pointe-Pelée. Les cercles gris représentent les sites d'échantillonnage où aucun crapet sac-à-lait n'a été détecté.
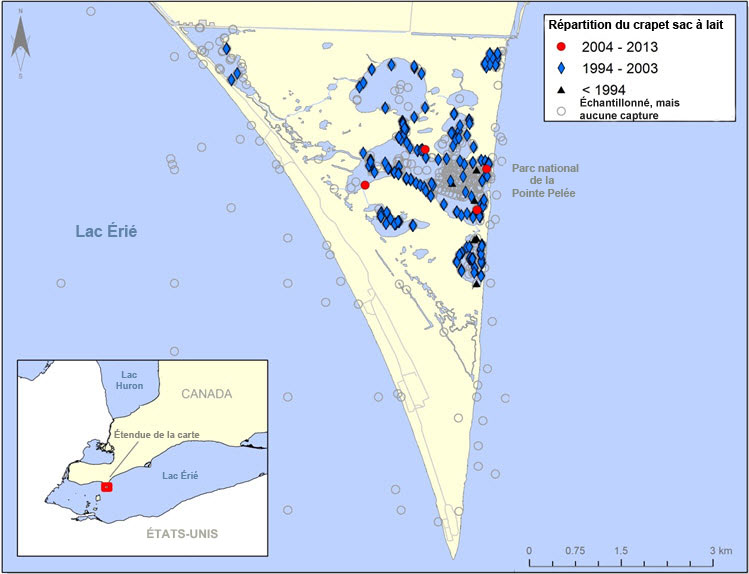
s.o.
Description longue pour la figure 3(b)
Carte montrant la répartition du crapet sac à lait dans le parc national de la Pointe Pelée. La répartition est indiquée pour trois périodes : avant 1994, 1994 2003 et 2004 2013.
Figure 3(c). Répartition du crapet sac-à-lait (Lepomis gulosus) dans la baie Rondeau. Les cercles gris représentent les sites d'échantillonnage où aucun crapet sac-à-lait n'a été détecté.
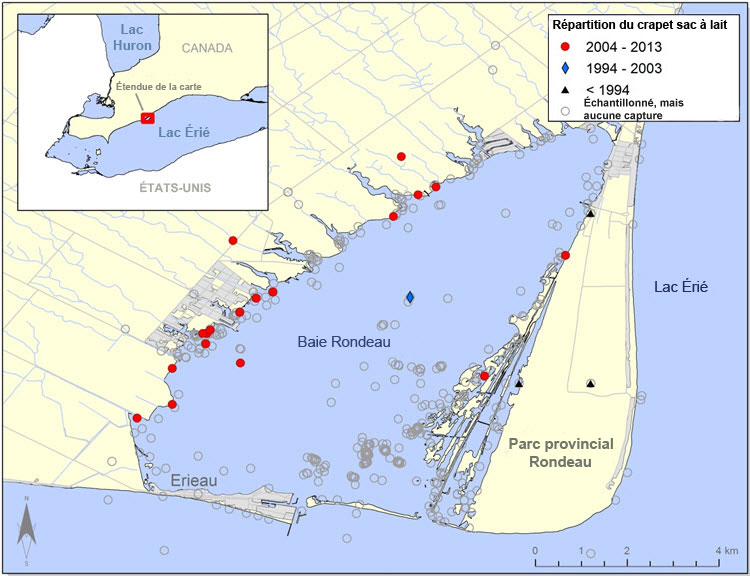
s.o.
Description longue pour la figure 3(c)
Carte montrant la répartition du crapet sac à lait dans la baie Rondeau. La répartition est indiquée pour trois périodes : avant 1994, 1994 2003 et 2004 2013.
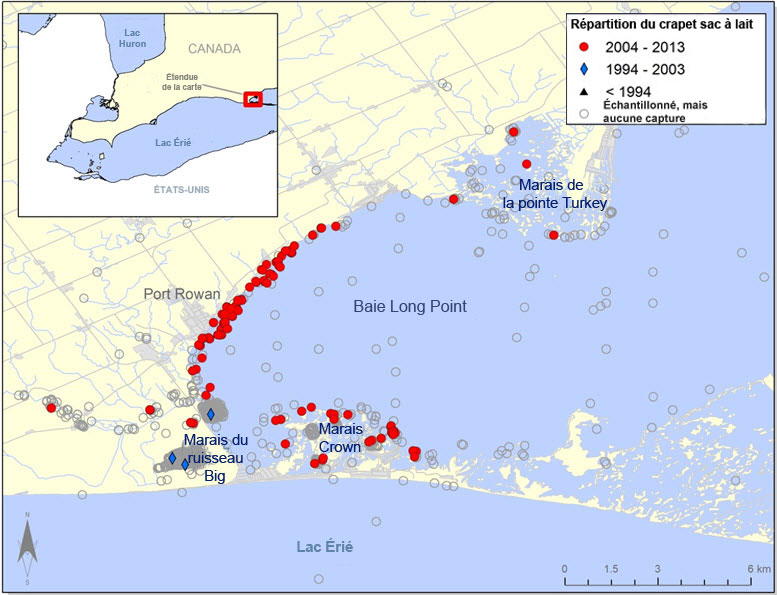
Figure 3(d). Répartition du crapet sac-à-lait (Lepomis gulosus) dans la baie Long Point et à proximité. Les cercles gris représentent les sites d'échantillonnage où aucun crapet sac-à-lait n'a été détecté.
s.o.
Description longue pour la figure 3(d)
Carte montrant la répartition du crapet sac à lait dans la baie Long Point. La répartition est indiquée pour trois périodes : avant 1994, 1994 2003 et 2004 2013.
Au Canada, le crapet sac-à-lait a seulement été observé dans 3 localités, toutes situées dans le bassin versant du lac Érié. La première mention date de 1966 et provient du parc provincial Rondeau (RPM F103-66; Crossman et Simpson, 1984), dans lequel l'espèce a par la suite été observée 2 fois en 1967 et 3 fois en 1968 (Crossman et Simpson, 1984). Le crapet sac-à-lait n'a pas été signalé de nouveau en eaux canadiennes avant 1983, lorsqu'un individu a été observé dans le lac Pond, dans le parc national de la Pointe-Pelée (ROM 42752; Crossman et Simpson, 1984). Après cette découverte dans le parc national de la Pointe-Pelée, 46 individus (28 adultes et 18 jeunes de l'année) ont été recueillis dans un seul site, du 3 juin au 18 octobre 1983 (Crossman et Simpson, 1984), venant ainsi confirmer la présence d'une population reproductrice en eaux canadiennes (Crossman et Simpson, 1984).
Les résultats des activités d'échantillonnage dans les sites occupés par le crapet sac-à-lait ces 10 dernières années laissent croire que toutes les populations se maintiennent (voir le tableau 1a-c). Des activités d'échantillonnage d'envergure dans des zones adjacentes aux sites des mentions historiques de l'espèce ont élargi l'aire de répartition connue de l'espèce dans la baie Long Point et la baie Rondeau. Une baisse de l'effort d'échantillonnage au cours de la même période dans le parc national de la Pointe-Pelée pourrait expliquer la réduction du nombre de points d'occurrence dans ce système.
| Plan d'eau | n | Année | Effort d'échantillonnage | Référence |
|---|---|---|---|---|
| Pointe Pelée | 0 | 1913-1982 | -15 années différentes dans cette période -principalement au moyen d'une senne |
Musée canadien de la nature (MCN), Musée royal de l'Ontario (MRO), personnel du parc Échelle nationale de la Pointe-Pelée (PNPP) [voir Surette (2006) pour les données complètes] |
| Pointe Pelée | 2 | 1983 | -verveux (< 24 h, 39 mouillages) | G. Mouland, données inédites (obtenues de J. Keitel, PNPP) |
| Pointe Pelée | IN (> 1) |
1989 | -senne (5 jours) -enquête auprès des pêcheurs (effort inconnu) |
E. Holm et D. Boehm (MRO, données inédites) K. Janoki et G. Mouland (Surette, 2006) |
| Pointe Pelée | 0 | 1992 | -enquête auprès des pêcheurs (effort inconnu) | T. Linke (Surette, 2006) |
| Pointe Pelée | 11 | 1993 | -trappe en filet (mouillage de 48 h, 3 sites, 2 campagnes) -senne (10 m, 5 traits) |
Dibble et al. (1995) |
| Pointe Pelée | IN (> 1) |
1997 | -senne (2 jours) -piège en plastique (5 jours) -pêche électrique par bateau (4,3 h) |
E. Holm, D. Boehm et M. Ciuk (ROM, données inédites) |
| Pointe Pelée | 0 | 2002 | -pêche électrique par bateau (4 sites) | N. Mandrak, données inédites |
| Pointe Pelée | 0 | 2002 | -verveux (mouillage de 24 h, 5 sites) -trappe en filet (mouillage de 24 h, 3 sites) |
N. Mandrak, données inédites |
| Pointe Pelée | 657 | 2002-2003 | -senne (55 campagnes) -pièges à ménés (80 campagnes) -pièges Windermere (80 campagnes) -trappe en filet (28 campagnes) -verveux (342 campagnes) |
Surette (2006) |
| Pointe Pelée | 1 | 2003 | -pêche électrique par bateau (100 m, 18 sites) -verveux (mouillage de 24 h, 8 sites) |
L. Bouvier, données inédites |
| Pointe Pelée | 0 | 2004 | -pêche électrique par bateau (100 m, 18 sites, 2 campagnes) -verveux (mouillage de 24 h, 8 sites, 2 campagnes) |
L. Bouvier, données inédites |
| Pointe Pelée | 1 | 2005 | -3 verveux appariés (2 gros et 1 petit, 2 sites) | Razavi (2006) |
| Pointe Pelée | 6 | 2009 | -verveux (mouillage de 24 h, 16 mouillages) | B. Glass, données inédites |
| Plan d'eau | n | Année | Effort d'échantillonnage | Référence |
|---|---|---|---|---|
| Baie Rondeau | 0 | 1921-1965 | 14 années différentes | MCN et MRO (MRO, données inédites) |
| Baie Rondeau | 1 | 1966 | Effort inconnu | Crossman et Simpson (1984) |
| Baie Rondeau | 2 | 1967 | Effort inconnu | Crossman et Simpson (1984) |
| Baie Rondeau | 5 | 1968 | Effort inconnu | Crossman et Simpson (1984) |
| Baie Rondeau | 2 | 1999 | Effort inconnu | MRO, données inédites |
| Baie Rondeau | 0 | 2002 | -pêche électrique par bateau (10 sites) | N. Mandrak, données inédites |
| Baie Rondeau | 0 | 2004 | -pêche électrique par bateau (> 1 000 s/500 m par site, 10 sites) -verveux (mouillage de 24 h, 28 sites) |
N. Mandrak, données inédites |
| Baie Rondeau | 2 | 2005 | -verveux (mouillage de 24 h, 24 sites) | N. Mandrak, données inédites |
| Baie Rondeau | 0 | 2005 | -senne bourse (1 trait, 3 sites; 2 traits, 5 sites; 3 traits, 14 sites) -senne à partir d'un bateau (1 trait, 5 sites) |
N. Mandrak, données inédites |
| Baie Rondeau | 3 | 2007 | -verveux (mouillage de 24 h, 128 mouillages) | B. Glass, données inédites |
| Baie Rondeau | 4 | 2008 | -verveux (mouillage de 24 h, 126 mouillages) | B. Glass, données inédites |
| Baie Rondeau | 5 | 2009 | -verveux (mouillage de 24 h, 78 mouillages) | B. Glass, données inédites |
| Baie Rondeau | 1 | 2009 | -verveux (effort inconnu) | M. Belore, ministère des Richesses naturelles de l'Ontario (MRNO), Unité de gestion du lac Érié (LEMU), données inédites |
| Baie Rondeau | 1 | 2013 | -verveux (mouillage de 24 h, 21 sites) | N. Mandrak, données inédites |
| Baie Rondeau | 0 | 2013 | -senne bourse (1 trait, 36 sites) -pièges lumineux quadrilobes (mouillage de 24 h, 21 sites) -chalut pélagique (100 m x 1 passage, 14 sites; 100 m x 3 passages, 1 site) |
N. Mandrak, données inédites |
| Baie Rondeau | 9 | 2013 | -mini verveux (mouillage de 24 h, 14 sites) | D. Marson, données inédites |
| Baie Rondeau | 0 | 2013 | -pêche électrique par bateau (4 x 100 m, 11 sites) | D. Marson, données inédites |
| Ruisseau Mill | 1 | 2013 | -verveux (4 sites) | J. Ciborowski, Université de Windsor, données inédites |
| Plan d'eau | n | Année | Effort d'échantillonnage | Référence |
|---|---|---|---|---|
| Baie Long Point | 0 | 1928-2003 | -18 années au cours de cette période, effort inconnu | MRNO, MRO et MCN (MRO, données inédites) |
| Marais du ruisseau Big | 0 | 1983-1985 | Effort inconnu | MCN et Université Wilfred Laurier (UWL) (MRO, données inédites) |
| Marais du ruisseau Big | 0 | 1979 | Effort inconnu | MCN et UWL (MRO, données inédites) |
| Marais du ruisseau Big | 0 | 2003 | -pêche électrique par bateau (50 m, 15 sites, 2 campagnes) -verveux (mouillage de 24 h, 4 sites, 2 campagnes) |
L. Bouvier, données inédites |
| Baie Long Point | 1 | 2003 | -pêche électrique par bateau (50 m, 18 sites, 2 campagnes) -verveux (mouillage de 24 h, 4 sites, 2 campagnes) |
L. Bouvier, données inédites |
| Baie Long Point | 0 | 2004 | -pêche électrique par bateau (50 m, 18 sites, 2 campagnes) -verveux (mouillage de 24 h, 4 sites, 2 campagnes) |
L. Bouvier, données inédites |
| Baie Long Point | 0 | 2004 | -pêche électrique par bateau (< 1 000 s [1 passage], 47 sites; > 1 000 s [2 passages], 10 sites) | N. Mandrak, données inédites |
| Marais du ruisseau Big | 4 | 2004 | -pêche électrique par bateau (50 m, 15 sites, 2 campagnes) -verveux (mouillage de 24 h, 4 sites, 2 campagnes) |
L. Bouvier, données inédites |
| Marais du ruisseau Big | 0 | 2005 | -senne (2 traits, 1 site) | N. Mandrak, données inédites |
| Baie Long Point | 0 | 2005 | -verveux (mouillage de 24 h, 24 sites) | N. Mandrak, données inédites |
| Marais du ruisseau Big | 11 | 2005 | -verveux (mouillage de 24 h, 26 sites) | N. Mandrak, données inédites |
| Baie Long Point | 0 | 2007 | -verveux (mouillage de 24 h, 58 sites) -senne (1 trait, 2 sites; 2 traits, 9 sites; 3 traits, 3 sites; 4 traits, 1 site) |
N. Mandrak, données inédites |
| Baie Long Point | 1 | 2007 | -senne (33 sites) | K. Oldenburg, MRNO, données inédites |
| Baie Long Point | 1 | 2007 | - pêche électrique par bateau (524-3 860 s, 9 sites) | N. Mandrak, données inédites |
| Ruisseau Big | 0 | 2008 | - pêche électrique par bateau (422-843 s, 10 sites) -senne à partir d'un bateau (1 trait, 3 sites; 3 traits, 6 sites; 4 traits, 1 site) -senne bourse (3 traits, 1 site) |
N. Mandrak, données inédites |
| Marais Crown | 0 | 2008 | -pièges à ménés (mouillage de 24 h, 9 sites) -senne (3 sites) |
K. Oldenburg, LEMU du MRNO, données inédites |
| Ruisseau Cedar | 0 | 2008 | -senne (3 sites) | K. Oldenburg, LEMU du MRNO, données inédites |
| Pointe Turkey | 0 | 2009 | -pièges à ménés (mouillage de 24 h, 12 sites) -verveux (22 sites) |
K. Oldenburg, LEMU du MRNO, données inédites |
| Barre de sable Bluff | 0 | 2009 | -pêche électrique (4 sites) -verveux (9 sites) -senne (4 sites) |
K. Oldenburg, LEMU du MRNO, données inédites |
| Baie Long Point | 141 | 2009 | -verveux (mouillage de 24 h, 368 campagnes) | Gislason et al. (2010) |
| Marais Crown | 4 | 2009 | -pêche électrique (5 sites) | K. Oldenburg, LEMU du MRNO, données inédites |
| Pointe Turkey | 1 | 2009 | -pêche électrique (8 sites) | K. Oldenburg, LEMU du MRNO, données inédites |
| Baie Long Point | 10 | 2010 | -verveux (mouillage de 24 h, 129 mouillages) | B. Glass, données inédites |
| Marais Murray | 1 | 2010 | -verveux (mouillage de 24 h, 23 mouillages) | J. Wilson, Long Point Conservation Authority (LPCA), données inédites |
| Ruisseau Big | 7 | 2011 | Effort inconnu | J. Wilson, LPCA, données inédites |
| Marais de la pointe Turkey | 1 | 2011 | Effort inconnu | J. Wilson, LPCA, données inédites |
| Baie Long Point | 35 | 2012 | -verveux (mouillage de 24 h, 47 sites) | N. Mandrak, données inédites |
| Baie Long Point | 11 | 2012 | -senne bourse (5 traits, 60 sites, 2 campagnes) | N. Mandrak, données inédites |
| Baie Long Point | 0 | 2013 | -senne bourse (5 traits, 34 sites) | N. Mandrak, données inédites |
| Baie Long Point | 0 | 2013 | -senne bourse (3 traits, 1 site) -pêche électrique par bateau (1 000 m, 2 sites; 800 m, 1 site; 400 m, 6 sites; 200 m, 2 sites) -trémail (0,5-0,75 h, 3 sites) |
D. Marson, données inédites |
| Baie Long Point | 3 | 2013 | -senne bourse (5 traits, 60 sites, 2 campagnes) | N. Mandrak, données inédites |
| Baie Long Point | 3 | 2013 | -mini verveux (mouillage de 24 h, 18 sites) | D. Marson, données inédites |
Pour examiner les tendances de la zone d'occurrence et de l'indice de zone d'occupation (IZO) selon la période d'évaluation antérieure (1994-2003) et toutes les mentions historiques (avant 2004), la période actuelle (2004-2013) est comparée séparément aux 10 années précédentes (1994-2003) et à toutes les mentions historiques (avant 2004). Les deux périodes historiques ne devraient pas être comparées entre elles, mais plutôt faire chacune l'objet d'une comparaison distincte avec la période actuelle.
Une comparaison de la zone d'occurrence actuelle (2004-2013) par rapport à celle des 2 périodes historiques (1994-2003 et avant 2004; voir la figure 3) indique une hausse de la zone d'occurrence. La zone d'occurrence actuelle (2004-2013; 2 408,62 km2) a augmenté de 54,2 % par rapport à celle des 10 dernières années (1994-2003; 1 561,70 km2) et de 47,9 % par rapport à toutes les mentions historiques (avant 2004; 1 628,36 km2).
L'IZO montre une tendance semblable, affichant une hausse lorsque les données actuelles (2004-2013) sont comparées aux données des 2 périodes historiques (1994-2003 et avant 2004). L'IZO actuel (2004-2013; 100 km2) a plus que triplé par rapport à celui des 10 années précédentes (1994-2003; 32 km2) et a plus que doublé par rapport à toutes les mentions historiques (avant 2004; 44 km2).
Il est difficile de déterminer la cause des hausses de la zone d'occurrence et de l'IZO, l'effort d'échantillonnage n'étant pas uniforme et les données sur les tendances à long terme n'étant pas disponibles. Les augmentations de ces deux paramètres peuvent être attribuables en partie à la hausse de l'effort d'échantillonnage dans les zones que l'on sait occupées par le crapet sac-à-lait (baie Long Point et baie Rondeau).
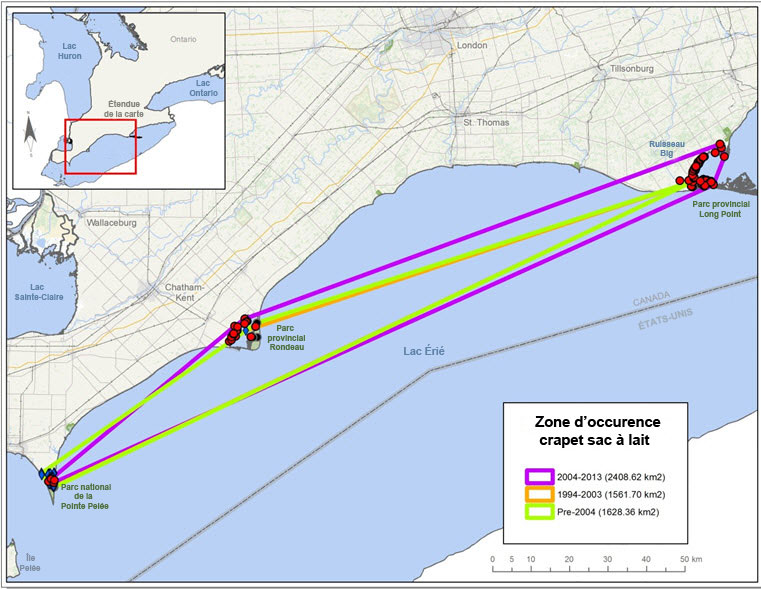
Description longue pour la figure 4
Carte illustrant la zone d'occurrence du crapet sac à lait au Canada selon la méthode de l'enveloppe convexe pour 3 périodes : 2004 2013 (2 408,62 km2), 1994 2003 (1 561,7 km2) et avant 2004 (1 628 km2).
Selon le Standards and Petitions Subcommittee de l'Union internationale pour la conservation de la nature UICN (IUCN, 2014), un taxon peut être considéré comme gravement fragmenté lorsque la plus grande partie de la zone d'occupation totale (> 50 %) est constituée de parcelles d'habitat qui sont :
- plus petites que ce qui est nécessaire pour soutenir une population viable et
- éloignées des autres parcelles d'habitat par de grandes distances.
Le crapet sac-à-lait répond au dernier critère puisque les populations sont séparées les unes des autres par plus de 50 km, et il n'y a que peu de milieux propices entre les populations, voire aucun. Cependant, il est peu probable que les populations actuelles puissent être considérées comme non viables; en effet, les données sur les tendances de l'espèce laissent croire que les populations sont viables aux trois sites. Ainsi, le crapet sac-à-lait n'est pas considéré comme très fragmenté.
La plus grande partie des relevés qui ont permis de déceler des crapets sac-à-lait ne visaient pas spécifiquement cette espèce. On a observé le crapet sac-à-lait au moyen des engins suivants : pêche électronique par bateau, verveux, senne, pièges à ménés et pièges Windermere. Le tableau 1 (a-c) présente un aperçu de tous les travaux d'échantillonnage connus qui ont été effectués dans les zones réputées être fréquentées par le crapet sac-à-lait (présentés par site, plan d'eau et année). Ce tableau donne résume également l'effort d'échantillonnage lors de chaque sortie d'échantillonnage, et si la sortie a permis d'observer des crapets sac-à-lait.
Le crapet sac-à-lait a été observé pour la première fois dans le parc national de la Pointe-Pelée en 1983. Surette (2006) fournit des renseignements détaillés sur les premiers échantillonnages de poissons sur la pointe Pelée de 1940 à 2003 (voir le tableau 1.1 dans Surette, 2006). Un total de 16 campagnes d'échantillonnage menées 15 années différentes au cours de la période de 1940 à 1983 n'ont pas permis de déceler la présence de l'espèce dans ce système, et ce, au moyen de divers engins d'échantillonnage, dont les suivants : senne, filets maillants, pièges à ménés, enquêtes auprès des pêcheurs et trappes en filet (voir le tableau 1a). La première mention de l'espèce consistait en 2 individus observés en 1983 (G. Mouland, données inédites). Par la suite, l'espèce a été rapportée en faibles nombres en 1989, en 1993 et en 1997. Lors d'une étude à grande échelle d'assemblages de poissons réalisée en 2002 et en 2003, 657 crapets sac-à-lait ont été observés dans le cadre de 87 campagnes d'échantillonnage sur 117 (Surette, 2006). Les étangs de la pointe Pelée ont fait de nouveau l'objet d'échantillonnages en 2004 (n = 0), en 2005 (n = 1) et en 2009 (n = 6), qui ont relevé de faibles effectifs de l'espèce. L'effectif beaucoup plus élevé observé en 2002-2003 par rapport à ceux des campagnes d'échantillonnage suivantes est probablement attribuable à la diminution de l'effort d'échantillonnage qui a suivi les relevés de 2002-2003 (voir le tableau 1).
Le crapet sac-à-lait qui a été observé dans la baie Rondeau en 1966 représente la première occurrence de cette espèce en eaux canadiennes (voir le tableau 1b). L'espèce n'a été la cible d'aucune étude dans ce système, mais des travaux d'échantillonnage d'envergure au moyen d'engins réputés être efficaces pour déceler les crapets sac-à-lait ont été effectués dans la baie Rondeau en 2007 (128 mouillages de verveux), en 2008 (126 mouillages de verveux) et en 2009 (78 mouillages de verveux; B. Glass, données inédites) et ont permis de détecter respectivement 3, 4 et 5 crapets sac-à-lait (B. Glass, données inédites). D'autres échantillonnages par verveux en 2013 ont permis la capture de 11 autres individus (D. Marson, données inédites; N. Mandrak, données inédites).
La première mention de l'espèce dans la baie Long Point et ses environs (ruisseau Big, marais du ruisseau Big et marais de la pointe Turkey) a été faite en 2003; il s'agissait d'un seul individu capturé par verveux (L. Bouvier, données inédites). Depuis cette mention, le complexe de la baie Long Point a été exhaustivement échantillonné (voir le tableau 1c). L'espèce a ainsi été observée annuellement dans le complexe de 2003 à 2013 (sauf en 2006 et en 2008). Le plus grand nombre de crapets sac-à-lait a été répertorié à l'occasion d'une activité de surveillance de la pêche commerciale aux poissons communs par verveux le long du rivage nord de la baie en 2009, où 141 crapets sac-à-lait ont été rapportés lors de 368 mouillages (Gislason et al., 2010). Le crapet sac-à-lait semble occuper toutes les aires de la baie Long Point intérieure, dont le marais de la pointe Turkey et le marais du ruisseau Big, mais ne semble pas se trouver dans la baie extérieure. Cette tendance était à prévoir compte tenu de l'absence de milieux propices à cet endroit.
Le crapet sac-à-lait est une espèce d'eau chaude qui préfère les milieux couverts de végétation dans les lacs, les cours d'eau à faible courant et les milieux humides (Holm et al., 2010; Page et Burr, 2011). Les individus occupent généralement les eaux peu profondes, et une grande partie des spécimens ont été capturés dans des eaux de moins de 2 m. Les seuils de tolérance à la teneur en oxygène sont inconnus pour les populations canadiennes, mais des crapets sac-à-lait ont survécu dans des systèmes pauvres en oxygène (jusqu'à 3,6 ppm) de l'Illinois lorsque la température de l'eau était de 20 °C (Larimore, 1957, in Becker, 1983). La description du substrat, sous forme de pourcentage de composition estimé, était disponible pour les sites où le crapet sac-à-lait a été décelé dans le complexe de la baie Long Point en 2005 (n = 11), en 2007 (n = 1) et en 2012 (n = 46). Les substrats étaient composés d'une combinaison de limon, de sable et de matière organique, et seulement 2 sites comprenaient de l'argile (seulement 10 % dans chaque site). Le type de substrat dominant le plus abondant dans l'ensemble des sites était le limon, suivi du sable.
L'habitat de fraye et d'alevinage correspondrait à l'habitat des adultes et caractérisé par des zones peu profondes (moins de 2 m) à végétation abondante, à la fois submergée et émergente (Becker, 1983; Lane et al., 1996a, b).
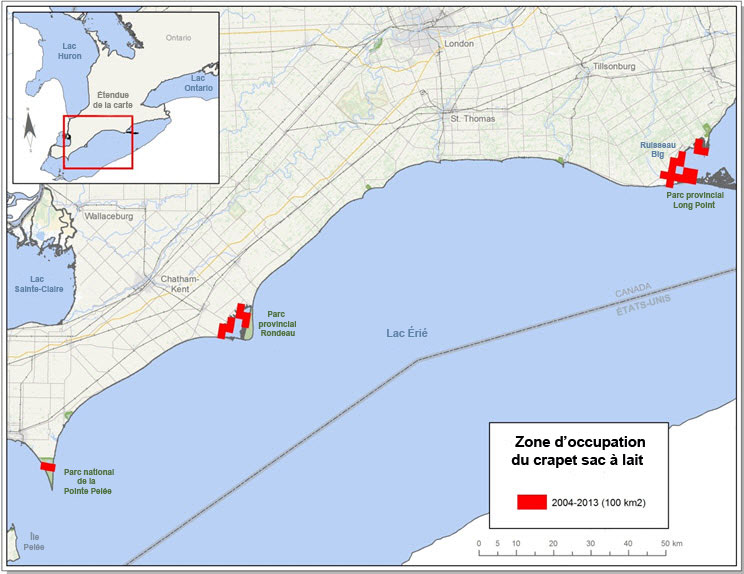
s.o.
Description longue pour la figure 5(a)
Carte illustrant l'indice de zone d'occupation (IZO) du crapet sac-à-lait au Canada pour la période de 2004 à 2013. L'IZO est de 100 km2.
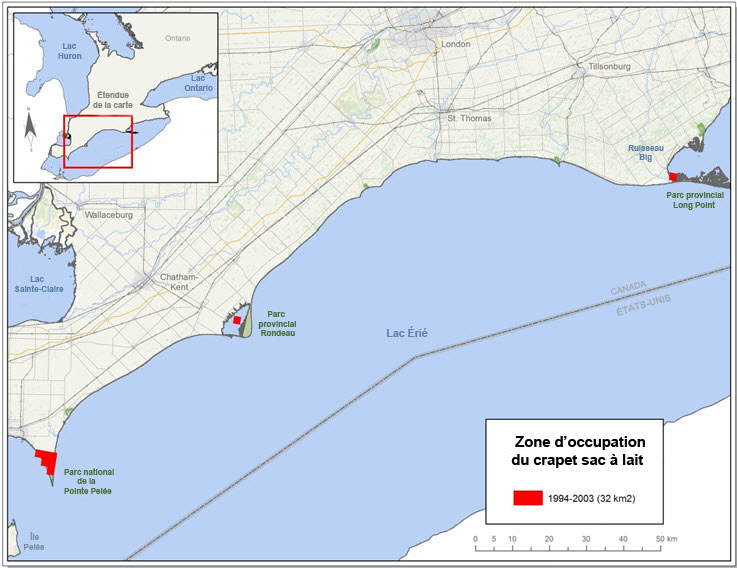
s.o.
Description longue pour la figure 5(b)
Carte illustrant l'indice de zone d'occupation (IZO) du crapet sac-à-lait au Canada pour la période de 1994 à 2003. L'IZO est de 32 km2.
s.o.
Description longue pour la figure 5(c)
Carte illustrant l'indice de zone d'occupation (IZO) du crapet sac-à-lait au Canada pour la période avant 2004. L'IZO est de 44 km2.
Figure 6. Composition du substrat (en %) dans les sites où le crapet sac-à-lait (Lepomis gulosus) a été observé en 2005 (n = 11), en 2007 (n = 1) et en 2012 (n = 46) dans la baie Long Point.
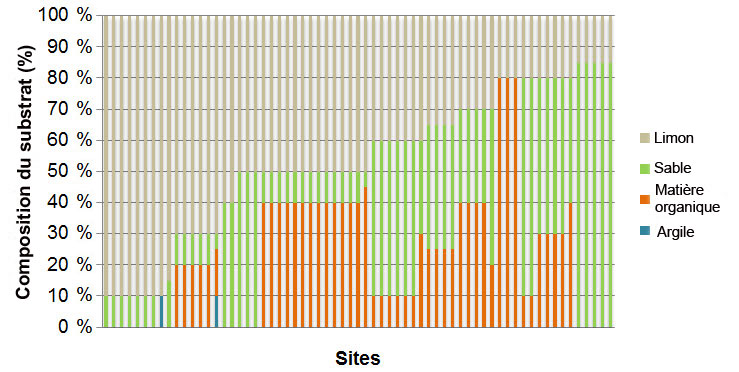
Description longue pour la figure 6
Graphique illustrant la composition du substrat (pourcentage de limon, de sable, de matière organique et d'argile) dans les sites où le crapet sac à lait a été observé en 2005, en 2007 et en 2012 dans la baie Long Point.
Considérées comme l'une des plus graves menaces pesant sur les populations de crapets sac-à-lait au Canada (voir la section MENACES ET FACTEURS LIMITATIFS), des modifications de l'habitat historique d'envergure ont eu lieu dans la baie Rondeau et sur la pointe Pelée. Dans la baie Rondeau, environ 70 % de la rive ouest a été récupérée à des fins agricoles ou résidentielles (Gilbert et Locke, 2007). De vastes milieux humides sur la rive nord-ouest ont été réduits à des parcelles isolées, séparées les unes des autres par des champs agricoles et des zones résidentielles (Gilbert et Locke, 2007). La première évaluation des milieux humides de la baie Rondeau a été réalisée au début des années 1980; on a alors estimé que les milieux humides restants couvraient environ 740 ha (Gilbert et al., 2007). Une estimation subséquente des milieux humides grâce à une couverture aérienne effectuée en 2006 indiquait que la superficie était de quelque 107 ha (169 ha avec les zones tampons) (Gilbert et al., 2007). De même, il est estimé que près de 60 % des milieux humides historiques de la pointe Pelée ont été asséchés et endigués de la fin du 19e siècle au milieu du 20e siècle à des fins agricoles (Dobbie et al., 2006).
L'introduction et l'établissement de macrophytes aquatiques envahissants ont aussi considérablement altéré l'habitat dans la baie Rondeau et la baie Long Point. Des peuplements importants de roseaux communs (Phragmites australis subsp. australis) dans la baie Long Point et la baie Rondeau ont réduit la superficie des milieux propices au crapet sac-à-lait (Gilbert et Locke, 2007; Badzinski et al., 2008).
En conditions de croissance optimales, le roseau commun peut coloniser rapidement les marais, tuant et remplaçant la végétation palustre indigène, ce qui augmente l'accrétion des substrats et, à terme, influe sur la composition et l'abondance de la flore indigène (Badzinksi et al., 2008 et les références qui y sont mentionnées). Une étude réalisée en 2006 visait à mesurer l'abondance et la répartition du roseau commun dans 5 complexes de marais de la baie Long Point. Elle a été conçue spécifiquement pour comparer la situation actuelle et la situation lors de la dernière évaluation, effectuée en 1999 (Wilcox et al., 2003; Badzinski et al., 2008). Dans l'ensemble, il a été noté que le roseau commun était largement réparti dans chaque complexe de marais et que son abondance avait grandement augmenté depuis l'évaluation de 1999 (Badzinski et al., 2008). Pour mesurer les changements d'abondance et de répartition, des orthophotos ont été utilisées pour une vérification au sol afin de déterminer l'emplacement et la taille des communautés végétales (Badzinski et al., 2008). Trois des 5 complexes de marais inclus dans cette étude sont particulièrement importants pour le crapet sac-à-lait, et on a décelé récemment des crapets sac-à-lait dans le marais du ruisseau Big, le marais Crown et le marais de la pointe Turkey (voir la figure 3d). Dans le marais du ruisseau Big, la couverture actuelle du roseau commun a été estimée à une superficie de 76 ha; comparativement aux estimations de 1999 (3 ha), cela représente une hausse annuelle de quelque 48 % (Badzinski et al., 2008). Une tendance similaire a été observée dans le marais Crown, où les valeurs historiques (8 ha), comparativement aux estimations de 2006 (48 ha), représentaient une hausse annuelle approximative de 27,8 % (Badzinski et al., 2008). Malheureusement, les tendances temporelles pour le marais de la pointe Turkey n'ont pas pu être obtenues, car les estimations de 1999 n'étaient pas disponibles. Les augmentations continues de la répartition et de l'abondance du roseau commun pourraient avoir un effet négatif sur les populations de crapets sac-à-lait en diminuant la qualité et la disponibilité de l'habitat.
Il est difficile de prévoir les effets à long terme qu'auront les changements climatiques sur la disponibilité de l'habitat du crapet sac-à-lait, qui pourraient lui être à la fois favorables et défavorables. Doka et al. (2006) ont réalisé une évaluation des conséquences prévues des changements climatiques sur les assemblages de poissons dans les milieux humides en évaluant la vulnérabilité des espèces de poissons aux changements climatiques.Une matrice de vulnérabilité a été calculée d'après la situation de l'espèce ainsi que d'après les associations de température et d'habitat (Doka et al., 2006). Les résultats indiquent que, sur les 99 espèces de poissons évaluées, le crapet sac-à-lait arrivait au deuxième rang parmi les espèces les plus vulnérables. Les effets prévus des changements climatiques incluaient la hausse de la température de l'eau ainsi que la diminution des niveaux d'eau et des fluctuations de ceux-ci (Mortsch, 1998; Lemmen et Warren, 2004). Tandis que l'augmentation de la température de l'eau peut accroître la dispersion et la colonisation du crapet sac-à-lait dans de nouveaux milieux, la diminution des niveaux d'eau peut restreindre l'habitat disponible dans les zones actuellement occupées par l'espèce (p. ex. baie Rondeau) ou faciliter l'invasion et l'expansion du roseau commun (p. ex. baie Long Point) (Badzinski et al., 2008).
On dispose de peu d'information sur les caractéristiques du cycle vital du crapet sac-à-lait au Canada, mais des données détaillées existent sur les populations de l'Illinois (Larimore, 1957, in Becker, 1983). L'information suivante provient du compte rendu de Larimore (1957) décrit dans le document de Becker (1983), sauf indication contraire.
La ponte commence en mai, atteint son sommet au début juin et ralentit au début juillet. La durée de la période de ponte peut différer selon les populations et est très variable d'une année à l'autre. Il a été montré que le crapet sac-à-lait peut frayer plusieurs fois au cours d'un été, lorsque la température de l'eau approche 21,5 °C. Le crapet sac-à-lait construit un nid sur un substrat de limon et de sable, parfois couvert de brindilles ou d'autres débris, à une profondeur de 0,6 à 0,8 m. Le mâle protège le nid et ventile activement les œufs fécondés.
Le crapet sac-à-lait atteint la maturité à 2 ans ou lorsqu'il mesure 89 mm (Carlander, 1969). La durée d'une génération serait d'environ 3 ans (COSEWIC, 2005). La fécondité est une fonction de la taille de l'individu, comme c'est le cas chez de nombreux poissons d'eau douce. Il a été observé que les femelles de 89 à 180 mm de longueur portaient de 4 500 à 37 500 œufs, tandis que les femelles d'une longueur de 94 à 137 mm en portaient de 17 200 à 63 200. On a estimé le taux de fécondité des crapets sac-à-lait vivant dans le lac Blackwater, en Caroline du Sud; les femelles comptaient de 798 à 34 257 œufs, et la fécondité pourrait être exprimée selon la relation suivante : log10F = -4,678 + 3,889 log10LT, où F = fécondité et LT = longueur totale (mm) (r2 = 0,67) (Panek et Cofield, 1978). Un œuf fécondé de crapet sac-à-lait a un diamètre de 0,95 à 1,03 mm. Les œufs fécondés éclosent en 34,5 h à des températures de l'eau variant de 25 à 26,4 °C.
L'âge maximal connu du crapet sac-à-lait est de huit ans (COSEWIC, 2005), et les taux de survie sont inconnus. Un histogramme illustrant la fréquence des tailles des individus échantillonnés sur la pointe Pelée en 2002 et en 2003 indique que la population comptait alors probablement au moins cinq classes d'âge (voir la figure 7; H. Surette, Université de Guelph, données inédites, in COSEWIC, 2005).
On sait que le crapet sac-à-lait s'hybride avec d'autres Centrarchidés (Childers, 1971). La viabilité des jeunes issus de l'hybridation de crapets sac-à-lait avec des crapets arlequins (L. macrochirus), des L. microlophus et des crapets verts (L. cyanellus) était respectivement de 58, 62 et 62 % (Childers, 1971). Ces estimations de la viabilité proviennent d'une expérience en laboratoire, et les taux d'hybridation et de viabilité hors laboratoire sont inconnus.
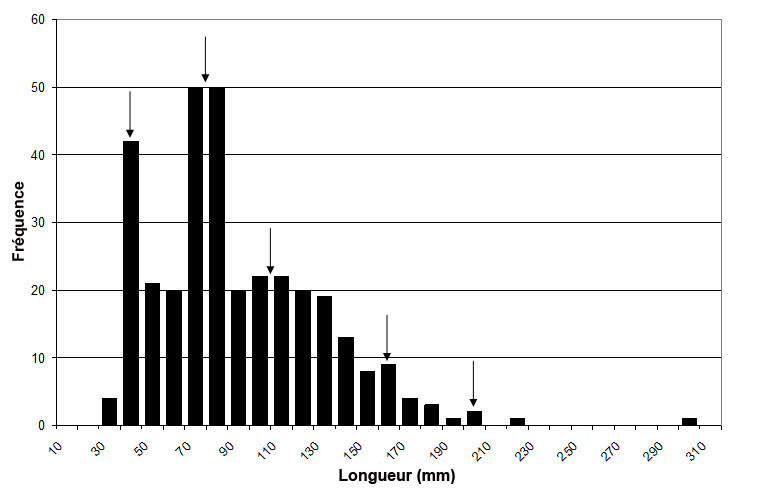
Description longue pour la figure 7
Chart illustrating the length-frequency relationship for Warmouth recorded from Point Pelee National Park in 2002 and 2003.
On en connaît peu sur la physiologie du crapet sac-à-lait. Cependant, il semblerait tolérant à de faibles teneurs en oxygène. Il a d'ailleurs été observé dans des systèmes pauvres en oxygène (aussi peu que 3,6 ppm) de l'Illinois lorsque la température de l'eau était de 20 °C (Larimore, 1957, in Becker, 1983). Aucune étude à ce jour ne cible l'adaptabilité du crapet sac-à-lait.
La capacité de dispersion et les tendances de déplacement du crapet sac-à-lait ont été étudiées dans 2 réseaux fluviaux de l'est du Tennessee (Gatz et Adams, 1994). Les tendances de déplacement de l'espèce et de 4 autres membres de la famille des Centrarchidés ont également été examinées durant une étude de marquage-recapture réalisée sur 3 ans (Gatz et Adams, 1994). Un total de 123 crapets sac-à-lait ont été marqués au cours de l'étude. Des chercheurs ont mené des échantillonnages tous les 3 mois au cours de l'étude, et 20 crapets sac-à-lait ont été recapturés (Gatz et Adams, 1994). La distance maximale qu'un individu a parcourue entre les captures était de 300 m (Gatz et Adams, 1994). En tenant compte de toutes les espèces (crapet rouge [Lepomis auratus], crapet arlequin, crapet de roche, achigan à grande bouche et crapet sac-à-lait), un total de 6 357 individus ont été marqués pendant l'étude, et 1 364 ont été recapturés (Gatz et Adams, 1994). Sur le nombre d'individus recapturés, 6 (1 crapet rouge, 1 achigan à grande bouche et 3 crapets arlequins) se sont déplacés sur de grandes distances (> 10 km, mais pas plus de 17,6 km). Même si cette étude n'a pas été réalisée en eaux canadiennes, on peut inférer que le crapet sac-à-lait a des capacités limitées de dispersion et de migration sur de grandes distances.
Le crapet sac-à-lait se nourrit à la fois en zones pélagiques et en zones benthiques. Il mange principalement des crustacés, des insectes aquatiques, des écrevisses, des mollusques et d'autres poissons (Carlander, 1969; Becker, 1983; COSEWIC, 2005). Les juvéniles se nourrissent essentiellement de plancton et de petits insectes, tandis que les adultes ajoutent à leur alimentation des écrevisses, des poissons et des insectes (McMahon et al., 1984 et les références qui y sont mentionnées). Tumlinson et al. (2007), dans leur analyse de l'alimentation de l'espèce, ont indiqué que sur les 133 estomacs de crapets sac-à-lait examinés, la plus grande partie contenait des naïades d'éphémères (Éphéméroptères) et des écrevisses.
Des indices circonstanciels laissent croire que le crapet sac-à-lait et le crapet vert pourraient être en compétition pour des ressources et que les zones abondantes en une de ces espèces semblent ne pas abriter l'autre espèce (DFO, données inédites). À titre d'exemple, le crapet sac-à-lait semble être abondant sur la pointe Pelée, où le crapet vert n'est pas détecté depuis 1975 (DFO, données inédites). Ce dernier est toutefois abondant dans le marais Hillman (milieux humides adjacents à la pointe Pelée), alors que le crapet sac-à-lait n'y a pas été observé. D'autres recherches s'imposent pour déterminer les possibles interactions compétitives entre ces deux espèces.
On ne dispose pas de renseignements spécifiques sur l'association du crapet sac-à-lait avec des macrophytes aquatiques indigènes et non indigènes. Cependant, l'abondance des crapets juvéniles (crapet arlequin, crapet vert, crapet à longues oreilles et crapet rouge) et l'utilisation que ces derniers font de l'habitat dans les différents peuplements de macrophytes ont été examinées (Collingsworth et Christopher, 2010). La densité des crapets et la densité des tiges de plantes ont été comparées dans les zones dépourvues de végétation, les peuplements de myriophylles en épi (Myriophyllum spicatum) et les peuplements de potamots noueux (Potomogeton nodosus) (Collingsworth et Christopher, 2010). Durant cette étude, la densité des crapets juvéniles était beaucoup plus élevée dans les milieux végétalisés que dans les milieux dépourvus de végétation; il n'y avait toutefois pas de différences notables entre les deux types de milieux végétalisés (Collingsworth et Christopher, 2010). Il a également été noté que, même si la densité des crapets ne différait pas selon le type de macrophyte, la structure par taille des crapets au sein des milieux végétalisés variait beaucoup. Par exemple, les plus petits crapets choisissaient les peuplements plus denses de myriophylles en épi, tandis que les individus de plus grande taille préféraient les peuplements de potamots noueux (Collingsworth et Christopher, 2010). Selon les auteurs, les peuplements denses de myriophylles en épi offraient aux crapets de petite taille une meilleure protection contre les prédateurs.
Comme les activités d'échantillonnage sont sporadiques et ont recours à divers engins de pêche, il est difficile d'inférer les tendances de la taille des populations de crapets sac-à-lait. On en sait très peu sur la taille des populations de l'espèce au Canada. Une étude de l'assemblage de poissons menée en 2002 et en 2003 dans le parc national de la Pointe-Pelée a permis de prendre 657 crapets sac-à-lait (H. Surette, données inédites). L'histogramme illustrant la fréquence des tailles de cette étude (voir la figure 7) indique une abondance de juvéniles, mais il faut faire preuve de prudence lors de l'interprétation de ces résultats puisqu'on ne sait pas si on a capturé plus d'une fois les mêmes juvéniles. De nombreux individus de grande taille ont été munis d'un transpondeur passif intégré (PIT; n = 93). Cependant, seuls 3 individus ont été recapturés, ce qui n'est pas suffisant pour estimer la taille de la population (COSEWIC, 2005). L'abondance de crapets sac-à-lait observée sur la pointe Pelée au cours de l'étude laisse croire à une population établie.
Depuis la première mention de l'espèce dans la baie Long Point en 2003, celle-ci a été décelée chaque année d'échantillonnage (sauf en 2008; n = 235 individus observés de 2003 à 2013). Le nombre d'individus détectés lors des différents relevés demeure faible, sauf lors du relevé de la pêche commerciale au verveux réalisé en 2009 (voir le tableau 1c; Gislason, 2009). Gislason (2009) a fait état de 141 crapets sac-à-lait à partir de 368 mouillages de verveux (0,38 prise par levée).
Un total de 36 crapets sac-à-lait ont été prélevés dans la baie Rondeau depuis la première mention de l'espèce dans ce système en 1966 (voir le tableau 1b). Un échantillonnage intensif a été effectué dans ce système à l'aide de verveux en 2004, 2005, 2007, 2008, 2009, pour un total de 426 mouillages de 24 h. En comparaison avec des travaux semblables dans la baie Long Point, le nombre de crapets sac-à-lait semble être relativement faible dans la baie Rondeau.
Il est impossible d'estimer la taille des populations puisque les données sont insuffisantes. Un échantillonnage uniforme, à l'aide d'engins de pêche susceptibles de capturer des crapets sac-à-lait, aiderait à obtenir une représentation plus précise de la taille et des tendances des populations dans le temps pour les trois populations restantes de crapets sac-à-lait au Canada.
À ce jour, aucune étude n'a déterminé l'abondance ou la taille des populations de crapets sac-à-lait au Canada.
À cause de la rareté des données historiques et de l'absence d'activités d'échantillonnage uniformes au fil du temps, il est impossible de déterminer les fluctuations ou les tendances des populations de crapets sac-à-lait.
Les populations de crapets sac-à-lait au Canada sont isolées les unes des autres, de même que des populations états-uniennes, par plus de 50 km. Les populations les plus proches sont celles se trouvant dans les affluents du lac Érié au Michigan et non pas celles du lac Érié en Ohio (Crossman et Simpson, 1984). L'espèce a reçu les cotes de conservation suivantes dans les États voisins : non en péril (S5) au Michigan, apparemment non en péril (S4) en Ohio, vulnérable (S3) en Pennsylvanie. Aucune cote ne s'applique (SNA) dans l'État de New York (NatureServe, 2014). Les vastes zones de milieux non propices entre les populations sources états-uniennes et les populations canadiennes actuelles rendent l'immigration peu probable. De plus, on pense que la capacité de dispersion est plus limitée chez le crapet sac-à-lait que chez les autres Centrarchidés (voir Gatz et Adams, 1994, et la section Dispersion et migration).
Une grande variété de menaces ont des effets négatifs sur le crapet sac-à-lait dans toute son aire de répartition. Nos connaissances de leurs incidences sur les populations de crapets sac-à-lait se limitent à la documentation générale puisque les données sur les causes et effets des menaces sont rares. Les plus grandes menaces à la survie et à la persistance des crapets sac-à-lait au Canada seraient liées aux modifications des systèmes naturels attribuables à l'élimination de la végétation aquatique et à la perte de milieux humides. On compte également la pollution résultant des pratiques agricoles et du développement.
Les menaces sont abordées et classées selon le calculateur des menaces (voir le tableau 2), d'après les méthodes et la terminologie de Salasky et al. (2008), de Master et al. (2009) et de l'UICN (IUCN, 2014). Les menaces décrites ci-dessous sont les principales qui pèsent sur le crapet sac-à-lait au Canada. La cote de l'impact global des menaces pesant sur l'espèce est moyenne-faible (voir l'annexe 1).
| No | Description de la menace | Impact | Impact description |
Portée | Gravité | Immédiateté |
|---|---|---|---|---|---|---|
| 7.0 | Modifications des systèmes naturels | CD | Moyen-faible | Restreinte | Extrême-modérée | Élevée |
| 7.3 | Autres modifications de l'écosystème | CD | Moyen-faible | Restreinte | Extrême-modérée | Élevée |
| 9.0 | Pollution | D | Faible | Grande | Légère | Élevée |
| 9.1 | Eaux usées domestiques et urbaines | - | Négligeable | Grande | Négligeable | Élevée |
| 9.3 | Effluents agricoles et sylvicoles | D | Faible | Grande | Légère | Élevée |
| 6.0 | Intrusions et perturbations humaines | - | Négligeable | Petite | Négligeable | Modérée |
| 6.3 | Travail et autres activités | - | Négligeable | Petite | Négligeable | Modérée |
| 1.0 | Développement résidentiel et commercial | - | Négligeable | Négligeable | Extrême | Élevée |
| 1.1 | Zones résidentielles et urbaines | - | Négligeable | Négligeable | Extrême | Élevée |
| 1.3 | Zones touristiques et récréatives | - | Négligeable | Négligeable | Élevée-modérée | Élevée |
| 5.0 | Utilisation des ressources biologiques | - | Négligeable | Généralisée | Négligeable | Élevée |
| 5.4 | Pêche et récolte de ressources aquatiques | - | Négligeable | Généralisée | Négligeable | Élevée |
| 8.0 | Espèces et gènes envahissants ou autrement problématiques | - | Inconnu | Généralisée | Inconnue | Élevée |
| 8.1 | Espèces exotiques (non indigènes) envahissantes | - | Inconnu | Généralisée | Inconnue | Élevée |
| 11.0 | Changements climatiques et phénomènes météorologiques violents | - | Inconnu | Généralisée | Inconnue | Élevée |
| 11.1 | Déplacement et altération de l'habitat | - | Inconnu | Généralisée | Inconnue | Élevée |
| 4.0 | Corridors de transport et de service | - | Inconnu | Petite | Inconnue | Inconnue |
| 4.3 | Voies de transport par eau | - | Inconnu | Petite | Inconnue | Inconnue |
L'une des plus grandes menaces pesant sur le crapet sac-à-lait est la perte de son habitat de prédilection, c'est-à-dire des zones peu profondes très végétalisées. La baie Rondeau a connu des modifications extensives. La plus grande partie des milieux humides se trouvant le long de la rive ouest a disparu à cause de l'excavation de fossés, de l'endiguement, du remplissage et du durcissement de la rive à des fins agricoles et résidentielles (Gilbert et al., 2007). Par le passé, des milieux humides bordaient toute la rive de la baie Rondeau et composaient un vaste système contigu (Gilbert et Locke, 2007). La première évaluation des milieux humides de la baie Rondeau a été menée au début des années 1980 et, à ce moment, le complexe de milieux humides sur la rive nord-ouest avait été réduit à des parcelles isolées totalisant quelque 740 ha. En 2006, les milieux humides ne faisaient qu'environ 107 ha (Gilbert et al., 2007).
Une situation semblable se déroule dans la région de la pointe Pelée, où il est estimé que près de 60 % des milieux humides historiques qui reliaient autrefois la pointe Pelée au marais Hillman ont été drainés et endigués à des fins agricoles, de la fin du 19e siècle au milieu du 20e siècle (Dobbie et al., 2006). Cette perte de milieux humides historiques a sans doute fait diminuer la superficie de l'habitat de prédilection de la population de crapets sac-à-lait de la pointe Pelée.
On sait que le comportement alimentaire de la carpe commune (Cyprinus carpio) a de graves effets négatifs sur les systèmes aquatiques; en effet, l'espèce déracine la végétation aquatique et augmente la turbidité (Lougheed et al., 1998, 2004). Ce comportement alimentaire altère considérablement les milieux humides indigènes et pourrait donc avoir des conséquences graves sur le crapet sac-à-lait, qui dépend de la végétation aquatique assurer de nombreuses fonctions vitales.
En 1994, une étude a été réalisée dans le parc national de la Pointe-Pelée (étang Sanctuary) pour trouver la source des fortes concentrations de nutriments qui entraînent la prolifération des algues (Mayer et al., 1999). On a déterminé que la décomposition de la matière organique était un mécanisme important faisant augmenter les concentrations de nutriments et que la remise en suspension des sédiments de fond, principalement par la carpe commune lorsqu'elle se nourrit, était probablement responsable des conditions hypereutrophiques (Mayer et al., 1999).
On sait aussi que les macrophytes aquatiques exotiques peuvent altérer considérablement le complexe de végétation aquatique en supplantant les végétaux indigènes. Au nombre de ses espèces végétales envahissantes, on compte le roseau commun, qui forme de denses peuplements monotypes, supplante les espèces indigènes (Gilbert et Locke, 2007) et réduit la superficie d'habitat en eaux libres. Le roseau commun est abondant dans les baies Rondeau et Long Point; non seulement le roseau commun réduit la diversité florale indigène (Gilbert et al., 2007; Badzinski et al., 2008), mais les peuplements à forte densité peuvent aussi diminuer l'habitat disponible pour le crapet sac-à-lait (voir la section Tendances en matière d'habitat pour plus de détails sur la propagation du roseau commun dans la baie Long Point).
Le myriophylle en épi est un autre macrophyte envahissant qui pourrait avoir des effets à la fois positifs et négatifs sur le crapet sac-à-lait. Collingsworth et Christopher (2010) ont indiqué que les petits crapets juvéniles préféraient les peuplements de myriophylles en épi aux peuplements de potamots noueux, ce qui laisse croire que les peuplements plus denses de myriophylles en épi pourraient offrir une meilleure protection contre la prédation (voir la section Relations interspécifiques pour plus de détails). Cependant, le myriophylle en épi croît en tapis denses qui bloquent la lumière du soleil pour les macrophytes submergés, augmentent les apports de phosphore et d'azote, accroissent le pH et la température et rend l'habitat potentiellement non propice au crapet sac-à-lait (Gilbert et al., 2007). Cet effet négatif peut être particulièrement pertinent pour les crapets sac-à-lait du parc national de la Pointe-Pelée et de la baie Rondeau, où le myriophylle en épi peut s'épanouir dans des conditions de croissance idéales. La communauté de macrophytes submergés dans les sections ouest, centre et nord de la baie Rondeau avait tendance à être dominée par le myriophylle en épi et la cornifle nageante (Ceratophyllum demersum), qui atteignent une densité élevée et une biomasse variant de 500 à 1 300 g m-2 poids sec (Gilbert et al., 2007). Des études sont nécessaires pour évaluer l'effet global du myriophylle en épi sur les populations de crapets sac-à-lait.
Les moules de la famille des Dreissenidés sont omniprésentes dans l'aire de répartition canadienne du crapet sac-à-lait. Les moules améliorent la clarté de l'eau dans certaines zones des Grands Lacs (Binding et al., 2007), ce qui augmente la croissance des macrophytes aquatiques indigènes et envahissants (Higgins et Vander Zanden, 2010). Cependant, l'effet net sur le crapet sac-à-lait ne peut être déterminé pour le moment.
On a récemment observé que la carpe de roseau (Ctenopharyngodon idella), originaire d'Eurasie, se reproduisait dans la baie Maumee, dans l'ouest du lac Érié (Chapman et al., 2013). La carpe de roseau est un herbivore envahissant réputé avoir des effets négatifs graves sur les macrophytes aquatiques (Wittmann et al., 2014). On ne sait pas si la carpe de roseau se propagera dans l'aire de répartition canadienne du crapet sac-à-lait au cours des dix prochaines années, mais, si c'est le cas, elle pourrait avoir une incidence grave sur l'habitat de celui-ci.
L'enlèvement de la végétation aquatique aux fins du développement résidentiel et récréatif et du transport est une modification de l'habitat qui nécessite une attention particulière. Le crapet sac-à-lait est très dépendant des zones peu profondes fortement végétalisées pour assurer nombre de ses fonctions vitales. On sait que l'espèce utilise ces zones pour la fraye et l'alevinage ainsi que pour chercher de la nourriture. La destruction et l'élimination de la végétation aquatique dans la zone littorale des lacs et des systèmes de milieux humides peuvent nuire à la population de crapets sac-à-lait. En plus des conséquences de l'enlèvement de la végétation, l'acte physique même d'enlever la végétation peut avoir des effets négatifs sur le crapet sac-à-lait. On a noté que l'enlèvement mécanique est préférable au traitement chimique (effet sur l'habitat, raisons esthétiques), car il réduit la demande en oxygène de la végétation en décomposition (Gilbert et al., 2007).
Des opérations d'enlèvement de la végétation ont eu lieu dans la baie Rondeau dans le passé (à grande échelle) et récemment (à petite échelle), principalement parce que la présence de macrophytes aquatiques submergés, à forte densité, pouvait nuire aux activités récréatives (Gilbert et al., 2007). Dans la baie, l'enlèvement chimique et mécanique, autorisé ou non, est courant.
Des activités d'enlèvement mécanique de faible envergure ont cours dans la baie Long Point (dans la zone d'occurrence du crapet sac-à-lait) et dans le parc national de la Pointe Pelée. Il n'y a eu aucune élimination de la végétation au moyen de traitement chimique dans le parc national de la Pointe Pelée (V. McKay, Agence Parcs Canada, comm. pers., in Bouvier et Mandrak, 2010) et, même si on a eu recours à des traitements chimiques dans la baie Long Point, il est maintenant courant d'employer la méthode mécanique.
La dégradation de l'habitat de prédilection du crapet sac-à-lait peut résulter de l'augmentation des charges en nutriments (nitrates et phosphore), laquelle peut découler du rejet d'engrais dans les plans d'eau, de l'apport de nutriments provenant d'usines de traitement des eaux usées et du ruissellement de nutriments à partir de tas de fumier. Ces teneurs accrues en nutriments peuvent entraîner la prolifération d'algues et, conséquemment, diminuer les teneurs en oxygène dissous lorsque les algues commencent à se dessécher (Gilbert et al., 2007). Les apports en nutriments sont considérés comme une menace importante dans la baie Long Point, le parc national de la Pointe-Pelée et la baie Rondeau, qui abritent tous le crapet sac-à-lait (Essex-Erie Recovery Team, 2008).
Des échantillons de nutriments prélevés en 2005 et en 2006 dans les affluents de la baie Rondeau durant 2 périodes d'échantillonnage (juin et août) ont été comparés aux lignes directrices provinciales sur la qualité de l'eau (le phosphore total ne doit pas dépasser 0,03 mg·L-1; Ontario Ministry of the Environment and Energy, 1994). Les résultats des échantillons provenant de tous les affluents en 2005, et de tous les affluents sauf un en 2006, dépassaient les lignes directrices (Gilbert et al., 2007). Ces concentrations élevées de nutriments seraient la cause principale de la prolifération d'algues, courante dans la baie Rondeau (Gilbert et al., 2007). Une fleur d'eau d'une épaisseur d'environ 1 m et couvrant 70 % (3 169 ha) de la surface de la baie Rondeau a été observée en 2005 (Gilbert et al., 2007). La fleur d'eau a considérablement altéré les concentrations d'oxygène dissous, qui ont chuté à 5 mg·L-1 (Gilbert et al., 2007). Elle s'est asséchée durant l'hiver et a entraîné le dépôt d'une épaisse matière organique sur les rives nord et est qui a étouffé l'habitat et créé des zones anoxiques (Gilbert et al., 2007).
L'augmentation des charges en sédiments et de la turbidité peuvent se faire au détriment de la survie et du rétablissement du crapet sac-à-lait. Celui-ci a été classé comme modérément intolérant à la turbidité, d'après son profil d'occurrence et d'abondance relative, dans le gradient de turbidité d'un milieu humide (Trebitz et al., 2007). L'augmentation des charges en sédiments et de la turbidité peuvent être attribuées à de mauvaises pratiques agricoles et de gestion des terres, à un mauvais entretien des canaux de drainage, à des activités de dragage et à l'enlèvement de la végétation riveraine (Staton et al., 2012). Parmi les effets négatifs indirects de la hausse de la turbidité sur le crapet sac-à-lait figure la diminution de l'habitat de prédilection causée par la baisse de la clarté de l'eau, qui entrave la pénétration de la lumière et diminue la croissance des macrophytes.
On a souligné le problème continu posé par l'envasement dans la baie Rondeau, où un système de drainage par tuyaux accroît l'envasement, en particulier lors de tempêtes (Gilbert et al., 2007). Une réduction des apports de sédiments de sources ponctuelles et diffuses contribuerait grandement à la remise en état de la baie Rondeau (Gilbert et al., 2007).
Dans le parc national de la Pointe-Pelée, la modification du transport des sédiments le long de la rive du lac Érié accroît l'érosion du cordon littoral, entraînant ainsi de plus en plus de brèches (Dobbie et al., 2006; Surette, 2006). Il s'ensuit un déclin de la qualité de l'eau, y compris une hausse de la turbidité dans le parc (V. McKay, Agence Parcs Canada, comm. pers., in Bouvier et Mandrak, 2010)
Un panache de turbidité évident naissant à l'embouchure du ruisseau Big est observé dans la baie intérieure Long Point (Bouvier et Mandrak, 2010). Même si les valeurs de turbidité ne sont actuellement pas disponibles pour cette région, on sait que l'étendue du panache de turbidité englobe la zone d'occurrence du crapet sac-à-lait et pourrait avoir un effet négatif sur l'habitat de celui-ci.
Les dommages fortuits causés aux crapets sac-à-lait durant la mise en œuvre des recherches scientifiques seraient minimaux. Des mesures de précaution sont prises pour veiller à ce que les dommages soient minimaux ou nuls lors de la récolte d'individus. De plus, des permis de prélèvement scientifique sont nécessaires pour l'échantillonnage de poissons dans les parcs provinciaux et nationaux de l'Ontario, et ces permis mentionnent que toutes les espèces en péril doivent être immédiatement remises à l'eau.
Un défi particulier se présente lorsque l'on examine les effets du développement sur le crapet sac-à-lait dans la baie Long Point puisque les différentes régions de la baie font face à divers niveaux de pression liés au développement. Le marais du ruisseau Big serait exposé à très peu de pressions parce qu'il se trouve dans une réserve nationale de faune, protégée et gérée par le Service canadien de la faune d'Environnement Canada. La rive nord-ouest de la baie fait face à des pressions accrues liées au développement résidentiel et à la construction de marinas.
Il reste un très faible pourcentage de couvert forestier naturel (~3,3 %) dans le bassin versant de la baie Rondeau. Il est estimé qu'environ 70 % de la rive ouest a été transformée à des fins agricoles et résidentielles (Gilbert et Locke, 2007). L'élargissement des terres pour des propriétés agricoles et résidentielles se fait aux dépens des milieux humides littoraux (Gilbert et Locke, 2007).
En Ontario, il est illégal d'utiliser les crapets sac-à-lait comme poissons-appâts (Ontario Ministry of Natural Resources, 2013). Cependant, comme c'est le cas dans la plupart des pêches, il est possible de capturer des poissons non ciblés à titre de prises accessoires lors de la récolte de poissons-appâts destinés aux pêches sportive et commerciale. La quantité de prises accessoires dépend de la répartition et de l'intensité de la récolte de poissons-appâts par rapport à la répartition du crapet sac-à-lait. Les prises accessoires de crapets sac-à-lait durant la récolte de poissons-appâts destinés à la pêche sportive sont actuellement inconnues à cause des pratiques de pêche sportive incertaines (Drake et Mandrak, 2014a). Par contre, Drake et Mandrak, 2014b ont pu estimer les pratiques de pêche commerciale. Ils ont évalué le potentiel de capturer accidentellement des crapets sac-à-lait dans les affluents des Grands Lacs et déterminé que la probabilité d'établir aléatoirement un site de pêche dans un cours d'eau abritant à la fois des poissons-appâts ciblés et des crapets sac-à-lait était de P = 0,000087 (probabilité inférieure à 1/11 000 sites). D'après un modèle de récolte générique, les relations estimées entre les prises accessoires et l'effort de pêche indiquaient qu'il faudrait 34 246 récoltes pour qu'une seule récolte ciblant une espèce donnée ait une probabilité médiane de 95 % de capturer accidentellement des crapets sac-à-lait (Drake et Mandrak, 2014b). Dans le cas des espèces non ciblées étroitement liées au crapet sac-à-lait que l'on s'attend à capturer fréquemment, comme le crapet de roche et le crapet-soleil (Lepomis gibbosus), seulement 17 récoltes seraient nécessaires pour qu'une récolte atteigne le seuil de 95 %. Les probabilités de capture estimées du crapet sac-à-lait étaient parmi les plus faibles de toutes les espèces vivant dans les eaux ontariennes. Une étude sur les poissons-appâts en Ontario (Drake, 2011; Drake et Mandrak, 2014a) n'a pas permis d'observer le crapet sac-à-lait durant l'échantillonnage des poissons-appâts de détaillants (n = 68) ou des poissons achetés (total cumulatif de 16 886 poissons) dans le sud de l'Ontario en juillet et en août 2007 et en février 2008 (Drake, 2011; Drake et Mandrak, 2014a).
En vertu du Règlement de pêche de l'Ontario (2007), le crapet sac-à-lait est considéré comme un « crapet » et peut être légalement pêché lorsque le pêcheur possède un permis de pêche sportive. Le permis de pêche écologique permet de conserver 25 crapets, et le permis régulier, 50 crapets. Un permis de pêche sportive distinct est nécessaire pour pêcher dans le parc national de la Pointe-Pelée. Les crapets ne sont pas la cible préférée des pêcheurs sportifs en Ontario; ils atteignent rarement une longueur assez grande pour intéresser les pêcheurs. Par conséquent, la pêche sportive a vraisemblablement un effet négligeable sur le crapet sac-à-lait.
Les crapets sac-à-lait peuvent faire partie des prises accessoires de la pêche commerciale. Une étude sur les effets de la pêche commerciale sur les espèces aquatiques en péril a été réalisée dans la baie Long Point en 2009 (Gislason et al., 2010). Lors de cette étude, on a procédé à la surveillance de 368 levées de verveux (pêche commerciale) afin d'y repérer des espèces aquatiques en péril, et on y a observé 141 crapets sac-à-lait (0,38 par levée; Gislason et al., 2010). Malheureusement, aucune estimation de l'abondance du crapet sac-à-lait n'est disponible pour la baie Long Point; il est donc difficile de déterminer la proportion de la population qui est touchée par les pratiques de pêche commerciale. Grâce à cette étude, un programme d'éducation a été mis en œuvre pour sensibiliser les pêcheurs aux espèces en péril qui peuvent se trouver dans leurs prises accessoires et qui doivent être remises à l'eau (N. Mandrak, comm. pers.). Une sensibilisation accrue permettra de diminuer les effets négatifs possibles de la pêche commerciale sur le crapet sac-à-lait. Il est également à noter que les effets de l'industrie de la pêche commerciale à la senne sur le crapet sac-à-lait dans la baie Long Point sont inconnus et doivent donc faire l'objet de recherches.
Le gobie à taches noires (Neogobius melanostomus) et les moules de la famille des Dreissenidés se rencontrent dans toute l'aire de répartition canadienne du crapet sac-à-lait. Les effets de ces espèces sur le crapet sac-à-lait sont inconnus. Les moules ont amélioré la clarté de l'eau dans certaines zones des Grands Lacs (Binding et al., 2007), ce qui a augmenté la croissance de macrophytes aquatiques indigènes et envahissants (Higgins et Vander Zanden, 2010). Cependant, l'effet net sur le crapet sac-à-lait ne peut être déterminé pour le moment.
Lors de discussions sur les effets des changements climatiques sur les populations de poissons au Canada, on a souligné les conséquences telles que la hausse des températures de l'eau et de l'air, la baisse des niveaux d'eau, la baisse de la durée du couvert de glace, l'augmentation de la fréquence de phénomènes météorologiques violents, l'émergence de maladies et la modification de la dynamique prédateur-proie, qui ont toutes des effets négatifs sur les poissons indigènes (Lemmen et Warren, 2004). D'après l'hypothèse selon laquelle la dispersion et la colonisation du crapet sac-à-lait dans les eaux canadiennes pourraient être restreintes par les températures de l'eau (Crossman et al., 1996), une hausse de la température de l'eau attribuable aux changements climatiques pourrait permettre une plus grande dispersion et la colonisation de nouveaux milieux. Inversement, le crapet sac-à-lait pourrait être particulièrement vulnérable aux effets des changements climatiques à cause des liens avec la température et l'habitat (Doka et al., 2006), ce qui entraîne des effets globaux négatifs sur les populations de crapets sac-à-lait. Cette hypothèse s'appuie sur la vulnérabilité des espèces de poissons aux changements climatiques, et le crapet sac-à-lait se classe au deuxième rang des espèces les plus vulnérables, comparativement à 98 autres espèces évaluées (Doka et al., 2006).
Le crapet sac-à-lait se trouve dans trois localités : la baie Rondeau, la pointe Pelée et la baie Long Point. Il n'y a actuellement aucune information disponible pour inférer la connectivité des populations à partir des évaluations génétiques. La capacité de dispersion limitée de l'espèce (voir la section Dispersion et migration), la présence de vastes zones d'habitat non propice empêchant les déplacements, et la nature non catastrophique et spatialement indépendante de la menace la plus grave touchant le crapet sac-à-lait (c.-à-d. la modification des systèmes naturels; voir la section Menaces et facteurs limitatifs) viennent appuyer la désignation de ces zones géographiques en tant que localités.
Le crapet sac-à-lait est actuellement inscrit à titre d'espèce préoccupante à l'annexe 1 de la Loi sur les espèces en péril (LEP). Cette inscription n'offre aucune protection à l'espèce ou à son habitat, mais nécessite la préparation d'un plan de gestion. Même si la LEP n'offre aucune protection directe au crapet sac-à-lait, les populations de cette espèce cohabitent avec d'autres espèces inscrites comme espèces menacées ou en voie de disparition (p. ex. lépisosté tacheté [Lepisosteus oculatus]; méné camus [Notropis anogenus]; sucet de lac [Erimyzon sucetta]), et peuvent ainsi recevoir une protection indirecte.
Le crapet sac-à-lait est également inscrit à titre d'espèce préoccupante en vertu de la Loi de 2007 sur les espèces en voie de disparition (LEVD) de l'Ontario, mais les espèces préoccupantes ne reçoivent pas de protection juridique aux termes de cette loi. Comme avec la LEP, cependant, le crapet sac-à-lait reçoit une protection indirecte puisqu'il cohabite avec des espèces inscrites comme espèces menacées ou en voie de disparition en vertu de la LEVD, ce qui lui offre une protection indirecte supplémentaire.
L'ensemble des poissons d'eau douce est géré en vertu de la Loi de 1997 sur la protection du poisson et de la faune; cette loi nécessite qu'un permis de collecte pour activités scientifiques soit délivré par le ministère des Richesses naturelles de l'Ontario.
La Loi sur les pêches du Canada était représentait auparavant une loi importante pour la protection directe de l'habitat du crapet sac-à-lait. Cependant, les récentes modifications à la Loi ont affaibli la protection offerte à l'habitat de l'espèce et assurent désormais seulement une protection dans les zones où des pêches commerciale, récréative et autochtone sont pratiquées. Il existe un chevauchement entre l'aire de répartition du crapet sac-à-lait et celle de diverses espèces pêchées à des fins commerciales et récréatives, ce qui fait en sorte que la nouvelle Loi sur les pêches vise toutes les localités actuellement occupées par le crapet sac-à-lait.
Le crapet sac-à-lait est actuellement désigné « espèce préoccupante » par le COSEPAC. L'espèce est désignée non en péril à l'échelle mondiale (G5) et non en péril à l'échelle nationale (N5) aux États-Unis (voir le tableau 3). L'espèce est considérée comme « non en péril » ou « apparemment non en péril » dans la plupart des États, sauf en Virginie (S2; en péril), en Pennsylvanie (S3; vulnérable) et en Illinois (S3S4; vulnérable/apparemment non en péril). Au Canada, le crapet sac-à-lait est classé « gravement en péril » à l'échelle nationale (N1) et provinciale (S1).
| Échelle mondiale | Échelle nationale États-Unis |
Échelle nationale Canada |
Échelle subnationale États-Unis |
Échelle subnationale Canada |
|---|---|---|---|---|
| G5 (Sept. 1996) |
N5 (Déc. 1996) |
N1 (Oct. 2012) |
S2 : Virginie S3 : Pennsylvanie |
S1 : Ontario |
| - | - | - | S3(?) : Maryland | - |
| - | - | - | S3S4 : Illinois | - |
| - | - | - | S4 : Arkansas, Indiana, Ohio, Wisconsin | - |
| - | - | - | S5 : Alabama, Louisiana, Michigan, Mississippi, Caroline du Nord, Oklahoma, Tennessee, Texas, Virginie | - |
| - | - | - | S4S5: Georgie, Kansas, Kentucky | - |
| - | - | - | SNA : Arizona, Delaware, District de Columbia, Idaho, Nevada, New Jersey, Nouveau-Mexique, New York, Oregon, État de Washington | - |
| - | - | - | SNR : Floride, Iowa, Minnesota, Missouri, Caroline du Sud | - |
Cotes de conservation : 1 = gravement en péril; 2 = en péril; 3 = vulnérable; 4 = apparemment non en péril; 5 = non en péril; SNA = non applicable; SNR = non classé.
Au Canada, les modifications à la Loi sur les pêches sont entrées en vigueur en novembre 2013. Ces modifications permettent seulement la protection de l'habitat des poissons visés par les pêches commerciale, récréative et autochtone. Puisque l'habitat du crapet sac-à-lait chevauche les zones de ces pêches, l'espèce reçoit une protection indirecte en vertu de la Loi. L'habitat de l'espèce peut également être protégé en vertu d'autres lois fédérales, dont la Loi canadienne sur l'évaluation environnementale.
Le crapet sac-à-lait est actuellement désigné « espèce préoccupante » en vertu de la LEP et de la LEVD, mais ces désignations n'offrent pas de protection supplémentaire de l'habitat. Cependant, le crapet sac-à-lait recevrait une protection indirecte dans le cadre de la Politique fédérale sur la conservation des terres humides (Environment Canada, 1991). Au nombre des lois ontariennes qui pourraient protéger l'habitat du crapet sac-à-lait, on compte la Loi sur la protection de l'environnement, la Loi sur les évaluations environnementales de l'Ontario, la Loi sur l'aménagement du territoire et la Loi sur les ressources en eau. En Ontario, les milieux aquatiques qui se trouvent sur des territoires réglementés par un office de protection de la nature sont protégés, aux termes de la Loi sur les offices de protection de la nature, contre le remblayage des milieux humides, l'aménagement des rives et les travaux réalisés dans les plaines d'inondation. Malgré ses protections juridiques, de nombreuses menaces qui pèsent sur le crapet sac-à-lait ne sont pas réglementées.
On sait que le crapet sac-à-lait occupe le parc national de la Pointe-Pelée et le parc provincial de la baie Rondeau; ainsi, son habitat pourrait être protégé davantage en vertu de la Loi sur les parcs nationaux et de la Loi sur les parcs provinciaux.
Andrew Doolittle a préparé les cartes de répartition et a effectué les calculs de l'indice de zone d'occupation (IZO) et de la zone d'occurrence.
Les autorités suivantes ont été contactées (et nous avons reçu une réponse) : Josh Keitel et Valerie Minelga (Agence Parcs Canada), Pat Chow-Fraser (Université McMaster), Jan Ciborowski (Université de Windsor), Sandy Dobbyn et Vivian Brownell (ministère des Richesses naturelles de l'Ontario), Paul Gagnon et Jennifer Wilson (Office de protection de la nature de la région de Long Point), Kurt Oldenburg et Megan Belore (ministère des Richesses naturelles de l'Ontario, Unité de gestion du lac Érié), Kevin Reid (Ontario Commercial Fisheries' Association), William Glass (Pêches et Océans Canada), Michael Oldham et Don Sutherland (Centre d'information sur le patrimoine naturel), Ken Tuininga (Environnement Canada), Neil Jones (COSEPAC) et David Gislason (Université de Guelph).
Nous avons contacté l'autorité suivante, mais n'avons reçu aucune réponse : Angela McConnell (Environnement Canada).
Badzinski, S.S., Proracki, S., Petrie, S.A., Richards, D. (2008). Changes in the distribution and abundance of common reed (Phragmites australis) between 1999 and 2006 in marsh complexes at Long Point - Lake Erie. Prepared for the Ontario Ministry of Natural Resources (consulté le 3 juillet 2014;).
Bailey, R.M., Fitch, J.E., Herald, E.S., Lachner, E.A., Lindsey, C.C., Robins, C.R., Scott, W.B. (1970). A list of scientific and common names of fishes from the United States and Canada. Third Edition. American Fisheries Society Special Publication 6 (consulté le 7 janvier 2014;).
Becker, G.C. (1983). Fishes of Wisconsin. The University of Wisconsin Press, Madison, WI. 1052 p.
Bermingham, E., Avise, J.C. (1986). Molecular zoogeography of freshwater fishes in the southeastern United States. Genetics 113:939-965.
Binding, C.E., Jerome, J.H., Bukata, R.P., Booty, W.G. (2007). Trends in water clarity of the lower Great Lakes from remotely sensed aquatic color. J Gt Lakes Res 33.
Bouvier, L.D., Mandrak, N.E. (2010). Information in support of a Recovery Potential Assessment of Spotted Gar (Lepisosteus oculatus) in Canada. DFO Can. Sci. Advis. Sec. Res. Doc. 2010/079. v + 23 p.
Carlander, K.D. (1969). Handbook of Freshwater Fishery Biology. Vol. 1. The Iowa State University Press, Ames, Iowa, USA. 432 p.
Chapman, D.C., Davis, J.J., Jenkins, J.A., Kocovsky, P.M., Miner, J.G., Farver, J., Jackson, P.R. (2013). First evidence of grass carp recruitment in the Great Lakes Basin. J Gt Lakes Res 39: 547-554.
Childers, W.F. (1971). Hybridization of fishes in North America (Family Centrarchidae (consulté le 12 décembre 2013;).
Collingsworth, P.D., Christopher, C.K. (2010). Abundance and habitat use of juvenile sunfish among different macrophyte stands. Lake Reservoir Manage 26:35-42.
COSEWIC (2005). COSEWIC assessment and update status report on the Warmouth Lepomis gulosus in Canada. Committee on the Status of Endangered Wildlife in Canada. Ottawa. vi + 16 p. [Également disponible en français : COSEPAC. (2005). Évaluation et Rapport de situation du COSEPAC sur le crapet sac-à-lait (Lepomis gulosus) au Canada – Mise à jour, Comité sur la situation des espèces en péril au Canada, Ottawa, vi + 18 p.]
COSEWIC (2011). Guidelines for recognizing designatable units below the species level. Committee on the Status of Endangered Wildlife in Canada. Ottawa (consulté le 21 juillet 2014;). [Également disponible en français : COSEPAC. (2011). Lignes directrices pour reconnaître les unités désignables, Comité sur la situation des espèces en péril au Canada, Ottawa.]
Crossman, E.J., Houston, J., Campbell, R.R. (1996). The status of the warmouth, Chaenobryttus gulosus, in Canada. Canadian Field Naturalist 110: 495-500.
Crossman, E.J., Simpson, R.C. (1984). Warmouth, Lepomis gulosus, a freshwater fish new to Canada. Canadian Field Naturalist 98:496-498.
Dibble, E.D., Hoover, J.J., Landin, M.C. (1995). Comparison of abundance and diversity of young fishes and macroinvertebrates between two Lake Erie wetlands. Technical Report, U.S. Army Corps of Engineers, Vicksburg, MS. 34 p.
Dobbie, T., McFadyen, T., Zorn, P., Keitel, J., Carlson, M. (2006). Point Pelee National Park of Canada: State of the Park Report 2006. Parks Canada Agency, Leamington, ON. 44 p. [Également disponible en français : Dobbie, T., McFadyen, T., Zorn, P., Keitel, J., Carlson, M. (2006). Parc national du Canada de la Pointe-Pelée – Rapport sur l'état du parc, 2006, Agence Parcs Canada, Leamington (Ont.), 47 p.]
Doka, S., Bakelaar, C., Bouvier, L.D. (2006). Chapter 6. Coastal wetland fish community assessment of climate change in the lower Great Lakes. In Great Lakes Coastal Wetland Communities: Vulnerability to Climate Change and Response to Adaptation Strategies. Edited by J.I.L. Mortsch, A. Hebb et S. Doka. Environment Canada and Fisheries and Oceans Canada, Toronto, ON. p. 101-128.
Drake, D.A.R (2011). Quantifying the likelihood of human-mediated movements of species and pathogens: the baitfish pathway in Ontario as a model system. Thèse (Ph.D.), University of Toronto, Toronto, ON. 295 p.
Drake, D.A.R, Mandrak, N.E. (2014a). Ecological risk of live bait fisheries: a new angle on selective fishing. Fisheries 39:201-211.
Drake, D.A.R., Mandrak, N.E. (2014b). Harvest models and stock co-occurrence: probabilistic methods for estimating bycatch. Fish Fish 15:23-42.
Environment Canada (1991). Federal Policy on Wetland Conservation (consulté le 3 juillet 2014;). [Également disponible en français : Environnement Canada. (1991). La politique fédérale de la conservation des terres humides .
Essex-Erie Recovery Team (2008). Recovery strategy for the fishes at risk of the Essex-Erie region: an ecosystem approach. Prepared for the Department of Fisheries and Oceans. Draft. 109 p.
Gatz, A.J., Adams, S.M. (1994). Patterns of movement of centratchids in two warmwater streams in eastern Tennessee. Ecol Freshw Fish 3:35-48.
Gilbert, J., Dunn, G., Locke, B. (2007). Rondeau Bay ecological assessment. Report prepared for the Ontario Ministry of Natural Resources. Port Dover, ON. May 2007. iv + 220 p.
Gilbert, J.M., Locke, B. (2007). Restoring Rondeau Bay's Ecological Integrity. A report funded by: The Lake Erie Management Unit, OMNR, the Canada/Ontario Agreement and the Lake Erie Habitat Restoration Section, Environment Canada. 40 p.
Gislason, D., Reid, K., Oldenburg, K. (2010). Assessment and mitigation of the effects of commercial fishing activities on aquatic Species at Risk in Long Point Bay. SARRFO Report - SARF151. 18 p.
Higgins, S.N., Vander Zanden, M.J. (2010). What a difference a species makes: a meta-analysis of dreissenid mussel impacts on freshwater ecosystems. Ecol Monogr 80:179-196.
Holm, E., Mandrak, N.E., Burridge, M. (2010). The ROM field guide to freshwater fishes of Ontario. Second Printing. Royal Ontario Museum, Toronto, ON. 462 p.
Hubble, P.M. (1966). Warmouth. In Inland Fisheries Management. Édité par A. Calhoun. California Fish Game, Sacramento, California. p. 546 p.
IUCN (2014). IUCN - CMP Unified Classification of Direct Threats. Version 3.2 (consulté le 5 juillet 2014; PDF file).
IUCN Standards and Petitions Subcommittee (2014). Guidelines for Using the IUCN Red List Categories and Criteria. Version 11. Prepared by the Standards and Petitions Subcommittee (consulté le 16 juin 2014; PDF file).
Lane, J.A., Portt, C.B., Minns, C.K. (1996a). Nursery habitat characteristics of Great Lakes fishes. Can. Manuscr. Rep. Fish. Aquat. Sci. 2338. v + 42 p.
Lane, J.A., Portt, C.B., Minns, C.K. (1996b). Spawning habitat characteristics of Great Lakes fishes. Can. Manuscr. Rep. Fish. Aquat. Sci. 2368. v + 48 p.
Larimore, R.W. (1957). Ecological life history of the warmouth (Centrarchidae). Ill Nat Hist Surv Bull 27:1-83.
Lemmen, D.S., Warren, F.J. (2004). Climate change impacts and adaptation: A Canadian perspective. Natural Resources Canada, Ottawa, Ontario. Natural Resources Canada. 174 p. [Également disponible en français : Lemmen, D.S., Warren, F.J. (2004). Impacts et adaptation liés aux changements climatiques : perspective canadienne, Ressources naturelles Canada, Ottawa (Ont.),190 p.]
Leslie, J.K., Timmins, C.A. (1998). Fish reproduction and distribution in a small tributary of Lake St. Clair. Canadian Technical Report of Fisheries and Aquatic Sciences No. 2253. Fisheries and Oceans Canada, Burlington, ON.
Leslie, J.K., Timmins, C.A., Pachkevich, A. (1999). Age 0 fishes in proximate systems: the Detroit River and Cedar Creek. Canadian Technical Report of Fisheries and Aquatic Sciences No. 2279. Fisheries and Oceans Canada, Burlington, ON.
Lougheed, V.L., Crosbie, B., Chow-Fraser, P. (1998). Predictions on the effect of common carp (Cyprinus carpio) exclusion on water quality, zooplankton, and submergent macrophytes in a Great Lakes wetland. Can J Fish Aquat Sci 55:1189-1197.
Lougheed, V.L., Theÿsmeÿer, T., Smith, T., Chow-Fraser, P. (2004). Carp exclusion, food-web interactions, and the restoration of Cootes Paradise Marsh. J Gt Lakes Res 30:44-57.
Master, L., Faber-Langendoen, D., Bittman, R., Hammerson, G.A., Heidel, B., Nichols, J., Ramsay, L., Tomaino, A. (2009). NatureServe Conservation Status Assessments: Factors for Assessing Extinction Risk. NatureServe, Arlington, Virginia. 57 p.
Mayer, T., Ptacek, C., Zanini, L. (1999). Sediments as a source of nutrients to hypereutrophic marshes of Point Pelee, Ontario, Canada. Water Res 33:1460-1470.
McMahon, T.E., Gebhart, G., Nelson, P.C. (1984). Habitat suitablity index models and instream flow suitabiltiy curves: Warmouth. Fish and Wildlife Service. 21 p.
Mortsch, L. (1998). Assessing the impact of climate change on the Great Lakes shoreline. Clim Change 40:391-416.
NatureServe (2014). NatureServe Explorer: An online encyclopedia of life [application Web]. Version 7.1. NatureServe, Arlington, Virginia (consulté le 19 novembre 2014;).
Ontario Ministry of Natural Resources (2013). Ontario Recreational Fishing Regulations Summary. 105 p. [Également disponible en français : Ministère des Richesses naturelles de l'Ontario. (2013). Résumé des règlements de la pêche sportive, 105 p.]
Ontario Ministry of the Environment and Energy (1994). Water Management, Policies, Guidelines, Provincial Water Quality Objectives of the Ministry of Environment and Energy. 32 p.
Page, L.M. et B.M. Burr. 1991. A field guide to freshwater fishes, North America; North of Mexico. Houghton Mifflin Company. Boston, Massachusetts. 432 p. + xii.
Page, L.M., Burr, B.M. (2011). Peterson Field Guide to Freshwater Fishes. Houghton Mifflin Company, Boston, MA. 663 p.
Page, L.M., Espinosa-Pérez, H., Findley, L.T., Gilbert, C.R., Lea, R.N., Mandrak, N.E., Mayden, R.L., Nelson, J.S. (2013) Common and Scientific Names of Fishes from the United States, Canada, and Mexico. Seventh Edition edition. 243 p.
Panek, F.M., Cofield, C.R. (1978). Fecundity of Bluegill and Warmouth from a South Carolina Blackwater Lake. The Progressive Fish-Culturalist 40:67-68.
Razavi, R. (2006). Assessing historical and present day fish habitat in the marshes of Point Pelee National Park. Thèse d'études spécialisées de niveau supérieur. McMaster University, Hamilton, Ontario, Canada. 65 p.
Salafsky, N., Salzer, D., Stattersfield, A.J., Hilton-Taylor, C., Neugarten, R., Butchart, S.H.M., Collen, B., Cox, N., Master, L.L., O'Connor, S., Wilkie, D. (2008). A standard lexicon for biodiversity conservation: Unified classifications of threats and actions. Conserv Biol 22:897-911.
Staton, S.K., Boyko, A.L., Dunn, S.E., Burridge, M. (2012). Recovery Strategy for the Spotted Gar (Lepisosteus oculatus) in Canada. vii + 57 p. [Également disponible en français : Staton, S.K., Boyko, A.L., Dunn, S.E., Burridge, M. (2012). Programme de rétablissement du lépisosté tacheté (Lepisosteus oculatus) au Canada, Série des programmes de rétablissement de la Loi sur les espèces en péril, Pêches et Océans Canada, Ottawa, ix + 67 p.]
Surette, H. (2006). Processes influencing temporal variation in fish species composition in Point Pelee National Park. Mémoire de maîtrise. Department of Integrative Biology, University of Guelph, Guelph, Ontario, Canada. 105 p.
Trautman, M.B. (1981). The Fishes of Ohio. 2nd edition. Ohio State University Press, Columbus, OH. 782 p.
Trebitz, A.S., Brazner, J.C., Brady, V.J., Axler, R., Tanner, D.K. (2007). Turbidity tolerances of Great Lakes coastal wetland fishes. N Am J Fish Manage 27:619-633.
Tumlison, R., Carroll, C.R., Greenwood, M. (2007). Summer food habits of young Grass Pickerel (Esox americanus), Warmouth (Lepomis gulosus), and Logperch (Percina caprodes) from a cove in Lake Ouachita, Garcland County, Arkansas. J Ark Acad Sci 61:134-136.
Van Meter, H.D., Trautman, M.B. (1970). An annotated list of the fishes of Lake Erie and its tributary waters exclusive of the Detroit River. The Ohio Journal of Science 70:65-78.
Wilcox, K.L., Petrie, S.A., Maynard, L.A., Meyer, S.W. (2003). Historical distribution and abundance of Phragmites australis at Long Point, Lake Erie, Ontario. J Gt Lakes Res 29:664-680.
Wittmann, M.E., Jerde, C.L., Howeth, J.G., Maher, S.P., Deines, A.M., Jenkins, J.A., Whitledge, G.W., Burbank, S.R., Chadderton, W.L., Mahon, A.R., Tyson, J.T., Gantz, C.A., Keller, R.P., Drake, J.M., Lodge, D.M. (2014). Grass carp in the Great Lakes region: establishment potential, expert perceptions, and re-evaluation of experimental evidence of ecological impact. Can J Fish Aquat Sci 71:992-999.
Lynn D. Bouvier est conseillère scientifique spécialiste des espèces en péril à Pêches et Océans Canada, à Burlington, en Ontario. Elle est titulaire d'un B.Sc. (avec distinction) en biologie marine et d'eau douce de l'Université de Guelph (2003). Mme Bouvier possède également une M.Sc. en zoologie de l'Université de Guelph (2006), dans le cadre de laquelle elle a étudié les effets de la connectivité aquatique des milieux humides sur les assemblages de poissons d'eau douce. Depuis plus de 10 ans, elle étudie les poissons et les moules d'eau douce des Grands Lacs. Elle s'intéresse à la biodiversité, aux poissons et aux moules en péril au Canada et à l'évaluation des menaces qui pèsent sur ces espèces.
Nicholas E. Mandrak (Ph.D.) est chercheur scientifique à Pêches et Océans Canada, à Burlington, en Ontario. Il s'intéresse à la biodiversité, à la biogéographie et à la conservation des poissons d'eau douce au Canada. M. Mandrack est le corédacteur de 35 rapports du COSEPAC et du Field Guide to Freshwater Fishes of Ontario (Musée royal de l'Ontario).
Aucune.
| Impact des menaces | Impact des menaces (descriptions) | Comptes des menaces de niveau 1 selon l'intensité de leur impact : Maximum de la plage d'intensité |
Comptes des menaces de niveau 1 selon l'intensité de leur impact : Minimum de la plage d'intensité |
|---|---|---|---|
| A | Très élevé | 0 | 0 |
| B | Élevé | 0 | 0 |
| C | Moyen | 1 | 0 |
| D | Faible | 1 | 2 |
| - | Impact global des menaces calculé : | Moyen | Faible |
| # | Menace | Impact (calculé) Critère |
Impact (calculé) |
Portée (10 prochaines années) |
Gravité (10 années ou 3 générations) |
Immédiateté | Commentaires |
|---|---|---|---|---|---|---|---|
| 1 | Développement résidentiel et commercial (en anglais seulement) | - | Négligeable | Négligeable (< 1 %) | Extrême (71-100 %) | Élevée (constante) | - |
| 1.1 | Habitations et zones urbaines | - | Négligeable | Négligeable (< 1 %) | Extrême (71-100 %) | Élevée (constante) | Des activités de développement ont déjà cours. Aucune prévision de croissance. Présence de chalets, mais aucun plan d'aménagement de nouveaux chalets. Cette menace existait dans le passé. Négligeable dans l'avenir. |
| 1.2 | Zones commerciales et industrielles | - | - | - | - | - | Effets continus attribuables à la marina existante. Construction d'une nouvelle marina peu probable. Faible perte d'habitat (perte de végétation) à cause du dragage. Sédimentation attribuable au dragage traitée au point 4.3. Élimination des mauvaises herbes (débroussaillage). Recolonisation rapide présumée. |
| 1.3 | Tourisme et espaces récréatifs | - | Négligeable | Négligeable (< 1 %) | Élevée-modérée (11-70 %) | Élevée (constante) | Sans objet |
| 2 | Agriculture et aquaculture (en anglais seulement) | - | - | - | - | - | - |
| 2.1 | Cultures annuelles et pluriannuelles de produits autres que le bois | - | - | - | - | - | Certains types de pollution continue traités à la menace 9.0. Aucune conversion de terres agricoles. |
| 2.2 | Plantations pour la production de bois et de pâte | - | - | - | - | - | Sans objet |
| 2.3 | Élevage et élevage à grande échelle | - | - | - | - | - | Sans objet |
| 2.4 | Aquaculture en mer et en eau douce | - | - | - | - | - | Sans objet |
| 3 | Production d'énergie et exploitation minière (en anglais seulement) | - | - | - | - | - | - |
| 3.1 | Forage pétrolier et gazier | - | - | - | - | - | Sans objet |
| 3.2 | Exploitation de mines et de carrières | - | - | - | - | - | Sans objet |
| 3.3 | Énergie renouvelable | - | - | - | - | - | Sans objet |
| 4 | Corridors de transport et de service (en anglais seulement) | - | Inconnu | Petite (1-10 %) | Inconnue | Inconnue | - |
| 4.1 | Routes et voies ferrées | - | - | - | - | - | Sans objet |
| 4.2 | Lignes de services publics | - | - | - | - | - | Sans objet |
| 4.3 | Transport par eau | - | Inconnu | Petite (1-10 %) | Inconnue | Inconnue | Navigation de plaisance dans la baie Rondeau (menace continue), mais aucun navire. Entretien et usage inconnus. Il faut vérifier si les mêmes voies de transport par eau sont utilisées ou si elles sont changées puisque cela influe sur la gravité. Les applications de diquat manquent de précision. |
| 4.4 | Trajectoires de vol | - | - | - | - | - | Sans objet |
| 5 | Utilisation des ressources biologiques (en anglais seulement) | - | Négligeable | Généralisée (71-100 %) | Négligeable (< 1 %) | Élevée (constante) | - |
| 5.1 | Chasse et prélèvement d'animaux terrestres | - | - | - | - | - | Sans objet |
| 5.2 | Cueillette de plantes terrestres | - | - | - | - | - | Sans objet |
| 5.3 | Exploitation forestière et récolte du bois | - | - | - | - | - | Sans objet |
| 5.4 | Pêche et récolte des ressources aquatiques | - | Négligeable | Généralisée (71-100 %) | Négligeable (< 1 %) | Élevée (constante) | Menace continue de la pêche récréative qui abaisse le taux de recrutement. Prises accessoires. Cependant, la menace n'est pas intensive. |
| 6 | Intrusions et perturbations humaines (en anglais seulement) | - | Négligeable | Petite (1-10 %) | Négligeable (< 1 %) | Modérée (peut-être à court terme, < 10 ans) | - |
| 6.1 | Activités récréatives | - | - | - | - | - | La navigation de plaisance n'influe pas directement sur la taille de la population. |
| 6.2 | Guerre, troubles civils et exercices militaires | - | - | - | - | - | Sans objet |
| 6.3 | Travaux et autres activités | - | Négligeable | Petite (1-10 %) | Négligeable (< 1 %) | Modérée (peut-être à court terme, < 10 ans) | Dommages fortuits minimes durant les recherches scientifiques. |
| 7 | Modification du système naturel (en anglais seulement) | CD | Moyen-faible | Restreinte-petite (1-30 %) | Extrême-modérée (11-100 %) | Élevée (constante) | - |
| 7.1 | Incendies et suppression des incendies | - | - | - | - | - | Sans objet |
| 7.2 | Barrages, gestion et utilisation de l'eau | - | - | - | - | - | Sans objet |
| 7.3 | Autres modifications de l'écosystème | CD | Moyen-faible | Restreinte-petite (1-30 %) | Extrême-modérée (11-100 %) | Élevée (constante) | Les activités agricoles passées (élimination de la végétation riveraine) sont historiques. Modifications en cours liées aux marinas, aux chalets et aux voies de transport prises en compte dans les menaces 1, 2 et 4. Possible avantage net de l'augmentation de la végétation submergée due à la hausse de la pénétration de la lumière. Conséquence possiblement négligeable. Espèces envahissantes altérant l'habitat (p. ex. conversion de milieux aquatiques en milieux terrestres). C'est le cas du roseau commun et du myriophylle en épi, qui altèrent également le pH et les teneurs en oxygène dissous dans les baies Long Point et Rondeau. Baisse des niveaux d'eau. Le comportement alimentaire de la carpe commune a de graves effets négatifs (déracinement de la végétation et hausse de la turbidité). Cette menace pourrait être sous-estimée si le roseau commun et le myriophylle en épi ont des effets plus importants que prévu puisque seul le roseau commun a été pris en compte dans les calculs. La carpe de roseau est maintenant établie dans le lac Érié. Établissement peu probable, mais possible, dans l'habitat du crapet sac-à-lait au cours des 10 prochaines années. Les moules zébrées augmentent la clarté de l'eau et altèrent l'habitat. |
| 8 | Espèces et gènes envahissants ou problématiques (en anglais seulement) | - | Inconnu | Généralisée (71-100 %) | Inconnue | Élevée (constante) | - |
| 8.1 | Espèces exotiques/non indigènes envahissantes | - | Inconnu | Généralisée (71-100 %) | Inconnue | Élevée (constante) | Menaces continues du roseau commun, du myriophylle en épi et de la carpe commune qui entraînent toutes l'altération de l'habitat et sont donc traitées à menace 7.3. Les effets du gobie à taches noires sont omniprésents dans la baie Long Point (à confirmer). Les moules zébrées ont augmenté la clarté de l'eau et entraîné des effets sur l'habitat (voir la menace 7.3) |
| 8.2 | Espèces indigènes problématiques | - | - | - | - | - | Sans objet |
| 8.3 | Introduction de matériel génétique | - | - | - | - | - | Sans objet |
| 9 | Pollution (en anglais seulement) | D | Faible | Grande (31-70 %) | Légère (1-10 %) | Élevée (constante) | - |
| 9.1 | Eaux usées domestiques et urbaines | - | Negligible | Grande (31-70 %) | Négligeable (< 1 %) | Élevée (constante) | Apport continu provenant des usines de traitement des eaux usées domestiques, mais les nutriments proviennent vraisemblablement du ruissellement agricole (voir menace 9.3). Les fosses septiques dans les baies Long Point et Rondeau nuisent à la qualité de l'eau. L'apport charge de nutriments cause la prolifération des algues dans le lac Érié. |
| 9.2 | Effluents industriels et militaires | - | - | - | - | - | Sans objet |
| 9.3 | Effluents agricoles et forestiers | D | Faible | Grande (31-70 %) | Légère (1-10 %) | Élevée (constante) | Le ruissellement et le drainage agricoles ont une incidence sur la qualité de l'eau et les charges en nutriments. L'apport de sédiments issus du drainage est aussi généralisé, mais les conséquences sont incertaines. Menace historique. |
| 9.4 | Détritus et déchets solides | - | - | - | - | - | Sans objet |
| 9.5 | Polluants atmosphériques | - | - | - | - | - | Sans objet |
| 9.6 | Énergie excessive | - | - | - | - | - | Sans objet |
| 10 | Phénomènes géologiques (en anglais seulement) | - | - | - | - | - | |
| 10.1 | Volcans | - | - | - | - | - | Sans objet |
| 10.2 | Tremblements de terre et tsunamis | - | - | - | - | - | Sans objet |
| 10.3 | Avalanches et glissements de terrain | - | - | - | - | - | Sans objet |
| 11 | Changement climatique et phénomènes météorologiques violents (en anglais seulement) | - | Inconnu | Généralisée (71-100 %) | Inconnue | Élevée (constante) | - |
| 11.1 | Déplacement et altération de l'habitat | - | Inconnu | Généralisée (71-100 %) | Inconnue | Élevée (constante) | Abordé à la menace 7.3 (conversion des milieux aquatiques). |
| 11.2 | Sécheresses | - | - | - | - | - | Baisse prévue des niveaux d'eau à cause de l'augmentation de l'évaporation due à la hausse des températures. Déclin inconnu prévu à cause de la sécheresse. Les changements dans les précipitations, les températures ou les sécheresses sont tous interreliés et sont abordés à la menace 11.1. |
| 11.3 | Températures extrêmes | - | - | - | - | - | Sans objet |
| 11.4 | Tempêtes et inondations | - | - | - | - | - | Changements des profils d'isolement des populations par rapport aux prédateurs (p. ex. gobie à taches noires) à cause des tempêtes. Effets indirects des espèces envahissantes abordés à la menace 8.1. |
Classification des menaces d'après l'IUCN-CMP, Salafsky et al. (2008).