Le traitement à l'acide tannique pour les artefacts en fer rouillé, publié antérieurement sous le titre Le traitement du fer à l'acide tannique – Notes de l'Institut canadien de conservation (ICC) 9/5
La Note de l'ICC 9/5 fait partie de la neuvième série des Notes de l'ICC (Métaux)
Mise en garde :
Dans cette Note, il est question de mesures qui auront des incidences sur l'aspect matériel de l'objet ou de procédés qui exigent l'utilisation de produits chimiques. Il faut donc agir avec prudence et, en cas de doute, demander l'aide d'une personne compétente.
Introduction
Les objets en fer sont souvent recouverts d'une couche de corrosion, dont l'épaisseur varie. Il ne s'agit parfois que d'une mince pellicule de rouille, mais elle peut également prendre la forme d'une épaisse couche qui défigure l'objet. La corrosion est particulièrement indésirable lorsqu'elle altère l'apparence de l'objet et nuit à son utilité à des fins d'exposition. De plus, comme le fer se corrode rarement d'une manière uniforme et homogène, il est moins bien protégé par les couches de corrosion que ne le sont certains autres métaux. Lorsque la corrosion n'est pas uniforme, la vapeur d'eau et l'oxygène peuvent pénétrer la surface d'un objet en fer et réagir avec le métal sous-jacent. À ce sujet, consulter le nº 9/1 des Notes de l'ICC : Comment reconnaître la corrosion active.
L'acide tannique est un acide organique complexe que l'on trouve dans des plantes. On le caractérise en général en indiquant l'espèce végétale dont il provient. Appliqué sur du fer, il réagit avec le métal et produit du tannate ferrique, une pellicule bleu-noir plutôt poreuse dont le niveau de protection dépend, dans une certaine mesure, de la méthode d'application. Il rend la surface de l'objet uniforme, ce qui en améliore l'apparence. Pour en savoir plus sur les effets du traitement du fer avec l'acide tannique, consulter Selwyn ( ).
Comme l'acide tannique produit une surface bleu-noir, il faut éviter de l'utiliser sur des objets qui avaient à l'origine un fini lustré ou étaient peints. Cependant, il convient au fer forgé et à la fonte, auxquels un fini bleu-noir s'harmonise bien.
À noter que l'application d'acide tannique n'élimine pas le besoin de régler les conditions ambiantes et ne permet pas non plus d'enlever les sels solubles d'objets touchés par de la corrosion active. À ce sujet, consulter le nº 9/6 des Notes de l'ICC : Le soin et le nettoyage du fer.
Préparation des surfaces en fer
Avant d'appliquer l'acide tannique au fer rouillé, s'assurer que toutes les surfaces sont exemptes de salissures, d'accrétions, d'huiles et de graisses. À ce sujet, consulter le nº 9/6 des Notes de l'ICC : Le soin et le nettoyage du fer. Idéalement, tout objet composite, c'est-à-dire formé de différents matériaux, doit être démonté. Si le démontage est impossible, s'assurer que l'acide tannique ne touche que le fer. L'acide tannique peut causer des taches permanentes sur des matériaux comme le bois, le papier, la laine, la soie, le cuir, l'os, la corne et l'ivoire.
Qu'elle soit mince ou épaisse, il n'est ni nécessaire ni souhaitable d'enlever la couche de corrosion avant l'application d'acide tannique.
Préparation de la solution acide
L'acide tannique se présente sous forme d'une poudre légère et floconneuse. Sa couleur va du brun au brun doré, selon le degré de raffinement du produit et le fabricant. Comme beaucoup de produits végétaux naturels, l'acide tannique est un mélange de polymères, ce qui signifie qu'il n'existe pas une composition unique et sa composition varie considérablement d'une marque de commerce à l'autre.
L'acide tannique constitue un risque pour la santé. Éviter l'inhalation de la poudre et tout contact avec la peau. Porter un masque anti-poussières durant la pesée ou le mélange de la poudre sèche. Pour des raisons pratiques, il est recommandé de préparer une solution d'acide tannique à 10 % (p/v) et de l'utiliser telle quelle ou, au besoin, diluée. Pour réduire le risque de moisissure, conserver la solution à 10 % (p/v) au réfrigérateur.
Préparation d'un litre de solution d'acide tannique à 10 % (p/v)
- 100 g d'acide tannique;
- 900 mL d'eau désionisée ou distillée;
- 50 mL d'éthanol;
- environ 2 mL d'acide phosphorique (H3PO4) dilué.
Remarques concernant les ingrédients :
- L'acide tannique étant très léger, une masse de 100 grammes est volumineuse. Pour mélanger ce produit, on doit utiliser un récipient d'une capacité d'au moins 1,5 à 2 litres.
- Utiliser de l'eau désionisée ou distillée. En effet, l'eau du robinet peut contenir des ions chlorure et autres sels dissous qui favorisent la corrosion du fer.
- L'éthanol sert d'agent mouillant qui accroît la pénétration de la solution dans les couches de corrosion poreuses et dans tous les interstices d'une surface de fer corrodé.
- L'acide phosphorique réduit le pH de la solution acide, ce qui augmente la quantité d'ions de fer dissout qui peut réagir avec l'acide tannique. Il n'y a pas lieu de se préoccuper de l'acide phosphorique résiduel, car cet acide réagit avec les ions de fer et donne du phosphate ferrique, qui protège le métal. D'autre part, comme la quantité d'acide utilisée dans la solution est très faible, on ne risque pas de voir un surplus d'acide phosphorique se cristalliser sur la surface de l'objet.
Matériel nécessaire :
- une balance;
- un récipient en verre à l'épreuve de la chaleur, d'une capacité d'au moins 1,5 litre;
- une pelle et une cuillère ou une tige à mélanger;
- un compte-gouttes;
- du papier indicateur de pH;
- un appareil de mesure gradué en millilitres (par exemple : un cylindre gradué);
- une plaque chauffante et un agitateur.
- de l'équipement de protection individuelle, y compris des gants, un masque anti-poussières, une protection pour les yeux et un sarrau ou un tablier long.
Mélange de la solution
L'acide tannique tache, le port des vêtements de protection (gants et un sarrau ou un tablier long) est donc conseillé. Des lunettes de sécurité doivent être portées. Si vos lunettes nuisent au port des lunettes de sécurité normales, un écran facial complet doit être utilisé. L'acide tannique est une poudre fine, il faut porter un masque anti-poussières pendant la préparation pour éviter de l'inhaler.
Mesurer et mélanger 800 mL d'eau désionisée ou distillée et 50 mL d'éthanol dans un récipient en verre. Les récipients en plastique sont à éviter, car on ne peut les chauffer.
Peser 100 g d'acide tannique. Si vous ne disposez pas d'une balance, il est possible d'en emprunter une du laboratoire d'une école voisine.
En remuant constamment le liquide, ajouter progressivement l'acide tannique à la solution d'eau et d'éthanol. Pour accélérer le processus de dissolution, chauffer la solution à feu doux sur une plaque chauffante. Lorsque l'acide tannique est dissous, ajouter suffisamment d'eau désionisée ou distillée (environ 100 mL) pour obtenir un volume total de 1 litre.
Vérifier le pH de la solution à l'aide d'un papier indicateur de pH. S'il est supérieur à 2,4, il faut le réduire en y ajoutant de l'acide phosphorique dilué.
Pour préparer une solution d'acide phosphorique dilué, verser 9 mL d'eau distillée ou désionisée dans un récipient de verre, puis y ajouter 1 mL d'acide phosphorique concentré (la concentration habituelle de l'acide phosphorique commercial est de 85 % p/p). Pour éviter toute réaction violente, toujours verser l'acide dans l'eau, et non l'inverse.
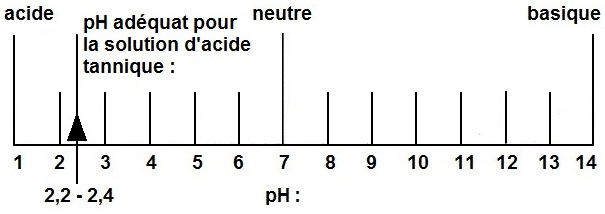
À l'aide d'un compte-gouttes, ajouter un peu d'acide phosphorique dilué à la solution d'acide tannique, en remuant constamment. Après l'ajout d'une dizaine de gouttes, mesurer de nouveau le pH. Poursuivre l'ajout d'acide avec le compte-gouttes jusqu'à ce que le pH se situe entre 2,2 et 2,4. En fonction du pH initial de l'acide tannique (consulter l'échelle du pH sur la figure 1), il faudra ajouter jusqu'à 50 gouttes (environ 2 mL) d'acide phosphorique dilué. L'acide phosphorique dilué non utilisé peut être jeté dans l'évier en prenant soin de faire couler l'eau du robinet en même temps.
Entreposer, préférablement au réfrigérateur, la solution d'acide tannique dans un récipient hermétique et bien identifié. L'étiquette doit indiquer la concentration de la solution, la composition, le pH, la date de préparation, le nom de la personne qui l'a préparé, les précautions à prendre lors de sa manipulation (gants, vêtements de protection), et les instructions pour en disposer (conformément aux règlements du gouvernement en vigueur dans votre localité).
Dilution de la solution-mère d'acide tannique
Pour obtenir un revêtement uniforme de tannate ferrique, il est préférable d'appliquer plusieurs couches d'une solution diluée d'acide tannique plutôt qu'une seule couche de solution concentrée. La solution d'acide tannique à 10 % (p/v) susmentionnée est trop concentrée pour donner de bons résultats. Dans la plupart des cas, il faut la ramener à 2 % (p/v) ou 3 % (p/v).
Pour une dilution facile, mélanger la solution à 10 % (p/v) à parts égales avec de l'eau désionisée (50/50), ce qui produit une solution à 5 % (p/v). Au besoin, diluer de nouveau la solution à 5 % (p/v) de la même façon. Il en résultera une solution à 2,5 % (p/v).
Vérifier par la suite le pH de la solution et, au besoin, ajouter encore quelques gouttes d'acide dilué, jusqu'à ce que le pH se situe entre 2,2 et 2,4.
Application de l'acide tannique
Préparer d'abord une surface de travail, de préférence une table débarrassée recouverte d'une feuille de polyéthylène dont les bords sont fixés. Deux brosses à poils durs, par exemple des brosses à dents, sont nécessaires : l'une pour appliquer l'acide, l'autre pour brosser l'objet lorsqu'il est sec. Comme l'opération peut être salissante, s'assurer que l'acide ne puisse pas éclabousser des surfaces qu'il pourrait tacher (notamment le bois ou les vêtements). Par beau temps, on peut réaliser ce travail à l'extérieur. Le port de vêtements de protection et des lunettes de sécurité est recommandé.
Verser une petite quantité de la solution d'acide tannique à 2,5 % (p/v) dans un récipient convenable, par exemple un bécher en Pyrex. Chauffer la solution jusqu'à environ 50 °C et l'appliquer à la surface de l'objet à l'aide d'une brosse. Lorsque la solution d'acide tannique dans le récipient noircit, la jeter et préparer une solution fraîche.
Pour répartir la solution de façon égale et y faire pénétrer de l'oxygène, continuer de brosser l'objet pendant que la solution sèche. L'objet aura ainsi une couleur uniforme.
On constate un changement rapide de teinte, commençant en général par les surfaces piquées de rouille. Dès que ces surfaces sont recouvertes d'une pellicule uniforme de tannate ferrique, la réaction cesse. L'acide tannique commence alors à réagir sur les plages moins corrodées. La présence d'acide phosphorique permet d'obtenir une réaction plus homogène sur toute la surface de l'objet. Dès que la première couche est sèche, frotter la surface du fer à l'aide d'une brosse sèche à poils durs pour enlever le tannate ferrique qui s'écaille. Appliquer ensuite une autre couche de la solution chauffée d'acide tannique, en continuant à brosser tout au long du séchage.
Répéter les étapes jusqu'à l'obtention d'une couche de l'épaisseur et de la couleur désirées.
Dans le cas d'objets cémentés et des aciers, les outils de coupe par exemple, il est possible que la réaction entre l'acide tannique et le fer produise une couche de couleur différente sur le tranchant. On peut également s'attendre à une apparence distincte du tannate ferrique aux points de soudure ou aux joints. La réaction à l'acide tannique sur les couches épaisses de corrosion sera plus lente que sur les couches minces de rouille ou sur le métal nu.
Maîtriser le processus d'application de la solution de tannate ferrique et obtenir les résultats escomptés peut nécessiter de la pratique. Si on utilise une solution d'acide tannique à 5 % plutôt qu'à 2,5 %, on obtient une pellicule plus épaisse et bien plus foncée. Tout excédent de tannate ferrique s'écaillera simplement de la surface.
Le soin des objets traités à l'acide tannique
Les revêtements de tannate ferrique ne sont pas des pare-vapeurs. Ils ne font que retarder ou freiner la corrosion en formant une couche protectrice sur le fer, mais leur action ne dure pas indéfiniment. Pour prolonger la protection, on recommande les mesures suivantes :
- conserver l'objet dans un endroit où l'humidité relative est stable, à environ 50 %. À ce sujet (consulter le nº 9/6 des Notes de l'ICC : Le soin et le nettoyage du fer);
- porter des gants pour manipuler l'objet;
- protéger la surface de l'objet de la poussière et de l'abrasion.
Il arrive que le revêtement de tannate ferrique soit transféré à d'autres matériaux par le contact. Il faut donc éviter tout contact entre les objets traités à l'acide tannique et d'autres objets faits de matériaux absorbants, comme le papier, les tissus, le cuir, l'os et le bois, qui se tachent facilement.
Si l'on aperçoit des taches de rouille qui percent le revêtement de tannate ferrique, il est bon de vérifier l'humidité relative du milieu et d'examiner soigneusement l'objet, pour s'assurer que ces taches ne résultent pas d'une contamination au chlorure. À ce sujet, voir le nº 9/6 des Notes de l'ICC : Le soin et le nettoyage du fer. Si la réapparition de la rouille semble causée par la détérioration du revêtement de tannate ferrique, il faut recommencer le traitement à l'acide tannique. Il n'est pas nécessaire d'enlever la première couche appliquée.
Il n'est pas nécessaire ou souhaitable d'appliquer sur une surface traitée avec de l'acide tannique un fini protecteur, comme une cire, de l'huile ou de la laque, lorsque l'objet est conservé à l'intérieur dans des conditions environnementales de musée. Les revêtements protecteurs tels que les cires et les laques n'empèchent pas la transmission des vapeurs d'eau et d'oxygène, ils la réduise seulement. Si l'objet commence à corroder, les revêtements peuvent être très difficiles à éliminer de la surface des couches de corrosion poreuses. Un revêtement d'acide tannique ne protège pas contre la corrosion si exposé à l'extérieur et il se dégradera rapidement. (Binnie et coll., ).
Pour en savoir plus sur la mise en réserve des objets en fer, consulter le nº 9/2 des Notes de l'ICC : Mise en réserve des métaux.
Fournisseurs
- Acide tannique
- Fournisseurs de produits chimiques
- Acide phosphorique
- Pharmacies, département de chimie d'écoles secondaires ou fournisseurs de produits chimiques.
- Éthanol
- Départements de chimie d'écoles secondaires ou fournisseurs de produits chimiques
- Brosses
- Magasins de matériel d'artiste ou quincailleries.
- Eau distillée
- Pharmacies ou quincailleries.
- Papier indicateur de pH
- Fournisseurs de produits chimiques.
Bibliographie
BINNIE, N.E., L. SELWYN, C. SCHLICHTING et D.A. RENNIE-BISAILLION. « Corrosion Protection of Outdoor Iron Artifacts Using Commercial Rust Converters », Journal of the International Institute for Conservation – Canadian Group, nº 20 ( ), p. 26-40.
SELWYN, L. Métaux et corrosion : Un manuel pour le professionnel de la conservation, Ottawa (Ontario), Institut canadien de conservation, .
par Judy Logan
Révision : Lyndsie Selwyn, Clifford Cook and Tara Grant
Première date de publication :
Révision : , ,
Also available in English.
Également publié en anglais.
© Gouvernement du Canada, Institut canadien de conservation,
ISSN : 1191-7237