L'acide perfluorooctanoïque (APFO) dans l'eau potable

Télécharger le rapport complet
(Format PDF, 941 Mo, 117 pages)
Organisation : Santé Canada
Type : Consultation
Date publiée : 2016-06-30
Sujets connexes
Table de matières
- Objet de la consultation
- Partie I. Vue d'ensemble et application
- Partie II. Science et considérations techniques
- 4.0 Propriétés, utilisations et sources dans l'environnement
- 5.0 Exposition
- 6.0 Méthodes d'analyse
- 7.0 Techniques de traitement
- 8.0 Cinétique et métabolisme
- 9.0 Effets sur la santé
- 9.1 Effets sur les humains
- 9.2 Effets chez les animaux de laboratoire
- 9.3 Mode d'action
- 10.0 Classification et évaluation
- 11.0 Justification
- 12.0 Références
- Annexe A : Élimination de l'APFO dans les usines de traitement d'eau potable de pleine grandeur - données rapportées
- Annexe B : Liste des acronymes
- Annexe C : Répercussions prévues par province et territoire
Objet de la consultation
Le Comité fédéral-provincial-territorial sur l'eau potable (CEP) a évalué l'information disponible sur l'acide perfluorooctanoïque dans le but d'élaborer une recommandation pour la qualité de l'eau potable et un document technique pour l'APFO dans l'eau potable. La présente consultation vise à solliciter des commentaires sur la recommandation proposée, la démarche suivie pour l'élaborer et les coûts possibles de sa mise en œuvre, ainsi que pour déterminer la disponibilité d'autres données d'exposition.
Le document propose une concentration maximale acceptable (CMA) de 0,0002 mg/L (0,2 µg/L) pour l'APFO dans l'eau potable, fondée sur les effets sur le foie chez les rats. Le document s'appuie sur les études et approches scientifiques présentement disponibles. Il incorpore une analyse détaillée du mode d'action et de la modélisation en vue d'établir une recommandation proposée pour l'APFO. Il renferme des renseignements relatifs à l'exposition ainsi que des méthodes d'analyse et des techniques de traitement qui pourraient être efficaces pour l'enlèvement de l'APFO aux échelles municipale et résidentielle.
Le CEP a demandé que le document soit rendu public aux fins de consultation. Les commentaires, avec justification pertinente le cas échéant, sont les bienvenus. Ils peuvent être envoyés au Secrétariat du CEP par courrier électronique (water_eau@hc-sc.gc.ca) ou au besoin par la poste au Secrétariat du CEP, Bureau de la qualité de l'eau et de l'air, Santé Canada, 3e étage, 269, avenue Laurier Ouest, IA 4903D, Ottawa (Ontario) K1A 0K9. Les commentaires doivent nous parvenir avant le 2 septembre 2016.
Les commentaires reçus dans le cadre de la consultation seront transmis, avec le nom et l'affiliation de leurs auteurs, aux membres concernés du CEP. Les personnes qui ne veulent pas que leur nom et leur affiliation soient communiqués aux membres du CEP doivent joindre à leurs commentaires une déclaration à cet égard.
Il est à noter que le présent document technique sera révisé après l'analyse des commentaires reçus et qu'une recommandation pour l'eau potable sera établie s'il y a lieu. Ce document devrait donc être considéré strictement comme une ébauche pour commentaires.
Partie I. Vue d'ensemble et application
1.0 Recommandation proposée
Une concentration maximale acceptable (CMA) de 0,0002 mg/L (0,2 µg/L) est proposée pour l'acide perfluorooctanoïque dans l'eau potable.
2.0 Sommaire
L'APFO est un composé artificiel qui ne se trouve pas naturellement dans l'environnement. Il est utilisé dans la fabrication de revêtements résistant à l'eau contenus dans divers produits grand public de même que dans certaines applications chimiques spécialisées telles que les mousses extinctrices, les fluides hydrauliques et les détachants de moquettes. Les concentrations dans l'environnement et, par conséquent, les niveaux d'exposition potentiels pourraient être plus élevés dans les régions proches des installations utilisant de grandes quantités d'APFO et à proximité des lieux où des incendies ont été éteints, si des mousses extinctrices à base d'APFO ont été utilisées.
Ce document technique passe en revue et évalue tous les risques connus pour la santé qui sont associés à la présence d'APFO dans l'eau potable. Il tient compte des nouvelles études et approches, ainsi que des limites des méthodes d'analyse et des techniques de traitement. D'après cet examen, la recommandation proposée pour l'APFO dans l'eau potable est une concentration maximale acceptable de 0,0002 mg/L (0,2 µg/L) pour la population générale.
À sa réunion de l'automne 2015, le Comité fédéral-provincial-territorial sur l'eau potable a examiné le document technique sur l'APFO dans l'eau potable et en a approuvé sa publication aux fins de consultation publique.
2.1 Effets sur la santé
Le Centre international de recherche sur le cancer (CIRC) a classé l'APFO et ses sels parmi les substances de groupe 2, c'est-à-dire susceptibles d'être cancérogènes pour l'être humain, d'après des preuves épidémiologiques limitées établissant des liens entre l'APFO et les cancers du testicule et du rein, et compte tenu de preuves limitées chez les animaux de laboratoire. Les effets non cancérogènes se produisant aux plus faibles niveaux d'exposition à l'APFO chez les animaux englobent des effets sur la reproduction et le développement, des effets sur le foie et des modifications touchant le niveau de lipides sériques.
Les effets cancérogènes et non cancérogènes ont tous deux été pris en considération dans l'établissement de la CMA proposée d'APFO dans l'eau potable. L'approche basée sur les effets non cancer, fondée sur la base des effets sur le foie chez le rat, a servi à calculer une CMA proposée qui protège la santé humaine à la fois des effets cancérogènes et non cancérogènes.
2.2 Exposition
Les Canadiens peuvent être exposés à l'APFO dans les aliments, les produits de consommation, la poussière et l'eau potable. L'exposition est principalement liée aux aliments et aux produits de consommation, mais la proportion provenant de l'eau potable peut être plus élevée pour les individus résidant dans des régions où l'eau potable est contaminée. Bien que la présence d'APFO ne soit pas régulièrement surveillée dans les usines de traitement de l'eau potable au Canada, une analyse a été effectuée à quelques endroits. Lorsque l'APFO est détecté dans l'eau potable, son niveau est généralement en dessous de 2 ou 3 ng/L.
2.3 Analyse et traitement
À ce jour, l'U.S. Environmental Protection Agency n'a approuvé aucune méthode pour l'analyse de l'APFO dans l'eau potable. Il existe certaines méthodes permettant de mesurer les niveaux d'APFO présents dans l'eau potable à des niveaux bien inférieurs à la CMA proposée. Elles nécessitent cependant des procédures rigoureuses de contrôle de la qualité pour donner des résultats justes.
Le choix et l'efficacité d'une stratégie pour l'enlèvement de l'APFO sont déterminés par plusieurs facteurs, tels que la composition chimique de l'eau brute, la concentration d'APFO et/ou d'autres substances perfluoroalkylée ainsi que les procédés de traitement déjà en place. Le traitement conventionnel n'est pas efficace pour enlever l'APFO. D'autres méthodes de traitement se montrent prometteuses, mais les études à pleine échelle sont limitées. La méthode d'adsorption sur du charbon actif peut permettre d'obtenir des concentrations d'APFO inférieures à la CMA proposée. Cependant, l'opération appropriée du système est essentielle pour faire en sorte que le rendement du charbon actif en grains (CAG) ne soit pas entravé par la présence de matière organique naturelle dans l'eau brute. Les techniques de filtration sur membrane (osmose inverse et nanofiltration) et d'échange d'anions pourraient aussi s'avérer efficaces. Bien qu'il n'existe aucun dispositif de traitement à résidentiel certifié pour éliminer l'APFO, les mêmes techniques de traitement devraient être efficaces à l'échelle résidentielle.
3.0 Application de la recommandation
Remarque : Des conseils spécifiques concernant l'application des recommandations pour l'eau potable devraient être obtenus auprès de l'autorité appropriée en matière d'eau potable dans le secteur de compétence concerné.
3.1 Surveillance
L'APFO est typiquement retrouvé dans les eaux souterraines et de surface contaminées par des rejets provenant d'installations industrielles, des rejets issus d'usines de traitement des eaux usées domestiques ou industrielles, des eaux pluviales d'orage, ou de l'application de sols modifiés par des biosolides. Il peut aussi se retrouver dans des eaux souterraines ou de surface qui sont probablement ou réellement atteintes par de la mousse à formation de pellicule aqueuse (mousse AFFF, utilisée pour l'extinction de feux). Tout comme d'autres contaminants d'eau souterraine, l'APFO peut atteindre les puits d'eau potable par la migration d'un panache d'eau souterraine contaminée. Il peut aussi atteindre l'eau souterraine par les émissions dans l'atmosphère provenant d'installations industrielles. Il est possible que des substances perfluoroalkyliques (SPFA) volatiles liées à des particules soient emportées par le vent à partir de sites d'élimination et qu'elles se déposent ensuite sur le sol ou l'eau de surface, ce qui explique la présence de substances chimiques anthropiques dans des lieux éloignés et dans des eaux non touchées par une source ponctuelle. L'APFO traverse le sol très lentement avant d'atteindre l'eau souterraine et plusieurs années peuvent s'écouler avant qu'il ne soit décelé dans la source d'eau.
Les services publics devraient caractériser leur source d'eau pour évaluer les concentrations d'APFO. Pour les sources d'eau dans lesquelles on retrouve un niveau d'APFO supérieur à la CMA proposée, il conviendrait d'effectuer une surveillance trimestrielle pour l'eau de surface, ou une surveillance semestrielle pour l'eau souterraine.
La fréquence de surveillance de l'eau traitée dépend de la technique de traitement utilisée par le service public. Les services publics qui utilisent un système à base de CAG pour éliminer l'APFO voudront probablement renforcer la surveillance de l'eau traitée en vue d'évaluer le rendement du système de CAG et de déterminer le moment propice pour la régénération. Un service public peut envisager de diminuer sa surveillance lorsqu'il dispose de données indiquant que la source d'eau est exempte d'APFO. Néanmoins, si l'on soupçonne que la contamination provient d'une mousse AFFF, le service public pourrait envisager de surveiller la présence d'autres acides perfluoroalkyliques (APFA; c.-à-d. les composés à chaîne plus courte tels que l'acide perfluorobutanoïque et le perfluorobutanesulfonate). Il est probable que ces autres APFA soient aussi présents sur des sites affectés par des mousses AFFF et sont généralement plus mobiles. Par conséquent, ils peuvent servir de signe avant-coureur d'une contamination de la source d'eau souterraine par l'APFO et le SPFO.
Partie II. Science et considérations techniques
4.0 Propriétés, utilisations et sources dans l'environnement
L'acide perfluorooctanoïque (APFO) est un composé anthropique à chaîne de huit atomes de carbone, dont sept sont perfluorés. Il appartient à la classe des acides perfluorocarboxyliques (APFC), eux-mêmes inclus dans la catégorie générale des substances perfluoalkyliques (PFA) qui, à leur tour, font partie des acides perfluoroalkyliques (Environnement Canada et Santé Canada, 2012). Aux fin du présent rapport, l'appellation APFO peut désigner l'acide libre (C8HF15O2; numéro CAS 335-67-1; 414,07 g/mol) ou sa base conjuguée (C8F15O2-; numéro CAS 45285-51-6). L'appellation de perfluorooctanoate d'ammonium (PFOA) désigne le sel d'ammonium (C8F15O2- NH4+; numéro de CAS 3825-26-1), son principal sel, tandis que K+APFO désigne le sel de potassium (numéro CAS 2395-00-8). Les principaux synonymes de l'APFO sont l'acide pentadécafluorooctanoïque, le perfluorooctanoate, C8, FC-143, le pentadécafluoro-acide-1 octanoïque, le pentadécafluoro-acide-n-octanoïque, l'acide perfluorocaprylique, l'acide perfluoroctanoïque, l'acide perfluoroheptanecarboxylique et l'acide octanoïque.
L'APFO est très soluble dans l'eau : les estimations varient de 3 500 mg/L en pH neutre ou alcalin à 9 500 mg/L dans de l'eau pure et peuvent diminuer jusqu'à 0,7 mg/L en pH acide (Kauck et Diesslin, 1951; Barton et coll., 2007; Environnement Canada et Santé Canada, 2012). La solubilité dépend de la constante de dissociation acide (pKa) de la forme acide. Les valeurs obtenues pour le pKa vont de -0,5 à 4 (Kissa, 1994; Burns et coll., 2008; Goss, 2008; ATSDR, 2009; Goss et Arp, 2009; Environnement Canada et Santé Canada, 2012), et les études semblent indiquer qu'avec un pKa aussi faible, la distribution de l'APFO dans l'environnement se fera majoritairement sous la forme anionique (Goss, 2008).
Les différentes portions de la molécule d'APFO combinent des propriétés hydrophobes et hydrophiles (Environnement Canada et Santé Canada, 2012). En raison de cette particularité, on s'attend à ce que l'APFO ait un comportement différent des substances chimiques hydrophobes traditionnelles. La présence des nombreuses couches octanol-eau empêche de déterminer directement le coefficient de partage octanol-eau (Koe). De plus, il est impossible de calculer les paramètres estimés à partir du Koe (tels que le Koc et le facteur de bioconcentration) en utilisant cette méthode (ATSDR, 2009; Environnement Canada et Santé Canada, 2012). Les valeurs du log Koe, estimées par modélisation, varient entre 3,62 et 6,30 (Arp et coll., 2006; Jasinski et coll., 2009; Environnement Canada et Santé Canada, 2012).
L'APFO est essentiellement non volatile, sa pression de vapeur étant de 2,24 × 10-5 atm à 20 °C (Barton et coll., 2007; ATSDR, 2009; Environnement Canada et Santé Canada, 2012). La constante de la loi d'Henry calculée pour cette substance est estimée à 2,4 x 10-5 atm-m3/mol (Barton et coll., 2007).
Les précurseurs de l'APFO (diesters de phosphate de polyfuoroakyle, fluorotélomères et acides phosphoniques perfluorés) constituent une source indirecte d'APFO dans l'environnement (Ellis et coll., 2004; D'Eon et coll., 2009; Lee, 2010).
Les principaux producteurs d'APFO se trouvent principalement aux États-Unis, en Europe et en Asie. Selon les renseignements obtenus auprès de l'industrie en 2004, il n'existerait aucun fabricant de substances perfluoroalkyliques et fluoroalkyliques au Canada. Néanmoins, le PFOA a été importé au pays dans des quantités variant entre 100 et 100 000 kg (Environnement Canada et Santé Canada, 2012). Le PFOA sert principalement d'adjuvant de polymérisation commerciale pour la production de polymères fluorés. Les fluoropolymères sont utilisés dans la fabrication de revêtements étanches et antitaches appliqués sur des tissus et tapis; des tuyaux, des câbles et des joints d'étanchéité; des revêtements antiadhésifs de batteries de cuisine; des produits de soins personnels. Le PFOA sert également d'ingrédient dans les dispersions aqueuses de polymères fluorés qui entrent dans la composition de peintures et d'additifs pour pellicules photographiques, et est utilisé dans l'industrie aérospatiale (p. ex., il est un ingrédient possible des mousses à formation de pellicule aqueuse [AFFF] utilisées pour combattre les incendies; Environnement Canada et Santé Canada, 2012). Les substances chimiques fluorées (précurseurs possibles de l'APFO) sont également utilisées dans le traitement de matériaux d'emballage alimentaire (Environnement Canada et Santé Canada, 2012), tels que les sacs de maïs à éclater utilisables au four à micro-ondes (Dolman et Pelzing, 2011). Il ne faut pas confondre le terme APFO avec les mélanges commerciaux contenant de l'APFO, car ceux-ci sont souvent mal caractérisés et pourraient comprendre n'importe quel produit qui contient même une infime quantité d'APFO (Environnement Canada et Santé Canada, 2012).
4.1 Sources dans l'eau
Le rejet de mousses AFFF utilisées dans les extincteurs constitue une source de contamination de l'eau par des APFA. Compte tenu de tendances géographiques et temporelles des APFA dans l'eau, on suppose que le rejet de mousses AFFF a entraîné un accroissement des quantités d'APFA dans les cours d'eau entourant l'aéroport international de Toronto (Awad et coll., 2011). Même si l'étude portait essentiellement sur la contamination au SPFO, étant donné qu'il s'agissait du principal APFA présent dans la mousse AFFF utilisée à cet endroit, il est plausible que les mousses AFFF contenant de l'APFO soient similairement responsables de concentrations accrues d'APFO dans les cours d'eau avoisinant les sites de déversement. Les données semblant confirmer la possibilité de contamination à proximité d'aires d'entraînement à la lutte contre les incendies comprennent des mesures de concentrations élevées d'APFO dans les eaux souterraines proches d'une base aérienne du Michigan (Moody et coll., 2003), sur un terrain d'entraînement à la lutte contre les incendies en Australie (Baduel et coll., 2015), et dans des puits privés d'eau potable situés à proximité d'un site industriel à Cologne en Allemagne (Weiß et coll., 2012).
Les concentrations élevées d'APFO mesurées dans l'eau de surface en aval d'usines de fabrication de composés fluorés ont également été prises en considération pour expliquer la présence possible d'APFO dans l'eau provenant de sources industrielles (Hansen et coll., 2002; Frisbee et coll., 2009).
Des études du bilan massique d'APFA dans les usines de traitement des eaux usées font couramment état de concentrations semblables ou supérieures d'APFO dans les effluents en comparaison avec les affluents bruts, ce qui permet de penser que la dégradation d'autres composés organiques fluorés (tels que les polymères fluorés) en APFO pourrait se produire durant le traitement des eaux usées (Clarke et Smith, 2011) et que les usines traditionnelles de traitement des eaux usées ne parviennent pas à éliminer les APFA (Ahrens, 2011). L'APFO a été détecté dans les effluents d'usines de traitement des eaux usées à des concentrations allant de 0,007 à 0,055 μg/L au Canada (Environnement Canada et Santé Canada, 2012) et à des concentrations moyennes variant entre 0,080 et 0,12 μg/L dans les effluents de sept lieux distincts aux É.-U. (Quinones et Snyder, 2009).
Bien que des mesures existent en Amérique du Nord et en Europe pour limiter la production, l'utilisation d'APFA et (ou) les principaux risques d'exposition connexes (cela concerne surtout le SPFO, mais aussi l'APFO dans une certaine mesure), l'utilisation généralisée des APFA au sein de l'environnement bâti continue de causer leur transfert vers les matières biosolides (boues) (Clarke et Smith, 2011). Par conséquent, l'utilisation de biosolides comme engrais pourrait constituer une source de contamination du sol et de l'eau par l'APFO (Clarke et Smith, 2011). Des concentrations élevées d'APFO ont été relevées dans l'eau de surface et dans l'eau de puits à Decatur en Alabama, après que des biosolides provenant d'une usine municipale de traitement des eaux usées (qui recevait des déchets provenant d'installations de production de composés fluorés) ont été appliqués sur des champs agricoles (Lindstrom et coll., 2011).
4.2 Devenir dans l'environnement
L'hydrosolubilité élevée de l'APFO et la volatilité négligeable de ses espèces ionisées semblent indiquer que les espèces d'APFO se répartiront principalement dans les milieux aquatiques (Environnement Canada et Santé Canada, 2012).
L'APFO peut se retrouver dans l'air, l'eau de surface, les sédiments, l'eau souterraine et le sol partout dans le monde (y compris dans l'Arctique). Deux voies de transport à grande distance ont été proposées pour expliquer cette omniprésence (Post et coll., 2012). La première voie a trait au transport atmosphérique des précurseurs volatiles (p.ex. : l'alcool fluorotélomérique), leur oxydation en APFO (et autres APFF) et, par la suite, leur retombée à la surface du sol ou de l'eau. La deuxième voie fait intervenir le transport à grande distance en milieu aqueux de carboxylates perfluorés sous forme anionique, tels que l'APFO, émis à proximité d'installations industrielles par les courants de surface (Butt et coll., 2010; Post et coll., 2012).
Les valeurs expérimentales du log Koe varient entre 1,2 et 4.5 (Dekleva, 2003; Higgins et Luthy, 2006; Prevedouros et coll., 2006; ATSDR, 2009; Environnement Canada et Santé Canada, 2012; Zareitalabad et coll., 2013). Les données semblent indiquer que la sorption de l'APFO peut raisonnablement être comparée à un processus de répartition assorti d'un log Koe de 2,8 en moyenne (Zareitalabad et coll., 2013).
L'APFO peut s'accumuler dans les tissus d'organismes vivant en milieu aquatique ou terrestre. Les données de bioaccumulation recueillies pour différentes espèces vivant dans les écosystèmes marin et terrestre indiquent que l'APFO présente un potentiel faible à modéré de s'accumuler dans l'organisme entier des espèces aquatiques, alors que l'accumulation peut se révéler plus forte dans certains organes ou tissus (p. ex. dans le foie et le sang) (Environnement Canada et Santé Canada, 2012). En résumé, le log des facteurs de bioaccumulation (FBA) de l'APFO varie entre 0,02 et 0,63 pour la truite, et entre 9,6 et 19,4 pour l'huître creuse du Pacifique. Le log des facteurs de concentration biologique (FCB) est évalué à 4 pour la truite arc-en-ciel (carcasse), varie entre 3,1 et 9,1 pour la carpe, est évalué à 1,8 pour le vairon à grosse tête (organisme entier) et varie entre 0,8 et 3 pour l'huître creuse du Pacifique. L'APFO peut aussi bioamplifier dans certains réseaux alimentaires (p. ex. chez les ours polaires) (Environnement Canada et Santé Canada, 2012).
Sous certaines conditions environnementales, l'APFO est incapable de s'hydrolyser, de se décomposer par photolyse ou de se biodégrader, et est considéré comme extrêmement persistant dans l'environnement (OCDE, 2006; Environnement Canada et Santé Canada, 2012). L'APFO résiste aussi à la dégradation microbienne (Liou et coll., 2010). En outre, la biodégradation des composés précurseurs pourrait causer des concentrations accrues d'APFO dans l'environnement (Ahrens, 2011; Clarke et Smith, 2011). Compte tenu de ses propriétés empiriques et physicochimiques, il a été conclu que l'APFO et ses sels répondent aux critères de persistance dans l'eau, le sol, les sédiments et l'air (demi-vie ≥ 182 jours dans le sol et dans l'eau, ≥ 365 jours dans les sédiments et ≥ 2 jours dans l'air) (Environnement Canada et Santé Canada, 2012).
5.0 Exposition
cLes Canadiens peuvent être exposés aux composés perfluorés présents dans les aliments, les produits de consommation, la poussière et l'eau potable. On estime que les principales sources de composés perfluorés sont les aliments et les produits de consommation, y compris les tapis et les vêtements traités chimiquement (Tittlemier et coll., 2007). Cela dit, le degré d'exposition par l'intermédiaire de l'eau potable peut augmenter chez les individus résidant dans des régions où l'eau courante est contaminée.
L'apport quotidien total d'acides perfluoroalkyliques est estimé à 410 ng/jour (estimations non fournies pour chaque composé individuel) chez la population générale du Canada (Tittlemier et coll., 2007). L'ingestion d'eau potable, évaluée à 0,3 ng/jour, ne contribue qu'une faible proportion de l'exposition globale. Bien que certaines données d'exposition soient disponibles, elles sont considérées insuffisantes pour justifier une modification du facteur alloué par défaut à l'eau potable de 20 %. Ce facteur attribué par défaut à l'eau potable est utilisé comme valeur seuil lorsque l'eau potable n'est pas une source importante d'exposition (Krishnan et Carrier, 2013). Par conséquent, cette valeur est applicable à l'APFO, même si l'eau n'est censée contribuer que peu à l'exposition de la population générale à cette substance.
5.1 Eau
Bien que la présence d'APFO ne soit pas régulièrement surveillée dans les usines de traitement de l'eau potable au Canada, une analyse a été effectuée dans certains lieux. Aucun APFO n'a été détecté (limite de détection de la méthode [LDM] de 0,51 ng/L) dans des échantillons d'eau brute ou traitée prélevés en 2012 dans deux usines de traitement de l'eau de Calgary (Alberta Environment and Water, 2013). Au Québec, des échantillons d'eau brute et d'eau traitée ont été prélevés mensuellement entre avril 2007 et mars 2008 dans sept sites différents (soit 84 échantillons d'eau brute et d'eau traitée). L'APFO a été détecté dans 75 % des échantillons d'eau traitée (LDM entre 0,3 et 0,6 ng/L), la valeur médiane étant de 2,5 ng/L. Le taux de détection et la concentration médiane étaient plus élevés dans les échantillons d'eau traitée que dans ceux d'eau brute, qui ont obtenu un taux de détection de 55 % et une valeur médiane de 2 ng/L, respectivement (ministère du Développement durable, de l'Environnement, de la Faune et des Parcs, 2012). La concentration d'APFO relevée à partir de cinq échantillons d'eau du robinet de Niagara-on-the-Lake en Ontario s'établissait à 2,1 ng/L (Mak et coll., 2009). Des concentrations plus faibles d'APFO (0,2 ng/L) ont été relevées à partir d'échantillons d'eau du robinet de Calgary et de Vancouver (Tanaka et coll., 2006).
Dans le cadre d'une enquête nationale menée par Santé Canada sur les nouveaux contaminants dans l'eau potable (y compris l'APFO), l'eau traitée et l'eau brute ont été surveillées en hiver et à l'été sur 35 sites en 2009, puis sur 30 sites en 2010. À l'été 2009, l'APFO a été détecté (LDM de 0,023 ng/L) dans 68 % des échantillons d'eau brute et dans 64 % des échantillons d'eau traitée, avec des moyennes de 0,067 ng/L et 0,071 ng/L, respectivement. Les concentrations d'APFO étaient légèrement plus faibles à l'hiver 2009, avec une moyenne de 0,057 ng/L dans les échantillons bruts (59 % de détection) et 0,056 ng/L dans les échantillons traités (55 % de détection). Les taux de détection de l'APFO étaient plus faibles dans les sites surveillés en 2010 : durant l'été, ces taux étaient de 18 % dans l'eau brute (moyenne de 0,066 ng/L) et de 15 % dans l'eau traitée (moyenne de 0,046 ng/L) tandis qu'en hiver, les taux observés étaient de 33 % dans l'eau brute (moyenne de 0,055 ng/L) et de 27 % dans l'eau traitée (moyenne de 0,05 ng/L) (Santé Canada, 2013a).
5.2 Aliments
On considère généralement que les aliments constituent la principale source d'exposition à l'APFO pour la majorité de la population canadienne, mais cette exposition par voie alimentaire est bien en deçà des valeurs considérées dangereuses pour l'humain. L'APFO a été mesuré dans une sélection d'échantillons composés d'aliments canadiens (fondés sur l'Étude canadienne sur l'alimentation totale réalisée en 2004 et sur d'autres échantillons recueillis entre1992 et 2001) servant à évaluer l'apport alimentaire. L'APFO a été détecté dans trois aliments composites sur 54 au total. Les concentrations d'APFO détectées (exprimées en poids) s'établissaient à 0,74 ng/g dans la pizza (l'échantillon était au-dessus de la limite de détection, mais en dessous de la limite de quantification), à 2,6 ng/g dans le rôti de bœuf et à 3,6 ng/g dans le maïs soufflé préparé au four à micro-ondes. Ces valeurs ont servi à estimer l'exposition quotidienne moyenne des Canadiens par l'alimentation, et l'on estime que les aliments apportent 250 ng/jour de composés perfluorés, dont 70 ng environ sont attribués à l'APFO (Tittlemier et coll., 2007).
Des aliments courants, achetés en magasin ou consommés dans les restaurants par les Canadiens, ont été recueillis à Whitehorse dans le territoire du Yukon en 1998 à des fins d'analyse pour y détecter la présence d'APFA. L'APFO a été détecté dans plusieurs échantillons composites (de 0,36 à 0,77 ng/g dans les biscuits, le fromage fondu, les poivrons, les viandes préparées en conserve et la pizza), mais toutes les mesures se situaient sous les limites de quantification (les valeurs variaient entre 0,65 et 1,52 ng/g) (Ostertag et coll., 2009a).
Les concentrations d'APFA dans les aliments traditionnels des Inuits du Nord du Canada ont été mesurées pour évaluer leur exposition alimentaire. L'APFO a rarement été détecté (9 % sur 68 échantillons au total) dans les aliments traditionnels prélevés à Chesterfield Inlet, à Igloolik, à Pond Inlet et à Qiqiktarjuak au Nunavut, entre 1997 et 1999.
L'APFO a été détecté notamment chez le phoque annelé (0,3 ng/g dans le foie et 0,1 ng/g dans le sang), chez l'eider du Nord (0,4 ng/g dans le corps entier), dans le foie de caribou (0,7 ng/g dans le foie cuit; et 0,1 ng/g dans le foie cru) et dans la panse de caribou crue (0,8 ng/g), les autres concentrations étant en dessous des limites de détection (valeurs inférieures à la fourchette de 0,1 à 0,6 ng/g) (Ostertag et coll., 2009 b).
L'APFO est un agent technologique du polytétrafluoroéthylène (PTFE) qui entre dans la fabrication de nombreux articles, notamment les batteries de cuisine antiadhésives. Des résidus d'APFO ont été détectés dans les films et batteries de cuisine au PTFE (Begley et coll., 2005). Néanmoins, seul un transfert minime d'APFO a été observé à la suite d'études portant sur la migration dans des substances à base aqueuse ou d'acides gras simulant des aliments (Begley et coll., 2005; Powley et coll., 2005; Washburn et coll., 2005; Sinclair et coll., 2007). L'APFO a également été détecté dans des sacs de maïs soufflé allant au micro-ondes (Begley et coll., 2005; Sinclair et coll., 2007; Dolman et Pelzing, 2011), ainsi que dans des papiers pour contact alimentaire traités aux tensioactifs phosphates de polyfluoroalkyles (PAP) ou aux di-perfluoro-alkyloxy-amino-acides (PAA) (Xu et coll., 2013). Les taux de migration de l'APFO à partir des papiers pour contact alimentaire traités avec ces composés variaient entre 7 % à 92 % pour cinq substances simulant des aliments (Xu et coll., 2013).
5.3 Air
On considère que l'apport d'APFO par inhalation chez les Canadiens est négligeable en raison de sa faible volatilité (Tittlemier et coll., 2007).
Les niveaux d'APFA dans l'air ambiant ont été déterminés dans une étude canadienne menée en 2007 à Vancouver (Shoeib et coll., 2011). Des échantillons d'APFO ont été prélevés au moyen d'échantillonneurs passifs installés dans des cours résidentielles pendant environ trois mois. L'APFO a été détecté dans quatre échantillons sur six (moins de 0,47 à 9,2 pg/m3; moyenne de1,4 pg/m3) (Shoeib et coll., 2011). Des concentrations semblables ont été mesurées dans l'Arctique canadien (baie Resolute, île Cornwallis au Nunavut) en 2004 avec une concentration moyenne (phases gazeuse et particulaire de l'air atmosphérique) de 1,4 pg/m3 (Stock et coll., 2007).
Le niveau d'APFO dans l'air intérieur dépend principalement de sa concentration dans les particules atmosphériques et, par conséquent, est lié aux niveaux présents dans la poussière intérieure, ainsi qu'au nombre, au type et à l'âge des sources potentielles (telles que la moquette, les meubles et la peinture) (Fraser et coll., 2012). À ce jour, les données disponibles sur les concentrations d'APFO dans l'air intérieur sont limitées à celles indiquées dans l'étude précitée, qui a été effectuée dans les résidences (Shoeib et coll., 2011). Les auteurs ont prélevé des échantillons d'APFO présent dans l'air intérieur au moyen d'échantillonneurs passifs installés pendant environ quatre semaines dans la chambre de 59 participants. L'alkyle perfluoré ionique dominant était l'APFO, dont la concentration géométrique moyenne était de 28 pg/m3 (moyenne arithmétique : 113 pg/m3; médiane : 21 pg/m3 et plage de 3,4 à 2 570 pg/m3).
5.4 Produits de consommation
En raison des modes d'utilisation de l'APFO, il est probable que les humains y sont exposés par leur contact avec certains produits de consommation ou par leur utilisation (Santé Canada, 2006). D'après les estimations, le traitement par solution chimique des tapis et des vêtements compte respectivement pour 120 ng et 12 ng par jour dans l'apport quotidien total de composés perfluorés par les Canadiens (Tittlemier et coll., 2007). Puisqu'il n'existe pas de données canadiennes sur l'exposition à l'APFO par l'intermédiaire des produits de consommation, ce sont les données d'autres pays que nous avons résumées ci-dessous.
L'APFO a été mesuré dans divers produits de consommation, y compris les hydrofuges, les textiles traités au fluorotélomère, les vêtements et les tapis, les mousses extinctrices aqueuses, les ustensiles antiadhésifs, les cires à parquet industrielles et les décapants pour cire, les peintures au latex, les produits de nettoyage pour le bureau et la maison, les soies et rubans dentaires recouverts de PTFE, ainsi que les films et rubans d'étanchéité enduits de PTFE (Begley et coll., 2005; Washburn et coll., 2005; Herzke et coll., 2012). L'APFO a également été mesuré dans les blocs de fartage de ski et les farts de glisse, par une étude de l'exposition professionnelle aux APFA présents dans l'air durant le fartage professionnel de skis (Freberg et coll., 2010).
5.5 Sol et poussières
D'après les estimations, les poussières contribuent 28 ng/jour à l'apport quotidien de composés perfluorés par les Canadiens (Tittlemier et coll., 2007). L'étude n'a pas évalué la contribution du sol dans l'apport quotidien aux composés perfluorés.
D'après les indications disponibles, les concentrations d'APFO dans la poussière des maisons canadienne varieraient entre 2,3 et 1 234 ng/g, la valeur médiane étant de 19,7 ng/g (soit une moyenne de 106 ng/g). On indique que l'âge du bâtiment et les revêtements de sol ont une corrélation importante avec la concentration d'alkyles perfluorés dans la poussière. Ainsi, les maisons anciennes et celles dont le plancher est recouvert de moins de tapis étaient marquées par des concentrations moindres d'APFA (Kubwabo et coll., 2005).
Dans une autre étude canadienne menée dans la ville de Vancouver, l'APFO a été détecté dans tous les échantillons de poussière domestique analysés (n = 132). Les concentrations de ce composée allaient de 1,9 à 1 390 ng/g (médiane = 30 ng/g et moyenne = 97 ng/g) (Shoeib et coll., 2011).
Nous n'avons trouvé aucune étude faisant état des niveaux d'APFO dans les sols. Il existe quelques données portant sur la présence de produits chimiques perfluorés dans les sols d'installations industrielles (telles que celles analysées par ATSDR, 2009).
5.6 Données de biosurveillance des êtres humains
Des études indiquent que l'âge et le sexe ont une influence sur le niveau d'APFO présent dans le sang humain. D'après les indications du cycle 1 (2007-2009) de l'Enquête canadienne sur les mesures de santé (ECMS), la concentration plasmatique d'APFO relevée chez les adultes de sexe masculin (moyenne géométrique = 2,94 ng/mL; IC de 95 % = 2,74 à 3,15, 95e percentile = 5,98 ng/mL, n = 1376) est plus élevée que chez les femmes d'âge adulte (moyenne géométrique = 2,17 ng/mL; IC de 95 % = 1,99 à 2,36, 95e percentile = 4,99 ng/ml, n = 1504) (Santé Canada, 2010). Cette tendance s'est maintenue dans le cycle 2 de l'étude (2009-2011) (Hommes - moyenne géométrique = 2,6 ng/mL, IC de 95 % : 2,4 à 2.9, 95e percentile = 6, n = 511; Femmes - moyenne géométrique = 2 ng/mL, IC de 95 % = 1,8 à 2,2, 95e percentile = 4,4 ng/mL, n = 506) (Santé Canada, 2013 b).
5.7 Exposition multi-voies par l'eau potable
La procédure d'évaluation de l'exposition par des voies multiples ne s'applique pas à l'APFO en raison du poids moléculaire élevé et de la faible volatilité de ce composé (Krishnan et Carrier, 2008). Par conséquent, il a été impossible d'évaluer les contributions relatives de l'exposition à l'APFO par inhalation et par voie cutanée pendant la douche et le bain. Compte tenu du poids moléculaire élevé de 414,07 et des propriétés ioniques de l'APFO à des niveaux de pH typiques dans l'eau potable, la volatilité et la pénétration cutanée devraient être faibles. En outre, les coefficients de perméabilité dermique mesurés dans des études in vitro laissent présager que la peau est imperméable à l'APFO dans des conditions normales (Fasano et coll., 2005; Franko et coll., 2012). Par conséquent, l'exposition à l'APFO par inhalation et par voie cutanée pendant la douche et le bain devrait être négligeable.
6.0 Méthodes d'analyse
À ce jour, la United States Environmental Protection Agency n'a approuvé aucune méthode d'analyse de l'APFO dans l'eau potable. Il existe des méthodes permettant de mesurer les niveaux d'APFO présents dans l'eau potable à des niveaux bien inférieurs à la CMA proposée. Elles nécessitent néanmoins des procédures rigoureuses de contrôle de la qualité pour donner des résultats précis.
6.1 Méthodes disponibles
La méthode EPA 537 ver. 1.1, la méthode 25101 de l'Organisation internationale de normalisation (ISO) et la méthode ETS-8-154.3 de 3M peuvent toutes être utilisés pour analyser l'APFO dans l'eau potable (3M, 2008; ISO, 2009; U.S. EPA, 2009a). Toutes les méthodes reposent sur une technique d'extraction en phase solide (EPS) suivie d'une chromatographie liquide (CL) couplée à la spectrométrie de masse en tandem (SM/SM) avec ionisation par électronébulisation (IE) fonctionnant en mode d'ions négatifs. À des fins d'analyse quantitative de l'APFO à l'état de traces dans l'eau potable, on choisit les conditions chromatographiques pour faire en sorte de co-éluer tous les isomères (linéaires et ramifiés).
Avec la méthode EPA, on fortifie un échantillon d'eau à l'aide d'étalons internes marqués, puis on le fait passer dans une cartouche d'extraction en phase solide en vue d'extraire les composés à analyser en plus des étalons internes correspondants. Les composés sont élués de la cartouche d'extraction, puis concentrés et injectés dans un système CL-SM/SM. Le spectre de masse et le temps de rétention des composés à analyser sont comparés aux étalons internes. La LDM pour l'APFO est de 1,7 ng/L (0,0017 µg/L) et le seuil minimal de niveau à rapporter (SMNR) est fixé à 5,1 ng/L (0,0051 µg/L) (U.S. EPA, 2009a). L'APFO est visé par la troisième règle de surveillance des contaminants non réglementés (Third Unregulated Contaminant Monitoring Rule, UCMR3) qui stipule qu'en ayant recours à la méthode 537 ver. 1.1, les services publics sont tenus, durant la procédure de surveillance, d'obtenir et de déclarer un niveau minimal de 20 ng/L (0,02 µg/L) pour l'APFO (U.S. EPA, 2012b).
Les résultats d'une épreuve interlaboratoires effectuée en 2006 (Taniyasu et coll., 2013) ont été utilisés pour déterminer si la méthode ISO 25101 était fiable pour analyser la présence d'APFO et de SPFO dans des échantillons d'eau de l'environnement et d'eau potable. Les fourchettes de précision intralaboratoire et interlaboratoire étaient de 3 à 7 % et de 15 à 22 %, respectivement pour l'ensemble des échantillons d'eau de l'environnement analysés en lien avec l'APFO. Le recouvrement des étalons internes pour l'APFO s'échelonnait de 91 à 98 % et les résultats ont confirmé que cette méthode d'analyse était fiable et utilisable pour analyser la présence d'APFO à partir d'échantillons d'eau de l'environnement. La méthode repose sur l'EPS et la CL-SM/SM et s'applique à la quantification des isomères linéaires et ramifiés d'APFO et de SPFO. Il est possible de séparer les isomères linéaires des isomères ramifiés en faisant appel à une colonne chromatographique particulière ainsi qu'à des conditions optimisées. On considère que la méthode ISO 25101 est adaptée à la détermination des niveaux d'APFO dans des échantillons d'eau potable non filtrée, dans l'eau souterraine et l'eau de surface avec des concentrations variant de 10 à 10 000 ng/L (0,01 à 10 µg/L) (ISO, 2009).
La méthode ETS-8-154.3 a été conçue et validée par 3M aux fins d'analyse de l'APFO dans des échantillons d'eau potable, d'eau souterraine et d'eau de surface. Les étapes d'analyse sont semblables à celles de la méthode 537 Ver 1.1 de l'EPA, et la limite de quantification (LQ) de l'APFO est de 25 ng/L (0,025 µg/L) dans ce cas (3M, 2008).
6.2 Défis de l'analyse
Malgré les améliorations considérables des méthodes d'analyse permettant de déterminer la présence de SPFA dans les échantillons d'eau de l'environnement, des défis, des incertitudes et des inconvénients subsistent toujours. Les difficultés importantes liées à l'analyse quantitative des SPFA à l'état de trace ont trait aux effets de matrice ainsi qu'à une contamination de fond des blancs analytiques. Les procédures de contrôle de qualité (CQ) sont essentielles pour produire des données précises (échantillons de matrice enrichis, doublons, essais de récupération avec échantillons enrichis, vérification de récupération des substituts). En outre, l'utilisation d'étalons internes marqués par un isotope est une pratique courante qui doit être utilisée dans l'analyse des SPFA.
6.2.1 Les effets de matrice
Bien que la CL-SM/SM soit une technique extrêmement sélective et sensible, cette méthode est vulnérable aux effets de matrice qui constituent l'une des principales incertitudes relatives à la quantification de l'APFO dans les échantillons d'eau de l'environnement (Martin et coll., 2004; Yamashita et coll., 2004; Taniyasu et coll., 2005; van Leeuwen et coll., 2006; Arsenault et coll., 2008). Les effets de matrice découlent de composants coextraits à partir d'un échantillon et qui entravent l'intensité du signal de l'analyte ciblé en supprimant ou en renforçant le signal du spectre. L'étendue des effets perturbants de matrice varie selon la nature de l'échantillon. Bien que les effets de matrice soient négligeables pour l'eau potable et l'eau souterraine (ISO, 2009), la quantification de l'APFO nécessite des procédures efficaces d'extraction et de nettoyage. L'objet de ces procédures est de séparer les composants de l'échantillon selon leurs propriétés chimiques et physiques, de concentrer l'analyte ciblé et de purifier l'extrait avant de pouvoir faire la détermination fondamentale. La technique la plus fréquemment utilisée pour extraire les SPFA des échantillons d'eau potable fait intervenir des cartouches EPS avec différents remplissages telles que les cartouches en phase inverse (C18) (Loewen et coll., 2005; Wolf et Reagen, 2011; Zainuddin et coll., 2012), les cartouches mixtes hydrophobes/polaires (HLB Oasis) (Yamashita et coll., 2004; Taniyasu et coll., 2005; Villaverde-de-Saa et coll., 2015) et les cartouches à échangeur d'anions faible (WAX) (Taniyasy et coll., 2005; 2013). Plusieurs études ont eu recours à une extraction liquide-liquide (ELL) pour extraire et concentrer les SPFA dans diverses matrices aqueuses de l'environnement avant de procéder à une CL-SM/SM, (Gonzales-Barreiro et coll., 2006; Szostek et coll., 2006; Backe et coll., 2013). Une étude de laboratoire a fait appel à l'extraction liquide-liquide (ELL) pour extraire des SPFA (C6-C12) à partir de l'eau du robinet (Gonzales-Barreiro et coll., 2006). La récupération de SPFA dont la chaîne carbonée est supérieure à C8 était de l'ordre de 80 à 93 %. Les auteurs ont indiqué que cette méthode était moins efficace que la technique d'ELS pour extraire les SPFA à chaîne courte (Gonzales-Barreiro et coll., 2006).
La procédure de nettoyage comporte une étape de rinçage après l'enrichissement de l'échantillon avec une cartouche d'EPS et est suivie d'une étape de filtration pour éliminer les substances solides de l'extrait final (Yamashita et coll., 2004; Larsen et Kaiser, 2007; van Leeuwen et Boer, 2007). Il convient de faire preuve de minutie pour éviter de contaminer l'extrait ou de perdre des SPFA durant la procédure de nettoyage. Avant de procéder à une extraction en phase solide, un traitement préalable de l'échantillon (filtration) pourrait être nécessaire pour faciliter l'extraction ou éliminer les éléments de la matrice qui perturberont les analyses (van Leeuwen et Boer, 2007; Ding et coll., 2012).
Le recours aux étalons internes marqués d'un isotope (analyse par dilution isotopique) est la méthode qui convient le mieux pour contribuer à la quantification des SPFA. Il est important d'utiliser les étalons internes marqués qui sont adaptés au composé natif qu'on souhaite analyser quantitativement. Les étalons internes marqués d'un isotope ont le même temps de rétention que les analytes ciblés (sauf en cas de séparation isomérique), et la surveillance de leur signal déterminera si le signal des analytes est supprimé ou renforcé. L'application de substituts ou d'étalons internes marqués d'un isotope précocement durant l'échantillonnage ou les étapes de préparation des échantillons permet de compenser les manques d'efficacité ou pertes durant l'extraction et d'autres étapes de préparation des échantillons (Martin et coll., 2004; Villagrassa et coll., 2006; Larsen et Kaiser, 2007). Wolf et Reagen (2011) indiquent que l'ajout d'étalons internes marqués avant le prélèvement d'un échantillon simplifie la procédure de préparation connexe. La méthode présentait une exactitude de 105 % et une précision de 12 % pour l'analyse d'APFO en laboratoire avec des échantillons d'eau Milli-Q (Wolf et Reagen, 2012).
Si l'on ne dispose pas d'étalons internes marqués, l'analyse quantitative de l'étalon, qui consiste à étudier les quantités connues de l'étalon dans l'échantillon, est une méthode de rechange qu'il convient d'utiliser lorsque les effets de matrice sont inévitables (Weremiuk et coll., 2006; Furdui et coll., 2007; van Leeuwen et coll., 2009).
L'utilisation de la SM/SM pour analyser la présence d'APFO permet de détecter la présence d'ions dérivés (de filiation). Le passage d'un rapport m/z de 413 (ion parent C7H15COO-) à un rapport m/z de 369 et de 169 (ions dérivés) est utilisé aux fins d'analyse quantitative de l'APFO (ISO, 2009; U.S. EPA, 2009a).
6.2.2 La contamination de fond des blancs analytiques
La présence de polymères fluorés, tels que le polytétrafluoroéthylène (PTFE) et les composés perfluoroalkoxy dans divers consommables de laboratoire constituent une source connue de contamination de fond. Le perfluorooctanoate d'ammonium et le perfluorononanoate d'ammonium sont des polymères fluorés utilisés en tant qu'adjuvants et font partie des produits courants de laboratoire. Ces polymères fluorés pourraient être à l'origine de niveaux de fond quantifiables de blancs analytiques, surtout lorsqu'on doit faire l'analyse quantitative de niveaux de trace dans des échantillons d'eau. Il faudrait éviter le contact avec ce genre de matériaux et produits de laboratoire pendant l'analyse d'APFO (Martin et coll., 2004; Yamashita et coll., 2004; ISO, 2009).
Yamashita et coll. (2004) ont étudié les sources de contamination de fond à diverses étapes d'analyse comprenant le prélèvement d'échantillons, l'extraction et la purification de l'échantillon avant l'analyse fondamentale. On a découvert que les bouteilles de polypropylène utilisées pour le prélèvement et le stockage d'échantillons, en plus des différents types de cartouches EPS et des réactifs aqueux purifiés, sont des sources de contamination des blancs analytiques par des SPFA. Taniyasu et coll. (2005) et Berger et coll. (2011) ont découvert que les contenants en polypropylène sont impropres au prélèvement et au stockage d'échantillons d'eau destinés à l'analyse d'acides perfluorocaroxyliques à longue chaîne, tels que les acides perfluoroundécanoïques et perfluorododécanoïques, en raison de l'adsorption des composés présents à la surface des contenants. Les auteurs recommandent d'utiliser des contenants en polyéthylène à haute densité ou en verre. Néanmoins, la méthode ISO 25101 et la méthode 537 de l'EPA déconseillent l'utilisation d'instruments en verre aux fins d'échantillonnage en raison d'une adsorption possible d'APFO sur les parois des contenants (ISO, 2009; U.S. EPA, 2009a). Les étapes de stockage et de conservation des échantillons précédant l'analyse fondamentale devraient prévenir les changements touchant la composition de la matrice et la concentration de l'analyte (van Leeuwen et coll., 2007).
Puisque les cartouches d'EPS constituent également une source de contamination possible, l'EPA (2009a) recommande de vérifier les dispositifs d'EPS avant toute analyse pour s'assurer qu'il n'y a aucun risque de contamination de l'échantillon. Plusieurs études ont été menées sur l'injection directe (ID) d'échantillons d'eau dans la CL-SM/SM. La méthode évite le recours à d'autres matériaux ainsi qu'à des procédés additionnels de préparation des échantillons, ce qui pourrait limiter toute contamination et les pertes éventuelles de composés cibles (Schultz et coll., 2006; Furdui et coll., 2008; Dickenson et Higgins, 2013).
Les tubes CLHP, les filtres en nylon, les bouchons de flacon d'échantillonnage automatique fabriqués en Téflon ou en Viton avec fluoropolymères, les capuchons de valve et les dégazeurs ont été désignés comme sources potentielles de contamination des blancs analytiques en présence d'APFO (Yamashita et coll., 2004; Taniyasu et coll., 2005; Schultz et coll., 2006; Larsen et Kaiser, 2007) et, dans une moindre mesure, en présence de SPFO (Yamashita et coll., 2004). Il est possible de diminuer la contamination de fond des instruments en remplaçant ou en évitant les pièces en polymères fluorés telles que le dégazeur (Arbuckle et coll., 2013) et en ayant recours au dégazage autonome des phases mobiles; en remplaçant les composants en polymères fluorés par des tubes en acier inoxydable et en polyétheréthercétone (PEEK), en installant une colonne de garde en amont, en rinçant abondamment le système de CL ou en diminuant la durée d'équilibration de la colonne de CL (Martin et coll., 2004; Yamashita et coll., 2004; Villagrassa et coll., 2006; Larsen et Kaiser, 2007; Nakayama et coll., 2007; Shoemaker et coll., 2009; Arbuckle et coll., 2013).
6.3 Rendement analytique
Les analyses ont connu des améliorations récentes par la disponibilité et l'utilisation d'étalons de grande qualité et d'étalons internes à isotopes stables pour compenser l'effet de matrice ainsi que les insuffisances liées à la procédure d'extraction et/ou à d'autres étapes de préparation des échantillons (Yamashita et coll., 2004; Lowen et coll., 2005; Taniyasu et coll., 2005; Nakayama et coll., 2007; Zainuddin et coll., 2012; Villaverde-de-Saa et coll., 2015). Il existe, à l'heure actuelle, plusieurs étalons de grande qualité pour les analyses dans le commerce, et la liste de ces étalons continue de s'accroître (van Leeuwen et coll., 2009, Berger et coll., 2011).
Au début des années 2000, les analyses quantitatives des SPFA étaient faussées par l'absence d'étalons analytiques, de substituts isotopiquement marqués et de substances de référence, et il existait une variabilité importante d'un laboratoire à l'autre. Deux études interlaboratoires réalisées pour analyser la présence de SPFA, y compris l'APFO et le SPFO dans des échantillons d'eau de l'environnement, ont mis en évidence un degré de précision variable. Dans la première étude réalisée entre 2004 et 2005 (van Leeuwen et coll., 2006), il s'avère que les facteurs ayant entraîné une faible concordance entre les laboratoires participants étaient les faibles concentrations d'APFO et de SPFO (inférieures à 20 ng/L) dans les échantillons d'eau; les normes de pureté peu élevées, l'effet de matrice élevé, et une forte contamination de fond des blancs analytiques. L'écart-type relatif (ETR) annoncé à la fin de l'étude était de 118 % pour l'APFO (van Leeuwen et coll., 2006). Dans la deuxième étude, les résultats obtenus par les laboratoires participants se sont améliorés grâce à l'atténuation des effets de matrice; à des normes de qualité communes plus élevées (pureté et composition isométrique) fournies par une seule source, et à l'utilisation d'étalons internes marqués en fonction de la masse. L'ETR déclaré à l'issue de cette étude était de 32 % pour l'APFO.
Les publications scientifiques font état de méthodes ayant recours à des procédures d'EPS et d'injection directe (DI) suivies d'une chromatographie en phase liquide couplée à la spectrométrie de masse en tandem avec ionisation par électronébulisation pour détecter la présence d'acides perfluoroalkyliques, y compris le SPFO dans les échantillons d'eau (Yamashita et coll., 2004; 2005; Taniyasu et coll., 2005; 2013; Furdui et coll., 2008; Hansen et coll., 2010; Berryman et coll., 2012; Zainuddin et coll., 2012; Villaverde-de-Saa et coll., 2015). Les détails concernant la procédure de préconditionnement des cartouches d'EPS, l'éluant, la procédure de nettoyage, les paramètres de quantifications de la SM et la procédure de contrôle de la qualité se rapportant à chaque méthode sont décrits dans les références précitées.
Une étude faisait état d'une limite de détection (LD) (rapport signal-bruit [S/B] = 3:1) de 0,28 ng/L et d'une LQ (S/B = 10:1) de 0,94 ng/L à l'aide d'une extraction en phase solide suivie d'une CL-SM/SM pour analyser l'APFO dans l'eau de surface. Un échantillon d'eau de 500 mL a été chargé dans une cartouche Oasis à échangeur d'anions faible, une portion de l'analyte cible a été éluée, séchée à l'azote gazeux et les échantillons ont été filtrés avant l'analyse. La valeur de récupération de 115 ± 6 % pour l'APFO a été calculée à l'aide d'étalons internes marqués d'un isotope (Sun et coll., 2011; Li et coll., 2011).
À l'aide d'une extraction en phase solide suivie d'une CL-SM/SM, Villaverde-de-Saa et coll. (2015) ont élaboré une méthode permettant de désigner sept APFC (C6-C12) et SPFO dans des échantillons d'eau de l'environnement. Un échantillon d'un litre d'eau, fortifié avec des étalons internes, a été chargé dans une cartouche Oasis HLB. La méthode indiquait une LD de 0,03 ng/L et une LQ de 0,11 ng/L pour l'APFO, (la LD et la LQ représentaient respectivement 3 fois et 10 fois l'écart-type). La valeur de récupération de 89 ± 4 % pour l'APFO a été calculée à l'aide d'étalons internes marqués d'un isotope.
Furdui et coll. (2008) ont étudié la concentration de SPFA dans des échantillons d'eau prélevés dans les Grands Lacs. L'analyse de neuf contaminants cibles, y compris l'APFO, a été effectuée en injectant les échantillons directement dans une CL-SM/SM. L'analyse quantitative a été réalisée en faisant appel à la correction des étalons internes et à la méthode des additions connues. Une dilution isotopique donne les résultats les plus exacts et les plus précis. La méthode présentait une LQ (signal-bruit = 10:1) de 0,5 ng/L pour l'APFO (Furdui et coll., 2008).
La province du Québec a annoncé les résultats de surveillance des SPFA dans 16 sites comportant notamment sept usines de traitement de l'eau potable. Au total, 226 échantillons (84 échantillons d'eau brute, 84 échantillons d'eau traitée et 58 échantillons d'eau de surface) ont été analysés. Des échantillons d'eau brute et d'eau traitée ont été prélevés chaque mois sur une période d'un an. L'échantillonnage d'eau de surface a été limité durant l'année. Les échantillons ont été analysés à l'aide de cartouches C18 et d'une CL-SM/SM en mode d'ionisation positive. Les limites de détection annoncées allaient de 0,5 à1 ng/L pour un échantillon de 250 mL d'eau non traitée, et de 0,3 à 0,6 ng/L pour 500 mL d'eau traitée. Afin de compenser et de corriger les variations liées aux instruments et aux effets de matrice, des étalons internes marqués d'un isotope ont été ajoutés avant la CL (Berryman et coll., 2012). Bien que la technique de photo-ionisation soit moins sensible que l'ionisation par électronébulisation, celle-ci est moins exposée aux effets de matrice (Martin et coll., 2004).
Berger et coll. (2004) ont comparé différentes techniques de spectroscopie de masse (SM haute résolution à temps de vol, SM en tandem de type triple quadripôle et la SM de type trappe ionique) combinées avec une chromatographie liquide à haute performance (CLHP) pour l'analyse de SPFA, y compris l'APFO. Les paramètres d'instruments tels que la température du nébuliseur, l'énergie de collision et la fragmentation du voltage des cônes ont été optimisés pour chaque technique de spectrométrie de masse. Le mode d'ionisation par électronébulisation négatif a été choisi pour tous les instruments. L'étude indique que les techniques de SM haute résolution à temps de vol et de SM en tandem triple quadripôle présentaient toutes les deux une sensibilité plus élevée que la SM de type trappe ionique pour l'ensemble des SPFO mis à l'essai. Bien que la SM de type trappe ionique présente une limite de détection supérieure et une gamme linéaire plus étroite, elle donne de meilleurs résultats pour la détermination expérimentale de la structure et l'analyse qualitative des isomères ramifiés de SPFA (Berger et coll., 2004; Jahnke et Berger, 2009).
L'analyse de composés SPFA dans les échantillons d'eau de l'environnement a été dominée par l'utilisation de la CL couplée à la SM ou la SM/SM, même si d'autres techniques telles que la résonance magnétique nucléaire (RMN) 19F et la chromatographie gazeuse (CG-SM) ont aussi été envisagées. L'analyse par RMN 19F est une méthode moins sensible et non spécifique en raison de la présence avérée de groupes de CF2 et de CF3 dans l'échantillon. Il est possible d'utiliser la chromatographie gazeuse (CG) pour déterminer la présence de SPFA neutres et volatiles ainsi que la présence d'alcools fluorotélomères. Des alkyles perfluorés sont produits par dérivation de manière à se prêter à l'analyse par CG. Néanmoins, l'utilisation des techniques de dérivatisation est limitée dans le cas de l'analyse des SPFA en raison de l'instabilité des composés qui en dérivent (Moody et coll., 2001; Villagrassa et coll., 2006).
7.0 Techniques de traitement
Les données disponibles et les valeurs de pKa calculées (2,8) indiquent que l'APFO est un acide fort qui se dissocie principalement en une forme chargée négativement (anion) à des pH enregistrés dans l'environnement (U.S. EPA, 2005; Lange et coll., 2006; Prevedouros et coll., 2006). Compte tenu des propriétés physico chimiques de la forme ionisée (pression de vapeur négligeable, solubilité élevée dans l'eau et sorption modérée par les matières solides), Prevedouros et coll. (2006) laissent entendre que l'APFO aurait une propension à s'accumuler à la surface de l'eau. Étant donné la nature hydrophobe et oléophobe de la chaîne d'alkyles fluorés et la nature hydrophile du groupe carboxylate, les effets hydrophobes et électrostatiques influencent probablement l'adsorption de l'APFO (Higgins et Luthy, 2006; Xiao et coll., 2011). La nature de la structure chimique de l'APFO (solides liaisons carbone-fluor (C-F)) rend cette substance résistante à l'hydrolyse et à la biodégradation ainsi qu'à plusieurs procédés de traitement chimique (Lange et coll., 2006; ATSDR, 2009).
7.1 Échelle municipale
Dickenson et Higgins (2013) ont évalué la capacité de toute une série de traitements à échelle réelle afin d'éliminer les SPFA, y compris l'APFO et le SPFO, dans les usines de réutilisation de l'eau brute ou de l'eau potable. Les chaînes de traitement variaient, mais comportaient généralement une coagulation suivie d'une séparation physique, d'une aération, d'une oxydation chimique, d'une irradiation aux rayons UV et d'une désinfection. Peu importe la chaîne de traitement appliquée, il y a eu peu, voire aucune diminution des concentrations d'APFO et de SPFO, ce qui a mené les auteurs à conclure que ces traitements constituent des méthodes inefficaces pour éliminer les SPFA.
Les techniques d'adsorption sur CAG et de filtration sur membrane semblent prometteuses pour éliminer l'APFO dans l'eau potable, car celles-ci permettent d'obtenir des concentrations inférieures à 0,2 µg/L dans l'eau traitée (Tang et coll., 2006; Lampert et coll., 2007; Wilhem et coll., 2008; Deng et coll., 2010; Takagi et coll., 2011; Appleman et coll., 2014). Afin d'atteindre une concentration d'APFO inférieure à 0,2 µg/L, le système de CAG doit être spécialement conçu et convenablement utilisé pour éliminer l'APFO dans l'eau potable. Les matières organiques naturelles (MON) présentes dans la source d'eau sont susceptibles de détériorer le rendement du CAG car ils sont en concurrence pour les sites d'adsorption et préchargent (souillent) les lits de CAG. Par conséquent, la capacité du CAG à éliminer efficacement l'APFO de l'eau potable dépend apparemment de la fréquence de régénération et/ou de remplacement du charbon (Kolstad 2010; Takagi et coll., 2011; Appleman et coll., 2014). Les études concernant les techniques de filtration sur membrane telles que l'osmose inverse (OI) et la nanofiltration (NF) à l'échelle de banc d'essai ont mis en évidence une élimination efficace de tous les SPFA à chaîne courte ou à chaîne longue mis à l'essai dans l'eau potable, y compris l'APFO. Bien que le procédé d'OI soit efficace, cette méthode de traitement a tendance à coûter cher (Steinle-Darling et coll., 2008); Quinones et Snyder, 2009; Appleman et coll., 2013; Flores et coll., 2013). Les résines échangeuses d'anions peuvent s'avérer efficaces pour éliminer l'APFO. Cependant, une évaluation complète de cette technique n'a pas encore été mise en œuvre pour l'élimination de l'APFO dans l'eau potable.
Le choix et l'efficacité d'une stratégie de traitement sont déterminés par plusieurs facteurs tels que la composition chimique de la source d'eau, la concentration d'APFO et/ou de la présence d'autres substances perfluoroalkyliques ainsi que l'existence préalable d'un procédé de traitement. Si des SPFA à chaîne longue sont détectés dans des sources d'eau potable, le service public pourrait envisager de mettre en œuvre des techniques de traitement telles que la CAG. Par contre, les services publics en présence de SPFA à chaîne courte dans leur eau brute pourraient plutôt choisir de mettre en œuvre une technique fondée sur l'OI ou la NF. Les techniques de traitement doivent être conçues spécialement pour éliminer les SPFA et doivent être utilisées convenablement pour atteindre les objectifs d'élimination des contaminants dans l'eau potable (Dickenson et Higgins, 2013).
Dickenson et Higgins (2013) et Rahman et coll. (2014) ont résumé la capacité d'élimination du SPFO dans l'eau potable par divers procédés et diverses chaînes de traitement.
L'annexe A présente une synthèse des taux d'élimination de l'APFO dans des usines pleine grandeur, avec indication des concentrations dans l'eau brute et l'eau traitée (Rahman et coll., 2014). Les données montrent que les techniques de traitement utilisées dans ces usines (exception faite pour le CAG, l'OI et la NF) n'ont pas réussi à éliminer l'APFO de manière appréciable. Elles montrent aussi que dans certains cas, les concentrations dans l'eau traitée étaient plus élevées que celles enregistrées dans l'eau brute, probablement en raison des composés précurseurs qui se dégradaient pour former de l'APFO en cours de traitement (Takagi et coll., 2008; Shivakoti et coll., 2010). Takagi et coll. (2011) postulent également que ces niveaux supérieurs relevés dans l'eau traitée pourraient provenir d'une désorption des filtres CAG utilisés sur de longues périodes sans réactivation et du lessivage de ces composés à partir des matériaux de traitement recouverts de Téflon.
7.1.1 Traitement conventionnel
Les procédés conventionnels de traitement de l'eau potable intègrent généralement la coagulation, la floculation, la sédimentation et la filtration, le tout suivi par une désinfection primaire et secondaire. Les coagulants couramment utilisés dans l'eau potable incluent le sulfate d'aluminium, l'hydroxyde de fer, le chlorure de fer, le chlorure de polyaluminium et des polymères adjuvants de floculation. Les matériaux de filtration peuvent comprendre le sable (matériau unique); le sable et l'anthracite (matériau double); ou le sable, l'anthracite et le grenat filtration sur lit mélangé ou lits multicouches). Le CAG peut aussi servir de matériau filtrant.
On a constaté que les techniques traditionnelles et à pleine échelle de traitement de l'eau sont inefficaces pour éliminer l'APFO dans les sources d'eau. Des échantillons prélevés dans plusieurs usines de traitement pleine grandeur et traditionnelles montrent qu'il n'existe essentiellement aucune différence entre les concentrations d'APFO relevées dans les affluents d'usine et celles observées dans l'eau après les étapes de coagulation, de sédimentation et de filtration sur sable (Loos et coll., 2007; Shivakoti et coll., 2009; Takagi et coll., 2011; Thompson et coll., 2011). De la même façon, Eschauzier et coll. (2012) ont indiqué que les filtrations lentes et rapides sur sable étaient inefficaces pour éliminer le SPFO et l'APFO. L'incapacité d'éliminer l'APFO et le SPFO à l'aide des traitements de l'eau traditionnels pourrait s'expliquer par la très faible concentration de ces composés dans l'eau et leur nature hydrophile qui rend leur élimination difficile par les procédés traditionnels (Rahman et coll., 2014). Ces observations concordent avec des études de laboratoire menées récemment dans le but d'éliminer l'APFO dans l'eau (Deng et coll., 2011; Xiao et coll., 2013).
Des essais de floculation (Xiao et coll., 2013) ont permis d'obtenir un taux d'élimination d'environ 3 % d'APFO dans l'eau d'arrivée avec une concentration de 0,083 µg/L (83 ng/L) d'APFO, une dose de 30 mg/L de sulfate d'aluminium et un pH de 7,9. Une efficacité d'élimination inférieure à 10 % a été déclarée avec des doses de sulfate d'aluminium allant de10 à 60 mg/L et un pH variant entre 6,5 et 8. Des taux d'élimination d'environ 25 % ont été observés à l'aide d'une coagulation accrue faisant appel à des doses de sulfate d'aluminium supérieures à 60 mg/L ainsi qu'à un pH variant entre 4,5 et 6,5. En général, l'efficacité d'élimination restait inférieure à 35 % dans les conditions de coagulation examinées (doses de sulfate d'aluminium allant de 3 à 110 mg/L et pH variant entre 4,5 et 8). La coagulation par ajout de chlorure de fer a donné des résultats semblables. Les auteurs indiquent que les taux d'élimination de l'APFO sont plus faibles que ceux du SPFO dans des conditions de coagulation usuelles ou améliorées, sans doute parce que l'APFO a une taille moléculaire moins grande et que cette substance a tendance à être moins hydrophobe.
Néanmoins, Deng et coll. (2011) ont démontré que l'ajout de charbon actif en poudre (CAP) avant le processus de coagulation permet d'améliorer l'efficacité d'élimination de l'APFO dans l'eau. Dans les expériences qui ont été réalisées, la concentration d'APFO qui était de 21,2 µg/L initialement a été ramenée à 5,8 µg/L par l'ajout d'une dose de 10 mg/L de chlorure de polyaluminium (CPA). Une concentration inférieure à 1 µg/L a été mesurée dans l'eau traitée après l'ajout de 10 mg/L de CPA et des doses de CAP allant jusqu'à 16 mg/L à des concentrations initiales d'APFO allant de 0,5 à 3 mg/L. L'étude a permis de constater que la concentration d'APFO dans l'eau traitée diminue en augmentant la turbidité initiale et la dose de CPA, alors qu'elle augmentait avec une hausse du pH ou de la température.
7.1.2 Adsorption
Les adsorbants ordinairement utilisés dans les traitements d'eau potable comprennent le charbon activé, l'alumine activée, les zéolites, l'argile, les oxydes métalliques, les hydroxydes et les carbonates (AWWA, 2011; U.S. EPA, 2012). Le CAG est utilisé dans un lit fixe, tandis que le CAP est, en général, ajouté directement à l'eau brute sous forme de poudre ou mélangée à l'eau brute pour former une bouillie.
Plusieurs études de laboratoire portant sur la cinétique d'adsorption de l'APFO et du SPFO indiquent que le CAP atteint un équilibre de sorption au bout de quatre heures comparativement à 168 heures pour le CAG, (Yu et coll., 2009), et que les pourcentages d'élimination des SPFA étaient généralement plus élevés avec le CAP qu'avec CAG (de 60 à 90 % contre 20 à 40 %, respectivement), pour un temps d'adsorption de10 minutes (Hansen et coll., 2010). Ces résultats s'expliquent probablement par la plus petite taille des particules de CAP et la plus grande surface spécifique par volume de charbon comparativement au CAG (Yu et coll., 2009; Hansen et coll., 2010). Si des SPFA sont présentes dans l'eau brute tout au long de l'année, Rahman et coll. (2014) suggèrent de privilégier la méthode d'adsorption sur CAG pour l'élimination de ces substances, le CAP étant mieux adapté aux remédiations à court terme en cas de déversement.
7.1.2.1 CAG
Des évaluations à pleine échelle de l'efficacité de l'adsorption du CAG pour éliminer l'APFO dans des sources d'eau potable ont donné des résultats mitigés. Plusieurs études détaillées à échelle réelle, spécialement conçues et mises en pratique pour éliminer les SPFA dans l'eau potable, ont permis d'obtenir une élimination fructueuse de l'APFO par le CAG avec un temps de contact en fût vide (TCFV) prolongé et un régime de régénération approprié (MDH, 2008a; Wilhem et coll., 2008; Rumsby et coll., 2009; Little Hocking Water Association, 2010; Appleman et coll., 2014). D'autres usines de traitement de l'eau ont obtenu des niveaux semblables d'APFO dans l'eau d'arrivée et l'eau traitée, ce qui semble indiquer que le CAG ne parvient à éliminer ce contaminant de façon partielle ou même pas du tout. Ces usines de traitement n'étaient pas spécialement conçues pour éliminer les SPFA de l'eau potable. Étant donné que le CAG était en place sur diverses périodes de temps, il est probable qu'un préchargement comportant des matières organiques naturelles (MON) a détérioré le rendement du CAG, entraînant ainsi un niveau semblable d'APFO dans l'eau d'arrivée et dans l'eau traitée (Shivakoti et coll., 2010; Takagi et coll., 2011; Eschauzier et coll., 2012, Flores et coll., 2013).
Un traitement à échelle réelle au CAG avec un débit de 1,5 m3/minute a spécialement été conçu pour éliminer les SPFA dans l'eau souterraine. Le système faisait appel à deux contacteurs à CAG en configuration principale/secondaire avec un TCFV de 13 minutes chacun. Le récipient principal a fonctionné pendant 10 mois environ et a traité 30 129 volumes de lit (VL) avant que la concentration d'APFO ne dépasse 0,05 µg/L. Le système de CAG a fait diminuer l'APFO dont la concentration dans l'eau d'arrivée était de l'ordre de 0,45 à 0,83 µg/L pour la ramener à une valeur inférieure à 0,05 µg/L dans l'eau traitée sortant du récipient secondaire, à raison de 72 775 VL (22 mois environ). À ce stade, l'eau du récipient principal atteignait 0,25 µg/L d'APFO, son charbon a été remplacé par un milieu vierge et le récipient a été placé en position secondaire (Appleman et coll., 2014). Un autre système de traitement à échelle réelle de 400 gpm (1,5 m3/minute) sur CAG s'est montré efficace pour éliminer l'APFO dans l'eau de surface, celui-ci étant parvenu à ramener la concentration de 0,9 μg/L dans l'eau d'arrivée jusqu'en dessous de la limite de détection de 0,01 µg/L dans l'eau traitée. Une hausse de la concentration d'APFO dans l'eau traitée a été observée après trois mois environ, avec des niveaux dépassant l'objectif de 0,1 μg/L dans l'eau traitée après cinq mois de fonctionnement (Wilhelm et coll., 2008; Rumsby et coll., 2009).
Le comportement et le devenir des SPFA, y compris l'APFO et le SPFO, ont été évalués par l'analyse de l'eau d'arrivée et de l'eau traitée prélevée à partir de plusieurs usines de traitement qui comportaient du CAG dans la chaîne de traitement. Ces usines de traitement n'étaient pas spécialement conçues pour éliminer les SPFA de l'eau potable. Le temps de rétention hydraulique a été pris en considération au moment d'évaluer l'efficacité de chacune des étapes de traitement (Shivakoti et coll., 2010; Takagi et coll., 2011; Eschauzier et coll., 2012; Flores et coll., 2013). Les études ont conclu que seule l'étape au CAG a été en mesure d'éliminer les SPFA dans l'eau potable. On fait état d'une élimination d'environ 50 % d'APFO lorsque la chaîne de traitement comportait un procédé de CAG (Eschauzier et coll., 2012; Flores et coll., 2013). Les paragraphes ci-dessous fournissent des renseignements plus détaillés sur certaines de ces études.
Une usine pleine grandeur traitant cinq millions de gallons par jour (MG/J), conçue pour éliminer les traces (ng/L) de contaminants organiques dans l'eau de surface, faisait appel à la filtration par les berges, à l'adoucissement, à l'oxydation avancée UV/H2O2, ainsi qu'à une filtration sur CAG biologiquement active et composée de six contacteurs. Le système de CAG fonctionnait en mode parallèle avec un TCFV de 10,5 minutes. L'analyse d'échantillons d'eau prélevés avant et après la filtration sur système de CAG a mis en évidence une diminution d'APFO dont la concentration est passée de 9,7 ng/L à une valeur inférieure à 5 ng/L (Appleman et coll., 2014).
Eschauzier et coll. (2012) ont surveillé les concentrations d'APFO et du SPFO dans une chaîne de traitement de l'eau potable faisant appel à la coagulation, à la filtration rapide sur sable, au passage à travers une dune, à l'adoucissement, à l'ozonisation et au traitement sur CAG. Seule l'étape du CAG a permis d'éliminer efficacement les SPFA. Le système à deux étages était constitué de contacteurs montés en configuration principale/secondaire. Sur les 40 filtres utilisés au total, 20 étaient montés en parallèle pour le premier étage, tandis que les 20 autres servaient au deuxième étage de filtration. Chaque filtre au CAG fonctionnait avec un débit de 348 m3/heure et un TCFV de 20 minutes, ce qui a permis d'obtenir un TCFV de 40 minutes au total. Des filtres au CAG vierges ont été installés au deuxième étage filtrant avant d'être transférés au premier étage au bout de 15 mois de fonctionnement. Après 15 mois additionnels, le charbon a été réactivé et remis en service comme filtre de deuxième étage. Le premier étage du système au CAG a permis d'obtenir une diminution d'environ 50 % de l'APFO dont la concentration moyenne était de 8,8 ng/L dans l'eau d'alimentation (Eschauzier et coll., 2012). Flores et coll. (2013) annoncent des résultats similaires (45 % d'élimination d'APFO) dans une usine de traitement de l'eau composée de 24 connecteurs au CAG régénéré une fois par an.
Takagi et coll. (2008, 2011) ont étudié le comportement, le devenir et l'efficacité d'élimination de l'APFO et du SPFO dans les procédés utilisés par plusieurs usines de traitement de l'eau potable comportant un système au CAG dans la chaîne de traitement. L'efficacité d'élimination de l'APFO et du SPFO était inférieure à 50 % pour de nombreuses usines de traitement. Le taux d'élimination négatif relevé dans certaines usines semble indiquer que la désorption produite par les filtres au CAG utilisés sur de longues périodes sans réactivation pourrait expliquer ces observations. Ces résultats négatifs pourraient aussi provenir de la formation d'APFO et du SPFO à partir de la dégradation de composés précurseurs présents dans l'eau brute (Takagi et coll., 2011). Par contre, une élimination d'APFO supérieure à 90 % a été observée pendant quatre mois dans une usine traitant 1,5 million de litres/jour après le remplacement du charbon dans le système au CAG. La chaîne de traitement faisait appel à la coagulation/sédimentation, à la filtration rapide sur sable et à deux contacteurs au CAG (charbon et coque de noix de coco) fonctionnant en mode parallèle. Pendant quatre mois, les deux contacteurs au CAG ont permis de diminuer les concentrations d'APFO, de l'ordre de 25 à 44 ng/L dans l'eau brute, sous la LQ de 0,7 ng/L. La concentration d'APFO dans l'eau filtrée au CAG a progressivement augmenté jusqu'à 13 ng/L au terme des huit mois de l'étude (Takagi et coll., 2011).
Les essais RSSCT (Rapid small-scale column tests) sont couramment utilisés à l'échelle du laboratoire pour évaluer le CAG. Appleman et coll. (2013) ont utilisé cette méthode pour comparer l'efficacité de trois différents types de CAG dans l'élimination de plusieurs SPFA, y compris l'APFO et le SPFO. Les expériences en colonne ont été réalisées avec un TCFV de 38 minutes faisant appel à de l'eau désionisée et à de l'eau de surface [1,7 mg/L carbone organique dissous (COD)], en ajoutant 1 µg/L de SPFA dans les deux cas. Les essais se sont déroulés sur 33 jours environ, à raison de 125 000 VL au total. Le rendement a varié selon le type de charbon utilisé et la chimie de l'eau, le CAG réussissant mieux à éliminer les SPFA dans l'eau désionisée. Sur les trois types de charbon utilisés, c'est le F300 qui a obtenu les meilleurs résultats. Dans les expériences menées avec de l'eau désionisée, une concentration supérieure à 0,02 µg/L d'APFO (la concentration de C0 étant de 2 % dans l'eau d'arrivée) a été observée dans 30 000 VL environ (soit une durée de 8 jours), tandis qu'une concentration d'eau filtrée de 0,05 µg/L (5 % of C0) a été mesurée après 56 000 VL. Néanmoins, la concentration dans l'eau filtrée a atteint 0,2 µg/L (20 % of C0) après 11 000 VL (durée de 3 jours), tandis qu'un progrès décisif (100 %) a été observé au bout de 26 000 VL d'eau de surface dopée. Bien que les essais RSSCT ne conviennent pas pour évaluer les effets d'un préchargement/encrassement des colonnes de CAG par le COD, les progrès décisifs et rapides obtenus avec de l'eau naturelle dopée démontrent que le COD entrave le rendement du CAG, car il est en concurrence directe avec les SPFA pour l'adsorption par le CAG (Appleman et coll., 2013).
L'efficacité d'élimination de l'APFO par le CAG est entravée par la présence de matières organiques naturelles (MON) dans la source d'eau, car celles-ci entrent en concurrence sur le site d'adsorption sur charbon et sont adsorbées de manière irréversible, ce qui entraîne une diminution de la capacité d'adsorption du composé cible. Lorsque la capacité d'adsorption du CAG est épuisée, celui-ci doit être retiré du contacteur et remplacé par du charbon neuf ou réactivé. On peut utiliser le CAG dans un réacteur à lit fixe, en tant que produit de remplacement d'un matériau filtrant existant (tel que le sable), à l'intérieur d'un filtre conventionnel, comme l'un des constituants d'un filtre rapide multicouches, ou dans un contacteur séparé. Le réacteur peut être situé au début de la chaîne de traitement dans un filtre à double couche ou en remplacement du sable, ou plus tard au cours du traitement en tant que contacteur de deuxième étage. La vitesse d'épuisement du CAG varie considérablement pour la même source d'eau selon la configuration du CAG employée. On utilise un filtre à double couche (CAG et sable) pour éliminer la turbidité et lorsque l'adsorption et l'élimination de contaminants sont combinées dans un procédé faisant intervenir un seul appareil. Le filtre à double couche (généralement situé après l'étape de sédimentation) est susceptible d'être exposé à des concentrations de COD plus élevées, ce qui entraîne un épuisement plus rapide du filtre. Un contacteur au CAG situé à la fin d'une chaîne de traitement sera moins vulnérable au préchargement ou à l'encrassement, étant donné que les étapes de traitement précédant le contacteur à CAG permettront de diminuer les concentrations de COD dans l'eau d'arrivée. Des contacteurs à CAG montés en configuration principale/secondaire permettent d'atteindre une concentration d'APFO inférieure à 0,2 µg/L dans l'eau traitée (Appleman et coll., 2014; Little Hocking Water Association, 2010). Cette stratégie de traitement contribuera à utiliser CAG au maximum de sa capacité et à réduire les coûts de fonctionnement (c.-à-d. le coût de remplacement du charbon) (Crittenden et coll., 2012).
Une surveillance étroite de toute diminution radicale de l'APFO (objectif de traitement) est nécessaire pour permettre au système de CAG de fonctionner efficacement. Les études indiquent qu'on réussit à éliminer l'APFO de l'eau potable lorsque le CAG est régénéré ou remplacé fréquemment (tous les 3 à 6 mois) (Wilhelm et coll., 2008; Rumsby et coll., 2009; Takagi et coll., 2011). Takagi et coll. (2011) ont observé que s'il est régénéré après une période supérieure à un an, le CAG ne parvient plus à éliminer efficacement l'APFO et le SPFO, et suggèrent par conséquent de régénérer le charbon deux ou trois fois par an. Un remplacement du CAG tous les trois mois environ a été nécessaire pour réduire la concentration d'APFO à une valeur inférieure à 0,004 µg/L dans un système où les concentrations de cette substance dans l'eau d'arrivée variaient entre 1,9 et 15 µg/L (Little Hocking Water Association, 2010). Une usine de traitement pleinement opérationnelle de 2 500 gpm qui faisait appel à deux contacteurs au CAG montés en série a permis une diminution radicale de l'APFO et du SPFO après 286 et 550 jours respectivement. Lorsqu'on a remplacé le CAG aussitôt après l'élimination de l'APFO, le système a permis de traiter 1,9 million de gallons d'eau pendant 23 mois (MDH, 2008a; Kolstad, 2010).
Eschauzier et coll. (2012) ont observé que l'efficacité d'élimination des SPFA par le CAG augmente proportionnellement à la chaîne carbonée et que les composés de sulfonate sont éliminés sur une période plus longue que les composés de carboxylate. Par contre, les SPFA à chaîne courte (surtout l'acide perfuorobutanoïque [APFB] et le sulfonate de perfluorobutane [SPFB]) ne sont pas éliminés par le CAG. Ces observations concordent avec des lots d'essais effectués antérieurement qui indiquaient que la sorption de SPFA sur charbon activé diminuait proportionnellement à la longueur de la chaîne carbonée et que l'adsorption des perfluorosulfonates est plus importante que les perfluorocarboxylates dont la longueur de la chaîne carbonée est identique (Ochoa-Herrera et Sierra-Alvarez, 2008; Hansen et coll., 2010; Dudley et coll., 2012; Appleman et coll., 2014). On a découvert que le pouvoir de sorption du CAG est supérieur pour les isomères linéaires que pour les isomères ramifiés de SPFO et d'APFO. La désorption des chaînes courtes de SPFA, causée par la concurrence avec les SPFA à chaîne longue ou la MON (tels que le COD) pour les sites de sorption, peut entraîner une présence accrue de SPFA à chaîne courte dans l'eau traitée (Eschauzier et coll. (2012).
7.1.2.2 CAP
Aucune donnée d'études à pleine échelle ne mentionne l'efficacité d'élimination de l'APFO par le charbon actif en poudre (CAP). La plupart des études publiées sur l'efficacité du CAP ont été effectuées en laboratoire. Dans certaines de ces études de laboratoire, les concentrations d'APFO étaient, en ordre de grandeur, plus élevées que celles observées dans les eaux naturelles. Néanmoins, les tendances observées pour le CAP en matière d'adsorption préférentielle (selon la longueur de la chaîne carbonée) et de concurrence avec les matières organiques naturelles (MON) sont semblables à celles observées pour le CAG (Hansen et coll., 2010; Dudley et coll., 2012).
Dudley et coll. (2012) ont évalué la capacité d'adsorption de dix SFPA de chaîne carbonée à longueur variable (de C4 à C10) avec du CAP disponible dans le commerce (coquille de noix de coco, lignite, bois et charbon bitumineux) et du CAP superfin (CAP-S) obtenu par concassage humide du CAP commercial. On a découvert que les substances à base de sulfonate étaient plus adsorbables que celles à base de carboxylate et que la cinétique de sorption était plus élevée avec le CAP-S qu'avec le CAP commercial. L'efficacité d'élimination des APFA augmente avec l'allongement de la chaîne carbonée (élimination négligeable des composés C4, mais élimination supérieure à 90 % pour les composés C7 à C10). Des études de lot ont permis de constater que la présence de MON diminue l'efficacité d'élimination des SPFA. Les auteurs concluent en outre qu'il est difficile d'éliminer les SPFA à chaîne courte de manière appréciable avec des doses raisonnables de CAP (Dudley et coll., 2012).
Yu et coll. (2009) ont étudié la cinétique et les isothermes de sorption de l'APFO et du SPFO sur du CAP, du CAG et une résine échangeuse d'anions. C'est la résine échangeuse d'anions qui a présenté la plus grande capacité de sorption de l'APFO, tandis que le CAP s'est avéré le matériau adsorbant à privilégier pour le SPFO. Une autre expérience de laboratoire a montré que le CAP et le CAG ont réussi à éliminer respectivement 88 % et 25 % de l'APFO, compte tenu d'une concentration initiale de 1,4 µg/L dans l'eau souterraine. La même étude a aussi permis d'observer que la sorption du SPFO était plus rapide sur le CAP que sur le CAG, ce qui semble indiquer que la taille du charbon activé a une influence sur la cinétique de sorption (Hansen et coll., 2010). Qu et coll. (2009) déduisent qu'il serait possible d'utiliser le CAP en tant que matériau pour éliminer efficacement l'APFO de l'eau, car la capacité d'élimination a augmenté de 51,1 % à 99,9 % lorsqu'on augmentait les doses de CAP de 0,1 à 10 g/L (la concentration initiale d'APFO étant de 20 mg/L).
7.1.3 Filtration sur membrane
Il existe quatre procédés de filtration sur membrane applicables au traitement de l'eau potable : la microfiltration (MF), l'ultrafiltration (UF), la nanofiltration et l'osmose inverse. Les membranes à faible pression telles que les membranes de MF et d'UF ne sont pas en mesure de rejeter les SPFA étant donné que leurs pores sont plus larges que le diamètre réel des molécules constituant ces substances (~1 nm) (Tsai et coll., 2010; Rahman et coll., 2014). Des études de laboratoire indiquent que le seuil de rétention des molécules des membranes de NF et d'OI constitue probablement le facteur le plus important dans l'élimination des SPFA. En général, les membranes de NF présentent un taux de rejet (95 %) inférieur à celui des membranes d'OI (supérieur à 99 %), ce qui correspond bien au fait que les membranes de NF ont des pores plus grands (Tang et coll., 2006, 2007; Steinle-Darling et Reinhard, 2008; Lipp et coll., 2010; Appleman et coll., 2013; Rahman et coll., 2014).
Les données scientifiques disponibles sur l'élimination de l'APFO et du SPFO dans les sources d'eau potable par la filtration sur membrane sont limitées à une installation d'eau potable faisant appel à l'OI (Flores et coll., 2013) et à plusieurs usines de réutilisation indirecte de l'eau potable (Quinones et Snyder, 2009; Appleman et coll., 2014). En raison de l'emplacement physique de ce type d'usines, on considère qu'elles pourraient avoir contribué grandement à la source d'eau utilisée par les installations de production d'eau potable ayant fait l'objet des études (Quinones et Snyder, 2009).
Même si un traitement conventionnel à échelle réelle s'est avéré inefficace pour éliminer l'APFO dans l'eau de surface, le taux d'élimination a atteint 92 % lorsque le processus de traitement conventionnel était suivi d'une OI (Flores et coll., 2013). L'eau d'alimentation du système d'OI était d'abord filtrée par un procédé de traitement conventionnel, puis mélangée à de l'eau souterraine. Lorsque la concentration d'APFO dans l'eau d'alimentation variait entre 15 et 26 ng/L (soit une moyenne de 21 ng/L), le système d'OI était capable de réduire ces concentrations à 2,1 ng/L (Flores et coll., 2013).
Deux usines de réutilisation indirecte de l'eau potable comportant des unités d'OI dans leur chaîne de traitement ont permis de réduire la concentration d'APFO sous la valeur de 55 ng/L dans l'eau traitée. Les deux systèmes d'OI avaient une vitesse de filtration de 12 gallons au pied carré par jour (gp2/j) (20 L/m2/h) et un taux de reprise d'eau allant de 80 à 85 %. Les concentrations d'APFO dans l'eau qui alimentait les unités d'OI allaient de 9,5 à 200 ng/L (Dickenson et Higgins, 2013; Appleman et coll., 2014). Une enquête portant sur plusieurs services d'alimentation en eau potable et usines de réutilisation indirecte de l'eau potable indique que les concentrations d'APFO dans l'eau traitée étaient comparables, dans presque tous les cas, aux niveaux qu'on retrouvait dans les échantillons d'eau brute. Néanmoins, un cas d'élimination a été constaté dans une usine de réutilisation de l'eau qui faisait appel à une membrane intégrant la MF et l'OI. Le système de membrane utilisé a permis de ramener la concentration d'APFO de 15 ng/L dans l'eau d'alimentation jusqu'en dessous de 5 ng/L dans l'eau traitée (Quinones et Snyder, 2009).
Des essais en laboratoire ont permis d'évaluer le comportement de rejet de membranes de filtration souillées et non souillées pour l'élimination de SPFA, y compris l'APFO (Appleman et coll., 2013). L'étude montre qu'une membrane plane et mince de NF en polyamide composite est capable de rejeter, dans une proportion de 93 à 99 %, tous les composés mis à l'épreuve. Un rejet supérieur à 97 % pour une concentration moyenne d'APFO de 664 ng/L (LQ = 20 ng/L) dans l'eau d'arrivée a été constaté dans toutes les expériences qui employaient des membranes neuves et de l'eau désionisée et dopée, des membranes neuves et de l'eau souterraine dopée, et des membranes souillées ainsi que de l'eau souterraine dopée. La couche souillée de la membrane de NF n'a eu aucun effet négatif sur le rejet d'APFO (Appleman et coll., 2013). Une autre étude de laboratoire a été réalisée avec une membrane d'OI (dont le seuil de rétention des molécules était de 100 Da) et trois membranes de NF (dont le seuil de rétention variant entre 200 et 360 Da) en vue d'extraire l'APFO. La membrane d'OI a atteint un rejet de 99,9 % d'APFO dont la concentration était de 3 500 ng/L dans l'eau d'alimentation, ce qui a permis d'obtenir une concentration de 3 à 6 ng/L dans le perméat. Le système d'OI fonctionnait avec un débit de 30 à 40 L/m2/h et une pression d'alimentation de 8 bars (116 lb/po2). Toutes les membranes de NF mises à l'essai ont atteint un taux de rejet de l'ordre de 95,5 à 99,8 % compte tenu d'une concentration moyenne d'APFO de 3000 ng/L, d'un débit de 70 L/m2/h et d'une pression de fonctionnement allant de 4 à 7 bars (de 58 à 101 lb/po2) (Lipp et coll., 2010).
Bien qu'il n'existe qu'un nombre limité de données sur le traitement par OI à échelle réelle et seulement des données de laboratoire sur le traitement par NF, on considère néanmoins que ces deux techniques sont efficaces pour éliminer l'APFO de l'eau potable (Appleman et coll., 2014). Les résultats des études sur la NF sont prometteurs étant donné que cette technique est moins énergivore que l'OI. La mise à l'essai des membranes de NF choisies pour éliminer l'APFO tant à l'échelle pilote qu'à l'échelle réelle constitue une étape importante pour les services publics qui envisagent d'utiliser cette technique comme procédé de traitement. Étant donné que l'exclusion par la taille est un mécanisme important de rejet des SPFA par les membranes de filtration, il faut envisager de choisir des membranes dont le seuil de rétention des molécules est inférieur à la taille de l'APFO.
Lorsqu'on effectue un traitement par OI, il faut tenir compte de l'élimination des rejets ainsi que du risque de corrosivité accrue de l'eau traitée. Comme le traitement par OI rejette une portion considérable de l'eau d'arrivée sous forme de saumure riche en contaminants, les rejets concentrés doivent être éliminés convenablement. (Duranceau et Taylor, 2011). L'élimination des contaminants peut causer un déséquilibre des minéraux, qui peut aggraver la corrosivité de l'eau traitée (Schock et Lytle, 2011). Dans la plupart des cas, il faut recourir à des mesures de corrosivité après le traitement.
7.1.4 Échange d'ions
Comme l'APFO prend une forme anionique à des valeurs de pH d'eau ambiante, les résines échangeuses d'anions devraient être en mesure de l'éliminer (Senevirathna et coll., 2010). Deux principaux mécanismes d'élimination de l'APFO par les résines échangeuses d'anions, soit les interactions électrostatiques et hydrophobiques, ont été proposés (Carter et coll., 2010; Deng et coll., 2010; Xiao et coll., 2012).
Appleman et coll. (2014) ont publié des résultats pour la seule application à échelle réelle connue de l'échange d'ions pour l'élimination de SPFA. Ce système n'a toutefois pas été spécifiquement conçu pour l'élimination de SPFA dans l'eau potable. Une installation mettant en œuvre des échangeurs d'ions à grande échelle de 350 gpm a réussi à réduire des concentrations d'APFO de l'ordre de 68 à 120 ng/L à une concentration moyenne de 24 ng/L dans l'eau souterraine. L'utilisation d'une résine basique puissante imprégnée d'oxyde de fer pour éliminer de l'arsenic a, en outre, fait l'objet d'une évaluation en vue de l'appliquer à l'élimination de l'APFO après que l'on ait utilisé cette résine pendant cinq et neuf mois. La résine échangeuse d'anions fortement basique très poreuse a éliminé plus de 75 % de l'APFO, a éliminé partiellement l'acide perfluoroheptanoïque (PFHpA) (46 %) et a éliminé grandement le SPFO (>92 %) et le perfluorohexanesulfonate (PFHxS) (97 %). Les composés de chaînes carbonées plus courtes, comme l'acide perfluorobutanoïque (APFB) et l'acide perfluorohexanoïque (PFHxA), ont été peu ou pas du tout éliminés. Les résultats ont également indiqué que la résine échangeuse d'anions a éliminé de manière préférentielle les acides perfluorosulfoniques au lieu des acides perfluorocarboxyliques.
Selon la concentration d'ions en solution et le type de résine choisi, les résines échangeuses présentent un certain degré de sélectivité de différents ions. Des évaluations en laboratoire de divers types de résines (c.-à-d., les résines échangeuses d'ions, les résines non échangeuses d'ions) utilisées pour éliminer les SPFA ont été signalées dans les ouvrages scientifiques (Lampert et coll., 2007; Carter et coll., 2010; Deng et coll., 2010; Senevirathna et coll., 2011; Xiao et coll., 2012; Chularueangaksorn et coll., 2013). Des essais cinétiques de lots réalisés avec une concentration initiale élevée d'APFO (mg/L) ont démontré une élimination supérieure à 99 % de l'APFO en 25 heures de contact avec une résine commerciale échangeuse d'anions, alors qu'une autre résine anionique n'avait éliminé que 37 % du composé. L'étude a également permis d'observer que les anions de SPFO étaient davantage éliminés que les anions d'APFO dans le processus d'échange ionique (Lampert et coll., 2007). Dans le cadre d'expériences en laboratoire, les résines échangeuses d'anions ont démontré une plus grande capacité d'élimination de SPFA que les résines non échangeuses d'anions (Chularueangaksorn et coll., 2013, 2014). Des colonnes à lit fixe en laboratoire ont permis de comparer le rendement des résines échangeuse d'anions et non échangeuses d'ions. Les essais ont été réalisés avec une concentration dans l'influent de 5 µg/L d'APFO pendant 120 jours d'opération. On a observé l'atteinte de l'objectif décisif de 0,5 µg/L avec des durées respectives de passage en colonne de 119 880 VL (111 jours) et de 68 040 VL (60 jours) par les résines échangeuses d'anions et non échangeuses d'ions (Chularueangaksorn et coll., 2013).
Alors que les conclusions indiquent que les résines anioniques avaient une meilleure capacité d'élimination d'APFO que les résines non échangeuses d'ions (Deng et coll., 2010; Chularueangaksorn et coll., 2013, 2014), on a également observé que les résines non échangeuses d'ions moyennement polaires ont démontré de meilleurs résultats que les résines non échangeuses d'ions non polaires en ce qui a trait à l'élimination de l'APFO dans l'eau (Xiao et coll., 2012).
Des études indiquent que le processus d'échange d'ions est une technologie prometteuse (Dickenson et Higgins, 2013) pour éliminer les APFA, dont l'APFO, dans l'eau potable. Il est toutefois nécessaire de réaliser d'autres études sur la sélectivité des résines, les limites relatives à la cinétique, l'incidence du COD, les taux de régénération et la présence d'ions concurrents, comme le sulfate et le nitrate, sur l'efficacité d'élimination (Dickenson et Higgins, 2013; Rahman et coll., 2013).
7.1.5 Oxydation, irradiation aux rayons UV et procédés d'oxydation avancée
Des procédés d'oxydation avancée (POA) ont été élaborés pour éliminer les contaminants qui résistent aux procédés de traitement par oxydation chimique plus communs. Ces procédés comprennent l'utilisation de combinaisons appropriées de lumière ultraviolette (UV), d'oxydants chimiques et de catalyseurs (p. ex., l'ozone, le peroxyde d'hydrogène, le dioxyde de titane) pour produire des radicaux hautement réactifs comme les radicaux hydroxyles, qui sont de puissants oxydants et qui réagissent rapidement et de manière non sélective avec les contaminants organiques.
Rahman et coll. (2014) ont résumé des études qui ont démontré la probabilité de la résistance des APFA, comme l'APFO, à l'oxydation, même si celle-ci est provoquée par l'ozone moléculaire et les radicaux hydroxyles. En raison de la faible réactivité de l'APFO à l'ozone et aux POA, il serait improbable que les procédés d'oxydation à base de chlore n'oxydent l'APFO dans des conditions normales d'eau potable. La résistance de l'APFO à l'oxydation est attribuable à l'effet d'écran des atomes de fluor et à la force des liaisons carbone-fluor (3M, 1999; ATSDR, 2009). Ces conclusions ont été confirmées dans les études d'usines de traitement d'eau à échelle réelle (Quinones et Snyder, 2009; Shivakoti et coll., 2010; Takagi et coll., 2011; Eschauzier et coll., 2012; Flores et coll., 2013) qui sont décrites ci-dessous.
Dans une étude menée sur de nombreux réseaux de distribution d'eau potable, Quinones et Snyder (2009) ont observé que l'APFO résistait à la chloration, à la chloramination et à l'ozonation, même en utilisant une combinaison d'autres procédés de traitement comme la coagulation/floculation, la filtration à lit profond et l'irradiation aux rayons UV. Des résultats obtenus auprès d'usines de traitement d'eau potable au Japon ont indiqué des concentrations similaires d'APFO dans des échantillons d'eau traitée avec le procédé d'ozonisation et dans des échantillons d'eau brute (Shivakoti et coll., 2010; Takagi et coll., 2011). Les doses d'ozone de l'ordre de 0,37 à 0,85 mg/L et une durée de contact aussi élevée que 120 minutes ont démontré que le procédé d'ozonisation n'était pas efficace pour dégrader l'APFO dans quatre réseaux de distribution (Takagi et coll., 2011). Thompson et coll. (2011) ont observé qu'une dose d'ozone de 5 mg/L associée à une durée de contact de 15 minutes dans l'eau recyclée s'avérait inefficace pour réduire les concentrations d'APFO de l'ordre de 7,1 à 12,4 ng/L.
Une usine de traitement à échelle réelle employant deux réacteurs UV, dont chacun était en mesure de traiter 3 MG/J d'eaux souterraines avec une dose de rayons UV de 80 mJ/cm2 et une transmission de rayons UV de 95 %, n'a pas été capable de réduire une concentration d'APFO dans l'influent de l'ordre de 11 à 15 ng/L. Une autre usine de traitement d'eau à échelle réelle de 5 MG/J a signalé qu'une dose de rayons UV de 500 MJ/cm2 combinée avec une dose de 4 mg/L de H2O2 s'avérait inefficace pour dégrader 19 ng/L d'APFO dans l'eau de surface (Appleman et coll., 2014). Les POA, l'oxydation et l'irradiation de rayons UV ne semblent pas efficaces pour éliminer l'APFO dans l'eau potable. L'ozone ou les POA peuvent toutefois oxyder les substances chimiques polyfluorées contrôlées qui pourraient être présentes dans l'eau brute, augmentant ainsi possiblement la concentration d'APFO et de SPFO dans l'eau traitée (Rahman et coll., 2014).
7.1.6 Aération/strippage à l'air
L'élimination de composés par le strippage à l'air repose sur le partage à l'équilibre des substances chimiques entre l'air et l'eau, qui est influencé par la surface de contact entre l'air et l'eau, ainsi que la température, la pression de la vapeur et le pH de l'eau.
Dickenson et Higgins (2013) ont évalué la présence de 23 SPFA (dont l'APFO et le SPFO) dans l'eau brute et l'eau potable traitée, ainsi qu'à diverses étapes le long de la chaîne de traitement. Ils ont constaté que l'aération était inefficace pour éliminer l'APFO et le SPFO (10 % d'élimination).
7.1.7 Filtration par les berges (biofiltration)
La filtration par les berges (FB) est une méthode de traitement d'eau potable selon laquelle l'eau de surface circule à travers les couches souterraines de sable et de gravier de la berge ou du lit d'une rivière jusqu'aux puits d'extraction, et les contaminants sont éliminés grâce aux procédés de filtration, de sorption, de dilution et de biodégradation.
Un réseau de distribution d'eau potable utilisant la FB combinée à une durée de séjour hydraulique d'environ 10 jours a observé un taux d'élimination approximatif de l'APFO de 30 %, un taux d'élimination variable de certaines SPFA et des augmentations dans les concentrations d'autres SPFA (Appleman et coll., 2014). Les auteurs ont conclu que cette variation était possiblement attribuable à la variabilité des concentrations d'influent causée par l'incidence des effluents d'eaux usées sur les sources d'eau potable et/ou la dégradation de composés précurseurs sur les berges. Dickenson et Higgins (2013) ont conclu qu'il était improbable que la FB élimine des concentrations significatives de SPFA.
7.1.8 Nouvelles techniques
Bien que d'autres technologies de traitement possibles visant à éliminer l'APFO et le SPFO s'avèrent intéressantes, elles font l'objet de recherches actives. Leur utilisation sur des eaux potables n'a pas encore été évaluée dans le cadre d'un projet pilote en laboratoire, ou d'études à échelle réelle, mais elle a été mentionnée dans des examens d'études effectuées par des consultants sur l'élimination de certaines SPFA dans l'eau potable et les eaux usées (Vecitis et coll., 2009; Eschauzier et coll., 2012).
7.1.8.1 Nanomatériaux et nanotechnologies
Les nanomatériaux sont mis au point pour certaines applications liées au traitement de l'eau potable, y compris l'échange d'ions, les procédés de sorption et d'oxydation et la réduction abiotique (p. ex., le fer nanozérovalent) (Boyd et coll., 2013). Divers nanomatériaux et diverses nanotechnologies se montrent prometteurs pour éliminer le SPFO, dont les nanotubes de carbone (NTC), les polymères à empreinte moléculaire (PEM) à base de chitosane, les membranes nanofibreuses électrofilées (MNFE) et la photocatalyse assistée de dioxyde de titane (TiO2) (Yu et coll., 2008; Deng et coll., 2012; Dai et coll., 2013). Les NTC sont des molécules de carbone composées de treillis de carbone susceptibles de prendre la forme de tubes. Le chitosane est un polysaccharide naturel reposant sur les coquilles des crustacés. Il est possible de le préparer comme une nanoparticule ou une fibre électrofilée dans les nanofibres (Sonia et Sharma, 2011; Zhao et coll., 2011a; Boyd et coll., 2013). L'impression moléculaire est une technique selon laquelle des sites précis de composés cibles sont construits sur un polymère afin que des matières absorbées spécifiques soient reconnues dans le processus de sorption. Les MNFE sont préparées par électrofilage de nanofibres de polymère ou de matériaux composites en polymère afin de créer des membranes de fibres non tissées de diamètres de l'ordre de plusieurs dizaines à des centaines de nanomètres (Greiner et Wendorff, 2007; Dai et coll., 2013; Boyd et coll., 2013).
Deng et coll. (2012) ont démontré l'efficacité des NTC pour l'élimination de contaminants perfluorés, dont l'APFO et le SPFO, dans des milieux aquatiques lorsque des interactions hydrophobiques faisaient partie de la sorption de contaminants perfluorés sur des NTC. La sorption des contaminants perfluorés a augmenté au rythme de la hausse de la longueur de la chaîne carbone-fluor avec le même groupe fonctionnel.
7.1.8.2 Photolyse et dégradation photochimique
Bien qu'on ait signalé qu'un procédé de traitement aux rayons UV à échelle réelle était inefficace pour éliminer l'APFO dans l'eau potable, plusieurs évaluations en laboratoire d'échantillons d'eaux synthétiques, d'eaux usées et d'eaux industrielles ont démontré que la lumière UV visible, les rayons UV en présence de persulfate, les rayons UV en présence de TiO2 et le perchlorate, les rayons UV en présence d'iodure et l'irradiation aux rayons UV au moyen d'ions radicaux de carbonates peuvent dégrader des concentrations d'APFO (Hori et coll., 2004a, 2005; Chen et Zhang, 2006; Chen et coll., 2007; Fujii et coll., 2007; Giri et coll., 2011, 2012, 2013; Dillert et coll., 2007; Panchangam et coll., 2009; Qu et coll., 2010).
Une étude en laboratoire a signalé un taux de dégradation et de défluoration de 87 % d'une concentration initiale d'APFO de 25 mg/L sous une irradiation de 185 nm de rayons UV en présence de persulfate. Comparativement à la photolyse directe, la réaction photochimique a accentué la dégradation de l'APFO. L'étude a permis d'observer la formation d'APFC à courte chaîne (Chen et Zhang, 2006). Une autre étude en laboratoire a démontré l'efficacité de l'anion radical de sulfate (SO4-) sur l'APFO décomposé dans une réaction photochimique. Les auteurs ont indiqué que la concentration d'APFO de 1,35 mmol a été complètement décomposée par le système photochimique au moyen de SO4- et de l'irradiation aux rayons UV visibles pendant quatre heures. L'étude a également démontré la formation d'APFC à courte chaîne de manière progressive (Hori et coll., 2005). Après l'irradiation aux rayons UV visibles sous 0,48 MPa d'oxygène, un taux de 89,5 % d'une concentration initiale d'APFO de 1,35 mmol s'est décomposé et on a observé la formation de CO2, F- et d'APFC à courte chaîne. Les auteurs ont également indiqué que les hétéropolyacides, en raison de leur grande stabilité, sont des photocatalyseurs intéressants dans les réactions de dégradation d'APFC. En présence d'hétéropolyacides, 7,44 µmol d'APFO en solution aqueuse s'est complètement dégradée après 24 heures d'irradiation aux rayons UV. Le photocatalyseur a accentué la dégradation d'APFO et a empêché la formation d'APFC à courte chaîne (Hori et coll., 2004a). Tang et coll. (2012) ont étudié l'efficacité de la technique des rayons UV de Fenton visant l'élimination de l'APFO dans l'eau et ont observé une dégradation et une défluoration presque complètes d'APFO en quelques heures, alors que l'APFO se dégradait difficilement par un système conventionnel de Fenton.
7.2 Échelle résidentielle
En général, il n'est pas recommandé d'utiliser des dispositifs de traitement de l'eau potable pour effectuer un traitement additionnel de l'eau traitée municipale. Dans les cas où l'eau potable d'une résidence provient d'un puits privé, un dispositif résidentiel de traitement de l'eau potable peut servir à réduire les concentrations d'APFO qui s'y trouvent.
Bien qu'il n'existe aucun dispositif de traitement résidentiel certifié visant à réduire la concentration d'APFO dans l'eau potable, les données disponibles suggèrent que le charbon actif résidentiel et l'osmose inverse peuvent atteindre des concentrations respectives d'APFO traité de 0,2 µg/L et de moins de 0,05 µg/L. En outre, les dispositifs de traitement utilisant l'échange d'anions peuvent être efficaces pour réduire les concentrations d'APFO.
Le ministère de la Santé du Minnesota (MDH, 2008b) a réalisé une étude sur l'efficacité des dispositifs de traitement d'eau aux points d'utilisation (PU) visant l'élimination de l'APFO, du SPFO et de l'APFB et a démontré que les filtres à charbon actif et d'OR ont été en mesure de réduire les concentrations d'APFO que l'on trouve généralement dans l'eau potable. On a par ailleurs réalisé des essais de dépistage en laboratoire et une évaluation sur le terrain des dispositifs installés dans les systèmes d'eau municipaux. Dans le cadre des tests en laboratoire, les échantillons d'eau évalués démontraient une concentration d'APFO de 3,0 µg/L et les objectifs cibles de rendement étaient de 0,2 µg/L. Les essais sur le terrain comprenaient la surveillance et l'échantillonnage de quatre dispositifs de charbon actif et sept dispositifs d'OR aux points d'utilisation installés à deux puits municipaux. L'un des puits démontrait des concentrations de 0,6 µg/L d'APFO, de 0,9 µg/L de SPFO et de 1,4 µg/L d'APFB, et le second ne comportait que des concentrations d'APFB (1,5 µg/L). On a installé un préfiltre de charbon actif sur tous les dispositifs d'OR (avant la membrane d'OR) et un filtre de polissage au charbon actif (après la membrane d'OR) après le traitement. Les résultats ont indiqué que tous les dispositifs d'OR et de charbon actif se sont avérés efficaces pour éliminer une concentration d'APFO inférieure à la limite de quantification de 0,2 µg/L et de la limite de détection de 0,05 µg/L, respectivement. Selon ces résultats, le charbon actif et l'OR devraient être efficaces pour réduire une concentration d'APFO dans l'eau potable inférieure à la CMA de 0,2 µg/L.
Santé Canada ne recommande pas de marques particulières de dispositifs de traitement de l'eau potable, mais conseille vivement aux consommateurs de n'utiliser que les dispositifs certifiés par un organisme de certification accrédité comme étant conformes aux normes appropriées de la NSF International (NSF) et de l'American National Standards Institute (ANSI). Ces normes ont été conçues pour garantir la sécurité de l'eau potable en aidant à assurer la sécurité matérielle et le rendement des produits qui entrent en contact avec l'eau potable. Les organismes de certification donnent l'assurance qu'un produit est conforme aux normes applicables; ils doivent être accrédités par le Conseil canadien des normes (CCN). Au Canada, les organismes qui suivent ont été accrédités par le CCN pour homologuer les appareils et matières servant à l'eau potable qui sont conformes aux normes NSF/ANSI (CCN, 2015) :
- Groupe CSA;
- NSF International (anglais seulement);
- Water Quality Association;
- UL LLC;
- Bureau de normalisation du Québec;
- International Association of Plumbing and Mechanical Officials (anglais seulement).
On peut obtenir une liste à jour des organismes de certification accrédités sur le site Web du CCN.
Les systèmes de filtration au charbon actif peuvent s'installer au robinet (au point d'utilisation) où à l'endroit où l'eau entre dans la résidence (au point d'entrée). Les systèmes d'OI sont conçus pour être installés au point d'utilisation, car de grandes quantités d'eau d'arrivée sont nécessaires pour obtenir le volume requis d'eau traitée, ce qui n'est pas pratique en général pour des systèmes de traitement résidentiels destinés au point d'entrée. Les systèmes d'OI devraient seulement être installés au point d'utilisation, car l'eau traitée par ceux-ci peut avoir un effet corrosif sur la plomberie. Il peut être nécessaire de prétraiter l'eau d'arrivée afin de réduire l'encrassement de la membrane et accroître sa durée de vie utile.
La technologie de traitement par échange d'ions utilisant des résines échangeuses d'anions peut également être utilisée pour éliminer l'APFO à l'échelle résidentielle. Les systèmes d'échange d'ions sont habituellement conçus et fabriqués pour un usage résidentiel par les fournisseurs ou les détaillants de systèmes de traitement de l'eau potable. Santé Canada recommande fortement aux particuliers qui utilisent ces systèmes de vérifier si ceux-ci sont fabriqués avec des matériaux conformes à la norme NSF/ANSI 61. Si un système d'échange d'ions est utilisé, l'eau pourrait devoir être filtrée par un filtre de CAG afin d'éliminer tout chlore ou toute chloramine (s'il est relié à un réseau d'approvisionnement en eau traitée) dans l'eau avant qu'elle n'atteigne la résine.
Avant d'installer un appareil de traitement, il faut faire analyser l'eau afin de déterminer sa chimie générale et de vérifier la présence et la concentration de dichlorométhane. L'eau qui pénètre dans le dispositif de traitement et l'eau traitée qui en sort devraient faire l'objet d'essais de contrôle périodiques par un laboratoire accrédité, pour s'assurer du bon fonctionnement du dispositif de traitement. Les appareils peuvent perdre de leur capacité d'élimination avec le temps et l'usure; il faut les entretenir et, parfois, les remplacer.
8.0 Cinétique et métabolisme
L'APFO est un composé qui ne se métabolise pas et qui est considéré comme étant chimiquement non réactif. L'absorption orale de l'APFO est rapide et complète (Kemper, 2003; Hundley et coll., 2006; Lau et coll., 2007). Une fois absorbé, l'APFO est restreint principalement au plasma et au liquide extracellulaire (Butenhoff et coll., 2004a; Han et coll., 2012) avant d'être excrété dans l'urine.
8.1 Absorption
L'APFO est rapidement et presque totalement absorbé dans la voie gastro-intestinale. Chez les rats, les études indiquent systématiquement que les taux d'absorption orale par gavage d'APFO s'élèvent à >93 % après l'administration d'une dose unique (0,1 à 25 mg/kg p.c.) (Johnson et Ober, 1979, 1999; Kemper, 2003; Cui et coll., 2010). Hundley et coll. (2006) ont relevé des taux d'absorption similaires chez les souris, les rats, les hamsters et les lapins après l'administration d'un seul bolus oral d'APFO à une dose de 10 mg/kg p.c. Les ratios d'absorption estimés étaient généralement plus élevés chez les mâles (les rats : 89 %, les souris : 82 %, les hamsters : 92 %) que chez les femelles (les rats : 76 %, les souris : 61 %, les hamsters : 75 %), sauf en ce qui concerne les lapins (88 % chez les deux sexes). Les concentrations plasmatiques d'APFO étaient environ de deux ou trois fois plus élevées chez les rats à jeun après l'administration d'un bolus oral unique de 10 mg/kg p.c. (Hinderliter et coll., 2006).
Bien qu'il n'existe aucune donnée d'étude contrôlée sur l'absorption orale d'APFO chez les humains, des études sur des résidents vivant dans des secteurs où l'eau potable est contaminée (Emmett et coll., 2006a; Wilhelm et coll., 2008) ont démontré des concentrations sériques élevées d'APFO. Emmett et coll. (2006a) ont d'ailleurs observé une corrélation entre le nombre de verres d'eau du robinet consommés par jour et les concentrations sanguines d'APFO, tout en indiquant qu'il s'agissait de la voie principale d'exposition pour les populations exposées à des concentrations élevées d'APFO dans l'eau potable.
Des études limitées sur l'exposition par voie cutanée ou par inhalation ont signalé une cinétique de l'APFO; les propriétés physicochimiques du composé suggèrent toutefois que ces voies d'exposition ne sont pas importantes lorsqu'on retrouve de l'APFO dans l'eau potable (voir la section 5.7).
8.2 Distribution
L'APFO est surtout présent dans le sérum/plasma (Johnson et Ober, 1999; Kudo et coll., 2007). Le volume de distribution, qui est semblable chez toutes les espèces (environ 170 mL/kg p.c.), suggère une distribution extracellulaire (Butenhoff et coll., 2004a; Han et coll. 2012). L'APFO est étroitement lié à la protéine sérique, qui joue un rôle important dans la distribution dans le sang et les tissus (Han et coll., 2005). L'APFO se lie principalement à l'albumine sérique dans le sang, puisqu'on estime que >90 % d'APFO dans le sérum se lie à l'albumine chez les rats et les humains (Han et coll., 2003). L'APFO peut également se lier dans une moindre mesure aux gammaglobulines, aux alplaglobulines, aux alpha-2-macroglobulines, aux transferrines et aux bêtalipoprotéines présentes dans le plasma (Kerstner-Wood et coll., 2003; Butenhoff et coll., 2012a). La liaison protéinique s'effectue également au niveau des organes et des tissus. Luebker et coll. (2002) ont révélé que l'APFO se liait in vitro aux protéines de liaison des acides gras du foie des rats. L'étude a également démontré que l'APFO se liait aux alpha-2μ globulines dans le foie et l'urine des rats; les constantes de dissociation étaient toutefois faibles comparativement aux autres ligands qui sont connus pour induire une néphropathie de gouttelettes hyalines (Han et coll., 2004).
Les cinétiques d'APFO ne sont pas linéaires à des doses élevées, probablement en raison de la saturation des transporteurs d'anions organiques (TAO) qui sont responsables de la réabsorption rénale à des doses importantes, ce qui entraîne un taux d'excrétion plus élevé à des doses élevées qu'à de faibles doses (Andersen et coll., 2006). Par ailleurs, dans certaines études, les augmentations des taux sériques n'étaient pas proportionnelles aux augmentations des doses, sauf à des doses plus faibles, et l'état d'équilibre était atteint plus rapidement que prévu à des doses élevées et à des cinétiques normales (4 à 5 demi-vies). Les cinétiques sont toutefois cohérentes avec les processus de premier ordre et les taux sériques sont proportionnels aux doses administrées à des doses plus faibles et plus près des concentrations qui reflètent bien les expositions environnementales des humains (Loveless et coll., 2006; Lou et coll., 2009). Cette absence de linéarité peut avoir une incidence sur la distribution de l'APFO; par exemple, à la suite de l'administration d'une dose intraveineuse unique de 17 mg/kg p.c. à des rats mâles, une proportion plus faible de la dose a été distribuée vers le foie (27 %), comparativement à 52 % à 0,4 mg/kg p.c. (Kudo et coll., 2007).
Peu de données ont été recueillies sur les tissus humains vers lesquels l'APFO est généralement distribué. Une concentration d'APFO a toutefois été détectée dans près de la moitié des échantillons de foies analysés (chez six hommes et six femmes de la Catalogne, en Espagne, âgés de 27 à 79 ans), et, alors que les concentrations étaient beaucoup plus élevées chez les hommes que chez les femmes (Kärrman et coll., 2010), elles étaient inférieures aux limites de dosage dans les foies des cadavres ayant subi une exposition environnementale (Olsen et coll., 2003a). Ni le liquide céphalo-rachidien (Harada et coll., 2007) ni la thyroïde (Pirali et coll., 2009) ne se sont avérés un lieu de cloisonnement pertinent pour l'APFO.
Chez les rats, les concentrations d'APFO étaient systématiquement plus élevées chez les mâles que chez les femelles à la suite d'expositions uniques ou répétées (Ylinen et coll., 1990; Kemper, 2003). On a attribué ces différences à une élimination plus rapide de l'APFO chez les femelles que chez les mâles. Chez les rats et les primates non humains, il ne semble pas y avoir de différences de concentrations d'APFO entre les sexes (Griffith et Long, 1980; Butenhoff et coll., 2004a; Lou et coll., 2009). Lou et coll. (2009) ont fait état de temps d'absorption de concentrations d'APFO similaires dans le sérum, le foie et les reins de souris CD-1 mâles et femelles après un seul gavage oral de 1 ou 10 mg/kg p.c. Des études de biosurveillance humaine ont également permis de noter des différences de concentrations d'APFO entre les sexes (voir la section 5.6). Comme la section 5.6 le décrit, l'Enquête canadienne sur les mesures de la santé (ECMS) indique que les taux sériques d'APFO chez les humains semblent être influencés par l'âge et le sexe. On a également observé cette incidence dans des études américaines, telles que la NHANES 1999-2008 (Kato et coll. 2011), ainsi que chez d'autres populations de référence (Harada et coll., 2004; Hölzer et coll., 2008; Ingelido et coll. 2010). Il a été démontré que les concentrations d'APFO diminuaient avec l'âge chez les hommes et qu'elles augmentaient chez les femmes (Kato et coll. 2011). Ce phénomène peut s'expliquer par les saignements menstruels, particulièrement chez les femmes nullipares (Ingelido et coll., 2010), la grossesse et la lactation. Cette hypothèse repose sur l'incidence de taux sériques plus élevés d'APFO chez les femmes primipares que chez les femmes multipares (Kim et coll., 2011), ainsi qu'une diminution importante des taux sériques d'APFO pendant la lactation (deux à sept semaines par rapport à trois à quatre mois après l'accouchement) (von Ehrenstein, 2009; Monroy et coll., 2008).
L'exposition à l'APFO peut survenir à travers le placenta ou par l'allaitement. Le transfert fœtal de concentrations d'APFO par le placenta a été démontré chez les rats (Hinderliter et coll., 2005) et chez les souris (Fenton et coll., 2009). Chez les humains, les concentrations d'APFO retrouvées dans le sang du cordon ombilical des nouveau-nés sont similaires aux concentrations retrouvées dans le sang de la mère (Tittlemier et coll., 2004; Midasch et coll., 2007; Monroy et coll., 2008; Beesoon et coll., 2011; Needham et coll., 2011; Gützkow et coll., 2012). Une étude menée dans une région témoin (c.-à-d., non contaminée par l'APFO) (Hölzer et coll., 2008) et une région présentant des concentrations environnementales élevées d'APFO (Mondal et coll., 2012) a par ailleurs révélé que les concentrations sériques détectées chez les jeunes enfants étaient supérieures aux concentrations sériques détectées chez les mères; les concentrations sériques étaient toutefois similaires chez les enfants et les mères qui vivaient dans un secteur présentant des concentrations élevées d'APFO dans l'eau potable (Hölzer et coll., 2008). On a de plus mesuré le transfert de l'APFO par l'allaitement chez différentes espèces de mammifères, dont les humains, les rats, les souris et les moutons (Hinderliter et coll., 2005; Fenton et coll., 2009; Kim et coll., 2011; Needham et coll., 2011). Les concentrations d'APFO dans le lait maternel étaient constamment inférieures à celles du plasma maternel (Hinderliter et coll., 2005; Fenton et coll., 2009); chez les humains, un examen des concentrations sériques chez la mère et dans le lait a démontré que les ratios sériques de lait maternel indiqués dans plusieurs études étaient d'environ 0,11-0,12 (Liu et coll., 2011). En outre, les concentrations d'APFO dans le lait maternel humain diminuent de façon importante pendant l'allaitement (Thomsen et coll., 2010), et un nombre croissant de bébés sont nourris au sein (Tao et coll., 2008; Kadar et coll., 2011).
8.3 Métabolisme
Les données disponibles indiquent que l'APFO ne se métabolise pas. Certaines études menées sur des rongeurs et des primates non humains ont révélé que la métabolisation de l'APFO n'est quantitativement pas importante et que l'APFO n'est pas métabolisé lorsqu'il est incubé avec des fractions misocromales d'homogénats d'intestin, de rein ou de foie d'humain ou de rat (Kemper et Nabb, 2005; EFSA, 2008; ATSDR, 2009).
8.4 Excrétion
Selon les espèces, on a observé des différences notoires en ce qui a trait à la demi-vie d'élimination de l'APFO, alors que celui-ci demeure dans le corps humain beaucoup plus longtemps que chez les autres espèces, y compris les primates non humains, les rats et les souris (Post et coll., 2012). Les demi-vies d'élimination du sérum chez les humains sont beaucoup plus longues que chez les primates non humains et les rats. Les différences liées à l'espèce et au sexe sont essentiellement attribuées à la cinétique d'élimination alors que, à des doses plus élevées, la cinétique de l'APFO chez les rongeurs et les primates ne suit pas des modèles simples de premier ordre ou de séparation (Andersen et coll., 2006). Les valeurs de demi-vies d'élimination sérique de l'APFO chez les humains découlent de données obtenues auprès de travailleurs retraités (moyenne arithmétique = 3,8 ans; intervalle = 1,5 à 9,1 ans; IC de 95 % = 3,1 à 4,4 ans; Olsen et coll. 2007). Chez les populations exposées dans leur milieu par la consommation d'eau potable contaminée par l'APFO, les valeurs de demi-vie pouvaient être estimées en analysant les déclins mesurés des concentrations sériques ou plasmiques d'APFO à la suite de l'arrêt des expositions grâce à la filtration de l'eau potable. Alors que la demi-vie moyenne géométrique en Allemagne a été fixée à 3,26 ans (intervalle = 1,03 à 14,67; aucun signalement d'IC de 95 %; Brede et coll., 2010), la valeur moyenne de la Vallée du Mid-Ohio correspond à 2,3 ans (IC de 95 % = 2,1 à 2,4 ans; aucun intervalle n'a été fourni; Bartell et coll., 2010). Une autre étude transversale menée dans la Vallée du Mid-Ohio (fondée sur des concentrations sériques initiales estimées et non mesurées) a démontré des valeurs de demi-vies de 2,9 à 10,1 ans (les valeurs variaient selon les concentrations sériques moyennes dans la communauté et le temps écoulé depuis la fin des expositions) (Seals et coll., 2011). Alors que la demi-vie de l'APFO chez les animaux varie selon les protocoles expérimentaux, elle se compte en jours et en semaines chez les rongeurs et les singes (voir le tableau 1).
| Espèce | Schéma posologique | Demi-vie moyenne (jours) | Référence |
|---|---|---|---|
| Rats | Dose orale unique de 0,1 mg/kg p.c.; suivis pendant 22 jours (M) ou 5 jours (F) | 8,41 ± 1,56Note de bas de page 1 (M) 0,13 ± 0,04Note de bas de page 1 (F) |
Kemper, 2003 |
| Dose orale unique de 0,1 mg/kg p.c.; suivis jusqu'à ce que l'APFO soit inférieur aux limites de quantification | 11,55 ± 2,36Note de bas de page 1 (M) 0,14 ± 0,05Note de bas de page 1 (F) |
||
| Dose orale unique de 1 mg/kg p.c.; suivis pendant 22 jours (M) ou 5 jours (F) | 5,76 ± 1,33Note de bas de page 1 (M) 0,14 ± 0,05Note de bas de page 1 (F) |
||
| Dose orale unique de 5 mg/kg p.c.; suivis pendant 22 jours (M) ou 5 jours (F) | 7,26 ± 1,21Note de bas de page 1 (M) 0,19 ± 0,03Note de bas de page 1 (F) |
||
| Dose orale unique de 25 mg/kg p.c.; suivis pendant 22 jours (M) ou 5jours (F) | 6,56 ± 1,60Note de bas de page 1 (M) 0,68 ± 0,41Note de bas de page 1 (F) |
||
| Dose intraveineuse unique de 1 mg/kg p.c.; suivis pendant 22 jours (M) ou 5 jours (F) | 7,73 ± 0,815Note de bas de page 1 (M) 0,12 ± 0,02Note de bas de page 1 (F) |
||
| Souris | Dose orale unique de 1 ou 10 mg/kg p.c.; suivies pendant une période pouvant aller jusqu'à 80 jours | 21,7 (19,5-24,1)Note de bas de page 2 (M) 15,6 (14,7-16,5)Note de bas de page 2 (F) |
Lou et coll., 2009 |
| Singes | Dose intraveineuse unique de 10 mg/kg p.c.; suivis pendant 123 jours | 20,9 ± 12,5 (M) 32,6 ± 8 (F) |
Butenhoff et coll., 2004 b |
| Dose orale quotidienne de 10 mg/kg p.c. pendant six mois; suivis pendant une période pouvant aller jusqu'à 147 jours après l'administration de la dose | 19,5Note de bas de page 3 (M) | ||
| Dose orale quotidienne de 20 mg/kg p.c. pendant six mois; suivis pendant une période pouvant aller jusqu'à 147 jours après l'administration de la dose | 20,8Note de bas de page 3 (M) | ||
| Humains | 26 anciens travailleurs comptant une moyenne de 31 années de travail et 2,6 années de retraite; les données externes d'exposition ne sont pas fournies | 1387 (1132-1606)Note de bas de page 2 | Olsen et coll., 2007 |
| 138 adultes et enfants, deux ans après la diminution des concentrations d'APFO dans l'eau potable; les doses ne sont pas fournies (Arnsberg, Allemagne) | 1190Note de bas de page 3 | Brede et coll., 2010 | |
| 200 adultes, environ un ou deux ans après la diminution des concentrations d'APFO dans l'eau potable; les doses ne sont pas fournies (Vallée du Mid-Ohio) | 840 (767-876)Note de bas de page 2 | Bartell et coll., 2010 | |
|
|||
L'excrétion par l'urine constitue la principale voie d'élimination de l'APFO chez les rats (particulièrement chez les femelles, dont les taux d'élimination par voie urinaire sont supérieurs à ceux des mâles) (Vanden Heuvel et coll., 1991; Kudo et coll., 2001) et chez les singes (Butenhoff et coll., 2002, 2004a). Le processus d'excrétion par l'urine comprend la filtration glomérulaire, la sécrétion dans le liquide tubulaire ainsi que la réabsorption à partir du liquide tubulaire. La filtration glomérulaire de l'APFO est limitée par le taux de liaison considérable de l'APFO aux protéines plasmatiques. On estime par ailleurs que la réabsorption rénale de l'APFO est stimulée par les protéines de TAO qui résident sur les membranes des cellules tubulaires proximales (Yang et coll., 2010; Han et coll., 2012), et qu'elle contribue aux différences entre les sexes en matière de clairance rénale (Yang et coll., 2009a). Contrairement au rat, il ne semble y avoir aucune différence entre les sexes en ce qui a trait à l'élimination de l'APFO par voie urinaire chez la souris (ATSDR 2009) ou chez le singe (Butenhoff et coll., 2004a). On a toutefois observé une tendance à la hausse (non linéaire) liée à la dose de l'excrétion urinaire de l'APFO chez les rats mâles (Butenhoff et coll., 2004b). Conformément aux observations chez les animaux auxquels on a administré de faibles doses, la relation entre une dose externe et une dose interne (taux sérique) est linéaire chez les humains qui sont exposés à l'APFO dans leur milieu (Clewell, 2009); une cinétique non linéaire - comme on le constate chez les animaux auxquels on a administré des doses plus élevées - pourrait toutefois survenir dans le cas d'expositions humaines plus importantes. On a toutefois remis en cause la pertinence de la clairance urinaire, car la clairance rénale de l'APFO était nettement inférieure que celle chez les animaux (Harada et coll., 2005).
L'excrétion biliaire et fécale contribue également à éliminer l'APFO, qui peut être assujetti à une recirculation entérohépatique importante (Vanden Heuvel et coll., 1991; Kudo et coll., 2001; Harada et coll., 2007; Kudo et coll., 2007). L'importance relative de l'excrétion fécale de l'APFO dépend de la clairance urinaire. L'excrétion fécale est moins importante que l'excrétion urinaire chez les rats (Harada et coll., 2007) et les singes (Butenhoff et coll., 2004a); les données sur les rats indiquent toutefois que la proportion d'excrétion par cette voie s'amplifie au fur et à mesure de l'augmentation des doses et des durées d'exposition (Cui et coll., 2010). La pertinence de cette voie d'excrétion chez les humains n'est pas claire. Harada et coll. (2007) ont démontré que le taux d'excrétion biliaire chez quatre humains était nettement plus élevé que le taux de clairance sérique par l'urine, et ont ainsi conclu que l'excrétion biliaire peut s'avérer une voie d'excrétion importante chez l'humain; ces données ne sont toutefois pas cohérentes avec le cas d'un homme dont les taux sériques d'APFO étaient élevés et chez qui on avait détecté de l'APFO dans l'urine, mais pas dans les excréments (Genius et coll., 2010).
Chez les femelles, la lactation peut constituer une voie d'excrétion importante comme le démontrent des études menées chez des souris (Abbott et coll. 2007) et des femmes (von Ehrenstein, 2009; Kim et coll., 2011). Les saignements menstruels peuvent s'avérer une voie d'excrétion importante chez les femmes (Harada et Koizumi, 2009) et contribuer aux différences de taux sériques qui ont été mesurées entre les sexes chez les humains.
8.5 Modèles pharmacocinétiques à base physiologique (PBPK)
De nombreux modèles plus ou moins complexes ont été élaborés afin de décrire la cinétique de l'APFO chez les animaux de laboratoire et les humains (Andersen et coll., 2006; Tan et coll., 2008; Loccisano et coll., 2011, 2012a, 2012 b, 2013). En raison de la nature non linéaire de la pharmacocinétique de l'APFO, selon laquelle l'élimination plus rapide est associée à une dose bolus élevée, les modèles physiologiques peuvent permettre d'améliorer les moyens d'examiner le paramètre de dose d'une voie d'élimination et d'une espèce à l'autre en vue d'évaluer les risques.
Le premier modèle qui a été élaboré pour l'APFO était un modèle biologique pharmacocinétique (PK) avec séparation pour les singes, qui comprenait la résorption rénale saturable de l'APFO filtré (Andersen et coll., 2006). Par ailleurs, les travaux ultérieurs qui ont été menés afin de peaufiner le modèle comprenaient l'ajout d'un compartiment hépatique et de fonctions dépendantes du temps en ce qui a trait à la liaison protéique et au volume de distribution afin d'adapter les données cinétiques liées au plasma, à l'urine et aux excréments de singes et de rats qui avaient reçu des doses élevées d'APFO par voie orale et par voie intraveineuse (Tan et coll. 2008). Les modèles PBPK de l'APFO pour les rats (Loccisano et coll., 2012a), les singes (Loccisano et coll., 2011) et les humains (Loccisano et coll., 2011) adultes sont fondés sur des modèles avec séparation. D'autres modèles de gestation et de lactation utilisant des rats (Loccisano et coll., 2012b) et des humains (Loccisano et coll., 2013) ont également été élaborés. Aucun modèle n'a été élaboré pour les souris, et aucun modèle de gestation et de lactation n'a été élaboré pour les singes. La structure de base du modèle PBPK était la même pour les trois espèces et comportait seulement des modifications physiologiques dépendantes du temps qui ont servi à décrire la gestation et la lactation ainsi que la dépendance temporelle de la liaison plasmatique et tissulaire. Les modèles comprenaient des compartiments tissulaires du tube digestif (pour les doses administrées par voie orale et dans l'alimentation), de la peau (pour les modèles humains et animaux seulement; pour les doses administrées par voie cutanée), du foie, de la graisse et des reins, et les tissus restants de l'organisme étaient regroupés ensemble (et non divisés en des compartiments bien ou mal perfusés). On a par ailleurs ajouté l'excrétion biliaire et l'élimination fécale de la dose bolus orale non absorbée ou de la dose d'exposition alimentaire dans le modèle pour les rats; en outre, la version du modèle pour les rats ne comprenait pas de compartiment pour la graisse (qui était comprise avec le reste du corps) ou le tube physiologique, que l'on décrivait comme étant un compartiment non physiologique. Le modèle PBPK suppose uniquement que la fraction plasmatique libre d'APFO peut être excrétée, résorbée ou absorbée dans les tissus. L'élimination plasmatique se décrit comme étant une filtration glomérulaire de la fraction libre dans un compartiment à filtrat. L'APFO filtré peut être soit éliminé dans l'urine ou résorbé dans les reins où il peut retourner dans la circulation générale. Les modèles parvenaient relativement bien à reproduire les données liées aux doses contrôlées qui ont été administrées aux rats (dans l'alimentation, par voie intraveineuse et par gavage oral; Loccisano et coll., 2012a) et aux singes (par voie intraveineuse et par gavage oral; Loccisano et coll., 2011). Alors qu'aucune donnée de dose contrôlée n'était disponible pour les humains, les données de biosurveillance (généralement pour un seul intervalle) se situaient dans des intervalles similaires à celles des simulations de modèles (selon les concentrations d'eau mesurées pour les populations biosurveillées ainsi que les hypothèses sur les habitudes d'ingestion; Loccisano et coll., 2011).
Bien que nous ayons envisagé d'utiliser les modèles de Loccisano des humains (2011), des singes (2011) et des rats (2012a) dans le cadre de l'évaluation actuelle (voir la section 10), nous avons plutôt décidé de recourir à un modèle utilisant des souris (qui a été reproduit à partir du modèle pour les rats sans être validé). Les particularités du modèle utilisé dans le cadre de la présente évaluation, dont les valeurs utilisées pour chacun des paramètres physiologiques et des paramètres propres aux substances chimiques, sont fournies dans l'étude de Campbell et Clewell (2013). On y décrit l'exposition comme étant un apport constant d'APFO chez les humains (ingestion de 1,5 L d'eau par jour) et on a laissé le modèle atteindre un état d'équilibre avant de déterminer si la concentration d'eau potable prévue était cohérente avec la mesure de la dose interne. Par prudence, on a utilisé la demi-vie la plus longue signalée (3,8 ans) afin d'obtenir la concentration d'eau potable la plus faible. La simulation pour les humains faisait référence à un adulte pesant 70 kg.
Le modèle pharmacocinétique d'Andersen et coll. (2006) a été modifié par Wambaugh et ses collègues (2013), qui ont ajouté un compartiment de tube digestif pour l'absorption orale et attribué une limite maximale à la distribution tissulaire. Les auteurs ont utilisé ce modèle afin de transposer les schémas de posologie et les valeurs disponibles liées aux doses minimales avec effet observé (LOEL), aux doses sans effet observé (NOEL) et aux doses de référence (DR) provenant de neuf études in vivo en paramètres de doses internes d'APFO (la zone située sous la courbe, la moyenne et les concentrations sériques maximales). Les données ont été modélisées pour les singes cynomolgus, les rats Sprague-Dawley mâles et femelles et les souris CD-1 et C57Bl/6. Une approche bayésienne a été utilisée afin de modéliser les différents paramètres physiologiques. Wambaugh et coll. (2013) ont déterminé que la concordance était relativement bonne entre les concentrations sériques prévues et les concentrations sériques mesurées (à la fin de l'étude), et qu'il y avait très peu de valeurs aberrantes. Ils ont également indiqué que les concentrations sériques moyennes et maximales étaient plus cohérentes parmi les effets nocifs. Les paramètres de doses des points de départ (PDD) étaient souvent les mêmes, indiquant ainsi une cohérence entre les espèces et les effets nocifs.
Nous n'avons pas considéré les contacts cutanés et par inhalation avec l'eau potable comme étant des voies d'exposition dans le cadre de cette étude, car nous croyons que leur contribution à l'exposition est négligeable (voir la section 5.7).
8.6 Extrapolation des animaux aux humains
Bien que les extrapolations des animaux aux humains fassent généralement l'objet de discussions à la suite des sélections de PDD potentiels, nous avons décidé d'examiner cette extrapolation plus tôt dans l'évaluation de l'APFO, car la forte variabilité entre les espèces était susceptible d'avoir une incidence sur la sélection des PDD. Les grandes différences entre les humains et les autres espèces en ce qui a trait à l'élimination de l'APFO doivent être prises en compte lorsque des études sur les animaux servent de base à des évaluations de risques d'une substance pour les humains. L'utilisation d'approches par défaut à l'égard de l'extrapolation des animaux aux humains - comme l'utilisation d'un facteur d'incertitude interespèce de 10 ou d'un facteur d'ajustement allométrique - pourrait ne pas être suffisante pour assurer la protection des humains dont les tissus cibles subissent des expositions internes plus longues. C'est la raison pour laquelle les approches propres à des substances chimiques qui pouvaient tenir compte des différences pharmacocinétiques entre les espèces et du comportement non linéaire de l'APFO ont fait l'objet d'un examen dans le cadre de l'évaluation des risques de l'APFO. Ces approches comprennent l'utilisation de facteurs d'ajustement propres aux substances chimiques (FASC) ainsi que la modélisation PBPK. Un exposé décrivant l'utilisation de chacune de ces approches est présenté ci-dessous, et de plus amples détails sont fournis dans un rapport préparé par Summit Toxicology (2015) à l'intention de Santé Canada.
8.6.1 Calcul des FASC
L'un des grands avantages de l'utilisation de facteurs d'ajustement propre aux substances chimiques (FASC) par rapport à l'utilisation de facteurs d'incertitude ou d'ajustement allométrique par défaut est que cette approche intègre à la fois les données liées aux espèces et les données propres à des substances chimiques. Malgré cette force, l'approche est fondée sur des valeurs uniques qui représentent la pharmacocinétique chez chacune des espèces, sans tenir compte nécessairement de la pharmacocinétique non linéaire.
Le respect des recommandations du Programme international sur la sécurité des substances chimiques (PISSC) à l'égard du calcul des FASC (PISSC, 2005) a permis de calculer la portion toxicocinétique du facteur d'incertitude interespèce (CAFI). Le PISSC recommande que le facteur d'incertitude interespèce de 10 soit divisé en valeurs de 4,0 (100,6) en ce qui a trait à la portion toxicocinétique (CAFI), et en valeurs de 2,5 (100,4) en ce qui a trait à l'aspect toxicodynamique (CAFI). La valeur de CAFI de 4,0 est remplacée par toute valeur de CAFI calculée selon les données propres à des substances chimiques (PISSC, 2005). Comme ces données n'étaient pas disponibles pour évaluer de façon quantitative les différences toxicodynamiques entre les espèces, aucune valeur de DAFI n'a été calculée.
L'équation suivante a été utilisée pour calculer le FICA (c.-à-d. en tenant compte des différences toxicocinétiques interespèces) :
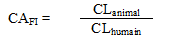
Figure 1 - Equivalent Textuel
Le CAFI pour l'APFO est calculé en divisant la clairance chez les animaux (CLanimal) par la clairance chez les humains (CLhumain).
où :
- CAFI = composante toxicocinétique du facteur d'incertitude interespèce;
- CL = clairance chez les animaux et les humains (p. ex., mL/kg p.c. par jour).
Chez les rats, une dose orale unique de 0,1 mg/kg p.c. par jour a été administrée aux rats Sprague-Dawley (4/sexe), qui ont été suivis pendant 22 jours (mâles) ou cinq jours (femelles) (Kemper et coll., 2003). À plusieurs reprises, on a relevé une clairance accrue et une diminution de la demi-vie chez les rates par rapport aux rats (voir la section 5); les femelles semblent excréter davantage l'APFO par voie urinaire que les mâles. La cause de ce phénomène n'est toutefois pas claire. C'est la raison pour laquelle les valeurs du CAFI sont présentées de façon séparée pour chaque sexe. Les taux de clairance chez les rats mâles et femelles étaient respectivement de 23,1 et de 777.
Puisqu'on n'a pas fourni de données directes sur la clairance chez les singes, les souris ou les humains, celle-ci doit être calculée en fonction des valeurs de demi-vies propres aux espèces à l'aide de l'équation suivante :
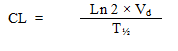
Figure 2 - Equivalent Textuel
La CL est calculée en multipliant le logarithme naturel de 2 par le volume de distribution (Vd) et en divisant le résultat par la demi-vie (T1/2) du composé.
où :
- CL est la clairance chez les animaux et les humains (L/kg p.c. par jour);
- ln 2 est le logarithme naturel de 2;
- Vd est le volume de distribution, qui est le volume théorique du sang dans lequel la quantité d'une substance chimique devrait être uniformément répartie pour produire la concentration sanguine observée; et
- T½ est la demi-vie d'un composé.
On a obtenu une demi-vie de 20,15 jours chez les singes cynomolgues en calculant la moyenne des demi-vies de singes à qui l'on avait administré une dose orale quotidienne de 10 et de 20 mg/kg p.c. pendant six mois et qui avaient été suivis pendant 147 jours après l'administration des doses (Butenhoff et coll., 2004a). Bien qu'aucun volume de distribution ne soit fourni pour les singes dans l'étude sur l'exposition chronique, on a obtenu une valeur moyenne de 190 mL/kg à partir de l'étude sur les doses uniques qui a été présentée dans la même publication (Butenhoff et coll., 2004a). Les valeurs de demi-vies chez les souris proviennent d'une étude au cours de laquelle on a administré une dose orale unique de 1 ou 10 mg/kg p.c. par jour aux souris CD-1 (3/sexe/dose) qui ont été suivies pendant une période pouvant aller jusqu'à 80 jours (Lou et coll., 2009); la valeur moyenne était de 18,7 jours. Chez les humains, on a calculé une demi-vie de 1387 jours (3,8 ans) à partir des baisses de concentrations sériques de 26 travailleurs qui avaient été, par le passé, exposés à l'APFO dans le cadre de leurs activités professionnelles et qui comptaient en moyenne 31 années de travail et 2,6 années de retraite (Olsen et coll., 2007). Malgré la disponibilité des valeurs de demi-vies des populations générales, on a choisi la demi-vie découlant des activités professionnelles parce qu'il s'agissait d'une donnée prudente et qu'elle correspondait à la plus longue demi-vie parmi les valeurs estimées à partir des données longitudinales (voir la section 8.4). Les valeurs liées au volume de distribution de l'APFO sont généralement relativement cohérentes entre les espèces (Thompson et coll., 2010); puisqu'aucune valeur liée aux volumes de distribution n'a été fournie dans les études portant sur les humains et les souris, on a utilisé une valeur de 200 mL/kg pour représenter une substance chimique dont la distribution est surtout extracellulaire. D'après l'équation ci-dessus, les valeurs de clairance résultantes s'élevaient à 6,5 mL/kg p.c. par jour chez les singes; 7,4 mL/kg p.c. par jour chez les souris et 0,1 mL/kg p.c. par jour chez les humains. D'après les ratios des valeurs de clairance entre les humains et les animaux qui ont été décrits ci-dessus, les valeurs moyennes du CAFI d'APFO qui ont été calculées pour les singes, les souris et les rats mâles et femelles étaient respectivement de 65, 74, 231 et 7774.
On a retenu la clairance comme paramètre de dose à utiliser pour le calcul des valeurs du CAFI parce que les données de ce paramètre étaient facilement accessibles chez la plupart des espèces et qu'elles pouvaient être calculées à partir des données des demi-vies chez les humains. En outre, l'utilisation de la clairance comme paramètre de dose constitue une hypothèse raisonnable pour les substances chimiques dotées d'une longue demi-vie. Selon les analyses préliminaires, les concentrations maximales pourraient permettre de mieux prévoir la toxicité de l'APFO en ce qui a trait à certains effets nocifs (Haber et coll., 2013); l'APFO n'a pas fait l'objet d'un examen dans le cadre de ces analyses. Bien que nous n'ayons pas exploré davantage cette hypothèse dans le cadre de la présente analyse, nous considérons qu'il est plus prudent d'utiliser la clairance comme alternative à l'utilisation de concentrations maximales en tant que paramètres de dose pour calculer la valeur de CAFI. Enfin, les ratios des niveaux de clairance sont habituellement considérés comme étant une base appropriée au calcul de la valeur de FICA seulement si l'on suppose que les cinétiques de premier ordre s'appliquent; toutefois, comme la clairance urinaire de l'APFO est complexe, cette hypothèse pourrait s'avérer inappropriée.
8.6.2 Modélisation PBPK
La modélisation PBPK est généralement utilisée afin de calculer les PDD pertinents pour l'humain, qui sont déterminés en appliquant un modèle PBPK pour l'humain aux paramètres des doses internes (p. ex., les concentrations d'APFO dans le plasma) qui ont été calculés ou mesurés chez les animaux. Avec des modèles qui ont été suffisamment validés, cette approche est considérée comme étant la méthode la plus solide pour réaliser des extrapolations des animaux aux humains. Nous ne faisons pas entièrement confiance aux modèles utilisant des humains, des singes et des rats, car différents codes de modèles ont été utilisés pour les différentes espèces et les correspondances entre les modèles et certains ensembles de données n'étaient pas optimales. En outre, notre compréhension limitée des raisons expliquant les différences de clairance entre les sexes qui ont été observées chez les rats signifie qu'il y a des faiblesses dans la façon dont celles-ci pourraient être traitées dans le modèle. Enfin, le principal inconvénient à utiliser une approche PBPK normale est que les modèles utilisant des humains n'ont pas été entièrement vérifiés. Les données sur les humains que l'on peut vérifier sont limitées aux études de biosurveillance qui ne permettent de réaliser que des estimations approximatives des scénarios d'exposition, et pour lesquelles les mesures des concentrations sériques n'ont généralement été calculées qu'une seule fois (des mesures à deux intervalles n'ont été prises que pour quelques populations). Bien que Loccisano et ses collègues n'aient pas élaboré de modèles PBPK utilisant des souris, les approches de modélisation de Santé Canada fondées sur des études sur des souris ont permis d'ajuster les modèles des rats à l'aide des données disponibles sur les souris. Puisque les données toxicocinétiques ne sont pas assez suffisantes pour vérifier si le modèle utilisant des souris est approprié, nous avons peu confiance en ce modèle. Par conséquent, nous n'avons pas suffisamment confiance dans les résultats des modèles PBPK pour nous en servir dans le calcul des PDD de l'évaluation des risques de l'APFO.
Comme autre approche que l'utilisation du modèle PBPK pour calculer les PDD, les ratios des paramètres des doses prévus dans le modèle PBPK ont été utilisés afin de calculer les valeurs de FICA pour les doses pertinentes. On pense que cette approche fournit des estimations plus solides des valeurs de FICA que les calculs traditionnels décrits à la section 8.6.1, car elle peut aborder la cinétique non linéaire de l'APFO, tout en déterminant les différentes valeurs à l'état d'équilibre pour les différentes doses orales administrées. En revanche, les valeurs de CAFI qui ont été calculées ci-dessus dépendent des doses spécifiques et des schémas de posologie utilisés dans des études pharmacocinétiques; des incertitudes découlent des valeurs obtenues dans ces études, car on a administré uniquement des doses uniques aux animaux, et les données sur les humains n'ont pas été obtenues à partir d'études sur l'administration de doses contrôlées. En outre, comme les valeurs de CAFI fondées sur la clairance constituent des rapports entre les faibles doses chez les humains et les doses élevées chez les animaux, les expositions entre les espèces ne sont pas du même ordre de grandeur; l'utilisation de la modélisation PBPK afin de calculer la valeur de CAFI permet de comparer de façon plus appropriée des doses du même ordre de grandeur.
La concentration d'APFO à l'état d'équilibre constitue le paramètre de dose choisi pour les valeurs de CAFI qui ont été calculées selon la modélisation PBPK. Elle a été sélectionnée, car il s'agit d'une donnée généralement pertinente pour les substances chimiques dotées d'une longue demi-vie et d'une hypothèse prudente. Bien que d'autres paramètres de doses - dont les concentrations maximales (Haber et coll., 2013) - pourraient permettre de prévoir davantage la toxicité de l'APFO en ce qui a trait à certains effets nocifs, aucune autre étude n'a été réalisée afin de mieux déterminer le paramètre de dose le plus approprié. Le plasma a été choisi comme tissu pertinent pour les concentrations à l'état d'équilibre, puisqu'il s'agit d'un paramètre qui peut servir de mesure approximative pour une grande variété d'organes en raison de la circulation du sang vers ces différents organes. Les concentrations à l'état d'équilibre du foie ont également été intégrées dans l'évaluation afin de comparer celles-ci aux valeurs de CAFI fondées sur le plasma, car des études pharmacocinétiques ont déterminé que le foie était l'organe principal de distribution de l'APFO et qu'il s'agissait d'un organe cible potentiel de la toxicité. Nous avons toutefois moins confiance dans les valeurs fondées sur le foie que dans les valeurs fondées sur le plasma, puisque très peu de données pharmacocinétiques sont disponibles pour vérifier si le modèle PBPK permet de déterminer les concentrations dans le foie. Les concentrations dans le foie n'ont pas été vérifiées pour les humains, les souris et les singes; en ce qui concerne les rats, une vérification minime a pu être réalisée, mais comme les données n'étaient disponibles que pour l'un des deux intervalles dans chacune des études, les comparaisons ne sont pas solides. En outre, l'utilisation de concentrations plasmatiques comme mesure approximative d'une variété d'organes simplifie l'application des valeurs de CAFI dans l'évaluation, qui est déjà complexe en raison de l'utilisation de valeurs de FICA propres aux espèces et aux doses.
À l'aide des modèles PBPK de Loccisano qui sont décrits à la section 8.5, on a pu obtenir des concentrations plasmatiques et hépatiques à l'état d'équilibre à diverses doses pour chacune des espèces. Les mêmes doses ont été utilisées pour chacune des espèces. Pour chaque cycle de dosage du modèle PBPK, les ratios de concentrations d'APFO à l'état d'équilibre chez les humains et les autres espèces ont été calculés afin d'obtenir des valeurs de FICA propres aux doses et aux espèces (Summit Toxicology, 2015). Les concentrations à l'état d'équilibre et les valeurs de FICA pour le plasma et le foie à des doses possiblement pertinentes sont énumérées dans le tableau 2.
Afin de sélectionner une valeur de CAFI pour chaque PDD, celui-ci est arrondi à la valeur inférieure le plus près dans la colonne des doses orales (c.-à-d., les valeurs de même ordre de grandeur sont utilisées). Tel qu'il est mentionné plus haut, nous avons peu confiance dans le modèle PBPK utilisant des souris. On recommande par ailleurs d'utiliser les valeurs de CAFI liées aux rats jusqu'à ce qu'un modèle PBPK soit élaboré en fonction des données disponibles sur les souris (Summit Toxicology, 2015).
| Mesure | Espèce | Dose (mg/kg p.c. par jour) | |||
|---|---|---|---|---|---|
| 0,001 | 0,01 | 0,1 | 1 | ||
| Prévisions des concentrations plasmatiques d'APFO à l'état d'équilibre (µg/mL) | Humains | 8,74 | 86,1 | 706 | 1493 |
| Singes | 0,17 | 1,61 | 11,5 | 38,9 | |
| Souris | 0,05Note de bas de page 1 | 0,47 | 4,74 | 47,4 | |
| Rats | 0,09 | 0,9 | 8,96 | 89,5 | |
| Prévisions des concentrations hépatiques d'APFO à l'état d'équilibre (µg/mL) | Humains | 19,2 | 189 | 1555 | 3289 |
| Singes | 0,37 | 3,58 | 25,5 | 88,3 | |
| Souris | NC | NC | NC | NC | |
| Rats | 0,32 | 3,16 | 31,6 | 316 | |
| FICA calculés à partir des prédictions des concentrations plasmatiques | Singes | 52 | 53 | 62 | 38 |
| SourisNote de bas de page 2 | 184 | 182 | 149 | 31 | |
| Rats | 97 | 96 | 79 | 17 | |
| FICA calculés à partir des prédictions des concentrations hépatiques | Singes | 52 | 53 | 61 | 37 |
| SourisNote de bas de page 2 | NC | NC | NC | NC | |
| Rats | 61 | 60 | 49 | 10 | |
|
|||||
8.6.3 Approche recommandée pour l'extrapolation interespèce
L'approche recommandée à l'égard de l'extrapolation interespèce est l'utilisation d'un modèle PBPK afin de calculer la composante de CAFI du FASC en utilisant les concentrations plasmatiques à l'état d'équilibre comme paramètre de dose. L'utilisation de concentrations plasmatiques assure la pertinence du paramètre de dose par rapport aux effets nocifs qui affectent une variété d'organes. Lorsqu'ils sont disponibles, les paramètres de doses propres aux organes sont généralement préférables aux valeurs fondées sur le sang; l'utilisation de paramètres plasmatiques dans le cadre de cette évaluation est toutefois cohérente avec l'application de la valeur de CAFI à une grande variété d'effets néfastes. Les valeurs de CAFI ont été calculées afin d'obtenir des paramètres pour le foie et de comparer ceux-ci avec les valeurs plasmatiques; le comportement de l'APFO dans le foie était similaire à celui dans le plasma, et les estimations des valeurs de CAFI étaient du même ordre dans les deux compartiments. Ces résultats indiquent que les valeurs plasmatiques constituent des mesures approximatives appropriées à utiliser dans le cadre d'un examen des effets hépatiques nocifs. Les valeurs fondées sur le foie chez les rats étaient légèrement inférieures, car il y avait davantage de données disponibles pour vérifier ce compartiment du modèle PBPK. Les valeurs de CAFI propres aux doses et aux espèces (pour les concentrations plasmatiques à l'état d'équilibre) dans le tableau 3 sont utilisées dans les sections 10.1 et 10.2.
Bien que les valeurs de CAFI dérivées du modèle PBPK aient été choisies comme approche recommandée dans le cadre de cette évaluation, plusieurs faiblesses ont été identifiées. Tel qu'il a été décrit plus haut, la valeur de CAFI était fondée sur le plasma plutôt que sur un organe en particulier. Les concentrations à l'état d'équilibre ont par ailleurs été sélectionnées pour servir de paramètre de dose, puisqu'elles permettaient de formuler une hypothèse prudente qui était pertinente à la nature du composé; aucun examen approfondi n'a été mené afin de déterminer si d'autres paramètres de dose (p. ex., des concentrations maximales) seraient plus appropriés pour évaluer les différents effets nocifs. L'état d'équilibre n'a également pas été atteint dans le modèle utilisant des humains à des doses inférieures à 0,1 mg/kg p.c. par jour. En outre, les modèles PBPK n'ont pas été élaborés spécialement pour la souris et ont été ajustés à partir du modèle appliqué aux rats sans qu'on utilise d'autres données pharmacocinétiques à des fins de vérification; on recommande toutefois d'appliquer les valeurs de CAFI pour les rats aux souris en l'absence de données solides pour cette espèce. De plus, les valeurs de CAFI pour les rats sont calculées en fonction uniquement de rats mâles malgré l'observation d'une clairance plus rapide -et, par conséquent, de plus grandes différences interespèces - observées chez les femelles.
Malgré ces faiblesses, nous pensions que l'utilisation du modèle PBPK pour calculer les valeurs de CAFI était équivalente ou plus solide par rapport aux autres approches potentielles d'extrapolation interespèce. L'approche sélectionnée intègre de façon quantitative les différences pharmacocinétiques entre les espèces; les cinétiques non linéaires de l'APFO sont toutefois traitées, ce qui ne peut être effectué avec l'approche par défaut de calcul des valeurs de CAFI. En outre, les valeurs de CAFI dérivées du modèle PBPK ne sont pas fondées sur des études pharmacocinétiques individuelles qui sont souvent des études à doses uniques et qui ne sont pas facilement comparables entre les espèces. L'approche idéale pour examiner les différences entre les espèces serait d'utiliser les concentrations sanguines de l'APFO - soit en utilisant des modèles pharmacocinétiques afin d'estimer les concentrations telles qu'elles sont employées par Wambaugh et ses collègues (2013), ou en utilisant les valeurs qui sont spécifiquement mesurées dans les études individuelles - comme PDD pour l'évaluation. Les modèles PBPK utilisant des humains qui seraient employés pour réaliser une extrapolation à partir de ces concentrations sériques ne peuvent être entièrement vérifiés selon les données pharmacocinétiques existantes sur les humains, ce qui diminue le niveau d'aisance à utiliser cette approche pour estimer des PDD précis. L'approche recommandée a été choisie comme moyen de quantifier les différences interespèces, tout en examinant la cinétique non linéaire de l'APFO, sans s'appuyer sur des estimations précises de PDD découlant du modèle PBPK.
9.0 Effets sur la santé
Le résumé de la documentation portant sur les effets sur la santé de l'APFO est principalement fondée sur un examen complet qui a été réalisé par un consultant (Sanexen Environmental Services Inc., 2013). Ce résumé comprend seulement les études directement pertinentes au calcul de la valeur basée sur la santé.
9.1 Effets sur les humains
9.1.1 Toxicité aiguë
Nous n'avons pu trouver aucun renseignement lié à des études épidémiologiques aiguës ou à court terme.
9.1.2 Toxicité subchronique et chronique
De nombreuses études épidémiologiques de qualité ont été menées. D'importantes cohortes de travailleurs et de populations exposées dans leur milieu ont fait l'objet de suivis, ce qui a permis d'observer des relations importantes entre l'exposition à l'APFO et les divers effets sur la santé, comme les biomarqueurs hématologiques et cliniques (le cholestérol et l'acide urique), le cancer (des testicules, du rein), la prééclampsie, les fonctions immunologiques, endocrines (thyroïde) et rénales et les effets sur la fécondité (qualité du sperme, poids à la naissance). Bien que toutes ces études comportent leurs limites dans une certaine mesure, notamment en ce qui a trait au modèle d'étude, aux biais et aux facteurs de confusion, le poids de la preuve liée aux humains fournit un solide argument en faveur des effets préjudiciables à la santé du composé. Ces renseignements devraient en principe appuyer le choix d'un effet sur la santé; le calcul d'une dose d'exposition sécuritaire pour les humains à partir d'études sur les humains demeure toutefois un défi en raison des difficultés que présente la caractérisation d'une relation dose-réponse avec les études actuelles. Leur utilisation dans le cadre de l'évaluation actuelle est importante afin de vérifier la pertinence de l'extrapolation des animaux aux humains. En outre, la surveillance des études à venir contribuera à déterminer l'exactitude des associations observées.
La plupart des études environnementales qui ont été menées auprès de populations exposées à l'APFO ont été réalisées dans la Vallée du Mid-Ohio dans le cadre du C8 Science Project. Le C8 Science Panel, composé d'épidémiologistes indépendants qui ont été sélectionnés conjointement par des avocats de la communauté et de l'entreprise DuPont, s'est réuni à la suite du règlement de recours collectif contre cette dernière. Le C8 Science Project, qui compte des résidents de communautés de l'Ohio et de la Virginie-Occidentale habitant dans des zones avoisinantes de l'usine de DuPont Washington Works, constitue la plus grande étude menée auprès d'une population exposée à l'APFO par l'eau potable. L'enquête sanitaire a été réalisée en 2005-2006 auprès de 69 000 personnes, incluant des enfants et des adultes. La concentration sérique moyenne d'APFO dans cette population était de 28,2 ng/mL, comparativement à une moyenne de 4,2 ng/mL dans la population américaine générale au cours de la même période (Frisbee et coll., 2009). Quelques études longitudinales et prospectives ont également été menées auprès de cette population à la suite d'une période de suivi. Certaines données récentes du projet n'ont pas encore été publiées dans des publications examinées par les pairs; les résumés de ces études -ainsi que les conclusions du groupe d'experts et de plus amples renseignements sur les membres de celui-ci - sont disponibles sur le site Web du C8 Science Panel.
9.1.2.1 Effets sur le foie
Bien qu'on ait observé un certain niveau d'association entre l'exposition à l'APFO et l'altération des enzymes hépatiques, aucune tendance claire n'a été définie. Une association négative entre l'APFO et la bilirubine et une association positive entre l'APFO et l'aspartate aminotransférase (AST) et la gammaglutamyle transpeptidase (GGT) ont été relevées chez des travailleurs (Sakr et coll., 2007a; Sakr et coll., 2007b). Des augmentations anormales des enzymes hépatiques (GPT et GGT) ont été signalées dans une étude transversale qui a été menée auprès d'adultes âgés de 18 ans et plus dans l'ensemble de la population américaine, particulièrement chez des personnes obèses ou des sujets qui avaient développé une résistance à l'insuline ou des syndromes métaboliques (Lin et coll., 2010). L'importance clinique des résultats obtenus au sein de la population exposée à l'APFO dans le cadre de leurs activités professionnelles n'est pas claire, car les ordres de grandeur des changements étaient petits et incohérents (Steenland et coll., 2010a). En outre, le nombre élevé des effets analysés augmente également la probabilité des résultats liés au hasard. L'interprétation causale des résultats issus de la population générale est limitée par le modèle d'étude, et l'analyse excluait plusieurs covariables.
9.1.2.2 Lipidémie
Plusieurs études ont associé une exposition accrue à l'APFO aux augmentations des taux sériques de cholestérol. Une étude récente menée auprès d'importantes cohortes de travailleurs et de résidents exposés à l'APFO dans leur milieu a révélé que le risque de développer une hypercholestérolémie s'accentuait avec une grande exposition à l'APFO comparativement à une exposition plus faible (Winquist et Steenland, 2014). Une petite étude longitudinale menée auprès de travailleurs en Italie a démontré une association positive entre l'APFO et le taux de cholestérol total (Costa et coll., 2009). Une étude transversale et une étude longitudinale ont été menées auprès des employés affectés à la production de l'entreprise DuPont. Dans le cadre de l'étude transversale, on a observé des associations positives entre l'APFO et le taux de cholestérol total, de cholestérol LDL et de cholestérol VDLD (Sakr et coll., 2007a). Dans le cadre de l'étude longitudinale, on a observé une association négative avec la bilirubine et on a relevé des associations positives entre les concentrations sériques d'APFO et le taux de cholestérol total après l'ajustement des facteurs de confusion (Sakr et coll., 2007b).
Les études sur les travailleurs affectés à la production de substances fluorées dans les usines américaines et européennes de 3M (Olsen et Zobel, 2007) ont révélé des résultats incohérents en ce qui a trait à l'association entre l'APFO et le cholestérol et les lipoprotéines. Une étude sur l'exposition professionnelle (Olsen et coll., 2012) a permis d'observer une hausse du taux de cholestérol HDL et une diminution du rapport entre le cholestérol total et le cholestérol HDL, et n'a démontré aucun changement dans les taux de cholestérol total et de cholestérol non HDL. Dans le cadre du C8 Health Project, on a constaté des associations entre les concentrations sériques d'APFO et différents composants sanguins, comme une augmentation des taux de cholestérol, chez des enfants et des adultes (Steenland et coll., 2009, Frisbee et coll., 2010, Kerger et coll., 2011). On a également observé des associations avec les lipoprotéines (LDL, HDL), bien que celles-ci soient incohérentes entre les études. On a par ailleurs constaté une association positive avec le cholestérol dans la population américaine générale (Nelson et coll., 2010), alors qu'une autre étude transversale réalisée dans la vallée du Mid-Ohio n'a pas permis de découvrir une telle association (Emmett et coll., 2006b). Une étude longitudinale menée auprès de 560 adultes (de 2005 à 2006, avec un suivi en 2010) a indiqué que le taux de cholestérol LDL diminuait avec la diminution des concentrations sériques d'APFO. On a constaté une tendance similaire (mais qui n'est pas statistiquement significative) pour le taux de cholestérol total; aucun changement n'a toutefois été dénoté pour le cholestérol HDL ou les triglycérides (Fitz-Simon et coll., 2013).
Dans l'ensemble, malgré une incohérence sur le plan de l'exposition et des effets observés, les données de l'étude transversale et de l'étude longitudinale indiquent un certain niveau d'association entre les concentrations sériques d'APFO et le taux de cholestérol total ou de cholestérol LDL observé chez différentes populations. L'association était généralement plus forte dans la population générale que chez les travailleurs. En tenant compte du poids de la preuve, le C8 Science Panel (2012a) a conclu qu'il y avait probablement un lien entre une cholestérolémie élevée et l'APFO. L'importance clinique est toutefois incertaine, compte tenu des incohérences des résultats, du mécanisme d'action inconnu, des limites inhérentes au modèle d'étude et de la faible ampleur des changements. Plus précisément, les conclusions et les associations qui ont été constatées dans les études de cohortes sont limitées par le risque d'erreurs de sélection et de mauvaise classification ainsi que les variables incontrôlées, puisqu'on a perdu certaines associations lors de la stratification par endroit des participants (Costa et coll., 2009; Winquist et Steenland, 2014).
9.1.2.3 Perturbations thyroïdiennes
Des effets incohérents sur les taux d'hormones thyroïdiennes ont été observés dans les populations exposées à l'APFO. Une étude sur l'exposition professionnelle réalisée auprès de 552 employés de trois usines différentes a révélé qu'il y avait une association négative entre l'APFO et la thyroxine libre, ainsi qu'une association positive entre l'APFO et la triiodothyronine après l'ajustement des facteurs confusionnels (Olsen et Zobel, 2007).Aucun ajustement n'a toutefois été apporté pour le SPFO, et les auteurs ont indiqué qu'ils n'avaient établi aucun lien entre l'APFO et les hormones thyroïdiennes, car les résultats étaient incohérents et se situaient dans les valeurs normales. Par ailleurs, deux autres études sur l'exposition professionnelle (Olsen et coll., 1998, 2003 b) n'ont révélé aucun lien important entre l'APFO et les taux de T3, de T4 ou de TSH. Plusieurs études transversales (le C8 Health Project et l'enquête NHANES) ont évalué la relation entre l'exposition environnementale à l'APFO et les fonctions thyroïdiennes. Ces études ont démontré des altérations dans les taux de thyroxine, le transfert de la T3, la sérum-albumine, l'hypothyroïdie chez les enfants et la maladie thyroïdienne chez les femmes (Chan et coll., 2011; Knox et coll., 2011b; Lopez-Espinosa et coll., 2012). La temporalité ne peut toutefois pas être établie avec le modèle d'étude et il est impossible de connaître les concentrations sériques de l'APFO avant le développement de la maladie thyroïdienne. Une étude menée en Corée du Sud (Kim et coll., 2011) a établi une corrélation positive entre les concentrations sériques d'APFO chez la mère et les taux de TSH chez le fœtus (mais pas des taux de T3 ou de T4) après l'ajustement des covariables.
9.1.2.4 Hypertension et effets cardiovasculaires
Des études transversales et de cohorte (Sakr et coll., 2007a; Costa et coll., 2009; Steenland et coll., 2010b) n'ont établi aucun lien constant entre les troubles cardiovasculaires et l'APFO. Par ailleurs, une étude de cohorte occupationnelle (Lundin et coll., 2009) a permis d'associer les longues expositions à l'APFO à un risque accru de maladie cérébrovasculaire, alors que des études transversales de la population américaine générale (Shankar et coll., 2012; Min et coll., 2013) les associaient à un risque de maladie cardiovasculaire, de maladie artérielle périphérique, de tension artérielle systolique et de marqueur d'inflammation. Ces résultats équivoques n'ont pas été confirmés dans d'autres études transversales (Leonard et coll., 2008; Sakr et coll., 2009; Steenland et Woskie, 2012) ni dans une autre étude transversale menée auprès de la population générale (Melzer et coll., 2010). Le C8 Science Panel a conclu qu'il n'y avait probablement aucun lien entre l'exposition à l'APFO et un diagnostic d'hypertension artérielle et d'une maladie coronarienne (y compris un infarctus du myocarde, une angine et un pontage coronarien) (C8 Science Panel, 2012a).
9.1.2.5 Effets sur les reins
Bien qu'on ait observé un lien entre les effets nocifs sur les reins et l'APFO, plusieurs facteurs limitent la généralisation des résultats à la population générale. Une étude de cohorte sur la mortalité menée auprès de 5 791 employés d'une usine de DuPont Chemical (Steenland et Woskie, 2012) a démontré un risque accru de développer une maladie rénale. Ce niveau de preuves ne permet pas de faire un lien de causalité entre une réduction de la fonction rénale et l'exposition à l'APFO, notamment parce qu'une altération de la fonction rénale pourrait entraîner une hausse des concentrations sériques de l'APFO. De même, si l'APFO induit des effets nocifs sur les reins, les concentrations élevées d'APFO sont susceptibles de modifier la fonction rénale. En outre, l'étude sur l'exposition professionnelle n'a permis d'observer qu'un petit nombre de cas (tel que l'attestait la grande marge d'erreur), et plusieurs travailleurs ont été perdus de vue pendant le suivi, augmentant ainsi le risque de biais de sélection. L'étude n'a pas pu par ailleurs s'appuyer sur les résultats d'une autre étude de cohorte non publiée menée dans la même région.
9.1.2.6 Diabète
Le lien possible entre l'APFO et le diabète a fait l'objet d'un examen dans certaines études sur la mortalité menées auprès de travailleurs qui étaient exposés à l'APFO dans le cadre de leurs activités professionnelles (Leonard et coll., 2008, Lundin et coll., 2009, Steenland et Woskie, 2012), ainsi que dans deux études environnementales sur la prévalence du diabète menées dans le cadre du C8 Health Project (MacNeil et coll., 2009, Groupe d'experts scientifiques du projet C8, 2012b). Les résultats des études sur l'exposition professionnelle des employés d'une usine de l'entreprise 3M située à Cottage Grove, au Minnesota, et de l'usine de polyfluorimère de DuPont, étaient incohérents. Étant donné que le diabète n'est généralement pas une maladie mortelle (et que celle-ci n'est pas nécessairement indiquée sur les certificats de décès) et que la mortalité n'est peut-être pas la meilleure façon d'étudier le diabète (C8 Science Panel, 2012b), les résultats fondés sur la prévalence du diabète dans les populations résidentielles exposées à l'APFO ne sont peut-être pas fiables. Les données disponibles provenant des études environnementales transversales menées dans le cadre du C8 Health Project (MacNeil et coll., 2009, C8 Science Panel, 2012b) suggèrent qu'il n'existe aucun lien entre l'APFO et le diabète de type II.
9.1.2.7 Immunosuppression
Bien que des études menées auprès de populations exposées à l'APFO dans leur milieu aient permis d'établir des liens entre les concentrations d'APFO et la diminution d'anticorps correspondant à diverses maladies, l'influence de l'exposition à l'APFO sur l'immunosuppression clinique (c.-à-d., l'incidence de maladies) semble plus ténue. Une étude menée auprès d'enfants a permis d'établir un lien inversé entre la réponse immunitaire et l'exposition à l'APFO (Grandjean et coll., 2012; Grandjean et Budtz-Jørgensen, 2013) et d'observer une corrélation négative entre l'exposition prénatale à l'APFO et les concentrations d'anticorps antidiphtériques. On a associé la concentration deux fois plus élevée d'APFO chez les enfants de cette population aux probabilités accrues de ne pas atteindre des taux normaux d'anticorps protecteurs pour le tétanos et la diphtérie à la suite d'une vaccination à l'âge de sept ans (Grandjean et coll., 2012). Le caractère prospectif, la taille de l'échantillon, le faible risque de biais de sélection et les objectifs définis permettent d'obtenir des résultats pertinents pour la population étudiée; la pertinence pour d'autres populations est toutefois discutable, puisque l'exposition accrue à d'autres immunosuppresseurs potentiels de cette région (les îles Féroé) n'a pas été prise en considération dans l'étude. L'exposition accrue à l'APFO a également été associée à une diminution des anticorps contre la rubéole (chez les enfants d'une cohorte de naissance prospective de femmes enceintes vivant en Norvège, 2007-2008) (Granum et coll., 2013) et la grippe (pour le virus de type A/H3N2 seulement). On a également observé un risque plus élevé de ne pas atteindre le seuil reconnu de la grippe A/H3N2 (Looker et coll., 2014). Une étude de cohorte prospective de femmes enceintes menée entre 2002 et 2005 au Japon (Okada et coll., 2012) a révélé que la quantité d'IgE dans le sang du cordon ombilical diminue avec l'exposition de la mère à l'APFO chez les nourrissons de sexe féminin.
Une cohorte danoise (1996-2002) (Fei et coll., 2010a) n'a pas associé des hospitalisations pour des infections à l'exposition prénatale à l'APFO; on a toutefois observé des associations positives entre l'exposition de la mère à l'APFO et le taux d'incidence de rhumes et de gastroentérites dans la cohorte de naissances norvégienne (Granum et coll., 2013).
Les différentes études présentent un certain niveau de cohérence, puisqu'elles ont généralement permis d'observer un lien entre l'exposition environnementale à l'APFO et les effets immunomodulateurs chez les enfants de différentes ethnies. La diversité des contextes de l'étude et la nature prospective des modèles d'étude par observation diminuent les risques d'associations erronées et permettent de mieux généraliser les résultats.
La taille de l'ensemble des données demeure toutefois relativement petite avec seulement cinq études, qui ont toutes été menées par observation. De plus, le risque de confusion résiduelle, de biais et de résultats liés au hasard ne peut être écarté. Bien que les études examinaient les effets sur le système immunitaire, les résultats n'étaient pas précis (différents effets mesurés), aucune relation claire entre les doses et la réponse n'a été établie et la plupart des associations étaient faibles. Les données comportaient souvent des résultats conflictuels et des variations entre les sexes, les immunoglobulines microbiennes spécifiques, les APFA, les infections, l'exposition de la mère par rapport à celle de l'enfant et le niveau de scolarité des enfants et d'autres caractéristiques. Ces failles empêchent la conclusion d'un mécanisme de facteurs de cause. De plus, la nature de l'association demeure imprécise.
9.1.2.8 Maladie auto-immune
Le C8 Science Panel (étude non publiée) a découvert qu'une exposition cumulative accrue à l'APFO augmentait le risque de développer une maladie intestinale inflammatoire, une constatation qui a été alimentée par l'établissement d'associations avec la colite ulcéreuse. Le C8 Science Panel a conclu qu'il y avait probablement un lien entre l'APFO et la colite ulcéreuse (C8 Science Panel, 2012c). Il n'y a toutefois pas de risque de biais de sélection, car le groupe d'experts a été en mesure de n'inclure qu'une seule partie de l'échantillon de la population, puisqu'il ne comptait que les participants dont les dossiers médicaux étaient accessibles et pour lesquels il était possible de calculer des estimations d'exposition. Ces résultats sont préoccupants et devraient être corroborés par de futures études.
9.1.3 Cancérogénicité
Plusieurs études de cohorte sur l'exposition professionnelle et environnementale à l'APFO ont été menées. Les études américaines sont considérées comme étant les études de plus haute qualité, car elles sont fondées sur des registres comportant tous les résidents d'une zone d'étude; elles ont été réalisées dans les districts présentant de grands contrastes mesurés de concentrations d'APFO dans l'eau; elles étaient liées aux données des registres du cancer; elles comportaient un vaste échantillon de population; et elles ont été ajustées afin de tenir compte des facteurs confusionnels.
Une étude de cas a été menée auprès des résidents du Mid-Ohio vivant près de l'usine de fabrication de Teflon de l'entreprise DuPont afin d'examiner le lien entre le cancer et l'exposition à l'APFO par l'absorption d'eau potable. L'étude a révélé que les concentrations élevées d'APFO étaient associées aux cancers des testicules à certains endroits (Vieira et coll., 2013). Parmi les effets cancérogènes, la probabilité de développer un cancer des testicules était uniquement élevée dans l'une des deux régions présentant une concentration élevée d'APFO dans l'eau potable. L'étude n'a signalé aucune hausse statistiquement significative de la probabilité de développer un cancer chez le nombre total de résidents exposés, dans les autres districts ou dans toute catégorie de niveau de dose (sauf en ce qui concerne la catégorie de dose maximale). L'incidence du cancer du rein a augmenté de façon importante dans l'un des districts et dans les deux niveaux plus élevés d'exposition individuelle. Aucune association importante n'a été signalée pour les cancers du sein, de la prostate et des ovaires ainsi que pour le lymphome non hodgkinien. Bien que cette étude démontre certains liens entre le cancer et l'exposition à l'APFO, la signification des résultats reliés aux cancers demeure incertaine, car aucune relation dose-réponse n'a été observée, la variabilité des estimations du risque était élevée, le nombre de cas était peu élevé, plusieurs effets avaient été calculés selon deux approches de modélisation (géographique et individuelle) et il y avait un risque de biais de classification de l'exposition (le manque de renseignements sur les antécédents résidentiels à tenir compte en ce qui a trait à la durée d'exposition, à la latence, à la migration et à d'autres enjeux concernant le moment d'exposition par rapport au cancer). L'analyse géographique (les résultats de l'incidence du cancer testiculaire dans l'étude menée au Mid-Ohio) portait sur les biais et le risque de confusion inhérents aux études écologiques.
On a associé l'exposition cumulative à l'APFO (estimations rétrospectives de concentrations sériques logarithmiques) au risque accru de déclaration de cancers des testicules, du rein et de la thyroïde chez une vaste cohorte (n = 32 254) de participants du C8 Health Project et d'employés de l'usine de fabrication de Teflon de l'entreprise DuPont âgés de 20 ans et plus (moyenne de 53 ans) après la stratification selon l'âge et l'ajustement des facteurs liés au tabagisme, à la consommation d'alcool, au sexe et à l'éducation (Barry et coll., 2013). Certains cas faisaient également partie des études de Barry et coll. (2013) et de Vieira et coll. (2013). Les associations qui étaient vraisemblablement moins attribuables au hasard uniquement (les valeurs p inférieures) étaient celles entre la concentration sérique logarithmique cumulative d'APFO et les risques de développer un cancer des testicules (selon les approches géographiques et individuelles à l'égard de l'étude de l'eau du district) et un cancer du rein (selon l'analyse résidentielle et l'approche individuelle). On a considéré que les associations avec le cancer de la thyroïde et le mélanome étaient liées au hasard en raison du manque de statistiques. Les associations étaient toutefois incohérentes entre les quartiles et les scénarios d'exposition (p. ex., résidentielle et géographique) après une période de suivi (avec très peu ou pas de cas de cancer des testicules depuis 2005, alors que les taux historiques indiquaient la prévision d'une incidence de cinq cas) et de perte en ce qui concerne les risques de cancer des testicules, du rein et de la thyroïde, comparativement avec les taux de la population américaine générale. En outre, l'IC de 95 % des ratios de hasard était importante, les tendances des risques de cancer des testicules, du rein et de la thyroïde ont été vraisemblablement attribuées au hasard dans au moins un scénario d'exposition, Barry et coll. (2013) ont mentionné la vraisemblance de l'exposition et des erreurs de classification des résultats, et les tendances signalées pour les cancers des testicules reposaient sur seulement six cas dans le groupe exposé à une dose élevée (C8 Science Panel, 2012 b; Barry et coll., 2013).
Une autre étude sur l'exposition professionnelle réalisée auprès de travailleurs du Minnesota a permis d'observer un risque accru de mortalité liée au cancer de la prostate; l'incertitude persiste toutefois en raison du nombre peu élevé de cas, ce qui entraîne un manque de précision dans les estimations des risques (Lundin et coll., 2009). Aucun excès statistiquement significatif de décès liés au cancer du rein, du foie, du pancréas, des testicules, de la thyroïde ou du sein n'a été signalé au cours d'une autre étude sur l'exposition professionnelle menée en Virginie-Occidentale (Leonard et coll., 2008) ou au cours de la période de suivi de six ans de cette cohorte, à l'exception d'un taux de mortalité excessif lié au cancer du rein (Steenland et Woskie, 2012). Il faut interpréter ces résultats avec prudence, car ceux-ci étaient reliés à un nombre peu élevé de cas, et le risque de biais de sélection était considérable.
Une étude de cohorte prospective réalisée auprès de la population générale du Danemark n'a permis de déceler aucune hausse de l'incidence du cancer de la prostate, de la vessie, du pancréas ou du foie, alors que les concentrations plasmatiques d'APFO (concentration plasmatique chez des hommes atteints du cancer : 6,8 ng/mL [5 à 95 % percentiles : 3,1 à 14,0]; des femmes atteintes du cancer : 6,0 ng/mL [5 à 95 % percentiles : 2,6 à 11,0]) étaient généralement inférieures à celles des cohortes américaines (moyenne de 76,5 ng/mL (SD = 208) en ce qui concerne la concentration sérique chez les hommes et de 42,3 ng/mL (écart-type = 118) chez les femmes d'une population d'une communauté exposée selon Frisbee et coll. [2009]; et aussi élevé qu'une moyenne de 2,210 ng/mL (écart-type = 6,4) dans le sérum des employés de fabrication d'APFO tel que le rapportent Olsen et Zobel [2007]) (Eriksen et coll., 2009). De plus, une petite étude de cas-témoins réalisée chez les Inuits du Groenland (Bonefeld-Jorgensen et coll., 2011) n'a fourni aucune preuve d'une relation entre l'APFO et le cancer du sein.
Le C8 Science Panel (2012b) a évalué le lien probable entre l'exposition à l'APFO et le cancer. Le « lien probable » défini par le groupe d'experts scientifiques signifie « qu'il est plus probable qu'improbable qu'il existe un lien entre l'exposition à l'APFO et une maladie humaine donnée parmi les membres d'un groupe compte tenu des données scientifiques disponibles ». Les cancers du rein et des testicules constituaient les types de cancers particuliers sur lesquels l'association était fondée. Il est toutefois impossible de déterminer la relation causale, puisque l'ensemble des données comportait des incohérences et que les risques de cancer étaient équivoques dans les études (manque de cohérence). En outre, l'interprétation du risque accru observé de formation de cancers du rein et des testicules est limitée par le risque de confusion résiduelle (parce que le modèle ne comprenait pas toutes les covariables et les autres expositions aux autres contaminants), les nombres peu élevés de cas, les incertitudes quant à la caractérisation de l'exposition (laquelle était estimée approximativement en fonction de la résidence dans une certaine zone) et le nombre élevé de résultats compris dans les modèles, augmentant ainsi la vraisemblance de résultats liés au hasard. Compte tenu de ces facteurs, il serait prématuré de fonder une recommandation sur le risque de cancer dans les études épidémiologiques sans avoir mieux compris la causalité possible entre l'APFO et les cancers observés. On propose de continuer la surveillance des preuves épidémiologiques afin de mieux comprendre la relation entre l'APFO et le risque de cancer.
9.1.4 Toxicité pour le développement et la reproduction
9.1.4.1 Toxicité pour le développement
Selon les données disponibles sur l'âge gestationnel, le poids et la grandeur à la naissance, la circonférence de la tête et de l'abdomen ou de la poitrine, les stades de développement, les fausses couches et les anomalies congénitales, les examens antérieurs des études épidémiologiques sur le développement ont permis de conclure que l'APFO ne devrait pas induire des effets sur le développement des humains (Olsen et coll., 2009). Bien qu'on observe des augmentations du risque de certains de ces résultats dans les études individuelles, il y avait un manque de cohérence entre les études. De nouvelles études environnementales ont démontré une association positive entre l'exposition prénatale à l'APFO et l'obésité chez la progéniture de sexe féminin à l'âge de 20 ans (Halldorsson et coll., 2012), ainsi qu'une association négative entre les concentrations sériques d'APFO chez la mère et le poids à la naissance et les paramètres anthropométriques connexes à la naissance (Apelberg et coll., 2007; Fei et coll., 2007; 2008 b; Andersen et coll., 2010; Maisonet et coll., 2012; Whitworth et coll., 2012a).
Les propriétés obésogènes de l'APFO et d'autres APFA ont fait l'objet d'une enquête dans le cadre d'une étude de cohorte prospective et d'un suivi à long terme (20 ans) menés auprès de femmes enceintes recrutées dans la cohorte nationale de naissances du Danemark (1988-1989) et de leur progéniture (Halldorsson et coll., 2012). À l'âge de 20 ans, la progéniture de sexe féminin des mères chez qui l'on avait observé des concentrations sériques élevées d'APFO était plus susceptible d'avoir un excès de poids et d'avoir une circonférence de taille élevée après l'ajustement des facteurs liés à l'éducation de la mère, à l'indice de masse corporelle (IMC), au tabagisme, à l'âge et au poids à la naissance du nourrisson. Cette grande étude longitudinale a également démontré une altération des biomarqueurs sériques se traduisant par une augmentation des concentrations d'APFO chez les mères (une augmentation du taux sérique d'insuline et de leptine et une baisse du taux d'adiponectine sérique chez la progéniture de sexe féminin), ce qui suggère une plausibilité biologique. L'analyse ne comprenait toutefois pas de facteurs confusionnels importants, comme l'activité physique et un régime alimentaire, ce qui est susceptible de donner lieu à des associations erronées. Les auteurs ont également indiqué que le suivi impossible constituait la principale limite de l'étude. D'autres études comportant de meilleurs ajustements et suivis auprès de différentes populations seraient nécessaires afin de confirmer les associations observées.
Les données qui sont actuellement disponibles concernant le lien entre l'APFO et un faible poids à la naissance ne sont pas cohérentes. Certaines études ont signalé des associations positives au sein de la population générale, alors que d'autres études n'ont rapporté aucune association dans la population générale et les communautés qui sont grandement exposées à l'APFO par l'absorption d'eau potable. Des études longitudinales réalisées auprès de l'ensemble des populations danoise et britannique ont démontré des associations inverses entre les concentrations plasmatiques d'APFO et le poids à la naissance (Fei et coll., 2007; Andersen et coll., 2010; Maisonet et coll., 2012). Une petite étude non publiée menée à partir des actes de naissance des participants des cohortes des communautés du C8 Health Project faisant l'objet de suivis a démontré un certain lien entre les concentrations sériques d'APFO et le faible poids à la naissance d'un bébé à terme; les résultats étaient toutefois incohérents et le degré d'importance n'a pas été fourni pour tous les résultats. Ces études représentent des constatations préoccupantes; la validité des résultats doit toutefois encore être confirmée, car ces études présentaient un risque de biais de sélection, de biais de rappel, de résultats liés au hasard, de covariables non contrôlées et d'absence d'une tendance de relation dose-réponse. En outre, aucune association importante entre les concentrations sériques d'APFO ou les concentrations d'APFO dans l'eau et un faible poids à la naissance n'a été décelée dans des études transversales ou dans des communautés grandement exposées (Nolan et coll., 2009; Stein et coll., 2009; Savitz et coll., 2012a; 2012b). Le C8 Science panel a conclu qu'il n'y avait probablement aucun lien entre l'APFO et un faible poids à la naissance (C8 Science Panel, 2011). Cependant, étant donné qu'on a trouvé que l'APFO était obésogène chez les souris (Hines et coll., 2009) et les humains (Halldorsson et coll., 2012), et qu'on sait que l'exposition in utero à de faibles doses d'obésogènes réduit le poids à la naissance (et favorise plus tard l'obésité; Holtcamp, 2012), le lien entre l'APFO et un poids faible à la naissance ne peut être exclu. On recommande donc de surveiller de près les nouvelles études en ce qui a trait à cet effet.
Une enquête sur les différents indicateurs de croissance fœtale en association avec l'exposition à l'APFO a donné des résultats équivoques. Les concentrations d'APFO dans le sang des mères de la cohorte de naissances nationale danoise (1996-2002) ont démontré des associations négatives avec la circonférence abdominale (avec une relation dose-réponse) et la grandeur à la naissance, après l'ajustement de plusieurs facteurs confusionnels pertinents (Fei et coll., 2008b). Comme ces associations ont été obtenues à partir d'importantes bases de données, il y a une possibilité d'erreurs de mesure et de codification des expositions et des résultats. Il y a également un risque de confusion résiduelle, comme les auteurs l'ont indiqué. Une étude transversale de la population générale (n = 293 accouchements simples) du Maryland (Apelberg et coll., 2007) a permis d'observer de faibles associations négatives avec la circonférence de la tête, l'indice pondéral et le poids à la naissance. Ces associations doivent être examinées avec prudence en raison des limites inhérentes au modèle d'étude. De plus, les autres études sur la population générale du Canada (Hamm et coll., 2010) ou du Japon (Washino et coll., 2009) n'ont permis d'établir aucune association entre les concentrations sériques d'APFO chez les mères et le poids à la naissance.
Les résultats des études transversales réalisées auprès de la population générale exposée à l'APFO dans le cadre du C8 Health Project (Fei et coll., 2008a; Hoffman et coll., 2010; Fei et Olsen, 2011; Stein et Savitz, 2011) n'ont pas permis de trouver de preuves concluantes de troubles du déficit de l'attention et d'hyperactivité (TDAH), de troubles d'apprentissage, de troubles du développement moteur ou de problèmes de comportement ou de coordination motrice.
9.1.4.2 Perturbations liées à la puberté et aux hormones sexuelles
Les concentrations sériques d'APFO ont été associées à un retard de puberté chez les jeunes filles (les probabilités sont réduites pour les 2e, 3e et 4e quartiles par rapport au quartile inférieur : retard de 142, 163 et 130 jours en ce qui concerne les premières règles, et retard de 155, de 158 ou de 183 jours en ce qui concerne un taux élevé d'œstradiol ou les premières règles) dans une étude transversale menée dans le cadre du C8 Health Project (Lopez-Espinosa et coll., 2011). D'autres examens s'imposent afin d'établir la nature de cette relation et de déterminer les mécanismes qui sont à la base de ces associations. Aucun lien n'a été établi entre l'APFO et les taux sériques d'œstradiol chez les groupes de femmes périménopausées et ménopausées (n = 25 957) du C8 Health Project (Knox et coll., 2011a).
9.1.4.3 Toxicité pour la reproduction
Aucune tendance évidente d'hypertension liée à la grossesse n'a été observée dans les études de cohorte menées auprès des résidentes de la Vallée du Mid-Ohio dans le cadre du C8Health Project et d'une étude transversale réalisée sur le comté de Washington (Savitz et coll., 2012 b; Nolan et coll., 2010; C8 Science Panel, 2011). Inversement, une étude prospective non publiée présentée par le C8 Science Panel (2011) a examiné des grossesses chez les participantes du C8 Health Project. Les quatre quintiles supérieurs présentaient de plus fortes probabilités d'hypertension liée à la grossesse; il n'y avait toutefois aucun modèle clair de relation dose-réponse. D'après cet ensemble de données, il serait prématuré de conclure qu'il y a un lien entre l'APFO et l'hypertension liée à la grossesse.
Dans l'ensemble, aucun lien défini n'a été établi entre l'APFO et la prééclampsie. Une étude menée auprès de résidentes de la Vallée du Mid-Ohio (des femmes enceintes entre 2000 et 2006) qui étaient exposées à l'eau potable contaminée par l'APFO (Stein et coll., 2009) n'a révélé aucune incidence accrue de prééclampsie. Une seconde étude a toutefois permis d'examiner le risque de prééclampsie parmi les participantes du C8 Health Project de 1990 à 2005 (Savitz et coll., 2012a). On a établi un faible lien entre les cas de prééclampsie signalés par les participantes et les concentrations sériques estimées d'APFO au moment de la grossesse, mais aucune tendance d'une relation dose-réponse n'a été observée. L'association a été renforcée lorsque l'étude a été restreinte aux grossesses survenues après 1999.
Un lien entre l'exposition à l'APFO et une diminution de la fécondité a été observé; les études n'étaient toutefois pas assez étoffées et les résultats n'étaient pas concluants. On a découvert que la diminution de la fertilité (une augmentation du temps d'attente avant une grossesse et des périodes de menstruation irrégulières) était associée aux concentrations plasmatiques d'APFO chez 1 240 femmes pares/nullipares; l'analyse ne comprenait toutefois pas de données liées à plusieurs facteurs de confusion (p. ex., la qualité du sperme, les incidences de fausses couches; Fei et coll., 2009). Une étude de cas-témoin sur des femmes pares qui participaient à l'Étude norvégienne de cohortes d'enfants et de mères a signalé des probabilités accrues d'hypofertilité (un temps d'attente supérieur à 12 mois avant une grossesse), alors qu'il n'y avait pas de risque accru d'hypofertilité chez les femmes nullipares (Whitworth et coll., 2012 b). Une étude de cohorte longitudinale réalisée au Danemark (Vestergaard et coll., 2012) n'a pas associé le temps d'attente avant une grossesse et la fécondité aux concentrations sériques d'APFO chez les femmes nullipares. Le manque d'ajustement des facteurs confusionnels et de cohérence des résultats remet en question le lien entre l'APFO et une baisse de fécondité.
Une étude de cohorte prospective a recruté 1 400 femmes enceintes (choisies au hasard parmi 43 045 femmes) au sein de la Cohorte de naissances nationale du Danemark (CNND, 1988-1989) afin de mesurer la concentration d'APFO dans leur plasma (Fei et coll., 2010b). Selon les entrevues téléphoniques, la période d'allaitement durait entre six et 18 mois après la naissance. Le risque d'une période plus courte d'allaitement augmentait avec l'accroissement de la concentration plasmatique d'APFO. Par exemple, le risque (soit l'indice de risque ajusté) d'une période d'allaitement plus courte (semaines) chez les femmes dont la concentration plasmatique d'APFO de > 7,0 ng/mL était de 1,4 (IC de 95 % : 1,2-1,7) fois plus élevée que chez les femmes présentant une concentration plasmatique d'APFO de < 3,9 ng/mL, après l'ajustement de l'âge de la mère à l'accouchement, l'IMC avant la grossesse, le statut socioéconomique de la mère, la consommation d'alcool et le tabagisme (la tendance d'une augmentation du risque avec l'accroissement de la comparaison au quatrième quartile était également significative). En outre, les probabilités (indice de risque ajusté) de sevrage avant l'âge de six mois étaient 1,23 fois plus élevées (IC de 95 % : 1,1 à 1,3) pour chaque hausse de 1 ng/mL de la concentration plasmatique d'APFO lorsque le modèle était restreint aux femmes multipares (la hausse n'était pas importante chez les femmes primipares), après les ajustements statistiques. On a observé une association similaire en ce qui a trait au sevrage avant l'âge de trois mois. Il serait toutefois nécessaire de mener d'autres études afin d'appuyer ces résultats, puisque la concentration plasmatique d'APFO n'a été mesurée qu'une seule fois, que seules 18 % des femmes admissibles ont participé à l'étude de CNND, qu'il y a un risque d'erreur de rappel des résultats (les mères pouvaient ne pas avoir déclaré de façon précise la date de sevrage) et que les auteurs n'ont pas exclu la possibilité qu'une causalité inverse puisse expliquer l'association (d'autant plus que cette association n'a pas été observée chez des femmes primipares et que les femmes ayant allaité plus longtemps leur bébé sont plus susceptibles de répéter l'expérience avec leurs prochains nourrissons, et que l'APFO est excrété dans le lait maternel, diminuant ainsi la concentration plasmatique).
Les études sur les liens entre l'exposition à l'APFO et la qualité du sperme ou les taux d'hormone sont rares, incohérentes et doivent être corroborées par des études de plus grande envergure afin d'être en mesure de mieux déterminer s'il y a bel et bien une relation. Une étude transversale réalisée auprès de 256 hommes de Durham, en Caroline du Nord, a révélé une corrélation positive entre les concentrations plasmatiques d'APFO et les taux sériques d'hormone lutéinisante. Il a toutefois été impossible de trouver un lien entre l'APFO et les mesures de qualité du sperme (Raymer et coll., 2012). On a été en mesure d'établir un lien positif entre l'APFO et la motilité du sperme chez un groupe d'hommes d'un pays, mais pas dans les deux autres pays étudiés (Groenland, Pologne et Ukraine). L'auteur a indiqué que le résultat positif pourrait être attribuable aux résultats liés au hasard (Toft et coll., 2012). Une étude prospective a suggéré que l'exposition in utero aux APFA pourrait avoir une incidence sur la qualité du sperme et les concentrations des hormones liées à la reproduction des hommes adultes; le mode de sélection des participants soulève par ailleurs des préoccupations (Vested et coll., 2013).
Compte du poids de la preuve, il est impossible d'exclure l'existence d'effets nocifs possibles de l'APFO sur le développement et la reproduction. D'importantes études de cohortes d'enfants de mères présentant des concentrations sériques élevées d'APFO ont signalé un risque accru d'une circonférence abdominale et d'une grandeur et d'un poids moins élevés à la naissance, ainsi qu'un surpoids et un large tour de taille 20 ans après la naissance. Ces résultats s'appuient sur les effets sur les biomarqueurs sériques (l'insuline, la leptine et l'adiponectine). En outre, des études ont permis d'observer une toxicité pour la reproduction, quoique dans une moindre mesure. Des études longitudinales ont associé le niveau supérieur d'exposition à l'APFO à un risque accru d'hypertension liée à la grossesse, de prééclampsie, de période plus courte d'allaitement, de qualité altérée de sperme et de fécondité réduite. Cependant, l'ensemble des données liées à chaque résultat individuel demeure relativement restreint, et les conclusions définitives sur la relation entre les résultats pour la reproduction et le développement et l'exposition à l'APFO sont principalement limitées par un manque de cohérence dans les résultats et une possibilité de confusion. Ces limites ne permettent pas de déterminer la nature de l'association pour le moment.
9.2 Effets chez les animaux de laboratoire
La grande majorité des études sur les animaux ont indiqué que l'exposition à l'APFO était liée à son sel d'ammonium (PFOA). On présume que les études qui n'ont pas identifié le sel utilisé dans le cadre de leur examen ont employé le sel d'ammonium étant donné qu'il s'agit du seul composé qui a été utilisé dans les études faisant mention du sel de l'APFO. Aucune étude n'a indiqué si la dose administrée renvoyait au composé de l'APFO ou particulièrement à l'ion de l'APFO, qui se distingue du sel d'ammonium. Les résumés décrits ci-après utilisent les concentrations et les doses indiquées par les auteurs. Cette approche est également utilisée dans le cadre des évaluations quantitatives; toutefois, comme l'ion de l'APFO compose 96 % du poids molaire de l'APFO et qu'il est libéré du composé à l'exposition, l'utilisation de doses de PFOA et d'APFO de manière interchangeable n'engendrait que des différences quantitatives mineures.
9.2.1 Toxicité aiguë
Les études sur la toxicité aiguë du PFOA et de l'APFO indiquent des valeurs de DL50 orale de >500 et 680 mg/kg p.c. respectivement chez les rats mâles CD et Sprague-Dawley (Glaza, 1997), 250-500 mg/kg p.c. et 430 mg/kg p.c. respectivement chez les rats femelles CD et Sprague-Dawley (Dean et Jessup, 1978; Glaza, 1997) et <1 000 mg/kg chez les rats Sherman-Wistar des deux sexes (Gabriel, 1976).
Aucune mortalité n'a été rapportée chez les rats Sprague-Dawley des deux sexes à la suite de l'exposition par inhalation à l'APFO à une dose de 18 600 mg/m3 pendant une heure (Rusch, 1979).
Les valeurs de DL50 cutanée chez les lapins correspondaient à >2 000 mg/kg p.c. ou 4 300 mg/kg p.c. (Glaza, 1995; Kennedy, 1985). Des valeurs plus élevées ont été obtenues chez les rats avec l'administration d'une DL50 de 7 000 mg/kg p.c. chez les mâles et de 7 500 mg/kg p.c. chez les femelles (Kennedy, 1985).
La section 9.2.5.5 analyse les études sur les troubles aigus de développement neurologique.
9.2.2 Exposition à court terme
Les études qui traitent de la toxicité de l'APFO après une exposition orale à court terme ont permis de déterminer trois principales cibles, soit les effets sur la reproduction et le développement (résumés à la section 9.2.5), les effets hépatiques et les effets sur les lipides sériques. Le retard du développement des glandes mammaires semble être la cible la plus sensible avec une LOAEL de 0,001 mg/kg p.c. par jour (concentration sérique d'APFO : 74,8 ng/mL; aucune NOAEL) chez les souris (voir la section 9.2.5.1). Les LOAEL les plus faibles pour l'évaluation des effets hépatiques étaient de 0,15 mg/kg p.c. par jour chez les souris adultes (Kennedy, 1987; NOAEL de 0,05 mg/kg p.c. par jour). Des effets sur les lipides sériques ont été observés à ≥0,3 mg/kg p.c. chez les rats (Loveless et coll., 2006, 2008). La présente section abordera en grande partie ces principaux effets observés aux doses minimales et ne traitera que brièvement des autres types de changements observés chez les animaux.
9.2.2.1 Effets hépatiques
L'hypertrophie hépatocellulaire chez les rats et les souris mâles (Perkins et coll., 2004; Loveless et coll., 2008) et une augmentation du poids du foie chez les rats (Kennedy, 1987) et les souris (Loveless et coll., 2006) constituaient les effets hépatiques observés aux doses minimales dans le cadre d'études à court terme. La présente section exposera plus en détail ces études et ne traitera que brièvement des autres effets hépatiques observés à des doses plus élevées.
La LOAEL la plus faible liée au poids du foie a été administrée chez les ratons exposés in utero à 0,1 mg/kg p.c. par jour pendant les jours de gestation (JG) de 1 à 17; la section 9.2.5.4 comprend de plus amples détails sur cette étude. Chez les adultes, les études qui ont observé des augmentations de poids du foie aux doses les plus faibles sont les études de Loveless et coll. (2006; avec une LOAEL de 0,3 mg/kg p.c. par jour) et de Kennedy (1987; avec une LOAEL de 0,15 mg/kg p.c. par jour et une NOAEL de 0,05 mg/kg p.c. par jour). Ces études sont présentées ci-dessous.
Une LOAEL de 0,3 mg/kg p.c. par jour (sans NOAEL) a été déterminée chez les souris CD-1 mâles (n = 10/dose) à la suite d'une exposition orale à l'APFO (0, 0,3, 1, 3, 10 ou 30 mg/kg p.c. par jour) pendant 14 jours (Loveless et coll, 2006). Différentes préparations d'APFO ont été utilisées (PFOA de type ramifié, linéaire ou ramifié et linéaire). La LOAEL renvoie à un poids du foie relativement accru chez les souris exposées à du PFOA ramifié (la plupart des études exposent les animaux à un mélange de PFOA principalement linéaire). Le poids du foie était également plus élevé chez les rats, mais seulement à une dose administrée à ≥1 mg/kg p.c. par jour. Le poids absolu du foie était considérablement plus élevé dans au moins une forme de PFOA à ≥1 mg/kg p.c. par jour chez les deux espèces. Chez les rats et les souris, les réponses du poids du foie aux formes linéaires et ramifiées de PFOA étaient similaires. Les mêmes chercheurs ont réalisé une étude de 29 jours en utilisant du PFOA linéaire et n'ont constaté aucune augmentation de poids du foie à une dose de 0,3 mg/kg p.c. par jour - le poids absolu du foie augmentait chez les deux espèces à ≥1 mg/kg p.c. par jour et le poids relatif du poids augmentait à ≥1 mg/kg p.c. par jour chez les souris et à ≥10 mg/kg p.c. par jour chez les rats (Loveless et coll., 2008). Cette dernière étude comprenait un groupe de récupération (avec une fin d'exposition au 23e jour de test chez les rats, et au 24e jour de test chez les souris) qui était exposé à une dose élevée (c.-à-d., 30 mg/kg p.c. par jour). On a encore noté des augmentations de poids du foie à la fin de l'étude chez les deux espèces.
Dans le cadre de l'étude utilisant la LOAEL la plus faible établie pour cet effet (Kennedy, 1987), les rats CD mâles et femelles ont été exposés à l'APFO à des doses de 0, 0,01, 0,03, 0,1, 0,3, 1, 3, 10 et 30 ppm dans leur nourriture (avec les hypothèses par défaut de Santé Canada de 1 ppm dans la nourriture = 0,05 mg/kg p.c. par jour chez les rats [Santé Canada, 1994], les doses approximatives étaient de 0,0005, 0,0015, 0,005, 0,015, 0,05, 0,15, 0,5 et de 1,5 mg/kg p.c. par jour) pendant 21 jours. Une augmentation du poids absolu et relatif du foie a été observée à ≥0,15 mg/kg par jour chez les rats mâles et femelles, avec une NOAEL de 0,05 mg/kg p.c. par jour. Dans le cadre de la même étude, on a également exposé les rats à l'APFO pendant 14 semaines et observé des augmentations à la dose minimale (30 ppm dans la nourriture, ce qui équivaut à 1,5 mg/kg p.c. par jour).
Un grand nombre d'études à court terme a permis d'observer des augmentations de poids du foie chez les animaux adultes à des doses plus élevées. Ces effets ont été observés chez les rats (Metrick et Marias, 1977; Goldenthal et coll., 1978a; Staples et coll., 1984; Kennedy et coll., 1986; Biegel et coll., 2001; Perkins et coll., 2004; Cui et coll., 2009) et chez les souris (Metrick et Marias, 1977; Liu et coll., 1996; Yang et coll., 2001, 2002; Lau et coll., 2006; Abbott et coll., 2007; Wolf et coll., 2007; DeWitt et coll., 2008; Son et coll., 2008; Qazi et coll., 2010; Yahia et coll., 2010). Les augmentations de poids du foie semblent généralement réversibles, puisqu'on ne les observait plus après la période d'exposition dans la plupart des études comportant une période de récupération (Palazzolo, 1993; Thomford, 2001a; Butenhoff et coll., 2002; Perkins et coll., 2004). Par contre, dans le cadre d'une étude sur des souris exposées à l'APFO pendant 10 jours, l'effet était toujours observé 10 jours après la fin de l'exposition (Yang et coll., 2001). Des augmentations de poids du foie ont également été observées chez des souris exposées à l'APFO in utero ou à l'âge péripubertaire; ces résultats sont présentés à la section 9.2.5.4.
L'étude qui a révélé la formation d'une hypertrophie hépatocellulaire à des doses minimales a exposé des rats Sprague-Dawley mâles (n=10 par groupe) et des souris CD-1 mâles (n=19-20 par groupe) à des doses d'APFO de 0, de 0,3, de 1, de 10 ou de 30 mg/kg p.c. par jour pendant 29 jours (Loveless et coll., 2008). L'incidence et la gravité de l'hypertrophie augmentaient avec la dose, et les effets étaient plus graves chez les souris. Dans le groupe de récupération exposé à des doses élevées, l'hypertrophie a perduré au-delà de la fin de l'étude, malgré la fin de l'exposition à la 23e (rat) ou à la 24e (souris) journée de l'étude.
L'étude la plus fiable révélant une NOAEL pour ce qui est du poids du foie et de l'hypertrophie hépatocellulaire a exposé des rats Crl:CD mâles (n =5 5 par dose) à des doses de 0, 0,06, 0,64, 1,94 et 6,5 mg/kg p.c. par jour dans la nourriture (Perkins et coll., 2004). L'étude comprenait deux groupes témoins; un groupe témoin nourri en parallèle à des doses élevées et un groupe ayant accès à de la nourriture à volonté. Les rats ont été répartis en groupes sacrifiés exposés pendant quatre, sept ou 13 semaines (n = 15 par dose par durée) et chaque dose (et pour les groupes témoins d'alimentation à volonté) était associée à un groupe de récupération qui était observé pendant huit autres semaines suivant la fin de l'exposition à la treizième semaine (n = 10 par dose). Des augmentations liées à la dose de l'incidence et de la gravité de l'hypertrophie ont été observées (tableau 3). La plupart des rats exposés à ≥0,64 mg/kg p.c. par jour présentaient une hypertrophie jugée minime à légère, dont la gravité était supérieure dans le groupe exposé à des doses élevées pendant 13 semaines; les effets n'ont pas persisté dans les groupes de récupération. L'hypertrophie n'a pas été accompagnée par des lésions dégénératives du foie. Le poids relatif du foie a augmenté à ≥0,64 mg/kg p.c. par jour dans le groupe exposé à l'APFO pendant quatre semaines, et à ≥1,94 mg/kg p.c. par jour à de plus longues durées d'exposition; les effets n'ont pas persisté dans les groupes de récupération.
| Dose (mg/kg p.c. par jour) | Durée d'exposition (semaine) | Degré de gravité de l'hypertrophie | |||
|---|---|---|---|---|---|
| Aucun | Minimale | Légère | Modéré | ||
| Groupe témoin nourri à volonté | 4 | 15 | 0 | 0 | 0 |
| 7 | 15 | 0 | 0 | 0 | |
| 13 | 15 | 0 | 0 | 0 | |
| 13 (récupération) | 10 | 0 | 0 | 0 | |
| Groupe témoin nourri ensemble | 4 | 15 | 0 | 0 | 0 |
| 7 | 15 | 0 | 0 | 0 | |
| 13 | 15 | 0 | 0 | 0 | |
| 13 (récupération) | S. O. | S. O. | S. O. | S. O. | |
| 0,06 | 4 | 15 | 0 | 0 | 0 |
| 7 | 15 | 0 | 0 | 0 | |
| 13 | 15 | 0 | 0 | 0 | |
| 13 (récupération) | 10 | 0 | 0 | 0 | |
| 0,64 | 4 | 3 | 12 | 0 | 0 |
| 7 | 3 | 12 | 0 | 0 | |
| 13 | 2 | 13 | 0 | 0 | |
| 13 (récupération) | 10 | 0 | 0 | 0 | |
| 1,94 | 4 | 0 | 7 | 8 | 0 |
| 7 | 0 | 14 | 1 | 0 | |
| 13 | 1 | 12 | 2 | 0 | |
| 13 (récupération) | 10 | 0 | 0 | 0 | |
| 6,5 | 4 | 0 | 5 | 9 | 0 |
| 7 | 0 | 6 | 9 | 0 | |
| 13 | 0 | 3 | 12 | 0 | |
| 13 (récupération) | 10 | 0 | 0 | 0 | |
Des études à doses plus élevées ont également révélé l'incidence d'une hypertrophie hépatocellulaire chez les souris (Yahia et coll., 2010) et les rats (Metrick et Marias, 1977; Goldenthal et coll., 1978a; Cui et coll., 2009).
Des études à court terme ont permis d'observer d'autres effets histologiques sur le foie à des doses plus élevées, dont une nécrose monocellulaire et focale chez les souris (Loveless et coll., 2008; Yahia et coll., 2010) et les rats (Metrick et Marias, 1977; Goldenthal et coll., 1978a; Loveless et coll., 2008; Cui et coll., 2009); une augmentation de la mitose chez les souris (Yahia et coll., 2010); une calcification légère chez les souris (Yahia et coll., 2010); un gonflement cytoplasmique des hépatocytes chez les rats (Metrick et Marias, 1977); et une vacuolisation cytoplasmique chez les rats (Cui et coll., 2009). Des effets histologiques ont également été observés sur les foies de rats exposés à l'APFO pendant deux ans, lesquels sont présentés à la section 9.2.3.
Des changements dans les taux sériques des marqueurs de lésions au foie ont été observés chez les souris exposées à des doses plus élevées que les LOAEL liées au poids du foie et à l'hypertrophie hépatocellulaire. Ces effets comprenaient une hausse des taux d'ALT (Son et coll., 2008; Yahia et coll., 2010), d'AST (Son et coll., 2008; Yahia et coll., 2010), de GGT (Yahia et coll., 2010) et d'ALP (Yahia et coll., 2010; Qazi et coll., 2010). On a également observé une hausse des taux d'ALP chez les rats (Kennedy et coll., 1986).
9.2.2.2 Effets sur les lipides sériques
Des altérations des paramètres des lipides sériques figurent parmi les effets observés aux doses d'exposition d'APFO les plus faibles chez des animaux adultes dans des études à court terme. Les effets comprennent les changements du taux de cholestérol HDL, de cholestérol total et de triglycérides. Bien que le taux de cholestérol total et de cholestérol HDL ait diminué dans la plupart des études menées sur les souris (Loveless et coll., 2006, 2008; Qazi et coll., 2010) et les rats (Loveless et coll., 2006, 2008), le taux de cholestérol total (ainsi que celui des phospholipides et des acides gras libres) a augmenté dans une étude à dose élevée menée sur des souris (Yahia et coll., 2010). Bien que certaines études (Loveless et coll., 2006; Yahia et coll., 2010) aient permis d'observer des augmentations des taux de triglycérides chez des souris, une autre étude a constaté des diminutions (Loveless et coll., 2008). Les taux de triglycérides ont diminué dans les deux études menées sur les rats (Loveless et coll., 2006, 2008).
Présentées de façon plus détaillée dans la section 9.2.2.1, les études qui ont permis d'observer des changements dans les lipides sériques aux doses les plus faibles ont toutes les deux été réalisées par Loveless et coll. (2006, 2008). Des LOAEL ont été administrées aux rats à des valeurs de 0,3 mg/kg p.c. par jour en ce qui a trait aux baisses des taux de cholestérol et de triglycérides (Loveless et coll., 2006, 2008), et de 0,3 mg/kg p.c. par jour en ce qui a trait aux baisses des taux de cholestérol HDL (Loveless et coll., 2008; en 2006, la LOAEL représentait seulement de 3 mg/kg p.c. par jour). La plupart des effets ont seulement été observés à des concentrations plus élevées chez les souris - dans l'étude de Loveless et coll. (2008), les LOAEL s'élevaient à 1 mg/kg p.c. par jour en ce qui concerne le cholestérol HDL, et 10 mg/kg p.c. par jour en ce qui concerne la baisse du taux de cholestérol total et de triglycérides, et la plupart des LOAEL s'élevaient à 3 mg/kg p.c. par jour dans l'étude de Loveless et coll. (2006). Faisaient exception les augmentations des taux de triglycérides, particulièrement chez les souris exposées à l'APFO linéaire et ramifiée, puisque les effets ont été observés à des doses de ≥0,3 mg/kg p.c. par jour.
Les effets sur le cholestérol et le cholestérol HDL ne semblent pas perdurer au-delà de la fin de l'exposition, car les taux de cholestérol total et de cholestérol HDL revenaient à des taux similaires à ceux des groupes témoins à la fin de l'exposition lors de la 23e journée (rat) ou de la 24e journée (souris) de l'étude menée sur 29 jours (Loveless et coll., 2008). Les taux de triglycérides chez les deux espèces continuaient d'être inférieurs à ceux des témoins après la période de récupération, mais, chez les souris, les taux avaient augmenté de manière assez importante pour en venir à être supérieurs à ceux du groupe exposé à des doses élevées pendant 29 jours.
Loveless et coll. (2006) ont examiné différentes formes d'APFO (ramifié, linéaire ou ramifié et linéaire). La forme linéaire (la forme qui est la plus souvent présentée dans les mélanges d'APFO utilisés dans les études) semblait être associée aux LOAEL chez les rats en ce qui concerne tous les résultats lipidiques. Chez les souris, alors que la forme d'APFO n'a pas semblé avoir d'effet sur le cholestérol HDL ou le cholestérol, le mélange linéaire/ramifié semblait être la seule forme n'ayant aucun effet sur les triglycérides.
D'autres études ont permis d'observer des augmentations des taux de triglycérides, de cholestérol total et d'acides gras libres à une dose de 10 mg/kg p.c. par jour chez les souris mères ICR (Yahia et coll., 2010) ainsi qu'une diminution du taux de cholestérol sérique total chez les souris C57BL/6 mâles (Qazi et coll., 2010).
9.2.2.3 Autres effets
D'autres effets que les effets hépatiques et hépatiques sériques ont été observés dans des études à court terme menées sur des animaux adultes exposés à l'APFO à des doses de ≥1 mg/kg p.c. par jour. Les études sont décrites brièvement ci-dessous.
Plusieurs études sur les souris (Yahia et coll., 2010) et les rats (Goldenthal et coll., 1978; Butenhoff et coll., 2004 b; Cui et coll., 2009) ont permis d'observer une augmentation du poids des reins à une dose de ≥1 mg/kg p.c. par jour. De nombreuses études ont démontré que les augmentations concernaient seulement le poids relatif, et non le poids absolu, des reins. Les effets étaient également souvent accompagnés par des effets histologiques (Butenhoff et coll., 2004 b; Cui et coll., 2009; Yahia et coll., 2010).
Des changements associés au poids des organes ayant des effets neurologiques sont survenus à des doses de ≥3 mg/kg p.c. par jour chez les singes. Ces observations correspondaient à l'augmentation du poids moyen de la glande pituitaire et à une diminution du poids absolu du cerveau (Goldenthal et coll., 1978). Les seuls effets neurologiques observés chez les animaux adultes exposés pendant une courte durée à l'APFO étaient l'activité réduite et la léthargie chez les rats (Cui et coll., 2009).
Des signes d'immunosuppression sont survenus à ≥3,75 mg/kg p.c. par jour chez les souris. Parmi ces signes, mentionnons la diminution des taux d'immunoglobulines, les changements de la cellularité et des sous-types de cellules immunitaires ainsi que les changements de l'expression de la cytokine (Yang et coll., 2001, 2002; DeWitt et coll., 2008; Loveless et coll., 2008; Son et coll., 2008; Qazi et coll., 2009, 2010). Une atrophie du thymus et de la rate a également été observée chez les souris (Yang et coll., 2001, 2002; Loveless et coll., 2008; Qazi et coll., 2009) et des changements histologiques ont été observés dans les organes des rats (Cui et coll., 2009; Qazi et coll., 2009). Des études menées sur les souris ont également indiqué une possibilité d'hypersensibilité causée par des expositions à l'APFO, une augmentation liée à la dose des teneurs sériques en histamine à ≥1 mg/kg p.c. par jour (Singh et coll., 2012) et un taux élevé d'IgE après la provocation à l'ovalbumine chez les souris exposées par voie cutanée à ≥18,75 mg/kg p.c. d'APFO par jour (Fairley et coll., 2007).
On a observé des effets sur d'autres organes à des doses de ≥10 mg/kg de p.c. par jour. Ces effets comprenaient l'hypertrophie et la vacuolisation de la zone glomérulée de la glande surrénale des rats (Butenhoff et coll., 2004b); la congestion pulmonaire, l'épaississement des parois épithéliales, l'infiltration et la vasodilatation des cellules chez les rats (Cui et coll., 2009);l'œdème pulmonaire chez les rats (Kennedy et coll., 1986); et la diminution du poids du cœur chez les singes (Goldenthal et coll., 1978).
La seule étude qui a indiqué des changements liés aux taux des hormones thyroïdiennes a démontré une diminution des taux de T3 et T4 libres et totaux chez les singes exposés à l'APFO pendant six mois (Butenhoff et coll., 2002). On a observé des diminutions de concentrations de T4 libre et total à des intervalles réguliers, notamment à la fin de l'exposition des singes à des taux de 10 ou 20 à 30 mg/kg p.c. par jour; à la fin de l'exposition (et non à des intervalles plus précoces), une diminution importante a également été observée pour le T4 total (mais non libre) à une dose de 3 mg/kg par jour. Une diminution de la concentration de T3 libre et total a également été observée à des intervalles réguliers (dont à la fin de l'exposition) chez les singes exposés à une dose se situant entre 20 et 30 mg/kg p.c. par jour; une diminution des concentrations de T3 total (mais pas libre) a également été observée à deux moments au milieu de l'étude, mais non à la fin de l'exposition chez les singes ayant été exposés à des faibles doses. Les effets étaient accompagnés d'augmentations importantes des concentrations de TSH à la fin de l'étude menée chez les singes exposés à 3 ou 10 mg/kg p.c. par jour (aucun effet à une dose élevée). L'étude de détermination des doses de quatre semaines menée sur les singes de Butenhoff (Thomford, 2001b) n'a relevé aucun effet sur les concentrations de TSH ou de T3 ou de T4 total ou libre.
De nombreuses études différentes ont démontré des pertes ou des gains de poids. Ces effets ont été observés à des LOAEL de 3 mg/kg p.c. par jour chez les rats (Metrick et Marias, 1977; Goldenthal et coll., 1978; Staples et coll. 1984; Kennedy et coll., 1986; Butenhoff et coll., 2004b; Cui et coll., 2010), de 3 mg/kg p.c. par jour chez les souris (Christopher et Marias, 1977; Lau et coll., 2006; Wolf et coll., 2007; Asakawa et coll., 2008; Son et coll., 2008; White et coll., 2009; Yahia et coll., 2010; Suh et coll., 2011) et de 30 mg/kg p.c. par jour chez les singes (Goldenthal et coll., 1978). Cet effet était accompagné d'une diminution de la consommation de nourriture à une dose de ≥5 mg/kg p.c. par jour chez les rats (Metrick et Marias, 1977; Butenhoff et coll., 2004 b; Cui et coll., 2009) et de 20,7 mg/kg p.c. par jour chez les souris (Asakawa et coll., 2008).
Des signes cliniques observés dans des études comprenaient des selles molles, de la diarrhée et des vomissements mousseux chez les singes (Goldenthal et coll., 1978), ainsi que des poils rudes, une faiblesse musculaire et une cyanose chez les souris (Christopher et Marias, 1977).
Peu d'études indiquaient une diminution de la mortalité chez les animaux. On a observé cet effet à des doses élevées dans des études sur les rats (Metrick et Marias, 1977; Staples et coll., 1984; Butenhoff et coll., 2004b), les souris (Christopher et Marias, 1977) et les singes (Goldenthal et coll., 1978b; Thomford, 2001a; Butenhoff et coll., 2002).
9.2.3 Exposition à long terme et cancérogénicité
En ce qui concerne la voie orale, nous avons ciblé deux études sur la toxicité chronique menées sur des animaux de laboratoire. Nous n'avons trouvé aucune étude portant sur l'exposition par inhalation ou par voie cutanée. Comme on l'a constaté dans certaines études sur la cancérogénicité à long terme, le poids constituait l'organe cible le plus sensible dans les études sur la chronicité (LOAEL = 1,3 mg/kg p.c. par jour chez les rats mâles en ce qui concerne l'augmentation des paramètres hépatiques sériques) (3M, 1983; Sibinski, 1987; Butenhoff et coll., 2012 b). D'autres effets observés chez les rats après l'exposition chronique à l'APFO comprennent une incidence accrue d'hyperplasie et de tumeurs dans divers tissus (les glandes mammaires chez les femelles, les cellules de Leydig, le pancréas et le foie chez les mâles) et une altération des concentrations sériques des hormones (3M, 1983; Sibinski, 1987; Biegel et coll., 2001).
La seule étude à avoir administré plus d'une dose a établi une LOAEL de 1,3 mg/kg p.c. par jour (aucune NOAEL) chez les rats mâles en ce qui concerne la toxicité pour le foie (3M, 1983; Sibinski, 1987; Butenhoff et coll., 2012b). Une dose de 0, 30 ou 300 ppm d'APFO (0, 1,3 ou 14,2 mg/kg p.c. par jour pour les mâles; et 0, 1,6 ou 16,1 mg/kg p.c. par jour pour les femelles) a été administrée pendant deux ans dans l'alimentation de rats Sprague-Dawley (50/sexe/groupe). La LOAEL de 30 ppm était fondée sur des hausses importantes des paramètres hépatiques sériques chez les mâles (l'alanine aminotransférase, l'aspartate aminotransférase, la phosphatase alcaline et l'albumine à plusieurs intervalles, dont les taux étaient encore élevés, quoique de façon non significative à une dose faible à la fin de l'exposition) et une augmentation liée à la dose de sialadénite chronique de la glande salivaire des mâles. Le taux d'incidence de l'hypertrophie hépatocellulaire était également élevé chez les deux groupes de traitement composés de mâles, dont la signification a seulement été atteinte à une dose maximale (l'incidence était de 0 % chez les groupes témoins, 12 % à une faible dose et 80 % à une dose élevée). D'autres effets chez les mâles comprennent une incidence accrue liée à la dose d'adénomes de cellules de Leydig qui est devenue statistiquement significative à 300 ppm (14,2 mg/kg p.c. par jour). Chez les rates, la première analyse de données a indiqué une augmentation liée à la dose de fibroadénomes mammaires qui est devenue statistiquement significative à ≥30 ppm; une plus récente analyse a toutefois été réalisée par un groupe de travail sur les pathologies qui a utilisé les critères actuels de diagnostic, laquelle a permis de conclure que le traitement de l'APFO n'a pas donné lieu à des lésions prolifératives dans les tissus mammaires (Hardisty et coll., 2010; Butenhoff et coll., 2012b). Des transformations non néoplasiques dans le foie (hypertrophie hépatocellulaire, infiltration de cellules mononucléaires des espaces portes ou dégénérescence cystoïde à une dose élevée) et dans les poumons (macrophages et hémorragies alvéolaires à une dose élevée) ont été observées et des lésions de cellules acineuses prolifératives ont été observées dans le pancréas des rates à une dose élevée. L'APFO n'a pas augmenté l'incidence de lésions néoplasiques ou non néoplasiques dans d'autres organes (la thyroïde, la glande pituitaire, la glande surrénale, les reins, l'utérus).
Une étude de suivi a été réalisée chez des rats CD mâles auxquels on avait administré de l'APFO dans leur nourriture (0 ou 300 ppm) pendant deux ans (dose quotidienne moyenne de 13,6 mg/kg p.c. par jour) (Biegel et coll., 2001). Deux groupes témoins ont été utilisés; le premier était un groupe nourri à volonté et le second était un groupe nourri en parallèle chez qui la ration alimentaire était contrôlée afin de correspondre à la ration alimentaire du groupe exposé à l'APFO. Les rats faisaient l'objet d'une évaluation au premier et au troisième mois et tous les trois mois par la suite afin de vérifier le statut hormonal, la prolifération de cellules dans le foie, les testicules et le pancréas et la prolifération de peroxysomes hépatiques. Le traitement avec l'APFO a augmenté le poids relatif du foie à toutes les étapes de l'étude (sauf au 24e mois) comparativement aux deux groupes témoins. L'activité de la bêta oxydation hépatique a augmenté de façon importante à toutes les étapes de l'étude, mais la prolifération de cellules n'a pas augmenté dans le foie. La prolifération de cellules acineuses pancréatiques a augmenté au 15e, au 18e et au 21e mois. La concentration sérique d'œstradiol a augmenté au cours de la première année de l'étude, soit au 6e et au 18e mois pour le taux sérique de LH, et au 6e mois pour le taux sérique de SFH; aucune tendance constante n'a été démontrée dans les changements de taux de testostérone sérique. Il y a eu une augmentation importante de tumeurs chez les animaux traités comparativement à l'un des groupes témoins ou aux deux groupes témoins en ce qui a trait à des adénomes des cellules de Leydig, des adénomes hépatiques, des adénomes des cellules acineuses et des adénomes et carcinomes combinés dans le pancréas. On a également observé une incidence accrue d'hyperplasie des cellules de Leydig et des cellules acineuses (Biegel et coll., 2001).
Bien que la LOAEL sur les effets hépatiques soit plus élevée dans les études sur la chronicité que dans les études à court terme, il est difficile d'établir des comparaisons, puisque la dose minimale utilisée dans l'étude sur la chronicité (1,3 mg/kg p.c. par jour) est plus élevée que les LOAEL utilisées dans les études à plus court terme sur les effets hépatiques (c.-à-d., 0,1 à 0,3 mg/kg p.c. par jour). Certains effets observés à ces faibles doses dans les études de plus courte durée, plus particulièrement sur l'hypertrophie hépatocellulaire chez les rats mâles (Loveless et coll., 2008), n'ont toutefois pas été observés aux doses minimales utilisées dans les études sur la chronicité (c.-à-d., la NOAEL chronique pour cet effet correspond à 1,3 mg/kg p.c. par jour).
9.2.4 Génotoxicité
La base de données sur la génotoxicité indique que les composés d'APFO ne sont pas mutagènes et qu'ils ne sont généralement pas génotoxiques (U.S. EPA, 2005; UK HPA, 2009; Environnement Canada et Santé Canada, 2012).
9.2.4.1 Observations in vitro
Les tests réalisés sur l'APFO (ou l'utilisation de ses sels d'ammonium ou de sodium) n'ont démontré aucun signe d'activité génotoxique lors de nombreux test d'Ames sur la mutation bactérienne et sur trois tests d'aberration chromosomique in vitro (deux sur des cellules de hamster et un sur des cellules humaines) (Environnement Canada et Santé Canada, 2012). Plus récemment, l'APFO (testé jusqu'à 1 000 µM) n'a révélé aucune activité mutagène lors du test umu (Oda et al., 2007) et du test d'Ames, avec ou sans activation métabolique S9 (Fernandez Freire et coll., 2008). L'APFO n'a pas augmenté les lésions oxydatives d'ADN (tel que mesuré lors d'un essai de Comet) des cellules testiculaires des rats exposés à 100 et 300 µM pendant 24 heures (Lindeman et coll., 2012). Chez les cellules d'hépatome humain HepG2, l'APFO (jusqu'à 400 µM pendant 24 h) n'a pas induit de génération d'espèces oxygénées réactives (EOR), de dommages aux brins uniques d'ADN ou de micronoyaux (Florentin et coll., 2011). Dans le cadre d'une autre étude sur l'utilisation de cellules humaines HepG2, l'APFO a induit une légère génération d'EOR (0,4-2 000 µM) sans générer de dommages détectables à l'ADN (200 µM) (Eriksen et coll., 2010).
Par ailleurs, des résultats positifs ont été obtenus lors d'un test sur des lésions chromosomiques de cellules de hamster et d'un test du micronoyau in vitro sur des cellules humaines, et l'APFO a causé des lésions oxydatives à l'ADN dans des cellules d'hépatome humain en culture (Environnement Canada et Santé Canada, 2012). L'APFO (200 µM) a induit une mutagénicité des cellules hybrides (AL) humaines-hamsters, et des EOR dépendantes de mitochondries ont démontré qu'elles jouaient un rôle important dans ce processus (Zhao et coll., 2011b).
9.2.4.2 Observations in vivo
Trois tests du micronoyau in vivo sur la moelle osseuse de la souris (jusqu'à 5 000 mg/kg p.c. par jour) ont été réalisés afin d'examiner le potentiel de génotoxicité de l'APFO (ainsi que de ses sels d'ammonium ou de sodium), mais n'ont fourni aucune preuve d'une telle activité. L'APFO a causé des lésions oxydatives à l'ADN dans le foie de rats traités par voie orale (200 ppm dans l'alimentation pendant deux semaines) ou par voie intrapéritonéale (100 mg/kg p.c., un dose) (Environnement Canada et Santé Canada, 2012).
9.2.5 Toxicité pour l'appareil reproducteur et pour le développement
La base de données sur les effets de l'APFO sur la reproduction et le développement est étoffée. Deux études portant sur deux générations de rats ont été élaborées (Butenhoff et coll., 2004b/York et coll., 2010; White et coll., 2011), et des paramètres de reproduction et de développement ont été examinés dans de nombreuses études portant sur une génération de rats, de souris et de singes. On a également exposé des souris à l'APFO en début de vie ou à l'âge péripubertaire (Johansson et coll., 2008, 2009; Yang et coll., 2009 b; Zhao et coll., 2010; Dixon et coll., 2012).
Les effets les plus sensibles qui ont été relevés sont un retard du développement des glandes mammaires chez les petits des souris (Macon et coll., 2011; White et coll., 2011), de l'obésité chez la progéniture femelle des souris à l'âge adulte (Hines et coll., 2009), des effets utérins chez les souris femelles immatures (Dixon et coll., 2012), des variations de poids du foie chez les ratons (Abbott et coll., 2007; Macon et coll., 2011; Onishchenko et coll., 2011) et un comportement neurologique altéré (Johansson et coll., 2008, 2009; Onishchenko et coll., 2011). Ces effets ont tous été observés à des niveaux d'exposition de ≤0,3 mg/kg p.c. par jour et seront examinés en détail plus bas. D'autres effets sur la reproduction et le développement ont été relevés à des doses plus élevées et seront décrits brièvement dans la présente section.
9.2.5.1 Effets sur les glandes mammaires
Les changements dans le développement des glandes mammaires (DGM) ont fait l'objet d'une seule étude chez les souris. Des études portant sur une génération (White et coll., 2007, 2009; Wolf et coll., 2007; Macon et coll., 2011), deux générations (White et coll., 2011) et l'âge péripubertaire (Yang et coll., 2009; Zhao et coll., 2010) ont démontré des retards du DGM. Les particularités du retard du DGM étaient par ailleurs très différentes de celles des groupes témoins à toutes les doses étudiées (≥0,001 mg/kg p.c. par jour) chez les générations F1 et maternelles (chez les petits et les mères). Les études ont principalement révélé un retard du DGM (une période aussi longue que 10 jours dans une étude qui a exposé des souris à 5 mg/kg p.c. par jour [White et coll., 2007]) et de moins bons résultats de DGMNote de bas de page 1 à de nombreux intervalles différents. Les structures précises de glandes mammaires qui ont été affectées comprenaient les canaux (retard et diminution de l'élongation et des embranchements des canaux), des canaux terminaux (CT) (diminution du nombre de CT stimulés), des bourgeons terminaux (BT) (retard dans le délai d'apparition, excès et diminution du nombre de BT) et de l'épithélium longitudinal (croissance réduite et tardive). Une étude a également révélé des densités plus élevées de foyers de teinte foncée, ainsi que d'autres changements histologiques à 18 mois (White et coll., 2009).
Trois études ont examiné le DGM à une dose de ≤1 mg/kg p.c. par jour (Macon et coll., 2011; White et coll., 2011; Tucker et coll., 2015) et seront décrites de façon plus détaillée ci-après, car les LOAEL de ces études sont les plus faibles parmi tous les résultats, y compris ceux observés dans les études d'exposition subchronique et chronique. Les autres études observant ces effets feront l'objet d'un résumé plus concis.
Une étude portant sur deux générations (White et coll., 2011) a indiqué que l'exposition des souris à de faibles doses d'APFO dans l'eau potable (5 µg/L) a retardé le développement des glandes mammaires chez les mères P0 et F1 et les petits F1 et F2, un effet qui a persisté jusqu'à l'âge adulte (au moins 63e JAN). Des souris CD-1 femelles parentales (P0) (n = 7 à 12 par groupe) ont été placées dans différents groupes de traitement et ont reçu :
- des doses quotidiennes d'APFO par gavage (0, 1 ou 5 mg/kg p.c. par jour : groupes témoin G1 et G5, respectivement) du 1er au 17e jour de gestation (JG);
- des concentrations d'APFO dans l'eau potable seulement (5 µg/L, groupe DW) du 7e au 17e JG;
- des doses d'APFO par gavage (1 mg/kg p.c. par jour du 1er au 17e JG) et dans l'eau potable (5 µg/L du 1er au 17e JG) (groupes G1+DW).
Le premier jour suivant la naissance des portées du groupe F1, celles-ci ont été regroupées et redistribuées à des mères de leur groupe respectif (n=12 à 13 nouveau-nés par portée). Les rejetons femelles F1 des groupes G1 et G5 n'ont pas été exposés après la naissance, alors que les rejetons femelles F1 des groupes DW et G1+DW ont été exposés à l'APFO par l'eau potable tout au long du reste de l'étude (n=2 à 10 mères F1 par groupe). Les rejetons femelles F1 ont été accouplés avec des mâles non exposés à l'APFO afin de produire la génération F2. Les rejetons femelles F2 des groupes DW et G1+DW ont été exposés à l'APFO par l'eau potable jusqu'à la fin de l'étude. On a réalisé des autopsies sur les femelles F1 et F2 au 42e JAN et au 63e JAN, ainsi que sur les mères F1 et les rejetons femelles F2 au 10e JAN et au 22e JAN (White et coll., 2011).
Dans le groupe P0 (c.-à-d, les mères exposées directement), on a observé une hausse importante de la note de l'échelle de DGM dans tous les groupes traités le 22e JAN, et ce, même à une dose minimale (5 µg/L dans l'eau potable du 7e au 17e JG). Ces résultats élevés tiennent compte du retard dans l'involution mammaire normale pendant le sevrage (au 22e JAN, la structure des glandes mammaires des animaux du groupe P0 était similaire à la structure normalement observée au pic de lactation au 10e JAN). Les auteurs n'ont fourni que des renseignements sur la quantité d'ingestion quotidienne d'APFO chez les mères P0 qui consommaient 5 µg/L d'eau potable (environ 0,05 µg par jour lors de la période de gestation, et 0,1 ug par jour lors de la période de lactation [1er au 2enbsp;JAN]). On estime que les doses quotidiennes moyennes étaient d'environ 0,001 mg/kg p.c. par jour lors de la période de gestation et de 0,004 mg/kg p.c. par jour lors de la période de lactation (selon les poids moyens approximatifs de 62 g lors de la période de gestation et de 25 g lors de la période de lactation; le gain pondéral moyen de la mère était de 25 g. Les auteurs n'ont pas indiqué le poids corporel initial des mères, mais on suppose qu'il était d'environ 25 g pour cette souche de souris). Nous avons, par conséquent, déduit que la LOAEL était de 0,001 mg/kg p.c. par jour.
Les ratons F1 de tous les groupes de traitement ont montré des résultats réduits de DGM (réduction de l'élongation et l'embranchement des canaux, retard dans le délai d'apparition des BT) jusqu'à neuf semaines (63e JAN, c.-à-d., le dernier intervalle). Chez les mères F1 (c.-à-d., les ratons F1), tous les groupes traités à l'APFO ont démontré des résultats réduits de DGM au 10e JAN; l'attribution de faibles résultats a persisté au 22 JAN dans le groupe G1+DW, alors que la note du groupe G5 était supérieure à celle du groupe témoin au 22e JAN (c.-à-d., un retard de l'involution normale). Chez les femelles F2, les résultats de DGM au 10e JAN et au 22e JAN différaient très peu de celles du groupe témoin; ce résultat peut être biaisé par les résultats inhabituellement faibles qui ont été attribués dans le groupe témoin. Des résultats réduits de façon importante ont été plus tard obtenus dans tous les groupes traités (42e JAN pour le groupe DW, G1+DW et G5 et 63e JAN pour le groupe G1), lesquelles ont été caractérisées par un excès de BT (White et coll., 2011).
En résumé, White et coll. (2011) ont démonté que l'ingestion de l'APFO modifie le développement des glandes mammaires chez les mères et les rejetons des souris CD-1 à la suite d'une exposition à des doses minimales pertinentes pour l'humain d'APFO (aussi faibles que 5 µg/L dans l'eau potable), ce qui induit des concentrations sériques d'APFO pertinentes pour l'humain chez les petits et les mères (plage d'environ 20 à 90 ng/mL). On a estimé que la dose correspondante (LOAEL) à une exposition maternelle était d'environ 0,001 et 0,004 mg/kg p.c. par jour lors de la période de gestation et de lactation, respectivement. Dans cette étude, les effets sont survenus indépendamment des variations de poids corporel, et les seuls effets nocifs qui ont été observés pour les mères étaient les changements liés aux glandes mammaires.
Macon et coll. (2011) ont réalisé deux études sur le DGM des souris CD-1, soit une étude menée en dernière phase de la gestation et une étude menée tout au long de la gestation. Dans l'étude menée en dernière phase de la gestation, on a exposé les mères (n = 13 par groupe) à l'APFO (0, 0,01, 0,1 et 1,0 mg/kg p.c. par jour) par gavage oral du 10e au 17e JG. Dans l'étude menée tout au long de la période de gestation, on a exposé les mères (n=13 par groupe) à des doses par gavage d'APFO de 0, 0,3, 1,0 ou 3,0 mg/kg p.c. par jour du 1er au 17e JG.
Les résultats de l'étude menée en dernière phase de la gestation indiquent une diminution considérable des résultats de DGM (chez tous les groupes traités, avec une relation proportionnelle à la dose) au 21e JAN. D'autres effets observés sur les glandes mammaires au 14e JAN (à 0,1 et 1,0 mg/kg p.c. par jour, respectivement) comprenaient une diminution de la croissance épithéliale longitudinale de 14,4 % et de 37,3 % par rapport au groupe témoin (diminution de 27,4 % et de 56,5 % comparativement au 1er JAN) et une diminution statistiquement significative des BT. Dans l'étude menée tout au long de la période de gestation, les effets observés à toutes les doses étaient proportionnels à la dose et comprenaient une diminution des résultats de DGM chez les rejetons femelles jusqu'à l'âge adulte (84e JAN). Les LOAEL utilisées dans les études menées en dernière phase de la gestation et tout au long de la gestation étaient de 0,01 et 0,3 mg/kg p.c. par jour, respectivement. Comme ces études n'ont révélé aucune diminution du poids corporel chez les petits, on ne peut affirmer que les retards de DGM étaient attribuables à la diminution du poids corporel.
Tucker et coll. (2015) ont étudié le DGM chez les jeunes femelles CD-1 et C57Bl/6 qui ont été exposées in utero à l'APFO. On a exposé les mères à des doses d'APFO administrées par gavage de 0, 0,01, 0,1, 0,3 et 1 mg/kg p.c. par jour du 1er au 17e JG. On a observé des tendances significatives liées à la dose en ce qui a trait aux diminutions des résultats de DGM chez les petits des deux souches. Chez les souris CD-1, les diminutions étaient importantes lorsqu'elles ont été mesurées au 21e JAN à une dose de ≥0,1 mg/kg p.c. par jour, laquelle a diminué à ≥0,01 mg/kg p.c. par jour au 35e JAN et au 56e JAN. La LOAEL qui a été administrée aux souris C57Bl/6 était légèrement supérieure avant de baisser de façon importante à ≥0,3 mg/kg p.c. par jour au 21e JAN et au 61e JAN. Les auteurs ont également noté des concentrations sériques moyennes d'APFO moins élevées chez les souris C57Bl/6 que chez les souris CD-1.
Bien que la LOAEL administrée pour calculer les résultats de DGM fût moins élevée chez les souris CD-1 que chez les souris C57Bl/6, les résultats de cette étude ne sont pas suffisants pour conclure que la souche était sensible à l'effet. Moins de souriceaux sont nés dans l'ensemble des groupes C57Bl/6, ce qui a diminué la taille d'échantillon de la souche. Cette situation était particulièrement marquante dans les groupes auxquels on avait administré 0,01 et 0,1 mg/kg p.c. par jour, qui comptaient entre huit et 22 souris CD-1, mais seulement entre deux et cinq souris C57Bl/6. Comme les résultats de DGM étaient similaires entre les souches à toutes les doses, la taille d'échantillon la plus faible pourrait avoir empêché d'atteindre un effet statistiquement significatif à des doses plus faibles administrées aux souris C57Bl/6. En outre, la période d'attribution de résultats de DGM était différente pour les souches qui ont été évaluées à des moments ultérieurs (les souris CD-1 ont été examinées au 21e, 35e et 56e JAN, alors que les souris C57Bl/6 ont seulement été examinées au 21e et au 61e JAN), ce qui pourrait également avoir une incidence sur les résultats; les résultats de DGM chez les souris du groupe témoin C57Bl/6 au 61e JAN étaient inférieures à celles des souris du groupe témoin CD-1 au 35e et 56e JAN.
Tucker et coll. (2015) ont également examiné d'autres effets sur la maturité sexuelle, mais n'ont observé aucun effet lié au traitement sur les taux d'œstradiol et de progestérone ou au moment de l'ouverture vaginale ou du premier cycle œstral dans l'une ou l'autre des deux souches.
De nombreuses autres études menées à des doses plus élevées ont permis de noter des retards du DGM à différents moments chez les souris femelles CD-1 (incluant les mères et les petits) exposées à des doses par gavage de ≥3 mg/kg p.c. par jour (White et coll., 2007, 2009; Wolf et coll., 2007). Ces retards du DGM sont étayés par des données indiquant un taux réduit d'expressions de l'ARNm des gènes de la famille de prolactines (à ≥2 mg/kg p.c. par jour; Suh et coll., 2011), et un retard dans l'expression de la lactotransferrine à une dose de 5 mg/kg p.c. par jour (White et coll., 2007).
Une étude sur des souris péripubertaires (début de l'administration des doses à 21 jours) a relevé des différences entre les souches, dont des retards importants dans le DGM à une dose de ≥5 mg/kg p.c. par jour chez les souris Balb/c, mais seulement à 10 mg/kg p.c. par jour chez les souris C57Bl/6 (aucune inhibition dans l'une ou l'autre des souches à 1 mg/kg p.c. par jour; on a plutôt observé une stimulation à cette dose chez les souris C57Bl/6) (Yang et coll., 2009 b). Une autre étude sur les souris péripubertaires (Zhao et coll., 2010) a relevé des effets à la seule dose utilisée dans le cadre de l'étude, soit 5 mg/kg p.c. par jour.
Bien que les retards dans le développement des glandes mammaires puissent parfois être associés à une perte de poids, deux études ont précisément indiqué avoir observé ces effets en l'absence de disparités de poids corporel (White et coll., 2007, 2009). Une étude a également relevé que l'effet n'était pas entièrement attribuable au sous-développement des petits et à une stimulation insuffisante par la tétée, puisque la différenciation des glandes mammaires fonctionnelles a été altérée avant la parturition et la lactation (c.-à-d., avant la stimulation de la glande par les petits) (White et coll., 2007; 5 mg/kg p.c. par jour).
La puberté accélérée (≥1 mg/kg p.c. par jour chez les souris M et 20 mg/kg p.c. par jour chez les souris F; Lau et coll., 2006), un retard dans la maturation sexuelle (séparation du prépuce et perméabilité vaginale chez les rats; uniquement à 30 mg/kg p.c. par jour; Butenhoff et coll., 2004b) et l'ouverture vaginale à un âge plus avancé (à ≥5 mg/kg p.c. par jour chez les souris C57BL/6, mais pas chez les souris Balb/c; Yang et coll., 2009 b) sont d'autres effets liés à la maturité sexuelle qui peuvent être observés.
9.2.5.2 Effets sur l'utérus
On a observé des changements histologiques dans l'utérus de souris CD-1 exposées à de faibles doses d'APFO (Dixon et coll., 2012). Des effets tels qu'un œdème endométrial, une hyperplasie de la muqueuse et des glandes endométriales, un œdème ainsi qu'une hypertrophie et une hyperplasie du myomètre se sont manifestés chez des souris immatures exposées du 18e au 20e JAN à une dose d'APFO par gavage de 0,01 mg/kg p.c. par jour. Aucun effet histologique aux deux doses maximales utilisées dans l'étude (0,1 et 1 mg/kg p.c. par jour) n'a été observé. L'étude a par ailleurs relevé une augmentation liée à la dose de la mucification (significative uniquement à la dose maximale) dans le col utérin et le vagin.
On a observé des effets différentiels sur le poids de l'utérus de souris. L'étude de Dixon et coll. (2012) n'a observé des augmentations de poids de l'utérus qu'au groupe auquel on avait administré la dose minimale (0,01 mg/kg p.c. par jour). La seule autre étude à avoir signalé des changements de poids de l'utérus était une étude de gavage étendue sur quatre semaines et au cours de laquelle on avait exposé des souris péripubertaires Balb/c et C57BL/6 à une dose de 0, 1, 5 ou 10 mg/kg p.c. par jour (Yang et coll., 2009 b). Chez les souris Balb/c, le poids de l'utérus a diminué à toutes les doses (≥1 mg/kg p.c. par jour), alors que chez les souris C57BL/6, le poids de l'utérus a augmenté à une dose de 1 mg/kg p.c. par jour et a diminué proportionnellement à des doses plus élevées, ce qui est devenu significatif seulement à une dose de 10 mg/kg p.c. par jour.
9.2.5.3 Obésité à l'âge adulte
On a remarqué que l'obésité à l'âge adulte se manifestait lorsqu'il y avait une relation dose-réponse non monotone chez les souris dans la seule étude qui portait sur cet effet (Hines et coll., 2009). On a par ailleurs observé des effets liés à la dose sur le poids corporel, le contrôle de l'appétit (augmentation de la concentration de leptine et d'insuline dans le sang) et la répartition de la graisse chez les souris femelles adultes CD-1 exposées in utero à l'APFO. Les souris en gestation (n=7-22 par groupe d'exposition à la dose) ont été exposées quotidiennement à l'APFO par gavage du 1er au 17e jour de gestation (JG) (à des doses d'APFO de 0, 0,01, 0,1, 0,3, 1, 3 et/ou 5 mg/kg p.c. par jour); on a sevré les petits à trois semaines, puis on a sélectionné de jeunes femelles qui ont reçu une alimentation normale pour le reste de l'étude.
À de faibles doses (0,01, 0,1 et 0,3 mg/kg p.c. par jour), les données indiquaient un gain de poids excessif chez les souris âgées entre 20 et 29 semaines, ce qui coïncidait avec une augmentation des taux de leptine et d'insuline dans le sang (d'environ 2,5 fois) à entre 21 et 33 semaines (Hines et coll. 2009). À des doses plus élevées, les poids tissulaires à 18 mois ont révélé une diminution du poids relatif du gras blanc abdominal à des doses de 1 et 5 mg/kg p.c. par jour (aucun effet observé à 3 mg/kg p.c. par jour) et une augmentation du poids relatif du tissu adipeux brun interscapulaire à des doses de 1 et 3 mg/kg p.c. par jour (aucun effet observé à 5 mg/kg p.c. par jour). Le poids corporel général diminuait à une dose d'exposition plus élevée (5 mg/kg p. c. par jour). On n'a observé aucun effet sur le poids corporel à des doses de 1 et 3 mg/kg p.c. par jour.
Des expériences similaires réalisées sur des souris ovariectomisées de la même portée exposée (l'ovariectomie a été réalisée au 21e et 22e JAN) n'ont indiqué aucun effet sur le poids corporel et le poids de la graisse abdominale, mais ont révélé une augmentation du poids relatif du tissu adipeux brun interscapulaire à une dose de 1 mg/kg p.c. par jour (aucun effet observé à 5 mg/kg par jour). Bien que ces dernières données fussent difficiles à interpréter, les auteurs ont conclu que les ovaires semblaient jouer un rôle important dans l'effet de surpoids en milieu de vie et ont proposé qu'un dérèglement possible des récepteurs PPAR et de son signal par les hormones ovariennes puisse être responsable des effets observés à de faibles doses (Hines et coll., 2009). Il convient toutefois de noter que l'exposition des souris âgées de huit semaines aux mêmes doses pendant la même période (17 jours) n'a entraîné aucun effet sur les mêmes résultats (voir la section 9.2.2.1), ce qui suggère que le moment de l'administration de la dose est une donnée importante pour l'induction des effets latents (Hines et coll., 2009).
9.2.5.4 Effets sur le développement du foie
Tel que la section 9.2.2.1 le décrit, les effets hépatiques constituent les effets non liés au développement les plus sensibles résultant de l'exposition à court terme à l'APFO. Des augmentations du poids du foie après l'exposition in utero ou péripubertaire à l'APFO ont également été observées.
La dose minimale d'exposition maternelle à laquelle on a observé des augmentations du poids du foie chez les petits exposés avant la naissance à l'APFO était de 0,1 mg/kg p.c. par jour (Abbott et coll., 2007). Dans le cadre de cette étude, on a exposé des souris 129S1/SvImJ (n = 5-22 mères/dose) à des doses par gavage de 0, 0,1, 0,3, 0,6, 1, 3, 5, 10 et 20 mg/kg p.c. par jour du 1er au 17e JG. On a observé des augmentations du poids du foie chez les petits à toutes les doses et l'effet s'est aggravé à des doses plus élevées.
Une autre étude a relevé des effets légers, mais importants à une dose de <1 mg/kg p.c. par jour; l'étude comportait seulement un groupe auquel on avait administré des doses de 0,3 mg/kg p.c. par jour (Onishchenko et coll., 2011). D'autres études sur les souris exposées in utero (Wolf et coll., 2007; White et coll., 2009, 2011;Macon et coll., 2011) ou à l'âge péripubertaire (Yang et coll., 2009b) ont relevé l'effet à ≥1 mg/kg p.c. par jour.
9.2.5.5 Effets sur le développement neurologique
Deux études ont relevé des effets neurocomportementaux chez les souris exposées in utero ou peu après la naissance aux doses minimales utilisées--0,3 mg/kg p.c. par jour (Onishchenko et coll., 2011) et 0,58 mg/kg p.c. par jour (Johansson et coll., 2008). Les effets se sont manifestés par des changements dans les niveaux d'activité des souris.
On a constaté qu'une exposition alimentaire des souris C57BL/6/Bkl (n = 6 mères/groupe) à 0 ou 0,3 mg/kg (le seul groupe de traitement) d'APFO à partir du 1er JG jusqu'à la fin de la gestation entraînait des changements liés au sexe dans le comportement exploratoire des petits (durant la première heure passée dans un nouvel environnement), notamment une augmentation des activités exploratrices chez les mâles et une diminution des activités chez les femelles (Onishchenko et coll., 2011). L'exposition prénatale à l'APFO a également diminué le nombre total de périodes d'inactivité pendant la phase de lumière chez les mâles et les femelles, ainsi que la phase de noirceur du cycle circadien des mâles. La coordination motrice était légèrement altérée chez les femelles seulement. On n'a par ailleurs relevé aucun effet sur l'activité locomotrice, le comportement lié à l'anxiété (test du labyrinthe en croix surélevé) et l'immobilité dans le test de la nage forcée ou la force musculaire.
Dans l'examen des effets sur le neurodéveloppement, on a déterminé une LOAEL de 0,58 mg/kg chez des souris mâles NMRI auxquels on a administré une dose unique par gavage d'APFO (0,58 ou 8,70 mg/kg) à 10 jours (Johansson et coll., 2008). On a testé le comportement spontané et l'accoutumance des souris à l'âge de deux et quatre mois, et on a exploré la susceptibilité de leur système cholinergique dans le cadre d'un test de comportement spontané provoqué par la nicotine à quatre mois (Johansson et coll., 2008). Les données indiquent des effets liés à la dose et au temps sur le comportement (comportement spontané anormal, manque d'accoutumance et susceptibilité accrue du système cholinergique), ce qui reflète les progrès d'un processus de dysfonction cérébrale induit au moment de la poussée de croissance du cerveau de la souris avant sa naissance. Les souris exposées à l'APFO ont démontré un comportement spontané altéré et une baisse de réponse à la nicotine aux deux doses. Les trois variables du test de comportement (la locomotion, le redressement et l'activité totale) ont été altérées, indiquant une hypoactivité pendant les 20 premières minutes et une hyperactivité dans les 20 dernières minutes (40 à 60 minutes après le début du test), et les effets s'aggravaient avec l'âge. Ces effets étaient accompagnés d'une augmentation significative des taux des protéines qui jouent un rôle important dans le développement normal du cerveau (la CaMKII, la GAP-43 et la synaptophysine dans l'hippocampe, la synaptophysine et la protéine tau dans le cortex cérébral et la protéine tau dans l'hippocampe) chez les souris exposées aux mêmes conditions néonatales (Johansson et coll., 2009).
9.2.5.6 Autres effets
On a observé à des doses plus élevées d'autres effets sur la reproduction et le développement que ceux qui ont été décrits plus haut dans cette section; la LOAEL liée au retard de l'ouverture des yeux (Abbott et coll., 2007) était établie à 0,6 mg/kg p.c. par jour, et tous les autres effets ont été observés à une dose de ≥1 mg/kg p.c. par jour.
Les autres effets sur la reproduction des souris comprenaient un nombre réduit d'implants (White et coll., 2011), une hausse du taux de résorption, de fœtus morts, de pertes d'embryons après l'implantation ou de pertes prénatales (White et coll., 2007; Suh et coll., 2011; White et coll., 2011;), y compris des augmentations de résorption ou de pertes de portées complètes (Lau et coll., 2006; Wolf et coll., 2007; White et coll., 2009), une diminution du poids du placenta (Suh et coll., 2011), un délai plus long avant la parturition (Lau et coll., 2006), une diminution du nombre de fœtus vivants (White et coll., 2011), une augmentation du nombre de petits mort-nés (Yahia et coll., 2010), une diminution de la survie des petits (Lau et coll., 2006; Wolf et coll., 2007; White et coll., 2009; 2011; Yahia et coll., 2010) et des changements histophatologiques dans le placenta des souris (Suh et coll., 2011).
Les autres effets sur le développement de la progéniture des souris comprenaient un retard de l'ouverture des yeux observé dans des études portant sur une génération (Lau et coll., 2006; Abbott et coll., 2007; Wolf et coll., 2007; White et coll., 2009), des effets sur le squelette observés dans des études portant sur une génération (l'une des études a permis d'observer une ossification altérée [fontanelle élargie, ossification réduite des sternèbres et de la calotte crânienne; Lau et coll., 2006], un retard dans l'ossification des phalanges relevé dans une autre étude, une augmentation de la fissure sternale et un retard dans la percée des incisives; Yahia et coll., 2010), une diminution du poids relatif de la rate, sans une relation dose-réponse claire (Hines et coll., 2009), une diminution du poids de fœtus ou des petits (Staples et coll., 1984; Lau et coll., 2006; Abbott et coll., 2007; White et coll., 2007; 2009; Wolf et coll., 2007; Yahia et coll., 2010; Suh et coll., 2011) et une augmentation du poids des fœtus (Yahia et coll., 2010).
Un retard de croissance (à ≥10 mg/kg p.c. par jour chez les souris M et 30 mg/kg p.c. par jour chez les souris F) et une augmentation de la mortalité après le sevrage (à 30 mg/kg p.c. par jour chez les souris F), avec l'absence d'effets sur la génération F2, constituent les seuls effets observés dans une étude portant sur deux générations de rats (Butenhoff et coll., 2004 b; York, 2002).
9.3 Mode d'action
Une analyse des modes d'action (MA) des effets se manifestant à des concentrations minimales d'APFO (c.-à-d., des tumeurs des cellules de Leydig, une hypertrophie hépatocellulaire et des changements dans les lipides sériques chez les rats, ainsi que des augmentations du poids du foie, une hypertrophie hépatocellulaire, de l'obésité, des retards de développement et des retards de développement des glandes mammaires chez les souris) a fait l'objet d'un examen. Seule une évaluation préliminaire des données a pu être réalisée pour la plupart des MA; une analyse des MA (Meek et coll., 2014) fondée sur des documents d'orientation récents (Meek et coll., 2014) a pu être réalisée pour les effets de prolifération des peroxysomes sur les résultats hépatiques. Au vu de l'analyse des MA, on ne considère aucun effet comme étant non pertinent pour les humains. Les résultats suggèrent toutefois que l'approche de l'apport quotidien tolérable (AQT) constitue la méthode la plus appropriée pour évaluer les risques de cancer. La section suivante comprend un résumé des résultats des évaluations des MA.
9.3.1 Mutagénicité à action directe
La mutagénicité à action directe et la réactivité relative à l'ADN ont été considérées comme étant des MA potentiels pour le développement de tumeurs des cellules de Leydig. Comme il en est question à la section 9.2.4, les données probantes indiquent principalement que l'APFO n'est pas mutagène, avec ou sans l'activation métabolique. Les résultats de la génotoxicité de l'APFO étaient négatifs dans un large éventail d'essais in vitro et in vivo. Des résultats positifs ont été seulement obtenus dans le cadre d'un test visant à déceler les aberrations chromosomiques sur des cellules de hamsters et d'un test du micronoyau sur les cellules humaines. On a par ailleurs observé une mutagénicité de cellules hybrides (AL) humaines-hamsters, mais il a été démontré que les EOR liées aux mitochondries jouaient un rôle important dans ce processus. Le modèle des tumeurs induites par l'APFO n'a également pas suivi celui des mutagènes typiques. Par exemple, les mutagènes causent habituellement des tumeurs dans de nombreux organes, mais l'APFO n'a affecté que les cellules testiculaires de Leydig, le foie et le pancréas (c.-à-d., les organes associés à la triade de tumeurs des récepteurs activés par les proliférateurs de peroxysomes alpha (PPARa) dans le cadre d'une étude (Biegel et coll., 2011), et seulement les cellules de Leydig dans une autre étude qui utilisait des doses similaires (Butenhoff et coll., 2012 b). En outre, les mutagènes provoquent souvent un taux d'incidence élevé de tumeurs qui surviennent tôt et à de faibles doses. Chez les animaux exposés à l'APFO, les tumeurs ont été observées seulement après une exposition d'une vie entière à des doses maximales et à de faibles incidences (10 à 14 %) dans les études sur l'APFO.
Une étude qui suggère que l'APFO agit comme promoteur de tumeurs appuie davantage l'hypothèse de l'activité non mutagène de l'APFO. On y a observé des tumeurs du foie--principalement l'hépatocarcinome--chez des rats qui ont été soumis à des protocoles d'initiation (c.-à-d., ils ont été exposés au diéthylnitrosamine mutagène) et qui ont été exposés à de la nourriture renfermant 0,015 % d'APFO (une dose équivalente à 7,5 mg/kg p.c. par jour fondée sur l'hypothèse de Santé Canada [1994] selon laquelle 1 ppm dans la nourriture équivaut à 0,05 mg/kg p.c. par jour chez les rats) de la 5e à la 28e semaine de l'étude (Abdellatif et coll., 1990). On a observé des tumeurs hépatiques chez 33 % des animaux (comparativement à 0 % chez les animaux témoins qui ont été initiés, mais pas exposés aux promoteurs de tumeurs); par conséquent, des effets ont été observés plus tôt (après six mois d'exposition à l'APFO et sept mois après l'initiation) et à un taux d'incidence supérieur à celui des études à des doses plus élevées menées sur des rats exposés uniquement à l'APFO.
Le poids de la preuve des MA des tumeurs (tel qu'il est examiné plus loin dans cette section) est plus solide que celui de la mutagénicité à action directe, ce qui suggère que l'extrapolation linéaire à des doses minimales n'est pas appropriée pour les tumeurs causées par l'APFO. Aucune autre analyse de MA n'est requise pour la mutagénicité à action directe, à moins que des données contradictoires ne soient publiées.
9.3.2 Prolifération des peroxysomes
La prolifération des peroxysomes était considérée comme étant un MA potentiel de l'hypertrophie hépatocellulaire chez les rats et les souris, des modifications des lipides sériques et des tumeurs hépatocellulaires chez les rats et de l'augmentation du poids et de l'obésité chez les souris. Comme il existe certaines données pour l'activité hépatique du RAPP chez les rats et les souris, l'analyse a porté principalement sur ce point. Étant donné que peu d'études ont mesuré directement l'impact du RAPP sur les autres résultats, il a été impossible d'établir un bilan exhaustif; des études sur des souris déficientes en PPAR indiquent toutefois une sensibilité décroissante aux effets sur la reproduction et le développement (y compris des pertes de portées, un retard de l'ouverture des yeux et une diminution du poids des petits [Abbott et coll., 2007]), mais pas les retards dans le développement des glandes mammaires (Zhao et coll., 2010). Les critères évolués de Bradford-Hill ont été utilisés afin d'évaluer le poids de la preuve du MA de prolifération des peroxysomes comme effets hépatiques. Un résumé est présenté ci-dessous.
On estime que trois principaux événements du MA de prolifération des peroxysomes induisent des effets histologiques hépatiques et des tumeurs hépatocellulaires. Ces principaux événements sont 1) l'activation des récepteurs hépatiques PPARa, engendrant 2) des voies de croissance cellulaire qui inhibent l'apoptose et/ou favorise la réplication cellulaire, ce qui entraîne éventuellement 3) la prolifération des hépatocytes (Corton et coll., 2014).
9.3.2.1 Événement clé no 1 - Activation des PPARa
On a observé une absence d'oxydation hépatique du palmitoyl-CoA chez les rats exposés à 0,3 mg/kg p.c. par jour d'APFO pendant 14 jours (Loveless et coll., 2006). La dose minimale à laquelle on a observé l'oxydation hépatique chez les rats s'élevait à 0,64 mg/kg p.c. par jour après quatre semaines d'exposition (Perkins et coll., 2004), et l'effet se manifestait régulièrement à des doses maximales (à ≥1 mg/kg p.c. par jour pendant 14 jours [Loveless et coll., 2006], à ≥1,94 mg/kg p.c. par jour pendant ≥4 semaines [Perkins et coll., 2004], à ≥2 mg/kg p.c. par jour pendant 14 jours [Liu et coll., 1996], à 7,5 mg/kg p.c. par jour pendant 23 semaines [Abdellatif et coll., 1990], 13,6 mg/kg p.c. par jour pendant ≥1 mois [Biegel et coll., 2011] et environ à 20 mg/kg p.c. par jour pendant ≤28 jours [Elcombe et coll., 2010]). On a observé chez les souris une oxydation hépatique du palmitoyl-CoA à des doses d'APFO plus faibles que chez les rats. L'effet a été mesuré à ≥0,3 mg/kg p.c. par jour pendant 14 jours d'exposition (Loveless et coll., 2006) et à des doses plus élevées dans d'autres études (Yang et coll., 2002; Minata et coll., 2010; Nakagawa et coll., 2012); on a observé, de plus, une expression accrue des gènes liés aux PPAR chez les souris de type sauvage, et non chez les souris humanisées avec ou sans activation des PPAR qui ont été exposées pendant deux semaines à ≥0,1 mg/kg p.c. par jour (Nakamura et coll., 2009). Chez les rats exposés à 13,6 mg/kg p.c. par jour d'APFO pendant deux ans, on n'a observé aucune hausse d'oxydation du palmitoyl-CoA dans les cellules de Leydig (Biegel et coll., 2011); la même étude n'a par ailleurs mesuré aucune augmentation de l'effet dans un modèle de proliférateur de peroxysomes (Wyeth-14,643 [WY]).
9.3.2.2 Événement clé no 2 - croissance de cellules altérées
Nous n'avons trouvé aucune étude sur les marqueurs des voies de croissance de cellules altérées.
9.3.2.3 Événement clé no 3 - prolifération des cellules
Une absence de prolifération des hépatocytes chez les rats exposés à 13,6 mg/kg p.c. par jour d'APFO entre un et 24 mois a été relevée alors qu'on observait la même chose une chez des animaux témoins positifs (c.-à-d., des souris exposées au gène WY) aux mêmes périodes (Biegel et coll., 2001). L'effet a été observé chez les rats exposés à environ 20 mg/kg p.c. par jour entre deux et 29 jours (Elcombe et coll., 2010). On a observé une augmentation liée à la dose de l'indice de marquage chez les souris de type sauvage et les souris déficientes en PPAR exposées pendant sept jours, et dont la signification de l'effet a été atteinte à 10 mg/kg p.c. par jour (mais non à 1 ou 3 mg/kg p.c. par jour) chez les deux souches (Wolf et coll., 2008).
On a mesuré la prolifération des cellules dans les cellules acineuses pancréatiques, mais pas dans les cellules de Leydig, chez les rats exposés à 13,6 mg/kg p.c. par jour pendant deux ans (Biegel et coll., 2011).
9.3.2.4 Évaluation des critères de Bradford-Hill
Concordance biologique -- l'activation des PPAR menant à une augmentation de la réplication des hépatocytes et des tumeurs hépatiques est un MA bien connu. On a observé des hausses de tumeurs testiculaires (cellules de Leydig), pancréatiques et hépatocellulaires chez les rats (Biegel et coll., 2011), lesquelles constituent la triade de tumeurs reconnue pour le MA de la prolifération des peroxysomes (Corton et coll., 2014); on a également observé une augmentation de la prolifération des cellules acineuses pancréatiques et de l'hyperplasie chez les rats (Biegel et coll., 2011). Il y a toutefois des incohérences dans cette observation, puisqu'on n'a pas observé de triade de tumeurs à une dose similaire dans une autre étude qui a été menée pendant deux ans sur des rats (Butenhoff et coll., 2012b). Des études sur la prolifération des peroxysomes et le développement de tumeurs dans ces cellules chez les souris (qui sont plus sensibles à la prolifération des peroxysomes que les rats) fourniraient potentiellement plus de renseignements utiles pour l'analyse des MA.
Caractère essentiel de l'événement clé -- des études sur les souris déficientes en PPAR (Yang et coll., 2002; Abbott et coll., 2007; Wolf et coll., 2008; Nakagawa et coll., 2012) ont fourni plus de renseignements dans l'évaluation de l'essentialité des événements clés des effets hépatiques; nous n'avons trouvé aucune étude sur les rats déficients en PPAR ayant été exposés à l'APFO. Dans l'étude d'Abbott et coll. (2007), on a observé une diminution de la sensibilité des souris déficientes en PPAR aux effets liés au poids du foie, ce qui appuie d'une certaine manière le MA de cet effet nocif; les effets liés au poids du foie sont encore observés (bien qu'à des doses plus élevées) chez les souris déficientes en PPAR, et l'hépatomégalie est induite dans une même mesure chez les souris de type sauvage et les souris déficientes en PPAR dans d'autres études (Yang et coll., 2002; Wolf et coll., 2008; Nakagawa et coll., 2012). L'augmentation de la prolifération des hépatocytes (telle qu'elle est mesurée par la hausse de l'indice de marquage) était également similaire entre les souris de type sauvage et les souris déficientes en PPAR (Wolf et coll., 2008). En outre, malgré une absence d'expression accrue de gènes liés aux PPAR chez les souris déficientes en PPAR et les souris humanisées avec activation des PPAR, des augmentations du poids du foie étaient similaires parmi ces souches et les souris de type sauvage (c.-à-d, les souris avec une augmentation de l'expression des PPAR) (Nakagawa et coll., 2012). Malgré ces similarités quantitatives entre les souches des effets non cancéreux sur le foie, on a observé des différences qualitatives - dont des différences dans l'apparence microscopique et l'ultrastructure des cellules hépatiques (Wolf et coll., 2008; Minata et coll., 2010). D'autres études qui exposent des souris déficientes en PPAR à des doses plus faibles et qui examinent d'autres résultats nocifs, ainsi que des études sur les rats déficients en PPAR, contribueraient à mieux évaluer le MA.
Correspondance temporelle et dose-réponse - On a observé une certaine corrélation dose-réponse du MA, comme l'activation des PPAR précède la prolifération des hépatocytes chez les rats; la prolifération des hépatocytes était toutefois absente à des doses pertinentes pour les tumeurs (Biegel et coll., 2001) et s'est produite seulement à des doses plus élevées que celles qui induisent une hypertrophie hépatocellulaire et une augmentation de poids (Elcombe et coll., 2010). La seule étude de prolifération des hépatocytes chez les souris indique son occurrence uniquement à des doses supérieures à celles auxquelles des augmentations de l'hypertrophie et du poids du foie ont été observées (Wolf et coll., 2008). En outre, l'absence de données sur les voies de croissance de cellules altérées empêche de déterminer si cet événement clé est déclenché par l'activation des PPAR et est précurseur de la prolifération d'hépatocytes.
La première manifestation (activation des PPAR) ne semble pas précéder les résultats hépatiques néfastes chez les rats. On a relevé une augmentation du poids du foie et une hypertrophie hépatocellulaire à une limite égale ou inférieure aux doses auxquelles on avait observé une activation des PPAR.
Cohérence (dans l'ensemble des espèces, des souches, des organes et des systèmes de test) -- tel qu'il est prévu, l'activation des PPAR débute à des doses plus faibles chez les souris que chez les rats et les singes en fonction des connaissances de la biologie des PPAR (Corton et coll., 2014). L'activation des PPAR n'est toutefois pas cohérente chez les singes, n'est pas accompagnée d'une prolifération de cellules et survient à des doses plus élevées que celles liées à des effets néfastes pour le foie.
Composés analogues -- La triade de tumeurs observées chez les rats mâles ainsi que l'augmentation du taux d'œstradiol sérique étaient similaires pour l'APFO et un proliférateur modèle de peroxysomes WY. L'effet hépatique chez les rats exposés au SPFO semble toutefois se manifester en l'absence de prolifération des peroxysomes, et on n'a pas observé la triade de tumeurs chez les rats exposés au SPFO.
Certaines données probantes sur les rats et les souris appuient l'incidence de la prolifération des peroxysomes en tant que mode d'action de l'hypertrophie hépatocellulaire. On a par ailleurs observé une triade caractéristique de tumeurs des proliférateurs des peroxysomes (cancers des testicules, du pancréas et du foie) chez les rats, et les doses auxquelles les tumeurs hépatocellulaires sont supérieures à celles qui avaient été administrées lors des manifestations clés du MA de la prolifération des peroxysomes. Des augmentations du poids du foie et une hypertrophie hépatocellulaire semblent toutefois se manifester à des doses plus faibles que celles qui avaient été administrées lors de l'activation des PPAR chez les rats; par conséquent, bien qu'il y ait une activation des PPAR chez les rats, celle-ci ne semble pas déclencher ces deux effets. Les études sur les souris déficientes en PPAR indiquent que la prolifération des peroxysomes pourrait jouer un rôle dans l'hypertrophie hépatocellulaire et l'augmentation du poids du foie, mais, malgré des différences qualitatives (c.-à-d., l'apparence) entre les souches, les similarités quantitatives entre les changements observés chez les souris déficientes en PPAR par rapport aux souris de type sauvage indiquent que d'autres MA jouent un rôle important dans la manifestation de ces effets. Parce que le MA de la prolifération des peroxysomes ne semble pas être le seul MA concerné, on ne peut exclure la signification pour l'humain des effets hépatiques non cancérogènes induits par l'APFO. En revanche, une analyse détaillée des MA a permis de conclure que les preuves du MA de la prolifération des peroxysomes en ce qui concerne les tumeurs au foie induites par l'APFO étaient solides. La pertinence de ces tumeurs pour les humains est limitée, puisque l'activation des PPARa par l'APFO est plus faible chez les humains que chez les rats. En outre, l'activation des PPARa par différents composés ne semble pas engendrer une prolifération hépatocellulaire et des tumeurs (Corton et coll., 2012; Klaunig et coll., 2012).
9.3.3 Perturbation des hormones sexuelles
Une perturbation des hormones sexuelles est un MA potentiel qui pourrait être envisagé pour les retards dans le développement des glandes mammaires chez les souris, l'obésité chez les souris exposées avant la naissance et les tumeurs des cellules de Leydig chez les rats. Il n'existe pas suffisamment de données pour être en mesure de réaliser une analyse quantitative des perturbations des hormones sexuelles; on a par ailleurs relevé peu d'observations différentes qui pourraient être pertinentes pour le MA des hormones sexuelles, y compris l'inhibition des effets utérins lorsque l'APFO était coadministré avec l'œstradiol (Dixon et coll., 2012), une amélioration des effets de l'œstradiol-17β dans une variété d'essais in vitro, mais avec une absence d'activité œstrogénique directe (Sonthithai et coll., 2015), le renversement des retards dans le développement de glandes mammaires avec le supplément des concentrations physiologiques d'œstradiol ou de progestérone (Zhao et coll., 2012), une augmentation des concentrations sériques d'œstradiol chez les rats mâles exposés pendant 1 à 12 mois (Biegel et coll., 2001), des changements de la genèse d'œstradiol (une diminution à des doses plus faibles et une augmentation à des doses plus élevées) dans un essai stéroïdogenèse in vitro (Rosenmai et coll., 2013), une absence de liaison ou d'activation par l'APFO des récepteurs d'œstrogènes humains in vitro (Ishibashi et coll., 2007) et des diminutions des taux de cholestérol, ce qui pourrait perturber la synthèse des testostérones (Li et coll., 2011). Si des études plus approfondies sur l'effet de l'APFO sur la perturbation des hormones sexuelles sont réalisées, ce MA potentiel pourrait faire l'objet d'un examen plus rigoureux.
9.3.4 Autres MA
Il n'existe pas suffisamment de données pour évaluer les autres MA potentiels examinés dans l'analyse des MA. Quelques données - particulièrement en ce qui a trait à l'activation des PPAR et de la prolifération des peroxysomes sont disponibles pour d'autres effets qui ne font pas partie de l'analyse des MA (c.-à-d. des effets qu'on a observés à des doses d'exposition plus élevées d'APFO).
10.0 Classification et évaluation
L'APFO et ses sels ont été classés comme étant possiblement cancérogènes pour les humains (Groupe 2B) par le CIRC qui s'est basé sur des données probantes épidémiologiques limitées qui démontraient des associations entre l'APFO et les cancers des testicules et du rein, ainsi que des données probantes limitées sur les animaux de laboratoire (Benbrahim-Tallaa et coll., 2014). Dans le cadre d'une évaluation en vertu de la Loi canadienne sur la protection de l'environnement, l'APFO, ses sels et ses précurseurs ont répondu aux critères de persistance et des effets nocifs à long terme ou immédiats sur l'environnement ou sa diversité biologique. On n'a pas jugé toutefois qu'ils étaient bioaccumulables ni qu'ils pénétraient dans l'environnement dans des conditions qui constituent ou peuvent constituer un danger au Canada pour la vie ou la santé humaine (Environnement Canada et Santé Canada, 2012).
On a utilisé l'approche de la dose de référence (BMD) autant que possible afin de calculer des PDD potentiels, car il s'agit d'une méthode fondée sur des données liées à toute la courbe dose-réponse de l'effet critique plutôt que sur des données provenant du groupe ayant reçu la NOAEL comme dose (PISSC, 1994). On a suggéré une limite de confiance inférieure de la dose de référence (BMDL) comme substitut approprié à la NOAEL (Crump, 1984). Plus précisément, une BMDL appropriée est définie comme étant une estimation à la limite inférieure de l'intervalle de confiance à 95 % de la dose correspondant à un niveau de risque de 1 à 10 % de plus que les niveaux de fond. La définition de la BMD comme limite de confiance inférieure tient compte de la puissance statistique et de la qualité des données (PISSC, 1994). On a calculé la dose de référence représentant une hausse de 10 % des effets nocifs par rapport aux taux de fond (BMD10) et leurs limites de confiance inférieures de 95 % (BMDL10) au moyen du logiciel Benchmark Dose de U.S. EPA (BMDS Version 2.6.0.86; U.S. EPA, 2015).
Il existe de grandes différences pharmacocinétiques entre les animaux et les humains, et une clairance plus faible (c.-à-d., des valeurs plus élevées de demi-vie) chez les humains que chez les rats, les souris et les singes. Ces différences donnent lieu à des doses tissulaires cibles plus élevées chez les humains lors de l'exposition aux mêmes doses externes que celles des animaux. Les approches par défaut à l'égard de l'extrapolation interespèces (p. ex., un facteur d'incertitude interespèces de 10, l'ajustement allométrique) ne sont toutefois pas considérées comme étant des méthodes qui protègent suffisamment les humains. Tel qu'il est décrit à la section 8.6, on a calculé les valeurs de CAFI (c.-à-d., l'élément du FASC reflétant les différences toxicocinétiques interespèces) en ayant recours à un modèle PBPK afin d'aborder les différences pharmacocinétiques entre les animaux et les humains. Comme on a calculé différentes valeurs de CAFI pour diverses doses, celles-ci peuvent également traiter la non-linéarité de la pharmacocinétique. L'approche comporte également des faiblesses, telle que le décrit de façon détaillée la section 8.6, dont l'utilisation de l'état d'équilibre de la concentration plasmatique comme mesure de dose, plutôt que la sélection de valeurs en fonction des organes ou de l'exploration permettant de déterminer si les autres mesures de doses (p. ex., des pics de concentration) sont plus appropriées. Nous avons toutefois déterminé, malgré les faiblesses, que cette approche était la meilleure des options offertes. Nous avons sélectionné celle-ci plutôt que l'utilisation de concentrations sériques comme PDD, parce que nous avons déterminé que les modèles humains PBPK n'étaient pas suffisamment solides pour obtenir des estimations précises des niveaux d'exposition correspondants aux PDD fondés sur le sérum.
10.1 Évaluation du risque de cancer
Les données épidémiologiques ont démontré un lien entre l'exposition à l'APFO et le risque accru d'incidence de cancers des testicules et du rein (voir la section 9.1.3). Les associations ont été observées dans des études épidémiologiques de grande envergure qui ont été réalisées dans une communauté présentant des concentrations élevées d'APFO dans l'eau (C8 Project). La relation de causalité et le point de départ ne peuvent toutefois pas être déterminés à partir de ces études en raison du manque de cohérence entre les études (aucun lien n'a été établi dans certaines études prospectives menées au Danemark et aux États-Unis). Nous avons également observé des contraintes dans les études relevant une association positive, notamment un risque de confusion résiduel (parce que le modèle ne comprenait pas de covariables et d'expositions aux autres contaminants), des nombres peu élevés de cas, des incertitudes quant à la caractérisation de l'exposition (estimations approximatives en fonction de la résidence dans une certaine région) et un nombre élevé de résultats compris dans le modèle, augmentant ainsi la probabilité d'observations liées au hasard.
Deux études sur l'exposition chronique ont relevé des adénomes testiculaires des cellules de Leydig chez des rats mâles Crl:CD BR (CD) exposés à l'APFO pendant deux ans. La première étude a observé ces adénomes à 13,6 mg/kg p.c. par jour (la seule dose testée dans l'étude; Biegel et coll., 2001); l'autre étude a relevé une augmentation liée à la dose des incidences d'adénomes, dont l'atteinte de la signification est survenue à une dose maximale (14,2 mg/kg p.c. par jour; 3M, 1983; Sibinski, 1987; Butenhoff et coll., 2012b). Les adénomes des cellules de Leydig étaient accompagnés par une hyperplasie des cellules de Leydig et une prolifération des cellules acineuses pancréatiques dans l'étude de Biegel et coll. (2001). Celle-ci a de plus permis d'observer des augmentations liées à la dose de fibroadénomes mammaires chez les rates, mais ceux-ci n'ont pas été considérés comme étant des lésions prolifératives selon les critères de diagnostic actuels.
Bien que l'on n'ait pas trouvé le mode d'action des tumeurs induites par l'APFO, la valeur probante des données suggère plus fortement que l'APFO est un composé non mutagène (voir les sections 9.2.4 et 9.3). Pour cette raison, l'approche de l'AQT est la méthode la plus appropriée pour calculer une valeur basée sur la santé pour le cancer.
L'étude de Butenhoff et coll. (2012b) représente la principale étude que nous avons sélectionnée pour évaluer les risques de cancer, puisqu'il s'agit de la seule étude sur l'exposition chronique qui utilise plus d'une dose. L'incidence de tumeurs des cellules de Leydig était respectivement de 0, 2 et 7 chez les rats exposés à 0, 1,3 et 14,2 mg/kg p.c. par jour. Puisqu'on a observé seulement une signification à une dose maximale, la NOAEL et la LOAEL pour les tumeurs des cellules de Leydig dans cette étude étaient respectivement de 1,3 et 14,2 mg/kg p.c. par jour. L'utilisation d'une modélisation des doses de référence n'est généralement pas recommandée pour les études comportant seulement deux groupes de doses (U.S. EPA, 2012b); nous avons utilisé cette approche aux fins de comparaison avec la NOAEL. Trois modèles (Log Logistic, Log Probit et Multistage) constituaient les meilleurs choix (ces trois modèles comportaient le critère d'information d'Akaike [CIA] le plus faible parmi tous les modèles examinés). Les valeurs de la LDR10 de ces trois modèles variaient de 1,06 à 1,26 mg/kg p.c. par jour, et étaient par conséquent similaires à la NOAEL de 1,3 mg/kg p.c. par jour, qui est utilisée comme PDD de l'analyse.
Afin de refléter les grandes différences interespèces en matière de pharmacocinétique, le point de départ équivalent humain (PDDEQH) peut être calculé en divisant la LDR10 par la valeur de CAFI comme suit :
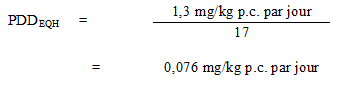
Figure 3 - Equivalent Textuel
Le PDDEQH est de 0,076 mg/kg p.c. par jour. Cette valeur est calculée en divisant la BMD10 associée aux tumeurs des cellules de Leydig chez les rats mâles, de 1,3 mg/kg p.c par jour, par la valeur de CAFI propre à la dose des rats d'environ 1 mg/kg p.c. par jour, 17.
Application :
- 1,3 mg/kg p.c. par jour représente la BMD10 associée aux tumeurs des cellules de Leydig chez les rats mâles (Butenhoff et coll., 2012b);
- 17 représente la valeur d' CAFI propre à la dose des rats d'environ 1 mg/kg p.c. par jour (comme le décrit la section 8.6.2).
On a calculé l'AQT comme suit à l'aide du PDDEQH calculé :
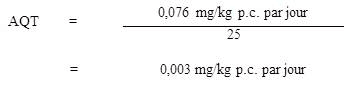
Figure 4 - Equivalent Textuel
L'AQT pour l'APFO est de 0,003 mg/kg p.c. par jour. Cette valeur est calculée en divisant le PDDEQH de 0,076 mg/kg p.c. par jour par le facteur d'incertitude composite, 25.
Application :
- 0,076 mg/kg p.c. par jour représente le PDDEQH associé à la NOAEL des tumeurs des cellules de Leydig chez les rats mâles (Butenhoff et coll., 2012b);
- 25 représente le facteur d'incertitude composite, tel que décrit ci-après.
Le facteur d'incertitude composite de 25 est le produit de deux éléments : le facteur d'incertitude interespèces (×2,5) et le facteur d'incertitude intraespèce (×10). La valeur de 2,5 est utilisée afin de refléter l'élément toxicodynamique du facteur d'incertitude interespèce par défaut, car les différences toxicocinétiques entre les rats et les humains ont déjà été intégrées lors du calcul du PDDEQH. Nous avons appliqué une valeur par défaut de 10 pour le facteur d'incertitude intraespèce. Nous avons présumé que la valeur par défaut était suffisante en l'absence de données sur les différences intraespèces. Bien que nous soyons conscients qu'il existe de grandes différences en matière de pharmacocinétique entre les espèces, l'insuffisance des données sur le mécanisme d'excrétion de l'APFO nous empêche de mener des enquêtes afin de déterminer si la variabilité pharmacocinétique serait également importante dans une population humaine. Les valeurs moyennes de demi-vie qui ont été calculées à partir des données longitudinales pour les différentes populations exposées précédemment à l'APFO étaient similaires (les moyennes de chaque population variaient entre 2,3 et 3,8 années; Olsen et coll., 2007; Bartell et coll., 2010; Brede et coll., 2010); toutefois, les études ayant fourni un écart de valeurs ont indiqué qu'il y avait environ dix fois plus de différences entre les estimations minimales et maximales des demi-vies. Si d'autres études sur l'APFO indiquent de façon constante une différence multipliée par dix dans la pharmacocinétique d'une population, un facteur d'incertitude intraespèce plus élevé pourrait être justifié afin d'assurer que les différences relatives à la pharmacodynamique entre les humains sont aussi abordées de façon quantitative.
La VBS dans l'eau potable peut être calculée comme suit à l'aide de l'AQT :
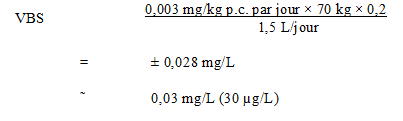
Figure 5 - Equivalent Textuel
La VBS pour l'APFO dans l'eau potable est de 0,03 mg/L (arrondie). Cette valeur est calculée en multipliant l'AQT de l'APFO pour le cancer, soit 0,003 mg/kg p.c. par jour, par 70 kg, le poids corporel moyen d'un adulte puis par le facteur d'attribution de l'eau potable, 0,2, et en divisant le résultat par 1.5 L/jour, le volume quotidien d'eau consommé par un adulte.
Application :
- 0,003 mg/kg p.c. par jour est l'AQT calculé ci-dessus;
- 70 kg est le poids corporel moyen d'un adulte;
- 0,2 est le facteur d'attribution par défaut pour l'eau potable qui a été utilisé comme valeur seuil, étant donné que l'eau potable n'est pas une source importante d'exposition et qu'il existe des preuves de la présence répandue du composé dans au moins un autre milieu (air, aliments, sol ou produits de consommation) (Krishnan et Carrier, 2013);
- 1,5 L/jour représente le volume quotidien d'eau consommé par un adulte; des expositions par inhalation ou voie cutanée de l'eau utilisée pour le bain ou la douche ne sont pas considérées comme étant des voies d'exposition significatives (comme le décrit la section 5.7).
10.2 Évaluation du risque d'effets autres que le cancer
Bien que les preuves épidémiologiques aient démontré un lien entre l'exposition à l'APFO et de nombreux effets sur la santé, tels que les dérèglements du système immunologique et des altérations du poids à la naissance et des taux de lipides (voir la section 9.1.3), il est impossible de calculer un PDD à partir de ces études en raison de certaines contraintes, notamment le modèle d'étude, les biais et les facteurs de confusion.
Les LOAEL les plus faibles de l'APFO étaient associés aux effets sur la reproduction et le développement chez les souris, avec des effets observés à des doses aussi faibles que 0,001 à 0,01 mg/kg p.c. par jour en ce qui concerne le retard du développement des glandes mammaires (Macon et coll., 2011; White et coll., 2011; Tucker et coll., 2015), de 0,01 mg/kg p.c. par jour en ce qui concerne les effets œstrogéniques dans l'utérus (Dixon et coll., 2012) et les changements de poids chez les adultes femelles exposées avant la naissance (Hines et coll., 2009) et de 0,6 mg/kg p.c. par jour en ce qui concerne le retard de l'ouverture des yeux (Abbott et coll., 2007). Ces effets n'ont pas constitué la base de l'évaluation des risques pour différentes raisons. On a exclu de l'évaluation les effets œstrogéniques dans l'utérus (œdème endométrial, hyperplasie de la muqueuse endométriales et des glandes, hypertrophie et hyperplasie du myomètre et augmentation du poids durant l'essai utérotrophique), car ils n'ont pas été associés à la dose - on a observé des augmentations importantes chez les souris exposées à seulement 0,01 mg/kg p.c. par jour, et non à des doses plus élevées (0,1 ou 1 mg/kg p.c. par jour; Dixon et coll., 2012). On a également observé une réponse non monotone en ce qui concerne les changements de poids corporel chez les souris femelles adultes exposées in utero, avec une augmentation de poids à 0,01 à 0,3 mg/kg p.c. par jour (et non de 1 mg/kg p.c. par jour) et des concentrations sériques de leptine et d'insuline à 0,01 et 0,1 mg/kg par jour (et non de 0,3 ou de 1 mg/kg p.c. par jour; Hines et coll., 2009). En outre, de légers changements (bien que significatifs) dans le développement des glandes mammaires et le poids corporel démontrent que ceux-ci sont liés au traitement, mais pas nécessairement au caractère nocif du composé - il n'y avait aucune preuve de consommation de lait insuffisant ou d'incapacité de se développer chez les petits des mères démontrant des changements dans le DGM, et les variations de poids étaient faibles (mesurées à <10 %). Aucune autre étude n'a corroboré l'observation du retard dans le développement des yeux à ≥0,6 mg/kg p.c. par jour chez la souris (Abbott et coll., 2007), puisque l'effet a été associé à une LOAEL de 3 mg/kg p.c. par jour (NOAEL = 1 mg/kg p.c. par jour; Lau et coll., 2006), et n'a pas été observé à 3 mg/kg p.c. par jour dans une autre étude (Albrecht et coll., 2013). Les effets sur le développement des glandes mammaires pourraient également être affectés par la sensibilité des souches--la majeure partie des effets à faible dose ont seulement été observés chez les souris exposées in utero, et d'autres souches étaient généralement seulement étudiées à des doses plus élevées et chez les souris péripubertaires. Une étude récente in utero qui comparaissait les DGM chez les souris CD-1 et C57Bl/6 à des doses de 0,01 à 1 mg/kg p.c. par jour a possiblement bien expliqué les effets à faible dose chez une seconde souche de souris, bien qu'à des doses légèrement supérieures (LOAEL -0,01 par rapport à 0,3 mg/kg p.c. par jour chez les souris CD-1 et C57Bl/6, respectivement); toutefois, une taille réduite d'échantillon à des doses minimales administrées aux souris C57Bl/6 (aussi peu que deux petits) pourrait avoir empêché d'observer des changements significatifs à des doses similaires administrées aux souris CD-1. Enfin, la sensibilité de l'espèce pourrait jouer un rôle dans l'apparition de ces effets, puisque des études portant sur une et deux générations de rats ont révélé des effets similaires uniquement à des doses beaucoup plus élevées, s'il y en avait; les NOAEL associées aux changements de poids corporel et au retard de la maturité sexuelle chez les petits étaient d'environ 3 mg/kg p.c. par jour (Staples et coll., 1984; Butenhoff et coll., 2004b) et 10 mg/kg p.c. par jour (Butenhoff et coll., 2004b), respectivement, et on n'a observé aucun effet sur l'indice de lactation jusqu'à 30 mg/kg p.c. par jour (Butenhoff et coll., 2004b). D'autres données probantes liées au potentiel de sensibilité des espèces sont fournies dans les études utilisant des souris dont les PPARa avaient été désactivés et qui étaient moins sensibles aux changements de poids corporel et à l'ouverture des yeux (Abbott et coll., 2007) et aux retards du DGM (Zhao et coll., 2012); l'activation des PPAR est plus sensible chez les souris que chez les autres espèces, dont les rats et les humains (Corton et coll., 2014). Bien que les données des études susmentionnées indiquent quelques effets sur la reproduction et le développement à des doses minimales, on ne considère pas actuellement que les données constituent une base appropriée pour l'évaluation quantitative des risques; si d'autres études démontrent toutefois une cohérence de ces effets chez d'autres espèces ou leur pertinence pour les humains, les résultats pourraient constituer une base plus appropriée pour l'évaluation de l'APFO.
Peu d'études épidémiologiques ont examiné les effets sur le développement décrits ci-haut, ce qui limite la capacité à conclure la pertinence de ces effets pour les humains. Les observations chez les humains reliés au gain de poids à l'adulte après des expositions développementales à l'APFO se limitaient à des probabilités accrues de surpoids chez les femmes et l'augmentation des biomarqueurs d'adiposité à 20 ans à la suite d'une exposition in utero (avec des concentrations sériques de 5,8 ng/mL chez la mère, comparativement à des concentrations de 2,3 ng/mL) (Halldorsson et coll., 2012). Les observations liées à l'œstrogène étaient limitées à un retard de la puberté chez les jeunes filles et de faibles liens entre la concentration d'APFO et une plus courte durée d'allaitement. Tel qu'il a été mentionné précédemment, une attention particulière doit être accordée avant de tirer des conclusions sur les effets sur la santé en s'appuyant sur ces études épidémiologiques. La nature des liens observés entre l'exposition à l'APFO et les effets sur le développement doivent faire l'objet d'une enquête plus approfondie en raison du manque de cohérence dans l'ensemble des études, de la non-spécificité des effets, de la mauvaise compréhension du mécanisme d'action, du seuil limite de signification, du manque de solidité et de l'absence d'une relation dose-réponse de nombreux résultats, ainsi que de la présence de diverses limites inhérentes au modèle d'étude, telles que la possibilité de confusion résiduelle, les biais causés par des erreurs de mesure de résultats et le hasard.
Bien que l'on ait observé des effets hépatiques à des doses légèrement supérieures que celles utilisées dans l'étude des effets sur la reproduction, on a quand même relevé des changements à des doses d'APFO de ≤0,3 mg/kg p.c. par jour. On a observé une augmentation du poids relatif du foie à ≥0,1 mg/kg par jour chez les souriceaux exposés avant la naissance (Abbott et coll., 2007; Macon et coll., 2011) et à ≥0,15 mg/kg p.c. par jour chez les souris adultes (Kennedy, 1987; Loveless et coll., 2006, 2008). On a observé des augmentations liées à la dose de l'incidence et de la gravité de l'hypertrophie hépatocellulaire à ≥0,3 mg/kg p.c. par jour chez les rats (Perkins et coll., 2004; Loveless et coll., 2008) et les souris (Loveless et coll., 2008) exposés de façon subchronique à l'APFO. Bien qu'on ait relevé des augmentations de l'hypertrophie hépatocellulaire et du poids du foie à des doses légèrement inférieures dans d'autres études, nous avons choisi l'étude de Perkins et coll. (2004) comme étant la principale étude qui était représentative de la base des données des effets. L'étude de Perkins indique une hypertrophie hépatocellulaire chez les rats mâles à une dose de ≥0,64 mg/kg p.c. par jour, ce qui représente un ordre de grandeur similaire à celui des études utilisant des LOAEL allant de 0,1 à 0,3 mg/kg p.c. par jour. L'un des principaux avantages que présente l'étude de Perkins est l'établissement d'une NOAEL (0,06 mg/kg p.c. par jour), car les LOAEL qui ont été indiquées dans la majorité des autres études à faibles doses correspondaient aux doses minimales administrées. Il est possible d'obtenir une NOAEL similaire de 0,05 mg/kg p.c. par jour dans l'étude de Kennedy et coll. (1987) lorsque les hypothèses de Santé Canada (1994) relatives à la consommation alimentaire et aux poids corporels chez les rats (Santé Canada, 1994) sont utilisées, mais les auteurs n'ont pas fourni de valeurs réelles de doses mesurées. Un autre avantage de l'étude de Perkins par rapport aux autres études à faibles doses est sa durée plus longue et ses durées d'exposition allant jusqu'à 13 semaines; en plus de groupes témoins nourris à volonté, l'étude a fourni des groupes témoins nourris en parallèle afin d'assurer que les effets ne soient pas attribuables aux quantités de nourriture consommées. Enfin, l'étude de Perkins a mesuré l'activité des PPARa, laquelle a seulement été augmentée à ≥1,94 mg/kg p.c. par jour; parce cela laisse entendre que l'hypertrophie hépatocellulaire n'était pas causée par la prolifération de peroxysomes, on ne peut exclure la pertinence de cet effet pour l'humain. Une NOAEL de 0,06 mg/kg p.c. par jour repose également sur la NOAEL la plus prudente des effets biochimiques hépatiques, laquelle a été estimée à 0,055 mg/kg p.c. par jour chez les rats mâles démontrant des taux accrus de phosphatase alcaline en plus d'une augmentation du poids du foie (Kennedy et coll., 1986) en ayant recours aux hypothèses par défaut liées au poids corporel et aux taux d'inhalation (Santé Canada, 1994) et à une échelle linéaire de l'exposition périodique à l'exposition continue. La NOAEL est également environ 10 fois plus faible que la NOAEL et 30 fois plus faible que la LOAEL qui ont été établies dans l'étude de la nécrose hépatique (0,56 et 1,72 mg/kg p.c. par jour, respectivement) observée chez des rats exposés pendant 90 jours (Goldenthal et coll., 1978a).
Bien que l'augmentation du poids du foie et l'hypertrophie hépatocellulaire peuvent parfois être considérées comme étant des effets adaptatifs plutôt que nocifs en soi, des preuves d'autres effets histologiques dans le foie à des concentrations plus élevées indiquent leur progression sous une exposition continue (ECETOC, 2002; Hall et coll., 2012). On a observé un effet histologique nocif (infiltration portale de cellules mononucléaires) dans le foie de rats mâles exposés à la même dose que celle administrée lors de l'observation d'augmentations importantes d'hypertrophies hépatocellulaires (14,2 mg/kg p.c. par jour d'APFO pendant deux ans; Butenhoff et coll., 2012b). Bien que cette dose soit beaucoup plus élevée que les points de départ les plus faibles liés à l'augmentation du poids du foie et à l'hypertrophie hépatocellulaire qui ont été observées dans les études subchroniques, nous proposons ces derniers comme étant des effets critiques dans le cadre de la présente évaluation, puisqu'il pourrait s'agir d'indicateurs sensibles de potentialité de progression des effets histologiques nocifs. D'autres effets histologiques observés chez les rats dans des études de plus courte durée comprenaient la nécrose à ≥1,72 mg/kg p.c. par jour (Goldenthal et coll., 1978a; Loveless et coll., 2008), la vacuolation cytoplasmique à ≥5 mg/kg p.c. par jour (Cui et coll., 2009) et les modifications de tissus adipeux, l'angiectasie, la congestion et les lésions acidophiles à 20 mg/kg p.c. par jour (Cui et coll., 2009). Par conséquent, l'augmentation du poids du foie et l'hypertrophie hépatocellulaire sont examinées dans l'évaluation de la relation dose-réponse - malgré la possibilité qu'il s'agisse d'effets adaptatifs plutôt que d'effets nocifs - comme moyen de prévenir les effets histologiques les plus graves observés dans d'autres études ou à des doses plus élevées. L'utilisation de paramètres prudents pour les effets hépatiques est également appuyée d'une certaine façon par des études épidémiologiques dans lesquelles on a observé quelques liens entre l'exposition à l'APFO et les augmentations d'enzymes hépatiques (dont l'AST, l'ALT et la GGT); les liens entre les concentrations sériques d'APFO et les effets hépatiques ne peuvent toutefois pas être utilisés pour tirer des conclusions définitives chez les humains en raison de limites, notamment le manque de cohérence et de spécificité des résultats, la faiblesse des effets et les plans d'étude présentant de nombreuses limites (p. ex., une étude qui ne permet pas de vérifier la temporalité). Les concentrations sériques auxquelles ces effets ont été observés chez les humains étaient de l'ordre de 1 000 ng/mL dans les études sur l'exposition professionnelle et de <10 ng/mL dans les études environnementales, ce qui était inférieur aux concentrations sériques associées à la NOAEL et le LOAEL de l'étude étendue sur 13 semaines de Perkins (7 100 et 41 000 ng/mL, respectivement).
On a également observé des changements dans les taux sériques de lipides près des doses auxquelles les effets hépatiques se manifestent. La dose la plus faible à laquelle on a observé des changements dans les taux sériques de lipides était de 0,3 mg/kg p.c. par jour chez les rats exposés pendant 14 jours (diminution du taux de cholestérol total; Loveless et coll., 2006) ou 29 jours (diminution du cholestérol total et du cholestérol HDL; Loveless et coll., 2008). Les changements typiques observés consistaient en des diminutions des taux de cholestérol total, de cholestérol HDL et de triglycérides. Il importe de tenir compte de ces effets dans l'évaluation des risques liés à l'APFO, car les études épidémiologiques ont généralement démontré des liens positifs entre l'APFO et les taux sériques de cholestérol. On a en outre observé des incohérences dans les effets non seulement entre les deux bases de données, mais également dans les bases de données sur la toxicologie (voir la section 9.2.2.2) et l'épidémiologie (voir la section 9.2.2.2). Des relations claires entre la dose et la réponse avaient tendance à être absentes des études sur les animaux. En raison de cette faiblesse, on n'a pas réalisé d'évaluations quantitatives des effets sur les lipides sériques; toutefois, selon la base de données actuelle, un AQT fondé sur les effets hépatiques devrait assurer une protection suffisante contre les changements lipidiques.
Afin de refléter les grandes différences interespèces en matière de pharmacocinétique, on a calculé un point de départ équivalent chez l'humain (PDDEQH) pour l'hypertrophie hépatocellulaire comme suit :
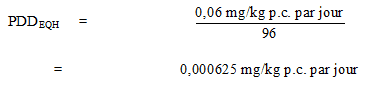
Figure 6 - Equivalent Textuel
Le PDDEQH est de 0,000625 mg/kg p.c. par jour. Cette valeur est calculée en divisant de 0,06 mg/kg p.c. par jour, la NOAEL pour l'hypertrophie hépatocellulaire, par 96, la valeur de CAFI
propre à la dose des rats d'environ 0,01 mg/kg p.c. par jour.Application :
- 0,06 mg/kg p.c. par jour représente la NOAEL pour l'hypertrophie hépatocellulaire de l'étude Perkins et coll. (2004), qui a été choisie pour représenter la base de données sur l'hypertrophie hépatocellulaire et les augmentations du poids du foie;
- 96 représente la valeur de CAFI liée à la dose pour les rats exposés à 0,01 mg/kg p.c. par jour (tel que le décrit la section 8.6.2).
On a calculé l'AQT non cancérogène comme suit à l'aide du PDDEQH calculé :
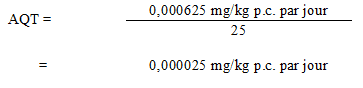
Figure 7 - Equivalent Textuel
L'AQT non cancérogène est de 0,000025 mg/kg p.c. par jour. Cette valeur est calculée en divisant le PDDEQH de 0,000625 mg/kg p.c. par jour, par 25, le facteur d'incertitude composite.
Application :
- 0,000625 mg/kg p.c. par jour représente le PDDEQH pour examiner l'hypertrophie hépatocellulaire, tel qu'il a été décrit ci-haut;
- 25 représente le facteur d'incertitude composite, tel qu'il est décrit ci-dessous.
Le facteur d'incertitude composé de 25 est le produit de deux éléments : le facteur d'incertitude interespèces (×2,5) et le facteur d'incertitude intraespèce (×10). La valeur de 2,5 est utilisée afin de refléter l'élément toxicodynamique du facteur d'incertitude interespèces par défaut, car les différences toxicocinétiques entre les rats et les humains ont déjà été intégrées lors du calcul du PDDEQH. Nous avons appliqué une valeur par défaut de 10 pour le facteur d'incertitude intraespèce. Nous avons présumé que la valeur par défaut était suffisante en l'absence de données sur les différences intraespèces. Bien que nous soyons conscients qu'il existe de grandes différences en matière de pharmacocinétique entre les espèces, l'insuffisance des données sur le mécanisme d'excrétion de l'APFO nous empêche de mener des enquêtes afin de déterminer si la variabilité pharmacocinétique serait également importante dans une population humaine. Les valeurs moyennes de demi-vie qui ont été calculées à partir des données longitudinales pour les différentes populations exposées précédemment à l'APFO étaient similaires (les moyennes de chaque population variaient entre 2,3 et 3,8 années; Olsen et coll., 2007; Bartell et coll., 2010; Brede et coll., 2010); toutefois, les études ayant fourni un écart de valeurs ont indiqué qu'il y avait environ dix fois plus de différences entre les estimations minimales et maximales des demi-vies. Si d'autres études sur l'APFO indiquent de façon constante une différence multipliée par dix dans la pharmacocinétique d'une population, un facteur d'incertitude intraespèce plus élevé pourrait être justifié afin d'assurer que les différences relatives à la pharmacodynamique entre les humains sont aussi abordées de façon quantitative. Nous n'avons utilisé aucun facteur d'incertitude pour l'extrapolation de l'exposition subchronique à chronique, puisque les effets hépatiques ont fait l'objet d'un examen dans une étude sur l'exposition chronique (Butenhoff et coll., 2012b) et que l'augmentation de la durée d'exposition n'a pas semblé aggraver les effets dans la principale étude sur le sujet (Perkins et coll., 2004).
La VBS dans l'eau potable peut être calculée comme suit à l'aide de l'AQT :
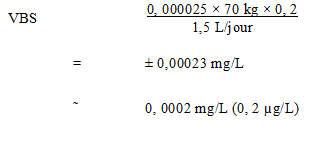
Figure 8 - Equivalent Textuel
La VBS pour l'APFO dans l'eau potable est de 0,0002 mg/L. Cette valeur est calculée en multipliant l'AQT non cancérogène pour l'APFO de 0,000025 mg/kg p.c. par jour, par 70 kg, le poids corporel moyen d'un adulte, puis par 0,2, le facteur d'attribution par défaut pour l'eau potable, et en divisant le résultat par 1.5 L/jour, le volume quotidien d'eau consommé par un adulte.
Application :
- 0,000025 mg/kg p.c. par jour est l'AQT calculé ci-dessus;
- 70 kg est le poids corporel moyen d'un adulte;
- 0,2 est le facteur d'attribution par défaut pour l'eau potable qui a été utilisé comme valeur seuil, étant donné que l'eau potable n'est pas une source importante d'exposition et qu'il existe des preuves de la présence répandue du composé dans au moins un autre milieu (air, aliments, sol ou produits de consommation) (Krishnan et Carrier, 2013);
- 1,5 L/jour représente le volume quotidien d'eau consommé par un adulte; des expositions par inhalation ou voie cutanée de l'eau utilisée pour le bain ou la douche ne sont pas considérées comme étant des voies d'exposition significatives (comme le décrit la section 5.7).
10.3 Comparaison des évaluations de risque de cancer et d'effets autres que le cancer
La VBS pour l'évaluation des effets non cancérogènes, qui était de 0,0002 mg/L pour l'hypertrophie hépatocellulaire chez les rats, est plus prudente que la VBS de 0,03 mg/L pour les tumeurs des cellules de Leydig. Nous considérons par conséquent que la VBS de 0,0002 mg/L qui a été calculée pour les effets non cancérogènes assure une protection suffisante contre les effets cancérogènes de l'APFO.
10.4 Considérations internationales
Un mémoire publié en 2009 par le U.S. EPA Office of Water indique un avis provisoire sur la santé de 0,4 μg/L (0,0004 mg/L) pour l'APFO (U.S. EPA, 2009 b). On a calculé cet avis à partir de la BMDL10 de 0,46 mg/kg p.c. associée à l'étude de l'augmentation du poids du foie de la mère à terme chez les souris exposées par gavage à l'APFO du 1er au 17e JG (Lau et coll., 2006). Cette BMDL10 se situe dans la plage des valeurs de BMDL10 associées à l'augmentation du poids chez les souris et les rats (0,29 à 0,74 mg/kg p.c. par jour) (EFSA, 2008, U.S. EPA, 2009 b). Un facteur d'incertitude de 2430 (10 pour les différences intraespèces, 3 pour les différences toxicodynamiques interespèces et 81 pour les différences toxicocinétiques interspéciques) a été appliquée à la BMDL10 à la suite de l'administration d'une dose de référence arrondie à 200 ng/kg p.c. par jour (0,2 μg/kg p.c. par jour) (U.S. EPA, 2009 b). Cette dose de référence a également été indiquée dans un mémoire publié en 2009 par le U.S. EPA Office of Solid Waste and Emergency Response (U.S. EPA, 2009c). Selon la politique de l'U.S. EPA, un APS (0,4 μg/L; 0,0004 mg/L) a également été calculé pour un enfant de 10 kg consommant 1 L d'eau par jour en utilisant l'hypothèse par défaut que l'eau potable constitue 20 % de l'exposition totale à l'APFO (U.S. EPA, 2009c).
Le New Jersey Department of Environmental Protection a établi une valeur guide préliminaire relative à la santé pour l'APFO dans l'eau potable de 0,04 μg/L (0,00004 mg/L) à partir de la NOAEL de 1,6 mg/kg p.c. par jour obtenue chez les rats exposés de façon chronique (Sibinski, 1987). À la dose maximale (16,1 mg/kg p.c. par jour), on a observé des diminutions du gain de poids corporel, des hématocrites, du nombre d'érythrocytes et des concentrations d'hémoglobines chez les rates. À l'aide de la modélisation pharmacocinétique, on a déterminé qu'une dose de 1,6 mg/kg par jour était équivalente à une concentration sérique moyenne d'APFO de 1 800 ng/mL chez les rats. On a appliqué un facteur d'incertitude de 100 pour la variation interespèce et intraespèce, ce qui a donné lieu à une concentration sérique maximale humaine cible d'APFO de 18 ng/mL. À l'aide de données d'une étude épidémiologique (Emmett et coll., 2006a), qui a relevé que l'ingestion d'APFO dans l'eau potable donnait lieu à une concentration sanguine d'APFO d'environ 100 fois supérieures à la concentration d'eau, on a estimé qu'une concentration d'eau de 0,18 ng/mL (0,18 μg/L ou 0,00018 mg/L) mènerait à une concentration sérique cible d'APFO. En se basant sur l'hypothèse par défaut selon laquelle l'eau potable contribue à 20 % de l'exposition totale d'APFO, la valeur-guide préliminaire relative à la santé a été établie à 0,04 μg/L (État du New Jersey, sans date).
Le Minnesota Department of Health a calculé une limite de risque sanitaire (LRS) de 0,3 μg/L (0,0003 mg/L). Cette valeur était fondée sur l'augmentation du poids du foie observée chez les singes exposés à ≥ 3 mg/kg p.c. par jour (Thomford, 2001a; Butenhoff et coll., 2002). Plus précisément, on a estimé la dose de référence (BMDL10) pour ces effets à une valeur de 23 000 ng/mL d'APFO dans le sérum des singes. On a calculé une dose équivalente pour les humains (DEH) de 2 300 ng/kg p.c. par jour en fonction de l'élimination de l'APFO chez les humains (à l'aide de données sur la demi-vie humaine afin d'estimer la clairance). On a appliqué un facteur d'incertitude de 30 (10 pour la variabilité humaine et 3 pour les différences toxicodynamiques interespèces) à la DEH, ce qui a donné lieu à une dose de référence de 77 ng/kg p.c. par jour (0,077 μg/kg p.c. par jour). Estimant que l'état d'équilibre dose/élimination survenait après 19 ans d'exposition, on a utilisé une dose au 95e percentile pondérée dans le temps pendant les 19 premières années de vie (0,053 L/kg p.c. par jour) en tant qu'ingestion quotidienne d'eau. Ceci, ainsi qu'une source relative de contribution de 20 %, a donné une LRS arrondie à 0,3 μg/L (MDH, 2008c, 2008d).
La UK Health Protection Agency (UK HPA, 2007, 2009) a calculé une recommandation relative à l'eau potable de 10 µg/L (0,01 mg/L) en fonction de l'AQT de 3 000 ng/kg p.c par jour (3 μg/kg p.c par jour) qui avait auparavant été calculé par le UK Committee on Toxicity of Chemicals in Food, Consumer Products and the Environment (UK COT, 2006). Cet AQT était fondée sur un PDD de 0,3 mg/kg p.c par jour, ce qui correspondait à la BMDL10 des augmentations de poids du foie de rats exposés pendant 13 semaines (données tirées de l'étude de Palazzolo, 1993 et Perkins et coll., 2004); cette valeur était similaire à la BMDL10 (,31 mg/kg p.c par jour) calculée pour la nécrose hépatique chez les rats mâles F0 et F1 (données tirées de l'étude de Butenhoff et coll., 2004 b). On a appliqué un facteur d'incertitude de 100 (variation intraespèce et interespèce). On a calculé la recommandation relative à l'eau potable (10 µg/L) à partir de l'AQT à l'aide d'un facteur d'attribution de 50 %, d'un poids corporel de 5 kg et d'un taux d'ingestion d'eau de 0,75 L par jour pour les bébés nourris à la bouteille (UK HPA, 2007).
Dans un document dans lequel on exprime une opinion scientifique sur les contaminants dans la chaîne alimentaire, le groupe CONTAM de la European Food Safety Authority (EFSA) a calculé un AQT de 1500 ng/kg p.c. par jour (1,5 μg/kg p.c. par jour) selon une BDML10 de 0,3 mg/kg p.c. par jour chez les rats (EFSA, 2008). Cette valeur renvoie à la BMDL10 minimale déterminée pour les effets sur le foie (Palazzolo, 1993; Butenhoff et coll., 2004 b; Perkins et coll., 2004) parmi ces doses (0,3 à 0,7 mg/kg p.c. par jour) calculées à partir d'un certain nombre d'études chez les souris (Lau et coll., 2006) et les rats mâles (Sibinski, 1987; Palazzolo, 1993; Butenhoff et coll., 2004 b; Perkins et coll., 2004). La BMDL10 est divisée par un facteur d'incertitude de 200 (10 pour les différences interespèces, 10 pour les différences intraespèces et 2 afin de compenser les incertitudes liées à la cinétique des doses internes).
11.0 Justification
L'APFO constitue un composé anthropogène utilisé dans la fabrication de revêtements résistant aux taches ou à l'eau pour divers produits de consommation. Les concentrations environnementales, et par conséquent les niveaux d'exposition potentiels, pourraient être plus importants près des installations qui utilisent des quantités élevées d'APFO et près de lieux où des incendies ont été éteints avec des mousses anti-incendie contenant de l'APFO. Les Canadiens peuvent être exposés à l'APFO dans les aliments, les produits de consommation, la poussière et l'eau potable. Bien que les principales sources d'APFO soient généralement les aliments et les produits de consommation, la proportion d'exposition par l'eau potable peut augmenter chez les personnes vivant dans des régions dont l'eau potable est contaminée. Selon ses propriétés physico-chimiques, l'exposition à l'APFO par les voies d'exposition cutanée ou d'inhalation pendant la douche ou le bain devrait être négligeable.
L'exposition chronique à l'APFO a été associée à des effets cancérogènes et non cancérogènes chez les animaux et les humains. On a calculé les VBS des deux effets, et une VBS plus prudente peut être calculée à partir des effets non cancérogènes.
Des études épidémiologiques ont démontré des associations entre l'exposition à l'APFO et plusieurs effets sur la santé non cancérogènes, comme les perturbations du système immunologique et les altérations du poids à la naissance et des taux de lipides. Ces études ne peuvent toutefois pas être utilisées pour calculer la VBS des effets non cancérogènes de l'APFO en raison des limites en ce qui a trait à la conception des études, leurs biais, les facteurs de confusion et les possibilités de résultats liés au hasard. Chez les animaux, les effets non cancérogènes observés aux plus faibles niveaux d'exposition comprennent des effets sur la reproduction et le développement, des effets hépatiques et des changements dans les taux sériques des lipides. Pour diverses raisons décrites à la section 10.2, le critère le plus approprié pour calculer une VBS pour l'APFO est l'hypertrophie hépatocellulaire (effets hépatiques) chez les rats, qui se manifestent aux mêmes concentrations que celles des changements dans les taux sériques des lipides. Une VBS de 0,0002 mg/L (0,2 µg/L) est calculée en utilisant l'approche AQT pour les effets non cancérogènes de l'APFO en fonction des effets hépatiques chez les rats. On considère que cette VBS assure une protection suffisante contre les effets cancérogènes ou non cancérogènes de l'APFO.
Une CMA de 0,0002 mg/L (0,2 µg/L) est proposée pour l'APFO dans l'eau potable. La CMA proposée pour l'APFO peut être mesurée par les méthodes d'analyse existantes et peut être atteintes par les techniques de traitement de l'eau potable aux échelles municipale et résidentielle. Dans le cadre de son processus continu de révision des recommandations, Santé Canada continuera, à suivre les nouvelles recherches à ce sujet, et recommandera au besoin toute modification jugée appropriée.
12.0 Références
3M Company (1983). Two year oral (diet) toxicity/carcinogenicity study of fluorochemical FC-143 in rats. Washington, DC: U.S. Environmental Protection Agency. Submitted to the U.S. Environmental Protection Agency under TSCA Section 8E. OTS0204926-1. [cité dans ATSDR (2009)].
3M Company (1999). The science of organic fluorochemistry. Letter of Frank D. Kover, Chief, Chemical Information and Testing Branch, Chemical Control Division, Office of Pollution Prevention and Toxics, U.S. EPA. Disponible à : www.fluoridealert.org/wp-content/pesticides/pfos.fr.final.docket.0006.pdf
3M Company (2008). Interim report #17-Analysis of Woodbury waste site water samples. Maplewood, Minnesota
Abbott, B.D., Wolf, C.J., Schmid, J.E., Das, K.P., Zehr, R.D., Helfant, L. et coll. (2007). Perfluorooctanoic acid induced developmental toxicity in the mouse is dependent on expression of peroxisome proliferator activated receptor-alpha. Toxicol. Sci., 98(2): 571-581.
Abdellatif, A.G., Préat, V., Vamecq, J., Nilsson, R. et Roberfroid, M. (1990). Peroxisome proliferation and modulation of rat liver carcinogenesis by 2,4-dichlorophenoxyacetic acid, 2,4,5-trichlorophenoxyacetic acid, perfluorooctanoic acid and nafenopin. Carcinogenesis, 11(11): 1899-1902.
Abe, T., Baba, H., Itoh, E. et Tanaka, K. (2001). Separation of perfluoroalkylsulfinic acids and perfluoroalkylsulfonic acids by ion-exclusion chromatioography. J. Chromatogr. A, 920:173-180.
Ahrens, L. (2011). Polyfluoroalkyl compounds in the aquatic environment: a review of their occurrence and fate. J. Environ. Monit., 13(1): 20-31.
Alberta Environment and Water (2013). Personal communication from Dr. Donald Reid.
Albrecht, P.P., Torsell, N.E., Krishnan, P., Ehresman, D.J., Frame, S.R., Chang, S.C., Butenhoff, J.L., Kennedy, G.L., Gonzalez, F.J. et Peters, J.M. (2013). A species difference in the peroxisome proliferator-activated receptor alpha-dependent response to the developmental effects of perfluorooctanoic acid. Toxicol. Sci., 131(2): 568-582.
Andersen, C.S., Fei, C., Gamborg, M., Nohr, E.A., Sørensen, T.I. et Olsen, J. (2010). Prenatal exposures to perfluorinated chemicals and anthropometric measures in infancy. Am. J. Epidemiol., 172(11): 1230-1237. Erratum in: Am. J. Epidemiol., 173(12):1475.
Andersen, M.E., Clewell, H.J., 3 rd, Tan, Y.M., Butenhoff, J.L. et Olsen, G.W. (2006). Pharmacokinetic modeling of saturable, renal resorption of perfluoroalkylacids in monkeys--probing the determinants of long plasma half-lives. Toxicology, 227(1-2): 156-164.
Apelberg, B.J., Witter, F.R., Herbstman, J.B., Calafat, A.M., Halden, R.U., Needham, L.L. et coll. (2007). Cord serum concentrations of perfluorooctane sulfonate (PFOS) and perfluorooctanoate (PFOA) in relation to weight and size at birth. Environ. Health Perspect, 115(11): 1670-1676.
Appleman, T.D., Dickenson, E.R.V., Bellona, C. et Higgins, C.P. (2013). Nanofiltration and granular activated carbon treatment of perfluoroalkyl acids. J. Hazard. Mater., 260(15): 740-746.
Appleman, T.D., Higgins, C.P., Quiñones, O., Vanderford, B.J., Kolstad, C., Zeigler-Holady, J.C. et Dickenson, E.R.V. (2014). Treatment of poly- and perfluoroalkyl substances in U.S. full-scale water treatment systems. Water Res. 51:246-255.
Arbuckle, T., Kubwabo, C., Walker, M., Davis, K., Lalonde, K. Kosarac, I., Wen, S. et Arnold, D. (2013). Umbilical cord blood levels of perfluoroalkyl acids and polybrominated flame retardants. Int. J. Hyg. Envir. Health, 216:184-194.
Arp, H.P.H., Niederer, C. et Goss, K.-U. (2006). Predicting the partitioning behaviour of highly fluorinated compounds. Environ. Sci. Technol., 40(23): 7298-7304.
Arsenault, G., Chittim, B., McAlees, A., McCrindle, R., Riddell, N. et Yeo, B. (2008). Some issue relating to the use of perfluorooctane sulfonate (PFOS) samples as reference standard. Chemosphere, 70:620-625.
Asakawa, A., Toyoshima, M., Harada, K.H., Fujimiya, M., Inoue, K. et Koizumi, A. (2008). The ubiquitous environmental pollutant perfluorooctanoicacid inhibits feeding behavior via peroxisome proliferator-activated receptor-alpha. Int J Mol Med, 21(4): 439-445.
Atkinson, C., Blake, S., Hall, T., Kanda, R. et Rumsby, P. (2008). Survey of the prevalence of perfluorooctane sulphonate (PFOS), perfluorooctanoic acid (PFOA) and related compounds in drinking water and their sources. WRc Ref: DEFRA 7585, February. Disponible à : http://dwi.defra.gov.uk/research/completed-research/reports/DWI70_2_212PFOS.pdf.
ATSDR (2009). Toxicological profile for perfluoroalkyls, draft for public comment. Agency for Toxic Substances and Disease Registry Disponible à : www.atsdr.cdc.gov/toxprofiles/tp.asp?id=1117&tid=237
Awad, E., Zhang, X., Bhavsar, S.P., Petro, S., Crozier, P.W., Reiner, E.J., Fletcher, R., Tittlemier, S.A. et Braekevelt, E. (2011). Long-term environmental fate of perfluorinated compounds after accidental release at Toronto airport. Environ. Sci. Technol., 45(19): 8081-8089.
AWWA. (2011). Water quality and treatment, a handbook of community water supplies. Sixth Edition. James K. Edzwald, Editor. American Water Works Association and McGraw-Hill. Denver, Colorado.
Backe, W, Thomas, J, Day, C et Field, J.A. (2013). Zwitterionic, cationic, and anionic fluorinated chemicals in aqueous film forming foam formulations and groundwater from U.S. military bases by non-aqueous large-volume injection HPLCMS/ MS. Environ. Sci. Technol., 47 (10): 5226-5234.
Baduel, C., Paxman, C.J. et Mueller J.F. (2015). Perfluoroalkyl substances in a firefighting training ground (FTG), distribution and potential future release. J. Hazard. Mater., 296: 46-53.
Barry, V., Winquist, A. et Steenland, K. (2013). Perfluorooctanoic acid (PFOA) exposures and incident cancers among adults living near a chemical plant. Environ. Health Perspect., 121(11-12): 1313-1318.
Bartell, S.M., Calafat, A.M., Lyu, C., Kato, K., Ryan, P.B. et Steenland, K. (2010). Rate of decline in serum PFOA concentrations after granular activated carbon filtration at two public water systems in Ohio and West Virginia. Environ. Health Perspect., 118(2): 222-228.
Barton, C.A., Kaiser, M.A. et Russell, M.H. (2007). Partitioning and removal of perfluorooctanoate during rain events: the importance of physical-chemical properties. J Environ Monit, 9: 539-46. [cité dans ATSDR (2009), Environnement Canada et Santé Canada (2012).]
Beesoon, S., Webster, G.M., Shoeib, M., Harner, T., Benskin, J.P. et Martin, J.W. (2011). Isomer profiles of perfluorochemicals in matched maternal, cord, and house dust samples: manufacturing sources and transplacental transfer. Environ. Health Perspect., 119(11): 1659-1664.
Begley, T.H., White, K., Honigfort, P., Twaroski, M.L., Neches, R. et Walker, R.A. (2005). Perfluorochemicals: potential sources of and migration from food packaging. Food Addit Contam, 22(10): 1023-1031. [cité dans ATSDR (2009), Fromme (2009).]
Benbrahim-Tallaa, L., Lauby-Secretan, B., Loomis, D., Guyton, K.Z., Grosse, Y., El Ghissassi, F., Bouvard, V., Guha, N., Mattock, H., Straif, K. et International Agency for Research on Cancer Monograph Working Group. (2014). Carcinogenicity of perfluorooctanoic acid, tetrafluoroethylene, dichloromethane, 1,2-dichloropropane, and 1,3-propane sultone. Lancet Oncol., 15(9): 924-925.
Benskin, J.P., De Silva, A.O. et Martin, J.W. (2010), Isomer profiling of perfluorinated substances as a tool for source tracking: a review of early findings and future application. Reviews of Environmental Contamination and Toxicology. P. de Voogt (ed.). Springer Science+Business Media, LLC.
Berger, U., Kaiser, M., Karrman, A., Barber, J. et van Leeuwen, S. (2011). Recent developments in trace analysis of poly-and perfluoroalkyl substances. Anal. Bional. Chem., 4000:1625-1635.
Berger, U., Langlois, I., Oehme, M. et Kallenborn, R. (2004). Comparison of three types of mass spectrometer for high-performance liquid chromatography/mass spectrometry analysis of perfluoroalkylated substances and fluorotelomer alcohol. Eur. J. Mass Spectrom. 10:579-588.
Berryman, D., Salhi, C., Bolduc, A., Deblois, C. et Tremblay, H. (2012). Les composés perfluorés dans les cours d'eau et l'eau potable du Québec méridional. Québec, Ministère du Développement durable, de l'Environnement, de la Faune et des Parcs, Direction du suivi de l'état de l'environnement.
Biegel, L.B., Hurtt, M.E., Frame, S.R., O'Conner, J.C. et Cook, J.C. (2001). Mechanisms of extrahepatic tumor induction by peroxisome proliferators in male CD rats. Toxicol. Sci., 60(1): 44-45.
Bonefeld-Jorgensen, E., Long, M., Bossi, R., Ayotte, P., Asmund, G., Kruger, T., et coll. (2011). Perfluorinated compounds are related to breast cancer risk in greenlandic inuit: A case control study. Environ. Health, 10(1): 88. Disponible à : www.ehjournal.net/content/10/1/88.
Boyd, G., Tucillo, M.E., Sandvig, A., Pelaez, M., Han, C. et Dionysious, D.D. (2013). Nanomaterials: Removal processes and beneficial applications in treatment. J. Am. Water Works Assoc.,105(12): 699-708.
Brede, E., Wilhelm, M., Göen, T., Müller, J., Rauchfuss, K., Kraft, M. et Hölzer, J.. (2010). Two-year follow-up biomonitoring pilot study of residents' and controls' PFC plasma levels after PFOA reduction in public water system in Arnsberg, Germany. Int. J. Hyg. Environ. Health, 213(3): 217-223.
Buck, R. C., Franklin, J., Berger, U., Conder, J. M., Cousins, I. T., de Voogt, P., Jensen, A. A.,Kannan, K., Mabury, S. A. et van Leeuwen, S. P. J. (2011). Perfluoroalkyl and polyfluoroalkylsubstances in the environment: terminology, classification, and origins. Integr. Environ. Assess. Manag., 7(4), 513-541.
Burns, D.C., Ellis, D.A., Li, H., McMurdo, C.J. et Webster, E. (2008). Experimental pKa determination for perfluorooctanoic acid (PFOA) and the potential impact of pKa concentration dependence on laboratory-measured partitioning phenomena and environmental modeling. Environ. Sci. Technol., 42(24): 9283-9288.
Butenhoff, J., Costa, G., Elcombe, C., Farrar, D., Hansen, K., Iwai, H. et coll. (2002). Toxicity of ammonium perfluorooctanoate in male cynomolgus monkeys after oral dosing for 6 months. Toxicol. Sci., 69(1): 244-257.
Butenhoff, J.L., Kennedy, G.L. et Hinderliter, P.M. (2004a). Pharmacokinetics of perfluorooctanoate in Cynomolgus monkeys. Toxicol. Sci., 82: 394-406.
Butenhoff, J.L., Kennedy, G.L., Frame, S.R., O'Conner, J.C. et York, R.G. (2004b). The reproductive toxicology of ammonium perfluorooctanoate (APFO) in the rat. Toxicology, 196(1-2): 95-116.
Butenhoff, J.L., Pieterman, E., Ehresman, D.J., Gorman, G.S., Olsen, G.W., Chang, S.C. et coll. (2012a). Distribution of perfluorooctanesulfonate and perfluorooctanoate into human plasma lipoprotein fractions. Toxicol. Lett.., 210(3): 360-365.
Butenhoff, J.L., Kennedy, G.L., Jr., Chang, S.C. et Olsen, G.W. (2012 b). Chronic dietary toxicity and carcinogenicity study with ammonium perfluorooctanoate in Sprague-Dawley rats. Toxicology, 298(1-3): 1-13.
Butt, C.M., Berger, U., Bossi, R. et Tomy, G.T. (2010). Levels and trends of poly- and perfluorinated compounds in the arctic environment. Sci. Total Environ., 408(15): 2936-2965.
C8 Science Panel (2011). C8 probable link reports (probable link evaluations for birth defects, pregnancy-induced hypertension and preeclampsia, miscarriage and stillbirths, preterm birth and low birth weight). Disponible à : www.c8sciencepanel.org/prob_link.html.
C8 Science Panel. (2012a). C8 probable link reports (probable link evaluations for heart disease, kidney disease, liver disease, osteoarthritis and parkinson's disease). Disponible à : www.c8sciencepanel.org/prob_link.html.
C8 Science Panel (2012b). C8 probable link reports (probable link evaluations for cancer and diabetes). Disponible à : www.c8sciencepanel.org/prob_link.html.
C8 Science Panel (2012c). C8 probable link reports (probable link evaluations for autoimmune disease, infectious disease, neurodevelopmental disorders in children, respiratory disease, stroke, and thyroid disease). Disponible à : www.c8sciencepanel.org/prob_link.html.
Campbell, J.L., Jr. et Clewell, H.J. III. (2013). Report on the perfluorooctanoic acid (PFOA) kinetic models and dosimetry. Final contract report to Health Canada.
Cao, M.H., Wang, B.B., Yu, H.S., Wang, L.L., Yuan, S.H., et Chen, J. (2010). Photochemical decomposition of perfluorooctanoic acid in aqueous periodate with VUV and UV light irradiation. J. Hazard. Mater., 179:1143-1146..
Carter, K.E. et Farrell, J. (2010). Removal of perfluorooctane and perfluorobutane sulfonate from water via carbon adsorption and ion exchange. Sep. Sci. Technol., 45:762-767.
CCN (2015).Accredited certification bodies. Standards Council of Canada. Disponible à : www.scc.ca/en/programs/product_cert/accredited_clients.shtml
Chan, E., Burstyn, I., Cherry, N., Bamforth, F. et Martin, J.W. (2011). Perfluorinated acids and hypothyroxinemia in pregnant women. Environ. Res., 111: 559-564.
Chen, J. et Zhang, P. (2006). Photodegradation of perfluorooctanoic acid in water under irradiation of 254 nm and 185 nm light by use of persulfate. Water Sci. Technol., 54(11-12):317-325.
Chen, J., Zhang, P-Y. et Liu, J. (2007). Photodegradation of perfluorooctanoic acid by 185 nm vacuum ultraviolet light. J. Environ. Sci., 19:387-390.
Christopher, B. et Marias, A.J. (1977). 28-Day oral toxicity study with FC-143 in albino mice, Final Report, Industrial Bio-Test Laboratories, Inc. Study No. 8532-10655, 3M Reference No. T-1742CoC, Lot 269. [cité dans OECD (2008).]
Chularueangaksorn, P., Tanaka, S., Fujii, S. et Kunacheva, C. (2013). Adsorption of perfluorooctanoic acid (PFOA) onto anion exchange resin, non-ion exchange resin, and granular activated carbon by batch and column. Desalination Water Treat., 52:6542-6548.
Chularueangaksorn, P., Tanaka, S., Fujii, S. et Kunacheva, C. (2014). Batch and column adsorption of perfluorooctane sulfonate on anion exchange resins and granular activated carbon. J. Appl. Polym. Sci., 131:39782-39788.
Clarke, B.O. et Smith, S.R. (2011). Review of 'emerging' organic contaminants in biosolids and assessment of international research priorities for the agricultural use of biosolids. Environ. Int., 37(1): 226-247.
Clewell, H. (2009). Pharmacokinetic modeling of PFOA and PFOS, USEPA, Washington DC. PowerPoint Presentation to USEPA.
Corton, J.C., Cunningham, M.L., Hummer, B.T., Lau, C., Meek, B., Peters, J.M., Popp, J.A., Rhomberg, L., Seed, J. et Klaunig, J.E. (2014). Mode of action framework analysis for receptor-mediated toxicity: the peroxisome proliferator-activated receptor alpha (PPARα) as a case study. Crit. Rev. Toxicol., 44(1):1-49.
Costa, G., Sartori, S. et Consonni, D. (2009). Thirty years of medical surveillance in perfluooctanoic acid production workers. J. Occup. Environ. Med., 51(3): 364-372. [cité dans Health Canada (2012).]
Crump, K.S. (1984). A new method for determining allowable daily intakes. Fundam. Appl. Toxicol., 4: 854-871.
Cui, L., Zhou, Q.F., Liao, C.Y., Fu, J.J. et Jiang, G.B. (2009). Studies on the toxicological effects of PFOA and PFOS on rats using histological observation and chemical analysis. Arch. Environ. Contam. Toxicol., 56(2): 338-349.
Cui, L., Liao, C.Y., Zhou, Q.F., Xia, T.M., Yun, Z.J. et Jiang, G.B. (2010). Excretion of PFOA and PFOS in male rats during a subchronic exposure. Arch. Environ. Contam. Toxicol., 58(1): 205-13.
Dai, Y., Niu, J., Yin, L., Xu, J. et Sun, K. (2013). Enhanced sorption of perfluorooctane sulfonate (PFOS) on carbon nanotube-filled electrospunnanofibrous membranes. Chemosphere, 93(8):1593-1599.
Dean, W.P. et Jessup, D.C. (1978). Acute oral toxicity (LD50) study in rats. International Research and Development Corporation, Study No. 137-091, May 5, 1978. U.S. Environmental Protection Agency Administrative Record 226-0419. [cité dans OECD (2008).]
Dekleva, L.A. (2003). Adsorption/desorption of ammonium perfluorooctanoate to soil (OECD 106). Prepared for E.I. du Pont de Nemours and Company. Sponsored by Association of Plastics Manufacturers in Europe (EMSER 17-03).
Deng, S., Yu, Q., Huang, J. et Yu, G. (2010). Removal of perfluorooctane sulfonate from wastewater by anion exchange resins: Effects of resin properties and solution chemistry. Water Res. 44(18):5188-5195.
Deng, S., Zhou, Q., Yu, G., Huang, J. et Fan, Q. (2011). Removal of perfluorooctanoate from surface water by polyaluminium chloride coagulation. Water Res., 45:1774-1780.
Deng, S., Zhang, Q., Nie, Y., Wei, H., Wang, B., Huang, J., Yu, G. et Xing, B. (2012). Sorption mechanisms of perfluorinated compounds on carbon nanotubes. Environ. Pollut. 168:138-144.
D'Eon, J.C., Crozier, P.W., Furdui, V.I., Reiner, E.J., Libelo, E.L. et Mabury, S.A. (2009). Observation of a commercial fluorinated material, the polyfluoroalkyl phosphoric acid diesters, in human sera, wastewater treatment plant sludge, and paper fibers. Environ. Sci. Technol., 43(12): 4589-4594. [cité dans Kato (2011).]
Dewitt, J.C., Copeland, C.B., Strynar, M.J. et Luebke, R.W. (2008). Perfluorooctanoic acid-induced immunomodulation in adult C57BL/6J or C57BL/6N female mice. Environ. Health Perspect., 116(5): 644-650.
Dickenson, E.R.V. et Higgins, C. (2013). The removal of perfluoroalklyl and polyfluoroalkly substances by North American water treatment practices. Water Research Foundation, Denver, Colorado. Draft Report. (in press)
Dillert, R., Bahnemann, D. et Hidaka, H.(2007). Light-induced degradation of perfluorocarboxylic acids in the presence of titanium dioxide. Chemosphere, 67:785-792.
Dixon, D., Reed, C.E., Moore, A.B., Gibbs-Flournoy, E.A., Hines, E.P., Wallace, E.A. et coll. (2012). Histopathologic changes in the uterus, cervix and vagina of immature CD-1 mice exposed to low doses of perfluorooctanoic acid (PFOA) in a uterotrophic assay. Reprod. Toxicol., 33(4): 506-512.
Dolman, S. et Pelzing, M. (2011). An optimized method for the determination of perfluorooctanoic acid, perfluorooctane sulfonate and other perfluorochemicals in different matrices using liquid chromatography/ion-trap mass spectrometry. J. Chromatogr. B Analyt. Technol. Biomed. Life Sci., 879(22): 2043-2050.
Dudley, L.-A., Lindstrom, A., Strynar, M., McMillan, L. et Knappe, D. (2012). Removal of perfluorinated compounds by powdered activated carbon: effects of adsorbent and background water characteristics. Presented at 2012 AWWA Annual Conference in Dallas, TX, June 10-14, 2012. 2012 Annual Conference Proceedings. American Water Works Association, Catalog No. ACE_0076609.
ECETOC (2002). Recognition of, and differentiation between, adverse and non-adverse effects in toxicology studies. European Centre for Ecotoxicology and Toxicology of Chemicals, Brussels, Belgium (Technical Report No. 85). Disponible à : members.ecetoc.org/Documents/Document/TR%20085.pdf.
EFSA (2008). Opinion of the scientific panel on contaminants in the food chain on perfluorooctane sulfonate (PFOS), perfluorooctanoic acid (PFOA) and their salts. European Food Safety Authority. EFSA Journal, 653:1-131. Disponible à : www.efsa.europa.eu/en/efsajournal/pub/653.htm.
Elcombe, C.R., Elcombe, B.M., Foster, J.R., Farrar, D.G., Jung, R., Chang, S-C, Kennedy, G.L. et Butenhoff, J.L. (2010). Hepatocellular hypertrophy and cell proliferation in Sprague-Dawley rats following exposure to ammonium perfluorooctanoate occurs through increased activation of the xenosensor nuclear receptors PPARα and CAR/PXR. Arch. Toxicol., 84(10): 787-798.
Ellis, D.A., Martin, J.W., De Silva, A.O., Mabury, S.A., Hurley, M.D., Sulbaek Andersen, M.P. et coll. (2004). Degradation of fluorotelomer alcohols: a likely atmospheric source of perfluorinated carboxylic acids. Environ. Sci. Technol., 38(12): 3316-3321.[ As cited in Kato (2011)]. Comment in: Environ. Sci. Technol.,38(12):215A-216A.
Emmett, E.A., Shofer, F.S., Zhang, H., Freeman, D., Desai, C. et Shaw, L.M. (2006a). Community exposure to perfluorooctanoate: Relationships between serum concentrations and exposure sources. J. Occup. Environ. Med., 48: 759-770.
Emmett, E.A., Zhang, H., Shofer, F.S., Freeman, D., Rodway, N.V., Desai, C. et coll. (2006b). Community exposure to perfluorooctanoate: Relationships between serum levels and certain health parameters. J. Occup. Environ. Med., 48(8): 771-779. [cité dans Steenland (2010), Health Canada (2012).]
Environnement Canada et Santé Canada (2012). Screening assessment report perfluorooctanoic acid, its salts, and its precursors. Disponible à : www.ec.gc.ca/ese-ees/370AB133-3972-454F-A03A-F18890B58277/PFOA_EN.pdf.
Eriksen, K.T., Sørensen, M., McLaughlin, J.K., Lipworth, L., Tjønneland, A., Overvad, K. et coll. (2009). Perfluorooctanoate and perfluorooctanesulfonate plasma levels and risk of cancer in the general Danish population. J. Natl. Cancer Inst., 101(8): 605-609.
Eriksen, K.T., Raaschou-Nielsen, O., Sørensen, M., Roursgaard, M., Loft, S. et Møller, P. (2010). Genotoxic potential of the perfluorinated chemicals PFOA, PFOS, PFBS, PFNA and PFHxA in human HepG2 cells. Mutat.. Res., 700(1-2): 39-43.
Eschauzier, C., Beerendonk, E., Scholte-Veenendaal, P. et De Voogt, P. (2012). Impact of treatment processes on the removal of perfluoroalkyl acids from the drinking water production chain. Environ. Sci. Technol., 46 (3):1708-1715.
Fairley, K.J., Purdy, R., Kearns, S., Anderson, S.E. et Meade, B. (2007). Exposure to the immunosuppressant, perfluorooctanoic acid, enhances the murine IgE and airway hyperreactivity response to ovalbumin. Toxicol. Sci., 97(2): 375--383.
Fasano, W.J., Kennedy, G.L., Szostek, B., Farrar, D.G., Ward, R.J., Haroun, L. et coll. (2005). Penetration of ammonium perfluorooctanoate through rat and human skin in vitro. Drug. Chem. Toxicol 28(1):79-90. [cité dans ATSDR (2009).]
Fei, C. et Olsen, J. (2011). Prenatal exposure to perfluorinated chemicals and behavioral or coordination problems at age 7 years. Environ. Health Perspect., 119(4): 573-578.
Fei, C., McLaughlin, J.K., Tarone, R.E. et Olsen, J. (2007). Perfluorinated chemicals and fetal growth: a study within the Danish National Birth Cohort. Environ. Health Perspect., 115(11): 16777-16782.
Fei, C., McLaughlin, J.K., Lipworth, L. et Olsen, J. (2008a). Prenatal exposure to perfluorooctanoate (PFOA) and perfluorooctanesulfonate (PFOS) and maternally reported developmental milestones in infancy. Environ. Health Perspect., 116(10): 1391-1395.
Fei, C., McLaughlin, J.K., Tarone, R.E. et Olsen, J. (2008b). Fetal growth indicators and perfluorinated chemicals: a study in the Danish National Birth Cohort. Am. J. Epidemiol., 168(1): 66-72.
Fei, C., McLaughlin, J.K., Lipworth, L. et Olsen, J. (2009). Maternal levels of perfluorinated chemicals and subfecundity. Hum. Reprod., 24(5): 1200-1205.
Fei, C., McLaughlin, J.K., Lipworth, L. et Olsen, J. (2010a). Prenatal exposure to PFOA and PFOS and risk of hospitalization for infectious diseases in early childhood. Environ. Res., 110: 773-777.
Fei, C., McLaughlin, J.K., Lipworth, L. et Olsen, J. (2010b). Maternal concentrations of perfluorooctanesulfonate (PFOS) and perfluorooctanoate (PFOA) and duration of breastfeeding. Scand. J. Work Environ. Health, 36(5): 413-421.
Fenton, S.E., Reiner, J.L., Nakayama, S.F., Delinsky, A.D., Stanko, J.P., Hines, E.P. et coll. (2009). Analysis of PFOA in dosed CD-1 mice. Part 2. Disposition of PFOA in tissues and fluids from pregnant and lactating mice and their pups. Reprod. Toxicol., 27(3-4): 365-372.
Fernandez Freire, P., Perez Martin, J.M., Herrero, O., Peropadre, A., de la Pena, E. et Hazen, M.J. (2008). In vitro assessment of the cytotoxic and mutagenic potential of perfluorooctanoic acid. Toxicol. In Vitro, 22(5): 1228-1233.
Filgo, A.J., Quist, E.M., Hoenerhoff, M.J., Brix, A.E., Kissling, G.E. et Fenton, S.E. (2014). Perfluorooctanoic acid (PFOA)-induced liver lesions in two strains of mice following developmental exposures: PPARα is not required. Toxicol. Pathol., 43: 558-568.
Fitz-Simon, N., Fletcher, T., Luster, M.I., Steenland, K., Calafat, A.M., Kato, K. et coll. (2013). Reductions in serum lipids with a 4-year decline in serum perfluorooctanoic acid and perfluorooctanesulfonic acid. Epidemiology, 24(4): 569-576. Erratum in: Epidemiology, 24(6):941.
Florentin, A., Deblonde, T., Diguio, N., Hautemaniere, A. et Hartemann, P. (2011). Impacts of two perfluorinated compounds (PFOS and PFOA) on human hepatoma cells: cytotoxicity but no genotoxicity? Int. J. Hyg. Environ. Health., 214(6): 493-499.
Flores, C., Ventura, F., Martin-Alonso, J. et Caixach, J. (2013). Occurrence of perfluorooctane sulfonate (PFOS) and perfluorooctanoate (PFOA) in N.E. Spanish surface water and their removal in a drinking water treatment plant that combines conventional and advanced treatment in parallel lines. Sci. Tot. Environ. 461: 618-626.
Franko, J., Meade, B.J., Frasch, H.F., Barbero, A.M. et Anderson, S.E. (2012). Dermal penetration potential of perfluorooctanoic acid (PFOA) in human and mouse skin. J. Toxicol. Environ. Health A., 75(1): 50-62.
Fraser, A.J., Webster, T.F., Watkins, D.J., Nelson, J.W., Stapleton, H.M., Calafat, A.M. et coll. (2012). Polyfluorinated compounds in serum linked to indoor air in office environments. Environ. Sci. Technol.., 46(2): 1209-1215.
Freberg, B.I., Haug, L.S., Olsen, R., Daae, H.L., Hersson, M., Thomsen, C. et coll. (2010). Occupational exposure to airborne perfluorinated compounds during professional ski waxing. Environ. Sci. Technol.., 44(19): 7723-7728.
Frisbee, S.J., Brooks, A.P., Jr., Maher, A., Flensborg, P., Arnold, S., Fletcher, T. et coll. (2009). The C8 health project: design, methods, and participants. Environ. Health Perspect, 117(12): 1873-1882.
Frisbee, S.J., Shankar, A., Knox, S.S., Steenland, K., Savitz, D.A., Fletcher, T. et coll. (2010). Perfluorooctanoic acid, perfluorooctanesulfonate, and serum lipids in children and adolescents: results from the C8 Health Project. Arch. Pediatr. Adolesc. Med., 164(9): 860-869.
Fromme, H., Tittlemier, S.A., Völkel, W., Wilhelm, M. et Twardella, D. (2009). Perfluorinated compounds--exposure assessment for the general population in Western countries. Int. J. Hyg. Environ. Health, 212(3): 239-270.
Fujii, S., Polprasert, C., Tanaka, S. et Lien, N.P.H. (2007). New POPs in the water environment: distribution, bioaccumulation and treatment of perfluorinated compounds - a review paper. J. Water Supply Res. T, 56(5): 313-326.
Furdui, V., Crozier, P., Reiner, E. et Mabury, S. (2008). Trace level determination of perfluorinated compounds in water by direct injection. Chemosphere 73:S24-S530.
Gabriel, K. (1976). Acute oral toxicity--rats. Biosearch, Inc., September 16. U.S. Environmental Protection Agency Administrative Record 226-0425. [cité dans OECD (2008)].
Genuis, S. J., Birkholz, D., Ralitsch, M. et Thibault, N. (2010). Human detoxification of perfluorinated compounds. Public Health, 124(7): 367-375.
Giri, R.R., Ozaki, H., Morigaki, T., Taniguchi, S. et Takanami, R. (2011). UV photolysis of perfluorooctanoic acid (PFOA) in dilute aqueous solution. Water Sci. Technol., 63(2): 276-282.
Giri, R.R, Ozaki, H., Okada, T., Taniguchi, S. et Takanami, R. (2012). Factors influencing UV photodecomposition of perfluorooctanoic acid in water. Chemi. Eng. J., 180: 197-203.
Giri, R. R., Ozaki, H., Guo, X., Takanami, R. et Taniguchi, S. (2013). Oxidative-reductive photodecomposition of perfluorooctanoic acid in water. Int. J. Environ. Sci. Te., DOI 10.1007/s13762-013-0312-2.
Glaza, S. (1995). Acute dermal toxicity study of T-6342 in rabbits. Corning Hazelton, Inc. Madison, WI. Project ID: HWI 50800374. 3M Company. St. Paul, MN. U.S. Environmental Protection Agency Administrative Record 226-0427. [cité dans OECD (2008)].
Glaza, S.M. (1997). Acute oral toxicity study of T-6669 in rats. Corning Hazleton Inc. Study No. CHW 61001760, January 10, 1997. U.S. Environmental Protection Agency Administrative Record 226-0420. [cité dans OECD (2008)].
Goldenthal, E.I. (1978). Ninety-day subacute rat toxicity study on Fluorad®Fluorochemical FC-143, International Research and Development Corporation, Study No. 137-089/090, U.S. Environmental Protection Agency Administrative Records 226-0441/0447. [cité dans Kudo (2003); EFSA (2008); OECD (2008)].
González-Barreiro, C., Elena Martínez-Carballo, E., Sitka, A., Scharf, S. et Gans, O. (2006). Method optimization for determination of selected perfluorinated alkylated substances in water samples. Anal. Bioanal. Chem., 386:2123-2132.
Goss, K.-U. (2008). The pKa values of PFOA and other highly fluorinated carboxylic acids. Environ. Sci. Technol., 42(2): 456-458. [cité dans Environnement Canada et Santé Canada (2012)].
Goss, K.-U. et Arp, H.P.H. (2009). Comment on "Experimental pKa determination for perfluorooctanoic acid (PFOA) and the potential impact of pKa concentration dependence on laboratory-measured partitioning phenomena and environmental modeling." Environ. Sci. Technol., 43(1): 5150-5151. [Addendum à Arp, H.P.H. et Goss, K.-U. (2009). Gas/particle partitioning behaviour of perfluorocarboxylic acids with terrestrial aerosols. Environ. Sci. Technol., 43:8542-8547]
Grandjean, P. et Budtz-Jørgensen, E. (2013). Immunotoxicity of perfluorinated alkylates: calculation of benchmark doses based on serum concentrations in children. Environ. Health, 12:35.
Grandjean, P., Andersen, E.W., Budtz-Jørgensen, E., Nielsen, F., Mølbak, K., Weihe, P., et Heilmann, C. (2012). Serum vaccine antibody concentrations in children exposed to perfluorinated compounds. JAMA, 307(4): 391-397. Commentaire dans : JAMA, 307(18):1910; réponse de l'auteur 1910-1. Errata dans : JAMA, 307(11):1142.
Granum, B., Haug, L.S., Namork, E., Stølevik, S.B., Thomsen, C., Aaberge, I.S., van Loveren, H., Løvik, M. et Nygaard, U.C. (2013). Pre-natal exposure to perfluoroalkyl substances may be associated with altered vaccine antibody levels and immune-related health outcomes in early childhood. J. Immunotoxicol., 10(4): 373-379.
Greiner, A. et Wendorff, J. (2007). Electrospinning: a fascinating method for the preparation of ultrathin fibers. Angew. Chem. Int. Ed., 46: 5670-5703.
Griffith, F. D. et Long, J. E. (1980). Animal toxicity studies with ammonium perfluorooctanoate. Am. Ind. Hyg. Assoc. J., 41(8): 576-583.
Gützkow, K.B., Haug, L.S., Thomsen, C., Sabaredzovic, A., Becher, G. et Brunborg, G. (2012). Placental transfer of perfluorinated compounds is selective--a Norwegian mother and child sub-cohort study. Int. J. Hyg. Environ. Health, 215(2): 216-219.
Haber, L.T., Dourson, M.L. et Mohapatra A. (2013). Development of chemical-specific adjustment factors for long-lived chemicals: PFOS as a model chemical. Poster presented at Society for Risk Analysis Annual Meeting, Baltimore, MD, December 8-11, 2013.
Hall, A.P., Elcombe, C.R., Foster, J.R., Harada, T., Kaufmann, W., Knippel, A., Küttler, K., Malarkey, D.E., Maronpot, R.R., Nishikawa, A., Nolte, T., Schulte, A., Strauss, V. et York, M.J. (2012). Liver hypertrophy: a review of adaptive (adverse and non-adverse) changes--conclusions from the 3rd International ESTP Expert Workshop. Toxicol Pathol., 40(7): 971-994.
Halldorsson, T.I., Rytter, D., Haug, L.S., Bech, B.H., Danielsen, I., Becher, G. et coll. (2012). Prenatal exposure to perfluorooctanoate and risk of overweight at 20 years of age: a prospective cohort study. Environ. Health Perspect., 120(5): 668-673.
Hamm, M.P., Cherry, N.M., Chan, E., Martin, J.W. et Burstyn, I. (2010). Maternal exposure to perfluorinated acids and fetal growth. J. Expo. Sci. Environ. Epidemiol., 20(7): 589-597.
Han, X., Snow, T.A., Kemper, R.A. et Jepson, G.W. (2003). Binding of perfluorooctanoic acid to rat and human plasma proteins. Chem. Res. Toxicol. 16: 775-781.
Han, X., Hinderliter, P.M., Snow, T.A. et Jepson, G.W. (2004). Binding of perfluorooctanoic acid to rat liver-form and kidney-form α2u-globulins. Drug Chem. Toxicol., 27(4): 341-360.
Han, X., Kemper, R.A. et Jepson, G.W. (2005). Subcellular distribution and protein binding of perfluorooctanoic acid in rat liver and kidney. Drug Chem. Toxicol., 28(2): 197-209.
Han, X., Nabb, D.L., Russell, M.H., Kennedy, G.L. et Rickard, R.W. (2012). Renal elimination of perfluorocarboxylates (PFCAs). Chem. Res. Toxicol., 25(1): 35-46.
Hansen, K.J., Johnson, H.O., Eldridge, J.S., Butenhoff, J.L. et Dick, L.A. (2002). Quantitative characterization of trace levels of PFOS and PFOA in the Tennessee River. Environ. Sci. Technol.., 36(8): 1681-1685.
Hansen, M.C., Børresen, M.H., Schlabach, M. et Cornelissen, G. (2010). Sorption of perfluorinated compounds from contaminated water to activated carbon. J. Soils Sediments, 10: 179-185.
Harada, K., Saito, N., Sasaki, K., Inoue, K. et Koizumi, A. (2003). Perfluoroocatne sulfonate contamination of drinking water in the Tama river, Japan: Estimated effects on resident serum levels. Environ. Contam. Toxicol. 71:31-36.
Harada, K., Saito, N., Inoue, K., Yoshinaga, T., Watanabe, T., Sasaki, S. et coll. (2004). The influence of time, sex and geographic factors on levels of perfluorooctane sulfonate and perfluorooctanoate in human serum over the last 25 years. J. Occup. Health, 46(2): 141-147.
Harada, K., Inoue, K., Morikawa, A., Yoshinaga, T. et Saito, N. (2005). Renal clearance of perfluorooctane sulfonate and perfluorooctanoate in humans and their species-specific excretion. Env. Res, 99: 653-261.
Harada, K.H., Hashida, S., Kaneko, T., Takenaka, K., Minata, M., Inoue, K. et coll. (2007). Biliary excretion and cerebrospinal fluid partition of perfluorooctanoate and perfluorooctane sulfonate in humans. Environ. Toxicol. Pharmacol, 24(2): 134-139.
Harada, K.H. et Koizumi, A. (2009). Environmental and biological monitoring of persistent fluorinated compounds in Japan and their toxicities. Environ. Health Prev. Med., 14(1): 7-19.
Hardisty, J.F., Willson, G.A., Brown, W.R., McConnell, E.E., Frame, S.R., Gaylor, D.W. et coll. (2010). Pathology Working Group review and evaluation of proliferative lesions of mammary gland tissues in female rats fed ammonium perfluorooctanoate (APFO) in the diet for 2 years. Drug. Chem. Toxicol., 33(2): 131-137.
Higgins, C.P. et Luthy, R.G. (2006). Sorption of perfluorinated surfactants on sediments. Environ. Sci. Technol. 40: 7251-7256.
Hinderliter, P.M., Mylchreest, E., Gannon, S.A., Butenhoff, J.L. et Kennedy, G.L., Jr. (2005). Perfluorooctanoate: Placental and lactational transport pharmacokinetics in rats. Toxicology, 211(1-2): 139-48.
Hinderliter, P.M., Han, X., Kennedy, G.L. et Butenhoff, J.L. (2006). Age effect on perfluorooctanoate (PFOA) plasma concentration in post-weaning rats following oral gavage with ammonium perfluorooctanoate (APFO). Toxicology, 225: 195-203.
Hines, E.P., White, S.S., Stanko, J.P., Gibbs-Flournoy, E.A., Lau, C. et Fenton, S.E. (2009). Phenotypic dichotomy following developmental exposure to perfluorooctanoic acid (PFOA) in female CD-1 mice: Low doses induce elevated serum leptin and insulin, and overweight in mid-life. Mol. Cell. Endocrinol, 304(1-2): 97-105.
Hoffman, K., Webster, T.F., Weisskopf, M.G., Weinberg, J. et Vieira, V.M. (2010). Exposure to polyfluoroalkyl chemicals and attention deficit/hyperactivity disorder in U.S. children 12-15 years of age. Environ. Health Perspect., 118(12): 1762-1767.
Holtcamp, W. (2012). Obesogens: an environmental link to obesity. Environ. Health Perspect., 120(2): a62-68.
Hölzer, J., Midasch, O., Rauchfuss, K., Kraft, M., Reupert, R., Angerer, J., Kleeschulte, P., Marschall, N. et Wilhelm, M. (2008). Biomonitoring of perfluorinated compounds in children and adults exposed to perfluorooctanoate-contaminated drinking water. Environ. Health Perspect.., 116(5): 651-657.
Hori, H., Hayakawa, E., Einaga, H., Kutsuna, S., Koike, K., Ibusuki, T., Kiatagawa, H. et Arakawa, R. (2004a). Decomposition of environmentally persistent pefluorooctanoic acid in water by photochemical approaches. Environ. Sci. Technol., 38: 6118-6124.
Hori, H., Hayakawa, E., Yamashita, N., Taniyasu, S., Nacata, F. et Kobayashi, Y. (2004b). High performance liquid chromatography with conductimetric detection of perfluorocarboxilic acids and perfluorosulfonates. Chemosphere 57:273-282.
Hori, H., Yamamoto, A., Hayakawa, E., Einaga, H., Taniyasu, S., Yamashita, N. et Kutsuna, S. (2005). Efficient decomposition of environmentally persistent pefluorocarboxylic acids by use of persulfate as a photochemical oxidant. Environ. Sci. Technol., 39: 2383-2388.
Hori, H., Yamamoto, A., Koike, K., Kutsuna, S., Osaka, I. et Arakawa, R. (2007). Photochemical decomposition of environmentally persistent short-chain perfluorocarboxylic acids in water mediated by iron(II)/(III) redox reactions. Chemosphere, 68: 572-578.
Hundley, S.G., Sarrif, A.M. et Kennedy, G.L. (2006). Absorption, distribution, and excretion of ammonium perfluorooctanoate (APFO) after oral administration to various species. Drug Chem. Toxicol., 29(2): 137-145.
Ingelido, A.M., Marra, V., Abballe, A., Valentini, S., Iacovella, N., Barbieri, P., Porpora, M.G., di Domenico, A. et De Felip, E. (2010). Perfluorooctanesulfonate and perfluorooctanoic acid exposures of the Italian general population. Chemosphere, 80(10): 1125-1130.
ISO (2009). ISO 25101 Water quality - Determination of perfluorooctanesulfonate (PFOS) and perfluorooctanoate (PFOA) - Method for unfiltered water samples using solid phase extraction and liquid chromatography with mass spectrometry. International Standardization Organization.
IPCS (1994). Assessing human health risks of chemicals: derivation of guidance values for health-based exposure limits. International Programme on Chemical Safety, Environmental Health Criteria 170, World Health Organization, Geneva, Switzerland.
IPCS (2005). Chemical-specific adjustment factors for interspecies differences and human variability: guidance document for use of data in dose/concentration-response assessment. International Programme on Chemical Safety, Harmonization Project Document No. 2. World Health Organization, Geneva, Switzerland.
Ishibashi, H., Ishida, H., Matsuoka, M., Tominaga, N. et Arizono, K. (2007). Estrogenic effects of fluorotelomer alcohols for human estrogen receptor isoforms alpha and beta in vitro. Biol. Pharm. Bull., 30(7): 1358-1359.
Jahnke, A. et Berger, U. (2009). Trace analysis of per- and polyfluorinated alkyl substances in various matrices-How do current method perform? J. Chromatogr. A 1216:410-421.
Japanese Industrial Standard (2011). JIS K 0450-70-10, Testing methods for perfluorooctanesulfonate (PFOS) and perfluorooctanoate (PFOA) in industrial water and wastewater.
Jasinski, M., Ellis. D.A., Webster, E., McMurdo, C. et Burns, D. (2009). The development of a 19F NMR technique for the simultaneous determination of the Kow and pKa of perfluorooctanoic acid (PFOA). Poster presentation at the Society of Environmental Toxicology and Chemistry (SETAC) 30th Annual Meeting in North America, November 19-23, 2009, New Orleans, Louisiana.
Johansson, N., Fredriksson, A. et Eriksson, P. (2008). Neonatal exposure to perfluorooctane sulfonate (PFOS) and perfluorooctanoic acid (PFOA) causes neurobehavioural defects in adult mice. Neurotoxicology, 29(1): 160-169.
Johansson, N., Eriksson, P. et Viberg, H. (2009). Neonatal exposure to PFOS and PFOA in mice results in changes in proteins which are important for neuronal growth and synaptogenesis in the developing brain. Toxicol. Sci., 108(2): 412-418.
Johnson, J. D. et Ober, R. E. (1979). Absorption of FC-95-14C in rats after a single oral dose. 3M. Submitted to the U.S. Environmental Protection Agency's Administrative Record. AR226-0007. [cité dans ATSDR (2009), EFSA (2008)].
Johnson, J.D. et Ober, R.E. (1999). Absorption of FC-143-14C in rats after a single oral dose. In: Exploratory 28-day oral toxicity study with telomer alcohol, telomer acrylate, PFHS, and PFOS (POS control) by daily gavage in the rat, w/CVR LTR DTD, 051500 (Sanitized) 3M. Submitted to the U.S. Environmental Protection Agency under TSCA Section FYI. OTS05001378S. [cité dans ATSDR (2009)].
Kadar, H., Veyrand, B., Barbarossa, A., Pagliuca, G., Legrand, A., Bosher, C. et coll. (2011). Development of an analytical strategy based on liquid chromatography-high resolution mass spectrometry for measuring perfluorinated compounds in human breast milk: application to the generation of preliminary data regarding perinatal exposure in France. Chemosphere, 85(3): 473-480.
Kärrman, A., Domingo, J.L., Llebaria, X., Nadal, M., Bigas, E., van Bavel, B. et Lindström G. (2010). Biomonitoring perfluorinated compounds in Catalonia, Spain: concentrations and trends in human liver and milk samples. Environ. Sci. Pollut. Res. Int., 17(3): 750-758.
Kato, K., Wong, L.Y., Jia, L.T., Kuklenyik, Z. et Calafat, A.M. (2011). Trends in exposure to polyfluoroalkyl chemicals in the U.S. Population: 1999-2008. Environ. Sci. Technol., 45(19): 8037-8045.
Kauck, E.A. et Diesslin, A.R. (1951). Some properties of perfluorocarboxylic acids. Ind Eng Chem, 43: 2332-2334.
Kemper, R.A. (2003). Perfluorooctanoic acid: Toxicokinetics in the rat. Association of Plastics Manufactures of Europe. Project ID: DuPont 7473. U.S. EPA public docket, administrative record. AR226-1499.
Kemper, R.A. et Nabb, D.L. (2005). In vitro studies in microsomes from rat and human liver, kidney, and intestine suggest that perfluorooctanoic acid is not a substrate for microsomal UDPglucuronosyltransferases. Drug Chem. Toxicol., 28(3): 281-287.
Kennedy, G.L. (1985). Dermal toxicity of ammonium perfluorooctanoate. Toxicol. Appl. Pharmacol., 81: 348-355. [cité dans OECD (2008)].
Kennedy, G.L., Jr. (1987). Increase in mouse liver weight following feeding of ammonium perfluorooctanoate and related fluorochemicals. Toxicol. Lett., 39(2-3): 295-300.
Kennedy, G.L.J., Hall, G.T., Brittelli, M.R., Barnes, J.R. et Chen, H.C. (1986). Inhalation toxicity of ammonium perfluorooctanoate. Food Chem. Toxicol., 24(12): 1325-1329.
Kerger, B.D., Copeland, T.L. et DeCaprio, A.P. (2011). Tenuous dose-response correlations for common disease states: case study of cholesterol and perfluorooctanoate/sulfonate (PFOA/PFOS) in the C8 Health Project. Drug Chem. Toxicol., 34(4): 396-404.
Kerstner-Wood, C., Coward, L. et Gorman, G. (2003). Protein binding of perfluorohexane sulfonate, perfluorooctane sulfonate and perfluorooctanoate to plasma (human, rat, and monkey), and various human-derived plasma protein fractions. Southern Research Institute. Submitted to the U.S. Environmental Protection Agency's Administrative Record. AR226-1354.
Kim, S., Choi, K., Ji, K., Seo, J., Kho, Y., Park, J., Hwang, I., Jeon, J., Yang, H. et Giesy, J.P. (2011). Trans-placental transfer of thirteen perfluorinated compounds and relations with fetal thyroid hormones. Environ. Sci. Technol., 45(17): 7465-7472.
Kissa, E. (1994). Fluorinated surfactants: synthesis, properties, applications. Marcel Dekker, Inc., New York, New York.
Kissa, E. (2001) Fluorinated surfactants and repellents (2nd edition revised and expanded). Marcel Dekker, Inc., New York, New York.
Klaunig, J.E., Hocevar, B.A. et Kamendulis, L.M. (2012). Mode of action analysis of perfluorooctanoic acid (PFOA) tumorigenicity and human relevance. Reprod. Toxicol., 33: 410-418.
Knox, S.S., Jackson, T., Javins, B., Frisbee, S.J., Shankar, A. et Ducatman, A.M. (2011a). Implications of early menopause in women exposed to perfluorocarbons. J. Clin. Endocrinol. Metab., 96(6): 1747-1753.
Knox, S.S., Jackson, T., Frisbee, S.J., Javins, B. et Ducatman, A.M. (2011 b). Perfluorocarbon exposure, gender and thyroid function in the C8 Health Project. J. Toxicol. Sci., 36(4): 403-410.
Kolstad, C. (2010). GAC treatment for PFCs in Oakdale. Breeze, 143: 14-15.
Krishnan, K. et Carrier, R. (2008). Approaches for evaluating the relevance of multiroute exposures in establishing guideline values for drinking water contaminants. J. Environ. Sci. Health C Environ. Carcinog. Ecotoxicol. Rev., 26(3): 300-316.
Krishnan, K. et Carrier, R. (2013). The use of exposure source allocation factor in the risk assessment of drinking-water contaminants. J. Toxicol. Environ. Health B Crit. Rev., 16(1): 39-51.
Kubwabo, C., Stewart, B., Zhu, J. et Marro, L. (2005). Occurrence of perfluorosulfonates and other perfluorochemicals in dust from selected homes in the city of Ottawa, Canada. J. Environ. Monit., 7(11): 1074-1078. [cité dans EFSA (2008); ATSDR (2009); Environnement Canada et Santé Canada (2012)].
Kudo, N., Suzuki, E., Katakura, M., Ohmori, K., Noshiro, R. et Kawashima, Y. (2001). Comparison of the elimination between perfluorinated fatty acids with different carbon chain length in rats. Chem. Biol. Interact., 134(2): 203-216.
Kudo, N., Sakai, A., Mitsumoto, A. e. a., Hibino, Y., Tsuda, T. et Kawashima, Y. (2007). Tissue distribution and hepatic subcellular distribution of perfluorooctanoic acid at low dose are different from those at high dose in rats. Biol. Pharm. Bull., 30(8): 1535-1540.
Lampert, D.J., Frisch, M.A. et Speitel.Jr, G.E. (2007). Removal of perfluorooctanoic acid and perfluorooctanesulfonate from wastewater by ion exchange. Practice Periodical of Hazardous, Toxic, and Radioactive Waste Management. 11: 60-68.
Lange, F.T., Schmidt, C. et Brauch, H-J.(2006). Perfluoroalkyl carboxylates and sulfonates, Rhine Water Works, The Netherlands, Association of River Waterworks - RIWA.
Larsen, B.S. et Kaiser, M.A., 2007. Challenges in perfluorocarboxylic acid measurement. Anal. Chem., 79: 3966-3973.
Lau, C., Thibodeaux, J.R., Hanson, R.G., Narotsky, M.G., Rogers, J.M., Lindstrom, A.B. et coll. (2006). Effects of perfluorooctanoic acid exposure during pregnancy in the mouse. Toxicol. Sci., 90(2): 510-518.
Lau, C., Anitole, K., Hodes, C., Lai, D., Pfahles-Hutchens, A. et Seed, J. (2007). Perfluoroalkyl acids: a review of monitoring and toxicological findings. Toxicol. Sci., 99: 366-394.
Lee, H., D'eon, J. et Mabury, S. A. (2010). Biodegradation of polyfluoroalkyl phosphates as a source of perfluorinated acids to the environment. Environ. Sci. Technol., 44: 3305-3310. [cité dans Kato (2011)].
Leonard, R.C., Kreckmann, K.H., Sakr, C.J. et Symons, J.M. (2008). Retrospective cohort mortality study of workers in a polymer production plant including a reference population of regional workers Ann. Epidemiol., 18: 15-22. [cité dans Steenland (2010); C8 Science Panel].
Li, Y., Ramdhan, D.H., Naito, H., Yamagishi, N., Ito, Y., Hayashi, Y. et coll. (2011). Ammonium perfluorooctanoate may cause testosterone reduction by adversely affecting testis in relation to PPARalpha. Toxicol. Lett., 205(3): 265-272.
Lide, D.R. (2003). CRC Handbook of Chemistry and Physics. CRC Press.
Lin, C.Y., Lin, L.Y., Chiang, C.K., Wang, W.J., Su, Y.N., Hung, K.Y. et coll. (2010). Investigation of the associations between low-dose serum perfluorinated chemicals and liver enzymes in US adults. Am. J. Gastroenterol., 105(6): 1354-1363.
Lindeman, B., Maass, C., Duale, N., Gützkow, K.B., Brunborg, G. et Andreassen, A. (2012). Effects of per- and polyfluorinated compounds on adult rat testicular cells following in vitro exposure. Reprod. Toxicol., 33(4): 531-537.
Lindstrom, A.B., Strynar, M.J., Delinsky, A.D., Nakayama, S.F., McMillan, L., Libelo, E.L., Neill, M. et Thomas, L. (2011). Application of WWTP biosolids and resulting perfluorinated compound contamination of surface and well water in Decatur, Alabama, USA. Environ. Sci. Technol., 45(19): 8015-8021.
Liou, J.S., Szostek, B., DeRito, C.M. et Madsen, E.L. (2010). Investigating the biodegradability of perfluorooctanoic acid. Chemosphere 80(2): 176-183.
Lipp, P., Sacher, F. et Baldauf, G. (2010). Removal of organic micro-pollutants during drinking water treatment by nanofiltration and reverse osmosis. Desalination Water Treat., 13(13): 226-237.
Little Hocking Water Association (2010). GAC filter C-8 sampling result summary. Disponible à : http://littlehockingwater.org/newsite/?cat=8
Liu, R.C., Hurtt, M.E., Cook, J.C. et Biegel, L.B. (1996). Effect of the peroxisome proliferator, ammonium perfluorooctanoate (C8), on hepatic aromatase activity in adult male Crl:CD BR (CD) rats. Fundam. Appl. Toxicol., 30(2): 220-228. [cité dans ATSDR (2009)].
Liu, J., Li, J., Liu, Y., Chan, H.M., Zhao, Y., Cai, Z. et Wu, Y. (2011). Comparison on gestation and lactation exposure of perfluorinated compounds for newborns. Environ. Int., 37(7): 1206-1212.
Loccisano, A.E., Campbell, J.L., Jr., Andersen, M.E. et Clewell, H.J., 3 rd. (2011). Evaluation and prediction of pharmacokinetics of PFOA and PFOS in the monkey and human using a PBPK model. Regul. Toxicol. Pharmacol., 59(1): 157-175.
Loccisano, A.E., Campbell, J.L., Jr., Butenhoff, J.L., Andersen, M.E. et Clewell, H.J., 3 rd. (2012a). Comparison and evaluation of pharmacokinetics of PFOA and PFOS in the adult rat using a physiologically based pharmacokinetic model. Reprod. Toxicol., 33(4): 452-467.
Loccisano, A.E., Campbell, J.L., Jr., Butenhoff, J.L., Andersen, M.E. et Clewell, H.J., 3 rd. (2012b). Evaluation of placental and lactational pharmacokinetics of PFOA and PFOS in the pregnant, lactating, fetal and neonatal rat using a physiologically based pharmacokinetic model. Reprod. Toxicol., 33(4): 468-90.
Loccisano, A.E., Longnecker, M.P., Campbell, J.L., Jr., Andersen, M.E. et Clewell, H.J., 3 rd. (2013). Development of PBPK models for PFOA and PFOS for human pregnancy and lactation life stages. J. Toxicol. Environ. Health A, 76(1): 25-57.
Looker, C., Luster, M.I., Calafat, A.M., Johnson, V.J., Burleson, G.R., Burleson, F.G. et Fletcher, T. (2014). Influenza vaccine response in adults exposed to perfluorooctanoate and perfluorooctanesulfonate. Toxicol. Sci.., 138(1): 76-88.
Loos.R., Wollgast, J., Huber, T. et Hanke, G. (2007). Polar herbicides, pharmaceutical products, perfluorooctanesulfonate (PFOS), perfluorooctanoate (PFOA), and nonylphenol and its carboxylates and ethoxylates in surface and tap waters around Lake Maggiore in Northern Italy. Anal. Bioanal. Chem., 387:1469-1478.
Lopez-Espinosa, M.J., Fletcher, T., Armstrong, B., Genser, B., Dhatariya, K., Mondal, D. et coll. (2011). Association of Perfluorooctanoic Acid (PFOA) and Perfluorooctane Sulfonate (PFOS) with age of puberty among children living near a chemical plant. Environ. Sci. Technol.., 45(19): 8160-8166.
Lopez-Espinosa, M.J., Mondal, D., Armstrong, B., Bloom, M.S. et Fletcher, T. (2012). Thyroid function and perfluoroalkyl acids in children living near a chemical plant. Environ. Health Perspect., 120(7): 1036-1041.
Lou, I., Wambaugh, J.F., Lau, C., Hanson, R.G., Lindstrom, A.B., Strynar, M.J., Zehr, R.D., Setzer, R.W. et Barton, H.A. (2009). Modeling single and repeated dose pharmacokinetics of PFOA in mice. Toxicol. Sci., 107(2): 331-341.
Loveless, S.E., Finlay, C., Everds, N.E., Frame, S.R., Gillies, P.J., O'Connor, J.C. et coll. (2006). Comparative responses of rats and mice exposed to linear/branched, linear, or branched ammonium perfluorooctanoate (APFO). Toxicology, 220(2-3): 203-217.
Loveless, S.E., Hoban, D., Sykes, G., Frame, S.R. et Everds, N.E. (2008). Evaluation of the immune system in rats and mice administered linear ammonium perfluorooctanoate. Toxicol. Sci.., 105(1): 86-96.
Lowen, M., Halldorson, T., Wang, F et Tomy, G. (2005). Fluorotelomer carboxylic acids and PFOS in rainwater from urban center in Canada. Environ. Sci. Technol. 39: 2944-2951.
Luebker, D.J., Hansen, K.J., Bass, N.M., Butenhoff, J.L. et Seacat, A.M. (2002). Interactions of fluorochemicals with rat liver fatty acid-binding protein. Toxicology, 176(3): 175-185.
Lundin, J.I., Alexander, B.H., Olsen, G.W. et Church, T.R. (2009). Ammonium perfluorooctanoate production and occupational mortality. Epidemiology, 20(6): 921-928.
MacNeil, J., Steenland, N.K., Shankar, A. et Ducatman, A. (2009). A cross-sectional analysis of type II diabetes in a community with exposure to perfluorooctanoic acid (PFOA). Environ. Res., 109(8): 997-1003.
Macon, M.B., Villanueva, L.R., Tatum-Gibbs, K., Zehr, R.D., Strynar, M.J., Stanko, J.P. et coll. (2011). Prenatal perfluorooctanoic acid exposure in CD-1 mice: low-dose developmental effects and internal dosimetry. Toxicol. Sci., 122(11): 134-145.
Maisonet, M., Terrell, M.L., McGeehin, M.A., Christensen, K.Y., Holmes, A., Calafat, A.M. et Marcus, M. (2012). Maternal concentrations of polyfluoroalkyl compounds during pregnancy and fetal and postnatal growth in British girls. Environ. Health Perspect., 120(10): 1432-1437.
Mak, Y.L., Taniyasu, S., Yeung, L.W.Y., Lu, G.H., Jin, L., Yang, Y.L., Lam, P.K.S., Kannan, K. et Yamashita, N. (2009). Perfluorinated compounds in tap water from China and several other countries. Environ. Sci. Technol. 43(13): 4824-4829.
Martin, J., Kannan, K., Berser, U., deVoogt, P., Field, J., Franklin, J., Giesy, J., Harner, T., Muir, D., Scott, B., Kaiser, M., Jarnberg, U., Jones, K., Mabury, S., Schroeder, H., Simcik, M., Sottani, C., Van Bavel., B., Karrmane, A., Lindstrom, G. et Van Leeuwen, S. (2004). Analytical challenges hamper perfluoroalkyl research. Environ. Sci. Technol., 38(13): 248A-255A.
Martin, M.T., Brennan, R.J., Hu, W., Ayanoglu, E., Lau, C., Ren, H., Wood, C.R., Corton, J.C., Kavlock, R.J. et Dix, D.J. (2007). Toxicogenomic study of triazole fungicides and perfluoroalkyl acids in rat livers predicts toxicity and categorizes chemicals based on mechanisms of toxicity. Toxicol. Sci., 97(2): 595-613.
Martin, J W., Asher, B J., Beesoon, S., Benskin, J P. et Ross, M.S. (2010). PFOS or PreFOS? Are perfluorooctanesulfonate precursors (PreFOS) important determinants of human and environmental perfluorooctanesulfonate (PFOS) exposure? J. Environ. Monitor., 12(11), 1979-2004.
MDH (2008a). Public 1071 health assessment: perfluorochemical 1072 contamination in Lake Elmo and Oakdale, Washington County, Minnesota. Minnesota Department of Health. Disponible à : www.health.state.mn.us/divs/eh/wells/waterquality/poudevicefinal.pdf
MDH (2008 b). Performance evaluation: Removal of perfluorochemicals (PFC's) with point-of-use (POU) water treatment devices. Final report, prepared for the state of Minnesota, Minnesota Department of Health by Philip C. Olsen and David J. Paulson, Water Science & Marketing, LLC. May. Disponible à : www.health.state.mn.us/divs/eh/wells/waterquality/poudevicefinal.pdf
MDH (2008c). Health risk limits for perfluorochemicals. Report to the Minnesota legislature. Final report. Minnesota Department of Health. January 15.
MDH (2008d). Health risk limits for groundwater 2008 rule revision. Perfluorooctanoic acid. Minnesota Department of Health.
Meek, M.E., Palermo, C.M., Bachman, A.N., North, C.M. et Lewis, J.R. (2014). Mode of action human relevance (species concordance) framework: Evolution of the Bradford Hill considerations and comparative analysis of weight of evidence. J. Appl. Toxicol., 34(6): 595-606.
Melzer, D., Rice, N., Depledge, M.H., Henley, W.E. et Galloway, T.S. (2010). Association between serum perfluorooctanoic acid (PFOA) and thyroid disease in the U.S. National Health and Nutrition Examination Survey. Environ. Health Perspect, 118(5): 686-692.
Metrick, M. et Marias, A.J. (1977). 28-day oral toxicity study with fc-143 in albino rats, Final Report, Industrial Bio-Test Laboratories, Inc. Study No. 8532-10654, 3M Reference No. T-1742CoC, Lot 269, September 29. [cité dans OECD (2008)].
Midasch, O., Drexler, H., Hart, N., Beckmann, M.W. et Angerer, J. (2007). Transplacental exposure of neonates to perfluorooctanesulfonate and perfluorooctanoate: a pilot study. Int. Arch. Occup. Environ Health, 80(7): 643-648.
Min, J.Y., Lee, K.J., Park, J.B. et Min, K.B. (2013). Perfluorooctanoic acid exposure is associated with elevated homocysteine and hypertension in US adults. Occup.Environ. Med., 69(9): 658-662.
Minata, M., Harada, K.H., Kärrman, A., Hitomi, T., Hirosawa, M., Murata, M., Gonzalez, F.J. et Koizumi A. (2010). Role of peroxisome proliferator-activated receptor-α in hepatobiliary injury induced by ammonium perfluorooctanoate in mouse liver. Ind. Health, 48: 96-107.
Ministère du Développement durable, de l'Environnement, de la Faune et des Parcs (2012). Les composés perfluorés dans les cours d'eau et l'eau potable du Québec méridonal. Gouvernement du Québec, Québec, Québec.
Mondal, D., Lopez-Espinosa, M.J., Armstrong, B., Stein, C.R. et Fletcher, T. (2012). Relationships of perfluorooctanoate and perfluorooctane sulfonate serum concentrations between mother-child pairs in a population with perfluorooctanoate exposure from drinking water. Environ. Health Perspect., 120(5): 752-757.
Monroy, R., Morrison, K., Teo, K., Atkinson, S., Kubwabo, C., Stewart, B. et Foster, W.G. (2008). Serum levels of perfluoroalkyl compounds in human maternal and umbilical cord blood samples. Environ. Res., 108(1): 56-62.
Moody, C.A., Kwan, W.C., Martin, J.W., Muir, D.C.G. et Mabury, S.A. (2001). Determination of perfluorinated surfactants in surface water samples by two independent analytical techniques: liquid chromatography/ tandem mass spectrometry and 19F NMR. Anal. Chem., 73: 2200-2206.
Moody, C.A., Hebert, G.N., Strauss, S.H. et Field, J.A. (2003). Occurrence and persistence of perfluorooctanesulfonate and other perfluorinated surfactants in groundwater at a fire-training area at Wurtsmith Air Force Base, Michigan, USA. J. Environ. Monit., 5(2): 341-345.
Nakayama, S., Strynar, M.., Helfant, L., Egeghy, P., Ye, X. et Lindstrom, A. (2007). Perfluorinated compounds in the Cape Fear Drainage basin in North Carolina. Environ. Sci. Technol., 41:5271-5276.
Nakamura, T., Ito, Y., Yanagiba, Y., Ramdhan, D.H., Kono, Y., Naito, H., Hayashi, Y., Li, Y., Aoyama, T., Gonzalez, F.J. et Nakajima, T. (2009). Microgram-order ammonium perfluorooctanoate may activate mouse peroxisome proliferator-activated receptor α, but not human PPARα. Toxicology, 265: 27-33.
Nakagawa, T., Ramdhan, D.H., Tanaka, N., Naito, H., Tamada, H., Ito, Y., Li, Y., Hayashi, Y., Yamagishi, N., Yanagiba, Y., Aoyama, T., Gonzalez, F.J. et Nakajima, T. (2012). Modulation of ammonium perfluorooctanoate-induced hepatic damage by genetically different PPARα in mice. Arch. Toxicol., 86: 63-74.
Needham, L. L., Grandjean, P., Heinzow, B., Jørgensen, P.J., Nielsen, F., Patterson, D. G., Jr., Sjödin, A., Turner, W.E. et Weihe, P. 2011. Partition of environmental chemicals between maternal and fetal blood and tissues. Environ. Sci. Technol., 45(3): 1121-1126.
Nelson, J.W., Hatch, E.E. et Webster, T.F. (2010). Exposure to polyfluoroalkyl chemicals and cholesterol, body weight, and insulin resistance in the general U.S. population. Environ. Health Perspect., 118(2): 197-202.
Nolan, L.A., Nolan, J.M., Shofer, F.S., Rodway, N.V. et Emmett, E.A. (2009). The relationship between birth weight, gestational age and perfluorooctanoic acid (PFOA)-contaminated public drinking water. Reprod. Toxicol.., 27(3-4): 231-238.
Nolan, L.A., Nolan, J.M., Shofer, F.S., Rodway, N.V. et Emmett, E.A. (2010). Congenital anomalies, labor/delivery complications, maternal risk factors and their relationship with perfluorooctanoic acid (PFOA)-contaminated public drinking water. Reprod. Toxicol.., 29(2): 147-155.
NSF/ANSI (2014). NSF International/American National Standards Institute Standard 61: Drinking water system components--health effects. NSF International, Ann Arbor, Michigan.
Ochoa-Herrera, V. et Sierra-Alvarez, R. (2008). Removal of perfluorinated surfactants by sorption onto granular activated carbon, zeolite and sludge. Chemosphere, 72: 1588-1593.
Oda, Y., Nakayama, S., Harada, K.H. et Koizumi, A. (2007). Negative results ofumu genotoxicity test of fluorotelomer alcohols and perfluorinated alkyl acids. Environ. Health Prev. Med., 12(5): 217-219.
OECD (2006). Perfluorooctanoic Acid (PFOA). SIDS Initial Assessment Report after SIAM 22 Paris, France, 18-21 April. Disponible à : www.oecd.org/ehs/pfc/.
Okada, E., Sasaki, S., Saijo, Y., Washino, N., Miyashita, C., Kobayashi, S. et coll. (2012). Prenatal exposure to perfluorinated chemicals and relationship with allergies and infectious diseases in infants. Environ. Res., 112: 118-125.
Olsen, G.W. et Zobel, L.R. (2007). Assessment of lipid, hepatic, and thyroid parameters with serum perfluorooctanoate (PFOA) concentrations in fluorochemical production workers. Int. Arch. Occup. Environ. Health, 81(2): 231-246.
Olsen, G.W., Gilliland, F.D., Burlew, M.M., Burris, J.M., Mandel, J.S. et Mandel, J.H. (1998). An epidemiologic investigation of reproductive hormones in men with occupational exposure to perfluorooctanoic acid. J. Occup. Environ. Med., 40(7): 614-622.
Olsen, G.W., Hansen, K.J., Stevenson, L.A., Burris, J.M. et Mandel, J.H. (2003a). Human donor liver and serum concentrations of perfluorooctanesulfonate and other perfluorochemicals. Environ. Sci. Technol., 37:888-891.
Olsen, G.W., Burris, J.M., Burlew, M.M. et Mandel, J.H. (2003b). Epidemiologic assessment of worker serum perfluorooctanesulfonate (PFOS) and perfluorooctanoate (PFOA) concentrations and medical surveillance examinations. J. Occup. Environ. Med., 45(3): 260-270.
Olsen, G.W., Burris, J.M., Ehresman, D.J., Froehlich, J.W., Seacat, A.M., Butenhoff, J.L. et coll. (2007). Half-life of serum elimination of perfluorooctanesulfonate, perfluorohexanesulfonate, and perfluorooctanoate in retired fluorochemical production workers. Environ. Health Perspect., 115(9): 1298-1305.
Olsen, G.W., Butenhoff, J.L. et Zobel, L.R. (2009). Perfluoroalkyl chemicals and human fetal development: an epidemiologic review with clinical and toxicological perspectives. Reprod. Toxicol., 27(3-4): 212-230.
Olsen, G., Ehresman, D.J., Buehrer, B.D., Gibson, B.A., Butenhoff, J.L. et Zobel, L.R. (2012). Longitudinal assessment of lipid and hepatic clinical parameters in workers involved with the demolition of perfluoroalkyl manufacturing facilities. J. Occup. Environ. Med., 54(8): 974-983.
Onishchenko, N., Fischer, C., Wan Ibrahim, W.N., Negri, S., Spulber, S., Cottica, D. et Ceccatelli, S. (2011). Prenatal exposure to PFOS or PFOA alters motor function in mice in a sex-related manner. Neurotox. Res., 19(3): 452-461.
Ostertag, S.K., Tague, B.A., Humphries, M.M., Tittlemier, S.A. et Chan, H.M. (2009). Estimated dietary exposure to fluorinated compounds from traditional foods among Inuit in Nunavut, Canada. Chemosphere, 75(9): 1165-1172.
Palazzolo, M.J. (1993). Thirteen-week dietary toxicity study with T-5180, ammonium perfluorooctanoate (CAS No. 3825-26-1) in male rats. Final Report. Laboratory Project Identification HWI 6329-100. Hazleton Wisconsin, Inc. U.S. Environmental Protection Agency Administrative Record 226-0449. [cité dans UK COT (2006); OECD (2008)].
Panchangam, S. C., Yu-Chen Lin, A., Shaik, K.L. et Lin, C-F.(2009). Decomposition of perfluorocarboxylic acids (PFCAs) by heterogeneous photocatalysis in acidic aqueous medium. Chemosphere 77: 242-248.
Perkins, R., Butenhoff, J., Kennedy, G. et Palazzolo, M. (2004). 13-Week dietary toxicity study of ammonium perfluorooctanoate (APFO) in male rats. Drug Chem. Toxicol., 27: 361-378.
Pirali, B., Negri, S., Chytiris, S., Perissi, A., Villani, L., La Manna, L., Cottica, D., Ferrari, M., Imbriani, M., Rotondi, M. et Chiovato, L. (2009). Perfluorooctane sulfonate and perfluorooctanoic acid in surgical thyroid specimens of patients with thyroid diseases. Thyroid, 19(12): 1407-1412.
Post, G.B., Cohn, P.D. et Cooper, K.R. (2012). Perfluorooctanoic acid (PFOA), an emerging drinking water contaminant: a critical review of recent literature. Environ. Res., 116: 93-117.
Post, G., Louis, J., Lippincott, L. et Procopio, N. (2013). Occurrence of perfluorinated compounds in raw water from New Jersey public drinking water system. Environ. Sci. Technol. 47:13266-13275.
Powley, C.R., Michalczyk, M.J., Kaiser, M.A. et Buxton, L.W. (2005). Determination of perfluorooctanoic acid (PFOA) extractable from the surface of commercial cookware under simulated cooking conditions by LC/MS/MS. Analyst., 130(9): 1299-1302. [cité dans Fromme (2009)].
Prevedouros, K., Cousins, I.T., Buck, R.C. et Korzeniowski, S.H. (2006). Sources, fate, and transport of perfluorocarboxylates. Environ. Sci. Technol., 40(1): 32-44.
Qazi, M.R., Bogdanska, J., Butenhoff, J.L., Nelson, B.D., DePierre, J.W. et Abedi-Valugerdi, M. (2009). High-dose, short-term exposure of mice to perfluorooctanesulfonate (PFOS) or perfluorooctanoate (PFOA) affects the number of circulating neutrophils differently, but enhances the inflammatory responses of macrophages to lipopolysaccharide (LPS) in a similar fashion. Toxicology, 262(3): 207-214.
Qazi, M.R., Abedi, M.R., Nelson, B.D., DePierre, J.W. et Abedi-Valugerdi, M. (2010). Dietary exposure to perfluorooctanoate or perfluorooctane sulfonate induces hypertrophy in centrilobular hepatocytes and alters the hepatic immune status in mice. Int. Immunopharmacol., 10(11): 1420-1427.
Qu. Y., Zhang, C., Li, F., Bo, X., Liu, G. et Zhou, Q. (2009). Equilibrium and kinetics study on the adsorption of perfluorooctanoic acid from aqueous solution onto powdered activated carbon. J. Hazard. Mater., 169: 146-152.
Quinones, O. et Snyder, S.A. (2009). Occurrence of perfluoroalkyl carboxylates and sulfonates in drinking water utilities and related waters from the United States. Environ. Sci. Technol., 43(24): 9089-9095.
Rahman, M.F., Peldszus, S. et Anderson, W.B. (2014). Behaviour and fate of perfluoroalkyl and polyfluoroalkyl substances (PFASs) in drinking water treatment: A review. Water Res. 50:318-340.
Raymer, J.H., Michael, L.C., Studabaker, W.B., Olsen, G.W., Sloan, C.S., Wilcosky, T. et coll. (2012). Concentrations of perfluorooctane sulfonate (PFOS) and perfluorooctanoate (PFOA) and their associations with human semen quality measurements. Reprod. Toxicol., 33(4): 419-427.
Ritter, L., Totman, C., Krishnan, K., Carrier, R., Vézina, A. et Morisset, V. (2007). Deriving uncertainty factors for threshold chemical contaminants in drinking water. J. Toxicol. Environ. Health B Crit. Rev., 10(7): 527-557.
Rosen, M.B., Abbott, B.D., Wolf, D.C., Corton, J.C., Wood, C.R., Schmid, J.E., Das, K.P., Zehr, R.D., Blair, E.T. et Lau, C. (2008). Gene profiling in the livers of wild-type and PPARα-null mice exposed to perfluorooctanoic acid. Toxicol. Pathol., 36: 592-607.
Rosen, M.B., Das, K.P., Wood, C.R., Wolf, C.J., Abbott, B.D. et Lau, C. (2013). Evaluation of perfluoroalkyl acid activity using primary mouse and human hepatocytes. Toxicology, 308: 129-137.
Rosenmai, A.K., Nielsen, F.K., Pedersen, M., Hadrup, N., Trier, X., Christensen, J.H. et coll. (2013). Fluorochemicals used in food packaging inhibit male sex hormone synthesis. Toxicol. Appl. Pharmacol., 266(1): 132-142.
Rumsby, P., McLaughlin, C. et Hall, T.(2009). Perfluorooctane sulphonate and perfluorooctanoic acid in drinking and environmental waters. Phil. Trans. Royal. Soc. 367:4119-4136.
Rusch, G. (1979). An acute inhalation study of T-2305 CoC in the rat. Bio/dynamics, Inc., Study No. 78-7184, May 3, 1979. U.S. Environmental Protection Agency Administrative Record 226-0417. [cité dans OECD (2002); EFSA (2008)].
Sakr, C.J., Kreckmann, K.H., Green, J.W., Gillies, P.J., Reynolds, J.L. et Leonard, R.C. (2007a). Cross-sectional study of lipids and liver enzymes related to a serum biomarker of exposure (ammonium perfluorooctanoate or APFO) as part of a general health survey in a cohort of occupationally exposed workers. J. Occup. Environ. Med., 49(10): 1086-1096.
Sakr, C.J., Leonard, R.C., Kreckmann, K.H., Slade, M.D. et Cullen, M.R. (2007b). Longitudinal study of serum lipids and liver enzymes in workers with occupational exposure to ammonium perfluorooctanoate. J. Occup. Environ. Med., 49(8): 872-879. Erratum dans : J. Occup. Environ. Med.. 49(11):1294.
Sakr, C., Symons, J.M., Kreckmann, K.H. et Leonard, R.C. (2009). Ischaemic heart disease mortality study among workers with occupational exposure to ammonium perfluorooctanoate. Occup. Environ. Med., 66(10): 699-703.
Sanexen Environmental Services Inc. (2013). Review of toxicological information on perfluorooctanoic acid (PFOA) to be used in the technical document for drinking water guidelines. Rapport final du contrat envoyé à Santé Canada.
Santé Canada. (1994). L'évaluation du risque à la santé humaine des substances d'intérêt prioritaire. Santé Canada, Ottawa, Ontario. Disponible à : www.hc-sc.gc.ca/ewh-semt/alt_formats/hecs-sesc/pdf/pubs/contaminants/approach/approach-fra.pdf
Santé Canada (2006). Rapport sur l'état des connaissances scientifiques - Le sulfonate de perfluorooctane, ses sels et ses précurseurs contenant la fraction C8F17SO2 ou C8F17SO3. Disponible à : http://www.hc-sc.gc.ca/ewh-semt/pubs/contaminants/pfos-spfo/index-fra.php
Santé Canada (2010). Rapport sur la biosurveillance humaine des substances chimiques de l'environnement au Canada : Résultats de l'Enquête canadienne sur les mesures de la santé Cycle 1 (2007 à 2009). Disponible à : www.hc-sc.gc.ca/ewh-semt/pubs/contaminants/chms-ecms/index-fra.php
Santé Canada. (2013a). Recherche de l'Enquête national APFO-SPFO 2009 et 2010. Chiffrier Excel. Santé Canada, Ottawa, Ontario.
Santé Canada. (2013b). Deuxième rapport sur la biosurveillance humaine des substances chimiques de l'environnement au Canada: Résultats de l'Enquête canadienne sur les mesures de la santé Cycle 2 (2009 à 2011). Disponible de : www.hc-sc.gc.ca/ewh-semt/pubs/contaminants/chms-ecms-cycle2/index-fra.php
Savitz, D.A., Stein, C.R., Bartell, S.M., Elston, B., Gong, J., Shin, H.M. et coll. (2012a). Perfluorooctanoic acid exposure and pregnancy outcome in a highly exposed community. Epidemiology, 23(3): 386-392.
Savitz, D.A., Stein, C.R., Elston, B., Wellenius, G.A., Bartell, S.M., Shin, H.M. et coll. (2012b). Relationship of perfluorooctanoic acid exposure to pregnancy outcome based on birth records in the Mid-Ohio Valley. Environ. Health Perspect., 120(8): 1201-1207.
Schultz, M., Barofsky, D. and Field, J. (2006). Quantitative determination of fluorinated alkyl substances by large-volume-injection liquid chromatography tandem mass spectrometryscharacterization of municipal wastewaters. Environ. Sci. Technol. 40:289-295.
Seals, R., Bartell, S.M. et Steenland, K. (2011). Accumulation and clearance of perfluorooctanoic acid (PFOA) in current and former residents of an exposed community. Environ. Health Perspect., 119(1): 119-124.
Senevirathna, S.T.M.L.D, Tanaka, S., Fujii, S., Kunacheva, C., Harada, H., Shivakoti, B.R. et Okamoto, R. (2010). A comparative study of adsorption of perfluorooctanesulfonate (PFOS) onto granular activated carbon, ion-exchange polymers and non-ion-exchange polymers. Chemosphere, 80: 647-651.
Senevirathna, S.T.M.L.D, Tanaka, S., Fujii, S., Kunacheva, C., Harada, H., Shivacoti, B., Dinh, H., Ariadas, T. (2011). Adsorption of four perfluorinated acids on non-ion exchange polymers sorbents. Water Sci. Technol., 63(10): 2106.
Shankar, A., Xiao, J. et Ducatman, A. (2012). Perfluorooctanoic acid and cardiovascular disease in US adults. Arch. Intern. Med., 172(18): 1397-1403. Comment in: Arch. Intern. Med. 172(18):1403-1405.
Shivakoti, B.R., Fujii, S., Nozoe, M., Tanaka, S. et Kunacheva, C. (2010). Perfluorinated chemicals (PFCs) in water purification plants (WPPs) with advanced treatment processes. Wa. Sci. Technol, 10(1): 87-95.
Shoeib, M., Harner, T., G, M.W. et Lee, S.C. (2011). Indoor sources of poly- and perfluorinated compounds (PFCS) in Vancouver, Canada: implications for human exposure. Environ. Sci. Technol., 45(19): 7999-8005.
Shoemaker, J., Boutin, B. et Grimmett, P. (2009). Development of a U.S. EPA drinking water method for the analysis of selected perfluoroalkyl acids by solid-phase extraction and LC-MS-MS. J. Chromatogr. Sci., 47(1):3-11.
Sibinski, L.J. (1987). Two-year oral (diet) toxicity/carcinogenicity study of fluorochemical FC-143 in rats. (Riker Experiment No. 0281CR0012). Vol 1-4. Riker Laboratories Inc./3M Company. St. Paul, Minnesota. 8 EHQ-1087-0394. Final Report, October 16, 1987. [cité dans U.S. EPA (2005); EFSA (2008); OECD (2008)]
Sinclair, E., Kim, S.K., Akinleye, H.B. et Kannan, K. (2007). Quantitation of gas-phase perfluoroalkyl surfactants and fluorotelomer alcohols released from nonstick cookware and microwave popcorn bags. Environ. Sci. Technol., 41: 1180-1185. [cité dans ATSDR (2009)].
Singh, T.S., Lee, S., Kim, H.H., Choi, J.K. et Kim, S.H. (2012). Perfluorooctanoic acid induces mast cell-mediated allergic inflammation by the release of histamine and inflammatory mediators. Toxicol. Lett., 210(1): 64-70.
Son, H.Y., Kim, S.H., Shin, H.I., Bae, H.I. et Yang, J.H. (2008). Perfluorooctanoic acid-induced hepatic toxicity following 21-day oral exposure in mice. Arch. Toxicol., 82(4): 239-246.
Sonia, T.A. et Sharma, C.P. (2011). Chitosan and its derivatives for drug delivery perspective. Adv. Polym. Sci., 243: 23-54.
Sonthithai, P., Suriyo, T., Thiantanawat, A., Watcharasit, P., Ruchirawat, M. et Satayavivad, J. (2015). Perfluorinated chemicals, PFOS and PFOA, enhance the estrogenic effects of 17β-estradiol in T47D human breast cancer cells. J. Appl. Toxicol. Accepted for publication. DOI: 10.1002/jat.3210.
Staples, R.E., Burgess, B.A. et Kerns, W.D. (1984). The embryo-fetal toxicity and teratogenic potential of ammonium perfluorooctanoate (APFO) in the rat. Fundam. Appl. Toxicol., 4(3 Pt 1): 429-440.
State of New Jersey (undated). Guidance for PFOA in drinking water at Pennsgrove Water Supply Company. Memorandum. From: Gloria Post, Ph.D., to: Barker Hamill.
Steenland, K. et Woskie, S. (2012). Cohort mortality study of workers exposed to perfluorooctanoic acid. Am J Epidemiol, 176(10): 909-917.
Steenland, K., Tinker, S., Frisbee, S., Ducatman, A. et Vaccarino, V. (2009). Association of perfluorooctanoic acid and perfluorooctane sulfonate with serum lipids among adults living near a chemical plant. Am. J. Epidemiol., 170(10): 1268-1278.
Steenland, K., Fletcher, T. et Savitz, D.A. (2010a). Epidemiologic evidence on the health effects of perfluorooctanoic acid (PFOA). Environ. Health Perspect., 118(8): 1100-1108.
Steenland, K., Tinker, S., Shankar, A. et Ducatman, A. (2010b). Association of perfluorooctanoic acid (PFOA) and perfluorooctane sulfonate (PFOS) with uric acid among adults with elevated community exposure to PFOA. Environ. Health Perspect., 118(2): 229-233.
Stein, C.R. et Savitz, D.A. (2011). Serum perfluorinated compound concentration and attention deficit/hyperactivity disorder in children 5-18 years of age. Environ. Health Perspect., 119(10): 1466-1471.
Stein, C.R., Savitz, D.A. et Dougan, M. (2009). Serum levels of perfluorooctanoic acid and perfluorooctane sulfonate and pregnancy outcome. Am. J. Epidemiol., 170(7): 837-846. Comment in: Am. J. Epidemiol., 171(1):131-132; author reply 132-133.
Steinle-Darling, E. et Reinhard, M. (2008). Nanofiltration for trace organic contaminant removal: structure, solution, and membrane fouling effects on the rejection of perfluorochemicals. Environ. Sci. Technol., 42, 5292-5297.
Stock, N.L., Furdui, V.I., Muir, D.C. et Mabury, S.A. (2007). Perfluoroalkyl contaminants in the Canadian Arctic: evidence of atmospheric transport and local contamination. Environ. Sci. Technol., 41(10): 3529-3536. [cité dans Fromme (2007); Butt (2010)].
Suh, C.H., Cho, N.K., Lee, C.K., Lee, C.H., Kim, D.H., Kim, J.H. et coll. (2011). Perfluorooctanoic acid-induced inhibition of placental prolactin-family hormone and fetal growth retardation in mice. Mol. Cell. Endocrinol., 337(1-2): 7-15.
Summit Toxicology (2015). Interspecies extrapolation for perfluorooctyl sulfonate (PFOS) and perfluorooctanoic acid (PFOA). Summit Toxicology, L.L.P. Report submitted to Health Canada.
Sun., H., LI, F., Zhang, T., Zhang, X., He., N., Song, Q., Zhao, L., Sun, L. et Sun, T. (2011). Perfluorinated compounds in surface waters and WWTPs in Shenyang, China: Mass flows and source analysis. Water Res., 45:4483-4490.
Szostek, B. Prickett, K.B. et Buck, R.C.(2006). Determination of fluorotelomer alcohol by liquid chromatography/tandem mass spectrometry in water. Rapid Commun. Mass Spectrom 20: 2837.
Takagi, S., Adachi, F., Miyano, K., Koizumi, Y., Tanaka, H., Watanabe, I., Tanabe, S. et Kannan, K. (2011). Fate of perfluorooctanesulfonate and perfluorooctanoate in drinking water treatment processes. Water Res., 45( 13): 3925-3932.
Takagi,S., Adachi, F., Miyano, K., Koizumi Ya, Tanaka, H., Mimura, M., Watanabe, I., Tanabe, S. et Kannan, K. (2008). Perfluorooctanesulfonate and perfluorooctanoate in raw and treated tap water from Osaka, Japan. Chemosphere, 72: 1409-1412.
Tan, Y.M., Clewell, H.J., 3 rd et Andersen, M.E. (2008). Time dependencies in perfluorooctylacids disposition in rat and monkeys: a kinetic analysis. Toxicol. Lett., 177(1): 38-47.
Tanaka, S., Fujii, S., Lien, N.P.H., Nozoe, M. Fukagawa, H., Wirojanagud, W., Anton, A. et Lindstrom, G.A. (2006). Simple pretreatment procedure in PFOS and PFOA water analysis and its application in several countries. International Symposium on Halogenated Environmental Organic Pollutants and POPs, Oslo, Norway, August 21-25.
Tang, C.Y., Fu, Q.S., Robertson, A.P., Criddle, C.S. et Leckie, J.O. (2006). Use of reverse osmosis membranes to remove perfluorooctanesulfonate (PFOS) from semiconductor wastewater. Environ. Sci. Technol., 40: 7343-7349.
Tang, C.Y., Shiangfu, Q., Criddle, C.S. et Leckie, J.O. (2007). Effect of flux (transmembrane pressure) and membrane properties on fouling and rejection of reverse osmosis and nanofiltration membranes treating perfluorooctanesulfonate containing wastewater. Environ. Sci. Technol., 41: 2008-2014.
Tang, C., Kwon, Y-N. et Leckie, J. (2009a). Effect of membrane chemistry and coating layer on physiochemical properties of thin film composite polyamide RO and NF membranes I. FTIR and XPS characterization of polyamide and coating layer chemistry. Desalination, 242: 149-167.
Tang, C., Kwon, Y-N. et Leckie, J. (2009b). Effect of membrane chemistry and coating layer on physiochemical properties of thin film composite polyamide RO and NF membranes II. Membrane physiochemical properties and their dependence on polyamide and coating layers. Desalination, 242: 168-182.
Tang, H., Xiang, Q., Lei, M., Yan, J., Zhu, L. et Zou, J. (2012). Efficient degradation of perfluorooctanoic acid by UV-Fenton process. Chem. Eng. J., 184: 156-162.
Taniyasu, S., Kannan, K., So, M.K., Gulkowska, A., Sinclair, E., Okazawa, T. et Yamashita, N. (2005). Analysis of fluorotelomer alcohols, fluorotelomer acids, and short- and long-chain perfluorinated acids in water and biota. J. Chromatogr. A, 1093: 89-97.
Taniyasu, S., Kannan, K., Wu, Q., Kwok, K.Y., Yeung, L.W.Y., Lam, P.K.S., Chittin, B., Kida, T., Takasagu, T., Tsuchiya, Y. et Yamashita, N. (2013). Inter-laboratory trials for analysis of perfluooroocatanesulfonate and perfluorooctanoate in water samples: Performance and recommendations. Anal. Chim. Acta, 770: 111-120.
Tao, L., Kannan, K., Wong, C.M., Arcaro, K.F. et Butenhoff, J.L. (2008). Perfluorinated compounds in human milk from Massachusetts, U.S.A. Environ. Sci. Technol., 42(8): 3096-3101.
Thomford, P.J. (2001a). 26-Week capsule toxicity study with ammonium perfluorooctanoate (APFO) in cynomolgus monkeys. Study performed by Covance Laboratories Inc., Madison Wisconsin 53704-2592 for APME Ad-hoc APFO Toxicology Working Group. Study No. Covance 6329-231, Completion Date December 18, 2001, 463 pp. U.S. Environmental Protection Agency Administrative Record 226-1052a. [cité dans OECD (2008); ATSDR (2009)].
Thomford, P.J. (2001b). 4-Week capsule toxicity study with ammonium perfluorooctanoate (APFO) in cynomolgus monkeys. APME Ad-Hoc APFO toxicology working group. [cité dans OECD (2008)].
Thompson, J., Lorber, M., Toms, L.M., Kato, K., Calafat, A.M. et Mueller, J.F. (2010). Use of simple pharmacokinetic modeling to characterize exposure of Australians to perfluorooctanoic acid and perfluorooctane sulfonic acid. Environ Int., 36(4): 390-397. Erratum in: Environ Int. 36(6): 647-648.
Thompson, J., Eaglesham, G., Reungoat, J., Poussade, Y., Bartkow, M., Lawrence, M., Mueller, J. F. (2011). Removal of PFOS, PFOA and other perfluoroalkyl acids at water reclamation plants in South East Queensland Australia. Chemosphere 82(1), 9-17.
Thomsen, C., Haug, L.S., Stigum, H., Frøshaug, M., Broadwell, S.L. et Becher, G. (2010). Changes in concentrations of perfluorinated compounds, polybrominated diphenyl ethers, and polychlorinated biphenyls in Norwegian breast-milk during twelve months of lactation. Environ. Sci. Technol.., 44(24): 9550-9556. Erratum in: Environ. Sci. Technol.., 45(7):3192.
Tittlemier, S., Ryan, J.J. et VanOostdam, J. (2004). Presence of anionic perfluorinated organic compounds in serum collected from Northern Canadian populations. Organohalogen Compd 66: 4009-4014. [cité dans Health Canada (2006, 2012)].
Tittlemier, S.A., Pepper, K., Seymour, C., Moisey, J., Bronson, R., Cao, X.L. et coll. (2007). Dietary exposure of Canadians to perfluorinated carboxylates and perfluorooctane sulfonate via consumption of meat, fish, fast foods, and food items prepared in their packaging. J. Agric. Food Chem., 55(8): 3203-3210.
Toft, G., Jönsson, B.A., Lindh, C.H., Giwercman, A., Spano, M., Heederik, D. et coll. (2012). Exposure to perfluorinated compounds and human semen quality in Arctic and European populations. Hum. Reprod., 27(8): 2532-2540.
Tsai, Y., Yu-Chen Lin, A., Weng, Y. et Li, K. (2010). Treatment of perfluorinated chemicals by electro-microfiltration. Environ. Sci. Technol., 44(20): 7914-7920.
Tucker, D.K., Macon, M.B., Strynar, M.J., Dagnino, S., Andersen, E. et Fenton, S.E. (2015). The mammary gland is a sensitive pubertal target in CD-1 and C57Bl/6 mice following perinatal perfluorooctanoic acid (PFOA) exposure. Reprod. Toxicol., 54: 26-36.
UK COT (2006). COT statement on the tolerable daily intake for perfluorooctanoic acid. UK Committee on Toxicity of Chemicals in Food, Consumer Products and the Environment. Disponible à : www.food.gov.uk/multimedia/pdfs/cotstatementpfoa200610.pdf
UK HPA (2007). Maximum acceptable concentrations of perfluorooctane sulfonate (PFOS) and perfluorooctanoic acid (PFOA) in drinking water. Disponible à : www.hpa.org.uk/webc/HPAwebFile/HPAweb_C/1194947397222
UK HPA (2009). HPA Compendium of chemical hazards. PFOS + PFOA. Version 1.
U.S.EPA (2005). Draft risk assessment of the potential human health effects associated with exposure to perfluorooctanoic acid and its salts. Office of Pollution Prevention and Toxics Risk Assessment Division. Disponible à : www.epa.gov/oppt/pfoa/pubs/pfoarisk.html
U.S. EPA (2009a). EPA Method 537, Determination of selected perfluorinated alkyl acids in drinking water by solid phase extraction and liquid chromatography/tandem mass spectrometry (LC/MS/MS). Version 1.1. September 2009. EPA/600/R-08/092.
U.S. EPA (2009b). Provisional health advisories for perfluorooctanoic acid (PFOA) and perfluorooctane sulfonate (PFOS). 1-5. US EPA Office of Water.
U.S. EPA (2009c). The toxicity of perfluoroactanoic acid (PFOA) and of percfluorooctanate sulfonate (PFOS). Memorandum. Office of Solid Waste and Emergency Response.
U.S. EPA (2012a). Drinking water treatability database. Disponible à : http://iaspub.epa.gov/tdb/pages/general/home.do.
U.S. EPA (2012b). UCMR3 laboratory approval requirements and information document. Version 2. Technical support center. Standards and Risk Management Division. Office of Groundwater and Drinking Water. U.S. Environmental Protection Agency, Cincinnati, Ohio 45268.
U.S. EPA (2015). Benchmark dose software (BMDS) Version 2.6.0.86 [Build: 2/4/2015]. National Center for Environmental Assessment. Available from: http://bmds.epa.gov
van Leeuwen, S. P. et de Boer, J. (2007). Extraction and clean-up strategies for the analysis of poly-and perfluoroalkyl substances in environmental and human matrices. J. Chromatogr. A, 1153(1-2):172-185.
van Leeuwen, S.P., Karrman, A., van Bevel, B., de Boer, J. et Lindstrom, G. (2006). Struggle of quality in determination of perfluorinated contaminants in environmental and human samples. Environ. Sci. Technol. 40:7854-7860.
van Leeuwen, S.P.J., Stewart, C.P., van der Veen, I., de Boer, J., (2009). Significant improvements in the analysis of perfluorinated compounds in water and fish: Results from an interlaboratory method evaluation study. J. Chromatogr. A, 1216: 401-409.
Vanden Heuvel, J.P., Kuslikis, B.I., Van Rafelghem, M.J. et Peterson, R.E. (1991). Tissue distribution, metabolism, and elimination of perfluorooctanoic acid in male and female rats. J. Biochem. Toxicol., 6(2): 83-92.
Vanden Heuvel, J.P., Thompson, J.T., Frame, S.R. et Gillies, P.J. (2006). Differential activation of nuclear receptors by perfluorinated fatty acid analogs and natural fatty acids: a comparison of human, mouse, and rat peroxisome proliferator-activated receptor-α, -β, and -γ, liver X receptor-β, and retinoid X receptor-α. Toxicol. Sci., 92(2): 476-489.
Vecitis, C.D., Park, H., Cheng, J., Mader, B.T. et Hoffmann, M.R. (2009). Treatment technologies for aqueous perfluorooctanesulfonate (PFOS) and perfluorooctanoate (PFOA). Front. Environ. Sci. Engin. China, 3(2): 129-151.
Vested, A., Ramlau-Hansen, C.H., Olsen, S.F., Bonde, J.P., Kristensen, S.L., Halldorsson, T.I. et coll. (2013). Associations of in utero exposure to perfluorinated alkyl acids with human semen quality and reproductive hormones in adult men. Environ. Health Perspect., 121(4): 453-458.
Vestergaard, S., Nielsen, F., Andersson, A.M., Hjøllund, N.H., Grandjean, P., Andersen, H.R. et coll. (2012). Association between perfluorinated compounds and time to pregnancy in a prospective cohort of Danish couples attempting to conceive. Hum. Reprod., 27(3): 873-880.
Vieira, V.M., Hoffman, K., Shin, H.M., Weinberg, J.M., Webster, T.F. et Fletcher, T. (2013). Perfluorooctanoic Acid exposure and cancer outcomes in a contaminated community: a geographic analysis. Environ. Health Perspect., 121(3): 318-323.
Villagrasa, M., deAlda, M.L. et Barcelo, D. (2006). Environmental analysis of fluorinated alkyl substances by liquid chromatography-(tandem) mass spectrometry: a review. Anal. Bioanal. Chem., 386: 953-972.
Villaverde-de-Saa, E., Fernandez-Lopez, M., Rodil, R., Quintana, J., Racamonde, I. et Cela, R. (2015). Solid phase extraction of perfluoroalkylated compounds from sea water. J. Sep. Sci. 38:1942-1950.
von Ehrenstein, O.S., Fenton, S.E., Kato, K., Kuklenyik, Z., Calafat, A.M. et Hines, E.P. (2009). Polyfluoroalkyl chemicals in the serum and milk of breastfeeding women. Reprod. Toxicol., 27(3-4):239-245.
Wambaugh, J.F., Setzer, R.W., Pitruzzello, A.M., Liu, J., Reif, D.M., Kleinstreuer, N.C., Wang, N.C., Sipes, N., Martin, M., Das, K., DeWitt, J.C., Strynar, M., Judson, R., Houck, K.A. et Lau C. (2013). Dosimetric anchoring of in vivo and in vitro studies for perfluorooctanoate and perfluorooctanesulfonate. Toxicol. Sci., 136(2): 308-327.
Washburn, S.T., Bingman, T.S., Braithwaite, S.K., Buck, R.C., Buxton, L.W., Clewell, H.J. et coll. (2005). Exposure assessment and risk characterization for perfluorooctanoate in selected consumer articles. Environ. Sci. Technol., 39(11): 3904-3910. [cité dans ATSDR (2009)].
Washino, N., Saijo, Y., Sasaki, S., Kato, S., Ban, S., Konishi, K. et coll. (2009). Correlations between prenatal exposure to perfluorinated chemicals and reduced fetal growth. Environ. Health Perspect., 1117(4): 660-667.
Weiß, O., Wiesmüller, G.A., Bunte, A., Göen, T., Schmidt, C.K., Wilhelm, M. et coll. (2012). Perfluorinated compounds in the vicinity of a fire training area--human biomonitoring among 10 persons drinking water from contaminated private wells in Cologne, Germany. Int. J. Hyg. Environ. Health, 215(2): 212-215.
Weremiuk, A. M., Gerstmann, S. et Frank, H. (2006). Quantitative determination of perfluorinated surfactants in water by LC-MS/MS. J. Sep. Sci., 29:2251-2255.
White, S.S., Calafat, A.M., Kuklenyik, Z., Villanueva, L., Zehr, R.D., Helfant, L. et coll. (2007). Gestational PFOA exposure of mice is associated with altered mammary gland development in dams and female offspring. Toxicol. Sci.., 96(1): 133-144.
White, S.S., Kato, K., Jia, L.T., Basden, B.J., Calafat, A.M., Hines, E.P. et coll. (2009). Effects of perfluorooctanoic acid on mouse mammary gland development and differentiation resulting from cross-foster and restricted gestational exposures. Reprod. Toxicol.., 27(3-4): 289-298.
White, S.S., Stanko, J.P., Kato, K., Calafat, A.M., Hines, E.P. et Fenton, S.E. (2011). Gestational and chronic low-dose PFOA exposures and mammary gland growth and differentiation in three generations of CD-1 mice. Environ. Health Perspect., 119(8): 1070-1076.
Whitworth, K.W., Haug, L.S., Baird, D.D., Becher, G., Hoppin, J.A., Skjaerven, R. et coll. (2012a). Perfluorinated compounds in relation to birth weight in the Norwegian Mother and Child Cohort Study. Am. J. Epidemiol., 175(12): 1209-1216.
Whitworth, K.W., Haug, L.S., Baird, D.D., Becher, G., Hoppin, J.A., Skjaerven, R. et coll. (2012b). Perfluorinated compounds and subfecundity in pregnant women. Epidemiology, 23(2): 257-263. Comment in: Epidemiology, 23(2):264-266.
Wilhelm, M., Kraft, M., Rauchfuss, K. et Holzer, J. (2008) Assessment and management of the first German case of a contamination with perfluorinated compounds (PFC) in the region Sauerland, North Rhine Westphalia. J. Toxicol. Environ. Health A,71(11-12): 725-733.
Wilhelm, M., Kraft, M., Rauchfuss, K. et Hölzer, J. (2008). Assessment and management of the first German case of a contamination with perfluorinated compounds (PFC) in the Region Sauerland, North Rhine-Westphalia. J Toxicol Environ Health A, 71(11-12): 725-733.
Winquist, A. et Steenland, K. (2014). Modeled PFOA exposure and coronary artery disease, hypertension, and high cholesterol in community and worker cohorts. Environ. Health Perspect.., 122(12): 1299-1305.
Wolf, S. et Reagen, W. (2011). Method for the determination of perfluotrinated compounds (PFCs) in water by solid-phase extraction and liquid chromatography/tandem mass spectrometry (LC/MS/MS). Anal. Methods, 3:1485-1493.
Wolf, C.J., Fenton, S.E., Schmid, J.E., Calafat, A.M., Kuklenyik, Z., Bryant, X.A. et coll. (2007). Developmental toxicity of perfluorooctanoic acid in the CD-1 mouse after cross-foster and restricted gestational exposures. Toxicol. Sci.., 95(2): 462-473.
Wolf, D.C., Moore, T., Abbott, B.D., Rosen, M.B., Das, K.P., Zehr, R.D., Lindstrom, A.B., Strynar, M.J. et Lau, C. (2008). Comparative hepatic effects of perfluorooctanoic acid and WY 14,643 in PPAR-α knockout and wild-type mice. Toxicol. Pathol., 36: 632-639.
Xiao, F., Davidsavor, K.J., Park, S., Nakayama, M.. et Phillips, B.R. (2012). Batch and column study: sorption of perfluorinated surfactants from water and co-solvent systems by Amberlite XAD resins. J. Colloid Interface Sci., 368: 505-511.
Xiao, F., Simcik, M.F. et Gulliver, J.S. (2013). Mechanisms for removal of perfluorooctanesulfonate (PFOS) and perfluorooctanoate (PFOA) from drinking water by conventional and enhanced coagulation. Water Res., 47: 49-56.
Xu, Y., Noonan, G.O. et Begley, T.H. (2013). Migration of perfluoroalkyl acids from food packaging to food simulants. Food Addit. Contam Part A, 30(5): 899-908.
Yahia, D., El-Nasser, M.A., Abedel-Latif, M., Tsukuba, C., Yoshida, M., Sato, I. et coll. (2010). Effects of perfluorooctanoic acid (PFOA) exposure to pregnant mice on reproduction. JToxicol. Sci.., 35(4): 527-533.
Yamashita, N., Kannan, K., Taniyasu, S., Horii, Y., Okazawa, T., Petrick, C. et Gamo, T. (2004). Analysis of perflulorinated acids at parts per quadrillion levels in seawater using liquid chromatograph tandem mass spectrometry. Environ. Sci. Technol. 38: 5522-5528.
Yang, Q., Xie, Y., Eriksson, A.M., Nelson, B.D. et DePierre, J.W. (2001). Further evidence for the involvement of inhibition of cell proliferation and development in thymic and splenic atrophy induced by the peroxisome proliferator perfluoroctanoic acid in mice. Biochem. Pharmacol., 62(8): 1133-1140.
Yang, Q., Xie, Y., Alexson, S.E.H., Dean Nelson, B. et DePierre, J.W. (2002). Involvement of the peroxisome proliferator-activated receptor alpha in the immunomodulation caused by peroxisome proliferators in mice. Biochem. Pharmacol., 63(10): 1893-1900.
Yang, C.-H., Glover, K.P. et Han, X. (2009a). Organic anion transporting polypeptide (Oatp) 1a1-mediated perfluorooctanoate transport and evidence for a renal reabsorption mechanism of Oatp1a1 in renal elimination of perfluorocarboxylates in rats. Toxicol. Lett., 190(2): 163-171.
Yang, C., Tan, Y.S., Harkema, J.R. et Haslam, S.Z. (2009 b). Differential effects of peripubertal exposure to perfluorooctanoic acid on mammary gland development in C57Bl/6 and Balb/c mouse strains. Reprod. Toxicol., 27(3-4):299-306.
Yang, C.-H., Glover, K.P. et Han, X. (2010). Characterization of cellular uptake of perfluorooctanoate via organic anion-transporting polypeptide 1a2, organic anion transporter 4, and urate transporter 1 for their potential roles in mediating human renal reabsorption of perfluorocarboxylates. Toxicol. Sci., 117(2): 294-302.
Ylinen, M., Kojo, A., Hanhijarvi, H. et Peura, P. (1990). Disposition of perfluorooctanoic acid in the rat after single and subchronic administration. Bull. Environ. Contam. Toxicol., 44(1): 46-53.
York, R.G. (2002). Oral (gavage) two-generation (one litter per generation) reproduction study of ammonium perfluorooctanoic (APFO) in rats. Argus Research Laboratories, Inc. Protocol Number: 418-020, Sponsor Study Number: T-6889.6, March 26, 2002. U.S. EPA AR226-1092. [cité dans U.S. EPA (2005)].
York, R.G., Kennedy, G.L., Jr., Olsen, G.W. et Butenhoff, J.L. (2010). Male reproductive system parameters in a two-generation reproduction study of ammonium perfluorooctanoate in rats and human relevance. Toxicology, 271(1-2): 64-72.
Yu, Q., Deng, S. et Yu, G. (2008). Selective removal of perfluorooctanesulfonate from aqueous solution using chitosan-based molecularly imprinted polymer adsorbents. Water Res.,.42(12): 3089-3097.
Yu, Q., Zhang, R., Deng, S., Huanga, J. et Yu, G. (2009). Sorption of perfluorooctane sulfonate and perfluorooctanoate on activated carbons and resin: Kinetic and isotherm study. Water Res., 43(4): 1150-1158.
Zainuddin, K., Zakaria, M. P., Al-Odaini, N., Bakhtiari, A.R et Latif, P.A.,(2012). Perfluorooctanoic acid (PFOA) and perfluorooctan sulfonate (PFOS) in surface water from the Langat river, Peninsular Malaysia. Environ. Forensic, 13:82-92.
Zareitalabad, P., Siemens, J., Hamer, M. et Amelung, W. (2013). Perfluorooctanoic acid (PFOA) and perfluorooctanesulfonic acid (PFOS) in surface waters, sediments, soils and wastewater - A review on concentrations and distribution coefficients. Chemosphere, 91(6): 725-732.
Zhao, Y., Tan, Y.S., Haslam, S.Z. et Yang, C. (2010). Perfluorooctanoic acid effects on steroid hormone and growth factor levels mediate stimulation of peripubertal mammary gland development in C57BL/6 mice. Toxicol. Sci.., 115(1): 214-224.
Zhao, L-M., Shi, L-E., Zhang, J-L., Chen, J-M., Shi, D-D., Yang, J. et Tang, Z-X. (2011a). Preparation and application of chitosan nanoparticles and nanofibers. Braz. J. Chem. Eng., 28(3):353.
Zhao, G., Wang, J., Wang, X., Chen, S., Zhao, Y., Gu, F. et coll. (2011b). Mutagenicity of PFOA in mammalian cells: role of mitochondria-dependent reactive oxygen species. Environ. Sci. Technol.., 45(4): 1638-1644.
Zhao, Y., Tan, Y.S., Strynar, M.J., Perez, G., Haslam, S.Z. et Yang, C. (2012). Perfluorooctanoic acid effects on ovaries mediate its inhibition of peripubertal mammary gland development in Balb/c and C57Bl/6 mice. Reprod. Toxicol., 33(4): 563-576.
Annexe A : Élimination de l'APFO dans les usines de traitement d'eau potable de pleine grandeur - données rapportées
| Source d'eau | Chaîne de traitementNote de bas de page 1 | Concentration dans l'influentNote de bas de page 2 (ng/L) | Concentration dand l'eau traitéeNote de bas de page 2 (ng/L) | % d'élimination de l'APFO | Référence |
|---|---|---|---|---|---|
| Eau souterraine | DBF, UV, Cl2 | 10 | 9,4 | 6 | Quinones et Snyder, 2009 |
| Eau de surface | O3, COA/FLOC, DBF, Cl2 | 1,4 | 1,4 | 0 | Quinones et Snyder, 2009 |
| Eau de surface | PAC, CHLM, DBF | 1,7 | 1.9 | -12 | Quinones et Snyder, 2009 |
| Eau de surface | Cl2, COA/FLOC, DBF, UV | 22 | 22 | 0 | Quinones et Snyder, 2009 |
| Installation de réutilisation indirecte à titre d'eau potable | MF/OI, UV/H2O2, BF | 41 | ND | 100 | Quinones et Snyder, 2009 |
| Installation de réutilisation indirecte à titre d'eau potable | Cl2, DL, BF | 29 | 57 | -97 | Quinones et Snyder, 2009 |
| Eau fluviale | FRS, O3, CAG, Cl2 | 1,0 (été) | 0,93 (été) | 7 | Takagi et coll., 2008 |
| Eau fluviale | FRS, O3, CAG, Cl2 | 0,87 (été) 3,2 (hiver) |
2,8 (été) 1,6 (hiver) |
-222 (été) 50 (hiver) |
Takagi et coll., 2008 |
| Eau fluviale | FRS, O3, CAG, Cl2 | Takagi et coll., 2008 | |||
| Eau de lac | FRS, CAG, Cl2 | 4,6 (été) 4,5 (hiver) |
0,16 (été) <0,1 (hiver) |
97 (été) >98 (hiver) |
Takagi et coll., 2008 |
| Eau fluviale, de lac, souterraine (7 usines) | FRS, Cl2 | 0,56 - 22 (été) 0,54 - 4.2 (hiver) |
0,45 - 22 (été) 0,37 - 4.5 (hiver) |
20 - 0 (été) 31 à -7 (hiver) |
Takagi et coll., 2008 |
| Eau fluviale | Membranes, Cl2 | 0,37 (été) 0,26 (hiver) |
0,29 (été) 0,20 (hiver) |
22 (été) 23 (hiver) |
Takagi et coll., 2008 |
| Eau de lac | FLS, Cl2 | 2,7 (été) 1,8 (hiver) |
2.3 (été) 1,9 (hiver) |
15 (été) -6 (hiver) |
Takagi et coll., 2008 |
| Eau fluviale | COA/FLOC/SED, FS, O3, CAG, Cl2 | 1,3 (été) 3,3 (hiver) |
3,7 (été) 1,3 (hiver) |
-185 (été) 60 (hiver) |
Takagi et coll., 2011 |
| Eau fluviale | COA/FLOC/SED, FS, O3, CAG, Cl2 | 1,6 (été) 3,3 (hiver) |
2,3 (été) 1,7 (hiver) |
44 (été) 48 (hiver) |
Takagi et coll., 2011 |
| Eau fluviale | COA/FLOC/SED, FS, O3, CAG, Cl2 | 1,2 (été) 2,8 (hiver) |
1,6 (été) 1,9 (hiver) |
-33 (été) 32 (hiver) |
Takagi et coll., 2011 |
| Eau fluviale | SED, O3, CAG, Cl2, FS | 1.4 (été) 3,3 (hiver) |
2,2 (été) 2,0 (hiver) |
-57 (été) 39 (hiver) |
Takagi et coll., 2011 |
| Eau de lac | COA/FLOC/SED, FS, CAG (réactivé), Cl2 | 4,4 (été) 4,1 (hiver) |
<0,5 (été) <0,5 (hiver) |
>89 (été) >88 (hiver) |
Takagi et coll., 2011 |
| Eau souterraine | UF, Cl2 | 16 | 16 | 0 | Atkinson et coll., 2008 |
| Eau souterraine | CAG (pas en activité), super chloration et déchloration | 135 | 130 | 3 | Atkinson et coll., 2008 |
| Eau souterraine | CAG (2 chaînes des CAG parallèles comportant chacune 6 fûts; les contacteurs sont matures et agissent comme des contacteurs biologiques; n'ont pas été regénérés pendant quelques années), Cl2 | 42 | 45 | -7 | Atkinson et coll., 2008 |
| Eau souterraine et de surface (60:40) | FLS, O3, CAG (6 fûts-aucune regénération pendant plusieurs années), Cl2 à l'aide de NaOCl- | 20, 6 | 25 | -21 | Atkinson et coll., 2008 |
| Eau souterraine | Cl2 à l'aide de NaOCl | Atkinson et coll., 2008 | |||
| Eau fluviale | COA/FLOC/SED, O3, CAG, FRS | 5,3 (août) 5,8 (oct.) |
9,4 (août) 6,4 (oct.) |
-77 (août) -10 (oct.) |
Shivakoti et coll., 2010) |
| Eau fluviale | COA/FLOC/SED, O3, CAG, FRS | 5,8 (août) 8,8 (oct.) |
3,9 (août) 4,2 (oct.) |
33 (août) 53 (oct.) |
Shivakoti et coll., 2010) |
| Eaux usées traitées | Dénitrification, pre-O3, COA/FLOC/SED, FAD, O3, CAG (agit comme un disque biologique), O3 | 2,2 (oct.)
3,7 (nov.) 3,6 (nov.) |
<NR (0,3) (oct.)
0,6 (nov.) 0,7 (nov.) |
100 (oct.)
84 (nov.) 81 (nov.) |
Thompson et coll., 2011 b |
| Eau fluviale | COA/FLOC/SED, FRS, Cl2 | 5,02 | 0,73 | 85 | Kunacheva et coll., 2010) |
| Eaux usées traitées | Clarificateur/ décanteur laminaire (FeCl3&(NH4)2SO4, ajout de NaOCl), UF, OI, UV+H2O2, stabilisation/ désinfection (ajout de chaux, CO2, NaOCl) |
38
39 23 |
<NR (0,5)
ND <NR (0,2) |
100
100 100 |
Thompson et coll., 2011 |
| Eau fluviale | COA/FLOC, FRS, O3, CAG, FLS | 8,2 | <0,23 | <97 | Eschauzer et coll., 2012 |
| Eau fluviale | Cl2, COA/FLOC, FRS, O3, CAG | 116 | 33 | 69 | Flores et coll., 2013 |
| Eau fluviale | Cl2, COA/FLOC, FRS, O3, CAG, UF, OI | 86 | 13 | 86 | Flores et coll., 2013 |
|
|||||
Annexe B : Liste des acronymes
- AFFF
- mousse à formation de pellicule aqueuse
- ALT
- alanine transaminase
- APFA
- acides perfluoroalkyliques
- APFC
- acides perfluorocarboxyliques à longue chaîne
- APFO
- acide perfluorooctanoïque
- AQT
- apport quotidien tolérable
- BMD
- dose de référence
- BMDL
- limite de confiance inférieure de la dose de référence
- BMDL 10
- limite de confiance inférieure à 95 % de la dose de référence pour une réponse de 10 %
- CAG
- charbon actif en grains
- CAP
- charbon actif en poudre
- CAS
- Chemical Abstracts Service
- CL
- chromatographie liquide
- CLHP
- chromatographie liquide à haute performance
- CMA
- concentration maximale acceptable
- DGM
- développement des glandes mammaires
- LOAEL
- dose minimale avec effet nocif observé
- NOAEL
- dose sans effet nocif observé
- EAF
- échangeur d'anions faible
- EAT
- étude sur l'alimentation totale
- ELL
- extraction liquide-liquide
- EPA
- Environmental Protection Agency (É.U.)
- EPS
- extraction en phase solide
- FASC
- facteur d'ajustement propre aux substances chimiques
- FB
- filtration par les berges
- IC
- intervalle de confiance
- ID
- injection directe
- IE
- ionisation par électronébulisation
- ISO
- Organisation internationale de normalisation
- JAN
- jour après la naissance
- JG
- jour de gestation
- LD
- limite de détection
- LD
- limite de dosage
- LDM
- limite de détection de la méthode
- LQ
- limite de quantification
- MA
- mode d'action
- MG
- moyenne géométrique
- MG/J
- millions de gallons par jour
- MON
- matières organiques naturelles
- NF
- nanofiltration
- OI
- osmose inverse
- PBPK
- pharmacocinétique à base physiologique
- PDD
- point de départ
- PDD EQH
- points de départ équivalents pour les humains
- PEFT polytétrafluoroéthylène
- PFA
- perfluoroalkyle
- PFOA
- perfluorooctanoate d'ammonium
- PI
- piège à ions
- PTFE
- polytétrafluoroéthylène
- SM/SM
- spectrométrie de masse en tandem
- SMNR
- seuil minimal de niveau à rapporter
- SPFA
- substances perfluoroalkyliques
- SPFO
- sulfonate de perfluorooctane
- TCFV
- temps de contact en fût vide
- UCMR3
- Third Unregulated Contaminant Monitoring Rule (É.U.)
- VBS
- valeur basée sur la santé
- VL
- volume de lit
Annexe C : Répercussions prévues par province et territoire
Veuillez noter que l'information suivante n'est pas dans les deux langues officielles puisque la source de l'information n'est pas assujettie à la Loi sur les langues officielles.
- Île-du-Prince-Édouard
- Aucun paragraphe n'a été soumis par la province.
- Terre-Neuve-et-Labrador
- Newfoundland and Labrador has not conducted monitoring for PFOA. Of the 305 surface water sources in the province, 258 (85%) are protected under the Water Resources Act. Of the 198 groundwater sources in the province, 59 (30%) are protected under the Water Resources Act. This provides for an extensive source water protection program that reduces the risk of contamination for drinking water sources.
As noted in the technical document, PFOA does not naturally occur in the environment and would only be relevant to areas that are subjected to industrial activities. The main cause for concern in NL would be the short-term use of fire-fighting foams for either property or forest fires.
The majority of Newfoundland and Labrador's drinking water systems do not have any treatment other than disinfection as 68% of the systems service very small populations (less than 500 people). Due to this fact, the ability for the majority of communities to treat for PFOA contamination would be limited. The cost would have to be assessed on a case by case basis but the risk of PFOA formation would be low to the protection of public water supplies.
The province will consider monitoring for PFOA if/when fire-fighting foams are utilized in public drinking water supply areas and is deemed relevant and if/when fire-fighting foams are utilized in single-dwelling homes on private wells when deemed relevant. - Nouvelle-Écosse
- Aucun paragraphe n'a été soumis par la province.
- Nouveau-Brunswick
- PFOA is not monitored in New Brunswick and it is not anticipated that this Guideline would have any impact on regulated drinking water facilities. However, we would have to consult with stakeholders to determine if source water characterization would be necessary and the associated impacts related to costs and the availability of analytical testing. If it was found in source waters this could result in an impact to that facility in terms of additional monitoring or treatment requirements.
- Québec
- Au Québec, étant donné que le PFOA ne fait pas l'objet d'une norme au Règlement sur la qualité de l'eau potable, les résultats disponibles découlent des campagnes d'échantillonnage réalisées par le Ministère dans le cadre Programme de surveillance de la qualité de l'eau potable.
Les résultats disponibles indiquent de très faibles concentrations mesurées de ce paramètre, très en-deçà de la CMA proposée. Plus précisément, en 2007 et 2008, 84 analyses de PFOA ont été réalisées à l'eau traitée de 7 installations de production d'eau potable alimentées en eau de surface. Ces installations avaient été sélectionnées puisqu'elles étaient localisées à des endroits où l'on était susceptible de détecter ces substances (ex. : villes d'importance en amont, présence d'industries de textiles). Les résultats indiquent que 75 % des échantillons prélevés ont présenté un résultat supérieur à la limite de détection et le PFOA a été détecté à au moins une occasion à l'eau traitée de toutes les installations échantillonnées. La concentration maximale mesurée était de 0,073 µg/L, ce qui est bien inférieur à la CMA proposée de 0,2 µg/L.
Considérant les résultats d'analyse disponibles, les impacts attendus de l'ajout d'une norme pour le PFOA à la réglementation, en fonction de la recommandation publiée par Santé Canada, seraient faibles. - Ontario
- Aucun paragraphe n'a été soumis par la province.
- Manitoba
- Aucun paragraphe n'a été soumis par la province.
- Saskatchewan
- The Water Security Agency (WSA) has reviewed the proposed guideline document for perfluorooctanoic acid (PFOA) in drinking water and agrees with the proposed MAC of 0.2 micrograms/L for PFOA in drinking water. A review of exposure data in drinking water/surface water in our database showed that there is no data for this compound in raw/treated water of the municipalities regulated by the WSA. Although, PFOA does not occur naturally in the environment and since its use is limited only to specialized applications, as noted in the guidelines Canadians can be exposed to PFOA in food, consumer products, dust and drinking water. The WSA notes that there are many challenges in analyzing for PFOA including the need for selection of an appropriate analytical method, appropriate analytical QA/QC measures, potentially high analytical cost, and no routine analytical laboratory capacity in Saskatchewan for PFOA, although some specialized research facilities with analytical capability does exist within the province. Since research has shown that treatment systems such as GAC filtration systems, membrane filtration systems are promising and effective in removing PFOA (some studies showed that the removal efficiency ranged between 95% and 99% for GAC and membrane systems) from drinking water, and since these types of treatment systems are in existence or are increasingly being adopted by the water treatment plants (WTPs) in the province, the WSA believes and expects that the new drinking water standard for PFOA can be achieved. Cost to some waterworks owners in the province where appropriate treatment technology does not already exist is anticipated if the guideline is adopted as a standard in Saskatchewan. Before adoption of a drinking water standard for PFOA in the province, local data collection is needed to fully assess the impact on waterworks in the province.
- Alberta
- Aucun paragraphe n'a été soumis par la province.
- Colombie-Britannique
- Aucun paragraphe n'a été soumis par la province.
- Yukon
- It is not anticipated that the proposed Guideline Technical Document for PFOA for consultation will have a significant impact on Yukon large public drinking water systems.
- Territoires du Nord-Ouest
- Aucun paragraphe n'a été soumis par le territoire.
- Nunavut
- Aucun paragraphe n'a été soumis par le territoire.