Recommandations pour la qualité de l'eau potable au Canada : document technique – benzo[a]pyrène
Notes
Table des matières
- Partie I. Vue d'ensemble et application
- Partie II. Science et considérations techniques
- 4.0 Propriétés, utilisations et sources dans l'environnement
- 5.0 Exposition
- 6.0 Méthodes d'analyse
- 7.0 Considérations relatives aux techniques de traitement et aux réseaux de distribution
- 7.1 Échelle municipale
- 7.2 Échelle résidentielle
- 8.0 Cinétique et métabolisme
- 9.0 Effets sur la santé
- 10.0 Classification et évaluation
- 11.0 Justification
- 12.0 Références
- Annexe A : Liste des acronymes
Partie I. Vue d'ensemble et application
1.0 Recommandation
Une concentration maximale acceptable (CMA) de 0,000 04 mg/L (0,04 µg/L) est établie pour le benzo[a]pyrène (BaP) dans l'eau potable.
2.0 Sommaire
En général, les concentrations de benzo[a]pyrène (BaP) dans l'eau potable sont très faibles au Canada. Il n'existe aucune utilisation industrielle ou commerciale du BaP au Canada, mais il est courant de le trouver dans l'environnement parce qu'il est généré par la combustion incomplète de la matière organique. On connaît des sources naturelles d'émissions de BaP (p. ex., les incendies de forêt, l'activité volcanique), mais les sources anthropiques telles que la combustion de combustibles fossiles, le chauffage résidentiel au bois, le bois traité à la créosote et les émissions des fours à coke en sont les principales sources d'émission dans l'environnement. On trouve du BaP tant dans les eaux de surface que dans les eaux souterraines, mais sa présence dans l'eau potable est principalement attribuable à son relargage à partir du revêtement des réservoirs de stockage de l'eau et des canalisations de distribution.
Dans le présent document technique, on recense et on évalue tous les risques que pose la présence de BaP dans l'eau potable pour la santé. On y intègre de nouvelles études et méthodologies, et on prend en considération la disponibilité des méthodes d'analyse et des techniques de traitement appropriées. Sur la base de cet examen, la recommandation pour le BaP dans l'eau potable est une concentration maximale acceptable (CMA) de 0,000 04 mg/L (0,04 μg/L).
2.1 Effets sur la santé
Le Centre international de Recherche sur le Cancer (CIRC) a classé le BaP dans le groupe 1, c'est-à-dire les substances cancérogènes pour l'homme, en se fondant sur des données suffisantes chez les animaux et des données solides indiquant que les mécanismes du cancer observé chez les animaux s'appliquent également à l'homme. Les études limitées menées chez les humains semblent indiquer l'existence d'un risque accru de cancer pour les personnes exposées à des mélanges de substances contenant du BaP, c'est-à-dire les personnes consommant de la viande calcinée, celles travaillant dans les fours à coke et les fumeurs. Chez le rongeur, l'exposition à long terme au BaP a induit divers types de tumeurs du préestomac, du foie, de l'œsophage, des poumons, de la langue, du larynx, de la cavité buccale, de la peau et des glandes mammaires. L'évaluation des risques de cancer a été fondée sur les tumeurs du préestomac (utilisées comme substitut pour tous les effets cancérogènes) observées chez les souris femelles.
Outre le cancer, on a noté divers effets sur la santé attribuables à l'exposition au BaP chez le rongeur, dont des effets neurologiques et sur le développement neurologique, et cela, à de faibles niveaux d'exposition. Cette évaluation considère les risques de cancer et d'effets autres que le cancer. La CMA pour le BaP dans l'eau potable est fondée sur l'évaluation des risques de cancer parce que celle-ci est plus protectrice et qu'il existe un plus haut niveau de confiance pour les effets cancérogènes du BaP que pour ses effets non cancérogènes.
2.2 Exposition
Les Canadiens peuvent être exposés au BaP par l'intermédiaire des aliments, de l'air, des produits de consommation, de l'eau potable, du sol et, dans certains cas, de leurs milieux de travail. Les aliments (p. ex., la viande calcinée) sont la principale source d'exposition au BaP. Il est rare que l'on détecte du BaP dans les approvisionnements d'eau potable au Canada, et lorsque cela se produit, les quantités détectées sont généralement faibles. Comme le BaP n'est pas volatil et qu'il n'est pas facilement absorbé par la peau, on a considéré que la contribution des expositions par voie cutanée et par inhalation à l'exposition globale par l'eau potable était négligeable.
2.3 Analyse et traitement
Lorsque l'on établit une recommandation pour la qualité de l'eau potable, il faut prendre en compte la capacité de mesurer le contaminant dans l'approvisionnement en eau potable et celle de l'en éliminer. On dispose de méthodes d'analyse permettant de mesurer de manière fiable le BaP présent dans l'eau potable à des niveaux inférieurs à la CMA.
Il existe des techniques de traitement tant à l'échelle municipale qu'à l'échelle résidentielle qui permettent de ramener les concentrations de BaP dans l'eau à des niveaux inférieurs à la CMA. La meilleure technique dont on dispose pour enlever le BaP de l'eau potable est le charbon actif en grains. À l'échelle municipale, les techniques existantes qui devraient être en mesure d'atteindre systématiquement des concentrations de BaP inférieures à la CMA sont le traitement conventionnel, le charbon actif en grains et le charbon actif en poudre.
À l'échelle résidentielle, même s'il n'existe pas actuellement de dispositifs de traitement certifiés pour l'élimination du BaP, les dispositifs de traitement faisant appel à des techniques telles que le charbon actif pourraient diminuer les concentrations de BaP dans l'eau potable à des valeurs inférieures à la CMA.
3.0 Application de la recommandation
Remarque : Des instructions spécifiques concernant l'application des recommandations doivent être obtenues auprès de l'autorité appropriée en matière d'eau potable dans le secteur de compétence concerné.
Le BaP est cancérogène pour l'homme, et l'exposition à quelque concentration que ce soit du produit, par l'intermédiaire de quelque milieu d'exposition que ce soit, y compris l'eau potable, peut accroître le risque de cancer. La recommandation pour l'eau potable est fondée sur une exposition pendant la vie entière (70 ans) au BaP dans l'eau potable.
La recommandation concernant un cancérogène est généralement établie à une concentration à laquelle l'accroissement du risque de cancer est considéré comme étant « essentiellement négligeable » pour une exposition pendant la vie entière à cette concentration dans l'eau potable. Dans le cadre des recommandations pour l'eau potable, Santé Canada entend par « essentiellement négligeable » une plage allant d'un nouveau cas de cancer de plus que le niveau de fond pour 100 000 personnes à un nouveau cas de cancer de plus que le niveau de fond pour un million de personnes (c.-à-d. 10-5 à 10-6). On vise un accroissement du risque de cancer de 10-6 lorsque l'exposition par d'autres sources que l'eau potable est significative. Dans le cas du BaP où les aliments constituent la principale source d'exposition, la CMA de 0,000 04 mg/L correspond à la concentration qui présenterait un risque essentiellement négligeable d'un nouveau cas de cancer de plus que le niveau de fond pour un million de personnes (c.-à-d. 10−6) exposées au BaP dans l'eau potable à sa CMA pendant toute une vie.
Dans le cas d'approvisionnements en eau potable où on enregistre des dépassements transitoires de la CMA, on conseille d'élaborer et de mettre en œuvre un plan pour remédier à ces situations. Dans le cas de dépassements prolongés qui ne peuvent être résolus par le biais de traitements, on devrait envisager d'utiliser une autre source d'eau potable.
3.1 Surveillance
Il faudrait effectuer une analyse des sources d'eau pour déterminer si elles contiennent du BaP. Une surveillance trimestrielle devrait être effectuée lorsque les eaux de surface sont touchées par des effluents d'eaux usées municipales, les eaux usées d'une raffinerie de pétrole ou des déversements d'hydrocarbures. De plus, les sources d'eau de surface qui ont été ou sont susceptibles d'avoir été contaminées par des dépôts d'hydrocarbures aromatiques polycycliques (HAP) (p. ex., à cause d'un incendie de forêt) devraient faire l'objet d'une surveillance. Une surveillance devrait aussi être effectuée sur les eaux souterraines affectées par une contamination de pétrole ou de HAP. Les services publics qui ont des données de base démontrant l'absence de BaP peuvent effectuer une surveillance moins fréquente.
Même si les composants et les revêtements du réseau de distribution doivent maintenant être conformes à des normes limitant le relargage de contaminants, les canalisations de distribution et les réservoirs de stockage installés avant 1980 peuvent libérer du BaP si des produits de goudron de houille (bitume) ou d'asphalte ont été employés pour les enduire. Il est recommandé de surveiller la présence de BaP et d'autres HAP dans les réseaux de distribution possédant ce type de revêtement. Une surveillance trimestrielle devrait être assurée à l'égard du BaP dans les secteurs du réseau de distribution où un revêtement de goudron de houille est susceptible d'avoir été utilisé, en particulier aux endroits où le temps de séjour est le plus long (p. ex., dans les culs-de-sac) ou lorsque ces secteurs connaissent des perturbations hydrauliques (p. ex., le remplacement d'une conduite principale). Les services publics qui ont des données de base démontrant l'absence de BaP dans le réseau de distribution peuvent effectuer une surveillance moins fréquente. Les autorités peuvent envisager de réduire l'échantillonnage si un protocole de rinçage approprié est en place.
3.2 Mesures d'atténuation
Dans les réseaux de distribution exploités de manière à favoriser la qualité de l'eau et à diminuer au maximum l'âge de l'eau, les rejets de BaP seront eux aussi minimaux. On recommande l'adoption des mesures ci-dessous pour aider à réduire la concentration de BaP issue du réseau de distribution :
- Appliquer les désinfectants aux doses requises.
- Éviter les variations du régime hydraulique et les coups de bélier. Des variations de la pression de l'eau de plus de 3 bar (45 psi) peuvent entraîner la mobilisation de particules contenant des HAP.
- Réduire le temps de séjour de l'eau dans le réseau de distribution. Les périodes de stagnation de plus de sept heures peuvent augmenter les concentrations de HAP.
- Rincer systématiquement le réseau de distribution pour s'assurer d'éliminer les particules s'y trouvant.
Partie II. Science et considérations techniques
4.0 Propriétés, utilisations et sources dans l'environnement
Le benzo[a]pyrène (BaP) (numéro de registre du Chemical Abstracts Service : 50-32-8) est une molécule relativement grosse faisant partie de la classe des hydrocarbures aromatiques polycycliques (HAP). Il compte cinq cycles non substitués. Il s'agit du HAP le mieux étudié. Sa formule chimique est C20H12, et sa masse moléculaire de 252,3 g/mol. Le BaP et d'autres HAP sont générés par la combustion ou la pyrolyse incomplète de matière organique. À pression et température ambiantes, le BaP est un solide jaune pâle relativement stable dégageant une faible odeur aromatique. Le BaP n'est pas facilement volatil ou réactif. Sa plage de fusion se situe entre 176,5 °C et 179,3 °C et sa plage d'ébullition entre 310 °C et 495 °C, et sa constante de la loi d'Henry est de 4,57 × 10−7 à 25 °C. Les coefficients de partage octanol-eau (log Koe) indiqués pour le BaP sont relativement élevés, se situant entre 5,97 et 6,35 (CIRC, 2010; OEHHA, 2010; HSDB, 2011; CHEMFATE, 2013; U.S. EPA, 2013). La solubilité du BaP dans l'eau est limitée (0,001 62 mg/L à 25 °C), mais le produit est très soluble dans les solvants organiques, notamment le chloroforme, le benzène, le toluène et le xylène (CIRC, 2010; HSDB, 2011; CHEMFATE, 2013; U.S. EPA, 2013). On n'a trouvé aucune donnée sur les seuils olfactif et gustatif du BaP (ATSDR, 1995; OEHHA, 2010).
Les HAP sont très répandus dans l'environnement, généralement à de faibles concentrations, bien qu'elles puissent être élevées à proximité des sources de HAP. Ils n'ont pas d'utilisation industrielle, et on ne les fabrique pas. Cependant, ils sont produits de manière naturelle lors des incendies de forêt et des éruptions volcaniques, et en plus grande quantité de manière anthropique, notamment par la combustion de combustibles fossiles, les émissions des fours à coke et les pratiques de gestion agricole. La source la plus importante est la combustion du bois dans les habitations; d'autres sources de HAP affectant les eaux de surface comprennent les dépôts atmosphériques, les déversements d'hydrocarbures, le traitement du pétrole, les rejets d'eaux usées municipales et les eaux de ruissellement en milieu urbain (ATSDR, 1995).
4.1 Devenir dans l'environnement
Les propriétés chimiques du BaP favorisent nettement sa sorption sur les particules, les sols et les sédiments (Mackay et Paterson, 1991). Ainsi, on estime qu'environ 82 % du BaP rejeté dans l'environnement se loge dans les sols, 17 % dans les sédiments, 1 % dans l'eau et moins de 1 % dans l'air (Hattemer-Frey et Travis, 1991). La demi-vie associée à l'évaporation du BaP dans l'eau est estimée à 43 jours, en supposant une profondeur de 1 m, un débit de 1 m/s et une vitesse du vent de 3 m/s (Irwin, 1997). L'adsorption sur les sols et les sédiments limite l'évaporation. Il peut également y avoir dégradation par photolyse près de la surface et par les bactéries dans les milieux naturels. La demi-vie dans le sol peut être de 2 jours à 1,9 ans (U.S. EPA, 2007). Le BaP est raisonnablement stable dans l'air et peut être transporté sur des distances considérables. Dans l'air, le BaP est dégradé par photolyse et par des réactions avec l'ozone et le dioxyde d'azote.
5.0 Exposition
Les aliments constituent une importante source d'exposition au BaP. Pour les non-fumeurs qui ne sont pas exposés au BaP dans le cadre de leur travail, on estime que 70 % de l'exposition aux HAP, y compris au BaP, est liée à l'alimentation, surtout aux céréales et aux légumes, sauf dans le cas des personnes consommant beaucoup de viande cuite à feu nu (Phillips, 1999). L'exposition par inhalation des produits de combustion peut également être une source notable; la contribution de l'ingestion d'eau potable et de sol à l'exposition totale au BaP est moindre quant à elle.
5.1 Eau
Les renseignements sur les concentrations de BaP dans les eaux souterraines sont rares. Comme il est fortement lié au sol, le BaP est peu susceptible d'être entraîné jusque dans les eaux souterraines par lessivage. Néanmoins, on a signalé la présence de concentrations allant jusqu'à 0,32 µg/L dans des eaux souterraines à proximité d'une usine de préservation du bois au Nouveau-Brunswick (WMS et coll., 1989).
Les concentrations moyennes de BaP dans les Grands Lacs se situent entre 0,03 et 0,7 ng/L (Gouvernement du Canada, 1991).
Les concentrations de BaP dans l'eau potable sont en général très faibles au Canada. On n'a généralement pas détecté de BaP dans l'eau potable en Ontario (Ontario Ministry of the Environment, 2013), en Colombie-Britannique (British Columbia Ministry of Health, 2013) ou en Saskatchewan (Saskatchewan Water Security Agency, 2013). Pour ces provinces, les limites de détection de la méthode (LDM) variaient de 0,001 à 1 µg/L, et les détections dans les échantillons étaient généralement inférieures ou égales à la LDM. Au Québec, les concentrations de BaP étaient inférieures à la limite de détection (de 0,002 à 0,01 µg/L) dans 97,6 % des 6678 échantillons prélevés dans des réseaux de distribution entre 2002 et 2012. Pour les échantillons renfermant des concentrations supérieures à la limite de détection, la concentration médiane était de 0,004 µg/L, 16 échantillons contenant une concentration de 0,04 µg/L ou plus (Ministère du Développement durable, de l'Environnement, de la Faune et des Parcs du Québec, 2013). On a décelé une concentration dépassant 0,04 µg/L dans quatre des 5711 échantillons prélevés au Nouveau-Brunswick (LDM de 0,001–0,5 µg/L) (Ministère de la Santé et du Mieux-être du Nouveau-Brunswick, 2013) et dans un de 268 échantillons prélevés en Nouvelle-Écosse (LDM se situant entre 0,009 et 0,01 µg/L) (Nova Scotia Department of Environment and Labour, 2013).
Les concentrations de BaP signalées dans l'eau potable aux États-Unis se situent entre 0 et 1 µg/L (1000 ng/L) (ATSDR, 1995), les concentrations typiques étant d'environ 0,000 55 µg/L (0,55 ng/L) (Santodonato et coll., 1981). Kolpin et coll. (2002) ont entrepris une étude à l'échelle nationale afin de déterminer la présence d'une série de produits pharmaceutiques, d'hormones et de contaminants organiques dans 139 cours d'eau de 30 états américains. Les chercheurs ont trouvé du BaP dans 85 échantillons, sa concentration maximale étant de 0,24 µg/L et sa concentration médiane de 0,04 µg/L. L'Organisation mondiale de la Santé (OMS, 2003) a indiqué que les concentrations de BaP dans l'eau potable se situent entre moins de 0,04 et 914 ng/L à l'échelle internationale.
5.1.1 Relargage à partir des revêtements de goudron de houille
Les concentrations de BaP dans l'eau traitée peuvent être supérieures aux concentrations mesurées dans l'eau non traitée à cause du relargage de BaP par le revêtement de goudron de houille contenant des HAP sur la paroi des conduites du réseau de distribution et des réservoirs de stockage d'eau potable (Basu et coll.; OMS, 2003; OEHHA, 2010). Avant 1980, on utilisait couramment l'asphalte ou le bitume comme matériaux de revêtement pour protéger contre la corrosion les conduites en fonte ou en fonte ductile, en béton et en acier employées pour acheminer l'eau potable, de même que les réservoirs utilisés pour stocker l'eau potable traitée (Basu et coll., 1987; OMS, 2003). Même si cette pratique a été en grande partie abandonnée, il reste des conduites, des réservoirs et des réservoirs de stockage possédant un tel revêtement, ce qui a été prouvé comme contribuant à accroître de façon notable les concentrations de BaP dans l'eau potable (Vu Duc et Huynh, 1981; Basu et coll., 1987; OEHHA, 2010). La présence de concentrations élevées de BaP dans des échantillons d'eau potable indique la présence de particules provenant de la détérioration de revêtements en goudron de houille ou en asphalte.
Dans une étude menée à l'échelle nationale aux Pays-Bas, on a examiné des échantillons d'eau potable à 120 endroits où les conduites principales d'eau potable étaient en fonte avec un revêtement de goudron de houille ou de bitume, et mesuré de fortes concentrations de BaP dans l'eau potable lors du rinçage (jusqu'à 22 μg/L), puis constaté une chute rapide des concentrations (concentration maximale de 2,1 μg/L) après ce rinçage; lorsque des réparations étaient effectuées sur les conduites principales, on a détecté des concentrations de HAP supérieures à 0,01 μg/L, soit la norme de qualité de l'eau potable aux Pays-Bas, pendant une période allant jusqu'à 40 jours pour certains sites d'échantillonnage (Blokker et coll., 2013).
Le niveau de relargage du BaP dépend d'un certain nombre de facteurs, dont l'âge de l'eau, les perturbations hydrauliques et l'état du revêtement des canalisations et des réservoirs. L'étude de Maier et coll. (2000) des facteurs ayant une incidence sur la mobilisation des HAP, dont le BaP, a montré que les variations rapides du régime hydraulique (p. ex., les coups de bélier, l'augmentation rapide de la vitesse d'écoulement) accroissant le temps de contact entre l'eau et le revêtement de goudron de houille, surtout dans le cas d'une eau stagnante en conditions anaérobies, pouvaient augmenter de manière importante le relargage du BaP. De plus amples détails sur cette étude sont présentés à la section 7.1.6.
5.2 Aliments
La principale source alimentaire de BaP est la viande calcinée. On estime qu'un steak grillé sur charbon de bois renferme en moyenne 9000 ng de BaP par kilogramme de viande. Au Canada, la viande, la volaille et le poisson (crus) contiennent jusqu'à 11,0 ng de BaP par kilogramme (Gouvernement du Canada, 1991). Cependant, on trouve aussi du BaP dans les céréales, les huiles, les fruits et les légumes. Dans une étude portant sur 200 aliments offerts aux États-Unis, on a mesuré des concentrations de BaP allant jusqu'à 0,51 ng/g dans les aliments autres que la viande, dont les produits laitiers, les pains, les céréales, les sucreries ainsi que les fruits et légumes frais, tandis que les produits carnés cuits renfermaient jusqu'à 4,86 ng de BaP par gramme (Kazerouni et coll., 2001). On estime qu'un adolescent moyen de 50 kg est exposé à 80 ng de BaP par kilogramme de poids corporel (p.c.) par jour à cause de la viande fumée et à 380 ng/kg p.c. par jour à cause de l'huile de canola (Shi et coll., 2010).
5.3 Air
La majeure partie du BaP présent dans l'air est rapidement adsorbée sur les particules atmosphériques, mais le produit peut également être présent sous forme de vapeur. Une étude menée dans 120 villes américaines a signalé des concentrations de BaP allant de 0,2 à 19,3 ng/m3 dans l'air (Pucknat, 1981). On a détecté des concentrations atteignant 460 ng/m3 à proximité d'une aluminerie à Shawinigan, au Québec (Ringuette et coll., 1993). De manière générale, les concentrations de HAP dans l'air ambiant culminent par temps froid parce que l'on chauffe davantage dans ces circonstances (OMS, 1998). On a enregistré des concentrations de HAP entre 1 et 30 ng/m3 dans diverses villes, mais elles peuvent atteindre 200 ng/m3 dans les grandes villes où la circulation routière est dense (OMS, 1998). La fumée du tabac, la cuisson au gaz et les appareils de chauffage sont des sources importantes de BaP dans l'air intérieur. Dans les zones polluées par la fumée du tabac, les concentrations de BaP vont de 400 à 760 000 ng/m3 (OEHHA, 2010).
5.4 Produits de consommation
Certains produits de consommation dont les shampooings à base de goudron contiennent du BaP. Le tabagisme est une source majeure de BaP. On estime que les cigarettes produites au Canada contiennent 6,1 ng de BaP par cigarette, tandis que les cigarettes importées en renferment approximativement 5,7 ng (Hammond et O'Connor, 2008). On estime que la teneur en BaP de la fumée principale se situe entre 5 et 80 ng par cigarette, celle dans la fumée secondaire étant plus forte (25 à 200 ng de BaP par cigarette; OEHHA, 2010).
5.5 Sol
Le BaP peut s'accumuler dans les sols en raison de ses propriétés hydrophobes. On estime que les concentrations de fond de BaP dans les sols en Ontario sont typiquement de 0,30 et de 0,039 mg/kg dans les espaces verts urbains et ruraux, respectivement (CCME, 2010). En Nouvelle-Angleterre, les concentrations de fond de BaP dans les sols se situent entre 0,04 et 13 mg/kg (Bradley et coll., 1994). Cependant, les concentrations de BaP dans les sols peuvent être considérablement plus fortes sur les sites industriels et à proximité de ceux-ci. Par exemple, on a mesuré des concentrations de BaP allant jusqu'à 1300 mg/kg sur le site d'une ancienne cokerie à Lasalle, au Québec (CCME, 2010), et l'OMS (1998) a signalé des concentrations atteignant 1000 mg/kg.
5.6 Exposition multivoies par l'eau potable
L'approche d'évaluation de l'exposition multivoies par l'eau potable établie par Krishnan et Carrier (2008) ne convient pas aux composés de masse moléculaire élevée comme le BaP. Cependant, il est peu probable que l'exposition cutanée attribuable à l'eau potable contribue de manière significative à l'exposition totale, puisque le BaP est une molécule hydrophobe qui est habituellement associée aux particules de sol, dont l'absorption et la distribution dans les tissus après une exposition cutanée sont limitées (voir les sections 8.1 et 8.2). Comme le BaP n'est pas très volatil, l'exposition par inhalation pendant le bain ou la douche est considérée comme négligeable. On suppose donc que la contribution de l'exposition par voie cutanée et par inhalation à l'exposition globale est négligeable.
6.0 Méthodes d'analyse
La United States Environmental Protection Agency (U.S. EPA) dispose actuellement de trois méthodes approuvées (méthodes 525.2, 550 et 550.1) pour l'analyse du BaP dans l'eau potable (U.S. EPA, 2009a). Il s'agit de méthodes générales pour l'analyse des composés organiques de synthèse faisant appel à une extraction liquide-liquide (ELL) ou à une extraction liquide-solide (ELS), suivie d'une chromatographie en phase gazeuse couplée à une spectrométrie de masse (CG-SM) ou d'une chromatographie en phase liquide haute performance (CLHP) pour séparer les analytes :
- La méthode 525.2 fait appel à une technique d'ELS, suivie d'une CG-SM sur colonne capillaire. La LDM se situe entre 0,032 et 0,23 µg/L (U.S. EPA, 1995, 2003). À l'origine, l'U.S EPA avait approuvé la méthode 525.1, qui a ensuite été remplacée par la méthode 525.2 plus sensible en 1995 (U.S. EPA, 2003, 2009a).
- La méthode 550 fait appel à une technique d'ELL et à une CLHP avec détection ultraviolette (UV) et par fluorescence. La LDM est de 0,029 µg/L (U.S. EPA, 1990, 2009a).
- La méthode 550.1 fait appel à une technique d'ELS et à une CLHP avec détection UV et par fluorescence. La LDM est de 0,016 µg/L (U.S. EPA, 1990, 2009a).
On peut aussi employer une méthode normalisée pour l'analyse du BaP dans l'eau potable (APHA et coll., 2012) : il s'agit de la méthode SM 6440B, qui fait appel à une ELL et à une CLHP et qui a une LDM de 0,02 µg/L.
Le seuil pratique d'évaluation quantitative (SPEQ) associé aux méthodes approuvées par l'U.S. EPA est de 0,0002 mg/L (0,2 µg/L) et est fondé sur la capacité des laboratoires à mesurer la concentration de BaP dans des limites raisonnables de précision et d'exactitude au moment de l'adoption de la réglementation (U.S. EPA, 1992). Les évaluations actuelles du SPEQ sont basées sur l'une ou l'autre des deux méthodes : 1) la concentration la plus faible que 75 % des laboratoires sont en mesure de quantifier dans les limites d'exactitude prescrites établies selon des données réelles relatives au rendement, si les données sont suffisantes; 2) la multiplication des limites supérieures des LDM pour prendre en compte la variabilité inhérente aux méthodes d'essai et aux instruments utilisés pour les analyses, lorsque les données sont insuffisantes. Pour établir le SPEQ, l'U.S. EPA préfère utiliser les données sur le rendement des laboratoires pour les méthodes approuvées au moment de l'examen plutôt que l'approche de la LDM.
Lors des premier et second examens sur six ans des National Primary Drinking Water Regulations en vigueur, l'U.S. EPA a déterminé qu'elle ne pouvait pas abaisser le SPEQ du BaP (U.S. EPA, 2003, 2009a, 2009b). L'analyse des deux ensembles de données utilisés pour ces deux examens a révélé l'absence de données en deçà de l'actuel SPEQ et que la variabilité des résultats des tests de rendement du second examen n'appuyait pas la diminution du SPEQ (U.S. EPA, 2009b).
L'U.S. EPA a employé deux autres méthodes pour déterminer si l'on pouvait établir un niveau estimé d'évaluation quantitative (NEEQ) inférieur au SPEQ : celle utilisant un seuil minimal de niveau à rapporter (SMNR) et celle de la multiplication de la LDM basée sur les méthodes d'analyse approuvées. Le NEEQ est une estimation de la limite inférieure possible du SPEQ. Il est fondé sur une analyse statistique des résultats des tests de rendement relatifs à une méthode ou sur le SMNR issu de l'ensemble de données. Les SMNR sont les limites d'analyse en laboratoire pour un grand nombre de laboratoires aux États-Unis. D'après les SMNR de plus de 55 487 dossiers recueillis entre 1998 et 2005, on a déterminé que seulement 55,4 % de ces valeurs étaient inférieures ou égales au SMNR global de 0,00002 mg/L. Comme le critère voulant que 80 % des valeurs de SMNR soient inférieures ou égales au SMNR global n'était pas respecté, l'U.S. EPA n'a pas fondé le SEEQ sur le SMNR global (U.S. EPA, 2009b). La multiplication de la LDM médiane des trois méthodes d'analyse approuvées (525.2, 550 et 550.1) par un facteur de 10 a donné un SPEQ possible de 0,0003 mg/L. Comme cette valeur est plus élevée que le SPEQ actuel; l'U.S. EPA a déterminé qu'il n'était pas possible d'abaisser le SPEQ du BaP, qui demeure donc de 0,0002 mg/L (0,2 μg/L; U.S. EPA, 2009b).
Il n'existe pas de programme centralisé équivalent pour la collecte et l'analyse statistique rigoureuse des données analytiques au Canada. Bien qu'il ne soit pas possible d'établir un SPEQ pour les laboratoires canadiens, certains d'entre eux pourraient être capables d'atteindre des niveaux d'évaluation quantitative plus bas.
Dans le cadre du processus d'examen des recommandations, plusieurs provinces ont examiné un certain nombre de laboratoires afin d'établir les LDM et les SMNR pouvant être obtenus pour l'analyse du BaP. Les LDM fournies par 15 laboratoires commerciaux, qui reposent sur des méthodes d'analyse variées dont les méthodes 525.2, 846, 3510, 3541 et 8270 de l'U.S. EPA et la SM6410B, se situaient entre 0,001 µg/L et 1,9 µg/L (n > 850 échantillons). Les seuils minimaux de niveau à rapporter du BaP (semblables au SMNR décrit ci-dessus) de ces mêmes laboratoires se situaient entre 0,001 et 6,5 µg/L. Onze des douze SMNR fournis étaient inférieurs ou égaux à 0,01 µg/L.
Les données limitées apparaissant plus haut confirment l'existence de méthodes d'analyse permettant de mesurer de façon fiable les concentrations de BaP inférieures ou égales à 0,01 µg/L. Les méthodes d'analyse ne devraient donc pas être un facteur limitant de la CMA. Les autorités responsables devraient établir des mesures de rendement lorsqu'elles indiquent la méthode d'analyse à employer (c.-à-d. le volume d'échantillon, les exigences d'échantillonnage, la conservation et le stockage des échantillons et la LDM).
7.0 Considérations relatives aux techniques de traitement et aux réseaux de distribution
7.1 Échelle municipale
Les usines de filtration de l'eau municipales faisant appel à des techniques de traitement conventionnel (coagulation, sédimentation, filtration et chloration) peuvent réduire les concentrations de HAP, comme le BaP, dans les sources d'eau potable (Sorrell et coll., 1980; Westerhoff et coll., 2005; Snyder et coll., 2007). En raison de son caractère hydrophobe, le BaP présent dans l'eau brute s'adsorbera sur les particules, et il sera ensuite éliminé par les procédés de traitement conventionnels (Sorrell et coll., 1980). Bien qu'il n'existe que des données limitées à pleine échelle sur l'enlèvement du BaP présent dans l'eau potable à l'aide des techniques de traitement conventionnel, celles-ci indiquent que les concentrations de BaP peuvent être réduites à des niveaux inférieurs à 0,01 µg/L grâce à ces mêmes techniques.
L'U.S. EPA indique que le charbon actif en grains (CAG) constitue la meilleure technique existante (MTE) pour éliminer le BaP de l'eau potable de manière à ce que la concentration du produit atteigne une valeur inférieure au Maximum Contaminant Level (niveau maximal de contaminant) de 0,0002 mg/L (0,2 µg/L) (U.S. EPA, 1992). Pour les systèmes de petite taille, les techniques pouvant atteindre cet objectif comprennent le CAG, le CAG au point d'utilisation et le charbon actif en poudre (CAP) (U.S. EPA, 1992). Les données disponibles indiquent que les concentrations de BaP peuvent être réduites à des niveaux bien en deçà de 0,01 µg/L à l'aide de CAG ou de CAP.
Le BaP est un contaminant préoccupant par sa présence possible dans les conduites en fonte ou en fonte ductile, en béton et en acier garnies d'un revêtement à base d'asphalte ou de goudron de houille, qui ont été installées principalement avant les années 1980 (Basu et coll., 1987). Le relargage du BaP à partir des conduites et des réservoirs de stockage peut être réglé en remplaçant ces composants, en limitant les variations du régime hydraulique, en évitant les fortes perturbations de débit (c.-à-d. les coups de bélier) et en réduisant le temps de séjour de l'eau dans le réseau de distribution (Maier et coll., 2000). La gestion des fluctuations hydrauliques dans le but de réduire au maximum le décrochement des biofilms ou la libération des dépôts de tartre contribuera aussi à limiter les rejets de BaP. En général, dans les réseaux de distribution exploités de manière à favoriser la qualité de l'eau et à réduire au maximum l'âge de l'eau, les rejets de BaP seront eux aussi réduits au maximum.
7.1.1 Procédés conventionnels de coagulation et de filtration et d'adoucissement à la chaux
Dans une étude sur l'efficacité d'enlèvement des HAP par des usines de traitement à pleine échelle, Sorrell et coll. (1980) ont constaté que les concentrations de BaP semblaient être considérablement réduites par un traitement conventionnel (c.-à-d., coagulation, sédimentation et filtration) suivi d'une chloration. L'efficacité du traitement semblait être étroitement liée à l'élimination des particules, ce qui a permis aux auteurs de conclure que le traitement conventionnel était en général efficace pour éliminer le BaP. Cependant, ils ont aussi noté que, dans certaines des études, on indiquait que du charbon actif était utilisé dans le cadre de procédés de traitement conventionnel, ce qui pourrait expliquer l'enlèvement accru de BaP. Les auteurs ont remarqué que, quand on détectait du BaP dans l'eau brute (en concentrations de 4 à 13 ng/L), le traitement réduisait les concentrations jusqu'à des valeurs inférieures à 1 ng/L (élimination de 75 à 92 % du produit) à tous les sites, sauf dans Jefferson Parish, en Louisiane, où la concentration était inférieure à 2 ng/L dans l'eau traitée.
Snyder et coll. (2007) ont étudié une série de perturbateurs endocriniens et de produits pharmaceutiques et de soins personnels, dont le BaP, pour évaluer leur élimination par les procédés de traitement de l'eau potable et de recyclage de l'eau. Les concentrations de BaP ont été déterminées par chromatographie en phase gazeuse couplée à une spectrométrie de masse en tandem (CG‑SM/SM). Le niveau de déclaration était de 10 ng/L, avec une LDM de 2,35 ng/L et une limite de détection de l'instrument de 4,3 pg/L (Trenholm et coll., 2006). Aux 20 usines de traitement de l'eau potable à pleine échelle étudiées, les concentrations de BaP dans l'eau brute étaient inférieures au niveau de déclaration de 10 ng/L (Snyder et coll. 2007). Seulement 13 des 20 usines employaient la coagulation et l'adoucissement à la chaux. Les auteurs ont constaté que la coagulation à l'aide d'alun ou de chlorure ferrique combinée à un adoucissement à la chaux permettait d'éliminer 50 à 80 % du BaP, sans toutefois préciser le nombre d'usines concernées et les concentrations dans l'eau brute. Cette étude contenait très peu de données portant de manière précise sur l'élimination du BaP.
Une étude à l'échelle de banc d'essai sur les procédés conventionnels de production d'eau potable portant sur trois eaux naturelles de qualité variable et une eau synthétique (modèle) enrichie avec un isolat de matière organique naturelle (MON) a été effectuée à une température de 20 °C, des pH de 5,5 et 8,5, une alcalinité de 38 mg/L de carbonate de calcium (CaCO3) et une concentration de carbone organique dissous de 3,5 mg/L (Westerhoff et coll., 2005; Snyder et coll., 2007). On a simulé un traitement conventionnel en effectuant un mélange rapide pendant 1 minute, suivi d'une période de floculation de 20 minutes et d'une période de clarification de 60 minutes. On a soumis l'eau à un traitement de coagulation à l'alun (doses de 30, 35 ou 40 mg/L) ou au chlorure ferrique (doses de 8,3 à 38 mg/L). L'adoucissement à la chaux a été effectué avec des doses d'hydroxyde de calcium se situant entre 53 et 238 mg/L et des doses de carbonate de sodium allant de 0 à 177 mg/L, jusqu'à atteindre un pH final de 11,3. Les concentrations initiales de BaP se situaient entre 39 et 115 ng/L. On a calculé que les concentrations dans l'eau traitée par coagulation à l'alun allaient de 10 à 34 ng/L (taux d'élimination de 68 à plus de 74 %) dans le cas des eaux naturelles et de 10 à 51 ng/L (taux d'élimination de 43 à 91 %) dans le cas de l'eau synthétique. Les concentrations calculées pour l'eau traitée par coagulation au chlorure ferrique étaient similaires, se situant entre 10 et 33 ng/L (taux d'élimination de 67 à 80 %) dans le cas des eaux naturelles et étant de 34 ng/L (taux d'élimination de 57 %) dans le cas de l'eau synthétique. Les concentrations calculées pour l'eau traitée par adoucissement à la chaux étaient également comparables, allant de 10 à 11 ng/L (taux d'élimination de plus de 74 % à plus de 90 %) dans le cas des eaux naturelles et étant de 46 ng/L (taux d'élimination de 47 %) pour l'eau synthétique. En conclusion, à petite échelle, le traitement conventionnel a permis de réduire des concentrations de BaP allant jusqu'à 105 ng/L pour les ramener à des valeurs inférieures à 34 ng/L dans des eaux naturelles. L'élimination du BaP contenu dans l'eau synthétique semblait moins efficace à pH élevé. Dans l'ensemble, l'alun a permis d'éliminer en moyenne 72 % du BaP (Westerhoff et coll., 2005). Le chlorure ferrique a enlevé 74 % du BaP présent dans l'eau, ce qui n'est pas très différent de l'adoucissement à la chaux qui a atteint un taux d'élimination du BaP de 82 % (Snyder et coll., 2007).
7.1.2 Charbon actif
Le charbon actif est utilisé pour le traitement de l'eau sous forme de CAG ou de CAP. La capacité d'adsorption du charbon actif à l'égard des composés organiques varie en fonction d'une série de facteurs, comme la compétition d'autres contaminants, la MON, la température ainsi que les propriétés physico-chimiques des composés organiques et du charbon (Speth, 1990).
7.1.2.1 Charbon actif en grains
Le CAG est la technique la plus couramment employée pour éliminer le BaP dans les petits systèmes de traitement en raison de sa simplicité, sa facilité d'utilisation, sa commodité et son accessibilité (Snoeyink, 1990; U.S. EPA, 1998). Lorsque l'on utilise du CAG, les contaminants diffusent à travers des granules adsorbantes et s'accumulent sur la surface interne des pores à mesure que l'eau traverse le contacteur.
Des études antérieures ont démontré l'efficacité du charbon actif dans l'élimination des HAP tels que le BaP. Basu et Saxena (1978) signalaient la présence de concentrations de BaP allant de 0,3 à 42,1 ng/L dans des eaux de surface utilisées comme source d'approvisionnement en eau potable dans quatre villes américaines (Huntington, en Virginie-Occidentale; Buffalo, dans l'État de New York; Pittsburgh et Philadelphie, en Pennsylvanie). À ces quatre usines de traitement de l'eau à pleine échelle, on utilisait un coagulant, du charbon actif (CAG, CAP, ou les deux) et du chlore dans la chaîne de traitement. Trois de ces usines utilisaient également de la chaux. Aucune précision n'a été fournie au sujet des conditions d'application des divers procédés (p. ex., la dose de coagulant, de charbon ou de chlore utilisée, le temps de contact). Les résultats d'analyse des échantillons prélevés à ces quatre usines de traitement de l'eau à pleine échelle ont montré que les concentrations de BaP dans l'eau traitée à l'aide de techniques conventionnels et de CAG se situaient entre 0,2 et 0,5 ng/L (taux d'élimination de 68 % à plus de 99 %). On a noté que le site où le taux d'élimination était le plus faible (Buffalo, dans l'État de New York) présentait également la plus faible concentration de BaP dans l'eau traitée et ne semblait pas utiliser de chaux dans le traitement. Sorrell et coll. (1980) ont examiné les résultats d'études à pleine échelle sur l'élimination des HAP et ont constaté que l'utilisation de charbon actif ne convenait pas nécessairement à l'élimination de faibles concentrations de HAP, comme le BaP, puisque l'efficacité d'élimination peut être plus faible lorsque les concentrations sont basses.
Stackelberg et coll. (2004) ont étudié une série de composés, dont le BaP, dans l'eau d'approvisionnement, l'eau filtrée et l'eau traitée d'une usine de traitement d'eau potable d'une capacité de 62 Mgallons/jour (235 ML/jour) faisant appel à un traitement conventionnel, à du CAP (pour le goût et l'odeur) et à du CAG (temps de contact de 1,5 à 3 minutes). Le BaP a été mesuré par ELL CG/SM en continu, et le niveau de déclaration était de 0,5 µg/L (les limites de détection n'étaient pas précisées). Les auteurs ont indiqué que du BaP était présent dans 42 % des 12 échantillons prélevés dans les cours d'eau alimentant l'usine et aux points d'échantillonnage de l'approvisionnement en eau brute de l'usine. À l'aide d'un graphique, on a estimé que les concentrations de BaP dans ces échantillons se situaient entre 0,04 et 0,09 µg/L, mais les auteurs n'ont pas détecté de BaP dans l'eau traitée (les limites de détection n'étaient pas précisées).
Dans une étude de suivi, Stackelberg et coll. (2007) ont analysé une série de composés, dont le BaP, dans l'eau d'approvisionnement, l'eau clarifiée, l'eau filtrée et l'eau traitée de cette même usine. Même si l'on utilisait encore un traitement conventionnel et du CAG à cette usine, certaines modifications avaient été apportées avant l'étude de 2007 : on n'ajoutait plus de CAP; la clarification (par floculation et sédimentation) avait été améliorée grâce à l'utilisation de microsable; la désinfection primaire avait dorénavant lieu après la clarification; et 9 % de l'eau de lavage à contre-courant décantée des filtres était recyclée et réacheminée au début du procédé. Les auteurs n'ont pas détecté de BaP dans l'eau d'approvisionnement, l'eau décantée, l'eau filtrée ou l'eau traitée. Cependant, des concentrations élevées de BaP ont été mesurées dans les solides secs issus des boues du bassin de décantation (48,5 µg/kg) et dans les sédiments provenant du lavage à contre-courant des filtres de CAG (15 µg/kg). On a enregistré une réduction de la concentration de BaP de 69 % (en poids) dans les solides entre les étapes de sédimentation et de filtration. Les auteurs ont attribué la présence de BaP dans les solides sans sa présence concomitante dans l'eau à des variations temporelles de l'échantillonnage. Autrement dit, du BaP était présent dans l'eau d'approvisionnement et en a été enlevé pendant une période où l'eau n'a pas fait l'objet d'un échantillonnage dans le cadre de l'étude.
7.1.2.2 Charbon actif en poudre
Dans la même étude à l'échelle du banc d'essai de Westerhoff et coll. (2005) décrite dans la section 7.1.1, les auteurs ont examiné l'efficacité du charbon actif en poudre (CAP) dans l'élimination du BaP en se servant d'une dose de 5 mg/L et en établissant le temps de contact à 4 heures. L'eau d'approvisionnement contenait une concentration de carbone organique dissous de 3,5 mg/L, son alcalinité était de 128 mg/L de CaCO3 et son pH initial de 7,9. Le BaP a été mesuré par CG-SM/SM. Le niveau de déclaration était de 10 ng/L, avec une LDM de 2,35 ng/L et une limite de détection de l'instrument de 4,3 ng/L (Trenholm et coll., 2006). Les concentrations initiales de BaP se situaient entre 66 et 155 ng/L, et les concentrations calculées pour l'eau traitée au CAP se situaient entre 9 et 36 ng/L (taux d'élimination de 69 à plus de 94 %), et cela pour toutes les eaux étudiées. Dans ces conditions, la concentration initiale moyenne de BaP de 110 ng/L a été réduite de 83 % dans les quatre eaux échantillonnées (concentration calculée dans l'eau traitée de 30 ng/L) (Westerhoff et coll., 2005; Snyder et coll., 2007). Il a également été établi que l'élimination des composés tels que le BaP par le CAP ne dépendait pas de la concentration initiale de BaP, mais que l'on pouvait améliorer le taux d'élimination en accroissant la dose de CAP (Westerhoff et coll., 2005; Snyder et coll., 2007). L'étude a aussi permis de déterminer que la valeur du Koe était un bon indicateur de l'efficacité d'élimination du procédé à l'égard de plusieurs des composés dans des conditions d'essai au CAP bien contrôlées (Westerhoff et coll., 2005).
7.1.3 Procédés d'oxydation
La formation de sous-produits, y compris ceux de la désinfection, par l'oxydation du BAP ou d'autres composés organiques présents dans l'eau d'approvisionnement devrait être prise en considération avant d'utiliser des procédés d'oxydation. Les types et les concentrations de sous-produits générés dépendent de la qualité de l'eau d'approvisionnement, des concentrations et des types d'oxydants et du temps de contact pour la réaction. Par exemple, les procédés d'oxydation avancée (POA), comme ozone et peroxyde d'hydrogène ou ozone et lumière UV, peuvent produire du bromate dans les eaux contenant des ions bromure (Fronk, 1987; Crittenden et coll., 2005). La présence de sous-produits peut nécessiter de recourir à d'autres traitements après les POA ou d'optimiser le procédé d'oxydation afin de réduire au maximum la formation de sous-produits.
7.1.3.1 Chloration, chloramination et oxydants mixtes
Dans des études à l'échelle du banc d'essai sur l'élimination du BaP effectuées par Westerhoff et coll. (2005), on a appliqué des doses de chlore suffisantes pour que la concentration résiduelle de chlore après 24 heures soit de 1 mg/L. Le chlore résiduel a été désactivé à l'aide d'acide ascorbique après l'échantillonnage pour empêcher toute réaction subséquente. Avec des doses de chlore allant de 2,5 à 6,75 mg/L à pH 5,5 dans de l'eau filtrée, on a réussi à oxyder plus de 75 % du BaP présent en concentrations de 30 à 115 ng/L. Les taux d'oxydation étaient supérieurs à 80 % lorsque le pH ambiant était de 7,0 ou plus pour une dose de chlore de 3 mg/L. Cette étude a aussi examiné les différences entre l'oxydation par le chlore et par la chloramine dans des conditions identiques du point de vue de la qualité de l'eau et des concentrations de BaP de 83 à 95 ng/L. On a évalué les résultats obtenus avec des doses de chloramine de 2 et de 3 mg/L en prélevant des échantillons après 24 et 168 heures de contact pour simuler les conditions dans le réseau de distribution (Westerhoff et coll., 2005; Snyder et coll., 2007). Le taux d'oxydation du BaP augmentait nettement avec la dose de chloramine et le temps de contact, les taux d'oxydation se situant entre 65 % et plus de 89 % (concentrations finales calculées allant de 15 à 33 ng/L).
Dans cette même étude (Westerhoff et coll., 2005; Snyder et coll., 2007), on a employé des oxydants mixtes et de l'eau de Javel pour générer des mélanges de chlore libre et de chlore combiné. Les oxydants mixtes peuvent contenir d'autres oxydants (p. ex., des radicaux hydroxyles), et l'étude a examiné simultanément le chlore à des fins de comparaison. On a ajouté des doses de chlore de 2 et de 3 mg/L à une concentration de BaP de 97 ng/L durant 24 heures de contact pour simuler les conditions dans le réseau de distribution,. En doses de 5 à 20 mg/L avec un temps de contact allant jusqu'à 20 minutes, les oxydants mixtes n'ont pas été efficaces pour oxyder le BaP, le taux d'oxydation atteint n'étant que de 30 % ou moins.
7.1.3.2 Ozonation et procédés d'oxydation avancés
Les POA font référence à l'utilisation de combinaisons d'oxydants chimiques (p. ex., l'ozone), de lumière UV et de catalyseurs (p. ex., le peroxyde d'hydrogène) pour générer des radicaux hautement réactifs, comme des radicaux hydroxyles, qui sont de puissants oxydants réagissant rapidement et de façon non sélective avec les contaminants organiques. Les propriétés physico-chimiques de l'eau à traiter, comme l'alcalinité, le pH, la MON, le fer et le manganèse ainsi que la turbidité, ont une profonde incidence sur les POA, puisqu'elles désactivent les radicaux hydroxyles libres ou absorbent la lumière UV utilisée pour produire les radicaux (Crittenden et coll., 2005).
Butković et coll. (1983) ont déterminé que la réaction du BaP avec un excès d'ozone dans de l'eau distillée suivait une cinétique de réaction du premier ordre. La demi-vie du BaP présent en concentration initiale de 18 µg/L, en présence d'ozone 10-4 M à pH 7, était de une seconde. D'après cette demi-vie, les auteurs ont estimé que l'ozonation d'eau potable à une dose de 1 mg/L oxyderait complètement le BaP et le détruirait. Une étude récente sur la cinétique de réaction du BaP dans les procédés d'ozonation corrobore ce résultat (Jin et coll., 2012).
Dans une étude à l'échelle du banc d'essai utilisant une dose de 0,5 ou de 2,5 mg/L d'ozone appliquée successivement (l'ozone en prétraitement) ou simultanément à la biodégradation, Yerushalmi et coll. (2006) ont constaté que le fait d'allonger le temps de contact de 10 à 60 minutes améliorait le taux d'oxydation du BaP. À 0,5 mg/L, le fait d'appliquer la dose successivement ou simultanément, quel que soit le temps de contact, n'a pas produit de différence notable. Cependant, à une dose de 2,5 mg/L, on a pu améliorer de manière importante le taux d'élimination du BaP en le faisant passer de 26 % pour un temps de contact de 20 minutes à 63 % pour un temps de contact de 60 minutes.
Snyder et coll. (2007) ont étudié l'efficacité de l'ozonation du point de vue de l'oxydation du BaP. Pour les quatre eaux échantillonnées soumises aux essais, le taux moyen d'élimination du BaP dépassait 80 % lorsqu'une dose d'ozone de 2,5 à 8,0 mg/L était ajoutée à l'eau filtrée, en se fondant sur une concentration d'ozone résiduel cible de 0,2 à 0,3 mg/L après 3 minutes et de zéro après 10 minutes (ce qui correspond à une valeur de concentration de désinfectant et de temps de contact associée à la désinfection primaire visant à éliminer les virus ou Giardia).
7.1.3.3 UV et procédés d'oxydation avancés
Snyder et coll. (2007) ont réalisé une étude à l'échelle du banc d'essai pour évaluer la capacité de la lumière UV et de la lumière UV avec du peroxyde d'hydrogène à diminuer la concentration de BaP dans des eaux de qualités variables (concentration dans l'eau brute : 104 à 332 ng/L) à l'aide d'une lampe à moyenne pression délivrant une dose de 40 ou de 1000 mJ/cm2. Le traitement à la lumière UV en dose de 40 mJ/cm2 (dose de désinfection typique) n'a pas permis de réduire le BaP de manière notable. Cependant, le traitement à la lumière UV en dose de 1000 mJ/cm2 a permis d'éliminer 63 à 82 % du BaP. L'utilisation d'un POA (ajout de 5 mg/L de peroxyde d'hydrogène avant l'exposition à une dose de 1000 mJ/cm2 de lumière UV) n'a pas permis d'améliorer de manière significative l'élimination du BaP.
Sanches et coll. (2011) ont évalué la capacité des lampes UV à basse pression à réduire les concentrations de BaP dans de l'eau de qualité laboratoire, de l'eau souterraine et de l'eau de surface. Avec une dose de lumière UV de 1500 mJ/cm2, on a pu décomposer efficacement le BaP. Le taux d'élimination était plus élevé dans l'eau souterraine (93 %) que dans l'eau de qualité laboratoire (79 %; concentration de 5,6 µM dans l'eau d'arrivée) ou l'eau de surface (48 %). Les auteurs ont conclu que la MON et la matière organique dissoute avaient probablement une incidence sur l'efficacité d'élimination.7.1.4 Séparation par membrane
Snyder et coll. (2007) ont réalisé une étude à l'échelle du banc d'essai sur l'élimination du BaP par les membranes de nanofiltration (NF) et d'ultrafiltration (UF). Ils ont étudié des membranes commerciales de NF et d'UF composites à film mince à l'aide de modules de membranes avec cellules à agitation en cul-de-sac qui sont efficaces pour évaluer la rétention relative de composés. Les membranes étaient constituées de polyimide ultramince revêtu soit d'un polyamide aromatique, soit d'un polyéthersulfone sulfoné. On a soumis trois eaux naturelles et une eau synthétique à la filtration sur membrane, à pH ambiant dans le cas des eaux naturelles (6,8 à 8,2) et à pH 7,5 dans le cas de l'eau synthétique. On a fait passer un premier volume de 300 mL de l'échantillon à travers la membrane, puis recueilli 200 mL de perméat. On a répété cette opération jusqu'à ce qu'on ait recueilli 1 L de perméat au total. Les concentrations de BaP dans les eaux au départ étaient de 40 à 155 ng/L, et les taux de rétention atteints se situaient entre plus de 75 % et plus de 94 % (concentrations calculées dans le perméat : 9 à 20 ng/L). Le taux de rétention du BaP était semblable pour les membranes de NF et les membranes d'UF.
7.1.5 Autres techniques de traitement
Une technique encore au stade expérimental permettrait d'éliminer les HAP, dont le BaP, de l'eau, mais les renseignements dont on dispose sont encore insuffisants pour évaluer pleinement son efficacité :
- Adsorption sur complexes organo-inorgano-argileux : Srinivasan et Folger (1990) ont comparé l'efficacité d'élimination du BaP des eaux industrielles des complexes organo-inorgano-argileux (COIA) et du CAG. Les COIA sont des adsorbants argileux ayant été modifiés à l'aide de polycations inorganiques et d'agents de surface cationiques. D'après leurs travaux antérieurs, l'orientation du carbone organique adsorbé et la quantité d'adsorbants organiques seraient deux facteurs dont l'incidence sur l'efficacité du sorbant serait déterminante. Comme le BaP est hydrophobe et que sa solubilité dans l'eau est relativement faible, il est facilement adsorbé sur les surfaces lipophiles des COIA.
7.1.6 Considérations relatives au réseau de distribution
La principale source de BaP se retrouvant dans l'eau potable est habituellement le revêtement à base de goudron de houille utilisé dans le réseau de distribution plutôt que l'eau d'approvisionnement (OMS, 2003). Même si les nouvelles canalisations que l'on installe ne sont plus munies de ce genre de revêtement, d'anciennes conduites à revêtement de goudron de houille demeurent en service (Maier et coll., 2000). On peut envisager la réfection ou le remplacement des conduites à revêtement de goudron de houille; l'avenue à privilégier est déterminée en fonction des conditions propres au site (p. ex., le matériau de fabrication des conduites, des signes de corrosion externe, l'estimation de la durée de vie restante et le diamètre des conduites). Il existe des stratégies de fonctionnement permettant de limiter les rejets de BaP dans le réseau de distribution jusqu'à ce que les canalisations munies d'un revêtement de goudron de houille puissent être remplacées.
Maier et coll. (2000) ont examiné les facteurs ayant une incidence sur la mobilisation de 13 HAP (dont le BaP) provenant du revêtement de goudron de houille des conduites d'eau principales. Une surveillance exhaustive a été exercée dans 22 zones d'approvisionnement en eau où l'on comptait 834 km de canalisations installées avant 1972. Ce programme de surveillance a révélé que la hausse des concentrations de HAP dépendait de la réduction de l'activité du biofilm microbien sur la paroi interne des conduites, du décollement du biofilm s'accompagnant de la libération de particules provenant des incrustations, de la perturbation du régime hydraulique et du temps de stagnation (rétention). Ces facteurs ont été étudiés de manière plus approfondie en laboratoire, à l'aide de bancs d'essai de tuyaux et sur le terrain.
On a étudié l'élimination du BaP dans le cadre d'études sur le terrain menées dans une zone d'approvisionnement en eau permettant de passer d'une eau d'approvisionnement désinfectée à une eau d'approvisionnement non désinfectée. Cinq expériences ont été effectuées, et les effets du chlore et du dioxyde de chlore sur le relargage des HAP ont été étudiés à des doses de 0,025 à 0,3 mg/L pendant une période allant jusqu'à 444 jours. Les auteurs ont constaté que l'augmentation des doses de chlore et de dioxyde de chlore entraînait une hausse de la concentration de plusieurs HAP dans le réseau de distribution, sans toucher les concentrations de BaP.
Maier et coll. (2000) ont exposé trois tronçons de 10 m d'un réseau de distribution possédant des conduites en fonte garnies d'un revêtement de goudron de houille à trois conditions différentes de qualité de l'eau, pour différents débits, niveaux de désinfection et régimes hydrauliques. On a procédé à un échantillonnage à 10 emplacements dans les tronçons, y compris avant et après le point d'application du désinfectant. Les auteurs ont confirmé que les concentrations de HAP augmentaient avec les doses de chlore et de dioxyde de chlore. De plus, ils ont noté que la diminution d'oxygène dans le réseau de distribution entraînait une baisse de l'activité microbienne du biofilm, produisant ainsi une hausse des concentrations de HAP.
Maier et coll. (2000) ont constaté que l'accroissement du temps de stagnation provoquait une hausse des concentrations de HAP et de la turbidité. De plus, ils ont montré qu'un pH inférieur à 5 causait une hausse importante des concentrations de HAP dans le réseau de distribution. Les perturbations hydrauliques augmentaient à la fois la turbidité et les concentrations de BaP (68 ng/L) et d'autres HAP. La filtration effectuée afin de réduire la turbidité, ramenait les concentrations de BaP à des valeurs inférieures à la limite de détection analytique.
Blokker et coll. (2013) ont mesuré les HAP, dont le BaP, dans diverses conditions de fonctionnement pour déterminer lesquelles d'entre elles étaient associées à des hausses des concentrations de HAP dans l'eau potable. Les auteurs ont prélevé des échantillons d'eau potable à 120 emplacements pendant le fonctionnement normal, pendant et après le rinçage des conduites et après le retrait d'une section de canalisation. Des échantillons ont été recueillis à chaque emplacement à 8 reprises sur une période de 2,5 semaines. Parmi les échantillons récoltés, 49 % des échantillons prélevés aux bouches d'incendie à faible débit et 61 % des échantillons prélevés aux bouches d'incendie à débit élevé contenaient des concentrations de BaP supérieures à 0,01 µg/L. Les concentrations maximales de BaP dans les diverses conditions de fonctionnement se situaient entre 0,003 et 22 µg/L. Les plus faibles concentrations provenaient des échantillons prélevés pendant le fonctionnement normal (sans perturbation) et les plus fortes des échantillons prélevés aux bouches d'incendie pendant le rinçage des conduites. Les concentrations diminuaient rapidement après le rinçage. Des concentrations élevées de HAP ont également été mesurées dans les échantillons recueillis après la réfection des conduites principales, et il a fallu jusqu'à 40 jours après la réfection pour les ramener au-dessous de la norme de 0,01 μg/L. Les auteurs ont constaté qu'il n'y avait pas de corrélation entre les concentrations de HAP et la turbidité ou la vitesse de rinçage.
Dans les essais en laboratoire effectués par Maier et coll. (2000), des coupons d'acier inoxydable revêtus de goudron de houille ont été exposés à de l'eau potable pendant 4 à 32 semaines. La surface de goudron de houille constituait le substrat de croissance du biofilm. Ces coupons ont ensuite été étudiés dans le cadre d'essais par lots afin de déterminer le taux de relargage sur une période de 24 heures dans diverses conditions. Les chercheurs ont noté que le biofilm avait un effet protecteur et que les concentrations de HAP générées par relargage étaient considérablement plus faibles en présence de biofilm sur les coupons. Ils se sont basés sur ces résultats pour recommander des stratégies visant à réduire les concentrations de HAP, dont le BaP, dans l'eau potable issue du réseau de distribution. Le fait d'appliquer les désinfectants aux doses requises, d'éviter les coups de bélier et les variations du régime hydraulique, et de réduire le temps de séjour ou la stagnation de l'eau dans le réseau de distribution contribuera à empêcher les concentrations de HAP d'augmenter. Il convient de rincer le réseau de distribution de manière systématique pour s'assurer d'éliminer toutes les particules s'y trouvant (Vreeburg, 2010). Cette affirmation est corroborée par les résultats obtenus par Maier et coll. (2000) et par Blokker et coll. (2013) au sujet de la présence de particules contenant des HAP pendant les perturbations et le rinçage.
Les matériaux utilisés à l'heure actuelle dans le réseau de distribution, qui répondent à la norme 61 de NSF International (NSF) et de l'American National Standards Institute (ANSI) (NSF/ANSI, 2013), ne devraient relarguer que de très faibles quantités de BaP dans l'eau potable. Pour que les matériaux obtiennent une certification de conformité à cette norme, ils ne peuvent pas libérer par relargage plus de 0,02 µg/L de BaP dans l'eau. Ce critère d'acceptation est la concentration permise par produit individuel (CPPI), laquelle est établie à partir des valeurs réglementaires de l'U.S. EPA à l'égard des contaminants (un dixième de la valeur réglementaire de 0,2 µg/L) (NSF/ANSI, 2013).
7.2 Échelle résidentielle
En général, il n'est pas recommandé d'utiliser des dispositifs à usage résidentiel pour traiter l'eau déjà traitée par les municipalités. Cependant, la migration de BaP à partir des conduites du réseau de distribution qui possèdent un revêtement de goudron de houille est une source possible de BaP dans les réseaux de distribution de l'eau potable. Dans ce cas, et dans celui où un particulier tire son eau potable d'un puits privé, il peut être indiqué d'employer un dispositif de traitement de l'eau potable à usage résidentiel pour réduire les concentrations de BaP présentes dans l'eau potable.
Santé Canada ne recommande pas de marques particulières de dispositifs de traitement de l'eau potable, mais conseille vivement aux consommateurs de n'utiliser que les dispositifs certifiés par un organisme de certification accrédité comme étant conformes aux normes appropriées de NSF/ANSI. Ces normes visent à protéger la qualité de l'eau potable en aidant à garantir l'innocuité des matériaux et le rendement des produits qui entrent en contact avec l'eau potable. Les organismes de certification garantissent qu'un produit est conforme aux normes en vigueur et doivent être accrédités par le Conseil canadien des normes (CCN). Au Canada, le CCN a accrédité les organismes suivants, qu'il autorise ainsi à certifier les dispositifs de traitement et les produits liés à l'eau potable qui respectent les normes NSF/ANSI (CCN, 2015) :
- CSA Group (www.csagroup.org – disponible en anglais seulement);
- NSF International (www.nsf.org – disponible en anglais seulement);
- Water Quality Association (www.wqa.org – disponible en anglais seulement);
- UL LLC (www.ul.com – disponible en anglais seulement);
- Bureau de normalisation du Québec (www.bnq.qc.ca); et
- International Association of Plumbing and Mechanical Officials (www.iapmo.org – disponible en anglais seulement).
Une liste à jour des organismes de certification accrédités peut être obtenue auprès du CCN (2015).
On trouve peu de renseignements dans les publications sur l'efficacité du traitement au CAG à l'échelle résidentielle et, à l'heure actuelle, il n'existe pas de dispositif de traitement à l'échelle résidentielle qui est certifié pour la réduction des concentrations de BaP dans l'eau potable. Des filtres au charbon peuvent s'installer au robinet (point d'utilisation) ou à l'endroit où l'eau entre dans l'habitation (point d'entrée). Certaines techniques de traitement au point d'entrée ou au point d'utilisation, comme celles qui font appel au charbon actif, peuvent ramener les concentrations de BaP dans l'eau potable au-dessous de la CMA. Aucun dispositif de traitement de l'eau potable n'est certifié spécifiquement pour l'élimination du BaP à l'heure actuelle, puisque ce produit n'est visé par aucune norme ANSI/NSF applicable aux unités de traitement de l'eau potable pour l'instant.
Avant d'installer un dispositif de traitement, il convient de faire analyser l'eau afin d'en caractériser la chimie générale et d'en vérifier la concentration de BaP. L'eau devrait être analysée régulièrement par un laboratoire accrédité à son entrée et à sa sortie du dispositif de traitement pour en vérifier l'efficacité. Les dispositifs fonctionnant par adsorption peuvent devenir moins efficaces avec l'usage et le temps et doivent donc être entretenus ou remplacés. Les consommateurs devraient vérifier la durée de vie prévue du matériel d'adsorption de leur dispositif de traitement conformément aux recommandations du fabricant et veiller à son entretien.
8.0 Cinétique et métabolisme
8.1 Absorption
Chez le rat, l'analyse des matières fécales a révélé qu'environ 60 % du BaP administré par voie orale en doses supérieures à 250 mg/kg p.c. par jour dans les aliments était absorbé (Chang, 1943). L'absorption du BaP à partir du tractus gastro-intestinal, évaluée par fluorescence du BaP sur les parois de l'estomac glandulaire de souris et de chats, semble être facilitée par sa solubilisation par les sels biliaires (Ermala et coll., 1951). La biodisponibilité du BaP par voie orale chez le rat a été estimée à 10 % (Foth et coll., 1988) ou à 40 % (Ramesh et coll., 2001b) selon la dose de BaP administrée (3 µg/kg p.c. ou 100 mg/kg p.c., respectivement). Les écarts quant à la quantité de BaP biodisponible pourraient être attribuables au fait que des doses plus élevées de BaP ont été employées dans la dernière des deux études, ce qui pourrait entraver l'extraction du produit par les fluides gastrointestinaux (Ramesh et coll., 2001b). L'absorption du BaP après son administration par voie orale dépend aussi de la présence d'huiles et de graisses dans le tractus gastro-intestinal (ATSDR, 1995) et elle est accrue par les solvants renfermant des constituants hydrophiles et hydrophobes (Ekwall et coll., 1951). Cette relation non linéaire entre la dose de BaP et sa biodisponibilité, de même que l'excipient employé auront une incidence sur l'absorption du BaP après une exposition par voie orale.
Environ 90 % du BaP radiomarqué inhalé a été éliminé des poumons de rats Fischer 344 en 30 minutes (Sun et coll., 1982). Chez les animaux de laboratoire, l'inhalation du BaP peut entraîner un passage rapide des poumons à la circulation systémique. Chez les rats exposés par inhalation par le nez seulement à du BaP sous forme d'aérosol de noir de carbone (0, 0,1, 1,0 et 2,5 mg/m3 pendant 4 heures), les concentrations plasmatiques maximales de BaP ont été atteintes en une heure; seules des quantités traces étaient encore détectables au bout de cinq heures (Ramesh et coll., 2001a). De manière similaire, environ 40 % de la dose de 1 μg/kg p.c. de BaP radiomarqué au 3H dissous dans le triéthyleneglycol, administrée à des rats par instillation intratrachéale, a été éliminée des poumons dans les cinq minutes suivant l'exposition; au bout de six heures, il ne restait environ que 5 % de la dose initiale (Weyand et Bevan, 1986). Ainsi, le BaP est absorbé rapidement après son inhalation. Comme on l'avait noté dans le cas de l'administration par voie orale, l'excipient est un facteur ayant une incidence importante sur l'absorption du BaP après une exposition par inhalation; le fait que le BaP soit associé avec des particules ou non et la taille de ces particules auront un effet sur son absorption (Creasia et coll., 1976).
L'exposition in vitro au BaP par voie cutanée à l'aide d'échantillons de peau de souris, de rats, de lapins, de cobayes, de ouistitis et d'humains a produit des taux d'absorption de 0,1 % à 10 %. L'induction d'enzymes métabolisant les médicaments dans la peau accroît la pénétration du BaP appliqué par voie topique, ce qui semble indiquer que le métabolisme du BaP est déterminant pour son absorption par voie cutanée (Kao et coll., 1985). L'excipient employé est un autre facteur ayant une incidence sur l'absorption du BaP par voie cutanée. Chez les macaques rhésus, le taux d'absorption du BaP était de 51 ± 22 % lorsque le produit était appliqué dans l'acétone et de 13,2 ± 3,4 % lorsqu'il était appliqué dans de la terre (Wester et coll., 1990). Les expériences in vitro sur de la peau de cadavres tendue au-dessus de sérum humain agissant comme fluide receveur ont montré qu'environ 1,4 % de la dose totale appliquée pénétrait dans la peau et que 0,01 % pénétrait dans le sérum lorsque le BaP était appliqué dans de la terre; lorsque l'on utilisait de l'acétone comme excipient, on détectait environ 24 % et 0,1 % de la dose totale appliquée dans la peau et dans le sérum, respectivement (Wester et coll., 1990).
8.2 Distribution
L'administration de BaP par voie orale peut mener à sa distribution rapide dans le sang, le foie et d'autres organes. Par exemple, chez les rats ayant reçu une dose de BaP de 100 mg/kg p.c. par voie orale, la plus grande quantité de BaP a été mesurée dans le sérum (~ 67 % de la dose totale non métabolisée) huit heures après l'exposition. Dans le foie, on a observé un profil de rétention du BaP en deux phases comportant des pics à environ 10 % de la dose totale métabolisée 2 et 24 heures après l'exposition (Ramesh et coll., 2001b). De manière similaire, le BaP a été distribué rapidement dans la circulation sanguine chez des rats exposés par voie orale chez qui on a détecté des concentrations mesurables une heure après son administration (Ramesh et coll., 2002).
Chez des animaux de laboratoire exposés par inhalation au BaP, on a noté des concentrations élevées de BaP dans les poumons peu après l'exposition, puis une distribution du produit aux divers organes par la circulation systémique. Après avoir instillé du BaP radiomarqué par voie intratrachéale à des rats, on a vu que la majeure partie de la dose administrée était distribuée dans les poumons (59,5 %), la carcasse (14,4 %) et le foie (12,5 %) dans les cinq minutes suivant l'exposition initiale. Six heures après l'exposition, la plus grande partie du BaP se trouvait dans l'intestin (45 % dans le contenu de l'intestin et 15 % dans les tissus), puis dans la carcasse (21,5 %), l'estomac (5,8 %), les poumons (5,2 %), le foie (4,6 %) et les reins (2,0 %). Le sang renfermait environ 4 % de la dose totale pendant les 15 premières minutes ayant suivi l'exposition et approximativement 1 à 2 % 0,5 à 6 heures après l'exposition (Weyand et Bevan, 1986). La nature de l'excipient (c'est-à-dire si le BaP administré était adsorbé sur des particules ou sous forme vaporisée) était un facteur important dans la distribution du BaP après inhalation (Creasia et coll., 1976).
Après l'application chez la souris d'une dose topique de 50 mg/kg p.c. de BaP radiomarqué au 3H, on a détecté le produit principalement dans la peau et des quantités négligeables dans le foie, les poumons et l'estomac (Carlson et coll., 1986). En outre, on a détecté du BaP dans l'urine et les globules blancs de patients à qui l'on avait appliqué un onguent au goudron de houille par voie topique (Godschalk et coll., 1998). Approximativement 13 à 51 % de la dose administrée, selon l'excipient employé, avait pénétré dans la peau chez les singes rhésus et 1 à 24 % chez les humains (Wester et coll., 1990). Ces résultats semblent indiquer que le BaP peut pénétrer dans la peau, mais qu'il y reste ensuite en majeure partie.
On a étudié la distribution systémique du BaP après une exposition par voie intraveineuse. Cinq minutes après l'exposition de rats à une dose de 15 mg/kg p.c. de BaP radiomarqué au 14C, on a constaté que, la majeure partie de la radioactivité se trouvait dans les poumons, puis dans le foie, le cœur, les reins, le sang, le cerveau, la rate, les testicules et les tissus adipeux (Moir et coll., 1998). Une étude plus récente (Marie et coll., 2010) a confirmé que le BaP était distribué dans divers organes et tissus chez les rats après son administration par voie intraveineuse. Deux heures après l'administration, la plus grande partie du BaP se trouvait dans les poumons (17,0 %), puis dans la peau (7,6 %), les tissus adipeux (2,5 %), le foie (2,3 %) et les reins (0,5 %).
On a aussi mesuré des concentrations accrues de BaP dans des fœtus de rats après son administration par voie orale dans de l'huile de maïs à des rates gravides. La plus forte concentration de BaP dans les tissus des fœtus a été détectée deux à trois heures après l'administration de 200 mg/kg p.c. aux mères, environ 1,5 % de la dose totale étant parvenue jusqu'aux fœtus (Shendrikova et Aleksandrov, 1974). Une autre étude a montré qu'il y avait passage transplacentaire de BaP après son inhalation par les mères, des métabolites étant présents chez les petits jusqu'à 15 jours après l'exposition pendant la gestation (Wu et coll., 2003).
8.3 Métabolisme
Le métabolisme du BaP a été bien étudié, et il a récemment été réexaminé par le CIRC (2010). Le récepteur des arylhydrocarbures (AhR) est le principal facteur de transcription qui régit l'activation des enzymes de phase I et de phase II. Une fois le BaP lié à l'AhR, le complexe BaP-AhR est transporté dans le noyau de la cellule où il forme un dimère avec la protéine de translocation nucléaire de l'AhR et se lie avec les promoteurs des gènes comportant des éléments de réponse de l'AhR, ce qui active la production d'enzymes (Michaelson et coll., 2011). Ainsi, le BaP induit son propre métabolisme en jouant le rôle tant d'inducteur que de substrat des enzymes métaboliques.
Dans le métabolisme de phase I, le BaP est converti en époxyde principalement par les enzymes du cytochrome P450 (CYP) (CYP1A1 et CYP1B1), mais aussi par d'autres enzymes, dont la prostaglandine-synthase (Trush et coll., 1982). Les époxydes du BaP sont hydratés par l'époxyde-hydrolase pour former des diols. Les aldo-céto reductases convertissent les diols de BaP en catéchols (Lan et coll., 2004). L'époxydation secondaire par les CYP donne des diols-époxydes. Le BaP-7,8-diol-9,10-époxyde (BPDE) est le diol-époxyde de BaP le plus mutagène et le plus étudié, formant des adduits covalents avec l'acide désoxyribonucléique (ADN) en position N2 de la désoxyguanosine (Fang et coll., 2001). Il est aussi possible que les CYP catalysent l'oxydation monoélectronique du BaP pour former un cation radical de BaP (Cavalieri et Rogan, 1992). Ces métabolites sont des composés génotoxiques directs qui forment des adduits instables avec les bases puriques (Straif et coll., 2005). De plus, les CYP peuvent subir un découplage de leurs réactions catalytiques, ce qui entraîne la production de superoxyde (·O2−) et d'autres espèces réactives de l'oxygène, dont le peroxyde d'hydrogène (H2O2) et des radicaux hydroxyle (HO·) (Shertzer et coll., 2004).
Pendant le métabolisme de phase II, les métabolites du BaP sont conjugués avec des groupements hydrophiles (glutathion, acide glucuronique ou sulfate) afin d'accroître leur solubilité dans l'eau, ce qui en permet l'excrétion par l'urine et les matières fécales (Garg et coll., 2008; Meinl et coll., 2008; Bock et Bock-Hennig, 2010). Les enzymes en jeu dans le métabolisme de phase II comprennent les glutathion-S-transférases, les uridine diphosphate–glucuronosyl transférases et les sulfotransférases.
Il est à noter que les rats mâles et femelles ne semblent pas métaboliser le BaP de la même façon. On a détecté des quantités considérablement plus faibles de métabolites dans les matières fécales et l'urine des femelles que dans celles des mâles après une exposition par voie orale (Van de Wiel et coll., 1993), bien qu'on ne sache pas si de telles différences surviennent chez d'autres espèces. Le principal métabolite détecté dans les matières fécales et l'urine des rats était le 3‑hydroxybenzo[a]pyrène, qui représentait environ 6 à 12 % de la dose totale de BaP administrée par voie orale (Van de Wiel et coll., 1993).
8.4 Excrétion
Chez le rat, après ingestion de BaP, 60 à 80 % de l'élimination du produit est attribuable à l'excrétion par les matières fécales (Foth et coll., 1988; Van de Wiel et coll., 1993). Par comparaison, la voie urinaire contribue relativement peu à l'excrétion du BaP, représentant moins de 1 % de l'excrétion après une exposition par voie orale. Chez les rats traités au BaP par infusion intraduodénale, l'intestin a absorbé environ 40 % du composé, et le taux d'extraction hépatique de premier passage représentait 40 %. On pense qu'environ 10 % de la dose originale subit une extraction pulmonaire (Foth et coll., 1988).
L'excrétion du produit après exposition par inhalation se fait essentiellement par les matières fécales et quelque peu par l'urine. L'inhalation par le nez seulement chez les rats d'une dose (unique ou sur une période de quatre semaines) de 4,8 mg/m3 de BaP radiomarqué a entraîné un taux d'excrétion par les matières fécales de 96 % (Wolff et coll., 1989).
Le BaP n'est pas facilement absorbé par l'organisme après exposition par voie cutanée; par conséquent, l'excrétion n'est pas en jeu.
8.5 Modèles PBPK
Les modèles pharmacocinétiques à base physiologique (PBPK) dont on dispose à l'heure actuelle ne sont pas adéquats pour décrire l'ensemble des expériences sur des animaux portant sur la pharmacocinétique du BaP. Une seule publication (Crowell et coll., 2011) présente un modèle PBPK décrivant les séries temporelles de données disponibles dans la littérature scientifique au sujet du BaP chez le rat et la souris. Cependant, ce modèle PBPK préliminaire n'utilise pas les valeurs physiologiques appropriées. En particulier, le débit cardiaque employé dans le modèle ne correspond pas aux valeurs de référence citées par Brown et coll. (1997). Les valeurs de débit sanguin de Crowell et coll. (2011) sont 10 à 100 fois plus faibles que les valeurs réelles citées par Brown et coll. (1997). Même après correction des valeurs de débit sanguin, les prédictions du modèle PBPK ne concordent pas avec les données présentées et validées par Crowell et coll. (2011). À cause de ce manque de cohérence, il est difficile de confirmer la structure du modèle et les processus pharmacocinétiques proposés dans ces travaux.
Dans une publication de Haddad et coll. (1998), on décrit un modèle PBPK relatif à la pharmacocinétique du pyrène, un autre HAP. Cependant, l'extrapolation de ce modèle PBPK au BaP a donné des résultats irréguliers à cause de l'incertitude associée aux constantes de fixations tissulaires employées dans le modèle. Dans une publication de Heredia-Ortiz et coll. (2011), on présentait un modèle toxicocinétique à compartiments pour décrire la pharmacocinétique du BaP chez le rat. Bien qu'il concorde avec les données expérimentales chez le rat, le modèle emploie des constantes de vitesse plutôt que des paramètres physiologiques. Ces constantes de vitesse correspondent aux données ajustées seulement et ne peuvent être extrapolées à d'autres espèces, comme l'homme ou la souris, ou à des conditions de dosage autres que celles employées dans l'étude.
Il faudra effectuer d'autres recherches sur les paramètres pharmacocinétiques tels que le partage sang-tissus et élaborer des modèles à partir de données sur la pharmacocinétique du BaP tirées de la littérature afin de correctement établir un lien entre la dose d'exposition au BaP et les mesures de doses internes.
9.0 Effets sur la santé
9.1 Effets chez les humains
9.1.1 Toxicité aiguë
On n'a trouvé aucune donnée sur la toxicité aiguë chez les humains.
9.1.2 Toxicité subchronique et chronique et cancérogénicité
Les données épidémiologiques sur le BaP se limitent aux expositions concomitantes à d'autres substances, dont d'autres HAP. L'exposition par voie orale a été étudiée surtout à partir de la consommation de viandes calcinées, tandis que l'exposition par inhalation a été évaluée en contexte professionnel dans les fours à coke, les alumineries et les usines sidérurgiques ainsi que chez les fumeurs. Dans chaque cas, l'exposition au BaP est survenue sous forme de mélange. Il n'est donc pas possible de tirer des conclusions valables au sujet de la cancérogénicité du BaP ou d'autres effets chroniques attribuables spécifiquement à l'exposition au BaP chez les humains. Même si on n'a pas pu formuler de conclusion à partir d'une seule étude, il est à noter que la plupart des études semblaient indiquer l'existence d'une association positive entre l'exposition au BaP par ingestion ou par inhalation et le cancer chez les humains.
9.1.2.1 Tumorigenèse et cancérogenèse
Des incidences accrues de tumeurs et de cancers étaient les éléments le plus souvent corrélés avec l'exposition au BaP chez les humains. L'exposition par voie alimentaire a été associée avec des cancers et des adénomes colorectaux (Butler et coll., 2003; Gunter et coll., 2005; Sinha et coll., 2005a, 2005b; Ferrucci et coll., 2012), des cancers du pancréas (Anderson et coll., 2005; Li et coll., 2007) et des cancers du poumon (Tram et coll., 2009). Dans d'autres études, on a examiné l'association entre l'exposition au BaP par voie orale et le cancer de la prostate, les lymphomes non hodgkiniens, le cancer du sein et le cancer de l'œsophage, et les résultats étaient négatifs ou non concluants (Cross et coll., 2005, 2006; Hakami et coll., 2008; Fu et coll., 2011). Les plus faibles doses de BaP auxquelles des effets ont été observés après une exposition par voie orale sont indiquées dans une étude d'Anderson et coll. (2005). L'étude portait sur l'ingestion d'amines hétérocycliques et de BaP par 193 personnes atteintes d'un cancer du pancréas et 674 témoins par leur consommation habituelle de viande préparée selon les méthodes courantes. On a enregistré une hausse de l'incidence de cancer, mise en évidence par les rapports des cotes de 2,0 (intervalle de confiance [IC] à 95 % : 1,1 à 3,7) et de 2,2 (IC à 95 % : 1,2 à 4,0) indiqués pour des doses médianes de BaP de 10,4 et de 53,7 ng/jour, respectivement. Il est à noter que les études sur la consommation de viande prenaient en compte l'exposition à divers composés mutagènes et cancérogènes et que les estimations de la concentration de BaP étaient fondées sur une remémoration de la consommation de viande, ce qui peut produire des résultats biaisés. Il est donc difficile d'interpréter les résultats des études décrites ci-dessus en raison du manque de données précises sur les doses ingérées.
Des études ont aussi associé l'inhalation de BaP à divers effets cancérogènes. On signale que, chez les fumeurs et les travailleurs exposés en contexte professionnel, les concentrations d'adduits de BPDE à l'ADN, qui sont propres à l'exposition au BaP, sont plus élevées (Haugen et coll., 1986; Perera et coll., 1988; Hemminki et coll., 1990; Izzotti et coll., 1991; De Flora et coll., 1993; Mumford et coll., 1993; Pan et coll., 1998). Les principaux effets cancérogènes observés dans le cadre d'expositions professionnelles au BaP étaient liés au cancer du poumon (Armstrong et coll., 1994; Friesen et coll., 2007; Armstrong et Gibbs, 2009; De Stefani et coll., 2009). Un rapport des cotes pour le cancer du poumon de 1,6 (IC à 95 % : 1,2 à 2,3) a été associé à une exposition cumulative de BaP de 0,85 à 1,96 μg/m3·année dans un complexe sidérurgique en Chine, même s'il y avait une exposition concomitante à d'autres HAP et à la poussière (Xu et coll., 1996). On a aussi estimé que l'incidence des cancers de la vessie augmentait de 2,3 % par μg/m3·année en supposant une période de latence de 10 ans chez les personnes travaillant dans une aluminerie exposées au BaP et à des matières solubles dans le benzène (Armstrong et coll., 1986).
Certains éléments semblent donc indiquer que l'exposition au BaP est associée à un risque excédentaire de cancer.
9.1.3 Toxicité pour la reproduction et le développement
Certaines données semblent indiquer l'existence d'un lien entre l'exposition aux HAP et la survenue d'effets néfastes sur la reproduction et le développement. Dans une étude, on a examiné l'exposition par voie alimentaire au BaP, entre autres HAP, pendant la grossesse et signalé une association significative avec la diminution du poids et de la longueur à la naissance. Cependant, ces effets n'étaient significatifs que chez les femmes dont la consommation de vitamine C était faible (Duarte-Salles et coll., 2012). Des études sur l'exposition par inhalation chez des femmes enceintes près d'une centrale thermique au charbon et à proximité des incendies au World Trade Center ont mis en évidence une association entre la présence d'adduits de BaP à l'ADN dans le sang ombilical et la diminution du poids des fœtus (Perera et coll., 2005; Tang et coll., 2006), mais aucun effet significatif sur la naissance n'a été noté dans une étude sur des minorités des quartiers centraux de ville exposées au BaP et à d'autres HAP (Perera et coll., 2004).
9.2 Effets chez les animaux de laboratoire
On dispose d'une vaste base de données sur les effets du BaP chez les animaux. Par conséquent, ce sont surtout les études dans lesquelles les renseignements sur la relation dose-réponse étaient adéquats qui sont décrites ci-dessous.
9.2.1 Toxicité aiguë
On a trouvé peu d'information sur la toxicité aiguë chez les animaux. On considère que la toxicité aiguë du BaP par voie orale est assez faible, sa dose létale moyenne (DL50) étant supérieure à 1600 mg/kg p.c. chez la souris (Awogi et Sato, 1989). L'injection intrapéritonéale de BaP a donné une DL50 de 232 mg/kg p.c. chez la souris. (Salamone, 1981). Chez le rat, l'injection sous-cutanée a mené à l'établissement d'une DL50 de 50 mg/kg p.c. (RTECS, 1994).
9.2.2 Exposition de courte durée
9.2.2.1 Toxicité rénale et hépatique
On a constaté une augmentation du poids du foie chez les rats mâles et femelles ayant reçu une dose de BaP de 30 mg/kg p.c. par jour par gavage ainsi que chez les rats mâles ayant reçu une dose de 10 mg/kg p.c. par gavage (5 jours/semaine pendant 90 jours) (Kroese et coll., 2001) et chez les rats mâles exposés à une dose de 90 mg/kg p.c. par jour (5 jours/semaine pendant 35 semaines) (De Jong et coll., 1999). Une vaste étude sur la relation dose-réponse a été menée sur des rats F-344 mâles et femelles ayant reçu par voie alimentaire une dose de BaP de 0, 5, 50 ou 100 mg/kg p.c. par jour pendant 90 jours. On a enregistré une hausse significative du rapport entre le poids du foie et le poids corporel chez les mâles traités à la plus forte dose (100 mg/kg p.c. par jour), mais pas chez les femelles, quelle que soit la dose (Knuckles et coll., 2001).
Dans une étude, on a administré par voie alimentaire à des rats F-344 mâles et femelles des doses de BaP de 5, 50 ou 100 mg/kg p.c. par jour pendant 90 jours. On a noté une augmentation des cylindres urinaires dans les reins des mâles traités aux doses intermédiaires et fortes, mais on n'a relevé aucun effet chez les femelles, quelle que soit la dose (Knuckles et coll., 2001).
Les éléments indiquant que le BaP aurait des effets sur les fonctions rénale et hépatique sont donc limités.
9.2.2.2 Toxicité cardiovasculaire
Deux études ont été menées sur la susceptibilité à l'athérosclérose après une exposition au BaP. On a noté une augmentation de la taille moyenne des lésions athéroscléreuses dans l'arbre et les racines aortiques chez les souris sujettes à l'athérosclérose (sans apoliprotéine E [ApoE]) ayant reçu du BaP par gavage en dose de 2,5 mg/kg p.c. par semaine pendant 24 semaines par rapport à des témoins traités à l'huile d'olive (Yang et coll., 2009). On a aussi observé une athérosclérose chez les souris sans ApoE ayant reçu du BaP par gavage en dose de 5 mg/kg p.c. deux fois en une semaine par rapport à des témoins traités à la tricapryline (Knaapen et coll., 2007).
Parmi les autres effets cardiovasculaires relevés figurait une augmentation du poids du cœur et des marqueurs de l'hypertrophie. On a noté une hausse du rapport entre le poids du cœur et le poids corporel ainsi que des marqueurs de l'hypertrophie chez des rats Sprague‑Dawley ayant reçu par injection intrapéritonéale une dose de BaP de 20 mg/kg p.c. par jour pendant 7 jours par rapport aux témoins traités à l'huile de maïs (Aboutabl et coll., 2009, 2011). Les effets cardiovasculaires néfastes du BaP pourraient également être transmis à la progéniture. Une étude semble indiquer que l'exposition in utero à du BaP en dose de 0,6 ou 1,2 mg/kg p.c. entre les 14e et 17e jours embryonnaires (par gavage de rates à capuchon Long-Evans gravides) prédispose les petits à des déficits fonctionnels au niveau du développement cardiovasculaire et à des troubles cardiaques plus tard au cours de leur vie (Jules et coll., 2012).
9.2.2.3 Neurotoxicité
Les principaux effets neurologiques observés après une exposition au BaP étaient une baisse de l'apprentissage et de la mémoire spatiaux. Xia et coll. (2011) ont administré du BaP à des rats Sprague-Dawley (0, 1,0, 2,5 ou 6,25 mg/kg p.c. par jour) sur une base quotidienne par injection intrapéritonéale pendant 13 semaines, puis ont soumis les animaux au test du labyrinthe aquatique de Morris. Ils ont constaté un retard dans la performance chez les rats traités avec une dose de 2,5 mg/kg p.c. par jour, alors qu'aucun effet significatif n'a été observé à la dose de 1,0 mg/kg p.c. par jour. De plus, cette étude a montré que d'autres effets observés, comme les taux de neurotransmetteurs et les paramètres relatifs au stress oxydatif dans l'hippocampe, étaient également sensibles au BaP, même à la plus faible dose. Parmi les autres effets neurocomportementaux signalés après une exposition au BaP figuraient un comportement agressif et une augmentation de l'activité sexuelle (Bouayed et coll., 2012), une diminution de l'anxiété (Grova et coll., 2008; Bouayed et coll., 2012) et une perturbation de l'activité motrice (Saunders et coll., 2006).
9.2.2.4 Immunotoxicité
L'exposition au BaP par diverses voies a été associée à une immunosuppression, mise en évidence par une diminution de la production d'anticorps et du poids du thymus, une inhibition des réponses lymphocytaires et d'autres altérations du système immunitaire.
On a enregistré une diminution du poids du thymus proportionnelle à la dose chez les rats après une période d'exposition par gavage de trois mois, les résultats étant significatifs à des doses de BaP supérieures à 15 g/kg p.c. chez les mâles et à 50 g/kg p.c. chez les femelles (Kroese et coll., 2001). On a observé une réduction de la production d'anticorps dans plusieurs études. Chez des souris B6C3F1 adultes ayant subi 10 injections sous-cutanées quotidiennes de BaP dans de l'huile de maïs (0, 50, 200 ou 400 mg/kg p.c.) sur 14 jours, on a noté une diminution du nombre de cellules formatrices d'anticorps, même à la plus faible dose d'exposition (Dean et coll., 1983). La baisse de la production d'anticorps à de faibles doses de BaP a en outre été démontrée chez des souris B6C3F1 femelles exposées à du BaP dans de l'huile de maïs en doses de 0, 5, 20 ou 40 mg/kg p.c. par injection sous-cutanée. Encore une fois, des changements étaient visibles dans la production d'anticorps à la plus faible dose (White et Holsapple, 1984). De plus, l'exposition in utero à une dose de 150 mg/kg p.c. par jour de BaP administrée par injection intrapéritonéale à des souris gravides aux jours 11 à 17 de la gestation a entraîné une immunosuppression, mesurée par la réduction de la capacité à produire des cellules formatrices d'anticorps chez les petits de 18 mois (Urso et Gengozian, 1984).
On a également relevé une inhibition des réponses lymphocytaires après exposition à du BaP. Chez des souris C57 et C3H de huit semaines exposées à du BaP par injection intrapéritonéale (0, 0,5, 5 ou 50 mg/kg p.c.), on a constaté une inhibition de la liaison des lymphocytes aux deux doses les plus élevées (Wojdani et Alfred, 1984). L'exposition in utero à une dose de 150 mg/kg p.c. par jour de BaP administrée par injection intrapéritonéale à des souris gravides aux jours 11 à 17 de la gestation a entraîné une diminution de la capacité des lymphocytes à participer à une réaction lymphocytaire mixte chez les rejetons à l'âge de 18 mois (Urso et Gengozian, 1984).
Parmi les autres immunotoxicités figuraient des effets sur le thymus et les cellules immunitaires autres que les lymphocytes. Dans une étude menée par De Jong et coll. (1999), des rats Wistar ont été exposés à du BaP par voie orale (0, 3, 10, 30 ou 90 mg/kg p.c. par jour) pendant 35 jours. À toutes les doses sauf la plus faible, on a noté une diminution du nombre d'érythrocytes, du nombre de lymphocytes B dans la rate, de même que du poids du thymus, autant de signes d'immunotoxicité. Chez les rats Wistar ayant reçu une dose de BaP de 150 mg/kg p.c. par jour par voie alimentaire pendant 30 jours, on a noté une diminution du nombre de cellules dans la moelle osseuse et la rate (Fischer et coll., 2011).9.2.3 Exposition de longue durée et cancérogénicité
Le Centre international de recherche sur le cancer (CIRC, 2012) a classé le BaP dans le groupe 1, c'est-à-dire les substances cancérogènes pour l'homme, en se fondant sur des données suffisantes chez les animaux et des données solides indiquant que les mécanismes du cancer observés chez les animaux s'appliquent également à l'homme. On a constaté que toutes les voies d'exposition causaient des effets cancérogènes localisés et systémiques. Les éléments indiquant une cancérogenèse chez les animaux sont présentés ci-dessous en fonction du site des tumeurs.
9.2.3.1 Tumeurs du tube digestif
Le site le plus sensible à la formation de tumeurs après une exposition par voie orale était le préestomac. Chez des souris A/J femelles (30 par dose) ayant été nourries avec des aliments contenant 0, 16 ou 98 mg/kg de BaP (dose totale de 0, 11 et 67 mg) pendant 260 jours, on a vu des tumeurs du préestomac se développer à toutes les doses d'exposition (Weyand et coll., 1995). Dans une autre étude, chez des souris B6C3F1 femelles (48 par dose) ayant été nourries avec des aliments contenant 0, 5, 25 ou 100 mg/kg de BaP (correspondant à environ 0, 0,7, 3,3 et 13,0 mg/kg p.c. par jour) pendant deux ans, on a vu se développer des tumeurs du préestomac aux doses de 25 et à 100 mg/kg et des tumeurs de l'œsophage à la dose de 100 mg/kg. L'incidence combinée de papillomes et de carcinomes du préestomac était de 1/48, 3/47, 36/46 et 46/47 pour les souris exposées respectivement à 0, 5, 25 et 100 mg/kg dans les aliments. On a aussi observé des tumeurs de la langue à la plus forte dose. Le BaP pur et un mélange complexe de goudron de houille contenant la même quantité de BaP avaient une capacité tumorigène similaire (Culp et coll., 1998). Dans une autre étude, chez des souris CFW mâles et femelles ayant été nourries avec des aliments contenant 0, 1, 10, 20, 30, 40, 45, 50, 100 ou 250 mg/kg de BaP (correspondant à environ 0, 0,1, 1,3, 2,6, 3,9, 5,2, 5,9, 6,5, 13,0 et 32,5 mg/kg p.c. par jour), on a vu des papillomes et des carcinomes malpighiens se développer dans le préestomac à toutes les doses supérieures à 40 mg/kg par rapport aux témoins, l'effet étant proportionnel à la dose. Cependant, les groupes utilisés dans cette étude étaient formés d'animaux des deux sexes et d'âges divers, et la durée d'exposition variait, ce qui rend l'interprétation des résultats difficile (Neal et Rigdon, 1967). Dans une autre étude sur l'exposition chronique, on a administré par gavage une dose de BaP de 0, 3, 10 ou 30 mg/kg p.c. par jour, 5 jours/semaine pendant 104 semaines à des rats Wistar mâles et femelles (52 sujets de chaque sexe par dose). Les mâles se sont montrés plus sensibles aux tumeurs du préestomac que les femelles, comme le montrait la présence de tumeurs à 3 mg/kg p.c. par jour chez les mâles et 10 mg/kg p.c. par jour chez les femelles. L'incidence combinée de papillomes et de carcinomes du préestomac était de 0/52, 7/52, 18/52 et 17/52 chez les mâles et de 1/52, 6/51, 30/51 et 50/52 chez les femelles à 0, 3, 10 et 30 mg/kg p.c. par jour, respectivement (Wester et coll., 2012). Dans une étude sur toute la durée de vie chez les rats, on a administré du BaP par gavage en dose de 0,1 mg/kg p.c., soit 5 jours/semaine, soit tous les 3 et 9 jours, causant ainsi un accroissement des tumeurs du préestomac. Cependant, l'administration de la même dose dans l'alimentation plutôt que par gavage (0,15 mg/kg p.c. 5 fois par semaine ou tous les 9 jours) n'a pas entraîné d'augmentation significative des tumeurs du préestomac (Brune et coll., 1981).
Dans une autre étude par ingestion, chez des souris B6C3F1 femelles (48 par dose) ayant été nourries avec des aliments contenant 0, 5, 25 ou 100 mg/kg de BaP pendant deux ans, on a vu des tumeurs de la langue se développer à la plus forte dose (Culp et coll., 1998). On a aussi observé des tumeurs du tube digestif après exposition par inhalation. Des hamsters mâles (24 par groupe) ont été traités avec du BaP par inhalation (0, 2,2, 9,5 ou 46,5 mg/m3) 4,5 heures/jour pendant 10 semaines, puis 3 heures/jour pendant le reste de leur vie (dose totale moyenne de 0, 29, 127 et 383 mg de BaP par animal). Chez les hamsters traités aux deux plus fortes doses, on a enregistré une hausse de l'incidence des papillomes et des carcinomes à cellules squameuses dans le tube digestif supérieur pour les doses aussi faibles que 9,5 mg/m3 (Thyssen et coll., 1981).
9.2.3.2 Tumeurs du foie
L'exposition de rats Wistar mâles et femelles (52 de chaque sexe par dose) à du BaP administré par gavage en doses de 0, 3, 10 ou 30 mg/kg p.c. par jour, 5 jours/semaine pendant 104 semaines a causé des tumeurs du foie chez les mâles et les femelles traités aux deux plus fortes doses (Wester et coll., 2012).
9.2.3.3 Tumeurs des voies respiratoires
On a observé des tumeurs des voies respiratoires après exposition au BaP par voie orale et par inhalation. Chez des souris A/J femelles (30 par dose) ayant été nourries avec des aliments contenant 0, 16 ou 98 mg/kg de BaP (dose totale de 0, 11 et 67 mg) pendant 260 jours, on a observé des tumeurs pulmonaires à toutes les doses (Weyand et coll., 1995). Dans une étude sur l'exposition par inhalation, des hamsters mâles (24 par groupe) ont été traités avec des doses de BaP de 0, 2,2, 9,5 ou 46,5 mg/m3 pendant 4,5 heures/jour sur une période de 10 semaines, puis 3 heures/jour pendant le reste de leur vie (doses totales moyennes de 0, 29, 127 et 383 mg de BaP par animal). Chez les hamsters traités aux deux plus fortes doses, on a enregistré une hausse de l'incidence des papillomes et des carcinomes à cellules squameuses dans les voies respiratoires supérieures (Thyssen et coll., 1981).
9.2.3.4 Tumeurs de la peau
L'application cutanée de BaP a également entraîné la formation de tumeurs chez les rongeurs. Les souris étaient particulièrement sensibles et développaient des tumeurs bénignes (des papillomes à cellules squameuses et des kérato-acanthomes) et malignes (surtout des carcinomes à cellules squameuses) lorsque l'on appliquait du BaP sur leur peau pendant une période prolongée (Poel, 1959, 1963; Roe et coll., 1970; Habs et coll., 1980, 1984; Sivak et coll., 1997). C'est dans une étude sur des souris C3H/HeJ que l'on a enregistré la plus faible dose à laquelle des tumeurs cutanées ont été observées. Chez des souris exposées à des niveaux de 0,5 ou de 5,0 µg de BaP dans le cyclohexanone et l'acétone appliqués sur une partie rasée de la peau du dos deux fois par semaine, on a observé le développement de tumeurs de la peau chez 20 % (5/30) et 90 % (27/30) des sujets, respectivement (Sivak et coll., 1997). On a également vu des tumeurs se développer dans des études sur l'exposition aiguë au BaP par voie cutanée, suivie d'expositions répétées à des promoteurs (Hoffmann et coll., 1972; Slaga et coll., 1978, 1980; Wood et coll., 1980; Cavalieri et coll., 1981, 1991; El‑Bayoumy et coll., 1982; LaVoie et coll., 1982; Weyand et coll., 1992).
9.2.3.5 Autres tumeurs
On a aussi observé des tumeurs des glandes mammaires après une ingestion de BaP. Chez des rats ayant reçu une dose de 50 µmol de BaP par gavage une fois par semaine pendant huit semaines, on a noté une hausse du nombre d'adénocarcinomes des glandes mammaires. Cependant, on ne connaît pas la plus faible dose à laquelle cet effet peut se manifester (El-Bayoumy et coll., 1995).
9.2.4 Génotoxicité
Il a été démontré que le BaP causait invariablement des mutations ponctuelles in vitro chez Salmonella typhimurium ainsi que des lésions chromosomiques dans les cellules de mammifères, y compris les cellules humaines, après activation métabolique. C'est pourquoi le BaP est souvent utilisé comme contrôle positif dans des essais biologiques sur d'autres composés. Dans la monographie publiée en 2010 par le CIRC, on répertorie tous les cas in vivo d'adduits de BaP à l'ADN observés dans la peau de souris après traitement topique, de même que dans les organes internes et les lymphocytes du sang après administration de BaP par voie orale, par inhalation ou par voie intrapéritonéale (CIRC, 2010). Parmi toutes les études in vivo examinées, c'est dans celle de Garner et coll. (1985) que l'on a administré la dose la plus faible ayant produit des adduits. Dans cette étude, des rats Wistar mâles ont reçu une dose unique de BaP (2 mg/kg p.c.) par injection intrapéritonéale, et on a détecté des adduits à l'ADN dans les poumons et le foie. En raison des très nombreux éléments indiquant que le BaP est génotoxique, on a retenu principalement les résultats obtenus in vivo.
Diverses études ont montré que le BaP induit des mutations. Le BaP a induit trois types de mutations Ki-ras du codon 12 dans les adénomes pulmonaires de souris A/J : GGT→TGT (56,3 %), GGT→GTT (25 %) et GGT→GAT (19 %) (Mass et coll., 1993). Le BaP a aussi induit des mutations du codon 13 (DiGiovanni et coll., 1993) et du codon 61 (Chakravarti et coll., 1995) du c-Ha-ras dans des papillomes cutanés de souris Sencar. Le BaP a provoqué, dans des fibroblastes d'embryons murins provenant de souris knock-in (Hupki) chez lesquelles on avait introduit le gène TP53 humain, des mutations similaires à celles observées dans les cancers du poumon causés par le tabagisme chez les humains (Liu et coll., 2005). Chez des souris mâles MutaMCMouse exposées à des doses de BaP de 25, 50 ou 75 mg/kg p.c. par jour pendant 28 jours, puis sacrifiées 3 jours après la dernière exposition, on a constaté une augmentation de la fréquence des mutants au niveau du transgène lacZ dans les poumons (Labib et coll., 2012), le foie, l'estomac glandulaire, l'intestin grêle et la moelle osseuse (Lemieux et coll., 2011) à toutes les doses. On a aussi noté une hausse proportionnelle à la dose des phénotypes mutants Pig-a chez ces souris (Lemieux et coll., 2011; Labib et coll., 2012). Dans une méta-analyse des études de génotoxicité in vivo antérieures, on a utilisé la méthode de la dose de référence (BMD) pour calculer la dose correspondant à un changement de 10 % de l'effet chez les animaux exposés par rapport aux témoins (BMD10) à partir de données d'essais biologiques sur la relation dose-réponse relative à l'induction de mutations chez les rongeurs transgéniques. On a déterminé des BMD10 d'à peine 2,08 mg/kg p.c. pour les mutations (Hernandez et coll., 2011).
On a aussi constaté que l'exposition au BaP accroissait la fréquence de micronoyaux. Awogi et Sato (1989) ont exposé des souris MS/Ae mâles à une dose unique de BaP de 62,5, 125, 250 ou 500 mg/kg p.c. par injection intrapéritonéale et mesuré la fréquence des micronoyaux dans leur moelle osseuse. Ils ont enregistré une augmentation des micronoyaux à toutes les doses, sauf la plus faible. Dans une autre étude, des souris HRA/SKh mâles ont été exposées à des doses de BaP de 0,5, 5, 50, 100 ou 500 µg par voie topique, en parallèle avec des témoins, et des échantillons ont été prélevés 24 heures après le traitement. On a noté un accroissement des micronoyaux à toutes les doses dans les kératinocytes de culture (He et Baker, 1991). Chez des souris MutaMCMouse mâles exposées par gavage à du BaP en doses de 25, 50 ou 75 mg/kg p.c. par jour pendant 28 jours et sacrifiées 3 jours après la dernière exposition, on a relevé des hausses significatives de la fréquence des réticulocytes micronucléés et des érythrocytes normochromes à toutes les doses (Lemieux et coll., 2011). Dans une méta-analyse des études de génotoxicité in vivo antérieures, on a utilisé la méthode de la BMD pour calculer la BMD10 à partir de données sur la relation dose-réponse relative à la fréquence de micronoyaux dans le sang; cette BM f10 était de 1,28 mg/kg p.c. (Hernandez et coll., 2011).
On dispose d'éléments probants montrant clairement que le BaP induit d'autres effets génotoxiques, dont des coupures simple brin et double brin d'ADN, des échanges de chromatides sœurs et des aberrations chromosomiques (ATSDR, 1995). Par exemple, chez des hamsters chinois mâles et femelles traités au BaP par injection intrapéritonéale à raison de 450 mg/kg p.c. par jour pendant deux jours consécutifs, on a noté une augmentation significative du nombre de métaphases des cellules de la moelle osseuse assortie d'aberrations chromosomiques et d'échanges de chromatides sœurs (Roszinsky-Kocher et coll., 1979). Chez des souris DBA/2 mâles ayant reçu deux doses de BaP de 10 ou de 100 mg/kg p.c. par voie intragastrique, on a noté une hausse significative de la fréquence des échanges de chromatides sœurs dans la moelle osseuse aux deux doses, alors qu'on n'a relevé qu'un faible effet chez les souris C57BL/6J mâles traitées avec des doses de 100 mg/kg p.c. (Wielgosz et coll., 1991). Chez des rats bruns ayant subi une exposition unique à une dose de BaP de 62,5 mg/kg p.c. administrée par voie intragastrique, on n'a pas observé d'induction de synthèse non programmée de l'ADN. Cependant, on a noté une augmentation significative des coupures simple brin d'ADN par rapport aux témoins (Mullaart et coll., 1989).
9.2.5 Toxicité pour la reproduction et le développement
9.2.5.1 Toxicité pour la reproduction
On a noté des effets sur la fertilité chez des animaux de laboratoire des deux sexes. Chez les rats Sprague-Dawley mâles, l'exposition par gavage à une dose de BaP de 1 ou de 5 mg/kg p.c. par jour pendant 90 jours a entraîné une baisse de la testostérone ainsi que des changements des macrophages testiculaires par rapport aux témoins (Zheng et coll., 2010). Divers effets ont été notés chez des rats Swiss albinos mâles exposés par voie orale à une dose de BaP de 50 mg/kg p.c. par jour pendant 10 jours (Arafa et coll., 2009) ainsi que chez des rats Sprague-Dawley mâles exposés par voie orale à une dose de BaP de 5 mg/kg p.c. par jour pendant 12 semaines (Chen et coll., 2011), notamment une diminution du nombre de spermatozoïdes, une augmentation du nombre de spermatozoïdes anormaux et des changements des taux de testostérone et d'enzymes testiculaires. On a également constaté la présence d'ovotoxicité chez des rongeurs adultes exposés au BaP. Par exemple, la production de l'hormone sexuelle 17β‑estradiol a été supprimée chez les rats femelles après une exposition à une dose de BaP de 5 ou 10 mg/kg p.c. par voie intragastrique tous les 2 jours pendant 60 jours (Xu et coll., 2010).
On a aussi observé des effets néfastes sur la reproduction pendant toute la vie adulte d'animaux de laboratoire exposés au BaP in utero. Dans une étude, les effets sur la reproduction chez les rejetons se produisaient à des doses plus faibles que chez les adultes directement exposés. On a enregistré une diminution des gestations et de la viabilité des portées chez les souris CD-1 exposées à une dose de BaP de 160 mg/kg p.c. par jour, tandis que l'exposition à des doses de BaP aussi faibles que 10 mg/kg p.c. par jour aux jours 7 à 16 de la gestation a entraîné une diminution de la fertilité chez les rejetons mâles et des effets marqués sur les tissus gonadiques, notamment une atrophie des tubes séminifères et un nombre accru de cellules interstitielles dans les testicules des rejetons mâles, de même que des réductions considérables des tissus ovariens chez les femelles. Parmi les autres signes indiquant l'existence d'effets transgénérationnels sur la reproduction figurent l'ovotoxicité chez les rejetons de souris NMRI traitées avec du BaP par gavage à raison de 10 mg/kg p.c. par jour aux jours 7 à 16 de la gestation (Kristensen et coll., 1995), de même qu'une réduction du poids des testicules et de la numération des spermatozoïdes chez les souris après un traitement avec du BaP en doses de 2 ou 10 mg/kg p.c. par jour aux jours 7 à 16 de la gestation (Nakamura et coll., 2012).
Dans l'ensemble, ces effets néfastes sur la reproduction ont été observés à des doses de BaP aussi faibles que 1 mg/kg p.c. par jour et de 2 mg/kg p.c. par jour chez les adultes et les petits, respectivement.
9.2.5.2 Toxicité pour le développement
Parmi les signes indiquant des effets toxiques sur le développement figuraient une diminution du taux de survie des fœtus ainsi que du poids à la naissance, une prédisposition au cancer à l'âge adulte, des effets sur le développement neurologique, des malformations ainsi que l'immunotoxicité.
On a enregistré un poids corporel réduit 20 et 42 jours après la naissance chez les petits de souris CD-1 traitées par gavage avec du BaP en doses de 40 ou de 160 mg/kg p.c. par jour aux jours 7 à 16 de la gestation, mais pas chez les sujets ayant reçu 10 mg/kg p.c. par jour (Mackenzie et Angevine, 1981). On a noté une diminution du taux de survie des fœtus à cause des résorptions et des mortinatalités ainsi qu'une incidence accrue de malformations fœtales chez les petits de souris exposées à des doses de BaP de 50 à 300 mg/kg p.c.par injection intraperitonéale pendant la gestation (Shum et coll., 1979). Chez les rates gravides ayant inhalé des concentrations de BaP de 25, 50 ou 100 µg/m3 4 heures/jour pendant 10 jours, on a enregistré jusqu'à 70 % de résorptions fœtales (Wu et coll., 2003).
L'exposition au BaP pendant le développement gestationnelaccroît l'incidence de cancers du poumon, du foie et des ovaires à l'âge adulte (examen de l'U.S. EPA, 2007). Le nombre de tumeurs touchant chaque site était significativement accru même chez les générations F2 à F5 non exposées issues de souris F1 exposées in utero par injection sous-cutanée, mais seulement dans le cas des sujets exposés à une dose très élevée de BaP de 150 mg/kg p.c. par jour (Urso et Gengozian, 1982, 1984; Turusov et coll., 1990). Dans une autre étude, on note que l'exposition par voie orale de rates gravides à des doses de BaP de 0,6 et de 1,2 mg/kg p.c. par jour peut prédisposer les petits à des troubles cardiaques plus tard au cours de leur vie (Jules et coll., 2012).
Les effets du BaP sur le développement neurologique chez les rongeurs ont été examinés dans plusieurs études. On a examiné le développement neurologique chez les souris exposées par le lait maternel produit par des mères exposées au BaP. L'exposition des mères à des doses de 2 et 20 mg/kg p.c. durant les 14 premiers jours de la lactation a entraîné une diminution significative des réflexes chez les petits et une altération de l'expression des gènes neuronaux. On a observé une perturbation du comportement dans le test du labyrinthe en croix surélevé plusieurs jours après la fin de l'exposition (Bouayed et coll., 2009). L'étude menée par Chen et coll. (2012) est l'étude la plus complète sur le développement neurologique, puisqu'elle portait sur une vaste gamme de concentrations de BaP (0, 0,02, 0,2 et 2 mg/kg p.c. par jour) et examinait les conséquences d'une exposition en début de vie sur le comportement anxieux et l'apprentissage spatial à l'âge adulte. On a administré du BaP par gavage à des rats Sprague-Dawley nouveau-nés des deux sexes aux jours 5 à 11 après la naissance, puis évalué leur développement neurologique à divers moments jusqu'au 75e jour après la naissance (début de l'âge adulte). On a observé peu d'effets sur les jalons du développement et sur les réponses sensorielles chez les sujets juvéniles, mais la neurotoxicité était plus apparente chez les jeunes adultes. Dans le test du labyrinthe en croix surélevé (qui mesure le comportement anxieux), on a noté des effets anxiolytiques significatifs à partir de 0,2 mg/kg p.c. par jour chez les mâles et de 0,02 mg/kg p.c. par jour chez les femelles. Dans le test du labyrinthe de Morris (labyrinthe aquatique mesurant l'apprentissage spatial), on a relevé des effets aux doses de 0,2 mg/kg p.c. par jour et plus chez les rats mâles et femelles. Selon cette étude, la dose minimale avec effet nocif observé (LOAEL) serait de 0,02 mg/kg p.c. par jour, soit la plus faible dose administrée. Cependant, il existe peu d'autres études pour corroborer ces effets sur le développement neurologique, surtout à des doses aussi faibles.
En outre, l'exposition in utero au BaP par injection intrapéritonéale d'une dose de 150 mg/kg p.c. par jour à des souris gravides aux jours 11 à 17 de la gestation a provoqué une immunosuppression en réduisant leur capacité à produire des cellules formatrices d'anticorps et une altération de la fonction des lymphocytes chez les petits âgés de 18 mois (Urso et Gengozian, 1984).
9.3 Toxicogénomique
De nombreuses études ont fait appel aux profils d'expression génique du génome entier (toxicogénomique) pour identifier les changements moléculaires à des stades précoces qui permettent de prédire le cancer et d'autres effets. Ces analyses permettent de déterminer et de quantifier les réponses cellulaires à l'exposition à un produit chimique grâce à l'analyse de l'activité de l'expression génique. La plupart de ces études ont été menées in vitro sur des cellules hépatiques (Hockley et coll., 2006, 2009; Michaelson et coll., 2011; Lizarraga et coll., 2012), du côlon (de Waard et coll., 2008; Hockley et coll., 2008), mammaires (Gwinn et coll., 2005; Keshava et coll., 2005; Gwinn et Weston, 2008), épithéliales pulmonaires (Hirano et coll., 2013), de la prostate (Hrubá et coll., 2011), amniotiques (Lu et coll., 2009, 2010) et épithéliales orales (Li et coll., 2008). Certaines de ces études portaient sur des cellules humaines normales non transformées et d'autres sur des cellules se rapportant aux organes touchés. Ces études ainsi que les études in vivo menées sur divers tissus ont été considérées comme les plus pertinentes, et sont donc décrites donc ci-dessous.
Dans deux études, on a examiné les profils d'expression des gènes hépatiques et pulmonaires chez des souris B6C3F1 mâles âgées de cinq semaines (5 par dose) traitées avec du BaP dans de l'huile de maïs administré par gavage en doses de 0 (huile de maïs seule), 5, 50, 150 ou 300 mg/kg p.c. par jour pendant 3 jours consécutifs (Halappanavar et coll., 2011; Yauk et coll., 2011). Des échantillons ont été prélevés en vue de l'analyse de l'expression génique 4 ou 24 heures après la dernière exposition. L'analyse de l'expression des gènes hépatiques chez les souris exposées à des doses de BaP de 150 ou de 300 mg/kg p.c. par jour pendant 3 jours a révélé qu'approximativement 836 et 1541 gènes, respectivement, étaient altérés par rapport aux gènes des témoins (régulés à la hausse ou à la baisse, avec un facteur de changement [FC] ≥ 1,5 et une valeur p ajustée en fonction d'un taux de fausses découvertes [TFD] ≤ 0,05). Dans les poumons de ces souris, 558 et 1267 gènes étaient différentiellement exprimés (FC ≥ 1,5 et p TFD ≤ 0,05) après une exposition à 150 et à 300 mg/kg p.c. par jour de BaP, respectivement, par rapport aux témoins. La réponse globale de l'expression génique dans le foie concordait avec la fonction physiologique connue de cet organe, y compris son rôle primordial dans la détoxification des composés xénobiotiques. La réponse de l'expression génique pulmonaire au BaP comprenait des changements des mécanismes biologiques intervenant dans la signalisation des récepteurs des lymphocytes B, l'inflammation, les réponses aux dommages à l'ADN et l'immunosuppression. Dans l'ensemble, ces mécanismes indiquent des changements profonds du métabolisme, de la réparation de l'ADN et du stress oxydatif survenant dans les poumons et le foie après une exposition par gavage. Tous ces mécanismes moléculaires confirment les propriétés cancérogènes du BaP.
Trois autres études ont été menées sur les réponses de l'expression des gènes des poumons, du foie et du préestomac chez des souris MutaMCMouse mâles âgées de 25 semaines (5 par groupe) exposées par gavage à du BaP dans de l'huile d'olive en doses de 0, 25, 50 ou 75 mg/kg p.c. par jour pendant 28 jours consécutifs (Labib et coll., 2012; Malik et coll., 2012). Les souris ont été sacrifiées 72 heures après la dernière exposition. Les analyses ont révélé des changements significatifs au niveau des produits de la transcription (et FC ≥ 1,5 et p TFD ≤ 0,05) de 6, 7 et 121 gènes dans le foie, de 20, 145 et 373 gènes dans les poumons, et de 9, 135 et 408 gènes dans le préestomac des souris des groupes exposés à 25, 50 et 75 mg/kg p.c. par jour, respectivement. Dans le foie, les gènes étaient principalement associés à des processus biologiques tels que le métabolisme des xénobiotiques et la signalisation p53 indiquant des dommages à l'ADN. Dans les poumons, on a aussi noté un enrichissement significatif de la signalisation p53 et d'autres mécanismes liés au cancer. Même si la voie de signalisation p53 était aussi perturbée dans le préestomac, les processus les plus enrichis concernaient le traitement et la présentation des antigènes, la réponse immunitaire, la chimiotaxie et la différenciation des kératinocytes, ce qui semble indiquer des réponses inflammatoires, immunitaires et aux dommages à l'ADN. Les résultats obtenus dans les poumons et dans le foie concordent avec les changements attendus de l'expression génique en réponse à une substance cancérogène génotoxique, tandis que les résultats enregistrés dans le préestomac indiquent d'autres mécanismes ayant trait à la cancérogenèse.
Les mécanismes moléculaires identifiés in vitro dans les cellules humaines traitées peuvent fournir des indications sur la pertinence de ces réponses dans les tissus humains. Par exemple, des mécanismes en jeu dans la régulation des cycles cellulaires, l'apoptose et l'anti-apoptose, l'assemblage de la chromatine et le stress oxydatif ont été relevés dans des lignées cellulaires de carcinomes du foie et du sein (cellules MCF-7 et HepG2) à des taux induisant une cytotoxicité minimale (Hockley et coll., 2006). Les cellules amniotiques humaines non transformées traitées avec du BPDE ont également répondu par des changements au niveau de la régulation du cycle cellulaire, de la croissance et de l'apoptose (Lu et coll., 2009, 2010). Ces résultats confirment que les résultats observés quant à la cancérogénicité chez les animaux de laboratoire se transposent chez les humains.
9.4 Mode d'action
Les analyses du mode d'action (MA) permettent de déterminer les mécanismes qui mènent aux effets toxiques et leur pertinence chez les humains. Étant donné les données extrêmement nombreuses indiquant la formation de tumeurs chez les animaux de laboratoire et les données limitées sur d'autres effets toxiques, on a concentré l'analyse du MA sur le développement des tumeurs. Le principal mécanisme en jeu dans l'initiation des tumeurs est lié à la formation de métabolites du BaP après liaison à l'AhR, comme on l'explique ci-dessous.
Les métabolites du BaP se sont invariablement montrés génotoxiques et mutagènes in vivo et in vitro, et l'exposition à des concentrations de BaP équivalant à celles que l'on trouve dans l'environnement a entraîné des cassures de brins d'ADN, la formation d'adduits à l'ADN de même que des aberrations chromosomiques chez des animaux de laboratoire (voir la section 9.2.4). Ainsi, on considère que la génotoxicité découlant des métabolites du BaP est le principal MA de la tumorigénèse induite par le BaP. La liaison du BaP à l'AhR est l'étape critique qui mène à la formation des métabolites. C'est pourquoi les souris dépourvues d'AhR n'ont pas développé de tumeurs après une exposition au BaP (Shimizu et coll., 2000), même s'il faut souligner que la présence d'autres produits chimiques capables d'induire les enzymes métaboliques indiquées ci-dessous peut contribuer en partie au métabolisme supplémentaire du BaP. La liaison du BaP à l'AhR a également lieu chez l'homme, bien que l'affinité de liaison peut grandement varier (Harper et coll., 2002) et ainsi avoir une incidence sur la sensibilité interindividuelle à l'exposition.
La liaison à l'AhR produit une induction des enzymes du P450, dont CYP1A1 et CYP1B1, qui sont responsables de la métabolisation du BaP en cations de carbone ou en époxydes génotoxiques comme le BPDE (Cavalieri et Rogan, 1995). La nécessité de ces enzymes pour le métabolisme du BaP est corroborée par les études de knock-out sur des animaux. Par exemple, les concentrations de BaP dans le sang chez des souris knock-out CYP1A1−/− et CYP1A1−/− CYP1B1−/− sont respectivement 25 et 75 fois plus élevées que chez les témoins, et ces souris sont moins sensibles à de nombreuses toxicités du BaP (Uno et coll., 2006). En outre, certaines données indiquent clairement que le BaP est métabolisé en métabolites réactifs chez les humains. Le BaP-7,8-dihydrodiol, un métabolite du BaP constituant un précurseur du métabolite génotoxique BPDE, est produit dans les microsomes de donneurs humains de foie et de poumons (Shimada et coll., 1989). De manière similaire, le 3-OH BaP est facilement détectable dans l'urine de personnes exposées au BaP en contexte professionnel, notamment dans les fours à coke et les installations de production d'électrodes en graphite (Forster et coll., 2008).
Les métabolites du BaP, en particulier le BPDE, forment des adduits covalents directement avec l'ADN, de même qu'avec des protéines. Par un mécanisme parallèle mais secondaire, les espèces réactives de l'oxygène générées comme sous-produits du métabolisme du BaP (par le cycle redox catéchol–quinone du BaP) peuvent aussi oxyder l'ADN (Lan et coll., 2004). La formation accrue d'adduits cause des changements héréditaires de l'ADN, comme le montrent les mutations observées dans divers systèmes d'essai (voir la section 9.2.4) et chez des non-fumeurs exposés au BaP (DeMarini et coll., 2001). Les données semblent donc indiquer que la génotoxicité des métabolites du BaP est la principale cause de la tumorigenèse et de la cancérogenèse chez les animaux de laboratoire. L'ensemble des éléments probants est suffisant pour permettre de conclure, comme le fait le CIRC (2010), que ce MA s'applique à l'homme.
10.0 Classification et évaluation
10.1 Évaluation des risques de cancer
Le Centre International de Recherche sur le Cancer (2010) a classé le BaP dans le groupe 1, c'est-à-dire les substances cancérogènes pour l'homme, en se fondant sur des données suffisantes chez les animaux et des données solides indiquant que les mécanismes du cancer observés chez les animaux s'appliquent également à l'homme. Les effets cancérogènes chez l'homme sont corroborés par les risques accrus de cancer chez les personnes consommant de la viande calcinée, chez les travailleurs des fours à coke et chez les fumeurs. Les rongeurs exposés de manière chronique au BaP développent tant des tumeurs au point d'entrée que des tumeurs découlant de la distribution systémique du BaP. Les tissus touchés comprennent le préestomac, le foie, l'œsophage, les poumons, la langue, le larynx, la cavité buccale, la peau et les glandes mammaires. Les analyses du MA de même que les données sur la génotoxicité in vivo et in vitro indiquent que les métabolites du BaP causent des dommages directs à l'ADN.
On a pris en compte deux études d'évaluation de l'induction de tumeurs chez la souris et le rat pour établir une valeur basée sur la santé (VBS) pour le BaP dans l'eau potable (Culp et coll., 1998; Wester et coll., 2012). Il s'agit de deux études d'exposition chronique employant des doses multiples et comportant un nombre suffisant d'animaux par groupe. De plus, les deux études s'appliquent à une exposition par voie orale au BaP. Chez des souris B6C3F1 femelles, on a noté une incidence accrue de papillomes et de carcinomes du préestomac, de l'œsophage et du larynx (Culp et coll., 1998). Chez des rats Wistar mâles et femelles, on a enregistré une incidence accrue de papillomes et de carcinomes du préestomac, du foie et de la cavité buccale (Wester et coll., 2012). Tous les effets ont été pris en compte dans le calcul de la VBS. On a eu recours à une modélisation de la BMD effectuée en utilisant la version 2.2 du logiciel BMDS (U.S. EPA, 2011) pour estimer la limite inférieure de l'intervalle de confiance à 95 % de la BMD10 (BMDL10) pour chaque effet cancérogène. Il a été déterminé que le préestomac était le tissu le plus sensible dans les deux études. Comme l'homme n'a pas de préestomac, l'utilisation de données relatives aux tumeurs du préestomac chez le rongeur pour prédire les risques de cancer associés à un produit chimique en particulier chez l'homme devrait répondre à certains critères, dont un MA cancérogène et l'induction de tumeurs à plusieurs sites et chez diverses espèces (Proctor et coll., 2007). Le BaP répond à ces critères, agissant selon un MA génotoxique, l'exposition au produit par voie orale causant des tumeurs à plusieurs sites chez diverses espèces et chez les deux sexes, et son MA en jeu dans la cancérogenèse étant compris et considéré comme applicable à l'homme. La plus faible BMDL10 déterminée en fonction des deux études était de 0,5389 mg/kg p.c. par jour (Moffat et coll., 2015), enregistrée chez les souris femelles à l'aide du modèle le mieux ajusté (log-logistique). Cette valeur a été utilisée comme point de départ afin d'établir une VBS pour le BaP.
Les modèles PBPK actuels ne sont pas adéquats pour élaborer une recommandation pour l'eau potable (voir la section 8.5), et l'on ne dispose pas de renseignements sur les différences de toxicocinétique et de toxicodynamique entre les espèces nécessaires à l'application de facteurs d'ajustement propres à un produit chimique donné. Par conséquent, on a ajusté le point de départ par mise à l'échelle allométrique, de manière à représenter plus correctement l'exposition humaine :
Dose équivalente chez l'homme = 0,5389 mg/kg p.c. par jour × (0,03 kg/70 kg)¼
= 0,07758 mg/kg p.c. par jour
où :
- 0,5389 mg/kg p.c. par jour est la plus faible BMDL10 déterminée pour les tumeurs du préestomac chez les souris femelles (Culp et coll., 1998; Moffat et coll., 2015);
- 0,03 kg est le poids corporel par défaut d'une souris;
- 70 kg est le poids corporel par défaut d'un humain adulte;
- (0,03 kg/70 kg)¼ est le facteur d'ajustement allométrique prenant en compte les différences interspécifiques de sensibilité au BaP.
On a utilisé la dose équivalente chez l'homme pour dériver le facteur de pente du cancer (FPC) :
FPC = 0,1/0,07758 mg/kg p.c. par jour
= 1,2890 (mg/kg p.c. par jour)-1
où :
- 0,1 est la dose de référence correspondant à un changement de 10 % de l'effet;
- 0,07758 mg/kg p.c. par jour est la dose équivalente chez l'homme calculée ci-dessus.
La dose associée avec chaque risque à vie est calculée en divisant le risque à vie correspondant par le FPC calculé ci-dessus.
| Risque à vie | Dose (mg/kg p.c. par jour) |
|---|---|
| 10−4 | 0,776 × 10−4 |
| 10−5 | 0,776 × 10−5 |
| 10−6 | 0,776 × 10−6 |
L'équation permettant de convertir une dose en concentration dans l'eau potable est la suivante :
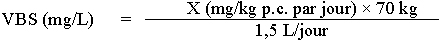
Équivalent textuel
La VBS, exprimée en mg/L, est calculée en multipliant la dose exprimée en mg/kg p.c. par jour par 70 kg (soit le poids corporel par défaut d'un humain adulte). Le produit obtenu est ensuite divisé par 1,5 L/jour (la consommation moyenne quotidienne d'eau d'un adulte).
où :
- X est la dose calculée ci-dessus;
- 70 kg est le poids corporel par défaut d'un humain adulte;
- 1,5 L/jour est la consommation moyenne quotidienne d'eau d'un adulte.
D'après les risques unitaires calculés, les concentrations estimées qui correspondent à des excès de risque de cancer à vie de 10-4, 10-5 et 10-6 chez l'homme sont les suivantes :
| Risque à vie | Concentration estimée dans l'eau potable (µg/L) |
|---|---|
| 10−4 | 4 |
| 10−5 | 0,4 |
| 10−6 | 0,04 |
Un excès de risque de cancer à vie de 10−6 ou moins est utilisé lorsque l'absorption par d'autres sources est considérable (Krishnan et Carrier, 2013). Comme il existe d'autres sources d'exposition significatives au BaP (soit les aliments), on a employé un excès de risque de cancer à vie de 10−6 pour établir une VBS de 0,04 µg/L.
10.2 Évaluation des risques autres que le cancer
Certains éléments indiquent que l'exposition au BaP entraîne des effets autres que le cancer, dont des effets neurologiques et sur le développement neurologique néfastes pouvant se manifester à de faibles doses. On a remarqué une performance retardée et des marqueurs de neurotoxicité dans l'hippocampe de rats auxquels on avait injecté 2,5 mg/kg p.c. par jour de BaP pendant 13 semaines (Xia et coll., 2011). Dans une étude portant sur des rats nouveau-nés exposés au BaP par voie orale aux jours 5 à 11 après leur naissance, on a constaté que les effets neurologiques néfastes, se traduisant par de piètres résultats obtenus au cours de deux tests du labyrinthe, s'aggravaient à l'âge adulte (résultats enregistrés aux jours 70 et 75 après la naissance comparativement à ceux obtenus aux jours 35 et 40 après la naissance dans le test du labyrinthe en croix surélevé et dans le test du labyrinthe de Morris, respectivement) (Chen et coll., 2012). Ces effets étaient significatifs à partir de doses de BaP aussi faibles que 0,02 mg/kg p.c. par jour chez les rats femelles dans le test du labyrinthe en croix surélevé et à partir de doses de 0,2 mg/kg p.c. par jour chez les rats mâles et femelles dans le test du labyrinthe de Morris.
Comme ces effets étaient significatifs à des doses de BaP d'au moins 0,2 mg/kg p.c. par jour, une NOAEL de 0,02 mg/kg p.c. par jour (soit 20 µg/kg p.c. par jour) peut être utilisé comme point de départ pour calculer l'apport quotidien tolérable (AQT). L'AQT pour les effets sur le développement neurologique est donc calculée de la façon suivante :
![L'équation utilisée pour calculer l'apport quotidien tolérable (AQT) pour le benzo[a]pyrène dans l'évaluation du risque d'effets autres que le cancer](/content/dam/phac-aspc/images/services/publications/healthy-living/guidelines-canadian-drinking-water-quality-guideline-technical-document-benzo-alpha-pyrene/fig02-fra.jpg)
Équivalent textuel
L'AQT pour le benzo[a]pyrène dans l'évaluation du risque d'effets autres que le cancer est de 0,0667 µg/kg p.c. par jour. Cette valeur est calculée en divisant la NOAEL , 20 µg/kg p.c. par jour, par le facteur d'incertitude, 300.
où :
- 0,02 mg/kg p.c. par jour est la NOAEL (Chen et coll., 2012)
- 300 est le facteur d'incertitude (× 10 pour la variation intraespèces; × 10 pour la variation interespèces; et × 3 pour tenir compte des lacunes dans la base de données).
Un facteur d'incertitude de 3 a été inclus pour tenir compte des lacunes dans la base de données sur les effets non-cancer du BaP, à cause des effets neurologiques et sur le développement neurologique, et parce que les données sur les effets à faible dose sont limitées, et qu'il existe des données limitées pour appuyer les MA non-cancer du BaP. En se servant de l'AQT calculé ci-dessus, une VBS peut être dérivée comme suit :
![L'équation utilisée pour calculer la valeur basée sur la santé (VBS) pour le benzo[a]pyrène dans l'eau potable pour l'évaluation du risque d'effets autres que le cancer](/content/dam/phac-aspc/images/services/publications/healthy-living/guidelines-canadian-drinking-water-quality-guideline-technical-document-benzo-alpha-pyrene/fig03-fra.jpg)
Équivalent textuel
La VBS pour le benzo[a]pyrène dans l’eau potable est de 0,6 µg/L (arrondie). Cette valeur est calculée en multipliant l’AQT non cancérogène de 0,0667 µg/kg p.c. par jour, par 70 kg, le poids corporel moyen d'un adulte, puis par 0,2, le facteur d'attribution par défaut pour l'eau potable, et en divisant le résultat par 1.5 L/jour, le volume quotidien d'eau consommé par un adulte.
où :
- 0,0667 µg /kg p.c. par jour correspond à l'AQT calculé ci-dessus;
- 70 kg correspond au poids corporel moyen d'un adulte;
- 0,2 est le facteur d'attribution par défaut pour l'eau potable, utilisé en tant que valeur seuil, comme l'eau potable n'est pas une source importante d'exposition et qu'il y a des preuves de présence généralisée dans au moins un autre milieu (air, aliments, sol ou produits de consommation) (Krishnan et Carrier, 2013).
- 1,5 L/jour correspond au volume quotidien d'eau consommée par un adulte; on ne considère pas que l'exposition par voie cutanée et par inhalation pendant les bains et les douches soit importante (comme il est décrit à la section 5.6).
10.3 Comparaison des évaluations de risques de cancer et d'effets autres que le cancer
On a dérivé une VBS de 0,04 µg/L pour les effets cancérogènes du BaP dans l'eau potable, basé sur la concentration associée à un risque à vie excédentaire de 10–6 pour l'effet critique de tumeurs le plus sensible (tumeurs du pré-estomac) chez les souris femelles. On a calculé une VBS de 0,6 µg/L pour les effets non cancérogènes, en fonction des effets neurologiques dans la progéniture de rats exposés au BaP. Puisque l'évaluation des risques de cancer produit une VBS pour le BaP plus protectrice que celle produite par l'évaluation des risques non-cancer, l'évaluation des risque de cancer est considérée déterminante pour établir une CMA pour le BaP dans l'eau potable. En outre, il existe un plus haut niveau de confiance pour les effets cancérogènes que pour les effets non cancérogènes du BaP. Par conséquent, la VBS de 0,000 04 mg/L (0,04 µg/L) qui a été calculée pour les effets cancérogènes est donc estimée comme étant suffisante pour protéger contre tous les cancers et contre les effets sur les développement du BaP.
10.4 Considérations internationales
On présente dans cette section les diverses lignes directrices et normes pour l'eau potable fixées par d'autres organisations internationales. Les limites varient en fonction de la date d'évaluation et des politiques et des approches employées, y compris le choix de l'étude principale et l'utilisation de différents taux de consommation, poids corporels et facteurs d'attribution.
L'U.S. EPA (1992) a établi à 0,2 µg/L son Maximum Contaminant Level pour le BaP dans l'eau potable, d'après les données de l'étude de Neal et Rigdon (1967). Un FPC de 7,3 (mg/kg p.c. par jour)-1 a été dérivé en utilisant la moyenne géométrique de quatre FPC calculés à partir d'hypothèses différentes, selon des études de Neal et Rigdon (1967) et de Brune et coll. (1981).
L'OMS (2011) a fixé une valeur de référence de 0,7 µg/L pour le BaP en 1996, ce qui correspond à un excès de risque de cancer à vie de 10−5. Cette valeur est également fondée sur l'étude de cancérogénicité par voie orale menée par Neal et Rigdon (1967). Cette valeur a été calculée à l'aide d'un modèle en deux étapes des mutations entre la naissance et la mort.
La California Environmental Protection Agency (OEHHA, 2010) a établi un objectif de santé publique de 0,007 µg/L et une concentration maximale de 0,2 µg/L pour le BaP dans l'eau potable, d'après les effets cancérogènes notés chez les animaux de laboratoire. Pour cela, l'organisation s'est basée sur des études portant sur des souris (Culp et coll., 1998) et des rats (Kroese et coll., 2001) plutôt que sur l'étude de Neal et Rigdon (1967) qui comporte d'importantes limitations. Les données de Kroese et coll. (2001) sont les mêmes que celles de Wester et coll. (2012). Un modèle du délai qui précède l'apparition de tumeurs a été employé pour obtenir la limite inférieure des estimations de la dose associée à une augmentation de 10 % de l'incidence des tumeurs de la cavité buccale chez les souris femelles et les rats des deux sexes, de même que des tumeurs du foie chez le rat. Les tumeurs de la cavité buccale et du préestomac chez les souris femelles étaient associées à la plus basse limite inférieure de la dose associée à une augmentation de 10 % de l'incidence des tumeurs. L'objectif de santé publique a été calculé d'après le pouvoir cancérogène, lequel a été déterminé en supposant une relation linéaire entre la dose et la réponse aux faibles doses, avec une correction pour l'âge et l'exposition en début de vie. Un niveau de protection de la santé de 4 µg/L a également été fixé d'après les données sur la toxicité rénale chez le rat tirées de l'étude de Knuckles et coll. (2001) afin de prendre en compte les effets autres que le cancer en se servant d'un facteur d'incertitude de 3000, d'une contribution relative de la source de 0,1 et de l'ingestion de 0,044 L/kg p.c. par jour.
11.0 Justification
Bien que le BaP ne soit ni fabriqué ni importé, il est très répandu dans l'environnement parce qu'il est généré par des processus naturels et anthropiques de combustion. Le réseau de distribution peut également être une source de contamination de l'eau potable par le BaP, car celui-ci peut être relargué à partir des revêtements en goudron de houille (bitume) ou en asphalte des réservoirs de stockage de l'eau et des canalisations du réseau de distribution. Cependant, l'eau potable n'est pas une source majeure d'exposition au BaP.
Le BaP a été classé dans le groupe 1, c'est-à-dire les substances cancérogènes pour l'homme, en se fondant sur des données suffisantes chez les animaux et des données solides indiquant que les mécanismes du cancer observés chez les animaux s'appliquent également à l'homme. Il existe des données probantes que l'exposition au BaP entraîne des effets autres que le cancer, dont des effets neurologiques et sur le développement neurologique chez les rongeurs, et cela, à de faibles niveaux d'exposition au BaP. Cette évaluation considère les risques de cancer et d'effets autres que le cancer. La CMA pour le BaP dans l'eau potable est fondée sur l'évaluation des risques de cancer parce que celle-ci est plus protectrice et qu'il existe un plus haut niveau de confiance pour les effets cancérogènes du BaP que pour ses effets non cancérogènes.
L'estimation du risque de cancer au cours de la vie associé à une exposition à des concentrations de BaP dans l'eau potable se situant entre 0,04 et 0,4 µg/L est considérée comme étant « essentiellement négligeable ». La recommandation concernant un cancérogène est généralement établie à une concentration à laquelle l'accroissement du risque de cancer est considéré comme étant « essentiellement négligeable » pour une exposition pendant la vie entière à cette concentration dans l'eau potable. Dans le cadre des recommandations pour la qualité de l'eau potable, Santé Canada entend par « essentiellement négligeable » une plage allant d'un nouveau cas de cancer de plus que le niveau de fond pour 100 000 personnes à un nouveau cas de cancer de plus que le niveau de fond pour un million de personnes (c.-à-d. 10-5 à 10-6). On vise un accroissement du risque de cancer de 10-6 lorsque l'exposition par d'autres sources que l'eau potable est significative. Dans le cas du BaP où les aliments constituent la principale source d'exposition, la CMA correspond à la concentration qui présenterait un risque essentiellement négligeable d'un nouveau cas de cancer de plus que le niveau de fond pour un million de personnes (c.-à-d. 10−6) exposées au BaP dans l'eau potable à sa CMA pendant toute une vie, prenant en considération le traitement.
En résumé, une CMA de 0,000 04 mg/L (0,04 µg/L) est établie pour le BaP en tenant compte des éléments suivants :
- Elle se situe dans la plage de risques considérés comme étant « essentiellement négligeables ».
- Elle est détectable et mesurable, avec une limite de détection de la méthode bien plus faible que la CMA. L'U.S. EPA a fixé un SPEQ de 0,0002 mg/L d'après la capacité des laboratoires à mesurer la concentration de BaP dans des limites raisonnables de précision et d'exactitude à l'aide de méthodes approuvées. Bien qu'il n'existe aucun processus similaire pour établir un SPEQ propre au Canada, une enquête limitée de laboratoires commerciaux révèle que ceux-ci sont capables de mesurer de façon fiable les concentrations de BaP inférieures ou égales à 0,01 µg/L.
- La CMA doit pouvoir être atteinte à un coût raisonnable. Les techniques de traitement à l'échelle municipale peuvent systématiquement enlever le BaP de l'eau potable jusqu'à des concentrations inférieures à la CMA de 0,04 µg/L. À l'échelle résidentielle, même s'il n'existe pas actuellement de dispositifs de traitement certifiés pour l'élimination du BaP, on s'attend à ce que les dispositifs de traitement faisant appel à des techniques telles que le charbon actif puissent enlever le BaP jusqu'à des niveaux inférieurs à la CMA.
12.0 Références
- Aboutabl, M.E., Zordoky, B.N. et El-Kadi, A.O. (2009). 3-Methylcholanthrene and benzo[a]pyrene modulate cardiac cytochrome P450 gene expression and arachidonic acid metabolism in male Sprague Dawley rats. Br. J. Pharmacol., 158(7): 1808–1819.
- Aboutabl, M.E., Zordoky, B.N., Hammock, B.D. et El-Kadi, A.O. (2011). Inhibition of soluble epoxide hydrolase confers cardioprotection and prevents cardiac cytochrome P450 induction by benzo[a]pyrene. J. Cardiovasc. Pharmacol., 57(3): 273–281.
- Anderson, K.E., Kadlubar, F.F., Kulldorff, M., Harnack, L., Gross, M., Lang, N.P., Barber, C., Rothman, N. et Sinha, R. (2005). Dietary intake of heterocyclic amines and benzo[a]pyrene: associations with pancreatic cancer. Cancer Epidemiol. Biomarkers Prev., 14(9): 2261–2265.
- APHA, AWWA and WEF (2012). Standard methods for the examination of water and wastewater. 22e édition. American Public Health Association, American Water Works Association and Water Environment Federation, Washington (DC).
- Arafa, H.M., Aly, H.A., Abd-Ellah, M.F. et El-Refaey, H.M. (2009). Hesperidin attenuates benzo[α]pyrene-induced testicular toxicity in rats via regulation of oxidant/antioxidant balance. Toxicol. Ind. Health, 25(6): 417–427.
- Armstrong, B.G., Tremblay, C.G., Cyr, D. et Thériault, G.P. (1986). Estimating the relationship between exposure to tar volatiles and the incidence of bladder cancer in aluminum smelter workers. Scand. J. Work Environ. Health, 12(5): 486–493.
- Armstrong, B., Tremblay, C., Baris, D. et Thériault, G. (1994). Lung cancer mortality and polynuclear aromatic hydrocarbons: a case–cohort study of aluminum production workers in Arvida, Quebec, Canada. Am. J. Epidemiol., 139(3): 250–262.
- Armstrong, B.G. et Gibbs, G. (2009). Exposure–response relationship between lung cancer and polycyclic aromatic hydrocarbons (PAHs). Occup. Environ. Med., 66(11): 740–746.
- ATSDR (1995). Toxicological profile for polycyclic aromatic hydrocarbons. Agency for Toxic Substances and Disease Registry, Public Health Service, U.S. Department of Health and Human Services, Atlanta, Georgia. Disponible à : www.atsdr.cdc.gov/toxprofiles/tp69.pdf
- Awogi, T. et Sato, T. (1989). Micronucleus test with benzo[a]pyrene using a single peroral administration and intraperitoneal injection in males of the MS/Ae and CD-1 mouse strains. Mutat. Res., 223(4): 353–356.
- Basu, D.K. et Saxena, J. (1978). Polynuclear aromatic hydrocarbons in selected US drinking water and their raw water sources. Environ. Sci. Technol., 12:795-798.
- Basu, D.K., Saxena, J., Stoss, F.W., Santodonato, J., Neal, M.W. et Kopfler, F.C. (1987). Comparison of drinking water mutagenicity with leaching of polycyclic aromatic hydrocarbons from water distribution pipes. Chemosphere, 16(10–12): 2595-2612.
- Blokker, E.J.M., van de Ven, B.M., de Jongh, C.M. et Slaats, P.G.G. (2013). Health implications of PAH release from coated cast iron drinking water distribution systems in the Netherlands. Environ. Health Perspect., 121(5): 600-606.
- Bock, K.W. et Bock-Hennig, B.S. (2010). UDP-glucuronosyltransferases (UGTs): from purification of Ah-receptor inducible UGT1A6 to coordinate regulation of subsets of CYPs, UGTs, and ABC transporters by nuclear receptors. Drug Metab. Rev., 42(1): 5–12.
- Bouayed, J., Bohn, T., Tybl, E., Kiemer, A.K. et Soulimani, R. (2012). Benzo[α]pyrene-induced anti-depressive-like behaviour in adult female mice: role of monoaminergic systems. Basic Clin. Pharmacol. Toxicol., 110(6): 544–550.
- Bouayed, J., Desor, F., Rammal, H., Kiemer, A.K., Tybl, E., Schroder, H., Rychen, G. et Soulimani, R. (2009). Effects of lactational exposure to benzo[α]pyrene (B[α]P) on postnatal neurodevelopment, neuronal receptor gene expression and behaviour in mice. Toxicology., 259: 97-106.
- Bradley, L.J., Magee, B.H. et Allen, S.L. (1994). Background levels of polycyclic aromatic hydrocarbons (PAH) and selected metals in New England urban soils. J. Soil Contam., 3(4): 349–361.
- Brown, R.P., Delp, M.D., Lindstedt, S.L., Rhomberg, L.R. et Beliles, R.P. (1997). Physiological parameter values for physiologically based pharmacokinetic models. Toxicol. Ind. Health, 13: 407-484.
- Brune, H., Deutsch-Wenzel, R.P., Habs, M., Ivankovic, S. et Schmähl, D. (1981). Investigation of the tumorigenic response to benzo[a]pyrene in aqueous caffeine solution applied orally to Sprague-Dawley rats. J. Cancer Res. Clin. Oncol., 102(2): 153–157.
- Butković V., Klasinc L., Orhanović M., et Turk, J. (1983). Reaction rates of polynuclear aromatic hydrocarbons with ozone in water. Environ. Sci. Technol., 17: 546-548.
- Butler, L.M., Sinha, R., Millikan, R.C., Martin, C.F., Newman, B., Gammon, M.D., Ammerman, A.S. et Sandler, R.S. (2003). Heterocyclic amines, meat intake, and association with colon cancer in a population-based study. Am. J. Epidemiol., 157(5): 434–445.
- Carlson, G.P., Fossa, A.A., Morse, M.A. et Weaver, P.M. (1986). Binding and distribution studies in the SENCAR mouse of compounds demonstrating a route-dependent tumorigenic effect. Environ. Health Perspect., 68: 53–60.
- Cavalieri, E., Rogan, E., Toth, B. et Munhall, A. (1981). Carcinogenicity of the environmental pollutants cyclopenteno-[cd]pyrene and cyclopentano[cd]pyrene in mouse skin. Carcinogenesis, 2: 277-281.
- Cavalieri, E.L. et Rogan, E.G. (1992). The approach to understanding aromatic hydrocarbon carcinogenesis. The central role of radical cations in metabolic activation. Pharmacol. Ther., 55(2): 183–199.
- Cavalieri, E.L. et Rogan, E.G. (1995). Central role of radical cations in metabolic activation of polycyclic aromatic hydrocarbons. Xenobiotica, 25(7): 677–688.
- Cavalieri, E.L., Higginbotham, S., Ramakrishna, N.V., Devanesan, P.D., Todorovic, R., Rogan, E.G. et Salmasi, S. (1991). Comparative dose-response tumorigenicity studies of benzo[alpha,I]pyrene versus 7,12-dimethylbenz[alpha]anthracene, benzo[alpha]pyrene and two dibenzo[alpha,I]pyrene dihydrodiols in mouse skin and rat mammary gland. Carcinogenesis, 12: 1939-1944.
- CCME (2010). Canadian soil quality guidelines: carcinogenic and other polycyclic aromatic hydrocarbons (PAHs) (environmental and human health effects). Document scientifique d'appui (révisé). Conseil canadien des ministres de l'Environnement (PN 1401). Disponible à : www.ccme.ca/files/Resources/supporting_scientific_documents/pah_soqg_ssd_1401.pdf
- CCN (2013). Répertoire des organismes de certification accrédités de produits, de processus et de services. Conseil canadien des normes, Ottawa (Ontario). Disponible à : /www.scc.ca/fr/accreditation/product-process-and-service-certification/directory-of-accredited-clients.
- Chakravarti, D., Pelling, J.C., Cavalieri, E.L. et Rogan, E.G. (1995). Relating aromatic hydrocarbon-induced DNA adducts and c-H-ras mutations in mouse skin papillomas: the role of apurinic sites. Proc. Natl. Acad. Sci. U.S.A., 92(22): 10422–10426.
- Chang, L.H. (1943). The fecal excretion of polycyclic hydrocarbons following their administration to the rat. J. Biol. Chem., 151(1): 93–99.
- CHEMFATE (2013). CHEMFATE entry form for Benzo[a]pyrene. SRC, Inc., Syracuse, New York. Disponible à : http://esc.syrres.com/scripts/CASCFcgi.exe?CASNUM=50328
- Chen, C., Tang, Y., Jiang, X., Qi, Y., Cheng, S., Qiu, C., Peng, B. et Tu, B. (2012). Early postnatal benzo[a]pyrene exposure in Sprague-Dawley rats causes persistent neurobehavioral impairments that emerge postnatally and continue into adolescence and adulthood. Toxicol. Sci., 125(1): 248–261.
- Chen, X., An, H., Ao, L., Sun, L., Liu, W., Zhou, Z., Wang, Y. et Cao, J. (2011). The combined toxicity of dibutyl phthalate and benzo[a]pyrene on the reproductive system of male Sprague Dawley rats in vivo. J. Hazard. Mater., 186(1): 835–841.
- CIRC (2010). Some non-heterocyclic polycyclic aromatic hydrocarbons and some related exposures. IARC Monogr. Eval. Carcinog. Risks Hum., 92: 1–853. Disponible à : http://monographs.iarc.fr/ENG/Monographs/vol92/mono92-6.pdf
- CIRC (2012). A review of human carcinogens: chemical agents and related occupations. IARC Monogr. Eval. Carcinog. Risks Hum., 100F: 111–144. Disponible à : http://monographs.iarc.fr/ENG/Monographs/vol100F/mono100F-14.pdf
- Creasia, D.A., Poggenburg, J.K., Jr. et Nettesheim, P. (1976). Elution of benzo[α]pyrene from carbon particles in the respiratory tract of mice. J. Toxicol. Environ. Health, 1(6): 967–975.
- Crittenden, J.C., Trussell, R.R., Hand, D.W., Howe, K.J. et Tchobanoglous, G. (2005). Water treatment: principles and design. 2e édition. John Wiley & Sons au nom de MWH.
- Cross, A.J., Peters, U., Kirsh, V.A., Andriole, G.L., Reding, D., Hayes, R.B. et Sinha, R. (2005). A prospective study of meat and meat mutagens and prostate cancer risk. Cancer Res., 65(24): 11779–11784.
- Cross, A.J., Ward, M.H., Schenk, M.J., Kulldorff, M., Cozen, W., Davis, S., Colt, J.S., Hartge, P., Cerhan, J.R. et Sinha, R. (2006). Meat and meat-mutagen intake and risk of non-Hodgkin lymphoma: results from a NCI-SEER case–control study. Carcinogenesis, 27(2): 293–297.
- Crowell, S.R., Amin, S.G., Anderson, K.A., Krishnegowda, G., Sharma, A.K., Soelberg, J.J., Williams, D.E. et Corley, R.A. (2011). Preliminary physiologically based pharmacokinetic models for benzo[a]pyrene and dibenzo[def,p]chrysene in rodents. Toxicol. Appl. Pharmacol., 257(3): 365–376.
- Culp, S.J., Gaylor, D.W., Sheldon, W.G., Goldstein, L.S. et Beland, F.A. (1998). A comparison of the tumors induced by coal tar and benzo[a]pyrene in a 2-year bioassay. Carcinogenesis, 19(1): 117–124.
- De Flora, S., Izzotti, A., D'Agostini, F., Rossi, G.A. et Balansky, R.M. (1993). Pulmonary alveolar macrophages in molecular epidemiology and chemoprevention of cancer. Environ. Health Perspect., 99: 249–252.
- De Jong, W.H., Kroese, E.D., Vos, J.G. et Van Loveren, H. (1999). Detection of immunotoxicity of benzo[a]pyrene in a subacute toxicity study after oral exposure in rats. Toxicol. Sci., 50(2): 214–220.
- De Stefani, E., Boffetta, P., Deneo-Pellegrini, H., Ronco, A.L., Aune, D., Acosta, G., Brennan, P., Mendilaharsu, M. et Ferro, G. (2009). Meat intake, meat mutagens and risk of lung cancer in Uruguayan men. Cancer Causes Control, 20(9): 1635–1643.
- de Waard, W.J., Aarts, J.M.M.J.G., Peijnenburg, A.A.C.M., Baykus, H., Talsma, E., Punt, A., de Kok, T.M.C.M., van Schooten, F.J. et Hoogenboom, L.A.P. (2008). Gene expression profiling in Caco-2 human colon cells exposed to TCDD, benzo[a]pyrene, and natural Ah receptor agonists from cruciferous vegetables and citrus fruits. Toxicol. In Vitro, 22(2): 396–410.
- Dean, J.H., Luster, M.I., Boorman, G.A., Lauer, L.D., Leubke, R.W. et Lawson, L. (1983). Selective immunosuppression resulting from exposure to the carcinogenic congener of benzopyrene in B6C3F1 mice. Clin. Exp. Immunol., 52(1): 199–206.
- DeMarini, D.M., Landi, S., Tian, D., Hanley, N.M., Li, X., Hu, F., Roop, B.C., Mass, M.J., Keohavong, P., Gao, W., Olivier, M., Hainaut, P. et Mumford, J.L. (2001). Lung tumor KRAS and TP53 mutations in nonsmokers reflect exposure to PAH-rich coal combustion emissions. Cancer Res., 61(18): 6679–6681.
- DiGiovanni, J., Beltran, L., Rupp, A., Harvey, R.G. et Gill, R.D. (1993). Further analysis of c-Ha-ras mutations in papillomas initiated by several polycyclic aromatic hydrocarbons and papillomas from uninitiated, promoter-treated skin in SENCAR mice. Mol. Carcinog., 8(4): 272–279.
- Duarte-Salles, T., Mendez, M.A., Morales, E., Bustamante, M., Rodríguez-Vicente, A., Kogevinas, M. et Sunyer, J. (2012). Dietary benzo[a]pyrene and fetal growth: effect modification by vitamin C intake and glutathione S-transferase P1 polymorphism. Environ. Int., 45(1): 1–8.
- Ekwall, P., Ermala, P. et Setala, K. (1951). Gastric absorption of 3,4-benzpyrene. II. The significance of the solvent for the penetration of 3,4-benzpyrene into the stomach wall. Cancer Res., 11(10): 758–763.
- El-Bayoumy, K., Chae, Y.H., Upadhyaya, P., Rivenson, A., Kurtzke, C., Reddy, B. et Hecht, S.S. (1995). Comparative tumorigenicity of benzo[a]pyrene, 1-nitropyrene and 2-amino-1-methyl-6-phenylimidazo[4,5-b]pyridine administered by gavage to female CD rats. Carcinogenesis, 16(2): 431–434.
- El-Bayoumy, K., Hecht, S.S., et Hoffmann, D. (1982). Comparative tumor initiating activity on mouse skin of 6-nitrobenzo[a]pyrene, 6-nitrochrysene, 3-nitroperylene, 1-nitropyrene and their parent hydrocarbons. Cancer Lett., 16: 333-337.
- Ermala, P., Setala, K. et Ekwall, P. (1951). Gastric absorption of 3,4-benzpyrene. I. The effect of physiological processes on absorption. Cancer Res., 11(10): 753–757.
- Fang, A.H., Smith, W.A., Vouros, P. et Gupta, R.C. (2001). Identification and characterization of a novel benzo[a]pyrene-derived DNA adduct. Biochem. Biophys. Res. Commun., 281(2): 383–389.
- Ferrucci, L.M., Sinha, R., Huang, W.Y., Berndt, S.I., Katki, H.A., Schoen, R.E., Hayes, R.B. et Cross, A.J. (2012). Meat consumption and the risk of incident distal colon and rectal adenoma. Br. J. Cancer, 106(3): 608–616.
- Fischer, A., Koeper, L.M. et Vohr, H.W. (2011). Specific antibody responses of primary cells from different cell sources are able to predict immunotoxicity in vitro. Toxicol. In Vitro, 25(8): 1966–1973.
- Forster, K., Preuss, R., Rossbach, B., Bruning, T., Angerer, J. et Simon, P. (2008). 3-Hydroxybenzo[a]pyrene in the urine of workers with occupational exposure to polycyclic aromatic hydrocarbons in different industries. Occup. Environ. Med., 65(4): 224–229.
- Foth, H., Kahl, R. et Kahl, G.F. (1988). Pharmacokinetics of low doses of benzo[a]pyrene in the rat. Food Chem. Toxicol., 26(1): 45–51.
- Friesen, M.C., Demers, P.A., Spinelli, J.J., Lorenzi, M.F. et Le, N.D. (2007). Comparison of two indices of exposure to polycyclic aromatic hydrocarbons in a retrospective aluminium smelter cohort. Occup. Environ. Med., 64(4): 273–278.
- Fronk, C.A. (1987). Destruction of volatile organic contaminants in drinking water by ozone treatment. Ozone Sci. Eng., 9: 265-288.
- Fu, Z., Deming, S.L., Fair, A.M., Shrubsole, M.J., Wujcik, D.M., Shu, X.O., Kelley, M. et Zheng, W. (2011). Well-done meat intake and meat-derived mutagen exposures in relation to breast cancer risk: the Nashville Breast Health Study. Breast Cancer Res. Treat., 129(3): 919–928.
- Garg, R., Gupta, S. et Maru, G.B. (2008). Dietary curcumin modulates transcriptional regulators of phase I and phase II enzymes in benzo[a]pyrene-treated mice: mechanism of its anti-initiating action. Carcinogenesis, 29(5): 1022–1032.
- Garner, R.C., Stanton, C.A., Martin, C.N., Harris, C.C. et Grafstrom, R.C. (1985). Rat and human explant metabolism, binding studies, and DNA adduct analysis of benzo[a]pyrene and its 6-nitro derivative. Cancer Res., 45(12): 6225–6231.
- Godschalk, R.W., Ostertag, J.U., Moonen, E.J., Neumann, H.A., Kleinjans, J.C. et van Schooten, F.J. (1998). Aromatic DNA adducts in human white blood cells and skin after dermal application of coal tar. Cancer Epidemiol. Biomarkers Prev., 7(9): 767-773.
- Gouvernement du Canada (1991). Les produits chimiques toxiques dans les Grands Lacs et leurs effets connexes. Vol. I. Les concentrations et les tendances des contaminants. Vol II. Les effets des contaminants.Environnement Canada, ministère des Pêches et des Océans et Santé Canada, Ottawa, Ontario (En 37-95/1990-1E).
- Grova, N., Schroeder, H., Farinelle, S., Prodhomme, E., Valley, A. et Muller, C.P. (2008). Sub-acute administration of benzo[a]pyrene (B[a]P) reduces anxiety-related behaviour in adult mice and modulates regional expression of N-methyl-d-aspartate (NMDA) receptors genes in relevant brain regions. Chemosphere, 73(1 Suppl.): S295–S302.
- Gunter, M.J., Probst-Hensch, N.M., Cortessis, V.K., Kulldorff, M., Haile, R.W. et Sinha, R. (2005). Meat intake, cooking-related mutagens and risk of colorectal adenoma in a sigmoidoscopy-based case–control study. Carcinogenesis, 26(3): 637–642.
- Gwinn, M.R. et Weston, A. (2008). Application of oligonucleotide microarray technology to toxic occupational exposures. J. Toxicol. Environ. Health A, 71(5): 315–324.
- Gwinn, M.R., Keshava, C., Olivero, O.A., Humsi, J.A., Poirier, M.C. et Weston, A. (2005). Transcriptional signatures of normal human mammary epithelial cells in response to benzo[a]pyrene exposure: a comparison of three microarray platforms. OMICS, 9(4): 334–350.
- Habs, M., Jahn, S.A.A. et Schmahl, D. (1984). Carcinogenic activity of condensate from coloquint seeds (Citrullus colocynthis) after chronic epicutaneous administration to mice. J. Cancer Res. Clin. Oncol., 108(1): 154–156.
- Habs, M., Schmahl, D. et Misfeld, J. (1980). Local carcinogenicity of some environmentally relevant polycyclic aromatic hydrocarbons after lifelong topical application to mouse skin. Arch Geschwulstforsch., 50: 266-274.
- Haddad, S., Withey, J., Laparé, S., Law, F. et Krishnan, K. (1998). Physiologically-based pharmacokinetic modeling of pyrene in the rat. Environ. Toxicol. Pharmacol., 5(4): 245–255.
- Hakami, R., Mohtadinia, J., Etemadi, A., Kamangar, F., Nemati, M., Pourshams, A., Islami, F., Nasrollahzadeh, D., Saberi-Firoozi, M., Birkett, N., Boffetta, P. et Malekzadeh, R. (2008). Dietary intake of benzo[a]pyrene and risk of esophageal cancer in north of Iran. Nutr. Cancer, 60(2): 216–221.
- Halappanavar, S., Wu, D., Williams, A., Kuo, B., Godschalk, R.W., Van Schooten, F.J. et Yauk, C.L. (2011). Pulmonary gene and microRNA expression changes in mice exposed to benzo[a]pyrene by oral gavage. Toxicology, 285(3): 133–141.
- Hammond, D. et O'Connor, R.J. (2008). Constituents in tobacco and smoke emissions from Canadian cigarettes. Tobacco Control, 17: 24–31.
- Harper, P.A., Wong, J.M.Y., Lam, M.S.M. et Okey, A.B. (2002). Polymorphisms in the human AH receptor. Chem. Biol. Interact., 141(1–2): 161–187.
- Hattemer-Frey, H.A. et Travis, C.C. (1991). Benzo-a-pyrene: environmental partitioning and human exposure. Toxicol. Ind. Health, 7(3): 141–157.
- Haugen, A., Becher, G., Benestad, C., Vahakangas, K., Trivers, G.E., Newman, M.J. et Harris, C.C. (1986). Determination of polycyclic aromatic hydrocarbons in the urine, benzo[a]pyrene diol epoxide–DNA adducts in lymphocyte DNA, and antibodies to the adducts in sera from coke oven workers exposed to measured amounts of polycyclic aromatic hydrocarbons in the work atmosphere. Cancer Res., 46(8): 4178–4183.
- He, S. and Baker, R.S.U. (1991). Micronuclei in mouse skin cells following in vivo exposure to benzo[a]pyrene, 7,12-dimethylbenz[a]anthracene, chrysene, pyrene and urethane. Environ. Mol. Mutagen., 17(3): 163–168.
- Hemminki, K., Grzybowska, E., Chorazy, M., Twardowska-Saucha, K., Sroczynski, J.W., Putman, K.L., Randerath, K., Phillips, D.H. et Hewer, A. (1990). Aromatic DNA adducts in white blood cells of coke workers. Int. Arch. Occup. Environ. Health, 62(6): 467–470.
- Heredia-Ortiz, R., Bouchard, M., Marie-Desvergne, C., Viau, C. et Maitre, A. (2011). Modeling of the internal kinetics of benzo[a]pyrene and 3-hydroxybenzo[a]pyrene biomarker from rat data. Toxicol. Sci., 122(2): 275–287.
- Hernandez, L.G., Slob, W., van Steeg, H. et van Benthem, J. (2011). Can carcinogenic potency be predicted from in vivo genotoxicity data?: a meta-analysis of historical data. Environ. Mol. Mutagen., 52(7): 518–528.
- Hirano, M., Tanaka, S. et Asami, O. (2013). Classification of polycyclic aromatic hydrocarbons based on mutagenicity in lung tissue through DNA microarray. Environ. Toxicol., 28(11): 652-659.
- Hockley, S.L., Arlt, V.M., Brewer, D., Giddings, I. et Phillips, D.H. (2006). Time- and concentration-dependent changes in gene expression induced by benzo[a]pyrene in two human cell lines, MCF-7 and HepG2. BMC Genomics, 7: 260. Disponible à : www.biomedcentral.com /1471-2164/7-260.
- Hockley, S.L., Arlt, V.M., Jahnke, G., Hartwig, A., Giddings, I. et Phillips, D.H. (2008). Identification through microarray gene expression analysis of cellular responses to benzo[a]pyrene and its diol-epoxide that are dependent or independent of p53. Carcinogenesis, 29(1): 202–210.
- Hockley, S.L., Mathijs, K., Staal, Y.C.M., Brewer, D., Giddings, I., Van Delft, J.H.M. et Phillips, D.H. (2009). Interlaboratory and interplatform comparison of microarray gene expression analysis of HepG2 cells exposed to benzo[a]pyrene. OMICS, 13(2): 115–125.
- Hrubá, E., Vondrácek, J., Líbalová, H., Topinka, J., Bryja, V., Soucek, K. et Machala, M. (2011). Gene expression changes in human prostate carcinoma cells exposed to genotoxic and nongenotoxic aryl hydrocarbon receptor ligands. Toxicol. Lett., 206(2): 178–188.
- HSDB (2011). Benzo[a]pyrene. Hazardous Substances Data Bank, U.S. National Library of Medicine, Bethesda, Maryland. Disponible à : http://toxnet.nlm.nih.gov
- Irwin, R. J. (1997). Benzo[a]pyrene (BaP). In: Environmental contaminants encyclopedia. Water Operations Branch, Water Resources Division, U.S. National Park Service, Fort Collins, Colorado.
- Izzotti, A., Balansky, R., Scatolini, L. et Coscia, N. (1991). Research on adducts of benzo[a]pyrene and DNA in different cells using synchronous fluorescence spectrophotometry. Boll. Soc. Ital. Biol. Sper., 67(9): 869–874.
- Jin, X., Peldszus, S. et Huck, P.M. (2012). Reaction kinetics of selected micropollutants in ozonation and advanced oxidation processes. Water Res., 46(19): 6519-6530.
- Jules, G.E., Pratap, S., Ramesh, A. et Hood, D.B. (2012). In utero exposure to benzo[a]pyrene predisposes offspring to cardiovascular dysfunction in later-life. Toxicology, 295(1–3): 56–67.
- Kao, J., Patterson, F.K. et Hall, J. (1985). Skin penetration and metabolism of topically applied chemicals in six mammalian species, including man: an in vitro study with benzo[a]pyrene and testosterone. Toxicol. Appl. Pharmacol., 81(3): 502–516.
- Kazerouni, N., Sinha, R., Hsu, C.H., Greenberg, A. et Rothman, N. (2001). Analysis of 200 food items for benzo[a]pyrene and estimation of its intake in an epidemiologic study. Food Chem. Toxicol., 39(5): 423–436.
- Keshava, C., Whipkey, D. et Weston, A. (2005). Transcriptional signatures of environmentally relevant exposures in normal human mammary epithelial cells: benzo[a]pyrene. Cancer Lett., 221(2): 201–211.
- Knaapen, A.M., Curfs, D.M., Pachen, D.M., Gottschalk, R.W., de Winther, M.P., Daemen, M.J. et Van Schooten, F.J. (2007). The environmental carcinogen benzo[a]pyrene induces expression of monocyte-chemoattractant protein-1 in vascular tissue: a possible role in atherogenesis. Mutat. Res., 621(1–2): 31–41.
- Knuckles, M.E., Inyang, F. et Ramesh, A. (2001). Acute and subchronic oral toxicities of benzo[a]pyrene in F-344 rats. Toxicol. Sci., 61(2): 382–388.
- Kolpin, D.W., Furlong, E.T., Meyer, M.T., Thurman, E.M., Zaugg, S.D., Barber, L.B., Buxton, H.T. (2002). Pharmaceuticals, hormones, and other organic wastewater contaminants in U.S. streams, 1999-2000: a national reconnaissance. Environ. Sci. Technol., 36(6): 1202-1211.
- Krishnan, K. et Carrier, R. (2008). Approaches for evaluating the relevance of multiroute exposures in establishing guideline values for drinking water contaminants. J. Environ. Sci. Health C Environ. Carcinog. Ecotoxicol. Rev., 26(3): 300–316.
- Krishnan, K. et Carrier, R. (2013). The use of exposure source allocation factor in the risk assessment of drinking-water contaminants. J. Toxicol. Environ. Health B Crit. Rev., 16 (1): 39-51.
- Kristensen, P., Eilertsen, E., Einarsdottir, E., Haugen, A., Skaug, V. et Ovrebo, S. (1995). Fertility in mice after prenatal exposure to benzo[a]pyrene and inorganic lead. Environ. Health Perspect., 103(6): 588-590.
- Kristensen, P., Eilertsen, E., Einarsdottir, E., Haugen, A., Skaug, V. et Ovrebo, S. (1995). Fertility in mice after prenatal exposure to benzo[a]pyrene and inorganic lead. Environ. Health Perspect., 103(6): 588–590.
- Kroese, E., Muller, J., Mohn, G. et Dortant, P.W. (2001). Tumorigenic effects in Wistar rats orally administered benzo[a]pyrene for two years (gavage studies). Implications for human cancer risks associated with oral exposure to polycyclic aromatic hydrocarbons. National Institute of Public Health and the Environment (RIVM), Bilthoven, Pays-Bas.
- Labib, S., Yauk, C., Williams, A., Arlt, V., Phillips, D.H., White, P. et Halappanavar, S. (2012). Sub-chronic oral exposure to benzo[a]pyrene leads to distinct transcriptomic changes in the lungs that are related to carcinogenesis. Toxicol. Sci., 129(1): 213–224.
- Lan, Q., Mumford, J.L., Shen, M., DeMarini, D.M., Bonner, M.R., He, X., Yeager, M., Welch, R., Chanock, S., Tian, L., Chapman, R.S., Zheng, T., Keohavong, P., Caporaso, N. et Rothman, N. (2004). Oxidative damage–related genes AKR1C3 and OGG1 modulate risks for lung cancer due to exposure to PAH-rich coal combustion emissions. Carcinogenesis, 25(11): 2177–2181.
- LaVoie, E.J., Amin, S., Hecht, S.S., Furuya, K., et Hoffmann. (1982). Tumour initiating activity of dihydrodiols of benzo[b]fluoranthene, benzo[j]fluoranthene, and benzo[k]fluoranthene. Carcinogenesis, 3(1): 49-52.
- Lemieux, C.L., Douglas, G.R., Gingerich, J., Phonethepswath, S., Torous, D.K., Dertinger, S.D., Phillips, D.H., Arlt, V.M. et White, P.A. (2011). Simultaneous measurement of benzo[a]pyrene-induced Pig-a and lacZ mutations, micronuclei and DNA adducts in Muta Mouse. Environ. Mol. Mutagen., 52(9): 756–765.
- Li, D., Day, R.S., Bondy, M.L., Sinha, R., Nguyen, N.T., Evans, D.B., Abbruzzese, J.L. et Hassan, M.M. (2007). Dietary mutagen exposure and risk of pancreatic cancer. Cancer Epidemiol. Biomarkers Prev., 16(4): 655–661.
- Li, J.Z., Pan, H.Y., Zheng, J.W., Zhou, X.J., Zhang, P., Chen, W.T. et Zhang, Z.Y. (2008). Benzo (a) pyrene induced tumorigenesity[sic] of human immortalized oral epithelial cells: transcription profiling. Chin. Med. J. (en anglais), 121(19): 1882–1890.
- Liu, Z., Muehlbauer, K.R., Schmeiser, H.H., Hergenhahn, M., Belharazem, D. et Hollstein, M.C. (2005). P53 mutations in benzo[a]pyrene-exposed human P53 knock-in murine fibroblasts correlate with P53 mutations in human lung tumors. Cancer Res., 65(7): 2583–2587.
- Lizarraga, D., Gaj, S., Brauers, K.J., Timmermans, L., Kleinjans, J.C. et Van Delft, J.H.M. (2012). Benzo[a]pyrene-induced changes in microRNA–mRNA networks. Chem. Res. Toxicol., 25(4): 838–849.
- Lu, X., Shao, J., Li, H. et Yu, Y. (2009). Early whole-genome transcriptional response induced by benzo[a]pyrene diol epoxide in a normal human cell line. Genomics, 93(4): 332–342.
- Lu, X., Shao, J., Li, H. et Yu, Y. (2010). Temporal gene expression changes induced by a low concentration of benzo[a]pyrene diol epoxide in a normal human cell line. Mutat. Res., 684(1–2): 74–80.
- Mackay, D. et Paterson, S. (1991). Evaluating the multimedia fate of organic chemicals: a level III fugacity model. Environ. Sci. Technol., 25(3): 427–436.
- Mackenzie, K.M. et Angevine, D.M. (1981). Infertility in mice exposed in utero to benzo[a]pyrene. Biol. Reprod., 24(1): 183–191.
- Maier M., Maier D., et Lloyd B.J. (2000). Factors influencing the mobilisation of polycyclic aromatic hydrocarbons (PAHs) from the coal-tar lining of water mains. Water Res., 34(3): 773-786.
- Malik, A.I., Williams, A., Lemieux, C.L., White, P.A. et Yauk, C.L. (2012). Hepatic mRNA, microRNA, and miR-34a-target responses in mice after 28 days exposure to doses of benzo[a]pyrene that elicit DNA damage and mutation. Environ. Mol. Mutagen., 53(1): 10–21.
- Marie, C., Bouchard, M., Heredia-Ortiz, R., Viau, C. et Maître, A. (2010). A toxicokinetic study to elucidate 3-hydroxybenzo[a]pyrene atypical urinary excretion profile following intravenous injection of benzo[a]pyrene in rats. J. Appl. Toxicol., 30(5): 402–410.
- Mass, M.J., Jeffers, A.J., Ross, J.A., Nelson, G., Galati, A.J., Stoner, G.D. et Nesnow, S. (1993). Ki-ras oncogene mutations in tumors and DNA adducts formed by benz[j]aceanthrylene and benzo[a]pyrene in the lungs of strain A/J mice. Mol. Carcinog., 8(3): 186–192.
- Meinl, W., Ebert, B., Glatt, H. et Lampen, A. (2008). Sulfotransferase forms expressed in human intestinal Caco-2 and TC7 cells at varying stages of differentiation and role in benzo[a]pyrene metabolism. Drug Metab. Dispos., 36(2): 276–283.
- Michaelson, J.J., Trump, S., Rudzok, S., Gräbsch, C., Madureira, D.J., Dautel, F., Mai, J., Attinger, S., Schirmer, K., von Bergen, M., Lehmann, I. et Beyer, A. (2011). Transcriptional signatures of regulatory and toxic responses to benzo-[a]-pyrene exposure. BMC Genomics, 12: 502 (doi:10.1186/1471-2164-12-502).
- Ministère de l'Environnement de l'Ontario (2013). Communication personnelle de S. Deshpande.
- Ministère de la Santé de la Colombie-Britannique. (2013). Communication personnelle de B. Boettger.
- Ministère de la Santé et du Mieux-être du Nouveau-Brunswick. (2013). Communication personnelle avec K. Gould.
- Ministère du Développement durable, de l'Environnement, de la Faune et des Parcs du Québec (2013). Communication personnelle de C. Robert.
- Moffat, I., Chepelev, N.L., Labib, S., Bourdon-Lacombe, J., Kuo, B., Buick, J.K., Lemieux, F., Williams, A., Halappanavar, S., Malik, A.I., Luijten, M., Aubrecht, J., Hyduke, D.R., Fornace, A.J. Jr, Swartz, C.D., Recio, L. et Yauk, C.L. (2015). Comparison of toxicogenomics and traditional approaches to inform mode of action and points of departure in human health risk assessment of benzo[a]pyrene in drinking water. Crit. Rev. Toxicol., 45(1):1–43.
- Moir, D., Viau, A., Chu, I., Withey, J. et McMullen, E. (1998). Pharmacokinetics of benzo[a]pyrene in the rat. J. Toxicol. Environ. Health, 53(7): 507–530.
- Mullaart, E., Buytenhek, M., Brouwer, A., Lohman, P.H.M. et Vijg, J. (1989). Genotoxic effects of intragastrically administered benzo[a]pyrene in rat liver and intestinal cells. Carcinogenesis, 10(2): 393–395.
- Mumford, J.L., Lee, X., Lewtas, J., Young, T.L. et Santella, R.M. (1993). DNA adducts as biomarkers for assessing exposure to polycyclic aromatic hydrocarbons in tissues from Xuan Wei women with high exposure to coal combustion emissions and high lung cancer mortality. Environ. Health Perspect., 99: 83–87.
- Nakamura, B.N., Mohar, I., Lawson, G.W., Cortes, M.M., Hoang, Y.D., Ortiz, L., Patel, R., Rau, B.A., McConnachie, L.A., Kavanagh, T.J. et Luderer, U. (2012). Increased sensitivity to testicular toxicity of transplacental benzo[a]pyrene exposure in male glutamate cysteine ligase modifier subunit knockout (Gclm−/−) mice. Toxicol. Sci., 126(1): 227–241.
- Neal, J. et Rigdon, R.H. (1967). Gastric tumors in mice fed benzo[a]pyrene: a quantitative study. Tex. Rep. Biol. Med., 25(4): 553–557.
- Nova Scotia Department of Environment and Labor. (2013). Communication personnelle avec Christina Mosher.
- NSF/ANSI (2012). NSF International/American National Standards Institute Standard 61: Drinking water system components—health effects. NSF International, Ann Arbor, Michigan.
- OEHHA (2010). Public health goals for chemicals in drinking water: benzo[a]pyrene. Office of Environmental Health Hazard Assessment, California Environmental Protection Agency, Sacramento, Californie). Disponible à : www.oehha.ca.gov/water/phg/pdf/091610Benzopyrene.pdf
- OMS (1998). Selected non-heterocyclic polycyclic aromatic hydrocarbons. Environmental Health Criteria 202. Programme international sur la sécurité des substances chimiques, Organisation mondiale de la Santé, Genève (Suisse). Disponible à : www.inchem.org/documents/ehc/ehc/ehc202.htm
- OMS (2003). Polynuclear aromatic hydrocarbons in drinking-water: background document for development of WHO Guidelines for Drinking-water quality. Organisation mondiale de la Santé, Genève (Suisse). WHO/SDE/WSH/03.04/59. Disponible à : www.who.int/water_sanitation_health/dwq/chemicals/polyaromahydrocarbons.pdf
- OMS (2011). Guidelines for drinking-water quality. 4th edition. Organisation mondiale de la Santé, Genève (Suisse). Disponible à : www.who.int/water_sanitation_health/publications/2011/dwq_guidelines/en/index.html
- Pan, G., Hanaoka, T., Yamano, Y., Hara, K., Ichiba, M., Wang, Y., Zhang, J., Feng, Y., Shujuan, Z., Guan, D., Gao, G., Liu, N. et Takahashi, K. (1998). A study of multiple biomarkers in coke oven workers—A cross-sectional study in China. Carcinogenesis, 19(11): 1963–1968.
- Perera, F.P., Hemminki, K., Young, T.L., Brenner, D., Kelly, G. et Santella, R.M. (1988). Detection of polycyclic aromatic hydrocarbon–DNA adducts in white blood cells of foundry workers. Cancer Res., 48(8): 2288–2291.
- Perera, F.P., Rauh, V., Whyatt, R.M., Tsai, W.Y., Bernert, J.T., Tu, Y.H., Andrews, H., Ramirez, J., Qu, L. et Tang, D. (2004). Molecular evidence of an interaction between prenatal environmental exposure and birth outcomes in a multiethnic population. Environ. Health Perpect., 112: 626-630.
- Perera, F.P., Tang, D., Rauh, V., Lester, K., Tsai, W.Y., Tu, Y.H., Weiss, L., Hoepner, L., Del Priore, G. et Lederman, S.A. (2005). Relationship among polycyclic aromatic hydrocarbon-DNA adducts, proximity to the World Trade Center, and effects on fetal growth. Environ. Health Perpect., 113: 1062-1067.
- Phillips, D.H. (1999). Polycyclic aromatic hydrocarbons in the diet. Mutat. Res., 443: 139-147.
- Poel, W.E. (1959). Effect of carcinogenic dosage and duration of exposure on skin-tumor induction in mice. J. Natl. Cancer Inst., 22: 19-43.
- Poel, W.E. (1963). Skin as a test site for the bioassay of carcinogens and carcinogen precursors. Natl. Cancer Inst. Monogr., 10: 611–625.
- Proctor, D.M., Gatto, N.M., Hong, S.J. et Allamneni, K.P. (2007). Mode-of-action framework for evaluating the relevance of rodent forestomach tumors in cancer risk assessment. Toxicol. Sci., 98(2): 313–326.
- Pucknat, A.W. (éd.) (1981). Health impacts of polynuclear aromatic hydrocarbons. Noyes Data Corp., Park Ridge, NJ, 271 pp. (Environmental Health Review No. 5).
- Ramesh, A., Greenwood, M., Inyang, F. et Hood, D.B. (2001a). Toxicokinetics of inhaled benzo[a]pyrene: plasma and lung bioavailability. Inhal. Toxicol., 13(6): 533–555.
- Ramesh, A., Hood, D.B., Inyang, F., Greenwood, M., Nyanda, A.M., Archibong, A.E. et Knuckles, M.E. (2002). Comparative metabolism, bioavailability, and toxicokinetics of benzo[a]pyrene in rats after acute oral, inhalation, and intravenous administration. Polycycl. Aromat. Compd., 22(3–4): 969–980.
- Ramesh, A., Inyang, F., Hood, D.B., Archibong, A.E., Knuckles, M.E. et Nyanda, A.M. (2001b). Metabolism, bioavailability, and toxicokinetics of benzo(α)pyrene in F-344 rats following oral administration. Exp. Toxicol. Pathol., 53(4): 275–290.
- Ringuette, S., Germain, A., Gonthier, C. et Perron, F. (1993). Présence des HAP dans l'environnement canadien : portrait de la situation. Préparé pour Environnement Canada, Conservation et protection, Région du Québec, Montréal (Québec) (Liste des substances d'intérêt prioritaire. Document de support nº 2).
- Roe, F.J., Peto, R., Kearns, F. et Bishop, D. (1970). The mechanism of carcinogenesis by the neutral fraction of cigarette smoke condensate. Br. J. Cancer, 24: 788-806.
- Roszinsky-Kocher, G., Basler, A. et Roehrborn, G. (1979). Mutagenicity of polycyclic hydrocarbons. V. Induction of sister-chromatid exchanges in vivo. Mutat. Res., 66(1): 65–67.
- RTECS (1994). Registry of Toxic Effects of Chemical Substances. MEDLARS Online Information Retrieval System, U.S. National Library of Medicine, Bethesda, Maryland.
- Salamone, M.F. (1981). Toxicity of 41 carcinogens and noncarcinogenic analogs. Dans : de Serres, F.J. et Ashby, J. (éd.). Progress in mutation research. Vol. 1. Evaluation of short-term tests for carcinogens. Report of the international corroborative program. Elsevier-North Holland, Amsterdam (Pays-Bas), p. 682–685.
- Sanches, S., Leitão, C., Penetra, A., Cardoso, V.V., Ferreira, E., Benoliel, M.J., Crespo, M.T. et Pereira, V.J. (2011). Direct photolysis of polycyclic aromatic hydrocarbons in drinking water sources. J Hazard. Mater., 192(3):1458-65.
- Santodonato, J., Howard, P. et Basu, D. (1981). Health and ecological assessment of polynuclear aromatic hydrocarbons. J. Environ. Pathol. Toxicol., 5(1): 1–364.
- Saskatchewan Water Security Agency (2013). Communication personnelle de S. Ferris.
- Saunders, C.R., Das, S.K., Ramesh, A., Shockley, D.C. et Mukherjee, S. (2006). Benzo[a]pyrene-induced acute neurotoxicity in the F-344 rat: role of oxidative stress. J. Appl. Toxicol., 26(5): 427–438.
- Shendrikova, I.A. et Aleksandrov, V.A. (1974). Comparative penetration of polycyclic hydrocarbons through the rat placenta into the fetus. Bull. Exp. Biol. Med., 77(2): 169–171.
- Shertzer, H.G., Clay, C.D., Genter, M.B., Chames, M.C., Schneider, S.N., Oakley, G.G., Nebert, D.W. et Dalton, T.P. (2004). Uncoupling-mediated generation of reactive oxygen by halogenated aromatic hydrocarbons in mouse liver microsomes. Free Radic. Biol. Med., 36(5): 618–631.
- Shi, Z., Dragin, N., Gálvez-Peralta, M., Jorge-Nebert, L.F., Miller, M.L., Wang, B. et Nebert, D.W. (2010). Organ-specific roles of CYP1A1 during detoxication of dietary benzo[a]pyrene. Mol. Pharmacol., 78(1): 46–57.
- Shimada, T., Martin, M.V., Pruess-Schwartz, D., Marnett, L.J. et Guengerich, F.P. (1989). Roles of individual human cytochrome P-450 enzymes in the bioactivation of benzo[a]pyrene, 7,8-dihydroxy-7,8-dihydrobenzo[a]pyrene, and other dihydrodiol derivatives of polycyclic aromatic hydrocarbons. Cancer Res., 49(22): 6304–6312.
- Shimizu, Y., Nakatsuru, Y., Ichinose, M., Takahashi, Y., Kume, H., Mimura, J., Fujii-Kuriyama, Y. et Ishikawa, T. (2000). Benzo[a]pyrene carcinogenicity is lost in mice lacking the aryl hydrocarbon receptor. Proc. Natl. Acad. Sci. U.S.A., 97(2): 779–782.
- Shum, S., Jensen, N.M. et Nebert, D.W. (1979). The murine Ah locus: in utero toxicity and teratogenesis associated with genetic differences in benzo[a]pyrene metabolism. Teratology, 20(3): 365–376.
- Sinha, R., Kulldorff, M., Gunter, M.J., Strickland, P. et Rothman, N. (2005a). Dietary benzo[a]pyrene intake and risk of colorectal adenoma. Cancer Epidemiol. Biomarkers Prev., 14(8): 2030–2034.
- Sinha, R., Peters, U., Cross, A.J., Kulldorff, M., Weissfeld, J.L., Pinsky, P.F., Rothman, N. et Hayes, R.B. (2005b). Meat, meat cooking methods and preservation, and risk for colorectal adenoma. Cancer Res., 65(17): 8034–8041.
- Sivak, A., Niemeier, R., Lynch, D., Beltis, K., Simon, S., Salomon, R., Latta, R., Belinky, B., Menzies, K., Lunsford, A., Cooper, C, Ross, A. et Bruner, R. (1997). Skin carcinogenicity of condensed asphalt roofing fumes and their fractions following dermal application to mice. Cancer Lett., 117: 113-123.
- Slaga, T.J., Gleason, G.L., Mills, G., Ewald, L., Fu, P.P., Lee, H.M., et Harvey, R.G. (1980). Comparison of the skin tumor-initiating activities of dihydrodiols and diol-epoxides of various polycyclic aromatic hydrocarbons. Cancer Res., 40: 1981-1984.
- Slaga, T.J., Huberman, E., Selkirk, J.K., Harvey, R.G., et Bracken, W.M. (1978). Carcinogenicity and mutagenicity of benz(a)anthracene diols and diol-epoxides. Cancer Res., 38: 1699-1704.
- Snoeyink, V.L. (1990). Adsorption of organic compounds. Dans : Water quality and treatment. 4e édition. American Water Works Association, Denver, Colorado.
- Snyder, S.A., Wert, E.C., Lei, H., Westerhoff, P. et Yoon, Y. (2007) Removal of EDCs and pharmaceuticals in drinking and reuse treatment processes. AWWA Research Foundation, American Water Works Association, Denver, Colorado (Report No. 91188).
- Sorrell, R.K., Brass, H. J., et Reding, R. (1980). A review of occurrences and treatment of polynuclear aromatic hydrocarbons in water, Environ.Int., 4(3): 245-254.
- Speth, T.F. (1990). Removal of volatile organic compounds from drinking water by adsorption. Dans : Ram, N.M., Christman, R.F. et Cantor, K.P. (éd.). Significance and treatment of volatile organic compounds in water supplies. Lewis Publishers, Chelsea, Michigan.
Srinivasan K.R. et Folger H.S. (1990). Use of inorgano-organo-clays in the removal of priority pollutants from industrial wastewaters: adsorption of benzo[a]pyrene and chlorophenols from aqueous solutions. Clay Clay Miner., 38(3): 287-293. - Stackelberg, P.E., Furlong, E.T., Meyer, M.T., Zaugg, S.D., Henderson, A.K. et Reissman, D.B. (2004). Persistence of pharmaceutical compounds and other organic wastewater contaminants in a conventional drinking-water-treatment plant. Sci. Total Environ., 329: 99-113.
Stackelberg, P.E., Gibs, J., Furlong, E.T., Meyer, M.T., Zaugg, S.D., et Lippincott, R.L. (2007). Efficiency of conventional drinking-water-treatment processes in removal of pharmaceuticals and other organic compounds. Sci. Total Environ., 377: 255-272. - Straif, K., Baan, R., Grosse, Y., Secretan, B., El Ghissassi, F., Cogliano, V., Drewski, D., Partanen, T., Vähäkangas, K., Stücker, I., Borlak, J., Feron, V.J., Marques, M.M., Gustavsson, P., Fletcher, T., Arey, J., Beland, F.A., Burchiel, S., Flowers, L., Herbert, R.A., Mukhtar, H., Nesnow, S., Penning, T.M., Sinha, R. et Shimada, T. (2005). Carcinogenicity of polycyclic aromatic hydrocarbons. Lancet Oncol., 6(12): 931–932.
- Sun, J.D., Wolff, R.K. et Kanapilly, G.M. (1982). Deposition, retention, and biological fate of inhaled benzo[a]pyrene adsorbed onto ultrafine particles and as a pure aerosol. Toxicol. Appl. Pharmacol., 65(2): 231–244.
- Tang, D., Li, T.Y, Liu, J.J., Chen, Y.H., Qu, L. et Perera, F. (2006). PAH-DNA adducts in cord blood and fetal and child development in a Chinese cohort. Environ. Health Perspect., 114: 1297-1300.
- Thyssen, J., Althoff, J., Kimmerle, G. et Mohr, U. (1981). Inhalation studies with benzo[a]pyrene in Syrian golden hamsters. J. Natl. Cancer Inst., 66(3): 575–577.
- Tram, K.L., Cross, A.J., Consonni, D., Randi, G., Bagnardi, V., Bertazzi, P.A., Caporaso, N.E., Sinha, R., Subar, A.F. et Landi, M.T. (2009). Intakes of red meat, processed meat, and meat mutagens increase lung cancer risk. Cancer Res., 69(3): 932–939.
- Trenholm, R.A., Vanderford, B.J., Holady, J.C., Rexing, D.J., et Snyder, S.A. (2006). Broad range analysis of endocrine disruptors and pharmaceuticals using gas chromatography and liquid chromatography tandem mass spectrometry. Chemosphere, 65: 1990-1998.
- Trush, M.A., Mimnaugh, E.G. et Gram, T.E. (1982). Activation of pharmacologic agents to radical intermediates. Implications for the role of free radicals in drug action and toxicity. Biochem. Pharmacol., 31(21): 3335–3346.
- Turusov, V.S., Nikonova, T.V. et Parfenov, Y.D. (1990). Increased multiplicity of lung adenomas in five generations of mice treated with benz(a)pyrene when pregnant. Cancer Lett., 55(3): 227–231.
- U.S. EPA (1990). Methods for determinations of organic compounds in drinking water—Supplement I. Office of Research and Development, U.S. Environmental Protection Agency, Washington, DC (EPA/600/4-90-020),.
- U.S. EPA (1992). Drinking water; National Primary Drinking Water Regulations—synthetic organic chemicals and inorganic chemicals; National Primary Drinking Water Regulations implementation; final rule. Fed. Regist. 57(138): 31776.
- U.S. EPA (1995). Methods for determinations of organic compounds in drinking water - Supplement III. Office of Research and Development ,U.S. Environmental Protection Agency, Washington, DC (EPA/600/R-95/131).
- U.S. EPA (1998). Small system compliance technology list for the non-microbial contaminants regulated before 1996. Office of Water, U.S. Environmental Protection Agency, Washington, DC (EPA 815-R-98-002).
- U.S. EPA (2003). Analytical feasibility support document for the six year review of existing National Primary Drinking Water Regulations (reassessment of feasibility for chemical contaminants). Targeting and Analysis Branch, Standards and Risk Management Division, Office of Ground Water and Drinking Water, Office of Water, U.S. Environmental Protection Agency, Washington, DC (EPA 815-R-03-003). Disponible à : www.epa.gov/safewater/standard/review/pdfs/support_6yr_analytical_final.pdf
- U.S. EPA (2007). Benzo[a]pyrene TEACH chemical summary. Toxicity and Exposure Assessment for Children's Health, U.S. Environmental Protection Agency, Washington, DC. Disponible à : www.epa.gov/teach/chem_summ/BaP_summary.pdf
- U.S. EPA (2009a). Analytical feasibility support document for the second six-year review of existing National Primary Drinking Water Regulations. Office of Water, U.S. Environmental Protection Agency, Cincinnati, Ohio (EPA 815-B-09-003).
- U.S. EPA (2009b). Development of estimated quantitation levels for the second six-year review of National Primary Drinking Water Regulations. Office of Water, U.S. Environmental Protection Agency, Cincinnati, Ohio (EPA 815-B-09-005).
- U.S. EPA (2011). Benchmark Dose Software (BMDS) version 2.2. Logiciel pouvant être téléchargé de l'U.S. Environmental Protection Agency. Disponivle à : www.epa.gov/NCEA/bmds/index.html
- U.S. EPA (2013). Estimation Program Interface SuiteTM for Microsoft® Windows, v 4.11. U.S. Environmental Protection Agency, Washington, DC.
- Uno, S., Dalton, T.P., Dragin, N., Curran, C.P., Derkenne, S., Miller, M.L., Shertzer, H.G., Gonzalez, F.J. et Nebert, D.W. (2006). Oral benzo[a]pyrene in Cyp1 knockout mouse lines: CYP1A1 important in detoxication, CYP1B1 metabolism required for immune damage independent of total-body burden and clearance rate. Mol. Pharmacol., 69(4): 1103–1114.
- Urso, P. et Gengozian, N. (1982). Alterations in the humoral immune response and tumor frequencies in mice exposed to benzo[a]pyrene and X-rays before or after birth. J. Toxicol. Environ. Health, 10(4–5): 817–835.
- Urso, P. et Gengozian, N. (1984). Subnormal expression of cell-mediated and humoral immune responses in progeny disposed toward a high incidence of tumors after in utero exposure to benzo[a]pyrene. J. Toxicol. Environ. Health, 14(4): 569–584.
- Van de Wiel, J.A.G., Fijneman, P.H.S., Duijf, C.M.P., Anzion, R.B.M., Theuws, J.L.G. et Bos, R.P. (1993). Excretion of benzo[a]pyrene and metabolites in urine and feces of rats: influence of route of administration, sex and long-term treatment. Toxicology, 80(2–3): 103–115.
- Vreeburg, J. (2010). Discolouration in drinking water systems: the role of particles clarified, IWA Publishing, London, R.-U.
- Vu Duc, T. et Huynh, C.K. (1981). Les micropolluants organiques dans l'eau. Résultats préliminaires sur les haloformes et les hydrocarbures aromatiques polycycliques. Med. Soc. Prev., 26: 315-316.
- Wester, P.W., Muller, J.J.A., Slob, W., Mohn, G.R., Dortant, P.M. et Kroese, E.D. (2012). Carcinogenic activity of benzo[a]pyrene in a 2 year oral study in Wistar rats. Food Chem. Toxicol., 50(3–4): 927–935.
- Wester, R.C., Maibach, H.I., Bucks, D.A.W., Sedik, L., Melendres, J., Liao, C. et DiZio, S. (1990). Percutaneous absorption of [14C]DDT and [14C]benzo[a]pyrene from soil. Fundam. Appl. Toxicol., 15(3): 510–516.
- Westerhoff, P., Yoon Y., Snyder S., et Wert E. (2005). Fate of endocrine-disruptor, pharmaceutical, and personal care product chemicals during simulated drinking water treatment processes. Environ. Sci. Technol., 39: 6649-6663.
- Weyand, E.H. et Bevan, D.R. (1986). Benzo[a]pyrene disposition and metabolism in rats following intratracheal instillation. Cancer Res., 46(11): 5655–5661.
- Weyand, E.H., Chen, Y.C., Wu, Y., Koganti, A., Dunsford, H.A. et Rodriguez, L.V. (1995). Differences in the tumorigenic activity of a pure hydrocarbon and a complex mixture following ingestion: benzo[a]pyrene vs manufactured gas plant residue. Chem. Res. Toxicol., 8(7): 949–954.
- Weyand, E.H., He, Z.M., Ghodrati, F., Wu, Y., Marshall, M.V. et Lavoie, E.J. (1992). Effect of fluorine substitution on benzo[j]fluoranthene genotoxicity. Chem. Biol. Interact., 84: 37-53.
- White, K.L., Jr. et Holsapple, M.P. (1984). Direct suppression of in vitro antibody production by mouse spleen cells by the carcinogen benzo[a]pyrene but not by the noncarcinogenic congener benzo(e)pyrene. Cancer Res., 44(8): 3388–3393.
- Wielgosz, S.M., Brauze, D. et Pawlak, A.L. (1991). Ah locus–associated differences in induction of sister-chromatid exchanges and in DNA adducts by benzo[a]pyrene in mice. Mutat. Res., 246(1): 129–137.
- WMS, Intera et NWRI (1989). Investigation of suspected PAH contamination of groundwater: Newcastle, New Brunswick. WMS Associates Ltd., Intera Technologies and National Water Research Institute, Fredericton (Nouveau-Brunswick), 29 p. (WMS 2988).
- Wojdani, A. et Alfred, L.J. (1984). Alterations in cell-mediated immune functions induced in mouse splenic lymphocytes by polycyclic aromatic hydrocarbons. Cancer Res., 44(3): 942–945.
- Wolff, M.S., Herbert, R., Marcus, M., Rivera, M., Landrigan, P.J. et Andrews, L.R. (1989). Polycyclic aromatic hydrocarbon (PAH) residues on skin in relation to air levels among roofers. Arch. Environ. Health, 44(3): 157-163.
- Wood, A.W., Levin, W., Chang, R.L., Huang, M.T., Ryan, D.E., Thomas, P.E., Lehr, R.E., Kumar, S., Koreeda, M., Akagi, H., Ittah, Y., Dansette, P., Yagi, H., Jerina, D.M. et Conney, A.H. (1976). Mutagenicity and tumor-initiation activity of cyclopenta(c,d)pyrene and structurally related compounds. Cancer Res., 40: 642-649.
- Wu, J., Ramesh, A., Nayyar, T. et Hood, D.B. (2003). Assessment of metabolites and AhR and CYP1A1 mRNA expression subsequent to prenatal exposure to inhaled benzo[a]pyrene. Int. J. Dev. Neurosci., 21(6): 333–346.
- Xia, Y., Cheng, S., He, J., Liu, X., Tang, Y., Yuan, H., He, L., Lu, T., Tu, B. et Wang, Y. (2011). Effects of subchronic exposure to benzo[a]pyrene (B[a]P) on learning and memory, and neurotransmitters in male Sprague-Dawley rat. Neurotoxicology, 32(2): 188–198.
- Xu, C., Chen, J.A., Qiu, Z., Zhao, Q., Luo, J., Yang, L., Zeng, H., Huang, Y., Zhang, L., Cao, J. et Shu, W. (2010). Ovotoxicity and PPAR-mediated aromatase downregulation in female Sprague-Dawley rats following combined oral exposure to benzo[a]pyrene and di-(2-ethylhexyl) phthalate. Toxicol. Lett., 199(3): 323–332.
- Xu, Z., Brown, L.M., Pan, G.W., Liu, T.F., Gao, G.S., Stone, B.J., Cao, R.M., Guan, D.X., Sheng, J.H., Yan, Z.S., Dosemeci, M., Fraumeni, J.F., Jr. et Blot, W.J. (1996). Cancer risks among iron and steel workers in Anshan, China, Part II: Case–control studies of lung and stomach cancer. Am. J. Ind. Med., 30(1): 7–15.
- Yang, H., Zhou, L., Wang, Z., Roberts, L.J., II, Lin, X., Zhao, Y. et Guo, Z. (2009). Overexpression of antioxidant enzymes in ApoE-deficient mice suppresses benzo[a]pyrene-accelerated atherosclerosis. Atherosclerosis, 207(1): 51–58.
- Yauk, C.L., Jackson, K., Malowany, M. et Williams, A. (2011). Lack of change in microRNA expression in adult mouse liver following treatment with benzo[a]pyrene despite robust mRNA transcriptional response. Mutat. Res., 722(2): 131–139.
- Yerushalmi, L., Nefil, S., Hausler, R. et Guiot, S.R. (2006). Removal of pyrene and benzo[a]pyrene from contaminated water by sequential and simultaneous ozonation and biotreatment. Water Environ. Res. 78(11): 2286-2292.
- Zheng, S.J., Tian, H.J., Cao, J. et Gao, Y.Q. (2010). Exposure to di(n-butyl)phthalate and benzo[a]pyrene alters IL-1β secretion and subset expression of testicular macrophages, resulting in decreased testosterone production in rats. Toxicol. Appl. Pharmacol., 248(1): 28–37.
Annexe A : Liste des acronymes
- ADN
- acide désoxyribonucléique
- AhR
- récepteur des arylhydrocarbures
- ANSI
- American National Standards Institute
- ApoE
- apoliprotéine E
- BaP
- benzo[a]pyrène
- BMD
- dose de référence
- BMD10
- dose de référence correspondant à un changement de 10 % de l'effet
- BMDL10
- limite inférieure de l'intervalle de confiance à 95 % de la dose de référence correspondant à un changement de 10 % de l'effet
- BPDE
- benzo[a]pyrène-7,8-diol-9,10-époxyde
- CAG
- charbon actif en grains
- CAP
- charbon actif en poudre
- CCN
- Conseil canadien des normes
- CG-SM
- chromatographie en phase gazeuse couplée à la spectrométrie de masse
- CG-SM/SM
- chromatographie en phase gazeuse couplée à une spectrométrie de masse en tandem
- CIRC
- Centre international de Recherche sur le Cancer
- CLHP
- chromatographie en phase liquide haute performance
- CMA
- concentration maximale acceptable
- COIA
- complexe organo-inorgano-argileux
- CYP
- cytochrome P450
- DL50
- dose létale moyenne
- ELL
- extraction liquide-liquide
- ELS
- extraction liquide-solide
- EPA
- Environmental Protection Agency (États-Unis)
- FC
- facteur de changement
- FPC
- facteur de pente du cancer
- FDR
- taux de fausses découvertes
- HAP
- hydrocarbure aromatique polycyclique
- IC
- intervalle de confiance
- Koe
- coefficient de partage octanol-eau
- LDM
- limite de détection de la méthode
- LOAEL
- dose minimale avec effet nocif observé
- MA
- mode d'action
- MON
- matière organique naturelle
- NF
- nanofiltration
- NEEQ
- niveau estimé d'évaluation quantitative
- NSF
- NSF International
- OMS
- Organisation mondiale de la Santé
- PBPK
- pharmacocinétique à base physiologique
- p.c.
- poids corporel
- POA
- procédé d'oxydation avancé
- SMNR
- seuil minimal de niveau à rapporter
- SPEQ
- seuil pratique d'évaluation quantitative
- UF
- ultrafiltration
- UV
- ultraviolet
- VBS
- valeur basée sur la santé

Télécharger le format de rechange
(Format PDF, 1.42 Mo, 2 pages)
Organisation : Santé Canada
Type : Lignes directrices
Publiée : 2016-01