Recommandations pour la qualité de l'eau potable au Canada : document technique – Escherichia coli

Télécharger le format de rechange
(Format PDF, 1,1 Mo, 58 pages)
Organisation : Santé Canada
Date publiée : Mars 2020
Table des matières
- Partie I : Vue d'ensemble et application
- Partie II. Science et considérations techniques
- 4.0 Importance d'E. coli dans l'eau potable
- 5.0 Méthodes d'analyse
- 6.0 Échantillonnage d'E. coli
- 7.0 Considérations relatives aux procédés de traitement et aux réseaux de distribution
- 8.0 Évaluation des risques
- 9.0 Justification
- 10.0 Références
- Annexe A : Arbre décisionnel relatif à l'analyse microbiologique régulière des systèmes à l'échelle municipale
- Annexe B : Arbre décisionnel relatif à l'analyse microbiologique régulière des systèmes à l'échelle résidentiellerésidentielle
- Annexe C : Liste des acronymes
Partie I : Vue d'ensemble et application
1.0 Recommandation
La concentration maximale acceptable (CMA) pour Escherichia coli d'E. coli dans l'eau potable est d'aucun microorganisme détectable par 100 mL.
2.0 Sommaire
Le présent document technique a été préparé en collaboration avec le Comité fédéral-provincial-territorial sur l'eau potable (CEP) pour évaluer toute l'information disponible sur E.coli.
E. coli est une espèce bactérienne qu'on trouve naturellement dans les intestins des humains et des animaux. Elle est présente en grand nombre dans les matières fécales et peut facilement être mesurée dans l'eau, ce qui en fait un indicateur utile de la contamination fécale pour les fournisseurs d'eau potable. E. coli est l'indicateur le plus utilisé pour détecter la contamination fécale dans les systèmes d'approvisionnement en eau potable du monde entier. Dans le cadre de programmes de surveillance de l'eau potable, la détection d'E. coli sert à fournir de l'information sur la qualité de la source d'approvisionnement en eau, le caractère adéquat du traitement et la salubrité de l'eau potable distribuée au consommateur.
2.1 Importance d'E. coli dans les systèmes d'approvisionnement en eau potable et leurs sources
On devrait recourir à la surveillance d'E. coli en combinaison avec d'autres indicateurs dans le cadre d'une approche de la source au robinet afin d'obtenir une eau potable de qualité acceptable. Puisque les sources d'approvisionnement en eau potable sont souvent touchées par une contamination fécale d'origine humaine ou animale, il est possible d'en déceler la présenced'E. coli. Sa présence dans un échantillon d'eau est considérée comme un bon indicateur de contamination fécale récente. Il est essentiel de pouvoir détecter une contamination de l'eau potable par des matières fécales, car les microorganismes pathogènes provenant de matières fécales d'origine humaine ou animale posent un grave danger pour la santé publique.
Dans le cadre d'une approche de gestion des risques pour les systèmes d'approvisionnement en eau potable, comme une approche de la source au robinet ou un plan de salubrité de l'eau, la surveillance d'E. coli sert à vérifier la qualité de l'eau pour démontrer que les barrières naturelles et les procédés de traitement en place assurent le degré de contrôle nécessaire. La détection d'E. coli dans l'eau potable indique une contamination fécale et, par conséquent, la présence possible d'agents pathogènes fécaux qui peuvent poser un risque pour la santé des consommateurs. Dans une source d'eau souterraine, la présence d'E. coli indique que l'eau souterraine est contaminée par des matières fécales, tandis que dans l'eau potable traitée, la présence d'E. coli peut indiquer que le traitement est inadéquat ou que l'eau traitée a été contaminée pendant la distribution. Si des analyses confirment la présence d'E. coli dans l'eau potable, les mesures qui peuvent être prises consistent notamment à aviser les autorités responsables, à émettre un avis d'ébullition de l'eau et à appliquer des mesures correctives.
Dans le cadre de la surveillance et de la vérification de l'eau potable, l'utilisation de multiples paramètres comme indicateurs de la qualité microbiologique générale de l'eau (comme les coliformes totaux, la numération des bactéries hétérotrophes) ou d'autres indicateurs de contamination fécale (entérocoques) est une bonne façon pour les services d'eau de renforcer le potentiel de reconnaissance des problèmes et donc de prendre les mesures appropriées.
2.2 Traitement
Les responsables de systèmes d'approvisionnements en eau potable alimentés par une eau de surface ou une eau souterraine directement soumises à l'influence d'une eau de surface qui respectent les recommandations relatives aux protozoaires entériques et aux virus entériques (élimination et/ou inactivation minimale de 3 log et élimination et/ou inactivation minimale de 4 log, respectivement). Les responsables de systèmes d'approvisionnements en eau potable alimentés par une eau souterraine qui satisfont aux recommandations relatives aux virus entériques (élimination et/ou inactivation minimale de 4 log) pourront atteindre la CMA proposée d'aucun microorganisme détectable d'E. coli par 100 mL. La détection d'E. coli dans l'eau potable indique qu'il y a un risque potentiel pour la santé découlant de la consommation de cette eau; toutefois, les tests de détection d'E. coli ne permettent pas à eux seuls de confirmer la présence ou l'absence d'agents pathogènes dans l'eau potable.
Pour les systèmes à l'échelle municipale, il est important d'appliquer une approche de surveillance qui comprend l'utilisation de multiples paramètres opérationnels et de vérification de la qualité de l'eau (p. ex. turbidité, mesures de désinfection, E. coli) pour assurer un traitement adéquat de l'eau et une qualité microbiologique acceptable. Dans le cas des systèmes à l'échelle résidentiels, des tests de détection réguliers d'E. coli combinés à une surveillance des processus critiques, des inspections physiques régulières et une évaluation de la source d'approvisionnement en eau peuvent servir à confirmer la qualité de l'approvisionnement d'eau potable.
2.3 Considérations internationales
La CMA pour E. coli est conforme aux recommandations sur l'eau potable établies par d'autres pays et organisations internationales. L'Organisation mondiale de la Santé, l'Union européenne, l'United States Environmental Protection Agency (U.S. EPA) et l'Australian National Health and Medical Research Council ont tous établi une limite de zéro E. coli par 100 mL.
3.0 Application de la recommandation
Remarque : Des conseils spécifiques concernant l'application des recommandations pour l'eau potable devraient être obtenus auprès de l'autorité responsable en matière d'eau potable dans le secteur de compétence concerné.
E. coli est l'organisme indicateur fécal le plus largement utilisé dans la gestion des risques liés à l'eau potable dans le monde. Dans le cas des systèmes à l'échelle municipale et à l'échelle résidentielleNote de bas de page 1, son rôle principal est de servir d'indicateur de la contamination fécale dans le cadre d'une surveillance de routine pour vérifier la qualité de l'approvisionnement de l'eau potable. Comme la présence d'E. coli indique une contamination fécale de l'eau potable, il y a un risque accru que des agents pathogènes entériques soient présents. Dans le cas de l'eau potable traitée et distribuée, la détection d'E. coli signifie que le traitement a été inadéquat ou qu'il y a eu une contamination après le traitement ou dans le réseau de distribution. Par conséquent, la détection d'E. coli dans n'importe quel système d'approvisionnement en eau potable est inacceptable.
La contamination par des matières fécales est souvent intermittente, et il est possible que l'analyse d'un seul échantillon ne permette pas de la déceler. Par conséquent, si une évaluation de la vulnérabilité ou une inspection d'un système d'approvisionnement en eau potable montre qu'une source d'approvisionnement non traitée ou que l'eau traitée (p. ex. pendant sa distribution ou son stockage) est susceptible d'être contaminée par des matières fécales, ou encore que le traitement est inadéquat, il faudrait considérer l'eau impropre à la consommation, quels que soient les résultats de l'analyse d'E. coli. La mise en œuvre d'une approche de gestion des risques aux systèmes d'approvisionnement en eau potable, comme l'approche de la source au robinet ou du plan de gestion de la sécurité sanitaire de l'eau, est la meilleure façon de réduire les agents pathogènes d'origine hydrique dans l'eau potable. Ces approches exigent une évaluation du système qui comprend les éléments suivants : caractérisation de la source d'approvisionnement en eau, description des procédés de traitement qui préviennent ou réduisent la contamination, mise en évidence des conditions qui peuvent entraîner une contamination, et application de mesures de contrôle pour atténuer ces risques grâce aux systèmes de traitement et réseau de distribution au consommateur.
Des concentrations d'E. coli non détectables par 100 mL d'eau à la sortie de la station de traitement devraient être atteintes pour toutes les systèmes d'approvisionnement en eau traitée. Le traitement des sources d'eau de surface ou d'eau souterraine sous l'influence directe d'eau de surface devrait comprendre une filtration adéquate (ou une technique permettant d'obtenir une réduction ou une inactivation logarithmique équivalente) et une désinfection. Le traitement des sources d'eau souterraine devrait inclure au minimum une élimination et une inactivation des virus entériques de 4 log (99,99 %). L'autorité responsable en matière d'eau potable dans le secteur de compétence concerné peut choisir de permettre qu'une source d'eau souterraine ait une réduction logarithmique inférieure à la recommandation de 4 log si l'évaluation du système d'approvisionnement en eau potable répond aux exigences provinciales ou territoriales en place pour assurer un risque minimal associé à la présence de virus entériques. Les responsables de systèmes d'approvisionnements en eau potable alimentés par une eau de surface ou une eau souterraine sous l'influence directe d'une eau de surface qui respectent les recommandations relatives aux protozoaires entériques et aux virus entériques (élimination et/ou inactivation minimale de 3 log, et élimination et/ou inactivation minimale de 4 log, respectivement) et les responsables de systèmes d'approvisionnements en eau potable alimentés par une eau souterraine qui satisfont aux exigences relatives aux virus entériques (élimination et/ou inactivation minimale de 4 log) peuvent permettre une élimination et une inactivation adéquates d'E. coli.Il se peut que les évaluations des sources d'approvisionnement en eau déterminent qu'une réduction logarithmique supérieure aux exigences minimales est nécessaire pour que l'eau ait une qualité microbiologique acceptable.
Le type et le niveau du traitement approprié devraient prendre en compte les fluctuations potentielles de la qualité de l'eau, y compris la dégradation de la qualité de l'eau à court terme ainsi que la variabilité de l'efficacité du traitement. Des essais pilotes ou des procédés d'optimisation peuvent être utiles pour déterminer la variabilité du traitement. Dans les systèmes comportant un réseau de distribution, il faudrait maintenir en tout temps un résidu de désinfectant dans l'ensemble du réseau. L'existence d'un résidu de désinfectant adéquat est une mesure importante pour contrôler la croissance microbienne pendant la distribution d'eau potable. Dans certaines conditions (p. ex. l'intrusion de virus ou de protozoaires provenant de l'extérieur du réseau de distribution), le résidu de désinfectant peut ne pas suffire pour assurer une inactivation efficace des agents pathogènes. Pour obtenir de plus amples renseignements sur la façon dont les évaluations des sources d'approvisionnement en eau, les technologies de traitement et l'exploitation des réseaux de distribution sont utilisées pour gérer les risques associés aux agents pathogènes présents dans l'eau potable, veuillez consulter les documents techniques sur les protozoaires entériques et les virus entériques de Santé Canada. Lors de la vérification de la qualité de l'eau potable traitée, les résultats des analyses de détection d'E. coli ainsi que l'information sur l'efficacité de l'installation de traitement et des réseaux de distribution devraient être pris en compte pour démontrer que l'eau a été traitée adéquatement et qu'elle est donc de qualité microbiologique acceptable. Les responsables de systèmes d'approvisionnement en eau potable devraient contacter l'autorité responsable en matière d'eau potable dans le secteur de compétence concerné pour obtenir une confirmation des exigences qui s'appliquent à leur système.
3.1 Systèmes d'approvisionnement en eau potable à l'échelle municipale
3.1.1 Surveillance d'E. coli dans l'eau à la sortie de la station de traitement
L'eau à la sortie d'une station de traitement devrait faire l'objet d'analyses de détection d'E. coli sur une base au moins hebdomadaire. La détection d'E. coli dans l'eau indique une défaillance grave du traitement, et cela est inacceptable. Les analyses de détection d'E. coli devraient être effectuées en combinaison avec d'autres indicateurs opérationnels, comme la surveillance d'un résidu de désinfectant et de la turbidité, dans le cadre d'une approche de la source au robinet ou d'un plan de gestion de la sécurité sanitaire de l'eau.
La fréquence requise pour toutes les analyses à la station de traitement est précisée par l'autorité responsable de l'eau potable. La pratique exemplaire consiste généralement de respecter une fréquence d'analyse supérieure à ce qui est requis au minimum, selon la taille du système, le nombre de consommateurs desservis, l'historique du système et d'autres considérations propres au site, comme les résultats des évaluations de la source d'approvisionnement. Les événements qui entraînent des changements dans l'état des sources d'approvisionnement en eau (p. ex. ruissellement printanier, tempêtes ou déversements d'eaux usées) sont associés à un risque accru de contamination fécale. Les services d'eau devront envisager d'autres échantillonnages au cours de ces événements.
3.1.2 Surveillance d'E. coli dans le réseau de distribution et dans les installations de stockage
Dans les réseaux de distribution et les installations de stockage de municipalités, le nombre d'échantillons prélevés aux fins d'analyse de détection d'E. coli devrait refléter la taille de la population desservie, et ne pas être inférieur à quatre échantillons par mois. Les points d'échantillonnage et la fréquence des analyses de détection d'E. coli à l'intérieur du réseau de distribution et des installations de stockage seront définis et approuvés par l'autorité responsable en matière d'eau potable.
Des changements dans l'état du réseau qui entraînent une interruption de l'approvisionnement ou des pressions transitoires faibles et négatives peuvent être associés à un risque accru de contamination fécale. Ces changements peuvent survenir au cours de l'exploitation ou de l'entretien courant du réseau de distribution (p. ex. démarrage et arrêt de la pompe, ouverture et fermeture des vannes) ou durant des événements imprévus comme des pannes de courant ou des ruptures de conduite maîtresse d'eau. Les indicateurs opérationnels (p. ex. résidu de désinfectant, surveillance de la pression) devraient être utilisés en conjonction avec les analyses de détection d'E. coli dans le cadre d'une approche de la source au robinet ou d'un plan de la salubrité de l'eau.
3.1.3 Avis
Si la présence d'E. coli est détectée dans un échantillon d'eau potable provenant d'un système d'approvisionnement en eau potable à l'échelle municipale (p. ex. de l'eau sortant d'une station de traitement ou celle d'un réseau de distribution ou d'une installation de stockage), le propriétaire ou l'exploitant de ce système et le laboratoire analysant les échantillons doivent prévenir immédiatement les autorités compétentes. Le propriétaire ou l'exploitant du réseau devrait aussi réaliser les tâches suivantes :
- Échantillonner à nouveau immédiatement et analyser le ou les sites ayant révélé la présence d'E. coli et des sites adjacents.
- Mener une évaluation pour veiller à ce que les procédés de traitement fonctionnent efficacement (cela pourrait comprendre la collecte de données sur l'efficacité du traitement de l'eau et d'autres données de surveillance);
- Prendre toute mesure corrective nécessaire (voir section 3.1.4) avant de reprendre les activités normales et de contrôle visant le système.
Si le nouvel échantillonnage et les analyses confirment la présence d'E. coli dans l'eau potable, le propriétaire ou l'exploitant du système doit immédiatement émettre un avis d'ébullition de l'eauNote de bas de page 2 en consultation avec les autorités responsables, et prendre les mesures correctives appropriées (section 3.1.4). Le propriétaire ou l'exploitant doit aussi collaborer avec les autorités responsables à la surveillance d'éventuelles éclosions de maladies d'origine hydrique.
De plus, lorsqu'une contamination par E. coli est décelée lors du premier échantillonnage - par exemple, des résultats positifs pour E. coli proviennent d'un seul site ou de plus d'un endroit du réseau de distribution - le propriétaire ou l'exploitant du système ou l'autorité responsable peut décider d'aviser immédiatement les consommateurs de faire bouillir leur eau potable ou d'utiliser un autre source d'eau potable réputé sûr et de prendre des mesures correctives sans attendre les résultats de confirmation. Un avis d'ébullition de l'eau doit être émis immédiatement s'il y a l'un des signes suivants :
- Défaillance importante d'un procédé de traitement essentiel;
- Maladie dans la communauté que l'on soupçonne d'être associée à l'eau potable.
Un arbre décisionnel est fourni à l'annexe A pour aider les propriétaires et les exploitants de système.
3.1.4 Mesures correctives
Si le ré-échantillonnage et l'analyse confirment la présence d'E. coli dans l'eau potable, le propriétaire ou l'exploitant du système d'approvisionnement et de distribution doit prendre les mesures correctives qui s'imposent, notamment :
- Vérifier l'intégrité du procédé de traitement;
- Vérifier si le fonctionnement du traitement est optimal;
- Vérifier l'intégrité du réseau de distribution;
- Vérifier la présence du résidu de désinfectant requis dans tout le réseau de distribution;
- Augmenter la dose de désinfectant, purger les conduites principales, nettoyer les réservoirs d'eau traitée (réservoirs municipaux et citernes domestiques) et vérifier s'il y a des raccordements croisés et des fuites de pression. L'autorité responsable doit être consultée au sujet de la procédure à suivre pour déchlorer l'eau rejetée dans l'environnement;
- Effectuer des échantillonnages aux sites ayant donné des résultats positifs pour E. coli et à des endroits adjacents, et analyser les échantillons. Il convient d'analyser au moins un échantillon prélevé en amont et un autre en aval des sites où l'on a prélevé les échantillons à l'origine, ainsi qu'un échantillon de l'eau traitée provenant de la station de traitement, prélevé au point où cette eau pénètre dans le réseau de distribution. D'autres échantillons de suivi doivent être prélevés et analysés selon un plan d'échantillonnage approprié pour le réseau de distribution. Les analyses effectuées doivent englober la détection d'E. coli et de coliformes totaux (comme indicateur général de la qualité microbiologique et d'un traitement inadéquat) et des paramètres de surveillance opérationnelle tels que la concentration résiduellesrésiduelles de désinfectant et la turbidité. Il est également possible d'effectuer des analyses pour déceler la présence d'entérocoques comme indicateur supplémentaire permettant de vérifier la présence d'une contamination fécale;
- Effectuer des recherches pour déterminer le problème et éviter qu'il se répète, et mesurer entre autres la qualité de l'eau brute (p. ex. caractéristiques bactériologiques, turbidité, couleur, matières organiques naturelles et conductivité) et sa variabilité;
- Continuer d'effectuer des échantillonnages à tous les endroits recensés pendant l'enquêteet d'analyser les échantillons (p. ex. caractéristiques bactériologiques, résidu de désinfectant, turbidité) pour confirmer l'ampleur du problème et vérifier si les mesures correctives portent fruit.
3.1.5 Annulation d'un avis d'ébullition de l'eau
Une fois que les mesures correctives appropriées ont été prises et seulement après qu'au moins deux séries consécutives d'échantillons bactériologiques, prélevés à 24 heures d'intervalle, ont donné des résultats négatifs, un avis d'ébullition de l'eau lié à E. coli peut être annulé. D'autres interventions et mesures de surveillance de la qualité de l'eau peuvent être exigées par l'autorité responsable en matière d'eau potable. Pour de plus amples renseignements sur les avis d'ébullition de l'eau, veuillez consulter le document de Santé Canada intitulé Conseils concernant l'émission et l'annulation des avis d'ébullition de l'eau dans les approvisionnements d'eau potable au Canada. À long terme, seuls un historique des données de surveillance bactériologique et opérationnelle ainsi que la validation de la conception du réseau, de son fonctionnement et de son entretien peuvent être utilisés pour confirmer la qualité de l'approvisionnement d'eau potable.
3.2 Systèmes d'approvisionnement en eau potable à l'échelle résidentielle
3.2.1 Surveillance d'E. coli dans l'eau provenant d'approvisionnements désinfectés et non désinfectés
La fréquence des analyses des systèmes d'approvisionnement à l'échelle résidentielle est déterminée par l'autorité responsable en matière d'eau potable dans le secteur de compétence concerné, laquelle devrait inclure les périodes où le risque de contamination de la source d'approvisionnement en eau potable est le plus élevé, par exemple, au début du printemps après le dégel, après une longue période de sécheresse ou après de fortes précipitations. Les propriétaires de puits privés devraient régulièrement vérifier (au moins deux fois par année) s'il y a présence d'E. coli dans leur puits, idéalement pendant ces mêmes périodes à risque. Les puits neufs ou réhabilités devraient également être testés avant leur première utilisation, pour confirmer leur salubrité microbiologique. L'autorité responsable en matière d'eau potable le secteur de compétence concerné doit être consultée au sujet de ses exigences particulières en matière de construction et d'entretien des puits.
3.2.2 Avis
Les systèmes à l'échelle résidentielle qui desservent le public peuvent être assujettis à des exigences réglementaires ou législatives et devraient faire l'objet de toute mesure précisée par l'autorité responsable en matière d'eau potable. Si la présence d'E. coli est détectée dans un échantillon d'eau potable provenant d'un système à l'échelle résidentielle desservant le public, le propriétaire ou l'exploitant du système et le laboratoire analysant les échantillons doivent prévenir immédiatement les autorités responsables. Le propriétaire ou l'exploitant du système doit aussi immédiatement à nouveau procéder à un échantillonnage et à une analyse de l'eau potable pour confirmer la présence d'E. coli. L'autorité responsable doit conseiller au propriétaire ou à l'exploitant du système de faire bouillir l'eau potable ou d'utiliser entre-temps un autre source d'eau potable réputé sûr. Si la présence d'E. coli est détectée dans un échantillon d'eau potable provenant d'un système à l'échelle résidentielle privée, les propriétaires devrait aussi être avisés de faire bouillir leur eau potable ou de faire appel à une autre source d'eau potable réputée sûre, et de procéder à un nouvel échantillonnage et une nouvelle analyse de leur eau potable pour confirmer la présence d'E. coli.
Si le nouvel échantillonnage confirme que la source est contaminée par E. coli, le propriétaire ou l'exploitant du système doit immédiatement prendre les mesures correctives appropriées (voir la section 3.2.3 et 3.2.4). Le propriétaire ou l'exploitant doit aussi collaborer avec les autorités responsables de la surveillance pour repérer d'éventuelles éclosions de maladies d'origine hydrique. Certains secteurs de compétence recommanderont, à titre de précaution, qu'on prenne immédiatement des mesures correctives sans attendre les résultats de confirmation. Un arbre décisionnel est fourni à l'annexe B pour aider les propriétaires et les exploitants de système.
3.2.3 Mesures correctives pour les sources d'approvisionnement désinfectées
La première étape, si elle n'a pas encore été entreprise, consiste à évaluer l'état du système d'approvisionnement en eau potable, y compris, s'il y a lieu, l'entrée d'eau, le puits, la tête de puits, la pompe, l'installation de traitement (y compris l'équipement d'alimentation en produits chimiques), la plomberie, les éléments empêchant l'entrée d'animaux (p. ex. oiseaux, vermine) et la zone avoisinante.
Il convient de corriger toute défaillance repérée. Si l'état physique des composantes est acceptable, une partie ou l'ensemble des mesures correctives suivantes peuvent s'imposer :
- Dans un système chloré, vérifier qu'il reste un résidu de désinfectant dans tout le système;
- Augmenter la dose de désinfectant, purger à fond le système et nettoyer les réservoirs d'eau traitée et les citernes domestiques. L'autorité responsable doit être consultée au sujet de la procédure à suivre pour déchlorer l'eau rejetée dans l'environnement;
- Pour les systèmes où la technologie de désinfection ne laisse pas de résidu de désinfectant, comme les UV, il peut être nécessaire de procéder à un traitement-choc au chlore dans le puits et la plomberie;
- S'assurer que le système de désinfection fonctionne correctement et qu'il est entretenu conformément aux directives du fabricant.
Une fois que les mesures correctives nécessaires ont été prises, il convient de prélever de nouveaux échantillons pour y détecter toute présence éventuelle d'E. coli et pour confirmer que le problème a été corrigé. Si le problème persiste, il faudrait envisager un traitement supplémentaire ou utiliser une nouvelle source d'approvisionnement en eau potable. Entre-temps, il convient de maintenir toutes les mesures de précaution prises au départ, par exemple, continuer de faire bouillir l'eau potable ou utiliser une autre source d'eau potable réputé sûre.
3.2.4 Mesures correctives pour les puits non désinfectés
Si ce n'est pas encore fait, il convient d'abord d'évaluer l'état du puits, de la tête de puits, de la pompe, de la plomberie et de la zone avoisinante, puis de corriger toute défaillance repérée. Si l'état physique des composantes est acceptable, il convient de prendre les mesures correctives qui suivent :
- Appliquer un traitement-choc au chlore au puits et au réseau de plomberie;
- Purger le réseau à fond et procéder à une autre analyse pour confirmer l'absence d'E. coli. Les analyses de confirmation devraient être retardées jusqu'à 48 heures après l'obtention de résultats négatifs pour la présence de résidu de chlore ou après 5 jours depuis le traitement du puits. Pour les réseaux résidentiels desservant le public, l'autorité responsable en matière d'eau potable peut déterminer la pratique qui est acceptable. L'autorité responsable doit également être consultée au sujet de la procédure à suivre pour déchlorer l'eau qui peut être rejetée dans l'environnement.
Si l'eau demeure contaminée après le traitement-choc au chlore, il importe de pousser les recherches pour déterminer les facteurs qui contribueraient à la contamination. Si ces facteurs ne peuvent être relevés ou corrigés, il faut envisager d'installer un dispositif de désinfection approprié, de reconstruire le puits ou de le remplacer. Il convient de faire bouillir l'eau potable avant sa consommation ou de continuer d'utiliser entre-temps une autre source d'eau potable réputée sûre.
3.2.5 Annulation d'un avis d'ébullition de l'eau
L'avis d'ébullition de l'eau devrait être annulé une fois que les mesures correctives appropriées ont été prises, et après qu'au moins deux séries consécutives d'échantillons prélevés à 24 heures d'intervalle ont donné des résultats négatifs pour la présence d'E. coli. Les autorités responsables de l'eau potable pourraient devoir prendre d'autres interventions et mesures de surveillance de la qualité de l'eau. Pour de plus amples renseignements sur les avis d'ébullition de l'eau, veuillez consulter le document de Santé Canada intitulé Conseils concernant l'émission et l'annulation des avis d'ébullition de l'eau dans les approvisionnements d'eau potable au Canada.Il convient de procéder à d'autres analyses trois à quatre mois plus tard pour vérifier que la contamination n'est pas réapparue. À long terme, seuls un historique des données de surveillance bactériologique et opérationnelle combiné à des inspections physiques régulières du système et à une évaluation de la source d'approvisionnement en eau peuvent être utilisés pour confirmer la qualité de l'eau potable.
Partie II. Science et considérations techniques
4.0 Importance d'E. coli dans l'eau potable
4.1 Description
Escherichia coli (E. coli) fait partie du groupe des bactéries coliformes, lequel fait partie de la famille des entérobactéries. Il s'agit d'une bactérie anaérobie facultative, à Gram négatif, non sporulée, en forme de bâtonnet. La grande majorité des E. coli sont des bactéries inoffensives qui vivent dans les intestins des humains et des animaux et qui contribuent à la digestion. Il existe aussi plusieurs types d'E. coli pathogènes, sont le sérotype bien connu O157:H7, qui a acquis des caractéristiques le rendant dangereux pour l'humain. Ces bactéries E. coli pathogènes, si elles sont présentes dans les sources d'approvisionnement en eau potable contaminées par des matières fécales humaines ou animales, peuvent être une cause importante des maladies entériques d'origine hydrique. La publication de Santé Canada Conseils sur les bactéries pathogènes d'origine hydrique (Santé Canada, 2013b) aborde en détail les E. coli pathogènes. Lorsqu'ils analysent des échantillons pour la présence d'E. coli, les responsables de systèmes d'approvisionnements en eau potable devraient comprendre que les méthodes d'analyse ont été conçues pour déceler les E. coli non pathogènes, dont la présence indique une contamination par des matières fécales. La présence d'E. coli signifie que l'eau potable pose un risque pour la santé, car elle contient des agents pathogènes provenant de matières fécales.
La complexité de l'espèce E. coli est mieux comprise grâce à l'utilisation de méthodes avancées de caractérisation moléculaire et à l'accumulation des données sur la séquence du génome entier (Lukjancenko et coll., 2010; Chaudhuri et Henderson, 2012; Gordon, 2013). À l'heure actuelle, il est reconnu que les souches d'E. coli peuvent être classées dans l'un des nombreux groupes phylogénétiques (A, B1, B2, C, D, E et F) en fonction des différences dans leur génotype. Les souches des différents groupes présentent aussi une certaine variation au niveau de leurs propriétés physiques et biologiques (p. ex. capacité d'utiliser différents éléments nutritifs), des habitats fécaux et environnementaux dans lesquels elles sont décelées et leur prédisposition à causer des maladies (Clermont et coll., 2000; Walk et coll., 2007; Tenaillon et coll., 2010; Chaudhuri et Henderson, 2012; Gordon, 2013; Jang et coll., 2017). D'autres recherches sont nécessaires pour mieux comprendre les répercussions pratiques de ces différences sur la microbiologie de l'eau potable et les conséquences pour la santé humaine (Van Elsas et coll., 2011; Gordon, 2013).
4.2 Sources
E. coli se trouve naturellement dans les intestins et les matières fécales des humains et d'une grande variété d'animaux. Cette bactérie est plus répandue chez les animaux à sang chaud (domestiques et sauvages), mais elle est aussi présente chez de nombreux animaux à sang froid (Gordon, 2013, Tenaillon et coll., 2010; Gordon et Cowling, 2003; Frick et coll., 2018). Dans les matières fécales humaines, E. coli est présente à une concentration se situant entre 107 et 109 cellules par gramme (Edberg et coll., 2000; Leclerc et coll., 2001; Tenaillon et coll., 2010; Ervin et coll., 2013). Leur nombre dans les matières fécales d'animaux domestiques (p. ex. animaux d'élevage et de compagnie) peut varier considérablement, mais il se situe généralement entre 104 et 109 cellules par gramme (Lefebvre et coll., 2006; Duriez et Topp, 2007; Diarra et coll., 2007; Tenaillon et coll., 2010; Ervin et coll., 2013). Les données sur la fréquence et l'abondance d'E. coli dans les matières fécales d'espèces animales sauvages sont peu nombreuses (Tenaillon et coll., 2010; Farnleitner et coll., 2010). Selon des études, la concentration d'E. coli dans les matières fécales d'animaux sauvages à sang chaud et à sang froid peut atteindre 104 à 109 cellules per gramme (Farnleitner et coll. 2010; Ervin et coll., 2013; Frick et coll., 2018). Comme les concentrations d'E. coli dans les matières fécales humaines et animales sont très élevées, il est possible de détecter une contamination de l'eau dans des volumes d'échantillon pratiques à recueillir et à transporter en vue d'une analyse en laboratoire.
Les sources de contamination fécale qui peuvent avoir des répercussions sur des approvisionnement de sources d'eau de surface ou d'eau souterraine comprennent les sources ponctuelles (p. ex. eaux usées et effluents industriels, fosses septiques et égouts sanitaires qui fuient) et les sources diffuses ou non ponctuelles (p. ex. ruissellement provenant des zones agricoles, urbaines et naturelles) (Gerba et Smith, 2005; Hynds et coll., 2012, 2014; Wallender et coll., 2014; Lalancette et coll., 2014; Staley et coll., 2016).
4.3 Survie
Une fois l'E. coli est excrété de l'animal-hôte dans un habitat secondaire, sa survie dépend de nombreux facteurs physiques et biologiques, dont la température, l'exposition au soleil, la présence et les types d'autre microflores, la disponibilité des nutriments et la capacité à persister dans les biofilms (Foppen et Schijven, 2006; Van Elsas et coll., 2011; Blaustein et coll., 2013; Jang et coll., 2017). L'apport de chacun des facteurs varie selon le type d'eau (p. ex. eau souterraine, de surface, traitée). Dans les milieux aquatiques, comme les conditions de survie sont beaucoup moins favorables que dans les intestins, les populations d'E. coli déclinent naturellement (Winfield et Groisman, 2003; Van Elsas et coll., 2011). Les résultats d'études sur le microcosme des eaux douces indiquent que les populations d'E. coli disparaissent rapidement, et s'abaissent de un à plusieurs logarithmes en 7 à 10 jours (Flint, 1987; Lim et Flint, 1989; Bogosian, 1996; Sampson et coll., 2006). Le déclin des populations est plus lent dans les eaux souterraines et les résultats des études sur les microcosmes indiquent des périodes d'une à deux semaines pour une réduction d'un logarithme (Keswick et coll., 1982; Filip et coll., 1986; John et Rose, 2005). La survie des populations d'E. coli dans les milieux naturels complexes n'est pas facile à prédire (Van Elsas et coll., 2011). Certaines études montrent que l'organisme a survécu plusieurs semaines à une température de 4 °C dans l'eau de lac (Sampson et coll., 2006) et 14 semaines à 10 °C dans de l'eau souterraine filtrée (0,45 µm) (Filip et coll., 1986).
En général, E. coli a une durée de vie semblable à celle d'autres bactéries entériques (Edberg et coll., 2000; John et Rose, 2004; Sinton et coll., 2007; Pachepsky et coll., 2014). Toutefois, cette durée est beaucoup plus courte que celle de microorganismes plus résistants comme les oocystes de protozoaire et de nombreux virus entériques (John et Rose, 2004; King et Monis, 2007; Kotwal et Cannon, 2014; Hamilton et coll., 2018). En raison de la vitesse du déclin dans les eaux naturelles et de la relative sensibilité de cette bactérie aux agressions de l'environnement, on considère que la présence d'E. coli dans les sources d'approvisionnement en eau est un signe d'une contamination fécale récente (Edberg et coll., 2000; OMS et OCDE, 2003).
Dans un milieu hydrique naturel ou artificiel (p. ex. réseau de distribution), lorsqu'ilse trouve dans des conditions non favorables à sa prolifération, E. coli s'adapte et entre dans un état viable, mais non cultivable (VMNC), où elle ne se développe pas dans des milieux de culture en laboratoire. Cependant, la bactérie demeure vivante et dotée d'une capacité de résurrection lorsque les conditions redeviennent favorables (Bjergbæk et Roslev, 2005). Cet état peut être induit par une large fourchette de facteurs de stress, dont l'absence de certains éléments nutritifs, le pH, la température, la quantité d'oxygène, la pression osmotique et l'exposition à des agents antimicrobiens tel que les désinfectants utilisés dans le traitement des sources d'approvisionnement en eau (Bjergbæk et Roslev, 2005; Li et coll., 2014, Chen et coll., 2018). Il s'agit d'une stratégie de survie primaire des bactéries qui a été observée chez de nombreuses espèces (Lee et coll., 2007; van der Kooij et van der Wielen, 2014). Une meilleure compréhension de l'état VMNC chez les bactéries pertinentes pour l'eau potable est nécessaire (Li et coll., 2014; van der Kooij et van der Wielen, 2014).
4.3.1 E. coli adaptée à l'environnement
La communauté scientifique reconnaît maintenant qu'E. coli peut survivre à long terme et croître dans des habitats situés à l'extérieur du tractus intestinal inférieur des humains et des animaux à condition que la pression exercée par certains facteurs (p. ex. température, disponibilité d'éléments nutritifs et d'eau, pH, rayonnement solaire et présence d'autres microorganismes) se situent dans la limite de tolérance d'E. coli (Ishii et coll., 2010; Van Elsas et coll., 2011; Byappanahalli et coll., 2012b; Tymensen et coll., 2015; Jang et coll., 2017). Il est également devenu évident que certaines souches d'E. coli peuvent s'adapter pour vivre indépendamment des matières fécales et devenir des membres naturalisés de la communauté microbienne dans des habitats environnementaux (Ishii et Sadowsky, 2008; Ishii et coll., 2010; Byappanahalli et coll., 2012b). Des génotypes d'E. coli distincts de ceux que l'on trouve dans les matières fécales humaines ou animales ont été découverts dans des sables, des sols, des sédiments, de la végétation aquatique, des déchets septiques et des eaux usées brutes (Gordon et coll., 2002; Byappanahalli et coll., 2006; Ksoll et coll., 2007; Ishii et Sadowsky, 2008; Ishii et coll., 2010; Badgley et coll., 2011; Zhi et coll., 2016). Au fil du temps, la recherche a démontré que des habitats environnementaux peuvent servir de sources potentielles pour la plupart des groupes de bactéries qui ont été utilisés pour détecter une contamination fécale de l'eau potable, notamment les coliformes totaux, les coliformes thermotolérants, E. coli et les entérocoques (Edberg et coll., 2000; Whitman et coll., 2003; Byappanahalli et coll., 2012a). Bien que ces résultats modifient la perception selon laquelle E. coli est exclusivement associé aux déchets fécaux, il est admis qu'E. coli est principalement d'origine fécale et demeure un indicateur valable de contamination fécale dans l'eau potable (voir la section 4.5). D'autres recherches sont nécessaires pour améliorer notre compréhension du comportement d'E. coli dans l'environnement.
4.4 Rôle d'E. coli comme indicateur de qualité de l'eau potable
Parmi les contaminants pouvant être présents dans l'eau potable, ce sont les microorganismes pathogènes provenant des matières fécales humaines et animales qui posent le plus grave danger pour la santé publique. Même si les techniques modernes de microbiologie permettent désormais la détection des bactéries, des virus et des protozoaires pathogènes, il n'est pas pratique de tenter d'isoler systématiquement ces microorganismes de l'eau potable (Payment et Pintar, 2006; Allen et coll., 2015). Pour cette raison, des organismes indicateurs sont utilisés pour évaluer la salubrité microbiologique de l'eau potable. Ces indicateurs sont moins difficiles, moins coûteux et moins longs à surveiller. Cela favorise l'analyse d'un plus grand nombre d'échantillons, ce qui donne une meilleure image globale de la qualité de l'eau et, par conséquent, une meilleure protection de la santé publique. Différents organismes indicateurs peuvent être utilisés à des fins précises dans la gestion des risques liés à l'eau potable, dans des domaines tels que l'évaluation des sources d'approvisionnement en eau, la surveillance opérationnelle, la validation des procédés de traitement de l'eau potable et la vérification de la qualité de l'eau potable (OMS, 2005).
À l'échelle mondiale, E. coli est l'indicateur de contamination fécale le plus largement utilisé dans les systèmes d'approvisionnement en eau potable (Edberg et coll., 2000; Payment et coll., 2003). E. coli est principalement associé aux matières fécales humaines et animales et on considère que sa présence est plus spécifique à une contamination fécale que celle d'autres bactéries indicatrices comme les coliformes thermotolérants ou les entérocoques (Edberg et coll., 2000; Standridge et coll., 2008; Lin et Ganesh, 2013). La bactérie E. coli est excrétée en grand nombre dans les matières fécales humaines et animales, elle ne prolifère généralement pas dans l'eau potable et peut être détectée rapidement, facilement et à peu de frais. Ces caractéristiques précises rendent E. coli très utile pour détecter une contamination fécale même lorsque la contamination est fortement diluée.
La bactérie E. coli sert principalement d'indicateur de contamination fécale pendant la surveillance pour vérifier la qualité microbiologique de l'eau potable. La vérification de la qualité de l'eau potable est un aspect fondamental d'une approche de la source au robinet ou d'un plan de gestion de la sécurité sanitaire de l'eau applicable aux systèmes d'approvisionnement en eau potable et qui comprend un volet de surveillance pour confirmer que le système dans son ensemble fonctionne comme prévu (Santé Canada, 2001; CCME, 2004; OMS, 2005). E. coli peut également être utilisé comme paramètre dans les évaluations des sources d'approvisionnement en eau et pendant les études menées sur des systèmes d'approvisionnement en eau potable après la mise en œuvre de mesures correctives ou dans le cadre d'une surveillance.
L'E. coli n'est pas un microorganisme de substitution pour des agents pathogènes dans l'eau (Santé Canada, 2019c, 2019d). De nombreuses études ont démontré que la présence d'E. coli ne prédit pas de façon fiable la présence d'agents pathogènes entériques ou non entériques précis d'origine hydrique (Wu et coll., 2011; Payment et Locas, 2011; Edge et coll., 2013; Hynds et coll., 2014; Lalancette et coll., 2014; Ashbolt, 2015; Falkinham et coll., 2015; Krkosek et coll., 2016; Fout et coll., 2017). Au cours du traitement de l'eau, le taux d'enlèvement physique d'E. coli est différent de celui de protozoaires entériques et de virus entériques; E. coli est aussi plus facilement inactivé par les désinfectants utilisés pour le traitement de l'eau potable que ces deux types de microorganismes (voir la section 7.0). La présence d'E. coli dans l'eau potable est un indicateur de la contamination récente de l'eau par des matières fécales et d'un grand risque pour la santé, que des agents pathogènes précis soient observés ou non.
4.4.1 Rôle dans les sources d'eau souterraine
La présence d'E. coli dans un puits d'eau souterraine indique que le puits a été contaminé par des matières fécales et que des mesures correctrices doivent être prises. (Voir les sections 3.1.3 et 3.2.2). La surveillance d'E. coli est un élément essentiel de la protection de la santé publique pour tous les systèmes d'approvisionnement en eau, désinfectés et non désinfectés. Les petits systèmes d'approvisionnement en eau potable, en particulier ceux alimentés par une eau souterraine non désinfectée, sont plus vulnérables aux effets de la contamination fécale et sont plus fréquemment associés à un résultat positif pour la présence d'indicateurs bactériologiques, notamment E. coli, que les grands réseaux (Cretikos et coll.,2010; Invik et coll., 2017; Messner et coll., 2017; Santé Canada, 2018d). Des études sur la qualité de l'eau souterraine des puits municipaux canadiens ont démontré l'importance des données historiques sur la présence d'E. coli dans l'eau souterraine brute lorsqu'il s'agit d'évaluer la sensibilité potentielle d'un puits à la contamination fécale (Payment et Locas, 2005; Locas et coll., 2007, 2008). La détection récurrente d'E. coli dans une source d'eau souterraine indique une dégradation de la qualité de la source et une présence plus probable d'agents pathogènes (Payment et Locas, 2005, 2011; Locas et coll., 2007, 2008; Fout et coll., 2017).
Des recherches sur des éclosions de maladies d'origine hydrique causées par de petites systèmes d'approvisionnement en eau potable ont également démontré l'utilité de la surveillance d'E. coli pour vérifier la présence d'une contamination fécale et l'efficacité du traitement d'une eau souterraine (Laursen et coll., 1994; Fogarty et coll., 1995; Engberg et coll., 1998; Novello, 2000; Olsen et coll., 2002; O'Connor, 2002a; Hrudey et hrudey, 2014; Government Inquiry into Havelock North Drinking Water, 2017; Kauppinen et coll., 2017). Des décès ont été associés à un certain nombre de ces éclosions, dont celle de la foire agricole du comté de Washington, à New York (1999), celle de Walkerton, en Ontario (2000) et celle de Havelock North, en Nouvelle-Zélande (2016) (Novello, 2000; O'Connor, 2002a; Hrudey et Hrudey, 2014; Government Inquiry into Havelock North Drinking Water, 2017).
L'eau souterraine provenant de puits privés est généralement perçue comme étant propre à la consommation par les consommateurs (Hynds et coll., 2013; Murphy et coll., 2017); toutefois, ce n'est pas toujours juste. Des études ont démontré que les puits privés peuvent donner des résultats positifs pour E. coli plus fréquemment que les systèmes à l'échelle municipale et les systèmes à l'échelle résidentielle qui fournissent de l'eau potable au public (Krolik et coll., 2013; Invik et coll., 2017; Saby et coll., 2017). De plus, des chercheurs ont estimé que la consommation d'eau provenant de puits privés contaminés et non réglementés pourrait être en grande partie responsable du fardeau total des maladies gastro-intestinales aiguës associées aux sources d'approvisionnement en eau potable (DeFelice et coll., 2016; Murphy et coll., 2016b).
L'information ci-dessus souligne l'importance d'analyser régulièrement tant l'eau souterraine non traitée que l'eau souterraine traitée pour améliorer la capacité d'un programme de surveillance à détecter des puits contaminés par des matières fécales. Des conseils supplémentaires sont disponibles pour les responsables de systèmes d'approvisionnements en eau potable, les propriétaires et les exploitants de systèmes afin d'aider à développer les meilleures pratiques pour contrôler et répondre aux dangers microbiologiques (CCME, 2004; OMS, 2012; AWWA, 2014).
4.4.2 Rôle dans les sources d'eau de surface
Bien que les relations semblent être propres au site, la surveillance de la présence d'E. coli dans l'eau brute peut fournir des données sur les répercussions causées par les sources de pollution fécale qui contaminent la source d'approvisionnement en eau potable et le moment où elles se produisent. De même, elle peut fournir de l'information sur les effets des mesures de protection des sources d'approvisionnement en eau ou de contrôle des dangers mises en œuvre dans le bassin versant. Les données sur E. coli dans les sources d'approvisionnement en eau peuvent également servir à fournir des renseignements supplémentaires pour évaluer les risques microbiologiques et les exigences de traitement des sources d'eau de surface (U.S. EPA, 2006b; Hamouda et coll., 2016).
Des corrélations entre des organismes indicateurs et des agents pathogènes peuvent parfois être observées dans les eaux fortement polluées, mais elles se détériorent rapidement en raison de la dilution et des différences dans le devenir et le transport des différents microorganismes dans différents milieux aquatiques (Payment et Locas, 2011). Lalancette et coll. (2014) ont constaté qu'E. coli était un bon indicateur potentiel de la concentration de Cryptosporidium dans des prises d'eau potable lorsque les sources d'approvisionnement en eau sont récemment contaminées par des eaux usées municipales proches, mais pas dans les prises d'eau où les sources étaient dominées par des sources de pollution fécale agricole ou rurale ou par des sources plus éloignées. Dans certaines études où la densité d'E. coli dépassait 100 UFC par 100 mL, des possibilités accrues de détection des agents pathogènes entériques (Campylobacter, Cryptosporidium, Salmonella et E. coli O157:H7) dans des échantillons d'eau de surface ont été mises en évidence (Van Dyke et coll., 2012, Banihashemi et coll., 2015; Stea et coll., 2015).
4.4.3 Rôle dans la surveillance du traitement
La détection d'E. coli dans l'eau immédiatement après le traitement ou à la sortie de la station de traitement dénote un traitement inadéquat et est inacceptable. Cretikos et coll. (2010) ont examiné les facteurs associés à la détection d'E. coli dans les systèmes publics d'approvisionnement en eau potable en Nouvelle-Galles-du-Sud, en Australie. Les systèmes non désinfectés et les petits systèmes d'approvisionnement en eau desservant moins de 500 personnes étaient les plus fortement associés à la détection d'E. coli. Des détections d'E. coli ont également été associées de façon importante à des systèmes désinfectés uniquement aux UV ou à une turbidité post-traitement plus élevée.
Des éclosions attribuables à l'eau potable ont été associées à des approvisionnements municipaux où les paramètres de qualité de l'eau (y compris E. coli) étaient inférieurs aux limites acceptables reconnues à l'époque (Hayes et coll., 1989; Maguire et coll., 1995; Goldstein et coll., 1996; Jack et coll., 2013). Les taux d'élimination d'E. coli sont différents selon les procédés physiques, et la bactérie est plus sensible aux désinfectants de l'eau potable que les virus entériques et les protozoaires. Bien que l'analyse de détection d'E. coli soit utile pour évaluer l'efficacité du traitement, elle n'est pas suffisante comme paramètre permettant d'isoler d'autres facteurs pour évaluer les répercussions sur ces agents pathogènes (Payment et coll., 2003). E. coli peut être employé dans le cadre du processus de vérification de la qualité de l'eau conjointement avec l'information sur l'efficacité du traitement pour établir que l'eau a été traitée adéquatement et qu'elle est donc d'une qualité microbiologique acceptable (Payment et coll., 2003; Stanfield et coll., 2003). Toutefois, dans le cadre d'une approche de la source au robinet ou d'un plan de gestion de la sécurité sanitaire de l'eau pour les systèmes d'approvisionnement en eau potable, la validation des procédés de traitement et de désinfection est également importante pour démontrer que le système peut fonctionner selon les besoins et atteindre les niveaux requis de réduction des dangers (CCME, 2004; OMS, 2005).
4.4.4 Rôle dans la surveillance du réseau de distribution
Des microorganismes peuvent pénétrer dans le réseau de distribution en résistant aux procédés de traitement et de désinfection durant un traitement inadéquat, ou encore, par suite d'une contamination post-traitement causée par des intrusions, des raccordements croisés ou pendant des travaux de construction ou de réparation.
La présence d'E. coli dans un échantillon du réseau de distribution peut indiquer que le traitement de la source d'approvisionnement en eau était inadéquat, ou que l'eau traitée a été contaminée par des matières fécales pendant la distribution. Des contaminations post-traitement causées, par exemple, par des raccordements croisés, des siphonages à rebours, des occurrences de pression transitoire négative ou faible, une contamination des réservoirs de stockage ou une contamination des conduites principales attribuable à des réparations, se sont révélées des causes de contamination du réseau de distribution liée à la maladie (Craun, 2002; Hunter et coll., 2005; Breitenmoser et coll., 2008; Falco et Williams, 2009; Laine et coll., 2011; Hrudey et Hrudey, 2014; Puleston et coll., 2014). Les éclosions de Nokia, en Finlande (2007) et d'Alamosa, au Colorado (2008) ont été liées à ce type de contamination (Falco et Williams, 2009; Laine et coll., 2011).
La détection d'E. coli devrait être sporadique et rare dans les installations de traitement et les réseaux de distribution bien conçus et bien exploités. Des rapports sur la qualité de l'eau fournis par de grands services municipaux d'eau potable au Canada ont démontré que le nombre d'échantillons du réseau de distribution qui sont positifs pour E. coli est généralement inférieur à 1 % par année (Santé Canada, 2018h). Les données démontrant la qualité de l'eau potable dans chaque province et territoire peuvent être obtenues auprès de l'autorité responsable en matière d'eau potable ou les services d'eau. La détection d'E. coli dans le réseau de distribution peut dénoter un risque accru d'exposition à des agents pathogènes entériques pour les consommateurs des régions touchées. Miles et coll. (2009) ont analysé des filtres au point d'utilisation se trouvant dans des distributeurs automatiques d'eau potable en Arizona pour évaluer la qualité microbiologique de grands volumes (p. ex. 1 000 à 17 000 L) d'eau potable traitée et distribuée, et ils ont observé que 60 % (3 sur 5) des filtres positifs pour E. coli étaient également positifs pour les entérovirus.
Les résultats d'études de systèmes modèles, à une échelle réduite et à une échelle réelle, ont démontré qu'E. coli peut s'accumuler en faibles quantités dans des biofilms de réseaux de distribution, principalement dans un état viable, mais non cultivable (Fass et coll. 1996; Williams et Braun-Howland, 2003; Juhna et coll., 2007; Lehtola et coll., 2007; Abberton et coll., 2016; Mezule et Juhna, 2016). Cependant, une fois intégré dans la matrice des biofilms, les concentrations d'E. coli sont contrôlées par la communauté microbienne naturelle par des processus tels que la prédation et la compétition pour les éléments nutritifs (Fass et coll. 1996; Abberton et coll., 2016; Mezule et Juhna, 2016). Par conséquent, la détection d'E. coli dans un réseau de distribution d'eau est un bon indicateur d'une contamination fécale récente. La présence d'E. coli dans tout échantillon prélevé dans un réseau de distribution ou des installations de stockage est inacceptable et devrait donner lieu à des mesures correctives (voir la section 3.1.3). Des conseils supplémentaires sont disponibles pour les responsables de systèmes d'approvisionnements en eau afin d'aider à développer les meilleures pratiques pour contrôler les dangers microbiologiques (CCME, 2004; AWWA, 2017; Hill et al., 2018).
4.4.5 Rôle d'E. coli dans la décision d'émettre des avis d'ébullition de l'eau
Les avis d'ébullition de l'eau sont des avis publics recommandant aux consommateurs de faire bouillir leur eau potable avant de la consommer afin d'éliminer tout microorganisme pathogène soupçonné ou confirmé dans l'eau. Ces avis s'inscrivent dans le cadre des activités de surveillance de l'eau potable et de protection de la santé publique à l'échelle du pays. Santé Canada (2015) fournit plus de renseignements sur l'émission et l'annulation des avis concernant l'eau potable.
Des données sur l'eau potable (principalement sur les avis d'ébullition de l'eau) sont recueillies par l'application sur les avis concernant la qualité de l'eau potable du Réseau canadien de renseignements sur la santé publique (RCRSP), une application Web sécurisée et en temps réel, et par les organismes de réglementation provinciaux et territoriaux. Les données provinciales, territoriales et municipales sur l'eau potable sont fournies par l'autorité responsable en matière d'eau potable dans le secteur de compétence concerné. Bien que les données du RCRSP ne brossent pas un tableau national complet, les tendances dégagées de ces données donnent un aperçu utile de la nature des avis d'ébullition de l'eau et des défis auxquels les systèmes d'approvisionnement en eau potable sont confrontés au Canada. Un examen des dossiers d'avis d'ébullition de l'eau disponibles au Canada (9 884 dossiers d'avis d'ébullition de l'eau émis entre 1984 et la fin de 2017) a révélé que 594 (6 %) des avis d'ébullition étaient diffusés par suite de la détection d'E. coli dans le système d'approvisionnement en eau potable (Santé Canada, 2018c). Les autres avis d'ébullition de l'eau ont été diffusés pour d'autres raisons, les plus courantes étant liées à l'équipement et au procédé (voir la figure 1).
Figure 1. Proportions globales des raisons pour lesquelles des avis d'ébullition de l'eau ont été émis*
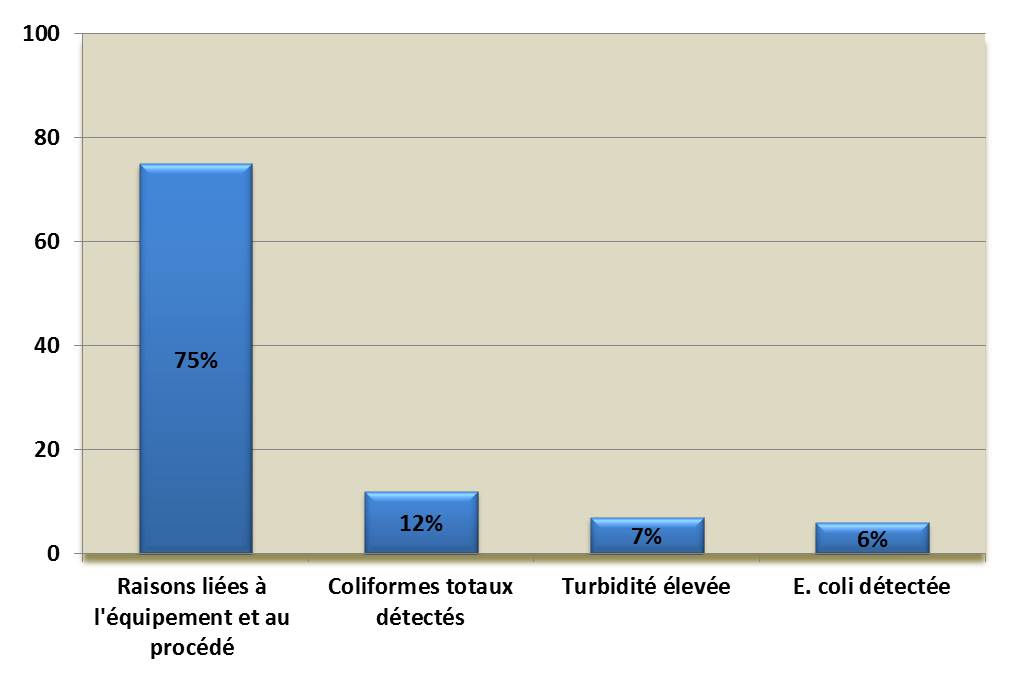
*Données de 1984 à 2017 (n = 9 884)
Équivalent textuel
La figure 1 est un diagramme à barres illustrant les proportions globales des raisons pour lesquelles des avis d'ébullition de l'eau ont été émis de 75% - raisons liées a l'équipement et au procédé, 12% - coliformes totaux détectés, 7% - turbidité elevée et 6% - E. coli détectée.
Plus de 99 % des 594 avis d'ébullition de l'eau associés à la détection d'E. coli ont été émis pour de petits systèmes d'approvisionnement en eau potable (voir la figure 2) et ils étaient presque également répartis entre les sources d'eau de surface et d'eau souterraine (voir la figure 3) (Santé Canada, 2018c). Plus de la moitié de ces avis ont été émis sans qu'aucun autre contexte opérationnel n'ait été consigné (voir la figure 4), ce qui peut indiquer qu'ils ont été émis uniquement en réponse à un résultat positif pour E. coli pendant l'échantillonnage de routine. Dans l'ensemble, les données confirment que les petits systèmes d'approvisionnement en eau potable font face à un risque accru de contamination. Les données soulignent également l'importance de la surveillance des paramètres opérationnels combinée à des analyses régulières de détection d'E. coli pour confirmer la qualité de l'approvisionnement de l'eau potable.
Figure 2. Population desservie par des systèmes d'approvisionnement en eau potable visés par des avis d'ébullition de l'eau liés à la détection d'E. coli*
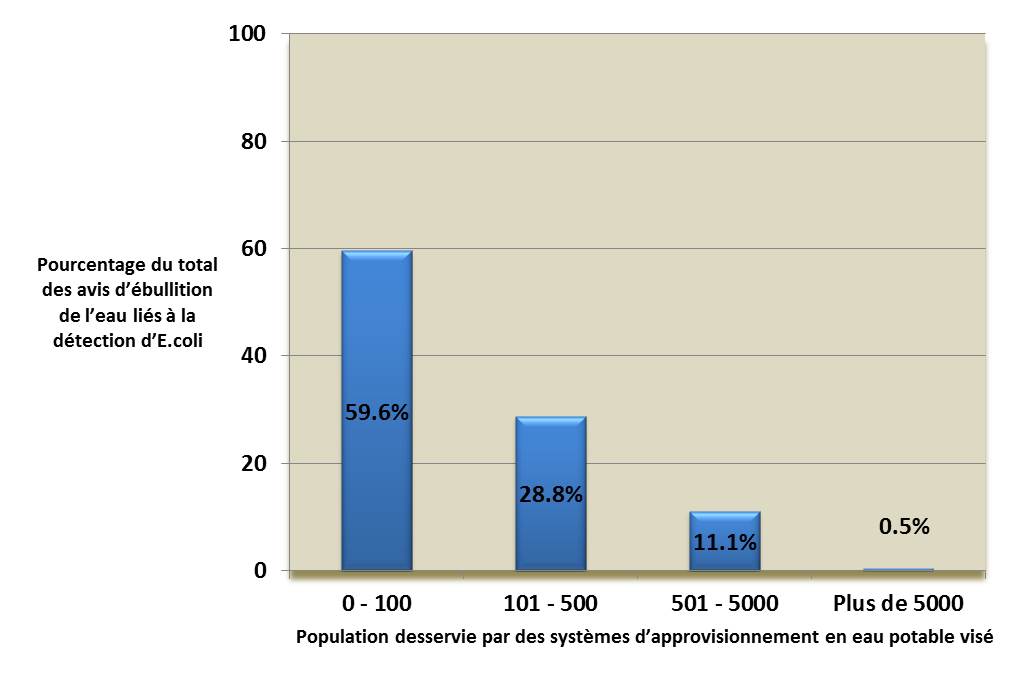
*Données de 1984 à 2017 (n = 9884)
Équivalent textuel
La figure 2 est un diagramme à barres illustrant la population desservie par des systèmes d'approvisionnement en eau potable visés par des avis d'ébullition de l'eau liés à la détection d'E. coli. 59,6% des réseaux d'eau potable concernés desservent de 0 à 100 personnes, 28,8% desservent de 101 à 500 personnes, 11,1 desservent de 501 à 5000 personnes et 0,5% desservent plus de 5000 personnes
Figure 3. Source d'approvisionnement en eau utilisée par les systèmes d'approvisionnement en eau potable visés par des avis d'ébullition de l'eau liés à la détection d'E. coli*

*Données de 1984 à 2017 (n = 9884)
Équivalent textuel
La figure 3 est un diagramme à barres illustrant la source d'approvisionnement en eau utilisée par les systèmes d'approvisionnement en eau potable visés par des avis d'ébullition de l'eau liés à la détection d'E. coli Les proportions montrent que 48% utilisent eau de surface, 46% utilisent eau souterraine et 6% utilisent autre source compris une eau mélanger, une eau acheminée par camion-citerne et une eau stockée en citerne.
Figure 4. Contexte opérationnel associé aux avis d'ébullition de l'eau liés à la détection d'E. coli*
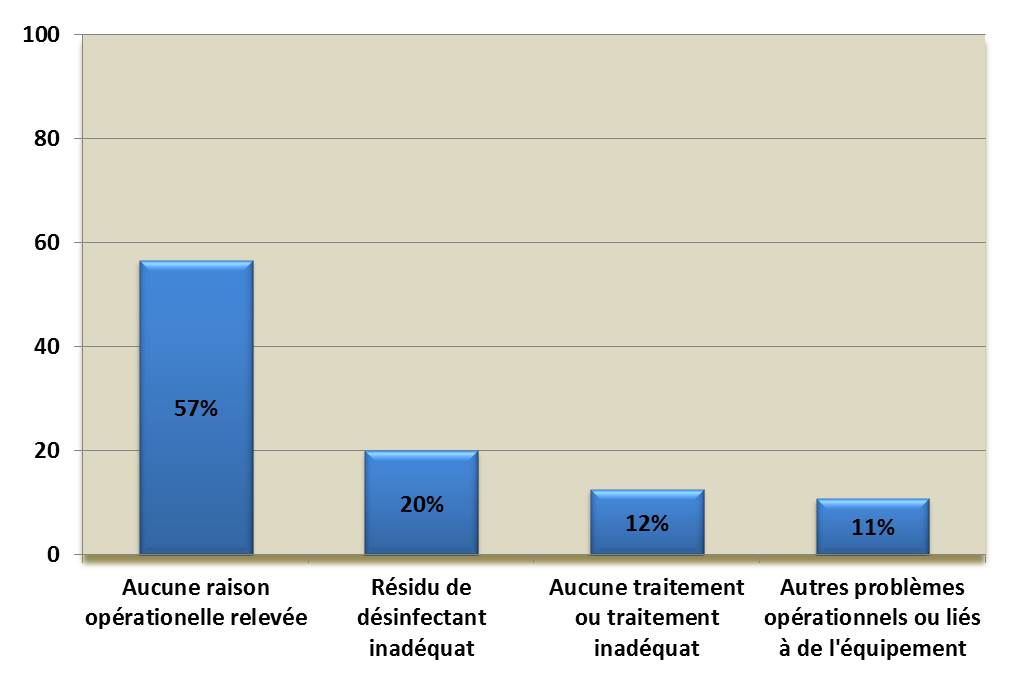
*Données de 1984 à 2017 (n = 9884)
Équivalent textuel
La figure 4 est un diagramme à barres illustrant le contexte opérationnel associé aux avis d'ébullition de l'eau liés à la détection d'E. coli. 57% n'identifient pas de raison opérationnelle, 20% identifient des résidus de désinfectant inadéquats, 12% identifient aucune traitement ou traitement inadéquat et 11% identifient autre problèmes opérationnels ou liés à de l'équipement.
5.0 Méthodes d'analyse
Toutes les analyses de détection d'E. coli doivent être effectuées conformément aux directives de l'autorité responsable en matière d'eau potable. Dans de nombreux cas, cette autorité recommande ou exige le recours à des laboratoires accrédités. Dans certains cas, il peut être nécessaire d'utiliser d'autres moyens pour analyser des échantillons en temps opportun, comme des analyses sur place au moyen de trousses d'analyse commerciales réalisées par des techniciens qualifiés. Il est important d'employer des méthodes validées ou normalisées pour que les décisions de santé publique soient prises correctement et sans délai. Lorsqu'ils achètent des services de laboratoire ou choisissent des méthodes d'analyse à effectuer à l'interne, les responsables de systèmes d'approvisionnements en eau potable devraient consulter le laboratoire d'analyse ou le fabricant au sujet de la sensibilité, de la spécificité et du délai d'exécution des méthodes. Afin de garantir la fiabilité des résultats, un programme d'assurance de la qualité (AQ), comprenant des procédures de contrôle de la qualité (CQ), devrait être en place. Les analyses effectuées à l'aide de trousses d'analyse doivent respecter les instructions du fabricant.
5.1 Méthodes fondées sur la culture
Les méthodes normalisées disponibles pour la détection d'E. coli dans l'eau potable sont résumées au tableau 1. Les méthodes qui ciblent E. coli reposent sur la présence de l'enzyme β-D-glucuronidase. Il s'agit d'une enzyme distinctive que l'on trouve dans la grande majorité des isolats d'E. coli. Le gène uidA qui code l'enzyme β-glucuronidase est présent dans plus de 97 % des isolats d'E. coli (Feng et coll., 1991; Martins et coll., 1993; Maheux et coll., 2009). Le gène peut également se trouver dans une faible proportion de souches de Shigella et de Salmonella et dans certaines souches d'autres espèces bactériennes, mais il est rarement présent dans d'autres coliformes (Feng et coll., 1991; Fricker et coll., 2008, 2010; Maheux et coll., 2008, 2017.). Bien que le sérotype d'E. coli O157:H7 et certaines souches de Shigella soient porteurs de séquences nucléotidiques du gène uidA, la plupart des isolats ne présentent aucune activité enzymatique (Feng et Lampel, 1994, Maheux et coll., 2011). Les méthodes de détection tirent également parti des caractéristiques biochimiques propres à E. coli et utilisent des additifs ajoutés au milieu de culture et des températures d'incubation pour inhiber la croissance des microorganismes de fond. Toutes les méthodes énumérées au tableau 1 sont capables de détecter les coliformes totaux et de différencier simultanément E. coli.
Lorsqu'il faut vérifier un résultat d'essai positif, il existe de nombreuses façons d'identifier E. coli parmid'autres coliformes et d'autres espèces de bactéries. Des analyses biochimiques pour différencier les membres de la famille des entérobactéries, y compris E. coli, ainsi que des milieux de culture commerciaux et des trousses d'identification pour vérifier la présence d'E. coli sont disponibles (APHA et coll., 2017; ISO, 2018). La confirmation de la présence d'E. coli peut également se faire en mettant en culture des échantillons positifs pour les coliformes dans un milieu qui révèle la présence de l'enzyme β-D-glucuronidase (APHA et coll., 2017). L'utilisation de plusieurs essais biochimiques pour la confirmation améliorera l'exactitude de l'identification (Maheux et coll., 2008).
| Organisation - Méthode | Milieu de croissance | Format des résultats | Coliformes totaux détectés (O/N) |
Délai d'exécution |
|---|---|---|---|---|
| Filtration sur membrane | ||||
| SM 9222 JTableau 1 Note de bas de page a U.S. EPA-S/OTableau 1 Note de bas de page bTableau 1 Note de bas de page c |
bouillon m-ColiBlue24® | P-A, C | O | 24 h |
| SM 9222 KTableau 1 Note de bas de page a U.S. EPA 1604Tableau 1 Note de bas de page bTableau 1 Note de bas de page c |
bouillon ou gélose MI | P-A, C | O | 24 h |
| ISO 9308-1:2014Tableau 1 Note de bas de page d U.S. EPA-S/OTableau 1 Note de bas de page bTableau 1 Note de bas de page c |
gélose CF Chromocult® | P-A, C | O | 21-24 h |
| Substrat enzymatique | ||||
| SM 9223 BaTableau 1 Note de bas de page a U.S. EPA-S/OTableau 1 Note de bas de page bTableau 1 Note de bas de page c |
milieu Colilert® | P-A, C | O | 24-28 h |
| SM 9223 BTableau 1 Note de bas de page a ISO 9308-2: 2012Tableau 1 Note de bas de page d U.S. EPA-N/ATableau 1 Note de bas de page bTableau 1 Note de bas de page c |
milieu Colilert-18® | P-A, C | O | 18-22 h |
| SM 9223 BTableau 1 Note de bas de page a U.S. EPA-N/ATableau 1 Note de bas de page bTableau 1 Note de bas de page c |
milieu Colisure® | P-A, C | O | 24-28 h |
| U.S. EPA-S/OTableau 1 Note de bas de page bTableau 1 Note de bas de page c | milieu E*Colite® | P-A | O | 28-48 h |
| U.S. EPA-S/OTableau 1 Note de bas de page bTableau 1 Note de bas de page c | bouillon Readycult®Coliforms 100 | P-A | O | 24 h |
| U.S. EPA-S/OTableau 1 Note de bas de page bTableau 1 Note de bas de page c | milieu Modified Colitag™ | P-A | O | 16-22 h |
| U.S. EPA-S/OTableau 1 Note de bas de page bTableau 1 Note de bas de page c | milieu Tecta™ EC/TC | P-A | O | 18 h |
S/O - sans objet; P-A - présence-absence; C - numération |
||||
Le recours à d'autres méthodes pourrait être autorisé dans d'autres secteurs de compétences (CEAEQ, 2018; MECP, 2019). Les résultats des méthodes d'analyse d'E. coli sont présentés sous forme de présence-absence (P-A) ou de numération (C) de bactéries. La méthode P-A ne fournit aucune information sur la concentration d'organismes dans l'échantillon. La quantification des organismes est parfois utilisée pour évaluer le degré de contamination et, à ce titre, elle est considérée comme un avantage des méthodes plus quantitatives. Pour le processus décisionnel, l'accent est mis sur la détection positive d'E. coli, peu importe la quantité; comme la recommandation pour E. coli dans l'eau potable est de zéro par 100 mL, les résultats qualitatifs sont suffisants pour protéger la santé publique.
5.1.1 Efficacité des méthodes de détection
Il y a des limitations à la capacité de détection des méthodes de culture fondées sur l'expression de l'enzyme β-glucuronidase pour identifier la présence d'E. coli (Maheux et coll., 2008; Zhang et coll., 2015). On a aussi constaté une variabilité dans le rendement des méthodes commercialisées de détection d'E. coli après avoir réalisé des essais en laboratoire avec des isolats provenant de différents milieux (p. ex. clinique, environnement), types d'eau et endroits géographiques (Bernasconi et coll., 2006; Olstadt et coll., 2007; Lange et coll., 2008; Maheux et coll., 2008; Maheux et coll., 2015a; 2015b; Martin et Gentry, 2016, Maheux et coll., 2017). Les facteurs qui peuvent influer sur la capacité des méthodes de culture à détecter E. coli comprennent : la variabilité naturelle du pourcentage de souches ne présentant aucune activité enzymatique β-D-glucuronidase dans la population source (Feng et Lampel, 1994; Maheux et coll., 2008), la composition des milieux (Hörman et Hänninen, 2006; Olstadt et coll., 2007; Maheux et coll., 2008, 2017; Fricker et coll., 2010; Martin et Gentry, 2016), la concentration des organismes et leur état physiologique (Ciebin et coll., 1995; Maheux et coll., 2008; Zhang et coll., 2015) et les caractéristiques de qualité de l'eau (Olstadt et coll., 2007).
Des méthodes normalisées ont été validées par rapport à des méthodes de référence établies pour s'assurer que la méthode produise des résultats acceptables (APHA et coll., 2017). Néanmoins, il est nécessaire d'évaluer continuellement l'efficacité des méthodes d'analyse d'E. coli et d'améliorer leur sensibilité et leur spécificité. L'exactitude des méthodes futures pourrait être améliorée grâce à des techniques avancées combinant des caractéristiques biochimiques et des tests moléculaires (Maheux et coll., 2008). Parmi les autres stratégies utiles, mentionnons les efforts déployés par des organismes d'approbation pour examiner régulièrement les critères de sélection et le rendement des méthodes, ainsi que le travail continu des fabricants pour optimiser les formulations de leurs milieux de culture (Zhang et coll., 2015). Les critères à prendre en considération lors de la conception d'études pour l'évaluation des méthodes microbiologiques sont abordés dans d'autres publications (Boubetra et coll., 2011; APHA et coll., 2017; Duygu et Udoh, 2017).5.2 Méthodes moléculaires
Étant donné les limites associées aux méthodes de culture pour détecter E. coli (p. ex. le temps requis pour l'analyse, l'absence d'universalité du signal de l'enzyme β-D-glucuronidase, leur incapacité à détecter les organismes VMNC), les méthodes moléculaires de détection demeurent intéressantes (Martins et coll., 1993; Heijnen et Medema, 2009; Mendes Silva et Domingues, 2015). Aucune méthode moléculaire de détection d'E. coli dans l'eau potable n'a été normalisée ni approuvée pour surveiller la conformité de l'eau potable.
Les méthodes de détection PCR (réaction en chaîne de la polymérase) sont les méthodes moléculaires les plus couramment décrites pour détecter les microorganismes dans l'eau (Maheux et coll., 2011; Gensberger et coll., 2014; Krapf et coll., 2016). Ces dernières années, le nombre de techniques disponibles a considérablement augmenté et les coûts associés à leur utilisation ont été considérablement réduits (Mendes Silva et Domingues, 2015). Cependant, la difficulté la plus importante associée à l'analyse par PCR d'échantillons d'eau potable demeure la nécessité d'offrir un seuil de détection suffisamment faible. Différentes méthodes moléculaires explorées pour la détection d'E. coli dans les sources d'approvisionnement d'eau sont décrites ailleurs (Botes et coll., 2013; Mendes Silva et Domingues, 2015). À l'heure actuelle, les seuils de détection signalés pour la grande majorité des méthodes décrites dans la littérature sont supérieures au seuil de sensibilité d'une bactérie E. coli par 100 mL requis pour l'analyse de l'eau potable (Heijnen et Medema 2009; Maheux et coll., 2011, Gensberger et coll., 2014; Mendes Silva et Domingues, 2015; Krapf et coll., 2016). Des travaux supplémentaires sont nécessaires pour optimiser davantage la sensibilité des méthodes moléculaires de détection d'E. coli et pour mettre au point des méthodes normalisées destinées à la surveillance systématique qui sont précises, fiables, faciles et abordables.5.3 Méthodes de surveillance rapide en ligne
Le besoin d'une surveillance plus rapide et plus fréquente d'E. coli dans les réseaux de distribution d'eau potable a amené les chercheurs à explorer des technologies de détection en ligne de la qualité de l'eau capables de détecter en temps réel une contamination par E. coli. Certains des capteurs étudiés se basent sur des mesures de l'impédance électrique (Kim et coll., 2015), de la fluorescence d'anticorps ou de marqueurs (Golberg et coll., 2014; Gutieérrez-del-Rio, 2018) ou de paramètres de qualité de l'eau tels que la conductivité, la numération des particules, le pH, la turbidité, l'absorbance UV, le carbone organique total, seuls ou en combinaison (Miles et coll., 2011; Ikonen et coll., 2017). La difficulté la plus importante associée aux méthodes potentielles de détection rapide en ligne est la nécessité d'obtenir une sensibilité à de très faibles concentrations d'E. coli (Kim et coll., 2015; Ikonen et coll., 2017). Parmi les autres obstacles, mentionnons les exigences en matière d'équipement, de formation des utilisateurs et d'interprétation des données (Golberg et coll., 2014; Ikonen et coll., 2017). Comme pour les méthodes moléculaires de détection, d'autres travaux sont nécessaires avant que les méthodes rapides puissent être utilisées à grande échelle.
6.0 Échantillonnage d'E. coli
6.1 Prélèvement des échantillons
Il faut prélever les échantillons suivant de bonnes procédures si l'on veut qu'ils soient représentatifs de l'eau à analyser. Il existe des directives facilitant le travail des responsables de systèmes d'approvisionnements en eau potable (OMS et OCDE, 2003; APHA et coll., 2017). Le prélèvement d'échantillons en vue d'une analyse microbiologique nécessite une bonne technique d'échantillonnage qui évite la contamination par les surfaces externes (p. ex. mains, robinet) au cours du prélèvement (OMS et OCDE, 2003; APHA et coll., 2017). On recommande aux préposés à l'échantillonnage de choisir soigneusement les lieux d'échantillonnage, d'éviter (ou sinon de désinfecter) les robinets susceptibles d'être contaminés (p.ex. près du fond d'un évier ou près du sol) et les robinets dont la propreté laisse à désirer (OMS et OCDE, 2003; APHA et coll., 2017).
En général, les échantillons destinés aux essais microbiologiques devraient être emballés avec des blocs réfrigérants, mais en évitant tout contact direct pour éviter le gel des échantillons. Il n'est pas recommandé d'emballer l'échantillon avec de la glace en morceaux, car elle pourrait contaminer l'échantillon. Pendant le transport, les échantillons doivent être conservés au frais, mais non congelés, à une température comprise entre 4 et 10 °C (Payment et coll., 2003; APHA et coll., 2017). Des appareils commerciaux sont disponibles pour vérifier le respect d'une température de transport adéquate. Pendant les mois d'été et d'hiver, des mesures supplémentaires peuvent être nécessaires pour maintenir la température optimale des échantillons pendant le transport. Ces étapes peuvent comprendre l'ajout de blocs réfrigérants supplémentaires ou une communication avec les messagers pour s'assurer que la glacière ne sera pas gardée dans des endroits de gel ou de chauffage excessif.
Pour éviter un changement imprévisible du nombre de bactéries, les échantillons d'E. coli doivent toujours être analysés le plus tôt possible après le prélèvement. Lorsqu'il existe des installations sur place ou lorsqu'un laboratoire accrédité se trouve à une distance acceptable, il est suggéré d'analyser les échantillons dans les 6 à 8 heures (Payment et coll., 2003; APHA et coll., 2017). Idéalement, pour l'analyse de détection d'E. coli dans des échantillons d'eau potable, la durée de conservation entre le prélèvement de l'échantillon et le début de son analyse ne devrait pas dépasser 30 heures (APHA et coll., 2017).
Il existe peu d'études sur les effets de la durée de conservation des échantillons d'eau sur la détection d'E. coli. Selon Ahammed et coll. (2003), la numération d'E. coli (concentration initiale = 21 nombre le plus probable (NPP)/100mL) dans les échantillons d'eau souterraine enrichis et conservés à 4 °C, s'est abaissée de 3 % et de 16 % après une conservation de 6 et 24 heures, respectivement. D'après d'autres études, des durées de conservation supérieures à 8 à 24 heures n'ont pas modifié considérablement la numération d'E. coli. Dans une étude sur les eaux de surface, Pope et coll. (2003) ont observé que les échantillons conservés à 4 °C et provenant de trois sites sur quatre n'étaient pas associés à une diminution significative de la numération (fourchette de concentration : 76 à 7 949 E. coli/100 mL) tant que la durée de conservation ne dépassait pas 48 heures. Bushon et coll. (2015) a étudié les effets de la durée de conservation de l'eau souterraine (fourchette de concentration : 3 à 63 UFC/100 mL) en comparant des échantillons contenant des E. coli analysés dans les 8 heures suivant le prélèvement par des méthodes décelant la présence ou l'absence avec des échantillons analysés dans les premières 18 à 30 heures à l'aide de méthodes quantitatives. Les données indiquent qu'une durée de conservation entre 8 heures et 18 à 30 heures n'a pas réduit le nombre d'E. coli détectés. Dans une autre étude sur l'eau souterraine, Maier et coll., (2015) ont fait état d'une baisse de la concentration d'E. coli dans des échantillons enrichis (fourchette : 72 à 130 UFC, volume non précisé) qui ne dépassait pas 10 % pour des échantillons conservés durant 48 heures. Ce constat laisse croire que les échantillons d'E. coli pourraient être analysés avec des méthodes courantes de détection et donner des résultats comparables, après au moins 8 heures suivant le prélèvement. Toutefois, les auteurs de l'étude ont aussi noté des variations dans le taux de survie d'E. coli selon certains endroits ou avec différents isolats (Pope et coll., 2003; Maier et coll., 2015). Par ailleurs, des études réalisées par McDaniels et ses collaborateurs (1985) et Ferguson (1994) montrent que la durée de conservation peut être plus cruciale pour les coliformes lorsque la concentration est faible.
Les conséquences d'une prolongation de la durée de conservation devraient être discutées avec l'autorité responsable en matière d'eau potable dans le secteur de compétence concerné. Plus précisément, il est important de tenir compte de la probabilité et des conséquences de la déclaration d'un résultat faussement négatif à la suite d'une baisse du nombre d'indicateurs bactériens pendant une conservation prolongée. Ce risque d'un résultat faussement négatif devrait être soupesé contre les conséquences associées à des échantillons rejetés ou non soumis si un service d'eau n'est pas en mesure de les faire livrer au laboratoire à l'intérieur des durées de conservation requises (Maier et coll., 2015).
Les responsable d'une installation de production d'eau potable devraient discuter avec le laboratoire des protocoles à utiliser pour rejeter ou analyser les échantillons qui ne respectent pas les exigences de durée de conservation. Pour les échantillons analysés malgré un dépassement de la durée de conservation, un résultat positif suffit comme preuve de contamination. Toutefois, un résultat négatif ne permet pas de confirmer l'absence d'une contamination. Lorsqu'un échantillon est rejeté, il est recommandé que les responsable d'une installation de production d'eau potable prélèvent immédiatement un autre échantillon au même endroit et l'analyse de nouveau. Lorsqu'on prévoit des durées de conservation longues, des essais sur place avec des méthodes d'essai commercialisées (voir le tableau 1), combinés à une formation appropriée et à des procédures de contrôle de la qualité, offrent une option d'analyse fiable et normalisée pour la vérification et la surveillance de la conformité. Les responsable d'une installation de production d'eau potable devraient d'abord consulter l'autorité responsable de l'eau potable au sujet de l'acceptabilité de cette pratique et de toute autre exigence qui pourrait s'appliquer. L'utilisation d'une procédure d'incubation retardée est une autre option pour responsable d'une installation de production d'eau potable qui ont de la difficulté à expédier des échantillons dans les délais recommandés. Un protocole d'incubation retardée pour les coliformes totaux a été décrit et il existe des méthodes de vérification pour confirmer la présence d'E. coli dans des échantillons associés à un résultat positif (APHA et coll., 2017). Ce protocole permet d'expédier au laboratoire une membrane ayant servi à filtrer un échantillon sur le site, cette membrane étant conservée dans un milieu destiné à préserver la viabilité des coliformes durant le transport (APHA et coll., 2017). Une fois au laboratoire, le filtre est transféré dans un milieu de culture fraichement préparé et est incubé (APHA et coll., 2017).
Les échantillons doivent être étiquetés conformément aux exigences spécifiées par l'autorité responsable de l'eau potable et le laboratoire d'analyse. Dans la plupart des cas, une grande partie de l'information et le numéro d'identification de la bouteille de prélèvement sont consignés sur les formulaires accompagnant les soumissions ainsi que dans la documentation relative à la chaîne de possession dans les cas où les échantillons sont prélevés à des fins judiciaires. Lorsque l'analyse est retardée, il est particulièrement important de noter la durée et la température de conservation de l'échantillon, car il faut en tenir compte dans l'interprétation des résultats. Les responsable d'une installation de production d'eau potable peuvent souhaiter consulter le laboratoire d'analyse pour connaître les exigences particulières concernant la soumission des échantillons.
Pour obtenir une estimation fiable du nombre d'E. coli dans une eau potable traitée, il faut analyser un volume d'au moins 100 mL d'eau. De plus petits volumes ou dilutions peuvent être plus pertinents pour analyser des échantillons provenant d'eaux riches en particules ou lorsque l'on peut s'attendre à un nombre élevé de bactéries. L'analyse de volumes d'eau potable plus importants peut accroître à la fois la sensibilité et la fiabilité des analyses. L'analyse d'échantillons de grand volume (20 L) à l'aide d'un filtre à capsule a été utile pour améliorer la détection des coliformes totaux (E. coli n'a pas été détectée) dans des échantillons du réseau de distribution de trois services d'eau potable au cours d'essais sur le terrain (Hargy et coll., 2010). D'autres études sur l'analyse d'échantillons de grands volumes sont nécessaires pour évaluer la valeur ajoutée des résultats. Les principales difficultés associées à l'échantillonnage de grands volumes sont d'interpréter correctement les résultats par rapport aux règlements en vigueur sur l'eau potable et d'optimiser les méthodologies pour qu'elles soient d'utilisation courante par les services d'eau. D'autres travaux statistiques et sur le terrain sont nécessaires pour examiner simultanément les paramètres suivants : volume de l'échantillon, fréquence de surveillance, méthode de détection, résultats faussement positifs et résultats faussement négatifs et coût.
6.2 Considérations relatives à la fréquence d'échantillonnage
Lorsqu'il s'agit de déterminer les exigences en matière de fréquence d'échantillonnage pour des réseaux municipaux, il est impossible d'appliquer une formule d'échantillonnage universelle en raison de différences fondamentales dans des facteurs tels que la qualité de la source d'approvisionnement d'eau, la pertinence et la capacité de traitement, la taille et la complexité du réseau de distribution (OMS, 2004). La fréquence d'échantillonnage devrait plutôt être déterminée par l'autorité responsable de l'eau potable après la prise en compte de conditions locales, comme les variations de la qualité de l'eau brute et les données historiques sur la qualité de l'eau traitée. Dans le cadre d'une surveillance opérationnelle et de la vérification d'un système de gestion de la qualité de l'eau potable utilisant une approche de la source au robinet ou d'un plan de gestion de la sécurité sanitaire de l'eau, l'eau sortant d'une station de traitement et dans le réseau de distribution devrait être analysée au moins une fois par semaine pour détecter la présence d'E. coli et quotidiennement pour déceler les résidus de désinfectant et des signes de turbidité.
Le tableau 2 fournit un guide sur la fréquence minimale d'échantillonnage recommandée pour détecter E. coli dans un réseau de distribution d'eau potable. Le nombre d'échantillons à analyser à des fins bactériologiques devrait être augmenté en fonction de la taille de la population desservie.
| Population desservie | Nombre minimal d'échantillons par moisTableau 2 Note de bas de page a |
|---|---|
| Jusqu'à 5 000 | 4 |
| 5 000 - 90 000 | 1 par 1 000 personnes |
| 90 000 et plus | Plus de 90 (1 par 10 000 personnes) |
|
|
La fréquence d'échantillonnage dans les réseaux municipaux et résidentiels peut varier dépendant du secteur de compétence concerné, mais elle devrait inclure les périodes où le risque de contamination de la source d'approvisionnement en eau est à son plus fort, comme pendant le dégel printanier, après de fortes pluies ou pendant des périodes de sécheresse. Des associations ont été observées entre des facteurs climatiques (périodes de grosses pluies, températures plus chaudes) et la détection d'E. coli dans de petits réseau d'eau souterraine sensibles à la contamination fécale (Valeo et coll., 2016; Invik et coll., 2017). Les phénomènes météorologiques extrêmes, comme les pluies intenses, les crues soudaines, les ouragans, les sécheresses et les incendies de forêt, peuvent avoir des répercussions importantes sur la qualité de l'eau et ils devraient augmenter en fréquence et en gravité avec les changements climatiques (Thomas et coll., 2006; Nichols et coll., 2009; Wallender et coll., 2014; Khan et coll., 2015; Staben et coll., 2015). Les services d'eau touchés par de tels événements devraient envisager d'effectuer des échantillonnages supplémentaires pendant et après leur survenance.
Il faut également prélever des échantillons dans les nouveaux puits ou dans les puits réhabilités avant leur première utilisation pour confirmer que leur qualité bactériologique est acceptable. Dans les réseaux municipaux, on peut envisager de prélever un plus grand nombre d'échantillons lorsque des changements surviennent dans l'exploitation habituelle de l'installation de traitement d'eau.
Il faut insister sur le fait que les fréquences suggérées dans le tableau 2 ci-dessus constituent des indications générales seulement. Dans bien des réseaux, l'eau à la sortie de la station de traitement et dans le réseau de distribution sera analysée pour détecter la présence d'E. coli à une fréquence bien au-delà de ces recommandations minimales. La pratique générale qui consiste à fonder les exigences d'échantillonnage sur la population desservie s'appuie sur le fait que les petits réseaux d'approvisionnement en eau desservent une petite population donc lerisque s'applique à moins de personne. Toutefois, les petits réseaux d'approvisionnement en eau présentent un plus grand nombre de lacunes dans leurs installations et ils sont responsables d'un plus grand nombre d'éclosions de maladies que les réseaux de plus grande taille (Schuster et coll., 2005, Wallender et coll., 2014; Murphy et coll., 2016a, 2016b). Il est important de mettre l'accent sur des inspections physiques régulières du réseau d'approvisionnement en eau et sur la surveillance des processus et des activités critiques pour tous les petites sources d'approvisionnement en eau potable et particulièrement pour ceux où il peut s'avérer difficile de procéder aux analyses à la fréquence requise (Robertson et coll., 2003; OMS, 2005).
Pour les sources d'approvisionnement ayant un historique d'eau de grande qualité, on peut recourir à un meilleur contrôle des procédés et à des inspections régulières comme moyen de réduire le nombre d'échantillons prélevés pour des analyses bactériologiques. En revanche, il se peut qu'il soit nécessaire de procéder à des analyses plus fréquentes lorsque la qualité de l'eau des sources varie.
Même si les fréquences d'échantillonnage recommandées pour la détection d'E. coli sont respectées, il faudrait tenir compte de certaines limitations lors de l'interprétation des résultats. Des études par simulation ont montré qu'il est très difficile de détecter une contamination dans un réseau de distribution, sauf si celle-ci se produit dans une conduite maîtresse d'eau, dans un réservoir, à la station de traitement, ou encore si elle subsiste et met en jeu des concentrations élevées (Speight et coll., 2004; van Lieverloo et coll., 2007). On a constaté une certaine amélioration des capacités de détection lorsque les programmes d'échantillonnage sont conçus pour que les échantillons soient prélevés sur plusieurs jours, notamment durant les fins de semaine et les jours fériés, au lieu d'un échantillonnage regroupé un seul jour par semaine (van Lieverloo et coll., 2007). Hrudey et Leiss (2003) ont fait valoir qu'il est difficile de bien interpréter les données tirées des programmes de surveillance des dangers environnementaux si la fréquence de détection du danger est faible. Les auteurs soulignent l'importance de recueillir des preuves à plus d'une source lorsqu'on gère les risques associés à une faible fréquence de danger pouvant entraîner des conséquences graves. Cela souligne l'importance de la surveillance opérationnelle des processus critiques et de l'utilisation d'indicateurs microbiologiques multiples dans la vérification de l'eau potable.
La concentration résiduelle de désinfectant doit être mesurée au moment où l'on prélève les échantillons pour l'analyse bactériologique. Les recommandations sur l'échantillonnage quotidien pour l'analyse de résidus de désinfectant et de la turbidité peuvent ne pas s'appliquer aux sources d'approvisionnement alimentées par de l'eau souterraine où la désinfection vise seulement à accroître la marge de sécurité. De plus amples renseignements sur la surveillance de la turbidité se trouvent dans le document technique sur la turbidité (Santé Canada, 2012a). D'autres paramètres peuvent être utilisés en plus d'E. coli dans le cadre du processus de vérification de la qualité de l'eau. Il s'agit notamment d'indicateurs de la qualité microbiologique générale de l'eau (coliformes totaux, numération des bactéries hétérotrophes sur plaque) et d'autres indicateurs de contamination fécale (p. ex., entérocoques, coliphages) (OMS et OCDE, 2003; OMS, 2005, 2014). On peut obtenir plus de détails dans les documents correspondants de Santé Canada (Santé Canada, 2012b, 2018a, 2019a).
6.3 Emplacement des points d'échantillonnage
Dans les réseaux municipaux, il appartient à l'autorité responsable en matière d'eau potable de choisir ou d'approuver l'emplacement des points d'échantillonnage. Les points d'échantillonnage sélectionnés peuvent varier en fonction des objectifs de surveillance. Par exemple, l'échantillonnage à des points fixes peut servir à dresser un historique de la qualité de l'eau dans le réseau de distribution alors que, si l'on procède à un échantillonnage à des points aléatoires (variable) dans tout le réseau de distribution, on obtiendra une meilleure vue d'ensemble du système. Une stratégie d'échantillonnage aléatoire comme la rotation des sites d'échantillonnage du réseau de distribution peut aussi augmenter la probabilité de détecter des problèmes de qualité de l'eau (OMS, 2014). Il est courant d'adopter une combinaison de points d'échantillonnage fixes et aléatoires (Narasimhan et coll., 2004). Speight et coll. (2004) ont publié une méthodologie pour élaborer des plans d'échantillonnage personnalisés des réseaux de distribution qui intègrent des points d'échantillonnage aléatoires.
Les sites d'échantillonnage devraient comprendre le point d'entrée dans le réseau de distribution et des points du réseau de distribution représentatifs de la qualité de l'eau fournie au consommateur. Si l'eau provient de plus d'une source, le choix des sites d'échantillonnage doit faire en sorte que chacune des différentes sources subisse un échantillonnage périodique de l'eau. Les plans des réseaux de distribution peuvent aider à connaître le sens de l'écoulement de l'eau et à choisir les points d'échantillonnage appropriés. L'accent devrait être mis sur les zones présentant des problèmes potentiels ou les zones où les conditions opérationnelles sont susceptibles de varier. Les zones où la durée de rétention de l'eau est longue (p. ex. des culs-de-sac), les zones de dépressurisation, les réservoirs, les emplacements en aval de réservoirs, les zones les plus éloignées de la station de traitement et les zones ayant déjà connu des problèmes sont des sites d'échantillonnage possibles. Il se peut que les évaluations des sources d'approvisionnement en eau et des réseaux permettent de déceler d'autres zones qui sont des sites d'échantillonnage pertinents.
Dans les réseaux résidentiels qui fournissent de l'eau potable à une population, on prélève en général les échantillons aux endroits recommandés par l'autorité responsable en matière d'eau potable.
7.0 Considérations relatives aux procédés de traitement et aux réseaux de distribution
Le principal objectif du traitement est de réduire le nombre d'organismes pathogènes et les facteurs de risque connexes pour les ramener à un niveau acceptable ou sécuritaire. Il est possible d'y parvenir grâce à un ou à plusieurs procédés de traitement qui les éliminent physiquement ou les rendent inactifs. Une approche de la source au robinet, y compris la protection des bassins versants ou des têtes de puits, l'optimisation des procédés de traitement et un réseau de distribution bien entretenu, est une approche universellement acceptée pour réduire la concentration des agents pathogènes entériques d'origine hydrique dans l'eau potable (O'Connor, 2002b; Santé Canada, 2001; CCME, 2004; OMS, 2012). La surveillance d'E. coli dans le cadre de la vérification de la qualité de l'eau traitée et distribuée est un élément important de cette approche. Pour obtenir de plus amples renseignements sur les exigences en matière de traitement et de désinfection de l'eau potable, on peut consulter les documents techniques suivants de Santé Canada : Protozoaires entériques : Giardia et Cryptosporidium et Les virus entériques (Santé Canada, 2012b, 2019d).
7.1 Traitement à l'échelle municipale
Il existe un éventail d'options permettant de traiter les sources d'approvisionnement en eau afin de fournir de l'eau potable d'excellente qualité. Le type et la qualité de l'eau de la source d'approvisionnement détermineront le degré de traitement nécessaire. En général, les sources d'approvisionnement en eau de surface ou en eau souterraine sous l'influence directe d'eau de surface (ESSIDES) doivent au moins subir comme traitement une filtration adéquate (ou un traitement à l'aide d'une technique permettant d'obtenir une réduction logarithmique équivalente) et une désinfection. Comme la plupart des eaux de surface et des ESSIDES peuvent être contaminées par des matières fécales, des procédés de traitement doivent être en place pour obtenir une élimination ou une inactivation d'au moins 3 log (99,9 %) de Giardia et de Cryptosporidium, et d'au moins 4 log (99,99 %) de virus entériques. Il faut évaluer les sources d'eau souterraine pour déterminer si la source d'approvisionnement est susceptible d'être contaminé par des virus entériques et des protozoaires. Pour les sources jugées sensibles aux virus, on devrait atteindre une élimination ou une inactivation des virus d'au moins 4 log. Un secteur de compétence peut juger acceptable qu'une source d'eau souterraine ne soit pas désinfectée si l'évaluation du réseau d'approvisionnement en eau potable satisfait aux exigences provinciales et territoriales en place qui assurent un risque minimal de présence de virus entériques (Santé Canada, 2018e).
Dans les réseaux comportant un réseau de distribution, il faudrait maintenir en tout temps un résidu de désinfectant. Il est essentiel que les objectifs d'élimination et d'inactivation soient atteints avant que l'eau ne parvienne au premier consommateur du réseau de distribution. Des mesures adéquates de contrôle des procédés et la formation des opérateurs sont aussi nécessaires pour assurer en tout temps l'efficacité des procédés de traitement (Smeets et coll., 2009; AWWA, 2011).
Dans l'ensemble, les éléments probants montrent que les agents pathogènes bactériens entériques sont beaucoup plus sensibles à la chloration que Giardia, Cryptosporidium, et de nombreux virus entériques, et plus sensibles à l'inactivation par UV que de nombreux virus entériques (Santé Canada, 2018d, 2018e). Par conséquent, l'eau qui répond aux exigences établies dans les recommandations relatives aux virus entériques et aux protozoaires entériques devrait être de qualité bactériologique acceptable, y compris afficher des concentrations d'E. coli non détectables par 100 mL d'eau à la sortie de la station de traitement.
7.1.1 Élimination physique
L'élimination physique des organismes indicateurs (E. coli, coliformes totaux, entérocoques) peut être réalisée à l'aide de diverses techniques, y compris une filtration avec procédé chimique, une filtration lente sur sable, une filtration sur diatomées et sur membrane ou une autre technique de filtration éprouvée. Les éliminations physiques logarithmiques d'organismes indicateurs (E. coli, coliformes totaux, entérocoques) déclarées pour plusieurs techniques de filtration sont présentées dans le tableau 3. On s'attend à ce que les membranes pour l'osmose inverse (OI) soient aussi efficaces que l'ultrafiltration, selon leur seuil de rétention moléculaire (LeChevallier et Au, 2004; Smeets et coll. 2006). Cependant, il n'existe actuellement aucune méthode pour valider l'élimination logarithmique des unités traitées par OI (Alspach, 2018).
| TechniqueTableau 3 Note de bas de page a | Élimination logarithmique | |||
|---|---|---|---|---|
| Minimum | Moyenne | Médiane | Maximum | |
| Filtrage classique | 1,0 | 2,1 | 2,1 | 3,4 |
| Filtrage direct | 0,8 | 1,4 | 1,5 | 3,3 |
| Filtrage lent sur sable | 1,2 | 2,7 | 2,4 | 4,8 |
| Microfiltrage | Non indiqué | Non indiqué | Non indiqué | 4,3 |
| Ultrafiltrage | Non indiqué | > 7 | Non indiqué | Non indiqué |
|
||||
7.1.2 Désinfection
La désinfection primaire est nécessaire pour protéger la santé publique, car elle tue ou inactive les protozoaires, les bactéries et les virus nocifs, tandis que la désinfection secondaire est utilisée pour maintenir un résidu dans le réseau de distribution. Un résidu de désinfectant dans la distribution aide à contrôler la reprise de la croissance bactérienne et offre une indication de l'intégrité du système (Santé Canada, 2009). On procède habituellement à la désinfection primaire après les traitements qui éliminent les particules et la matière organique. Cette stratégie contribue à inactiver efficacement les agents pathogènes et à réduire au minimum la formation de sous-produits de désinfection. À propos de la désinfection microbienne de l'eau potable, il est important de noter que le terme « inactivation » signifie que l'agent pathogène n'est plus infectieux et ne peut se reproduire dans un hôte convenable, mais qu'il peut encore être présent.
Les cinq désinfectants souvent utilisés pour le traitement de l'eau potable sont les suivants : le chlore libre, la monochloramine (chloramine), l'ozone, le dioxyde de chlore et la lumière UV. Le chlore libre est le produit chimique le plus souvent utilisé pour la désinfection primaire, parce qu'il est facile de s'en procurer, qu'il est relativement peu coûteux et qu'il fournit un résidu qui peut aussi être utilisé pour la désinfection secondaire. La chloramine est beaucoup moins réactive que le chlore libre, a une efficacité de désinfection inférieure et est généralement réservée à la désinfection secondaire. L'ozone et le dioxyde de chlore sont des désinfectants primaires efficaces contre les bactéries, les virus et les protozoaires, mais ils sont habituellement plus coûteux et plus difficiles à appliquer, en particulier dans les petits réseaux. L'ozone se dégrade rapidement après avoir été appliqué et ne peut donc pas être utilisé pour une désinfection secondaire. Le dioxyde de chlore n'est pas non plus recommandé pour la désinfection secondaire parce qu'il se dégrade relativement vite (Santé Canada, 2008a). Grâce à un processus physique, la lumière UV assure une inactivation efficace des bactéries, des protozoaires et de la plupart des virus entériques, à l'exception des adénovirus, qui nécessitent une dose élevée pour son inactivation. Comme l'ozone et le dioxyde de chlore, la lumière UV est très efficace pour la désinfection primaire, mais il faut utiliser en complément un autre désinfectant (habituellement du chlore ou de la chloramine) pour la désinfection secondaire.
7.1.2.1 Désinfection chimique
Il est possible de prédire l'efficacité des désinfectants chimiques d'après la concentration résiduelle d'un désinfectant en particulier et les facteurs qui influent sur son efficacité, surtout la température, le pH, le temps de contact et le degré de désinfection requis (AWWA, 2011). Cette relation est communément appelée « concept CT », où CT représente le produit de « C » (concentration résiduelle d'un désinfectant, en mg/L) par « T » (temps de contact avec le désinfectant, en minutes) pour un microorganisme particulier dans des conditions définies (p. ex. la température et le pH). Pour tenir compte de la dégradation du désinfectant, on détermine habituellement la concentration résiduelle à la sortie de la chambre de contact plutôt que d'utiliser la dose appliquée ou la concentration initiale. Pour calculer le temps de contact, on se sert le plus souvent d'une valeur T10 qui correspond à la durée de rétention pendant laquelle le temps de contact requis est atteint ou dépassé pour 90 % de l'eau. On peut estimer cette valeur T10 en multipliant la durée de rétention hydraulique théorique (c.-à-d. le volume du réservoir divisé par le débit) par l'efficacité hydraulique de la chambre de contact. L'United States Environmental Protection Agency (U.S. EPA, 1991) fournit l'efficacité hydraulique pour des exemples de chambres de contact. Un essai de traçage hydraulique peut aussi être effectué pour déterminer le temps de contact réel en fonction du débit de la station. Comme la valeur T dépend de la construction hydraulique de la station de traitement d'eau, améliorer les caractéristiques hydrauliques (c.-à-d. augmenter l'efficacité hydraulique) est plus efficace qu'accroître la dose de désinfectant pour respecter les exigences relatives à CT.
Le tableau 4 présente des valeurs CT pour une inactivation à 99 % (2 log) d'E. coli par le chlore, le dioxyde de chlore, la chloramine et l'ozone. On a également indiqué, pour des fins de comparaison, les valeurs CT pour Giardia lamblia et pour des virus. D'après les valeurs CT, comparativement à la plupart des protozoaires et des virus, les bactéries E. coli sont plus faciles à inactiver à l'aide des désinfectants chimiques courants. Le tableau 4 montre également que la chloramine est un désinfectant beaucoup moins puissant que le chlore libre, le dioxyde de chlore ou l'ozone, puisqu'il faut des concentrations ou des temps de contact beaucoup plus élevés pour atteindre le même taux d'inactivation. La chloramine n'est donc pas recommandée comme désinfectant primaire.
Dans une installation de traitement fonctionnant correctement, les valeurs CT indiquées pour Giardia ou les virus entraîneront une inactivation très supérieure à 99 % pour les bactéries. La documentation indique que la sensibilité à la désinfection chimique des bactéries entériques pathogènes Salmonella, Campylobacter et E. coli O157:H7 est comparable à celle des E. coli non pathogènes (Lund, 1996; Rice et coll., 1999; Wojcicka et coll., 2007; Chauret et coll., 2008; Rasheed et coll., 2016; Jamil et coll., 2017). Les valeurs CT publiées pour ces bactéries pathogènes sont peu nombreuses. Des études en laboratoire ont montré qu'une inactivation de 2 à 4 log d'E. coli O157:H7 peut être obtenue avec des valeurs CT inférieures à 0,3 mg min/L pour le chlore libre et supérieures à 30 mg min/L pour la monochloramine (Chauret et coll., 2008; Wojcicka et coll., 2007).
| Agent de désinfection | pH | E. coliTableau 4 Note de bas de page a (mg·min/L) [5 °C] |
Giardia lambliaTableau 4 Note de bas de page b (mg·min/L) [5 °C] |
VirusTableau 4 Note de bas de page c (mg·min/L) [5-15 °C] |
|---|---|---|---|---|
| Chlore libre | 6-7 | 0,034-0,05 | 70-99 | 0,01-12 |
| Chloramines | 8-9 | 95-180 | 1 470 | 360-6 476 |
| Dioxyde de chlore | 6-7 | 0,4-0,75 | 17 | 0,17-6,7 |
| Ozone | 6-7 | 0,02 | 1,3 | 0,006-0,5 |
|
||||
7.1.2.2 Désinfection aux rayons UV
Pour la désinfection par les rayons UV, le produit de la multiplication de l'intensité lumineuse « I » (mesurée en mW/cm2 ou W/m2) et du temps « T » (mesuré en secondes) est la dose calculée (fluence) en mJ/cm2 pour un microorganisme donné. Cette relation est appelée concept IT.
Le tableau 5 présente les inactivations logarithmiques découlant de la désinfection aux rayons UV. En raison de son importance comme indicateur de santé publique, on a utilisé E. coli comme espèce bactérienne représentative. À des fins de comparaison, le tableau comprend les doses de rayons UV dans le cas de protozoaires et de virus représentatifs. D'après un examen des données sur l'inactivation à l'aide de rayons UV, pour les organismes représentatifs, il faut une dose de rayons UV comparable pour inactiver dans la même mesure les bactéries (ici, E. coli) et les protozoaires, tandis que certains virus sont beaucoup plus résistants.
Les organismes non pathogènes E. coli, Salmonella, Campylobacter et pathogènes E. coli (y compris E. coli O157:H7) présentent des sensibilités similaires à la désinfection aux rayons UV (Sommer et coll., 2000; Smeets et coll., 2006; Zimmer-Thomas et coll., 2007). Dans des études sur des souches pathogènes d'E. coli, on a obtenu une inactivation de 2 à 6 log avec des doses de rayons UV allant de 3 à 12,5 mJ/cm2 (Sommer et coll., 2000; Zimmer-Thomas et coll., 2007).
Les bactéries ont des mécanismes de défense naturels pour renverser les dommages photochimiques causées par la lumière UV (p. ex. photoréactivation et réparation dans l'obscurité) (Hijnen et coll., 2006). Des études expérimentales utilisant des populations d'E. coli à haute densité ont montré que de faibles degrés de réparation à l'obscurité sont possibles dans l'eau potable avec de faibles doses de lumière UV (Zimmer-Thomas et coll., 2007; Bohrerova et coll., 2015). Les données actuelles laissent croire que, dans le cas des stations de traitement de l'eau dont les réacteurs UV bien entretenus administrent une dose UV minimale de 40 mJ/cm2 suivie d'un temps de contact avec un résidu de désinfectant approprié, la réparation par E. coli des dommages causés par les rayons UV ne devrait pas être préoccupante (Zimmer-Thomas et coll., 2007; Bohrerova et coll., 2015).
| Inactivation logarithmique | E. coliTableau 5 Note de bas de page aTableau 5 Note de bas de page c | CryptosporidiumTableau 5 Note de bas de page a | AdénovirusTableau 5 Note de bas de page b | RotavirusTableau 5 Note de bas de page b | GiardiaTableau 5 Note de bas de page a |
|---|---|---|---|---|---|
| 1 | 1,5-5 | 2,5 | 10-76 | 7,1-10 | 2,1 |
| 2 | 2,8-9 | 5,8 | 26-137 | 14,8-26 | 5,2 |
| 3 | 4,1-14 | 12 | 39-199 | 23-44 | 11 |
| 4 | 5,0-18 | 22 | 51-261 | 36-61 | 22 |
|
|||||
7.1.3 Réseau de distribution
Un réseau de distribution bien entretenu est un élément essentiel d'une approche de la source au robinet ou d'un plan de gestion de la sécurité sanitaire de l'eau pour assurer la salubrité de l'eau potable (Santé Canada, 2001; CCME, 2004; OMS, 2014; AWWA 2017). On sait que la qualité de l'eau du réseau de distribution se détériore en raison de divers problèmes, notamment la reprise de la croissance bactérienne dans les biofilms à long terme et les dommages transitoires ou introductions à court terme qui peuvent résulter des activités quotidiennes ainsi qu'une contamination croisée accidentelle ou une contamination intentionnelle. D'importantes perturbations de la qualité de l'eau dans le réseau de distribution (p. ex. résultant de refoulements, de raccordements croisés, de travaux de construction ou de réparations) ont été associées à des éclosions de maladies d'origine hydrique (Risebro et coll., 2007; Craun et coll., 2010, Hrudey et Hrudey, 2014). Un dysfonctionnement ou des lacunes au cours d'activités d'exploitation courantes (p. ex. perte d'intégrité d'une conduite, perte de pression, manque de résidus adéquats) peuvent également contribuer à accroître le risque de maladies gastro-intestinales chez les consommateurs (Ercumen et coll., 2014). La qualité de l'eau dans le réseau de distribution devrait faire l'objet d'une surveillance régulière (p. ex. indicateurs microbiens, résidu de désinfectant, turbidité, pH), des programmes d'exploitation et d'entretien devraient être en place (p. ex. nettoyage des conduites principales, vérification des raccordements croisés, gestion des biens) et une hygiène rigoureuse doit être pratiquée pendant tout travail de construction, réparation ou entretien de conduites principales afin que l'eau potable soit acheminée jusqu'au consommateur avec une perte minimale de sa qualité (Kirmeyer et coll., 2001, 2014).
L'eau traitée peut subir une désinfection secondaire à sa sortie de la station de traitement ou aux points de rechloration du réseau de distribution. Le chlore libre et la chloramine sont les produits chimiques couramment utilisés pour fournir un résidu de désinfectant. La chloramine pénètre mieux dans les biofilms que le chlore libre, mais ce dernier agit plus efficacement là où il pénètre (Lee et coll., 2011, Pressman et coll., 2012). Lorsque la chloramine est utilisée comme désinfectant résiduel dans les réseaux de distribution d'eau potable, les procédés de traitement doivent être optimisés pour assurer la stabilité de la chloramine (rapport de poids entre Cl2:NH3 de 4,5:1 - 5:1, pH supérieur à 8,0) (Santé Canada, 2019b).
La fonction principale du résidu de désinfectant est de conférer une protection contre la reprise de la croissance bactérienne (LeChevallier et Au, 2004). Le résidu peut également servir de sentinelle qui annonce une variation de la qualité de l'eau. Une baisse de la concentration résiduelle peut indiquer des lacunes du procédé de traitement, un traitement inadéquat, une contamination du réseau ou une rupture dans l'intégrité du réseau de distribution (LeChevallier, 1998; Haas, 1999; O'Connor, 2002a; AWWA, 2017). La capacité d'un désinfectant secondaire de réguler la croissance microbienne en continu dans le réseau de distribution dépend du type de résidu (c.-à-d. le chlore libre ou la chloramine), de la concentration, du temps de contact, de la demande en résidu (attribuable à l'eau et aux matières présentes ou entrant dans le réseau de distribution), des effets protecteurs des biofilms et de la résistance au désinfectant des microorganismes présents (LeChevallier et Au, 2004). Des chercheurs ont remarqué qu'un résidu de chlore « détectable » n'est pas suffisant pour restreindre efficacement la croissance bactérienne dans le réseau de distribution (Gagnon et coll., 2008; Wahman et Pressman, 2015). C'est l'autorité responsable de l'eau potable qui fixe les exigences précises concernant les concentrations résiduelles de désinfectant, qui peuvent varier d'une province ou d'un territoire à l'autre.
La seule surveillance d'E. coli pourrait ne pas permettre de détecter des problèmes de détérioration de la qualité de l'eau dans un réseau de distribution. Dans le traitement de l'eau potable, le développement de biofilms et leur potentiel de capture d'agents pathogènes entériques et opportunistes d'origine hydrique qui peuvent présenter diverses capacités de survie, de multiplication et de rejet dans le réseau de distribution est préoccupant (Ashbolt, 2015). Des pressions transitoires faibles et négatives peuvent entraîner une contamination du réseau de distribution attribuable à l'introduction d'agents provenant de l'extérieur des conduites ou de raccordements croisés ou d'un refoulement provenant d'installations domestiques, industrielles ou institutionnelles (Gullick et coll., 2004). Un résidu de désinfectant secondaire peut ne pas inactiver suffisamment des organismes pathogènes introduits dans le réseau de distribution (Payment et coll., 1999; Betanzo et coll., 2008). En cas de contamination fécale ou d'une détérioration de la qualité microbiologique de l'eau, la purge (p. ex. purge classique, purge unidirectionnelle) et la chloration sont des mesures correctives importantes (Szabo et Minamyer, 2014). Toutefois, si elles ne sont pas mises en œuvre correctement, les procédés de purge peuvent mobiliser et disséminer les dépôts et contaminer le réseau de distribution au lieu de favoriser une élimination contrôlée. Il est donc important que les services d'eau recherchent et mettent en œuvre la technique de purge la plus adéquate pour régler un problème préoccupant ayant des conséquences sur la qualité microbiologique de l'eau. Les responsables de systèmes d'approvisionnements en eau potable peuvent obtenir des recommandations sur la gestion de la qualité de l'eau dans un réseau de distribution d'eau potable auprès d'autres sources (Santé Canada, 2019a).
Dans les collectivités éloignées, l'un des problèmes pertinents est le risque de contamination entre la source d'approvisionnement en eau traitée et le point de consommation pour les ménages et les entreprises qui utilisent l'eau acheminée par camion-citerne ou des réservoirs sur place. Des études menées dans des communautés des Premières Nations et des Inuits ont permis d'observer que des échantillons d'eau prélevés dans des réservoirs domestiques d'eau (Farenhorst et coll., 2017) ou dans des camions de livraison d'eau ou des robinets recevant de l'eau acheminée par camion-citerne (Daley et coll., 2017; Farenhorst et coll., 2017; Mi et coll., 2019) présentaient une probabilité accrue de détection d'E. coli comparativement aux sources d'approvisionnement en eau courante. On a également constaté que des échantillons d'eau du robinet prélevés chez des ménages recevant de l'eau acheminée par camion-citerne présentaient des concentrations de chlore libre inférieures à celles enregistrées dans les sources d'approvisionnement en eau potable acheminée par des conduites (Daley et coll., 2017; Farenhorst et coll., 2017). Ces études soulignent l'importance de bonnes pratiques de gestion pour le transport et la conservation de l'eau potable dans ces communautés afin de réduire le risque de contamination. Il incombe à l'autorité responsable en matière d'eau potable dans le secteur de compétence concerné de fournir des lignes directrices précises sur les exigences en matière d'exploitation, d'entretien et de surveillance de l'eau acheminée par camion-citerne et des citernes ou réservoirs d'eau potable. On peut également trouver de l'information dans d'autres publications (Agriculture et Agroalimentaire Canada, 2006; Affaires indiennes et du Nord Canada, 2006; Santé Canada, 2013a).
7.2 Traitement à l'échelle résidentielle
Le traitement à l'échelle résidentielle s'applique aussi aux petites installationsd'approvisionnement en eau potable. Les éléments probants indiquent que les petites sources privés et communautaires d'approvisionnement en eau potable sont plus vulnérables à une contamination et sont plus souvent associées à des éclosions de maladies d'origine hydrique que les grands réseaux municipaux d'approvisionnement en eau potable (Schuster et coll. 2005; Murphy et coll., 2016b, Messner et coll., 2017). Pour les petits puits d'eau souterraine qui sont sensibles à une contamination fécale et qui fournissent de l'eau potable à une population, la désinfection est le meilleur moyen de protéger la santé publique (Payment et Locas, 2011). On peut trouver de plus amples renseignements sur la caractérisation des risques dans les petits systèmes dans d'autres sources (OMS, 2012).
Dans les cas où l'eau potable d'un ménage provient d'un puits privé, il faut évaluer la vulnérabilité de la source à une contamination fécale. Bien qu'il soit difficile pour des propriétaires d'effectuer une évaluation détaillée de la vulnérabilité de leurs puits à une contamination fécale, des mesures peuvent être prises pour réduire au maximum le risque de contamination d'un puits. Les autorités provinciales et territoriales fournissent habituellement des conseils sur la construction, l'entretien, la protection et l'analyse des puits. Si l'information disponible est insuffisante pour déterminer si un puits est vulnérable à la contamination par des matières fécales, le traitement du puits est un moyen de réduire le risque. En général, l'eau de surface n'est pas recommandée comme source d'approvisionnement en eau à l'échelle résidentielle, à moins qu'elle ne soit correctement filtrée, désinfectée, et surveillée pour en assurer la qualité.
Il existe plusieurs possibilités de traitement des sources d'approvisionnement en eau afin de fournir une eau potable d'excellente qualité, exempte d'agents pathogènes. Il y a notamment la filtration ou la désinfection au moyen de composés chlorés ou de lumière UV. Ces méthodes s'apparentent aux procédés de traitement municipaux, mais elles sont appliquées à plus petite échelle. Bon nombre de ces méthodes ont été intégrées à des dispositifs au point d'entrée, qui traitent toute l'eau entrant dans le réseau, ou à des dispositifs au point d'utilisation, qui traitent l'eau en un seul endroit, comme au robinet de la cuisine. En raison des risques pour la santé publique liés à l'utilisation d'une eau potable contaminée par des microorganismes, si des dispositifs au point d'utilisation sont utilisés au lieu d'un système au point d'entrée, tous les points d'eau utilisés pour boire, préparer des aliments et des boissons, assurer l'hygiène ou laver la vaisselle devraient être équipés de dispositifs de traitement au point d'utilisation.
L'autorité responsable en matière d'eau potable dans le secteur de compétence concerné devrait fournir des conseils précis sur les méthodes qui peuvent être utilisées dans les petits réseaux. Santé Canada ne recommande aucune marque particulière de dispositif de traitement de l'eau potable, mais conseille fortement aux consommateurs d'utiliser des dispositifs dont la conformité aux normes pertinentes de NSF International (NSF) /American National Standards Institute (ANSI) est attestée par un organisme de certification agréé. Ces normes ont été conçues pour protéger la qualité de l'eau potable en veillant à la sécurité des matériaux et à l'efficacité des produits qui entrent en contact avec l'eau potable.
Les organismes de certification fournissent l'assurance qu'un produit est conforme aux normes applicables et sont accrédités par le Conseil canadien des normes (CCN). Au Canada, les organismes suivants ont été accrédités par le CCN à certifier les dispositifs et les matériaux utilisés pour le traitement de l'eau potable comme satisfaisant aux normes NSF/ANSI (CCN, 2019) :
- Groupe CSA;
- NSF International;
- Water Quality Association
- Underwriters Laboratories Inc.;
- Truesdail Laboratories Inc.;
- Bureau de normalisation du Québec; et
- International Association of Plumbing & Mechanical Officials.
On peut obtenir une liste à jour des organismes de certification accrédités auprès du Conseil canadien des normes (2019).
Pour les sources résidentielles d'approvisionnement en eau désinfectées au chlore liquide, il faut utiliser des solutions d'hypochlorite certifiées conformes à la norme NSF/ANSI/CAN 60 (NSF/ANSI/CAN, 2018b) et suivre les recommandations de manutention et de conservation de l'hypochlorite qui sont présentées dans un document technique (Santé Canada, 2018b).
Pour les dispositifs de désinfection aux rayons UV, la norme NSF/ANSI 55 définit des critères d'efficacité de deux catégories de dispositifs certifiés : les dispositifs de classe A et les dispositifs de classe B (NSF/ANSI, 2019). Les dispositifs de classe A suivant la norme NSF/ANSI 55 sont conçus pour administrer une dose d'UV au moins équivalente à 40 mJ/cm2 pour inactiver les microorganismes, soit les bactéries, les virus, les oocytes de Cryptosporidium et les kystes de Giardia, qui contaminent l'eau. Cependant, ils ne sont pas conçus pour traiter des eaux usées ou encore des eaux contaminées par des eaux usées brutes, et ils doivent être installés pour une eau limpide à l'œil. Les dispositifs de classe B suivant la norme NSF 55 ne sont pas conçus pour la désinfection d'une eau microbiologiquement insalubre. Ces dispositifs ne sont certifiés que pour le traitement bactéricide supplémentaire de sources publiques d'approvisionnement en eau potable désinfectée ou d'autres sources d'eau potable qui ont été analysées et jugées acceptables pour la consommation humaine.
Certains secteurs de compétence peuvent exiger des réseaux semi-publics qu'ils administrent une dose de rayons UV de 186 mJ/cm2 en présence d'adénovirus (p. ex. sous l'influence d'eaux usées). Les systèmes UV, conçus conformément au UV Disinfection Guidance Manual de l'U.S. EPA, sont offerts sur le marché et administrent 186 mJ/cm2 et une transmission UV supérieure à 68 % pour un débit pouvant aller jusqu'à 24 gallons américains par minute (U.S. EPA, 2006c).
Les membranes d'osmose inverse ont une taille de pores plus petite que les bactéries et les virus et pourraient constituer une barrière physique. Cependant, la norme NSF/ANSI 58 (NSF/ANSI, 2018a) ne comprend pas d'allégations de réduction du nombre de bactéries ou de virus. Il est important de noter que les systèmes d'osmose inverse ne sont destinés qu'à une installation au point d'utilisation. En effet, l'eau traitée par un système d'osmose inverse peut être corrosive pour les éléments internes de la plomberie. Ces systèmes exigent aussi de grandes quantités d'eau d'arrivée pour que le volume d'eau potable requis soit obtenu et ils ne conviennent généralement pas à une installation au point d'entrée.
Les membranes d'ultrafiltration ont des pores plus petits dont la taille varie entre 0,005 et 0,05 µm et elles pourraient généralement fournir une barrière physique contre les bactéries et les virus, bien qu'il n'existe aucune norme NSF/ANSI pour les systèmes résidentiels d'ultrafiltration. Pour les réseaux de distribution d'eau potable nécessitant une grande capacité de filtration, certaines unités d'ultrafiltration respectant la norme NSF/ANSI 419 (NSF/ANSI, 2018c) ont été testées pour leur capacité de réduction des virus; ces unités permettent aussi de réduire les bactéries. Cependant, la résolution de l'analyse directe de l'intégrité n'est pas suffisante pour valider l'élimination logarithmique de bactéries ou de virus. On devrait contacter l'autorité responsable de l'eau potable dans le secteur de compétence visé pour vérifier l'acceptabilité et/ou le champ d'application de ces unités.
Pour s'assurer de l'efficacité d'un dispositif de traitement, le propriétaire ou l'exploitant d'un réseau ou le propriétaire de la résidence devrait régulièrement demander à un laboratoire accrédité d'analyser l'eau à l'entrée et à la sortie du dispositif de traitement pour y détecter E. coli et les coliformes totaux. Comme la capacité d'élimination des dispositifs diminue avec le temps et l'utilisation, il faut les entretenir ou les remplacer. Les consommateurs doivent vérifier la longévité prévue des éléments de leur dispositif de traitement selon les recommandations du fabricant, et établir un calendrier d'entretien clair. Les dispositifs de traitement doivent être inspectés et entretenus selon le calendrier d'entretien et les recommandations du fabricant.
8.0 Évaluation des risques
Une évaluation des risques associés à E. coli fondée sur la santé n'est pas appropriée puisque cette bactérie n'est utilisée qu'en tant qu'organisme indicateur. Des évaluations des risques ont été effectuées pour certains microorganismes ayant des effets sur la santé, comme les protozoaires entériques et les virus entériques (Santé Canada, 2019c, 2019d).
8.1 Considérations internationales
D'autres pays et organisations multinationales utilisent E. coli comme organisme indicateur dans la surveillance de l'eau potable. Les Directives de qualité pour l'eau de boisson de l'OMS (OMS, 2017) recommandent E. coli comme premier indicateur à privilégier dans les programmes de surveillance de la vérification dans le cadre d'une approche de gestion de la qualité de l'eau potable fondée sur un plan de salubrité de l'eau. E. coli ou les coliformes thermotolérants ne doivent pas être détectés dans tout échantillon d'eau directement destinée à la consommation ou dans tout échantillon d'eau traitée prélevé à l'entrée du réseau de distribution ou dans ce dernier (volume d'échantillon de 100 mL). Des mesures d'enquête immédiates doivent être prises en cas de détection d'E. coli (OMS, 2017).
Aux États-Unis, la modification proposée à la Revised Total Coliform Rule (réglement révisé sur les coliformes totaux) de l'U.S. EPA (U.S. EPA, 2013) s'applique à tous les réseaux publics d'approvisionnement en eau et elle précise un maximum contaminant level (concentration maximale de contaminant, MCL) et un maximum contaminant level goal (objectif de niveau maximum de contaminant, MCLG) de zéro pour E. coli dans tout échantillon d'eau potable (volume standard de 100 mL). La détection d'E. coli dans tout contrôle de routine ou échantillon répété enfreint le règlement du MCL.
La Groundwater Rule (règlement sur l'eau souterraine) de l'U.S. EPA (U.S. EPA, 2006a) s'applique aux systèmes publics d'approvisionnement en eau qui utilisent l'eau souterraine. En vertu de ce règlement, les réseaux qui ne suppriment pas 4 log de virus doivent déclencher une surveillance de la source d'approvisionnement en eau, en vertu de laquelle les réseaux avisés de la présence de coliformes totaux positifs doivent vérifier la présence d'indicateur de matières fécales (c.-à-d. E. coli, entérocoques ou coliphages).
La Directive relative à la qualité des eaux destinées à la consommation humaine de l'UE définit les exigences législatives pour tous ses États membres (UE, 1998). En vertu de la Directive, E. coli est classé comme paramètre de la partie A pour vérifier l'efficacité des mesures en place permettant de réduire les risques pour la santé humaine tout au long de la chaîne d'approvisionnement en eau et la salubrité et la propreté de l'eau au point de conformité. La norme de l'UE pour E. coli correspond à une valeur de zéro par 100 mL (UE, 1998).
Les lignes directrices australiennes sur l'eau potable (NHMRC, NRMMC, 2017) précisent que pour la vérification de la qualité microbiologique de l'eau potable, un programme d'analyse régulière doit être mis en place pour l'indicateur E. coli autant que possible. Selon ces lignes directrices, la mesure d'E. coli comme indicateur efficace à court terme de la qualité de l'eau dans le réseau de distribution n'est pas détectée dans un échantillon minimum de 100 mL d'eau potable.
9.0 Justification
E. coli est l'indicateur le plus répandu pour détecter une contamination fécale dans les installations d'approvisionnement en eau potable du monde entier. En tant qu'indicateur de la présence de matières fécales, E. coli est principalement associé aux matières fécales humaines et animales et est plus spécifique aux matières fécales que d'autres groupes indicateurs comme les coliformes totaux, les coliformes thermotolérants et les entérocoques. Le nombre élevé de cette bactérie dans les matières fécales et sa capacité à être mesurée facilement et à peu de frais en font un indicateur utile pour détecter une contamination fécale qui a été réduite à de faibles concentrations dans des milieux d'eau potable. Un autre avantage de l'utilisation d'E. coli comme indicateur de la présence de matières fécales est que de nombreuses méthodes d'analyse détectent les coliformes totaux tout en détectant simultanément E. coli de manière distincte. Dans le cadre d'une surveillance de l'eau potable, le recours à plusieurs paramètres comme indicateurs de la qualité microbiologique générale de l'eau (comme les coliformes totaux, la numération des bactéries hétérotrophes) ou d'autres indicateurs de contamination fécale (entérocoques) est une bonne façon pour les les responsables de systèmes d'approvisionnements en eau potable de renforcer la probabilité de déceler les problèmes et donc de mettre en œuvre des mesures. Le recours à E. coli en tant qu'indicateur n'est pas sans limites. E. coli est plus facilement inactivé par les stress environnementaux et les désinfectants présents dans l'eau potable que de nombreux agents pathogènes d'origine hydrique, en particulier, les virus entériques et les protozoaires entériques. Néanmoins, E. coli est un important indicateur de l'efficacité des procédés de traitement mis en place pour éliminer ou inactiver ces organismes.
Les recommandations actuelles sur l'eau potable privilégient l'adoption d'un système de gestion de la qualité de l'eau potable qui utilise une approche de la source au robinet ou d'un plan de gestion de la sécurité sanitaire de l'eau. Dans un système de gestion de l'eau potable où les dangers du réseau d'approvisionnement en eau potable sont maîtrisés et où des paramètres de surveillance opérationnelle sont en place pour montrer que le système fonctionne adéquatement, E. coli joue un rôle important dans la vérification de la qualité de l'eau potable. La surveillance de la présence d'E. coli permet de vérifier l'efficacité des mesures de contrôle du réseau en place pour produire une eau microbiologiquement acceptable.
La détection d'E. coli dans l'eau potable indique des lacunes d'un ou de plusieurs contrôles dans le réseau et l'existence d'une voie de contamination fécale qui pourrait atteindre le consommateur, ce qui est inacceptable. Par conséquent, la recommandation pour la présence d'E. coli dans les réseaux d'approvisionnement en eau potable est une concentration maximale acceptable d'aucun microorganisme détectable par 100 mL.
10.0 Références
- Abberton, C.L., Bereschenko, L., van der Wielen, P.W.J.J. et Smith, C.J. (2016). Survival, biofilm formation, and growth potential of environmental and enteric Escherichia coli strains in drinking water microcosms. Appl. Environ. Microbiol., 82(17): 5320-5331.
- Affaires autochtones et du Nord Canada (2006). Protocole pour la salubrité de l'eau potable dans les communautés des Premières Nations. Affaires autochtones et du Nord Canada, Gatineau (Québec). Accès : https://www.aadnc-aandc.gc.ca/fra/1100100034913/1100100034920
- Affaires indiennes et du Nord Canada (2006). Protocole pour la salubrité de l'eau potable dans les communautés des Premières Nations. Affaires autochtones et du Nord Canada, Gatineau, Québec. Accès : https://www.aadnc-aandc.gc.ca/fra/1100100034913/1100100034920
- Agriculture et Agroalimentaire Canada (2006). La qualité de l'eau, ça compte : Comment maintenir la salubrité de l'eau domestique dans les citernes et les réservoirs d'eau à la ferme. Agriculture et Agroalimentaire Canada, Ottawa, Ontario. TRE-120-2006-02.
- Ahammed, M.M. (2003). Effect of holding time and temperature on bacterial counts. Indian J. Environ. Health, 45(3): 209-212.
- Allen, M.J., Edberg, S.C., Clancy, J.L. et Hrudey, S.E. (2015). Drinking water microbial myths. Crit. Rev. Microbiol., 41(3): 366-373.
- Alspach, B.(2018). Pathogen Rejection in Potable Reuse: The Role of NF/RO and Importance of Integrity Testing: J. Am. Water Works Assoc., 110 (3):39-44.
- APHA, AWWA et WEF (2017). Standard methods for the examination of water and wastewater. 23rd edition. American Public Health Association, American Water Works Association and Water Environment Federation, Washington, DC.
- Ashbolt, N.J. (2015). Environmental (saprozoic) pathogens of engineered water systems: Understanding their ecology for risk assessment and management. Pathogens, 4(2): 390-405.
- AWWA (2011). Water quality and treatment: A handbook of community water supplies. 6th. Edzwald, J.K. (ed.). McGraw-Hill, New York.
- AWWA (2014). Small Systems Field Guide, Water and Wastewater. American Water Works Association Denver, CO.
- AWWA (2017). Manual of Water Supply Practices M68- Water Quality in Distribution Systems. American Water Works Association, Denver, CO.
- Badgley, B.D., Ferguson, J., Heuvel, A.V., Kleinheinz, G.T., McDermott, C.M., Sandrin, T.R., Kinzelman, J., Junion, E.A., Byappanahalli, M.N., Whitman, R.L. et Sadowsky, M.J. (2011). Multi-scale temporal and spatial variation in genotypic composition of cladophora-borne Escherichia coli populations in Lake Michigan. Water Res., 45(2): 721-731.
- Banihashemi, A., Van Dyke, M.I. et Huck, P.M. (2015). Detection of viable bacterial pathogens in a drinking water source using propidium monoazide-quantitative PCR. J. Water Supply Res. T., 64(2): 139-148.
- Bernasconi, C., Volponi, G. et Bonadonna, L. (2006). Comparison of three different media for the detection of E. coli and coliforms in water. Water Sci. Technol., 54(3): 141-145.
- Betanzo, E.W., Hofmann, R., Hu, Z., Baribeau, H. et Alam, Z. (2008). Modeling the impact of microbial intrusion on secondary disinfection in a drinking water distribution system. J. Environ. Eng., 134(4): 231-237.
- Bjergbæk, L.A., Roslev, P. (2005). Formation of nonculturable Escherichia coli in drinking water. J. Appl. Microbiol., 99 (5):1090-1098.
- Blaustein, R.A., Pachepsky, Y., Hill, R.L., Shelton, D.R. et Whelan, G. (2013). Escherichia coli survival in waters: Temperature dependence. Water Res., 47(2): 569-578.
- Bogosian, G., Sammons, L.E., Morris, P.J.L., O'Neil, J.P., Heitkamp, M.A. et Weber, D.B. (1996). Death of the Escherichia coli K-12 strain W3110 in soil and water. Appl. Environ. Microbiol., 62(11): 4114-4120.
- Bohrerova, Z., Rosenblum, J. et Linden, K.G. (2015). Importance of recovery of E. coli in water following ultraviolet light disinfection. J. Env. Eng. (United States), 141(6).
- Botes, M., De Kwaadsteniet, M. et Cloete, T.E. (2013). Application of quantitative PCR for the detection of microorganisms in water. Anal. Bioanal. Chem., 405(1): 91-108.
- Boubetra, A., Nestour, F.L., Allaert, C., Feinberg, M. (2011). Validation of alternative methods for the analysis of drinking water and their application to Escherichia coli. Appl. Environ. Microbiol., 77 (10): 3360-3367.
- Breitenmoser, A., R. Fretz, J. Schmid, A. Besl, et R. Etter. 2011. Outbreak of acute gastroenteritis due to a washwater-contaminated water supply, Switzerland, 2008. J. Water Health. 9(3): 569-576.
- Bushon, R.N., Brady, A.M.G. et Lindsey, B.D. (2015). Holding-time and method comparisons for the analysis of fecal-indicator bacteria in groundwater. Environ. Monit. Assess., 187(11).
- Byappanahalli, M.N., Whitman, R.L., Shively, D.A., Sadowsky, M.J. et Ishii, S. (2006). Population structure, persistence, and seasonality of autochthonous Escherichia coli in temperate, coastal forest soil from a Great Lakes watershed. Environ. Microbiol., 8 (3):504-513.
- Byappanahalli, M.N., Nevers, M.B., Korajkic, A., Staley, Z.R. et Harwood, V.J. (2012a). Enterococci in the environment. Microbiol. Mol. Biol. Rev., 76: 685-706.
- Byappanahalli, M.N., Yan, T., Hamilton, M.J., Ishii, S., Fujioka, R.S., Whitman, R.L. et Sadowsky, M.J. (2012b). The population structure of Escherichia coli isolated from subtropical and temperate soils. Sci. Total Environ., 417-418: 273-279.
- CCME (2004). De la source au robinet : Guide d'application de l'approche à barrières multiples pour une eau potable saine. Conseil canadien des ministres de l'environnement. Winnipeg (Manitoba) Accès :
- https://www.ccme.ca/files/Resources/fr_water/fr_source_to_tap/mba_guidance_doc_f.pdf
- CEAEQ (2018). Centre d'Expertise en Analyse Environmentale du Québec. Lignes directrices concernant les travaux analytiques en microbiologie, DR-12-SCA-02, Québec, Ministère du Développement durable, de l'Environnement et de la Lutte contre les changements climatiques, 2018, 38 p.
- Chaudhuri, R.R. et Henderson, I.R. (2012). The evolution of the Escherichia coli phylogeny. Infect. Genet. Evol., 12(2): 214-226.
- Chauret, C., Smith, C. et Baribeau, H. (2008). Inactivation of Nitrosomonas europaea and pathogenic Escherichia coli by chlorine and monochloramine. J. Water Health, 6(3): 315-322.
- Chen, S., Li, X., Wang, Y., Zeng, J., Ye, C., Li, X., Guo, L., Zhang, S., et Yu, X. (2018). Induction of Escherichia coli into a VBNC state through chlorination/chloramination and differences in characteristics of the bacterium between states. Water Res., 142:279-288.
- Ciebin, B.W., Brodsky, M.H., Eddington, R., Horsnell, G., Choney, A., Palmateer, G., Ley, A., Joshi, R. et Shears, G. (1995). Comparative evaluation of modified m-FC and m-TEC media for membrane filter enumeration of Escherichia coli in water. Appl. Environ. Microbiol., 61(11): 3940-3942.
- Clermont, O., Bonacorsi, S. et Bingen, E. (2000). Rapid and simple determination of the Escherichia coli phylogenetic group. Appl. Environ. Microbiol., 66(10): 4555-4558.
- CCN (2019). Répertoire des organismes de certification accrédités de produits, de processus et de services. Conseil canadien des normes, Ottawa (Ontario). Consulté en décembre 2019. Accès : http://www.scc.ca/fr/accreditation/certification-de-produits-procedes-et-services/repertoire-des-organismes-de-certification-accredites
- Craun, G.F., Nwachuku, N., Calderon, R.L., et Craun, M.F. (2002). Outbreaks in drinking-water systems, 1991-1998. J. Environ. Health, 65 (1): 16-23.
- Craun, G.F., Brunkard, J.M., Yoder, J.S., Roberts, V.A., Carpenter, J., Wade, T., Calderon, R.L., Roberts, J.M., Beach, M.J. et Roy, S.L. (2010). Causes of outbreaks associated with drinking water in the united states from 1971 to 2006. Clin. Microbiol. Rev., 23(3): 507-528.
- Cretikos, M., Byleveld, P., Durrheim, D.N., Porigneaux, P., Merritt, T., et Leask, S. (2010). Supply system factors associated with microbiological drinking water safety in regional New South Wales, Australia, 2001-2007. J Water Health, 8 (2):257-268.
- Daley, K., Truelstrup Hansen, L., Jamieson, R.C., Hayward, J.L., Piorkowski, G.S., Krkosek, W., Gagnon, G.A., Castleden, H., MacNeil, K., Poltarowicz, J., Corriveau, E., Jackson, A., Lywood, J. et Huang, Y. (2017). Chemical and microbial characteristics of municipal drinking water supply systems in the Canadian Arctic. Environ. Sci. Pollut. R., (Epub ahead of print) doi: 10.1007/s11356-017-9423-5.
- Defelice, N.B., Johnston, J.E., et Gibson, J.M. (2016). Reducing emergency department visits for acute gastrointestinal illnesses in North Carolina (USA) by extending community water service. Environ. Health Perspect., 124 (10):1583-1591.
- Diarra, M.S., Silversides, F.G., Diarrassouba, F., Pritchard, J., Masson, L., Brousseau, R., Bonnet, C., Delaquis, P., Bach, S., Skura, B.J. et Topp, E. (2007). Impact of feed supplementation with antimicrobial agents on growth performance of broiler chickens, Clostridium perfringens and Enterococcus counts, and antibiotic resistance phenotypes and distribution of antimicrobial resistance determinants in Escherichia coli isolates. Appl. Environ. Microbiol., 73 (20): 6566-6576.
- Duriez, P. et Topp, E. (2007). Temporal dynamics and impact of manure storage on antibiotic resistance patterns and population structure of Escherichia coli isolates from a commercial swine farm. Appl. Environ. Microbiol., 73 (17): 5486-5493.
- Duygu, D.Y. et Udoh, A.U. (2017). Validation of microbiological testing methods. Trakya University Journal of Natural Sciences, 18(1): 65-69.
- Edberg, S.C., Rice, E.W., Karlin, R.J. et Allen, M.J. (2000). Escherichia coli: The best biological drinking water indicator for public health protection. J. Appl. Microbiol. Symposium Supplement, 88(29): 106s-116s.
- Edge, T.A., Khan, I.U.H., Bouchard, R., Guo, J., Hill, S., Locas, A., Moore, L., Neumann, N., Nowak, E., Payment, P., Yang, R., Yerubandi, R. et Watson, S. (2013). Occurrence of waterborne pathogens and Escherichia coli at offshore drinking water intakes in Lake Ontario. Appl. Environ. Microbiol., 79(19): 5799-5813.
- Engberg, J., Gerner-Smidt, P., Scheutz, F., Nielsen, E.M., On, S.L.W., et Mølbak, K. (1998). Water-borne Campylobacter jejuni infection in a Danish town - A 6-week continuous source outbreak. Clinical Microbiology and Infection, 4 (11): 648-656.
- Ercumen, A., Gruber, J.S. et Colford Jr., J.M. (2014). Water distribution system deficiencies and gastrointestinal illness: A systematic review and meta-analysis. Environ. Health Perspect., 122(7): 651-660.
- Ervin, J.S., Russell, T.L., Layton, B.A., Yamahara, K.M., Wang, D., Sassoubre, L.M., Cao, Y., Kelty, C.A., Sivaganesan, M., Boehm, A.B., Holden, P.A., Weisberg, S.B. et Shanks, O.C. (2013). Characterization of fecal concentrations in human and other animal sources by physical, culture-based, and quantitative real-time PCR methods. Water Res., 47(18): 6873-6882.
- UE (1998). Directive 98/83/CE du Conseil du 3 novembre 1998 relative à la qualité des eaux destinées à la consommation humaine. Journal officiel de l'Union européenne.L 330/32 5.12.98.
- Falco, R., et S.I. Williams. 2009. Waterborne Salmonella Outbreak in Alamosa, Colorado. March and April 2008: Outbreak Identification, Response and Investigation. Denver, Colo.: Colorado Department of Public Health and Environment. Safe Drinking Water Program, Water Quality Division.
- Falkinham, J.O.,III, Pruden, A. et Edwards, M. (2015). Opportunistic premise plumbing pathogens: Increasingly important pathogens in drinking water. Pathogens, 4(2): 373-386.
- Farenhorst, A., Li, R., Jahan, M., Tun, H.M., Mi, R., Amarakoon, I., Kumar, A. et Khafipour, E. (2017). Bacteria in drinking water sources of a First Nation reserve in Canada. Sci. Total Environ., 575: 813-819.
- Farnleitner, A.H., Ryzinska-Paier, G., Reischer, G.H., Burtscher, M.M., Knetsch, S., Kirschner, A.K.T., Dirnböck, T., Kuschnig, G., Mach, R.L., et Sommer, R. (2010). Escherichia coli and enterococci are sensitive and reliable indicators for human, livestock and wildlife faecal pollution in alpine mountainous water resources. J. Appl. Microbiol. 109 (5): 1599-1608.
- Fass, S., Dincher, M.L., Reasoner, D.J., Gatel, D. et Block, J.-. (1996). Fate of Escherichia coli experimentally injected in a drinking water distribution pilot system. Water Res., 30(9): 2215-2221.
- Feng, P., Lum, R. et Chang, G.W. (1991). Identification of uidA gene sequences in β-D-glucuronidase-negative Escherichia coli. Appl. Environ. Microbiol., 57(1): 320-323.
- Feng, P. et Lampel, K.A. (1994). Genetic analysis of uidA expression in enterohaemorrhagic Escherichia coli serotype O157:H7. Microbiology, 140(8): 2101-2107.
- Frick, C., Vierheilig, J., Linke, R., Savio, D., Zornig, H., Antensteiner, R., Baumgartner, C., Bucher, C., Blaschke, A.P., Derx, J., Kirschner, A.K.T., Ryzinska-Paier, G., Mayer, R., Seidl, D., Nadiotis-Tsaka, T., Sommer, R., et Farnleitner, A.H. (2018). Poikilothermic animals as a previously unrecognized source of fecal indicator bacteria in a backwater ecosystem of a large river. Appl. Environ. Microbiol. 84 (16), art. no. e00715-18.
- Filip, Z., Kaddu-Mulindwa, D. et Milde, G. (1986). Survival and adhesion of some pathogenic and facultative pathogenic micro-organisms in groundwater. Water Sci. Technol., 19(7): 1189.
- Flint, K.P. (1987). The long-term survival of Escherichia coli in river water. J. Appl. Bacteriol., 63(3): 261-270.
- Fogarty, J., Thornton, L., Hayes, C., Laffoy, M., O'flanagan, D., Devlin, J., et Corcoran, R. (1995). Illness in a community associated with an episode of water contamination with sewage. Epidemiol. Infect., 114 (2):289-295.
- Foppen, J.W.A. et Schijven, J.F. (2006). Evaluation of data from the literature on the transport and survival of Escherichia coli and thermotolerant coliforms in aquifers under saturated conditions. Water Res., 40(3): 401-426.
- Fout, G.S., Borchardt, M.A., Kieke, B.A., Jr. et Karim, M.R. (2017). Human virus and microbial indicator occurrence in public-supply groundwater systems: Meta-analysis of 12 international studies. Hydrogeol. J., 25(4): 903-919.
- Fricker, C.R., DeSarno, M., Warden, P.S. et Eldred, B.J. (2008). False-negative β-D-glucuronidase reactions in membrane lactose glucuronide agar medium used for the simultaneous detection of coliforms and Escherichia coli from water. Lett. Appl. Microbiol., 47(6): 539-542.
- Fricker, C.R., Warden, P.S. et Eldred, B.J. (2010). Understanding the cause of false negative β-D-glucuronidase reactions in culture media containing fermentable carbohydrate. Lett. Appl. Microbiol., 50(6): 547-551.
- Gagnon, G.A., Baribeau, H., Rutledge, S.O., Dumancic, R., Oehmen, A., Chauret, C. et Andrews, S. (2008). Disinfectant efficacy in distribution systems: A pilot-scale assessment. J. Water Supply Res. T., 57(7): 507-518.
- Gensberger, E.T., Polt, M., Konrad-Köszler, M., Kinner, P., Sessitsch, A. et Kostić, T. (2014). Evaluation of quantitative PCR combined with PMA treatment for molecular assessment of microbial water quality. Water Res., 67: 367-376.
- Gerba, C.P. et Smith Jr., J.E. (2005). Sources of pathogenic microorganisms and their fate during land application of wastes. J. Environ. Qual., 34(1): 42-48.
- Golberg, A., Linshiz, G., Kravets, I., Stawski, N., Hillson, N.J., Yarmush, M.L., Marks, R.S. et Konry, T. (2014). Cloud-enabled microscopy and droplet microfluidic platform for specific detection of Escherichia coli in water. PLoS ONE, 9 (1), art. no. e86341.
- Goldstein, S.T., Juranek, D.D., Ravenholt, O., Hightower, A.W., Martin, D.G., Mesnik, J.L., Griffiths, S.D., Bryant, A.J., Reich, R.R. et Herwaldt, B.L. (1996). Cryptosporidiosis: An outbreak associated with drinking water despite state-of-the-art water treatment. Ann. Intern. Med., 124(5): 459-468.
- Gordon, D.M., Bauer, S. et Johnson, J.R. (2002). The genetic structure of Escherichia coli populations in primary and secondary habitats. Microbiology, 148(5): 1513-1522.
- Gordon, D.M. (2013). The ecology of Escherichia coli. In: Escherichia coli: Pathotypes and Principles of Pathogenesis: Second Edition. Donnenberg, M.S. (ed.) Academic Press. London. pp. 3-20.
- Government Inquiry into Havelock North Drinking Water (2017). Report of the Havelock North drinking water inquiry: Stage 2. December 2017, Auckland, New Zealand. ISBN: 978-0-473-39743-2. Available at: https://www.dia.govt.nz/Government-Inquiry-into-Havelock-North-Drinking-Water
- Gutiérrez-del-Río, I., Marín, L., Fernández, J., Millán, M.Á.S., Ferrero, F.J., Valledor, M., Campo, J.C., Cobián, N., Méndez, I., et Lombó, F. (2018). Development of a biosensor protein bullet as a fluorescent method for fast detection of Escherichia coli in drinking water. PLoS ONE, 13 (1), art. no. e0184277.
- Gullick, R.W., LeChevallier, M.W., Svindland, R.C. et Friedman, M.J. (2004). Occurrence of transient low and negative pressures in distribution systems. J. Am. Water Works Assoc., 96(11): 52-66.
- Haas, C.N. (1999). Benefits of using a disinfectant residual. J. Am. Water Works Assoc., 91(1): 65-69.
- Hamilton, K.A., Waso, M., Reyneke, B., Saeidi, N., Levine, A., Lalancette, C., Besner, M.-C., Khan, W., et Ahmed, W. (2018). Cryptosporidium and Giardia in wastewater and surface water environments. J. Environ. Qual., 47 (5):1006-1023.
- Hamouda, M.A., Anderson, W.B., Van Dyke, M.I., Douglas, I.P., McFadyen, S.D., et Huck, P.M. (2016). Scenario-based quantitative microbial risk assessment to evaluate the robustness of a drinking water treatment plant. Water Qual. Res. J. Can., 51 (2), pp. 81-96.
- Hargy, T.M., Rosen, J., Lechevallier, M., Friedman, M. et Clancy, J.L. (2010). A high-volume sampling method for total coliform and E. coli. J. Am. Water Works Assoc., 102(3): 79-86.
- Hayes, E.B., Matte, T.D., O'brien, T.R., Mckinley, T.W., Logsdon, G.S., Rose, J.B., Ungar, B.L.P., Word, D.M., Wilson, M.A., Long, E.G., Hurwitz, E.S., Juranek, D.D. et Fishman, A.P. (1989). Large community outbreak of cryptosporidiosis due to contamination of a filtered public water supply. N. Engl. J. Med., 320(21): 1372-1376.
- Heijnen, L. et Medema, G. (2009). Method for rapid detection of viable Escherichia coli in water using real-time NASBA. Water Res., 43(12): 3124-3132.
- Hijnen, W.A.M., Beerendonk, E.F. et Medema, G.J. (2006). Inactivation credit of UV radiation for viruses, bacteria and protozoan (oo)cysts in water: Water Res., 40(1): 3-22.
- Hill, A.S., Friedman, M., Hallett, M., Salo-Zieman, V., Booth, S., Hanson, A., Gupta, K., Akagi, Y., Kochiss, C.,Koperski, L., Igoe, P., Kirby, L. et Harper, W. (2018). Use of flushing as a corrective action under the revised total coliform rule. Water Research Foundation. Denver, CO.Hoff, J.C. (1986). Inactivation of microbial agents by chemical disinfectants. U.S. Environmental Protection Agency, Cincinnati, OH (EPA/600/S2-86/067).
- Hörman, A. et Hänninen, M.-. (2006). Evaluation of the lactose Tergitol-7, m-Endo LES, Colilert 18, Readycult Coliforms 100, Water-Check-100, 3M Petrifilm EC and DryCult Coliform test methods for detection of total coliforms and Escherichia coli in water samples. Water Res., 40(17): 3249-3256.
- Hrudey, S.E. et Leiss, W. (2003). Risk management and precaution: Insights on the cautious use of evidence. Environ. Health Persp., 111 (13):1577-1581.
- Hrudey, S.E. et E.J. Hrudey. 2014 Ensuring Safe Drinking Water - Learning from Frontline Experience with Contamination. American Water Works Association. Denver, CO. 269pp.
- Hunter, P.R., Chalmers, R.M., Hughes, S. et Syed, Q. (2005). Self-reported diarrhea in a control group: a strong association with reporting of low-pressure events in tap water. Clin. Infect. Dis., 40: e32-e34.
- Hynds, P.D., Misstear, B.D. et Gill, L.W. (2012). Development of a microbial contamination susceptibility model for private domestic groundwater sources. Water Resour. Res., 48(12).
- Hynds, P.D., Misstear, B.D. et Gill, L.W. (2013). Unregulated private wells in the Republic of Ireland: Consumer awareness, source susceptibility and protective actions. J. Environ. Manage., 127: 278-288.
- Hynds, P.D., Thomas, M.K. et Pintar, K.D.M. (2014). Contamination of groundwater systems in the US and Canada by enteric pathogens, 1990-2013: A review and pooled-analysis. Plos One, 9(5).
- Ikonen, J., Pitkänen, T., Kosse, P., Ciszek, R., Kolehmainen, M. et Miettinen, I.T. (2017). On-line detection of Escherichia coli intrusion in a pilot-scale drinking water distribution system. J. Environ. Manage., 198: 384-392.
- Invik, J., Barkema, H.W., Massolo, A., Neumann, N.F. et Checkley, S. (2017). Total coliform and Escherichia coli contamination in rural well water: Analysis for passive surveillance. J. Water Health, 15(5): 729-740.
- Ishii, S. et Sadowsky, M.J. (2008). Escherichia coli in the environment: Implications for water quality and human health. Microbes Environ., 23(2): 101-108.
- Ishii, S., Yan, T., Vu, H., Hansen, D.L., Hicks, R.E. et Sadowsky, M.J. (2010). Factors controlling long-term survival and growth of naturalized Escherichia coli populations in temperate field soils. Microbes Environ., 25(1): 8-14.
- ISO (2018) ISO ICS 07.100.20 - Microbiologie de l'eau. Organisation internationale de normalisation. Genève, Suisse. Accès : https://www.iso.org/fr/ics/07.100.20/x/
- Jack, S., Bell, D. et Hewitt, J. (2013). Norovirus contamination of a drinking water supply at a hotel resort. N. Z. Med. J., 126(1387): 98-107.
- Jamil, A., Farooq, S. et Hashmi, I. (2017). Ozone disinfection efficiency for indicator microorganisms at different pH values and temperatures. Ozone: Science and Engineering, 39(6): 407-416.
- Jang, J., Hur, H.-., Sadowsky, M.J., Byappanahalli, M.N., Yan, T. et Ishii, S. (2017). Environmental Escherichia coli: Ecology and public health implications-a review. J. Appl. Microbiol., 123(3): 570-581.
- Juhna, T., Birzniece, D., Larsson, S., Zulenkovs, D., Sharipo, A., Azevedo, N.F., Ménard-Szczebara, F., Castagnet, S., Féliers, C. et Keevil, C.W. (2007). Detection of Escherichia coli in biofilms from pipe samples and coupons in drinking water distribution networks. Appl. Environ. Microbiol., 73(22): 7456-7464.
- Kauppinen, A., Pitkänen, T. et Miettinen, I.T. (2017). Persistent norovirus contamination of groundwater supplies in two waterborne outbreaks. Food Environ. Virol., : 1-12.
- Keswick, B.H., Secor, S.L., Gerba, C.P. et Cech, I. (1982). Survival of enteric viruses and indicator bacteria in groundwater. J. Environ. Sci. Heal. A., 17(6): 903-912.
- Khan, S.J., Deere, D., Leusch, F.D.L., Humpage, A., Jenkins, M., et Cunliffe, D. (2015). Extreme weather events: Should drinking water quality management systems adapt to changing risk profiles? Water Res., 85: 124-136.
- Kim, M., Jung, T., Kim, Y., Lee, C., Woo, K., Seol, J.H. et Yang, S. (2015). A microfluidic device for label-free detection of Escherichia coli in drinking water using positive dielectrophoretic focusing, capturing, and impedance measurement. Biosens. Bioelectron., 74: 1011-1015.
- King, B.J., et Monis, P.T. (2007). Critical processes affecting Cryptosporidium oocyst survival in the environment. Parasitology, 134 (3): 309-323.
- Kirmeyer, G.J., Friedman, M., Martel, K., Howie, D., LeChevallier, M., Abbaszadegan, M., Karim, M., Funk, J. et Harbour, J. (2001). Pathogen intrusion into the distribution system. AWWA Research Foundation and American Water Works Association, Denver, CO.
- Kirmeyer, G.J., Thomure, T.M., Rahman, R., Marie, J.L., LeChevallier, M.W., Yang, J., Hughes, D.M. et Schneider, O. (2014). Effective microbial control strategies for main breaks and depressurization. Water Research Foundation, Denver, CO.
- Kotwal, G., et Cannon, J.L. (2014). Environmental persistence and transfer of enteric viruses. Curr. Opin. Virol., 4: 37-43.Krapf, T., Kuhn, R.M., Kauf, P., Corinne, H.G.-. et Fieseler, L. (2016). Quantitative real-time PCR does not reliably detect single fecal indicator bacteria in drinking water. Wat. Sci. Tech.-W. Sup., 16(6): 1674-1682.
- Krkosek, W., Reed, V. et Gagnon, G.A. (2016). Assessing protozoan risks for surface drinking water supplies in Nova Scotia, Canada. J. Water Health, 14(1): 155-166.
- Krolik, J., Maier, A., Evans, G., Belanger, P., Hall, G., Joyce, A. et Majury, A. (2013). A spatial analysis of private well water Escherichia coli contamination in Southern Ontario. Geospatial Health, 8(1): 65-75.
- Ksoll, W.B., Ishii, S., Sadowsky, M.J. et Hicks, R.E. (2007). Presence and sources of fecal coliform bacteria in epilithic periphyton communities of Lake Superior. Appl. Environ. Microbiol., 73(12): 3771-3778.
- Laine, J., E. Huovinen, M.J. Virtanen, M. Snellman, J. Luomio, P. Ruutu, E. Kujansuu, R. Vuento, T. Pitkanen, I. Miettinen, J. Herrala, O. Lepisto, J. Antonen, J. Helenius, M.-L. Hanninen, L. Maunula, J. Mustonen, M. Kuusi, et the Pirkanmaa Outbreak Study Group. (2011). An extensive gastroenteritis outbreak after drinking-water contamination by sewage effluent, Finland. Epidemiol. Infect. 139(7): 1105-1113.
- Lalancette, C., Papineau, I., Payment, P., Dorner, S., Servais, P., Barbeau, B., Di Giovanni, G.D. et Prévost, M. (2014). Changes in Escherichia coli to Cryptosporidium ratios for various fecal pollution sources and drinking water intakes. Water Res., 55: 150-161.
- Lange, B., Strathmann, M. et Oßmer, R.(2013). Performance validation of chromogenic coliform agar for the enumeration of Escherichia coli and coliform bacteria. Lett. in Appl. Microbiol., 57 (6):547-553.
- Laursen, E., Mygind, O., Rasmussen, B., et Ronne, T. (1994). Gastroenteritis: A waterborne outbreak affecting 1600 people in a small Danish town. J. Epidemiol. Commun. H., 48 (5): 453-458.
- LeChevallier, M.W. et Au, K.K. (2004). Water treatment and pathogen control: Process efficiency in achieving safe drinking water. IWA Publishing, London, UK, on behalf of the World Health Organization, Geneva.
- LeChevallier, M.W. (1998). Benefits of employing a disinfectant residual in distribution systems. Water Supp., 16(3-4): 61-73.
- Leclerc, H., Mossel, D.A.A., Edberg, S.C. et Struijk, C.B. (2001). Advances in the bacteriology of the coliform group: Their suitability as markers of microbial water safety. Annu. Rev. Microbiol., 55: 201-234.
- Lee, D.-G., Park, S. et Kim, S.-J. (2007). Influence of Pipe Materials and VBNC Cells on Culturable Bacteria in a Chlorinated Drinking Water Model System. J. Microbiol. Biotechnol., 17(9): 1558-1562.
- Lee, W.H., Wahman, D.G., Bishop, P.L. et Pressman, J.G. (2011). Free chlorine and monochloramine application to nitrifying biofilm: Comparison of biofilm penetration, activity, and viability. Environ. Sci. Technol., 45(4): 1412-1419.
- Lefebvre, B., Malouin, F., Roy, G., Giguère, K. et Diarra, M.S. (2006). Growth performance and shedding of some pathogenic bacteria in feedlot cattle treated with different growth-promoting agents. J. Food Prot., 69 (6):1256-1264.
- Lehtola, M.J., Torvinen, E., Kusnetsov, J., Pitkänen, T., Maunula, L., Von Bonsdorff, C.-., Martikainen, P.J., Wilks, S.A., Keevil, C.W. et Miettinen, I.T. (2007). Survival of Mycobacterium avium, Legionella pneumophila, Escherichia coli, and calicivirases in drinking water-associated biofilms grown under high-shear turbulent flow. Appl. Environ. Microbiol., 73(9): 2854-2859.
- Li, L., Mendis, N., Trigui, H., Oliver, J.D. et Faucher, S.P. (2014). The importance of the viable but non-culturable state in human bacterial pathogens. Front Microbiol. 5(258) 1-20.
- Lim, C.-. et Flint, K.P. (1989). The effects of nutrients on the survival of Escherichia coli in lake water. J. Appl. Bacteriol., 66(6): 559-569.
- Lin, J. et Ganesh, A. Water quality indicators: Bacteria, coliphages, enteric viruses(2013). Int. J. Environ. Heal. R., 23 (6): 484-506.
- Locas, A., Barthe, C., Barbeau, B., Carrière, A. et Payment, P. (2007). Virus occurrence in municipal groundwater sources in Quebec, Canada. Rev. can. microbiol. = Can. J. Microbiol., 53(6) : 688-694.
- Locas, A., Barthe, C., Margolin, A.B. et Payment, P. (2008). Groundwater microbiological quality in Canadian drinking water municipal wells. Rev. can. microbiol. = Can. J. Microbiol., 54(6) : 472-478.
- Lukjancenko, O., Wassenaar, T.M. et Ussery, D.W. (2010). Comparison of 61 sequenced Escherichia coli genomes. Microb. Ecol., 60(4): 708-720.
- Lund, V. (1996). Evaluation of E. coli as an indicator for the presence of Campylobacter jejuni and Yersinia enterocolitica in chlorinated and untreated oligotrophic lake water. Water Res., 30(6): 1528-1534.
- Maguire, H.C., Holmes, E., Hollyer, J., Strangeways, J.E.M., Foster, P., Holliman, R.E. et Stanwell-Smith, R. (1995). An outbreak of cryptosporidiosis in South London: What value the p value ? Epidemiol. Infect., 115(2): 279-287.
- Maheux, A.F., Huppé, V., Boissinot, M., Picard, F.J., Bissonnette, L., Bernier, J.-.T. et Bergeron, M.G. (2008). Analytical limits of four β-glucuronidase and β-galactosidase-based commercial culture methods used to detect Escherichia coli and total coliforms. J. Microbiol. Methods, 75(3): 506-514.
- Maheux, A.F., Picard, F.J., Boissinot, M., Bissonnette, L., Paradis, S. et Bergeron, M.G. (2009). Analytical comparison of nine PCR primer sets designed to detect the presence of Escherichia coli/Shigella in water samples. Water Res., 43(12): 3019-3028.
- Maheux, A.F., Bissonnette, L., Boissinot, M., Bernier, J.T., Huppé, V., Picard, F.J., Bérubé, E. et Bergeron, M.G. (2011). Rapid concentration and molecular enrichment approach for sensitive detection of Escherichia coli and Shigella species in potable water samples. Appl. Environ. Microbiol., 77(17): 6199-6207.
- Maheux, A.F., Dion-Dupont, V., Bisson, M.-A., Bouchard, S., Jubinville, É., Nkuranga, M., Rodrigue, L., Bergeron, M.G., et Rodriguez, M.J. (2015a). Multiparametric comparison of chromogenic-based culture methods used to assess the microbiological quality of drinking water and the mFC method combined with a molecular confirmation procedure. J. Water Health, 13 (1):67-72.
- Maheux, A.F., Dion-Dupont, V., Bouchard, S., Bisson, M.-A., Bergeron, M.G. et Rodriguez, M.J. (2015b). Comparison of four ß-glucuronidase and ß-galactosidasebased commercial culture methods used to detect Escherichia coli and total coliforms in water. J. Water Health, 13 (2): 340-352.
- Maheux, A.F., Bouchard, S., Bérubé, E. et Bergeron, M.G. (2017). Comparison of MI, Chromocult® coliform, and Compass CC chromogenic culture-based methods to detect Escherichia coli and total coliforms in water using 16S rRNA sequencing for colony identification. J. Water Health, 15(3): 353-359.
- Maier, A., Krolik, J., Fan, S., Quintin, P., McGolrick, D., Joyce, A. et Majury, A. (2015). Evaluating appropriate maximum holding times for private well water samples. Dossier santé environnementale (revue de l'Institut canadien des inspecteurs en santé publique (CIPHI)) = Environmental Health Review (Journal of the Canadian Institute of Public Health Inspectors (CIPHI)). 58: 35-40.
- Martin, E.C. et Gentry, T.J. (2016). Impact of enumeration method on diversity of Escherichia coli genotypes isolated from surface water. Lett. Appl. Microbiol., 63 (5): 369-375.
- Martins, M.T., Rivera, I.G., Clark, D.L., Stewart, M.H., Wolfe, R.L. et Olson, B.H. (1993). Distribution of uidA gene sequences in Escherichia coli isolates in water sources and comparison with the expression of β-glucuronidase activity in 4- methylumbelliferyl-β-D-glucuronide media. Appl. Environ. Microbiol., 59(7): 2271-2276.
- McDaniels, A.E., Bordner, R.H., Gartside, P.S., Haines, J.R., Brenner, K.P. et Rankin, C.C. (1985). Holding effects on coliform enumeration in drinking water samples. Appl. Environ. Microbiol., 50(4): 755-762.
- Mendes Silva, D. et Domingues, L. (2015). On the track for an efficient detection of Escherichia coli in water: A review on PCR-based methods. Ecotoxicol. Environ. Saf., 113: 400-411.
- Messner, M.J., Berger, P. et Javier, J. (2017). Total coliform and E. coli in public water systems using undisinfected ground water in the United States. Int. J. Hyg. Environ. Health, 220(4): 736-743.
- Mezule, L. et Juhna, T. (2016). Effect of labile organic carbon on growth of indigenous Escherichia coli in drinking water biofilm. Chemical Engineering Transactions. 49: 619-624.
- Mi, R., Patidar, R., Farenhorst, A., Cai, Z., Sepehri, S., Khafipour, E., et Kumar, A. (2019). Detection of fecal bacteria and antibiotic resistance genes in drinking water collected from three First Nations communities in Manitoba, Canada FEMS Microbiol. Lett., 366 (6).
- Miles, S.L., Gerba, C.P., Pepper, I.L., et Reynolds, K.A. (2009). Point-of-use drinking water devices for assessing microbial contamination in finished water and distribution systems. Environ. Sci. Technol., 43 (5): 1425-1429.
- Miles, S.L., Sinclair, R.G., Riley, M.R. et Pepper, I.L. (2011). Evaluation of select sensors for real-time monitoring of Escherichia coli in water distribution systems. Appl. Environ. Microbiol., 77(8): 2813-2816.
- MEPP (2019). Protocol of Accepted Drinking Water Testing Methods. Version 2.0. Laboratory Services Branch 2002. Ontario Ministry of the Environment, Conservation and Parks. Consulté en septembre 2019. Accès : https://www.ontario.ca/page/accepted-drinking-water-testing-methods.
- Murphy, H.M., Thomas, M.K., Medeiros, D.T., McFadyen, S. et Pintar, K.D.M. (2016a). Estimating the number of cases of acute gastrointestinal illness (AGI) associated with Canadian municipal drinking water systems. Epidemiol. Infect., 144(7): 1371-1385.
- Murphy, H.M., Thomas, M.K., Schmidt, P.J., Medeiros, D.T., McFadyen, S. et Pintar, K.D.M. (2016b). Estimating the burden of acute gastrointestinal illness due to Giardia, Cryptosporidium, Campylobacter, E. coli O157 and norovirus associated with private wells and small water systems in Canada. Epidemiol. Infect., 144(7): 1355-1370.
- Murphy, H.M., Prioleau, M.D., Borchardt, M.A. et Hynds, P.D. (2017). Review: Epidemiological evidence of groundwater contribution to global enteric disease, 1948-2015. Hydrogeol. J., 25 (4): 981-1001.
- Narasimhan, R., Brereton, J., Abbaszadegan, M., Alum, A. et Ghatpande, P. (2004). Sample collection procedures and locations for bacterial compliance monitoring. AWWA Research Foundation, Denver, CO.
- NHMRC, NRMMC (2017) Australian Drinking Water Guidelines Paper 6 National Water Quality Management Strategy (Version 3.4 Updated October 2017). National Health and Medical Research Council, National Resource Management Ministerial Council, Commonwealth of Australia, Canberra.
- Nichols, G., Lane, C., Asgari, N., Verlander, N.Q. et Charlett, A. (2009). Rainfall and outbreaks of drinking water related disease and in England and Wales. J. Water Health, 7(1): 1-8.
- Novello, A. (2000). The Washington County Fair Outbreak Report. Albany, New York State Department of Health: 108 pp.
- NSF/ANSI (2018a). Standard 58: Reverse osmosis drinking water treatment systems. NSF International, Ann Arbor, Michigan.
- NSF/ANSI/CAN (2018b). Standard 60: Drinking water treatment chemicals: Health effects. NSF International, Ann Arbor, Michigan.
- NSF/ANSI (2018c). Standard 419: Public drinking water equipment performance - Filtration. NSF International, Ann Arbor, Michigan.
- NSF/ANSI (2019). Standard 55: Ultraviolet microbiological water treatment systems. NSF International, Ann Arbor, Michigan.O'Connor, D.R. (2002a).
- Rapport de la Commission d'enquête sur Walkerton : les événements de mai 2000 et les questions connexes, première partie. Ministère du Procureur général de l'Ontario (ISBN : 0-7794-2932-X).
- O'Connor, D.R. (2002b). Rapport de la Commission d'enquête sur Walkerton : stratégie pour la salubrité de l'eau potable, deuxième partie. Ministère du Procureur général de l'Ontario (ISBN : 0-7794-2934-6).
- Olsen, S.J., Miller, G., Breuer, T., Kennedy, M., Higgins, C., Walford, J., McKee, G., Fox, K., Bibb, W., et Mead, P. (2002). A waterborne outbreak of Escherichia coli O157:H7 infections and hemolytic uremic syndrome: Implications for rural water systems. Emerg. Infect. Dis., 8(4): 370-375.
- Olstadt, J., Schauer, J.J., Standridge, J. et Kluender, S. (2007). A comparison of ten USEPA approved total coliform/E. coli tests. J. Water Health, 5(2): 267-282.
- OMS (2004). Directives de qualité pour l'eau de boisson. 3e édition. Organisation mondiale de la Santé, Genève, Suisse.
- OMS (2005). Managing drinking-water quality from catchment to consumer. World Health Organization, Geneva, Switzerland.
- OMS (2012). Planifier la gestion de la sécurité sanitaire de l'eau pour l'approvisionnement en eau des petites communautés. Organisation mondiale de la Santé, Genève (Suisse). Accès : https://www.who.int/water_sanitation_health/publications/small-comm-water_supplies/fr/.
- OMS (2014). Water safety in distribution systems. WHO Document Production Services, Geneva, Switzerland.
- OMS (2017). Directives de qualité pour l'eau de boisson : quatrième édition intégrant le premier additive. Organisation mondiale de la Santé, Genève.
- OMS et OCDE (2003). Assessing Microbial Safety of Drinking Water - Improving approaches and methods. World Health Organization and Organisation for Economic Co-operation and Development. IWA Publishing, London UK. pp 1-295.
- Pachepsky, Y.A., Blaustein, R.A., Whelan, G., et Shelton, D.R. (2014). Comparing temperature effects on Escherichia coli, Salmonella, and Enterococcus survival in surface waters. Lett. Appl Microbiol., 59 (3), pp. 278-283.
- Payment, P. (1999). Poor efficacy of residual chlorine disinfectant in drinking water to inactivate waterborne pathogens in distribution systems. Rev. can. microbiol. = Can. J. Microbiol., 45(8) : 709-715.
- Payment, P. et Locas, A. (2005). Évaluation et contrôle de la qualité virologique des eaux souterraines. Projet: 3331-24-02-01. Institut Armand-Frappier, Institut national de la recherche scientifique. Laval, Québec
- Payment, P. et Locas, A. (2011). Pathogens in water: Value and limits of correlation with microbial indicators. Ground Water, 49(1): 4-11.
- Payment, P. et Pintar, K. (2006). Waterborne pathogens: a critical assessment of methods, results and data analysis. Rev. Sci. Eau, 19: 233-245.
- Payment, P., Waite, M. et Dufour, A. (2003). Chapter 2: Introducing parameters for the assessment of drinking water quality. In: Assessing microbial safety of drinking water. Dufour, A. et al. eds. World Health Organization and The Organization for Economic Co-operation and Development. IWA Publishing, London, UK. Pp. 47-77.
- Pope, M.L., Bussen, M., Feige, M.A., Shadix, L., Gonder, S., Rodgers, C., Chambers, Y., Pulz, J., Miller, K., Connell, K. et Standridge, J. (2003). Assessment of the effects of holding time and temperature on Escherichia coli densities in surface water samples. Appl. Environ. Microbiol., 69(10): 6201-6207.
- Pressman, J.G., Lee, W.H., Bishop, P.L. et Wahman, D.G. (2012). Effect of free ammonia concentration on monochloramine penetration within a nitrifying biofilm and its effect on activity, viability, and recovery. Water Res., 46(3): 882-894.
- Puleston, R.L., Mallaghan, C.M., Modha, D.E., Hunter, P.R., Nguyen-Van-Tam, J.S., Regan, C.M., Nichols, G.L., et Chalmers, R.M. (2014). The first recorded outbreak of cryptosporidiosis due to Cryptosporidium cuniculus (formerly rabbit genotype), following a water quality incident (2014) J. Water Health, 12 (1), pp. 41-50.
- Rasheed, S., Hashmi, I. et Campos, L. (2016). Inactivation of Escherichia coli and Salmonella with chlorine in drinking waters at various pH and temperature levels. Proceedings of the Pakistan Academy of Sciences, 53(2B): 83-92.
- Rice, E.W., Clark, R.M. et Johnson, C.H. (1999). Chlorine inactivation of Escherichia coli O157:H7. Emerg. Infect. Dis., 5(3): 461-463.
- Risebro, H.L., Doria, M.F., Andersson, Y., Medema, G., Osborn, K., Schlosser, O. et Hunter, P.R. (2007). Fault tree analysis of the causes of waterborne outbreaks. J. Water Health, 5(Suppl. 1): 1-18.
- Robertson, W., Stanfield, G., Howard, G. et Bartram, J. (2003). Chapter 6 - Monitoring the quality of drinking water during storage and distribution. In: Assessing microbial safety of drinking water. Dufour, A. et al. eds. World Health Organization and The Organization for Economic Co-operation and Development. IWA Publishing, London, UK. Pp. 179-204.
- Saby, M., Larocque, M., Pinti, D.L., Barbecot, F., Gagné, S., Barnetche, D. et Cabana, H. (2017). Regional assessment of concentrations and sources of pharmaceutically active compounds, pesticides, nitrate, and E. coli in post-glacial aquifer environments (Canada). Sci. Total Environ., 579: 557-568.
- Sampson, R.W., Swiatnicki, S.A., Osinga, V.L., Supita, J.L., McDermott, C.M. et Kleinheinz, G.T. (2006). Effects of temperature and sand on E. coli survival in a Northern lake water microcosm. J Water Health, 4(3): 389-393.
- Santé Canada (2001). La salubrité de l'eau potable au Canada, de la prise d'eau au robinet : un document cadre. Préparé par un groupe de travail du Sous-comité fédéral-provincial-territorial sur l'eau potable du Comité fédéral-provincial-territorial de l'hygiène du milieu et du travail. Décembre, 2001. Santé Canada, Ottawa (Canada). Consulté en octobre 2019. Accès : https://www.canada.ca/fr/sante-canada/services/sante-environnement-milieu-travail/rapports-publications/qualite-eau/salubrite-eau-potable-canada-prise-eau-robinet-document-cadre-sante-canada-2001.html
- Santé Canada (2006). Recommandations pour la qualité de l'eau potable au Canada : les trihalométhanes. Bureau de la qualité de l'eau et de la santé, Direction générale de la santé environnementale et de la sécurité des consommateurs, Santé Canada, Ottawa (Ontario). Accès : https://www.canada.ca/fr/sante-canada/services/publications/vie-saine/recommandations-pour-qualite-eau-potable-canada-trihalomethanes.html
- Santé Canada (2008a). Recommandations pour la qualité de l'eau potable au Canada : document technique : le chlorite et le chlorate. Bureau de l'eau, de l'air et des changements climatiques, Direction générale de la santé environnementale et de la sécurité des consommateurs, Santé Canada, Ottawa (Ontario). Disponible à : https://www.canada.ca/fr/sante-canada/services/publications/vie-saine/recommandations-pour-qualite-eau-potable-canada-document-technique-chlorite-et-chlorate.html
- Santé Canada (2008b). Recommandations pour la qualité de l'eau potable au Canada : document technique : les acides haloacétiques. Bureau de l'eau, de l'air et des changements climatiques, Direction générale de la santé environnementale et de la sécurité des consommateurs, Santé Canada, Ottawa (Ontario). Accès : https://www.canada.ca/fr/sante-canada/services/publications/vie-saine/recommandations-pour-qualite-eau-potable-canada-document-technique-acides-haloacetiques.html
- Santé Canada (2009) Recommandations pour la qualité de l'eau potable au Canada : document technique : le chlore. Bureau de l'eau, de l'air et des changements Accès : https://www.canada.ca/fr/sante-canada/services/publications/vie-saine/recommandations-pour-qualite-eau-potable-canada-chlore-document-technique.html
- Santé Canada (2011). Recommandations pour la qualité de l'eau potable au Canada : document technique : N-nitrosodiméthylamine. Bureau de l'eau, de l'air et des changements climatiques, Direction générale de la santé environnementale et de la sécurité des consommateurs, Santé Canada, Ottawa (Ontario). Accès : https://www.canada.ca/fr/sante-canada/services/publications/vie-saine/recommandations-pour-qualite-eau-potable-canada-document-technique-n-nitrosodimethylamine-ndma.html
- Santé Canada (2012a). Recommandations pour la qualité de l'eau potable au Canada : document technique - la turbidité. Bureau de la qualité de l'eau et de l'air, Direction générale de la santé environnementale et de la sécurité des consommateurs, Santé Canada, Ottawa (Ontario). Accès : https://www.canada.ca/fr/sante-canada/services/publications/vie-saine/recommandations-pour-qualite-eau-potable-canada-turbidite.html
- Santé Canada (2012b). Recommandations pour la qualité de l'eau potable au Canada : document technique : les coliformes totaux. Bureau de la qualité de l'eau et de l'air, Direction générale de la santé environnementale et de la sécurité des consommateurs, Santé Canada, Ottawa (Ontario). Accès : https://www.canada.ca/fr/sante-canada/services/publications/vie-saine/recommandations-pour-qualite-eau-potable-canada-document-technique-coliformes-totaux.html
- Santé Canada (2013a). Conseils pour un approvisionnement en eau potable salubre dans les secteurs de compétence fédérale : version 2. Bureau de la qualité de l'eau et de l'air, Direction générale de la santé environnementale et de la sécurité des consommateurs, Santé Canada, Ottawa (Ontario). Accès : https://www.canada.ca/fr/sante-canada/services/publications/vie-saine/conseils-pour-approvisionnement-eau-potable-salubre-secteurs-competence-federale-version-2.html
- Santé Canada (2013b). Conseils sur les bactéries pathogènes d'origine hydrique. Bureau de la qualité de l'eau et de l'ai, Direction générale de la santé environnementale et de la sécurité des consommateurs, Santé Canada, Ottawa (Ontario). Accès : https://www.canada.ca/fr/sante-canada/services/publications/vie-saine/conseils-bacteries-pathogenes-origine-hydrique.html
- Santé Canada (2015). Conseils concernant l'émission et l'annulation des avis d'ébullition de l'eau dans les approvisionnements d'eau potable au Canada. Bureau de la qualité de l'eau et de l'air, Direction générale de la santé environnementale et de la sécurité des consommateurs, Santé Canada, Ottawa (Ontario). Accès : https://www.canada.ca/fr/sante-canada/services/publications/vie-saine/conseils-concernant-emission-et-annulation-avis-ebullition-eau-approvisionnements-eau-potable-canada.html
- Santé Canada (2018a). Conseils sur l'utilisation des entérocoques comme bactéries indicatrices dans les sources d'approvisionnement en eau potable canadiennes - en préparation. Bureau de la qualité de l'eau et de la santé, Direction générale de la santé environnementale et de la sécurité des consommateurs, Santé Canada, Ottawa, Ontario.
- Santé Canada (2018b). Recommandations pour la qualité de l'eau potable au Canada : document technique - bromate. Bureau de la qualité de l'eau et de l'air, Direction générale de la santé environnementale et de la sécurité des consommateurs, Santé Canada, Ottawa (Ontario). Accès : https://www.canada.ca/fr/sante-canada/services/publications/vie-saine/recommandations-pour-qualite-eau-potable-canada-document-technique-bromate/document-reference.html
- Santé Canada (2018c). Communications personnelles avec T. Beattie. Analyse basée sur les données de la Module des avis concernant l'eau potable de la Réseau canadien de renseignements sur la santé publique (RCRSP).
- Santé Canada (2018d). Résumé des données de surveillance sur E. coli tirées de rapports annuels sur la qualité de l'eau potable publiés par des services canadiens d'alimentation en eau potable. Disponible sur demande.
- Santé Canada (2019a). Conseils sur la surveillance de la stabilité biologique de l'eau potable dans les réseaux de distribution- en préparation. Document for public consultation. Water and Air Quality Bureau, Healthy Environments and Consumer Safety Branch, Health Canada, Ottawa, Ontario.
- Santé Canada (2019b). Recommandations pour la qualité de l'eau potable au Canada : document technique - Chloramines. Water Quality and Health Bureau, Healthy Environments and Consumer Safety Branch, Health Canada, Ottawa, Ontario. Accès : https://www.canada.ca/fr/sante-canada/services/publications/vie-saine/recommandations-pour-qualite-eau-potable-canada-document-technique-chloramines.html
- Santé Canada (2019c). Recommandations pour la qualité de l'eau potable au Canada : document technique : protozoaires entériques : Giardia et Cryptosporidium. Bureau de la qualité de l'eau et de l'air, Direction générale de la santé environnementale et de la sécurité des consommateurs, Santé Canada, Ottawa (Ontario). Accès : https://www.canada.ca/fr/sante-canada/services/sante-environnement-milieu-travail/rapports-publications/qualite-eau/protozoaires-enteriques-giardia-cryptosporidium.html
- Santé Canada (2019d). Recommandations pour la qualité de l'eau potable au Canada : document technique : les virus entériques. Bureau de la qualité de l'eau et de l'air, Direction générale de la santé environnementale et de la sécurité des consommateurs, Santé Canada, Ottawa (Ontario). Accès : https://www.canada.ca/fr/sante-canada/services/publications/vie-saine/recommandations-pour-qualite-eau-potable-canada-document-technique-virus-enteriques.html
- Schuster, C.J., Ellis, A.G., Robertson, W.J., Charron, D.F., Aramini, J.J., Marshall, B.J. et Medeiros, D.T. (2005). Infectious disease outbreaks related to drinking water in Canada, 1974-2001. Can. J. Public Health, 96(4): 254-255.
- Sinton, L., Hall, C., et Braithwaite, R. (2007). Sunlight inactivation of Campylobacter jejuni and Salmonella enterica, compared with Escherichia coli, in seawater and river water. J. Water Health, 5 (3): 357-365.
- Smeets, P., Rietveld, L., Hijnen, W., Medema, G. et Stenstrom, T-A. (2006). Efficacy of water treatment processes. in: MicroRisk - microbiological risk assessment: A scientific basis for managing drinking water safety from source to tap. April 2006. (available from: www.kwrwater.nl).
- Smeets, P.W.M.H., Medema, G.J. et Van Dijk, J.C. (2009). The Dutch secret: How to provide safe drinking water without chlorine in the Netherlands. Drink. Water Eng. Sci., 2(1): 1-14.
- Sommer, R., Lhotsky, M., Haider, T. et Cabaj, A. (2000). UV inactivation, liquid-holding recovery, and photoreactivation of Escherichia coli O157 and other pathogenic Escherichia coli strains in water. J. Food Prot., 63(8): 1015-1020.
- Speight, V.L., Kalsbeek, W.D. et DiGiano, F.A. (2004). Randomized stratified sampling methodology for water quality in distribution systems. J. Water Resour. Plann. Manage., 130(4): 330-338.
- St Laurent, J. et Mazumder, A. (2012). The influence of land-use composition on fecal contamination of riverine source water in Southern British Columbia. Water Resour. Res., 48(12).
- Staben, N., Nahrstedt, A., et Merkel, W. (2015). Securing safe drinking water supply under climate change conditions. Water Sci. Technol.-W. Sup., 15 (6): 1334-1342.
- Staley, Z.R., Grabuski, J., Sverko, E., et Edge, T.A. (2016). Comparison of microbial and chemical source tracking markers to identify fecal contamination sources in the Humber River (Toronto, Ontario, Canada) and associated storm water outfalls. Appl. Environ. Microbiol., 82 (21):6357-6366.
- Standridge, J. (2008). E. coli as a public health indicator of drinking water quality. J. Am. Water Works Assoc., 100(2): 65-75.
- Statistique Canada (2013a). Enquête sur les ménages et l'environnement (EME), 2011.
- Stanfield, G., LeChevallier, M. et Snozzi, M. (2003). Chapter 5: Treatment Efficiency In: Assessing microbial safety of drinking water. Dufour, A. al. eds. World Health Organization and The Organization for Economic Co-operation and Development. IWA Publishing, London, UK. pp. 159-178.
- Stea, E.C., Truelstrup Hansen, L., Jamieson, R.C. et Yost, C.K. (2015). Fecal contamination in the surface waters of a rural and an urban-source watershed. J. Environ. Qual., 44(5): 1556-1567.
- Szabo, J. et Minamyer, S. (2014). Decontamination of chemical agents from drinking water infrastructure: A literature review and summary. Environ. Int., 72: 119-123.
- Tenaillon, O., Skurnik, D., Picard, B. et Denamur, E. (2010). The population genetics of commensal Escherichia coli. Nat. Rev. Microbiol., 8(3): 207-217.
- Thomas, M.K., Charron, D.F., Waltner-Toews, D., Schuster, C., Maarouf, A.R. et Holt, J.D. (2006). A role of high impact weather events in waterborne disease outbreaks in Canada, 1975-2001. Int. J. Environ. Health Res., 16(3): 167-180.
- Tymensen, L.D., Pyrdok, F., Coles, D., Koning, W., Mcallister, T.A., Jokinen, C.C., Dowd, S.E. et Neumann, N.F. (2015). Comparative accessory gene fingerprinting of surface water Escherichia coli reveals genetically diverse naturalized population. J. Appl. Microbiol., 119(1): 263-277.
- UE (1998). Directive 98/83/CE du Conseil du 3 novembre 1998 relative à la qualité des eaux destinées à la consommation humaine. Journal officiel des Communautés européennes. L 330/32 5.12.98.
- U.S. EPA (1991). Guidance manual for compliance with the filtration and disinfection requirements for public water systems using surface water sources. U.S. Environmental Protection Agency, Washington, DC.
- U.S. EPA (1999). EPA guidance manual: Disinfection profiling and benchmarking. U.S. Environmental Protection Agency, Washington, DC. (EPA-815-R-99-013).
- U.S. EPA (2006a). 40 CFR parts 9, 141 and 142. National primary drinking water regulations: Ground water rule. final rule. U.S. Environmental Protection Agency, Washington, DC. Fed. Regist., 71(216): 65573-65660.
- U.S. EPA (2006b). National Primary Drinking Water Regulations: Long Term 2 Enhanced Surface Water Treatment; final rule. U.S. Environmental Protection Agency, Washington, DC. Fed. Regist., 71(3):678-671; 782-783.
- U.S. EPA (2006c). Ultraviolet disinfection guidance manual. Office of Water, U.S. Environmental Protection Agency, Washington, DC (Report No. EPA/815/R-06/007).
- U.S. EPA (2013). National primary drinking water standards: Revisions to the total coliform rule. final rule. U.S. Environmental Protection Agency, Washington, DC. Fed. Regist., 78(30): 10269.
- U.S. EPA (2017a). Analytical methods approved for compliance monitoring under the groundwater rule. Office of Water, U.S. Environmental Protection Agency, Washington, DC. EPA 821-F-17-004.
- U.S. EPA (2017b). Analytical methods approved for compliance monitoring under the revised total coliform rule. Office of Water, U.S. Environmental Protection Agency, Washington, DC. EPA 821-F-17-004.
- Valeo, C., He, J., Checkley, S. et Neumann, N. (2016). Rainfall and microbial contamination in Alberta well water. J. Environ. Eng. Sci., 11(1): 18-28.
- van der Kooij, D. et van der Wielen, P.W.J.J. (2014). Chapter 15 - Research needs. In: Microbial growth in drinking-water supplies: Problems, causes, control and research needs. IWA Publishing, London, UK. Pp. 423-443
- Van Dyke, M.I., Ong, C.S.L., Prystajecky, N.A., Isaac-Renton, J.L. et Huck, P.M. (2012). Identifying host sources, human health risk and indicators of Cryptosporidium and Giardia in a Canadian watershed influenced by urban and rural activities. J. Water Health, 10(2): 311-323.
- Van Elsas, J.D., Semenov, A.V., Costa, R. et Trevors, J.T. (2011). Survival of Escherichia coli in the environment: Fundamental and public health aspects. ISME J., 5(2): 173-183.
- van Lieverloo, J.H.M., Mesman, G.A.M., Bakker, G.L., Baggelaar, P.K., Hamed, A. et Medema, G. (2007). Probability of detecting and quantifying faecal contaminations of drinking water by periodically sampling for E. coli: A simulation model study. Water Res., 41(19): 4299-4308.
- Wahman, D.G. et Pressman, J.G. (2015). Distribution system residuals-is "detectable" still acceptable for chloramines? J. Am. Water Works Assoc., 107(8): 53-63.
- Walk, S.T., Alm, E.W., Calhoun, L.M., Mladonicky, J.M. etWhittam, T.S. (2007). Genetic diversity and population structure of Escherichia coli isolated from freshwater beaches. Environ. Microbiol., 9(9): 2274-2288.
- Wallender, E.K., Ailes, E.C., Yoder, J.S., Roberts, V.A., et Brunkard, J.M. (2014). Contributing Factors to Disease Outbreaks Associated with Untreated Groundwater. Groundwater, 52 (6): 886-897.
- Whitman, R.L., Shively, D.A., Pawlik, H., Nevers, M.B. et Byappanahalli, M.N. (2003). Occurrence of Escherichia coli and enterococci in Cladophora (Chlorophyta) in nearshore water and beach sand of Lake Michigan. Appl. Environ. Microbiol., 69: 4714-4719.
- Williams, M.M. et Braun-Howland, E.B. (2003). Growth of Escherichia coli in model distribution system biofilms exposed to hypochlorous acid or monochloramine. Appl. Environ. Microbiol., 69(9): 5463-5471.
- Winfield, M.D., Groisman, E.A. (2003). Role of nonhost environments in the lifestyles of Salmonella and Escherichia coli. Appl. Environ. Microbiol., 69 (7): 3687-3694.
- Wojcicka, L., Hofmann, R., Baxter, C., Andrews, R.C., Auvray, I., Lière, J., Miller, T., Chauret, C. et Baribeau, H. (2007). Inactivation of environmental and reference strains of heterotrophic bacteria and Escherichia coli O157:H7 by free chlorine and monochloramine. J. Water Supply Res. T., 56(2): 137-150.
- Wu, J., Long, S.C., Das, D. et Dorner, S.M. (2011). Are microbial indicators and pathogens correlated? A statistical analysis of 40 years of research. J. Water Health, 9(2): 265-278.
- Wu, J., Rees, P., et Dorner, S. (2011). Variability of E. coli density and sources in an urban watershed. J. Water Health, 9: 94-106.
- Zhang, Y., Hong, P.-., LeChevallier, M.W. et Liu, W.-. (2015). Phenotypic and phylogenetic identification of coliform bacteria obtained using 12 coliform methods approved by the U.S. Environmental Protection Agency. Appl. Environ. Microbiol., 81(17): 6012-6023.
- Zhi, S., Banting, G., Li, Q., Edge, T.A., Topp, E., Sokurenko, M., Scott, C., Braithwaite, S., Ruecker, N.J., Yasui, Y., McAllister, T., Chui, L. et Neumann, N.F. (2016). Evidence of naturalized stress-tolerant strains of Escherichia coli in municipal wastewater treatment plants. Appl. Environ. Microbiol., 82(18): 5505-5518.
- Zimmer-Thomas, J.L., Slawson, R.M. et Huck, P.M. (2007). A comparison of DNA repair and survival of Escherichia coli O157:H7 following exposure to both low- and medium- pressure UV irradiation. J. Water Health, 5(3): 407-415.
Annexe A : Arbre décisionnel relatif à l'analyse microbiologique régulière des systèmes à l'échelle municipale
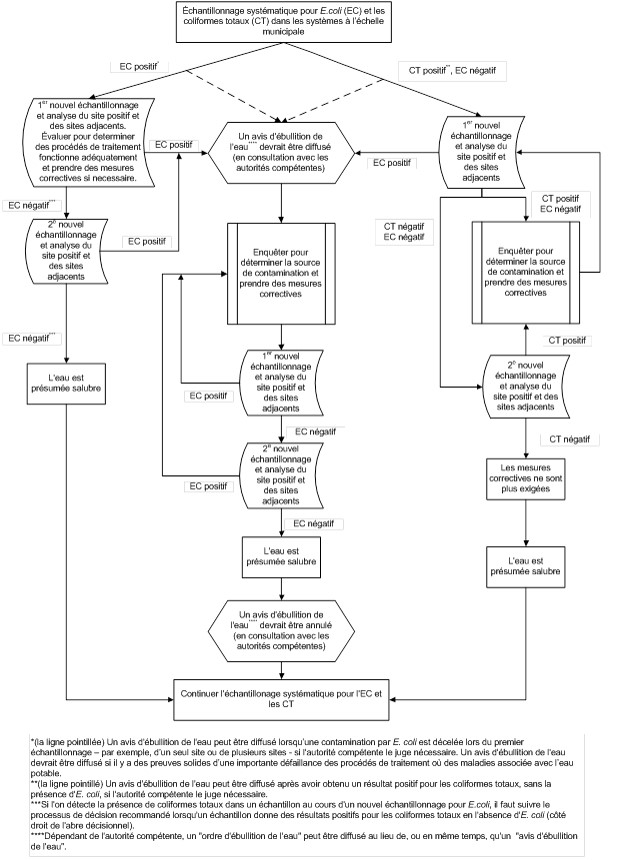
Équivalent textuel
Les mesures recommandées si l'analyse microbiologique régulière de l'eau des systèmes publics révèle une contamination par E. coli ou des coliformes totaux sont présentées sous forme d'arbre décisionnel. Les éléments constitutifs de cet arbre sont des cases, reliées par une flèche unidirectionnelle et renfermant chacune une mesure recommandée. Le cheminement le long de l'arbre et, par conséquent, les mesures recommandées dépendent des résultats de l'analyse microbiologique des échantillons. Du côté gauche, se trouvent les mesures à prendre si l'analyse révèle la présence d'E. coli, du côté droit, celles qui s'imposent en présence de coliformes totaux, mais non d'E. coli. Si un avis d'ébullition de l'eau a été diffusé, il faut choisir les mesures du centre.
Du côté gauche de l'arbre décisionnel, si E. coli est trouvé lors de l'analyse régulière, la mesure recommandée est de diffuser un avis d'ébullition de l'eau en collaboration avec les autorités compétentes. Si un seul site est contaminé, la mesure recommandée est de prélever d'autres échantillons (1er nouvel échantillonnage) au site positif et aux sites adjacents à la recherche d'E. coli et de coliformes totaux (*). Si l'analyse révèle de nouveau la présence d'E. coli au site positif, la mesure recommandée est de diffuser un avis d'ébullition de l'eau en collaboration avec les autorités compétentes. Certaines autorités diffusent un tel avis même si la contamination ne concerne qu'un site. Si le 1er nouvel échantillonnage révèle que le site qui était positif est exempt d'E. coli et de coliformes totaux, la mesure recommandée est de prélever d'autres échantillons (2e échantillonnage) à ce site et aux sites adjacents. Si un de ces sites s'avère contaminé par E. coli, la mesure recommandée est de diffuser un avis d'ébullition de l'eau en collaboration avec les autorités compétentes. Si le 2e nouvelle échantillonnage révèle que les sites sont exempts d'E. coli et de coliformes totaux, l'eau est présumée salubre et la mesure recommandée est de s'en tenir ensuite aux échantillonnages systématiques.
Il faut suivre le cheminement du côté droit de l'arbre décisionnel si l'analyse d'un échantillon révèle la présence de coliformes totaux, mais non d'E. coli. Par conséquent, si des coliformes totaux sont trouvés au 1er ou au 2e nouvel échantillonnage à la recherche d'E. coli, ou, si l'analyse régulière révèle la présence de coliformes totaux, mais non d'E. coli, la mesure recommandée est de prélever d'autres échantillons (1er nouvel échantillonnage) au site positif et aux sites adjacents, à la recherche d'E. coli et de coliformes totaux (**). Si l'analyse révèle la présence d'E. coli, la mesure recommandée est de diffuser un avis d'ébullition de l'eau en collaboration avec les autorités compétentes. Un tel avis peut être diffusé en présence d'une contamination par des coliformes totaux, mais non par E. coli, lorsque les autorités compétentes le jugent nécessaire. Si le site positif et les sites adjacents s'avèrent exempts de coliformes totaux et d'E. coli lors du 1er nouvel échantillonnage , la mesure recommandée est de prélever d'autres échantillons (2e nouvel échantillonnage) à tous ces sites, à la recherche d'E. coli et de coliformes totaux. S'ils s'avèrent une fois de plus exempts d'E. coli et de coliformes totaux, aucune mesure supplémentaire ne s'impose et l'eau est présumée salubre. La mesure recommandée est alors de s'en tenir ensuite aux échantillonnages systématiques. Si l'analyse révèle une contamination par des coliformes totaux, mais non par E. coli, la mesure recommandée est d'enquêter pour trouver la source de contamination et de prendre des mesures correctives, puis de retourner au haut de l'arbre décisionnel, à la case renfermant la mesure « 1er nouvel échantillonnage et analyse du site positif et des sites adjacents » (***).
Dans tous les cas où un avis d'ébullition de l'eau s'impose selon l'arbre décisionnel, il faut suivre le cheminement prévu au centre de celui-ci (****). Une fois l'avis diffusé, les mesures recommandées sont d'abord d'enquêter pour trouver la source de contamination et de prendre des mesures correctives, puis de prélever d'autres échantillons (1er nouvel échantillonnage) aux sites positifs et aux sites adjacents. Si E. coli est découvert à l'analyse, les flèches renvoient aux étapes antérieures de l'enquête et des mesures correctives. Sinon, il est recommandé de prélever d'autres échantillons (2e nouvel échantillonnage) aux sites positifs et aux sites adjacents. Si l'analyse révèle une contamination par E. coli, les flèches de l'arbre décisionnel renvoient aux étapes antérieures de l'enquête et des mesures correctives. Sinon, l'eau est présumée salubre, et la mesure recommandée est d'annuler l'avis d'ébullition de l'eau en collaboration avec les autorités compétentes et de s'en tenir ensuite aux échantillonnages systématiques.
Annexe B : Arbre décisionnel relatif à l'analyse microbiologique régulière des systèmes à l'échelle résidentiellerésidentielle

Équivalent textuel
Les mesures recommandées si l'analyse microbiologique régulière de l'eau des systèmes à l'échelle résidentielle révèle une contamination par E. coli ou des coliformes totaux sont présentées sous forme d'arbre décisionnel (*). Les éléments constitutifs de cet arbre sont des cases reliées par une flèche unidirectionnelle et renfermant chacune une mesure recommandée. Le cheminement le long de l'arbre, et, par conséquent, les mesures recommandées, dépendent des résultats de l'analyse microbiologique des échantillons. Du côté gauche, se trouvent les mesures à prendre si l'analyse a révélé la présence d'E. coli et qu'un avis d'ébullition de l'eau a été diffusé (**), et du côté droit, celles qui s'imposent en présence de coliformes totaux, mais non d'E. coli.
Du côté gauche de l'arbre décisionnel, si l'analyse régulière révèle la présence d'E. coli, la mesure recommandée est de diffuser un avis d'ébullition de l'eau en collaboration avec les autorités compétentes.
Il faut suivre le cheminement du côté droit de l'arbre décisionnel si l'analyse d'un échantillon révèle la présence de coliformes totaux, mais non d'E. coli. Selon ce cheminement, la mesure recommandée est de prélever d'autres échantillons (1er nouvel échantillonnage) au site positif et aux sites adjacents à la recherche d'E. coli et de coliformes totaux (***). Si l'analyse révèle la présence d'E. coli, la mesure recommandée est de diffuser un avis d'ébullition de l'eau en collaboration avec les autorités compétentes. Un tel avis peut être diffusé en présence de coliformes totaux, mais non d'E. coli, lorsque les autorités compétentes le jugent nécessaire. Si les sites visés par le nouvel échantillonnage s'avèrent encore exempts de coliformes totaux et d'E. coli, la mesure recommandée est de prélever d'autres échantillons (2e nouvel échantillonnage) aux sites positifs et aux sites adjacents, à la recherche d'E. coli et de coliformes totaux. Si l'analyse révèle la présence d'E. coli, la mesure recommandée est de diffuser un avis d'ébullition de l'eau en collaboration avec les autorités compétentes. S'il n'y a toujours ni E. coli ni coliformes totaux, aucune mesure supplémentaire ne s'impose et l'eau est présumée salubre. La mesure recommandée est alors de s'en tenir ensuite aux échantillonnages systématiques. Si l'analyse révèle la présence de coliformes totaux, mais non d'E. coli dans n'importe lequel des sites où d'autres échantillons ont été prélevés, la mesure recommandée dépend de l'étendue de la contamination, de l'historique du système, des exigences de l'autorité compétente ainsi que de la présence ou de l'absence d'éclosion (***). Ce pourra être soit d'enquêter pour trouver la source de contamination et de prendre des mesures correctives, puis de prélever d'autres échantillons (1er nouvel échantillonnage) aux sites positifs et aux sites adjacents, soit de diffuser un avis d'ébullition de l'eau en collaboration avec les autorités compétentes. Dans le premier cas, si l'analyse révèle l'absence d'E. coli et de coliformes totaux, la mesure recommandée est de prélever d'autres échantillons (2e nouvel échantillonnage) à la recherche d'E. coli et de coliformes totaux. Si les résultats d'analyse sont négatifs, l'eau est alors présumée salubre et la mesure recommandée est de s'en tenir aux échantillonnages systématiques. Si au 1er ou au 2e nouvel échantillonnage l'analyse révèle encore la présence d'E. coli ou de coliformes totaux, la mesure recommandée est de diffuser un avis d'ébullition de l'eau en collaboration avec les autorités compétentes.
Dans tous les cas où un avis d'ébullition de l'eau s'impose selon l'arbre décisionnel, les mesures recommandées sont d'abord d'enquêter pour trouver la source de contamination et de prendre des mesures correctives, et, ensuite, de prélever d'autres échantillons (1er nouvel échantillonnage) aux sites positifs et aux sites adjacents. Si E. coli ou des coliformes totaux sont découverts à l'analyse, les flèches renvoient aux étapes antérieures de l'enquête et des mesures correctives. Sinon, il est recommandé de prélever d'autres échantillons (2e nouvel échantillonnage) aux sites positifs et aux sites adjacents à la recherche d'E. coli et de coliformes totaux. Si l'analyse révèle une contamination par E. coli ou des coliformes totaux, les flèches de l'arbre décisionnel renvoient aux étapes antérieures de l'enquête et des mesures correctives. Sinon, l'eau est présumée salubre, et la mesure recommandée est d'annuler l'avis d'ébullition de l'eau en collaboration avec les autorités compétentes et de s'en tenir ensuite aux échantillonnages systématiques.
Annexe C : Liste des acronymes
- ANSI
- American National Standards Institute
- AQ
- assurance de la qualité
- CCN
- Conseil canadien des normes
- CMA
- concentration maximale acceptable
- CT
- concentration résiduelle de désinfectant par durée de contact du désinfectant
- CQ
- contrôle de la qualité
- E. coli
- Escherichia coli
- ESSIDES
- eau souterraine sous l'influence directe d'eau de surface
- MCL
- niveau maximum de contaminant (États-Unis)
- MCLG
- objectif de niveau maximum de contaminant (États-Unis)
- NPP
- nombre le plus probable
- NSF
- NSF International
- P-A
- présence-absence
- PCR
- amplification par la polymérase avec transcription inverse
- OI
- osmose inverse
- RCRSP
- Réseau canadien de renseignements sur la santé publique
- UFC
- unité formant colonie
- UE
- Union européenne
- U.S. EPA
- Environmental Protection Agency (États-Unis)
- UV
- ultraviolet
- VMNC
- viable mais non cultivable
- Note de bas de page 1
-
Aux fins du présent document, un système d'approvisionnement en eau à l'échelle résidentielle s'entend d'un système doté d'aucun réseau de distribution ou d'un réseau limité qui fournit de l'eau au public à partir d'une installation qui n'est pas reliée au système municipal. Mentionnons notamment les système privés d'approvisionnement en eau potable et les puits communautaires ainsi que des établissements comme les écoles, les foyers de soins personnels, les garderies, les hôpitaux, les hôtels et les restaurants. La définition d'un système d'approvisionnement à l'échelle résidentielle peut varier selon les secteurs de compétence.
- Note de bas de page 2
-
Pour les besoins du présent document, on entend par « avis d'ébullition de l'eau » tout communiqué public émis par l'autorité responsable en matière d'eau potable dans le secteur de compétence concerné avisant la population de faire bouillir l'eau, soit par mesure de précaution, soit par suite d'une éclosion de maladie. Le terme utilisé peut varier selon le secteur de compétence. Il arrive également que le terme « ordre d'ébullition de l'eau » soit utilisé à la place du terme « avis d'ébullition de l'eau » ou conjointement avec lui.