Résumé de l'évaluation du risque associé au coronavirus du syndrome respiratoire du Moyen-Orient (MERS-CoV) pour la santé publique au Canada
L'évaluation des risques est régulièrement examinée et mise à jour au besoin.
Mise à jour : 22 novembre 2018
Dernières nouvelles
- Le résumé de l'evénement, la courbe épidémiologique et la carte de la répartition spatiale ont été mis à jour de manière à représenter les cas déclarés depuis la dernière mise à jour (13 juillet 2017) : Au total, 227 nouveaux cas ont été signalés, dont 137 entre le 1er janvier et 30 octobre, 2018.
- Le Résumé de la documentation scientifique a été révisé pour inclure les nouveaux documents publiés sur la détection du MERS-CoV chez l'alpaga, les variations entre les profils épidémiologiques selon qu'il s'agit de cas MERS liés ou non à une éclosion, et les nouvelles données probantes sur l'efficacité des mesures de prévention et de contrôle des infections (PCI).
- De plus amples renseignements sur les sources de transmission zoonotique et secondaire sont fournis.
Résumé
- Le risque pour la santé publique que pose le MERS-CoV au Canada reste faible.
- À ce jour, aucun cas de MERS n'a été signalé au Canada.
- En date du 30 octobre 2018, 2 266 cas, dont 804 ont conduit à un décès (taux de létalité ~ 35 %) ont été signalés par 27 pays depuis l'émergence du virus en 2012, avec environ 80 % des cas signalés par le Royaume d'Arabie saoudite.
- L'infection est associée à une exposition à des dromadaires infectés ou à un contact avec des personnes infectées, le plus souvent en milieu de soins.
- La menace la plus probable pour la population canadienne demeure le risque d'importation au Canada par des voyageurs infectés au Moyen-Orient.
Évaluation du risque
Pour l'instant, le risque pour la santé publique au Canada associé au MERS-CoV est considéré comme faible selon les renseignements disponibles. Le risque peut évoluer à mesure que de nouveaux renseignements surviennent.
Le MERS-CoV est considéré comme un virus zoonotique, car son transmission à l'humain serait associée à un contact direct ou indirect avec des chameaux ou des produits de chameaux. Les données actuelles suggèrent que les chameaux sont l'hôte réservoir du MERS-CoV et la source animale de l'infection humaine par le MERS-CoV. Cependant, il existe également des preuves de transmission interhumaine puisque des grappes de cas de MERS ont été signalées chez des personnes ayant eu des contacts étroits avec des personnes infectées et dans les milieux de soins. Bien qu'aucune transmission interhumaine n'ait été observée dans les collectivités, une transmission interhumaine a été observée dans des ménages des pays touchés. La plupart des cas humains de MERS-CoV signalés à ce jour sont le résultat d'une transmission interhumaine en milieu de soins.
Les infections par le MERS-CoV se produisent en grande partie dans la péninsule arabique. La menace la plus probable pour la population canadienne demeure le risque d'importation au Canada par des voyageurs infectés au Moyen-Orient. Aucun cas de MERS n'a encore été signalé au Canada.
Résumé de la situation
Depuis janvier 2018, le nombre de cas d'infection par le MERS est demeuré relativement stable avec 20 cas ou moins signalés chaque mois. Entre le 1er janvier et le 30 octobre 2018, 137 cas de MERS ont été signalés, dont 42 ont conduit à un décès (taux de létalité = 31 %)(World Health Organization [WHO] Regional Office for the Eastern Mediterranean, 2018a).
La répartition par âge et par sexe des cas signalés entre janvier et le 30 octobre 2018 est demeurée relativement stable par rapport aux années précédentes : 82 % d'hommes dont l'âge médian était de 57 ans (de 2013 à 2017, les chiffres variaient entre 62 % et 82 % d'hommes âgés entre 47 ans et 55 ans) (World Health Organization [WHO] Regional Office for the Eastern Mediterranean, 2018a). À la dernière mise à jour, la proportion des cas signalant une exposition à un cas d'infection par le MERS était de 59 %. Ceci est attribuable aux éclosions nosocomiales signalées en juin 2017. Depuis, parmi les cas pour lesquels des antécédents d'exposition à des chameaux ont été signalés (n = 122), la proportion des cas signalant une exposition à des chameaux avant l'apparition des symptômes a été de 64 %.
Depuis janvier 2018, seuls six pays (Arabie saoudite, Malaisie, Oman, Émirats arabes unis, Royaume-Uni de Grande-Bretagne et d'Irlande du Nord et République de Corée) ont signalés des cas de MERS, soit une répartition moins vaste qu'à la même période au cours des années précédentes (total de 5 à 14 pays entre 2013 et 2017).
À l'échelle mondiale, depuis avril 2012, 2 266 cas de MERS ont été signalés (figure 1), dont au moins 804 ont conduit au décès (taux de létalité d'environ 35 %) (World Health Organization [WHO], 2018b). C'est en 2014 que le plus grand nombre de cas a été déclaré (n = 758 cas) (World Health Organization [WHO] Regional Office for the Eastern Mediterranean, 2018b). Depuis 2014, le nombre de cas signalés annuellement a diminué, passant de 672 cas déclarés en 2015 à 250 en 2017 (World Health Organization [WHO] Regional Office for the Eastern Mediterranean, 2018b). Le nombre de cas d'infection par le MERS-CoV dans le monde sous-estime probablement le fardeau réel de la maladie, puisque les systèmes de surveillance sont souvent incapables de recenser les cas bénins et asymptomatiques. Pour les dernières mises à jour sur les cas et les décès, veuillez consulter le site Web de l'OMS sur le MERS-CoV (en anglais uniquement).
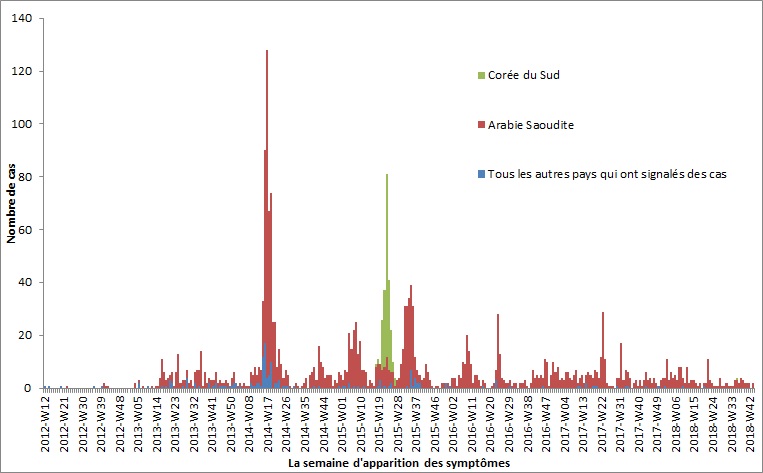
Figure 1 - Description textuel
À l'échelle mondiale, depuis avril 2012, 2 266 cas de MERS ont été signalés (figure 1), dont au moins 804 ont conduit au décès (taux de létalité d'environ 35 %). C'est en 2014 que le plus grand nombre de cas a été déclaré (n = 758 cas). Depuis 2014, le nombre de cas signalés annuellement a diminué, passant de 672 cas déclarés en 2015 à 250 en 2017.
Remarque : La courbe épidémiologique a été préparée à l'aide des données compilées par le Réseau mondial d'information en santé publique (RMISP) de l'Agence de la santé publique du Canada et le bulletin sur les flambées épidémiques de l'Organisation mondiale de la Santé (n = 2125). Cette figure exclut 132 cas signalés par l'OMS entre 2012-2017 et les cas dont la semaine de l'apparition des symptômes ou la date du signalement n'ont pas été signalées ou font l'objet d'une enquête.
Géographiquement, 27 pays d'Amérique du Nord, d'Europe, du Moyen-Orient, d'Afrique du Nord et d'Asie ont signalé des cas importés et des cas de MERS contractés localement, dont la majorité (environ 83 %) provenait de l'Arabie saoudite (figure 2) (World Health Organization [WHO], 2018a). À ce jour, le plus grand nombre de cas ayant été déclarés à l'extérieur du Moyen-Orient concernent la Corée du Sud (en 2015) : la majorité des 186 cas signalés étaient associés à une grande éclosion dans plusieurs hôpitaux (Normile, 2015).
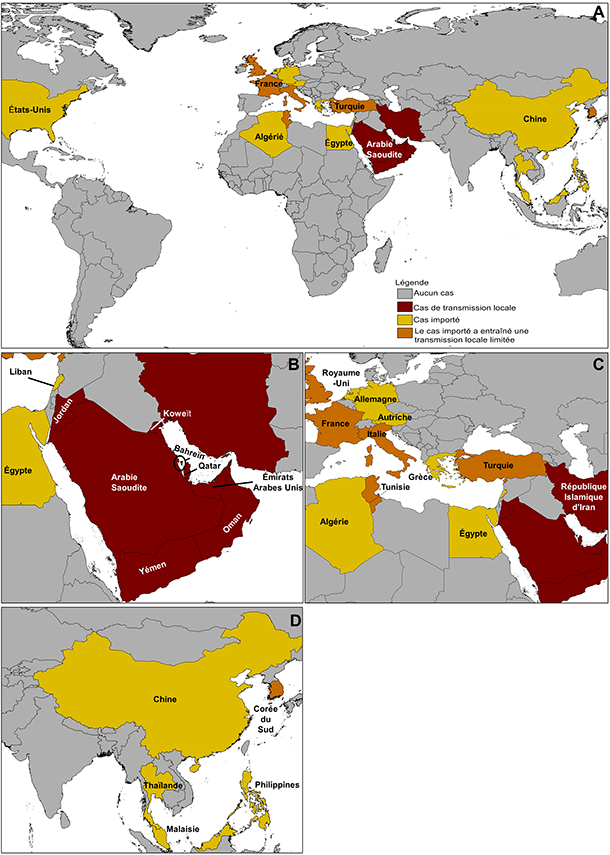
Figure 2 - Description textuel
Géographiquement, 27 pays d'Amérique du Nord, d'Europe, du Moyen-Orient et d'Asie ont signalé des cas importés et des cas de MERS contractés localement, dont la majorité (environ 80 %) provenait de l'Arabie saoudite.
Remarque : La carte a été préparée à l'aide des renseignements compilés par l'Organisation mondiale de la santé.
Sommaire de la littérature
Le syndrome respiratoire du Moyen-Orient (MERS) est une maladie respiratoire virale causée par un Bêta-coronavirus de lignée C ayant émergé dans la population humaine en 2012. Depuis 2012, l'OMS a signalé 2266 cas humains confirmés, dont plus de 804 ont mené au décès de la personne infectée. Les profils épidémiologiques du MERS reflètent les infections zoonotiques sporadiques ayant une transmission amplifiée d'humain à humain dans les milieux de soins de santé. Les éclosions de grande envergure du MERS résultent principalement de transmissions nosocomiales dans les établissements de soins de santé en raison de lacunes dans les mesures de prévention et de contrôle des infections. Certaines de ces éclosions d'envergure ont mené à une transmission limitée au sein de la collectivité dans les ménages; cependant, aucune transmission soutenue d'humain à humain n'a été observée.
L'infection humaine par le MERS-CoV présente un large éventail de tableaux cliniques, de l'infection asymptomatique à des cas cliniques d'infections aiguës sévères (Fehr, Channappanavar, & Perlman, 2017). Parmi les symptômes cliniques communs, on compte la fièvre, la toux et l'essoufflement, lesquels peuvent évoluer en pneumonie aiguë, en syndrome de détresse respiratoire aiguë (SDRA), en arrêt du fonctionnement de multiples organes et entraîner le décès. Des cas symptomatiques et bénins ont également été signalés (Arabi Y.M. et al., 2017; Fehr et al., 2017). Les cas graves sont souvent observés chez les patients âgés ou les personnes atteintes de maladies comorbides (Alhamlan et al., 2017).
La répartition des cas dans le temps est caractérisée par l'introduction des cas primaires zoonotiques suivis d'une augmentation du nombre de cas secondaires, résultats d'éclosions nosocomiales et de lacunes dans les mesures de prévention et de contrôle des infections (PCI). L'analyse de la répartition dans le temps des cas de MERS entre 2012 et 2014 a suggéré une tendance saisonnière qui augmente de mars à avril chaque année. À l'époque, les spécialistes avaient lié cette tendance saisonnière au vêlage et au sevrage des dromadaires. Toutefois, cette tendance n'a pas été invariablement observée d'année en année depuis 2014 (Hemida et al., 2017).
Différents profils d'âge et de sexe sont observés parmi les cas primaires et secondaires. Les cas primaires (cas sans antécédents de contact avec un cas de MERS) sont principalement observés chez les hommes plus âgés : le risque le plus élevé de contracter une infection concerne le groupe d'âge de 50 à 59 ans (Gossner et al., 2016; World Health Organization [WHO] Regional Office for the Eastern Mediterranean, 2017b). On a associé cette tendance à l'élevage de dromadaires, activité populaire parmi les hommes d'âge moyen et à la retraite (Gossner et al., 2016). Les cas secondaires (cas sans antécédents de contact avec un cas de MERS) sont principalement observés chez les groupes plus jeunes avec une répartition égale entre les sexes. Les personnes de 30 à 39 ans sont les plus à risque de contracter l'infection (Gossner et al., 2016; World Health Organization [WHO] Regional Office for the Eastern Mediterranean, 2017b).
Plus de 80 % des cas ont été signalés dans la péninsule arabique. Cette répartition géographique a été associée à la forte densité de dromadaires dans cette région (Gossner et al., 2016; Hemida et al., 2017). De plus amples renseignements sur la répartition géographique de l'infection par le MERS-CoV chez le dromadaire peuvent être consultés sur le site Web de l'Organisation des Nations Unies pour l'alimentation et l'agriculture (en anglais seulement).
Source de transmission zoonotique
Les recherches menées à ce jour laissent entendre que le MERS-CoV vient des chauves-souris (Sharif-Yakan & Kanj, 2014). Le séquençage génomique et l'analyse phylogénique des chauves-souris de l'Arabie saoudite et de l'Afrique appuient cette théorie, puisque des similitudes ont été détectées entre les séquences du coronavirus des chauves-souris et le MERS-CoV (Ithete et al., 2013; Memish et al., 2013; Wang et al., 2014). De nombreuses études sur l'émergence et la transmission du MERS-CoV semblent indiquer le rôle des chameaux comme un réservoir et une source principale d'infection zoonotique en raison de (1) la forte prévalence d'anticorps du MERS-CoV chez les chameaux dans la péninsule arabique, l'Afrique du Nord et l'Afrique orientale; (2) la détection du MERS-CoV par l'entremise de la technique de transcription inverse suivie d'une réaction en chaîne de la polymérase (RT-PCR) dans les sécrétions respiratoires, les excréments et le lait des dromadaires; et (3) les similitudes dans la séquence génomique des virus isolés chez les personnes infectées et les chameaux (Omrani, Al-Tawfiq, & Memish, 2015). Tout porte à croire que le MERS-CoV a été détecté chez les chameaux depuis plus de 20 ans (depuis au moins 1992) (Alagaili et al., 2014; Corman et al., 2014). Des études de vérification menées chez les chameaux laissent entendre que le MERS est une infection respiratoire légère entraînant peu ou pas de signe de maladie (Adney et al., 2014). Selon les études séro-épidémiologiques réalisées sur d'autres animaux d'élevage, les alpagas sont les seuls autres animaux d'élevage chez lesquels des anticorps propres au MERS-CoV ont été cernés; toutefois, aucun cas humain avec une exposition aux alpagas n'a été signalé à ce jour (Reusken et al., 2016).
Bien que la voie de transmission des chameaux aux humains ne soit pas entièrement comprise, il est probable que les infections zoonotiques causées par le MERS-CoV sont le résultat d'un contact direct ou indirect avec des chameaux infectés ou des produits dérivés de chameaux infectés (p. ex. le lait cru) (Gossner et al., 2016). La détection de l'ARN de MERS-CoV dans le lait de chamelle suggère une possible transmission du virus d'origine alimentaire par la consommation de lait cru (Reusken et al., 2014).
Les études épidémiologiques montrent un plus grand risque d'infection par le MERS-CoV chez les personnes exposées à des chameaux, comparativement à la population en général (Muller M.A. et al., 2015; World Health Organization [WHO], 2015b). À ce jour, les infections humains de source zoonotiques ont seulement été signalées dans des pays de la péninsule arabique où la prévalence du virus est élevée et où il est répandu au sein de la population de chameaux. D'autres études doivent être menées afin de bien comprendre le rôle que l'interaction entre les humains et les animaux joue dans la transmission de cette maladie.
Source de transmission secondaire
La transmission secondaire du MERS-CoV a été largement associée aux éclosions nosocomiales; cependant, des grappes familiales ont également été signalées (Abroug et al., 2014; Memish, Zumla, Al-Hakeem, Al-Rabeeah, & Stephens, 2013). Les éclosions nosocomiales du MERS ont joué un rôle important dans l'accroissement de l'ampleur des cas signalés. À ce jour, des éclosions en milieu hospitalier à grande échelle ont été signalées en Arabie saoudite et en Corée du Sud. Le manque de prévention et de contrôle des infections (PCI) (p. ex. le surpeuplement, l'isolation tardive des cas, et le manque de connaissances sur les définitions de cas de MERS parmi les travailleurs de la santé), de même que la transmission dans les hôpitaux et entre les hôpitaux, les propagateurs de virus extrêmement efficaces et les contacts avec les personnes asymptomatiques, sont quelques-uns des facteurs qui ont contribué à ces éclosions en milieu hospitalier (Al-Tawfiq & Perl, 2015). Il a été démontré que l'observance stricte des mesures de PCI peut donner lieu à la détection rapide des cas et à une réduction importante du nombre de cas secondaires dans les éclosions nosocomiales, et qu'elle permet la détection précoce de nouveaux cas (El Bushra et al., 2017).
Une éclosion en Corée du Sud, qui a débuté en mai 2015, est la plus grande éclosion nosocomiale du MERS à l'extérieur du Moyen-Orient. Un individu ayant voyagé dans quatre pays du Moyen-Orient, qui était propagateurs de virus extrêmement efficace, serait à l'origine de cette éclosion (Kim et al., 2017). Ce dernier aurait infecté ses proches parents, des patients avec qui il a partagé une chambre d'hôpital, ainsi que des travailleurs de la santé qui lui ont fourni des soins à son retour en Corée du Sud. Ces expositions ont eu lieu avant que l'on soupçonne un cas de MERS-CoV et que l'on pose le diagnostic. L'éclosion en Corée du Sud a été déclarée terminée le 23 décembre 2015 (Normile, 2015). Les données actuelles tirées d'études sur la recherche des contacts suggèrent que la transmission s'est limitée aux contacts étroits dans la communauté (Memish, Zumla, & Assiri, 2013).
Vaccins contre le MERS-CoV
Il n'existe aucun vaccin ou traitement antiviral efficace pour le MERS-CoV. Toutefois, des recherches sont en cours, et de nombreux vaccins expérimentaux ciblés pour les humains sont en cours d'élaboration. Ces vaccins expérimentaux utilisent un large éventail de plateformes, y compris les vaccins à virus entier (vivants et atténués, et inactivés), les vaccins à virus vectorisés, les vaccins à ADN, et les vaccins à base de protéines (Okba, Raj, & Haagmans, 2017). Jusqu'à présent, un seul vaccin expérimental est passé à l'élaboration clinique : un vaccin à ADN ayant démontré qu'il peut générer des anticorps protecteurs contre le MERS-CoV chez les souris, les chameaux et les singes est passé à la phase 1 des essais cliniques humains en février 2016 (Modjarrad, 2016). Ce vaccin expérimental a également été testé chez les dromadaires. En outre, un essai d'innocuité de phase 1 pour un vaccin constitué du virus modifié de la vaccine d'Ankara ayant réduit l'élimination du virus et ayant généré des anticorps protecteurs et une immunité dans les muqueuses est actuellement prévu (Alharbi, 2017).
Caractéristiques du virus
Le MERS-CoV est un virus enveloppé et un virus à ARN monocaténaire appartenant à la famille des Coronaviridae (Fehr et al., 2017). Bien qu'il soit causé par le même genre de coronavirus que le syndrome respiratoire aigu sévère (SRAS) [de genre Bêta-coronavirus], le MERS-CoV se distingue par le fait qu'il appartient à la lignée C, tandis que le SRAS appartient à la lignée B (Arabi Y.M. et al., 2017). L'entrée du MERS-CoV dans les cellules hôtes est médiée par ses protéines de spicule (S), lesquelles sont liées au récepteur cellulaire hôte, soit la dipeptidyl peptidase-4 (DPP-4) (Fehr et al., 2017). Dans le cas du SRAS, de vastes mutations ont permises au virus de s'adapter au récepteur cellulaire humain, soit l'enzyme de conversion de l'angiotensine 2 (ECA2) ce qui a permis une augmentation de la transmission interhumaine (Chinese SARS Molecular Epidemiology Consortium, 2004). Bien que des isolats de virus provenant de chameaux et d'humains ont été séquencés et ont démontrés que le MERS-CoV a fait l'objet d'une recombinaison et de changements génétiques depuis son introduction dans la population humaine en 2012 (Sabir et al., 2016), aucun de ces changements n'a permis une adaptation à la récepteur cellulaire humain DPP-4 plus efficace. En fait, l'analyse des isolats viraux de l'éclosion en Corée du Sud ayant une mutation dans le domaine de liaison au récepteur a démontré une affinité réduite à la DPP-4 humaine (Kim et al., 2016). Étant donné l'ampleur de l'éclosion en Corée du Sud, ces résultats compliquent davantage le rôle que jouent la protéine S et la DPP-4 dans l'adaptation humaine de ce virus.
Recommandations pour le Canada
Surveillance
On encourage les professionnels de la santé à maintenir la vigilance à l'égard des cas d'infection par le MERS-CoV, et à aviser les ministères de la Santé publique concernés lorsqu'une personne fait l'objet d'une enquête diagnostique. La définition nationale de cas pour le MERS-CoV doit être utilisée dans le cadre de la surveillance du MERS-CoV. Pour obtenir des conseils quant aux objectifs et aux activités de surveillance, veuillez vous reporter aux Lignes directrices nationales sur la surveillance des cas d'infection par le coronavirus du syndrome respiratoire du Moyen-Orient (MERS-CoV).
On demande aux provinces et aux territoires de signaler les cas confirmés d'infection par le MERS-CoV à l'Agence de la santé publique du Canada au moyen du Formulaire de déclaration des cas d'agents pathogènes respiratoires émergents et les infections respiratoires aiguës sévères (IRAS).
Laboratoire
Les analyses en laboratoire doivent être réalisées conformément au Protocole d'enquête microbiologique concernant les infections respiratoires aiguës sévères (IRAS) du Réseau des laboratoires de santé publique du Canada. Veuillez vous conformer aux lignes directrices en matière de prévention et de contrôle des infections lors de la collecte des échantillons des voies respiratoires. Soyez au courant des approches prises dans votre compétence.
Une confirmation en laboratoire est obtenue par détection du virus à l'aide (a) d'un test d'amplification des acides nucléiques (TAAN) propre au MERS-CoV, avec, au maximum, deux cibles distinctes ou séquençages; (b) d'une isolation du virus dans une culture de tissusNote de bas de page 1; (c) ou d'analyses sérologiques menées à partir de sérum testé dans un Centre collaborateur de l'Organisation mondiale de la santé (OMS) dont les méthodes d'analyses sont bien établies. Les premiers tests de dépistage du MERS-CoV peuvent être effectués dans certains laboratoires (c.-à-d. principalement les laboratoires provinciaux de santé publique); cependant, ces cas sont considérés comme des cas probables en attente de la confirmation par le Laboratoire national de microbiologie (LNM). Les laboratoires dont des échantillons se sont révélés positifs (MERS-CoV) doivent acheminer ces échantillons à leur laboratoire de santé publique local. Ce dernier organisera alors les tests de confirmation au LNM.
Pour obtenir de plus amples renseignements, veuillez vous reporter aux Lignes directrices nationales provisoires sur la surveillance des cas d'infection par le coronavirus du syndrome respiratoire du Moyen-Orient (MERS-CoV).
L'OMS a publié des recommandations provisoires pour les analyses en laboratoire du MERS-CoV (septembre 2014).
Conseils de santé aux voyageurs
L'Agence publie des conseils de santé aux voyageurs expliquant aux voyageurs et au public canadien les risques potentiels, et elle recommande des mesures à adopter pour réduire ces risques. Les conseils de santé aux voyageurs relatifs au MERS-CoV sont publiés sur le site Web du Gouvernement du Canada.
Prévention des infections
Aucun vaccin ni traitement prophylactique n'est disponible pour prévenir l'infection par le MERS-CoV. On rappelle aux établissements de soins de santé qu'il est important de mettre en œuvre systématiquement des mesures de prévention et de contrôle des infections visant à réduire le risque d'exposition et de transmission au sein d'établissement de soins de santé. Les établissements de soins de santé qui recevront des patients atteints d'une infection par le MERS-CoV présumée ou confirmée doivent prendre les mesures appropriées pour diminuer le risque de transmission du virus à d'autres patients, aux travailleurs de la santé ou aux visiteurs. Le site Web de l'Agence de la santé publique du Canada affiche les recommandations quant aux mesures de prévention et de contrôle des infections à prendre pour tout patient présentant une infection présumée ou confirmée par le MERS-CoV dans un établissement de soins actifs. Ces lignes directrices sont mises à jour à mesure que de nouveaux renseignements deviennent disponibles.
Comme il n'existe actuellement aucun vaccin pour prévenir l'infection par le MERS-CoV, pour se protéger des maladies respiratoires en voyageant au Moyen-Orient et en Asie du Sud-Est, on recommande aux Canadiens de se laver les mains fréquemment, d'éviter le contact avec les personnes à risque et de se toucher les yeux et le nez avec les mains non lavées, et de désinfecter les surfaces fréquemment touchées.
Biosécurité
Le MERS-CoV est classé comme un anthropopathogène du groupe de risque 3, c'est-à-dire que ce virus peut entraîner une maladie grave chez l'humain. Il y a un faible risque pour la santé publique puisque les probabilités de transmission du virus dans la communauté semblent faibles. Le niveau de confinement 3 est requis pour tous les travaux prolifératifs (in vitro ou in vivo). Les activités de diagnostic non-propagative peuvent être effectuées au niveau de confinement 2 en suivant les procédures opérationnelles additionnelles décrites dans l'Avis de biosécurité : Coronavirus du syndrome respiratoire du Moyen-Orient (MERS-CoV).
References
Disponibles en anglais seulement
- Abroug, F., Slim, A., Ouanes-Besbes, L., Hadj Kacem, M. A., Dachraoui, F., Ouanes, I., et al. (2014). Family cluster of Middle East Respiratory Syndrome coronavirus infections, Tunisia, 2013. Emerging Infectious Diseases, 20(9), 1527-1530. doi:10.3201/eid2009.140378 [doi]
- Adney, D. R., van Doremalen, N., Brown, V. R., Bushmaker, T., Scott, D., de Wit, E., et al. (2014). Replication and shedding of MERS-CoV in upper respiratory tract of inoculated dromedary camels. Emerging Infectious Diseases, 20(12), 1999-2005. doi:10.3201/eid2012.141280 [doi]
- Alagaili, A. N., Briese, T., Mishra, N., Kapoor, V., Sameroff, S. C., Burbelo, P. D., et al. (2014). Middle East Respiratory Syndrome coronavirus infection in dromedary camels in Saudi Arabia. MBio, 5(2), e00884-14. doi:10.1128/mBio.00884-14 [doi]
- Alhamlan, F. S., Majumder, M. S., Brownstein, J. S., Hawkins, J., Al-Abdely, H. M., Alzahrani, A., et al. (2017). Case characteristics among Middle East Respiratory Syndrome coronavirus outbreak and non-outbreak cases in Saudi Arabia from 2012 to 2015. BMJ Open, 7(1), e011865-2016-011865. doi:10.1136/bmjopen-2016-011865 [doi]
- Alharbi, N. K. (2017). Vaccines against Middle East Respiratory Syndrome coronavirus for humans and camels. Reviews in Medical Virology, 27(2), 10.1002/rmv.1917. Epub 2016 Oct 27. doi:10.1002/rmv.1917 [doi]
- Al-Tawfiq, J. A., & Perl, T. M. (2015). Middle East Respiratory Syndrome coronavirus in healthcare settings. Current Opinion in Infectious Diseases, 28(4), 392-396. doi:10.1097/QCO.0000000000000178 [doi]
- Arabi Y.M., Balkhy H.H., Hayden F.G., Bouchama A., Luke T., Baillie J.K., et al. (2017). Middle East Respiratory Syndrome. New England Journal of Medicine, 376(6), 584-594.
- Chinese SARS Molecular Epidemiology Consortium. (2004). Molecular evolution of the SARS coronavirus during the course of the SARS epidemic in China. Science (New York, N.Y.), 303(5664), 1666-1669. doi:10.1126/science.1092002 [doi]
- Corman, V. M., Jores, J., Meyer, B., Younan, M., Liljander, A., Said, M. Y., et al. (2014). Antibodies against MERS coronavirus in dromedary camels, Kenya, 1992-2013. Emerging Infectious Diseases, 20(8), 1319-1322.
- El Bushra, H. E., Al Arbash, H. A., Mohammed, M., Abdalla, O., Abdallah, M. N., Al-Mayahi, Z. K., et al. (2017). Outcome of strict implementation of infection prevention control measures during an outbreak of Middle East Respiratory Syndrome. American Journal of Infection Control, 45(5), 502-507. doi:S0196-6553(17)30003-2 [pii]
- Fehr, A. R., Channappanavar, R., & Perlman, S. (2017). Middle East Respiratory Syndrome: Emergence of a pathogenic human coronavirus. Annual Review of Medicine, 68, 387-399. doi:10.1146/annurev-med-051215-031152 [doi]
- Gossner, C., Danielson, N., Gervelmeyer, A., Berthe, F., Faye, B., Kaasik Aaslav, K., et al. (2016). Human-dromedary camel interactions and the risk of acquiring zoonotic Middle East Respiratory Syndrome coronavirus infection. Zoonoses and Public Health, 63(1), 1-9. doi:10.1111/zph.12171 [doi]
- Hemida, M. G., Elmoslemany, A., Al-Hizab, F., Alnaeem, A., Almathen, F., Faye, B., et al. (2017). Dromedary camels and the transmission of Middle East Respiratory Syndrome coronavirus (MERS-CoV). Transboundary and Emerging Diseases, 64(2), 344-353. doi:10.1111/tbed.12401 [doi]
- Ithete, N. L., Stoffberg, S., Corman, V. M., Cottontail, V. M., Richards, L. R., Schoeman, M. C., et al. (2013). Close relative of human Middle East Respiratory Syndrome coronavirus in bat, South Africa. Emerging Infectious Diseases, 19(10), 1697-1699. doi:10.3201/eid1910.130946 [doi]
- Kim,K.H., Tandi, T.E., Choi, J.W., Moon, J.M., & M.S. Kim (2017). Middle East respiratory syndrome coronavirus (MERS-CoV) outbreak in South Korea, 2015: epidemiology, characteristics and public health implications. Journal of Hospital Infection, 95:207-213. doi:10.1016/j.jhin.2016.10.008 [doi]
- Kim, Y., Cheon, S., Min, C. K., Sohn, K. M., Kang, Y. J., Cha, Y. J., et al. (2016). Spread of mutant Middle East Respiratory Syndrome coronavirus with reduced affinity to human CD26 during the South Korean outbreak. MBio, 7(2), e00019-16. doi:10.1128/mBio.00019-16 [doi]
- Memish, Z. A., Mishra, N., Olival, K. J., Fagbo, S. F., Kapoor, V., Epstein, J. H., et al. (2013). Middle East Respiratory Syndrome coronavirus in bats, Saudi Arabia. Emerging Infectious Diseases, 19(11), 1819-1823. doi:10.3201/eid1911.131172 [doi]
- Memish, Z. A., Zumla, A. I., Al-Hakeem, R. F., Al-Rabeeah, A. A., & Stephens, G. M. (2013). Family cluster of Middle East Respiratory Syndrome coronavirus infections. The New England Journal of Medicine, 368(26), 2487-2494. doi:10.1056/NEJMoa1303729 [doi]
- Memish, Z.A., Zumla, Al., Assiri, A. (2013). Middle East respiratory syndrome coronavirus infections in health care workers. The New England Journal of Medicine, 369(9): 884-886. doi: 10.1056/NEJMc1308698
- Modjarrad, K. (2016). MERS-CoV vaccine candidates in development: The current landscape. Vaccine, 34(26), 2982-2987. doi:10.1016/j.vaccine.2016.03.104 [doi]
- Muller M.A., Meyer B., Corman V.M., AlMasri M., Turkestani A., Ritz D., et al. (2015). Presence of Middle East Respiratory Syndrome coronavirus antibodies in saudi arabia: A nationwide, cross-sectional, serological study. The Lancet Infectious Diseases, 15(5), 559-564.
- Normile, D. (2015, December 23 2015). South Korea finally MERS-free.Science Magazine, Okba, N. M., Raj, V. S., & Haagmans, B. L. (2017). Middle East Respiratory Syndrome coronavirus vaccines: Current status and novel approaches. Current Opinion in Virology, 23, 49-58. doi:S1879-6257(16)30148-1 [pii]
- Omrani, A. S., Al-Tawfiq, J. A., & Memish, Z. A. (2015). Middle East Respiratory Syndrome coronavirus (MERS-CoV): Animal to human interaction. Pathogens and Global Health, 109(8), 354-362. doi:10.1080/20477724.2015.1122852 [doi]
- Reusken, C.B., Farag, E.A., Jonges, M., Godeke, G.J., El-Sayed, A.M., Pas, S.D., et al. (2014). Middle East respiratory syndrome coronavirus (MERS-CoV) RNA and neutralising antibodies in milk collected according to local customs from dromedary camels, Qatar, April 2014. Eurosurveillance, 19(23)
- Reusken, C. B., Schilp, C., Raj, V. S., De Bruin, E., Kohl, R. H., Farag, E. A., et al. (2016). MERS-CoV infection of alpaca in a region where MERS-CoV is endemic. Emerging Infectious Diseases, 22(6), 1129-1131. doi:10.3201/eid2206.152113 [doi]
- Sabir, J. S., Lam, T. T., Ahmed, M. M., Li, L., Shen, Y., Abo-Aba, S. E., et al. (2016). Co-circulation of three camel coronavirus species and recombination of MERS-CoVs in saudi arabia. Science (New York, N.Y.), 351(6268), 81-84. doi:10.1126/science.aac8608 [doi]
- Sharif-Yakan, A., & Kanj, S. S. (2014). Emergence of MERS-CoV in the Middle East: Origins, transmission, treatment, and perspectives. PLoS pathogens, PLoS, 10(12)
- Wang, Q., Qi, J., Yuan, Y., Xuan, Y., Han, P., Wan, Y., et al. (2014). Bat origins of MERS-CoV supported by bat coronavirus HKU4 usage of human receptor CD26. Cell Host & Microbe, 16(3), 328-337. doi:10.1016/j.chom.2014.08.009 [doi]
- World Health Organization [WHO]. (2015a). Media centre: WHO statement on the tenth meeting of the IHR emergency committee regarding MERS. Retrieved April 1, 2017.
- World Health Organization [WHO]. (2015b). Summary of current situation, literature update and risk assessment: July 7, 2015. Retrieved April 25, 2017
- World Health Organization [WHO]. (2018a). Coronavirus infections: Disease outbreak news. Retrieved November 22, 2018.
- World Health Organization [WHO]. (2018b). Middle East Respiratory Syndrome coronavirus (MERS-CoV). Retrieved November 15, 2018.
- World Health Organization [WHO] Regional Office for the Eastern Mediterranean. (2018a). MERS situation update, October 2018. Retrieved November 15, 2018.
- World Health Organization [WHO] Regional Office for the Eastern Mediterranean. (2017b). MERS situation update, january-february 2017. Retrieved May 15, 2017.