Ligne directrice canadienne sur la biosécurité : Gestion du programme de biosécurité

Téléchargez en format PDF
(Format PDF, 6,14 Mo, 77 pages)
Organisation : Agence de la santé publique du Canada
Cat. : HP45-33/2023F-PDF
ISBN : 978-0-660-47919-4
Pub. : 220806
Date Publiée : 2023-03-31
Table des matières
- Préface
- Abréviations et sigles
- 1. Introduction
- 2. Planifier un programme de biosécurité
- 3. Mettre en œuvre le programme de biosécurité
- 4. Amélioration continue du programme de biosécurité
- 5. Glossaire
- 6. Références
Préface
Au Canada, la manipulation ou l'entreposage des agents pathogènes humains et des toxines de groupe de risque 2 (GR2), GR3 et GR4 est réglementé par l'Agence de la santé publique du Canada (ASPC) en vertu de la Loi sur les agents pathogènes humains et les toxines (LAPHT) et du Règlement sur les agents pathogènes humains et les toxines (RAPHT). En vertu de la Loi sur la santé des animaux (LSA) et du Règlement sur la santé des animaux (RSA), l'ASPC et l'Agence canadienne d'inspection des aliments (ACIA) réglementent l'importation d'agents zoopathogènes ou d'une partie de ceux-ci (p. ex. une toxine), d'animaux exposés de manière naturelle ou expérimentale à un agent zoopathogène ou à une partie de celui-ci (p. ex. une toxine), ainsi que des produits ou sous-produits animaux (p. ex. des tissus, du sérum) ou d'autres organismes porteurs d'un agent zoopathogène ou d'une partie de celui-ci (p. ex. une toxine).
La figure suivante illustre la hiérarchie des documents qu'utilisent l'ASPC et l'ACIA pour surveiller les activités de biosécurité et de biosûreté. Chaque niveau de la pyramide correspond à un type de document. Les documents sont placés en ordre de priorité du haut de la pyramide vers le bas. Les lois et les règlements se trouvent au sommet de la pyramide, car ce sont ces documents qui confèrent à l'ASPC et à l'ACIA leur autorité légale. Le matériel d'orientation et les éléments techniques se trouvent au bas de la pyramide, car ils sont uniquement destinés à résumer les recommandations et les connaissances scientifiques.
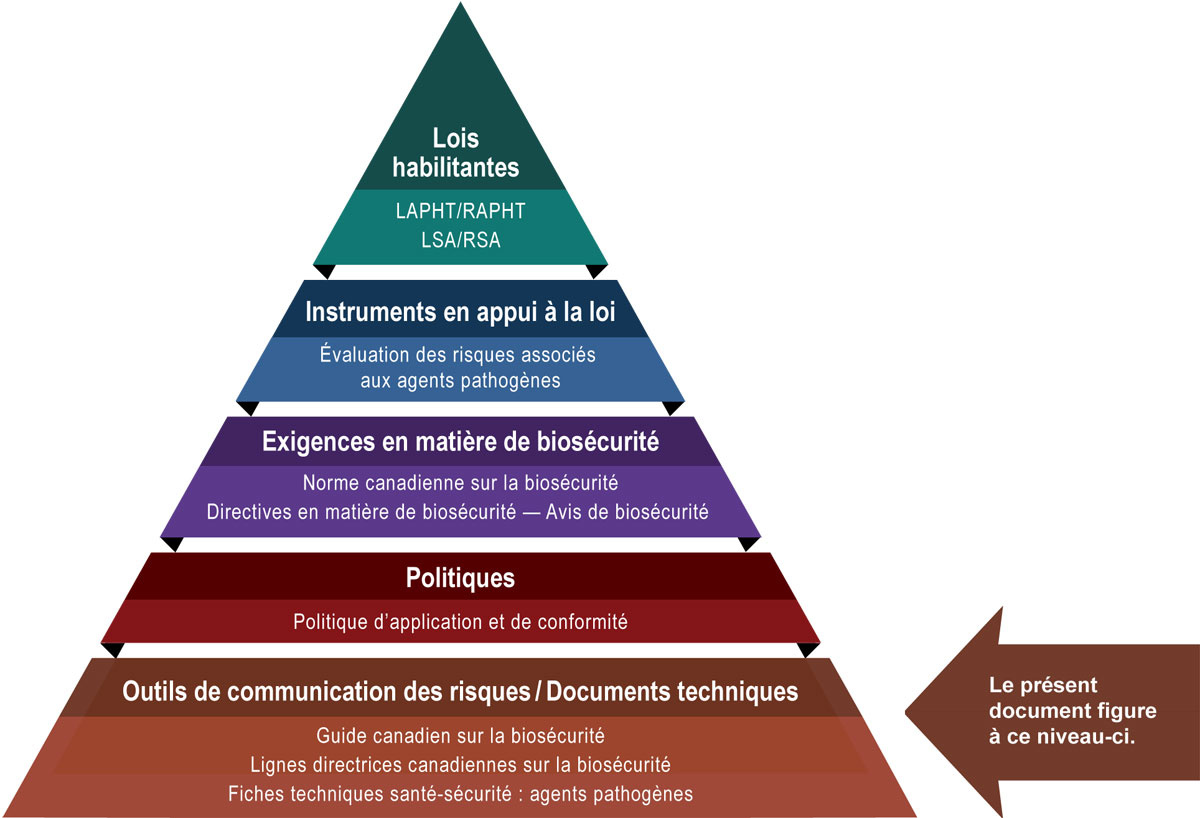
Figure 1 - Texte descriptif
Figure sous la forme d'une pyramide représentant la hiérarchie des documents utilisés par l'ASPC pour superviser les opérations de biosécurité et de biosûreté. Chacun des cinq niveaux de la pyramide correspond à un type de document, dont l'ordre de préséance augmente du bas vers le haut.
Au sommet se trouve la législation habilitante, c'est-à-dire la LAPHT, le RAPHT, la LSA et le RSA, qui transmet les autorités légales à l'ASPC. Au-dessous des lois et des règlements figurent les Instruments à l'appui de la législation, et ceux-ci sont les évaluations des risques associés aux agents pathogènes. La prochaine étape est intitulée les Exigences en matière de biosécurité, notamment la Norme canadienne sur la biosécurité, les Directives en matière de biosécurité et les Avis de biosécurité. Le deuxième niveau du bas est Documents de politique, soit la Politique de conformité et d'application de la loi. Le matériel d'orientation et les pièces techniques trouvés au bas de la pyramide, sous l'en-tête des Outils de communication des risques et documents techniques, visent seulement à résumer les recommandations et les informations scientifiques. Il s'agit notamment du Guide canadien sur la biosécurité, des Lignes directrices canadiennes sur la biosécurité et des Fiches techniques santé-sécurité : agents pathogènes.
La ligne directrice Gestion du programme de biosécurité a été élaborée par l'ASPC et l'ACIA dans le cadre d'une série de publications électroniques visant à approfondir les concepts de biosécurité et de biosûreté abordés dans l'édition actuelle du Guide canadien sur la biosécurité (GCB), qui constitue le document d'accompagnement de la Norme canadienne sur la biosécurité (NCB). La présente ligne directrice fournit des renseignements et des considérations qui pourraient aider à l'élaboration et la mise en œuvre des politiques et des procédures dont les organisations ont besoin pour protéger les membres de leur personnel, la communauté et l'environnement contre les agents pathogènes et les toxines qui sont manipulés et entreposés au sein de leurs installations. De telles politiques et procédures en matière de biosécurité comprennent celles qui sont nécessaires pour satisfaire aux exigences de la LAPHT, du RAPHT, de la LSA et du RSA, ainsi qu'aux exigences applicables énoncées dans la NCBNote de bas de page 1Note de bas de page 2. En adoptant une approche globale, les politiques et les procédures en matière de biosécurité peuvent être élargies de façon à aborder d'autres risques biologiques présents au sein d'une organisation, le cas échéant, comme des activités qui comportent des agents pathogènes d'animaux aquatiques, des phytoravageurs, des arthropodes et de nouveaux organismesNote de bas de page 3Note de bas de page 4Note de bas de page 5.
Abréviations et sigles
- ABCSE
- Agent biologique à cote de sécurité élevée
- ACIA
- Agence canadienne d'inspection des aliments
- ASB
- Agent de la sécurité biologique
- ASPC
- Agence de la santé publique du Canada
- CIB
- Comité institutionnel de biosécurité
- ELR
- Évaluation locale des risques
- EPI
- Équipement de protection individuel
- ESB
- Enceinte de sécurité biologique
- GCB
- Guide canadien sur la biosécurité
- GR
- Groupe de risque (c.-à-d. GR1, GR2, GR3, GR4)
- LAPHT
- Loi sur les agents pathogènes humains et les toxines
- LSA
- Loi sur la santé des animaux
- NC
- Niveau de confinement (c.-à-d. NC1, NC2, NC3, NC4)
- NCB
- Norme canadienne sur la biosécurité
- PFVA
- Planifier, Faire, Vérifier, Agir
- PON
- Procédure opératoire normalisée
- RAPHT
- Règlement sur les agents pathogènes humains et les toxines
- RSA
- Règlement sur la santé des animaux
1. Introduction
Les mots en caractères gras sont définis dans le glossaire à la section 5.
Un programme de biosécurité englobe toute une série de mesures visant à identifier et à quantifier les risques de biosécurité et de biosûreté associés aux matières réglementées qui sont manipulées et entreposées dans une installation, ainsi qu'à mettre en œuvre des mesures d'atténuation appropriées afin de réduire ces risques. Le programme de biosécurité peut également s'appliquer à d'autres matières biologiques, comme les microorganismes de groupe de risque 1 (GR1), les lignées cellulaires, les produits et les sous-produits animaux et les échantillons cliniques humains, lesquels peuvent être réglementés ou non. Ce système utilisé à l'échelle de l'organisation sert à créer et à maintenir un cadre de biosécurité qui s'intègre à la structure de gouvernance générale. Le programme de biosécurité peut être un système autonome ou être combiné à d'autres programmes (p. ex. la santé et la sécurité au travail, la sûreté) de façon à produire un programme complet de biosécurité, de santé, de sécurité et de sûreté au travail.
Les microorganismes sont classés dans l'un des quatre groupes de risque (c.-à-d. du GR1 au GR4) en fonction des résultats obtenus dans le cadre d'une évaluation des risques associés à l'agent pathogène. Celle-ci est effectuée afin d'évaluer les caractéristiques inhérentes à un organisme qui contribuent au risque que celui-ci présente pour une personne ou un animal, ainsi que la santé publique et la population animale. Les niveaux de confinement font référence aux exigences physiques en matière de confinement et aux exigences opérationnelles minimales qu'une zone de confinement (c.-à-d. un espace physique déterminé qui satisfait aux exigences d'un niveau de confinement donné) requiert pour la manipulation sécuritaire de matières réglementées. Il existe quatre niveaux de confinement, allant du niveau d'un laboratoire de base pour le travail effectué avec des matières biologiques (c.-à-d. le niveau de confinement 1 [NC1]) aux installations hautement sophistiquées pour le travail avec les agents pathogènes à plus haut risque (c.-à-d. le niveau de confinement 4 [NC4]). En général, le groupe de risque d'un agent pathogène est le même que le niveau de confinement auquel il doit être manipulé (c.-à-d. les agents pathogènes du GR2 sont habituellement manipulés au NC2); lorsque ce n'est pas le cas, l'Agence de santé publique du Canada (ASPC) et l'Agence canadienne d'inspection des aliments (ACIA) peuvent élaborer des directives en matière de biosécurité afin de clarifier les exigences en matière de confinementNote de bas de page 6.
Par ailleurs, les exigences peuvent varier selon le type d'espace de travail, y compris les espaces de travail en laboratoire, les aires de production à grande échelle, les espaces de travail avec des animaux et les espaces où des prions ou des agents biologiques à cote de sécurité élevée (ABCSE) sont manipulés.
Le niveau de complexité et de détail du programme de biosécurité varie selon la nature et la taille de l'organisation, les types d'agents pathogènes qui sont manipulés et les activités qui sont réalisées. Par exemple, une petite entreprise au sein de laquelle un seul agent pathogène à faible risque est manipulé dans une seule salle constituant un espace de travail en laboratoire de NC2 disposera d'un programme de biosécurité moins complexe qu'une grande entreprise ou une université dotée de plusieurs campus où sont effectuées des activités in vivo, de recherche et de diagnostic comportant des agents pathogènes présentant un niveau de risque allant de faible à élevé (c.-à-d. GR2, GR3, GR4). Peu importe la taille et la complexité de l'organisation, tous les éléments du programme de biosécurité s'appliquent, mais la manière dont ces éléments sont mis en œuvre peut varier d'une organisation à l'autre. Un programme de biosécurité efficace permet de promouvoir et de renforcer des pratiques de travail sécuritaires, d'améliorer la biosécurité de manière générale, d'accroître la conformité aux exigences réglementaires applicables et de favoriser une culture de biosécurité au sein de l'organisation.
Une gestion proactive est essentielle à la réussite d'un programme de biosécurité. Un processus normalisé de gestion de programme aide les organisations à identifier, évaluer, contrôler et surveiller de manière efficace les risques associés à la manipulation et l'entreposage d'agents pathogènes et de toxines. Cela diminue les risques d'incidents de biosécurité et de biosûreté et permet d'établir une intervention organisationnelle appropriée en cas d'incident. Au sein de l'organisation, la gestion efficace du programme de biosécurité peut améliorer la conformité, le rendement en matière de sécurité ainsi que l'efficacité. En dehors de l'organisation, la gestion du programme de biosécurité est essentielle pour protéger la communauté contre les agents pathogènes et les toxines qui sont manipulés et entreposés sur place.
La gestion efficace du programme de biosécurité peut être réalisée en suivant le cycle de gestion Planifier, Faire, Vérifier, Agir (PFVA)Note de bas de page 7Note de bas de page 8Note de bas de page 9.
La figure 1-1 démontre la façon dont le cycle PFVA peut être appliqué pour mettre en place et maintenir un programme de biosécurité : Planifier — identifier et évaluer les dangers et les risques de biosécurité et de biosûreté; Faire — mettre en œuvre et documenter les mesures d'atténuation; Vérifier — effectuer des activités de surveillance planifiées et adaptées du programme et de ses éléments; Agir — adapter et modifier les processus afin d'améliorer continuellement le programme.
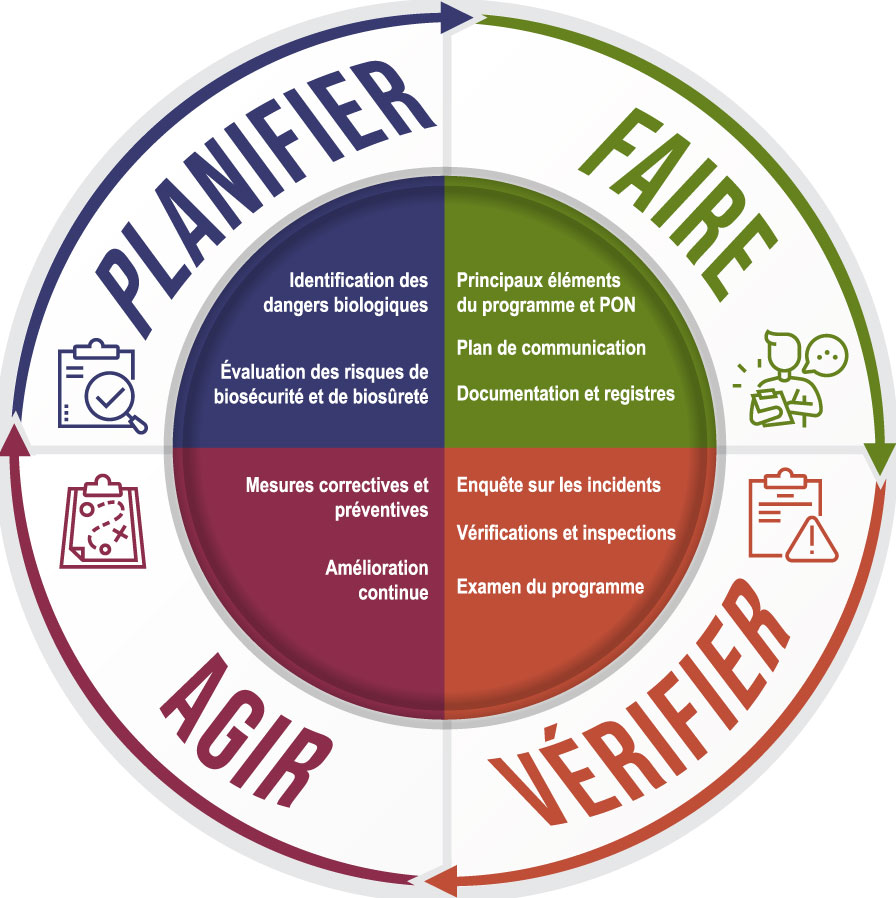
Figure 1-1 - Texte Descriptif
Figure sous la forme d'un cycle à quatre quadrants. Le premier quadrant correspond à la partie Planifier du cycle et énumère l'identification des risques biologiques et l'évaluation des risques de biosécurité et biosûreté en tant que composants. Le deuxième quadrant représente la partie Faire du cycle et comprend les principaux éléments du programme et PON, le plan de communication et la documentation et registres. Le troisième quadrant est indiqué comme la partie Vérifier du cycle et comprend les enquêtes sur les incidents, les vérifications et les inspections et l'examen du programme en tant que composants de cette section. Le dernier quadrant est la partie Agir du cycle et comprend les actions correctives et préventives et l'amélioration continue en tant que composants.
1.1 Portée
La ligne directrice Gestion du programme de biosécurité fournit des recommandations complètes sur la façon d'élaborer, de mettre en œuvre et de gérer un programme de biosécurité au sein des installations où sont manipulés et entreposés des agents pathogènes humains, des agents pathogènes d'animaux terrestres et des toxines. La ligne directrice décrit les étapes essentielles à suivre pour l'élaboration et la mise en œuvre d'un programme de biosécurité complet, ce qui comprend la planification, la mise en œuvre, l'examen et l'amélioration du programme. La présente ligne directrice est destinée à être utilisée conjointement avec la NCBNote de bas de page 10.
Les renseignements fournis dans le présent document sont présentés à titre indicatif seulement et ne doivent pas être interprétés comme des exigences. Les parties réglementées peuvent choisir d'adopter d'autres approches pour satisfaire aux exigences énoncées dans la NCB.
1.2 Comment utiliser la ligne directrice Gestion du programme de biosécurité
Une liste détaillée de toutes les abréviations et de tous les sigles utilisés dans la présente ligne directrice se trouve au début du document. Chaque mot ou terme est épelé au long à sa première utilisation dans la ligne directrice, suivi de l'abréviation entre parenthèses. Après avoir été définie, l'abréviation est utilisée exclusivement dans le reste du document. Un glossaire complet des définitions des termes techniques se trouve à la section 5 du présent document. Les termes définis dans le glossaire apparaissent en caractères gras à leur première utilisation dans la ligne directrice. Lorsqu'une recommandation est associée à une exigence donnée de la NCB, la ou les matrices d'exigences sont citées en référence (p. ex. la matrice 4.1 de la NCB). Une liste complète de références et d'autres ressources est fournie au section 6.
2. Planifier un programme de biosécurité
La première étape de la planification d'un programme de biosécurité consiste à déterminer les besoins de l'organisation (selon la fonction du programme et les évaluations des risques), à identifier les mesures d'atténuation des risques et à déterminer les ressources humaines et financières requises pour mettre en œuvre les mesures d'atténuation identifiées.
Bien que le présent document porte sur la biosécurité et la protection de la santé publique, de la population animale et de l'environnement, bon nombre des éléments, y compris le programme lui-même, peuvent être intégrés dans des programmes existants de santé, de sécurité et de sûreté d'une organisation afin d'utiliser plus efficacement les ressources. Comme les organisations peuvent être assujetties à diverses exigences (p. ex. des accords, des exigences réglementaires, des normes nationales et internationales), la combinaison des éléments communs et des processus internes peut permettre de concentrer les efforts et de réduire le nombre de ressources nécessaires. Par exemple, une seule inspection interne peut permettre d'évaluer la conformité aux exigences relatives aux matières biologiques, chimiques et radioactives. De même, des exigences en matière de déclaration à l'interne peuvent être intégrées à un seul système destiné à répondre à tout incident, y compris ceux associés à des matières biologiques, des produits chimiques, la technologie de l'information, la radiation, la santé et la sécurité, ainsi que la sûreté.
2.1 Promouvoir une culture de biosécurité
Une culture de biosécurité solide, axée sur la responsabilité et la responsabilisation, constitue un élément essentiel de la réussite d'un programme de biosécuritéNote de bas de page 11. Un engagement manifeste à l'égard de la biosécurité de la part de la haute direction peut renforcer et appuyer une culture de biosécurité, dont la réussite nécessite également un engagement de la part des membres du personnel à tous les niveaux de l'organisation. L'importance et l'état de la biosécurité au sein d'une organisation est véhiculée lorsque la biosécurité devient une valeur fondamentale de l'organisation. Elle est également mise en évidence par la quantité de ressources qui sont consacrées à la mise sur pied, à la mise en œuvre, au maintien, à la révision et à l'amélioration du programme de biosécurité. Une participation et une promotion actives et visibles de la haute direction dans les activités liées à la biosécurité contribuent à faire ressortir davantage l'engagement qui a été pris à l'égard de la biosécurité.
L'élaboration d'une politique claire et d'un ensemble d'objectifs liés à la biosécurité, ainsi que la participation précoce et active des membres du personnel à tous les niveaux de l'organisation favorisent la prise en main et la responsabilité en ce qui concerne la biosécurité. Un engagement personnel peut être maintenu grâce à une communication ouverte et cohérente dans un environnement réceptif et non punitifNote de bas de page 11. Une forte culture de biosécurité peut permettre de renforcer le respect des exigences relatives à la biosécurité et d'intégrer la sensibilisation à l'égard de la biosécurité dans toutes les activités qui sont menées au sein d'une installation.
2.1.1 Rôles et responsabilités
Les rôles et les responsabilités de toutes les personnes impliquées dans le programme de biosécurité doivent être clairement définis, documentés et communiqués afin d'assurer l'efficacité de la gestion du programme. La définition des rôles permet d'identifier et de gérer les conflits d'intérêts possibles. Par ailleurs, lorsque les personnes comprennent bien leurs rôles et leurs responsabilités, elles sont en mesure de contextualiser la façon dont elles contribuent au programme de biosécurité de l'organisation dans son ensemble.
2.1.1.1 Haute direction
À titre de dirigeants dans leur organisation, les membres de la haute direction occupent une position unique pour diriger l'élaboration d'un programme de biosécurité et promouvoir une culture de biosécurité auprès de tous les membres du personnel. Certaines des responsabilités de la haute direction peuvent comprendre les tâches suivantesNote de bas de page 7Note de bas de page 12 :
- créer un ou plusieurs mécanismes (p. ex. une politique, un code, une stratégie) qui soulignent leur engagement à l'égard de la gestion et du contrôle des risques de biosécurité et de biosûreté au sein de l'organisation;
- allouer suffisamment de ressources humaines et financières pour assurer la biosécurité au sein de l'organisation;
- définir les rôles, les responsabilités et les pouvoirs liés au programme de biosécurité, les attribuer aux membres du personnel de l'organisation, ou désigner l'autorité compétente pour le faire (p. ex. l'agent de la sécurité biologique [ASB]), et les communiquer à tous les membres du personnel;
- réviser et approuver le Plan de surveillance administrative à l'égard des agents pathogènes et des toxines dans un contexte de recherche lorsque des recherches scientifiques comportant des agents pathogènes et des toxines sont effectuéesNote de bas de page 12;
- assurer la surveillance du programme de biosécurité, notamment en prenant part au processus d'examen du programme;
- assister aux réunions des comités de biosécurité (ou désigner un cadre supérieur pour y participer);
- favoriser une communication continue entre les membres du personnel et les autorités internes (p. ex. la haute direction, l'ASB) au sujet des questions et des préoccupations liées à la biosécurité en adoptant une approche non punitive.
2.1.1.2 Titulaire de permis visant des agents pathogènes et des toxines et importateur d'agents pathogènes d'animaux terrestres
En vertu de la Loi sur les agents pathogènes humains et les toxines (LAPHT), pour entreprendre des activités réglementées avec des agents pathogènes humains et des toxines, il faut généralement détenir un permis visant des agents pathogènes et des toxines (ci-après, un « permis ») délivré par l'ASPC. Bien que toutes les personnes qui réalisent sciemment des activités réglementées soient tenues responsables, le titulaire de permis a des obligations précises en ce qui a trait au programme de biosécurité et à sa gestion. Le titulaire de permis est responsable, entre autres, de désigner un ASB et de communiquer toutes les conditions du permis, y compris toutes les exigences applicables énoncées dans la LAPHT, le RAPHT et la NCB, à quiconque effectue des activités en vertu de ce permis. Bien que le titulaire de permis puisse être une personne morale, les responsabilités quotidiennes du titulaire de permis relèveront généralement des cadres supérieurs de l'organisation ou d'une autre personne autorisée. Lors de la désignation d'un membre approprié de la haute direction pour assumer le rôle de titulaire de permis (ou pour assumer les responsabilités d'un titulaire de permis) pour l'installation ou l'organisation, il convient notamment de choisir une personne qui :
- est autorisée à prendre des décisions ayant des répercussions financières et juridiques;
- est autorisée à prendre des décisions associées à la conformité avec la LAPHT et le RAPHT, et prendra ces décisions en fonction des recommandations internes de l'organisation;
- est appuyée par les accords de surveillance administrative existants de l'organisation;
- est en mesure d'influencer des décisions et des comportements à tous les niveaux de l'organisation;
- connaît les risques organisationnels généraux liés à la manipulation et à l'entreposage d'agents pathogènes humains et de toxines au sein de l'installation.
Dans les installations où un agent pathogène d'animaux terrestres ou une toxine a été importé en vertu d'un permis d'importation d'agents pathogènes d'animaux terrestres délivré par l'ACIA, la personne identifiée en tant que demandeur sur le permis est responsable des matières réglementées qui sont importées. Le demandeur pourrait être la personne qui utilisera la matière biologique (p. ex. le chercheur principal, un chercheur, un technicien), un cadre supérieur ou l'organisation (c.-à-d. une personne morale). Dans l'éventualité où le demandeur est la personne qui utilisera la matière, il est important d'assurer un suivi auprès de l'ASB en ce qui a trait aux agents pathogènes d'animaux terrestres et aux toxines importés.
2.1.1.3 Agent de la sécurité biologique
Le titulaire de permis ou le titulaire de permis d'importation d'agents pathogènes d'animaux terrestres désigne un ASB [LAPHT 36(1), matrice 4.1 de la NCB) afin qu'il supervise les pratiques en matière de biosécurité, fournisse des conseils et des recommandations concernant les enjeux liés au programme de biosécurité et agisse comme personne-ressource principale pour communiquer avec l'ASPC et l'ACIA. L'ASB, qui est responsable de superviser les pratiques en matière de biosécurité et de biosûreté (et souvent l'élaboration et la mise en œuvre du programme de biosécurité), joue un rôle essentiel dans le cadre du programme de biosécurité de l'organisation. La LAPHT, le RAPHT et la NCB ont été conçus pour soutenir le rôle de l'ASB, lequel consiste à améliorer le système de responsabilisation interne de l'organisation, en précisant les qualifications, les fonctions et les pouvoirs de ce dernier. Il est donc essentiel que l'ASB connaisse la portée des responsabilités et de l'autorité qu'il détient. L'ASB est le représentant de la biosécurité qui est responsable, le cas échéant, de :
- s'assurer de la précision et de l'exhaustivité des demandes de documents législatifs;
- communiquer avec l'ASPC et l'ACIA;
- promouvoir et surveiller la conformité envers la législation applicable (la LAPHT, le RAPHT, la LSA, le RSA), les conditions relatives aux permis et aux permis d'importation d'agents pathogènes d'animaux terrestres, le manuel de biosécurité et les procédures opératoires normalisées (PON);
- participer à l'élaboration et à la mise à jour des PON et du manuel de biosécurité;
- participer aux enquêtes internes menées à la suite d'incidents.
Toute personne peut être désignée comme ASB, qu'elle effectue un travail à l'intérieur (p. ex. un technicien, un agent de la sécurité, un enquêteur principal) ou à l'extérieur (p. ex. un entrepreneur tiers) de l'organisation, pourvu qu'elle détienne les qualifications appropriées et puisse consacrer suffisamment de temps et de ressources pour effectuer son travail de façon efficace et efficiente. Les qualifications d'un ASB comprennent les suivantesNote de bas de page 13 :
- connaissance de la microbiologie à un niveau approprié aux risques associés aux agents pathogènes et aux toxines manipulés et entreposés en vertu du permis ou du permis d'importation d'agents pathogènes d'animaux terrestres;
- connaissance des dispositions de la LAPHT, du RAPHT, de la LSA, du RSA et de toute loi fédérale ou provinciale/territoriale applicable;
- connaissance des politiques, des normes et des pratiques en matière de biosécurité et de biosûreté applicables et appropriées aux agents pathogènes et aux toxines manipulés et entreposés en vertu du permis ou du permis d'importation d'agents pathogènes d'animaux terrestres.
Les ASB peuvent acquérir les connaissances appropriées en combinant l'éducation, la formation et l'expérience.
Une grande organisation avec un programme de biosécurité complexe ou plusieurs emplacements pourrait nécessiter un ASB à temps plein, ainsi que du personnel de soutien consacré à ce domaine (p. ex. des experts ou des conseillers en biosûreté). Dans d'autres cas, le poste d'ASB pourrait ne pas nécessiter un engagement à temps plein ou une ressource consacrée à une fin particulière (p. ex. un technicien de laboratoire qui accomplit d'autres fonctions peut agir à titre d'ASB au sein d'une petite organisation une fonction du programme simple). Au moment d'allouer des ressources au programme de biosécurité, la haute direction peut estimer le temps qu'il faut consacrer pour s'acquitter des fonctions liées au poste selon la taille, la complexité et les besoins de l'organisation.
2.1.1.4 Comité institutionnel de biosécurité
Bien que ce ne soit pas exigé, un comité institutionnel de biosécurité (CIB) peut être mis sur pied afin d'aider à gérer le programme de biosécurité en agissant à titre de groupe indépendant consacré à l'examen des enjeux liés à la biosécurité et à la biosûreté au sein de l'organisation. La taille d'un CIB peut varier selon la complexité de l'organisation. Les membres qui composent un tel comité reflètent les divers domaines professionnels et l'expertise scientifique de l'organisationNote de bas de page 7. Le CIB peut demander l'avis de spécialistes de départements ayant une expertise pertinente et peut à l'occasion solliciter l'aide d'experts indépendants dans des domaines connexes, d'experts en biosûreté, d'autorités locales, et de l'ASPC ou l'ACIA. Le cas échéant, les membres du CIB communiqueraient avec l'ASPC ou l'ACIA par l'entremise de l'ASB (matrice 4.1 de la NCB).
Les mandats documentés peuvent aider à éclaircir certains éléments importants, comme les membres du CIB, la fréquence des réunions, les exigences en matière de quorum pour la prise de décision, les considérations liées aux rapports (p. ex. la fréquence et le format des rapports à la haute direction) et les considérations liées à la communication régulière avec l'ASB. Les mandats peuvent également définir la portée des travaux du comité. Par exemple, le CIB pourrait participer à l'élaboration des politiques et des codes de pratique organisationnels en matière de biosécurité et de biosûreté ainsi qu'examiner les travaux proposés qui impliquent des matières biologiques. Les autres fonctions du comité pourraient comprendre la contribution à l'élaboration des évaluations des risques (p. ex. par la prestation d'une expertise en la matière, l'examen des évaluations réalisées), à l'examen en matière de biosécurité et de biosûreté des propositions de recherche (p. ex. pour évaluer la possibilité de double usage de la recherche sur les sciences de la vie) et à la médiation dans des différends relatifs aux questions de biosécurité.
2.1.1.5 Membres du personnel
À titre de travailleurs de première ligne, les membres du personnel jouent un rôle primordial dans la réussite d'un programme de biosécurité. Lorsque les membres du personnel sont déterminés à assurer la biosécurité et la biosûreté, ils utilisent les mesures appropriées qui sont à leur disposition (p. ex. des PON, de l'équipement de protection individuel [EPI], des dispositifs de confinement primaire). Les membres du personnel sont également dans une position unique qui permet d'observer les lacunes et de les signaler à la direction, ce qui survient seulement s'ils sont conscients des enjeux et sont motivés à préserver la biosécurité et la biosûreté, et s'ils peuvent signaler des problèmes sans crainte de représailles.
Bien que l'organisation se doive d'offrir un environnement de travail sécuritaire et l'équipement nécessaire pour que les activités soient menées de façon sécuritaire, les membres du personnel sont responsables d'utiliser de façon appropriée les ressources qui leur sont fournies (p. ex. les PON, l'EPI) afin de prévenir l'exposition des membres du personnel, le rejet accidentel hors du confinement, et les incidents relatifs à la sûreté qui impliquent des matières réglementées ou des ressources connexes (p. ex. des renseignements sensibles)Note de bas de page 14. En fait, toute personne qui effectue sciemment une activité réglementée avec un agent pathogène humain ou une toxine doit prendre toutes les précautions raisonnables pour protéger la santé et la sécurité du public en fonction des risques présentés par cette activité [LAPHT 6]; la LAPHT et le RAPHT comportent d'autres obligations dont les personnes doivent s'acquitterNote de bas de page 13.
La formation sur la biosécurité et la biosûreté vise à préparer les membres du personnel à la manipulation responsable des agents pathogènes et des toxines et à mieux les sensibiliser aux enjeux liés à la biosécurité et la biosûreté. Les membres du personnel de l'installation peuvent communiquer avec l'ASB, le CIB et les membres de la haute direction s'ils croient que les ressources disponibles sont insuffisantes ou que celles-ci pourraient être accrues ou être allouées plus efficacement afin d'améliorer la biosécurité et la biosûretéNote de bas de page 15. Les membres du personnel peuvent également contribuer au programme de biosécurité en participant à l'élaboration de politiques ou de procédures, et en faisant la promotion active de pratiques de travail sécuritaires et d'un environnement de travail sûr.
2.1.2 Politique de biosécurité
La politique de biosécurité constitue le document général d'orientation sur la biosécurité sur lequel s'appuyer pour élaborer un programme de biosécurité. Elle jette les bases d'une culture de biosécurité et de biosûreté solide en démontrant l'engagement que prend la haute direction à l'égard de la biosécurité et de la biosûreté. La politique de biosécurité définit les principes et les objectifs de biosécurité de l'organisation afin de gérer de manière appropriée les risques liés à la biosécurité et à la biosûreté et établit l'engagement à l'égard de la biosécurité et de la biosûreté en décrivant les rôles et les responsabilités liés à la sécurité et à la sûreté. À l'interne, la politique est adaptée aux enjeux de biosécurité propres à l'organisation comme les activités menées dans la zone de confinement, les produits et les services, le contexte relatif aux menaces et les vulnérabilités possibles de l'organisation, et sert à guider les membres du personnel en ce qui concerne les procédures appropriées en matière de biosécurité et de biosûreté. D'un point de vue externe, la politique de biosécurité énonce les engagements de l'organisation à l'égard de la biosécurité, de la biosûreté et du respect des objectifs de rendementNote de bas de page 8.
2.1.2.1 Objectifs et cibles
Les objectifs et les cibles définissent les priorités de l'organisation en ce qui a trait à la biosécurité et la biosûreté. Outre les exigences législatives, réglementaires et celles énoncées dans la NCB, ils tiennent compte des exigences qui s'appliquent à l'organisation dans son ensemble et à certains éléments spécifiques (p. ex. les départements, les installations, les fonctions). Au moment d'établir des objectifs et des cibles, il est important de mettre l'accent sur des mesures précises, lesquelles décrivent la façon dont :
- la direction est déterminée à traiter et à gérer de façon appropriée les risques associés aux agents pathogènes, aux toxines, aux matières infectieuses et aux ressources connexes;
- les risques associés aux activités de travail prévues seront déterminés;
- les mesures d'atténuation réduiront les risques;
- les pratiques et les procédures en matière de biosécurité et de biosûreté seront mises en œuvre de façon efficace;
- les pratiques et les procédures seront surveillées (p. ex. une évaluation interne peut être effectuée sur une base régulière, à l'improviste) afin de confirmer qu'elles sont toujours suivies;
- le personnel pourra assister à une formation appropriée en matière de biosécurité et de biosûreté (c.-à-d. le programme de formation).
Les objectifs qui sont SMART (c.-à-d. spécifiques, mesurables, atteignables, réalistes, et temporels) sont plus susceptibles de mener à la réalisation d'un butNote de bas de page 16. Un plan d'action bien établi peut aider une organisation à atteindre et à revoir ses objectifs en ce qui a trait au programme de biosécurité. Selon la complexité du programme, il peut s'avérer utile d'attribuer des responsabilités pour des tâches individuelles (p. ex. la surveillance des procédures) et d'établir des échéanciers pour l'examen des objectifsNote de bas de page 7.
2.2 Évaluations des risques de biosécurité et de biosûreté
La première étape de la planification d'un programme de biosécurité consiste à déterminer les besoins de l'organisation, conformément à la fonction du programme, ainsi que les ressources requises pour manipuler et entreposer de manière sécuritaire et sûre des agents pathogènes et des toxines.
Les évaluations des risques servent à identifier les dangers et à catégoriser et à établir les priorités des risques connexes. Elles font partie intégrante d'un programme de biosécurité, sont basées sur une combinaison de données scientifiques, de politiques et de jugements d'experts et peuvent évoluer au fur et à mesure que le niveau de compréhension scientifique progressera. Une méthodologie systématique permettra d'obtenir des résultats plus cohérents, peu importe qui a procédé à l'évaluation. Les descriptions des probabilités (p. ex. faibles, probables, fréquentes), la gravité des conséquences (p. ex. mineures, modérées, critiques) et le niveau de tolérance au risque de l'organisation (c.-à-d. acceptable ou inacceptable) peuvent être définies et utilisées dans les évaluationsNote de bas de page 7. Les évaluations des risques peuvent également permettre de déterminer si les mesures d'atténuation existantes sont suffisantes et contribuer à identifier les stratégies supplémentaires d'atténuation des risques qui doivent être mises en œuvre pour réduire les risques à un niveau acceptableNote de bas de page 7Note de bas de page 17.
Plusieurs différents types d'évaluations des risques sont nécessaires pour les aspects distincts du programme de biosécurité, comme il est indiqué au tableau 2-1Note de bas de page 18Note de bas de page 19. Les évaluations des risques doivent être réalisées au début de la mise en œuvre de nouveaux programmes ou projets, lorsque des changements se produisent, à la suite d'événements qui pourraient être pertinents en ce qui a trait à la biosécurité et la biosûreté (p. ex. des incidents, des changements réglementaires) et dans le cadre d'un processus d'examen régulierNote de bas de page 7.
| Type d'évaluation des risques | Portée de l'évaluation des risques | Exemple et description d'un danger ou menace évalué dans le cadre de l'évaluation des risques |
|---|---|---|
| Évaluation globale des risques | Une évaluation générale qui fournit une vue d'ensemble (c.-à-d. à l'échelle organisationnelle) de la biosécurité et de la biosûreté afin de déterminer quels sont les dangers grâce à un examen systématique de l'éventail des agents pathogènes et des toxines, des membres du personnel, des emplacements et des activités prévues. Les résultats de cette évaluation orienteront le choix des mesures d'ingénierie et des contrôles administratifs, et des pratiques et des procédures opérationnelles, et éclaireront le programme de biosécurité dans son ensemble. | Compétences des membres du personnel : Les compétences des membres du personnel qui travaillent avec des agents pathogènes et des toxines sont variées, allant des scientifiques hautement qualifiés, des superviseurs de laboratoire et des techniciens aux nouveaux employés inexpérimentés en passant par les étudiants en formation. Une organisation d'enseignement ou de formation ayant un taux de roulement élevé de membres du personnel moins expérimentés, de stagiaires ou d'étudiants pourrait anticiper différents dangers que ceux déterminés par une organisation ayant une expertise bien établie. Les personnes qui peuvent entrer dans une zone de confinement comprennent les visiteurs, le personnel chargé du nettoyage et de l'entretien et les entrepreneurs, ayant tous des compétences variées. |
| Évaluation des risques associés à l'agent pathogène | Une évaluation des risques de danger pour les humains, les animaux et l'environnement. Les caractéristiques inhérentes de l'agent pathogène (p. ex. la pathogénicité, la transmissibilité, la gamme d'hôtes) ainsi que les risques associés avec sa manipulation et son entreposage sont pris en considération. | Dangers biologiques : Les agents pathogènes et les toxines qui sont manipulés ou entreposés dans une installation, y compris toute matière (p. ex. le surnageant de culture, le sang, les tissus) ou tout animal qui est susceptible d'en contenir. |
| Évaluation des risques de biosûreté | Une évaluation des risques qui consiste à définir et à classer par ordre de priorité les matières réglementées et les autres ressources connexes (p. ex. l'équipement, les animaux, les renseignements sensibles, les membres du personnel, le matériel non infectieux), à évaluer la probabilité des menaces, les vulnérabilités et les conséquences associées, ainsi qu'à recommander des stratégies d'atténuation appropriées afin de protéger ces ressources contre des événements de biosûreté. | Vol, mésusage et détournement : La facilité avec laquelle les individus peuvent accéder sans autorisation à un espace sécurisé dans l'édifice (p. ex. une zone de confinement) augmente les risques de vol, de mésusage, de détournement ou de rejet intentionnel non autorisé de ressources biologiques (p. ex. des matières réglementées) et de ressources connexes (p. ex. de l'équipement, du matériel non infectieux, des animaux, des renseignement sensibles). L'accès non autorisé peut également mener à des incidents de biosûreté tels que le sabotage d'infrastructure ou d'équipement essentiel au bioconfinement. Le fait de comprendre le contexte des menaces (c.-à-d. la possibilité d'un événement de biosûreté, les capacités des adversaires et les agents pathogènes ou les renseignements sensibles recherchés) et les vulnérabilités de l'organisation peut aider à évaluer la probabilité et les risques associés avec un accès non autorisé. |
| Évaluations locales des risques (ELR) | Des évaluations propres à un endroit en particulier réalisées pour repérer les dangers en fonction des matières biologiques utilisées et des activités (p. ex. la culture d'un agent pathogène, la centrifugation, le pipetage, l'entrée dans une zone de confinement ou la sortie de celle-ci) qui sont menées et pour éclairer l'élaboration de PON décrivant des pratiques de travail sécuritaires. | Activités de laboratoire : Le type de travail réalisé influencera le risque. Les dangers liés aux activités peuvent être associés aux manipulations en laboratoire (p. ex. des activités de pipetage ou de mélange peuvent produire des aérosols infectieux), mais également à l'installation (p. ex. entrer dans une zone de confinement ou en sortir, enfiler de l'EPI). |
2.2.1 Identifier les dangers ou menaces potentiels
L'identification de tous les dangers potentiels liés aux agents pathogènes et aux toxines au sein d'une organisation facilite la réalisation d'une évaluation précise des risques associés aux activités prévues. Les exemples des types de dangers qui peuvent être pris en considération dans le cadre d'un processus de gestion d'un programme de biosécurité et être identifiés grâce à différentes évaluations des risques sont indiqués dans le tableau 2-1.
Une identification complète et efficace des dangers est effectuée en recueillant, en documentant clairement et en communiquant des renseignements d'une manière telle que les autres peuvent examiner facilement le processus et les résultats qui en découlentNote de bas de page 20. Une méthodologie ou une approche normalisée peut être adoptée dans le cadre de l'identification de dangers, quelles que soient la nature et la complexité de l'installationNote de bas de page 7. L'ASB et le CIB qui soutient ce dernier peuvent mener à bien le processus d'identification des dangers à l'aide de renseignements et de recommandations fournis par des experts internes et externes sur la sécurité, la sûreté et la gestion du programme de biosécurité. Les ressources pour l'évaluation des dangers peuvent comprendre:
- des sources de renseignements propres aux agents pathogènes (p. ex. les fiches techniques santé-sécurité : agents pathogènes (FTSSP), ePATHogène - la base de données sur les groupes de risque)Note de bas de page 21Note de bas de page 22;
- des évaluations des risques complètes (p. ex. des évaluations des risques associés aux agents pathogènes, une évaluation des risques de biosûreté, des ELR);
- des rapports d'enquête sur les incidents;
- des évaluations des menaces par des experts en sûreté;
- des renseignements publiés (p. ex. des renseignements évalués par les pairs, des normes de l'industrie);
- des groupes de discussion détenant une expertise à l'interne et à l'externe.
2.2.2 Détermination des mesures d'atténuation
Diverses mesures de contrôle physique et procédures opérationnelles peuvent contribuer à atténuer les risques associés à la manipulation et à l'entreposage d'agents pathogènes et de toxines. Les résultats des évaluations des risques servent à déterminer quelles autres mesures d'atténuation sont nécessaires et à quel moment celles-ci doivent être mises en œuvre pour assurer le maintien de la biosécurité et la biosûreté. Bon nombre des mesures d'atténuation identifiées devraient déjà être en place à titre de condition spécifique du permis ou du permis d'importation d'agents pathogènes d'animaux terrestres (y compris les exigences applicables de la NCB).
Le choix des mesures d'atténuation pourrait être envisagé de manière progressive selon leur efficacité, y compris la substitution, les mesures d'ingénierie et d'autres solutions physiques, les pratiques de travail sécuritaires (p. ex. afin d'éviter la production d'aérosols), les contrôles administratifs (p. ex. la formation, les PON) et l'EPINote de bas de page 20. Plusieurs méthodes d'atténuation (p. ex. les mesures physiques, les mesures opérationnelles, l'EPI) peuvent être combinées pour travailler en synergie afin de diminuer les risques associés à la manipulation ou l'entreposage d'agents pathogènes et de toxines, ce qui, dans certains cas, fournit la redondance nécessaire pour atténuer les risques plus élevés (p. ex. au NC3, au NC4). Des exemples de mesures d'atténuation à envisager figurent au tableau 2-2.
| Mesure d'atténuation | Description de la mesure d'atténuation |
|---|---|
| Substitution | La substitution par une toxine ou un agent pathogène présentant un risque plus faible (p. ex. une souche atténuée par rapport à une souche parentale) ou par un équipement présentant un risque plus faible (p. ex. le plastique par rapport au verre) peut diminuer la dépendance aux mesures d'ingénierie et aux contrôles opérationnels et doit être considérée si ces derniers donnent des résultats similaires. Dans certains cas, les mesures d'ingénierie et les contrôles opérationnels existants peuvent être suffisants si l'agent pathogène, la toxine ou l'équipement ont été substitués par une solution de rechange présentant un risque plus faible. |
| Confinement physique | La structure physique et les mesures d'ingénierie qui empêchent l'exposition aux agents pathogènes et aux toxines et leur rejet de l'installation. Cela comprend les structures qui composent la zone de confinement, comme les murs, les planchers, les plafonds, les sas et les box. Il s'agit également des systèmes d'ingénierie qui contribuent au confinement physique. Ces systèmes comprennent les systèmes de chauffage, ventilation et air climatisé (CVAC), les systèmes de décontamination (p. ex. un autoclave, un système de décontamination des effluents) et les dispositifs de confinement primaire (p. ex. les enceintes de sécurité biologique [ESB], les étagères à cages ventilées). |
| Systèmes de sûreté | Des systèmes qui empêchent l'accès non autorisé intentionnel et involontaire à l'installation ou à des espaces définis au sein de celle-ci. Ces systèmes peuvent comprendre une sécurité physique (p. ex. des fenêtres incassables, un système de contrôle d'accès, des portes verrouillées) et des procédures administratives (p. ex. un processus d'obtention d'accès, l'identification de l'autorité interne en mesure d'accorder l'accès). Pour ce qui est des agents pathogènes et des toxines présentant un risque plus élevé, une sûreté appropriée peut comprendre des barrières physiques et une protection calibrée (p. ex. des barrières physiques ou des barrières perçues telles que des clôtures, des barrières ou des aménagements paysagers délimitant le périmètre du site; une séquence de portes de haute sécurité et de contrôles d'accès, lesquelles restreignent l'accès aux espaces menant à des agents pathogènes ou des toxines et aux systèmes informatiques contenant des renseignements sensibles ou à possibilité de double usage). |
| Surveillance administrative | Un mécanisme qui est mis en place au sein d'une organisation afin d'identifier, de gérer et de contrôler de façon administrative les risques de biosécurité et de biosûreté. Cela comprend plusieurs des éléments fondamentaux du programme de biosécurité, tel qu'exigé dans le Plan de surveillance administrative à l'égard des agents pathogènes et des toxines dans un contexte de recherche de l'organisation. Une surveillance interne des agents pathogènes et des toxines ainsi que des ressources connexes peut être assurée par l'ASB, le CIB ou la haute direction. |
| Gestion du personnel | Les procédures définies qui sont mises en œuvre pendant et après les processus d'embauche pour autoriser les membres du personnel à accéder à une zone de confinement (c.-à-d. seulement aux membres du personnel qui répondent à toutes les exigences) et, surtout, refuser l'autorisation à ceux qui ne répondent pas aux exigences nécessaires. De telles procédures empêchent l'entrée non autorisée dans l'installation de ceux qui ne répondent pas aux exigences minimales. La gestion du personnel peut comprendre l'évaluation de la compétence, l'évaluation continue des membres du personnel et de la fiabilité, la formation documentée et, pour les personnes qui manipulent des ABCSE, l'identification des situations pouvant avoir une incidence sur la capacité d'une personne à obtenir et à maintenir une habilitation de sécurité en vertu de la LAPHT. |
| Pratiques et procédures de travail | Les procédures liées aux pratiques de travail sécuritaires (p. ex. les PON pour l'entrée et la sortie, les bonnes pratiques microbiologiques, l'enfilement et le retrait de l'EPI, la décontamination, la déclaration d'incident) et un système définissant le contrôle des documents. Les PON liées aux pratiques de travail sécuritaires sont fondées sur les ELR et visent à empêcher les expositions et le rejet d'agents pathogènes et de toxines hors du confinement. |
| EPI | Les procédures définies relatives à la sélection, à l'utilisation et à l'entretien de l'EPI et les systèmes qui en facilitent la disponibilité (p. ex. l'achat et le lavage de sarraus). Dans une zone de confinement de gros animaux, et lors de certains incidents (p. ex. un déversement de matières biologiques à l'extérieur d'un dispositif de confinement primaire), l'EPI offre la seule barrière entre l'utilisateur et les toxines et les agents pathogènes et les toxines présents. |
3. Mettre en œuvre le programme de biosécurité
La taille et la complexité d'une organisation dictent les particularités de son programme de biosécurité. Il existe toutefois des éléments fondamentaux qui, lorsqu'ils sont montés sur une base solide de planification et d'engagement, offrent un cadre solide pour mettre sur pied un programme efficace. La mise en œuvre de ces éléments correspond à la phase « Faire » du cycle PFVA. Les éléments fondamentaux du programme de biosécurité, lesquels sont décrits ci-dessous, sont plus facilement normalisés au sein d'une installation lorsque tous les niveaux de l'organisation participent à leur élaboration.
3.1 Éléments fondamentaux du programme de biosécurité
La gestion et mise en œuvre efficace d'un programme de biosécurité nécessite la documentation détaillée de tous les éléments fondamentaux afin que ceux-ci soient facilement accessibles à la haute direction. Les éléments fondamentaux du programme de biosécurité comprennent les politiques, les pratiques et les plans institutionnels de biosécurité qui contribuent au programme de biosécurité dans son ensemble. La portée des travaux de l'organisation influenceront la façon dont ces éléments sont élaborés et documentés. Des besoins en matière de confinement ou de biosûreté plus stricts, fondés sur des évaluations des risques, donneront généralement des renseignements plus détaillés. Ces documents peuvent être élaborés grâce aux contributions de personnes ayant de l'expertise dans divers domaines, comme le CIB, des membres du personnel de recherche ou du personnel technique, des experts en sûreté et un conseiller médical, au besoin.
Cette collecte de documents constitue l'outil le plus efficace pour la documentation et la communication des objectifs du programme de biosécurité, mais seulement s'ils sont exhaustifs, mis à jour régulièrement et bien communiqués à ceux qui ont besoin de ces renseignements. Un résumé, une version abrégée ou des descriptions, le cas échéant, peuvent être élaborés spécifiquement pour les membres du personnel afin de les sensibiliser davantage à la façon dont les procédures, les activités et les processus sont liés les uns aux autres. Un outil efficace permet de fournir une orientation claire sur la façon de répondre aux objectifs et aux cibles du programme de biosécurité.
Ces renseignements peuvent être conservés sous la forme d'un seul document exhaustif (p. ex. un manuel de biosécurité) qui s'applique à toutes les installations afin que les renseignements soient facilement accessibles à tous les membres du personnel. Ces renseignements peuvent également être conservés dans un document central contenant des renseignements qui s'appliquent à toute l'organisation et comprendre des documents distincts pour les différentes installations ou zones de confinement ou les divers départements de l'organisation (Matrice 4.1 de la NCB) afin de ne pas submerger les membres du personnel avec des renseignements dont ils n'ont pas besoin et, dans certains cas, auxquels ils ne devraient pas avoir accès (p. ex. des renseignements sensibles). Des liens ou des renvois aux éléments propres aux installations ou aux zones de confinement et aux PON pour les pratiques de travail sécuritaires peuvent être fournis à ceux qui en ont besoin, en fonction de leurs activités de travail et des zones de confinement au sein desquelles ils travaillentNote de bas de page 8. De cette façon, la version imprimée de chaque élément peut ou non être localisée dans un seul emplacement physique. Par exemple, dans les zones de NC3 et de NC4, les descriptions du programme de formation et du programme de surveillance médicale peuvent être entreposées à l'extérieur de la zone de confinement, alors que les PON peuvent être conservées à l'intérieur de la zone de confinement où elles sont requises.
3.1.1 Procédures opératoires normalisées relatives aux pratiques de travail sécuritaires
Les PON offrent aux membres du personnel un accès facile aux instructions détaillées qui les protègent, la communauté et eux-mêmes, contre les risques que présentent les agents pathogènes et les toxines qui sont manipulés et entreposés au sein de l'installation. Les PON sont propres aux activités (p. ex. l'entrée et la sortie, l'enfilement de l'EPI) et aux travaux qui sont réalisés dans la zone de confinement, et sont fondées sur des ELR. Les processus liés à la documentation, à l'examen, à la mise à jour et à l'approbation des PON sont aussi documentés dans les PON.
En plus des pratiques de travail sécuritaires qui s'appliquent à une zone de confinement précise, des PON à l'échelle de l'organisation (p. ex. pour la gestion des déchets, l'entretien de l'équipement, la vérification régulière des ESB) peuvent être élaborées. Les PON peuvent également indiquer la personne qui est chargée de vérifier que l'entretien a bel et bien été effectué, ainsi que la façon dont le personnel peut vérifier si l'équipement peut être utilisé en toute sécurité (p. ex. en identifiant la dernière date des essais dans les ESB, en vérifiant les lectures des jauges et le courant d'air vers l'intérieur avant d'utiliser les ESB).
3.1.2 Conception physique
Une description de la conception physique des zones de confinement permet de contextualiser les PON (p. ex. où enfiler l'EPI, où se laver les mains). Selon le type d'espace de travail en laboratoire, une description générale peut être suffisante, alors qu'une représentation plus détaillée (avec les plans d'étage) peut être nécessaire pour les installations avec des critères plus stricts. L'utilisation de plans d'étage ou de plans « conformes à l'exécution » pour représenter visuellement la zone de confinement et les espaces attenants peut aider les membres du personnel à identifier les principales caractéristiques physiques de l'espace qui contribuent au confinement (p. ex. le périmètre de la zone de confinement, les sas, les sondes de surveillance de pression différentielle, les box, les salles de nécropsie). Par ailleurs, le fait de fournir une représentation visuelle (p. ex. des schémas) de la barrière de confinement peut aider le personnel à identifier rapidement la ou les portes critiques qui sont essentielles au maintien du confinement là où un courant d'air vers l'intérieur est fourni ainsi qu'à reconnaître l'endroit où l'EPI (p. ex. des gants, des couvre-chaussures, des blouses jetables) dédié à l'espace doit être retiré au moment de quitter. Dans certains cas (p. ex. dans les locaux de l'installation où sont manipulés ou entreposés des ABCSE, les niveaux de confinement élevés), l'accès à certains renseignements liés à la conception physique peut être restreint aux membres du personnel autorisés. Afin d'appuyer les stratégies d'atténuation en matière de sûreté, il est important que les renseignements détaillés associés à la conception physique soient partagés selon le besoin de savoir.
Plan de biosûreté
Un plan de biosûreté décrit les mesures de sûreté qui doivent être mises en œuvre pour prévenir la perte, le vol, le mésusage, le détournement ou le rejet non autorisé intentionnel d'agents pathogènes, de toxines et de ressources connexes. Toutes les installations doivent avoir un plan de biosûreté qui contient tous les éléments obligatoires énoncés dans la matrice 4.1 de la NCB.
La complexité et le niveau de détail du plan de biosûreté dépendront de la nature des activités de l'organisation, des risques de biosûreté présentés par les agents pathogènes et les toxines ainsi que les ressources connexes, y compris les renseignements sensibles en leur possessionNote de bas de page 23. Par exemple, il est peu probable qu'une petite installation de NC2 où sont seulement effectuées des activités réglementées à très faible possibilité de double usage avec des agents pathogènes de GR2 nécessite des dispositifs de protection au même niveau qu'une installation où sont manipulés des ABCSE ou des agents pathogènes de GR3 ou GR4. Les dispositifs de protection ont également tendance à être plus stricts pour les installations où le travail implique des animaux ou est lié au développement ou à la production de vaccins. La complexité des mesures de sûreté et le niveau de détail du plan de biosûreté dependent toujours des résultats de l'évaluation des risques de biosûreté, laquelle est réalisée par l'organisation.
Le plan de biosûreté peut contenir des renseignements sensibles et l'accès à ce dernier ne doit être accordé qu'aux membres du personnel qui en ont besoin. Les plans de biosûreté caviardés, qui ne contiennent pas de détails critiques sur le plan de la sûreté (p. ex. des détails menant à des faiblesses en matière de sûreté physique, les emplacements précis des ABCSE) mais comprennent des stratégies en matière de biosûreté (p. ex. des procédures pour la déclaration d'activités ou de personnes suspectes, les techniques d'enquête de sécurité sur le personnel) peuvent être rendus disponibles à d'autres membres du personnel de l'installation qui en ont besoin. Cette version peut comprendre des (ou renvoyer aux) PON qui portent spécifiquement sur la biosûreté (p. ex. les demandes d'accès) et peut servir lors de la formation du personnel. Elle peut également décrire la façon dont la possibilité de double usage d'une recherche, y compris les résultats de cette recherche (p. ex. de nouveaux agents pathogènes, de nouvelles procédures, des renseignements), sera identifiée, évaluée, gérée et contrôlée, tel qu'exigé dans le Plan de surveillance administrative à l'égard des agents pathogènes et des toxines dans un contexte de recherche de l'organisationNote de bas de page 12. Le fait de fournir de tels renseignements aux membres du personnel les aidera à mieux comprendre les processus concernés, ainsi que leurs responsabilités et celles d'autres intervenants de l'organisation (p. ex. l'ASB, la haute direction, le CIB). Le plan de biosûreté peut également décrire la formation en matière de biosûreté fournie aux membres du personnel afin d'identifier et de déclarer des menaces ou des incidents possibles. Des renseignements supplémentaires en matière de formation sur la biosécurité et la biosûreté sont disponibles sur le Portail de la formation de l'ASPCNote de bas de page 24.
3.1.4 Programme de surveillance médicale
Le programme de surveillance médicale vise à prévenir, détecter et traiter les maladies liées à l'exposition à des agents pathogènes ou à des toxines. Il offre également des mécanismes d'intervention qui permettent la détection et l'évaluation rapides d'une intoxication ou une infection contractée en laboratoire (ICL) à la suite d'une exposition afin d'assurer un traitement précoce de façon à prévenir et à réduire la gravité de la maladie ainsi que d'empêcher la transmission secondaire dans la communauté. En raison du large éventail d'agents pathogènes et de toxines manipulés, et des différents types de domaines de travail et de recherche qui ont lieu au Canada, il n'existe aucune approche unique à l'égard de la surveillance qui serait appropriée pour toutes les installations. Chaque programme de surveillance médicale, même le besoin d'en avoir un, doit être adapté aux agents pathogènes et aux toxines qui peuvent être rencontrés et aux besoins de l'installation en fonction de l'évaluation globale des risques et des ELR. Le programme de surveillance médicale comprend l'évaluation des aspects de la santé des membres du personnel qui peuvent avoir une incidence sur la probabilité d'infection (p. ex. l'état immunitaire) et met l'accent sur la prévention et le traitement des infections (p. ex. des vaccins, une prophylaxie pré-exposition et post-exposition). Le chevauchement et le dédoublement des efforts peuvent être réduits en élargissant le programme de façon à inclure certains aspects de la santé en milieu de travail, comme l'exposition aux produits chimiques, les allergies (p. ex. au latex, aux pellicules animales, à la poussière), les facteurs ergonomiques (p. ex. la fatigue physique) et le bruit excessif dans le cadre d'un programme exhaustif de santé et de sécurité au travail.
Une infection causée par un agent pathogène ou une exposition à une toxine n'entraîne pas toujours rapidement l'apparition de symptômes ou d'une maladie apparente. Par ailleurs, les infections peuvent être symptomatiques ou asymptomatiques. La mise en œuvre de pratiques de surveillance médicale visant à identifier une séroconversion peut permettre de reconnaître ou de confirmer des infections ou des maladies récentes ou antérieures. La séroconversion peut se produire après l'infection initiale et l'élimination de l'agent pathogène et, dans le cas de certains agents pathogènes (p. ex. le virus de l'immunodéficience humaine [VIH], Mycobacterium tuberculosis, le virus de l'hépatite C, certains champignons, les prions), peut indiquer une période de latence après l'infection avant l'apparition de la maladie.
La confidentialité des renseignements médicaux doit être protégée (p. ex. un professionnel de la santé devrait les conserver) dans la mesure du possible et conformément aux politiques institutionnelles. Par exemple, si un rapport à l'employeur est requis à la suite d'une évaluation, le professionnel de la santé peut simplement rendre sa décision (p. ex. « répond aux exigences médicales », « ne répond pas aux exigences ») à l'employeur sans fournir de détails sur les raisons qui y sont associées. À la suite d'un incident d'exposition concernant plus d'une personne, l'employeur peut être informé par le biais d'un rapport anonymisé indiquant qu'une personne a subi un traitement (ou non) et le résultat (p. ex. une infection, l'absence d'infection, résolu avec un traitement).
Le programme de surveillance médicale peut comprendre des évaluations médicales préalables à l'affectation, des situations où une vaccination peut être requise, la surveillance médicale continue du personnel et un plan d'intervention post-exposition et de traitement de maladie. Ces éléments sont décrits dans les sections qui suivent.
3.1.4.1 Évaluation médicale préalable à l'affectation
L'évaluation médicale préalable à l'affectation donne l'occasion d'évaluer des conditions qui peuvent influencer la vulnérabilité d'une personne à une infection ou une maladie, ou la capacité de traiter la maladie à la suite de l'infection. Ces conditions peuvent comprendre :
- des conditions ou des problèmes de santé préalables et en cours (p. ex. un traitement immunosuppressif, une infection par le VIH, une grossesse) qui peuvent avoir une incidence sur la vulnérabilité aux infections ou la gravité de l'infection, le cas échéant;
- des médicaments pris actuellement;
- des allergies ou des sensibilités (p. ex. à des médicaments, des animaux, des allergènes environnementaux);
- des immunisations ou des infections naturelles préalables (p. ex. les oreillons, la grippe) qui peuvent conférer une immunité aux agents pathogènes manipulés.
Au cours de l'évaluation médicale préalable à l'affectation, il serait possible d'envisager de prélever un échantillon de sérum aux fins d'analyse afin de déterminer l'immunité préexistante résultant d'une vaccination ou d'une infection préalable. Le sérum peut également être entreposé à long terme afin d'établir une séroréactivité de référence aux fins de comparaison avec les échantillons prélevés à la suite d'une exposition possible.
Les exigences médicales doivent être clairement documentées (p. ex. dans les PON). Il est recommandé que le professionnel de la santé ait accès aux renseignements (p. ex. sur un formulaire) afin de l'informer clairement de la raison de l'évaluation (p. ex. les agents pathogènes qui seront manipulés) et des points à inclure dans l'évaluation.
3.1.4.2 Vaccination
Les vaccins sont des produits biologiques réglementés qui sont administrés afin de provoquer une réponse immunitaire protectrice. Il existe un grand nombre de vaccins autorisés par Santé Canada qui sont disponibles sur le marché, et les risques et les avantages de leur utilisation dans un contexte de travail peuvent être discutés avec un professionnel de la santé. La plupart des Canadiens reçoivent plusieurs vaccins au cours de leur enfance et de leur adolescence afin de les protéger d'une infection (p. ex. la diphtérie, la polio, le tétanos, la rougeole, la varicelle, le virus du papillome humain, le virus de l'hépatite B). Dans certains cas, l'immunité conférée par la vaccination peut décroître avec le temps (p. ex. le tétanos, la rougeole), ce qui peut être vérifié avec des titres d'anticorps, et la vaccination peut être répétée au besoin (c.-à-d. « une injection de rappel »), par exemple, pour atténuer les risques biologiquesNote de bas de page 25.
3.1.4.3 Surveillance médicale continue
Une surveillance médicale continue (p. ex. une évaluation de santé annuelle) donne l'occasion de détecter des changements dans l'état de santé d'une personne qui pourraient accroître le risque d'infection ou de maladie (p. ex. des changements dans le système immunitaire, une grossesse, un nouveau médicament, un stress accru). Elle donne également l'occasion de détecter des infections passées inaperçues, en particulier pour les agents pathogènes qui peuvent causer une infection asymptomatique, ou qui peuvent causer une infection latente, des symptômes bénins ou des symptômes de maladies courantes (p. ex. un simple rhume, une grippe). Cela permet de détecter et de traiter l'infection avant qu'une maladie grave ne se développe ou ne se propage dans la communauté. Par exemple, bien que la plupart des cas d'infection causés par le virus de l'hépatite C soient asymptomatiques, une détection et un traitement précoces peuvent prévenir de graves dommages au foie qui pourraient survenir au cours de l'infection.
3.1.4.4 Plan d'intervention post-exposition
Les étapes à suivre immédiatement après que soit survenue une exposition à un agent pathogène ou à une toxine pourraient être comprises dans le plan d'intervention d'urgence. Les PON peuvent comprendre des renseignements propres aux agents pathogènes ou aux toxines, le cas échéant. Un prestataire ou un professionnel de la santé au travail, le CIB, l'ASB, le conseiller en santé et sécurité au travail ou le spécialiste en maladies infectieuses peut être consulté pour établir un plan d'intervention optimal en cas d'exposition soupçonnée aux différents agents pathogènes et aux toxines, déterminer les considérations relatives aux types d'expositions (p. ex. cutanée, par les muqueuses, par inhalation) et les dispositions qui ont été prises pour que des mesures préventives et des traitements médicaux soient disponibles à la suite d'une exposition (p. ex. une antitoxine, une prophylaxie post-exposition), tout particulièrement pour ceux qui ne le sont pas habituellement. Un lien avec un établissement local de soins de santé (p. ex. un centre médical, un hôpital) peut accélérer le diagnostic et le traitement pour les agents pathogènes présentant des risques plus élevés et les agents pathogènes et les toxines qui sont inhabituels ou difficiles à diagnostiquer.
3.1.5 Plan d'intervention d'urgence
Le plan d'intervention d'urgence prépare le personnel à prendre les mesures appropriées en cas d'accidents (p. ex. un déversement, de l'EPI endommagé), d'urgences médicales, de panne de courant, de perte de confinement ou d'autres situations d'urgence prévisibles afin de prévenir une exposition à des agents pathogènes et à des toxines ou le rejet de ceux-ci hors du confinement. Les mesures d'intervention doivent être appropriées pour l'ampleur et la nature des situations d'urgence possibles, peuvent comprendre des procédures de nettoyage, de désinfection et de pansement de plaies ou de parties du corps qui ont été exposées, et peuvent indiquer les endroits où obtenir de l'aide médicale à l'intérieur ou à l'extérieur de l'organisation.
Au moment d'élaborer un plan d'intervention d'urgence, l'organisation devra inclure les coordonnées de la ou des personnes à informer en cas d'incident. L'établissement d'une « chaîne de notifications » facilite la notification des personnes appropriées afin que ces dernières entreprennent rapidement une mesure d'intervention; la chaîne de notifications peut inclure des superviseurs, des responsables du programme et de la zone de confinement, la direction, l'ASB et les autorités réglementaires (p. ex. l'ASPC, l'ACIA) ou publiques (p. ex. les forces policières, le service des incendies) pertinentesNote de bas de page 26. La notification bien coordonnée des autorités publiques peut être particulièrement importante pour les urgences relatives à la sûreté, telles qu'un tireur actif, une cyberattaque empêchant le fonctionnement normal, le vol de matières réglementées ou de ressources connexes (des renseignements sensibles), la détection d'un intrus dans l'édifice (p. ex. un ancien employé mécontent) ou la présence d'activistes possiblement hostiles au périmètre du site.
3.1.6 Programme de formation
Un programme de formation est essentiel à la mise en œuvre efficace d'un programme de biosécurité et peut comprendre de l'éducation (p. ex. l'apprentissage de connaissances théoriques dans une salle de classe, des cours en ligne), de la formation (p. ex. le développement de compétences spécifiques) et de la supervision. Les besoins actuels et futurs en matière de formation pour l'organisation sont identifiés dans le cadre d'une évaluation des besoins en matière de formation qui est révisée annuellementNote de bas de page 23. En suivant une formation, les membres du personnel peuvent en apprendre davantage sur les caractéristiques des agents pathogènes qu'ils utilisent, les mesures d'atténuation appropriées visant à prévenir une exposition à ces derniers et leur rejet, et les mesures de sûreté en place pour prévenir les incidents de biosûretéNote de bas de page 8. Cela comprend la formation initiale et la formation annuelle de perfectionnement sur le plan d'intervention d'urgence. La mise sur pied d'un programme de formation visant à informer et à éduquer les gens quant aux responsabilités qu'ils assument au sein de la zone de confinement et dans l'organisation joue un rôle essentiel dans la réussite du programme de biosécuritéNote de bas de page 25. La biosécurité et la biosûreté peuvent seulement être assurées lorsque toutes les personnes au sein d'une organisation suivent les procédures établies.
Afin de soutenir et de promouvoir la conformité, un programme de formation exhaustif met en évidence :
- les risques associés aux activités de travail;
- les moyens de prévenir l'exposition aux dangers;
- l'importance de satisfaire aux exigences relatives à la biosécurité et à la biosûreté;
- les rôles et les responsabilités spécifiques des membres du personnel;
- les conséquences qui pourraient découler du non-respect des PON.
Il est recommandé que le programme de formation tienne compte des responsabilités de chacun (p. ex. des gestionnaires, des superviseurs, des membres du personnel de laboratoire) et de la compréhension et des connaissances existantes du sujet à l'étude par les membres du personnel. Le programme de formation en matière de biosécurité et de biosûreté peut comprendreNote de bas de page 7Note de bas de page 26 :
- les objectifs et les buts du programme de formation;
- la façon d'effectuer des évaluations des besoins en matière de formation et le moment propice pour le faire;
- les personnes qui sont chargées de compiler le matériel de formation et d'offrir les séances de formation;
- les moments auxquels les séances de formation auront lieu et leur fréquence (p. ex. pour les membres du personnel incapables de participer à une session donnée, aux fins de requalification);
- la façon dont les séances de formation se dérouleront (c.-à-d. à l'échelle de l'organisation par rapport à une formation propre au site, la façon dont le matériel sera présenté);
- le public cible de séances de formation spécifiques;
- les responsabilités liées à la tenue à jour des registres de formation;
- les restrictions sur l'autorisation des membres du personnel à avoir accès à une zone de confinement sans supervision ou les restrictions visant à les empêcher d'effectuer des tâches jusqu'à ce qu'ils aient terminé leur formation;
- la façon dont l'efficacité de la formation est établie (p. ex. par des évaluations, des exercices).
Un programme de formation efficace tient compte de toutes les personnes qui travaillent directement avec des matières biologiques et des personnes qui pourraient entrer indirectement en contact avec celles-ci (p. ex. les membres du personnel chargés de l'entretien, du nettoyage et de la sécurité). La formation peut être adaptée à des groupes spécifiques au sein des membres du personnel en fonction de leur travail dans la zone de confinement (p. ex. un technicien ou un technologue de laboratoire qui cultive un agent pathogène, un préposé à l'entretien qui remplace des ampoules). La formation peut également être pertinente pour les membres du personnel chargés de la mise en œuvre des stratégies d'atténuation énoncées dans le plan de biosûreté, afin qu'ils puissent mieux comprendre les raisons pour lesquelles des mesures de sûreté spécifiques ont été mises en place et doivent être suivies.
3.1.7 Décontamination et gestion des déchets
Un système efficace de gestion des déchets empêche les déchets biologiques dangereux non traités (y compris les déchets liquides) de se mêler aux déchets ordinaires ou de se déverser dans les égouts sanitaires, empêchant ainsi un rejet de matières contaminées hors du confinement. Il est essentiel afin de réduire le risque pour les membres du personnel et prévenir l'exposition de la communauté à des agents pathogènes et à des toxines. Les procédures de décontamination et d'élimination doivent respecter toutes les lois applicables (c.-à-d. fédérales, provinciales ou territoriales, et municipales). Celles-ci peuvent comprendre des PON relatives à la séparation (p. ex. les déchets pointus ou tranchants, les déchets liquides, les déchets solides), l'étiquetage, la décontamination, la validation, la vérification et la collecte de déchets biologiques dangereux générés au sein de l'installation.
Les considérations relatives à la gestion des déchets peuvent comprendre les suivantes :
- les procédures de préparation pour l'élimination des déchets (p. ex. la collecte, la mise en sac);
- la séparation des déchets et l'étiquetage aux fins d'identification;
- les méthodes de décontamination (p. ex. l'incinération, les autoclaves, les désinfectants chimiques) pour les différents types de déchets générés (p. ex. les déchets infectieux de laboratoire, des effluents liquides, des objets pointus ou tranchants, des tissus animaux infectés, des matières non infectieuses);
- le déplacement de déchets contaminés à l'extérieur de la zone de confinement vers un autre emplacement pour la décontamination (p. ex. dans un contenant étiqueté étanche);
- la validation des méthodes de décontamination et les vérifications régulières;
- le recours aux services d'entreprises tierces d'élimination des déchets, le cas échéant, y compris la vérification de leur conformitéNote de bas de page 28.
3.2 Plan de communication
Le fait d'instaurer une communication cohérente, crédible et claire permet de favoriser la compréhension et l'établissement de relations de coopérationNote de bas de page 8. Une communication ouverte et transparente renforce la confiance au sein d'une organisation ainsi que de la communauté environnante. Un plan de communication permet de définir l'objectif et l'approche que l'organisation adoptera pour aborder des questions de biosécurité au sein de l'organisation et à l'externeNote de bas de page 8. Par ailleurs, un plan de communication efficace vise à répondre aux préoccupations publiques sur les risques associés à l'installation et à ses activités. Il comprend un engagement précoce et continu avec toutes les parties concernées. Les considérations relatives à l'élaboration du plan de communication peuvent comprendre les suivantesNote de bas de page 29 :
- les rôles et les responsabilités;
- des modèles, des formats ou des documents normalisés;
- les procédures visant à promouvoir la communication à l'interne;
- les procédures de communication de renseignements sensibles ou confidentiels, y compris les procédures visant à obtenir une autorisation;
- les procédures de gestion de la communication avec des parties externes;
- un processus d'escalade visant à résoudre les conflits, les préoccupations ou les enjeux liés à la communication.
Les renseignements peuvent être diffusés de plusieurs façons (p. ex. de façon verbale, sur des médias physiques [c.-à-d. écrits ou imprimés], par voie électronique) et peuvent comprendre des renseignements qui sont affichés dans des endroits publics, dans des communications par courriel, sur des sites Web, sur des fiches d'information et sur des forums. Il est préférable que toutes les communications officielles soient documentées et entreposées dans un emplacement accessible, sécuritaire et sûr.
3.2.1 Communication interne
Outre la formation, un système de communication interne efficace offre au personnel les renseignements dont ils ont besoin concernant le programme de biosécurité, y compris les dangers associés aux activités de l'organisation. Les employés sont plus susceptibles d'être motivés et engagés à atteindre les objectifs et les buts du programme de biosécurité s'ils sont tenus au courant des enjeux liés au programme de biosécurité, y compris son examen et les modifications qui en découlentNote de bas de page 8Note de bas de page 27.
Il est possible de favoriser une culture de biosécurité et de biosûreté en faisant preuve d'ouverture dans le partage de renseignements, en incitant à poser des questions et en faisant preuve d'autocritiqueNote de bas de page 30. L'adoption d'une approche non punitive (p. ex. en ne cherchant pas à attribuer la faute, mais plutôt en décrivant les incidents en fonction de leurs causes fondamentales, tout en omettant les renseignements personnels ou les données d'identification) motive davantage les employés à déclarer les incidents, les pratiques non sécuritaires et les changements de comportement des membres du personnel (p. ex. une menace interne possible). La communication entre les membres du personnel à tous les niveaux et dans toutes les fonctions de l'organisation est essentielle pour gérer de façon efficace le programme de biosécurité. Ainsi, il est recommandé que la haute direction accorde la priorité à la communication avec les membres du personnel et encourage la communication verticale et latérale entre les départements et les équipes.
La tenue régulière de réunions d'équipe, départementales et interdépartementales (y compris les réunions du CIB et les communications fréquentes avec l'ASB) facilite une communication et une discussion ouvertes et actives concernant le programme de biosécurité. La fréquence des réunions et les méthodes de diffusion des renseignements qui y sont associés (p. ex. des ordres du jour, des procès-verbaux, des comptes rendus de décision) peuvent être décrites dans le plan de communication. Un aperçu des sujets et des résultats des réunions peut être mis à la disposition des membres du personnel afin que ces derniers demeurent à l'affût des activités de biosécurité et de biosûreté qui sont menées, même s'ils ne participent pas aux réunions.
3.2.2 Communication externe
Le plan de communication peut comprendre des procédures visant à fournir de façon proactive ou réactive aux parties externes (p. ex. le secteur public, les organismes de réglementation, les organismes de financement, les médias) des renseignements pertinents ou d'intérêt, y compris sur les activités scientifiques qui sont menées au sein de l'installation et les avantages qu'en retire le public. Ces procédures peuvent servir à favoriser la confiance et l'engagement, deux éléments qui profiteront à l'organisme et à la communauté élargie. Une approche de communication efficace peut mettre l'accent sur les aspects positifs des activités de l'organisation (p. ex. le développement d'un vaccin, le fait qu'une zone de confinement soit un lieu sécuritaire pour manipuler des agents pathogènes et des toxines), ce qui peut comprendre des descriptions de mesures d'atténuation ainsi que des rapports d'audits internes et externes et des constatations dans le cadre de la description des dangers.
Un système efficace et bien planifié visant à recevoir, prioriser et documenter les communications de parties externes, ainsi qu'à y répondre, tout en dirigeant rapidement la correspondance externe à la bonne personne ou au bon département, permet de fournir rapidement des réponses aux questions et aux préoccupations externes. La gestion rapide et claire des communications externes renforce la confiance de la communauté en favorisant une meilleure compréhension et de meilleures relations professionnelles coopératives avec les parties externes et en faisant la promotion de l'image professionnelle de l'organisation. Il est possible d'éviter les mauvaises interprétations ou les mauvaises compréhensions de l'information en assurant la cohérence du format et du contenu des communications externes et en utilisant un langage simple, tout en évitant les termes techniques et les abréviations. De même, la tenue des registres liés aux communications externes et aux réponses aux demandes de renseignement externes donne un point de référence pour rédiger des réponses cohérentes aux demandes de renseignements similaires (c.-à-d. des réponses normalisées)Note de bas de page 8Note de bas de page 27.
3.3 Registres et documents
Les systèmes de gestion des registres et des documents peuvent améliorer l'efficacité et la conformité au programme de biosécurité. La façon dont l'organisation recueille et tient à jour les registres et les documents reflète la culture et les besoins de celle-ci. Par exemple, la taille de l'organisation, la fonction du programme, les exigences réglementaires et législatives et la complexité des processus et des systèmes internes constituent des éléments qui influencent l'approche à l'égard de la tenue à jour (et de la conservation) de registres et de documents.
3.3.1 Gestion des documents
La documentation par écrit des procédures ou des activités prévues est essentielle pour assurer une gestion quotidienne efficace du programme de biosécurité. Les documents peuvent être stockés sur n'importe quel support (p. ex. sur papier, par voie électronique) qui convient bien à l'organisation, tant et aussi longtemps que celui-ci demeure utile, lisible, facilement compréhensible et accessible aux membres du personnel qui en ont besoin et, le cas échéant, aux parties externes qui le demandent. Il existe diverses méthodes de contrôle de documents, y compris l'élaboration d'un processus normalisé pour créer, modifier et mettre à jour des documents et maintenir des systèmes efficaces de diffusion (p. ex. pour aviser le personnel de mises à jour ou de la sortie de nouveaux documents) et de conservation (p. ex. afin d'éviter l'élimination de documents requis) des documentsNote de bas de page 8Note de bas de page 27. Un programme de contrôle des documents est plus efficace lorsque :
- la personne-ressource et l'affiliation, le cas échéant (p. ex. une équipe, un groupe, un département), ou une ressource pour un document spécifique sont facilement identifiées;
- les documents font régulièrement l'objet d'un examen, d'une mise à jour et d'une approbation par le personnel autorisé, au besoin;
- la dernière version de chaque document est facilement trouvée et accessible aux membres du personnel qui en ont besoin;
- les documents désuets sont retirés ou archivés, conformément aux exigences relatives à la conservation (Matrice 4.9 de la NCB).
3.3.2 Gestion des registres
Les registres fournissent des preuves écrites et détaillées des activités qui ont été réalisées ou des résultats qui ont été obtenus dans le cadre du programme de biosécurité. Les registres peuvent prendre la forme, par exemple, de registres de validation et de vérification, de registres de formation, de rapports d'enquête sur les incidents et d'inventaires. Un système qui respecte les politiques et les normes existantes relatives à la tenue à jour de registres peut faciliter la préparation des examens et des audits et aider l'organisation à répondre aux exigences réglementairesNote de bas de page 31. Les processus qui définissent l'identification, la tenue à jour et la distribution des registres peuvent être décrits dans les PONNote de bas de page 8. Un programme efficace de gestion des registres :
- favorise la tenue à jour de registres lisibles, identifiables et accessibles qui permettent de retrouver l'activité, le produit ou l'élément du programme de biosécurité qui a mené à leur création;
- aide à répondre aux exigences relatives à la conservation des documents;
- favorise le stockage des registres dans un lieu sûr dont l'accès est réservé aux membres du personnel autorisé;
- peut être associé à un système de déclaration comportant des notifications en cas d'écarts par rapport à un ensemble de limites acceptables;
- peut être utilisé pour l'amélioration continue.
3.3.2.1 Inventaire
Un système d'inventaire empêche la perte et le vol d'agents pathogènes et de toxines par la création, la tenue à jour et le recoupement de la liste des ressources biologiques entreposées avec les matières réellement présentes. Il peut être intégré dans un système d'inventaire plus large qui fait le suivi de matières nouvellement acquises ainsi que l'envoi ou le transfert de matières. La tenue à jour d'un inventaire des matières réglementées qui sont entreposées à long terme (c.-à-d. plus de 30 jours) constitue un élément exigé de tout programme de biosécurité (Matrice 4.9 de la NCB). Bien que le format de l'inventaire ne soit pas spécifié, il doit faire référence au groupe de risque et à l'emplacement où sont entreposées les matières. Par ailleurs, l'inventaire des agents pathogènes et des toxines présentant des risques plus élevés (p. ex. des agents pathogènes de GR3 et de GR4, des toxines ABCSE) doit indiquer précisément l'agent pathogène ou la toxine (p. ex. le genre, l'espèce ou la souche de l'agent pathogène; l'état physique; la quantité présente dans une installation ou une zone de confinement précise) et être suffisamment détaillé pour permettre de détecter la perte ou le vol de matières. Par exemple, les renseignements sur la date de réception, de transfert ou de production de la matière, le renvoi à un bon de commande ou la personne qui a entreposé l'agent pathogène peuvent faciliter l'identification de renseignements supplémentaires liés à l'agent pathogène (p. ex. les conditions de culture, le nombre de passages, les renseignements sur les spécifications).
Les facteurs à prendre en considération au moment de développer un système de contrôle des inventaires comprennent :
- des méthodes normalisées de documentation de l'ensemble des ressources (biologiques) qui sont entreposés à long terme dans une installation;
- l'étiquetage clair et précis des récipients qui contiennent des matières biologiques;
- un format qui est accessible et facile à mettre à jour par des personnes autorisées (p. ex. un registre écrit, une base de données électronique, une feuille de calcul);
- des mesures de sûreté afin de permettre un accès limité aux personnes autorisées;
- l'augmentation de la fréquence des audits et des mesures de responsabilisation pour les agents pathogènes et les toxines présentant des risques plus élevés;
- des politiques décrivant des calendriers pour les examens et les audits des inventaires.
Les examens ou les audits sont nécessaires pour vérifier que les nouveaux agents pathogènes ou les nouvelles toxines (p. ex. obtenus d'autres sources, de nouvelles cultures, générés par une modification génétique) ont été saisis dans l'inventaire et que les matières qui ne sont plus entreposées sur les lieux (p. ex. elles ont été transférées, inactivées ou détruites de façon appropriée) sont retirées de l'inventaire. La fréquence de l'examen dépendra des risques associés aux matières, des résultats des audits précédents, de l'identification de matières perdues ou d'incidents connexes.
4. Amélioration continue du programme de biosécurité
Un programme de biosécurité efficace est souple et peut être adapté rapidement afin de remédier aux faiblesses ou aux lacunes qui ont été identifiées. Les résultats des différents types d'examens qui sont décrits dans le présent chapitre peuvent permettre de déterminer les domaines pouvant être améliorés et les recommandations relatives aux mesures ou aux ressources nécessairesNote de bas de page 7. De plus, ces résultats peuvent indiquer les aspects du programme qui sont réussis ou servir à guider les améliorations qui devraient être apportées dans d'autres domaines du programme de biosécurité. Toute modification proposée devra être approuvée par la haute direction qui pourrait établir l'ordre des priorités liées à la mise en œuvre des mesures d'atténuation, conformément aux risques et aux ressources humaines et financières disponibles.
Les examens du programme de biosécurité peuvent comprendre des évaluations réactionnaires d'éléments particuliers du programme (p. ex. à la suite d'un incident), des examens proactifs et prévus des éléments sélectionnés (p. ex. un audit, une inspection) et des examens complets de tout le programme. Les risques associés aux activités menées avec des agents pathogènes et des toxines et aux ressources connexes peuvent influencer la fréquence et la portée de telles évaluations (c.-à-d. de plus grands risques peuvent justifier des examens plus fréquents et rigoureux).
4.1 Enquête sur un incident
En cas d'incident, une enquête approfondie permettra de déterminer la ou les causes fondamentales de l'incident ainsi que les mesures d'atténuation appropriées nécessaires; celles-ci peuvent comprendre des améliorations à apporter aux mesures existantes ainsi que de nouvelles mesures visant à prévenir une récurrence ou à diminuer les conséquences liées à un autre incident similaire. Un examen approfondi de chacun des rapports d'enquêtes sur les incidents confirmera si les causes fondamentales ont été identifiées pour tous les facteurs contributifs, alors que l'examen de plusieurs rapports permettra de déterminer les tendances (p. ex. les causes fondamentales communes) qui pourraient devoir nécessiter la prise de mesures d'atténuation à l'échelle de l'organisation. Les résultats des enquêtes sur les incidents peuvent servir à mettre à jour les éléments du programme de biosécurité (p. ex. le programme de formation, les PON, les plans d'intervention d'urgence) afin de prévenir ou d'atténuer les incidents futurs.
4.2 Inspections et audits internes
Un examen des éléments du programme de biosécurité peut prendre place pendant ou après des audits et des inspections afin d'identifier les dangers de manière proactive, vérifier la conformité avec les exigences en matière de biosécurité et de biosûreté et identifier les lacunes et les points à améliorer dans le programme de biosécurité d'une organisation donnée. Bon nombre d'organisations mettent en œuvre un programme d'inspection coopératif en vertu duquel le personnel est chargé d'effectuer des autoévaluations récurrentes. De tels programmes d'inspection sont habituellement combinés à des inspections moins fréquentes, mais plus approfondies par l'ASB, des membres du CIB ou un entrepreneur tiers. L'ASB est responsable de présenter les conclusions des inspections périodiques au titulaire de permis ou au titulaire de permis d'importation d'agents pathogènes d'animaux terrestres, le cas échéant (Matrice 4.1 de la NCB). Les attentes à l'égard de la fréquence et de la portée des inspections et des audits peuvent être décrites dans les PON de l'organisation. Des inspections et des audits aléatoires et à l'improviste servent à vérifier la conformité continue aux exigences et aux procédures applicables en matière de biosécurité ainsi qu'à identifier les lacunes. Des audits et des inspections aléatoires ou prévues liées au programme de biosécurité peuvent comprendreNote de bas de page 7 :
- des inspections informelles régulières des espaces et surfaces de travail (p. ex. par des superviseurs, des membres du personnel);
- des examens des documents et des registres;
- des inventaires;
- des rapports d'incident;
- des résultats d'autoévaluations;
- des résultats des registres de validation et de vérification;
- des PON et des preuves de conformité de celles-ci;
- des évaluations de l'entretien et de la performance de l'équipement;
- des évaluations de l'installation.
La mise en place d'un processus d'évaluation officiel pour examiner et évaluer la conformité et l'efficacité du programme de biosécurité de l'organisation aidera l'ASB à donner rapidement suite aux lacunes ciblées, à fixer des dates cibles pour les mesures correctives et à vérifier la mise en œuvre des mesures correctives. Les audits et les inspections visent à promouvoir la conformité et non à blâmer qui que ce soit (c.-à-d. identifier les points à améliorer). La personne qui effectue l'audit (p. ex. l'ASB) peut travailler en collaboration avec le personnel de l'installation afin de déterminer les mesures immédiates et à long terme appropriées à prendre pour corriger les lacunes, tout en établissant les priorités liées à la mise en œuvre des mesures en fonction des risques.
Les facteurs à prendre en considération au moment d'élaborer un programme d'audit ou d'inspection peuvent comprendreNote de bas de page 7 :
- la portée de l'audit ou de l'inspection;
- la fréquence des audits et des inspections, en fonction d'une ELR et des antécédents de conformité;
- la procédure relative aux audits et aux inspections;
- la façon dont les résultats de l'audit et de l'inspection seront mesurés et déclarés;
- les renseignements permettant d'établir si des audits et des inspections à l'improviste pourraient être réalisées.
Les résultats d'un audit ou d'une inspection peuvent être fournis à la haute direction, au titulaire de permis, au titulaire de permis d'importation d'agents pathogène d'animaux terrestres ou à l'ASB sous forme de rapport écrit ou électronique. Le rapport peut contenir les conclusions (p. ex. des lacunes, des tendances, des observations positives) et des recommandations de mesures correctives et préventivesNote de bas de page 27. Des paramètres (p. ex. le nombre et la gravité des non-conformités) et les métadonnées connexes (p. ex. les tendances au fil du temps) peuvent servir à faire le suivi du rendement du programme de biosécurité d'une année à l'autre et à évaluer si les cibles du programme de biosécurité sont atteintes.
4.3 Examen du programme de biosécurité et de la gestion
Les examens prévus de tout le programme de biosécurité aident à maintenir la pertinence, l'adéquation et l'efficacité du programmeNote de bas de page 7. L'organisation peut choisir d'élaborer des rapports périodiques (p. ex. mensuels, trimestriels, annuels, bisannuels) dans le cadre desquels les réalisations sont évaluées par rapport aux cibles et aux objectifs établis. Il n'est pas impératif que la fréquence des examens et celle des rapports correspondent. Certains aspects peuvent justifier des examens plus fréquents (p. ex. des PON, de la formation), particulièrement lorsque les audits et les inspections internes soulèvent des enjeux qui y sont liés. D'autre part, un examen approfondi de tout le programme de biosécurité peut seulement être accompli une ou deux fois dans un cycle d'un permis ou d'un permis d'importation d'agents pathogènes d'animaux terrestres, puisqu'il s'agit d'un exercice qui peut s'avérer très long. Un tiers externe peut être embauché pour réaliser une analyse du programme de biosécurité en vue d'évaluer si les buts et les objectifs organisationnels sont atteints et de déterminer quelles sont les lacunes du programmeNote de bas de page 7Note de bas de page 8Note de bas de page 27.
L'examen du programme de biosécurité peut comprendre des renseignements obtenus à partirNote de bas de page 7Note de bas de page 20 :
- d'audits et d'inspections;
- d'enquêtes sur les incidents;
- de données sur la conformité en ce qui a trait aux indicateurs de retard (p. ex. le nombre et la gravité des non-conformités, le nombre et la gravité des incidents) et aux indicateurs de tendance (p. ex. le pourcentage des membres du personnel qui ont suivi une formation);
- de communications internes, y compris les suggestions et les commentaires du personnel et du CIB;
- de l'état des activités d'évaluation des risques;
- de l'état des mesures préventives et correctives;
- de mesures de suivi des examens précédents;
- de décisions de la direction (p. ex. des ordres du jour, des comptes rendus de décisions de réunions)
- de changements (p. ex. organisationnels, à la fonction du programme) qui pourraient avoir une incidence sur le programme de biosécurité.
L'examen complet du programme répond à des questions plus larges que les examens périodiques, dont les questions suivantes :
- Est-ce que les bonnes procédures, les bons processus et les bons plans sont en place pour répondre aux cibles et aux objectifs énoncés dans la politique de biosécurité?
- Le programme de biosécurité est-il compris et communiqué de façon appropriée ainsi que mis en œuvre et maintenu au sein de l'organisation?
- Les dangers sont-ils identifiés et gérés de façon efficace?
- La conformité réglementaire est-elle atteinte?
- Le processus d'inspection est-il efficace?
- Les PON sont-elles efficaces?
4.4 Mise en œuvre des mesures correctives et préventives
Pour combler les lacunes du programme de biosécurité, il pourrait être nécessaire de mettre en œuvre des solutions à court terme qui les corrigent directement (c.-à-d. des mesures correctives) ainsi que des approches systémiques à long terme (c.-à-d. des mesures préventives). Les mesures correctives répondent aux enjeux ou aux problèmes (p. ex. les causes fondamentales d'un incident) qui ont mené à un incident, alors que les mesures préventives répondent à des problèmes ou à des enjeux identifiés qui pourraient mener à un incidentNote de bas de page 32.
Les principales étapes à suivre pour appliquer les mesures correctives et préventives sont les suivantesNote de bas de page 7 :
- Identifier les lacunes et les causes fondamentales des incidents.
- Élaborer des mesures visant à empêcher que des problèmes surviennent ou reviennent. Bien que des solutions possibles puissent être déterminées grâce à une analyse des causes fondamentales ou à des processus similaires, elles pourraient nécessiter de l'orientation ou du soutien de la part d'experts externes (p. ex. des enquêteurs en milieu de travail, des experts en biosécurité, des ingénieurs, des experts en la matière).
- Mettre en œuvre les mesures proposées et élaborées. Les considérations relatives à la mise en œuvre comprennent l'établissement des priorités des mesures nécessaires selon le risque qu'elles atténueront, les menaces et la probabilité que des incidents surviennent, ainsi que les ressources et le temps nécessaires pour mettre en œuvre les mesures. Bien que de courts délais puissent être établis pour mettre en œuvre des solutions rapides (p. ex. la mise à jour de PON, la réparation d'équipement, l'offre de formation de rattrapage) afin d'éviter la récurrence d'incidents similaires, la mise en œuvre de mesures complexes ou vastes (p. ex. une nouvelle infrastructure de l'édifice) peut nécessiter beaucoup de temps.
- Documenter et surveiller l'efficacité de ces mesures afin de faire face aux enjeux sous-jacents au sein de l'organisation.
Un plan d'action peut être élaboré avec des échéanciers réalistes pour la mise en œuvre des mesures correctives et préventives, ainsi que des échéanciers sur la façon dont l'efficacité des nouvelles mesures sera vérifiée et à quel momentNote de bas de page 8.
4.5 Gestion du changement
L'amélioration du programme de biosécurité entraînera un certain changement, ce qui peut comprendre des modifications mineures aux PON, la mise en œuvre de nouvelles PON et le remaniement, les rénovations et la réaffectation d'une zone de confinement. Les changements peuvent être réactionnaires; par exemple, ils peuvent découler d'un incident, de l'introduction d'un nouvel agent pathogène ou de l'imposition externe d'exigences (p. ex. des changements législatifs). Ils peuvent aussi être proactifs, par exemple, en cherchant à améliorer l'efficience, l'efficacité et les marges de sécurité et de sûreté, ou simplement en tenant le programme de biosécurité à jour et pertinent. Peu importe la nature des changements qui ont été apportés, l'amélioration d'un aspect du programme de biosécurité peut avoir une incidence sur d'autres aspects. L'utilisation de méthodes et de procédures normalisées (p. ex. des PON) visant à gérer de manière efficace toutes les modifications apportées au programme de biosécurité ou à ses éléments réduira au minimum les répercussions du changement. Une gestion efficace du changement comprendra :
- un processus visant à tenir informés l'ASB et la haute direction de tout changement prévu afin d'assurer que les mesures appropriées soient prises (p. ex. un processus d'approbation, en informant l'ASPC ou l'ACIA au besoin);
- une évaluation de l'avantage du changement par rapport aux répercussions possibles sur d'autres domaines de la biosécurité et de la biosûreté. Un changement en apparence bénéfique pour un aspect (p. ex. simplifier l'entrée dans une zone de confinement pour augmenter l'efficacité du travail) peut avoir des effets néfastes inattendus sur un autre (p. ex. un risque accru lié à la biosûreté);
- un processus d'approbation établi;
- un plan de mise en œuvre du changement, ce qui peut comprendre la mise à jour ou l'élaboration de nouvelles PON, la planification de la mise en suspens des activités pour effectuer des rénovations ou installer un nouvel équipement, ou l'ajout d'un nouvel agent pathogène;
- un processus pour communiquer le plan aux membres du personnel, notamment lorsque le changement entrera en vigueur, et assurer que la formation soit effectuée et documentée, le cas échéant.
4.6 Amélioration continue
Le processus PFVA est un cycle continu qui, une fois établi, n'a ni commencement ni fin. À la fin d'un cycle complet, les mesures nouvellement appliquées amorcent le commencement du nouveau cycle; cette progression est importante pour adapter et améliorer continuellement le programme de biosécurité. Un effort et un soutien continus du programme de biosécurité à tous les niveaux de l'organisation sont nécessaires pour poursuivre la lancée et maintenir la pertinence du programme afin que celui-ci continue de respecter l'engagement de l'organisation à l'égard de la biosécurité et de la biosûreté.
5. Glossaire
Bien que certaines des définitions fournies dans le glossaire soient universellement reconnues, beaucoup d'entre elles ont été établies expressément pour la NCB, le Guide canadien sur la biosécurité (GCB) ou la Ligne directrice canadienne sur la biosécurité : Gestion du programme de biosécurité. Par conséquent, certaines définitions pourraient ne pas s'appliquer aux installations qui ne sont pas visées par la NCB.
| Terme | Définition |
|---|---|
| Accident | Événement imprévu ayant causé des blessures, un préjudice ou des dommages. |
| Activité réglementée | Activité visée par le paragraphe 7(1) de la Loi sur les agents pathogènes humains et les toxines, à savoir : posséder, manipuler ou utiliser des agents pathogènes humains ou des toxines; les produire; les entreposer; permettre à quiconque d'y avoir accès; les transférer; les importer ou les exporter; les rejeter ou les abandonner de toute autre manière; les éliminer. |
| Agent de la sécurité biologique (ASB) | Personne désignée pour superviser les pratiques en matière de biosécurité et de biosûreté dans une installation. |
| Agent pathogène | Microorganisme, acide nucléique, protéine ou autre agent infectieux transmissible ayant la capacité de causer une maladie ou une infection chez l'humain ou l'animal. Les agents pathogènes humains et les agents zoopathogènes classés peuvent être trouvés à l'aide de la base de données sur les groupes de risque ePATHogène offerte par l'Agence de la santé publique du Canada. |
| Agent pathogène d'animaux terrestres | Microorganisme, acide nucléique, protéine ou autre agent infectieux transmissible ayant la capacité de cause une maladie ou une infection chez les animaux terrestres; y compris ceux dérivés de la biotechnologie. Ceux-ci comprennent les agents pathogènes ayant la capacité de causer une maladie chez les oiseaux et les amphibiens, mais ce terme ne s'applique pas aux agents pathogènes qui causent des maladies seulement chez les animaux aquatiques ou les invertébrés. Ceci comprend également les agents pathogènes d'animaux terrestres ou une partie de ceux-ci (p. ex. une toxine) présents sur ou dans des produits ou des sous-produits animaux, ou d'autres organismes. |
| Agents biologiques à cote de sécurité élevée (ABCSE) | Sous-ensemble d'agents pathogènes humains et de toxines qui présentent un risque accru en matière de biosûreté en raison de la possibilité qu'ils soient utilisés comme arme biologique. Au paragraphe 10 du Règlement sur les agents pathogènes humains et les toxines (RAPHT), les ABCSE sont identifiés comme des agents pathogènes et des toxines « précisés ». Les ABCSE comprennent donc tous les agents pathogènes de groupe de risque 3 (GR3) et de GR4 qui se retrouvent sur la Liste des agents pathogènes humains et animaux et des toxines réglementés à l'exportation, publiée par le Groupe d'Australie et modifiée de temps à autre, à l'exception du virus Duvenhage, du virus rabique et de tous les autres du genre Lyssavirus, du virus de la stomatite vésiculaire, ainsi que du virus de la chorioméningite lymphocytaire. Les ABCSE comprennent aussi toutes les toxines qui se trouvent à la fois à l'annexe 1 de la Loi sur les agents pathogènes humains et les toxines et sur la Liste des agents pathogènes humains et animaux et des toxines réglementés à l'exportation et qui sont présentes en quantités supérieures aux quantités seuils énoncées au paragraphe 10(2) du RAPHT. |
| Barrière de confinement | Structures physiques ou barrières qui créent une limite entre les espaces « propres » et les espaces « sales » ou entre les zones à plus faible risque de contamination et celles à risque plus élevé (p. ex. entre les espaces de travail en laboratoire, les aires de production à grande échelle, les salles animalières, les box et les salles de nécropsie, et l'extérieur de cette aire de confinement). La barrière de confinement est elle-même créée par les murs, les portes, les planchers et les plafonds qui entourent physiquement les espaces à l'intérieur du confinement, ainsi que par le courant d'air vers l'intérieur aux portes critiques (là où un courant d'air vers l'intérieur est exigé). |
| Bioconfinement | Voir « Confinement ». |
| Biosécurité | Ensemble des principes, des technologies et des pratiques liés au confinement mis en œuvre pour empêcher l'exposition involontaire à des agents pathogènes et à des toxines, ou leur rejet accidentel. |
| Biosûreté | Ensemble des mesures de sûreté visant à prévenir la perte, le vol, le mésusage, le détournement ou le rejet volontaire de matières réglementées ou d'autres ressources connexes (p. ex. les membres du personnel, l'équipement, les matières non infectieuses, les animaux, les renseignements sensibles). |
| Bonnes pratiques microbiologiques | Code de déontologie fondamental régissant toutes les activités de laboratoire comportant des matières biologiques. Ce code sert à protéger les membres du personnel de laboratoire et à prévenir la contamination de leur milieu de travail et des échantillons utilisés. |
| Box | Salle ou espace conçu pour héberger un ou plusieurs animaux où la salle elle-même sert de confinement primaire. Ces espaces servent à héberger des gros animaux (p. ex. du bétail, des cerfs) ou des petits animaux qui sont hébergés dans des cages ouvertes (c.-à-d. pas des cages de confinement primaire). |
| Cause fondamentale | Le facteur ou la raison la plus fondamentale ou sous-jacente d'un incident. |
| Communauté | Comprend à la fois la communauté humaine (c.-à-d. le public) et la population animale. |
| Confinement | Ensemble de paramètres de conception physique et de pratiques opérationnelles visant à protéger les membres du personnel, le milieu de travail immédiat et la communauté contre toute exposition à des matières biologiques. Dans le même contexte, le terme « bioconfinement » est aussi employé. |
| Courant d'air vers l'intérieur | Courant d'air qui s'écoule constamment des zones dont le niveau de confinement ou le risque de contamination est plus bas vers les zones dont le niveau de confinement ou le risque de contamination est plus élevé, et ce, en raison d'une pression différentielle de l'air négative à l'intérieur de la zone de confinement, créée par un système de ventilation. Le courant d'air vers l'intérieur protège les espaces « propres » contre le rejet d'agents pathogènes aéroportés, d'aérosols infectieux et de toxines aérosolisées. |
| Danger | Source possible de dommage, de tort, ou d'effets indésirables. Dans le contexte de la biosécurité, des objets (p. ex. des objets pointus ou tranchants, des aiguilles), des matières (p. ex. des agents pathogènes, des toxines), des animaux (p. ex. des morsures, des égratignures) et des situations (p. ex. une défaillance du système de confinement) en sont des exemples. |
| Déchet | Matière solide ou liquide produite par une installation et destinée à être éliminée. |
| Décontamination | Procédé qui consiste à traiter des matières et des surfaces pour que leur manipulation soit sécuritaire et qu'elles soient relativement exemptes de microorganismes, de toxines ou de prions. La décontamination s'effectue par désinfection, inactivation ou stérilisation. |
| Déplacement | Fait de déplacer (p. ex. amener, apporter, conduire, relocaliser) des personnes, des matières (y compris des matières réglementées) ou des animaux entre deux emplacements du même édifice. Le déplacement peut se faire de différentes manières : à l'intérieur d'une même zone de confinement, vers une autre zone de confinement et vers un autre emplacement dans le même édifice. |
| Désinfectant | Agent chimique ayant la capacité d'éliminer le matériel biologique viable sur les surfaces ou dans les déchets liquides. L'efficacité peut varier selon les propriétés de l'agent chimique, la concentration, la durée de conservation et le temps de contact. |
| Dispositif de confinement primaire | Appareil ou équipement conçu pour empêcher le rejet de matières réglementées et assurer le confinement primaire (c.-à-d. former une barrière physique entre les matières réglementées et la personne et/ou le milieu de travail). Les enceintes de sécurité biologique, les isolateurs, les centrifugeuses munies de godets ou de rotors étanches, l'équipement de procédé, les fermenteurs, les bioréacteurs, les cages de micro-isolation et les étagères à cages ventilées en sont des exemples. |
| Document législatif | Les documents législatifs délivrés par l'Agence de la santé publique du Canada comprennent les suivants :
Les documents législatifs délivrés par l'Agence canadienne d'inspection des aliments s'appliquent aux agents pathogènes non indigènes d'animaux terrestres, aux agents pathogènes d'animaux terrestres présents dans des animaux, des produits ou des sous-produits animaux, ou dans d'autres organismes, et aux animaux infectés ou intoxiqués de manière naturelle ou expérimentale avec un agent pathogène d'animaux terrestres. Ces documents comprennent les suivants :
|
| Enceinte de sécurité biologique (ESB) | Dispositif de confinement primaire qui offre une protection aux membres du personnel, à l'environnement et aux produits (selon la catégorie d'ESB) lors de travaux avec des matières biologiques. |
| Entreposage à long terme | Dans le contexte de la Norme canadienne sur la biosécurité, le fait de posséder des matières réglementées plus de 30 jours après leur réception ou leur création. |
| Équipement de protection individuel (EPI) | Équipement ou vêtement porté par les membres du personnel à titre de barrière afin de réduire le risque d'exposition aux matières biologiques. Des exemples d'EPI comprennent les sarraus, les blouses, les vêtements de protection couvrant toutes les parties du corps, les gants, les chaussures de sécurité, les lunettes de sécurité, les masques et les appareils de protection respiratoire. |
| Espace de travail en laboratoire | Espace à l'intérieur d'une zone de confinement conçu et équipé de façon à pouvoir y mener des activités in vitro (p. ex. à des fins de diagnostic, d'enseignement et de recherche). |
| Évaluation des besoins en matière de formation | Évaluation qui vise à cerner les besoins actuels et futurs en ce qui concerne la formation des membres du personnel de l'installation (c.-à-d. de l'organisation, de la zone de confinement), y compris la formation, la formation de perfectionnement et la requalification, et les lacunes du programme de formation existant. |
| Évaluation des risques associés à l'agent pathogène | Évaluation des caractéristiques inhérentes à un agent biologique (c.-à-d. un microorganisme, une protéine, un acide nucléique, ou une matière biologique en comportant des parties) qui détermine la classification du groupe de risque. Une évaluation des risques associés à l'agent pathogène comporte l'analyse de quatre facteurs de risque clés, y compris la pathogénicité (c.-à-d. l'infectivité et la virulence), les mesures pré- et post-exposition, la transmissibilité et l'impact sur la population animale (c.-à-d. la gamme d'hôtes, la distribution naturelle et l'impact économique). |
| Évaluation des risques de biosûreté | Évaluation des risques qui consiste à définir et à classer par ordre de priorité les matières réglementées et les autres ressources connexes (p. ex. l'équipement, les animaux, les renseignements sensibles, les membres du personnel, le matériel non infectieux), à évaluer la probabilité des menaces, les vulnérabilités et les conséquences associées, ainsi qu'à recommander des stratégies d'atténuation appropriées afin de protéger ces ressources contre des événements de biosûreté. |
| Évaluation globale des risques | Évaluation générale qui appuie le programme de biosécurité dans son ensemble et qui peut comprendre plusieurs zones de confinement au sein d'une organisation. L'évaluation globale des risques détermine quels sont les dangers, les risques et quelles sont les stratégies d'atténuation pour les activités proposées comportant des matières réglementées. Les stratégies d'atténuation et de gestion des risques tiennent compte du type de programme de biosécurité nécessaire pour prévenir l'exposition des membres du personnel aux matières réglementées ainsi que le rejet de celles-ci. |
| Évaluation locale des risques (ELR) | Évaluation propre à un endroit en particulier réalisée pour repérer les dangers associés aux activités menées ainsi qu'aux matières réglementées utilisées. Cette évaluation permet d'élaborer des stratégies d'atténuation des risques et des stratégies de gestion des risques, qui doivent être intégrées aux paramètres de conception relatifs au confinement physique et aux pratiques opérationnelles de l'installation. |
| Événement de biosûreté | Acte délibéré qui implique des matières réglementées, des renseignements sensibles ou de l'équipement qui pourrait causer une maladie ou du tort à des personnes, des animaux ou aux deux, ainsi qu'à l'organisation. |
| Exposition | Contact ou proximité étroite avec des agents pathogènes ou des toxines pouvant respectivement causer une infection ou une intoxication. Les voies d'exposition comprennent l'inhalation, l'ingestion, l'inoculation et l'absorption. |
| Fonction du programme | Description des travaux qui seront effectués dans une zone de confinement. Cette description comprend, entre autres, la portée des travaux (p. ex. des activités de diagnostic, d'enseignement, de recherche, de production à grande échelle, de travail in vitro ou in vivo), la liste des agents pathogènes et des toxines qui seront manipulés ou entreposés, la liste des espèces animales qu'implique le travail in vivo avec des agents pathogènes et des toxines dans la zone de confinement, ainsi que la liste des procédures qui peuvent générer des aérosols. |
| Groupe de risque (GR) | Groupe dans lequel un agent biologique (c.-à-d. un microorganisme, une protéine, un acide nucléique, ou une matière biologique contenant des parties de ceux-ci) est classé en fonction de ses caractéristiques inhérentes, comme la pathogénicité, la virulence, la transmissibilité et l'existence d'un traitement prophylactique ou thérapeutique efficace. Le groupe de risque indique quel est le risque pour la santé des personnes et du public ainsi que pour la santé des animaux et des populations animales. |
| Habilitation de sécurité en vertu de la Loi sur les agents pathogènes humains et les toxines (LAPHT) | Autorisation délivrée par l'Agence de la santé publique du Canada, en vertu de l'article 34 de la LAPHT, à la suite d'une vérification des antécédents et de la cote de fiabilité d'une personne. |
| Haute direction | Autorité ultimement responsable de la délégation appropriée des pouvoirs en matière de biosécurité. La haute direction est chargée de s'assurer que le programme de biosécurité dispose de ressources suffisantes, que les exigences légales sont respectées, que l'ordre de priorité des préoccupations à l'égard de la biosécurité est bien établi et que celles-ci sont abordées adéquatement. |
| Importation | Activité qui consiste à introduire au Canada (p. ex. transférer, transporter) des matières réglementées en provenance d'un autre pays ou juridiction. Dans le contexte de la Norme canadienne sur la biosécurité, ce terme ne s'applique pas aux activités auxquelles la Loi de 1992 sur le transport des marchandises dangereuses s'applique. |
| In vivo | Du latin « dans le vivant »; se rapporte à une expérience menée dans un organisme vivant (p. ex. une étude des effets d'un traitement antibiotique sur des modèles animaux). |
| Incident | Événement ou situation pouvant causer une blessure, du mal, une infection, une intoxication, une maladie ou un dommage. Les accidents et ceux évités de justesse sont considérés comme des incidents. |
| Inspection | Mesures prises dans le but de vérifier si une organisation se conforme ou non à la Loi sur les agents pathogènes humains et les toxines, au Règlement sur les agents pathogènes humains et les toxines, à la Loi sur la santé des animaux et/ou au Règlement sur la santé des animaux, ou afin de prévenir la non-conformité. |
| Installation | Structure, édifice ou espace défini à l'intérieur d'une structure ou d'un édifice dans lesquels sont manipulées ou entreposées des matières réglementées. Il peut s'agir d'un unique laboratoire de recherche ou de diagnostic, d'une aire de production à grande échelle ou d'une zone où des animaux sont hébergés. Ce terme peut également désigner un ensemble de salles de ce type ou un édifice où se trouvent plusieurs espaces de ce type. |
| Intoxication et infection contractée en laboratoire (ICL) | Infection ou intoxication résultant d'une exposition à des agents pathogènes, des matières infectieuses, des animaux infectés ou des toxines manipulés ou entreposés dans la zone de confinement. |
| Inventaire | Liste des ressources biologiques d'une zone de confinement répertoriant les matières réglementées pour leur entreposage à long terme (c.-à-d. plus de 30 jours) à l'intérieur comme à l'extérieur de la zone de confinement. |
| Laboratoire | Espace à l'intérieur d'une installation ou l'installation elle-même où des matières biologiques sont manipulées. |
| Lacune | Observation de non-conformité avec les exigences applicables de la Norme canadienne sur la biosécurité, d'une directive en matière de biosécurité, de la Loi sur les agents pathogènes humains et les toxines, du Règlement sur les agents pathogènes humains et les toxines, de la Loi sur la santé des animaux ou du Règlement sur la santé des animaux. |
| Maladie | Trouble structural ou fonctionnel touchant un humain ou un animal vivant, ou une partie du corps de ceux-ci. Les maladies sont causées par une infection ou une intoxication et se manifestent généralement par des signes et des symptômes caractéristiques. |
| Manipulation ou entreposage | « Manipulation ou entreposage » comprend la possession, la manipulation, l'utilisation, la production, l'entreposage, le transfert, l'importation, l'exportation, le rejet, l'élimination ou l'abandon de matières réglementées, ainsi que le fait de permettre l'accès à de telles substances. Cela comprend donc toutes les activités réglementées comportant des agents pathogènes humains ou des toxines énoncées au paragraphe 7(1) de la Loi sur les agents pathogènes humains et les toxines. Tous les temps de verbe et toutes les variations de « manipulation ou entreposage » sont également utilisés dans ce contexte. |
| Manuel de biosécurité | Ensemble de documents propres à une installation dans lesquels sont décrits les éléments fondamentaux d'un programme de biosécurité (p. ex. le plan de biosûreté, la formation, l'équipement de protection individuel) qui s'appliquent à la zone de confinement. Les renseignements peuvent être présentés sous la forme d'un seul document papier ou électronique ou d'un ensemble de documents. |
| Matière biologique | Microorganismes, protéines ou acides nucléiques pathogènes ou non pathogènes, ou toute autre matière biologique pouvant contenir un de ces éléments, en partie ou en entier, ou d'autres agents infectieux. Les bactéries, les virus, les champignons, les prions, les toxines, les organismes génétiquement modifiés, les acides nucléiques, les échantillons de tissus, les échantillons de diagnostic, les échantillons environnementaux, les vaccins vivants et les isolats d'un agent pathogène ou d'une toxine (p. ex. les cultures pures, les suspensions, les spores purifiées) sont tous des exemples de microorganismes. |
| Matière infectieuse | Tout isolat d'un agent pathogène ou toute matière biologique qui contient des agents pathogènes humains ou des agents zoopathogènes, et qui présente donc un risque pour la santé humaine ou animale. |
| Matière réglementée | Dans le contexte de la Norme canadienne sur la biosécurité, les matières réglementées comprennent :
|
| Membre du personnel autorisé | Personne ayant reçu le droit de pénétrer dans une zone de confinement sans supervision par l'autorité interne responsable (p. ex. le directeur de cette zone, l'agent de la sécurité biologique, une autre personne à laquelle cette responsabilité a été confiée). Pour obtenir ce statut, il faut satisfaire à diverses exigences en matière de formation et faire preuve de compétence envers les procédures opératoires normalisées, selon ce qui est jugé nécessaire par l'installation. |
| Microorganisme | Entité microbiologique cellulaire ou non cellulaire ne pouvant pas raisonnablement être décelable à l'œil nu et ayant la capacité de se répliquer ou de transférer son matériel génétique. Les microorganismes comprennent les bactéries, les champignons, les virus et les parasites, qu'ils soient pathogènes ou non. |
| Niveau de confinement (NC) | Exigences minimales liées au confinement physique et aux pratiques opérationnelles visant la manipulation sécuritaire des matières réglementées dans les laboratoires, les aires de production à grande échelle et les environnements de travail avec des animaux. Il existe quatre niveaux de confinement, allant du niveau de base (c.-à-d. NC1) au niveau le plus élevé (c.-à-d. NC4). |
| Non-conformité | État de non-conformité aux exigences législatives (p. ex. la Loi sur les agents pathogènes humains et les toxines, le Règlement sur les agents pathogènes humains et les toxines, la Loi sur la santé des animaux, le Règlement sur la santé des animaux, les conditions du permis visant des agents pathogènes et des toxines et du permis d'importation d'agents pathogènes d'animaux terrestres). |
| Pathogénicité | Capacité d'un agent pathogène de causer une maladie chez un hôte humain ou animal. |
| Permis | Voir « Permis visant des agents pathogènes et des toxines ». |
| Permis d'importation d'agents pathogènes d'animaux terrestres | Permis délivré par l'Agence de la santé publique du Canada ou l'Agence canadienne d'inspection des aliments permettant, en vertu des alinéas 51a) et 51b) du Règlement sur la santé des animaux, l'importation au Canada d'agents pathogènes d'animaux terrestres ou d'une partie de ceux-ci (p. ex. une toxine); ou d'animaux, de produits ou de sous-produits animaux (p. ex. des tissus, du sérum), ou d'autres organismes porteurs d'un agent pathogène d'animaux terrestres ou d'une partie de celui-ci (p. ex. une toxine). |
| Permis visant des agents pathogènes et des toxines | Autorisation délivrée par l'Agence de la santé publique du Canada :
Dans le même contexte, le terme « permis » est aussi employé. |
| Plan d'intervention d'urgence (PIU) | Document énonçant les mesures à prendre et les parties responsables en cas d'urgence, par exemple en cas : de déversement, d'exposition, ou de rejet de matières réglementées; de fuite d'un animal; de blessure ou de maladie chez un membre du personnel; de panne de courant; ou de toute autre situation d'urgence. |
| Porte critique | Toute porte d'une zone de confinement, d'un box ou d'une salle de nécropsie où le maintien d'un courant d'air vers l'intérieur est exigé. |
| Possibilité de double usage | Propriétés d'un agent pathogène ou d'une toxine, d'une méthode scientifique, de la propriété intellectuelle, ou d'une autre ressource connexe qui leur permettent d'être utilisés autant pour mener des activités scientifiques légitimes (p. ex. à des fins commerciales, médicales ou de recherche) que d'être volontairement mal utilisés pour causer du tort ou une maladie. Les agents pathogènes et les toxines qui pourraient être utilisés comme arme biologique (p. ex. pour du bioterrorisme), une méthode qui facilite la propagation de tels agents pathogènes dans un contexte de laboratoire non traditionnel, ou la découverte qu'une certaine mutation confère une résistance à tous les traitements disponibles sont des exemples de ressources à possibilité de double usage. |
| Prion | Petite particule protéique infectieuse généralement reconnue comme étant impliquée dans le développement d'un certain groupe de maladies neurodégénératives chez l'humain et l'animal, à savoir les encéphalopathies spongiformes transmissibles. |
| Procédure opératoire normalisée (PON) | Document qui normalise, en fonction d'une évaluation locale des risques, les procédures et les pratiques de travail sécuritaires utilisées dans le cadre d'activités réalisées avec des matières réglementées dans une zone de confinement. Les protocoles expérimentaux, les procédures d'entrée et de sortie, les protocoles de décontamination et les procédures d'intervention en cas d'urgence sont des exemples de PON. |
| Production à grande échelle | Activités de production ou de pré-production, y compris des cultures in vitro, qui impliquent des volumes importants de matières réglementées. Les activités à grande échelle diffèrent des activités à l'échelle du laboratoire ou du banc d'essai selon l'équipement utilisé, puisqu'elles sont généralement effectuées dans des fermenteurs, des bioréacteurs et d'autres systèmes fermés. |
| Programme de biosécurité | Programme qui décrit les politiques et les plans institutionnels qui facilitent la manipulation et l'entreposage sécuritaire des matières réglementées, et qui préviennent leur rejet hors de la zone de confinement. Les éléments fondamentaux d'un programme de biosécurité comprennent un manuel de biosécurité, un programme de formation exhaustif, un programme de surveillance médicale, un plan d'intervention d'urgence, des procédures opératoires normalisées et un plan de biosûreté. |
| Programme de surveillance médicale | Programme conçu pour prévenir et déceler les maladies liées à une exposition à des matières réglementées chez les membres du personnel. L'accent est principalement mis sur la prévention, mais le programme prévoit un mécanisme d'intervention par lequel une infection ou une intoxication possible est décelée et traitée avant qu'il n'en résulte une atteinte ou une maladie grave et pour réduire la possibilité de propagation de la maladie dans la communauté. |
| Recherche scientifique | Selon la définition de l'article 1 du Règlement sur les agents pathogènes humains et les toxines, il s'agit d'une enquête ou d'une recherche systématique menée dans un domaine de la science ou de la technologie au moyen d'activités réglementées, telles que :
|
| Rejet | Libération de matières réglementées hors d'un système de confinement ou d'une zone de confinement (p. ex. découlant d'une fuite, d'une pulvérisation, d'un dépôt, d'une décharge, d'une vaporisation). |
| Risque | Probabilité qu'un événement indésirable (p. ex. un accident, un incident, un bris de confinement) survienne et les conséquences de cet événement. |
| Salle de nécropsie | Salle située à l'intérieur de la zone de confinement, où sont menées des nécropsies et des dissections d'animaux à l'extérieur d'un dispositif de confinement primaire. |
| Sas | Salle ou ensemble de salles situées à l'intérieur de la zone de confinement permettant de séparer les espaces « propres » des espaces « sales » (c.-à-d. séparer les zones à plus faible risque de contamination de celles à plus haut risque). Les sas sont utilisés pour franchir la barrière de confinement (entrée et sortie du personnel, du matériel et des animaux), pour entrer dans les salles animalières, les box ou les salles de nécropsie, et en ressortir. La présence d'un sas facilite le maintien des pressions différentielles de l'air négatives dans les zones de confinement où un courant d'air vers l'intérieur est exigé. Le sas peut également fournir un espace approprié aux points d'entrée ou de sortie pour enfiler, retirer et ranger l'équipement de protection individuel dédié et supplémentaire, lorsqu'exigé. |
| Système de décontamination | Équipement dont la capacité à permettre la manipulation sécuritaire de matières en les rendant relativement exemptes de microorganismes, de toxines ou de prions a été validée. Les autoclaves, les incinérateurs, les digesteurs et les systèmes de décontamination des effluents sont des exemples de systèmes de décontamination. |
| Système de décontamination des effluents | Équipement raccordé à la plomberie qui utilise la chaleur ou des procédés chimiques pour décontaminer les déchets liquides (c.-à-d. les effluents) produits dans la zone de confinement avant leur rejet dans les égouts sanitaires. |
| Toxine (microbienne) | Substance toxique produite par un microorganisme, ou dérivée de celui-ci, qui peut avoir des effets graves sur la santé humaine ou animale. Les toxines humaines sont énumérées à l'annexe 1 et à la partie 1 de l'annexe 5 de la Loi sur les agents pathogènes humains et les toxines. |
| Transfert | Changement de possession (c.-à-d. de propriété) de matières réglementées entre des personnes qui travaillent dans une même installation ou dans des installations différentes (c.-à-d. le déplacement hors du ou des endroits énoncés dans le permis visant des agents pathogènes et des toxines ou le permis d'importation d'agents pathogènes d'animaux terrestres vers tout autre endroit). |
| Validation | Fait de confirmer qu'une méthode permet d'atteindre l'objectif souhaité et convient à l'usage auquel elle est destinée grâce à des données probantes objectives. La validation peut être l'observation que des conditions particulières ont été respectées (p. ex. confirmer à l'aide d'indicateurs biologiques, d'indicateurs chimiques ou de dispositifs de surveillance paramétriques situés à des endroits difficiles à décontaminer qu'un cycle précis d'autoclavage peut décontaminer une charge représentative de déchets). |
| Vérification | Surveillance régulière de l'équipement et des procédés visant à confirmer leur efficacité continue entre les validations (p. ex. une mise à l'essai de la performance d'un autoclave en utilisant des indicateurs biologiques, la visualisation des jauges de courant d'air pour confirmer la fonction du ventilateur d'une enceinte de sécurité biologique). La comparaison de l'exactitude d'une pièce d'équipement avec celle prévue par une norme ou une procédure opératoire normalisée applicable est un exemple de vérification. |
| Zone de confinement | Espace physique qui répond aux exigences liées à un niveau de confinement donné. Il peut s'agir d'une salle unique (p. ex. un laboratoire de niveau de confinement 2 [NC2]), d'une série de salles situées dans un même endroit (p. ex. plusieurs espaces de travail en laboratoire de NC2 non adjacents, mais verrouillables) ou d'une série de salles adjacentes (p. ex. des salles de NC3 comprenant des espaces de laboratoire réservés à certaines activités et des salles animalières ou des box séparés). Les espaces réservés au soutien de la zone, y compris les sas équipés de douches, les vestiaires « propres » et les vestiaires « sales », là où ils sont exigés, font partie de la zone de confinement. |
| Zone de confinement de gros animaux (Zone GA) | Zone de confinement d'animaux constituée d'une ou de plusieurs salles voisines ou adjacentes de niveau de confinement identique, où des animaux sont hébergés dans des box (c.-à-d. que la salle elle-même sert de confinement primaire). Une zone GA peut comprendre des box qui hébergent de gros animaux, comme du bétail ou des cervidés, ou des box qui hébergent de petits animaux, comme des souris ou des ratons laveurs, dans des cages ouvertes et non des cages de confinement primaire. Les salles de nécropsie, lorsqu'elles sont présentes, sont considérées comme faisant partie d'une zone GA. |
6. Références
- Note de bas de page 1
-
Règlement sur les agents pathogènes humains et les toxines (DORS/2015-44).
- Note de bas de page 2
-
Règlement sur la santé des animaux (C.R.C., ch. 296).
- Note de bas de page 3
-
Gouvernement du Canada. (2010). Normes relatives au confinement des installations manipulant des agents pathogènes d'animaux aquatiques, 1re éd, Ottawa, ON, Canada : Gouvernement du Canada. Disponible à l'adresse https://www.inspection.gc.ca/sante-des-animaux/animaux-aquatiques/importation/pathogenes/installations/fra/1377962925061/1377963021283
- Note de bas de page 4
-
Gouvernement du Canada. (2007). Normes sur le confinement des installations manipulant des phytoravageurs, 1re éd, Ottawa, ON, Canada : Gouvernement du Canada. Disponible à l'adresse https://www.inspection.gc.ca/protection-des-vegetaux/phytoravageurs-especes-envahissantes/bioconfinement/normes-sur-le-confinement/fra/1412353866032/1412354048442.
- Note de bas de page 5
-
Règlement sur les renseignements concernant les substances nouvelles (organismes) (DORS/2005-248).
- Note de bas de page 6
-
Gouvernement du Canada. Directives et avis en matière de biosécurité. Disponible à l'adresse https://www.canada.ca/fr/sante-publique/services/biosecurite-biosurete-laboratoire/directives-avis-avis-speciaux-matiere-biosecurite.html
- Note de bas de page 7
-
CEN Workshop 55 ‒ CEN Workshop Agreement (CWA) 16393:2012, Laboratory biorisk management - Guidelines for the implementation of CWA 15793:2008. (2012). Bruxelles, Belgique : Comité européen de normalisation.
- Note de bas de page 8
-
Burnett, L. C. (2006). Biological safety program management. Dans Fleming, D. O. et Hunt, D. L. (éds.). Biological safety : Principles and practices, 4e éd., p. 405-415, Washington, DC, États-Unis : ASM Press.
- Note de bas de page 9
-
ISO 14001:2015, Systèmes de management environnemental - Exigences et lignes directrices pour son utilisation. (2015). Genève, Suisse : Organisation internationale de normalisation.
- Note de bas de page 10
-
Gouvernement du Canada. (2022). Norme canadienne sur la biosécurité, 3e éd., Ottawa, ON, Canada : Gouvernement du Canada. Disponible à l'adresse : https://www.canada.ca/fr/sante-publique/services/normes-lignes-directrices-canadiennes-biosecurite/troisieme-edition.html
- Note de bas de page 11
-
Perkins, D., Danskin, K. et Rowe, A. E. (2017). Fostering an International Culture of Biosafety, Biosecurity, and Responsible Conduct in the Life Sciences. Science & Diplomacy, 6(3).
- Note de bas de page 12
-
Gouvernement du Canada. (2015). Plan de surveillance administrative à l'égard des agents pathogènes et des toxines dans un contexte de recherche ‒ Éléments requis et lignes directrices, Ottawa, ON, Canada : Gouvernement du Canada. Disponible à l'adresse https://www.canada.ca/fr/sante-publique/services/biosecurite-biosurete-laboratoire/programme-delivrance-permis/plan-surveillance-administrative-a-egard-agents-pathogenes-toxines-contexte-recherche-elements-requis-lignes-directrices.html
- Note de bas de page 13
-
Loi sur les agents pathogènes humains et les toxines (L.C. 2009, ch. 24).
- Note de bas de page 14
-
Règlement canadien sur la santé et la sécurité au travail (DORS/86-304).
- Note de bas de page 15
-
Red River College. (2019). Biological Safety Manual. Page consultée le 15 décembre 2022 à l'adresse https://www.rrc.ca/wp-content/uploads/sites/36/2019/12/Biosafety-Manual-2019.pdf
- Note de bas de page 16
-
Doran, G.T. (1981). There's a S.M.A.R.T. way to write management's goals and objectives. Management Review, 70 (11):35-36.
- Note de bas de page 17
-
Gouvernement du Canada. (2018). Ligne directrice canadienne sur la biosécurité : Évaluation locale des risques. Ottawa, ON, Canada : Gouvernement du Canada. Disponible à l'adresse https://www.canada.ca/fr/sante-publique/services/normes-lignes-directrices-canadiennes-biosecurite/directrices.html
- Note de bas de page 18
-
Gouvernement du Canada. (2018). Ligne directrice canadienne sur la biosécurité : Évaluation des risques associés à l'agent pathogène. Ottawa, ON, Canada : Gouvernement du Canada. Disponible à l'adresse https://www.canada.ca/fr/sante-publique/services/normes-lignes-directrices-canadiennes-biosecurite/directrices.html
- Note de bas de page 19
-
Gouvernement du Canada. (2018). Ligne directrice canadienne sur la biosécurité : Effectuer une évaluation des risques de biosûreté. Ottawa, ON, Canada : Gouvernement du Canada. Disponible à l'adresse https://www.canada.ca/fr/sante-publique/services/normes-lignes-directrices-canadiennes-biosecurite/directrices.html
- Note de bas de page 20
-
United States Department of Labor. (date inconnue). Hazard identification and assessment. Page consultée le 22 décembre 2022 à l'adresse https://www.osha.gov/safety-management/hazard-Identification
- Note de bas de page 21
-
Gouvernement du Canada. Fiche technique santé-sécurité : agents pathogènes. Disponible à l'adresse https://www.canada.ca/fr/sante-publique/services/biosecurite-biosurete-laboratoire/fiches-techniques-sante-securite-agents-pathogenes-evaluation-risques.html
- Note de bas de page 22
-
Gouvernement du Canada. ePATHogène - la base de données sur les groupes de risque. Disponible à l'adresse https://health.canada.ca/fr/epathogene
- Note de bas de page 23
-
Gouvernement du Canada. (2016). Ligne directrice canadienne sur la biosécurité : Élaboration d'un plan de biosûreté exhaustif. Ottawa, ON, Canada : Gouvernement du Canada. Disponible à l'adresse https://www.canada.ca/fr/sante-publique/services/normes-lignes-directrices-canadiennes-biosecurite/directrices.html
- Note de bas de page 24
-
Gouvernement du Canada. Portail de la formation de l'ASPC. Disponible à l'adresse https://training-formation.phac-aspc.gc.ca/?lang=fr
- Note de bas de page 25
-
Gouvernement du Canada. Guide canadien d'immunisation. Disponible à l'adresse https://www.canada.ca/fr/sante-publique/services/guide-canadien-immunisation.html
- Note de bas de page 26
-
United States Department of Health and Human Services, United States Centers for Disease Control and Prevention et United States National Institutes of Health. (2020). Biosafety in Microbiological and Biomedical Laboratories, 6e éd., Washington, DC, États-Unis : United States Government Printing Office.
- Note de bas de page 27
-
ISO 14004:2016, Systèmes de management environnemental - Lignes directrices générales pour la mise en application. (2016). Genève, Suisse : Organisation internationale de normalisation.
- Note de bas de page 28
-
CSA Z317.10:F15 Manipulation des déchets de soins de santé. (C2020). Toronto, ON, Canada : Association canadienne de normalisation.
- Note de bas de page 29
-
Project Managements Docs. (date inconnue). Communications Management Plan Template. Page consultée le 15 décembre 2022 à l'adresse http://www.projectmanagementdocs.com/project-planning-templates/communications-management-plan.html#axzz5LjAzhyVV
- Note de bas de page 30
-
Pentella, M. A. (2017). Components of a Biosafety Program for a Clinical Laboratory. Dans Wooley, D. P. et Byers, K. B. (éds.). Biological safety: Principles and practices, 5e éd., p. 687-694, Washington, DC, États-Unis : ASM Press.
- Note de bas de page 31
-
Laserfiche. (date inconnue). What's the Difference Between Document and Records Management? Page consultée le 15 décembre 2022 à l'adresse https://www.laserfiche.com/ecmblog/whats-the-difference-between-document-and-records-management/
- Note de bas de page 32
-
Quality Progress. (2005). Corrective vs. Preventive Action. Page consultée le 5 janvier 2023 à l'adresse http://asq.org/quality-progress/2005/03/problem-solving/corrective-vs-preventive-action.html