La tuberculose : La résistance aux antituberculeux au Canada – 2014
Remerciements
La Division de surveillance de la santé et de l'épidémiologie de l'Agence de la santé publique du Canada tient à remercier les membres du Réseau technique canadien de laboratoires de tuberculose et leurs équipes, ainsi que les collègues du Laboratoire national de microbiologie, pour leur contribution et leur participation au Système canadien de surveillance des laboratoires de tuberculose.
Table des matières

Télécharger le format de rechange
(Format PDF, 1,42 Mo, 60 pages)
Sujets connexes
Liste des figures
- Figure 1 : Nombre d'isolats du complexe Mycobacterium tuberculosis testés, par province ou territoire d'origine : 2014
- Figure 2 : Pourcentage des isolats présentant une certaine résistance à l'isoniazide, à la pyrazinamide, à la rifampicine, et à l'éthambutol, 2014
- Figure 3 : Pourcentage des isolats présentant une certaine résistance à l'isoniazide, à la pyrazinamide, à la rifampicine, et à l'éthambutol, de 2004 à 2014
- Figure 4 : Profils de résistance aux antituberculeux selon le pourcentage d'isolats testés, 2014
- Figure 5 : Profils de résistance aux antituberculeux selon le pourcentage d'isolats testés, 2004 à 2014
Liste des tableaux
- Tableau 1 :Concentrations critiques pour les épreuves courantes de sensibilité aux antituberculeux
- Tableau 2 : Nombre d'isolats du complexe Mycobacterium tuberculosis déclarés par province/territoire de déclaration et d'origin, 2014
- Tableau 3 : Nombre total d'isolats du complexe Mycobacterium tuberculosis et nombre et pourcentage d'entre eux présentant une certaine résistance, tels que les isolats de tuberculose multirésistante et de tuberculose ultrarésistante, déclarés au Canada, de 2004 à 2014
- Tableau 4 : Profil général de résistance aux antituberculeux déclarée au Canada, de 2004 à 2014
- Tableau 5 : Résultats des épreuves systématiques de sensibilité aux antituberculeux des isolats du complexe Mycobacterium tuberculosis en Alberta, de 2004 à 2014
- Tableau 6 : Résultats des épreuves systématiques de sensibilité aux antituberculeux des isolats du complexe Mycobacterium tuberculosis en Colombie-Britannique, de 2004 à 2014
- Tableau 7 : Résultats des épreuves systématiques de sensibilité aux antituberculeux des isolats du complexe Mycobacterium tuberculosis au Manitoba, de 2004 à 2014
- Tableau 8 : Résultats des épreuves systématiques de sensibilité aux antituberculeux des isolats du complexe Mycobacterium tuberculosis au Nouveau-Brunswick, de 2004 à 2014
- Tableau 9 : Résultats des épreuves systématiques de sensibilité aux antituberculeux des isolats du complexe Mycobacterium tuberculosis à Terre-Neuve-et-Labrador, de 2004 à 2014
- Tableau 10 : Résultats des épreuves systématiques de sensibilité aux antituberculeux des isolats du complexe Mycobacterium tuberculosis aux Territoires du Nord-Ouest, de 2004 à 2014
- Tableau 11 : Résultats des épreuves systématiques de sensibilité aux antituberculeux des isolats du complexe Mycobacterium tuberculosis en Nouvelle-Écosse, de 2004 à 2014
- Tableau 12 : Résultats des épreuves systématiques de sensibilité aux antituberculeux des isolats du complexe Mycobacterium tuberculosis au Nunavut, de 2004 à 2014
- Tableau 13 : Résultats des épreuves systématiques de sensibilité aux antituberculeux des isolats du complexe Mycobacterium tuberculosis en Ontario, de 2004 à 2014
- Tableau 14 : Résultats des épreuves systématiques de sensibilité aux antituberculeux des isolats du complexe Mycobacterium tuberculosis à l'Île-du-Prince-Édouard, de 2004 à 2014
- Tableau 15 : Résultats des épreuves systématiques de sensibilité aux antituberculeux des isolats du complexe Mycobacterium tuberculosis au Québec, de 2004 à 2014
- Tableau 16 : Résultats des épreuves systématiques de sensibilité aux antituberculeux des isolats du complexe Mycobacterium tuberculosis en Saskatchewan, de 2004 à 2014
- Tableau 17 : Résultats des épreuves systématiques de sensibilité aux antituberculeux des isolats du complexe Mycobacterium tuberculosis au Yukon, de 2004 à 2014
- Tableau 18 : Isolats de tuberculose multirésistante et de tuberculose ultrarésistante déclarés par province/territoire d'origine, 2014
- Tableau 19 : Répartition provinciale/territoriale des isolats de tuberculose résistante de tout type, de tuberculose multirésistante et de tuberculose ultrarésistante au Canada, de 2004 à 2014
- Tableau 20 : Résistance aux antituberculeux par sexe et par groupe d'âge au Canada, 2014
Liste des annexes
Acronymes et abréviations
- Alb.
- Alberta
- AK
- Amikacine
- ASPC
- Agence de la santé publique du Canada
- BCG
- Bacille de Calmette-Guérin
- C.-B.
- Colombie-Britannique
- CLSI
- Clinical and Laboratory Standards Institute
- CM
- Capréomycine
- CMTB
- Complexe Mycobacterium tuberculosis
- CNRM
- Centre national de référence en mycobactériologie
- EMB
- Éthambutol
- ETH
- Éthionamide
- Î.-P.-É.
- Île-du-Prince-Édouard
- IC
- Intervalle de confiance
- INH
- Isoniazide
- KM
- Kanamycine
- LIN
- Linézolide
- M. africanum
- Mycobacterium africanum
- M. bovis
- Mycobacterium bovis
- M. canetti
- Mycobacterium canetti
- M. caprae
- Mycobacterium caprae
- M. microti
- Mycobacterium microti
- M. pinnipedii
- Mycobacterium pinnipedii
- M. tuberculosis
- Mycobacterium tuberculosis
- Man.
- Manitoba
- MOX
- Moxifloxacine
- N.-B.
- Nouveau-Brunswick
- N.-É.
- Nouvelle-Écosse
- Nt
- Nunavut
- OFL
- Ofloxacine
- Ont.
- Ontario
- PAS
- Acide para-aminosalicylique
- ProvLab
- Laboratoire provincial de santé publique (Alberta)
- PZA
- Pyrazinamide
- Qc
- Québec
- RBT
- Rifabutine
- RLSPC
- Réseau des laboratoires de santé publique du Canada
- RMP
- Rifampicine
- RTCLT
- Réseau technique canadien des laboratoires de tuberculose
- Sask.
- Saskatchewan
- SCSLT
- Système canadien de surveillance des laboratoires de tuberculose
- SM
- Streptomycine
- T.-N.-L.
- Terre-Neuve-et-Labrador
- T.N.-O.
- Territoires du Nord-Ouest
- TB
- Tuberculose
- TB-MR
- Tuberculose multirésistante
- TB-UR
- Tuberculose ultrarésistante
- Yn
- Yukon
Introduction
Les souches de bacilles tuberculeux pharmacorésistantes menacent grandement de saper les efforts de prévention et de lutte contre la tuberculose (TB) au Canada. Bien que la tuberculose pharmacorésistante ne soit pas encore considérée comme étant un problème majeur au Canada, elle représente tout de même un problème potentiel, puisque les Canadiens voyagent fréquemment à l'étranger et de nombreuses personnes s'établissant au Canada proviennent de pays où l'incidence de la tuberculose, de même que la pharmacorésistance associée, sont élevées.
Le Système canadien de surveillance des laboratoires de tuberculose (SCSLT) a été créé en 1998 en réponse à une inquiétude grandissante à l'échelle mondiale à l'égard de la résistance aux antituberculeux. Il a été mis sur pied par la Division de la lutte antituberculeuse de Santé Canada du Bureau du VIH/sida, des MTS et de la tuberculose du Laboratoire de lutte contre la maladie, en collaboration avec le Réseau technique canadien des laboratoires de tuberculose (RTCLT) et les laboratoires participants. Le SCSLT a été conçu pour surveiller les tendances et les profils émergents de la résistance aux antituberculeux au Canada et est actuellement géré par l'Agence de la santé publique du Canada (ASPC).
Le présent rapport fait partie d'une série de rapports de surveillance annuels qui contiennent les données recueillies au moyen du SCSLT. Plus précisément, le présent rapport fournit des détails sur le niveau global de résistance aux antituberculeux déclaré au Canada pour la période de 2004 à 2014; une attention particulière ayant été accordée à l'année 2014.
Les données présentées dans ce rapport serviront de base aux mesures de santé publique, ainsi qu'à l'élaboration et à l'évaluation des politiques et des programmes en la matière.
Contexte
Profils de pharmacorésistance
La résistance aux antituberculeux est déterminée au moyen d'épreuves de sensibilité d'échantillons cliniques prélevés chez des personnes atteintes de tuberculose à culture positiveNote de bas de page 1. On dit que les personnes atteintes présentent une tuberculose pharmacorésistante si la souche de Mycobacterium tuberculosis responsable de leur maladie est résistante à un ou plusieurs des quatre antituberculeux majeurs, à l'isoniazide, à la rifampicine, à la pyrazinamide ou à l'éthambutol. Les profils de résistance suivants sont décrits dans le présent rapport :
- Monorésistance - résistance à un seul antituberculeux majeur (isoniazide, rifampicine, éthambutol ou pyrazinamide).
- Polyrésistance (autres profils) - résistance à plus d'un antituberculeux majeur, à l'exclusion de la résistance à la fois à l'isoniazide et à la rifampicine.
- Tuberculose multirésistante (TB-MR) - résistance à l'isoniazide et à la rifampicine avec ou sans résistance à d'autres antituberculeux.
- Tuberculose ultrarésistante (TB-UR) - tuberculose résistante à l'isoniazide et à la rifampicine ainsi qu'à une fluoroquinolone et à au moins un des trois antituberculeux mineurs injectables (amikacine, capréomycine ou kanamycine).Note de bas de page 2
Normes et épreuves de résistance aux antituberculeux au Canada
Le RTCLT a pour mission de promouvoir l'excellence, la standardisation et l'assurance de la qualité dans les services de mycobactériologie. Il consiste en un réseau pancanadien composé de directeurs techniques ou scientifiques de laboratoires de tuberculose provinciaux et territoriaux (Annexe I).
Les objectifs du RTCLT sont les suivants :
- normaliser les méthodologies de laboratoire;
- améliorer les pratiques opérationnelles et les exigences physiques en matière de biosécurité;
- mettre en œuvre des lignes directrices en matière de biosécurité;
- participer aux programmes nationaux de surveillance et de vérification de la compétence;
- échanger des services et des renseignements sur les nouvelles technologies.
Au Canada, les méthodes d'analyse en laboratoire, y compris le choix des médicaments et des concentrations critiques utilisés lors d'épreuves systématiques de sensibilité aux antituberculeux, sont conformes aux normes de laboratoire recommandées.Note de bas i, Note de bas de page 3,Note de bas de page 4 Les laboratoires participants du RTCLT évaluent systématiquement la sensibilité des isolats de Mycobacterium tuberculosis ou du complexe Mycobacterium tuberculosis (CMTB) aux antituberculeux majeurs au moyen de la méthode fluorométrique BACTEC® MGIT 960. Le tableau 1 présente la liste des antituberculeux majeurs et mineurs recommandés et les concentrations critiques recommandées pour les analyses.Note de bas de page 3,Note de bas de page 4
Les épreuves de sensibilité aux antituberculeux mineurs varient selon les provinces et territoires. En règle générale, les isolats sont soumis à des tests de résistance à l'amikacine, à la kanamycine, à la capréomycine, à l'éthionamide, au linézolide, à l'ofloxacine, à la moxifloxacine, à l'acide para-aminosalicylique et à la rifabutine.
Méthodologie
Aperçu du Système canadien de surveillance des laboratoires de tuberculose
Le SCSLT est un système de surveillance basé sur les isolats qui vise à recueillir des données sur la résistance aux antituberculeux dans tout le Canada. Les résultats des épreuves de sensibilité de tous les isolats uniques ayant été soumis à ces épreuves au cours de l'année civile précédente sont soumis volontairement chaque année par les laboratoires de tuberculose provinciaux à l'ASPC aux fins d'intégration dans le SCSLT. Parmi les laboratoires participants figurent les membres du RTCLT (qui représentent toutes les provinces et tous les territoires).
La collecte des données destinées au SCSLT s'effectue au moyen d'un formulaire de déclaration standard (Annexe II) rempli manuellement ou transmis par voie électronique. Des procédures normalisées d'enregistrement des données sont appliquées à toutes les données afin de créer un ensemble de données nationales. Les renseignements suivants sont soumis à l'ASPC :
- date de réception de l'isolat ou de l'échantillon au laboratoire;
- numéro d'identification de l'échantillon fourni par le laboratoire;
- province ou territoire où l'isolat a été testé;
- province ou territoire d'où provient l'isolat;
- sexe de la personne dont provient l'isolat;
- date de naissance de la personne dont provient l'isolat ou âge au moment de l'analyse;
- résultats des épreuves de sensibilité (médicament testé et concentration de médicament testée).
Les données sont soumises pour tous les cas confirmés pour lesquels le CMTB, y compris les espèces M. tuberculosis, M. africanum, M. canetti, M. caprae, M. microti, M. pinnipedii ou M. bovis, a été mis en évidence par culture. Les résultats peuvent être soumis au niveau de l'espèce ou au niveau du CMTB uniquement sans identification de l'espèce. Certains laboratoires soumettent également des résultats pour la souche M. bovis BCG, reliée à des complications survenant à la suite d'un vaccin contre la tuberculose, souvent observées chez les patients immunodéprimés. Ces résultats sont exclus du présent rapport, étant donné que cette souche n'est pas infectieuse.
Tous les laboratoires participants effectuent des épreuves de résistance à l'isoniazide, à l'éthambutol et à la rifampicine, des antituberculeux majeurs. Bien que, en vertu des Normes canadiennes pour la lutte antituberculeuse (7e édition), les laboratoires doivent procéder à des épreuves de sensibilité à la pyrazinamideNote de bas de page 1, la Colombie-Britannique n'évalue pas systématiquement la résistance à ce médicament. Cependant, si une résistance à un antituberculeux majeur est détectée, la Colombie-Britannique analysera alors les isolats pour évaluer la résistance à la pyrazinamide.
Sont ensuite soumis les résultats des épreuves de sensibilité aux antituberculeux mineurs des isolats présentant une résistance à l'isoniazide et à la rifampicine. Afin d'écarter la possibilité de tuberculose ultrarésistante, les laboratoires doivent déclarer les résultats pour au moins une des fluoroquinolones (ofloxacine, moxifloxacine ou levofloxacine) et au moins un des antituberculeux injectables (amikacine, kanamycine et capréomycine).
Tous les provinces et territoires n'ont pas la capacité d'effectuer des épreuves de sensibilité aux médicaments. Ceux qui n'ont pas cette capacité assurent la préparation des isolats et les transmettent à d'autres laboratoires provinciaux aux fins d'analyse. Dans certains cas, le laboratoire qui analyse l'échantillon soumet les résultats à l'ASPC au nom de la province ou du territoire d'origine.
Le Laboratoire de santé publique et de référence en microbiologie du Centre de contrôle des maladies de la Colombie-Britannique procède aux épreuves de sensibilité aux antituberculeux majeurs et rend compte de leurs résultats pour la Colombie-Britannique et le Yukon. Le Laboratoire provincial de santé publique (ProvLab) de l'Alberta effectue les tests sur les isolats et communique les résultats pour l'Alberta et les Territoires du Nord-Ouest, tandis que le Laboratoire central de santé publique de l'Ontario effectue les tests et communique les résultats pour l'Ontario et le Nunavut. Le Centre national de référence en mycobactériologie (CNRM)Note de bas ii, au Manitoba, effectue les épreuves de sensibilité aux antituberculeux majeurs pour le compte de Terre-Neuve-et-Labrador, du Manitoba, du Nouveau-Brunswick, de la Nouvelle-Écosse et de l'Île-du-Prince-Édouard. Dans ce cas, le Centre renvoie les résultats des tests à la province d'origine, qui soumet elle-même ses résultats à l'ASPC. Toutes les autres provinces effectuent leurs propres épreuves de sensibilité et ne déclarent pas systématiquement les résultats au nom d'une autre province ou d'un autre territoire.
Au Canada, quatre laboratoires procèdent à des épreuves de sensibilité aux antituberculeux mineurs : le ProvLab de l'Alberta, le Laboratoire central de santé publique de l'Ontario, le Laboratoire de santé publique du Québec et le CNRM. Ce dernier évalue la sensibilité des isolats aux antituberculeux mineurs pour tous les territoires et provinces qui ne sont pas équipés pour effectuer ces épreuves dans leurs propres laboratoires. Sur demande, le Centre national de référence en mycobactériologie peut également analyser des isolats soumis par un laboratoire provincial afin de confirmer le profil de résistance. Les résultats des tests réalisés par le CNRM sont retournés au laboratoire provincial ayant soumis les isolats aux fins d'analyse, puis le laboratoire transmet ces résultats à l'ASPC.
Tableaux et présentation des résultats
Le présent rapport fournit un aperçu de la résistance aux antituberculeux observée au Canada pour la période de 2004 à 2014. Certaines données sont présentées par province ou territoire ainsi que par âge et par sexe, dans la mesure du possible. Les données de 2014 (la dernière année de déclaration pour laquelle des données sont disponibles) sont mises en évidence, de même que les tendances importantes dans le temps.
Les données présentées dans le présent rapport ont été extraites de la base de données du SCSLT le 30 mars 2015 et ont été validées par le laboratoire déclarant. Les résultats des cultures positives obtenues au cours d'une année civile sont comptabilisés dans les statistiques de l'année en question; les résultats obtenus ultérieurement sont consignés dans le rapport de l'année suivante. Par exemple, si le laboratoire a reçu un échantillon le 20 décembre 2014 et que la croissance de M. tuberculosis n'a été observée qu'en janvier 2015, ces résultats seront inclus dans le rapport de 2015.
Il est possible d'obtenir les échantillons soumis au laboratoire pour les épreuves de sensibilité aux antituberculeux dès que le patient reçoit le diagnostic ou à tout moment durant le traitement. Selon la durée du traitement, un patient pourrait subir de nombreux tests pendant plusieurs années. C'est pourquoi le nombre d'isolats décrits dans le présent rapport n'équivaut pas au nombre de cas à culture positive déclarés au moyen du système de surveillance des cas au cours de la même période. En effet, un cas de tuberculose à culture positive n'est déclaré qu'une fois, au cours de l'année du diagnostic, mais la résistance aux antituberculeux peut être évaluée de façon répétée pendant plusieurs années, jusqu'à ce que le cas soit guéri ou que le traitement prescrit soit terminé. S'il est confirmé que deux échantillons proviennent de la même personne au cours d'une année civile donnée, seul le résultat de sensibilité le plus récent est conservé.
Aucune procédure statistique n'a été utilisée pour les analyses comparatives du présent rapport et aucune technique statistique n'a été appliquée pour tenir compte des données manquantes. Les données des tableaux contenant de petites cellules (n ≤ 5) n'ont pas été supprimées puisqu'elles ne semblaient pas présenter de risque d'identification de cas individuels. Ces procédures sont conformes à la directive de l'ASPC sur la collecte, l'utilisation et la diffusion de l'information sur la santé publiqueNote de bas de page 5.
Résultats
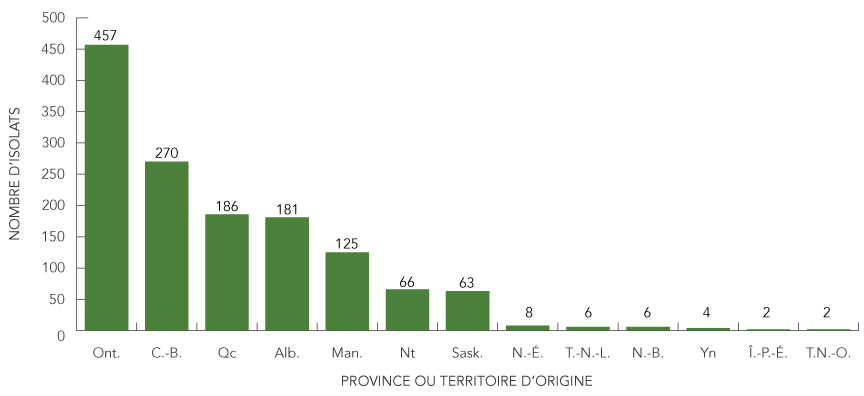
En 2014, les résultats des épreuves de sensibilité aux antituberculeux de 1 393 isolats ont été communiqués à l'ASPC. Parmi ces isolats, 790 (56,7 %) ont été déclarés comme faisant partie d'un CMTB dont l'espèce était connue (786 étaient identifiés comme M. tuberculosis, deux comme M. africanum et deux comme M. bovis), et 586 (42,1 %) ont été déclarés comme appartenant à un CMTB d'une espèce inconnue. Dix-sept isolats (1,2 %) étaient identifiés comme M. bovis BCG (13 provenant de l'Ontario, trois de l'Alberta et un du Manitoba) et ont été exclus des analyses ultérieures (données non représentées). Les résultats de laboratoire de 1 376 isolats du CMBT ont été analysés aux fins du présent rapport. Le tableau 2 présente la répartition du nombre d'isolats par province ou territoire de signalement ou d'origine. La figure 1 illustre le nombre d'isolats du CMBT testés par province ou territoire d'origine.
Figure 1 : Nombre d'isolats du complexe Mycobacterium tuberculosis testés par province ou territoire d'origine, 2014
Description de la figure 1
Le graphique à barres présente la répartition du nombre d'isolats testés par province ou territoire d'origine. L'axe horizontal représente les provinces et les territoires. L'axe vertical représente le nombre d'isolats de 0 à 500, par tranche de 50.
En ordre décroissant, le nombre d'isolats testés par province ou territoire d'origine pour 2014 se présentait comme suit :
| Province ou territoire d'origine | Nombre d'isolats déclarés |
|---|---|
| Ontario | 457 |
| Colombie-Britannique | 270 |
| Québec | 186 |
| Alberta | 181 |
| Manitoba | 125 |
| Nunavut | 66 |
| Saskatchewan | 63 |
| Nouvelle-Écosse | 8 |
| Terre-Neuve-et-Labrador | 6 |
| Nouveau-Brunswick | 6 |
| Yukon | 4 |
| Île-du-Prince-Édouard | 2 |
| Territoires du Nord-Ouest | 2 |
Pour la période de 2004 à 2014, des résultats d'épreuves de sensibilité ont été déclarés pour 14 813 isolats (tableau 3). Entre 2004 et 2014, 1 382 (9,3 %) des isolats testés présentaient une résistance à un ou plusieurs antituberculeux majeurs, 168 (1,1 %) étaient multirésistants et sept (< 0,1 %) étaient ultrarésistants (tableau 3).
Résistance aux antituberculeux majeurs
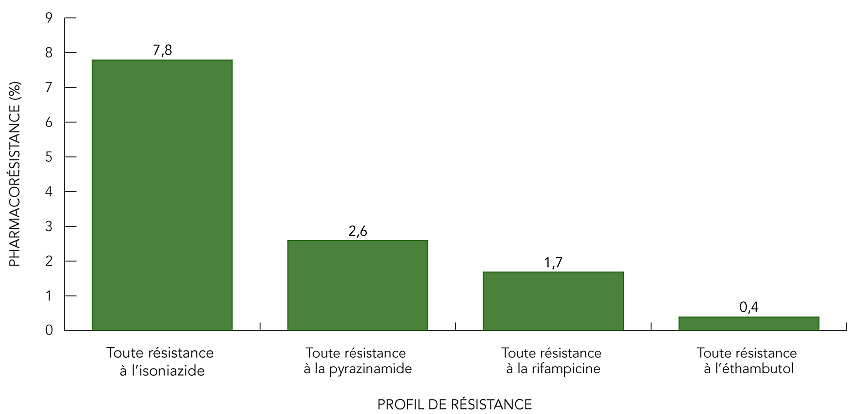
En 2014, les 1 376 isolats du CMTB ont tous fait l'objet d'une épreuve de sensibilité à l'isoniazide, à la rifampicine et à l'éthambutol, et 1 143 isolats (83 %) ont été soumis à une épreuve de sensibilité à la pyrazinamide (tableau 4). Cent sept (7,8 %) isolats testés étaient résistants à l'isoniazide, 30 (2,6 %) étaient résistants à la pyrazinamide, 24 (1,7 %) étaient résistants à la rifampicine et six (0,4 %) étaient résistants à l'éthambutol (figure 2).
Figure 2 : Pourcentage des isolats présentant une certaine résistance à l'isoniazide, à la pyrazinamide, à la rifampicine et à l'éthambutol, 2014
Description de la figure 2
Le graphique à barres indique le pourcentage du nombre total d'isolats présentant une résistance à chacun des quatre antituberculeux majeurs. L'axe horizontal représente les médicaments testés; de gauche à droite, l'isoniazide (INH), la pyrazinamide (PZA), la rifampicine (RMP) et l'éthambutol (EMB). L'axe vertical représente le pourcentage de pharmacorésistance de 0 à 9 %, par tranche de 1 %.
| Profil de résistance | Pharmacorésistance (%) |
|---|---|
| Toute résistance à l'isoniazide | 7,8 % |
| Toute résistance à la pyrazinamide | 2,6 % |
| Toute résistance à la rifampicine | 1,7 % |
| Toute résistance à l'éthambutol | 0,4 % |
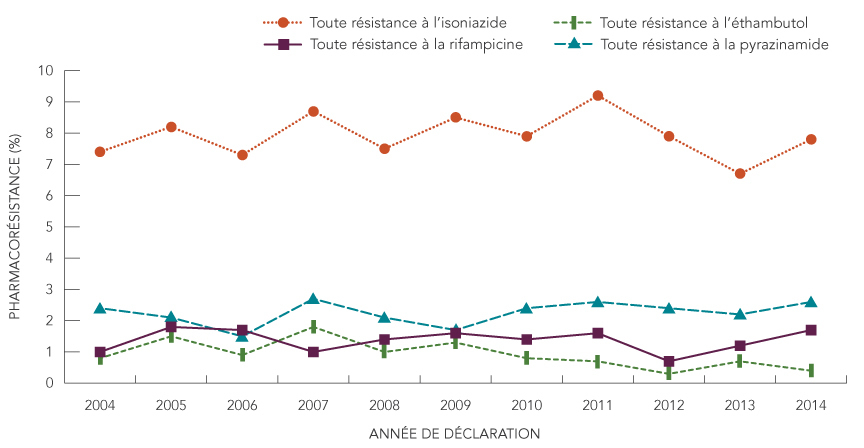
La figure 3 présente l'évolution dans le temps du pourcentage d'isolats résistants à chacun des antituberculeux majeurs pour la période de 2004 à 2014. On a constaté une très faible variation de la proportion d'isolats présentant une certaine résistance. Pour la période de 2004 à 2014, 7,9 % (plage : 6,7 % à 9,2 %) de tous les isolats testés étaient résistants à l'isoniazide (tableau 4). La résistance à l'éthambutol, à la rifampicine et à la pyrazinamide est demeurée inférieure à 3 %.
Figure 3 : Pourcentage des isolats présentant une certaine résistance à l'isoniazide, à la pyrazinamide, à la rifampicine et à l'éthambutol, de 2004 à 2014
Description de la figure 3
Le graphique linéaire affiche le pourcentage d'isolats présentant une résistance à chacun des quatre antituberculeux majeurs de 2004 à 2014. Chaque ligne représente l'un des quatre médicaments. L'axe horizontal représente l'année de déclaration de 2004 à 2014. L'axe vertical représente le pourcentage de pharmacorésistance de 0 à 10 %, par tranche de 1 %.
Le pourcentage d'isolats indiquant une certaine résistance à l'isoniazide, à la rifampicine, à l'éthambutol et à la pyrazinamide pour la période de 2004 à 2014, se présente comme suit :
| Pharmacorésistance ( %) | Année de déclaration | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| 2004 | 2005 | 2006 | 2007 | 2008 | 2009 | 2010 | 2011 | 2012 | 2013 | 2014 | |
| Toute résistance à l'isoniazide | 7,4 % | 8,2 % | 7,3 % | 8,7 % | 7,5 % | 8,5 % | 7,9 % | 9,2 % | 7,9 % | 6,7 % | 7,8 % |
| Toute résistance à la rifampicin | 1,0 % | 1,8 % | 1,7 % | 1,0 % | 1,4 % | 1,6 % | 1,4 % | 1,6 % | 0,7 % | 1,2 % | 1,7 % |
| Toute résistance à l'éthambutol | 0,8 % | 1,5 % | 0,9 % | 1,8 % | 1,0 % | 1,3 % | 0,8 % | 0,7 % | 0,3 % | 0,7 % | 0,4 % |
| Toute résistance à la pyrazinamide | 2,4 % | 2,1 % | 1,5 % | 2,7 % | 2,1 % | 1,7 % | 2,4 % | 2,6 % | 2,8 % | 2,2 % | 2,6 % |
Monorésistance
Dans l'ensemble, en 2014, 131 isolats de tuberculose (9,5 % de tous les isolats testés) ont présenté une résistance à au moins un des quatre antituberculeux majeurs (tableau 4). La majorité d'entre eux (108, 82,4 %) étaient monorésistants. De ceux-ci, 84 (77,8 %) étaient monorésistants à l'isoniazide, 19 (17,6 %) étaient monorésistants à la pyrazinamide et cinq (4,6 %) étaient monorésistants à la rifampicine. Aucun des isolats n'était monorésistant à l'éthambutol (tableaux 5 à 17). Pour la période de 2004 à 2014, 7,7 % de l'ensemble des isolats testés étaient monorésistants, le taux étant à son plus haut en 2011, à 9 %, et à son plus bas en 2013, à 6,7 % (tableau 4).
Pour la période de 2004 à 2014, il a été observé que 28 isolats (0,2 % de l'ensemble des isolats testés) étaient monorésistants à la rifampicine. De ce nombre, 15 (53,6 %) provenaient de la Colombie-Britannique, six (21,4 %) de l'Ontario, deux (7,1 %) de l'Alberta et du Québec, et un (3,6 %) de la Saskatchewan, des Territoires du Nord-Ouest et du Nunavut. À l'exception des années 2004 et 2010, au cours desquelles aucun isolat monorésistant à la rifampicine n'avait été déclaré, entre un et trois isolats monorésistants à la rifampicine ont été signalés chaque année entre 2005 et 2014. En 2006, on a signalé huit (0,6 %) isolats monorésistants à la rifampicine ont été déclarés, ce qui représente un chiffre inhabituellement élevé sur une période d'une année (tableaux 5 à 17).
Polyrésistance, tuberculose multirésistante et tuberculose ultrarésistante aux antituberculeux
En 2014, quatre isolats (0,3 %) étaient résistants à au moins deux antituberculeux majeurs, à l'exclusion de la résistance à la fois à l'isoniazide et à la rifampicine (tableau 4). Ces quatre isolats étaient résistants à la fois à l'isoniazide et à la pyrazinamide en plus d'être sensibles à la rifampicine et à l'éthambutol. Entre 2004 et 2014, 64 (0,4 %) isolats ont été déclarés comme étant polyrésistants. De ce nombre, 29 (45,3 %) étaient résistants à l'isoniazide et à l'éthambutol, tandis que 26 (40,6 %) étaient résistants à l'isoniazide et à la pyrazinamide. Des neuf isolats restants, six étaient résistants à l'isoniazide, à l'éthambutol et à la pyrazinamide, deux étaient résistants à la rifampicine et à la pyrazinamide et un était résistant à l'éthambutol et à la pyrazinamide (tableaux 5 à 17).
En 2014, 19 (1,4 %) de tous les isolats testés étaient résistants à la fois à l'isoniazide et à la rifampicine (ce qui en fait des souches au moins TB-MR). De ces 19 isolats, dix (52,6 %) étaient résistants uniquement à l'isoniazide et à la rifampicine, trois (15,8 %) étaient également résistants à l'éthambutol, deux (10,5 %) étaient également résistants à la pyrazinamide et quatre (21 %) étaient résistants également à la fois a à la pyrazinamide et à l'éthambutol (tableau 18).
Afin d'écarter la possibilité de TB-UR, les 19 isolats qui se sont révélés résistants à la fois à l'isoniazide et à la rifampicine ont tous été soumis ensuite à des épreuves de sensibilité à certains antituberculeux mineurs. Seize (84,2 %) de ces isolats étaient sensibles à la fois aux antituberculeux injectables et aux fluoroquinolones, un (5,2 %) était résistant à un antituberculeux injectable, mais était sensible aux fluoroquinolones et un (5,2 %) était résistant à une fluoroquinolone, mais était sensible aux antituberculeux injectables (données non représentées). Le dernier isolat était résistant à au moins un des antituberculeux injectables et à une fluoroquinolone. Par conséquent, en 2014, 18 isolats ont été identifiés comme étant TB-MR et un présentait une TB-UR. La figure 4 présente les profils de résistance aux antituberculeux sous forme de pourcentage des isolats testés en 2014.
Figure 4 : Profils de résistance aux antituberculeux selon le pourcentage d'isolats testés, 2014
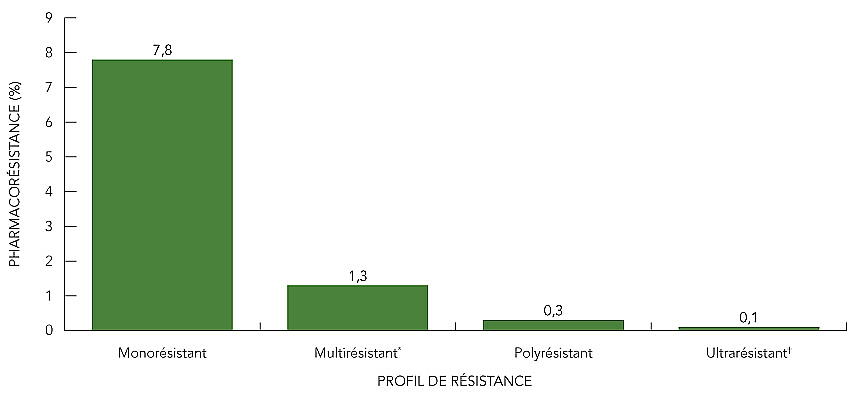
* La tuberculose multirésistante est une tuberculose qui est résistante à l'isoniazide et à la rifampicine, mais qui ne répond pas à la définition de tuberculose ultrarésistante.
†La tuberculose ultrarésistante est une tuberculose résistante à l'isoniazide et à la rifampicine, qu'à une fluoroquinolone et à au moins un des trois antituberculeux mineurs injectables (amikacine, capréomycine et kanamycine).
Description de la figure 4
Le graphique à barres affiche le pourcentage du nombre total d'isolats testés en 2014 qui présentaient une certaine pharmacorésistance, par type de résistance. L'axe horizontal représente les profils de résistance des isolats, tels que la monorésistance, la multirésistance, la polyrésistance et l'ultrarésistance et d'autres profils. L'axe vertical représente le pourcentage de pharmacorésistance de 0 à 9 %, par tranche de 1 %.
Les profils de pharmacorésistance selon le pourcentage d'isolats testés en 2014 se présentent comme suit :
| Profil de résistance | Pharmacorésistance (%) |
|---|---|
| Monorésistant | 7,8 % |
| Multirésistant | 1,3 % |
| Polyrésistant | 0,3 % |
| Ultrarésistant | 0,1 % |
Prendre note que la tuberculose multirésistante est une tuberculose qui est résistante, à tout le moins, à l'isoniazide et à la rifampicine, mais qui ne répond pas à la définition de tuberculose ultrarésistante. La tuberculose ultrarésistante est une tuberculose résistante à l'isoniazide et à la rifampicine, ainsi qu'à une fluoroquinolone et à au moins un des trois antituberculeux mineurs injectables (amikacine, capréomycine et kanamycine).
Pour la période de 2004 à 2014, 168 isolats ont été classés comme TB-MR, ce qui représentait 1,1 % des isolats testés au cours de cette période (tableau 4). Sept isolats ont été classés comme TB-UR, ce qui équivaut à une moyenne annuelle inférieure à 0,1 % du nombre total d'isolats testés pour cette période. Une moyenne de 15 isolats TB-MR a été déclarée chaque année, avec un minimum de huit cas (0,6 % de tous les isolats) en 2012 et un maximum de 22 cas (1,6 % de tous les isolats testés) en 2005.
La figure 5 montre le profil général de résistance aux antituberculeux déclarée sous forme de pourcentage des isolats testés pour la période de 2004 à 2014. Malgré de petites fluctuations du pourcentage d'isolats présentant divers profils de résistance, aucune tendance importante n'a été observée au cours de cette période.
Figure 5 : Profils de résistance aux antituberculeux selon le pourcentage d'isolats testés, 2004 à 2014
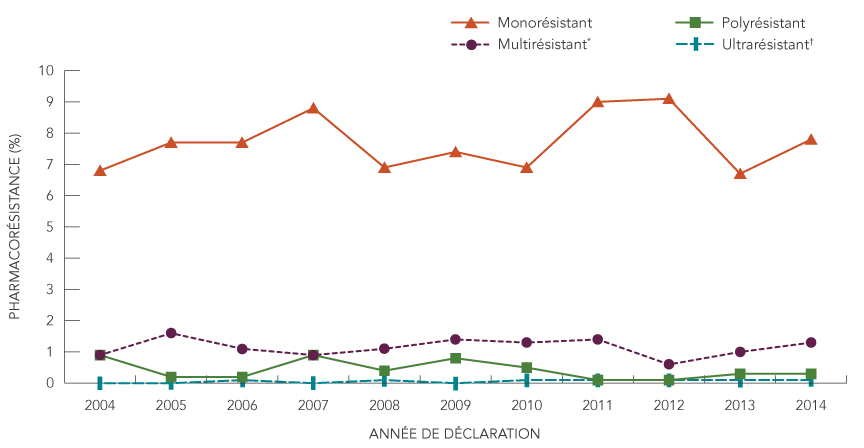
* La tuberculose multirésistante est une tuberculose qui est résistante à l'isoniazide et à la rifampicine, mais qui ne répond pas à la définition de tuberculose ultrarésistante.
† La tuberculose ultrarésistante est une tuberculose résistante à l'isoniazide et à la rifampicine, qu'à une fluoroquinolone et à au moins un des trois antituberculeux mineurs injectables (amikacine, capréomycine et kanamycine).
Description de la figure 5
Le graphique linéaire affiche le pourcentage d'isolats présentant une résistance selon le profil de résistance aux antituberculeux, de 2004 à 2014. Les différents types de résistance présentés pour les isolats comprennent la monorésistance, la multirésistance, la polyrésistance et l'ultrarésistance.
Les profils de résistance aux antituberculeux selon le pourcentage d'isolats testés pendant la période de 2004 à 2014 se présentent comme suit :
| Profil de résistance | Année de déclaration | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| 2004 | 2005 | 2006 | 2007 | 2008 | 2009 | 2010 | 2011 | 2012 | 2013 | 2014 | |
| Monorésistant | 6,8 % | 7,7 % | 7,7 % | 8,8 % | 6,9 % | 7,4 % | 6,9 % | 9,0 % | 9,1 % | 6,7 % | 7,8 % |
| Multirésistant | 0,9 % | 1,6 % | 1,1 % | 0,9 % | 1,1 % | 1,4 % | 1,3 % | 1,4 % | 0,6 % | 1,0 % | 1,3 % |
| Polyrésistant | 0,9 % | 0,2 % | 0,2 % | 90,0 % | 40,0 % | 0,8 % | 0,5 % | 0,1 % | 0,1 % | 0,3 % | 0,3 % |
| Ultrarésistant | 0,0 % | 0,0 % | 0,1 % | 0,0 % | 0,1 % | 0,0 % | 0,1 % | 0,1 % | 0,1 % | 0,1 % | 0,1 % |
Prendre note que la tuberculose multirésistante est une tuberculose qui est résistante, à tout le moins, à l'isoniazide et à la rifampicine, mais qui ne répond pas à la définition de tuberculose ultrarésistante. La tuberculose ultrarésistante est une tuberculose résistante à l'isoniazide et à la rifampicine, ainsi qu'à une fluoroquinolone et à au moins un des trois antituberculeux mineurs injectables (amikacine, capréomycine et kanamycine).
Répartition géographique
Dans l'ensemble, le nombre total d'isolats testés et déclarés en 2014 (1 376) était semblable à celui déclaré en 2013 (1 381) (tableau 2). En 2014, la majorité des isolats déclarés provenait de cinq provinces : Ontario (33,2 %); Colombie-Britannique (19,6 %); Québec (13,5 %); Alberta (13,2 %) et Manitoba (9,1 %). La Saskatchewan représentait moins de 5 % des isolats déclarés, alors que les territoires (Territoires du Nord-Ouest, Nunavut et Yukon) et les provinces de l'Atlantique (Nouveau-Brunswick, Terre-Neuve-et-Labrador, Nouvelle-Écosse et Île-du-Prince-Édouard) représentaient moins de 7 % des isolats déclarés en 2014.
Tous les isolats provenant des Territoires du Nord-Ouest, du Nunavut, du Yukon, du Nouveau-Brunswick, de Terre-Neuve-et-Labrador et de l'Île-du-Pince-Édouard étaient complètement sensibles à tous les antituberculeux majeurs testés. Des 19 isolats résistants à la fois à l'isoniazide et à la rifampicine ayant été déclarés en 2014, quatre provenaient de l'Alberta, six de la Colombie-Britannique, sept de l'Ontario et deux du Québec (tableau 18).
Pour la période de 2004 à 2014, les 168 isolats TB-MR provenaient tous de six provinces : l'Alberta, la Colombie-Britannique, le Manitoba, l'Ontario, le Québec et la Saskatchewan (tableau 19). Sur les sept isolats identifiés comme ultrarésistants, cinq provenaient de l'Ontario, un du Manitoba et un du Québec.
Les tableaux 5 à 17 présentent les résultats des épreuves systématiques de sensibilité des isolats du CMTB aux antituberculeux pour la période de 2004 à 2014, par province et territoire.
Données démographiques
En 2014, l'âge ou la date de naissance étaient disponibles pour toutes les personnes chez lesquelles les 1 376 isolats déclarés ont été prélevés, sauf une (tableau 20). Des 131 isolats pharmacorésistants, 22,9 % provenaient de personnes âgées de 25 à 34 ans et 20,6 % ont été prélevés chez des personnes âgées de 35 à 44 ans. 1,6 % des isolats ont été prélevés chez des personnes âgées de moins de 15 ans (tableau 20). L'isolat TB-UR a été prélevé chez une personne âgée de 25 à 34 ans.
En 2014, le sexe était connu pour les personnes chez lesquelles 1 374 (99,9 %) des 1 376 isolats ont été prélevés (tableau 20). Les hommes représentaient 56,6 % des isolats déclarés en 2014 (tableau 20). Quant aux femmes, elles représentaient 51,9 % des isolats présentant une certaine résistance; la moitié des cas étaient des isolats résistants à la fois à l'isoniazide et à la rifampicine. L'isolat TB-UR a été prélevé chez une femme.
Discussion
Dans de nombreuses régions du monde, la pharmacorésistance constitue une difficulté majeure à surmonter pour la prévention et le contrôle de la tuberculose. L'Europe de l'Est et l'Asie centrale continuent d'afficher la proportion la plus élevée de cas de TB-UR dans le monde.Note de bas de page 6
Les organismes résistants à la fois à l'isoniazide et à la rifampicine rendent les efforts de traitement et de prévention considérablement plus difficiles, car les antituberculeux efficaces sont limités. Les données publiées par l'Organisation mondiale de la Santé indiquent qu'à l'échelle mondiale, en 2012, environ 3,6 % (IC à 95 % : 2,1 %-5,1 %) des nouveaux cas de tuberculose et 20,2 % (IC à 95 % : 13,3 %-27,2 %) des cas de tuberculose déjà traités étaient TB-MR.Note de bas de page 6 Bien que les données recueillies au moyen du SCSLT n'établissent pas de distinction entre les isolats des nouveaux cas de tuberculose et ceux des cas déjà traités, le fait que seulement 1,3 % des isolats testés en 2014 étaient TB-MR constitue une observation nettement inférieure aux estimations à l'échelle mondiale. En outre, l'identification de sept cas de TB-UR sur la période de 2004 à 2014 indique que la TB-UR reste une maladie relativement rare au Canada.
Dans l'ensemble, le pourcentage d'isolats présentant une résistance aux antituberculeux majeurs au Canada pendant la période de 2004 à 2014 n'a subi aucun changement notable; toutefois, la répartition géographique n'est pas demeurée la même. Le pourcentage d'isolats provenant de l'Ontario a diminué, tandis que le nombre d'isolats prélevés en Alberta et en Colombie-Britannique a augmenté par rapport au nombre de déclarations présentées lors des années précédentes. Cela pourrait indiquer un changement dans la répartition générale des cas de tuberculose au Canada, et une surveillance accrue s'avère nécessaire.
Forces et limites
Le SCSLT est le fruit d'une collaboration réussie entre les gouvernements fédéral, provinciaux et territoriaux et le RTCLT. Le principal objectif du SCSLT est de surveiller les tendances et les profils émergents de la résistance aux antituberculeux au Canada. Ce rapport présente des données détaillées sur l'incidence de la résistance aux antituberculeux majeurs et mineurs au Canada, réparties par province ou territoire et, dans la mesure du possible, par âge et par sexe. En tant que principale source de données nationales sur la résistance aux antituberculeux au Canada, les données contenues dans le présent rapport fournissent des renseignements opportuns pour les mesures de santé publique, ainsi que pour l'élaboration et l'évaluation des politiques et des programmes.
Avant l'analyse et la préparation du rapport, toutes les données ont été examinées pour repérer les erreurs, les incohérences et les données manquantes. Les laboratoires qui soumettent des isolats ont reçu un rapport de synthèse de leurs données aux fins d'examen. Une fois validées par les laboratoires déclarants, les données ont été intégrées à la base de données du SCSLT. Toutefois, comme la plupart des données de surveillance, les données du présent rapport peuvent contenir des erreurs de codage, de déclaration et de traitement.
Les données publiées précédemment font l'objet de mises à jour lorsque des déclarations sont soumises en retard ou que des révisions sont reçues des laboratoires participants. Les révisions apportées aux données déclarées antérieurement sont prises en compte dans les rapports suivants. Par conséquent, les données présentées dans ce rapport sont considérées comme étant les plus récentes et elles remplacent les données précédemment publiées dans cette série de rapports.
Malgré les efforts déployés pour s'assurer que les déclarations multiples pour une même personne au cours d'une année donnée sont supprimées, il est possible, compte tenu des renseignements d'identification minimaux disponibles pour chaque isolat (âge et sexe), que des déclarations multiples pour une même personne soient incluses dans la base de données. On s'attend à ce que ce biais soit minime, compte tenu du processus de validation auprès des fournisseurs de données.
Les données démographiques et cliniques recueillies au moyen du SCSLT sont limitées. Aucunes données ne sont recueillies sur l'origine ethnique, les renseignements diagnostiques et cliniques ou le résultat du traitement. Une plus grande quantité de données démographiques et de données cliniques sur les personnes d'où proviennent les isolats de bacilles tuberculeux permettrait de réaliser une évaluation épidémiologique plus approfondie des profils de pharmacorésistance au Canada. En outre, d'après les données recueillies à partir de ce système de surveillance, il est impossible de distinguer une pharmacorésistance primaire d'une résistance acquise ni de faire la différence entre les profils de résistance des nouveaux cas et ceux des cas traités de nouveau. Toutefois, le rapport intitulé La tuberculose au Canada, qui fournit un aperçu du nombre total de cas de tuberculose actifs déclarés et des taux d'incidence correspondants au Canada selon certaines caractéristiques démographiques et cliniques, présente des données basées sur des cas (et non sur des isolats) sur la pharmacorésistance primaire et acquise au Canada, lesquelles ne sont pas présentées ici. Ensemble, ces deux rapports fournissent un aperçu complet des données de surveillance des cas de tuberculose et de la résistance aux antituberculeux à l'échelle nationale.
Habituellement, seuls les isolats de TB-MR ou d'autres profils de tuberculose ultrarésistante font l'objet d'épreuves de sensibilité à certains antituberculeux mineurs. Bien que le Clinical and Laboratory Standards Institute (CLSI) recommande d'évaluer la résistance aux antituberculeux mineurs des isolats monorésistants à l'isoniazide, ainsi que des autres isolats polyrésistants mais non multirésistants, cette recommandation n'est pas toujours respectée au Canada. Les isolats autres que ceux de la TB-MR peuvent être résistants à une fluoroquinolone, car cette famille d'antibiotiques est largement utilisée dans le traitement des infections respiratoires. Dans une certaine mesure, notre compréhension de l'émergence de la résistance aux antituberculeux mineurs au Canada en est donc limitée.
Conclusion
Les données recueillies à ce jour au moyen du SCSLT indiquent que la présence de tuberculose pharmacorésistante au Canada est présentement plus faible que ce qui s'observe en moyenne dans le monde et que les chiffres restent relativement stables depuis le début de la déclaration. Cependant, le SCSLT continue de jouer un rôle vital dans la surveillance de la résistance aux antituberculeux au Canada en vue de répondre à une inquiétude grandissante à l'échelle mondiale à l'égard de la résistance aux antituberculeux et de l'émergence de souches de TB-UR.
Annexes
Annexe I : Laboratoires participants du Réseau technique canadien des laboratoires de tuberculose (RTCLT)
Laboratoire provincial de santé publique
Calgary
Cary Shandro
Technologue, Mycobactériologie
Dr Greg Tyrrell
Microbiologiste clinique
Graham Tipples
Directeur scientifique/médical
Colombie-Britannique
Centre de contrôle des maladies de la Colombie-Britannique, Laboratoire de santé publique et de référence en microbiologie
Vancouver
Dre Mabel Rodrigues
Chef de section, Laboratoire de mycobactériologie/TB
Dr Patrick Tang
Microbiologiste médical
Dre Judy L. Isaac-Renton
Directrice, Services de laboratoire
Manitoba
Services diagnostiques Manitoba Health Sciences Centre
Winnipeg
Assunta Rendina
Technologue responsable, Mycobactériologie
Doug Swidinsky
Technologue principal
Nouveau-Brunswick
Service de médecine de laboratoire Hôpital régional de Saint John
Saint John
Hope MacKenzie
Superviseure-TLM3, Laboratoire NC3
Dr Duncan Webster
Microbiologiste médical/Maladies infectieuses
Dr Marek Godlewski
Directeur de laboratoire
Terre-Neuve-et-Labrador
Laboratoire de santé publique de Terre-Neuve-et-Labrador
St. John's
Audrey Martin
Technologue II
Lourens Robberts
Directeur et microbiologiste clinique
Territoires du Nord-Ouest
Hôpital territorial Stanton
Yellowknife
Sherrill Webber
Technologue II, Microbiologie
Carolyn Russell
Responsable de laboratoire
Cheryl Case
Gestionnaire
Services thérapeutiques et diagnostiques
Nouvelle-Écosse
Service de pathologie et de médecine de laboratoire Queen Elizabeth II Health Sciences Centre
Halifax
Sherry Maston
Division de la microbiologie médicale
Dr David Haldane
Directeur, Réseau des laboratoires provinciaux de santé publique et des agents pathogènes spéciaux
Dr Todd Hatchette
Directeur, Pathologie et médecine de laboratoire
Hôpital général de Qikiqtani
Iqaluit
Santé en laboratoire
Laboratoire central de santé publique Agence de protection et de promotion de la santé de l'Ontario
Toronto
Kevin May
Chef de l'exploitation, Mycobactériologie
Dre Frances Jamieson
Microbiologiste médicale, Tuberculose et Mycobactériologie
Alex Marchand-Austin
Gestionnaire, Surveillance des laboratoires et gestion des données
Laboratoire de santé publique du Québec
Institut national de santé publique du Québec
Sainte-Anne-de-Bellevue
Hafid Soualhine
Chef, Mycobactériologie et actinomycètes aérobies
Dre Cécile Tremblay
Directrice
Laboratoire de lutte contre les maladies de la Saskatchewan
Regina
Rita Thomas
Technologue, Tuberculose/Bactériologie
Dre Christine Turenne
Microbiologiste
Dr Paul Levett
Microbiologiste
Dr David Alexander
Microbiologiste
Dr Greg Horsman
Directeur, Saskatchewan Health
Laboratoire national de microbiologie
Agence de la santé publique du Canada
Winnipeg
Joyce Wolfe
Gestionnaire de programme, Mycobactériologie
Annexe II : Rapport sur la sensibilité des souches du complexe M. tuberculosis aux antimicrobiens
Veuillez noter

Annexe III : Tableaux de données
| Antituberculeux | Concentration critiqueTableau 1 note de bas de page *, (mg/l) BACTEC®960 | Remarques | |
|---|---|---|---|
| Antituberculeux majeurs | Isoniazide (INH) | 0,1 | Lorsque l'on détecte une résistance à l'INH à la concentration de 0,1 mg/L, les tests sont répétés avec 0,4 mg/L d'INH pour déterminer le degré de résistance. Néanmoins, l'isolat est signalé comme résistant avec la valeur seuil de 0,1 mg/L. |
| Rifampicine (RMP) | 1,0 | ||
| Éthambutol (EMB) | 5,0 | ||
| Pyrazinamide (PZA) | 100,0 | Les épreuves ne sont pas systématiquement effectuées pour les isolats provenant de la Colombie-Britannique. | |
| Antituberculeux mineurs | Amikacine (AK) | 1,0 | |
| Capréomycine (CM) | 2,5 | ||
| Éthionamide (ETH) | 5,0 | ||
| Kanamycine (KM) | 2,5 | ||
| Linézolide (LIN) | 1,0 | ||
| Moxifloxacine (MOX) | 0,3 | ||
| Ofloxacine (OFL) | 2,0 | ||
| Acide para-aminosalicylique (PAS) | 4,0 | ||
| Rifabutine (RBT) | 0,5 | ||
| Streptomycine (SM) | 1,0 | ||
|
|||
| Province de déclaration | Canada | Province d'origine | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| T.-N.-L. | Î.-P.-É. | N.-É. | N.-B. | Qc. | Ont. | Man. | Sask. | Alb. | C.-B. | Yn | T.N.-O. | Nt | ||
| T.-N.-L. | 6 | 6 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 |
| N.-É. | 10 | 0 | 2 | 8 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 |
| N.-B. | 6 | 0 | 0 | 0 | 6 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 |
| Qc. | 183 | 0 | 0 | 0 | 0 | 183 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 |
| Ont. | 523 | 0 | 0 | 0 | 0 | 3 | 457 | 0 | 0 | 0 | 2 | 0 | 0 | 61 |
| Man. | 125 | 0 | 0 | 0 | 0 | 0 | 0 | 125 | 0 | 0 | 0 | 0 | 0 | 0 |
| Sask. | 63 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 63 | 0 | 0 | 0 | 0 | 0 |
| Alb. | 188 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 180 | 1 | 0 | 2 | 5 |
| C.-B. | 272 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 1 | 267 | 4 | 0 | 0 |
| Total | 1 376 | 6 | 2 | 8 | 6 | 186 | 457 | 125 | 63 | 181 | 270 | 4 | 2 | 66 |
| Année de déclaration | Nombre total d'isolats du CMTB déclarés | Résistants à un ou plusieurs antituberculeux majeurs | Tuberculose multirésistanteTableau 3 note de bas de page * | Tuberculose ultrarésistanteTableau 3 note de bas de page † | |||
|---|---|---|---|---|---|---|---|
| nombre | pourcentage(%) | nombre | pourcentage (%) | nombre | pourcentage (%) | ||
| 2004 | 1 376 | 119 | 8,6 | 12 | 0,9 | 0 | 0,0 |
| 2005 | 1 335 | 128 | 9,6 | 22 | 1,6 | 0 | 0,0 |
| 2006 | 1 389 | 126 | 9,1 | 15 | 1,1 | 1 | 0,1 |
| 2007 | 1 267 | 133 | 10,5 | 11 | 0,9 | 0 | 0,0 |
| 2008 | 1 356 | 116 | 8,6 | 15 | 1,1 | 1 | 0,1 |
| 2009 | 1 331 | 127 | 9,5 | 18 | 1,4 | 0 | 0,0 |
| 2010 | 1 279 | 112 | 8,8 | 17 | 1,3 | 1 | 0,1 |
| 2011 | 1 319 | 139 | 10,5 | 18 | 1,4 | 1 | 0,1 |
| 2012 | 1 404 | 139 | 9,9 | 8 | 0,6 | 1 | 0,1 |
| 2013 | 1 381 | 112 | 8,1 | 14 | 1,0 | 1 | 0,1 |
| 2014 | 1 376 | 131 | 9,5 | 18 | 1,3 | 1 | 0,1 |
| Total | 14 813 | 1 382 | 9,3 | 168 | 1,1 | 7 | <0,1 |
Abréviation : CMTB, complexe Mycobacterium tuberculosis
|
|||||||
| Année de déclaration | ||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 2004 | 2005 | 2006 | 2007 | 2008 | 2009 | 2010 | 2011 | 2012 | 2013 | 2014 | Total | |||||||||||||
| n | % | n | % | n | % | n | % | n | % | n | % | n | % | n | % | n | % | n | % | n | % | n | % | |
| Nombre total d'isolats testés | 1 376 | 100,0 | 1 335 | 100,0 | 1 389 | 100,0 | 1 267 | 100,0 | 1 356 | 100,0 | 1 331 | 100,0 | 1 279 | 100,0 | 1 319 | 100,0 | 1 404 | 100,0 | 1 381 | 100,0 | 1 376 | 100,0 | 14 813 | 100,0 |
| Isolats testés qui étaient sensibles | 1 257 | 91,4 | 1 207 | 90,4 | 1 263 | 90,9 | 1 134 | 89,5 | 1 240 | 91,4 | 1 204 | 90,5 | 1 167 | 91,2 | 1 180 | 89,5 | 1 265 | 90,1 | 1 269 | 91,9 | 1 245 | 90,5 | 13 431 | 90,7 |
| Isolats affichant une certaine résistance aux antituberculeux majeurs | ||||||||||||||||||||||||
| Toute résistance à l'isoniazide | 102 | 7,4 | 109 | 8,2 | 101 | 7,3 | 110 | 8,7 | 102 | 7,5 | 113 | 8,5 | 101 | 7,9 | 122 | 9,2 | 111 | 7,9 | 93 | 6,7 | 107 | 7,8 | 1 171 | 7,9 |
| Toute résistance à la rifampicine | 14 | 1,0 | 24 | 1,8 | 24 | 1,7 | 13 | 1,0 | 19 | 1,4 | 21 | 1,6 | 18 | 1,4 | 21 | 1,6 | 10 | 0,7 | 17 | 1,2 | 24 | 1,7 | 205 | 1,4 |
| Toute résistance à l'éthambutol | 11 | 0,8 | 20 | 1,5 | 12 | 0,9 | 23 | 1,8 | 13 | 1,0 | 17 | 1,3 | 10 | 0,8 | 9 | 0,7 | 4 | 0,3 | 10 | 0,7 | 6 | 0,4 | 135 | 0,9 |
| Toute résistance à la pyrazinamideTableau 4 note de bas de page * | 26 | 2,4 | 22 | 2,1 | 16 | 1,5 | 27 | 2,7 | 22 | 1,7 | 18 | 2,4 | 25 | 2,6 | 28 | 2,4 | 33 | 2,4 | 26 | 2,2 | 30 | 2,6 | 273 | 2,6 |
| Isolats résistants à un ou plusieurs antituberculeux majeurs | 119 | 8,6 | 128 | 9,6 | 126 | 9,1 | 133 | 10,5 | 116 | 8,6 | 127 | 9,5 | 112 | 8,8 | 139 | 10,5 | 139 | 9,9 | 112 | 8,1 | 131 | 9,5 | 1 382 | 9,3 |
| Monorésistant | 94 | 6,8 | 103 | 7,7 | 107 | 7,7 | 111 | 8,8 | 94 | 6,9 | 98 | 7,4 | 88 | 6,9 | 119 | 9,0 | 128 | 9,1 | 93 | 6,7 | 108 | 7,8 | 1 143 | 7,7 |
| Multirésistant Tableau 4 note de bas de page † | 12 | 0,9 | 22 | 1,6 | 15 | 1,1 | 11 | 0,9 | 15 | 1,1 | 18 | 1,4 | 17 | 1,3 | 18 | 1,4 | 8 | 0,6 | 14 | 1,0 | 18 | 1,3 | 168 | 1,1 |
| Polyrésistant | 13 | 0,9 | 3 | 0,2 | 3 | 0,2 | 11 | 0,9 | 6 | 0,4 | 11 | 0,8 | 6 | 0,5 | 1 | 0,1 | 2 | 0,1 | 4 | 0,3 | 4 | 0,3 | 64 | 0,4 |
| UltrarésistantTableau 4 note de bas de page ‡ | 0 | 0,0 | 0 | 0,0 | 1 | 0,1 | 0 | 0,0 | 1 | 0,1 | 0 | 0,0 | 1 | 0,1 | 1 | 0,1 | 1 | 0,1 | 1 | 0,1 | 1 | 0,1 | 7 | <0,1 |
|
||||||||||||||||||||||||
| Année de déclaration | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 2004 | 2005 | 2006 | 2007 | 2008 | 2009 | 2010 | 2011 | 2012 | 2013 | 2014 | ||||||||||||
| n | % | n | % | n | % | n | % | n | % | n | % | n | % | n | % | n | % | n | % | n | % | |
| Isolats soumis à des tests de résistance à l'INH, à la RMP, à l'EMB et à la PZATableau 5 note de bas de page * | 94 | 100,0 | 129 | 100,0 | 104 | 100,0 | 98 | 100,0 | 134 | 100,0 | 159 | 100,0 | 107 | 100,0 | 156 | 100,0 | 163 | 100,0 | 154 | 100,0 | 181 | 100,0 |
| Isolats sensibles à tous les antituberculeux majeurs | 82 | 87,2 | 115 | 89,1 | 95 | 91,3 | 92 | 93,9 | 123 | 91,8 | 145 | 91,2 | 96 | 89,7 | 133 | 85,3 | 148 | 90,8 | 140 | 90,9 | 165 | 91,2 |
| Résistants à un ou plusieurs antituberculeux majeurs | 12 | 12,8 | 14 | 10,9 | 9 | 8,7 | 6 | 6,1 | 11 | 8,2 | 14 | 8,8 | 11 | 10,3 | 23 | 14,7 | 15 | 9,2 | 14 | 9,1 | 16 | 8,8 |
| Tuberculose monorésistante | ||||||||||||||||||||||
| INH | 7 | 7,4 | 10 | 7,8 | 7 | 6,7 | 5 | 5,1 | 8 | 6,0 | 8 | 5,0 | 6 | 5,6 | 14 | 9,0 | 10 | 6,1 | 9 | 5,8 | 11 | 6,1 |
| RMP | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,6 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,6 |
| EMB | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| PZA | 2 | 2,1 | 0 | 0,0 | 1 | 1,0 | 1 | 1,0 | 0 | 0,0 | 3 | 1,9 | 0 | 0,0 | 2 | 1,3 | 3 | 1,8 | 4 | 2,6 | 0 | 0,0 |
| Total | 9 | 9,6 | 10 | 7,8 | 8 | 7,7 | 6 | 6,1 | 8 | 6,0 | 12 | 7,5 | 6 | 5,6 | 16 | 10,3 | 13 | 8,0 | 13 | 8,4 | 12 | 6,6 |
| Polyrésistante | ||||||||||||||||||||||
| INH et PZA | 1 | 1,1 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,6 | 1 | 0,9 | 0 | 0,0 | 1 | 0,6 | 0 | 0,0 | 0 | 0,0 |
| INH et EMB | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,7 | 1 | 0,6 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| INH, EMB et PZA | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,9 | 0 | 0,0 | 0 | 0,0 | 1 | 0,6 | 0 | 0,0 |
| Total | 1 | 1,1 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,7 | 2 | 1,3 | 2 | 1,9 | 0 | 0,0 | 1 | 0,6 | 1 | 0,6 | 0 | 0,0 |
| Tuberculose multirésistanteTableau 5 note de bas de page † | ||||||||||||||||||||||
| INH et RMP | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,6 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| INH, RMP et EMB | 0 | 0,0 | 1 | 0,8 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| INH, RMP, EMB, AK, KM et RBT | 1 | 1,1 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| INH, RMP, EMB et PZA | 0 | 0,0 | 1 | 0,8 | 0 | 0,0 | 0 | 0,0 | 1 | 0,7 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| INH, RMP, EMB, PZA et RBT | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,6 |
| INH, RMP, EMB, PZA et SM | 0 | 0,0 | 1 | 0,8 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| INH, RMP, EMB, PZA, SM, OFL, MOX, ETH et RBT | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,6 |
| INH, RMP, EMB, PZA, SM et RBT | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,7 | 0 | 0,0 | 1 | 0,9 | 1 | 0,6 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| INH, RMP, EMB et SM | 0 | 0,0 | 0 | 0,0 | 1 | 1,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| INH, RMP, EMB, SM et OFL | 1 | 1,1 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| INH, RMP, ETH et RBT | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 2 | 1,3 | 0 | 0,0 | 0 | 0,0 | 1 | 0,6 |
| INH, RMP, PZA, SM et ETH | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,6 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| INH, RMP, PZA, SM, OFL et RBT | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,9 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| INH, RMP, PZA, SM et RBT | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,9 | 1 | 0,6 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| INH, RMP et RBT | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,6 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| INH, RMP et SM | 0 | 0,0 | 1 | 0,8 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| INH, RMP, SM, ETH et RBT | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,6 |
| INH, RMP, SM et RBT | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,6 | 0 | 0,0 | 0 | 0,0 |
| Total | 2 | 2,1 | 4 | 3,1 | 1 | 1,0 | 0 | 0,0 | 2 | 1,5 | 0 | 0,0 | 3 | 2,8 | 7 | 4,5 | 1 | 0,6 | 0 | 0,0 | 4 | 2,2 |
Abréviations : AK, amikacine; EMB, éthambutol; ETH, éthionamide; INH, isoniazide; KM, kanamycine; MOX, moxifloxacine; OFL, ofloxacine; PAS, acide para-aminosalicylique; PZA, pyrazinamide; RBT, rifabutine; RMP, rifampicine; SM, streptomycine.
|
||||||||||||||||||||||
| Année de déclaration | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 2004 | 2005 | 2006 | 2007 | 2008 | 2009 | 2010 | 2011 | 2012 | 2013 | 2014 | ||||||||||||
| n | % | n | % | n | % | n | % | n | % | n | % | n | % | n | % | n | % | n | % | n | % | |
| Isolats soumis à des tests de résistance à l'INH, à la RMP et à l'EMBTableau 6 note de bas de page *Tableau 6 note de bas de page † | 263 | 100,0 | 204 | 100,0 | 275 | 100,0 | 231 | 100,0 | 254 | 100,0 | 239 | 100,0 | 204 | 100,0 | 194 | 100,0 | 254 | 100,0 | 223 | 100,0 | 270 | 100,0 |
| Isolats sensibles à tous les antituberculeux majeurs | 237 | 90,1 | 182 | 89,2 | 257 | 93,5 | 210 | 90,9 | 230 | 90,6 | 215 | 90,0 | 185 | 90,7 | 170 | 87,6 | 231 | 90,9 | 204 | 91,5 | 235 | 87,0 |
| Résistants à un ou plusieurs antituberculeux majeurs | 26 | 9,9 | 22 | 10,8 | 18 | 6,5 | 21 | 9,1 | 24 | 9,4 | 24 | 10,0 | 19 | 9,3 | 24 | 12,4 | 23 | 9,1 | 19 | 8,5 | 35 | 13,0 |
| Tuberculose monorésistante | ||||||||||||||||||||||
| INH | 13 | 4,9 | 11 | 5,4 | 7 | 2,5 | 13 | 5,6 | 18 | 7,1 | 22 | 9,2 | 16 | 7,8 | 21 | 10,8 | 21 | 8,3 | 19 | 8,5 | 25 | 9,3 |
| RMP | 0 | 0,0 | 2 | 1,0 | 6 | 2,2 | 0 | 0,0 | 3 | 1,2 | 1 | 0,4 | 0 | 0,0 | 1 | 0,5 | 0 | 0,0 | 0 | 0,0 | 2 | 0,7 |
| EMB | 1 | 0,4 | 4 | 2,0 | 3 | 1,1 | 4 | 1,7 | 0 | 0,0 | 0 | 0,0 | 1 | 0,5 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| PZA | 3 | 1,1 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,5 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| Total | 17 | 6,5 | 17 | 8,3 | 16 | 5,8 | 17 | 7,4 | 21 | 8,3 | 23 | 9,6 | 18 | 8,8 | 22 | 11,3 | 21 | 8,3 | 19 | 8,5 | 27 | 10,0 |
| Polyrésistante | ||||||||||||||||||||||
| RMP et PZA | 2 | 0,8 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| INH et PZA | 4 | 1,5 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,5 | 0 | 0,0 | 0 | 0,0 | 2 | 0,7 |
| INH et EMB | 1 | 0,4 | 1 | 0,5 | 0 | 0,0 | 2 | 0,9 | 0 | 0,0 | 1 | 0,4 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| Total | 7 | 2,7 | 1 | 0,5 | 0 | 0,0 | 2 | 0,9 | 0 | 0,0 | 1 | 0,4 | 0 | 0,0 | 1 | 0,5 | 0 | 0,0 | 0 | 0,0 | 2 | 0,7 |
| Tuberculose multirésistanteTableau 6 note de bas de page ‡ | ||||||||||||||||||||||
| INH et RMP | 0 | 0,0 | 0 | 0,0 | 1 | 0,4 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| INH, RMP, EMB, PZA, ETH et RBT | 1 | 0,4 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| INH, RMP, EMB, PZA, KM, CM, ETH et RBT | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,4 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| INH, RMP, EMB, PZA et PAS | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,4 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| INH, RMP, EMB, PZA et RBT | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,4 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| INH, RMP, EMB, PZA, SM, ETH, RBT et PAS | 0 | 0,0 | 0 | 0,0 | 1 | 0,4 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| INH, RMP, EMB, PZA, SM, KM et RBT | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,4 | 0 | 0,0 | 0 | 0,0 |
| INH, RMP, EMB, PZA, SM, OFL, ETH, RBT et PAS | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,4 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| INH, RMP, EMB, PZA, SM et RBT | 0 | 0,0 | 1 | 0,5 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| INH, RMP, EMB et RBT | 1 | 0,4 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| INH, RMP, EMB, SM, ETH et RBT | 0 | 0,0 | 1 | 0,5 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,4 |
| INH, RMP, EMB, SM, ETH, RBT et PAS | 0 | 0,0 | 1 | 0,5 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| INH, RMP, ETH et RBT | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,4 |
| INH, RMP, PZA et RBT | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,4 |
| INH, RMP, PZA, SM et RBT | 0 | 0,0 | 1 | 0,5 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,5 | 0 | 0,0 | 1 | 0,4 | 0 | 0,0 | 0 | 0,0 |
| INH, RMP, PZA, SM, RBT et PAS | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,5 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| INH, RMP et RBT | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,4 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 2 | 0,7 |
| INH, RMP, SM et RBT | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,4 |
| Total | 2 | 0,8 | 4 | 2,0 | 2 | 0,7 | 2 | 0,9 | 3 | 1,2 | 0 | 0,0 | 1 | 0,5 | 1 | 0,5 | 2 | 0,8 | 0 | 0,0 | 6 | 2,2 |
Abréviations : CM, capréomycine; EMB, éthambutol; ETH, éthionamide; INH, isoniazide; KM, kanamycine; MOX, moxifloxacine; OFL, ofloxacine; PAS, acide para-aminosalicylique; PZA, pyrazinamide; RBT, rifabutine; RMP, rifampicine; SM, streptomycine.
|
||||||||||||||||||||||
| Année de déclaration | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 2004 | 2005 | 2006 | 2007 | 2008 | 2009 | 2010 | 2011 | 2012 | 2013 | 2014 | ||||||||||||
| n | % | n | % | n | % | n | % | n | % | n | % | n | % | n | % | n | % | n | % | n | % | |
| Isolats soumis à des tests de résistance à l'INH, à la RMP, à l'EMB et à la PZATableau 7 note de bas de page * | 122 | 100,0 | 94 | 100,0 | 119 | 100,0 | 84 | 100,0 | 116 | 100,0 | 106 | 100,0 | 113 | 100,0 | 97 | 100,0 | 123 | 100,0 | 148 | 100,0 | 125 | 100,0 |
| Isolats sensibles à tous les antituberculeux majeurs | 121 | 99,2 | 92 | 97,9 | 113 | 95,0 | 75 | 89,3 | 111 | 95,7 | 99 | 93,4 | 99 | 87,6 | 90 | 92,8 | 113 | 91,9 | 144 | 97,3 | 120 | 96,0 |
| Résistants à un ou plusieurs antituberculeux majeurs | 1 | 0,8 | 2 | 2,1 | 6 | 5,0 | 9 | 10,7 | 5 | 4,3 | 7 | 6,6 | 14 | 12,4 | 7 | 7,2 | 10 | 8,1 | 4 | 2,7 | 5 | 4,0 |
| Tuberculose monorésistante | ||||||||||||||||||||||
| INH | 0 | 0,0 | 2 | 2,1 | 6 | 5,0 | 7 | 8,3 | 4 | 3,4 | 4 | 3,8 | 10 | 8,8 | 5 | 5,2 | 10 | 8,1 | 4 | 2,7 | 5 | 4,0 |
| RMP | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| EMB | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| PZA | 1 | 0,8 | 0 | 0,0 | 0 | 0,0 | 1 | 1,2 | 0 | 0,0 | 1 | 0,9 | 1 | 0,9 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| Total | 1 | 0,8 | 2 | 2,1 | 6 | 5,0 | 8 | 9,5 | 4 | 3,4 | 5 | 4,7 | 11 | 9,7 | 5 | 5,2 | 10 | 8,1 | 4 | 2,7 | 5 | 4,0 |
| Polyrésistante | ||||||||||||||||||||||
| INH et PZA | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,9 | 1 | 0,9 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| INH et EMB | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 1,2 | 0 | 0,0 | 1 | 0,9 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| Total | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 1,2 | 0 | 0,0 | 2 | 1,9 | 1 | 0,9 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| Tuberculose multirésistanteTableau 7 note de bas de page † | ||||||||||||||||||||||
| INH et RMP | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,9 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| INH, RMP, EMB, PZA, SM, AK, KM, CM, ETH et PAS | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 1,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| INH, RMP, PZA, SM et RBT | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,9 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| INH, RMP et RBT | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 1,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| Total | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,9 | 0 | 0,0 | 1 | 0,9 | 2 | 2,1 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| Tuberculose ultrarésistanteTableau 7 note de bas de page ‡ | ||||||||||||||||||||||
| INH, RMP, EMB, PZA, KM, OFL, ETH et RBT | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,9 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| Total | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,9 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
Abréviations : AK, amikacine; CM, capréomycine; EMB, éthambutol; ETH, éthionamide; INH, isoniazide; KM, kanamycine; MOX, moxifloxacine; OFL, ofloxacine; PAS, acide para-aminosalicylique; PZA, pyrazinamide; RBT, rifabutine; RMP, rifampicine; SM, streptomycine.
|
||||||||||||||||||||||
| Année de déclaration | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 2004 | 2005 | 2006 | 2007 | 2008 | 2009 | 2010 | 2011 | 2012 | 2013 | 2014 | ||||||||||||
| n | % | n | % | n | % | n | % | n | % | n | % | n | % | n | % | n | % | n | % | n | % | |
| Isolats soumis à des tests de résistance à l'INH, à la RMP, à l'EMB et à la PZATableau 8 note de bas de page * | 11 | 100,0 | 5 | 100,0 | 3 | 100,0 | 5 | 100,0 | 3 | 100,0 | 10 | 100,0 | 9 | 100,0 | 5 | 100,0 | 4 | 100,0 | 3 | 100,0 | 6 | 100,0 |
| Isolats sensibles à tous les antituberculeux majeurs | 10 | 90,9 | 4 | 80,0 | 3 | 100,0 | 5 | 100,0 | 3 | 100,0 | 10 | 100,0 | 7 | 77,8 | 5 | 100,0 | 3 | 75,0 | 2 | 66,7 | 6 | 100,0 |
| Résistants à un ou plusieurs antituberculeux majeurs | 1 | 9,1 | 1 | 20,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 2 | 22,2 | 0 | 0,0 | 1 | 25,0 | 1 | 33,3 | 0 | 0,0 |
| Tuberculose monorésistante | ||||||||||||||||||||||
| INH | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 2 | 22,2 | 0 | 0,0 | 0 | 0,0 | 1 | 33,3 | 0 | 0,0 |
| RMP | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| EMB | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| PZA | 1 | 9,1 | 1 | 20,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 25,0 | 0 | 0,0 | 0 | 0,0 |
| Total | 1 | 9,1 | 1 | 20,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 2 | 22,2 | 0 | 0,0 | 1 | 25,0 | 1 | 33,3 | 0 | 0,0 |
Abréviations : EMB, éthambutol; INH, isoniazide; PZA, pyrazinamide; RMP, rifampicine. Notes de bas de page du Tableau 8
|
||||||||||||||||||||||
| Année de déclaration | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 2004 | 2005 | 2006 | 2007 | 2008 | 2009 | 2010 | 2011 | 2012 | 2013 | 2014 | ||||||||||||
| n | % | n | % | n | % | n | % | n | % | n | % | n | % | n | % | n | % | n | % | n | % | |
| Isolats soumis à des tests de résistance à l'INH, à la RMP, à l'EMB et à la PZA | 8 | 100,0 | 6 | 100,0 | 11 | 100,0 | 5 | 100,0 | 5 | 100,0 | 10 | 100,0 | 9 | 100,0 | 5 | 100,0 | 5 | 100,0 | 11 | 100,0 | 6 | 100,0 |
| Isolats sensibles à tous les antituberculeux majeurs | 8 | 100,0 | 5 | 83,3 | 11 | 100,0 | 5 | 100,0 | 5 | 100,0 | 10 | 100,0 | 9 | 100,0 | 5 | 100,0 | 5 | 100,0 | 11 | 100,0 | 6 | 100,0 |
| Résistants à un ou plusieurs antituberculeux majeurs | 0 | 0,0 | 1 | 16,7 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| Tuberculose monorésistante | ||||||||||||||||||||||
| INH | 0 | 0,0 | 1 | 16,7 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| RMP | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| EMB | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| PZA | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| Total | 0 | 0,0 | 1 | 16,7 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
Abréviations : EMB, éthambutol; INH, isoniazide; PZA, pyrazinamide; RMP, rifampicine. |
||||||||||||||||||||||
| Année de déclaration | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 2004 | 2005 | 2006 | 2007 | 2008 | 2009 | 2010 | 2011 | 2012 | 2013 | 2014 | ||||||||||||
| n | % | n | % | n | % | n | % | n | % | n | % | n | % | n | % | n | % | n | % | n | % | |
| Isolats soumis à des tests de résistance à l'INH, à la RMP, à l'EMB et à la PZA | 9 | 100,0 | 6 | 100,0 | 4 | 100,0 | 14 | 100,0 | 13 | 100,0 | 10 | 100,0 | 5 | 100,0 | 8 | 100,0 | 6 | 100,0 | 3 | 100,0 | 2 | 100,0 |
| Isolats sensibles à tous les antituberculeux majeurs | 9 | 100,0 | 6 | 100,0 | 3 | 75,0 | 14 | 100,0 | 13 | 100,0 | 9 | 90,0 | 4 | 80,0 | 8 | 100,0 | 6 | 100,0 | 3 | 100,0 | 2 | 100,0 |
| Résistants à un ou plusieurs antituberculeux majeurs | 0 | 0,0 | 0 | 0,0 | 1 | 25,0 | 0 | 0,0 | 0 | 0,0 | 1 | 10,0 | 1 | 20,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| Tuberculose monorésistante | ||||||||||||||||||||||
| INH | 0 | 0,0 | 0 | 0,0 | 1 | 25,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 20,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| RMP | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 10,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| EMB | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| PZA | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| Total | 0 | 0,0 | 0 | 0,0 | 1 | 25,0 | 0 | 0,0 | 0 | 0,0 | 1 | 10,0 | 1 | 20,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
Abréviations : EMB, éthambutol; INH, isoniazide; PZA, pyrazinamide; RMP, rifampicine. |
||||||||||||||||||||||
| Année de déclaration | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 2004 | 2005 | 2006 | 2007 | 2008 | 2009 | 2010 | 2011 | 2012 | 2013 | 2014 | ||||||||||||
| n | % | n | % | n | % | n | % | n | % | n | % | n | % | n | % | n | % | n | % | n | % | |
| Isolats soumis à des tests de résistance à l'INH, à la RMP, à l'EMB et à la PZATableau 11 note de bas de page * | 9 | 100,0 | 7 | 100,0 | 8 | 100,0 | 5 | 100,0 | 3 | 100,0 | 7 | 100,0 | 8 | 100,0 | 7 | 100,0 | 9 | 100,0 | 9 | 100,0 | 8 | 100,0 |
| Isolats sensibles à tous les antituberculeux majeurs | 9 | 100,0 | 6 | 85,7 | 8 | 100,0 | 5 | 100,0 | 3 | 100,0 | 7 | 100,0 | 5 | 62,5 | 7 | 100,0 | 9 | 100,0 | 8 | 88,9 | 5 | 62,5 |
| Résistants à un ou plusieurs antituberculeux majeurs | 0 | 0,0 | 1 | 14,3 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 3 | 37,5 | 0 | 0,0 | 0 | 0,0 | 1 | 11,1 | 3 | 37,5 |
| Tuberculose monorésistante | ||||||||||||||||||||||
| INH | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 12,5 | 0 | 0,0 | 0 | 0,0 | 1 | 11,1 | 3 | 37,5 |
| RMP | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| EMB | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| PZA | 0 | 0,0 | 1 | 14,3 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 12,5 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| Total | 0 | 0,0 | 1 | 14,3 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 2 | 25,0 | 0 | 0,0 | 0 | 0,0 | 1 | 11,1 | 3 | 37,5 |
| Polyrésistante | ||||||||||||||||||||||
| INH et PZA | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 12,5 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| Total | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 12,5 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
Abréviations : EMB, éthambutol; INH, isoniazide; PZA, pyrazinamide; RMP, rifampicine.
|
||||||||||||||||||||||
| Année de déclaration | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 2004 | 2005 | 2006 | 2007 | 2008 | 2009 | 2010 | 2011 | 2012 | 2013 | 2014 | ||||||||||||
| n | % | n | % | n | % | n | % | n | % | n | % | n | % | n | % | n | % | n | % | n | % | |
| Isolats soumis à des tests de résistance à l'INH, à la RMP, à l'EMB et à la PZA | 16 | 100,0 | 28 | 100,0 | 37 | 100,0 | 25 | 100,0 | 51 | 100,0 | 50 | 100,0 | 71 | 100,0 | 64 | 100,0 | 65 | 100,0 | 42 | 100,0 | 66 | 100,0 |
| Isolats sensibles à tous les antituberculeux majeurs | 16 | 100,0 | 28 | 100,0 | 37 | 100,0 | 24 | 96,0 | 51 | 100,0 | 49 | 98,0 | 70 | 98,6 | 62 | 96,9 | 65 | 100,0 | 42 | 100,0 | 66 | 100,0 |
| Résistants à un ou plusieurs antituberculeux majeurs | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 4,0 | 0 | 0,0 | 1 | 2,0 | 1 | 1,4 | 2 | 3,1 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| Tuberculose monorésistante | ||||||||||||||||||||||
| INH | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 4,0 | 0 | 0,0 | 1 | 2,0 | 1 | 1,4 | 1 | 1,6 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| RMP | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 1,6 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| EMB | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| PZA | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| Total | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 4,0 | 0 | 0,0 | 1 | 2,0 | 1 | 1,4 | 2 | 3,1 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
Abréviations : EMB, éthambutol; INH, isoniazide; PZA, pyrazinamide; RMP, rifampicine. |
||||||||||||||||||||||
| Année de déclaration | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 2004 | 2005 | 2006 | 2007 | 2008 | 2009 | 2010 | 2011 | 2012 | 2013 | 2014 | ||||||||||||
| n | % | n | % | n | % | n | % | n | % | n | % | n | % | n | % | n | % | n | % | n | % | |
| Isolats soumis à des tests de résistance à l'INH, à la RMP, à l'EMB et à la PZATableau 13 note de bas de page * | 599 | 100,0 | 553 | 100,0 | 567 | 100,0 | 538 | 100,0 | 479 | 100,0 | 488 | 100,0 | 496 | 100,0 | 507 | 100,0 | 493 | 100,0 | 511 | 100,0 | 457 | 100,0 |
| Isolats sensibles à tous les antituberculeux majeurs | 539 | 90,0 | 487 | 88,1 | 504 | 88,9 | 466 | 86,6 | 427 | 89,1 | 428 | 87,7 | 456 | 91,9 | 454 | 89,5 | 429 | 87,0 | 458 | 89,6 | 407 | 89,1 |
| Résistants à un ou plusieurs antituberculeux majeurs | 60 | 10,0 | 66 | 11,9 | 63 | 11,1 | 72 | 13,4 | 52 | 10,9 | 60 | 12,3 | 40 | 8,1 | 53 | 10,5 | 64 | 13,0 | 53 | 10,4 | 50 | 10,9 |
| Tuberculose monorésistante | ||||||||||||||||||||||
| INH | 46 | 7,7 | 44 | 8,0 | 39 | 6,9 | 50 | 9,3 | 33 | 6,9 | 39 | 8,0 | 27 | 5,4 | 39 | 7,7 | 45 | 9,1 | 27 | 5,3 | 30 | 6,6 |
| RMP | 0 | 0,0 | 0 | 0,0 | 1 | 0,2 | 1 | 0,2 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,2 | 2 | 0,4 | 1 | 0,2 |
| EMB | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,2 | 1 | 0,2 | 1 | 0,2 | 0 | 0,0 | 0 | 0,0 | 1 | 0,2 | 0 | 0,0 | 0 | 0,0 |
| PZA | 3 | 0,5 | 7 | 1,3 | 9 | 1,6 | 9 | 1,7 | 6 | 1,3 | 4 | 0,8 | 2 | 0,4 | 6 | 1,2 | 10 | 2,0 | 8 | 1,6 | 11 | 2,4 |
| Total | 49 | 8,2 | 51 | 9,2 | 49 | 8,6 | 61 | 11,3 | 40 | 8,4 | 44 | 9,0 | 29 | 5,8 | 45 | 8,9 | 57 | 11,6 | 37 | 7,2 | 42 | 9,2 |
| Polyrésistante | ||||||||||||||||||||||
| EMB et PZA | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,2 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| INH et EMB | 3 | 0,5 | 2 | 0,4 | 3 | 0,5 | 1 | 0,2 | 2 | 0,4 | 3 | 0,6 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,2 | 0 | 0,0 |
| INH et PZA | 1 | 0,2 | 0 | 0,0 | 0 | 0,0 | 2 | 0,4 | 0 | 0,0 | 0 | 0,0 | 1 | 0,2 | 0 | 0,0 | 1 | 0,2 | 2 | 0,4 | 1 | 0,2 |
| INH, EMB et PZA | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 2 | 0,4 | 2 | 0,4 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| Total | 4 | 0,7 | 2 | 0,4 | 3 | 0,5 | 4 | 0,7 | 4 | 0,8 | 5 | 1,0 | 1 | 0,2 | 0 | 0,0 | 1 | 0,2 | 3 | 0,6 | 1 | 0,2 |
| Tuberculose multirésistanteTableau 13 note de bas de page † | ||||||||||||||||||||||
| INH et RMP | 1 | 0,2 | 0 | 0,0 | 2 | 0,4 | 0 | 0,0 | 0 | 0,0 | 1 | 0,2 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| INH, RMP, AK, CM et RBT | 0 | 0,0 | 0 | 0,0 | 1 | 0,2 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| INH, RMP, CM, ETH et RBT | 1 | 0,2 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| INH, RMP, CM et RBT | 0 | 0,0 | 0 | 0,0 | 1 | 0,2 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| INH, RMP, EMB, ETH et RBT | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,2 | 0 | 0,0 |
| INH, RMP, EMB, PZA, AK, CM, ETH et RBT | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,2 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| INH, RMP, EMB, PZA, CM et RBT | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,2 | 0 | 0,0 | 0 | 0,0 |
| INH, RMP, EMB, PZA, ETH et RBT | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 2 | 0,4 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| INH, RMP, EMB, PZA et RBT | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,2 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,2 |
| INH, RMP, EMB, PZA, RBT et PAS | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,2 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| INH, RMP, EMB, PZA et SM | 0 | 0,0 | 1 | 0,2 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,2 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| INH, RMP, EMB, PZA, SM, ETH et RBT | 0 | 0,0 | 1 | 0,2 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,2 | 1 | 0,2 | 0 | 0,0 | 1 | 0,2 | 0 | 0,0 |
| INH, RMP, EMB, PZA, SM, ETH, RBT et PAS | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,2 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| INH, RMP, EMB, PZA, SM, OFL, ETH et RBT | 1 | 0,2 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| INH, RMP, EMB, PZA, SM, OFL, MOX, ETH et RBT | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,2 | 0 | 0,0 |
| INH, RMP, EMB, PZA, SM, OFL et RBT | 0 | 0,0 | 1 | 0,2 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| INH, RMP, EMB, PZA, SM et RBT | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,2 | 1 | 0,2 | 1 | 0,2 | 0 | 0,0 | 1 | 0,2 | 0 | 0,0 | 1 | 0,2 | 0 | 0,0 |
| INH, RMP, EMB et RBT | 0 | 0,0 | 0 | 0,0 | 2 | 0,4 | 1 | 0,2 | 1 | 0,2 | 2 | 0,4 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| INH, RMP, EMB, SM, AK et CM | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,2 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| INH, RMP, EMB, SM, ETH et RBT | 0 | 0,0 | 1 | 0,2 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,2 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| INH, RMP, EMB, SM, ETH, RBT et PAS | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,2 | 0 | 0,0 |
| INH, RMP, EMB, SM, KM, RBT et PAS | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,2 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| INH, RMP, EMB, SM, OFL, ETH et RBT | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,2 | 1 | 0,2 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| INH, RMP, EMB, SM, OFL, MOX, ETH et RBT | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,2 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| INH, RMP, EMB, SM, OFL et RBT | 0 | 0,0 | 1 | 0,2 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| INH, RMP, EMB, SM et RBT | 0 | 0,0 | 2 | 0,4 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,2 | 1 | 0,2 |
| INH, RMP, ETH et RBT | 0 | 0,0 | 0 | 0,0 | 1 | 0,2 | 0 | 0,0 | 1 | 0,2 | 1 | 0,2 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,2 | 0 | 0,0 |
| INH, RMP, ETH, RBT et PAS | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,2 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| INH, RMP, OFL, ETH et RBT | 2 | 0,3 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| INH, RMP, OFL, ETH, RBT et PAS | 0 | 0,0 | 0 | 0,0 | 1 | 0,2 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| INH, RMP, PZA, ETH et RBT | 0 | 0,0 | 1 | 0,2 | 1 | 0,2 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| INH, RMP, PZA et RBT | 1 | 0,2 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| INH, RMP, PZA et SM | 1 | 0,2 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| INH, RMP, PZA, SM, ETH et RBT | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,2 | 1 | 0,2 | 1 | 0,2 | 1 | 0,2 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| INH, RMP, PZA, SM, OFL, MOX et RBT | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,2 | 0 | 0,0 | 0 | 0,0 |
| INH, RMP, PZA, SM et RBT | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,2 | 0 | 0,0 | 1 | 0,2 | 1 | 0,2 |
| INH, RMP et RBT | 0 | 0,0 | 3 | 0,5 | 1 | 0,2 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,2 | 0 | 0,0 | 0 | 0,0 | 2 | 0,4 | 0 | 0,0 |
| INH, RMP et SM | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,2 | 1 | 0,2 | 0 | 0,0 |
| INH, RMP, SM, CM et RBT | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,2 |
| INH, RMP, SM, ETH et RBT | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,2 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| INH, RMP, SM, ETH, RBT et PAS | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,2 |
| INH, RMP, SM, KM, ETH et RBT | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,2 | 0 | 0,0 | 0 | 0,0 |
| INH, RMP, SM, OFL, ETH et RBT | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,2 | 1 | 0,2 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| INH, RMP, SM et RBT | 0 | 0,0 | 2 | 0,4 | 0 | 0,0 | 0 | 0,0 | 3 | 0,6 | 1 | 0,2 | 1 | 0,2 | 1 | 0,2 | 1 | 0,2 | 2 | 0,4 | 1 | 0,2 |
| Total | 7 | 1,2 | 13 | 2,4 | 10 | 1,8 | 7 | 1,3 | 7 | 1,5 | 11 | 2,3 | 10 | 2,0 | 7 | 1,4 | 5 | 1,0 | 13 | 2,5 | 6 | 1,3 |
| Tuberculose ultrarésistanteTableau 13 note de bas de page ‡ | ||||||||||||||||||||||
| INH, RMP, AK, CM, OFL, ETH et RBT | 0 | 0,0 | 0 | 0,0 | 1 | 0,2 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| INH, RMP, EMB, PZA, CM, OFL, ETH, RBT et PAS | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,2 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| INH, RMP, EMB, PZA, SM, KM, OFL, MOX, ETH et RBT | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,2 | 0 | 0,0 | 0 | 0,0 |
| INH, RMP, EMB, PZA, SM, KM, OFL, MOX, ETH, RBT et PAS | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,2 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| INH, RMP, EMB, PZA, SM, KM, OFL, MOX, RBT, ETA et PAS | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,2 |
| Total | 0 | 0,0 | 0 | 0,0 | 1 | 0,2 | 0 | 0,0 | 1 | 0,2 | 0 | 0,0 | 0 | 0,0 | 1 | 0,2 | 1 | 0,2 | 0 | 0,0 | 1 | 0,2 |
Abréviations : AK, amikacine; CM, capréomycine; EMB, éthambutol; ETH, éthionamide; INH, isoniazide; KM, kanamycine; MOX, moxifloxacine; OFL, ofloxacine; PAS, acide para-aminosalicylique; PZA, pyrazinamide; RBT, rifabutine; RMP, rifampicine; SM, streptomycine.
|
||||||||||||||||||||||
| Année de déclaration | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 2004 | 2005 | 2006 | 2007 | 2008 | 2009 | 2010 | 2011 | 2012 | 2013 | 2014 | ||||||||||||
| n | % | n | % | n | % | n | % | n | % | n | % | n | % | n | % | n | % | n | % | n | % | |
| Isolats soumis à des tests de résistance à l'INH, à la RMP, à l'EMB et à la PZA | 1 | 100,0 | 1 | 100,0 | 0 | 0 | 0 | 0 | 0 | 0 | 1 | 100,0 | 1 | 100,0 | 3 | 100,0 | 0 | 0 | 0 | 0 | 2 | 100,0 |
| Isolats sensibles à tous les antituberculeux majeurs | 1 | 100,0 | 1 | 100,0 | 0 | 0 | 0 | 0 | 0 | 0 | 1 | 100,0 | 1 | 100,0 | 2 | 66,7 | 0 | 0 | 0 | 0 | 2 | 100,0 |
| Résistants à un ou plusieurs antituberculeux majeurs | 0 | 0,0 | 0 | 0,0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0,0 | 0 | 0,0 | 1 | 33,3 | 0 | 0 | 0 | 0 | 0 | 0,0 |
| Tuberculose monorésistante | ||||||||||||||||||||||
| INH | 0 | 0,0 | 0 | 0,0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0 | 0 | 0 | 0 | 0,0 |
| RMP | 0 | 0,0 | 0 | 0,0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0 | 0 | 0 | 0 | 0,0 |
| EMB | 0 | 0,0 | 0 | 0,0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0 | 0 | 0 | 0 | 0,0 |
| PZA | 0 | 0,0 | 0 | 0,0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0,0 | 0 | 0,0 | 1 | 33,3 | 0 | 0 | 0 | 0 | 0 | 0,0 |
| Total | 0 | 0,0 | 0 | 0,0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0,0 | 0 | 0,0 | 1 | 33,3 | 0 | 0 | 0 | 0 | 0 | 0,0 |
| Année de déclaration | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 2004 | 2005 | 2006 | 2007 | 2008 | 2009 | 2010 | 2011 | 2012 | 2013 | 2014 | ||||||||||||
| n | % | n | % | n | % | n | % | n | % | n | % | n | % | n | % | n | % | n | % | n | % | |
| Isolats soumis à des tests de résistance à l'INH, à la RMP, à l'EMB et à la PZATableau 15 note de bas de page * | 207 | 100,0 | 226 | 100,0 | 201 | 100,0 | 200 | 100,0 | 210 | 100,0 | 171 | 100,0 | 197 | 100,0 | 205 | 100,0 | 209 | 100,0 | 205 | 100,0 | 186 | 100,0 |
| Isolats sensibles à tous les antituberculeux majeurs | 190 | 91,8 | 207 | 91,6 | 173 | 86,1 | 177 | 88,5 | 188 | 89,5 | 156 | 91,2 | 179 | 90,9 | 180 | 87,8 | 187 | 89,5 | 187 | 91,2 | 167 | 89,8 |
| Résistants à un ou plusieurs antituberculeux majeurs | 17 | 8,2 | 19 | 8,4 | 28 | 13,9 | 23 | 11,5 | 22 | 10,5 | 15 | 8,8 | 18 | 9,1 | 25 | 12,2 | 22 | 10,5 | 18 | 8,8 | 19 | 10,2 |
| Tuberculose monorésistante | ||||||||||||||||||||||
| INH | 11 | 5,3 | 14 | 6,2 | 21 | 10,4 | 12 | 6,0 | 15 | 7,1 | 7 | 4,1 | 11 | 5,6 | 18 | 8,8 | 13 | 6,2 | 12 | 5,9 | 10 | 5,4 |
| RMP | 0 | 0,0 | 0 | 0,0 | 1 | 0,5 | 1 | 0,5 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| EMB | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| PZA | 4 | 1,9 | 4 | 1,8 | 4 | 2,0 | 4 | 2,0 | 4 | 1,9 | 2 | 1,2 | 5 | 2,5 | 6 | 2,9 | 9 | 4,3 | 4 | 2,0 | 7 | 3,8 |
| Total | 15 | 7,2 | 18 | 8,0 | 26 | 12,9 | 17 | 8,5 | 19 | 9,0 | 9 | 5,3 | 16 | 8,1 | 24 | 11,7 | 22 | 10,5 | 16 | 7,8 | 17 | 9,1 |
| Polyrésistante | ||||||||||||||||||||||
| INH et PZA | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,5 | 1 | 0,5 | 0 | 0,0 | 1 | 0,5 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| INH et EMB | 1 | 0,5 | 0 | 0,0 | 0 | 0,0 | 3 | 1,5 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| Total | 1 | 0,5 | 0 | 0,0 | 0 | 0,0 | 4 | 2,0 | 1 | 0,5 | 0 | 0,0 | 1 | 0,5 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| Tuberculose multirésistanteTableau 15 note de bas de page † | ||||||||||||||||||||||
| INH, RMP, EMB, ETH et RBT | 0 | 0,0 | 0 | 0,0 | 1 | 0,5 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| INH, RMP, EMB, PZA et RBT | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,6 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| INH, RMP, EMB, PZA, SM et ETH | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,5 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| INH, RMP, EMB, PZA, SM, KM, ETH, RBT et PAS | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,5 | 0 | 0,0 |
| INH, RMP, EMB, PZA, SM et RBT | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,5 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| INH, RMP, EMB et RBT | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,5 | 0 | 0,0 | 1 | 0,6 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| INH, RMP, EMB, SM et RBT | 0 | 0,0 | 0 | 0,0 | 1 | 0,5 | 1 | 0,5 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| INH, RMP, PZA, ETH et RBT | 0 | 0,0 | 1 | 0,4 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| INH, RMP, PZA et RBT | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,5 |
| INH, RMP, PZA, SM, AK, KM et CM | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,5 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| INH, RMP, PZA, SM, KM, CM et ETH | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,6 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| INH, RMP et RBT | 1 | 0,5 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,6 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| INH, RMP, SM et RBT | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,5 | 2 | 1,2 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,5 |
| Total | 1 | 0,5 | 1 | 0,4 | 2 | 1,0 | 2 | 1,0 | 2 | 1,0 | 6 | 3,5 | 1 | 0,5 | 1 | 0,5 | 0 | 0,0 | 1 | 0,5 | 2 | 1,1 |
| Tuberculose ultrarésistanteTableau 15 note de bas de page ‡ | ||||||||||||||||||||||
| INH, RMP, EMB, PZA, SM, AK, KM, CM, OFL, MOX, ETH et RBT | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,5 | 0 | 0,0 |
| Total | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 0,5 | 0 | 0,0 |
Abréviations : AK, amikacine; CM, capréomycine; ETH, éthionamide; KM, kanamycine; MOX, moxifloxacine; OFL, ofloxacine; PAS, acide para-aminosalicylique; RBT, rifabutine; RMP, rifampicine; SM, streptomycine.
|
||||||||||||||||||||||
| Année de déclaration | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 2004 | 2005 | 2006 | 2007 | 2008 | 2009 | 2010 | 2011 | 2012 | 2013 | 2014 | ||||||||||||
| n | % | n | % | n | % | n | % | n | % | n | % | n | % | n | % | n | % | n | % | n | % | |
| Isolats soumis à des tests de résistance à l'INH, à la RMP, à l'EMB et à la PZA | 34 | 100,0 | 74 | 100,0 | 58 | 100,0 | 60 | 100,0 | 81 | 100,0 | 77 | 100,0 | 54 | 100,0 | 66 | 100,0 | 72 | 100,0 | 71 | 100,0 | 63 | 100,0 |
| Isolats sensibles à tous les antituberculeux majeurs | 32 | 94,1 | 72 | 97,3 | 57 | 98,3 | 59 | 98,3 | 79 | 97,5 | 72 | 93,5 | 51 | 94,4 | 62 | 93,9 | 68 | 94,4 | 69 | 97,2 | 60 | 95,2 |
| Résistants à un ou plusieurs antituberculeux majeurs | 2 | 5,9 | 2 | 2,7 | 1 | 1,7 | 1 | 1,7 | 2 | 2,5 | 5 | 6,5 | 3 | 5,6 | 4 | 6,1 | 4 | 5,6 | 2 | 2,8 | 3 | 4,8 |
| Tuberculose monorésistante | ||||||||||||||||||||||
| INH | 2 | 5,9 | 2 | 2,7 | 1 | 1,7 | 1 | 1,7 | 2 | 2,5 | 3 | 3,9 | 2 | 3,7 | 4 | 6,1 | 1 | 1,4 | 1 | 1,4 | 0 | 0,0 |
| RMP | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 1,6 |
| EMB | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| PZA | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 3 | 4,2 | 1 | 1,4 | 1 | 1,6 |
| Total | 2 | 5,9 | 2 | 2,7 | 1 | 1,7 | 1 | 1,7 | 2 | 2,5 | 3 | 3,9 | 2 | 3,7 | 4 | 6,1 | 4 | 5,6 | 2 | 2,8 | 2 | 3,2 |
| Polyrésistante | ||||||||||||||||||||||
| INH et PZA | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 1,6 |
| INH et EMB | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 1,3 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| Total | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 1,3 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 1,6 |
| Tuberculose multirésistanteTableau 16 note de bas de page * | ||||||||||||||||||||||
| INH, RMP et RBT | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 1,9 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| INH, RMP et SM | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 1,3 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| Total | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 1,3 | 1 | 1,9 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
Abréviations : EMB, éthambutol; INH, isoniazide; PZA, pyrazinamide; RBT, rifabutine; RMP, rifampicine; SM, streptomycine.
|
||||||||||||||||||||||
| Année de déclaration | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 2004 | 2005 | 2006 | 2007 | 2008 | 2009 | 2010 | 2011 | 2012 | 2013 | 2014 | ||||||||||||
| n | % | n | % | n | % | n | % | n | % | n | % | n | % | n | % | n | % | n | % | n | % | |
| Isolats soumis à des tests de résistance à l'INH, à la RMP et à l'EMBTableau 17 note de bas de page * | 3 | 100,0 | 2 | 100,0 | 2 | 100,0 | 2 | 100,0 | 7 | 100,0 | 3 | 100,0 | 5 | 100,0 | 2 | 100,0 | 1 | 100,0 | 1 | 100,0 | 4 | 100,0 |
| Isolats sensibles à tous les antituberculeux majeurs | 3 | 100,0 | 2 | 100,0 | 2 | 100,0 | 2 | 100,0 | 7 | 100,0 | 3 | 100,0 | 5 | 100,0 | 2 | 100,0 | 1 | 100,0 | 1 | 100,0 | 4 | 100,0 |
Abréviations : EMB, éthambutol; INH, isoniazide; PZA, pyrazinamide; RMP, rifampicine.
|
||||||||||||||||||||||
| Canada | Province d'origine | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| T.-N.-L. | Î.-P.-É. | N.-É. | N.-B. | Qc | Ont. | Man. | Sask. | Alb. | C.-B. | Yn | T.N.-O. | Nt | ||
| Nombre total d'isolats du CMTB testés | 1 376 | 6 | 2 | 8 | 6 | 186 | 457 | 125 | 63 | 181 | 270 | 4 | 2 | 66 |
| Tuberculose multirésistanteTableau 18 note de bas de page * | ||||||||||||||
| Isoniazide et rifampicine | 10 | 0 | 0 | 0 | 0 | 1 | 3 | 0 | 0 | 2 | 4 | 0 | 0 | 0 |
| Isoniazide, rifampicine et éthambutol | 3 | 0 | 0 | 0 | 0 | 0 | 1 | 0 | 0 | 0 | 2 | 0 | 0 | 0 |
| Isoniazide, rifampicine et pyrazinamide | 2 | 0 | 0 | 0 | 0 | 1 | 1 | 0 | 0 | 0 | 0 | 0 | 0 | 0 |
| Isoniazide, rifampicine et pyrazinamide | 3 | 0 | 0 | 0 | 0 | 0 | 1 | 0 | 0 | 2 | 0 | 0 | 0 | 0 |
| Total | 18 | 0 | 0 | 0 | 0 | 2 | 6 | 0 | 0 | 4 | 6 | 0 | 0 | 0 |
| Tuberculose ultrarésistanteTableau 18 note de bas de page † | ||||||||||||||
| Isoniazide, rifampicine, pyrazinamide, éthambutol, streptomycine, kanamycine, ofloxacine, moxifloxacine et rifabutine | 1 | 0 | 0 | 0 | 0 | 0 | 1 | 0 | 0 | 0 | 0 | 0 | 0 | 0 |
| Total | 1 | 0 | 0 | 0 | 0 | 0 | 1 | 0 | 0 | 0 | 0 | 0 | 0 | 0 |
Abréviations : Alb., Alberta; C.-B., Colombie-Britannique; Î.-P.-É., Île-du-Prince-Édouard; Man., Manitoba; N.-B., Nouveau-Brunswick; N.-É., Nouvelle-Écosse; Nt, Nunavut; Ont., Ontario; Qc, Québec; Sask., Saskatchewan; T.-N.-L., Terre-Neuve-et-Labrador; T.N.-O., Territoires du Nord-Ouest; Yn, Yukon.
|
||||||||||||||
| Province d'origine | Nombre total d'isolats du CMTB déclarés | Résistants à un ou plusieurs antituberculeux majeurs | Tuberculose multirésistanteTableau 19 note de bas de page * | Tuberculose ultrarésistanteTableau 19 note de bas de page † | |||
|---|---|---|---|---|---|---|---|
| nombre | pourcentage (%) | nombre | pourcentage (%) | nombre | pourcentage (%) | ||
| Ontario | 5 688 | 633 | 11,1 | 96 | 1,7 | 5 | 0,1 |
| Colombie-Britannique | 2 611 | 255 | 9,8 | 23 | 0,9 | 0 | 0,0 |
| Québec | 2 217 | 226 | 10,2 | 19 | 0,9 | 1 | 0,0 |
| Alberta | 1 479 | 145 | 9,8 | 24 | 1,6 | 0 | 0,0 |
| Manitoba | 1 247 | 70 | 5,6 | 4 | 0,3 | 1 | 0,1 |
| Saskatchewan | 710 | 29 | 4,1 | 2 | 0,3 | 0 | 0,0 |
| Nunavut | 515 | 5 | 1,0 | 0 | 0,0 | 0 | 0,0 |
| Terre-Neuve-et-Labrador | 81 | 1 | 1,2 | 0 | 0,0 | 0 | 0,0 |
| Nouvelle-Écosse | 80 | 8 | 10,0 | 0 | 0,0 | 0 | 0,0 |
| Territoires du Nord-Ouest | 80 | 3 | 3,8 | 0 | 0,0 | 0 | 0,0 |
| Nouveau-Brunswick | 64 | 6 | 9,4 | 0 | 0,0 | 0 | 0,0 |
| Yukon | 32 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| Île-du-Prince-Édouard | 9 | 1 | 11,1 | 0 | 0,0 | 0 | 0,0 |
| Canada | 14 813 | 1 382 | 9,3 | 168 | 1,1 | 7 | <0,1 |
|
|||||||
| Groupe d'âge et sexe | Isolats déclarés | Résistants à un ou plusieurs antituberculeux majeurs | Tuberculose multirésistanteTableau 20 note de bas de page * | Tuberculose ultrarésistanteTableau 20 note de bas de page † | |||||
|---|---|---|---|---|---|---|---|---|---|
| nombre | pourcentage(%) | nombre | pourcentage (%) | nombre | pourcentage (%) | nombre | pourcentage (%) | ||
| 0 à 4 ans | Hommes | 8 | 0,6 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| Femmes | 4 | 0,3 | 1 | 0,8 | 1 | 5,6 | 0 | 0,0 | |
| Inconnu | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | |
| Total | 12 | 0,9 | 1 | 0,8 | 1 | 5,6 | 0 | 0,0 | |
| 5 à 14 ans | Hommes | 12 | 0,9 | 1 | 0,8 | 0 | 0,0 | 0 | 0,0 |
| Femmes | 10 | 0,7 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | |
| Inconnu | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | |
| Total | 22 | 1,6 | 1 | 0,8 | 0 | 0,0 | 0 | 0,0 | |
| 15 à 24 ans | Hommes | 93 | 6,8 | 4 | 3,1 | 1 | 5,6 | 0 | 0,0 |
| Femmes | 81 | 5,9 | 9 | 6,9 | 1 | 5,6 | 0 | 0,0 | |
| Inconnu | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | |
| Total | 174 | 12,6 | 13 | 9,9 | 2 | 11,1 | 0 | 0,0 | |
| 25 to 34 ans | Hommes | 116 | 8,4 | 9 | 6,9 | 3 | 16,7 | 0 | 0,0 |
| Femmes | 134 | 9,7 | 21 | 16,0 | 2 | 11,1 | 1 | 100,0 | |
| Inconnu | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | |
| Total | 250 | 18,2 | 30 | 22,9 | 5 | 27,8 | 1 | 100,0 | |
| 35 à 44 ans | Hommes | 103 | 7,5 | 11 | 8,4 | 0 | 0,0 | 0 | 0,0 |
| Femmes | 113 | 8,2 | 16 | 12,2 | 3 | 16,7 | 0 | 0,0 | |
| Inconnu | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | |
| Total | 216 | 15,7 | 27 | 20,6 | 3 | 16,7 | 0 | 0,0 | |
| 45 à 54 ans | Hommes | 120 | 8,7 | 9 | 6,9 | 2 | 11,1 | 0 | 0,0 |
| Femmes | 70 | 5,1 | 7 | 5,3 | 1 | 5,6 | 0 | 0,0 | |
| Inconnu | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | |
| Total | 190 | 13,8 | 16 | 12,2 | 3 | 16,7 | 0 | 0,0 | |
| 55 à 64 ans | Hommes | 110 | 8,0 | 12 | 9,2 | 1 | 5,6 | 0 | 0,0 |
| Femmes | 49 | 3,6 | 5 | 3,8 | 0 | 0,0 | 0 | 0,0 | |
| Inconnu | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | |
| Total | 159 | 11,6 | 17 | 13,0 | 1 | 5,6 | 0 | 0,0 | |
| 65 à 74 ans | Hommes | 90 | 6,5 | 12 | 9,2 | 1 | 5,6 | 0 | 0,0 |
| Femmes | 50 | 3,6 | 4 | 3,1 | 0 | 0,0 | 0 | 0,0 | |
| Inconnu | 1 | 0,1 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | |
| Total | 141 | 10,2 | 16 | 12,2 | 1 | 5,6 | 0 | 0,0 | |
| 75 ans et plus | Hommes | 127 | 9,2 | 5 | 3,8 | 1 | 5,6 | 0 | 0,0 |
| Femmes | 83 | 6,0 | 5 | 3,8 | 1 | 5,6 | 0 | 0,0 | |
| Inconnu | 1 | 0,1 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | |
| Total | 211 | 15,3 | 10 | 7,6 | 2 | 11,1 | 0 | 0,0 | |
| Inconnu | Hommes | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
| Femmes | 1 | 0,1 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | |
| Inconnu | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | |
| Total | 1 | 0,1 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | |
| Total | Hommes | 779 | 56,6 | 63 | 48,1 | 9 | 50,0 | 0 | 0,0 |
| Femmes | 595 | 43,2 | 68 | 51,9 | 9 | 50,0 | 1 | 100,0 | |
| Inconnu | 2 | 0,1 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | |
| Total | 1 376 | 100,0 | 131 | 100,0 | 18 | 100,0 | 1 | 100,0 | |
|
|||||||||