Normes nationales sur l'évaluation de la couverture vaccinale : Recommandations du Réseau canadien des registres d'immunisation
1. Introduction/contexte
Partout au Canada, les programmes d'immunisation financés par l'État sont offerts pour l'immunisation systématique des enfants contre la diphtérie, la coqueluche, le tétanos, la poliomyélite, l'Haemophilus influenzae de type B, la rougeole, les oreillons, la rubéole (RRO) et les infections par le virus de l'hépatite BNote de bas de page i. Depuis 2000, de nouveaux programmes ont été instaurés au Canada à la suite de recommandations formulées par le Comité consultatif national de l'immunisation (CCNI). Chaque vaccin est administré en fonction des calendriers d'immunisation provinciaux/territoriaux, qui varient légèrement d'une province ou d'un territoire à l'autre. Pour surveiller la protection de la population contre les maladies évitables par la vaccination, la couverture est considérée comme un indicateur important de l'état de santé. Il s'agit d'une mesure sensible, qui peut être utilisée en tant que mesure indirecte pour évaluer les services et les systèmes de santé, ainsi que les interventions en santéNote de bas de page iiNote de bas de page iii. En outre, il est utile de surveiller les tendances nationales en matière de couverture vaccinale au fil du temps, car cela contribue à l'évaluation des programmes et des progrès réalisés par rapport à un objectifNote de bas de page iv.
Les données concernant la couverture vaccinale sont souvent recueillies et communiquées à l'échelle locale, provinciale, territoriale et nationale. Les normes nationales relatives aux rapports sur la couverture vaccinale au Canada ont été publiées en 2005Note de bas de page v. Selon ces normes, la couverture vaccinale nationale devrait être évaluée avant le 2e, le 7e et le 17e anniversaire de naissance, et suivant le calendrier d'immunisation pour les enfants d'âge scolaire, par antigène, et elle devrait être rapportée annuellement à partir des données des registres d'immunisation, ou aux deux ans, à l'aide d'enquêtes. Les normes ont été élaborées dans le but de faciliter la collecte de données agrégées, permettre de comparer la couverture vaccinale au sein des provinces et des territoires et définir une méthode normalisée pour mesurer la couverture vaccinale au Canada. Les défis à surmonter actuellement en ce qui concerne la collecte et la déclaration des données sur la couverture vaccinale sont les suivants :
- Manque de régularité et de cohérence sur le plan de la collecte des données
- Méthodes d'évaluation de la couverture vaccinale non uniformisées
- Absence de définitions normalisées pour les rapports (p. ex. numérateur, dénominateur)
- Hétérogénéité des calendriers d'immunisation d'une province et d'un territoire à l'autre
La définition de normes nationales aux fins des rapports sur la couverture vaccinale vise à faire ce qui suit :
- Faciliter le partage de l'information ayant trait à l'immunisation entre les gouvernements fédéral, provinciaux et territoriaux, tout en renforçant les capacités en matière de rapports des registres d'immunisation ou d'autres systèmes d'information.
- Produire une mesure agrégée de la couverture vaccinale à l'échelle nationale.
- Contribuer à la création de registres d'immunisation provinciaux/territoriaux uniformisés, laquelle est un objectif important de la Stratégie nationale d'immunisationNote de bas de page vi.
La mise à jour des normes nationales relatives aux rapports sur la couverture vaccinale au Canada établies en 2012, et leur examen en 2014, dénotent l'évolution, au fil des années, des priorités en matière de rapports sur la couverture vaccinale au Canada. En outre, tandis que les normes précédentes relatives à la couverture vaccinale étaient surtout axées sur la déclaration d'estimations de la couverture vaccinale provenant de données d'enquête, cette mise à jour revoit les normes pour rendre celles-ci applicables aux registres d'immunisation électroniques, aux enquêtes ou à d'autres méthodes de collecte de données. Les révisions apportées aux normes ont été faites à la suite d'une consultation auprès des provinces et des territoires.
Notre rapport décrit les méthodes utilisées pour élaborer les normes nationales relatives aux rapports sur la couverture vaccinale de 2005 et 2008, ainsi que les recommandations mises à jour formulées par le Réseau canadien des registres d'immunisation (RCRI) en 2012, puis révisées en 2014. Le présent document décrit les normes relatives à la déclaration de la couverture vaccinale chez les enfants de 2 ans; en 2012, le RCRI a également décidé de tenir compte d'autres groupes d'âge. Nous espérons qu'un réseau national des registres d'immunisation sera mis en place au Canada et que ces normes de déclaration fourniront un « étalon-or » pour la production de rapports sur la couverture vaccinale.
2. Méthodes
En 2004, des représentants provinciaux et territoriaux du Réseau canadien des registres d'immunisation (RCRI) ont répondu à une enquête concernant les normes utilisées pour la déclaration des données sur la couverture vaccinale. Les résultats de l'enquête ont été présentés lors de la réunion du RCRI, parrainée par Santé Canada (SC), qui s'est tenue en juillet 2004. Au cours de la réunion, les participants ont discuté des objectifs principaux relatifs aux rapports sur la couverture vaccinale, puis procédé à l'ébauche de recommandations à cet égard. En plus de l'enquête, un examen de la documentation traitant de l'évaluation de la couverture vaccinale à l'échelle nationale et internationale est venu enrichir ces débats, dont les conclusions figurent dans le rapport complet (disponible auprès de l'Agence de la santé publique du Canada [ASPC]).
En octobre 2004, le Comité canadien sur l'immunisation (CCI) a demandé à ce que le Programme d'agents de surveillance sur le terrain soit chargé d'améliorer les rapports sur la couverture vaccinale et a donné la priorité à cette tâche en réalisant le premier projet de collaboration des agents de surveillance sur le terrain (AST). En 2005, une série de normes relatives à la déclaration de données sur la couverture vaccinale au Canada a été publiée dans le Relevé des maladies transmissibles au Canada (RMTC)Note de bas de page v.
En octobre 2006, le British Columbia Centre for Disease Control (BC CDC) a mené une enquête, qu'il a présentée au RCRI; ce dernier a confirmé que l'adoption de normes nationales en matière de couverture vaccinale n'est pas uniforme à l'échelle du pays. S'appuyant sur ces résultats, le RCRI a déterminé qu'il est nécessaire de clarifier les points suivants :
- Raisons pour lesquelles les provinces et les territoires n'adoptent pas des normes nationales sur la couverture vaccinale
- Capacité de ces normes à uniformiser les taux de couverture provinciale afin d'améliorer la comparabilité
Au cours de l'hiver 2007, l'ASPC, par l'intermédiaire du Programme d'AST de l'Alberta, du Manitoba et de la Saskatchewan, a mené un projet pilote dans le but d'étudier la faisabilité de l'extraction et de l'analyse des données des registres d'immunisation provinciaux en suivant les normes nationales relatives aux rapports sur la couverture vaccinale de 2005. L'objectif de ce projet pilote était de cerner les lacunes des normes de déclaration existantes et d'expliquer pourquoi les normes ne sont pas adoptées de manière uniforme. Un plan d'analyse a été élaboré à partir des normes nationales existantes en matière de rapports sur la couverture vaccinale. Si une lacune était relevée, d'autres critères étaient définis, s'il était jugé nécessaire de le faire, afin d'effectuer une analyse complète. Au nombre de ces critères supplémentaires, mentionnons la définition d'un calendrier d'immunisation commun pour les provinces participantes et l'établissement de définitions de certains termes tels que « dose valide », « délai de grâce », etc., lesquels sont définis différemment par les provinces et les territoires. Lorsqu'il n'y avait pas de définition, les définitions utilisées actuellement dans les provinces et les territoires ont été utilisées. À la fin du projet pilote, on a demandé à chaque province d'évaluer le processus et le niveau d'effort requis pour mettre en œuvre les normes de 2005. On a ensuite comparé les estimations de la couverture produites par chaque province.
Les résultats du projet pilote ont été présentés au RCRI en juin 2007 et un groupe de travail composé d'AST et de membres du RCRI a été formé et chargé d'examiner les normes. En février 2012, le RCRI s'est réuni pour examiner et réviser les normes exposées dans le présent document afin de confirmer les recommandations. Le RCRI a examiné ces normes à l'automne 2014, et les mises à jour fournies étaient incluses.
La version définitive remaniée des normes nationales relatives aux rapports sur la couverture de 2014 est présentée dans le présent document.
3. Résultats
Les résultats et les recommandations qui ont émané du projet pilote de 2007 sont les suivants :
Principaux résultats
- Les taux de couverture globale entre les provinces sont comparables lorsqu'on utilise les mêmes normes de déclaration des données sur la couverture vaccinale. La couverture vaccinale à jour à 24 mois pour le vaccin antirougeoleux, antiourlien et antirubéoleux (RRO) se situait entre 83 % et 87 %; pour le vaccin contenant l'anatoxine diphtérique, l'anatoxine tétanique et un anticoquelucheux acellulaire (DTCa), elle se situait entre 67 % et 75 %.
- La capacité à appliquer les normes nationales variait selon le registre. L'ensemble des normes de déclaration nationales de 2005 pouvait être appliqué; cependant, les autres définitions élaborées pour ce projet (p. ex. doses valides, inclusion d'exemptions/contre-indications, dénominateur uniforme) ne s'appliquaient pas toujours en raison du manque d'information ou de fonctionnalité dans les registres.
- Les obstacles à l'application de normes nationales cernés étaient, notamment : temps limité pour concevoir d'autres programmes de normes nationales en matière de déclaration et manque de détail dans les normes nationales.
Recommandations/Prochaines étapes
- Les normes nationales doivent être applicables à la fois aux données des registres et aux données d'enquête. Les données des registres d'immunisation sont plus riches et permettent de produire des rapports plus élaborés que les données de l'enquête à laquelle les normes de rapport de 2005 étaient destinées.
- Il faut préciser la méthode à utiliser pour analyser les normes nationales.
- Il faut définir plus précisément les termes suivants :
- Doses valides
- Motifs de non-immunisation (c.-à-d. exemptions et contre-indications)
- Immunisation conforme au calendrier et immunisation à jour
- Dénominateur correspondant à la population
- Fournir des directives claires sur la façon de gérer :
- les données propres à la population autochtone (Premières Nations qui reçoivent le vaccin dans les réserves, Premières Nations hors réserves, Inuits et Métis);
- les calendriers d'immunisation aux fins de production de rapports nationaux.
Recommandations relatives aux rapports sur la couverture vaccinale nationale (février 2012)
Il a été recommandé de déclarer deux mesures générales de la couverture vaccinale à l'échelle nationale et d'inclure les immunisations qui sont :
- « à jour »,
- « conformes au calendrier ».
Ces mesures peuvent être calculées à l'aide des données des registres ou des données provenant d'autres sources (p. ex. enquête, données de facturation des médecins, etc.). Dans chaque mesure, les définitions de certains éléments essentiels à l'analyse sont précisées davantage; nous fournissons un exemple pour illustrer leur utilisation. Certains des éléments communs aux trois résultats sont définis à la section « Règles générales » (tableau 2) qui suit les résultats (Mesure no 1 et no 2).
Il a été recommandé d'utiliser les données pour évaluer la couverture des vaccins administrés dans le cadre de programmes d'immunisation en milieu scolaire et de programmes d'immunisation s'adressant aux adultes, ainsi que celles contenues dans les registres des clients.
Le calendrier d'immunisation figurant au tableau 1 décrit les exigences en matière d'immunisation à satisfaire pour atteindre les cibles de couverture vaccinale recommandées.
Calendrier d'immunisation
Le calendrier d'immunisation aux fins de la déclaration nationale devrait être fondé sur les critères minimaux communs utilisés dans tous les calendriers provinciaux au moment de la production des rapports (p. ex. chaque année). Les calendriers d'immunisation des provinces et des territoires varient, mais ils tiennent compte des recommandations actuelles du Comité consultatif national de l'immunisation (CCNI)Note de bas de page viii. Depuis février 2012, les exigences sont les suivantes :
À jour
Immunisation À JOUR à 2 ans, 7 ans et vaccins administrés dans le cadre d'un programme scolaire
- Calendrier d'immunisation systématique :
- Avant 24 mois :
- ≥ 4 doses du DTCa-VPI(3)Note de bas de page ix-Hib(4) (2, 4, 6, 18 mois)
- 1 dose du vaccin RRO (12 mois)
- 3 doses du vaccin conjugué contre le pneumocoque (2, 4, [6 RÉ], entre 12 et 15 mois)
- 1 à 4 doses du vaccin antiméningococcique conjugué (avant 12 mois)
- 2 doses du vaccin contre la varicelle (12 mois, 18 mois)
- HB durant la petite enfance (3 doses) ou préadolescence (2 ou 3 doses)
- ≥ 1 dose du vaccin antigrippal
- 2 doses du vaccin contre le rotavirus (2 mois, 4 mois)
- Avant 7 ans
- ≥ 5 doses du DTCa-VPI(4)Note de bas de page ix-Hib(4) (2, 4, 6, 18 mois, entre 4 et 6 ans)
- 2 doses du vaccin RRO (12 ET 18 mois OU entre 4 et 6 ans)
- 3 doses du vaccin conjugué contre le pneumocoque (2, 4, [6 RÉ], entre 12 et 15 mois)
- 1 à 4 doses du vaccin antiméningococcique conjugué (2, 4, 6 et 12 mois)
- 2 doses du vaccin contre la varicelle (12 mois, 18 mois)
- HB durant la petite enfance (3 doses) ou préadolescence (2 ou 3 doses)
- ≥ 1 dose du vaccin antigrippal
- Avant 17 ans
- ≥ 6 doses du DTCa-VPI(4)Note de bas de page ix-Hib(4) (2, 4, 6, 18 mois, entre 4 et 6 ans, et entre 14 et 16 ans)
- 2 doses du vaccin RRO (12 ET 18 mois OU entre 4 et 6 ans)
- 3 doses du vaccin conjugué contre le pneumocoque (2, 4, [6 RÉ], entre 12 et 15 mois)
- 1 à 4 + 1 doses du vaccin antiméningococcique conjugué (2, 4, 6 et 12 mois et préadolescence)
- 2 doses du vaccin contre la varicelle (12 mois, 18 mois)
- HB durant la petite enfance (3 doses) ou préadolescence (2 ou 3 doses)
- ≥ 1 dose du vaccin antigrippal
- 3 doses du VPH (entre 9 et 18 ans, à 0, 2, 6 mois d'intervalle)
- Avant 24 mois :
- Retard dans le calendrier d'immunisation
- Calendrier d'immunisation systématique des enfants de 24 mois ou de moins de 7 ans n'ayant pas été immunisés dans leur petite enfance :
- DTCa-VPI :
- 4 doses (première visite, 2, 2 et de 6 à 12 mois plus tard)
- dcaT :
- 1 dose entre de 14 à 16 ans
- Hib :
- si la première dose a été donnée entre 2 et 11 mois : 3 doses
- si la première dose a été donnée entre 12 et 14 mois : 2 doses
- si la première dose a été donnée entre 15 et 23 mois : 1 dose
- RRO-Var :
- 2 doses (première visite, puis 2 mois plus tard)
- Vaccin conjugué contre le pneumocoque (2 et 4 mois) :
- si la première dose a été donnée entre 2 et 6 mois : 4 doses (SYSTÉMATIQUE)
- si la première dose a été donnée entre 7 et 11 mois : 3 doses
- si la première dose a été donnée entre 12 et 21 mois : 2 doses
- si la première dose a été donnée entre 22 et 23 mois : 1 dose
- Vaccin antiméningococcique conjugué :
- s'il a été administré pour la première fois à 12 mois et plus : 1 dose la première visite + 1 dose à l'âge de 12 ans
- HB
- 3 doses (à la première visite, à 2 mois et entre 6 et 12 mois plus tard)
- VPH
- 3 doses (dès l'âge de 9 ans)
- DTCa-VPI :
- Calendrier d'immunisation systématique des enfants de 7 ans et plus jusqu'à 17 ans qui n'ont pas été immunisés dans leur petite enfance
- dcaT :
- 4 doses (à la première visite, à 2 mois, entre 6 et 12 mois et 10 ans plus tard)
- VPI
- 3 doses (à la première visite, à 2 mois et entre 6 et 12 mois plus tard)
- RRO-Var :
- 1 à 2 doses (à la première visite, puis 2 mois plus tard)
- Vaccin antiméningococcique conjugué :
- 1 dose (à la première visite)
- HB
- 3 doses (à la première visite, 2 mois et/ou entre 6 et 12 mois plus tard)
- VPH
- 3 doses (dès l'âge de 9 ans, à la première visite, 2 mois plus tard, puis 6 à 12 mois plus tard)
- dcaT :
- Calendrier d'immunisation systématique des enfants de 24 mois ou de moins de 7 ans n'ayant pas été immunisés dans leur petite enfance :
Conforme au calendrier
Immunisation CONFORME AU CALENDRIER
Même calendrier que celui de la couverture « à jour ». Toutefois, l'intervalle entre les doses et le moment d'administrer les doses sont déterminés par les lignes directrices sur les périodes d'admissibilité, d'échéance et de retardNote de bas de page vii.
- Remarque 1 : En ce qui concerne la vaccination conforme au calendrier, les antigènes ne sont pas tous comparables dans l'ensemble des provinces et des territoires. Pour évaluer la couverture vaccinale des vaccins contre l'hépatite B, la pneumonie et le méningocoque du groupe C (Men-C), le nombre de doses requises par seuil d'âge variera selon les provinces et les territoires,car les calendriers d'immunisation varient.
- Remarque 2 : Par définition, les enfants qui ne participent pas à un programme d'immunisation systématique dès la petite enfance (c.-à-d. retard dans le calendrier) ne sont pas pris en compte dans le calcul de la couverture vaccinale de l'immunisation systématique conforme au calendrier. Par conséquent, aucun autre calendrier n'est fourni pour calculer l'immunisation conforme au calendrier.
- Guide canadien d'immunisation, novembre 2012.
- Programmes d'immunisation subventionnés par l'État au Canada – Calendrier d'immunisation systématique des nourrissons et des enfants incluant les projets spéciaux et les programmes de rappel, Agence de la santé publique du Canada, en collaboration avec la Coalition canadienne des infirmières et infirmiers pour l'immunisation (CNCI), décembre 2012.
- Lignes directrices nationales sur les périodes d'admissibilité, d'échéance et de retard pour les fins des registres d'immunisation : Recommandations provisoires du Groupe de travail sur la normalisation des données du Réseau canadien des registres d'immunisation, Relevé des maladies transmissibles au Canada (RMTC), 15 mars 2004, volume 30.
Résultats recommandés pour les mesures de la couverture vaccinale nationale
Mesure no 1 : Immunisation à jour
Définition
A reçu la série complète de doses vaccinales valides requises avant l'âge de 1 an ou de 2 ans (reportez-vous au tableau 2 pour connaître la définition d'une dose valide). Les doses valides doivent être reçues pendant la période recommandée afin de maximiser l'immunogénicité de chaque vaccin; de plus, il faut prendre en considération l'intervalle recommandé entre l'administration de chaque dose.
Utilisation prévue
Mesure de la protection de la population.
Numérateur
Le nombre d'enfants ayant reçu toutes les doses requises valides avant l'âge de 2 ans.
Justification des groupes d'âge
La mesure de la couverture vaccinale avant l'âge de 2 ans est utile pour faire des comparaisons à l'échelle nationale et internationale, comme il s'agit d'un âge de référence très utilisé, ainsi que pour mesurer l'administration de la série complète de vaccins donnée aux enfants.
Mesures de la couverture à jour
Les trois mesures suivantes sont recommandées pour produire des rapports sur la couverture vaccinale à jour. Les enfants qui satisfont aux exigences suivantes avant l'âge de 2 ans sont considérés comme étant « à jour » et doivent être inclus dans le numérateur :
- Par antigène : L'estimation de la couverture vaccinale individuelle est déclarée à chacun des antigènes suivants, et aux posologies indiquées, ce qui donne une mesure unique de la couverture vaccinale par antigène.
- Avant l'âge de 2 ans : 4 doses de D, T, Ca, 3 doses par personne du VPI et du PCV-13, 1 dose de Ro, Or, Ru, Men-C, Var et InfNote de bas de page x
- Avant l'âge de 7 ans : DTCa (5 doses)-VPI (4)-Hib (4) + 2 doses Ro, 1 dose de Or et de Ru
- Avant l'âge de 17 ans : DTCa (6 doses)-VPI (4)-Hib (4)+ 2 doses Ro, une dose de Or et de Ru
- Série d'antigènes excluant les nouveaux vaccinsNote de bas de page xi : Une mesure de la couverture vaccinale, qui englobe tous les antigènes et les posologies suivants, est produite, ce qui donne une mesure à jour.
- Avant l'âge de 2 ans : DTCa(4 doses)-IPV (3)-Hib (4) + RRO (1 OU 2)+ PCV-13 (2 ou 3 selon l'âge à la première dose) + Men-C (1 à 3 selon l'âge à la première dose) + Var1 (2) + Inf (1)
- Avant l'âge de 7 ans : DTCa (5 doses)-VPI (4)-Hib (4) + RRO (2)
- Avant l'âge de 17 ans : DTCa (6 doses)-VPI (4)-Hib (4) + RRO (2)
- Tous les antigènesNote de bas de page xii : Une mesure de la couverture vaccinale, qui englobe tous les antigènes et les posologies suivants, est produite, ce qui donne une mesure à jour.
- Avant l'âge de 2 ans : DTCa (4 doses)-VPI (3)-Hib (4) + RRO (1 ou 2) + PCV-13 (2 ou 3 selon l'âge à la première dose) + Men-C (1 à 3 selon l'âge à la première dose) + Var1 (2) + HB durant la petite enfance (3 ou préadolescence, 2 ou 3) + Inf (1) + Rot (2)
- Avant l'âge de 7 ans : DTCa (5 doses)-VPI (4)-Hib (4) + RRO (2) + PCV-13 (2 ou 3 selon l'âge à la première dose) + Men-C (1 à 3 selon l'âge à la première dose) + Var1 (2) + HB durant la petite enfance (3 ou préadolescence, 2 ou 3)
+ Inf (1) + Rot (2) - Avant l'âge de 17 ans : DTCa (6 doses)-VPI (4)-Hib (4) + RRO (2) + PCV-13 (2 ou 3 selon l'âge à la première dose) + Men-C (1 à 3 selon l'âge à la première dose) + Var1 (2) + HB durant la petite enfance (3 ou préadolescence, 2 ou 3) + Inf (1) + Rot (2) + VPH (3)
Dénominateur
Pour la couverture vaccinale avant l'âge de 2 ans :
- Tous les enfants qui ont un « dossier actif »Note de bas de page xiii dans la cohorte de naissance (c.-à-d. registre de la population) et atteignent l'âge de 2 ans au cours de la période visée par l'évaluation (c.-à-d. tous les enfants qui ont fêté leur deuxième anniversaire de naissance au cours de l'année civile [p. ex. du 1er janvier au 31 décembre]). Le dénominateur doit comprendre tous les enfants qui sont exemptés du vaccin ou pour lesquels le vaccin est contre-indiqué (veuillez consulter le tableau 2 pour connaître la définition des exemptions et des contre-indications).
Les provinces et les territoires qui s'appuient sur les registres d'immunisation pour faire l'évaluation de la couverture vaccinale doivent entreprendre des évaluations périodiques afin de confirmer l'intégralité du dénominateur correspondant à leur population.
Calcul de la couverture
Le calcul suivant doit être effectué à chaque antigène ou combinaison d'antigènes :
Données de registre
- x
- Nombre d'enfants ayant un dossier actif dans le registre, qui ont suivi au complet le calendrier d'immunisation systématique des enfants avant l'âge de 1 an (ou 2 ans) dans la province
- y
- Nombre total d'enfants ayant un dossier actif dans le registre provincial, qui atteignent l'âge de 1 an ou 2 ans pendant la période visée
Données d'enquête
- x
- Nombre d'enfants dans l'échantillon de l'enquête qui ont suivi au complet le calendrier d'immunisation avant l'âge de 1 an (ou 2 ans)
- y
- Nombre total d'enfants dont les parents ont répondu à l'enquête
Exemple 1
Un enfant atteint l'âge de 2 ans le 15 mars 2006. La couverture est évaluée en 2006; par conséquent, cet enfant est admissible et inclus dans la cohorte de naissance visée par l'évaluation de la couverture vaccinale. L'enfant a reçu l'ensemble des doses recommandées de chaque antigène; toutefois, certaines d'entre elles n'étaient pas valides (p. ex. 2e dose du vaccin DTCa-VPI-Hib), et certaines autres avaient dépassé l'âge fixé dans le calendrier (p. ex. la 4e dose à recevoir après l'âge de 2 ans). Cet enfant ne serait donc pas inclus dans le numérateur « à jour ».
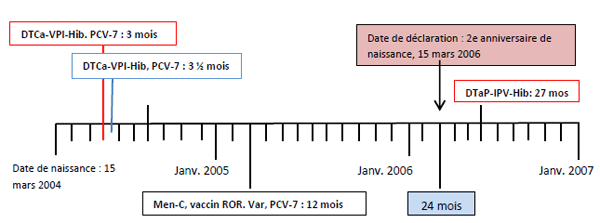
Description de la figure de l'exemple 1
Cette figure présente un exemple de la façon dont le statut « à jour » est déterminé par les activités de vaccination. L'échelle de temps présente les intervalles annuels depuis la date de naissance d'un enfant né le 15 mars 2004. Chaque case le long de l'échelle de temps représente une dose unique, ce qui comprend les antigènes administrés et l'âge auquel le vaccin a été administré. Les antigènes administrés comprennent le vaccin contenant l'anatoxine diphtérique, l'anatoxine tétanique et un anticoquelucheux acellulaire (DTCa), un vaccin antipoliomyélitique (VPI), un vaccin contre l'Haemophilus influenza de type b (Hib) à l'âge de 3, 3,5, 6 et 27 mois; un vaccin contre le pneumocoque (PCV-7) à l'âge de 3, 3,5 et 12 mois ainsi qu'un vaccin contre la rougeole, les oreillons et la rubéole (ROR), la varicelle (Var), le pneumocoque (PCV-7) et le méningocoque (Men-C) à l'âge de 12 mois. Dans cet exemple, l'enfant serait admissible à une évaluation de la couverture vaccinale pendant la période visée, soit 2006, indiquée dans la case de la période de déclaration. Cet enfant a reçu toutes les doses recommandées de chaque antigène, cependant, la deuxième dose du vaccin DTCa-VPI-Hib et celle du vaccin PCV-7 à l'âge de 3,5 mois ne sont pas valides (c.-à-d. administrées trop tôt) et la quatrième dose du vaccin DTCa-VPI-Hib a été administrée en retard (c.-à-d. qu'elle est reçue après le deuxième anniversaire). Le deuxième anniversaire est indiqué par la case « 24 mois ». Par conséquent, cet enfant ne serait pas considéré comme étant « à jour » pour le vaccin PCV-7 et la série d'antigènes comprenant le vaccin DTCa-VPI-Hib.
| Par antigène | Doses reçues avant l'âge de 2 ans | À jour? | Raison |
|---|---|---|---|
| Diphtérie/tétanos/polio/coqueluche/Haemophilus influenzae de type B | 3 | Non | 3 doses reçues avant l'âge de 2 ans, mais 1 dose reçue après l'âge de 2 ans. 2e dose non valide, car elle a été reçue trop tôt |
| PCV-7 | 3 | Non | 2e dose reçue trop tôt, donc non valide et non comptabilisée |
| Rougeole, oreillons et rubéole | 1 | Oui | 1 dose reçue avant l'âge de 2 ans |
| Men-C | 1 | Oui | 1 dose reçue avant l'âge de 2 ans |
| Varicelle | 1 | Oui | 1 dose reçue avant l'âge de 2 ans |
| Par série d'antigènes moins les nouveaux vaccins | |||
| DTCa-VPI, Hib, vaccin RRO | 3-3-1 | Non | 4e dose de DTCa-VPI, Hib reçue après l'âge de 2 ans |
| Par série d'antigènes, incluant tous les vaccins | |||
| DTCa-IPV, Hib, vaccin RRO, Men-C, PCV-7, Var | 3-3-1-1-3-1 | Non | 4e dose de DTCa-VPI, Hib reçue après l'âge de 2 ans |
Mesure de la couverture no 2 : Immunisation conforme au calendrier
Définition
A reçu la série complète de doses vaccinales avant l'âge de 1 an ou 2 ans. Ces lignes directrices précisent également une marge de un mois après l'administration de la dose. Cette marge de un mois permet d'immuniser un enfant un mois après la date prévue en lui administrant la dose établie dans le calendrier d'immunisation présenté au tableau 1. Un mois correspond à quatre semaines (28 jours) ou à un certain nombre de jours civils déterminé dans le protocole de programmation utilisé. Les doses doivent être administrées en respectant les intervalles définis dans les lignes directrices nationales sur les périodes d'admissibilité, d'échéance et de retard.
Veuillez consulter le tableau 2 pour une définition plus précise de la couverture « conforme au calendrier » et des notes sur la programmation.
Utilisation prévue
La couverture conforme au calendrier est une mesure du succès de l'exécution des programmes d'immunisation et de l'administration des ressources.
Numérateur
Nombre d'enfants ayant reçu toutes les doses valides requises pour être conformes au calendrier selon le seuil d'âge précisé.
Les trois mesures suivantes sont recommandées pour produire des rapports sur la couverture vaccinale conforme au calendrier. Les enfants qui satisfont aux exigences suivantes avant l'âge de 1 an et de 2 ans sont considérés comme ayant été immunisés « conformément au calendrier » et doivent être inclus dans le numérateur :
- Par antigène
- L'estimation de la couverture vaccinale individuelle est déclarée à chacun des antigènes, selon le seuil d'âge qui prend en compte uniquement les doses requises pour cet antigène à cet âge. Dès qu'une seule dose d'un antigène particulier est donnée en retard (ou trop tôt), l'enfant n'est plus considéré comme immunisé conformément au calendrier relativement à cet antigène. - Veuillez consulter le calendrier d'immunisation au tableau 1.
- Tous les antigènes moins les nouveaux vaccins
- Une mesure de la couverture vaccinale à chaque seuil d'âge, qui englobe tous les antigènes et les posologies suivants, est produite. - Veuillez consulter le calendrier d'immunisation au tableau 1.
- Tous les antigènes
- Une mesure de la couverture vaccinale, qui englobe tous les antigènes et les posologies suivants, est produite, ce qui donne une mesure de l'immunisation conforme au calendrier. - Veuillez consulter le calendrier d'immunisation au tableau 1.
Dénominateur
Pour la couverture vaccinale avant l'âge de 1 an ou 2 ans :
- Tous les enfants qui ont un « dossier actif »Note de bas de page xiii dans la cohorte de naissance (c.-à-d. registre de la population) et qui atteignent l'âge de 1 an ou 2 ans au cours de la période visée par l'évaluation (c.-à-d. tous les enfants qui ont fêté leur premier ou leur deuxième anniversaire de naissance au cours de l'année civile [p. ex. du 1er janvier au 31 décembre]). Le dénominateur doit comprendre tous les enfants qui sont exemptés du vaccin ou auxquels le vaccin est contre-indiqué (veuillez consulter le tableau 2 pour connaître la définition des exemptions et des contre-indications).
Exemple 2
Scénario avec un enfant dont l'immunisation n'est pas conforme au calendrier
L'enfant atteint l'âge de 2 ans le 15 mars 2006 (c.-à-d. il atteint l'âge de 2 ans pendant la période visée, soit 2006). Toutes les doses requises de chaque antigène sont reçues avant le 2e anniversaire de l'enfant, mais elles n'ont pas été administrées au bon moment ni selon l'intervalle requis.
Extrait des lignes directrices sur les périodes d'admissibilité, d'échéance et de retard.
- 3e dose du vaccin DTCa
- Admissibilité
- 28 jours après la deuxième dose
- Échéance
- 2 mois après la deuxième dose
- Retard
- 3 mois après la deuxième dose
L'administration de la troisième dose du vaccin DTCa est « conforme au calendrier » seulement si elle est faite entre 28 jours suivant l'administration de la 2e dose et l'âge de 6 mois (p. ex. avant 3 mois à partir de la 2e dose). Dans le scénario ci-dessous, la 3e dose a été administrée en retard, donc l'immunisation de l'enfant n'est pas considérée comme étant « conforme au calendrier ».
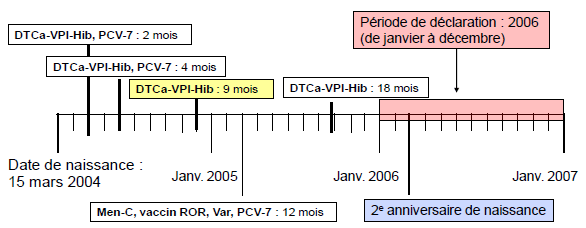
Description de la figure de l'exemple 2
Cette figure présente un exemple de la façon dont le statut « conforme au calendrier » est déterminé par les activités de vaccination. L'échelle de temps présente les intervalles annuels depuis la date de naissance d'un enfant né le 15 mars 2004. Chaque case le long de l'échelle de temps représente une dose unique, ce qui comprend les antigènes administrés et l'âge auquel le vaccin a été administré. Les antigènes administrés comprennent le vaccin contenant l'anatoxine diphtérique, l'anatoxine tétanique et un anticoquelucheux acellulaire (DTCa), un vaccin antipoliomyélitique (VPI), un vaccin contre l'Haemophilus influenza de type b (Hib) à l'âge de 2, 4, 9 et 18 mois; un vaccin contre le pneumocoque (PCV-7) à l'âge de 2, 4 et 12 mois ainsi qu'un vaccin contre la rougeole, les oreillons et la rubéole (ROR), la varicelle (Var), le méningocoque (Men-C) à l'âge de 12 mois. Dans cet exemple, l'enfant serait admissible à une évaluation de la couverture vaccinale pendant la période visée, soit 2006, indiquée dans la case de la période de déclaration. Toutes les doses requises de chaque antigène ont été reçues avant le deuxième anniversaire de l'enfant. Toutefois, toutes les doses n'ont pas été reçues au bon moment et aux bons intervalles entre chaque dose. La troisième dose des vaccins DTCa-VPI-Hib et PCV-7 administrée à l'âge de 9 mois est seulement « conforme au calendrier » si elle est administrée entre 28 jours à compter de la deuxième dose et la fin du sixième mois de vie (p. ex. d'ici trois mois à compter de la deuxième dose). Dans cet exemple, la troisième dose a été administrée en retard, par conséquent, cet enfant ne serait pas considéré comme étant « conforme au calendrier » pour la série d'antigène comprenant le vaccin DTCa-VPI-Hib.
Tableau 2 - Recommandations nationales relatives aux normes de rapport sur l'évaluation de la couverture - Terminologie générale
1. Doses valides
- Définition
- Dose qui est jugée protectrice pour la personne et qui doit être incluse dans les rapports sur la couverture vaccinale. Une dose valide est administrée après le nombre minimal de jours spécifié à partir de l'administration de la première dose de cet antigène ou à partir de la naissance. Une dose est non valide si elle a été donnée plus tôt que la période d'« admissibilité » pour chaque vaccin.
- Considérations / Justification
- Les lignes directrices sur les périodes d'admissibilité, d'échéance et de retard doivent être utilisées pour définir l'intervalle entre chaque dose et l'admissibilité à la première dose.
2. Délai de grâce
- Définition
- Le délai de grâce fait référence au délai autorisé avant l'admissibilité de la dose, au cours duquel une dose administrée reste considérée comme valide. Aux fins des rapports sur la couverture vaccinale, les doses valides ne comprennent actuellement aucun délai de grâce pour les antigènes.
- Considérations / Justification
-
Aux États-Unis, l'Advisory Committee on Immunization Practices (ACIP) recommande un délai de grâce de quatre jours, ce qui signifie que si une dose est administrée quatre jours avant son échéance, elle est considérée malgré cela comme étant valide et n'a pas besoin d'être administrée de nouveau. Cette règle est destinée aux fins de l'évaluation de la couverture vaccinale et ne doit pas être utilisée dans la planification de l'administration des vaccins. Les recherches réalisées en Colombie-Britannique par le Centre de contrôle des maladies de la Colombie-Britannique ont montré que l'utilisation des délais de grâce n'a pas d'effet significatif sur la couverture vaccinale.
Il peut exister actuellement des variations quant aux critères relatifs aux doses valides, car certaines provinces et certains territoires incorporent des délais de grâce et ont parfois des politiques qui permettent de considérer comme étant valide une dose du vaccin RRO administrée précocement. Le délai de grâce est souvent fondé sur une décision subjective avant de consigner la dose dans le registre d'immunisation. À l'avenir, si l'on décide d'utiliser les délais de grâce, il faudra statuer sur un délai de grâce commun à chaque province et territoire.
3. Exemptions et contre-indications
- Définition
- Aux fins des déclarations nationales, l'ensemble des exemptions et des contre-indications devraient être inclus, sans distinction, dans le dénominateur. À l'heure actuelle, les exemptions et les contre-indications ne peuvent pas être mesurées dans l'ensemble des provinces et des territoires.
- Considérations / Justification
-
Lorsqu'il se fait, l'enregistrement des exemptions et des contre-indications varie d'une province ou d'un territoire à l'autre. En outre, il est difficile de consigner les enfants pour lesquels un vaccin est contre-indiqué parce qu'ils ne se présentent pas pour se faire vacciner et ne sont pas identifiés comme tels dans le registre. À l'avenir, lorsque les registres seront disponibles par l'intermédiaire d'un réseau national dans toutes les provinces et tous les territoires, et que les contre-indications et les exemptions pourront plus facilement être suivies, les définitions devraient être les suivantes :
- Exemption
- Le client est exempté pour des motifs médicaux, religieux ou philosophiques. L'immunité acquise à la suite d'une maladie ou d'une vaccination antérieure est un exemple médical.
- Contre-indications
- Dans certains cas, il est décidé délibérément de ne pas administrer un vaccin, et cela est consigné dans le système électronique d'information sur la santé publique. Une contre-indication indique que l'agent immunisant ne doit pas être administré, car les risques l'emportent sur les avantages pour la santé du receveur.
4. Données propres aux populations autochtones (Premières Nations/Inuits/Métis)
- Définition
-
La Constitution canadienne reconnaît trois groupes de peuples autochtones : les Premières Nations, les Métis et les Inuits. Les membres des Premières Nations vivent dans des réserves et hors de réserves.
Aux fins des rapports nationaux, il est recommandé que les données des provinces et des territoires comprennent un identifiant désignant les membres d'une Première Nation (dans les réserves et hors des réserves)/Inuits/Métis au moment de leur collecte. Par exemple, sans identifiant, la couverture vaccinale des membres des Premières Nations qui vivent dans des réserves sera probablement sous-estimée, si ceux-ci reçoivent leurs vaccins hors de la réserve.
Certaines provinces/territoires ont mis en place des mécanismes pour ventiler les données relatives aux Premières Nations/Inuits/Métis provenant de leurs registres d'immunisation. Dans les provinces et les territoires où il est possible de ventiler ces données dans le registre, il est recommandé d'inclure ces données dans le numérateur et le dénominateur pour calculer la couverture vaccinale. - Considérations / Justification
-
La Direction générale de la santé des Premières nations et des Inuits (DGSPNI) de Santé Canada fournit ou soutient l'exécution des programmes d'immunisation destinés aux membres des Premières Nations vivant dans les réserves, lesquels correspondent aux calendriers d'immunisation de la province où se trouve la réserve. Les données sur la couverture vaccinale dans les réserves sont communiquées par les communautés des Premières Nations aux bureaux régionaux de la DGSPNI en Alberta, en Saskatchewan, au Manitoba, en Ontario, au Québec et dans la région de l'Atlantique (soit le Nouveau-Brunswick, la Nouvelle-Écosse, l'Île-du-Prince-Édouard et Terre-Neuve-et-Labrador). - Il faudrait envisager de mettre en place un mécanisme permettant d'intégrer ces données dans les registres provinciaux.
- Les données sur l'immunisation des membres des Premières Nations (dans les réserves et hors des réserves), les Inuits et les Métis inscrites dans les registres provinciaux et territoriaux sont souvent incomplètes ou ne sont pas recueillies à l'aide d'une méthode standard dans chaque province ou territoire, entraînant une sous-estimation de la couverture. Cela s'explique par plusieurs facteurs : lorsque les membres des Premières Nations/Inuits/Métis sont inclus dans les registres provinciaux et territoriaux, ces registres n'utilisent bien souvent aucun identifiant, ou alors, les identifiants utilisés sont incomplets (p. ex. ils requièrent une déclaration volontaire, mais en général, peu le font).
- Dans certaines provinces, l'immunisation des Premières Nations qui vivent dans des réserves ne sera consignée dans le registre provincial que si les vaccins sont reçus à l'extérieur des réserves.
Lorsqu'il y a des données particulières sur les Premières Nations dans les registres provinciaux et territoriaux, le terme « Premières Nations » est parfois défini de façon différente selon la province ou le territoire, car il n'existe pas de définition normalisée.
Pour surveiller les changements et cerner les tendances, évaluer l'efficacité des programmes et orienter la prise de décision fondée sur des données probantes, il faut disposer de données ventilées sur l'immunisation chez les Premières Nations (dans les réserves et hors des réserves)/Inuits/Métis. Il est nécessaire de recueillir des données sur l'immunisation à l'aide d'une approche standardisée et coordonnée dans l'ensemble des provinces et des territoires.
5. Dénominateur
- Définition
-
Le dénominateur à utiliser pour calculer la couverture correspond à tous les enfants dans le registre de la « population » ayant l'âge visé, pendant l'année de l'évaluation. Le dénominateur doit se fonder sur les dossiers « actifs » seulement, c'est-à-dire les enfants résidant dans la province au cours de la période qui fait l'objet de l'évaluation de la couverture. Dans certaines provinces et certains territoires, cela peut inclure tous les dossiers qui renferment des numéros d'assurance-maladie actifs pendant la période en question.
Les dossiers des personnes qui sont « actives » au moment de l'analyse, mais qui, dans le passé, n'étaient pas inscrites de façon continue au régime d'assurance-maladie de la province doivent être inclus dans le dénominateur. Les données sources utilisées dans le registre de la « population » pourraient correspondre, par exemple, à une base de données sur les personnes inscrites au registre, à une base de données sur la facturation des médecins ou à une base de données des numéros d'assurance-maladie. - Considérations / Justification
- Le suivi et la migration à l'intérieur et à l'extérieur d'une province ou d'un territoire sont parfois difficiles, et ils varient suivant la province ou le territoire. Certaines provinces utilisent, dans leurs bases de données sur les personnes inscrites au registre, des marques signalant les déplacements, qui permettent de comptabiliser les migrations, tandis que d'autres font cela manuellement. En outre, le suivi des dossiers des personnes dont l'inscription au régime d'assurance-maladie est discontinue est souvent incomplet, car les prestations ne sont pas toujours transférées pendant de courtes périodes où la personne est absente de la province.
6. Période de conformité au calendrier
- Définition
-
Une marge de un mois suivant le moment où il est recommandé d'administrer une dose de vaccin est autorisée aux fins des rapports sur la couverture vaccinale conforme au calendrier. Cette marge de un mois permet d'immuniser un enfant un mois après la date prévue dans le calendrier d'immunisation présenté au tableau 1.
- Remarque
- Aux fins de programmation et de comparaisons, la marge de un mois doit être exprimée en nombre de jours civils « réels »; cela signifie que la variation du nombre de jours d'un mois à l'autre est prise en compte (p. ex. entre 28 et 31 jours). Les provinces qui définissent déjà la marge de un mois comme étant une période de 28 jours peuvent continuer à utiliser cette définition, car la différence n'est pas censée avoir une incidence significative sur la couverture. L'analyse provinciale a fait ressortir une légère différence dans la couverture (c.-à-d. 0,1 %) lorsque l'analyse de l'immunisation conforme au calendrier est effectuée selon les jours civils et non un intervalle fixe de 28 jours.
- Autres calendriers
- Les enfants qui ne participent pas à un programme d'immunisation systématique dès la toute petite enfance (c.-à-d. qui commencent tardivement) ne sont pas pris en compte dans le calcul de la couverture conforme au calendrier. Cependant, d'autres calendriers, présentés au tableau 1, peuvent être suivis par les personnes qui ont reçu un vaccin en retard; de cette façon, on considérera celles-ci, dans l'évaluation de la couverture vaccinale, comme étant immunisées conformément au calendrier.
- Considérations / Justification
- La couverture conforme au calendrier est une mesure de l'exécution des programmes d'immunisation et de la conformité avec le calendrier d'immunisation systématique dans une province donnée. L'immunisation conforme au calendrier donne parfois lieu à une sous-estimation de la proportion d'enfants qui sont complètement protégés contre une maladie évitable par la vaccination, car l'enfant reste considéré comme étant entièrement immunisé, si le calendrier pour les vaccins reçus en retard est suivi.
7. Fréquence des déclarations et période de l'année
- Définition
-
Chaque province et chaque territoire devraient évaluer et déclarer les données sur la couverture vaccinale annuellement. Un rapport annuel sur la couverture vaccinale nationale, produit par l'
ASPC, inclura des estimations fondées à la fois sur les enquêtes nationales sur la vaccination et sur des évaluations provinciales ou territoriales, de même qu'une annexe précisant la méthodologie utilisée et la définition des cohortes d'âge.
- Données de registre
- Évaluation sur une base annuelle.
- Données d'enquête
- Évaluation aux deux ans. Dans le cas des enfants et des adolescents, l'évaluation devrait être effectuée à l'automne, pour tenir compte des exigences du milieu scolaire. (applicable aux enfants de 7 ans et de 17 ans).
- Considérations / Justification
- Dès que les registres d'immunisation seront pleinement fonctionnels à l'échelle nationale, il est recommandé que les données relatives à la couverture vaccinale qui y figurent soient déclarées annuellement. Cela dit, il faudrait maintenir la capacité des registres de fournir des rapports plus fréquents, selon les besoins liés à la planification et à l'évaluation des programmes ainsi qu'à l'étude de nouveaux programmes d'immunisation.
Conclusions
L'ébauche des normes nationales relatives aux rapports sur la couverture vaccinale est fondée sur un examen complet des normes de déclaration nationales et internationales et a été acceptée par consensus par les membres du RCRI. La définition de normes relatives à la production de rapports sur la couverture vaccinale nationale est une étape importante, qui nous conduira à la diffusion optimale de l'information et nous permettra d'assurer la comparabilité entre les estimations des provinces et des territoires et les estimations nationales de la couverture vaccinale.
Les normes nationales pourraient être mises à jour de nouveau dans l'avenir; les révisions dépendront des changements apportés aux programmes, ainsi que d'autres facteurs, comme l'instauration de nouveaux programmes d'immunisation et la création d'un réseau national des registres d'immunisation, qui pourrait modifier la façon de mesurer la couverture vaccinale.
Abréviations
- DCaT
- Vaccin combiné contre la diphtérie, la Coqueluche et le Tétanos
- VPI
- Vaccin Inactivé contre la Poliomyélite
- RRO
- Rougeole, Rubéole, Oreillons
- RoT
- Rotavirus
- HB
- Hépatite B
- VPH
- Virus du Papillome Humain
- HiB
- Haemophilus influenzae de type b
- Var
- Varicelle