Archivée - Résistance aux antituberculeux 2017

 Téléchargez cet article en format PDF
Téléchargez cet article en format PDFPublié par : L'Agence de la santé publique du Canada
Numéro : Volume 44-11 : Infections liées aux soins de santé et résistance aux antimicrobiens
Date de publication : 1er novembre 2018
ISSN : 1719-3109
Soumettre un article
À propos du RMTC
Naviguer
Volume 44-11, le 1er novembre 2018 : Infections liées aux soins de santé et résistance aux antimicrobiens
Surveillance
La résistance aux antituberculeux au Canada : 2017
M LaFreniere1, H Hussain1,2, J Vachon1
Affiliations
1 Centre de la lutte contre les maladies transmissibles et les infections, Agence de la santé publique du Canada, Ottawa (Ontario)
2 École de santé publique Dalla Lana, Université de Toronto, Toronto (Ontario)
Correspondance
Citation proposée
LaFreniere M, Hussain H, Vachon J. La résistance aux antituberculeux au Canada : 2017. Relevé des maladies transmissibles au Canada 2018;44(11):330-6. https://doi.org/10.14745/ccdr.v44i11a04f
Mots-clés : tuberculose, résistance, tuberculose multirésistante, tuberculose ultrarésistante, isolats, surveillance, isoniazide, rifampine, éthambutol, pyrazinamide
Résumé
Contexte : La tuberculose (TB) pharmacorésistante est un problème de santé publique mondial. Au Canada, des systèmes de surveillance sont en place depuis 20 ans pour suivre ce phénomène.
Objectif : Décrire les tendances en matière de pharmacorésistance parmi les isolats de la TB déclarés au Canada en 2017, selon le type de résistance, ainsi que l’emplacement géographique, les données démographiques et l’origine des cas, et comparer les données actuelles à celles des 10 années précédentes.
Méthodes : Les données analysées proviennent de deux sources. Le Système canadien de surveillance des laboratoires de tuberculose (SCSLT) est un système de surveillance de laboratoire des isolats. Il a servi à obtenir des renseignements sur les résultats des épreuves de sensibilité aux antituberculeux ainsi que sur la province ou le territoire, le sexe et l’âge des personnes à l’origine des échantillons. Le Système canadien de déclaration des cas de tuberculose (SCDCT) est un système de surveillance fondé sur les cas comportant des renseignements sur les cas de TB active et de retraitement au Canada. Il a été utilisé pour l’obtention de données sur l’origine des cas, qu’elle soit de personnes nées à l’étranger, de personnes autochtones nées au Canada ou de personnes non autochtones nées au Canada. L’analyse est descriptive, et la comparaison a été effectuée contre les données de 2007 à 2016 provenant de ces deux sources.
Résultats : En 2017, la résistance aux antituberculeux de 1 515 isolats de TB a été analysée; 123 de ces isolats (8,1 %) présentaient une résistance à au moins un antituberculeux majeur. Parmi ces derniers, 103 correspondaient à des souches de TB monorésistante; six, à des souches de TB polyrésistante et 14, à des souches de TB multirésistante (TB-MR). On n’a signalé aucune souche de tuberculose ultrarésistante (TB-UR) parmi ces isolats. Une pharmacorésistance a été signalée dans sept provinces ou territoires (Colombie‑Britannique, Alberta, Saskatchewan, Manitoba, Ontario, Québec et Nouveau‑Brunswick). Parmi les isolats provenant de personnes de sexe féminin, 63 (9,5 %) étaient pharmacorésistants, tandis que chez les personnes de sexe masculin, 60 isolats (7,0 %) étaient pharmacorésistants. Chez les personnes âgées de 25 à 34 ans, la pharmacorésistance était présente dans un plus grand pourcentage d’isolats (n = 29, 23,6 %). Selon l’origine, 1 072 (11 %) des cas de TB déclarés de 2005 à 2015 chez des personnes nées à l’étranger étaient pharmacorésistants. Chez les personnes non autochtones nées au Canada et les Autochtones nés au Canada, 143 (9 %) et 54 (2 %) des cas de TB étaient pharmacorésistants, respectivement. Comparativement aux années précédentes, le nombre d’isolats testés a légèrement augmenté (passant de 1 267 à 1 515); toutefois, on a observé une diminution du pourcentage d’isolats pour lesquels on a signalé une pharmacorésistance (de 10,5 % en 2007 à 8,1 % en 2017).
Conclusion : Le taux de pharmacorésistance de la TB est demeuré faible en 2017 au Canada.
Introduction
La tuberculose (TB) est une maladie infectieuse aérogène qui touche principalement les poumons et est causée par la bactérie Mycobacterium tuberculosis. Il s’agit d’une des maladies infectieuses les plus souvent déclarées à l’échelle mondiale Note de bas de page 1. En 2016, l’Organisation mondiale de la Santé (OMS) estimait que 10,4 millions de personnes avaient reçu un diagnostic de TB active Note de bas de page 1. Bien qu’on puisse guérir la TB, M. tuberculosis peut venir à présenter une résistance à un traitement antituberculeux. En 2016, l’OMS estimait qu’à l’échelle mondiale, 4,1 % des nouveaux cas et 19 % des cas déjà traités présentaient une tuberculose multirésistante (TB-MR) ou une TB résistante à la rifampine Note de bas de page 1.
Au Canada, l’incidence de la TB dans la population générale demeure faible, soit 4,8 cas pour 100 000 habitants; toutefois, certaines sous-populations sont touchées de façon disproportionnelle. Parmi les cas de TB déclarés à l’Agence de la santé publique du Canada (ASPC) en 2016, 70 % touchaient des personnes nées à l’extérieur du Canada. En outre, le taux dans l’ensemble de la population autochtone était de 23,5 cas pour 100 000 habitants et, chez les Inuit, il était de 170,1 pour 100 000 habitants Note de bas de page 2.
On surveille la TB pharmacorésistante depuis 20 ans au Canada, en raison de l’importance de la maladie à l’échelle internationale, en ce qui a trait à la santé publique et à l’éventualité que des souches pharmacorésistantes de TB se propagent au pays. Toutefois, la pharmacorésistance demeure rare parmi les cas de TB signalés au Canada. Au cours de la dernière décennie, les tendances en matière de pharmacorésistance sont demeurées stables et faibles, la résistance à au moins un antituberculeux majeur variant de 8,2 à 10,5 %. Au cours de la même période, la TB-MR est restée rare, le pourcentage d’isolats multirésistants variant de 0,6 à 1,6 % Note de bas de page 3.
Le présent rapport de surveillance a pour objectif de décrire les tendances en matière de pharmacorésistance parmi les isolats de la TB déclarés au Canada en 2017, selon le type de résistance, l’emplacement géographique, les données démographiques et l’origine des cas, et de comparer les données actuelles à celles des 10 années précédentes.
Méthodologie
Définitions
Les Normes canadiennes pour la lutte antituberculeuse classent les tendances en matière de résistance aux antituberculeux comme suit Note de bas de page 4 :
- Monorésistance : Résistance à un seul antituberculeux majeur (isoniazide, rifampicine, éthambutol ou pyrazinamide)
- Polyrésistance : Résistance à plus d’un antituberculeux majeur, à l’exclusion de la résistance à la fois à l’isoniazide et à la rifampicine
- Tuberculose multirésistante (TB-MR) : TB causée par des bactéries résistantes à l’isoniazide ET à la rifampicine avec ou sans résistance à d’autres antituberculeux
- Tuberculose ultrarésistante (TB-UR) : TB causée par des bactéries résistantes à l’isoniazide ET à la rifampicine AINSI QU’À toute fluoroquinolone ET à au moins un des trois antituberculeux mineurs injectables (amikacine, capréomycine ou kanamycine)
Sources de données
Les données analysées proviennent de deux systèmes de surveillance, soit le Système canadien de surveillance des laboratoires de tuberculose (SCSLT) et le Système canadien de déclaration des cas de tuberculose (SCDCT).
Système canadien de surveillance des laboratoires de tuberculose
Le SCSLT est un système dont la surveillance est fondée sur les isolats analysés en laboratoire. Les isolats des cas positifs à l’égard de la TB sont soumis à une épreuve de sensibilité aux antituberculeux, et le laboratoire qui effectue l’analyse transmet ensuite les résultats à l’ASPC sur une base volontaire.
Le présent article comporte les résultats des épreuves de sensibilité aux antituberculeux majeurs et à d’autres antituberculeux, le cas échéant, ainsi que le sexe, l’âge et la province ou le territoire des personnes à l’origine des échantillons. Dans la mesure du possible, un seul ensemble de résultats à l’épreuve de sensibilité aux antituberculeux a été inclus pour chaque cas dans notre analyse. Nous avons repéré les doublons éventuels par le biais du sexe, de la date de naissance ou de l’âge, ainsi que de la province ou du territoire, et demandé des éclaircissements auprès du laboratoire ayant fourni les résultats. Le nombre d’isolats a été vérifié par les laboratoires ayant fourni les résultats afin d’assurer l’exhaustivité du rapport et de clarifier toute incohérence relative aux données.
Système canadien de déclaration des cas de tuberculose
Alors que le SCSLT recueille des données sur les isolats de M. tuberculosis, le SCDCT est un système de surveillance fondé sur les cas qui comporte des renseignements sur les cas de TB active et de retraitement au Canada. Le SCDCT recueille certaines données relatives à la pharmacorésistance des cas de TB lorsque les autorités sanitaires provinciales et territoriales signalent ces cas à l’ASPC.
Dans le présent article, nous avons utilisé les renseignements du SCDCT pour obtenir des données sur l’origine, qui est définie comme une personne née à l’étranger, une personne autochtone née au Canada ou une personne non autochtone née au Canada. On peut trouver de plus amples renseignements sur le SCDCT dans le rapport La tuberculose au Canada 2012 Note de bas de page 5. Les plus récentes données disponibles pour la présente analyse dataient de 2015.
Analyse des données
Les données ont été triées et analysées à l’aide des logiciels SAS Enterprise Guide, version 5.1 (Cary, Caroline du Nord, États-Unis) et Microsoft Excel 2010 (Redmond, Washington, États-Unis). Tous les isolats ayant produit un résultat positif en culture en ce qui a trait au complexe Mycobacterium tuberculosis, particulièrement M. tuberculosis, M. africanum, M. canetti, M. caprae, M. microti, M. pinnipedii ou M. bovis, ont été inclus dans les analyses. Les isolats de TB positifs à l’égard du bacille de Calmette Guérin (BCG) dérivé de M. bovis ont été exclus des analyses.
Des analyses descriptives ont été menées sur les données de 2017 concernant la résistance, l’emplacement géographique et les données démographiques, ainsi que sur les données de 2015 ayant trait à l’origine. Ces analyses ont ensuite été comparées aux tendances des 10 années antérieures.
Résultats
Tendances en matière de résistance aux antituberculeux
En 2017, les résultats des épreuves de sensibilité aux antituberculeux de 1 534 isolats ont été transmis à l’ASPC. Parmi ces isolats, 19 étaient positifs à l’égard du BCG dérivé de M. bovis et n’ont pas été inclus dans l’analyse (Figure 1). Dans l’ensemble des 1 515 isolats inclus, 123 (8,1 %) présentaient une résistance à au moins un antituberculeux majeur, et 1 392 (91,9 %) étaient sensibles à tous les antituberculeux majeurs.
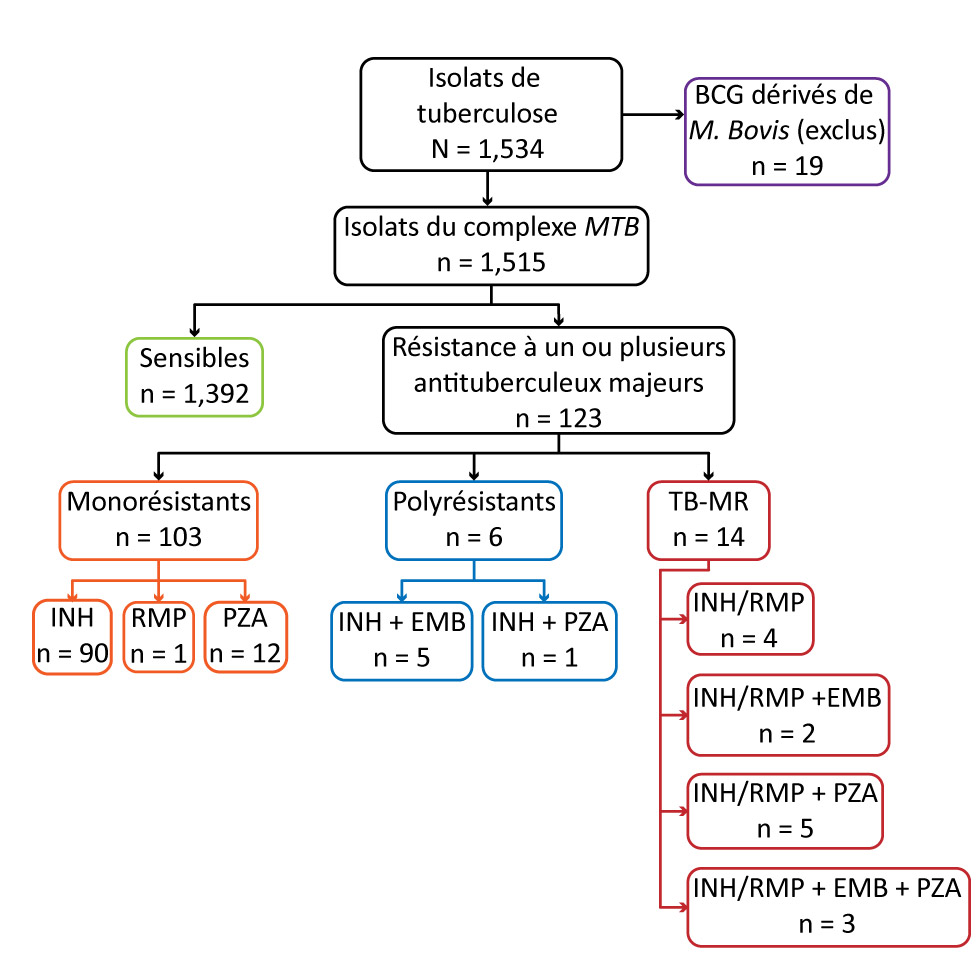
Figure 1 : Nombre d’isolats de tuberculose soumis à une épreuve de sensibilité aux antituberculeux et résultats, Canada, 2017
Description textuelle : Figure 1
Figure 1 : Nombre d’isolats de tuberculose soumis à une épreuve de sensibilité aux antituberculeux et résultats, Canada, 2017
La figure 1 est un organigramme illustrant le nombre d'isolats de tuberculose soumis à une épreuve de sensibilité aux antituberculeux et les résultats obtenus au Canada en 2017. La première case représente le nombre total d'isolats de tuberculose N = 1 534, avec une flèche pointant vers la zone de texte mentionnant M. bovis. BCG (exclus) n = 19. Immédiatement au-dessous de la zone Total des isolats se trouve une zone de texte indiquant les isolats du complexe MTB n = 1 515. Immédiatement ci-dessous, il débouche dans une zone de texte à gauche, Sensible n = 1 392, et dans la zone de texte à droite, indique toute résistance aux antituberculeux de première ligne n = 123. À partir de cette zone, il se divise en trois zones de texte. Monorésistant; Polyrésistant et TB-MDR. Sous Monorésistant, n = 103, trois zones de texte supplémentaires: INH n = 90, RMP n = 1 et PZA n = 12. Sous Polyrésistant n = 6, il y a deux zones de texte supplémentaires; INH + EMB n = 5 et NHI + PZA n = 1. Sous la TB-MDR, n = 14 sont quatre zones; INH / RMP n = 4, INH / RMP + EMB n = 2, INH / RMP + PZA n = 5 et INH / RMP + EMB + PZA n = 3.
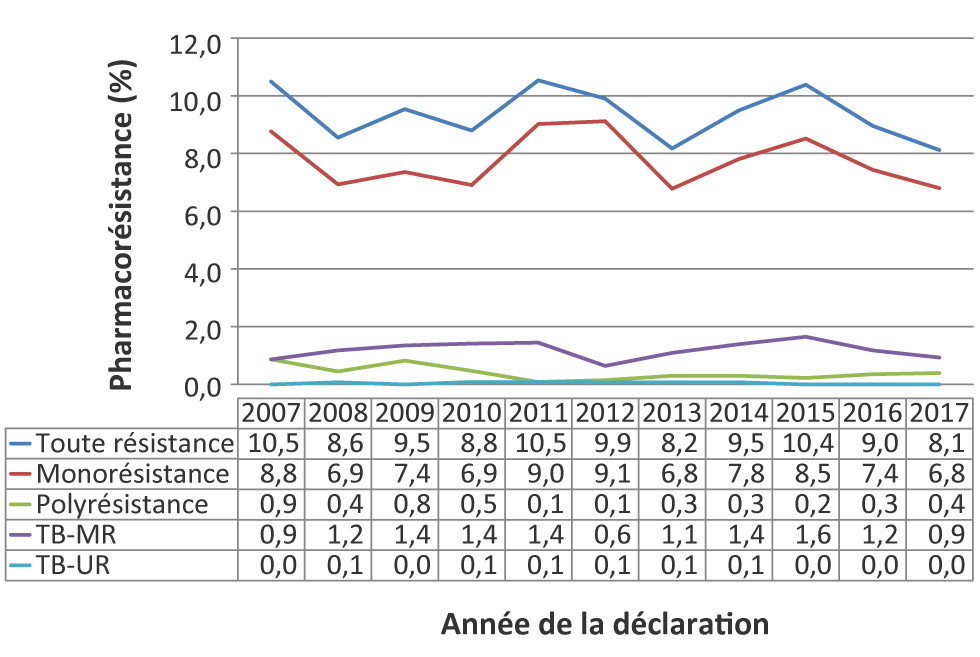
Bien que le nombre d’isolats positifs à l’égard de la TB ayant été soumis à une épreuve de sensibilité aux antituberculeux ait légèrement augmenté dans l’ensemble depuis 2007 (de 1 267 isolats), le nombre d’isolats déclarés résistants à au moins un antituberculeux a fluctué d’une année à l’autre et s’est soldé par une faible diminution globale du pourcentage d’isolats pour lesquels on a signalé une pharmacorésistance (de 10,5 % en 2007 à 8,1 % en 2017) (Figure 2).
Figure 2 : Proportion d’isolats de tuberculose pour lesquels on a signalé une pharmacorésistance, selon le type de pharmacorésistance, Canada, 2007 à 2017
Description textuelle : Figure 2
| Pharmacorésistance (%) | Année de la déclaration | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| 2007 | 2008 | 2009 | 2010 | 2011 | 2012 | 2013 | 2014 | 2015 | 2016 | 2017 | |
| Toute résistance | 10,5 | 8,6 | 9,5 | 8,8 | 10,5 | 9,9 | 8,2 | 9,5 | 10,4 | 9,0 | 8,1 |
| Monorésistance | 8,8 | 6,9 | 7,4 | 6,9 | 9,0 | 9,1 | 6,8 | 7,8 | 8,5 | 7,4 | 6,8 |
| Polyrésistance | 0,9 | 0,4 | 0,8 | 0,5 | 0,1 | 0,1 | 0,3 | 0,3 | 0,2 | 0,3 | 0,4 |
| TB-MR | 0,9 | 1,2 | 1,4 | 1,4 | 1,4 | 0,6 | 1,1 | 1,4 | 1,6 | 1,2 | 0,9 |
| TB-UR | 0,0 | 0,1 | 0,0 | 0,1 | 0,1 | 0,1 | 0,1 | 0,1 | 0,0 | 0,0 | 0,0 |
Monorésistance
La monorésistance était le type de résistance le plus fréquemment signalé. En 2017, parmi les isolats résistants à au moins un antituberculeux majeur, 103 (83,7 %) étaient monorésistants. Parmi ceux-ci, 90 étaient résistants à l’isoniazide seulement, 12 au pyrazinamide seulement, et un à la rifampine seulement. Aucun isolat n’était monorésistant à l’éthambutol (Figure 1). Ces résultats sont conformes aux données antérieures; depuis 2015, de 2007 à 2017, on observe une légère tendance à la baisse (Figure 2).
Polyrésistance
En 2017, six isolats (0,4 %) étaient polyrésistants : cinq étaient résistants à la fois à l’isoniazide et à l’éthambutol, et un était résistant tant à l’isoniazide qu’au pyrazinamide (Figure 1). Comparativement aux années antérieures, le pourcentage d’isolats qui étaient polyrésistants est demeuré faible (Figure 2).
TB-MR et TB-UR
En 2017, 14 (0,9 %) isolats ont été signalés comme étant résistants à la fois à l’isoniazide et à la rifampine (avec ou sans résistance à d’autres antituberculeux) et, par conséquent, ont été considérés comme des souches de TB-MR. Parmi eux, quatre étaient résistants de l’isoniazide et de la rifampine combinées, cinq étaient résistants à l’isoniazide, à la rifampine et au pyrazinamide, et deux étaient résistants à l’isoniazide, à la rifampine et à l’éthambutol. Trois isolats étaient résistants à l’ensemble des quatre antituberculeux majeurs (Figure 1). De 2007 à 2017, 172 (1,1 %) isolats de TB ont été signalés comme étant de type TB-MR; durant cette période, le pourcentage signalé était faible, et la tendance générale, stable (Figure 2).
Au Canada, en 2017, aucun isolat n’a été déclaré de type TB-UR. Même si deux isolats étaient résistants à l’isoniazide, à la rifampine et à toute fluoroquinolone, et que deux autres étaient résistants à l’isoniazide, à la rifampine et à au moins un antituberculeux injectables, aucun n’était résistant à l’ensemble des quatre antituberculeux. Depuis 2007, au Canada, seulement six isolats ont produit des résultats positifs permettant de les classer comme TB-UR; le plus récent a été signalé en 2014.
Distribution géographique
En 2017, l’Ontario a déclaré le plus grand nombre d’isolats (559 isolats, soit 36,9 %), suivi par la Colombie-Britannique, avec 260 isolats (17,2 %), de l’Alberta, avec 199 (13,1 %), du Québec, avec 183 (12,1 %), du Manitoba, avec 157 (10,4 %), de la Saskatchewan, avec 64 (4,2 %), et du Nunavut, avec 60 (4,0 %). Terre-Neuve-et-Labrador, la Nouvelle-Écosse, le Nouveau-Brunswick, le Yukon et les Territoires du Nord-Ouest ont signalé 2,2 % du total des isolats analysés en 2017. En 2017, le Nunavut a soumis près de deux fois plus d’isolats pour des épreuves de sensibilité aux antituberculeux qu’en 2016, probablement en raison du nombre accru de cas de TB dans cette jurisdiction Note de bas de page 6. On n’a déclaré aucun cas de TB à l’Île-du-Prince-Édouard en 2017.
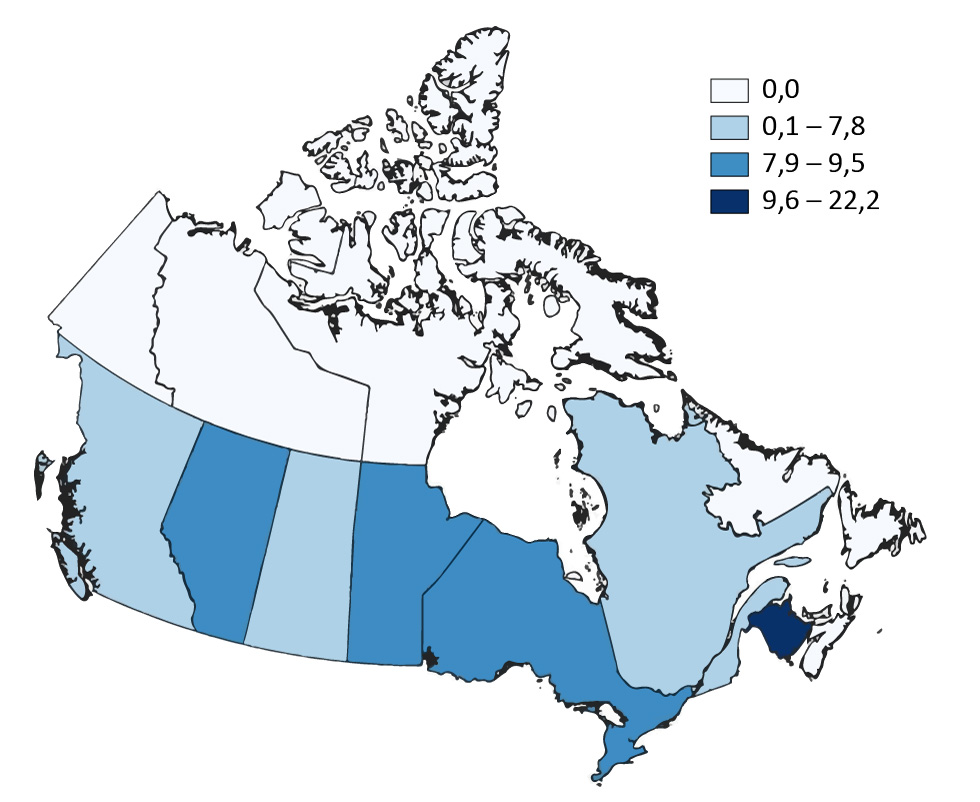
Parmi toutes les provinces et tous les territoires, la Colombie-Britannique, l’Alberta, la Saskatchewan, le Manitoba, l’Ontario, le Québec et le Nouveau-Brunswick ont signalé l’un ou l’autre des types de pharmacorésistance en 2017 (Figure 3). Dans le cas de la Colombie-Britannique, de l’Alberta, de la Saskatchewan, du Manitoba, de l’Ontario et du Québec, la proportion d’isolats présentant une résistance à un ou plusieurs antituberculeux variait de 6,9 à 9,5 %. Parmi les neuf isolats soumis par le Nouveau-Brunswick, deux présentaient une résistance à un ou plusieurs antituberculeux (22,2 %). Le Nunavut, Terre‑Neuve‑et‑Labrador, la Nouvelle‑Écosse, le Yukon et les Territoires du Nord‑Ouest n’ont signalé aucun isolat pharmacorésistant en 2017.
Figure 3 : Proportion (%) d’isolats présentant une résistance à un ou plusieurs antituberculeux selon la province ou le territoire, Canada, 2017
Description textuelle : Figure 3
| Canada 2017 | Province ou Territoire | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| T.-N.-L. | Î.-P.-É | N.-É. | N.-B. | Qc | Ont. | Man. | Sask. | Alb. | C.-B. | Yn | T.N.-O. | Nt | |
| Proportion | 0,0 | 0,0 | 0.0 | 22,2 | 7,7 | 9,1 | 8,9 | 7,8 | 9,5 | 6,9 | 0,0 | 0,0 | 0,0 |
Sur l’ensemble des 14 isolats de type TB-MR signalés en 2017, l’Ontario en comptait sept, le Nouveau-Brunswick, le Québec et la Colombie-Britannique en ont déclaré deux chacun, et l’Alberta en comptait un.
Distribution selon le sexe
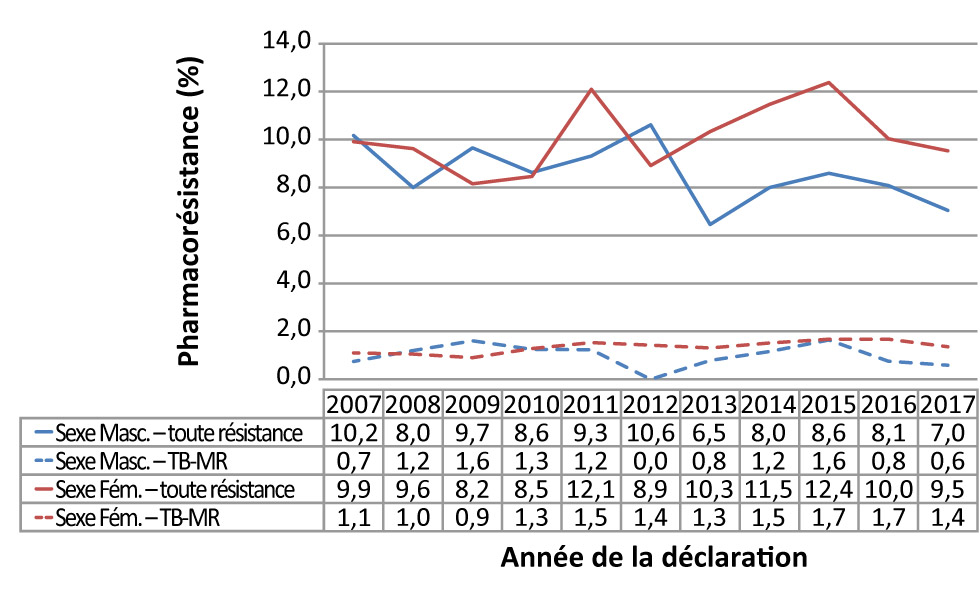
En 2017, 60 (7,0 %) des isolats provenant de personnes de sexe masculin et 63 (9,5 %) de ceux provenant de personnes de sexe féminin présentaient une résistance à un ou plusieurs antituberculeux majeurs (Figure 4). Depuis 2007, le pourcentage d’isolats présentant une résistance à un ou plusieurs antituberculeux majeurs selon le sexe fluctue. Cependant, dans l’ensemble, le pourcentage a diminué chez les personnes de sexe masculin (68 isolats, soit 10,2 %), et une réduction semblable s’observe chez les personnes de sexe féminin (54 isolats, soit 9,5 %). De 2007 à 2012, les pourcentages d’isolats pour lesquels on a signalé une pharmacorésistance étaient comparables chez les personnes de sexe masculin et les personnes de sexe féminin, mais depuis lors, on observe une plus grande proportion d’isolats présentant une pharmacorésistance chez les personnes de sexe féminin (Figure 4). Parmi les 14 isolats de type TB-MR, cinq provenaient de personnes de sexe masculin et neuf, de personnes de sexe féminin. De 2007 à 2017, le pourcentage d’isolats classés comme TB-MR chez les deux sexes est demeuré faible et stable, variant de 0,1 à 1,6 % des isolats provenant de personnes de sexe masculin, et de 0,9 à 1,7 % des isolats provenant de personnes de sexe féminin. Sur les six isolats de type TB-UR signalés de 2007 à 2017, cinq provenaient de personnes de sexe féminin.
Figure 4 : Pourcentage d’isolats de tuberculose pour lesquels on a signalé une pharmacorésistance, selon le sexe et le type de pharmacorésistance, Canada, 2007 à 2017
Description textuelle : Figure 4
| Pharmacorésistance (%) | Année de la déclaration | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| 2007 | 2008 | 2009 | 2010 | 2011 | 2012 | 2013 | 2014 | 2015 | 2016 | 2017 | |
| Sexe Masc. – toute résistance | 10,2 | 8,0 | 9,7 | 8,6 | 9,3 | 10,6 | 6,5 | 8,0 | 8,6 | 8,1 | 7,0 |
| Sexe Masc. – TB-MR | 0,7 | 1,2 | 1,6 | 1,3 | 1,2 | 0,0 | 0,8 | 1,2 | 1,6 | 0,8 | 0,6 |
| Sexe Fém. – toute résistance | 9,9 | 9,6 | 8,2 | 8,5 | 12,1 | 8,9 | 10,3 | 11,5 | 12,4 | 10,0 | 9,5 |
| Sexe Fém. – TB-MR | 1,1 | 1,0 | 0,9 | 1,3 | 1,5 | 1,4 | 1,3 | 1,5 | 1,7 | 1,7 | 1,4 |
Distribution selon l’âge
En 2017, les isolats provenant de personnes de moins de 15 ans représentaient une très petite proportion du total testé par les laboratoires et de ceux présentant une pharmacorésistance (Figure 5). Seulement 46 (3 %) des isolats provenaient de ce groupe d’âge. Deux présentaient une pharmacorésistance, mais aucun n’était de type TB-MR. En revanche, les isolats provenant du groupe d’âge des 25 à 34 ans représentaient la plus grande proportion d’échantillons testés (260 isolats, soit 17,2 %) et la plus importante proportion présentant une pharmacorésistance (29 isolats, soit 23,6 %) et du type TB-MR (six isolats, soit 42,9 %).
Dans tous les autres groupes d’âge, le nombre total d’isolats variait de 160 (10,6 %) chez les personnes de 65 à 74 ans, à 248 (16,4 %) chez celles de 75 ans ou plus. Le pourcentage d’isolats présentant une résistance variait de 6,5 % (huit isolats) chez les personnes de 65 à 74 ans, à 19,5 % (24 isolats) chez celles de 35 à 44 ans. Le nombre d’isolats du type TB-MR variait d’un dans les groupes d’âge de 15 à 24, de 35 à 44, de 45 à 54 et de 65 à 74 ans, respectivement, à deux dans les groupes d’âge de 55 à 64 ans et de 75 ans et plus, respectivement.
Figure 5 : Pourcentage d’isolats de tuberculose pour lesquels on a signalé une pharmacorésistance, selon le groupe d’âge et le type de résistance, Canada, 2017
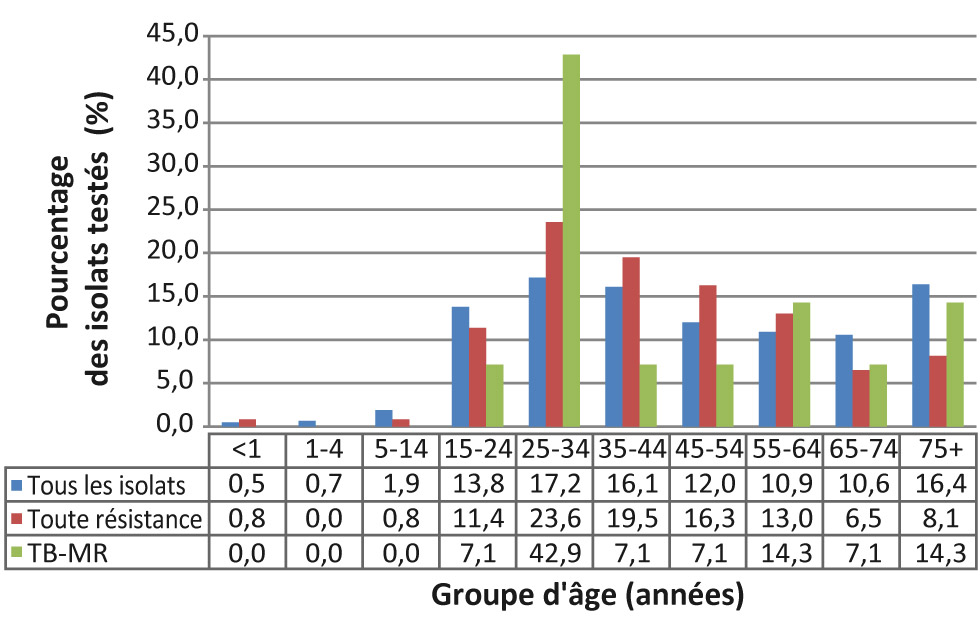
Description textuelle : Figure 5
| Pourcentage d’isolats testés (%) | Groupe d’âge | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| Moins de 1 | 1-4 | 5-14 | 15-24 | 25-34 | 35-44 | 45-54 | 55-64 | 65-74 | 75 et plus | |
| Tous les isolats | 0,5 | 0,7 | 1,9 | 13,8 | 17,2 | 16,1 | 12,0 | 10,9 | 10,6 | 16,4 |
| Toute résistance | 0,8 | 0,0 | 0,8 | 11,4 | 23,6 | 19,5 | 16,3 | 13,0 | 6,5 | 8,1 |
| TB-MDR | 0,0 | 0,0 | 0,0 | 7,1 | 42,9 | 7,1 | 7,1 | 14,3 | 7,1 | 14,3 |
Distribution selon l’origine
De 2005 à 2015, le SCDCT a reçu 9 745 déclarations de cas positifs à l’égard de la TB active touchant des personnes nées à l’étranger; 1 050 (11 %) de ces cas présentaient une résistance à un ou plusieurs antituberculeux majeurs, et 151 (1,5 %) étaient de type TB-MR. On comptait 2 711 cas de TB touchant des Autochtones nés au Canada, dont 67 (2 %) qui présentaient une pharmacorésistance; aucun n’était de type TB-MR. Parmi les 1 588 cas de TB chez des personnes non autochtones nées au Canada, 149 (9 %) présentaient une résistance à au moins un antituberculeux majeur, et sept (0,5 %) étaient de type TB-MR. De tous les cas de type TB-MR, 96 % provenaient de personnes nées à l’étranger, et 4 %, de personnes nées au Canada, autochtones ou non autochtones.
Voir en Annexe la liste des tableaux supplémentaires pouvant être fournis sur demande.
Discussion
Au Canada, les taux de pharmacorésistance parmi les isolats positifs à l’égard de la TB sont demeurés relativement bas en 2017. Au nombre de ces isolats, 8,1 % étaient résistants à un ou plusieurs des antituberculeux majeurs, et 0,9 % étaient de type TB-MR. Aucun isolat du type TB-UR n’a été signalé au Canada depuis 2014. De 2007 à 2017, les taux de résistance aux antituberculeux sont demeurés relativement faibles. Bien qu’on observe une augmentation du nombre d’isolats positifs à l’égard de la TB déclarés en 2017, comparativement à 2007, la proportion d’isolats présentant une résistance à au moins un des antituberculeux majeurs a diminué au fil du temps.
En général, les tendances en matière de résistance aux antituberculeux reflètent les tendances générales des cas de TB active au Canada qui sont déclarés au SCDCT. L’Ontario continue à présenter la majorité des isolats et des cas positifs à l’égard de la pharmacorésistance, ainsi que le nombre le plus élevé de cas de TB active signalés au Canada. Cette situation n’est pas surprenante, étant donné que l’Ontario a la plus grande population de toutes les provinces et tous les territoires canadiens, et qu’elle reçoit le pourcentage annuel le plus élevé d’immigrants au Canada (39,0 % des immigrants au Canada en 2016) Note de bas de page 7.
De 2007 à 2017, environ la moitié des provinces et territoires (soit le Yukon, les Territoires du Nord-Ouest, le Nunavut, la Nouvelle-Écosse, l’Île-du-Prince-Édouard et Terre-Neuve-et-Labrador) n’ont déclaré aucun cas de TB-MR. Ces provinces et territoires ont de petites populations et comptent pour un nombre restreint de l’ensemble des cas de TB déclarés annuellement au Canada. Comme on l’observe dans l’ensemble des cas de TB déclarés au Canada Note de bas de page 2, la pharmacorésistance continue d’être plus fréquemment signalée parmi les isolats provenant de personnes âgées de 25 à 34 ans (42,9 % de TB-MR).
Les personnes nées à l’étranger comptaient pour 71 % du total des cas de TB déclarés au Canada en 2015 Note de bas de page 8 et constituaient également une plus grande proportion des cas de TB-MR (96 %). Cette situation pourrait s’expliquer par un traitement incomplet d’un épisode antérieur de TB ou par l’acquisition d’une souche pharmacorésistante dans le pays d’origine Note de bas de page 4.
Le présent rapport de surveillance est sujet à quelques limites. En ce qui concerne la qualité des données, il y a un risque d’erreurs de déclaration, de données manquantes et de doublons; toutefois, tous les efforts ont été déployés afin de repérer et de retirer les résultats supplémentaires d’isolats provenant d’une même personne et de corriger les erreurs, au moyen de plusieurs étapes de validation par les laboratoires ayant fourni les résultats. Comme le SCSLT est un système de surveillance fondé sur les résultats de laboratoire, les données démographiques disponibles sont limitées, et les isolats signalés ne peuvent pas être directement associés aux données de surveillance fondées sur les cas du SCDCT. Par conséquent, nous sommes actuellement dans l’impossibilité de caractériser les données du SCSLT selon l’origine ethnique, le pays de naissance ou l’issue du traitement, comme d’autres pays et organismes le font Note de bas de page 1Note de bas de page 9Note de bas de page 10. Afin de dresser un portrait épidémiologique plus exhaustif de la résistance aux antituberculeux au Canada, les données du SCDCT ont été utilisées pour décrire les cas de TB présentant une pharmacorésistance en fonction de l’origine ethnique. Les renseignements concernant la pharmacorésistance consignés dans le SCDCT sont assez complets (98 %) Note de bas de page 11 et raisonnablement comparables aux données du SCSLT, mais certains écarts irréconciliables peuvent exister entre les deux.
La pharmacorésistance demeure une préoccupation à l’échelle mondiale, alors que la TB-MR continue de se propager partout dans le monde Note de bas de page 1. Au Canada, malgré des taux de pharmacorésistance constamment faibles, il demeure important de poursuivre la surveillance des tendances émergentes en matière de résistance aux antituberculeux, car le risque d’importation au Canada de souches pharmacorésistantes de TB reste possible. Le SCSLT sera continuellement mis à jour, à mesure que de nouvelles technologies de détection de la pharmacorésistance (p. ex. séquençage du génome entier) et de nouveaux antituberculeux (p. ex. bédaquiline, délamanide) seront offerts.
Déclaration des auteurs
M. L. – Conceptualisation, méthodologie, logiciel, validation, analyse officielle, rédaction (ébauche initiale)
H. H. – Conceptualisation, logiciel, validation, analyse officielle, rédaction (révision) et édition
J. V. – Conceptualisation, rédaction (révision) et édition, supervision
Conflit d’intérêts
Aucun.
Remerciements
La Division de surveillance de la santé et de l’épidémiologie du Centre de la lutte contre les maladies transmissibles et les infections de l’Agence de la santé publique du Canada aimerait remercier les membres du Réseau technique canadien des laboratoires de tuberculose et leurs équipes, ainsi que ses collègues du Laboratoire national de microbiologie pour leur contribution et leur participation au Système canadien de surveillance des laboratoires de tuberculose.
Financement
Ce travail a été appuyé par l’Agence de la santé publique du Canada dans le cadre de son mandat de base.
Annexe : Liste des tableaux supplémentaires fournis sur demande
Tableau supplémentaire 1 : Nombre total et pourcentage d’isolats du complexe Mycobacterium tuberculosis présentant une résistance, du type multirésistant et du type ultrarésistant, selon l’année, de 2007 à 2017, au Canada
Tableau supplémentaire 2 : Tendances globales de la résistance aux antituberculeux signalée au Canada, de 2007 à 2017
Tableau supplémentaire 3 : Résultats des épreuves systématiques de sensibilité aux antituberculeux des isolats du complexe Mycobacterium tuberculosis provenant de l’Alberta, de 2007 à 2017
Tableau supplémentaire 4 : Résultats des épreuves systématiques de sensibilité aux antituberculeux des isolats du complexe Mycobacterium tuberculosis provenant de la Colombie-Britannique, de 2007 à 2017
Tableau supplémentaire 5 : Résultats des épreuves systématiques de sensibilité aux antituberculeux des isolats du complexe Mycobacterium tuberculosis provenant du Manitoba, de 2007 à 2017
Tableau supplémentaire 6 : Résultats des épreuves systématiques de sensibilité aux antituberculeux des isolats du complexe Mycobacterium tuberculosis provenant du Nouveau-Brunswick, de 2007 à 2017
Tableau supplémentaire 7 : Résultats des épreuves systématiques de sensibilité aux antituberculeux des isolats du complexe Mycobacterium tuberculosis provenant de Terre-Neuve-et-Labrador, de 2007 à 2017
Tableau supplémentaire 8 : Résultats des épreuves systématiques de sensibilité aux antituberculeux des isolats du complexe Mycobacterium tuberculosis provenant des Territoires du Nord-Ouest, de 2007 à 2017
Tableau supplémentaire 9 : Résultats des épreuves systématiques de sensibilité aux antituberculeux des isolats du complexe Mycobacterium tuberculosis provenant de la Nouvelle-Écosse, de 2007 à 2017
Tableau supplémentaire 10 : Résultats des épreuves systématiques de sensibilité aux antituberculeux des isolats du complexe Mycobacterium tuberculosis provenant du Nunavut, de 2007 à 2017
Tableau supplémentaire 11 : Résultats des épreuves systématiques de sensibilité aux antituberculeux des isolats du complexe Mycobacterium tuberculosis provenant de l’Ontario, de 2007 à 2017
Tableau supplémentaire 12 : Résultats des épreuves systématiques de sensibilité aux antituberculeux des isolats du complexe Mycobacterium tuberculosis provenant de l’Île-du-Prince-Édouard, de 2007 à 2017
Tableau supplémentaire 13 : Résultats des épreuves systématiques de sensibilité aux antituberculeux des isolats du complexe Mycobacterium tuberculosis provenant du Québec, de 2007 à 2017
Tableau supplémentaire 14 : Résultats des épreuves systématiques de sensibilité aux antituberculeux des isolats du complexe Mycobacterium tuberculosis provenant de la Saskatchewan, de 2007 à 2017
Tableau supplémentaire 15 : Résultats des épreuves systématiques de sensibilité aux antituberculeux des isolats du complexe Mycobacterium tuberculosis provenant du Yukon, de 2007 à 2017
Tableau supplémentaire 16 : Isolats de souches de tuberculose multirésistante et de tuberculose ultrarésistante selon la province ou le territoire d’origine, 2017
Tableau supplémentaire 17 : Nombre total d’isolats du complexe Mycobacterium tuberculosis selon la province ou le territoire d’origine et les ayant déclarés, 2017
Tableau supplémentaire 18 : Répartition provinciale et territoriale selon la présence d’une résistance à tout antituberculeux, la souche de tuberculose multirésistante et la souche de tuberculose ultrarésistante au Canada, de 2007 à 2017
Tableau supplémentaire 19 : Résistance aux antituberculeux selon le sexe et le groupe d’âge au Canada, 2017