Coûts associés aux infections résistantes aux antimicrobiens au Canada, 2019

 Téléchargez cet article en format PDF
Téléchargez cet article en format PDFPublié par : L'Agence de la santé publique du Canada
Numéro : Volume 48-11/12, novembre/décembre 2022 : Utilisation et intendance des antimicrobiens
Date de publication : novembre/décembre 2022
ISSN : 1719-3109
Soumettre un article
À propos du RMTC
Naviguer
Volume 48-11/12, novembre/décembre 2022 : Utilisation et intendance des antimicrobiens
Aperçu
Coûts des hôpitaux et des ressources connexes associés aux infections résistantes aux antimicrobiens au Canada, 2019
Alan Diener1, Hui Wang1, Miriam Nkangu2
Affiliations
1 Unité de politique, recherche, économie et analyse, Direction générale de la politique stratégique, Santé Canada, Ottawa, ON
2 École d'épidémiologie et de santé publique, Université d'Ottawa, Ottawa, ON
Correspondance
Citation proposée
Diener A, Wang H, Nkangu M. Coûts des hôpitaux et des ressources connexes associés aux infections résistantes aux antimicrobiens au Canada, 2019. Relevé des maladies transmissibles au Canada 2022;48(11/12):582−93. https://doi.org/10.14745/ccdr.v48i1112a06f
Mots-clés : résistance aux antimicrobiens, Staphylococcus aureus résistant à la méthicilline, Clostridioides difficile, coûts hospitaliers, ressources en matière de santé
Résumé
Contexte : La résistance aux antimicrobiens (RAM) se produit lorsque des micro-organismes deviennent résistants au traitement par des antibiotiques standards, ou de première intention. Ces infections posent un énorme fardeau sur la société en raison de la prolongation des séjours à l'hôpital et de l'augmentation de la morbidité et de la mortalité, ce qui entraîne une hausse des coûts médicaux et une perte de ressources. L'objectif de cet article est d'estimer les coûts hospitaliers associés à deux des plus importants organismes résistants aux antibiotiques : le Staphylococcus aureus résistant à la méthicilline (SARM) et le Clostridioides difficile (C. difficile), pour le Canada, pour l'année 2019, ainsi que la valeur de l'utilisation d'autres ressources attribuée à la perte de production causée par l'invalidité et la mortalité prématurée.
Méthodes : La Base de données sur les congés des patients a été utilisée pour l'analyse selon un processus en deux étapes : d'abord, le nombre de cas pour chaque diagnostic a été estimé; ensuite, un coût moyen par cas a été évalué, qui a été utilisé pour multiplier le nombre de cas afin d'obtenir les coûts totaux. Les coûts ont été évalués à l'aide d'un modèle de régression, en tenant compte des variables démographiques et d'autres variables confondantes importantes.
Résultats : Au total, 16 070 et 9 889 cas d'infections à C. difficile et d'infections à SARM, respectivement, ont été recensés au Canada en 2019, entraînant un nombre estimé de 1 743 décès prématurés. La majorité des cas sont survenus dans les groupes d'âge plus élevés. Les coûts hospitaliers attribuables à ces infections s'élevaient à plus de 125 millions de dollars, tandis que les coûts indirects des ressources se situaient entre 18,8 et 146,9 millions de dollars.
Conclusion : La quantification des résultats associés aux infections résistantes aux antimicrobiens fournit des renseignements précieux aux décideurs et constitue une première étape essentielle dans la compréhension des impacts économiques totaux de la RAM.
Introduction
La résistance aux antimicrobiens (RAM) est une menace sérieuse et croissante pour la santé publique au Canada et dans le monde entier Note de bas de page 1 Note de bas de page 2 Note de bas de page 3. Si rien n'est fait, les coûts économiques mondiaux pourraient dépasser les 100 000 billions de dollars d'ici 2050, et le Canada pourrait voir son produit intérieur brut (PIB) diminuer de plus de 20 milliards de dollars Note de bas de page 2 Note de bas de page 3 Note de bas de page 4 Note de bas de page 5. On parle de résistance aux antimicrobiens lorsque les micro-organismes deviennent résistants au traitement par les antibiotiques standards, ou de première intention. Ces dernières années, de plus en plus de microbes sont devenus résistants aux antibiotiques actuels et peu de nouveaux antimicrobiens ont été mis sur le marché, ce qui a entraîné une augmentation des maladies attribuables à des infections auparavant traitables.
Ces infections représentent un énorme fardeau pour la société, car les patients sont confrontés à une morbidité et une mortalité accrues. De plus, la RAM alourdit la charge sur le système de santé en augmentant la durée des séjours à l'hôpital et en nécessitant des ressources et des traitements plus coûteux, qui pourraient être utilisés pour traiter d'autres affections. En l'absence de traitement efficace, les infections résistantes aux antimicrobiens persistent, avec un risque de propagation de l'infection à d'autres personnes.
Deux des principaux organismes résistants aux antibiotiques sont le Staphylococcus aureus résistant à la méthicilline (SARM) et le Clostridioides difficile (C. difficile). Le SARM peut également être résistant à d'autres antibiotiques de première intention comme l'oxacilline et la cloxacilline. Le Staphylococcus aureus (S. aureus) est présent sur la peau ou les surfaces muqueuses de 20 à 30 % de la population saine et est également connu pour provoquer une infection systémique Note de bas de page 6. Le SARM, un type spécifique de bactérie staphylocoque, peut être présent sur la peau ou les surfaces muqueuses des populations saines et des patients hospitalisés, ainsi que sur les surfaces environnementales et peut pénétrer dans l'organisme par des lésions cutanées, des voies respiratoires, des sites chirurgicaux et (ou) des plaies ouvertes et des cathéters intraveineux, et peut provoquer des infections graves et parfois mortelles en milieu hospitalier. Le C. difficile est une importante infection associée aux soins de santé qui entraîne une morbidité et une mortalité significatives. Il s'agit de la cause la plus fréquente de diarrhée infectieuse dans les hôpitaux et peut passer d'un état asymptomatique à une menace pour la vie. La plupart des cas se produisent chez des patients âgés et présentant d'autres conditions médicales sous-jacentes. Il se propage rapidement dans les établissements de santé par contact direct, car il est naturellement résistant à de nombreux antimicrobiens utilisés pour traiter d'autres infections, et les spores de C. difficile présentes dans l'environnement ont tendance à être résistantes aux désinfectants couramment utilisés Note de bas de page 7.
Outre les coûts médicaux directs, les infections résistantes aux antimicrobiens entraînent d'autres pertes de ressources en raison de la diminution de la production résultant de l'invalidité et de la mortalité prématurée. Si l'augmentation de la RAM se poursuit, le fardeau futur associé à la RAM pourrait également augmenter de manière significative à cause de son impact sur l'ensemble du système de soins de santé. Par exemple, comme l'ont noté Smith et Coast (2012), si la résistance aux antimicrobiens devait se poursuivre sans intervention, nous pourrions être confrontés à un monde dans lequel il n'y a plus aucun antibiotique efficace disponible pour les situations dans lesquelles ils sont actuellement utilisés de manière routinière Note de bas de page 8.
À l'heure actuelle, il existe peu d'études de coûts de la RAM qui soient méthodologiquement solides, complètes et comparables. Des examens systématiques récents portant sur les coûts de la RAM ont révélé une grande variation des résultats en raison des méthodologies employées, du type de résistance étudié et des éléments de coût inclus Note de bas de page 8 Note de bas de page 9 Note de bas de page 10. Par exemple, Naylor et al. ont constaté que les coûts excessifs du système de santé variaient d'un montant négligeable à 1 milliard de dollars par an, tandis que le fardeau économique variait de 21 832 dollars par cas à 3 000 milliards de dollars de perte du PIB Note de bas de page 9. Le tableau 1 résume les résultats de ces examens systématiques et des études canadiennes récentes qui ont porté sur le fardeau économique de la RAM Note de bas de page 11 Note de bas de page 12 Note de bas de page 13 Note de bas de page 14. Il convient de noter la grande variation des estimations de coûts attribuable aux raisons susmentionnées (tous les coûts afférents ont été convertis en dollars canadiens de 2019 en utilisant les valeurs de la parité du pouvoir d'achat et ont été gonflés en conséquence).
| Référence (année de publication) | Région | Type d'infection | Type d'étude | Coûts estimésNote de bas de page a |
|---|---|---|---|---|
| Smith et Coast (2013) | International | La RAM en général | Examen systématique | De 5 $ à plus de 74 000 $ par épisode de patient |
| Levy et al. (2015) | Canada | C. difficile | Modèle économique utilisant des sources de données multiples | 291 millions de dollars en frais d'hospitalisation 13 millions de dollars en frais médicaux communautaires 11 millions de dollars en perte de productivité |
| Thampi et al. (2015) | Ontario, Canada | SARM | Étude multicentrique sur les coûts | 14 100 dollars en coûts directs par patient hospitalisé |
| Zhang et al. (2016) | États-Unis | C. difficile | Méta-analyse | 28 756 $ par patient |
| Naylor et al. (2018) | International | La RAM en général | Examen systématique | Coûts du système de santé : jusqu'à 1 milliard de dollars par an Fardeau économique : 29 595 $ par cas à plus de 3 billions de dollars de pertes du PIB |
| Conseil des académies canadiennes (2018) | Canada | La RAM en général | Examen d'une sélection d'études canadiennes | 16 979 $ par patient SARM 18 773 $ par patient RAM 1,5 milliard de dollars en coûts hospitaliers totaux liés à la RAM |
| Zhen et al. (2019) | International | SARM | Examen systématique | De 9 998 $ à 242 599 $ par patient |
|
||||
Le Conseil des académies canadiennes (CAC) a récemment estimé les impacts sur la santé, les aspects sociaux et économiques actuels et futurs de la RAM au Canada Note de bas de page 2. Sur la base d'un examen de plusieurs études canadiennes, les auteurs ont estimé un coût moyen de 16 280 dollars par patient atteint de SARM. En examinant les études de coûts d'autres infections résistantes aux antimicrobiens, la CAC a estimé que le coût moyen d'un cas hospitalier de RAM était de 18 000 $. Les études incluses dans l'analyse de la CAC avaient tendance à être des études à petite échelle, dont beaucoup ne comprenaient que des données provenant d'un ou deux établissements hospitaliers. Sur la base de ces estimations de coûts, le total des coûts hospitaliers associés à la RAM a été estimé à 1,4 milliard de dollars en 2018. D'ici 2050, la RAM devrait coûter 6 milliards de dollars au système de santé canadien si le taux d'infection actuel se maintient. De plus, le rapport estime que la perte cumulée du PIB à cause de la RAM entre 2018 et 2050 serait de 268 milliards de dollars si aucun changement n'était apporté au taux d'infection actuel.
Malgré les préoccupations importantes de chercheurs, comme Smith et Coast, qui préviennent que si l'on ne s'attaque pas correctement à la RAM, nous nous dirigeons vers un système de santé radicalement différent de celui que nous connaissons, les décideurs ont besoin d'estimations précises du fardeau global actuel de la RAM. Il est important de bien comprendre la situation actuelle sur laquelle peuvent se baser les projections et la modélisation des coûts futurs liés à la RAM. Des données valides sur les coûts liés à la RAM au Canada fourniraient des renseignements précieux sur l'ampleur de son fardeau, permettraient de combler les lacunes dans les données et fourniraient des données et des éléments probants pour l'analyse des politiques.
L'objectif de cet article était d'estimer les coûts hospitaliers et la valeur de la perte de production associés aux infections résistantes aux antimicrobiens, plus précisément le SARM et les infections à C. difficile, au Canada pour 2019. L'incidence des infections résistantes aux antimicrobiens était basée uniquement sur le diagnostic, à partir de données administratives; aucune distinction n'a été faite entre les infections acquises dans le cadre des soins de santé et celles acquises dans la communauté. Les infections résistantes aux antimicrobiens causées par d'autres bactéries ont été exclues en raison du manque de données valides et fiables.
Méthodes
Sources de données
La principale source de données utilisée dans l'analyse a été la base de données sur les congés des patients (BDCP) de l'Institut canadien d'information sur la santé, de 2010 à 2019. La BDCP contient des données administratives sur les sorties d'hôpital, les diagnostics et les caractéristiques des patients. Les établissements de toutes les provinces et de tous les territoires, à l'exception du Québec, sont tenus de déclarer leurs données à la BDCP. En plus de l'utilisation des variables standards de la BDCP, des données sur le coût d'un séjour hospitalier standard et sur la pondération de l'intensité des ressources associée à chaque sortie d'hôpital ont été obtenues. Cela a permis d'estimer les coûts associés à chaque sortie. Le coût d'un séjour hospitalier standard fournit un coût pour le patient standard, tandis que la pondération de l'intensité des ressources permet d'ajuster le coût en fonction des caractéristiques et des diagnostics des patients. Toutes les analyses ont été effectuées pour les données de 2010 à 2019. Les résultats transversaux concernaient l'année la plus récente, soit 2019, tandis que les autres données ont permis d'examiner la RAM au Canada au fil du temps. L'analyse a été limitée aux personnes de 18 ans et plus en raison de la faible incidence dans les groupes d'âge plus jeunes.
Bien que des données administratives plutôt que des données de surveillance aient été utilisées dans l'analyse, une étude récente a révélé que la BDCP était exceptionnellement performante dans l'identification des cas de SARM par rapport aux données de surveillance en Ontario et en Alberta (r = 0,79 pour l'Ontario, r = 0,92 pour l'Alberta pour l'ensemble des infections à SARM et r = 0,95 pour les infections du sang à SARM en Ontario) Note de bas de page 15. Ainsi, nous sommes convaincus que les taux d'incidence produits à l'aide de la BDCP étaient des estimations valides.
Pour chaque sortie d'hôpital consignée, la BDCP contient jusqu'à vingt-cinq diagnostics possibles selon les codes de la dixième révision de la Classification internationale des maladies (CIM-10). Pour chaque sortie consignée, le diagnostic principal (MRDx) est indiqué, défini comme « le diagnostic ou l'état qui peut être décrit comme étant principal du séjour du patient à l'hôpital. S'il y a plus d'une de ces conditions, celle qui est considérée comme la principale en ce qui concerne la durée de séjour (DS) ou l'utilisation des ressources est sélectionnée » Note de bas de page 16. Tous les autres diagnostics (jusqu'à 24) ont été considérés comme des diagnostics secondaires. Pour cette analyse, tous les cas de SARM et d'infections à C. difficile (ICD) ont été identifiés (se reporter au tableau 2 pour les codes CIM-10 spécifiques utilisés dans l'analyse).
| Diagnostic | Code(s) CIM-10 |
|---|---|
| ICD | A04.7 |
| SARM, non-IS | B95.6 (S. aureus) et U82.1 (résistance à la méthicilline) et dans la même éclosionNote de bas de page a |
| SARM, IS | B95.6 (S. aureus) et U82.1 (résistance à la méthicilline) et A49 (infection du sang), et dans la même éclosion ou A41.0 (septicémie due à un staphylocoque) et U82.1 (résistance à la méthicilline) et dans la même éclosionNote de bas de page a |
|
|
Comme la BDCP n'inclut pas les données de la province du Québec, les valeurs ajustées selon l'âge pour les coûts et la mortalité pour le Québec ont été estimées, sur la base des résultats obtenus de la BDCP, et incluses dans les valeurs totales. Ainsi, toutes les valeurs du fardeau total représentent des estimations pour l'ensemble du Canada. Les résultats sont présentés en dollars canadiens de 2019.
Taux d'incidence
L'incidence et les coûts des infections à SARM ont été divisés en infections du sang (IS) et non sanguines (non-IS) en raison des différences entre les patients et les protocoles de traitement. Avant 2009, pour classer un cas comme étant un SARM, l'observation devait inclure à la fois 1) un diagnostic de résistance à la méthicilline et 2) un diagnostic d'infection à Staphylocoque. En 2009, un indicateur de série a été présentée dans la BDCP pour noter si les deux diagnostics étaient liés; ainsi, pour être considérée comme un cas de SARM, l'observation devait inclure les deux diagnostics et les deux diagnostics devaient être établis comme faisant partie de la même éclosion. L'incidence et les coûts des diagnostics de C. difficile ont été estimés séparément pour les cas où le C. difficile apparaissait soit comme le diagnostic principal, soit comme un diagnostic secondaire (ICD MRDx et ICD non-MRDx, respectivement).
Coûts hospitaliers
Les coûts différentiels, c'est-à-dire les coûts associés au traitement des affections en sus des coûts associés au reste du séjour à l'hôpital, ont été estimés de deux manières. Tout d'abord, le coût moyen des séjours des patients ayant reçu ou non le diagnostic en question a été estimé. La différence entre les deux estimations a ensuite été considérée comme étant les coûts différentiels attribuables à l'infection spécifique. Le défi de cette approche est que la probabilité d'une infection liée à la RAM augmente avec l'âge, la durée de séjour, le nombre de comorbidités et la raison de l'admission. Ainsi, les coûts différentiels non ajustés évalués de cette manière sont susceptibles de surestimer les coûts différentiels réels qui peuvent être valablement attribués à la seule présence de l'infection.
Pour tenir compte des effets de confusion susmentionnés, le modèle de régression suivant a été utilisé pour estimer les coûts supplémentaires associés au traitement des infections résistantes aux antimicrobiens :
Coût = β0 + β1MRSA_non_BL + β2MRSA_BL + β3CDI_non_mrdx + β4Comorbidites
+ ∑γiISHMTi + ∑λiPROVi 5+ βSex + β6LOS + e
Où :
- Coût = le logarithme du coût par sortie d'hôpital
- MRSA_non_BL = 1 si un diagnostic de SARM non sanguin est présent
- MRSA_BL = 1 si le diagnostic de SARM sanguin est présent
- CDI_non_mrdx = 1 si le diagnostic de C. difficile est présent en tant que condition comorbide
- Comorbidités = nombre de comorbidités diagnostiquées (à l'exclusion des infections résistantes aux antimicrobiens)
- ISHMTi = 1 si le diagnostic principal du patient figure dans le code i de l'International Short List of Hospital Morbidity Tabulation (ISHMT) (à l'exclusion du code C. difficile)
- PROV = une variable muette pour la province
- Sexe = 1, si femme
- LOS = durée de séjour associée à l'observation
Le modèle utilisé incluait des variables pour le diagnostic principal (pour tenir compte des différentes raisons d'admission), le nombre de comorbidités (basé sur les dossiers dans la BDCP), le sexe et la province. Les coefficients bêta estimés ont été utilisés pour estimer les coûts différentiels associés aux infections. Plus précisément, les coefficients des variables associées aux infections (β1, β2, β3) ont été transformés pour indiquer le pourcentage d'augmentation des coûts moyens qui pourrait être attribuable à l'infection (SARM ou C. difficile).
Pour les personnes chez qui le C. difficile était un diagnostic secondaire ou dont le diagnostic de SARM était toujours un diagnostic secondaire, les coûts différentiels associés à ce diagnostic ont été estimés.
Les données sur les coûts présentent généralement un étalement à droite, car les coûts ne peuvent pas être négatifs et la plupart des observations sont proches de zéro, avec plusieurs observations présentant des coûts relativement élevés. Ainsi, un modèle loglinéaire a été utilisé, permettant un bien meilleur ajustement. Les coefficients bêta résultants, une fois transformés, peuvent être interprétés comme les coûts différentiels attribuables à la présence d'infections à SARM ou à C. difficile, respectivement, en tenant compte de l'âge, du diagnostic, du sexe, des comorbidités et d'autres facteurs pertinents. Des régressions séparées ont été effectuées par groupe d'âge pour tenir compte des différences selon l'âge. Une fois que le coût différentiel a été estimé, il est multiplié par le nombre de cas pour ce diagnostic. Pour les patients classés comme ayant le C. difficile comme diagnostic principal, tous les coûts associés à ce séjour à l'hôpital ont été employés.
Le diagnostic principal, pour chaque observation, a été codé selon l'ISHMT. L'ISHMT est un système de classification basé sur les chapitres de la CIM-10, qu'il décompose ensuite en 130 catégories de diagnostic. Les codes de l'ISHMT ont été utilisés pour définir les diagnostics, car ils représentent un nombre gérable de diagnostics bien définis, tout en étant suffisamment granulaires pour être significatifs.
Estimations de la mortalité
Pour estimer la valeur de la perte de production due à la mortalité prématurée attribuable aux infections résistantes aux antimicrobiens, il a fallu estimer la mortalité accrue attribuable aux infections employées dans l'analyse. Alors que le C. difficile est une cause possible de décès répertoriée, les décès attribuables aux infections au SARM sont codés autrement, ce qui rend difficile l'obtention d'estimations valides et fiables sur le nombre de décès attribuables au SARM Note de bas de page 17. Une régression logistique séparée avec une variable binaire indiquant si le patient est décédé ou a eu son congé de l'hôpital a été utilisée pour estimer le taux de mortalité pour chacun des cinq groupes d'âge, notamment 18 à 34 ans, 35 à 54 ans, 55 à 64 ans, 65 à 74 ans et 75 ans et plus. Les coefficients de cette régression produisent les logarithmes de la cote exprimant la chance (log-odds), à partir desquels il a été possible d'estimer les rapports de cotes pour les taux de mortalité associés à chaque infection. Plus précisément, le modèle suivant a été mis en œuvre :
Décès = β0 + β1MRSA_non_BL + β2MRSA_BL + β3CDiff_non_mrdx + β4Comorbidites
+ ∑γiISHMTi + ∑λiPROVi + β5Sex + β6LOS + e
Où :
- Décès = 1 si le patient est décédé, 0 sinon
- Toutes les autres variables ont été définies précédemment
Pour estimer le nombre total de décès attribuables à chaque type d'infection liée à la RAM, on a obtenu à partir des données le taux de mortalité par âge pour tous les patients sortis de l'hôpital et le nombre de patients infectés à cause de la RAM. Ensuite, le taux de mortalité spécifique à l'infection peut être calculé en multipliant le rapport de cotes de l'infection spécifique et le taux de mortalité global. Enfin, le nombre estimé de décès pour l'infection peut être estimé en multipliant le taux de mortalité spécifique à l'infection et le nombre d'infections dans le groupe d'âge.
Valeur de la production perdue
Pour obtenir une estimation plus complète de la charge économique, la valeur de la production perdue, tant pour l'invalidité que pour la mortalité prématurée, attribuable aux infections résistantes aux antimicrobiens, a également été estimée. Deux approches sont généralement utilisées pour estimer les pertes de production dans les études sur le coût de la maladie : l'approche du coût de friction et l'approche du capital humain Note de bas de page 18. Cette approche du coût de friction suppose qu'un travailleur décédé sera éventuellement remplacé par des personnes faisant actuellement partie du bassin de chômeurs, une fois que les personnes à la recherche d'un emploi auront trouvé un employeur offrant actuellement un emploi (i.e. la période de friction), trois mois étant une période couramment employée Note de bas de page 19. En revanche, l'approche fondée sur le capital humain mesure la valeur du manque à gagner brut sur toute la durée de la vie, ce qui donne lieu à des estimations beaucoup plus importantes; en d'autres termes, l'approche fondée sur le capital humain suppose que la production d'une personne est perdue pendant toute sa vie active. Compte tenu du débat en cours sur la méthode appropriée et des taux de chômage généralement plus élevés (l'approche des coûts de friction a été proposée à l'origine pendant les périodes de chômage élevé), les deux méthodes ont été employées pour accroître la comparabilité des résultats.
La durée de l'absence du travail due à l'absentéisme ou à la mortalité prématurée a été estimée selon les deux approches et a ensuite été multipliée par un taux de salaire moyen. La durée de séjour supplémentaire dans les hôpitaux attribuables à ces infections a été déterminée sur la base des coûts supplémentaires estimés précédemment pour en évaluer le temps perdu en raison de l'absentéisme. Le temps d'absence du travail a été multiplié par les gains moyens par âge (en tant qu'indicateur du produit marginal). Le revenu moyen et le taux d'emploi des personnes de 15 ans et plus ont été obtenus de Statistique Canada Note de bas de page 20 Note de bas de page 21.
Résultats
Taux d'incidence
La figure 1 montre l'incidence des infections à C. difficile et à SARM de 2010 à 2019. L'incidence des infections à C. difficile a diminué depuis 2015, passant de 7,1 cas pour 1 000 sorties d'hôpital à 5,8 cas pour 1 000 sorties d'hôpital en 2019 (2,0 comme diagnostic principal et 3,8 comme diagnostic secondaire). En examinant les diagnostics de résistance à la méticilline et d'infection à Staphylocoque, on a observé qu'en 2010 (la première année après la présentation d'indicateur de série), tous les cas avaient à la fois un diagnostic de résistance à la méticilline et d'infection à Staphylocoque, et seulement 85 % étaient dans la même éclosion. La majorité (76 %) des infections diagnostiquées comme étant à la fois résistantes à la méthicilline et présentant une infection du sang à Staphylocoque se trouvaient également dans la même éclosion. En 2011, le pourcentage est passé à 97 % et à 85 %, et en 2019, les pourcentages se sont stabilisés à 99 % et à 88 %, respectivement. Il a probablement fallu un certain temps pour que le codage soit appliqué de manière appropriée. En 2019, le taux global d'infections à SARM était de 3,6 pour 1 000 sorties d'hôpital — 2,6 pour les non-IS et 1,0 pour les SARM-IS. Notez que les infections du sang à SARM ont augmenté régulièrement depuis 2010 et ont plus que doublé entre 2010 et 2019; passant de 0,4 à 1,0 cas pour 1 000 sorties d'hôpital. Ces conclusions sont conformes aux résultats des études de surveillance canadiennes; toutefois, en raison des différences de méthodologies, les résultats ne sont pas directement comparables Note de bas de page 1 Note de bas de page 7.
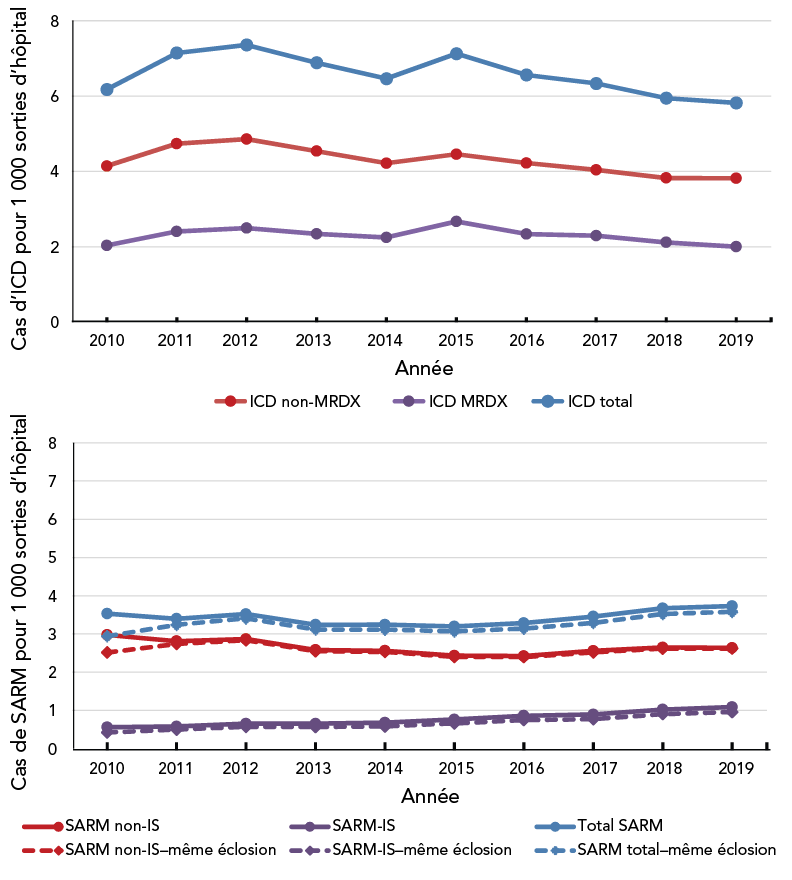
Figure 1 - Description textuelle
La figure 1 montre l'incidence des infections à Clostridioides difficile (ICD) et à Staphylococcus aureus résistant à la méthicilline (SARM) de 2010 à 2019. L'incidence des ICD a diminué depuis 2015, passant de 7,1 cas pour 1 000 sorties d'hôpital à 5,8 cas pour 1 000 sorties d'hôpital en 2019 (2,0 comme diagnostic principal et 3,8 comme diagnostic secondaire).
En 2019, le taux global d'infections à SARM était de 3,6 par 1 000 sorties d'hôpital — 2,6 pour les infections non sanguines et 1,0 pour les infections du sang à SARM. Les infections du sang à SARM n'ont cessé d'augmenter depuis 2010 et ont plus que doublé entre 2010 et 2019, passant de 0,4 à 1,0 cas pour 1 000 sorties d'hôpital.
Un indicateur de série indiquant si les diagnostics de résistance à la méthicilline et d'infections à staphylocoques sont interreliés, a été présentée pour la première fois en 2010. La même année, 85 % des infections dues à la résistance à la méthicilline et au staphylocoque (SARM total) se trouvaient dans la même éclosion, et 76 % des infections du sang dues au SARM (IS à SARM) dans la même éclosion. Ces pourcentages ont augmenté à 97 % et à 85 % en 2011 et se sont stabilisés à 99 % et à 88 % en 2019, respectivement.
Infections à Clostridioides difficile
| Cas | 2010 | 2011 | 2012 | 2013 | 2014 | 2015 | 2016 | 2017 | 2018 | 2019 |
|---|---|---|---|---|---|---|---|---|---|---|
| ICD non-MRDx | 4,142 | 4,737 | 4,858 | 4,538 | 4,215 | 4,456 | 4,223 | 4,041 | 3,826 | 3,816 |
| ICD MRDx | 2,034 | 2,408 | 2,498 | 2,344 | 2,247 | 2,670 | 2,337 | 2,294 | 2,117 | 2,002 |
| ICD total | 6,176 | 7,145 | 7,356 | 6,883 | 6,462 | 7,126 | 6,561 | 6,335 | 5,943 | 5,818 |
Infections à Staphylococcus aureus résistant à la méthicilline
| Cas | 2010 | 2011 | 2012 | 2013 | 2014 | 2015 | 2016 | 2017 | 2018 | 2019 |
|---|---|---|---|---|---|---|---|---|---|---|
| SARM non-IS | 2,9752 | 2,8147 | 2,8674 | 2,5844 | 2,5622 | 2,4334 | 2,4240 | 2,5606 | 2,6486 | 2,6385 |
| SARM-IS | 0,5595 | 0,5846 | 0,6552 | 0,6582 | 0,6830 | 0,7655 | 0,8638 | 0,8971 | 1,0249 | 1,0903 |
| Total SARM | 3,5347 | 3,3993 | 3,5226 | 3,2426 | 3,2452 | 3,1989 | 3,2878 | 3,4577 | 3,6735 | 3,7288 |
| SARM non-IS — même éclosion | 2,5167 | 2,7410 | 2,8366 | 2,5492 | 2,5322 | 2,4046 | 2,3950 | 2,5176 | 2,6191 | 2,6207 |
| SARM-IS — même éclosion | 0,4237 | 0,4988 | 0,5719 | 0,5688 | 0,5828 | 0,6631 | 0,7473 | 0,7725 | 0,9052 | 0,9597 |
| SARM total — même éclosion | 2,9404 | 3,2398 | 3,4085 | 3,1180 | 3,1150 | 3,0677 | 3,1422 | 3,2901 | 3,5243 | 3,5804 |
En 2019, plus de 2,1 millions de sorties d'hôpital ont été incluses dans la BDCP. Le tableau 3 présente des statistiques récapitulatives pour l'échantillon global et les personnes présentant soit une infection à SARM, soit une ICD. Les patients atteints de n'importe quel type d'infection avaient une durée de séjour moyenne beaucoup plus longue; toutefois, il convient de noter que la différence entre la durée de séjour moyenne de l'ensemble de l'échantillon et celle des patients atteints d'infections résistantes aux antimicrobiens est attribuable à de nombreux facteurs. Les personnes atteintes d'infections à C. difficile avaient tendance à être plus âgées, et celles atteintes de SARM avaient tendance à être plus jeunes que l'ensemble de l'échantillon. Alors que l'âge moyen de l'ensemble de l'échantillon a augmenté au cours de la période d'étude, l'âge moyen des personnes atteintes de ces infections a légèrement diminué. Les hommes étaient plus susceptibles que les femmes d'avoir reçu un diagnostic d'infection au SARM. Le tableau 4 montre les taux d'incidence des infections résistantes aux antimicrobiens par groupe d'âge. Comme on pouvait s'y attendre, les personnes de 75 ans et plus présentaient les taux globaux les plus élevés, sauf que les infections à SARM ont atteint un pic chez les personnes de 35 à 54 ans.
| Type d'infection | Incidence (cas pour 1 000 sorties d'hôpital) | Pourcentage de femmes | Durée de séjour moyenne (jours) | Âge moyen (années) |
|---|---|---|---|---|
| Échantillon complet | s.o. | 57,0 % | 7,6 | 59,5 |
| Aucune infection | s.o. | 57,0 % | 7,5 | 59,5 |
| ICD (MRDx) comme diagnostic principal | 2,00 | 58,9 % | 11,7 | 70,6 |
| ICD, en tant que non-MRDx | 3,82 | 51,1 % | 31,7 | 68,8 |
| ICD (total) | 5,82 | 53,8 % | 24,8 | 69,4 |
| SARM non-IS | 2,62 | 40,5 % | 22,6 | 58,4 |
| SARM, IS | 0,96 | 38,6 % | 25,4 | 57,5 |
| SARM (total) | 3,58 | 40,0 % | 23,3 | 58,2 |
|
||||
| Groupe d'âge (années) | ICD, MRDx | ICD, non-MRDx | ICD, total | SARM, non-IS | SARM, IS | SARM, total |
|---|---|---|---|---|---|---|
| 18 à 34 | 0,537 | 0,994 | 1,531 | 1,970 | 0,758 | 2,728 |
| 35 à 54 | 1,119 | 2,492 | 3,611 | 3,805 | 1,455 | 5,261 |
| 55 à 64 | 1,929 | 4,315 | 6,244 | 3,055 | 1,141 | 4,195 |
| 65 à 74 | 2,415 | 5,028 | 7,443 | 2,509 | 0,909 | 3,418 |
| 75 ans et plus | 3,312 | 5,472 | 8,785 | 2,105 | 0,701 | 2,806 |
| Total | 2,002 | 3,816 | 5,818 | 2,621 | 0,960 | 3,580 |
|
||||||
Coûts hospitaliers
Les coûts non ajustés étaient relativement élevés, comme prévu, et variaient de plus de 19 000 $ par patient (SARM, non-IS) à plus de 30 000 $ par patient (ICD). Comme indiqué précédemment, cela est probablement dû au fait que les personnes souffrant de RAM ont des durées de séjour plus longues, nécessitant plus de ressources, en raison d'autres caractéristiques. Pour obtenir les coûts différentiels ajustés, des régressions distinctes ont été effectuées pour chaque groupe d'âge (les principaux résultats des régressions sont présentés en appendice, au tableau A1 et au tableau A2). Le tableau 5 présente les estimations des coûts différentiels par groupe d'âge). Les coûts différentiels moyens dans tous les groupes d'âge étaient de 2 301 $ et de 3 654 $ pour les cas de SARM sans IS et les cas de SARM avec IS, respectivement, ce qui donne un coût hospitalier total du SARM estimé à 24,4 millions de dollars. Pour le C. difficile, le coût moyen des patients ayant un diagnostic principal était de 11 056 $ par patient et les coûts supplémentaires associés à un diagnostic secondaire de C. difficile étaient de 3 749 $. Les coûts hospitaliers totaux associés à C. difficile ont été estimés à 100,7 millions de dollars.
| Groupe d'âge (années) |
Tous les diagnostics (coût moyen) |
ICD, MRDx (coût différentiel) |
ICD, non-MRDx (coût différentiel) |
SARM, non-IS (coût différentiel) |
SARM, IS (coût différentiel) |
|---|---|---|---|---|---|
| 18 à 34 | 5 251 $ | 7 297 $ | 2 806 $ | 1 411 $ | 1 828 $ |
| 35 à 54 | 8 001 $ | 7 866 $ | 3 883 $ | 1 694 $ | 2 589 $ |
| 55 à 64 | 10 785 $ | 10 153 $ | 3 731 $ | 2 271 $ | 3 022 $ |
| 65 à 74 | 11 414 $ | 12 389 $ | 4 057 $ | 2 309 $ | 5 006 $ |
| 75 ans et plus | 12 098 $ | 11 806 $ | 3 641 $ | 2 408 $ | 5 802 $ |
| Moyenne | 9 721 $ | 11 056 $ | 3 479 $ | 2 031 $ | 3 654 $ |
|
|||||
Estimations de la mortalité
Les sorties d'hôpital fournissent des renseignements sur l'état à la sortie; cependant, il n'a pas été précisé si un patient est décédé à l'intérieur ou à l'extérieur de l'hôpital. Selon la BDCP, le nombre observé de décès dus à une infection à C. difficile, à SARM non-IS et à SARM-IS était respectivement de 1 455, de 353 et de 351. Comme aucune cause de décès n'est notée pour ces patients dans les données, la mortalité pourrait être due à d'autres risques concurrents, comme les comorbidités ou le vieillissement, plutôt qu'à la seule infection liée à la RAM.
Afin de prévenir la surestimation de la mortalité liée à la RAM, des régressions logistiques ont été effectuées pour les patients de chaque groupe d'âge afin d'estimer les taux de décès attribuables aux infections, ajustés en fonction du sexe, du nombre de comorbidités et du groupe de diagnostic de l'ISHMT. Les résultats ont clairement montré une relation positive entre le nombre de décès et l'âge des patients. Le tableau A2 présente les rapports de cotes obtenus à partir des résultats de la régression, et le tableau 6 montre le nombre de décès estimés attribuables aux infections à C. difficile et à SARM, pour l'ensemble du Canada. Selon les estimations, le nombre de décès attribuables à C. difficile, aux infections par le SARM non-IS et par le SARM-IS était de 1 309, de 257 et de 177, respectivement. La majorité des décès estimés, près de 70 %, sont survenus chez les personnes de 75 ans et plus
| Type d'infection | Âge (années) | Mortalité totale | ||||
|---|---|---|---|---|---|---|
| 18 à 34 | 35 à 54 | 55 à 64 | 65 à 74 | 75 ans et plus | ||
| ICD, tout | 2 | 28 | 98 | 206 | 975 | 1 309 |
| SARM, non-IS | 2 | 23 | 34 | 54 | 144 | 257 |
| SARM, IS | 2 | 17 | 25 | 49 | 84 | 177 |
| Total | 6 | 68 | 157 | 309 | 1 203 | 1 743 |
|
||||||
Valeur de la production perdue
Le tableau 7 montre la durée de séjour supplémentaire associée aux infections résistantes aux antimicrobiens. La durée moyenne de séjour a été multipliée par le nombre de cas, le taux de salaire moyen et le taux d'emploi pour obtenir la valeur de la perte de production due à la morbidité, qui s'est élevée à 5,6 millions de dollars. La valeur de la perte de production due à la mortalité prématurée a été estimée à 13,2 millions de dollars en utilisant l'approche des coûts de friction, et à 141,4 millions de dollars en utilisant l'approche du capital humain. Cette constatation est conforme à d'autres résultats. La valeur de la production perdue est la plus importante pour les personnes de 35 à 64 ans, en raison des revenus et des emplois plus élevés dans ces groupes d'âge.
| Type d'infection | Âge (années) | ||||
|---|---|---|---|---|---|
| 18 à 34 | 35 à 54 | 55 à 64 | 65 à 74 | 75 ans et plus | |
| ICD, MRDxNote de bas de page b | 6,9 | 7,5 | 9,3 | 12,6 | 13,5 |
| ICD, non-MRDx | 1,9 | 2,6 | 2,5 | 3,0 | 3,5 |
| SARM, non-IS | 1,0 | 1,1 | 1,5 | 1,7 | 2,3 |
| SARM, IS | 1,3 | 1,7 | 2,0 | 3,6 | 5,5 |
|
|||||
Total des coûts
Le tableau 8 résume le fardeau accru en termes de mortalité et de coûts économiques associés aux infections résistantes aux antimicrobiens au Canada en 2019. Les infections résistantes aux antimicrobiens ont entraîné 1 743 décès supplémentaires et ont représenté un coût économique total compris entre 143,8 et 272 millions de dollars.
| Type d'infection | Nombre de cas | Augmentation de la mortalité | Coûts hospitaliersNote de bas de page b | Perte de productionNote de bas de page b (invalidité) | Perte de productionNote de bas de page b (mortalité prématurée) | Coût totalNote de bas de page b | |
|---|---|---|---|---|---|---|---|
| MCF | MCH | ||||||
| ICD, toute | 16 070 | 1 309 | 100,65 $ | 3,99 $ | 9,92 $ | 66,90 $ | 114,56 $–171,54 $ |
| SARM, non-IS | 7 238 | 257 | 14,70 $ | 0,93 $ | 1,95 $ | 42,62 $ | 17,5 $–58,26 $ |
| SARM, IS | 2 651 | 177 | 9,69 $ | 0,64 $ | 1,34 $ | 31,82 $ | 11,6 $–42,15 $ |
| Total | 25 959 | 1 743 | 125,04 $ | 5,56 $ | 13,22 $ | 141,35 $ | 143,8 $–271,95 $ |
|
|||||||
Discussion
En 2019, au Canada, on a estimé à 16 070 et à 9 989 le nombre de cas d'infections à C. difficile et à SARM, respectivement, ce qui a entraîné environ 1 743 décès prématurés. La majorité des cas sont survenus dans les groupes d'âge plus élevés, et près de 70 % des décès prématurés sont survenus chez les personnes de 75 ans et plus. Les coûts annuels liés aux hôpitaux s'élevaient à plus de 125 millions de dollars, tandis que la valeur de la production perdue était estimée entre 18,8 millions et 146,9 millions de dollars; les coûts économiques totaux se situaient entre 143,8 millions et 272 millions de dollars. Compte tenu des hypothèses utilisées et du fait que seulement deux types d'infections résistantes aux antimicrobiens ont été incluses dans l'analyse, ces résultats peuvent être considérés comme des valeurs inférieures du fardeau économique des infections résistantes aux antimicrobiens au Canada.
Les estimations de la durée de séjour, de la mortalité attribuable et des coûts différentiels étaient conformes à celles trouvées dans la littérature, bien qu'elles se situent à l'extrémité inférieure. Ce résultat n'est pas inattendu, étant donné que la méthodologie employée pour l'estimation des coûts hospitaliers était susceptible de produire des estimations prudentes. De plus, l'analyse a tenté de tenir compte de facteurs susceptibles d'influencer le risque d'infections résistantes aux antimicrobiens et les coûts totaux, notamment l'âge, la durée de séjour, le nombre de comorbidités et le diagnostic principal. Les différences dans les coûts hospitaliers par patient étaient probablement dues à l'estimation des coûts différentiels, plutôt que des coûts moyens.
Les comparaisons directes avec la littérature antérieure sont difficiles en raison du large éventail de résultats inclus, de perspectives et de méthodologies employées. Naylor et al. Note de bas de page 9 ont noté qu'une grande partie des données antérieures sur le fardeau économique de la RAM n'utilisaient pas les techniques établies de modélisation économique de la santé; ils ont formulé des recommandations pour la recherche sur le fardeau économique de la RAM, que nous avons tenté de suivre. Il s'agissait notamment d'utiliser un échantillon de population représentatif, de tenir compte des variables de confusion (y compris les comorbidités et l'âge), de décrire les données utilisées et la façon dont les taux ont été calculés, et de décrire clairement le modèle utilisé.
Limites
Bien qu'elle ait tenté de prendre en compte de nombreuses covariables liées aux infections résistantes aux antimicrobiens, l'analyse présentait plusieurs limites. Comme indiqué précédemment, l'analyse n'a pas fait de distinction entre les infections acquises dans le cadre des soins de santé et celles acquises dans la communauté. Les différences entre ces deux groupes de patients peuvent affecter les résultats globaux et devraient idéalement être prises en compte. En outre, les données utilisées portaient sur les sorties d'hôpital et non sur les personnes. Il n'a donc pas été possible de tenir compte des réadmissions éventuelles. Le fait de disposer de telles données permettrait de mieux estimer le nombre de cas de RAM globaux plutôt que les épisodes. En ce qui concerne ce dernier point, les infections résistantes aux antimicrobiens peuvent avoir un impact sur la santé à long terme et donc entraîner des coûts. Par exemple, Nanwa et al. ont mené une étude longitudinale de cohorte appariée en Ontario, au Canada, qui a estimé les coûts sur trois ans associés à l'ICD. Ils ont constaté que les coûts étaient supérieurs à 31 000 $ et à 37 000 $ (en dollars canadiens de 2014) pour les patients admis de façon non urgente et urgente Note de bas de page 22.
Conclusion
La quantification des résultats associés aux infections résistantes aux antimicrobiens fournit des renseignements précieux aux décideurs et constitue une première étape essentielle dans la compréhension des impacts économiques totaux de la RAM. La quantification de ces résultats est également une donnée importante qui peut être utilisée dans les évaluations économiques des politiques visant à réduire les impacts futurs de la RAM.
Déclaration des auteurs
A. D. — Conceptualisation, méthodologie, rédaction–révision et édition, analyse formelle
H. W. — Rédaction–révision et édition, analyse formelle
M. N. — Rédaction–projet original, analyse formelle
Intérêts concurrents
Aucun.
Remerciements
Les auteurs tiennent à remercier K. Amartunga, K. Eng, D. Gravel Tropper, M. Latendresse, B. Ney, L. Pelude, J. Shurgold ainsi que deux arbitres anonymes pour leurs commentaires précieux sur une version antérieure de ce manuscrit. Toutes les erreurs sont les nôtres.
Financement
Aucun.
Références
- Note de bas de page 1
-
Agence de la santé publique du Canada. Rapport de 2021 du Système canadien de surveillance de la résistance aux antimicrobiens. Ottawa, ON : ASPC; 2022. https://www.canada.ca/fr/sante-publique/services/publications/medicaments-et-produits-sante/rapport-2021-systeme-canadien-surveillance-resistance-antimicrobiens.html
- Note de bas de page 2
-
Conseil des académies canadiennes. Quand les antibiotiques échouen. Comité d'experts sur les incidences socioéconomiques potentielles de la résistance aux antimicrobiens au Canada. Ottawa, ON : CAC; 2019. https://www.rapports-cac.ca/reports/les-incidences-socioeconomiques-potentielles-de-la-resistance-aux-antimicrobiens-au-canada/?_gl=1*u5b4qv*_ga*MTQ5MTQyNjMwNi4xNjY5MzE1MjE2*_ga_FQ44VJSZFT*MTY2OTkyOTkyMC4zLjEuMTY2OTkyOTkyNS4wLjAuMA..
- Note de bas de page 3
-
Antimicrobial Resistance Collaborators. Global burden of bacterial antimicrobial resistance in 2019: a systematic analysis. Lancet 2022;399(10325):629–55. https://doi.org/10.1016/S0140-6736(21)02724-0
- Note de bas de page 4
-
UK Government. Review on Antimicrobial Resistance. Antimicrobial resistance: tackling a crisis for the health and wealth of nations. London (UK): UK Government; 2014. https://amr-review.org/sites/default/files/AMR%20Review%20Paper%20-%20Tackling%20a%20crisis%20for%20the%20health%20and%20wealth%20of%20nations_1.pdf
- Note de bas de page 5
-
UK Government. Review on Antimicrobial Resistance. Tackling Drug Resistant Infections Globally: Final Report and Recommendations. London (UK): UK Government; 2014. https://amr-review.org/sites/default/files/160518_Final%20paper_with%20cover.pdf
- Note de bas de page 6
-
Lucet JC, Regnier B. Screening and decolonization: does methicillin-susceptible Staphylococcus aureus hold lessons for methicillin-resistant S. aureus? Clin Infect Dis 2010;51(5):585–90. https://doi.org/10.1086/655695
- Note de bas de page 7
-
Agence de la santé publique du Canada. Canadian Système canadien de surveillance de la résistance aux antimicrobiens -Rapport de 2017: Ottawa, ON : ASPC; 2018. https://www.canada.ca/fr/sante-publique/services/publications/medicaments-et-produits-sante/systeme-canadien-surveillance-resistance-antimicrobiens-2017-rapport-resume.html
- Note de bas de page 8
-
Smith R, Coast J. The economic burden of antimicrobial resistance: Why it is more serious than current studies suggest. London School of Hygiene and Tropical Medicine: 2012. https://researchonline.lshtm.ac.uk/id/eprint/639028/1/DH_AMR_final_report_30-10-12_with_appendix.pdf
- Note de bas de page 9
-
Naylor NR, Atun R, Zhu N, Kulasabanathan K, Silva S, Chatterjee A, Knight GM, Robotham JV. Estimating the burden of antimicrobial resistance: a systematic literature review. Antimicrob Resist Infect Control 2018;7:58. https://doi.org/10.1186/s13756-018-0336-y
- Note de bas de page 10
-
Smith R, Coast J. The true cost of antimicrobial resistance. BMJ 2013;346 f1493:f1493. https://doi.org/10.1136/bmj.f1493
- Note de bas de page 11
-
Levy AR, Szabo SM, Lozano-Ortega G, Lloyd-Smith E, Leung V, Lawrence R, Romney MG. Incidence and Costs of Clostridium difficile Infections in Canada. Open Forum Infect Dis 2015;2(3):ofv076. https://doi.org/10.1093/ofid/ofv076
- Note de bas de page 12
-
Thampi N, Showler A, Burry L, Bai AD, Steinberg M, Ricciuto DR, Bell CM, Morris AM. Multicenter study of health care cost of patients admitted to hospital with Staphylococcus aureus bacteremia: impact of length of stay and intensity of care. Am J Infect Control 2015;43(7):739–44. https://doi.org/10.1016/j.ajic.2015.01.031
- Note de bas de page 13
-
Zhang S, Palazuelos-Munoz S, Balsells EM, Nair H, Chit A, Kyaw MH. Cost of hospital management of Clostridium difficile infection in United States-a meta-analysis and modelling study. BMC Infect Dis 2016;16(1):447. https://doi.org/10.1186/s12879-016-1786-6
- Note de bas de page 14
-
Zhen X, Lundborg CS, Sun X, Hu X, Dong H. Economic burden of antibiotic resistance in ESKAPE organisms: a systematic review. Antimicrob Resist Infect Control 2019;8:137. https://doi.org/10.1186/s13756-019-0590-7
- Note de bas de page 15
-
Ramirez Mendoza JY, Daneman N, Elias MN, Amuah JE, Bush K, Couris CM, Leeb K. A Comparison of Administrative Data Versus Surveillance Data for Hospital-Associated Methicillin-Resistant Staphylococcus aureus Infections in Canadian Hospitals. Infect Control Hosp Epidemiol 2017;38(4):436–43. https://doi.org/10.1017/ice.2016.302
- Note de bas de page 16
-
Institut canadien dinformation sur la santé. Normes canadiennes de codification de la CIM-10-CA et la CCI. Ottawa, ON : ICIS; 2012. https://secure.cihi.ca/estore/productSeries.htm?locale=fr&pc=PCC189
- Note de bas de page 17
-
Dubberke ER, Gerding DN, Classen D, Arias KM, Podgorny K, Anderson DJ, Burstin H, Calfee DP, Coffin SE, Fraser V, Griffin FA, Gross P, Kaye KS, Klompas M, Lo E, Marschall J, Mermel LA, Nicolle L, Pegues DA, Perl TM, Saint S, Salgado CD, Weinstein RA, Wise R, Yokoe DS. Strategies to prevent clostridium difficile infections in acute care hospitals. Infect Control Hosp Epidemiol 2008;29 Suppl 1:S81–92. https://doi.org/10.1086/591065
- Note de bas de page 18
-
Pike J, Grosse SD. Friction cost estimates of productivity costs in cost-of-illness studies in comparison with human capital estimates: a review. Appl Health Econ Health Policy 2018;16(6):765–78. https://doi.org/10.1007/s40258-018-0416-4
- Note de bas de page 19
-
Koopmanschap MA, Rutten FF, van Ineveld BM, van Roijen L. The friction cost method for measuring indirect costs of disease. J Health Econ 1995;14(2):171–89. https://doi.org/10.1016/0167-6296(94)00044-5
- Note de bas de page 20
-
Statistique Canada. Tableau : 11-10-0239-01. Revenu des particuliers selon le groupe d'âge, le sexe et la source de revenu, Canada, provinces et certaines régions métropolitaines de recensement. Ottawa, ON : StatCan; 2021. https://www150.statcan.gc.ca/t1/tbl1/fr/tv.action?pid=1110023901&request_locale=fr
- Note de bas de page 21
-
Statistique Canada. Tableau : 14-10-0020-01 Taux de chômage, taux d'activité et taux d'emploi selon le niveau de scolarité atteint, données annuelles. Ottawa, ON : StatCan; 2021. https://www150.statcan.gc.ca/t1/tbl1/fr/tv.action?pid=1410002001&request_locale=fr
- Note de bas de page 22
-
Nanwa N, Kwong JC, Krahn M, Daneman N, Lu H, Austin PC, Govindarajan A, Rosella LC, Cadarette SM, Sander B. The Economic Burden of Hospital-Acquired Clostridium difficile Infection: A Population-Based Matched Cohort Study. Infect Control Hosp Epidemiol 2016;37(9):1068–78. https://doi.org/10.1017/ice.2016.122
Appendice : Liste des tableaux
Tableau A1 : Résultats de la régression des coûts différentiels
Tableau A2 : Résultats de la régression de la mortalité
| Groupe d'âge | Variable indépendante | CoefficientNote de bas de page a | Erreur standard | Statistiques T | Statistiques de régression |
|---|---|---|---|---|---|
| 18 à 34 | C. difficile, non-MRDx | 0,428 2 | 0,022 1 | 19,37 | Nombre d'observations : 398 445 Statistique F : 3 964,2 Probabilité > F : < ,000 1 R-carré : 0,573 R-carré aj. : 0,573 |
| SARM, non-IS | 0,238 0 | 0,015 9 | 14,93 | ||
| SARM, IS | 0,298 7 | 0,025 6 | 11,68 | ||
| Femme | -0,036 3 | 0,002 3 | -15,93 | ||
| Durée du séjour | 0,030 1 | 0,000 1 | 323,55 | ||
| Comorbidités | 0,077 7 | 0,000 3 | 223,69 | ||
| Constant | 7,808 3 | 0,016 2 | 482,12 | ||
| 35 à 54 | C. difficile, non-MRDx | 0,395 6 | 0,016 7 | 23,70 | Nombre d'observations : 401 292 Statistique F : 3 965,0 Probabilité > F : < ,000 1 R-carré : 0,575 R-carré aj. : 0,575 |
| SARM, non-IS | 0,192 1 | 0,013 7 | 14,04 | ||
| SARM, IS | 0,280 3 | 0,022 0 | 12,75 | ||
| Femme | -0,021 3 | 0,002 0 | -10,74 | ||
| Durée du séjour | 0,027 4 | 0,000 1 | 340,48 | ||
| Comorbidités | 0,080 7 | 0,000 4 | 230,28 | ||
| Constant | 7,787 0 | 0,018 6 | 417,89 | ||
| 55 à 64 | C. difficile, non-MRDx | 0,297 1 | 0,015 3 | 19,47 | Nombre d'observations : 326 065 Statistique F : 3 192,3 Probabilité > F : < ,000 1 R-carré : 0,566 R-carré aj. : 0,566 |
| SARM, non-IS | 0,191 1 | 0,018 1 | 10,53 | ||
| SARM, IS | 0,247 0 | 0,029 6 | 8,35 | ||
| Femme | -0,010 0 | 0,002 1 | -4,80 | ||
| Durée du séjour | 0,024 8 | 0,000 1 | 326,28 | ||
| Comorbidités | 0,081 5 | 0,000 4 | 223,42 | ||
| Constant | 7,801 5 | 0,024 8 | 315,15 | ||
| 65 à 74 | C. difficile, non-MRDx | 0,304 1 | 0,012 6 | 24,08 | Nombre d'observations : 403 732 Statistique F : 4 221,8 Probabilité > F : < ,000 1 R-carré : 0,578 R-carré aj. : 0,578 |
| SARM, non-IS | 0,184 2 | 0,017 8 | 10,33 | ||
| SARM, IS | 0,363 7 | 0,029 6 | 12,30 | ||
| Femme | -0,001 2 | 0,001 8 | -0,65 | ||
| Durée du séjour | 0,023 8 | 0,000 1 | 388,35 | ||
| Comorbidités | 0,079 6 | 0,000 3 | 262,67 | ||
| Constant | 7,952 4 | 0,024 0 | 331,05 | ||
| 75 ans et plus | C. difficile, non-MRDx | 0,263 1 | 0,009 9 | 26,63 | Nombre d'observations : 606 518 Statistique F : 6 794,8 Probabilité > F : < ,000 1 R-carré : 0,595 R-carré aj. : 0,595 |
| SARM, non-IS | 0,181 5 | 0,015 9 | 11,44 | ||
| SARM, IS | 0,391 7 | 0,027 5 | 14,25 | ||
| Femme | 0,006 5 | 0,001 5 | 4,34 | ||
| Durée du séjour | 0,021 5 | 0,000 0 | 559,10 | ||
| Comorbidités | 0,076 0 | 0,000 2 | 328,88 | ||
| Constant | 8,391 4 | 0,024 3 | 345,42 | ||
|
|||||
| Groupe d'âge | Variable indépendante | Rapport de cotes | Erreur standard | Khi-carré de Wald | Statistiques de régression |
|---|---|---|---|---|---|
| 18 à 34 | C. difficile, toute | 1,095 | 0,303 | 0,090 | Nombre d'observations : 398 445 Rapport de vraisemblance : 6 205,05 Probabilité > F : < 0,000 1 R-carré : 0,016 R-carré remis à l'échelle maximale : 0,407 1 |
| SARM, non-IS | 0,684 | 0,371 | 1,049 | ||
| SARM, IS | 2,123 | 0,285 | 6,956 | ||
| 35 à 54 | C. difficile, toute | 1,178 | 0,137 | 1,430 | Nombre d'observations : 401 292 Rapport de vraisemblance : 19 382,09 Signification du modèle : < 0,000 1 R-carré : 0,047 2 R-carré remis à l'échelle maximale : 0,369 9 |
| SARM, non-IS | 0,901 | 0,181 | 0,330 | ||
| SARM, IS | 1,815 | 0,157 | 14,367 | ||
| 55 à 64 | C. difficile, toute | 1,179 | 0,098 | 2,864 | Nombre d'observations : 326 065 Rapport de vraisemblance : 27 465,87 Signification du modèle : < 0,000 1 R-carré : 0,080 8 R-carré remis à l'échelle maximale : 0,330 8 |
| SARM, non-IS | 0,838 | 0,172 | 1,059 | ||
| SARM, IS | 1,595 | 0,167 | 7,805 | ||
| 65 à 74 | C. difficile, toute | 1,113 | 0,074 | 2,068 | Nombre d'observations : 403 732 Rapport de vraisemblance : 44 814,01 Signification du modèle : < 0,000 1 R-carré : 0,105 1 R-carré remis à l'échelle maximale : 0,331 2 |
| SARM, non-IS | 0,884 | 0,129 | 0,904 | ||
| SARM, IS | 2,172 | 0,143 | 29,419 | ||
| 75 ans et plus | C. difficile, toute | 1,584 | 0,047 | 95,419 | Nombre d'observations : 606 518 Rapport de vraisemblance : 84 928,33 Signification du modèle : < 0,000 1 R-carré : 0,130 7 R-carré remis à l'échelle maximale : 0,288 8 |
| SARM, non-IS | 0,973 | 0,095 | 0,082 | ||
| SARM, IS | 1,715 | 0,126 | 18,212 | ||
|
|||||

Cette œuvre est mise à disposition selon les termes de la Licence Creative Commons Attribution 4.0 International