Choix d’équipement de protection individuelle pour les travailleurs de la santé qui soignent les fièvres hémorragiques virales

 Téléchargez cet article en format PDF (158 ko)
Téléchargez cet article en format PDF (158 ko)Publié par : L'Agence de la santé publique du Canada
Numéro : RMTC : Volume 51-1, janvier 2025 : Mesures de protection individuelle
Date de publication : janvier 2025
ISSN : 1719-3109
Soumettre un article
À propos du RMTC
Naviguer
Volume 51-1, janvier 2025 : Mesures de protection individuelle
Revue systématique
Existe-t-il suffisamment de données probantes pour éclairer les décisions en matière de choix d’équipements de protection individuelle pour les travailleurs de la santé soignant les patients atteints de fièvre hémorragique virale?
Amanda Graham1, Steven Ettles1, Maureen McGrath1, Toju Ogunremi1, Jennifer Selkirk1, Natalie Bruce1
Affiliation
1 Centre de lutte contre les maladies transmissibles et les infections, Agence de la santé publique du Canada, Ottawa, ON
Correspondance
Citation proposée
Graham A, Ettles S, McGrath M, Ogunremi T, Selkirk J, Bruce N. Existe-t-il suffisamment de données probantes pour éclairer les décisions en matière de choix d'équipements de protection individuelle pour les travailleurs de la santé soignant les patients atteints de fièvre hémorragique virale? Relevé des maladies transmissibles au Canada 2025;51(1):8–17. https://doi.org/10.14745/ccdr.v51i01a02f
Mots-clés : équipement de protection individuelle, ÉPI, travailleurs de la santé, transmission, contamination, exposition, fièvre hémorragique virale, filovirus, Ebola
Résumé
Contexte : En septembre 2022, les autorités sanitaires ougandaises ont déclaré une éclosion de la maladie à virus Ebola, causée par le virus Ebola Soudan. Une revue rapide a été réalisée pour mettre à jour les lignes directrices de l'Agence de la santé publique du Canada (l'Agence) concernant les mesures de prévention et de contrôle des infections à Ebola dans les établissements de santé, afin de se préparer à l'apparition potentielle de cas.
Objectif : Résumer les données disponibles relatives à l'utilisation des équipements de protection individuelle (ÉPI) par les travailleurs de la santé pour prévenir l'exposition aux fièvres hémorragiques virales (FHV) et en entraver la transmission, notamment la maladie à virus Ebola.
Méthodes : Les bases de données électroniques ont été consultées afin de repérer les données probantes évaluées par des pairs, publiées entre juillet 2014 et octobre 2022. Les études primaires et les revues de la littérature évaluées par les pairs, en anglais ou en français, portant sur l'ÉPI pour protéger contre les FHV et les filovirus dans le contexte des soins de santé ont été prises en compte dans cette revue rapide. Deux évaluateurs ont mené les processus d'analyse de la littérature, à l'aide du logiciel d'analyse systématique DistillerSR® et du kit d'évaluation critique de l'Agence de la santé publique du Canada pour la prévention et le contrôle des infections. Une analyse du milieu de la littérature grise a également été réalisée afin d'éclairer la revue rapide.
Résultats : La recherche dans les bases de données a permis de trouver 417 citations, et 29 études ont été jugées éligibles pour une évaluation critique. Au total, 20 études ont été incluses dans le processus de réalisation d'une synthèse narrative des données probantes. La solidité de la base de données probantes était limitée en ce qui concerne l'efficacité comparative de différents types d'ÉPI pour supprimer le risque d'exposition des travailleurs de la santé à la maladie et de transmission de celle-ci Quatre études ont porté sur l'exposition aux FHV et sa transmission. Seize études ont fourni des données sur d'autres sujets connexes, tels que la simulation d'une contamination et des essais en laboratoire pour tester l'intégrité des ÉPI.
Conclusion : Il existe peu de données probantes permettant de tirer des conclusions sur l'efficacité comparative des ÉPI pour prévenir l'exposition aux FHV et leur transmission parmi les travailleurs de la santé. Il est donc nécessaire de mener des recherches supplémentaires pour déterminer l'ÉPI optimal pour protéger les travailleurs de la santé contre l'exposition aux FHV et la transmission celles-ci.
Introduction
Les fièvres hémorragiques virales (FHV) sont un groupe de maladies provoquées par des virus enveloppés possédant un génome à ARN simple brin, appartenant à six taxons, à savoir les Filovirus (i.e., virus Ebola et Marburg), les Arenavirus, les Flavivirus, les Hantavirus, les Nairovirus et les Phenuivirus Note de bas de page 1. La première description de la maladie d'Ebola (EBOD) a été émise en 1976 lors de deux éclosions simultanées dans deux pays différents, à savoir le Soudan du Sud et la République démocratique du Congo. Cette maladie est causée par six espèces de virus, dont quatre sont pathogènes pour les humains Note de bas de page 2Note de bas de page 3. Avant 2014, un total de 2 387 cas avaient été enregistrés dans des éclosions rurales localisées en Afrique, le taux de avec une mortalité brute global étant de 67 % Note de bas de page 1Note de bas de page 2. En 2014, une éclosion survenue en Afrique de l'Ouest, qui a duré deux ans, a enregistré une transmission urbaine intense et a entraîné plus de 28 000 cas, de nombreux pays, dont l'Italie, le Mali, le Nigeria, le Sénégal, l'Espagne, le Royaume-Uni et les États-Unis, ayant signalé des cas importés Note de bas de page 4Note de bas de page 5.
La transmission interhumaine du virus Ebola se produit par contact direct (i.e., à travers la peau ou les muqueuses non intactes) avec le sang ou d'autres liquides corporels (comme les selles, l'urine, les vomissures, la salive, la sueur, le sperme) d'une personne atteinte, ou indirectement par contact avec des surfaces environnementales et matières contaminées par du sang ou d'autres liquides corporels Note de bas de page 1Note de bas de page 2Note de bas de page 4. Le risque de transmission augmente en fonction de la quantité de matériel infectieux à laquelle l'individu est exposé Note de bas de page 5. Les enquêtes menées à ce jour n'ont pas mis en évidence de transmission entre humains de la maladie à virus Ebola en l'absence de contact direct avec un cas infecté Note de bas de page 3Note de bas de page 4.
L'utilisation d'équipements de protection individuelle (ÉPI) efficaces est essentielle pour prévenir l'infection et la transmission nosocomiales chez les travailleurs de la santé qui soignent les patients soupçonnés ou confirmés d'être atteint des FHV. Un contact direct avec des cas confirmés ou soupçonnés d'être atteints de la maladie sans précautions adéquates de prévention et de contrôle de l'infection (PCI) peut entraîner une infection et une mortalité du personnel soignant. Rien qu'en Sierra Leone, en Guinée et au Libéria, 513 décès sur un total de 881 travailleurs de la santé infectés ont été signalés en 2015 Note de bas de page 4. À l'heure actuelle, il y a peu de consensus sur les ÉPI les plus sûrs pour protéger les travailleurs de la santé de l'exposition au virus Ebola, et les recommandations varient souvent d'une administration à l'autre. Malgré l'absence de consensus général, les recommandations canadiennes en matière de PCI sont élaborées selon une approche de précaution priorisant la santé et la sécurité des travailleurs de la santé.
En septembre 2022, les autorités sanitaires ougandaises ont déclaré une nouvelle éclosion de maladie d'Ebola causée par le virus Ebola Soudan qui a entraîné 142 cas confirmés, 22 cas probables, 55 décès confirmés et 87 patients guéris Note de bas de page 2Note de bas de page 6. Aucun cas n'a été signalé au Canada. Compte tenu de l'évolution de la situation épidémiologique, une revue rapide de la littérature a été réalisée afin d'étayer la mise à jour des lignes directrices de l'Agence de santé publique du Canada (l'Agence) relatives aux mesures de prévention de la maladie Ebola dans les établissements de soins de santé. Cette revue résume les données disponibles sur l'utilisation des ÉPI par les travailleurs de la santé pour supprimer les risques d'exposition aux FHV et la transmission de celles-ci, notamment la maladie à virus Ebola des ÉPI.
Méthodes
Recherche documentaire et critères d'admissibilité
Les stratégies de recherche électronique ont été élaborées par les auteurs en consultation avec un bibliothécaire de la Bibliothèque de Santé Canada. Les bases de données Embase, MEDLINE, Global Health et Scopus ont été consultées en octobre 2022. Les études publiées en anglais ou en français entre juillet 2014 et octobre 2022 ont été prises en compte dans cette revue.
Notre recherche visait à répondre à la question suivante : Quelles sont les publications relatives à l'utilisation des ÉPI par le personnel de santé pour prévenir la transmission des fièvres hémorragiques virales et l'exposition à celles-ci? Les termes de recherche utilisés couvraient une grande variété de milieux et de professions de soins, ainsi que des articles d'ÉPI. Les termes de recherche, ainsi que les critères de population, d'exposition, d'intervention, de contrôle et de résultats pour la recherche documentaire figurent dans le tableau 1.
| PICO | Critères de recherche |
|---|---|
| Population | Personnel Diététicien, services alimentaires, technicien médical d'urgence, infirmier auxiliaire autorisé, technologue en radiologie médicale, technologue de laboratoire médical, sage-femme, infirmier praticien, paramédical, médecin, adjoint au médecin, infirmier autorisé, infirmier autorisé adjoint, infirmier auxiliaire autorisé, thérapeute respiratoire, services environnementaux, personnel de nettoyage, phlébotomiste, porteurs, travailleurs du secteur des transports Type de soins : Soins aigus, soins hospitaliers, soins d'urgence, soins intensifs, soins ambulatoires, soins de santé communautaire, soins à domicile, soins de répit, soins palliatifs, soins de longue durée, soins continus complexes, soins de réadaptation, soins préhospitaliers, soins de convalescence, soins de santé mentale |
| Exposition | Fièvre hémorragique virale, filovirus, Ebola, Lassa, Marbourg, virus de Crimée-Congo, maladie à virus Ebola (MVE), maladie à Ebolavirus Soudan (MVES) |
| Interventions | Équipement de protection individuelle (ÉPI), blouses, gants, respirateurs, N95, appareil de protection respiratoire à épuration d'air motorisé, protection du visage, masques, visières, protection des yeux, lunettes, tabliers, Tyvek, combinaison, bottes, couvre-bottes, couvre-chaussures, cagoule |
| Comparaisons | Sans objet pour l'instant |
| Résultats | Exposition (événement) Transmission (événement), propagation Contamination, auto-contamination |
Abréviations : ÉPI, équipement de protection individuelle; MVE, maladie à virus Ebola; MVES, maladie à Ebolavirus Soudan; PICO, population, exposure, intervention, comparison and outcomes |
|
Sélection des études et extraction des données
Les doublons ont été repérés et supprimés. Un outil de sélection a été développé dans Excel® pour un premier dépistage afin de vérifier que les paramètres d'inclusion étaient respectés. Deux évaluateurs indépendants ont procédé à une sélection supplémentaire des titres et des résumés en utilisant le logiciel DistillerSR®, afin d'évaluer la conception/le format de l'étude et la pertinence de l'utilisation des ÉPI. En raison de l'ampleur des résultats, la portée des études admissibles à l'inclusion a été réduite pour n'inclure que celles directement liées à l'utilisation de l'ÉPI par rapport aux résultats d'intérêt, sur la base de l'avis éclairé de l'évaluateur. Les articles d'actualité, les éditoriaux, les commentaires, les articles d'opinion, les lignes directrices, les déclarations de politique générale, les analyses de coûts et les articles à caractère juridique ou éthique ont été exclus. En outre, les études portant sur l'élaboration de protocoles, ainsi que sur l'épuisement par la chaleur et le confort pendant l'utilisation des ÉPIS, ont également été exclues.
L'objectif principal de la revue étant d'éclairer les orientations nationales en matière de PCI, les études ont été limitées à celles menées dans les pays membres du Groupe des vingt, et la Nouvelle-Zélande a été rajoutée lors de la phase d'examen complet du texte, afin de garantir l'applicabilité de l'étude au contexte canadien.
Un outil de sélection des textes à évaluer (DistillerSR) a été mis au point, ce qui a permis d'exclure les études sur la base des critères susmentionnées et pour récupérer les détails pertinents sur la conception de l'étude, la méthodologie et les résultats qualitatifs et quantitatifs concernant les ÉPI pertinents. L'examen complet des textes a été effectué par deux évaluateurs indépendants. Les incompatibilités ont été résolues par le biais d'une discussion permettant de renforcer le consensus entre les évaluateurs, et un troisième évaluateur a été invité à apporter sa contribution en cas d'impossibilité d'y parvenir.
Les articles inclus dans cette revue ont fait l'objet d'une évaluation critique à l'aide de la Trousse d'outils de l'évaluation critique des Lignes directrices pour la prévention et le contrôle des infections de l'Agence Note de bas de page 7. Cette trousse d'outils est utilisée pour évaluer les données probantes de manière systématique dans plusieurs domaines, notamment les évaluations de la population étudiée et des méthodes d'échantillonnage, la validité interne et externe, l'éthique et le contrôle des facteurs de confusion et des biais. Un résultat sommaire a été attribué à l'étude sur la base de la force de la conception, de la qualité globale et du caractère direct des données probantes.
Synthèse des données probantes
Une synthèse narrative des données probantes a été réalisée afin de repérer les points communs des études, les domaines de consensus et de divergence, ainsi que les lacunes dans la base de données probantes.
Résultats
Aperçu des études incluses
Les résultats de la méthode PRISMA (Preferred Reporting Items for Systematic Reviews and Meta-Analyses) sont présentés dans la figure 1. Vingt études ont été incluses dans l'analyse : huit études de laboratoire, deux essais contrôlés randomisés, trois essais contrôlés non randomisés, une étude transversale, quatre rapports de cas et deux revues de la littérature. Un résumé des données incluses se trouve dans l'appendice en tant que matériel supplémentaire.
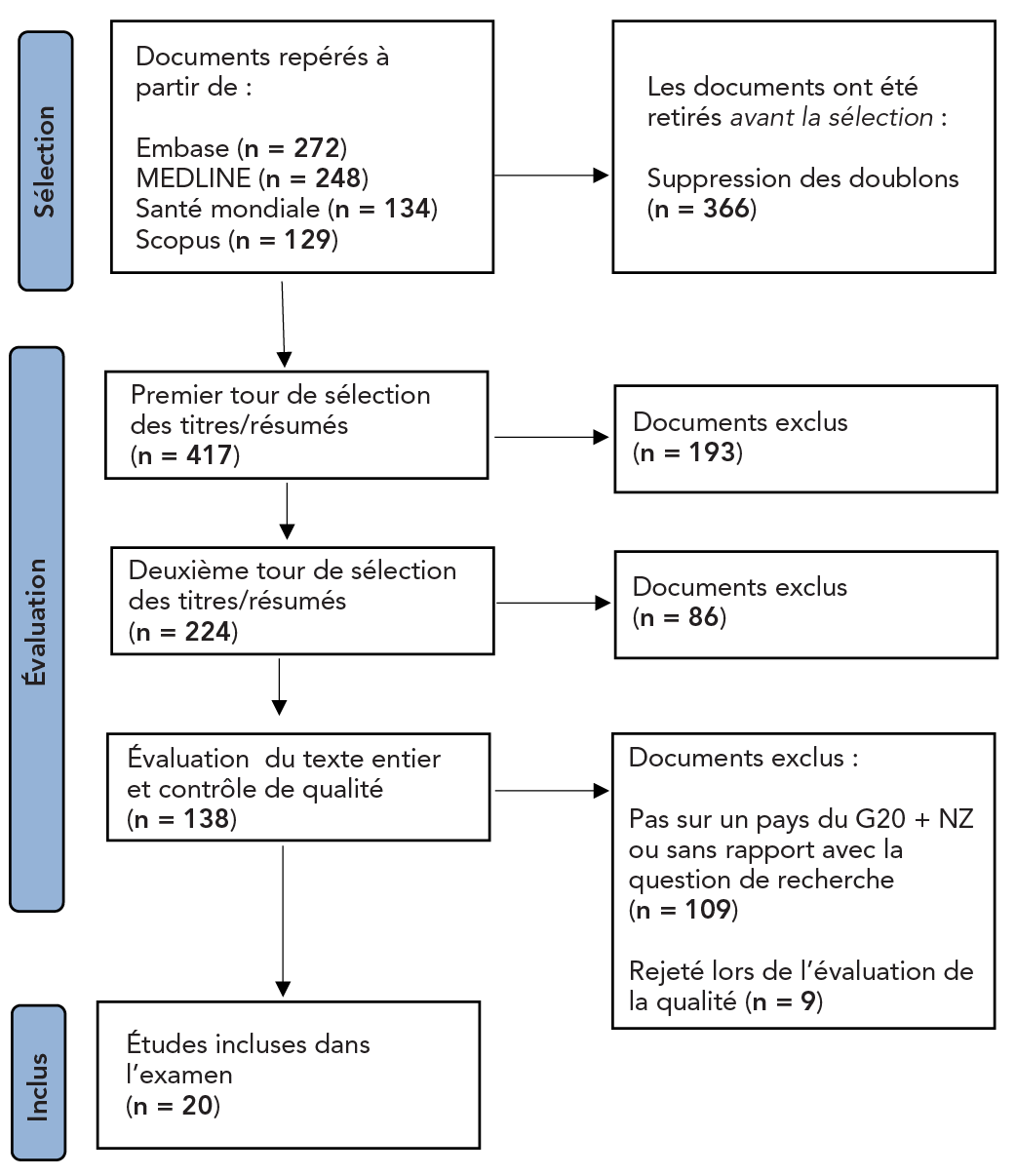
Figure 1 : Équivalent textuel
L'étape initiale de sélection des articles a permis d'inclure un total de 783 articles sur la base de la méthode PICO) (critères de population, d'exposition, d'intervention, de contrôle et de résultats). Deux cent soixante-douze articles ont été repérés dans Embase, 248 dans MEDLINE, 134 dans Global Health et 129 dans Scopus. À ce stade, 366 doublons ont été repérés et supprimés, ce qui a permis de sélectionner 417 articles. La sélection a commencé par une première série de titres et de résumés, qui a abouti à l'exclusion de 193 articles et à l'inclusion de 224. Une deuxième sélection des titres et des résumés a été effectuée, excluant 86 articles supplémentaires et en incluant 138. L'examen complet du texte et l'évaluation de la qualité ont permis d'exclure 109 articles parce qu'ils n'avaient pas été rédigés dans un pays du Groupe des vingt, à l'exception de la Nouvelle-Zélande. Neuf autres articles ont été exclus en raison des résultats de l'évaluation de la qualité. Au total, 20 articles ont passé toutes les étapes de la sélection et ont été inclus dans cette étude.
Abréviations : G20 + NZ, pays du Groupe des vingt plus la Nouvelle-Zélande; PRISMA, Preferred Reporting Items for Systematic reviews and Meta-Analyses
Contamination par fluorescence
Trois études Note de bas de page 8Note de bas de page 9Note de bas de page 10 ont évalué la contamination à l'aide de virus de substitution fluorescents, simulant des virus enveloppés et des virus nus. Dans chaque simulation, les participants ont revêtu un ensemble complet d'ÉPI complet couramment utilisé pour protéger contre les maladies infectieuses à haut risque. Dans deux études menées par Casanova et al., les chercheurs ont principalement cherché à mesurer la contamination décelable des ÉPI et des individus, repérée par des marques fluorescentes Note de bas de page 8Note de bas de page 9. Dans les deux études, aucun virus de substitution enveloppé n'a été détecté après le retrait de l'ÉPI, mais plusieurs cas de contamination par des virus nus ont été relevés, en particulier sur les sous-gants des participants. La détection d'une contamination, au niveau des sous-gants, mais pas sur les mains, suggère que les mesures d'hygiène des mains lors du retrait des gants protègent contre l'autocontamination par des virus enveloppés et nus.
L'étude de Mumma et al. Note de bas de page 10, a effectué une analyse des modes de défaillance et de leurs effets ainsi qu'une analyse par arbre de défaillances afin de cerner et de quantifier le risque d'erreurs dans un protocole de retrait des ÉPI. Pendant que les participants simulaient les soins aux patients, en démontrant le protocole de retrait de l'ÉPI conçu spécifiquement pour protection contre le virus Ebola, les risques liés aux modes de défaillance ont été repérés et quantifiés. La mesure dans laquelle les erreurs ont contribué à l'autocontamination a été définie. Trois groupes de modes de défaillance, caractérisés par leur fréquence et leur gravité, présentent des indices de risque plus élevé. Il s'agit notamment d'erreurs liées à la pratique de l'hygiène des mains, d'une mauvaise utilisation des ÉPI (en particulier au niveau des mains et des poignets) et d'une mauvaise manipulation des ÉPI (en particulier les cagoules comportant l'appareil de protection respiratoire à épuration d'air motorisé). Une étude ultérieure menée par Mumma et al. Note de bas de page 11 a utilisé une méthodologie semblable pour cerner les erreurs potentielles dans le processus de retrait des ÉPI et leur fréquence. Corroborant les résultats de l'étude précédente, l'hygiène des mains et le retrait de l'appareil de protection respiratoire à épuration d'air motorisé ont été associés à un risque d'erreur plus élevé. Le retrait du vêtement extérieur et des couvre-bottes a également révélé un risque d'erreur supérieur à la moyenne dans le processus de retrait de l'ÉPI.
Comparaison des ensembles d'équipements de protection individuelle
Chughtai et al. Note de bas de page 12 ont testé dix protocoles d'ÉPI établis pour la protection contre la maladie Ebola. Le niveau d'autocontamination parmi les participants était plus faible pour les protocoles d'ÉPI exigeant l'utilisation des blouses que pour ceux exigeant l'utilisation des combinaisons. Les appareils de protection respiratoire à épuration d'air motorisé se sont révélés plus protecteurs que les appareils respiratoires N95, ce qui pourrait s'expliquer par un risque plus faible d'autocontamination grâce aux moins d'articles d'ÉPI et à la mise en place d'un système de retrait assisté.
Une étude réalisée par Suen et al. Note de bas de page 13, comparant l'efficacité de trois types d'ÉPI, a signalé certaines différences de contamination entre les ensembles. L'ÉPI standard pour protection contre Ebola (ÉPI1), qui comprend une combinaison allant du cou à la cheville, une blouse imperméable, des gants doubles en nitrile et une cagoule, a été comparé à un autre ensemble d'ÉPI pour protection contre Ebola (ÉPI2) : une combinaison à fermeture frontale, un tablier en plastique et des gants doubles. Les ÉPI1 et ÉPI2 comprennent des bottes, un écran facial et un respirateur N95, et ont été comparés à un ensemble d'ÉPI de référence utilisé pour les pratiques de routine et les procédures génératrices d'aérosols (ÉPI3). L'étude a révélé que les vêtements des participants étaient moins souvent contaminés par de petites taches lors du retrait de l'ÉPI1 (médiane de 5,00 petites taches de contamination), par rapport à l'ÉPI2 et à l'ÉPI3 (médiane de 7,00 taches). L'étude a révélé que les vêtements des participants étaient moins souvent contaminés par de petites taches lors du retrait de l'ÉPI1 (médiane de 5,00 petites taches de contamination), par rapport à l'ÉPI2 et à l'ÉPI3 (médiane de 7,00 taches). En outre, les ensembles d'ÉPI conçus spécifiquement pour protection contre Ebola (ÉPI1, ÉPI2) ont généralement fait preuve de moins de contamination que l'ÉPI de référence (ÉPI3).
Hall et al. Note de bas de page 14 ont comparé un ensemble d'ÉPI de base (masque chirurgical, tablier de longueur standard, une paire de gants courts, ses propres chaussures) aux protocoles d'ÉPI établis utilisés dans les unités de traitement des maladies à haut risque au Royaume-Uni. Sur l'ensemble des protocoles, 1 584 contaminations ont été enregistrées après la fin d'un exercice de simulation, et douze contaminations après le retrait de l'ÉPI. Les manquements repérés étaient liés à une défaillance du protocole ou à des complications dans les processus de retrait de l'ÉPI. Dans une étude de suivi, Poller et al. Note de bas de page 15 ont reproduit les tests en utilisant un nouvel ensemble d'ÉPI pour les maladies infectieuses à haut risque, mis au point par un groupe de travail d'experts. Alors que la fréquence des événements de contamination post-simulation était comparable à celle observée par Hall et al., aucune contamination résiduelle n'a été observée après le retrait du nouvel ensemble d'ÉPI. Les principales caractéristiques de l'ensemble comprenaient l'utilisation d'un respirateur FFP3, d'une cagoule résistante au transfert d'infection, d'une visière intégrale, d'une blouse chirurgicale renforcée et résistante aux fluides se fixant à l'arrière, d'un tablier large et extra long en plastique d'épaisseur moyenne, de trois couches de gants et de bottes chirurgicales de type Wellington.
Un essai contrôlé randomisé Note de bas de page 16 a utilisé un seul ensemble d'ÉPI conçu pour le traitement d'Ebola, mais a comparé deux groupes de formation différents pour évaluer la contamination par fluorescence dans chaque groupe après avoir subi une contamination simulée. Les deux groupes ont reçu une formation de base en matière de PCI et d'ÉPI. Le groupe d'intervention a reçu une formation beaucoup plus axée sur le travail d'équipe, comprenant des stratégies, une définition des rôles et des responsabilités et une démonstration du processus de retrait. Un examen nous a permis de constater que l'autocontamination était significativement plus faible dans le groupe d'intervention que dans le groupe de contrôle.
Évaluation de l'intégrité des équipements de protection individuelle
Gao et al. Note de bas de page 17 ont testé treize marques de gants en nitrile (n = 8) et en latex (n = 5), en examinant la résistance à la traction et l'allongement final sans (contrôle) et avec une à six applications de désinfectant à base d'alcool. Dans l'ensemble, le désinfectant à base d'alcool a eu peu ou pas d'effet sur l'élongation de la plupart des gants, mais a entraîné une diminution de la résistance à la traction pour certains gants en nitrile après un maximum de six applications. Malgré cela, tous les gants en nitrile, à l'exception de deux gants relativement fins, ont continué à répondre aux normes de la National Fire Protection Association en matière de résistance à la tension et d'élongation.
Nikiforuk et al. Note de bas de page 18 ont mesuré la persistance dans l'environnement du virus Ebola et de l'ARN viral sur divers matériaux d'ÉPI. Le virus Ebola est resté viable sur tous les matériaux entre 24 et 72 heures après l'inoculation, sauf sur les gants (moins d'une heure) et les lunettes (moins de 24 heures). La pénétration du virus Ebola à travers les ÉPI a été mesurée à l'aide d'échantillons secs et saturés de solution saline d'une cagoule, d'une combinaison et d'un respirateur, qui ont également été traités avec le tampon au phosphate. Les échantillons saturés se sont révélés moins protecteurs que les matériaux secs. Des résultats comparables ont été observés lorsque des échantillons secs et saturés d'un masque chirurgical et de deux respirateurs ont été testés. Dans l'ensemble, les ÉPIS saturés ont fourni moins de protection que les échantillons secs, avec une pénétration du virus Ebola dans sept des 21 échantillons saturés, contre un des 21 échantillons secs des mêmes matériaux.
Jaques et al. Note de bas de page 19 a effectué des tests utilisant différents niveaux de pression, sur des blouses d'isolation et des combinaisons afin de mesurer la résistance des parties continues et discontinues des vêtements à la pénétration de fluides corporels simulés. Dans l'ensemble, une pression plus élevée a entraîné des taux de défaillance plus importants pour tous les types de vêtements, que ce soit dans les régions continues ou discontinues. Dans les parties discontinues, les combinaisons qui présentaient des taux de défaillance élevés au niveau des coutures, et des fermetures à glissière n'offraient pas de protection, mais les coutures thermosoudées étaient plus performantes. Seul un modèle de vêtement, une blouse, a démontré une protection de près de 100 % pour l'ensemble du vêtement, avec un seul échec sur 42 tests.
Rapports de cas
Quatre rapports de cas ont été inclus, décrivant les mesures de PCI prises pour les soins des patients soupçonnés ou confirmés comme étant atteints de la maladie Ebola ou d'autres FHV Note de bas de page 20Note de bas de page 21Note de bas de page 22Note de bas de page 23. Il y avait très peu de rapports sur les articles ou ensembles spécifiques d'ÉPI utilisés pour les soins aux patients, et peu de détails ont été fournis sur la capacité de l'ÉPI à prévenir les risques d'exposition et de transmission. Malgré leurs limites, ces études ne pouvaient pas être raisonnablement exclues sur la base des critères d'inclusion établis et ont donc été prises en compte dans l'analyse.
Revue de la littérature :
Deux revues de la littérature ont été incluses dans l'analyse. Hersi et al. Note de bas de page 24 ont évalué les avantages et les inconvénients de l'ÉPI spécifique à l'Ebola par rapport à un ÉPI potentiellement moins robuste dans le contexte des travailleurs de la santé soignant des patients atteints de filovirus. Malgré une méthodologie exhaustive, les données disponibles sont insuffisantes pour tirer des conclusions sur l'efficacité et les inconvénients potentiels d'un ÉPI robuste par rapport à l'autre solution.
Licina et al. Note de bas de page 25 ont évalué l'effet des appareils de protection respiratoire à épuration d'air motorisé pour la protection respiratoire contre les maladies infectieuses très virulentes, y compris la maladie Ebola par rapport à d'autres dispositifs tels que les respirateurs N95/FFP2, sur les taux d'infection et de contamination des travailleurs de la santé. Des taux d'infection équivalents ont été démontrés dans les cohortes utilisant des appareils de protection respiratoire à épuration d'air motorisé par rapport à d'autres protections respiratoires appropriées. La revue a repéré quelques preuves de faible qualité indiquant les avantages de ces appareils respiratoires, par rapport à d'autres protections respiratoires, pour la protection du porteur contre la contamination croisée et dans les études de simulation de retrait d'ÉPI.
Évaluations de la qualité
Vingt-neuf études ont fait l'objet d'une évaluation de la qualité à l'aide de la Trousse d'outil de l'évaluation critique de l'Agence Note de bas de page 7. Neuf études ont été rejetées à ce stade en raison de leur manque de pertinence par rapport à notre question de recherche. Sur les 20 études incluses, deux études ont été évaluées comme étant de haute qualité Note de bas de page 17Note de bas de page 18, 14 comme étant de qualité moyenne et quatre comme étant de faible qualité. Pour toutes les études, le caractère direct des données probantes a été déterminé comme étant une extrapolation, car les résultats étaient liés à une question de recherche différente, ou ont été étudiés dans des conditions artificielles. Les résultats complets de l'évaluation de la qualité figurent dans le tableau 2.
| Étude (référence) | Conception de l'étude | Solidité de la conceptionNote de bas de page a | Caractère direct des données probantes | Qualité globale de l'étude |
|---|---|---|---|---|
| Andonian et al., 2019 Note de bas de page 16 | ECR | Solide | Extrapolation | Moyen |
| Bell et al., 2022 Note de bas de page 26 | ECR | Solide | Extrapolation | Faible |
| Barratt et al., 2015 Note de bas de page 20 | Rapport de cas | Faible | Extrapolation | Moyen |
| Casanova et al., 2018 Note de bas de page 8 | Étude en laboratoire | Solide | Extrapolation | Moyen |
| Casanova et al., 2016 Note de bas de page 9 | ECNR | Solide | Extrapolation | Faible |
| Chughtai et al., 2018 Note de bas de page 12 | Étude en laboratoire | Solide | Extrapolation | Moyen |
| Cummings et al., 2016 Note de bas de page 21 | Rapport de cas | Faible | Extrapolation | Faible |
| Drew et al., 2016 Note de bas de page 27 | ECNR | Solide | Extrapolation | Moyen |
| Gao et al., 2016 Note de bas de page 17 | Étude en laboratoire | Solide | Extrapolation | Élevée |
| Hall et al., 2018 Note de bas de page 14 | ECNR | Solide | Extrapolation | Faible |
| Haverkort et al., 2016 Note de bas de page 22 | Rapport de cas | Faible | Extrapolation | Moyen |
| Hersi et al., 2015 Note de bas de page 24 | Revue de la littérature | Sans objetNote de bas de page b | Extrapolation | Moyen |
| Jaques et al., 2016 Note de bas de page 19 | Étude en laboratoire | Solide | Extrapolation | Moyen |
| Lehmann et al., 2017 Note de bas de page 23 | Rapport de cas | Faible | Extrapolation | Moyen |
| Licina et al., 2020 Note de bas de page 25 | Revue de la littérature | Sans objetNote de bas de page b | Extrapolation | Moyen |
| Mumma et al., 2019 Note de bas de page 11 | Étude transversale | Faible | Extrapolation | Moyen |
| Mumma et al., 2018 Note de bas de page 10 | Étude en laboratoire | Solide | Extrapolation | Moyen |
| Nikiforuk et al., 2017 Note de bas de page 18 | Étude en laboratoire | Solide | Extrapolation | Élevée |
| Poller et al., 2018 Note de bas de page 15 | Étude en laboratoire | Solide | Extrapolation | Moyen |
| Suen et al., 2018 Note de bas de page 13 | Étude en laboratoire | Solide | Extrapolation | Moyen |
Note de bas de tableau 2
Abréviations : ECNR, essai contrôlé non randomisé; ECR, essai contrôlé randomisé
|
||||
Discussion
L'analyse a permis de repérer 20 études pertinentes portant sur l'utilisation des ÉPI dans le contexte des FHV, telle que la maladie Ebola, dans des pays à revenu élevé. Une évaluation de la qualité des preuves a été réalisée, étant donné la qualité faible à moyenne de la plupart des études Note de bas de page 19; malheureusement, la faible qualité de nombreuses études a limité notre capacité d'extrapolation à des scénarios réels. Nous avons conclu que les données probantes étaient insuffisantes pour tirer des conclusions sur l'efficacité comparative des ÉPI pour prévenir l'exposition aux FHV, y compris la maladie Ebola, et leur transmission aux travailleurs de la santé. Compte tenu de ce manque d'éléments probants sur l'efficacité des ÉPI, la détermination des ensembles d'ÉPI pour la maladie Ebola devrait envisager une approche de précaution.
Neuf études aux méthodologies variées ont permis de détecter la contamination à l'aide de marqueurs fluorescents. Deux études ont montré que l'utilisation de l'ÉPI contre les maladies infectieuses à haut risque n'entraînait pas d'autocontamination, ce qui suggère que les ensembles sont efficaces. En outre, les études comparant les ensembles d'ÉPI spécifiques conçus pour la maladie Ebola/les maladies infectieuses à haut risque aux ÉPIS de base ou de routine ont systématiquement montré que les ensembles d'ÉPI plus robustes protègent nettement mieux contre la contamination Note de bas de page 13Note de bas de page 14Note de bas de page 15. Cependant, il est difficile de comparer l'efficacité des combinaisons d'ÉPI améliorées en raison de l'hétérogénéité des ensembles comparés entre les études, des méthodes utilisées pour simuler et enregistrer la contamination, des différences dans la déclaration de la contamination et des variations dans la formation et l'expérience des participants. En raison de la diversité de la portée et de la méthodologie des études indépendantes qui répondaient aux critères d'inclusion, il n'a pas été possible de réaliser une méta-analyse qui résumerait quantitativement les conclusions générales des résultats. Il est donc difficile de tirer des conclusions sur les effets protecteurs d'éléments individuels ou de combinaisons d'ÉPI. La plupart des ensembles varient considérablement en ce qui concerne le protège-corps, les gants, les couvre-chefs et les chaussures. D'autres aspects des protocoles (lorsqu'ils sont signalés) varient également, notamment l'hygiène des mains et l'aide au déshabillage.
Trois études de laboratoire de qualité moyenne à supérieure Note de bas de page 17Note de bas de page 18Note de bas de page 19 utilisant des méthodologies différentes ont évalué l'intégrité des ÉPI, en examinant la dégradation des matériaux des ÉPI et la pénétration du virus Ebola, d'un virus de substitution ou de fluides corporels simulés à travers les échantillons. Les équipements de protection individuelle testés comprenaient des gants Note de bas de page 17Note de bas de page 18, des blouses et des combinaisons Note de bas de page 18Note de bas de page 19, des masques chirurgicaux et des respirateurs Note de bas de page 18. Ces études ont montré que les ÉPI considérés étaient généralement résistants à la dégradation due à l'utilisation des rince-mains à base d'alcool et que les ÉPI saturés d'humidité tendaient à offrir une protection moindre que les ÉPI secs, ce qui montre qu'il est important d'éviter la contamination par les fluides corporels et la transpiration excessive lors de l'enfilage des vêtements. D'autres travaux devraient être menés pour élucider les performances comparatives d'autres modèles d'ÉPI afin de déterminer ceux qui offrent la meilleure protection en cas de saturation en eau et de pression induite par l'activité.
Malgré le fait qu'ils disposaient d'une méthodologie bien conçue et complète, Hersi et al. Note de bas de page 24 n'ont pas été en mesure de conclure à l'efficacité des différents types d'ÉPI pour les travailleurs de la santé prodiguant des soins aux patients atteints de FHV, en raison de problèmes comparables liés au corpus de preuves, tels que la faible qualité des études et l'hétérogénéité des composants de l'ÉPI et de la présentation des résultats. Ce résultat est conforme à nos conclusions.
Lors de l'examen du rôle de l'appareil de protection respiratoire à l'épuration d'air motorisé Note de bas de page 25, les enquêteurs n'ont pas été en mesure de trouver des différences de protection par rapport à d'autres formes de protection respiratoire. Ce résultat est en contradiction avec les travaux de Chughtai et al. Note de bas de page 12, qui a montré que les appareils de protection respiratoire à épuration d'air motorisé offraient une meilleure protection que les respirateurs N95. Bien que les travaux de Chughtai et al. présentent un certain nombre de limites, d'autres travaux sont nécessaires pour déterminer la véritable sécurité de l'utilisation des appareils de protection respiratoire et leur rôle dans l'autocontamination, lors des soins aux patients atteints de FHV.
Un autre problème a été relevé : les rapports sur l'ÉPI dans les études étaient souvent incohérents, un certain nombre d'études ne citant les ensembles d'ÉPI que comme des ceux conçus pour les maladies à haut risque ou spécifiquement pour Ebola, ce qui rendait difficile la détermination des composants individuels et leur comparabilité avec l'ÉPI utilisé dans d'autres études. En outre, les étapes d'enfilage et de retrait d'équipement n'ont souvent pas été indiquées, ce qui constitue un autre obstacle à la comparaison des résultats.
Points forts et limites
L'un des points forts de cette étude est l'utilisation d'un formulaire de sélection et d'extraction de données normalisé dans un logiciel de gestion des références, ce qui a permis de réduire les biais et de garantir l'intégrité des données grâce à un processus cohérent de collecte de données et d'établissement de rapport. Les résultats ont également fait l'objet d'une évaluation critique afin de déterminer les domaines de biais, et certaines études ont été exclues en raison d'une méthodologie jugée médiocre. Un autre point fort de cette étude est que les critères de recherche excluaient les pays en dehors du Groupe des vingt et de la Nouvelle-Zélande, afin de garantir la compatibilité des résultats avec les établissements de santé canadiens lors de l'élaboration des recommandations pratiques en matière de soins intensifs de santé. En outre, l'ajout de critères multiples au cours du processus de sélection a facilité la sélection d'études plus comparables et plus pertinentes par rapport à la question de recherche, ce qui a permis d'améliorer notre analyse.
L'une des faiblesses de cette étude est le nombre limité d'études incluses et l'hétérogénéité globale de la méthodologie et des résultats. La plupart des études étaient également limitées par des échantillons de petite taille (moins de 20 participants). Compte tenu de ces problèmes et de l'impossibilité de procéder à une analyse statistique plus poussée, il a été difficile de tirer des conclusions définitives à partir des données disponibles, ce qui a eu une incidence sur notre capacité à formuler des conclusions fondées sur des éléments probants.
Conclusions et orientations futures
À notre connaissance, il s'agit de la première analyse documentaire réalisée au Canada visant à répondre à la question de recherche : Que dispose-t-on comme littérature relative à l'utilisation d'ÉPI par les travailleurs de la santé pour prévenir la transmission des fièvres hémorragiques virales et l'exposition à celles-ci dans les pays à revenu élevé? Cette synthèse donne un aperçu important de l'état des connaissances sur ce sujet et indique les domaines nécessitant une exploration plus approfondie.
Dans l'ensemble, les données disponibles ne permettent pas de tirer des conclusions sur l'efficacité comparative des ÉPI pour prévenir l'exposition aux FHV et leur transmission aux travailleurs de la santé. Le corpus actuel de données bénéficierait d'une comparaison plus solide des différents composants et modèles d'ÉPI, en utilisant des méthodes normalisées pour la collecte et la communication des données afin de garantir la comparabilité entre les études. Il y a une lacune importante en matière de modèles d'étude solides (tels que les essais contrôlés randomisés et les études impliquant un grand nombre de participants), qui produiraient des résultats plus robustes et permettraient une analyse statistique et une modélisation. Si possible, la réalisation d'un plus grand nombre d'études au cours d'éclosions de FHV ou pendant les soins prodigués aux patients atteints de maladie Ebola donnerait une meilleure idée des résultats obtenus dans le monde réel par rapport aux études de simulation.
Déclaration des auteurs
- A. G. — Conceptualisation, méthodologie, analyse formelle, interprétation, rédaction de la version originale, rédaction–révision et édition
- S. E. — Conceptualisation, méthodologie, analyse formelle, interprétation, rédaction de la version originale, rédaction–révision et édition
- M. M. — Conceptualisation, méthodologie, analyse formelle, interprétation, rédaction de la version originale, rédaction–révision et édition
- T. O. — Conceptualisation, rédaction–révision et édition
- J. S. — Conceptualisation, méthodologie, analyse formelle, interprétation, rédaction de la version originale, rédaction–révision et édition
- N. B. — Conceptualisation, rédaction–révision et édition
Intérêts concurrents
Aucun des chercheurs n'a de conflit d'intérêts dans cette étude.
Identifiants ORCID
Aucun.
Remerciements
Les auteurs souhaitent remercier les bibliothécaires de la bibliothèque de Santé Canada et de l'Agence de santé publique du Canada pour leur contribution aux premiers résultats de recherche de cette revue.
Financement
Le travail effectué dans le cadre de cette étude a été soutenu par l'Agence de santé publique du Canada dans le cadre de son mandat.
Références
- Notes de bas de page 1
-
Clément C, Adhikari NK, Lamontagne F. Evidence-Based Clinical Management of Ebola Virus Disease and Epidemic Viral Hemorrhagic Fevers. Infect Dis Clin North Am 2019;33(1):247–64. https://doi.org/10.1016/j.idc.2018.10.013
- Notes de bas de page 2
-
World Health Organization. Ebola Virus Disease. Geneva, CH: WHO; 2023. [Consulté le 20 fév. 2023]. https://www.who.int/news-room/fact-sheets/detail/ebola-virus-disease#
- Notes de bas de page 3
-
Sivanandy P, Jun PH, Man LW, Wei NS, Mun NF, Yii CA, Ying CC. A systematic review of Ebola virus disease outbreaks and an analysis of the efficacy and safety of newer drugs approved for the treatment of Ebola virus disease by the US Food and Drug Administration from 2016 to 2020. J Infect Public Health 2022;15(3):285–92. https://doi.org/10.1016/j.jiph.2022.01.005
- Notes de bas de page 4
-
World Health Organization. WHO: Ebola situation report 2 September 2015. Geneva, CH: WHO; 2015. [Consulté le 23 fév. 2023]. https://apps.who.int/iris/handle/10665/183955
- Notes de bas de page 5
-
UK Health Security Agency. Ebola: overview, history, origins and transmission. London, UK: UK HAS; 2023. [Consulté le 21 fév. 2023]. https://www.gov.uk/government/publications/ebola-origins-reservoirs-transmission-and-guidelines/ebola-overview-history-origins-and-transmission
- Notes de bas de page 6
-
World Health Organization. Ebola—Uganda, 2022. Geneva, CH: WHO; 2023. [Consulté le 19 oct. 2023]. https://www.who.int/emergencies/situations/ebola-uganda-2022
- Notes de bas de page 7
-
Agence de la santé publique du Canada. Infection prevention and control guidelines: critical appraisal tool kit. Ottawa, ON: ASPC; 2016. [Consulté le 15 mars 2023]. https://publications.gc.ca/site/fra/470818/publication.html
- Notes de bas de page 8
-
Casanova LM, Erukunuakpor K, Kraft CS, Mumma JM, Durso FT, Ferguson AN, Gipson CL, Walsh VL, Zimring C, DuBose J, Jacob JT; Centers for Disease Control and Prevention Epicenters Program, Division of Healthcare Quality Promotion. Assessing Viral Transfer During Doffing of Ebola-Level Personal Protective Equipment in a Biocontainment Unit. Clin Infect Dis 2018;66(6):945–9. https://doi.org/10.1093/cid/cix956
- Notes de bas de page 9
-
Casanova LM, Teal LJ, Sickbert-Bennett EE, Anderson DJ, Sexton DJ, Rutala WA, Weber DJ; CDC Prevention Epicenters Program. Assessment of self-contamination during removal of personal protective equipment for Ebola patient care. Infect Control Hosp Epidemiol 2016;37(10):1156–61. https://doi.org/10.1017/ice.2016.169
- Notes de bas de page 10
-
Mumma JM, Durso FT, Ferguson AN, Gipson CL, Casanova L, Erukunuakpor K, Kraft CS, Walsh VL, Zimring C, DuBose J, Jacob JT; Centers for Disease Control and Prevention Epicenters Program, Division of Healthcare Quality Promotion. Human Factors Risk Analyses of a Doffing Protocol for Ebola-Level Personal Protective Equipment: Mapping Errors to Contamination. Clin Infect Dis 2018;66(6):950–8. https://doi.org/10.1093/cid/cix957
- Notes de bas de page 11
-
Mumma JM, Durso FT, Casanova LM, Erukunuakpor K, Kraft CS, Ray SM, Shane AL, Walsh VL, Shah PY, Zimring C, DuBose J, Jacob JT. Common Behaviors and Faults When Doffing Personal Protective Equipment for Patients With Serious Communicable Diseases. Clin Infect Dis 2019;69 Suppl 3:S214–20. https://doi.org/10.1093/cid/ciz614
- Notes de bas de page 12
-
Chughtai AA, Chen X, Macintyre CR. Risk of self-contamination during doffing of personal protective equipment. Am J Infect Control 2018;46(12):1329–34. https://doi.org/10.1016/j.ajic.2018.06.003
- Notes de bas de page 13
-
Suen LK, Guo YP, Tong DW, Leung PH, Lung D, Ng MS, Lai TK, Lo KY, Au-Yeung CH, Yu W. Self-contamination during doffing of personal protective equipment by healthcare workers to prevent Ebola transmission. Antimicrob Resist Infect Control 2018;7:157. https://doi.org/10.1186/s13756-018-0433-y
- Notes de bas de page 14
-
Hall S, Poller B, Bailey C, Gregory S, Clark R, Roberts P, Tunbridge A, Poran V, Evans C, Crook B. Use of ultraviolet-fluorescence-based simulation in evaluation of personal protective equipment worn for first assessment and care of a patient with suspected high-consequence infectious disease. J Hosp Infect 2018;99(2):218–28. https://doi.org/10.1016/j.jhin.2018.01.002
- Notes de bas de page 15
-
Poller B, Tunbridge A, Hall S, Beadsworth M, Jacobs M, Peters E, Schmid ML, Sykes A, Poran V, Gent N, Evans C, Crook B; High Consequence Infectious Diseases Project Working Group. A unified personal protective equipment ensemble for clinical response to possible high consequence infectious diseases: A consensus document on behalf of the HCID programme. J Infect 2018;77(6):496–502. https://doi.org/10.1016/j.jinf.2018.08.016
- Notes de bas de page 16
-
Andonian J, Kazi S, Therkorn J, Benishek L, Billman C, Schiffhauer M, Nowakowski E, Osei P, Gurses AP, Hsu YJ, Drewry D, Forsyth ER, Vignesh A, Oresanwo I, Garibaldi BT, Rainwater-Lovett K, Trexler P, Maragakis LL. Effect of an Intervention Package and Teamwork Training to Prevent Healthcare Personnel Self-contamination During Personal Protective Equipment Doffing. Clin Infect Dis 2019;69 Suppl 3:S248–55. https://doi.org/10.1093/cid/ciz618
- Notes de bas de page 17
-
Gao P, Horvatin M, Niezgoda G, Weible R, Shaffer R. Effect of multiple alcohol-based hand rub applications on the tensile properties of thirteen brands of medical exam nitrile and latex gloves. J Occup Environ Hyg 2016;13(12):905–14. https://doi.org/10.1080/15459624.2016.1191640
- Notes de bas de page 18
-
Nikiforuk AM, Cutts TA, Theriault SS, Cook BW. Challenge of Liquid Stressed Protective Materials and Environmental Persistence of Ebola Virus. Sci Rep 2017;7(1):4388. https://doi.org/10.1038/s41598-017-04137-2
- Notes de bas de page 19
-
Jaques PA, Gao P, Kilinc-Balci S, Portnoff L, Weible R, Horvatin M, Strauch A, Shaffer R. Evaluation of gowns and coveralls used by medical personnel working with Ebola patients against simulated bodily fluids using an Elbow Lean Test. J Occup Environ Hyg 2016;13(11):881–93. https://doi.org/10.1080/15459624.2016.1186279
- Notes de bas de page 20
-
Barratt R. Infection prevention and control lessons learned from the management of the first suspected Ebola virus disease case admitted to a New Zealand hospital. Healthc Infect 2015;20:78–80. https://doi.org/10.1071/HI15006
- Notes de bas de page 21
-
Cummings KJ, Choi MJ, Esswein EJ, de Perio MA, Harney JM, Chung WM, Lakey DL, Liddell AM, Rollin PE. Addressing Infection Prevention and Control in the First U.S. Community Hospital to Care for Patients With Ebola Virus Disease: Context for National Recommendations and Future Strategies. Ann Intern Med 2016;165(1):41–9. https://doi.org/10.7326/M15-2944
- Notes de bas de page 22
-
Haverkort JJ, Minderhoud AL, Wind JD, Leenen LP, Hoepelman AI, Ellerbroek PM. Hospital Preparations for Viral Hemorrhagic Fever Patients and Experience Gained from Admission of an Ebola Patient. Emerg Infect Dis 2016;22(2):184–91. https://doi.org/10.3201/eid2202.151393
- Notes de bas de page 23
-
Lehmann C, Kochanek M, Abdulla D, Becker S, Böll B, Bunte A, Cadar D, Dormann A, Eickmann M, Emmerich P, Feldt T, Frank C, Fries J, Gabriel M, Goetsch U, Gottschalk R, Günther S, Hallek M, Häussinger D, Herzog C, Jensen B, Kolibay F, Krakau M, Langebartels G, Rieger T, Schaade L, Schmidt-Chanasit J, Schömig E, Schüttfort G, Shimabukuro-Vornhagen A, von Bergwelt-Baildon M, Wieland U, Wiesmüller G, Wolf T, Fätkenheuer G. Control measures following a case of imported Lassa fever from Togo, North Rhine Westphalia, Germany, 2016. Euro Surveill 2017;22(39):17–00088. https://doi.org/10.2807/1560-7917.ES.2017.22.39.17-00088
- Notes de bas de page 24
-
Hersi M, Stevens A, Quach P, Hamel C, Thavorn K, Garritty C, Skidmore B, Vallenas C, Norris SL, Egger M, Eremin S, Ferri M, Shindo N, Moher D. Effectiveness of personal protective equipment for healthcare workers caring for patients with filovirus disease: A rapid review. PLoS One 2015;10(10):e0140290. https://doi.org/10.1371/journal.pone.0140290
- Notes de bas de page 25
-
Licina A, Silvers A, Stuart RL. Use of powered air-purifying respirator (PAPR) by healthcare workers for preventing highly infectious viral diseases-a systematic review of evidence. Syst Rev 2020;9(1):173. https://doi.org/10.1186/s13643-020-01431-5
- Notes de bas de page 26
-
Bell T, Smoot J, Patterson J, Smalligan R, Jordan R. Ebola virus disease: the use of fluorescents as markers of contamination for personal protective equipment. IDCases 2015;2(1):27–30. https://doi.org/10.1016/j.idcr.2014.12.003
- Notes de bas de page 27
-
Drew JL, Turner J, Mugele J, Hasty G, Duncan T, Zaiser R, Cooper D. Beating the spread developing a simulation analog for contagious body fluids. Simul Healthc 2016;11(2):100–5. https://doi.org/10.1097/SIH.0000000000000157
Appendice
Du matériel supplémentaire est disponible sur demande auprès de l’auteur : steven.ettles@phac-aspc.gc.ca.

Cette œuvre est mise à disposition selon les termes de la Licence Creative Commons Attribution 4.0 International