Rapport coût/efficacité des stratégies de vaccination contre le VRS chez les âgées canadiennes

 Téléchargez cet article en format PDF (266 ko)
Téléchargez cet article en format PDF (266 ko)Publié par : L'Agence de la santé publique du Canada
Numéro : RMTC : Volume 51-2/3, février/mars 2025 : Économie de la santé en santé publique
Date de publication : février 2025
ISSN : 1719-3109
Soumettre un article
À propos du RMTC
Naviguer
Volume 51-2/3, février/mars 2025 : Économie de la santé en santé publique
Économie de la santé
Rapport coût/efficacité des stratégies de vaccination contre le virus respiratoire syncytial chez les personnes âgées canadiennes : une comparaison multimodèles
Monica Rudd1,2, Alison E Simmons1,2, Gebremedhin B Gebretekle1, Ashleigh R Tuite1,2
Affiliations
1 Centre pour les programmes d'immunisation, Agence de la santé publique du Canada, Ottawa, ON
2 École de santé publique Dalla Lana, Université de Toronto, Toronto, ON
Correspondance
Citation proposée
Rudd M, Simmons AE, Gebretekle GB, Tuite AR. Rapport coût/efficacité des stratégies de vaccination contre le virus respiratoire syncytial chez les personnes âgées canadiennes : une comparaison multimodèles. Relevé des maladies transmissibles au Canada 2025;51(2/3):61−75. https://doi.org/10.14745/ccdr.v51i23a01f
Mots-clés : virus respiratoire syncytial, vaccination, analyse coût/utilité, économie de la santé, modélisation
Résumé
Contexte : Deux vaccins contre le virus respiratoire syncytial (VRS) sont actuellement autorisés au Canada pour les adultes de 60 ans et plus.
Objectif : Effectuer une comparaison multimodèles afin d'explorer l'incidence d'autres hypothèses structurelles et méthodologiques sur l'estimation du rapport coût/efficacité des programmes de vaccination des adultes contre le VRS.
Méthodes : Nous avons comparé trois modèles statiques coût/utilité mis au point par l'Agence de la santé publique du Canada, GSK et Pfizer à l'aide d'un ensemble commun de paramètres d'entrée. Chaque modèle a évalué les rapports coût/efficacité différentiels séquentiels en dollars canadiens de 2023 par année de vie ajustée par la qualité (AVAQ) pour un ensemble de politiques de substitution, l'admissibilité au vaccin étant déterminée par des combinaisons d'âge et de statut de maladie chronique. Les résultats ont été calculés pour chaque vaccin séparément dans le cadre de scénarios prévoyant une protection vaccinale de deux ou trois ans, en utilisant la perspective du système de santé et un taux d'actualisation annuel de 1,5 %.
Résultats : Les trois modèles coût/utilité ont été globalement concordants pour l'ensemble des scénarios modélisés. Dans tous les scénarios, l'accent a été mis sur la vaccination des personnes présentant une AMC plutôt que sur des politiques plus larges basées sur l'âge. La vaccination contre le virus respiratoire syncytial pour les personnes de plus de 70 ans présentant une maladie chronique a été le plus souvent identifiée comme la politique optimale en utilisant un seuil de coût/efficacité de 50 000 $/AVAQ. Si l'on considère uniquement les politiques fondées sur des critères d'âge, la vaccination des personnes de plus de 80 ans est rentable à ce seuil.
Conclusion : Une comparaison multimodèles des modèles canadiens de coût/utilité montre que les programmes de vaccination contre le VRS sont susceptibles d'être rentables pour certains groupes d'adultes plus âgés au Canada. Ces résultats sont cohérents d'un modèle à l'autre, malgré les différences de structure du modèle.
Introduction
Le virus respiratoire syncytial (VRS) est l'une des principales causes d'infections respiratoires au Canada, un fardeau de la maladie important chez les jeunes enfants et les personnes âgées Note de bas de page 1. Le virus respiratoire syncytial était à l'origine d'environ 4,8 % des hospitalisations pour infections respiratoires aiguës chez les adultes canadiens de plus de 50 ans entre 2012 et 2015 Note de bas de page 2. Les taux de mortalité hospitalière augmentent avec l'âge et chez les personnes souffrant d'affections médicales chroniques Note de bas de page 2Note de bas de page 3Note de bas de page 4.
Avec l'autorisation récente de deux vaccins pour les adultes de plus de 60 ans au Canada, les décideurs politiques évaluent l'utilisation de ces produits dans cette population, et notamment s'il convient de recommander des programmes de vaccination financés par l'État Note de bas de page 5. Les considérations économiques sont un élément important de ces processus de décision.
Nous avons récemment effectué une analyse du rapport coût/efficacité de diverses options de programmes de vaccination pour les personnes âgées au Canada Note de bas de page 6, afin d'orienter les prochaines recommandations du Comité consultatif national de l'immunisation (CCNI) sur l'utilisation des vaccins contre le VRS chez les personnes âgées. Cette analyse a montré que la vaccination des personnes âgées peut être rentable, en fonction de la conception du programme. Nous avons notamment montré que les programmes axés sur la vaccination des personnes souffrant d'une maladie chronique les exposant à un risque accru de VRS devraient présenter une meilleure rentabilité que les programmes plus généraux basés sur l'âge.
Si les évaluations économiques basées sur des modèles peuvent fournir des renseignements utiles aux décideurs, il est important d'étudier l'incidence de l'incertitude sur les résultats, afin d'éviter de prendre des décisions sous-optimales. Des analyses de sensibilité peuvent être effectuées pour tester l'incertitude due aux entrées du modèle et aux hypothèses des paramètres. Bien que les modifications des hypothèses relatives à la structure du modèle puissent être évaluées dans le cadre d'analyses de scénarios, ces analyses peuvent s'avérer complexes. Les études comparatives multimodèles peuvent être utilisées pour traiter l'incertitude due à la structure du modèle et à la méthodologie Note de bas de page 7Note de bas de page 8, et sont recommandées dans les lignes directrices du CCNI pour les évaluations économiques Note de bas de page 9. En comparant les résultats de modèles économiques mis au point de manière indépendante avec des paramètres d'entrée normalisés, les chercheurs sont en mesure d'évaluer dans quelle mesure les résultats dérivés des modèles sont fiables face aux différences dans la formulation mathématique des modèles et les choix méthodologiques, offrant ainsi une plus grande confiance dans l'évaluation de ces données probantes.
Nous avons effectué une comparaison multimodèles de trois modèles économiques coût/utilité, afin d'évaluer la fiabilité des résultats concernant le rapport coût/efficacité des options du programme de vaccination contre le VRS chez les personnes âgées au Canada par rapport à la variation des hypothèses et de la structure du modèle.
Méthodes
Sélection du modèle
La comparaison multimodèles a été réalisée pour soutenir le CCNI et faisait partie d'un ensemble de données économiques prises en compte lors de l'élaboration des recommandations relatives à l'utilisation des vaccins contre le VRS chez les adultes canadiens. Outre le modèle élaboré par l'Agence de la santé publique du Canada (l'Agence) Note de bas de page 6, nous avons axé nos efforts sur les modèles des fabricants dont le produit a été approuvé pour utilisation chez les adultes canadiens de plus de 60 ans pour la saison 2024–2025 du VRS (Arexvy [GSK] et Abrysvo [Pfizer]). GSK et Pfizer ont fourni leurs modèles, qui ont été mis au point à l'aide de Microsoft Excel Note de bas de page 10. Le nouveau paramétrage du modèle et les nouvelles analyses ont été effectués par notre équipe.
Cadre d'économie de la santé
Nous avons évalué tous les modèles dans une population de 100 000 adultes canadiens de plus de 50 ans. Bien que les vaccins actuels contre le VRS aient été autorisés pour la population de 60 ans et plus au moment de l'analyse, nous avons inclus certaines stratégies de vaccination qui prenaient en compte une limite d'âge inférieure de 50 ans, une indication d'âge inférieur étant actuellement à l'étude Note de bas de page 11. La population a été répartie par groupe d'âge Note de bas de page 12 et selon un haut risque ou un risque moyen en fonction de la présence ou de l'absence de maladie chronique les exposant à un risque accru de VRS Note de bas de page 13. Les résultats d'intérêt estimés par le modèle comprenaient le nombre de consultations externes, de visites aux urgences, d'hospitalisations, de décès et d'événements indésirables attribuables au VRS après la vaccination, les pertes d'années de vie ajustées par la qualité (AVAQ), les coûts de la vaccination et les coûts des soins de santé. Nous avons calculé les coûts de vaccination attendus, les coûts médicaux imputables au VRS et les pertes d'AVAQ pour une série de programmes de vaccination possibles. Nous avons évalué l'incidence des programmes de vaccination utilisant Arexvy ou Abrysvo, pour un horizon politique de deux à trois ans, en fonction de la durée supposée de la protection vaccinale. Tous les modèles ont débuté en septembre de la première année, afin de couvrir le début attendu de la saison typique du VRS (avant la pandémie de SRAS-CoV-2), la vaccination ayant lieu au début de la première saison. Les pertes d'AVAQ sur la durée de vie ont été calculées dans le cas de la mortalité due au VRS. Tous les coûts et les pertes d'AVAQ ont été actualisés à un taux de 1,5 % par an Note de bas de page 9. Les coûts et les AVAQ ont été utilisés pour calculer les rapports coût/efficacité différentiels (RCED) séquentiels pour toutes les options stratégiques envisagées. Cette analyse a pris en compte la perspective du système de santé uniquement.
Aperçu des modèles et normalisation
Chaque modèle coût/utilité présentait des caractéristiques uniques nous obligeant à adapter les hypothèses d'entrée pour les rendre directement comparables, comme décrit ci-dessous. Le tableau 1 donne un aperçu des principales caractéristiques des modèles de l'Agence, de GSK et de Pfizer.
| Attribut du modèle | ASPC | GSK | Pfizer |
|---|---|---|---|
| Dynamique | Statique | Statique | Statique |
| Agrégation | Individuel | Cohorte | Cohorte |
| Groupes d'âges (années) | 50 à 59, 60 à 64, 65 à 69, 70 à 74, 75 à 79, 80 et plus | 50 à 59, 60 à 64, 65 à 69, 70 à 74, 75 à 79, 80 et plus | 18 à 49Note de bas de page a, 50 à 59, 60 à 69, 70 à 79, 80 et plus |
| Strates de risque | Deux strates représentant les personnes présentant ou non une affection chronique | Strates non explicitement modélisées. Les adultes à risque moyen et à haut risque ont été modélisés en cohortes distinctes | Deux ou trois strates de risque, permettant aux personnes de passer à des strates de risque plus élevé au fur et à mesure qu'elles vieillissent |
| Résultats liés au VRS | Consultation externe, visite aux urgences, hospitalisation, soins intensifs | VRS-IVRS (consultation externe ou visite aux urgences), VRS-IVRI (hospitalisation) | Non médicalement pris en charge, consultation externe, visite aux urgences, hospitalisation |
| Caractère saisonnier | Répartition mensuelle des cas annuels | « Facteur de saisonnalité » multipliant le nombre de cas mensuels attendus | Répartition mensuelle des cas annuels |
| EV | EV distincts pour l'hospitalisation et la consultation externe. Déclin sur 36 mois modélisé à l'aide d'un modèle de régression polynomiale cubique | EV distincts pour le VRS-IVRS et le VRS-IVRI. Efficacité du premier mois réduite de moitié. Déclin linéaire entre les mois 1 à 7, 7 à 18, 18 et plus | Quatre courbes d'EV pour l'hospitalisation, la visite aux urgences, la consultation externe et le VRS non médicalement pris en charge. Décroissance linéaire entre les mois 0 à 3, 3 à 6, 6 à 12, 12 à 18, 18 à 24, 24 à 36 |
| ESSI | Local et systémique | Local et systémique | Non modélisé |
| Calendrier de vaccination | Septembre et octobre 2024 | 1er octobre 2024 | Septembre et octobre 2024 |
| Horizon de temps | Trois ans. L'EV de la troisième année dans le scénario à deux ans est supposée être nulle | N'importe quel nombre entier | N'importe quel nombre entier, mais l'horizon de la vie entière doit être utilisé pour saisir les pertes d'AVAQ dues à la mortalité provenant du VRS |
Note de bas de tableau 1
Abréviations : ASPC, Agence de la santé publique du Canada; AVAQ, année de vie ajustée par la qualité; ESSI, effets secondaires suivant l'immunisation; EV, efficacité du vaccin; IVRI, infection des voies respiratoires inférieures; IVRS, infection des voies respiratoires supérieures; VRS, virus respiratoire syncytial
|
|||
Modèle de l'Agence de la santé publique du Canada
Le modèle de l'Agence est un modèle statique basé sur l'individu avec cinq groupes d'âge et deux strates de risque. Il inclut les résultats suivants concernant le VRS : consultations externes, visites aux urgences, hospitalisation sans unité de soins intensifs (USI), hospitalisation avec USI et décès Note de bas de page 6. Les hospitalisations sans USI et les hospitalisations avec USI ont été regroupées pour simplifier l'hospitalisation et permettre la comparaison avec d'autres modèles. On suppose que les ESSI sont proportionnels à l'ensemble des vaccins administrés. Le modèle inclut des pertes d'AVAQ sur toute la durée de vie pour la mortalité due au VRS et utilise un horizon de politique fixe de trois ans.
Modèle de Pfizer
Le modèle de Pfizer est un modèle de cohorte statique avec cinq groupes d'âge et deux ou trois strates de risque. La structure du modèle a été décrite précédemment Note de bas de page 14 et les données d'entrée du modèle ont été adaptées au contexte canadien. Comme il y a moins de groupes d'âge dans ce modèle que dans les politiques de substitution envisagées (décrites ci-dessous), nous avons fusionné certains groupes d'âge, en utilisant des moyennes pondérées en fonction de la population lorsque les hypothèses d'entrée différaient entre les groupes d'âge fusionnés.
Le modèle inclut les coûts et les pertes d'AVAQ pour les cas non médicalement pris en charge, les consultations externes, les visites aux urgences, les hospitalisations et les décès. Par souci de cohérence avec le modèle de l'Agence, nous avons exclu les coûts et les pertes d'AVAQ associés aux cas non médicalement pris en charge. Les effets secondaires suivant l'immunisation ne sont pas explicitement pris en compte dans ce modèle. Nous avons ajouté le coût attendu du traitement de ces effets (0,67 $ par personne vaccinée) au coût d'administration du vaccin, mais nous n'avons pas été en mesure d'intégrer les pertes d'AVAQ attendues. Bien que le modèle présente un horizon temporel spécifié par l'utilisateur, un horizon temporel à vie est nécessaire pour comptabiliser pleinement les pertes d'AVAQ dues à la mortalité par le VRS. Enfin, contrairement aux autres modèles, le modèle Pfizer suppose que les paramètres spécifiques à l'âge sont linéaires par morceaux entre les groupes d'âge par incréments d'un an, comme l'illustre la figure 1.
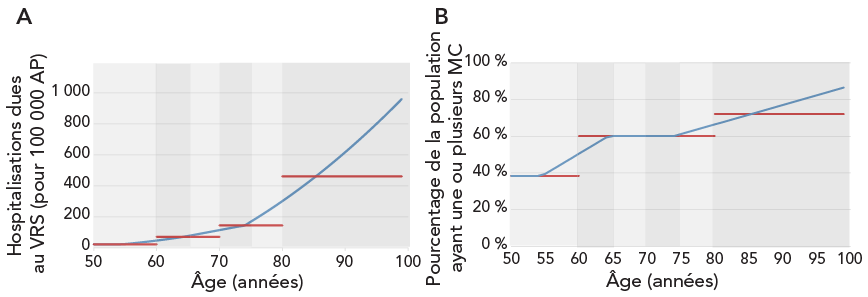
Figure 1 : Équivalent textuel
| Âge (années) |
Hospitalisations dues au VRS (pour 100 000 années-personnes) |
|
|---|---|---|
| ASPC | Pfizer | |
| 50 | 22,65 | 22,65 |
| 51 | 22,65 | 22,65 |
| 52 | 22,65 | 22,65 |
| 53 | 22,65 | 22,65 |
| 54 | 22,65 | 22,65 |
| 55 | 22,65 | 24,40 |
| 56 | 22,65 | 28,36 |
| 57 | 22,65 | 32,57 |
| 58 | 22,65 | 37,04 |
| 59 | 22,65 | 41,75 |
| 60 | 71,25 | 46,72 |
| 61 | 71,25 | 51,94 |
| 62 | 71,25 | 57,42 |
| 63 | 71,25 | 63,14 |
| 64 | 71,25 | 69,12 |
| 65 | 71,25 | 76,22 |
| 66 | 71,25 | 83,82 |
| 67 | 71,25 | 91,43 |
| 68 | 71,25 | 99,03 |
| 69 | 71,25 | 106,63 |
| 70 | 144,6 | 114,23 |
| 71 | 144,6 | 121,83 |
| 72 | 144,6 | 129,44 |
| 73 | 144,6 | 137,04 |
| 74 | 144,6 | 144,73 |
| 75 | 144,6 | 169,09 |
| 76 | 144,6 | 194,14 |
| 77 | 144,6 | 219,87 |
| 78 | 144,6 | 246,30 |
| 79 | 144,6 | 273,41 |
| 80 | 461,1 | 301,21 |
| 81 | 461,1 | 329,70 |
| 82 | 461,1 | 358,88 |
| 83 | 461,1 | 388,74 |
| 84 | 461,1 | 419,29 |
| 85 | 461,1 | 450,53 |
| 86 | 461,1 | 482,46 |
| 87 | 461,1 | 515,08 |
| 88 | 461,1 | 548,38 |
| 89 | 461,1 | 582,37 |
| 90 | 461,1 | 617,05 |
| 91 | 461,1 | 652,42 |
| 92 | 461,1 | 688,48 |
| 93 | 461,1 | 725,22 |
| 94 | 461,1 | 762,65 |
| 95 | 461,1 | 800,77 |
| 96 | 461,1 | 839,58 |
| 97 | 461,1 | 879,07 |
| 98 | 461,1 | 919,26 |
| 99 | 461,1 | 960,13 |
| Âge (années) |
Pourcentage de la population ayant une ou plusieurs MC | |
|---|---|---|
| ASPC | Pfizer | |
| 50 | 38,4 % | 38,4 % |
| 51 | 38,4 % | 38,4 % |
| 52 | 38,4 % | 38,4 % |
| 53 | 38,4 % | 38,4 % |
| 54 | 38,4 % | 38,4 % |
| 55 | 38,4 % | 39,4 % |
| 56 | 38,4 % | 41,6 % |
| 57 | 38,4 % | 43,8 % |
| 58 | 38,4 % | 46,1 % |
| 59 | 38,4 % | 48,3 % |
| 60 | 60,1 % | 50,5 % |
| 61 | 60,1 % | 52,7 % |
| 62 | 60,1 % | 54,9 % |
| 63 | 60,1 % | 57,1 % |
| 64 | 60,1 % | 59,3 % |
| 65 | 60,1 % | 60,1 % |
| 66 | 60,1 % | 60,1 % |
| 67 | 60,1 % | 60,1 % |
| 68 | 60,1 % | 60,1 % |
| 69 | 60,1 % | 60,1 % |
| 70 | 60,1 % | 60,1 % |
| 71 | 60,1 % | 60,1 % |
| 72 | 60,1 % | 60,1 % |
| 73 | 60,1 % | 60,1 % |
| 74 | 60,1 % | 60,1 % |
| 75 | 60,1 % | 61,2 % |
| 76 | 60,1 % | 62,2 % |
| 77 | 60,1 % | 63,3 % |
| 78 | 60,1 % | 64,3 % |
| 79 | 60,1 % | 65,4 % |
| 80 | 72,1 % | 66,5 % |
| 81 | 72,1 % | 67,5 % |
| 82 | 72,1 % | 68,6 % |
| 83 | 72,1 % | 69,6 % |
| 84 | 72,1 % | 70,7 % |
| 85 | 72,1 % | 71,7 % |
| 86 | 72,1 % | 72,8 % |
| 87 | 72,1 % | 73,9 % |
| 88 | 72,1 % | 74,9 % |
| 89 | 72,1 % | 76,0 % |
| 90 | 72,1 % | 77,0 % |
| 91 | 72,1 % | 78,1 % |
| 92 | 72,1 % | 79,2 % |
| 93 | 72,1 % | 80,2 % |
| 94 | 72,1 % | 81,3 % |
| 95 | 72,1 % | 82,3 % |
| 96 | 72,1 % | 83,4 % |
| 97 | 72,1 % | 84,4 % |
| 98 | 72,1 % | 85,5 % |
| 99 | 72,1 % | 86,6 % |
Abréviation : ASPC, Agence de la santé publique du Canada
Notes de bas de page figure 1
Abréviations : ASPC, Agence de la santé publique du Canada; AVAQ, année de vie ajustée par la qualité; ESSI, effets secondaires suivant l’immunisation; EV, efficacité du vaccin; IVRI, infection des voies respiratoires inférieures; IVRS, infection des voies respiratoires supérieures; VRS, virus respiratoire syncytial
- Figure 1 note de bas de page a
-
Les données de linéarité par morceaux de Pfizer sont indiquées en bleu et les données d'uniformité de l'Agence de la santé publique du Canada et de GSK sont indiquées en rouge
- Figure 1 note de bas de page b
-
Les résultats sont présentés pour A) l'incidence des hospitalisations associées au VRS pour 100 000 années-personnes et B) la prévalence des affections médicales chroniques
Modèle de GSK
Le modèle de GSK est un modèle de cohorte statique comprenant jusqu'à sept groupes d'âge. La structure du modèle a été décrite précédemment Note de bas de page 14Note de bas de page 15 et les paramètres d'entrée du modèle ont été adaptés à la population canadienne. Toutes les personnes de chaque groupe d'âge sont supposées avoir l'âge le plus bas. Par conséquent, nous avons échelonné les groupes d'âge pour commencer au milieu des tranches d'âge souhaitées, afin que les groupes d'âge aient le même âge moyen et les mêmes années de vie perdues dans le cas de la mortalité par le VRS. Le modèle ne modélise pas explicitement les strates de risque, mais en traitant les personnes à haut risque et à risque faible en cohortes distinctes, nous avons obtenu le même effet. Comme dans les autres modèles, les pertes d'AVAQ sur toute la durée de vie sont prises en compte pour la mortalité due au VRS, mais l'utilisateur peut choisir un horizon temporel de deux ou trois ans.
Plutôt que de modéliser l'efficacité du vaccin (EV) comme une protection directe contre les résultats de l'utilisation du système de santé, tels que les consultations externes et les hospitalisations, le modèle original suppose que toutes les infections respiratoires aiguës à VRS (VRS-IRA) conduisent à une infection des voies respiratoires supérieures (VRS-IVRS) ou à une infection des voies respiratoires inférieures (VRS-IVRI). Des niveaux différents d'utilisation des ressources de santé sont alors supposés, selon qu'une personne est atteinte du VRS-IVRS ou du VRS-IVRI. Nous avons modifié cette formulation en modélisant le VRS-IVRI comme équivalent au VRS nécessitant une hospitalisation, et le VRS-IVRS comme entraînant des consultations externes ou des visites aux urgences, avec des probabilités proportionnelles au nombre de cas de chaque issue, stratifié selon l'âge et le risque, estimé dans le modèle de l'Agence.
La vaccination dans le modèle GSK confère deux niveaux de protection : contre le VRS-IVRI et contre tous les VRS-IRA. Dans le modèle original, l'EV contre le VRS-IRA et le VRS-IVRI était basée sur les résultats des essais cliniques et l'EV pour le VRS-IVRS était calculée sur la base des deux autres données d'entrée de l'EV. Pour cette analyse, nous avons calculé les profils de décroissance du VRS-IRA pour chaque strate d'âge à risque, de telle sorte que l'EV contre le VRS-IVRS qui en résulte corresponde aux hypothèses d'EV contre les consultations externes et les visites aux urgences dans les autres modèles.
Paramètres d'entrée
Les paramètres d'entrée communs ont été basés sur ceux utilisés dans l'analyse coût/utilité de l'Agence, qui a préféré les données canadiennes lorsqu'elles étaient disponibles et, dans le cas contraire, les données provenant d'autres administrations ou des avis d'experts Note de bas de page 6. Une description complète des paramètres d'entrée utilisés est publiée séparément Note de bas de page 6, et les valeurs utilisées dans la présente analyse sont fournies dans le tableau A1 (voir l'appendice) à titre de référence. Certains paramètres clés sont décrits ci-dessous.
Les proportions par âge des personnes présentant une ou plusieurs maladies chroniques ont été basées sur les estimations de la prévalence au Canada des maladies pulmonaires obstructives chroniques, de l'obésité (indice de masse corporelle autodéclaré supérieur ou égal à 30 kg/m3), de l'hypertension artérielle, du cancer, des maladies cardiaques et des séquelles d'un accident vasculaire cérébral, du diabète ou de la démence Note de bas de page 13. On a supposé que la couverture vaccinale suivait l'administration du vaccin antigrippal Note de bas de page 16. Les coûts de vaccination comprenaient les frais d'administration et le prix de la liste publique canadienne de 230 $ par dose pour les deux vaccins. On a supposé que l'efficacité du vaccin contre le VRS nécessitant une consultation externe ou une hospitalisation était égale à l'efficacité publiée contre les infections légères et graves à VRS, et qu'elle diminuait sur une période de deux ou trois ans, les estimations pour la période de trois ans étant basées sur l'extrapolation des données existantes, qui étaient limitées à deux saisons de VRS au moment de l'analyse Note de bas de page 17Note de bas de page 18Note de bas de page 19. L'incidence par âge des hospitalisations associées au VRS a été estimée sur la base des résultats d'études canadiennes Note de bas de page 2, avec un facteur de sous-détection des cas supposé de 1,5 fois Note de bas de page 4. Les infections par le virus respiratoire syncytial ont été considérées comme saisonnières, la plupart des cas survenant entre janvier et mars Note de bas de page 20. Le cas échéant, en raison des hypothèses structurelles des modèles, nous avons adapté les paramètres d'entrée pour qu'ils aient des effets équivalents d'un modèle à l'autre, mais la logique sous-jacente des modèles n'a pas été modifiée.
Comparaison des modèles
Comme décrit ci-dessus, nous avons modélisé séparément l'utilisation des vaccins Abrysvo (Pfizer) ou Arexvy (GSK) en supposant une durée de protection de deux ou trois ans après la vaccination, l'EV étant supposée s'estomper au cours de la période concernée. Outre l'absence de vaccination, nous avons évalué 19 politiques de substitution en utilisant différentes combinaisons de critères d'admissibilité en matière d'âge et de comorbidité pour chaque scénario Note de bas de page 6 :
- Politiques basées sur l'âge : tous les adultes de plus de 60, 65, 70, 75 ou 80 ans ont été considérés comme admissibles
- Politiques basées sur le risque médical : tous les adultes de plus de 60, 65, 70, 75 ou 80 ans et présentant une ou plusieurs maladies chroniques ont été considérés comme admissibles
- Politiques basées sur l'âge et le risque médical : tous les adultes dépassant un seuil d'âge général, ainsi que les adultes présentant une maladie chronique dépassant une fourchette de seuils d'âge inférieurs (50 ou 60 ans) ont été considérés comme admissibles
Bien que les trois modèles utilisent un horizon à vie pour les pertes d'AVAQ dues à la mortalité par le VRS, chacun d'entre eux présente des horizons politiques différents pour évaluer l'incidence des programmes de vaccination. Puisque l'EV est supposée être limitée (i.e., qu'un maximum de trois ans a été pris en compte dans cette analyse), ces différents horizons n'ont pas eu d'incidence sur les comparaisons des RCED. Dans les comparaisons graphiques des frontières coût/efficacité, nous avons utilisé les coûts nets du programme et les effets par rapport à l'absence de vaccination pour tenir compte des différences dans les horizons temporels des modèles.
Résultats
La figure 2 présente une comparaison des frontières coût/efficacité pour les trois modèles utilisant des hypothèses d'EV pour Abrysvo (Pfizer) et Arexvy (GSK) dans les scénarios de décroissance à deux ans et à trois ans. Les trois modèles ont été globalement concordants dans les quatre scénarios. Les modèles de l'Agence et de GSK ont défini les mêmes politiques de substitution comme potentiellement rentables, la politique optimale dépendant du seuil de coût/efficacité. Le modèle de Pfizer présente des résultats globaux comparables, mais définit une politique supplémentaire, la vaccination des personnes à haut risque de plus de 65 ans, comme une option potentiellement rentable. Cette politique a toujours fait l'objet d'une dominance étendue (i.e., qu'elle n'est pas rentable quel que soit le seuil de coût/efficacité) dans les modèles de l'Agence et de GSK. Pour tous les modèles, toutes les politiques définies comme potentiellement rentables étaient basées sur le risque ou basées sur l'âge et le risque. Les stratégies basées sur l'âge n'ont jamais été définies comme des options rentables. Nous avons constaté qu'une politique de vaccination des personnes à haut risque de 80 ans et plus dominait une politique d'absence de vaccination dans tous les modèles utilisant l'EV supposée de l'un ou l'autre vaccin.
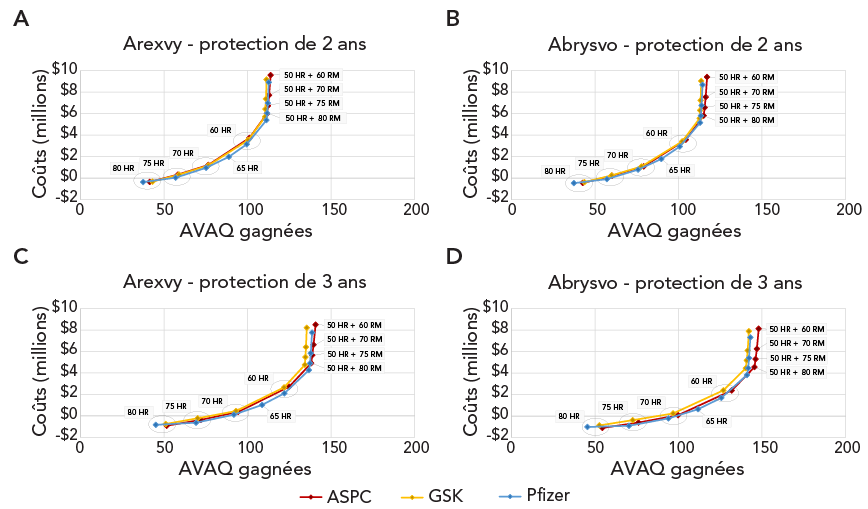
Figure 2 : Équivalent textuel
| Politique | ASPC | GSK | Pfizer | |||
|---|---|---|---|---|---|---|
| AVAQ gagnées | Coûts (millions de dollars) |
AVAQ gagnées | Coûts (millions de dollars) |
AVAQ gagnées | Coûts (millions de dollars) |
|
| 80 HR | 42,65 | −0,45 | 43,68 | −0,39 | 37,38 | −0,47 |
| 75 HR | 60,19 | 0,21 | 59,97 | 0,25 | 57,13 | −0,10 |
| 70 HR | 79,15 | 1,09 | 77,83 | 1,07 | 75,81 | 0,78 |
| 65 HR | Dominance élargie | Dominance élargie | Dominance élargie | Dominance élargie | 89,73 | 1,78 |
| 60 HR | 104,37 | 3,57 | 102,21 | 3,41 | 100,75 | 2,93 |
| 80 RM – 50 HR | 115,09 | 5,82 | 112,65 | 5,57 | 112,89 | 5,15 |
| 75 RM – 50 HR | 115,62 | 6,57 | 112,92 | 6,30 | 113,40 | 5,80 |
| 70 RM – 50 HR | 116,26 | 7,54 | 113,20 | 7,24 | 113,76 | 6,75 |
| 60 RM – 50 HR | 117,10 | 9,41 | 113,57 | 9,04 | 114,34 | 8,67 |
| Politique | ASPC | GSK | Pfizer | |||
|---|---|---|---|---|---|---|
| AVAQ gagnées | Coûts (millions de dollars) |
AVAQ gagnées | Coûts (millions de dollars) |
AVAQ gagnées | Coûts (millions de dollars) |
|
| 80 HR | 41,36 | −0,37 | 43,09 | −0,33 | 37,51 | −0,37 |
| 75 HR | 58,31 | 0,32 | 59,00 | 0,33 | 56,93 | 0,04 |
| 70 HR | 76,56 | 1,23 | 76,45 | 1,17 | 75,17 | 0,96 |
| 65 HR | Dominance élargie | Dominance élargie | Dominance élargie | Dominance élargie | 88,74 | 1,99 |
| 60 HR | 101,10 | 3,74 | 100,26 | 3,53 | 99,48 | 3,15 |
| 80 RM – 50 HR | 111,60 | 5,99 | 110,44 | 5,70 | 111,28 | 5,39 |
| 75 RM – 50 HR | 112,18 | 6,74 | 110,70 | 6,43 | 111,77 | 6,03 |
| 70 RM – 50 HR | 112,86 | 7,71 | 110,98 | 7,37 | 112,10 | 6,99 |
| 60 RM – 50 HR | 113,79 | 9,58 | 111,33 | 9,17 | 112,66 | 8,91 |
| Politique | ASPC | GSK | Pfizer | |||
|---|---|---|---|---|---|---|
| AVAQ gagnées | Coûts (millions de dollars) |
AVAQ gagnées | Coûts (millions de dollars) |
AVAQ gagnées | Coûts (millions de dollars) |
|
| 80 HR | 54,46 | −1,11 | 52,62 | −0,88 | 45,45 | −1,02 |
| 75 HR | 76,05 | −0,61 | 72,62 | −0,38 | 70,33 | −0,90 |
| 70 HR | 99,70 | 0,07 | 96,74 | 0,24 | 93,99 | −0,23 |
| 65 HR | Dominance élargie | Dominance élargie | Dominance élargie | Dominance élargie | 111,68 | 0,64 |
| 60 HR | 131,77 | 2,37 | 126,83 | 2,39 | 125,64 | 1,69 |
| 80 RM – 50 HR | 145,50 | 4,55 | 140,32 | 4,46 | 141,03 | 3,82 |
| 75 RM – 50 HR | 146,16 | 5,30 | 140,81 | 5,18 | 141,74 | 4,46 |
| 70 RM – 50 HR | 146,91 | 6,27 | 141,40 | 6,11 | 142,21 | 5,41 |
| 60 RM – 50 HR | 147,99 | 8,13 | 142,11 | 7,90 | 143,01 | 7,32 |
| Politique | ASPC | GSK | Pfizer | |||
|---|---|---|---|---|---|---|
| AVAQ gagnées | Coûts (millions de dollars) |
AVAQ gagnées | Coûts (millions de dollars) |
AVAQ gagnées | Coûts (millions de dollars) |
|
| 80 HR | 51,52 | −0,92 | 51,00 | −0,76 | 45,06 | −0,84 |
| 75 HR | 71,96 | −0,37 | 70,14 | −0,23 | 69,14 | −0,64 |
| 70 HR | 94,39 | 0,36 | 93,04 | 0,44 | 91,81 | 0,10 |
| 65 HR | Dominance élargie | Dominance élargie | Dominance élargie | Dominance élargie | 108,72 | 1,01 |
| 60 HR | 124,81 | 2,72 | 121,84 | 2,65 | 122,08 | 2,10 |
| 80 RM – 50 HR | 138,03 | 4,91 | 134,29 | 4,75 | 136,73 | 4,26 |
| 75 RM – 50 HR | 138,72 | 5,66 | 134,60 | 5,48 | 137,39 | 4,89 |
| 70 RM – 50 HR | 139,51 | 6,63 | 134,97 | 6,42 | 137,83 | 5,84 |
| 60 RM – 50 HR | 140,69 | 8,49 | 135,41 | 8,22 | 138,58 | 7,76 |
Notes de bas de page figure 2
Abréviations : Abrysvo, vaccin contre le virus respiratoire syncytial fabriqué par Pfizer; Arexvy, vaccin contre le virus respiratoire syncytial fabriqué par GSK; ASPC, Agence de la santé publique du Canada; AVAQ, année de vie ajustée par la qualité; EV, efficacité du vaccin; HR; haut risque; RM, risque moyen
- Figure 2 note de bas de page a
-
Les résultats sont présentés pour les scénarios suivants : A) données d'EV d'Arexvy avec une protection décroissante sur 2 ans, B) données d'EV d'Abrysvo avec une protection décroissante sur 2 ans, C) données d'EV d'Arexvy avec une protection décroissante sur 3 ans et D) données d'EV d'Abrysvo avec une protection décroissante sur 3 ans. Les étiquettes indiquent la stratégie de vaccination. Par souci de clarté, seules les stratégies qui se situaient à la frontière du rapport coût/efficacité sont présentées. Toutes les autres stratégies ont été dominées ou exclues par une dominance élargie et n'étaient pas des options rentables, quel que soit le seuil de coût/efficacité utilisé. Les tableaux 2 et 3 présentent les rapports coût/efficacité différentiels pour les stratégies non dominantes. Comme décrit dans les méthodes, les coûts et les AVAQ gagnées sont présentés par rapport à l'absence de vaccination, afin de permettre une comparaison entre les modèles
Scénarios de protection vaccinale sur deux ans
Les RCED séquentiels pour toutes les politiques qui n'ont pas été dominées ou largement dominées dans le scénario de protection vaccinale sur deux ans sont présentés dans le tableau 2. Par rapport à la vaccination des personnes à haut risque de 80 ans et plus, les modèles de l'Agence et de GSK ont estimé des RCED séquentiels compris entre 38 029 $/AVAQ et 41 325 $/AVAQ pour une politique de vaccination des personnes à haut risque de plus de 75 ans, alors que le modèle de Pfizer présentait des RCED d'environ 20 000 $/AVAQ. À l'exception du modèle de Pfizer paramétré avec les estimations d'EV d'Arexvy, tous les RCED séquentiels pour la politique relative aux adultes à haut risque de 70 ans et plus étaient inférieurs au seuil de coût/efficacité couramment utilisé de 50 000 $/AVAQ par rapport à la vaccination des adultes à haut risque de 75 ans et plus. Le RCED séquentiel pour le modèle de Pfizer utilisant les estimations d'EV d'Arexvy n'était que légèrement supérieur à ce seuil, soit 50 388 $/AVAQ. Le modèle Pfizer est le seul à estimer qu'une politique de vaccination des personnes à haut risque de plus de 65 ans pourrait être une option rentable, avec des RCED séquentiels de 71 933 $/AVAQ à 75 457 $/AVAQ par rapport à une politique pour les adultes à haut risque de 70 ans et plus. Pour tous les modèles, le RCED séquentiel d'une politique de vaccination de toutes les personnes à haut risque de plus de 60 ans était d'environ 100 000 $/AVAQ par rapport à la vaccination des adultes à haut risque de 70 ans (modèles de l'Agence et de GSK) ou de 65 ans (modèle de Pfizer) et plus. Au-delà de ce seuil, les politiques les plus rentables étaient toutes celles qui consistaient à vacciner les personnes à haut risque de plus de 50 ans et les groupes d'âge de plus en plus bas de personnes sans maladie chronique. Les politiques strictement fondées sur l'âge n'ont jamais été considérées comme des options rentables, quel que soit le modèle utilisé.
| Politique | Arexvy | Abrysvo | ||||
|---|---|---|---|---|---|---|
| ASPC | GSK | Pfizer | ASPC | GSK | Pfizer | |
| 80 ans ou plus à HR | - | - | - | - | - | - |
| 75 ans ou plus à HR | 40 660 $ | 41 325 $ | 21 219 $ | 38 029 $ | 39 199 $ | 18 682 $ |
| 70 ans ou plus à HR | 49 502 $ | 48 068 $ | 50 388 $ | 46 157 $ | 45 591 $ | 47 309 $ |
| 65 ans ou plus à HR | Dominance élargie | 75 457 $ | Dominance élargie | 71 933 $ | ||
| 60 ans ou plus à HR | 102 356 $ | 99 485 $ | 108 641 $ | 98 583 $ | 96 188 $ | 104 544 $ |
| 80 ans et plus à RM et 50 ans et plus à HR | 214 052 $ | 212 578 $ | 189 414 $ | 209 131 $ | 206 540 $ | 182 774 $ |
| 75 ans et plus à RM et 50 ans et plus à HR | 1 317 114 $ | 2 865 566 $ | 1 329 263 $ | 1 421 826 $ | 2 784 588 $ | 1 265 781 $ |
| 70 ans et plus à RM et 50 ans et plus à HR | 1 421 897 $ | 3 391 567 $ | 2 829 476 $ | 1 519 503 $ | 3 298 674 $ | 2 703 549 $ |
| 60 ans et plus à RM et 50 ans et plus à HR | 2 013 359 $ | 5 059 381 $ | 3 449 849 $ | 2 235 963 $ | 4 920 460 $ | 3 286 184 $ |
Note de bas de tableau 2
Abréviations : Abrysvo, vaccin contre le virus respiratoire syncytial fabriqué par Pfizer; Arexvy, vaccin contre le virus respiratoire syncytial fabriqué par GSK; ASPC, Agence de la santé publique du Canada; HR; haut risque; RM, risque moyen; -, sans objet
|
||||||
Scénarios de protection vaccinale sur trois ans
Le tableau 3 présente les RCED séquentiels pour toutes les politiques qui n'ont pas été dominées ou largement dominées dans le cadre d'un scénario supposant que la protection vaccinale se prolonge jusqu'à la troisième saison. Comme on pouvait s'y attendre, les RCED pour ces scénarios étaient inférieurs à leurs équivalents dans les scénarios sur deux ans, en raison de la durée supposée plus longue de la protection vaccinale. Les RCED séquentiels pour une politique de vaccination des personnes à haut risque de plus de 70 ans se situaient entre 25 727 $/AVAQ et 32 907 $/AVAQ par rapport à la vaccination des adultes à haut risque de plus de 80 ans. Comme pour le scénario de protection vaccinale sur deux ans, seul le modèle de Pfizer a défini la vaccination des personnes à haut risque de plus de 65 ans comme une option rentable, avec des RCED séquentiels de 48 856 $/AVAQ à 53 647 $/AVAQ par rapport à une politique destinée aux adultes à haut risque de 70 ans et plus. La vaccination des personnes à haut risque de plus de 60 ans a donné lieu à des RCED compris entre 71 513 $/AVAQ et 81 335 $/AVAQ par rapport à la vaccination des adultes à haut risque de 70 ans (modèles de l'Agence et de GSK) ou de 65 ans et plus (Pfizer). À des seuils de coût/efficacité plus élevés, comme dans les scénarios de protection vaccinale sur deux ans, les politiques fondées sur l'âge et le risque, qui comprennent la vaccination des personnes à haut risque de plus de 50 ans et des groupes d'âge de plus en plus bas de personnes à risque moyen, ont été définies comme des options rentables. Les politiques fondées sur l'âge n'ont jamais été rentables par rapport à ces autres options.
| Politique | Arexvy | Abrysvo | ||||
|---|---|---|---|---|---|---|
| ASPC | GSK | Pfizer | ASPC | GSK | Pfizer | |
| 80 ans ou plus à HR | - | - | - | - | - | - |
| 75 ans ou plus à HR | 26 834 $ | 27 801 $ | 8 269 $ | 23 169 $ | 24 695 $ | 4 745 $ |
| 70 ans ou plus à HR | 32 907 $ | 29 320 $ | 32 736 $ | 28 814 $ | 25 727 $ | 28 557 $ |
| 65 ans ou plus à HR | Dominance élargie | 53 647 $ | Dominance élargie | 48 856 $ | ||
| 60 ans ou plus à HR | 77 338 $ | 76 430 $ | 81 335 $ | 71 776 $ | 71 513 $ | 75 674 $ |
| 80 ans et plus à RM et 50 ans et plus à HR | 165 771 $ | 169 258 $ | 147 249 $ | 158 601 $ | 153 336 $ | 138 356 $ |
| 75 ans et plus à RM et 50 ans et plus à HR | 1 090 178 $ | 2 350 773 $ | 975 340 $ | 1 135 141 $ | 1 461 416 $ | 905 774 $ |
| 70 ans et plus à RM et 50 ans et plus à HR | 1 219 926 $ | 2 534 807 $ | 2 132 683 $ | 1 290 424 $ | 1 560 714 $ | 1 984 098 $ |
| 60 ans et plus à RM et 50 ans et plus à HR | 1 588 568 $ | 4 112 609 $ | 2 577 733 $ | 1 717 449 $ | 2 547 744 $ | 2 394 941 $ |
Note de bas de tableau 3
Abréviations : Abrysvo, vaccin contre le virus respiratoire syncytial fabriqué par Pfizer; Arexvy, vaccin contre le virus respiratoire syncytial fabriqué par GSK; ASPC, Agence de la santé publique du Canada; HR; haut risque; RM, risque moyen; -, sans objet
|
||||||
Politiques fondées sur l'âge
Bien que les politiques fondées sur l'âge n'aient jamais été considérées comme rentables par rapport aux options fondées sur le risque ou sur l'âge et le risque, elles peuvent être préférées par certains décideurs sur la base d'autres considérations, telles que la réduction potentielle de la complexité de la mise en œuvre du programme. Nous avons donc effectué une sous-analyse des scénarios de protection vaccinale sur deux ans, en nous limitant aux politiques basées sur l'âge (tableau 4). Les RCED séquentiels pour une politique de vaccination de toutes les personnes de plus de 80 ans se situaient entre 3 161 $/AVAQ et 6 194 $/AVAQ par rapport à l'absence de vaccination. Il est peu probable que les politiques incluant des personnes plus jeunes soient considérées comme rentables à un seuil de coût/efficacité de 50 000 $/AVAQ. Les modèles de l'Agence et de GSK ont estimé les RCED entre 78 637 $/AVAQ et 85 805 $/AVAQ pour une politique de vaccination de toutes les personnes de plus de 75 ans par rapport à une politique pour toutes les personnes de plus de 80 ans. Toutefois, le modèle de Pfizer présente un RCED compris entre 50 090 $/AVAQ et 53 205 $/AVAQ dans ce scénario. Les politiques plus étendues fondées sur l'âge présentaient des RCED de plus en plus élevés et il était peu probable qu'elles soient considérées comme rentables aux seuils couramment utilisés.
| Politique | Arexvy | Abrysvo | ||||
|---|---|---|---|---|---|---|
| ASPC | GSK | Pfizer | ASPC | GSK | Pfizer | |
| Aucune vaccination | - | - | - | - | - | - |
| 80 ans et plus à RM et à HR | 5 391 $ | 6 194 $ | 5 883 $ | 3 261 $ | 4 838 $ | 3 161 $ |
| 75 ans et plus à RM et à HR | 82 326 $ | 85 805 $ | 53 205 $ | 78 637 $ | 82 607 $ | 50 090 $ |
| 70 ans et plus à RM et à HR | 99 045 $ | 100 332 $ | 100 829 $ | 94 264 $ | 96 651 $ | 96 496 $ |
| 65 ans et plus à RM et à HR | Dominance élargie | 136 241 $ | Dominance élargie | 131 165 $ | ||
| 60 ans et plus à RM et à HR | 172 061 $ | 172 531 $ | 201 336 $ | 167 226 $ | 167 515 $ | 194 749 $ |
Note de bas de tableau 3
Abréviations : Abrysvo, vaccin contre le virus respiratoire syncytial fabriqué par Pfizer; Arexvy, vaccin contre le virus respiratoire syncytial fabriqué par GSK; ASPC, Agence de la santé publique du Canada; HR; haut risque; RM, risque moyen; -, sans objet
|
||||||
Discussion
Notre comparaison de trois modèles canadiens de coût/utilité a montré que les programmes de vaccination contre le VRS pour les personnes âgées pourraient être une intervention rentable, en particulier lorsque ces programmes sont axés sur les groupes de population présentant le risque le plus élevé de VRS. Ces résultats sont globalement concordants entre les scénarios envisagés. Les politiques jugées optimales aux seuils de coût/efficacité couramment utilisés sont généralement cohérentes. De plus, les RCED estimés différaient peu entre les deux vaccins considérés.
En utilisant des paramètres d'entrée harmonisés, tous les modèles ont systématiquement défini les politiques basées sur le risque médical comme étant optimales par rapport aux politiques basées uniquement sur l'âge. Une différence entre les modèles concerne l'identification d'une politique de vaccination des adultes à haut risque de plus de 65 ans comme potentiellement rentable uniquement avec le modèle Pfizer. En utilisant les deux autres modèles, cette option politique a été largement dominée, d'autres options politiques offrant un meilleur rapport qualité-prix. Cette différence est probablement due à la façon dont les modèles utilisent les données variables en fonction de l'âge. Bien que l'hypothèse des modèles de l'Agence et de GSK de valeurs constantes pour chaque groupe d'âge soit plus proche des données de base, les hypothèses de gradient d'âge utilisées par le modèle de Pfizer pourraient être considérées comme plus réalistes par certains décideurs.
Bien que la majorité des autres évaluations économiques publiées à ce jour sur la vaccination contre le VRS chez les personnes âgées soient axées uniquement sur des stratégies basées sur l'âge, les tendances générales observées dans notre analyse peuvent être comparées à d'autres études. Une analyse systématique des évaluations économiques des vaccins contre le VRS chez les adultes, réalisée aux États-Unis et à Hong Kong, a montré que dans la plupart des études, les programmes de vaccination proposés à tous les adultes de 60 ou 65 ans et plus n'étaient probablement pas rentables si l'on utilise un seuil de 50 000 $/AVAQ, à moins d'une réduction substantielle du prix des vaccins Note de bas de page 21. Comme dans notre analyse, les études qui ont pris en compte plusieurs seuils d'âge pour les programmes de vaccination ont constaté que les RCED étaient plus faibles lorsque les programmes étaient plus restrictifs en ce qui concerne l'admissibilité à l'âge Note de bas de page 14Note de bas de page 22. Une récente évaluation économique canadienne a examiné les politiques de vaccination des résidents des maisons de soins de longue durée, seules ou parallèlement à la vaccination des adultes vivant en communauté en fonction de l'âge Note de bas de page 23. Cette étude a utilisé une analyse de seuil pour définir le prix maximum du vaccin à partir duquel la vaccination serait rentable pour un seuil de 50 000 $/AVAQ, et a constaté que des prix plus élevés étaient acceptables pour des stratégies de vaccination limitées aux résidents des maisons de soins de longue durée, où le risque de VRS est le plus élevé. Le prix maximum acceptable du vaccin a été réduit lorsque l'âge d'admissibilité des adultes vivant dans la communauté a été élargi à des âges plus jeunes Note de bas de page 23.
Cette analyse présente certaines limites qui doivent être prises en compte lors de l'interprétation de nos résultats. Tous les modèles inclus dans notre comparaison étaient statiques et ne prenaient pas en compte les effets indirects des programmes de vaccination. Par conséquent, ces modèles peuvent sous-estimer les économies potentielles en termes de coûts et d'AVAQ de ces programmes, ce qui conduit à considérer comme optimales des options politiques moins ambitieuses. Ensuite, aucune analyse d'une perspective sociétale n'a été effectuée et l'incidence possible de la vaccination pour la prévention du VRS non médicalement pris en charge n'a pas été prise en compte. Nos résultats pourraient sous-estimer les avantages des programmes de vaccination. Enfin, nous avons limité notre analyse à un petit nombre de scénarios et n'avons pas effectué d'analyses de sensibilité. Toutefois, étant donné la cohérence de nos résultats entre les modèles, la valeur d'une exploration plus approfondie de l'incidence de l'incertitude des paramètres est probablement faible pour cette analyse comparative.
Conclusion
La comparaison multimodèles montre que les programmes de vaccination contre le VRS sont probablement rentables pour certains sous-groupes d'adultes canadiens plus âgés, en particulier ceux dont les maladies chroniques les exposent à un risque accru de VRS. Ces résultats sont fiables par rapport aux autres hypothèses structurelles du modèle.
Déclaration des auteurs
- M. R. — Conceptualisation, analyse formelle, rédaction de la version originale
- A. E. S. — Conceptualisation, rédaction–révision et édition
- G. B. G. — Conceptualisation, rédaction–révision et édition
- A. R. T. — Conceptualisation, rédaction–révision et édition
Intérêts concurrents
Aucun.
Identifiants ORCID
- Monica Rudd – 0009-0001-9109-9872
- Alison E Simmons – 0000-0001-8780-9467
- Gebremedhin B Gebretekle – 0000-0002-2485-505X
- Ashleigh R Tuite – 0000-0002-4373-9337
Remerciements
Le modèle coût/utilité canadien de GSK pour les personnes âgées a été élaboré par Sydney George (GSK, Mississauga, Canada), Michael Dolph (Cytel, Toronto, Canada), Yufan Ho (GSK, Singapour), Dessi Loukov (GSK, Mississauga, Canada), Emily Matthews (Cytel, Toronto, Canada), Shreena Malaviya (Cytel, Toronto, Canada), Janine Xu (GSK, Mississauga, Canada) et Daniel Molnar (GSK, Wavre, Belgique). Le modèle coût/utilité canadien de Pfizer pour les adultes a été élaboré par Ahuva Averin (Avalere Health, Boston, États Unis [É.-U.]), Mark Atwood (Avalere Health, Boston, É.-U.), Derek Weycker (Avalere Health, Boston, É.-U.), Erin Quinn (Avalere Health, Boston, É.-U.), Alexandra Goyette (Pfizer Canada, Kirkland, Canada) et Reiko Sato (Pfizer, New York, É.-U.). Les auteurs remercient les membres du groupe de travail sur le VRS du Comité consultatif national de l'immunisation, qui ont donné leur rétroaction sur les paramètres du modèle.
Financement
Aucun.
Références
- Notes de bas de page 1
-
Wu M, Wu Q, Liu D, Zu W, Zhang D, Chen L. The global burden of lower respiratory infections attributable to respiratory syncytial virus in 204 countries and territories, 1990–2019: findings from the Global Burden of Disease Study 2019. Intern Emerg Med 2024;19(1):59–70. https://doi.org/10.1007/s11739-023-03438-x
- Notes de bas de page 2
-
ElSherif M, Andrew MK, Ye L, Ambrose A, Boivin G, Bowie W, David MP, Gruselle O, Halperin SA, Hatchette TF, Johnstone J, Katz K, Langley JM, Loeb M, MacKinnon-Cameron D, McCarthy A, McElhaney JE, McGeer A, Poirier A, Pirçon JY, Powis J, Richardson D, Semret M, Smith S, Smyth D, Trottier S, Valiquette L, Webster D, McNeil SA, LeBlanc JJ; Serious Outcomes Surveillance (SOS) Network of the Canadian Immunization Research Network (CIRN) and the Toronto Invasive Bacterial Diseases Network (TIBDN). Leveraging influenza virus surveillance From 2012 to 2015 to characterize the burden of respiratory syncytial virus disease in Canadian adults ≥50 years of age hospitalized with acute respiratory illness. Open Forum Infect Dis 2023;10(7):ofad315. https://doi.org/10.1093/ofid/ofad315
- Notes de bas de page 3
-
Mac S, Shi S, Millson B, Tehrani A, Eberg M, Myageri V, Langley JM, Simpson S. Burden of illness associated with Respiratory Syncytial Virus (RSV)-related hospitalizations among adults in Ontario, Canada: A retrospective population-based study. Vaccine 2023;41(35):5141–9. https://doi.org/10.1016/j.vaccine.2023.06.071
- Notes de bas de page 4
-
McLaughlin JM, Khan F, Begier E, Swerdlow DL, Jodar L, Falsey AR. Rates of medically attended RSV among US adults: a systematic review and meta-analysis. Open Forum Infect Dis 2022;9(7):ofac300. https://doi.org/10.1093/ofid/ofac300
- Notes de bas de page 5
-
Killikelly A, Shane A, Yeung MW, Tunis M, Bancej C, House A, Vaudry W, Moore D, Quach C. Analyse des lacunes visant à évaluer le niveau de préparation des Canadiens à l’introduction des vaccins contre le virus respiratoire syncytial : compte rendu d’une retraite d’experts. Relevé des maladies transmissibles au Canada 2020;46(4):71–8. https://doi.org/10.14745/ccdr.v46i04a02f
- Notes de bas de page 6
-
Tuite AR, Simmons AE, Rudd M, Cernat A, Gebretekle GB, Yeung MW, Killikelly A, Siu W, Bachan SA, Brousseau N, Tunis M. Respiratory syncytial virus vaccination strategies for older Canadian adults: a cost-utility analysis. medRxiv 2024;2024.03.20.24304630. https://doi.org/10.1101/2024.03.20.24304630
- Notes de bas de page 7
-
den Boon S, Jit M, Brisson M, Medley G, Beutels P, White R, Flasche S, Hollingsworth TD, Garske T, Pitzer VE, Hoogendoorn M, Geffen O, Clark A, Kim J, Hutubessy R. Guidelines for multi-model comparisons of the impact of infectious disease interventions. BMC Med 2019;17(1):163. https://doi.org/10.1186/s12916-019-1403-9
- Notes de bas de page 8
-
Drolet M, Bénard É, Jit M, Hutubessy R, Brisson M. Model comparisons of the effectiveness and cost-effectiveness of vaccination: A systematic review of the literature. Value Health 2018;21(10):1250–8. https://doi.org/10.1016/j.jval.2018.03.014
- Notes de bas de page 9
-
Agence de la santé publique du Canada. Comité consultatif national de l'immunisation (CCNI) : Lignes directrices pour l'évaluation économique des programmes de vaccination au Canada. Ottawa, ON: ASPC; 2023. https://www.canada.ca/fr/sante-publique/services/immunisation/comite-consultatif-national-immunisation-ccni/methodes-processus/integration-donnees-economiques-recommandations-federales-relatives-vaccins/lignes-directrices-evaluation-programmes-vaccination-canada.html
- Notes de bas de page 10
-
Microsoft Corporation. Microsoft Excel. 2018. https://www.microsoft.com/en-ca/microsoft-365/excel
- Notes de bas de page 11
-
Santé Canada. Présentations de médicaments et de produits de santé en cours d'examen (PCE) : Suppléments aux présentations en cours d'examen. Ottawa, ON : Santé Canada; 2024. [Consulté le 27 févr. 2024]. https://www.canada.ca/fr/sante-canada/services/examen-et-approbation-medicaments-et-produit-sante/presentations-cours-examen/supplements-presentations-cours-examen.html
- Notes de bas de page 12
-
Statistique Canada. Tableau 17-10-0057-01. Population projetée, selon le scénario de projection, l’âge et le genre, au 1er juillet (x 1 000). Ottawa, ON : StatCan; 2022. [Consulté le 5 janv. 2024]. https://www150.statcan.gc.ca/t1/tbl1/fr/tv.action?pid=1710005701&request_locale=fr
- Notes de bas de page 13
-
Statistique Canada. Tableau 13-10-0777-01. Nombre et pourcentage d'adultes (âgés de 18 ans et plus) de la population à domicile ayant des problèmes de santé sous-jacents, par âge et sexe (période de deux ans). Ottawa, ON : StatCan; 2020. https://www150.statcan.gc.ca/t1/tbl1/fr/tv.action?pid=1310077701&request_locale=fr
- Notes de bas de page 14
-
Ortega-Sanchez I. Economics of vaccinating U.S. adults ≥60 years-old against respiratory syncytial virus [slides presented at Advisory Committee on Immunization Practices (ACIP) meeting June 21, 2023]. Atlanta, GA: CDC; 2023. [Consulté le 27 févr. 2024]. https://www.cdc.gov/acip/downloads/slides-2023-06-21-23/05-RSV-Adults-Ortega-Sanchez-508.pdf
- Notes de bas de page 15
-
Molnar D, La EM, Verelst F, Poston S, Graham J, Van Bellinghen LA, Curran D. Public health impact of the adjuvanted RSVPreF3 vaccine for respiratory syncytial virus prevention among older adults in the United States. Infect Dis Ther 2024;13(4):827–44. https://doi.org/10.1007/s40121-024-00939-w
- Notes de bas de page 16
-
Agence de la santé publique du Canada. Enquête sur la couverture vaccinale contre la grippe saisonnière, 2022–2023. Rapport final. Ottawa, ON: ASPC; 2023. https://publications.gc.ca/collections/collection_2023/aspc-phac/H14-315-2023-fra.pdf
- Notes de bas de page 17
-
Friedland L. Manufacturer presentation: GSK season 2 safety & efficacy; coadministration with influenza vaccine [slides presented at Advisory Committee on Immunization Practices (ACIP) meeting June 21, 2023]. Atlanta, GA: CDC; 2023. [Consulté le 27 févr. 2024]. https://www.cdc.gov/acip/downloads/slides-2023-06-21-23/03-RSV-Adults-Friedland-508.pdf
- Notes de bas de page 18
-
Ison MG, Papi A, Athan E, Feldman RG, Langley JM, Lee DG, Leroux-Roels I, Martinon-Torres F, Schwarz TF, van Zyl-Smit RN, Verheust C, Dezutter N, Gruselle O, Fissette L, David MP, Kostanyan L, Hulstrøm V, Olivier A, Van der Wielen M, Descamps D; AReSVi-006 Study Group. AReSVi-006 Study Group. Efficacy and safety of respiratory syncytial virus (RSV) prefusion F protein vaccine (RSVPreF3 OA) in older adults over 2 RSV seasons. Clin Infect Dis 2024;78(6):1732–44. https://doi.org/10.1093/cid/ciae010
- Notes de bas de page 19
-
Gurtman A. Manufacturer presentation: Pfizer season 2 safety & efficacy; coadministration with influenza vaccine [slides presented at Advisory Committee on Immunization Practices (ACIP) meeting June 21, 2023]. Atlanta, GA: CDC; 2023. [Consulté le 27 févr. 2024]. https://www.cdc.gov/acip/downloads/slides-2023-06-21-23/02-RSV-Adults-Gurtman-508.pdf
- Notes de bas de page 20
-
Agence de la santé publique du Canada. Détection de virus des voies respiratoires au Canada. Ottawa, ON : ASPC; 2024. [Consulté le 27 févr. 2024]. https://www.canada.ca/fr/sante-publique/services/surveillance/detection-virus-voies-respiratoires-canada.html
- Notes de bas de page 21
-
Canadian Agency for Drugs and Technologies in Health. Cost-effectiveness of respiratory syncytial virus vaccines for adults: Technology review. Ottawa, ON : CADTH; 2024. https://pubmed.ncbi.nlm.nih.gov/38588351/
- Notes de bas de page 22
-
Hutton D. Economic analysis of RSV vaccination in older adults [slides presented at Advisory Committee on Immunization Practices (ACIP) meeting June 21, 2023]. Atlanta, GA: CDC; 2023. [Consulté le 27 févr. 2024]. https://www.cdc.gov/acip/downloads/slides-2023-06-21-23/04-RSV-Adults-Hutton-508.pdf
- Notes de bas de page 23
-
Shoukat A, Bawden CE, Röst G, LeBlanc JJ, Galvani AP, Langley JM, Moghadas SM. Impact and cost-effectiveness analyses of vaccination for prevention of respiratory syncytial virus disease among older adults in Ontario: A Canadian Immunization Research Network (CIRN) study. Vaccine 2024;42(7):1768–76. https://doi.org/10.1016/j.vaccine.2024.02.041
- Notes de bas de page 24
-
Shi T, Vennard S, Jasiewicz F, Brogden R, Nair H, RESCEU Investigators. Disease burden estimates of Respiratory Syncytial Virus related acute respiratory infections in adults with comorbidity: a systematic review and meta-analysis. J Infect Dis 2022;226 Suppl 1:S17–21. https://doi.org/10.1093/infdis/jiab040
- Notes de bas de page 25
-
Bernardo CO, Gonzalez-Chica D, Stocks N. Influenza-like illness and antimicrobial prescribing in Australian general practice from 2015 to 2017: a national longitudinal study using the MedicineInsight dataset. BMJ Open 2019;9(4):e026396. https://doi.org/10.1136/bmjopen-2018-026396
- Notes de bas de page 26
-
Chen KA. Ingen Tv, Smith BT, Fitzpatrick T, Whelan M, Parpia AS, Alessandrini J, Buchan SA. Neighbourhood-level burden of social risk factors on respiratory syncytial virus hospitalization in Ontario, Canada, 2016-2019. medRxiv 2024:2024.02.27.24303436. https://doi.org/10.1093/ofid/ofae384
- Notes de bas de page 27
-
Statistique Canada. Tableau 13-10-0114-01. Espérance de vie et autres éléments de la table complète de mortalité, estimations sur trois ans, Canada, toutes les provinces sauf l’Île-du-Prince-Édouard. Ottawa. ON : StatCan; 2023. [Consulté le 5 janv. 2024]. https://doi.org/10.25318/1310011401-fra
- Notes de bas de page 28
-
Agence de la santé publique du Canada. Couverture vaccinale contre la grippe saisonnière au Canada, 2022–2023. Ottawa, ON : ASPC; 2023. https://www.canada.ca/fr/sante-publique/services/immunisation-vaccins/couvertures-vaccinales/resultats-enquete-grippe-saisonniere-2022-2023/rapport-complet.html
- Notes de bas de page 29
-
World Health Organization. Revising global indicative wastage rates: a WHO initiative for better planning and forecasting of vaccine supply needs. Geneva, CH: WHO 2019. https://www.who.int/docs/default-source/immunization/tools/revising-wastage-concept-note.pdf
- Notes de bas de page 30
-
Melgar M, Britton A, Roper LE, Talbot HK, Long SS, Kotton CN, Havers FP. Use of respiratory syncytial virus vaccines in older adults: recommendations of the Advisory Committee on Immunization Practices - United States, 2023. MMWR Morb Mortal Wkly Rep 2023;72(29):793–801. https://doi.org/10.15585/mmwr.mm7229a4
- Notes de bas de page 31
-
O’Reilly R, Kwong JC, McGeer A, To T, Sander B. The cost-effectiveness of a pneumococcal conjugate vaccine (PCV13) program for older adults (65+) in Ontario, Canada in the context of infant immunization and changing serotype distributions. Society for Medical Decision Making 39th Annual North American Meeting; 22-25 October 2017; Pittsburgh, PA.
- Notes de bas de page 32
-
Robertson G. What you need to know about RSV this flu season. The Globe and Mail, 15 September 2023. [Consulté le 19 oct. 2023]. https://www.theglobeandmail.com/canada/article-rsv-virus-vaccines-treatments/
- Notes de bas de page 33
-
Sander B, Kwong JC, Bauch CT, Maetzel A, McGeer A, Raboud JM, Krahn M. Economic appraisal of Ontario’s Universal Influenza Immunization Program: a cost-utility analysis. PLoS Med 2010;7(4):e1000256. https://doi.org/10.1371/journal.pmed.1000256
- Notes de bas de page 34
-
Canadian Institute for Health Information. An overview of physician payments and cost per service. Ottawa, ON: CIHI; 2022. [Consulté le 5 janv. 2024]. https://www.cihi.ca/en/health-workforce-in-canada-in-focus-including-nurses-and-physicians/an-overview-of-physician
- Notes de bas de page 35
-
Alliance for Healthier Communities. Emergency department costs averted attributed to community health centres in Ontario. 2022. [Consulté le 5 janv. 2024]. https://www.allianceon.org/sites/default/files/CHC_ED_Costs_Averted_Feb_9.pdf
- Notes de bas de page 36
-
Lee BY, Ercius AK, Smith KJ. A predictive model of the economic effects of an influenza vaccine adjuvant for the older adult (age 65 and over) population. Vaccine 2009;27(16):2251–7. https://doi.org/10.1016/j.vaccine.2009.02.024
- Notes de bas de page 37
-
Comité consultatif national de l'immunisation. Recommandations sur l'utilisation du vaccin conjugué 15-valent (PNEU-C-15) contre le pneumocoque et 20-valent (PNEU-C-20) contre le pneumocoque chez les adultes : Annexe de données économiques supplémentaires. Ottawa, ON : ASPC; 2023. [Consulté le 27 avr. 2023]. https://www.canada.ca/en/public-health/services/immunization/national-advisory-committee-on-immunization-naci/public-health-level-recommendations-use-pneumococcal-vaccines-adults-including-use-15-valent-20-valent-conjugate-vaccines/economic-evidence-supplementary-appendix.html
- Notes de bas de page 38
-
Yan J, Xie S, Johnson JA, Pullenayegum E, Ohinmaa A, Bryan S, Xie F. Canada population norms for the EQ-5D-5L. Eur J Health Econ 2024;25(1):147–55. https://doi.org/10.1007/s10198-023-01570-1
- Notes de bas de page 39
-
Herring WL, Zhang Y, Shinde V, Stoddard J, Talbird SE, Rosen B. Clinical and economic outcomes associated with respiratory syncytial virus vaccination in older adults in the United States. Vaccine 2022;40(3):483–93. https://doi.org/10.1016/j.vaccine.2021.12.002
- Notes de bas de page 40
-
Mao Z, Li X, Korsten K, Bont L, Butler C, Wildenbeest J, Coenen S, Hens N, Bilcke J, Beutels P; RESCEU Investigators. Economic burden and health-related quality of life of Respiratory Syncytial Virus and influenza infection in European community-dwelling older adults. J Infect Dis 2022;226 Suppl 1:S87–94. https://doi.org/10.1093/infdis/jiac069
- Notes de bas de page 41
-
Zeevat F, Luttjeboer J, Paulissen JH, van der Schans J, Beutels P, Boersma C, Postma MJ; RESCEU Investigators. Exploratory analysis of the economically justifiable price of a hypothetical RSV vaccine for older adults in the Netherlands and the United Kingdom. J Infect Dis 2022;226 Suppl 1:S102–9. https://doi.org/10.1093/infdis/jiab118
- Notes de bas de page 42
-
Meijboom MJ, Pouwels KB, Luytjes W, Postma MJ, Hak E. RSV vaccine in development: assessing the potential cost-effectiveness in the Dutch elderly population. Vaccine 2013;31(52):6254–60. https://doi.org/10.1016/j.vaccine.2013.10.023
- Notes de bas de page 43
-
Statistique Canada. Tableau 98-10-0022-01. Âge (en années), âge moyen et âge médian et genre : Canada, provinces et territoires, divisions de recensement et subdivisions de recensement. Ottawa, ON : StatCan; 2022. [Consulté le 5 janv. 2024]. https://doi.org/10.25318/9810002201-fra
- Notes de bas de page 44
-
Prosser LA. Economic analysis of vaccination with mRNA booster dose against COVID-19 among adults [slides presented at Advisory Committee on Immunization Practices (ACIP) meeting Sep 12, 2023]. Atlanta, GA: CDC; 2023. [Consulté le 29 janv. 2024]. https://stacks.cdc.gov/view/cdc/132890
Appendice
| Paramètre | Base | Intervalle | Référence |
|---|---|---|---|
| Répartition de la population (%) | |||
| 50 à 59 ans | 31,7 | – | Statistique Canada Note de bas de page 12 |
| 60 à 64 ans | 17,5 | – | |
| 65 à 69 ans | 15,8 | – | |
| 70 à 74 ans | 12,8 | – | |
| 75 à 79 ans | 9,9 | – | |
| 80 ans et plus | 12,2 | – | |
| % de la population ayant une ou plusieurs maladie chronique | |||
| 50 à 59 ans | 38,4 | – | Statistique Canada Note de bas de page 13 |
| 60 à 79 ans | 60,1 | – | |
| 80 ans et plus | 72,1 | – | |
| % mensuel des cas annuels de VRS | |||
| Septembre | 1,2 | – | Système de surveillance de la détection des virus respiratoires (moyenne de 9 saisons, 2010–2011 à 2018–2019) Note de bas de page 20 |
| Octobre | 1,9 | – | |
| Novembre | 5,5 | – | |
| Décembre | 14,2 | – | |
| Janvier | 17,6 | – | |
| Février | 21,1 | – | |
| Mars | 17,0 | – | |
| Avril | 11,0 | – | |
| Mai | 5,6 | – | |
| Juin | 2,6 | – | |
| Juillet | 1,3 | – | |
| Août | 1,1 | – | |
| Rapport de cotes pour les soins ambulatoires médicalement pris en charge chez les adultes présentant une ou plusieurs maladies chroniques | |||
| Tous les âges | 1,1 | – | Shi et al., 2022 Note de bas de page 24 |
| % de patients nécessitant une hospitalisation avec un ou plusieurs maladies chroniques | |||
| Tous les âges | 98,2 | – | ElSherif et al., 2023 Note de bas de page 2 |
| Facteur de sous-détection du VRS médicalement pris en charge chez les adultes | |||
| Tous les âges | 1,5 | 1–2 | McLaughlin et al., 2022 Note de bas de page 4 |
| Incidence annuelle des cas de VRS médicalement pris en charge et nécessitant une consultation externe pour 100 000 habitants (non ajustée pour tenir compte de la sous-détection) | |||
| 50 à 59 ans | 261,9 | 186,5–337,3 | ElSherif et al., 2023 Note de bas de page 2; McLaughlin et al., 2022 Note de bas de page 4; Système de surveillance de la détection des virus respiratoires Note de bas de page 20 |
| 60 à 69 ans | 604,1 | 472,8–707,8 | |
| 70 à 79 ans | 780,0 | 625,1–934,1 | |
| 80 ans et plus | 2 487,1 | 2 097,1–2 877,2 | |
| Incidence annuelle des cas de VRS médicalement pris en charge nécessitant une visite aux urgences pour 100 000 habitants (non ajustée pour tenir compte de la sous-détection) | |||
| 50 à 59 ans | 16,8 | 12,0–21,6 | ElSherif et al., 2023 Note de bas de page 2; McLaughlin et al., 2022 Note de bas de page 4; Système de surveillance de la détection des virus respiratoires Note de bas de page 20 |
| 60 à 69 ans | 43,3 | 33,9–50,7 | |
| 70 à 79 ans | 68,5 | 54,9–82,0 | |
| 80 ans et plus | 218,3 | 184,1–252,5 | |
| Incidence annuelle des hospitalisations attribuables au VRS pour 100 000 habitants (non ajustée pour la sous-détection) | |||
| 50 à 59 ans | 15,1 | 10,8–19,5 | ElSherif et al., 2023 Note de bas de page 2; Système de surveillance de la détection des virus respiratoires Note de bas de page 20 |
| 60 à 69 ans | 47,5 | 37,2–55,7 | |
| 70 à 79 ans | 96,4 | 77,3–115,4 | |
| 80 ans et plus | 307,4 | 259,2–355,6 | |
| % de patients hospitalisés pour un VRS nécessitant une admission en USI | |||
| Tous les âges | 13,7 | 10,2–17,9 | ElSherif et al., 2023 Note de bas de page 2 |
| % de patients atteints de VRS médicalement pris en charge à qui l'on a prescrit un antimicrobien | |||
| Tous les âges | 50 | 14–89 | Bernardo et al., 2019 Note de bas de page 25; ElSherif et al., 2023 Note de bas de page 2 |
| Mortalité due au VRS par hospitalisation (%) | |||
| 50 à 64 ans | 7,2 | 5,4–9,5 | Chen et al., 2024 Note de bas de page 26 |
| 65 à 74 ans | 6,6 | 5,2–8,4 | |
| 75 ans et plus | 10,1 | 9,0–11,3 | |
| Taux de mortalité toutes causes confondues (par an, pour 1 000 habitants) | |||
| Tous les âges | Taux spécifiques à l'âge | – | Statistique Canada Note de bas de page 27 |
| Couverture vaccinale (%), avec maladie chronique | |||
| 50 à 59 ans | 58,6 | – | Enquête sur la couverture vaccinale contre la grippe saisonnière, 2022–2023 Note de bas de page 28 |
| 60 à 64 ans | 59,9 | – | |
| 65 à 69 ans | 65,2 | – | |
| 70 à 79 ans | 82,7 | – | |
| 80 ans et plus | 83,4 | – | |
| Couverture vaccinale (%), sans maladie chronique | |||
| 50 à 59 ans | 36,7 | – | Enquête sur la couverture vaccinale contre la grippe saisonnière, 2022–2023 Note de bas de page 28 |
| 60 à 64 ans | 49,4 | – | |
| 65 à 69 ans | 61,1 | – | |
| 70 à 79 ans | 74,9 | – | |
| 80 ans et plus | 74,8 | – | |
| Efficacité du vaccin (%), Arexvy (GSK) | |||
| VRS en consultation externe — saison 1 (suivi à 7 mois) |
82,6 | – | Friedland, 2023 Note de bas de page 17; Ison et al., 2024 Note de bas de page 18; hypothèse pour la saison 3 |
| VRS en consultation externe — saison 2 (suivi à 6 mois) |
56,1 | – | |
| VRS en consultation externe — saison 3 | 18,7 | – | |
| VRS hospitalisé — saison 1 (suivi à 7 mois) |
94,1 | – | |
| VRS hospitalisé — saison 2 (suivi à 6 mois) |
64,2 | – | |
| VRS hospitalisé — saison 3 | 21,4 | – | |
| Efficacité du vaccin (%), Abrysvo (Pfizer) | |||
| VRS en consultation externe — saison 1 (suivi à 7 mois) |
65,1 | – | Gurtman, 2023 Note de bas de page 19; hypothèse pour la saison 3 |
| VRS en consultation externe — saison 2 (suivi à 4 mois) |
48,9 | – | |
| VRS en consultation externe — saison 3 | 16,3 | – | |
| VRS hospitalisé — saison 1 (suivi à 7 mois) |
88,9 | – | |
| VRS hospitalisé — saison 2 (suivi à 4 mois) |
78,6 | – | |
| VRS hospitalisé — saison 3 | 26,2 | – | |
| Taux de perte de vaccins (%) | |||
| Tous les âges | 5 | – | OMS, 2019 Note de bas de page 29 |
| Effets secondaires suivant l'immunisation (%) | |||
| Événement indésirable local grave | 0,51 | 0,16–1,84 | Melgar et al., 2023 Note de bas de page 30 |
| Événement indésirable systémique grave | 0,57 | 0,10–2,35 | |
| Coût d'administration du vaccin par dose ($) | |||
| Tous les âges | 18 | 13–22 | O'Reilly et al., 2017 Note de bas de page 31 |
| Coût de la vaccination par dose ($) | |||
| Arexvy (GSK) | 230 | 100–230 | Robertson, 2023 Note de bas de page 32 |
| Abrysvo (Pfizer) | 230 | 100–230 | |
| Coûts attribuables par personne hospitalisée en raison du VRS ($) | |||
| Hospitalisation (6 mois) | 32 228 | 31 622–32 836 | Mac et al., 2023 Note de bas de page 3 |
| Hospitalisation, décès à l'hôpital | 27 534 | 22 027–33 041Note de bas de page a | |
| Coûts par personne atteinte du VRS traitée en ambulatoire ($) | |||
| Visite d'un professionnel de la santé | 62 | 48–82 | Sander et al., 2010 Note de bas de page 33; ICIS Note de bas de page 34; Alliance pour des communautés en santé Note de bas de page 35 |
| Visite aux urgences | 340 | 302–509 | |
| Coûts médicaux directs en cas d'effet indésirable local grave après la vaccination ($) | |||
| Moins de 65 ans | 62 | 48–82 | Sander et al., 2010 Note de bas de page 33; ICIS Note de bas de page 34; Lee et al., 2009 Note de bas de page 36 |
| 65 ans et plus | 63 | 49–83 | |
| Coûts médicaux directs en cas d'effet indésirable systémique grave après la vaccination ($) | |||
| Moins de 65 ans | 62 | 48–82 | Sander et al., 2010 Note de bas de page 33; ICIS Note de bas de page 34; Lee et al., 2009 Note de bas de page 36 |
| 65 ans et plus | 66 | 51–87 | |
| Coûts de transport ($) | |||
| Coûts de déplacement pour les soins hospitaliers | 417 | 210–623 | CCNII Note de bas de page 37 |
| Utilité de la santé en arrière-plan | |||
| 50 à 59 ans | 0,848 | – | Yan et al., 2023 Note de bas de page 38 |
| 60 à 64 ans | 0,839 | – | |
| 65 à 74 ans | 0,867 | – | |
| 75 ans et plus | 0,861 | – | |
| Perte d'AVAQ, en ambulatoire, avec ou sans visite aux urgences | |||
| Tous les âges | 0,0056 | 0,0037–0,0075 | Herring et al., 2022 Note de bas de page 39; Mao et al., 2022 Note de bas de page 40; Zeevat et al., 2022 Note de bas de page 41; Meijboom et al., 2013 Note de bas de page 42 |
| Perte d'AVAQ, hospitalisation | |||
| Tous les âges | 0,020 | 0,017–0,030 | Herring et al., 2022 Note de bas de page 39; Mao et al., 2022 Note de bas de page 40; Zeevat et al., 2022 Note de bas de page 41; Meijboom et al., 2013 Note de bas de page 42 |
| Perte d'AVAQ, décès | |||
| 50 à 59 ans | 20,26 | – | Yan et al., 2023 Note de bas de page 38; Statistique Canada Note de bas de page 27Note de bas de page 43 |
| 60 à 64 ans | 16,74 | – | |
| 65 à 69 ans | 14,29 | – | |
| 70 à 74 ans | 11,75 | – | |
| 75 à 79 ans | 9,38 | – | |
| 80 ans et plus | 5,84 | – | |
| Perte d'AVAQ, effet secondaire suivant l'immunisation | |||
| Événement indésirable local grave | 0,0003 | 0,0002–0,0004 | Prosser, 2023 Note de bas de page 44; hypothèse |
| Événement indésirable systémique grave | 0,0004 | 0,0003–0,0005 | |
Abréviations : AVAQ, année de vie ajustée par la qualité; CCNI, Comité consultatif national de l'immunisation; ICIS, Institut canadien d'information sur la santé; OMS, Organisation mondiale de la Santé; USI, unité de soins intensifs; VRS, virus respiratoire syncytial; –, sans objet Notes de bas de page
|
|||

Cette œuvre est mise à disposition selon les termes de la Licence Creative Commons Attribution 4.0 International