Comparaison des vaccins pneumococciques conjugués 13-, 15- et 20-valents dans la population pédiatrique canadienne

 Téléchargez cet article en format PDF (505 ko)
Téléchargez cet article en format PDF (505 ko)Publié par : L'Agence de la santé publique du Canada
Numéro : RMTC : Volume 51-2/3, février/mars 2025 : Économie de la santé en santé publique
Date de publication : février 2025
ISSN : 1719-3109
Soumettre un article
À propos du RMTC
Naviguer
Volume 51-2/3, février/mars 2025 : Économie de la santé en santé publique
Économie de la santé
Comparaison des vaccins pneumococciques conjugués 13-, 15- et 20-valents dans la population pédiatrique canadienne : une analyse coût/utilité
Alison E Simmons1,2, Gebremedhin B Gebretekle1, Robert Pless1, Aleksandra Wierzbowski1, Matthew Tunis1, Ashleigh R Tuite1,2
Affiliations
1 Direction générale des programmes sur les maladies infectieuses et de la vaccination, Agence de la santé publique du Canada, Ottawa, ON
2 École de santé publique Dalla Lana, Université de Toronto, Toronto, ON
Correspondance
Citation proposée
Simmons AE, Gebretekle GB, Pless R, Wierzbowski A, Tunis M, Tuite AR. Comparaison des vaccins pneumococciques conjugués 13-, 15- et 20-valents dans la population pédiatrique canadienne : une analyse coût/utilité. Relevé des maladies transmissibles au Canada 2025;51(2/3):76–91. https://doi.org/10.14745/ccdr.v51i23a02f
Mots-clés : infection à pneumocoque, vaccination, analyse coût/utilité, économie de la santé, modélisation
Contexte : Deux vaccins pneumococciques conjugués, couvrant 15 et 20 sérotypes de Streptococcus pneumoniae (Pneu-C-15 et Pneu-C-20, respectivement), ont été récemment approuvés pour une utilisation dans la population pédiatrique canadienne.
Objectif : Évaluer le rapport coût/efficacité de Pneu-C-15 et Pneu-C-20 chez les nourrissons non vaccinés qui commencent une vaccination systématique contre le pneumocoque, par rapport au vaccin conjugué 13-valent actuellement utilisé (Pneu-C-13).
Méthodes : Un modèle de cohorte statique a été utilisé pour estimer les rapports coût/efficacité différentiels séquentiels (RCED en dollars canadiens de 2022 par année de vie ajustée par la qualité [AVAQ]) de Pneu-C-13, Pneu-C-15 et Pneu-C-20 dans la population pédiatrique commençant leur série primaire. Les coûts et les résultats ont été calculés sur un horizon temporel de 10 ans au niveau du programme et sur un horizon temporel à vie au niveau de l'individu, et actualisés à un taux de 1,5 % par an. Nous avons étudié l'incidence des incertitudes liées aux paramètres et aux hypothèses du modèle dans le cadre d'analyses de scénarios et de sensibilité.
Résultats : L'utilisation systématique de Pneu-C-20 et, dans une moindre mesure, de Pneu-C-15 devrait réduire le fardeau de l'infection à pneumocoque, par rapport à Pneu-C-13. Sur la base des hypothèses de coût du produit, les RCED séquentiels pour Pneu-C-15 et Pneu-C-20 étaient de 58 800 $ et 135 200 $ par AVAQ gagnée du point de vue du système de santé et de 18 272 $ et 93 416 $ par AVAQ gagnée du point de vue de la société, à l'exclusion des effets indirects. Une réduction de 5 % ou plus des maladies attribuables à un sérotype en raison des effets indirects du vaccin a donné lieu à des RCED inférieurs à 30 000 $ par AVAQ gagnée pour Pneu-C-15 et Pneu-C-20, la stratégie optimale étant déterminée par l'ampleur de la réduction des maladies pneumococciques et par le temps nécessaire pour y parvenir.
Conclusion : Il est présumé que Pneu-C-15 et Pneu-C-20 augmentent les AVAQ chez les enfants canadiens par rapport à Pneu-C-13 et à ce qu'ils soient des interventions rentables.
Introduction
L'infection à pneumocoque (IP), causée par la bactérie Streptococcus pneumoniae, est à l'origine d'une morbidité et d'une mortalité importantes dans le monde, en particulier chez les enfants, les personnes âgées et les personnes immunodéprimées. Bien que S. pneumoniae colonise fréquemment le nasopharynx humain sans provoquer de maladie, il peut être à l'origine de maladies graves invasives (e.g., méningite et bactériémie) et, plus fréquemment, non invasives (e.g., pneumonie d'origine communautaire à pneumocoques [POCP] et otite moyenne aiguë [OMA]) Note de bas de page 1. Plus de 100 types capsulaires distincts, ou sérotypes, de S. pneumoniae ont été recensés, mais la majorité des cas d'infections invasives à pneumocoque (IPI) sont attribués à un sous-ensemble de ces sérotypes Note de bas de page 2Note de bas de page 3.
La modélisation des maladies infectieuses est souvent utilisée pour étayer les décisions relatives au vaccin pneumococcique en raison de la dynamique complexe des sérotypes observée au fil des ans dans le cadre des calendriers de vaccination antérieurs. Au début des années 2000, les premiers vaccins pneumococciques conjugués (Pneu-C-7 et Pneu-C-10) ont été autorisés au Canada et ont été administrés dans le cadre de programmes de vaccination à fonds publics. En 2009, le vaccin Pneu-C-13 a été homologué et en 2010, le Comité consultatif national de l'immunisation (CCNI) du Canada a recommandé que les enfants en bonne santé reçoivent 2+1 doses de Pneu-C-13 à l'âge de deux, quatre et 12–15 mois ou 3+1 doses de Pneu-C-13 à l'âge de deux, quatre, six et 12-18 mois Note de bas de page 4. Le vaccin Pneu-C-13 comprend les sérotypes 1, 3, 4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19A, 19F et 23F. Deux vaccins pneumococciques conjugués, couvrant 15 et 20 sérotypes de S. pneumoniae, ont été autorisés par Santé Canada pour une utilisation dans les populations pédiatriques le 8 juillet 2022 (Pneu-C-15) et le 21 juillet 2023 (Pneu-C-20). Le vaccin Pneu-C-15 comprend les sérotypes de Pneu-C-13 ainsi que les sérotypes 22F et 33F, et le vaccin Pneu-C-20 comprend les sérotypes de Pneu-C-13 ainsi que les sérotypes 8, 10A, 11A, 12F, 15B, 22F et 33F Note de bas de page 5Note de bas de page 6.
Après l'introduction de Pneu-C-13, l'incidence des IIP causées par les 13 sérotypes de S. pneumoniae inclus dans le vaccin a diminué dans tous les groupes d'âge Note de bas de page 7Note de bas de page 8Note de bas de page 9. Toutefois, l'incidence globale des IIP est restée relativement inchangée dans tous les groupes d'âge en raison du remplacement des sérotypes de S. pneumoniae et de la persistance de certains sérotypes de Pneu-C-13 Note de bas de page 10Note de bas de page 11. Entre 2016 et 2020, une augmentation importante des IIP causées par les sérotypes 19F et 11A a été observée chez les enfants de moins de cinq ans au Canada Note de bas de page 12. Le sérotype 19F est inclus dans Pneu-C-13, Pneu-C-15 et Pneu-C-20, alors que le sérotype 11A n'est inclus que dans Pneu-C-20.
Étant donné que Pneu-C-15 et Pneu-C-20 couvrent un plus grand nombre de sérotypes, nous avons réalisé une évaluation économique basée sur un modèle, afin d'évaluer le rapport coût/efficacité de leur utilisation dans la population pédiatrique canadienne par rapport à la norme de soins actuelle.
L'examen systématique de l'AMC s'est concentré sur la question de savoir si les vaccins conjugués antipneumococciques constituent une intervention rentable chez les adultes de moins de 65 ans présentant un risque d'IP. Nous avons mené un examen systématique distinct pour répondre à la question stratégique de savoir si le Pneu-C-21 est rentable pour la prévention d'IP chez les adultes âgés de 18 ans et plus. L'objectif de cette analyse était d'identifier les études publiées plus récemment et d'inclure tous les adultes, y compris ceux âgés de 65 ans et plus.
Méthodes
Nous avons mis au point un modèle statique de cohorte de Markov pour quantifier l'incidence sur la santé de trois stratégies de vaccination pédiatrique contre le pneumocoque chez les nourrissons jamais vaccinés. Nous avons comparé le calendrier de 2+1 doses de Pneu-C-13 (politique actuelle), Pneu-C-15 et Pneu-C-20. Les résultats de santé associés à S. pneumoniae du modèle de cohorte ont été utilisés pour étayer une analyse coût/utilité. Les résultats comprenaient l'incidence de l'IIP, de la POCP non invasive et de l'OMA, les hospitalisations, les décès, les coûts, les années de vie ajustées par la qualité (AVAQ) et les rapports coût/efficacité différentiels (RCED). Au moment de l'analyse, le CCNI n'avait pas encore publié de recommandations pour l'utilisation de Pneu-C-15 et de Pneu-C-20 dans la population pédiatrique. Cette analyse économique a été réalisée pour soutenir l'élaboration des recommandations du CCNI, et des détails supplémentaires sur les données économiques prises en compte sont disponibles en ligne Note de bas de page 13.
Structure du modèle
Notre modèle a suivi une cohorte de population ouverte et multiâges sur une période de 10 ans. Les taux de natalité et de mortalité au sein de la cohorte ont été déterminés à partir des projections démographiques canadiennes Note de bas de page 14Note de bas de page 15Note de bas de page 16. Les individus étaient exempts d'IP à l'entrée dans le modèle, mais pouvaient développer une IIP, une POCP et une OMA au cours de leur vie (figure 1, tableau 1). Un sous-ensemble de personnes atteintes d'IIP a développé des séquelles post-méningite. Il a été présumé que l'IIP était traitée en milieu hospitalier, que la POCP était traitée en milieu hospitalier ou ambulatoire et que l'OMA était traitée en milieu ambulatoire. L'incidence, les coûts et les conséquences sanitaires de l'OMA ont été limités aux personnes de moins de 10 ans Note de bas de page 17.
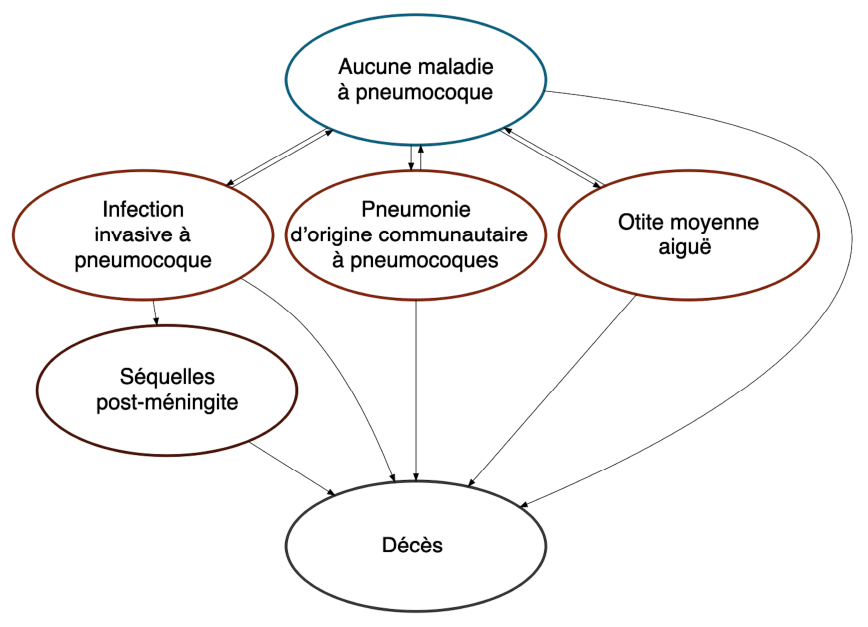
Figure 1 : Équivalent textuel
Schéma du modèle pneumococcique dans lequel la relation entre différents états de santé est représentée avec des ovales étiquetés avec chaque état de santé et des flèches représentant comment les individus peuvent passer d'un état de santé à un autre. Il y a une relation bidirectionnelle entre « aucune maladie à pneumocoque » et les états « infection invasive à pneumocoque », « pneumonie extrahospitalière à pneumocoque » et « otite moyenne aiguë », indiquant que les individus peuvent développer une maladie pneumococcique et récupérer. Il y a un mouvement unidirectionnel depuis « infection invasive à pneumocoque » vers « séquelles post-méningite », indiquant que certaines personnes développeront des conséquences à long terme de l'infection et ne récupéreront pas. Les individus peuvent passer à l'état « décès » à partir de n'importe quel autre état de santé et ne peuvent pas quitter cet état une fois qu'ils y entrent.
Notes de bas de page figure 1
- Figure 1 note de bas de page a
-
Les personnes vaccinées et non vaccinées ont connu les mêmes états de santé, le risque étant modifié en fonction du statut vaccinal, du type de vaccin reçu et du temps écoulé depuis la vaccination
- Figure 1 note de bas de page b
-
Les séquelles post-méningite comprennent des séquelles auditives et neurologiques
| Paramètre | Base | Plage | Référence(s) |
|---|---|---|---|
| Incidence de l'IIP (pour 100 000 habitants) | |||
| Moins de 2 ans | 14,5 | - | SCSMDO, 2019; programme SCI, 2019 Note de bas de page 18 |
| 2 à 4 ans | 10,2 | - | |
| 5 à 17 ans | 2,1 | - | |
| 18 à 49 ans | 5,2 | - | |
| 50 à 64 ans | 13,6 | - | |
| 65 ans et plus | 23,8 | - | |
| Incidence de la POC (pour 100 000 habitants) | |||
| Moins de 5 ans | 4 991,1 | - | Nasreen et al., 2022 Note de bas de page 19 |
| 5 à 17 ans | 1 249,0 | - | |
| 18 à 39 ans | 815,9 | - | |
| 40 à 64 ans | 1 529,9 | - | |
| 65 à 74 ans | 3 095,7 | - | |
| 75 à 84 ans | 5 398,1 | - | |
| 85 ans et plus | 10 122,7 | - | |
| Incidence de l'OMA (pour 100 000 habitants) | |||
| Moins de 5 ans | 25 467,6 | - | Nasreen et al., 2022 Note de bas de page 19 |
| 5 à 17 ans | 7 225,9 | - | |
| 18 à 39 ans | 2 204,4 | - | |
| 40 à 64 ans | 2 058,6 | - | |
| 65 à 74 ans | 1 954,7 | - | |
| 75 à 84 ans | 1 857,4 | - | |
| 85 ans et plus | 1 621,4 | - | |
| Risque relatif d'IP dans un contexte d'incidence plus élevée | |||
| Moins de 2 ans | 6,8 | - | SCSMDO, 2019; programme SCI, 2015–2019 Note de bas de page 18 |
| 2 à 4 ans | 0,9 | - | |
| 5 à 17 ans | 3,9 | - | |
| 18 à 49 ans | 2,1 | - | |
| 50 à 64 ans | 2,1 | - | |
| 65 ans et plus | 2,4 | - | |
| Proportion de patients atteints de POC attribuée à la bactérie S. pneumoniae (%) | |||
| Moins de 1 an | 6,0 | 5,1–9,1 | King, 2023; LeBlanc et al., 2022; Groupe d'étude PERCH (Pneumonia Etiology Research for Child Health), 2019 Note de bas de page 20Note de bas de page 21Note de bas de page 22 |
| 1 à 15 ans | 12,0 | 10,1–18,2 | |
| 16 à 49 ans | 19,5 | 17,3–21,7 | |
| 50 à 64 ans | 19,0 | 17,3–20,7 | |
| 65 ans et plus | 11,2 | 10,4–12,1 | |
| Proportion de patients atteints d'une OMA attribuée à la bactérie S. pneumoniae (%) | |||
| Moins de 18 ans | 17 | 14–22 | Kim et al., 2017; King, 2023 Note de bas de page 20Note de bas de page 23 |
| Proportion de patients atteints d'une POCP pris en charge en milieu hospitalier (%) | |||
| Moins de 65 ans | 4,6 | 2,2–9,3 | O'Reilly et al., 2023 Note de bas de page 24 |
| 65 ans et plus | 12,3 | 7,9–18,6 | |
| Proportion de patients atteints d'une IIP avec méningite (%) | |||
| Moins de 1 an | 16,9 | 13,3–21,1 | Morrow et al., 2007 Note de bas de page 17 |
| 1 à 4 ans | 4,6 | 3,0–6,8 | |
| 5 à 9 ans | 8,7 | 4,1–15,9 | |
| 10 à 19 ans | 8,5 | 5,1–13,3 | |
| 20 à 64 ans | 5,1 | 3,9–6,4 | |
| 65 ans et plus | 3,1 | 2,2–4,1 | |
| Proportion de patients atteints de méningite et présentant des séquelles post-méningitiques à long terme (%) | |||
| Séquelles neurologiques | 12,2 | 5,3–19,1 | Jit, 2010 Note de bas de page 25 |
| Perte auditive | 8,2 | 4,5–11,9 | |
| Proportion de patients atteints d'OMA ayant bénéficié de la pose d'un tube auriculaire (%) | |||
| Moins de 10 ans | 6 | 4–12 | Institut canadien d'information sur la santé, 2020; Chuck et al., 2010; Nasreen et al., 2022; Hypothèse Note de bas de page 19Note de bas de page 26Note de bas de page 27 |
| Létalité des cas d'IIP (%) | |||
| Moins de 1 an | 11,8 | 11,2–12,3 | Wijayasri et al., 2019 Note de bas de page 7 |
| 1 à 4 ans | 1,6 | 0,8–2,7 | |
| 5 à 49 ans | 5,7 | 4,9–6,7 | |
| 50 à 64 ans | 10,9 | 9,9–12 | |
| 65 ans et plus | 17,2 | 16,2–18,3 | |
| Létalité des cas de POCP (patients hospitalisés) (%) | |||
| Moins de 10 ans | 1,0 | 0,3–3,1 | LeBlanc et al., 2022; Morrow et al., 2007; Hypothèse Note de bas de page 17Note de bas de page 22 |
| 10 à 15 ans | 1,6 | 0,6–4,3 | |
| 16 à 49 ans | 3,8 | 1,7–7,0 | |
| 50 à 64 ans | 4,8 | 2,7–7,1 | |
| 65 ans et plus | 9,9 | 7,7–12,3 | |
| Répartition des sérotypes de vaccins (%), moins de 2 ans | |||
| ST3 | 8 | - | Laboratoire national de microbiologie, 2019 Note de bas de page 18 |
| Pneu-C-13/non-ST3 | 9 | - | |
| Pneu-C-15/non-Pneu-C-13 | 21 | - | |
| Pneu-C-20/non-Pneu-C-15 | 19 | - | |
| TNV | 43 | - | |
| Distribution des sérotypes de vaccins (%), 2 à 4 ans | |||
| ST3 | 11 | - | Laboratoire national de microbiologie, 2019 Note de bas de page 18 |
| Pneu-C-13/non-ST3 | 16 | - | |
| Pneu-C-15/non-Pneu-C-13 | 16 | - | |
| Pneu-C-20/non-Pneu-C-15 | 23 | - | |
| TNV | 33 | - | |
| Distribution des sérotypes de vaccins (%), 5 à 17 ans | |||
| ST3 | 8 | - | Laboratoire national de microbiologie, 2019 Note de bas de page 18 |
| Pneu-C-13/non-ST3 | 23 | - | |
| Pneu-C-15/non-Pneu-C-13 | 20 | - | |
| Pneu-C-20/non-Pneu-C-15 | 14 | - | |
| TNV | 35 | - | |
| Distribution des sérotypes de vaccins (%), 18 à 49 ans | |||
| ST3 | 10 | - | Laboratoire national de microbiologie, 2019 Note de bas de page 18 |
| Pneu-C-13/non-ST3 | 32 | - | |
| Pneu-C-15/non-Pneu-C-13 | 11 | - | |
| Pneu-C-20/non-Pneu-C-15 | 21 | - | |
| TNV | 26 | - | |
| Distribution des sérotypes de vaccins (%), 50 à 64 ans | |||
| ST3 | 12 | - | Laboratoire national de microbiologie, 2019 Note de bas de page 18 |
| Pneu-C-13/non-ST3 | 32 | - | |
| Pneu-C-15/non-Pneu-C-13 | 11 | - | |
| Pneu-C-20/non-Pneu-C-15 | 21 | - | |
| TNV | 26 | - | |
| Répartition des sérotypes de vaccins (%), 65 ans et plus | |||
| ST3 | 13 | - | Laboratoire national de microbiologie, 2019 Note de bas de page 18 |
| Pneu-C-13/non-ST3 | 16 | - | |
| Pneu-C-15/non-Pneu-C-13 | 15 | - | |
| Pneu-C-20/non-Pneu-C-15 | 14 | - | |
| TNV | 42 | - | |
Abréviations : IP, infection à pneumocoque; IIP, infection invasive à pneumocoque; OMA, otite moyenne aiguë; Pneu-C, vaccin pneumococcique conjugué; POC, pneumonie d'origine communautaire; POCP, pneumonie d'origine communautaire à pneumocoques; SCI, Surveillance circumpolaire internationale; SCSMDO, Système canadien de surveillance des maladies à déclaration obligatoire; ST3, sérotype 3; TNV, type non vaccinal; -, sans objet |
|||
Lors de l'entrée dans le modèle, une proportion de chaque cohorte de naissance a été vaccinée à l'âge de deux, quatre et douze mois, sur la base de la couverture vaccinale estimée de Pneu-C-13 (tableau 2) Note de bas de page 28. Il a été présumé que la vaccination réduisait le risque d'IP en raison des sérotypes inclus dans le vaccin. Nous avons supposé que l'efficacité réelle du vaccin (ER) pour Pneu-C-15 et Pneu-C-20 était équivalente à l'ER pour Pneu-C-13. Tous les vaccins présentaient une ER plus faible contre le sérotype 3 que contre les autres sérotypes vaccinaux. Dans ce modèle, la protection conférée par le vaccin a commencé après la deuxième dose et s'est atténuée sur une période de 15 ans Note de bas de page 29. Le modèle de base n'a pas pris en compte les effets indirects de la vaccination, notamment l'immunité collective et le remplacement des sérotypes.
| Paramètre | Base | Plage | Référence(s) |
|---|---|---|---|
| Couverture vaccinale (%) | |||
| 2 doses | 87 | - | HypothèseNote de bas de page a |
| 2+1 doses | 84,5 | - | Enquête nationale sur la couverture vaccinale des enfants (ENCVE), 2022 Note de bas de page 28 |
| Efficacité réelle de Pneu-C pour 2+1 doses (%) | |||
| TV-PI | 85 | 67–96 | Farrar et al., 2022; Prasad et al., 2023; Hypothèse Note de bas de page 29Note de bas de page 30 |
| ST3-PI | 33 | 10–66 | Farrar et al., 2022; Prasad et al., 2023; Hypothèse Note de bas de page 29Note de bas de page 30 |
| TV-POCP | 64 | 50–72 | Prasad et al., 2023; Stoecker 2023; Hypothèse (basée sur des données sur les adultes pour l'ER relative pour l'IIP vs. la POCP) Note de bas de page 29Note de bas de page 31 |
| ST3-POCP | 25 | 19–28 | Hypothèse (basée sur l'IIP) |
| TV-OMA | 54 | 40–64 | Eskola, 2001 Note de bas de page 32 |
| ST3-OMA | 21 | 15–25 | Hypothèse (basée sur l'IIP) |
| Efficacité réelle de Pneu-C pour 2 doses | |||
| % d'ER obtenu avec les deux premières doses de la série | 75 | 60–90 | Andrews et al., 2014; Hypothèse Note de bas de page 33 |
| Durée de la protection | |||
| Pneu-C | 15 ans : stable pendant 5 ans, diminution linéaire jusqu'à 0 sur 10 ans | - | Prasad et al., 2023 Note de bas de page 29 |
Note de bas de tableau 2
Abréviations : IIP, infection invasive à pneumocoque; Pneu-C, vaccin pneumococcique conjugué; POCP, pneumonie d'origine communautaire à pneumocoques; ST3-OMA, otite moyenne aiguë de sérotype 3; ST3-PI, pneumococcie invasive de sérotype 3; ST3-POCP, pneumonie d'origine communautaire à pneumocoques de sérotype 3; ER, efficacité réelle du vaccin; TV-OMA, otite moyenne aiguë de type vaccinal; TV-PI, pneumococcie invasive de type vaccinal; TV-POCP, pneumonie d'origine communautaire à pneumocoques de type vaccinal; -, sans objet
|
|||
Analyse coût/utilité
Nous avons utilisé les résultats de notre modèle pour réaliser une analyse coût/utilité des trois stratégies de vaccination sur un horizon temporel programmatique de 10 ans. Un horizon temporel de toute une vie a été utilisé au niveau individuel (i.e., que toutes les conséquences à long terme de l'IP accumulées au cours de la vie d'un individu ont été incluses). Le coût présumé par dose dans notre scénario de référence était de 71,50 $ pour Pneu-C-13, 78,10 $ pour Pneu-C-15 et 90,10 $ pour Pneu-C-20 (tableau 3). Une analyse non publiée réalisée par l'Agence de la santé publique du Canada a révélé que les prix des vaccins négociés au Canada pour l'ensemble des programmes de vaccination représentaient généralement 30 % à 50 % des prix contractuels aux États-Unis. Nous avons appliqué un taux d'actualisation de 40 % aux prix publics des vaccins des Centres pour le contrôle et la prévention des maladies des États-Unis pour estimer le coût par dose dans notre scénario de référence Note de bas de page 34. Les coûts et les utilités ont été dérivés principalement des données de surveillance canadiennes et des études publiées, et par hypothèse (tableau 3, tableau 4). Nous avons appliqué un taux d'actualisation de 1,5 % aux AVAQ et aux coûts, les coûts étant gonflés en dollars canadiens de 2022 Note de bas de page 35. Les estimations probabilistes du modèle ont été basées sur 10 000 simulations. Pour chaque simulation du modèle, les paramètres ont été tirés de distributions, les résultats ont été calculés pour chaque scénario et les résultats récapitulatifs des 10 000 simulations ont été calculés. Les valeurs assorties d'intervalles dans les tableaux 1 à 4 indiquent les paramètres du modèle qui ont été échantillonnés de manière probabiliste pour tenir compte de l'incertitude (i.e, échantillonnés à partir de distributions bêta pour les probabilités et les utilités et de distributions gamma pour les coûts). Le modèle a été construit en R et les paramètres spécifiant les distributions (forme et échelle pour les distributions gamma et forme1 et forme2 pour les distributions bêta) ont été estimés en utilisant les moyennes et les intervalles spécifiés Note de bas de page 36Note de bas de page 37. Nous avons mené nos analyses à la fois du point de vue du système de santé et du point de vue de la société. Outre les coûts liés aux résultats de santé et au système de santé, ce dernier comprend également les coûts non pris en charge par le système de santé publique (e.g., les coûts directs à la charge du patient, la perte de productivité) Note de bas de page 38.
| Paramètre | Base ($) | Intervalle ($) | Référence(s) |
|---|---|---|---|
| Coût par dose de vaccin | |||
| Administration du vaccin | 16,77 | 12,58–20,96 | O'Reilly et al., 2017 Note de bas de page 39 |
| Pneu-C-13 | 71,5 | - | Centres pour le contrôle et la prévention des maladies; Hypothèse Note de bas de page 34 |
| Pneu-C-15 | 78,1 (9,2 % plus élevé que Pneu-C-13) | 72,2–87,9 (1 %–23 % plus élevé que Pneu-C-13) | |
| Pneu-C-20 | 90,1 (26,1 % plus élevé que Pneu-C-13) | 78,6–107,2 (10 %–50 % plus élevé que Pneu-C-13) | |
| Coût par cas d'IIP | |||
| Moins de 5 ans | 20 468 | 17 422–23 755 | Base de données sur les congés des patients, 2015–2019Note de bas de page 40Note de bas de page 41Note de bas de page 42Note de bas de page 43 |
| 5 à 17 ans | 14 717 | 12 510–17 100 | |
| 18 à 49 ans | 28 812 | 26 559–31 155 | |
| 50 à 64 ans | 29 146 | 27 363–30 984 | |
| 65 à 74 ans | 28 955 | 26 727–31 271 | |
| 75 ans et plus | 21 501 | 20 001–23 054 | |
| Coût par cas de POCP pris en charge en milieu hospitalier | |||
| Moins de 18 ans | 7 345 | 7 189–7 545 | O'Reilly et al., 2023 Note de bas de page 24 |
| 18 à 64 ans | 14 185 | 13 708–14 686 | |
| 65 ans et plus | 14 179 | 13 931–14 433 | |
| Coût par cas de POCP pris en charge en milieu ambulatoire | |||
| Moins de 18 ans | 450 | 438–461 | O'Reilly et al., 2023 Note de bas de page 24 |
| 18 à 64 ans | 1 187 | 1 154–1 221 | |
| 65 ans et plus | 3 343 | 3 283–3 400 | |
| Coût par cas d'OMA, à l'exclusion de la pose d'un tube auriculaire | |||
| Moins de 2 ans | 260 | 258–301 | Gaboury et al, 2010; Hypothèse Note de bas de page 44 |
| 2 à 9 ans | 178 | 148–207 | |
| Coût de l'intervention chirurgicale pour la pose d'un tube auriculaire | 1 790 | 1 340–2 240Note de bas de page a | Institut canadien d'information sur la santé, 2020 Note de bas de page 26 |
| Coût des soins pour les patients souffrant de séquelles post-méningite (par an) | |||
| Coût annuel des soins pour les personnes souffrant de séquelles auditives | 2 783,3 | 2 087,5–3 479,2Note de bas de page a | Christensen et al., 2014 Note de bas de page 45 |
| Coût annuel des soins pour les personnes souffrant de séquelles neurologiques | 9 262,4 | 6 946,8–11 578,0Note de bas de page a | Christensen et al., 2014 Note de bas de page 45 |
| Coûts directs | |||
| Médicaments, moins de 65 ans | 18,1 | 13,6–22,6 | American Academy of Pediatrics, 2021; Metlay et al, 2019; Ministère de la Santé de l'Ontario, 2022; Conseil d'examen du prix des médicaments brevetés Canada, 2019–2020 Note de bas de page 46Note de bas de page 47Note de bas de page 48Note de bas de page 49 |
| Transport vers les soins hospitaliers | 139 | 29–333 | Agence du revenu du Canada, 2022; Colbert, 2020; Base de données sur les congés des patients, 2015–2019 Note de bas de page 40Note de bas de page 41Note de bas de page 42Note de bas de page 43Note de bas de page 50Note de bas de page 51 |
| Transport vers les soins ambulatoires | 3,7 | 2,8–4,6Note de bas de page a | Agence du revenu du Canada, 2022; Pong et Pitblado 2005 Note de bas de page 51Note de bas de page 52 |
| Augmentation relative des coûts directs dans un contexte de coûts plus élevés | |||
| Cas en milieu hospitalier | 1,8 | - | CCNII Note de bas de page 53 |
| Cas en milieu ambulatoire | 1,2 | - | |
| Déplacement pour un cas en milieu ambulatoire | 33 | - | |
| Journées de travail perdues (16 ans et plus) | |||
| IIP ou POCP en milieu hospitalier | 15 | 9–29 | Pasquale et al., 2019 Note de bas de page 54 |
| POCP en milieu ambulatoire | 5,4 | 1,8–6,3 | |
| Réduction de l'emploi chez les patients souffrant de séquelles post-méningite (%) | |||
| Séquelles auditives | 25 | 15–35 | Bizier et al., 2016; Jiang et al., 2012 Note de bas de page 55Note de bas de page 56 |
| Séquelles neurologiques | 98 | 75–100 | Jiang et al., 2012; Hypothèse Note de bas de page 56 |
| Journées de travail perdues pour les aidants, IIP | |||
| Moins de 5 ans | 11,2 | 9,4–13,0 | Base de données sur les congés des patients, 2015–2019 Note de bas de page 40Note de bas de page 41Note de bas de page 42Note de bas de page 43 |
| 5 à 15 ans | 9,9 | 7,8–12,0 | |
| 16 ans et plus | 5,4 | 1,5–10,8 | Wyrwich et al., 2015 Note de bas de page 57 |
| Journées de travail perdues pour les aidants, POCP en milieu hospitalier | |||
| Moins de 5 ans | 4,2 | 4,2–4,3 | Base de données sur les congés des patients, 2015–2019 Note de bas de page 40Note de bas de page 41Note de bas de page 42Note de bas de page 43 |
| 5 à 15 ans | 5,0 | 7,8–12,0 | |
| 16 ans et plus | 5,4 | 1,5–10,8 | Wyrwich et al., 2015 Note de bas de page 57 |
| Journées de travail perdues pour les aidants, POCP en milieu ambulatoire | |||
| Moins de 16 ans | 5,4 | 1,8–6,3 | Pasquale et al., 2019; Hypothèse Note de bas de page 54 |
| 16 ans et plus | 1,1 | 1,0–1,2 | Dubé et al., 2011 Note de bas de page 58 |
| Journées de travail perdues pour les aidants, OMA | |||
| OMA | 1,3 | 0,8–1,7 | Barber et al., 2014; Dubé et al., 2011 Note de bas de page 58Note de bas de page 59 |
| Pose d'un tube auriculaire | 2,1 | – | Petit et al., 2003 Note de bas de page 60 |
| Journées de travail perdues pour les aidants, séquelles | |||
| Séquelles auditives (annuelles) | 0 | – | Hypothèse |
| Séquelles neurologiques (annuelles) | 190 | 146–240Note de bas de page a | Ganapathy et al., 2015 Note de bas de page 61 |
| Journées de travail perdues pour les aidants, vaccination | |||
| Visite chez le professionnel de la santé pour la vaccination | 0,5 | – | Hypothèse |
| Revenu d'emploi moyen ($) | |||
| Adultes de 16 ans et plus | Valeurs spécifiques à l'âge | – | Statistique Canada Note de bas de page 62 |
| Soignant | 58 811 | – | |
| Taux de population active (%) | |||
| Adultes de 16 ans et plus | Valeurs spécifiques à l'âge | – | Statistique Canada Note de bas de page 63 |
| Aidant (25 à 54 ans) | 87 | – | |
Note de bas de tableau 3
Abréviations : CCNI, Comité consultatif national de l'immunisation; IIP, infection invasive à pneumocoque; OMA, otite moyenne aiguë; Pneu-C, vaccin pneumococcique conjugué; POCP, pneumonie d'origine communautaire à pneumocoques; –, sans objet
|
|||
| Paramètre | Base | Plage | Référence(s) |
|---|---|---|---|
| Utilité de la santé en arrière-plan | |||
| Moins de 6 ans | 0,97 | 0,96–0,98 | Molina et al., 2023; Hypothèse Note de bas de page 64 |
| 6 à 11 ans | 0,95 | 0,94–0,96 | Molina et al., 2023 Note de bas de page 64 |
| 12 à 17 ans | 0,89 | 0,87–0,91 | Yan et al., 2023 Note de bas de page 65 |
| 18 à 24 ans | 0,879 | 0,863–0,895 | |
| 25 à 34 ans | 0,881 | 0,864–0,898 | |
| 35 à 44 ans | 0,878 | 0,863–0,893 | |
| 45 à 54 ans | 0,855 | 0,838–0,872 | |
| 55 à 64 ans | 0,839 | 0,822–0,856 | |
| 65 à 74 ans | 0,867 | 0,849–0,885 | |
| 75 ans et plus | 0,861 | 0,835–0,887 | |
| Décrément de l'utilité de l'IIP | |||
| Moins de 19 ans | 0,028 | 0,0165–0,0308 | Tang et al., 2022; Hypothèse Note de bas de page 66 |
| 19 à 64 ans | 0,0533 | 0,0425–0,0547 | |
| 65 ans et plus | 0,0745 | 0,0001–0,0745 | |
| Décrément de l'utilité de la POCP en milieu ambulatoire | |||
| Moins de 19 ans | 0,0004 | 0,0001–0,0329 | Tang et al., 2022 Note de bas de page 66 |
| 19 à 64 ans | 0,0094 | 0,0001–0,0205 | |
| 65 ans et plus | 0,0586 | 0,0271–0,0659 | |
| Décrément de l'utilité de la POCP en milieu hospitalier | |||
| Moins de 19 ans | 0,0105 | 0,001–0,0155 | Tang et al., 2022; Hypothèse Note de bas de page 66 |
| 19 à 64 ans | 0,0396 | 0,0001–0,168 | |
| 65 ans et plus | 0,1154 | 0,0068–0,29 | |
| Décrément de l'utilité de l'OMA | |||
| Moins de 10 ans | 0,0016 | 0–0,1461 | Tang et al., 2022 Note de bas de page 66 |
| Décrément de l'utilité des séquelles auditives (par an) | |||
| Moins de 19 ans | 0,2137 | 0,07–0,72 | Tang et al., 2022 Note de bas de page 66 |
| 19 ans et plus | 0,365 | 0,273–0,418 | Tang et al., 2022; Hypothèse Note de bas de page 66 |
| Décrément de l'utilité des séquelles neurologiques (par an) | |||
| Moins de 19 ans | 0,2456 | 0,16–0,49 | Tang et al., 2022 Note de bas de page 66 |
| 19 ans et plus | 0,5278 | 0,22–0,783 | Tang et al., 2022; Hypothèse Note de bas de page 66 |
Abréviations : IIP, infection invasive à pneumocoque; OMA, otite moyenne aiguë; Pneu-C, vaccin pneumococcique conjugué; POCP, pneumonie d'origine communautaire à pneumocoques |
|||
Afin de comparer les trois stratégies de vaccination, nous avons effectué une analyse coût/efficacité séquentielle Note de bas de page 38. En bref, les trois stratégies de vaccination ont été classées du coût le plus faible au coût le plus élevé. Les coûts différentiels et les AVAQ gagnées ont été comparés entre une stratégie donnée et la stratégie suivante la moins coûteuse. Une stratégie de vaccination a été considérée comme dominée si au moins une autre stratégie de vaccination devait permettre d'obtenir des AVAQ supplémentaires à un coût moindre.
Scénarios et analyses de sensibilité
Nous avons effectué une analyse de scénario pour estimer l'incidence potentielle des effets indirects du vaccin sur le RCED, en incluant une diminution exponentielle de l'incidence de l'IP causée par les sérotypes spécifiques à Pneu-C-15 (i.e., 22F et 33F) et les sérotypes spécifiques à Pneu-C-20 (i.e., 8, 10A, 11A, 12F, 15B, 22F et 33F) dans tous les groupes d'âge. Nous avons inclus un déclin exponentiel allant de 0 % à 50 %, les effets commençant un an après la mise en œuvre du programme de vaccination et prenant de cinq à dix ans pour atteindre leur effet maximal.
Nous avons également évalué le rapport coût/efficacité des trois stratégies de vaccination dans un contexte où les coûts sont plus élevés et l'incidence de l'IP plus forte, comme dans la région circumpolaire Note de bas de page 18Note de bas de page 67. Les risques relatifs spécifiques à l'âge ont été calculés en comparant l'incidence des IIP au Yukon, dans les Territoires du Nord-Ouest et au Nunavut à celle de l'ensemble du Canada (y compris les territoires) Note de bas de page 18. Une mesure relative de l'augmentation des coûts associés aux soins médicaux au Yukon, dans les Territoires du Nord-Ouest et au Nunavut par rapport à l'ensemble du Canada a été extraite d'une analyse économique des vaccins pneumococciques chez les personnes âgées Note de bas de page 53. Nous avons appliqué ces multiplicateurs aux résultats de santé attribués à S. pneumoniae et aux coûts pertinents dans notre analyse du cas de référence.
En plus d'une analyse de sensibilité probabiliste, nous avons effectué des analyses de sensibilité déterministes afin d'examiner la fiabilité des résultats du scénario de référence par rapport à nos hypothèses. En premier lieu, nous avons examiné l'incidence de la variation des paramètres clés du modèle dans notre scénario de référence dans le cadre d'une analyse de sensibilité à sens unique. Les paramètres variaient dans un intervalle de valeurs (tableaux 1 à 4). Deuxièmement, compte tenu de l'incertitude des prix de Pneu-C-15 et de Pneu-C-20, nous avons effectué une analyse de sensibilité à deux niveaux. Nous avons fait varier le prix différentiel de Pneu-C-15 et de Pneu-C-20 pour qu'il soit jusqu'à 50 % plus élevé que le prix présumé de Pneu-C-13. Ensuite, nous avons réduit l'incidence de la POCP et de l'OMA dans notre modèle, en tenant compte des données de la Colombie-Britannique Note de bas de page 19. Les données de l'Ontario ont servi de base à notre analyse du cas de référence. Enfin, nous avons réduit le nombre de cas d'OMA, probablement évitables par l'utilisation de Pneu-C-15 ou de Pneu-C-20 par rapport à Pneu-C-13. Cela reflète l'incidence plus faible de l'OMA attribuée aux sérotypes vaccinaux Pneu-C-15 et Pneu-C-20 aux États-Unis Note de bas de page 68.
Bien que le Canada n'ait pas fixé de seuil de coût/efficacité, nous avons utilisé deux seuils courants, 30 000 $ par AVAQ et 60 000 $ par AVAQ, dans nos analyses de scénario et de sensibilité à des fins d'illustration Note de bas de page 69Note de bas de page 70.
Notre étude suit les normes consolidées de rapport d'évaluation économique de la santé (CHEERS) 2022 de la Professional Society for Health Economics and Outcomes Research (ISPOR).
Résultats
L'utilisation de Pneu-C-15 et de Pneu-C-20 a permis d'éviter, sur une période de 10 ans, des effets de santé supplémentaires attribuables à S. pneumoniae, par rapport à l'utilisation continue de Pneu-C-13 (figure 2). En moyenne, Pneu-C-15 a permis d'éviter 221 (écart interquartile [EI] : 206–233) cas d'IIP, 337 (EI : 533–976), cas de POCP en milieu hospitalier, 7 428 (EI : 6 965–7 885) cas de POCP en milieu ambulatoire et 51 143 (EI : 47 184–55 089) cas d'OMA dans la population canadienne par rapport à l'utilisation continue de Pneu-C-13 dans notre scénario de référence. Le vaccin Pneu-C-20 a permis d'éviter 468 (EI : 436–494) cas d'IIP, 730 (EI : 533–976) cas de POCP en milieu hospitalier, 16 084 (EI : 15 082–17 071) cas de POCP en milieu ambulatoire et 109 527 (EI : 101 054–117 926) cas d'OMA comparé à Pneu-C-13.
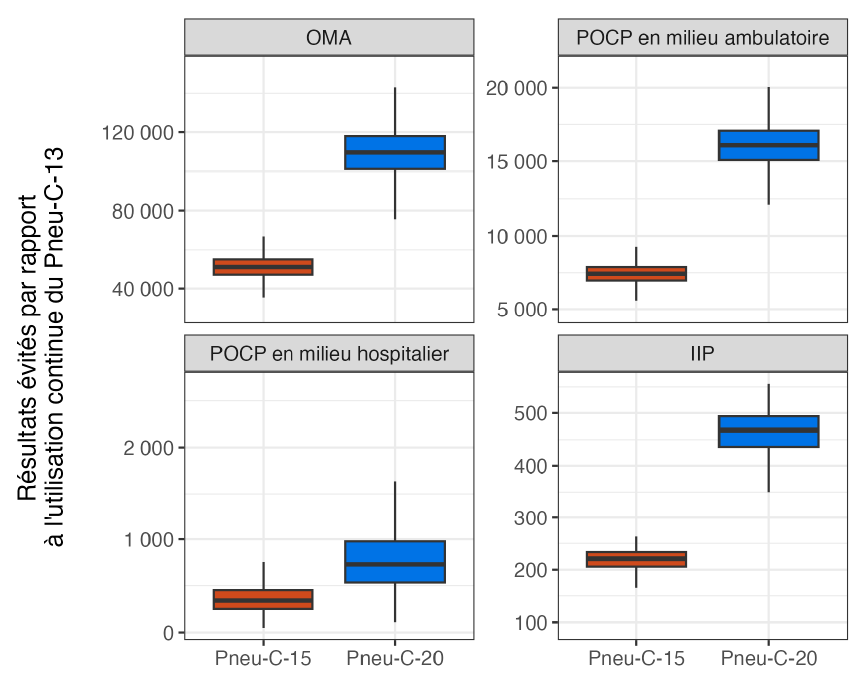
Figure 2 : Équivalent textuel
| Stratégie | Résultat | Minimum | Limite inférieure | Médiane | Limite supérieure | Maximum | |
|---|---|---|---|---|---|---|---|
| 1 | Pneu-C-15 | OMA | 35 369 | 47 183 | 51 143 | 55 089 | 66 903 |
| 2 | Pneu-C-20 | OMA | 75 773 | 101 054 | 109 527 | 117 926 | 14 3075 |
| 3 | Pneu-C-15 | POCP en milieu ambulatoire | 5 588 | 6 965 | 7 428 | 7 885 | 9 263 |
| 4 | Pneu-C-20 | POCP en milieu ambulatoire | 12 098 | 15 082 | 16 084 | 17 071 | 20 049 |
| 5 | Pneu-C-15 | POCP en milieu hospitalier | 50 | 246 | 337 | 451 | 756 |
| 6 | Pneu-C-20 | POCP en milieu hospitalier | 107 | 533 | 730 | 976 | 1 638 |
| 7 | Pneu-C-15 | IIP | 165 | 206 | 221 | 233 | 263 |
| 8 | Pneu-C-20 | IIP | 350 | 436 | 468 | 494 | 556 |
Notes de bas de page figure 2
Abréviations : IIP, infection invasive à pneumocoque; OMA, otite moyenne aiguë; Pneu-C, vaccin pneumococcique conjugué; POCP, pneumonie d'origine communautaire à pneumocoques
- Figure 2 note de bas de page a
-
Les résultats sont présentés pour 10 000 simulations de modèles
Du point de vue du système de santé, le remplacement de Pneu-C-13 par Pneu-C-15 devrait permettre de gagner en moyenne 497 AVAQ et coûter 30 millions de dollars supplémentaires sur 10 ans (tableau 5). Le remplacement de Pneu-C-13 par Pneu-C-20 devrait permettre de gagner en moyenne 1 039 AVAQ et coûter 103 millions de dollars supplémentaires sur dix ans. Du point de vue sociétal, Pneu-C-15 devrait coûter 9 millions de dollars supplémentaires et Pneu-C-20 60 millions de dollars supplémentaires sur 10 ans par rapport à l'utilisation continue de Pneu-C-13. Du point de vue du système de santé, Pneu-C-15 est plus susceptible d'être la stratégie optimale à des seuils de coût/efficacité compris entre 43 000 $ et 127 000 $ par AVAQ (figure 3). Au-delà de 127 000 $ par AVAQ, Pneu-C-20 est plus susceptible d'être la stratégie optimale. Du point de vue sociétal, Pneu-C-15 est plus susceptible d'être la stratégie optimale à des seuils de coût/efficacité compris entre 3 000 $ et 86 000 $ par AVAQ, et Pneu-C-20 à des seuils supérieurs à 86 000 $ par AVAQ.
| Stratégie | Effet (AVAQ perdues) |
Coût (millions de dollars) |
RCED séquentiel ($/AVAQ) |
|---|---|---|---|
| Perspective du système de santé | |||
| Pneu-C-13 | 229 769 | 4 945 | - |
| Pneu-C-15 | 229 272 | 4 975 | 58 823 |
| Pneu-C-20 | 228 730 | 5 048 | 135 289 |
| Perspective sociétale | |||
| Pneu-C-13 | 229 769 | 432 243 | - |
| Pneu-C-15 | 229 272 | 432 252 | 18 272 |
| Pneu-C-20 | 228 730 | 432 303 | 93 416 |
Abréviations : AVAQ, année de vie ajustée par la qualité; Pneu-C, vaccin pneumococcique conjugué; RCED, rapport coût/efficacité différentiel |
|||
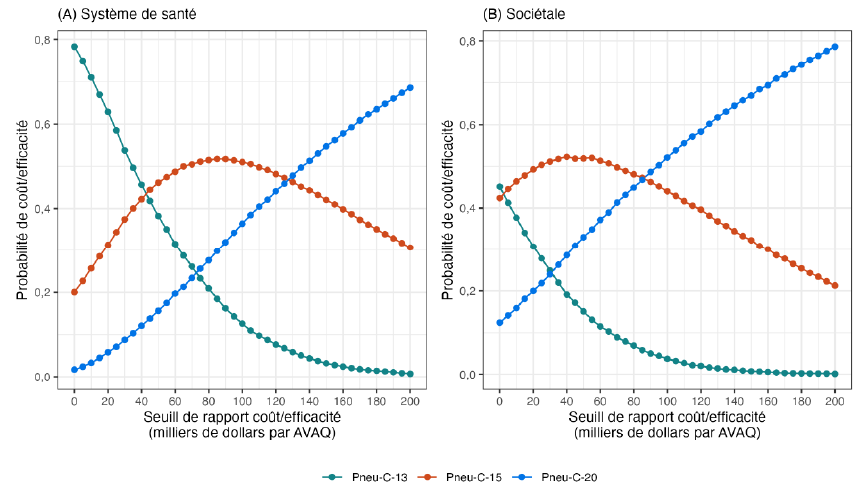
Figure 3 : Équivalent textuel
Ce graphique linéaire à deux panneaux montre le pourcentage de simulations pour lesquelles chaque stratégie de vaccination était optimale pour un seuil de rentabilité donné. Le panneau A montre les résultats pour la perspective du système de santé et le panneau B montre les résultats pour la perspective sociétale. L'axe des x est étiqueté « Seuil de rapport coût/efficacité (milliers de dollars par AVAQ) » et l'échelle va de 0 à 200. L'axe des y est étiqueté « Probabilité de coût/efficacité » et va de 0 à 0,8. Il y a des lignes sur le graphique pour chaque stratégie de vaccination : Pneu-C-13, Pneu-C-15, et Pneu-C-20, et les lignes montrent la probabilité qu'une stratégie donnée soit optimale pour un seuil de rentabilité donné, basée sur 10 000 simulations du modèle. Pour la perspective du système de santé, à des valeurs de seuil basses, Pneu-C-13 a la probabilité la plus élevée. Pour des valeurs de seuil entre 43 000 $ et 127 000 $, Pneu-C-15 a la probabilité la plus élevée. Au-dessus de 127 000 $, Pneu-C-20 a la probabilité la plus élevée. Pour la perspective sociétale, Pneu-C-15 a la probabilité la plus élevée pour des seuils de 3 000 $ à 86 000 $, avec Pneu-C-20 ayant la probabilité la plus élevée pour des seuils supérieurs à 86 000 $.
Abréviations : AVAQ, année de vie ajustée par la qualité; Pneu-C, vaccin pneumococcique conjugué
La prise en compte des effets indirects mène des RCED plus faibles en raison de la réduction de l'IP parmi les membres de la population qui n'ont pas reçu le vaccin (figure 4). À un seuil de coût/efficacité de 30 000 $ par AVAQ, une réduction de 5 % de l'IP causée par les sérotypes supplémentaires contenus dans Pneu-C-15 sur une période de six ans ferait de ce vaccin la stratégie optimale. À un seuil de coût/efficacité de 30 000 $ par AVAQ, une diminution de 10 % ou plus de l'IP causée par les sérotypes supplémentaires contenus dans Pneu-C-20 sur une période de cinq ans ferait de ce vaccin la stratégie de préférence. D'une perspective sociétale, des effets indirects encore plus faibles feraient de Pneu-C-15 ou de Pneu-C-20 la stratégie optimale.
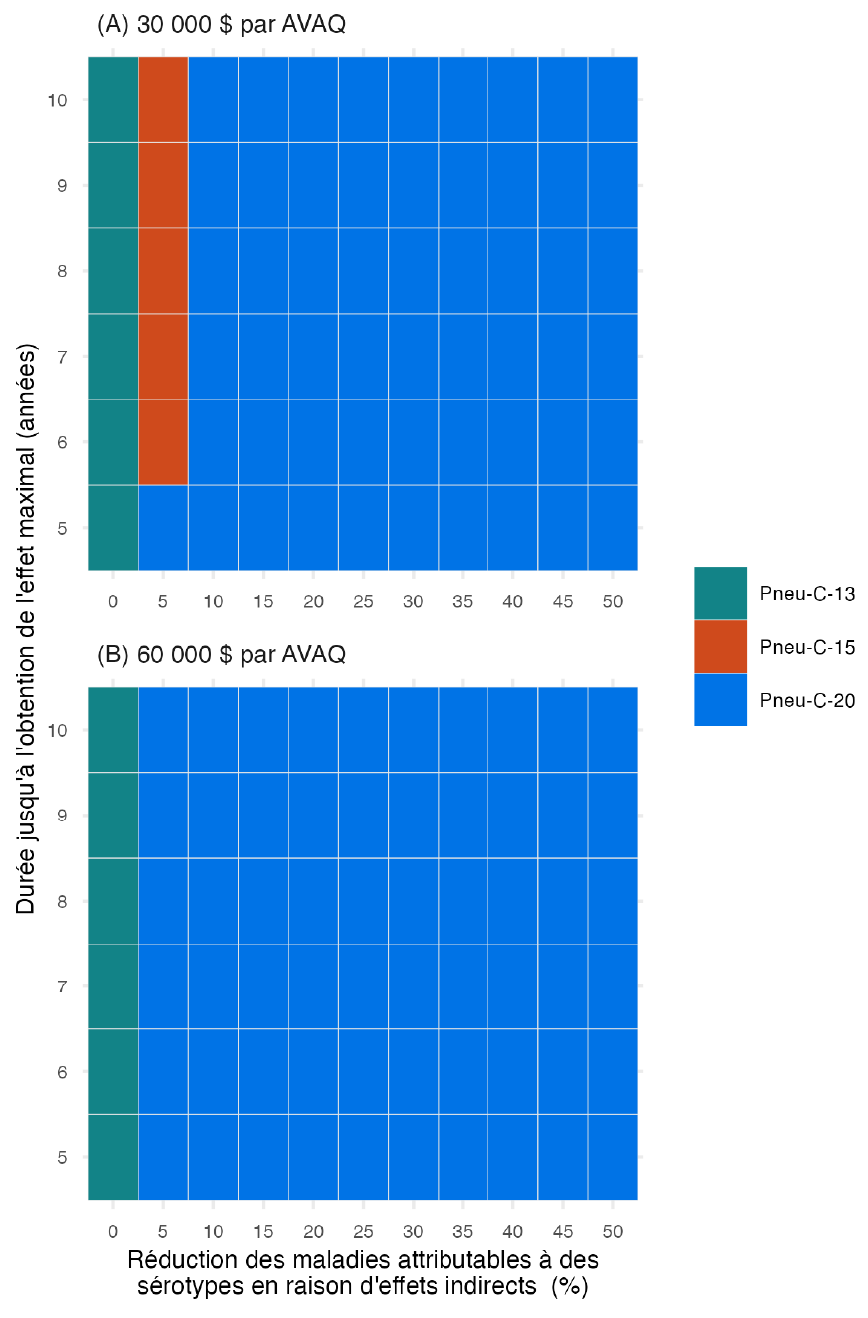
Figure 4 : Équivalent textuel
Cette figure à deux panneaux montre comment la stratégie la plus coût-efficace change lorsque les effets indirects sont incorporés. Le panneau A montre les résultats pour un seuil de coût-efficacité de 30 000 $ par AVAQ et le panneau B montre les résultats pour 60 000 $ par AVAQ. Pour chaque figure, l'axe des x montre la réduction en pourcentage de la maladie pneumococcique due aux sérotypes supplémentaires contenus dans Pneu-C-15 ou Pneu-C-20, et varie de 0 % à 50 % par incréments de 5 %. L'axe des y montre le temps nécessaire jusqu'à ce que l'effet maximal soit atteint, allant de 5 à 10 ans. Pour chaque combinaison de valeurs des axes x et y, il y a un carré ombré qui montre quelle stratégie est optimale pour le seuil de coût-efficacité associé. Dans les deux panneaux, Pneu-C-13 est la stratégie optimale lorsque la valeur de l'axe des x est de 0, représentant l'hypothèse de base de l'absence d'effets indirects. Pour le panneau supérieur, Pneu-C-15 est la stratégie optimale lorsque l'ampleur des effets indirects est de 5 % et le temps nécessaire pour atteindre cet effet est de six ans ou plus. Pour le reste des combinaisons de paramètres au seuil de 30 000 $ par AVAQ, Pneu-C-20 est la stratégie optimale. Pour le panneau inférieur, le reste du graphique montre que Pneu-C-20 est la stratégie optimale pour le seuil de 60 000 $ par AVAQ.
Notes de bas de page figure 4
Abréviations : AVAQ, année de vie ajustée par la qualité; Pneu-C, vaccin pneumococcique conjugué
- Figure 4 note de bas de page a
-
Les résultats sont fonction du pourcentage de réduction de la maladie attribuable au sérotype dû aux effets indirects et du temps nécessaire pour atteindre l'effet maximal
Dans un contexte de coûts et d'incidence d'IP plus élevés, Pneu-C-15 a permis d'éviter en moyenne 925 (EI : 859–979) cas d'IIP, 1 116 (EI : 855–1 545), cas de POCP en milieu hospitalier, 25 638 (EI : 24 055–27 254) cas de POCP en milieu ambulatoire et 190 760 (EI : 175 466–205 884) cas d'OMA en moyenne sur 10 ans par rapport à l'utilisation continue de Pneu-C-13 (l'appendice, figure A1). Le vaccin Pneu-C-20 a permis d'éviter 1 808 (EI : 1 680–1 914) cas d'IIP, 2 294 (EI : 1 683–3 039), cas de POCP en milieu hospitalier, 50 446 (EI : 47 333–53 624) cas de POCP en milieu ambulatoire et 373 543 (EI : 343 610–403 099) cas d'OMA comparé à Pneu-C-13. Le vaccin Pneu-C-20 domine (i.e., qu'il est moins coûteux et plus efficace que les vaccins Pneu-C-13 et Pneu-C-15) du point de vue du système de santé et de la société (l'appendice, tableau A1). Le vaccin Pneu-C-20 est dominant, avec des coûts inférieurs et moins d'AVAQ perdues que la stratégie actuelle (i.e., Pneu-C-13) et que Pneu-C-15.
Les conclusions de notre scénario de référence reposent sur plusieurs hypothèses que nous avons examinées dans le cadre d'analyses de sensibilité. Dans notre analyse de sensibilité à sens unique des paramètres du modèle, le prix du vaccin était le paramètre le plus influent (non représenté). Lorsque les prix relatifs des vaccins Pneu-C-15 et Pneu-C-20 par rapport à Pneu-C-13 ont été augmentés par rapport à leurs valeurs dans le scénario de référence, Pneu-C-13 est resté la stratégie présentant le RCED le plus bas (figure 5). Au seuil de 30 000 $ par AVAQ, Pneu-C-15 était la stratégie optimale lorsque l'augmentation relative de son prix était de 5 % ou moins par rapport au prix de Pneu-C-13. Le vaccin Pneu-C-20 était la stratégie optimale lorsque l'augmentation relative de son prix était de 10 % ou moins par rapport au prix de Pneu-C-13. Au seuil de 60 000 $ par AVAQ, Pneu-C-15 ou Pneu-C-20 étaient la stratégie optimale lorsque l'augmentation relative de leurs prix était de 5 % ou de 15 % ou moins que le prix de Pneu-C-13, respectivement. Une incidence plus faible de la POCP et de l'OMA a conduit à des RCED séquentiels de plus de 100 000 $ par AVAQ pour Pneu-C-15 et de plus de 200 000 $ par AVAQ pour Pneu-C-20. De plus, une distribution des sérotypes d'OMA plus proche de celle des États-Unis, qui diffère de la distribution des sérotypes d'IIP au Canada, entraîne des RCED séquentiels de plus de 100 000 $ par AVAQ pour Pneu-C-15 et Pneu-C-20.

Figure 5 : Équivalent textuel
Ce figure à deux panneaux montre comment la stratégie la plus rentable change pour différents prix relatifs par dose de Pneu-C-15 et de Pneu-C-20 par rapport à Pneu-C-13, dont le prix présumé est de 71,50 $ par dose. L'axe des x montre l'augmentation en pourcentage du prix par dose de Pneu-C-15 par rapport à Pneu-C-13 et l'axe des y montre l'augmentation en pourcentage du prix par dose de Pneu-C-20 par rapport à Pneu-C-13. Les intervalles pour les deux axes vont de 0 % à 50 %. Le panneau A présente les résultats pour un seuil de coût/efficacité de 30 000 $ par AVAQ et le panneau B les résultats pour 60 000 $ par AVAQ. Pour chaque combinaison de valeurs des axes x et y, un carré ombré indique laquelle des trois stratégies, Pneu-C-13, Pneu-C-15 ou Pneu-C-20, est la stratégie optimale pour le seuil de coût/efficacité donné. Pour le panneau supérieur, qui utilise un seuil de coût/efficacité de 30 000 $, Pneu-C-13 est la stratégie optimale, sauf si l'augmentation relative du prix de Pneu-C-15 est de 5 % ou moins, ou si l'augmentation relative du prix de Pneu-C-20 est de 10 % ou moins. Pour le panneau inférieur, qui utilise un seuil de coût/efficacité de 60 000 $, Pneu-C-13 est la stratégie optimale, sauf si l'augmentation relative du prix par dose de Pneu-C-15 est de 5 % ou moins, ou que l'augmentation relative du prix de Pneu-C-20 est de 15 % ou moins.
Notes de bas de page figure 5
Abréviations : AVAQ, année de vie ajustée par la qualité; Pneu-C, vaccin pneumococcique conjugué
- Figure 5 note de bas de page a
-
Des rapports coût/efficacité différentiels ont été calculés pour une gamme de prix par dose pour Pneu-C-15 et Pneu-C-20, allant de 0 % à 50 % de plus que le prix de Pneu-C-13
- Figure 5 note de bas de page b
-
La stratégie optimale a été identifiée pour des seuils de coût/efficacité de 30 000 $ et 60 000 $ par AVAQ du point de vue du système de santé
Discussion
Nous avons réalisé une évaluation économique pour estimer l'incidence sur la santé et le rapport coût/efficacité du remplacement de Pneu-C-13 par Pneu-C-15 ou par Pneu-C-20 pour une utilisation systématique dans la population pédiatrique au Canada. Les résultats de notre scénario de référence ont montré que Pneu-C-15 et Pneu-C-20 ont permis d'éviter des cas supplémentaires d'IIP, de POCP et d'OMA par rapport à l'utilisation continue de Pneu-C-13. Dans notre scénario de référence, Pneu-C-15 devrait atteindre un seuil de 58 823 $ par AVAQ du point de vue du système de santé et de 18 272 $ par AVAQ du point de vue de la société pour être considéré comme rentable. Le vaccin Pneu-C-20 devrait atteindre un seuil de 135 289 $ par AVAQ du point de vue du système de santé et de 93 416 $ par AVAQ du point de vue de la société pour être considéré comme rentable. En revanche, si l'on tient compte des effets indirects modérés du vaccin (e.g., une réduction de 5 % ou plus de l'IP attribuable au sérotype), Pneu-C-15 et Pneu-C-20 peuvent tous deux être considérés comme rentables à des seuils inférieurs à 30 000 $ par AVAQ du point de vue du système de santé et de la société. Dans un contexte de coûts et d'incidence d'IP plus élevés, Pneu-C-20 domine les autres stratégies de vaccination.
Une analyse comparative récente de trois modèles de coût/utilité menée aux États-Unis a comparé Pneu-C-20 à Pneu-C-15 ou Pneu-C-13 selon un calendrier 3+1 chez les enfants de moins de deux ans Note de bas de page 71. Elle a montré des tendances semblables à celles de notre analyse, Pneu-C-20 devant entraîner le gain le plus important en termes de résultats de santé par rapport aux autres vaccins. Du point de vue de la société, les résultats varient entre les trois modèles inclus, avec des RCED pour Pneu-C-20 allant de dominant à 162 700 $ par AVAQ par rapport à Pneu-C-15. Les modèles inclus dans cette analyse étaient tous statiques, mais différaient en termes de structure, d'horizon analytique, d'hypothèses sur les effets indirects de la protection et de paramètres clés, soulignant davantage la sensibilité des résultats de ces évaluations économiques fondées sur des modèles aux hypothèses et aux paramètres d'entrée des modèles Note de bas de page 13.
Le rapport coût/efficacité estimé des différents vaccins conjugués dépendait en partie de la présence ou de l'absence d'effets indirects. Après l'introduction de Pneu-C-13 dans les populations pédiatriques, l'incidence des IIP causées par les sérotypes contenus dans le vaccin a diminué dans tous les groupes d'âge Note de bas de page 7Note de bas de page 8, mais l'incidence globale des IIP dans la population n'a pas diminué de manière substantielle Note de bas de page 10. Dans plusieurs pays, dont le Canada, l'introduction de vaccins pneumococciques conjugués (Pneu-C-7, Pneu-C-10 et Pneu-C-13) a entraîné une augmentation de l'incidence des IIP causées par des sérotypes non inclus dans les vaccins, quel que soit l'âge Note de bas de page 72Note de bas de page 73. Dans notre analyse de référence, nous avons pris soin de ne pas inclure les effets indirects, compte tenu de l'incertitude des effets de l'immunité collective et du remplacement des sérotypes. Dans notre analyse de scénario, nous avons modélisé les effets indirects comme une diminution des infections pneumococciques dans la population plus large ne recevant pas les vaccins conjugués à valent plus élevé.
L'incertitude concernant le prix des vaccins dans le contexte canadien complique l'interprétation de nos résultats, étant donné l'influence des prix de Pneu-C-15 et de Pneu-C-20 sur les RCED estimés. Dans l'analyse de sensibilité, nous avons démontré qu'à des prix différentiels inférieurs au prix par dose de Pneu-C-13, les deux vaccins à valent plus élevé peuvent être des options rentables. Notre analyse donne une indication des prix auxquels l'un ou l'autre vaccin peut devenir la stratégie optimale sur la base des seuils couramment utilisés.
Limites
Comme nous avons utilisé un modèle statique, notre approche n'a pas entièrement pris en compte la dynamique de transmission associée aux effets de l'immunité collective et au remplacement des sérotypes. Les futures évaluations économiques des vaccins pneumococciques conjugués devraient envisager d'utiliser des modèles dynamiques pour étayer les analyses coût/utilité, afin de mieux rendre compte de ces effets Note de bas de page 74.
De plus, notre évaluation économique était axée sur les enfants commençant leur série de vaccinations contre le pneumocoque. Nous n'avons pas évalué le rapport coût/efficacité des trois stratégies chez les enfants qui étaient à mi-parcours de leur série de vaccins ni l'incidence d'un éventuel programme de rattrapage. Nos estimations de l'incidence de l'IP ont pris en compte les enfants présentant un risque faible autant qu'un risque élevé d'IP. Nous n'avons pas identifié la stratégie de vaccination optimale de manière indépendante parmi les enfants présentant un risque élevé d'IP en dehors d'un contexte de coûts élevés.
Conclusion
Notre étude fournit des données probantes de l'incidence que Pneu-C-15 et Pneu-C-20 pourraient avoir sur la réduction du fardeau de l'IP au Canada par rapport à l'utilisation continue de Pneu-C-13. Bien que les RCED soient relativement élevés dans l'analyse du scénario de référence, les deux vaccins ont le potentiel d'améliorer la santé de manière rentable si les prix des vaccins sont plus bas ou en présence d'effets indirects dans l'ensemble de la population après l'introduction du vaccin.
Déclaration des auteurs
- A. S. — Conceptualisation, analyse formelle, rédaction de la version originale
- G. G. — Conceptualisation, analyse formelle, rédaction–révision et édition
- R. P. — Conceptualisation, rédaction–révision et édition
- A. W. — Conceptualisation, rédaction–révision et édition
- M. T. — Conceptualisation, rédaction–révision et édition
- A. T. — Conceptualisation, analyse, modélisation, rédaction–révision et édition, supervision
Intérêts concurrents
Aucun.
Identifiants ORCID
- Alison E Simmons — 0000-0001-8780-9467
- Gebremedhin B Gebretekle — 0000-0002-2485-505X
- Robert Pless — 0009-0004-4779-0844
- Aleksandra Wierzbowski — 0009-0002-7139-8450
- Matthew Tunis — 0000-0003-2092-9143
- Ashleigh R Tuite — 0000-0002-4373-9337
Remerciements
Les auteurs remercient les membres du groupe de travail sur le pneumocoque du Comité consultatif national de l'immunisation, qui ont donné leur rétroaction durant la mise au point du modèle.
Financement
Aucun.
Références
- Notes de bas de page 1
-
Scelfo C, Menzella F, Fontana M, Ghidoni G, Galeone C, Facciolongo NC. Pneumonia and Invasive Pneumococcal Diseases: The Role of Pneumococcal Conjugate Vaccine in the Era of Multi-Drug Resistance. Vaccines (Basel) 2021;9(5):420. https://doi.org/10.3390/vaccines9050420
- Notes de bas de page 2
-
van Hoek AJ, Andrews N, Waight PA, George R, Miller E. Effect of serotype on focus and mortality of invasive pneumococcal disease: coverage of different vaccines and insight into non-vaccine serotypes. PLoS One 2012;7(7):e39150. https://doi.org/10.1371/journal.pone.0039150
- Notes de bas de page 3
-
Greenberg D, Givon-Lavi N, Newman N, Bar-Ziv J, Dagan R. Nasopharyngeal carriage of individual Streptococcus pneumoniae serotypes during pediatric pneumonia as a means to estimate serotype disease potential. Pediatr Infect Dis J 2011;30(3):227–33. https://doi.org/10.1097/INF.0b013e3181f87802
- Notes de bas de page 4
-
Desai S, McGeer A, Quach-Thanh C, Elliott D; approuvée par le CCNI. Mise à jour sur l’utilisation des vaccins conjugués contre le pneumocoque chez les enfants : Une déclaration d’un comité consultatif (DCC) : Comité consultatif national de l’immunisation (CCNI). Relevé des maladies transmissibles au Canada 2010;36(DCC-12):1–23. https://doi.org/10.14745/ccdr.v36i00a12f
- Notes de bas de page 5
-
Greenberg D, Hoover PA, Vesikari T, Peltier C, Hurley DC, McFetridge RD, Dallas M, Hartzel J, Marchese RD, Coller BG, Stek JE, Abeygunawardana C, Winters MA, MacNair JE, Pujar NS, Musey L. Safety and immunogenicity of 15-valent pneumococcal conjugate vaccine (PCV15) in healthy infants. Vaccine 2018;36(45):6883–91. https://doi.org/10.1016/j.vaccine.2018.02.113
- Notes de bas de page 6
-
Hurley D, Griffin C, Young M, Scott DA, Pride MW, Scully IL, Ginis J, Severs J, Jansen KU, Gruber WC, Watson W. Safety, Tolerability, and Immunogenicity of a 20-Valent Pneumococcal Conjugate Vaccine (PCV20) in Adults 60 to 64 Years of Age. Clin Infect Dis 2021;73(7):e1489–97. https://doi.org/10.1093/cid/ciaa1045
- Notes de bas de page 7
-
Wijayasri S, Hillier K, Lim GH, Harris TM, Wilson SE, Deeks SL. The shifting epidemiology and serotype distribution of invasive pneumococcal disease in Ontario, Canada, 2007-2017. PLoS One 2019;14(12):e0226353. https://doi.org/10.1371/journal.pone.0226353
- Notes de bas de page 8
-
Waye A, Chuck AW. Value Added by the Prevnar 13 Childhood Immunization Program in Alberta, Canada (2010-2015). Drugs Real World Outcomes 2015;2(3):311–8. https://doi.org/10.1007/s40801-015-0037-2
- Notes de bas de page 9
-
Agence de la santé publique du Canada. Maladies évitables par la vaccination : Rapport de surveillance en date du 31 décembre 2019. Ottawa, ON : ASPC; 2024. https://www.canada.ca/fr/sante-publique/services/publications/vie-saine/maladies-evitables-vaccination-rapport-surveillance-2019.html
- Notes de bas de page 10
-
Agence de la santé publique du Canada. Comité consultatif national de l'immunisation. Recommandations au niveau de la santé publique sur l’utilisation des vaccins contre le pneumocoque chez les adultes, y compris l’utilisation des vaccins conjugués 15-valent et 20-valent. Ottawa, ON : ASPC: 2023. https://www.canada.ca/fr/sante-publique/services/immunisation/comite-consultatif-national-immunisation-ccni/recommandations-niveau-sante-publique-utilisation-vaccins-contre-pneumocoque-adultes-compris-utilisation-vaccins-conjugues-15-valent-20-valent.html
- Notes de bas de page 11
-
Lewnard JA, Hanage WP. Making sense of differences in pneumococcal serotype replacement. Lancet Infect Dis 2019;19(6):e213–20. https://doi.org/10.1016/S1473-3099(18)30660-1
- Notes de bas de page 12
-
Golden A, Griffith A, Demczuk W, Lefebvre B, McGeer A, Tyrrell G, Zhanel G, Kus J, Hoang L, Minion J, Van Caeseele P, Smadi H, Haldane D, Zahariadis G, Mead K, Steven L, Strudwick L, Li A, Mulvey M, Martin I. Surveillance des pneumococcies invasives au Canada, 2020. Relevé des maladies transmissibles au Canada 2022;48(9):438–49. https://doi.org/10.14745/ccdr.v48i09a04f
- Notes de bas de page 13
-
Agence de la santé publique du Canada. Comité consultatif national de l'immunisation. Résumé de la déclaration du CCNI du 11 mars 2024 : Recommandations pour les programmes de santé publique concernant l’utilisation de vaccins contre le pneumocoque chez les enfants, y compris l’utilisation des vaccins conjugués 15-valent et 20-valent. Ottawa, ON : ASPC; 2024. https://www.canada.ca/fr/sante-publique/services/publications/vaccins-immunisation/comite-consultatif-national-immunisation-resume-recommandations-programmes-sante-publique-utilisation-vaccins-contre-pneumocoque-enfants-compris-utilisation-vaccins-conjugues-15-valent-20-valent.html
- Notes de bas de page 14
-
Statistique Canada. Tableau 98-10-0027-01. Âge (en années), âge moyen et âge médian et genre : Canada et régions de tri d'acheminement. Ottawa, ON : StatCan; 2021. [Consulté le 31 mars 2023]. https://www150.statcan.gc.ca/t1/tbl1/fr/tv.action?pid=9810002701
- Notes de bas de page 15
-
Statistique Canada. Tableau 13-10-0837-01. Espérance de vie et autres éléments de la table complète de mortalité, estimations sur un an, Canada, toutes les provinces sauf l’Île-du-Prince-Édouard. Ottawa, ON : StatCan; 2022. [Consulté le 31 mars 2023]. https://www150.statcan.gc.ca/t1/tbl1/fr/tv.action?pid=1310083701&request_locale=fr
- Notes de bas de page 16
-
Statistique Canada. Tableau 17-10-0057-01. Population projetée, selon le scénario de projection, l’âge et le genre, au 1er juillet (x 1 000). Ottawa, ON : StatCan; 2022. [Consulté le 31 mars 2023]. https://www150.statcan.gc.ca/t1/tbl1/fr/tv.action?pid=1710005701&request_locale=fr
- Notes de bas de page 17
-
Morrow A, De Wals P, Petit G, Guay M, Erickson LJ. The burden of pneumococcal disease in the Canadian population before routine use of the seven-valent pneumococcal conjugate vaccine. Can J Infect Dis Med Microbiol 2007;18(2):121–7. https://doi.org/10.1155/2007/713576
- Notes de bas de page 18
-
Agence de la santé publique du Canada. Pneumococcies invasives. Ottawa, ON : ASPC; 2023. https://www.canada.ca/fr/sante-publique/services/immunisation/maladies-pouvant-etre-prevenues-vaccination/pneumococcies-invasives/professionels.html
- Notes de bas de page 19
-
Nasreen S, Wang J, Sadarangani M, Kwong JC, Quach C, Crowcroft NS, Wilson SE, McGeer A, Morris SK, Kellner JD, Sander B, Kus JV, Hoang L, Marra F, Fadel SA. Estimating population-based incidence of community-acquired pneumonia and acute otitis media in children and adults in Ontario and British Columbia using health administrative data, 2005-2018: a Canadian Immunisation Research Network (CIRN) study. BMJ Open Respir Res 2022;9(1):e001218. https://doi.org/10.1136/bmjresp-2022-001218
- Notes de bas de page 20
-
King L. Pediatric outpatient ARI visits and antibiotic use attributable to serotypes in higher valency PCVs [slides presented at Advisory Committee on Immunization Practices (ACIP) meeting February 22, 2023]. Atlanta, GA: CDC; 2023. [Consulté le 14 mars 2023]. https://www.cdc.gov/vaccines/acip/meetings/downloads/slides-2023-02/slides-02-22/Pneumococcal-03-King-508.pdf
- Notes de bas de page 21
-
Pneumonia Etiology Research for Child Health (PERCH) Study Group. Causes of severe pneumonia requiring hospital admission in children without HIV infection from Africa and Asia: the PERCH multi-country case-control study. Lancet 2019;394(10200):757–79. https://doi.org/10.1016/S0140-6736(19)30721-4
- Notes de bas de page 22
-
LeBlanc JJ, ElSherif M, Ye L, MacKinnon-Cameron D, Ambrose A, Hatchette TF, Lang AL, Gillis HD, Martin I, Demczuk WH, Andrew MK, Boivin G, Bowie W, Green K, Johnstone J, Loeb M, McCarthy AE, McGeer A, Semret M, Trottier S, Valiquette L, Webster D, McNeil SA. Recalibrated estimates of non-bacteremic and bacteremic pneumococcal community acquired pneumonia in hospitalized Canadian adults from 2010 to 2017 with addition of an extended spectrum serotype-specific urine antigen detection assay. Vaccine 2022;40(18):2635–46. https://doi.org/10.1016/j.vaccine.2022.02.081
- Notes de bas de page 23
-
Kim SH, Jeon EJ, Hong SM, Bae CH, Lee HY, Park MK, Byun JY, Kim MG, Yeo SG. Bacterial Species and Antibiotic Sensitivity in Korean Patients Diagnosed with Acute Otitis Media and Otitis Media with Effusion. J Korean Med Sci 2017;32(4):672–8. https://doi.org/10.3346/jkms.2017.32.4.672
- Notes de bas de page 24
-
O’Reilly R, Lu H, Kwong JC, McGeer A, To T, Sander B. The epidemiology and healthcare costs of community-acquired pneumonia in Ontario, Canada: a population-based cohort study. J Med Econ 2023;26(1):293–302. https://doi.org/10.1080/13696998.2023.2176679
- Notes de bas de page 25
-
Jit M. The risk of sequelae due to pneumococcal meningitis in high-income countries: a systematic review and meta-analysis. J Infect 2010;61(2):114–24. https://doi.org/10.1016/j.jinf.2010.04.008
- Notes de bas de page 26
-
Canadian Institute for Health Information. Implantable medical devices in Canada: Insights into high-volume procedures and associated costs. Ottawa, ON: CIHI; 2020. https://secure.cihi.ca/free_products/implantable-medical-devices-report-en.pdf
- Notes de bas de page 27
-
Chuck AW, Jacobs P, Tyrrell G, Kellner JD. Pharmacoeconomic evaluation of 10- and 13-valent pneumococcal conjugate vaccines. Vaccine 2010;28(33):5485–90. https://doi.org/10.1016/j.vaccine.2010.05.058
- Notes de bas de page 28
-
Agence de la santé publique du Canada. Faits saillants de l'Enquête nationale sur la couverture vaccinale des enfants (ENCVE), 2019). Ottawa, ON : ASPC; 2023. https://www.canada.ca/fr/sante-publique/services/publications/vaccins-immunisation/2019-faits-saillants-enquete-nationale-couverture-vaccinale-enfants.html
- Notes de bas de page 29
-
Prasad N, Stoecker C, Xing W, Cho BH, Leidner AJ, Kobayashi M. Public health impact and cost-effectiveness of 15-valent pneumococcal conjugate vaccine use among the pediatric population of the United States. Vaccine 2023;41(18):2914–21. https://doi.org/10.1016/j.vaccine.2023.03.045
- Notes de bas de page 30
-
Farrar J, Nsofor C, Childs L, Kobayashi M, Pilishvili T, editors. Systematic Review of 13-Valent Pneumooccal Conjugate Vaccine Effectiveness Against Pneumonia Among Children. 12th International Symposium on Pneumococci and Pneumococcal Diseases: Toronto, ON; 2022. https://isppd2022.kenes.com/
- Notes de bas de page 31
-
Stoecker C. Economic assessment of routine PCV20 for children [slides presented at Advisory Committee on Immunization Practices (ACIP) meeting June 22, 2023]. Atlanta, GA: CDC; 2023. [Consulté le 24 juin 2023]. https://www.cdc.gov/vaccines/acip/meetings/downloads/slides-2023-06-21-23/02-Pneumococcal-Stoecker-508.pdf
- Notes de bas de page 32
-
Eskola J, Kilpi T, Palmu A, Jokinen J, Haapakoski J, Herva E, Takala A, Käyhty H, Karma P, Kohberger R, Siber G, Mäkelä PH; Finnish Otitis Media Study Group. Efficacy of a pneumococcal conjugate vaccine against acute otitis media. N Engl J Med 2001;344(6):403–9. https://doi.org/10.1056/NEJM200102083440602
- Notes de bas de page 33
-
Andrews NJ, Waight PA, Burbidge P, Pearce E, Roalfe L, Zancolli M, Slack M, Ladhani SN, Miller E, Goldblatt D. Serotype-specific effectiveness and correlates of protection for the 13-valent pneumococcal conjugate vaccine: a postlicensure indirect cohort study. Lancet Infect Dis 2014;14(9):839–46. https://doi.org/10.1016/S1473-3099(14)70822-9
- Notes de bas de page 34
-
Centers for Disease Control and Prevention. VFC CDC Vaccine Price List Archives. Atlanta, GA: CDC; 2024. https://www.cdc.gov/vaccines/programs/vfc/awardees/vaccine-management/price-list/2022/2022-04-01.html
- Notes de bas de page 35
-
Statistique Canada. Tableau 18-10-0005-01. Indice des prix à la consommation, moyenne annuelle, non désaisonnalisé. Ottawa, ON : StatCan; 2024. [Consulté le 31 mars 2023]. https://www150.statcan.gc.ca/t1/tbl1/fr/tv.action?pid=1810000501&request_locale=fr
- Notes de bas de page 36
-
R Core Team. R: A language and environment for statistical computing [Software]. 4.0 ed. Vienna (AT): R Foundation for Statistical Computing; 2020. [Consulté le 5 janv. 2024]. https://www.r-project.org/
- Notes de bas de page 37
-
Devleesschauwer B, Torgerson P, Charlier J, Levecke B, Praet N, Roelandt S, Smit S, Dorny P, Bervens D, Speybroeck N. Package “prevalence” Oct 14, 2022: Tools for prevalence assessment studies. R package version 0.4.1. 2022. https://cran.r-project.org/package=prevalence
- Notes de bas de page 38
-
Agence de la santé publique du Canada. Comité consultatif national de l'immunisation (CCNI) : Lignes directrices pour l'évaluation économique des programmes de vaccination au Canada. Ottawa, ON : ASPC; 2024. https://www.canada.ca/fr/sante-publique/services/immunisation/comite-consultatif-national-immunisation-ccni/methodes-processus/integration-donnees-economiques-recommandations-federales-relatives-vaccins/lignes-directrices-evaluation-programmes-vaccination-canada.html
- Notes de bas de page 39
-
O’Reilly RK, McGeer A, To T, Sander B. The Cost-Effectiveness of a Pneumococcal Conjugate Vaccine (PCV13) Program for Older Adults (65+) in Ontario, Canada: Update on the use of pneumococcal vaccine in immunocompetent adults 65 years of age and older – A Public Health Perspective in the Context of Infant Immunization and Changing Serotype Distributions. Pittsburgh, PA: Society for Medical Decision Making; 2017. https://smdm.org/meeting/39th-annual-north-american-meeting
- Notes de bas de page 40
-
Canadian Institute for Health Information. Data Quality Documentation, Discharge Abstract Database - Current-Year Information, 2015–2016. Ottawa, ON: CIHI; 2016. [Consulté le 31 mars 2023]. https://www.cihi.ca/sites/default/files/document/dad-data-quality_15-16_en.pdf
- Notes de bas de page 41
-
Canadian Institute for Health Information. Data Quality Documentation Discharge Abstract Database - Current-Year Information 2018–2019. Ottawa, ON: CIHI; 2019. [Consulté le 31 mars 2023]. https://www.cihi.ca/sites/default/files/document/current-year-information-dad-2018-2019-en-web.pdf
- Notes de bas de page 42
-
Canadian Institute for Health Information. Data Quality Documentation, Discharge Abstract Database - Current-Year Information, 2016–2017. Ottawa, ON: CIHI; 2017. [Consulté le 31 mars 2023]. https://www.cihi.ca/sites/default/files/document/current-year_information_dad_2016-2017-en-web.pdf
- Notes de bas de page 43
-
Canadian Institute for Health Information. Data Quality Documentation, Discharge Abstract Database - Current-Year Information, 2017–2018. Ottawa, ON: CIHI; 2018. [Consulté le 31 mars 2023]. https://www.cihi.ca/sites/default/files/document/current-year-information-dad-2017-2018-en-web.pdf
- Notes de bas de page 44
-
Gaboury I, Coyle K, Coyle D, Le Saux N. Treatment cost effectiveness in acute otitis media: A watch-and-wait approach versus amoxicillin. Paediatr Child Health 2010;15(7):e14–8. https://doi.org/10.1093/pch/15.7.e14
- Notes de bas de page 45
-
Christensen H, Trotter CL, Hickman M, Edmunds WJ. Re-evaluating cost effectiveness of universal meningitis vaccination (Bexsero) in England: modelling study. BMJ 2014;349:g5725. https://doi.org/10.1136/bmj.g5725
- Notes de bas de page 46
-
Ontario Ministry of Health. Formulary/Comparative Drug Index (CDI) Edition 43. Toronto, ON: MOHLTC; 2024. [Consulté le 31 mars 2023]. https://www.ontario.ca/document/ontario-drug-benefit-odb-formulary-comparative-drug-index-cdi-and-monthly-formulary-0
- Notes de bas de page 47
-
Committee on Infectious Diseases, American Academy of Pediatrics. Red Book: 2021–2024 Report of the Committee on Infectious Diseases, 32nd Edition. Kimberlin DW, Barnett ED, Lynfield R, Sawyer MH, editors. Itasca, IL; American Academy of Pediatrics; 2021. ISBN-13; 978-1-61002-735-9
- Notes de bas de page 48
-
Metlay JP, Waterer GW, Long AC, Anzueto A, Brozek J, Crothers K, Cooley LA, Dean NC, Fine MJ, Flanders SA, Griffin MR, Metersky ML, Musher DM, Restrepo MI, Whitney CG. Diagnosis and Treatment of Adults with Community-acquired Pneumonia. An Official Clinical Practice Guideline of the American Thoracic Society and Infectious Diseases Society of America. Am J Respir Crit Care Med 2019;200(7):e45–67. https://doi.org/10.1164/rccm.201908-1581ST
- Notes de bas de page 49
-
Patented Medicine Prices Review Board Canada. Dispensing fee policies in public drug plans, 2019/20. Ottawa, ON: PMPRB; 2020. [Consulté le 24 mars 2023]. http://www.pmprb-cepmb.gc.ca/CMFiles/NPDUIS/refdocs/ReferenceDoc_Dispensing_Fees_2019-20_EN.pdf
- Notes de bas de page 50
-
Colbert Y. 'My jaw dropped,' says Ontario woman of $12K air ambulance bill in Nova Scotia. CBC News. 2020 Nov 27. [Consulté le 31 mars 2023]. https://www.cbc.ca/news/canada/nova-scotia/ground-and-air-ambulance-fees-health-care-universal-health-care-1.5817284
- Notes de bas de page 51
-
Agence du revenu du Canada. Avantages relatifs aux automobiles ou véhicules à moteur – Allocations ou remboursements fournis à un employé pour l’utilisation de son propre véhicule. Ottawa, ON : ARC; 2024. [Consulté le 31 mars 2023]. https://www.canada.ca/fr/agence-revenu/services/impot/entreprises/sujets/retenues-paie/avantages-allocations/automobile/allocations-frais-automobile-vehicule-a-moteur.html
- Notes de bas de page 52
-
Pong RW, Pitblado JR. Geographic distribution of physicians in Canada: beyond how many and where. Ottawa, ON: Canadian Institute for Health Information; 2006. https://secure.cihi.ca/estore/productFamily.htm?locale=en&pf=PFC609
- Notes de bas de page 53
-
Agence de la santé publique du Canada Canada. Recommandations au niveau de la santé publique sur l’utilisation des vaccins contre le pneumocoque chez les adultes, y compris l’utilisation des vaccins conjugués 15-valent et 20-valent. Ottawa, ON : ASPC; 2023. https://www.canada.ca/fr/sante-publique/services/immunisation/comite-consultatif-national-immunisation-ccni/recommandations-niveau-sante-publique-utilisation-vaccins-contre-pneumocoque-adultes-compris-utilisation-vaccins-conjugues-15-valent-20-valent.html
- Notes de bas de page 54
-
Pasquale CB, Vietri J, Choate R, McDaniel A, Sato R, Ford KD, Malanga E, Yawn BP. Patient-reported consequences of community-acquired pneumonia in patients with chronic obstructive pulmonary disease. Chronic Obstr Pulm Dis (Miami) 2019;6(2):132–44. https://doi.org/10.15326/jcopdf.6.2.2018.0144
- Notes de bas de page 55
-
Bizier C, Contreras R, Walpole A. Enquête canadienne sur l'incapacité, 2012 : Les troubles auditifs chez les Canadiens âgés de 15 ans et plus, 2012. Ottawa, ON : StatCan; 2016. [Consulté le 31 mars 2023]. https://www150.statcan.gc.ca/n1/pub/89-654-x/89-654-x2016002-fra.htm
- Notes de bas de page 56
-
Jiang Y, Gauthier A, Annemans L, van der Linden M, Nicolas-Spony L, Bresse X. Cost-effectiveness of vaccinating adults with the 23-valent pneumococcal polysaccharide vaccine (PPV23) in Germany. Expert Rev Pharmacoecon Outcomes Res 2012;12(5):645–60. https://doi.org/10.1586/erp.12.54
- Notes de bas de page 57
-
Wyrwich KW, Yu H, Sato R, Powers JH. Observational longitudinal study of symptom burden and time for recovery from community-acquired pneumonia reported by older adults surveyed nationwide using the CAP Burden of Illness Questionnaire. Patient Relat Outcome Meas 2015;6:215–23. https://doi.org/10.2147/PROM.S85779
- Notes de bas de page 58
-
Dubé E, De Wals P, Gilca V, Boulianne N, Ouakki M, Lavoie F, Bradet R. Burden of acute otitis media on Canadian families. Can Fam Physician 2011;57(1):60–5.
- Notes de bas de page 59
-
Barber C, Ille S, Vergison A, Coates H. Acute otitis media in young children - what do parents say? Int J Pediatr Otorhinolaryngol 2014;78(2):300–6. https://doi.org/10.1016/j.ijporl.2013.11.030
- Notes de bas de page 60
-
Petit G, De Wals P, Law B, Tam T, Erickson LJ, Guay M, Framarin A. Epidemiological and economic burden of pneumococcal diseases in Canadian children. Can J Infect Dis 2003;14(4):215–20. https://doi.org/10.1155/2003/781794
- Notes de bas de page 61
-
Ganapathy V, Graham GD, DiBonaventura MD, Gillard PJ, Goren A, Zorowitz RD. Caregiver burden, productivity loss, and indirect costs associated with caring for patients with poststroke spasticity. Clin Interv Aging 2015;10:1793–802. https://doi.org/10.2147/CIA.S91123
- Notes de bas de page 62
-
Statistique Canada. Tableau 11-10-0239-01. Revenu des particuliers selon le groupe d'âge, le sexe et la source de revenu, Canada, provinces et certaines régions métropolitaines de recensement. Ottawa, ON : StatCan; 2024. [Consulté le 31 mars 2023]. https://www150.statcan.gc.ca/t1/tbl1/fr/tv.action?pid=1110023901&request_locale=fr
- Notes de bas de page 63
-
Statistique Canada. Tableau 14-10-0327-02. Taux de chômage, taux d'activité et taux d'emploi selon le genre, données annuelles. Ottawa, ON : StatCan; 2023. [Consulté le 31 mars 2023]. https://www150.statcan.gc.ca/t1/tbl1/fr/tv.action?pid=1410032702&request_locale=fr
- Notes de bas de page 64
-
Molina M, Humphries B, Guertin JR, Feeny D, Tarride JE. Health Utilities Index Mark 3 scores for children and youth: population norms for Canada based on cycles 5 (2016 and 2017) and 6 (2018 and 2019) of the Canadian Health Measures Survey. Health Rep 2023;34(2):29–39. https://doi.org/10.25318/82-003-x202300200003-eng
- Notes de bas de page 65
-
Yan J, Xie S, Johnson JA, Pullenayegum E, Ohinmaa A, Bryan S, Xie F. Canada population norms for the EQ-5D-5L. Eur J Health Econ 2024;25(1):147–55. https://doi.org/10.1007/s10198-023-01570-1
- Notes de bas de page 66
-
Tang Z, Matanock A, Jeon S, Leidner AJ. A review of health-related quality of life associated with pneumococcal disease: pooled estimates by age and type of disease. J Public Health (Oxf) 2022;44(2):e234–40. https://doi.org/10.1093/pubmed/fdab159
- Notes de bas de page 67
-
Bruce MG, Deeks SL, Zulz T, Bruden D, Navarro C, Lovgren M, Jette L, Kristinsson K, Sigmundsdottir G, Jensen KB, Lovoll O, Nuorti JP, Herva E, Nystedt A, Sjostedt A, Koch A, Hennessy TW, Parkinson AJ. International Circumpolar Surveillance System for invasive pneumococcal disease, 1999-2005. Emerg Infect Dis 2008;14(1):25–33. https://doi.org/10.3201/eid1401.071315
- Notes de bas de page 68
-
Kaur R, Fuji N, Pichichero ME. Dynamic changes in otopathogens colonizing the nasopharynx and causing acute otitis media in children after 13-valent (PCV13) pneumococcal conjugate vaccination during 2015-2019. Eur J Clin Microbiol Infect Dis 2022;41(1):37–44. https://doi.org/10.1007/s10096-021-04324-0
- Notes de bas de page 69
-
Pichon-Riviere A, Drummond M, Palacios A, Garcia-Marti S, Augustovski F. Determining the efficiency path to universal health coverage: cost-effectiveness thresholds for 174 countries based on growth in life expectancy and health expenditures. Lancet Glob Health 2023;11(6):e833–42. https://doi.org/10.1016/S2214-109X(23)00162-6
- Notes de bas de page 70
-
Ochalek JM, Lomas JR, Claxton KP. Assessing health opportunity costs for the Canadian health care systems. North York, ON: University of York (Commissioned report); 2018. https://pure.york.ac.uk/portal/en/publications/assessing-health-opportunity-costs-for-the-canadian-health-care-s
- Notes de bas de page 71
-
Ayabina D. Summary of three economic analyses of the use of 20-valent pneumococcal conjugate vaccine (PCV20) in children in the United States [slides presented at Advisory Committee on Immunization Practices meeting June 22, 2023]. Atlanta, GA: CDC; 2023. [Consulté le 11 janv. 2024]. https://www.cdc.gov/vaccines/acip/meetings/downloads/slides-2023-06-21-23/03-Pneumococcal-Ayabina-508.pdf
- Notes de bas de page 72
-
Weinberger DM, Malley R, Lipsitch M. Serotype replacement in disease after pneumococcal vaccination. Lancet 2011;378(9807):1962–73. https://doi.org/10.1016/S0140-6736(10)62225-8
- Notes de bas de page 73
-
Feikin DR, Kagucia EW, Loo JD, Link-Gelles R, Puhan MA, Cherian T, Levine OS, Whitney CG, O’Brien KL, Moore MR; Serotype Replacement Study Group. Serotype-specific changes in invasive pneumococcal disease after pneumococcal conjugate vaccine introduction: a pooled analysis of multiple surveillance sites. PLoS Med 2013;10(9):e1001517. https://doi.org/10.1371/journal.pmed.1001517
- Notes de bas de page 74
-
Pitman R, Fisman D, Zaric GS, Postma M, Kretzschmar M, Edmunds J, Brisson M; ISPOR-SMDM Modeling Good Research Practices Task Force. Dynamic transmission modeling: a report of the ISPOR-SMDM Modeling Good Research Practices Task Force--5. Value Health 2012;15(6):828–34. https://doi.org/10.1016/j.jval.2012.06.011
Appendice
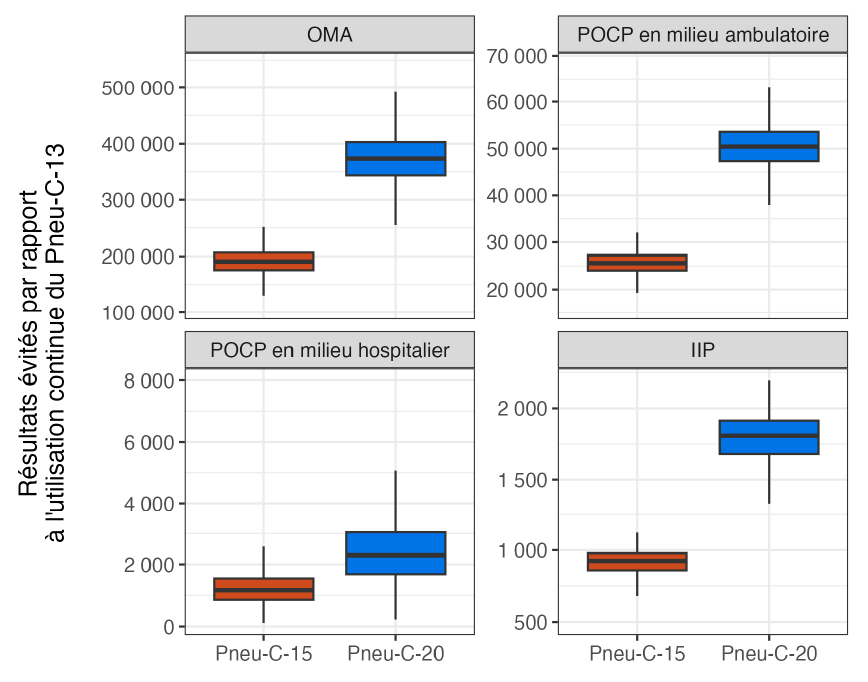
Figure A1 : Équivalent textuel
| Stratégie | Resultat | Minimum | Limite inférieure | Médiane | Limite supérieure | Maximum | |
|---|---|---|---|---|---|---|---|
| 1 | Pneu-C-15 | OMA | 130 032 | 175 466 | 190 760 | 205 884 | 251 450 |
| 2 | Pneu-C-20 | OMA | 254 800 | 343 610 | 373 543 | 403 099 | 492 212 |
| 3 | Pneu-C-15 | POCP en milieu ambulatoire | 19 275 | 24 055 | 25 638 | 27 254 | 32 051 |
| 4 | Pneu-C-20 | POCP en milieu ambulatoire | 37 922 | 47 333 | 50 446 | 53 624 | 63 057 |
| 5 | Pneu-C-15 | POCP en milieu hospitalier | 115 | 855 | 1 166 | 1 545 | 2 577 |
| 6 | Pneu-C-20 | POCP en milieu hospitalier | 227 | 1 683 | 2 294 | 3 039 | 5 071 |
| 7 | Pneu-C-15 | IIP | 680 | 859 | 925 | 979 | 1 123 |
| 8 | Pneu-C-20 | IIP | 1 330 | 1 680 | 1 808 | 1 914 | 2 194 |
Abréviations : IIP, infection invasive à pneumocoque; OMA, otite moyenne aiguë; Pneu-C, vaccin pneumococcique conjugué; POCP, pneumonie d'origine communautaire à pneumocoques
Footnote- Figure A1 note de bas de page
-
Les résultats sont présentés pour 10 000 simulations de modèles
| Stratégie | Effet (AVAQ perdues) |
Coût (millions de dollars) |
RCED séquentiel ($/AVAQ) |
|---|---|---|---|
| Perspective du système de santé | |||
| Pneu-C-20 | 15 794 | 541 539 | - |
| Pneu-C-15 | 15 819 | 543 513 | Dominé par Pneu-C-20 |
| Pneu-C-13 | 15 897 | 545 613 | Dominé par Pneu-C-20 |
| Perspective sociétale | |||
| Pneu-C-20 | 541 539 | 445 465 | - |
| Pneu-C-15 | 543 513 | 455 579 | Dominé par Pneu-C-20 |
| Pneu-C-13 | 545 613 | 445 760 | Dominé par Pneu-C-20 |
Abréviations : AVAQ, année de vie ajustée par la qualité; Pneu-C, vaccin pneumococcique conjugué; RCED, rapport coût/efficacité différentiel; -, sans objet |
|||

Cette œuvre est mise à disposition selon les termes de la Licence Creative Commons Attribution 4.0 International