Poids de la preuve : Principes généraux et applications actuelles à Santé Canada

Télécharger le format de rechange
(Format PDF, 725 Ko, 25 pages)
Organisation : Santé Canada
Publiée : 2019-01-08
Cat. : H129-69/2018F-PDF
ISBN : 978-0-660-27302-0
Préparé par l'équipe spéciale du poids de la preuve du Groupe de travail sur l'évaluation des risques scientifiques
T. TaoNote de bas de page 1, Y. BhullerNote de bas de page 2, Y. BonvalotNote de bas de page 3, M. HillNote de bas de page 4, A. KleinNote de bas de page 5, G. KozakNote de bas de page 6, I. PlanteNote de bas de page 7, and N. RobertNote de bas de page 8
| Version | Date | Section ou paragraphe modifié | Changement(s) apporté(s) |
|---|---|---|---|
| 1 | Novembre 2011 | - | Publication initiale du document final. |
| 2 | Mai 2018 | Historique de la révision du document | Section ajoutée pour suivre les révisions. |
| Annexe 2 | Secteurs de programme, interprétations et applications mises à jour. | ||
| 8.0 Références | Section 8.0 ajoutée; liste des références mise à jour dans l'ensemble du document. |
Table des matières
- 1. Introduction
- 2. Objet et portée
- 3. Rôle dans l'évaluation des risques
- 4. Principes généraux
- 5. Application à Santé Canada
- 6. Contexte international
- 7. Conclusions
- 8. Références
- Annexe 1
- Annexe 2
- Annexe 3
1. Introduction
Le poids de la preuve est fréquemment cité comme le fondement de l'élaboration des conclusions d'une évaluation des risques. Toutefois, les interprétations multiples du poids de la preuve et l'absence de consensus sur le sens de cette expression pourraient potentiellement compromettre la communication entre les diverses parties du processus décisionnel. Pour contrer ce problème, une analyse de la méthode du poids de la preuve a été amorcée par la Direction des politiques scientifiques de Santé Canada en 2010, dans le cadre d'un projet dirigé par le Groupe de travail sur l'évaluation des risques scientifiques. Par l'examen des interprétations actuelles et le choix des pratiques exemplaires potentielles, cette analyse vise à améliorer l'uniformité et la cohérence des évaluations des risques dans l'ensemble du Ministère.
2. Objet et portée
Le présent document vise à informer la haute direction sur les évaluations des risques par le poids de la preuve à Santé Canada, en présentant un aperçu de ce qui suit :
- rôle dans l'évaluation des risques scientifiques;
- principaux principes directeurs;
- application dans le cadre de divers programmes d'évaluation des risques à Santé Canada.
En outre, le présent document explicatif constitue une ressource ministérielle à valeur ajoutée contenant de l'information contextuelle de haut niveau ainsi que des principes directeurs qui complètent les lignes directrices, les procédures ou les outils qui s'appliquent à un programme.
Certes, le poids de la preuve peut être utilisé pour la prise de décisions dans un contexte de gestion des risques (c'est-à-dire évaluer la preuve scientifique par rapport à d'autres facteurs stratégiques), mais cet aspect ne sera pas traité puisque ce n'est pas le propos du présent documentNote de bas de page 9.3. Rôle dans l'évaluation des risques
En règle générale, une évaluation des risques scientifiques comporte les étapes suivantes : définition et caractérisation du danger, évaluation de l'exposition, et caractérisation des risques. En outre, ce type d'évaluation fait partie intégrante de la prise d'une décision éclairée, qui englobe également la gestion et la communication du risque.
Le poids de la preuve dans le contexte de l'évaluation des risques est défini dans le Cadre décisionnel de Santé Canada pour la détermination, l'évaluation et la gestion des risques pour la santé (Santé Canada, 2000) comme suit :
« Mesure qualitative tenant compte de la nature et de la qualité des études scientifiques destinées à étudier le risque lié à un agent. Les incertitudes qui découlent de l'insuffisance et de la non-disponibilité de données scientifiques amènent souvent les scientifiques à faire des inférences, à émettre des hypothèses et à porter des jugements afin de caractériser un risque. « Évaluer le poids de la preuve » se dit du fait de porter des jugements sur le risque en se fondant sur des renseignements scientifiques »
La description ci-dessus renvoie implicitement à deux concepts fréquemment associés à la terminologie employée pour traiter du poids de la preuve :
- Ensemble de la preuve : types et sources de renseignements à recueillir et à prendre en compte pour évaluation subséquente;
- Appréciation de la preuve : façon dont les diverses sources de données probantes sont évaluées puis intégrées dans une conclusion ou une recommandation globale.
Diverses interprétations de l'expression « toutes les preuves » disponibles ou pertinentes à ce jour, peuvent influer sur ce que l'on entend par l'ensemble de la preuve. Ce concept offre la possibilité d'utiliser des études ou des renseignements qui peuvent ne pas être considérés comme suffisants s'ils sont pris isolément, mais qui peuvent constituer, s'ils sont associés à d'autres études ou renseignements, une argumentation complète par le « poids de la preuve » à l'appui des conclusions d'une évaluation des risques. De plus, la preuve évaluée initialement et la décision subséquente peuvent être réévaluées à une date ultérieure, compte tenu de renseignements qui n'étaient pas disponibles au moment de l'évaluation initiale.
Ce second concept méthodologique d'appréciation de la preuve s'applique à la plupart des évaluations des risques. Bien que les méthodes et les outils utilisés pour l'évaluation et l'intégration des preuves puissent varier (p. ex. méthode quantitative ou qualitative) et dépendre du contexte, les principes généraux du processus d'évaluation et d'intégration restent les mêmes.
4. Principes généraux
L'interdépendance des deux concepts susmentionnés et les principes généraux de la méthode du poids de la preuve ci-dessous, sont présentés à l'annexe 1 aux fins d'illustration seulement. Le concept de l'ensemble de la preuve englobe les principes généraux 4.1, 4.2 et 4.3, tandis que le concept méthodologique de l'appréciation de la preuve peut être constitué des principes généraux 4.4 et 4.5. Peu importe l'interprétation des termes employés, les étapes suivantes s'appliquent à l'établissement d'une argumentation par le « poids de la preuve » à l'appui d'une conclusion ou d'une recommandation découlant d'une évaluation des risques.
4.1 Collecte de « toutes » les preuves disponibles
Plusieurs sources et types de preuve peuvent être recueillis ou présentés et pris en compte dans le contexte de « toutes les preuves » disponibles à ce jour. Selon les exigences réglementaires en matière de données, la gamme complète de sources et de types de preuve peut inclure les suivants : essais cliniques contrôlés, études exclusives, réalisées par une tierce partie ou une entreprise, renseignements examinés par les pairs, documents scientifiques publiés, rapports d'expert, rapports d'analyse et de décision d'organismes de réglementation, rapports d'incident, effets indésirables communiqués aux organismes de réglementation et données non publiées.
4.2 Évaluation d'études distinctes
Les critères généraux d'inclusion ou d'exclusion sont utiles pour l'examen de « toutes » les données probantes recueillies pour examen ultérieur. Bien que le champ d'application et les termes précis des critères interdépendants d'examen comme « qualité », « fiabilité », « pertinence », etc. peuvent varier selon le programme ou l'organisme de réglementation, les principes sous-jacents sont les mêmes. Une évaluation peut comporter le recours à un système de notation et/ou au meilleur jugement professionnel. Les études acceptables qui répondent aux normes d'inclusion font l'objet d'une évaluation plus poussée au cours des étapes subséquentes de la méthode du poids de la preuve et les études inacceptables peuvent être rejetées. Par exemple, des données non publiées ou qui ne se rapportent pas aux paramètres de mesure d'une évaluation des risques, peuvent être rejetées ou recevoir une valeur probante plus faible au moment du regroupement des éléments de preuve. Au besoin, la justification de l'inclusion ou de l'exclusion d'études peut être étayée dans le rapport pertinent.
4.3 Regroupement des éléments de preuve
Les types et les sources de données probantes sont diversifiés et leur niveau de détail varie considérablement. Selon le contexte de l'évaluation des risques, des études ou des sources de données sont souvent examinées en tant qu'éléments de preuve distincts, ou elles sont jugées en combinaison avec des études ou des données semblables en tant qu'« élément de preuve » particulier. Ces éléments de preuve peuvent être classés en fonction de caractéristiques communes comme la source ou le type de donnée (p. ex. données animales, données humaines, essais cliniques, et données documentaires). Des éléments de preuve distincts peuvent aussi être définis selon des sous-catégories du risque comme le danger, l'exposition, la santé humaine, la sécurité de l'environnement ou d'autres caractéristiques comme des études qui corroborent ou infirment une certaine conclusion. Ces éléments de preuve peuvent encore être subdivisés en d'autres éléments plus précis. Par exemple, le « danger » peut être divisé par organe du corps (danger pour le foie, les reins, le cerveau, etc.)
4.4 Évaluation des éléments de preuve
Les éléments de preuve sont évalués en fonction de divers critères qui dépendent des paramètres de l'évaluation. Les évaluations des risques peuvent être fondées sur des hypothèses et conçues pour l'obtention d'un « oui » ou d'un « non » à des questions (p. ex. la substance x est-elle cancérogène?). Dans ce cas, chacun des éléments de preuve (p. ex. études de cancérogénicité, études de génotoxicité ou données mécanistes) peut être évalué selon des critères comme la force ou la solidité de la preuve à l'appui ou à l'encontre d'une conclusion donnée pour chaque élément particulier.
D'autres évaluations des risques peuvent comporter des questions plus générales (p. ex. quel produit ou quelle source est la cause probable de l'épidémie de la maladie y?). Dans de ce cas, certains éléments de preuve, comme des données épidémiologiques, peuvent être évalués en fonction de critères précis comme la force de l'association, la corrélation, la spécificité, la temporalité, le gradient biologique et la dose-réponse, la plausibilité, la cohérence, les données probantes expérimentales, et l'analogie (p. ex. les critères Bradford Hill (1965) pour l'inférence causale). Selon le contexte de l'élément de preuve en cause, d'autres critères non mentionnés ici pourraient aussi s'appliquer. L'évaluation peut être quantitative (attribution d'un poids ou d'une valeur à chaque élément de preuve évalué, sous la forme de probabilités ou de valeurs alphanumériques) ou qualitative (description à l'aide d'adjectifs comme « faible » ou « fort ») ou implicite (sous la forme de modèles logiques et de diagrammes de décision qui soulignent par défaut l'importance de certains éléments de preuve par rapport à d'autres).
Les valeurs attribuées ou les descriptions correspondent à la « force » relative d'un élément de preuve, sur laquelle l'incertitude et la variabilité des ensembles de données contribuant à chaque élément
de preuve ont une incidence négative. Parmi les documents du Ministère contenant des explications détaillées sur l'incertitude et la variabilité on compte notamment les deux documents suivants : Cadre d'application de la précaution dans un processus décisionnel scientifique en gestion du risque (Bureau du Conseil privé, 2003) et Guide de la Direction générale des produits de santé et des aliments portant sur la réalisation des évaluations des risques pour la santé des humains (Santé Canada, 2011).
4.5 Intégration des éléments de preuve multiples
Le recours au meilleur jugement professionnel est une méthode qualitative qui permet de déterminer la contribution relative de chaque élément de preuve à la conclusion globale en une seule étape. D'autres méthodes plus systématiques d'intégration quantitative peuvent aussi être employées. Elles consistent à attribuer à chaque élément de preuve une note qui peut être modifiée par des facteurs de pondération correspondant à l'importance relative de l'élément parmi l'ensemble des éléments de preuve. Puis, une formule mathématique permet d'obtenir une valeur finale. Toutefois, le processus de notation est difficile à appliquer dans un contexte comme l'évaluation des risques, en raison de la grande complexité des différentes sources de renseignements disponibles.
L'intégration des valeurs probantes ou du poids des données est un processus itératif qui est répété à plusieurs niveaux : à l'intérieur d'une étude, parmi des études similaires pour l'attribution d'une valeur collective à un élément de preuve en particulier, et parmi des éléments de preuve multiples pour l'obtention d'une conclusion ou d'une recommandation globale découlant d'une évaluation des risques. Par exemple, pour déterminer si un composé chimique affecte le foie, les constatations des essais cliniques chimiques sont examinées puis intégrées ainsi que la valeur attribuée à l'organe et les données histopathologiques dans le cadre d'une seule étude ou de plusieurs études semblables (p. ex. pour évaluer la dose-réponse). Pour intégrer les valeurs de plusieurs études en vue d'obtenir le paramètre d'une évaluation donnée (p. ex. si un composé est cancérogène), des études de cancérogénicité, des études de génotoxicité, ou des données mécanistes peuvent être examinées puis intégrées. Pour l'obtention de conclusions concernant le risque global, il est nécessaire d'intégrer des éléments de preuve relatifs au danger et à l'exposition. L'intégration des risques pour la santé humaine et des risques pour l'environnement peut contribuer à établir un profil général des risques.
5. Application à Santé Canada
L'évaluation de la preuve scientifique est un élément crucial de l'évaluation des risques et de la prise de décisions à Santé Canada. De plus, pour de nombreux programmes réglementaires au Ministère, les conclusions d'une évaluation des risques (appelée « caractérisation des risques ») sont souvent élaborées en fonction de la vraisemblance de l'association entre une substance ou une activité particulière et les effets sur la santé qui y sont associés. Dans ce contexte, la méthode du poids de la preuve est fréquemment citée comme le fondement de l'élaboration des conclusions d'une évaluation des risques à l'aide des meilleurs renseignements disponibles à ce jour, qui peuvent être recueillis, évalués et intégrés à l'aide de diverses méthodes qualitatives et quantitatives.
Le mandat et l'étendue de l'évaluation des risques et/ou des activités de gestion des risques des divers programmes varient considérablement dans l'ensemble du Ministère (voir le Guide d'introduction sur l'évaluation scientifique des risques à Santé Canada, Saner, 2010). Chaque programme est réalisé compte tenu des contraintes imposées par la réglementation pertinente. Les différences sur le plan de la réglementation et des objectifs d'un programme ont une incidence sur la période dont disposent les intéressés pour évaluer chaque activité ou produit particuliers, sur la quantité et la qualité de l'information qui est disponible à ce jour aux fins de l'évaluation, et sur le degré de flexibilité pour l'interprétation et le recours à la valeur probante de la preuve comme méthode d'évaluation des risques. Les lignes directrices internationales visant divers domaines et le contexte du secteur auquel peuvent souvent s'appliquer des règlements harmonisés à l'échelle mondiale, ont aussi une incidence sur chaque programme. Les enjeux variés et le contexte dans lequel les décisions en matière de réglementation sont prises, et l'ampleur des possibilités et des recommandations de gestion des risques potentiels qui peuvent être envisagées, diffèrent aussi selon les programmes ainsi qu'à l'intérieur d'un programme.
Un sondage a été mené pour déterminer comment la méthode du poids de la preuve était appliquée un peu partout au Ministère. Toutes les directions générales ont répondu, y compris la Direction générale des produits de santé et des aliments (DGPSA), la Direction générale de la santé environnementale et de la sécurité des consommateurs (DGSESC), et l'Agence de réglementation de la lutte antiparasitaire (ARLA). Les principes généraux de la méthode du poids de la preuve sont appliqués par la plupart des programmes visés par l'enquête. Plus particulièrement, la plupart des évaluations des risques comportent les étapes suivantes : collecte et évaluation d'études et de sources distinctes de données probantes, regroupement des études pour constituer des éléments de preuve contextuels, et évaluation et intégration des éléments de preuve multiples dans une conclusion ou recommandation globale. La plupart des directions générales chargées des programmes estiment que le poids de la preuve englobe les concepts de l'ensemble de la preuve (c.-à-d. les données probantes à recueillir et à prendre en compte) et de l'appréciation de la preuve (c.-à-d. façon dont les données probantes sont évaluées puis intégrées dans une conclusion finale) (voir l'annexe 2).
L'utilisation de critères et d'outils particuliers dépend du contexte, et ceux-ci sont indiqués dans les lignes directrices, les procédures d'exploitation standard, les documents de travail, etc., relatifs au programme. Des documents de programme décrivant l'application de la méthode du poids de la preuve ont été élaborés à cette fin, lorsque c'était estimé nécessaire. Par exemple :
- Poids de la preuve : Facteurs à considérer pour la prise de mesures appropriées et en temps opportun dans une situation d'enquête sur une éclosion de maladie d'origine alimentaire (Santé Canada, Agence de la santé publique du Canada et Agence canadienne d'inspection des aliments; 2011);
- Framework for Initiating and Conducting Risk Analysis Activities on Microbial Hazards in Food (Santé Canada, 2017)
- Guide d'intervention en matière d'enquête sur les aliments (Agence canadienne d'inspection des aliments, 2017)
- Document de principes : Paramètre des facteurs d'exposition généraux utilisés pour les évaluations de l'exposition alimentaire, professionnelle et résidentielle (Santé Canada, 2014)
- L'évaluation des risques pour les sites contaminés fédéraux au Canada : Guide supplémentaire sur l'évaluation des risques pour la santé humaine liés aux aliments d'origine locale (ERSaliments) (Santé Canada, 2010)
- Avis aux demandeurs de licence de mise en marché : critères de preuve et modèle d'évaluation des preuves (Direction des produits de santé naturels et sans ordonnance, 2010);
- Cheminement des demandes de licences de mise en marché des produits de santé naturels utilisés comme remèdes traditionnels (Direction des produits de santé naturels et sans ordonnance, 2012a)
- Cheminement des demandes de licence de mise en marché des produits de santé naturels qui font l'objet d'allégations santé fondées sur des preuves modernes (Direction des produits de santé naturels et sans ordonnance, 2012b)
Documents de programme de nature plus générale :
- Guide de la Direction générale des produits de santé et des aliments portant sur la réalisation des évaluations des risques pour la santé des humains (Santé Canada, 2011)
- Cadre d'évaluation scientifique des risques liés aux micro-organismes réglementés en vertu de la Loi canadienne sur la protection de l'environnement (1999) (Environnement Canada, Santé Canada, 2013);
- Lignes directrices sur la méthodologie d'évaluation tous risques 2012–2013 (Sécurité publique Canada 2018)
Tel que susmentionné, la documentation sur la méthode d'évaluation des risques et la justification pour l'inclusion ou l'exclusion de certaines sources de données probantes est un élément crucial du processus décisionnel. De la même façon, bien que la méthode du poids de la preuve soit utilisée systématiquement pour la plupart des évaluations des risques dans l'ensemble du Ministère, l'utilisation explicite des termes décrivant le poids de la preuve n'est pas toujours étayée. Dans certains cas, des expressions associées au poids de la preuve sont employées, mais l'application précise de la méthode du poids de la preuve n'est pas expliquée en détail.
À l'occasion, la terminologie associée au poids de la preuve est utilisée lorsqu'il est fait mention de niveaux de preuve ou des normes de qualité de certaines études. Dans certains cas, des termes associés au poids de la preuve sont employés au lieu de termes décrivant la force de la conclusion ou de la recommandation globale, ou au lieu d'expressions juridiques comme « prépondérance de la preuve », qui signifie simplement « plus probable que le contraire ».
Toutefois, la majorité des rapports d'évaluation des risques contiennent une description narrative logique des forces ou des faiblesses relatives des divers éléments de preuve pris en compte. La plupart du temps, les divers éléments de preuve sont regroupés et intégrés dans une conclusion finale fondée sur le meilleur jugement professionnel et non sur une formule mathématique. Une description narrative de la justification est habituellement offerte pour ce type de jugement, expliquant notamment pourquoi certains éléments de preuve sont plus importants que d'autres pour l'établissement de la conclusion ou de la recommandation découlant de l'évaluation des risques. Cependant, certains rapports ne contiennent que des listes des éléments de preuve évalués puis présentent directement de l'évaluation globale des risques, sans mention explicite des liens entre les divers éléments de preuve ou de la justification qui sous-tend le processus d'intégration.
6. Contexte international
La méthode du poids de la preuve est couramment appliquée par la plupart des organismes de l'évaluation des risques à l'échelle internationale et bien qu'il existe plusieurs définitions du poids de la preuve, il n'y a aucune définition ou orientation normalisée, universelle ou convenue par tous, concernant la manière de réaliser une analyse par le poids de la preuve. Par exemple, le Comité scientifique de l'Autorité européenne de sécurité des aliments (EFSA) a publié récemment un guide sur l'utilisation de la méthode du poids de la preuve et du concept de « l'ensemble de la preuve » dans lequel on explique que « l'évaluation par le poids de la preuve est un processus qui intègre les preuves afin de déterminer le soutien relatif à des réponses possibles à une question scientifique. Le terme « poids de la preuve » lui-même correspond à la mesure dans laquelle les preuves soutiennent les réponses possibles à une question scientifique. » (traduction libre)
La United States Environmental Protection Agency (US EPA, 2003) fait mention du poids de la preuve dans diverses lignes directrices, tant dans le contexte de l'ensemble de la preuve que dans le contexte méthodologique de l'appréciation des éléments de preuve multiples. En voici un exemple :
« La méthode du poids de la preuve consiste en un examen de toute l'information pertinente dans une évaluation intégrative qui prend en compte tous les types de preuves disponibles, la quantité et la qualité des preuves, les points forts et les limites associés à chaque type de preuve et explique comment les divers types de preuve cadrent les uns avec les autres. » (traduction libre)
Cependant, dans un examen du processus du système Integrated Risk Information System (IRIS) de l'EPA, le National Research Council (2014) a conclu :
« L'examen systématique et l'analyse par le poids de la preuve ont été décrits par le passé de façons variées, et les termes sont parfois utilisés de façon interchangeable; ce manque de précision dans la terminologie utilisée entraîne une certaine confusion sur la signification des termes dans la pratique… Le comité voit l'analyse par le poids de la preuve comme un processus fondé sur le jugement pour évaluer les points forts des preuves afin d'inférer une causalité. Cependant, le comité a conclu que l'expression telle qu'elle est utilisée dans la pratique est devenue trop vague et de peu d'utilité scientifique. Une évaluation du IRIS doit permettre d'apprécier les risques d'un produit chimique pour la santé humaine, et ce, en intégrant une variété d'éléments de preuve. Par conséquent, le comité considère le terme intégration des preuves plus utile et plus apte à décrire le processus qui suit la réalisation des examens systématiques. » (traduction libre)
De la même manière, le Centre national d'évaluation environnementale de l'EPA (2015) adopte une méthode intégrée pour effectuer des évaluations scientifiques dans le cadre des examens des normes nationales de la qualité de l'air ambiant :
« L'US EPA intègre des preuves provenant de l'ensemble des disciplines scientifiques ou des types d'études et caractérise le poids de la preuve pour les relations… et utilise les résultats de toutes les études dont la pertinence et la qualité sont jugées adéquates par rapport aux critères… prend en compte des aspects tels que les points forts, la cohérence et la plausibilité biologique de la preuve, et élabore des déterminations de causalité sur la nature des relations… comprend l'évaluation des points forts et des points faibles dans la collecte générale des études dans toutes les disciplines. » (traduction libre)
L'Agence européenne des produits chimiques (ECHA, 2011 et 2016) mentionne des interprétations concernant le contexte méthodologique de l'appréciation de la preuve comme suit :
« La méthode du poids de la preuve renvoie communément à la combinaison de preuves provenant de sources multiples pour évaluer la propriété examinée. Cette technique peut par conséquent être utile, lorsque par exemple chaque élément d'information ou un test seul ne suffisent pas à répondre à une exigence d'information normative, mais qu'il est possible de combiner les points forts et les points faibles d'études individuelles pour aboutir à une conclusion pour une propriété en particulier.
Le terme poids de la preuve n'est ni un terme scientifiquement bien défini ni un concept convenu formalisé caractérisé par des procédures et des outils définis. Il peut cependant être considéré comme une méthode fondée sur des preuves qui comprend une évaluation du poids (valeur) relatif des différents éléments de l'information disponible qui ont été recueillis. L'application de ce concept peut être effectuée de manière objective en utilisant une procédure normalisée ou en sollicitant le jugement d'experts. Des facteurs tels que la qualité des données, la cohérence des résultats, la nature et la gravité des effets, la pertinence de l'information, influeront sur le poids donné aux preuves disponibles. » (traduction libre)
Ce concept de l'appréciation de la preuve est complété par le concept de l'ensemble de la preuve dans le Règlement REACH (Registration, Evaluation, Authorisation and Restriction of Chemicals) (ECHA, 2017) :
« Le poids de la preuve provenant de plusieurs sources d'information indépendantes peut être suffisant pour formuler l'hypothèse ou conclure qu'une substance possède ou non une propriété dangereuse particulière, alors que l'information de chaque source distincte seule est jugée insuffisante pour appuyer cette notion.
Le poids de la preuve provenant de l'utilisation de nouvelles méthodes de test, non incluses encore dans les méthodes de test indiquées dans l'article 13(3), ou provenant d'une méthode de test internationale reconnue par la Commission ou l'Agence comme équivalente, peut être suffisant pour conclure qu'une substance possède ou non une propriété dangereuse particulière.
Lorsque le poids de la preuve de la présence ou non d'une propriété dangereuse particulière est suffisant :
- des essais supplémentaires sur des animaux vertébrés ne sont pas nécessaires;
- des essais supplémentaires ne portant pas sur des animaux vertébrés ne sont pas nécessaires.
Dans tous les cas, des documents adéquats et fiables doivent être fournis. » (traduction libre)
Le Programme international sur la sécurité des substances chimiques de l'Organisation mondiale de la santé a publié deux documents d'orientation sur l'incertitude dans l'évaluation des risques : Uncertainty and Data Quality in Exposure Assessment (Incertitude et qualité des données dans l'évaluation de l'exposition) (OMS, 2008), qui traite explicitement du poids de la preuve : « dans la mesure du possible, l'effet combiné des différentes sources d'incertitude sur les prévisions d'exposition ou de risque, éventuellement fondé sur une méthode du poids de la preuve en l'absence de données quantitatives, devrait être également pris en compte »; et Guidance Document on Evaluating and Expressing Uncertainty in Hazard Characterization (Document d'orientation sur l'évaluation et l'expression de l'incertitude dans la caractérisation du risque) (OMS, 2017).
L'Organisation des Nations Unies pour l'alimentation et l'agriculture et l'Organisation mondiale de la santé (FAO/OMS, 2009) ont discuté de l'utilisation d'une méthode du poids de la preuve pour caractériser les risques microbiologiques dans les aliments : « le poids de la preuve devrait être évalué selon des critères scientifiques clairement définis. À mesure que les critères sont satisfaits, le poids de la preuve indique un risque plus crédible. » La FAO ou l'OMS ont prévu que « les déterminations par le poids de la preuve prendront de plus en plus de place dans les évaluations des risques des agents pathogènes microbiologiques dans les aliments. »
L'Organisation de coopération et de développement économiques (OCDE, 2015, 2017, 2018) définit le poids de la preuve comme « un jugement complet, intégré, souvent qualitatif sur la portée et la qualité de l'information qui soutient une hypothèse pour laquelle les méthodes et les outils varient en fonction du contexte. » La méthode du poids de la preuve est utilisée dans le cadre de l'OCDE « Adverse Outcome Pathway [AOP]/Mode Of Action [MOA]) » (Voie des effets indésirables/Mode d'action) visant à élaborer et à utiliser des méthodes de test et d'évaluation intégrées (Integrated Approaches to Testing and Assessment [IATA]) :
« L'évaluation de l'information existante ou la génération de données supplémentaires dans le cadre d'une méthode de test et d'évaluation intégrée peuvent être exécutées à l'aide d'une méthode du poids de la preuve non formalisée ou de méthodes prédéfinies et structurées telles que des stratégies d'essai séquentielles, des stratégies d'analyses intégrées ou leur combinaison. » (traduction libre)
Concernant l'utilisation d'une méthode du poids de la preuve, le codex Alimentarius (2014) met en garde contre le fait que « le poids de la preuve qui intègre des données quantitatives et qualitatives pourrait permettre une estimation du risque qualitative seulement. »
Ensemble, les définitions ci-dessus d'importants partenaires internationaux cadrent avec les interprétations actuelles de la méthode du poids de la preuve de Santé Canada.
7. Conclusions
Alors que certains outils et méthodes sont souvent associés au contexte des divers secteurs de programme, les principes sous-jacents de la méthode du poids de la preuve, selon laquelle des sources multiples d'information sont recueillies, évaluées et intégrées dans une conclusion globale, sont couramment appliqués dans l'ensemble du Ministère et ils sont estimés conformes à la pratique internationale.
À l'heure actuelle, il n'y a pas d'incohérence quant à l'application de haut niveau de la méthode générale du poids de la preuve. Des incohérences se produisent plutôt lorsque des termes associés au poids de la preuve sont utilisés dans le contexte des normes de qualité de diverses études ou de la force d'une conclusion ou d'une recommandation globale.
Puisque chaque évaluation des risques s'inscrit dans un contexte particulier, et qu'il existe une multitude d'outils et de critères applicables, il est particulièrement important d'étayer clairement l'application de la méthode du poids de la preuve. Une harmonisation est possible et la conformité à une simple liste de contrôle serait un pas vers cet objectif (voir l'annexe 3). Les secteurs de programme sont encouragés à prendre des mesures pertinentes (p. ex. mise à jour des lignes directrices internes) pour améliorer davantage dans les rapports d'évaluation des risques, l'information à l'appui des possibilités subséquentes de gestion des risques ou des décisions réglementaires. Cette information consiste notamment en des explications détaillées sur ce que l'on entend par « poids de la preuve », au besoin. En outre, des graphiques présentant les éléments de preuve, des profils ou des tableaux peuvent être utiles aux évaluateurs des risques tout comme aux gestionnaires des risques en tant qu'outils supplémentaires de communication.
8. Références
- Bradford Hill A. 1965. The environment and disease: association or causation? Proc R Soc Med. 58(5) : 295–300.
- Agence canadienne d'inspection des aliments. 2017. Guide d'intervention en matière d'enquête sur les aliments. Disponible à : www.inspection.gc.ca/aliments/systemes-de-production-d-aliments-salubres/rappels-d-aliments- et-mesures-d-urgence/guide-sur-les-aliments/fra/1378402475724/1378403080658?chap=0 (consulté le 16-03-2018)
- Bureau du Conseil privé du Canada. 2003. Cadre d'application de la précaution dans un processus décisionnel scientifique en gestion du risque. Disponible à : http://publications.gc.ca/collections/Collection/CP22-70-2003F.pdf (consulté le 15-03-2018)
- Codex Alimentarius. 2014. Principes et directives régissant la conduite de l'évaluation des risques microbiologiques (CAC/ GL 30–1999). Disponible à : www.fao.org/fao-who-codexalimentarius/codex-texts/guidelines/fr/ (consulté le 20-03-2018)
- ECHA : Agence européenne des produits chimiques. 2011. Guide des exigences d'information et évaluation de la sécurité chimique – Chapitre R.4 : Évaluation de l'information disponible. Disponible à : https://echa.europa.eu/documents/ 10162/13643/information_requirements_r4_en.pdf/d6395ad2-1596-4708-ba86-0136686d205e (consulté le 19-03-2018).
- ECHA. 2016. Guide pratique : Comment utiliser les alternatives aux essais sur les animaux pour remplir vos obligations d'information dans le cadre de l'enregistrement au titre de REACH. Disponible à : https://echa.europa.eu/documents/ 10162/13655/practical_guide_how_to_use_alternatives_fr.pdf/87246232-f0e8-46bf-a69a-9ab32530de5c (consulté le 19-03-2018)
- ECHA. 2017. Version consolidée du Règlement REACH : Règlement (CE) no 1907/2006 du Parlement européen et du Conseil du 18 décembre 2006 concernant l'enregistrement, l'évaluation et l'autorisation des substances chimiques, ainsi que les restrictions applicables à ces substances (REACH). Disponible à : https://echa.europa.eu/regulations/reach/legislation (consulté le 19-03-2018)
- Environnement Canada, Santé Canada. 2013. Cadre d'évaluation scientifique des risques liés aux micro-organismes réglementés en vertu de la Loi canadienne sur la protection de l'environnement (1999). Disponible à : www.ec.gc.ca/ subsnouvelles-newsubs/default.asp?lang=Fr&n=120842D5-1 (consulté le 16-03-2018)
- EFSA : Autorité européenne de sécurité des aliments. 2017a. Guidance on the use of the weight of evidence approach in scientific assessments. EFSA Journal 2017; 15(8):4971. Disponible à : http://onlinelibrary.wiley.com/doi/10.2903/ j.efsa.2017.4971/epdf (consulté le 15-03-2018)
- EFSA. 2017b. Revised Draft for Internal Testing: Guidance on Uncertainty in EFSA Scientific Assessment. Disponible à : https://www.efsa.europa.eu/sites/default/files/160321DraftGDUncertaintyInScientificAssessment.pdf (consulté le 15-03-2018)
- EPA : United States Environmental Protection Agency. 2003. A Summary of General Assessment Factors for Evaluating the Quality of Scientific and Technical Information. Disponible à : www.epa.gov/sites/production/files/2015-01/documents/ assess2.pdf (consulté le 19-03-2018)
- EPA : United States Environmental Protection Agency. 2015. Preamble to the Integrated Science Assessments (ISA). Disponible à : https://cfpub.epa.gov/ncea/isa/recordisplay.cfm?deid=310244 (consulté le 29-03-2018)
- FAO/OMS : Organisation des Nations Unies pour l'alimentation et l'agriculture et Organisation mondiale de la santé. 2009. Caractérisation des risques liés aux dangers microbiologiques d'origine alimentaire Série 17. Disponible à www.fao.org/3/a-at660f.pdf (consulté le 20-03-2018)
- Santé Canada. 2000. Cadre décisionnel de Santé Canada pour la détermination, l'évaluation et la gestion des risques pour la santé. Disponible à : www.canada.ca/content/dam/hc-sc/migration/hc-sc/ahc-asc/alt_formats/hpfb-dgpsa/ pdf/pubs/risk-risques-fra.pdf (consulté le 15-03-2018)
- Santé Canada. 2010. L'évaluation des risques pour les sites contaminés fédéraux au Canada : Guide supplémentaire sur l'évaluation des risques pour la santé humaine liés aux aliments d'origine locale (ERSaliments). Disponible à : http://publications.gc.ca/collections/collection_2012/sc-hc/H128-1-11-641-fra.pdf (consulté le 16-03-2018)
- Santé Canada. 2011. Guide de la Direction générale des produits de santé et des aliments portant sur la réalisation des évaluations des risques pour la santé des humains. Disponible à : http://mysource.hc-sc.gc.ca/sites/default/files/ guide_dgpsa_realisation_ersh.pdf (consulté le 15-03-2018)
- Santé Canada. 2014. Document de principes : Paramètre des facteurs d'exposition généraux utilisés pour les évaluations de l'exposition alimentaire, professionnelle et résidentielle. Disponible à : www.canada.ca/fr/sante-canada/services/ securite-produits-consommation/rapports-publications/pesticides-lutte-antiparasitaire/politiques-lignes-directrices/ document-principes/2014/parametres-facteurs-exposition-generaux-utilises-evaluations-exposition-alimentaire- professionnelle-residentielle-spn2014-01.html (consulté le 16-03-2018)
- Santé Canada. 2017. Framework for Initiating and Conducting Risk Analysis Activities on Microbial Hazards in Food. Cat. : H164-198/2017E-PDF, ISBN: 978-0-660-06811-4, Pub : 160231. Disponible à : publications@hc-sc.gc.ca
- Santé Canada, Agence de la santé publique du Canada, Agence canadienne d'inspection des aliments. 2011. Poids de la preuve : Facteurs à considérer pour la prise de mesures appropriées et en temps opportun dans une situation d'enquête sur une éclosion de maladie d'origine alimentaire. Disponible à : www.canada.ca/content/dam/hc-sc/migration/hc-sc/fn-an/ alt_formats/pdf/pubs/securit/2011-food-illness-outbreak-eclosion-malad-ailments-fra.pdf (consulté le 16-03-2018)
- National Research Council. 2014. Review of EPA's Integrated Risk Information System (IRIS) Process. Committee to Review the IRIS Process; Board on Environmental Studies and Toxicology; Division on Earth and Life Studies. National Academies of Sciences, Engineering, Medicine – National Academies Press. Disponible à : http://nap.edu/18764 (consulté le 19-03-2018)
- Direction des produits de santé naturels et sans ordonnance, Santé Canada. 2010. Avis aux demandeurs de licence de mise en marché – présentation d'allégations relative à l'utilisation traditionnelle : Critères de preuve et modèle d'évaluation des preuves. Disponible à : www.canada.ca/fr/sante-canada/services/medicaments-produits-sante/ naturels-sans-ordonnance/legislation-lignes-directrices/documents-reference/presentations-allegations-relatives- utilisation-traditionnelle-criteres-preuve-modele-evaluation-preuves.html (consulté le 16-03-2018)
- Direction des produits de santé naturels et sans ordonnance, Santé Canada. 2012a. Cheminement des demandes de licences de mise en marché des produits de santé naturels utilisés comme remèdes traditionnels. Disponible à : www.canada.ca/fr/sante-canada/services/medicaments-produits-sante/naturels-sans-ordonnance/legislation-
lignes-directrices/documents-reference/cheminement-demandes-licence-mise-marche-remedes-traditionnels.html
(consulté le 16-03-2018) - Direction des produits de santé naturels et sans ordonnance, Santé Canada. 2012b. Cheminement des demandes de licence de mise en marché des produits de santé naturels qui font l'objet d'allégations santé fondées sur des preuves modernes. Disponible à : www.canada.ca/fr/sante-canada/services/medicaments-produits-sante/naturels-sans-ordonnance/ legislation-lignes-directrices/documents-reference/cheminement-demandes-licence-mise-marche-allegations- sante-fondees-preuves-modernes.html (consulté le 16-03-2018)
- OCDE : Organisation de coopération et de développement économiques. 2015. Report of the Workshop on a Framework for the Development and Use of Integrated Approaches to Testing and Assessment. Series on Testing and Assessment No. 215, ENV/JM/MONO(2015)22. Disponible à : www.oecd.org/officialdocuments/publicdisplaydocumentpdf/?cote=ENV/JM/ MONO(2015)22&doclanguage=en (consulté le 20-03-2018)
- OCDE. 2017. Revised Guidance Document on Developing and Assessing Adverse Outcome Pathways. Series on Testing & Assessment No. 184, ENV/JM/MONO(2013)6. Disponible à : www.oecd.org/officialdocuments/publicdisplaydocumentpdf/ ?cote=env/jm/mono(2013)6&doclanguage=en (consulté le 20032018)
- OCDE. 2018. Users' Handbook Supplement to the Guidance Document for Developing and Assessing AOPs. Series on Testing & Assessment No. 233, Series on Adverse Outcome Pathways No. 1, ENV/JM/MONO(2016)12. Disponible à : https://one.oecd.org/document/ENV/JM/MONO(2016)12/en/pdf (consulté le 20-03-2018)
- Sécurité publique Canada. 2018. Lignes directrices sur la méthodologie d'évaluation tous risques 2012–2013. Disponible à : www.securitepublique.gc.ca/cnt/rsrcs/pblctns/ll-hzrds-ssssmnt/index-fr.aspx (consulté le 16-03-2018)
- Saner M. 2010. Guide d'introduction sur l'évaluation scientifique des risques à Santé Canada. SC Pub. : 100140; Cat. : H22-4/3-2010; ISBN : 978-1-100-15377-3. Disponible à : www.canada.ca/content/dam/hc-sc/migration/hc-sc/sr-sr/ alt_formats/pdf/pubs/about-apropos/2010-scientif-ris-fra.pdf (consulté le 16-03-2018)
- OMS (Organisation mondiale de la santé). 2008. Programme international sur la sécurité des substances chimiques. Uncertainty and Data Quality in Exposure Assessment. Disponible à : www.who.int/ipcs/publications/methods/ harmonization/exposure_assessment.pdf?ua=1 (consulté le 15-03-2018)
- OMS. 2017. Programme international sur la sécurité des substances chimiques. Guidance Document on Evaluating and Expressing Uncertainty in Hazard Characterization. Disponible à : http://apps.who.int/iris/bitstream/handle/ 10665/259858/9789241513548-eng.pdf?sequence=1 (consulté le 15-03-2018)
Annexe 1
Représentation graphique de la méthode du poids de la preuve dans le contexte de l'évaluation des risques scientifiques
Ensemble de la preuve: interprétations conceptuelles de la nature et de l'étendue des preuves à prendre en compte
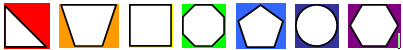
1. Collecte de « toutes » les preuves
Équivalent textuel
L'étape 1 illustre la collecte de toutes les preuves, qui est représentée par 7 formes multicolores, ou «preuves».
2. Évaluation d'études distinctes (sur le plan de la « qualité », de la « pertinence », etc.)
(*Nota: Certaines études peuvent ne pas répondre à tous les critères mais elles pourraient quand même être prises en compte si, en combinaison avec d'autres études, elles contribuent à une argumentation par le poids de la preuve.)

Équivalent textuel
L'étape 2 illustre le processus d'évaluation d'études individuelles en conservant certaines preuves (en utilisant une flèche intitulée «inclusion») et en supprimant deux des formes multicolores de la preuve (en utilisant une flèche intitulée «exclusion»).
3. Regroupement des éléments de preuve
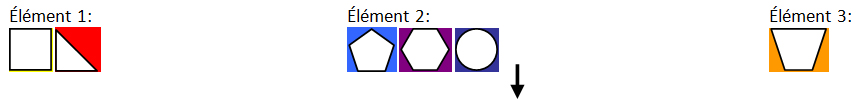
Équivalent textuel
L'étape 3 illustre trois «éléments de preuve» distinctes en catégorisant les formes multicolores en élément de preuve 1, 2 ou 3.
Appréciation de la preuve: méthodes d'évaluation des divers éléments de preuve pour la formulation d'une conclusion finale
4. Évaluation des éléments de preuve (causalité, danger, exposition, etc.)
5. Intégration des éléments de preuve multiples
| Éléments de preuve | Critères évalués (Faible…. Fort): | Description qualitative |
|---|---|---|
Élément 1 |
|
(Faible…Fort) |
Élément 2 |
|
(Faible…Fort) |
Élément 3 |
|
(Faible…Fort) |
Conclusion générale |
L'argument, en termes de poids de la preuve, selon lequel le produit Y est la source de contamination pour l'éclosion de maladie d'origine alimentaire X est (Faible…Fort) |
|
|
||
| Critères évalués | Description qualitative |
|---|---|
| Rigueur de l'ensemble des données | limiteé |
| Puissance de l'ensemble des données | limiteé |
| Corroboration et concordance | limiteé |
| Plausibilité/cohérence biologique | limiteé |
| Poids de l'ensemble de la preuve fondé sur les effets neurocomportementaux chez les rongeurs de l'exposition à des doses inférieures aux DSENO établies pour la toxicité pour la reproduction et le développement | limiteé |
|
|
Annexe 2
| Programme | Ensemble de la preuveAnnex 2 Note de bas de page * : interprétations conceptuellesde la nature et de l'étendue des sources de données probantes à prendre en compte |
Appréciation de la preuveAnnex 2 Note de bas de page ** : méthodes d'évaluation et d'intégration des divers éléments de preuve pour la formulation d'une conclusion finale |
|||
|---|---|---|---|---|---|
| Prise en compte de tous les éléments de preuves disponibles à ce jour, par opposition à un sous-ensemble de données | Prise en compte d'études qui, prises isolément, peuvent ne pas satisfaire à tous les critères, mais qui contribuent à une argumentation par le poids de la preuve lorsqu'elles sont combinées | Qualitative [p. ex. liste, meilleur jugement professionnel] | Semi-quantitative [p. ex. critères de causalité, modèles logiques, notation alphanumérique ou indexation] | Quantitative (p. ex. techniques probabilistes ou analyse décisionnelle multicritères | |
| Direction générale de la santé environnementale et de la sécurité des consommateurs (DGSESC) | |||||
| BQEAAnnex 2 Note de bas de page 1 / Eau | |||||
| BEACC / Air | |||||
| Substances nouvelles BECSAnnex 2 Note de bas de page 2 | |||||
| Substances existantes BERSEAnnex 2 Note de bas de page 3 | |||||
| DSSERAnnex 2 Note de bas de page 4 | |||||
| DSPCAnnex 2 Note de bas de page 5 | |||||
| Direction générale des produits de santé et des aliments (DGPSA) | |||||
| DPTAnnex 2 Note de bas de page 6 | |||||
| DPBTGAnnex 2 Note de bas de page 7 / Produits biologiques | |||||
| DPSAnnex 2 Note de bas de page 8 | |||||
| DPSNAnnex 2 Note de bas de page 9 | |||||
| DMVAnnex 2 Note de bas de page 10 | |||||
| DAAnnex 2 Note de bas de page 11 / Aliments nouveaux | |||||
| DA / Étiquetage nutritionnel et allégations | |||||
| DA / Dangers microbiens | |||||
| Agence de réglementation de la lutte antiparasitaire (ARLA) | |||||
| DESAnnex 2 Note de bas de page 12 | |||||
|
|||||
Annexe 3
Liste de contrôle pour étayer clairement la méthode du poids de la preuve
Lorsque des termes associés au poids de la preuve sont employés, préciser le sens voulu par rapport aux concepts suivants :
- Ensemble de la preuve : interprétations conceptuelles de la nature et de l'étendue des sources de données probantes à prendre en compte;
- Appréciation de la preuve : méthode d'évaluation et d'intégration des éléments de preuve multiples.
L'information qui suit est-elle consignée dans le processus d'évaluation des risques?
- preuves recueillies : toutes les données disponibles à ce jour, chaque source et chaque type de données;
- preuves incluses pour étude ultérieure, et pourquoi (critères d'inclusion);
- preuves rejetées, et pourquoi (critères d'exclusion);
- éléments de preuve regroupés (énumérer les études sous chaque élément de preuve);
- critères d'évaluation appliqués aux éléments de preuve, et système de notation utilisé (s'il y a lieu);
- valeur ou poids attribué à chaque élément de preuve (p. ex. descriptions, valeur alphanumérique);
- méthode d'intégration (p. ex. meilleur jugement professionnel, formule mathématique, cadre de critères);
- conclusion ou recommandation(s) globale(s).
Notes de bas de page
- Note de bas de page 1
-
Division de la bioéthique et intégrations des politiques, Direction de la politique de la science, DPS, Ottawa, ON
- Note de bas de page 2
-
Direction de l'évaluation sanitaire, ARLA, Ottawa, ON
- Note de bas de page 3
-
Programme de santé environnementale, Région du Québec, DGRP, Longueuil, QC
- Note de bas de page 4
-
Bureau de l'évaluation et du contrôle des substances nouvelles, Direction de la sécurité des milieux, DGSESC, Ottawa, ON
- Note de bas de page 5
-
Centre de l'évaluation des produits radiopharmaceutiques et biothérapeutiques, Direction des produits biologiques et des thérapies génétiques, DGPSA, Ottawa, ON
- Note de bas de page 6
-
Bureau de dangers microbiens, Direction des aliments, DGPSA, Ottawa, ON
- Note de bas de page 7
-
Bureau de la gestion des risques et de la science, Direction des produits de santé commercialisés, DGPSA, Ottawa, ON
- Note de bas de page 8
-
Bureau d'évaluation du risque des substances existantes, Direction de la sécurité des milieux, DGPSA, Ottawa, ON
- Note de bas de page 9
-
Les termes « preuve », « information » et « donnée » sont employés ici indifféremment et dans un contexte scientifique général. Ils ne correspondent pas à la définition juridique stricte d'une preuve qui serait « admissible » dans un tribunal.