Ébauche d’évaluation préalable - Groupe des acides naphtalènesulfoniques et de leurs sels (ANS)
Titre officiel : Ébauche d’évaluation préalable - Groupe des acides naphtalènesulfoniques et de leurs sels (ANS)
Numéros de registre du Chemical Abstracts Service
1321-69-3, 25322-17-2, 25619-56-1, 57855-77-3, 60223-95-2, 68425-61-6
Environnement et Changement climatique Canada
Santé Canada
Juillet 2020
Sommaire
En vertu de l’article 68 ou 74 de la Loi canadienne sur la protection de l’environnement (1999) (LCPE), les ministres de l’Environnement et de la Santé ont procédé à l’évaluation préalable de six des sept substances appelées collectivement « groupe des acides naphtalènesulfoniques et leurs sels » dans le cadre du Plan de gestion des produits chimiques. Ces six substances ont été considérées d’intérêt prioritaire pour une évaluation, car elles satisfaisaient aux critères de catégorisation du paragraphe 73(1) de la LCPE ou en raison d’autres préoccupations liées à la santé humaine ou à l’environnement. Trois substances de ce groupe visées par la présente évaluation ne satisfaisaient pas aux critères de catégorisation, mais ont été désignées d’intérêt prioritaire en suivant l’approche décrite pour l’Identification des priorités d’évaluation des risques. Au départ, le groupe comportait une septième substance, mais d’autres démarches ont permis de déterminer qu’elle était peu préoccupante. Un autre rapportNote de bas de page 1 présente les conclusions relatives à cette substance. La présente évaluation préalable porte donc sur les six substances énumérées dans le tableau ci-dessous. Ces six substances seront désignées sous le nom de « groupe des acides naphtalènesulfoniques et leurs sels (ANS) ». Nous donnons dans ce tableau leur numéro de registre du Chemical Abstracts Service (no CASNote de bas de page 2 ), leur nom sur la Liste intérieure (LI) et l’acronyme utilisé dans le présent document.
| No CAS | Nom sur la LI | Acronyme |
|---|---|---|
| 1321-69-3 | naphtalènesulfonate de sodium | NSNa |
| 25322-17-2b | acide dinonylnaphtalènesulfonique | ADNNS |
| 25619-56-1b | bis(dinonylnaphtalènesulfonate) de baryum | DNNSBa |
| 57855-77-3c | bis(dinonylnaphtalènesulfonate) de calcium | DNNSCa |
| 60223-95-2b | acide dinonylnaphtalènedisulfonique | ADNNDS |
| 68425-61-6 | acide diisopropylnaphtalènesulfonique, composé avec la cyclohexylamine (1:1) | CDINSA |
a Toutes ces substances sont des substances de composition inconnue ou variable, des produits de réactions complexes ou des matières biologiques (UVCB).
b La démarche d’Identification des priorités d’évaluation des risques a déterminé que cette substance était prioritaire.
c Cette substance n’est pas visée par le paragraphe 73(1) de la LCPE, mais elle a été incluse dans l’évaluation, car elle était considérée prioritaire en raison d’autres préoccupations pour la santé humaine.
Les six substances du groupe ANS sont produites commercialement et n’existent pas naturellement dans l’environnement. Elles ont été visées par des enquêtes menées en vertu de l’article 71 de la LCPE. Selon les renseignements soumis, entre 100 000 et 1 000 000 kg de NSNa et moins de 1 000 kg de DNNSCa ont été produits au Canada. Les autres substances n’y sont pas produites, mais entre 1000 kg et 100 000 kg de chacune y ont été importés. Ces substances sont diversement utilisées dans des combustibles, des lubrifiants, des peintures et revêtements et matériaux à base de caoutchouc, et pour l’extraction du pétrole et du gaz naturel ou le traitement de l’eau.
Les risques posés par le NSNa à l’environnement ont été caractérisés à l’aide de la Classification des risques écologiques des substances organiques (CRE). Il s’agit d’une approche basée sur le risque qui tient compte de plusieurs paramètres liés au danger et à l’exposition et assigne un classement du risque après pondération de plusieurs éléments de preuve. Selon les résultats de la CRE, il est improbable que le NSNa ait des effets nocifs sur l’environnement.
Nous avons évalué les risques pour l’environnement posés par les cinq autres substances du groupe des ANS à partir d’une combinaison de données empiriques et de données sur les dangers posés par des substances analogues, qui nous ont éclairés sur le devenir et les effets de ces substances. L’estimation des dangers de ces substances a été regroupée en raison de similitudes de leurs structures chimiques et de leurs effets. De même, l’exposition de l’environnement a été considérée pour l’ensemble du groupe, puisqu‘il est présumé que l’on peut substituer une des substances par un autre
dans des applications industrielles. Certaines d’entre elles pourraient être persistantes et bioaccumulatives. Les scénarios d’exposition de l’évaluation environnementale incluaient leur rejet dans l’environnement aquatique dû à la préparation d’huiles lubrifiantes, à l’utilisation de fluides d’usinage, à la formulation de peintures et revêtements, à la formulation de produits pétroliers et gaziers et a l’utilisation industrielle de peintures. Ont aussi été prises en compte l’exposition du sol découlant de l’application de biosolides et l’exposition dans les sédiments. Nous avons trouvé qu’aux niveaux actuels d’exposition, ces cinq membres du groupe des ANS présentaient un faible risque.
Compte tenu de tous les éléments de preuve avancés dans la présente ébauche d’évaluation préalable, les six substances du groupe des ANS présentent un faible risque d’effets nocifs sur l’environnement. Il est conclu que les six substances du groupe des ANS ne satisfont pas aux critères de l’alinéa 64a) ou b) de la LCPE, car elles ne pénètrent pas dans l’environnement en une quantité ou concentration ni dans des conditions de nature à avoir, immédiatement ou à long terme, un effet nocif sur l’environnement ou sa diversité biologique, ou à mettre en danger l’environnement essentiel pour la vie.
En ce qui concerne la santé humaine, le DNNSBa et le CDINSA ont été évalué en suivant l’approche suivie pour l’Évaluation préalable rapide des substances pour lesquelles l’exposition de la population générale est limitée, pour déterminer si une substance requiert une évaluation supplémentaire sur la base de l’exposition potentielle, directe ou indirecte, de la population générale. Cette approche a permis d’établir que le potentiel d’exposition de la population générale au DNNSBa et au CDINSA était négligeable, indiquant une faible probabilité de risque pour la santé humaine. Nous considérons donc qu’aux niveaux actuels d’exposition, le DNNSBa et le CDINSA sont peu préoccupants pour la santé humaine.
Dans le cas des quatre autres substances, les Canadiens peuvent principalement être exposés à l’ADNNS, au DNNSCa et à l’ADNNDS par l’eau potable, alors que le NSNa n’est pas rejeté dans l’environnement. Bien que certains matériaux d’emballage contenant de l’ADNNS, utilisé comme agent antistatique, puissent entrer en contact direct avec les aliments, l’exposition due à de tels emballages alimentaires devrait être négligeable. L’emploi de produits disponibles pour les consommateurs ne devrait pas exposer la population générale au NSNa, à l’ADNNS et à l’ADNNDS. À cause de sa présence dans un lubrifiant en aérosol à usage général, des inhalations et des expositions cutanées intermittentes au DNNSCa pourraient avoir lieu.
Selon les classifications de la cancérogénicité, de la génotoxicité et de la toxicité pour le développement et la reproduction faites par d’autres organismes nationaux ou internationaux, le NSNa ne constitue pas un grave danger pour la santé humaine. Nous n’avons donc pas poussé plus loin les recherches sur ses effets potentiels sur la santé humaine, car la population générale du Canada ne devrait pas y être exposée. Puisqu’il existait peu de données sur les effets sur la santé de l’ADNNS, du DNNSCa et de l’ADNNDS, nous avons utilisé la lecture croisée pour éclairer la caractérisation de leurs effets sur la santé. Sur la base d’études de laboratoire réalisées sur des substances structurellement proches, nous considérons que les effets critiques de l’ADNNS, du DNNSCa et de l’ADNNDS sur la santé sont la formation de cristaux dans les reins et des effets sur la thyroïde. La comparaison des niveaux d’exposition à l’ADNNS ou à l’ADNNDS à partir de milieux environnementaux aux concentrations causant des effets sur la santé a conduit à calculer des marges qui sont considérées adéquates pour tenir compte des incertitudes des bases de données sur les effets sur la santé et l’exposition. De même, la comparaison des niveaux d’exposition au DNNSCa du aux milieux environnementaux ou à l’utilisation de lubrifiants contenant du DNNSCa et des concentrations causant des effets sur la santé a permis de calculer des marges qui sont considérées adéquates pour tenir compte des incertitudes des bases de données sur les effets sur la santé et l’exposition.
À la lumière des renseignements contenus dans la présente ébauche d’évaluation préalable, il est conclu que les six substances du groupe des ANS ne satisfont pas aux critères de l’alinéa 64c) de la LCPE, car elles ne pénètrent pas dans l’environnement en une quantité ou concentration ni dans des conditions de nature à constituer un danger au Canada pour la vie ou la santé humaine.
Il est proposé de conclu que les six substances du groupe des ANS ne satisfont à aucun des critères de l’article 64 de la LCPE.
1. Introduction
En vertu de l’article 68 ou 74 de la Loi canadienne sur la protection de l’environnement (1999) [LCPE] (Canada 1999], les ministres de l’Environnement et de la Santé ont procédé à l’évaluation préalable de six des sept substances appelées collectivement « Groupe des acides naphtalènesulfoniques et leurs sels » dans le cadre du Plan de gestion des produits chimiques, afin d’établir si elles constituent ou pourraient constituer un risque pour l’environnement ou la santé humaine. Trois substances ont été identifiées d’intérêt prioritaire pour une évaluation, car elles satisfont aux critères de catégorisation du paragraphe 73(1) de la LCPE ou en raison d’autres préoccupations liées à la santé humaine ou à l’environnement (ECCC, SC [modifié 2017]). Les trois autres substances ont été ajoutées après avoir été identifiées d’intérêt prioritaire dans le cadre de l’approche de Détermination des priorités en matière d’évaluation des risques (ECCC, SC 2015, Environnement Canada, Santé Canada 2014).
Le groupe des ANS contenait au départ une septième substance, le butylnaphtalènesulfonate de sodium (no CASNote de bas de page 3 25638-17-9). Or, elle a été étudiée au moyen du Document sur l’approche scientifique : Classification du risque écologique des substances organiques (CRE) (ECCC 2016a) et de l’approche suivie pour l’Évaluation préalable rapide des substances pour lesquelles l’exposition de la population générale est limitée (ECCC, SC 2018a), et jugée peu préoccupante pour la santé humaine et l’environnement. Elle ne sera donc pas étudiée davantage dans la présente évaluation. Le lecteur trouvera les conclusions relatives à cette substance dans le rapport de l’Évaluation rapide de substances auxquelles l’exposition de la population générale est limitée (ECCC, SC 2018a). Les six substances visées par la présente évaluation préalable seront désignées ci-après sous le nom de « groupe des ANS ».
Le risque pour l’environnement posé par l’une des substances du groupe des ANS, le NSNa (no CAS 1321-69-3), a été caractérisé en utilisant la Classification du risque écologique des substances organiques (CRE), une approche basée sur les risques qui tient compte de plusieurs paramètres liés au danger et à l’exposition, avec une pondération des éléments de preuve pour déterminer la classification des risques. Puisque la CRE a déterminé que le potentiel d’effets nocifs du NSNa sur l’environnement était faible (ECCC 2016 b), son impact sur l’environnement ne sera pas pris en compte davantage dans la présente évaluation, bien que les risques pour la santé humaine seront abordés.
Étant donné que l’ADNNS, le DNNSBa, le DNNSCa, l’ADNNDS et le CDINSA peuvent potentiellement être utilisé de manières et dans des applications similaires, le potentiel de risque pour l’environnement a été évalué en faisant des hypothèses d’exposition similaires pour tout le groupe. Toutefois, le risque pour la santé humaine a été évalué individuellement.
En ce qui concerne la santé humaine, nous avons évalué le DNNSBa et le CDINSA en suivant l’approche d’évaluation préalable rapide de l’exposition de la population générale à des substances à effet limité (ECCC, SC 2018). Dans le cadre de cette approche, le potentiel d’exposition directe est évalué sur la base de considérations comme la présence avérée de la substance dans un produit utilisé par la population générale, et le potentiel d’exposition indirecte a été adapté de l’approche générale présentée dans le document sur l’Approche fondée sur le seuil de préoccupation toxicologique (SPT) pour certaines substances (Santé Canada 2016). À partir de l’évaluation des expositions directe et indirecte menée dans le cadre de ladite approche, l’exposition de la population générale au DNNSBa et au CDINSA a été jugée négligeable. Nous considérons donc qu’aux niveaux actuels d’exposition, le DNNSBa et le CDINSA sont peu préoccupants pour la santé humaine.
Pour la présente ébauche d’évaluation préalable, nous avons pris en compte des renseignements sur les propriétés chimiques, le devenir dans l’environnement, les dangers, les utilisations et l’exposition. Des données pertinentes ont été identifiées jusqu’en avril 2019. Nos conclusions reposent sur des données empiriques tirées d’études critiques et les résultats de modélisation. Nous avons aussi pris en compte des renseignements pertinents présentés dans des évaluations réalisées par d’autres juridictions.
La présente ébauche d’évaluation préalable a été préparée par le personnel du Programme d’évaluation des risques de la LCPE de Santé Canada et d’Environnement et Changement climatique Canada, elle inclut des intrants d’autres programmes de ces ministères. Les parties de la présente évaluation préalable portant sur la santé humaine et l’environnement ont été soumises à des examens ou des consultations externes. Geoff Granville (GCGranville Consulting Corp) et James Armitage (AES Environmental Services, Inc.) ont formulé des commentaires sur les parties techniques touchant l’environnement. Les commentaires sur les parties techniques relatives à la santé humaine ont été formulés par Theresa Lopez, Jennifer Flippin, et Joan Garey, de Tetra Tech. De plus, le document sur la Classification du risque écologique (SCR) des substances organiques (ECCC, 2016a) a été soumis au jugement par les pairs et a fait l’objet d’une période de 60 jours de commentaires du public. Le document sur l’Évaluation préalable rapide des substances avec une exposition limitée pour la population générale (ECCC, SC 2018) a aussi été soumis aux commentaires du public pendant une période de 60 jours. Bien que des commentaires externes aient été pris en compte, Santé Canada et Environnement et Changement climatique Canada assument la responsabilité du contenu final et des conclusions de la présente évaluation préalable.
La présente ébauche d’évaluation préalable repose sur des renseignements critiques pour déterminer si ces substances satisfont aux critères de l’article 64 de la LCPE. Pour ce faire, nous avons examiné des données scientifiques et suivi une approche basée sur le poids de la preuve et le principe de précaution.Note de bas de page 4 Dans le présent document, nous présentons ces données critiques et les analyses sur lesquelles se fondent les conclusions proposées.
2. Identité des substances
Le tableau 2‑1 donne le numéro du registre CAS, le nom sur la Liste intérieure des substances (LIS) et l’acronyme des six substances du groupe des ANS.
Chaque substance de ce groupe est considéré être un UVCBNote de bas de page 5 (substance de composition inconnue ou variable, produits de réactions complexes ou matières biologiques) puisque ni la position du groupe sulfonate ni celle du groupe alkyle sur les deux cycles sur le naphtalène ne sont précisées. De plus, les groupes nonyles de certaines d’entre elles peuvent se présenter être linéaires ou ramifiés. À des fins de simplicité, la géométrie exacte (linéaire ou ramifiée) n’est pas représentée dans les structures représentatives.Version:1.0 StartHTML:0000000298 EndHTML:0000038379 StartFragment:0000038339 EndFragment:0000038339 SourceURL:file:///G:/Web%20Unit/Existing%20Substances/12%20-%20Assessments%20Reports/CMP3/Naphthalene%20sulfonic%20acids%20and%20salts/DSAR/Web%20Conversion/20200529-NSAs-DSAR-FR_CGEdits.docx
| No CAS (acronyme) | Nom sur la LIS | Structure chimique représentative et formule moléculaire | Masse moléculaire(g/mol) |
|---|---|---|---|
| 1321-69-3 (NSNa) | naphtalènesulfonate de sodium | ![[Na+].CC(C)c1cc(C(C)C)c(c2ccc(C)cc12)S([O-])(=O)=O](/content/dam/eccc/images/pded/nsas/20200604-t21a.jpg) C10H8O3SNa C10H8O3SNa | 230,22 |
| 25322-17-2 (ADNNS) | acide dinonylnaphtalènesulfonique | 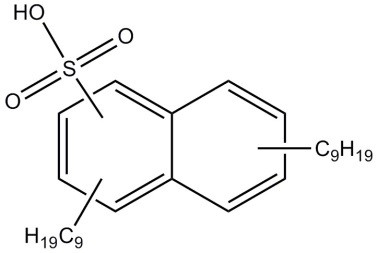 C28H44O3S C28H44O3S | 460,72 |
| 25619-56-1 (DNNSBa) | bis(dinonylnaphtalènesulfonate) de baryum | 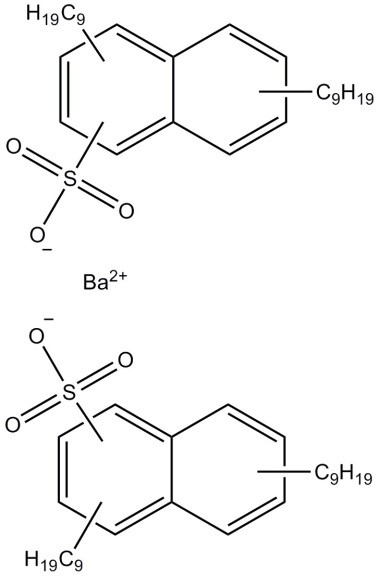 C56H88O6S2Ba C56H88O6S2Ba | 1056,75 |
| 57855-77-3 (DNNSCa) | bis(dinonylnaphtalènesulfonate) de calcium | 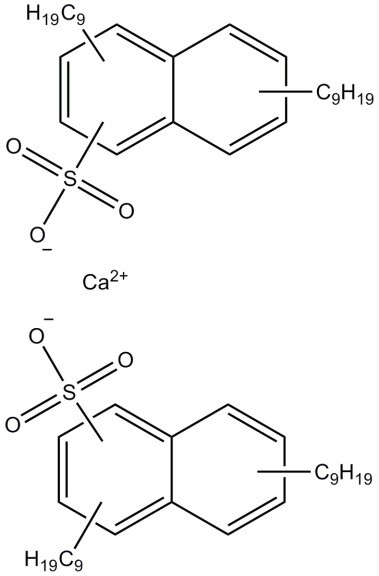 C56H88O6S2Ca C56H88O6S2Ca | 959,50 |
| 60223-95-2 (ADNNDS) | acide dinonylnaphtalènedisulfonique | 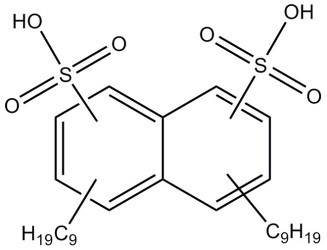 C28H44O6S2 C28H44O6S2 | 540,78 |
| 68425-61-6 (CDINSA) | acide diisopropylnaphtalènesulfonique, composé avec la cyclohexylamine (1/1) | 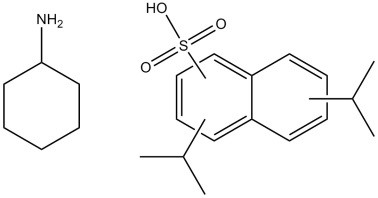 C6H13N.C16H20O3S C6H13N.C16H20O3S | 391,57 |
2.1 Choix des analogues et utilisation de modèles QSAR
Nous avons suivi une approche de lecture croisée à partir de substances analogues et des résultats de modèles de (Q)SAR (relations structure-activité (quantitatives)), le cas échéant, pour éclairer les évaluations relatives à l’environnement et la santé humaine. Nous avons choisi des analogues présentant une structure et/ou une fonction similaires à celles des substances du groupe (p. ex. propriétés physicochimiques, toxicocinétique), pour lesquels existaient des données empiriques pertinentes utilisables pour une lecture croisée. L’applicabilité des modèles QSAR a été déterminée au cas par cas. Les détails des données de lecture croisée et des modèles QSAR utilisés pour éclairer les évaluations relatives à l’environnement et la santé humaine du groupe des ANS sont discutés plus en détail dans les parties pertinentes du présent rapport et dans l’annexe F. Nous donnons dans le tableau 2-2 l’identité et les structures chimiques des analogues utilisés pour éclairer la présente évaluation. Nous donnons dans le tableau 2-3 une indication des données de lecture croisée disponibles pour différents paramètres.
| No CAS (acronyme) | Nom sur la LIS [nom commun] | Structure chimique et formule moléculaire | Masse moléculaire (g/mol) |
|---|---|---|---|
| 120-18-3 (AN2S) | acide naphtalène-2-sulfonique | 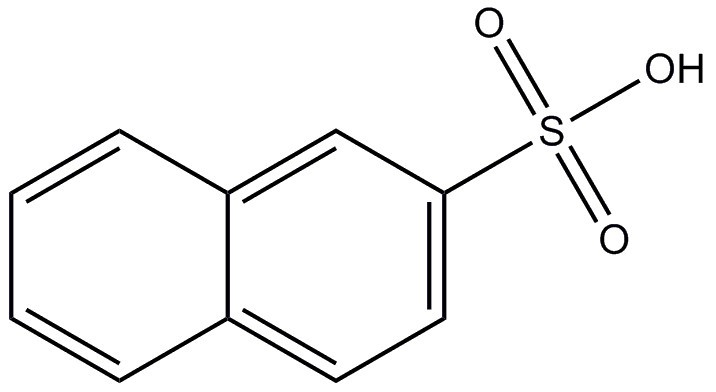 C10H8O3S C10H8O3S | 208,23 |
| 68153-01-5 | acides naphtalènesufoniques | 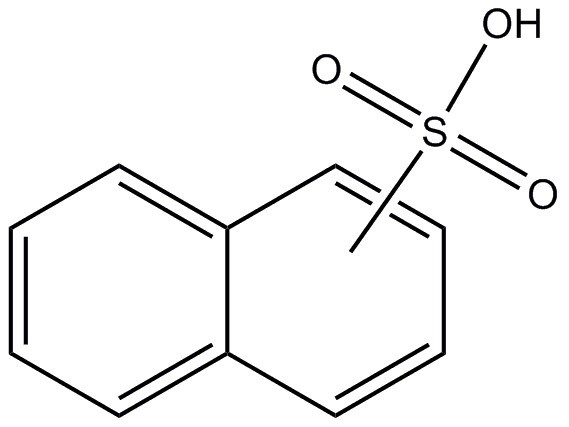 C10H8O3S C10H8O3S | 208,23 |
| 91078-64-7 | Acides naphtalènesulfoniques, dérivés butylés ramifiés et linéaires, sels de sodium[n(butyl linéaire ou ramifié)naphtalène (msulfonates) de m(sodium)] | ![[(C4H9)n]C1=CC2=C(C=C1)C=C([(SO3Na)m])C=C2](/content/dam/eccc/images/pded/nsas/20200604-t22b.jpg) m = 1-2, n = 1-3 m = 1-2, n = 1-3 | 288,29 à 551,46 |
| No de la Comm. Europ.a, b 939-714-0 ((ADANS riche en C9) | acides di(alkyl en C8-10 ramifié riche en C9) naphtalènesulfoniques(au milieu) [sont aussi représentés les acides mono(alkyl en C8-10 ramifié riche en C9) (en haut) et tri(alkyl en C8-10 ramifié riche en C9) naphtalènesulfoniques] (en bas) | ![[R]C1=CC=C(C=C(S(=O)(O)=O)C=C2)C2=C1](/content/dam/eccc/images/pded/nsas/20200604-t22d1.jpg) ![[R]C1=C([R])C=C(C=C(S(=O)(O)=O)C=C2)C2=C1](/content/dam/eccc/images/pded/nsas/20200604-t22d2.jpg) ![[R]C1=C([R])C=C(C=C(S(=O)(O)=O)C=C2[R])C2=C1](/content/dam/eccc/images/pded/nsas/20200604-t22d3.jpg) R = C8-C10 R = C8-C10 | S.O. |
| No de la Comm. europ.a, b 939-718-2 (DANSBa riche en C9) | bis[(dialkyl ramifié en C8-10 riche en C9) naphtalènesulfonates] de baryum [Sont aussi montrés les bis[(monoalkyl ramifié en C8-10 riche en C9 et trialkyl ramifiés en C8-10 riche en C9) naphtalènesulfonates de baryum] | ![[R]C1=CC=C2C(C=CC(S(=O)([O-])=O)=C2)=C1.[Ba+2]](/content/dam/eccc/images/pded/nsas/20200604-t22e1.jpg)
![[R]C1=C([R])C=C2C(C=CC(S(=O)([O-])=O)=C2)=C1.[Ba+2]](/content/dam/eccc/images/pded/nsas/20200604-t22e2.jpg)
![[R]C1=C([R])C=C2C(C=CC(S(=O)([O-])=O)=C2[R])=C1.[Ba+2]](/content/dam/eccc/images/pded/nsas/20200604-t22e3.jpg) R = C8-C10 R = C8-C10 | 776,18 à 1393,39 |
| No de la Comm. europ.a, b 939-717-7 (DANSCa riche en C9) | bis[(dialkyl ramifié en C8-10 riche en C9) naphtalènesulfonates] de calcium Sont aussi montré les bis[(monoalkyl ramifié en C8-10 riche en C9s et trialkyl ramifié en C8-10 riche en C9) naphtalènesulfonates] de calcium | ![[R]C1=CC=C2C(C=CC(S(=O)([O-])=O)=C2)=C1.[Ca+2]](/content/dam/eccc/images/pded/nsas/20200604-t22f1.jpg) ![[R]C1=C([R])C=C2C(C=CC(S(=O)([O-])=O)=C2)=C1.[Ca+2]](/content/dam/eccc/images/pded/nsas/20200604-t22f2.jpg) ![[R]C1=C([R])C=C2C(C=CC(S(=O)([O-])=O)=C2[R])=C1.[Ca+2]](/content/dam/eccc/images/pded/nsas/20200604-t22f3.jpg) R = C8-C10 R = C8-C10 | 678,24 à 1296,15 |
| No de la Comm. europ.a 947‑977-8 | acides naphtalènesulfoniques, produits de la réaction avec du 2‑méthypropanol, sels de sodium | ![CC(C)CC1=CC=C(S(=O)([O-])=O)C2=CC=C(CC(C)C)C=C21.[Na+]](/content/dam/eccc/images/pded/nsas/20200604-t22g.jpg) C18H23O3SNa C18H23O3SNa | 342,43 |
| S.O.a | alkylsulfates, alcanesulfonates et (alc‑1-ène)sulfonates | S.O. | S.O. |
| N/Aa (ALBS en C10-11) | (alkyl linéaire en C10-11) benzènesulfonates de sodium | ![O=S(C1=CC=CC([R])=C1)([O-])=O.[Na+]](/content/dam/eccc/images/pded/nsas/20200604-t22h.jpg) R = C10-C11 R = C10-C11 | 320,42 à 334,45 |
| S.O.a | alcanesulfonates en C14-17 | S.O. | S.O. |
| S.O.a (ALBS en C10-13)b | (alkyl linéaire en C10-13) benzènesulfonates de sodium | ![O=S(C1=CC=CC([R])=C1)([O-])=O.[Na+]](/content/dam/eccc/images/pded/nsas/20200604-t22i.jpg) R = C10-C13 R = C10-C13 | 320,42 à 362,50 |
| 68909-82-0b | Acide diisopropylnaphtalènesulfonique, dérivés méthylés, sels de sodium [méthyl(di(propane-2-yl)) naphtalènesulfonates de sodium | ![[Na+].CC(C)c1cc(C(C)C)c(c2ccc(C)cc12)S([O-])(=O)=O](/content/dam/eccc/images/pded/nsas/20200604-t22j.jpg) | 328,40 |
Abréviation – S.O. : sans objet
a Il n’y a pas de no CAS pour cette substance, ou celui-ci est inconnu.
b La formule moléculaire de cette substance n’apparaît pas en raison de la complexité de sa structure.
| No CAS de l’analogue (acronyme) | Nom | Données physico-chimiques et environnement-ales | Données sur les effets sur la santé |
|---|---|---|---|
| 120-18-3 (AN2S) | acide naphatalène-2-sulfonique | persistance | S.O.a |
| 68153-01-5 | acides naphtalènesulfoniques | écotoxicité | S.O.a |
| 91078-64-7 | n(butyl linéaire ou ramifié)naphtalène (msulfonates) de m(sodium) | bioaccumulation, écotoxicité | S.O.a |
| 68909-82-0 | méthyl(di(propane-2-yl)) naphtalènesulfonates de sodium | écotoxicité | S.O.a |
| No de la Comm. europb 939-714-0 ((DANS riche en C9) | acides di(alkyl en C8-10 ramifié riche en C9)naphtalènesulfoniques | persistance, écotoxicité | Toxicité pour la reproduction et le développement, génotoxicité |
| No de la Comm. europ. 939-718-2 ((DANSBa riche en C9) | bis[(dialkyl ramifié en C8-10 riche en C9) naphtalènesulfonates] de baryum | hydrosolubilité | Toxicité pour la reproduction et le développement, génotoxicité |
| No de la Comm. europ. 939-717-7 (DANSCa riche en C9) | bis[(dialkyl ramifié en C8-10 riche en C9) naphtalènesulfonates] de calcium | hydrosolubilité | Toxicité subaiguë, toxicité subchronique |
| No de la Comm. europ.b 947-977-8 | acides naphtalènesulfoniques, produits de la réaction avec du 2-méthypropanol, sels de sodium | persistance | S.O.a |
| S.O.b | alkylsulfates, alcanesulfonates et (alc-1‑ène)sulfonates | bioaccumulation | S.O.a |
| S.O.b ALS en C10-11 | (alkyl linéaire en C10‑11) benzènesulfonates de sodium | bioaccumulation | S.O.a |
| S.O.b | alcanesulfonates en C14-17 | persistance | S.O.a |
| S.O.b ALS en C10-13 | (alkyl linéaire en C10-13) benzènesulfonates de sodium | persistance | S.O.a |
Abréviation – S.O. : sans objet
a Il n’est pas nécessaire de connaître les effets sur la santé de ces substances, étant donné qu’elles ne sont pas utilisées comme analogues pour l’évaluation relative à la santé humaine.
b Il n’y a pas de no CAS pour cette substance, ou celui-ci est inconnu.
3. Propriétés physiques et chimiques
Les tableaux 3-1 et 3-2 résument les données sur les propriétés physiques et chimiques des substances du groupe des ANS, dont les valeurs retenues indiquées pour chaque propriété. Le tableau 3-1 donne les valeurs retenues des propriétés physiques et chimiques de l’ADNNDS et de l’ADNNS, dont les composantes organiques dissociées de l’ADNNS, du DNNSCa et du DNNSBa. Le tableau 3‑2 donne les valeurs pour le CDINSA et le NSNa. Dans ces tableaux, les valeurs présentées sont les résultats de modélisation, sauf indication contraire. Les résultats modélisés ont été produits pour les variantes structurelles linéaires et ramifiées de l’ADNNS et de l’ADNNDS, le cas échéant, et lorsque les résultats étaient différents, une moyenne des deux valeurs a été utilisée pour la présente évaluation.
Toutes ces substances ont une très faible constante de dissociation acide (pKa) et devraient donc être complètement ionisées (c.-à-d. anioniques) dans des solutions aqueuses dont le pH ambiant est de 6 à 9. L’ionisation se produit par la perte d’un ion hydrogène de chacune des fonctions acides sulfoniques, conduisant à un anion sulfonate (ACD/Percepta c1997-2017). Cependant, puisque nombre des modèles de type RQSA reposent sur des méthodes d’addition de fragments (p. ex., EPI Suite c2000-2012), ils ne fonctionnent habituellement qu’avec la forme neutre d’un produit chimique comme intrant. En conséquence, seule la forme non ionisée de ces substances a été modélisée, le cas échéant. Pour cette raison, les propriétés physiques et chimiques du DNNSBa et du DNNSCa n’ont pas été modélisées. Elles ont plutôt été déduites, au besoin, à partir de l’analogue de l’ADNNS, qui représente leur composante organique. De même, les données sur le CDINSA et le NSNa présentées dans le tableau 3-2 concernent les formes neutres de leurs anions. Les formes ionisées de ces substances devraient avoir une volatilité et une constante de Henry inférieures à celles des formes neutres modélisées au moyen d’EPI Suite.
La solubilité dans l’eau du DNNSBa, du DNNSCa et de l’ADNNDS (tableau 3-1) a été mesurée au moyen de la méthode par agitation en flacon de l’OCDE, à la différence que les échantillons ont été agités pendant trois jours au lieu de 24 heures, et traités aux ultrasons quatre heures/jour pendant ces trois jours. Même avec l’agitation et le traitement aux ultrasons additionnels, les solubilités de ces substances se sont avérées très faibles à faibles (communication personnelle de la Division de la recherche sur les contaminants aquatiques d’Environnement et Changement climatique Canada (ECCC) à la Division de l'évaluation écologique d’ECCC, juin 2019, non référencée). Dans les dossiers REACH sur l’ADNNDS et les substances analogues DANSBa et DANSCa riches en C9, les solubilités dans l’eau mesurées rapportées étaient supérieures de plusieurs ordres de grandeur (tableau 3-1). En ce qui concerne l’ADNNDS, son dossier REACH contenait bien quelques détails au sujet de l’étude sur la solubilité dans l’eau, mais il y était indiqué que la mesure avait été faite à un pH de 1,1-2,1 auquel une solubilité encore est attendue (ACD/Percepta c1997-2017). Les mesures de solubilité dans l’eau du DANSBa et du DANSCa riches en C9 ont été obtenues pour un pH de 6,1 à 7,5 (ECHA 2018b, 2018d).
À la vue de leurs structures chimiques, les substances du groupe des ANS devraient généralement avoir des caractéristiques types de surfactants anioniques. Dans l’eau, les surfactants ont tendance à s’agréger à l’interface entre deux phases (p. ex. octanol et eau) et, lorsque les concentrations sont suffisamment élevées, à former des micelles. Pour ces raisons, les méthodes de test typiques employées pour étudier la partition des surfactants (c.-à-d. log Koe) ainsi que leur solubilité dans l’eau, comme la méthode 117 de l’OCDE (méthode par HPLC) et la méthode 107 de l’OCDE (méthode (méthode par agitation en flacon), ne donnent habituellement pas des résultats précis ou fiables, qui ne conviennent donc pas à ce groupe de substances (McWilliams et Payne 2011). La plupart des ANS ont des propriétés de surfactants, car ils comportent des chaînes alkyles hydrophobes de 8 à 18 atomes de carbone (Farn 2006), ainsi que des groupes sulfonates anioniques. Cependant, étant donné l’absence d’un groupe alkyle dans le NSNa et les groupes d’alkyles à chaîne courte du CDINSA, ces deux substances ne devraient être que minimalement surfactantes.
Les coefficients de partage carbone organique-eau (log Kco) de l’ADNNS, de l’ADNNDS et du CDINSA ont été retenus en se basant sur l’équation décrite dans Abraham et coll. (1994) et les résultats du modèle d’ACD/Percepta (c1997-2017). Cette approche est basée sur des relations linéaires d'énergie libre à plusieurs paramètres (RLELpp) pour évaluer le partage entre l’eau et la matière organique à l’équilibre de composés organiques. L’approche RLELpp est considérée plus précise que d’autres méthodes traditionnelles pour l’estimation du Koc de composés polaires et de composés ayant des interactions précises avec la matière organique, en raison de la prise en compte de plusieurs types d’interactions moléculaires (avec l’eau et/ou la matière organique) comme contributions aux changements d’énergie libre (Nguyen et coll. 2005). Toutefois, l’approche RLELpp n’est pas idéal pour estimer Koc car il ne tient pas compte des interactions électrostatiques qui existeraient en présence de substances ionisées comme les ANS.
| Propriété | ADNNS (DNNSCa, DNNSBa)a | ADNNDS | Référence(s) |
|---|---|---|---|
| État physique | N. D. | solide | ECHA 2018a |
| Point de fusion (°C) | 153 | 121b | Médiane des modèles (MPBPWIN 2008, TEST 2016); ECHA 2018a |
| Pression de vapeur (Pa) | 1,03 x 10-10 | 2,33 x 10-16 | Médiane des modèles (MPBPWIN 2008) |
| Constante de Henry (Pa·m3/mol) | 2,82 x 10-3 | 1,32 x 10-9 | HENRYWIN 2008 (méthode des liaisons) |
| Solubilité dans l’eau (mg/L) | N.D. (ADNNS) 0,0039 (DNNSCa) 0,011 (DNNSBa) | 2,00 | Rapport interne d’ECCC non publié, Division de la recherche sur les contaminants aquatiques, daté du 26 avril 2019, non référencé |
| Solubilité dans l’eau (mg/L) | 0,23 (ADNNS)b 0,27 (DNNSCa)b 0,21 (DNNSBa)b | 2,00 x 103 b | Lecture croisée à partir de l’ADAN riche en C9, du DANSCa riche en C9 et du DANSBa riche C9 (ECHA 2018b, 2018c, 2018d), ECHA 2018a |
| Solubilité dans l’eau (mg/L) de l’anion, pH 5-9 | 0.003 (ADNNS) N.D. (DNNSCa) N.D. (DNNSBa) | 0,18 | ACD/Percepta c1997-2017 |
| Log Koc (sans dimension) | 5,09 | 4,31 | Abraham et coll. 1994 et ACD/Percepta c1997-2017 |
| Dmax (nm) | N.D. | 19,7 | Simulation tirée de ECHA 2018a |
| pKa1 (sans dimension) | 0,4-0,7 | -2,2-1,1 | ACD/Percepta c1997-2017 |
Abréviations : N.D. = non disponible
a Les valeurs pour le DNNSBa et le DNNSCa sont déduites par lecture croisée de celles de l’ADNNS, à l’exception de la solubilité dans l’eau.
b Les valeurs sont des données empiriques
| Propriété | CDINSA | NSNaa | Références pour le CDINSA et le NSNa |
|---|---|---|---|
| État physique | N.D. | Solide | ECHA 2019a |
| Point de fusion (°C) | 164 | 115,5b | Médiane des modèles (MPBPWIN 2008, TEST 2016) |
| Pression de vapeur (Pa) | 5,07 x 10-7 | 2,51 x 10-5 | Médiane des modèles (MPBPWIN 2008) |
| Constante de Henry (Pa·m3/mol) | 9,42 x 10-5 | NR | HENRYWIN 2008 (méthode des liaisons) |
| Solubilité dans l’eau (mg/L) | 1,98 x 102 | 6,01x104 b | Médiane des modèles (ACD/Percepta c1997-2017, WATERNT 2010, WSKOWWIN 2010, VCCLab 2005); valeur expérimentale (EPI Suite c2000-2012) |
| Log Kow (sans dimension) | 2,92 | 0,85b | Médiane des modèles (ACD/Percepta c1997-2017, p RLELpp, VCCLab 2005, KOWWIN 2010); médiane des valeurs expérimentales (base de données ACD/Percepta) |
| Log Koc (sans dimensions) | 3,28 | NR | Abraham et coll. 1994 et ACD/Percepta c1997-2017 |
| pKa1 (sans dimension) | 0,7 | NR | ACD/Percepta c1997-2017 |
Abréviations : N.D. = non disponible; NR, non requis pour l’évaluation
a Les propriétés physiques et chimiques du NSNa sont déduites par lecture croisée de celles d’analogues afin d’obtenir des données empiriques ou modélisées pour le AN2S.
b Les valeurs sont des données empiriques
4. Sources et utilisations
Les six substances du groupe des ANS sont produites commercialement et ne sont pas présentes naturellement dans l’environnement.
Les six substances ont été visées par des enquêtes menées en vertu de l’article 71 de la LCPE (Canada 2012, Canada 2017). Le tableau 4-1 présente un résumé des renseignements rapportées sur les quantités totales produites et importées pour le groupe des ANS.
| Nom commun | Quantité totale produitea (kg) | Quantité totale importéea (kg) | Année de déclaration | Référence de l’enquête |
|---|---|---|---|---|
| NSNa | 100 000 – 1 000 000 | ND | 2015 | ECCC 2018 |
| ADNNS | ND | 10 000 – 100 000 | 2015 | ECCC 2018 |
| DNNSBa | ND | 37 975 | 2015 | ECCC 2018 |
| DNNSCa | 110 | 10 000 – 100 000 | 2011 | Environnement Canada 2013 |
| ADNNDS | ND | 1000 – 10 000 | 2015 | ECCC 2018 |
| CDINSA | ND | 10 000 – 100 000 | 2011 | Environnement Canada 2013 |
ND – non déclaré avec un seuil de déclaration de 100 kg
a Les valeurs représentent les quantités déclarées en réponse aux enquêtes menées en vertu de l’article 71 de la LCPE (Environnement Canada 2013, ECCC 2018). Consultez les enquêtes pour connaître les détails sur les inclusions et les exclusions (annexes 2 et 3).
Le tableau 4-2 présente un résumé des principales utilisations non confidentielles des substances du groupe des ANS, rapportées lors d’enquêtes menées en vertu de l’article 71 de la LCPE (Environnement Canada 2013, ECCC 2018). Les principales utilisations rapportées pour le NSNa n’ont pas été indiquées dans le tableau 4-2 en raison de revendications de confidentialité.
| Principales utilisationsa | ADNNS | DNNSBa | DNNSCa | ADNNDS | CDINSA |
|---|---|---|---|---|---|
| Carburants et produits connexes, mélanges ou articles manufacturés | O | O | N | N | N |
| Lubrifiants et graisses | N | O | O | N | N |
| Extraction pétrolière et gazière | O | N | N | N | O |
| Peintures et revêtements | O | O | N | O | N |
| Matières en caoutchouc | O | N | N | N | N |
| Traitement de l’eau | O | N | N | N | N |
Abréviations : O = oui, utilisation rapportée pour cette substance; N = non, utilisation non rapportée pour cette substance
a Utilisations non confidentielles rapportées en réponse aux enquêtes menées en vertu de l’article 71 de la LCPE (Environnement Canada 2013, ECCC 2018). Consultez les enquêtes pour connaître les détails sur les inclusions et les exclusions (annexes 2 et 3).
Au Canada, le NSNa est présent en tant que formulant dans des produits de lutte antiparasitaire homologués (communication personnelle, courriel de l’Agence de réglementation de la lutte antiparasitaire (ARLA) de Santé Canada au Bureau de l’évaluation des risques des substances existantes (BERSE) de Santé Canada, janvier 2018, non référencée). L’ADNNS peut être utilisé comme agent antistatique pour la production d’agents de rétention utilisés pour dans la fabrication du papier et du papier cartonné pouvant entrer directement en contact avec des aliments (communication personnelle, courriel de la Direction des aliments de Santé Canada au BERSE de Santé Canada, janvier 2018; non référencé). Le DNNSCa peut servir de lubrifiant pour de l’équipement ou des pièces de machinerie quand le lubrifiant n’entre pas en contact avec des aliments (communication personnelle, courriel de la Direction des aliments de Santé Canada au BERSE de Santé Canada, août 2016, non référencé). Le DNNSCa sert également d’inhibiteur de corrosion dans certains lubrifiants tout usage (FSS 2018).
Aux États-Unis, les principales utilisations des substances du groupe des ANS sont les suivantes : production de substances organiques de base, de produits pétrochimiques, de peintures et revêtements, d’huiles et graisses lubrifiantes à base de pétrole, pour des activités dans des raffineries de pétrole, pour le forage, l’extraction et le soutien du secteur pétrolier et gazier (Chemview c2013- ). Dans l’Union européenne, il est rapporté que l’ADNNDS est utilisé dans des peintures et des revêtements (ECHA 2018a).
5. Rejets dans l’environnement
Les rejets potentiels dans l’environnement des substances de ce groupe peuvent provenir d’installations industrielles qui les utilisent pour le mélange d’huiles lubrifiantes, comme fluides d’usinage, pour la formulation de produits pétroliers et gaziers ou pour la formulation de peintures et revêtements. La plupart de ces utilisations mèneraient à des rejets indirects dans l’environnement par les systèmes de traitement des eaux uséesNote de bas de page 6 (STEU). De plus, des rejets indirects dans les sols peuvent être dus à l’épandage de biosolides provenant des STEU sur les terres.
6. Devenir et comportement dans l’environnement
6.1 Distribution dans l’environnement
En raison des utilisations prévues des substances du groupe des ANS et de leurs propriétés physico-chimiques, ces substances devraient être principalement rejetées par des systèmes de traitement des eaux usées d’installations industrielles.
Les ANS devraient être entièrement ionisés (chargés négativement) dans l’environnement ambiant, tel que mentionné à la section 3. Ainsi, ces substances devraient avoir de faibles pressions de vapeur et se répartir en grande partie dans l’eau plutôt que dans l’air.
Lorsqu’elles sont rejetées dans l’eau, certaines de ces substances, comme le CDINSA et l’ADNNDS, devraient se retrouver dans la colonne d’eau et les sédiments, compte tenu de leurs propriétés physico-chimiques comme leur solubilité dans l’eau faible à élevée. Le CDINSA est très soluble et demeurera probablement en grande partie dans la colonne d’eau. Puisque ces substances ont une charge négative dans les conditions ambiantes, elles auront probablement une adsorption plus faible dans les sols et les sédiments que ce que laisseraient croire leurs log Kco, calculées pour leur forme neutre.
Le CDINSA a une solubilité dans l’eau moyenne et, en tant que tel, devrait se dissoudre dans l’eau. L’ADNNDS, l’ADNNS et les sels métalliques de l’ADNNS ont une faible solubilité dans l’eau et ne devraient donc pas se dissoudre significativement dans le milieu aquatique. Pour cette raison, l’ADNNDS, l’ADNNS et les sels métalliques de l’ADNNS devraient se retrouver en grande partie dans les sédiments lorsqu’ils sont rejetés dans l’eau, et rester liés aux particules de sol lorsqu’ils y sont rejetés (c.-à-d. qu’ils demeureraient dans le sol). La sorption très élevée du DNNSCa et du DNNSBa dans les sédiments a été confirmée par une étude sur la sorption/désorption menée avec un sédiment composite et du sable (rapport interne non publié d’ECCC, Division de la recherche sur les contaminants aquatiques, 26 avril 2019, non référencé). Pendant la phase de désorption de l’expérience, les concentrations aqueuses de DNNSCa et de DNNSBa étaient inférieures à la limite de détection de la méthode. En raison de leur faible solubilité, il a été assumé qu’à des concentrations pertinentes sur le plan environnemental ces ANS se lieront au sable ou aux sédiments, peu importe la teneur en carbone organique ou en argile du matériau adsorbant. En revanche, l’ADNNDS a été détecté dans les sédiments et dans l’eau pendant la phase de désorption de l’expérience. L’ADNNDS ne semblait également pas se sorber sur le sable (rapport interne d’ECCC non publié, Division de la recherche sur les contaminants aquatiques, 26 avril 2019, non référencé).
Compte tenu des utilisations prévues de ces substances, elles ne devraient pas être rejetées dans l’air. Puisqu’elles ont toutes des pressions de vapeur négligeables et des constantes de Henry faibles, la probabilité qu’une volatilisation se produise depuis le sol ou les eaux de surface devrait être faible, indiquant que l’air n’est pas un milieu d’intérêt pour la présente évaluation. Les propriétés physico-chimiques de ces substances, comme une pression de vapeur négligeable, une faible constante de Henry et une mobilité faible à modérée dans les milieux de l’environnement indiquent que ces substances ne seront probablement pas transportées sur de grandes distances.
Compte tenu des renseignements susmentionnés, l’eau, les sédiments et le sol seront les milieux d’intérêt pour la caractérisation des dangers présentés par les substances du groupe des ANS.
6.2 Persistance dans l’environnement
Aucune donnée empirique sur la biodégradation des substances du groupe des ANS n’a été trouvée. Cependant, nous avons trouvé certains renseignements sur la biodégradation d’autres alkylnaphtalènesulfonates. La biodégradation des alkylnaphtalènesulfonates comportant des groupes ramifiés, du propane-2-yl au 3-méthylbutyl, est décrite comme « marginale au mieux » (Swisher 1987). Toutefois, la biodégradation des alkylnaphtalènesulfonates comportant des groupes linéaires était plus rapide, celles avec des chaînes plus longues se dégradant plus rapidement. Au moyen d’une culture d’E. coli, Kölbel (1964) a montré que le composé n-butylique ne se dégradait pas après 30 jours, tandis que le composé n-hexylique se dégradait totalement en 24-30 et le dérivé n‑octylique en 5-15 jours.
Les substances analogues avaient des potentiels de dégradation hautement variables. Lors d’un test de 28 jours réalisé selon la ligne directrice 301 A de l’OCDE (test d’élimination du carbone organique dissous [COD]), l’acide naphtalène-2-sulfonique, un analogue proche du NSNa, a été biodégradé à plus de 90 %. Il a donc été déterminé qu’il était facilement biodégradable (ECHA 2019a). Pour les ANS à chaîne plus longue, l’ADANS riche en C9 a été utilisé en tant qu’analogue. Lors d’un test de dégagement de CO2 de 29 jours réalisé selon la ligne directrice 301 B de l’OCDE, il a été établi qu’il ne se dégrade qu’à 14‑17 % et, donc, qu’il ne se biodégrade pas facilement (ECHA 2018b). De plus, la biodégradation des produits de la réaction de l’ANS avec le 2-méthylpropanol, sels de sodium, a été de 0 % lors d’un test de 28 jours en flacon fermé réalisé en suivant la ligne directrice 301 D de l’OCDE (ECHA 2018e). Toutefois, les auteurs de cette étude ont indiqué que l’absence de biodégradation n’indique pas nécessairement que la substance est de nature persistante, la rigueur des procédures de test en flacon fermé peuvent plutôt possiblement expliquer la persistance (ECHA 2018e).
La biodégradation d’autres surfactants anioniques a été examinée pour mieux définir le potentiel de biodégradation. Dans un extrait sur les surfactants tiré de l’Ullmann’s Encyclopedia of Industrial Chemistry (Kosswig 2012), il est indiqué que les surfactants comportant des groupes hydrophobes dérivés d’hydrocarbures peuvent être oxydés par un procédé enzymatique et être biodégradés dans des conditions aérobies. L’attaque enzymatique qui mène à la biodégradation se produit le plus souvent au niveau du groupe hydrophobe. Il a été montré que les (alkyl linéaire en C10-C13)benzènesulfonates et les (alcane en C14-C17 )sulfonates (des surfactants anioniques comparables) se biodégradent lors de divers tests. Lors d’un test modifié de l’OCDE, ces substances ont exhibé respectivement une biodégradation de 94 % et de 88‑96 % (% COD), et lors de tests en flacon fermé des biodégradations respectives de 55-65 % et 63-95 % (% BOD). Étant donné que certaines substances du groupe des ANS comportent des groupes aliphatiques ramifiés, qui peuvent considérablement ralentir la dégradation (Kosswig 2012), les données sur ces surfactants anioniques ne sont utilisées qu’à titre de renseignements complémentaires. Il n’est pas possible de faire des tests de dégradation anaérobie avec ce groupe de substances, car il n’existe aucune méthode validée pour les tests avec des surfactants (Kosswig 2012).
Des approches de modélisation, dont celles avec les programmes CATALOGIC (2014) et BIOWIN (2010), ont été suivies en tant que source d’élément de preuve additionnel sur la biodégradation. Spécifiquement, les prédictions de demi-vie de biodégradation obtenues avec le programme CATALOGIC (2014) sont de moins de 182 jours pour l’ADNNS, l’ADNNDS et le CDINSA. Toutefois, ces prédictions ont été jugées hors du domaine d’application du programme et n’ont donc été utilisées que dans le cadre d’une approche pondérée de poids de la preuve en conjonction avec les données susmentionnées sur des analogues. Les prédictions obtenues avec le programme BIOWIN 3 (2010) sont en accord, indiquant que la dégradation de ces trois substances prendra de quelques semaines à quelques mois. Pour compenser les données analogues conflictuelles susmentionnées et le fait que la structure des ANS peut varier (c.‑à-d. qu’ils peuvent comporter des groupes alkyles linéaires ou ramifiés), une gamme de demi-vies de biodégradation allant de 92 à 200 jours a été utilisé pour la modélisation de l’exposition dans le sol (section 7.2.8).
D’après les données empiriques sur les analogues des ANS et les (alkyle ramifié)naphthalènesulfonates présentées ci-dessus, il est probable que les ANS persisteront dans l’eau, les sols et les sédiments (p. ex. ils auront des demi-vies supérieures à 182 jours dans l’eau et le sol ou supérieures à 365 jours dans les sédiments).
6.3 Potentiel de bioaccumulation
Le coefficient de partage octanol-eau (log Koe) peut servir à éclairer la bioaccumulation de substances, car c’est un indicateur de la capacité d’une substance de se répartir dans les tissus adipeux. Cependant, les substances de ce groupe étant des surfactants anioniques, elles s’accumulent dans l’interface entre les régions hydrophiles et hydrophobes lors d’un test sur le log Koe. Ce log Koe ne fournit donc pas une mesure précise de leur partage ou leur bioaccumulation.
Les données expérimentales sur le facteur de bioconcentration (FBC) de l’ADNNDS, des données modélisées ainsi que des données sur le FBC d’autres surfactants anioniques, dont l’ALBS, ont été utilisées pour caractériser le potentiel de bioaccumulation des ANS. Les valeurs du FBC de l’ADNNDS suite à des expositions de huit semaines à 0,1 mg/L et 1 mg/L étaient respectivement inférieures à 2,0 L/kg et 0,19 L/kg (tableau 6-1), indiquant un faible potentiel de bioaccumulation.
| Substance | Organisme testé | Concentration expérimentale(durée) | FBC(L/kg) | Référence |
|---|---|---|---|---|
| ADNNDS | Poisson (Cyprinus carpio) | 0,1 mg/L (8 semaines) | < 2,0 | ECHA 2018a |
| ADNNDS | Poisson (C. carpio) | 1 mg/L (8 semaines) | < 0,19 | ECHA 2018a |
Les valeurs du FBC des ANS ont été modélisées au moyen du modèle BIONIC (2016), un modèle conçu pour les substances organiques monoprotiques ionisantes (tableau 6-2). L’ADNNDS étant diprotique, les résultats pour l’ADNNDS ont été exclus. Ces valeurs indiquent que l’ADNNS, le DNNSBa et le DNNSCa se bioaccumuleront dans une grande mesure chez les poissons, tandis que le CDINSA ne semble pas se bioaccumuler.
| Substance | FBC (L/kg) |
|---|---|
| ADNNS | 9954 |
| DNNSBa | 6035 |
| DNNSCa | 6035 |
| CDINSA | 4 |
La bioaccumulation d’autres surfactants anioniques a été examinée. Les descriptions générales des mécanismes d’accumulation des surfactants sont mentionnées dans EOSCA (2000). Par exemple, il a été montré que l’absorption à partir de la colonne d’eau est le mécanisme d’accumulation le plus important pour les composés organiques hydrophobes (Bartell et coll. 1998). Un rapport d’évaluation initiale sur les alkylsulfates, les alcanesulfonates et les (alc‑1‑ène)sulfonates (OCDE 2007) indique que les données expérimentales (non fournies) donnaient des FBC ≤ 73 L/kg, pour des chaînes de carbone ayant jusqu’à 16 atomes de carbone. Il a été déterminé qu’« aucune bioaccumulation significative » ne devrait avoir lieu. Les FBC expérimentaux pour les (alkyle linéaire en C10 ou C11)benzènesulfonates (ALBS), couramment utilisés comme surfactants anioniques représentatifs, chez Pimephales promelas allaient de 1,7 à 6,1 L/kg, indiquant également un faible potentiel de bioaccumulation de ces substances (Tolls et coll. 1997).
En résumé, d’après les données modélisées, l’ADNNS, le DNNSBa, le DNNSCa et le CDINSA semblent pouvoir être bioaccumulés, alors que d’après les données expérimentales l’ADNNDS ne semble pas l’être.
7. Potentiel d’effets nocifs sur l’environnement
7.1 Évaluation des effets sur l’environnement
Il existe peu de données expérimentales sur la toxicité des substances évaluées, pour tous les milieux. C’est pourquoi l’évaluation de ces effets repose en grande partie sur des données d’analogues.
7.1.1 Mode/mécanisme d’action
Aucune information sur le mode d’action des ANS n’a été trouvée dans la littérature. Trois profileurs ont été utilisés pour établir le mode d’action (MdA) de ces substances, tels qu’ils figurent dans la Classification du risque écologique des substances organiques (CRE) (ECCC 2016a). Le profileur ASTER s’est avéré le plus fiable, indiquant la narcose de référence comme mode d’action de l’ADNNS, de l’ADNNDS et du CDINSA. En conséquence, il a été déterminé que les substances du groupe des ANS n’ont pas de mode d’action spécifique. Cela a éclairé le choix de facteurs d’évaluation appropriés.
7.1.2 Effets sur les espèces aquatiques
Des données empiriques sur l’ADNNDS dans le milieu aquatique sont disponibles dans un dossier REACH (ECHA 2018a). Des données pertinentes sur des analogues sont également disponibles dans le dossier REACH de l’ADANS riche en C9 (ECHA 2018b). La fiabilité des études avec des poissons, des invertébrés et des algues a été évaluée. D’après les données empiriques et les données sur un analogue, les algues sont l’espèce aquatique la plus sensible à l’ADNNDS et à la substance analogue. Les études clés sur la toxicité aquatique des substances du groupe des ANS et d’un analogue proche sont résumées dans le tableau 7-3.
Les données sur l’ADNNDS pour les invertébrés ont été obtenues de son dossier REACH (ECHA 2018a). Lors d’une étude menée en suivant la ligne directrice 202 de l’OCDE (test d’immobilisation aiguë sur Daphnia sp.) et la méthode C.2 de l’UE (toxicité aiguë chez Daphnia), des jeunes Daphnia magna ont été exposés à 5 concentrations d’ADNNDS. Les concentrations n’ont été rapportées qu’en tant que concentrations nominales. Cependant, les concentrations mesurées auraient été égales à 97 à 112 % des valeurs nominales. Le paramètre toxicologique utilisé dans cette étude était une CE50 nominale à 48 h de 87 mg/L.
Les données du dossier REACH (ECHA 2018a) sur la toxicité de l’ADNNDS pour les algues étaient obtenues à partir de l’ADANS riche en C9 (ECHA 2018b), sachant que la substance analogue est beaucoup moins soluble que l’ADNNDS. Lors de deux études menées en suivant la ligne directrice 201 de l’OCDE (algue, test d’inhibition de la croissance), Pseudokirchneriella subcapitata a été exposée à sept concentrations d’ADANS riche en C9, substance achetée en tant qu’UVCB à 100 %. En raison de la faible solubilité de l’ADANS riche en C9, des fractions adaptées à l’eau (FAE) ont été utilisées pour des tests, et des vitesses d’absorption nominales ont été rapportées ainsi que des concentrations mesurées. Les concentrations mesurées ont diminué de manière significative (de 17 à 76 %) après 72 heures en raison de l’adhérence à la verrerie. Bien que plusieurs paramètres toxicologiques aient été rapportés (CE50, CSEO, CE10), seules les valeurs de CE10 ont été prises en compte dans le choix de la valeur critique de toxicité, car les auteurs de l’étude les considèrent les plus précises pour déterminer le profil dose-réponse du test.
Des données sur la toxicité des acides naphtalènesulfoniques (no CAS 68153-01-5) pour les poissons, les algues et les invertébrés ont été rapportées, ainsi que des données supplémentaires sur la toxicité des n(butyl ramifié ou linéaire)naphtalène-msulfonates de msodium (no CAS 91078-64-7) (Greim et al. 1994). Aucun renseignement de base n’a été fourni sur les méthodes de test, les résultats ayant été soumis par un laboratoire externe. Toutefois, le document a été revu par des pairs et ces données ont été jugées acceptables en tant que telles pour une utilisation dans une approche basée sur le poids de la preuve en conjonction avec d’autres données expérimentales et sur des analogues. Les données supplémentaires sur la toxicité aquatique des substances analogues sont présentées dans le tableau A-1 de l’annexe A.
Deux espèces, l’amphipode Hyalella azteca et l’escargot Planorbella pilsbryi, ont été exposées au DNNSBa, au DNNSCa et à l’ADNNS pendant 96 heures. Seules des concentrations nominales en pourcentage de la solution saturée en ANS ont été rapportées. Le DNNSACa s’est révélé le plus nocif pour les deux espèces, suivi de l’ADNNS et du DNNSBa. Les trois solutions d’ANS se sont révélées plus nocives pour le H. azteca que pour le P. pilsbryi (rapport interne non publié d’ECCC, Division de la recherche sur les contaminants aquatiques, 26 avril 2019; non référencé). Comme aucun paramètre conventionnel n’a été rapporté, ces espèces n’ont pas été incluses dans l’approche factorielle d’évaluation pour le calcul d’une concentration estimée sans effet (CESE).
Le rapport susmentionné comprend une étude de 21 jours sur l’exposition des embryons et des larves de tête-de-boule (P. promelas). Des embryons de tête‑de-boule nouvellement fécondés ont été mis en suspension dans une tasse dans l’eau au-dessus de sédiments contenant des ANS à des concentrations nominales d’ADNNDS et de DNNSCa allant jusqu’à 2000 mg/kg. L’exposition au DNNSCa a provoqué une légère diminution du nombre d’œufs éclos, mise en évidence par un taux de 98 % observé dans le groupe témoin contre 81 % dans le groupe le plus exposé. Aucun effet n’a été observé suite à l’exposition à l’ADNNDS (rapport interne non publié d’ECCC, Division de la recherche sur les contaminants aquatiques, 26 avril 2019). Lors d’une autre étude, des embryons de grenouilles (Silurana tropicalis) ont été exposés à de l’eau recouvrant du sable additionné de 75 mg/kg de DNNSCa, de 8 heures après la fécondation jusqu’au pic de leur métamorphose. À partir de la douzième semaine environ, des retards de développement importants ont été observés dans le groupe exposé par rapport au groupe témoin. Par ailleurs, une diminution de la taille corporelle a été rapportée, le poids corporel total moyen des grenouilles ayant atteint le pic de métamorphose à 0,75 g dans le groupe de contrôle et à 0,60 g dans le groupe exposé au DNNSCa (rapport interne non publié d’ECCC, Division de la recherche sur les contaminants aquatiques, 26 avril 2019; non référencé)(Matten et al. 2018).
La valeur critique de toxicité (VCT) de l’ADANS riche en C9 retenue pour l’inhibition du rendement de l’espèce algale P. subcapitata était une CE10 à 72 h de 0,16 mg/L, tel que rapporté dans son dossier REACH (ECHA 2018 b).
Pour calculer la CESE, la VCT a été divisée par un facteur d’évaluation (FE), qui tient compte de diverses extrapolations et sources d’incertitude. Un facteur de normalisation des paramètres (FNP) est pris en compte pour l’extrapolation d’un cadre temporel à court terme (aigu) à un cadre temporel à long terme (chronique), ainsi que d’effets létaux (c.-à-d. la mortalité) à des effets sublétaux (p. ex. croissance, reproduction), et de niveaux d’effet médians (p. ex. CE50) à des niveaux d’effet faible (p. ex. CE10). Le FA tient également compte du nombre d’espèces et de catégories d’espèces représentées dans l’ensemble des données de toxicité (facteur de variation des espèces, FVE), et du mode d’action plus toxique de la substance par rapport à la narcose de référence (facteur de mode d’action, FMdA). Le facteur d’évaluation (FA) final est obtenu en multipliant le FNP, le FVE et le FMdA.
Comme la VCT est calculée pour une étude chronique basée sur un paramètre sublétal à effets faibles, le FNP est égal à 1. Le mode d’action des ANS est celui d’une narcose non polaire (de référence) (section 7.1.1). Par conséquent, le FMdA est aussi égal à 1. L’ensemble de données de toxicité aquatique combinées de l’ADNNDS et la substance analogue, l’ADANS riche en C9, comprend trois espèces de trois catégories (plantes, invertébrés et vertébrés). Par conséquence, une valeur de VNP de 5 a été utilisée. Le FE total de 5 (FNP × FVE × FMdA = 1 × 5 × 1) a été appliqué à la VCT, donnant une CESE aquatique de 32 µg/L.
| Nom commun de la substance | Organisme testé | Paramètre | Valeur (mg/L) | Référence |
|---|---|---|---|---|
| ADNNDS | Invertébré (D. magna) | CE50 à 48 h | 87 | ECHA 2018a |
| ADANS riche en C9 | Poisson (C. carpio) | CL50 à 96 h | > 0,28 | ECHA 2018b |
| ADANS riche en C9 | Invertébré (D. magna) | CE50 à 48 h | > 0,27 | ECHA 2018b |
| ADANS riche en C9 | Algue (P. subcapitata) | CE50 à 72 h (vitesse de croissance) | > 9,60 | ECHA 2018b |
| ADANS riche en C9 | Algue (P. subcapitata) | CE50 à 72 h(rendement) | 2,4 | ECHA 2018b |
| ADANS riche en C9 | Algue (P. subcapitata) | CE10 à 72 h (vitesse de croissance) | 0,8 | ECHA 2018b |
| ADANS riche en C9 | Algue (P. subcapitata) | CE10 à 72 h (vitesse de croissance) | 0,7 | ECHA 2018b |
| ADANS riche en C9 | Algue (P. subcapitata) | CE10 à 72 h(rendement) | 0,2 | ECHA 2018b |
| ADANS riche en C9A | Algue (P. subcapitata) | CE10 à 72 h(rendement) | 0,16 | ECHA 2018b |
7.1.3 Effets sur les organismes vivant dans les sédiments
Les effets de l’ADNNDS, du DNNSCa et du DNNSBa sur deux espèces d’invertébrés (H. azteca et Tubifex tubifex) ont été étudiés au moyen de tests d’exposition chronique au substrat, en suivant la méthode standard E1706-05 de l’ASTM (2010). Pour les tests avec T. tubifex, les concentrations nominales utilisées étaient comprises entre 200 et 10 000 mg d’ANS par kg en poids sec de sédiment, tandis que pour les tests avec H. azteca, les concentrations utilisées étaient comprises entre 100 et 2000 mg d’ANS par kg en poids sec de sédiment. Les organismes testés ont été exposés pendant 28 jours (rapport interne non publié d’ECCC, Division de la recherche sur les contaminants aquatiques, 26 avril 2019, non référencé; Matten et al. 2018). Les concentrations nominales avec effet pour les deux espèces sont résumées dans le tableau 7-2.
La VCT retenue pour les sédiments est une CE50 à 28 jours de 205 mg/kg pour la production de jeunes T. tubifex. Pour la convertir en une CESE, la VCT a été multipliée par un facteur d’évaluation global de 100. Ce facteur comprend un FNP de 5 pour tenir compte de l’extrapolation de niveaux d’effet médian (c’est-à-dire CE50) à des niveaux d’effet faible, d’un facteur de mode d’action de 1 (pour la narcose non polaire) et d’un FVE de 20, car une seule catégorie d’organismes est représentée, à savoir les invertébrés. Le résultat est une CESE de 2,05 mg/kg pour les sédiments.
| Nom commun de la substance | Organisme testé | Paramètre | Valeur (mg/kg poids sec) |
|---|---|---|---|
| DNNSBa | Amphipode (H. azteca) | CL50 sur 28 j | 832 |
| DNNSBa | Amphipode (H. azteca) | CE50 sur 28 j (croissance) | 709 |
| DNNSBa | Amphipode (H. azteca) | CE50 sur 28 j (biomasse) | 699 |
| DNNSBa | Ver à boue (T. tubifex) | CL50 sur 28 j | 1598 |
| DNNSBa | Ver à boue (T. tubifex) | CE50 sur 28 j (production de cocons) | 803 |
| DNNSBa | Ver à boue (T. tubifex) | CE50 sur 28 j (production de jeunes) | 398 |
| DNNSCa | Amphipode (H. azteca) | CL50 sur 28 j | 648 |
| DNNSCa | Amphipode (H. azteca) | CE50 sur 28 j (croissance) | 424 |
| DNNSCa | Amphipode (H. azteca) | CE50 sur 28 j (biomass) | 373 |
| DNNSCa | Ver à boue (T. tubifex) | CL50 sur 28 j | 1279 |
| DNNSCa | Ver à boue (T. tubifex) | CE50 sur 28 j (production de cocons) | 419 |
| DNNSCa | Ver à boue (T. tubifex) | CE50 sur 28 j (production de jeunes) | 205 |
| DNNDSA | Ver à boue (T. tubifex) | CE50 sur 28 j (production de cocons) | 3412 |
| DNNDSA | Ver à boue (T. tubifex) | CE50 sur 28 j (production de jeunes) | 2336 |
| DNNDSA | Ver à boue (T. tubifex) | CL50 sur 28 j | > 10 000 |
a Références : rapport interne non publié d’ECCC, Division de la recherche sur les contaminants aquatiques, 26 avril 2019; non référencé ; Matten et al. 2019
7.1.4 Effets sur les organismes vivant dans le sol
Les données sur la toxicité des ANS dans les sols étaient très limitées. Il existait des données tirées d’une étude sur les vers de terre réalisée avec la substance analogue méthyl(di(propane-2-yl))naphtalènesulfonates de sodium (no CAS 68909-82-0) (ECHA 2019b). En suivant la ligne directrice de l’OCDE sur la reproduction des vers de terre, des vers de terre (Eisenia fetida) adultes ont été exposés à la substance testée à des concentrations nominales allant de 15,63 à 500 mg/kg poids sec de sol artificiel, pendant 8 semaines. Les résultats clés (nominaux) de cette étude sont résumés dans le tableau 7 3. Aucune différence statistiquement significative n’a été constatée pour la reproduction ni pour le gain de poids corporel à des concentrations allant jusqu’à 250 mg/kg de poids sec. Cependant, à 500 mg/kg de poids sec, la reproduction (mesurée à 8 semaines) et le gain de poids corporel (mesuré à 28 jours) ont baissé de manière significative. Aucun symptôme pathologique ni aucun changement de comportement n’a été observé pendant la période du test.
La VCT retenue pour le sol pour la reproduction des vers de terre était la CSEO à 8 semaines de 250 mg/kg poids sec (tableau 7-3). Pour la convertir en CESE, elle a été multipliée par un facteur d’évaluation global de 50 a, qui comprenait un FNP de 1, car aucune extrapolation n’était nécessaire pour normaliser ce paramètre vu qu’il s’agit d’une CSEO chronique, par un facteur pour le mode d’action de 1 (pour la narcose non polaire) et par un FVE de 50, car les données n’étaient disponibles que pour une catégorie d’organismes et une espèce. La valeur de la CESE est donc de 5 mg/kg.
| Paramètre | Valeur (mg/kg poids sec) |
|---|---|
| CE50 è 8 semaines (reproduction) | 398 |
| CSEO à 8 semaines (reproduction) | 250 |
| CMEO à 8 semaines (reproduction) | 500a |
| CSEO à 8 semaines (mortalité) | 500 |
Abréviations : CSEO : concentration sans effet observé; CMEO : concentration minimale avec effet observé; CEx : Concentration causant un effet chez x % de la population
a valeur sans limite
7.2 Évaluation de l’exposition de l’environnement
Les substances du groupe des ANS pourraient être utilisées de manière interchangeable pour des applications industrielles. Par conséquent, dans le cadre de la présente évaluation, les scénarios d’exposition de l’environnement tiennent compte de l’ADNNS, du DNNSBa, du DNNSCa, de l’ADNNDS et de l’ACDINS collectivement, en assumant qu’une des substances pourrait être substituée par une autre pour une application donnée et que, par conséquent, le total de l’ADNNS, du DNNSBa, du DNNSCa, de l’ADNNDS et de l’ACDINS rapportés par les entreprises individuelles est pris en compte. Les scénarios d’exposition sont basés sur des renseignements soumis pour ces substances en réponse à des enquêtes menées en vertu de l’article 71 de la LCPE (Environnement Canada 2013, ECCC 2018). Les scénarios d’exposition utilisés pour la présente évaluation incluent les rejets aquatiques dus au mélange d’huiles lubrifiantes, à l’utilisation de fluides d’usinage, à la formulation de peintures et revêtements, à la formulation de produits pétroliers et gaziers et à l’utilisation industrielle de peintures. L’exposition dans les sols due à l’épandage de biosolides sur des terres et l’exposition dans des sédiments en équilibre avec la colonne d’eau sont estimées en tant qu’extension de scénarios aquatiques. Chacun de ces scénarios est décrit plus en détail ci-après.
Aucun scénario d’exposition n’a été établi pour l’utilisation des ANS dans des lubrifiants et graisses. Il a été déterminé que leur utilisation comme lubrifiants entraînerait une exposition de l’environnement minimale ou nulle, ces produits étant généralement recyclés ou éliminés dans des installations de traitement des déchets conformes aux programmes provinciaux/territoriaux. Ainsi, ils ne devraient donc pas être rejetés dans l’environnement.
Aucun scénario d’exposition n’a pas non plus été étudié pour l’utilisation des ANS dans des produits d’extraction du pétrole et du gaz naturel, car lors des applications sur les champs pétrolifères, les eaux de traitement et les déchets ne sont généralement pas rejetés dans un égout ni dans le milieu aquatique. L’injection pour la stimulation des puits et l’injection en profondeur de l’eau de traitement sont les méthodes d’élimination les plus courantes en Amérique du Nord (OCDE 2012).
7.2.1 Concentrations mesurées dans les milieux de l’environnement et les eaux usées
Les seules données trouvées sur les concentrations environnementales mesurées des ANS au Canada étaient des concentrations dans les effluents de quatre systèmes de traitement des eaux usées domestiques (STEU). L’ADNNDS, le DNNSBa et le DNNSCa n’ont pas été détectés (limites de détection de la méthode de 0,46 à 3,6 µg/L) dans les effluents de ces quatre installations, qui appliquaient soit un traitement primaire, soit un traitement en lagune (communication personnelle, courriel de la Section de recherche et de surveillance du PGPC à la Division de l’évaluation environnementale d’ECCC, 15 juillet 2019, non référencé). Certaines installations de travail des métaux et de formulation de produits pétroliers et gaziers rejettent leurs effluents dans ces quatre STEU. Toutefois, on ignore si elles utilisent des ANS ou, dans un tel cas, si elles ont effectivement rejeté des ANS pendant les périodes d’échantillonnage des STEU.
7.2.2 Calcul des CEE et hypothèses générales
Les expositions environnementales sont estimées et présentées sous forme de concentrations environnementales estimées (CEE). Les CEE aquatiques ont été calculées à l’aide de l’équation suivante :
avec,
CEE = concentration environnementale estimée (μg/L)
Q = quantité utilisée par site et par an (kg/an)
L = pertes dans les eaux usées (fraction)
E = efficacité d’élimination des STEU (fraction)
D = volume de dilution quotidien (L/jour)
N = nombre de jours de rejet
109 = facteur de conversion de kg à μg (μg/kg)
Il existe des différences dans les propriétés physiques/chimiques des ANS, qui affectent la façon dont ils se répartissent dans l’environnement. Par exemple, la solubilité varie de plusieurs ordres de grandeur et le potentiel de sorption varie également de manière significative parmi les substances du groupe des ANS. Ces propriétés ont été prises en compte pour le calcul des CEE. En raison du manque de données sur les ANS, l’efficacité d’élimination des STEU a été estimée à partir des données pour un groupe de substances analogues. Le taux d’élimination moyen des (alkyl linéaire)benzènesulfonates (ALBS) par les différents systèmes est d’environ 90 % (OCDE 2005). Comme il existe des différences entre le potentiel de dégradation des ALBS et celui des ANS (section 5.2), le taux d’élimination des ANS plus solubles qui se lient moins fortement aux solides (par exemple, l’ACDINS et l’ADNNDS) a été assumé être la moitié de celui des ALBS. Par conséquent, le taux d’élimination de ces substances est estimé à 45 %. Dans le cas des ANS ayant une forte affinité avec les solides, le taux d’élimination par les STEU a été assumé à 99 %. Par conséquent, les estimations d’exposition ont été faites en utilisant les taux d’élimination les plus bas (45 %) et les plus élevés (99 %) pour obtenir une gamme de CEE potentielles. Les volumes de dilution quotidiens sont calculés en multipliant le débit d’effluent des STEU ou des installations déversant leur rejet dans un plan d’eau par le facteur de dilution du plan d’eau récepteur. Dans tous les cas, les CEE aquatiques ont été calculées en utilisant un facteur de dilution basé sur le 10e percentile du débit faible du plan d’eau récepteur et plafonné à un facteur de dilution maximum de 10 %.
Les CEE aquatiques représentent les concentrations potentielles de substances présentes dans le plan d’eau récepteur à proximité du point de rejet d’un STEU. Les valeurs de CEE obtenues pour chaque scénario d’exposition et un résumé des hypothèses clés sont donnés dans l’annexe B. Les rejets potentiels dus au nettoyage et au transport des conteneurs, y compris lors du chargement et du déchargement, ne sont pas pris en compte dans la présente évaluation.
7.2.3 Scénario d’exposition 1 : mélange d’huiles lubrifiantes
D’après les renseignements soumis pour ces substances en réponse à des enquêtes menées en vertu de l’article 71 de la LCPE (Environnement Canada 2013, ECCC 2018), l’une des principales utilisations des ANS est comme additif dans des lubrifiants. Par conséquent, un scénario a été élaboré pour refléter les rejets potentiels des ANS par les installations de mélange d’huiles lubrifiantes au Canada dans les systèmes de traitement des eaux usées, puis dans les plans d’eau. Plus de 10 entreprises au Canada produisent et/ou mélangent des lubrifiants. Elles sont situées dans différentes régions du pays.
La CEE aquatique a été calculée pour une installation de mélange générique représentative en se basant sur des données compilées provenant de différentes sources. Le scénario est basé sur les quantités importées par un certain nombre d’entreprises, dont la valeur moyenne a été utilisée comme valeur représentative. Il est assumé que l’effluent de l’installation représentative serait rejeter après passage dans une STEU secondaire, tertiaire ou lagunaire hors site. Le volume de dilution quotidien retenu est représentatif du secteur des mélanges d’huiles lubrifiantes. Voir le tableau B-1 de l’annexe B pour un résumé des hypothèses.
Les CEE aquatiques génériques calculées se situent dans une gamme de 0,05 à 2,87 µg/L.
7.2.4 Scénario d’exposition 2 : utilisation de fluides d’usinage
D’après les renseignements soumis pour ces substances en réponse à des enquêtes menées en vertu de l’article 71 de la LCPE (Environnement Canada 2013, ECCC 2018), les ANS sont utilisés comme agent anticorrosion ou antitartre dans des fluides d’usinage utilisés pour le revêtement de pièces métalliques. Un scénario a donc été élaboré pour refléter les éventuels rejets des ANS dans les systèmes de traitement des eaux usées par les installations de revêtement de pièces métalliques qui utilisent des fluides d’usinage.
L’utilisation dans les fluides métallurgiques peut avoir lieu dans plusieurs installations à travers le Canada, de taille et de lieu d’exploitation différents. On ne dispose pas de renseignements spécifiques sur les utilisateurs de fluides d’usinage contenant des ANS. Le présent scénario est basé sur une situation générique dans laquelle une installation industrielle utilise des fluides d’usinage (contenant des ANS) tout au long de l’année.
Les paramètres tels que la capacité de production, le facteur d’émission et le nombre de jours de rejet ont été basés sur des données tirées du document de l’OCDE sur les scénarios d’émission portant sur l’utilisation des fluides d’usinage. Le volume de dilution quotidien retenu est la valeur du 10e percentile de la distribution du volume de dilution quotidien correspondant à une variété d’usines exerçant des activités qui font appel à l’utilisation de tels fluides. Il est assumé que les installations exerçant de telles activités ont un certain système de traitement de leurs eaux usées sur place, sous forme de séparateur huile/eau par exemple, avant de les rejeter dans le réseau d’égouts pour un traitement ultérieur dans une STEU. Le tableau B-2 de l’annexe B contient un résumé des hypothèses faites pour calculer les CEE.
Les CEE aquatiques obtenues pour un tel scénario vont de 0,06 à 3,38 µg/L.
7.2.5 Scénario d’exposition 3 : formulation de peintures et revêtements
D’après les renseignements soumis lors d’enquêtes menées en vertu de l’article 71 de la LCPE (Environnement Canada 2013, ECCC 2018), ces substances sont utilisées comme régulateurs de procédé ainsi que comme agents oxydants et réducteurs pour la formulation industrielle des peintures et revêtements. Ce scénario est basé sur l’utilisation des ANS pour la formulation des peintures et revêtements. Les rejets par ces installations devraient entrer dans les systèmes de traitement des eaux usées avant d’être rejetés dans l’environnement.
Le scénario est basé sur la plus importante quantité importée de NSA déclarée par une installation de formulation de ce secteur. Le volume de dilution quotidien retenu correspond à la valeur du 10e percentile d’une distribution du volume de dilution quotidien calculée pour le secteur des peintures et revêtements. Un résumé des hypothèses clés faites pour ce scénario est donné dans le tableau B-3 de l’annexe B.
Les CEE aquatiques calculées pour ce scénario vont de 0,05 à 2,64 µg/L.
7.2.6 Scénario d’exposition 4 : formulation de produits pétroliers et gaziers
D’après les renseignements soumis lors d’enquêtes menées en vertu de l’article 71 de la LCPE (Environnement Canada 2013, ECCC 2018), des ANS sont utilisés comme auxiliaire de traitement dans des produits utilisés pour l’extraction du pétrole et du gaz naturel. Ce scénario a donc porté sur le rejet des ANS dans les systèmes de traitement des eaux usées provenant de la formulation de produits utilisés pour l’extraction du pétrole et du gaz.
Les CEE ont été évaluées pour un scénario générique d’une installation de fabrication de produits pour l’extraction du pétrole et du gaz qui rejette ces produits dans une installation de traitement secondaire ou tertiaire des eaux usées. Le volume de dilution quotidien retenu correspond à la valeur du 10e percentile d’une distribution des volumes de dilution quotidiens de différentes installations industrielles. Consultez le tableau B-4 de l’annexe B pour un résumé des hypothèses faites pour calculer la CEE.
Les CEE obtenues pour ce scénario vont de 0,07 à 3,83 µg/L.
7.2.7 Scénario d’exposition 5 : utilisation industrielle de peintures
D’après les soumissions faites en vertu de l’article 71 de la LCPE et les renseignements communiqués par l’Association canadienne des constructeurs de véhicules (ACCV) (communication personnelle, courriel de l’ACCV à la Division des produits d’ECCC, 2 août 2019, non référencé), des ANS sont utilisés industriellement dans des peintures, y compris par le secteur automobile. Un scénario a donc été élaboré pour refléter les éventuels rejets des ANS dans les systèmes de traitement des eaux usées par les installations qui utilisent des peintures pour la fabrication d’équipements d’origine pour automobile (EOA).
La peinture des EOA est automatisée et les pertes de peinture à la pulvérisation sont collectées dans des cabines à aspiration par le sol ou à aspiration par les côtés dans lesquelles l’eau est utilisée presque exclusivement pour collecter les pertes (EPA 1996). Le scénario générique de l’EPA pour le revêtement par pulvérisation des pièces automobiles (EPA 1996) a été adapté pour calculer la CEE pour un site d’activités de peinture, en utilisant l’équation suivante:
avec,
Q = quantité utilisée (kg/an)
ET = efficacité moyenne de transfert dans les procédés de pulvérisation (fraction)
E = efficacité d’élimination du système de traitement des eaux usées (STEU) (fraction)
D = volume de dilution quotidien (L/jour)
N = nombre de jours de rejet (jour/année)
La CEE aquatique a été calculée à partir de données compilées provenant de différentes sources. Les paramètres tels que le nombre de jours de rejet ont été basés sur les données du scénario générique de l’EPA pour le revêtement par pulvérisation des automobiles (EPA 1996), tandis que l’efficacité du transfert a été basée sur le document de l’OCDE décrivant le scénario d’émission de l’industrie du revêtement (OCDE 2009). Les paramètres tels que les méthodes de déchargement, les systèmes de traitement sur site et hors site, et le débit des eaux usées ont été basés sur des renseignements représentant les installations de fabrication automobile pertinentes du Canada. La quantité utilisée correspond à la limite supérieure de la gamme des valeurs importées déclarées (ECCC 2018). Consultez le tableau B-5 de l’annexe pour un résumé des hypothèses faites pour calculer les CEE.
Les CEE aquatiques ainsi obtenues vont de 0,19 à 10,54 µg/L.
7.2.8 Exposition dans les sédiments
Une approche de partage à l’équilibre sédiments-eau a été utilisée pour estimer la CEE des ANS dans les sédiments de fond. Cette approche est basée sur le guide de l’Agence européenne des produits chimiques pour l’estimation de l’exposition environnementale dans des sédiments en suspension (ECHA 2012) et sur une approche de partage à l’équilibre pour les sédiments de fond décrite par le National Center for Environmental Assessment de l’EPA (EPA 2003). À l’équilibre, la CEE dans les sédiments de fond est en corrélation linéaire avec la concentration dans la phase aqueuse de l’eau sus-jacente. Les caractéristiques typiques des sédiments en suspension et des sédiments de fond suggérées par Gobas (2007 et 2010) ont été utilisées pour l’estimation. La CEE dans les sédiments de fond (en mg/kg) est typiquement calculée au moyen de l’équation suivante :
Avec,
Ctotal = concentration totale dans la colonne d’eau (mg/L)
KCO = coefficient de partage carbone organique-eau pour les sédiments en suspension ou de fond (L/kg CO)
Des gammes de CEE dans les sédiments de fond, normalisées à 3 % de carbone organique (une teneur typique en carbone organique dans les sédiments de fond des rivières et des lacs du Canada), ont été calculées pour les scénarios 1 à 5 susmentionnés. Une valeur de log KCO de 3,28 a été utilisée comme valeur représentative pour les ANS plus solubles, comme l’ACDINS, tandis qu’une valeur de log KCO de 5,09 a été utilisée pour les ANS moins solubles, comme l’ADNNS. Les valeurs de KCO ont été jumelées pour les calculs avec un taux d’élimination approprié (par exemple, l’élimination la plus élevée était associée à un KCO élevé, et l’élimination la plus faible à un KCO peu élevé). Ces valeurs sont très prudentes, car elles représentent les formes neutres de ces substances. Les valeurs réelles de KCO devraient être beaucoup plus faibles. Les CEE des sédiments sont fournies dans le tableau 7-4. Un résumé d’autres hypothèses faites est fourni dans les tableaux B-6 à B-10 de l’annexe B. Il est à noter que la concentration totale dans la colonne d’eau a été calculée en utilisant les débits du 50e percentile plutôt que ceux du 10e. Cela a été fait afin de refléter une période d’exposition plus proche de la moyenne nécessaire dans les plans d’eau récepteurs pour atteindre l’équilibre dans les sédiments.
| Scénario | CEE (mg/kg) |
|---|---|
| 1- Mélange d’huiles lubrifiantes | 0,06 - 0,09 |
| 2- Utilisation de fluides d’usinage | 0,08 - 0,13 |
| 3- Formulation de peintures et revêtements | 0,09 - 0,15 |
| 4- Formulation de produits pétroliers et gaziers | 0,11 - 0,17 |
| 5- Utilisation industrielle de peintures | 0,38 - 0,59 |
7.2.9 Épandage de biosolides sur des terres
Ce scénario portait sur l’épandage des ANS sur des terres sous forme de biosolides provenant de systèmes de traitement des eaux usées. Une gamme de CEE pour le sol a été calculée pour les scénarios 1 à 5 susmentionnés et comme extension de ces scénarios aquatiques.
La CEE pour le sol après 10 ans d’épandage de biosolides et en tenant compte de la biodégradation comme mécanisme de perte est calculée par itération des équations ci-dessous. Les concentrations ont été déterminées sur une base annuelle immédiatement après l’épandage et à la fin de l’année (après que la dégradation se soit produite, mais avant l’épandage subséquent) pour une période de 10 ans.
Au début de l’année (immédiatement après l’épandage) :
(notez que )
A la fin de l’année (après dégradation):
Où,
CEEdébut = concentration environnementale estimée dans le sol au début de l’année suivant l’épandage de biosolides (avant dégradation) (mg/kg)
CEEfin = Concentration environnementale estimée dans le sol à la fin de l’année (après dégradation), avant l’épandage ultérieur de biosolides (mg/kg)
t = numéro de l’année d’épandage des biosolides (y), de 1 à 10
Cs = Concentration de la substance dans les biosolides (mg/kg poids sec)
V = vitesse d’épandage annuel de biosolides sur les sols (kg/m2.an)
p = profondeur de mélange du sol (m)
ρ = masse volumique du sol sec (kg/m3)
Une demi-vie de 92 à 200 jours a été estimée pour les ANS. La concentration des ANS dans le sol n’augmente pas fortement au cours de la période de 10 ans et les concentrations dans le sol sont maximales juste après l’épandage (diminuant ensuite de manière significative au cours de l’année). Les CEE calculées au début de la 10ème année pour chaque scénario sont données dans le tableau 7-5. Un résumé des hypothèses faites est fourni dans les tableaux B‑11 à B-16 de l’annexe B.
| Scénario | CEE (mg/kg) |
|---|---|
| 1- Mélange d’huiles lubrifiantes | 0,11 – 0,33 |
| 2- Utilisation de fluides d’usinage | 0,66 – 1,91 |
| 3- Formulation de peintures et revêtements | 0,63 – 1,81 |
| 4- Formulation de produits pétroliers et gaziers | 0,18 – 0,53 |
| 5- Utilisation industrielle de peintures | 0,18 – 0,51 |
7.3 Caractérisation des risques pour l’environnement
L’approche adoptée pour la présente évaluation ayant trait à l’environnement consistait à examiner les renseignements pour l’évaluation et à tirer des conclusions basées sur le poids de la preuve et le principe de précaution. Des éléments de preuve ont été rassemblés pour déterminer le potentiel de risques pour l’environnement au Canada dû aux substances du groupe des ANS. Les éléments de preuve pris en compte comprennent ceux évalués pour la présente évaluation qui étayent la caractérisation des risques pour l’environnement au Canada. Des éléments de preuve secondaires ou indirects ont également été pris en compte, y compris des décisions réglementaires et la classification du danger ou les caractéristiques du devenir déterminées par d’autres organismes de réglementation.
7.3.1 Classification du risque écologique (CRE) des substances organiques
La Classification du risque écologique (CRE) des substances organiques a permis de déterminer que le NSNa présente un faible potentiel d’effets nocifs sur l’environnement (ECCC 2016a). La CRE est une approche basée sur les risques qui tient compte de plusieurs paramètres liés au danger et à l’exposition et d’une pondération des différents éléments de preuve pour déterminer la classification du risque. Cette approche est résumée dans l’annexe C. Des données critiques et des facteurs ayant servi à développer le profil spécifique au NSNa sont présentés dans u document d’ECCC (2016b).
Compte tenu du fait que la CRE attribue un faible danger et une faible exposition au NSNa, cette substance a été classée comme présentant un faible potentiel de risques pour l’environnement. Il est donc improbable que cette substance soit préoccupante pour l’environnement au Canada.
7.3.2 Analyse des quotients de risque
Nous avons réalisé des analyses de quotients de risque en comparant les diverses estimations d’exposition (CEE; voir la section Évaluation de l’exposition environnementale) avec les renseignements sur l’écotoxicité (CESE; voir la section Évaluation des effets sur l’environnement) pour déterminer s’il existe un potentiel d’effets nocifs sur l’environnement au Canada. Nous avons calculé des quotients de risque (QR) en divisant la CEE par la CESE pour les milieux de l’environnement pertinents et les scénarios d’exposition associés. Nous donnons dans les tableaux 7-6, 7-7 et 7-8 les quotients de risque dans le milieu aquatique, les sols et les sédiments, calculés respectivement pour les substances du groupe des ANS.
| Scénario d’exposition | CEE en milieu aquatique (μg/L) | CESE en milieu aquatique (μg/L) | QR en milieu aquatique |
|---|---|---|---|
| Mélange d’huiles lubrifiantes | 0,05 – 2,87 | 32 | 0 – 0,09 |
| Utilisation de fluides d’usinage | 0,06 – 3,38 | 32 | 0 – 0,11 |
| Formulation de peintures et revêtements | 0,05 – 2,64 | 32 | 0 – 0,08 |
| Formulateur industriel de produits pétroliers et gaziers | 0,07 – 3,83 | 32 | 0 – 0,12 |
| Utilisation industrielle de peintures | 0,19 – 10,54 | 32 | 0,09 – 0,33 |
| Scénario d’exposition | CEE dans les sédiments (mg/kg de poids sec) | CESE dans les sédiments (mg/kg de poids sec) | QR dans les sédiments |
|---|---|---|---|
| Mélange d’huiles lubrifiantes | 0,06 – 0,09 | 2,05 | 0,03 – 0,05 |
| Utilisation de fluides d’usinage | 0,08 – 0,13 | 2,05 | 0,04 – 0,06 |
| Formulation de peintures et revêtements | 0,09 – 0,15 | 2,05 | 0,05 – 0,07 |
| Formulateur industriel de produits pétroliers et gaziers | 0,11 – 0,17 | 2,05 | 0,05 – 0,08 |
| Utilisation industrielle de peintures | 0,38 – 0,59 | 2,05 | 0,18 – 0,29 |
| Scénario d’exposition | CEE dans le sol (mg/kg) | CESE dans le sol (mg/kg) | QR dans le sol |
|---|---|---|---|
| Mélange d’huiles lubrifiantes | 0,11 – 0,33 | 5 | 0,02 – 0,07 |
| Utilisation de fluides d’usinage | 0,66 – 1,91 | 5 | 0,13 – 0,38 |
| Formulation de peintures et revêtements | 0,63 – 1,81 | 5 | 0,13 – 0,36 |
| Formulateur industriel de produits pétroliers et gaziers | 0,18 – 0,53 | 5 | 0,04 – 0,11 |
| Utilisation industrielle de peintures | 0,18 – 0,51 | 5 | 0,04 – 0,10 |
Les QR des tableaux 7-6, 7-7 et 7-8 sont tous inférieurs à un, ce qui indique que les ANS présentent un faible potentiel d’effets nocifs sur les organismes aquatiques ou vivant dans les sédiments ou les sols suite à leur rejet potentiel par l’industrie.
7.3.3 Éléments de preuve pris en compte
Pour caractériser les risques pour l’environnement associés aux substances du groupe des ANS, nous avons pris en compte des renseignements techniques sur divers éléments de preuve (tel que discuté dans les sections pertinentes du présent document), et les avons pondéré qualitativement. Les éléments de preuve clés appuyant la conclusion de l’évaluation sont présentés dans le tableau 7-9, une discussion globale sur le poids de la preuve étant faite à la section 7.3.4. Le niveau de confiance fait référence à l’influence combinée de la qualité et de la variabilité des données, aux lacunes dans les données, à la causalité, à la plausibilité et de toute extrapolation requise. La pertinence fait référence à l’impact d’un élément de preuve sur la détermination du potentiel d’effets nocifs sur l’environnement au Canada. Les qualificateurs utilisés pour l’analyse vont de faible à élevé, la pondération assignée à chaque élément étant de cinq niveau.
| Élément de preuve | Niveau confiancea | Pertinence pour l’évaluationb | Pondérationc | |
|---|---|---|---|---|
| Similarité de la structure chimique aux fins de lecture croisée – devenir et effets | Modéré | Élevée | Modérée à élevée | |
| Similarité de la structure chimique aux fins de lecture croisée – ADNNS par rapport à DNNSBa et DNNSCa | Élevé | Élevée | Élevée | |
| Propriétés physico-chimiques | Faible | Modérée | Faible à modérée | |
| Distribution dans l’environnement | Modéré | Modérée | Modérée | |
| Persistance dans l’environnement | Faible | Élevée | Modérée | |
| Transport sur de grandes distances | Modéré | Faible | Faible à modérée | |
| Bioaccumulation dans les organismes aquatiques | Modéré | Modérée | Modérée | |
| Mode d’action ou autres données non observablesd | Faible | Modérée | Faible à modérée | |
| CESE pour les organismes aquatiques | Modéré | Élevée | Modérée à élevée | |
| CESE pour les organismes vivant dans les sols | Faible | Élevée | Modérée | |
| CESE pour les organismes vivant dans les sédiments | Modéré | Élevée | Modérée à élevée | |
| CEE dans l’eau | Modéré | Élevée | Modérée à élevée | |
| CEE dans les sols | Modéré | Élevée | Modérée à élevée | |
| CEE dans les sédiments | Modéré | Élevée | Modérée à élevée | |
| QR pour l’eau | Modéré | Élevée | Modérée à élevée | |
| QR pour les sols | Modéré | Élevée | Modérée à élevée | |
| QR pour les sédiments | Modéré | Élevée | Modérée à élevée | |
a Le niveau de confiance est déterminé en fonction de la qualité des données, de leur variabilité et des lacunes dans les données (adéquation des données).
b La pertinence fait référence à l’impact de l’élément de preuve sur l’évaluation.
c Une pondération est assignée à chaque élément de preuve en fonction de la pondération globale combinée du niveau de confiance et de la pertinence de l’évaluation.
d Les paramètres non observables font référence aux paramètres autres que la mortalité, la croissance et la reproduction (ces paramètres sont désignés comme ayant des effets sur les populations).
7.3.4 Pondération et détermination du potentiel d’effets nocifs sur l’environnement au Canada
Une combinaison de données expérimentales, modélisées et/ou obtenues par lecture croisée, selon les renseignements disponibles, a permis d’éclairer les propriétés physico-chimiques et d’autres paramètres sélectionnés pour les ANS. La pondération des éléments de preuve appuyant les paramètres sélectionnés varie selon la source (données obtenues expérimentalement ou par modélisation) et traduit les limites de l’ensemble de données.
Compte tenu de l’incertitude associée à la modélisation de ces substances, qui ont des propriétés ionisantes et tensioactives, nous nous sommes basés sur la lecture croisée et des données empiriques pour l’évaluation du risque quand cela était possible et sur des gammes de valeurs pour évaluer l’exposition, afin d’atténuer l’impact de ces incertitudes sur l’évaluation globale.
Il n’existe aucune donnée empirique sur le transport des ANS sur de grandes distances dans l’environnement. Étant donné leurs propriétés physico-chimiques (pression de vapeur négligeable, solubilité dans l’eau faible à moyenne, faible mobilité dans le sol prévue), les ANS ne devraient pas être transportés sur de grandes distances.
La persistance dans l’environnement a été évaluée au moyen de données empiriques sur d’autres acides naphtalènesulfoniques, sur des substances analogues, ainsi que sur des résultats modélisés. Selon certaines données empiriques sur la biodégradation et les données modélisées, les ANS persisteront assez longtemps dans l’environnement pour entraîner une toxicité chronique.
Il existe peu de données empiriques sur la bioaccumulation des ANS. Les données sur l’ADNNDS ont été utilisées en combinaison avec les données modélisées pour les autres ANS. Le manque de données empiriques sur les substances autres que l’ADNNDS signifie que seul un niveau de confiance modéré peut être accordé à la détermination que certains ANS sont bioaccumulables.
Des outils de profilage chimique (notamment l’outil ASTER de l’approche de CRE) ont permis d’éclairer la caractérisation du mode d’action, étant donné qu’aucun renseignement n’a été identifié dans la littérature. Les CESE pour les organismes aquatiques, vivant dans les sédiments et dans les sols ont été déterminées à partir d’ensembles de données assez petits, qui contenaient des données obtenues par lecture croisée sur des organismes aquatiques et vivant dans les sols, résultant en un niveau de confiance dans les CESE faible à modéré.
La fiabilité des CEE tient compte de divers facteurs, dont le taux d’élimination des STEU, les données sur les propriétés physiques et chimiques, la quantité utilisée, le facteur d’émission industrielle et le volume quotidien de dilution des eaux du milieu récepteur. Les taux d’élimination des STEU, basés sur l’élimination d’une classe de substances analogues (ALBS), sont peu fiables à titre de données de lecture croisée pour les ANS. Toutefois, la situation a été atténuée en utilisant une gamme de valeurs (45-99 % des ALBS). Des gammes de valeurs ont également été utilisées pour d’autres paramètres des scénarios d’exposition, dont les valeurs de log Kco dans les scénarios relatifs aux sédiments et les demi-vies de biodégradation dans les scénarios relatifs aux sols, afin de compenser le manque de certitude associé à ces valeurs et tenir compte des différences possibles entre les valeurs des divers ANS.
Les quantités utilisées prises en compte pour les scénarios d’exposition sont basées sur les renseignements soumis lors d’enquêtes menées en vertu de l’article 71 de la LCPE. Étant donné qu’il existait peu de données sur les quantités utilisées, les quantités importées ont été utilisées pour les calculs dans les scénarios d’exposition. De plus, il manquait des renseignements sur les clients des importateurs de ces substances. En l’absence de données complètes, plusieurs hypothèses ont été faites afin de calculer les CEE. Par exemple, il a été assumé que les quantités déclarées lors des collectes de données de deux années (2011 et 2015) sont représentatives des quantités utilisées pour cette année-là. De plus, pour l’ensemble des scénarios d’exposition, en raison du manque de données sur les quantités utilisées par installation, il a été assumé que la quantité totale importée déclarée par une entreprise pourrait être utilisée dans chacune de ses installations. Comme il existait peu de données sur la composition en pourcentage des produits contenant des ANS, ce paramètre a été établi à partir de fiches signalétiques (FS) pertinentes et de documents de l’OCDE sur les scénarios d’émission.
Les données sur le volume quotidien de dilution des eaux utilisées pour les scénarios d’exposition sont jugées fiables, car elles sont basées sur des données industrielles provenant de bases de données du gouvernement canadien et sur des données mesurées ou calculées sur le débit des cours d’eau récepteurs. Les facteurs d’émission industrielle sont des estimations réalisées à partir de sources génériques (publications de l’OCDE) plutôt que de données spécifique au site. En raison des données limitées, tel que susmentionné, le niveau de confiance dans les CEE est modéré.
D’après les QR et les autres renseignements susmentionnés, le potentiel d’effets nocifs sur l’environnement au Canada dus aux substances du groupe des ANS est faible.
7.3.5 Sensibilité de la conclusion aux incertitudes clés
Étant donné le manque de données physico-chimiques expérimentales sur les substances de ce groupe, la présente évaluation s’est appuyée sur des données modélisées et une méthode de lecture croisée pour déterminer le comportement et le devenir des substances dans l’environnement et caractériser leurs effets sur l’environnement. Chaque milieu de l’environnement a été caractérisé au moyen r de données appropriées (données empiriques sur une substance du groupe ou un proche analogue) et, donc, il est improbable qu’une modification des propriétés physico-chimiques d’une substance ait une incidence sur la conclusion tirée.
L’évaluation des risques posés par les substances ayant des propriétés ionisantes et tensioactives pose un défi, car il est difficile de mesurer leurs propriétés physiques et chimiques ainsi que leur toxicité lors d’études empiriques. Ces substances posent aussi des problèmes du point de vue de la modélisation, ce qui ajoute un degré d’incertitude aux conclusions de l’évaluation. Le recours à des propriétés physico-chimiques d’une validité sujette à caution pour ces substances (comme log Koe) a été réduit au minimum autant que possible pour l’évaluation du potentiel de bioaccumulation et de persistance, et une gamme de valeurs a été utilisée pour les paramètres pertinents des scénarios d’exposition, comme les valeurs de log Kco et de demi-vies de biodégradation. Par conséquent, des renseignements supplémentaires sur ces propriétés auraient probablement un faible impact sur nos conclusions.
Tel que décrit à la section 7.3.4, il existait peu de données sur l’utilisation industrielle et sur la composition des produits sur lesquelles baser les scénarios d’exposition. De meilleures données auraient permis d’accroître le niveau de confiance dans les CEE. Toutefois, elles n’auraient probablement pas conduit à modifier la conclusion de ces scénarios d’exposition, étant donné les très faibles CEE et QR.
8. Potentiel d’effets nocifs sur la santé humaine
Le DNNSBa et le CDINSA ont été étudiés dans le cadre de l’approche suivie pour l’évaluation préalable rapide des substances pour lesquelles l’exposition de la population générale est limitée (ECCC, SC 2018). Dans le cadre de cette approche, Santé Canada a déterminé si les substances nécessitaient une évaluation plus approfondie du potentiel d’effets nocifs sur la santé humaine en se basant sur le potentiel d’expositions directe et indirecte de la population générale. Le potentiel d’exposition directe a été évalué en se basant sur des facteurs comme la preuve de présence de la substance dans un produit utilisé par la population générale, tandis que le potentiel d’exposition indirecte est tiré d’une approche générale décrite dans le document sur l’Approche fondée sur le seuil de préoccupation toxicologique (SPT) pour certaines substances (Santé Canada 2016). D’après l’évaluation des expositions directe et indirecte menée dans le cadre de cette approche, l’exposition de la population générale au DNNSBa et au CDINSA a été jugée négligeable. Par conséquent, ces substances sont considérées peu préoccupantes pour la santé humaine aux niveaux d’exposition actuels. D’autres détails sur les données et les éléments pris en compte pour l’approche basée sur le SPT sont présentées dans le document sur cette approche (Santé Canada 2016).
8.1 Évaluation de l’exposition
8.1.1 Milieux de l’environnement et aliments
NSNa
Nous n’avons trouvé aucun rapport sur la concentration de NSNa dans les milieux de l’environnement ou la poussière au Canada, ni ailleurs. Les seules utilisations déclarées lors d’enquêtes menées en vertu de l’article 71 de la LCPE (Environnement Canada 2013, ECCC 2018) étaient de nature industrielle et n’entraînaient pas de rejet dans l’environnement ou d’exposition pour la population générale (communication personnelle, courriel d’une partie prenante au Bureau de l’évaluation du risque des substances existantes (BERSE) de Santé Canada, août 2018, non référencé) (Section 7.3.1).
ADNNS, DNNSCa et DNNDSA
La présence d’ADNNS, de DNNSCa ou de DNNDSA dans les milieux de l’environnement ou la poussière au Canada ou ailleurs n’a pas été rapportée. Tel qu’indiqué à la section 6.1, étant donné leurs propriétés physico-chimiques, ces substances devraient se répartir principalement dans l’eau, le sol et les sédiments lorsqu’elles sont rejetées dans l’environnement, et les utilisations actuelles au Canada indiquent que ces milieux sont des milieux d’intérêt dans l’environnement. D’après les renseignements déclarés sur ces substances lors d’enquêtes menées en vertu de l’article 71 de la LCPE (Environnement Canada 2013, ECCC 2018) et des communications avec l’Association canadienne des constructeurs de véhicules [ACCV] (communication personnelle, courriel de l’ACCV à la Division des produits d’ECCC, 2 août 2019, non référencé), ces substances sont utilisées dans des contextes industriels au Canada et peuvent être rejetées dans l’environnement suite au traitement d’eaux usées et à l’épandage de biosolides. La concentration environnementale estimée (CEE) la plus élevée était de 10,54 µg/L pour l’eau dans le cas des rejets potentiels d’ANS provenant d’installations qui utilisent des peintures pour la fabrication d’équipement d’origine (FEM) pour automobiles (section 7.2) dans les systèmes de traitement des eaux usées. Dans le cadre d’une approche prudente, nous avons estimé l’absorption d’ADNNS, de DNNSCa et de DNNDSA par la population générale due à l’eau potable en nous basant sur la CEE la plus élevée d’un scénario d’émission industrielle. Les estimations maximales de l’absorption quotidienne due à l’eau potable se situaient entre 0,19 (9 à 13 ans et 14 à 18 ans) et 1,38 µg/kg pc/jour (0 à 5 mois, nourris à la préparation pour nourrissons). L’exposition due au sol est considérée négligeable, et l’exposition due à l’air devrait être nulle (annexe D).
L’exposition à l’ADNNS due aux aliments en raison de son utilisation comme agent antistatique pour la production d’un adjuvant de rétention pour la fabrication de papier et de carton en contact direct avec les aliments devrait être négligeable (communication personnelle, courriels de la Direction des aliments de Santé Canada au BERSE de Santé Canada, octobre 2018 et avril 2019, non référencé). L’absorption estimée la plus élevée due à l’eau potable (1,38 µg/kg pc/jour pour les nourrissons de 0 à 5 mois nourris à la préparation) a été retenue pour la caractérisation des risques (annexe D).
L’exposition au DNNSCa due aux aliments en raison de son utilisation potentielle comme lubrifiant pour des pièces d’équipement ou de machine ne devrait pas avoir lieu, étant donné qu’il n’y a aucun contact entre le lubrifiant et les aliments (communication personnelle, courriel de la Direction des aliments de Santé Canada au BERSE de Santé Canada, août 2016, non référencé).
8.1.2 Produits disponibles pour les consommateurs
NSNa, ADNNS et DNNDSA
La présence de NSNa, d’ADNNS et de DNNDSA n’a pas été identifiée dans des produits disponibles pour les consommateurs au Canada. Par conséquent, l’exposition de la population générale à ces substances due à ces produits ne devrait pas se produire.
DNNSCa
Le DNNSCa est utilisé comme inhibiteur de corrosion (1-5 %) dans un lubrifiant en aérosol à usage général (FSS 2018). Ce produit devrait être utilisé sporadiquement par la population générale, pouvant entraîner une exposition par inhalation et par voie cutanée. Nous avons résumé dans le tableau 8‑1 les expositions estimées au DNNSCa, par événement, dues à l’utilisation d’un tel lubrifiant. Les détails sur les paramètres utilisés pour l’estimation de l’exposition sont présentés à l’annexe E.
| Scénario pour le produit (groupe d’âge) | Concentration dans le produit | Expositition par inhalationa (mg/kg pc) | Exposition par voie cutanéea (mg/kg pc) | Exposition combinée par inhalation et par voie cutanéea (mg/kg pc) |
|---|---|---|---|---|
| Lubrifiant en aérosol à usage général, exposition intermittente (adultes de 19 ans ou plus) | 5 %b | 2,2 × 10-3 | 1,1 × 10-2 | 1,4 × 10-2 |
a L’absorption par inhalation ou par voie cutanée est assumée être de 100 % (équivalente à une absorption orale).
b La concentration maximale figurant dans la FSS a servi à estimer les expositions.
8.2 Évaluation des effets sur la santé
NSNa
En se basant sur les classifications de la cancérogénicité, de la génotoxicité et de la toxicité pour le développement ou pour la reproduction établie par d’autres organismes nationaux ou internationaux, le NSNa n’a pas été identifié comme posant un danger important pour la santé humaine. Cette substance ne figure pas non plus sur la Liste des substances extrêmement préoccupantes candidates en vue d’une autorisation de l’Agence européenne des produits chimiques (ECHA 2018f). Des études plus poussées sur les effets de cette substance sur la santé ne sont pas nécessaires, étant donné que la population générale du Canada ne devrait pas y être exposée.
ADNNS, DNNSCa et DNNDSA
L’EPA des États-Unis a publié un document sur la caractérisation préalable des dangers de plusieurs dinonylnaphtalènes dans le cadre de son programme d’évaluation des substances chimiques produites en grande quantité (HPV Challenge Program), qui traitait de l’ADNNS et du DNNSCa (EPA 2012). Les deux substances ont été évaluées en tant que sous-catégorie, et des données sur leur toxicité aiguë par voie orale, par inhalation et par voie cutanée ainsi que sur leurs propriétés irritantes et sensibilisantes pour les yeux et la peau étaient disponibles. Cependant, aucune donnée sur la toxicité à dose répétée, la toxicité pour la reproduction ou le développement, la génotoxicité ou la cancérogénicité n’a été identifiée.
Un dossier REACH sur l’ADNNDS contenant des données empiriques sur la toxicité aiguë est disponible (ECHA 2018a). Les autres données disponibles sur les effets sur la santé de l’ADNNDS contenues dans le dossier REACH sont basées sur une lecture croisée à partir des données sur l’ADANS riche en C9, le DANSCa riche en C9 et l’DANSBa riche en C9 (ECHA 2018b, 2018c, 2018d).
L’ADNNS, le DNNSCa et l’ADNNDS ont des structures chimiques similaires : ils ont tous un cycle naphtalénique avec un ou deux substituants acide sulfonique et deux alkyles en C9, ramifiés ou linéaires. Le DNNSCa étant un sel métallique alcalino‑terreux de l’ADNNS, il est présumé se dissocier en un anion de l’ADNNS et en un cation métallique au moment de l’ingestion et de l’absorption, et devrait présenter des effets toxicologiques semblables à ceux de l’ADNNS. Étant donné que la base globale de données toxicologiques empiriques sur ces substances est limitée (aucune donnée disponible sur la toxicité à dose répétée ni sur la génotoxicité) et que les substances ont une structure globale similaire, une seule évaluation des effets sur la santé sera présentée pour l’ADNNS, le DNNSCa et l’ADNNDS, et une approche de lecture croisée sera utilisée. (Malgré des solubilités dans l’eau différentes, l’ADNNDS est jugé suffisamment semblable à l’ADNNS et au DNNSCa aux fins d’une lecture croisée.)
Pour la caractérisation des effets sur la santé humaine de l’ADNNS, du DNNSCa et de l’ADNNDS, l’ADANS riche en C9, le DANSCa riche en C9 et le DANSBa riche en C9 ont été utilisés comme analogues. Ces trois substances riches en C9 sont considérés comme des analogues appropriés, car ce sont des mélanges des acides (alkyl en C8-C10)naphtalènesulfoniques correspondants, qui contiennent soit de l’ADNNS soit du DNNSCa comme composant principal. Les composants acides monoalkylnaphtalènesulfoniques et acides trialkylnaphtalènesulfoniques (avec un ou trois substituants alkyles) de ces ADANS sont également considérés comme des analogues appropriés en raison de leur similarité structurale avec l’ADNNS, le DNNSCa et l’ADNNDS.
Génotoxicité
L’ADANS riche en C9 (ECHA 2018b) et le DANSBa riche en C9 (ECHA 2018d) ont tous deux donnés lors de tests Ames, avec ou sans activation métabolique, des résultats négatifs pour la mutagénicité pour toutes les souches de S. typhimurium et d’E. colicoli jusqu’à la concentration maximale testée (5000 µg/plaque de gélose). Une cytotoxicité a été observée à 1000 µg/plaque de gélose et plus pour l’ADANS riche en C9 et à 333 µg/plaque de gélose ou plus pour le DANSBa riche en C9.
Lors d’un test à la thymidine kinase sur des cellules de lymphome de souris, le DANSBa riche en C9 a donné des résultats négatifs pour la mutagénicité dans les cellules de mammifère jusqu’à la concentration maximale testée (90 µg/mL), avec ou sans activation métabolique, avec une cytotoxicité observée à partir de de 50 µg/mL (avec activation) et de 70 µg/mL (sans activation) [ECHA 2018d]. Lors d’une étude d’aberration chromosomique, le DANSBa riche en C9 a donné des résultats négatifs pour la clastogénicité jusqu’à une concentration maximale de 250 µg/mL, avec ou sans activation métabolique (ECHA 2018d).
Aucune étude sur la génotoxicité du DANSBa riche en C9 n’a été identifiée.
De plus, la modélisation prédictive QSAR n’a produit aucune alerte structurale pour la génotoxicité des structures représentatives de ces substances (Derek Nexus 2018, Leadscope Model Applier 2018, TIMES 2016).
En se basant sur ces résultats, il a été déterminé que l’ADNNS, le DNNSCa et l’ADNNDS ne sont probablement pas génotoxiques.
Il n’existe aucune étude sur la cancérogénicité de l’ADANS riche en C9 ou de ses sels.
Toxicité à dose répétée
Dans le cadre d’une étude à dose répétée de 14 jours, des rats Wistar adultes mâles et femelles (n = 3 pour chaque sexe et chaque dose) ont reçu par gavage par voie oral des doses de 0, 80, 250 ou 750 mg/kg pc/jour de DANSCa riche en C9 dans du (méthanesulfinyl)méthane (ECHA 2018c). Les résultats comprennent une augmentation non significative des niveaux de phosphate inorganique et de l’activité de la phosphatase alcaline (PA) et de la glutamate pyruvate transaminase (GPT), ainsi qu’une concentration totale en protéines moindre chez les femelles à la dose testée maximale, sans effet nocif manifeste observé quelle que soit la dose. Les auteurs de l’étude ont établi une CSENO de 750 mg/kg pc/jour (dose maximale testée). Comparativement à une étude à dose répétée de 28 jours réalisée en suivant la ligne directrice de l’OCDE, cette étude a été faite avec moins d’animaux par sexe et par dose, une durée moindre et moins de paramètres étudiés.
Dans le cadre d’une étude à dose répétée de 90 jours, des rats Wistar adultes mâles et femelles (n = 10 pour chaque sexe et chaque dose) ont reçu par gavage par voie orale des doses de 0, 100, 300 ou 1000 mg/kg pc/jour de DANSCa riche en C9 dans de l’huile de maïs (ECHA 2018c). Six femelles sont mortes après avoir reçu une dose de 1000 mg/kg pc/jour, et une nécropsie a révélé des effets sur les voies gastro-intestinales (p. ex., ulcération, hyperplasie des cellules pavimenteuses, hyperkératose et épaississement de la paroi du préestomac, atrophie et érosion de la muqueuse, et intestins distendus), une atrophie de la moelle osseuse et un petit thymus. À la dose de 1000 mg/kg pc/jour, d’importants changements dans les paramètres biochimiques suivants ont été observés : activité du GPT (baisse chez les mâles, hausse chez les femelles), cholestérol (baisse chez les mâles et les femelles), phosphate (hausse chez les mâles), acide biliaire (baisse chez les mâles), albumine (baisse chez les femelles), potassium (baisse chez les femelles) et calcium (hausse chez les femelles). À 300 et 1000 mg/kg pc/jour, on a observé chez les animaux survivants une baisse irréversible importante du gain moyen de poids corporel accompagnée d’une augmentation de la consommation alimentaire, d’ulcères et d’effets inflammatoires sur le tube digestif ainsi que des variations considérables du poids relatif ou absolu du thymus (baisse chez les mâles et les femelles), du foie (baisse chez les mâles, hausse chez les femelles), des reins (hausse chez les mâles et les femelles) et des glandes surrénales (hausse chez les mâles et les femelles). De plus, d’importants changements aux paramètres hématologiques suivants ont été observés : temps de coagulation (baisse chez les mâles et les femelles), neutrophiles (hausse chez les femelles), lymphocytes, plaquettes et réticulocytes (baisse chez les femelles). Des observations histopathologiques réalisées à 300 et 1000 mg/kg pc/jour ont révélé une lymphocytolyse et une déplétion lymphocytaire accrues dans le thymus des mâles et des femelles, une hausse de l’hypertrophie des cellules folliculaires de la thyroïde chez les mâles et une présence accrue de macrophages alvéolaires dans les poumons des mâles. Une atrophie vaginale et une inactivité de l’utérus ont aussi été observées chez les femelles à une dose de 300 mg/kg pc/jour. Par conséquent, une CSENO de 100 mg/kg pc/jour pour le DANSCa riche en C9 a été établie en se basant sur les effets sur le poids corporel et des organes et des modifications aux voies gastro-intestinales et au système hématopoïétique observées à la dose de 300 mg/kg pc/jour.
Des études à dose répétée ont été réalisées avec l’ADANS riche en C9 et le DANSBa riche en C9 sous la forme d’études combinées de toxicité à dose répétée et de dépistage de la toxicité pour la reproduction et le développement. Les résultats sont présentés dans la section suivante.
Aucune étude à dose répétée pour d’autres voies d’exposition (cutanée ou par inhalation) n’a été identifiée.
Aucune étude à dose répétée à long terme n’a été identifiée.
Toxicité pour le développement et la reproduction
Dans le cadre d’une étude combinée de toxicité à dose répétée et de dépistage de la toxicité pour la reproduction et le développement, des rats Wistar adultes mâles et femelles (n=10 pour chaque sexe et dose) ont reçu par gavage par voie orale 0, 95, 298 ou 893 mg/kg pc/jour (doses analytiques) d’ADANS riche en C9 dans du propane-1,2-diol (ECHA 2018b). Les mâles ont été exposés pendant 31 jours, tandis que les femelles l’ont été pendant 41-52 jours. Les petits ayant survécu ont été sacrifiés entre les jours de lactation 5 et 7. À 893 mg/kg pc/jour, cinq animaux ont été sacrifiés in extremis. Les mâles adultes survivants présentaient un poids corporel ou un gain de poids corporel moyens inférieurs à ceux du groupe témoin tout au long de la période d’accouplement. Les mâles du groupe ayant reçu la dose maximale ont aussi présenté un nombre moyen de globules blancs statistiquement significativement plus élevé. De plus, tant les adultes mâles que femelles présentaient une activité plus élevée du GPT et de la PA ainsi qu’un taux de cholestérol plus bas que ceux du groupe témoin. Des observations histopathologiques ont été faites dans le tube gastro-intestinal, le thymus, les poumons et le foie des adultes survivants. Les paramètres microscopiques observés chez les sujets sacrifiés tôt étaient généralement de nature et d’intensité semblables à celles observées chez les animaux survivants. À 298 mg/kg pc/jour, une activité accrue de la PA chez les femelles adultes ainsi qu’un taux de cholestérol plus bas chez les mâles adultes ont été observés, une femelle ayant été sacrifiée in extremis 27 jours après l’accouplement. À 893 mg/kg pc/jour, les jeunes femelles présentaient au jour de lactation 4 un poids corporel moyen beaucoup plus bas que celui du groupe témoin, ce qui ne pouvait être attribuable à de la négligence maternelle ou à des effets secondaires découlant de changements au poids corporel et à la consommation alimentaire de la mère. Toutefois, aucun autre paramètre lié au développement examiné lors de l’étude n’a eu d’effet nocif (indice et durée de gestation, parturition, soins maternels et développement des petits au début de la période postnatale comprenant mortalité, signes cliniques et paramètres macroscopiques). Aucun paramètre de toxicité pour la reproduction n’a été affecté chez les rats adultes mâles et femelles (indices de reproduction, de fertilité et de conception, intervalle précoïtal, spermatogenèse et nombre de corps jaunes et de sites d’implantation). Par conséquent, la CSENO pour la toxicité parentale est de 95 mg/kg pc/jour, basée sur des changements dans les paramètres cliniques de biochimie à 298 mg/kg pc/jour et de la toxicité systémique observée à 893 mg/kg pc/jour, tandis que la CSENO pour les effets sur le développement est de 298 mg/kg pc/jour, basée sur les changements au poids corporel moyen des petits à 893 mg/kg pc/jour. La CSENO pour les effets sur la reproduction est de 893 mg/kg pc/jour en raison de l’absence d’effet observé à la dose maximale testée.
Dans le cadre d’une étude combinée de toxicité à dose répétée et de dépistage de la toxicité pour la reproduction et le développement, des rats Wistar adultes mâles et femelles (n = 10 pour chaque sexe et chaque dose) ont reçu par gavage par voie orale 0, 17, 55 ou 165 mg/kg pc/jour (corrigées en fonction de la pureté finale des UVCB) de DANSBa riche en C9 (ECHA 2018d). Les mâles ont été exposés pendant 29 jours, tandis que les femelles l’ont été pendant 42‑55 jours. Les petits ayant survécu ont été sacrifiés entre les jours de lactation 5 et 7. Parmi les adultes exposés à la dose de 165 mg/kg pc/jour, une hausse statistiquement non significative de la fréquence de cristaux tubulaires dans les reins d’un mâle et d’une femelle a été observée, ainsi que de faibles ou minimes cas de dilatation des tubules, d’hypertrophie épithéliale et de présence de cylindres granulaires chez la femelle. De plus, les femelles ont présenté une baisse réversible de l’activité motrice et une faible hausse de l’hypertrophie et de l’hyperplasie de l’épithélium de la glande thyroïde. Aucun effet lié au traitement n’a été observé sur les paramètres de reproduction (indices de reproduction, de fertilité et de conception, intervalle précoïtal, spermatogenèse et nombre de corps jaunes et de sites d’implantation) ou de développement (indice et durée de gestation, parturition, soins maternels et développement des petits au début de la période postnatale comprenant mortalité, signes cliniques, poids corporel et paramètres macroscopiques) étudiés chez les rats adultes ou leurs petits. Par conséquent, la CSENO pour la toxicité pour les parents a été établie à 55 mg/kg pc/jour en se basant sur des effets sur les reins et la thyroïde observés à 165 mg/kg pc/jour, tandis que la CSENO pour les effets sur la reproduction et le développement a été établie à 165 mg/kg pc/jour en raison de l’absence d’effet à la dose maximale testée.
Aucune étude sur la toxicité du DANSCa riche C9 pour la reproduction ou le développement n’est disponible.
8.3 Caractérisation des risques pour la santé humaine
DNNSBa et CDINSA
Le DNNSBa et le CDINSA ont été étudiés dans le cadre de l’approche suivie pour l’Évaluation préalable rapide des substances pour lesquelles l’exposition de la population générale est limitée (ECCC, SC 2018). D’après l’évaluation de l’exposition directe et de l’exposition indirecte réalisée dans le cadre de cette approche, l’exposition de la population générale au DNNSBa ou au CDINSA a été jugée négligeable. Par conséquent, ces deux substances ont été jugées peu préoccupantes pour la santé humaine aux niveaux d’exposition actuels.
NSNa
La population générale ne devrait pas être exposée au NSNa par les milieux de l’environnement, les aliments ou l’utilisation de produits disponibles pour les consommateurs. Par conséquent, les risques pour la santé humaine sont considérés faibles.
ADNNS, DNNSCa et ADNNDS
Comme les données sur les effets de l’ADNNS, du DNNSCa et de l’ADNNDS sur la santé étaient limitées, une approche de lecture croisée faisant appel aux données sur les effets des analogues DANSA riche en C9, DANSCa riche en C9 et DANSBa riche en C9 sur la santé a été suivie. En se basant sur les renseignements sur les analogues, il est improbable que l’ADNNS, le DNNSCa et l’ADNNDS soient génotoxiques. Aucune étude à dose répétée à long terme n’a été trouvée pour l’ADNNS, le DNNSCa, l’ADNNDS et leurs analogues. Cependant, une DSENO de 100 mg/kg pc/jour a été établie en se basant sur les effets sur l’organisme, les variations de poids des organes et les modifications observées dans le tube gastro-intestinal chez des animaux de laboratoire ayant reçu une dose de 300 mg/kg pc/jour lors d’une étude d’exposition par voie orale de 90 jours à du DANSCa riche en C9. Une DSENO de 55 mg/kg pc/jour a été établie en se basant sur les effets sur les reins et la glande thyroïde (présence de cristaux tubulaires dans les reins et hyperplasie ou hypertrophie de l’épithélium de la glande thyroïde) observés à la dose suivante de 165 mg/kg pc/jour chez les parents des rejetons lors de tests de dépistage de la toxicité pour la reproduction et le développement menée avec l’analogue DANSBa riche en C9.
La DSENO de 55 mg/kg pc/jour établie à partir de tests de dépistage de la toxicité pour la reproduction et le développement est considérée prudente pour ce qui est des effets observés à plus long terme, et elle a été utilisée pour caractériser les risques associés à des expositions quotidiennes par voie orale au DNNSCa, à l’ADNNS et à l’ADNNDS dues aux milieux de l’environnement ou aux aliments, et à des expositions intermittentes au DNNSCa par inhalation et par voie cutanée dues à l’utilisation d’un lubrifiant en aérosol à usage général. Toutes les valeurs pertinentes d’exposition et de danger pour les substances du groupe des ANS, ainsi que les marges d’exposition résultantes, pour déterminer le risque sont données dans le tableau 8‑2.
| Scénario d’exposition (groupe d’âge) | Substance | Exposition systémique (mg/kg pc/jour) | Niveau d’effet critique (mg/kg pc/jour) | Paramètre critique pour la santé | ME |
|---|---|---|---|---|---|
| Milieux de l’environ-nement (nourrissons nourris aux préparations âgés de 0 à 5 mois) | DNNSCa, ADNNS et ADNNDS | 1,38 x 10-3(quotidien-nement) | 55 (DSENO pour l’analogue DANSBa riche en C9) | Présence de cristaux tubulaires dans les reins, et hyperplasie ou hypertrophie de l’épithélium de la glande thyroïde | 39 900 |
| Lubrifiant en aérosol à usage général, exposition combinée par inhalation et voie cutanéea (adultes, âgés de 19 ans ou plus) | DNNSCa | 1,4 x 10-2(par exposition) | 55 (DSENO pour l’analogue DANSBa riche en C9) | Présence de cristaux tubulaires dans les reins et hyperplasie ou hypertrophie de l’épithélium de la glande thyroïde | 3 900 |
Abréviation : ME, marge d’exposition
a L’absorption par voie cutanée et par inhalation sont supposées être de 100 % (équivalant à l’absorption par voie orale)
En comparant les estimations de l’exposition quotidienne (DNNSCa, ADNNS et ADNNDS) et de l’exposition par évènement (DNNSCa) au niveau d’effet critique, des marges d’exposition (ME) d’environ 39 900 et 3 900 sont respectivement calculées. Ces marges calculées sont jugées adéquates pour tenir compte des incertitudes des bases de données sur l’exposition et les effets sur la santé.
8.4 Incertitudes de l’évaluation des risques pour la santé humaine
Les sources clés d’incertitude sont présentées dans le tableau suivant.
| Principales sources d’incertitude | Impact |
|---|---|
| Pas de données sur la présence d’ADNNS, de DNNSCa et d’ADNNDS dans les milieux de l’environnement disponibles. | +/- |
| L’utilisation d’un lubrifiant en aérosol contenant du DNNSCa est associée à un potentiel d’exposition par voie cutanée ou par inhalation. Cependant, il n’existe aucune étude de toxicité propre à une voie pour l’exposition au DNNSCa ou à ses analogues par inhalation ou par voie cutanée. La caractérisation des risques associés à l’exposition au DNNSCa par inhalation et par voie cutanée est basée sur l’extrapolation d’une voie à une autre. | +/- |
| Les données empiriques sur les effets sur la santé spécifiques à une substance, y compris celles d’études sur le danger par exposition chronique à l’ADNNS, au DNNSCa et à l’ADNNDS, ainsi qu’à leurs analogues, étaient limitées ou indisponibles. | +/- |
| Les données sur les effets sur la santé des analogues étaient limitées et n’étaient accessibles que sous forme de sommaires d’études rigoureux versés aux dossiers REACH. | +/- |
| La nature UVCB des analogues crée de l’incertitude pour identifier quel composant provoque les effets observés sur la santé. | +/- |
+ = incertitude pouvant entraîner une surestimation de l’exposition/du risque; - = incertitude pouvant entraîner une sous-estimation de l’exposition/du risque; +/- = potentiel inconnu de surestimer ou de sous-estimer le risque.
9. Conclusion
Compte tenu de tous les éléments de preuve avancés dans la présente ébauche d’évaluation préalable, les six substances du groupe des ANS présentent un faible risque d’effets nocifs sur l’environnement. Il est conclu que ces six substances ne satisfont à aucun des critères de l’alinéa 64a) ou 64b) de la LCPE, car ils ne pénètrent pas dans l’environnement en une quantité ou concentration ni dans des conditions de nature à avoir, immédiatement ou à long terme, un effet nocif sur l’environnement ou sa diversité biologique, ou à mettre en danger l’environnement essentiel pour la vie.
En se basant sur les renseignements présentés dans la présente ébauche d’évaluation préalable, il est conclu que les six substances du groupe des ANS ne satisfont à aucun des critères de l’alinéa 64c) de la LCPE, car ils ne pénètrent pas dans l’environnement en une quantité ou concentration ni dans des conditions de nature à constituer un danger au Canada pour la vie ou la santé humaine.
Il est donc conclu que les six substances du groupe des ANS ne satisfont à aucun des critères de l’article 64 de la LCPE.
Références
Abraham M.H., Chadha H.S., Whiting G.S., et Mitchell R.C.; 1994; Hydrogen bonding. 32. An analysis of water-octanol and water-alkane partitioning and the Δlog P parameter of seiler; J. Pharm. Sci., 83(8), p. 1085‑1100 [disponible en anglais seulement].
ACD/Percepta [module de prévision]; c1997-2017; Toronto (ON) : Advanced Chemistry Development Inc. [disponible en anglais seulement].
Alberta Environment; 2009; Guidelines for the application of municipal wastewater sludges to agricultural lands [PDF]; Edmonton (Alberta) : Alberta Environment [consulté le 11 décembre 2018] [disponible en anglais seulement].
Bartell S.M., LaKind J.S., Moore J.A. et Anderson P.; 1998; Bioaccumulation of hydrophobic organic chemicals by aquatic organisms: a workshop summary; Int. J. Environ. Pollut., 9, p. 3-25 [cité dans EOSCA 2000] [disponible en anglais seulement].
BIONIC Model; 2016, ver. 2.0; A mechanistic mass balance model for predicting bioconcentration factors (BCFs) of ionizable organic chemicals in fish; modèle développé par James Armitage et Frank Wania (Université de Toronto, Canada), Trevor Brown (Université Dalhousie, Canada), Don Mackay (Université Trent, Canada) et John Arnot (ARC, Arnot Research and Consulting, Canada) [disponible en anglais seulement].
[BIOWIN] Biodegradation Probability Program for Microsoft Windows [estimation model]; 2010, ver. 4.10; Washington (DC): US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY): Syracuse Research Corporation [disponible en anglais seulement].
Boethling R.S., Howard P.H., Beauman J.A. et Larosche M.E.; 1995; Factors for intermedia extrapolations in biodegradability assessment; Chemosphere, 30(4), p. 741–752 [disponible en anglais seulement].
Canada, ministère de l’Environnement; 2012; Loi canadienne sur la protection de l’environnement (1999) : avis concernant certaines substances de la Liste intérieure [PDF]; Gazette du Canada, Partie I, vol. 146, no 48, supplément.
Canada, ministère de l’Environnement; 2017; Loi canadienne sur la protection de l’environnement (1999) : avis concernant les substances visées par la mise à jour de l’inventaire de 2017 [PDF]; Gazette du Canada, Partie I, vol. 151, no 2.
CATALOGIC [modèle sur le devenir dans l’environnement et l’écotoxicité]; 2014, ver. 5.11.15; Bourgas (Bulgarie) : Université “Prof. Dr. Assen Zlatarov”, Laboratoire de chimie mathématique [disponible en anglais seulement].
ChemView [base de données]; 2013- ; Search results for CAS RNs 25322-17-2, 25619-56-1, 57855-77-3, 60223-95-2 and 68425-61-6; Washington (DC): US Environmental Protection Agency [mise à jour le 26 octobre 2018, consultée le 19 septembre 2018] [disponible en anglais seulement].
[ConsExpo Web] Consumer Exposure Web Model; 2016; Bilthoven (Pays-Bas) : Rijksinstituut voor Volksgezondheid en Milieu [Institut national pour la santé publique et l’environnement] [disponible en anglais seulement.]
Derek Nexus [toxicity prediction module]; 2018, ver. 6.0.1; Leeds (R.-U.) : Lhasa Limited [accès réservé] [disponible en anglais seulement].
[ECCC] Environnement et Changement climatique Canada; 2016a; Document sur l’approche scientifique : classification du risque écologique des substances organiques; Ottawa (ON), gouvernement du Canada.
[ECCC] Environnement et Changement climatique Canada; 2016b;Suporting documentation: data used to create substance-specific hazard and exposure profiles and assign risk; Gatineau (QC) : ECCC; Information in support of the science approach document: ecological risk classification of organic substances; accessible sur demande : substances@ec.gc.ca [disponible en anglais seulement].
[ECCC] Environnement et Changement climatique Canada ; 2018; Données de la mise à jour de l’inventaire de la LIS recueillies en vertu de l’article 71 de la Loi canadienne sur la protection de l’environnement, 1999 : Avis concernant les substances incluses dans la mise à jour de l’inventaire de 2017 ; Données préparées par : Environnement et Changement climatique Canada, Santé Canada : Programme des substances existantes.
[ECCC, SC] Environnement et Changement climatique Canada, Santé Canada; 2015; Identification des priorités d’évaluation des risques : résultats de l’examen de 2015 [consulté le 5 mars 2020].
[ECCC, SC] Environnement et Changement climatique Canada, Santé Canada; [modifié le 12 mars 2017]; Catégorisation; Ottawa (ON) : gouvernement du Canada [consulté le 14 novembre 2018].
[ECCC, SC] Environnement et Changement climatique Canada, Santé Canada; 2018; Évaluation préalable rapide des substances pour lesquelles l’exposition de la population générale est limitée; Ottawa (ON) : gouvernement du Canada.
[ECHA] Agence européenne des produits chimiques; 2012; Guidance on information requirements and chemical safety assessment, ver. 2.1; Helsinki (Finlande) : European Chemicals Agency (Environmental exposure estimation; Chapter R.16) [disponible en anglais seulement].
[ECHA] Agence européenne des produits chimiques; 2016; Guidance on information requirements and chemical safety assessment. Chapter R.16: Environmental exposure estimation, version 3.0; Helsinki (Finlande) : ECHA [disponible en anglais seulement].
[ECHA] Agence européenne des produits chimiques; 2018a; Registration dossier: Dinonylnaphthalenedisulphonic acid; CAS RN 60223-95-2; Helsinki (Finlande) : ECHA [consulté le 4 décembre 2018] [disponible en anglais seulement].
[ECHA] Agence européenne des produits chimiques; 2018b; Registration dossier: di C8-C10, branched, C9 rich, alkylnaphthalene sulphonic acid; EC number 939-714-0; Helsinki (Finlande) : ECHA [consulté le 3 décembre 2018] [disponible en anglais seulement].
[ECHA] Agence européenne des produits chimiques; 2018c; Registration dossier: calcium bis(di C8-C10, branched, C9 rich, alkylnaphthalene sulphonic acid); EC number 939-717-7; Helsinki (Finlande) : ECHA [consulté le 4 septembre 2018] [disponible en anglais seulement].
[ECHA] Agence européenne des produits chimiques; 2018d; Registration dossier: barium bis (di C8-C10, branched, C9 rich, alkylnaphthalene sulphonic acid); EC number 939-718-2; Helsinki (Finlande) : ECHA [consulté le 222 août 2018] [disponible en anglais seulement].
[ECHA Agence européenne des produits chimiques; 2018e; Registration dossier: Naphthalene sulfonic acid, reaction products with isobutanol,sodium salts;EC number 947-977-8; Helsinki (Finlande) : ECHA [mis à jour le 13 juin 2018] [disponible en anglais seulement].
[ECHA] Agence européenne des produits chimiques; 2018f; Candidate List of Substances of Very High Concern for Authorisation [Internet]; Helsinki (Finlande) : European Chemicals Agency [consulté le 3 décembre 2018] [disponible en anglais seulement].
[ECHA] Agence européenne des produits chimiques; 2019a; Registration dossier: 2-Naphthalenesulfonic acid; CAS RN 120-18-3; Helsinki (Finlande) : ECHA [mis à jour le 7 mars 2019; consulté le 2 mai 2019] [disponible en anglais seulement].
[ECHA] Agence européenne des produits chimiques; 2019b; Registration dossier: Naphthalene sulfonic acid, bis(1-methylethyl)-, Me derivs., sodium salts; CAS RN 68909-82-0; Helsinki (Finlande) : ECHA [mis à jour le 14 juillet 2019] [disponible en anglais seulement].
Environnement Canada; 2013; Données de la Mise à jour de l’inventaire de la LIS recueillies en vertu du de l’article 71 de la Loi canadienne sur la protection de l’environnement de 1999 : Avis concernant certaines substances inanimées (chimiques) inscrites sur la Liste intérieure; Données préparées par Environnement Canada et Santé Canada, Programme des substances existantes.
Environnement Canada, Santé Canada; 2014; Approche d’identification des substances chimiques et des polymères jugés prioritaires pour l’évaluation des risques en vertu de la Partie 5 de la Loi canadienne sur la protection de l’environnement de 1999 [LCPE (1999)]; Ottawa (ON) : gouvernement du Canada [consulté le 5 mars 2020].
[EOSCA] European Oilfield Speciality Chemicals Association; 2000; Bioaccumulation potential of surfactants: A review [consulté en septembre 2018] [disponible en anglais seulement].
[EPA] Environmental Protection Agency des États-Unis; 1996; Generic scenario for automobile spray coating - Draft report; Washington (DC): US EPA, Office of Pollution Prevention and Toxics [disponible en anglais seulement].
[EPA] Environmental Protection Agency des États-Unis; 2003; Exposure and human health reassessment of 2,3,7,8-tetrachlorodibenzo-p-dioxin (TCDD) and related compounds; Washington (DC): US EPA, National Center for Environmental Assessment, Report No.: EPA/600/P-00/001Cb. Part I: Estimating exposure to dioxin-like compounds; Volume 3: Site-specific assessment procedures; Chapter 4: Estimating exposure media concentrations. 14 p. [disponible en anglais seulement].
[EPA] Environmental Protection Agency des États-Unis; 2011; Exposure factors handbook; Washington (DC): US EPA, National Center for Environmental Assessment, Office of Research and Development [consulté le 20 février 2018] [disponible en anglais seulement].
[EPA] Environmental Protection Agency des États-Unis; 2012; Screening level hazard characterization of high production volume chemicals: Dinonylnaphthalene category; Washington (DC): US EPA, Office of Pollution Prevention and Toxics [consulté le 20 février 2018] [disponible en anglais seulement].
[EPI Suite] Estimation Program Interface Suite for Microsoft Windows [estimation model]; c2000-2012, ver. 4.11; Washington (DC): US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY): Syracuse Research Corporation [disponible en anglais seulement].
Farn R.J. éditeur; Chemistry and Technology of Surfactants [PDF]; Blackwell Publishing Ltd, R.‑U. [cité dans ECCC 2015] [disponible en anglais seulement].
[FS] Fiche signalétique; 2014; NAXAN DI-AN; Harrison (OH): Nease Performance Chemicals LLC [consulté au printemps 2018] [disponible en anglais seulement].
[FSS] Fiche signalétique de sécurité; 2018; Termin-8R [PDF]; Toronto (ON) : Spectra Products [consulté le 11 février 2019] [disponible en anglais seulement].
Gobas F.; 2007; Development and review of a generic water–sediment modelling framework for organic chemicals; Burnaby (C.-B.) : Université Simon Fraser, Faculty of Environment; rapport préparé pour Environnement Canada [disponible en anglais seulement].
Gobas F.; 2010; Comments on approach to sediment exposure approach; Burnaby (C.-B.) : Université Simon Fraser, Faculty of Environment; rapport préparé pour Environnement Canada [disponible en anglais seulement].
Greim H., Ahlers J., Bias R., Broecker B., Hollander H., Gelbke H.-P., Klimisch H.-J., Mangelsdorf I., Paetz A., Schong N. et coll.; 1994; Toxicity and ecotoxicity of sulfonic acids: Structure-activity relationships; Chemosphere, 28(12), p. 2203-2236 [disponible en anglais seulement].
[HENRYWIN] Henry’s Law Constant Program for Microsoft Windows [estimation model]; 2011, ver. 3.20; Washington (DC): US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY): Syracuse Research Corporation [disponible en anglais seulement].
Kim M., Guerra P., Theocharides M., Barclay K., Smyth S.A. et Alaee M.; 2013; Polybrominated diphenyl ethers in sewage sludge and treated biosolids: effect factors and mass balance; Water Res., 47, p. 6496‑6505 [disponible en anglais seulement].
[KOAWIN] Octanol-Air Partition Coefficient Program for Microsoft Windows [estimation model]; 2010, ver. 1.10; Washington (DC): US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY): Syracuse Research Corporation [disponible en anglais seulement].
Kölbel H., Kurzendörfer P. et Zahiruddin M.; 1964; Constitution and properties of surfactants. IV. Influence of structure on the aerobic biodegradation of anionic surfactants; Tenside, 1, p. 7-18 [cité dans Swisher, 1987] [disponible en anglais seulement].
Kosswig K.; 2012; Surfactants; dans Ullmann’s Encyclopedia of Industrial Chemistry, vol. 35; Weinheim : Wiley-VCH Verlag GmbH & Co., p. 431-505 [disponible en anglais seulement].
[KOWWIN] Octanol-Water Partition Coefficient Program for Microsoft Windows [estimation model]; 2010, ver. 1.68; Washington (DC): US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY): Syracuse Research Corporation [disponible en anglais seulement].
Leadscope Model Applier [prediction module]; 2016, ver. 2.1; Columbus (OH): Leadscope Inc. [accès réservé] [disponible en anglais seulement].
Lee Y., Chen L., Fang H., Hu J. et Zhang P. inventeurs; Dow Global Technologies LLC, assignee; 2011 July 21; Alkyd coating formulations; World Intellectual Property Organization WO 085520. [disponible en anglais seulement].
McWilliams P. et Payne G.; 2011; Bioaccumulation potential of surfactants: a review; Royal Society of Chemistry and the European Oilfield Speciality Chemicals Association [consulté en septembre 2018] [disponible en anglais seulement].
Matten K.J., Gillis P.L., Toito J., Milani D., Bartlett A.J., Parrott J.L., Balakrishnan V. et Prosser R.S.; 2018; Effect characterization of three naphthalene sulfonates (NSAs) on freshwater biota and their environmental concentrations in Ontario river sediments (poster); Society of Environmental Toxicology and Chemistry North America, Sacramento (CA) [disponible en anglais seulement].
[MPBPWIN] Melting Point Boiling Point Program for Microsoft Windows [estimation model]; 2010, ver. 1.43; Washington (DC): US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY): Syracuse Research Corporation [disponible en anglais seulement].
[New EQC] New Equilibrium Criterion Model; 2011, ver. 1.00 (bêta); Peterborough (ON) : Université Trent, Canadian Centre for Environmental Modelling and Chemistry [disponible en anglais seulement].
Nguyen T.H., Goss K.-U. et Ball W.P.; 2005; Critical Review: Polyparameter linear free energy relationships for estimating the equilibrium partition of organic compounds between water and the natural organic matter in soils and sediments; Environ. Sci. Technol., 39(4), p. 913-924 [disponible en anglais seulement].
[OCDE] Organisation de coopération et de développement économiques; 2004; Emission scenario document on lubricants and lubricant additives [PDF]; Paris (France) : OCDE, Direction de l’environnement (Series on Emission Scenario Documents No. 10; Report No.: ENV/JM/MONO(2004)21, JT00174617) [consulté le 19 décembre 2018] [disponible en anglais seulement].
[OCDE] Organisation de coopération et de développement économiques; 2005; SIDS initial assessment report: Linear Alkylbenzene Sulfonates (LAS) [PDF]; SIAM [SIDS Initial Assessment Meeting], 20 avril 2005 : Paris (France) [consulté en novembre 2018] [disponible en anglais seulement].
[OCDE] Organisation de coopération et de développement économiques; 2007; SIDS Initial Assessment Profile (SIAP): Alkyl Sulfates, Alkane Sulfonates, and alpha-Olefin Sulfonates category; CoCAM-2 [Cooperative Chemicals Assessment Meeting], 17-18 octobre 2007 [consulté en septembre 2018] [disponible en anglais seulement].
[OCDE] Organisation de coopération et de développement économiques; 2009; Emissions Scenario Document on Coating Industry (Paints, Laquers, and Varnishes) [PDF]; Paris (France) : OCDE, Direction de l’environnement (Series on Emission Scenario Documents No. 22; Report No. ENV/JM/MONO(2009)24) [consulté en janvier 2019] [disponible en anglais seulement].
[OCDE] Organisation de coopération et de développement économiques; 2011; Emission Scenario Document on the use of Metalworking Fluids [PDF]; Paris (France) : OCDE, Direction de l’environnement (Series on Emission Scenario Documents No. 28, Report No. ENV/JM/MONO(2011)18) [consulté en janvier 2019] [disponible en anglais seulement].
[OCDE] Organisation de coopération et de développement économiques; 2012; Emission Scenario Document on Chemicals used in oil well production [PDF]; Paris (France) : OCDE, Direction de l’environnement (Series on Emission Scenario Documents No. 31, Report No. ENV/JM/MONO(2012)7) [consulté en mars 2019] [disponible en anglais seulement].
[RIVM] Rijksinstituut voor Volksgezondheid en Milieu [Institut national pour la santé publique et l’environnement]; 2009; The ConsExpo spray model – Modelling and experimental validation of the inhalation exposure of consumers to aerosols from spray cans and trigger sprays [PDF]; Bilthoven (Pays-Bas) : RIVM, rapport numéro 320 104 005/2009 [consulté le 11 février 2019] [disponible en anglais seulement].
[RIVM] Rijksinstituut voor Volksgezondheid en Milieu [Institut national pour la santé publique et l’environnement]; 2014; General fact sheet: General default parameters for estimating consumer exposure – Updated version 2014 [PDF]; Bilthoven (Pays-Bas) : RIVM, rapport numéro : 090013003 [consulté le 11 février 2019] [disponible en anglais seulement].
[RIVM] Rijksinstituut voor Volksgezondheid en Milieu [Institut national pour la santé publique et l’environnement]; 2018; Cleaning products fact sheet: Default parameters for estimating consumer exposure – Updated version 2018 [PDF]; Bilthoven (Pays-Bas) : RIVM, rapport numéro 2016-0179 [consulté le 11 février 2019] [disponible en anglais seulement].
Santé Canada; 1998; Exposure factors for assessing total daily intake of priority substances by the general population of Canada; rapport non publié; Ottawa (ON) : Santé Canada, Direction de l’hygiène du milieu [disponible en anglais seulement].
Santé Canada; 2015; Tableau de la consommation des aliments fondé sur l’Enquête sur la santé dans les collectivités canadiennes, cycle 2.2, Nutrition (2004), réalisée par Statistique Canada, fichier partagé, Ottawa (ON).
Statistique Canada; 2004; Canadian Community Health Survey, Cycle 2.2: General Health Component, fichier partagé [disponible en anglais seulement].
Swisher R.D.; 1987; Surfactant Biodegradation, 2ème édition, Marcel Dekker Inc., New York [disponible en anglais seulement].
[TEST] Toxicity Estimation Software Tool; 2016, ver. 4.2; Washington (DC): US Environmental Protection Agency [disponible en anglais seulement].
[TIMES] Tissue MEtabolism Simulator [prediction module]; 2018, ver. 2.27.19; Bourgas (Bulgarie) : Université “Prof. Dr. Assen Zlatarov”, Laboratoire de chimie mathématique [disponible en anglais seulement].
Tolls J., Haller M., De Graaf I., Thijssen M.A.T.C. et Sijm D.T.H.M.; 1997; Bioconcentration of LAS: experimental determination and extrapolation to environmental mixtures; Environ. Sci. Technol., 31, p. 3426-3431 [cité dans EOSCA 2000 [PDF] [disponible en anglais seulement].
Tolls J., Haller M., Labee E., Verweij M. et D.T.H.M. Sijm; 2000; Experimental determination of bioconcentration of the non-ionic surfactant alcohol ethoxylate; Environ. Toxicol. Chem., 19, p. 646-653 [cité dans EOSCA 2000 [PDF] [disponible en anglais seulement].
[VCCLab] Virtual Computational Chemistry Laboratory. ALOGPS [interface autre qu’en Java]; 2005, ver. 2.1; Munich (Allemagne) : VCCLab [Tetko I.V., Gasteiger J., Todeschini R., Mauri A., Livingstone D., Ertl P., Palyulin V.A., Radchenko E.V., Zefirov N.S., Makarenko A.S. et coll.,2005, Virtual computational chemistry laboratory - design and description. J. Comput. Aid Mol. Des., 19, p. 453-463 [disponible en anglais seulement].
[WATERNT] Water Solubility Program [estimation model]; 2010, ver. 1.01; Washington (DC): US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY): Syracuse Research Corporation [disponible en anglais seulement].
Williams J.H.; 1999; Regulations on additions of sludge-borne metals to soil and their adaptation to local conditions; dans L’Hermite P. éditeur : Treatment and use of sewage sludge and liquid agricultural wastes, 243-250; Londres (R.-U.) : Commission of the European Communities [disponible en anglais seulement].
[WSKOWWIN] Water Solubility for Organic Compounds Program for Microsoft Windows [estimation model]; 2010, ver. 1.42; Washington (DC): US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY): Syracuse Research Corporation [disponible en anglais seulement].
Annexe A. Données additionnelles sur les effets sur l’environnement
| Nom commun (no CAS) | Organisme testé | Paramètre | Valeur (mg/L) |
|---|---|---|---|
| Acides naphtalènesulfoniques (68153-01-5) | Poisson (non précisé) | CL50 96 h | 100-500 |
| Acides naphtalènesulfoniques (68153-01-5) | Invertébré (D. magna) | CE50 24 h | 85 |
| Acides naphtalènesulfoniques (68153-01-5) | Invertébré (D. magna) | CE50 48 h | 34 |
| Acides naphtalènesulfoniques (68153-01-5) | Algue (non précisée) | CE10 96 h | 73,3 |
| Acides naphtalènesulfoniques (68153-01-5) | Algue (non précisée) | CE50 96 h | 54,3 |
| (Butyl linéaire ou ramifié)naphtalènesulfonates de sodium (91078-64-7) | Poisson (non précisé) | CL0 48 h | 20 |
| (Butyl linéaire ou ramifié)naphtalènesulfonates de sodium (91078-64-7) | Poisson (non précisé) | CL100 48 h | 100 |
Abréviations : CLx, concentration létale pour x % de la population; CEx, concentration entraînant un effet sur x % de la population
Annexe B. Évaluation de l’exposition de l’environnement : résumé des hypothèses
| Variable | Valeur | Unité | Autres commentaires |
|---|---|---|---|
| Quantité | 2 400 | kg/an | ECCC (2013, 2018), quantité moyenne d’ANS utilisée par les installations de mélange de lubrifiant, d’après les déclarations sur les quantités importées lors d’enquêtes menées en vertu de l’article 71 de la LCPE. Il est assumé que la quantité entière importée par une entreprise pourrait être utilisée dans une seule installation. |
| Facteur d’émission | 0,25 | Pourcent | OCDE (2004), il s’agit du facteur d’émission du pire cas pour une usine de mélange de lubrifiants. |
| Jours de rejet | 50 | Jour/an | OCDE (2004), le nombre de jours est déterminé en convertissant la quantité totale d’ANS utilisée dans une installation en quantité de produit formulé dans cette installation, et en convertissant ensuite le tonnage de produit en nombre de jours à l’aide de la référence pertinente; cette conversion a été basée sur la concentration maximale (1 %) d’ANS dans un lubrifiant, d’après les renseignements de la FS d’un produit. |
| Taux d’élimination (sur le site) | 0 | Pourcent | Aucun |
| Taux d’élimination (hors du site) | 45-99 | Pourcent | Le taux d’élimination allait de 45 à 99 % pour tenir compte des différentes propriétés physiques et chimiques des ANS. |
| Volume de dilution quotidien | 22 982 400 | L/jour | Les volumes de dilution quotidiens sont calculés en multipliant le débit d’effluent du STEU par le facteur de dilution (FD) du plan d’eau récepteur. Un FD maximal de 10 est utilisé lorsque le FD réel est supérieur à 10. Cette valeur correspond à une valeur représentative pour le secteur du mélange d’huiles lubrifiantes au Canada. |
| Variable | Valeur | Unité | Autres commentaires |
|---|---|---|---|
| Quantité | 161,24 | kg/an | OCDE (2011), estimation de la masse d’ANS manipulée dans une installation, déterminée à l’aide du volume géométrique moyen des fluides d’usinage à base d’huile manipulés dans une installation (16 124 L/an), de la masse volumique du fluide d’usinage (1 kg/L) et de la concentration des ANS dans les fluides d’usinage (1 %). |
| Facteur d’émission | 11 | Pourcent | OCDE (2011), le facteur d’émission associé aux fluides d’usinage varie de 11 à 100 %, lequel prend en compte les rejets de nettoyants de résidus d’huiles sur les surfaces de métal, la manutention des matières premières, la finition et d’autres procédés. Le coefficient d’émission le plus bas (11 %) a été utilisé. |
| Jours de rejet | 247 | Jour/an | OCDE (2011), il est assumé que le nombre de jours de rejet par défaut des installations utilisant des fluides d’usinage est égal au nombre de jours d’exploitation par défaut. |
| Taux d’élimination (sur le site) | 45 | Pourcent | L’OCDE (2011) indique que la plupart des sites utilisant des fluides d’usinage font traiter leurs eaux usées sur le site avant de déverser leurs effluents dans un STEU. Par conséquent, le taux d’élimination sur le site a été supposé équivalent au taux d’élimination du traitement secondaire le plus bas. |
| Taux d’élimination (hors du site) | 45-99 | Pourcent | Le taux d’élimination varie de 45 à 99 % pour tenir compte des différentes propriétés physiques et chimiques des ANS. |
| Volume de dilution quotidien | 6 430 000 | L/jour | Les volumes de dilution quotidiens sont calculés en multipliant le débit d’effluent du STEU par le facteur de dilution (FD) du plan d’eau récepteur. Un FD maximal de 10 est appliqué lorsque le FD réel est supérieur à 10. Cette valeur correspond au 10e centile de la distribution des volumes de dilution quotidiens pour les étangs, les STEU secondaires et tertiaires associés aux installations utilisant des fluides d’usinage au Canada. |
| Variable | Valeur | Unité | Autres commentaires |
|---|---|---|---|
| Quantité | 3162 | kg/an | ECCC (2013 et 2018), la plus importante quantité importée déclarée lors d’enquêtes menées conformément à l’article 71 de la LCPE a été convertie en une gamme de 1000 à 10 000 kg/an, 3162 kg/an correspondant à la valeur médiane sur une échelle logarithmique. Il est assumé que la quantité entière importée par une entreprise pourrait être utilisée dans une seule installation. |
| Facteur d’émission | 0,505 | Pourcent | OCDE (2009), facteur d’émission associé à la fabrication d’un lot standard de revêtements aqueux quand les matières premières brutes sont sous forme de poudre. |
| Jours de rejet | 300 | Jour/an | EC 2003, Guide technique, tableau B2.10, p. 260 |
| Taux d’élimination (sur le site) | 0 | Pourcent | Aucun |
| Taux d’élimination (hors du site) | 45-99 | Pourcent | Le taux d’élimination variait de 45 à 99 % pour tenir compte des différentes propriétés physiques et chimiques des ANS. |
| Volume de dilution quotidien | 11 105 000 | L/jour | Les volumes de dilution quotidiens sont calculés en multipliant le débit d’effluent du STEU par le facteur de dilution (FD) du plan d’eau récepteur. Un FD maximal de 10 est appliqué lorsque le FD réel est supérieur à 10. Cette valeur correspond au 10e centile de la distribution des volumes de dilution quotidiens pour les installations de formulation de peinture et revêtements au Canada, qui prend en compte les étangs et les STEU secondaires et tertiaires. |
| Variable | Valeur | Unités | Autres commentaires |
|---|---|---|---|
| Quantité | 3162 | kg/an | ECCC (2013 et 2018), la plus importante quantité importée déclarée lors d’enquêtes menées en vertu de l’article 71 de la LCPE a été convertie en une gamme de 1000 à 10 000 kg/an, 3162 kg/an correspondant à la valeur médiane sur une échelle logarithmique. Il est assumé que la quantité entière importée par une entreprise a pu être utilisée dans n’importe laquelle de ses installations. |
| Facteur d’émission | 0,3 | Pourcent | EC (2003), Guide technique, tableau A2.1, p. 221. Même si 2 % est le coefficient d’émission déterminé à partir des tableaux du Guide technique pour la quantité utilisée donnée, d’après les procédures de lavage des récipients utilisés pour la formulation, une valeur de 0,3 % a été jugée plus appropriée. Il est attendu que des solvants puissent être utilisés pour le lavage des récipients et que, par conséquent, 2 % serait une surestimation des rejets dans les eaux usées. |
| Jours de rejet | 60 | Jour/an | EC (2003), Guide technique, tableau B2.8, p. 256; le nombre de jours est déterminé en convertissant la quantité totale d’ANS utilisée dans une installation en quantité de produit formulé, puis en convertissant le tonnage de produit en nombre de jours en utilisant la référence pertinente; cette conversion a été basée sur la concentration de 10 % d’ANS dans un produit d’extraction de pétrole et de gaz, d’après les renseignements d’une FS d’un produit. |
| Taux d’élimination (sur le site) | 0 | Pourcent | Aucun |
| Taux d’élimination (hors du site) | 45-99 | Pourcent | Le taux d’élimination variait de 45 à 99 % pour tenir compte des différentes propriétés physiques et chimiques des ANS. |
| Volume de dilution quotidien | 22 697 000 | L/jour | Les volumes de dilution quotidiens sont calculés en multipliant le débit d’effluents du STEU par le facteur de dilution (FD) du plan d’eau récepteur. Un FD maximal de 10 est appliqué lorsque le FD réel est supérieur à 10. Cette valeur correspond au 10e centile de la distribution des volumes de dilution quotidiens pour les STEU secondaires et tertiaires associés à une série d’installations industrielles au Canada. |
| Variable | Valeur | Unité | Autres commentaires |
|---|---|---|---|
| Quantité | 1000 | kg/an | ECCC (2018), la plus importante quantité importée déclarée lors de la mise à jour de la Liste intérieure des substances a été convertie en une gamme de 1000 à 10 000 kg/an, la limite supérieure de la gamme ayant été utilisée. Il est assumé que la quantité entière importée par une entreprise a pu être utilisée dans l’installation. |
| Efficacité de transfert | 65 | Pourcent | OCDE (2009), il s’agit de l’efficacité de transfert moyenne pour les procédés de pulvérisation utilisés pour la fabrication d’équipement d’automobile d’origine. |
| Jours de rejet | 21 | Jour/an | OCDE (2009), EPA (1996), le nombre de jours est déterminé en convertissant la quantité totale d’ANS utilisée dans une installation en quantité de produit utilisée à l’installation, puis en convertissant le tonnage de produit en nombre de jours en utilisant la référence pertinente; cette conversion a été basée sur la concentration maximale (1,5 %) (Lee et coll. 2011) de surfactant dans une formulation de revêtement basée sur les renseignements de brevets. |
| Taux d’élimination (sur le site) | 90 | Pourcent | EPA (1996). Efficacité d’élimination des solides basée sur l’exploitation d’une usine pilote d’élimination des solides de peinture dans une cabine à eau. |
| Taux d’élimination (hors du site) | 45-99 | Pourcent | Le taux d’élimination variait de 45 à 99 % pour tenir compte des différentes propriétés physiques et chimiques des ANS. |
| Volume de dilution quotidien (pour le calcul en milieu aquatique) | 86 969 000 | L/jour | Les volumes de dilution quotidiens sont calculés en multipliant le débit d’effluent du STEU par le facteur de dilution (FD) du plan d’eau récepteur. Un FD maximal de 10 est appliqué lorsque le FD réel est supérieur à 10. Cette valeur correspond au 10e percentile de la distribution des volumes de dilution quotidiens associés à une installation de fabrication d’automobiles canadienne choisie et au facteur de dilution du site. |
| Variable | Valeur | Unité | Autres commentaires |
|---|---|---|---|
| Volume de dilution quotidien | 40 176 000 | L/jour | Les volumes de dilution quotidiens sont calculés en multipliant le débit d’effluent du STEU par le facteur de dilution (FD) du plan d’eau récepteur. Un FD maximal de 10 est appliqué lorsque le FD réel est supérieur à 10. Cette valeur correspond à une valeur représentative pour le secteur du mélange d’huiles lubrifiantes au Canada, basée sur le débit au 50e percentile. |
| Concentration totale dans la colonne d’eau (Ctotal) | 0,03-1,64 | mg/L | Les concentrations en milieu aquatique ont été calculées à l’aide du volume de dilution quotidien indiqué ci-dessus. Les autres intrants sont les mêmes que pour le scénario aquatique. |
| Variable | Valeur | Unité | Autres commentaires |
|---|---|---|---|
| Volume de dilution quotidien | 9 731 600 | L/jour | Les volumes de dilution quotidiens sont calculés en multipliant le débit d’effluent du STEU par le facteur de dilution (FD) du plan d’eau récepteur. Un FD maximal de 10 est appliqué lorsque le FD réel est supérieur à 10. Cette valeur correspond au 10e percentile de la distribution des volumes de dilution quotidiens basé sur le débit au 50e percentile pour les étangs et les STEU secondaires et tertiaires associés aux installations utilisant des fluides d’usinage au Canada. |
| Concentration totale dans la colonne d’eau (Ctotal) | 0,04-2,23 | mg/L | Les concentrations en milieu aquatique ont été calculées à l’aide du volume de dilution quotidien susmentionné. Les autres intrants sont les mêmes que pour le scénario aquatique. |
| Variable | Valeur | Unité | Autres commentaires |
|---|---|---|---|
| Volume de dilution quotidien | 11 105 000 | L/jour | Les volumes de dilution quotidiens sont calculés en multipliant le débit d’effluent du STEU par le facteur de dilution (FD) du plan d’eau récepteur. Un FD maximal de 10 est appliqué lorsque le FD réel est supérieur à 10. Cette valeur correspond au 10e percentile de la distribution des volumes de dilution quotidiens, basée sur le débit au 50e percentile pour les étangs, et les STEU secondaires et tertiaires associés aux installations de formulation de peinture et revêtements au Canada. |
| Concentration totale dans la colonne d’eau (Ctotal) | 0,05-2,64 | mg/L | Les concentrations en milieu aquatique ont été calculées à l’aide du volume de dilution quotidien susmentionné. Les autres intrants sont les mêmes que pour le scénario aquatique. |
| Variable | Valeur | Unité | Autres commentaires |
|---|---|---|---|
| Volume de dilution quotidien | 29 384 000 | L/jour | Les volumes de dilution quotidiens sont calculés en multipliant le débit d’effluent du STEU par le facteur de dilution (FD) du plan d’eau récepteur. Un FD maximal de 10 est appliqué lorsque le FD réel est supérieur à 10. Cette valeur correspond au 10e percentile de la distribution des volumes de dilution quotidiens, basée sur le débit au 50e percentile pour les STEU secondaires et tertiaires associés à toutes les installations industrielles au Canada. |
| Concentration totale dans la colonne d’eau (Ctotal) | 0,05-2,96 | mg/L | Les concentrations en milieu aquatique ont été calculées à l’aide du volume de dilution quotidien susmentionné. Les autres intrants sont les mêmes que pour le scénario aquatique. |
| Variable | Valeur | Unité | Autres commentaires |
|---|---|---|---|
| Volume de dilution quotidien (pour le calcul de la Ctotale dans le calcul pour les sédiments) | 86 969 000 | L/jour | Les volumes de dilution quotidiens sont calculés en multipliant le débit d’effluent du STEU par le facteur de dilution (FD) du plan d’eau récepteur. Un FD maximal de 10 est appliqué lorsque le FD réel est supérieur à 10. Cette valeur correspond au 10e percentile de la distribution des volumes de dilution quotidiens, basée sur le débit au 50e percentile pour les étangs, les STEU secondaires et tertiaires associés à une certaine installation canadienne de fabrication d’automobiles et le FD du site. |
| Concentration totale dans la colonne d’eau (Ctotal) | 0-0,01 | mg/L | Les concentrations en milieu aquatique ont été recalculées à l’aide du 10e percentile des volumes de dilution quotidiens basé sur le 50e percentile des débits. Les autres intrants sont les mêmes que pour le scénario en milieu aquatique. |
| Variable | Valeur | Unité | Commentaires |
|---|---|---|---|
| Fraction de l’élimination par sorption dans le STEU (Rsorption) | 45-99 | Pourcent | Le taux d’élimination variait de 45 à 99 % pour tenir compte des différentes propriétés physiques et chimiques des ANS. |
| Taux de production de biosolides (PB) | 104 | mg/L | Valeur par défaut basée sur les données sur le terrain de plusieurs systèmes de traitement secondaire (Kim et coll. 2013); utilisée pour calculer la concentration de substance dans les biosolides (Cs). |
| Vitesse d’épandage annuel de biosolides (E) | 0,83 | kg/m2-an | Au Canada, la vitesse maximale d’épandage est réglementée par les provinces et les territoires et elle varie. La vitesse la plus élevé est en Alberta et a été utilisée comme valeur par défaut (Alberta Environment 2009). |
| Nombre d’années d’épandage de biosolides (n) | 10 | An | Une période de 10 années consécutives est suggérée par l’Agence européenne des produits chimiques (ECHA 2016) pour le calcul de l’exposition sur les terres où des biosolides ont été épandus. |
| Profondeur de mélange dans le sol (p) | 0,2 | m | Valeur par défaut. Une profondeur de mélange dans le sol de 20 cm est suggérée par l’Agence européenne des produits chimiques (ECHA 2016) pour le calcul de l’exposition sur les terres où des biosolides ont été épandus. |
| Masse volumique du sol sec (ρ) | 1200 | kg/m3 | Valeur par défaut rapportée pour la masse volumique du sol (sec) par Williams (1999). |
| Demi-vie de biodégradation dans le sol | 92-200 | jour | CATALOGIC (2014) |
| Variable | Valeur | Unité | Commentaires |
|---|---|---|---|
| Concentration de la substance dans les biosolides (Cs) | 30,95-68,09 | mg/kg poids sec | La Cs est déterminée au moyen de l’équation suivante : avec Qs (kg/jour) est la masse de substance rejetée quotidiennement dans le STEU, Esorption est la fraction de la substance éliminée par sorption, D est le débit du STEU retenu, en L/jour, et PB est le taux de production de biosolides par litre d’eaux usées en mg/L. Voir les valeurs ci-dessous et dans le tableau B‑11. |
| Masse de substance rejetée quotidiennement dans le STEU (Qs) | 0,02 | kg/jour | Qs est calculé à partir de la quantité de substance annuelle à l’installation, multipliée par le facteur d’émission (provenant d’un scénario en milieu aquatique) et moyennée pour l’année en divisant par 365 jours; valeur utilisée pour calculer la concentration de la substance dans les biosolides (Cs). |
| Débit du STEU (D) | 2 298 240 | L/jour | Cette valeur est basée sur le même volume de dilution quotidien que celui utilisé pour le scénario en milieu aquatique, et assume un facteur de dilution de 10; valeur utilisée pour calculer la concentration de la substance dans les biosolides (Cs). |
| Variable | Valeur | Unité | Commentaires |
|---|---|---|---|
| Concentration de la substance dans les biosolides (Cs) | 179,85-395,66 | mg/kg poids sec | La Cs est déterminée au moyen de l’équation suivante : avec Qs (kg/jour) est la masse de substance rejetée quotidiennement dans le STEU, Esorption est la fraction de la substance éliminée par sorption, D est le débit du STEU retenu, en L/jour, et PB est le taux de production de biosolides par litre d’eaux usées en mg/L. Voir les valeurs ci-dessous et dans le tableau B‑ 11. |
| Masse de substance rejetée quotidiennement dans le STEU (Qs) | 0,027 | kg/jour | On calcule Qs à partir de la quantité de substance rejetée annuellement à l’installation, multipliée par le facteur d’émission (provenant d’un scénario en milieu aquatique) et moyennée pour l’année en divisant par 365 jours; valeur utilisée pour calculer la concentration de la substance dans les biosolides (Cs). |
| Débit du STEU (D) | 643 000 | L/jour | Cette valeur est basée sur le même volume de dilution quotidien que celui utilisé pour le scénario en milieu aquatique, et assume un facteur de dilution de 10; valeur utilisée pour calculer la concentration de la substance dans les biosolides (Cs). |
| Variable | Valeur | Unité | Commentaires |
|---|---|---|---|
| Concentration de la substance dans les biosolides (Cs) | 170,46-375,01 | mg/kg poids sec | La Cs est déterminée au moyen de l’équation suivante : Avec Qs (kg/jour) est la masse de substance rejetée quotidiennement dans le STEU, Esorption est la fraction de la substance éliminée par sorption, D est le débit du STEU retenu, en L/jour, et PB est le taux de production de biosolides par litre d’eaux usées en mg/L. Voir les valeurs ci-dessous et dans le tableau B‑ 11. |
| Masse de substance rejetée quotidiennement dans le STEU (Qs) | 0,04 | kg/jour | Qs est calculé à partir de la quantité de substance rejetée annuellement à l’installation, multipliée par le facteur d’émission (provenant d’un scénario en milieu aquatique) et moyennée pour l’année en divisant par 365 jours; valeur utilisée pour calculer la concentration de la substance dans les biosolides (Cs). |
| Débit du STEU (D) | 1 110 500 | L/jour | Cette valeur est basée sur le même volume de dilution quotidien que celui utilisé pour le scénario en milieu aquatique, et suppose un facteur de dilution de 10; valeur utilisée pour calculer la concentration de la substance dans les biosolides (Cs). |
| Variable | Valeur | Unité | Autres commentaires |
|---|---|---|---|
| Concentration de la substance dans les biosolides (Cs) | 49,54-109,0 | mg/kg poids sec | La Cs est déterminée au moyen de l’équation suivante : Avec Qs (kg/jour) est la masse de substance rejetée quotidiennement dans le STEU, Esorption est la fraction de la substance éliminée par sorption, D est le débit du STEU retenu, en L/jour, et PB est le taux de production de biosolides par litre d’eaux usées en mg/L. Voir les valeurs ci-dessous et dans le tableau B‑ 11. |
| Masse de substance rejetée quotidiennement dans le STEU (Qs) | 0,03 | kg/jour | Qs est calculé à partir de la quantité de substance rejetée annuellement à l’installation, multipliée par le facteur d’émission (provenant d’un scénario en milieu aquatique) et moyennée pour l’année en divisant par 365 jours; valeur utilisée pour calculer la concentration de la substance dans les biosolides (Cs). |
| Débit du STEU (D) | 2 269 700 | L/jour | Cette valeur est basée sur le même volume de dilution quotidien que celui utilisé pour le scénario en milieu aquatique, et suppose un facteur de dilution de 10; valeur utilisée pour calculer la concentration de la substance dans les biosolides (Cs). |
| Variable | Valeur | Unité | Commentaires |
|---|---|---|---|
| Concentration de la substance dans les biosolides (Cs) | 47,71-104,96 | mg/kg poids sec | La Cs est déterminée au moyen de l’équation suivante : Avec Qs (kg/jour) est la masse de substance rejetée quotidiennement dans le STEU, Esorption est la fraction de la substance éliminée par adsorption, D est le débit du STEU retenu, en L/jour, et PB est le taux de production de biosolides par litre d’eaux usées en mg/L. Voir les valeurs ci-dessous et dans le tableau B‑ 11. |
| Masse de substance rejetée quotidiennement dans le STEU (Qs) | 0,10 | kg/jour | Qs est calculé à partir de la quantité de substance rejetée annuellement à l’installation, multipliée par le facteur d’émission (provenant d’un scénario en milieu aquatique) et moyennée pour l’année en divisant par 365 jours; valeur utilisée pour calculer la concentration de la substance dans les biosolides (Cs). |
| Débit du STEU (D) | 8 696 900 | L/jour | Cette valeur est utilisée pour représenter le débit au 10e percentile du plan d’eau récepteur associé au STEU dans lequel l’installation rejette la substance; cette valeur est basée sur le volume de dilution quotidien utilisé pour le scénario en milieu aquatique, en supposant un facteur de dilution de 10; valeur utilisée pour calculer la concentration de substance dans les biosolides (Cs). |
Annexe C. Approche de classification des risques écologiques des substances organiques (CRE)
La CRE est une approche basée sur le risque qui tient compte de plusieurs paramètres liés au danger et à l’exposition et d’une pondération de différents éléments de preuve pour le classement du risque. Les différents éléments de preuve sont combinés pour distinguer les substances présentant une puissance faible ou élevée (danger) et un potentiel d’exposition faible ou élevé dans divers milieux. Une telle approche permet de réduire l’incertitude globale de la caractérisation du risque comparativement à une approche qui reposerait sur un paramètre unique dans un seul milieu (p. ex., la concentration létale médiane [CL50]). Dans cette section, les paragraphes suivants résument l’approche, qui est décrite en détail dans ECCC (2016).
Les données sur les propriétés physico-chimiques, le devenir (les demi-vies chimiques dans divers milieux et biotes, les coefficients de partage et la bioconcentration dans les poissons), l’écotoxicité aiguë chez les poissons et le volume de substance importée ou produite au Canada proviennent de la littérature scientifique, de bases de données empiriques (p. ex. Boîte à outils QSAR de l’OCDE 2016) et des réponses à des enquêtes menées en vertu de l’article 71 de la LCPE, ou bien ont été produites à l’aide des modèles de type QSAR (relation quantitative structure‑activité) et de devenir du bilan massique ou de bioaccumulation. Ces données ont servi à d’intrants pour d’autres modèles de bilan massique ou à compléter les profils de risque et d’exposition d’une substance.
Les profils de danger reposent principalement sur des paramètres tels que le mode d’action toxique, la réactivité chimique, les seuils de toxicité interne dérivés du réseau trophique, la biodisponibilité et l’activité chimique et biologique. Les profils d’exposition sont aussi basés sur plusieurs paramètres, dont les vitesses d’émission potentielles, la persistance globale et le potentiel de transport à grande distance. Les profils de danger et d’exposition ont été comparés aux critères de décision afin de classer les potentiels de danger et d’exposition de chaque substance organique comme faible, modéré ou élevé. D’autres règles (p. ex., constance de la classification, marge d’exposition) ont été appliquées afin d’améliorer les classements préliminaires du danger et de l’exposition.
Une matrice de risque a été utilisée pour attribuer à chaque substance un risque potentiel faible, moyen ou élevé, basé sur les classements du danger et de l’exposition. Les classements du risque potentiel obtenus avec la CRE ont été vérifiés en suivant une approche en deux étapes. La première étape consistait à faire passer de modéré ou élevé à faible la classification du risque dans le cas des substances dont la vitesse d’émission estimée dans l’eau est faible après traitement des eaux usées, représentant un potentiel d’exposition faible. La deuxième étape consistait à examiner la classification de faible potentiel de risque faible à l’aide de scénarios de risque à l’échelle locale relativement prudents (c.-à-d. dans la zone entourant directement la source ponctuelle de rejet), conçus pour être protecteurs de l’environnement, afin de déterminer si le classement du risque potentiel devrait être revu à la hausse.
La CRE est basée sur une approche pondérée pour réduire au minimum tout surclassement ou sous-classement du danger, de l’exposition et du risque subséquent. Une description détaillée des approches équilibrées suivies pour traiter d’incertitudes est présentée dans ECCC (2016). Voici une description de deux des domaines d’incertitude les plus importants. Des valeurs de toxicité aiguë empiriques ou modélisées erronées pourraient entraîner des modifications du classement du danger, en particulier dans le cas des paramètres reposant sur des valeurs de résidus dans les tissus (c.-à-d. mode d’action toxique), dont bon nombre sont des valeurs estimées à l’aide de modèles QSAR (boîte à outils QSAR de l’OCDE 2016). L’incidence d’une telle erreur est toutefois atténuée par le fait qu’une surestimation de la létalité médiane donnera lieu à une valeur prudente (protectrice) des résidus dans les tissus qui sera utilisée lors de l’analyse des résidus corporels critiques (RCC). L’erreur due à une sous‑estimation de la toxicité aiguë sera atténuée par le recours à d’autres paramètres du danger tels que la structure associée au mode d’action, à la réactivité ou à l’affinité de liaison aux œstrogènes. Les changements ou les erreurs touchant les quantités chimiques pourraient donner lieu à un classement de l’exposition différent, puisque les classements de l’exposition et du risque sont très sensibles aux taux d’émission et aux quantités utilisées. Les résultats de la CRE illustrent donc l’exposition et le risque au Canada, d’après les quantités actuellement utilisées, et pourraient ne pas représenter les tendances futures.
Annexe D. Expositions potentielles des humains à l’ADNNS dues aux milieux de l’environnement ou aux aliments
| Voie d’exposition | 0 à 5 mois, nourris aux prépa-rations | 6 à 11 moisb | 1 anc | 2 à 3 ansd | 4 à 8 anse | 9 à 13 ansf | 14 à 18 ansg | 19 ans et plush |
|---|---|---|---|---|---|---|---|---|
| Eau potablei | 1,38 | 0,88 | 0,34 | 0,30 | 0,24 | 0,19 | 0,19 | 0,22 |
| Aliments | s.o. | s.o. | s.o. | s.o. | s.o. | s.o. | s.o. | s.o. |
| Absorption totale | 1,38j | 0,88 | 0,34 | 0,30 | 0,24 | 0,19 | 0,19 | 0,22 |
Abréviations : s.o., sans objet
a Assumé peser 6,3 kg (Santé Canada 2015) et boire 0,826 L d’eau par jour (Santé Canada 1998). Il est assumé que les nourrissons âgés de moins d’un an ne consomment de l’eau potable que dans les préparations pour nourrissons et que ceux nourris au sein ne consomment pas d’eau potable.
b Assumé peser 9,1 kg (Santé Canada 2015) et boire 0,764 L d’eau par jour (Santé Canada 1998). Il est assumé que les nourrissons de moins d’un an ne consomment de l’eau potable que dans les préparations pour nourrissons et que ceux nourris au sein ne consomment pas d’eau potable.
c Assumé peser 11 kg (Santé Canada 2015) et boire 0,36 L d’eau par jour (Santé Canada 1998).
d Assumé peser 15 kg (Santé Canada 2015) et boire 0,43 L d’eau par jour (Santé Canada 1998).
e Assumé peser 23 kg (Santé Canada 2015) et boire 0,53 L d’eau par jour (Santé Canada 1998).
f Assumé peser 42 kg (Santé Canada 2015) et boire 0,74 L d’eau par jour (Santé Canada 1998).
g Assumé peser 62 kg (Santé Canada 2015) et boire 1,09 L d’eau par jour (Santé Canada 1998).
hAssumé peser 74 kg (Santé Canada 2015) et boire 1,53 L d’eau par jour (Santé Canada 1998).
i Une concentration maximale d’ADNNS, de DNNSCa et d’ADNNDS de 10,54 mg/L dans les eaux usées a été utilisée pour estimer l’absorption de ces substances due à l’eau potable.
j Absorption totale maximale par toutes les voies d’exposition.
Annexe E. Paramètres utilisés pour estimer l’exposition humaine au DNNSCa due à l’utilisation d’un lubrifiant en aérosol à usage général
L’exposition à un lubrifiant en aérosol à usage général contenant jusqu’à 5 % de DNNSCa a été estimée au moyen du modèle ConsExpo Web (ConsExpo Web 2016). Les hypothèses suivantes ont été faites : l’utilisateur était un adulte âgé de 19 ans ou plus, d’un poids corporel de 74 kg; vitesse d’inhalation de 15,1 m3/jour (Santé Canada 2015). Sauf indication contraire, les paramètres par défaut pour le modèle ConsExpo Web pour un lubrifiant pénétrant en pulvérisateur ont été choisis d’après la General Fact Sheet (RIVM 2014), la Cleaning Product Fact Sheet (RIVM 2018) et la documentation sur le modèle ConsExpo pour la pulvérisation (RIVM 2009). L’absorption par inhalation et par voie cutanée a été assumée de façon prudente être de 100 %.
| Scénario et voie d’exposition | Paramètres utilisés pour le modèle ConsExpo Web |
|---|---|
Lubrifiant en aérosol à usage général, inhalation | Modèle : exposition à la pulvérisation – pulvérisation Durée de la pulvérisation : 10 secondes (d’après le mode d’emploi du fabricant du produit) Durée d’exposition : 60 minutes (RIVM 2018) Fraction massique : 0,05 (FSS 2018) Volume de la pièce : 34 m3 (valeur par défaut pour un garage, RIVM 2014) Hauteur de la pièce : 2,5 m (RIVM 2014) Vitesse de renouvellement de l’air : 1,5/h (valeur par défaut pour un garage, RIVM 2014) Vitesse de production massique : 1,5 g/s (pour le lubrifiant pénétrant dans une bombe aérosol, RIVM 2009) Fraction atmosphérique : 0,2 (RIVM 2018) Masse volumique non volatile : 1,8 g/cm3 (RIVM 2018) Diamètre maximal des particules inhalées : 15 mm (RIVM 2018) Type de distribution granulométrique des aérosols : log-normale (diamètre médian : 23,3 mm, coefficient de variation arithmétique : 1,3, diamètre maximal : 50 mm; RIVM 2009) |
Lubrifiant en aérosol à usage général, voie cutanée | Modèle : contact direct avec le produit – taux constant Superficie exposée : 2185 cm2 (mains et avant-bras; Statistique Canada 2004 et EPA 2011) Fraction massique : 0,05 (FSS 2018) Vitesse de contact : 100 mg/min (RIVM 2018) Durée du rejet : 10 secondes (même durée que pour la pulvérisation) |
Annexe F. Tableau récapitulatif de la lecture croisée faite pour les paramètres d’effet sur la santé
| Facteur pris en compte | Justification |
|---|---|
| 1. Structure chimique. L’accent a été mis sur les analogues qui contenaient un cycle naphtalène, une ou plusieurs chaînes alkyles et un ou deux groupes sulfonates. | Les analogues qui ont une structure chimique similaire et/ou qui sont métabolisés par des voies similaires en produits de dégradation similaires devraient avoir des profils de toxicité similaires. Les analogues trouvés dont les métabolites toxiques connus ne devraient pas provenir de la métabolisation de la cible n’ont pas été pris en compte. |
| 2. Métabolites similaires (prévus ou observés). En utilisant les modèles OASIS TIMES pour l’auto-oxydation et le métabolisme in vivo et in vitro chez le rat, les analogues et les substances d’intérêt ont tous produit des profils métaboliques similaires. | Les analogues qui ont une structure chimique similaire et/ou qui sont métabolisés par des voies similaires en produits de dégradation similaires devraient avoir des profils de toxicité similaires. Les analogues trouvés dont les métabolites toxiques connus ne devraient pas provenir de la métabolisation de la cible n’ont pas été pris en compte. |
| 3. Propriétés physico-chimiques similaires. L’accent a été mis sur les structures chimiques dont la masse moléculaire, la solubilité dans l’eau et la pression de vapeur étaient similaires. | Les analogues qui ont des propriétés physico-chimiques similaires peuvent avoir des profils de toxicologie et une biodisponibilité similaires. |
| 4. Disponibilité des données sur les effets sur la santé | Seuls les analogues disposant de données sur le danger de qualité suffisante et d’une couverture des voies et des durées d’exposition pertinentes dans le cadre des scénarios d’exposition ont été jugés applicables pour les besoins d’extrapolation. |
| Nom chimique | ADNNS | DNNSCa | ADNNDS |
|---|---|---|---|
Toxicité aiguëa, b | DL50 orale > 5 000 mg/kg p.c. | DL50 orale > 5 000 mg/kg p.c. | DL50 orale = 2 035 mg/kg p.c. |
Génotoxicité | Ames : négatif | Ames : négatif | Ames : négatif |
Études d’exposition par voie orale à court terme | DSENO = 55 mg/kg p.c./jour | DSENO = 55 mg/kg p.c./jour | DSENO = 55 mg/kg p.c./jour |
Études d’exposition subchronique par voie orale | DSENO = 100 mg/kg p.c./jour | DSENO = 100 mg/kg p.c./jour | DSENO = 100 mg/kg p.c./jour |
Études de toxicité pour la reproduction et le développement par voie orale | DSENO = 165 mg/kg p.c./jour | DSENO = 165 mg/kg p.c./jour | DSENO = 165 mg/kg p.c./jour |
Cancérogénicité | n.d. | n.d. | n.d. |
Abréviations : DL50, la dose létale requise pour tuer 50 % de la population; CL50, la concentration létale requise pour tuer 50 % de la population; n.d., non déterminé
a US EPA 2012
b ECHA 2018a
