Ébauche d’évaluation préalable groupe des éthers
Titre officiel : Ébauche d’évaluation préalable - Groupe des éthers
Numéros de registre du Chemical Abstracts Service :
- 60-29-7
- 101-84-8
- 115-10-6
- 34590-94-8
Environnement et Changement climatique Canada
Santé Canada
Mars 2021
Résumé
En vertu de l’article 68 ou de l’article 74 de la Loi canadienne sur la protection de l’environnement (1999) [LCPE], le ministre de l’Environnement et la ministre de la Santé ont procédé à l’évaluation préalable des quatre substances collectivement appelées « groupe des éthers » dans le Plan de gestion des produits chimiques. L’évaluation des substances de ce groupe a été jugée d’intérêt prioritaire, car elles satisfaisaient aux critères de catégorisation énoncés au paragraphe 73(1) de la LCPE ou en raison d’autres préoccupations pour la santé humaine. Leurs numéros de registre du Chemical Abstracts Service (NR CASNote de bas de page 1), leurs noms sur la Liste intérieure des substances (LIS), leurs noms communs et leurs abréviations apparaissent dans le tableau ci-dessous.
| NR CAS | Nom dans la LIS | Nom commun | Abréviation |
|---|---|---|---|
| 60-29-7 | oxyde de diéthyle | éther diéthylique | DEE |
| 101-84-8 | oxyde de diphényle | éther diphénylique | DPE |
| 115-10-6a | oxyde de diméthyle | éther diméthylique | DME |
| 34590-94-8 |
(2‑méthoxyméthyléthoxy) propanol |
éther méthylique de dipropylène glycol | DPGME |
a Cette substance n’a pas été désignée en vertu du paragraphe 73(1) de la LCPE, mais est incluse dans la présente évaluation, car elle est considérée d’intérêt prioritaire en raison d’autres préoccupations pour la santé humaine.
Le DEE, le DPE et le DME sont naturellement présents à de faibles concentrations dans certains aliments, mais le DPGME n’est pas naturellement présent dans l’environnement. Les quatre substances du groupe des éthers ont été visées par des enquêtes menées en vertu de l’article 71 de la LCPE. Les renseignements soumis indiquent que le DEE et le DPE ne sont pas fabriqués au Canada au-delà du seuil de déclaration de 100 kg, tandis que 100 000 à 1 000 000 kg de DME et 10 000 à 100 000 kg de DPGME ont été synthétisés au Canada en 2011. Les quatre substances ont également été importées au Canada en quantités allant de 487 199 à 1 287 772 kg. Les utilisations déclarées sont très variées, la plupart des substances étant utilisées dans divers secteurs : assainisseurs d’air, automobile, avions et transports, nettoyage et ameublement, carburants et produits connexes, extraction du pétrole et du gaz naturel, peintures et revêtements.
Au Canada, les substances du groupe des éthers peuvent également être utilisées comme composants dans les matériaux d’emballage alimentaire, les auxiliaires technologiques alimentaires, les agents technologiques alimentaires, les ingrédients médicinaux ou non médicinaux dans les désinfectants, les médicaments à usage humain ou vétérinaire et les produits de santé naturels, les cosmétiques et divers autres produits de consommation, et comme formulants dans les produits antiparasitaires.
Les risques pour l’environnement associés aux quatre substances du groupe des éthers ont été caractérisés selon l’approche dite Classification du risque écologique (CRE) des substances organiques, laquelle est une méthode fondée sur le risque qui tient compte de plusieurs paramètres liés au danger et à l’exposition, et sur une pondération de multiples éléments de preuve. Les profils des dangers reposent principalement sur des paramètres liés au mode d’action toxique, à la réactivité chimique, aux seuils de toxicité interne établis dans le réseau trophique, à la biodisponibilité et à l’activité chimique et biologique. Parmi les paramètres pris en compte pour les profils d’exposition figurent la vitesse d’émission potentielle, la persistance globale et le potentiel de transport sur de grandes distances. Une matrice de risque est utilisée pour attribuer aux substances un degré faible, moyen ou élevé de préoccupation potentielle, selon leurs profils de danger et d’exposition. D’après les résultats de la CRE, il est improbable que les substances du groupe des éthers soient nocives pour l’environnement.
Compte tenu de tous les éléments de preuve contenus dans la présente ébauche d’évaluation préalable, le DEE, le DPE, le DME et le DPGME présentent un faible risque d’effets nocifs pour l’environnement. Il est proposé de conclure que le DEE, le DPE, le DME et le DPGME ne satisfont pas aux critères énoncés aux alinéas 64a) ou 64b) de la LCPE, car ils ne pénètrent pas dans l’environnement en une quantité ou concentration ou dans des conditions de nature à avoir, immédiatement ou à long terme, un effet nocif sur l’environnement ou sur la diversité biologique, ou à mettre en danger l’environnement essentiel pour la vie.
Pour la population générale au Canada, les sources principales d’exposition aux substances du groupe des éthers sont l’utilisation de produits de consommation qui contiennent ces substances, ainsi que les milieux environnementaux et les aliments. Nous avons choisi les scénarios qui donnent les niveaux d’exposition les plus élevés pour caractériser l’exposition potentielle des Canadiens aux substances du groupe des éthers par l’utilisation de produits de consommation, les milieux environnementaux et les aliments.
Selon les renseignements disponibles, la population générale devrait être exposée au DEE par les milieux environnementaux et par l’utilisation de divers produits de consommation tels que les lotions corporelles, les produits contre les cors et les cals, et les liquides de démarrage automobile. D’après des études en laboratoire, les effets les plus critiques du DEE étaient les changements de poids corporel, la toxicité hépatique et l’augmentation de la mortalité en cas d’exposition orale, et la toxicité hépatique en cas d’exposition par inhalation. Une substance structurellement similaire, l’éther diisopropylique (DIPE), a également été utilisée pour éclairer l’évaluation des effets du DEE sur la santé.
On prévoit que la population générale sera exposée au DPE par les milieux environnementaux et en raison de son utilisation potentielle comme aromatisant alimentaire, et de l’utilisation de divers produits de consommation tels que les désodorisants et les crèmes pour les mains. Sur la base d’études en laboratoire, les effets les plus critiques de l’exposition au DPE par voie orale et par inhalation à long terme étaient la modification du poids corporel.
L’exposition de la population générale au DME devrait se faire via les milieux environnementaux et l’utilisation de divers produits tels que les écrans solaires en aérosol. Sur la base d’études en laboratoire, l’effet critique du DME était la diminution du taux de survie chez les rats exposés par inhalation à long terme.
Bien que l’utilisation de produits de consommation puisse entraîner une exposition potentielle par inhalation et par voie cutanée au DPGME, l’exposition à cette substance a été caractérisée qualitativement, car on juge qu’elle présente un faible potentiel de danger. Aucune des études disponibles n’a trouvé que le DPGME induisait un effet nocif. Une substance structurellement similaire, l’éther méthylique de propylène glycol (PGME), a également été utilisée pour éclairer l’évaluation des effets du DPGME sur la santé.
Si on compare les niveaux d’exposition au DEE, au DPE et au DME par l’environnement et les produits de consommation, ainsi que l’exposition au DPE par les aliments en raison de son utilisation potentielle comme aromatisant alimentaire, aux niveaux auxquels des effets sur la santé se produisent, on obtient des marges jugées adéquates pour compenser des incertitudes dans les bases de données sur les effets sur la santé et l’exposition. On juge que le DPGME présente un faible potentiel de danger, et le risque pour la santé humaine est jugé faible.
À la lumière des renseignements contenus dans la présente ébauche d’évaluation préalable, il est proposé de conclure que le DEE, le DPE, le DME et le DPGME ne satisfont pas aux critères de l’alinéa 64c) de la LCPE, car ils ne pénètrent pas dans l’environnement en une quantité ou concentration ou dans des conditions de nature à constituer un danger au Canada pour la vie ou la santé humaines.
Il est proposé de conclure que le DEE, le DPE, le DME et le DPGME ne satisfont à aucun des critères énoncés à l’article 64 de la LCPE.
1. Introduction
En vertu de l’article 68 ou de l’article 74 de la Loi canadienne sur la protection de l’environnement (1999) [LCPE], le ministre de l’Environnement et la ministre de la Santé ont procédé à l’évaluation préalable des quatre substances collectivement appelées « groupe des éthers » dans le Plan de gestion des produits chimiques afin de déterminer si ces substances présentent ou peuvent présenter un risque pour l’environnement ou la santé humaine. L’évaluation des substances de ce groupe a été jugée d’intérêt prioritaire, car elles satisfaisaient aux critères de catégorisation énoncés au paragraphe 73(1) de la LCPE ou en raison d’autres préoccupations pour la santé humaine (ECCC, SC [modifié 2017]).
Les risques pour l’environnement occasionnés par les substances du groupe des éthers ont été caractérisés en suivant la démarche de Classification du risque écologique (CRE) des substances organiques (ECCC 2016a). La CRE décrit le danger d’une substance au moyen de paramètres clés, notamment le mode d’action toxique, la réactivité chimique, les seuils de toxicité interne dérivés du réseau alimentaire, la biodisponibilité et l’activité chimique et biologique, et tient compte de l’exposition possible des organismes dans les milieux aquatiques et terrestres en fonction de facteurs comme les vitesses d’émission potentielles, la persistance globale et le potentiel de transport atmosphérique à grande distance. Les divers éléments de preuve sont combinés afin de déterminer quelles substances nécessitent une évaluation plus poussée de leur potentiel d’effets nocifs sur l’environnement ou présentant une faible probabilité de tels effets.
Le DEE a été étudié par l’Agence de protection de l’environnement des États-Unis (USEPA) et la Commission du Sénat allemand d’étude des risques sanitaires posés par les produits chimiques dans les lieux de travail (Commission MAK). Le DPE a été étudié par la Commission européenne (CE), l’Agence européenne de sécurité des aliments (EFSA), le Comité mixe de l’Organisation pour l’alimentation et l’agriculture et de l’Organisation mondiale de la santé d’experts des additifs alimentaires (JECFA), la Commission MAK et l’USEPA. Le DME a été examiné par l’USEPA, la Commission MAK et l’EFSA. Le DPGME a été examiné par la Commission MAK, le ministère de la Santé de l’Australie (AJGH) et le Programme d’évaluation coopérative des produits chimiques de l’Organisation de coopération et de développement économiques (OCDE). Un rapport d’évaluation initiale (SIAR) de l’Ensemble de données de dépistage (SIDS) de l’OCDE est aussi disponible. Ces évaluations ont servi à étayer la caractérisation des effets sur la santé de la présente évaluation préalable.
Pour la présente ébauche d’évaluation préalable, nous avons pris en compte des renseignements sur les propriétés chimiques, le devenir dans l’environnement, les dangers, les utilisations et l’exposition, y compris des renseignements soumis par des parties intéressées. Nous avons tenu compte des données pertinentes publiées jusqu’en septembre 2019. Des données empiriques tirées d’études clés ainsi que des résultats obtenus à l’aide de modèles ont été utilisés pour arriver aux conclusions proposées.
La présente ébauche d’évaluation préalable a été préparée par le personnel des programmes d’évaluation des risques de la LCPE travaillant à Santé Canada et Environnement et Changement climatique Canada. Elle inclut des contributions d’autres programmes de ces ministères. Les parties de la présente évaluation préalable portant sur la santé humaine ont fait l’objet d’examens externes. Des commentaires sur les parties techniques concernant la santé humaine ont été reçus de Supratik Kar, Jerzy Leszczynski et Ole Jalob Nøstbakken de Risk Sciences International. La partie de l’évaluation du risque écologique repose sur le document de la CRE (publié le 30 juillet 2016), lequel a fait l’objet d’un examen externe par des pairs et d’une période de consultation publique de 60 jours. Bien que les commentaires externes aient été pris en compte, Santé Canada et Environnement et Changement climatique Canada demeurent responsables du contenu final et des conclusions de la présente ébauche d’évaluation préalable.
La présente ébauche d’évaluation préalable repose sur des renseignements permettant de déterminer si les substances satisfont aux critères énoncés à l’article 64 de la LCPE. Pour ce faire, nous avons étudié les renseignements scientifiques et les avons intégrés en suivant une démarche fondée sur le poids de la preuve et le principe de prudenceNote de bas de page 2. Dans le présent document, nous présentons ces renseignements essentiels et les éléments sur lesquels reposent les conclusions proposées.
2. Identité des substances
Les numéros de registre du Chemical Abstracts Service (numéro CAS), les noms dans la Liste intérieure des substances (LIS), les noms communs et les abréviations des diverses substances du groupe des éthers sont présentés dans le tableau 2-1. Dans le cadre de l’exercice de catégorisation, le DPGME a été considéré comme une substance distincte au sens de la LCPE (ECCC, SC [modifié 2017]). Cependant, en raison de son mélange d’isomères avec le substituant méthyle en position 1 ou 2, il est reconnu que cette substance possède les caractéristiques d’un UVCB (substance de composition inconnue ou variable, produit de réactions complexes ou matière biologique).
| NR CAS (abréviation) | Nom dans la LIS (autres noms) | Structure chimique et formule moléculaire | Masse moléculaire (g/mol) |
|---|---|---|---|
| 60-29-7 (DEE) | oxyde de diéthyle (éther diéthylique) | 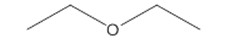 C4H10O C4H10O |
74,12 |
| 101-84-8 (DPE) | oxyde de diphényle (éther diphénylique) | 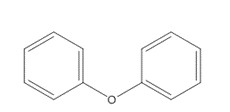 C12H10O C12H10O |
170,21 |
| 115-10-6 (DME) | oxyde de diméthyle (éther méthylique, diméthyléther) | 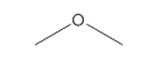 C2H6O C2H6O |
46,07 |
| 34590-94-8 (DPGMEa, b) | (2‑méthoxyméthyléthoxy) propanol (éther méthylique de dipropylène glycol) | 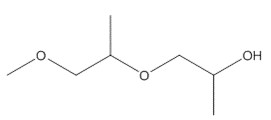 C7H16O3 C7H16O3 |
148,20 |
a Le DPGME possède les caractéristiques d’un UVCB (substance de composition inconnue ou variable, produit de réactions complexes ou matière biologique).
b La structure chimique de l’isomère 1 est représentée.
2.1 Choix des analogues et utilisation de modèles QSAR
Nous avons utilisé la méthode dite de « lecture croisée » faisant appel à des données sur des substances analogues et aux résultats des modèles de relations (quantitatives) structure-activité (modèles QSAR), le cas échéant, pour éclairer l’évaluation relative à la santé humaine. Les analogues choisis présentaient des structures ou des fonctionnalités similaires aux substances de ce groupe (p. ex., toxicocinétique et propriétés physico-chimiques similaires), et les données empiriques pertinentes les concernant pouvaient être utilisées pour une lecture croisée des substances pour lesquelles on disposait de peu de données empiriques. Ainsi, on a déterminé l’applicabilité des modèles QSAR au cas par cas. Dans les sections pertinentes du présent rapport, nous présentons plus de précisions sur les données de lecture croisée et les modèles QSAR choisis pour éclairer l’évaluation des effets des substances du groupe des éthers sur la santé humaine.
Le tableau 2-2 présente les données sur l’identité et la structure chimique des analogues utilisés pour étayer la présente évaluation. Les données sur les propriétés physico-chimiques et le danger des analogues apparaissent à l’annexe A.
| NR CAS(acronyme ou abréviation) | Nom sur la LIS ou autre nom (autres noms) | Structure chimique et formule moléculaire | Masse moléculaire (g/mol) |
|---|---|---|---|
| 108-20-3 (DIPE) | Oxyde de diisopropyle (éther diisopropylique) | 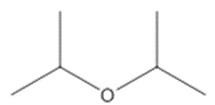 C6H14O C6H14O |
102,18 |
| 1320-67-8 (PGME) | 1-méthoxypropan-2-ol(éther monométhylique du propylèneglycol) | 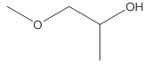 C4H10O2 C4H10O2 |
90,12 |
Le DIPE (NR CAS 108-20-3) a été utilisé comme analogue par l’USEPA pour éclairer l’évaluation des effets du DEE sur la santé humaine, et son utilisation a été jugée appropriée sur la base de similitudes structurelles, notamment la longueur de la chaîne, la position du groupe éther et le mécanisme d’action (USEPA 2014).
Le PGME (NR CAS 1320-67-8) a été utilisé comme analogue par l’OCDE pour éclairer l’évaluation des effets du DPGME sur la santé humaine, et son utilisation a été jugée appropriée sur la base de similitudes structurelles, des propriétés physico-chimiques et de la toxicocinétique (OCDE 2001).
3. Propriétés physiques et chimiques
le tableau 3-1 résume les données sur les propriétés physiques et chimiques des substances du groupe des éthers. Lorsque les données expérimentales sur une propriété étaient peu nombreuses ou inexistantes, nous avons utilisé des modèles QSAR (relations quantitatives structure-activité) pour obtenir des prédictions. D’autres propriétés physiques et chimiques sont présentées dans ECCC (2016b).
| Propriété | DEE | DPE | DME | DPGME | Référence |
|---|---|---|---|---|---|
| État physique | liquide | solide | gaz | liquide | S.O. |
| Point de fusion (°C) | -116 | 27 | -142 | -83 | ChemIDplus 1993- |
| Pression de vapeur (Pa) | 7,17 × 104 | 3,00 | 5,93 × 105 | 73,3 | ChemIDplus 1993- |
| Constante de la loi d’Henry (Pa m³/mol) | 1,25 × 102 | 28,3 | 1,01 × 102 a | 1,08 × 10−2a | ChemIDplus 1993- |
| Hydrosolubilité (mg/L) | 6,04 × 104 | 18,0 | 4,60 × 104 | 1,00 × 106 | ChemIDplus 1993- |
| Log Koe (sans dimension) | 0,89 | 4,21 | 0,1 | -0,35a | ChemIDplus 1993- |
Abréviations : S.O. = sans objet; Koe = coefficient de partage octanol-eau.
a Valeurs modélisées.
4. Sources et utilisations
On a signalé que de faibles concentrations de DEE, DME et DPE étaient naturellement dans certains aliments (Nijssen 2018; OMS 2004). Le DPGME n’existe pas naturellement dans l’environnement.
Toutes les substances du groupe des éthers ont été visées par des enquêtes menées en vertu de l’article 71 de la LCPE (Canada 2009, 2012). Nous résumons au tableau 4‑1 les données soumises sur les quantités totales des substances du groupe.
| Nom commun | Quantité fabriquée totale a (kg) | Quantité totale importée a (kg) | Année de déclaration | Référence de l’enquête |
|---|---|---|---|---|
| DEE | ND b | 914298 | 2011 | Environnement Canada, 2013 |
| DPE | ND b | 100000 – 1000000 | 2008 | Environnement Canada, 2009 |
| DME | 100000 – 1000000 | 487199 | 2011 | Environnement Canada, 2013 |
| DPGME | 10000 – 100000 | 1287772 | 2011 | Environnement Canada, 2013 |
Abréviation : ND = Valeur non déclarée.
a Les valeurs représentent les quantités déclarées lors des enquêtes menées en vertu de l’article 71 de la LCPE (Environnement Canada 2009, 2013). Veuillez consulter les enquêtes pour connaître les inclusions et exclusions particulières (annexes 2 et 3).
b Aucune quantité fabriquée n’a été déclarée pour la substance au‑delà du seuil de déclaration de 100 kg, pour l’année de déclaration en question.
Le tableau 4-2 résume les principales utilisations des substances du groupe des éthers selon les renseignements communiqués lors des enquêtes menées en vertu de l’article 71 de la LCPE (Environnement Canada 2009, 2013). Le tableau 4-3 présente les autres utilisations possibles des substances du groupe répertoriées au Canada.
| Principales utilisations a | DEE | DPE | DME | DPGME |
|---|---|---|---|---|
| Adhésifs et produits d’étanchéité | N | N | O | N |
| Assainisseurs d’air | N | N | O | O |
| Voiture, aéronef et transport | N | N | O | O |
| Entretien des voitures | N | N | N | O |
| Matériaux de construction | N | N | N | O |
| Nettoyage et entretien des meubles | N | N | O | O |
| Appareils électriques et électroniques | N | N | N | O |
| Matières explosives | O | N | N | N |
| Tissus, textiles et articles en cuir | N | N | N | O |
| Combustibles et produits, mélanges ou articles manufacturés connexes | O | N | N | O |
| Fluide caloporteur | N | O | N | N |
| Encre, encres en poudre et colorants | N | N | N | O |
| Lubrifiants et graisses | N | N | N | O |
| Extraction pétrolière et gazière | O | N | N | O |
| Peintures et revêtements | N | N | O | O |
| Soins personnels | N | N | O | N |
| Matériaux plastiques et caoutchoucs | N | N | N | O |
| Solvant | N | N | N | O |
Abréviations : O = oui, utilisation déclarée pour cette substance; N = non, utilisation non déclarée pour cette substance.
a Renseignements non confidentiels sur les utilisations déclarées en réponse aux enquêtes menées en vertu de l’article 71 de la LCPE (Environnement Canada, 2009, 2013). Veuillez consulter les enquêtes pour connaître les inclusions et exclusions particulières (annexes 2 et 3).
| Utilisation | DEE | DPE | DME | DPGME |
|---|---|---|---|---|
| Matériaux d’emballage alimentairea | N | N | N | Ob |
| Auxiliaires technologiques alimentairesa | O | N | O | N |
| Aromatisanta | N | O | N | N |
| Ingrédients médicinaux ou non médicinaux utilisés dans les désinfectants, et les médicaments à usage humain ou vétérinairec | O | N | O | O |
| Ingrédients des produits de santé naturels inscrits dans la BDIPSNd | O | O | O | O |
| Ingrédients médicinaux ou non médicinaux utilisés dans les produits de santé naturels homologuése | O | N | O | O |
| Substance utilisée dans les cosmétiques déclarée en vertu du Règlement sur les cosmétiquesf | O | O | O | O |
| Produit de formulation dans des produits antiparasitaires homologuésg | N | O | O | O |
Abréviations : O = utilisation indiquée pour cette substance; N = utilisation non indiquée pour cette substance.
a Communications personnelles, courriels de la Direction des aliments (DA), Santé Canada, au Bureau d’évaluation du risque des substances existantes (BERSE), Santé Canada, 2018 et 2019; sans référence.
b Substance utilisée comme solvant dans la fabrication d’enduits et d’encres d’impression qui ne présentent pas de risque de contact avec les aliments.
c Communication personnelle, courriel de la Direction des produits thérapeutiques (DPT), Santé Canada, au BERSE, Santé Canada, 2018; sans référence.
d BDIPSN (modifiée 2019); communications personnelles, courriels de la Direction des produits de santé naturels et sans ordonnance (DPSNSO), Santé Canada, au BERSE, Santé Canada, 2018; sans référence.
e BDPSNH (modifiée en 2018).
f Communication personnelle, courriel de la Direction de la sécurité des produits de consommation et des produits dangereux (DSPCPD), Santé Canada, au BERSE, Santé Canada, 2018; sans référence.
g Communication personnelle, courriel de l’Agence de réglementation de la lutte antiparasitaire (ARLA), Santé Canada, au BERSE, Santé Canada, 2018; sans référence.
Nous avons trouvé, en plus des utilisations indiquées ci‑dessus, d’autres utilisations des substances du groupe des éthers au Canada. Le DEE est présent dans les fluides de démarrage des automobiles (FDS 2017a). Le DPE est présent dans les désodorisants (FDS 2016a) et dans un nettoyant pour salle de bain (FDS 2017b). Le DME est utilisé dans les produits d’étanchéité, la craie à marquer ou en aérosol (FDS 2015a; FDS 2019a), les produits en aérosol pour la réparation de murs (FDS 2015a), la mousse isolante de bâtiment (FDS 2017d), la peinture en aérosol pour tissu (FDS 2018a), les produits de protection des pneus (FDS 2015b), les nettoyants pour les taches de sel (FDS 2015c) et les attractifs pour chevreuils (FDS 2018b). Le DPGME est présent dans une crème décapante pour salle de bain (FDS 2016e), un produit d’entretien du cuir (FDS 2016f), un produit de traitement des tissus (FDS 2014a) et un gaz poivré (FDS 2014b, 2016h).
5. Potentiel d’effets nocifs sur l’environnement
5.1 Caractérisation des risques pour l’environnement
Les risques pour l’environnement occasionnés par les substances du groupe des éthers ont été caractérisés en suivant la démarche de classification du risque écologique (CRE) des substances organiques (ECCC 2016a). La CRE est une méthode fondée sur les risques qui tient compte de plusieurs paramètres liés au danger et à l’exposition et qui repose sur la pondération de plusieurs éléments de preuve. Les divers éléments de preuve sont combinés afin de faire la distinction entre des substances plus ou moins puissantes et un potentiel plus ou moins élevé d’exposition dans divers milieux. Une telle approche permet de réduire l’incertitude globale de la caractérisation du risque comparativement à une approche qui reposerait sur un unique paramètre dans un seul milieu (p. ex. la concentration létale médiane, CL50). La méthode, décrite en détail par ECCC (2016a), est résumée dans ce qui suit.
Les données sur les propriétés physico-chimiques, le devenir (demi-vies chimiques dans divers milieux et biotes, coefficients de partage et bioconcentration dans les poissons), l’écotoxicité aiguë pour les poissons et les volumes de produits chimiques importés et fabriqués au Canada proviennent de publications scientifiques, de bases de données empiriques accessibles (p. ex., la boîte à outils QSAR de l’OCDE, 2016), et des réponses aux enquêtes menées en vertu de l’article 71 de la LCPE, ou ont été produites à l’aide de la modélisation de la relation (quantitative) structure-activité (QSAR) ou du devenir du bilan massique ou de la bioaccumulation. Ces données ont été utilisées comme données d’entrées d’autres modèles de bilan massique ou pour compléter les profils d’exposition et de danger de la substance.
Nous avons déterminé les profils de dangers en nous fondant principalement sur les mesures du mode d’action toxique, de la réactivité chimique, des seuils de toxicité internes basés sur les réseaux trophiques, de la biodisponibilité et de l’activité chimique et biologique. Les profils d’exposition sont également fondés sur plusieurs paramètres, dont le taux d’émission potentielle, la persistance globale et le potentiel de transport sur de grandes distances. Les profils de risque et d’exposition ont été comparés aux critères de décision afin de classer les risques et le potentiel d’exposition de chaque substance comme faible, moyen ou élevé. Des règles supplémentaires ont été appliquées (p. ex., constance de la classification, marge d’exposition) pour raffiner les classifications préliminaires du risque et de l’exposition.
Nous avons utilisé une matrice de risque pour classer le risque associé à chaque substance comme étant faible, modéré ou élevé, suivant la classification du danger et de l’exposition. Les risques classés selon la CRE ont été vérifiés par une démarche en deux étapes. La première étape consistait à modifier à la baisse la classification du risque (qui passe de modéré ou élevé à faible) des substances présentant un faible taux estimé d’émission dans l’eau après le traitement des eaux usées, ce qui constitue un faible risque d’exposition. La deuxième étape consistait à revoir les résultats de classification faibles à la lumière de scénarios de risque relativement prudents à l’échelle locale (c.-à-d. dans la zone à proximité immédiate du point de rejet) conçus pour protéger l’environnement, afin de déterminer si le risque devrait être reclassé à un niveau supérieur.
La CRE est fondée sur une approche pondérée pour réduire au minimum la possibilité d’une classification trop haute ou trop basse du danger, de l’exposition et du risque subséquent. Une description détaillée des approches équilibrées de traitement des incertitudes est présentée dans ECCC (2016a). Dans ce qui suit, nous décrivons deux des domaines d’incertitude les plus importants. Des valeurs de toxicité aiguë empiriques ou modélisées erronées pourraient conduire à des modifications du classement du danger, en particulier dans le cas des paramètres liés à des valeurs de résidus dans les tissus (le mode d’action toxique), dont un grand nombre sont prévues à partir de modèles QSAR (OCDE, QSAR Toolbox 2014). Toutefois, l’incidence de ce type d’erreur est atténuée par le fait qu’une surestimation de la létalité médiane donnera une valeur prudente (protectrice) des résidus dans les tissus qui servira à l’analyse critique des résidus corporels. L’erreur due à une sous-estimation de la toxicité aiguë sera atténuée grâce à l’utilisation d’autres paramètres de risque tels que le profil structurel du mode d’action, la réactivité ou l’affinité de liaison à l’estrogène. Les changements ou les erreurs touchant les quantités chimiques pourraient mener à un classement différent de l’exposition, les classements de l’exposition et du risque étant très sensibles à la vitesse d’émission et aux quantités utilisées. Les classements obtenus au moyen de la CRE reflètent donc l’exposition et le risque au Canada compte tenu des quantités utilisées actuellement (déterminées par estimations), mais pourraient ne pas rendre compte des tendances futures.
Les données essentielles et les facteurs à considérer, utilisés pour élaborer les profils spécifiques des substances du groupe des éthers, ainsi que les résultats de la classification du danger, de l’exposition et des risques figurent dans ECCC (2016b).
La classification des dangers et de l’exposition pour les quatre substances du groupe des éthers est résumée dans le tableau 5-1.
| Substance | Classification du danger (CRE) | Classification de l’exposition (CRE) | Classification du risque (CRE) |
|---|---|---|---|
| DEE | faible | faible | faible |
| DPE | faible | faible | faible |
| DME | faible | élevée | faible |
| DPGME | faible | faible | faible |
Compte tenu de la classification de danger faible et d’exposition faible selon les renseignements examinés par l’approche CRE, le DEE, le DPE et le DPGME ont été classés comme présentant un faible risque écologique. Il est peu probable que ces substances soient préoccupantes pour l’environnement au Canada.
D’après les renseignements examinés selon l’approche CRE, le DME a été classé comme substance présentant un potentiel d’exposition élevé, en raison de sa longue persistance globale et des importantes quantités importées chaque année, d’après les réponses fournies à une enquête menée en vertu de l’article 71 de la LCPE (Environnement Canada 2013). Le DME a été classé comme substance présentant un faible potentiel de danger, et donc, un faible risque écologique. Bien que les profils d’emploi actuels donnent lieu à un fort potentiel d’exposition, il est peu probable que le DME, compte tenu de son faible potentiel de danger, suscite des préoccupations pour l’environnement au Canada.
6. Potentiel d’effets nocifs sur la santé humaine
6.1 Évaluation de l’exposition
Nous présentons dans cette section les données sur l’exposition potentielle aux substances du groupe des éthers par les milieux naturels, par les aliments et par l’utilisation de produits de consommation. Étant donné que l’on juge que le DPGME a un faible potentiel de danger (voir la section 6.2.4), aucune estimation quantitative d’exposition de la population générale n’a été réalisée. En ce qui concerne le DEE, le DPE et le DME, les scénarios sentinelles donnant une exposition maximale pour chaque groupe d’âge sont présentés afin de caractériser le risque. Des détails supplémentaires sur les scénarios d’exposition figurent à l’annexe B.
6.1.1 DEE
Milieux naturels et aliments
Le DEE a déjà été trouvé dans l’environnement canadien et ailleurs dans le monde. Chan et coll. (1990) ont mesuré le DEE dans l’air intérieur de 12 maisons au Canada, et dans l’air ambiant autour. Lors du premier échantillonnage en 1986, ils avaient détecté du DEE dans les échantillons d’air intérieur de 5 des 12 maisons, avec une concentration maximale de 2 µg/m³, mais non dans les échantillons d’air environnant. Lors des prélèvements ultérieurs, en 1987, 6 maisons ont été échantillonnées, et on a détecté du DEE dans un échantillon d’air intérieur (647 µg/m³) et dans un échantillon d’air ambiant (24 µg/m³).Outre sa présence dans l’air, le DEE a été détecté séparément dans un réseau de puits de surveillance et dans un aquifère d’épandage, près de la décharge de Gloucester, en Ontario, avec une concentration maximale de 658 µg/L et une fréquence de détection de 68 % (Lesage et coll. 1990). En l’absence de données de surveillance des sols au Canada, nous avons modélisé la fugacité de niveau III à l’aide du logiciel ChemCAN v6.00 pour simuler les rejets de DEE au Canada. D’après les quantités fabriquées et importées totales combinées déclarées (Environnement Canada 2013), la concentration prévue de cette substance dans le sol a été jugée négligeable. Les concentrations maximales mesurées de DEE dans l’air intérieur et l’air ambiant autour des maisons canadiennes (647 µg/m³ et 24 µg/m³, respectivement) et dans un aquifère canadien (658 µg/L) ont été utilisées pour caractériser l’exposition des Canadiens au DEE par l’environnement. L’ingestion maximale estimée de DEE provenant des milieux environnementaux pour la population canadienne était de 0,44 mg/kg p.c./j, ce qui correspond à l’ingestion par les enfants de 1 an (voir l’annexe C pour de plus amples renseignements).
Ailleurs dans le monde, on a signalé la présence du DEE dans des échantillons d’air prélevés dans divers lieux, notamment à l’intérieur de voitures en Espagne, au Japon et en Allemagne (avec des concentrations atteignant 25,2 µg/m³), dans l’air intérieur d’un immeuble de plusieurs étages après des rénovations importantes en Allemagne (avec des concentrations atteignant 330 µg/m³) et dans l’air ambiant en Espagne (avec des concentrations atteignant 0,09 µg/m³) (Buters et coll. 2007; Cadena et coll. 2018; Chan et coll. 1990; Hippelein et coll. 2006; Moreno et coll. 2019; Rabaud et coll. 2003; Raboni et coll. 2015; Ramirez et coll. 2010; Smet et coll. 1999; Tokumura et coll. 2006; Veijanen et coll. 2011). Le DEE a également été détecté dans des échantillons d’eau provenant d’eaux souterraines en Alaska, au Colorado, au Connecticut, en Géorgie et au Kansas (avec des concentrations atteignant 17 µg/L) et dans une zone humide en Arizona (concentration de 0,1 µg/L) (Apodaca et coll. 2002; Gonthier et coll. 2011; Keefe et coll. 2004; Lesage et coll. 1990; Mullaney et coll. 1999; Pope et coll. 2002; Roy et coll. 2001).
Aucun renseignement définitif n’est disponible concernant l’utilisation du DEE dans les aliments vendus au Canada. On sait que le DEE est utilisé dans les auxiliaires technologiques alimentaires dans divers pays étrangers, et pourrait l’être au Canada. Si c’est le cas, l’exposition au DEE par les aliments, résultant de cette utilisation au Canada, devrait être négligeable (communications personnelles, courriels de la Direction des aliments (DA), Santé Canada, au BERSE, Santé Canada, février 2018 et septembre 2019; sans référence).
Le DEE serait également présent à l’état naturel à de faibles concentrations dans certains aliments (Nijssen 2018; OMS 2004). Les données sur la présence de DEE utilisées pour estimer l’exposition à celui‑ci par les aliments provenaient de la base de données sur les composés volatils dans les aliments (Nijssen 2018), qui faisait état d’une concentration de 0,15 ppm dans les pommes fraîches et d’une présence qualitative dans d’autres aliments. Pour chaque catégorie d’aliment et de boisson dans la base de données, la concentration maximale signalée pour le DEE a été appliquée de manière prudente afin de représenter la catégorie d’aliment (p. ex., la concentration maximale signalée dans les pommes de 0,15 ppm a été appliquée à toutes les pommes). Nous avons estimé l’exposition alimentaire au DEE au Canada due à sa présence naturelle dans les aliments en multipliant la consommation d’aliments par la quantité de DEE présente dans ces aliments. Les estimations de la consommation alimentaire moyenne et du 90e centile ont été basées sur l’ingestion alimentaire individuelle d’une journée « mangeurs seulement » déclarée par les répondants à l’Enquête sur la santé dans les collectivités canadiennes (ESCC) de 2004 pour les nourrissons jusqu’à 12 moisNote de bas de page 3, et dans l’ESCC de 2015 pour tous les autres groupes d’âge (Statistique Canada 2004a, 2015). La moyenne et le 90e centile de l’exposition alimentaire estimés de cette manière pour les différents groupes d’âge sont présentés dans le tableau 6‑1. Pour certains groupes d’âge, le nombre de répondants à l’enquête était insuffisant pour générer des données de consommation et les estimations correspondantes de l’exposition (communications personnelles, courriels de la DA, Santé Canada, au BERSE, Santé Canada, 2018 et 2019; sans référence).
| - | 0 à 5 mois | 6 à 11 mois | 1 an | 2 à 3 ans | 4 à 8 ans | 9 à 13 ans | 14 à 18 ans | 19 ans et plus |
|---|---|---|---|---|---|---|---|---|
| Moyenne | N.D. | 1,61 | 1,43 | 1,43 | 1,12 | 0,62 | 0,44 | 0,33 |
| 90e centile | N.D. | 3,86 | 2,50 | 2,35 | 1,97 | 1,00 | 0,80 | 0,57 |
Abréviation : N.D. = valeur non disponible.
L’ingestion estimée maximale de DEE résultant de sa présence naturelle dans les aliments était pour les enfants de 6 à 11 mois, soit 1,61 μg/kg p.c./j (moyenne) ou 3,86 μg/kg p.c./j (90e centile). La présence naturelle dans les aliments n’a pas été examinée plus à fond, car l’exposition potentielle est plus faible que l’exposition combinée à d’autres sources environnementales.
Produits de consommation
Le DEE est présent dans un liquide de démarrage pour moteurs à combustion (FDS 2017a) et dans des produits de soins personnels, comme des lotions corporelles (communication personnelle, courriel de la Direction de la sécurité des produits de consommation et des produits dangereux (DSPCPD), Santé Canada, au BERSE, Santé Canada, 2018; sans référence), et des produits pour éliminer les cors, les cals et les verrues (communications personnelles, courriels de la DPSNSO, Santé Canada, au BERSE, Santé Canada, 2018 et 2019; sans référence). En raison de sa très forte pression de vapeur (7,17 × 104 Pa), l’exposition au DEE découlant de l’utilisation de ces produits de consommation devrait surtout se faire par inhalation. On ne prévoit pas d’exposition par voie orale, et l’exposition systémique par voie cutanée devrait être minime par rapport à l’inhalation, car la peau n’absorbe pas facilement le DEE (Commission MAK 1996). Le tableau 6‑2 résume l’exposition estimée au DEE résultant de l’utilisation de ces produits, pour le groupe d’âge le plus exposé.
| Scénario d’utilisation du produit (groupe d’âge) | Concentration du produit | Exposition par inhalationa (mg/kg p.c./j) |
|---|---|---|
| Lotion corporelle, exposition quotidienne (19 ans et plus) | 3 %b | 3,2 × 10-2 |
| Produit contre les cors et les cals, par événement (9 à 13 ans) | 57 %c | 7,8 × 10-2 |
| Fluide de démarrage, par événement (19 ans et plus) | 60 %d | 0,63 |
a On présume une absorption à 100 % pour l’exposition par inhalation.
b Communication personnelle, courriel de la DSPCPD, Santé Canada, au BERSE, Santé Canada, 2018; sans référence.
c DailyMed 2019.
d FDS 2017a.
6.1.2 DPE
Milieux naturels et aliments
Le DPE a été détecté dans des milieux environnementaux au Canada et ailleurs dans le monde. On n’a trouvé aucune mesure de la concentration de DPE dans les milieux environnementaux canadiens, bien que Rogers et coll. (1986) aient mené une étude à la station de traitement des eaux usées (STEU) d’Iona Island, en Colombie-Britannique, où le DPE a été trouvé comme composant des fractions basiques et neutres des eaux usées et des boues. Ailleurs dans le monde, le DPE a été mesuré dans l’air intérieur des salons de coiffure en Espagne (avec des concentrations atteignant 130 µg/m³) (Ronda et coll. 2009), et dans l’eau de bassins de cours d’eau en Slovaquie (avec des concentrations atteignant 4,4 µg/L) (Slobodnik et coll. 2010).
Étant donné l’absence de données de surveillance canadiennes (où le DPE aurait été mesuré), nous avons réalisé une modélisation de la fugacité de niveau III à l’aide de ChemCAN v6.00 pour simuler les rejets de DPE au Canada. En combinant toutes les quantités fabriquées et importées déclarées (Environnement Canada 2013), nous prévoyons une concentration de 0,00628 µg/m³ dans l’air et de 0,0552 µg/L dans l’eau. Ces concentrations ont été utilisées pour caractériser l’exposition des Canadiens au DPE par les milieux environnementaux. La concentration prévue de cette substance dans le sol était de l’ordre du ng/g ce qui se traduit par une ingestion négligeable.
Aucune information définitive sur l’utilisation du DPE dans les aliments vendus au Canada n’est disponible. Le DPE est connu pour être employé comme aromatisant alimentaire ailleurs dans le monde, et il est possible que cette substance soit également présente comme aromatisant dans les aliments vendus au Canada (Burdock 2010). Le JECFA a évalué l’utilisation du DPE comme aromatisant alimentaire (OMS 2004), et a estimé l’ingestion par personne et par jour aux États‑Unis à 5 µg (environ 0,1 µg/kg p.c./j pour une personne de 60 kg), d’après les volumes de production annuels déclarés par l’industrie alimentaire dans les enquêtes sur les volumes produits (NAS 1989, IOFI 1995, Lucas 1999, cité dans OMS 2004). Le JECFA a conclu que cette substance ne présente « aucun problème de sécurité aux niveaux d’ingestion actuels lorsqu’elle est utilisée comme agent aromatisant ». Étant donné l’absence de données sur l’utilisation éventuelle du DPE comme aromatisant alimentaire dans les aliments vendus au Canada, il est acceptable d’utiliser l’estimation de l’ingestion par personne aux États-Unis, établie par le JECFA pour estimer l’exposition des Canadiens au DPE lorsqu’il est utilisé comme aromatisant alimentaire (communications personnelles, courriels de la DA, Santé Canada, au BERSE, Santé Canada, 2018 et 2019; sans référence).
Le DPE serait également présent à l’état naturel, à de faibles concentrations dans certains aliments (Nijssen 2018; OMS 2004). Les données sur la présence du DPE utilisées pour estimer l’exposition à cette substance par les aliments proviennent de la base de données sur les composés volatils dans les aliments (Nijssen 2018), qui fait état d’une concentration de 0,5 ppm dans les câpres et d’une présence qualitative de DPE dans d’autres aliments. Pour chaque catégorie d’aliment et de boisson dans la base de données, la concentration maximale signalée pour le DPE a été appliquée de manière prudente pour représenter la catégorie d’aliment (p. ex., la concentration maximale de 0,5 ppm signalée dans des câpres a été appliquée à toutes les câpres). L’exposition au DPE au Canada par les aliments, en raison de sa présence naturelle dans ceux-ci, a été estimée avec la même méthode que celle utilisée pour le DEE (voir la section 6.1.1). On estime ainsi l’exposition moyenne par voie alimentaire de 0,061 µg/kg p.c./j pour les Canadiens de 19 ans et plus. L’exposition alimentaire correspondante au 90e centile ne peut être estimée en raison du manque de données. Pour les autres groupes d’âge, le nombre de répondants à l’enquête était insuffisant pour générer des données de consommation et les estimations correspondantes de l’exposition (communications personnelles, courriels de la DA, Santé Canada, au BERSE, Santé Canada, 2018 et 2019; sans référence). La présence naturelle du DPE dans les aliments n’est pas prise en compte dans cette évaluation, car l’exposition potentielle est plus faible par rapport à l’exposition potentielle liée à l’utilisation d’agents technologiques alimentaires, et par rapport à l’exposition combinée provenant d’autres sources environnementales.
Le JECFA a estimé l’ingestion à 5 µg par personne et par jour aux États‑Unis (sur la base des volumes de production annuels déclarés par l’industrie alimentaire dans les enquêtes sur les volumes produits) pour calculer l’ingestion journalière de DPE par les agents technologiques alimentaires.
L’ingestion maximale estimée de DPE provenant des milieux environnementaux et des aliments pour la population canadienne était de 0,557 µg/kg p.c./j, ce qui correspond à l’ingestion pour les nourrissons de 6 à 11 mois (voir l’annexe C pour plus de détails).
Produits de consommation
Le DPE est présent dans divers produits de consommation, notamment dans les désodorisants domestiques utilisés à l’intérieur (FDS 2016a) et dans les crèmes pour les mains (communication personnelle, courriel de la DSPCPD, Santé Canada, au BERSE, Santé Canada, 2018; sans référence).
Les Canadiens peuvent être exposés quotidiennement au DPE lors de l’utilisation de désodorisant et de crème pour les mains. Le tableau 6‑3 résume l’exposition quotidienne estimée au DPE par inhalation lors de l’utilisation de ces produits pour le groupe d’âge le plus exposé.
Bien qu’il existe un potentiel d’exposition intermittente au DPE par voie cutanée et par inhalation (p. ex., par l’utilisation de nettoyants pour salle de bain) et un potentiel d’exposition quotidienne par voie cutanée (p. ex., par l’utilisation de crème pour les mains), ces expositions n’ont pas été quantifiées en raison de l’absence d’effets nocifs observés dans une étude de 13 semaines par voie cutanée chez le rat et d’une étude de 33 jours par inhalation chez le rat (voir la section 6.2.2 pour plus de détails)
| Scénario d’utilisation du produit (groupe d’âge) | Concentration du produit | Exposition par inhalationa (mg/kg p.c./j) |
|---|---|---|
| Désodorisant pour intérieur, exposition quotidienne (1 an) | 5 %b | 2,3 × 10-2 |
| Crème pour les mains, exposition quotidienne (19 ans et plus) | 5 %c | 1,7 × 10-2 |
Abréviation : S.O. = sans objet.
a On présume une absorption à 100 % pour l’exposition par inhalation.
b FDS 2016a.
c Communication personnelle, courriel de la DSPCPD, Santé Canada, au BERSE, Santé Canada, 2018; sans référence.
6.1.3 DME
Milieux naturels et aliments
Le DME a été déclaré à l’Inventaire national des rejets de polluants (INRP). Le rejet le plus élevé par une seule installation a été déclaré en 2017, soit 28 tonnes dans l’air, et les rejets de cette substance sont désignés comme étant des émissions fugitives ou de stockage (INRP 2017). SCREEN3 est un modèle de dispersion atmosphérique préliminaire, à distribution gaussienne, permettant d’évaluer les concentrations de polluants provenant de diverses sources (SCREEN3 2011). On a estimé que les émissions de DME provenaient d’une source étendue, d’après la base de données propres à l’installation. On a utilisé les données suivantes : un taux d’émission de 5,73 × 10-5 g/m2·s (d’après les données d’émissions atmosphériques de l’INRP et des renseignements propres à l’installation), une hauteur de récepteur de 1,74 m (Curry et coll. 1993), une superficie d’émission efficace de 130 m × 119 m et une hauteur de source de 6 m (jugement professionnel), ainsi que des données météorologiques urbaines et complètes (par défaut). Pour les événements d’exposition se produisant sur une année, on peut s’attendre à ce que la direction des vents dominants soit plus variable et non corrélée avec la direction du vent pour un événement unique. Par conséquent, on peut déterminer la concentration d’exposition maximale amortie sur un an en multipliant l’exposition maximale d’une heure par un facteur d’échelle de 0,08 pour les émissions par une source ponctuelle (USEPA 1992). Toutefois, ces facteurs d’échelle ne sont pas utilisés pour les émissions par une source non ponctuelle. Pour éviter la surestimation des expositions à des sources diffuses, un facteur de mise à l’échelle de 0,2 a été utilisé pour obtenir les concentrations d’exposition annuelle à partir de la valeur maximale d’une heure d’exposition, obtenue avec le modèle SCREEN3. On obtient ainsi une concentration estimée de 123 µg/m³ dans l’air ambiant, d’après la distance (119 m) où la concentration calculée est maximale.
À l’étranger, le DME a été détecté dans l’air intérieur des salons de coiffure en Espagne (avec des concentrations atteignant 90 µg/m³) et dans l’air ambiant en Suisse (avec une concentration moyenne de 0,60 µg/m³ et une concentration de 1,40 µg/m³ au 95e centile) (Gaeggeler et coll. 2008; Ronda et coll. 2009). Pellizzari et coll. (1982) ont également signalé la détection qualitative de DME dans 1 de 12 échantillons de lait maternel aux États‑Unis.
En l’absence de données canadiennes sur l’eau et le sol, nous avons modélisé la fugacité de niveau III à l’aide du programme ChemCAN v6.00 pour simuler les rejets de DME au Canada. En utilisant les quantités fabriquées et importées totales combinées déclarées (Environnement Canada 2013), nous avons prévu une concentration dans l’eau de 0,058 µg/L et une concentration jugée négligeable dans le sol.
Les concentrations dans l’air ambiant, d’après un modèle de dispersion dans l’air (123 µg/m³) et dans l’eau par modélisation de la fugacité (0,058 µg/L), ont été utilisées pour caractériser l’exposition des Canadiens au DME par les milieux environnementaux. L’ingestion maximale estimée de DME par les milieux naturels pour la population canadienne était de 0,089 mg/kg p.c./j, ce qui correspond à l’ingestion par les enfants de 1 an (voir l’annexe C).
Aucun renseignement définitif n’est disponible concernant l’utilisation du DME dans les aliments vendus au Canada. On sait que le DME est utilisé dans les auxiliaires technologiques alimentaires dans le monde. Il est également potentiellement utilisé dans les auxiliaires technologiques alimentaires au Canada. Si c’est le cas, l’exposition au DME par les aliments résultant de cette utilisation au Canada devrait être négligeable (communications personnelles, courriels de la DA, Santé Canada, au BERSE, Santé Canada, 2018 et 2019; sans référence).
Le DME est censément présent à l’état naturel à de faibles concentrations dans certains aliments tels que les pommes de terre et le vinaigre (Nijssen 2018; OMS 2004), mais sa présence n’a pas été quantifiée. Par conséquent, l’exposition au DME naturellement dans les aliments n’a pas été estimée dans la présente évaluation (communications personnelles, courriels de la DA, Santé Canada, au BERSE, Santé Canada, 2018 et 2019; sans référence).
Produits de consommation
Le DME est présent dans les produits en aérosol, y compris la craie à marquer en aérosol (FDS 2017c), les adhésifs (p. ex., adhésifs à usage général, temporaire pour le tissu, garniture de toit automobile) (Environnement Canada 2013; FDS 2018a), finition du bois d’intérieur (FDS 2019b), produit en aérosol pour la réparation des murs intérieurs (FDS 2015a), mousse pour l’isolation des bâtiments (FDS 2017d), protecteur de pneus (FDS 2015b), détachant (FDS 2015c), revêtement pour la doublure de caisse des camions (FDS 2018d), protecteur antirouille pour automobile (FDS 2017e), peinture pour tissu (FDS 2018b) et enduit de bijoux (FDS 2016b). On trouve également du DME dans les produits de soins personnels, notamment les laques, les colorants capillaires temporaires en aérosol, les autobronzants en aérosol (communication personnelle, courriel de la DSPCPD, Santé Canada, au BERSE, Santé Canada, 2018; sans référence), les désinfectants en mousse pour les mains (communications personnelles, courriels de la DPSNSO, Santé Canada, au BERSE, Santé Canada, 2018 et 2019; sans référence) et les écrans solaires en aérosol (communication personnelle, courriel de la DPT, Santé Canada, au BERSE, Santé Canada, 2018; sans référence). D’après les renseignements disponibles, la principale fonction du DME dans ces produits est d’agir comme propulseur.
Le DME est également un ingrédient d’un attractif pour animaux en aérosol qui peut être utilisé pour la chasse au chevreuil depuis une cache en hauteur ou à l’affût, sur des pistes olfactives, dans des éraflures simulées ou lorsqu’il est appliqué sur un leurre (FDS 2018c). L’exposition au DME pendant l’utilisation devrait être minime, car cette substance, présente dans les produits de consommation, n’est utilisée qu’à l’extérieur.
En raison de la pression de vapeur très élevée du DME (5,93 × 105 Pa) et de son état physique (gaz à la température normale), l’exposition au DME lors de l’utilisation des produits de consommation devrait se faire principalement par inhalation. L’exposition par voie orale ne devrait pas se produire et l’exposition par voie cutanée devrait être minime par rapport à l’inhalation, car le DME agit comme propulseur et retourne en phase gazeuse lorsqu’il est expulsé par la bonbonne ou le récipient. Le scénario de l’utilisation comme écran solaire par pulvérisation fournit les valeurs estimées maximales d’exposition quotidienne au DME avec une concentration dans le produit de 40 % (communication personnelle, courriel de la DPT, Santé Canada, au BERSE, Santé Canada, 2018; sans référence), et l’exposition par inhalation est estimée à 0,61 mg/kg p.c./j, où l’on suppose une absorption à 100 % par inhalation.
6.1.4 DPGME
Puisque que nous jugeons que le DPGME présente un faible potentiel de danger (voir la section 6.2.4), nous n’avons fait aucune estimation quantitative d’exposition de la population générale.
Milieux naturels et aliments
Nous n’avons trouvé aucune donnée de surveillance environnementale du DPGME au Canada. À l’étranger, le DPGME a été mesuré dans l’air intérieur de maisons suédoises (avec des concentrations atteignant 9,16 μg/m³) et dans les salles de stockage d’un musée allemand (avec une concentration moyenne de 12 μg/m³) (Choi et coll. 2010; Schieweck et coll. 2005). De plus, le DPGME a été mesuré à raison de 0,6 μg/L dans l’eau traitée d’une station de traitement des eaux usées en France (Bruchet et coll. 2007).
Bien que le DPGME puisse être utilisé comme solvant dans la fabrication d’enduits, de revêtements et d’encres d’impression utilisés dans les matériaux d’emballage alimentaire, ces matériaux ne présentent aucun risque de contact par les aliments, et on ne prévoit pas d’exposition au DPGME par les aliments (communications personnelles, courriels de la DA, Santé Canada, au BERSE, Santé Canada, 2018 et 2019; sans référence).
Produits de consommation
Le DPGME est présent dans les produits de consommation, notamment les désodorisants (FDS 2015d, 2017f), les encres (FDS 2016g), les dégraissants et les désinfectants (FDSM 2010, 2018e), les nettoyants (FDS 2016c, 2016d, 2015e), les convertisseurs de rouille (FDS 2016e), les crèmes décapantes pour salle de bain (FDS 2016f), les peintures et revêtements (FDS 2015f, 2018f), les restaurateurs de meubles (FDS 2010), les produits d’entretien du cuir (FDS 2016g), les lubrifiants (FDS 2015g), les produits automobiles (FDS 2015h), les produits de traitement des tissus (FDS 2014a) et le gaz poivré (FDS 2014b, 2016i). Le DPGME est également présent dans divers produits de soins personnels, dont les hydratants et les crèmes, les shampoings et les revitalisants, les nettoyants, le maquillage, le vernis à ongles et d’autres produits de coiffure (communication personnelle, courriel de la DSPCPD, Santé Canada, au BERSE, Santé Canada, février 2018; sans référence). L’utilisation de ces produits peut entraîner une exposition potentielle par inhalation et par voie cutanée au DGPME.
6.2 Évaluation des effets sur la santé
6.2.1 DEE
Le DEE a été évalué ailleurs dans le monde par l’USEPA (1987, 2009a, 2014) et la commission MAK (Commission MAK 1996). Un dossier REACH est également disponible (ECHA c2007-2019).
Toxicité à doses répétées
Des rats Sprague Dawley (8 par dose/sexe), des souris ICR (24 par dose/sexe) et des cobayes Hartley (8 par dose/sexe) ont été exposés à 1 000 ou 10 000 ppm (3 031, 30 031 mg/m³) de DEE pendant 24 h/j, pendant 35 jours par inhalation pour tout le corps (USEPA 2009a, Commission MAK 1996). Un groupe témoin était présent pour chaque groupe d’exposition. Aucun effet nocif n’a été observé chez les rats. Les seuls effets liés au traitement chez les cobayes ont été une diminution importante de la prise de poids corporel et un taux de mortalité élevé (25 %) dans le groupe ayant reçu la dose maximale. Les souris étaient l’espèce la plus sensible; à 10 000 ppm, 25 % des animaux étaient morts dans les 20 jours. À 1 000 ppm, le poids absolu et relatif du foie des souris avait augmenté de manière significative chez les mâles (26 % et 11 % respectivement), et à 10 000 ppm des changements similaires, mais plus prononcés, ont été observés chez les mâles et les femelles (76 % et 86 % chez les mâles, 59 % et 66 % chez les femelles). Des lésions dégénératives ont été constatées dans le foie des souris exposées à 10 000 ppm, mais pas à 1 000 ppm. Aucun autre organe n’a été touché chez les espèces testées. Sur la base de ces résultats, on a calculé des CSENO de 10 000 ppm (30 031 mg/m³) pour les rats et de 1 000 ppm (3 031 mg/m³) pour les cobayes, et une CMENO de 1 000 ppm pour les souris.
Dans une étude de toxicité subchronique par voie orale (USEPA 2009a), des rats Sprague Dawley (30 par dose/sexe) ont reçu par gavage du DEE dissous dans de l’huile de maïs à raison de 0, 500, 2 000 ou 3 500 mg/kg p.c./j pendant 90 jours. La mortalité est survenue dans les groupes ayant reçu les doses moyenne et élevée (7 % et 25 % respectivement), et on a observé une décoloration des poumons, du foie et de l’estomac, ainsi que des altérations de la muqueuse lisse de l’estomac. Une réduction significative de la prise de poids corporel a été observée chez les mâles des groupes exposés à la dose moyenne et à la dose élevée, et chez les femelles des groupes exposés à la dose élevée. Parmi les autres effets observés dans le groupe ayant reçu la dose élevée, mentionnons une diminution de la consommation alimentaire, une anesthésie légère, une diminution du poids absolu des organes et la modification de l’activité de l’alanine aminotransférase (ALT) et du taux de cholestérol. Compte tenu des effets sur le poids corporel, des modifications hépatiques et de la mortalité chez les rats à la dose de 2 000 mg/kg p.c./j, une DSENO de 500 mg/kg p.c./j a été établie.
Génotoxicité et cancérogénicité
À la lumière des renseignements disponibles, le DEE n’est pas jugé génotoxique (Commission MAK 1996, USEPA 2009a).
Aucune étude de cancérogénicité n’est disponible pour le DEE. On a plutôt utilisé le DIPE comme substance de substitution pour caractériser les dangers du DEE au niveau de l’examen préalable de l’EPA (USEPA 2014). L’EPA s’est basée sur les critères d’effet pour le développement et la génotoxicité à des doses répétées de DIPE pour éclairer l’évaluation des effets du DEE sur la santé, mais n’a pas utilisé les renseignements sur la cancérogénicité du DIPE. L’EPA n’a pas établi de dose de référence (DRf) pour la cancérogénicité du DEE en raison d’un manque de données appropriées (USEPA 2009a).
Toxicité pour la reproduction et le développement
Un certain nombre d’études menées sur des rats et des souris ont examiné les effets de l’inhalation du DEE sur le développement des fœtus, les paramètres du sperme et les organes reproducteurs mâles, avec des résultats contradictoires (Commission MAK 1996). Cependant, aucune de ces études ne suivait une ligne directrice établie et n’utilisait des concentrations proches ou supérieures aux valeurs rapportées pour la CL50 par inhalation (95 000-220 000 mg/m³). Ainsi, les effets observés peuvent être liés à l’hypoxie ou au stress maternel (Commission MAK 1996).
L’EPA (2014) a utilisé les résultats des études menées avec le DIPE pour éclairer l’évaluation des critères de toxicité du DEE pour le développement. Des rates Sprague Dawley gravides (22 par concentration) ont été exposées par inhalation à des vapeurs de DIPE à 430, 3 095 ou 6 745 ppm (1 800, 12 940 ou 28 200 mg/m³) pendant 6 h/j, aux jours de gestation (JG) 6 à 15. Les résultats ont montré que les mères présentaient une légère réduction de la prise de poids corporel et de la consommation alimentaire aux concentrations moyenne et élevée, et les différences par rapport aux témoins n’étaient statistiquement significatives que pendant la période de traitement (JG 6 à 16), ce qui semble indiquer une possible aversion pour la nourriture pendant la première semaine de l’étude (USEPA 2011). La seule observation faite chez les fœtus était une augmentation significative de la fréquence de l’ossification rudimentaire (ossification petite, discrète) ou de la présence de 14e côtes courtes (longueur inférieure à la moitié de la longueur des côtes précédentes) dans les groupes ayant reçu les concentrations moyenne et élevée. En l’absence d’autres anomalies fœtales, ces effets ne sont pas jugés nocifs.
6.2.2 DPE
Plusieurs organismes internationaux ont évalué le DPE, notamment l’EPA (USEPA 2010, 2017), le Conseil de l’UE (CE 2012), l’EFSA (2011, 2012), le JECFA (OMS 2004) et la commission allemande MAK (2004). En outre, il existe un dossier REACH pour le DPE (ECHA c2007-2019).
Toxicité à doses répétées
Nous avons trouvé plusieurs études à doses répétées dans lesquelles le DPE avait été administré par inhalation, par voie cutanée ou par voie orale. Dans certaines études, le DPE a été administré sous forme d’un mélange appelé Therminol A ou Dowtherm A, qui contient 73,5 % de DPE et 26,5 % de diphényle (NR CAS 92-52-4).
Des rats mâles (20 par concentration), des lapins mâles (4 par concentration) et des chiens mâles (2 par concentration) ont été exposés à 35 ou 71 mg/m³ de DPE dans un appareil d’exposition du corps entier pendant 7 h/j, 5 j/sem pendant 33 jours (USEPA 2017). Un troisième groupe de rats mâles et femelles (10 par sexe) a été exposé à 142 mg/m³ de DPE pendant 27 jours. On a constaté une irritation localisée des yeux et du nez à 71 mg/m³, mais aucun autre effet lié au traitement. En raison de l’absence d’effets nocifs, on a établi une CSENO de 142 mg/m³, qui était la concentration maximale de l’essai.
Dans une étude alimentaire de 13 semaines (Johnson et coll. 1992, CE 2012), des rats Sprague Dawley mâles et femelles (10 par dose/sexe) ont reçu 0, 200, 1 000 ou 5 000 ppm de DPE (0, 11,7, 60,7 ou 301,1 mg/kg p.c./j pour les mâles et 0, 14,5, 73,9 ou 334,8 mg/kg p.c./j pour les femelles). Des groupes supplémentaires de rats (10 par dose/sexe) ont été conservés pour observation pendant une période de récupération de 4 semaines après la période d’alimentation de 13 semaines. Les effets observés sur la santé comprenaient une diminution significative de la prise de poids corporel et de la consommation alimentaire à la dose maximale d’essai chez les mâles, et aux doses moyenne et élevée chez les femelles. Cependant, comme le poids corporel et la consommation alimentaire avaient augmenté de manière significative pendant la période de récupération, les auteurs ont attribué les effets antérieurs à l’insipidité de la substance dans les aliments, plutôt qu’à un effet lié au traitement. Compte tenu de l’incertitude associée à cette étude, et en raison de données insuffisantes fournies, une DSENO de 15 mg/kg p.c./j a été établie sur la base d’une diminution de la prise de poids corporel chez les femelles à 74 mg/kg p.c./j.
Dans une étude par voie cutanée de 13 semaines (Api et Ford 2003, USEPA 2017), des rats Sprague Dawley mâles et femelles (12 par dose/sexe) ont été exposés quotidiennement au DPE sous pansement semi-occlusif 6 h/j à 0, 100, 300 ou 1 000 mg/kg p.c./j. Aucune lésion histopathologique n’a été observée dans aucun des organes examinés. Une augmentation significative du poids relatif et absolu du foie a été observée chez les mâles à 300 mg/kg p.c./j, mais il ne s’agissait pas d’un effet proportionnel à la dose. À 1 000 mg/kg p.c./j, on a observé une augmentation significative du poids relatif du cerveau, des reins et du foie. Chez les femelles, le poids relatif du foie a augmenté de façon significative à 300 mg/kg p.c./j, et le poids relatif et absolu du foie a augmenté à la dose maximale d’essai. Compte tenu de l’absence d’effets histopathologiques sur les organes affectés, de l’absence de modification significative des paramètres sanguins ou urinaires et de l’absence de relation dose-réponse, les auteurs de l’étude ont conclu que le DPE n’induisait aucun effet systématique nocif et ont estimé que les modifications du poids des organes n’avaient pas de signification biologique. Ainsi, on a établi une DSENO à 1 000 mg/kg p.c./j, qui était la dose maximale d’essai.
Un mélange de Therminol A (73,5 % de DPE) a été administré par inhalation avec exposition du corps entier à des rats Sprague Dawley (25 par dose/sexe) sous forme d’aérosol à des concentrations de 0, 7,4, 37,5 ou 95,6 mg de DPE/m³ pendant 6 h/j, 5 j/sem pendant 7 ou 14 semaines (USEPA 2017). Chez les animaux exposés pendant 14 semaines, on a observé une réduction significative de la prise de poids corporel chez les mâles et les femelles à 95,6 mg de DPE/m³ pendant les semaines 2 à 6. On a observé une réduction du nombre de globules blancs chez les mâles dans les groupes exposés à des concentrations faible et moyenne, mais l’effet n’était pas proportionnel à la dose. En outre, on a constaté un poids relatif significativement plus faible du foie (chez les mâles et les femelles), du cerveau et de la rate (chez les femelles) dans le groupe ayant reçu la concentration maximale, mais cela peut être attribué à la réduction du poids corporel. Les auteurs ont attribué une CSENO de 37,5 mg de DPE/m³ sur la base des changements de poids corporel à 95,6 mg de DPE/m³.
Génotoxicité et cancérogénicité
Le DPE n’est pas jugé génotoxique, comme le démontrent plusieurs essais in vitro et in vivo (USEPA 2017).
Dans une étude de cancérogénicité de 13 mois, des rats albinos mâles (8 animaux/dose) ont reçu un régime alimentaire contenant du DPE à raison de 530 mg/kg p.c./j, ou sous forme de mélange de Therminol A (73,5 % de DPE) à 396 mg de DPE/kg p.c./j. Aucune tumeur ni aucun effet pathologique lié au traitement n’a été observé chez les animaux traités avec du DPE seul ou en mélange (OMS 2004).
Toxicité pour la reproduction et le développement
Dans une étude à doses répétées par voie alimentaire chez le rat, les organes reproducteurs des deux sexes ont été examinés au niveau macroscopique et histopathologique, et aucun effet nocif lié au traitement n’a été constaté (Johnson et coll. 1992, CE 2012).
Il n’existe aucune étude de toxicité pour la reproduction ou le développement du DPE lorsque celui‑ci ne fait pas partie d’un mélange.
Dans une étude de toxicité pour le développement (USEPA 2017, ECHA c2007-2019), un mélange de Therminol A contenant 73,5 % de DPE a été administré dans de l’huile de maïs à des rates Sprague Dawley gravides (24 animaux/dose) par gavage à 0, 36,75, 147 et 367,5 mg de DPE/kg p.c./j entre les JG 6 et 15. Les animaux ont été euthanasiés au JG 20 et on a examiné les mères et les fœtus pour vérifier les signes de toxicité clinique et pour le développement. Chez les mères, on a observé une diminution non significative de la prise de poids corporel à la dose la plus faible. À 147 mg de DPE/kg p.c./j, on a noté une réduction significative de la prise de poids corporel (20 % de moins que chez les témoins) et de la consommation alimentaire, ainsi qu’une salivation et des taches dans la zone ano-génitale. Ces effets étaient plus graves à la dose maximale d’essai, deux mères étant mortes à cette dose. Chez les fœtus, aucune toxicité manifeste n’a été observée à aucune des doses d’essai, y compris des malformations du squelette, des tissus mous ou des malformations externes. Ainsi, la DSENO pour la toxicité maternelle a été établie à 36,75 mg de DPE/kg p.c./j sur la base de la modification du poids corporel à 147 mg de DPE/kg p.c./j. La DSENO pour la toxicité pour le développement a été établie à 367,5 mg de DPE/kg p.c./j, ce qui était la dose maximale d’essai.
6.2.3 DME
Plusieurs organismes internationaux ont évalué le DME, notamment l’USEPA (2009b), l’EFSA (2009, 2015) et la commission MAK en Allemagne (Commission MAK 1990). En outre, il existe un dossier REACH pour le DME (ECHA c2007-2019). Dans un rapport initial sur la priorisation des substances chimiques produites en grande quantité en fonction de leur risque, l’EPA a recommandé que le DME soit classé comme faiblement prioritaire en raison de son faible danger pour la santé humaine (USEPA 2009b).
Toxicité à doses répétées
Comme le DME est un gaz à la température du corps, des animaux ont été exposés à la substance par inhalation dans toutes les études de toxicité à doses répétées qui étaient disponibles.
Aucun effet critique sur la santé par inhalation n’a été signalé dans deux études à court terme et une étude de toxicité subchronique chez le rat à des concentrations de DME atteignant 94 211 mg/m³ (Commission MAK 1990). Dans une étude de toxicité chronique (Commission MAK 1990), des rats Wistar mâles et femelles (25 par dose/sexe) ont été exposés à du DME à 0, 197, 1 964 ou 18 830 ppm (0, 371, 3 701 ou 35 480 mg/m³) pendant 6 h/j, 5 j/sem pendant 30 semaines. On n’a constaté aucun effet sur le poids corporel, la consommation alimentaire, les signes cliniques ou l’œil. Aucune anomalie dans l’hématologie ou l’analyse d’urine n’a été observée, sauf un niveau significativement plus élevé de l’activité de l’AST chez les mâles exposés à 1 964 ppm seulement et de l’activité de l’ALT chez les mâles et les femelles exposés à 18 830 ppm. En outre, on a observé une réduction significative du poids relatif du foie (8 % de moins que chez les témoins) chez les mâles ayant reçu la concentration maximale de l’essai.
Dans une étude de cancérogénicité de deux ans, réalisée selon les bonnes pratiques de laboratoire (Commission MAK 1990), des rats Crl:CD mâles et femelles (100 par dose/sexe) ont été exposés à des vapeurs de DME à 0, 2 000, 10 000 ou 25 000 ppm (0, 3 768, 18 842 ou 47 105 mg/m³) pendant 6 h/j, 5 j/sem pendant 104 semaines. Les résultats les plus notables étaient l’augmentation significative du poids corporel et la baisse non significative de la durée de vie des rats mâles dans les groupes aux concentrations moyenne et élevée à la fin de la période d’étude. Dans le groupe ayant reçu la concentration maximale, les mâles ont montré une diminution du nombre d’érythrocytes, une augmentation du poids de la rate et des signes de congestion de la rate après 6 mois, ainsi qu’une histologie osseuse normale. Dans le même groupe, les femelles ont montré une diminution du nombre d’érythrocytes après 3 mois. Ces changements n’ont toutefois pas été notés plus tard. Hormis les observations faites au niveau de la rate, on n’a observé aucun effet histopathologique dans d’autres organes. Le nombre de masses observées chez les rates était plus élevé dans tous les groupes étudiés que dans le groupe témoin, y compris la présence de tumeurs mammaires à la dose maximale d’essai. Toutefois, les auteurs de l’étude n’ont pas considéré cet effet comme étant lié au traitement, car la fréquence des masses et des tumeurs dans le groupe témoin était faible par rapport aux données historiques. Par conséquent, une CSENO de 2 000 ppm (3 768 mg/m³) a été établie en raison d’un taux de survie réduit chez les rats mâles aux concentrations moyenne et élevée.
Génotoxicité et cancérogénicité
Le DME n’est pas jugé génotoxique, comme l’ont démontré plusieurs essais in vitro (Commission MAK 1990, USEPA 2009b, ECHA c2007-2019).
Dans l’étude de cancérogénicité de 2 ans chez les rats décrite précédemment (Commission MAK 1990), on a estimé que le DME n’induisait pas d’effet cancérogène.
Toxicité pour la reproduction et le développement
Aucune étude de toxicité pour la reproduction n’a été trouvée pour le DME. De plus, on n’a constaté aucun effet nocif lors de l’examen macroscopique et histopathologique des organes reproducteurs mâles et femelles dans plusieurs études par inhalation à court et à long terme avec exposition répétée chez les rats et chez les hamsters.
Deux études sur la toxicité du DME pour le développement le rat sont disponibles (CIVO 1981, Haskell Labs 1983, USEPA 2009b, Commission MAK 1990), dans lesquelles des rates Wistar et Crl:CD gravides ont été exposées à du DME jusqu’à 28 000 ppm (52 758 mg/m³), pendant 6 h/j des JG 6 à 16. Aucune toxicité maternelle n’a été observée dans aucun des groupes traités. Aucune malformation des tissus mous liée au traitement n’a été observée chez les fœtus de tous les groupes traités. La fréquence de côtes lombaires surnuméraires (tant unilatérales que bilatérales) était significativement plus élevée dans les groupes traités que dans les groupes témoins, mais la signification biologique de cette observation a été jugée incertaine par les examinateurs de l’étude (Haskell Labs 1983, Commission MAK 1990). Des différences significatives dans l’ossification des phalanges des membres postérieurs ainsi que des vertèbres cervicales et thoraciques ont également été observées. Cependant, les auteurs et les examinateurs des études ont considéré que ces différences n’étaient pas liées au traitement, en raison de l’absence d’une relation concentration-réponse claire, et ils les ont attribuées à une variation normale de l’ossification chez cette souche d’animaux (Commission MAK 1990).
6.2.4 DPGME
Le DPGME a été évalué au niveau international par l’OCDE (2001) et la commission MAK d’Allemagne (Commission MAK 1993). Des études de l’ECETOC (Gribble 2005) et de la Cosmetic Ingredients Review (Robinson et coll. 2009) sur les effets des éthers de glycol sur la santé, y compris le DPGME, sont également disponibles. En outre, il existe un dossier REACH pour le DPGME (ECHA c2007-2019). Lors d’une réunion d’évaluation initiale (SIAM) de l’Ensemble de données de dépistage (SIDS), l’OCDE a recommandé que le DPGME soit classé comme substance faiblement prioritaire pour l’évaluation des risques, en raison de son faible profil de dangerosité (OCDE 2001). De même, dans une évaluation multichimique de niveau I des risques pour la santé humaine réalisée par le ministère de la Santé de l’Australie (AJGH 2018), le DPGME a été classé parmi les substances chimiques qui ne sont pas considérées comme présentant un risque déraisonnable pour la santé des travailleurs ou du grand public.
Toxicité à doses répétées
Des études de toxicité par voie orale, cutanée et par inhalation à doses répétées sont disponibles pour le DPGME.
Dans huit études distinctes par inhalation, des souris, des rats, des lapins, des cobayes et des singes exposés à des concentrations de DPGME atteignant 300 ppm (1 818 mg/m³) pendant 6 à 7 h/j pendant 2 à 31 semaines n’ont pas subi d’effets nocifs (OCDE 2001). Il convient de noter que la concentration de 300 ppm est la plus élevée possible pour les vapeurs de DPGME à la température et à la pression normales.
Dans une étude par voie orale à court terme (OCDE 2001), des rats Sprague Dawley (5 par dose/sexe) ont reçu par gavage 0, 40, 200 ou 1 000 mg/kg p.c./j de DPGME pendant 28 jours. La DSENO a été établie à 1 000 mg/kg p.c./j en raison de l’absence d’effets significatifs sur le plan biologique à la dose maximale d’essai.
Aucun effet nocif n’a été observé chez les rats Wistar mâles (8 par dose) exposés à 0, 100 ou 1 000 mg/kg p.c./j de DPGME par voie cutanée sous pansement occlusif et semi-occlusif pour 4 h/j, 5 j/sem, pendant 4 semaines (OCDE 2001). Dans une étude par voie cutanée semi-occlusive, des lapins mâles (5 à 7 par dose) ont été exposés à 0, 950, 2 850, 4 750 ou 9 510 mg/kg p.c./j de DPGME pendant 5 j/sem et 90 jours (OCDE 2001). On a observé une irritation cutanée mineure, une narcose et quelques décès chez les animaux exposés à 4 750 mg/kg p.c./j et plus. Par conséquent, la DSENO a été établie à 2 850 mg/kg p.c./j.
Génotoxicité et cancérogénicité
Plusieurs essais in vitro (OCDE 2001) ont montré que DPGME n’était pas génotoxique.
Aucune étude de cancérogénicité n’est disponible pour le DPGME. Cependant, les études de toxicité subchronique et chronique sur des rats, des lapins, des cobayes et des singes n’ont pas relevé de fréquence significative de tumeurs lorsque 300 ppm (la concentration maximale atteignable) de DPGME a été administré par inhalation pendant 7 h/j, 5 j/sem jusqu’à 31 semaines (OCDE 2001).
L’OCDE (2001) a utilisé un produit chimique substitut, le PGME, pour évaluer le potentiel cancérogène du DPGME dans le cadre d’une étude par inhalation de 2 ans sur des rats Fischer et des souris B6C3F1 qui furent exposés à 0, 300, 1 000 ou 3 000 ppm (0, 1 106, 3 686, 11 058 mg/m³) de PGME pendant 6 h/j, 5 j/sem (OCDE 2001). Aucun signe de cancérogénicité n’a été observé chez ces deux espèces à toutes les concentrations de l’essai, y compris la concentration maximale.
Toxicité pour la reproduction et le développement
Aucune étude de toxicité pour la reproduction n’est disponible pour le DPGME. Cependant, aucun effet marqué ou histopathologique n’a été observé dans les testicules ou les ovaires de rats et de lapins mâles et femelles exposés au DPGME par inhalation pendant 90 jours (OCDE 2001).
Aucune toxicité pour les mères ou les fœtus n’a été observée dans deux études dans lesquelles des rates Fischer 344 et des lapines néo-zélandaises gravides ont été exposées à des doses atteignant 300 ppm de DPGME par inhalation du corps entier aux JG 6-15 (rats) et aux JG 7-19 (lapins) pendant 6 h/j (OCDE 2001).
6.3 Caractérisation des risques pour la santé humaine
Les tableaux 6-4 à 6-6 énumèrent les valeurs d’exposition et de danger pertinentes pour le DEE, le DPE et le DME, ainsi que les marges d’exposition (ME) qui en résultent, pour la détermination du risque.
Une DSENO de 500 mg/kg p.c./j, basée sur les changements dans la prise de poids corporel, les effets sur le foie et l’augmentation de la mortalité chez les rats ayant reçu 2 000 ou 3 500 mg/kg p.c./j de DEE par gavage oral (USEPA 2009a), a été utilisée comme critère d’effet le plus pertinent pour l’exposition par voie orale. Il convient de noter que les doses moyenne et élevée sont supérieures à la DL50 du DEE par voie orale (1 568 mg/kg p.c.; USEPA 2014).
Une CMENO de 3 031 mg/m³ (DMENOaju = 4 256 mg/kg p.c./j) a été jugée le critère d’effet le plus pertinent pour l’exposition par inhalation, d’après une augmentation du poids du foie à 3 031 mg/m³ de DEE et l’augmentation de la dégénérescence du foie et de la mortalité à 30 031 mg/m³ de DEE chez les souris exposées par inhalation pendant 35 jours (USEPA 2009a). La souris était l’espèce la plus sensible dans cette étude (par rapport au rat et au cobaye), et tous les animaux ont été exposés en continu pendant 35 jours. L’exposition à la lotion corporelle devrait se faire par inhalation, principalement en raison de la pression de vapeur élevée du DEE. Une comparaison avec l’étude de 35 jours par inhalation a donc été jugée appropriée.
Sur la base des paramètres prudents utilisés pour estimer l’exposition, les ME résultantes pour la voie orale et l’inhalation sont jugées adéquates pour compenser les incertitudes dans les bases de données sur l’exposition au DEE et les effets sur la santé.
| Substance | Scénario d’exposition | Exposition systémique (mg/kg p.c./j)a | Critère d’effet critique (mg/kg p.c./j) | Effet critique | ME |
|---|---|---|---|---|---|
| DEE | Milieu environnemental, exposition quotidienne (enfants de 1 an)e | 0,44b | DSENO = 500 (étude par gavage oral de 13 semaines chez le rat) | Changements dans la prise de poids corporel, effets sur le foie et mortalité accrue chez les rats à 2 000 mg/kg p.c./j | 1136 |
| DEE | Lotion corporelle, exposition quotidienne (19 ans et plus) | 3,2 × 10-2 c | DMENOaju = 4 256d (étude par inhalation de 35 jours chez la souris) | Toxicité du foie chez les souris, à la dose ajustée de 4 256 mg/kg p.c./jd | 133000 |
| DEE | Produit contre les cors et les cals, par événement (9 à 13 ans) | 7,8 × 10-2 c | DMENOaju = 4 256d (étude par inhalation de 35 jours chez la souris) | Toxicité du foie chez les souris, à la dose ajustée de 4 256 mg/kg p.c./jd | 54564 |
| DEE | Fluide de démarrage, par événement (19 ans et plus) | 0,63 c | DMENOaju = 4 256d (étude par inhalation de 35 jours chez la souris) | Toxicité du foie chez les souris, à la dose ajustée de 4 256 mg/kg p.c./jd | 6756 |
Abréviations : ME = marge d’exposition; DSENO = dose sans effet nocif observé; DMENOaju = dose minimale entraînant un effet nocif observé, valeur ajustée.
a L’exposition systémique est calculée à partir de la « dose externe le jour de l’exposition », à l’aide du logiciel ConsExpo Web (2016), qui présume prudemment une absorption de 100 % par inhalation et par voie cutanée. Cette valeur représente la somme des doses externes pour plusieurs événements qui ont lieu la même journée, le cas échéant. Voir l’annexe C pour de plus amples renseignements.
b Représente la somme de l’exposition par voie orale et par inhalation.
c Représente l’exposition par inhalation.
d On calcule les critères d’effet critiques en convertissant les concentrations sans effet nocif observé (CSENO) ou les concentrations minimales entraînant un effet nocif observé (CMENO) d’après les études de toxicité par inhalation en doses internes qui tiennent compte du taux d’inhalation des animaux (m³/j), du poids corporel (kg) et des facteurs d’ajustement temporel (Durée de l’exposition en heures/24; jours d’exposition dans une semaine/7), sauf indication contraire. Les taux d’inhalation des animaux ont été établis d’après l’équation présentée dans Bide et coll. (2000). Le poids corporel des animaux a été établi d’après les rapports d’étude lorsqu’ils étaient disponibles; sinon, on a utilisé la valeur par défaut présentée dans Meek et coll. (1994).
e L’exposition au DEE par les aliments au Canada, en raison de sa présence possible dans les auxiliaires technologiques alimentaires, devrait être négligeable. La présence naturelle dans les aliments n’est pas prise en compte, car l’exposition potentielle est plus faible que l’exposition combinée due à d’autres sources environnementales.
Une DSENO de 15 mg/kg p.c./j, basée sur les changements dans la prise de poids corporel chez les rates exposées à 74 mg/kg p.c./j de DPE dans les aliments pendant 13 semaines (Johnson et coll. 1992, CE 2012), a été jugée le critère d’effet le plus pertinent pour l’exposition par voie orale. La réduction de la consommation alimentaire due à des problèmes de sapidité de la substance a peut-être contribué à la diminution de la prise de poids corporel observée. Cependant, les données disponibles pour valider cette hypothèse sont limitées. En outre, des effets similaires ont été observés chez des rates gravides exposées à un mélange contenant du DPE par gavage oral, et une réduction significative de la prise de poids corporel avait été observée à partir de 147 mg/kg p.c./j de DPE. Ainsi, une DSENO de 15 mg/kg p.c./j est jugée appropriée, car elle assurerait la protection contre tout effet potentiel sur le poids corporel qui pourrait se produire à des doses plus élevées.
Une CSENO de 37,5 mg de DPE/m³ (DSENOaju = 6 mg/kg p.c./j), basée sur les variations du poids corporel chez les rats exposés par inhalation à 95,6 mg de DPE/m³ pendant 6 h/j, 5 j/sem pendant 13-14 semaines (USEPA 2017), a été considérée comme étant le critère d’effet le plus pertinent pour l’exposition par inhalation à long terme. Cette étude a été jugée appropriée pour caractériser le risque posé par l’exposition aux crèmes pour les mains, car la voie d’exposition la plus probable pour cette substance serait par inhalation en raison de sa pression de vapeur modérée et de son faible taux d’absorption cutanée (environ 20 % de 1 000 mg/kg p.c./j de DPE étaient absorbés par les rats sur 72 h, comme il est décrit dans Api et Ford 2003, USEPA 2017), et l’absence d’effets nocifs chez les rats lorsque du DPE était administré par voie cutanée jusqu’à 1 000 mg/kg p.c./j pendant 13 semaines.
Pour caractériser le risque lié à l’exposition par voie cutanée et par inhalation à court terme, on a également tenu compte du fait qu’on n’avait pas noté d’effets nocifs chez les rats lorsque le DPE était administré par voie cutanée jusqu’à 1 000 mg/kg p.c./j pendant 13 semaines, et qu’il n’y avait également pas d’effets nocifs par inhalation jusqu’à la concentration maximale d’essai de 142 mg/m³ pendant 27 jours. Par conséquent, on n’a pas calculé de marges d’exposition pour l’exposition par voie cutanée et par inhalation à court terme, et le risque pour la santé humaine est jugé faible, selon les scénarios pertinents.
Par conséquent, les ME résultantes pour les scénarios d’exposition par voie orale et par inhalation à long terme sont jugées adéquates pour compenser les incertitudes dans les bases de données sur les effets sur la santé et l’exposition au DPE.
| Substance | Scénario d’exposition | Exposition systémique (mg/kg p.c./j)a |
Critère d’effet critique (mg/kg p.c./j) |
Effet critique | ME |
|---|---|---|---|---|---|
| DPE | Milieu environnemental et aliments, exposition quotidienne (enfants de 6 à 11 mois) | 5,6 × 10-4 b | DSENO = 15 (étude par le régime alimentaire chez le rat de 13 semaines) | Changements dans la prise de poids corporel chez les rates à 74 mg/kg p.c./j | 27000 |
| DPE | Désodorisant domestique, exposition quotidienne (enfants de 1 an) | 2,3 × 10-2 c | DSENOaju = 6 d (étude par inhalation chez le rat de 14 semaines) | Changements dans la prise de poids corporel chez le rat à la dose ajustée de 15 mg/kg p.c./jd | 261 |
| DPE | Crème pour les mains, exposition quotidienne (19 ans et plus) | 1,7 × 10-2 c | DSENOaju = 6 d (étude par inhalation chez le rat de 14 semaines) | Changements dans la prise de poids corporel chez le rat à la dose ajustée de 15 mg/kg p.c./jd | 353 |
Abréviations : ME = marge d’exposition; DSENOaju = dose sans effet nocif observé, avec valeur ajustée.
a L’exposition systémique est calculée à partir de la « dose externe le jour de l’exposition », à l’aide du logiciel ConsExpo Web (2016), qui présume prudemment une absorption à 100 % par inhalation et par voie cutanée. Cette valeur représente la somme des doses externes pour plusieurs événements qui ont lieu la même journée, le cas échéant. Voir l’annexe C pour de plus amples renseignements.
b Représente la somme de l’exposition par voie orale et par inhalation.
c Représente l’exposition par inhalation.
d On calcule les critères d’effet critiques en convertissant les concentrations sans effet nocif observé (CSENO) ou concentrations minimales entraînant un effet nocif observé (CMENO) d’après les études de toxicité par inhalation en doses internes qui tiennent compte du taux d’inhalation des animaux (m³/j), du poids corporel (kg) et des facteurs d’ajustement temporel (heures d’exposition/24; jours d’exposition par semaine/7), sauf indication contraire. Les taux d’inhalation des animaux ont été établis d’après l’équation présentée dans Bide et coll. (2000). Le poids corporel des animaux a été établi d’après les rapports d’étude lorsqu’ils étaient disponibles; sinon, on a utilisé la valeur par défaut présentée dans Meek et coll. (1994).
Une CSENO de 3 768 mg/m³ (CSENOaju = 590 mg/kg p.c./j), basée sur la diminution du taux de survie chez les rats mâles exposés à 18 842 ou 47 105 mg/m³ de DME par inhalation pendant 6 h/j, 5 j/sem pendant 2 ans (Commission MAK 1990) a été choisie comme critère d’effet le plus pertinent pour l’exposition par inhalation à long terme. Les ME résultantes sont jugées adéquates pour lever les incertitudes dans les bases de données sur les effets sur la santé et l’exposition au DME.
Pour ce qui est de l’exposition par inhalation à court terme, on a conclu à l’absence d’effets nocifs chez les rats exposés au DME pendant 10 jours jusqu’à 94 211 mg/m³. Ainsi, les ME pour l’exposition par inhalation à court terme n’ont pas été calculées, et le risque pour la santé humaine a été jugé faible, d’après les scénarios pertinents.
| Substance | Scénario d’exposition | Exposition systémique (mg/kg p.c./j)a |
Critère d’effet critique (mg/kg p.c./j) |
Paramètre d’effet critique pour la santé | ME |
|---|---|---|---|---|---|
| DME | Milieu environnemental, exposition quotidienne (enfants de 1 an) | 8,9 × 10-2 b | DSENOaju = 590d (étude par inhalation de 2 ans chez le rat) | Réduction du taux de survie chez les rats mâles à la dose ajustée de 2955 mg/kg p.c./j d | 6600 |
| DME | Écran solaire en aérosol, exposition quotidienne (enfants de 1 an) | 0,61c | DSENOaju = 590d (étude par inhalation de 2 ans chez le rat) | Réduction du taux de survie chez les rats mâles à la dose ajustée de 2955 mg/kg p.c./j d | 967 |
Abréviations : ME = marge d’exposition; DSENOaju = dose sans effet nocif observé.
a L’exposition systémique est calculée à partir de la « dose externe le jour de l’exposition », à l’aide du logiciel ConsExpo Web (2016), qui présume prudemment une absorption à 100 % par inhalation et par voie cutanée. Cette valeur représente la somme des doses externes pour plusieurs événements qui ont lieu la même journée, le cas échéant. Voir l’annexe C pour de plus amples renseignements.
b Représente la somme de l’exposition par voie orale et par inhalation.
c Représente l’exposition par inhalation.
d On calcule les critères d’effet critiques en convertissant les concentrations sans effet nocif observé (CSENO) ou concentrations minimales entraînant un effet nocif observé (CMENO) d’après les études de toxicité par inhalation en doses internes qui tiennent compte du taux d’inhalation des animaux (m³/j), du poids corporel (kg) et des facteurs d’ajustement temporel (heures d’exposition/24; jours d’exposition par semaine/7), sauf indication contraire. Les taux d’inhalation des animaux ont été établis d’après l’équation présentée dans Bide et coll. (2000). Le poids corporel des animaux a été établi d’après les rapports d’étude lorsqu’ils étaient disponibles; sinon, on a utilisé la valeur par défaut présentée dans Meek et coll. (1994).
Le DPGME est considéré comme ayant un faible potentiel de danger, car aucun effet nocif n’a été observé après l’exposition par voie orale ou cutanée jusqu’à la dose limite, ou à la suite de l’exposition par inhalation jusqu’à la concentration maximale atteignable et compte tenu des données disponibles indiquant un faible risque d’effet génotoxique sur la reproduction ou le développement. En outre, d’après les données de cancérogénicité obtenues par lecture croisée de l’analogue PGME, le DPGME n’est pas susceptible d’être cancérogène. Par conséquent, aucune estimation quantitative de l’exposition n’a été faite et le risque pour la santé humaine est jugé faible.
6.4 Incertitudes de l’évaluation des risques pour la santé humaine
Les plus importantes sources d’incertitude sont présentées dans le tableau suivant.
| Source clé d’incertitude | Incidence |
|---|---|
| Il y a un manque de données de surveillance canadiennes pour les substances du groupe des éthers dans les milieux environnementaux (p. ex., l’air et l’eau). | +/- |
| Il y a un manque d’études sur la cancérogénicité, la toxicité pour la reproduction et avec doses répétées à long terme pour le DEE. | +/- |
| L’utilisation d’un mélange eutectique (Therminol A) dans certaines études sur les dangers du DPE entraîne une incertitude quant à la détermination du composant à l’origine des effets observés sur la santé. | +/- |
+ = incertitude quant au potentiel de surestimation de l’exposition/risque; – = incertitude quant au potentiel de sous‑estimation du risque d’exposition; +/ – = potentiel inconnu de surestimation ou de sous-estimation du risque.
7. Conclusion
Compte tenu de tous les éléments de preuve contenus dans la présente ébauche d’évaluation préalable, le DEE, le DPE, le DME et le DPGME présentent un faible risque d’effets nocifs pour l’environnement. Il est proposé de conclure que le DEE, le DPE, le DME et le DPGME ne satisfont pas aux critères énoncés aux alinéas 64a) ou 64b) de la LCPE, car ils ne pénètrent pas dans l’environnement en une quantité ou concentration ou dans des conditions de nature à avoir, immédiatement ou à long terme, un effet nocif sur l’environnement ou sur la diversité biologique, ou à mettre en danger l’environnement essentiel pour la vie.
À la lumière des renseignements contenus dans la présente ébauche d’évaluation préalable, il est proposé de conclure que le DEE, le DPE, le DME et le DPGME ne satisfont pas aux critères de l’alinéa 64c) de la LCPE, car ils ne pénètrent pas dans l’environnement en une quantité ou concentration ou dans des conditions de nature à constituer un danger au Canada pour la vie ou la santé humaines.
Il est proposé de conclure que le DEE, le DPE, le DME et le DPGME ne satisfont à aucun des critères énoncés à l’article 64 de la LCPE.
Références
[AGDH] Australian Government Department of Health. 2018. Tier I Human Health Assessments INVENTORY MULTI-TIERED ASSESSMENT AND PRIORITISATION (IMAP) FRAMEWORK. Sydney (AU): Department of Health, National Industrial Chemicals Notification and Assessment Scheme. [Consulté le 11 septembre 2019.] (En anglais seulement.)
Api A and Ford R. 2003. « Evaluation of the dermal subchronic toxicity of diphenyl ether in the rat ». Food and Chemical Toxicology 41(2):259-64. (En anglais seulement.)
Apodaca L, Bails J et Smith M. 1997. « Water quality in shallow alluvial aquifers, Upper Colorado Riwer Basin, Colorado, 1997 ». J Am Water Resour Assoc. 38(1):133-149. (En anglais seulement.)
[BDIPSN] Base de données sur les ingrédients de produits de santé naturels [base de données]. [Modifiée le 26 septembre 2019.] Ottawa (ON), Santé Canada.
[BDPP] Base de données sur les produits pharmaceutiques [base de données]. [Modifiée le 17 juillet 2015]. Ottawa (ON), Gouvernement du Canada. [Consulté le 25 septembre 2019.]
[BDPSNH] Base de données sur les produits de santé naturels homologués [base de données]. [Modifiée le 6 février 2018]. Ottawa (ON), Santé Canada.
Bide RW, Armour SJ et Yee E. 2000. « Allometric respiration/body mass data for animals to be used for estimates of inhalation toxicity to young adult humans ». J Appl Toxicol 20(4):273-90. (En anglais seulement.)
Boîte à outils QSAR de l’OCDE. 2014. Paris (FR), Organisation de coopération et de développement économiques, Laboratoire de chimie mathématique.
Burdock, GA. 2010. Fenaroli’s handbook of flavor ingredients. 6e éd. Boca Raton (FL): CRC Press. (En anglais seulement.)
Buters JT, Schober W, Gutermuth J, Jakob T, Aguilar-Pimentel A, Huss-Marp J, Traidl-Hoffmann C, Mair S, Mair S, Mayer F, Breuer K, Behrendt H. et coll. 2007. « Toxicity of parked motor vehicle indoor air ». Environ Sci Technol. 41(7):2622-2629. (En anglais seulement)
Cadena E, Adani F, Font X et Artola A. 2018. « Including an odor impact potential in life cycle assessment of waste treatment plants ». Int J Environ Sci Technol. 15:2193–2202. (En anglais seulement.)
Canada, Ministère de l’Environnement. 2009. « Loi canadienne sur la protection de l’environnement (1999) : Avis concernant certaines substances inanimées (chimiques) inscrites sur la Liste intérieure [PDF] ». Gazette du Canada, Partie I, vol. 143, no 40, p. 2945-2967.
Canada, Ministère de l’Environnement. 2012. « Loi canadienne sur la protection de l’environnement (1999) – Avis concernant certaines substances de la Liste intérieure [PDF] ». Gazette du Canada, Partie I, vol. 146, no 48, Supplément.
Canada. [1978]. Règlement sur les aliments et drogues. C.R.C., ch. 870.
Canada. 1999. « Loi canadienne sur la protection de l’environnement (1999) ». L.C. 1999, ch. 33. Gazette du Canada. Partie III, vol. 22, no 3.
[CE] Commission européenne. 2012. Recommendation from the scientific committee on occupational exposure limits for diphenyl ether. European Commission. Rapport no SCOEL/SUM/182. (En anglais seulement.)
Chan C, Vainer L, Martin J, Williams D. 1990. « Determination of organic contaminants in residential indoor air using an adsorption-thermal desorption technique ». J Air Waste Manage Assoc. 40(1):62-7. (En anglais seulement.)
ChemCAN [level III fugacity model of 24 regions of Canada]. 2003. Version 6.00. Peterborough (ON): Trent University, Canadian Centre for Environmental Modelling and Chemistry. (En anglais seulement.)
ChemIDplus [base de données]. 1993- . Bethesda (MD): US National Library of Medicine. [Actualisé le 20 juillet 2016, consulté le 25 septembre 2019.] (En anglais seulement.)
CIVO Institute. 1981. Initial submission: Inhalation embryotoxicity/teratogenicity studies witii dimethylether in rats with cover letfer dated 08/24/92. Pays-Bas : DuPont. Report No. OTS 0555244. Disponible à partir de NTIS, Springfield, VA. (En anglais seulement.)
Commission MAK. 1990. Dimethyl ether [documentation sur la concentration maximale au travail, 1990]. Wiley-VCH Verlag GmbH & Co. (En anglais seulement.)
Commission MAK. 1993. Dipropylene glycol monomethyl ether [documentation sur la concentration maximale au travail, 1993]. Wiley-VCH Verlag GmbH & Co. (En anglais seulement.)
Commission MAK. 1996. Diethyl ether [documentation sur la concentration maximale au travail, 1999.] Wiley-VCH Verlag GmbH & Co. (En anglais seulement.)
Commission MAK. 2004. Diphenylether (Dampf) [documentation sur la concentration maximale au travail en allemand, 2004]. Wiley-VCH Verlag GmbH & Co. (En anglais seulement.)
Curry P, Kramer G, Newhook R, Sitwell J, Somers D, Tracy B et Oostdam JV. 1993. Reference values for Canadian populations. Produit par le groupe de travail sur les valeurs de référence de la Direction de l’hygiène du milieu. Santé Canada. 1988 (mise à jour en 1993). (En anglais seulement.)
DailyMed [base de données]. 2019. Search result for Freezone. Bethesda (MD): US National Library of Medicine. [Actualisé le 19 septembre 2019, consulté le 27 septembre 2019.] (En anglais seulement.)
[ECCC, SC] Environnement et Changement climatique Canada, Santé Canada. [Modifié le 12 mars 2017.] Catégorisation. Ottawa (ON), Gouvernement du Canada. [Consulté le 25 septembre 2019.]
[ECCC] Environnement et Changement climatique Canada. 2016a. Document sur l’approche scientifique : classification du risque écologique des substances organiques. Ottawa (ON), Gouvernement du Canada.
[ECCC] Environnement et Changement climatique Canada. 2016b. Supporting documentation: data used to create substance-specific hazard and exposure profiles and assign risk classifications. Gatineau (QC): ECCC. Information in support of the science approach document: ecological risk classification of organic substances. Disponible à : substances@ec.gc.ca.
[ECHA] Agence européenne des produits chimiques. c2007-2019. Registered substances database; search results for CAS RNs 60-29-7, 101-84-8, 115-10-6, 34590-94-8. Helsinki (FI): ECHA. [Consulté le 26 septembre 2019.] (En anglais seulement.)
[EFSA] Autorité européenne de sécurité des aliments. 2009. « Safety in use of dimethyl ether as an extraction solvent ». EFSA Journal 7(3):984. (En anglais seulement.)
[EFSA] Autorité européenne de sécurité des aliments. 2011. « Scientific Opinion on Flavouring Group Evaluation 59, Revision 1 (FGE.59Rev1): Consideration of aliphatic and aromatic ethers evaluated by JECFA (61st meeting and 63rd meeting) structurally related to aliphatic, alicyclic and aromatic ethers including anisole derivatives evaluated by EFSA in FGE.23 Rev2 (2010) ». Parme, Italie : Autorité européenne de sécurité des aliments. EFSA Journal, No. 2158. (En anglais seulement.)
[EFSA] Autorité européenne de sécurité des aliments. 2012. « Scientific Opinion on the safety and efficacy of aromatic ethers including anisole derivatives (chemical group 26) when used as feed additives for all animal species ». EFSA Journal 2012;10(5):2678 (En anglais seulement.)
[EFSA] Autorité européenne de sécurité des aliments. 2015. « Panel on Food Contact Materials, Enzymes, Flavourings and Processing Aids (CEF). Scientific opinion on the safety of use of dimethyl ether as an extraction solvent under the intended conditions of use and the proposed maximum residual limits ». EFSA Journal 13(7):4174. (En anglais seulement.)
Environnement Canada. 2009. « DSL Inventory Update Phase 1 data collected under the Canadian Environmental Protection Act, 1999, section 71: Notice with respect to certain substances on the Domestic Substances List ». Données préparées par : Environnement Canada, Santé Canada; Programme des substances existantes. (En anglais seulement.)
Environnement Canada. 2013. « DSL Inventory Update data collected under the Canadian Environmental Protection Act, 1999, section 71: Notice with respect to certain substances on the Domestic Substances List ». Données préparées par : Environnement Canada, Santé Canada; Programme des substances existantes. (En anglais seulement.)
[FDEM] Fiche de sécurité des matières. 2010. Motorcycle Degreaser [PDF]. Hauppauge (NY): Finishi Line Technologies Inc. [Consulté le 19 septembre 2019.] (En anglais seulement.)
[FDS] Fiche de données de sécurité. 2010. Neutral Floor Cleaner [PDF]. Miramar (US): For Life Products, Inc. [Consulté le 19 septembre 2019.] (En anglais seulement.)
[FDS] Fiche de données de sécurité. 2014a. Mace Pepper Gun - Refill Cartridge [PDF]. Cleveland (US): Mace Security International [Consulté le 19 septembre 2019.] (En anglais seulement.)
[FDS] Fiche de données de sécurité. 2014b. Restorative Water Repellent for Outerwear and Apparel [PDF]. St. Paul (US): New Business Ventures [Consulté le 19 septembre 2019.] (En anglais seulement.)
[FDS] Fiche de données de sécurité. 2015a. Homax Spray Spackling [PDF]. Longueuil CA): PPG Revêtement Architecturaux Canada [Consulté le 11 septembre 2019.]
[FDS] Fiche de données de sécurité. 2015b. Simoniz Tire Foam. Repentigny (QC): Auto-Chem Incoporated [Consulté le 11 septembre 2019.] (En anglais seulement.)
[FDS] Fiche de données de sécurité. 2015c. Salt Eraser. Brampton (CA): Empack Spraytech Incorporated [Consulté le 11 septembre 2019.] (En anglais seulement.)
[FDS] Fiche de données de sécurité. 2015d. Febreze Noticeables Air Freshener [PDF]. Toronto (CA): Procter & Gamble Inc [Consulté le 19 septembre 2019.] (En anglais seulement.)
[FDS] Fiche de données de sécurité. 2015e. Ultra power remover [PDF]. Chicago (US): Rust-Oleum Corporation [Consulté le 19 septembre 2019.] (En anglais seulement.)
[FDS] Fiche de données de sécurité. 2015f. Stainless Steel Basecoat [PDF]. St. Louis (US): Giani, Inc. [Consulté le 19 septembre 2019.] (En anglais seulement.)
[FDS] Fiche de données de sécurité. 2015g. Teflon Penetrant [PDF]. Suffolk County (US): Finish Line Technologies, Inc. [Consulté le 20 septembre 2019.] (En anglais seulement.)
[FDS] Fiche de données de sécurité. 2015h. Restore Black [PDF]. St. Paul (US): Automotive Aftermarket [Consulté le 20 septembre 2019.] (En anglais seulement.)
[FDS] Fiche de données de sécurité. 2016a. Febreze Small Spaces Mediterranean Lavender [PDF]. Toronto (CA): Proctor & Gamble Incorporated [Consulté le 11 septembre 2019] (En anglais seulement.)
[FDS] Fiche de données de sécurité. 2016b. Tarnish-Me-Not [PDF]. Passaic County (US): Tarnish Me Not [Consulté le 11 septembre 2019.] (En anglais seulement.)
[FDS] Fiche de données de sécurité. 2016c. Graffiti Remover [PDF]. Chicago (US): Rust-Oleum Corporation [Consulté le 19 septembre 2019.] (En anglais seulement.)
[FDS] Fiche de données de sécurité. 2016d. Spa jet cleaner [PDF]. Alpharetta (US)[Consulté le 19 septembre 2019.] (En anglais seulement.)
[FDS] Fiche de données de sécurité. 2016e. Rust converter [PDF]. Fulf Breeze (US): Radical Rafts, Inc. [Consulté le 19 septembre 2019.] (En anglais seulement.) (En anglais seulement.)
[FDS] Fiche de données de sécurité. 2016f. Tub & Tile Etch [PDF]. Toronto (CA), Rust-Oleum Consumer Brands Canada [Consulté le 19 septembre 2019]
[FDS] Fiche de données de sécurité. 2016g. Herman Survivors Liquid Silicone [PDF]. Durham (US): Implus Footcare LLC [Consulté le 19 septembre 2019.] (En anglais seulement.)
[FDS] Fiche de données de sécurité. 2016h. 1915 Classic Inks [PDF]. Cleveland (US): Mace Security International [Consulté le 19 septembre 2019.] (En anglais seulement.)
[FDS] Fiche de données de sécurité. 2016i. 10% Pepper Stream [PDF]. Erie County(US): International Imaging Materials, Inc [Consulté le 19 septembre 2019.] (En anglais seulement.)
[FDS] Fiche de données de sécurité. 2017a. Kleen-Start Starting Fluid [PDF]. Toronto (CA): Kleen-Flo Tumbler Industries Limited [Consulté le 6 septembre 2019.] (En anglais seulement.)
[FDS] Fiche de données de sécurité. 2017b. Arm & Hammer Scrub Free Bathroom Cleaner [PDF]. Mercer County (US): Church & Dwight [Consulté le 11 septembre 2019.] (En anglais seulement.)
[FDS] Fiche de données de sécurité. 2017c. Rust-Oleum Spray Chalk, yellow [PDF]. Vaughan (CA), Rust-Oleum Consumer Brands Canada [Consulté le 11 septembre 2019.]
[FDS] Fiche de données de sécurité. 2017d. LePage Quad Window and Door Foam [PDF]. Hartford County (US): Henkel Corporation [Consulté le 11 septembre 2019.] (En anglais seulement.)
[FDS] Fiche de données de sécurité. 2017e. Rust Check Rust Converter [PDF]. Mississauga (CA): Rust Check Corporation [Consulté le 11 septembre 2019.] (En anglais seulement.)
[FDS] Fiche de données de sécurité. 2017f. Air Wick Liquid Electrical - Fresh Waters [PDF]. Mississauga (ON): Reckiit Benckiser LLC. [Consulté le 19 septembre 2019.] (En anglais seulement.)
[FDS] Fiche de données de sécurité. 2018a. Headliner Adhesive [PDF]. St. Paul (US): 3M [Consulté le 11 septembre 2019.] (En anglais seulement.)
[FDS] Fiche de données de sécurité. 2018b. Tulip Color Shot Instant Fabric Color [PDF]. Fresno (US): Duncan Enterprises [Consulté le 11 septembre 2019.] (En anglais seulement.)
[FDS] Fiche de données de sécurité. 2018c. Buck Bomb Doe “P” Bomb [PDF]. Cedar Rapids (US): Buck Bomb Incorporated [Consulté le 11 septembre 2019.] (En anglais seulement.)
[FDS] Fiche de données de sécurité. 2018d. EZ Liner [PDF]. Mississauga (CA): Dominion Sure Seal Limited [Consulté le 11 septembre 2019.] (En anglais seulement.)
[FDS] Fiche de données de sécurité. 2018e. Nettoyant dégraissant. Montréal (CA), LAVO [Consulté le 19 septembre 2019.]
[FDS] Fiche de données de sécurité. 2018f. WDCARE 4X177ML VARA POLY TUBE SEMI GLOSS [PDF]. Vaughan (ON), Rust-Oleum Canada [Consulté le 19 septembre 2019.]
[FDS] Fiche de données de sécurité. 2019a. Krylon Professional Marking Chalk [PDF]. Mississauga (CA): Krylon Products Group [Consulté le 11 septembre 2019.] (En anglais seulement.)
[FDS] Fiche de données de sécurité. 2019b. Varathane Diamond Wood Finish – Interior [PDF]. Vaughan (CA), Rust-Oleum Canada [Consulté le 11 septembre 2019.]
Ficheux AS, Chevillotte G, Wesolek N, Morisset T, Dornic N, Bernard A, Bertho A, Romanet A, Leroy L, Mercat AC, Creusot T, Simon E et Roudot AC. 2016. « Consumption of cosmetic products by the French population second part: Amount data ». Food and Chemical Toxicology 90: 130-141. (En anglais seulement.)
Ficheux AS, Wesolek N, Chevillotte G et Roudot AC. 2015. « Consumption of cosmetic products by the French population. First part: Frequency data ». Food and Chemical Toxicology 78: 159-169. (En anglais seulement.)
Gaeggeler K, Prevot A, Dommena J, Legreid G, Reimann S et Baltensperger U. 2008. « Residential wood burning in an Alpine valley as a source for oxygenated volatile organic compounds, hydrocarbons and organic acids ». Atmos Environ 42:8278-87. (En anglais seulement.)
Gonthier G, Lawrence S, Peck M et Holloway G. 2011. « Groundwater conditions and studies in the Augusta–Richmond County Area, Georgia, 2008-2009 ». Atlanta, Georgia : U.S. Geological Survey. 45 p. Scientific Investigations Report 2011–5188. (En anglais seulement.)
Gribble M. 2005. The toxicology of glycol ethers and its relevance to man. ECETOC. (En anglais seulement.)
Haskell Labs. 1983. Initial submission: Evaluation of embryotoxicity and teratogenicity studies w/dimethylether (dme) in rats with cover letter dated 082492. Rapport final. Pays-Bas : DuPont. Rapport no NTIS/OTS 0546404. Disponible à partir de NTIS, Springfield, VA, USA. (En anglais seulement.)
Hefner Jr R, Leong B, Kociba R et Gehring P. 1975. « Repeated inhalation toxicity of diphenyl oxide in experimental animals ». Toxicol Appl Pharmacol 33(1):78-86. (En anglais seulement.)
Hippelein M. 2006. « Analysing selected VVOCs in indoor air with solid phase microextraction (SPME): a case study ». Chemosphere. 65:271–277. (En anglais seulement.)
[INRP] Inventaire national des rejets de polluants. [Base de données]. 2017. Gatineau (QC), Environnement Canada.
[IOFI] International Organization of the Flavour Industry, 1995. European Inquiry on Volume of Use. Submitted to WHO by the Flavor and Extract Manufacturers’ Association of the United States, Washington DC, États-Unis. (En anglais seulement.)
Johnson W, Ehrlich J, Hatoum N et Yermakoff J. 1992. « Thirteen-week oral (diet) toxicity study of diphenyl ether in rats ». Toxicologist 12(1992):117. (En anglais seulement.)
Keefe SH, Barber LB, Runkel RL et Ryan JN. 2004. « Fate of volatile organic compounds in constructed wastewater treatment wetlands ». Environ Sci Technol. 38(7):2209-16. (En anglais seulement.)
Lesage S, Jackson R, Priddle M et Riemann P. 1990. « Occurrence and fate of organic solvent residues in anoxic groundwater at the Gloucester landfill, Canada », Environ Sci Technol. 24(4):559-566. (En anglais seulement.)
Loretz LG, Api AM, Babcock L, Barraj LM, Burdick J, Cater KC, Jarrett G, Mann S, Pan YHL, Re TA, Renskers KJ et Scrafford CG. 2008. « Exposure data for cosmetic products: Facial cleanser, hair conditioner, and eye shadow ». Food Chem Toxicol 46: 1516-1524. (En anglais seulement.)
Lucas, C.D. et coll., dir. 1999. 1995 Poundage and technical effects update summary. Washington, DC, Flavor and Extract Manufacturers’ Association of the United States. (En anglais seulement.)
Meek M, Newhook R, Liteplo R et Armstrong V. 1994. « Approach to assessment of risk to human health for priority substances under the canadian environmental protection act. » Journal of Environmental Science & Health Part C 12(2):105-34. (En anglais seulement.)
Moreno T, Pacitto A, Fernandez A, Amato F, Marco E, Grimalt J, Buonanno G, et Querol X. 2019. « Vehicle interior air quality conditions when travelling by taxi ». Environ Res.172:529-542. (En anglais seulement.)
Mullaney J, Mondazzi R et Stone J. 1999. /Hydrogeology and water quality of the Nutmeg Valley Area, Wolcott and Waterbury, Connecticut/. Denver: U.S. Geological Survey. 89 pages. Water-Resources Investigations Report 99-4081. (En anglais seulement.)
[NAS] National Academy of Sciences. 1989. 1987 Poundage and Technical Effects Update of Substances Added to Food, Committee on Food Additives Survey Data, Food and Nutrition Board, Institute of Medicine, National Academy of Sciences, Washington DC, USA. (En anglais seulement.)
Nijssen LM, Ingen-Visscher CA et van Donders JJH [dir.]. 1963-2018. VCF (Volatile Compounds in Food): base de données, Version 16.6.1, 2018. Triskelion B.V. Zeist, Netherlands. (En anglais seulement.)
[OCDE] Organisation de coopération et de développement économiques. 2001. SIDS initial assessment report: Dipropylene glycol methyl ether: CAS No. 34590-94-8. SIAM [SIDS Initial Assessment Meeting] 12. Paris, France. (En anglais seulement.)
[OMS] Organisation mondiale de la santé. 2004. « Evaluation of certain food additives and contaminants: sixty-first meeting of the Joint FAO/WHO Expert Committee on Food Additives ». WHO Technical Report Series: 922. Geneva. Organisation mondiale de la santé. (En anglais seulement.)
[OCDE] Organisation de coopération et de développement économiques. 2001. SIDS initial assessment report: Dipropylene glycol methyl ether: CAS No. 34590-94-8. SIAM [SIDS Initial Assessment Meeting] 12. Paris, France. (En anglais seulement.)
[OMS] Organisation mondiale de la santé. 2004. « Evaluation of certain food additives and contaminants: sixty-first meeting of the Joint FAO/WHO Expert Committee on Food Additives ». WHO Technical Report Series: 922. Geneva. Organisation mondiale de la santé. (En anglais seulement.)
Pellizzari E, Hartwell T, Harris B, Waddell R et Whitaker D.1982. « Purgeable organic compounds in mother’s milk ». Bull Environ Contam Toxicol. 28(3):322-8. (En anglais seulement.)
Pope LM, Bruce BW, Rasmussen PP et Milligan CR. 2002. « Quality of shallow ground water in areas of recent residential and commercial development, Wichita, Kansas, 2000 ». Denver: U.S. Geological Survey. 67 pages. Water-Resources Investigations Report 02–4228 (En anglais seulement.)
PubChem. 2004- . Bethesda (MD): US National Library of Medicine, National Center for Biotechnology Information. [Consulté le 26 septembre 2019.] (En anglais seulement.)
Rabaud N, Ebeler S, Ashbaugh L et Flocchini R. 2003. « Characterization and quantification of odorous and non-odorous volatile organic compounds near a commercial dairy in California ». Atmos Environ 37:933–940. (En anglais seulement.)
Raboni M, Torretta V, Urbini G et Viotti P. 2015. « Automotive shredder residue: a survey of the hazardous organic micro-pollutants spectrum in landfill biogas ». Waste Manag Res 33(1), 48-54. (En anglais seulement.)
Ramírez N, Cuadras A, Rovira E, Borrull F et Marcé R. 2010. « Comparative study of solvent extraction and thermal desorption methods for determining a wide range of volatile organic compounds in ambient air ». Talanta 82:719–727. (En anglais seulement.)
Robinson V, Bergfeld WF, Belsito DV, Klaassen CD, Marks JG, Shank RC, Slaga TJ, Snyder PW et Andersen FA. 2009. « Final report on the safety assessment of PPG-2 methyl ether, PPG-3 methyl ether, and PPG-2 methyl ether acetate ». Int J Toxicol 28(6_suppl):162S-74S. (En anglais seulement.)
Rogers IH, Birtwell IK et Kruzynski GM.1986. « Organic extractables in municipal wastewater Vancouver, British Columbia ». Water Qual Res J Can 21(2):187-204. (En anglais seulement.)
Santé Canada. [Modifié le 14 décembre 2015]. Liste critique des ingrédients de cosmétiques : Liste des ingrédients dont l’usage est interdit dans les cosmétiques. Ottawa (ON), Gouvernement du Canada. [Consulté le 25 septembre 2019.]
Santé Canada. 2015a. Tableau de la consommation des aliments fondée sur l’Enquête sur la santé dans les collectivités canadiennes, cycle 2.2, Nutrition (2004), fichier partagé. Ottawa (ON).
Santé. Canada 2015b. Keep calm and use hand sanitizer – how much and how often. Non publié, Bureau de l’évaluation des risques pour les substances existantes et Bureau de l’évaluation et du contrôle des substances nouvelles, Santé Canada. Présenté au Forum scientifique de Santé Canada 2015. (En anglais seulement.)
SCREEN3 [modèle informatique]. 2011. Ver. 3.5.0. Research Triangle Park (NC): US Environmental Protection Agency, Office of Air Quality Planning and Standards, Emissions, Monitoring, and Analysis Division. (En anglais seulement.)
Slobodnik J, Mrafkova L, Carere M, Ferrara F, Pennelli B, Schüürmann G, von der Ohe P.C. 2010. « Identification of river basin specific pollutants and derivation of environmental quality standards: A case study in the Slovak Republic ». Trends Analyt Chem 41:133-145. (En anglais seulement.)
Smet E, Langenhove H et Bo I. 1999. « The emission of volatile compounds during the aerobic and the combined anaerobic/aerobic composting of biowaste ». Atmos Environ 33:1295-1303. (En anglais seulement.)
Statistique Canada. 2004a. Enquête sur la santé dans les collectivités canadiennes (ESCC) - Cycle 2.2 : Nutrition. Fichiers de partage. Ottawa, ON. Canada. Estimations générées à l’aide de SAS 9.3 [GRID] à SAS EG 5.1.
Statistique Canada. 2004b. Enquête sur la santé dans les collectivités canadiennes, Cycle 2.2 : Volet général sur la santé. Fichiers de partage.
Statistique Canada. 2015. Enquête sur la santé dans les collectivités canadiennes (ESCC) 2015 Fichiers de partage. Ottawa, ON. Canada. Estimations générées à l’aide de SAS 9.3 [GRID] à SAS EG 5.1.
Tokumura M, Hatayama R, Tatsu K, Naito T, Takeda T, Raknuzzaman M, Habibullah-Al-Mamun M et Masunaga S. 2006. « Car indoor air pollution by volatile organic compounds and aldehydes in Japan ». AIMS Environ Sci. 3(3): 362-381. (En anglais seulement.)
[USEPA]. 1987. Health Effects Assessment for Ethyl Ether. Washington, DC: U.S. Environmental Protection Agency. Rapport no EPA/600/8-88/039. (En anglais seulement.)
[USEPA]. 1992. Screening procedures for estimating the air quality impact of stationary sources, revised [PDF]. Washington (DC): U.S. Environmental Protection Agency, Office of Air Quality. Rapport no EPA-454/R-92-019. (En anglais seulement.)
[USEPA]. 2009a. Provisional peer-reviewed toxicity values for ethyl ether. Washington, DC: U.S. Environmental Protection Agency. Rapport no EPA/690/R-09/022F. (En anglais seulement.)
[USEPA]. 2009b. Dimethyl ether Initial Risk-Based Prioritization of HPV Chemicals. Washington (DC): U.S. Environmental Protection Agency. [Consulté le 28 août 2019.] (En anglais seulement.)
[USEPA]. 2010. Diphenyl oxide Screening Level Hazard Characterization. Washington (DC): U.S. Environmental Protection Agency. [Consulté le 28 août 2019.] (En anglais seulement.)
[USEPA]. 2011. Exposure Factors Handbook: 2011 Edition. Washington (DC): National Center for Environmental Assessment, Office of Research and Development, U.S. Environmental Protection Agency. (En anglais seulement.)
[USEPA]. 2014. Diethyl ether Screening Level Hazard Characterization. Washington (DC): U.S. Environmental Protection Agency. [Consulté le 28 août 2019.] (En anglais seulement.)
[USEPA]. 2017. Provisional peer-reviewed toxicity values for diphenyl ether. Washington (DC): U.S. Environmental Protection Agency. Rapport no EPA/690/R-17/009F. (En anglais seulement.)
Veijanen A et Lehtinen J. 2011. « Odour monitoring by combined TD–GC–MS–sniff technique and dynamic olfactometry at the wastewater treatment plant of low H2S concentration ». Water Air Soil Pollut. 218:185–196. (En anglais seulement.)
Wu X, Bennett DH, Ritz B, Cassady DL, Lee K et Hertz-Picciotto I. 2010. « Usage pattern of personal care products in California households ». Food Chem Toxicol 48: 3109-3119. (En anglais seulement.)
Annexes
Annexe A. Résumé des données obtenues par lecture croisée pour les effets sur la santé
| Propriété | DEE (cible) | DIPE (analogue) |
|---|---|---|
| Structure |  |
 |
| État physique | Liquide | Liquide |
| Point de fusion (°C) | –116a | -86,8a |
| Pression de vapeur (Pa) | 7,17 × 104 a | 1,99 × 104 a |
| Constante de la loi d’Henry (Pa·m³/mol) | 1,25 × 102 a | 2,31 × 102 a |
| Solubilité dans l’eau (mg/L) | 6,04 × 104 a | 8,8 × 104 a |
| Log Koe (sans dimension) | 0,89a | 1,52a |
| Génotoxicité | Négatif | S.O. |
| Exposition à court terme par voie orale | N.D. | S.O. |
| Exposition par inhalation, court terme |
DMENOaju = 4 256 mg/kg p.c./j (étude par inhalation de 35 jours chez la souris; toxicité pour le foie et mortalité) |
S.O. |
| Exposition à court terme par voie cutanée | N.D. | S.O. |
| Toxicité subchronique, voie orale |
DSENO = 500 mg/kg p.c./j (étude par gavage oral de 13 semaines chez le rat; variation du poids corporel et mortalité accrue) |
S.O. |
| Toxicité subchronique, inhalation | S.O. | S.O. |
| Toxicité subchronique, voie cutanée | N.D. | S.O. |
| Chronique par voie orale | N.D. | S.O. |
| Toxicité chronique, inhalation | N.D. | S.O. |
| Toxicité chronique, voie cutanée | N.D. | S.O. |
| Cancérogénicité | S.O. | S.O. |
| Toxicité pour la reproduction et/ou le développement |
CSENO = 28 200 mg/m³ (données obtenues par lecture croisée du DIPE) |
CSENO = 28 200 mg/m³ (étude par inhalation pour le développement chez le rat; aucun effet nocif; aucun effet nocif sur les fœtus) |
Abréviations : S.O. = sans objet; N.D. = valeur non disponible.
a ChemIDplus 1993-
| Propriété |
DPGME (cible) |
PGME (analogue) |
|---|---|---|
| Structure |  |
 |
| État physique | Liquide | Liquide |
| Point de fusion (°C) | –83b | -95c |
| Pression de vapeur (Pa) | 7,33 × 101 b | 1,2c |
| Constante de la loi d’Henry (Pa·m³/mol) | 1,08 × 10−2 a | 9,3 × 10−2 c |
| Solubilité dans l’eau (mg/L) | 1,00 × 106 b | 1,00 × 105 c |
| Log Koe (sans dimension) | –0,35a | -0,49c |
| Génotoxicité | Négatif | S.O. |
| Exposition à court terme par voie orale |
DSENO = 1 000 mg/kg p.c./j (étude par voie orale de 28 jours chez le rat; aucun effet nocif) |
S.O. |
| Exposition par inhalation, court terme |
CSENO = 1818 mg/m³ (études de 2 semaines chez le rat et la souris; aucun effet nocif) |
S.O. |
| Exposition à court terme par voie cutanée |
DSENO = 1 000 mg/kg p.c./j (étude de 4 semaines chez le rat; aucun effet nocif) |
S.O. |
| Toxicité subchronique, voie orale | N.D. | S.O. |
| Toxicité subchronique, inhalation |
CSENO = 1818 mg/m³ (études de 13 semaines chez le rat et le lapin; aucun effet nocif) |
S.O. |
| Toxicité subchronique, voie cutanée |
DSENO = 2 850 mg/kg p.c./j (étude de 90 jours chez le lapin; irritation cutanée mineure, narcose et mort) |
S.O. |
| Chronique par voie orale | N.D. | S.O. |
| Toxicité chronique, inhalation |
CSENO = 1 818 mg/m³ (études de 31 semaines chez le rat, le lapin, le cobaye et le singe; aucun effet nocif) |
S.O. |
| Toxicité chronique, voie cutanée | N.D. | S.O. |
| Cancérogénicité |
CSENO = 11 058 mg/m³ (données obtenues par lecture croisée du PGME) |
CSENO = 11 058 mg/m³ (étude de cancérogénicité par inhalation de 2 ans chez le rat et la souris; aucun effet cancérogène) |
| Toxicité pour la reproduction et/ou le développement |
CSENO = 1818 mg/m³ (études de toxicité pour le développement par inhalation chez le rat et le lapin; aucun effet nocif sur les fœtus) |
S.O. |
Abréviations : S.O. = sans objet; N.D. = valeur non disponible.
a Valeurs modélisées.
b ChemIDplus (1993-).
c PubChem 2004-.
Annexe B. Paramètres utilisés pour estimer l’exposition humaine au DEE, au DPE et au DME par les produits de consommation
L’estimation de l’exposition des humains par les produits de consommation a été faite à l’aide du logiciel ConsExpo Web (ConsExpo Web 2016). Sauf indication contraire dans les scénarios d’exposition ci‑dessous, les paramètres par défaut du modèle ConsExpo Web ont été utilisés. Les paramètres par défaut ont été sélectionnés d’après les fiches d’information General Fact Sheet (RIVM 2014) et Cleaning Product Fact Sheet (RIVM 2018) et la documentation du modèle d’aérosol de ConsExpo (RIVM 2009) et la Cosmetics Fact Sheet (RIVM 2006). Par prudence, on a présumé que le taux d’absorption par inhalation était de 100 % pour le DEE, le DPE et le DME, et que le taux d’absorption par la voie cutanée était de 100 % pour le DPE.
Les taux d’inhalation et les poids corporels des utilisateurs sont précisés dans le document de Santé Canada 2015a, et sont résumés dans le tableau A-1.
| Groupe d’âge | Taux d’inhalation (m³/jour) | Poids corporel (kg) |
|---|---|---|
| 19 ans et plus | 15,1 | 74 |
| 14 à 18 ans | 15,9 | 62 |
| 9 à 13 ans | 13,9 | 42 |
| 4 à 8 ans | 11,1 | 23 |
| 2 à 3 ans | 9,2 | 15 |
| 1 an | 8,0 | 11 |
|
Scénario d’exposition, voie d’exposition et groupe d’âge |
Paramètres utilisés dans ConsExpo Web |
|---|---|
|
Lotion corporelle (exposition quotidienne), inhalation, 19 ans et plus a |
Modèle : Exposition à la vapeur – rejet instantané Fréquence d’utilisation : 1/j (Ficheux 2015; Wu 2010) Durée de l’exposition : 24 h (RIVM 2006) Quantité de produit : 10 g (Ficheux 2016) Fraction du poids : 0,03 (communication personnelle, courriel de la DSPCPD, Santé Canada, au BERSE, Santé Canada, février 2018; sans référence) Volume de la pièce : 80 m³ (jugement professionnel; ce volume devrait être représentatif du mélange dans l’air intérieur pendant la journée) Taux de ventilation : 1/h (jugement professionnel) |
|
Produit contre les cors et les cals (par exposition), inhalation, 9 à 13 ans |
Modèle : Exposition à la vapeur – rejet instantané Durée de l’exposition : 10 min. (jugement professionnel) Quantité de produit : 0,7 g (selon les instructions d’utilisation figurant dans la Base de données sur les produits de santé naturels homologués de Santé Canada, ce qui correspond à 2 gouttes de 0,5 mL chacune, avec une masse volumique de 0,7 g/mL pour le DEE) Fraction du poids : 0,57 (DailyMed 2019) Volume de la pièce : 10 m³ (valeur par défaut pour les salles de bain, RIVM 2014) Taux de ventilation : 2,0/h (valeur par défaut pour les salles de bain, RIVM 2014) |
|
Fluide de démarrage (par événement), inhalation, 19 ans et plus |
Modèle : Exposition à la vapeur – rejet instantané Durée de l’exposition : 30 min. (jugement professionnel) Quantité de produit : 12 g (utilisation présumée de 5 pulvérisations de 2 secondes chacune, d’après les instructions pour un produit similaire, avec un taux de production massique de 1,2 g/s (RIVM 2009)) Fraction du poids : 0,6 (FDS 2017c) Volume de la pièce : 34 m³ (valeur par défaut pour les garages, RIVM 2014) Taux de ventilation : 1,5/h (valeur par défaut pour les garages, RIVM 2014) |
a Le groupe d’âge des 19 ans et plus a été sélectionné, car le produit correspondant ne devrait être utilisé que par des adultes. Des groupes d’âge plus jeunes ont été pris en compte pour d’autres produits similaires, ce qui a permis de réduire l’exposition par kg.
|
Scénario d’exposition, voie d’exposition et groupe d’âge |
Paramètres utilisés dans ConsExpo Web |
|---|---|
|
Désodorisant domestique (exposition quotidienne), inhalation, 1 an |
Modèle : Exposition à la vapeur – rejet instantané Durée de l’exposition : 24 h (jugement professionnel) Quantité de produit : 0,18 g (l’emballage indique que 5,5 mL durent 30 jours, masse volumique présumée de 1 g/mL (USEPA CEM, guide d’utilisation)) Fraction du poids : 0,05 (FDS 2016a) Volume de la pièce : 20 m³ (valeur par défaut pour une pièce générique, RIVM 2014) Taux de ventilation : 0,6/h (valeur par défaut pour une pièce générique, RIVM 2014) |
|
Crème pour les mains (exposition quotidienne), inhalation, 19 ans et plus |
Modèle : Exposition à la vapeur – rejet instantané Durée de l’exposition : 24 h (jugement professionnel) Fréquence d’utilisation : 1/jour (ajustements apportés à la quantité de produit pour tenir compte de l’estimation prudente d’une durée d’exposition de 24 heures (Ficheux 2015) Quantité de produit : 3,2 g (car la quantité appliquée est de 1,6 g, et on suppose que la crème pour les mains est utilisée deux fois par jour, ajustement de la superficie basé sur les données de Ficheux 2016) Fraction du poids : 0,05 (communication personnelle, courriel de la DSPCPD, Santé Canada, au BERSE, Santé Canada, 2018; sans référence) Volume de la pièce : 80 m³ (jugement professionnel; ce volume devrait être représentatif du mélange dans l’air intérieur pendant la journée) Taux de ventilation : 1/h (jugement professionnel) Température d’application : 37 °C |
|
Scénario d’exposition, voie d’exposition et groupe d’âge |
Paramètres utilisés dans ConsExpo Web |
|---|---|
|
Écran solaire en aérosol (exposition quotidienne), inhalation, 1 an |
Modèle : Exposition à la vapeur – rejet instantané Fréquence d’utilisation : 1/jour (ajustements apportés à la quantité de produit pour tenir compte de l’estimation prudente d’une durée d’exposition de 24 heures (Ficheux 2015) Durée de l’exposition : 24 h (jugement professionnel) Quantité de produit : 4 g (quantité appliquée de 2,5 g, et on prévoit que l’écran solaire en aérosol est utilisé 1,6 fois par jour; Ficheux 2016) Fraction du poids : 0,4 (communication personnelle, courriel de la DPT, Santé Canada, au BERSE, Santé Canada, 2018; sans référence) Volume de la pièce : 80 m³ (jugement professionnel; ce volume devrait être représentatif du mélange dans l’air intérieur pendant la journée) Taux de ventilation : 1/h (jugement professionnel) |
Annexe C. Estimations de l’ingestion quotidienne par groupe d’âge au sein de la population générale du Canada
| Voie d’exposition | 0 à 5 moisa (nourrissons allaités)b | 0 à 5 mois a (nourrissons allaités avec préparation)c | 6 à 11 moisd | 1 ane | 2 à 3 ansf | 4 à 8 ansg | 9 à 13 ansh | 14 à 18 ansi | 19 ans et plusj |
|---|---|---|---|---|---|---|---|---|---|
| Air ambiantk | 1,76 | 1,76 | 1,78 | 2,18 | 1,84 | 1,45 | 9,93×10-1 | 7,69×10-1 | 6,12×10-1 |
| Air intérieurl | 3,32×102 | 3,32×102 | 3,36×102 | 4,12×102 | 3,47×102 | 2,73×102 | 1,87×102 | 1,45×102 | 1,16×102 |
| Eau potablem | S.O. | 8,63×101 | 5,52×101 | 2,15×101 | 1,89×101 | 1,52×101 | 1,16×101 | 1,16×101 | 1,36×101 |
| Ingestion totale | 3,34×102 | 4,19×102 | 3,92×102 | 4,35×102 | 3,67×102 | 2,89×102 | 2,00×102 | 1,57×102 | 1,29×102 |
Abréviation : S.O., sans objet.
a On présume que le nourrisson pèse 6,3 kg (Santé Canada 2015a), respire 3,7 m³ d’air par jour (USEPA 2011 [modifié]) et ingère 21,6 mg de poussière par jour (Wilson et Meridian 2015 [modifié]). On présume qu’aucune ingestion de sol n’a lieu sur la base des pratiques courantes des personnes qui s’occupent des nourrissons.
b On présume que les nourrissons allaités seulement consomment 0,744 L de lait maternel par jour (Santé Canada 2018), et on présume que le lait maternel constitue la seule source alimentaire.
c On présume que les nourrissons nourris avec une préparation seulement consomment 0,826 L d’eau par jour (Santé Canada 2018), qui est utilisée pour reconstituer la préparation. Pour plus de renseignements, voir la note de bas de page sur l’eau potable.
d On présume que le tout-petit pèse 9,1 kg (Santé Canada 2015a), respire 5,4 m³ d’air par jour (USEPA 2011 [modifié]), boit 0 L d’eau par jour (Santé Canada 2017), ingère 7,3 mg de sol par jour et ingère 27,0 mg de poussière par jour (Wilson et Meridian 2015 [modifié]). Pour les nourrissons allaités, on présume qu’ils consomment 0,632 L de lait maternel par jour (Santé Canada 2018). Pour les nourrissons nourris avec une préparation, on présume qu’ils consomment 0,764 L d’eau par jour (Santé Canada 2018), qui est utilisée pour reconstituer la préparation. Pour plus de renseignements, voir la note de bas de page sur l’eau potable.
e On présume que l’enfant pèse 11,0 kg (Santé Canada 2015a), respire 8,0 m³ d’air par jour (USEPA 2011 [modifié]), boit 0,36 L d’eau par jour (Santé Canada 2017), ingère 8,8 mg de sol par jour et ingère 35,0 mg de poussière par jour (Wilson et Meridian 2015 [modifié]).
f On présume que l’enfant pèse 15 kg (Santé Canada 2015a), respire 9,2 m³ d’air par jour (USEPA 2011 [modifié]), boit 0,43 L d’eau par jour (Santé Canada 2017), ingère 6,2 mg de sol par jour et ingère 21,4 mg de poussière par jour (Wilson et Meridian 2015 [modifié]).
g On présume que l’enfant pèse 23 kg (Santé Canada 2015a), respire 11,1 m³ d’air par jour (USEPA 2011 [modifié]), boit 0,53 L d’eau par jour (Santé Canada 2017), ingère 8,7 mg de sol par jour et ingère 24,4 mg de poussière par jour (Wilson et Meridian 2015 [modifié]).
h On présume que l’enfant pèse 42 kg (Santé Canada 2015a), respire 13,9 m³ d’air par jour (USEPA 2011 [modifié]), boit 0,74 L d’eau par jour (Santé Canada 2017), ingère 6,9 mg de sol par jour et ingère 23,8 mg de poussière par jour (Wilson et Meridian 2015 [modifié]).
i On présume que l’adolescent pèse 62 kg (Santé Canada 2015a), respire 15,9 m³ d’air par jour (USEPA 2011 [modifié]), boit 1,09 L d’eau par jour (Santé Canada 2017), ingère 1,4 mg de sol par jour et ingère 2,1 mg de poussière par jour (Wilson et Meridian 2015 [modifié]).
j On présume que l’adulte pèse 74 kg (Santé Canada 2015a), respire 15,1 m³ d’air par jour (USEPA 2011 [modifié]), boit 1,53 L d’eau par jour (Santé Canada 2017), ingère 1,6 mg de sol par jour et ingère 2,6 mg de poussière par jour (Wilson et Meridian 2015 [modifié]).
k La concentration maximale dans l’air ambiant des maisons canadiennes (24 µg/m³) a été utilisée pour estimer de manière prudente la limite supérieure de l’ingestion quotidienne due à l’exposition par l’air ambiant (Chan et coll. 1990). L’hypothèse selon laquelle les Canadiens passent 3 heures par jour à l’extérieur est utilisée (Santé Canada 1998).
l La concentration maximale dans l’air intérieur des maisons canadiennes (647 µg/m³) a été utilisée pour estimer de manière prudente la limite supérieure de l’ingestion quotidienne due à l’exposition par l’air intérieur (Chan et coll. 1990). On a présumé que les Canadiens passent 21 heures par jour à l’intérieur (Santé Canada, 1998).
m La concentration maximale mesurée dans un réseau de puits de surveillance et un aquifère d’épandage (658 µg/L) à la décharge de Gloucester (Canada) a été utilisée pour estimer de manière prudente la limite supérieure de l’ingestion quotidienne due à l’exposition à l’eau potable (Lesage et coll. 1990).
| Voie d’exposition | 0 à 5 moisa (nourrissons allaités)b | 0 à 5 moisa (nourrissons allaités avec préparation)c | 6 à 11 moisd | 1 ane | 2 à 3 ansf | 4 à 8 ansg | 9 à 13 ansh | 14 à 18 ansi | 19 ans et plusj |
|---|---|---|---|---|---|---|---|---|---|
| Airk | 3,69×10-3 | 3,69×10-3 | 3,73×10-3 | 4,57×10-3 | 3,85×10-3 | 3,03×10-3 | 2,08×10-3 | 1,61×10-3 | 1,28×10-3 |
| Eau potablel | S.O. | 7,24×10-3 | 4,63×10-3 | 1,81×10-3 | 1,58×10-3 | 1,27×10-3 | 9,73×10-4 | 9,70×10-4 | 1,14×10-3 |
| Aliments et boissonsm | S.O. | S.O. | 5,49×10-1 | 4,55×10-1 | 3,33×10-1 | 2,17×10-1 | 1,19×10-1 | 8,06×10-2 | 6,76×10-2 |
| Ingestion totale | 3,69×10-3 | 1,00×10-2 | 5,57×10-1 | 4,61×10-1 | 3,38×10-1 | 2,21×10-1 | 1,22×10-1 | 8,32×10-2 | 7,00×10-2 |
Abréviation : S.O., sans objet.
a On présume que le nourrisson pèse 6,3 kg (Santé Canada 2015a), respire 3,7 m³ d’air par jour (USEPA 2011 [modifié]) et ingère 21,6 mg de poussière par jour (Wilson et Meridian 2015 [modifié]). On présume qu’aucune ingestion de sol n’a lieu sur la base des pratiques courantes des personnes qui s’occupent des nourrissons.
b On présume que les nourrissons allaités seulement consomment 0,744 L de lait maternel par jour (Santé Canada 2018), et on présume que le lait maternel constitue la seule source alimentaire.
c On présume que les nourrissons nourris avec une préparation seulement consomment 0,826 L d’eau par jour (Santé Canada 2018), qui est utilisée pour reconstituer la préparation. Pour plus de renseignements, voir la note de bas de page sur l’eau potable.
d On présume que le tout-petit pèse 9,1 kg (Santé Canada 2015a), respire 5,4 m³ d’air par jour (USEPA 2011 [modifié]), boit 0 L d’eau par jour (Santé Canada 2017), ingère 7,3 mg de sol par jour et ingère 27,0 mg de poussière par jour (Wilson et Meridian 2015 [modifié]). Pour les nourrissons allaités, on présume qu’ils consomment 0,632 L de lait maternel par jour (Santé Canada 2018). Pour les nourrissons nourris avec une préparation, on présume qu’ils consomment 0,764 L d’eau par jour (Santé Canada 2018), qui est utilisée pour reconstituer la préparation. Pour plus de renseignements, voir la note de bas de page sur l’eau potable.
e On présume que l’enfant pèse 11,0 kg (Santé Canada 2015a), respire 8,0 m³ d’air par jour (USEPA 2011 [modifié]), boit 0,36 L d’eau par jour (Santé Canada 2017), ingère 8,8 mg de sol par jour et ingère 35,0 mg de poussière par jour (Wilson et Meridian 2015 [modifié]).
f On présume que l’enfant pèse 15 kg (Santé Canada 2015a), respire 9,2 m³ d’air par jour (USEPA 2011 [modifié]), boit 0,43 L d’eau par jour (Santé Canada 2017), ingère 6,2 mg de sol par jour et ingère 21,4 mg de poussière par jour (Wilson et Meridian 2015 [modifié]).
g On présume que l’enfant pèse 23 kg (Santé Canada 2015a), respire 11,1 m³ d’air par jour (USEPA 2011 [modifié]), boit 0,53 L d’eau par jour (Santé Canada 2017), ingère 8,7 mg de sol par jour et ingère 24,4 mg de poussière par jour (Wilson et Meridian 2015 [modifié]).
h On présume que l’enfant pèse 42 kg (Santé Canada 2015a), respire 13,9 m³ d’air par jour (USEPA 2011 [modifié]), boit 0,74 L d’eau par jour (Santé Canada 2017), ingère 6,9 mg de sol par jour et ingère 23,8 mg de poussière par jour (Wilson et Meridian 2015 [modifié]).
i On présume que l’adolescent pèse 62 kg (Santé Canada 2015a), respire 15,9 m³ d’air par jour (USEPA 2011 [modifié]), boit 1,09 L d’eau par jour (Santé Canada 2017), ingère 1,4 mg de sol par jour et ingère 2,1 mg de poussière par jour (Wilson et Meridian 2015 [modifié]).
j On présume que l’adulte pèse 74 kg (Santé Canada 2015a), respire 15,1 m³ d’air par jour (USEPA 2011 [modifié]), boit 1,53 L d’eau par jour (Santé Canada 2017), ingère 1,6 mg de sol par jour et ingère 2,6 mg de poussière par jour (Wilson et Meridian 2015 [modifié]).
k Aucune donnée de surveillance de l’air ambiant au Canada n’a été trouvée. D’après une estimation de 6,28 ng/L, pour un scénario de rejet de 100 % dans l’air selon ChemCAN v6.00, avec l’hypothèse prudente que les quantités totales étaient rejetées dans une seule région du Canada, c.‑à‑d. la région des plaines à forêts mixtes de l’Ontario.
l Rogers et coll. (1986) ont indiqué que le DPE était un composant des fractions basiques/neutres des eaux usées et des boues sur l’île d’Iona en Colombie-Britannique, mais la concentration de DPE n’a pas été déterminée. Par conséquent, on n’a pas trouvé de données de surveillance dans lesquelles le DPE a été mesuré au Canada. D’après une estimation de 0,0552 µg/L pour un scénario de rejet de 100 % dans l’eau selon ChemCAN v6.00, avec l’hypothèse prudente que les quantités totales étaient rejetées dans une seule région du Canada, c.‑à‑d. la région des plaines à forêts mixtes de l’Ontario, avec un facteur d’émission de 100 % et un taux d’élimination de 0 % par le traitement des eaux usées (dans le cas des rejets dans l’eau).
m On ne dispose d’aucun renseignement définitif concernant le potentiel d’utilisation du DPE dans les aliments vendus au Canada. Pour calculer l’ingestion quotidienne de DPE, sous forme d’aromatisant alimentaire, on a utilisé l’estimation d’ingestion par habitant du JECFA de 5 µg par personne et par jour pour les États‑Unis (d’après les volumes de production annuelle déclarés par l’industrie dans les enquêtes sur les volumes produits) (voir la section 6.1.2).
| Voie d’exposition | 0 à 5 moisa (nourrissons allaités)b | 0 à 5 mois a (nourrissons allaités avec préparation)c | 6 à 11 moisd | 1 ane | 2 à 3 ansf | 4 à 8 ansg | 9 à 13 ansh | 14 à 18 ansi | 19 ans et plusj |
|---|---|---|---|---|---|---|---|---|---|
| Airk | 7,21×101 | 7,21×101 | 7,28×101 | 8,93×101 | 7,53×101 | 5,92×101 | 4,06×101 | 3,15×101 | 2,50×101 |
| Eau potablel | S.O. | 7,60×10-3 | 4,87×10-3 | 1,90×10-3 | 1,66×10-3 | 1,34×10-3 | 1,02×10-3 | 1,02×10-3 | 1,20×10-3 |
| Ingestion totale | 7,21×101 | 7,21×101 | 7,28×101 | 8,93×101 | 7,53×101 | 5,92×101 | 4,06×101 | 3,15×101 | 2,50×101 |
Abréviation : S.O., sans objet.
a On présume que le nourrisson pèse 6,3 kg (Santé Canada 2015a), respire 3,7 m³ d’air par jour (USEPA 2011 [modifié]) et ingère 21,6 mg de poussière par jour (Wilson et Meridian 2015 [modifié]). On présume qu’aucune ingestion de sol n’a lieu sur la base des pratiques courantes des personnes qui s’occupent des nourrissons.
b On présume que les nourrissons allaités seulement consomment 0,744 L de lait maternel par jour (Santé Canada 2018), et on présume que le lait maternel constitue la seule source alimentaire.
c On présume que les nourrissons nourris avec une préparation seulement consomment 0,826 L d’eau par jour (Santé Canada 2018), qui est utilisée pour reconstituer la préparation. Pour plus de renseignements, voir la note de bas de page sur l’eau potable.
d On présume que le tout-petit pèse 9,1 kg (Santé Canada 2015a), respire 5,4 m³ d’air par jour (USEPA 2011 [modifié]), boit 0 L d’eau par jour (Santé Canada 2017), ingère 7,3 mg de sol par jour et ingère 27,0 mg de poussière par jour (Wilson et Meridian 2015 [modifié]). Pour les nourrissons allaités, on présume qu’ils consomment 0,632 L de lait maternel par jour (Santé Canada 2018). Pour les nourrissons nourris avec une préparation, on présume qu’ils consomment 0,764 L d’eau par jour (Santé Canada 2018), qui est utilisée pour reconstituer la préparation. Pour plus de renseignements, voir la note de bas de page sur l’eau potable.
e On présume que l’enfant pèse 11,0 kg (Santé Canada 2015a), respire 8,0 m³ d’air par jour (USEPA 2011 [modifié]), boit 0,36 L d’eau par jour (Santé Canada 2017), ingère 8,8 mg de sol par jour et ingère 35,0 mg de poussière par jour (Wilson et Meridian 2015 [modifié]).
f On présume que l’enfant pèse 15 kg (Santé Canada 2015a), respire 9,2 m³ d’air par jour (USEPA 2011 [modifié]), boit 0,43 L d’eau par jour (Santé Canada 2017), ingère 6,2 mg de sol par jour et ingère 21,4 mg de poussière par jour (Wilson et Meridian 2015 [modifié]).
g On présume que l’enfant pèse 23 kg (Santé Canada 2015a), respire 11,1 m³ d’air par jour (USEPA 2011 [modifié]), boit 0,53 L d’eau par jour (Santé Canada 2017), ingère 8,7 mg de sol par jour et ingère 24,4 mg de poussière par jour (Wilson et Meridian 2015 [modifié]).
h On présume que l’enfant pèse 42 kg (Santé Canada 2015a), respire 13,9 m³ d’air par jour (USEPA 2011 [modifié]), boit 0,74 L d’eau par jour (Santé Canada 2017), ingère 6,9 mg de sol par jour et ingère 23,8 mg de poussière par jour (Wilson et Meridian 2015 [modifié]).
i On présume que l’adolescent pèse 62 kg (Santé Canada 2015a), respire 15,9 m³ d’air par jour (USEPA 2011 [modifié]), boit 1,09 L d’eau par jour (Santé Canada 2017), ingère 1,4 mg de sol par jour et ingère 2,1 mg de poussière par jour (Wilson et Meridian 2015 [modifié]).
j On présume que l’adulte pèse 74 kg (Santé Canada 2015a), respire 15,1 m³ d’air par jour (USEPA 2011 [modifié]), boit 1,53 L d’eau par jour (Santé Canada 2017), ingère 1,6 mg de sol par jour et ingère 2,6 mg de poussière par jour (Wilson et Meridian 2015 [modifié]).
k D’après les données de l’INRP sur les émissions atmosphériques et des renseignements propres aux installations, on a choisi le modèle SCREEN3 de l’USEPA pour estimer la concentration dans l’air ambiant (123 µg/m³).
l Aucune donnée de surveillance de l’eau potable au Canada n’a été trouvée. D’après une estimation de 0,058 µg/L pour un scénario de rejet de 100 % dans l’eau selon ChemCAN v6.00, avec l’hypothèse prudente que les quantités totales étaient rejetées dans une seule région du Canada, c.‑à‑d. la région des plaines à forêts mixtes de l’Ontario, avec un facteur d’émission de 100 % et un taux d’élimination de 0 % par le traitement des eaux usées (dans le cas des rejets dans l’eau).
