Ébauche de l’évaluation préalable du groupe des thiophosphates d’alkyle
Titre officiel : Ébauche de l’évaluation préalable du groupe des thiophosphates d’alkyle
Numéros d’identification confidentiels :
- 11145‑3
- 11105‑8
Environnement et Changement climatique Canada
Santé Canada
Mars 2021
Synopsis
En vertu de l’article 74 de la Loi canadienne sur la protection de l’environnement de 1999 (LCPE), les ministres de l’Environnement et de la Santé ont réalisé l’évaluation préalable de deux substances appelées collectivement groupe des thiophosphates d’alkyle (TPAE). Les substances de ce groupe ont été jugées d’intérêt prioritaire pour une évaluation car elles satisfont aux critères de catégorisation du paragraphe 73(1) de la LCPE. Nous donnons dans le tableau ci-après leurs noms en nomenclature de l’Union internationale de chimie pure et appliquée (UICPA) ou leurs appellations commerciales, leurs numéros de registre du Chemical Abstracts Service (no CASNote de bas de page 1), ainsi que leurs numéros d’identification confidentiels (NIC).
| Acronyme | Nom de la substance | No CASb | NICc |
|---|---|---|---|
| TPAE-1a | Produits de la réaction du 4‑méthylpentan-2-ol et du pentasulfure de diphosphore, propoxylés, estérifiés avec du pentaoxyde de diphosphore, sels de tert-alcanamine en C12-14 | 91745-46-9 | 11145-3 |
| TPAE-2a | Phosphorothioate de O,O-dibutyle, mélange de sels d’alcanamines en C8, C16 ou C18d | Non disponible | 11105-8 |
a Cette substance est un UVCB (substances de composition inconnue ou variable, produits de réaction complexes ou matières biologiques).
b No CAS, numéro de registre du Chemical Abstracts Service.
c NIC, numéro d’identification confidentiel.
d Ceci est un nom commercial. Cette substance comporte deux constituants principaux qui ont chacun un nom en nomenclature de l’UICPA.
Les deux substances décrites ci-dessus et visées par la présente évaluation préalable seront appelées ci-après TPAE-1 et TPAE-2. Il a été déterminé dans le cadre du projet d’examen des revendications d’identité confidentielle de substances que les identités de ces substances ne sont plus considérées comme des renseignements commerciaux confidentiels et, en conséquence, elles sont divulguées dans le présent document.
D’après les renseignements recueillis en réponse à une enquête menée en vertu de l’article 71 de la LCPE, de 100 000 à 1 000 000 kg de TPAE-1 et 500 kg de TPAE-2 ont été importés au Canada en 2011. Ces substances sont utilisées au Canada dans des lubrifiants industriels et pour automobile. Le TPAE-1 est également utilisé dans des fluides pour le travail des métaux.
Les deux substances de ce groupe sont composées principalement d’anions de dithiophosphate ou de thiophosphate d’alkyle et de leurs contre-ions d’amine aliphatique primaire. Le TPAE-1 est la substance la plus complexe des deux, comportant environ dix composants majeurs dont des dithiophosphates, des thiophosphates et des phosphates d’alkyle, en plus d’un thiophosphate neutre. À l’exception du composant neutre du TPAE-1, tous les composants de ces substances sont ionisés dans des conditions environnementales ambiantes et certains, en particulier les contre-ions d’amine aliphatique, ont des propriétés tensio-actives.
Les données empiriques sur l’écotoxicité des substances complètes, ainsi que celles sur les amines aliphatiques, ont été utilisées pour calculer des valeurs critiques de toxicité pour les substances de ce groupe. Ces données indiquent que les composants (di)thiophosphate d’alkyle et amine aliphatique des TPAE présentent une toxicité chronique élevée pour les organismes aquatiques, et que les composants amine aliphatique ont une toxicité chronique faible à modérée pour les organismes vivant dans les sols. Il a aussi été mis en évidence que le TPAE-1 est biodégradé très lentement. Ces substances devraient persister dans l’environnement assez longtemps pour causer une toxicité chronique. Toutefois, elles ne sont pas hautement bioaccumulatives.
Les potentiels de rejet dans l’environnement les plus élevés sont dus à deux utilisations industrielles des TPAE, à savoir la formulation de lubrifiants et l’utilisation dans des fluides pour le travail des métaux. Les concentrations des composants représentatifs du TPAE-1 dans l’environnement aquatique associées aux rejets dus à ces utilisations, suite à un traitement des eaux usées, ont été estimées et comparées aux concentrations estimées sans effet pour les organismes aquatiques. De plus, les concentrations des composants amine aliphatique du TPAE-1 dans les sols, suite à une application de biosolides provenant d’usines de traitement des eaux usées, ont été estimées et comparées aux concentrations estimées sans effet pour les organismes vivant dans les sols. En se basant sur ces comparaisons, il a été déterminé que le TPAE-1 peut poser un risque pour les organismes aquatiques et ceux vivant dans les sols dû à son utilisation dans des fluides pour le travail des métaux. En se basant sur les profils d’utilisation actuels, il est improbable que le TPAE-2 pose un risque à ces organismes.
Compte tenu de tous les éléments de preuve avancés dans l’ébauche d’évaluation préalable, il existe un risque d’effets nocifs du TPAE-1 sur l’environnement. Il est proposé de conclure que le TPAE-1 satisfait aux critères de l’alinéa 64 a) de la LCPE, car il pénètre ou peut pénétrer dans l’environnement en une quantité ou concentration ou dans des conditions qui ont ou peuvent avoir un effet nocif immédiat ou à long terme sur l’environnement ou sa diversité biologique. Toutefois, il est proposé de conclure que le TPAE-1 ne satisfait pas aux critères de l’alinéa 64 b) de la LCPE, car il ne pénètre pas dans l’environnement en une quantité ou concentration ni dans des conditions qui constituent ou peuvent constituer un danger pour l’environnement essentiel à la vie.
Compte tenu de tous les éléments de preuve avancés dans l’ébauche d’évaluation préalable, il existe un faible risque d’effets nocifs du TPAE-2 sur l’environnement. Il est proposé de conclure que le TPAE-2 ne satisfait pas aux critères des alinéas 64 a) et 64 b) de la LCPE, car il ne pénètre pas dans l’environnement en une quantité ou concentration ou dans des conditions qui ont ou peuvent avoir un effet nocif immédiat ou à long terme sur l’environnement ou sa diversité biologique ou qui constituent ou peuvent constituer un danger pour l’environnement essentiel à la vie.
En ce qui a trait à la santé humaine, le TPAE-2 a déjà fait l’objet d’une évaluation lors de l’Évaluation préalable rapide des substances pour lesquelles l’exposition de la population générale est limitée. Il a alors été déterminé que le potentiel d’exposition directe ou indirecte de la population générale était négligeable. Le TPAE-2 est donc jugé peu préoccupant pour la santé humaine aux niveaux actuels d’exposition.
Nous n’avons trouvé aucune mesure de concentration de TPAE-1 dans les milieux de l’environnement au Canada, ni ailleurs. Toutefois, des rejets dans l’environnement ont été estimés pour cette substance pour la formulation de lubrifiants et pour l’utilisation dans des fluides pour le travail des métaux. Les effets critiques sur la santé incluaient des effets sur les glandes surrénales et des effets sur le système nerveux. La comparaison des estimations d’exposition par voie orale due à l’eau potable et des niveaux associés à des effets critiques lors d’études en laboratoire a conduit à calculer des marges d’exposition jugées adéquates pour tenir compte des incertitudes des bases de données sur les expositions et les effets sur la santé humaine.
Compte tenu des renseignements présentés dans la présente ébauche d’évaluation préalable, il est proposé de conclure que ces deux substances du groupe des thiophosphates d’alkyle ne satisfont pas aux critères de l’alinéa 64 c) de la LCPE, car elles ne pénètrent pas dans l’environnement en une quantité ou concentration ni dans des conditions qui constituent ou peuvent constituer un danger au Canada pour la vie ou la santé humaine.
Il est donc proposé de conclure que le TPAE-1 satisfait à un ou plusieurs des critères de l’article 64 de la LCPE, alors que le TPAE-2 ne satisfait à aucun d’eux.
Il est aussi proposé de conclure que le TPAE-1 satisfait aux critères de persistance, mais pas à ceux de bioaccumulation, du Règlement sur la persistance et la bioaccumulation de la LCPE.
1. Introduction
En vertu de l’article 74 de la Loi canadienne sur la protection de l’environnement de 1999 (LCPE) (Canada 1999), les ministres de l’Environnement et de la Santé ont réalisé l’évaluation préalable de deux substances appelées collectivement groupe des thiophosphates d’alkyle (TPAE) afin de déterminer si elles présentent ou peuvent présenter un risque pour l’environnement ou la santé humaine. Les substances de ce groupe ont été jugées d’intérêt prioritaire pour une évaluation, car elles satisfont aux critères de catégorisation du paragraphe 73(1) de la LCPE (ECCC, SC [modifié en 2017]). Les substances de ce groupe ont des structures chimiques similaires, ces deux substances comportant des anions dithiophosphate ou thiophosphate d’alkyle et des contre-ions amine aliphatique primaire. La première des deux substances visée par la présente évaluation préalable a le numéro de registre du Chemical Abstracts Service (no CAS[1]) 91745-46-9 et le numéro d’identification confidentiel (NIC) 11145-3. La seconde a le NIC 11105-8, mais pas de no CAS. Ci-après, ces substances sont respectivement désignées par les acronymes TPAE-1 et TPAE-2. Nous donnons à la section 2 plus de renseignements sur l’identité de ces substances, y compris leurs noms en nomenclature de l’Union internationale de chimie pure et appliquée (UICPA) ou leurs noms commerciaux.
Il a été déterminé lors de la phase pilote du Projet d’examen des revendications d’identité confidentielle de substances que les identités de ces substances ne sont plus considérées comme des renseignements commerciaux confidentiels. Ce projet découle de l’Approche pour divulguer des renseignements confidentiels et favoriser la transparence dans la gestion des produits chimiques (l’Approche) (Canada 2018). Il est établi dans ce document de politique plusieurs mesures pour améliorer la transparence de la gestion des produits chimiques au Canada, y compris l’introduction d’un examen des revendications de confidentialité pour des identités de substance après une période de dix ans. Pour mettre en œuvre cette partie de l’Approche, un projet pilote a été initié pour examiner le cas de 24 substances de la Liste intérieure des substances (LIS), y compris ceux du TPAE-1 et du TPAE-2. Grâce à ce processus, les déclarants du TPAE‑1 et du TPAE-2 ont confirmé qu’ils ne requièrent plus d’identité confidentielle pour ces deux substances et, en conséquence, nous divulguons ces identités dans le présent document.
Le TPAE-2 a été évalué en suivant l’approche de l’Évaluation préalable rapide des substances pour lesquelles l’exposition de la population générale est limitée (ECCC, SC 2018), et il a été montré que cette substance est peu préoccupante pour la santé humaine.
Pour la présente ébauche d’évaluation préalable, nous avons tenu compte de renseignements sur les propriétés chimiques, le devenir dans l’environnement, les dangers, les utilisations et expositions, y compris de renseignements additionnels soumis pas des parties intéressées. Des données pertinentes ont été identifiées jusqu’en septembre 2018, et une recherche bibliographique ciblée a été faite jusqu’en mars 2020. Des données empiriques tirées d’études clés et des résultats de modélisation ont été utilisés pour tirer nos conclusions. Quand ils étaient pertinents, nous avons tenu compte de renseignements présentés dans des évaluations d’autres juridictions.
La présente ébauche d’évaluation préalable a été préparée par le personnel travaillant au programme d’évaluation des risques de la LCPE de Santé Canada et d’Environnement et Changement climatique Canada. Elle inclut des intrants d’autres programmes de ces deux ministères. La partie portant sur l’environnement a fait l’objet d’un examen externe. Des commentaires sur les parties techniques pertinentes pour l’environnement ont été faits par James Armitage (AES Environmental Services Inc.), Connie Gaudet et Meredith Curren. Bien que des commentaires de l’extérieur aient été pris en compte, Santé Canada et Environnement et Changement climatique Canada restent responsables du contenu et des conclusions de la présente évaluation.
La présente ébauche d’évaluation préalable est centrée sur des renseignements critiques pour déterminer si ces substances satisfont aux critères de l’article 64 de la LCPE en examinant des renseignements scientifiques et en suivant une approche basée sur le poids de la preuve et le principe de précautionNote de bas de page 2. Nous présentons dans la présente ébauche d’évaluation préalable les renseignements critiques et les éléments pris en compte à partir desquels nous avons tiré nos conclusions.
2. Identité des substances
Les deux substances de ce groupe sont des UVCB (substances de composition inconnue ou variable, produits de réaction complexes ou matières biologiques). Les UVCB sont des substances dérivées de sources naturelles ou de réactions complexes qui ne peuvent pas être caractérisées en termes de constituants chimiques, car leur composition est trop complexe ou variable. Un UVCB n’est pas un mélange défini de substances discrètes, et il est considéré comme une substance simple. Nous donnons dans le tableau 2-1 le NIC des substances, ainsi que leur nom descriptif et, si disponible, leur numéro CAS.
| Acronyme | Nom de la substance | No CAS | No CE | NIC |
|---|---|---|---|---|
| TPAE-1 |
Produits de la réaction du 4‑méthylpentan-2-ol et du pentasulfure de diphosphore, propoxylés, estérifiés avec du pentaoxyde de diphosphore, sels de tert-alcanamines en C12-14a (Alcanamines en C12-14, produits de la réaction avec de l’hexanol, de l’oxyde de phosphore (P2O5), du sulfure de phosphore (P2S5) et du méthyloxiraneb |
91745-46-9 | 294-716-2d, 931-384-6 | 11145-3 |
| TPAE-2 | Phosphorothioate de O,O‑dibutyle, mélange de sels d’alcanamines en C8, C16 ou C18c | Non disponible | Non disponible | 11105-8 |
Abréviations : no CAS = numéro de registre du Chemical Abstracts Service; no CE = numéro de la Communauté européenne; NIC = numéro d’identification confidentiel.
a Nom de substance utilisé dans le rapport d’évaluation de REACH.
b Nom de la substance associé au no CAS.
c Ceci est un nom commercial. La substance comporte deux composants principaux qui ont chacun un no CAS (voir le tableau 2-3).
d Ce no CE est lié au no CAS. L’autre no CE ne l’est pas.
Le TPAE-1 est composé d’une variété de phosphorodithioates/phosphorothioates d’alkyle et de phosphates d’alkyle, qui sont tous des anions accompagnés de leurs contre-ions de tert-alcanamine en C12-14, à l’exception d’un composant neutre (tableau 2-2). Les renseignements de l’industrie mentionnent environ 10 structures majeures pour cette substance, qui sont présentes dans le produit commercial en concentrations variables, accompagnées du cation amine aliphatique (Présentation de projet 2018; tableau 2-2). Les structures présentent en quantités molaires les plus importantes sont des amines aliphatiques, étant donné qu’elles sont les contre-ions de toutes les autres structures ioniques présentes dans cet UVCB, et il est estimé qu’elles représentent environ 40 % des molécules du mélange, soit environ 25 % du poids. Les données sur la composition de la substance fournies à Environnement et Changement climatique Canada (ECCC) et Santé Canada (HC), basées sur des analyses d’un seul échantillon par chromatographie en phase liquide/spectrométrie de masse et par résonance magnétique nucléaire du phosphore (Présentation de projet 2018; ECHA 2019a), ne comportaient pas les pourcentages de chacune des structures majeures, mais plutôt les gammes de pourcentages assignées à chaque groupe de structures.
| Numéro de la structure | Masse moléculaire (g/mol)a | Représentation de la structure chimique |
|---|---|---|
| Amine aliphatiqueb | 185,35 | 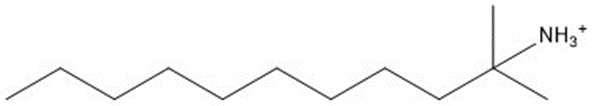 |
| 1 | 356,52 | 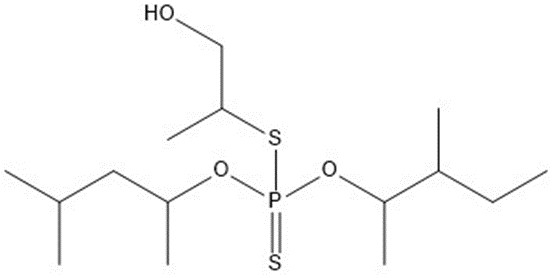 |
| 2 | 436,51 | 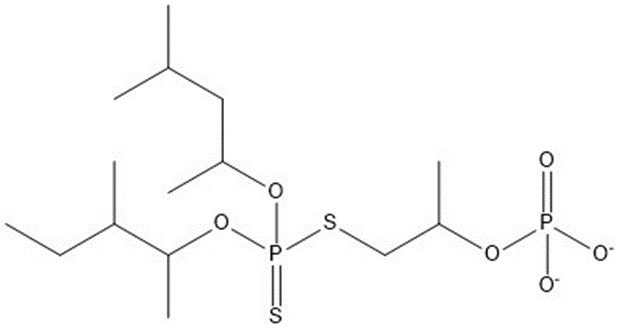 |
| 3 | 775,02 | 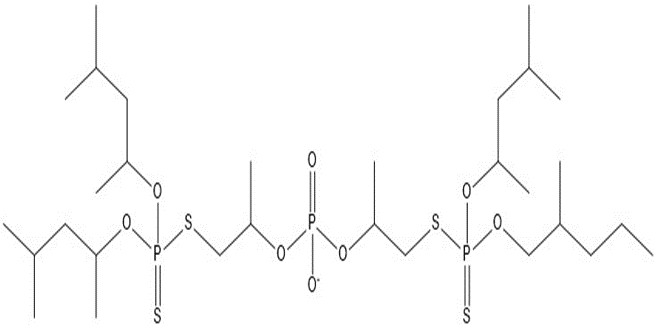 |
| 4 | 520,67 | 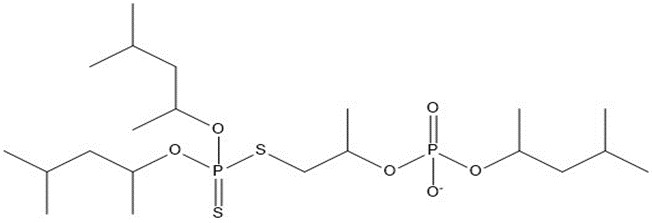 |
| 5 | 282,38 | 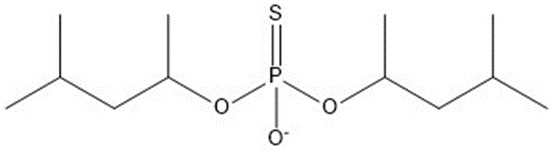 |
| 6 | 346,29 | 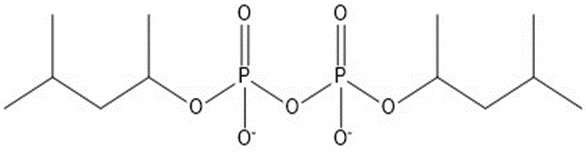 |
| 7 | 586,62 | 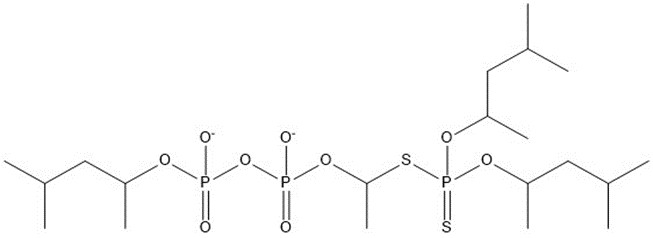 |
| 8 | 855,00 | 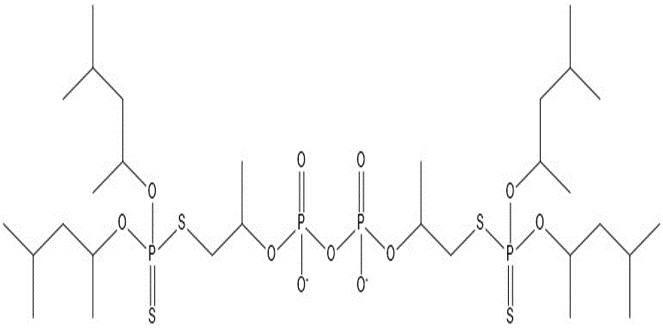 |
| 9 | 182,15 | 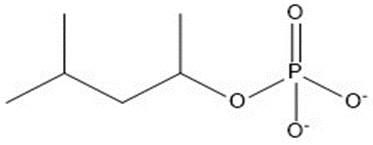 |
| 10 | 250,31 | 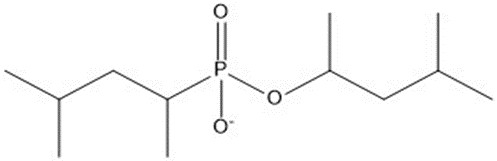 |
a Les masses des structures représentatives ne comprennent pas celles des contre-ions d’amine aliphatique.
b La structure représentative présentée est celle d’une tert-alcanamine en C12. Le composant amine aliphatique présent dans l’UVCB est un mélange de tert-alcanamines en C12-14.
| Constituant | Nom UICPA | No CAS ou no CE |
|---|---|---|
| Constituant A | Phosphorothioates d’O,O-dibutyle, sels d’alcanamines en C16 ou C18 saturées ou insaturées | No CE 947-129-7a |
| Constituant B | Hydrogénothiophosphate d’O,O-dibutyle, composé avec de l’octanamine (1/1) | 93964-99-9 |
Abréviation : no CAS = numéro de registre du Chemical Abstracts Service; no CE = numéro de la Communauté européenne; UICPA = Union internationale de chimie pure et appliquée.
a Aucun no CAS assigné.
Le TPAE-2 est enregistré dans le cadre du règlement REACH (Registration, Evaluation, Authorisation and Restriction of Chemicals) de l’Union européenne sous chacun de ses deux principaux composants (voir le tableau 2-3), plutôt que comme substance simple (tel que décrit dans le tableau 2-1). Toutefois, les constituants individuels ne sont produits et distribués qu’ensemble, et ne sont pas vendus commercialement séparément (communication personnelle, lettre de parties intéressées de l’industrie à Environnement et Changement climatique Canada, du 20 novembre 2017; non référencé). Le constituant A (tableau 2-3) représente la plus grande partie du TPAE-2, soit environ 84 % de son poids, et 12 % pour le constituant B. Le composant thiophosphate d’alkyle est présent dans les constituants A et B du TPAE-2, la composition du composant amine aliphatique étant différente (tableau 2-4). Le composant amine aliphatique du constituant A est variable. Toutefois, ka structure représentative de l’amine du constituant A comportant 18 atomes (représentée dans le tableau 2-4) représente 60 À 80 % de ce constituant (ECHA 2018a). Le composant amine aliphatique du constituant B est constitué d’un élément majeur avec moins de 10 % en poids d’impuretés. Des renseignements plus détaillés sur la composition des constituants A et B du TPAE-2 sont donnés dans leurs dossiers REACH (ECHA 2017, 2018a). Le reste du TPAE-2 (environ 4 % en poids) est un mélange d’alcanamines n’ayant pas réagi, dont celles de no CAS 40165-68-2 [(9Z)-N-((9Z)-octadéc-9-ènyl)octadéc-9-èn-1-amine], 112-90-3 [(9Z)-octadéc-9-èn-1-amine] et 111-86-4 [octanamine] (communication personnelle, courriel d’une partie intéressée de l’industrie à Environnement et Changemant climatique Canada, 25 avril 2018; non référencé).
| Structure | Masse moléculaire (g/mol)a | Représentation de la structure chimique |
|---|---|---|
| 11105-8, thiophosphate d’alkyle (constituants A et B) | 226.27 | ![O-]P(OCCCC)(OCCCC)=S](/content/dam/eccc/images/pded/tpaes/20210118-Table2-4-1.jpg) |
| 11105-8, amine en C18 (constituant A) | 269.52 | 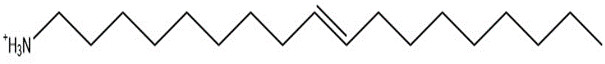 |
| 11105-8, amine en C8 (constituant B) | 129.24 | 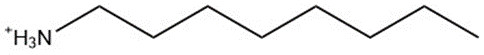 |
2.1 Sélection d’analogues et utilisation de modèles (Q)SAR
Nous avons suivi une approche de lecture croisée en utilisant des données d’analogues et les résultats de modèles (Q)SAR (relation quantitative structure-activité), si nécessaire, pour informer l’évaluation ayant trait à l’environnement. Les analogues retenus avaient des structures et/ou des fonctions similaires à celles de substances de ce groupe (p. ex. propriétés physico-chimiques similaires, même mécanisme d’action toxique), et des données empiriques pertinentes sur ceux-ci étaient disponibles pour permettre une lecture croisée avec celles des substances du groupe des TPAE, pour lesquelles les données empiriques étaient limitées. Les noms et structures des analogues utilisés pour le présent rapport sont confidentiels, étant donné qu’ils ont été déclarés en vertu du Règlement sur les renseignements concernant les substances nouvelles (RRSN). Toutefois, ils ont des structures presque similaires à certaines des structures représentatives du TPAE-1 en ce qu’ils comportent des entités phosphorodithioates d’alkyle ionisées associées à des sels d’amines aliphatiques ramifiées. Il est bon toutefois de noter que le choix d’analogues d’UVCB comporte une plus grande incertitude que dans le cas de substances discrètes, en raison de la diversité des composants et de la variabilité de la composition. L’utilisation de données sur l’écotoxicité d’analogues est discutée plus en détail à la section 6.1.
L’applicabilité de modèles (Q)SAR a été déterminée au cas par cas. Des détails sur les données de lecture croisée et les modèles (Q)SAR retenus pour informer l’évaluation ayant trait à l’environnement du groupe des TPAE sont donnés dans les sections pertinentes du présent rapport.
| Analogue | Solubilité dans l’eau | Koe | Données sur la biodégradation | Données sur l’écotoxicité | Données sur la santé humaine |
|---|---|---|---|---|---|
| DNS substance 1 | O | O | N | N | NR |
| DNS substance 2 | O | O | O | O | NR |
Abréviations : O = oui; N = non; NR = non requis; DNS = déclaration de nouvelle substance
3. Propriétés physiques et chimiques
Nous donnons dans le tableau 3-1 des données mesurées et modélisées sur les propriétés physiques et chimiques des deux substances du groupe des TPAE, alors que les données sur les substances analogues sont données à l’Annexe A. Étant donné la complexité des TPAE et celle des substances analogues, qui sont des UVCB ionisés, il existe des défis intrinsèques à la mesure des leurs propriétés physiques et chimiques. Ces données peuvent donc être associées à une incertitude significative.
| - | TPAE-1 | TPAE-2, constituant A | TPAE-2, constituant B |
|---|---|---|---|
| État physique (20 °C) | liquide | liquide | liquide |
| Point de fusion (°C) | -6 (point d’écoulement) | < -20 | < -20 |
| Point d’ébullition (°C à 101,3 kPa) | 198 (initial) | 215 (initial) | 201 (initial) |
| Pression de vapeur (Pa) | 3,2 x 10-2 | 2,2 x 10-2 | 1,8 |
| Densité (sans unité) | 1,02 à 15,6 °C | 0,938 à 20 °C | 0,969 à 20 °C |
| Solubilité dans l’eau (mg/L au taux de charge en mg/L) | 39,5 à 100 | 20,7 à 10 000 | 4,9 à 10 000 |
| Solubilité dans l’eau (mg/L au taux de charge en mg/L) | 138 à 1000 | 15,4 à 1000 | 4,7 à 100 000 |
| log Koe (sans dimension) | Gamme : < 0,30 à > 7,1a | Amines aliphatiques en C16-18 : 4,61 (± 5,2) | Amines aliphatiques en C8 : 1,07 (± 0,24) |
| log Koe (sans dimension) | ND | Phosphorothioate de dibutyle : 2,73 (± 1,8) | Phosphorothioate de dibutyle : 1,37 (± 0,36) |
| log Koc (sans dimension) | < 1,25 à ≤ 5,09b | Amines aliphatiques en C16-18 : 3,42c | ND |
| log Koc (sans dimension) | ND | Phosphorothioate de dibutyle : 2,51c | ND |
Notes : les références pour les constituants A et B du TPAE-2 sont tirées d’ECHA 2018a et d’ECHA 2017, respectivement. La référence pour les données sur le TPAE-1 est tirée d’ECHA 2019a.
Abréviations : NA = non disponible; Koe = coefficient de partage octanol-eau; Koc = coefficient de partage carbone organique-eau.
a 38 % de la surface avait un Koe > 7,1, 24 % un Koe de 1,8 et 9,8 % un Koe de 4,9.
b 68 % de la surface avait un Koc < 1,25, 32 % un Koc de 1,36 à ≤ 5,09.
c Calcul basé sur des modèles QSAR (ECHA 2017, 2018a).
La caractérisation analytique du TPAE-2 rapportée dans des études sur l’écotoxicité suggère que les sels amine-thiophosphate se dissocient dans des systèmes aqueux (section 6.1.2), et il est assumé que le TPAE-1 se dissocie aussi dans l’eau. Les propriétés physico-chimiques des composants représentatifs thiophosphate et amine des TPAE ont été prises en compte en plus de celles des UVCB complets rapportées dans le tableau 3-1. Toutes les structures représentatives du TPAE-1 et du TPAE-2 sont ionisées, à l’exception d’un composant neutre du TPAE-1. Il est prédit que les composants dithio/thio/phosphate d’alkyle de ces structures sont tous des acides forts, avec des log pKa prédits dans la gamme 0,8-2,7 (ACD/Percepta c1997-2012). Ils seront donc presque complètement ionisés (chargés négativement) aux pH pertinents pour l’environnement dans la gamme 5-9. Toutes les amines aliphatiques primaires ont un pKa d’environ 10,5 (ECCC, SC 2021) et, en conséquence, sont ionisées à presque 100 % (chargées négativement) aux pH pertinents pour l’environnement dans la gamme 5-9.
Il est prédit que les structures (di)thiophosphate d’alkyle ont des propriétés tensio‑actives, étant donné que les composants/structures ont tous des tensions superficielles prédites d’environ 28-29 dyn/cm (TEST 2016), une valeur bien inférieure à 60 dyn/cm en dessous de laquelle les substances sont considérées avoir des propriétés tensio-actives (CE 1992). Les amines aliphatiques ont aussi des propriétés tensio‑actives (ECCC, SC 2021).
Nous avons aussi utilisé des modèles (Q)SAR pour obtenir des valeurs pour des propriétés physico-chimiques des composants (di)thiophosphate d’alkyle et amine aliphatique de ces substances (tableau 3-3). Il serait bon de noter que ces modèles (p. ex. EPI Suite c2000-2012, AIEPS c2010-2012, CATALOGIC 2014), à l’exception du modèle ACD/Percepta (c1997-2012), ne sont pas conçus pour modéliser des formes ionisées de ces substances, qui sont les formes de la plupart de ces structures représentatives aux pH ambiants des eaux naturelles (5 à 9). Le logiciel TEST (Toxicity Estimation Software Tool) (2016) fait des prédictions basées sur les substances les plus similaires disponibles dans l’ensemble d’apprentissage, qui peuvent être ionisées ou non.
Étant donné les incertitudes intrinsèques à la modélisation des propriétés physiques/chimiques de substances ionisées et de celles ayant des propriétés tensio‑actives, il a été décidé d’utiliser une structure de dithiophosphate d’alkyle représentative (structure 1) du TPAE-1, qui est la seule structure non ionisée, pour représenter les propriétés physiques/chimiques des composants (di)thiophosphate d’alkyle et phosphate d’alkyle de cette substance. Cette structure ayant un log Koe prédit de 5,4 à 5,9, ce choix est considéré prudent pour la modélisation de paramètres tels que la bioaccumulation. Une tert-alcanamine en C12 est utilisée pour représenter les contre‑ions du TPAE-1, qui sera appelé composant amine aliphatique du TPAE-1.
Des propriétés physico-chimiques d’autres structures du TPAE-1 ont été modélisées. Toutefois, nous ne sommes pas certains de la validité de certains résultats dans le cas de substances ionisées. Ces valeurs n’ont donc pas été rapportées dans le tableau 3-2. Les masses moléculaires et tailles de ces structures sont très variables (tableau 2-2) et, en conséquence, leurs propriétés prédites sont aussi très variables. Le log D des principales structures à un pH de 7 va de -3,8 (structure 10) à 6,9 (structure 3) et la solubilité dans l’eau à un pH de 7 de 1,5 mg/L (structure 3) à 1 x 106 mg/L (structure 10) (ACD/Percepta c1997-2012). Toutefois, il est prédit qu’elles ont toutes une faible pression de vapeur (< 0,13 Pa) (ACD/Percepta c1997-2012).
| - | Structure 1, TPAE-1 | Composant thiophosphate d’alkyle, TPAE-2a | Référence |
|---|---|---|---|
| log Koe (sans dimension) | 5,9 | ND | KOWWIN (2010) |
| log D à pH 7 (sans dimension) | 5,4 | -1,1 | ACD/Percepta (c1997-2012 ) |
| Solubilité dans l’eau (mg/L) | 0,055 – 1,1b | 3,7 x 105 | ACD/Percepta (c1997-2012 ) |
| Pression de vapeur (Pa, 20 °C) | 5,2 x 10-5 | 6,6 x 10-3 | EPI Suite (c2000‑2012) |
| Constante de Henry (Pa.m3/mol) | 7,0 x 10-3 | 2,0 x 10-1 | HENRYWIN (2008), méthode Bond |
| log Kco (sans dimension) | 3,1- 3,7c | 2,6 | KOCWIN (2010), méthode MCI |
Abréviations : log D = log du rapport de distribution octanol-eau; Koe = coefficient de partage octanol-eau; Koc = coefficient de partage carbon organique-eau; MCI = molecular connectivity index.
a La modélisation est basée sur la forme neutre de ce composant, à l’exception du log D et de la solubilité dans l’eau.
b Solubilités dans l’eau estimées au moyen des modèles suivants : WSKOWWIN (2010), WATERNT (2010) et ACD/Percepta (c1997-2012).
c Estimation de 3,7 basée sur le Koe.
La détermination des propriétés physico-chimiques des amines aliphatiques est compliquée en raison de leurs propriétés tensio-actives et ioniques, tel que discuté plus en détail dans le rapport d’évaluation de ce groupe de substances (ECCC, SC 2021). Nous avons utilisé ACD/Percepta (c1997-2012) pour modéliser la solubilité dans l’eau des amines aliphatiques, afin de compléter les données expérimentales limitées (ECCC, SC 2021). Étant donné que le comportement de bioconcentration et de partage des substances tensio-actives et ionisées ne correspond pas bien à leur Koe (ECCC, SC 2021), d’autres paramètres ont été utilisés pour décrire le comportement de partage des amines aliphatiques, dont le coefficient de partage solide-eau (Kd), un coefficient de partage carbone organique-eau spécifique aux cations (Kco-cation), un coefficient de partage pour les interactions ioniques avec les argiles (KCEC) et le coefficient de partage membrane-eau (Kme) (ECCC, SC 2021). La tendance générale de ces coefficients de partage est que la proportion d’amines aliphatiques se retrouvant dans les sols, argiles ou membranes croît avec la longueur de la chaîne. Les propriétés physico-chimiques modélisées ou mesurées des structures représentatives des amines aliphatiques du groupe des TPAE sont résumées dans le tableau 3-3.
| Structure | pKaa | Solubilité dans l’eau (mg/L) à pH 7 (pH 6‑9)a | Pression de vapeur à 20 °C (Pa)b |
|---|---|---|---|
| TPAE-1 amine aliphatique en C12 | 10,5 | 18 400 (941 - 22 300) | 6,1 |
| TPAE-2, constituant B, amine aliphatique en C8 | 10,5 | 197 000 (10 500 – 235 000) | 129(E), 131 |
| TPAE-2, constituant A, amine aliphatique en C18 | 10,5 | 4,6 (0,21 -5,6) | 0,012 |
Abréviations : pKa = constante de dissociation acide; E = valeur expérimentale (tirée de la base de données d’EPI Suite c2000-2012).
a Modélisé avec ACD/Percepta c1997-2012.
b Modélisé avec EPI Suite c2000-2012.
4. Sources, utilisations et rejets
Les deux substances du groupe des TPAE ont été visées par une enquête menée en vertu de l’article 71 de la LCPE (Canada 2012). Il a été rapporté en 2011 que les deux ont été importées au Canada, mais qu’aucune n’y a été produite au-dessus du seuil de déclaration de 100 kg (tableau 4-1).
| Substance | Importation totalea (kg) | Production totalea(kg) |
|---|---|---|
| TPAE-1 | 100000 to 1000000 | ND |
| TPAE-2 | 500 | ND |
Abréviations : ND = non déclaré au-dessus du seuil de déclaration de 100 kg.
a Les valeurs reflètent les quantités rapportées en réponse à une enquête menée en vertu de l’article 71 de la LCPE (Environnement Canada 2013). Voir l’enquête pour les inclusions et exclusions spécifiques (annexes 2 et 3).
Les deux substances de ce groupe sont utilisées au Canada dans des lubrifiants industriels et pour automobile et comme additifs de lubrifiants (ECCC 2015). Une des utilisations rapportées du TPAE-1 est comme lubrifiant pour la manufacture de machinerie (ECCC 2015). Pour la présente évaluation, ceci a été interprété comme une utilisation dans des fluides pour le travail des métaux, pour procurer une protection contre l’oxydation, la corrosion ou des températures/pressions extrêmes. Les fluides pour le travail des métaux peuvent être utilisés par diverses industries, dont celles de l’aviation, de la construction navale, de l’automobile, de la production d’équipement électronique, des transports ou autres. Les TPAE peuvent aussi être utilisés comme additif dans des produits de lubrification re-raffinés, produits à partir huiles usées qui sont retraitées dans des installations spécialisées.
La seule utilisation identifiée du TPAE-2 au Canada est en tant que composant d’huiles hydrauliques, avec une teneur recommandée de moins de 1 % dans l’huile formulée (communication personnelle, courriel d’une partie intéressée de l’industrie à Environnement et Changement climatique Canada, du 12 septembre 2018; non référencé). Toutefois, le TPAE-2 peut aussi être utilisé comme additif anti-usure exempt de cendre dans des huiles pour engrenages (automobiles et industrielles), des huiles hydrauliques, des huiles pour compresseur et des huiles pour moteur de camion léger (communication personnelle, courriel d’une partie intéressée de l’industrie à Environnement et Changement climatique Canada, du 12 septembre 2018; non référencé). En Europe, il est utilisé pour la production de véhicules et de machinerie, en tant qu’adjuvant de fabrication, et comme réactif de laboratoire (ECHA 2017, 2018a).
Les utilisations des TPAE pouvant conduire à des rejets dans l’environnement sont la formulation de produits et, dans le cas du TPAE-1, l’utilisation dans des fluides pour le travail des métaux. La plupart des installations utilisant des TPAE rejetteraient leurs effluents vers des systèmes de traitement des eaux usées (STEU) hors site, dans lesquels les TPAE peuvent se retrouver dans les boues. Il est donc aussi possible que des TPAE présents dans les biosolides produits par des STEUNote de bas de page 3 puissent être épandus sur des terres agricoles. Nous discutons de ces scénarios de rejet potentiel à la section 6.2.
Les fluides usés à base d’huile utilisés pour le travail des métaux sont collectés et éliminés quand ils ne satisfont plus aux exigences provinciales/territoriales. De petites quantités de ces fluides usés, à base d’huile ou d’eau, peuvent pénétrer dans les circuits d’eaux usées et se retrouver dans des STEU. L’élimination des TPAE présents dans d’autres huiles lubrifiantes ne devrait pas conduire à des rejets significatifs dans l’environnement, étant donné qu’il existe des règlements provinciaux/territoriaux qui requièrent le recyclage des huiles lubrifiantes (Environnement Canada, Santé Canada 1994, Environnement Canada 2011, ChemInfo Services 2016).
5. Devenir et comportement dans l’environnement
5.1 Distribution environnementale
Ci-après, nous décrivons qualitativement la distribution des composants des TPAE, y compris des amines aliphatiques à longue chaîneNote de bas de page 4, dans les différents milieux de l’environnement (air, eau, sol, sédiments et biote), basée sur des propriétés physiques et chimiques mesurées/modélisées. Les modèles de fugacité actuels ne sont pas conçus pour traiter le devenir environnemental de substances ionisées ou tensio‑actives comme les TPAE. Nous ne les avons donc pas utilisés.
Les composants des TPAE, pour la plupart ionisés dans des conditions typiques, devraient avoir une faible pression de vapeur et ne seront donc pas volatils (EPA 2010). La volatilisation d’une substance chimique à partir de l’eau ou d’un sol humide est décrite pas sa constante de Henry (CH), qui peut être mesurée expérimentalement, mais qui est typiquement estimée en tant que rapport entre la pression de vapeur et la solubilité dans l’eau. Bien que des modèles QSAR soient disponibles pour estimer des CH, les valeurs mesurées pour les substances ionisées peuvent différer significativement de celles estimées (ECETOC 2003)Note de bas de page 5. Aucune CH expérimentale ni aucune CH calculée à partir de valeurs de solubilité dans l’eau et de pression de vapeur de haute qualité n’a été trouvée pour les TPAE ou les amines aliphatiques à longue chaîne. En général, les substances tensio-actives devraient avoir une volatilisation négligeable (Boethling et Mackay 2000).
Quand ils sont rejetés dans l’eau, les composants amine aliphatique (en raison de leur charge positive et de leurs propriétés tensio-actives) sont adsorbés sur les solides en suspension, la matière organique et les sédiments. Les cations organiques chargés aux pH pertinents pour l’environnement, comme les amines aliphatiques, sont sorbés suite à des interactions ioniques et non ioniques sur des sites d’échange de cations chargés négativement dans la matière organique et les argiles (Droge et Goss 2013a, 2013b). La structure 1 non chargée du TPAE-1 devrait aussi être fortement sorbée sur la matière organique en raison de son log KOC prédit élevé. Certains des composants (di)thiophosphate d’alkyle plus grands peuvent aussi se retrouver sur les sédiments malgré leur charge négative, étant donné qu’ils ont des log D modérés à élevés (tableau 3-3). Les composants thiophosphate plus petits devraient toutefois rester principalement dans l’eau, étant donné leurs solubilités dans l’eau prédites élevées (de plus de 1000 à plus de 10 000 mg/L) et leurs log D faibles (tableau 3-3).
De même, lorsqu’elles sont rejetées dans les sols (p. ex. par épandage de boues/biosolides sur des terres agricoles), la structure 1 et certaines des structures plus grandes du TPAE-1 devraient être adsorbées sur des particules du sol. Les composants d’amine aliphatique à longue chaîne seront aussi fortement adsorbés sur des particules du sol. Toutefois, les thiophosphates et les phosphates d’alkyle, plus petits, plus solubles dans l’eau et chargés négativement ne devraient pas se lier aux particules du sol. Donc, certains des composants des TPAE se lieront aux particules du sol alors que d’autres ne le feront pas.
Les composants amine aliphatique à longue chaîne des TPAE ne devraient pas être transportés à grande distance dans l’air ou l’eau en raison de leur volatilité faible à modérée, de leur liaison aux particules du sol et aux sédiments et de leur relativement rapide biodégradation dans l’environnement. De plus, les TPAE et les amines aliphatiques devraient avoir de très courtes durées de vie dans l’atmosphère étant donné qu’ils réagissent avec les radicaux hydroxyles (section 5.2.1). Il semble donc improbable qu’ils puissent être transportés à grande distance dans l’atmosphère. Il est possible que certains thiophosphates d’alkyle du TPAE-1 soit transportés à grande distance dans l’eau, certains étant très solubles et le TPAE-1 semblant être persistant dans l’eau (section 5.2.2). Le TPAE-2 n’est pas persistant dans l’eau (section 5.2.2) et il est donc improbable qu’il soit transporté à grande distance dans l’eau.
5.2 Persistance dans l’environnement
5.2.1 Dégradation abiotique
Dans le cas du TPAE-1, aucune étude sur l’hydrolyse n’a été réalisée pour l’homologation REACH, une telle étude n’étant pas considérée techniquement faisable (ECHA 2018a). Aucune donné fiable n’a été obtenue pour l’hydrolyse du constituant A du TPAE-2, en raison de ses effets tensio-actifs et d’une mauvaise réponse de l’appareil (ECHA 2018a). Aucune étude sur l’hydrolyse du constituant B du TPAE-2 n’a été réalisée. Toutefois, le composant thiophosphate d’alkyle du TPAE-2 était stable en solution pendant 48 à 72 heures lors de tests sur l’écotoxicité (section 6.1.2). En se basant sur ces renseignements, les composants (di)thiophosphate d’alkyle des TPAE ne semblent pas être hydrolysés rapidement. Les composants amine aliphatique ne seront pas non plus hydrolysés en raison du manque de groupes hydrolysables (ECCC, SC 2021).
Les TPAE ne devraient pas être rejetés dans l’air, étant donné leurs utilisations prévues et leurs propriétés physico-chimiques. En raison de sa réaction avec les ions hydroxyles, la demi-vie atmosphérique modélisée de la structure 1 du TPAE-1 est de 0,6 heure (AOPWIN 2010), indiquant qu’elle n’est pas persistante dans l’air. Les formes neutres des autres (di)thiophosphates d’alkyle du TPAE-1 et du TPAE-2 ont aussi des demi-vies inférieures à 2 heures dans l’air, en raison de réactions avec les ions hydroxyles (AOPWIN 2010), ces composés ne devrait donc pas être considérés persistants dans l’air. Toutefois, la structure 1 devrait être fortement sorbée (68 à 84 %) sur des particules atmosphériques (AEROWIN 2010) et, en conséquence, peuvent être résistantes à la dégradation dans l’atmosphère. Les plus grandes structures du TPAE-1 ont un Koe plus élevés et peuvent aussi être fortement sorbées sur des particules présentes dans l’atmosphère.
Les amines aliphatiques ne devraient pas non plus être persistantes dans l’air, étant donné qu’il est probable qu’elles y soient dégradées en raison de leurs réactions avec des radicaux hydroxyles et l’ozone (AOPWIN 2010). Les demi-vies des amines aliphatiques réagissant avec les radicaux hydroxyles et l’ozone vont respectivement de 0,4 à 3,2 heures et de 0,7 à 2,1 heures (AOPWIN 2010). Il est donc improbable que les composants des TPAE soient persistants dans l’air.
5.2.2 Biodégradation dans l’eau
TPAE-1
Lors de tests sur la biodégradation aérobie du TPAE-1 complet, il a été montré qu’il avait une très faible biodégradabilité immédiate dans l’eau, avec des valeurs allant de ‑ 0,3 à 9,8 % d’évolution du CO2 en 28 jours, même si les microbes avaient été pré‑adaptés à la substance testée dans deux des tests (tableau 5-1). Une faible biodégradabilité de 20 % en 28 jours a aussi été observée pour l’analogue RSN 2 similaire au TPAE-1 (tableau 5-1).
Les TPAE devant se dissocier dans des environnements aquatiques, les biodégradations des composants du TPAE-1 ont été étudiées séparément en plus de celle de la substance complète. Les données modélisées pour la structure 1 correspondent aux données empiriques de biodégradation pour la substance complète. Le modèle CATALOGIC (2014) prédit une demande biologique en oxygène (DBO) à 28 jours (% dégradé) de 4,0 ± 3,0 % pour la structure 1, avec une demi-vie ultime de plus d’un an, 3 mois. Les résultats obtenus avec le modèle BIOWIN 5 (modèle linéaire MITI) et le modèle BIOWIN 6 (modèle non linéaire MITI) (BIOWIN 2008) indiquent que la structure 1 a une faible biodégradabilité, bien que les résultats du modèle BIOWIN 3 (modèle de biodégradation ultime) indiquent une biodégradation allant de quelques semaines à quelques mois. Les tert-alcanamines en C10-14 ne sont pas facilement biodégradables, avec une biodégradation mesurée par la consommation d’O2 ou la production de CO2 de 22 % ou moins lors de tests de 28 jours (tableau 5-1). Toutefois, certains de ces tests ont été faits avec des concentrations de substance testée de 10 mg/L ou plus, que l’on pensait toxiques pour les microbes. Il est possible que les tert-alcanamines en C12-14 puissent être biodégradées à long terme. La biodégradation immédiate (28 jours) des tert-alcanamines en C12-14 est de 18 à 22 %, et leur demi-vie de biodégradation ultime est d’environ 3 mois (CATALOGIC 2014). En résumé, les données empiriques et les données modélisées suggèrent que les composants (di)thiophosphate d’alkyle du TPAE-1 seront persistants dans l’eau, alors que les composants amine aliphatique peuvent être biodégradés en quelques mois.
TPAE-2
Lors de tests aérobies de production de CO2, il a été montré que les constituants A et B subissent respectivement une biodégradation de 75 et 80 % en 28 jours (tableau 5-1). La biodégradation plus élevée observée pour cette substance peut être attribuable à ses composants nettement plus petits que ceux du TPAE-1, dont plusieurs ont des masses moléculaires dans la gamme 700-1000 g/mol, alors que celle la plus grande structure du TPAE-2 (le constituant A, amine aliphatique en C18) est de 494 g/mol. Les composants di)thiophosphate d’alkyle et amine du TPAE-1 sont aussi beaucoup plus ramifiés que ceux du TPAE-2, une caractéristique qui peut inhiber la biodégradation.
Les résultats de la modélisation du composant thiophosphate d’alkyle du TPAE-2 correspondent généralement aux données expérimentales sur la substance complète. La DBO à 28 jours prédite par le modèle CATALOGIC (2014) n’est que de 10 % (± 28 %). Toutefois, cette prédiction n’est pas considérée robuste, étant donné que 54 % des fragments de la substance ne font pas partie de l’ensemble d’apprentissage du modèle. L’estimation faite avec le modèle BIOWIN 3 indique une biodégradation ultime de quelques jours à quelques semaines (BIOWIN 2008).
Il a aussi été montré que les composants amine aliphatique du TPAE-2 sont hautement biodégradés. Lors de tests de l’OCDE, il a été rapporté que l’octadécanamine (amine primaire en C18 de no CAS 124‑30‑1) et l’octanamine (amine primaire en C8 de no CAS 111-86-4) sont facilement biodégradable (tableau 5-1). Pour les alcanamines de coco en C8-C18 (no CAS 61788-46-3), il existe deux études sur la biodégradation immédiate qui est de 56 à 67 % (tableau 5-1), des valeurs qui sont proches de la valeur d’acceptation de 60 % ou supérieures Les résultats de la modélisation indiquent aussi que ces composants auront des demi-vies ultimes de l’ordre de semaines dans l’eau (BIOWIN 2008, CATALOGIC 2014).
En résumé, les données existantes suggèrent que les composants thiophosphate d’alkyle et amine aliphatique du TPAE-2 se dégraderont rapidement dans l’environnement.
| Substance | Conditions du test (méthode) | Résultat du test (28 jours) | Référence |
|---|---|---|---|
| TPAE-1, substance complète | Biodégradabilité immédiate aérobie dans l’eau, test de production de CO2 (méthode D-5864-95 de l’ASTM) | 3,6 +/- 4,5 %a | ECHA 2019a |
| TPAE-1, substance complète | Biodégradabilité immédiate aérobie dans l’eau, test de production de CO2 (OCDE 301B) | -10 +/- 0,3 %a | ECHA2019a |
| TPAE-1, substance complète | Biodégradabilité immédiate aérobie dans l’eau, test de production de CO2 (OCDE 301B) | 7,4 +/- 2,4% | ECHA 2019a |
| TPAE-1, substance complète | Biodégradabilité immédiate aérobie dans l’eau, test de production de CO2 (OCDE 301B, UE méthode C.4‑C et ISO 10634:1995(E)). |
-4,7 %b -2,7 %c |
ECHA 2019a |
| TPAE-2 constituant A | Biodégradabilité immédiate aérobie dans l’eau, test de production de CO2 (OCDE 301B) | 75 % | ECHA 2018a |
| TPAE-2, constituant B | Biodégradabilité immédiate aérobie dans l’eau, test de production de CO2 (OCDE 301B) | 80 % | ECHA 2017 |
| Analogue RSN 2 | OCDE 301B | 20 % (production de CO2) | LCPE Programme des substances nouvelles |
| CE 701-175-2, tert-alcanamies en C10-14, constituantd | Biodégradabilité immédiate : test en flacon fermé, consommation de O2 (OCDE 301D) | 22 % | ECHA 2019b |
| CE 701-175-2, tert-alcanamines en C10-14, constituante | Biodégradabilité immédiate : consommation de O2 (OCDE 301D), OCDE 301F), production de CO2 (méthode D 5864-95 de l’ASTM) | -18,1 à 4,3 % | ECHA 2019b |
| Octadécanamine (C18) (no CAS 124-30-1) | OCDE 301F | 70 % | ECHA 2018c |
| Alcanamines de coco (C8-C18) (no CAS 61788‑46-3) | OCDE 301B, OCDE 301D | 56 % (consommation d’O2), 58 %, 67,3 % (production de CO2) | Akzo Nobel 1992a, ECHA 2018c |
| Octanamine (C8) (no CAS 111-86-4) | Diverses méthodes de l’OCDE | 73 à 99 % | ECHA 2019c |
a Pour ces études, la boue testée était pré-adaptée à la matière à tester pendant 14 jours avant le commencement des tests de biodégradabilité de 28 jours. La pré-adaptation n’a pas été utilisée lors d’autres études sur le TPAE-1.
b La matière à tester était appliquée sur le milieu par pré-application sur du gel de silice.
c La matière à tester était ajoutée au milieu de test en la pré-dissolvant dans de l’huile de silicone.
d Aucune analyse de la matière testée fournie.
e Analyse de la matière à tester, PRIMENE 81-R, fournie pour deux des tests : 74 % C12, 14 % C11, 11 % C10.
5.2.3 Biodégradation dans les sols
Aucune donnée sur la biodégradation dans les sols des TPAE ou des analogues RSN n’est disponible. Des données existaient sur la biodégradation de l’amine aliphatique hexadécanamine (C16), ainsi que sur deux substances analogues aux amines aliphatiques, les ammoniums quaternaires chlorures d’(alkyl en C12-C18)(hydroxythyl) diméthylammoniums et chlorures d’(alkyl en C22)triméthylammoniums (ECCC, SC 2021). En raison du pourcentage relativement élevé de 14CO2 produit lors des tests réalisés avec ces substances (55 à 73 %), ainsi que du temps de dissipation à 50 % dans les sols de 8 à 41 jours, il a été déterminé que la biodégradation était un processus prédominant de dissipation de ces substances et que les microorganismes du sol étaient capables de dégrader les amines aliphatiques à longue chaîne (ECCC, SC 2021).
En se basant sur les données susmentionnées, les composants amine aliphatique des TPAE ne devraient pas être persistants dans les sols. Toutefois, les composants (di)thiophosphate d’alkyle hautement ramifiés du TPAE-1 devraient être quant à eux persistants dans les sols.
5.2.4 Biodégradation dans les sédiments
Nous n’avons trouvé aucune étude sur la biodégradation des TPAE ou des amines aliphatiques à longue chaîne dans des sédiments.
Dans les conditions aérobies des premiers centimètres de sédiments, les demi-vies des composants (di)thiophosphate d’alkyle et amine aliphatique devraient être similaires à celles dans les sols. Les composants amine aliphatique ne devraient donc pas y être persistants alors que les demi-vies des composants (di)thiophosphate d’alkyle devraient dépendre de leur niveau de ramification, ceux plus petits et moins ramifiés du TPAE-2 devraient être dégradés rapidement alors que ceux plus grands et plus ramifiés du TPAE-1 pourraient y persister.
Les structures représentatives du TPAE-1, y compris les amines aliphatiques, devraient subir une très lente biodégradation anaérobie (BIOWIN 2008). Nous n’avons trouvé aucun test sur la biodégradation des TPAE ou des amines aliphatiques primaires dans des sédiments dans des conditions anaérobies (ECCC, SC 2021). La plupart des sédiments sont anoxiques à une profondeur de plus de quelques centimètres. Il est donc assumé avec prudence que ces substances seront persistantes dans des conditions anaérobies, telles que celles présentes dans les couches de sédiments anoxiques. Cette hypothèse est en accord avec le rapport européen sur l’évaluation des risques posés par les amines aliphatiques primaires (CE 2008). Pour les composants amine aliphatique, ceci correspond aussi aux concentrations accumulées élevées de cations de substances tensio-actives observées sur le terrain dans des sédiments (Lara-Martin et al. 2010).
5.3 Potentiel de bioaccumulation
5.3.1 Potentiel de bioaccumulation des composants (di)thiophosphate d’alkyle
Une étude sur le facteur de bioconcentration (FBC) chez la truite arc-en-ciel (Oncorhynchus mykiss) a été réalisée avec la structure 1 du TPAE-1, une structure neutre (non ionisée), en tant que substance de remplacement du TPAE-1 complet (Présentation de projet 2018, dossier d’homologation REACH, non référencé). L’étude n’a pas été réalisée sur l’UVCB lui-même, sa composition complexe ne convenant pas à des tests de bioconcentration classiques. Pour le test sur le FBC, la molécule de remplacement radiomarquée, pure à 99 %, a été testée à deux concentrations dans de l’eau, 0,25 et 2,8 μg/L (valeurs moyennes mesurées), en utilisant un solvant comme vecteur (diméthylformamide à 0,1 mL/L). Pendant une période d’absorption de 35 jours et une période de dépuration de 62 jours le poisson a semblé normal et en bonne santé. Des concentrations d’équilibre dans les tissus des poissons ont été atteintes après 31 jours. Les résultats de cette étude ont montré que cette substance à un FBC d’équilibre de 436 et un BFC cinétique de 834, pour le poisson entier. Ces résultats montrent que cette substance ne subit pas de bioconcentration significative chez le poisson. Il a été noté que les concentrations mesurées de la substance testée étaient substantiellement inférieure (39 à 67 %) aux concentrations cibles, indiquant que la substance testée pouvaient constituer un problème.
Une modélisation de la bioaccumulation a été faite pour la structure représentative 1 du TPAE-1 au moyen de BCFBAF (2010). Cette substance a un log Koe prédit de 5,9 (tableau 3-2). Pour un poisson de niveau trophique moyen, le FBC et le FBA sont respectivement estimés à 1015 et 2023 L/kg poids humide, prédisant que cette structure a un facteur de bioaccumulation modéré (entre 1000 et 5000 L/kg).
Il existe une incertitude quant à savoir si le FBC et le FBA estimés pour la structure 1 peuvent s’appliquer à certaines des autres structures ionisées du TPAE-1. Il est prédit que certaines des structures plus grandes de cette substance, malgré le fait qu’elles soient ionisées, ont de faibles solubilités dans l’eau et des log D élevés, suggérant qu’elles peuvent avoir des propriétés de bioaccumulation.
Aucun test sur la bioaccumulation du TPAE-2 ou des analogues RSN 1 et 2 n’a été réalisé. Toutefois, le composant thiophosphate d’alkyle du TPAE-2 a un Koe mesuré inférieur à 5 (tableau 3-1) et est ionisé, il ne devrait donc pas être fortement bioaccumulé.
5.3.2 Potentiel de bioaccumulation des amines aliphatiques à longue chaîne
Nous n’avons trouvé qu’une seule étude expérimentale sur le FBC de l’hexadécanamine chez la carpe (Cyprinus carpio), réalisée par Akzo Nobel (2006). Le FBC de 2400 L/kg calculé pour le poisson complet lors de cette étude à long terme (11 mois) est considéré être une estimation prudente (ECCC, SC 2021). Il existe aussi une étude avec la truite arc-en-ciel sur l’absorption et la distribution dans les tissus de substances tensio-actives, dont des amines aliphatiques en C9 à C16 (McLachlan 2018). Bien que la durée de l’étude soit trop courte pour déterminer des FBC d’équilibre, les BFC à 7 jours pour les substances individuelles allaient d’environ 3 à 1000 L/kg poids humide, des valeurs correspondant aux FBC prédits par d’autres au moyen du modèle BIONIC (McLachlan 2018). Des données sur l’analogue alkyl(triméthyl)ammonium (ATMA) ont aussi été prises en compte. Un examen de substances tensio-actives réalisé par Krop et de Voogt (2007) a montré que les ATMA à chaîne en C12 ou moins ont un FBC d’environ 100 L/kg ou moins en eau douce, ces valeurs ayant été déterminées indirectement (Versteeg et Shorter 1991, Schlechtriem et al. 2015). Schlechtriem et al. (2015) ont estimé que le FBC pour un ATMA en C16-18 est de 1960 L/kg, en utilisant des vitesses d’absorption et de dépuration tirées de Versteeg et Shorter (1991). En tenant compte de tous les renseignements disponibles, il est déterminé que les amines aliphatiques à longue chaîne n’ont pas un potentiel de bioaccumulation élevé dans les organismes aquatiques (ECCC, SC 2021).
Nous avons résumé dans le tableau 5‑2 les données clés sur le potentiel de bioconcentration des composants des TPAE chez les organismes aquatiques.
| Substance | Organisme testé | Concentration expérimentale, durée et renseignements sur le modèle | FBC ou FBA (L/kg) |
|---|---|---|---|
| Structure 1 du TPAE-1 | Truite arc-en-ciel (Oncorhynchus mykiss) | 0,25 et 2,8 µg/L (35 jours d’absorption, 62 jours de dépuration) | FBC = 834 |
| Structure 1 du TPAE-1 | NA | Poisson de niveau trophique moyen, modèle BCFBAF (2012), y compris la biotransformation |
FBC = 1015 FBA = 2023 |
| Hexadécanamine (C16) | Carp (Cyprinus carpio) | 3 µg/L, 11 mois | FBC = 2400 |
Abréviation : NA = non applicable
Les données mesurées, modélisées et sur les analogues indiquent toutes que les composants (di)thiophosphate d’alkyle des TPAE ont un faible potentiel de bioaccumulation. Les données expérimentales et modélisées sur les amines aliphatiques à longue chaîne et leurs analogues indiquent un potentiel modéré de bioaccumulation.
6. Potentiel d’effets nocifs sur l’environnement
6.1 Évaluation des effets sur l’environnement
6.1.1 Mode/mécanisme d’action
Les composants (di)thiophosphate d’alkyle des TPAE ont des similarités structurelles avec certains pesticides de type thiophosphate, dithiophosphate et organophosphate (OP) (p. ex. éthion, disulfoton, diméthoate). Ces pesticides agissent comme neurotoxines en désactivant l’acétylcholinestérase (AChE) qui hydrolyse le neurotransmetteur acétylcholine (Sparling 2016). Bien qu’ils soient très toxiques pour les insectes, la plupart des OP ont une toxicité modérée à faible pour les oiseaux et les mammifères, les poissons ayant tendance à y être plus sensibles que les mammifères (Sparling 2016).
Toutefois, les composants (di)thiophosphate d’alkyle et d’OP des TPAE ont des différences structurelles significatives par rapport à ces pesticides, il est donc incertain s’ils exhiberont aussi un mode d’action (MA) d’inhibition de l’AChE. Ces différences incluent la masse moléculaire, la longueur et le degré de ramification de la chaîne alkyle et l’ionisation (c.-à-d. que la majorité des structures des TPAE sont ionisées alors que les pesticides ne le sont pas). Elles pourraient toutes affecter leur potentiel d’interaction avec les TPAE et inhiber l’AChE. De plus, les tests de toxicité des TPAE indiquent un profil de danger aquatique plus faible par rapport aux pesticides de type (di)thiophosphate les plus comparables (voir la section 6.1.2), suggérant qu’il puisse y avoir des différences dans le MA, ou au moins dans sa puissance. Les profils de l’éthion et du diméthoate dans la Boîte à outils QSAR de l’OCDE (2017) indiquent qu’ils ont un mécanisme d’action lié à la liaison covalente, y compris la liaison aux protéines liée à une sensibilisation cutanée et la liaison à l’ADN (substitution nucléophile SN2), et qu’ils ont été classés comme ayant un MA spécifique selon le schéma de classification de Verhaar. À l’opposé, il n’y a pas d’alertes pour les composants (di)thiophosphate d’alkyle du TPAE-1, bien qu’ils y en aient pour la liaison à l’ADN (SN2), et ils sont aussi classés comme ayant un MA spécifique par Verhaar.
Il existe aussi une incertitude au sujet du MA des composants amine aliphatique à longue chaîne des TPAE. Bien qu’il existe des preuves pour suggérer que ces substances ont un MA narcotique non spécifique, il n’est pas certain que ce MA concerne tous les organismes, ou que certains puissent être plus susceptibles à ces substances en raison d’interactions ioniques spécifiques (ECCC, SC 2021).
En conclusion, il existe une incertitude au sujet des MA des composants (di)thiophosphate d’alkyle et amine aliphatique des TPAE. Aux fins de la présente évaluation, ces deux composants sont considérés avoir un MA associé à une toxicité plus élevée que celle de la narcose non polaire.
6.1.2 Effets sur les organismes aquatiques
Les études sur la toxicité des TPAE en milieu aquatique incluent des études sur la toxicité aiguë du TPAE-1 pour les poissons et des études sur la toxicité aiguë des deux TPAE pour Daphnia magna et des algues. Dans le cas du TPAE-1, il existe une étude sur la toxicité chronique pour D. magna. L’ECHA a fait des résumés de toutes ces études (ECHA 2017, 2018a, 2019a). Nous les avons brièvement résumées dans le tableau 6-1 ci-après. Toutes les études susmentionnées ont été réalisées avec des fractions adaptées à l’eau (FAE) de la substance à tester, et tous les résultats ont été rapportés en tant que taux de charge nominale. Pour le TPAE-1, les études ne comportaient pas d’analyses chimiques, sauf dans le cas de l’étude sur la toxicité aiguë pour D. magna, étude pour laquelle les niveaux de carbone organique total (COT) des solutions de test ont été mesurés. Les tests sur les constituants A et B du TPAE-2 incluent des analyses chimiques des composants de la substance testée, tel que discuté ci-après.
| Substance | Organisme testé | Paramètre | Valeur nominale (mg/L) | Référence |
|---|---|---|---|---|
| TPAE-1 | Rainbow trout (Oncorhynchus mykiss) | LL50 à 96 h | 24 | Présentation de projet 2018 |
| TPAE-1 | Tête-de-boule (Pimephales promelas) | LL50 à 96 h | 8,5 | Présentation de projet 2018 |
| TPAE-2 (no CAS 97808-07-6), constituant A | Truite arc-en-ciel (Oncorhynchus mykiss) | LL50 à 96 h | > 0,028 | ECHA 2018a |
| TPAE-1 | Daphnia magna | CE50 à 48 h (immobilisation) | 91,4 | Présentation de projet 2018 |
| TPAE-1 | Daphnia magna | CE50 à 21 j (immobilisation) | 0,91 | Présentation de projet 2018 |
| TPAE-1 | Daphnia magna | CE50 à 21 j (reproduction) | 0,66 | Présentation de projet 2018 |
| TPAE-2, constituant A | Daphnia magna | CE50 à 48 h (immobilisation) | 0,071 | ECHA 2018a |
| TPAE-2, constituant B | Daphnia magna | CE50 à 48 h (immobilisation) | 31 | ECHA 2017 |
| TPAE-1 | Algue (Selenastrum capricornutum)a | CE50 à 72 h (vitesse de croissance) | 16 | Présentation de projet 2018 |
| TPAE-1 | Algue (Selenastrum capricornutum)a | CE50 à 72 h (rendement) | 6,3 | Présentation de projet 2018 |
| TPAE-2, constituant A | Algue (Pseudokirchneriella subcapitata)a | CE50 à 72 h (vitesse de croissance) | 0,028 | ECHA 2018a |
| TPAE-2, constituant A | Algue (Pseudokirchneriella subcapitata)a | CE50 à 72 h (rendement) | 0,026 | ECHA 2018a |
| TPAE-2, constituant A | Algue (Pseudokirchneriella subcapitata)a | CE10 à 72 h (rendement) | 0,022 | ECHA 2018a |
| TPAE-2, constituant B | Algue (Pseudokirchneriella subcapitata)a | CE50 à 72 h (vitesse de croissance) | 3 | ECHA 2017 |
| TPAE-2, constituant B | Algue (Pseudokirchneriella subcapitata)a | CE50 à 72 h (rendement) | 1,8 | ECHA 2017 |
Abréviations : CEX = charge de la substance testée résultant en un effet spécifique (p.ex. immobilisation, croissance) chez X % des espèces exposées à la FAE; LL50 = charge létale médiane de la substance testée résultant en une mortalité de 50 % chez la population exposée à la FAE; FAE = fraction adaptée à l’eau, milieu aqueux contenant seulement la fraction de la substance dissoute ou présente en tant que dispersion ou émulsion stable.
a P. subcapitata et S. capricornutum sont une même espèce.
Pour l’étude sur la toxicité aiguë du TPAE-1 pour D. magna, le COT n’a été analysé que dans les solutions testées fraîches. Ces analyses indiquent que la solution testée à 30,5 mg/L (nominal) contenait seulement 3,8 fois plus de COT que la solution à 1 mg/L (0,53 mg/L COT) et que la solution à 99,5 mg/L n’en contenait que 9,6 fois plus que la solution à 1 mg/L (ECHA 2019b), indiquant de faibles niveaux de dissolution de la substance testée dans les solutions de FAE par rapport à la solution à 1 mg/L (nominal). Lors de l’étude sur le TPAE-1 avec la tête-de-boule, il a été noté que la plupart des solutions dans les contenants des tests étaient troubles avec des films en surface (Présentation de projet 2018), indiquant aussi un faible niveau de dissolution de la substance testée.
Dans le cas du TPAE-2, les études sur la toxicité en milieu aquatique incluaient des analyses chimiques par chromatographie en phase liquide/spectrométrie de masse (CLHP/SM) (ECHA 2017, 2018a). Pour les tests sur le constituant A, la concentration d’amines insaturées en C18 a été mesurée, et pour les tests sur le constituant B c’est la concentration d’acide dibutylthiophosphorique (ADBTP) qui l’a été. Ces mesures ont été faites dans la solution testée au commencement et à la fin des périodes de test (ECHA 2017, 2018a). Le composant d’amine en C18 n’était pas stable durant les tests. Les concentrations des préparations testées de 0,013 mg/L à 0 h et de 0,017 mg/L à 72 h n’étaient plus respectivement que de 0,0062 mg/L à 24 h et de 0,0085 mg/L à 96 h, des déclins d’environ 48 et 50 % en 24 heures. Pendant le test statique avec D. magna, la concentration d’amines en C18 avait décliné d’environ 94 % en 48 heures, passant de 0,083 mg/L (concentration nominale de 0,10 mg/L) à 0,005 mg/L. D’une valeur mesurée de 0,042 mg/L à 0 h, la concentration d’amines en C18 passait à une valeur inférieure à la limite de dosage de 0,0019 mg/L. Ceci n’était pas inattendu, les amines aliphatiques étant connues pouvoir d’adsorber sur les contenants ainsi que sur le biote (ECCC, SC 2021). Contrairement aux amines, les concentrations d’ADBTP semblaient être stables pendant les périodes de 48 à 72 h lors des tests statiques avec D. magna et l’algue (ECHA 2017, 2018a).
En se basant sur les analyses faites lors des tests avec le TPAE-2, il est fait l’hypothèse que les concentrations des composants d’amine aliphatiques ont aussi grandement déclinées avec le temps lors des tests sur la toxicité en milieu aquatique du TPAE-1, alors que celles des composants de (di)thiophosphate d’alkyle sont restées stables.
Une comparaison de la toxicité aiguë (CE50) de ces substances pour D. magna montre que celle du constituant A (0,071 mg/L) du TPAE-2 est de 3 ordres de grandeur supérieure à celle du constituant B (31 mg/L) et du TPAE-1 (91 mg/L). Comme dans le cas de D. magna, les études ont montré que le constituant A était plus toxique pour les algues, de 2 ordres de grandeur, que le constituant B et le TPAE-1. Les différences de toxicité de ces substances peuvent être attribuables aux différences de toxicité des composants amine aliphatique de longueur de chaîne différente (C16/18 et C8, la toxicité croissant avec la longueur de la chaîne), mais aussi à des variations expérimentales.
6.1.2.1 Données sur des analogues
Des données sur l’écotoxicité de l’analogue RSN 2 ont été soumises en vertu du Règlement sur les renseignements concernant les substances nouvelles, dont des données sur la toxicité aiguë pour les poissons et les daphnés et des données sur la toxicité chronique pour les daphnés et les algues. Ce dithiophosphate d’alkyle est structurellement similaire à certaines des structures représentatives du TPAE-1, malgré des différences dans les propriétés physico/chimiques (section 3). Des problèmes similaires à ceux observés pour les TPAE ont été rapportés lors des tests avec cette substance. Un protocole de FAE a été utilisé en raison de la faible solubilité dans l’eau et de la nature complexe de la matière testée. Les résultats ont donc été rapportés en tant que taux de charge nominaux. Les solutions de FAE ont été filtrées, car le milieu testé était trouble avec des dispersions blanches, avec des globules de la matière testée au fond du contenant, à la surface de l’eau et sur les parois à la fin de la période de mélange de 24 h. Aucune analyse chimique n’a été faite lors de ces études sur la toxicité, seules des valeurs nominales des paramètres ont donc été rapportées.
Il a été montré que l’analogue RSN 2 a une toxicité nominale similaire à celle du TPAE‑1 complet pour tous les organismes étudiés. Lors des tests avec O. mykiss, l’analogue RSN 2 avait une LL50 à 96 heures de 56 mg/L. Lors d’une étude sur la toxicité chronique pour D. magna, les LL50 à 21 jours étaient respectivement de 2,5 et 3,2 mg/L pour la reproduction et l’immobilisation. La CE50 aiguë à 48 heures était de 15 mg/L pour les daphnés. La CE50 à 21 jours pour la reproduction de D. magna était le paramètre le plus sensible pour les deux substances. Pour les algues vertes, la CE50 à 72 heures (biomasse) était de 5,1 mg/L.
6.1.2.2 Données sur les pesticides
Les données sur les pesticides éthion et sulfotep, qui ont des structures de thiophosphate d’alkyle similaires à certaines des structures représentatives du TPAE-1, ont été comparées aux données empiriques sur la toxicité de la substance complète des TPAE. L’utilisation de ces deux pesticides n’est pas homologuée au Canada (Santé Canada 2019). Les arthropodes, comme des insectes, ou pour les organismes aquatiques, des crustacés, comme les daphnés, devraient être la classe d’organismes la plus sensible à ces pesticides. Les données sur les daphnés pour l’éthion et le sulfotep sont disponibles dans la base de données ECOTOX (2000-2019). Pour chacune de ces substances, il existait deux études sur la toxicité aiguë pour D. magna. Les CE50 à 48 heures pour l’éthion étaient de 4,6 x 10-5 et 5,6 x 10-5 mg/L, alors que pour le sulfotep la CE50 et la CL50 à 48 heures étaient de 2,3 x 10-3 et 2,5 x 10-3 mg/L. Les valeurs de toxicité aiguë pour D. magna étaient de 7,1 x 10-2 mg/L pour le TPAE-2 et de 91,4 mg/L pour le TPAE-1. Étant donné les différences entre les structures chimiques des TPAE et celles de ces deux pesticides, les données sur le danger de ces pesticides ont été prises en compte avec un poids de la preuve pour le potentiel de danger plutôt que de les utiliser directement comme lecture croisée pour les TPAE.
6.1.2.3 Données modélisées
Nous avons entrepris une modélisation de la toxicité des composants (di)thiophosphate/organophosphate d’alkyle des TPAE. Toutefois, les résultats de la modélisation n’ont pas en définitive été inclus dans le présent rapport en raison d’incertitudes sur l’exactitude des prédictions. La modélisation de la toxicité de substances ionisées est généralement problématique, les modèles disponibles étant principalement basés sur le Koe (p. ex. ECOSAR c2000-2016, AIEPS c2010-2012, CATALOGIC 2014) et ne tenant pas compte de la nature ionique des substances. De plus, les ensembles d’apprentissage des modèles ne conviennent pas aux composants (di)thiophosphate d’alkyle des TPAE. Les ensembles d’apprentissage des modèles TEST (2016) et AIEPS (c2010‑2012) ne comportent pas de substances similaires aux composants (di)thiophosphate d’alkyle, et ceux du modèle ECOSAR (c2000-2016) pour les classes de substances applicables (dithiophosphate et thiophosphate) étaient basés principalement sur des données sur des pesticides qui, tel que précédemment discuté, comportent une incertitude quant au fait qu’elles soient des substances de remplacement appropriées pour les TPAE puisqu’elles sont considérablement plus toxiques. Le modèle CATALOGIC (2014) n’était pas en mesure de produire des estimations de toxicité pour les composants (di)thiophosphate d’alkyle, prédisant uniquement que ces substances ont un mode d’action plus réactif qu’une narcose de base, donc seules des valeurs « inférieures à » ont été produites.
Il existe un ensemble important de données empiriques sur les amines aliphatiques à longue chaîne (ECCC, SC 2021), une modélisation de la toxicité des composants amine aliphatique n’était donc pas nécessaire, bien que ces substances auraient été difficiles à modéliser en raison de leurs propriétés ioniques et tensio-actives. Aucune modélisation des composants des TPAE n’a donc été faite.
6.1.2.4 Sélection et standardisation des valeurs critiques de toxicité (VCT) et calcul des concentrations estimées sans effet (CESE)
Deux VCT ont été retenues pour les TPAE, une pour les composants (di)thiophosphate d’alkyle et une pour les composants amine aliphatique.
6.1.2.4.1 VCT et CESE pour les composants thiophosphate
En raison du manque de données modélisées appropriées ou sur des analogues pour les composants (di)thiophosphate d’alkyle, la VCT a été basée sur les données de toxicité empiriques pour le TPAE-1 et le TPAE-2 complets. Ces données ont été prises en compte en tant que groupe, puisque le TPAE-1 comporte des composants qui contiennent soit un dithiophosphate d’alkyle soit un thiophosphate d’alkyle (tableau 2-2), et que les structures de ces substances sont similaires. Le paramètre le plus sensible pour ces deux substances est la CE10 à 72 h de 0,022 mg/L pour les algues pour le rendement dans le cas du TPAE-2 (tableau 6-1). La qualité de cette étude a été évaluée et jugée acceptable.
Pour calculer la CESE pour les composants (di)thiophosphate d’alkyle, la VCT a été divisée par un facteur d’évaluation (FE). Les FE tiennent compte de diverses extrapolations et sources d’incertitude. Un facteur de standardisation du paramètre (FSP) est pris en compte pour une extrapolation du court terme (aigu) au long terme (chronique), des effets létaux (p. ex. mortalité) à des effets sublétaux (p. ex. croissance, reproduction) et des niveaux d’effet médians (CE50) à des niveaux d’effet faibles (CE10). Les FE tiennent aussi compte du nombre d’espèces et de catégories d’organisme représentées dans l’ensemble de données sur la toxicité (facteur de variation des espèces; FVE) et du fait de savoir si la substance a un mode d’action plus toxique que la narcose de base (facteur de mode d’action, FMA). Le FE final est calculé en multipliant FSP par FVE et FMA. La VCT étant pour une étude chronique avec un paramètre pour des effets sublétaux faibles, le FSP est égal à un. Le mode d’action des composants (di)thiophosphate d’alkyle des TPAE étant suspecté plus toxique qu’une narcose non polaire (section 6.1.1), un FMA de 2 a été appliqué à la VCT. Ceci est un FMA relativement faible, l’ensemble de données incluant la classe d’organismes la plus sensible pour le MA d’inhibition de l’AChE, les arthropodes, tels que des insectes, ou des organismes aquatiques, crustacés tels que les daphnés. L’ensemble des données combinées sur la toxicité aquatique de TPAE-1 et du TPAE-2 qui inclut un total de quatre espèces de trois catégories (plantes, invertébrés et vertébrés), tel que décrit précédemment, est un ensemble modérément riche en données et un FVE de 2 a donc été utilisé. Un FE global de 4 (FSP × FVE × FMA = 1 × 2 × 2) a donc été appliqué à la VCT de CTV de 22 µg/L, donnant une CESE de 5,5 µg/L.
6.1.2.4.2 Calcul de la VCT et de la CESE pour les composants amine aliphatique
La VCT pour les composants amine aliphatique des TPAE a été tirée de l’évaluation des amines aliphatiques (ECCC, SC 2021). Une VCT et une CESE ont été utilisées pour les amines aliphatiques à longue chaîne en milieu aquatique, basées sur la toxicité similaire observée de ces substances (ECCC, SC 2021). Nous avons trouvé des données sur la toxicité en milieu aquatique des amines aliphatiques à longue chaîne pour 11 espèces de trois catégories d’organismes, poissons, invertébrés et algues. La VCT est tirée d’une étude sur une algue, Desmodesmus subspicatus, avec la N,N‑diméthylhexadécanamine (no CAS 112-69-6), une amine tertiaire avec une chaîne alkylique en C16, dont la CE10 pour la biomasse est de 0,43 µg/L (mesurée) (ECHA 2019d). Pour convertir cette VCT en une CESE, la VCT a été divisée par les facteurs suivants : un FSP de 1, ce paramètre étant pour un effet faible tiré d’une étude sur la toxicité chronique; un FVE de 1, en raison de l’ensemble de données sur la toxicité relativement grand et complet; un FMA de 2, pour tenir compte de l’incertitude sur le mode d’action des amines aliphatiques (ECCC, SC 2021). Une CESE de 0,22 µg/L a donc été calculée.
6.1.3 Effets sur les organismes vivant dans les sédiments
Nous n’avons trouvé aucune donnée sur la toxicité des sédiments (empirique ou modélisée) pour les deux TPAE ou pour des substances RSN analogues. Il n’a donc pas été possible de calculer une CESE dans les sédiments pour les composants (di)thiophosphate d’alkyle des TPAE. Toutefois, des données étaient disponibles sur les amines aliphatiques à longue chaîne.
Des données sur la toxicité dans les sédiments des amines aliphatiques à longue chaîne et des ammoniums quaternaires à longue chaîne (substances analogues) étaient disponibles. Elles provenaient de cinq études sur la toxicité chronique pour trois espèces : trois études avec le nématode Caenorhabditis elegans, une étude avec le moucheron Chironomus riparius et une étude avec le ver Lumbriculus variegatus. Ces études sont décrites dans un document d’ECCC et SC (2021). Il a été montré que les toxicités des amines aliphatiques à longue chaîne et des substances analogues sont similaires. Le paramètre le plus sensible tiré d’une étude acceptable, une CE10 nominale de 11 mg/kg poids sec, était pour des effets sur la reproduction et la biomasse de l’amine aliphatique à longue chaîne N-(alkyl de suif hydrogéné)propane-1,3-diamine (no CAS 68603-64-5) avec L. variegatus. La VCT représente une toxicité sublétale à long terme pour de faibles effets, aucun facteur d’évaluation n’est donc nécessaire pour une extrapolation aiguë-chronique. Néanmoins, puisque l’ensemble de données représente seulement trois espèces d’une catégorie d’organismes (invertébrés), un facteur d’évaluation de 20 a été utilisé pour tenir compte de la variation entre espèces. De plus, un facteur d’évaluation de 2 a été utilisé pour tenir compte de l’incertitude sur le mode d’action de ces substances. La VCT a donc été divisée par un facteur global de 40, conduisant à une CESE de 0,275 mg/kg ps.
6.1.4 Effets sur les organismes vivant dans les sols
Nous n’avons trouvé aucune donnée sur la toxicité dans les sols (empirique ou modélisée) pour les deux TPAE ou pour des substances RSN analogues. Il n’a donc pas été possible de calculer une CESE dans les sols pour les composants (di)thiophosphate d’alkyle des TPAE. Toutefois, des données sur la toxicité dans les sols des amines aliphatiques à long chaîne étaient disponibles.
Des données sur la toxicité dans les sols d’amines aliphatiques étaient disponibles pour six espèces de deux catégories d’organismes (producteurs primaires et invertébrés), tel que décrit dans un document d’ECCC et SC (2021). Le paramètre le plus sensible était une CE25 à 21 jours de 52 mg/kg pour des DMANote de bas de page 6 en C12-14 pour le colza (longueur des pousses) (ECHA 2015), qui a été retenue comme VCT pour le calcul de la CESE. La VCT représentant une exposition aiguë (court terme) pour des plantes, un facteur d’évaluation de 5 a été appliqué pour l’extrapolation à une valeur à long terme (chronique). Les données sur la toxicité n’étant disponibles qu’en nombre limité, un facteur de 5 pour la variation entre espèces a été appliqué, en plus d’un FMA de 2. Un FE de 50 a été appliqué à cette valeur (FSP × FVE × FMA = 5 × 5 × 2), donnant une CESE de 1 mg/kg poids sec. Cette CESE sera utilisée pour les composants amine aliphatique des TPAE.
6.2 Évaluation de l’exposition de l’environnement
Nous n’avons préparé des scénarios d’exposition quantitatifs que pour le TPAE-1, en raison des quantités beaucoup plus faibles de TPAE-2 utilisées (tableau 4-1). De plus, le TPAE-2 n’est pas utilisé dans des fluides pour le travail des métaux. Le rapport exposition/risque pour le TPAE-2 est décrit qualitativement à la section 6.3.1.
Des scénarios d’exposition ont été préparés pour : 1) la formulation de lubrifiants; 2) l’utilisation dans des fluides pour le travail des métaux; 3) l’application de biosolides provenant de STEU recevant les eaux d’utilisateurs industriels de fluides pour le travail des métaux.
Aucun scénario n’a été préparé pour l’utilisation de TPAE dans d’autres lubrifiants et graisses, car il a été déterminé que l’exposition de l’environnement due à cette utilisation serait faible ou nulle, ces produits étant recyclés ou éliminés dans des installations pour déchets et n’étant donc pas rejetés dans l’environnement.
6.2.1 Concentrations mesurées dans les milieux de l’environnement et les eaux usées
Nous n’avons trouvé aucune concentration environnementale pour les TPAE ou les amines aliphatiques au Canada, ni ailleurs.
6.2.2 Calcul des concentrations environnementales estimées (CEE) et hypothèses générales
La modélisation de l’exposition au TPAE-1 a été faite en se basant sur deux structures représentatives de cette substance, la structure 1 (composé organique neutre) représentant les composants (di)thiophosphate d’alkyle et le composant amine aliphatique (ionisable) (tableau 2-2). La justification pour le choix de la structure 1 est donnée à la section 3. Le composant amine aliphatique a été choisi, car c’est le contre‑ion de toutes les autres structures majeures de cette substance (section 2). Ces deux structures ont été prises en compte individuellement pour la modélisation des STEU. Des hypothèses ont été faites sur les pourcentages massiques de ces structures représentatives du TPAE-1, basées sur l’analyse chimique d’un seul échantillon de cette substance, tel que décrit à la section 2. En se basant sur cette analyse, il a été assumé que les composants (di)thiophosphate d’alkyle, représentés par la structure 1, représentent environ 75 % du poids de cette substance, le composant amine aliphatique représentant les autres 25 %.
Pour les deux scénarios industriels décrits ci-après, nous avons utilisé le modèle SimpleTreat 3.1 (2003) pour modéliser le traitement secondaire sur place dans un STEU, avec un taux d’élimination de 76 % pour la structure 1. Pour le composant amine aliphatique, le taux d’élimination était de 96 %, basé sur des données empiriques sur des amines aliphatiques (ECCC, SC 2021), et il est assumé que ce taux représente l’élimination après un traitement primaire et un traitement secondaire. De plus, un prétraitement sur place avec un séparateur huile/eau a aussi été assumé, avec un taux d’élimination de 50 % des TPAE, étant donné leur solubilité et leur masse volumique (OCDE 2011).
Les CEE en milieu aquatique pour les amines aliphatiques ont ensuite été ajustées pour calculer la fraction dissoute libre qui sera biodisponible, afin de reconnaître qu’une fois rejetées dans des eaux de surface, une fraction des amines aliphatiques sera sorbée sur la matière organique et ne sera plus biodisponible. Tel que décrit dans l’évaluation du groupe des amines aliphatiques (ECCC, SC 2021), en assumant une concentration moyenne de COT de 13,05 mg/L dans des eaux de surface au Canada, la fraction dissoute libre du composant d’amine aliphatique en C12-14 du TPAE-1 serait de 93,7 %.
Les scénarios d’exposition sont brièvement décrits ci-après. Des détails supplémentaires sont donnés dans le document d’ECCC (2020).
6.2.3 Scénario d’exposition 1 : formulation de lubrifiants
Le mélange de TPAE avec d’autres composants pour produire des produits lubrifiants dans des installations industrielles peut conduire à des rejets dans l’environnement. Les entreprises qui formulent des produits lubrifiants sont situées à divers endroits à travers le Canada. Pour estimer ces rejets, nous avons utilisé les renseignements sur les installations de formulation de lubrifiants au Canada, tels que leurs capacités de mélange, les quantités maximales potentiellement utilisées, les débits d’eaux usées, les méthodes de rejet (directes ou indirectes), les systèmes de traitement sur le site ou hors du site et les facteurs de dilution pour les plans d’eau récepteurs.
Ce scénario est basé sur la quantité potentielle manipulée dans une installation canadienne. Il est assumé que la substance est utilisée en continue durant toute l’année. La masse de TPAE-1 manipulée a été fournie par les entreprises qui l’importent (communication personnelle, courriels de parties intéressées industrielles à Environnement et Changement climatique Canada, février 2018; non référencé). Pour ce scénario, un facteur d’émission de 0,25 %, basé sur le document OCDE (2204) a été utilisé. Il tient compte des rejets dans les eaux usées dus à la manipulation de la matière brute, au mélange, au conditionnement, au nettoyage des sols et à d’autres processus. Le taux d’élimination d’un séparateur huile/eau sur le site (50 %) est tiré d’OCDE (2011). Tel que précédemment discuté, un taux d’élimination pour un traitement secondaire dans un STEU (sur le site ou hors du site) a aussi été utilisé. Une installation peut rejeter ses effluents directement dans des eaux de surface ou les faire passer dans un STEU pour qu’ils soient ensuite rejetés dans des eaux de surface.
En se basant sur les renseignements spécifiques à une installation et sur les renseignements susmentionnés, la CEE aquatique la plus élevée calculée pour ce scénario est de 1,9 µg/L pour la structure 1 et de 0,106 µg/L pour le composant amine aliphatique. En tenant compte de la concentration dissoute libre, la CEE pour le composant amine aliphatique est de 0,099 µg/L.
6.2.4 Scénario d’exposition 2 : utilisation de fluides pour le travail des métaux
À travers le Canada, de multiples installations de diverses tailles utilisent des TPAE dans des fluides pour le travail des métaux. Les renseignements spécifiques sur les utilisateurs et les quantités utilisées de fluides pour le travail des métaux contenant des TPAE ne sont pas connus. Pour calculer une CEE dans les eaux de surface, nous avons utilisé les paramètres suivants : le volume de fluide manipulé dans une installation, la concentration de TPAE-1 dans divers fluides, le facteur d’émission pour cette substance rejetée dans des eaux usées, le taux d’élimination de la substance dans un STEU, le débit d’effluent et le facteur de dilution d’un plan d’eau récepteur.
Ce scénario tient compte d’une situation représentative dans laquelle une installation industrielle utilise des fluides pour le travail des métaux à base d’huiles et manipule du TPAE-1 en continu pendant l’année. Le volume des fluides manipulés dans cette installation a été tiré de la moyenne géométrique aux États-Unis (OCDE 2011). La concentration des TPAE dans les fluides à base d’huiles va de 5 à 20 % (Brinksmeier et al. 2015). Nous avons utilisé une concentration de 10 % pour le présent scénario. Un facteur d’émission de 11 % a été utilisé. Ce facteur tient compte des rejets de la substance dans les eaux usées lors de la manipulation de la matière brute, du nettoyage des huiles résiduelles présentes sur les surfaces métalliques, de la finition et d’autres processus (OCDE 2011). Des taux d’élimination moyens ont été utilisés pour le séparateur huile/eau utilisé sur le site et pour les systèmes de traitement secondaire utilisés, la plupart des installations rejetant leurs eaux usées dans un STEU après un traitement secondaire. De plus, l’effluent d’un STEU est dilué dans le plan d’eau récepteur. Le volume quotidien de dilutionNote de bas de page 7 pour le plan d’eau récepteur utilisé est le 10ème percentile d’une distribution pour des installations industrielles manipulant potentiellement la substance, distribution qui était basée sur des données industrielles tirées de bases de données du gouvernement du Canada et sur des données mesurées ou calculées sur les débits des plans d’eau récepteurs.
Ce scénario a conduit à calculer une CEE aquatique de 10,1 µg/L pour la structure 1 et de 0,56 µg/L pour le composant amine aliphatique. En tenant compte de la concentration dissoute libre, la CEE pour le composant amine aliphatique est de 0,52 µg/L.
6.2.5 Scénario d’exposition 3 : épandage de biosolides
La CEE pour les sols a été calculée en tant qu’extension du scénario en milieu aquatique pour les fluides pour le travail des métaux décrit plus haut, les installations de ce type dirigeant leurs eaux usées vers un STEU hors site. Certaines installations de mélange de lubrifiants envoient aussi leurs eaux usées vers des STEU hors site. Toutefois, ces rejets sont très inférieurs à ceux des installations de fluides pour le travail des métaux et, en conséquence, ce scénario d’épandage de biosolides est basé sur la CEE aquatique du scénario pour les fluides pour le travail des métaux. Les biosolides produits par les STEU peuvent être épandus sur des terres agricoles en tant qu’amendement.
La quantité de composant amine aliphatique du TPAE-1 accumulée dans les 20 premiers cm de sol après 10 années consécutives d’épandage de biosolides une fois par an a été estimée en suivant une approche décrite dans un document de l’ECHA (2016). Ce calcul est basé sur la quantité rejetée dans un STEU par un utilisateur industriel. Nous n’avons pas calculé de CEE pour les sols pour la structure 1 en raison du manque de données nécessaires sur la toxicité dans les sols, empiriques, modélisées ou sur un analogue. Nous avons utilisé une demi-vie de biodégradation dans les sols de 96 jours pour le composant amine aliphatique, basée sur une modélisation de la biodégradation faite avec CATALOGIC (2014), et la dégradation a été assumée avoir une cinétique de premier ordre. Les concentrations ont été déterminées sur une base annuelle immédiatement après l’épandage et à la fin de l’année (365 jours) avant l’épandage subséquent, pendant une période de 10 ans. Nous avons assumé qu’il n’y avait aucune perte de TPAE par volatilisation, lixiviation ou ruissellement (ECCC 2020).
En raison du manque de renseignements, il a été assumé que tout le composant amine aliphatique éliminé dans le STEU resterait dans les boues. Nous avons aussi utilisé le 10ème percentile du débit des STEU canadiens avec traitement secondaire recevant des eaux usées d’installations de fluides pour le travail des métaux pour le calcul de la CEE.
En suivant cette approche, une CEE de 1,20 mg/kg poids sec a été calculée pour les sols pour le composant amine aliphatique.
6.2.6 Sédiments
Étant donné que nous n’avons trouvé aucune donnée sur l’exposition dans des sédiments pour les TPAE et très peu de données sur les amines aliphatiques (ECCC, SC 2021), nous n’avons pas calculé de CEE pour les composants du TPAE-1. Il n’est pas actuellement possible de modéliser la distribution dans les sédiments des concentrations des composants amine aliphatique et (di)thiophosphate d’alkyle (tel que représenté par la structure 1), en raison des propriétés uniques des composés tensio‑actifs et du manque de mesures sur le terrain. Bien qu’il puisse y avoir une sorption sur des particules de sédiment et une exposition potentielle des organismes benthiques, le niveau d’exposition est incertain. Pour le déterminer quantitativement, il est nécessaire de faire un échantillonnage environnemental. Toutefois, étant donné les propriétés de cette substance (persistance attendue des composants des TPAE dans les sédiments et partage attendu des composants neutre et (di)thiophosphate d’alkyle à longue chaîne et des composants amine aliphatique dans les sédiments) ainsi que les concentrations calculées pour les systèmes aquatiques, les organismes vivant dans les sédiments devraient être exposés aux TPAE.
6.3 Caractérisation des risques pour l’environnement
L’approche suivie pour la présente évaluation ayant trait à l’environnement était d’examiner des renseignements et d’en tirer des conclusions en tenant compte du poids de la preuve et du principe de précaution. Des preuves ont été rassemblées afin de déterminer le potentiel d’effets nocifs des TPAE ou de leurs composants sur l’environnement au Canada. Les éléments de preuve pris en compte incluaient ceux évalués pour la caractérisation des risques de la présente évaluation préalable, ainsi que des éléments de preuve indirects ou secondaires dont des décisions réglementaires, des classifications du danger et des caractéristiques du devenir établies par d’autres organismes de réglementation.
6.3.1 Analyse de quotient de risque
Des analyses de quotient de risque ont été faites pour le TPAE-1 en comparant les diverses estimations de l’exposition (section 6.2) aux renseignements sur l’écotoxicité (section 6.1), afin de déterminer s’il existe un potentiel d’effets nocifs sur l’environnement au Canada. Des quotients de risque (QR) ont été calculés séparément pour deux composants représentatifs du TPAE-1, les composants (di)thiophosphate d’alkyle, représentés par la structure 1, et la tert-alcanamine en C12 représentant les contre-ions d’amines aliphatiques. Les QR ont été calculés en divisant la CEE par la CESE pour les milieux de l’environnement pertinents et les scénarios d’exposition associés, tels que rapportés ci-après dans les tableaux 6-2 et 6-3.
| Scénario (milieu) | CEE | CESE | QR |
|---|---|---|---|
| Formulation de lubrifiants (eau) | 1,9 µg/L | 5,5 µg/L | 0,35 |
| Fluides pour le travail des métaux (eau) | 10,1 µg/L | 5,5 µg/L | 1,8 |
Abréviation : CEE = concentration environnementale estimée; CESE = concentration estimée sans effet; QR = quotient de risque
a La modélisation de la CEE a été faite avec les propriétés physiques et chimiques de la structure 1, alors que la CESE est basée sur des données sur la toxicité de la substance complète.
| Scénario (milieu) | CEEa | CESE | RQ |
|---|---|---|---|
| Formulation de lubrifiants (eau) | 0,099 µg/L | 0,22 µg/L | 0,45 |
| Fluides pour le travail des métaux (eau) | 0,52 µg/L | 0,22 µg/L | 2,4 |
| Fluides pour le travail des métaux (sol, épandage de biosolides) | 1,2 mg/kg ps | 1 mg/kg ps | 1,2 |
Abréviation : CEE = concentration environnementale estimée; CESE = concentration estimée sans effet; QR = quotient de risque
a Les valeurs de la CEE pour les scénarios d’exposition aux composants d’amine aliphatique dans l’eau ont été ajustées pour tenir compte des concentrations dissoutes libres à une concentration moyenne de COT.
Pour les deux structures représentatives, les QR en milieu aquatique sont inférieurs à 1 pour le scénario de formulation de lubrifiants et supérieurs à 1 pour le scénario de fluides pour le travail des métaux (tableaux 6-2 et 6-3). Ils sont également supérieurs à 1 pour les sols pour le composant amine aliphatique pour les scénarios d’épandage de biosolides et de fluides pour le travail des métaux.
La quantité de TPAE-2 utilisée au Canada est au moins 200 fois inférieure à celle du TPAE-1, et le TPAE-2 n’est pas utilisé dans des fluides pour le travail des métaux (section 4). Les QR pour le TPAE-2 utilisé pour la formulation de lubrifiants devraient donc être inférieurs à 1.
6.3.2 Prise en compte des éléments de preuve
Pour caractériser les risques posés à l’environnement par les TPAE, nous avons tenu compte des renseignements techniques de divers éléments de preuve (tel que discuté dans les sections pertinentes du présent rapport) et y avons associé un poids de la preuve. Les éléments de preuve clés à partir desquels nous avons tiré nos conclusions sont présentés dans le tableau 6-4, avec une discussion globale du poids de la preuve rapportée à la section 6.3.3. Le niveau de confiance fait référence à l’influence combinée de la qualité et de la variabilité des données, des lacunes dans les données, de leur causalité, de leur plausibilité et à toute extrapolation requise. La pertinence fait référence à l’impact de l’élément de preuve sur la détermination du potentiel d’effets nocifs sur l’environnement au Canada. Les qualificateurs utilisés pour l’analyse allaient de faible à élevé, avec une pondération possible à cinq niveaux.
| Élément de preuve | Niveau de confiancea | Pertinence pour l’évaluationb | Pondération assignéec |
|---|---|---|---|
| Similarité de la structure à des fins de lecture croisée | modéré | élevée | modérée à élevée |
| Devenir et comportement dans l’environnement (nature ionique) | modéré | modérée | modérée |
| Persistance dans l’environnement, composants (di)thiophosphate d’alkyle et amine aliphatique | élevé | élevée | élevée |
| Transport à grande distance | modéré | faible | faible à modérée |
| Bioaccumulation dans des organismes aquatiques, composants (di)thiophosphate d’alkyle et amine aliphatique | modéré | modéré | modéré |
| Mode d’action, composants (di)thiophosphate d’alkyle et amine aliphatique | modéré | modéré | modéré |
| CESE pour les organismes aquatiques, composants (di)thiophosphate d’alkyle | modéré | élevée | modérée à élevée |
| CESE pour les organismes aquatiques, composants amine aliphatique | élevé | élevée | élevée |
| CESE pour les organismes vivant dans les sols, composant amine aliphatique | modéré | élevée | modérée à élevée |
| CEE aquatiques | modéré | élevée | modérée à élevée |
| CEE pour les sols | modéré | élevée | modérée à élevée |
| QR pour l’eau | modéré | élevée | modérée à élevée |
| QR pour les sols | modéré | élevée | modérée à élevée |
Abréviation : CEE = concentration environnementale estimée; CESE = concentration estimée sans effet; QR = quotient de risque
a Le niveau de confiance est déterminé en fonction de la qualité des données, de leur variabilité et des lacunes dans les données (c.-à-d. existe-t-il des données à cette fin?).
b La pertinence fait référence à l’impact de la preuve sur l’évaluation.
c Une pondération globale est assignée à chaque élément de preuve en fonction du niveau de confiance et de la pertinence pour l’évaluation.
6.3.3 Pondération pour déterminer le potentiel d’effets nocifs sur l’environnement au Canada
La CESE pour les composants (di)thiophosphate d’alkyle et organophosphate du TPAE-1 est basée sur des données sur la toxicité des TPAE complets, alors que la CESE pour le composant amine aliphatique du TPAE-1 l’est sur des données empiriques sur des amines aliphatiques à longue chaîne. Les paramètres sur la toxicité de la substance complète sont exprimés en tant que taux de charge nominaux. On ne sait pas quel ou quels composants des TPAE sont responsables de la toxicité (p. ex. amine aliphatique ou (di)thiophosphate d’alkyle), ce qui ne confère qu’une confiance modérée à la CESE. La CESE en milieu aquatique pour le composant amine aliphatique du TPAE-1 est basée sur un large ensemble de données empiriques sur la toxicité aquatique des amines aliphatiques, et elle est donc considérée fiable. L’ensemble de données sur la toxicité dans les sols des amines aliphatiques n’est pas important, la confiance dans cette CESE n’est donc que modérée. Les composants (di)thiophosphate d’alkyle et amine aliphatique ont tous deux une toxicité chronique élevée pour les organismes aquatiques, alors que les amines aliphatiques ont une toxicité chronique faible à modérée pour les organismes vivant dans les sols. Il existe des données empiriques sur le devenir et le comportement dans l’environnement des amines aliphatiques (p. ex. leur forte sorption sur des matrices de l’environnement, coefficient de partage empirique sol-eau). Toutefois, nous n’avons trouvé aucune donnée empirique sur le devenir et le comportement dans l’environnement des composants (di)thiophosphate d’alkyle des TPAE (autre que des données sur la biodégradation de la substance complète). Les données empiriques ou modélisées sur la biodégradation indiquent que le TPAE-1 sera persistant dans l’environnement assez longtemps pour causer une toxicité chronique. De plus, le TPAE-1 est rejeté continuellement par les installations industrielles.
Les composants des TPAE ne sont pas considérés persistants dans l’air et ne sont pas rejetés dans l’air. Ils ne subissent donc pas de transport atmosphérique à grande distance vers des régions éloignées. Il a été montré que le TPAE-1 est persistant dans l’eau en raison de sa très faible vitesse de biodégradation, accroissant ainsi la durée et l’étendue spatiale de l’exposition des organismes. Il a été montré que le TPAE-2 est biodégradé beaucoup plus vite que le TPAE-1, probablement en raison de considérations structurales, tel que discuté à la section 5.2, et il n’est donc pas persistant. En se basant sur des données empiriques ou modélisées sur la structure 1 du TPAE-1 et sur des amines aliphatiques, il a été conclu que les TPAE ne sont pas bioaccumulés.
La fiabilité des CEE aquatiques repose sur un certain nombre de facteurs, dont le taux d’élimination des STEU, la quantité utilisée, le facteur d’émission et le volume de dilution quotidien du plan du milieu récepteur. Le taux d’élimination des STEU pour la structure 1, modélisé au moyen de SimpleTreat (2003), est considéré modérément fiable. La performance de SimpleTreat (2003) pour modéliser Kd (le coefficient de partage solides-eau) a été vérifiée avec des données mesurées pour les HAP (Étude d’ECCC, non référencée), et elle est considérée très fiable. Néanmoins, ceci dépend aussi de la fiabilité des données physicochimiques de la substance modélisée, qui n’est que modérée pour la structure 1, ces données étant basées entièrement sur des données modélisées et non sur des données mesurées. Le taux d’élimination des STEU pour les amines aliphatiques est considéré fiable, étant donné qu’il est basé sur des données empiriques. Les données sur les quantités industrielles de TPAE utilisées pour la formulation de lubrifiants sont considérées fiables, ayant été obtenues directement de parties intéressées industrielles, alors que celles utilisées pour les fluides pour le travail des métaux sont basées sur un document sur les émissions de l’OCDE (2011), représentant des pratiques génériques. Les données sur le volume quotidien de dilution sont considérées fiables, étant donné qu’elles sont basées sur des données industrielles tirées de bases de données du gouvernement canadien et sur des données mesurées ou calculées sur les débits des plans d’eau récepteurs. Les facteurs d’émission sont des estimations provenant de sources génériques (p. ex. publications de l’OCDE), plutôt que des données spécifiques à un site. Les facteurs susmentionnés conduisent à une confiance modérée dans les CEE aquatiques.
La CEE pour les sols a été déterminée en suivant une approche générique basée sur le taux provincial d’épandage de biosolides maximal permis au Canada. Cette approche inclut la biodégradation dans le sol, mais sans autre perte due à la volatilisation, à la lixiviation ou au ruissellement, pendant une période de 10 ans. La CEE pour les sols est aussi basée sur certains des paramètres utilisés pour la CEE aquatique comme les propriétés physicochimiques, les quantités industrielles utilisées et le facteur d’émission industriel. La confiance dans le CEE pour les sols est donc aussi modérée.
Les quotients de risque indiquent que le TPAE-1 peut avoir des effets nocifs sur les organismes aquatiques ou vivant dans les sols dans les milieux de l’environnement au Canada, effets dus à son utilisation dans des fluides pour le travail des métaux. Nous avons déterminé que la formulation de lubrifiants contenant des TPAE ne pose pas de risque pour l’environnement. Il est improbable que l’utilisation de TPAE dans des lubrifiants entraîne des effets nocifs sur l’environnement au Canada, la majorité de ces produits étant recyclés dans des installations à cet effet.
Certains composants des TPAE rejetés dans l’eau devraient se retrouver dans les sédiments (p. ex. les amines aliphatiques) et pourraient s’y accumuler avec le temps étant donné leur persistance dans ce milieu. Nous avons assumé que les utilisations industrielles de TPAE prises en compte pour les scénarios d’exposition conduisent à des rejets continus dans l’environnement. Les données empiriques sur la toxicité des amines aliphatiques et de leurs analogues dans les sédiments indiquent une toxicité chronique relativement faible. Toutefois, nous n’avons trouvé aucun renseignement sur la toxicité des TPAE (substance complète), des composants (di)thiophosphate d’alkyle ou de leurs analogues due à une exposition dans des sédiments, ni sur la concentration des composants des TPAE dans les sédiments.
Le danger posé à l’environnement par le TPAE-1 a été classé de la manière suivante par l’ECHA (Agence européenne des produits chimiques) : toxique pour la vie aquatique avec des effets à long terme (ECHA 2018b). Le danger du constituant A du TPAE-2 a été classé ainsi par l’ECHA : cette substance est très toxique pour la vie aquatique, toxique avec des effets à long terme (ECHA 2018e). D’après son écotoxicité, le danger du constituant B du TPAE-2 n’est pas étiqueté dangereux, mais est étiqueté dangereux pour ce qui est de ses effets liés à la santé humaine (ECHA 2019e).
Bien qu’il soit improbable que les expositions actuelles de l’environnement canadien au TPAE-2 soient préoccupantes, le TPAE-2 est considéré présenté un niveau de danger élevé pour les organismes aquatiques. Il pourrait donc devenir préoccupant pour l’environnement canadien si les expositions venaient à augmenter.
6.3.4 Sensibilité de la conclusion aux principales incertitudes
Les substances ayant des propriétés ioniques et tensio-actives posent un défi pour l’évaluation des risques, car leurs propriétés physicochimiques et leurs toxicités sont difficiles à mesurer lors d’études empiriques et sont aussi difficiles à modéliser, ce qui ajoute de l’incertitude aux conclusions de l’évaluation. Ce défi a été traité en modélisant une structure représentative non ionique du TPAE-1 et en ne tenant compte que d’études empiriques valides sur les TPAE, les amines aliphatiques et des analogues. Une autre source d’incertitude des QR est que la CESE des composants (di)thiophosphate d’alkyle du TPAE-1 est basée sur des données sur la toxicité de la substance complète, alors que le CEE a été modélisée en se basant les propriétés physicochimiques de la structure 1 uniquement. La CEE pour les composants (di)thiophosphate d’alkyle n’est donc pas représentative de la gamme complète des propriétés physicochimiques de cette substance. Le choix de la structure 1 pour la modélisation de la CEE est considéré prudent en raison de son log Koe relativement élevé, de 5,4 à 5,9.
Bien que les données sur l’écotoxicité des deux TPAE soient limitées, le grand ensemble de données empiriques sur la toxicité des amines aliphatiques à longue chaîne (y compris les substances analogues) indique que les composants des TPAE ont une toxicité élevée pour les organismes aquatiques ou vivant dans les sols.
Les scénarios d’exposition aux TPAE ont été élaborés en se basant sur des renseignements obtenus lors d’enquêtes menées en vertu de l’article 71 de la LCPE et lors de suivis avec les parties intéressées industrielles. En l’absence de données, des hypothèses réalistes ont été faites afin d’estimer les CEE. Pour les scénarios d’exposition, des données empiriques sur les propriétés physiques et chimiques des composants des TPAE, en particulier des composants (di)thiophosphate d’alkyle, ainsi que des données plus spécifiques sur les facteurs d’émission industriels permettraient une plus grande certitude dans les valeurs des CEE. Toutefois, il est improbable que ces renseignements puissent conduire à une modification de nos conclusions sur les risques dus à ces expositions, étant donné les faibles CESE.
Certains composants des TPAE rejetés dans l’eau devraient se retrouver dans les sédiments et pourraient s’y accumuler avec le temps, certaines structures représentatives devant être persistantes dans les sédiments. Nous n’avons pas pu déterminer le risque posé aux organismes vivant dans les sédiments en raison du manque de renseignements sur les concentrations environnementales des composants des TPAE dans les sédiments à proximité des points de rejet des effluents, ainsi que du manque de renseignements sur la toxicité des composants des TPAE autres que les amines aliphatiques pour les organismes vivant dans les sédiments. La disponibilité de tels renseignements aurait pu accroître la confiance dans les éléments de preuve utilisés pour tirer nos conclusions, mais n’aurait pas conduit à une modification de la conclusion globale.
7. Potentiel d’effets nocifs sur la santé humaine
7.1 Évaluation de l’exposition
Le TPAE-2 a fait partie de l’Évaluation préalable rapide des substances pour lesquelles l’exposition de la population générale est limitée (ECCC, SC 2018). Pour cette évaluation, le potentiel d’exposition directe a été déterminé pour les substances présentes ou utilisées dans un produit utilisé par la population générale. Le potentiel d’exposition indirecte des substances considérées avoir un faible potentiel d’exposition directe a ensuite été évalué. Suite à cette analyse, le potentiel d’exposition de la population générale au TPAE-2 a été jugée négligeable.
D’après les renseignements soumis en réponse à une enquête menée en vertu de l’article 71 de la LCPE, il n’y a eu aucune production de TPAE-1 au Canada pendant l’année civile 2011. L’utilisation rapportée pour cette substance était la fabrication de machinerie. Il ne devrait donc pas y avoir d’exposition de la population générale à cette substance (Environnement Canada 2013).
Nous n’avons trouvé aucune donnée sur des mesures de la concentration de TPAE-1 dans des milieux de l’environnement au Canada ni ailleurs.
Les estimations de l’exposition au TPAE-1 due à l’eau potable ont été basées sur la somme des CEE aquatiques des deux composants (décrites dans les tableaux 6-2 et 6‑3) associées à des rejets de cette substance dans l’environnement par des installations de travail des métaux (voir la section 6.2.4 pour plus de détails). L’absorption journalière totale la plus élevée (due à la consommation d’eau potable) de TPAE-1 par la population générale était de 1,39 µg/kg pc/jour (pour les enfants de moins de 6 mois). L’absorption journalière totale pour les autres groupes d’âge et les paramètres utilisés pour estimer l’exposition sont décrits à l’Annexe B. Il se peut que les expositions estimées au TPAE-1 dues à la consommation d’eau potable soient très prudentes, étant donné que la CEE a été calculée afin de représenter la concentration dans l’eau à proximité du point de rejet et que la dilution supplémentaire et l’élimination potentielles durant le traitement de l’eau potable n’ont pas été pris en compte.
7.2 Évaluation des effets sur la santé
Des données sur les effets sur la santé du TPAE-1 ont été rapportées lors de la soumission du numéro CE 931-384-6 pour REACH (ECHA 2007-2018a).
Il existe une étude à court terme à dose répétée pour le TPAE-1 (Rapport d’étude anonyme 2002a). Lors de cette étude, quatre groupes de 10 rats femelles et de 10 rats mâles CD Sprague-Dawley ont reçus 0, 50, 150 ou 500 mg/kg pc/jour de la substance par gavage, pendant 28 jours. Des augmentations du poids absolu et du poids relatif du foie et des glandes surrénales et du poids absolu du cœur ont été observées chez les femelles du groupe ayant reçu la dose la plus élevée. Des modifications histopathologiques ont été observées chez les groupes ayant reçu la dose élevée ou la dose moyenne, dont des effets sur les glandes surrénales (augmentation de la vacuolisation corticale et hypertrophie) et les reins (incidence accrue de gouttelettes hyalines). Des tests neurocomportementaux ont mis en évidence un écartement moindre du pied d’atterrissage chez les femelles des groupes ayant reçu une dosse élevée ou moyenne. Aucune modification liée au traitement n’a été observée lors d’un examen microscopique du système nerveux central. En se basant sur les effets observés chez le groupe ayant reçu la dose moyenne, une DSENO de 50 mg/kg pc/jour a été établie pour cette étude.
Des données sur la toxicité pour la reproduction tirées d’un test de dépistage 421 de l’OCDE sont disponibles pour le TPAE-1. Pour cette étude (Rapport d’étude anonyme 2010), des rats Wistar, en groupes de 10 mâles et 10 femelles, ont reçu 0, 15, 150 ou 750 mg/kg pc/jour par gavage pendant jusqu’à 56 jours. Des observations cliniques chez les animaux recevant la dose élevée ont conduit à réduire la dose à 500 mg/kg pc/jour à partir du jour 5. Les femelles recevant 750 mg/kg pc/jour exhibaient des tremblements occasionnels avant la réduction de la dose à 500 mg/kg pc/jour. Le gain de poids corporel cumulatif des animaux des deux sexes du groupe recevant la dose élevée était statistiquement réduit pendant la dernière semaine de gestation. Aucun effet sur le poids corporel n’a été observé chez les femelles et les mâles recevant la dose moyenne ou faible. Une incidence accrue d’hypertrophie/vacuolisation des glandes interstitielles des ovaires a été observée chez les femelles recevant la dose élevée, bien que cette augmentation ne soit pas statistiquement significative. À la dose élevée, il y avait une diminution statistiquement significative de l’indice de naissances vivantes. Aucune perte pré- ou post-implantation statistiquement significative n’a été observée, ni aucun effet lié au traitement sur les taux de conception. Les auteurs de l’étude ont indiqué que la substance n’avait des effets nocifs sur la reproduction qu’aux doses toxiques pour la mère. Ils ont rapporté une DSENO de 150 mg/kg pc/jour. Ils ont aussi indiqué qu’une DSEO de 15 mg/kg pc/jour était appropriée pour la toxicité pour la reproduction et le développement, basée sur une DMEO de 150 mg/kg pc/jour pour des effets non statistiquement significatifs sur la reproduction et le développement (Rapport d’étude anonyme 2010).
D’après les données disponibles (ECHA 2007-2018a), cette substance n’est pas génotoxique. Des épreuves Ames in vitro ont donné des résultats négatifs pour cinq souches de Salmonella typhimurium, avec ou sans activation métabolique (Rapport d’étude anonyme 1996). De plus, lors de tests no 476 de l’OCDE, tests in vitro sur la mutation de gènes de cellules de mammifères, la substance s’est avérée non mutagène (Rapport d’étude anonyme 2009). Les données disponibles indiquent aussi que cette substance n’est pas génotoxique (aberration chromosomique) in vivo, d’après les résultats de tests de micronoyaux érythrocytes mammifères (Rapport d’étude anonyme 2002b).
7.3 Caractérisation des risques pour la santé humaine
L’exposition potentielle au TPAE-2 a été évaluée dans le cadre de l’Évaluation préalable rapide des substances pour lesquelles l’exposition de la population générale est limitée (ECCC, SC 2018). Elle a été considérée négligeable et, en conséquence, cette substance a été jugée peu préoccupante pour la santé humaine.
Le paramètre d’effet critique du TPAE-1 sur la santé a été établi à 50 mg/kg pc/jour, basé sur des effets observés sur les glandes surrénales et des effets potentiels neurotoxiques et/ou comportementaux lors d’une étude à court terme à dose répétée. Une exposition de la population générale due à la consommation d’eau potable est possible. La comparaison du niveau d’effet critique et de l’exposition potentielle estimée la plus élevée (1,39 x 10-3 mg/kg pc/jour pour les enfants de moins de 6 mois) a conduit à calculer une marge d’exposition de plus de 35 000. Pour les autres groupes d’âge, cette marge est plus importante.
En se basant sur les paramètres prudents utilisés pour la modélisation de l’exposition des humains due aux rejets potentiels de TPAE-1 dans l’environnement, il est jugé que les marges calculées sont adéquates pour tenir compte des incertitudes des bases de données sur les effets sur la santé et l’exposition.
7.4 Incertitudes de l’évaluation des risques pour la santé humaine
Nous donnons dans le tableau suivant les sources principales d’incertitude de l’évaluation.
| Principale source d’incertitude | Impact |
|---|---|
| Il existe un manque de donnée sur l’occurrence du TPAE-1 dans l’environnement au Canada. Il y a donc une incertitude sur l’occurrence et les concentrations environnementales estimées de cet UVCB, tel que discuté à la section 6.3.4. | +/- |
| Il y a un manque de donnée sur la toxicité chronique du TPAE-1. | +/- |
+/- = potentiel inconnu de sous-estimation ou de surestimation du risque.
8. Conclusion
En tenant compte de tous les éléments de preuve avancés dans la présente ébauche d’évaluation préalable, il existe un risque d’effet nocif du TPAE-1 sur l’environnement. Il est proposé de conclure que le TPAE-1 satisfait aux critères de l’alinéa 64 a) de la LCPE, car il pénètre ou peut pénétrer dans l’environnement en une quantité ou concentration ou dans des conditions qui ont ou peuvent avoir un effet nocif immédiat ou à long terme sur l’environnement ou sa diversité biologique. Toutefois, il est proposé de conclure que le TPAE‑1 ne satisfait pas aux critères de l’alinéa 64 b) de la LCPE, car il ne pénètre pas dans l’environnement en une quantité ou concentration ni dans des conditions qui constituent ou peuvent constituer un danger pour l’environnement essentiel à la vie.
En tenant compte de tous les éléments de preuve avancés dans la présente ébauche d’évaluation préalable, il existe un faible risque d’effet nocif du TPAE-2. Il est proposé de conclure que le TPAE-2 ne satisfait pas aux critères des alinéas 64 a) et 64 b) de la LCPE, car il ne pénètre pas dans l’environnement en une quantité ou concentration ni dans des conditions qui ont ou peuvent avoir un effet nocif immédiat ou à long terme sur l’environnement ou sa diversité biologique ou qui constituent ou peuvent constituer un danger pour l’environnement essentiel à la vie.
En tenant compte de tous les éléments de preuve avancés dans la présente ébauche d’évaluation préalable, il est proposé de conclure que le TPAE-1 et le TPAE-2 ne satisfont pas aux critères de l’alinéa 64 c) de la LCPE, car ils ne pénètrent pas dans l’environnement en une quantité ou concentration ni dans des conditions qui constituent ou peuvent constituer un danger au Canada pour la vie ou la santé humaine.
Il est donc proposé de conclure donc que le TPAE-1 satisfait aux critères de l’article 64 de la LCPE et que le TPAE-2 n’y satisfait pas.
Il est aussi proposé de conclure aussi que le TPAE-1 satisfait aux critères de persistance, mais pas à ceux de bioaccumulation, du Règlement sur la persistance et la bioaccumulation de la LCPE.
Références
ACD/Percepta [moduel de prédiction module]; c1997-2012; Toronto (ON) : Advanced Chemistry Development Inc. (disponible en anglais seulement).
[AEROWIN] Atmospheric particulate sorption program for Microsoft Windows [modèle d’estimation]; 2010; ver. 1.00; Washington (DC): US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY): Syracuse Research Corporation (disponible en anglais seulement).
[AIEPS] Artificial Intelligence Expert Predictive System; c2010-2012; ver. 3.0; Gatineau (QC) : Environnement Canada; modèle développé par Stephen Niculescu (disponible en anglais seulement).
Akzo Nobel; 1992; Biodegradability of Armeen CD. Report No.: CRL F91125; Arnhem (Pays-Bas) : Akzo Research Laboratories [cité dans EPA 2003] (disponible en anglais seulement).
Akzo Nobel; 2006; Bioconcentration of 1-Hexadecylamine (C16 primary amine) in the carp, Cyprinus carpio, under flow-through conditions; Arnhem (Pays-Bas) : Akzo Research Laboratories [cité dans CE 2008] (disponible en anglais seulement).
[AOPWIN] Atmospheric Oxidation Program for Microsoft Windows [modèle d’estimation]; 2010; ver. 1.92a; Washington (DC): US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY): Syracuse Research Corporation (disponible en anglais seulement).
Armitage J., Arnot J., Wania F. et Mackay D.; 2013; Development and evaluation of a mechanistic bioconcentration model for ionogenic organic chemicals in fish; Environ. Tox. Chem., 32(1), p. 115-128 (disponible en anglais seulement).
[ASTM] American Standard Test Method International; 2000; ASTM D5864-95 Standard Test Method for Determining Aerobic Aquatic Biodegradation of Lubricants or Their Components (compte requis); West Conshohocken (PA) [consultéle 12 mars 2020] (disponible en anglais seulement).
[BCFBAF] Bioaccumulation Program for Microsoft Windows [modèle d’estimation]; 2010; ver. 3.01; Washington (DC): US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY): Syracuse Research Corporation (disponible en anglais seulement).
[BIOWIN] Biodegradation Probability Program for Microsoft Windows [modèle d’estimation]; 2008; ver. 4.10; Washington (DC): US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY): Syracuse Research Corporation (disponible en anglais seulement).
Blakemore G. et Forbis A.; 1991; Chronic toxicity of Di-Syston technical to Daphnia magna under flow-through test conditions. Data evaluation record; Kansas City (MO): Mobay Corporation; rapport no 032501, étude no 33896, MRID no : 419358-02 (disponible en anglais seulement).
Boethling R. et Mackay D.; 2000; Handbook of property estimation methods for chemicals; New York (NY) : Lewis Publisher (disponible en anglais seulement).
Boîte à outils QSAR de l’OCDE; 2017; ver. 4.1; Paris (France) : Organisation de coopération et de développement économiques, Laboratoire de chimie mathématique (disponible en anglais seulement).
Canada; 1999; Loi canadienne sur la protection de l’environnement, L.C. 1999, ch. 33; Gazette du Canada, Partie III, vol. 22, no 3.
Canada; 2000; Loi canadienne sur la protection de l’environnement : Règlement sur la persistance et la bioaccumulation, DORS/2000-107, C.P. 2000-348, 23 mars 2000.
Canada, ministère de l’Environnement; 2012; Loi canadienne sur la protection de l’environnement : Avis concernant certaines substances de la Liste inérieure [PDF]; Gazette du Canada, Partie I, vol. 146, no 48, supplément.
Canada; 2018; Approche pour divulguer des renseignements confidentiels et favoriser la transparence dans la gestion des produits chimiques [mise à jour du 23 octobre 2018, consultée le 10 juin 2020].
CATALOGIC [modèle sur le devenir et le comportement dans l’environnement]; 2014; ver. 5.11.15; Bourgas (Bulgarie) : Université « Prof. Dr. Assen Zlatarov », Laboratoire de chimie mathématique (disponible en anglais seulement).
[CE] Communauté européenne; 1992; A.5. Surface Tension [PDF]; rapport no 67/548/EEC, méthode L383 A; Official Journal of the European Communities, p.47-53 [consulté le 12 mars 2020] (disponible en anglais seulement).
[CE] Communauté européenne; 2008; European Union draft risk assessment report: Primary aliphatic amines [PDF]; Luxembourg : Office des publications officielles des Communautés européennes [consulté le 12 mars 2020] (disponible en anglais seulement).
ChemInfo Services; 2016; Technical Study on the Use, Exposure, and Release Potential of Used Lubricating Oils and Associated Substances; préparé pour Santé Canada; rapport confidentiel (disponible en anglais seulement).
Droge S.T. et Goss K.U.; 2013a; Development and evaluation of a new sorption model for organic cations in soil: Contributions from organic matter and clay minerals; Environ. Sci. Technol., 47(24), p. 14233‑14241 (disponible en anglais seulement).
Droge S.T.J. et Goss K.U.; 2013b; Ion-exchange affinity of organic cations to natural organic matter: influence of amine type and nonionic interactions at two different pHs; Environ. Sci. Technol., 47, p. 798‑806 (disponible en anglais seulement).
[ECCC] Environnement et Changement climatique Canada; 2015; Données de la mise à jour II de l’inventaire de la LIS collectées en vertu de la Loi canadienne sur la protection de l’environnement 1999 : Avis concernant certaines substances de la Liste intérieure; Données préparées par ECCC et Santé Canada, Programme des substances existantes.
[ECCC] Environnement et Changement climatique Canada; 2020; Supporting Documentation for the Ecological Exposure Assessment of TPAEs; Gatineau (QC), disponible auprès de substances@ec.gc.ca (disponible en anglais seulement).
[ECCC, SC] Environnement et Changement climatique Canada, Santé Canada; 2015; Identification des priorités d’évaluation des risques : résultats de l’examen de 2015; Ottawa (ON) : gouvernement du Canada [consulté le 12 mars 2020].
[ECCC, SC] Environnement et Changement climatique Canada, Santé Canada; [modifié le 12 mars 2017]; Catégorisation des substances chimiques; Ottawa (ON) : gouvernement du Canada [consulté le 12 mars 2020].
[ECCC, SC] Environnement et Changement climatique Canada, Santé Canada; 2018; Évaluation préalable rapide des substances pour lesquelles l’exposition de la population générale est limitée; gouvernement du Canada [consulté le 12 mars 2020].
[ECCC, SC] Environnement et Changement climatique Canada, Santé Canada; 2021; Évaluation préalable des amines aliphatiques; Ottawa (ON) : gouvernement du Canada.
[ECETOC] European Centre for Ecotoxicology and Toxicology of Chemicals; 2003; Environmental risk assessment of difficult substances; rapport no 88; Bruxelles (Belgique) : ECETOC, 109 p. (disponible en anglais seulement).
[ECHA] Agence européenne des produits chimiques; 2015; Registration Dossier: Hexadecyldimethylamine CAS RN 112-69-6; Helsinki (Finlande) : ECHA [mis à jour le 13 avril 2015; consulté en octobre 2018] (disponible en anglais seulement).
[ECHA] Agence européenne des produits chimiques; 2016; Guidance on Information Requirements and Chemical Safety Assessment. Chapter R. 16: Environmental Exposure Estimation; version 3.0 [PDF] [consulté le 12 mars 2020] (disponible en anglais seulement).
[ECHA] Agence européenne des produits chimiques; 2017; Registration Dossier: O,O-dibutyl hydrogen thiophosphate, compound with 1-octylamine (1:1) CAS RN 93964-99-9; Helsinki (Finlande) : ECHA [mis à jour le 14 aoûtl 2017; consulté le 19 novembre 2018] (disponible en anglais seulement).
[ECHA] Agence européenne des produits chimiques; 2018a; Registration Dossier: Amines, C16-18-(even numbered, saturated and unsaturated) alkyl, O,O-di-Bu phosphorothioates; EC No. 947-129-7; Helsinki (Finlande) : ECHA [mis à jour le 13 mars 2018; consulté le 19 novembre 2018] (disponible en anglais seulement).
[ECHA] Agence européenne des produits chimiques; 2018b; Substance Information for Reaction products of bis(4-methylpentan-2-yl) dithiophosphoric acid with phosphorus oxide, propylene oxide and amines, C12-14-alkyl (branched); EC No. 931-384-6; Helsinki (Finlande) : ECHA [mis à jour le 15 août 2018; consulté le 13 mars 2019] (disponible en anglais seulement).
[ECHA] Agence européenne des produits chimiques; Registration Dossier: Octadecylamine, CAS RN 124-30-1; Helsinki (Finlande) : ECHA [mis à jour le 10 janvier 2018; consulté le 6 avril 2018] (disponible en anglais seulement).
[ECHA] Agence européenne des produits chimiques; 2019a; Registration Dossier: Reaction products of bis(4-methylpentan-2-yl) dithiophosphoric acid with phosphorus oxide, propylene oxide and amines, C12-14-alkyl (branched); EC No. 931-384-6; Helsinki (Finlande) : ECHA [mis à jour l6 mars 2019; consulté le 13 mars 2019] (disponible en anglais seulement).
[ECHA] Agence européenne des produits chimiques; 2019b; Registration Dossier: Amines, C10-14 tert-alkyl; EC 701-175-2; Helsinki (Finlande) : ECHA [mis à jour le 7 février 2019; consulté le 27 mars 2019] (disponible en anglais seulement).
[ECHA] Agence européenne des produits chimiques; 2019c; Registration Dossier: Octylamine; CAS RN 111-86-4; Helsinki (Finlande) : ECHA [mis à jour le 6 février 2019; consulté le 27 mars 2019] (disponible en anglais seulement).
[ECHA] Agence européenne des produits chimiques; 2019d; Registration Dossier: Hexadecyldimethylamine; CAS RN 112-69-6; Helsinki (Finlande) : ECHA [mis à jour le 9 février 2019; consulté le 18 février 2020] (disponible en anglais seulement).
[ECHA] Agence européenne des produits chimiques; 2019e; Registration Dossier: O,O-dibutyl hydrogen thiophosphate, compound with 1-octylamine (1:1); CAS RN 93964-99-9; Helsinki (Finlande) : ECHA [mis à jour le 25 janvier 2019; consulté le 13 mars 2019] (disponible en anglais seulement).
[ECOSAR] ECOlogical Structure-Activity Relationship Model Class Program [modèle d’estimation]; c2000-2016; ver. 2.0; Washington (DC): US Environmental Protection Agency, Office of Chemical Safety and Pollution Prevention [consulté le 12 mars 2020] (disponible en anglais seulement).
ECOTOX] ECOTOXicology database [base de données]; 2000-2019; ver. 5.1; Washington (DC): US Environmental Protection Agency, Office of Research and Development; National Health and Environmental Effects Research Laboratory; Mid-Continent Ecology Division [mise à jour le 14 mars 2019, consultée le 14 mars 2019] (disponible en anglais seulement).
Environnement Canada; 2011; Suivi à propos de la décision finale sur l’évaluation des rejets d’huiles moteur usées dans l’environnement [PDF] [consulté le 12 mars 2020].
Environnement Canada; 2013; Données de la Mise à jour de l'inventaire de la LIS recueillies en vertu de l’article 71 de la Loi canadienne sur la protection de l'environnement, 1999: Avis concernant certaines substances de la Liste intérieure; Données préparées par: Environnement Canada et Santé Canada; Programme des substances existantes.
Environnement Canada, Santé Canada; 1994; Waste Crankcase Oils. Priority Substances List Assessment Report [PDF]; Ottawa (ON) : gouvernement du Canada [consulté le 12 mars 2020] (disponible en anglais seulement).
[EPA] Environmental Protection Agency des États-Unis; 2003; Appendix A – Robust Summaries for Reliable Studies, FND Ether Amines category HPV Chemicals Challenge; Washington (DC): US EPA, Toxicology/ Regulatory Services, Inc. Docket No.: 201-14978 (disponible en anglais seulement).
[EPA] Environmental Protection Agency des États-Unis; 2010; Screening-level hazard characterization: Fatty Nitrogen Derived amines category; Washington (DC): US EPA, Office of Pollution Prevention and Toxics (disponible en anglais seulement).
[EPI Suite] Estimation Program Interface Suite for Microsoft Windows [modèle d’estimation]; c2000-2012; ver. 4.11; Washington (DC): US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY): Syracuse Research Corporation [consulté le 12 mars 2020] (disponible en anglais seulement).
[HENRYWIN] Henry’s Law Constant Program for Microsoft Windows [modèle d’estimation]; 2008; ver. 3.20; Washington (DC): US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY): Syracuse Research Corporation (disponible en anglais seulement).
Johnson W.W. et Finley M.T.; 1980; Handbook of aquatic toxicity of chemicals to fish and aquatic invertebrates; Washington (DC): U.S. Fish and Wildlife Service, Resource Publication No.: 137, 98 p. (disponible en anglais seulement).
[KOCWIN] Organic Carbon Partition Coefficient Program for Microsoft Windows [modèle d’estimation]; 2010; ver. 2.00; Washington (DC): US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY): Syracuse Research Corporation (disponible en anglais seulement).
[KOWWIN] Octanol-Water Partition Coefficient Program for Microsoft Windows [modèle d’estimation]; 2010; ver. 1.68; Washington (DC): US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY): Syracuse Research Corporation (disponible en anglais seulement).
Krop H. et de Voogt P.; 2007; Bioconcentration factors of surfactants in seawater; Amsterdam (Pays‑Bas) : IVAM UvA BV (disponible en anglais seulement).
Lara-Martin P.A., Li X., Bopp R.F. et Brownawell B.J.; 2010; Occurrence of alkyltrimethylammonium compounds in urban estuarine sediments: Behentrimonium as a new emerging contaminant; Environ. Sci. Technol., 44, p. 7569-7575 (disponible en anglais seulement).
McLachlan M.; 2018; CEFIC ECO37 D-BASS: Development of a bioaccumulation assessment strategy for surfactants. Deliverable D8: Report on tissue-distribution for 2 surfactant mixtures; Stockholm (Suède) : Université de Stockholm, Département de science de l’environnement et de chimie analytique (ACES), 17 p. (disponible en anglais seulement).
[OCDE] Organisation de coopération et de développement économiques; 1992; Test No. 301: Ready Biodegradability, OECD Guidelines for the Testing of Chemicals, Section 3, OECD Publishing; Paris (France) (disponible en anglais seulement).
[OCDE] Organisation de coopération et de développement économiques; 2004; Emission scenario document on lubricants and lubricant additives [PDF]; Paris (France) : OCDE, Direction de l’environnement (Series on Emission Scenario Documents No. 10; Report No.: ENV/JM/MONO(2004)21, JT00174617) [consulté le 12 mars 2020] (disponible en anglais seulement).
[OCDE] Organisation de coopération et de développement économiques; 2011; Emission scenario document on the use of metalworking fluids [PDF]; Paris (France): OCDE, Direction de l’environnement (Series on Emission Scenario Documents No. 28, Report No. ENV/JM/MONO(2011)18 [consulté le 12 mars 2020] (disponible en anglais seulement).
Owojori O.J., Waszak K. et Roembke J.; 2014; Avoidance and reproduction tests with the predatory mite Hypoaspis aculeifer: Effects of different chemical substances; Environ. Toxicol. Chem., 33(1), p. 230-237 (disponible en anglais seulement).
Présentation d’étude; 2018; étude confidentielle non publiée soumise à Environnement et Changement climatique Canada (ECCC) dans le cadre de l’initiative du Plan de gestion des produits chimiques; Gatineau (QC) : ECCC, Division de la mobilisation et de l’élaboration de programmes; Présentation reçue le 4 avril 2018 (disponible en anglais seulement).
Rapport d’étude anonyme; 1996; OECD Guideline 471 Bacterial Reverse Mutation Assays Study (tel que cité dans ECHA 2019a) [consulté le 15 novembre 2018] (disponible en anglais seulement).
Rapport d’étude anonyme; 2002a; Short-term Repeated Dose Toxicity Study in Rats (tel que cité dans ECHA 2019a) [consulté le 15 novembre 2018] (disponible en anglais seulement).
Rapport d’étude anonyme; 2002b; EPA OPPTS 870.5395 In Vivo Mammalian Cytogenetics Tests: Erythrocytes Micronucleus Assay (tel que cité dans ECHA 2019a) [consulté le 15 novembre 2018] (disponible en anglais seulement).
Rapport d’étude anonyme; 2009; OECD Guideline 476 In Vitro Mammalian Cell Gene Mutation Test (tel que cité dans ECHA 2019a) [consulté le 15 novembre 2018] (disponible en anglais seulement).
Rapport d’étude anonyme; 2010; OECD Guideline 421 Reproduction/Developmental Toxicity Screening Test (tel que cité dans ECHA 2019a) [consulté le 15 novembre 2018] (disponible en anglais seulement).
Santé Canada; 2015; Tableau de la consommation des aliments, Enquête sur la santé dans les collectivités canadiennes, cycle 2.2, Nutrition (2004), dossier partagé; Ottawa (ON).
Santé Canada; 2017; Tableau de la consommation d’eau, Enquête sur la santé dans les collectivités canadiennes, cycle 2.2, Nutrition (2004), dossier partagé; Ottawa (ON).
Santé Canada; 2018; Draft backgrounder document on default values for breast milk and formula intakes; rapport non publié; Ottawa (ON) : gouvernement du Canada (disponible en anglais seulement).
Santé Canada; 2019; Base de données sur l’information sur les produits antiparasitaires – Recherche d’un principe actif [consultée le 25 juillet 2019].
Schlechtriem C., Nendza M., Hahn S., Zwintscher A., Schüürmann G. et Kühne R.; 2014; Contribution of non-lipid based processes to the bioaccumulation of chemicals; Dessau-Roßlau (Allemagne) : Recherche environnementale du ministère fédéral de l’Environnement, Conservation de la nature et sûreté nucléaire; rapport no UBA-FB 00, 92 p. (disponible en anglais seulement).
SimpleTreat [sewage treatment plant removal model]; 2003; ver. 3.1; Bilthoven (Pays-Bas) : Rijksinstituut voor Volksgezondheid en Milieu (RIVM) [Institut national pour la santé publique et l’environnement], Laboratoire d’évaluation du risque écologique, B.P. 1, 3720 BA Bilthoven, Pays-Bas (disponible en anglais seulement).
Sparling D.W.; 2016; Ecotoxicology Essentials: Environmental contaminants and their biological effects on animals and plants; Academic Press, Elsevier Inc., États-Unis, chapitre 5, Current Use Pesticides, p. 109-147 (disponible en anglais seulement).
[TEST] Toxicity Estimation Software Tool; 2016; ver. 4.2.1; Washington (DC): US Environmental Protection Agency (disponible en anglais seulement).
Versteeg D.J. et Shorter S.J.; 1991; Effect of organic carbon on the uptake and toxicity of quaternary ammonium compounds to the fathead minnow, pimephales promelas; Cincinnati (OH): The Procter & Gamble Company, Environmental Safety Department (disponible en anglais seulement).
Versar Inc.; 1986; Standard scenarios for estimating exposure to chemical substances during use of consumer products. Vol. II. Consumer use of used motor oil; Springfield (VA): Versar Inc., préparé pour l’Environmental Protection Agency des États-Unis (disponible en anglais seulement).
[WATERNT] Water Solubility Program [estimation model]; 2010; ver. 1.01; Washington (DC): US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY): Syracuse Research Corporation (disponible en anglais seulement).
[WSKOWWIN] Water Solubility for Organic Compounds Program for Microsoft Windows [modèle d’estimation]; 2010; ver. 1.42; Washington (DC): US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY): Syracuse Research Corporation (disponible en anglais seulement).
Annexes
Annexe A. Propriétés physiques et chimiques des substances analogues du Programme de renseignements concernant les substances nouvelles (PRSN)
| Propriété | Analogue RNS 1 | Analogue RSN 2 |
|---|---|---|
| États physique (20 °C) | liquide | liquide |
| Point de fusion (°C) | -12 (point d’écoulement) | -20,2 (point d’écoulement) |
| Point d’ébullition (°C à 101,3 kPa) | 180 (initial) – 569 (final) | 240 |
| Pression de vapeur (Pa) | 2,95 à 24 °C | 1,8 x 10-4 |
| Densité (sans unité) | 1,014 à 15,6 °C | 1,02 à 20 °C |
| Solubilité dans l’eau (mg/L) | TC 70,1 à 500 | compt P 838, compt S 938; compt amine TC 2140; TC 5500 |
| Solubilité dans l’eau (mg/L) | 729 à 10 000 LR | FS : insoluble |
| log Koe (sans dimension) | Majorité des composants > 6, minorité des composants 3,0, 4,2, 4,3 | 0,76 |
| log Koc (sans dimension) | 1,9 – 2,4 | NA |
Notes : Les références des substances analogues sont confidentielles.
Abréviations: compt. = composant; TC = taux de charge; Koe = coefficient de partage octanol-eau; Koc = coefficient de partage carbone organique-eau; P = phosphate; S = soufre.
Annexe B. Absorption journalière estimée de TPAE-1 des humains due à une exposition par voir orale
| Catégorie d’âge | Eau potablea |
|---|---|
| 0 à 5 moisb (nourris avec une préparation)c | 1,39 |
| 6 à 11 moisd | 0,89 |
| 1 ane | 0,35 |
| 2 à 3 ansf | 0,30 |
| 4 à 8 ansg | 0,24 |
| 9 à 13 ansh | 0,19 |
| 14 à 18 ansi | 0,19 |
| 19 ans ou plusj | 0,22 |
a 10,62 µg/L tel que rapporté en tant que somme des CEE pour les rejets de TPAE-1 par des installations industrielles, en assumant une valeur au 10ème percentile (voir la section 6.2.4).
b En assumant un poids de 6,3 kg (Santé Canada 2015). Il est assumé qu’aucune ingestion d’huile due à des pratiques typiques de soins n’a lieu.
c Nourris exclusivement avec des préparations pour bébés, en assumant boire 0,826 L d’eau par jour (Santé Canada 2018), l’eau étant utilisée pour reconstituer la préparation. Voie la note de bas de page sur l’eau potable pour plus de détails.
d En assumant un poids de 9,1 kg (Santé Canada 2015), une consommation de 0 L d’eau par jour (Santé Canada 2017). Pour les enfants allaités, il est assumé une consommation de 0,632 L de lait maternel par jour (Santé Canada 2018). Pouyr les enfants nourris avec de la préparation, il est assumé une consommation de 0,764 L d’eau par jour (Santé Canada 2018), l’eau étant utilisée pour reconstituer la préparation. Voir la note de bas de page (a) pour plus de détails sur l’eau potable.
e En assumant un poids de 11,0 kg (Santé Canada 2015), une consommation d’eau de 0,36 L par jour (Santé Canada 2017).
f En assumant un poids de 15,0 kg (Santé Canada 2015), une consommation d’eau de 0,43 L par jour (Santé Canada 2017).
g En assumant un poids de 23,0 kg (Santé Canada 2015), une consommation d’eau de 0,53 L par jour (Santé Canada 2017).
h En assumant un poids de 42,0 kg (Santé Canada 2015), une consommation d’eau de 0,74 L par jour (Santé Canada 2017).
i En assumant un poids de 62,0 kg (Santé Canada 2015), une consommation d’eau de 1,09 L par jour (Santé Canada 2017).
j En assumant un poids de 74,0 kg (Santé Canada 2015), une consommation d’eau de 1,53 L par jour (Santé Canada 2017).
