Ébauche d’évaluation préalable - pipérazine
Titre officiel : Ébauche d’évaluation préalable - pipérazine
Numéro de registre du Chemical Abstracts Service
110-85-0
Environnement et Changement climatique Canada
Santé Canada
Mars 2021
Sommaire
En vertu de l’article 68 de la Loi canadienne sur la protection de l’environnement (1999) (LCPE), les ministres de l’Environnement et de la Santé ont effectué une évaluation préalable de la pipérazine. Le numéro de registre du Chemical Abstracts Service (no CASNote de bas de page 1) pour la pipérazine est 110-85-0. Cette substance a été jugée d’intérêt prioritaire pour une évaluation en raison de préoccupations pour la santé humaine.
La pipérazine n’est pas présente à l’état naturel dans l’environnement. D’après les données obtenues dans le cadre d’une enquête menée en vertu de l’article 71 de la LCPE, pour l’année de déclaration 2008, aucun répondant n’a indiqué qu’il avait fabriqué la substance au delà du seuil de déclaration de 100 kg. Cependant, entre 10 000 et 100 000 kg de pipérazine ont été importés au Canada pour une utilisation commerciale dans des peintures et des enduits, et comme intermédiaire chimique dans les industries, notamment dans les systèmes de captage et de stockage du carbone. Les données obtenues dans le cadre d’autres programmes de Santé Canada ainsi que les fiches de données de sécurité (FDS) des produits ont permis de trouver d’autres utilisations au Canada, notamment comme ingrédient médicinal dans des médicaments antiparasitaires à usage humain et vétérinaire, et comme comonomère dans les adhésifs époxydes. La substance est possible utilisée comme aromatisant dans les aliments vendus au Canada.
Les risques environnementaux associés à la pipérazine ont été caractérisés à l’aide de l’approche de Classification du risque écologique (CRE) des substances organiques, c’est-à-dire une approche basée sur le risque qui considère plusieurs paramètres liés au danger et à l’exposition et classe les risques après une pondération de plusieurs données probantes. Les profils de danger reposent principalement sur des paramètres liés au mode d’action toxique, à la réactivité chimique, aux seuils de toxicité interne dérivés du réseau trophique, à la biodisponibilité et à l’activité chimique et biologique. Parmi les paramètres pris en compte pour la détermination des profils d’exposition, on retrouvé le taux d’émission potentiel, la persistance globale et le potentiel de transport à grande distance. Une matrice de risques est utilisée pour attribuer aux substances un potentiel faible, moyen ou élevé à partir de leurs profils de danger et d’exposition. Selon les résultats de l’analyse CRE, il est peu probable que la pipérazine cause des dommages à l’environnement.
Compte tenu de tous les éléments de preuve contenus dans la présente ébauche d’évaluation préalable, la pipérazine présente un risque faible de causer des effets nocifs pour l’environnement. Il est proposé de conclure que la pipérazine ne satisfait pas aux critères énoncés aux alinéas 64a) et b) de la LCPE, car elle ne pénètre pas dans l’environnement en une quantité ou concentration ou dans des conditions de nature à avoir, immédiatement ou à long terme, un effet nocif sur l’environnement ou sur la diversité biologique, ou à mettre en danger l’environnement essentiel pour la vie.
Dans une étude canadienne de l’air intérieur, on n’a pas détecté de pipérazine ni trouvé de donnée de surveillance de la pipérazine dans l’environnement. La pipérazine devrait se répartir dans l’eau si elle est rejetée dans l’environnement et ne devrait pas être stable dans l’air. Par conséquent, l’exposition des Canadiens à la pipérazine dans les milieux naturels a été estimée d’après les rejets potentiels à grande échelle dans les eaux de surface et les rejets dans l’air par des sources ponctuelles.
Des effets neurologiques ont été constatés par l’Organisation de coopération et de développement économiques, tout comme l’indique le Rapport d’évaluation des risques de l’Union européenne. Ces effets sont, en l’occurrence, des effets critiques sur la santé, d’après des rapports cliniques et des études sur les humains ayant reçu la pipérazine dans un médicament antiparasitaire. La pipérazine est également classée par l’Agence européenne des produits chimiques comme une substance toxique pour la reproduction et un sensibilisant respiratoire.
La pipérazine peut être rejetée dans l’environnement (c. à d. dans l’air et dans l’eau) lorsqu’elle est utilisée dans des applications industrielles, notamment dans les systèmes de captage et de stockage du carbone (également appelés épurateurs de gaz). D’après une comparaison des estimations de l’exposition à la pipérazine dans les milieux naturels et des concentrations auxquelles des effets critiques sont observés, les marges sont jugées suffisantes pour tenir compte des incertitudes dans les bases de données sur les effets sur la santé et l’exposition. D’après l’estimation de la consommation par habitant aux États Unis réalisée par le Comité mixte FAO/OMS d’experts des additifs alimentaires (JECFA), l’exposition des Canadiens à la pipérazine et celle découlant de son utilisation comme aromatisant alimentaire est jugée négligeable et le risque pour la santé humaine est jugé faible.
L’exposition de la population générale canadienne à la pipérazine peut découler de son utilisation dans des produits de consommation contenant des adhésifs époxydes. À la lumière d’une comparaison de la concentration de l’exposition à la pipérazine par voie cutanée et par inhalation estimée avec les concentrations auxquelles des effets critiques sont observés, les marges sont jugées suffisantes pour tenir compte des incertitudes dans les bases de données sur l’exposition et les effets sur la santé.
À la lumière des renseignements contenus dans la présente ébauche d’évaluation préalable, il est proposé de conclure que la pipérazine ne satisfait pas au critère énoncé à l’alinéa 64c) de la LCPE, car elle ne pénètre pas dans l’environnement en une quantité ou concentration ou dans des conditions de nature à constituer un danger au Canada pour la vie ou la santé humaines.
Il est proposé de conclure que la pipérazine ne satisfait à aucun des critères énoncés à l’article 64 de la LCPE.
1. Introduction
En vertu de l’article 68 de la Loi canadienne sur la protection de l’environnement (1999) [LCPE] (Canada 1999), les ministres de l’Environnement et de la Santé ont réalisé une évaluation préalable de la pipérazine afin de déterminer si cette substance pose ou peut poser des risques pour l’environnement ou la santé humaine. Cette substance a été jugée d’intérêt prioritaire pour une évaluation en raison d’autres préoccupations pour la santé humaine (ECCC, SC [modifié en 2017]).
Le risque pour l’environnement associé à la pipérazine a été caractérisé selon l’approche de la Classification du risque écologique (CRE) des substances organiques (ECCC 2016a). La CRE permet de décrire le danger posé par une substance à l’aide de paramètres clés, notamment le mode d’action toxique, la réactivité chimique, les seuils de toxicité interne dérivés du réseau trophique, la biodisponibilité et l’activité chimique et biologique, et d’évaluer l’exposition potentielle des organismes en milieux aquatique et terrestre en fonction de facteurs comme le taux d’émission potentiel, la persistance globale et le potentiel de transport atmosphérique à grande distance. Les diverses données probantes sont combinées afin de déterminer quelles substances nécessitent une évaluation plus poussée de leur potentiel à causer des effets nocifs pour l’environnement ou ont une faible probabilité de causer des effets nocifs pour l’environnement.
La substance visée par la présente évaluation a été examinée au niveau international par l’Organisation de coopération et de développement économiques (OCDE), et il existe pour cette substance un profil d’évaluation initiale (SIAP) de l’ensemble des données de dépistage (SIDS) de l’OCDE. Ces évaluations sont soumises à un examen rigoureux (dont un examen par des pairs) et sont approuvées par les autorités gouvernementales internationales. Santé Canada et Environnement et Changement climatique Canada sont des participants actifs à ces processus et considèrent ces évaluations comme fiables. Le rapport final d’évaluation du processus de l’OCDE a été publié sous forme de Rapport d’évaluation des risques de l’Union européenne (EU RAR). Dans la présente évaluation préalable, le SIAP de l’OCDE et le RAR de l’UE ont été utilisés pour éclairer la caractérisation des effets sur la santé.
La présente ébauche d’évaluation préalable tient compte des renseignements sur les propriétés chimiques, le devenir dans l’environnement, les dangers, les utilisations et l’exposition à la substance, y compris d’autres renseignements présentés par des intervenants. Les données pertinentes ont été recensées jusqu’en août 2019. Des données empiriques tirées d’études clés ainsi que des résultats de modélisation ont servi à tirer les conclusions proposées.
La présente ébauche d’évaluation préalable a été préparée par le personnel du Programme d’évaluation des risques de la LCPE travaillant à Santé Canada et à Environnement et Changement climatique Canada. Elle comprend des données provenant d’autres programmes de ces deux ministères. La partie de l’évaluation portant sur l’environnement repose sur le document décrivant la CRE (publié le 30 juillet 2016), lequel a fait l’objet d’un examen externe et d’une consultation publique de 60 jours.
La présente ébauche d’évaluation préalable se concentre sur les données essentielles permettant de déterminer si une substance répond aux critères énoncés à l’article 64 de la LCPE, en examinant les données scientifiques et en utilisant une approche fondée sur le poids de la preuve et le principe de prudenceNote de bas de page 2. À cette fin, nous avons examiné les données critiques et nous avons tenu compte des facteurs sur lesquels la conclusion proposée est basée.
2. Identité de la substance
Le tableau 2‑1 présente le no CASNote de bas de page 3 de la pipérazine et son nom dans la Liste intérieure des substances (LIS).
| No CAS | Nom dans la LIS | Structure chimique et formule moléculaire | Masse moléculaire (g/mol) |
|---|---|---|---|
| 110-85-0 | Pipérazine | 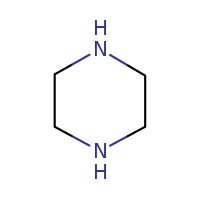 C4H10N2 C4H10N2 | 86,1 |
3. Propriétés physiques et chimiques
Le tableau 3‑1 présente un résumé des propriétés physiques et chimiques de la pipérazine. ECCC (2016 b) présente d’autres propriétés physico-chimiques.
| Propriété | Valeur | Référence clé |
|---|---|---|
| État physique | Solide | ECHA c2007-2019 |
| Point de fusion (°C) | 106 @ 101,325 kPa | ECHA c2007-2019 |
| Pression de vapeur (Pa) | 39 | ECHA c2007-2019 |
| Solubilité dans l’eau (mg/L) | 150 000 | ECHA c2007-2019 |
| Log Koe (sans dimension) | -1,24 | ECHA c2007-2019 |
| pKa1 (sans dimension) | 9,7 | ECHA c2007-2019 |
| pKa2 (sans dimension) | 5,3 | ECHA c2007-2019 |
Abréviations : Koe = coefficient de partage octanol-eau; pKa = constante de dissociation acide.
4. Sources et utilisations
La pipérazine a fait l’objet d’une enquête menée en vertu de l’article 71 de la LCPE (Canada 2009). La substance n’a pas été fabriquée en quantité supérieure au seuil de déclaration de 100 kg au cours de l’année civile 2008 au Canada. Les quantités totales importées déclarées au cours de cette même année étaient comprises entre 10 000 et 100 000 kg pour une utilisation commerciale dans des peintures et des enduits, et comme intermédiaire chimique en milieu industriel, y compris dans les systèmes de captage et de stockage du carbone (Environnement Canada 2009). La substance est également utilisée dans des adhésifs industriels (SDS 2017b; SDS 2017c; SDS 2019), des liants plastiques époxydes (SDS 2016) et des adhésifs automobiles (SDS 2017a) disponibles pour les consommateurs, en l’occurrence des trousses de réparation automobile. Au Canada, la pipérazine est également utilisée comme ingrédient médicinal dans des médicaments antiparasitaires, soit un médicament à usage humain et sept à usage vétérinaire (communication personnelle, courriel de la Direction des produits thérapeutiques, Santé Canada, au Bureau de l’évaluation du risque des substances existantes, Santé Canada, janvier 2019) et comme composant d’enduits utilisés dans les revêtements de sol dans les établissements de transformation des aliments (communication personnelle, courriel de la Direction des aliments, Santé Canada, au Bureau de l’évaluation du risque des substances existantes, Santé Canada, février 2019). Aucune donnée définitive n’est disponible concernant l’utilisation potentielle de la pipérazine comme aromatisant dans les aliments vendus au Canada. Cependant, comme cette substance est connue, ailleurs dans le monde, pour être utilisée comme aromatisant alimentaire, il est possible qu’elle soit présente comme telle dans les aliments vendus au Canada (communication personnelle, courriel de la Direction des aliments, Santé Canada à la Direction de la sécurité des milieux, Santé Canada, février 2019; sans référence).
Dans le monde, la pipérazine est utilisée pour la fabrication des résines polyamides pour modifier certaines propriétés physiques des polyamides, notamment le point de fusion. Les résines polyamides peuvent être utilisées dans les adhésifs thermofusibles et comme liants dans l’impression flexographique (brochure du produit, 2007). Cependant, la pipérazine est incorporée dans la structure du polyamide et il n’en reste que des traces (UE 2005).
5. Potentiel d’effets nocifs sur l’environnement
Le risque écologique de la pipérazine a été caractérisé selon l’approche de la Classification du risque écologique (CRE) des substances organiques (ECCC 2016a). La CRE est une approche basée sur les risques qui tient compte de plusieurs paramètres liés au danger et à l’exposition, et sur la pondération de plusieurs données probantes. Les divers éléments de preuve sont combinés afin de pouvoir distinguer les substances présentant une puissance faible ou élevée et un potentiel d’exposition faible ou élevé dans divers milieux. Cette approche permet de réduire l’incertitude associée à la caractérisation des risques, contrairement à une approche qui serait basée sur un seul paramètre mesuré dans un seul milieu (p. ex., CL50). Elle est résumée dans les paragraphes suivants et elle est décrite en détail dans un document d’ECCC (2016a).
Les données sur les propriétés physico-chimiques, le devenir (demi-vies chimiques dans divers milieux et biotes, coefficients de partage et bioconcentration dans les poissons), l’écotoxicité aiguë pour les poissons et les volumes de produits chimiques importés et fabriqués au Canada proviennent de publications scientifiques, de bases de données empiriques accessibles (p. ex., la boîte à outils QSAR de l’OCDE, 2014), et des réponses aux enquêtes menées en vertu de l’article 71 de la LCPE, ou ont été produites à l’aide de la modélisation de la relation quantitative structure-activité (QSAR) ou du devenir du bilan massique ou de la bioaccumulation. Ces données ont été utilisées comme paramètres d’entrée dans d’autres modèles de bilan massique ou pour compléter les profils de danger et d’exposition à la substance.
Les profils de danger étaient basés principalement sur des paramètres représentant le mode d’action toxique, la réactivité chimique, les seuils de toxicité interne dérivés du réseau trophique, la biodisponibilité et l’activité chimique et biologique. Les profils d’exposition étaient également basés sur plusieurs paramètres, dont la vitesse d’émission potentielle, la persistance globale et le potentiel de transport à grande distance. On a comparé les profils de danger et d’exposition aux critères de décision afin de les classer comme faibles, modérés ou élevés. Des règles supplémentaires ont été appliquées (p. ex., cohérence de la classification, marge d’exposition) pour affiner les classifications préliminaires du danger ou de l’exposition.
Une matrice de risque a été utilisée pour assigner à chaque substance un risque faible, moyen ou élevé basé sur le classement de son danger et de son exposition. Les classifications du risque au moyen de la CRE ont été vérifiées en suivant une approche en deux étapes. La première étape consistait à modifier à la baisse le classement du risque (de modéré ou élevé à faible) des substances présentant un faible taux de rejet dans l’eau estimé après le traitement des eaux usées, ce qui constitue un faible potentiel d’exposition. La deuxième étape consistait à réévaluer le risque jugé faible en utilisant des scénarios de risque relativement prudents et à échelle locale (c.-à-d. le risque dans la zone entourant directement le point de rejet), conçus pour protéger l’environnement, afin de déterminer si le classement du risque devrait être augmenté.
La CRE est fondée sur une approche pondérée pour réduire au minimum la possibilité d’un classement trop élevé ou trop faible du danger et de l’exposition ainsi que du risque subséquent. Une description détaillée des approches équilibrées de traitement des incertitudes est présentée dans ECCC (2016a). Nous présentons ci-dessous deux des plus importantes sources d’incertitudes. Des valeurs de toxicité aiguë empiriques ou modélisées erronées pourraient mener à modifier le classement du danger, en particulier dans le cas des paramètres basés sur les concentrations de résidus dans les tissus (c.-à-d. mode d’action toxique), dont un grand nombre sont prédites à partir de modèles QSAR (OCDE QSAR Toolbox 2014). Toutefois, l’incidence de ce type d’erreur est atténuée par le fait qu’une surestimation de la létalité médiane donnera une valeur prudente (protectrice) des résidus dans les tissus qui servira à l’analyse des résidus corporels critiques. Une erreur due à une sous-estimation de la toxicité aiguë sera atténuée par le recours à d’autres paramètres de danger, tels que le profilage structurel du mode d’action, la réactivité et/ou l’affinité de liaison à l’œstrogène. Les changements ou les erreurs touchant les quantités chimiques pourraient mener à un classement différent de l’exposition, les classements de l’exposition et du risque étant très sensibles au taux d’émission et aux quantités utilisées. Les classements obtenus au moyen de la CRE représentent donc l’exposition et le risque au Canada compte tenu des quantités utilisées actuellement (déterminées par estimations), mais pourraient ne pas rendre compte des tendances futures.
Les données critiques et les considérations sur lesquelles nous avons élaboré les profils de la pipérazine ainsi que les résultats de la classification du danger, de l’exposition et du risque sont présentés dans ECCC 2016b.
En se basant sur les classements de faible danger et de faible exposition établis à partir des données prises en compte pour la CRE, le potentiel de risque de la pipérazine pour l’environnement a été classé comme faible. Il est peu probable que cette substance cause des préoccupations pour l’environnement au Canada.
6. Potentiel de causer des effets nocifs pour la santé humaine
6.1 Évaluation de l’exposition
6.1.1 Milieux naturels et aliments
La pipérazine n’a pas été détectée dans une étude portant sur l’air intérieur avec échantillonnage dans 50 maisons de la ville de Québec, entre 2008 et 2010 (CNRC 2011). Aucune autre donnée de surveillance environnementale canadienne ou ailleurs dans le monde concernant la pipérazine n’a été trouvée.
La pipérazine peut être rejetée dans l’environnement lorsqu’elle est utilisée dans des applications industrielles, notamment dans les systèmes de captage et de stockage du carbone (également appelés épurateurs de gaz). Les épurateurs de gaz éliminent le dioxyde de carbone des gaz de combustion industriels en faisant passer les gaz de combustion dans un mélange de solvant d’amines contenant de la pipérazine. Les groupes fonctionnels aminés réagissent facilement avec le dioxyde de carbone pour produire (dans le cas de la pipérazine) de la pipérazine-carbamate. Alors que les gaz de combustion épurés sont rejetés dans l’atmosphère, le carbamate est remis en circulation dans une chambre de chauffage où la pipérazine est régénérée pour être réutilisée et le dioxyde de carbone est acheminé vers un dispositif de stockage. Au cours de ce processus, la formation de la pipérazine-carbamate réduit la quantité de pipérazine libre dans le solvant de l’épurateur (ce qui réduit donc la pression partielle et la volatilité de la pipérazine), entraînant ainsi une réduction des émissions fugitives de pipérazine (Closmann et coll. 2009; Shell 2013).
L’exposition potentielle des Canadiens vivant à proximité d’installations industrielles équipées d’épurateurs de gaz a été modélisée sous forme de rejet par une source ponctuelle, car la pipérazine a une demi‑vie calculée dans l’air de 0,8 heure et ne devrait donc pas se disperser largement dans l’atmosphère. Une concentration maximale sur 1 heure de 2,67 µg/m³ (à une distance de 1 200 m de la source) a été calculée à l’aide du logiciel SCREEN3 (2013) pour estimer l’aspiration d’air des résidents vivant à proximité d’une usine équipée d’un épurateur de gaz. Les paramètres d’entrée et les résultats du modèle SCREEN3 sont décrits à l’annexe A.
La pipérazine est instable dans l’air et il est peu probable que sa présence entraîne une exposition au‑delà de celles qui se produisent à proximité d’une source ponctuelle de rejet. Cependant, elle est très soluble et stable dans l’eau. Par conséquent, les rejets industriels dans les eaux de surface peuvent parcourir de grandes distances et pénétrer dans les réseaux d’eau potable. Afin de déterminer l’exposition environnementale potentielle à la pipérazine pour la population générale du Canada (ne vivant pas nécessairement à proximité des épurateurs de gaz industriels), on a calculé des estimations sur la base des rejets potentiels à grande échelle dans les eaux de surface à l’aide du Chiffrier pour l’eau potable de l’Unité d’évaluation environnementale (Santé Canada 2015a). Les paramètres d’entrée comprenaient les quantités totales maximales importées déclarées en réponse à une enquête menée en vertu de l’article 71 de la LCPE (c.‑à‑d. 100 000 kg), un pourcentage prudent de rejets dans les eaux usées de 5 % (pour les scénarios de rejets industriels), un pourcentage d’élimination par les systèmes de traitement des eaux usées (STEU) de 83 % (ECCC 2016b), et un débit de 0,823 m³/s dans le plan d’eau récepteur. L’estimation résultante de la concentration de pipérazine dans les eaux de surface était de 48,6 µg/L et a été utilisée pour estimer l’exposition à la pipérazine par la consommation d’eau potable.
Aucun cas de présence de pipérazine dans les aliments canadiens n’a été relevé. Au Canada, la pipérazine est utilisée comme composant des revêtements de sol dans les établissements de transformation des aliments. La population générale ne devrait pas être exposée à la pipérazine en raison de cette utilisation (communication personnelle, courriel de la Direction des aliments, Santé Canada, au Bureau de l’évaluation du risque des substances existantes, Santé Canada, février 2019).
Aucune donnée définitive n’est disponible concernant l’utilisation possible de la pipérazine dans les aliments vendus au Canada. Cependant, comme cette substance est reconnue comme aromatisant alimentaire ailleurs dans le monde, il est possible qu’elle soit présente comme aromatisant dans les aliments vendus au Canada. Le Comité mixte FAO/OMS d’experts des additifs alimentaires (JECFA) a évalué l’utilisation de la pipérazine comme aromatisant alimentaire et a estimé que la consommation par habitant de cette substance est de 0,09 µg/j (0,001 µg/kg p.c./j sur la base d’un poids corporel de 60 kg) pour la population américaine âgée de 1 an et plus. Cette estimation était basée sur les volumes de production annuels déclarés par l’industrie alimentaire (EFSA 2015; Gavin 2007, tel que présenté dans JECFA 2009). JECFA a déterminé que cette substance ne présente aucun problème de sécurité aux concentrations actuelles ingérées lorsqu’elle est utilisée comme aromatisant. En l’absence de données sur l’utilisation réelle, le cas échéant, de la pipérazine comme aromatisant alimentaire dans les aliments vendus au Canada, l’estimation du JECFA (2009) de l’ingestion par habitant aux États-Unis est considérée comme une estimation acceptable de l’exposition alimentaire potentielle de la population canadienne à cette substance en raison de cette utilisation dans les aliments. L’exposition cumulée estimée à la pipérazine par l’environnement et les aliments pour la population générale varie de 1,54 à 7,94 µg/kg p.c./j, les nourrissons de moins de 6 mois nourris au lait maternisé étant les plus exposés, principalement par l’eau potable (voir l’annexe B pour les paramètres d’entrée et les estimations de la dose journalière).
6.1.2 Produits de consommation
Lorsque la pipérazine est utilisée comme ingrédient médicinal dans des médicaments à usage vétérinaire, le traitement des animaux domestiques consiste généralement à administrer par voie orale deux comprimés au plus par mois. Lorsqu’il est administré sous forme liquide, le médicament est appliqué directement sur l’aliment de l’animal selon le même calendrier. L’exposition humaine potentielle est jugée faible pour cette utilisation, étant donné la courte durée de manipulation, le contact minime avec le médicament et la fréquence d’administration du médicament antiparasitaire.
La pipérazine peut également être utilisée dans les trousses de réparation automobile (SDS 2017a), et dans les colles plastiques époxydes pour petits projets (SDS 2016). Lorsqu’elle est formulée dans des adhésifs époxydes, la pipérazine serait présente à des concentrations inférieures à 1 % et serait entièrement consommée après durcissement. Tous les adhésifs époxydes trouvés dans les produits disponibles pour les consommateurs et formulés avec de la pipérazine étaient fournis avec une seringue préchargée et préparée pour délivrer simultanément les parties A et B de l’époxyde. L’époxyde en deux parties se mélange pendant l’application grâce à de multiples chicanes décalées à l’intérieur du cylindre de la seringue. Ainsi, l’exposition potentielle à la pipérazine est éliminée pendant l’étape de mélange/chargement et le risque d’exposition pendant l’application est réduit. Sur ConsExpo Web (2019), la fiche d’information sur les colles à deux composants (RIVM 2007) a été utilisée pour estimer l’exposition à la pipérazine par voie cutanée et par inhalation (voir l’annexe C pour les détails et les paramètres d’entrée du scénario). L’exposition générale ainsi estimée pour un adulte de 19 ans ou plus à la pipérazine provenant d’une colle époxyde utilisée pour la réparation automobile (le scénario sentinelle) était de 33,4 µg/kg p.c./exposition (par inhalation) et de 6,8 µg/kg p.c./exposition (par voie cutanée).
6.2 Évaluation des effets sur la santé
Le SIAP de l’OCDE (OCDE 2004), qui a été présenté lors de la 18e réunion d’évaluation du SIAMNote de bas de page 4 de l’OCDE, et le RAR de l’UE (UE 2005) ont été utilisés pour éclairer la caractérisation des effets sur la santé pour la présente évaluation préalable.
Une recherche dans la documentation scientifique a été menée à partir de l’année précédant la 18e réunion du SIAM de l’OCDE, soit de janvier 2003 à août 2019. On n’a trouvé aucune étude des effets sur la santé pouvant avoir une incidence sur la caractérisation des risques, publiée par l’OCDE (2004) et l’UE (2005). L’ECHAECHA (c2007-2019) a classé la pipérazine comme substance toxique pour la reproduction (Repr 2) et comme sensibilisant cutané et respiratoire de catégorie 1 (ECHA 2008).
Le RAR de l’UE (2005) a indiqué que la pipérazine est facilement absorbée par le tube digestif chez les porcs. La principale voie d’élimination de la pipérazine et de ses métabolites est l’urine. La cinétique de l’absorption et de l’élimination chez les humains et les porcs s’est avérée similaire (OCDE 2004). En l’absence de données sur l’absorption par voie cutanée ou par inhalation, on a supposé une absorption de 100 % pour les deux voies (UE 2005).
D’après l’évaluation des données concernant l’utilisation de la pipérazine comme antiparasitaire chez l’humain, l’UE (UE 2005) a établi une dose minimale entraînant un effet nocif observé (DMENO) aiguë de 110 mg/kg pour les effets neurologiques (UE 2005, OCDE 2004). L’étude critique utilisée pour calculer la DMENO aiguë est celle de Padelt et coll. (1966). Cette étude a été menée sur 89 enfants (41 garçons et 48 filles), qui ont été traités par la pipérazine après avoir reçu un diagnostic d’infection aux oxyures. La pipérazine a été administrée par voie orale à une dose de 90 à 130 mg/kg deux fois par jour, les doses étant administrées à 12 heures d’intervalle. Les variations à l’électroencéphalogramme (EEG) ont été mesurées un jour avant et un jour après le traitement. On a mesuré des EEG anormaux chez 33 des 89 enfants. Cependant, comme il n’y avait aucun autre signe de neurotoxicité, le degré de nocivité associé aux anomalies de l’EEG devrait être minime (UE 2005). Par conséquent, cette étude n’a pas été considérée comme une étude clé pour la caractérisation des risques pour la présente évaluation.
L’UE (2005) a établi une DMENO de 30 mg/kg p.c./j pour la pipérazine d’après les effets neurologiques observés chez des patients humains traités par voie orale pendant 3 à 7 jours. L’UE (2005) a calculé cette DMENO d’après l’évaluation d’un certain nombre de rapports cliniques et d’études portant sur des résultats neurologiques, y compris des effets anormaux sur les mesures de l’EEG. L’évaluation de l’OCDE (2004) indique que cette DMENO était basée sur la « documentation de cas rares de neurotoxicité constatés dans la pratique clinique humaine ». L’UE (2005) a utilisé la DMENO de 30 mg/kg p.c./j comme principal résultat de l’étude de toxicité à doses répétées pour caractériser les risques pour les humains exposés à la substance par l’environnement (p. ex., eau potable, air), ainsi que pour l’exposition professionnelle (UE 2005)Note de bas de page 5.
La pipérazine ne devrait pas être génotoxique. La substance s’est révélée négative dans le test d’Ames et dans l’essai d’aberration chromosomique in vitro chez les mammifères (cellules ovariennes de hamsters chinois), avec et sans activation métabolique. Le résultat de la pipérazine s’est également révélé négatif dans l’essai du micronoyau in vivo (OCDE 2004). On a de plus déterminé qu’il est peu probable que la pipérazine soit cancérogène (OCDE 2004).
La pipérazine a été classée comme substance toxique pour la reproduction. Cette classification s’appuie sur une étude sur deux générations de rats Sprague-Dawley CD (essai no 416 des Lignes directrices de l’OCDE) réalisée par Wood et Brooks (1994), qui a également été considérée comme l’étude clé sur la reproduction par l’OCDE (2004). Dans cette étude, une dose sans effet nocif observé (DSENO) de 125 mg/kg p.c./j a été établie d’après des effets sur la fertilité à 300 mg/kg p.c./j (UE 2005; OCDE 2004). La DMENO de 300 mg/kg p.c./j a été établie d’après un indice de gestation réduit, une diminution du nombre de sites d’implantation et une diminution de la taille des portées observées chez les rats à cette dose (UE 2005). Des effets sur le développement ont été observés lors d’une étude chez le lapin. Toutefois, les effets n’ont été observés qu’à des doses toxiques pour la mère (UE 2005; Ridgeway 1987).
D’après les données obtenues sur des animaux, des observations faites chez les humains et provenant d’études épidémiologiques en milieu professionnel, il a été démontré que l’exposition à la pipérazine et à ses sels provoque une dermatite allergique ainsi qu’une sensibilisation respiratoire, mais aucun point de départ n’a pu être déterminé à partir de ces études (UE 2005).
6.3 Caractérisation du risque pour la santé humaine
La pipérazine a été classée par l’ECHA comme substance toxique présumée pour la reproduction (catégorie 2), dans le Système général harmonisé (SGH) de classification et d’étiquetage des produits chimiques. L’ECHA a également classé la pipérazine comme sensibilisant cutané et respiratoire de catégorie 1 (ECHA 2008).
L’effet critique pour la toxicité à doses répétées a été établi sous forme de DMENO de 30 mg/kg p.c./j, d’après les effets neurologiques constatés lors de l’évaluation d’un certain nombre de rapports et d’études cliniques réalisés dans le cadre du RAR de l’UE (UE 2005).
La population générale peut être exposée à la pipérazine par l’environnement et l’alimentation. L’exposition générale estimative à la pipérazine par les milieux naturels et la voie alimentaire était comprise entre 1,54 et 7,94 µg/kg p.c./j, les nourrissons de moins de 6 mois nourris au lait maternisé étant les plus exposés, principalement par l’eau potable (voir l’annexe B pour plus de détails). La comparaison de l’exposition estimative par voie orale à la pipérazine avec la dose entraînant un effet critique (30 mg/kg p.c./j) donne des marges d’exposition (ME) de 3 700 ou plus. Les ME sont jugées suffisantes pour tenir compte des incertitudes dans les bases de données sur l’exposition et les effets sur la santé. Comme le critère d’effet neurologique est inférieur à la DSENO de 125 mg/kg p.c./j établie pour la toxicité pour la reproduction, les ME calculées sont également suffisantes pour cet effet.
La population générale du Canada peut également être exposée à la pipérazine en utilisation certains adhésifs époxydes dans les produits disponibles pour les consommateurs. L’exposition résultant de cette utilisation a été estimée à 33,4 µg/kg p.c./exposition (inhalation) et à 6,8 µg/kg p.c./exposition (voie cutanée) pour les adultes de 19 ans ou plus. La comparaison de l’exposition systémique estimative combinée à la dose avec effet critique (30 mg/kg p.c./j) donne une ME de 746. La ME pour les effets sur la reproduction serait encore plus élevée. Les ME pour les effets neurologiques et les effets sur la reproduction sont jugées suffisantes pour tenir compte des incertitudes dans les bases de données sur l’exposition et les effets sur la santé. Bien que l’exposition de la population générale aux concentrations actuelles de pipérazine ne soit pas préoccupante, cette substance est considérée comme ayant un effet préoccupant sur la santé en raison de ses effets potentiels sur le système reproducteur. Par conséquent, elle pourrait être préoccupante pour la santé humaine si l’exposition devait augmenter.
6.4 Incertitudes de l’évaluation des risques pour la santé humaine
Les sources clés d’incertitude sont présentées dans le tableau suivant.
| Principales sources d’incertitudes | Impact |
|---|---|
| Il n’existe pas de données canadiennes sur la présence de pipérazine dans les aliments. C’est pourquoi les valeurs utilisées pour calculer la dose alimentaire de pipérazine proviennent exclusivement du JECFA (2009) et reposent sur une approche de dose maximisée dérivée d’une enquête (MSDI)a. | +/- |
| Il n’existe pas de données canadiennes sur la présence de pipérazine dans l’eau potable. C’est pourquoi les valeurs utilisées pour calculer l’exposition par voie orale par l’eau potable ont été modélisées sur la base de la quantité maximale déclarée dans le commerce au Canada. | + |
+ = incertitude liée au risque de surestimer l’exposition ou le risque; - = incertitude liée au risque de causer une sous-estimation de l’exposition ou du risque; +/- = risque non connu de surestimer ou de sous-estimer l’exposition ou le risque.
a JECFA a estimé l’exposition due à une éventuelle utilisation comme aromatisant en utilisant l’approche MSDI, qui est basée sur la quantité déclarée de l’aromatisant introduit dans la chaîne alimentaire par année dans une région donnée (dans ce cas‑ci, les États‑Unis). Cette valeur est corrigée pour tenir compte des sous‑déclarations, en supposant que seulement 80 % de la quantité produite annuellement est déclaré, et que 10 % de la population concernée consommerait des aliments contenant l’aromatisant.
7. Conclusion
Compte tenu de tous les éléments de preuve contenus dans la présente ébauche d’évaluation préalable, il est proposé de conclure que la pipérazine ne satisfait pas aux critères énoncés aux alinéas 64a) et b) de la LCPE, car elle ne pénètre pas dans l’environnement en une quantité ou concentration ou dans des conditions de nature à avoir, immédiatement ou à long terme, un effet nocif sur l’environnement ou sur la diversité biologique, ou à mettre en danger l’environnement essentiel pour la vie.
À la lumière des renseignements contenus dans la présente ébauche d’évaluation préalable, il est proposé de conclure que la pipérazine ne satisfait pas au critère énoncé à l’alinéa 64c) de la LCPE, car elle ne pénètre pas dans l’environnement en une quantité ou concentration ou dans des conditions de nature à constituer un danger au Canada pour la vie ou la santé humaines.
Il est proposé de conclure que la pipérazine ne satisfait à aucun des critères énoncés à l’article 64 de la LCPE.
Référence
Canada. 1999. Loi canadienne sur la protection de l’environnement, 1999. L.C. 1999, ch. 33. Gazette du Canada, Partie III, vol. 22, n° 3.
Canada, ministère de l’Environnement. 2009. Loi canadienne sur la protection de l’environnement, 1999 : Avis concernant certaines substances inanimées (chimiques) inscrites sur la Liste intérieure [PDF]. Gazette du Canada, Partie I, vol. 143, n° 40, p. 2945-2956.
Closmann F, Nguyen T, Rochelle GT. 2009. MDEA/Piperazine as a solvent for CO2 capture [PDF]. Energy Procedia. Vol. 1, no. 1, p. 1351-1357. (Disponible en anglais seulement)
[ConsExpo Web] Consumer Exposure Web Model. 2019. Ver. 1.0.6. Bilthoven (NL): Rijksinstituut voor Volksgezondheid en Milieu [Institut national pour la santé publique et l’environnement]. [Consulté le 27 août 2019]. (Disponible en anglais seulement)
Curry P, Kramer G, Newhook R, Sitwell J, Somers D, Tracy B, Oostdam JV. 1993. Reference values for Canadian populations. Prepared by the Environmental Health Directorate Working Group on reference values. Health Canada. 1988 (Mis à jour en 1993). (Disponible en anglais seulement)
[ECCC] Environnement et Changement climatique Canada. 2016a. Document sur l’approche scientifique : Classification du risque écologique des substances organiques. Ottawa (Ont.) : gouvernement du Canada.
[ECCC] Environnement et Changement climatique Canada. 2016 b. Documents justificatifs : données utilisées pour créer des profils de danger et d’exposition propres à la substance et attribuer un classement par rapport aux risques. Gatineau (QC) : ECCC. Données à l’appui au document sur l’approche scientifique : Classification du risque écologique des substances organiques. Disponible sur demande à : substances@ec.gc.ca. (Disponible en anglais seulement)
[ECCC, SC] Environnement et Changement Canada, Santé Canada. [Modifié le 12 mars 2017]. Catégorisation. Ottawa (Ont.) : gouvernement du Canada. [Consulté le 9 septembre 2019].
[ECHA] European Chemicals Agency. c2007-2019. Registered substances database; search results for CAS RN 110-85-0. Helsinki (FI): ECHA. [Mis à jour le 29 juillet 2019; consulté le 22 août 2019]. (Disponible en anglais seulement)
[ECHA] European Chemicals Agency. 2008. Summary of Classification and Labelling [for CAS RN 110‑85‑0]. Helsinki (FI): ECHA. [Consulté le 2 décembre 2020]. (Disponible en anglais seulement)
[EFSA] European Food Safety Authority. 2015. Scientific Opinion on Flavouring Group Evaluation 86, Revision 2 (FGE.86Rev2): Consideration of aliphatic and arylalkyl amines and amides evaluated by JECFA (65th meeting). EFSA Journal: 13(1). 3998. (Disponible en anglais seulement)
[EFFA] European Flavour and Fragrance Association. 2005. European inquiry on volume use. Private communication to the Flavor and Extract Manufacturers Association, Washington, DC, USA. Submitted to WHO by the International Organization of the Flavor Industry, Brussels, Belgium. (Disponible en anglais seulement)
Environnement Canada. 2009. Données de la Mise à jour de l’inventaire de la LIS recueillies en vertu de l’article 71 de la Loi canadienne sur la protection de l’environnement (1999) : Avis concernant certaines substances inanimées (chimiques) inscrites sur la Liste intérieure. Données préparées par : Environnement Canada, Santé Canada; Programme des substances existantes.
Gavin CL, Williams MC, Hallagan JB. 2007. FEMA 2005 poundage and technical effects update survey. Washington (DC): Flavor and Extract Manufacturers Association. (Disponible en anglais seulement)
[JECFA] Joint FAO/WHO Expert Committee on Food Additives. 2006. Evaluation of Certain Food Additives. WHO Technical Report Series No. 934. Sixty-fifth report. Geneva (CH): World Health Organization. [Consulté le 26 août 2019]. (Disponible en anglais seulement)
[JECFA] Joint FAO/WHO Expert Committee on Food Additives. 2009. Evaluation of Certain Food Additives. WHO Technical Report Series No. 952. Sixty-ninth report. Geneva (CH): World Health Organization. [Consulté le 25 octobre 2019]. (Disponible en anglais seulement)
[CNRC] Conseil national de recherches du Canada. Won D, Lusztyl E. 2011. Data gathering on chemicals released to indoor air of residences from building materials and furnishings. Rapport final. Ottawa (Ont.) : Conseil national de recherches du Canada. Rapport no : B3332.2. (Disponible en anglais seulement)
[OCDE] Organisation de coopération et de développement économiques. 2004. SIDS Initial Assessment Profile (SIAP). Piperazine. Paris (FR): OECD, Environment Directorate. SIAM 18, 20-23 avril 2004. [Consulté le 20 août 2019]. (Disponible en anglais seulement)
[OCDE] Boîte à outils QSAR [outil d’extrapolation]. 2014. Version 3.3. Paris (FR): Organisation de coopération et de développement économiques, Laboratory of Mathematical Chemistry. (Disponible en anglais seulement)
Product brochure. 2007. Ethyleneamines A global profile of products and services [PDF]. The Woodlands (TX): Huntsman Corporation [Consulté le 28 janvier 2021]. (Disponible en anglais seulement)
Padelt B, Bruhn B, Nicolai A. 1966. Das Hirnstrombild vor und nach Kurzzeitbehandlung der Enterobiasis mit Piperazinderivaten. Padiatr. Grenzgeb. 5, 1-9. [Mentionné dans UE 2005]. (Disponible en anglais seulement)
Ridgway P. 1987. Piperazine phosphate. Rabbit teratology study. Report to Reckitt and Coleman from Toxicol Laboratories Ltd., Ledbury, Herefordshire. Unpublished. [Mentionné dans UE 2005]. (Disponible en anglais seulement)
[RIVM] Rijksinstituut voor Volksgezondheid en Milieu [Institut national pour la santé publique et l’environnement]. 2007. Do-it-yourself products fact sheet: to assess the risks for the consumer [PDF]. Bilthoven (NL): RIVM. Report No.: 320104007/2007. [Consulté le 27 août 2019]. (Disponible en anglais seulement)
Santé Canada. 1996. Norme d’étiquetage - Médicament : Anthelminthiques [PDF]. Ottawa (Ont.) : gouvernement du Canada [Consulté le 1er octobre 2019].
Santé Canada. 2015a. Feuilles de calcul sur l’eau potable de l’Unité d’évaluation environnementale. [format Excel]. Ottawa (Ont.) : gouvernement du Canada. [Consulté le 26 août 2019]. (Disponible en anglais seulement)
Santé Canada. 2015 b. Tableau de la consommation des aliments fondé sur l’Enquête sur la santé dans les collectivités canadiennes, cycle 2.2, Nutrition (2004), fichier partagé. Ottawa (Ont.) : gouvernement du Canada.
Santé Canada. 2017. Tableau de la consommation d’eau fondé sur l’Enquête sur la santé dans les collectivités canadiennes, cycle 2.2, Nutrition (2004), fichier partagé. Ottawa (Ont.) : gouvernement du Canada.
Santé Canada. 2018. Ébauche de fiche d’information sur les valeurs par défaut pour l’absorption dans le lait maternel et les préparations pour nourrissions. Rapport non publié. Ottawa (Ont.) : gouvernement du Canada. (Disponible en anglais seulement)
SCREEN3 [computer model]. 2013. Ver. 3.5.0. Research Triangle Park (NC): US Environmental Protection Agency, Office of Air Quality Planning and Standards, Emissions, Monitoring, and Analysis Division. (Disponible en anglais seulement)
[SDS] Safety Data Sheet. 2016. Plastic Bonder (Black) – Syringe – Parts B [PDF]. Sulphur Springs (TX): J-B Weld Company, LLC [Consulté le 15 juillet 2019]. (Disponible en anglais seulement)
[SDS] Safety Data Sheet. 2017a. 3M Universal Adhesive Plastic bonding adhesive [PDF]. London (ON): 3M Canada Company [Consulté le 12 juin 2019]. (Disponible en anglais seulement)
[SDS] Safety Data Sheet. 2017 b. LOCTITE E-30UT Epoxy [PDF]. Mississauga (ON): Henkel Canada Corporation [Consulté le 5 juin 2019]. (Disponible en anglais seulement)
[SDS] Safety Data Sheet. 2017c. PF7770 Pliogrip Urethane structural adhesive [PDF]. Milton (ON): Pro Form Products Ltd. [Consulté le 5 juin 2019]. (Disponible en anglais seulement)
[SDS] Safety Data Sheet. 2019. Plastic bonding adhesive [PDF]. Oakville (ON): Ford Motor Company of Canada [Consulté le 5 juin 2019] (Disponible en anglais seulement)
Shell. 2013. Shell global solutions technology portfolio. Hague (NL): Shell Inc. [Consulté le 10 janvier 2020]. (Disponible en anglais seulement)
SimpleTreat [sewage treatment plant removal model]. 1997. Ver. 3.0. Bilthoven (NL): Rijksinstituut voor Volksgezondheid en Milieu (RIVM) [Institut national pour la santé publique et l’environnement], Laboratory for Ecological Risk Assessment. (Disponible en anglais seulement)
[UE] Union européenne. 2005. Risk Assessment Report (RAR): Piperazine CAS No 110-85-0. Final report. Brussels (BE): EU. [Consulté le 20 août 2019]. (Disponible en anglais seulement)
[US EPA] United States Environmental Protection Agency. 1992 [Modifié]. Screening procedures for estimating the air quality impact of stationary sources [PDF]. Revised. Research Triangle Park (NC): US EPA, Office of Air and Radiation, Office of Air Quality Planning and Standards. EPA-454/R-92-019. [Consulté le 26 novembre 2019]. (Disponible en anglais seulement)
[US EPA] United States Environmental Protection Agency. 1999. Estimates of stack heights and exit gas velocities for TRI facilities in OPPT’s risk-screening environmental indicators model [PDF]. Washington (DC): US EPA, Office of Pollution Prevention and Toxics.[Consulté le 26 novembre 2019]. (Disponible en anglais seulement)
[US EPA] United States Environmental Protection Agency. 2011 [Modifié]. Chapter 6: Inhalation Rates. Exposure Factors Handbook 2011 Edition (Final) [PDF]. Washington (DC): US EPA. EPA/600/R-09/052F. (Disponible en anglais seulement)
Wood E, Brooks PN. 1994. Piperazine hydrochloride: Dietary two generation reproduction study in the rat. Report to Akzo Nobel from Safepharm Laboratories Ltd., Derby. Unpublished. [Mentionné dans UE 2005]. (Disponible en anglais seulement)
Annexe A. Paramètres d’entrée dans SCREEN3 pour la modélisation de la dispersion et l’estimation des concentrations de pipérazine à proximité des épurateurs de gaz industriels
| Paramètre d’entrée | Valeur du paramètre |
|---|---|
| Type de source | Ponctuelle |
| Taux d’émissiona (g/s) | 0,317 |
| Hauteur de la source de rejetb (m) | 15 |
| Diamètre intérieur de la cheminéeb (m) | 0,1 |
| Vitesse des gaz à la sortie de la cheminéec (m/s) | 4,0 |
| Température à l’émissionb (K) | 358 |
| Température de l’air ambiantd (K) | 293 |
| Hauteur du récepteure (m) | 1,74 |
| Milieu urbain ou rurald | Milieu urbain |
| Rabattement par les bâtiments? | Non |
| Hauteur du terrain supérieure à la hauteur de la cheminée? | Non |
| Hauteur du terrain supérieure à la base de la cheminée? | Non |
| Données météorologiquesd | 1 (données météorologiques complètes) |
| Distance minimale et maximale d’utilisationb | 1 200 à 5 000 m |
| Facteur de conversion de l’exposition annuellef | 0,2 |
a Valeur basée sur un taux d’émission de 10 000 kg/an (10 % du volume [jugement professionnel], quantité déclarée dans le commerce au Canada) (Environnement Canada 2009), pendant 365 jours (24 heures par jour).
b Jugement professionnel.
c Jugement professionnel; à l’aide de la vitesse médiane des gaz à la sortie, mentionnée dans US EPA (1999), on obtient l’estimation de rejet la plus élevée.
d Valeur par défaut dans SCREEN3 (1996).
e Curry et coll., 1993.
f Un facteur de conversion de 0,2 est utilisé pour estimer la concentration maximale de pipérazine sur une période d’un an, d’après les résultats de SCREEN3 (qui consistent en estimation pour une période de 1 heure). Ce facteur tient compte de la variation du vent et des conditions météorologiques dans le temps (US EPA 1992 [modifié]).
| Distance (m) | Concentration après 1 heure (µg/m³) a | Concentration annuelle (µg/m³) b |
|---|---|---|
| 1200 | 13,36 | 2,67 |
| 1300 | 11,93 | 2,39 |
| 1400 | 10,75 | 2,15 |
| 1500 | 9,76 | 1,95 |
| 2000 | 6,56 | 1,31 |
| 2500 | 4,87 | 0,97 |
| 3000 | 3,84 | 0,77 |
| 4000 | 2,66 | 0,53 |
| 5000 | 2,03 | 0,41 |
a SCREEN3 (2013).
b Un facteur d’ajustement de 0,2 est utilisé pour estimer la concentration maximale de pipérazine sur une période d’un an, d’après les résultats de SCREEN3 (qui consistent en estimation pour une période de 1 heure). Ce facteur tient compte de la variation du vent et des conditions météorologiques dans le temps et est fondé sur le jugement professionnel (US EPA 1992 [modifié]).
Annexe B. Dose journalière estimée due à l’exposition des humains à la pipérazine par voie orale
| Voie d’exposition | 0 à 5 moisa (allaités)b | 0 à 5 mois a (nourris à la préparation pour nourrissons)c | 6 à 11 moisd | 1 ane | 2 à 3 ansf | 4 à 8 ansg | 9 à 13 ansh | 14 à 18 ansi | 19 ans et plusj |
|---|---|---|---|---|---|---|---|---|---|
| Airk | 1,57 | 1,57 | 1,59 | 1,94 | 1,63 | 1,29 | 0,88 | 0,69 | 0,55 |
| Eau potablel | S.O. | 6,37 | 4,08 | 1,59 | 1,39 | 1,12 | 0,86 | 0,85 | 1,00 |
| Aliments et boissonsm | S.O. | S.O. | S.O. | 0,002 | 0,002 | 0,002 | 0,002 | 0,002 | 0,002 |
| Absorption totale | 1,57 | 7,94 | 5,66 | 3,53 | 3,03 | 2,41 | 1,74 | 1,54 | 1,55 |
Abréviation : S.O. = sans objet.
a On présume un poids de 6,3 kg (Santé Canada 2015 b).
b Valeurs seulement pour les nourrissons allaités et consommant 0,744 L de lait maternel par jour (Santé Canada 2018), et on présume que le lait maternel constitue la seule source alimentaire.
c Valeurs seulement pour les nourrissons nourris à la préparation pour nourrissons et consommant 0,826 L d’eau par jour (Santé Canada 2018), eau qui est utilisée pour reconstituer la préparation pour nourrissons. Pour plus de renseignements, veuillez consulter la note de bas de page sur l’eau potable.
d On présume un poids de 9,1 kg (Santé Canada 2015 b). Pour les nourrissons allaités, on présume qu’ils ne consomment pas d’eau potable, mais boivent 0,632 L de lait maternel par jour (Santé Canada 2018). Pour les nourrissons nourris à la préparation pour nourrissons, on présume qu’ils consomment 0,764 L d’eau par jour (Santé Canada 2018), eau qui est utilisée pour reconstituer la préparation pour nourrissons. Pour plus de renseignements, veuillez consulter la note de bas de page sur l’eau potable.
e On présume un poids de 11,0 kg (Santé Canada 2015 b), et une consommation d’eau par jour de 0,36 L (Santé Canada 2017).
f On présume un poids de 15 kg (Santé Canada 2015 b), et une consommation d’eau par jour de 0,43 L (Santé Canada 2017).
g On présume un poids de 23 kg (Santé Canada 2015 b), et une consommation d’eau par jour de 0,53 L (Santé Canada 2017).
h On présume un poids de 42 kg (Santé Canada 2015 b), et une consommation d’eau par jour de 0,74 L (Santé Canada 2017).
i On présume un poids de 62 kg (Santé Canada 2015 b), et une consommation d’eau par jour de 1,09 L (Santé Canada 2017).
j On présume un poids de 74 kg (Santé Canada 2015 b), une inspiration de 15,1 m³ d’air par jour (US EPA 2011 [modifié]), et une consommation d’eau par jour de 1,53 L (Santé Canada 2017).
k Une valeur de 2,67 µg/m³ a été estimée à l’aide de SCREEN3 (2013) pour déterminer la dose d’exposition par l’air ambiant et l’air intérieur pour les personnes vivant à proximité d’une installation industrielle équipée d’un épurateur de gaz. Les paramètres d’entrée et les résultats des scénarios de modélisation avec SCREEN3 sont décrits à l’annexe A.
l Aucune donnée de surveillance de l’eau potable au Canada n’a été trouvée. On a présumé que 5 % de la quantité déclarée maximale (100 000 kg) de pipérazine dans le commerce au Canada étaient rejetés vers un plan d’eau de surface. Après le traitement des eaux usées (taux d’élimination de 82,7 %), on a calculé une concentration de pipérazine dans l’eau potable de 48,6 µg/L (Santé Canada 2015a; SimpleTreat 1997).
m On n’a trouvé aucune donnée sur la présence de la substance dans les aliments au Canada. L’ingestion de pipérazine à la suite de son utilisation comme aromatisant alimentaire a été estimée par habitant (population américaine, 1 an et plus) à 0,09 µg/j (0,0015 µg/kg p.c./j, pour un poids corporel de 60 kg). Cette estimation était basée sur les volumes de production annuels déclarés par l’industrie alimentaire (EFSA 2005; Gavin 2007, comme présenté dans JECFA 2009).
Annexe C. Paramètres du scénario d’exposition aux polymères époxydes à deux composants
ConsExpo Web (2019) a été utilisé pour estimer l’exposition par inhalation et par voie cutanée à la pipérazine provenant d’adhésifs époxydes à deux composants. Nous nous sommes appuyés sur la fiche d’information de produits de bricolage (RIVM, 2007) pour estimer l’exposition par absorption, estimation qui a été améliorée grâce à certains renseignements sur le produit. Le scénario d’exposition par mélange et chargement a été exclu, car tous les produits de consommation contenant ces époxydes utilisaient un dispositif qui prémélange l’époxyde pendant l’application. Par conséquent, seul le scénario d’exposition lors de l’application a été pris en compte. Un scénario d’utilisation des adhésifs époxydes pour automobile a été choisi, car on a jugé qu’il présentait le plus grand potentiel d’exposition compte tenu de la quantité de produit utilisée.
| Paramètre d’entrée | Valeur du paramètre |
|---|---|
| Concentration (%) | 0,5 (SDS 2017a) |
| Quantité de produit (g) | 200 |
| Fréquence (par année) | 3 |
| Durée d’exposition (min) | 240 |
| Modèle d’inhalation | Exposition à la vapeur, évaporation |
| Volume de la pièce (m³) | 20 |
| Taux de ventilation (nombre de renouvellements de l’air par heure) | 0,6 |
| Taux d’inhalation (m³/j) a | 15,1 |
| Taux d’inhalation (%) | 100 |
| Superficie du rejet (m2) | 0,5 |
| Coefficient de transfert massique (m/h) | 10 |
| Matrice des masses moléculaires (g/mol) | 3 000 |
| Modèle cutané | Contact direct, application instantanée |
| Quantité de produit (g) | 0,1 |
| Absorption cutanée (%) | 100 |
a On suppose que l’utilisateur est un adulte de 19 ans ou plus.
