Évaluation préalable groupe des thiols
Titre officiel : Évaluation préalable groupe des thiols
Numéros d’enregistrement du Chemical Abstracts Service
75-18-3, 150-60-7, 25103-58-6, 71159-90-5
Environnement et Changement climatique Canada
Santé Canada
Octobre 2018
Catalogue : En14-340/2018F-PDF
ISBN : 978-0-660-28183-4
Sommaire
En vertu de l’article 68 ou 74 de la Loi canadienne sur la protection de l’environnement 1999 (LCPE), la ministre de l’Environnement et du Changement climatique et la ministre de la Santé ont produit une évaluation préalable portant sur quatre des six substances appelées collectivement « groupe des thiols » dans le Plan de gestion des produits chimiques. Ces quatre substances ont été considérées comme prioritaires pour une évaluation, car elles satisfont aux critères de catégorisation du paragraphe 73(1) de la LCPE ou ont été déclarées d’intérêt prioritaire en raison d’autres préoccupations liées à la santé humaine. Grâce à d’autres méthodes, on a ultérieurement déterminé que deux des six substances sont peu préoccupantes, et les décisions les concernant sont présentées dans une évaluation préalable distincteNote de bas de page 1 . Par conséquent, la présente évaluation préalable porte sur les quatre substances décrites dans le tableau ci-dessous. Ces quatre substances, qui font l’objet de la présente évaluation préalable, seront ci‑après désignées « groupe des thiols ». Les numéros d’enregistrement du Chemical Abstracts Service (No CASNote de bas de page 2 ), le nom sur la Liste intérieure (LI) et le nom commun figurent dans le tableau ci‑dessous.
No CAS |
Nom figurant sur la Liste intérieure des substances |
Nom commun |
75-18-3a |
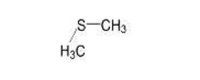
Sulfure de diméthyle |
Sulfure de diméthyle |
150-60-7 |
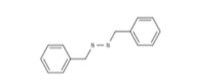
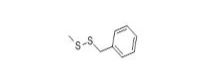
Disulfure de dibenzyle |
Disulfure de dibenzyle |
25103-58-6 b |
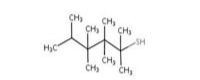
tert-Dodécanethiol |
tert-Dodécanethiol |
71159-90-5 |
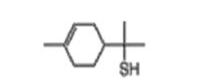
alpha,alpha,4-Triméthylcyclohex-3-ène-1-méthanethiol |
alpha,alpha,4-Triméthylcyclohex-3-ène-1-méthanethiol |
a Cette substance n’a pas été désignée en vertu du paragraphe 73(1) de la LCPE, mais est visée par la présente évaluation préalable, car elle est considérée d’intérêt prioritaire en raison d’autres préoccupations liées à la santé humaine.
b Ce composé est une UVCB (substance de composition inconnue ou variable, produits de réaction complexes ou matières biologiques).
Selon les renseignements fournis aux termes de l’article 71 de la LCPE, il n’y a eu au Canada aucune déclaration de production supérieure au seuil de déclaration de 100 kg de tert-dodécanethiol en 2008 ou de sulfure de diméthyle, de disulfure de dibenzyle ou d’alpha,alpha,4-triméthylcyclohex-3-ène-1-méthanethiol en 2011, mais entre 10 000 et 100 000 kg de sulfure de diméthyle et entre 100 000 et 1 000 000 kg de tert‑dodécanethiol ont été importés au Canada en 2011 et en 2008, respectivement. Il n’y a eu aucune déclaration d’importation supérieure au seuil de déclaration de 100 kg de disulfure de dibenzyle ou d’alpha,alpha,4-triméthylcyclohex-3-ène-1-méthanethiol au Canada en 2011.
Le sulfure de diméthyle, le disulfure de dibenzyle et l’alpha,alpha,4-triméthylcyclohex-3-ène-1-méthanethiol peuvent être utilisés en tant qu’agents aromatisants dans les aliments. Le tert-dodécanethiol a été reconnu comme un composant des emballages d’aliments et peut également être présent sous forme d’impureté dans des peintures et des revêtements. Le sulfure de diméthyle est importé en tant qu’agent odorisant dans le gaz naturel, tandis que le tert-dodécanethiol est utilisé dans des revêtements en vinyle, des produits du papier, et des matériaux en plastique, en caoutchouc et en métal.
Les risques pour l’environnement associés aux substances du groupe des thiols ont été caractérisés au moyen de la Classification du risque écologique (CRE) des substances organiques, approche fondée sur les risques qui tient compte de plusieurs paramètres liés au danger et à l’exposition et basés sur une pondération des éléments de preuve. Les profils de danger sont établis principalement d’après des paramètres liés au mode d’action toxique, à la réactivité chimique, aux seuils de toxicité interne dérivés du réseau trophique, à la biodisponibilité et à l’activité biologique et chimique. Parmi les paramètres pris en compte pour les profils d’exposition figurent la vitesse d’émission potentielle, la persistance globale et le potentiel de transport à grande distance. La méthode utilise une matrice des risques pour attribuer à ces substances un degré de préoccupation potentielle faible, modéré ou élevé, en fonction de leurs profils de danger et d’exposition. La CRE a permis de déterminer que les quatre substances du groupe des thiols ont un faible potentiel d’effets nocifs sur l’environnement.
Compte tenu de tous les éléments de preuve contenus dans la présente évaluation préalable, le sulfure de diméthyle, le disulfure de dibenzyle, le tert‑dodécanethiol et l’alpha,alpha,4-triméthylcyclohex-3-ène-1-méthanethiol présentent un faible risque d’effets nocifs sur l’environnement. Il est conclu que le sulfure de diméthyle, le disulfure de dibenzyle, le tert-dodécanethiol et l’alpha,alpha,4-triméthylcyclohex-3-ène-1-méthanethiol ne satisfont pas aux critères énoncés aux alinéas 64a) ou b) de la LCPE, car ils ne pénètrent pas dans l’environnement en une quantité ou concentration ou dans des conditions de nature à avoir, immédiatement ou à long terme, un effet nocif sur l’environnement ou sur la diversité biologique, ou à mettre en danger l’environnement essentiel pour la vie.
Dans son évaluation du sulfure de diméthyle, l’Organisation pour la coopération et le développement économiques (OCDE) n’a pas déterminé que cette substance a des effets préoccupants sur la santé humaine. Le Comité mixte FAO/OMS (Organisation des Nations Unies pour l’alimentation et l’agriculture/Organisation mondiale de la santé) d’experts des additifs alimentaires (JECFA) a déterminé que l’utilisation de sulfure de diméthyle, de disulfure de dibenzyle et d’alpha,alpha,4-triméthylcyclohex-3-ène-1-méthanethiol en tant qu’agents aromatisants dans les aliments ne posait aucune préoccupation sur le plan de l’innocuité. Dans son évaluation du tert-dodécanethiol, l’OCDE a noté des effets sur le foie des animaux de laboratoire.
Le sulfure de diméthyle est importé comme agent odorisant dans le gaz naturel, et l’exposition potentielle de la population générale résultant de cette utilisation devrait être limitée. Il existe un potentiel d’exposition alimentaire au sulfure de diméthyle, au disulfure de benzyle et à l’alpha,alpha,4-triméthylcyclohex-3-ène-1-méthanethiol découlant de leurs utilisations possibles en tant qu’agents aromatisants dans les aliments. Le tert‑dodécanethiol est utilisé dans certains emballages d’aliments (p. ex. revêtements), mais l’exposition découlant de cette utilisation est jugée négligeable. Le tert-dodécanethiol peut également être présent sous forme d’impureté dans certaines peintures et certains revêtements. Aucun rapport ne signale la présence de disulfure de dibenzyle et d’alpha,alpha,4-triméthylcyclohex-3-ène-1-méthanethiol dans les produits offerts aux consommateurs au Canada. D’après la prise en compte des évaluations d’autres organisations et des utilisations limitées, les risques posés par les substances du groupe des thiols pour la santé humaine sont considérés comme faibles. Dans le cas du tert-dodécanethiol, selon une comparaison entre, d’une part, les concentrations auxquelles les Canadiens peuvent être exposés en raison de sa présence sous forme d’impureté dans certaines peintures et certains revêtements, et, d’autre part, les concentrations associées à des effets sur la santé établies à partir d’études en laboratoire, aucune préoccupation pour la santé humaine n’a été relevée.
À la lumière des renseignements contenus dans la présente évaluation préalable, il est conclu que le sulfure de diméthyle, le disulfure de dibenzyle, le tert-dodécanethiol et l’alpha,alpha,4-triméthylcyclohex-3-ène-1-méthanethiol ne satisfont pas aux critères énoncés à l’alinéa 64c) de la LCPE, car ils ne pénètrent pas dans l’environnement en une quantité ou concentration ou dans des conditions de nature à constituer un danger au Canada pour la vie ou la santé humaines.
Il est conclu que le sulfure de diméthyle, le disulfure de dibenzyle, le tert‑dodécanethiol et l’alpha,alpha,4-triméthylcyclohex-3-ène-1-méthanethiol ne satisfont pas aux critères énoncés à l’article 64 de la LCPE.
1. Introduction
En vertu de l’article 68 ou 74 de la Loi canadienne sur la protection de l’environnement 1999 (LCPE) (Canada, 1999), la ministre de l’Environnement et du Changement climatique et la ministre de la Santé ont produit une ébauche d’évaluation préalable portant sur quatre des six substances appelées collectivement « groupe des thiols » dans le Plan de gestion des produits chimiques, afin de déterminer si ces quatre substances présentent ou peuvent présenter un risque pour l’environnement et la santé humaine. Ces quatre substances ont été considérées comme prioritaires pour une évaluation, car elles satisfont aux critères de catégorisation du paragraphe 73(1) de la LCPE ou ont été déclarées d’intérêt prioritaire en raison de préoccupations liées à la santé humaine (ECCC, SC [modifié 2017]).
Les deux autres substances [no CASNote de bas de page 3 60-24-2, 2-mercaptoéthanol; no CAS 73984-93-7, 5-(tert-dodécyldithio)-1,3,4-thiadiazole-2(3H)-thione] ont été prises en compte dans les documents sur l’approche scientifique intitulés « Classification du risque écologique de substances organiques » et « Approche fondée sur le seuil de préoccupation toxicologique (SPT) pour certaines substances » (ECCC, 2016a; ECCC SC, 2017) et ont été considérées comme peu préoccupantes pour la santé humaine et l’environnement. Elles ne seront donc pas plus prises en compte dans la présente évaluation. Les conclusions tirées pour ces deux substances sont données dans l’ébauche d’évaluation préalable « Substances jugées comme étant peu préoccupantes au moyen de l’approche de la Classification du risque écologique des substances organiques et l’approche fondée sur le seuil de préoccupation toxicologique (SPT) pour certaines substances » (ECCC, SC, 2017). Les quatre substances faisant l’objet de la présente évaluation préalable seront ci-après désignées « groupe des thiols ».
Deux substances du groupe des thiols examinées dans la présente ébauche ont fait l’objet d’études internationales par l’Organisation pour la coopération et le développement économiques (OCDE), dans le cadre du Programme d’évaluation coopérative des produits chimiques, et l’ensemble des données d’évaluation (Screening Information Data Set, ou SIDS) ainsi que les rapports d’évaluation initiale (Initial Assessment Reports, ou SIAR) sont disponibles. Ces évaluations sont soumises à un examen rigoureux (y compris par des pairs) et à des processus d’approbation par des autorités gouvernementales internationales. Santé Canada et Environnement et Changement climatique Canada sont des participants actifs à ces processus et considèrent ces évaluations comme fiables. Les SIARS de l’OCDE portant sur le sulfure de diméthyle et la catégorie des thiols aliphatiques en C8 à C12 ont servi à éclairer la caractérisation des effets sur la santé de la présente évaluation préalable (OCDE, 2006; OCDE, 2011). De plus, les effets sur la santé de trois des substances du groupe (sulfure de diméthyle, disulfure de dibenzyle et alpha,alpha,4-triméthylcyclohex-3-ène-1-méthanethiol) en tant qu’agents aromatisants dans les aliments ont été évalués par le Comité mixte FAO/OMS (Organisation des Nations Unies pour l’alimentation et l’agriculture/Organisation mondiale de la santé) d’experts des additifs alimentaires (JECFA), dont les évaluations servent également à appuyer la caractérisation des effets sur la santé de la présente évaluation préalable (OMS, 2000).
Les risques pour l’environnement associés aux substances du groupe des thiols ont été caractérisés au moyen de l’approche de la CRE (ECCC, 2016a), qui décrit les dangers posés par une substance en utilisant des paramètres clés, dont le mode d’action toxique, la réactivité chimique, les seuils de toxicité interne dérivés du réseau trophique, la biodisponibilité et l’activité biologique et chimique. La CRE tient compte de l’exposition possible des organismes des milieux terrestres ou aquatiques en se fondant sur des facteurs tels que la vitesse d’émission potentielle, la persistance globale et le potentiel de transport atmosphérique à grande distance. Les divers éléments de preuve sont combinés afin de déterminer si les substances nécessitent une évaluation plus poussée de leur potentiel d’effets nocifs sur l’environnement ou si elles présentent un faible risque de tels effets.
La présente évaluation préalable tient compte des renseignements sur les propriétés chimiques, le devenir dans l’environnement, les dangers, les utilisations et l’exposition, ainsi que des renseignements supplémentaires soumis par les intervenants. Les données pertinentes ont été relevées jusqu’en novembre 2016. Les données empiriques obtenues d’études clés, ainsi que certains résultats provenant de modèles, ont servi à formuler les conclusions. Lorsqu’elle était disponible et pertinente, l’information présentée dans des évaluations réalisées par d’autres autorités a été prise en considération.
La présente évaluation préalable a été préparée par le personnel du Programme d’évaluation des risques de la LCPE travaillant à Santé Canada et à Environnement et Changement climatique Canada. Elle inclut des données provenant d’autres programmes de ces deux ministères. Le volet sur les effets sur l’environnement de la présente évaluation repose sur le document sur la CRE (publié le 30 juillet 2016), qui a fait l’objet d’un examen par des pairs et d’une période de commentaires du public de 60 jours. Par ailleurs, l’ébauche de la présente évaluation préalable (publiée le 22 juillet 2017) a été soumise à une période de consultation publique de 60 jours. Bien que des commentaires de l’extérieur aient été pris en compte, Environnement et Changement climatique Canada et Santé Canada restent responsables du contenu final et des conclusions de la présente évaluation préalable.
La présente évaluation préalable repose sur des renseignements permettant de déterminer si les substances satisfont aux critères énoncés à l’article 64 de la LCPE. À cette fin, nous avons examiné les renseignements scientifiques et suivi une approche basée sur une pondération des éléments de preuve et le principe de précaution.Note de bas de page 4 Nous présentons dans la présente évaluation préalable les renseignements critiques et les considérations à partir desquels les conclusions ont été tirées.
2. Identité des substances
Les numéros CAS, les noms figurant sur la Liste intérieure des substances (LIS) et les noms communs de chacune des substances du groupe des thiols sont présentés dans le tableau 2-1. Il est possible d’obtenir une liste d’autres noms de ces composés chimiques (p. ex. leurs noms commerciaux) dans les National Chemical Inventories (NCI [modifié 2017]).
No CAS |
Nom dans la LIS |
Nom commun |
Structure chimique et formule moléculaire |
Masse moléculaire (g/mol) |
| 75-18-3 | Sulfure de diméthyle |
Sulfure de diméthyle |
C2H6S |
62.13 |
| 150-60-7 | Disulfure de dibenzyle |
Disulfure de dibenzyle |
C14H14S2 |
246.39 |
| 25103-58-6a | Tert-dodécanethiol |
Tert-dodécanethiol |
C12H26S |
202.41 |
| 71159-90-5 | Alpha, alpha, 4-triméthyl-3-cyclohex-3-ène-1 méthanethiol | Alpha,alpha,4-triméthylcyclohex- 3-ène-1-méthanethiol |
C10H18S |
170.31 |
a Le tert-dodécanethiol est un UVCB (substances de composition inconnue ou variable, produits de réaction complexes ou matières biologiques) dont la longueur et le degré de ramification sont variables – la structure caractéristique présentée ici est C12H26.
2.1 Sélection des analogues
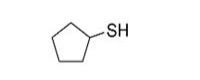
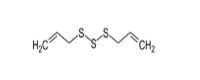
Des métabolites potentiels, décrits dans l’évaluation du JECFA sur l’innocuité des agents aromatisants, dont des substances du groupe des thiols (OMS, 2000), ont été utilisés comme analogues pour appuyer l’évaluation des effets du disulfure de dibenzyle et de l’alpha,alpha,4-triméthylcyclohex-3-ène-1-méthanethiol sur la santé humaine. Plus précisément, des données sur la santé humaine existent pour le disulfure de benzyle et de méthyle (no CAS 699-10-5), le cyclopentanethiol (no CAS 1679-07-8) et le trisulfure de diallyle (no CAS 2050-87-5); ces données ont servi à appuyer l’évaluation. Nous donnons dans le tableau 2‑2 des renseignements sur l’identité de ces analogues.
No CAS |
LIS ou autre nom (nom commun) |
Structure chimique et formule moléculaire |
Masse moléculaire (g/mol) |
699-10-5 |
Disulfure de benzyle et de méthyle |
|
170.30 |
1679-07-8 |
Cyclopentanethiol |
|
102.20 |
2050-87-5 |
Trisulfure de diallyle |
|
178.33 |
a Tel qu’il est décrit dans OMS (2000).
3. Propriétés physiques et chimiques
Un résumé des propriétés physiques et chimiques des substances du groupe des thiols est fourni dans le tableau 3‑1, avec une gamme de valeurs indiquée pour chaque propriété. Quand les données expérimentales sur une propriété étaient limitées ou inaccessibles, les données sur les analogues ont été utilisées pour obtenir des données croisées et/ou des modèles de relation (quantitative) structure-activité (R[Q]SAR) ont été utilisés pour générer les valeurs prédites pour la substance. D’autres propriétés physiques et chimiques sont présentées dans le document ECCC (2016b).
Propriété |
Sulfure de diméthylea |
Disulfure de dibenzyleab |
Tert-dodécanethiolc |
Alpha,alpha,4-triméthylcyclohex- 3-ène-1-méthanethiold |
Point de fusion (°C) |
-98,3 |
71,5 |
3,7 |
3,0 |
Point d’ébullition (°C) |
37,3 |
376-384 |
215 |
295 |
Pression de vapeur (Pa) |
66928 |
0,0036 |
22,80 |
14,13 |
Hydrosolubilité (mg/L) |
22000 |
0,75 |
0,43 |
5,49 |
Log Koe (sans dimension) |
0,92 |
5,29 |
5,85 |
4,74 |
Abréviation : Koe = coefficient de partage octanol‑eau.
a ChemIDplus 2018.
b ChemSpider 2015 : le point d’ébullition est déterminé expérimentalement; la pression de vapeur et l’hydrosolubilité sont prédites par EPISuite.
c ChemSpider, 2015 : toutes les valeurs sont prédites par EPISuite.
d ChemSpider, 2015 : le point d’ébullition est déterminé expérimentalement; le point de fusion, la pression de vapeur, l’hydrosolubilité et le log Koe sont prédits par EPISuite.
4. Sources et utilisations
Le sulfure de diméthyle est naturellement présent dans de nombreux types d’aliments tels que le lait, les œufs, le bœuf, le fromage, les fraises, le brocoli et le chou (Kim et Kim, 2014; Klein et al., 2016). Le disulfure de dibenzyle est naturellement présent dans une variété d’aliments, et l’alpha,alpha,4-triméthylcyclohex- 3-ène-1-méthanethiol est naturellement présent dans le jus de pamplemousse (OMS, 2000). Le tert‑dodécanethiol n’est pas présent naturellement dans l’environnement.
Les quatre substances du groupe des thiols ont été incluses dans les enquêtes effectuées en vertu de l’avis aux termes de l’article 71 de la LCPE. Le tableau 4‑1 fournit un résumé des données déclarées sur les quantités totales de tert-dodécanethiol et de sulfure de diméthyle produites et importées en 2008 ou 2011 (Environnement Canada, 2009, 2014). La production et l’importation de disulfure de dibenzyle et d’alpha,alpha,4-triméthylcyclohex-3-ène-1-méthanethiol en 2011 n’ont pas été déclarées dans l’enquête de 2011 réalisée aux termes de l’article 71 (Environnement Canada, 2014).
Nom commun |
Quantité totale (kg) |
Quantité importée totale (kg)b |
Année de déclaration |
Référence de l’enquête |
Sulfure de diméthyle |
s. o. |
10 000 – 100 000 |
2011 |
Environnement Canada, 2014 |
Tert-dodécanethiol |
s. o. |
100 000 – |
2008 |
Environnement Canada, 2009 |
Abréviations : s. o. = sans objet.
a Les valeurs reflètent les quantités déclarées en réponse à une enquête menée aux termes de l’article 71 de la LCPE (Environment Canada, 2014). Consulter l’enquête pour connaître les inclusions et les exclusions spécifiques (annexes 2 et 3).
b Les quantités importées sont rapportées sous forme de fourchettes de valeur pour éviter de divulguer des renseignements commerciaux confidentiels.
En ce qui a trait aux utilisations canadiennes, le sulfure de diméthyle est utilisé comme agent odorisant dans le gaz naturel, tandis que le tert-dodécanethiol est utilisé comme intermédiaire, adjuvant de polymérisation, agent de séparation des solides, régulateur de viscosité et régulateur de procédés (Environnement Canada, 2009, 2014). Du sulfure de diméthyle est également rejeté pendant le procédé kraft. Le tert‑dodécanethiol entre dans la composition de certains emballages d’aliments (communication personnelle, courriel de la Direction des aliments de Santé Canada au Bureau d’évaluation du risque des substances existantes [BERSE] de Santé Canada, juillet 2016) et est également utilisé dans la fabrication d’autres produits tels que les matériaux en métal, en papier, en plastique et en caoutchouc (Environnement Canada, 2009). Le tert-dodécanethiol peut se trouver dans des produits utilisés par les consommateurs, par exemple les revêtements de sol en vinyle et les produits du papier, et peut être présent sous forme d’impureté dans certains produits de bricolage (p. ex peintures et revêtements) (Environnement Canada, 2009).
Aucune de ces quatre substances ne figure dans la Base de données sur les produits pharmaceutiques ou dans la base de données interne sur les ingrédients non médicinaux de la Direction des produits thérapeutiques en tant que médicaments sur ordonnance, de médicaments sans ordonnance ou de médicament à usage vétérinaire au Canada (communication personnelle de la Direction des produits thérapeutiques de Santé Canada au BERSE, juin 2016). Le sulfure de diméthyle, le disulfure de dibenzyle et l’alpha,alpha,4-triméthylcyclohex-3-ène-1-méthanethiol figurent dans la Base de données d’ingrédients de produits en santé naturels (BDIPSN) en tant qu’agents non médicinaux utilisés comme exhausteurs de goût dans les produits de santé naturels (PSN), à des doses maximales de 0,25, 0,0012 et de 0,00056 mg/kg p.c./j, respectivement. Toutefois, aucune de ces substances ne figure dans la Base de données des produits de santé naturels homologués (BDPSNH) en tant que substances présentes dans des PSN homologués (BDIPSN [modifié 2018], BDPSNH [modifié 2018], communication personnelle, courriel de la Direction des produits de santé naturels et sans ordonnance de Santé Canada au BERSE, juin 2016). Trois des quatre substances du groupe des thiols (soit le sulfure de diméthyle, le disulfure de dibenzyle et l’alpha,alpha,4-triméthylcyclohex-3-ène-1-méthanethiol) pourraient être utilisées comme agents aromatisants dans les aliments. Une des substances du groupe, le tert‑dodécanethiol, est une composante de certains emballages d’aliments (revêtements) (communication personnelle, courriel de la Direction des aliments de Santé Canada au BERSE, juillet 2016). L’utilisation des substances du groupe des thiols comme additifs alimentaires n’est pas autorisée au Canada (communication personnelle, courriel de la Direction des aliments de Santé Canada au BERSE, juillet 2016).
Aucun rapport ne fait état de la présence de ces substances dans les produits cosmétiques au Canada (communication personnelle de la Direction de la sécurité des produits de consommation de Santé Canada au BERSE, juillet 2016). Le sulfure de diméthyle et le disulfure de dibenzyle figurent sur la liste des produits de formulation de l’Agence de réglementation de la lutte antiparasitaire (ARLA); toutefois, seul le sulfure de diméthyle est présent dans des produits homologués. Plus précisément, le sulfure de diméthyle est présent en tant que parfum dans plusieurs produits tels que les insectifuges et les insecticides (communication personnelle, courriels de l’ARLA au BERSE, juillet 2016).
5. Potentiel d’effets nocifs sur l’environnement
5.1 Caractérisation des risques pour l’environnement
Les risques pour l’environnement associés aux substances du groupe des thiols ont été caractérisés au moyen de la Classification du risque écologique (CRE) des substances organiques (ECCC, 2016a), approche fondée sur les risques qui tient compte de plusieurs paramètres liés au danger et à l’exposition et basés sur une pondération des éléments de preuve. Les divers éléments de preuve sont combinés afin de faire la différence entre des substances présentant une puissance plus ou moins élevée et un potentiel d’exposition plus ou moins élevé dans divers milieux. Cette approche permet de réduire l’incertitude globale de la caractérisation des risques comparativement à une approche reposant sur un seul paramètre dans un seul milieu (p. ex. CL50). L’approche, qui est décrite en détail par ECCC (2016a), est résumée ci-dessous.
Nous avons colligé les données sur les propriétés physicochimiques, le devenir (demi‑vie chimique dans divers milieux et le biote, coefficient de partage, bioconcentration dans les poissons), l’écotoxicité aiguë chez les poissons et les quantités produites et importées au Canada, à partir des publications scientifiques, des bases de données empiriques disponibles (par ex. boîte à outils RQSA de l’OCDE) et des réponses aux enquêtes menées en vertu de l’article 71 de la LCPE. Nous avons produit d’autres données à partir de la relation quantitative structure-activité (RQSA) ou les modèles du devenir du bilan massique ou de la bioaccumulation. Ces données ont été utilisées comme intrants dans d’autres modèles de bilan massique ou pour compléter les profils d’exposition et de danger de la substance.
Les profils de danger ont été établis principalement à partir de paramètres liés au mode d’action toxique, à la réactivité chimique, aux seuils de toxicité interne dérivés du réseau trophique, à la biodisponibilité et à l’activité chimique et biologique. Parmi les multiples paramètres pris en compte pour les profils d’exposition figurent la vitesse d’émission potentielle, la persistance globale et le potentiel de transport à grande distance. Les profils de danger et d’exposition ont été comparés aux critères de décision afin de classer les potentiels de danger et d’exposition de chaque substance organique comme faibles, modérés ou élevés. Des règles supplémentaires ont été appliquées (p. ex. régularité de la classification, marge d’exposition) pour raffiner les classifications préliminaires du danger et de l’exposition.
Une matrice des risques a été utilisée pour assigner une classification faible, modérée ou élevée au risque potentiel posé par chaque substance, en fonction des classifications du danger et de l’exposition. Les classifications du risque potentiel au moyen de la CRE ont été vérifiées en suivant une approche en deux étapes. La première étape servait à ajuster les résultats de la classification du risque de modéré ou élevé à faible pour les substances présentant une faible vitesse d’émission estimée dans l’eau après traitement des eaux usées, ce qui représente un faible potentiel d’exposition. La deuxième étape servait à revoir les résultats d’une classification du potentiel de risque faible d’après des scénarios de risque relativement prudents, d’échelle locale (c.-à-d. dans la zone la plus proche d’une source ponctuelle de rejet) et conçus pour protéger l’environnement, afin de déterminer si la classification du risque potentiel devrait être accrue.
La CRE est basée sur une approche pondérée afin de réduire au minimum toute surclassification ou sous-classification du danger et de l’exposition et du risque subséquent. Les approches équilibrées pour tenir compte des incertitudes sont décrites en détail dans ECCC (2016a). Nous décrivons ci-après deux des zones d’incertitude les plus importantes. Les erreurs dans les valeurs de toxicité aiguë empiriques ou modélisées pourraient conduire à des changements de la classification du danger, en particulier en ce qui a trait aux paramètres reposant sur des valeurs de résidus dans les tissus (c.-à-d. mode d’action toxique), dont de nombreux sont des valeurs prédites à partir de modèles RQSA. Cependant, l’impact de ces erreurs est atténué par le fait qu’une surestimation de la létalité médiane donnera une valeur prudente (protectrice) pour les résidus dans les tissus aux fins d’analyse des résidus corporels critiques (RCC). De même, toute erreur de sous-estimation de la toxicité aiguë est atténuée par le recours à d’autres paramètres du danger, comme le profil structural du mode d’action, la réactivité et/ou l’affinité pour les récepteurs d’œstrogènes. Les changements ou les erreurs dans les quantités chimiques pourraient mener à des classifications différentes de l’exposition, la classification de l’exposition et du risque étant hautement sensible à la vitesse d’émission et aux quantités utilisées. Les résultats de la CRE reflètent donc l’exposition et le risque au Canada d’après les quantités actuellement utilisées et pourraient ne pas refléter des tendances futures.
Les données critiques et les facteurs pris en compte pour produire les profils spécifiques de chacune des quatre substances du groupe des thiols ainsi que les résultats de la classification du danger, de l’exposition et du risque sont présentés dans ECCC (2016b).
Les classifications du danger et de l’exposition des quatre substances du groupe des thiols sont résumées dans le tableau 5-1.
Nom commun |
Classification CRE du danger |
Classification CRE de l’exposition |
Classification CRE du risque |
Sulfure de diméthyle |
Faible |
Faible |
Faible |
Disulfure de dibenzyle |
Modéré |
Faible |
Faible |
Tert-dodécanethiol |
Modéré |
Faible |
Faible |
Alpha,alpha,4-triméthylcyclohex-3-ène-1-méthanethiol |
Élevé |
Faible |
Faible |
Selon les données découlant de la CRE, l’alpha,alpha,4-triméthylcyclohex-3-ène-1-méthanethiol est classé comme étant un faible potentiel d’exposition. L’alpha,alpha,4-triméthylcyclohex-3-ène-1-méthanethiol a été classé par la CRE comm ayant un danger élevé d’après le mode d’action, qui est réactif, le potentiel élevé d’effets nocifs sur les réseaux trophiques aquatiques étant donné son potentiel de bioaccumulation. En outre, les alertes structurelles de la boîte à outils de l’OCDE ont permis de relever que cette substance peut se lier à l’ADN et à des protéines. Elle a été d’abord classée comme ayant un potentiel modéré de risque pour l’environnement, mais la classification du risque a été modifiée à la baisse, passant à un potentiel faible de risque pour l’environnement à la suite de la correction effectuée en fonction des quantités actuelles utilisées (voir section 7.1.1 du document sur l’approche de la CRE, ECCC, 2016a). Les effets potentiels et comment ils pourraient se manifester dans l’environnement n’ont pas été examinés plus en profondeur, car l’exposition à cette substance est faible. Compte tenu des profils d’utilisation actuels, il est peu probable que cette substance soit préoccupante pour l’environnement au Canada.
Selon les données examinées dans le cadre de la CRE, le disulfure de dibenzyle et le tert-dodécanethiol ont été classés comme ayant un faible potentiel d’exposition. D’après la classification, ces deux substances ont un potentiel de danger modéré, d’après le mode d’action toxique, qui est réactif, et un potentiel modéré de causer des effets nocifs sur les réseaux trophiques aquatiques, compte tenu leur potentiel de bioaccumulation. En outre, les alertes structurales de la boîte à outils de l’OCDE ont perms d’établir que ces substances pourraient se lier à des protéines. Les effets potentiels et la façon dont ils pourraient se manifester dans l’environnement n’ont pas été étudiés plus en profondeur étant donné la faible exposition à ces substances. Sur la base des profils d’utilisation actuels, il est peu probable que ces substances soulèvent des préoccupations à l’égard de l’environnement au Canada.
Compte tenu du faible danger et de la faible exposition relevés à l’aide des données examinées lors de la CRE, le sulfure de diméthyle a été classé comme ayant un faible potentiel de risque pour l’environnement. Par conséquent, il est peu probable que cette substance soit préoccupante pour l’environnement au Canada.
6. Potentiel d’effets nocifs sur la santé humaine
6.1 Évaluaton de l’exposition
Milieux environnementaux
Au Canada, aucune concentration supérieure aux limites de détection des substances du groupe des thiols n’a été mesurée dans l’air intérieur, l’air extérieur, l’eau potable ou le sol. Dans le cadre d’un programme de surveillance de la qualité de l’air ambiant, les concentrations de certains composés dans des échantillons d’air prélevés en amont et en aval d’un lieu d’enfouissement en Ontario ont été mesurées pour examiner leurs effets potentiels. Le sulfure de diméthyle n’était pas présent en des concentrations détectables dans ces échantillons d’air prélevés en amont et en aval (City of Hamilton, 2009).
Les résultats de certaines études donnent à penser que du sulfure de diméthyle peut être émis à partir de lieux d’enfouissement, de stations de traitement des eaux usées, de fabriques de pâte kraft et d’installations de compostage (City of Hamilton, 2009; Kotowska et al., 2012; Kangas et al., 1984; Drimal et al., 2010; Goyer, 1990; Catalan et al., 2009), et la substance a été détectée à des concentrations de l’ordre des parties par milliard (ppb) dans l’air intérieur en Corée (Susaya et al., 2011). Toutefois, puisque le sulfure de diméthyle n’a pas été détecté dans l’air extérieur au Canada, que les concentrations en aval de lieux d’enfouissement étaient inférieures aux niveaux de détection et que les utilisations sont limitées (présence de sulfure de diméthyle en tant qu’agent odorisant dans le gaz naturel et de tert‑dodécanethiol dans des produits importés), les rejets dans l’environnement, et par conséquent l’exposition des milieux environnementaux à ces substances, devraient être limités. L’exposition des milieux environnementaux n’a donc pas été quantifiée.
Aliments
Le Food Chemicals Codex (FCC) indique que deux des substances du groupe des thiols, soit le sulfure de diméthyle et le disulfure de dibenzyle, sont des agents aromatisants (FCC USP, 2016). Le sulfure de diméthyle, le disulfure de dibenzyle et l’alpha,alpha,4-triméthylcyclohex-3-ène-1-méthanethiol figurent sur la liste du Fenaroli’s Handbook of Flavor Ingredients (Burdock, 2010). Ce même ouvrage indique également que le sulfure de diméthyle est présent naturellement dans une variété d’aliments et que l’alpha,alpha,4-triméthylcyclohex-3-ène-1-méthanethiol est présent naturellement dans le jus de pamplemousse (Burdock, 2010). Il est raisonnable de s’attendre à ce que la source prédominante d’exposition alimentaire au sulfure de diméthyle soit sa présence naturelle dans les aliments. L’Union européenne autorise également l’utilisation du sulfure de diméthyle, du disulfure de dibenzyle et de l’alpha,alpha,4-triméthylcyclohex-3-ène-1-méthanethiol en tant qu’agents aromatisants dans les aliments (base de données des arômes dans les aliments de l’Union européenne). Il n’existe aucune donnée concernant l’utilisation potentielle de ces trois thiols comme agents aromatisants dans les aliments au Canada (communication personnelle de la Direction des aliments de Santé Canada au BERSE de Santé Canada, juillet 2016).
Le Comité mixte FAO/OMS d’experts des additifs alimentaires (JECFA) a évalué un groupe d’agents aromatisants dont faisaient partie les thiols lors de sa 53e réunion (OMS, 2000). Les absorptions estimées de thiols examinées par le JECFA et incluses dans la présente évaluation sont résumées dans le tableau 6-1 ci-dessous.
Substance (no CAS) |
Absorptions (µg/kg p.c./j) |
Sulfure de diméthyle (75-18-3) |
Europe : 10 États-Unis : 9 |
Disulfure de dibenzyle (150-60-7) |
Europe : 0,0002 États-Unis : 0,002 |
Alpha,alpha,4-triméthylcyclohex- 3-ène-1-méthanethiol (71159-90-5) |
Europe : 0,01 États-Unis : 0,01 |
L’une des substances de ce groupe, le tert-dodécanethiol, entre également dans la composition d’emballages d’aliments. Toutefois, l’exposition alimentaire à partir de cette source devrait être négligeable (communication personnelle, courriel de la Direction des aliments de Santé Canada au BERSE, août 2016).
Produits disponibles aux consommateurs
Comme nous l’avons décrit dans la section sur les utilisations, le sulfure de diméthyle sert d’agent odorisant dans le gaz naturel (Environnement Canada, 2014) puisqu’il a un faible seuil olfactif (aussi faible que 2 ppb; OCDE, 2011). L’exposition découlant de cette source ne devrait pas être importante pour la population générale du Canada, compte tenu de l’odeur désagréable de cette substance ainsi que du potentiel limité d’exposition (p. ex. fuite de gaz accidentelle).
Quant au tert-dodécanethiol, une enquête réalisée aux termes de l’article 71 de la LCPE a révélé sa présence potentielle, sous forme d’impureté, dans des peintures et des revêtements, à des concentrations de moins de 0,1 % dans les produits finaux (Environnement Canada, 2014). Au moyen de la version 4.1 de ConsExpo (ConsExpo 2006; voir l’annexe A), l’exposition de la population générale découlant de l’utilisation de peintures à l’eau contenant 0,1 % de tert-dodécanethiol (exposition par inhalation – concentration moyenne par événement : 0,67 mg/m3; exposition accidentelle par voie cutanée : 51 µg/kg p.c.) a été estimée. Il est à noter que l’absorption cutanée complète a été présumée; toutefois, d’après le flux (Jmax) dérivé des propriétés physicochimiques du tert-dodécanethiol (Kroes et al., 2007), l’absorption cutanée est considérée comme beaucoup plus basse. L’exposition découlant de la présence potentielle de tert-dodécanethiol dans les revêtements de vinyle n’a pas été modélisée, car elle devrait être négligeable (Environnement Canada, 2014).
En ce qui concerne le disulfure de dibenzyle et l’alpha,alpha,4-triméthylcyclohex-3-ène-1-méthanethiol, l’enquête menée aux termes de l’article 71 de la LCPE n’a révélé aucune utilisation dans des produits offerts aux consommateurs au Canada (Environnement Canada, 2011).
6.2 Évaluation des effets sur la santé
Sulfure de diméthyle
Les renseignements sur les effets sur la santé de cette substance sont tirés du rapport d’évaluation initiale (SIAR) du sulfure de diméthyle de l’OCDE (OCDE, 2006). Une revue de la littérature de la période commençant l’année précédant le SIAR de l’OCDE et se terminant en juillet 2016 n’a pas permis de trouver de nouvelles études qui modifieraient la caractérisation du danger et du risque posés par cette substance.
L’OCDE (2006) n’a pas trouvé d’études bien menées portant sur la toxicocinétique, le métabolisme et la distribution du sulfure de diméthyle. Par contre, une étude limitée a permis de constater que, à la suite d’une seule exposition aiguë à des vapeurs de sulfure de diméthyle, celui-ci était largement distribué dans tous les tissus (OCDE, 2006). Les sulfures d’alkyle sont réputés s’oxyder pour devenir, chez les mammifères, des sulfoxydes, puis des sulfones (Terazawa et al., 1991, tel que cité dans OCDE, 2006).
Des études sur la toxicité aiguë par inhalation, voie orale et voie cutanée étaient accessibles, mais les données sur les voies orale et cutanée étaient limitées. Comme l’a rapporté l’OCDE (2006), des rats ont été exposés pendant 4 heures à des concentrations de 0, 800, 3 000, 6 000, 12 000, 24 000, 36 000, 39 000, 42 000, 45 000 ou 48 000 ppm (soit environ 0, 2,03, 7,61, 15,2, 30,4, 60,9, 91,3, 98,9, 106, 114 ou 122 mg/L) de vapeur de sulfure de diméthyle, puis observé pendant 14 jours après l’exposition. La mortalité a été observée chez certains animaux exposés à des concentrations égales ou supérieures à 36 000 ppm, et la CL50 a été établie à 40 250 ppm (102 mg/L) chez les mammifères (Tansy et al., 1981, tel que cité dans OCDE, 2006). Dans une autre étude sur la toxicité aiguë par inhalation, des souris ayant reçu des doses de 6,8, 11,6, 23,6, 34,0, ou 50,6 % (soit 68 000, 116 000, 236 000, 340 000 ou 506 000 ppm) sont toutes mortes dans les 8 minutes environ suivant l’administration de la dose de 6,8 % (environ 173 mg/L) (Terazawa et al., 1991, tel que cité dans OCDE, 2006). Selon des études limitées sur la toxicité aiguë par voie orale, aucune mortalité et aucun effet n’ont été observés chez des souris traitées avec 5 000 mg/kg p.c. ou chez des rates gravides traitées avec 1 000 mg/kg p.c./j pendant 14 jours (Elf Atochem, 1995; WIL Research Laboratories, 2004, tel que cité dans OCDE, 2006). Enfin, une étude sur l’exposition par voie cutanée a rapporté une DL50 de > 5 g/kg p.c. (>5 000 mg/kg p.c.) chez des lapins, mais aucune durée d’exposition n’est mentionnée (Opdyke, 1979, tel que cité dans OCDE, 2006).
Comme le résume l’OCDE (2006), des études in vitro (essai de mutation inverse bactérienne et essai de dommages et de réparations à l’ADN) et in vivo (test des micronoyaux chez la souris) ont obtenu des résultats négatifs (Nakamura et al., 1990; Microbiological Associates Inc., 1995a; Microbiological Associates, 1995b, tel que cité dans OCDE, 2006). Aucune étude sur la cancérogénicité n’a été trouvée.
Dans une étude sur l’exposition par voie orale (gavage) à doses répétées, des rats mâles et femelles ont reçu des doses de 2,5, de 25 et de 250 mg/kg p.c./j de sulfure de diméthyle pendant 2, 6 ou 14 semaines (Butterworth et al., 1975, tel que cité dans OMS, 2000, et OCDE, 2006)Note de bas de page 5 . Une augmentation du poids relatif du cerveau et une diminution du poids absolu du cœur ont été observées après 2 semaines et après 6 semaines, respectivement, chez les femelles du groupe ayant reçu la dose la plus élevée. Après 14 semaines, le poids absolu du petit intestin (à toutes les doses) était significativement plus élevé chez les rats mâles que chez les individus du groupe témoin (le poids relatif de l’intestin était plus élevé aux doses de 25 et de 250 mg/kg p.c./j). Des différences propres au sexe dans le poids relatif de la thyroïde ont également été observées chez les mâles et les femelles ayant reçu pendant 14 semaines des doses de 250 mg/kg p.c./j (diminution des poids relatif et absolu de la thyroïde chez les femelles et augmentation du poids relatif de la thyroïde chez les mâles). Aucun effet histopathologique lié au traitement n’a été observé dans les organes susmentionnés. Aucune anomalie n’a été observée dans les testicules et les ovaires, et aucun effet lié au traitement n’a été observé sur le poids corporel, la consommation de nourriture, la consommation d’eau, l’hématologie et la chimie du sang. La dose sans effet nocif observé (DSENO) a été établie à 250 mg/kg p.c./j, soit la dose la plus élevée administrée (OCDE, 2006).
Dans une étude sur les effets de la toxicité par voie orale (gavage) sur le développement, des rates gravides (25/groupe) ont reçu des doses de 100, de 500 ou de 1 000 mg/kg p.c./j de sulfure de diméthyle aux jours de gestation (JG) 6 à 19 (WIL Research Laboratories, LLC, 2004, tel que cité dans OCDE, 2006). Aucun effet lié au traitement sur le poids corporel des mères, la consommation de nourriture, la croissance intra-utérine, le nombre de fœtus, le poids des fœtus et la survie n’a été observé. En outre, aucune malformation fœtale ou variation sur le plan du développement n’a été observée dans les groupes traités. La DSENO a été établie à 1 000 mg/kg p.c./j, soit la dose la plus élevée administrée (OCDE, 2006).
Disulfure de dibenzyle et alpha,alpha,4-triméthylcyclohex- 3-ène-1-méthanethiol
Le JECFA a évalué l’innocuité d’un groupe d’agents aromatisants, dont le sulfure de diméthyle, le disulfure de dibenzyle et l’alpha,alpha,4-triméthylcyclohex-3-ène-1-méthanethiol (OMS, 2000). Une revue de la littérature de la période commençant l’année précédant l’évaluation de l’innocuité du JECFA et se terminant en juillet 2016 a permis de trouver deux autres études publiées par l’Autorité européenne de sécurité des aliments (EFSA) qui auraient un impact sur la caractérisation du danger et du risque de ces substances (EFSA, 2009, 2014).
Le JECFA a conclu que les agents aromatisants comprenant des thiols, dont le disulfure de dibenzyle et l’alpha,alpha,4-triméthylcyclohex-3-ène-1-méthanethiol, ne présentent pas d’inquiétudes sur le plan de l’innocuité aux niveaux d’absorption estimés.
Les épreuves d’Ames, avec ou sans activation métabolique, avec administration de disulfure de dibenzyle ont donné des résultats négatifs à des concentrations de 10, de 100 et de 300 µg/plaque et des résultats positifs à la concentration la plus élevée de 600 µg/plaque (Gao Y et al., 1993). Toutefois, les résultats d’une autre épreuve d’Ames (avec ou sans activation) à des concentrations 6 fois plus élevées de disulfure de dibenzyle (soit 3 600 µg/plaque) étaient négatifs (OMS, 2000; EFSA, 2009).
L’OMS (2000) a classé le disulfure de dibenzyle dans la catégorie III, qui regroupe les substances aux caractéristiques structurales ne permettant pas de forte présomption initiale d’innocuité ou pouvant même laisser croire à une toxicité importante, et l’alpha,alpha,4-triméthylcyclohex-3-ène-1-méthanethiol, dans la catégorie II, qui regroupe les substances aux caractéristiques structurales présentant une innocuité moindre que les substances de catégorie I, mais qui ne laissent pas entrevoir une toxicité. Les substances de cette catégorie peuvent contenir des groupes fonctionnels réactifs.
En ce qui concerne l’évaluation des effets sur la santé de ces deux substances, le JECFA a considéré le disulfure de benzyle et de méthyle (no RN 699-10-5) et le cyclopentanethiol (no CAS 1679-07-8) comme des substances connexes aux fins de l’évaluation de l’innocuité du disulfure de dibenzyle et de l’alpha,alpha,4-triméthylcyclohex-3-ène-1-méthanethiol, respectivement (OMS, 2000). L’évaluation de ces substances connexes est fondée sur le fait que celles-ci sont des métabolites potentiels du disulfure de dibenzyle et de l’alpha,alpha,4-triméthylcyclohex-3-ène-1-méthanethiol. La dose sans effet observé (DSEO) utilisée dans l’évaluation de l’innocuité du disulfure de dibenzyle réalisée par le JECFA est de 1,2 mg/kg p.c./j (seule dose administrée) d’après une étude de 90 jours sur des doses répétées de disulfure de benzyle et de méthyle chez des rats. La DSEO utilisée dans l’évaluation de l’innocuité de l’alpha,alpha,4-triméthylcyclohex-3-ène-1-méthanethiol réalisée par le JECFA est de 0,56 mg/kg p.c./j (seule dose administrée) d’après une étude de 90 jours sur des doses répétées de cyclopentanethiol.
Dans les examens externes des décisions du JECFA par l’EFSA, cette dernière est d’accord avec la conclusion du JECFA selon laquelle le disulfure de dibenzyle ne présente aucune inquiétude sur le plan de l’innocuité (EFSA, 2009). Quant à l’alpha,alpha,4-triméthylcyclohex-3-ène-1-méthanethiol, l’EFSA (2011ab) a conclu que cette substance n’a pas pu être adéquatement évaluée selon la procédure de l’OMS (2000), les monothiols connexes posant des inquiétudes sur le plan de la génotoxicité. Cette opinion a été mise à jour en 2014, après que des données sur la génotoxicité d’une substance connexe (2-méthyl-4-oxopentane-2-thiol) eurent montré des effets génotoxiques néfastes, corroborant ainsi les préoccupations de l’EFSA quant à la génotoxicité potentielle de l’alpha,alpha,4-triméthylcyclohex-3-ène-1-méthanethiol (McGarry, 2012, tel que cité dans EFSA, 2014). Toutefois, l’EFSA (2014) n’a pas terminé son évaluation de cette substance puisque le comité était d’avis qu’il n’existait pas de DSENO adéquate pour l’alpha,alpha,4-triméthylcyclohex-3-ène-1-méthanethiol ou pour des substances considérées comme des analogues à structures similaires.
Tert-dodécanethiol
Les données sur les effets sur la santé de cette substance sont tirées de SIAR de l’OCDE sur le tert-dodécanethiol (OCDE, 2011). Une revue de la littérature de la période commençant l’année précédant les SIAR de l’OCDE et se terminant en juillet 2016 n’a pas permis de trouver d’études qui modifieraient la caractérisation du danger et du risque posés par cette substance.
L’OCDE (2011) n’a pas trouvé d’études bien menées portant sur la toxicocinétique, le métabolisme et la distribution du tert-dodécanethiol. Le tert-dodécanethiol est un irritant cutané et oculaire et pourrait être un sensibilisant cutané (OCDE, 2011).
Des études sur la toxicité aiguë par voie cutanée, voie orale et inhalation étaient accessibles. Comme l’a rapporté l’OCDE (2011), des lapins blancs néo-zélandais ont reçu des doses de 6,83, 10,25, 15,28 et 23,07 g/kg p.c. de tert‑dodécanethiol par voie cutanéeNote de bas de page 6 . Les huit lapins du groupe ayant reçu une dose de 15,28 g/kg p.c. sont morts trois à quatre jours après le traitement, et la DL50 a été modélisée et établie à 12,6 g/kg p.c. (soit 12 600 mg/kg p.c.) (OCDE, 2011). Dans une étude sur la toxicité aiguë par voie orale, des rats Sprague-Dawley ont reçu des doses de 4,56, 6,84, 10,25 et 15,38 g/kg p.c. Les huit rats des deux groupes ayant reçu les plus fortes doses sont morts, et la DL50 modélisée était de 6,8 g/kg p.c. (soit 6 800 mg/kg p.c.) (OCDE, 2011). Deux autres études sur les rats ont rapporté des DL50 par voie cutanée de 4 380 mg/kg p.c. et de > 5 000 mg/kg p.c. (OCDE, 2011). Une étude limitée sur la toxicité aiguë par inhalation (1 dose administrée, 12 mg/L) chez des rats Sprague-Dawley (5 mâles et 5 femelles) n’a rapporté aucun cas de mortalité (OCDE, 2011). D’autres études limitées sur la toxicité aiguë par inhalation sont décrites dans OCDE (2011).
Des études de l’exposition subchronique par inhalation au tert-dodécanethiol chez des rats, des souris et des chiens sont accessibles. Des rats Charles River CD ont été exposés à 26 ppm (220 mg/m3) et à 98 ppm (810 mg/m3, vapeur saturée) 6 heures par jour, 5 jours par semaine, sur une période de 4 semaines. Les mâles ayant reçu la dose la plus élevée ont montré les changements statistiquement significatifs suivants : diminutions du poids corporel et de la consommation de nourriture, et augmentations de la production de créatinine. Des augmentations du poids du foie liées à l’exposition ont également été observées; toutefois, aucun changement microscopique n’a été constaté. Aux deux doses, les rats mâles ont affiché une légère dégénérescence des tubules rénaux et des kystes granuleux, tandis que les femelles ayant reçu la dose la plus élevée ont montré des signes d’hydronéphrose (OCDE, 2011). Chez des souris CD-1, le tert-dodécanethiol a été administré à des doses de 25 ppm (210 mg/m3) et de 109 ppm (900 mg/m3) 6 heures par jour, 5 jours par semaine, sur une période de 4 semaines. Un mâle et une femelle du groupe ayant reçu la dose la plus élevée sont morts, et les animaux survivants de ce groupe ont montré des signes d’alopécie et de desquamation, de même que des baisses du nombre d’érythrocytes et de l’hématocrite et des hausses d’autres paramètres liés aux érythrocytes, baisses et hausses qui étaient significatives sur le plan statistique. En outre, les souris femelles du groupe ayant reçu la dose la plus forte ont présenté des hausses de teneurs en alanine aminotransférase, en azote uréique dans le sang et en phosphatase alcaline, et des baisses du poids des ovaires. D’autres effets chez les souris traitées avec la plus forte dose ont également été observés (OCDE, 2011). À la dose la plus faible, les femelles ont présenté une glycémie élevée et un poids du foie accru, et, chez les deux sexes, une hypertrophie et une décoloration du foie ainsi qu’une hypertrophie hépatocellulaire ont été observées (tant à la dose la moins élevée qu’à la dose la plus élevée) (OCDE, 2011). Dans une étude sur l’exposition par inhalation, des chiens ont reçu des doses de 25 ppm (210 mg/m3) et de 109 ppm (900 mg/m3) 6 heures par jour, 5 jours par semaine, pendant 4 semaines. Les animaux du groupe ayant reçu la dose la plus élevée ont présenté des hausses de teneurs en alanine aminotransférase et en azote uréique dans le sang. Des augmentations liées à la dose du poids du foie et une hypertrophie hépatocellulaire, à la dose la plus élevée, ont également été observées chez les deux sexes (OCDE, 2011). Compte tenu des similarités en termes d’effets observés dans le foie et les reins à la dose la plus faible dans les trois études, la concentration minimale avec effet nocif observé (CMENO) a été établie à 25 à 26 ppm (210 à 220 mg/m3) (OCDE, 2011).
Des études in vitro sur la génotoxicité ont donné des résultats principalement négatifs (Ames, lymphome de souris, chromatides sœurs) et un résultat équivoque (essai d’aberration chromosomique) (OCDE, 2011). Aucune étude in vivo sur la génotoxicité ou la cancérogénicité n’a été trouvée.
Des études sur la toxicité par inhalation pour le développement des rats et des souris ont été menées. Des rates COBS-CD gravides ont reçu une dose de 22,6 ppm (190 mg/m3) ou de 88,6 ppm (730 mg/m3) du jour de gestation (JG) 6 au JG 19, à raison de 6 heures par jour. Des césariennes ont été réalisées le jour 20. Aucun effet lié au traitement n’a été observé dans les fœtus ou les mères; toutefois, le gain en poids corporel des mères a semblé subir une baisse liée à la dose (OCDE, 2011). Une rate ayant reçu la dose la plus élevée est morte, mais la cause de la mort n’a pas été déterminée. L’OCDE (2011) a établi la concentration sans effet nocif observé (CSENO) à 88,6 ppm pour les paramètres d’effet de la toxicité pour les mères et pour le développement. Chez les souris gravides (CD-1), du tert-dodécanethiol a été administré à des doses de 22,6 ppm (190 mg/m3) et de 88,6 ppm (730 mg/m3) du jour de gestation 6 au jour de gestation 16, à raison de 6 heures par jour. Aucun changement statistiquement significatif n’a été relevé quant au poids corporel ou aux malformations fœtales. D’autres paramètres (p. ex. nombre moyen d’implantations totales et poids corporel des fœtus) étaient comparables aux valeurs témoins. Aucune malformation fœtale liée au traitement n’a été remarquée. Toutefois, une souris ayant reçu la dose la plus faible est morte, mais la cause de la mort n’a pas pu être déterminée. En 2011, l’OCDE a indiqué que, chez les rats et les souris exposés par inhalation au tert-dodécanethiol, aucune toxicité pour les mères ou pour le développement liée au traitement n’a été observée à concentrations allant jusqu’à 88,6 ppm (730 mg/m3)(OCDE, 2011).
6.3 Caractérisation des risques pour la santé humaine
Les principales études critiques aux fins de la caractérisation du danger sont résumées dans les SIAR de l’OCDE. Le tableau 6‑2 fournit toutes les valeurs pertinentes liées à l’exposition aux thiols présents dans ce groupe et au danger qu’ils posent, ainsi que la marge d’exposition (ME) qui en découle, aux fins de la détermination des risques.
Substance |
Scénario d’exposition |
Absorptions |
Niveau d’effet critique |
ME |
Tert-dodécanethiol |
Exposition par inhalation à des peintures |
0,60 mg/m3 a |
CSENO : 730 mg/m3 6 h/j à partir du JG 6 au JG 19 chez des rates gravides ou du JG 6 au JG 16 chez des souris gravides; fondée sur la dose maximale sans effet qui a été administréeb |
1 216 |
Abréviations : CSENO = concentration sans effet nocif observé.
a Selon la modélisation de ConsExpo pour l’exposition de la population générale.
b Tel que rapporté par l’OCDE (2011).
Les ME sont jugées adéquates pour rendre compte des incertitudes dans les bases de données.
Les sources d’exposition de la population générale du Canada au sulfure de diméthyle, au disulfure de dibenzyle et à l’alpha,alpha,4-triméthylcyclohex-3-ène-1-méthanethiol résultent de l’utilisation de ces substances comme agents aromatisants dans les aliments.
En ce qui concerne le disulfure de dibenzyle et l’alpha,alpha,4-triméthylcyclohex-3-ène-1-méthanethiol, d’après les données disponibles sur la toxicité et le métabolisme ainsi que les faibles absorptions estimées dérivées à partir des populations des États-Unis et de l’Union européenne, le JECFA a conclu que l’utilisation de ces substances en tant qu’agents aromatisants dans les aliments ne soulevait aucune inquiétude du point de vue de l’innocuité (OMS, 2000). De plus, il a été rapporté qu’à une faible concentration (0,004 ppm) l’alpha,alpha,4-triméthylcyclohex-3-ène-1-méthanethiol a une saveur semblable à celle du pamplemousse, tandis qu’à une concentration 10 fois plus élevée il a une odeur de pneu brûlé (Young et al., 2006). Les propriétés de ces agents aromatisants limitent en soi leur absorption. Étant donné que les expositions à ces substances sont considérées comme négligeables au Canada et que celles-ci ne semblent pas utilisées à d’autres fins, le risque pour la population générale posé par ces substances est considéré comme faible.
Pour le tert-dodécanethiol, la population générale peut être exposée par l’intermédiaire de l’utilisation de peintures et de revêtements, et la principale voie d’exposition est l’inhalation. Les études sur la toxicité aiguë par inhalation n’ont pas établi de paramètres d’effet pour l’utilisation en évaluant l’exposition à de faibles concentrations de tert-dodécanethiol dans l’air issues d’activités de peinture. Comme il est indiqué dans le tableau 6-2, une ME de 1 216 a été obtenue en comparant la valeur estimée de l’exposition par inhalation au tert-dodécanethiol au cours d’une activité de peinture et l’absence d’effet observé à la dose la plus élevée administrée lors d’une étude sur la toxicité par inhalation pour le développement (OCDE, 2011). Cette ME est considérée comme appropriée pour tenir compte des incertitudes potentielles dans les bases de données sur le danger et l’exposition.
La population générale peut également être exposée par voie cutanée au tert‑dodécanethiol par l’intermédiaire de l’utilisation de peintures et de revêtements (0,22 µg/kg p.c./événement). Toutefois, cette exposition ne devrait pas inquiéter, vu les faibles concentrations de la substance dans ces produits (sous forme d’impureté : < 0,1 %). En outre, comme il a été mentionné dans la section sur l’exposition, le tert‑dodécanethiol a une faible valeur d’absorption cutanée prévue (10 %); par conséquent, la valeur estimée du degré d’exposition par voie cutanée actuellement modélisée est prudente. De plus, les risques potentiels pour la santé humaine résultant de l’exposition à la substance dans des emballages d’aliments sont considérés comme négligeables puisque cette exposition est faible.
6.4 Incertitudes dans l’évaluation des risques pour la santé humaine
La principale incertitude entourant l’évaluation de l’exposition alimentaire découle du fait que Santé Canada ne possède pas de donnée sur les concentrations de ces substances dans les aliments vendus sur le marché canadien aujourd’hui, le cas échéant. Toutefois, les absorptions estimées considérées par le JECFA dans son évaluation de ces agents aromatisants sont considérées comme représentatives des expositions au Canada.
La présente évaluation a pris en considération l’évaluation du JECFA selon laquelle ces substances (sulfure de diméthyle, disulfure de dibenzyle et alpha,alpha,4-triméthylcyclohex-3-ène-1-méthanethiol) sont sécuritaires en tant qu’agents aromatisants dans les aliments aux niveaux d’absorption estimés. L’évaluation du JECFA repose sur l’hypothèse d’une faible toxicité des métabolites potentiels de ces substances, mais la toxicité des métabolites du disulfure de dibenzyle et de l’alpha,alpha,4-triméthylcyclohex-3-ène-1-méthanethiol n’est pas connue.
7. Conclusion
Compte tenu de tous les éléments de preuve contenus dans la présente évaluation préalable, le sulfure de diméthyle, le disulfure de dibenzyle, le tert‑dodécanethiol et l’alpha,alpha,4-triméthylcyclohex-3-ène-1-méthanethiol présentent un faible risque d’effets nocifs sur l’environnement. Il est proposé de conclure que le sulfure de diméthyle, le disulfure de dibenzyle, le tert-dodécanethiol et l’alpha,alpha,4-triméthylcyclohex-3-ène-1-méthanethiol ne satisfont pas aux critères énoncés aux alinéas 64a) ou b) de la LCPE, car ils ne pénètrent pas dans l’environnement en une quantité ou concentration ou dans des conditions de nature à avoir, immédiatement ou à long terme, un effet nocif sur l’environnement ou sur la diversité biologique, ou à mettre en danger l’environnement essentiel pour la vie.
À la lumière des renseignements contenus dans la présente évaluation préalable, il est conclu que le sulfure de diméthyle, le disulfure de dibenzyle, le tert‑dodécanethiol et l’alpha,alpha,4-triméthylcyclohex-3-ène-1-méthanethiol ne satisfont pas aux critères énoncés à l’alinéa 64c) de la LCPE, car ils ne pénètrent pas dans l’environnement en une quantité ou concentration ou dans des conditions de nature à constituer un danger au Canada pour la vie ou la santé humaines.
Il est conclu que le sulfure de diméthyle, le disulfure de dibenzyle, le tert‑dodécanethiol et l’alpha,alpha,4-triméthylcyclohex-3-ène-1-méthanethiol ne satisfont pas aux critères énoncés à l’article 64 de la LCPE.
Références
[BDIPSN] Base de données d’ingrédients de produits de santé naturels [base de données]. [modifié le 25 juin 2018]. Ottawa (Ontario) : Gouvernement du Canada. [consulté le 5 janvier 2018].
[BDPSNH] Base de données des produits de santé naturels homologués [Base de données]. [modifiée le 6 février 2018]. Ottawa (Ontario) : Gouvernement du Canada. [consulté le 5 janvier 2018].
Burdock, G. 2010. Fenaroli’s Handbook of Flavor Ingredients, sixth ed. CRC Press, Boca Raton, FL. (disponible en anglais seulement)
Butterworth, K.R., Carpanini, F.M.B., Gaunt, I.F. Hardy, J., Kiss, I.S. and Gangolli, S. D. 1975. Short-term toxicity of dimethyl sulphide in the rat. Fd. Cosmet.Toxicol. 13:15-22 [cite dans OCDE, 2006] (disponible en anglais seulement)
Canada. 1999. Loi canadienne sur la protection de l’environnement, 1999. L.C. 1999, ch.33. Gazette du Canada Partie III, vol. 22, n° 3. [consulté le 22 février 2016].
Catalan L, Liang V, Johnson A, Jia C, O'Connor B, Walton C. 2009. Emissions of reduced sulphur compounds from the surface of primary and secondary wastewater clarifiers at a Kraft Mill. Environ Monit Assess. 156(1-4):37-49. (disponible en anglais seulement)
ChemIDplus [base de données]. 2018. Bethesda, MD: National Institutes of Health; [consulté le 25 juin 2018]. (disponible en anglais seulement)
Chemspider [base de données]. 2015.London, UK: Royal Society of Chemistry; [Consulté le 22 février 2016]. (disponible en anglais seulement)
City of Hamilton. 2009. Ambient Air Monitoring Program Year 2009 [PDF], City of Hamilton Glanbrook Landfill, Binbrook, Ontario. [consulté le 22 novembre 2016]. (disponible en anglais seulement)
[ConsExpo] Consumer Exposure Model. 2006. Version 4.1. Bilthoven (NL): Rijksinstituut voorVolksgezondheid en Milieu (National Institute for Public Health and the Environment). [consulté le 22 févier 2016]. (disponible en anglais seulement)
Drimal M, Koppová K, Klöslová Z, Fabiánová E. 2010. Environmental exposure to hydrogen sulfide in central Slovakia (Ruzomberok area) in context of health risk assessment. Cent Eur J Public Health. 18(4):224-9. (disponible en anglais seulement)
[ECCC] Environnement et Changement climatique Canada. 2016a. Document sur l’approche scientifique : classification du risque écologique des substances organiques. Ottawa (Ontario) : Gouvernement du Canada.
[ECCC] Environnement et Changement climatique Canada; 2016b; Gatineau (QC) : données utilisées pour créer des profils d'exposition et de danger spécifiques des substances et assigner des classifications des risques pour la Classification des risques écologiques des substances organiques. Disponible de : substances@ec.gc.ca
[ECCC, SC] Environnement et Changement climatique Canada, Santé Canada. [modifié le 12 mars 2017]. Catégorisation. Ottawa (Ontario) : Gouvernement du Canada. [consulté le 20 novembre 2016].
[ECCC, SC] Environnement et Changement climatique Canada, Santé Canada. 2017. Ébauche d’évaluation préalable Substances jugées comme étant peu préoccupantes au moyen de l’approche de la Classification du risque écologique des substances organiques et de l’approche fondée sur le seuil de préoccupation toxicologique (SPT) pour certaines substances. Ottawa (Ontario) : Gouvernement du Canada.
[EFSA] European Food Safety Authority. 2009. Flavouring Group Evaluation 8 (FGE.08): Aliphatic and alicyclic mono-, di-, tri-, and polysulfide s with or without additional oxygenated functional groups from chemical group 20. [Consulté le 22 février 2016]. (disponible en anglais seulement)
[EFSA] European Food Safety Authority. 2011a. Scientific Opinion on Flavouring Group Evaluation 74, Revision 1 (FGE.74Rev1): Consideration of Simple Aliphatic Sulfide s and Thiols evaluated by the JECFA (53rd and 61st meeting) Structurally related to Aliphatic and Alicyclic Mono-, Di-, Tri-, and Polysulfide s with or without Additional Oxygenated Functional Groups from Chemical Group 20 evaluated by EFSA in FGE.08Rev1 (2009). [Consulté le 22 février 2016]. (disponible en anglais seulement)
[EFSA] European Food Safety Authority. 2011b. Scientific Opinion on Flavouring Group Evaluation 74, Revision 2 (FGE.74Rev2): Consideration of Simple Aliphatic Sulfide s and Thiols evaluated by the JECFA (53rd and 61st meeting) Structurally related to Aliphatic and Alicyclic Mono-, Di-, Tri-, and Polysulfide s with or without Additional Oxygenated Functional Groups from Chemical Group 20 evaluated by EFSA in FGE.08Rev3 (2011). [Consulté le 22 février 2016]. (disponible en anglais seulement)
[EFSA] European Food Safety Authority. 2014. Scientific Opinion on Flavouring Group Evaluation 91, Revision 2 (FGE.91Rev2): Consideration of simple aliphatic and aromatic sulfides and thiols evaluated by the JECFA (53rd and 68th meetings) structurally related to aliphatic and alicyclic mono-, di-, tri-, and polysulfide s with or without additional oxygenated functional groups evaluated by EFSA in FGE.08Rev5 (2012). [Consulté le 22 février 2016]. (disponible en anglais seulement)
Elf Atochem SA. 1995. Biodegradabilite du Dimethyl Sulfure. Report 50794/HT [cite dans OCDE 2006] (disponible en anglais seulement)
Environnement Canada. 2009. Données de la mise à jour de l’inventaire de la LIS recueillies en vertu de la Loi canadienne sur la protection de l’environnement, 1999, article 71 : Avis concernant certaines substances inanimées (chimiques) sur la Liste intérieure des substances. Données préparées par : Environnement Canada, Santé Canada; Programme des substances existantes.
Environnement Canada; 2014; Résultats de l'examen préalable rapide des substances identifiées à la Phase 2 de la mise à jour de la Liste intérieure des substances – Chiffrier détaillé; Division de l'évaluation environnementale, Environnement Canada, Gatineau, QC, Canada.
[EPI Suite] Estimation Program Interface Suite for Microsoft Windows [estimation model]. c2000-2012. Ver. 4.11. Washington (DC): US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY): Syracuse Research Corporation. [Consulté le 22 février 2016]. (disponible en anglais seulement)
European Union Food Flavourings Database [Database]. [Consulté le 22 novembre 2016]. (disponible en anglais seulement)
[FCC] Food Chemicals Codex. 2016 National Academy of Sciences, Washington, DC. In: The United States Pharmacopeia-National Formulary (USP39–NF34). [Consulté le 22 novembre 2016]. (disponible en anglais seulement)
Gao Y, Wang G, Fan P, Wang T. 1993. Mutagenic and teratogenic effects of BDS. Weisheng Dulixue Zazhi 7(4):214-16. (disponible en anglais seulement)
Goyer N. 1990. Evaluation of occupational exposure to sulfur compounds in paper pulp kraft mills. Am IndHyg Assoc J. 51(7):390-4. (disponible en anglais seulement)
Kangas J, Jäppinen P, Savolainen H. 1984. Exposure to hydrogen sulfide, mercaptans and sulfur dioxide in pulp industry. Am Ind Hyg Assoc J. 45(12):787-90. (disponible en anglais seulement)
Kim KH, Kim YH. 2014. Composition of key offensive odorants released from fresh food materials. Atmos Environ 89:443–52. (disponible en anglais seulement)
Klein F, Platt SM, Farren NJ, Detournay A, Bruns EA, Bozzetti C, Daellenbach KR, Kilic D, Kumar NK, Pieber SM, Slowik JG, Temime-Roussel B, Marchand N, Hamilton JF, Baltensperger U, Prévôt AS, El Haddad I. 2016. Characterization of Gas-Phase Organics Using Proton Transfer Reaction Time-of-Flight Mass Spectrometry: Cooking Emissions. Environ Sci Technol. 50(3):1243-50. (disponible en anglais seulement)
Kotowska U, Zalikowski M, Isidorov VA. 2012. HS-SPME/GC-MS analysis of volatile and semi-volatile organic compounds emitted from municipal sewage sludge, Environ. Monit Asses 184(5):2893-2907. (disponible en anglais seulement)
Kroes R, Renwick AG, Feron V, Galli CL, Gibney M, Greim H, Guy RH, Lhuguenot JC, van de Sandt JJ. 2007. Application of the threshold of toxicological concern (TTC) to the safety evaluation of cosmetic ingredients. Food Chem Toxicol. 45(12):2533-62. (disponible en anglais seulement)
McGarry S, 2012. Audited Draft Report. Reverse mutation in five histidine-requiring strains of Salmonella typhimurium. 2-Mercapto-4-methylpentan-2-one. Covance Laboratories Ltd. Study no. 8261928. September 2012. Unpublished report submitted by EFFA to FLAVIS Secretariat [cited in EFSA 2014](disponible en anglais seulement)
Microbiological Associates, Inc. 1995a. Micronucleus cytogenetic assay in mice. Laboratory Study No. G95AT25.122. Submitted to Elf Atochem North America, Inc. Philadelphia, PA [cité dans OCDE, 2006] (disponible en anglais seulement)
Microbiological Associates, Inc. 1995b. Salmonella/Escherichia coli closed-phase preincubation mutagenicity assay with an independent repeat assay. Laboratory Study No. G95AT25.502003. Submitted to Elf Atochem North America, Inc. Philadelphia, PA [cité dans OCDE, 2006] (disponible en anglais seulement)
Nakamura, S., Oda, Y. and Ugawa, M. 1990. Induction of umu Gene Expression in Salmonella typhimurium TA1535/p SK1002 by Dimethyl Sulfoxide (DMSO). Mutation Research, 229(1):11-15 [cité dans OCDE, 2006] (disponible en anglais seulement)
[NCI] National Chemical Inventory [Database]. [modifié le 15 mai 2017]. [consulté le 20 juillet 2016]. (disponible en anglais seulement)
[OCDE]. 2006. SIDS Initial Assessment Report: Dimethyl Sulfide. [Consulté le 22 février 2016]. (disponible en anglais seulement)
[OCDE]. 2011. SIDS initial Assessment Report: C8 - C12 Aliphatic Thiols Category. [Consulté le 18 mai 2017]. (disponible en anglais seulement)
[OMS]. Organisation mondiale de la Santé. 2000. Joint FAO/WHO Expert Committee on Food Additives (JECFA). Safety Evaluation of Certain Food Additives and Contaminants. WHO Food Additives Series 44. [consulté le 20 juillet 2016]. (disponible en anglais seulement)
Opdyke, D. L. J. 1979. Fragrance Raw Materials Monograph, Dimethyl Sulfide. Fd. Cosmet. Toxicol.17:365-367 [cité dans OCDE, 2006] (disponible en anglais seulement)
[RIVM] Rijksinstituut voor Volksgezondheid en Milieu [National Institute for Public Health and the Environment]. 2006. General fact sheet: limiting conditions and reliability, ventilation, room size, body surface area: updated version for ConsExpo 4. Bilthoven (NL): RIVM. Report No.: 320104002/2006. [Consulté le 22 novembre 2016]. (disponible en anglais seulement)
[RIVM] Rijksinstituut voor Volksgezondheid en Milieu [National Institute for Public Health and the Environment]. 2007. Paint products fact sheet: to assess the risks for the consumer: updated version for ConsExpo 4 [PDF]. Bilthoven (NL): RIVM. Report No.: 320104008/2007. [Consulté le 22 février 2016]. (disponible en anglais seulement)
Susaya J, Kim KH, Phana NT, Kim JC. 2011. Assessment of reduced sulfur compounds in ambient air as malodor components in an urban area Atmos Environ 45(20):3381–90. (disponible en anglais seulement)
Tansy, M.F., Kendall, F.M., Fantasia, J., Landin, W.E. and Oberly, R. 1981. Acute and subchronic toxicity studies of rats exposed to vapors of methyl mercaptan and other reduced-sulfur compounds, J. Toxicol. Environ. Health, 8:71-88 [cité dans OCDE, 2006] (disponible en anglais seulement)
Terazawa K, Mizukami K, Wu B, Takatori T. 1991. Fatality due to inhalation of dimethyl sulfide in a confined space: a case report and animal experiments. Int J Legal Med 104(3):141-4. [cité dans OCDE, 2006]. (disponible en anglais seulement)
WIL Research Laboratories, LLC. 2004. A prenatal developmental toxicity study of dimethyl sulfide in rats. Report # WIL-495002. Unpublished study sponsored by the Dimethyl Sulfide Producers Association [cité dabs OCDE, 2006](disponible en anglais seulement)
Young KW, Danielewska-Nikiel B, Munro IC. 2006. An evaluation of the maximized survey-derived daily intake (MSDI) as a practical method to estimate intake of flavouring substances. Food Chem Toxicol. 44(11):1849-67. (disponible en anglais seulement)
Annexe A. Exposition cutanée et par inhalation à la peinture murale chez l’humain
Les expositions chez l’humain ont été estimées en utilisant le scénario ConsExpo pour la peinture murale à l’eau à appliquer au pinceau/rouleau (RIVM, 2007). Toutes les valeurs par défaut recommandées pour ce scénario ont été utilisées, sauf pour les paramètres mentionnés ci-après.
Concentration de tert-dodécanethiol dans la peinture murale = 0,1 % (Environnement Canada, 2009)
Masse moléculaire du tert-dodécanethiol = 202 g/mol
Pression de vapeur du tert-dodécanethiol = 22,8 Pa
Koe du tert-dodécanethiol = 5,85 10log
Paramètres utilisés pour calculer l’exposition par inhalation et par voie cutanée à la peinture murale
Modèle d’inhalation : exposition à la vapeur : évaporation
Durée d’exposition : 132 minutes
Volume de la pièce : 20 m3
Taux de ventilation : 0,6/h
Quantité de produit : 1,25E3 grammes
Surface exposée : 10 m2
Durée d’application : 120 minutes
Température d’application : 20 oC
Matrice de la masse moléculaire : 120 g/mol
Taux de transfert de masse : 0,223 m/min (Thibodeaux)
Absorption par inhalation : 100 %
Taux d’inhalation : 16,2 m3/j
Modèle d’exposition cutanée : contact cutané direct avec le produit : taux constant
Surface exposée : 0,367 cm2 (RIVM, 2006)
Taux de contact : 30 mg/min
Durée d’émission : 120 minutes
Absorption cutanée : 100 %