Évaluation préalable - isobutylène sulfuré
Titre officiel : Évaluation préalable - 2-méthylprop-1-ène sulfuré (isobutylène sulfuré)
Numéro d’enregistrement du Chemical Abstracts Service
68511-50-2
Environnement et Changement climatique Canada
Santé Canada
Mai 2022
No de cat. : En84-291/2022F-PDF
ISBN 978-0-660-42829-1
Sommaire
Conformément à l’article 74 de la Loi canadienne sur la protection de l’environnement (1999) (LCPE), les ministères de l’Environnement et de la Santé ont mené une évaluation préalable du 2-méthylprop-1-ène sulfuré (numéro de registre CASNote de bas de page 1 68511-50-2), aussi appelé isobutylène sulfuré. Il a été déterminé que cette substance devait être évaluée en priorité, car elle satisfaisait aux critères de catégorisation énoncés au paragraphe 73(1) de la LCPE.
L’isobutylène sulfuré fait partie des substances de composition inconnue ou variable, produits de réaction complexes ou matières biologiques (UVCB) et n’est pas présent à l’état naturel dans l’environnement. Les résultats d’une enquête menée en 2011 en vertu de l’article 71 de la LCPE ont montré que la quantité d’isobutylène sulfuré produite au Canada ne dépassait pas le seuil de déclaration de 100 kg et qu’entre 10 000 et 100 000 kg de la substance ont été importés. Il a été indiqué que cette substance était principalement utilisée au Canada comme lubrifiant et additif dans les lubrifiants et les graisses.
Le risque pour l’environnement associé à l’isobutylène sulfuré a été caractérisé à l’aide de la classification du risque écologique (CRE) des substances organiques, une méthode fondée sur le risque qui tient compte de plusieurs paramètres évaluant à la fois le danger et l’exposition dans le but de classer le risque en fonction d’une pondération des éléments de preuve. Les profils de danger reposent principalement sur des paramètres comme le mode d’action toxique, la réactivité chimique, les seuils de toxicité interne induite par le réseau trophique, la biodisponibilité et l’activité chimique et biologique. Les paramètres pris en compte dans les profils d’exposition comprennent le taux d’émission potentiel, la persistance globale et le potentiel de transport à longue distance. Une matrice des risques permet d’attribuer un niveau de risque faible, modéré ou élevé aux substances en fonction de leurs profils de danger et d’exposition. Selon les résultats de la CRE, l’isobutylène sulfuré est considéré comme étant peu susceptible de causer des effets nocifs sur l’environnement.
Compte tenu de tous les éléments de preuve contenus dans la présente évaluation préalable, l’isobutylène sulfuré présente un faible risque d’effets nocifs sur l’environnement. Il est conclu que l’isobutylène sulfuré ne satisfait aux critères énoncés à l’alinéa 64a) ou 64b) de la LCPE, car il ne pénètre pas dans l’environnement en une quantité ou concentration ni dans des conditions de nature à avoir, immédiatement ou à long terme, un effet nocif sur l’environnement ou sur la diversité biologique, ou à mettre en danger l’environnement essentiel pour la vie.
D’après les données existantes, la population générale pourrait être exposée à l’isobutylène sulfuré lors de l’utilisation de produits de consommation (lubrifiants et graisses) et par l’intermédiaire de l’eau potable, en raison des rejets industriels.
D’après les observations faites en laboratoire, les effets critiques découlant d’une exposition cutanée à l’isobutylène sulfuré étaient une diminution du gain de poids corporel et des effets hématologiques. D’après les effets observés en laboratoire pour une substance similaire, l’effet critique sur la santé à la suite d’une exposition orale sur une longue durée était la diminution du poids des petits chez le rat.
La comparaison des niveaux d’exposition de la population générale aux niveaux associés aux effets critiques sur la santé montre que les marges d’exposition sont jugées adéquates pour tenir compte des incertitudes dans les bases de données relatives aux effets sur la santé et à l’exposition.
À la lumière des renseignements contenus dans la présente évaluation préalable, il est conclu que l’isobutylène sulfuré ne satisfait pas aux critères de l’alinéa 64c) de la LCPE, car il ne pénètre pas dans l’environnement en une quantité ou concentration ou dans des conditions de nature à constituer un danger au Canada pour la vie ou la santé humaines.
Il est donc conclu que l’isobutylène sulfuré ne satisfait à aucun des critères énoncés à l’article 64 de la LCPE.
1. Introduction
En vertu de l’article 74 de la Loi canadienne sur la protection de l’environnement (1999) (LCPE) (Canada, 1999), les ministères de l’Environnement et de la Santé ont réalisé une évaluation préalable de l’isobutylène sulfuré afin de déterminer si cette substance présentait ou pouvait présenter un risque pour l’environnement ou la santé humaine. Il a été déterminé que l’isobutylène sulfuré devait être évalué en priorité, car il satisfaisait au critère de catégorisation énoncé au paragraphe 73(1) de la LCPE.
Les risques posés à l’environnement par l’isobutylène sulfuré ont été caractérisés à l’aide de l’approche de classification des risques écologiques (CRE) des substances organiques (ECCC, 2016a). La CRE permet de décrire le danger posé par une substance à l’aide de paramètres clés, notamment le mode d’action toxique, la réactivité chimique, les seuils de toxicité interne induite par le réseau trophique, la biodisponibilité et l’activité chimique et biologique et d’évaluer l’exposition potentielle des organismes aquatiques et terrestres en fonction de facteurs comme la vitesse potentielle d’émission, la persistance globale et le potentiel de transport atmosphérique sur de grandes distances. La combinaison des divers éléments de preuve permet de déterminer quelles substances requièrent une évaluation approfondie de leur potentiel d’effets nocifs sur l’environnement ou présentent une faible probabilité d’avoir de tels effets.
La présente évaluation préalable tient compte des renseignements sur les propriétés chimiques, le devenir dans l’environnement, les dangers, les utilisations et l’exposition, ainsi que des renseignements supplémentaires soumis par les intervenants. Des données pertinentes ont été trouvées jusqu’en mai 2019. Nos conclusions reposent sur des données empiriques tirées d’études clés et des résultats de modélisations. Quand ils étaient disponibles et pertinents, nous avons tenu compte de renseignements présentés dans des évaluations faites par d’autres instances, c’est-à-dire l’United States Environmental Protection Agency (US EPA) et le ministère de la Santé de l’Australie.
La présente évaluation préalable a été rédigée par les responsables du Programme d’évaluation des risques de la LCPE à Santé Canada et Environnement et Changement climatique Canada. Elle inclut des contributions issues d’autres programmes menés par ces deux ministères. Les parties de la présente évaluation portant sur la santé humaine ont fait l’objet d’un examen ou de consultations externes. Les commentaires sur les parties techniques contenues dans ce volet ont été formulés par Jennifer Flippin, Theresa Lopez et Joan Garey, toutes affiliées à Tetra Tech. La partie de l’évaluation du risque pour l’environnement repose sur le document de la CRE (publié le samedi 30 juillet 2016), lequel a fait l’objet d’un examen externe par des pairs et d’une période de consultation publique de 60 jours. De plus, l’ébauche de la présente évaluation préalable (publiée le 4 juillet 2020) a fait l’objet d’une consultation publique de 60 jours. Bien que les commentaires de l’extérieur aient été pris en compte, le contenu définitif et les résultats de la présente évaluation préalable demeurent la responsabilité de Santé Canada et d’Environnement et Changement climatique Canada.
La présente évaluation préalable repose sur des renseignements permettant de déterminer si les substances satisfont aux critères énoncés à l’article 64 de la LCPE. Pour ce faire, les renseignements scientifiques ont été étudiés et intégrés à une approche fondée sur le poids de la preuve et le principe de prudence.Note de bas de page 2 Cette évaluation préalable présente les renseignements essentiels et les considérations qui ont permis de tirer la conclusion proposée.
2. Identité de la substance
Le numéro de registre du Chemical Abstracts Service (no CASNote de bas de page 3 ) et le nom figurant sur la Liste intérieure des substances (LIS) de la substance individuelle figurent dans le tableau 2-1.
| No CAS | Nom sur la LIS (nom commun) | Structure chimique représentativea | Poids moléculaire (g/mol)a |
|---|---|---|---|
|
b |
2-méthylprop-1-ène sulfuréb (isobutylène sulfuré) |
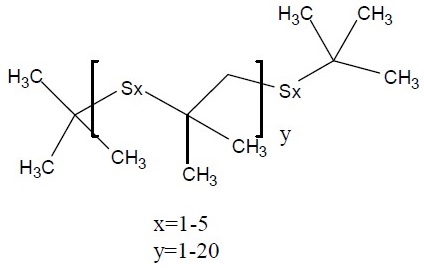 |
160 à 1 600 (moyenne de 480) |
a US EPA, 2009
b UVCB, c.-à-d. substance de composition inconnue ou variable, produit de réactions complexes ou matière biologique. Ces matières sont issues de sources naturelles ou de réactions complexes et elles ne peuvent pas être caractérisées sur le plan de leurs constituants chimiques en raison de leur composition trop complexe ou trop variable. Les UVCB ne sont pas des mélanges intentionnels de substances précises et sont considérées comme des substances uniques.
2.1 Sélection d’analogues
Lorsque la situation s’y prêtait, une approche par lecture croisée utilisant des données d’analogues a permis d’évaluer les effets de la substance sur la santé humaine. On a choisi des analogues dont la structure ou la fonction étaient semblables à celles de l’isobutylène sulfuré (d’après leurs propriétés physico-chimiques, leur réactivité et leur métabolisme) et pour lesquels on possède des données empiriques. L’annexe A présente de plus amples détails sur les facteurs pris en compte pour la sélection des analogues. Les détails de la lecture croisée choisie utilisée pour éclairer l’évaluation des risques pour la santé humaine posés par l’isobutylène sulfuré suivent ci-dessous.
L’EPA (2009) a fait l’évaluation de l’isobutylène sulfuré en le regroupant avec des substances semblables de la catégorie des polysulfures d’alkyle, et avec des alcènes C15-18- α-sulfurés. Ce regroupement était fonction de la similarité structurelle, de la réactivité limitée, de la faible activité biologique, de la très faible solubilité dans l’eau et de la faible pression de vapeur des substances incluses.
Une liste des analogues utilisés dans la présente évaluation est fournie dans le tableau 2-2. Pour en savoir plus au sujet des propriétés physico-chimiques présentées plus haut, consultez l’annexe A.
| No CAS (sigle/abréviation) | Nom dans la LIS (nom commun) | Formule développée | Poids moléculaire (g/mol) |
|---|---|---|---|
|
67124-09-8 |
1-(tert-dodécylthio) propan-2-ol (1-(tert-dodécylthio)propan-2-ol) |
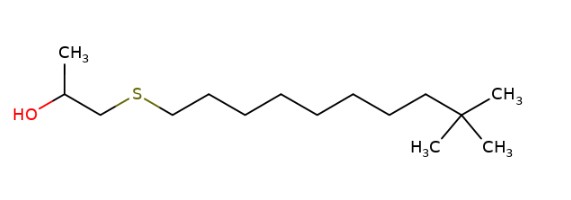 |
160 à 1 600 (moyenne de 480) |
|
68425-16-1a |
Polysulfures, di-tert-nonyl |
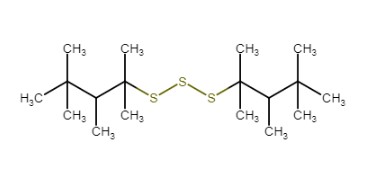 |
Non précisé |
|
67762-55-4a |
Alcènes, C15-18- α-sulfurés |
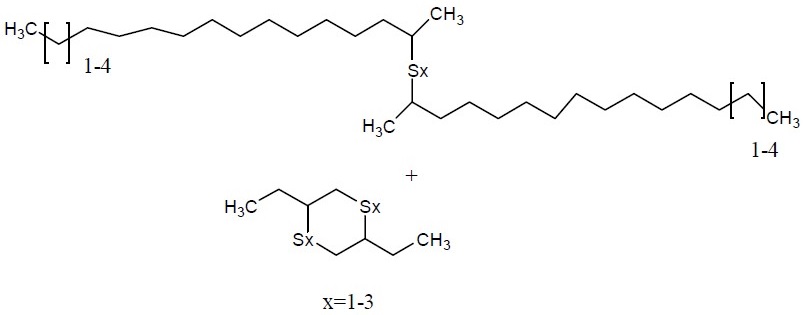 |
Non précisé |
a UVCB, c.-à-d. substance de composition inconnue ou variable, produit de réactions complexes ou matière biologique. Ces matières sont issues de sources naturelles ou de réactions complexes et elles ne peuvent pas être caractérisées sur le plan de leurs constituants chimiques en raison de leur composition trop complexe ou trop variable. Les UVCB ne sont pas des mélanges intentionnels de substances précises et sont considérées comme des substances uniques.
3. Propriétés physico-chimiques
Le tableau 3-1 présente un résumé des propriétés physiques et chimiques de l’isobutylène sulfuré. D’autres propriétés physiques et chimiques ont été décrites dans un document d’ECCC (2016b).
| Propriété | Valeur ou intervalle | Principales références |
|---|---|---|
|
État physique |
Liquide |
US EPA, 2009 |
|
Pression de vapeur (Pa) |
1,0 × 10−6 - 2,7 |
US EPA, 2009 |
|
Hydrosolubilité (mg/L) |
6,3 × 10−6 - 2,7 |
US EPA, 2009 |
|
log Koe (sans dimension) |
5,1 à > 6 a |
US EPA, 2009 |
|
log Kco (sans dimension) |
11,98 |
US EPA, 2009 |
Abréviations : Koe, coefficient de partage octanol-eau; Kco, coefficient de partage carbone organique-eau
a À une température de 25 °C et un pH de 6,8
4. Sources et utilisations
L’isobutylène sulfuré a été visé par une enquête menée en vertu de l’article 71 de la LCPE (Canada, 2012). Au cours de l’année civile 2011, aucune production en quantité supérieure au seuil de déclaration de 100 kg n’a été signalée au Canada, et une importation au Canada de 10 000 à 100 000 kg a été déclaréeNote de bas de page 4 (Environnement Canada, 2013). Au Canada, l’isobutylène sulfuré est utilisé comme lubrifiant et additif dans les lubrifiants et les graisses, y compris dans des produits offerts aux consommateurs (Environnement Canada, 2013; ECCC, 2016c; FDS, 2019).
Parmi les autres utilisations possibles au Canada, notons l’utilisation comme lubrifiant pour les équipements et les pièces de machines dans les installations de transformation des aliments, qui ne devraient pas entrer en contact avec les aliments (communication personnelle; courriel de la Direction des aliments, Santé Canada, adressé au Bureau de l’évaluation du risque des substances existantes, Santé Canada, et daté du 1er février 2019; non cité).
5. Risque d’effets nocifs sur l’environnement
5.1 Caractérisation des risques pour l’environnement
Les risques posés à l’environnement par l’isobutylène sulfuré ont été caractérisés à l’aide de l’approche de classification des risques écologiques (CRE) des substances organiques (ECCC, 2016a). La CRE est une approche fondée sur le risque qui tient compte de plusieurs paramètres liés au danger et à l’exposition et d’une pondération des différents éléments probants pour classer les risques. Les divers éléments de preuve sont rassemblés pour que l’on puisse distinguer des autres substances celles qui présentent une toxicité faible ou élevée et un risque d’exposition faible ou élevé dans divers milieux. Cette façon de faire permet de réduire l’incertitude globale liée à la caractérisation des risques par rapport à une approche reposant sur un seul paramètre mesuré dans un seul milieu (p. ex. la concentration létale médiane [CL50]). La partie qui suit résume cette approche, décrite en détail dans un document d’ECCC (2016a).
Les profils de danger reposent principalement sur des paramètres comme le mode d’action toxique, la réactivité chimique, les seuils de toxicité interne induite par le réseau trophique, la biodisponibilité et l’activité chimique et biologique. Les profils d’exposition ont aussi été élaborés à l’aide de plusieurs paramètres, dont le taux d’émission potentielle, la persistance globale et le potentiel de transport à longue distance. La comparaison des profils de danger et d’exposition avec les critères de décision a permis de classer le danger et le risque d’exposition associé à chaque substance selon qu’ils étaient faibles, moyens ou élevés. D’autres règles ont été appliquées (p. ex. cohérence de la classification, marge d’exposition) pour améliorer les classifications préliminaires de danger ou d’exposition. Cependant, dans le cas de l’isobutylène sulfuré, les profils de danger et d’exposition n’ont pu être établis entièrement en raison de l’absence d’une structure représentative permettant d’estimer les propriétés nécessaires et de l’absence de données empiriques sur ces propriétés. Par conséquent, une classification manuelle du danger et de l’exposition a été réalisée par l’examen des constituants UVCB et à l’aide des renseignements obtenus grâce à l’enquête menée conformément à l’article 71 de la LCPE et de décisions fondées sur l’examen de substances similaires et du jugement d’un spécialiste.
Une matrice des risques a permis de classer le risque associé à chaque substance, selon qu’il était faible, modéré ou élevé, à partir de la classification du danger et de l’exposition. Les classifications du risque obtenues à l’aide de la CRE ont subi une vérification en deux étapes. La première étape a consisté à modifier à la baisse la classification du risque (qui passe de modéré ou élevé à faible) des substances présentant une valeur estimée faible du taux d’émission dans l’eau après traitement des eaux usées, ce qui représente un faible risque d’exposition. La deuxième étape a consisté à revoir les résultats de classification faible à la lumière de scénarios de risque relativement prudents à l’échelle locale (c. à d. dans la zone à proximité du point de rejet) conçus pour protéger l’environnement, afin de déterminer si la classification du risque devrait être reclassée à un niveau supérieur.
La CRE est une approche pondérée qui vise à réduire au minimum le risque d’une surclassification ou d’une sous-classification du danger, de l’exposition et du risque subséquent. Les approches équilibrées utilisées pour réduire les incertitudes sont décrites en détail dans un document d’ECCC (2016a). Dans ce qui suit, nous décrivons deux des zones d’incertitude les plus importantes. Des valeurs de toxicité aiguë empiriques ou modélisées erronées pourraient conduire à des modifications du classement du danger, en particulier dans le cas des paramètres liés à des valeurs de résidus dans les tissus (c.-à-d. mode d’action toxique), dont de nombreux sont prédites à partir de modèles QSAR (Boîte à outils QSAR de l’OCDE, 2014). Les répercussions de ce type d’erreur sont toutefois atténuées par le fait qu’une surestimation de la CL50 donnera une valeur prudente (protectrice) de résidus dans les tissus qui servira à l’analyse des résidus corporels critiques. L’erreur due à une sous-estimation de la toxicité aiguë sera atténuée par le recours à d’autres paramètres du danger tels que la structure associée au mode d’action, la réactivité ou l’affinité de liaison aux œstrogènes. Les changements ou erreurs touchant les quantités de substances chimiques peuvent conduire à des classifications différentes de l’exposition, car la classification de l’exposition et du risque est très sensible au taux d’émission et aux quantités utilisées. Les classifications obtenues au moyen de la CRE reflètent donc l’exposition et le risque au Canada, compte tenu des quantités vraisemblablement utilisées actuellement, mais pourraient ne pas rendre compte des tendances futures.
Les données essentielles et les éléments pris en compte pour produire les profils et les classifications du danger, de l’exposition et du risque associés à l’isobutylène sulfuré sont présentés dans ECCC (2016b).
D’après le classement de danger faible et de faible exposition établi au moyen des données examinées selon l’approche de la CRE, le potentiel de risque pour l’environnement associé à l’isobutylène sulfuré est faible. Il est peu probable que cette substance suscite des préoccupations pour l’environnement au Canada.
6. Potentiel d’effets nocifs sur la santé humaine
6.1 Évaluation de l’exposition
Produits de consommation
L’isobutylène sulfuré a, en tant qu’ingrédient, été décelé dans des lubrifiants et graisses automobiles offerts aux consommateurs, à une concentration allant jusqu’à 5 % (FDS, 2019). L’utilisation de ces produits peut exposer la population générale à la substance, par exemple pour ceux qui effectuent eux-mêmes l’entretien de leur véhicule. On ne s’attend pas à une exposition par inhalation à cause de la faible pression de vapeur de la substance. L’exposition, qui devrait se faire principalement par voie cutanée, est estimée à 0,12 mg/kg p.c. par événement pour les adultes. L’information sur la méthode et les paramètres utilisés pour obtenir les estimations de l’exposition par voie cutanée à l’isobutylène sulfuré se trouve à l’annexe B.
Alimentation
L’isobutylène sulfuré peut être utilisé dans les usines de transformation des aliments au Canada, où il sert de lubrifiant pour les équipements et les machines; il ne devrait donc pas y avoir de contact avec les aliments (communication personnelle; courriel de la Direction des aliments, Santé Canada, adressé au Bureau de l’évaluation du risque des substances existantes, Santé Canada, et daté du 1er février 2019; non cité).
Environnement
L’isobutylène sulfuré n’a pas été détecté dans l’environnement au Canada ni ailleurs. Les concentrations dans l’environnement ont été modélisées à l’aide de ChemCAN (ChemCAN, 2003) et du volume total d’importation au Canada (Environnement Canada, 2013). D’après le modèle obtenu, l’exposition à l’isobutylène sulfuré dans l’air et le sol devrait être négligeable.
L’ingestion de la substance dans l’eau potable résultant d’éventuels rejets industriels a été modélisée à l’aide de la feuille de calcul sur l’eau potable de l’Unité d’évaluation environnementale (UEE) (Santé Canada, 2015a) et des quantités totales importées déclarées dans le commerce canadien en 2011 (Environnement Canada, 2013). L’information sur les paramètres du modèle se trouve dans le tableau C-1 (annexe C). La concentration maximale modélisée au 50e centile dans les eaux de surface des 10 milieux récepteurs était de 1,1 µg/L. Cette concentration dans les eaux de surface a entraîné une absorption quotidienne estimée de 2,0 × 10-5 à 1,4 × 10-4 mg/kg p.c./jour (pour les personnes de 19 ans et plus et les enfants de 0 à 5 mois nourris au lait maternisé, respectivement). Les données sur l’ingestion de la substance dans l’eau potable pour les différentes tranches d’âge se trouvent dans le tableau C-2 (annexe C). L’utilisation d’une concentration modélisée d’eau de surface pourrait donner une estimation prudente de l’absorption par l’eau potable étant donné qu’il est probable que l’eau sera traitée avant sa distribution pour la consommation.
6.2 Évaluation des effets sur la santé
L’isobutylène sulfuré a fait l’objet d’une évaluation par l’US EPA (Screening-Level Hazard Characterization) dans le cadre de son examen des sulfures d’alkyle (US EPA, 2009). L’évaluation de l’US EPA ainsi que toutes les données disponibles sur l’isobutylène sulfuré et ses analogues ont servi à caractériser les effets sur la santé.
Toxicité à doses répétées
Une étude menée avec des doses répétées sur une courte durée mesurant l’exposition par la voie cutanée sur une peau intacte ou éraflée a été réalisée chez le lapin. Les animaux de laboratoire ont été exposés pendant quatre semaines à 0, 200 ou 2 000 mg/kg p.c./jour d’isobutylène sulfuré (six animaux/sexe/dose). Une dose sans effet nocif observé (DSENO) de 200 mg/kg p.c./jour a été établie sur la base des effets hématologiques (augmentation des monocytes, du chlorure et de la globuline et diminution de l’activité de la phosphatase alcaline) à la dose suivante, soit 2 000 mg/kg p.c./jour. Une irritation grave a été observée aux deux doses, mais à la dose inférieure, elle était plus intense et a été attribuée aux éraflures (US EPA, 2009).
Une autre étude de toxicité a été menée chez des lapins blancs de Nouvelle-Zélande dans laquelle on a administré des doses répétées à court terme pour mesurer l’exposition par voie cutanée. Les lapins ont été exposés pendant trois semaines à 140, 560 ou 2 240 mg/kg p.c./jour d’isobutylène sulfuré (10 animaux/dose). Les auteurs ont établi une dose minimale avec effet observé (DMEO) de 140 mg/kg p.c./jour en fonction de signes cliniques de toxicité (érythème modéré à sévère, œdème, hyperplasie épithéliale, peau craquelée, saignement et coloration) et de la toxicité générale (AGDH, 2006). La gravité des effets était progressive sur la durée de l’étude. Les valeurs de l’analyse d’urine étaient normales dans tous les groupes, et les cas sporadiques de poumons et de foie foncés, d’intestins rouges et gonflés, de reins pâles ou de rate petite ou grise à l’autopsie n’ont pas été considérés comme liés au traitement. Pour cette étude, l’EPA (2009) a établi la DSENO à 2 240 mg/kg p.c./jour (la dose étudiée la plus élevée) en fonction de l’absence d’effet dose-dépendant dans les groupes traités et a noté que les signes cliniques observés étaient liés à la manipulation et non à la substance étudiée.
Une étude de toxicité subchronique avec doses répétées administrées par voie cutanée pour examiner les effets sur le développement a été réalisée chez des rats Sprague-Dawley. Les animaux de laboratoire ont été exposés pendant 13 semaines à 0, 500 ou 2 000 mg/kg p.c./jour d’isobutylène sulfuré non dilué et à 0, 10, 50, 100, 250 ou 500 mg/kg p.c./jour d’isobutylène sulfuré dilué dans de l’huile minérale (10 animaux/sexe/dose). Une DSENO de 100 mg/kg p.c./jour a été établie par l’auteur en fonction d’une diminution de la prise de poids corporel chez les mâles, d’une augmentation de la production de neutrophiles, d’une diminution de la production de globules rouges et d’effets locaux (réactions cutanées modérées à graves comme un érythème ou un œdème) observés chez les deux sexes à la dose subséquente, soit 250 mg/kg p.c./jour. Bien qu’une augmentation de globules blancs ait également été constatée à 100 mg/kg p.c./jour, l’US EPA ne l’a pas considérée comme étant nocive. À la concentration la plus élevée, soit 500 mg/kg p.c./jour, les effets mentionnés plus haut ont augmenté en gravité. En outre, les reins des rats mâles traités avec des doses non diluées de 500 ou 2 000 mg/kg p.c./jour présentaient un poids accru des reins corrélé avec une augmentation de la formation de gouttelettes hyalines liée à la dose. L’auteur mentionne qu’il s’agit d’un signe de néphropathie à gouttelettes hyalines (US EPA, 2009).
Aucune étude à doses répétées par voie orale n’a été trouvée pour l’isobutylène sulfuré. Les analogues alcènes C15-C18- α-sulfurés (no CAS 67762-55-4) et les polysulfures di-tert-nonyl, (no CAS 68425-16-1) ont été pris en considération en fonction des données disponibles. L’US EPA et le National Industrial Chemicals Notification and Assessment Scheme de l’Australie ont également jugé les alcènes C15-C18- α-sulfurés comme un analogue adéquat de l’isobutylène sulfuré, appartenant à la même classe de polysulfures d’alkyle (AGDH, 2006; US EPA, 2009). Le di-tert-nonyl n’a pas été inclus dans les rapports susmentionnés, mais il a été considéré comme un analogue adéquat et les données qui lui sont associées ont servi à étayer l’évaluation. Malgré des différences de structure, de propriétés physiques et chimiques et de réactivité, la plupart des alertes structurelles étaient similaires.
Selon des informations soumises dans un dossier d’enregistrement REACH, une étude préalable de toxicité à doses répétées combinée à une étude de toxicité pour la reproduction et le développement a été menée avec des alcènes C15-C18- α-sulfurés. Des rats Wistar Han (10 animaux/sexe/dose) ont reçu par voie orale 0, 100, 300 ou 1 000 mg/kg p.c./jour pendant 29 jours pour les mâles et 45 jours pour les femelles. Aucun signe clinique observable, ni aucune modification des paramètres hématologiques et de biochimie clinique, ni aucun changement microscopique et macroscopique n’ont été constatés. Une DSENO de 1 000 mg/kg p.c./jour a été établie par les auteurs, ce qui représente la dose la plus élevée à l’étude (ECHA, 2013).
D’après des données soumises dans un dossier d’enregistrement REACH, une étude préalable de toxicité à doses répétées combinée à une étude de toxicité pour le développement a été réalisée avec des polysulfures di-tert-nonyl. Des rats Sprague-Dawley (6 à 12 animaux/sexe/dose) ont reçu par gavage 0, 50, 250 ou 1 000 mg/kg p.c./jour de la substance pendant 29 jours. Le rétablissement d’un groupe satellite dans le groupe témoin et le groupe ayant reçu la dose élevée a fait l’objet d’une surveillance pendant deux semaines. Deux décès ont été constatés chez des femelles, peut-être à la suite d’une erreur de gavage; ils n’ont pas été considérés comme liés à la substance à l’étude. Aucun changement toxicologique important n’a été observé, peu importe le groupe, en ce qui concerne le poids corporel, la consommation alimentaire, l’hématologie, la chimie clinique, l’analyse d’urine, la pathologie clinique et l’histopathologie. Aucun signe clinique n’a été observé dans le groupe ayant reçu la dose la plus élevée pendant la phase d’administration de la dose et de rétablissement de l’étude. Une DSENO de 1 000 mg/kg p.c./jour a été établie par les auteurs, ce qui représente la dose la plus élevée à l’étude (ECHA, 1995).
Toxicité pour la reproduction et le développement
Aucune étude sur les effets de l’isobutylène sulfuré sur la reproduction et le développement n’a été trouvée. Les données disponibles sur les analogues 1-(tert-dodécylthio) propan-2-ol (no CAS 67124-09-8), les alcènes C15-C18- α-sulfurés (no CAS 67762-55-4) et les polysulfures di-tert-nonyl (no CAS 68425-16-1) ont été prises en considération.
Comme cela est décrit dans la section sur la toxicité à doses répétées, une étude préalable de la toxicité par voie orale pour la reproduction et le développement a été menée avec des alcènes C15-C18- α-sulfurés chez des rats Wistar Han. Les animaux de laboratoire ont été exposés pendant 29 jours pour les mâles et 45 jours pour les femelles à 0, 100, 300 ou 1 000 mg/kg p.c./jour (10 animaux/sexe/dose). Aucun effet lié au traitement sur les paramètres de reproduction, l’indice et la durée de gestation, la parturition, les soins maternels et le développement postnatal précoce des petits n’a été observé. Le poids corporel des petits est considéré comme n’ayant pas été touché par le traitement et se situait dans les valeurs historiques normales. Une DSENO de 1 000 mg/kg p.c./jour a été établie, ce qui représente la dose la plus élevée à l’étude (ECHA, 2013).
Comme cela est décrit dans la section sur la toxicité à doses répétées, une étude expérimentale de toxicité à doses répétées combinée à une étude de toxicité pour le développement par voie orale a été menée avec des polysulfures di-tert-nonyl chez des rats Sprague-Dawley. Les animaux de laboratoire ont été exposés à 50, 250 ou 1 000 mg/kg p.c./jour (25 animaux/dose) jusqu’au 20e jour de gestation. Aucun effet toxique lié au traitement chez la mère ou d’effets sur le développement n’a été observé. À la dose de 1 000 mg/kg p.c./jour, une légère augmentation de la perte post-implantation a été constatée chez une femelle, mais on croit qu’elle n’est pas liée au traitement. Une DSENO de 1 000 mg/kg p.c./jour a été établie, ce qui représente la dose la plus élevée à l’étude (ECHA, 1997).
Le 1-(tert-dodécylthio)propan-2-ol (no CAS 67124-09-8) a également été choisi comme un analogue sur la base des données disponibles et ses propriétés physico-chimiques et de réactivité semblables à celles de la substance à l’étude. Il a également été évalué par le National Industrial Chemicals Notification and Assessment Scheme et dans le cadre de la caractérisation préalable des dangers associés aux sulfures d’alkyle effectuée par l’US EPA avec l’isobutylène sulfuré.
Sur la base des données soumises dans un dossier d’enregistrement REACH, les effets du 1-(tert-dodécylthio)propan-2-ol sur la reproduction ont été examinés dans une étude de toxicité par voie orale sur une génération de rats Sprague-Dawley. Les animaux de laboratoire ont été exposés pendant trois mois à 50, 167 ou 500 mg/kg p.c./jour (28 animaux/sexe/groupe). Une DSENO de 167 mg/kg p.c./jour a été établie par les auteurs en fonction de la diminution du poids des petits à la dose suivante, soit 500 mg/kg p.c./jour, en l’absence de toxicité parentale (ECHA, 2002). Les autres paramètres examinés dans l’étude sans changements significatifs liés au traitement sont les signes cliniques, la consommation alimentaire, la fonction reproductive (cycle œstral, mesures chez les spermatozoïdes, rendement de la reproduction), la pathologie clinique et l’histopathologie des parents. Aucun effet indésirable lié au traitement sur la viabilité, les signes cliniques et la pathologie clinique des petits n’a été observé (ECHA, 2002).
Génotoxicité
Dans une étude de mutation réverse sur les bactéries in vitro, les souches TA98, TA100, TA1535, TA1537 et TA1538 de Salmonella typhimurium ont été exposées à de l’isobutylène sulfuré dans du DMSO à 0,01, 0,05, 0,1, 0,5 ou 1 μL/plaque en présence et en l’absence d’activation métabolique. L’isobutylène sulfuré n’était pas mutagène dans cet essai (US EPA, 2009).
Dans un test du micronoyau in vivo, des souris B63CF1 (5 animaux/sexe/dose) ont reçu 3 500 mg/kg p.c./jour d’isobutylène sulfuré par injection intrapéritonéale. L’isobutylène sulfuré n’a pas entraîné la formation de micronoyaux dans l’essai (EPA, 2009).
Un autre test du micronoyau in vivo a été réalisé chez des rats avec exposition par voie cutanée. Les animaux ont été exposés pendant 13 semaines à de l’isobutylène sulfuré (5 animaux/sexe/dose). Les micronoyaux ont été analysés à partir d’échantillons de moelle osseuse fémorale prélevés 24 heures après la dernière administration par voie cutanée. L’isobutylène sulfuré n’a pas entraîné la formation de micronoyaux dans l’essai (EPA, 2009).
Sur la base de ces résultats, l’isobutylène sulfuré ne devrait pas être génotoxique.
Cancérogénicité
Aucune étude sur la cancérogénicité n’a été relevée pour l’isobutylène sulfuré ni pour aucune substance analogue. Une analyse des alertes structurelles à l’aide de la Boîte à outils QSAR de l’OCDE (2016) n’a relevé aucune alerte structurelle pour la cancérogénicité de l’isobutylène sulfuré ou de ses substances analogues.
6.3 Caractérisation des risques pour la santé humaine
Le tableau 6-1 présente toutes les valeurs pertinentes d’exposition et de danger pour l’isobutylène sulfuré ainsi que les marges d’exposition qui en résultent, pour la détermination des risques.
| Scénario d’exposition | Estimation de l’exposition | Dose critique | Paramètre d’effet critique | Marge d’exposition |
|---|---|---|---|---|
|
Lubrifiant pour automobiles; voie cutanée; adulte; aiguë |
0,12 mg/kg p.c. par événement |
100 mg/kg p.c./jour (DSENO) |
En fonction d’une diminution des gains de poids corporel chez les mâles, d’une augmentation de la production de neutrophiles, d’une diminution de la production de globules rouges ainsi que des effets locaux observés à la dose suivante, soit 250 mg/kg p.c./jour, dans une étude par voie cutanée de 13 semaines. |
833 |
|
Consommation d’eau potable; voie orale; 0 à 5 mois; quotidienne |
1,4 × 10-4 mg/kg p.c./jour |
167 mg/kg p.c./jour (DSENO) |
En fonction de la diminution du poids des petits observée à la dose suivante, soit 500 mg/kg p.c./jour, dans une étude de trois mois sur la toxicité pour la reproduction par voie orale sur une génération (menée avec l’analogue 1-(tert-dodécylthio)propan-2-ol). |
> 1 000 000 |
Abréviations : ME, marge d’exposition; DSENO, dose sans effet nocif observé.
Ces marges d’exposition sont jugées adéquates pour tenir compte des incertitudes dans les bases de données relatives aux effets sur la santé et à l’exposition.
6.4 Incertitudes de l’évaluation des risques pour la santé humaine
Les principales sources d’incertitude sont présentées dans le tableau ci-dessous.
| Principale source d’incertitudes | Incidence |
|---|---|
|
Absence de détection de l’isobutylène sulfuré dans l’environnement |
+/− |
|
Aucune étude de cancérogénicité ou de chronicité trouvée pour l’isobutylène sulfuré ou l’un de ses analogues |
+/− |
|
Aucune étude sur la toxicité pour la reproduction ou le développement trouvée pour l’isobutylène sulfuré |
+/− |
+ = incertitude quant au potentiel de surestimation du risque; – = incertitude quant au potentiel de sous-estimation du risque; +/ – = potentiel de surestimation ou de sous-estimation du risque inconnu
7. Conclusion
Compte tenu de tous les éléments de preuve contenus dans la présente évaluation préalable, l’isobutylène sulfuré présente un faible risque d’effets nocifs sur l’environnement. Il est conclu que l’isobutylène sulfuré ne satisfait aux critères énoncés à l’alinéa 64a) ou 64b) de la LCPE, car il ne pénètre pas dans l’environnement en une quantité ou concentration ni dans des conditions de nature à avoir, immédiatement ou à long terme, un effet nocif sur l’environnement ou sur la diversité biologique, ou à mettre en danger l’environnement essentiel pour la vie.
À la lumière des renseignements contenus dans la présente évaluation préalable, il est conclu que l’isobutylène sulfuré ne satisfait pas aux critères de l’alinéa 64c) de la LCPE, car il ne pénètre pas dans l’environnement en une quantité ou concentration ou dans des conditions de nature à constituer un danger au Canada pour la vie ou la santé humaines.
Il est donc conclu que l’isobutylène sulfuré ne satisfait à aucun des critères énoncés à l’article 64 de la LCPE.
Références
[AGDH] Australian Government Department of Health. 2006. 1-Decene, sulfurized. Sydney (AU): Department of Health, National Industrial Chemicals Notification and Assessment Scheme (NICNAS). Full Public Report [consulté le 27 février 2019].
Canada. 1999. Loi canadienne sur la protection de l’environnement (1999). L.C. 1999, ch. 33. Gazette du Canada, partie III, vol. 22, no 3.
Canada, ministère de l’Environnement. 2012. Loi canadienne sur la protection de l’environnement (1999) : Avis concernant certaines substances de la Liste intérieure [PDF]. Gazette du Canada, partie I, vol. 146, no 48, supplément.
ChemCAN [level III fugacity model of 24 regions of Canada]. 2003. Version 6.00. Peterborough (Ontario) : Université Trent, Canadian Centre for Environmental Modelling and Chemistry.
ChemIDplus [base de données]. 1993-. Bethesda (MD) : US National Library of Medicine [consulté le 4 mars 2019].
ChemSpider [base de données]. 2015. Royal Society of Chemistry [consulté le 5 mai 2019].
[ECCC] Environnement et Changement climatique Canada. 2016a. Document sur l’approche scientifique : Classification du risque écologique des substances organiques. Ottawa (Ontario) : gouvernement du Canada.
[ECCC] Environnement et Changement climatique Canada. 2016b. Supporting documentation: data used to create substance-specific hazard and exposure profiles and assign risk classifications. Gatineau (Québec) : ECCC. Renseignements à l’appui du Document sur l’approche scientifique : Classification du risque écologique des substances organiques. Disponible sur demande : substances@ec.gc.ca.
[ECCC] Environnement et Changement climatique Canada. 2016c. Données recueillies dans le cadre d’une initiative de collecte de données ciblée pour les évaluations du Plan de gestion des produits chimiques (automne 2016). Données préparées par ECCC et Santé Canada, Programme des substances existantes.
[ECCC, SC] Environnement et Changement climatique Canada, Santé Canada [modifié le 12 mars 2017]. Catégorisation. Ottawa (Ontario) : gouvernement du Canada.
[ECHA] Agence européenne des produits chimiques. 1995. Guidance on the safe use of the substance: Polysulfides, di-tert-dodecyl; 68425-15-0 [consulté le 27 février 2019]. (disponible en anglais seulement)
[ECHA] Agence européenne des produits chimiques. 1997. Guidance on the safe use of the substance: Polysulfides, di-tert-dodecyl; 68425-15-0 [consulté le 27 février 2019]. (disponible en anglais seulement)
[ECHA] Agence européenne des produits chimiques. 2002. Guidance on the safe use of the substance: 1-(tert-dodecylthio)propan-2-ol; 67124-09-8 [consulté le 27 février 2019]. (disponible en anglais seulement)
[ECHA] Agence européenne des produits chimiques. 2013. Guidance on the safe use of the substance: Alkenes, C15-18 α-, sulfurized; 67762-55-4 [consulté le 27 février 2019]. (disponible en anglais seulement)
Environnement Canada. 2013. Données de la Mise à jour de l’inventaire de la LIS recueillies en vertu de l’article 71 de la Loi canadienne sur la protection de l’environnement de 1999 : Avis concernant certaines substances de la Liste intérieure. Données préparées par : Environnement Canada, Santé Canada; Programme des substances existantes.
[EPI Suite] Estimation Program Interface Suite for Microsoft Windows [estimation model]. c2000-2012. Vers. 4.11. Washington (DC) : United States Environmental Protection Agency. (disponible en anglais seulement)
Santé Canada. 2015a. Environmental Assessment Unit Drinking Water Spreadsheets [format Excel]. Ottawa (Ontario) : Santé Canada [consulté le 8 avril 2016].
Santé Canada. 2015b. Tableau de la consommation alimentaire obtenu à l’aide de Statistique Canada, Enquête sur la santé dans les collectivités canadiennes, Cycle 2.2, Nutrition (2004). Fichier de partage. Ottawa.
Santé Canada. 2017. Tableau de la consommation d’eau obtenu à l’aide de Statistique Canada, Enquête sur la santé dans les collectivités canadiennes, Cycle 2.2, Nutrition (2004). Fichier de partage. Ottawa.
Santé Canada. 2018. Draft backgrounder document on default values for breast milk and formula intakes. Rapport inédit. Ottawa (Ontario) : gouvernement du Canada.
Boîte à outils QSAR de l’OCDE [outil de lecture croisée]. 2016. Vers. 4.1. Paris (France) : Organisation de coopération et de développement économiques, Laboratoire de chimie mathématique.
Office of Pollution Prevention and Toxics; Syracuse (NY) : Syracuse Research Corporation.
[FDS] Fiche de données de sécurité. 2019. ValvolineMC GRAISSE TOUT-CLIMAT 10/400 G. Valvoline LLC [consulté le 1er mai 2019].
[US EPA] United States Environmental Protection Agency. 2009. Screening-Level Hazard Characterization: Alkyl Sulfides Category.
Versar, Inc. 1986. Standard scenarios for estimating exposure to chemical substances during use of consumer products. Vol. II. Consumer use of used motor oil. Springfield (VA) : Versar, Inc. Préparé pour l’United States Environmental Protection Agency.
Annexes
Annexe A. Approche par lecture croisée
| Considérations | Justification |
|---|---|
|
1) Structure chimique. L’accent a été mis sur les analogues ayant des schémas de ramification similaires (isobutyle, di-tertbutyle, isopropyle, etc.) et considérés comme des mono- ou polysulfures. Les structures chimiques contenant de la cyclicité ou des schémas de ramification complexes n’ont pas été prises en compte lors de la lecture croisée. En outre, les substances chimiques structurellement similaires contenant des groupes réactifs supplémentaires (azote, aluminium, oxygène) n’ont pas été prises en compte. |
Les analogues présentant une structure chimique similaire devraient avoir des profils de toxicité similaires. |
|
2) Alertes structurelles communes. |
Les analogues présentant des alertes structurelles similaires devraient présenter une plus grande similarité en matière de toxicité. |
|
3) Propriétés physico-chimiques similaires. L’accent a été mis sur les structures chimiques ayant des poids moléculaires, des solubilités dans l’eau, des pressions de vapeur et des log Koe similaires. |
Les analogues ayant des propriétés physico-chimiques similaires peuvent potentiellement avoir des profils toxicologiques similaires. |
|
4) Métabolisme (une analyse du métabolisme a été réalisée à l’aide de la boîte à outils de l’OCDE et OASIS TIMES). |
Les analogues ont des voies métaboliques similaires. Les principales réactions impliquent des hydroxylations ou la conversion en acides. Étant donné que toutes les substances, à l’exception du no CAS 67124-09-8, représentent des UVCB, les exercices de modélisation ont été limités aux données SMILES accessibles dans des bases de données telles que la Boîte à outils QSAR ou ChemID. |
| No CAS | 68511-50-2 | 67762-55-4 | 67124-09-8 | 68425-16-1 |
|---|---|---|---|---|
|
Nom |
2-méthylprop-1-ène sulfuré (substance cible) |
Alcènes, C15-18- α-sulfurés |
1-(tert-dodécylthio)propan-2-ol |
Polysulfures di-tert-nonyl |
|
Structure |
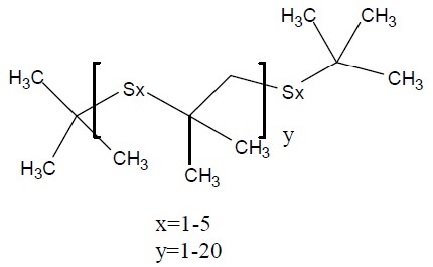 |
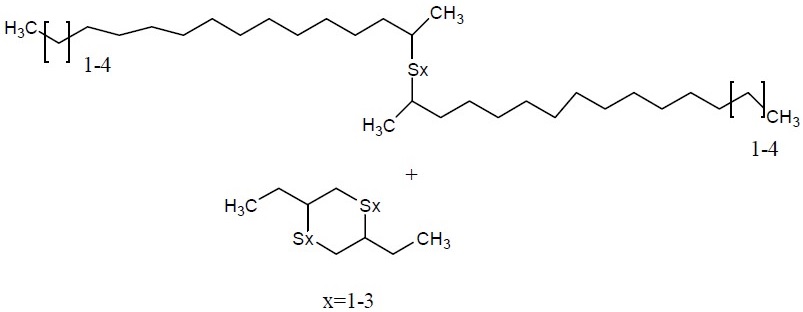 |
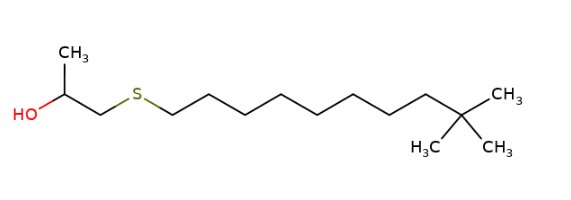 |
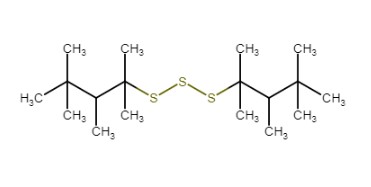 |
|
Poids moléculaire (g/mol) |
210b |
Non précisé |
260c |
Non précisé |
|
Point d’ébullition (°C) |
140d |
ND |
164a |
236a |
|
Pression de vapeur (en Pa, à 25 °C) |
1,0 × 10−6 – 2,7 d |
0,052a |
0,63a |
0a |
|
Hydrosolubilité (mg/L) à 25 °C |
6,3 × 10−6 – 2,7 d |
0,0056a |
4,84a |
2,6 × 10-4a |
|
log Koe (sans dimension) |
5,1 à > 6 d |
9,4a |
5,7a |
5,2a |
|
Toxicité à doses répétées (mg/kg p.c./jour) |
Rats – 13 semaines, voie cutanée Doses : 10, 50, 100, 250 et 500 DSENO = 100 et DMENO = 250, d’après l’observation d’une diminution de la prise de poids corporel chez les mâles et de divers effets hématologiques Lapins – 4 semaines, voie cutanée Doses : 200 et 2 000 DSENO = 200 DMENO = 2 000 en fonction des effets hématologiques et de la chimie clinique Lapins – 3 semaines, voie cutanée Doses : 140, 560 et 2 240 DMENO = 140 (longue durée) en fonction des signes cliniques et de la toxicité systémique (hyperplasie épithéliale, érythème sévère) |
Rats – 29 à 45 jours, voie orale Doses : 0, 100, 300 et 1 000 DSENO = 1000 |
- |
Rats – 29 jours, voie orale Doses : 50, 250 et 1000 DSENO = 1000 |
|
Toxicité pour la reproduction et le développement (mg/kg p.c./jour) |
- |
Toxicité pour le développement (4 mois) Doses : 100, 300 et 1000 DSENO = 1000 Aucune toxicité parentale ou pour le développement observée |
Toxicité pour la reproduction sur une génération (9 mois) Doses : 50, 167 et 500 DSENO = 167 DMENO = 500 en fonction d’une diminution significative du poids des petits |
Toxicité pour le développement Doses : 50, 250 et 1000 DSENO = 1000 Aucun effet lié au traitement n’a été observé pour ce qui est de la toxicité maternelle, de l’embryofœto-toxicité ou des effets tératogènes |
|
Génotoxicité |
Négatif Non mutagène, non cytotoxique |
S. o. |
S. o. |
S. o. |
|
Cancérogénicité (mg/kg p.c./jour) |
S. o. |
S. o. |
S. o. |
S. o. |
Abréviations : PM, poids moléculaire; Koe, coefficient de partage octanol-eau; ND, non disponible; S. o., sans objet; DSENO, dose sans effet nocif observé; DMENO, dose minimale avec effet nocif observé
a ECHA
b Boîte à outils QSAR, 2004-
c ChemIDplus, 1993-
d US EPA
Annexe B. Paramètres d’estimation de l’exposition par les produits de consommation au Canada
Les estimations de l’exposition ont été calculées en fonction d’un poids corporel de 74 kg pour une personne de 19 ans et plus (Santé Canada, 2015b). Les paramètres de l’exposition estimée par voie cutanée pour les produits offerts aux consommateurs sont décrits dans le tableau B-1.
| Produit (substance) | Hypothèses |
|---|---|
|
Lubrifiant pour automobiles |
Scénario de produit : application de lubrifiant – petite tâche (bout des doigts, deux mains) (Versar inc., 1986) Par voie cutanée Exposition quotidienne estimée par voie cutanée : C (concentration d’isobutylène sulfuré) = 5 % (FDS, 2019) |
Annexe C. Paramètres pour estimer l’exposition par l’eau potable
| Paramètre | Donnée |
|---|---|
|
Scénario |
Rejet industriel |
|
Taux d’élimination de l’usine de traitement des eaux usées (%) |
62,89a |
|
Nombre de sites industriels |
1b |
|
Nombre de jours de rejet (par année) |
250b |
|
Rejet quotidien dans les eaux usées (%) |
4c |
|
Débit du milieu récepteur (m³/s) |
21b |
a ECCC, 2016a.
b Valeur par défaut de la feuille de calcul sur l’eau potable de l’UEE pour le milieu récepteur qui présente la concentration la plus élevée dans les eaux de surface.
c En fonction d’un taux de 3 % de résidus dans les contenants et de 1 % de résidus dans les canalisations de transfert ou la machinerie de traitement pour une substance liquide.
| Groupe d’âge | Exposition par l’eau potable (mg/kg p.c./jour)a, b |
|---|---|
|
0 à 5 mois (allaitement au sein)c, d |
S. o. |
|
0 à 5 mois (allaitement au sein)c, e |
1,4 x 10-4 |
|
6 à 11 moisf |
9,0 x 10-5 |
|
1 ang |
4,0 x 10-5 |
|
2 à 3 ansh |
3,0 x 10-5 |
|
4 à 8 ansi |
2,0 x 10-5 |
|
9 à 13 ansj |
2,0 x 10-5 |
|
14 à 18 ansk |
2,0 x 10-5 |
|
19 ans et plusl |
2,0 x 10-5 |
Abréviations : S. O., sans objet.
a Basé sur une estimation de la concentration dans les eaux de surface modélisée à partir de la feuille de calcul sur l’eau potable de l’UEE en utilisant les paramètres du tableau C-1.
b L’utilisation d’une concentration modélisée d’eau de surface aura tendance à surestimer l’ingestion de la substance dans l’eau potable étant donné que l’eau devrait être traitée avant sa distribution pour la consommation.
c Poids supposé de 6,3 kg (Santé Canada, 2015b).
d On présume que les nourrissons allaités exclusivement consomment 0,744 L de lait maternel par jour (Santé Canada, 2018), et on présume que le lait maternel constitue la seule source alimentaire.
e On présume que les nourrissons nourris à la préparation exclusivement consomment 0,826 L d’eau par jour (Santé Canada, 2018), qui est utilisée pour reconstituer la préparation.
f Poids supposé de 9,1 kg (Santé Canada, 2015b). Pour les nourrissons allaités, on présume qu’ils consomment 0,632 L de lait maternel par jour (Santé Canada, 2018). Pour les nourrissons nourris à la préparation, on présume qu’ils consomment 0,764 L d’eau par jour (Santé Canada, 2018), eau servant à reconstituer la préparation.
g Poids supposé de 11,0 kg (Santé Canada, 2015b) et consommation d’eau établie à 0,36 L par jour (Santé Canada, 2017).
h Poids supposé de 15 kg (Santé Canada, 2015b) et consommation d’eau établie à 0,43 L par jour (Santé Canada, 2017).
i Poids supposé de 23 kg (Santé Canada, 2015b) et consommation d’eau établie à 0,53 L par jour (Santé Canada, 2017).
j Poids supposé de 42 kg (Santé Canada, 2015b) et consommation d’eau établie à 0,74 L par jour (Santé Canada, 2017).
k Poids supposé de 62 kg (Santé Canada, 2015b) et consommation d’eau établie à 1,09 L par jour (Santé Canada, 2017).
l Poids supposé de 74 kg (Santé Canada, 2015b) et consommation d’eau établie à 1,53 L par jour (Santé Canada, 2017).
