Évaluation préalable pour le Défi concernant l'acétate de 2-éthoxyéthyle
Numéro de registre du Chemical Abstracts Service 111-15-9
Environnement Canada
Santé Canada
Février 2009
Table des matières
- Synopsis
- Introduction
- Identité de la substance
- Propriétés physiques et chimiques
- Sources
- Utilisations
- Rejets dans l'environnement
- Devenir dans l'environnement
- Persistance et potentiel de bioaccumulation
- Potentiel d'effets nocifs sur l'environnement
- Potentiel d'effets nocifs sur la santé humaine
- Conclusion
- Références
- Annexe 1. Concentration d'acétate de 2-éthoxyéthyle dans les produits de consommation 1 selon le modèle ConsExpo 4.1 (RIVM, 2006)
- Annexe 2. Sommaire 1 des renseignements au sujet des effets de l'acétate de 2-éthoxyéthyle (no CAS 111-15-9) sur la santé
Synopsis
Conformément à l'article 74 de la Loi canadienne sur la protection de l'environnement (1999) [LCPE (1999)], les ministres de l'Environnement et de la Santé ont effectué une évaluation préalable de l'acétate de 2-éthoxyéthyle, dont le numéro de registre du Chemical Abstracts Service est 111-15-9. Une priorité élevée a été accordée à la prise de mesures à l'égard de cette substance lors de la catégorisation visant la Liste intérieure dans le cadre du Défi, car on considère que l'acétate de 2-éthoxyéthyle présente le plus fort risque d'exposition pour les particuliers au Canada et il a été classé sur la base de sa toxicité sur le plan du développement et de la reproduction par la Commission européenne. La substance ne répondait pas aux critères environnementaux de la catégorisation relatifs à la persistance, au potentiel de bioaccumulation et à la toxicité intrinsèque pour les organismes aquatiques. Par conséquent, la présente évaluation de l'acétate de 2-éthoxyéthyle porte principalement sur les risques pour la santé humaine.
Selon les renseignements déclarés conformément à l'article 71 de la LCPE (1999), la fabrication de l'acétate de 2-éthoxyéthyle au Canada pendant l'année civile 2006 n'a pas dépassé le seuil de déclaration de 100 kg par année. Au total, selon les quantités déclarées en 2006, entre 10 000 et 100 000 kg ont été importés au Canada. L'acétate de 2-éthoxyéthyle est principalement utilisé dans les solvants, les peintures, les revêtements et les solutions de nettoyage dans les milieux industriels.
On suppose que l'exposition de la population à l'acétate de 2-éthoxyéthyle se fait principalement par l'air. D'après les renseignements très limités dont on dispose sur les concentrations dans les milieux environnementaux et les résultats de la modélisation de la fugacité de cette substance, l'exposition dans l'environnement global devrait être faible. Même si l'acétate de 2-éthoxyéthyle est principalement utilisé dans les milieux industriels, l'exposition des consommateurs serait faible. Les observations faites chez les animaux de laboratoire et les travailleurs exposés montrent que les effets sur la santé associés à l'exposition à l'acétate de 2-éthoxyéthyle sont principalement liés à la toxicité sur le plan du développement et de la reproduction et au système hématologique. La marge entre l'estimation de la limite supérieure des concentrations dans l'air intérieur et les concentrations entraînant des effets chez les humains exposés professionnellement et les animaux de laboratoire est considérée suffisamment protectrice.
Étant donné que les marges entre les estimations prudentes de l'exposition à l'acétate de 2-éthoxyéthyle lors de l'utilisation des produits, d'une part, et les concentrations entraînant des effets critiques chez les travailleurs exposés et les animaux de laboratoire, d'autre part, pourraient être adéquates, on conclut que l'acétate de 2-éthoxyéthyle ne pénètre pas dans l'environnement en une quantité ou concentration ou dans des conditions de nature à constituer un danger au Canada pour la vie ou la santé humaines.
D'après les faibles risques pour l'environnement que présentent l'acétate de 2-éthoxyéthyle et ses rejets attendus et compte tenu de la faible exposition de l'environnement à cette substance, celle-ci ne pénètre pas dans l'environnement en une quantité ou concentration ou dans des conditions de nature à avoir, immédiatement ou à long terme, un effet nocif sur l'environnement ou sur la diversité biologique, ou encore à mettre en danger l'environnement essentiel pour la vie. L'acétate de 2-éthoxyéthyle ne remplit pas les critères de la persistance et du potentiel de bioaccumulation énoncés dans le Règlement sur la persistance et la bioaccumulation.
Cette substance s'inscrira dans la prochaine mise à jour de l'inventaire de la Liste intérieure des substances (LIS). De plus, des activités de recherche et de surveillance viendront, s'il y a lieu, appuyer la vérification des hypothèses formulées au cours de l'évaluation préalable et, le cas échéant, l'efficacité des mesures de contrôle possibles définies à l'étape de la gestion des risques.
Compte tenu des renseignements disponibles, l'acétate de 2-éthoxyéthyle ne remplit aucun des critères de l'article 64 de la LCPE (1999).
Introduction
La Loi canadienne sur la protection de l'environnement (1999) [LCPE (1999)] (Canada , 1999) impose aux ministres de l'Environnement et de la Santé de procéder à une évaluation préalable des substances qui répondent aux critères de catégorisation énoncés dans la Loi, afin de déterminer si elles présentent ou sont susceptibles de présenter un risque pour l'environnement ou la santé humaine. Selon les résultats de cette évaluation, les ministres peuvent proposer de ne rien faire à l'égard de la substance, de l'inscrire sur la Liste des substances d'intérêt prioritaire (LSIP) en vue d'une évaluation plus détaillée, ou de recommander son inscription sur la Liste des substances toxiques de l'annexe 1 de la Loi et, s'il y a lieu, sa quasi-élimination.
En se fondant sur l'information fournie dans le cadre de la catégorisation, les ministres ont jugé qu'une attention hautement prioritaire devait être accordée à un certai n nombre de substances, à savoir :
- celles qui répondent à tous les critères environnementaux de la catégorisation, notamment la persistance (P), le potentiel de bioaccumulation (B) et la toxicité intrinsèque (Ti) pour les organismes aquatiques, et que l'on croit être commercialisées;
- celles qui répondent aux critères de la catégorisation pour le plus fort risque d'exposition (PFRE) ou qui présentent un risque d'exposition intermédiaire (REI) et qui ont été jugées particulièrement dangereuses pour la santé humaine, compte tenu du classement attribué par d'autres organismes nationaux ou internationaux quant à la cancérogénicité, la génotoxicité ou la toxicité sur le plan du développement ou de la reproduction.
Le 9 décembre 2006, les ministres ont donc publié un avis d'intention dans la Partie I de la Gazette du Canada (Canada , 2006) dans lequel ils priaient l'industrie et les autres parties intéressées de fournir, selon un calendrier déterminé, des renseignements précis qui pourraient servir à étayer l'évaluation des risques, ainsi qu'à élaborer et à évaluer les meilleures pratiques de gestion des risques et de bonne gestion des produits pour ces substances jugées hautement prioritaires.
L'acétate de 2 éthoxyéthyle est une substance dont l'évaluation des risques pour la santé humaine a été jugée hautement prioritaire, car on considère qu'il présente le PFRE et il a été classé par d'autres organismes sur la base de sa toxicité sur le plan du développement et de la reproduction.
Le volet du Défi portant sur cette substance a été lancé le 18 août 2007 au moyen d'un avis paru dans le Gazette du Canada (Canada, 2007a). En même temps a été publié le profil de la substance, qui présentait l'information technique (obtenue avant décembre 2005) sur laquelle a reposé sa catégorisation. De nouveaux renseignements sur la substance ont été communiqués en réponse au Défi (Environnement Canada, 2008).
Même si l'évaluation des risques que présente l'acétate de 2 éthoxyéthyle pour la santé humaine a été jugée hautement prioritaire, cette substance ne répond pas aux critères relatifs à la persistance, au potentiel de bioaccumulation ou à la toxicité intrinsèque pour les organismes aquatiques. La présente évaluation est donc axée principalement sur les renseignements présentant de l'intérêt pour l'évaluation des risques touchant la santé humaine.
Les évaluations préalables effectuées aux termes de la LCPE (1999) mettent l'accent sur les renseignements essentiels pour déterminer si une substance répond aux critères de toxicité des substances chimiques au sens de l'article 64 de la Loi :
« 64. [...] est toxique toute substance qui pénètre ou peut pénétrer dans l'environnement en une quantité ou concentration ou dans des conditions de nature à :
- avoir, immédiatement ou à long terme, un effet nocif sur l'environnement ou sur la diversité biologique;
- mettre en danger l'environnement essentiel pour la vie; ou
- constituer un danger au Canada pour la vie ou la santé humaines. »
Les évaluations préalables visent à examiner des renseignements scientifiques et à tirer des conclusions fondées sur la méthode du poids de la preuve et le principe de prudence, conformément aux dispositions de la LCPE (1999).
La présente évaluation préalable prend en considération les renseignements sur les propriétés chimiques, les dangers, les utilisations et l'exposition, y compris ceux fournis dans le cadre du Défi. Les données pertinentes pour l'évaluation préalable de l'acétate de 2 éthoxyéthyle ont été trouvées dans des publications originales, des rapports de synthèse et d'évaluation et des rapports de recherche de parties intéressées ainsi que d'autres documents consultés lors de recherches documentaires menées récemment, jusqu'en décembre 2007 (exposition) et jusqu'en septembre 2007 (effets sur la santé). Les études importantes ont fait l'objet d'une évaluation critique; les résultats de la modélisation ont pu être utilisés dans la formulation des conclusions. L'évaluation des risques pour la santé humaine comprend l'examen des données pertinentes à l'évaluation de l'exposition (non professionnelle) de la population dans son ensemble et des renseignements sur les dangers pour la santé (principalement fondés sur des évaluations réalisées par d'autres organismes suivant la méthode du poids de la preuve et ayant servi à déterminer le caractère prioritaire de la substance). Les décisions concernant la santé humaine reposent sur la nature de l'effet critique retenu et/ou sur l'écart entre les valeurs prudentes des concentrations entraînant un effet et les estimations de l'exposition, en tenant compte de la confiance accordée au caractère exhaustif des bases de données sur l'exposition et les effets dans le contexte d'une évaluation préalable. La présente évaluation préalable ne constitue pas un examen exhaustif ou critique de toutes les données disponibles. Elle fait plutôt état des éléments d'information les plus importants pour appuyer la conclusion.
La présente ébauche d'évaluation préalable a été préparée par le personnel du Programme d'évaluation des substances existantes de Santé Canada et d'Environnement Canada et elle intègre les résultats d'autres programmes exécutés par ces ministères. Cette évaluation préalable a fait l'objet d'une consultation indépendante par des pairs. Des commentaires sur les portions techniques concernant la santé humaine ont été reçus d'experts scientifiques désignés et dirigés par la Toxicology Excellence for Risk Assessment (TERA), notamment John Christopher (California Department of Toxic Substances Control), Michael Jayjock (The Lifeline Group) et Joan Strawson (TERA). Des commentaires concernant ces sections ont aussi été reçus de ToxEcology - Environmental Consulting Ltd. Bien que les commentaires externes aient été pris en considération, Santé Canada et Environnement Canada assument la responsabilité du contenu final et des résultats de l'évaluation préalable. De plus, une version provisoire de la présente évaluation préalable a fait l'objet d'une consultation publique de 60 jours. Bien que les commentaires externes aient été pris en considération, Santé Canada et Environnement Canada assument la responsabilité du contenu final et des résultats de l'évaluation préalable. Les principales données et considérations sur lesquelles repose la présente évaluation sont résumées ci-après.
Identité de la substance
L'acétate de 2-éthoxyéthyle est l'ester du 2-éthoxyéthanol (Wenninger et McEwen, 1997). Les acétates de l'éther monoalkylique de l'éthylèneglycol, comme l'acétate de 2-éthoxyéthyle, sont habituellement produits par estérification de l'éther glycolique particulaire avec de l'acide acétique, de l'anhydride de l'acide acétique ou du chlorure (NIOSH, 1991). L'acétate de 2 -éthoxyéthyle est défini comme un liquide incolore à l'odeur caractéristique douce et fruitée (Commission européenne, 2005). C'est aussi un produit soluble dans l'eau (Nikitakis et McEwen, 1990). Des renseignements additionnels sur l'identité de l'acétate de 2 éthoxyéthyle sont présentés dans le tableau 1.
| Numéro de registre du Chemical Abstracts Service (no CAS) | 111-15-9 |
|---|---|
| Nom dans la LIS | Acétate de 2-éthoxyéthyle |
| Noms relevés dans les National Chemical Inventories (NCI)Note de bas de tableau a | Ethanol, 2-ethoxy-, 1-acetate (TSCA) Acétate de 2-éthoxyéthyle (EINECS) |
| Autres noms | Ethyleneglycol monoethyl ether acetate; Cellosolve acetate; Acetate, ethoxyethyl; Acetate, 2-ethoxyethyl; 2-Ethoxyethanol Acetate; 2-Ethoxyethylethanoate; 2-Ethoxyethyl acetone; 1-Acetoxy-2-ethoxyethane; 2-Ethoxy acetate; 2-Ethoxyethanol acetate; 2-Ethoxyethanol acetate ester; Acetic acid, 2-ethoxyethyl ester; Ethyl cellosolve acetate; Ethyl glycol acetate; Ethylene glycol acetate monoethyl ether; Ethylene glycol ethyl ether acetate; Ethylene glycol monoethyl ether monoacetate; Glycol monoethyl ether acetate; O-Ethylglycol acetate; Oxitol acetate; Poly-Solv EE acetate |
| Groupe chimique (groupe de la LIS) |
Produits chimiques organiques |
| Sous-groupe chimique | Esters |
| Formule chimique | C6H12O3 |
| Structure chimique | 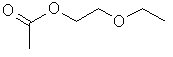 |
| Simplified Molecular Input Line Entry System (SMILES) | O=C(OCCOCC)C |
| Masse moléculaire | 132,16 g/mol |
Propriétés physiques et chimiques
Le tableau 2 résume les propriétés physiques et chimiques (valeurs expérimentales et modélisées) de l'acétate de 2-éthoxyéthyle.
| Type | Valeur | Température (°C)Note de bas de tableau b | RéférencesNote de bas de tableau c | |
|---|---|---|---|---|
| Point de fusion (°C) | expérimental | -61,7 | PhysProp, 2006; Lewis, 2007 |
|
| Point d'ébullition (°C) | expérimental | 156; 156,4 | PhysProp, 2006; Budavari, 1996 |
|
| Masse volumique | 0,9730; 0,975 | 20; 25 | Kirk-Othmer, 1980; Budavari, 1996 | |
| Pression de vapeur (Pa) | expérimental | 270; 326,64 | 20; 25 | Kirk-Othmer. 1980; Daubert et Danner, 1989 |
| Constante de la loi de Henry (Pa·m3/mol) |
expérimental | 3,24 × 10-4 (3,2 × 10-6 atm·m3/mol)Note de bas de tableau d |
25 | PhysProp, 2006; |
| Log Koe (coefficient de partage octanol/eau) (sans dimension) |
expérimental | 0,24 | Hüls, 1989a | |
| Log Kco (coefficient de partage carbone organique/eau) (sans dimension) |
modélisé | 0,32 | 25 | PCKOCWIN, 2000 |
| Log Kco (sans dimension) |
modélisé | 1,62 | 25 | ACD, 2007 |
| Solubilité dans l'eau (mg/L) | expérimental | 2,47 × 105 | 15 à 25 | Yalkowsky et Dannenfelser, 1992 |
| Solubilité dans l'eau (mg/L) | expérimental | 2,29 × 105 | 20 | Kirk-Othmer, 1980 |
Sources
La plupart des rapports produits ont permis d'observer que l'acétate de 2 éthoxyéthyle ne devrait pas être présent naturellement dans l'environnement (Commission européenne , 2005; IPCS , 1990; NPI , 2006), mais une étude a révélé des émissions biogéniques rejetées par certaines essences de bois dans la région méditerranéenne (Peñuelas et Llusià, 2001).
Les sources anthropiques d'acétate de 2 éthoxyéthyle comprennent notamment les procédés de fabrication d'acétates par estérification normale du 2 éthoxyéthanol avec de l'anhydride de l'acide acétique ou acide de chlorure, et avec un catalyseur acide (OMS , 1990; Kirk Othmer, 1980).
D'après les renseignements fournis en réponse à une enquête effectuée en application de l'article 71 de la LCPE (1999), l'acétate de 2 éthoxyéthyle n'a pas été fabriqué au Canada en 2006 en une quantité dépassant le seuil de déclaration de 100 kg. La quantité totale importée au Canada au cours de la même année civile se situait entre 10 000 et 100 000 kg (Environnement Canada, 2008).
Tous les fabricants d'acétate de 2-éthoxyéthyle de l'Union européenne ont mis un terme à leur production en 2002, et il n'est pas attendu que la production ou l'importation de cette substance ne reprennent (Commission européenne, 2006).
Utilisations
Les éthers glycoliques font en général l'objet d'une vaste gamme d'utilisations. On les trouve notamment comme agents de couplage dans diverses spécialités chimiques et comme intermédiaires dans la fabrication de plastifiants et de solvants. L'acétate de 2-éthoxyéthyle est largement utilisé comme solvant industriel pour décaper les laques et les vernis, comme retardateur résistant à l'opalescence et comme solvant pour la nitrocellulose, les huiles, les résines, les colorants, les peintures et les teintures. Il est aussi utilisé dans les procédés photographiques et photolithographiques et sert de solvant générique dans une grande variété d'agents nettoyants (IPCS, 1990). De plus, il entre dans la composition des laques pour automobiles pour retarder l'évaporation et donner un lustre très brillant. Sa fonction première consiste à dissoudre les constituants des mélanges dans les systèmes aqueux et non aqueux, et à conserver les mélanges en solution jusqu'aux derniers stades d'évaporation (Montgomery, 2000; NPI, 2006). Il peut aussi servir à la fabrication d'adhésifs et dans l'industrie des semiconducteurs (ACGIH, 1991; Kim et al,. 1999; NPI, 2006). Comme substance chimique intermédiaire, l'acétate de 2 éthoxyéthyle pourrait être utilisé dans la synthèse du 2 éthoxyéthylcyanoacrylate, qui entre dans la fabrication des cyanoacrylates à faible odeur (HSDB, 2005).
D'après les déclarations faites en conformité avec l'article 71 de la LCPE (1999), les utilisations de l'acétate de 2 éthoxyéthyle au Canada comprennent la fabrication de solvants, de peintures, de revêtements et de solutions de nettoyage à des fins industrielles (Environnement Canada, 2008).
L'acétate de 2 éthoxyéthyle figure sur la liste des matières utilisées pour la fabrication d'adhésifs, lesquels peuvent entrer dans la composition d'articles destinés à emballer, à transporter ou à contenir des aliments aux États -Unis (U S FDA, 2007). Bien qu'il ait aussi été utilisé comme solvant dans la fabrication de revêtements et d'adhésifs dans le secteur de l'emballage des aliments au Canada dans le passé (il y a quinze ans), aucune utilisation actuelle connue de cette substance dans ce secteur au Canada n'est reconnue (communication personnelle avec la Section des matériaux d'emballage alimentaire et des additifs indirects de la Direction générale des produits de santé et des aliments de Santé Canada le 18 avril 2008; non référencée).
L'acétate de 2-éthoxyéthyle figure dans l'International Cosmetic Ingredient Dictionary and Handbook en tant que solvant et agent diminuant la viscosité (Wenninger et McEwen, 1997). Pendant longtemps, l'acétate de 2-éthoxyéthyle a été utilisé dans les produis de maquillage pour les yeux (30 à 100 %) et dans les hydratants pour la peau (1 à 3 %). Toutefois, l'utilisation d'acétate de 2 éthoxyéthyle et de 2 éthoxyéthyle est aujourd'hui interdite dans la fabrication de cosmétiques au Canada (SDC, 2008), de même que dans l'Union européenne (Commission européenne, 1999).
L'utilisation d'éthers glycoliques constitués d'hydrocarbure aliphatique à chaîne droite et courte comprenant de l'acétate de 2 éthoxyéthyle et du 2 éthoxyéthyle, a progressivement diminué au cours des 20 dernières années à l'échelle mondiale (Johanson et Rick, 1996; De Kettenis, 2005; US EPA, 2005). La United States Environmental Protection Agency (EPA) a indiqué que l'acétate de 2 éthoxyéthyle et le 2 éthoxyéthanol n'entraient plus dans la fabrication de produits destinés à la consommation aux États-Unis et qu'un avis doit être publié pour toute nouvelle utilisation importante de ces substances (US EPA, 2005).
Rejets dans l'environnement
La plus importante exposition à l'acétate de 2-éthoxyéthyle dans l'environnement est causée par son rejet direct dans l'atmosphère lorsqu'il est utilisé comme solvant à évaporation (IPCS, 1990). Le tableau 3 présente le sommaire des rejets relevés dans l'Inventaire national des rejets polluants (INRP) entre 1994 et 2006 (INRP, 2007). Le total des rejets sur place signalés concernent principalement les rejets atmosphériques. L'augmentation de la quantité de rejets d'acétate de 2-éthoxyéthyle au cours des dernières années est principalement causée par une société ontarienne.
| Année de déclaration | Nombre d'entreprises ayant présenté une déclaration | Total des rejets sur place (tonnes) | Année de déclaration | Nombre d'entreprises ayant présenté une déclaration | Total des rejets sur place(tonnes) |
|---|---|---|---|---|---|
| 2006 | 2 | 1,4 | 1999 | 6 | 4,4 |
| 2005 | 1 | 1,6 | 1998 | 6 | 4,4 |
| 2004 | 2 | 1,8 | 1997 | 8 | 33 |
| 2003 | 3 | 1,5 | 1996 | 6 | 0,31 |
| 2002 | 3 | 0,13 | 1995 | 7 | 4,4 |
| 2001 | 4 | 0,12 | 1994 | 3 | 0,00 |
| 2000 | 4 | 0,15 |
Devenir dans l'environnement
Un modèle de fugacité de niveau III a été utilisé en fonction des propriétés physicochimiques de la substance (tableau 2). Les résultats sont présentés dans le tableau 4 et indiquent que l'acétate de 2-éthoxyéthyle devrait demeurer en grande partie dans le milieu où il est rejeté.
| Fraction de la substance se répartissant dans l'air (%) | Fraction de la substance se répartissant dans l'eau (%) | Fraction de la substance se répartissant dans le sol (%) | Fraction de la substance se répartissant dans le sédiment (%) | |
|---|---|---|---|---|
| Rejets de la substance dans l'air (100%) | 50,8 | 19,5 | 29,7 | 0,03 |
| Rejets de la substance dans l'eau (100%) | 0,02 | 99,8 | 0,01 | 0,17 |
| Rejets de la substance dans le sol (100%) | 0,15 | 21,1 | 78,7 | 0,04 |
Persistance et potentiel de bioaccumulation
Persistance
Une fois libéré dans l'environnement, l'acétate de 2-éthoxyéthyle ne devrait pas être persistant dans l'air, l'eau, le sol ou les sédiments. Le tableau 5 présente un résumé des prévisions sur la persistance fondées sur des données modélisées et empiriques.
| Processus du devenir | Type de données | Valeur pour la dégradation | Paramètre/unités | Références |
|---|---|---|---|---|
| Biodégradation | modélisé | 0,823 | t½ (jours) | AOPWIN, 2000 |
| Réaction avec les OH dans l'air |
empirique | 0,45 | t½ (jours) | Atkinson, 1989 |
| Biodégradation dans l'eau |
modélisé | 15 | t½ (jours) | BIOWIN, 2000 (modèle d'enquête sur la dégradation ultime) |
| Biodégradation dans l'eau |
modélisé | 0,915 | probabilité | BIOWIN, 2000 (modèle non linéaire Ministry of International Trade and Industry, Japon (MITI)) |
L'acétate de 2-éthoxyéthyle réagit sous l'effet des rayons du soleil et au contact d'autres substances chimiques présentes dans l'atmosphère, et se décompose habituellement en hydroesters, en hydroxyacides, en hydroxycarbonyles, en nitrates de peroxyacétyle et en formaldéhyde (NPI, 2006). Une réactivité photochimique élevée de l'acétate de 2 éthoxyéthyle a aussi été observée en présence de d'oxydes d'azote lors d'essais en chambres à smog (Yanagihara et al., 1977).
La majeure partie des rejets d'acétate de 2-éthoxyéthyle devrait se déposer au sol et dans l'eau par l'intermédiaire des précipitations, car la phase gazeuse de la substance se dissout dans l'eau à son contact (NPI, 2006). La substance devrait s'hydrolyser rapidement pour ensuite se biodégrader en dioxyde de carbone et en eau dans des conditions aérobies. Dans des conditions anaérobies, les principaux produits terminaux de l'acétate de 2-éthoxyéthyle sont le méthane et le dioxyde de carbone (IPCS, 1990). Dans le sol, l'acétate de 2-éthoxyéthyle est décomposé par les bactéries (NPI, 2006).
D'après un ratio d'extrapolation de 1:1:4 de la demi-vie de biodégradation dans l'eau, le sol et les sédiments (Boethling et al., 1995), la demi-vie dans le sol est inférieure à 182 jours, alors que celle dans les sédiments est inférieure à 365 jours. Cela indique que l'acétate de 2 éthoxyéthyle ne devrait pas être persistant dans le sol, ni dans les sédiments.
Si l'on applique la méthode du poids de la preuve aux données figurant ci-dessus, l'acétate de 2 éthoxyéthyle ne répond pas au critère de la persistance tel qu'il est défini dans le Règlement sur la persistance et la bioaccumulation (Canada, 2000), et ce, ni pour l'air (demi-vie supérieur(e) ou égal(e) à 2 jours), ni pour l'eau ou le sol (demi-vie supérieur(e) ou égal(e) à 182 jours), ni pour les sédiments (demi-vie supérieur(e) ou égal(e) à 365 jours).
Potentiel de bioaccumulation
Les données modélisées sur le potentiel de bioaccumulation de l'acétate de 2-éthoxyéthyle présentées au tableau 6 indiquent que cette substance ne devrait pas se bioaccumuler dans l'environnement.
| Paramètre | Valeur en poids humide (L/kg) |
Références |
|---|---|---|
| Facteur de bioaccumulation (FBA) | 1,18 | Gobas FBA T2MTL (Arnot et Gobas, 2003) |
| Facteur de bioconcentration (FBC) | 1,15 | Gobas FBC 5 % T2LTL (Arnot et Gobas, 2003) |
| FBC | 1,29 | ACD, 2007 |
| FBC | 14,37 | OASIS Forecast, 2005 |
| FBC | 3,16 | BCFWIN, 2000 |
Le modèle modifié du facteur de bioaccumulation (FBA; aussi appelé BAF) de Gobas pour le niveau trophique intermédiaire, chez les poissons, donne un FBA de 1,18 L/kg en poids humide, ce qui indique une faible probabilité de bioconcentration ou de bioamplification de cette substance dans l'environnement. Les modèles du facteur de bioconcentration (FBC) fournissent aussi un élément du poids de la preuve à l'appui du faible potentiel de bioconcentration de la substance.
Si on applique la méthode du poids de la preuve, l'acétate de 2 éthoxyéthyle ne répond pas au critère de la bioaccumulation (FBC, FBA supérieur(e) ou égal(e) à 5 000) tel qu'il est défini dans le Règlement sur la persistance et la bioaccumulation (Canada, 2000).
Potentiel d'effets nocifs sur l'environnement
Tel qu'il est indiqué ci- après dans la section de l'évaluation de l'exposition pour la santé humaine, les concentrations de l'acétate de 2 éthoxyéthyle sont prévues être faibles dans l'air, l'eau et le sol.
Les résultats expérimentaux sur la toxicité aquatique présentés au tableau 7 indiquent que les valeurs de CL50 létales médianes aiguës étaient de beaucoup supérieures à 1,0 mg/L, ce qui montre que l'acétate de 2 éthoxyéthyle n'est pas nocif pour les organismes aquatiques à des concentrations relativement faibles. La fourchette des valeurs prévues dans le tableau 7 indique que la toxicité aiguë de l'acétate de 2 éthoxyéthyle est faible à modérée pour les organismes aquatiques, et qu'il est peu probable que cette substance nuise les organismes aquatiques à des concentrations relativement faibles.
| Organisme d'essai | Type d'essai | Paramètre | Valeur (mg/L) |
|---|---|---|---|
| Daphnia | aiguë | CL502 | 560 |
| Crevette | aiguë | CL50 | 4 000 |
| Poisson | aiguë | CL50 | 40 à 197 |
Les rejets déclarés d'acétate de 2 éthoxyéthyle sont essentiellement dans l'air. Lorsque l'acétate de 2 éthoxyéthyle se libère dans l'atmosphère, il se disperse rapidement et les concentrations résultantes dans l'air sont faibles. Étant donné que les rejets atmosphériques provenant de produits finis qui contiennent cette substance seraient diffus à partir d'un grand nombre de petites sources plutôt que de quelques importantes sources ponctuelles, les concentrations résultantes d'acétate de 2 éthoxyéthyle dans l'air seraient faibles. Puisque les rejets dans l'eau déclarés sont faibles, on peut donc conclure que l'exposition des organismes aquatiques à l'acétate de 2 éthoxyéthyle serait minime.
Comme il est indiqué précédemment, l'acétate de 2- éthoxyéthyle ne remplit pas les critères de la persistance ou du potentiel de bioaccumulation tels qu'ils sont définis dans le Règlement sur la persistance et la bioaccumulation (Canada, 2000). D'après les données disponibles, il est improbable que l'acétate de 2-éthoxyéthyle ait des effets nuisibles sur l'environnement au Canada.
Incertitudes dans l'évaluation des risques pour l'environnement
On s'est servi de modèles de relation quantitative structure-activité (RQSA) pour estimer la persistance et la bioaccumulation. Or, l'utilisation de ces modèles à cette fin comporte des incertitudes. En outre, la valeur du Koe, qui est une donnée d'entrée pour les modèles RQSA, a aussi été estimée.
Il existe une incertitude concernant l'exposition à l'acétate de 2 éthoxyéthyle, mais on suppose que les concentrations dans les différents milieux naturels sont faibles.
Potentiel d'effets nocifs sur la santé humaine
Évaluation de l'exposition
Les estimations concernant l'absorption d'acétate de 2-éthoxyéthyle dans divers milieux n'ont pas été calculées pour cette évaluation à cause d'un manque de données. Aucune donnée n'a été trouvée sur les concentrations d'acétate de 2 éthoxyéthyle dans l'environnement au Canada, sauf dans une étude sur l'air ambiant menée à Windsor, en Ontario, pendant laquelle on a observé que la concentration d'acétate de 2 éthoxyéthyle se situait en deçà de la limite de détection de 0, 55 à 2,9 µg/m3 (MEEO, 1994). Les estimations modélisées fondées sur les rejets industriels dans l'atmosphère fournies par l'INRP en 2006 (INRP, 2007) indiquent que les concentrations d'acétate de 2 éthoxyéthyle dans l'air, l'eau et le sol ne devraient pas atteindre des niveaux importants (exprimées en ng/m3, en ng/L et en ng/g respectivement) (ChemCAN , 2003). De manière similaire, les concentrations d'acétate de 2-éthoxyéthyle dans la nourriture et les boissons ne devraient pas être importantes d'après les renseignements disponibles concernant les utilisations et les propriétés physiques et chimiques de cette substance.
La plus forte concentration d'acétate de 2 éthoxyéthyle dans l'air intérieur, soit de 130 µg/m3, a été mesurée dans six échantillons dans le cadre d'une étude menée en Italie (De Bortotli et al., 1986), alors que, dans d'autres études à plus grande échelle menées en Finlande (n = 50 échantillons) et en Allemagne (n = 89 échantillons), les concentrations d'acétate de 2 éthoxyéthyle dans l'air intérieur n'atteignaient pas plus de 5 µg/m3 (Jungers et Sheldon , 1987; Kostiainen , 1995; Schleibinger et al., 2001). On présume donc que l'ensemble de la population au Canada n'est probablement pas exposée à des concentrations de plus de 5 µg/m3 dans l'air intérieur, concentration la plus élevée mesurée lors des études approfondies (Schleibinger et al., 2001). De plus, avec le déclin de l'utilisation de l'acétate de 2 éthoxyéthyle en Europe et aux États -Unis (Commission européenne , 2006; U.S. EPA, 2005), les concentrations élevées mesurées lors des échantillonnages antérieurs ne sont probablement plus représentatifs du degré d'exposition actuel. Des émissions d'acétate de 2 éthoxyéthyle, à partir d'un produit fini (revêtement de sol en chlorure de polyvinyl) ou pendant l'utilisation d'un produit (séchoir à cheveux), ont été rapportées dans des études danoises. Ceci pourrait contribuer au niveau d'acétate de 2 éthoxyéthyle dans l'environnement extérieur (Lundgren et al., 1999; Danish Ministry of Environment , 2005).
Bien que les données soient limitées concernant la présence d'acétate de 2-éthoxyéthyle dans les produits de consommation, les renseignements disponibles révèlent que cette substance est utilisée dans les peintures (AkzoNobel, 2005), les peintures en aérosol (Borden Inc., 1987, 1985), lubrifiant en aérosol (Dow Corning Corp., 2007), les photorésines (Injectorall Electronics Corp., 1992) et les trousses de réparation pour désembueurs de vitre arrière (Permatex Inc., 2001). La Household Products Database des États-Unis (HPD, 2007) signale aussi deux vernis dont la liste des composants comprend l'acétate de 2-éthoxyéthyle. Toutefois, la concentration indiquée est de 0 %.. Bien que des données aient aussi été trouvées sur la concentration d'acétate de 2-éthoxyéthyle dans une peinture pour yacht (AkzoNobel, 2005), l'utilisation de ce produit a été limitée à l'usage professionnel et n'a pas été considérée comme suffisamment répandue pour extrapoler les résultats à l'ensemble de la population. De manière similaire, tous les autres produits ont soit été déterminer ne pas être en commerce sur el marché canadien ou on été condiréré être utilisé lors d'activités limité ou spécialisé. Ainsi, des scénarios d'exposition à partir de produits de consommation n'ont pas été développés.
Les estimations concernant l'exposition à l'acétate de 2-éthoxyéthyle constituent d'importantes sources d'incertitude, car un nombre très limité de données ont été trouvées sur les concentrations de cette substance dans l'environnement et dans les produits de consommation au Canada.
Évaluation des effets sur la santé
L'annexe 1 présente un résumé des données disponibles sur les effets de l'acétate de 2-éthoxyéthyle sur la santé.
La Commission européenne a classé l'acétate de 2-éthoxyéthyle dans la catégorie 2, avec les mentions de risque R60 (Peut altérer la fertilité) et R61 (Risque pendant la grossesse d'effets néfastes pour l'enfant) (ESIS, 2007). De plus, une évaluation de la toxicité de l'acétate de 2-éthoxyéthyle, du 2-méthoxyéthanol et de son groupe fonctionnel acétate (l'acétate de 2-méthoxyéthanol) ainsi que du 2-éthoxyéthanol a été menée dans le cadre du Programme international sur la sécurité des substances chimiques (PISSC). Il a été conclu que les principaux effets préoccupants sur la santé humaine de ces substances concernent la toxicité sur le plan du développement et la toxicité testiculaire et hématologique. Ces conclusions sont appuyées par de nombreuses données cohérentes concernant les effets sur les animaux et par quelques données concernant les effets sur les humains (PISSC, 1990). Comme l'acétate de 2-éthoxyéthyle est rapidement hydrolysé en 2-éthoxyéthanol par les estérases présentes dans divers tissus corporels, les renseignements sur la toxicité du 2-éthoxyéthanol sont jugés pertinents pour l'évaluation de son groupe fonctionnel acétate. D'après le Rapport d'évaluation de la Liste des substances d'intérêt prioritaire (LSIP) préparé sur le 2-éthoxyéthanol aux termes de la LCPE (1999), les effets sur la santé jugés critiques touchent aussi la reproduction, le développement et le système hématologiqueNote de bas de page 1 (Environnement Canada et Santé Canada, 2002).
Des effets sur la reproduction ont été observés chez des souris exposées à de l'acétate de 2-éthoxyéthyle par voie orale pendant 5 semaines ou plus. Une atrophie des testicules dépendante de la dose a été observée chez les souris exposées par gavage à de l'acétate de 2 éthoxyéthyle pendant cinq semaines, et la dose minimale avec effet (nocif) observé [DME(N)O ] était de 1 000 mg/kg poids corporel par jour (mg/kg-p.c./j) (Nagano etal., 1979, 1984). Lors d'une étude de reproduction continue, on a observé une diminution du nombre de portées par couple, du nombre de nouveau-nés par portée, de la viabilité des nouveau-nés et du poids corporel des ftus à des concentrations de 1 860 mg/kg p oids corporel par jour ou plus dans l'eau potable. Tandis que, à des doses plus élevées, on a noté une diminution importante de l'indice de fertilité, du poids des testicules et de l'épididyme ainsi que de la densité du sperme, et une augmentation du nombre d'anomalies des spermatozoïdes. Des modifications histopathologiques dans les testicules et l'épididyme ont aussi été notées (Gulati et al., 1985; Morrissey et al., 1989; Chapin et Sloane , 1997).
On a observé des effets sur le développement chez des rongeurs et des lapins exposés à l'acétate de 2 éthoxyéthyle par voies orale et cutanée ainsi que par inhalation. À la suite de l'exposition par voie orale, une réduction importante du nombre de portées par couple fertile, du poids corporel des ftus et de la viabilité des nouveau-nés a été observée chez les souris exposées à de l'acétate de 2 éthoxyéthyle à 1 ou 2 % dans de l'eau potable (1 860 ou 3 000 mg/kg p oids corporel par jour respectivement), ceci en l'absence de toxicité chez les mères. Aucun effet n'a été observé chez les souris auxquelles on a administré de l'acétate de 2 éthoxyéthyle à 0,5 % (930 mg/kg-p.c. par jour) (Gulati et al., 1985; Morrissey et al., 1989; Chapin et Sloane, 1997). Lors d'études portant sur l'exposition par inhalation de différentes souches de rates et de lapines en gestation à de l'acétate de 2 éthoxyéthyle, on a noté une incidence significativement accrue des variations viscérales et squelettiques en divers sites, une augmentation de la résorption ftale, une réduction de la viabilité et du poids corporel des ftus en présence de toxicité chez les mères à une dose de 100 parties par million (ppm) (550 mg/m3) ou plus, et ce, chez les deux espèces. Aucun effet n'a été observé à 50 ppm (275 mg/m3) (Tinston et al. 1983; Doe, 1984; Nelson et al., 1984; Tyl et al., 1988). Les lapines, plus sensibles que les rates, ont montré une augmentation significative du nombre de résorptions totales des portées à une dose de 200 à 300 ppm (1 099 à 1 649 mg/m3), alors que de tels effets n'ont été observés chez les rates qu'à une concentration de 600 ppm (3 298 mg/m3) (Nelson et al., 1984; Tyl et al., 1988). Au cours de la seule étude disponible sur la toxicité par voie cutanée sur le plan du développement, on a observé une incidence significativement accrue des variations cardiovasculaires et squelettiques, une augmentation de la résorption ftale et une diminution du poids corporel et de la viabilité des ftus chez les rats exposés à une dose de 5 826 mg/kg-p.c. par jour d'acétate de 2 éthoxyéthyle, la seule dose testée. On a également noté une toxicité chez les mères à cette concentration (Hardin et al., 1984).
Le système hématologique est aussi l'une des principales cibles de l'acétate de 2 éthoxyéthyle. Les effets ont été observés de façon constante chez des animaux de laboratoire à la suite d'expositions aiguës ou répétées par inhalation. La concentration minimale avec effet (nocif) observé (CME[N]O) d'acétate de 2 éthoxyéthyle dans une étude d'inhalation aïgue était de 62 ppm (341 mg/m3); elle est fondée sur la fragilité osmotique accrue des érythrocytes des rats femelles (Carpenter et al., 1956). Lors des études sur la toxicité sur le plan du développement décrites plus haut, on a observé, chez les lapines mères, une diminution liée à la concentration du nombre de plaquettes et une moyenne élevée du volume corpusculaire et, chez les rates mères, une diminution du nombre de globules rouges ainsi que de leur taille, du taux d'hémoglobine et d'hématocrite ainsi qu'une augmentation du nombre de globules blancs, et ce, à une dose de 100 ppm (550 mg/m3) ou plus chez les deux espèces. La CSE(N)O était de 50 ppm (275 mg/m3) (Tyl etal., 1988). De plus, une leucopénie a été observée chez les souris exposées par voie orale à une dose de 1 000 mg/kg-p.c. par jour ou plus, mais non à une dose de 500 mg/kg-p.c. par jour (Nagano etal., 1979, 1984).
Aucun essai biologique à long terme sur des animaux de laboratoire n'est connu concernant l'acétate de 2-éthoxyéthyle. Puisque cette substance est rapidement hydrolysée en 2-éthoxyéthanol par les estérases présentes dans divers tissus corporels (Environnement Canada et Santé Canada, 2002), les données sur la cancérogénicité et la toxicité chronique du 2-éthoxyéthanol sont considérées comme pertinentes pour son groupe fonctionnel acétate. Un rapport d'étude a été trouvé concernant la toxicité chronique du 2-éthoxyéthanol, étude pendant laquelle des rats et des souris ont été exposés à la substance par voie orale. On n'a pas observé d'augmentation du nombre de tumeurs, mais les données histopathologiques étaient limitées. Toutefois, on a signalé que les testicules étaient les principaux organes ciblés chez les deux espèces (Melnick, 1984). D'après l'évaluation des renseignements disponibles sur la génotoxicité du 2 éthoxyéthanol et de l'acétate de 2 éthoxyéthyle (la base de données étant plus limitée pour cette dernière substance), il a été conclu dans le Rapport d'évaluation de la Liste des substances d'intérêt prioritaire (Environnement Canada et Santé Canada, 2002) que le 2 éthoxyéthanol « aurait, tout au plus, un faible pouvoir d'induction de changements cytogénétiques, mais aucune donnée n'indique que cette substance provoque des mutations ». L'acétate de 2 éthoxyéthyle n'a pas provoqué de mutation génique dans diverses souches du Salmonella typhimurium (Slesinski et al., 1988; JCIETIC , 2000) ou de l'Escherichiacoli (JCIETIC , 2000), avec ou sans activation métabolique. Bien que la clastogénicité de l'acétate de 2 éthoxyéthyle dans les cellules ovariennes de hamsters chinois ait été augmentée par l'activation métabolique lors des essais in vitro, l'acétate de 2 éthoxyéthyle n'a pas provoqué la formation de micronoyaux dans les cellules de moelle osseuse des souris lors des essais in vivo (Slesinski et al., 1988).
Des effets sur le plan de la reproduction et du développement ont aussi été observés chez des humains exposés aux éthers glycoliques, notamment l'acétate de 2 éthoxyéthyle dans leur milieu de travail. Bien que l'exposition à une concentration moyenne pondérée dans le temps (MPT) d'acétate de 2 éthoxyéthyle de 0,51 ppm (2,8 mg/m3) n'ait pas affecté les cycles menstruels des femmes exposées dans une usine de fabrication de moniteurs à cristaux liquides (Chia et al., 1997), plusieurs études épidémiologiques ont révélé que des risques significativement élevés d'avortement spontané et/ou de difficulté à concevoir (hypofertilité) et de malformations congénitales étaient liés à l'exposition professionnelle des mères à un mélange d'éthers glycoliques, notamment l'acétate de 2 éthoxyéthyle, le 2 éthoxyéthanol et le 2 méthoxyéthanol (Gray et al., 1993, 1996; Beaumont et al., 1995; Schenker et al., 1995; Swan et al., 1995; Correa et al., 1996; Ha et al., 1996; Schenker, 1996; Swan et Forest, 1996; Cordier et al., 1997, 2001). Toutefois, le rôle relatif que joue l'acétate de 2 éthoxyéthyle dans ces effets observés ne peut pas être clarifié, car les données disponibles indiquent que le 2 méthoxyéthanol ou son groupe fonctionnel acétate pourraient entraîner des effets similaires à des degrés d'exposition plus faibles, sur des animaux de laboratoire (Environnement Canada et Santé Canada, 2002). Lors de la revue de l'une de ces études (Maldonado et al., 2003), on a affirmé que les éléments de preuve disponibles au moment de l'étude étaient insuffisants pour déterminer si l'exposition professionnelle aux éthers glycoliques cause des malformations congénitales.
En ce qui concerne les effets hématologiques, il a été signalé dans une étude transversale que l'exposition à une concentration moyenne géométrique d'acétate de 2-éthoxyéthyle de 9,34 ppm (51,2 mg/m3) était liée à une diminution significative des taux d'hémoglobine et d'hématocrite chez les femmes exposées à la substance dans une usine de sérigraphie, mais non chez les hommes qui, en moyenne, étaient exposés à de plus faibles concentrations (Loh et al., 2003). Lors des enquêtes de suivi, les effets hématologiques chez les travailleuses n'étaient plus aussi importants ni même présents un an ou plus après la mise en uvre de mesures de protection sur les lieux de travail (Chen et al., 2007). Lors d'une autre étude transversale, des effets hématologiques, comme l'augmentation du nombre de cas de leucopénie, ont aussi été observés chez des hommes exposés dans un chantier naval. La MPT d'acétate de 2 éthoxyéthyle sur les lieux de travail variait entre 1,76 et 3,03 ppm (9, 67 à 16,65 mg/m3), les plus fortes concentrations atteignant entre 8, 12 et 18,27 ppm (44, 6 à 100,4 mg/m3). Les travailleurs observés dans cette étude étaient aussi exposés à d'autres solvants, mais pas à d'autres éthers glycoliques (Kim et al., 1999). Lors de la seule étude épidémiologique menée sur le potentiel de génotoxicité de l'acétate de 2 éthoxyéthyle, aucun effet cytogénétique (échange de chromatides surs ou induction de micronoyaux) n'a été observé chez des fabricants de vernis exposés à des éthers glycoliques, dont l'acétate de 2 éthoxyéthyle, à des concentrations allant jusqu'à 3,07 ppm (20,34 mg/m3) (Söhnlein et al., 1993).
Bien que l'analyse approfondie du mode d'action échappe à la portée de la présente évaluation préalable, on admet que la toxicité générale de l'acétate de 2-éthoxyéthyle se manifeste par l'intermédiaire de son principal métabolite, l'acide 2-éthoxyacétique (ECETOC, 2005).
Le degré de confiance en la base de données sur la toxicité sur le plan du développement et de la reproduction et sur les effets hématologiques de l'acétate de 2 éthoxyéthyle est élevé, car des données cohérentes obtenues à partir d'essais sur différents animaux de laboratoire et selon différentes voies d'administration sont disponibles. Ces données sont aussi appuyées par quelques observations épidémiologiques de même que par des renseignements sur la toxicité du 2 éthoxyéthanol et de l'acide 2 éthoxyacétique (Environnement Canada et Santé Canada, 2002). Toutefois, les renseignements sont limités en ce qui concerne les effets chroniques et la cancérogénicité de l'acétate de 2-éthoxyéthyle.
Caractérisation des risques pour la santé humaine
Si l'on prend en considération la classification fondée sur la méthode du poids de la preuve établie par la Commission européenne, qui fait de l'acétate de 2 éthoxyéthyle une substance de catégorie 2, compte tenu de sa toxicité sur le plan du développement et de la reproduction (ESIS , 2007), les évaluations effectuées par un autre organisme international (PISSC , 1990) et par Santé Canada (Environnement Canada et Santé Canada, 2002), ainsi que les données pertinentes dont on dispose, on conclut que les effets critiques de l'acétate de 2 éthoxyéthyle sont, aux fins de la caractérisation des risques que pose cette substance pour la santé humaine : la toxicité sur le plan du développement et de la reproduction, et les effets hématologiques. Par conséquent, lorsque des données suffisantes sont disponibles, des marges d'exposition sont ainsi calculées à partir des plus faibles degrés d'exposition provoquant ces effets critiques et des estimations de l'exposition de la population à l'acétate de 2 éthoxyéthyle.
L'exposition à l'acétate de 2-éthoxyéthyle de l'ensemble de la population devrait se produire principalement par l'air intérieur. La comparaison entre, d'une part, la concentration d'acétate de 2-éthoxyéthyle (9,67 mg/m3) à laquelle des effets hématologiques nocifs ont été observés chez des travailleurs (Kim et al., 1999) (même s'il est reconnu que ces travailleurs étaient aussi exposés à d'autres substances ayant des effets similaires) et, d'autre part, la plus forte concentration observée dans les études sur la qualité de l'air intérieur considérées les plus pertinentes pour évaluer le degré d'exposition actuel au Canada (c.-à-d. 5 µg/m3; Schleibinger, 2001) génère une marge d'exposition d'environ 1 930. Par ailleurs, la comparaison entre les CME(N)O les plus faibles, auxquelles une toxicité sur le plan du développement et des effets hématologiques ont été observés chez des animaux de laboratoire (550 mg/m3) (Tyl et al., 1988), liée à cette concentration dans l'air intérieur, génère une plus grande marge d'exposition (110 000). Ces marges sont jugées adéquates pour tenir compte des incertitudes dans la base de données, à la lumière de la nature conservatrice de l'exposition estimée et des niveaux d'effets critiques lors des études sur les humains et les animaux de laboratoire.
Les prpduits de consomamtion potentiel contenant de l'acétate de 2-éthoxyéthyle on soit été trouvé ne pas être pas présent sur le marché canadien ou ont été considérés être utilisés dans des activités limitées ou spécialiséesé Ainsi, l'exposition à l'acétate de 2-éthoxyéthyle via les produits de consommation n'est pas prévue être significative.
Incertitudes dans l'évaluation des risques pour la santé humaine
La quantification précise de l'exposition de la population à l'acétate de 2-éthoxyéthyle présent dans le milieu est associée à un certain degré d'incertitude, et ce, même si l'on s'attend à ce que les degrés d'exposition soient très faibles. Il y a aussi une incertitude associée au manque de données suffisantes sur les concentrations de l'acétate de 2 éthoxyéthyle dans l'environnement et sur la présence de l'acétate de 2 éthoxyéthyle dans les produits de consommation utilisés au Canada. Les sources d'information disponibles indiquent que l'acétate de 2 éthoxyéthyle n'est actuellement pas utilisé dans les produits et donc n'entraînerait pas un risque important d'exposition pour la population générale.
Même si la quantification des différences de sensibilité aux effets de l'acétate de 2 éthoxyéthyle entre les animaux de laboratoire, les humains et la population dans son ensemble échappe à la portée de la présente évaluation préalable, il convient de noter que des effets hématologiques ont été signalés chez des travailleurs à des concentrations moindres que les concentrations avec effets observées lors des essais sur des animaux de laboratoire. Vu le nombre insuffisant de données, des incertitudes demeurent au sujet du potentiel de cancérogénicité de l'acétate de 2 éthoxyéthyle, même si les résultats des études portant sur la génotoxicité ainsi que les données préliminaires sur la toxicité chronique du 2 éthoxyéthanol ne portent pas à croire que l'acétate de 2 éthoxyéthyle est cancérogène. De plus, il y a aussi des incertitudes liées à l'absence d'études portant sur la toxicité pour la reproduction chez les animaux de laboratoire exposés par inhalation (la voie ayant le plus de rapport à l'exposition de la population). Toutefois, l'information de la base de données disponible concernant d'autres paramètres observés chez les animaux exposés par voie orale, par voie cutanée ou par inhalation ne porte pas à croire que les effets critiques de toxicité pour la reproduction résultant de l'exposition par inhalation d'acétate de 2 éthoxyéthyle seraient plus faibles que les effets liés aux autres voies d'exposition.
Conclusion
Étant donné les marges entre les estimations prudentes de l'exposition, à partir de sources environnementales, et les concentrations entraînant des effets critiques sur le développement et des effets hématologiques chez les animaux de laboratoire ou chez les travailleurs exposés, on peut conclure que l'acétate de 2 éthoxyéthyle n'est pas jugé « toxique » au sens de l'alinéa 64c) de la LCPE (1999), car il ne pénètre pas dans l'environnement en une quantité ou à une concentration, ou dans des conditions de nature à constituer un danger pour la vie ou la santé humaines au Canada.
D'après les renseignements présentés dans le présent rapport d'évaluation préalable, l'acétate de 2 éthoxyéthyle ne pénètre pas dans l'environnement en une quantité ou à une concentration, ou dans des conditions de nature à avoir, immédiatement ou à long terme, un effet nocif sur l'environnement ou sa diversité biologique, ni à mettre en danger l'environnement essentiel pour la vie.
En conséquence, il est conclu que l'acétate de 2 éthoxyéthyle n'est pas une « substance toxique » au sens de l'article 64 de la LCPE (1999). De plus, l'acétate de 2 éthoxyéthyle ne répond pas aux critères de la persistance et de la bioaccumulation tels qu'ils sont définis dans le Règlement sur la persistance et la bioaccumulation (Canada, 2000).
Références
[ACD] Advances Chemistry Development. 2007. Valeurs calculées à l'aide du logiciel Advanced Chemistry Development (ACD/Labs), version 9.04 pour Solaris (© 1994-2007), présenté dans la base de données SciFinder. [consultée le 25 juillet 2007].
[ACGIH] American Conference on Governmental Industrial Hygienists. 1991. American Conference of Governmental Industrial Hygienists. Documentation of the threshold limit values and biological exposure indices. Sixième édition. Cincinnati (OH) : ACGIH. Pages 567-568.
[AOPWIN] Atmospheric Oxidation Program for Windows [modèle d'estimation]. 2000. Version 1.91. Washington (DC) : U.S. Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY) : Syracuse Research Corporation. http://www.epa.gov/oppt/exposure/pubs/episuite.htm
Arnot , J.A., Gobas , F.A. 2003. A generic QSAR for assessing the bioaccumulation potential of organic chemicals in aquatic food webs. QSAR Comb.Sci. [Internet] 22(3):337 -345. [accès restreint]. http://www3.interscience.wiley.com/journal/104557877/home_
Atkinson, R. 1989. Kinetics and mechanisms of the gas-phase reactions of the hydroxyl radical with organic compounds. J. Phys. Chem. Ref. Data. Monograph No. 1.
Azko Nobel. 2005. Fiches signalétiques (diverses). http://www.awlgrip.com/support/msds/Pages/MSDS.aspx
[BCFWIN] BioConcentration Factor Program for Windows [modèle d'estimation]. 2000. Version 2.15. Washington (DC) : U.S. Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY) : Syracuse Research Corporation. http://www.epa.gov/oppt/exposure/pubs/episuite.htm
Beaumont, J.J., Swan, S.H., Hammond, S.K., Samuels, S.J., Green, R.S., Hallock, M.F., Dominguez, C., Boyd, P., Schenker, M.B. 1995. Historical cohort investigation of spontaneous abortion in the semiconductor health study: epidemiologic methods and analysis of risk in fabrication overall and in fabrication work groups. Am. J. Ind. Med. 43:440-446.
[BIOWIN] Biodegradation Probability Program for Windows [modèle d'estimation]. 2000. Version 4.02. Washington (DC) : U.S. Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY) : Syracuse Research Corporation. http://www.epa.gov/oppt/exposure/pubs/episuite.htm
Boethling, R.S., Howard, P.H., Beauman, J.A., Larosche, M.E. 1995. Factors for intermedia extrapolations in biodegradability assessment. Chemosphere 30(4):741-752.
Borden Inc. 1985. Fiches signalétiques du produit Krylon Interior/Exter Enamel Aerosol 1809. http://www.biosci.ohio-state.edu/safety/MSDS/KRYLON%20ENAMEL%20AEROSOL.htm
Borden Inc. 1987. Fiches signalétiques du produit SPARVAR S-100 GLOSSY WHITE (OLD FORM). Date : 01/01/1987. http://hazard.com/msds/f2/bdw/bdwyf.html
Budavari, S. (éd.). 1996. The Merck Index - An encyclopedia of chemicals, drugs, and biologicals. Douzième édition. Whitehouse Station (NJ) : Merck and Co., Inc., p. 640.
Canada. 1999. Loi canadienne sur la protection del'environnement (1999). L.C., 1999, ch. 33. http://canadagazette.gc.ca/partIII/1999/g3-02203.pdf
Canada. 2000. Loi canadienne sur la protection de l'environnement (1999) : Règlement sur la persistance et la bioaccumulation, C.P. 2000-348, 23 mars 2000, DORS/2000-107, Gazette du Canada, Partie II, vol. 134, no 7, p. 607-612. Ottawa : Imprimeur de la Reine. http://canadagazette.gc.ca/partII/2000/20000329/pdf/g2-13407.pdf
Canada. 2002. Loi canadienne sur la protection de l'environnement (1999) : Liste des substances d'intérêt prioritaire : rapport d'évaluation : 2-Éthoxyéthanol. Ottawa : Environnement Canada, Santé Canada. no de catalogue En 40-215/64F. http://www.hc-sc.gc.ca/ewh-semt/pubs/contaminants/psl2-lsp2/index-fra.php
Canada. 2006. Ministère de l'Environnement, Ministère de la Santé. Loi canadienne sur la protection de l'environnement (1999) : Avis d'intention d'élaborer et de mettre en ouvre des mesures d'évaluation et de gestion des risques que certaines substances présentent pour la santé des Canadiens et leur environnement Ottawa : Travaux publics et Services gouvernementaux Canada. Gazette du Canada, Partie 1, vol. 140, no 49, p. 4109-4117. http://canadagazette.gc.ca/partI/2006/20061209/pdf/g1-14049.pdf
Canada. 2007a. Ministère de l'Environnement, ministère de la Santé. 2006. Profil de substance pour le Défi aux intervenants : Acétate de 2-éthoxyéthyle, no CAS 111-15-9. /ese-ees/24089F6A-CC0E-B0E4-F9FC-0F223DFF5ABD/batch3_111-15-9_fr.pdf
Canada. 2007. Ministère de l'Environnement, Ministère de la Santé. Loi canadienne sur la protection de l'environnement (1999) : Avis concernant les substances du groupe 3 du Défi. Gazette du Canada. Partie I, vol. 141 , no 33 , p. 435 - 459. http://canadagazette.gc.ca/partI/2007/20070818/pdf/g1-14133.pdf
Carpenter , C.P., Smyth, H.F. 1946. Chemical burns of the rabbit cornea. Am. J. Ophthalmol. 29:1363 -1372. [cité dans ECETOC, 2005].
Carpenter CP. 1947. Cellosolve (queries and minor notes). J.Am.Med.Assoc. 135: 880.
Carpenter, C.P., Pozzani, U.C., Weil, C.S., Nair, J.H., Keck, G.A., Smyth, H.F. 1956. The toxicity of butyl cellosolve solvent. AMA Arch. Ind. Health 14:114-131.
[CCRIS] Chemical Carcinogenesis Research Information System [Internet]. 2003. Record for Ethylene glycol monoethyl ether acetate. No CAS : 111-15-9. Bethesda (MD) : National Library of Medicine (États-Unis). [mise à jour en 2004]. http://toxnet.nlm.nih.gov/cgi-bin/sis/htmlgen?CCRIS
Chapin, R.E., Sloane, R.A. 1997. Reproductive assessment by continuous breeding: evolving study design and summaries of ninety studies; ethylene glycol monoethyl ether acetate. Environ.Health Perspect. 105 (suppl. 1):199-395; 221-222.
[ChemCAN]. 2003. ChemCAN: level III fugacity model of 24 regions of Canada. Version 6.00. Peterborough (Ont.) : Canadian Centre for Environmental Modelling and Chemistry, Université Trent. http://www.trentu.ca/academic/aminss/envmodel/models/CC600.html
Chen, H.I., Liou, S.H., Hsieh, M.H., Shih, T.S., Sun, C.W., Wu, T.N., Chang, H.Y., Loh, C.H. 2007. Hematological follow-up of an intervention program adding rubber glove-wearing to local ventilation for 2-ethoxyethanol acetate-exposed workers. J. Occup. Health 48(6):462-73.
Chia, S.E., Foo, S.C., Khoo, N.Y., Jeyaratnam, J. 1997. Menstrual patterns of workers exposed to low levels of 2-ethoxyethylacetate (EGEEA). Am. J. Ind. Med. 43:440-446 {± 2}.
Commission européenne. 2006. Risk assessment: of 24.02.2006. 2-Ethoxyethyl acetate. (no CAS 111 -15 -9, no EINECS : 203-839-2). Dortmund (Allemagne). Human Health Section. Federal Institute for Occupational Safety and Health Notification Unit.
Commission européenne. 2005. Risk assessment: of 24.02.2005. 2-Ethoxyethyl acetate. Dortmund (Allemagne) : Federal Institute for Occupational Safety and Health Notification Unit.
Commission européenne. 1999. The rules governing cosmetic products in the European Union, vol. 1, Cosmetics legislation, Cosmetic products. Directive du Conseil 76/768. Annexe II. Commission européenne, Direction générale Entreprises et industries, produits pharmaceutiques et cosmétiques. http://www.leffingwell.com/cosmetics/vol_1en.pdf
Cordier, S., Bergeret, A., Goujard, J., Ha, M.C., Aymé, S., Bianchi, F., Calzolari, E., De Walle, H.E.K., Knill-Jones, R., Candela, S., Dale, I., Dananché, B., de Vigan, C., Fevotte, J., Kiel, G., Mandereau, L. 1997. Congenital malformations and maternal occupational exposure to glycol ethers. Epidemiology 8:355-63.
Cordier, S., Szabova, E., Fevotte, J., Bergeret, A., Plackova, S., Mandereau, L. 2001. Congenital malformations and maternal exposure to glycol ethers in the Slovak Republic. Epidemiology 12:592-3.
Correa, A., Gray, R.H., Cohen, R., Rothman, N., Shah, F., Seacat, H., Corn, M. 1996. Ethylene glycol ethers and risks of spontaneous abortion and subfertility. Am. J.Epidemiol. 143:707-17.
Daubert, T.E., Danner, R.P. 1989. Physical and thermodynamic properties of pure chemicals data compilation. Washington (DC) : Taylor et Francis.
De Bortoli, N., Knöppel, H., Pecchio, E., Peil, A., Rogora, L., Schauenburg, H., Schlitt, H., Vissers, H. 1986. Concentrations of selected organic pollutants in indoor and outdoor air in northern Italy. Environ. Int. 12:343-350.
De Kettenis, P. 2005. The historic and current use of glycol ethers: a picture of change. Toxicol. Lett. 156: 5-11.
Doe , J.E. 1984. Ethylene glycol monoethyl ether and ethylene glycol monoethyl ether acetate teratology studies. Environ. Health Perspect. 57: 33 -41.
Dow Corning Corporation. 2007. Fiches signalétiques du produit MolyKote® 3402C Spray. http://www2.dowcorning.com/DataFiles/090007b280ca8bdc.pdf
Eastman Chemical Products, Inc. 1982. Fiche signalétique. NTIS/OTS 0505466. p. 1-8. Springfield (VA) : US Department of Commerce. [cité dans ECETOC, 2005].
Eastman Kodak Company. 1958. Données inédites. Corporate Health, Safety and Environment. [cité dans ECB , 2000].
Eastman Kodak Company. 1968. Données inédites. Corporate Health, Safety and Environment. [cité dans ECB, 2000].
[ECB] European Chemicals Bureau. 2000. IUCLID dataset for 2-ethoxyethyl acetate (no CAS 111-15-9). http://ecb.jrc.it/esis/
[ECETOC] European Centre for Ecotoxicology and Toxicology of Chemicals. 2005. The toxicology of glycol ethers and its relevance to man. Rapport technique no 95, vol. II. 4.10. Profil de la substance : EGEEA (no CAS 111-15-9). Bruxelles (Belgique) : ECETOC.
[ECOTOX] ECOTOXicology database [Internet]. 2006.Washington (DC) : U.S. Environmental Protection Agency, Office of Research and Development; U.S. Environmental Protection Agency, National Health and Environmental Effects Research Laboratory's, Mid-Continent Ecology Division. http://cfpub.epa.gov/ecotox
Environnement Canada. 2008. Données sur les substances du lot 3 recueillies en vertu de l'article 71 de la Loi canadienne sur la protection de l'environnement (1999) : Avis concernant les substances du lot 3 du Défi. Préparé par Environnement Canada et Santé Canada dans le cadre du Programme des substances existantes.
Environnement Canada et Santé Canada. 2002. Liste des substances d'intérêt prioritaire - Rapport d'évaluation du 2-Ethoxyethanol [Internet]. Ottawa (Ont.) : Environnement Canada; Santé Canada. http://www.hc-sc.gc.ca/ewh-semt/pubs/contaminants/psl2-lsp2
Environnement Canada. 2007. Inventaire national des rejets de polluants [INRP]. Gatineau (Québec). [consulté en septembre 2007]. http://www.ec.gc.ca/pdb/querysite/query_f.cfm
[EQC] EQuilibrium Criterion. Version 2.02 du modèle. 2003. Peterborough (Ont.) : Université Trent, Canadian Centre for Environmental Modelling and Chemistry. http://www.trentu.ca/academic/aminss/envmodel/models/EQC2.html
[ESIS] European Chemical Substances Information System. 2006. 2007. Version 5. Acétate de 2-éthoxyéthyle, no CAS 111-15-9. http://ecb.jrc.it/esis/
Gig Sanit. 1988. 53(10):78. [cité dans RTECS , 1993 , ECB , 2000].
Gray , R.H., Corn , M., Cohen , R., Correa , A., Hakim , R., Hou , W., Shah , F., Zauer , H. 1993. Final report. The Johns Hopkins University retrospective and prospective studies of reproductive health among IBM employees in semiconductor manufacturing. Baltimore (MD [États -Unis]) : The Johns Hopkins University. [cité dans Swan et Forest , 1996; Maldonado et al., 2003].
Gray, R.H., Correa, A., Hakim, R., Cohen, R., Corn, M., Shah, F., Rothman, N., Hou, W., Secat, H. 1996. Ethylene glycol ethers and reproductive health in semiconductor workers. Occup. Hyg. 2:331-338.
Gulati, D.K., Barnes, L.H., Russell, S., Poonacha, K.B., Lamb, J.C. 1985. Ethylene Glycol Monoethyl Ether Acetate. Reproduction and fertility assessment in CD-1 mice when administered in drinking water. Final report, NTP-85-320. PB 86-139565. Research Triangle Park (C.N.) : US Department of Health and Human Services, National Institutes of Health, National Institute of Environmental Health Sciences, National Toxicology Program. National Toxicology Program, National Institute of Environmental Health Sciences.
Ha, M.C., Cordier, S., Dananche, B., Bergeret, A., Mandereau, L., Bruno, F. 1996. Congenital malformations and occupational exposure to glycol ethers: a European collaborative case-control study. Occup. Hyg. 2:417-421.
Hardin, B.D., Goad, P.T., Burg, J.R. 1984. Developmental toxicity of four glycol ethers applied cutaneously to rats. Environ. Health Perspect. 57:69-74.
[HPD] Household Products Database [base de données sur Internet]. 2007. 2 -Ethoxyethanol acetate. Bethesda (MD [États-Unis]) : National Library of Medicine. [consultée le 8 mai 2008]. http://household products.nlm.nih.gov/
[HSDB] Hazardous Substances Data Bank [base de données sur Internet]. 2005. Ethylene glycol monoethyl ether acetate. Bethesda (MD [États-Unis]) : National Library of Medicine. [mise à jour le 26 juin 2005; cité en juin 2007]. http://toxnet.nlm.nih.gov/cgi-bin/sis/htmlgen?HSDB
Hüls, A.G. 1989a. Verteilungskoeffizient n-Octanol - Wasser für "Altstoffe". Rapport d'essai daté du 10 janvier 1989. [cité dans Commission européenne, 2005].
Hüls, A.G. 1989b. Bestimmung der Mutagenität von Ethyglykolacetat in Salmonella/Säuger-Mikrosomen-Mutagenitätstest nach Ames, gemäß Eg-Richtlinie 84/449/EGW B14. Rapport inédit. AM-89/22. Schöberl, Ps-Biologie/Toxikologie. Marl (Allemagne) : Hüls. [cité dans ECETOC , 2005].
Injectorall Electronics Corp. 1992. Fiche signalétique de la résine positive PC197. http://www.injectorall.com/MSDS197.htm
[INRP] Inventaire national des rejets de polluants [base de données sur Internet]. 2007. Gatineau (Qc), Environnement Canada. [consulté le 5 juillet 2007]. http://www.ec.gc.ca/pdb/querysite/query_e.cfm
[JCIETIC] Japan Chemical Industry Ecology-Toxicology and Information Center. 2000. Mutagenicity test data of existing chemical substances based on the toxicity investigation system of the industrial safety and health law. Suppl. 2 [cité dans CCRIS, 2004].
Johanson, G., Rick, U. 1996. Use and use patterns of glycol ethers in Sweden. Occup. Hyg. 2:105-110.
Johnson, W. Jr. 2002. CIR (Cosmetic Ingredient Review). Final report on the safety assessment of ethoxyethanol and ethoxyethanol acetate. Int.J.Toxicol. 21(suppl. 1):9 -62.
Jungers, R.H., Sheldon, L.S. 1987. Characterization of volatile organic chemicals in public access buildings. In: Proceedings of the Fourth International Conference on Indoor Air Quality and Climate. Vol. 1. Berlin (Allemagne) : Institute for Water, Soil, and Air Hygiene. Pages 144-148.
Kennah , H.F., Hignet, S., Laux , P.E., Dorko , J.D., Barrow, C.S. 1989. An objective procedure for quantitating eye irritation based upon changes of corneal thickness. Fundam. Appl. Toxicol. 12:258 -268. [cité dans ECETOC, 2005].
Kim, Y., Lee, N., Sakai, T., Kim, J.S., Yang, J.S., Park, S., Lee, C.R., Cheong, H.K., Moon, Y. 1999. Evaluation of exposure to ethylene glycol monoethyl ether acetates and their possible haematological effects on shipyard painters. Occup. Environ. Med. 46:280-286.
Kirk-Othmer. 1980. Encyclopaedia of chemical technology, vol. 11. Glycols (ethylene and propylene). Troisième édition. New York (NY): Wiley. [cité dans Commission européenne , 2005].
Kostiainen, R. 1995. Volatile organic compounds in the indoor air of normal and sick houses. Atmos. Environ. 29(6):693-702.
Lewis, R.J. Sr. 2007. Hawley's Condensed Chemical Dictionary. Quinzième édition. Hoboken (NJ) : John Wiley & Sons. Page 529.
Loh, C.H., Shih, T.S., Liou, S.H., Lin, Y.C., Hsieh, A.T., Chen, C.Y., Liao, G.D. 2003. Haematological effets among silk screening workers exposed to 2-ethoxy ethyl acetate. Occup. Environ. Med. 60:e7.
Lundgren, B., Jonsson, B., Ek-Olausson, B. 1999. Material emission of chemicals - PVC flooring materials. Indoor Air 9:202-208.
Maldonado, G., Delzell, E., Tyl, R.W., Sever, L.E. 2003. Occupational exposure to glycol ethers and human congenital malformations. Int. Arch. Occup. Environ. Health 72(3):142-50.
Melnick, R.L. 1984. Toxicities of ethylene glycol and ethylene glycol monoethyl ether in Fisher 344/N rats and B6C3F1 mice. Environ. Health Perspect. 57:147- 155.
[MITI] Ministry of International Trade & Industry (Japon), Basic Industries Bureau, Chemical Products Safety Division. 1992. Biodegradation and bioaccumulation data of existing chemicals based on the CSCL Japan. Tokyo (Japon), Japan Chemical Industry Ecology-Toxicology & Information Centre.
[MEEO] Ministère de l'Environnement et de l'Énergie de l'Ontario. 1994. Windsor Air Quality Study: TAGA 6000 survey results. Windsor Air Quality Committee; Imprimeur de la Reine pour l'Ontario (PIBS 3152E; ISBN 0-7778-2831-6, automne 1994).
Ministère de l'Environnement du Danemark. 2005. Emission and evaluation of chemical substances from selected electrical and electronic products - part 2. Survey of Chemical Substances in Consumer Products, no 66. Agence de protection de l'environnement.
Montgomery , J.H. 2000. Groundwater chemicals desk reference. Boca Raton (FL) : CRC Press.
Morrissey, R.E., Lamb, J.C., Morris, R.W., Chapin, R.E., Gulati, D.K., Heindel, J.J. 1989. Results and evaluations of 48 continuous breeding reproduction studies conducted in mice. Fundam. Appl. Toxicol. 13:747-77.
Nagano, K., Nakayama, E., Koyano, M., Oobayashi, H., Adachi, H., Yamada, T. 1979. Testicular atrophy of mice induced by ethylene glycol mono alkyl ethers. Sanyo Igaku(Jpn J. Ind. Health) 21:29-35 (en japonais, avec résumé et tableaux en anglais).
Nagano, K., Nakayama, E., Oobayashi, H., Nishizawa, T., Okuda, H., Yamazaki, K. 1984. Experimental studies on toxicity of ethylene glycol alkyl ethers in Japan. Environ. Health Perspect. 57:75 84.
[NCI] National Chemical Inventories [base de données sur CD-ROM]. 2007. Columbus (OH), American Chemical Society. [consultée en novembre 2007]. http://www.cas.org/products/cd/nci/index.html
Nelson, B.K., Setzer, J.V., Brightwell, W.S., Mathinos, P.R., Kuczuk, M.H., Weaver, T.E., Goad, P.T. 1984. Comparative inhalation teratogenicity of four glycol ether solvents and an amino derivative in rats. Environ. Health Perspect. 57:261-271.
Nikitakis, J.M., McEwen, G.N. Jr. (éd.) 1990. CTFA compendium of cosmetic ingredient composition - descriptions. I. Washington (DC) : CTFA. [cité dans Johnson, 2002].
[NIOSH] National Institute for Occupational Safety and Health. 1991. Criteria for a recommended standard. Occupational exposure to ethylene glycol monomethyl ether, ethylene glycol monoethyl ether, and their acetates. (DHHS [NIOSH] publication no 91, p. 119.) Cincinnnati (OH) : US Department of Health and Human Services, Public Health Service, Centers for Disease Control and Prevention, NIOSH. [cité dans Johnson, 2002].
[NLM] National Library of Medicine. 2005. Hazardous Substances Data Bank (HSDB). http://www.toxnet.nlm.nih.gov/cgi-bin/sis/htmlgen?HSDB
[NPI] National Pollutant Inventory. 2006. Substance fact sheet. 2-Ethoxyethanol acetate. Parkes (AU) : Australian Government, Department of the Environment, Water, Heritage and the Arts. [consulté le 21 janvier 2008]. http://www.npi.gov.au/cgi-bin/npireport.pl?proc=substance;substance=37#Details
[OASIS Forecast] Optimized Approach based on Structural Indices Set [Internet]. 2005. Version 1.20. Bourgas (Bulgarie) : Prof. Assen Zlatarov University, Laboratoire de chimie mathématique. http://oasis-lmc.org/?section=software
Peñuelas, J., Llusià, J. 2001. Seasonal patterns of non-terpenoid C6-C10 VOC emission from seven Mediterranean woody species. Chemosphere 45:237-244.
[PCKOCWIN] Organic Carbon Partition Coefficient Program for Windows [modèle d'estimation]. 2000. Version 1.66. Washington (DC) : U.S. Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY) : Syracuse Research Corporation. http://www.epa.gov/oppt/exposure/pubs/episuite.htm
Permatex, Inc. 2001. Fiche signalétique du produit Quick Grid TM Repair Kit.05FO CG. Hartford (CT) : Permatex, Inc. https://corporateportal.ppg.com/NR/rdonlyres/9B08C0E3-63DD-47CE-8BB7-3DEAC80D4BE0/0/permatex_15067_msds.pdf
[PISSC] Programme international sur la sécurité des substances chimiques. 1990. 2 -Methoxyethanol, 2-ethoxyethanol, and their acetates. Genève (Suisse) : Organisation mondiale de la santé. (Critères d'hygiène de l'environnement no 115). Financé conjointement par le Programme des Nations -Unies pour l'environnement, l'Organisation internationale du travail et l'Organisation mondiale de la santé. http://www.inchem.org/documents/ehc/ehc/ehc115.htm
[PhysProp] Interactive PhysProp Database [Internet]. 2006. Syracuse (NY) : Syracuse Research Corporation. http://www.syrres.com/esc/physdemo.htm
Pozzani, U.C., Weil, C.S., Carpenter, C.P. 1959. The toxicological basis of threshold limit values. 5. The experimental inhalation of vapor mixtures by rats, with notes upon the relationship between single dose inhalation and single dose oral data. Am. Ind. Hyg. Ass. J. 20:364-369.
[RIVM] Rijksinstituut voor Volksgezondheid en Milieu. 2006. Modèle d'exposition des consommateurs (ConsExpo) [Internet]. Version 4.1. Pays-Bas : The National Institute for Public Health and the Environment (Rijksinstituut voor Volksgezondheid en Milieu). http://www.rivm.nl/en/healthanddisease/productsafety/ConsExpo.jsp#tcm:13-42840
Schenker, M.B., Gold, E.B., Beaumont, J.J., Eskenazi, B., Hammond, S.K., Lasley, B.L., McCurdy, S.A., Samuels, J.J., Saiki, C.L., Swan, S.H. 1995. The association of spontaneous abortion and other reproductive effects with work in the semiconductor industry. Am. J. Ind. Med. 28 :639-659.
Schenker, M.B. 1996. Reproductive health effects of glycol ether exposure in the semiconductor industry. Occup. Hyg. 2:367-372.
Schleibinger , H., Hott , U., Marchl , D., Braun , P., Plieninger , P., Ruden , H. 2001.
VOC-concentrations in Berlin indoor environments between 1988 and 1999. Gefahrst Reinhalt Luft 61(1 -2):26 -38.
[SDC] Système de déclaration des cosmétiques [base de données exclusive]. 2008. Ottawa (Ont.) : Santé Canada. [mis à jour en mars 2008 et consulté en avril 2008].
Shaw, G.M., Velie, E.M., Katz, E.A., Morland, K.B., Schaff, D.M., Nelson, V. 1999. Maternal Occupational and hobby chemical exposures as risk factors for neural tube defects. Epidemiology 10:124-129.
Shell Chemical Co. Non daté. Rapport inédit. [cité dans Tyl et al., 1988].
Slesinski, R.S., Guzzie, P.J., Tyler, T.R. 1988. Cytotoxicity and genotoxic potential of ethylene glycol monethyl ether acetate (EGEE.Ac) in a battery of short term test systems. Environ. Molec. Mutagen 11(suppl. 11):97 (résumé).
Smyth, H.F., Seaton, J., Fisher, L. 1941. The single dose toxicity of some glycols and derivatives. J. Ind. Hyg. Toxicol. 23:259-68.
Söhnlein, B., Letzel, S., Weltle, D., Rüdiger, H.W., Angerer, J. 1993. Occupational chronic exposure to organic solvents. XIV. Examinations concerning the evaluation of a limit value for 2-ethoxyethanol and 2-ethoxyethyl acetate and genotoxic effects of these glycol ethers. Int. Arch. Occup. Environ. Health 64(7):479-484.
Swan, S.H., Beaumont, J.J., Hammond, S.K., VonBehren, J., Green, R.S., Hallock, M.F., Woskie, S.R., Hines, C.J., Schenker, M.B. 1995. Historical cohort study of spontaneous abortion among fabrication workers in the semiconductor health study: agent-level analysis. Am. J. Ind. Med. 28 :751-769.
Swan, S.H., Forest, W. 1996. Reproductive risks of glycol ethers and other agents used in semiconductor manufacturing. Occup. Hyg. 2:373-385.
Tinston, D.J., Doe, J.E., Killick, M., Thomas, M. 1983. Ethylene glycol monoethyl ether acetate (EEAc). Inhalation teratogenicity study in rabbits. Imperial Chemical Industries PLC. Report No. CTL/P/840 to Chemical Manufacturers Association.
Truhaut, R., Dutertre -Catella, H., Phu-Lich, N., Huyen, V.N. 1979. Comparative toxicological study of ethylglycol acetate and butylglycol acetate. Toxicol. Appl. Pharmacol. 51:117-127.
Tyl, R.W., Pritts, I.M., France, K.A., Fisher, L.C., Tyler, T.R. 1988. Developmental toxicity evaluation of inhaled 2-ethoxyethanol acetate in Fischer 344 rats and New Zealand white rabbits. Fundam. Appl. Toxicol. 10:20-39.
[US EPA] U.S. Environmental Protection Agency. 2005. 2-Ethoxyethanol, 2-ethoxyethanol acetate, 2-methoxyethanol, and 2-methoxyethanol acetate; Significant New Use Rule. Fed Regist 70(228):71401 -71406. http://www.epa.gov/EPA-TOX/2005/November/Day-29/t23421.htm
[US FDA] U.S. Food and Drug Administration. 2007. Indirect food additives: Adhesives and components of coatings. Adhesives. 21CFR175.105 (Code of Federal Regulations. Titre 21, volume 3. [révisé le 1er avril 2007 ; consulté en juillet 2008]. Rockville (MD) : US Department of Health and Human Services. http://www.accessdata.fda.gov/scripts/cdrh/cfdocs/cfcfr/CFRSearch.cfm
Von Oettingen WF, Jirouch EA. 1931. The pharmacology of ethylene glycol and some of its derivatives in relation to their chemical constitution and physical properties. J. Pharmacol. Exp. Ther. 42:355-372. [cité dans ECETOC, 2005].
Wenninger, J.A., McEwen, G.N. 1997. International cosmetic ingredient dictionary and handbook. Septième édition. Washington (DC) : Cosmetic, Toiletry, and Fragrance Association. Page 505. [cité dans Johnson, 2002].
Yalkowsky, S.H., Dannenfelser, R.M. 1992. The Aquasol database of aqueous solubility. Cinquième édition. Tucson (AZ) : University of Arizona , College of Pharmacy.
Yanagihara, S., Shimada, I., Shinoyama, E., Chisaka, P., Saito, K. 1977. Photochemical reactivities of hydrocarbons. In Proceeding of the Fourth International Clean Air Congress. Tokyo (Japon); Mai. Tokyo (Japon) : Clean Air Society. p. 472-477.
Zissu D. 1995. Experimental study of cutaneous tolerance to glycol ethers. Contact Dermatitis
Annexe 1. Concentration d'acétate de 2-éthoxyéthyle dans les produits de consommation 1 selon le modèle ConsExpo 4.1 (RIVM, 2006)
| Scénarios concernant les produits de consommation | Les hypothèses suivantes ont été utilisées pour tous les scénarios :
|
Estimation de l'exposition |
| Peinture en aérosol | Fraction massique d'acétate de 2-éthoxyéthyle : 5 % (Borden Inc., 1985). Inhalation Durée d'exposition de 20 minutes, volume de la pièce de 34 m3, taux de ventilation de 1,5 h-1, taux de génération de masse de 0,33 g/sec, durée de pulvérisation de 15 minutes, fraction de la substance dans l'air de 1, fraction massique des particules non volatiles de 0,3, masse volumique des particules non volatiles de 1,5 g/cm 3, hauteur de la pièce de 2,25 m, diamètre de coupure de 15 µm et fraction non inhalable de 1. Voie cutanée Contact cutané direct avec le produit - taux constant. Taux de contact de 100 mg/min, durée du rejet : 15 minutes. |
Inhalation - concentration moyenne par événement = 18,7 mg/m3 Voie cutanée - dose aiguë = 1,06 mg/kg |
Annexe 2. Sommaire 1 des renseignements au sujet des effets de l'acétate de 2-éthoxyéthyle (no CAS 111-15-9) sur la santé
| Paramètre | Doses ou concentrations minimales entraînant un effet/résultats |
|---|---|
| Toxicité aiguë | Dose létale médiane (DL50) la plus faible, par voie orale (cochon d'Inde) = 1 910 mg/kg-p.c. (Smyth et al., 1941; Carpenter, 1947) DL50 la plus faible, par voie cutanée (souris) = 10 300 mg/kg-p.c. (Carpenter, 1947) CL50 la plus faible, par inhalation (rat) = 8 250 mg/m3 (Shell Chemical Co. [non daté]) Plus faible CME(N)O par inhalation (rat, femelle) = 62 ppm (341 mg/m3), fondée sur l'effet hémolytique sur la fragilité osmotique des érythrocytes (Carpenter et al., 1956). |
| Toxicité à court terme, doses répétées | DME(N)O la plus faible, par voie orale (souris) = 1 000 mg/kg-p.c. par jour (5 souris mâles/groupe, gavage, 5 semaines), fondée sur l'atrophie testiculaire et la leucopénie dépendantes de la dose observée. Dose sans effet (nocif) observé (DSE(N)O) = 500 mg/kg-p.c./j (Nagano et al., 1979, 1984). DME(N)O la plus faible, par voie cutanée (rat) = 5 826 mg/kg-p.c./j (seule dose testée, 18 rates gravides/groupe, 4 fois par jour, jours de gestation 7 à 16), d'après les effets de toxicité chez les mères, notamment la diminution significative du gain en poids corporel et du poids de l'utérus chez les mères (Hardin et al., 1984). CME(N)O la plus faible, par inhalation (rat et lapin) = 100 ppm (550 mg/m3) (24 lapines gravides/groupe, 6 heures par jour, jours de gestation 6 à 18; 30 rats femelles/groupe, 6 heures par jour, jours de gestation 6 à 15), d'après les effets de toxicité chez les mères, notamment la diminution significative du gain en poids corporel, les changements dans les paramètres hématologiques, l'augmentation du poids absolu du foie et l'accentuation des signes cliniques; DSE(N)O = 50 ppm (275 mg/m3 (Tyl et al., 1988). |
| Toxicité subchronique | CME(N)O la plus faible, par inhalation (rat et lapin) = 200 ppm (1 099 mg/m3 (2 lapins/sexe/groupe; 10 rats/sexe/groupe; 4 heures par jour, 5 jours par semaine, pendant 10 mois). Cette concentration a été la seule utilisée au cours de l'étude. Des lésions discrètes causées par une néphrite tubulaire de même qu'une dégénérescence évidente de l'épithélium et la présence de cylindres urinaires hyalins et granuleux ont été observées dans les reins des lapins mâles et femelles ainsi que des rats mâles (mais non des rats femelles) (Truhaut et al., 1979). DME(N)O la plus faible, par voie orale (souris) = 2 % dans de l'eau potable (3 000 mg/kg-p.c./j) (20 souris Swiss CD/sexe/groupe, dose administrée dans de l'eau potable pendant 119 jours), d'après la diminution significative du poids corporel chez les souris mâles F0 lors d'une étude de reproduction continue (Gulati et al., 1985; Morrissey et al., 1989; Chapin et Sloane, 1997) Aucune donnée recensée sur la toxicité subchronique par voie cutanée. |
| Toxicité chronique et cancérogénicité | Aucune donnée recensée sur la toxicité chronique et la cancérogénicité |
| Toxicité sur le plan du réproduction | DME(N)O la plus faible, par voie orale (souris) = 1 000 mg/kg-p.c./j (5 souris mâles/groupe, gavage, 5 semaines), d'après l'atrophie testiculaire dépendante de la dose observée. DSE(N)O = 500 mg/kg-p.c./j (Nagano et al., 1979, 1984) Lors d'une étude de reproduction continue (souris mâles et femelles, dose administrée dans de l'eau potable pendant 2 générations), une DME(N)O de 1,0 % (1 860 mg/kg-p.c./j) a été établie d'après la diminution : du nombre de nouveau-nés par portée; de la viabilité des nouveau-nés; du poids corporel des ftus. À une dose plus élevée (3 000 mg/kg-p.c./j), une réduction significative de l'indice de fertilité et du poids des testicules de même qu'une augmentation importante de l'incidence d'anomalies des spermatozoïdes ont été observées à la génération F0, alors qu'une réduction significative du poids de l'épididyme et de la densité du sperme ainsi que des changements histopathologiques prononcés dans les testicules et l'épididyme ont été observés à la génération F1. Des modifications importantes dans le poids du foie ont aussi été notées à la génération F1. DSE(N)O = 0,5 % (930 mg/kg-p.c./j) (Gulati et al., 1985; Morrissey et al., 1989; Chapin et Sloane, 1997). |
| Toxicité sur le plan du développement | DME(N)O la plus faible, par voie orale (souris) = 1 % dans de l'eau potable (1 860 mg/kg-p.c./j) (souris mâles et femelles, étude de reproduction continue), d'après la diminution significative du nombre de portées par couple fertile et la baisse du poids corporel des ftus et de la viabilité des nouveau-nés, ceci en l'absence de toxicité chez les mères. DSE(N)O = 0,5 % dans de l'eau potable (930 mg/kg-p.c./j) (Gulati et al., 1985; Morrissey et al., 1989; Chapin et Sloane, 1997). DME(N)O la plus faible, par voie cutanée (rat) = 5 826 mg/kg-p.c./j (seule dose testée, 18 rats/groupe, 4 fois par jour, jours de gestion 7 à 16). Une hausse significative de l'incidence des variations cardiovasculaires et squelettiques au niveau des côtes et des vertèbres, un retard de l'ossification, une hausse des résorptions ftales et une diminution du poids corporel des ftus et de leur viabilité ont été notés. Une toxicité chez les mères a également été observée (voir ci-dessus) (Hardin et al., 1984). CME(N)O la plus faible, par inhalation (rat et lapin) = 100 ppm (550 mg/m3) (30 rats F344/groupe, jours de gestation 6 à 15; 24 lapins de la race néo-zélandais blanc/groupe, jours de gestation 6 à 18), d'après la hausse significative de l'incidence des variations viscérales et squelettiques observée chez les ftus. À des concentrations plus élevées (200 à 300 ppm), une hausse significative de l'incidence des variations externes et viscérales (particulièrement au niveau des systèmes cardiovasculaire et rénal chez les deux espèces et au niveau du système pulmonaire chez le lapin), des variations et des malformations squelettiques (en divers sites) chez les ftus, une hausse des résorptions ftales et une réduction du poids corporel et de la viabilité des ftus ont été observées. CSE(N)O = 50 ppm (275 mg/m3). Une toxicité chez les mères a été observée à une concentration de 100 à 300 ppm (voir ci-dessus) (Tyl et al., 1988). |
| Génotoxicité et paramètres connexes : in vivo | Résultats négatifs : Cellules de moelle osseuse de souris après injection intrapéritonéale (Slesinski et al., 1988) |
| Génotoxicité et paramètres connexes : in vitro | Mutagénicité Mutation de souches de l'Escherichia coli WP2uvrA/pKM101, avec et sans activation métabolique (JCIETIC, 2000). Mutation sur le locus HGPRT dans les cellules CHO, avec et sans activation métabolique (Slesinski et al., 1988). Échange de chromatides surs Test de clastogénicité sur des cellules CHO (aucun détail additionnel), résultats positifs avec activation; résultats faiblement positifs sans activation (Slesinski et al., 1988). |
| Sensibilisation | Résultats négatifs sur le cobaye (Zissu, 1995). |
| Irritation | Irritation cutanée Irritation oculaire |
| Paramètre | Doses ou concentrations minimales entraînant un effet/résultats |
|---|---|
| Génotoxicité | Aucune augmentation de l'incidence d'ECS (échange de chromatides surs) ou d'induction de micronoyaux n'a été notée chez 19 travailleurs d'une usine de production de vernis exposés à un mélange d'éthers glycoliques renfermant de l'acétate de 2-éthoxyéthyle, en comparaison avec 15 témoins (l'âge et le tabagisme des sujets et des témoins étaient assez similaires). La concentration d'acétate de 2-éthoxyéthyle dans l'usine de production de vernis se trouvait dans la fourchette de 0,1 à 3,7 ppm (0,55 à 20,34 mg/m3) (Söhnlein et al., 1993). |
| Toxicité sur le plan de la reproduction et du développement | Cycles menstruels Avortement spontané Des conclusions similaires ont été tirées à partir d'études sur des cohortes, notamment une étude rétrospective (561 grossesses chez des femmes exposées et 589 grossesses chez les conjointes des hommes exposés) et une étude prospective (148 femmes), menées dans deux usines de fabrication de semiconducteurs IBM. Parmi les éthers glycoliques utilisés sur les lieux de travail figuraient l'éther diméthylique du diéthylèneglycol et/ou l'acétate de 2-éthoxyéthyle. Lors de l'étude rétrospective de cohorte, des RR significativement accrus d'avortement spontané ont été observés chez les femmes susceptibles d'avoir été exposées à des concentrations élevées (RR 2,8; IC à 95 % = 1,4 à 5,6), mais non chez les conjointes des hommes exposés. Lors de l'étude rétrospective de cohorte, des RR significativement accrus d'avortement spontané ont été observés chez les femmes susceptibles d'avoir été exposées à des concentrations élevées (RR = 2,8; IC à 95 % = 1,4 à 5,6), mais non chez les conjointes des hommes exposés. Les résultats n'étaient pas significatifs. De plus, lors de l'étude rétrospective de cohorte, l'odd-ratio (OR) d'hypofertilité (difficulté à concevoir pendant plus d'un an) était aussi significativement accru chez les femmes susceptibles d'avoir été exposées à des concentrations élevées (440 grossesses, OR = 3,9; IC 95 à % = 1,4 à 11,4), et une hausse non significative des risques d'hypofertilité a été observée chez les conjointes d'hommes susceptibles d'avoir été exposés à des concentrations élevées (495 grossesses, OR = 1,6; IC à 95 % = 0,6 à 3,8). Aucune estimation sur les taux d'exposition n'a été fournie (Gray, 1993; Gray et al., 1996; Correa et al., 1996). Malformations congénitales Lors de deux études cas-témoins, des risques accrus de malformations congénitales ont été associés à l'exposition professionnelle des mères à un mélange d'éthers glycoliques. Une étude (984 cas, 1 134 témoins) visait des travailleurs de diverses occupations en Europe occidentale (Ha et al., 1996; Cordier et al., 1997) et l'autre étude (196 cas, 196 témoins) a été menée en Slovaquie (Cordier et al., 2001). Ces études n'ont fourni aucun renseignement concernant les risques propres à l'exposition à l'acétate de 2-éthoxyéthyle. |
| Effets hématologiques | Une étude transversale a été menée auprès de travailleurs ayant été exposés à de fortes concentrations (n = 29 : 17 hommes et 12 femmes) et de travailleurs n'ayant pas été exposés ou ayant été peu exposés (n = 56 : 29 hommes et 27 femmes) dans une usine de sérigraphie. La concentration moyenne géométrique (CMG) d'acétate de 2-éthoxyéthyle était de 7,4 ppm (fourchette de 1,35 à 16,5 ppm), soit 40,66 mg/m3 (fourchette de 7,42 à 90,68 mg/m3); la CMG chez les travailleuses était de 9,34 ppm (51,2 mg/m3); la CMG chez les travailleurs était de 4,87 ppm (26,8 mg/m3). La CMG chez les travailleurs et travailleuses n'ayant pas été exposés ou ayant été peu exposés (n = 26) était de 0,07 ppm (fourchette d'une concentration non détectable à 3,62 ppm), soit 0,39 mg/m3 (fourchette d'une concentration non détectable à 19,9 mg/m3). Les valeurs moyennes des taux d'hémoglobine et d'hématocrite chez les travailleuses ayant été fortement exposées étaient significativement plus faibles (12 femmes exposées, 27 témoins). Aucun effet n'a été observé chez les hommes exposés (Loh et al., 2003). Lors des enquêtes de suivi menées un an (11 personnes exposées, 24 témoins) ou trois ans (11 personnes exposées, 19 témoins) après la mise en place d'une politique sur le port de gants en caoutchouc et l'amélioration des systèmes de ventilation sur les lieux de travail, plus aucune différence significative sur le plan des paramètres hématologiques n'a été observée entre les femmes ayant été fortement exposées et les femmes témoins. Les auteurs ont affirmé que, puisque l'acétate de 2-éthoxyéthyle est le composant principal du solvant de nettoyage pour les écrans, les travailleurs sont susceptibles d'être exposés à de petites quantités de méthylisobutylcétone et de toluène (Chen et al., 2007). Des effets hématologiques liés à l'exposition à l'acétate de 2-éthoxyéthyle ont été signalés dans une autre étude transversale chez des peintres de chantier naval (hommes) ayant été fortement exposés (n = 30; moyenne d'années de travail = 8,0 ± 5,4 [écart-type]) ou peu exposés (n = 27; moyenne d'années de travail = 11,0 ± 0,7 [écart-type]) et un groupe témoin (principalement des employés de bureau) (n = 41; moyenne d'années de travail = 11,0 ± 6,6 [écart-type]). La concentration MPT d'acétate de 2-éthoxyéthyle dans le scénario de forte exposition était de 3,03 ppm (16,65 mg/m3, atteignant jusqu'à 18,27 ppm (100,4 mg/m3); la concentration MPT d'acétate de 2-éthoxyéthyle dans les zones à faible exposition était de 1,76 ppm (9,67 mg/m3), atteignant jusqu'à 8,12 ppm (44,6 mg/m3). L'occurrence de cas de leucopénie était significativement accrue dans les groupes exposés (6 sur 57 =11 %). Dans le groupe fortement exposé, le nombre moyen de globules blancs et de granulocytes a fortement diminué et le volume corpusculaire moyen a augmenté significativement en comparaison avec le groupe témoin. Les travailleurs faisant partie des groupes exposés étaient aussi exposés à d'autres substances chimiques (toluène, xylène, butanol, éthylbenzène, alcool isopropylique, éthanol, acétate d'éthyle, acétate de butyle, méthylisobutylcétone et nonane), mais non à d'autres éthers glycoliques (Kim et al., 1999). |