Évaluation préalable pour le Défi concernant le
Archivée
3-[Éthyl[3-méthyl-4-[(6-nitrobenzothiazol-2-yl)azo]phényl] amino]propiononitrile
(Disperse Red 179)
Numéro de registre du Chemical Abstracts Service
16586-42-8
3-[[4-[(5,6-Dichlorobenzothiazol-2-yl)azo]phényl] éthylamino]propiononitrile
(DAPEP)
Numéro de registre du Chemical Abstracts Service
25176-89-0
Environnement Canada
Santé Canada
Mars 2010
- Sommaire
- Introduction
- Identité de la substance
- Définition des substances analogues et estimation des proprités physiques et chimiques
- Sources
- Utilisations
- Rejets dans l'environnement
- Devenir dans l'environnement
- Persistance et potentiel de bioaccumulation
- Potentiel d'effets nocifs écologiques nocifs
- Potentiel d'effets nocifs sur la santé humaine
- Conclusion
- Références
- Annexe 1 : Sommaire de rigueur d'études pour les études clés
- Annexe 2 : Table de résumé des données du modèle BTP
- Annexe 3 : Estimations de la limite supérieure de l'exposition au Disperse Red 179 et au DAPEP découlant des textiles
- Annexe 4 : Estimations de l'exposition découlant des textiles teints
- Annexe 5 : Prévisions des modèles R(Q)SA pour le Disperse Red 179 (16586-42-8) et ses produits de clivage azoïques potentiels
- Annexe 6 : Produits de clivage azoïques potentiels et analogues structurels du Disperse Red 179
- Annexe 7 : Prévisions des modèles R(Q)SA pour le DAPEP (isomère 5,6-dichloro du Disperse Red 153), l'isomère 6,7-dichloro du Disperse Red 153 et leurs produits de clivage azoïques potentiels
- Annexe 8 : Produits de clivage azoïques potentiels et analogues structurels du DAPEP (isomère 5,6-dichloro) et du Disperse Red 153 (mélange d'isomères)
Conformément à l'article 74 de la Loi canadienne sur la protection de l'environnement, 1999[LCPE (1999)], les ministres de l'Environnement et de la Santé ont effectué une évaluation préalable du 3-[[4-[(5,6-Dichlorobenzothiazol-2-yl)azo]phényl] éthylamino]propiononitrile (Disperse Red 179), dont le numéro de registre du Chemical Abstracts Service est 16586-42-8; et du 3-[[4-[(5,6-Dichlorobenzothiazol-2-yl)azo]phényl] éthylamino]propiononitrile (DAPEP), dont le numéro de registre du Chemical Abstracts Service est 25176-89-0. Ces substances ont été identifiées lors de l'évaluation préalable comme hautement prioritaires et incluses dans le cadre du défi, car elles se sont avérées répondre aux critères de catégorisation écologiques de persistance, de potentiel de bioaccumulation et de toxicité intrinsèque pour les organismes non humains et que l'on pense être commercialisées au Canada.
Les substances Disperse Red 179 et DAPEP n'ont pas été considérées comme hautement prioritaires pour l'évaluation des risques potentiels pour la santé humaine, d'après l'application de la simple exposition et des outils de danger développés par Santé Canada pour la catégorisation de substances dans la Liste intérieure des substances. Par conséquent, cette évaluation est centrée sur les renseignements correspondant à l'évaluation des risques écologiques.
Le Disperse Red 179 et le DAPEP sont des substances organiques utilisées au Canada principalement comme agents de teinture rouge pour fibres synthétiques des vêtements et textiles domestiques. En raison de leur structure et de leur usage similaires, le Disperse red 179 et le DAPEP sont évalués ensemble dans ce rapport.Ces substances ne sont pas naturellement produites dans l'environnement. Leur fabrication n'est pas signalée au Canada; toutefois, 400 kg de Disperse Red 179 et 100 kg de DAPEP ont été importés dans le pays en 2006 pour être utilisés dans l'industrie du textile.
D'après des modèles d'utilisation signalés au Canada et certaines hypothèses, la plupart de ces substances devraient finir dans des sites d'élimination des déchets. Environ 17 % du Disperse Red 179 et du DAPEP sont estimés être rejetés dans l'eau et aucun rejet n'est prédit dans l'air et dans le sol.Le Disperse Red 179 et le DAPEP présentent une solubilité très faible dans l'eau et l'octanol (d'après des données analogues et modélisées). Le Disperse Red 179 et le DAPEP sont présents dans l'environnement principalement sous forme de particules fines non volatiles, ils sont relativement stables d'un point de vue chimique, ils ont tendance à se répartir dans les sédiments, sous l'action de la pesanteur, s'ils sont rejetés dans les eaux de surface et ils se répartiraient probablement dans les sols s'ils étaient rejetés dans l'air.
D'après leurs propriétés physiques et chimiques ainsi que des données expérimentales de biodégradation, le Disperse Red 179 et le DAPEP devraient être persistants dans l'environnement, soit dans tous les milieux dans des conditions aérobies. De nouvelles données expérimentales sur des analogues, des données modélisées ainsi que l'avis des experts indiquent que ces teintures présentent un faible potentiel d'accumulation dans les tissus adipeux des organismes. Les substances répondent donc aux critères de persistance, mais non à ceux de bioaccumulation énoncés dans le Règlement sur la persistance et la bioaccumulation.En outre, de nouvelles données sur la toxicité de produits chimiques analogues indiquent que ces substances représentent un danger faible à modéré pour les organismes aquatiques.
Aux fins de la présente évaluation préalable, deux scénarios d'exposition très prudents représentant les rejets industriels et domestiques dans l'environnement aquatique ont été appliqués. Le premier scénario simulait le rejet du Disperse Red 179 et du DAPEP dans l'environnement aquatique après l'utilisation de chaque teinture dans une opération industrielle.Le deuxième scénario simulait le rejet du Disperse Red 179 et du DAPEP dans l'environnement aquatique après leur utilisation domestique.Les concentrations environnementales prévues dans l'eau pour chaque scénario étaient inférieures aux concentrations sans effet prévues, calculées pour les organismes pélagiques.
L'exposition potentielle de la population générale au Disperse Red 179 et au DAPEP présents dans les milieux naturels devrait être négligeable. L'exposition au Disperse Red 179 et au DAPEP par les produits de consommation devrait être faible compte tenu de l'utilisation prévue du produit (teinture dans les textiles synthétiques) dans le cas d'expositions fortuites, notamment lorsque de jeunes enfants portent ces produits à leur bouche.
Les données empiriques limitées définies pour Disperse Red 179 et au DAPEP, les métabolites et analogues potentiels, ensemble avec les relations quantitatives structure-activités (RQSA),. Les prédictions semblent indiquer que ces substances peuvent présenter un risque potentiel pour la santé humaine.
Bien que les données empiriques limitées indiquent un risque d’exposition au Disperse Red 179 et au DAPEP, l’expossition de la population canadienne à ces substances en raison de leur utilisation dans les textiles devrait être faible. Par conséquent, le risque pour la santé humaine est faible.
D'après les informations disponibles, le Disperse Red 179 et le DAPEP ne répondent à aucun critère de l'article 64 de la Loi canadienne sur la protection de l'environnement, 1999.
Puisque ces substances sont inscrites sur la Liste intérieure des substances, leur importation et leur fabrication au Canada ne requièrent pas de déclaration aux termes du paragraphe 81(1). Étant donné les propriétés dangereuses potentielles de ces substances, on craint que des utilisations nouvelles non décelées ni évaluées fassent en sorte qu'elles répondent aux critères de l'article 64 de la LCPE (1999). Par conséquent, il est recommandé de modifier la Liste intérieure des substances en vertu du paragraphe 87(3) de la Loi afin d'indiquer que le paragraphe 81(3) s'applique à ces substances. Ainsi, toute fabrication, importation ou utilisation de ces dernières devra être déclarée et faire l'objet d'une évaluation des risques pour l'environnement et la santé humaine
De plus, des activités de recherche et de surveillance viendront, le cas échéant, appuyer la vérification des hypothèses formulées au cours de l'évaluation préalable.
La Loi canadienne sur la protection de l'environnement, 1999[LCPE (1999)] (Canada 1999) exige que les ministres de l'Environnement et de la Santé procèdent à une évaluation préalable des substances qui répondent aux critères de la catégorisation énoncés dans la Loi, afin de déterminer si elles présentent ou sont susceptibles de présenter un risque pour l'environnement ou la santé humaine.
D'après les informations obtenues dans le cadre de la catégorisation, les ministres ont identifié un certain nombre de substances hautement prioritaires pour lesquelles entreprendre une action. Ces substances comprennent celles qui
- répondent à tous les critères environnementaux de la catégorisation, notamment la persistance (P), le potentiel de bioaccumulation (B) et la toxicité intrinsèque pour les organismes aquatiques (Ti), et que l'on pense être commercialisées au Canada et/ou
- répondent aux critères de catégorisation pour le plus fort risque d'exposition (PFRE) ou qui présentent un risque d'exposition intermédiaire (REI) et qui ont été jugées particulièrement dangereuses pour la santé humaine, compte tenu des classifications qui ont été établies par d'autres organismes nationaux ou internationaux concernant leur cancérogénicité, leur génotoxicité ou leur toxicité pour le développement ou la reproduction.
Le 9 décembre 2006, les ministres ont donc publié un avis d'intention dans la Partie I de la Gazette du Canada(Canada, 2006), qui encourageait l'industrie et les autres intervenants intéressés à fournir dans des délais précis, des renseignements spécifiques qui pourraient servir à étayer l'évaluation des risques et à élaborer les meilleures pratiques en matière de gestion des risques et en intendance des produits pour les substances jugées hautement prioritaires.
Les substances 3-[[4-[(5,6-Dichlorobenzothiazol-2-yl)azo]phényl] éthylamino]propiononitrile (Disperse Red 179) et 3-[[4-[(5,6-Dichlorobenzothiazol-2-yl)azo]phényl] éthylamino]propiononitrile (DAPEP), ont été identifiées comme hautement prioritaires pour l'évaluation du risque écologique, car elles se sont révélées persistantes, bio-accumulatives et naturellement toxiques pour les organismes aquatiques et sont supposées être commercialisées au Canada. Le Défi portant sur ces substances a été publié dans la Gazette du Canadale 30 août 2008 (Canada, 2008).En même temps, un profil pour chaque substance a été publié.Ces profils présentaient les informations techniques obtenues avant décembre 2005 et sur lesquelles reposait leur catégorisation.En réponse au Défi, des soumissions d'informations relatives à la persistance, au danger et à l'utilisation de ces substances ont été reçues.
Bien que le Diperse Red 179 et le DAPEP aient été déterminés comme hautement prioritaires pour l'évaluation par rapport à l'environnement, ils ne répondaient pas aux critères du plus fort risque d'exposition ou du risque d'exposition intermédiaire et un danger élevé pour la santé humaine d'après les classifications de cancérogénicité, de génotoxicité, de toxicité pour le développement ou la reproduction établies par d'autres organismes nationaux ou internationaux.
Les évaluations préalables effectuées aux termes de la LCPE (1999) mettent l'accent sur les renseignements jugés essentiels pour déterminer si une substance répond aux critères de l'article 64 de la Loi.
Les évaluations préalables étudient les renseignements scientifiques et tirent des conclusions en intégrant sur la méthode du poids de la preuve et le principe de précaution.
La présente évaluation préalable prend en considération les renseignements sur les propriétés chimiques, les dangers, les utilisations de la substance en question et l’exposition à celle-ci, y compris l’information supplémentaire fournie dans le cadre du Défi. Des données pertinentes à l'évaluation préalable de cette substance sont tirées de publications originales, de rapports de synthèse et d’évaluation, de rapports de recherche de parties intéressées et d’autres documents consultés au cours de recherches documentaires menées récemment, jusqu'au 31 décembre 2009.. Les informations disponibles et pertinentes présentées dans les évaluations du danger d'autres juridictions ont été prises en compte.L'évaluation préalablene constitue pas un examen exhaustif ou critique de toutes les données disponibles. Elle présente plutôt les études les plus critiques et les éléments de preuve relatifs à la conclusion.
Le Disperse Red 179 et le DAPEP sont évalués ensemble dans ce rapport d'évaluation préalable Les données sur les propriétés physiques et chimiques de ces teintures manquent et vu les similitudes de leur structure et de leur usage respectifs, des analogues acceptables ont été identifiés et possèdent des données pertinentes soutenant l'évaluation écologique de ces deux teintures.
La présente évaluation préalable a été préparée par le personnel du Programme des substances existantes de Santé Canada et d’Environnement Canada et elle intègre les résultats d’autres programmes exécutés par ces ministères. La section écologique de la présenteévaluation a fait l'objet d'une étude consignée par des pairs ou d'une consultation de ces derniers. Par ailleurs, l'ébauche de cette évaluation préalable a fait l’objet d’une période de commentaires du public de 60 jours.Alors que les commentaires externes aient été pris en considération, Santé Canada et Environnement Canada assument la responsabilité du contenu final et des résultats de l'évaluation préalable.Les principales données et considérations sur lesquelles repose la présente évaluation sont résumées ci-après
Pour les besoins de ce document, la substance 3-[[4-[(5,6-Dichlorobenzothiazol-2-yl)azo]phényl] éthylamino]propiononitrile- (n° CAS16586-42-8), sera appelée Disperse Red 179, au lieu de NBATP, qui était utilisé dans le profil de substance. Le « Disperse Red 179 » est défini par le Colour Index (CII 2002-) comme une combinaison de deux numéros de registre CAS(n° CAS 61951-64-2 et n° CAS16195-64-8). Les substances associées aux n° CAS16586-42-8 et 61951-64-2 sont identiques, car toutes deux ont des noms scientifiques identiques (NCI, 2009), des structures chimiques identiques (ChemID, 2009; CII, 2002-) et le même numéro du Colour Index, C.I. 11290 (CII, 2002-). D'après le Colour Index, une substance chimique précise peut avoir plus d'un n° CAS, notamment dans le domaine des teintures, selon que la substance a été déclarée au Chemical Abstracts sous son nom chimique complet ou sous son nom C.I. générique (CII 2002-). Ainsi, dans cet exemple particulier, le n° CAS 61951-64-2 se rapporte au nom C.I. Disperse Red 179, alors que le n° CAS16586-42-8 correspond en fait au nom chimique 3-[[4-[(5,6-Dichlorobenzothiazol-2-yl)azo]phényl] éthylamino]propiononitrile]. Cependant, le n° CAS16195-64-8 ne se trouve pas sur la liste d'inventaire du Chemical Abstract Service (NCI, 2009) et aucune substance n'est ni n'a jamais été associée à ce n° CAS(Chemical Abstract Service, communication personnelle, source non citée). Par conséquent, le Disperse Red 179 n'est pas un mélange de deux numéros CAS, mais un produit chimique discret listé sous le n° CAS 16586428 (voir le tableau 1a).
La substance 3-[[4-[(5,6-Dichlorobenzothiazol-2-yl)azo]phényl] éthylamino]propiononitrile (n° CAS25176-89-0), est parfois appelée Disperse Red 153. Toutefois, le Disperse Red 153, qui est enregistré sous le n° CAS78564-87-1 (CI 111370), est en fait un mélange de deux isomères structurels (Nakagawa, 1996; CII, 2002- ). Un isomère est enregistré sous le n° CAS25176-89-0 (C.I. 111371) et l'autre n'a pas de n° CASenregistré, mais un numéro d'enregistrement du Colour Index, C.I. 111372 (CII 2002- ). Ces deux substances sont des isomères structurels (même formule chimique); dès lors, on prévoit que les propriétés du mélange chimique ressemblent beaucoup à celles du n° CAS 25176-89-0. Aux fins du présent document, le n° CAS 25176-89-0 sera appelé le DAPEP, un acronyme tiré de son nom d'inventaire (voir tableau 1b).
Tableau 1 a. Identité de la substance pour le Disperse Red 179
| Numéro de registre du Chemical Abstracts Service (n° CAS) | 16586-42-8 |
| Nom dans la LIS | 3-[Éthyl[3-méthyl-4-[(6-nitrobenzothiazol-2-yl)azo]phényl] amino]propiononitrile |
| Noms1 du National Chemical Inventories (NCI) | 3-[Éthyl[3-méthyl-4-[(6-nitrobenzothiazol-2-yl)azo]phényl] amino]propiononitrile- (TSCA) 3-[Éthyl[3-méthyl-4-[(6-nitrobenzothiazol-2-yl)azo]phényl] amino]propiononitrile- (AICS, PICCS, ASIA-PAC) 3-[Éthyl[3-méthyl-4-[(6-nitrobenzothiazol-2-yl)azo]phényl] amino]propiononitrile (EINECS, ECL) C.I. Violet Disperse 052 (ECL) C.I. ROUGE DISPERSE 179 (PICCS) |
| Autres noms | 3-[N-Ethyl-4-[(6-nitro-2-benzothiazolyle)azo]-m-toluidino]propionitrileC.I. 112290, C.I. Violet Disperse 52 Rouge Disperse79, Violet Disperse 52 Kayalon Polyester Rubine BL-SKayalon Polyester Rubine BL-S 200 Propionitrile, 3-[N-éthyl-4-[(6-nitro-2-benzothiazolyl)azo]-m-toluidino]-3-(éthyle{3-méthyl-4-[(6-nitrobenzothiazol-2-yl)azo]phényle}amino)propiononitrile |
| Groupe chimique (LIS) | Produits chimiques organiques définis |
| Principale classe chimique ou utilisation | Colorant azoïque organique dispersé |
| Principale sous-classe chimique | Colorant benzothiazole mono-azoïque |
| Formule chimique | C19H18N6O2S |
| Structure chimique |  |
| SMILES2 | N(=O)(=O)c(ccc(nc(N=Nc(c(cc(N(CCC(#N))CC)c1)C)c1)s2)c23)c3 |
| Masse moléculaire | 394,45 g/mol |
| 1 National Chemical Inventories (NCI), 2009; AICS (Inventaire australien des substances chimiques); ASIA-PAC (Listes des substances Asie-Pacifique); ECL (Liste coréenne des produits chimiques existants); EINECS (Inventaire européen des substances chimiques commerciales existantes); PICCS (Inventaire philippin des produits et des substances chimiques); TSCA (Inventaire des substances chimiques de la Loi sur le contrôle des substances toxiques). 2 Simplified Molecular Line Input Entry System (SMILES). |
|
Tableau 1b. Identité de substance pour le DAPEP
| Numéro de registre du Chemical Abstracts Service (n° CAS) | 25176-89-0 |
| Nom dans la LIS | 3-[[4-[(5,6-Dichlorobenzothiazol-2-yl)azo]phényl] éthylamino]propiononitrile |
| Noms1 du National Chemical Inventories (NCI) | 3-[[4-[(5,6-Dichlorobenzothiazol-2-yl)azo]phényl] éthylamino]propiononitrile- (AICS, PICCS, ASIA-PAC) 3-[[4-[(5,6-Dichlorobenzothiazol-2-yl)azo]phényl]éthylamino]propiononitrile(EINECS) 3-[[4-[(5,6-Dichlorobenzothiazol-2-yl)azo]phényl] éthylamino]propionontrile (PICCS) |
| Autres noms | Propionitrile, 3-[p-[(5,6-dichloro-2-benzothiazolyl)azo]-N-ethylanilino]-3-({4-[(5,6-Dichlorobenzothiazol-2-yl)azo]phényl}éthylamino)propiononitrile |
| Groupe chimique (LIS) | Produits chimiques organiques définis |
| Principale classe chimique ou utilisation | Colorant azoïque organique dispersé |
| Principale sous-classe chimique | Colorant benzothiazole mono-azoïque |
| Formule chimique | C18H15Cl2N5S |
| Structure chimique |  |
| SMILES | c12N=C(N=Nc3ccc(N(CC)CCC(#N))cc3)Sc1cc(Cl)c(Cl)c2 |
| Masse moléculaire | 404,32 g/mol |
| 1 National Chemical Inventories (NCI), 2009; AICS (Inventaire australien des substances chimiques); ASIA-PAC (Listes des substances Asie-Pacifique); EINECS (Inventaire européen des substances chimiques commerciales existantes); PICCS (Inventaire philippin des produits et des substances chimiques). 2 Simplified Molecular Line Input Entry System (SMILES). |
|
Peu de données expérimentales sont disponibles pour le Disperse Red 179 ou le DAPEP. Lors de l'atelier sur les relations quantitatives structure-activité (RQSA) parrainé par Environnement Canada en 1999 (Environnement Canada, 2000), les experts en modélisation invités ont identifié de nombreuses classes structurelles de pigments et de teintures en « difficiles à modéliser », à l'aide des RQSA.Les propriétés physiques et chimiques de plusieurs classes structurelles de teintures et de pigments (y compris les teintures acides et dispersées) ne sont pas soumises à une prédiction de modèles, car elles sont considérées comme « hors du domaine de modèles d'applicabilité » (par exemple les domaines de paramètres structurels et/ou de propriété).En conséquence, pour déterminer l'utilité potentielle, les domaines d'applicabilité des domaines RQSA aux teintures et aux pigments sont évalués au cas par cas.
Environnement Canada a estimé qu'il était inapproprié d'utiliser des modèles RQSA pour prévoir la plupart des propriétés physiques et chimiques du Disperse Red 179 et du DAPEP et, par conséquent, il a eu recours à une méthode fondée sur les données déduites à partir d'analogues afin de déterminer les propriétés physiques et chimiques approximatives données au tableau 3. Ces propriétés ont été utilisées par la suite pour d'autres modélisations et éléments d'information au cours de cette évaluation.
Un analogue est un produit chimique structurellement similaire à la substance en évaluation et doit par conséquent avoir des propriétés physiques et chimiques similaires, un comportement similaire dans l'environnement et/ou une toxicité similaire. Si des données expérimentales sont disponibles pour un paramètre spécifique lié à une substance analogue, on peut utiliser ces dernières, directement ou après modification, pour estimer la valeur du paramètre concerné pour la substance évaluée.
Pour trouver des analogues acceptables, une revue des données pour plusieurs colorants azoïques dispersés a été effectuée (Anliker et al., 1981; Anliker et Moser, 1987; Baughman et Perenich, 1988; Savarino et al., 1989; Yen et al., 1989; Yen et al., 1991; Brown, 1992; Peters et Gbadamosi, 1992; Peters et al., 1992; ETAD, 1995; Sijm et al., 1999; Maradiya, 2004). Ces composés possèdent des similitudes structurelles au Disperse Red 179 et au DAPEP, mais partagent également d'autres caractéristiques importantes qui en font des analogues convenables.Ces dernières comprennent des propriétés affectant leur devenir dans l'environnement, comme des masses moléculaires élevées (généralement > 320 g/mol), des diamètres transversaux similaires (de 1,31 à 2,11 nm), des structures de particules solides, une décomposition à plus de 110 °C et une « dispersibilité » dans l'eau (c.-à-d. pas réellement « solubles »). De plus, elles ont une pression de vapeur négligeable et sont conçues pour être stables en conditions environnementales.
Le Disperse Red 179 et le DAPEP sont des substances analogues en raison des similitudes de leur structure chimique et de leur masse moléculaire Les deux substances contiennent les groupes fonctionnels azoïque, benzothiazyle et cyanuré et tous deux sont utilisés comme colorants pour textiles.Cependant, il faut s'attendre à de légères différences au niveau des propriétés physiques et chimiques et du comportement entre les deux substances. On prévoit que le Disperse Red 179 a une plus grande solubilité dans l'eau et un plus faible log Koe que le DAPEP en raison de la présence d'un groupe nitré fixé à son noyau benzothiazyle.De façon similaire, les deux atomes de chlore fixés au groupe benzothialzyle du DAPEP vont probablement diminuer sa solubilité dans l'eau et augmenter son log Koe.
L'information structurelle relative aux colorants azoïques dispersés analogues du Disperse Red 179 et du DAPEP est présentée dans les tableaux 2a et 2b. Certaines propriétés physiques et chimiques (voir le tableau 3), données empiriques sur la bioaccumulation (voir le tableau 6) et données empiriques sur la toxicité (voir le tableau 7) de ces analogues ont été utilisées pour établir le poids de la preuve et pour appuyer les décisions présentées dans cette ébauche d'évaluation préalable.
Tableau 2a. Information disponible pour le Disperse Red 179 et le DAPEP ainsi que pour plusieurs analogues structurels
| n° CAS | Nom commun | Nom dans la LIS | Structure chimique de l'analogue | Données empiriques disponibles | |
|---|---|---|---|---|---|
| i. | 25176-89-0 | DAPEP | 3-[[4-[(5,6- Dichloro- benzothiazol-2- yl)azo]phényl] éthylamino] propiononitrile |
 |
Persistance, toxicité aquatique |
| ii. | 16586-42-8 | Disperse Red 179 | 3-[Éthyl[3- méthyl-4-[(6- nitrobenzothiazol- 2-yl)azo]phényl] amino] propiononitrile- |
 |
Persistance, toxicité aquatique |
| iii. | 68133-69-7 | s.o. | Propanenitrile, 3-((2-(acétyloxy) éthyl)(4-(2-(6- nitro-2- benzothiazolyl) diazényl)phényl) amino)- |
 |
Point de fusion, solubilité dans l'octanol, solubilité dans l'eau, log Koe |
| iv | 70198-17-3 | s.o. | Ethanol, 2-((4- (2-(6-chloro-2- benzothiazolyl) diazenyl)phényle) éthylamino)-, 1-acétate |
 |
Toxicité pour les organismes aquatiques |
| v | 5261-31-4 | Disperse Orange 30 | Acétate de 2- [N-(2-cyanoéthyl)- 4-[2,6-dichloro-4- nitrophényl)azo] anilino]éthyle |
 |
Facteur de bioconcentration; (FBC), toxicité aquatique |
| vi. | 31482-56-1 | Disperse Orange 25 | Propanenitrile, 3- (Ethyl(4-((4- nitrophenyl)azo) phenyl)amino)- |
 |
Toxicité pour les organismes aquatiques |
| vii | 3179-89-3 | Disperse Red 17 | Ethanol, 2,2¢-((3- méthyl-4-(2-(4- nitrophényl)diazényl) phényl)amino)bis- |
 |
Toxicité pour les organismes aquatiques |
| viii | 16889-10-4 | Disperse Red 73 | 2-({4-[(2- Cyanoéthyl)(2- phényléthyl)amino] phenyl}azo)-5- nitrobenzonitrile |
 |
Toxicité pour les organismes aquatiques |
Il faut souligner que l'on dénombre diverses incertitudes liées à l'utilisation des données disponibles sur les propriétés physiques et chimiques, la toxicité et la bioaccumulation des substances qui apparaissent dans le tableau 2a. Toutes ces substances appartiennent à la même classe chimique, soit celle des colorants azoïques dispersés (caractérisés par une liaison azoïque) et ont, en majorité, des masses moléculaires semblables (tableau 3b) et sont utilisées à des fins industrielles similaires. Toutefois, il existe des différences entre ces substances associées à leurs différences de taille moléculaire et leur groupe fonctionnel unique, notamment la présence ou l'absence des groupes fonctionnels benzothiazyle, cyano, nitro et/ou ester, ou la présence d'atomes halogènes, comme du chlore sur l'un des noyaux aromatiques. De plus, les différences de résultats pour des substances peuvent également être dues à une erreur analytique pendant les essais. Il en découle que ces analogues ont des valeurs empiriques déterminées de solubilité dans l'eau qui varient de plus de quatre ordres de grandeur, soit dans une plage allant de 10-5 à 0,69 mg/L. Il serait préférable d'utiliser des données empiriques (par exemple pour l'hydrosolubilité et le log Koe) propres aux substances soumises à une évaluation. Toutefois, en raison du manque de données dans tous les domaines pour les teintures dispersées monoazoïques au benzothiazyle, les données analogues présentées sont considérées comme la seule preuve raisonnable pour l'évaluation de ces deux substances. La variabilité des données disponibles a été prise en compte.
Tableau 2b. Comparaison des analogues structuraux et le Disperse Red 179 et le DAPEP1
| n° CAS | Nom commun | Masse moléculaire (g/mol) | Similarité structurelle | Diamètre transversal minimum et maximum (DMax) en (nm) | ||
|---|---|---|---|---|---|---|
| par rapport au Disperse Red 179 (%) | par rapport au DAPEP (%) | |||||
| 1 ChemID (2009); valeur présentée si > 60 %. Le tableau 3 contient les propriétés physiques et chimiques expérimentales et modélisées du Disperse Red 179 et du DAPEP, ainsi que des analogues structurels qui se rapportent à leur devenir dans l'environnement. |
||||||
| i. | 16586-42-9 | Disperse Red 179 | 394,45 | 100 | 82,33 | 1,31–2,11 |
| ii. | 25176-89-0 | DAPEP | 404,32 | 82,33 | 100 | 1,41–2,08 |
| iii. | 68133-69-7 | s.o. | 438,5 | 89,76 | 78,47 | 1,96–2,32 |
| iv | 70198-17-3 | s.o. | 402,90 | 73,71 | 84,2 | 1,87–2,31 |
| v | 5261-31-4 | Disperse Orange 30 | 450,28 | < 60 | < 60 | 1,40–2,10 |
| vi. | 31482-56-1 | Disperse Orange 25 | 323,35 | < 60 | < 60 | 1,37–1,95 |
| vii | 3179-89-3 | Disperse Red 17 | 344,36 | < 60 | < 60 | 1,41–1,86 |
| viii | 16889-10-4 | Disperse Red 73 | 348,36 | < 60 | < 60 | 1,31–1,93 |
Tableau 3. Propriétés physiques et chimiques du Disperse Red 179, du DAPEP et d'analogues disponibles
| Produit chimique | Type1 | Valeur | Température (°C) |
Référence |
|---|---|---|---|---|
| 1 Les valeurs extrapolées utilisées pour le Disperse Red 179 et le DAPEP sont basées sur l'évidence sur les teintures dispersées présentées à Environnement Canada dans le cadre des Règles de notification des nouvelles substances (Produits chimiques et polymères) (ETAD, 1995) et les preuves disponibles auprès d'autres analogues de teinture dispersée trouvées dans la littérature. 2 L'expression « point de fusion » est utilisée, mais serait mieux définie par un point de décomposition, car les teintures dispersées sont connues pour se carboniser à de fortes températures (supérieures à 200 °C) au lieu de fondre. 3 La valeur inférieure du point de fusion mesurée par Peters et Gbadamosi (1992) peut provenir d'une erreur analytique ou d'une variation dans les mesures. 4 Cette valeur de point de fusion se réfère à l'isomère structurel du n° CAS25176-89-0 qui, avec le DAPEP, constitue le mélange n° CAS 78564-87-1. 5 Le point d'ébullition ne s'applique généralement pas aux teintures dispersées. Pour les teintures en poudre, la carbonisation ou la décomposition interviennent à de fortes températures au lieu de bouillir.Pour les liquides et les pâtes, l'ébullition ne se produit que pour le composant solvant, alors que le solide non évaporé se décompose ou se carbonise (ETAD, 1995). 6 La solubilité de plusieurs teintures dispersées à 25 et 80 °C a été utilisée par Baughman et Perenich (1988) pour calculer la constante de la Loi de Henry pour ces teintures. Ces valeurs sont présentées ici sous forme de plage, afin d'illustrer la constante attendue de la Loi de Henry pour le Red Disperse 179 et le DAPEP. 7 Ces valeurs ont été modélisées à l'aide de la « Méthode expérimentale d'ajustement des valeurs » de KOWWIN (2000), qui estimait le log Koe des substances d'après la valeur expérimentale du log Koe de 4,08 pour le no CAS analogue 68133-69-7 (Sijm et al., 1999). 8 Les valeurs expérimentales du log Koe ont été mesurées par Yen et al., (1989) au point de saturation de la teinture, à l'aide de la méthode d'équilibrage des lots. Cette valeur est faiblement fiable, dans la mesure où les systèmes de lots ne sont pas l'idéal pour déterminer de grands coefficients de partage (Yen et al., 1989). 9 Cette valeur expérimentale du log Koe(qui représente une estimation de limite inférieure) a été déterminée à l'aide de la méthode de brassage lent (De Bruijn et al., 1989). 10 Les valeurs du log Kco sont basées sur des calculs réalisés par Baughman et Perenich (1988) à l'aide d'une plage de solubilités mesurées pour des teintures commerciales et un point de fusion supposé de 200 °C. 11 Ces valeurs ont été modélisées à l'aide de la « Méthode expérimentale d'ajustement des valeurs » de WATERNT (2002), qui estimait la solubilité des substances dans l'eau d'après les valeurs de solubilité dans l'eau du n° CAS analogue 68133-69-7. La solubilité dans l'eau de l'analogue (0,0485 55 mg/L) est une moyenne géométrique des valeurs expérimentales de solubilité du n° CAS68133-69-7 (Sijm et al., 1999). 12 La variation de la valeur de solubilité dans l'eau s'explique par la forme polymorphe de la structure cristalline des teintures. Chaque forme morphologique possède son propre point de fusion et son enthalpie de fusion, ce qui donne une solubilité différente (Sijm et al., 1999). |
||||
| État physique | ||||
| Disperse Red 179 | Poudre | Environnement Canada, 2009a | ||
| Poudre granulaire | Sarex Overseas, 1995 | |||
| DAPEP | Poudre | Environnement Canada, 2009a | ||
| Disperse Red 153 (n° CAS 78564-87-1) | Analogue | Poudre ou granulé rougeâtre | S.M.S Technology, non daté | |
| Point de fusion2(°C) | ||||
| DAPEP | Expérimental | 219-220 | Peters et al., 1992 | |
| 177-1803 | Peters et Gbadamosi, 1992 | |||
| N° CAS inconnu (Isomère structurel du DAPEP) | Expérimental (analogue) | 181-1824 | Peters et al., 1992 | |
| N° CAS 68133-69-7 | Expérimental (analogue) | 172 | Yen et al., 1989 | |
| 167 | Sijm et al., 1999 | |||
| N° CAS 3771-31-1 | Expérimental (analogue) | 228-230 | Maradiya, 2004 | |
| N° CAS 68083-97-6 | Expérimental (analogue) | 242-243 | Maradiya, 2004 | |
| Disperse Orange 30 | Expérimental (analogue) | 126,9-128,5 | ETAD, 2005 | |
| Colorants benzothiazyles azoïques dispersés | Données déduites à partir d'analogues | 114-230 | Peters et al., 1992 | |
| 141-269 | Peters et Gbadamosi, 1992 | |||
| 119-243 | Savarino et al., 1989 | |||
| Point d'ébullition5 (°C) | ||||
| Non applicable | ||||
| Densité (kg/m3) | ||||
| Disperse Red 153 (no CAS 78564-87-1) | Non disponible | 950 | S.M.S Technology, non daté | |
| Pression de vapeur (Pa) | ||||
| Colorants azoïques dispersés | Données déduites à partir d'analogues | 5.33 × 10-12 à 5,33 × 10-5 (4 ×10-14 à 4 × 10-7 mm Hg) | 25 | Baughman et Perenich, 1988 |
| Constante de la loi de Henry (Pa·m3/mol) | ||||
| Colorants azoïques dispersés | Données déduites à partir d'analogues6 | 10-8 à 0,1 (10-13 à 10-6 atm m3/mol) | Baughman et Perenich, 1988 | |
| Log Koe(coefficient de partage octanol-eau) (sans dimensions) | ||||
| Disperse Red 179 | Modelisé7 | 5,09 | KOWWIN, 2000 | |
| DAPEP | Modelisé7 | 6,01 | KOWWIN, 2000 | |
| N° CAS68133-69-7 | Expérimental (analogue) | 4,6 (± 3,35)8 | Yen et al., 1989 | |
| 4,089 | Sijm et al., 1999 | |||
| Disperse Orange 30 | Expérimental (analogue) | 4,2 | Brown, 1992 | |
| Colorants azoïques dispersés | Données déduites à partir d'analogues | 1,79 à 5,07 | Baughman et Perenich, 1988 | |
| > 2 à 5,1 | Anliker et al., 1981; Anliker et Moser, 1987 | |||
| de 3,74 à > 5,8 | Sijm et al., 1999 | |||
| Log Koe(coefficient de partage du carbone organique) (sans dimensions) | ||||
| Colorants azoïques dispersés | Données déduites à partir d'analogues, calculé10 | 3,4 à 4,2 | Baughman et Perenich, 1988 | |
| Solubilité dans l'eau (mg/L) | ||||
| Disperse Red 179 | Modélisé11 | 0,0119 18 | WATERNT, 2002 | |
| DAPEP | Modélisé11 | 0,004 2083 | WATERNT, 2002 | |
| N° CAS 68133-69-7 | Expérimental (analogue) | 0,021 ± 0,004 0,690 ± 0,17012 | Sijm et al., 1999 | |
| 0,0079 ± 0,0014 | Yen et al., 1989 | |||
| Colorants azoïques dispersés | Données déduites à partir d'analogues | < 0,01 | Anliker et Moser, 1987 | |
| 1,19 × 10-5 à 35,46 | Baughman et Perenich, 1988 | |||
| Solubilité dans le n-octanol (mg/L) | ||||
| N° CAS 68133-69-7 | Expérimental (analogue) | 66 ± 6 | Sijm et al., 1999 | |
| Colorants azoïques dispersés | Données déduites à partir d'analogues | 81 à 2 430 | 20 | Anliker et Moser, 1987 |
| 14,1 à 3 000 | 20 | Sijm et al., 1999 | ||
| pKa (constante de dissociation d'acide) (sans dimensions) | ||||
| Disperse Red 179 | Modélisé | 1,9 | ACD/pKa DB, 2005 | |
| DAPEP | Modélisé | 2,05 | ACD/pKa DB, 2005 | |
Le Disperse Red 179 et le DAPEP ne sont pas naturellement produits dans l'environnement.
Des informations récentes ont été recueillies dans des études sur le domaine menées pendant les années 2005 et 2006 dans le cadre des avis de la Gazette du Canadapubliés en application de l'article 71 de la LCPE (1999) (Canada, 2006b, 2008). Ces avis réclamaient des données sur la fabrication canadienne et les quantités des substances importées au Canada. Dans l'avis de 2006, on demandait également de fournir des données sur les quantités de Disperse Red 179 et de DAPEP utilisées.
En réponse à l'avis en application de l’article 71 de la LCPE (1999) pour l'année civile 2006, aucune fabrication de Disperse Red 179 ou de DAPEP n'a été signalée au-delà du seuil de 100 kg/an. Toutefois, une seule entreprise signalait l'importation de 400 kg de Disperse Red 179 et 100 kg de DAPEP au Canada en 2006 (le pays exportateur n'a pas été identifié) (Environnement Canada, 2009a). De plus, quatre entreprises ont déclaré avoir utilisé 400 kg de Disperse Red 179 en 2006, tandis que quatre autres entreprises ont déclaré avoir utilisé 180 kg de DAPEP en 2006. La quantité plus importante de 180 kg/an de DAPEP par rapport à la quantité importée de 100 kg pour l'année 2006 est vraisemblablement due à des stocks inutilisés des années précédentes.
Deux autres intervenants ont aussi indiqué un intérêt pour ces substances.
Les informations reçues en réponse à l'avis en application de l’article 71 de la LCPE (1999) pour l'année civile 2005 déterminaient qu'entre 100 et 1000 kg de Disperse Red 179 étaient commercialisés au Canada (Environnement Canada, 2006).Aucun rapport de fabrication ou d'importation de DAPEP au Canada, supérieure ou égale au seuil de 100 kg au cours de l'année civile 2005 n'a été reçu en réponse au même avis (Environnement Canada, 2006).Toutefois, une partie prenante a été identifiée comme ayant un intérêt pour ces substances.
Les quantités signalées dans la Liste intérieure des substances (LIS) comme fabriquée, importée ou commercialisée au Canada au cours de l'année civile 1986 pour le Disperse Red 179 se situaient entre 1 000 et 10 000 kg. Les quantités signalées dans la LIS comme fabriquées, importées ou commercialisées au Canada au cours de l'année civile 1986 pour le DAPEP se situaient entre 100 et 1 000 kg.
La production de Disperse Red 179 aux États-Unis a été estimée entre 10 000 et 500 000 livres au cours de chacune des années suivantes : 1986, 1990, 1994 et 1998 (US EPA, 2009). Toutefois, aucune quantité n'a été signalée pour 2002 (US EPA, 2009).Le DAPEP n'a pas été produit aux États-Unis pendant cette période (US EPA, 2009).
Les informations sur les utilisations au cours des années civiles 2005 et 2006 ont été rassemblées en réponse à l'avis en application de l’article 71 de la LCPE (1999) (Canada, 2006b, 2008).
En 2006, l'entreprise qui importe le Disperse Red 179 et le DAPEP a identifié son activité comme « Distributeur en gros de produits chimiques et produits associés (sauf agricoles) ». Le Disperse Red 179 est signalé comme étant utilisé comme teinture dans le colorant chimique Foron Rubine RD-S, alors que le DAPEP est utilisé dans le colorant chimique Foron Scarlet RD-S (Environnement Canada, 2009a).Le Disperse Red 179 a été signalé dans le commerce au Canada en 2005, dans le même groupe d'activités appelé « Distributeur en gros de produits chimiques (sauf agricoles) et de produits associés » (Environnement Canada, 2006).
Les codes LIS d'utilisation suivants ont été identifiés pour le Disperse Red 179 pendant la dénomination LIS (1984-1986) : « Colorant - pigment/teinture/colorant/encre » et « Textile, Produit ». Seul le code d'utilisation de LIS « Colorant - pigment/teinture/colorant/encre » a été identifié pour le DAPEP.
Une analyse de l'information technique disponible révèle que le Disperse Red 179 et le DAPEP sont utilisés comme teinture rouge dans la fabrication de textiles (Environnement Canada, 2009a). . Le Disperse Red 179 et le DAPEP peuvent être utilisés comme agents de teinture pour les fibres synthétiques comme le polyester et le nylon dans les vêtements et les textiles domestiques (CII 2002– ; Choi et al.,2007; Environnement Canada, 2009a).
Selon les informations reçues en réponse à l'avis en application de l’article 71 de la LCPE (1999), pour l'année 2006, le rejet direct le plus important de colorant dans l'environnement a lieu dans l'industrie textile après le processus de teinture, lorsque le colorant non fixé est éliminé des fibres et rejeté avec les eaux usées.La plupart des usines textiles au Canada rejettent leurs eaux usées vers des stations de traitement avec des capacités primaires ou secondaires, soit municipales, soit situées sur leurs installations (Environnement Canada, 2009a).
Débit massique
Pour estimer les rejets potentiels de substances dans l'environnement à différent stades de leur cycle de vie, un débitmètre massique a été développé (Environnement Canada, 2009b). Les données empiriques sur les rejets de substances particulières dans l'environnement sont rarement disponibles.En conséquence, pour chaque type d'utilisation identifié pour la substance, la proportion et la quantité rejetée vers les divers milieux naturels sont estimées, comme c'est le cas pour la proportion de substance chimiquement transformée ou envoyée pour l'élimination des déchets.À moins que des informations particulières sur le taux ou le potentiel de rejet de la substance issue de décharges et d'incinérateurs soient disponibles, le débitmètre massique ne prend pas en compte quantitativement les rejets hors site vers l'environnement, issus de sites d'élimination des déchets.
Les hypothèses et les paramètres d'entrée utilisés dans les estimations de rejet sont basés sur des informations tirées d'un certain nombre de sources, comprenant des réponses aux études règlementaires, de Statistique Canada, des sites Internet de fabricants, de bases de données et de documents techniques et d'informations et d'hypothèses professionnelles. Sont particulièrement pertinents les facteurs d'émission, qui sont généralement exprimés en fraction d'une substance rejetée dans l'environnement, notamment pendant sa fabrication, son traitement et l'utilisation associée avec des processus industriels.Les sources de ces informations comprennent des documents de scenarios d'émission, souvent développés sous les auspices de l'organisation de coopération et de développement économiques (OCDE), et les hypothèses par défaut utilisées par différents organismes internationaux de règlementation des produits chimiques.On note que le niveau d'incertitude pour la masse de substance et la quantité rejetée dans l'environnement augmentent généralement vers la fin de son cycle de vie.
Tableau 4. Rejets et pertes estimés de Disperse Red 179 et de DAPEP dans les milieux naturels, transformation de produits chimiques pendant le cycle de vie et transfert vers des sites d'élimination des déchets, d'après le débitmètre massique
| Devenir | Proportion de la masse (%)1 | Principal stade du cycle de vie impliqué2 | |
|---|---|---|---|
| 1 Pour chaque substance, les informations issues des documents suivants de l'OCDE sur les scénarios d'émission ont été utilisées pour estimer les rejets dans l'environnement et la répartition de la substance, tel qu'il est résumé dans ce tableau : Formulation d'adhésifs (OCDE, 2004) et usines textiles de fabrication de laine (OCDE, 2007). Les hypothèses spécifiques utilisées dans le calcul de ces estimations sont résumées dans Environnement Canada (2009c) et dans Environnement Canada (2009d). 2 Stade(s) applicable(s) : production, formulation, usage industriel, usage domestique, durée de vie de l'article/produit, élimination des déchets. 3 Eaux usées avant toute forme de traitement sur site industriel ou hors site municipal. |
|||
| Rejeté vers des milieux récepteurs : | |||
| Vers le sol | 0 | Cycle de vie entier | |
| Dans l'air | 0 | Cycle de vie entier | |
| Vers les eaux usées3 | 17,1 | Fabrication de produits, usage domestique | |
| Chimiquement transformés (incinération) | 2,5 | Élimination des déchets | |
| Transférés vers des sites d'élimination des déchets (par exemple, décharge, incinération) | 80,5 | Élimination des déchets | |
D'après les informations de Statistique Canada et une analyse faite conjointement par Environnement Canada et Industrie Canada, il est reconnu que des colorants peuvent être importés dans des articles manufacturés. En suivant la proposition de Statistique Canada, un ratio de 30:70 (textiles manufacturés au Canada contre ceux importés) a été utilisé pour estimer la quantité de colorant importé en produits colorés (Environnement Canada, 2009a).La quantité importée de 400 kg pour le Disperse Red 179 et la quantité utilisée de 180 kg pour le DAPEP pour l'année 2006 ont été incluses dans les calculs de l'outil de débit massique, lesquels ont donné des quantités totales approximatives de 1 128 kg et 508 kg, respectivement, pour le Disperse Red 179 et le DAPEP commercialisés au Canada.
Les résultats indiquent que le Disperse Red 179 et le DAPEP peuvent se trouver en grandes quantités dans des sites d'élimination de déchets (80,5 % ou 908 kg/an de Disperse Red 179 et 408 kg/an de DAPEP), en raison du rejet éventuel d'articles fabriqués qui en contiennent. Une petite fraction des déchets solides est incinérée, ce qui peut engendrer la transformation chimique de la substance.Surtout d'après les informations contenues dans les documents de scénarios d'émission de l'OCDE pour le traitement et les usages associés avec ce type de substance (OCDE, 2004, 2007), on estime que 17,1 % (192 kg/an de Disperse Red 179 et 87 kg/an de DAPEP) peuvent être rejetés dans les eaux usées, provenant principalement d'activités associées à leur usage industriel (7,9 %), mais également de la durée de vie de produits contenant les substances, comme les rejets associés à la blanchisserie (9,2 %). Bien que ces teintures ne soient pas prises en considération dans l'outil de débit massique, il convient de noter qu'elles peuvent être épandues sur des sols agricoles et des pâturages au Canada du fait de leur présence dans les boues activées de l'épuration des eaux usées qui sont utilisées couramment pour enrichir le sol. La perte potentielle dans les eaux souterraines issue de la partie des substances qui parviennent à s'introduire dans des sites d'enfouissement (par l'élimination d'articles manufacturés) devrait être limitée. Pour l'évaluation écologique, l'environnement aquatique est considéré comme le milieu critique (d'après les rejets des usines de traitement des eaux usées).
Bien qu'une part importante des substances finisse dans des sites d'enfouissement (par l'élimination d'articles manufacturés), à partir desquels peut exister une fuite potentielle vers la nappe phréatique, le milieu aquatique est considéré comme milieu critique, puisque ni le Disperse Red 179, ni le DAPEP ne seront liés à une matière quelconque et tous deux auront par conséquent la possibilité d'être plus biodisponibles.
Comme l'indiquent les résultats du débitmètre massique (tableau 4), les substances Disperse Red 179 et DAPEP sont supposées être rejetées dans les effluents d'eaux usées au cours de processus industriels et d'usages domestiques (Environnement Canada, 2009c, 2009d). Les valeurs élevées du log Koe (analogues 4,08 à 4,6, données déduites à partir d'analogues > 4 et valeurs modélisées 5,09 à 6,01) et du log Kco (données déduites à partir d'analogues 3,4 à 4,2) (voir le tableau 2) indiquent que ces substances peuvent avoir une affinité pour les solides.Toutefois, le log Kco est une valeur calculée (voir la note de bas de page 3 au-dessous du tableau 2) pour les colorants azoïques dispersés sans groupe benzothiazyle fonctionnel et le potentiel d'adsorption des structures particulaires solides de colorants n'est généralement pas bien compris.Par conséquent, le degré de ce comportement particulier pour les deux substances évaluées est incertain.
Le Disperse Red 179 et le DAPEP ne se biodégradent pas rapidement en conditions aérobies (voir le tableau 5). Le Disperse Red 179 et le DAPEP sont utilisés sous forme de poudres avec une solubilité limitée dans l'eau (voir le tableau 2).En solution, le Disperse Red 179 et le DAPEP se comportent comme des bases, avec un très faible pKa estimé (respectivement 2,05 et 1,9; voir le tableau 2).Par conséquent les formes dissoutes de l'une ou l'autre substance ne devraient pas s'ioniser dans l'eau à des pH correspondant au milieu naturel (6 à 8 pour les eaux de surface). En raison de leur faible solubilité, ces substances devraient se comporter comme des dispersions colloïdales lorsqu'elles sont rejetées dans l'eau (Yen et al., 1991). On les trouvera par conséquent principalement sous forme solide ou adsorbée sur des particules en suspension et éventuellement enfoncées dans les sédiments du fond, où elles devraient rester sous une forme relativement indisponible biologiquement. Yen et al., (1989) ont conclu que les colorants dispersés ont tendance à s'accumuler en abondance dans les sédiments et les biotes, à moins qu'ils ne soient dégradés à des vitesses comparables à leur assimilation. Selon Razo-Flores et al. (1997), les colorants azoïques finissent par se retrouver dans des sédiments anaérobies, dans des aquifères ou dans les eaux souterraines en raison de leur nature récalcitrante dans le milieu anaérobie Yen et al., (1991) ont observé qu'un analogue azoïque benzothiazyle était transformé en conditions anaérobies dans les sédiments par hydrolyse et réduction, et ont conclu que la plupart des colorants azoïques ne persistent probablement pas dans les systèmes sédimentaires anaérobies.
La vitesse de volatilisation à partir de la surface de l'eau est proportionnelle à la constante de la loi de Henry (Baughman et Perenich, 1988). Baughman et Perenich (1988) précisent également que la volatilisation à partir de systèmes aquatiques ne représente pas un processus de perte important pour les colorants dispersés. Cette déclaration est conforme aux valeurs faibles à négligeables déduites à partir d'analogues de la constante de la loi de Henry (10-8 à 0,1 Pa·m3/mol, tableau 3), ainsi qu'à la faible pression de vapeur analogue (5,33 × 10-12 à 5,33 x 10-5, tableau 3). D'après ces données d'analogue et de données déduites à partir d'analogues pour les colorants azoïques dispersés, le transport dans l'air dû à la perte de cette substance issue de la surface de sols humides et secs ne devrait pas être important.Ces données sont cohérentes avec l'état physique (structure particulaire solide) du Disperse Red 179 et du DAPEP; cet état n'en fait probablement pas des candidats à la volatilisation.
Persistance dans l'environnement
Aucune donnée de surveillance environnementale ayant trait à la présence de Disperse Red 179 ou de DAPEP dans l’environnement canadien (air, eau, sol et sédiments) n'a été relevée.
Selon L'Association écologique et toxicologique des fabricants de colorants et de pigments organiques, les colorants sont, avec quelques exceptions, considérés essentiellement comme non biodégradables en conditions aérobies (ETAD, 1995). Une évaluation répétée de la biodégradabilité prête et inhérente à l'aide de tests de dépistage acceptés (voir les directives de l'OCDE pour les tests sur les produits chimiques) a confirmé cette hypothèse (Pagga et Brown, 1986; ETAD, 1992).D'après la structure chimique du Disperse Red 179 et du DAPEP, il n'existe aucune raison de soupçonner que la biodégradation sera différente de celle décrite en général pour les colorants (ETAD, 1995).
Certains colorants azoïques dispersés, comprenant les composés benzothiazyles, se sont révélés subir une dégradation anaérobie relativement rapide dans les sédiments en profondeur, où les conditions anoxiques prévalent (Yen et al., 1991; Baughman et Weber, 1994; Weber et Adams, 1995). Les colorants dispersés pénètrent le système aquatique principalement sous forme de dispersion de fines particules en suspension et s'installent éventuellement dans les couches aérobies des sédiments de surface, où ils vont persister jusqu'à ce que l'enfouissement des sédiments crée des conditions de réduction.La vitesse de dépôt des sédiments et l'importance de la bioturbation varient d'un site à l'autre et il est donc très difficile d'établir le temps de séjour des colorants dans les couches de sédiments aérobies.Il est toutefois probable que dans de nombreux cas il soit supérieur à 365 jours.Une fois sous conditions anaérobies ou de réduction, les colorants azoïques peuvent subir une dégradation rapide en constituants amines aromatiques substitués, comme l'ont démontré Yen et al., (1991) qui ont mesuré les valeurs de demi-vie de réduction dans des sédiments compactés à température ambiante, de 1,9 à 2,0 jours pour un colorant azoïque benzothiazyle (n° CAS 68133-69-7).Toutefois, la plupart des organismes aquatiques ne devraient pas être exposés à ces produits de transformation après biodégradation dans les sédiments anoxiques profonds, en partie parce que le contact avec les sédiments anoxiques est susceptible d'être limité et en partie parce que les produits de dégradation d'amines devraient être étroitement liés aux sédiments et avoir, par conséquent, une très faible biodisponibilité (Weber et al., 2001; Colon et al., 2002).Par conséquent, les produits de dégradation ne présentent probablement pas de problème écologique.
Des données empiriques de biodégradation ont été soumises par le secteur en réponse à l'avis en application de l’article 71 de la LCPE (1999), pour l'année civile 2006 (Environnement Canada, 2009a).Des études inhérentes de biodégradabilité qui ont évalué la biodégradabilité aérobie dans un milieu aquaux de Foron Rubin RD-S (produit commercial contenant du n° CAS16586-42-8) et du Disperse Red 153 (produit commercial contenant du n° CAS 25176-89-0) ont déterminé qu'aucun composé n'était biodégradable (BMG, 2001, 2003a). Ces tests ont été effectués conformément aux directives de l'OCDE pour les tests sur les produits chimiques, test n° 302B-1992, « Biodégradabilité inhérente : Test de Zahn-Wellens/EMPA. » Bien que le protocole utilisé pour ces deux études était acceptable, subsiste un manque général d'information sur les substances utilisées pour chaque test. La solubilité des composés testés n'est signalée dans aucune étude.Dans la première étude, ni la proportion de Disperse Red 179 (n° CAS 16586-42-8) dans le produit Foron Rubin RD-S du commerce, ni les autres composants de ce produit du commerce n'ont été signalés.Dans la deuxième étude, la proportion de DAPEP présent dans le Disperse Red 153 (n° CAS78564-87-1), qui est en fait un mélange de DAPEP et d'un autre isomère structurel (Nakagawa, 1996; CII 2002- ), n'est pas indiquée.
L'absence de dégradation pourrait s'expliquer par l'inhibition bactérienne provoquée par la toxicité du Disperse Red 179 et du DAPEP. Toutefois, des études sur les essais d'inhibition de la respiration effectuées sur les mêmes composés selon les Lignes directrices de l'OCDE pour les essais de produits chimiques, n° 209-1984, ont déterminé que les boues activées ne montraient aucun effet toxique important de l'une ou l'autre substance soumise à ces essais (BMG, 2000a, 2003b). La CE20 et la CE80 pour le Foron Rubin RD-S (n° CAS 16586-42-8) et le Disperse Red 153 (qui contient du n° CAS 25176-89-0) ont été estimés comme étant respectivement supérieurs à 1 000 mg/L et 4 000 mg/L (BMG, 2000a, 2003b).D'après ces informations supplémentaires, les deux études inhérentes de biodégradabilité sont estimées acceptables, malgré le manque de clarté concernant la composition des substances test (voir l'annexe 1).
Le tableau 5a présente les données empiriques de biodégradation (BMG, 2001, 2003a) qui ne montre aucune biodégradation sur 28 jours dans un test inhérent de biodégradation pour le Foron Rubin RD-S et le Disperse Red 153. Ces essais indiquent que la demi-vie dans un milieu aqueux oxique sera probablement supérieure à 182 jours (6 mois) et que, par conséquent, les substances seront probablement persistantes dans des conditions aérobies dans ce milieu environnemental.
Tableau 5a. Données empiriques de dégradabilité inhérente pour le Disperse Red 179 et le DAPEP
| Substance | Milieu | Processus du devenir | Valeur de dégradation | Résultat de dégradation/ unités | Référence |
|---|---|---|---|---|---|
| Foron Rubin RD-S (Disperse Red 179) |
Eau/ boues activées |
Biodégradation | 0 | Biodégradation à 28 jours/% | BMG, 2003a |
| Disperse Red 153 (DAPEP) |
Eau/ boues activées |
Biodégradation | 0 | Biodégradation à 28 jours/% | BMG, 2001 |
Alors que peu de données expérimentales sur la dégradation du Disperse Red 179 et du DAPEP sont disponiblese, une méthode RQSA basée sur le poids de la preuve a également été appliquée à l'aide des modèles de dégradation indiqués au tableau 5b. Bien que le rejet du Disperse Red 179 et du DAPEP doive se faire vers les eaux usées, leur temps de séjour dans la colonne d'eau, dû à leur faible solubilité et leur comportement comme dispersions colloïdales, peut être court avant qu'ils ne s'enfouissent dans les sédiments. Cependant, compte tenu du manque de données à ce sujet, la persistance dans l'eau a été examinée à l'aide de modèles de prévision RQSA sur la biodégradation.L'analyse suivante s'applique principalement à la portion de cette substance qui est présente dans l'environnement sous forme dissoute, en reconnaissant qu'une proportion importante pourrait probablement exister sous forme dispersée de particules solides. Le tableau 5b résume les résultats des modèles RQSA disponibles sur la dégradation dans l'eau du Disperse Red 179 et du DAPEP.
Tableau 5b. Données modélisées de dégradation du Disperse Red 179 et du DAPEP
| Processus du devenir | Modèle et base du modèle | Substance | Résultat et prévision du modèle | Demi-vie extrapolée (jours) |
|---|---|---|---|---|
| 1 Le résultat est une valeur numérique. 2 Le résultat est un pourcentage de probabilité. |
||||
| Eau | ||||
| Biodégradation (aérobie) | BIOWIN, 2000 Sous-modèle 3 : Étude d'expert (biodégradation ultime) |
Disperse Red 179 | 1,4451 « se biodégrade très lentement » |
> 182 |
| DAPEP | 1,25491 « se biodégrade très lentement » |
> 182 | ||
| Biodégradation (aérobie) | BIOWIN, 2000 Sous-modèle 5 : Probabilité linéaire du MITI |
Disperse Red 179 | -0,46862 « se biodégrade très lentement » |
> 182 |
| DAPEP | -0,33952 « se biodégrade très lentement » |
> 182 | ||
| Biodégradation (aérobie) | BIOWIN, 2000 Sous-modèle 6 : Probabilité non linéaire du MITI |
Disperse Red 179 | 02 « se biodégrade très lentement » |
> 182 |
| DAPEP | 02 « se biodégrade très lentement » |
> 182 | ||
| Biodégradation (aérobie) | TOPKAT, 2004 Probabilité |
Disperse Red 179 | 0.02 « se biodégrade très lentement » |
> 182 |
| DAPEP | « se biodégrade très lentement » | > 182 | ||
| Biodégradation (aérobie) | CATABOL, 2008 % DBO (demande biologique en oxygène) |
Disperse Red 179 | % DBO = 3,3 « Se biodégrade très lentement » |
> 182 |
| DAPEP | % DBO = 3,1 « Se biodégrade très lentement » |
> 182 | ||
Les résultats du tableau 5b montrent que les deux modèles de probabilité BIOWIN (5 et 6) indiquent que ces substances se biodégradent lentement et que leur demi-vie dans l'eau serait supérieure à 182 jours. En fait, les résultats de probabilité des deux modèles sont bien inférieurs à 0,3, ce qui est la limite suggérée par Aronson et al., (2006) pour identifier des substances comme ayant une demi-vie > 60 jours (d'après les modèles de probabilité du MITI). Le résultat du modèle de dégradation ultime (BIOWIN 3), à savoir « se biodégrade très lentement », pourrait signifier 180 à 240 jours (US EPA, 2002a; Aronson et al., 2006). La conclusion générale de BIOWIN (2000) est que ces substances ne sont pas facilement biodégradables.
D'autres modèles récents de dégradation (CATABOL et TOPKAT) prévoient que le Disperse Red 179 et le DAPEP ne subissent pas de minéralisation dans une période de 28 jours, avec une probabilité ou une importance de biodégradation dans les limites des produits chimiques très persistants. Le TOPKAT, qui simule le test de biodégradation sur 28 jours du MITI japonais, a produit une probabilité de 0 pour les deux substances. Ce résultat est bien inférieur au seuil suggéré pour les substances persistantes dans ce modèle (< 0,3) (0,7 est la limite suggérée pour les produits chimiques non persistants) (TOPKAT, 2004). CATABOL ne prévoyait qu'un taux de biodégradation de 3,3 % et 3,1 % pour le Disperse Red 179 et le DAPEP, respectivement, d'après l'essai sur la biodégradation immédiate de l'OCDE 301 (% DBO). Ceci a été suggéré comme signifiant « probablement persistant » (Aronson et Howard, 1999) et ayant une demi-vie dans l'eau > 182 jours. Les valeurs modélisées dans le tableau 5b sont jugées fiables, comme leurs ensembles d'étalonnage contiennent plusieurs substances chimiques ayant une structure comparable.
Lorsque les résultats des tests empiriques de dégradation inhérente, ainsi que les modèles de prévisions, sont pris en compte ensemble, il existe un consensus suggérant que la demi-vie de dégradation ultime dans l'eau est > 182 jours, ce qui est cohérent avec ce à quoi on pourrait s'attendre pour les produits chimiques utilisés comme colorants dispersés (c.-à-d. fabriqués pour être relativement insolubles et durables). En utilisant un ratio de 1:1:4 pour l'extrapolation des demi-vies eau:sol:sédiment (Boethling et al., 1995), la demi-vie dans le sol est également > 182 jours et la demi-vie dans les sédiments oxiques est > 365 jours.
D'après les résultats des données expérimentales, la modélisation prédictive et l'avis des experts (ETAD, 2005), le Disperse Red 179 et le DAPEP répondent aux critères de persistance dans l'eau et le sol (demi-vies dans le sol et l'eau = 182 jours et demi-vie dans les sédiments = 365 jours), comme énoncés dans le Règlement sur la persistance et la bioaccumulation (Canada, 2000).
Potentiel de bioaccumulation
Aucune donnée de facteur expérimental de bioaccumulation (FBA) et/ou de facteur de bioconcentration (FBC) pour le Disperse Red 179 ou le DAPEP n'étaient disponibles; par conséquent, des données empiriques de tests de bioconcentration pour les poissons utilisant la substance analogue Disperse Orange 30 (Shen et Hu, 2008) ont été utilisées pour déterminer le potentiel de bioaccumulation des substances sujettes à cette évaluation.
La structure chimique et le poids moléculaire du Disperse Orange 30 sont similaires à ceux du DAPEP et particulièrement du Disperse Red 179, avec les plus grandes différences étant que le Disperse Orange 30 possède un groupe ester, mais ne possède pas de groupe fonctionnel benzothiazyle. La biodisponibilité de la plupart des colorants dispersés est généralement jugée très faible (et celle-ci limite le potentiel de bioaccumulation). Néanmoins, compte tenu des considérations structurelles uniquement, il est possible que le potentiel de bioaccumulation du DAPEP soit légèrement supérieur au potentiel de bioaccumulation du Disperse Red 179 en raison de la présence des deux atomes de chlore sur son groupe benzothiazyle.
Une étude de bioconcentration du Disperse Orange 30 a révélé qu'il est peu susceptible de s'accumuler dans les poissons (Shen et Hu, 2008). Cette étude a été effectuée conformément aux directives de l'OCDE pour les tests sur les produits chimiques, test n° 305B-1996, Bioconcentration : test semi-statique sur les poissons. La bioconcentration du Disperse Orange 30 chez le poisson zèbre (Brachydanio rerio) a été déterminée par un test semi-statique sur 28 jours, avec renouvellement du milieu de test tous les deux jours.Un test d'exposition à une concentration nominale de 20 mg/L (concentration moyenne mesurée de 0,028 ~ 0,28 mg/L) a été réalisé (conformément au résultat d'un test de toxicité aiguë sur les poissons), dans le but de vérifier le potentiel de bioconcentration de la substance testée.Des échantillons des deux solutions de test et des organismes d'essai ont été pris du 26e jour au 28e jour de la période de test d'exposition sur 28 jours.Les échantillons ont été préparés en extrayant le composant lipidique des poissons testés.La concentration mesurée de la substance de test, le contenu lipidique des poissons et le calcul du facteur de bioconcentration sont rapportés dans le tableau 6a.
Tableau 6a. Concentration mesurée du Disperse Orange 30, contenu lipidique des poissons et calcul du facteur de bioconcentration
| Traitements(20 mg/L) | Durée d'échantillonnage | ||
|---|---|---|---|
| 26e jour | 27e jour | 28e jour | |
| Concentration mesurée de la substance de test dans les solutions extraites (mg/L) | < 0,028 | < 0,028 | < 0,028 |
| Contenu de la substance test dans les lipides du poisson (mg) | < 1,68 | < 1,68 | < 1,68 |
| Poids total du poisson (g) | 2,07 | 2,13 | 2,53 |
| Concentration de la substance test dans le Cp du poisson (mg/kg) | < 0,81 | < 0,79 | < 0,66 |
| Concentration mesurée de la substance test dans le Ce de l'eau (mg/L) | 0,028 ~ 0,28 | 0,028 ~ 0,28 | 0,028 ~ 0,28 |
| Contenu lipidique du poisson (%) | 0,81 | 0,57 | 1,25 |
| Facteur de bioconcentration | < 100 | < 100 | < 100 |
| Facteur de bioconcentration moyen | < 100 | ||
L'étude de Shen et Hu (2008) a été révisée et considérée comme acceptable (voir l'annexe 1). Le manque de détection dans les extraits de poissons (< 0,028 mg/L) suggère une solubilité limitée dans les lipides et/ou un potentiel limité de partage dans les tissus des poissons des systèmes aqueux (plus probablement les deux).Toutefois, il existe une incertitude associée aux valeurs limites dans toute étude, car la « vraie » valeur n'est pas connue.
Étant donné la structure de la substance et le comportement probable de cette classe de colorants dispersés dans les systèmes aqueux, un faible résultat de facteur de bioconcentration est probable. La plupart des colorants dispersés, comme leur nom l'indique, existent sous forme de particules susceptibles de dispersion, avec des fractions vraiment solubles limitées.La solubilité peut toutefois être augmentée en ajoutant des groupements fonctionnels polaires à la molécule. Le Disperse Orange 30 contient certains de ces groupes de solubilisation (nitreux) et l'on peut donc s'attendre à un certain degré de solubilité dans l'eau. En supposant que la concentration de la solution dans l'essai était égale à la plus faible valeur de l'hydrosolubilité, soit 0,028 mg/L, et en utilisant une concentration dans les poissons de 0,81 mg/kg comme une estimation de la pire éventualité, le FBC pourrait être calculé comme inférieur à 100.
L'étude ci-dessus sert de première preuve pour soutenir le manque de potentiel de bioaccumulation du Disperse Red 179 et du DAPEP et d'autres recherches soutiennent cette conclusion. Anliker et al., (1981) ont signalé des valeurs expérimentales de bioaccumulation chez les poissons pour 18 colorants mono azoïques dispersés, obtenues selon les méthodes de test spécifiées par le ministère japonais du commerce international et de l'industrie (MITI). Exprimé en fonction du poids du corps humide des poissons, ces facteurs log de bioaccumulation allaient de 0,00 à 1,76 (Anliker et al., 1981).Les numéros de registre des produits chimiques et les structures chimiques n'ont pas été signalés dans cette étude et limitent par conséquent l'utilité de cette étude pour les besoins de données déduites à partir d'analogues liés au Disperse Red 179 et au DAPEP. Toutefois, les études de suivi, qui fournissaient les structures chimiques pour les colorants dispersés testés, ont confirmé un faible potentiel de bioaccumulation pour 10 colorants nitroazoïques, avec des facteurs logarithmiques de bioaccumulation allant de 0,3 à 1,76 (Anliker et Moser, 1987; Anliker et al., 1988). Des études disponibles du MITI soutiennent également un faible potentiel de bioaccumulation pour les colorants azoïques dispersés.Les FBC déclarés pour trois colorants azoïques dispersés (nos CAS40690-89-9, 61968-52-3 et 71767-67-4) testés à une concentration de 0,01 mg/L variaient de moins de 0,3 à 47 (MITI, 1992).Une étude d'accumulation effectuée par Brown (1987) a également montré qu'aucun des 12 colorants dispersés testés ne s'accumulait pendant une étude sur huit semaines sur des carpes.
Bien que l'on prévoie que le manque de biodisponibilité importante dans l'eau et les aliments atténue fortement le potentiel d'assimilation de la plupart des colorants dispersés, le log Koe empirique pour un analogue proche, basé sur les données de Sijm et al. (1999), suggère que le Disperse Red 179 et le DAPEP pourraient être solubles dans les lipides, si les conditions environnementales favorisent la biodisponibilité de ces substances pour les poissons.
Des valeurs corrigées du log Koe, soit 5,09 et 6,01, ont été estimées pour le Disperse Red 179 et le DAPEP à partir de la valeur connue et acceptable du log Koe de 4,08 (Sijm et al., 1999) pour l'analogue proche portant le n° CAS 68133-69-7, en utilisant la méthode d'ajustement de la valeur expérimentale de KOWWIN (2000). Dans la méthode EVA, l'estimation commence avec le log Koeexpérimental du composé similaire.La structure similaire est ensuite modifiée en soustrayant et en ajoutant des fragments pour « construire » le composé estimé.L'estimation devient ensuite la somme de la valeur expérimentale et la valeur des modifications du fragment.
Dès lors, une valeur de log Koe de 4,08 pour l'analogue n° CAS 68133-69-7 et les valeurs corrigées élevées du log Koe de 5,09 et 6,01 pour le Disperse Red 179 et le DAPEP, respectivement (tableau 2), sont les deux seuls renseignements qui indiquent que ces substances peuvent présenter un potentiel de bioaccumulation important. Malgré leurs valeurs élevées de log Koe, il manque la preuve de la bioaccumulation des colorants azoïques dispersés (Anliker et al., 1981; Anliker et Moser, 1987; MITI, 1992). Les auteurs ayant trouvé de fortes valeurs de log Koe et de faibles facteurs concomitants de bioaccumulation pour les colorants azoïques dispersés suggèrent que les faibles facteurs d'accumulation peuvent être dus dans certains cas à la faible liposolubilité absolue de ces substances (Brown, 1987) ou à leur poids moléculaire relativement élevé (généralement de 450 à 550 g/mol). Une faible liposolubilité et un poids moléculaire élevé rendent difficile le transport dans les membranes des poissons (Anliker et al., 1981; Anliker et Moser, 1987). Il est également probable que le manque de biodisponibilité et la capacité de partage limitée dans des conditions de tests de facteur de bioconcentration, ainsi que dans la dégradation métabolique in vivo, limitent l'accumulation dans les lipides des poissons.
Il a été établi par l'ETAD (1995) que les caractéristiques moléculaires indiquant l'absence de bioaccumulation sont un poids moléculaire > 450 g/mol et un diamètre transversal > 1,05 nm. Des recherches récentes effectuées par Dimitrov et al. (2002), Dimitrov et al., (2005) et le BBM (2008) suggèrent que la probabilité qu'une molécule traverse les membranes cellulaires par diffusion passive diminue de façon importante, alors que le diamètre transversal maximum (Dmax) augmente. La probabilité d'une diffusion passive décroît sensiblement lorsque le diamètre transversal est supérieur à ~1,5 nm et diminue de façon plus importante lorsque les molécules ont un diamètre transversal > 1,7 nm. Sakuratani et al., (2008) ont également étudié l'effet du diamètre transversal sur la diffusion passive dans une série de tests sur environ 1 200 produits chimiques nouveaux et existants. Ils ont observé que les substances qui n'ont pas un potentiel de bioconcentration très élevé ont souvent un Dmax > 2,0 nm et un diamètre effectif (Deff) > 1,1 nm.
Le Disperse Red 179 et le DAPEP ont un poids moléculaire de 394,45 et 404,32 g/mol, respectivement (voir le tableau 1), et leurs structures moléculaires sont relativement peu compliquées. Ces deux caractéristiques indiquent une certaine capacité de bioaccumulation de ces substances. Il n'existe aucune relation claire qui permette d'établir des seuils stricts de taille moléculaire pour l'évaluation du potentiel de bioaccumulation; toutefois, une réduction de la vitesse d'absorption peut être associée à l'augmentation du diamètre transversal, comme l'ont démontré Dimitrov et al. (2002, 2005). Le diamètre maximal du Disperse Red 179 et du DAPEP (et leurs conformères) varie de 1,3 à 2,108 nm et de 1,414 à 2,075 nm, respectivement (BBM, 2008), ce qui indiquerait qu'en ce qui concerne ce colorant, il y a une possibilité de réduction importante du taux d'absorption dans l'eau et de la biodisponibilité in vivo.
D'après un manque d'accumulation dans les essais de bioconcentration sur la substance analogue Disperse Orange 30 et d'autres colorants azoïques dispersés correspondants, ainsi que les grandes tailles moléculaires du Disperse Red 179 et du DAPEP, ces substances devraient avoir un faible potentiel de bioaccumulation. Par conséquent, le Disperse Red 179 et le DAPEP ne répondent pas aux critères de bioaccumulation (FBC ou FBA = 5 000, énoncés dans le Règlement sur la persistance et la bioaccumulation (Canada, 2000).
Évaluation des effets écologiques
A – Dans le milieu aquatique
Peu de données empiriques sur l'écotoxicité ont été identifiées pour le Disperse Red 179 ou le DAPEP. Des études sur la toxicité aigüe de deux produits du commerce contenant du Disperse Red 179 et du DAPEP, réalisées à l'aide de Poecilia reticulata (guppy) ont été soumises à Environnement Canada en janvier 2009 (BMG, 2000b, 2003c).Les deux études ont été menées selon la procédure 203 du guide de l'OCDE (test de toxicité aigüe du poisson) et la directive 92/69/EEC de la CEE (toxicité aigüe pour les poissons).Les résultats des deux études sont présentés dans le tableau 7a.
Dans la première étude, la toxicité du Disperse Red 179 a été recherchée à l'aide d'un test de dépistage de la toxicité aquatique, avec le produit Foron Rubin RD-S du commerce (BMG, 2003c). Le test signalait une CL50 aiguë à 96 heures entre 10 et 100 mg/L et une concentration sans effet observé (CSEO) > 10 mg/L, en fonction de concentrations nominales. Ces résultats peuvent être interprétés comme signifiant qu'il n'y a pas d'effets observés à saturation de la substance testée.Une évaluation de la fiabilité de l'étude à l'aide d'un sommaire de rigueur d'étude a trouvé que l'étude a été jugée comme étant de « faible confiance », en raison du manque de détails sur la substance testée (annexe 1).De fait, ni la proportion de Disperse Red 179 dans le Foron Rubin RD-S, ni la solubilité du Foron Rubin RD-S ne sont signalées.
La deuxième étude sur le test de toxicité aquatique (BMG, 2000b) a été menée sur le Disperse Red 153, substance qui contient du DAPEP et un isomère structurel du DAPEP, dans des proportions inconnues (Nakagawa et al., 1996; CII, 2002– ). L'essai a déterminé une concentration sans effet observé (CSEO) de 100 mg/L. Ce résultat peut être interprété dans le sens où aucun effet aigu n'a été observé à saturation de la substance. Comme pour l'étude précédente, l'étude est considérée comme étant de « faible confiance » en raison du manque de détails sur la substance testée (annexe 1).
Bien que l'on considère les deux études comme étant de faible confiance, les résultats obtenus dans les deux études sont typiques pour les colorants azoïques dispersés.
Tableau 7a. Données empiriques sur la toxicité aquatique du Disperse Red 179 et du DAPEP
| Substance d'essai | Organisme d'essai | Type d'essai | Paramètre ultime | Valeur (mg/L) | Référence |
|---|---|---|---|---|---|
| 1 CL50 : concentration d'une substance estimée létale pour 50 % des organismes d'essai. 2 CSEO : la concentration sans effets observés est la plus haute concentration lors d'un test de toxicité qui n'entraîne pas d'effet statistiquement significatif comparé aux contrôles. |
|||||
| Foron Rubin RD-S (Disperse Red 179) | Poecilia reticulata (guppy) | Aigu (96 heures) | CL501 | 10 à 100 mg/L | BMG, 2003c |
| CSEO2 | > 10 mg/L | ||||
| C.I. Disperse Red 153 | Poecilia reticulata (guppy) | Aigu (96 heures) | CSEO2 | > 100 mg/L | BMG, 2000b |
Des données empiriques sur la toxicité sont aussi disponibles pour un autre analogue proche des deux substances, l'éthanol, 2-((4-(2-(6-chloro-2-benzothiazolyl)diazenyl)phényl)ethylamino), 1-acétate, n° CAS 70198-17-3 (voir le tableau 7b). La masse moléculaire de ce colorant benzothiazyle mono-azoïque dispersé (404,9 g/mol) et sa structure moléculaire sont identiques à celles du Disperse Red 179 et du DAPEP. Le test de toxicité statique à 96 heures de la substance, ajoutée aux aquariums dans un vecteur d'acétone à 0,05%, a été mené avec des daphnies, des plathelminthes, des vairons à grosse tête et des escargots (Laboratoire de Santé, Sécurité et facteurs humains, 1978).Les résultats indiquaient une toxicité faible pour le vairon à grosse tête et les escargots (valeurs de CL50 > 100 mg/L) et une toxicité faible pour les plathelminthes (CL50 = 32 mg/L), mais une toxicité élevée pour les daphnies (CL50 = 0,12 mg/L) (Laboratoire de Santé, Sécurité et facteurs humains, 1978).La faible valeur de toxicité de 0,12 mg/L pour les daphnies est préoccupante, mais ces données sont considérées comme peu fiables, puisque la fiabilité du test de toxicité n'a pu être évaluée à cause d'un manque général de détails signalé dans l'étude et de l'âge de l'étude ellemême.
Environnement Canada a reçu des données éco-toxicologiques sur une substance structurellement identique dans les Règles de notification des nouvelles substances (Produits chimiques et polymères) (Environnement Canada, 1994) (voir le tableau 7b). La masse moléculaire de cette substance déclarée était de 418,35 g/mol, ce qui est identique à la masse moléculaire du Disperse Red 179 et du DAPEP.Les résultats du test de toxicité statique à 96 heures sur la truite arc-en-ciel, sur une substance contenant 5 % de la substance déclarée a révélé que la CL50 pour ces espèces est de 10 mg/L. Cependant, alors que cette valeur de toxicité suggère une toxicité aigüe de modérée à faible pour les poissons, elle n'a pas été considérée comme indicatrice du matériel notifié, à cause de la faible concentration de la substance déclarée dans le produit testé.
Tableau 7b. Données empiriques sur la toxicité aquatique d'analogues proches du Disperse Red 179 et du DAPEP
| Nom usuel ou n° CAS | Organisme d'essai | Durée (heures) | Paramètre ultime | Fiabilité de l'étude | Valeur (mg/L) | Référence |
|---|---|---|---|---|---|---|
| 1CL50 – La concentration d'une substance estimée létale pour 50 % des organismes d'essai. | ||||||
| N° CAS 70198-17-3 | Vairons à grosse tête | 96 | CL501 | Non disponible | > 100 | Laboratoire de Santé, Sécurité et facteurs humains, 1978 |
| Escargots | 96 | CL501 | Non disponible | > 100 | ||
| Plathelminthes | 96 | CL501 | Non disponible | 32 | ||
| Daphnies | 96 | CL501 | Non disponible | 0,12 | ||
| Confidentiel | Truite arc-en-ciel |
96 | CL501 | Confiance faible | 10 | Environnement Canada, 1994 |
Des données empiriques sur la toxicité sont disponibles pour l'analogue proche Disperse Orange 30 (voir le tableau 7c). Selon une étude soumise à Environnement Canada pour le compte de l'ETAD (Brown, 1992), CL50 après 96 heures de 710 mg/L pour le poisson zèbre, une CE50 après 48 heures de 5,8 mg/L pour le Daphnia magna, et une CE50après 72 heures de 6,7 mg/L (pour la croissance) pour le Scenedesmus subspicatusont été obtenues expérimentalement d'après une étude de toxicité utilisant le Disperse Orange 30. Cependant, les études d'origine n'ont pas été fournies et leur fiabilité ne peut donc être vérifiée.Un autre résultat pour le Disperse Orange 30 a établi une CL50 pour la truite arc-en-ciel (Oncorhynchus mykiss) > 700 mg/L (Sandoz, 1975).Cependant, après examen, cette étude a été considérée irrecevable (voir l'annexe 1).Finalement, une autre étude de toxicité aiguë, utilisant la truite arc-en-ciel et soumise à Environnement Canada en août 2008, indiquait une CL50 à 96 heures > 100 mg/L (Safepharm Laboratories Ltd., 1990).L'évaluation de la fiabilité de l'étude utilisant un sommaire de rigueur d'étude, a estimé que l'étude était de « faible confiance » à cause du manque de détails (annexe 1).
Tableau 7c. Données empiriques sur la toxicité aquatique de l'analogue Disperse Orange 30
| Organisme d'essai | Type d'essai | Durée (heures) | Paramètre ultime | Fiabilité de l'étude | Valeur (mg/L) | Référence |
|---|---|---|---|---|---|---|
| 1 CL50 – La concentration d'une substance estimée létale pour 50% des organismes d'essai. 2 CE50 - La concentration d'une substance qui est jugée causer un effet toxique sublétal chez 50 % des organismes d'essai. 3 CI50 – La concentration d'une substance estimée inhiber la croissance pour 50% des organismes d'essai. |
||||||
| Truite arc-en-ciel |
Aigu | 48 | CL501 | Inacceptable | > 700 | Sandoz, 1975 |
| Truite arc-en-ciel |
Aigu | 96 | CL50 | Confiance faible | > 100 | Safepharm Laboratories Ltd., 1990 |
| Poisson zèbre | Aigu | 96 | CL50 | Non disponible | 710 | Brown, 1992 |
| Daphnia magna | Aigu | 48 | CE502 | Non disponible | 5,8 | |
| Scenedesmus subspicatus | Aigu | 72 | CE50 | Non disponible | 6,7 | |
| Bactéries | Aigu | s.o. | CI503 | Non disponible | > 100 | |
Dans une autre étude, un résumé qui a été soumis à Environnement Canada pour le compte de l'ETAD (Brown, 1992), 11 colorants dispersés ont été testés sur les organismes suivants : poisson zèbre, Daphnia magna, algues et bactéries. Dans cette étude, des colorants dispersés (composants non azoïques) avaient des niveaux de toxicité signalés < 1 mg/L pour les algues.Cependant, Brown (1992) a signalé que l'inhibition de la croissance pour les algues était largement due à l'absorption de la lumière par les colorants, plutôt que par l'activité biologique.Trois des colorants dispersés testés par Brown (1992) sont des analogues du Disperse Red 179 et du DAPEP.Ce sont le Disperse Red 73, le Disperse Orange 25 et le Disperse Red 17 (tableau 7c). Ces analogues ont montré une toxicité modérée chez D. magna (CE50 à 48 heures = 23 à 110 mg/L) et une toxicité modérée à faible chez le poisson zèbre (CL50 à 96 heures = 17 à 268 mg/L) (voir le tableau 7d).Une toxicité modérée a aussi été observée pour la croissance des algues (une CE50 pour la croissance = 7 à 54mg/L) et aucune toxicité n'a été détectée pour les bactéries (CI50 > 100 mg/L).Les détails de l'expérience sur les colorants testés n'ont pas été fournis, limitant fortement l'évaluation de ces études (Brown, 1992).Cependant, ces données ont été considérées utilisables et sont inclues dans cette évaluation préalable comme faisant partie du poids de la preuve, étant donné qu'elles sont en accord avec d'autres données et avec l'échelle attendue des valeurs d'écotoxicité pour ces structures.Ces valeurs devraient donc également suggérer que ni le Disperse Red 179, ni le DAPEP ne sont fortement dangereux pour les organismes aquatiques.
Tableau 7d. Données empiriques sur la toxicité aquatique d'analogues du Disperse Red 179 et du DAPEP
| Nom usuel ou n° CAS | Organisme d'essai | Durée (heures) | Paramètre ultime | Valeur (mg/L) | Référence |
|---|---|---|---|---|---|
| 1 CL50 – La concentration d'une substance estimée létale pour 50 % des organismes d'essai. 2 CE50 – La concentration d'une substance qui est jugée causer un effet toxique sublétal chez 50 % des organismes d'essai. 3 CI50 – La concentration d'une substance estimée inhiber la croissance pour 50 % des organismes d'essai. s.o. : sans objet |
|||||
| Disperse Red 73 | Poisson zèbre | 96 | CL501 | 17 | Brown, 1992 |
| Daphnia magna | 48 | CE502 | 23 | ||
| Scenedesmus subspicatus | 72 | CE502 | > 10 | ||
| Bactéries | s.o. | CI503 | > 100 | ||
| Disperse Red 17 | Poisson zèbre | 96 | CL501 | 103 | Brown, 1992 |
| Daphnia magna | 48 | CE502 | 98 | ||
| Scenedesmus subspicatus | 72 | CE502 | 7 | ||
| Bactéries | s.o. | CI503 | > 100 | ||
| Disperse Orange 25 | Poisson zèbre | 96 | CL501 | 268 | Brown, 1992 |
| Daphnia magna | 48 | CE502 | 110 | ||
| Scenedesmus subspicatus | 72 | CE502 | 54 | ||
| Bactéries | s.o. | CI503 | > 100 | ||
| Disperse Yellow 3 | Vairon à grosse tête | 96 | CL501 | > 180 | Little et Lamb, 1973 |
En général, en raison de leur faible solubilité (< 1 mg/L), les colorants dispersés sont supposés avoir un impact écologique faiblement aigu (Hunger, 2003). À l'exception de la seule faible valeur de CL50 à 96 heures observée pour les daphnies (Laboratoire de santé, Sécurité et Facteurs humains, 1978), les résultats des études empiriques de toxicité avec les deux substances évaluées et plusieurs analogues, sont cohérentes avec cette attente, indiquant des valeurs de CL50 dans la plage de 5 à 340 mg/L, avec la Daphnia étant l'organisme testé le plus sensible (valeurs de CE50/CL50 de 4,5 à 100 mg/L).Bien que l'interprétation des résultats de ces tests soit compliquée par le fait que ces valeurs d'effet soit basé sur des concentrations nominales parfois supérieures à 10 000 fois la solubilité estimée de la substance (c.-à-d. 0,011 92 mg/L pour le Disperse Red 179; 0,004 208 mg/L pour le DAPEP; 0,021 à 0,69 mg/L pour l'analogue n° CAS68133-69-7), elles représentent effectivement les pires charges environnementales possibles.
Les informations empiriques d'écotoxicité disponibles pour les analogues du Disperse Red 179 et du DAPEP indiquent ainsi que le Disperse Red 179 et le DAPEP ne sont pas susceptibles d'être fortement dangereux pour les organismes aquatiques.
B – Dans d'autres milieux environnementaux
Etant donné que le Disperse Red 179 et le DAPEP peuvent potentiellement être rejetés dans le sol à partir d'eaux usées ou de terres agricoles, il serait préférable d'obtenir des données sur la toxicité des organismes contenus dans le sol. Ceci est pertinent car il a été montré que les colorants sont fortement absorbés et retenus dans les boues activées des stations d'épuration des eaux usées (Tincher, 1988). Cependant, on n'a trouvé aucune étude pertinente sur les effets écologiques de ces composés ou de leurs analogues dans d'autres milieux que l'eau. En dépit de l'absence d'étude appropriée sur les effets écologiques de ces composés dans le sol, compte tenu des données sur la toxicité pour les organismes aquatiques et vu leur absence de potentiel de bioaccumulation et leur faible biodisponibilité, ces composés ne devraient pas vraiment être toxiques pour les organismes vivant dans le sol. Pour les mêmes raisons, le potentiel de toxicité est également susceptible d'être faible concernant les espèces oxiques vivant dans les sédiments, bien que ceci ne puisse être justifié, étant donné le manque d'informations sur la toxicité de l'ensemble des organismes contenus dans les sédiments pour ces substances ou des analogues acceptables.En outre, le potentiel de toxicité du Disperse Red 179 et du DAPEP dans les sédiments anoxiques sera faible étant donné la faible biodisponibilité de leurs produits de digestion anaérobie.
Évaluation de l'exposition écologique
Aucune donnée sur les concentrations de ces substances dans l'eau n'a été identifiée au Canada; par conséquent, les concentrations dans l'environnement sont estimées à partir d'informations disponibles, comprenant les quantités estimées de ces substances dans le commerce, les taux de rejet et le volume des masses d'eau réceptrices.
Rejets industriels
Le Disperse Red 179 et le DAPEP peuvent être utilisés en faibles volumes dans certaines installations industrielles et peuvent être rejetés dans l'eau où ils resteront pour une période indéterminée avant de décanter dans les sédiments. Étant donné que le Disperse Red 179 et le DAPEP sont analogues, un scénario d'exposition unique a été modélisé pour les deux substances, afin de déterminer une concentration environnementale estimée (CEE) dans l'environnement aquatique.Plusieurs sites industriels ont été identifiés comme sources potentielles de rejets dans l'eau et un site a été sélectionné pour l'évaluation d'un scénario le plus défavorable dû aux plus grandes quantités de substances utilisées.Des hypothèses prudentes ont été émises concernant la quantité de substance traitée et rejetée, le nombre de jours de traitement et le taux d'élimination des stations d'épuration des eaux usées.La concentration environnementale estimée pour le Disperse Red 179 et le DAPEP a été calculée en se basant sur l'utilisation combinée d'une quantité de 510 kg/an (respectivement 350 kg/an et 160 kg/an pour le Disperse Red 179 et le DAPEP), sur lesquels 22 % sont supposés être rejetés sur une période de 250 jours, résultant du processus de coloration lorsque le colorant non fixé est éliminé des fibres et rejeté dans les eaux usées (Environnement Canada, 2009a, 2009b, 2009c, 2009d).Les 22 % rejetés dans les eaux usées (égouts) par les activités industrielles représentent une estimation prudente, tirée du débitmètre massique (Environnement Canada, 2009b, 2009c, 2009d). On a alors supposé que la quantité rejetée était déversée directement dans une usine locale de traitement des eaux usées, avec un taux d'élimination de zéro pour les substances. Le Disperse Red 179 et le DAPEP dans les effluents d'une usine de traitement des eaux usées étaient supposés être rejetés vers une masse d'eau réceptrice ayant une capacité de dilution 10 fois supérieure à celle du débit des effluents. En fonction du volume rejeté estimé le plus élevé possible et des hypothèses susmentionnées, la concentration la plus élevée de Disperse Red 179 et de DAPEP dans les eaux réceptrices est de 1,7 × 10-5 mg/L (Environnement Canada, 2009e).
Rejets de consommation (Mega Flush)
Comme on trouve du Disperse Red 179 et du DAPEP dans les produits de consommation et qu'on déclare des rejets de ces substances dans l'eau (égouts), d'après les résultats de l'outil de débit massique (Environnement Canada, 2009c, 2009d). Mega Flush (modèle de tableur d'Environnement Canada pour l'estimation des rejets dans les canalisations issus des produits de consommation) a été utilisé pour estimer la concentration potentielle des substances dans plusieurs cours d'eau récepteurs d'effluents d'usines de traitement des eaux usées, vers lesquelles les produits de consommation contenant les substances sont susceptibles d'avoir été rejetés (Environnement Canada, 2009f) . Le modèle de tableur est conçu pour fournir ces estimations en fonction des hypothèses prudentes concernant la quantité de substances utilisées et rejetées par les consommateurs.Par défaut, nous supposons que les taux d'élimination primaires et secondaires des usines de traitement des eaux usées sont de 0 %, les pertes dues à l'utilisation sont de 100 %, l'utilisation domestique de la substance étant sur 365 jours/an et le débit des eaux réceptrices sur tous les sites du dixième centile (estimation basse).Ces estimations sont réalisées pour environ 1 000 sites de rejet à travers le Canada, ce qui représente la majorité des plus importantes usines de traitement des eaux usées dans le pays.
L'équation et les données utilisées pour calculer la concentration environnementale estimée du Disperse Red 179 dans les masses d'eau réceptrices sont décrites dans Environnement Canada (2009f). Un scénario a été réalisé en supposant une quantité totale consommée de 104 kg/an prévue d'être rejetée dans les égouts (9,2 % de la masse totale), en conséquence du blanchissage d'articles manufacturés qui contiennent ce colorant (articles importés ou fabriqués au Canada) (Environnement Canada, 2009c). Selon ce scénario, l'outil estime que la CEE du Disperse Red 179 dans les cours d'eau récepteurs varie entre 1,3 × 10-5 et 1,6 × 10-4 mg/L..
Un scénario semblable pour les rejets issus des utilisations des consommateurs a été utilisé pour prévoir la CEE du DAPEP (Environnement Canada, 2009h). Le scénario a été réalisé pour le DAPEP en supposant une quantité totale de 47 kg/an (9,2 % de la masse totale) perdue dans les égouts pendant le blanchissage des articles manufacturés qui contiennent ce colorant. Des taux d'élimination semblables de 0 % ont été utilisés. Selon ce scénario, l'outil estime que la CEE du DAPEP dans les cours d'eau récepteurs varie entre 5,9 × 10-6 et 7,2 × 10-5 mg/L.
Caractérisation du risque écologique
La démarche suivie dans cette évaluation écologique a consisté à examiner un certain nombre informations complémentaires et à tirer des conclusions d'après la méthode du poids de la preuve et en prenant les précautions requises par la LCPE (1999). Les éléments de preuve pris en compte comprenaient les résultats de calculs prudents du quotient de risque ainsi que des renseignements sur la persistance, la bioaccumulation, la toxicité inhérente, les sources et le devenir des substances.
On s'attend à ce que le Disperse Red 179 et le DAPEP soient persistants dans l'eau, le sol et les sédiments dans des conditions aérobies; on s'attend également à ce que leur potentiel de bioaccumulation soit bas. Les faibles volumes d'importation au Canada des deux substances indiquent un faible potentiel de rejet dans l'environnement canadien, malgré leur utilisation industrielle, commerciale et domestique.Une fois rejetés dans l'environnement aquatique, ils se trouveront principalement dans les sédiments. On s'attend également à ce que dans l'ensemble, elles présentent un potentiel faible à modéré de toxicité pour les organismes aquatiques.
Des estimations d'exposition prudentes intégrant l'analyse du quotient de risque d'exposition, avec une information sur la toxicité, ont été réalisées pour le milieu aquatique, afin de déterminer s'il existe un danger potentiel pour l'environnement au Canada. Une concentration estimée sans effet (CESE) pour les deux substances a été estimée de façon prudente d'après la CL50 en 96 heures extrêmement faible de 0,12 mg/L (Health, Safety, and Human Factors Laboratory, 1978) pour les daphnies à l'aide de la substance analogue n° CAS 70198-17-3. Il s'agit de la valeur analogue expérimentale la plus faible tirée des données de toxicité aiguë relevées et elle est un ordre de grandeur inférieur à la deuxième plus faible valeur de toxicité. On a appliqué un facteur de 100 pour tenir compte de l'extrapolation de la toxicité aiguë à la toxicité chronique (à long terme) et de l'extrapolation des résultats en laboratoire pour une espèce à d'autres espèces potentiellement sensibles sur le terrain. La concentration estimée sans effet qui en résulte est de 0,0012 mg/L.
Lorsqu'il est compare aux concentrations environnementales estimées prudentes calculées ci-dessus pour le scenario des rejets industriels, le quotient de risque résultant pour les rejets industriels dans l'environnement aquatique (concentration environnementale/concentration estimée sans effet) est de 0,000 009/0,0012 = 0,0077 pour les rejets combines de Disperse Red et de DAPEP. En conséquence, on estime que les concentrations de Disperse Red 179 ou de DAPEP sur les eaux de surface au Canada, provenant des rejets industriels pour un site canadien soumis au scénario le plus défavorable, ont peu de chance de causer des effets indésirables sur les populations d'organismes aquatiques.Étant donné que ce scénario de rejet industriel fournit une estimation prudente de l'exposition et du risque, les résultats indiquent un faible potentiel de nocivité écologique, résultant de l'exposition locale et du point d'origine des rejets industriels dans l'environnement aquatique.
En ce qui concerne l'exposition découlant de rejets dans les canalisations à l'aide de scénarios modérément prudents d'utilisation domestique, les CEE estimées avec Mega Flush ne dépassent la CESE sur aucun site (c'est-à-dire que tous les quotients de risque sont très inférieurs à 1) (Environnement Canada, 2009g, 2009h). Ceci indique que les rejets domestiques jetés dans l'évier de Disperse Red 179 et de DAPEP ne semblent pas devoir nuire aux organismes aquatiques.
En conséquence, d'après les preuves disponibles, le Disperse Red 179 et le DAPEP ne sont pas en mesure de nuire à l'environnement canadien.
Incertitudes dans l'évaluation des risques pour l'environnement
Il existe des incertitudes dans cette évaluation des risques en raison d'un manque de données sur les propriétés physiques et chimiques du Disperse Red 179 et du DAPEP, notamment leur hydrosolubilité et leurs coefficients de partage octanol-eau et carbone-eau. Cependant, des méthodes d'analyse de données déduites à partir d'analogues, des données analogues proches et des données modélisées utilisant la méthode d'ajustement de la valeur expérimentale d'EPIsuite (2008), ont été utilisées afin de combler les données manquantes importantes avec une marge d'erreur acceptable.
L'évaluation de la persistance est limitée par l'incertitude sur le taux de dégradation dans les sédiments anaérobies et la mesure pour laquelle la dégradation a lieu dans ces sédiments, et si les produits de dégradation (par exemple, les amines) seraient biologiquement disponibles. Néanmoins, il apparaît clairement que la dégradation anaérobie de la partie biodisponible de colorants azoïques dans les sédiments en amines constitutives, est beaucoup plus rapide (demi-vies dans l'ordre des jours) que la biodégradation aérobie. Bien que l'on ne s'attende pas à ce que les produits de dégradation amine soient biodisponibles, parce qu'ils se forment uniquement dans les sédiments anoxiques relativement profonds et qu'ils peuvent se lier étroitement aux sédiments par l'addition néophilique et le couplage radicalaire oxydant (Weber et al., 2001; Colon et al. 2002), cette question est une source d'incertitude pour l'évaluation de la toxicité du Disperse Red 179 et du DAPEP.
Des incertitudes sont associées également à la fraction des substances dont on présume qu'elle est rejetée pendant l'utilisation (c'est-à-dire pendant les activités industrielles et l'utilisation des produits de consommation) et au manque d'information sur les concentrations environnementales au Canada du Disperse Red 179 et du DAPEP. Ces incertitudes ont été prises en charge en formulant des hypothèses prudentes dans chacun des exercices de modélisation.
Les concentrations expérimentales, associées à la toxicité intrinsèque pour les organismes aquatiques, constituent une source additionnelle d'incertitude, dans le sens où elles dépassent la solubilité du produit chimique dans l’eau. Malgré ceci, la faible solubilité des substances et leur biodisponibilité limitée due à leur taille moléculaire indiquent que le Disperse Red 179 et le DAPEP ne sont pas extrêmement dangereux pour les organismes aquatiques.
Également, en ce qui concerne l'écotoxicité, basée sur le comportement de partage prévu de ces produits chimiques, l'importance du sol et des sédiments comme milieux d'exposition importants n'est pas bien résolue par les données disponibles sur les effets. En effet, les seules données sur les effets qui ont été trouvées s’appliquent principalement aux expositions aquatiques pélagiques, même si la colonne d’eau peut ne pas être le moyen le plus préoccupant à long terme. Néanmoins, d'après la toxicité aquatique relativement faible de ces substances et la faible commercialisation des masses, le potentiel nocif pour les organismes vivant dans les sols et les sédiments devrait également être faible.
Évaluation de l'exposition
Aucune mesure du Disperse Red 179 ou du DAPEP dans l'environnement n'a été relevée dans la littérature scientifique. D'après les renseignements sur les rejets, les concentrations dans les milieux naturels devraient être négligeables.
Les colorant dispersés tels que le Disperse Red 179 et le DAPEP sont utilisés dans l'industrie du textile afin de colorer les tissus synthétiques comme les polyesters et les polyamides. Les colorants dispersés tirent leur nom du processus de teinture utilisé (APE du Danemark, 1998). En raison de leur faible solubilité dans l'eau, les composés de colorant sont traditionnellement moulus en vue d'obtenir une fine poudre qui est ensuite dispersée dans de l'eau. Les molécules de colorant hydrophobes s'adsorbent alors au textile hydrophobe. La chaleur permet ensuite l'absorption du colorant par le textile (Chudgar et Oakes, 2003). Le Disperse Red 179 et le DAPEP ne créent pas de liaisons chimiques avec le textile; ainsi, la migration est possible. Ils peuvent être utilisés comme agents de teinture des fibres synthétiques destinées aux vêtements personnels ou au linge de maison.
Les estimations de la limite supérieure d'exposition ont été calculées pour deux scénarios. Le premier scénario analysait la voie cutanée quand un individu porte des vêtements faits en tissu teints avec ces substances, tandis que le second analysait la voie orale résultant du mâchonnement d'un tissu teint avec ces substances par des nourrissons et des jeunes enfants. On considère qu'il s'agit des voies d'exposition les plus probables La limite supérieure d'exposition pour tout contact direct ou indirect avec des textiles teints avec ces substances. Les doses internes maximales provenant de l'exposition cutanée au Disperse Red 179 et au DAPEP ont été estimées entre 0,1 et 4 µg/kg de poids corporel (p.c.) par jour pour tous les groupes d'âges portant des vêtements neuf, non lavé et présentant des propriétés d'indégorgeabilité bonnes à faibles (ETAD, 2004). Pour les bébés et enfants âgés les expositions par voie buccale sont estimées à moins de 0,002 µg/kg p.c. par jour, Une étude récente a déterminé que la quantité de colorant dispersé migrant sur la peau de volontaires humains était de 300 à 600 fois plus faible que celle émise par les stimulants sudorifiques (Meinke et al., 2009). Cela soutient la nature prudente des estimés d’exposition de limite supérieure. En outre, on estime que les colorants présents dans les textiles sont relâchés principalement au moment du lavage. Donc toutes expositions potentielles relâcheraient avec le temps. Des renseignements détaillés concernant les hypothèses utilisées dans ces calculs sont proposés aux annexes III et IV.
Évaluation des effets sur la santé
Disperse Red 179 (n° CAS 16586-42-8)
Une seule étude sur le Disperse Red 179 (cité en tant que Disperse Violet 52) dans un essai de génotoxicité in vitro sur les indicateurs (test umu/SOS); celui-ci a fait état de résultats positifs avec une activation de la fraction S9 et de résultats négatifs sans l'activation de cette fraction (Kosaka et Nakamura, 1990). Les résultats des modèles de prévision RQSA sur le Disperse Red 179 étaient mitigés pour les paramètres de cancérogénicité et de génotoxicité (CASETOX (2008), DEREK (2008), Leadscope Model Applier (Leadscope, 2009) et Toxtree (2009)) (annexe 5). Étant donné que les données disponibles étaient limitées en matière de toxicité potentielle du Disperse Red 179, des renseignements pertinents relatifs aux métabolites et analogues potentiels de cette substance ont également été pris en considération.
Comme le Disperse Red 179 est un membre de la famille des substances azoïques, les renseignements important sur l’effets des produits de clivage azoïques potentiels sur la santé ont été pris en considération dans cette évaluation préalable. Il a été démontré que certaines substances azoïques peuvent subir un clivage réducteur diffusé par des enzymes azoréductases présentes dans les tissus des mammifères ainsi que dans les bactéries intestinales et cutanées (Platzek et al., 1999; Golka et al., 2004; Chen, 2006; Xu et al., 2007; Stingley et al., 2010). Bien que l'on reconnaisse que le degré de réduction azoïque est vraisemblablement influencé par divers facteurs (p. ex. solubilité du composé d'origine, présence et position des substituants moléculaires), en l'absence de données propres aux produits chimiques, on présume que l'exposition à une substances azoïque peut également entraîner une exposition à ses produits de clivage connexes, habituellement les amines aromatiques. Dès lors, les produits de clivage azoïques prévus pour le Disperse Red 179 – à savoir le 6-nitro-2-aminobenzothiazole (n° CAS 6285-57-0) et le 3-[(4-amino-3-méthylphényl)éthylamino]propanenitile]- (n° CAS 105294-34-6) (annexe 6) – sont aussi pris en considération dans cette évaluation préalable.
Le métabolite prévu n° CAS 6285-57-0 a été soumis à des essais de mutagénicité in vitro dans plusieurs études. Trois études distinctes ont montré des resultats positifs dans les souches TA98, TA100 et TA1538 du Salmonella typhimuriumavec et sans activation de la fraction S9, tandis que les souches TA1535 et TA1537 étaient positives uniquement sans activation de la fraction S9 (NTP, 1982, 1983; Seifried, 2006). On n'a observé aucune mutagénicité dans les cellules de lymphomes de souris avec ou sans activation de la fraction S9 pour cette substance (Seifried et al., 2006). Une activité cancérogène potentielle a aussi été signalée pour le n° CAS 6285-57-0 a aussi été liée une activité carcinogénique basée sur la similarité avec des composés nitrés aromatiques cancérogènes (Helmes et al., 1982). Aucune donnée empirique sur la toxicité n'était disponible pour le n° CAS 105294-34-6, l'autre produit de clivage azoïque prévu du Disperse Red 179. Les résultats de la modélisation RQSA pour les paramètres de cancérogénicité et de génotoxicité étaient mitigés pour ces deux produits de clivage azoïques potentiels (voir l'annexe 5).
Le seul analogue pertinent relevé, le Disperse Red 145 (n° CAS 25510-81-0), a produit un résultat positif lors du test umu/SOS avec et sans activation de la fraction S9 dérivée du foie (Kosaka et Nakamura, 1990).Il convient de noter également que la classe des colorants azoïques aminobenzothiazoles a été signalée par la Environmental Protection Agency (EPA) des États-Unis comme une catégorie de substance chimique du New Chemicals Program (NCP) visé par la Toxic Substances Control Act (TSCA), en raison des inquiétudes quant aux risques que posent les substances connexes et les métabolites potentiels (US EPA, 2002).
L'information obtenue concernant le Disperse Red 179, ses produits de clivage azoïques potentiels et un analogue structurel (Disperse Red 145) indique que certains risques potentiels pourraient être associés à Dispered Red 179. Toutefois, le niveau de confiance à l'égard de la base de données toxicologiques est réputé faible, en raison des données empiriques limitées pour cette substance.
DAPEP (25176-89-0)
Aucune donnée empirique sur la toxicité n'a été trouvée pour le DAPEP. Cependant, comme le DAPEP est un des deux isomères qui constituent le Disperse Red 153 (n° CAS 78564-87-1), [1] les données relatives à cette substance sont jugées représentatives du DAPEP. Une seule étude a révélé que le Disperse Red 153 était négatif lors du test umu/SOS avec et sans activation de la fraction S9 (Kosaka et Nakamura, 1990). En outre, les résultats des modèles de prévision RQSA sur les deux isomères du Disperse Red 153 étaient mitigés pour les paramètres de cancérogénicité et de génotoxicité (voir l'annexe 7). Étant donné que seules des données limitées étaient disponibles en matière de toxicité potentielle du DAPEP et du Disperse Red 153, des renseignements pertinents relatifs aux métabolites et aux analogues potentiels ont également été pris en considération.
Comme le DAPEP est un membre de la famille des substances azoïques, les produits de clivage azoïques potentiels du DAPEP – à savoir, le 2-amino-5,6-dichlorobenzothiazole (n° CAS 24072-75-1) et le 3-[(4-aminophényl)éthylamino]propanenitrile (n° CAS 100894-10-8) (voir l'annexe 8) – sont pris en considération dans cette évaluation préalable (consulter la section précédente pour connaître la justification).
Le métabolite prévu n° CAS 24072-75-1 (2-amino-5,6-dichlorobenzothiazole) a été soumis à des essais de mutagénicité in vivo et in vitro. La mutagénicité de cette substance était négative tant chez le Salmonella typhimurium (NTP, 1986a; Seifried et al., 2006) que dans les cellules de lymphomes de souris. 2006). La substance n'a pas provoqué la formation de micronoyaux chez des souris mâles ou femelles exposées par voie orale par leur alimentation dans le cadre d'une étude de toxicité subchronique inédite (NTP, 1993; Witt et al., 2000). Bien que l'ensemble de données exhaustif pour cette étude soit inédit et indisponible dans l'immédiat (NTP, 1986b), un rapport concis du National Toxicology Program des États-Unis a indiqué que certains effets histopathologiques dans le foie et les reins ont été observés chez des rats et des souris. Toutefois, l'incidence et les doses n'ont pas été fournies (NTP, 2000). Il convient de noter également que l'US EPA a relevé la classe des colorants azoïques aminobenzothiazoles en partie en raison de préoccupations relatives à la neurotoxicité du « 2-aminobenzothiazole chloré » en tant que produit de clivage réducteur (US EPA, 2002). Aucune donnée empirique sur la toxicité n'a été définie pour les autres métabolites potentiels n° CAS 100894-10-8 ou CAS25150-27-0 (le produit de clivage azoïque prévu de l'autre isomère dichloro présent dans le Disperse Red 153, se reporter à l'annexe 8 pour la structure). Les résultats de la modélisation RQSA sur la cancérogénicité et la génotoxicité étaient mitigés pour tous les métabolites de clivage azoïques prévus pour le DAPEP et l'isomère 6,7'-dichloro du Disperse Red 153 (voir l'annexe 7).
Disperse Red 153 (n° CAS78564-87-1, un mélange d'isomères comprenant le DAPEP, déjà abordé ci-dessus) et du Disperse Red 152 (n° CAS78564-86-0) ont été relevé comme des analogues potentiels de DAPEP. Le Disperse Red 152 est aussi un mélange d'isomères 5,6'- et 6,7'-dichloro, il est semblable au Disperse Red 153 (voir l'annexe 8 pour la structure) et il a donné un résultat négatif similaire à ceux du test umu/SOS (Kosaka et Nakamura, 1990). Bien que des analogues limités aient été relevés pour le DAPEP d'après les critères susmentionnés, il convient de noter également que la classe des colorants azoïques aminobenzithiazoles à laquelle appartient le DAPEP a été relevé par l'US EPA. comme une catégorie de substance chimique du New Chemicals Program (NCP) visé par la Toxic Substances Control Act (TSCA), en raison des inquiétudes quant aux risques que posent les substances connexes et les métabolites potentiels (US EPA, 2002).
L'information toxicologique limitée obtenue concernant le DAPEP, leurs produits de clivage azoïques potentiels et un analogue structurel (Disperse Red 153) indique que certains risques potentiels pourraient être associés au DAPEP. Toutefois, le niveau de confiance à l'égard de la base de données toxicologiques est réputé faible, en raison des données empiriques limitées disponibles pour cette substance.
Caractérisation du risque pour la santé humaine
Bien que seules des données empiriques limitées aient été relevées pour le Disperse Red 179 et le DAPEP, leurs produits de clivage azoïques et analogues potentiels, les données connexes, ainsi que les résultats RQSA mitigés, indiquent que des propriétés dangereuses. Cependant, les données disponibles limitées en ce qui concerne les risques empêchent le choix d'une dose avec effet critique à utiliser dans la caractérisation du risque de cette substance.
Le Disperse Red 179 et le DAPEP appartiennent au groupe des substances azoïques qui peuvent rejeter des amines aromatiques par clivage réducteur de la liaison azoïque. Bien que les données sur les risques concernant les amines aromatiques précises associées au Disperse Red 179 et au DAPEP soient limitées, la base de données collective sur la toxicité des amines aromatiques en tant que groupe chimique (Vineis et Pirastu, 1997; Benigni et Passerini, 2002; Talaska, 2003) laisse entendre que ces substances peuvent constituer une source d'inquiétude.
L'exposition potentielle de la population générale au Disperse Red 179 et au DAPEP présents dans les milieux naturels devrait être négligeable.
L'exposition de l'ensemble de la population canadienne au Disperse Red 179 et au DAPEP résultant du port de vêtements teints par tous les groupes d'âge et du mâchonnement fortuit de tissus par des enfants a quantifiée et est faible.
Comme l'exposition de l'ensemble de la population canadienne devrait être faible en raison de l'utilisation de la substance en tant que colorant pour textiles synthétiques, le risque prévu pour la santé humaine découlant des risques potentiels est réputé faible.
Incertitudes de l'évaluation des risques pour la santé humaine
Des incertitudes existent quant à l'évaluation de l'exposition. Aucune information n'était disponible quant aux facteurs de migration et à la solubilité du Disperse Red 179 et du DAPEP. Les sources d'exposition ont été caractérisées globalement en tant que tissus synthétiques, étant donné qu'aucun produit de consommation précis n'a été trouvé. Cependant, le niveau de confiance est élevé parce que les estimations relatives à l'exposition sont prudentes, pour les raisons suivantes. Le facteur de migration utilisé dans l'évaluation correspond à une exposition quotidienne à des tissus neufs, non lavés et présentant une indégorgeabilité faible, alors que l'on considère que le rejet de la substance se produit principalement pendant le lavage. En outre, une étude a démontré que la quantité de colorant dispersé migrant sur la peau de volontaires humains était beaucoup plus faible que celle rejetée en solution.
Le niveau de confiance à l'égard de la base de données toxicologiques pour ces substances est jugé très faible. Il y a des données limitées sur les risques associés au Disperse Red 179 et DAPEP. Il y a également un manque de renseignements sur le potentiel qu’ont ces substances de devenir des substances clivage azoïques, un aspect majeur pris en compte lors de l’évaluation de la toxicité des substances azotiques.
D'après les renseignements présentés dans la présente évaluation préalable, ni le Disperse Red 179, ni le DAPEP ne pénètrent dans l'environnement en une quantité ou une concentration ou dans des conditions qui ont ou peuvent avoir, immédiatement ou à long terme, un effet nocif sur l'environnement ou sur sa diversité biologique; par ailleurs, ces substances ne constituent ni ne peuvent présenter un danger pour l'environnement essentiel à la vie.
Bien que les données empiriques de modélisation pour les substances soient limitées, leurs métabolites et analogues potentiels indiquent un risque potentiel, d'après la prise en considération des renseignements limités sur les effets de la santé et la faible exposition même négligeable de l'ensemble de la population au Disperse Red 179 et au DAPEP, il est conclu que le Disperse Red 179 et le DAPEP ne pénètrent pas dans l’environnement en quantités, à des concentrations ou dans des conditions qui constituent ou peuvent constituer un danger pour la vie ou la santé humaine au Canada.
Par conséquent, il est conclu que le Disperse Red 179 et le DAPEP ne correspondent pas à la définition de « substance toxique » énoncée dans l’article 64 de la LCPE (1999). De plus, ces substances répondent au critère de la persistance, mais pas à ceux de la bioaccumulation énoncés dans le Règlement sur la persistance et la bioaccumulation (Canada, 2000).
Puisque ces substances sont inscrites sur la Liste intérieure des substances, leur importation et leur fabrication au Canada ne requièrent pas de déclaration aux termes du paragraphe 81(1). Étant donné les propriétés dangereuses potentielles de ces substances, on craint que des utilisations nouvelles non décelées ni évaluées fassent en sorte qu'elles répondent aux critères de l'article 64 de la LCPE (1999). Par conséquent, il est recommandé de modifier la Liste intérieure des substances en vertu du paragraphe 87(3) de la Loi afin d'indiquer que le paragraphe 81(3) s'applique à ces substances. Ainsi, toute fabrication, importation ou utilisation de ces dernières devra être déclarée et faire l'objet d'une évaluation des risques pour l'environnement et la santé humaine.
De plus, s'il y a lieu, des activités de recherche et de surveillance viendront appuyer la vérification des hypothèses formulées au cours de l'évaluation préalable.
Considérations dans le cadre d'un suivi
Le Disperse Red 179 et le DAPEP appartiennent à un groupe des substances azoïques qui peuvent se métaboliser en amines aromatiques et qui, en tant que groupe chimique connu pour présenter des propriétés dangereuses, notamment la cancérogénicité. Par conséquent, des activités supplémentaires (p. ex. recherche, contrôle et surveillance, évaluation) pourraient être entreprises afin de caractériser le risque pour la santé humaine au Canada relatif à ces lots de substances azoïques plus larges.
ACD/pKaDB [module de prédiction]. 2005. Version 9.04. Toronto (Ont.) : Advanced Chemistry Development. Accès : http://www.acdlabs.com/products/phys_chem_lab/pka/
Anliker, R., Clarke, E.A., Moser, P. 1981. Use of the partition coefficient as an indicator of bioaccumulation tendency of dyestuffs in fish. Chemosphere 10(3):263-274.
Anliker, R., Moser, P. 1987. The limits of bioaccumulation of organic pigments in fish: their relation to the partition coefficient and the solubility in water and octanol. Ecotoxicol. and Environ. Safety 13:43-52.
Anliker, R., Moser, P., Poppinger, D. 1988. Bioaccumulation of dyestuffs and organic pigments in fish. Relationships to hydrophobicity and steric factors. Chemosphere17(8):1631-1644.
Aronson, D., Boethling, B., Howard, P., Stiteler, W. 2006. Estimating biodegradation half-lives for use in chemical screening. Chemosphere 63:1953-1960.
Aronson, D., Howard, P.H. 1999. Evaluating potential POP/PBT compounds for environmental persistence. North Syracuse (NY) : Syracuse Research Corp., Environmental Science Centre. No rapport : SRCTR99020.
Baughman, G.L., Perenich, T.A. 1988. Fate of dyes in aquatic systems: I. Solubility and partitioning of some hydrophobic dyes and related compounds. Environ. Toxicol. Chem.7(3):183-199.
Baughman, G.L., Weber, E.J. 1994. Transformation of dyes and related compounds in anoxic sediment: kinetics and products. Environ. Sci. Technol. 28(2):267-276.
[BBM] Baseline Bioaccumulation Model. 2008. Gatineau (Qc) : Environnement Canada, Division des substances existantes. [modèle élaboré d'après Dimitrov et al., 2005]. [consulté le 21 novembre 2008]. Disponible sur demande.
Benigni, R., Passerini, L. 2002. Carcinogenicity of the aromatic amines: from structure–activity relationships to mechanisms of action and risk assessment. Mutat. Res.511(3):191-206.
[BIOWIN] Biodegradation Probability Program for Windows [modèle d'estimation]. 2000. Version 4.02. Washington (DC) : U.S. Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY) : Syracuse Research Corporation. Accès : http://www.epa.gov/oppt/exposure/pubs/episuite.htm
BMG. 2000a. C.I. Disperse Red 153, Test for inhibition of oxygen consumption by activated sludges: Respiration Inhibition Test. BMG report no. 800/b-00, décembre 2000.
BMG. 2000b. Foron Rubin RD-S Presskuchen trocken, 96-hour acute toxicity to Poecilia reticulata (Guppy): Limit Test (100 mg/L). BMG report no. 800/a-00, décembre 2000.
BMG. 2001. C.I. Disperse Red 153, Inherent biodegradability – Evaluation of the aerobic biodegradability in an aqueous medium: Zahn-Wellens/EMPA test. BMG report no. 800/c-00, janvier 2001.
BMG. 2003a. Foron Rubin RD-S Presskuchen trocken, Inherent biodegradability – Evaluation of the aerobic biodegradability in an aqueous medium: Zahn-Wellens/EMPA test. BMG report no. 709/c-03, octobre 2003.
BMG. 2003b. Foron Rubin RD-S Presskuchen trocken, Test for inhibition of oxygen consumption by activated sludges: Respiration Inhibition Test. BMG report no. 709/a-03, octobre 2003.
BMG. 2003c. Foron Rubin RD-S Presskuchen trocken, 96-hour acute toxicity to Poecilia reticulata (Guppy): Screening Test. BMG report no. 709/b-03, octobre 2003.
Boethling, R.S., Howard, P.H., Beauman, J.A., Larosche, M.E. 1995. Factors for intermedia extrapolations in biodegradability assessment. Chemosphere. 30(4):741-752.
Brown D. 1987. Effects of colorants in the aquatic environment. Ecotoxicol. Environ. Safety 13:139-147.
Brown, D. (ICI Group Environmental Laboratory, Brixham, UK). 1992. Environmental assessment of dyestuffs. Rédigé pour le compte de l'Ecological and Toxicological Association of the Dyes and Organic Pigments Manufacturers, Bâle, Suisse, ETAD ecological sub-committee project E3020. Présenté à Environnement Canada.
Canada. 1999. Loi canadienne sur la protection de l'environnement (1999), L.C., ch. 33, Gazette du Canada. Partie III, vol. 22, no 3. Ottawa : Imprimeur de la Reine. Accès : http://www.canlii.org/fr/ca/legis/lois/lc-1999-c-33/derniere/lc-1999-c-33.html
Canada. 2000. Loi canadienne sur la protection de l'environnement (1999) : Règlement sur la persistance et la bioaccumulation, C.P. 2000-348, 23 mars 2000, DORS/2000-107, Gazette du Canada. Partie II, vol. 134, no 7, p. 607-612. Ottawa : Imprimeur de la Reine. Accès : http://www.gazette.gc.ca/archives/p2/2000/2000-03-29/pdf/g2-13407.pdf
Canada. Ministère de l'Environnement, Ministère de la Santé. 2006a. Loi canadienne sur la protection de l'environnement (1999) : Avis d'intention d'élaborer et de mettre en œuvre des mesures d'évaluation et de gestion des risques que certaines substances présentent pour la santé des Canadiens et leur environnement, Gazette du Canada. Partie I, vol. 140, no 49, p. 4109-4117. Ottawa : Imprimeur de la Reine. Accès : http://www.gazette.gc.ca/archives/p1/2006/2006-12-09/pdf/g1-14049.pdf
Canada. Ministère de l'Environnement, Ministère de la Santé. 2006b. Loi canadienne sur la protection de l'environnement (1999) : Avis concernant certaines substances considérées comme priorités pour suivi. Gazette du Canada. Partie I, vol. 140, no 9, p. 435-459. Accès : http://www.gazette.gc.ca/archives/p1/2006/2006-03-04/pdf/g1-14009.pdf
Canada. Ministère de l'Environnement, Ministère de la Santé. 2008. Loi canadienne sur la protection de l'environnement (1999) : Avis de septième divulgation d'information technique concernant les substances identifiées dans le Défi.Gazette du Canada. Partie I, vol. 142, no 35, p. 2497-2501. Ottawa : Imprimeur de la Reine. Accès : http://www.gazette.gc.ca/rp-pr/p1/2008/2008-08-30/pdf/g1-14235.pdf
CASETOX [module de prévision]. 2008. Version 2.0. Beachwood (OH) : MultiCASE. [consulté le 30 sept. 2009]. Accès : http://www.multicase.com/products/prod03.htm[réserve de consultation].
Chen, H. 2006. Recent advances in azo dye degrading enzyme research. Curr. Protein Pept. Sci. 7:101111.
[CATABOL] Probabilistic assessment of biodegradability and metabolic pathways [modèle informatique]. c2004-2008. Version 5.10.2. Bourgas (Bulgarie) : Bourgas Prof. Assen Zlatarov University, Laboratory of Mathematical Chemistry. Accès : http://oasis-lmc.org/?section=software&swid=1
[ChemID] ChemID Plus Advanced. [base de données sur Internet]. 2009. [consultée le 20 avril 2009]. U.S. National Library of Medicine (MD), National Institute of Health. Accès : http://chem.sis.nlm.nih.gov/chemidplus/
Chen, H. 2006. Recent advances in azo dye degrading enzyme research. Curr. Protein Pept. Sci. 7:101111.
Choi, J.H., Kim, M.H., Park, J.S., Jeon, J.M., Kim, D.O., Towns, A.D. 2007. Coloration of poly(lactic acid) with disperse dyes. II. Dyeing characteristics and color fastness. Fibers and Polymers 8(1):37-42.
Chudgar, R.J., Oakes, J. 2003. Dyes, azo. In: Kirk-Othmer encyclopedia of chemical technology, édition en ligne. Accès : http://mrw.interscience.wiley.com/emrw/9780471238966/kirk/article/azochud.a01/
current/abstract? hd=All,azoandhd=All,dye [réserve de consultation]
[CII] Color Index International [base de donnée en ligne]. 2002. 4e éd. Research Triangle Park (NC) : American Association of Textile Chemists and Colorists. [consultée le 25 mars 2009]. Accès : http://www.colour-index.org/
Clariant. 1996. IUCLID dataset for C.I. Disperse Blue 79 (no CAS 12239-34-8).
Colon, D., Weber, E., Baughman, G. 2002. Sediment-associated reactions of aromatic amines. 2. QSAR development. Environ. Sci. Technol. 35(12):2443-2450.
[ConsExpo] Consumer Exposure Model [en ligne]. 2006. Version 4.1. Bilthoven (Pays-Bas) : Rijksinstituut voor Volksgezondheid en Milieu (Institut national néérlandais de la santé publique et de l'environnement). Accès : http://www.rivm.nl/en/healthanddisease/productsafety/ConsExpo.jsp#tcm:13–42840
[CPOPs] Modèle canadien de POP. 2008. Gatineau (Qc) : Environnement Canada, Division des substances existantes; Bourgas (Bulgarie) : Bourgas Prof. Assen Zlatarov University, Laboratory of Mathematical Chemistry. [Modèle élaboré à partir de celui de Mekenyan et al., 2005]. Disponible sur demande.
[Danish EPA] Danish Environmental Protection Agency. 1998. Azocolorants in Textiles and Toys, Environmental and Health Assessment. Environmental Project, no. 416 1998. Accès : http://www2.mst.dk/common/Udgivramme/Frame.asp? http://www2.mst.dk/udgiv/Publications/1998/87-7909-136-9/html/helepubl_eng.htm
de Bruijn, J., Busser, F., Seinen, W., Hermens, J. 1989. Determination of octanol/water partition coefficients for hydrophobic organic chemicals with the “slow-stirring” method. Environ. Toxicol. Chem. 8:499-512.
[DEREK] Deductive Estimation of Risk from Existing Knowledge [module de prévision sur CD ROM]. 2008. Version 10.0.2. Cambridge (MA) : Harvard University, LHASA Group. [consulté le 30 sept. 2009]. Accès : http://www.lhasalimited.org/index.php? cat=2&sub_cat=2# [réserve de consultation].
Dimitrov, S., Dimitrova, N., Parkerton, T., Comber, M., Bonnell, M., Mekenyan, O. 2005. Base-line model for identifying the bioaccumulation potential of chemicals. SAR QSAR Environ. Res. 16(6):531-554.
Dimitrov, S.D., Dimitrova, N.C., Walker, J.D., Veith, G.D., Mekenyan, O.G. 2002. Predicting bioconcentration factors of highly hydrophobic chemicals. Effects of molecular size. Pure Appl. Chem. 74(10):1823-1830.
[Environ] ENVIRON International Corporation. 2003a. Voluntary Children’s Chemical Evaluation Program Pilot (VCCEPP)–Tier 1 assessment of the potential health risks to children associated with exposure to the commercial pentabromodiphenyl ether product and appendices [en ligne]. Emerville (CA) : ENVIRON International Corporation. [Accès : http://www.epa.gov/oppt/vccep/pubs/chem22a.html]
[Environ] ENVIRON International Corporation. 2003b. Voluntary Children’s Chemical Evaluation Program Pilot (VCCEPP)–Tier 1 assessment of the potential health risks to children associated with exposure to the commercial octabromodiphenyl ether product and appendices [en ligne]. Emerville (CA) : ENVIRON International Corporation. [Accès : http://www.epa.gov/oppt/vccep/pubs/chem23a.h]
[ECOSAR] Ecological Structural Activity Relationships [en ligne]. 2004. Version 0.99h. Washington (DC) : U.S. Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY) : Syracuse Research Corporation. Accès : www.epa.gov/oppt/exposure/pubs/episuite.htm
Environnement Canada, Division de l'évaluation des produits chimiques. 2000. Environmental Categorization for Persistence Bioaccumulation and Inherent Toxicity of Substances on the Domestic Substances List Using QSARs (juillet 2000). Rapport final. Environnement Canada.
Environnement Canada. 1994. Soumission de l'essai de toxicité aiguë pour le poisson conformément au Règlement sur les renseignements concernant les substances nouvelles. Données présentées à la Division des substances nouvelles d'Environnement Canada.
Environnement Canada. 2006.Données pour certaines substances recueillies en vertu de l'article 71 de la Loi canadienne sur la protection de l'environnement (1999) : Avis concernant certaines substances considérées comme priorités pour suivi. Données préparées par Environnement Canada, Santé Canada, Programme des substances existantes.
Environnement Canada. 2009a. Données sur les substances du lot 7 recueillies en vertu de l'article 71 de la Loi canadienne sur la protection de l'environnement (1999) : Avis concernant certaines substances identifiées dans le septième lot du Défi. Données produites par la Division des substances existantes, Environnement Canada.
Environnement Canada. 2009b. Guidance for conducting ecological assessments under CEPA, 1999: science resource technical series, technical guidance module: Mass Flow Tool. Document de travail préliminaire. Gatineau (Qc) : Environnement Canada, Division des substances existantes.
Environnement Canada. 2009c. Assumptions, limitations and uncertainties of the mass flow tool for Disperse Red 179, CAS RN 16586-42-8. Document provisoire interne. Gatineau (Qc) : Environnement Canada, Division des substances existantes. Disponible sur demande.
Environnement Canada. 2009d. Assumptions, limitations and uncertainties of the mass flow tool for DAPEP, CASRN 25176-89-0. Document provisoire interne. Gatineau (Qc) : Environnement Canada, Division des substances existantes. Disponible sur demande.
Environnement Canada. 2009e. Site Specific Analysis report: CAS RN 16586-42-8 &25176-89-0, rapport inédit. Gatineau (Qc) : Environnement Canada, Division des évaluations écologiques.
Environnement Canada. 2009f. Mega Flush report: CASRN 16586-42-8, 2009-04-28. Rapport inédit. Gatineau (Qc) : Environnement Canada, Division des substances existantes.
Environnement Canada. 2009g. Mega Flush report: CASRN 25176-89-0, 2009-04-28. Rapport inédit. Gatineau (Qc) : Environnement Canada, Division des substances existantes.
[EPIsuite] Estimation Programs Interface Suite for Microsoft Windows [modèle d'estimation]. 2008. Version 4.0. Washington (DC) : U.S. Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY) : Syracuse Research Corporation. Accès : http://www.epa.gov/oppt/exposure/pubs/episuite.htm
[ETAD] Ecological and Toxicological Association of Dyes and Organic Pigments Manufacturers. 1983. Extractability of dyestuffs from textiles. Basel (Suisse) : Ecological and Toxicological Association of Dyes and Organic Pigments Manufacturers. ETAD Project A 4007.
[ETAD] Ecological and Toxicological Association of Dyes and Organic Pigments. Affiliés canadiens, Dayan, J., Trebitz, H. 1995. Health and environmental information on dyes used in Canada. Rapport inédit présenté à Environnement Canada, Division des substances existantes. En page couverture : An overview to assist in the implementation of the New Substances Notification Regulations under the Canadian Environmental Protection Act.
[ETAD] The Ecological and Toxicological Association of Dyes and Organic Pigments Manufacturers. 2004. Setting a risk based detection limit of sensitizing disperse dyes on textiles. Accès : www.etad.com/documents/Downloads/publications/detectionlimit.pdf
[ETAD] Ecological and Toxicological Association of Dyes and Organic Pigments Manufacturers. 2005. ETAD data for DSL categorization and screening, présenté à Environnement Canada le 27 octobre 2005. Rapport d'étude préparé par Intertek ASG, no de référence 2005/CC0157-001/REGIS.
Golka, K., Kopps, S., Myslaket, Z.W. 2004. Carcinogenicity of azo colorants: influence of solubility and bioavailability. Toxicology Letters 151:203-210
Health, Safety, and Human Factors Laboratory. 1978. Basic Toxicity of 2-[4-[(6-chloro-2-benzothiazolylazo)phenyl]-ethylamino]ethyl acetate. Toxicology Section, Health, Safety, and Human Factors Laboratory. Rapport soumis par la Eastman Kodak Company en 1992 à la U.S. Environmental Protection Agency Registration and Agreement for the TSCA 8(a) Compliance Audit Program.
Santé Canada. 1998. Exposure factors for assessing total daily intake of priority substances by the general population of Canada. Rapport inédit. Ottawa (Ont.) : Santé Canada, Direction de l'hygiène du milieu.
Helmes, C.T., Fung, V.A., Lewin, B., McCaleb, K.E., Malko, S., Pawlovich, A.M. 1982. A study of aromatic nitro compounds for the selection of candidates for carcinogen bioassay. J. Environ. Sci. Health A Environ. Sci. Eng. Toxic Hazard Subst. Control17:75-128.
Hunger, K., éd. 2003. Industrial dyes; chemistry, properties, applications. Weinheim (Allemagne) : WILEY-VCH Verlag GmbH & Co. KGaA.
Kosaka, H., Nakamura, S. 1990. Genotoxicity of synthetic dyes in umu test using Salmonella typhimurium TA1535/pSK1002 (1). Jpn. J. Ind. Health. 32:89-104. (cité également dans Reifferscheid & Heil, 1996)
[KOWWIN] Octanol-Water Partition Coefficient Program for Microsoft Windows [modèle d'estimation]. 2000. Version 1.67. Washington (DC) : U.S. Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY) : Syracuse Research Corporation. Accès : www.epa.gov/oppt/exposure/pubs/episuite.htm
Kraetke, R.M., Platzek, T. 2005. Exposure to chemicals in clothing textiles: methods and models [en ligne]. Abstract for Poster 74 at the conference “Occupational and environmental exposure of skin to chemicals--2005.” Washington (DC) : National Institute for Occupational Safety and Health. Accès : http://www.cdc.gov/niosh/topics/skin/OEESC2/AbPost074Kraetke.html
[Leadscope] Leadscope Model Applier [module de prévision]. 2009. Version 1.2.0-3. Columbus (OH) : Leadscope, Inc. [consulté le 30 sept. 2009]. Accès : http://www.leadscope.com/all_products.php[réserve de consultation].
Little, L.W., Lamb, J.C. III. 1973. Acute toxicity of 46 selected dyes to the fathead minnow, Pimephales promelas.Dyes and the Environment - Reports on Selected Dyes and Their Effects. American Dye Manufacturers Institute, Inc. 1:130.
Maradiya, H.R. 2004. Disperse dyes based on 2-aminoheterocycles. J. Saudi Chem. Soc. 8(3):495-504.
Meinke, M., Abdollahnia, M., Gähr, Platzek, T., Sterry, W., Lademann, J. 2009. Migration and penetration of a fluorescent textile dye into the skin – in vivo versus in vitro methods. Experimental Dermatology18(9):789-792.
Mekenyan, G., Dimitrov, S.D., Pavlov, T.S., Veith, G.D. 2005. POPs: a QSAR system for creating PBT profiles of chemicals and their metabolites. SAR QSAR Environ. Res.16(1-2):103-133.
[MITI] Ministry of International Trade & Industry (Japon), Basic Industries Bureau, Chemical Products Safety Division. 1992. Biodegradation and bioaccumulation data of existing chemicals based on the CSCL Japan. Tokyo (Japon) : Japan Chemical Industry Ecology-Toxicology & Information Centre.
Mortelmans, K., Haworth, S., Lawlor, T., Speck, W., Tainer, B., Zeiger, E. 1986. Salmonella mutagenicity tests: II. Results from the testing of 270 chemicals. Environ. Mutagen.8:1-119
Nakagawa, M., Kawai, K., Kawai, K. 1996. Multiple azo disperse dye sensitization mainly due to group sensitizations to azo dyes. Contact Dermatitis 34:6-11.
[NCI] National Chemical Inventories [base de données sur cédérom]. 2009. Columbus (OH) : American Chemical Society. [consultée le 11 mars 2009]. Accès : http://www.cas.org/products/cd/nci/index.html
Noriris, B., Smith, S. 2002. Research into the mouthing behaviour of children up to 5 years old. Rapport commandé par le Ministère du commerce et de l'industrie du Royaume-Uni [traduction], Londres (Royaume-Uni).
[NTP] National Toxicology Program. 1982. Study ID 70250: Test result for an in vitro genetic toxicology test (mutagenicity in Salmonella) for 2-amino-6-nitrobenzothiazole (6285-57-0). Research Triangle Park (NC) : National Institutes of Health's National Institute of Environmental Health Sciences (NIEHS). [base de donnée du NTP consultée le 23 nov. 2009]. Accès :
http://ntp-apps.niehs.nih.gov/ntp_tox/index.cfm? fuseaction=salmonella.salmonellaData&study_no=
702501&cas_no=6285%2D57%2D0&endpointlist=SA [cité également dans Mortelmans et al., 1986]
[NTP] National Toxicology Program. 1983. Study ID 832791: Test result for an in vitro genetic toxicology test (mutagenicity in Salmonella) for 2-amino-6-nitrobenzothiazole (6285-57-0). Research Triangle Park (NC) : National Institutes of Health's National Institute of Environmental Health Sciences (NIEHS). [base de données du NTP consultée le 23 nov. 2009]. Accès : http://ntp-apps.niehs.nih.gov/ntp_tox/index.cfm? fuseaction=salmonella.salmonellaData&study_no=
832791&cas_no=6285%2D57%2D0&endpointlist=SA [cité également dans Mortelmans et al., 1986]
[NTP] National Toxicology Program. 1986a. Study ID 461292: Test result for an in vitro genetic toxicology test (mutagenicity in Salmonella) for 5,6'-dichloro-2-benzothiazolamine (24072-75-1). Research Triangle Park (NC) : National Institutes of Health's National Institute of Environmental Health Sciences (NIEHS). [base de données du NTP consultée le 23 nov. 2009]. Accès : http://ntp-apps.niehs.nih.gov/ntp_tox/index.cfm? fuseaction=salmonella.overallresults&cas_no=
24072-75-1&endpointlist=SA [cité également dans Mortelmans et al., 1986
[NTP] National Toxicology Program. 1986b. Study ID C61712: Short-term toxicity studies (2-week, 13-week, dosed-feed) in rats and mice for 5,6'-dichloro-2-benzothiazolamine (24072-75-1). (aucun rapport de toxicité publié). Accès : http://ntp-apps.niehs.nih.gov/ntp_tox/index.cfm? fuseaction=shorttermbioassaydata.datasearch&chemical_name=5%2C6-Dichloro-2-benzothiazolamine&cas_no=24072-75-1&study_no=C61712&study_length=13%20Weeks
[NTP] National Toxicology Program. 1993. Study ID A42046: Test result for in vivo micronucleus induction in male and female mice for 5,6'-dichloro-2-benzothiazolamine (24072-75-1). Research Triangle Park (NC) : National Institutes of Health's National Institute of Environmental Health Sciences (NIEHS). [base de données du NTP consultée le 23 nov. 2009]. Accès : http://ntp-apps.niehs.nih.gov/ntp_tox/index.cfm? fuseaction=micronucleus.choosestudytype&cas_no=24072-75-1&endpointlist=MN[cité également dansWitt et al., 2000]
[NTP] National Toxicology Program. 2000. Short-term study toxicity. Prechronic toxicity for 5,6'-dichloro-2-benzothiazolamine (24072-75-1). Study ID C61712. Research Triangle Park (NC) : National Institutes of Health's National Institute of Environmental Health Sciences (NIEHS). [base de données du NTP consultée le 23 nov. 2009]. Accès : http://ntp-server.niehs.nih.gov/index.cfm? objectid=03621D4C-B63D-AED4-CB677FD7CC46D300
[OASIS Forecast] Optimized Approach based on Structural Indices Set [en ligne]. 2005. Version 1.20. Bourgas (Bulgarie) : Bourgas Prof. Assen Zlatarov University, Laboratory of Mathematical Chemistry. Accès : http://oasis-lmc.org/?section=software
[OCDE] Organisation de coopération et de développement économiques. 2004. Emission scenario document on adhesive formulation [en ligne]. Rapport final. Paris (France) : Direction de l'environnement de l'OCDE. (Series on Emission Scenario Documents). Accès : http://ascouncil.org/news/adhesives/docs/EPAFormulation.pdf
[OCDE] Organisation de coopération et de développement économiques. 2007. Draft emission scenario on textile manufacturing wool mills [en ligne]. Paris (France) : OCDE, Direction de l'environnement. Rapport no : ENV/JM/EEA(2004)8/1/REV, JT00175156. Accès : http://www.oecd.org/dataoecd/2/47/34003719.pdf
Pagga, U., Brown, D. 1986. The degradation of dyestuffs: Part II Behaviour of dyestuffs in aerobic biodegradation tests. Chemosphere 15(4):479-491.
Peters, A.T., Gbadamosi, N.M.A. 1992. 5,6-(6,7-) dichlorobenzothiazolylazo dyes for synthetic-polymer fibres. Dyes and Pigments 18:115-123.
Peters, A.T., Tsatsaroni, E., Xisai, M. 1992. Hetarylazo disperse dyes derived from 5,6-dichloro- and 6,7-dichloro-2 aminobenzothiazoles. Dyes and Pigments 20:41-51.
Platzek, T., Lang, C., Grohmann, G., Gi, U.S., Baltes, W. 1999. Formation of a carcinogenic aromatic amine from an azo dye by human skin bacteria in vitro. Human & Experimental Toxicology 18:552-559.
Razo-Flores, E., Luijten, M., Donlon, B., Lettinga, G., Field, J. 1997. Biodegradation of selected azo dyes under methanogenic conditions. Wat. Sci. Tech. 36(6-7):65-72.
Refferscheid, G., Heil, J. 1996. Validation of the SOS/umu test using results of 486 chemicals and comparison with the Ames test and carcinogenicity data. Mut. Res. 369:129-145.
[RIVM] Rijksinstituut voor Volksgezondheid en Milieu. 2005. ConsExpo 4.0. Consumer exposure and uptake models. Manuel du programme [en ligne]. Report No.: 320104004/2005. Bilthoven (Pays-Bas) : RIVM (Institut national néérlandais de la santé publique et de l'environnement). [consulté le 16 nov. 2009]. Accès : http://rivm.openrepository.com/rivm/bitstream/10029/7307/1/320104004.pdf
S.M.S Technology Co., Ltd. [date inconnue]. Material Safety Data Sheet (MSDS) for Navacron Disperse Scarlet GS [en ligne]. Accès : http://www.intonline.org/product/nava-doc/navacron-msds/9-Navacron%20dyes/msds(Navacron%20Scarlet%20GS).pdf
Safepharm Laboratories Ltd. 1990. Acute toxicity to rainbow trout. Project number 47/781. No de déclaration dans le cadre du défi : 11347.
Sakuratani, Y., Noguchi, Y., Kobayashi, K., Yamada, J., Nishihara, T. 2008. Molecular size as a limiting characteristic for bioconcentration in fish. J. Environ. Biol. 29(1):89-92.
Sandoz. 1975. Acute Fish Toxicity (Rainbow trout), 48 hr. Données tirées à partir des questionnaires volontaires relatifs aux substances contenues dans le lot 5 du Plan de gestion des produits chimiques. Préparé par Environnement Canada.
Sandoz. 1975. Voluntary Data Submission under Section 71.
Sarex Overseas. 1995. Material Safety Data Sheet (MSDS) for SARAPERSE RED 4G [en ligne]. Accès : http://www.sarex.com/dyesmsds/PS616.HTM
Savarino, P., Viscardi, G., Carpignano, R., Barni, E. 1989. Technical properties and photofading of disperse heterocyclic azo dyes. Dyes and Pigments 10:269-283.
Seifried, H.E., Seifried, R.M., Clarke, J.J., Junghans, T.B., San, R.H. 2006. A compilation of two decades of mutagenicity test results with the Ames Salmonella typhimurium and L5178Y mouse lymphoma cell mutation assays. Chem. Res. Toxicol. 19:627-44.
Shen, G., Hu, S. (Environmental Testing Laboratory, Shanghai Academy of Environmental Sciences, Shanghai, Chine). 2008. Bioconcentration Test of C.I. Disperse Orange 30 in Fish, préparé par Environmental Testing Laboratory, Shanghai Academy of Environmental Sciences, Shanghai (Chine) pour Dystar au nom de l'Ecological and Toxicological Association of the Dyes and Organic Pigments Manufacturers (ETAD), Bâle (Suisse). Rapport no S-070-2007. Présenté à Environnement Canada en avril 2008, no de déclaration dans le cadre du défi 8351.
Sijm, D.T.H.M., Schuurmann, G., deVries, P.J., Opperhuizen, A. 1999. Aqueous solubility, octanol solubility, and octanol/water partition coefficient of nine hydrophobic dyes. Environ. Toxicol. Chem. 18(6):1109-1117.
Stingley, R., Zou, W., Heinze, T., Chen, H., Cerniglia, C. 2009. Metabolism of azo dyes by human skin microbiota. J. Med.Microbiol. le 3 sept. 2009. [paru en ligne avant impression].
Talaska, G. 2003. Aromatic amines and human urinary bladder cancer: exposure sources and epidemiology. J. Environ. Sci. Health C. Environ. Carcinog. Ecotoxicol. Rev. 21(1):2943.
Tincher, W.C. 1988. Dyes in the environment: dyeing wastes in landfill. Étude commanditée par le US Operating Committee de l'ETAD.
[TOPKAT] Toxicity Prediction Program [en ligne]. 2004. Version 6.2. San Diego (CA) : Accelrys Software Inc. Accès : http://www.accelrys.com/products/topkat/index.html
Toxtree. Version 1.60. 2009. Logiciel conçu par Ideaconsult Ltd, Bulgarie.
[US EPA] U.S. Environmental Protection Agency. 2002. PBT Profiler Methodology [en ligne]. Washington (DC) : US EPA, Office of Pollution Prevention and Toxics. [consulté en août 2008]. Accès : http://www.pbtprofiler.net/methodology.asp
[US EPA] United States Environmental Protection Agency. 2002b. TSCA New Chemicals Program (NCP) Chemical Categories: Aminobenzothiozole Azo Dyes. Accès : http://www.epa.gov/oppt/newchems/pubs/cat02.htm#Aminobenzothiazole%20Azo%20Dyes
[US EPA] U.S. Environmental Protection Agency. 2009. Inventory update reporting, past IUR data: Nonconfidential production volume information submitted by companies under the 1986, 1990, 1994, 1998, and 2002 Inventory Update Reporting Regulation: CAS RN 16586-42-8 & CAS RN 25176-89-0 [en ligne]. Washington (DC) : U.S. Environmental Protection Agency. [consulté le 25 mars 2009]. Accès : http://www.epa.gov/oppt/iur/tools/data/2002-vol.htm
[WATERNT] Water Solubility Program [modèle d'estimation]. 2002. Version 1.00. Washington (DC) : U.S. Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY) : Syracuse Research Corporation. Accès : www.epa.gov/oppt/exposure/pubs/episuite.htm
[WSKOWWIN] Water Solubility for Organic Compounds Program for Microsoft Windows [modèle d'estimation]. 2000. Version 1.41. Washington (DC) : U.S. Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY) : Syracuse Research Corporation. Accès : www.epa.gov/oppt/exposure/pubs/episuite.htm
Weber, E.J., Adams, R.L. 1995. Chemical and sediment-mediated reduction of the azo dye disperse blue 79. Environ. Sci. Technol. 29(5):1163-1170.
Weber, E.J., Colon, D., Baughman, G.L. 2001. Sediment-associated reactions of aromatic amines. 1. Elucidation of sorption mechanisms. Environ. Sci. Technol. 35(12):2470-2475.
Witt, K.L., Knapton, A., Wehr, C.M., Hook, G.J., Mirsalis, J., Shelby, M.D., MacGregor, J.T. 2000. Micronucleated erythrocyte frequency in peripheral blood of B6C3F(1) mice from short-term, prechronic, and chronic studies of the NTP carcinogenesis bioassay program. Environ. Mol. Mutagen. 36(3):163-94.
Xu, H., Heinze, T.M., Chen, S., Cerniglia, C.E., Chen, H. 2007. Anaerobic Metabolism of 1-Amino-2-Naphthol-Based Azo Dyes (Sudan Dyes) by Human Intestinal Microflora. Appl. Environ. Microbiol. 73:7759-62.
Yen, C.C., Perenich, T.A., Baughman, G.L. 1989. Fate of dyes in aquatic systems II. Solubility and octanol/water partition coefficients of disperse dyes. Environ. Toxicol. Chem.8(11):981-986.
Yen, C.C., Perenich, T.A., Baughman, G.L. 1991. Fate of commercial disperse dyes in sediments. Environ. Toxicol. Chem. 10:1009-1017.
Évaluation de données expérimentales selon la méthode de Kollig* : hydrosolubilité
| Élément | Pondération | Réponse | Note | |
|---|---|---|---|---|
| * Kollig, H.P., 1988. Criteria for evaluating the reliability of literature data on environmental process constants. Environ Toxicol Chem 17:287-311. ** Le code de fiabilité pour les études éco-toxicologiques de catégorisation de LIS a été utilisé. |
||||
| Référence : Sijm DTHM, Schuurmann G, De Vries PJ et Opperhuizen A., 1999. Aqueous solubility, octanol solubility, and octanol/water partition coefficient of nine hydrophobic dyes. Environ. Toxicol. Chem. 18(6):1109-1117. | ||||
| Substance d'essai : N° CAS : 68133-69-7 | ||||
| Paramètre : Solubilité dans l'eau | ||||
| Pourriez-vous répéter l'expérience avec des informations disponibles? | 5 | Oui | 4 | |
| Un objectif clair a-t-il été fixé? | 1 | Oui | 1 | |
| La qualité de l'eau est-elle caractérisée ou identifiée (distillée ou désionisée)? | 2 | Oui, distillée | 2 | |
| Les résultats sont-ils présentés en détail, clairement et de façon intelligible? | 3 | Oui | 2 | |
| Les données proviennent-elles d'une source principale et non pas d'un article référencé? | 3 | Source principale | 3 | |
| Le produit chimique a-t-il été testé à des concentrations inférieures à sa solubilité dans l'eau? | 5 | s.o. | s.o. | |
| Des particules étaient-elles absentes? | 2 | Supposé | 2 | |
| Un produit chimique de référence à constante connue a-t-il été testé? | 3 | Non | 0 | |
| D'autres processus de devenir ont-ils été envisagés? | 5 | s.o. | s.o. | |
| Un contrôle (à blanc) a-t-il eu lieu? | 3 | Non indiqué | 0 | |
| La température a-t-elle été maintenue constante? | 5 | Non indiqué mais supposé. La solubilité dans l'eau a été estimée à l'aide d'une colonne de générateur comme l'a fait Opperhuizen, 1986 | 5 | |
| L'expérience a-t-elle été réalisée à température ambiante (15 à 30 °C)? | 3 | Non indiqué mais supposé. | 3 | |
| La pureté du produit chimique testé atelle été signalée (> 98 %)? | 3 | Non, mais les produits chimiques ont été obtenus auprès de Bayer AG, puis recristallisés en dichlorométhane afin d'ôter tout additif avant utilisation | 3 | |
| L'identité du produit chimique a-t-elle été prouvée? | 3 | Oui, garantie par Bayer AG | 3 | |
| L'origine du produit chimique a-t-elle été signalée? | 1 | Oui, Bayer AG | 1 | |
| Note : | 29/37 = 78 % | |||
| Degré de fiabilité** | 2 Confiance satisfaisante | |||
| Commentaires | ||||
Évaluation de données expérimentales selon la méthode de Kollig* : coefficient de partage octanol-eau (Koe)
| Élément | Pondération | Réponse | Note | |
|---|---|---|---|---|
| * Kollig, H.P., 1988. Criteria for evaluating the reliability of literature data on environmental process constants. Environ. Toxicol. Chem.17:287-311. ** Le code de fiabilité pour les études éco-toxicologiques de catégorisation de LIS a été utilisé. |
||||
| Référence :Sijm DTHM, Schuurmann G, De Vries PJ et Opperhuizen A., 1999. Aqueous solubility, octanol solubility, and octanol/water partition coefficient of nine hydrophobic dyes. Environ. Toxicol. Chem. 18(6):1109-1117. | ||||
| Substance d'essai : N° CAS : 68133-69-7 | ||||
| Paramètre :Coefficient de partage octanol/eau) (Koe) | ||||
| Pourriez-vous répéter l'expérience avec des informations disponibles? | 5 | Oui | 5 | |
| Un objectif clair a-t-il été fixé? | 1 | Oui | 1 | |
| La qualité de l'eau est-elle caractérisée ou identifiée (distillée ou désionisée)? | 2 | Distillée | 2 | |
| Les résultats sont-ils présentés en détail, clairement et de façon intelligible? | 3 | Oui | 3 | |
| Les données proviennent-elles d'une source principale et non pas d'un article référencé? | 3 | Oui | 3 | |
| Le produit chimique a-t-il été testé à des concentrations inférieures à sa solubilité dans l'eau? | 5 | s.o. | s.o. | |
| Des particules étaient-elles absentes? | 2 | Oui | 2 | |
| Un produit chimique de référence à constante connue a-t-il été testé? | 3 | Non | 0 | |
| D'autres processus de devenir ont-ils été envisagés? | 5 | s.o. | s.o. | |
| Un contrôle (à blanc) a-t-il eu lieu? | 3 | Non indiqué | 0 | |
| La température a-t-elle été maintenue constante? | 5 | Oui, utilisé le protocole de la méthode de brassage lent de De Bruijn et al., 1989 | 5 | |
| L'expérience a-t-elle été réalisée à température ambiante (15 à 30 °C)? | 3 | Oui, 25 °C (protocole de la méthode de brassage lent de De Bruijn et al., 1989) | 3 | |
| La pureté du produit chimique testé a-t-elle été signalée (> 98 %)? | 3 | Non, mais les produits chimiques ont été obtenus auprès de Bayer AG, puis recristallisés en dichlorométhane afin d'ôter tout additif avant utilisation | 3 | |
| L'identité du produit chimique a-t-elle été prouvée? | 3 | Oui, garantie par Bayer AG | 3 | |
| L'origine du produit chimique a-t-elle été signalée? | 1 | Oui, Bayer AG | 1 | |
| Note : | 31/37 = 83 % | |||
| Degré de fiabilité** | 1 Confiance élevée | |||
| Commentaires | ||||
Formulaire pour sommaires de rigueur d'études : persistance dans l'eau, les sédiments et les sols
| Non | Élément | Pondération | Oui/Non | Veuillez préciser | |
|---|---|---|---|---|---|
| 1 | Référence : Foron Rubin RD-S Presskuchen trocken (Disperse Red 179) Biodégradabilité Intrinsèque – Évaluation de la biodégradabilité aérobie en milieu aqueux : Test ZahnWellens/EMPA. Rapport BMG no. 709/c-03, octobre 2003. Soumis à Environnement Canada dans l'étude de l'article 71 (Environnement Canada, 2009a) | ||||
| 2 | Identité de la substance : n° CAS | s.o. | n | Non précisé, mais il s'agit du Disperse Red 179 (16586428) | |
| 3 | Identité de la substance : nom(s) chimique(s) | s.o. | n | Foron Rubin RD-S | |
| 4 | Composition chimique de la substance | 2 | n | Seul le contenu carbone organique total est mentionné. Aucune mention de produits secondaires. | |
| 5 | Pureté chimique | 1 | n | Le produit commercial luimême, Foron Rubine RD-S, est testé. Il contient 34,3% en poids de 16586-42-8. | |
| Méthode | |||||
| 6 | Référence | 1 | O | Le test est celui de Zahn-Wellens/EMPA | |
| 7 | Méthode de l'OCDE, de l'UE, nationale ou autre méthode standard? | 3 | O | ||
| 8 | Justification de la/du méthode/protocole si une méthode non standard a été utilisée | 2 | Non applicable | ||
| 9 | BPL (bonne pratique de laboratoire) | 3 | n | Pas clairement indiqué | |
| Conception/conditions du test | |||||
| 10 | Type de test (hydrolyse, biodégradation, etc.) | s.o. | o | Biodégradation | |
| 11 | Type de conditions du test (aérobie ou anaérobie) | s.o. | O | Aérobie | |
| 12 | Milieu du test (eau, sédiment ou sol) | s.o. | O | Boues activées | |
| 13 | Durée du test | s.o. | O | 28 jours | |
| 14 | Contrôles négatifs ou positifs? | 1 | O | Contrôle positif au diéthylène glycol | |
| 15 | Nombre de répétitions (incluant les contrôles) | 1 | O | 2 répétitions pour le test, 2 répétitions pour l'essai à blanc et 1 pour le contrôle du test | |
| 16 | Concentrations mesurées rapportées? | 3 | O | La dégradation du matériel de test a été suivie par la détermination du carbone inorganique (CI) à intervalles réguliers. Les concentrations des produits chimiques à étudier n'ont pas été mesurées pendant le test. | |
| 17 | Méthode/instrument analytique | 1 | O | Le carbone inorganique (CI) a été déterminé de la même façon que le produit chimique organique défini sans laver les échantillons avant analyse. | |
| Détails sur la biodégradation | |||||
| 18 | Type de biodégradation (immédiate ou intrinsèque) signalée? | 2 | o | Biodégradation intrinsèque recherchée selon le test Zahn-Wellens | |
| 19 | Lorsque le type de biodégradation (immédiate ou intrinsèque) n'est pas signalé, une information indirecte permet-elle l'identification du type de biodégradation? | 1 | s.o. | ||
| 20 | Origine de l'inoculum | 1 | O | Il est mentionné que l'inoculum provient d'une usine de traitement des déchets. Cependant, le nom de l'usine n'est pas mentionné. | |
| 21 | Concentration de l'inoculum ou nombre de micro-organismes | 1 | O | 0,2 g/L de matière sèche | |
| 22 | L'inoculum a-t-il été préconditionné et la préadaptation rapportée? | 1 | N | ||
| 23 | L'inoculum a-t-il été préconditionné et la préadaptation a-t-elle été appropriée à la méthode utilisée? | s.o. | s.o. | ||
| 24 | Température | 1 | O | 22 ± 0,5°C, en chambre obscure | |
| 25 | Le pourcentage de dégradation du composé de référence a-t-il atteint les niveaux requis avant le 14e jour? | s.o. | O | Le diéthylèneglycol a été dégradé à 99% avant le 14ème jour. | |
| 26 | Sol : humidité du sol signalée? | 1 | s.o. | ||
| 27 | Sol et sédiments : contenu en matière organique du sol (MOS) de base signalé? | 1 | s.o. | ||
| 28 | Sol et sédiments : teneur en argile signalée? | 1 | s.o. | ||
| 29 | Sol et sédiments : CEC (capacité d'échange cationique) signalée? | 1 | s.o. | ||
| Détails sur l'hydrolyse | |||||
| 30 | Valeurs du pH signalées? | 1 | s.o. | ||
| 31 | Température | 1 | s.o. | ||
| 32 | Les concentrations appropriées de la substance ont-elles été utilisées? | s.o. | |||
| 33 | Si un solvant a été utilisé, l'a-t-il été de manière appropriée? | s.o. | |||
| Détails sur la photo-dégradation | |||||
| 34 | Température | 1 | s.o. | ||
| 35 | Source lumineuse | 1 | s.o. | ||
| 36 | Spectre lumineux (nm) | 1 | s.o. | ||
| 37 | Intensité relative en fonction de l'intensité lumineuse du soleil | 1 | s.o. | ||
| 38 | Spectre d'une substance | 1 | s.o. | ||
| 39 | Photolyse indirecte :Sensibilisateur (type) | 1 | s.o. | ||
| 40 | Photolyse indirecte :concentration du sensibilisateur | 1 | s.o. | ||
| Résultats | |||||
| 41 | Critère d'évaluation et valeur | s.o. | s.o. | Dégradation de 0%. L'élimination du composé à 99% est dûe à l'absorption ou à la sédimentation, non à la biodégradation. | |
| 42 | Produits de dégradation | s.o. | |||
| 43 | Note : ... % | 68,2 | |||
| 44 | Code de fiabilité d'Environnement Canada : | 2 | |||
| 45 | Catégorie de fiabilité (élevée, satisfaisante, basse) : | Confiance satisfaisante | |||
Formulaire pour sommaires de rigueur d'études : persistance dans l'eau, les sédiments et les sols
| Non | Élément | Pondération | Oui/Non | Veuillez préciser | |
|---|---|---|---|---|---|
| 1 | Référence : 13365Submission028, CI Disperse Red 153. Biodégradabilité Intrinsèque – Évaluation de la biodégradabilité aérobie en milieu aqueux : Rapport BMG n° 800/c-00 (n° CAS 25176-89-0), janvier 2000. Soumis à Environnement Canada dans l'étude de l'article 71 (Environnement Canada, 2009a) |
||||
| 2 | Identité de la substance : n° CAS | s.o. | n | N° CAS 25176-89-0 |
|
| 3 | Identité de la substance : nom(s) chimique(s) | s.o. | n | C.I. Disperse Red 153 | |
| 4 | Composition chimique de la substance | 2 | n | Seul le contenu carbone organique total est mentionné. Pas de mention de produits secondaires (c'està-dire que c'est à 100 % du 25176-89-0). | |
| 5 | Pureté chimique | 1 | n | Le produit testé est le C.I. Disperse Red 153 | |
| Méthode | |||||
| 6 | Référence | 1 | O | Le test est celui de Zahn-Wellens/EMPA | |
| 7 | Méthode de l'OCDE, de l'UE, nationale ou autre méthode standard? | 3 | O | ||
| 8 | Justification de la/du méthode/protocole si une méthode non standard a été utilisée | 2 | s.o. | ||
| 9 | BPL (bonne pratique de laboratoire) | 3 | n | Pas clairement indiqué | |
| Conception/conditions du test | |||||
| 10 | Type de test (hydrolyse, biodégradation, etc.) | s.o. | o | Biodégradation | |
| 11 | Type de conditions du test (aérobie ou anaérobie) | s.o. | O | Aérobie | |
| 12 | Milieu du test (eau, sédiment ou sol) | s.o. | O | Boues activées | |
| 13 | Durée du test | s.o. | O | 28 jours | |
| 14 | Contrôles négatifs ou positifs? | 1 | O | Contrôle positif au diéthylène glycol | |
| 15 | Nombre de répétitions (incluant les contrôles) | 1 | O | 2 répétitions pour le test, 2 répétitions pour l'essai à blanc et 1 pour le contrôle du test | |
| 16 | Concentrations mesurées rapportées? | 3 | O | La dégradation du matériel de test a été suivie par la détermination du carbone organique dissous (DOC) à intervalles réguliers. Les concentrations des produits chimiques à étudier n'ont pas été mesurées pendant le test. | |
| 17 | Méthode/instrument analytique | 1 | O | Le produit chimique organique défini a été déterminé en double avec un analyseur Shimadzu 5050 de TOC, par le mode NPOC. Le carbone inorganique (CI) a été déterminé de la même façon que le produit chimique organique défini sans laver les échantillons avant analyse. | |
| Détails sur la biodégradation | |||||
| 18 | Type de biodégradation (immédiate ou intrinsèque) signalée? | 2 | O | Biodégradation intrinsèque recherchée selon le test ZahnWellens | |
| 19 | Lorsque le type de biodégradation (immédiate ou intrinsèque) n'est pas signalé, une information indirecte permet-elle l'identification du type de biodégradation? | 1 | s.o. | ||
| 20 | Origine de l'inoculum | 1 | O | Il est mentionné que l'inoculum provient d'une usine de traitement des déchets. Cependant, le nom de l'usine n'est pas mentionné. | |
| 21 | Concentration de l'inoculum ou nombre de microorganismes | 1 | O | 0,2 g/L de matière sèche | |
| 22 | L'inoculum a-t-il été préconditionné et la préadaptation rapportée? | 1 | N | ||
| 23 | L'inoculum a-t-il été préconditionné et la préadaptation a-t-elle été appropriée à la méthode utilisée? | s.o. | s.o. | ||
| 24 | Température | 1 | O | 22 ± 0,5 °C, en chambre obscure | |
| 25 | Le pourcentage de dégradation du composé de référence a-t-il atteint les niveaux requis avant le 14e jour? | s.o. | O | Le composé de référence a atteint 87 % de dégradation après 14 jours. | |
| 26 | Sol : humidité du sol signalée? | 1 | s.o. | ||
| 27 | Sol et sédiments : contenu en matière organique du sol (MOS) de base signalé? | 1 | s.o. | ||
| 28 | Sol et sédiments : teneur en argile signalée? | 1 | s.o. | ||
| 29 | Sol et sédiments : CEC (capacité d'échange cationique) signalée? | 1 | s.o. | ||
| Détails sur l'hydrolyse | |||||
| 30 | Valeurs du pH signalées? | 1 | s.o. | ||
| 31 | Température | 1 | s.o. | ||
| 32 | Les concentrations appropriées de la substance ont-elles été utilisées? | s.o. | |||
| 33 | Si un solvant a été utilisé, l'a-t-il été de manière appropriée? | s.o. | |||
| Détails sur la photo-dégradation | |||||
| 34 | Température | 1 | s.o. | ||
| 35 | Source lumineuse | 1 | s.o. | ||
| 36 | Spectre lumineux (nm) | 1 | s.o. | ||
| 37 | Intensité relative en fonction de l'intensité lumineuse du soleil | 1 | s.o. | ||
| 38 | Spectre d'une substance | 1 | s.o. | ||
| 39 | Photolyse indirecte :sensibilisateur (type) | 1 | s.o. | ||
| 40 | Photolyse indirecte :concentration de sensibilisateur | 1 | s.o. | ||
| Résultats | |||||
| 41 | Critère d'évaluation et valeur | s.o. | s.o. | Non dégradé | |
| 42 | Produits de dégradation | s.o. | |||
| 43 | Note : ... % | 68,2 | |||
| 44 | Code de fiabilité d'Environnement Canada : | 2 | |||
| 45 | Catégorie de fiabilité (élevée, satisfaisante, basse) : | Confiance satisfaisante | |||
Formulaire pour sommaires de rigueur d'études : toxicité intrinsèque pour les organismes aquatiques
| Non | Élément | Pondération | Oui/Non | Veuillez préciser | |
|---|---|---|---|---|---|
| 1 | Référence : 13365 Submission 025 Foron Rubin RD-S Presskuchen trocken (Disperse Red 179) 96-hr Acute Toxicity to Poecilia reticulata (Guppy). Rapport BMG n° 709/b-03, octobre 2003. Soumis à Environment Canada dans l'étude de l'article 71 (Environnement Canada, 2009a) | ||||
| 2 | Identité de la substance : n° CAS | s.o. | O | Le produit chimique testé est le Foron Rubin RD-S Presskuchen trocken | |
| 3 | Identité de la substance : nom(s) chimique(s) | s.o. | O | Foron Rubin RD-S Presskuchen trocken (Disperse Red 179) | |
| 4 | Composition chimique de la substance | 2 | N | Composition du produit non présentée | |
| 5 | Pureté chimique | 1 | N | Indiquée par l'article 71, pas l'étude de toxicité. Le test indique un ingrédient à 100 % actif, ce qui est impossible selon l'article 71. | |
| 6 | Persistance/stabilité de la substance d'essai en solution aquatique signalée? | 1 | N | Pas d'information | |
| Méthode | |||||
| 7 | Référence | 1 | O | Le test a été réalisé selon le guide de procédure 203 de l'OCDE et la directive EEC 92/69/EEC | |
| 8 | Méthode de l'OCDE, de l'UE, nationale ou autre méthode standard? | 3 | O | OCDE et Communauté économique européenne | |
| 9 | Justification de la/du méthode/protocole si une méthode non standard a été utilisée | 2 | Non applicable | ||
| 10 | BPL (bonne pratique de laboratoire) | 3 | N | Non précisé | |
| Organisme d'essai | |||||
| 11 | Identité de l'organisme : nom | s.o. | O | Poecilia reticulata (guppy) | |
| 12 | Nom latin ou noms latin et commun signalés? | 1 | O | Poecilia reticulata (guppy) | |
| 13 | Âge/stade du cycle biologique de l'organisme d'essai | 1 | N | Le stade du cycle biologique des organismes d'essai n'est pas précisé, mais on pense qu'il existe des divergences dues aux variations de longueur et surtout de poids. | |
| 14 | Longueur et/ou poids | 1 | O | Ceci est un problème, car de grandes variations peuvent être observées entre les poissons. | |
| 15 | Sexe | 1 | N | ||
| 16 | Nombre d'organismes par répétition | 1 | O | Minimum autorisé par protocole d'essai : 7 poissons | |
| 17 | Taux de chargement de l'organisme | 1 | O | Les taux de chargement de l'organisme sont < 1 g de poisson/L. Ils sont de 0,533 pour 100 mg/L, de 0,563 pour 10 mg/L et de 0,538 pour 1 mg/L. | |
| 18 | Type de nourriture et périodes d'alimentation pendant la période d'acclimatation | 1 | O | ||
| Conception/conditions du test | |||||
| 19 | Type de test (aigu ou chronique) | s.o. | O | Aigu | |
| 20 | Type d'expérience (laboratoire ou terrain) | s.o. | O | Laboratoire | |
| 21 | Voies d'exposition (nourriture, eau, les deux) | s.o. | O | Eau | |
| 22 | Durée d'exposition | s.o. | O | 96 heures | |
| 23 | Contrôles négatifs ou positifs (veuillez préciser) | 1 | O | Positif | |
| 24 | Nombre de répétitions (incluant les contrôles) | 1 | O | Un total de 4 répétitions (1 pour chaque concentration et 1 pour le contrôle) | |
| 25 | Concentrations nominales rapportées? | 1 | O | 4 incluant le contrôle | |
| 26 | Concentrations mesurées rapportées? | 3 | N | En fait, la toxicité signalée dépasse la solubilité du composé | |
| 27 | Type de nourriture et périodes d'alimentation pendant les tests à long terme | 1 | Non applicable | ||
| 28 | Les concentrations ont-elles été mesurées périodiquement (particulièrement lors du test chronique)? | 1 | N | ||
| 29 | Les conditions du milieu d'exposition correspondaient-elles au produit chimique particulier signalé? (par exemple, pour la toxicité du métal : pH, DOC/TOC, dureté de l'eau, température) | 3 | O | ||
| 30 | Photopériode et intensité lumineuse | 1 | O | Photopériode de 16, aucune idée de l'intensité réelle | |
| 31 | Préparation de la solution de stock et d'essai | 1 | O | Étant donné la solubilité limitée dans l'eau, les concentrations d'essai individuelles ont été préparées en ajoutant les quantités respectives d'une solution de stock acétonique aux récipients en verre vides. Après évaporation complète du solvant, l'eau du robinet a été ajoutée.Des détails sur les solutions du stock sont aussi disponibles. | |
| 32 | Un agent solubilisant/émulsifiant a-t-il été utilisé si le produit chimique était faiblement soluble ou instable? | 1 | O | Étant donné la solubilité limitée dans l'eau, les concentrations d'essai individuelles ont été préparées en ajoutant les quantités respectives d'une solution de stock acétonique aux récipients en verre vides. Après évaporation complète du solvant, l'eau du robinet a été ajoutée. | |
| 33 | Si un solubilisant/émulsifiant a été utilisé, sa concentration a-t-elle été signalée? | 1 | N | Non, mais l'acétone s'est évaporé. | |
| 34 | Si un solubilisant/émulsifiant a été utilisé, son écotoxicité a-t-elle été signalée? | 1 | N | L'acétone s'est évaporée et était donc absente. | |
| 35 | Intervalles de contrôle analytique | 1 | N | ||
| 36 | Méthodes statistiques utilisées | 1 | N | ||
| Informations relatives à la qualité des données | |||||
| 37 | Le critère d'évaluation a-t-il été directement causé par la toxicité du produit chimique et non par l'état de santé de l'organisme (par exemple, lorsque la mortalité lors du contrôle est > 10 %) ou des effets physiques (par exemple, « effet d'ombrage »)? | s.o. | |||
| 38 | L'organisme d'essai correspondait-il à l'environnement canadien? | 3 | N | ||
| 39 | Les conditions du test (pH, température, DO, etc.) étaient-elles adaptées à l'organisme d'essai? | 1 | O | Le pH était un peu élevé (8,1 à 8,5); les concentrations en oxygène étaient normales (6,9 à 7,9 mg/L). | |
| 40 | Le type de système et sa conception (statique, semi-statique, flux continu, scellé ou ouvert, etc.) correspondent-ils aux propriétés de la substance et à la nature/aux habitudes de l'organisme? | 2 | O | ||
| 41 | Le pH de l'eau du test se situait-il dans la plage habituelle pour l'environnement canadien (6 à 9)? | 1 | O | ||
| 42 | La température de l'eau du test se situait-elle dans la plage habituelle pour l'environnement canadien (5 à 27 °C)? | 1 | O | ||
| 43 | La valeur de la toxicité était-elle inférieure à la solubilité dans l'eau du produit chimique? | 3 | N | ||
| Résultats | |||||
| 44 | Valeurs de la toxicité (préciser le critère d'évaluation et la valeur) | s.o. | s.o. | ||
| 45 | Autres critères d'évaluation signalés : par exemple, FBC/FBA, CMEO/CSEO (préciser)? | s.o. | O | CSEO > 10 mg/L basé sur une concentration nominale | |
| 46 | Autres effets indésirables (par exemple, cancérogénicité, mutagénicité) signalés? | s.o. | O | Perte de coordination, hypoactivité et nage sur le dos ont aussi été signalées. | |
| 47 | Note : ... % | 50,0 | |||
| 48 | Code de fiabilité d'Environnement Canada : | 3 | |||
| 49 | Catégorie de fiabilité (élevée, satisfaisante, basse) : | Confiance basse | |||
Formulaire pour sommaires de rigueur d'études : toxicité intrinsèque pour les organismes aquatiques
| Non | Élément | Poids | Oui/Non | Veuillez préciser |
|---|---|---|---|---|
| 1 | Référence : 13365 Submission 026 C.I. Disperse Red 153. 96-hour Acute Toxicity to Poecilia reticulata (Guppy) Limit Test (100 mg/L). Rapport BMG n° 800/a-00 soumis à Environnement Canada dans l'étude de l'article 71 (Environnement Canada, 2009a) | |||
| 2 | Identité de la substance : n° CAS | s.o. | 25176-89-0 | |
| 3 | Identité de la substance : nom(s) chimique(s) | s.o. | C.I. Disperse Red 153 | |
| 4 | Composition chimique de la substance | 2 | N | La substance est identifiée comme étant le C.I. Disperse Red 153, Lot n° 99L094 Contrôle 100811B, avec un ingrédient actif à 100 %. Peu d'informations. |
| 5 | Pureté chimique | 1 | N | Le rapport d'essai mentionne une pureté de 100%, mais il reste à déterminer si cela concerne la pureté à 100 % du produit commercial ou bien du n° CAS. |
| 6 | Persistance/stabilité de la substance d'essai en solution aquatique signalée? | 1 | N | Pas d'information |
| Méthode | ||||
| 7 | Référence | 1 | O | Le test a été réalisé selon le guide de procédure 203 de l'OCDE et la directive EEC 92/69/EEC |
| 8 | Méthode de l'OCDE, de l'UE, nationale ou autre méthode standard? | 3 | O | OCDE et Communauté économique européenne |
| 9 | Justification de la/du méthode/protocole si une méthode non standard a été utilisée | 2 | Non applicable | |
| 10 | BPL (bonne pratique de laboratoire) | 3 | N | Non précisé |
| Organisme d'essai | ||||
| 11 | Identité de l'organisme : nom | s.o. | O | Poecilia reticulata (guppy) |
| 12 | Nom latin ou noms latin et commun signalés? | 1 | O | Poecilia reticulata (guppy) |
| 13 | Âge/stade du cycle biologique de l'organisme d'essai | 1 | N | Le stade du cycle biologique des organismes d'essai n'est pas précisé, mais on pense qu'il existe des divergences dues aux variations de longueur et surtout de poids. |
| 14 | Longueur et/ou poids | 1 | O | Ceci est un problème, car de grandes variations peuvent être observées entre les poissons. |
| 15 | Sexe | 1 | N | |
| 16 | Nombre d'organismes par répétition | 1 | O | Minimum autorisé par protocole d'essai : 7 poissons |
| 17 | Taux de chargement de l'organisme | 1 | O | Les taux de chargement de l'organisme sont < 1 gramme de poisson/L. De 0,584 g pour 100 mg/L. |
| 18 | Type de nourriture et périodes d'alimentation pendant la période d'acclimatation | 1 | O | |
| Conception/conditions du test | ||||
| 19 | Type de test (aigu ou chronique) | s.o. | O | Aigu |
| 20 | Type d'expérience (laboratoire ou terrain) | s.o. | O | Laboratoire |
| 21 | Voies d'exposition (nourriture, eau, les deux) | s.o. | O | Eau |
| 22 | Durée d'exposition | s.o. | O | 96 heures |
| 23 | Contrôles négatifs ou positifs (veuillez préciser) | 1 | O | Positif |
| 24 | Nombre de répétitions (incluant les contrôles) | 1 | O | Deux répétitions (100 mg/L et contrôle) |
| 25 | Concentrations nominales rapportées? | 1 | O | Une seule concentration nominale |
| 26 | Concentrations mesurées rapportées? | 3 | N | |
| 27 | Type de nourriture et périodes d'alimentation pendant les tests à long terme | 1 | Non applicable | |
| 28 | Les concentrations ont-elles été mesurées périodiquement (particulièrement lors du test chronique)? | 1 | N | |
| 29 | Les conditions du milieu d'exposition correspondaient-elles au produit chimique particulier signalé? (par exemple, pour la toxicité du métal : pH, DOC/TOC, dureté de l'eau, température) | 3 | O | |
| 30 | Photopériode et intensité lumineuse | 1 | O | Photopériode de 16, aucune idée de l'intensité réelle. |
| 31 | Préparation de la solution de stock et d'essai | 1 | O | Étant donné la solubilité limitée dans l'eau, les concentrations d'essai individuelles ont été préparées en ajoutant les quantités respectives d'une solution de stock acétonique aux récipients en verre vides. Après évaporation complète du solvant, l'eau du robinet a été ajoutée.Des détails sur les solutions du stock sont aussi disponibles. |
| 32 | Un agent solubilisant/émulsifiant a-t-il été utilisé si le produit chimique était faiblement soluble ou instable? | 1 | O | Étant donné la solubilité limitée dans l'eau, les concentrations d'essai individuelles ont été préparées en ajoutant les quantités respectives d'une solution de stock acétonique aux récipients en verre vides. Après évaporation complète du solvant, l'eau du robinet a été ajoutée. |
| 33 | Si un solubilisant/émulsifiant a été utilisé, sa concentration a-t-elle été signalée? | 1 | N | Non, mais l'acétone s'est évaporé. |
| 34 | Si un solubilisant/émulsifiant a été utilisé, son écotoxicité a-t-elle été signalée? | 1 | N | L'acétone s'est évaporée et était donc absente. |
| 35 | Intervalles de contrôle analytique | 1 | N | |
| 36 | Méthodes statistiques utilisées | 1 | N | |
| Informations relatives à la qualité des données | ||||
| 37 | Le critère d'évaluation a-t-il été directement causé par la toxicité du produit chimique et non par l'état de santé de l'organisme (par exemple, lorsque la mortalité lors du contrôle est > 10 %) ou des effets physiques (par exemple, « effet d'ombrage »)? | s.o. | ||
| 38 | L'organisme d'essai correspondait-il à l'environnement canadien? | 3 | N | |
| 39 | Les conditions du test (pH, température, DO, etc.) étaient-elles adaptées à l'organisme d'essai? | 1 | O | Le pH était un peu élevé (8,6 à 8,9); la concentration en oxygène était normales (7,5 à 7,9 mg/L). |
| 40 | Le type de système et sa conception (statique, semi-statique, flux continu, scellé ou ouvert, etc.) correspondent-ils aux propriétés de la substance et à la nature/aux habitudes de l'organisme? | 2 | O | |
| 41 | Le pH de l'eau du test se situait-il dans la plage habituelle pour l'environnement canadien (6 à 9)? | 1 | O | |
| 42 | La température de l'eau du test se situait-elle dans la plage habituelle pour l'environnement canadien (5 à 27 °C)? | 1 | O | |
| 43 | La valeur de la toxicité était-elle inférieure à la solubilité dans l'eau du produit chimique? | 3 | N | |
| Résultats | ||||
| 44 | Valeurs de la toxicité (préciser le critère d'évaluation et la valeur) | s.o. | s.o. | |
| 45 | Autres critères d'évaluation signalés : par exemple, FBC/FBA, CMEO/CSEO (préciser)? | s.o. | O | CSEO > 100 mg/L basé sur des concentrations nominales |
| 46 | Autres effets indésirables (par exemple, cancérogénicité, mutagénicité) signalés? | s.o. | O | Perte de coordination, hypoactivité et nage sur le dos ont aussi été recherchées. |
| 47 | Note : ... % | 50,0 | ||
| 48 | Code de fiabilité d'Environnement Canada : | 3 | ||
| 49 | Catégorie de fiabilité (élevée, satisfaisante, basse) : | Confiance basse | ||
Formulaire pour sommaires de rigueur d'études : organismes aquatiques B
| Non | Élément | Pondération | Oui/Non | Veuillez préciser | ||
|---|---|---|---|---|---|---|
| 1 | Référence : Shen G, and Hu S. 2008. Bioconcentration Test of C.I. Disperse Orange 30 in Fish. Préparé par Environmental Testing Laboratory, Académie des Sciences de l'Environnement de Shanghai, Shanghai, Chine, pour Dystar au nom de l'Association écologique et toxicologique des fabricants de colorants et de pigments organiques (ETAD), Bâle, Suisse. Rapport n° S-070-2007. Soumis à Environnement Canada en Avril 2008. Soumission au défi ID n° 8351. | |||||
| 2 | Identité de la substance : n° CAS | s.o. | O | 5261-31-4 | ||
| 3 | Identité de la substance : nom(s) chimique(s) | s.o. | O | Propanenitrile, 3-[[2-(acétyloxy)éthyle][4-[(2,6-dichloro-4-nitrophényl)azo]phényl]amino]- | ||
| 4 | Composition chimique de la substance | 2 | N | |||
| 5 | Pureté chimique | 1 | N | |||
| 6 | Persistance/stabilité de la substance d'essai en solution aquatique signalée? | 1 | N | |||
| 7 | Si le matériau d'essai est radio-marqué, la/les position(s) précise(s) de l'/des atome(s) marqué(s) et le pourcentage de radioactivité associé aux impuretés ont-ils été signalés? | 2 | s.o. | |||
| Méthode | ||||||
| 8 | Référence | 1 | O | Guide de l'OCDE pour le test des produits chimiques n° 305B-1996 | ||
| 9 | Méthode de l'OCDE, de l'UE, nationale ou autre méthode standard? | 3 | O | OCDE | ||
| 10 | Justification de la/du méthode/protocole si une méthode non standard a été utilisée | 2 | ||||
| 11 | BPL (bonne pratique de laboratoire) | 3 | N | |||
| Organisme d'essai | ||||||
| 12 | Identité de l'organisme : nom | s.o. | O | Poisson zèbre, Brachydanio rerio | ||
| 13 | Nom latin ou noms latin et commun signalés? | 1 | O | Les deux | ||
| 14 | Âge/stade du cycle biologique de l'organisme d'essai | 1 | N | |||
| 15 | Longueur et/ou poids | 1 | O | Longueur moyenne du corps 3,91 ± 0,18 cm et poids moyen du corps 0,32 ± 0,06 g | ||
| 16 | Sexe | 1 | N | |||
| 17 | Nombre d'organismes par répétition | 1 | O | 7 | ||
| 18 | Taux de chargement de l'organisme | 1 | O | 20 mg/L | ||
| 19 | Type de nourriture et périodes d'alimentation pendant la période d'acclimatation | 1 | O | Mise au régime avec un poisson du commerce jusqu'à un jour avant le début du test | ||
| Conception/conditions du test | ||||||
| 20 | Type d'expérience (laboratoire ou terrain) | s.o. | O | Laboratoire | ||
| 21 | Voies d'exposition (nourriture, eau, les deux) | s.o. | O | Eau | ||
| 22 | Durée d'exposition | s.o. | O | 28 jours | ||
| 23 | Nombre de répétitions (incluant les contrôles) | 1 | O | |||
| 24 | Concentrations | 1 | O | 20 mg/L | ||
| 25 | Type/composition de la nourriture et périodes d'alimentation pendant le test | 1 | O | Les poissons étaient nourris deux heures avant le renouvellement de l'eau. | ||
| 26 | Si le ratio FBC/FBA dérivait de la concentration chimique dans l'organisme et dans l'eau, la durée de l'expérience était-elle égale à ou supérieure au temps nécessaire pour que les concentrations chimiques atteignent un état stable? | 3 | O | 28 jours | ||
| 27 | Si le ratio FBC/FBA provenait de la concentration chimique dans l'organisme et dans l'eau, les concentrations mesurées dans l'eau et dans l'organisme ont-elles été signalées? | 3 | O | |||
| 28 | Les concentrations dans l'eau du test ont-elles été mesurées périodiquement? | 1 | O | Sur trois jours distincts | ||
| 29 | Les conditions du milieu d'exposition correspondaient-elles au produit chimique particulier signalé? (par exemple, pour la toxicité du métal : pH, DOC/TOC, dureté de l'eau, température) | 3 | O | Oui, tous les deux jours | ||
| 30 | Photopériode et intensité lumineuse | 1 | O | 12:12 | ||
| 31 | Préparation de la solution de stock et d'essai | 1 | O | |||
| 32 | Intervalles de contrôle analytique | 1 | O | Tous les deux jours pour l'oxygène dissous, le pH et la température | ||
| 33 | Méthodes statistiques utilisées | 1 | O | |||
| 34 | Le solubilisant/émulsifiant a-t-il été utilisé si le produit chimique était faiblement soluble ou instable? | s.o. | N | |||
| Informations relatives à la qualité des données | ||||||
| 35 | L'organisme d'essai correspondait-il à l'environnement canadien? | 3 | O | |||
| 36 | Les conditions du test (pH, température, DO, etc.) étaient-elles adaptées à l'organisme d'essai? | 1 | O | |||
| 37 | Le type de système et sa conception (statique, semi-statique, flux continu, scellé ou ouvert, etc.) correspondent-ils aux propriétés de la substance et à la nature/aux habitudes de l'organisme? | 2 | O | Semi-statique | ||
| 38 | Le pH de l'eau du test se situait-il dans la plage habituelle pour l'environnement canadien (6 à 9)? | 1 | O | 7,22–7,84 | ||
| 39 | La température de l'eau du test se situaitelle dans la plage habituelle pour l'environnement canadien (5 à 27 °C)? | 1 | O | 22–23 | ||
| 40 | Le contenu lipidique (ou FBA/FBC lipidiquement normalisé) a-t-il été signalé? | 2 | O | |||
| 41 | Les concentrations mesurées d'un produit chimique dans l'eau du test étaient-elles inférieures à la solubilité dans l'eau du produit chimique? | 3 | N | |||
| 42 | Si une substance d'essai radio-marquée a été utilisée, la détermination du FBC étaitelle basée sur le composé d'origine (c'est-à-dire, pas sur la totalité des résidus radio-marqués)? | 3 | s.o. | |||
| Résultats | ||||||
| 43 | Critères d'évaluation (FBA, FBC) et valeurs | s.o. | s.o. | FBC | ||
| 44 | FBA et FBC définis comme : 1) le ratio de concentration chimique dans l'organisme et dans l'eau, ou 2) le ratio de l'assimilation chimique et les constantes du taux d'élimination | s.o. | s.o. | 1 | ||
| 45 | Le FBA/FBC était-il issu d'un 1) échantillon de tissu ou 2) organisme entier? | s.o. | s.o. | 2 | ||
| 46 | Le FBA/FBC 1) moyen ou 2) maximum at-il été utilisé? | s.o. | s.o. | 1 | ||
| 47 | Note : ... % | 75,0 | ||||
| 48 | Code de fiabilité d'Environnement Canada : | 2 | ||||
| 49 | Catégorie de fiabilité (élevée, satisfaisante, basse) : | Confiance satisfaisante | ||||
| 50 | Commentaires | La présente procédure est basée sur des conditions semi-statiques (renouvellement des solutions du test tous les deux jours). Par conséquent, les produits chimiques d'essai ayant une très faible solubilité dans l'eau peuvent aussi être caractérisés par leur potentiel de bioconcentration, sans ajouter de solvants ou d'autres substances auxiliaires qui pourraient affecter les résultats. | ||||
Formulaire pour sommaire de rigueur d'étude : Ti aquatique
| Non | Élément | Pondération | Oui/Non | Veuillez préciser | |||
|---|---|---|---|---|---|---|---|
| 1 | Référence : Sandoz. 1975. Toxicité aiguë du poisson (truite arc-en-ciel) 48 heures | ||||||
| 2 | Identité de la substance : noCAS | s.o. | O | 5261-31-4 | |||
| 3 | Identité de la substance : nom(s) chimique(s) | s.o. | O | ||||
| 4 | Composition chimique de la substance | 2 | N | ||||
| 5 | Pureté chimique | 1 | N | ||||
| 6 | Persistance/stabilité de la substance d'essai en solution aquatique signalée? | 1 | N | ||||
| Méthode | |||||||
| 7 | Référence | 1 | O | ||||
| 8 | Méthode de l'OCDE, de l'UE, nationale ou autre méthode standard? | 3 | O | ||||
| 9 | Justification de la/du méthode/protocole si une méthode non standard a été utilisée | 2 | |||||
| 10 | BPL (bonne pratique de laboratoire) | 3 | O | ||||
| Organisme d'essai | |||||||
| 11 | Identité de l'organisme : nom | s.o. | O | Truite arc-en-ciel | |||
| 12 | Nom latin ou noms latin et commun signalés? | 1 | O | ||||
| 13 | Âge/stade du cycle biologique de l'organisme d'essai | 1 | N | ||||
| 14 | Longueur et/ou poids | 1 | O | ||||
| 15 | Sexe | 1 | N | ||||
| 16 | Nombre d'organismes par répétition | 1 | N | ||||
| 17 | Taux de chargement de l'organisme | 1 | N | ||||
| 18 | Type de nourriture et périodes d'alimentation pendant la période d'acclimatation | 1 | N | ||||
| Conception/conditions du test | |||||||
| 19 | Type de test (aigu ou chronique) | s.o. | O | Aigu | |||
| 20 | Type d'expérience (laboratoire ou terrain) | s.o. | O | Laboratoire | |||
| 21 | Voies d'exposition (nourriture, eau, les deux) | s.o. | |||||
| 22 | Durée d'exposition | s.o. | O | 48 | |||
| 23 | Contrôles négatifs ou positifs (veuillez préciser) | 1 | N | ||||
| 24 | Nombre de répétitions (incluant les contrôles) | 1 | N | ||||
| 25 | Concentrations nominales rapportées? | 1 | N | ||||
| 26 | Concentrations mesurées rapportées? | 3 | N | ||||
| 27 | Type de nourriture et périodes d'alimentation pendant les tests à long terme | 1 | N | ||||
| 28 | Les concentrations ont-elles été mesurées périodiquement (particulièrement lors du test chronique)? | 1 | N | ||||
| 29 | Les conditions du milieu d'exposition correspondaient-elles au produit chimique particulier signalé? (par exemple, pour la toxicité du métal : pH, DOC/TOC, dureté de l'eau, température) | 3 | N | ||||
| 30 | Photopériode et intensité lumineuse | 1 | N | ||||
| 31 | Préparation de la solution de stock et d'essai | 1 | N | ||||
| 32 | Un agent solubilisant/émulsifiant a-t-il été utilisé si le produit chimique était faiblement soluble ou instable? | 1 | N | ||||
| 33 | Si un solubilisant/émulsifiant a été utilisé, sa concentration a-t-elle été signalée? | 1 | |||||
| 34 | Si un solubilisant/émulsifiant a été utilisé, son écotoxicité a-t-elle été signalée? | 1 | |||||
| 35 | Intervalles de contrôle analytique | 1 | N | ||||
| 36 | Méthodes statistiques utilisées | 1 | N | ||||
| Informations relatives à la qualité des données | |||||||
| 37 | Le critère d'évaluation a-t-il été directement causé par la toxicité du produit chimique et non par l'état de santé de l'organisme (par exemple, lorsque la mortalité lors du contrôle est > 10 %) ou des effets physiques (par exemple, « effet d'ombrage »)? | s.o. | |||||
| 38 | L'organisme d'essai correspondait-il à l'environnement canadien? | 3 | O | ||||
| 39 | Les conditions du test (pH, température, DO, etc.) étaient-elles adaptées à l'organisme d'essai? | 1 | N | ||||
| 40 | Le type de système et sa conception (statique, semistatique, flux continu, scellé ou ouvert, etc.) correspondent-ils aux propriétés de la substance et à la nature/aux habitudes de l'organisme? | 2 | N | ||||
| 41 | Le pH de l'eau du test se situait-il dans la plage habituelle pour l'environnement canadien (6 à 9)? | 1 | N | ||||
| 42 | La température de l'eau du test se situait-elle dans la plage habituelle pour l'environnement canadien (5 à 27 °C)? | 1 | O | ||||
| 43 | La valeur de la toxicité était-elle inférieure à la solubilité dans l'eau du produit chimique? | 3 | N | ||||
| Résultats | |||||||
| 44 | Valeurs de la toxicité (préciser le critère d'évaluation et la valeur) | s.o. | s.o. | CL50 à 48 heures > 700 mg/L | |||
| 45 | Autres critères d'évaluation signalés : par exemple, FBC/FBA, CMEO/CSEO (préciser)? | s.o. | |||||
| 46 | Autres effets indésirables (par exemple, cancérogénicité, mutagénicité) signalés? | s.o. | |||||
| 47 | Note : ... % | 28,9 | |||||
| 48 | Code de fiabilité d'Environnement Canada : | 4 | |||||
| 49 | Catégorie de fiabilité (élevée, satisfaisante, basse) : | Non satisfaisante | |||||
| 50 | Commentaires | ||||||
Formulaire pour sommaire de rigueur d'étude : Ti aquatique
| Non | Élément | Pondération | Oui/Non | Veuillez préciser | |
|---|---|---|---|---|---|
| 1 | Référence : Safepharm Laboratories Ltd. 1990. Acute toxicity to rainbow trout. Numéro de projet 47/781 | ||||
| 2 | Identité de la substance : n° CAS | s.o. | O | 5261-31-4 | |
| 3 | Identité de la substance : nom(s) chimique(s) | s.o. | O | ||
| 4 | Composition chimique de la substance | 2 | N | ||
| 5 | Pureté chimique | 1 | N | ||
| 6 | Persistance/stabilité de la substance d'essai en solution aquatique signalée? | 1 | N | ||
| Méthode | |||||
| 7 | Référence | 1 | N | ||
| 8 | Méthode de l'OCDE, de l'UE, nationale ou autre méthode standard? | 3 | N | ||
| 9 | Justification de la/du méthode/protocole si une méthode non standard a été utilisée | 2 | N | ||
| 10 | BPL (bonne pratique de laboratoire) | 3 | s.o. | ||
| Organisme d'essai | |||||
| 11 | Identité de l'organisme : nom | s.o. | Truite arc-en-ciel | ||
| 12 | Nom latin ou noms latin et commun signalés? | 1 | O | ||
| 13 | Âge/stade du cycle biologique de l'organisme d'essai | 1 | O | ||
| 14 | Longueur et/ou poids | 1 | O | ||
| 15 | Sexe | 1 | s.o. | ||
| 16 | Nombre d'organismes par répétition | 1 | O | De trois à dix | |
| 17 | Taux de chargement de l'organisme | 1 | O | 0,70 g poids du corps/L | |
| 18 | Type de nourriture et périodes d'alimentation pendant la période d'acclimatation | 1 | s.o. depuis le test aigu | ||
| Conception/conditions du test | |||||
| 19 | Type de test (aigu ou chronique) | s.o. | Aigu | ||
| 20 | Type d'expérience (laboratoire ou terrain) | s.o. | Laboratoire | ||
| 21 | Voies d'exposition (nourriture, eau, les deux) | s.o. | Eau | ||
| 22 | Durée d'exposition | s.o. | 96 heures | ||
| 23 | Contrôles négatifs ou positifs (veuillez préciser) | 1 | O | Positif | |
| 24 | Nombre de répétitions (incluant les contrôles) | 1 | O | Deux pour l'étude définitive | |
| 25 | Concentrations nominales rapportées? | 1 | O | 3 | |
| 26 | Concentrations mesurées rapportées? | 3 | N | ||
| 27 | Type de nourriture et périodes d'alimentation pendant les tests à long terme | 1 | s.o. | ||
| 28 | Les concentrations ont-elles été mesurées périodiquement (particulièrement lors du test chronique)? | 1 | N | ||
| 29 | Les conditions du milieu d'exposition correspondaient-elles au produit chimique particulier signalé? (par exemple, pour la toxicité du métal : pH, DOC/TOC, dureté de l'eau, température) | 3 | O | ||
| 30 | Photopériode et intensité lumineuse | 1 | N | ||
| 31 | Préparation de la solution de stock et d'essai | 1 | N | ||
| 32 | Un agent solubilisant/émulsifiant a-t-il été utilisé si le produit chimique était faiblement soluble ou instable? | 1 | N | ||
| 33 | Si un solubilisant/émulsifiant a été utilisé, sa concentration a-t-elle été signalée? | 1 | s.o. | ||
| 34 | Si un solubilisant/émulsifiant a été utilisé, son écotoxicité a-t-elle été signalée? | 1 | s.o. | ||
| 35 | Intervalles de contrôle analytique | 1 | O | ||
| 36 | Méthodes statistiques utilisées | 1 | N | ||
| Informations relatives à la qualité des données | |||||
| 37 | Le critère d'évaluation a-t-il été directement causé par la toxicité du produit chimique et non par l'état de santé de l'organisme (par exemple, lorsque la mortalité lors du contrôle est > 10 %) ou des effets physiques (par exemple, « effet d'ombrage »)? | s.o. | O | ||
| 38 | L'organisme d'essai correspondait-il à l'environnement canadien? | 3 | O | ||
| 39 | Les conditions du test (pH, température, DO, etc.) étaient-elles adaptées à l'organisme d'essai? | 1 | O | ||
| 40 | Le type de système et sa conception (statique, semi-statique, flux continu, scellé ou ouvert, etc.) correspondent-ils aux propriétés de la substance et à la nature/aux habitudes de l'organisme? | 2 | s.o. | ||
| 41 | Le pH de l'eau du test se situait-il dans la plage habituelle pour l'environnement canadien (6 à 9)? | 1 | N | Pas de pH donné | |
| 42 | La température de l'eau du test se situait-elle dans la plage habituelle pour l'environnement canadien (5 à 27 °C)? | 1 | O | ||
| 43 | La valeur de la toxicité était-elle inférieure à la solubilité dans l'eau du produit chimique? | 3 | N | La solubilité de l'eau pour cette substance était de 0,07. | |
| Résultats | |||||
| 44 | Valeurs de la toxicité (préciser le critère d'évaluation et la valeur) | s.o. | CL50 à 96 heures > 100 mg/L | ||
| 45 | Autres critères d'évaluation signalés : par exemple, FBC/FBA, CMEO/CSEO (préciser)? | s.o. | N | ||
| 46 | Autres effets indésirables (par exemple, cancérogénicité, mutagénicité) signalés? | s.o. | N | ||
| 47 | Note : ... % | 43,6 | |||
| 48 | Code de fiabilité d'Environnement Canada : | 3 | |||
| 49 | Catégorie de fiabilité (élevée, satisfaisante, basse) : | Confiance basse | |||
| 50 | Commentaires | ||||
Annexe 2 : Tableau sommaire des intrants des modèles de la persistance, de la bioaccumulation et de la toxicité
Données du modèle pour le Disperse Red 179 (n° CAS 16586-42-8)
| Devenir physique et chimique | Devenir | Devenir | Profils de persistance, bioaccumulation et toxicité | Persistance | |
|---|---|---|---|---|---|
| 1 Dérivé de log Kco 2 Dérivé des données FBC 3 Valeur par défaut 4 Dérivé d'une demi-vie dans l'eau |
|||||
| Paramètres d’entrée des modèles | EPI Suite (tous les modèles, notamment AOPWIN, KOCWIN, BCFWIN, BIOWIN et ECOSAR) |
STP (1) Traitement AS (2) Traitement simple (3) (les données requises sont différentes selon le modèle) |
Modèle FBC/ Gobas |
Modèle de POP canadien (y compris CATABOL) |
TOPKAT |
| Code SMILES | N(=O)(=O)c (ccc(nc (N=Nc (c(cc(N(CCC (#N))CC)c1) C)c1) s2)c23) c3 |
N(=O)(=O)c (ccc(nc (N=Nc (c(cc(N(CCC (#N))CC)c1) C)c1)s2)c23) c3 |
N(=O)(=O)c (ccc(nc (N=Nc (c(cc(N(CCC (#N))CC)c1) C)c1)s2)c23) c3 |
N(=O)(=O)c (ccc(nc (N=Nc (c(cc(N(CCC (#N))CC)c1) C)c1)s2)c23) c3 |
|
| Masse moléculaire (g/mol) | 394,45 | 394,45 (1, 2, 3) | |||
| Point de fusion (°C) | 172 Point de fusion de l'analogue CASn° 68133697 (Yen et al., 1989) |
||||
| Point d’ébullition (°C) | |||||
| Température des données (ºC) | 20 | ||||
| Masse volumique (kg/m3) | 1,52 (2) | ||||
| Pression de vapeur (Pa) | 4,53 × 10-7 B (1, 3) (pression de vapeur du Disperse Blue 79, Clariant, 1996) |
||||
| Constante de la loi de Henry (Pa·m3/mol) | 0,001 (3) La constante de la loi de Henry est la plus haute valeur en données déduites à partir d'analogues utilisée pour représenter le pire scénario (Baughman et Perenich, 1988, comme cité dans l'ébauche SAR) |
||||
Log Kae (coefficient de partage air-eau; sans dimension) |
|||||
Log Koe (coefficient de partage octanol-eau, sans dimension) |
5,09 [Valeur modélisée à l'aide de la méthode d'ajustement de la valeur expérimentale du modèle KNOWWIN (2000), qui a estimé le log Koe des substances d'après la valeur expérimentale du log Koe, soit 4,08, pour l'analogue n° CAS 68133-69-7 (Sijm et al.,1999)] |
La même que EPIWEB | La même que EPIWEB | Identique à EPIWEB | Identique à EPIWEB |
Koe (coefficient de partage octanol-eau, sans dimension) |
123 027 (2, 3) | ||||
Log Kco (coefficient de partage carbone organique/eau – L/kg) |
|||||
| Solubilité dans l'eau (mg/L) | 0,012 [Valeur modélisée à l'aide de la méthode d'ajustement de la valeur expérimentale du modèle WATERNT (2002), qui a estimé l'hydrosolubilité des substances en fonction de la valeur de l'hydrosolubilité de l'analogue n° CAS68133-69-7. L'hydrosolubilité de l'analogue (0,048 mg/L) est une moyenne géométrique des valeurs expérimentales de solubilité du n° CAS 68133-69-7 (Sijm et al.,1999)] |
0,02 (1, 3) | |||
Log Koa (coefficient de partage octanol-air, sans dimension) |
|||||
| Coefficient de partage sol-eau (L/kg)1 | |||||
| Coefficient de partage sédiments-eau (L/kg)1 | |||||
| Coefficient de partage particules en suspension-eau (L/kg)1 | 12365 (2) | ||||
| Coefficient de partage poisson-eau (L/kg)2 | |||||
| Coefficient de partage aérosol-eau (sans dimension)3 | |||||
| Coefficient de partage végétation-eau (sans dimension)1 | |||||
| Enthalpie (Koe) | |||||
| Enthalpie (Kae) | |||||
| Demi-vie dans l'air (jours) | |||||
| Demi-vie dans l’eau (jours) | |||||
| Demi-vie dans les sédiments (jours) | |||||
| Demi-vie dans le sol (jours) | |||||
| Demi-vie dans la végétation (jours)4 | |||||
| Constante cinétique de métabolisme (1/jours) | |||||
| Constante cinétique de biodégradation (jour-1 ou heure-1) – préciser | 0,032 (2, 1/jour) 0,77 (3, 1/heure) |
||||
| Demi-vie de biodégradation en clarificateur primaire (t1/2-p; h) | 217 heures (1) | ||||
| Demi-vie de biodégradation en bassin d’aération (t1/2-s; h) | 21,7 heures (1) | ||||
| Demi-vie de biodégradation en bassin de décantation (t1/2-s; h) | 21,7 heures (1) | ||||
Intrants du modèle pour le DAPEP (n° CAS25176-89-0)
| Devenir physique et chimique | Devenir | Devenir | Profils de persistance, bioaccumulation et toxicité | Persistance | |
|---|---|---|---|---|---|
| Paramètres d’entrée des modèles | EPI Suite (tous les modèles, notamment AOPWIN, KOCWIN, BCFWIN, BIOWIN et ECOSAR) |
STP (1) Traitement AS (2) Traitement simple (3) (les données requises sont différentes selon le modèle) |
Modèle FBC/FBA Arnot- Gobas |
Modèle de POP canadien (CATABOLl) |
TOPKAT |
| Code SMILES | c12N=C(N= Nc3ccc(N (CC)CCC (#N))cc3) Sc1cc(Cl)c (Cl)c2 |
c12N=C(N= Nc3ccc(N (CC)CCC (#N))cc3) Sc1cc(Cl) c(Cl)c2 |
c12N=C(N= Nc3ccc(N (CC)CCC (#N))cc3) Sc1cc(Cl) c(Cl)c2 |
c12N=C(N= Nc3ccc(N (CC)CCC (#N))cc3) Sc1cc(Cl) c(Cl)c2 |
c12N=C(N= Nc3ccc(N (CC)CCC (#N))cc3) Sc1cc(Cl) c(Cl)c2 |
| Masse moléculaire (g/mol) | 404,32 | 404,32 (1, 2, 3) | |||
| Point de fusion (°C) | * | 220 Point de fusion pour CAS# 25176-89-0 (Peters et al. 1992) |
|||
| Point d’ébullition (°C) | * | ||||
| Température des données (ºC) | 20 | ||||
| Masse volumique (kg/m3) | 1,64 (2) | ||||
| Pression de vapeur (Pa) | * | 4.53x10-7 B (1, 3) (pression de vapeur pour le Disperse blue 79, Clariant 1996) |
|||
| Constante de la loi de Henry (Pa·m3/mol) | * | 0.001 (3) La valeur la plus élevée de lecture a été utilisée afin de présenter le pire scénario (Baughman and Perenich, 1988, tel que cité dans le SAR) |
|||
Log Kae (coefficient de partage air-eau; sans dimension) |
|||||
Log Koe (coefficient de partage octanol-eau, sans dimension) |
6,01 [Valeur modélisée à l'aide de la méthode d'ajustement de la valeur expérimentale du modèle KNOWWIN (2000), qui a estimé le log Koe des substances d'après la valeur expérimentale du log Koe, soit 4,08, pour l'analogue n° CAS 68133-69-7 (Sijm et al., 1999)] |
La même que EPIWEB | La même que EPIWEB | Identique à EPIWEB | Identique à EPIWEB |
Koe (coefficient de partage octanol-eau, sans dimension) |
102329 (2, 3) | ||||
Log Kco (coefficient de partage carbone organique/eau – L/kg) |
|||||
| Solubilité dans l'eau (mg/L) | 0,004 [Valeur modélisée à l'aide de la méthode d'ajustement de la valeur expérimentale du modèle WATERNT (2002), qui a estimé l'hydrosolubilité des substances en fonction de la valeur de l'hydrosolubilité de l'analogue n° CAS68133-69-7. L'hydrosolubilité de l'analogue (0,048 mg/L) est une moyenne géométrique des valeurs expérimentales de solubilité du n° CAS 68133-69-7 (Sijm et al., 1999)] |
0,007 (1, 3) | |||
Log Koa (coefficient de partage octanol-air, sans dimension) |
|||||
| Coefficient de partage sol-eau (L/kg)1 | |||||
| Coefficient de partage sédiments-eau (L/kg)1 | |||||
| Coefficient de partage particules en suspension-eau (L/kg)1 | 42247 (2) | ||||
| Coefficient de partage poisson-eau (L/kg)2 | |||||
| Coefficient de partage aérosol-eau (sans dimension)3 | |||||
| Coefficient de partage végétation-eau (sans dimension)1 | |||||
| Enthalpie (Koe) | |||||
| Enthalpie (Kae) | |||||
| Demi-vie dans l'air (jours) | |||||
| Demi-vie dans l’eau (jours) | |||||
| Demi-vie dans les sédiments (jours) | |||||
| Demi-vie dans le sol (jours) | |||||
| Demi-vie dans la végétation (jours)4 | |||||
| Constante cinétique de métabolisme (1/jours) | * | ||||
| Constante cinétique de biodégradation (jour-1 ou heure-1) – préciser | 0,48 (2, 1/jour) 0.020 (3, 1/heure) |
||||
| Demi-vie de biodégradation en clarificateur primaire (t1/2-p; h) | 347 heures (1) | ||||
| Demi-vie de biodégradation en bassin d’aération (t1/2-s; h) | 34,7 heures (1) | ||||
| Demi-vie de biodégradation en bassin de décantation (t1/2-s; h) | 34,7 heures (1) |
Annexe 3 : Estimations de la limite supérieure de l'exposition au Disperse Red 179 et au DAPEP découlant des textiles
| Produit de consommation | Estimations de la limite supérieure de l'exposition (mg/kg p.c. par jour) au Disperse Red 179 et au DAPEP par divers groupes d'âge1 | ||||
|---|---|---|---|---|---|
| de 0 à 6 mois2 | de 0,5 à 4 ans3 | de 5 à 11 ans4 | de 12 à 19 ans5 | 20 ans et plus6 | |
| 1 L'estimation de la limite supérieure de la fraction lixiviable se situe entre 0,03 % pour les textiles grand-teint (ETAD, 2004) et 0,5 % pour les textiles présentant une faible indégorgeabilité (Kraetke et Platzek, 2005). 2 En supposant que le nourrisson pèse 7,5 kg, que sa surface corporelle (sans les mains et la tête) représente 0,28 m2 (Santé Canada, 1998) et qu'il passe 23 minutes par jour à mâchonner le tissu (Norris et Smith, 2002). 3 En supposant que l'enfant pèse 15,5 kg, que sa surface corporelle (sans les mains et la tête) représente 0,46 m2 (Santé Canada, 1998) et qu'il passe 29 minutes par jour à mâchonner le tissu (Norris et Smith, 2002). 4 En supposant que l'enfant pèse 31 kg et que sa surface corporelle (sans les mains et la tête) représente 0,80 m2 (Santé Canada, 1998). 5 En supposant que l'adolescent pèse 59,4 kg et que sa surface corporelle (sans les mains et la tête) représente 1,4 m2 (Santé Canada, 1998). 6 En supposant que la personne pèse 70,9 kg et que sa surface corporelle (sans les mains et la tête) représente 1,6 m2 (Santé Canada, 1998). |
|||||
| Cutanée : port de textiles | (0,2 - 4) x 10-3 | (0,2 - 3) x 10-3 | (0,2 - 3) x 10-3 | (0,1 - 2) x 10-3 | (0,1 - 2) x 10-3 |
| Voie orale : mâchonnement | 0,002 x 10-3 | 0,001 x 10-3 | s.o. | s.o. | s.o. |
| Scénarios – produits de consommation | Hypothèses | Estimation de la limite supérieure de l'exposition |
|---|---|---|
| 1 On présume que ce chiffre équivaut à la quantité de tissu en contact avec la peau. 2 Quantité de produit = densité du tissu ´ quantité de tissu ´ concentration = (100 g/m2) ´ (0,28 m2) ´ (1 % en poids) = 0,28 g 3 La quantité maximale de colorant retirée par de la salive simulée à partir de textiles destinés aux enfants après 4 h se chiffrait à 0,13 %; 0,5 % est utilisé pour représenter la limite supérieure. |
||
| Port d'un vêtement teint confectionné à partir de tissu synthétique | Scénario d'exposition : ConsExpo 4.0, contact cutané direct avec le produit – migration (RIVM, 2005). Exemple pour les nourrissons âgés de 0 à 6 mois. Concentration : 1 % par poids (Kraetke et Platzek, 2005) Densité du tissu : 100 g/m2 (Kraetke et Platzek, 2005) Hypothèses générales
Voie cutanée
|
Dose cutanée chronique interne = 0,004 mg/kg p.c. par jour |
| Mâchonnement de textiles teints | L'exposition est estimée ci-dessous pour les nourrissons âgés de 0 à 6 mois (poids corporel : 7,5 kg). Valeur d'absorption journalière estimée pour l'ingestion résultant du mâchonnement : = où : WS = solubilité dans l'eau du Disperse Red et du DAPEP (déduite pour les colorants azoïques = 0,69 mg/L (Baughman et Perenich, 1988) Vs = débit de salive = 0,22 mL/min (Environ, 2003a, b) CF = conversion du litre en mL = 0,001 L/mL FR = extraction partielle par la salive = 0,5 % (ETAD, 1983)3 AFo = facteur d'absorption par voie orale = 1 EF = fréquence d'exposition fondée sur le comportement d'absorption orale = 23 min/jour (Norris et Smith, 2002) BW = poids corporel = 7,5 kg pour les nourrissons âgés de 0 à 6 mois (Santé Canada, 1998) = (0,69 mg/L × 0,22 mL/min × 0,001 L/mL × 0,005 × 1 × 23 min)/ 7,5 kg = 6 x 10-6 mg/kg p.c. par jour |
Dose orale chronique interne = 6 x 10-6 mg/kg p.c. par jour |
Annexe 5 : Prévisions des modèles R(Q)SA pour le Disperse Red 179 (16586-42-8) et ses produits de clivage azoïques potentiels
Prévisions en matière de cancérogénicité
| ID | n° CAS | Derek1 | Toxtree2 | Model Applier3 | Casetox4 | |||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Cancer | SA gtx | Cancer | m-rat | f-rat | m-souris | f-souris | m-rat | f-rat | m-souris | f-souris | ||
| Composé d'origine | 16586-42-8 | P | P | N | P | IC | ND | ND | ND | ND | ND | ND |
| Métabolite 1 | 6285-57-0 | P | P | - | P | P | ND | IC | P | N | N | P |
| Métabolite 2 | 105294-34-6 | P | P | N | P | N | P | N | ND | ND | ND | ND |
Prévisions en matière de génotoxicité
| ID | n° CAS | Ames | ChrAb | Induction de micronoyaux | ||||||
|---|---|---|---|---|---|---|---|---|---|---|
| Derek | TT5 | MA | CT | MA | CT6 | TT | MA | CT | ||
| N° CAS : numéro de registre du Chemical Abstracts Service; ChrAb : aberration chromosomique; CT : Casetox; f : femelle; IC : non concluant; ID : identification; m : mâle; MA : Model Applier; N : négative; ND : hors du champ d'application du domaine; SA gtx : alerte structurelle indiquant la cancérogénicité génotoxique; P : positive; TT : Toxtree; - : aucun résultat 1 [DEREK] Deductive Estimation of Risk from Existing Knowledge [module de prévision sur cédérom]. 2008. Version 10.0.2. Cambridge (MA) : Harvard University, LHASA Group. [consulté le 30 septembre 2009]. Accès : http://www.lhasalimited.org/index.php? cat=2&sub_cat=2# [réserve de consultation]. 2 Toxtree version 1.60. 2009. Réalisé par Ideaconsult Ltd, Bulgarie. 3 [Leadscope] Leadscope Model Applier [module de prévision]. 2009. Version 1.2.0-3. Columbus (OH): Leadscope, Inc. [consulté le 30 septembre 2009]. Accès : http://www.leadscope.com/all_products.php[réserve de consultation]. 4 CASETOX [module de prévision]. 2008. Version 2.0. Beachwood (OH) : MultiCASE. [consulté le 30 septembre 2009]. Accès : http://www.multicase.com/products/prod03.htm[réserve de consultation]. 5Souche TA100 du Salmonella typhimurium. 6 Essai in vitro (dans des cellules ovariennes de hamster chinois en culture). 7 Résultat négatif faible. |
||||||||||
| Composé d'origine | 16586-42-8 | P | P | P | ND | ND | IC | P | ND | ND |
| Métabolite 1 | 6285-57-0 | P | - | P | ND | ND | ND | P | N7 | P |
| Métabolite 2 | 105294-34-6 | P | P | P | P | N | P | P | N | IC |
| Fondement de la considération | Nom et n° de registre du CAS | Structure |
|---|---|---|
| 1 Coefficient de Tanimoto = 92 (recherche de similitude dans SciFinder). | ||
| Produit de clivage azoïque potentiel | 6285-57-0 2-amino-6-nitrobenzothiazole |
 |
| Produit de clivage azoïque potentiel | 105294-34-6 3-[(4-amino-3-méthylphényl)éthylamino]propanenitile |
 |
| Analogue structurel1 | 25510-81-0 Disperse Red 145 |
 |
Annexe 7 : Prévisions des modèles R(Q)SA pour le DAPEP (isomère 5,6-dichloro du Disperse Red 153), l'isomère 6,7-dichloro du Disperse Red 153 et leurs produits de clivage azoïques potentiels
Prévisions en matière de cancérogénicité
| ID | n° CAS | Derek1 | Toxtree2 | Model Applier3 | Casetox4 | |||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Cancer | SA gtx | Cancer | m-rat | f-rat | m-souris | f-souris | m-rat | f-rat | m-souris | f-souris | ||
| Composé d'origine 1 | 25176-89-0 | P | P | N | P | N | ND | ND | ND | ND | ND | ND |
| Composé d'origine 2 (isomère 6,7'-dichloro) | 78564-87-1 | P | P | N | P | N | ND | ND | ND | ND | ND | ND |
| M-1 | 24072-75-1 | P | P | - | IC | IC | ND | ND | ND | N | N | P |
| M 2 | 25150-27-0 | P | P | - | IC | IC | ND | ND | ND | ND | N | N |
| M 3 | 100894-10-8 | - | P | N | N | N | N | N | ND | ND | ND | ND |
Prévisions en matière de génotoxicité
| ID | n° CAS | Ames | ChrAb | Induction de micronoyaux | ||||||
|---|---|---|---|---|---|---|---|---|---|---|
| Derek | TT5 | MA | CT | MA | CT6 | TT | MA | CT | ||
| N° CAS : numéro de registre du Chemical Abstracts Service; ChrAb : aberration chromosomique; CT : Casetox; f : femelle; IC : non concluant; ID : identification; m : mâle; MA : Model Applier; N : négative; ND : hors du champ d'application du domaine; SA gtx : alerte structurelle indiquant la cancérogénicité génotoxique; P : positive; TT : Toxtree; - : aucun résultat 1 [DEREK] Deductive Estimation of Risk from Existing Knowledge [module de prévision sur cédérom]. 2008. Version 10.0.2. Cambridge (MA) : Harvard University, LHASA Group. [consulté le 30 septembre 2009]. Accès : http://www.lhasalimited.org/index.php? cat=2&sub_cat=2# [réserve de consultation]. 2 Toxtree version 1.60. 2009. Réalisé par Ideaconsult Ltd, Bulgarie. 3 [Leadscope] Leadscope Model Applier [module de prévision]. 2009. Version 1.2.0-3. Columbus (OH): Leadscope, Inc. [consulté le 30 septembre 2009]. Accès : http://www.leadscope.com/all_products.php[réserve de consultation]. 4 CASETOX [module de prévision]. 2008. Version 2.0. Beachwood (OH) : MultiCASE. [consulté le 30 septembre 2009]. Accès : http://www.multicase.com/products/prod03.htm[réserve de consultation]. 5 Souche TA100 du Salmonella typhimurium. 6 Essai in vitro (dans des cellules ovariennes de hamster chinois en culture). |
||||||||||
| Composé d'origine | 25176-89-0 | P | P | N | ND | ND | P | P | ND | ND |
| Composé d'origine 2 (isomère 6,7'-dichloro) | 78564-87-1 | P | P | N | ND | ND | ND | P | N | N |
| M-1 | 25150-27-0 | P | - | N | N | N | ND | P | IC | N |
| M 2 | 105294-34-6 | P | P | P | P | N | P | P | N | IC |
| M 3 | 100894-10-8 | - | P | IC | ND | N | P | P | N | N |
Annexe 8 : Produits de clivage azoïques potentiels et analogues structurels du DAPEP (isomère 5,6-dichloro) et du Disperse Red 153 (mélange d'isomères)
| Fondement de la considération | Nom et n° de registre du CAS | Structure |
|---|---|---|
| 1 Coefficient de Tanimoto = 90 (recherche de similitude dans SciFinder). | ||
| Produit de clivage azoïque potentiel (DAPEP, isomère 5,6'-dichloro du Disperse Red 153) | 24072-75-1 2-amino-5,6- dichlorobenzothiazole |
 |
| Produit de clivage azoïque potentiel (isomère 6,7'-dichloro du Disperse Red 153) | 25150-27-0 6,7-dichloro-2- benzothiazolamine |
 |
| Produit de clivage azoïque potentiel (deux isomères du Disperse Red 153) | 100894-10-8 3-[(4-aminophényl) éthylamino] propanenitrile - |
 |
| Analogue structurel1 | 78564-86-0 Disperse Red 152 |
 |
Note de bas de page
Cette page Web a été archivée dans le Web
L'information dont il est indiqué qu'elle est archivée est fournie à des fins de référence, de recherche ou de tenue de documents. Elle n'est pas assujettie aux normes Web du gouvernement du Canada et elle n'a pas été modifiée ou mise à jour depuis son archivage. Pour obtenir cette information dans un autre format, veuillez communiquer avec nous.
Archivée
3-[Éthyl[3-méthyl-4-[(6-nitrobenzothiazol-2-yl)azo]phényl] amino]propiononitrile
(Disperse Red 179)
Numéro de registre du Chemical Abstracts Service
16586-42-8
3-[[4-[(5,6-Dichlorobenzothiazol-2-yl)azo]phényl] éthylamino]propiononitrile
(DAPEP)
Numéro de registre du Chemical Abstracts Service
25176-89-0
Environnement Canada
Santé Canada
Mars 2010
- Sommaire
- Introduction
- Identité de la substance
- Définition des substances analogues et estimation des proprités physiques et chimiques
- Sources
- Utilisations
- Rejets dans l'environnement
- Devenir dans l'environnement
- Persistance et potentiel de bioaccumulation
- Potentiel d'effets nocifs écologiques nocifs
- Potentiel d'effets nocifs sur la santé humaine
- Conclusion
- Références
- Annexe 1 : Sommaire de rigueur d'études pour les études clés
- Annexe 2 : Table de résumé des données du modèle BTP
- Annexe 3 : Estimations de la limite supérieure de l'exposition au Disperse Red 179 et au DAPEP découlant des textiles
- Annexe 4 : Estimations de l'exposition découlant des textiles teints
- Annexe 5 : Prévisions des modèles R(Q)SA pour le Disperse Red 179 (16586-42-8) et ses produits de clivage azoïques potentiels
- Annexe 6 : Produits de clivage azoïques potentiels et analogues structurels du Disperse Red 179
- Annexe 7 : Prévisions des modèles R(Q)SA pour le DAPEP (isomère 5,6-dichloro du Disperse Red 153), l'isomère 6,7-dichloro du Disperse Red 153 et leurs produits de clivage azoïques potentiels
- Annexe 8 : Produits de clivage azoïques potentiels et analogues structurels du DAPEP (isomère 5,6-dichloro) et du Disperse Red 153 (mélange d'isomères)
Conformément à l'article 74 de la Loi canadienne sur la protection de l'environnement, 1999[LCPE (1999)], les ministres de l'Environnement et de la Santé ont effectué une évaluation préalable du 3-[[4-[(5,6-Dichlorobenzothiazol-2-yl)azo]phényl] éthylamino]propiononitrile (Disperse Red 179), dont le numéro de registre du Chemical Abstracts Service est 16586-42-8; et du 3-[[4-[(5,6-Dichlorobenzothiazol-2-yl)azo]phényl] éthylamino]propiononitrile (DAPEP), dont le numéro de registre du Chemical Abstracts Service est 25176-89-0. Ces substances ont été identifiées lors de l'évaluation préalable comme hautement prioritaires et incluses dans le cadre du défi, car elles se sont avérées répondre aux critères de catégorisation écologiques de persistance, de potentiel de bioaccumulation et de toxicité intrinsèque pour les organismes non humains et que l'on pense être commercialisées au Canada.
Les substances Disperse Red 179 et DAPEP n'ont pas été considérées comme hautement prioritaires pour l'évaluation des risques potentiels pour la santé humaine, d'après l'application de la simple exposition et des outils de danger développés par Santé Canada pour la catégorisation de substances dans la Liste intérieure des substances. Par conséquent, cette évaluation est centrée sur les renseignements correspondant à l'évaluation des risques écologiques.
Le Disperse Red 179 et le DAPEP sont des substances organiques utilisées au Canada principalement comme agents de teinture rouge pour fibres synthétiques des vêtements et textiles domestiques. En raison de leur structure et de leur usage similaires, le Disperse red 179 et le DAPEP sont évalués ensemble dans ce rapport.Ces substances ne sont pas naturellement produites dans l'environnement. Leur fabrication n'est pas signalée au Canada; toutefois, 400 kg de Disperse Red 179 et 100 kg de DAPEP ont été importés dans le pays en 2006 pour être utilisés dans l'industrie du textile.
D'après des modèles d'utilisation signalés au Canada et certaines hypothèses, la plupart de ces substances devraient finir dans des sites d'élimination des déchets. Environ 17 % du Disperse Red 179 et du DAPEP sont estimés être rejetés dans l'eau et aucun rejet n'est prédit dans l'air et dans le sol.Le Disperse Red 179 et le DAPEP présentent une solubilité très faible dans l'eau et l'octanol (d'après des données analogues et modélisées). Le Disperse Red 179 et le DAPEP sont présents dans l'environnement principalement sous forme de particules fines non volatiles, ils sont relativement stables d'un point de vue chimique, ils ont tendance à se répartir dans les sédiments, sous l'action de la pesanteur, s'ils sont rejetés dans les eaux de surface et ils se répartiraient probablement dans les sols s'ils étaient rejetés dans l'air.
D'après leurs propriétés physiques et chimiques ainsi que des données expérimentales de biodégradation, le Disperse Red 179 et le DAPEP devraient être persistants dans l'environnement, soit dans tous les milieux dans des conditions aérobies. De nouvelles données expérimentales sur des analogues, des données modélisées ainsi que l'avis des experts indiquent que ces teintures présentent un faible potentiel d'accumulation dans les tissus adipeux des organismes. Les substances répondent donc aux critères de persistance, mais non à ceux de bioaccumulation énoncés dans le Règlement sur la persistance et la bioaccumulation.En outre, de nouvelles données sur la toxicité de produits chimiques analogues indiquent que ces substances représentent un danger faible à modéré pour les organismes aquatiques.
Aux fins de la présente évaluation préalable, deux scénarios d'exposition très prudents représentant les rejets industriels et domestiques dans l'environnement aquatique ont été appliqués. Le premier scénario simulait le rejet du Disperse Red 179 et du DAPEP dans l'environnement aquatique après l'utilisation de chaque teinture dans une opération industrielle.Le deuxième scénario simulait le rejet du Disperse Red 179 et du DAPEP dans l'environnement aquatique après leur utilisation domestique.Les concentrations environnementales prévues dans l'eau pour chaque scénario étaient inférieures aux concentrations sans effet prévues, calculées pour les organismes pélagiques.
L'exposition potentielle de la population générale au Disperse Red 179 et au DAPEP présents dans les milieux naturels devrait être négligeable. L'exposition au Disperse Red 179 et au DAPEP par les produits de consommation devrait être faible compte tenu de l'utilisation prévue du produit (teinture dans les textiles synthétiques) dans le cas d'expositions fortuites, notamment lorsque de jeunes enfants portent ces produits à leur bouche.
Les données empiriques limitées définies pour Disperse Red 179 et au DAPEP, les métabolites et analogues potentiels, ensemble avec les relations quantitatives structure-activités (RQSA),. Les prédictions semblent indiquer que ces substances peuvent présenter un risque potentiel pour la santé humaine.
Bien que les données empiriques limitées indiquent un risque d’exposition au Disperse Red 179 et au DAPEP, l’expossition de la population canadienne à ces substances en raison de leur utilisation dans les textiles devrait être faible. Par conséquent, le risque pour la santé humaine est faible.
D'après les informations disponibles, le Disperse Red 179 et le DAPEP ne répondent à aucun critère de l'article 64 de la Loi canadienne sur la protection de l'environnement, 1999.
Puisque ces substances sont inscrites sur la Liste intérieure des substances, leur importation et leur fabrication au Canada ne requièrent pas de déclaration aux termes du paragraphe 81(1). Étant donné les propriétés dangereuses potentielles de ces substances, on craint que des utilisations nouvelles non décelées ni évaluées fassent en sorte qu'elles répondent aux critères de l'article 64 de la LCPE (1999). Par conséquent, il est recommandé de modifier la Liste intérieure des substances en vertu du paragraphe 87(3) de la Loi afin d'indiquer que le paragraphe 81(3) s'applique à ces substances. Ainsi, toute fabrication, importation ou utilisation de ces dernières devra être déclarée et faire l'objet d'une évaluation des risques pour l'environnement et la santé humaine
De plus, des activités de recherche et de surveillance viendront, le cas échéant, appuyer la vérification des hypothèses formulées au cours de l'évaluation préalable.
La Loi canadienne sur la protection de l'environnement, 1999[LCPE (1999)] (Canada 1999) exige que les ministres de l'Environnement et de la Santé procèdent à une évaluation préalable des substances qui répondent aux critères de la catégorisation énoncés dans la Loi, afin de déterminer si elles présentent ou sont susceptibles de présenter un risque pour l'environnement ou la santé humaine.
D'après les informations obtenues dans le cadre de la catégorisation, les ministres ont identifié un certain nombre de substances hautement prioritaires pour lesquelles entreprendre une action. Ces substances comprennent celles qui
- répondent à tous les critères environnementaux de la catégorisation, notamment la persistance (P), le potentiel de bioaccumulation (B) et la toxicité intrinsèque pour les organismes aquatiques (Ti), et que l'on pense être commercialisées au Canada et/ou
- répondent aux critères de catégorisation pour le plus fort risque d'exposition (PFRE) ou qui présentent un risque d'exposition intermédiaire (REI) et qui ont été jugées particulièrement dangereuses pour la santé humaine, compte tenu des classifications qui ont été établies par d'autres organismes nationaux ou internationaux concernant leur cancérogénicité, leur génotoxicité ou leur toxicité pour le développement ou la reproduction.
Le 9 décembre 2006, les ministres ont donc publié un avis d'intention dans la Partie I de la Gazette du Canada(Canada, 2006), qui encourageait l'industrie et les autres intervenants intéressés à fournir dans des délais précis, des renseignements spécifiques qui pourraient servir à étayer l'évaluation des risques et à élaborer les meilleures pratiques en matière de gestion des risques et en intendance des produits pour les substances jugées hautement prioritaires.
Les substances 3-[[4-[(5,6-Dichlorobenzothiazol-2-yl)azo]phényl] éthylamino]propiononitrile (Disperse Red 179) et 3-[[4-[(5,6-Dichlorobenzothiazol-2-yl)azo]phényl] éthylamino]propiononitrile (DAPEP), ont été identifiées comme hautement prioritaires pour l'évaluation du risque écologique, car elles se sont révélées persistantes, bio-accumulatives et naturellement toxiques pour les organismes aquatiques et sont supposées être commercialisées au Canada. Le Défi portant sur ces substances a été publié dans la Gazette du Canadale 30 août 2008 (Canada, 2008).En même temps, un profil pour chaque substance a été publié.Ces profils présentaient les informations techniques obtenues avant décembre 2005 et sur lesquelles reposait leur catégorisation.En réponse au Défi, des soumissions d'informations relatives à la persistance, au danger et à l'utilisation de ces substances ont été reçues.
Bien que le Diperse Red 179 et le DAPEP aient été déterminés comme hautement prioritaires pour l'évaluation par rapport à l'environnement, ils ne répondaient pas aux critères du plus fort risque d'exposition ou du risque d'exposition intermédiaire et un danger élevé pour la santé humaine d'après les classifications de cancérogénicité, de génotoxicité, de toxicité pour le développement ou la reproduction établies par d'autres organismes nationaux ou internationaux.
Les évaluations préalables effectuées aux termes de la LCPE (1999) mettent l'accent sur les renseignements jugés essentiels pour déterminer si une substance répond aux critères de l'article 64 de la Loi.
Les évaluations préalables étudient les renseignements scientifiques et tirent des conclusions en intégrant sur la méthode du poids de la preuve et le principe de précaution.
La présente évaluation préalable prend en considération les renseignements sur les propriétés chimiques, les dangers, les utilisations de la substance en question et l’exposition à celle-ci, y compris l’information supplémentaire fournie dans le cadre du Défi. Des données pertinentes à l'évaluation préalable de cette substance sont tirées de publications originales, de rapports de synthèse et d’évaluation, de rapports de recherche de parties intéressées et d’autres documents consultés au cours de recherches documentaires menées récemment, jusqu'au 31 décembre 2009.. Les informations disponibles et pertinentes présentées dans les évaluations du danger d'autres juridictions ont été prises en compte.L'évaluation préalablene constitue pas un examen exhaustif ou critique de toutes les données disponibles. Elle présente plutôt les études les plus critiques et les éléments de preuve relatifs à la conclusion.
Le Disperse Red 179 et le DAPEP sont évalués ensemble dans ce rapport d'évaluation préalable Les données sur les propriétés physiques et chimiques de ces teintures manquent et vu les similitudes de leur structure et de leur usage respectifs, des analogues acceptables ont été identifiés et possèdent des données pertinentes soutenant l'évaluation écologique de ces deux teintures.
La présente évaluation préalable a été préparée par le personnel du Programme des substances existantes de Santé Canada et d’Environnement Canada et elle intègre les résultats d’autres programmes exécutés par ces ministères. La section écologique de la présenteévaluation a fait l'objet d'une étude consignée par des pairs ou d'une consultation de ces derniers. Par ailleurs, l'ébauche de cette évaluation préalable a fait l’objet d’une période de commentaires du public de 60 jours.Alors que les commentaires externes aient été pris en considération, Santé Canada et Environnement Canada assument la responsabilité du contenu final et des résultats de l'évaluation préalable.Les principales données et considérations sur lesquelles repose la présente évaluation sont résumées ci-après
Pour les besoins de ce document, la substance 3-[[4-[(5,6-Dichlorobenzothiazol-2-yl)azo]phényl] éthylamino]propiononitrile- (n° CAS16586-42-8), sera appelée Disperse Red 179, au lieu de NBATP, qui était utilisé dans le profil de substance. Le « Disperse Red 179 » est défini par le Colour Index (CII 2002-) comme une combinaison de deux numéros de registre CAS(n° CAS 61951-64-2 et n° CAS16195-64-8). Les substances associées aux n° CAS16586-42-8 et 61951-64-2 sont identiques, car toutes deux ont des noms scientifiques identiques (NCI, 2009), des structures chimiques identiques (ChemID, 2009; CII, 2002-) et le même numéro du Colour Index, C.I. 11290 (CII, 2002-). D'après le Colour Index, une substance chimique précise peut avoir plus d'un n° CAS, notamment dans le domaine des teintures, selon que la substance a été déclarée au Chemical Abstracts sous son nom chimique complet ou sous son nom C.I. générique (CII 2002-). Ainsi, dans cet exemple particulier, le n° CAS 61951-64-2 se rapporte au nom C.I. Disperse Red 179, alors que le n° CAS16586-42-8 correspond en fait au nom chimique 3-[[4-[(5,6-Dichlorobenzothiazol-2-yl)azo]phényl] éthylamino]propiononitrile]. Cependant, le n° CAS16195-64-8 ne se trouve pas sur la liste d'inventaire du Chemical Abstract Service (NCI, 2009) et aucune substance n'est ni n'a jamais été associée à ce n° CAS(Chemical Abstract Service, communication personnelle, source non citée). Par conséquent, le Disperse Red 179 n'est pas un mélange de deux numéros CAS, mais un produit chimique discret listé sous le n° CAS 16586428 (voir le tableau 1a).
La substance 3-[[4-[(5,6-Dichlorobenzothiazol-2-yl)azo]phényl] éthylamino]propiononitrile (n° CAS25176-89-0), est parfois appelée Disperse Red 153. Toutefois, le Disperse Red 153, qui est enregistré sous le n° CAS78564-87-1 (CI 111370), est en fait un mélange de deux isomères structurels (Nakagawa, 1996; CII, 2002- ). Un isomère est enregistré sous le n° CAS25176-89-0 (C.I. 111371) et l'autre n'a pas de n° CASenregistré, mais un numéro d'enregistrement du Colour Index, C.I. 111372 (CII 2002- ). Ces deux substances sont des isomères structurels (même formule chimique); dès lors, on prévoit que les propriétés du mélange chimique ressemblent beaucoup à celles du n° CAS 25176-89-0. Aux fins du présent document, le n° CAS 25176-89-0 sera appelé le DAPEP, un acronyme tiré de son nom d'inventaire (voir tableau 1b).
Tableau 1 a. Identité de la substance pour le Disperse Red 179
| Numéro de registre du Chemical Abstracts Service (n° CAS) | 16586-42-8 |
| Nom dans la LIS | 3-[Éthyl[3-méthyl-4-[(6-nitrobenzothiazol-2-yl)azo]phényl] amino]propiononitrile |
| Noms1 du National Chemical Inventories (NCI) | 3-[Éthyl[3-méthyl-4-[(6-nitrobenzothiazol-2-yl)azo]phényl] amino]propiononitrile- (TSCA) 3-[Éthyl[3-méthyl-4-[(6-nitrobenzothiazol-2-yl)azo]phényl] amino]propiononitrile- (AICS, PICCS, ASIA-PAC) 3-[Éthyl[3-méthyl-4-[(6-nitrobenzothiazol-2-yl)azo]phényl] amino]propiononitrile (EINECS, ECL) C.I. Violet Disperse 052 (ECL) C.I. ROUGE DISPERSE 179 (PICCS) |
| Autres noms | 3-[N-Ethyl-4-[(6-nitro-2-benzothiazolyle)azo]-m-toluidino]propionitrileC.I. 112290, C.I. Violet Disperse 52 Rouge Disperse79, Violet Disperse 52 Kayalon Polyester Rubine BL-SKayalon Polyester Rubine BL-S 200 Propionitrile, 3-[N-éthyl-4-[(6-nitro-2-benzothiazolyl)azo]-m-toluidino]-3-(éthyle{3-méthyl-4-[(6-nitrobenzothiazol-2-yl)azo]phényle}amino)propiononitrile |
| Groupe chimique (LIS) | Produits chimiques organiques définis |
| Principale classe chimique ou utilisation | Colorant azoïque organique dispersé |
| Principale sous-classe chimique | Colorant benzothiazole mono-azoïque |
| Formule chimique | C19H18N6O2S |
| Structure chimique | 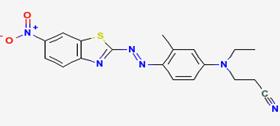 |
| SMILES2 | N(=O)(=O)c(ccc(nc(N=Nc(c(cc(N(CCC(#N))CC)c1)C)c1)s2)c23)c3 |
| Masse moléculaire | 394,45 g/mol |
| 1 National Chemical Inventories (NCI), 2009; AICS (Inventaire australien des substances chimiques); ASIA-PAC (Listes des substances Asie-Pacifique); ECL (Liste coréenne des produits chimiques existants); EINECS (Inventaire européen des substances chimiques commerciales existantes); PICCS (Inventaire philippin des produits et des substances chimiques); TSCA (Inventaire des substances chimiques de la Loi sur le contrôle des substances toxiques). 2 Simplified Molecular Line Input Entry System (SMILES). |
|
Tableau 1b. Identité de substance pour le DAPEP
| Numéro de registre du Chemical Abstracts Service (n° CAS) | 25176-89-0 |
| Nom dans la LIS | 3-[[4-[(5,6-Dichlorobenzothiazol-2-yl)azo]phényl] éthylamino]propiononitrile |
| Noms1 du National Chemical Inventories (NCI) | 3-[[4-[(5,6-Dichlorobenzothiazol-2-yl)azo]phényl] éthylamino]propiononitrile- (AICS, PICCS, ASIA-PAC) 3-[[4-[(5,6-Dichlorobenzothiazol-2-yl)azo]phényl]éthylamino]propiononitrile(EINECS) 3-[[4-[(5,6-Dichlorobenzothiazol-2-yl)azo]phényl] éthylamino]propionontrile (PICCS) |
| Autres noms | Propionitrile, 3-[p-[(5,6-dichloro-2-benzothiazolyl)azo]-N-ethylanilino]-3-({4-[(5,6-Dichlorobenzothiazol-2-yl)azo]phényl}éthylamino)propiononitrile |
| Groupe chimique (LIS) | Produits chimiques organiques définis |
| Principale classe chimique ou utilisation | Colorant azoïque organique dispersé |
| Principale sous-classe chimique | Colorant benzothiazole mono-azoïque |
| Formule chimique | C18H15Cl2N5S |
| Structure chimique | 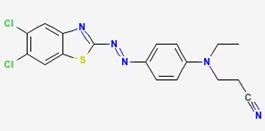 |
| SMILES | c12N=C(N=Nc3ccc(N(CC)CCC(#N))cc3)Sc1cc(Cl)c(Cl)c2 |
| Masse moléculaire | 404,32 g/mol |
| 1 National Chemical Inventories (NCI), 2009; AICS (Inventaire australien des substances chimiques); ASIA-PAC (Listes des substances Asie-Pacifique); EINECS (Inventaire européen des substances chimiques commerciales existantes); PICCS (Inventaire philippin des produits et des substances chimiques). 2 Simplified Molecular Line Input Entry System (SMILES). |
|
Peu de données expérimentales sont disponibles pour le Disperse Red 179 ou le DAPEP. Lors de l'atelier sur les relations quantitatives structure-activité (RQSA) parrainé par Environnement Canada en 1999 (Environnement Canada, 2000), les experts en modélisation invités ont identifié de nombreuses classes structurelles de pigments et de teintures en « difficiles à modéliser », à l'aide des RQSA.Les propriétés physiques et chimiques de plusieurs classes structurelles de teintures et de pigments (y compris les teintures acides et dispersées) ne sont pas soumises à une prédiction de modèles, car elles sont considérées comme « hors du domaine de modèles d'applicabilité » (par exemple les domaines de paramètres structurels et/ou de propriété).En conséquence, pour déterminer l'utilité potentielle, les domaines d'applicabilité des domaines RQSA aux teintures et aux pigments sont évalués au cas par cas.
Environnement Canada a estimé qu'il était inapproprié d'utiliser des modèles RQSA pour prévoir la plupart des propriétés physiques et chimiques du Disperse Red 179 et du DAPEP et, par conséquent, il a eu recours à une méthode fondée sur les données déduites à partir d'analogues afin de déterminer les propriétés physiques et chimiques approximatives données au tableau 3. Ces propriétés ont été utilisées par la suite pour d'autres modélisations et éléments d'information au cours de cette évaluation.
Un analogue est un produit chimique structurellement similaire à la substance en évaluation et doit par conséquent avoir des propriétés physiques et chimiques similaires, un comportement similaire dans l'environnement et/ou une toxicité similaire. Si des données expérimentales sont disponibles pour un paramètre spécifique lié à une substance analogue, on peut utiliser ces dernières, directement ou après modification, pour estimer la valeur du paramètre concerné pour la substance évaluée.
Pour trouver des analogues acceptables, une revue des données pour plusieurs colorants azoïques dispersés a été effectuée (Anliker et al., 1981; Anliker et Moser, 1987; Baughman et Perenich, 1988; Savarino et al., 1989; Yen et al., 1989; Yen et al., 1991; Brown, 1992; Peters et Gbadamosi, 1992; Peters et al., 1992; ETAD, 1995; Sijm et al., 1999; Maradiya, 2004). Ces composés possèdent des similitudes structurelles au Disperse Red 179 et au DAPEP, mais partagent également d'autres caractéristiques importantes qui en font des analogues convenables.Ces dernières comprennent des propriétés affectant leur devenir dans l'environnement, comme des masses moléculaires élevées (généralement > 320 g/mol), des diamètres transversaux similaires (de 1,31 à 2,11 nm), des structures de particules solides, une décomposition à plus de 110 °C et une « dispersibilité » dans l'eau (c.-à-d. pas réellement « solubles »). De plus, elles ont une pression de vapeur négligeable et sont conçues pour être stables en conditions environnementales.
Le Disperse Red 179 et le DAPEP sont des substances analogues en raison des similitudes de leur structure chimique et de leur masse moléculaire Les deux substances contiennent les groupes fonctionnels azoïque, benzothiazyle et cyanuré et tous deux sont utilisés comme colorants pour textiles.Cependant, il faut s'attendre à de légères différences au niveau des propriétés physiques et chimiques et du comportement entre les deux substances. On prévoit que le Disperse Red 179 a une plus grande solubilité dans l'eau et un plus faible log Koe que le DAPEP en raison de la présence d'un groupe nitré fixé à son noyau benzothiazyle.De façon similaire, les deux atomes de chlore fixés au groupe benzothialzyle du DAPEP vont probablement diminuer sa solubilité dans l'eau et augmenter son log Koe.
L'information structurelle relative aux colorants azoïques dispersés analogues du Disperse Red 179 et du DAPEP est présentée dans les tableaux 2a et 2b. Certaines propriétés physiques et chimiques (voir le tableau 3), données empiriques sur la bioaccumulation (voir le tableau 6) et données empiriques sur la toxicité (voir le tableau 7) de ces analogues ont été utilisées pour établir le poids de la preuve et pour appuyer les décisions présentées dans cette ébauche d'évaluation préalable.
Tableau 2a. Information disponible pour le Disperse Red 179 et le DAPEP ainsi que pour plusieurs analogues structurels
| n° CAS | Nom commun | Nom dans la LIS | Structure chimique de l'analogue | Données empiriques disponibles | |
|---|---|---|---|---|---|
| i. | 25176-89-0 | DAPEP | 3-[[4-[(5,6- Dichloro- benzothiazol-2- yl)azo]phényl] éthylamino] propiononitrile |
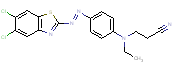 |
Persistance, toxicité aquatique |
| ii. | 16586-42-8 | Disperse Red 179 | 3-[Éthyl[3- méthyl-4-[(6- nitrobenzothiazol- 2-yl)azo]phényl] amino] propiononitrile- |
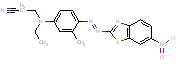 |
Persistance, toxicité aquatique |
| iii. | 68133-69-7 | s.o. | Propanenitrile, 3-((2-(acétyloxy) éthyl)(4-(2-(6- nitro-2- benzothiazolyl) diazényl)phényl) amino)- |
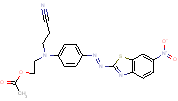 |
Point de fusion, solubilité dans l'octanol, solubilité dans l'eau, log Koe |
| iv | 70198-17-3 | s.o. | Ethanol, 2-((4- (2-(6-chloro-2- benzothiazolyl) diazenyl)phényle) éthylamino)-, 1-acétate |
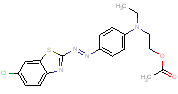 |
Toxicité pour les organismes aquatiques |
| v | 5261-31-4 | Disperse Orange 30 | Acétate de 2- [N-(2-cyanoéthyl)- 4-[2,6-dichloro-4- nitrophényl)azo] anilino]éthyle |
 |
Facteur de bioconcentration; (FBC), toxicité aquatique |
| vi. | 31482-56-1 | Disperse Orange 25 | Propanenitrile, 3- (Ethyl(4-((4- nitrophenyl)azo) phenyl)amino)- |
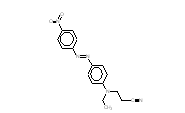 |
Toxicité pour les organismes aquatiques |
| vii | 3179-89-3 | Disperse Red 17 | Ethanol, 2,2¢-((3- méthyl-4-(2-(4- nitrophényl)diazényl) phényl)amino)bis- |
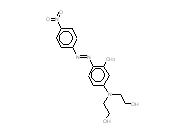 |
Toxicité pour les organismes aquatiques |
| viii | 16889-10-4 | Disperse Red 73 | 2-({4-[(2- Cyanoéthyl)(2- phényléthyl)amino] phenyl}azo)-5- nitrobenzonitrile |
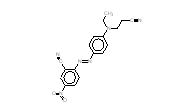 |
Toxicité pour les organismes aquatiques |
Il faut souligner que l'on dénombre diverses incertitudes liées à l'utilisation des données disponibles sur les propriétés physiques et chimiques, la toxicité et la bioaccumulation des substances qui apparaissent dans le tableau 2a. Toutes ces substances appartiennent à la même classe chimique, soit celle des colorants azoïques dispersés (caractérisés par une liaison azoïque) et ont, en majorité, des masses moléculaires semblables (tableau 3b) et sont utilisées à des fins industrielles similaires. Toutefois, il existe des différences entre ces substances associées à leurs différences de taille moléculaire et leur groupe fonctionnel unique, notamment la présence ou l'absence des groupes fonctionnels benzothiazyle, cyano, nitro et/ou ester, ou la présence d'atomes halogènes, comme du chlore sur l'un des noyaux aromatiques. De plus, les différences de résultats pour des substances peuvent également être dues à une erreur analytique pendant les essais. Il en découle que ces analogues ont des valeurs empiriques déterminées de solubilité dans l'eau qui varient de plus de quatre ordres de grandeur, soit dans une plage allant de 10-5 à 0,69 mg/L. Il serait préférable d'utiliser des données empiriques (par exemple pour l'hydrosolubilité et le log Koe) propres aux substances soumises à une évaluation. Toutefois, en raison du manque de données dans tous les domaines pour les teintures dispersées monoazoïques au benzothiazyle, les données analogues présentées sont considérées comme la seule preuve raisonnable pour l'évaluation de ces deux substances. La variabilité des données disponibles a été prise en compte.
Tableau 2b. Comparaison des analogues structuraux et le Disperse Red 179 et le DAPEP1
| n° CAS | Nom commun | Masse moléculaire (g/mol) | Similarité structurelle | Diamètre transversal minimum et maximum (DMax) en (nm) | ||
|---|---|---|---|---|---|---|
| par rapport au Disperse Red 179 (%) | par rapport au DAPEP (%) | |||||
| 1 ChemID (2009); valeur présentée si > 60 %. Le tableau 3 contient les propriétés physiques et chimiques expérimentales et modélisées du Disperse Red 179 et du DAPEP, ainsi que des analogues structurels qui se rapportent à leur devenir dans l'environnement. |
||||||
| i. | 16586-42-9 | Disperse Red 179 | 394,45 | 100 | 82,33 | 1,31–2,11 |
| ii. | 25176-89-0 | DAPEP | 404,32 | 82,33 | 100 | 1,41–2,08 |
| iii. | 68133-69-7 | s.o. | 438,5 | 89,76 | 78,47 | 1,96–2,32 |
| iv | 70198-17-3 | s.o. | 402,90 | 73,71 | 84,2 | 1,87–2,31 |
| v | 5261-31-4 | Disperse Orange 30 | 450,28 | < 60 | < 60 | 1,40–2,10 |
| vi. | 31482-56-1 | Disperse Orange 25 | 323,35 | < 60 | < 60 | 1,37–1,95 |
| vii | 3179-89-3 | Disperse Red 17 | 344,36 | < 60 | < 60 | 1,41–1,86 |
| viii | 16889-10-4 | Disperse Red 73 | 348,36 | < 60 | < 60 | 1,31–1,93 |
Tableau 3. Propriétés physiques et chimiques du Disperse Red 179, du DAPEP et d'analogues disponibles
| Produit chimique | Type1 | Valeur | Température (°C) |
Référence |
|---|---|---|---|---|
| 1 Les valeurs extrapolées utilisées pour le Disperse Red 179 et le DAPEP sont basées sur l'évidence sur les teintures dispersées présentées à Environnement Canada dans le cadre des Règles de notification des nouvelles substances (Produits chimiques et polymères) (ETAD, 1995) et les preuves disponibles auprès d'autres analogues de teinture dispersée trouvées dans la littérature. 2 L'expression « point de fusion » est utilisée, mais serait mieux définie par un point de décomposition, car les teintures dispersées sont connues pour se carboniser à de fortes températures (supérieures à 200 °C) au lieu de fondre. 3 La valeur inférieure du point de fusion mesurée par Peters et Gbadamosi (1992) peut provenir d'une erreur analytique ou d'une variation dans les mesures. 4 Cette valeur de point de fusion se réfère à l'isomère structurel du n° CAS25176-89-0 qui, avec le DAPEP, constitue le mélange n° CAS 78564-87-1. 5 Le point d'ébullition ne s'applique généralement pas aux teintures dispersées. Pour les teintures en poudre, la carbonisation ou la décomposition interviennent à de fortes températures au lieu de bouillir.Pour les liquides et les pâtes, l'ébullition ne se produit que pour le composant solvant, alors que le solide non évaporé se décompose ou se carbonise (ETAD, 1995). 6 La solubilité de plusieurs teintures dispersées à 25 et 80 °C a été utilisée par Baughman et Perenich (1988) pour calculer la constante de la Loi de Henry pour ces teintures. Ces valeurs sont présentées ici sous forme de plage, afin d'illustrer la constante attendue de la Loi de Henry pour le Red Disperse 179 et le DAPEP. 7 Ces valeurs ont été modélisées à l'aide de la « Méthode expérimentale d'ajustement des valeurs » de KOWWIN (2000), qui estimait le log Koe des substances d'après la valeur expérimentale du log Koe de 4,08 pour le no CAS analogue 68133-69-7 (Sijm et al., 1999). 8 Les valeurs expérimentales du log Koe ont été mesurées par Yen et al., (1989) au point de saturation de la teinture, à l'aide de la méthode d'équilibrage des lots. Cette valeur est faiblement fiable, dans la mesure où les systèmes de lots ne sont pas l'idéal pour déterminer de grands coefficients de partage (Yen et al., 1989). 9 Cette valeur expérimentale du log Koe(qui représente une estimation de limite inférieure) a été déterminée à l'aide de la méthode de brassage lent (De Bruijn et al., 1989). 10 Les valeurs du log Kco sont basées sur des calculs réalisés par Baughman et Perenich (1988) à l'aide d'une plage de solubilités mesurées pour des teintures commerciales et un point de fusion supposé de 200 °C. 11 Ces valeurs ont été modélisées à l'aide de la « Méthode expérimentale d'ajustement des valeurs » de WATERNT (2002), qui estimait la solubilité des substances dans l'eau d'après les valeurs de solubilité dans l'eau du n° CAS analogue 68133-69-7. La solubilité dans l'eau de l'analogue (0,0485 55 mg/L) est une moyenne géométrique des valeurs expérimentales de solubilité du n° CAS68133-69-7 (Sijm et al., 1999). 12 La variation de la valeur de solubilité dans l'eau s'explique par la forme polymorphe de la structure cristalline des teintures. Chaque forme morphologique possède son propre point de fusion et son enthalpie de fusion, ce qui donne une solubilité différente (Sijm et al., 1999). |
||||
| État physique | ||||
| Disperse Red 179 | Poudre | Environnement Canada, 2009a | ||
| Poudre granulaire | Sarex Overseas, 1995 | |||
| DAPEP | Poudre | Environnement Canada, 2009a | ||
| Disperse Red 153 (n° CAS 78564-87-1) | Analogue | Poudre ou granulé rougeâtre | S.M.S Technology, non daté | |
| Point de fusion2(°C) | ||||
| DAPEP | Expérimental | 219-220 | Peters et al., 1992 | |
| 177-1803 | Peters et Gbadamosi, 1992 | |||
| N° CAS inconnu (Isomère structurel du DAPEP) | Expérimental (analogue) | 181-1824 | Peters et al., 1992 | |
| N° CAS 68133-69-7 | Expérimental (analogue) | 172 | Yen et al., 1989 | |
| 167 | Sijm et al., 1999 | |||
| N° CAS 3771-31-1 | Expérimental (analogue) | 228-230 | Maradiya, 2004 | |
| N° CAS 68083-97-6 | Expérimental (analogue) | 242-243 | Maradiya, 2004 | |
| Disperse Orange 30 | Expérimental (analogue) | 126,9-128,5 | ETAD, 2005 | |
| Colorants benzothiazyles azoïques dispersés | Données déduites à partir d'analogues | 114-230 | Peters et al., 1992 | |
| 141-269 | Peters et Gbadamosi, 1992 | |||
| 119-243 | Savarino et al., 1989 | |||
| Point d'ébullition5 (°C) | ||||
| Non applicable | ||||
| Densité (kg/m3) | ||||
| Disperse Red 153 (no CAS 78564-87-1) | Non disponible | 950 | S.M.S Technology, non daté | |
| Pression de vapeur (Pa) | ||||
| Colorants azoïques dispersés | Données déduites à partir d'analogues | 5.33 × 10-12 à 5,33 × 10-5 (4 ×10-14 à 4 × 10-7 mm Hg) | 25 | Baughman et Perenich, 1988 |
| Constante de la loi de Henry (Pa·m3/mol) | ||||
| Colorants azoïques dispersés | Données déduites à partir d'analogues6 | 10-8 à 0,1 (10-13 à 10-6 atm m3/mol) | Baughman et Perenich, 1988 | |
| Log Koe(coefficient de partage octanol-eau) (sans dimensions) | ||||
| Disperse Red 179 | Modelisé7 | 5,09 | KOWWIN, 2000 | |
| DAPEP | Modelisé7 | 6,01 | KOWWIN, 2000 | |
| N° CAS68133-69-7 | Expérimental (analogue) | 4,6 (± 3,35)8 | Yen et al., 1989 | |
| 4,089 | Sijm et al., 1999 | |||
| Disperse Orange 30 | Expérimental (analogue) | 4,2 | Brown, 1992 | |
| Colorants azoïques dispersés | Données déduites à partir d'analogues | 1,79 à 5,07 | Baughman et Perenich, 1988 | |
| > 2 à 5,1 | Anliker et al., 1981; Anliker et Moser, 1987 | |||
| de 3,74 à > 5,8 | Sijm et al., 1999 | |||
| Log Koe(coefficient de partage du carbone organique) (sans dimensions) | ||||
| Colorants azoïques dispersés | Données déduites à partir d'analogues, calculé10 | 3,4 à 4,2 | Baughman et Perenich, 1988 | |
| Solubilité dans l'eau (mg/L) | ||||
| Disperse Red 179 | Modélisé11 | 0,0119 18 | WATERNT, 2002 | |
| DAPEP | Modélisé11 | 0,004 2083 | WATERNT, 2002 | |
| N° CAS 68133-69-7 | Expérimental (analogue) | 0,021 ± 0,004 0,690 ± 0,17012 | Sijm et al., 1999 | |
| 0,0079 ± 0,0014 | Yen et al., 1989 | |||
| Colorants azoïques dispersés | Données déduites à partir d'analogues | < 0,01 | Anliker et Moser, 1987 | |
| 1,19 × 10-5 à 35,46 | Baughman et Perenich, 1988 | |||
| Solubilité dans le n-octanol (mg/L) | ||||
| N° CAS 68133-69-7 | Expérimental (analogue) | 66 ± 6 | Sijm et al., 1999 | |
| Colorants azoïques dispersés | Données déduites à partir d'analogues | 81 à 2 430 | 20 | Anliker et Moser, 1987 |
| 14,1 à 3 000 | 20 | Sijm et al., 1999 | ||
| pKa (constante de dissociation d'acide) (sans dimensions) | ||||
| Disperse Red 179 | Modélisé | 1,9 | ACD/pKa DB, 2005 | |
| DAPEP | Modélisé | 2,05 | ACD/pKa DB, 2005 | |
Le Disperse Red 179 et le DAPEP ne sont pas naturellement produits dans l'environnement.
Des informations récentes ont été recueillies dans des études sur le domaine menées pendant les années 2005 et 2006 dans le cadre des avis de la Gazette du Canadapubliés en application de l'article 71 de la LCPE (1999) (Canada, 2006b, 2008). Ces avis réclamaient des données sur la fabrication canadienne et les quantités des substances importées au Canada. Dans l'avis de 2006, on demandait également de fournir des données sur les quantités de Disperse Red 179 et de DAPEP utilisées.
En réponse à l'avis en application de l’article 71 de la LCPE (1999) pour l'année civile 2006, aucune fabrication de Disperse Red 179 ou de DAPEP n'a été signalée au-delà du seuil de 100 kg/an. Toutefois, une seule entreprise signalait l'importation de 400 kg de Disperse Red 179 et 100 kg de DAPEP au Canada en 2006 (le pays exportateur n'a pas été identifié) (Environnement Canada, 2009a). De plus, quatre entreprises ont déclaré avoir utilisé 400 kg de Disperse Red 179 en 2006, tandis que quatre autres entreprises ont déclaré avoir utilisé 180 kg de DAPEP en 2006. La quantité plus importante de 180 kg/an de DAPEP par rapport à la quantité importée de 100 kg pour l'année 2006 est vraisemblablement due à des stocks inutilisés des années précédentes.
Deux autres intervenants ont aussi indiqué un intérêt pour ces substances.
Les informations reçues en réponse à l'avis en application de l’article 71 de la LCPE (1999) pour l'année civile 2005 déterminaient qu'entre 100 et 1000 kg de Disperse Red 179 étaient commercialisés au Canada (Environnement Canada, 2006).Aucun rapport de fabrication ou d'importation de DAPEP au Canada, supérieure ou égale au seuil de 100 kg au cours de l'année civile 2005 n'a été reçu en réponse au même avis (Environnement Canada, 2006).Toutefois, une partie prenante a été identifiée comme ayant un intérêt pour ces substances.
Les quantités signalées dans la Liste intérieure des substances (LIS) comme fabriquée, importée ou commercialisée au Canada au cours de l'année civile 1986 pour le Disperse Red 179 se situaient entre 1 000 et 10 000 kg. Les quantités signalées dans la LIS comme fabriquées, importées ou commercialisées au Canada au cours de l'année civile 1986 pour le DAPEP se situaient entre 100 et 1 000 kg.
La production de Disperse Red 179 aux États-Unis a été estimée entre 10 000 et 500 000 livres au cours de chacune des années suivantes : 1986, 1990, 1994 et 1998 (US EPA, 2009). Toutefois, aucune quantité n'a été signalée pour 2002 (US EPA, 2009).Le DAPEP n'a pas été produit aux États-Unis pendant cette période (US EPA, 2009).
Les informations sur les utilisations au cours des années civiles 2005 et 2006 ont été rassemblées en réponse à l'avis en application de l’article 71 de la LCPE (1999) (Canada, 2006b, 2008).
En 2006, l'entreprise qui importe le Disperse Red 179 et le DAPEP a identifié son activité comme « Distributeur en gros de produits chimiques et produits associés (sauf agricoles) ». Le Disperse Red 179 est signalé comme étant utilisé comme teinture dans le colorant chimique Foron Rubine RD-S, alors que le DAPEP est utilisé dans le colorant chimique Foron Scarlet RD-S (Environnement Canada, 2009a).Le Disperse Red 179 a été signalé dans le commerce au Canada en 2005, dans le même groupe d'activités appelé « Distributeur en gros de produits chimiques (sauf agricoles) et de produits associés » (Environnement Canada, 2006).
Les codes LIS d'utilisation suivants ont été identifiés pour le Disperse Red 179 pendant la dénomination LIS (1984-1986) : « Colorant - pigment/teinture/colorant/encre » et « Textile, Produit ». Seul le code d'utilisation de LIS « Colorant - pigment/teinture/colorant/encre » a été identifié pour le DAPEP.
Une analyse de l'information technique disponible révèle que le Disperse Red 179 et le DAPEP sont utilisés comme teinture rouge dans la fabrication de textiles (Environnement Canada, 2009a). . Le Disperse Red 179 et le DAPEP peuvent être utilisés comme agents de teinture pour les fibres synthétiques comme le polyester et le nylon dans les vêtements et les textiles domestiques (CII 2002– ; Choi et al.,2007; Environnement Canada, 2009a).
Selon les informations reçues en réponse à l'avis en application de l’article 71 de la LCPE (1999), pour l'année 2006, le rejet direct le plus important de colorant dans l'environnement a lieu dans l'industrie textile après le processus de teinture, lorsque le colorant non fixé est éliminé des fibres et rejeté avec les eaux usées.La plupart des usines textiles au Canada rejettent leurs eaux usées vers des stations de traitement avec des capacités primaires ou secondaires, soit municipales, soit situées sur leurs installations (Environnement Canada, 2009a).
Débit massique
Pour estimer les rejets potentiels de substances dans l'environnement à différent stades de leur cycle de vie, un débitmètre massique a été développé (Environnement Canada, 2009b). Les données empiriques sur les rejets de substances particulières dans l'environnement sont rarement disponibles.En conséquence, pour chaque type d'utilisation identifié pour la substance, la proportion et la quantité rejetée vers les divers milieux naturels sont estimées, comme c'est le cas pour la proportion de substance chimiquement transformée ou envoyée pour l'élimination des déchets.À moins que des informations particulières sur le taux ou le potentiel de rejet de la substance issue de décharges et d'incinérateurs soient disponibles, le débitmètre massique ne prend pas en compte quantitativement les rejets hors site vers l'environnement, issus de sites d'élimination des déchets.
Les hypothèses et les paramètres d'entrée utilisés dans les estimations de rejet sont basés sur des informations tirées d'un certain nombre de sources, comprenant des réponses aux études règlementaires, de Statistique Canada, des sites Internet de fabricants, de bases de données et de documents techniques et d'informations et d'hypothèses professionnelles. Sont particulièrement pertinents les facteurs d'émission, qui sont généralement exprimés en fraction d'une substance rejetée dans l'environnement, notamment pendant sa fabrication, son traitement et l'utilisation associée avec des processus industriels.Les sources de ces informations comprennent des documents de scenarios d'émission, souvent développés sous les auspices de l'organisation de coopération et de développement économiques (OCDE), et les hypothèses par défaut utilisées par différents organismes internationaux de règlementation des produits chimiques.On note que le niveau d'incertitude pour la masse de substance et la quantité rejetée dans l'environnement augmentent généralement vers la fin de son cycle de vie.
Tableau 4. Rejets et pertes estimés de Disperse Red 179 et de DAPEP dans les milieux naturels, transformation de produits chimiques pendant le cycle de vie et transfert vers des sites d'élimination des déchets, d'après le débitmètre massique
| Devenir | Proportion de la masse (%)1 | Principal stade du cycle de vie impliqué2 | |
|---|---|---|---|
| 1 Pour chaque substance, les informations issues des documents suivants de l'OCDE sur les scénarios d'émission ont été utilisées pour estimer les rejets dans l'environnement et la répartition de la substance, tel qu'il est résumé dans ce tableau : Formulation d'adhésifs (OCDE, 2004) et usines textiles de fabrication de laine (OCDE, 2007). Les hypothèses spécifiques utilisées dans le calcul de ces estimations sont résumées dans Environnement Canada (2009c) et dans Environnement Canada (2009d). 2 Stade(s) applicable(s) : production, formulation, usage industriel, usage domestique, durée de vie de l'article/produit, élimination des déchets. 3 Eaux usées avant toute forme de traitement sur site industriel ou hors site municipal. |
|||
| Rejeté vers des milieux récepteurs : | |||
| Vers le sol | 0 | Cycle de vie entier | |
| Dans l'air | 0 | Cycle de vie entier | |
| Vers les eaux usées3 | 17,1 | Fabrication de produits, usage domestique | |
| Chimiquement transformés (incinération) | 2,5 | Élimination des déchets | |
| Transférés vers des sites d'élimination des déchets (par exemple, décharge, incinération) | 80,5 | Élimination des déchets | |
D'après les informations de Statistique Canada et une analyse faite conjointement par Environnement Canada et Industrie Canada, il est reconnu que des colorants peuvent être importés dans des articles manufacturés. En suivant la proposition de Statistique Canada, un ratio de 30:70 (textiles manufacturés au Canada contre ceux importés) a été utilisé pour estimer la quantité de colorant importé en produits colorés (Environnement Canada, 2009a).La quantité importée de 400 kg pour le Disperse Red 179 et la quantité utilisée de 180 kg pour le DAPEP pour l'année 2006 ont été incluses dans les calculs de l'outil de débit massique, lesquels ont donné des quantités totales approximatives de 1 128 kg et 508 kg, respectivement, pour le Disperse Red 179 et le DAPEP commercialisés au Canada.
Les résultats indiquent que le Disperse Red 179 et le DAPEP peuvent se trouver en grandes quantités dans des sites d'élimination de déchets (80,5 % ou 908 kg/an de Disperse Red 179 et 408 kg/an de DAPEP), en raison du rejet éventuel d'articles fabriqués qui en contiennent. Une petite fraction des déchets solides est incinérée, ce qui peut engendrer la transformation chimique de la substance.Surtout d'après les informations contenues dans les documents de scénarios d'émission de l'OCDE pour le traitement et les usages associés avec ce type de substance (OCDE, 2004, 2007), on estime que 17,1 % (192 kg/an de Disperse Red 179 et 87 kg/an de DAPEP) peuvent être rejetés dans les eaux usées, provenant principalement d'activités associées à leur usage industriel (7,9 %), mais également de la durée de vie de produits contenant les substances, comme les rejets associés à la blanchisserie (9,2 %). Bien que ces teintures ne soient pas prises en considération dans l'outil de débit massique, il convient de noter qu'elles peuvent être épandues sur des sols agricoles et des pâturages au Canada du fait de leur présence dans les boues activées de l'épuration des eaux usées qui sont utilisées couramment pour enrichir le sol. La perte potentielle dans les eaux souterraines issue de la partie des substances qui parviennent à s'introduire dans des sites d'enfouissement (par l'élimination d'articles manufacturés) devrait être limitée. Pour l'évaluation écologique, l'environnement aquatique est considéré comme le milieu critique (d'après les rejets des usines de traitement des eaux usées).
Bien qu'une part importante des substances finisse dans des sites d'enfouissement (par l'élimination d'articles manufacturés), à partir desquels peut exister une fuite potentielle vers la nappe phréatique, le milieu aquatique est considéré comme milieu critique, puisque ni le Disperse Red 179, ni le DAPEP ne seront liés à une matière quelconque et tous deux auront par conséquent la possibilité d'être plus biodisponibles.
Comme l'indiquent les résultats du débitmètre massique (tableau 4), les substances Disperse Red 179 et DAPEP sont supposées être rejetées dans les effluents d'eaux usées au cours de processus industriels et d'usages domestiques (Environnement Canada, 2009c, 2009d). Les valeurs élevées du log Koe (analogues 4,08 à 4,6, données déduites à partir d'analogues > 4 et valeurs modélisées 5,09 à 6,01) et du log Kco (données déduites à partir d'analogues 3,4 à 4,2) (voir le tableau 2) indiquent que ces substances peuvent avoir une affinité pour les solides.Toutefois, le log Kco est une valeur calculée (voir la note de bas de page 3 au-dessous du tableau 2) pour les colorants azoïques dispersés sans groupe benzothiazyle fonctionnel et le potentiel d'adsorption des structures particulaires solides de colorants n'est généralement pas bien compris.Par conséquent, le degré de ce comportement particulier pour les deux substances évaluées est incertain.
Le Disperse Red 179 et le DAPEP ne se biodégradent pas rapidement en conditions aérobies (voir le tableau 5). Le Disperse Red 179 et le DAPEP sont utilisés sous forme de poudres avec une solubilité limitée dans l'eau (voir le tableau 2).En solution, le Disperse Red 179 et le DAPEP se comportent comme des bases, avec un très faible pKa estimé (respectivement 2,05 et 1,9; voir le tableau 2).Par conséquent les formes dissoutes de l'une ou l'autre substance ne devraient pas s'ioniser dans l'eau à des pH correspondant au milieu naturel (6 à 8 pour les eaux de surface). En raison de leur faible solubilité, ces substances devraient se comporter comme des dispersions colloïdales lorsqu'elles sont rejetées dans l'eau (Yen et al., 1991). On les trouvera par conséquent principalement sous forme solide ou adsorbée sur des particules en suspension et éventuellement enfoncées dans les sédiments du fond, où elles devraient rester sous une forme relativement indisponible biologiquement. Yen et al., (1989) ont conclu que les colorants dispersés ont tendance à s'accumuler en abondance dans les sédiments et les biotes, à moins qu'ils ne soient dégradés à des vitesses comparables à leur assimilation. Selon Razo-Flores et al. (1997), les colorants azoïques finissent par se retrouver dans des sédiments anaérobies, dans des aquifères ou dans les eaux souterraines en raison de leur nature récalcitrante dans le milieu anaérobie Yen et al., (1991) ont observé qu'un analogue azoïque benzothiazyle était transformé en conditions anaérobies dans les sédiments par hydrolyse et réduction, et ont conclu que la plupart des colorants azoïques ne persistent probablement pas dans les systèmes sédimentaires anaérobies.
La vitesse de volatilisation à partir de la surface de l'eau est proportionnelle à la constante de la loi de Henry (Baughman et Perenich, 1988). Baughman et Perenich (1988) précisent également que la volatilisation à partir de systèmes aquatiques ne représente pas un processus de perte important pour les colorants dispersés. Cette déclaration est conforme aux valeurs faibles à négligeables déduites à partir d'analogues de la constante de la loi de Henry (10-8 à 0,1 Pa·m3/mol, tableau 3), ainsi qu'à la faible pression de vapeur analogue (5,33 × 10-12 à 5,33 x 10-5, tableau 3). D'après ces données d'analogue et de données déduites à partir d'analogues pour les colorants azoïques dispersés, le transport dans l'air dû à la perte de cette substance issue de la surface de sols humides et secs ne devrait pas être important.Ces données sont cohérentes avec l'état physique (structure particulaire solide) du Disperse Red 179 et du DAPEP; cet état n'en fait probablement pas des candidats à la volatilisation.
Persistance dans l'environnement
Aucune donnée de surveillance environnementale ayant trait à la présence de Disperse Red 179 ou de DAPEP dans l’environnement canadien (air, eau, sol et sédiments) n'a été relevée.
Selon L'Association écologique et toxicologique des fabricants de colorants et de pigments organiques, les colorants sont, avec quelques exceptions, considérés essentiellement comme non biodégradables en conditions aérobies (ETAD, 1995). Une évaluation répétée de la biodégradabilité prête et inhérente à l'aide de tests de dépistage acceptés (voir les directives de l'OCDE pour les tests sur les produits chimiques) a confirmé cette hypothèse (Pagga et Brown, 1986; ETAD, 1992).D'après la structure chimique du Disperse Red 179 et du DAPEP, il n'existe aucune raison de soupçonner que la biodégradation sera différente de celle décrite en général pour les colorants (ETAD, 1995).
Certains colorants azoïques dispersés, comprenant les composés benzothiazyles, se sont révélés subir une dégradation anaérobie relativement rapide dans les sédiments en profondeur, où les conditions anoxiques prévalent (Yen et al., 1991; Baughman et Weber, 1994; Weber et Adams, 1995). Les colorants dispersés pénètrent le système aquatique principalement sous forme de dispersion de fines particules en suspension et s'installent éventuellement dans les couches aérobies des sédiments de surface, où ils vont persister jusqu'à ce que l'enfouissement des sédiments crée des conditions de réduction.La vitesse de dépôt des sédiments et l'importance de la bioturbation varient d'un site à l'autre et il est donc très difficile d'établir le temps de séjour des colorants dans les couches de sédiments aérobies.Il est toutefois probable que dans de nombreux cas il soit supérieur à 365 jours.Une fois sous conditions anaérobies ou de réduction, les colorants azoïques peuvent subir une dégradation rapide en constituants amines aromatiques substitués, comme l'ont démontré Yen et al., (1991) qui ont mesuré les valeurs de demi-vie de réduction dans des sédiments compactés à température ambiante, de 1,9 à 2,0 jours pour un colorant azoïque benzothiazyle (n° CAS 68133-69-7).Toutefois, la plupart des organismes aquatiques ne devraient pas être exposés à ces produits de transformation après biodégradation dans les sédiments anoxiques profonds, en partie parce que le contact avec les sédiments anoxiques est susceptible d'être limité et en partie parce que les produits de dégradation d'amines devraient être étroitement liés aux sédiments et avoir, par conséquent, une très faible biodisponibilité (Weber et al., 2001; Colon et al., 2002).Par conséquent, les produits de dégradation ne présentent probablement pas de problème écologique.
Des données empiriques de biodégradation ont été soumises par le secteur en réponse à l'avis en application de l’article 71 de la LCPE (1999), pour l'année civile 2006 (Environnement Canada, 2009a).Des études inhérentes de biodégradabilité qui ont évalué la biodégradabilité aérobie dans un milieu aquaux de Foron Rubin RD-S (produit commercial contenant du n° CAS16586-42-8) et du Disperse Red 153 (produit commercial contenant du n° CAS 25176-89-0) ont déterminé qu'aucun composé n'était biodégradable (BMG, 2001, 2003a). Ces tests ont été effectués conformément aux directives de l'OCDE pour les tests sur les produits chimiques, test n° 302B-1992, « Biodégradabilité inhérente : Test de Zahn-Wellens/EMPA. » Bien que le protocole utilisé pour ces deux études était acceptable, subsiste un manque général d'information sur les substances utilisées pour chaque test. La solubilité des composés testés n'est signalée dans aucune étude.Dans la première étude, ni la proportion de Disperse Red 179 (n° CAS 16586-42-8) dans le produit Foron Rubin RD-S du commerce, ni les autres composants de ce produit du commerce n'ont été signalés.Dans la deuxième étude, la proportion de DAPEP présent dans le Disperse Red 153 (n° CAS78564-87-1), qui est en fait un mélange de DAPEP et d'un autre isomère structurel (Nakagawa, 1996; CII 2002- ), n'est pas indiquée.
L'absence de dégradation pourrait s'expliquer par l'inhibition bactérienne provoquée par la toxicité du Disperse Red 179 et du DAPEP. Toutefois, des études sur les essais d'inhibition de la respiration effectuées sur les mêmes composés selon les Lignes directrices de l'OCDE pour les essais de produits chimiques, n° 209-1984, ont déterminé que les boues activées ne montraient aucun effet toxique important de l'une ou l'autre substance soumise à ces essais (BMG, 2000a, 2003b). La CE20 et la CE80 pour le Foron Rubin RD-S (n° CAS 16586-42-8) et le Disperse Red 153 (qui contient du n° CAS 25176-89-0) ont été estimés comme étant respectivement supérieurs à 1 000 mg/L et 4 000 mg/L (BMG, 2000a, 2003b).D'après ces informations supplémentaires, les deux études inhérentes de biodégradabilité sont estimées acceptables, malgré le manque de clarté concernant la composition des substances test (voir l'annexe 1).
Le tableau 5a présente les données empiriques de biodégradation (BMG, 2001, 2003a) qui ne montre aucune biodégradation sur 28 jours dans un test inhérent de biodégradation pour le Foron Rubin RD-S et le Disperse Red 153. Ces essais indiquent que la demi-vie dans un milieu aqueux oxique sera probablement supérieure à 182 jours (6 mois) et que, par conséquent, les substances seront probablement persistantes dans des conditions aérobies dans ce milieu environnemental.
Tableau 5a. Données empiriques de dégradabilité inhérente pour le Disperse Red 179 et le DAPEP
| Substance | Milieu | Processus du devenir | Valeur de dégradation | Résultat de dégradation/ unités | Référence |
|---|---|---|---|---|---|
| Foron Rubin RD-S (Disperse Red 179) |
Eau/ boues activées |
Biodégradation | 0 | Biodégradation à 28 jours/% | BMG, 2003a |
| Disperse Red 153 (DAPEP) |
Eau/ boues activées |
Biodégradation | 0 | Biodégradation à 28 jours/% | BMG, 2001 |
Alors que peu de données expérimentales sur la dégradation du Disperse Red 179 et du DAPEP sont disponiblese, une méthode RQSA basée sur le poids de la preuve a également été appliquée à l'aide des modèles de dégradation indiqués au tableau 5b. Bien que le rejet du Disperse Red 179 et du DAPEP doive se faire vers les eaux usées, leur temps de séjour dans la colonne d'eau, dû à leur faible solubilité et leur comportement comme dispersions colloïdales, peut être court avant qu'ils ne s'enfouissent dans les sédiments. Cependant, compte tenu du manque de données à ce sujet, la persistance dans l'eau a été examinée à l'aide de modèles de prévision RQSA sur la biodégradation.L'analyse suivante s'applique principalement à la portion de cette substance qui est présente dans l'environnement sous forme dissoute, en reconnaissant qu'une proportion importante pourrait probablement exister sous forme dispersée de particules solides. Le tableau 5b résume les résultats des modèles RQSA disponibles sur la dégradation dans l'eau du Disperse Red 179 et du DAPEP.
Tableau 5b. Données modélisées de dégradation du Disperse Red 179 et du DAPEP
| Processus du devenir | Modèle et base du modèle | Substance | Résultat et prévision du modèle | Demi-vie extrapolée (jours) |
|---|---|---|---|---|
| 1 Le résultat est une valeur numérique. 2 Le résultat est un pourcentage de probabilité. |
||||
| Eau | ||||
| Biodégradation (aérobie) | BIOWIN, 2000 Sous-modèle 3 : Étude d'expert (biodégradation ultime) |
Disperse Red 179 | 1,4451 « se biodégrade très lentement » |
> 182 |
| DAPEP | 1,25491 « se biodégrade très lentement » |
> 182 | ||
| Biodégradation (aérobie) | BIOWIN, 2000 Sous-modèle 5 : Probabilité linéaire du MITI |
Disperse Red 179 | -0,46862 « se biodégrade très lentement » |
> 182 |
| DAPEP | -0,33952 « se biodégrade très lentement » |
> 182 | ||
| Biodégradation (aérobie) | BIOWIN, 2000 Sous-modèle 6 : Probabilité non linéaire du MITI |
Disperse Red 179 | 02 « se biodégrade très lentement » |
> 182 |
| DAPEP | 02 « se biodégrade très lentement » |
> 182 | ||
| Biodégradation (aérobie) | TOPKAT, 2004 Probabilité |
Disperse Red 179 | 0.02 « se biodégrade très lentement » |
> 182 |
| DAPEP | « se biodégrade très lentement » | > 182 | ||
| Biodégradation (aérobie) | CATABOL, 2008 % DBO (demande biologique en oxygène) |
Disperse Red 179 | % DBO = 3,3 « Se biodégrade très lentement » |
> 182 |
| DAPEP | % DBO = 3,1 « Se biodégrade très lentement » |
> 182 | ||
Les résultats du tableau 5b montrent que les deux modèles de probabilité BIOWIN (5 et 6) indiquent que ces substances se biodégradent lentement et que leur demi-vie dans l'eau serait supérieure à 182 jours. En fait, les résultats de probabilité des deux modèles sont bien inférieurs à 0,3, ce qui est la limite suggérée par Aronson et al., (2006) pour identifier des substances comme ayant une demi-vie > 60 jours (d'après les modèles de probabilité du MITI). Le résultat du modèle de dégradation ultime (BIOWIN 3), à savoir « se biodégrade très lentement », pourrait signifier 180 à 240 jours (US EPA, 2002a; Aronson et al., 2006). La conclusion générale de BIOWIN (2000) est que ces substances ne sont pas facilement biodégradables.
D'autres modèles récents de dégradation (CATABOL et TOPKAT) prévoient que le Disperse Red 179 et le DAPEP ne subissent pas de minéralisation dans une période de 28 jours, avec une probabilité ou une importance de biodégradation dans les limites des produits chimiques très persistants. Le TOPKAT, qui simule le test de biodégradation sur 28 jours du MITI japonais, a produit une probabilité de 0 pour les deux substances. Ce résultat est bien inférieur au seuil suggéré pour les substances persistantes dans ce modèle (< 0,3) (0,7 est la limite suggérée pour les produits chimiques non persistants) (TOPKAT, 2004). CATABOL ne prévoyait qu'un taux de biodégradation de 3,3 % et 3,1 % pour le Disperse Red 179 et le DAPEP, respectivement, d'après l'essai sur la biodégradation immédiate de l'OCDE 301 (% DBO). Ceci a été suggéré comme signifiant « probablement persistant » (Aronson et Howard, 1999) et ayant une demi-vie dans l'eau > 182 jours. Les valeurs modélisées dans le tableau 5b sont jugées fiables, comme leurs ensembles d'étalonnage contiennent plusieurs substances chimiques ayant une structure comparable.
Lorsque les résultats des tests empiriques de dégradation inhérente, ainsi que les modèles de prévisions, sont pris en compte ensemble, il existe un consensus suggérant que la demi-vie de dégradation ultime dans l'eau est > 182 jours, ce qui est cohérent avec ce à quoi on pourrait s'attendre pour les produits chimiques utilisés comme colorants dispersés (c.-à-d. fabriqués pour être relativement insolubles et durables). En utilisant un ratio de 1:1:4 pour l'extrapolation des demi-vies eau:sol:sédiment (Boethling et al., 1995), la demi-vie dans le sol est également > 182 jours et la demi-vie dans les sédiments oxiques est > 365 jours.
D'après les résultats des données expérimentales, la modélisation prédictive et l'avis des experts (ETAD, 2005), le Disperse Red 179 et le DAPEP répondent aux critères de persistance dans l'eau et le sol (demi-vies dans le sol et l'eau = 182 jours et demi-vie dans les sédiments = 365 jours), comme énoncés dans le Règlement sur la persistance et la bioaccumulation (Canada, 2000).
Potentiel de bioaccumulation
Aucune donnée de facteur expérimental de bioaccumulation (FBA) et/ou de facteur de bioconcentration (FBC) pour le Disperse Red 179 ou le DAPEP n'étaient disponibles; par conséquent, des données empiriques de tests de bioconcentration pour les poissons utilisant la substance analogue Disperse Orange 30 (Shen et Hu, 2008) ont été utilisées pour déterminer le potentiel de bioaccumulation des substances sujettes à cette évaluation.
La structure chimique et le poids moléculaire du Disperse Orange 30 sont similaires à ceux du DAPEP et particulièrement du Disperse Red 179, avec les plus grandes différences étant que le Disperse Orange 30 possède un groupe ester, mais ne possède pas de groupe fonctionnel benzothiazyle. La biodisponibilité de la plupart des colorants dispersés est généralement jugée très faible (et celle-ci limite le potentiel de bioaccumulation). Néanmoins, compte tenu des considérations structurelles uniquement, il est possible que le potentiel de bioaccumulation du DAPEP soit légèrement supérieur au potentiel de bioaccumulation du Disperse Red 179 en raison de la présence des deux atomes de chlore sur son groupe benzothiazyle.
Une étude de bioconcentration du Disperse Orange 30 a révélé qu'il est peu susceptible de s'accumuler dans les poissons (Shen et Hu, 2008). Cette étude a été effectuée conformément aux directives de l'OCDE pour les tests sur les produits chimiques, test n° 305B-1996, Bioconcentration : test semi-statique sur les poissons. La bioconcentration du Disperse Orange 30 chez le poisson zèbre (Brachydanio rerio) a été déterminée par un test semi-statique sur 28 jours, avec renouvellement du milieu de test tous les deux jours.Un test d'exposition à une concentration nominale de 20 mg/L (concentration moyenne mesurée de 0,028 ~ 0,28 mg/L) a été réalisé (conformément au résultat d'un test de toxicité aiguë sur les poissons), dans le but de vérifier le potentiel de bioconcentration de la substance testée.Des échantillons des deux solutions de test et des organismes d'essai ont été pris du 26e jour au 28e jour de la période de test d'exposition sur 28 jours.Les échantillons ont été préparés en extrayant le composant lipidique des poissons testés.La concentration mesurée de la substance de test, le contenu lipidique des poissons et le calcul du facteur de bioconcentration sont rapportés dans le tableau 6a.
Tableau 6a. Concentration mesurée du Disperse Orange 30, contenu lipidique des poissons et calcul du facteur de bioconcentration
| Traitements(20 mg/L) | Durée d'échantillonnage | ||
|---|---|---|---|
| 26e jour | 27e jour | 28e jour | |
| Concentration mesurée de la substance de test dans les solutions extraites (mg/L) | < 0,028 | < 0,028 | < 0,028 |
| Contenu de la substance test dans les lipides du poisson (mg) | < 1,68 | < 1,68 | < 1,68 |
| Poids total du poisson (g) | 2,07 | 2,13 | 2,53 |
| Concentration de la substance test dans le Cp du poisson (mg/kg) | < 0,81 | < 0,79 | < 0,66 |
| Concentration mesurée de la substance test dans le Ce de l'eau (mg/L) | 0,028 ~ 0,28 | 0,028 ~ 0,28 | 0,028 ~ 0,28 |
| Contenu lipidique du poisson (%) | 0,81 | 0,57 | 1,25 |
| Facteur de bioconcentration | < 100 | < 100 | < 100 |
| Facteur de bioconcentration moyen | < 100 | ||
L'étude de Shen et Hu (2008) a été révisée et considérée comme acceptable (voir l'annexe 1). Le manque de détection dans les extraits de poissons (< 0,028 mg/L) suggère une solubilité limitée dans les lipides et/ou un potentiel limité de partage dans les tissus des poissons des systèmes aqueux (plus probablement les deux).Toutefois, il existe une incertitude associée aux valeurs limites dans toute étude, car la « vraie » valeur n'est pas connue.
Étant donné la structure de la substance et le comportement probable de cette classe de colorants dispersés dans les systèmes aqueux, un faible résultat de facteur de bioconcentration est probable. La plupart des colorants dispersés, comme leur nom l'indique, existent sous forme de particules susceptibles de dispersion, avec des fractions vraiment solubles limitées.La solubilité peut toutefois être augmentée en ajoutant des groupements fonctionnels polaires à la molécule. Le Disperse Orange 30 contient certains de ces groupes de solubilisation (nitreux) et l'on peut donc s'attendre à un certain degré de solubilité dans l'eau. En supposant que la concentration de la solution dans l'essai était égale à la plus faible valeur de l'hydrosolubilité, soit 0,028 mg/L, et en utilisant une concentration dans les poissons de 0,81 mg/kg comme une estimation de la pire éventualité, le FBC pourrait être calculé comme inférieur à 100.
L'étude ci-dessus sert de première preuve pour soutenir le manque de potentiel de bioaccumulation du Disperse Red 179 et du DAPEP et d'autres recherches soutiennent cette conclusion. Anliker et al., (1981) ont signalé des valeurs expérimentales de bioaccumulation chez les poissons pour 18 colorants mono azoïques dispersés, obtenues selon les méthodes de test spécifiées par le ministère japonais du commerce international et de l'industrie (MITI). Exprimé en fonction du poids du corps humide des poissons, ces facteurs log de bioaccumulation allaient de 0,00 à 1,76 (Anliker et al., 1981).Les numéros de registre des produits chimiques et les structures chimiques n'ont pas été signalés dans cette étude et limitent par conséquent l'utilité de cette étude pour les besoins de données déduites à partir d'analogues liés au Disperse Red 179 et au DAPEP. Toutefois, les études de suivi, qui fournissaient les structures chimiques pour les colorants dispersés testés, ont confirmé un faible potentiel de bioaccumulation pour 10 colorants nitroazoïques, avec des facteurs logarithmiques de bioaccumulation allant de 0,3 à 1,76 (Anliker et Moser, 1987; Anliker et al., 1988). Des études disponibles du MITI soutiennent également un faible potentiel de bioaccumulation pour les colorants azoïques dispersés.Les FBC déclarés pour trois colorants azoïques dispersés (nos CAS40690-89-9, 61968-52-3 et 71767-67-4) testés à une concentration de 0,01 mg/L variaient de moins de 0,3 à 47 (MITI, 1992).Une étude d'accumulation effectuée par Brown (1987) a également montré qu'aucun des 12 colorants dispersés testés ne s'accumulait pendant une étude sur huit semaines sur des carpes.
Bien que l'on prévoie que le manque de biodisponibilité importante dans l'eau et les aliments atténue fortement le potentiel d'assimilation de la plupart des colorants dispersés, le log Koe empirique pour un analogue proche, basé sur les données de Sijm et al. (1999), suggère que le Disperse Red 179 et le DAPEP pourraient être solubles dans les lipides, si les conditions environnementales favorisent la biodisponibilité de ces substances pour les poissons.
Des valeurs corrigées du log Koe, soit 5,09 et 6,01, ont été estimées pour le Disperse Red 179 et le DAPEP à partir de la valeur connue et acceptable du log Koe de 4,08 (Sijm et al., 1999) pour l'analogue proche portant le n° CAS 68133-69-7, en utilisant la méthode d'ajustement de la valeur expérimentale de KOWWIN (2000). Dans la méthode EVA, l'estimation commence avec le log Koeexpérimental du composé similaire.La structure similaire est ensuite modifiée en soustrayant et en ajoutant des fragments pour « construire » le composé estimé.L'estimation devient ensuite la somme de la valeur expérimentale et la valeur des modifications du fragment.
Dès lors, une valeur de log Koe de 4,08 pour l'analogue n° CAS 68133-69-7 et les valeurs corrigées élevées du log Koe de 5,09 et 6,01 pour le Disperse Red 179 et le DAPEP, respectivement (tableau 2), sont les deux seuls renseignements qui indiquent que ces substances peuvent présenter un potentiel de bioaccumulation important. Malgré leurs valeurs élevées de log Koe, il manque la preuve de la bioaccumulation des colorants azoïques dispersés (Anliker et al., 1981; Anliker et Moser, 1987; MITI, 1992). Les auteurs ayant trouvé de fortes valeurs de log Koe et de faibles facteurs concomitants de bioaccumulation pour les colorants azoïques dispersés suggèrent que les faibles facteurs d'accumulation peuvent être dus dans certains cas à la faible liposolubilité absolue de ces substances (Brown, 1987) ou à leur poids moléculaire relativement élevé (généralement de 450 à 550 g/mol). Une faible liposolubilité et un poids moléculaire élevé rendent difficile le transport dans les membranes des poissons (Anliker et al., 1981; Anliker et Moser, 1987). Il est également probable que le manque de biodisponibilité et la capacité de partage limitée dans des conditions de tests de facteur de bioconcentration, ainsi que dans la dégradation métabolique in vivo, limitent l'accumulation dans les lipides des poissons.
Il a été établi par l'ETAD (1995) que les caractéristiques moléculaires indiquant l'absence de bioaccumulation sont un poids moléculaire > 450 g/mol et un diamètre transversal > 1,05 nm. Des recherches récentes effectuées par Dimitrov et al. (2002), Dimitrov et al., (2005) et le BBM (2008) suggèrent que la probabilité qu'une molécule traverse les membranes cellulaires par diffusion passive diminue de façon importante, alors que le diamètre transversal maximum (Dmax) augmente. La probabilité d'une diffusion passive décroît sensiblement lorsque le diamètre transversal est supérieur à ~1,5 nm et diminue de façon plus importante lorsque les molécules ont un diamètre transversal > 1,7 nm. Sakuratani et al., (2008) ont également étudié l'effet du diamètre transversal sur la diffusion passive dans une série de tests sur environ 1 200 produits chimiques nouveaux et existants. Ils ont observé que les substances qui n'ont pas un potentiel de bioconcentration très élevé ont souvent un Dmax > 2,0 nm et un diamètre effectif (Deff) > 1,1 nm.
Le Disperse Red 179 et le DAPEP ont un poids moléculaire de 394,45 et 404,32 g/mol, respectivement (voir le tableau 1), et leurs structures moléculaires sont relativement peu compliquées. Ces deux caractéristiques indiquent une certaine capacité de bioaccumulation de ces substances. Il n'existe aucune relation claire qui permette d'établir des seuils stricts de taille moléculaire pour l'évaluation du potentiel de bioaccumulation; toutefois, une réduction de la vitesse d'absorption peut être associée à l'augmentation du diamètre transversal, comme l'ont démontré Dimitrov et al. (2002, 2005). Le diamètre maximal du Disperse Red 179 et du DAPEP (et leurs conformères) varie de 1,3 à 2,108 nm et de 1,414 à 2,075 nm, respectivement (BBM, 2008), ce qui indiquerait qu'en ce qui concerne ce colorant, il y a une possibilité de réduction importante du taux d'absorption dans l'eau et de la biodisponibilité in vivo.
D'après un manque d'accumulation dans les essais de bioconcentration sur la substance analogue Disperse Orange 30 et d'autres colorants azoïques dispersés correspondants, ainsi que les grandes tailles moléculaires du Disperse Red 179 et du DAPEP, ces substances devraient avoir un faible potentiel de bioaccumulation. Par conséquent, le Disperse Red 179 et le DAPEP ne répondent pas aux critères de bioaccumulation (FBC ou FBA = 5 000, énoncés dans le Règlement sur la persistance et la bioaccumulation (Canada, 2000).
Évaluation des effets écologiques
A – Dans le milieu aquatique
Peu de données empiriques sur l'écotoxicité ont été identifiées pour le Disperse Red 179 ou le DAPEP. Des études sur la toxicité aigüe de deux produits du commerce contenant du Disperse Red 179 et du DAPEP, réalisées à l'aide de Poecilia reticulata (guppy) ont été soumises à Environnement Canada en janvier 2009 (BMG, 2000b, 2003c).Les deux études ont été menées selon la procédure 203 du guide de l'OCDE (test de toxicité aigüe du poisson) et la directive 92/69/EEC de la CEE (toxicité aigüe pour les poissons).Les résultats des deux études sont présentés dans le tableau 7a.
Dans la première étude, la toxicité du Disperse Red 179 a été recherchée à l'aide d'un test de dépistage de la toxicité aquatique, avec le produit Foron Rubin RD-S du commerce (BMG, 2003c). Le test signalait une CL50 aiguë à 96 heures entre 10 et 100 mg/L et une concentration sans effet observé (CSEO) > 10 mg/L, en fonction de concentrations nominales. Ces résultats peuvent être interprétés comme signifiant qu'il n'y a pas d'effets observés à saturation de la substance testée.Une évaluation de la fiabilité de l'étude à l'aide d'un sommaire de rigueur d'étude a trouvé que l'étude a été jugée comme étant de « faible confiance », en raison du manque de détails sur la substance testée (annexe 1).De fait, ni la proportion de Disperse Red 179 dans le Foron Rubin RD-S, ni la solubilité du Foron Rubin RD-S ne sont signalées.
La deuxième étude sur le test de toxicité aquatique (BMG, 2000b) a été menée sur le Disperse Red 153, substance qui contient du DAPEP et un isomère structurel du DAPEP, dans des proportions inconnues (Nakagawa et al., 1996; CII, 2002– ). L'essai a déterminé une concentration sans effet observé (CSEO) de 100 mg/L. Ce résultat peut être interprété dans le sens où aucun effet aigu n'a été observé à saturation de la substance. Comme pour l'étude précédente, l'étude est considérée comme étant de « faible confiance » en raison du manque de détails sur la substance testée (annexe 1).
Bien que l'on considère les deux études comme étant de faible confiance, les résultats obtenus dans les deux études sont typiques pour les colorants azoïques dispersés.
Tableau 7a. Données empiriques sur la toxicité aquatique du Disperse Red 179 et du DAPEP
| Substance d'essai | Organisme d'essai | Type d'essai | Paramètre ultime | Valeur (mg/L) | Référence |
|---|---|---|---|---|---|
| 1 CL50 : concentration d'une substance estimée létale pour 50 % des organismes d'essai. 2 CSEO : la concentration sans effets observés est la plus haute concentration lors d'un test de toxicité qui n'entraîne pas d'effet statistiquement significatif comparé aux contrôles. |
|||||
| Foron Rubin RD-S (Disperse Red 179) | Poecilia reticulata (guppy) | Aigu (96 heures) | CL501 | 10 à 100 mg/L | BMG, 2003c |
| CSEO2 | > 10 mg/L | ||||
| C.I. Disperse Red 153 | Poecilia reticulata (guppy) | Aigu (96 heures) | CSEO2 | > 100 mg/L | BMG, 2000b |
Des données empiriques sur la toxicité sont aussi disponibles pour un autre analogue proche des deux substances, l'éthanol, 2-((4-(2-(6-chloro-2-benzothiazolyl)diazenyl)phényl)ethylamino), 1-acétate, n° CAS 70198-17-3 (voir le tableau 7b). La masse moléculaire de ce colorant benzothiazyle mono-azoïque dispersé (404,9 g/mol) et sa structure moléculaire sont identiques à celles du Disperse Red 179 et du DAPEP. Le test de toxicité statique à 96 heures de la substance, ajoutée aux aquariums dans un vecteur d'acétone à 0,05%, a été mené avec des daphnies, des plathelminthes, des vairons à grosse tête et des escargots (Laboratoire de Santé, Sécurité et facteurs humains, 1978).Les résultats indiquaient une toxicité faible pour le vairon à grosse tête et les escargots (valeurs de CL50 > 100 mg/L) et une toxicité faible pour les plathelminthes (CL50 = 32 mg/L), mais une toxicité élevée pour les daphnies (CL50 = 0,12 mg/L) (Laboratoire de Santé, Sécurité et facteurs humains, 1978).La faible valeur de toxicité de 0,12 mg/L pour les daphnies est préoccupante, mais ces données sont considérées comme peu fiables, puisque la fiabilité du test de toxicité n'a pu être évaluée à cause d'un manque général de détails signalé dans l'étude et de l'âge de l'étude ellemême.
Environnement Canada a reçu des données éco-toxicologiques sur une substance structurellement identique dans les Règles de notification des nouvelles substances (Produits chimiques et polymères) (Environnement Canada, 1994) (voir le tableau 7b). La masse moléculaire de cette substance déclarée était de 418,35 g/mol, ce qui est identique à la masse moléculaire du Disperse Red 179 et du DAPEP.Les résultats du test de toxicité statique à 96 heures sur la truite arc-en-ciel, sur une substance contenant 5 % de la substance déclarée a révélé que la CL50 pour ces espèces est de 10 mg/L. Cependant, alors que cette valeur de toxicité suggère une toxicité aigüe de modérée à faible pour les poissons, elle n'a pas été considérée comme indicatrice du matériel notifié, à cause de la faible concentration de la substance déclarée dans le produit testé.
Tableau 7b. Données empiriques sur la toxicité aquatique d'analogues proches du Disperse Red 179 et du DAPEP
| Nom usuel ou n° CAS | Organisme d'essai | Durée (heures) | Paramètre ultime | Fiabilité de l'étude | Valeur (mg/L) | Référence |
|---|---|---|---|---|---|---|
| 1CL50 – La concentration d'une substance estimée létale pour 50 % des organismes d'essai. | ||||||
| N° CAS 70198-17-3 | Vairons à grosse tête | 96 | CL501 | Non disponible | > 100 | Laboratoire de Santé, Sécurité et facteurs humains, 1978 |
| Escargots | 96 | CL501 | Non disponible | > 100 | ||
| Plathelminthes | 96 | CL501 | Non disponible | 32 | ||
| Daphnies | 96 | CL501 | Non disponible | 0,12 | ||
| Confidentiel | Truite arc-en-ciel |
96 | CL501 | Confiance faible | 10 | Environnement Canada, 1994 |
Des données empiriques sur la toxicité sont disponibles pour l'analogue proche Disperse Orange 30 (voir le tableau 7c). Selon une étude soumise à Environnement Canada pour le compte de l'ETAD (Brown, 1992), CL50 après 96 heures de 710 mg/L pour le poisson zèbre, une CE50 après 48 heures de 5,8 mg/L pour le Daphnia magna, et une CE50après 72 heures de 6,7 mg/L (pour la croissance) pour le Scenedesmus subspicatusont été obtenues expérimentalement d'après une étude de toxicité utilisant le Disperse Orange 30. Cependant, les études d'origine n'ont pas été fournies et leur fiabilité ne peut donc être vérifiée.Un autre résultat pour le Disperse Orange 30 a établi une CL50 pour la truite arc-en-ciel (Oncorhynchus mykiss) > 700 mg/L (Sandoz, 1975).Cependant, après examen, cette étude a été considérée irrecevable (voir l'annexe 1).Finalement, une autre étude de toxicité aiguë, utilisant la truite arc-en-ciel et soumise à Environnement Canada en août 2008, indiquait une CL50 à 96 heures > 100 mg/L (Safepharm Laboratories Ltd., 1990).L'évaluation de la fiabilité de l'étude utilisant un sommaire de rigueur d'étude, a estimé que l'étude était de « faible confiance » à cause du manque de détails (annexe 1).
Tableau 7c. Données empiriques sur la toxicité aquatique de l'analogue Disperse Orange 30
| Organisme d'essai | Type d'essai | Durée (heures) | Paramètre ultime | Fiabilité de l'étude | Valeur (mg/L) | Référence |
|---|---|---|---|---|---|---|
| 1 CL50 – La concentration d'une substance estimée létale pour 50% des organismes d'essai. 2 CE50 - La concentration d'une substance qui est jugée causer un effet toxique sublétal chez 50 % des organismes d'essai. 3 CI50 – La concentration d'une substance estimée inhiber la croissance pour 50% des organismes d'essai. |
||||||
| Truite arc-en-ciel |
Aigu | 48 | CL501 | Inacceptable | > 700 | Sandoz, 1975 |
| Truite arc-en-ciel |
Aigu | 96 | CL50 | Confiance faible | > 100 | Safepharm Laboratories Ltd., 1990 |
| Poisson zèbre | Aigu | 96 | CL50 | Non disponible | 710 | Brown, 1992 |
| Daphnia magna | Aigu | 48 | CE502 | Non disponible | 5,8 | |
| Scenedesmus subspicatus | Aigu | 72 | CE50 | Non disponible | 6,7 | |
| Bactéries | Aigu | s.o. | CI503 | Non disponible | > 100 | |
Dans une autre étude, un résumé qui a été soumis à Environnement Canada pour le compte de l'ETAD (Brown, 1992), 11 colorants dispersés ont été testés sur les organismes suivants : poisson zèbre, Daphnia magna, algues et bactéries. Dans cette étude, des colorants dispersés (composants non azoïques) avaient des niveaux de toxicité signalés < 1 mg/L pour les algues.Cependant, Brown (1992) a signalé que l'inhibition de la croissance pour les algues était largement due à l'absorption de la lumière par les colorants, plutôt que par l'activité biologique.Trois des colorants dispersés testés par Brown (1992) sont des analogues du Disperse Red 179 et du DAPEP.Ce sont le Disperse Red 73, le Disperse Orange 25 et le Disperse Red 17 (tableau 7c). Ces analogues ont montré une toxicité modérée chez D. magna (CE50 à 48 heures = 23 à 110 mg/L) et une toxicité modérée à faible chez le poisson zèbre (CL50 à 96 heures = 17 à 268 mg/L) (voir le tableau 7d).Une toxicité modérée a aussi été observée pour la croissance des algues (une CE50 pour la croissance = 7 à 54mg/L) et aucune toxicité n'a été détectée pour les bactéries (CI50 > 100 mg/L).Les détails de l'expérience sur les colorants testés n'ont pas été fournis, limitant fortement l'évaluation de ces études (Brown, 1992).Cependant, ces données ont été considérées utilisables et sont inclues dans cette évaluation préalable comme faisant partie du poids de la preuve, étant donné qu'elles sont en accord avec d'autres données et avec l'échelle attendue des valeurs d'écotoxicité pour ces structures.Ces valeurs devraient donc également suggérer que ni le Disperse Red 179, ni le DAPEP ne sont fortement dangereux pour les organismes aquatiques.
Tableau 7d. Données empiriques sur la toxicité aquatique d'analogues du Disperse Red 179 et du DAPEP
| Nom usuel ou n° CAS | Organisme d'essai | Durée (heures) | Paramètre ultime | Valeur (mg/L) | Référence |
|---|---|---|---|---|---|
| 1 CL50 – La concentration d'une substance estimée létale pour 50 % des organismes d'essai. 2 CE50 – La concentration d'une substance qui est jugée causer un effet toxique sublétal chez 50 % des organismes d'essai. 3 CI50 – La concentration d'une substance estimée inhiber la croissance pour 50 % des organismes d'essai. s.o. : sans objet |
|||||
| Disperse Red 73 | Poisson zèbre | 96 | CL501 | 17 | Brown, 1992 |
| Daphnia magna | 48 | CE502 | 23 | ||
| Scenedesmus subspicatus | 72 | CE502 | > 10 | ||
| Bactéries | s.o. | CI503 | > 100 | ||
| Disperse Red 17 | Poisson zèbre | 96 | CL501 | 103 | Brown, 1992 |
| Daphnia magna | 48 | CE502 | 98 | ||
| Scenedesmus subspicatus | 72 | CE502 | 7 | ||
| Bactéries | s.o. | CI503 | > 100 | ||
| Disperse Orange 25 | Poisson zèbre | 96 | CL501 | 268 | Brown, 1992 |
| Daphnia magna | 48 | CE502 | 110 | ||
| Scenedesmus subspicatus | 72 | CE502 | 54 | ||
| Bactéries | s.o. | CI503 | > 100 | ||
| Disperse Yellow 3 | Vairon à grosse tête | 96 | CL501 | > 180 | Little et Lamb, 1973 |
En général, en raison de leur faible solubilité (< 1 mg/L), les colorants dispersés sont supposés avoir un impact écologique faiblement aigu (Hunger, 2003). À l'exception de la seule faible valeur de CL50 à 96 heures observée pour les daphnies (Laboratoire de santé, Sécurité et Facteurs humains, 1978), les résultats des études empiriques de toxicité avec les deux substances évaluées et plusieurs analogues, sont cohérentes avec cette attente, indiquant des valeurs de CL50 dans la plage de 5 à 340 mg/L, avec la Daphnia étant l'organisme testé le plus sensible (valeurs de CE50/CL50 de 4,5 à 100 mg/L).Bien que l'interprétation des résultats de ces tests soit compliquée par le fait que ces valeurs d'effet soit basé sur des concentrations nominales parfois supérieures à 10 000 fois la solubilité estimée de la substance (c.-à-d. 0,011 92 mg/L pour le Disperse Red 179; 0,004 208 mg/L pour le DAPEP; 0,021 à 0,69 mg/L pour l'analogue n° CAS68133-69-7), elles représentent effectivement les pires charges environnementales possibles.
Les informations empiriques d'écotoxicité disponibles pour les analogues du Disperse Red 179 et du DAPEP indiquent ainsi que le Disperse Red 179 et le DAPEP ne sont pas susceptibles d'être fortement dangereux pour les organismes aquatiques.
B – Dans d'autres milieux environnementaux
Etant donné que le Disperse Red 179 et le DAPEP peuvent potentiellement être rejetés dans le sol à partir d'eaux usées ou de terres agricoles, il serait préférable d'obtenir des données sur la toxicité des organismes contenus dans le sol. Ceci est pertinent car il a été montré que les colorants sont fortement absorbés et retenus dans les boues activées des stations d'épuration des eaux usées (Tincher, 1988). Cependant, on n'a trouvé aucune étude pertinente sur les effets écologiques de ces composés ou de leurs analogues dans d'autres milieux que l'eau. En dépit de l'absence d'étude appropriée sur les effets écologiques de ces composés dans le sol, compte tenu des données sur la toxicité pour les organismes aquatiques et vu leur absence de potentiel de bioaccumulation et leur faible biodisponibilité, ces composés ne devraient pas vraiment être toxiques pour les organismes vivant dans le sol. Pour les mêmes raisons, le potentiel de toxicité est également susceptible d'être faible concernant les espèces oxiques vivant dans les sédiments, bien que ceci ne puisse être justifié, étant donné le manque d'informations sur la toxicité de l'ensemble des organismes contenus dans les sédiments pour ces substances ou des analogues acceptables.En outre, le potentiel de toxicité du Disperse Red 179 et du DAPEP dans les sédiments anoxiques sera faible étant donné la faible biodisponibilité de leurs produits de digestion anaérobie.
Évaluation de l'exposition écologique
Aucune donnée sur les concentrations de ces substances dans l'eau n'a été identifiée au Canada; par conséquent, les concentrations dans l'environnement sont estimées à partir d'informations disponibles, comprenant les quantités estimées de ces substances dans le commerce, les taux de rejet et le volume des masses d'eau réceptrices.
Rejets industriels
Le Disperse Red 179 et le DAPEP peuvent être utilisés en faibles volumes dans certaines installations industrielles et peuvent être rejetés dans l'eau où ils resteront pour une période indéterminée avant de décanter dans les sédiments. Étant donné que le Disperse Red 179 et le DAPEP sont analogues, un scénario d'exposition unique a été modélisé pour les deux substances, afin de déterminer une concentration environnementale estimée (CEE) dans l'environnement aquatique.Plusieurs sites industriels ont été identifiés comme sources potentielles de rejets dans l'eau et un site a été sélectionné pour l'évaluation d'un scénario le plus défavorable dû aux plus grandes quantités de substances utilisées.Des hypothèses prudentes ont été émises concernant la quantité de substance traitée et rejetée, le nombre de jours de traitement et le taux d'élimination des stations d'épuration des eaux usées.La concentration environnementale estimée pour le Disperse Red 179 et le DAPEP a été calculée en se basant sur l'utilisation combinée d'une quantité de 510 kg/an (respectivement 350 kg/an et 160 kg/an pour le Disperse Red 179 et le DAPEP), sur lesquels 22 % sont supposés être rejetés sur une période de 250 jours, résultant du processus de coloration lorsque le colorant non fixé est éliminé des fibres et rejeté dans les eaux usées (Environnement Canada, 2009a, 2009b, 2009c, 2009d).Les 22 % rejetés dans les eaux usées (égouts) par les activités industrielles représentent une estimation prudente, tirée du débitmètre massique (Environnement Canada, 2009b, 2009c, 2009d). On a alors supposé que la quantité rejetée était déversée directement dans une usine locale de traitement des eaux usées, avec un taux d'élimination de zéro pour les substances. Le Disperse Red 179 et le DAPEP dans les effluents d'une usine de traitement des eaux usées étaient supposés être rejetés vers une masse d'eau réceptrice ayant une capacité de dilution 10 fois supérieure à celle du débit des effluents. En fonction du volume rejeté estimé le plus élevé possible et des hypothèses susmentionnées, la concentration la plus élevée de Disperse Red 179 et de DAPEP dans les eaux réceptrices est de 1,7 × 10-5 mg/L (Environnement Canada, 2009e).
Rejets de consommation (Mega Flush)
Comme on trouve du Disperse Red 179 et du DAPEP dans les produits de consommation et qu'on déclare des rejets de ces substances dans l'eau (égouts), d'après les résultats de l'outil de débit massique (Environnement Canada, 2009c, 2009d). Mega Flush (modèle de tableur d'Environnement Canada pour l'estimation des rejets dans les canalisations issus des produits de consommation) a été utilisé pour estimer la concentration potentielle des substances dans plusieurs cours d'eau récepteurs d'effluents d'usines de traitement des eaux usées, vers lesquelles les produits de consommation contenant les substances sont susceptibles d'avoir été rejetés (Environnement Canada, 2009f) . Le modèle de tableur est conçu pour fournir ces estimations en fonction des hypothèses prudentes concernant la quantité de substances utilisées et rejetées par les consommateurs.Par défaut, nous supposons que les taux d'élimination primaires et secondaires des usines de traitement des eaux usées sont de 0 %, les pertes dues à l'utilisation sont de 100 %, l'utilisation domestique de la substance étant sur 365 jours/an et le débit des eaux réceptrices sur tous les sites du dixième centile (estimation basse).Ces estimations sont réalisées pour environ 1 000 sites de rejet à travers le Canada, ce qui représente la majorité des plus importantes usines de traitement des eaux usées dans le pays.
L'équation et les données utilisées pour calculer la concentration environnementale estimée du Disperse Red 179 dans les masses d'eau réceptrices sont décrites dans Environnement Canada (2009f). Un scénario a été réalisé en supposant une quantité totale consommée de 104 kg/an prévue d'être rejetée dans les égouts (9,2 % de la masse totale), en conséquence du blanchissage d'articles manufacturés qui contiennent ce colorant (articles importés ou fabriqués au Canada) (Environnement Canada, 2009c). Selon ce scénario, l'outil estime que la CEE du Disperse Red 179 dans les cours d'eau récepteurs varie entre 1,3 × 10-5 et 1,6 × 10-4 mg/L..
Un scénario semblable pour les rejets issus des utilisations des consommateurs a été utilisé pour prévoir la CEE du DAPEP (Environnement Canada, 2009h). Le scénario a été réalisé pour le DAPEP en supposant une quantité totale de 47 kg/an (9,2 % de la masse totale) perdue dans les égouts pendant le blanchissage des articles manufacturés qui contiennent ce colorant. Des taux d'élimination semblables de 0 % ont été utilisés. Selon ce scénario, l'outil estime que la CEE du DAPEP dans les cours d'eau récepteurs varie entre 5,9 × 10-6 et 7,2 × 10-5 mg/L.
Caractérisation du risque écologique
La démarche suivie dans cette évaluation écologique a consisté à examiner un certain nombre informations complémentaires et à tirer des conclusions d'après la méthode du poids de la preuve et en prenant les précautions requises par la LCPE (1999). Les éléments de preuve pris en compte comprenaient les résultats de calculs prudents du quotient de risque ainsi que des renseignements sur la persistance, la bioaccumulation, la toxicité inhérente, les sources et le devenir des substances.
On s'attend à ce que le Disperse Red 179 et le DAPEP soient persistants dans l'eau, le sol et les sédiments dans des conditions aérobies; on s'attend également à ce que leur potentiel de bioaccumulation soit bas. Les faibles volumes d'importation au Canada des deux substances indiquent un faible potentiel de rejet dans l'environnement canadien, malgré leur utilisation industrielle, commerciale et domestique.Une fois rejetés dans l'environnement aquatique, ils se trouveront principalement dans les sédiments. On s'attend également à ce que dans l'ensemble, elles présentent un potentiel faible à modéré de toxicité pour les organismes aquatiques.
Des estimations d'exposition prudentes intégrant l'analyse du quotient de risque d'exposition, avec une information sur la toxicité, ont été réalisées pour le milieu aquatique, afin de déterminer s'il existe un danger potentiel pour l'environnement au Canada. Une concentration estimée sans effet (CESE) pour les deux substances a été estimée de façon prudente d'après la CL50 en 96 heures extrêmement faible de 0,12 mg/L (Health, Safety, and Human Factors Laboratory, 1978) pour les daphnies à l'aide de la substance analogue n° CAS 70198-17-3. Il s'agit de la valeur analogue expérimentale la plus faible tirée des données de toxicité aiguë relevées et elle est un ordre de grandeur inférieur à la deuxième plus faible valeur de toxicité. On a appliqué un facteur de 100 pour tenir compte de l'extrapolation de la toxicité aiguë à la toxicité chronique (à long terme) et de l'extrapolation des résultats en laboratoire pour une espèce à d'autres espèces potentiellement sensibles sur le terrain. La concentration estimée sans effet qui en résulte est de 0,0012 mg/L.
Lorsqu'il est compare aux concentrations environnementales estimées prudentes calculées ci-dessus pour le scenario des rejets industriels, le quotient de risque résultant pour les rejets industriels dans l'environnement aquatique (concentration environnementale/concentration estimée sans effet) est de 0,000 009/0,0012 = 0,0077 pour les rejets combines de Disperse Red et de DAPEP. En conséquence, on estime que les concentrations de Disperse Red 179 ou de DAPEP sur les eaux de surface au Canada, provenant des rejets industriels pour un site canadien soumis au scénario le plus défavorable, ont peu de chance de causer des effets indésirables sur les populations d'organismes aquatiques.Étant donné que ce scénario de rejet industriel fournit une estimation prudente de l'exposition et du risque, les résultats indiquent un faible potentiel de nocivité écologique, résultant de l'exposition locale et du point d'origine des rejets industriels dans l'environnement aquatique.
En ce qui concerne l'exposition découlant de rejets dans les canalisations à l'aide de scénarios modérément prudents d'utilisation domestique, les CEE estimées avec Mega Flush ne dépassent la CESE sur aucun site (c'est-à-dire que tous les quotients de risque sont très inférieurs à 1) (Environnement Canada, 2009g, 2009h). Ceci indique que les rejets domestiques jetés dans l'évier de Disperse Red 179 et de DAPEP ne semblent pas devoir nuire aux organismes aquatiques.
En conséquence, d'après les preuves disponibles, le Disperse Red 179 et le DAPEP ne sont pas en mesure de nuire à l'environnement canadien.
Incertitudes dans l'évaluation des risques pour l'environnement
Il existe des incertitudes dans cette évaluation des risques en raison d'un manque de données sur les propriétés physiques et chimiques du Disperse Red 179 et du DAPEP, notamment leur hydrosolubilité et leurs coefficients de partage octanol-eau et carbone-eau. Cependant, des méthodes d'analyse de données déduites à partir d'analogues, des données analogues proches et des données modélisées utilisant la méthode d'ajustement de la valeur expérimentale d'EPIsuite (2008), ont été utilisées afin de combler les données manquantes importantes avec une marge d'erreur acceptable.
L'évaluation de la persistance est limitée par l'incertitude sur le taux de dégradation dans les sédiments anaérobies et la mesure pour laquelle la dégradation a lieu dans ces sédiments, et si les produits de dégradation (par exemple, les amines) seraient biologiquement disponibles. Néanmoins, il apparaît clairement que la dégradation anaérobie de la partie biodisponible de colorants azoïques dans les sédiments en amines constitutives, est beaucoup plus rapide (demi-vies dans l'ordre des jours) que la biodégradation aérobie. Bien que l'on ne s'attende pas à ce que les produits de dégradation amine soient biodisponibles, parce qu'ils se forment uniquement dans les sédiments anoxiques relativement profonds et qu'ils peuvent se lier étroitement aux sédiments par l'addition néophilique et le couplage radicalaire oxydant (Weber et al., 2001; Colon et al. 2002), cette question est une source d'incertitude pour l'évaluation de la toxicité du Disperse Red 179 et du DAPEP.
Des incertitudes sont associées également à la fraction des substances dont on présume qu'elle est rejetée pendant l'utilisation (c'est-à-dire pendant les activités industrielles et l'utilisation des produits de consommation) et au manque d'information sur les concentrations environnementales au Canada du Disperse Red 179 et du DAPEP. Ces incertitudes ont été prises en charge en formulant des hypothèses prudentes dans chacun des exercices de modélisation.
Les concentrations expérimentales, associées à la toxicité intrinsèque pour les organismes aquatiques, constituent une source additionnelle d'incertitude, dans le sens où elles dépassent la solubilité du produit chimique dans l’eau. Malgré ceci, la faible solubilité des substances et leur biodisponibilité limitée due à leur taille moléculaire indiquent que le Disperse Red 179 et le DAPEP ne sont pas extrêmement dangereux pour les organismes aquatiques.
Également, en ce qui concerne l'écotoxicité, basée sur le comportement de partage prévu de ces produits chimiques, l'importance du sol et des sédiments comme milieux d'exposition importants n'est pas bien résolue par les données disponibles sur les effets. En effet, les seules données sur les effets qui ont été trouvées s’appliquent principalement aux expositions aquatiques pélagiques, même si la colonne d’eau peut ne pas être le moyen le plus préoccupant à long terme. Néanmoins, d'après la toxicité aquatique relativement faible de ces substances et la faible commercialisation des masses, le potentiel nocif pour les organismes vivant dans les sols et les sédiments devrait également être faible.
Évaluation de l'exposition
Aucune mesure du Disperse Red 179 ou du DAPEP dans l'environnement n'a été relevée dans la littérature scientifique. D'après les renseignements sur les rejets, les concentrations dans les milieux naturels devraient être négligeables.
Les colorant dispersés tels que le Disperse Red 179 et le DAPEP sont utilisés dans l'industrie du textile afin de colorer les tissus synthétiques comme les polyesters et les polyamides. Les colorants dispersés tirent leur nom du processus de teinture utilisé (APE du Danemark, 1998). En raison de leur faible solubilité dans l'eau, les composés de colorant sont traditionnellement moulus en vue d'obtenir une fine poudre qui est ensuite dispersée dans de l'eau. Les molécules de colorant hydrophobes s'adsorbent alors au textile hydrophobe. La chaleur permet ensuite l'absorption du colorant par le textile (Chudgar et Oakes, 2003). Le Disperse Red 179 et le DAPEP ne créent pas de liaisons chimiques avec le textile; ainsi, la migration est possible. Ils peuvent être utilisés comme agents de teinture des fibres synthétiques destinées aux vêtements personnels ou au linge de maison.
Les estimations de la limite supérieure d'exposition ont été calculées pour deux scénarios. Le premier scénario analysait la voie cutanée quand un individu porte des vêtements faits en tissu teints avec ces substances, tandis que le second analysait la voie orale résultant du mâchonnement d'un tissu teint avec ces substances par des nourrissons et des jeunes enfants. On considère qu'il s'agit des voies d'exposition les plus probables La limite supérieure d'exposition pour tout contact direct ou indirect avec des textiles teints avec ces substances. Les doses internes maximales provenant de l'exposition cutanée au Disperse Red 179 et au DAPEP ont été estimées entre 0,1 et 4 µg/kg de poids corporel (p.c.) par jour pour tous les groupes d'âges portant des vêtements neuf, non lavé et présentant des propriétés d'indégorgeabilité bonnes à faibles (ETAD, 2004). Pour les bébés et enfants âgés les expositions par voie buccale sont estimées à moins de 0,002 µg/kg p.c. par jour, Une étude récente a déterminé que la quantité de colorant dispersé migrant sur la peau de volontaires humains était de 300 à 600 fois plus faible que celle émise par les stimulants sudorifiques (Meinke et al., 2009). Cela soutient la nature prudente des estimés d’exposition de limite supérieure. En outre, on estime que les colorants présents dans les textiles sont relâchés principalement au moment du lavage. Donc toutes expositions potentielles relâcheraient avec le temps. Des renseignements détaillés concernant les hypothèses utilisées dans ces calculs sont proposés aux annexes III et IV.
Évaluation des effets sur la santé
Disperse Red 179 (n° CAS 16586-42-8)
Une seule étude sur le Disperse Red 179 (cité en tant que Disperse Violet 52) dans un essai de génotoxicité in vitro sur les indicateurs (test umu/SOS); celui-ci a fait état de résultats positifs avec une activation de la fraction S9 et de résultats négatifs sans l'activation de cette fraction (Kosaka et Nakamura, 1990). Les résultats des modèles de prévision RQSA sur le Disperse Red 179 étaient mitigés pour les paramètres de cancérogénicité et de génotoxicité (CASETOX (2008), DEREK (2008), Leadscope Model Applier (Leadscope, 2009) et Toxtree (2009)) (annexe 5). Étant donné que les données disponibles étaient limitées en matière de toxicité potentielle du Disperse Red 179, des renseignements pertinents relatifs aux métabolites et analogues potentiels de cette substance ont également été pris en considération.
Comme le Disperse Red 179 est un membre de la famille des substances azoïques, les renseignements important sur l’effets des produits de clivage azoïques potentiels sur la santé ont été pris en considération dans cette évaluation préalable. Il a été démontré que certaines substances azoïques peuvent subir un clivage réducteur diffusé par des enzymes azoréductases présentes dans les tissus des mammifères ainsi que dans les bactéries intestinales et cutanées (Platzek et al., 1999; Golka et al., 2004; Chen, 2006; Xu et al., 2007; Stingley et al., 2010). Bien que l'on reconnaisse que le degré de réduction azoïque est vraisemblablement influencé par divers facteurs (p. ex. solubilité du composé d'origine, présence et position des substituants moléculaires), en l'absence de données propres aux produits chimiques, on présume que l'exposition à une substances azoïque peut également entraîner une exposition à ses produits de clivage connexes, habituellement les amines aromatiques. Dès lors, les produits de clivage azoïques prévus pour le Disperse Red 179 – à savoir le 6-nitro-2-aminobenzothiazole (n° CAS 6285-57-0) et le 3-[(4-amino-3-méthylphényl)éthylamino]propanenitile]- (n° CAS 105294-34-6) (annexe 6) – sont aussi pris en considération dans cette évaluation préalable.
Le métabolite prévu n° CAS 6285-57-0 a été soumis à des essais de mutagénicité in vitro dans plusieurs études. Trois études distinctes ont montré des resultats positifs dans les souches TA98, TA100 et TA1538 du Salmonella typhimuriumavec et sans activation de la fraction S9, tandis que les souches TA1535 et TA1537 étaient positives uniquement sans activation de la fraction S9 (NTP, 1982, 1983; Seifried, 2006). On n'a observé aucune mutagénicité dans les cellules de lymphomes de souris avec ou sans activation de la fraction S9 pour cette substance (Seifried et al., 2006). Une activité cancérogène potentielle a aussi été signalée pour le n° CAS 6285-57-0 a aussi été liée une activité carcinogénique basée sur la similarité avec des composés nitrés aromatiques cancérogènes (Helmes et al., 1982). Aucune donnée empirique sur la toxicité n'était disponible pour le n° CAS 105294-34-6, l'autre produit de clivage azoïque prévu du Disperse Red 179. Les résultats de la modélisation RQSA pour les paramètres de cancérogénicité et de génotoxicité étaient mitigés pour ces deux produits de clivage azoïques potentiels (voir l'annexe 5).
Le seul analogue pertinent relevé, le Disperse Red 145 (n° CAS 25510-81-0), a produit un résultat positif lors du test umu/SOS avec et sans activation de la fraction S9 dérivée du foie (Kosaka et Nakamura, 1990).Il convient de noter également que la classe des colorants azoïques aminobenzothiazoles a été signalée par la Environmental Protection Agency (EPA) des États-Unis comme une catégorie de substance chimique du New Chemicals Program (NCP) visé par la Toxic Substances Control Act (TSCA), en raison des inquiétudes quant aux risques que posent les substances connexes et les métabolites potentiels (US EPA, 2002).
L'information obtenue concernant le Disperse Red 179, ses produits de clivage azoïques potentiels et un analogue structurel (Disperse Red 145) indique que certains risques potentiels pourraient être associés à Dispered Red 179. Toutefois, le niveau de confiance à l'égard de la base de données toxicologiques est réputé faible, en raison des données empiriques limitées pour cette substance.
DAPEP (25176-89-0)
Aucune donnée empirique sur la toxicité n'a été trouvée pour le DAPEP. Cependant, comme le DAPEP est un des deux isomères qui constituent le Disperse Red 153 (n° CAS 78564-87-1), [1] les données relatives à cette substance sont jugées représentatives du DAPEP. Une seule étude a révélé que le Disperse Red 153 était négatif lors du test umu/SOS avec et sans activation de la fraction S9 (Kosaka et Nakamura, 1990). En outre, les résultats des modèles de prévision RQSA sur les deux isomères du Disperse Red 153 étaient mitigés pour les paramètres de cancérogénicité et de génotoxicité (voir l'annexe 7). Étant donné que seules des données limitées étaient disponibles en matière de toxicité potentielle du DAPEP et du Disperse Red 153, des renseignements pertinents relatifs aux métabolites et aux analogues potentiels ont également été pris en considération.
Comme le DAPEP est un membre de la famille des substances azoïques, les produits de clivage azoïques potentiels du DAPEP – à savoir, le 2-amino-5,6-dichlorobenzothiazole (n° CAS 24072-75-1) et le 3-[(4-aminophényl)éthylamino]propanenitrile (n° CAS 100894-10-8) (voir l'annexe 8) – sont pris en considération dans cette évaluation préalable (consulter la section précédente pour connaître la justification).
Le métabolite prévu n° CAS 24072-75-1 (2-amino-5,6-dichlorobenzothiazole) a été soumis à des essais de mutagénicité in vivo et in vitro. La mutagénicité de cette substance était négative tant chez le Salmonella typhimurium (NTP, 1986a; Seifried et al., 2006) que dans les cellules de lymphomes de souris. 2006). La substance n'a pas provoqué la formation de micronoyaux chez des souris mâles ou femelles exposées par voie orale par leur alimentation dans le cadre d'une étude de toxicité subchronique inédite (NTP, 1993; Witt et al., 2000). Bien que l'ensemble de données exhaustif pour cette étude soit inédit et indisponible dans l'immédiat (NTP, 1986b), un rapport concis du National Toxicology Program des États-Unis a indiqué que certains effets histopathologiques dans le foie et les reins ont été observés chez des rats et des souris. Toutefois, l'incidence et les doses n'ont pas été fournies (NTP, 2000). Il convient de noter également que l'US EPA a relevé la classe des colorants azoïques aminobenzothiazoles en partie en raison de préoccupations relatives à la neurotoxicité du « 2-aminobenzothiazole chloré » en tant que produit de clivage réducteur (US EPA, 2002). Aucune donnée empirique sur la toxicité n'a été définie pour les autres métabolites potentiels n° CAS 100894-10-8 ou CAS25150-27-0 (le produit de clivage azoïque prévu de l'autre isomère dichloro présent dans le Disperse Red 153, se reporter à l'annexe 8 pour la structure). Les résultats de la modélisation RQSA sur la cancérogénicité et la génotoxicité étaient mitigés pour tous les métabolites de clivage azoïques prévus pour le DAPEP et l'isomère 6,7'-dichloro du Disperse Red 153 (voir l'annexe 7).
Disperse Red 153 (n° CAS78564-87-1, un mélange d'isomères comprenant le DAPEP, déjà abordé ci-dessus) et du Disperse Red 152 (n° CAS78564-86-0) ont été relevé comme des analogues potentiels de DAPEP. Le Disperse Red 152 est aussi un mélange d'isomères 5,6'- et 6,7'-dichloro, il est semblable au Disperse Red 153 (voir l'annexe 8 pour la structure) et il a donné un résultat négatif similaire à ceux du test umu/SOS (Kosaka et Nakamura, 1990). Bien que des analogues limités aient été relevés pour le DAPEP d'après les critères susmentionnés, il convient de noter également que la classe des colorants azoïques aminobenzithiazoles à laquelle appartient le DAPEP a été relevé par l'US EPA. comme une catégorie de substance chimique du New Chemicals Program (NCP) visé par la Toxic Substances Control Act (TSCA), en raison des inquiétudes quant aux risques que posent les substances connexes et les métabolites potentiels (US EPA, 2002).
L'information toxicologique limitée obtenue concernant le DAPEP, leurs produits de clivage azoïques potentiels et un analogue structurel (Disperse Red 153) indique que certains risques potentiels pourraient être associés au DAPEP. Toutefois, le niveau de confiance à l'égard de la base de données toxicologiques est réputé faible, en raison des données empiriques limitées disponibles pour cette substance.
Caractérisation du risque pour la santé humaine
Bien que seules des données empiriques limitées aient été relevées pour le Disperse Red 179 et le DAPEP, leurs produits de clivage azoïques et analogues potentiels, les données connexes, ainsi que les résultats RQSA mitigés, indiquent que des propriétés dangereuses. Cependant, les données disponibles limitées en ce qui concerne les risques empêchent le choix d'une dose avec effet critique à utiliser dans la caractérisation du risque de cette substance.
Le Disperse Red 179 et le DAPEP appartiennent au groupe des substances azoïques qui peuvent rejeter des amines aromatiques par clivage réducteur de la liaison azoïque. Bien que les données sur les risques concernant les amines aromatiques précises associées au Disperse Red 179 et au DAPEP soient limitées, la base de données collective sur la toxicité des amines aromatiques en tant que groupe chimique (Vineis et Pirastu, 1997; Benigni et Passerini, 2002; Talaska, 2003) laisse entendre que ces substances peuvent constituer une source d'inquiétude.
L'exposition potentielle de la population générale au Disperse Red 179 et au DAPEP présents dans les milieux naturels devrait être négligeable.
L'exposition de l'ensemble de la population canadienne au Disperse Red 179 et au DAPEP résultant du port de vêtements teints par tous les groupes d'âge et du mâchonnement fortuit de tissus par des enfants a quantifiée et est faible.
Comme l'exposition de l'ensemble de la population canadienne devrait être faible en raison de l'utilisation de la substance en tant que colorant pour textiles synthétiques, le risque prévu pour la santé humaine découlant des risques potentiels est réputé faible.
Incertitudes de l'évaluation des risques pour la santé humaine
Des incertitudes existent quant à l'évaluation de l'exposition. Aucune information n'était disponible quant aux facteurs de migration et à la solubilité du Disperse Red 179 et du DAPEP. Les sources d'exposition ont été caractérisées globalement en tant que tissus synthétiques, étant donné qu'aucun produit de consommation précis n'a été trouvé. Cependant, le niveau de confiance est élevé parce que les estimations relatives à l'exposition sont prudentes, pour les raisons suivantes. Le facteur de migration utilisé dans l'évaluation correspond à une exposition quotidienne à des tissus neufs, non lavés et présentant une indégorgeabilité faible, alors que l'on considère que le rejet de la substance se produit principalement pendant le lavage. En outre, une étude a démontré que la quantité de colorant dispersé migrant sur la peau de volontaires humains était beaucoup plus faible que celle rejetée en solution.
Le niveau de confiance à l'égard de la base de données toxicologiques pour ces substances est jugé très faible. Il y a des données limitées sur les risques associés au Disperse Red 179 et DAPEP. Il y a également un manque de renseignements sur le potentiel qu’ont ces substances de devenir des substances clivage azoïques, un aspect majeur pris en compte lors de l’évaluation de la toxicité des substances azotiques.
D'après les renseignements présentés dans la présente évaluation préalable, ni le Disperse Red 179, ni le DAPEP ne pénètrent dans l'environnement en une quantité ou une concentration ou dans des conditions qui ont ou peuvent avoir, immédiatement ou à long terme, un effet nocif sur l'environnement ou sur sa diversité biologique; par ailleurs, ces substances ne constituent ni ne peuvent présenter un danger pour l'environnement essentiel à la vie.
Bien que les données empiriques de modélisation pour les substances soient limitées, leurs métabolites et analogues potentiels indiquent un risque potentiel, d'après la prise en considération des renseignements limités sur les effets de la santé et la faible exposition même négligeable de l'ensemble de la population au Disperse Red 179 et au DAPEP, il est conclu que le Disperse Red 179 et le DAPEP ne pénètrent pas dans l’environnement en quantités, à des concentrations ou dans des conditions qui constituent ou peuvent constituer un danger pour la vie ou la santé humaine au Canada.
Par conséquent, il est conclu que le Disperse Red 179 et le DAPEP ne correspondent pas à la définition de « substance toxique » énoncée dans l’article 64 de la LCPE (1999). De plus, ces substances répondent au critère de la persistance, mais pas à ceux de la bioaccumulation énoncés dans le Règlement sur la persistance et la bioaccumulation (Canada, 2000).
Puisque ces substances sont inscrites sur la Liste intérieure des substances, leur importation et leur fabrication au Canada ne requièrent pas de déclaration aux termes du paragraphe 81(1). Étant donné les propriétés dangereuses potentielles de ces substances, on craint que des utilisations nouvelles non décelées ni évaluées fassent en sorte qu'elles répondent aux critères de l'article 64 de la LCPE (1999). Par conséquent, il est recommandé de modifier la Liste intérieure des substances en vertu du paragraphe 87(3) de la Loi afin d'indiquer que le paragraphe 81(3) s'applique à ces substances. Ainsi, toute fabrication, importation ou utilisation de ces dernières devra être déclarée et faire l'objet d'une évaluation des risques pour l'environnement et la santé humaine.
De plus, s'il y a lieu, des activités de recherche et de surveillance viendront appuyer la vérification des hypothèses formulées au cours de l'évaluation préalable.
Considérations dans le cadre d'un suivi
Le Disperse Red 179 et le DAPEP appartiennent à un groupe des substances azoïques qui peuvent se métaboliser en amines aromatiques et qui, en tant que groupe chimique connu pour présenter des propriétés dangereuses, notamment la cancérogénicité. Par conséquent, des activités supplémentaires (p. ex. recherche, contrôle et surveillance, évaluation) pourraient être entreprises afin de caractériser le risque pour la santé humaine au Canada relatif à ces lots de substances azoïques plus larges.
ACD/pKaDB [module de prédiction]. 2005. Version 9.04. Toronto (Ont.) : Advanced Chemistry Development. Accès : http://www.acdlabs.com/products/phys_chem_lab/pka/
Anliker, R., Clarke, E.A., Moser, P. 1981. Use of the partition coefficient as an indicator of bioaccumulation tendency of dyestuffs in fish. Chemosphere 10(3):263-274.
Anliker, R., Moser, P. 1987. The limits of bioaccumulation of organic pigments in fish: their relation to the partition coefficient and the solubility in water and octanol. Ecotoxicol. and Environ. Safety 13:43-52.
Anliker, R., Moser, P., Poppinger, D. 1988. Bioaccumulation of dyestuffs and organic pigments in fish. Relationships to hydrophobicity and steric factors. Chemosphere17(8):1631-1644.
Aronson, D., Boethling, B., Howard, P., Stiteler, W. 2006. Estimating biodegradation half-lives for use in chemical screening. Chemosphere 63:1953-1960.
Aronson, D., Howard, P.H. 1999. Evaluating potential POP/PBT compounds for environmental persistence. North Syracuse (NY) : Syracuse Research Corp., Environmental Science Centre. No rapport : SRCTR99020.
Baughman, G.L., Perenich, T.A. 1988. Fate of dyes in aquatic systems: I. Solubility and partitioning of some hydrophobic dyes and related compounds. Environ. Toxicol. Chem.7(3):183-199.
Baughman, G.L., Weber, E.J. 1994. Transformation of dyes and related compounds in anoxic sediment: kinetics and products. Environ. Sci. Technol. 28(2):267-276.
[BBM] Baseline Bioaccumulation Model. 2008. Gatineau (Qc) : Environnement Canada, Division des substances existantes. [modèle élaboré d'après Dimitrov et al., 2005]. [consulté le 21 novembre 2008]. Disponible sur demande.
Benigni, R., Passerini, L. 2002. Carcinogenicity of the aromatic amines: from structure–activity relationships to mechanisms of action and risk assessment. Mutat. Res.511(3):191-206.
[BIOWIN] Biodegradation Probability Program for Windows [modèle d'estimation]. 2000. Version 4.02. Washington (DC) : U.S. Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY) : Syracuse Research Corporation. Accès : http://www.epa.gov/oppt/exposure/pubs/episuite.htm
BMG. 2000a. C.I. Disperse Red 153, Test for inhibition of oxygen consumption by activated sludges: Respiration Inhibition Test. BMG report no. 800/b-00, décembre 2000.
BMG. 2000b. Foron Rubin RD-S Presskuchen trocken, 96-hour acute toxicity to Poecilia reticulata (Guppy): Limit Test (100 mg/L). BMG report no. 800/a-00, décembre 2000.
BMG. 2001. C.I. Disperse Red 153, Inherent biodegradability – Evaluation of the aerobic biodegradability in an aqueous medium: Zahn-Wellens/EMPA test. BMG report no. 800/c-00, janvier 2001.
BMG. 2003a. Foron Rubin RD-S Presskuchen trocken, Inherent biodegradability – Evaluation of the aerobic biodegradability in an aqueous medium: Zahn-Wellens/EMPA test. BMG report no. 709/c-03, octobre 2003.
BMG. 2003b. Foron Rubin RD-S Presskuchen trocken, Test for inhibition of oxygen consumption by activated sludges: Respiration Inhibition Test. BMG report no. 709/a-03, octobre 2003.
BMG. 2003c. Foron Rubin RD-S Presskuchen trocken, 96-hour acute toxicity to Poecilia reticulata (Guppy): Screening Test. BMG report no. 709/b-03, octobre 2003.
Boethling, R.S., Howard, P.H., Beauman, J.A., Larosche, M.E. 1995. Factors for intermedia extrapolations in biodegradability assessment. Chemosphere. 30(4):741-752.
Brown D. 1987. Effects of colorants in the aquatic environment. Ecotoxicol. Environ. Safety 13:139-147.
Brown, D. (ICI Group Environmental Laboratory, Brixham, UK). 1992. Environmental assessment of dyestuffs. Rédigé pour le compte de l'Ecological and Toxicological Association of the Dyes and Organic Pigments Manufacturers, Bâle, Suisse, ETAD ecological sub-committee project E3020. Présenté à Environnement Canada.
Canada. 1999. Loi canadienne sur la protection de l'environnement (1999), L.C., ch. 33, Gazette du Canada. Partie III, vol. 22, no 3. Ottawa : Imprimeur de la Reine. Accès : http://www.canlii.org/fr/ca/legis/lois/lc-1999-c-33/derniere/lc-1999-c-33.html
Canada. 2000. Loi canadienne sur la protection de l'environnement (1999) : Règlement sur la persistance et la bioaccumulation, C.P. 2000-348, 23 mars 2000, DORS/2000-107, Gazette du Canada. Partie II, vol. 134, no 7, p. 607-612. Ottawa : Imprimeur de la Reine. Accès : http://www.gazette.gc.ca/archives/p2/2000/2000-03-29/pdf/g2-13407.pdf
Canada. Ministère de l'Environnement, Ministère de la Santé. 2006a. Loi canadienne sur la protection de l'environnement (1999) : Avis d'intention d'élaborer et de mettre en œuvre des mesures d'évaluation et de gestion des risques que certaines substances présentent pour la santé des Canadiens et leur environnement, Gazette du Canada. Partie I, vol. 140, no 49, p. 4109-4117. Ottawa : Imprimeur de la Reine. Accès : http://www.gazette.gc.ca/archives/p1/2006/2006-12-09/pdf/g1-14049.pdf
Canada. Ministère de l'Environnement, Ministère de la Santé. 2006b. Loi canadienne sur la protection de l'environnement (1999) : Avis concernant certaines substances considérées comme priorités pour suivi. Gazette du Canada. Partie I, vol. 140, no 9, p. 435-459. Accès : http://www.gazette.gc.ca/archives/p1/2006/2006-03-04/pdf/g1-14009.pdf
Canada. Ministère de l'Environnement, Ministère de la Santé. 2008. Loi canadienne sur la protection de l'environnement (1999) : Avis de septième divulgation d'information technique concernant les substances identifiées dans le Défi.Gazette du Canada. Partie I, vol. 142, no 35, p. 2497-2501. Ottawa : Imprimeur de la Reine. Accès : http://www.gazette.gc.ca/rp-pr/p1/2008/2008-08-30/pdf/g1-14235.pdf
CASETOX [module de prévision]. 2008. Version 2.0. Beachwood (OH) : MultiCASE. [consulté le 30 sept. 2009]. Accès : http://www.multicase.com/products/prod03.htm[réserve de consultation].
Chen, H. 2006. Recent advances in azo dye degrading enzyme research. Curr. Protein Pept. Sci. 7:101111.
[CATABOL] Probabilistic assessment of biodegradability and metabolic pathways [modèle informatique]. c2004-2008. Version 5.10.2. Bourgas (Bulgarie) : Bourgas Prof. Assen Zlatarov University, Laboratory of Mathematical Chemistry. Accès : http://oasis-lmc.org/?section=software&swid=1
[ChemID] ChemID Plus Advanced. [base de données sur Internet]. 2009. [consultée le 20 avril 2009]. U.S. National Library of Medicine (MD), National Institute of Health. Accès : http://chem.sis.nlm.nih.gov/chemidplus/
Chen, H. 2006. Recent advances in azo dye degrading enzyme research. Curr. Protein Pept. Sci. 7:101111.
Choi, J.H., Kim, M.H., Park, J.S., Jeon, J.M., Kim, D.O., Towns, A.D. 2007. Coloration of poly(lactic acid) with disperse dyes. II. Dyeing characteristics and color fastness. Fibers and Polymers 8(1):37-42.
Chudgar, R.J., Oakes, J. 2003. Dyes, azo. In: Kirk-Othmer encyclopedia of chemical technology, édition en ligne. Accès : http://mrw.interscience.wiley.com/emrw/9780471238966/kirk/article/azochud.a01/
current/abstract? hd=All,azoandhd=All,dye [réserve de consultation]
[CII] Color Index International [base de donnée en ligne]. 2002. 4e éd. Research Triangle Park (NC) : American Association of Textile Chemists and Colorists. [consultée le 25 mars 2009]. Accès : http://www.colour-index.org/
Clariant. 1996. IUCLID dataset for C.I. Disperse Blue 79 (no CAS 12239-34-8).
Colon, D., Weber, E., Baughman, G. 2002. Sediment-associated reactions of aromatic amines. 2. QSAR development. Environ. Sci. Technol. 35(12):2443-2450.
[ConsExpo] Consumer Exposure Model [en ligne]. 2006. Version 4.1. Bilthoven (Pays-Bas) : Rijksinstituut voor Volksgezondheid en Milieu (Institut national néérlandais de la santé publique et de l'environnement). Accès : http://www.rivm.nl/en/healthanddisease/productsafety/ConsExpo.jsp#tcm:13–42840
[CPOPs] Modèle canadien de POP. 2008. Gatineau (Qc) : Environnement Canada, Division des substances existantes; Bourgas (Bulgarie) : Bourgas Prof. Assen Zlatarov University, Laboratory of Mathematical Chemistry. [Modèle élaboré à partir de celui de Mekenyan et al., 2005]. Disponible sur demande.
[Danish EPA] Danish Environmental Protection Agency. 1998. Azocolorants in Textiles and Toys, Environmental and Health Assessment. Environmental Project, no. 416 1998. Accès : http://www2.mst.dk/common/Udgivramme/Frame.asp? http://www2.mst.dk/udgiv/Publications/1998/87-7909-136-9/html/helepubl_eng.htm
de Bruijn, J., Busser, F., Seinen, W., Hermens, J. 1989. Determination of octanol/water partition coefficients for hydrophobic organic chemicals with the “slow-stirring” method. Environ. Toxicol. Chem. 8:499-512.
[DEREK] Deductive Estimation of Risk from Existing Knowledge [module de prévision sur CD ROM]. 2008. Version 10.0.2. Cambridge (MA) : Harvard University, LHASA Group. [consulté le 30 sept. 2009]. Accès : http://www.lhasalimited.org/index.php? cat=2&sub_cat=2# [réserve de consultation].
Dimitrov, S., Dimitrova, N., Parkerton, T., Comber, M., Bonnell, M., Mekenyan, O. 2005. Base-line model for identifying the bioaccumulation potential of chemicals. SAR QSAR Environ. Res. 16(6):531-554.
Dimitrov, S.D., Dimitrova, N.C., Walker, J.D., Veith, G.D., Mekenyan, O.G. 2002. Predicting bioconcentration factors of highly hydrophobic chemicals. Effects of molecular size. Pure Appl. Chem. 74(10):1823-1830.
[Environ] ENVIRON International Corporation. 2003a. Voluntary Children’s Chemical Evaluation Program Pilot (VCCEPP)–Tier 1 assessment of the potential health risks to children associated with exposure to the commercial pentabromodiphenyl ether product and appendices [en ligne]. Emerville (CA) : ENVIRON International Corporation. [Accès : http://www.epa.gov/oppt/vccep/pubs/chem22a.html]
[Environ] ENVIRON International Corporation. 2003b. Voluntary Children’s Chemical Evaluation Program Pilot (VCCEPP)–Tier 1 assessment of the potential health risks to children associated with exposure to the commercial octabromodiphenyl ether product and appendices [en ligne]. Emerville (CA) : ENVIRON International Corporation. [Accès : http://www.epa.gov/oppt/vccep/pubs/chem23a.h]
[ECOSAR] Ecological Structural Activity Relationships [en ligne]. 2004. Version 0.99h. Washington (DC) : U.S. Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY) : Syracuse Research Corporation. Accès : www.epa.gov/oppt/exposure/pubs/episuite.htm
Environnement Canada, Division de l'évaluation des produits chimiques. 2000. Environmental Categorization for Persistence Bioaccumulation and Inherent Toxicity of Substances on the Domestic Substances List Using QSARs (juillet 2000). Rapport final. Environnement Canada.
Environnement Canada. 1994. Soumission de l'essai de toxicité aiguë pour le poisson conformément au Règlement sur les renseignements concernant les substances nouvelles. Données présentées à la Division des substances nouvelles d'Environnement Canada.
Environnement Canada. 2006.Données pour certaines substances recueillies en vertu de l'article 71 de la Loi canadienne sur la protection de l'environnement (1999) : Avis concernant certaines substances considérées comme priorités pour suivi. Données préparées par Environnement Canada, Santé Canada, Programme des substances existantes.
Environnement Canada. 2009a. Données sur les substances du lot 7 recueillies en vertu de l'article 71 de la Loi canadienne sur la protection de l'environnement (1999) : Avis concernant certaines substances identifiées dans le septième lot du Défi. Données produites par la Division des substances existantes, Environnement Canada.
Environnement Canada. 2009b. Guidance for conducting ecological assessments under CEPA, 1999: science resource technical series, technical guidance module: Mass Flow Tool. Document de travail préliminaire. Gatineau (Qc) : Environnement Canada, Division des substances existantes.
Environnement Canada. 2009c. Assumptions, limitations and uncertainties of the mass flow tool for Disperse Red 179, CAS RN 16586-42-8. Document provisoire interne. Gatineau (Qc) : Environnement Canada, Division des substances existantes. Disponible sur demande.
Environnement Canada. 2009d. Assumptions, limitations and uncertainties of the mass flow tool for DAPEP, CASRN 25176-89-0. Document provisoire interne. Gatineau (Qc) : Environnement Canada, Division des substances existantes. Disponible sur demande.
Environnement Canada. 2009e. Site Specific Analysis report: CAS RN 16586-42-8 &25176-89-0, rapport inédit. Gatineau (Qc) : Environnement Canada, Division des évaluations écologiques.
Environnement Canada. 2009f. Mega Flush report: CASRN 16586-42-8, 2009-04-28. Rapport inédit. Gatineau (Qc) : Environnement Canada, Division des substances existantes.
Environnement Canada. 2009g. Mega Flush report: CASRN 25176-89-0, 2009-04-28. Rapport inédit. Gatineau (Qc) : Environnement Canada, Division des substances existantes.
[EPIsuite] Estimation Programs Interface Suite for Microsoft Windows [modèle d'estimation]. 2008. Version 4.0. Washington (DC) : U.S. Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY) : Syracuse Research Corporation. Accès : http://www.epa.gov/oppt/exposure/pubs/episuite.htm
[ETAD] Ecological and Toxicological Association of Dyes and Organic Pigments Manufacturers. 1983. Extractability of dyestuffs from textiles. Basel (Suisse) : Ecological and Toxicological Association of Dyes and Organic Pigments Manufacturers. ETAD Project A 4007.
[ETAD] Ecological and Toxicological Association of Dyes and Organic Pigments. Affiliés canadiens, Dayan, J., Trebitz, H. 1995. Health and environmental information on dyes used in Canada. Rapport inédit présenté à Environnement Canada, Division des substances existantes. En page couverture : An overview to assist in the implementation of the New Substances Notification Regulations under the Canadian Environmental Protection Act.
[ETAD] The Ecological and Toxicological Association of Dyes and Organic Pigments Manufacturers. 2004. Setting a risk based detection limit of sensitizing disperse dyes on textiles. Accès : www.etad.com/documents/Downloads/publications/detectionlimit.pdf
[ETAD] Ecological and Toxicological Association of Dyes and Organic Pigments Manufacturers. 2005. ETAD data for DSL categorization and screening, présenté à Environnement Canada le 27 octobre 2005. Rapport d'étude préparé par Intertek ASG, no de référence 2005/CC0157-001/REGIS.
Golka, K., Kopps, S., Myslaket, Z.W. 2004. Carcinogenicity of azo colorants: influence of solubility and bioavailability. Toxicology Letters 151:203-210
Health, Safety, and Human Factors Laboratory. 1978. Basic Toxicity of 2-[4-[(6-chloro-2-benzothiazolylazo)phenyl]-ethylamino]ethyl acetate. Toxicology Section, Health, Safety, and Human Factors Laboratory. Rapport soumis par la Eastman Kodak Company en 1992 à la U.S. Environmental Protection Agency Registration and Agreement for the TSCA 8(a) Compliance Audit Program.
Santé Canada. 1998. Exposure factors for assessing total daily intake of priority substances by the general population of Canada. Rapport inédit. Ottawa (Ont.) : Santé Canada, Direction de l'hygiène du milieu.
Helmes, C.T., Fung, V.A., Lewin, B., McCaleb, K.E., Malko, S., Pawlovich, A.M. 1982. A study of aromatic nitro compounds for the selection of candidates for carcinogen bioassay. J. Environ. Sci. Health A Environ. Sci. Eng. Toxic Hazard Subst. Control17:75-128.
Hunger, K., éd. 2003. Industrial dyes; chemistry, properties, applications. Weinheim (Allemagne) : WILEY-VCH Verlag GmbH & Co. KGaA.
Kosaka, H., Nakamura, S. 1990. Genotoxicity of synthetic dyes in umu test using Salmonella typhimurium TA1535/pSK1002 (1). Jpn. J. Ind. Health. 32:89-104. (cité également dans Reifferscheid & Heil, 1996)
[KOWWIN] Octanol-Water Partition Coefficient Program for Microsoft Windows [modèle d'estimation]. 2000. Version 1.67. Washington (DC) : U.S. Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY) : Syracuse Research Corporation. Accès : www.epa.gov/oppt/exposure/pubs/episuite.htm
Kraetke, R.M., Platzek, T. 2005. Exposure to chemicals in clothing textiles: methods and models [en ligne]. Abstract for Poster 74 at the conference “Occupational and environmental exposure of skin to chemicals--2005.” Washington (DC) : National Institute for Occupational Safety and Health. Accès : http://www.cdc.gov/niosh/topics/skin/OEESC2/AbPost074Kraetke.html
[Leadscope] Leadscope Model Applier [module de prévision]. 2009. Version 1.2.0-3. Columbus (OH) : Leadscope, Inc. [consulté le 30 sept. 2009]. Accès : http://www.leadscope.com/all_products.php[réserve de consultation].
Little, L.W., Lamb, J.C. III. 1973. Acute toxicity of 46 selected dyes to the fathead minnow, Pimephales promelas.Dyes and the Environment - Reports on Selected Dyes and Their Effects. American Dye Manufacturers Institute, Inc. 1:130.
Maradiya, H.R. 2004. Disperse dyes based on 2-aminoheterocycles. J. Saudi Chem. Soc. 8(3):495-504.
Meinke, M., Abdollahnia, M., Gähr, Platzek, T., Sterry, W., Lademann, J. 2009. Migration and penetration of a fluorescent textile dye into the skin – in vivo versus in vitro methods. Experimental Dermatology18(9):789-792.
Mekenyan, G., Dimitrov, S.D., Pavlov, T.S., Veith, G.D. 2005. POPs: a QSAR system for creating PBT profiles of chemicals and their metabolites. SAR QSAR Environ. Res.16(1-2):103-133.
[MITI] Ministry of International Trade & Industry (Japon), Basic Industries Bureau, Chemical Products Safety Division. 1992. Biodegradation and bioaccumulation data of existing chemicals based on the CSCL Japan. Tokyo (Japon) : Japan Chemical Industry Ecology-Toxicology & Information Centre.
Mortelmans, K., Haworth, S., Lawlor, T., Speck, W., Tainer, B., Zeiger, E. 1986. Salmonella mutagenicity tests: II. Results from the testing of 270 chemicals. Environ. Mutagen.8:1-119
Nakagawa, M., Kawai, K., Kawai, K. 1996. Multiple azo disperse dye sensitization mainly due to group sensitizations to azo dyes. Contact Dermatitis 34:6-11.
[NCI] National Chemical Inventories [base de données sur cédérom]. 2009. Columbus (OH) : American Chemical Society. [consultée le 11 mars 2009]. Accès : http://www.cas.org/products/cd/nci/index.html
Noriris, B., Smith, S. 2002. Research into the mouthing behaviour of children up to 5 years old. Rapport commandé par le Ministère du commerce et de l'industrie du Royaume-Uni [traduction], Londres (Royaume-Uni).
[NTP] National Toxicology Program. 1982. Study ID 70250: Test result for an in vitro genetic toxicology test (mutagenicity in Salmonella) for 2-amino-6-nitrobenzothiazole (6285-57-0). Research Triangle Park (NC) : National Institutes of Health's National Institute of Environmental Health Sciences (NIEHS). [base de donnée du NTP consultée le 23 nov. 2009]. Accès :
http://ntp-apps.niehs.nih.gov/ntp_tox/index.cfm? fuseaction=salmonella.salmonellaData&study_no=
702501&cas_no=6285%2D57%2D0&endpointlist=SA [cité également dans Mortelmans et al., 1986]
[NTP] National Toxicology Program. 1983. Study ID 832791: Test result for an in vitro genetic toxicology test (mutagenicity in Salmonella) for 2-amino-6-nitrobenzothiazole (6285-57-0). Research Triangle Park (NC) : National Institutes of Health's National Institute of Environmental Health Sciences (NIEHS). [base de données du NTP consultée le 23 nov. 2009]. Accès : http://ntp-apps.niehs.nih.gov/ntp_tox/index.cfm? fuseaction=salmonella.salmonellaData&study_no=
832791&cas_no=6285%2D57%2D0&endpointlist=SA [cité également dans Mortelmans et al., 1986]
[NTP] National Toxicology Program. 1986a. Study ID 461292: Test result for an in vitro genetic toxicology test (mutagenicity in Salmonella) for 5,6'-dichloro-2-benzothiazolamine (24072-75-1). Research Triangle Park (NC) : National Institutes of Health's National Institute of Environmental Health Sciences (NIEHS). [base de données du NTP consultée le 23 nov. 2009]. Accès : http://ntp-apps.niehs.nih.gov/ntp_tox/index.cfm? fuseaction=salmonella.overallresults&cas_no=
24072-75-1&endpointlist=SA [cité également dans Mortelmans et al., 1986
[NTP] National Toxicology Program. 1986b. Study ID C61712: Short-term toxicity studies (2-week, 13-week, dosed-feed) in rats and mice for 5,6'-dichloro-2-benzothiazolamine (24072-75-1). (aucun rapport de toxicité publié). Accès : http://ntp-apps.niehs.nih.gov/ntp_tox/index.cfm? fuseaction=shorttermbioassaydata.datasearch&chemical_name=5%2C6-Dichloro-2-benzothiazolamine&cas_no=24072-75-1&study_no=C61712&study_length=13%20Weeks
[NTP] National Toxicology Program. 1993. Study ID A42046: Test result for in vivo micronucleus induction in male and female mice for 5,6'-dichloro-2-benzothiazolamine (24072-75-1). Research Triangle Park (NC) : National Institutes of Health's National Institute of Environmental Health Sciences (NIEHS). [base de données du NTP consultée le 23 nov. 2009]. Accès : http://ntp-apps.niehs.nih.gov/ntp_tox/index.cfm? fuseaction=micronucleus.choosestudytype&cas_no=24072-75-1&endpointlist=MN[cité également dansWitt et al., 2000]
[NTP] National Toxicology Program. 2000. Short-term study toxicity. Prechronic toxicity for 5,6'-dichloro-2-benzothiazolamine (24072-75-1). Study ID C61712. Research Triangle Park (NC) : National Institutes of Health's National Institute of Environmental Health Sciences (NIEHS). [base de données du NTP consultée le 23 nov. 2009]. Accès : http://ntp-server.niehs.nih.gov/index.cfm? objectid=03621D4C-B63D-AED4-CB677FD7CC46D300
[OASIS Forecast] Optimized Approach based on Structural Indices Set [en ligne]. 2005. Version 1.20. Bourgas (Bulgarie) : Bourgas Prof. Assen Zlatarov University, Laboratory of Mathematical Chemistry. Accès : http://oasis-lmc.org/?section=software
[OCDE] Organisation de coopération et de développement économiques. 2004. Emission scenario document on adhesive formulation [en ligne]. Rapport final. Paris (France) : Direction de l'environnement de l'OCDE. (Series on Emission Scenario Documents). Accès : http://ascouncil.org/news/adhesives/docs/EPAFormulation.pdf
[OCDE] Organisation de coopération et de développement économiques. 2007. Draft emission scenario on textile manufacturing wool mills [en ligne]. Paris (France) : OCDE, Direction de l'environnement. Rapport no : ENV/JM/EEA(2004)8/1/REV, JT00175156. Accès : http://www.oecd.org/dataoecd/2/47/34003719.pdf
Pagga, U., Brown, D. 1986. The degradation of dyestuffs: Part II Behaviour of dyestuffs in aerobic biodegradation tests. Chemosphere 15(4):479-491.
Peters, A.T., Gbadamosi, N.M.A. 1992. 5,6-(6,7-) dichlorobenzothiazolylazo dyes for synthetic-polymer fibres. Dyes and Pigments 18:115-123.
Peters, A.T., Tsatsaroni, E., Xisai, M. 1992. Hetarylazo disperse dyes derived from 5,6-dichloro- and 6,7-dichloro-2 aminobenzothiazoles. Dyes and Pigments 20:41-51.
Platzek, T., Lang, C., Grohmann, G., Gi, U.S., Baltes, W. 1999. Formation of a carcinogenic aromatic amine from an azo dye by human skin bacteria in vitro. Human & Experimental Toxicology 18:552-559.
Razo-Flores, E., Luijten, M., Donlon, B., Lettinga, G., Field, J. 1997. Biodegradation of selected azo dyes under methanogenic conditions. Wat. Sci. Tech. 36(6-7):65-72.
Refferscheid, G., Heil, J. 1996. Validation of the SOS/umu test using results of 486 chemicals and comparison with the Ames test and carcinogenicity data. Mut. Res. 369:129-145.
[RIVM] Rijksinstituut voor Volksgezondheid en Milieu. 2005. ConsExpo 4.0. Consumer exposure and uptake models. Manuel du programme [en ligne]. Report No.: 320104004/2005. Bilthoven (Pays-Bas) : RIVM (Institut national néérlandais de la santé publique et de l'environnement). [consulté le 16 nov. 2009]. Accès : http://rivm.openrepository.com/rivm/bitstream/10029/7307/1/320104004.pdf
S.M.S Technology Co., Ltd. [date inconnue]. Material Safety Data Sheet (MSDS) for Navacron Disperse Scarlet GS [en ligne]. Accès : http://www.intonline.org/product/nava-doc/navacron-msds/9-Navacron%20dyes/msds(Navacron%20Scarlet%20GS).pdf
Safepharm Laboratories Ltd. 1990. Acute toxicity to rainbow trout. Project number 47/781. No de déclaration dans le cadre du défi : 11347.
Sakuratani, Y., Noguchi, Y., Kobayashi, K., Yamada, J., Nishihara, T. 2008. Molecular size as a limiting characteristic for bioconcentration in fish. J. Environ. Biol. 29(1):89-92.
Sandoz. 1975. Acute Fish Toxicity (Rainbow trout), 48 hr. Données tirées à partir des questionnaires volontaires relatifs aux substances contenues dans le lot 5 du Plan de gestion des produits chimiques. Préparé par Environnement Canada.
Sandoz. 1975. Voluntary Data Submission under Section 71.
Sarex Overseas. 1995. Material Safety Data Sheet (MSDS) for SARAPERSE RED 4G [en ligne]. Accès : http://www.sarex.com/dyesmsds/PS616.HTM
Savarino, P., Viscardi, G., Carpignano, R., Barni, E. 1989. Technical properties and photofading of disperse heterocyclic azo dyes. Dyes and Pigments 10:269-283.
Seifried, H.E., Seifried, R.M., Clarke, J.J., Junghans, T.B., San, R.H. 2006. A compilation of two decades of mutagenicity test results with the Ames Salmonella typhimurium and L5178Y mouse lymphoma cell mutation assays. Chem. Res. Toxicol. 19:627-44.
Shen, G., Hu, S. (Environmental Testing Laboratory, Shanghai Academy of Environmental Sciences, Shanghai, Chine). 2008. Bioconcentration Test of C.I. Disperse Orange 30 in Fish, préparé par Environmental Testing Laboratory, Shanghai Academy of Environmental Sciences, Shanghai (Chine) pour Dystar au nom de l'Ecological and Toxicological Association of the Dyes and Organic Pigments Manufacturers (ETAD), Bâle (Suisse). Rapport no S-070-2007. Présenté à Environnement Canada en avril 2008, no de déclaration dans le cadre du défi 8351.
Sijm, D.T.H.M., Schuurmann, G., deVries, P.J., Opperhuizen, A. 1999. Aqueous solubility, octanol solubility, and octanol/water partition coefficient of nine hydrophobic dyes. Environ. Toxicol. Chem. 18(6):1109-1117.
Stingley, R., Zou, W., Heinze, T., Chen, H., Cerniglia, C. 2009. Metabolism of azo dyes by human skin microbiota. J. Med.Microbiol. le 3 sept. 2009. [paru en ligne avant impression].
Talaska, G. 2003. Aromatic amines and human urinary bladder cancer: exposure sources and epidemiology. J. Environ. Sci. Health C. Environ. Carcinog. Ecotoxicol. Rev. 21(1):2943.
Tincher, W.C. 1988. Dyes in the environment: dyeing wastes in landfill. Étude commanditée par le US Operating Committee de l'ETAD.
[TOPKAT] Toxicity Prediction Program [en ligne]. 2004. Version 6.2. San Diego (CA) : Accelrys Software Inc. Accès : http://www.accelrys.com/products/topkat/index.html
Toxtree. Version 1.60. 2009. Logiciel conçu par Ideaconsult Ltd, Bulgarie.
[US EPA] U.S. Environmental Protection Agency. 2002. PBT Profiler Methodology [en ligne]. Washington (DC) : US EPA, Office of Pollution Prevention and Toxics. [consulté en août 2008]. Accès : http://www.pbtprofiler.net/methodology.asp
[US EPA] United States Environmental Protection Agency. 2002b. TSCA New Chemicals Program (NCP) Chemical Categories: Aminobenzothiozole Azo Dyes. Accès : http://www.epa.gov/oppt/newchems/pubs/cat02.htm#Aminobenzothiazole%20Azo%20Dyes
[US EPA] U.S. Environmental Protection Agency. 2009. Inventory update reporting, past IUR data: Nonconfidential production volume information submitted by companies under the 1986, 1990, 1994, 1998, and 2002 Inventory Update Reporting Regulation: CAS RN 16586-42-8 & CAS RN 25176-89-0 [en ligne]. Washington (DC) : U.S. Environmental Protection Agency. [consulté le 25 mars 2009]. Accès : http://www.epa.gov/oppt/iur/tools/data/2002-vol.htm
[WATERNT] Water Solubility Program [modèle d'estimation]. 2002. Version 1.00. Washington (DC) : U.S. Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY) : Syracuse Research Corporation. Accès : www.epa.gov/oppt/exposure/pubs/episuite.htm
[WSKOWWIN] Water Solubility for Organic Compounds Program for Microsoft Windows [modèle d'estimation]. 2000. Version 1.41. Washington (DC) : U.S. Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY) : Syracuse Research Corporation. Accès : www.epa.gov/oppt/exposure/pubs/episuite.htm
Weber, E.J., Adams, R.L. 1995. Chemical and sediment-mediated reduction of the azo dye disperse blue 79. Environ. Sci. Technol. 29(5):1163-1170.
Weber, E.J., Colon, D., Baughman, G.L. 2001. Sediment-associated reactions of aromatic amines. 1. Elucidation of sorption mechanisms. Environ. Sci. Technol. 35(12):2470-2475.
Witt, K.L., Knapton, A., Wehr, C.M., Hook, G.J., Mirsalis, J., Shelby, M.D., MacGregor, J.T. 2000. Micronucleated erythrocyte frequency in peripheral blood of B6C3F(1) mice from short-term, prechronic, and chronic studies of the NTP carcinogenesis bioassay program. Environ. Mol. Mutagen. 36(3):163-94.
Xu, H., Heinze, T.M., Chen, S., Cerniglia, C.E., Chen, H. 2007. Anaerobic Metabolism of 1-Amino-2-Naphthol-Based Azo Dyes (Sudan Dyes) by Human Intestinal Microflora. Appl. Environ. Microbiol. 73:7759-62.
Yen, C.C., Perenich, T.A., Baughman, G.L. 1989. Fate of dyes in aquatic systems II. Solubility and octanol/water partition coefficients of disperse dyes. Environ. Toxicol. Chem.8(11):981-986.
Yen, C.C., Perenich, T.A., Baughman, G.L. 1991. Fate of commercial disperse dyes in sediments. Environ. Toxicol. Chem. 10:1009-1017.
Évaluation de données expérimentales selon la méthode de Kollig* : hydrosolubilité
| Élément | Pondération | Réponse | Note | |
|---|---|---|---|---|
| * Kollig, H.P., 1988. Criteria for evaluating the reliability of literature data on environmental process constants. Environ Toxicol Chem 17:287-311. ** Le code de fiabilité pour les études éco-toxicologiques de catégorisation de LIS a été utilisé. |
||||
| Référence : Sijm DTHM, Schuurmann G, De Vries PJ et Opperhuizen A., 1999. Aqueous solubility, octanol solubility, and octanol/water partition coefficient of nine hydrophobic dyes. Environ. Toxicol. Chem. 18(6):1109-1117. | ||||
| Substance d'essai : N° CAS : 68133-69-7 | ||||
| Paramètre : Solubilité dans l'eau | ||||
| Pourriez-vous répéter l'expérience avec des informations disponibles? | 5 | Oui | 4 | |
| Un objectif clair a-t-il été fixé? | 1 | Oui | 1 | |
| La qualité de l'eau est-elle caractérisée ou identifiée (distillée ou désionisée)? | 2 | Oui, distillée | 2 | |
| Les résultats sont-ils présentés en détail, clairement et de façon intelligible? | 3 | Oui | 2 | |
| Les données proviennent-elles d'une source principale et non pas d'un article référencé? | 3 | Source principale | 3 | |
| Le produit chimique a-t-il été testé à des concentrations inférieures à sa solubilité dans l'eau? | 5 | s.o. | s.o. | |
| Des particules étaient-elles absentes? | 2 | Supposé | 2 | |
| Un produit chimique de référence à constante connue a-t-il été testé? | 3 | Non | 0 | |
| D'autres processus de devenir ont-ils été envisagés? | 5 | s.o. | s.o. | |
| Un contrôle (à blanc) a-t-il eu lieu? | 3 | Non indiqué | 0 | |
| La température a-t-elle été maintenue constante? | 5 | Non indiqué mais supposé. La solubilité dans l'eau a été estimée à l'aide d'une colonne de générateur comme l'a fait Opperhuizen, 1986 | 5 | |
| L'expérience a-t-elle été réalisée à température ambiante (15 à 30 °C)? | 3 | Non indiqué mais supposé. | 3 | |
| La pureté du produit chimique testé atelle été signalée (> 98 %)? | 3 | Non, mais les produits chimiques ont été obtenus auprès de Bayer AG, puis recristallisés en dichlorométhane afin d'ôter tout additif avant utilisation | 3 | |
| L'identité du produit chimique a-t-elle été prouvée? | 3 | Oui, garantie par Bayer AG | 3 | |
| L'origine du produit chimique a-t-elle été signalée? | 1 | Oui, Bayer AG | 1 | |
| Note : | 29/37 = 78 % | |||
| Degré de fiabilité** | 2 Confiance satisfaisante | |||
| Commentaires | ||||
Évaluation de données expérimentales selon la méthode de Kollig* : coefficient de partage octanol-eau (Koe)
| Élément | Pondération | Réponse | Note | |
|---|---|---|---|---|
| * Kollig, H.P., 1988. Criteria for evaluating the reliability of literature data on environmental process constants. Environ. Toxicol. Chem.17:287-311. ** Le code de fiabilité pour les études éco-toxicologiques de catégorisation de LIS a été utilisé. |
||||
| Référence :Sijm DTHM, Schuurmann G, De Vries PJ et Opperhuizen A., 1999. Aqueous solubility, octanol solubility, and octanol/water partition coefficient of nine hydrophobic dyes. Environ. Toxicol. Chem. 18(6):1109-1117. | ||||
| Substance d'essai : N° CAS : 68133-69-7 | ||||
| Paramètre :Coefficient de partage octanol/eau) (Koe) | ||||
| Pourriez-vous répéter l'expérience avec des informations disponibles? | 5 | Oui | 5 | |
| Un objectif clair a-t-il été fixé? | 1 | Oui | 1 | |
| La qualité de l'eau est-elle caractérisée ou identifiée (distillée ou désionisée)? | 2 | Distillée | 2 | |
| Les résultats sont-ils présentés en détail, clairement et de façon intelligible? | 3 | Oui | 3 | |
| Les données proviennent-elles d'une source principale et non pas d'un article référencé? | 3 | Oui | 3 | |
| Le produit chimique a-t-il été testé à des concentrations inférieures à sa solubilité dans l'eau? | 5 | s.o. | s.o. | |
| Des particules étaient-elles absentes? | 2 | Oui | 2 | |
| Un produit chimique de référence à constante connue a-t-il été testé? | 3 | Non | 0 | |
| D'autres processus de devenir ont-ils été envisagés? | 5 | s.o. | s.o. | |
| Un contrôle (à blanc) a-t-il eu lieu? | 3 | Non indiqué | 0 | |
| La température a-t-elle été maintenue constante? | 5 | Oui, utilisé le protocole de la méthode de brassage lent de De Bruijn et al., 1989 | 5 | |
| L'expérience a-t-elle été réalisée à température ambiante (15 à 30 °C)? | 3 | Oui, 25 °C (protocole de la méthode de brassage lent de De Bruijn et al., 1989) | 3 | |
| La pureté du produit chimique testé a-t-elle été signalée (> 98 %)? | 3 | Non, mais les produits chimiques ont été obtenus auprès de Bayer AG, puis recristallisés en dichlorométhane afin d'ôter tout additif avant utilisation | 3 | |
| L'identité du produit chimique a-t-elle été prouvée? | 3 | Oui, garantie par Bayer AG | 3 | |
| L'origine du produit chimique a-t-elle été signalée? | 1 | Oui, Bayer AG | 1 | |
| Note : | 31/37 = 83 % | |||
| Degré de fiabilité** | 1 Confiance élevée | |||
| Commentaires | ||||
Formulaire pour sommaires de rigueur d'études : persistance dans l'eau, les sédiments et les sols
| Non | Élément | Pondération | Oui/Non | Veuillez préciser | |
|---|---|---|---|---|---|
| 1 | Référence : Foron Rubin RD-S Presskuchen trocken (Disperse Red 179) Biodégradabilité Intrinsèque – Évaluation de la biodégradabilité aérobie en milieu aqueux : Test ZahnWellens/EMPA. Rapport BMG no. 709/c-03, octobre 2003. Soumis à Environnement Canada dans l'étude de l'article 71 (Environnement Canada, 2009a) | ||||
| 2 | Identité de la substance : n° CAS | s.o. | n | Non précisé, mais il s'agit du Disperse Red 179 (16586428) | |
| 3 | Identité de la substance : nom(s) chimique(s) | s.o. | n | Foron Rubin RD-S | |
| 4 | Composition chimique de la substance | 2 | n | Seul le contenu carbone organique total est mentionné. Aucune mention de produits secondaires. | |
| 5 | Pureté chimique | 1 | n | Le produit commercial luimême, Foron Rubine RD-S, est testé. Il contient 34,3% en poids de 16586-42-8. | |
| Méthode | |||||
| 6 | Référence | 1 | O | Le test est celui de Zahn-Wellens/EMPA | |
| 7 | Méthode de l'OCDE, de l'UE, nationale ou autre méthode standard? | 3 | O | ||
| 8 | Justification de la/du méthode/protocole si une méthode non standard a été utilisée | 2 | Non applicable | ||
| 9 | BPL (bonne pratique de laboratoire) | 3 | n | Pas clairement indiqué | |
| Conception/conditions du test | |||||
| 10 | Type de test (hydrolyse, biodégradation, etc.) | s.o. | o | Biodégradation | |
| 11 | Type de conditions du test (aérobie ou anaérobie) | s.o. | O | Aérobie | |
| 12 | Milieu du test (eau, sédiment ou sol) | s.o. | O | Boues activées | |
| 13 | Durée du test | s.o. | O | 28 jours | |
| 14 | Contrôles négatifs ou positifs? | 1 | O | Contrôle positif au diéthylène glycol | |
| 15 | Nombre de répétitions (incluant les contrôles) | 1 | O | 2 répétitions pour le test, 2 répétitions pour l'essai à blanc et 1 pour le contrôle du test | |
| 16 | Concentrations mesurées rapportées? | 3 | O | La dégradation du matériel de test a été suivie par la détermination du carbone inorganique (CI) à intervalles réguliers. Les concentrations des produits chimiques à étudier n'ont pas été mesurées pendant le test. | |
| 17 | Méthode/instrument analytique | 1 | O | Le carbone inorganique (CI) a été déterminé de la même façon que le produit chimique organique défini sans laver les échantillons avant analyse. | |
| Détails sur la biodégradation | |||||
| 18 | Type de biodégradation (immédiate ou intrinsèque) signalée? | 2 | o | Biodégradation intrinsèque recherchée selon le test Zahn-Wellens | |
| 19 | Lorsque le type de biodégradation (immédiate ou intrinsèque) n'est pas signalé, une information indirecte permet-elle l'identification du type de biodégradation? | 1 | s.o. | ||
| 20 | Origine de l'inoculum | 1 | O | Il est mentionné que l'inoculum provient d'une usine de traitement des déchets. Cependant, le nom de l'usine n'est pas mentionné. | |
| 21 | Concentration de l'inoculum ou nombre de micro-organismes | 1 | O | 0,2 g/L de matière sèche | |
| 22 | L'inoculum a-t-il été préconditionné et la préadaptation rapportée? | 1 | N | ||
| 23 | L'inoculum a-t-il été préconditionné et la préadaptation a-t-elle été appropriée à la méthode utilisée? | s.o. | s.o. | ||
| 24 | Température | 1 | O | 22 ± 0,5°C, en chambre obscure | |
| 25 | Le pourcentage de dégradation du composé de référence a-t-il atteint les niveaux requis avant le 14e jour? | s.o. | O | Le diéthylèneglycol a été dégradé à 99% avant le 14ème jour. | |
| 26 | Sol : humidité du sol signalée? | 1 | s.o. | ||
| 27 | Sol et sédiments : contenu en matière organique du sol (MOS) de base signalé? | 1 | s.o. | ||
| 28 | Sol et sédiments : teneur en argile signalée? | 1 | s.o. | ||
| 29 | Sol et sédiments : CEC (capacité d'échange cationique) signalée? | 1 | s.o. | ||
| Détails sur l'hydrolyse | |||||
| 30 | Valeurs du pH signalées? | 1 | s.o. | ||
| 31 | Température | 1 | s.o. | ||
| 32 | Les concentrations appropriées de la substance ont-elles été utilisées? | s.o. | |||
| 33 | Si un solvant a été utilisé, l'a-t-il été de manière appropriée? | s.o. | |||
| Détails sur la photo-dégradation | |||||
| 34 | Température | 1 | s.o. | ||
| 35 | Source lumineuse | 1 | s.o. | ||
| 36 | Spectre lumineux (nm) | 1 | s.o. | ||
| 37 | Intensité relative en fonction de l'intensité lumineuse du soleil | 1 | s.o. | ||
| 38 | Spectre d'une substance | 1 | s.o. | ||
| 39 | Photolyse indirecte :Sensibilisateur (type) | 1 | s.o. | ||
| 40 | Photolyse indirecte :concentration du sensibilisateur | 1 | s.o. | ||
| Résultats | |||||
| 41 | Critère d'évaluation et valeur | s.o. | s.o. | Dégradation de 0%. L'élimination du composé à 99% est dûe à l'absorption ou à la sédimentation, non à la biodégradation. | |
| 42 | Produits de dégradation | s.o. | |||
| 43 | Note : ... % | 68,2 | |||
| 44 | Code de fiabilité d'Environnement Canada : | 2 | |||
| 45 | Catégorie de fiabilité (élevée, satisfaisante, basse) : | Confiance satisfaisante | |||
Formulaire pour sommaires de rigueur d'études : persistance dans l'eau, les sédiments et les sols
| Non | Élément | Pondération | Oui/Non | Veuillez préciser | |
|---|---|---|---|---|---|
| 1 | Référence : 13365Submission028, CI Disperse Red 153. Biodégradabilité Intrinsèque – Évaluation de la biodégradabilité aérobie en milieu aqueux : Rapport BMG n° 800/c-00 (n° CAS 25176-89-0), janvier 2000. Soumis à Environnement Canada dans l'étude de l'article 71 (Environnement Canada, 2009a) |
||||
| 2 | Identité de la substance : n° CAS | s.o. | n | N° CAS 25176-89-0 |
|
| 3 | Identité de la substance : nom(s) chimique(s) | s.o. | n | C.I. Disperse Red 153 | |
| 4 | Composition chimique de la substance | 2 | n | Seul le contenu carbone organique total est mentionné. Pas de mention de produits secondaires (c'està-dire que c'est à 100 % du 25176-89-0). | |
| 5 | Pureté chimique | 1 | n | Le produit testé est le C.I. Disperse Red 153 | |
| Méthode | |||||
| 6 | Référence | 1 | O | Le test est celui de Zahn-Wellens/EMPA | |
| 7 | Méthode de l'OCDE, de l'UE, nationale ou autre méthode standard? | 3 | O | ||
| 8 | Justification de la/du méthode/protocole si une méthode non standard a été utilisée | 2 | s.o. | ||
| 9 | BPL (bonne pratique de laboratoire) | 3 | n | Pas clairement indiqué | |
| Conception/conditions du test | |||||
| 10 | Type de test (hydrolyse, biodégradation, etc.) | s.o. | o | Biodégradation | |
| 11 | Type de conditions du test (aérobie ou anaérobie) | s.o. | O | Aérobie | |
| 12 | Milieu du test (eau, sédiment ou sol) | s.o. | O | Boues activées | |
| 13 | Durée du test | s.o. | O | 28 jours | |
| 14 | Contrôles négatifs ou positifs? | 1 | O | Contrôle positif au diéthylène glycol | |
| 15 | Nombre de répétitions (incluant les contrôles) | 1 | O | 2 répétitions pour le test, 2 répétitions pour l'essai à blanc et 1 pour le contrôle du test | |
| 16 | Concentrations mesurées rapportées? | 3 | O | La dégradation du matériel de test a été suivie par la détermination du carbone organique dissous (DOC) à intervalles réguliers. Les concentrations des produits chimiques à étudier n'ont pas été mesurées pendant le test. | |
| 17 | Méthode/instrument analytique | 1 | O | Le produit chimique organique défini a été déterminé en double avec un analyseur Shimadzu 5050 de TOC, par le mode NPOC. Le carbone inorganique (CI) a été déterminé de la même façon que le produit chimique organique défini sans laver les échantillons avant analyse. | |
| Détails sur la biodégradation | |||||
| 18 | Type de biodégradation (immédiate ou intrinsèque) signalée? | 2 | O | Biodégradation intrinsèque recherchée selon le test ZahnWellens | |
| 19 | Lorsque le type de biodégradation (immédiate ou intrinsèque) n'est pas signalé, une information indirecte permet-elle l'identification du type de biodégradation? | 1 | s.o. | ||
| 20 | Origine de l'inoculum | 1 | O | Il est mentionné que l'inoculum provient d'une usine de traitement des déchets. Cependant, le nom de l'usine n'est pas mentionné. | |
| 21 | Concentration de l'inoculum ou nombre de microorganismes | 1 | O | 0,2 g/L de matière sèche | |
| 22 | L'inoculum a-t-il été préconditionné et la préadaptation rapportée? | 1 | N | ||
| 23 | L'inoculum a-t-il été préconditionné et la préadaptation a-t-elle été appropriée à la méthode utilisée? | s.o. | s.o. | ||
| 24 | Température | 1 | O | 22 ± 0,5 °C, en chambre obscure | |
| 25 | Le pourcentage de dégradation du composé de référence a-t-il atteint les niveaux requis avant le 14e jour? | s.o. | O | Le composé de référence a atteint 87 % de dégradation après 14 jours. | |
| 26 | Sol : humidité du sol signalée? | 1 | s.o. | ||
| 27 | Sol et sédiments : contenu en matière organique du sol (MOS) de base signalé? | 1 | s.o. | ||
| 28 | Sol et sédiments : teneur en argile signalée? | 1 | s.o. | ||
| 29 | Sol et sédiments : CEC (capacité d'échange cationique) signalée? | 1 | s.o. | ||
| Détails sur l'hydrolyse | |||||
| 30 | Valeurs du pH signalées? | 1 | s.o. | ||
| 31 | Température | 1 | s.o. | ||
| 32 | Les concentrations appropriées de la substance ont-elles été utilisées? | s.o. | |||
| 33 | Si un solvant a été utilisé, l'a-t-il été de manière appropriée? | s.o. | |||
| Détails sur la photo-dégradation | |||||
| 34 | Température | 1 | s.o. | ||
| 35 | Source lumineuse | 1 | s.o. | ||
| 36 | Spectre lumineux (nm) | 1 | s.o. | ||
| 37 | Intensité relative en fonction de l'intensité lumineuse du soleil | 1 | s.o. | ||
| 38 | Spectre d'une substance | 1 | s.o. | ||
| 39 | Photolyse indirecte :sensibilisateur (type) | 1 | s.o. | ||
| 40 | Photolyse indirecte :concentration de sensibilisateur | 1 | s.o. | ||
| Résultats | |||||
| 41 | Critère d'évaluation et valeur | s.o. | s.o. | Non dégradé | |
| 42 | Produits de dégradation | s.o. | |||
| 43 | Note : ... % | 68,2 | |||
| 44 | Code de fiabilité d'Environnement Canada : | 2 | |||
| 45 | Catégorie de fiabilité (élevée, satisfaisante, basse) : | Confiance satisfaisante | |||
Formulaire pour sommaires de rigueur d'études : toxicité intrinsèque pour les organismes aquatiques
| Non | Élément | Pondération | Oui/Non | Veuillez préciser | |
|---|---|---|---|---|---|
| 1 | Référence : 13365 Submission 025 Foron Rubin RD-S Presskuchen trocken (Disperse Red 179) 96-hr Acute Toxicity to Poecilia reticulata (Guppy). Rapport BMG n° 709/b-03, octobre 2003. Soumis à Environment Canada dans l'étude de l'article 71 (Environnement Canada, 2009a) | ||||
| 2 | Identité de la substance : n° CAS | s.o. | O | Le produit chimique testé est le Foron Rubin RD-S Presskuchen trocken | |
| 3 | Identité de la substance : nom(s) chimique(s) | s.o. | O | Foron Rubin RD-S Presskuchen trocken (Disperse Red 179) | |
| 4 | Composition chimique de la substance | 2 | N | Composition du produit non présentée | |
| 5 | Pureté chimique | 1 | N | Indiquée par l'article 71, pas l'étude de toxicité. Le test indique un ingrédient à 100 % actif, ce qui est impossible selon l'article 71. | |
| 6 | Persistance/stabilité de la substance d'essai en solution aquatique signalée? | 1 | N | Pas d'information | |
| Méthode | |||||
| 7 | Référence | 1 | O | Le test a été réalisé selon le guide de procédure 203 de l'OCDE et la directive EEC 92/69/EEC | |
| 8 | Méthode de l'OCDE, de l'UE, nationale ou autre méthode standard? | 3 | O | OCDE et Communauté économique européenne | |
| 9 | Justification de la/du méthode/protocole si une méthode non standard a été utilisée | 2 | Non applicable | ||
| 10 | BPL (bonne pratique de laboratoire) | 3 | N | Non précisé | |
| Organisme d'essai | |||||
| 11 | Identité de l'organisme : nom | s.o. | O | Poecilia reticulata (guppy) | |
| 12 | Nom latin ou noms latin et commun signalés? | 1 | O | Poecilia reticulata (guppy) | |
| 13 | Âge/stade du cycle biologique de l'organisme d'essai | 1 | N | Le stade du cycle biologique des organismes d'essai n'est pas précisé, mais on pense qu'il existe des divergences dues aux variations de longueur et surtout de poids. | |
| 14 | Longueur et/ou poids | 1 | O | Ceci est un problème, car de grandes variations peuvent être observées entre les poissons. | |
| 15 | Sexe | 1 | N | ||
| 16 | Nombre d'organismes par répétition | 1 | O | Minimum autorisé par protocole d'essai : 7 poissons | |
| 17 | Taux de chargement de l'organisme | 1 | O | Les taux de chargement de l'organisme sont < 1 g de poisson/L. Ils sont de 0,533 pour 100 mg/L, de 0,563 pour 10 mg/L et de 0,538 pour 1 mg/L. | |
| 18 | Type de nourriture et périodes d'alimentation pendant la période d'acclimatation | 1 | O | ||
| Conception/conditions du test | |||||
| 19 | Type de test (aigu ou chronique) | s.o. | O | Aigu | |
| 20 | Type d'expérience (laboratoire ou terrain) | s.o. | O | Laboratoire | |
| 21 | Voies d'exposition (nourriture, eau, les deux) | s.o. | O | Eau | |
| 22 | Durée d'exposition | s.o. | O | 96 heures | |
| 23 | Contrôles négatifs ou positifs (veuillez préciser) | 1 | O | Positif | |
| 24 | Nombre de répétitions (incluant les contrôles) | 1 | O | Un total de 4 répétitions (1 pour chaque concentration et 1 pour le contrôle) | |
| 25 | Concentrations nominales rapportées? | 1 | O | 4 incluant le contrôle | |
| 26 | Concentrations mesurées rapportées? | 3 | N | En fait, la toxicité signalée dépasse la solubilité du composé | |
| 27 | Type de nourriture et périodes d'alimentation pendant les tests à long terme | 1 | Non applicable | ||
| 28 | Les concentrations ont-elles été mesurées périodiquement (particulièrement lors du test chronique)? | 1 | N | ||
| 29 | Les conditions du milieu d'exposition correspondaient-elles au produit chimique particulier signalé? (par exemple, pour la toxicité du métal : pH, DOC/TOC, dureté de l'eau, température) | 3 | O | ||
| 30 | Photopériode et intensité lumineuse | 1 | O | Photopériode de 16, aucune idée de l'intensité réelle | |
| 31 | Préparation de la solution de stock et d'essai | 1 | O | Étant donné la solubilité limitée dans l'eau, les concentrations d'essai individuelles ont été préparées en ajoutant les quantités respectives d'une solution de stock acétonique aux récipients en verre vides. Après évaporation complète du solvant, l'eau du robinet a été ajoutée.Des détails sur les solutions du stock sont aussi disponibles. | |
| 32 | Un agent solubilisant/émulsifiant a-t-il été utilisé si le produit chimique était faiblement soluble ou instable? | 1 | O | Étant donné la solubilité limitée dans l'eau, les concentrations d'essai individuelles ont été préparées en ajoutant les quantités respectives d'une solution de stock acétonique aux récipients en verre vides. Après évaporation complète du solvant, l'eau du robinet a été ajoutée. | |
| 33 | Si un solubilisant/émulsifiant a été utilisé, sa concentration a-t-elle été signalée? | 1 | N | Non, mais l'acétone s'est évaporé. | |
| 34 | Si un solubilisant/émulsifiant a été utilisé, son écotoxicité a-t-elle été signalée? | 1 | N | L'acétone s'est évaporée et était donc absente. | |
| 35 | Intervalles de contrôle analytique | 1 | N | ||
| 36 | Méthodes statistiques utilisées | 1 | N | ||
| Informations relatives à la qualité des données | |||||
| 37 | Le critère d'évaluation a-t-il été directement causé par la toxicité du produit chimique et non par l'état de santé de l'organisme (par exemple, lorsque la mortalité lors du contrôle est > 10 %) ou des effets physiques (par exemple, « effet d'ombrage »)? | s.o. | |||
| 38 | L'organisme d'essai correspondait-il à l'environnement canadien? | 3 | N | ||
| 39 | Les conditions du test (pH, température, DO, etc.) étaient-elles adaptées à l'organisme d'essai? | 1 | O | Le pH était un peu élevé (8,1 à 8,5); les concentrations en oxygène étaient normales (6,9 à 7,9 mg/L). | |
| 40 | Le type de système et sa conception (statique, semi-statique, flux continu, scellé ou ouvert, etc.) correspondent-ils aux propriétés de la substance et à la nature/aux habitudes de l'organisme? | 2 | O | ||
| 41 | Le pH de l'eau du test se situait-il dans la plage habituelle pour l'environnement canadien (6 à 9)? | 1 | O | ||
| 42 | La température de l'eau du test se situait-elle dans la plage habituelle pour l'environnement canadien (5 à 27 °C)? | 1 | O | ||
| 43 | La valeur de la toxicité était-elle inférieure à la solubilité dans l'eau du produit chimique? | 3 | N | ||
| Résultats | |||||
| 44 | Valeurs de la toxicité (préciser le critère d'évaluation et la valeur) | s.o. | s.o. | ||
| 45 | Autres critères d'évaluation signalés : par exemple, FBC/FBA, CMEO/CSEO (préciser)? | s.o. | O | CSEO > 10 mg/L basé sur une concentration nominale | |
| 46 | Autres effets indésirables (par exemple, cancérogénicité, mutagénicité) signalés? | s.o. | O | Perte de coordination, hypoactivité et nage sur le dos ont aussi été signalées. | |
| 47 | Note : ... % | 50,0 | |||
| 48 | Code de fiabilité d'Environnement Canada : | 3 | |||
| 49 | Catégorie de fiabilité (élevée, satisfaisante, basse) : | Confiance basse | |||
Formulaire pour sommaires de rigueur d'études : toxicité intrinsèque pour les organismes aquatiques
| Non | Élément | Poids | Oui/Non | Veuillez préciser |
|---|---|---|---|---|
| 1 | Référence : 13365 Submission 026 C.I. Disperse Red 153. 96-hour Acute Toxicity to Poecilia reticulata (Guppy) Limit Test (100 mg/L). Rapport BMG n° 800/a-00 soumis à Environnement Canada dans l'étude de l'article 71 (Environnement Canada, 2009a) | |||
| 2 | Identité de la substance : n° CAS | s.o. | 25176-89-0 | |
| 3 | Identité de la substance : nom(s) chimique(s) | s.o. | C.I. Disperse Red 153 | |
| 4 | Composition chimique de la substance | 2 | N | La substance est identifiée comme étant le C.I. Disperse Red 153, Lot n° 99L094 Contrôle 100811B, avec un ingrédient actif à 100 %. Peu d'informations. |
| 5 | Pureté chimique | 1 | N | Le rapport d'essai mentionne une pureté de 100%, mais il reste à déterminer si cela concerne la pureté à 100 % du produit commercial ou bien du n° CAS. |
| 6 | Persistance/stabilité de la substance d'essai en solution aquatique signalée? | 1 | N | Pas d'information |
| Méthode | ||||
| 7 | Référence | 1 | O | Le test a été réalisé selon le guide de procédure 203 de l'OCDE et la directive EEC 92/69/EEC |
| 8 | Méthode de l'OCDE, de l'UE, nationale ou autre méthode standard? | 3 | O | OCDE et Communauté économique européenne |
| 9 | Justification de la/du méthode/protocole si une méthode non standard a été utilisée | 2 | Non applicable | |
| 10 | BPL (bonne pratique de laboratoire) | 3 | N | Non précisé |
| Organisme d'essai | ||||
| 11 | Identité de l'organisme : nom | s.o. | O | Poecilia reticulata (guppy) |
| 12 | Nom latin ou noms latin et commun signalés? | 1 | O | Poecilia reticulata (guppy) |
| 13 | Âge/stade du cycle biologique de l'organisme d'essai | 1 | N | Le stade du cycle biologique des organismes d'essai n'est pas précisé, mais on pense qu'il existe des divergences dues aux variations de longueur et surtout de poids. |
| 14 | Longueur et/ou poids | 1 | O | Ceci est un problème, car de grandes variations peuvent être observées entre les poissons. |
| 15 | Sexe | 1 | N | |
| 16 | Nombre d'organismes par répétition | 1 | O | Minimum autorisé par protocole d'essai : 7 poissons |
| 17 | Taux de chargement de l'organisme | 1 | O | Les taux de chargement de l'organisme sont < 1 gramme de poisson/L. De 0,584 g pour 100 mg/L. |
| 18 | Type de nourriture et périodes d'alimentation pendant la période d'acclimatation | 1 | O | |
| Conception/conditions du test | ||||
| 19 | Type de test (aigu ou chronique) | s.o. | O | Aigu |
| 20 | Type d'expérience (laboratoire ou terrain) | s.o. | O | Laboratoire |
| 21 | Voies d'exposition (nourriture, eau, les deux) | s.o. | O | Eau |
| 22 | Durée d'exposition | s.o. | O | 96 heures |
| 23 | Contrôles négatifs ou positifs (veuillez préciser) | 1 | O | Positif |
| 24 | Nombre de répétitions (incluant les contrôles) | 1 | O | Deux répétitions (100 mg/L et contrôle) |
| 25 | Concentrations nominales rapportées? | 1 | O | Une seule concentration nominale |
| 26 | Concentrations mesurées rapportées? | 3 | N | |
| 27 | Type de nourriture et périodes d'alimentation pendant les tests à long terme | 1 | Non applicable | |
| 28 | Les concentrations ont-elles été mesurées périodiquement (particulièrement lors du test chronique)? | 1 | N | |
| 29 | Les conditions du milieu d'exposition correspondaient-elles au produit chimique particulier signalé? (par exemple, pour la toxicité du métal : pH, DOC/TOC, dureté de l'eau, température) | 3 | O | |
| 30 | Photopériode et intensité lumineuse | 1 | O | Photopériode de 16, aucune idée de l'intensité réelle. |
| 31 | Préparation de la solution de stock et d'essai | 1 | O | Étant donné la solubilité limitée dans l'eau, les concentrations d'essai individuelles ont été préparées en ajoutant les quantités respectives d'une solution de stock acétonique aux récipients en verre vides. Après évaporation complète du solvant, l'eau du robinet a été ajoutée.Des détails sur les solutions du stock sont aussi disponibles. |
| 32 | Un agent solubilisant/émulsifiant a-t-il été utilisé si le produit chimique était faiblement soluble ou instable? | 1 | O | Étant donné la solubilité limitée dans l'eau, les concentrations d'essai individuelles ont été préparées en ajoutant les quantités respectives d'une solution de stock acétonique aux récipients en verre vides. Après évaporation complète du solvant, l'eau du robinet a été ajoutée. |
| 33 | Si un solubilisant/émulsifiant a été utilisé, sa concentration a-t-elle été signalée? | 1 | N | Non, mais l'acétone s'est évaporé. |
| 34 | Si un solubilisant/émulsifiant a été utilisé, son écotoxicité a-t-elle été signalée? | 1 | N | L'acétone s'est évaporée et était donc absente. |
| 35 | Intervalles de contrôle analytique | 1 | N | |
| 36 | Méthodes statistiques utilisées | 1 | N | |
| Informations relatives à la qualité des données | ||||
| 37 | Le critère d'évaluation a-t-il été directement causé par la toxicité du produit chimique et non par l'état de santé de l'organisme (par exemple, lorsque la mortalité lors du contrôle est > 10 %) ou des effets physiques (par exemple, « effet d'ombrage »)? | s.o. | ||
| 38 | L'organisme d'essai correspondait-il à l'environnement canadien? | 3 | N | |
| 39 | Les conditions du test (pH, température, DO, etc.) étaient-elles adaptées à l'organisme d'essai? | 1 | O | Le pH était un peu élevé (8,6 à 8,9); la concentration en oxygène était normales (7,5 à 7,9 mg/L). |
| 40 | Le type de système et sa conception (statique, semi-statique, flux continu, scellé ou ouvert, etc.) correspondent-ils aux propriétés de la substance et à la nature/aux habitudes de l'organisme? | 2 | O | |
| 41 | Le pH de l'eau du test se situait-il dans la plage habituelle pour l'environnement canadien (6 à 9)? | 1 | O | |
| 42 | La température de l'eau du test se situait-elle dans la plage habituelle pour l'environnement canadien (5 à 27 °C)? | 1 | O | |
| 43 | La valeur de la toxicité était-elle inférieure à la solubilité dans l'eau du produit chimique? | 3 | N | |
| Résultats | ||||
| 44 | Valeurs de la toxicité (préciser le critère d'évaluation et la valeur) | s.o. | s.o. | |
| 45 | Autres critères d'évaluation signalés : par exemple, FBC/FBA, CMEO/CSEO (préciser)? | s.o. | O | CSEO > 100 mg/L basé sur des concentrations nominales |
| 46 | Autres effets indésirables (par exemple, cancérogénicité, mutagénicité) signalés? | s.o. | O | Perte de coordination, hypoactivité et nage sur le dos ont aussi été recherchées. |
| 47 | Note : ... % | 50,0 | ||
| 48 | Code de fiabilité d'Environnement Canada : | 3 | ||
| 49 | Catégorie de fiabilité (élevée, satisfaisante, basse) : | Confiance basse | ||
Formulaire pour sommaires de rigueur d'études : organismes aquatiques B
| Non | Élément | Pondération | Oui/Non | Veuillez préciser | ||
|---|---|---|---|---|---|---|
| 1 | Référence : Shen G, and Hu S. 2008. Bioconcentration Test of C.I. Disperse Orange 30 in Fish. Préparé par Environmental Testing Laboratory, Académie des Sciences de l'Environnement de Shanghai, Shanghai, Chine, pour Dystar au nom de l'Association écologique et toxicologique des fabricants de colorants et de pigments organiques (ETAD), Bâle, Suisse. Rapport n° S-070-2007. Soumis à Environnement Canada en Avril 2008. Soumission au défi ID n° 8351. | |||||
| 2 | Identité de la substance : n° CAS | s.o. | O | 5261-31-4 | ||
| 3 | Identité de la substance : nom(s) chimique(s) | s.o. | O | Propanenitrile, 3-[[2-(acétyloxy)éthyle][4-[(2,6-dichloro-4-nitrophényl)azo]phényl]amino]- | ||
| 4 | Composition chimique de la substance | 2 | N | |||
| 5 | Pureté chimique | 1 | N | |||
| 6 | Persistance/stabilité de la substance d'essai en solution aquatique signalée? | 1 | N | |||
| 7 | Si le matériau d'essai est radio-marqué, la/les position(s) précise(s) de l'/des atome(s) marqué(s) et le pourcentage de radioactivité associé aux impuretés ont-ils été signalés? | 2 | s.o. | |||
| Méthode | ||||||
| 8 | Référence | 1 | O | Guide de l'OCDE pour le test des produits chimiques n° 305B-1996 | ||
| 9 | Méthode de l'OCDE, de l'UE, nationale ou autre méthode standard? | 3 | O | OCDE | ||
| 10 | Justification de la/du méthode/protocole si une méthode non standard a été utilisée | 2 | ||||
| 11 | BPL (bonne pratique de laboratoire) | 3 | N | |||
| Organisme d'essai | ||||||
| 12 | Identité de l'organisme : nom | s.o. | O | Poisson zèbre, Brachydanio rerio | ||
| 13 | Nom latin ou noms latin et commun signalés? | 1 | O | Les deux | ||
| 14 | Âge/stade du cycle biologique de l'organisme d'essai | 1 | N | |||
| 15 | Longueur et/ou poids | 1 | O | Longueur moyenne du corps 3,91 ± 0,18 cm et poids moyen du corps 0,32 ± 0,06 g | ||
| 16 | Sexe | 1 | N | |||
| 17 | Nombre d'organismes par répétition | 1 | O | 7 | ||
| 18 | Taux de chargement de l'organisme | 1 | O | 20 mg/L | ||
| 19 | Type de nourriture et périodes d'alimentation pendant la période d'acclimatation | 1 | O | Mise au régime avec un poisson du commerce jusqu'à un jour avant le début du test | ||
| Conception/conditions du test | ||||||
| 20 | Type d'expérience (laboratoire ou terrain) | s.o. | O | Laboratoire | ||
| 21 | Voies d'exposition (nourriture, eau, les deux) | s.o. | O | Eau | ||
| 22 | Durée d'exposition | s.o. | O | 28 jours | ||
| 23 | Nombre de répétitions (incluant les contrôles) | 1 | O | |||
| 24 | Concentrations | 1 | O | 20 mg/L | ||
| 25 | Type/composition de la nourriture et périodes d'alimentation pendant le test | 1 | O | Les poissons étaient nourris deux heures avant le renouvellement de l'eau. | ||
| 26 | Si le ratio FBC/FBA dérivait de la concentration chimique dans l'organisme et dans l'eau, la durée de l'expérience était-elle égale à ou supérieure au temps nécessaire pour que les concentrations chimiques atteignent un état stable? | 3 | O | 28 jours | ||
| 27 | Si le ratio FBC/FBA provenait de la concentration chimique dans l'organisme et dans l'eau, les concentrations mesurées dans l'eau et dans l'organisme ont-elles été signalées? | 3 | O | |||
| 28 | Les concentrations dans l'eau du test ont-elles été mesurées périodiquement? | 1 | O | Sur trois jours distincts | ||
| 29 | Les conditions du milieu d'exposition correspondaient-elles au produit chimique particulier signalé? (par exemple, pour la toxicité du métal : pH, DOC/TOC, dureté de l'eau, température) | 3 | O | Oui, tous les deux jours | ||
| 30 | Photopériode et intensité lumineuse | 1 | O | 12:12 | ||
| 31 | Préparation de la solution de stock et d'essai | 1 | O | |||
| 32 | Intervalles de contrôle analytique | 1 | O | Tous les deux jours pour l'oxygène dissous, le pH et la température | ||
| 33 | Méthodes statistiques utilisées | 1 | O | |||
| 34 | Le solubilisant/émulsifiant a-t-il été utilisé si le produit chimique était faiblement soluble ou instable? | s.o. | N | |||
| Informations relatives à la qualité des données | ||||||
| 35 | L'organisme d'essai correspondait-il à l'environnement canadien? | 3 | O | |||
| 36 | Les conditions du test (pH, température, DO, etc.) étaient-elles adaptées à l'organisme d'essai? | 1 | O | |||
| 37 | Le type de système et sa conception (statique, semi-statique, flux continu, scellé ou ouvert, etc.) correspondent-ils aux propriétés de la substance et à la nature/aux habitudes de l'organisme? | 2 | O | Semi-statique | ||
| 38 | Le pH de l'eau du test se situait-il dans la plage habituelle pour l'environnement canadien (6 à 9)? | 1 | O | 7,22–7,84 | ||
| 39 | La température de l'eau du test se situaitelle dans la plage habituelle pour l'environnement canadien (5 à 27 °C)? | 1 | O | 22–23 | ||
| 40 | Le contenu lipidique (ou FBA/FBC lipidiquement normalisé) a-t-il été signalé? | 2 | O | |||
| 41 | Les concentrations mesurées d'un produit chimique dans l'eau du test étaient-elles inférieures à la solubilité dans l'eau du produit chimique? | 3 | N | |||
| 42 | Si une substance d'essai radio-marquée a été utilisée, la détermination du FBC étaitelle basée sur le composé d'origine (c'est-à-dire, pas sur la totalité des résidus radio-marqués)? | 3 | s.o. | |||
| Résultats | ||||||
| 43 | Critères d'évaluation (FBA, FBC) et valeurs | s.o. | s.o. | FBC | ||
| 44 | FBA et FBC définis comme : 1) le ratio de concentration chimique dans l'organisme et dans l'eau, ou 2) le ratio de l'assimilation chimique et les constantes du taux d'élimination | s.o. | s.o. | 1 | ||
| 45 | Le FBA/FBC était-il issu d'un 1) échantillon de tissu ou 2) organisme entier? | s.o. | s.o. | 2 | ||
| 46 | Le FBA/FBC 1) moyen ou 2) maximum at-il été utilisé? | s.o. | s.o. | 1 | ||
| 47 | Note : ... % | 75,0 | ||||
| 48 | Code de fiabilité d'Environnement Canada : | 2 | ||||
| 49 | Catégorie de fiabilité (élevée, satisfaisante, basse) : | Confiance satisfaisante | ||||
| 50 | Commentaires | La présente procédure est basée sur des conditions semi-statiques (renouvellement des solutions du test tous les deux jours). Par conséquent, les produits chimiques d'essai ayant une très faible solubilité dans l'eau peuvent aussi être caractérisés par leur potentiel de bioconcentration, sans ajouter de solvants ou d'autres substances auxiliaires qui pourraient affecter les résultats. | ||||
Formulaire pour sommaire de rigueur d'étude : Ti aquatique
| Non | Élément | Pondération | Oui/Non | Veuillez préciser | |||
|---|---|---|---|---|---|---|---|
| 1 | Référence : Sandoz. 1975. Toxicité aiguë du poisson (truite arc-en-ciel) 48 heures | ||||||
| 2 | Identité de la substance : noCAS | s.o. | O | 5261-31-4 | |||
| 3 | Identité de la substance : nom(s) chimique(s) | s.o. | O | ||||
| 4 | Composition chimique de la substance | 2 | N | ||||
| 5 | Pureté chimique | 1 | N | ||||
| 6 | Persistance/stabilité de la substance d'essai en solution aquatique signalée? | 1 | N | ||||
| Méthode | |||||||
| 7 | Référence | 1 | O | ||||
| 8 | Méthode de l'OCDE, de l'UE, nationale ou autre méthode standard? | 3 | O | ||||
| 9 | Justification de la/du méthode/protocole si une méthode non standard a été utilisée | 2 | |||||
| 10 | BPL (bonne pratique de laboratoire) | 3 | O | ||||
| Organisme d'essai | |||||||
| 11 | Identité de l'organisme : nom | s.o. | O | Truite arc-en-ciel | |||
| 12 | Nom latin ou noms latin et commun signalés? | 1 | O | ||||
| 13 | Âge/stade du cycle biologique de l'organisme d'essai | 1 | N | ||||
| 14 | Longueur et/ou poids | 1 | O | ||||
| 15 | Sexe | 1 | N | ||||
| 16 | Nombre d'organismes par répétition | 1 | N | ||||
| 17 | Taux de chargement de l'organisme | 1 | N | ||||
| 18 | Type de nourriture et périodes d'alimentation pendant la période d'acclimatation | 1 | N | ||||
| Conception/conditions du test | |||||||
| 19 | Type de test (aigu ou chronique) | s.o. | O | Aigu | |||
| 20 | Type d'expérience (laboratoire ou terrain) | s.o. | O | Laboratoire | |||
| 21 | Voies d'exposition (nourriture, eau, les deux) | s.o. | |||||
| 22 | Durée d'exposition | s.o. | O | 48 | |||
| 23 | Contrôles négatifs ou positifs (veuillez préciser) | 1 | N | ||||
| 24 | Nombre de répétitions (incluant les contrôles) | 1 | N | ||||
| 25 | Concentrations nominales rapportées? | 1 | N | ||||
| 26 | Concentrations mesurées rapportées? | 3 | N | ||||
| 27 | Type de nourriture et périodes d'alimentation pendant les tests à long terme | 1 | N | ||||
| 28 | Les concentrations ont-elles été mesurées périodiquement (particulièrement lors du test chronique)? | 1 | N | ||||
| 29 | Les conditions du milieu d'exposition correspondaient-elles au produit chimique particulier signalé? (par exemple, pour la toxicité du métal : pH, DOC/TOC, dureté de l'eau, température) | 3 | N | ||||
| 30 | Photopériode et intensité lumineuse | 1 | N | ||||
| 31 | Préparation de la solution de stock et d'essai | 1 | N | ||||
| 32 | Un agent solubilisant/émulsifiant a-t-il été utilisé si le produit chimique était faiblement soluble ou instable? | 1 | N | ||||
| 33 | Si un solubilisant/émulsifiant a été utilisé, sa concentration a-t-elle été signalée? | 1 | |||||
| 34 | Si un solubilisant/émulsifiant a été utilisé, son écotoxicité a-t-elle été signalée? | 1 | |||||
| 35 | Intervalles de contrôle analytique | 1 | N | ||||
| 36 | Méthodes statistiques utilisées | 1 | N | ||||
| Informations relatives à la qualité des données | |||||||
| 37 | Le critère d'évaluation a-t-il été directement causé par la toxicité du produit chimique et non par l'état de santé de l'organisme (par exemple, lorsque la mortalité lors du contrôle est > 10 %) ou des effets physiques (par exemple, « effet d'ombrage »)? | s.o. | |||||
| 38 | L'organisme d'essai correspondait-il à l'environnement canadien? | 3 | O | ||||
| 39 | Les conditions du test (pH, température, DO, etc.) étaient-elles adaptées à l'organisme d'essai? | 1 | N | ||||
| 40 | Le type de système et sa conception (statique, semistatique, flux continu, scellé ou ouvert, etc.) correspondent-ils aux propriétés de la substance et à la nature/aux habitudes de l'organisme? | 2 | N | ||||
| 41 | Le pH de l'eau du test se situait-il dans la plage habituelle pour l'environnement canadien (6 à 9)? | 1 | N | ||||
| 42 | La température de l'eau du test se situait-elle dans la plage habituelle pour l'environnement canadien (5 à 27 °C)? | 1 | O | ||||
| 43 | La valeur de la toxicité était-elle inférieure à la solubilité dans l'eau du produit chimique? | 3 | N | ||||
| Résultats | |||||||
| 44 | Valeurs de la toxicité (préciser le critère d'évaluation et la valeur) | s.o. | s.o. | CL50 à 48 heures > 700 mg/L | |||
| 45 | Autres critères d'évaluation signalés : par exemple, FBC/FBA, CMEO/CSEO (préciser)? | s.o. | |||||
| 46 | Autres effets indésirables (par exemple, cancérogénicité, mutagénicité) signalés? | s.o. | |||||
| 47 | Note : ... % | 28,9 | |||||
| 48 | Code de fiabilité d'Environnement Canada : | 4 | |||||
| 49 | Catégorie de fiabilité (élevée, satisfaisante, basse) : | Non satisfaisante | |||||
| 50 | Commentaires | ||||||
Formulaire pour sommaire de rigueur d'étude : Ti aquatique
| Non | Élément | Pondération | Oui/Non | Veuillez préciser | |
|---|---|---|---|---|---|
| 1 | Référence : Safepharm Laboratories Ltd. 1990. Acute toxicity to rainbow trout. Numéro de projet 47/781 | ||||
| 2 | Identité de la substance : n° CAS | s.o. | O | 5261-31-4 | |
| 3 | Identité de la substance : nom(s) chimique(s) | s.o. | O | ||
| 4 | Composition chimique de la substance | 2 | N | ||
| 5 | Pureté chimique | 1 | N | ||
| 6 | Persistance/stabilité de la substance d'essai en solution aquatique signalée? | 1 | N | ||
| Méthode | |||||
| 7 | Référence | 1 | N | ||
| 8 | Méthode de l'OCDE, de l'UE, nationale ou autre méthode standard? | 3 | N | ||
| 9 | Justification de la/du méthode/protocole si une méthode non standard a été utilisée | 2 | N | ||
| 10 | BPL (bonne pratique de laboratoire) | 3 | s.o. | ||
| Organisme d'essai | |||||
| 11 | Identité de l'organisme : nom | s.o. | Truite arc-en-ciel | ||
| 12 | Nom latin ou noms latin et commun signalés? | 1 | O | ||
| 13 | Âge/stade du cycle biologique de l'organisme d'essai | 1 | O | ||
| 14 | Longueur et/ou poids | 1 | O | ||
| 15 | Sexe | 1 | s.o. | ||
| 16 | Nombre d'organismes par répétition | 1 | O | De trois à dix | |
| 17 | Taux de chargement de l'organisme | 1 | O | 0,70 g poids du corps/L | |
| 18 | Type de nourriture et périodes d'alimentation pendant la période d'acclimatation | 1 | s.o. depuis le test aigu | ||
| Conception/conditions du test | |||||
| 19 | Type de test (aigu ou chronique) | s.o. | Aigu | ||
| 20 | Type d'expérience (laboratoire ou terrain) | s.o. | Laboratoire | ||
| 21 | Voies d'exposition (nourriture, eau, les deux) | s.o. | Eau | ||
| 22 | Durée d'exposition | s.o. | 96 heures | ||
| 23 | Contrôles négatifs ou positifs (veuillez préciser) | 1 | O | Positif | |
| 24 | Nombre de répétitions (incluant les contrôles) | 1 | O | Deux pour l'étude définitive | |
| 25 | Concentrations nominales rapportées? | 1 | O | 3 | |
| 26 | Concentrations mesurées rapportées? | 3 | N | ||
| 27 | Type de nourriture et périodes d'alimentation pendant les tests à long terme | 1 | s.o. | ||
| 28 | Les concentrations ont-elles été mesurées périodiquement (particulièrement lors du test chronique)? | 1 | N | ||
| 29 | Les conditions du milieu d'exposition correspondaient-elles au produit chimique particulier signalé? (par exemple, pour la toxicité du métal : pH, DOC/TOC, dureté de l'eau, température) | 3 | O | ||
| 30 | Photopériode et intensité lumineuse | 1 | N | ||
| 31 | Préparation de la solution de stock et d'essai | 1 | N | ||
| 32 | Un agent solubilisant/émulsifiant a-t-il été utilisé si le produit chimique était faiblement soluble ou instable? | 1 | N | ||
| 33 | Si un solubilisant/émulsifiant a été utilisé, sa concentration a-t-elle été signalée? | 1 | s.o. | ||
| 34 | Si un solubilisant/émulsifiant a été utilisé, son écotoxicité a-t-elle été signalée? | 1 | s.o. | ||
| 35 | Intervalles de contrôle analytique | 1 | O | ||
| 36 | Méthodes statistiques utilisées | 1 | N | ||
| Informations relatives à la qualité des données | |||||
| 37 | Le critère d'évaluation a-t-il été directement causé par la toxicité du produit chimique et non par l'état de santé de l'organisme (par exemple, lorsque la mortalité lors du contrôle est > 10 %) ou des effets physiques (par exemple, « effet d'ombrage »)? | s.o. | O | ||
| 38 | L'organisme d'essai correspondait-il à l'environnement canadien? | 3 | O | ||
| 39 | Les conditions du test (pH, température, DO, etc.) étaient-elles adaptées à l'organisme d'essai? | 1 | O | ||
| 40 | Le type de système et sa conception (statique, semi-statique, flux continu, scellé ou ouvert, etc.) correspondent-ils aux propriétés de la substance et à la nature/aux habitudes de l'organisme? | 2 | s.o. | ||
| 41 | Le pH de l'eau du test se situait-il dans la plage habituelle pour l'environnement canadien (6 à 9)? | 1 | N | Pas de pH donné | |
| 42 | La température de l'eau du test se situait-elle dans la plage habituelle pour l'environnement canadien (5 à 27 °C)? | 1 | O | ||
| 43 | La valeur de la toxicité était-elle inférieure à la solubilité dans l'eau du produit chimique? | 3 | N | La solubilité de l'eau pour cette substance était de 0,07. | |
| Résultats | |||||
| 44 | Valeurs de la toxicité (préciser le critère d'évaluation et la valeur) | s.o. | CL50 à 96 heures > 100 mg/L | ||
| 45 | Autres critères d'évaluation signalés : par exemple, FBC/FBA, CMEO/CSEO (préciser)? | s.o. | N | ||
| 46 | Autres effets indésirables (par exemple, cancérogénicité, mutagénicité) signalés? | s.o. | N | ||
| 47 | Note : ... % | 43,6 | |||
| 48 | Code de fiabilité d'Environnement Canada : | 3 | |||
| 49 | Catégorie de fiabilité (élevée, satisfaisante, basse) : | Confiance basse | |||
| 50 | Commentaires | ||||
Annexe 2 : Tableau sommaire des intrants des modèles de la persistance, de la bioaccumulation et de la toxicité
Données du modèle pour le Disperse Red 179 (n° CAS 16586-42-8)
| Devenir physique et chimique | Devenir | Devenir | Profils de persistance, bioaccumulation et toxicité | Persistance | |
|---|---|---|---|---|---|
| 1 Dérivé de log Kco 2 Dérivé des données FBC 3 Valeur par défaut 4 Dérivé d'une demi-vie dans l'eau |
|||||
| Paramètres d’entrée des modèles | EPI Suite (tous les modèles, notamment AOPWIN, KOCWIN, BCFWIN, BIOWIN et ECOSAR) |
STP (1) Traitement AS (2) Traitement simple (3) (les données requises sont différentes selon le modèle) |
Modèle FBC/ Gobas |
Modèle de POP canadien (y compris CATABOL) |
TOPKAT |
| Code SMILES | N(=O)(=O)c (ccc(nc (N=Nc (c(cc(N(CCC (#N))CC)c1) C)c1) s2)c23) c3 |
N(=O)(=O)c (ccc(nc (N=Nc (c(cc(N(CCC (#N))CC)c1) C)c1)s2)c23) c3 |
N(=O)(=O)c (ccc(nc (N=Nc (c(cc(N(CCC (#N))CC)c1) C)c1)s2)c23) c3 |
N(=O)(=O)c (ccc(nc (N=Nc (c(cc(N(CCC (#N))CC)c1) C)c1)s2)c23) c3 |
|
| Masse moléculaire (g/mol) | 394,45 | 394,45 (1, 2, 3) | |||
| Point de fusion (°C) | 172 Point de fusion de l'analogue CASn° 68133697 (Yen et al., 1989) |
||||
| Point d’ébullition (°C) | |||||
| Température des données (ºC) | 20 | ||||
| Masse volumique (kg/m3) | 1,52 (2) | ||||
| Pression de vapeur (Pa) | 4,53 × 10-7 B (1, 3) (pression de vapeur du Disperse Blue 79, Clariant, 1996) |
||||
| Constante de la loi de Henry (Pa·m3/mol) | 0,001 (3) La constante de la loi de Henry est la plus haute valeur en données déduites à partir d'analogues utilisée pour représenter le pire scénario (Baughman et Perenich, 1988, comme cité dans l'ébauche SAR) |
||||
Log Kae (coefficient de partage air-eau; sans dimension) |
|||||
Log Koe (coefficient de partage octanol-eau, sans dimension) |
5,09 [Valeur modélisée à l'aide de la méthode d'ajustement de la valeur expérimentale du modèle KNOWWIN (2000), qui a estimé le log Koe des substances d'après la valeur expérimentale du log Koe, soit 4,08, pour l'analogue n° CAS 68133-69-7 (Sijm et al.,1999)] |
La même que EPIWEB | La même que EPIWEB | Identique à EPIWEB | Identique à EPIWEB |
Koe (coefficient de partage octanol-eau, sans dimension) |
123 027 (2, 3) | ||||
Log Kco (coefficient de partage carbone organique/eau – L/kg) |
|||||
| Solubilité dans l'eau (mg/L) | 0,012 [Valeur modélisée à l'aide de la méthode d'ajustement de la valeur expérimentale du modèle WATERNT (2002), qui a estimé l'hydrosolubilité des substances en fonction de la valeur de l'hydrosolubilité de l'analogue n° CAS68133-69-7. L'hydrosolubilité de l'analogue (0,048 mg/L) est une moyenne géométrique des valeurs expérimentales de solubilité du n° CAS 68133-69-7 (Sijm et al.,1999)] |
0,02 (1, 3) | |||
Log Koa (coefficient de partage octanol-air, sans dimension) |
|||||
| Coefficient de partage sol-eau (L/kg)1 | |||||
| Coefficient de partage sédiments-eau (L/kg)1 | |||||
| Coefficient de partage particules en suspension-eau (L/kg)1 | 12365 (2) | ||||
| Coefficient de partage poisson-eau (L/kg)2 | |||||
| Coefficient de partage aérosol-eau (sans dimension)3 | |||||
| Coefficient de partage végétation-eau (sans dimension)1 | |||||
| Enthalpie (Koe) | |||||
| Enthalpie (Kae) | |||||
| Demi-vie dans l'air (jours) | |||||
| Demi-vie dans l’eau (jours) | |||||
| Demi-vie dans les sédiments (jours) | |||||
| Demi-vie dans le sol (jours) | |||||
| Demi-vie dans la végétation (jours)4 | |||||
| Constante cinétique de métabolisme (1/jours) | |||||
| Constante cinétique de biodégradation (jour-1 ou heure-1) – préciser | 0,032 (2, 1/jour) 0,77 (3, 1/heure) |
||||
| Demi-vie de biodégradation en clarificateur primaire (t1/2-p; h) | 217 heures (1) | ||||
| Demi-vie de biodégradation en bassin d’aération (t1/2-s; h) | 21,7 heures (1) | ||||
| Demi-vie de biodégradation en bassin de décantation (t1/2-s; h) | 21,7 heures (1) | ||||
Intrants du modèle pour le DAPEP (n° CAS25176-89-0)
| Devenir physique et chimique | Devenir | Devenir | Profils de persistance, bioaccumulation et toxicité | Persistance | |
|---|---|---|---|---|---|
| Paramètres d’entrée des modèles | EPI Suite (tous les modèles, notamment AOPWIN, KOCWIN, BCFWIN, BIOWIN et ECOSAR) |
STP (1) Traitement AS (2) Traitement simple (3) (les données requises sont différentes selon le modèle) |
Modèle FBC/FBA Arnot- Gobas |
Modèle de POP canadien (CATABOLl) |
TOPKAT |
| Code SMILES | c12N=C(N= Nc3ccc(N (CC)CCC (#N))cc3) Sc1cc(Cl)c (Cl)c2 |
c12N=C(N= Nc3ccc(N (CC)CCC (#N))cc3) Sc1cc(Cl) c(Cl)c2 |
c12N=C(N= Nc3ccc(N (CC)CCC (#N))cc3) Sc1cc(Cl) c(Cl)c2 |
c12N=C(N= Nc3ccc(N (CC)CCC (#N))cc3) Sc1cc(Cl) c(Cl)c2 |
c12N=C(N= Nc3ccc(N (CC)CCC (#N))cc3) Sc1cc(Cl) c(Cl)c2 |
| Masse moléculaire (g/mol) | 404,32 | 404,32 (1, 2, 3) | |||
| Point de fusion (°C) | * | 220 Point de fusion pour CAS# 25176-89-0 (Peters et al. 1992) |
|||
| Point d’ébullition (°C) | * | ||||
| Température des données (ºC) | 20 | ||||
| Masse volumique (kg/m3) | 1,64 (2) | ||||
| Pression de vapeur (Pa) | * | 4.53x10-7 B (1, 3) (pression de vapeur pour le Disperse blue 79, Clariant 1996) |
|||
| Constante de la loi de Henry (Pa·m3/mol) | * | 0.001 (3) La valeur la plus élevée de lecture a été utilisée afin de présenter le pire scénario (Baughman and Perenich, 1988, tel que cité dans le SAR) |
|||
Log Kae (coefficient de partage air-eau; sans dimension) |
|||||
Log Koe (coefficient de partage octanol-eau, sans dimension) |
6,01 [Valeur modélisée à l'aide de la méthode d'ajustement de la valeur expérimentale du modèle KNOWWIN (2000), qui a estimé le log Koe des substances d'après la valeur expérimentale du log Koe, soit 4,08, pour l'analogue n° CAS 68133-69-7 (Sijm et al., 1999)] |
La même que EPIWEB | La même que EPIWEB | Identique à EPIWEB | Identique à EPIWEB |
Koe (coefficient de partage octanol-eau, sans dimension) |
102329 (2, 3) | ||||
Log Kco (coefficient de partage carbone organique/eau – L/kg) |
|||||
| Solubilité dans l'eau (mg/L) | 0,004 [Valeur modélisée à l'aide de la méthode d'ajustement de la valeur expérimentale du modèle WATERNT (2002), qui a estimé l'hydrosolubilité des substances en fonction de la valeur de l'hydrosolubilité de l'analogue n° CAS68133-69-7. L'hydrosolubilité de l'analogue (0,048 mg/L) est une moyenne géométrique des valeurs expérimentales de solubilité du n° CAS 68133-69-7 (Sijm et al., 1999)] |
0,007 (1, 3) | |||
Log Koa (coefficient de partage octanol-air, sans dimension) |
|||||
| Coefficient de partage sol-eau (L/kg)1 | |||||
| Coefficient de partage sédiments-eau (L/kg)1 | |||||
| Coefficient de partage particules en suspension-eau (L/kg)1 | 42247 (2) | ||||
| Coefficient de partage poisson-eau (L/kg)2 | |||||
| Coefficient de partage aérosol-eau (sans dimension)3 | |||||
| Coefficient de partage végétation-eau (sans dimension)1 | |||||
| Enthalpie (Koe) | |||||
| Enthalpie (Kae) | |||||
| Demi-vie dans l'air (jours) | |||||
| Demi-vie dans l’eau (jours) | |||||
| Demi-vie dans les sédiments (jours) | |||||
| Demi-vie dans le sol (jours) | |||||
| Demi-vie dans la végétation (jours)4 | |||||
| Constante cinétique de métabolisme (1/jours) | * | ||||
| Constante cinétique de biodégradation (jour-1 ou heure-1) – préciser | 0,48 (2, 1/jour) 0.020 (3, 1/heure) |
||||
| Demi-vie de biodégradation en clarificateur primaire (t1/2-p; h) | 347 heures (1) | ||||
| Demi-vie de biodégradation en bassin d’aération (t1/2-s; h) | 34,7 heures (1) | ||||
| Demi-vie de biodégradation en bassin de décantation (t1/2-s; h) | 34,7 heures (1) |
Annexe 3 : Estimations de la limite supérieure de l'exposition au Disperse Red 179 et au DAPEP découlant des textiles
| Produit de consommation | Estimations de la limite supérieure de l'exposition (mg/kg p.c. par jour) au Disperse Red 179 et au DAPEP par divers groupes d'âge1 | ||||
|---|---|---|---|---|---|
| de 0 à 6 mois2 | de 0,5 à 4 ans3 | de 5 à 11 ans4 | de 12 à 19 ans5 | 20 ans et plus6 | |
| 1 L'estimation de la limite supérieure de la fraction lixiviable se situe entre 0,03 % pour les textiles grand-teint (ETAD, 2004) et 0,5 % pour les textiles présentant une faible indégorgeabilité (Kraetke et Platzek, 2005). 2 En supposant que le nourrisson pèse 7,5 kg, que sa surface corporelle (sans les mains et la tête) représente 0,28 m2 (Santé Canada, 1998) et qu'il passe 23 minutes par jour à mâchonner le tissu (Norris et Smith, 2002). 3 En supposant que l'enfant pèse 15,5 kg, que sa surface corporelle (sans les mains et la tête) représente 0,46 m2 (Santé Canada, 1998) et qu'il passe 29 minutes par jour à mâchonner le tissu (Norris et Smith, 2002). 4 En supposant que l'enfant pèse 31 kg et que sa surface corporelle (sans les mains et la tête) représente 0,80 m2 (Santé Canada, 1998). 5 En supposant que l'adolescent pèse 59,4 kg et que sa surface corporelle (sans les mains et la tête) représente 1,4 m2 (Santé Canada, 1998). 6 En supposant que la personne pèse 70,9 kg et que sa surface corporelle (sans les mains et la tête) représente 1,6 m2 (Santé Canada, 1998). |
|||||
| Cutanée : port de textiles | (0,2 - 4) x 10-3 | (0,2 - 3) x 10-3 | (0,2 - 3) x 10-3 | (0,1 - 2) x 10-3 | (0,1 - 2) x 10-3 |
| Voie orale : mâchonnement | 0,002 x 10-3 | 0,001 x 10-3 | s.o. | s.o. | s.o. |
| Scénarios – produits de consommation | Hypothèses | Estimation de la limite supérieure de l'exposition |
|---|---|---|
| 1 On présume que ce chiffre équivaut à la quantité de tissu en contact avec la peau. 2 Quantité de produit = densité du tissu ´ quantité de tissu ´ concentration = (100 g/m2) ´ (0,28 m2) ´ (1 % en poids) = 0,28 g 3 La quantité maximale de colorant retirée par de la salive simulée à partir de textiles destinés aux enfants après 4 h se chiffrait à 0,13 %; 0,5 % est utilisé pour représenter la limite supérieure. |
||
| Port d'un vêtement teint confectionné à partir de tissu synthétique | Scénario d'exposition : ConsExpo 4.0, contact cutané direct avec le produit – migration (RIVM, 2005). Exemple pour les nourrissons âgés de 0 à 6 mois. Concentration : 1 % par poids (Kraetke et Platzek, 2005) Densité du tissu : 100 g/m2 (Kraetke et Platzek, 2005) Hypothèses générales
Voie cutanée
|
Dose cutanée chronique interne = 0,004 mg/kg p.c. par jour |
| Mâchonnement de textiles teints | L'exposition est estimée ci-dessous pour les nourrissons âgés de 0 à 6 mois (poids corporel : 7,5 kg). Valeur d'absorption journalière estimée pour l'ingestion résultant du mâchonnement : = où : WS = solubilité dans l'eau du Disperse Red et du DAPEP (déduite pour les colorants azoïques = 0,69 mg/L (Baughman et Perenich, 1988) Vs = débit de salive = 0,22 mL/min (Environ, 2003a, b) CF = conversion du litre en mL = 0,001 L/mL FR = extraction partielle par la salive = 0,5 % (ETAD, 1983)3 AFo = facteur d'absorption par voie orale = 1 EF = fréquence d'exposition fondée sur le comportement d'absorption orale = 23 min/jour (Norris et Smith, 2002) BW = poids corporel = 7,5 kg pour les nourrissons âgés de 0 à 6 mois (Santé Canada, 1998) = (0,69 mg/L × 0,22 mL/min × 0,001 L/mL × 0,005 × 1 × 23 min)/ 7,5 kg = 6 x 10-6 mg/kg p.c. par jour |
Dose orale chronique interne = 6 x 10-6 mg/kg p.c. par jour |
Annexe 5 : Prévisions des modèles R(Q)SA pour le Disperse Red 179 (16586-42-8) et ses produits de clivage azoïques potentiels
Prévisions en matière de cancérogénicité
| ID | n° CAS | Derek1 | Toxtree2 | Model Applier3 | Casetox4 | |||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Cancer | SA gtx | Cancer | m-rat | f-rat | m-souris | f-souris | m-rat | f-rat | m-souris | f-souris | ||
| Composé d'origine | 16586-42-8 | P | P | N | P | IC | ND | ND | ND | ND | ND | ND |
| Métabolite 1 | 6285-57-0 | P | P | - | P | P | ND | IC | P | N | N | P |
| Métabolite 2 | 105294-34-6 | P | P | N | P | N | P | N | ND | ND | ND | ND |
Prévisions en matière de génotoxicité
| ID | n° CAS | Ames | ChrAb | Induction de micronoyaux | ||||||
|---|---|---|---|---|---|---|---|---|---|---|
| Derek | TT5 | MA | CT | MA | CT6 | TT | MA | CT | ||
| N° CAS : numéro de registre du Chemical Abstracts Service; ChrAb : aberration chromosomique; CT : Casetox; f : femelle; IC : non concluant; ID : identification; m : mâle; MA : Model Applier; N : négative; ND : hors du champ d'application du domaine; SA gtx : alerte structurelle indiquant la cancérogénicité génotoxique; P : positive; TT : Toxtree; - : aucun résultat 1 [DEREK] Deductive Estimation of Risk from Existing Knowledge [module de prévision sur cédérom]. 2008. Version 10.0.2. Cambridge (MA) : Harvard University, LHASA Group. [consulté le 30 septembre 2009]. Accès : http://www.lhasalimited.org/index.php? cat=2&sub_cat=2# [réserve de consultation]. 2 Toxtree version 1.60. 2009. Réalisé par Ideaconsult Ltd, Bulgarie. 3 [Leadscope] Leadscope Model Applier [module de prévision]. 2009. Version 1.2.0-3. Columbus (OH): Leadscope, Inc. [consulté le 30 septembre 2009]. Accès : http://www.leadscope.com/all_products.php[réserve de consultation]. 4 CASETOX [module de prévision]. 2008. Version 2.0. Beachwood (OH) : MultiCASE. [consulté le 30 septembre 2009]. Accès : http://www.multicase.com/products/prod03.htm[réserve de consultation]. 5Souche TA100 du Salmonella typhimurium. 6 Essai in vitro (dans des cellules ovariennes de hamster chinois en culture). 7 Résultat négatif faible. |
||||||||||
| Composé d'origine | 16586-42-8 | P | P | P | ND | ND | IC | P | ND | ND |
| Métabolite 1 | 6285-57-0 | P | - | P | ND | ND | ND | P | N7 | P |
| Métabolite 2 | 105294-34-6 | P | P | P | P | N | P | P | N | IC |
| Fondement de la considération | Nom et n° de registre du CAS | Structure |
|---|---|---|
| 1 Coefficient de Tanimoto = 92 (recherche de similitude dans SciFinder). | ||
| Produit de clivage azoïque potentiel | 6285-57-0 2-amino-6-nitrobenzothiazole |
 |
| Produit de clivage azoïque potentiel | 105294-34-6 3-[(4-amino-3-méthylphényl)éthylamino]propanenitile |
 |
| Analogue structurel1 | 25510-81-0 Disperse Red 145 |
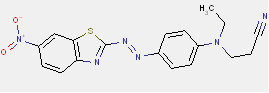 |
Annexe 7 : Prévisions des modèles R(Q)SA pour le DAPEP (isomère 5,6-dichloro du Disperse Red 153), l'isomère 6,7-dichloro du Disperse Red 153 et leurs produits de clivage azoïques potentiels
Prévisions en matière de cancérogénicité
| ID | n° CAS | Derek1 | Toxtree2 | Model Applier3 | Casetox4 | |||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Cancer | SA gtx | Cancer | m-rat | f-rat | m-souris | f-souris | m-rat | f-rat | m-souris | f-souris | ||
| Composé d'origine 1 | 25176-89-0 | P | P | N | P | N | ND | ND | ND | ND | ND | ND |
| Composé d'origine 2 (isomère 6,7'-dichloro) | 78564-87-1 | P | P | N | P | N | ND | ND | ND | ND | ND | ND |
| M-1 | 24072-75-1 | P | P | - | IC | IC | ND | ND | ND | N | N | P |
| M 2 | 25150-27-0 | P | P | - | IC | IC | ND | ND | ND | ND | N | N |
| M 3 | 100894-10-8 | - | P | N | N | N | N | N | ND | ND | ND | ND |
Prévisions en matière de génotoxicité
| ID | n° CAS | Ames | ChrAb | Induction de micronoyaux | ||||||
|---|---|---|---|---|---|---|---|---|---|---|
| Derek | TT5 | MA | CT | MA | CT6 | TT | MA | CT | ||
| N° CAS : numéro de registre du Chemical Abstracts Service; ChrAb : aberration chromosomique; CT : Casetox; f : femelle; IC : non concluant; ID : identification; m : mâle; MA : Model Applier; N : négative; ND : hors du champ d'application du domaine; SA gtx : alerte structurelle indiquant la cancérogénicité génotoxique; P : positive; TT : Toxtree; - : aucun résultat 1 [DEREK] Deductive Estimation of Risk from Existing Knowledge [module de prévision sur cédérom]. 2008. Version 10.0.2. Cambridge (MA) : Harvard University, LHASA Group. [consulté le 30 septembre 2009]. Accès : http://www.lhasalimited.org/index.php? cat=2&sub_cat=2# [réserve de consultation]. 2 Toxtree version 1.60. 2009. Réalisé par Ideaconsult Ltd, Bulgarie. 3 [Leadscope] Leadscope Model Applier [module de prévision]. 2009. Version 1.2.0-3. Columbus (OH): Leadscope, Inc. [consulté le 30 septembre 2009]. Accès : http://www.leadscope.com/all_products.php[réserve de consultation]. 4 CASETOX [module de prévision]. 2008. Version 2.0. Beachwood (OH) : MultiCASE. [consulté le 30 septembre 2009]. Accès : http://www.multicase.com/products/prod03.htm[réserve de consultation]. 5 Souche TA100 du Salmonella typhimurium. 6 Essai in vitro (dans des cellules ovariennes de hamster chinois en culture). |
||||||||||
| Composé d'origine | 25176-89-0 | P | P | N | ND | ND | P | P | ND | ND |
| Composé d'origine 2 (isomère 6,7'-dichloro) | 78564-87-1 | P | P | N | ND | ND | ND | P | N | N |
| M-1 | 25150-27-0 | P | - | N | N | N | ND | P | IC | N |
| M 2 | 105294-34-6 | P | P | P | P | N | P | P | N | IC |
| M 3 | 100894-10-8 | - | P | IC | ND | N | P | P | N | N |
Annexe 8 : Produits de clivage azoïques potentiels et analogues structurels du DAPEP (isomère 5,6-dichloro) et du Disperse Red 153 (mélange d'isomères)
| Fondement de la considération | Nom et n° de registre du CAS | Structure |
|---|---|---|
| 1 Coefficient de Tanimoto = 90 (recherche de similitude dans SciFinder). | ||
| Produit de clivage azoïque potentiel (DAPEP, isomère 5,6'-dichloro du Disperse Red 153) | 24072-75-1 2-amino-5,6- dichlorobenzothiazole |
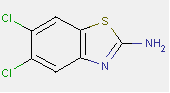 |
| Produit de clivage azoïque potentiel (isomère 6,7'-dichloro du Disperse Red 153) | 25150-27-0 6,7-dichloro-2- benzothiazolamine |
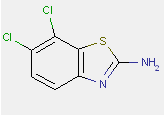 |
| Produit de clivage azoïque potentiel (deux isomères du Disperse Red 153) | 100894-10-8 3-[(4-aminophényl) éthylamino] propanenitrile - |
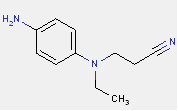 |
| Analogue structurel1 | 78564-86-0 Disperse Red 152 |
 |