Résumés du COSEPAC sur les espèces terrestres admissibles pour ajout ou reclassification à l’annexe 1 - janvier 2018
Pour un résumé des justifications de la désignation par le COSEPAC du statut d’espèces individuelles et leur biologie, les menaces, la répartition et d’autres informations. Pour une explication détaillée de la situation de conservation d’une espèce individuelle, veuillez vous référer au rapport du COSEPAC pour cette espèce, qui est aussi disponible sur le Registre public des espèces en péril.
ou contactez :
Secrétariat du COSEPAC
a/s Service canadien de la faune
Environnement Canada
Ottawa (Ontario) K1A 0H3
- Aster d'Anticosti
- Bruant à face noire
- Bruant noir et blanc
- Caribou (Population de la toundra)
- Caribou (Population des monts Torngat)
- Caribou (Population migratrice de l'Est)
- Chimaphile maculée
- Coccinelle à bandes transverses
- Couleuvre gaufre de Say
- Criquet des Îles-de-la-Madeleine
- Entosthodon rouilleux
- Escargot-tigre à bandes de l’Est
- Gros-bec errant
- Hespérie du Sonora
- Monarque
- Puffin à pieds roses
- Scirpe de Long
- Téloschiste ocellé (Population boréale et des Prairies)
- Téloschiste ocellé (Population des Grands Lacs)
- Tortue mouchetée (Population des Grands Lacs et du Saint-Laurent)
- Tortue peinte de l'Ouest (Population de la côte du Pacifique)

Photo: © Atlantic Canada Conservation Data Centre
Description longue
Symphyotrichum anticostense
Plantes vasculaires
Préoccupante
Québec, Nouveau-Brunswick
Cette plante clonale est limitée aux rives calcaires de plus grandes rivières (et occasionnellement de lacs) dans l’Est du Québec et au Nouveau-Brunswick. Au moins 95 % de sa petite aire de répartition mondiale se trouve au Canada. Les espèces envahissantes menacent la qualité de l’habitat et il y a certaines indications qu’une hybridation localisée et le broutage par les cerfs peuvent affecter de façon minimale la persistance de la population à des échelles locales. Depuis la dernière évaluation en 2000 où l’espèce a été évaluée comme étant « menacée », des recherches exhaustives ont mené à la documentation de plusieurs nouvelles sous-populations. Les sous-populations semblent être stables.
L’aster d’Anticosti est une herbacée de 10 à 75 cm de hauteur qui s’étend au moyen de longs rhizomes pour former des colonies clonales peu denses. Ses étroites feuilles allongées et rigides sont quelque peu coriaces, souvent arquées, et ont des marges entières ou très finement dentées. Ses fleurs forment des capitules portés sur de longs pédoncules et composés de fleurs tubulaires jaunes et de fleurs ligulées (semblables à des pétales) violettes. L’aster d’Anticosti est une espèce apparue à l’Holocène (il y a moins de 11 700 ans) par hybridation entre l’aster de Nouvelle-Belgique et l’aster boréal. Son identification fondée seulement sur sa morphologie n’est pas entièrement fiable, particulièrement au Nouveau-Brunswick, principalement en raison de sa ressemblance aux formes à feuilles étroites de l’aster de Nouvelle-Belgique. Il présente un intérêt à titre de rare espèce d’origine postglaciaire endémique à la région qui pousse en association avec de nombreuses autres espèces végétales dont la conservation est préoccupante au sein de communautés de rives fluviales calcaires importantes à l’échelle régionale.. Description longue situé dans la paragraphe précédent.. Description longue situé dans la paragraphe précédent.
L’aster d’Anticosti est une espèce rare endémique au nord-est de l’Amérique du Nord qui est présente dans trois régions distinctes : 1) l’île d’Anticosti, au Québec, 2) la région du lac Saint-Jean, au Québec, et 3) la région englobant les parties sud et est de la péninsule gaspésienne, le nord-est du Nouveau-Brunswick (réseaux hydrographiques de la rivière Restigouche et du fleuve Saint-Jean) et le nord-est du Maine (rivière Aroostook, un affluent du fleuve Saint-Jean). Chacune de ces régions pourrait correspondre à une origine hybride indépendante de l’espèce, mais les données sur leur caractère génétiquement distinct sont actuellement insuffisantes pour justifier qu’on les considère comme des unités désignables distinctes.
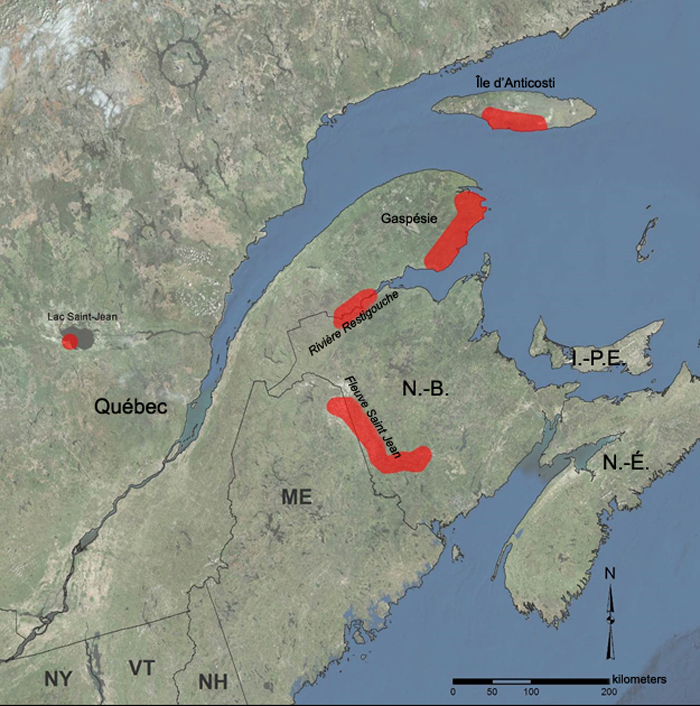
Aire de répartition mondiale de l’aster d’Anticosti (source de l’image aérienne : Esri World Imagery Basemap).
L’aster d’Anticosti pousse dans la zone annuellement inondée de grandes rivières, et parfois sur des rives semblables de grands lacs. Il est étroitement associé à un sol calcaire sur un substrat rocheux sédimentaire. Il occupe le plus souvent de larges bandes peu inclinées de grève (galets, gravier ou sable) ou de roche-mère à végétation éparse ou absente, entre les lignes de hautes et de basses eaux. À un site, l’aster d’Anticosti a largement colonisé les emprises de route et de voie ferrée au bord d’une rivière, ce qui montre sa capacité à profiter d’habitats perturbés.
L’aster d’Anticosti est une espèce vivace coloniale qui se propage par voie végétative au moyen de rhizomes. Ainsi, les individus génétiquement distincts peuvent sans doute persister de nombreuses années. On ignore toutefois la durée de vie des tiges ou segments de rhizomes individuels. L’espèce est probablement pollinisée par des insectes. Elle fleurit de la fin de juillet à la fin de septembre et disperse ses semences de la mi-août à la fin de l’automne. Le transport par l’eau est vraisemblablement son plus important mode de dispersion. Ses individus peuvent fleurir dès la première année, mais, sur le terrain, il lui faut sans doute plus de temps pour atteindre sa maturité sexuelle.
On estime que la population totale d’asters d’Anticosti au Canada se situe quelque part entre 410 000 et 1 063 000 tiges réparties dans 18 sous-populations pour lesquelles l’identification de l’espèce est jugée fiable (1 au lac Saint-Jean, 7 sur l’île d’Anticosti et 10 dans la région de la Gaspésie et de l’ouest du Nouveau-Brunswick). Les sous-populations de cette dernière région représentent au moins 95 % de la population mondiale connue de l’espèce. La rivière Restigouche (N.-B. et Québec) abrite la plus grande occurrence connue (centaines de milliers de tiges) qui s’étend sur un tronçon d’environ 80 km de la rivière. Ailleurs, les sous-populations les plus grandes sont celles de la Grande Rivière et des rivières Bonaventure et Petit Pabos, en Gaspésie (>68 000, >20 000 et >5 000 tiges, respectivement). Toutes les autres sous-populations sont estimées à quelques milliers de tiges ou moins. On ne croit pas que les sous-populations aient connu de changement important depuis la dernière évaluation de la situation de l’espèce en 2000.
La construction de grands barrages dans le réseau hydrographique du fleuve Saint-Jean (N.-B.) et au lac Saint-Jean (Qc) a causé une perte historique considérable d’habitat potentiel. La concurrence d’espèces végétales exotiques envahissantes, particulièrement l’alpiste roseau (Phalaris arundinacea), constitue une menace importante pour les sous-populations du fleuve Saint-Jean, au Nouveau-Brunswick. Ces plantes nuisent peut-être dans une moindre mesure à d’autres sous-populations, et cette menace augmentera probablement en gravité et en étendue. Sur l’île d’Anticosti, le broutage par le cerf de Virginie introduit et surabondant semble avoir un effet négatif considérable. L’hybridation constante avec l’aster de Nouvelle-Belgique pourrait causer la perte localisée d’intégrité génétique de l’espèce chez les sous-populations du Nouveau-Brunswick et de la Gaspésie. Les activités sur les plages liées au développement résidentiel et à la villégiature à proximité constituent une menace modérée pour la population isolée du lac St-Jean. Les autres menaces possibles semblent très mineures. La spécificité de l’habitat constitue un important facteur limitatif pour l’aster d’Anticosti, car l’habitat qui lui est propice ne représente qu’une très petite partie du paysage dans son aire de répartition.
L’aster d’Anticosti est inscrit comme espèce menacée à l’annexe 1 de la Loi sur les espèces en péril du gouvernement fédéral. Au Nouveau-Brunswick, il est désigné espèce en voie de disparition et protégé par la Loi sur les espèces en péril de la province. Au Québec, il est désigné espèce menacée et protégé par la Loi sur les espèces menacées ou vulnérables. Il est désigné vulnérable (G3) à l’échelle mondiale et a les cotes nationalesN3 (vulnérable) au Canada et N1 (gravement en péril) aux États-Unis et les cotes infranationales S3 (vulnérable) au Québec, S2S3 (en péril à vulnérable) au Nouveau-Brunswick et S1 (gravement en péril) au Maine.
Source : COSEPAC. 2017. Évaluation et Rapport de situation du COSEPAC sur l’aster d’Anticosti (Symphyotrichum anticostense) au Canada. Comité sur la situation des espèces en péril au Canada. Ottawa. xiv + 60 p.

Photo: © Mark Gilmore
Description longue
Zonotrichia querula
Oiseaux
Préoccupante
Territoires du Nord-Ouest, Nunavut, Alberta, Saskatchewan, Manitoba, Ontario
Cet oiseau septentrional qui niche au sol est le seul oiseau chanteur à se reproduire exclusivement au Canada. Les données des Recensements des oiseaux de Noël dans les lieux d’hivernage du Midwest américain montrent un déclin significatif à long terme de 59 % au cours des 35 dernières années, dont 16 % au cours de la dernière décennie. L’espèce pourrait être touchée par les changements climatiques sur les lieux de reproduction, tandis que les menaces qui pèsent sur les lieux d’hivernage sont entre autres la perte d’habitat, l’utilisation de pesticides, la mortalité routière et la prédation par les chats féraux.
Le Bruant à face noire est un bruant de grande taille doté d’un capuchon et d’une bavette noirs distinctifs. Les individus des deux sexes ont un plumage semblable. Les oiseaux non nicheurs et ceux se trouvant dans leur première année ont un plumage similaire, une bonne partie de la bavette et des motifs faciaux noirs présents chez les individus nicheurs étant absents chez eux. Cet oiseau est le seul passereau qui ne niche qu’au Canada.
Le Bruant à face noire, présent seulement en Amérique du Nord, est un oiseau qui migre en zone tempérée sur de longues distances. Il niche le long de la limite forestière dans le nord du Canada (Territoires du Nord-Ouest, Nunavut, Saskatchewan, Manitoba et, irrégulièrement, Ontario). Il hiverne dans le centre du Midwest américain (régulièrement au Nebraska, au Kansas, en Oklahoma et au Texas, et irrégulièrement en Arkansas, au Missouri, en Iowa et au Dakota du Sud). Comme l’accès à son aire de reproduction est limité, on en sait relativement peu sur l’espèce au Canada.
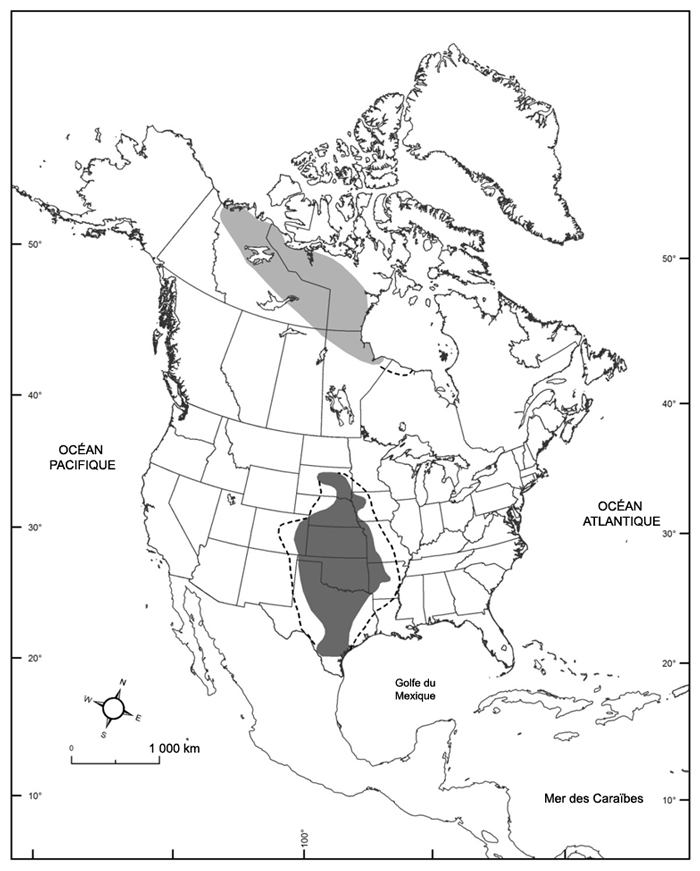
Répartition mondiale du Bruant à face noire en période de reproduction (gris pâle; adaptation à partir de James et al., 1976; Cadman, 2007) et d’hivernage (gris foncé; adaptation à partir de National Audubon Society, 2015; eBird, 2016; Norment et al., 2016), y compris les occurrences irrégulières (lignes tiretées).
Le Bruant à face noire préfère une mosaïque de terrain élevé et de toundra parsemée de lacs. Les territoires de reproduction incluent habituellement des conifères; les densités les plus élevées sont observées dans les peuplements forestiers dominés par l’épinette ou le mélèze, émaillés d’arbustes ayant généralement moins de un mètre de hauteur. En hiver et durant la migration, l’espèce fréquente divers habitats, notamment des fourrés riverains, des prairies, des lisières de forêts, des haies et des fourrés de saules.
Le Bruant à face noire est une espèce socialement monogame qui se nourrit de fruits, de graines et d’insectes. Durant la saison de reproduction, il dépend d’abord principalement des fruits, puis il modifie son régime alimentaire pour y inclure davantage d’insectes et de graines au fil de la saison, au fur et à mesure que la couverture de neige disparaît. Les nids sont construits par les femelles, qui couvent aussi les oeufs; ils sont placés sur le sol là où la végétation dense peut les dissimuler. Les couvées comptent en moyenne 4,07 oeufs, la fourchette étant de 3 à 5. L’incubation dure de 12 à 13,5 jours, et les oisillons quittent le nid après 8,5 à 10 jours. Des études effectuées dans le secteur de la rivière Thelon (Territoires du Nord-Ouest) ont montré un taux d’éclosion de 76 %, un pourcentage d’oisillons ayant quitté le nid de 62,5 % et un taux global de succès de nidification de 47,5 %, la moyenne étant de 2,07 oisillons ayant quitté le nid par couple.
La population mondiale, qui se reproduit exclusivement au Canada, est estimée à entre 500 000 et 5 000 000 d’individus, les plus récentes estimations se situant autour de 2 000 000 d’individus.
D’après les données obtenues du Recensement des oiseaux de Noël, le Bruant à face noire a connu un déclin annuel à long terme significatif de 2,58 % entre 1980 et 2014. Cela représente une baisse totale des effectifs de 59 % sur les 35 dernières années. Pour la plus récente période décennale (2004 à 2014), les données du Recensement montrent un déclin de 1,77 % par année, pour une perte cumulative de 16 %.
À la grandeur des lieux d’hivernage du Midwest américain, la conversion de prairies et de terres périphériques à des fins agricoles pourrait être un facteur du déclin du Bruant à face noire. L’épandage de pesticides un peu partout dans l’aire d’hivernage a été lié au déclin de l’espèce; l’incidence relative de ce facteur est inconnue, mais elle est probablement négative et pourrait être grave.
Au sein de l’aire de reproduction, les préoccupations incluent la perte d’habitat liée au déboisement près de la limite septentrionale de l’aire de répartition de l’espèce. Ce déboisement est dû aux feux de forêt, à l’exploitation de mines et de carrières, et aux changements climatiques, qui pourraient réduire l’habitat de reproduction convenable tout en permettant aux ectoparasites et aux mammifères prédateurs, comme le renard roux, d’étendre leur répartition vers le nord.
Des études supplémentaires doivent être effectuées pour évaluer l’espèce tout au long de son cycle de vie annuel et pour étudier l’importance relative des différentes menaces qui la guettent dans ses lieux de reproduction et d’hivernage.
Le Bruant à face noire, ses nids et ses oeufs sont protégés au Canada par la Loi sur la convention concernant les oiseaux migrateurs. Cette loi interdit la vente et la possession d’oiseaux migrateurs et de leurs nids, et toute activité qui nuit aux oiseaux migrateurs, à leurs oeufs ou à leurs nids, sauf exceptions autorisées par le Règlement sur les oiseaux migrateurs. L’espèce est également protégée aux États-Unis aux termes de la Migratory Birds Treaty Act.
Le Bruant à face noire est classé « non en péril à l’échelle mondiale » par NatureServe. Au Canada, l’espèce est classée « non en péril » à l’échelle nationale, « non en péril » en Alberta et en Saskatchewan, et « vulnérable » au Manitoba et dans les Territoires du Nord-Ouest. Le COSEPAC a évalué l’espèce comme étant préoccupante en avril 2017.
Source : COSEPAC. 2017. Évaluation et Rapport de situation du COSEPAC sur le Bruant à face noire (Zonotrichia querula) au Canada. Comité sur la situation des espèces en péril au Canada. Ottawa. xi + 43 p.

Photo: © Marcel Gahbauer
Description longue
Calamospiza melanocorys
Oiseaux
Menacée
Alberta, Saskatchewan, Manitoba
Cet oiseau chanteur des prairies se trouve à la limite septentrionale de son aire de répartition dans les Prairies canadiennes. L’espèce est nomade, les populations reproductrices changent considérablement d’endroits d’une année à l’autre pour suivre les conditions favorables à l’échelle du paysage régional, recherchant les pointes d’abondance de sauterelles. Par conséquent, les estimations de la population fluctuent considérablement et viennent compliquer l’estimation des tendances à court terme. Cependant, les données à long terme montrent un déclin de 98 % depuis 1970. Au cours de la plus grande partie de la dernière décennie, cette tendance est restée fortement négative. La conversion de l’habitat de prairies et l’utilisation d’insecticides sont réputées être les principales menaces qui pèsent sur l’espèce.
Le Bruant noir et blanc est un gros bruant trapu à courte queue et au bec relativement volumineux. Les mâles ont un plumage nuptial noir et blanc distinctif, mais, en dehors de la période de reproduction, ils ressemblent aux femelles. Les femelles ont un plumage brun grisâtre avec des rayures noires sur les parties supérieures, et leurs ailes sont brun foncé avec une tache alaire blanchâtre. Les juvéniles ont un motif de coloration semblable à celui des femelles, mais ils sont de couleur chamois et présentent plus de rayures.
Aucune sous-espèce n’a été décrite pour cette espèce, qui est la seule du genre Calamospiza. Le Bruant noir et blanc est l’oiseau emblématique de l’État du Colorado.

Photo: © Marcel Gahbauer
Description longue
Le Bruant noir et blanc se reproduit seulement dans les prairies du centre-ouest de l’Amérique du Nord, depuis le sud des Prairies canadiennes jusque dans le nord du Mexique, en passant par les Grandes Plaines du centre des États-Unis. Au Canada, le Bruant noir et blanc est présent dans le sud-est de l’Alberta, le sud de la Saskatchewan et le sud-ouest du Manitoba. En dehors de la période de reproduction, le Bruant noir et blanc se trouve dans le sud-ouest des États-Unis et le centre-nord du Mexique.
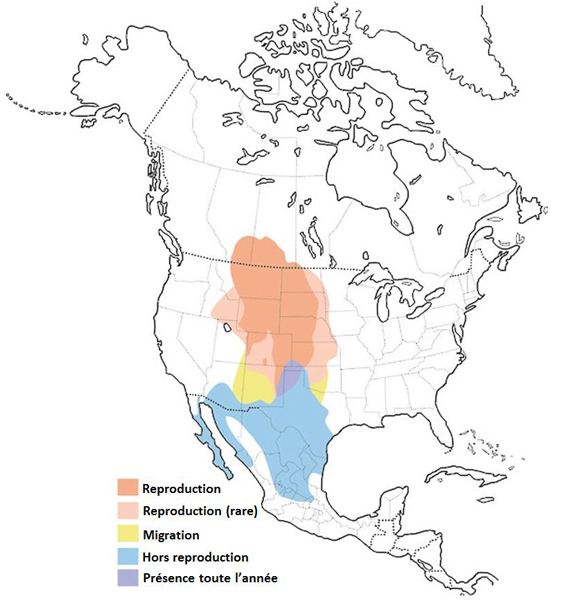
Répartition du Bruant noir et blanc en Amérique du Nord. Les aires de reproduction, de migration, de présence hors reproduction et de présence toute l’année sont représentées.
Source: Carte fournie par Birds of America online (Birds of North America), Cornell Lab of Ornithology.
Le Bruant noir et blanc est présent dans divers habitats de prairie, notamment dans les prairies à graminées courtes et mixtes, les champs en jachère envahis de mauvaises herbes, les pâturages et les terres agricoles. Il préfère nicher dans des milieux où se combinent graminées, végétation arbustive et sol dénudé. Les arbustes ou les grandes graminées qui se trouvent près des nids offrent une protection contre le soleil et les prédateurs. Au Canada, l’espèce semble utiliser des zones agricoles, comme les champs de foin, les prairies cultivées et les fossés en bordure de routes, en plus des prairies indigènes. En dehors de la période de reproduction, le Bruant noir et blanc se trouve dans des milieux plats et ouverts, notamment dans des plaines, des terres cultivées, des champs et des plaines désertiques.
Le Bruant noir et blanc nicherait une fois par an, pondant de 3 à 5 oeufs par couvée. La moyenne de jeunes par nid quittant le nid se situe entre 1,2 et 3,1 selon le type d’habitat.
Le Bruant noir et blanc a évolué en s’adaptant à l’instabilité environnementale qui caractérise son habitat de prairie. Cette espèce est très nomade d’une année à l’autre. Ce comportement semble s’être développé pour suivre les conditions idéales d’habitat dans un paysage changeant. La période de nidification du Bruant noir et blanc coïncide aussi avec l’abondance maximale de sauterelles, une composante majeure de son régime alimentaire. La sélection des sites de nidification se fait de façon à réduire le stress thermique pour les oeufs et les oisillons, ainsi que pour les mâles au plumage foncé qui couvent. Une fois que les oisillons quittent le nid, le mâle et la femelle se partagent la couvée et continuent à prendre soin des jeunes chacun de leur côté, stratégie qui réduit la prédation et augmente l’efficacité de recherche de nourriture, particulièrement lors des sécheresses.
Les Bruants noir et blanc sont fréquemment les hôtes de Vachers à tête brune, mais ils ne semblent pas avoir développé de stratégie d’évitement contre ce parasitisme de couvée. De nombreux prédateurs se nourrissent de Bruants noir et blanc, notamment des rapaces nocturnes et diurnes, des chats, des coyotes, des spermophiles, des belettes et des couleuvres.
Les Bruants noir et blanc ont évolué parmi les bisons d’Amérique et d’autres grands herbivores indigènes dans leurs lieux de reproduction. Ils dépendent donc dans une certaine mesure du broutage, qui maintient leur habitat de reproduction, particulièrement dans les prairies à grandes graminées.
Le total de la population reproductrice mondiale de Bruants noir et blanc est de 10 millions d’individus, dont environ 160 000 individus se reproduisent au Canada. De 1970 à 2014, l’espèce a décliné d’environ 3,2 % par année en Amérique du Nord et de 8,6 % par année au Canada, soit des pertes cumulatives de 77 % et 98 %, respectivement. De 2005 à 2015, les taux de déclin ont accéléré, soit un déclin de 6 % par année en Amérique du Nord et un déclin de 14 % par année au Canada. L’espèce devrait perdre la moitié de sa population totale restante d’ici les 16 prochaines années. Cependant, la variabilité interannuelle de la répartition et de l’abondance des Bruants noir et blanc, causée par le caractère très nomade de l’espèce, pourrait fausser les résultats des tendances à court terme des populations régionales. L’examen des tendances mobiles sur 10 ans au Canada (dans lesquelles un point pour chaque année représente le pourcentage moyen de variation annuelle au cours de la décennie précédente) montre une tendance vers des tendances fortement négatives tant dans le court terme (2005-2015) que dans le long terme (1980-2015), bien qu’il existe une grande variabilité dans le temps. L’interpolation à partir du déclin à long terme permet d’estimer que le déclin de la population canadienne au cours de la dernière décennie a été de 59 %.
On sait peu de choses à propos des menaces pesant spécifiquement sur la population canadienne de Bruants noir et blanc. Dans une grande partie des Grandes Plaines, la perte, la dégradation et la fragmentation d’habitat attribuables à l’agriculture, à l’urbanisation et à l’extraction de ressources, ainsi que les effets causés par des pesticides, sont considérés comme les principales menaces pesant sur l’espèce.
L’habitat de prairie est l’un des écosystèmes les plus menacés en Amérique du Nord. Au Canada, plus de 70 % du paysage de prairie a été dégradé ou converti depuis la colonisation par les Européens principalement en raison de l’agriculture et de l’urbanisation, et une grande partie des prairies restantes sont très fragmentées.
Bien que certains Bruants noir et blanc se reproduisent dans des paysages agricoles, leur succès de reproduction pourrait être plus faible dans ces milieux à cause du labourage, du fauchage et de l’application de pesticides. Les pesticides sont une grande menace pour les Bruants noir et blanc, car, en plus d’avoir des effets létaux directs, ils appauvrissent les populations de proies, telles que les sauterelles.
L’exploitation pétrolière et gazière dans les prairies a aussi contribué à la perte et à la fragmentation d’habitat pour les Bruants noir et blanc; la perturbation sensorielle qui y est associée est aussi préoccupante. L’augmentation des parcs éoliens et solaires constitue une menace croissante. Les lignes électriques associées à ces parcs peuvent favoriser la présence de prédateurs aviaires et de Vachers à tête brune, ce qui menace la survie et la productivité des Bruants noir et blanc.
Les changements climatiques seraient une menace croissante pour les Bruants noir et blanc. Le réchauffement continu, jumelé à des sécheresses plus fréquentes et plus intenses ainsi qu’à des tempêtes plus importantes, affectera probablement négativement l’espèce. Dans de telles conditions, les Bruants noir et blanc pondront moins d’oeufs et les taux de survie des oeufs et des oisillons diminueront, alors que les inondations causées par des précipitations extrêmes pourraient aussi augmenter la mortalité chez les adultes.
Un certain nombre de facteurs limitatifs rend les Bruants noir et blanc susceptibles au déclin. Cette espèce dépend fortement de la disponibilité de la couverture végétale pour réduire le stress thermique lors de la nidification. Les Bruants noir et blanc sont vulnérables aux conditions de sécheresse, qui réduisent l’abondance de leur principale proie (les sauterelles) et les exposent à une compétition accrue avec d’autres espèces d’oiseaux de prairie, d’où une réduction du taux de recrutement. À l’inverse, ils sont aussi vulnérables aux épisodes de fortes pluies dans leurs lieux de reproduction et aux fluctuations de la disponibilité de graines dans leurs quartiers d’hiver.
Le Bruant noir et blanc est protégé en vertu de lois fédérales comme la Loi de 1994 sur la convention concernant les oiseaux migrateurs, au Canada, le Migratory Bird Treaty Act, aux États-Unis, et la Convention for the Protection of Migratory Birds and Game Mammals (convention pour la protection des oiseaux migrateurs et des mammifères chassés), au Mexique. Le Bruant noir et blanc est aussi protégé par des lois provinciales comme le Alberta Wildlife Act, le Saskatchewan Wildlife Act et le Manitoba Wildlife Act. Aucune de ces lois n’a de dispositions précises sur la protection de l’habitat.
Le Bruant noir et blanc est inscrit à la liste rouge de l’UICN dans la catégorie « préoccupation mineure ». NatureServe le désigne comme non en péril à l’échelle mondiale et comme non en péril dans les lieux de reproduction et à l’extérieur de ceux-ci aux États-Unis, parce qu’il est commun et largement réparti. Pour l’ensemble du Canada, NatureServe classe l’espèce comme apparemment non en péril à non en péril, ce qui reflète une certaine inquiétude pour le long terme à cause des déclins et d’autres facteurs. Le Bruant noir et blanc est classé non en péril en Alberta, apparemment non en péril à non en péril en Saskatchewan et gravement en péril au Manitoba.
Le Bruant noir et blanc est considéré comme une espèce d’importance continentale aux termes du Plan nord-américain de conservation des oiseaux terrestres de Partenaires d’envol, parce qu’il s’agit d’un oiseau commun qui connaît un déclin abrupt.
Source : COSEPAC. 2017. Évaluation et Rapport de situation du COSEPAC sur le Bruant noir et blanc (Calamospiza melanocorys) au Canada. Comité sur la situation des espèces en péril au Canada. Ottawa. xii + 45 p.

Photo: © Anne Gunn
Description longue
Rangifer tarandus
Mammifères
Menacée
Yukon, Territoires-du-Nord-Ouest, Nunavut, Alberta, Saskatchewan, Manitoba
Les individus de cette population donnent naissance à ses petits dans la toundra arctique ouverte, et la plupart des sous-populations (hardes) hivernent dans de vastes forêts subarctiques. Bien connue pour ses grands regroupements, ses longues migrations, et son importante valeur culturelle et sociale pour les peuples autochtones du Nord et autres Canadiens, ses 14 ou 15 sous-populations se trouvent du nord-est de l’Alaska à l’ouest de la baie d’Hudson et sur l’île de Baffin. Comptant plus de 2 millions d’individus au début des années 1990, la population actuelle est estimée à environ 800 000 individus. La plupart des sous-populations ont connu un déclin dramatique, mais deux d’entre elles sont en croissance, incluant la harde de caribous de la Porcupine. Pour 70 % de la population qui présentent suffisamment de données pour quantifier les tendances, le déclin est estimé à 56 % au cours des trois dernières générations (depuis 1989), dont plusieurs des plus grandes hardes ayant fait l’objet, depuis leurs effectifs les plus élevés, d’un déclin supérieur à 80 %. Les données de relevés disponibles pour un autre 25 % de la population totale indiquent également des déclins. Des indications obtenues des peuples autochtones locaux et des études scientifiques portent à croire que les effectifs de la plupart des hardes ont subi des fluctuations naturelles par le passé; cependant, les données démographiques disponibles n’indiquent aucun signe de rétablissement rapide en ce moment, et les menaces cumulatives sont sans précédent historique. Le statut répond aux critères de la catégorie « en voie de disparition » en raison d’une réduction des effectifs supérieure ou égale à 50%, mais la catégorie « menacée » est recommandée car, dans l’ensemble, cette population ne semble pas faire face actuellement à une disparition imminente. Malgré des déclins inquiétants dans la majeure partie de l’aire de répartition, l’abondance numérique actuelle de la harde de caribous de la Porcupine et la prise de nombreuses mesures de gestion par les gouvernements, les conseils de gestion des ressources fauniques, et les communautés appuient la catégorie « menacée » en tant qu’un statut de conservation plus approprié. La situation de ces sous-populations devra faire l’objet d’un étroit suivi et pourrait justifier une réévaluation d’ici cinq ans.
Tous les caribous et rennes du monde ne constituent qu’une seule espèce de cervidés (Rangifer tarandus) et sont présents dans les régions arctiques et subarctiques ainsi que dans les forêts du Nord. Le caribou de la toundra se distingue par de longues migrations et un comportement très grégaire, se déplaçant souvent en groupes de plusieurs centaines ou de plusieurs milliers d’individus. En tant qu’herbivore de taille relativement grande avec une vaste aire de répartition et un effectif élevé, le caribou de la toundra constitue une population clé qui joue un rôle écologique et culturel important dans les écosystèmes nordiques.
Les découvertes archéologiques liées au suivi de la répartition de l’humain et du caribou de la toundra par rapport au retrait des glaciers il y a environ 8 000 ans, dans les régions centrales de la toundra, et il y a aussi longtemps que 12 000 à 15 000 ans, dans le centre de l’aire de répartition de la sous-population de la Porcupine, montrent clairement l’importance du caribou de la toundra pour le peuplement du nord du Canada. Le caribou de la toundra a été et demeure une ressource importante pour les habitants du nord du Canada; dans certains cas, l’importance de cette population est telle que des familles la suivent au fil de sa migration. Les activités de chasse dont la population fait l’objet, principalement celles aux fins de subsistance, ont une valeur économique directe importante. Le caribou de la toundra contribue à l’économie du Nord par l’intermédiaire du tourisme faunique et de la chasse récréative. De plus, il a une valeur culturelle incalculable pour les habitants dans l’ensemble des aires de répartition de ses sous-populations.
L’aire de répartition mondiale du caribou de la toundra s’étend de l’Alaska à l’ouest du Groenland et elle est continue dans l’ensemble du nord du territoire continental du Canada, du nord-ouest du Yukon à l’île de Baffin. La limite nord de cette aire correspond à la côte continentale dans l’Arctique, et la limite sud correspond à la région nord de la Saskatchewan, de l’Alberta et du Manitoba. Les activités et les méthodes d’échantillonnage varient selon les sous-populations, ce qui donne lieu à des différences dans l’interprétation de la structure de celles-ci; 14 ou 15 sous-populations sont reconnues dans le présent rapport. Certaines sont combinées afin d’obtenir des estimations des tendances et de l’abondance de la population, pour un total de 13 unités. Dix sous-populations ont systématiquement été reconnues au cours des dernières décennies, principalement en fonction de leur fidélité aux aires de mise bas.
La fluctuation de l’abondance de chaque sous-population a une incidence sur la répartition. Quand l’abondance du caribou de la toundra baisse, la répartition de la population (en particulier en hiver) change et la distance de migration à l’automne et avant la mise bas diminue. Les sous-populations continentales de caribous de la toundra migrent généralement vers la côte arctique pour mettre bas, et elles sont présentes dans la toundra de l’écozone du Bas-Arctique à l’été et à l’automne. Les sous-populations de l’ouest et du centre du continent passent habituellement l’hiver dans la forêt boréale des écozones de la taïga de la Cordillère, de la taïga des plaines et de la taïga du Bouclier.
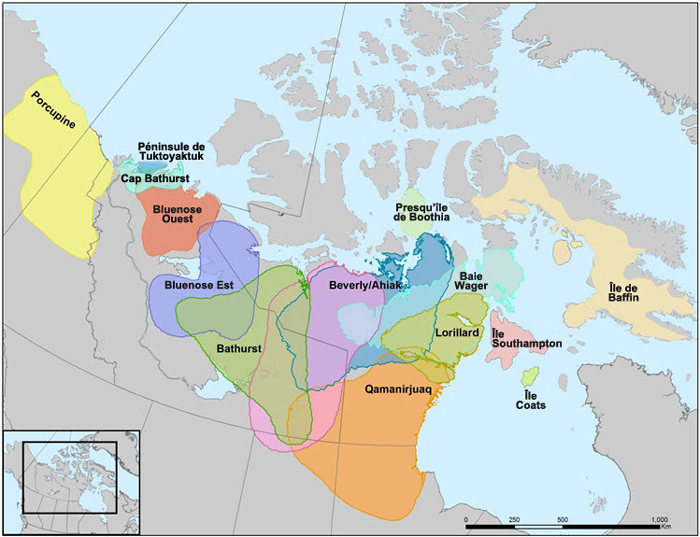
Répartition des sous-populations de caribous de l’unité désignable du caribou de la toundra. Carte préparée par Bonnie Fournier, gouvernement des Territoires du Nord-Ouest.
Les besoins en matière d’habitat dépendent en partie des besoins alimentaires, qui varient en fonction du moment du cycle de reproduction annuel du caribou et des coûts nutritionnels de ce cycle par rapport à la courte saison de croissance végétale et aux longs hivers dans les régions arctiques et subarctiques. Le caribou est une espèce généraliste sur le plan de l’alimentation, en particulier en été, et il se nourrit de graminées, de carex, d’arbustes et de plantes herbacées non graminoïdes, selon le stade de la croissance végétale plutôt que selon l’espèce végétale. Le caribou de la toundra a besoin de vastes territoires annuels (d’une superficie de plusieurs centaines de milliers de kilomètres carrés) afin d’avoir accès à une gamme de milieux de rechange pour s’adapter aux variations annuelles dans l’environnement, notamment sur le plan de la couverture de neige, de la croissance végétale, du risque de prédation ou du risque d’infestation par des parasites. Les caractéristiques de l’habitat qui sont importantes pour la mise bas comprennent celles qui réduisent le risque de prédation et qui maximisent l’apport nutritionnel, et ces caractéristiques varient d’une aire de mise bas à l’autre. Les besoins alimentaires dépendent du moment du cycle de reproduction annuel par rapport à la courte saison de croissance végétale et aux longs hivers qui caractérisent les régions arctiques et subarctiques. Dans les aires d’estivage, le caribou recherche des milieux où le harcèlement par les insectes est moindre et où la nourriture est de grande qualité. La plupart des sous-populations passent l’hiver dans la forêt boréale, mais plusieurs demeurent dans la toundra tout l’hiver.
Au cours des trois générations précédentes, une certaine réduction a été observée sur le plan de l’habitat à la suite de la fragmentation naturelle des aires d’hivernage causée par les feux de forêt et de l’augmentation de la présence humaine (c.-à-d. infrastructure) dans les aires de répartition du caribou. Toutefois, l’habitat à l’extérieur de l’aire d’hivernage boisée est encore largement intact à l’échelle du paysage. Les tendances générales à la hausse de la population humaine donneront lieu à une augmentation du développement économique (développement industriel, routes et circulation) dans les territoires utilisés par le caribou de la toundra.
Le caribou met habituellement bas pour la première fois à l’âge de trois ans, mais il peut également mettre bas à l’âge de deux ans quand les conditions sont favorables. Les femelles donnent naissance à un seul petit et peuvent se reproduire chaque année en l’absence de stress nutritionnel. La mise bas est grandement synchronisée et a habituellement lieu au cours d’une période de deux semaines en juin. Le caribou est une espèce polygyne. Les migrations annuelles et le comportement grégaire constituent les caractéristiques les plus évidentes de la plupart des sous-populations de caribous de la toundra. Ces caractéristiques constituent des adaptations à une longue saison hivernale durant laquelle les températures froides, le refroidissement éolien et la neige imposent des coûts énergétiques élevés. Ces coûts sont assumés par l’intermédiaire d’une réduction des besoins en énergie de maintien et de la mobilisation des réserves de gras et de protéines.
La prédation est un facteur qui a une incidence importante sur de nombreuses facettes de l’écologie du caribou puisque les déplacements et les choix d’habitat de l’espèce visent souvent sur la réduction au minimum de l’exposition aux prédateurs. Une gamme de prédateurs et de détritivores dépendent du caribou de la toundra : l’ours grizzli (Ursus arctos) est un prédateur efficace des nouveau-nés, tandis que le loup gris (Canis lupus, appelé ci-après« loup ») est un prédateur de toutes les classes d’âge et de sexe à longueur d’année. Les agents pathogènes (y compris des virus, des bactéries, des helminthes et des protozoaires), en combinaison avec les insectes, jouent un rôle important dans l’écologie du caribou, et les effets varient d’effets subtils sur la reproduction à des maladies cliniques ou à la mort.
L’effectif actuel de la population de caribous de la toundra est estimé à environ 800 000 individus. Entre 1986 et le milieu des années 1990, l’effectif de la population a dépassé le cap des deux millions, avant de connaître un déclin qui persiste encore aujourd’hui. Parmi les treize unités de sous-populations utilisées pour estimer l’abondance, huit sont en déclin, deux connaissent une augmentation, et trois ont un effectif inconnu. Le pourcentage médian de déclin sur trois générations du nombre total de caribous de la toundra se chiffre à 56,8 % (intervalle de -50,8 à -59,0 %), selon la somme des changements survenus dans sept sous-populations pour lesquelles les données de relevés sont suffisantes, ces sous-populations comptant pour près de 70 % de la population actuelle totale. Quatre de ces sept sous-populations ont connu un déclin supérieur à 80 % au cours de cette période, une autre a connu un déclin médian de 39 % caractérisé par une variabilité marquée, et les deux autres ont connu une augmentation. Les données de relevés disponibles suggèrent également un déclin pour trois autres sous-populations, qui représentent environ 25 % de la population totale. L’évolution actuelle de trois autres sous-populations est inconnue en raison de l’absence de relevés récents.
Les connaissances traditionnelles autochtones (CTA) et l’étude scientifique suggèrent que les sous-populations de caribous de la toundra connaissent des périodes d’effectif élevé et faible (fluctuations) qui peuvent ressembler à des cycles de population. Les données sont toutefois insuffisantes pour inférer de façon systématique l’existence d’un cycle naturel d’augmentation pour l’ensemble des sous-populations. Les données démographiques disponibles ainsi que les changements cumulatifs touchant l’environnement, les milieux et les régimes de récolte pour nombre de ces sous-populations sont sans précédent, et il serait donc risqué de supposer qu’un rétablissement naturel aura lieu, du moins jusqu’aux valeurs enregistrées dans les années 1990, pour de nombreuses sous-populations.
Le climat et les conditions météorologiques ont des effets non linéaires complexes et en cascade sur d’autres facteurs limitatifs importants pour le caribou de la toundra, y compris la disponibilité de la nourriture, la prédation, les parasites et les maladies. Tant d’aspects de l’écologie du caribou sont touchés par les conditions météorologiques qu’un climat plus chaud pourrait avoir un ensemble important, mais complexe d’effets positifs et négatifs.
Au cours des dernières décennies, les activités d’exploration et de développement industriel ont augmenté dans les territoires utilisés par le caribou de la toundra, et plusieurs territoires utilisés par des sous-populations comptent maintenant plusieurs nouvelles mines et des centaines de permis de prospection, de concessions minières et de baux d’exploitation minière. En outre, la chasse de subsistance et la chasse récréative peuvent constituer des causes de mortalité importantes et ainsi accroître le taux de déclin et donner lieu à une population de taille réduite. Les concentrations de contaminants chimiques dans les tissus sont généralement faibles à l’heure actuelle. L’évolution des conditions dans les territoires utilisés par le caribou comprend également la complexité administrative et politique d’un ensemble de revendications territoriales réglées et non réglées, avec des changements dans les limites de compétence et les mandats. La complexité des rapports entre les différentes compétences - organismes politiques, organismes de gestion des terres et organismes de gestion des ressources fauniques -, combinée à la nature migratoire du caribou et à son utilisation de vastes territoires saisonniers, compliquent la mise en œuvre des mesures de gestion.
La protection des sous-populations de caribous de la toundra par les compétences provinciales et territoriales est assurée par l’intermédiaire de la réglementation de la récolte et de la protection de l’habitat. Le régime de cogestion constitue une responsabilité de gestion partagée entre les gouvernements et les organismes établis par les dispositions législatives relatives aux revendications territoriales et par des accords multilatéraux renouvelables entre des administrations publiques (pour les sous-populations de la Porcupine, de Beverly et de Qamanirjuaq). La sous-population de la Porcupine est la seule sous-population de caribous de la toundra couverte par un accord international signé par le Canada et les États-Unis en 1987. Le COSEPAC a évalué pour la première fois l’unité désignable (UD) du caribou de la toundra en novembre 2016 et l’a jugée comme étant menacée. À l’heure actuelle, cette UD ne figure pas aux annexes de la Loi sur les espèces en péril (LEP) du Canada. La situation générale du caribou au Canada en 2015 ne sera connue qu’en août 2017, quand le rapport sur la situation générale des espèces de 2015 sera publié. Cette classification pancanadienne s’appliquera à l’ensemble des UD du caribou et ne visera pas spécifiquement le caribou de la toundra. La cote territoriale attribuée au caribou de la toundra en 2015 est « vulnérable à apparemment non en péril » au Yukon et « sensible » dans les Territoires du Nord-Ouest. À l’heure actuelle, il n’y a pas de classement particulier pour le caribou de la toundra au Nunavut, mais pour l’ensemble des UD, la cote générale attribuée à l’échelle territoriale au Nunavut est « apparemment non en péril ». Les aires fédérales protégées dans lesquelles les utilisations industrielles des terres sont exclues, mais où la chasse de subsistance est permise, comptent pour environ 6 % des territoires utilisés par le caribou de la toundra et comprennent huit parcs nationaux.
Source : COSEPAC. 2016. Évaluation et Rapport de situation du COSEPAC sur le caribou (Rangifer tarandus), population de la toundra, au Canada. Comité sur la situation des espèces en péril au Canada. Ottawa. xiv + 147 p.

Photo: © Charles Jutras
Description longue
Rangifer tarandus
Mammifères
En voie de disparition
Nunavut, Québec, Terre-Neuve-et-Labrador
Cette population est limitée à la péninsule d’Ungava dans l’est du Québec, dans le nord du Labrador et au Nunavut (Killiniq et les îles adjacentes). Aucune tendance quantitative n’est disponible, car les données de relevés sont limitées, mais la population totale a été estimée à 5 000 individus en 1980 et à 930 individus en 2014, ce qui semble indiquer un déclin significatif. Les connaissances traditionnelles autochtones indiquent également un déclin. La population correspond au statut d’espèce « en voie de disparition », car une seule population compte l’ensemble des 698 animaux matures estimés, un déclin de la population est évident et devrait se poursuivre en raison des taux de récolte et d’une diminution de la qualité de l’habitat associée aux changements climatiques. La population pourrait faire face à une disparition imminente en raison du faible nombre d’individus restants.
Le caribou (Rangifer tarandus) est un cervidé de taille moyenne. Il possède des pattes relativement longues et de gros sabots qui facilitent ses déplacements dans la neige épaisse des milieux nordiques. Le caribou est au coeur de la culture, de la spiritualité et de la subsistance de nombreuses collectivités autochtones du Nord, et est également important pour des non-Autochtones du Canada. Les caribous présentent une grande variabilité sur le plan morphologique, écologique et comportemental à l’échelle de leur aire de répartition circumpolaire. En 2011, le COSEPAC a établi 12 unités désignables (UD) pour le caribou; le présent rapport de situation porte sur la population migratrice de l’Est (population ME; UD 4) et sur la population des monts Torngat (population des MT; UD 10).
La population ME comprend quatre sous-populations, soit celle du cap Churchill, située sur le littoral de la baie d’Hudson, à la frontière entre le Manitoba et l’Ontario; celle du sud de la baie d’Hudson, principalement située plus au sud et à l’est, dans le nord de l’Ontario; celle de la rivière aux Feuilles (Leaf River), dans le nord du Québec; et celle de la rivière George, au Québec et au Labrador. La superficie de l’aire de répartition combinée est de plus de 1,5 million de km2. Les caribous des MT forment une seule population et occupent un territoire d’environ 28 000 km2 dans les monts Torngat, dans le nord du Labrador, le nord du Québec et le Nunavut (Killiniq et îles adjacentes).
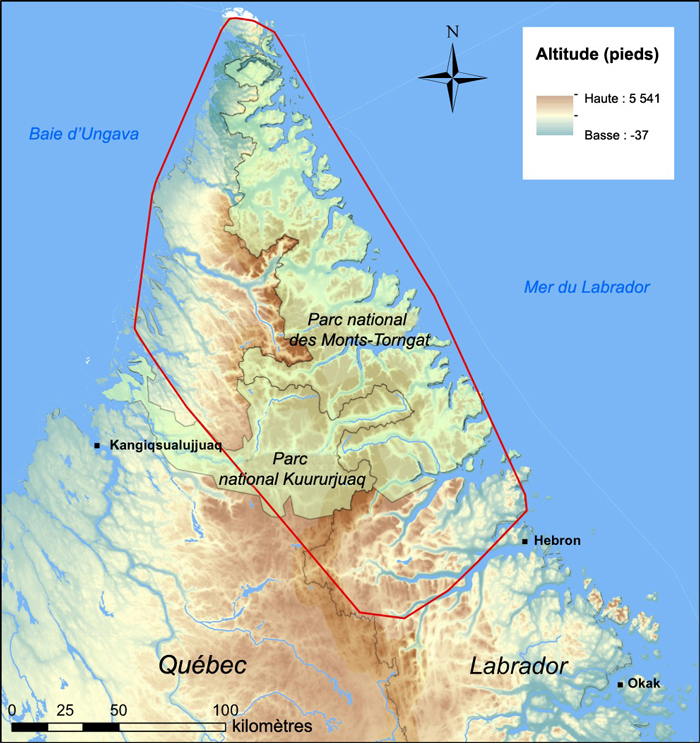
Aire de répartition estimée de la sous-population de caribous des monts Torngat, représentée par le polygone rouge. Ce polygone, qui indique l’emplacement de 35 caribous adultes suivis par satellite entre 2011 et 2015, est fondé sur la méthode du plus petit polygone convexe à 100 % (Source : Courturier et Mitchell Foley, 2014; Caribou Ungava).
Les caribous migrateurs de l’Est utilisent principalement la toundra durant la période de mise bas et en été, et occupent la taïga et surtout la forêt boréale durant l’hiver. Les caribous des monts Torngat utilisent les zones alpines des plateaux montagneux des monts Torngat et les vallées adjacentes de même que des zones côtières. La mise bas a lieu sur des versants montagneux, dans des îles et sur des plateaux alpins.
La longévité du caribou est habituellement de moins de 10 ans chez les mâles et de moins de 15 ans chez les femelles. La majorité des femelles âgées de 3 ans ou plus donnent naissance à un seul petit par année, ce qui fait que le taux de reproduction du caribou est plus faible que celui des autres cervidés d’Amérique du Nord. La primiparité peut survenir à l’âge de 2 ans lorsque les conditions de l’habitat sont favorables. On estime la durée d’une génération à 6 à 7 ans.
La taille minimale de la population ME s’élève à 227 513 caribous de tous âges, selon les plus récentes estimations totales établies pour les sous-populations de la rivière aux Feuilles (2016) et de la rivière George (2016) ainsi que les plus récentes estimations minimales établies pour les sous-populations du cap Churchill (2007) et du sud de la baie d’Hudson (2011). Le nombre estimatif de caribous matures est de 170 636. Le nombre de caribous matures de la population ME il y a trois générations (18 – 21 ans) est estimé à 833 774, ce qui donne un déclin de 80 % sur trois générations. Les connaissances traditionnelles autochtones corroborent le déclin de la sous-population de la rivière George.
Il est établi que les sous-populations de l’est de l’aire de répartition de la population ME fluctuent (selon les connaissances traditionnelles autochtones et des données historiques), mais on ignore si les effectifs pourront augmenter de nouveau en raison de la présence de nouvelles menaces. Les caribous appartenant à ces UD sont associés au lichen et à la toundra dominée par les graminées, mais le paysage de la toundra change à cause du réchauffement climatique. Le nombre de caribous de la sous-population de la rivière George (qui constituait, jusqu’à récemment, la plus grande sous-population de caribous migrateurs de l’Est) a diminué, et les menaces qui pèsent sur les sous-populations de la rivière George et de la rivière aux Feuilles sont considérées comme importantes.
Le nombre de caribous de la population des MT a été estimé à environ 5 000 dans les années 1980 et à 930 (dont 698 caribous matures) au printemps 2014, ce qui correspond à une réduction de plus de 80 % en 35 ans environ (approximativement 4 – 5 générations). Les connaissances traditionnelles autochtones corroborent ce déclin. Il n’existe aucune donnée sur les variations de population sur une période de trois générations.
Les caribous sont sensibles aux perturbations. Le développement industriel, et plus particulièrement l’exploitation minière et les réseaux routiers qui y sont associés, représente une menace pour les caribous ME. La récolte excessive de caribous ME et de caribous des MT contribue au déclin des populations. Les populations sont généralement restreintes par la disponibilité de la nourriture, mais la chasse de subsistance et la chasse sportive peuvent constituer un facteur limitatif lorsque les populations sont petites ou en déclin. Un parasite, le Besnoitia tarandi, est apparu dans les sous-populations de l’est de la population ME au milieu des années 2000 et pourrait avoir une incidence sur la productivité du caribou. Les changements climatiques, qui ont des effets sur la qualité de l’habitat et la disponibilité des ressources, semblent également constituer une menace pour les populations de caribous, compte tenu de l’augmentation du couvert arbustif dans la toundra. Selon le calculateur des menaces, l’impact des menaces est considéré comme « très élevé à élevé » pour le caribou ME, et « élevé » pour le caribou des MT.
Le COSEPAC a évalué la situation du caribou ME (en voie de disparition) en avril 2017, et la situation du caribou des MT (en voie de disparition) en novembre 2016. En 2016, l’UICN a modifié la cote attribuée à la population mondiale de caribous, la faisant passer de « préoccupation mineure » à « vulnérable ». La cote mondiale attribuée au caribou par NatureServe est G5 (non en péril; dernière mise à jour en 2012), mais aucune cote n’a été établie pour les différentes UD reconnues par le COSEPAC. La cote provisoire accordée en 2015 aux caribous du Labrador (principalement à la sous-population de la rivière George) est S1S2 (gravement en péril à en péril).
Source : COSEPAC. 2017. Évaluation et Rapport de situation du COSEPAC sur le caribou (Rangifer tarandus), population migratrice de l’Est et population des monts Torngat, au Canada. Comité sur la situation des espèces en péril au Canada, Ottawa, xix + 80 p.

Photo: © Steeve Côté
Description longue
Rangifer tarandus
Mammifères
En voie de disparition
Manitoba, Ontario, Québec, Terre-Neuve-et-Labrador
La population migratrice de caribou est composée de quatre sous-populations présentes depuis les côtes de l’ouest de la baie d’Hudson jusqu’au Labrador. La population est actuellement estimée à 170 636 individus matures, estimation qui révèle un déclin global de 80 % des effectifs sur 3 générations (18-21 ans). Le déclin devrait se poursuivre à cause de la surexploitation et d’une diminution de la qualité de l’habitat associée aux changements climatiques et aux activités de développement. Deux sous-populations en déclin renferment environ 99 % de la population migratrice de l’Est : celle de la rivière George a connu un déclin de 99 % sur 3 générations et celle de la rivière Leaf, un déclin de 68 % sur 2 générations. La taille des populations migratrices de caribou fluctue, mais l’on craint que les menaces récentes et prévues limitent la croissance d’une population qui est actuellement à son niveau le plus bas enregistré. Les menaces semblent être moins courantes dans les deux sous-populations de l’ouest, lesquelles représentent environ seulement 4% de la population totale existante. La plupart des autres caribous font partie de la sous-population de la rivière Leaf, qui continue de connaître un déclin.
Le caribou (Rangifer tarandus) est un cervidé de taille moyenne. Il possède des pattes relativement longues et de gros sabots qui facilitent ses déplacements dans la neige épaisse des milieux nordiques. Le caribou est au coeur de la culture, de la spiritualité et de la subsistance de nombreuses collectivités autochtones du Nord, et est également important pour des non-Autochtones du Canada. Les caribous présentent une grande variabilité sur le plan morphologique, écologique et comportemental à l’échelle de leur aire de répartition circumpolaire. En 2011, le COSEPAC a établi 12 unités désignables (UD) pour le caribou; le présent rapport de situation porte sur la population migratrice de l’Est (population ME; UD 4) et sur la population des monts Torngat (population des MT; UD 10).
La population ME comprend quatre sous-populations, soit celle du cap Churchill, située sur le littoral de la baie d’Hudson, à la frontière entre le Manitoba et l’Ontario; celle du sud de la baie d’Hudson, principalement située plus au sud et à l’est, dans le nord de l’Ontario; celle de la rivière aux Feuilles (Leaf River), dans le nord du Québec; et celle de la rivière George, au Québec et au Labrador. La superficie de l’aire de répartition combinée est de plus de 1,5 million de km2. Les caribous des MT forment une seule population et occupent un territoire d’environ 28 000 km2 dans les monts Torngat, dans le nord du Labrador, le nord du Québec et le Nunavut (Killiniq et îles adjacentes).
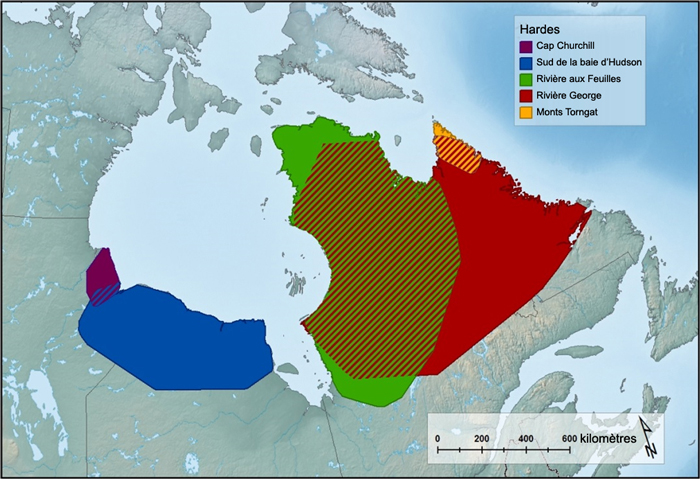
Répartition approximative de la population de caribous des monts Torngat et des quatre sous-populations de caribous migrateurs de l’Est. Les zones hachurées correspondent aux aires de chevauchement des sous-populations. L’aire de répartition indiquée pour la sous-population de la rivière George date d’avant 1999, c’est-à-dire d’avant son rétrécissement. (Source : Pond et al., 2016; données inédites de Caribou Ungava et des gouvernements de l’Ontario, du Québec et de Terre-Neuve-et-Labrador). (Carte produite par A. Filion, Secrétariat du COSEPAC).
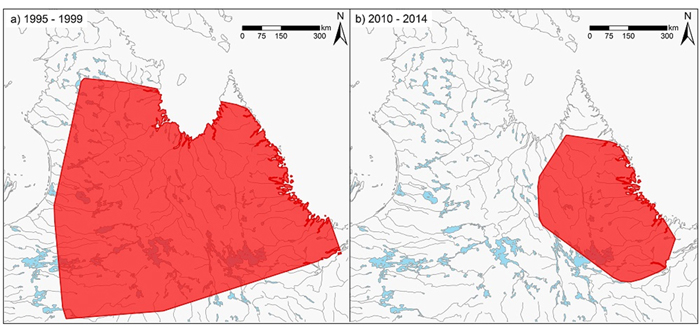
Répartition comparée de la sous-population de la rivière George à la fin des années 1990 et durant la période 2010 – 2014. Les polygones, qui représentent la position des caribous suivis par satellite, sont fondés sur la méthode du plus petit polygone convexe à 100 %. La diminution de l’aire de répartition est d’environ 85% (Source : gouvernement du Québec, gouvernement de Terre-Neuve-et-Labrador, Caribou Ungava).
Description longue
Les caribous migrateurs de l’Est utilisent principalement la toundra durant la période de mise bas et en été, et occupent la taïga et surtout la forêt boréale durant l’hiver. Les caribous des monts Torngat utilisent les zones alpines des plateaux montagneux des monts Torngat et les vallées adjacentes de même que des zones côtières. La mise bas a lieu sur des versants montagneux, dans des îles et sur des plateaux alpins.
La longévité du caribou est habituellement de moins de 10 ans chez les mâles et de moins de 15 ans chez les femelles. La majorité des femelles âgées de 3 ans ou plus donnent naissance à un seul petit par année, ce qui fait que le taux de reproduction du caribou est plus faible que celui des autres cervidés d’Amérique du Nord. La primiparité peut survenir à l’âge de 2 ans lorsque les conditions de l’habitat sont favorables. On estime la durée d’une génération à 6 à 7 ans.
La taille minimale de la population ME s’élève à 227 513 caribous de tous âges, selon les plus récentes estimations totales établies pour les sous-populations de la rivière aux Feuilles (2016) et de la rivière George (2016) ainsi que les plus récentes estimations minimales établies pour les sous-populations du cap Churchill (2007) et du sud de la baie d’Hudson (2011). Le nombre estimatif de caribous matures est de 170 636. Le nombre de caribous matures de la population ME il y a trois générations (18 – 21 ans) est estimé à 833 774, ce qui donne un déclin de 80 % sur trois générations. Les connaissances traditionnelles autochtones corroborent le déclin de la sous-population de la rivière George.
Il est établi que les sous-populations de l’est de l’aire de répartition de la population ME fluctuent (selon les connaissances traditionnelles autochtones et des données historiques), mais on ignore si les effectifs pourront augmenter de nouveau en raison de la présence de nouvelles menaces. Les caribous appartenant à ces UD sont associés au lichen et à la toundra dominée par les graminées, mais le paysage de la toundra change à cause du réchauffement climatique. Le nombre de caribous de la sous-population de la rivière George (qui constituait, jusqu’à récemment, la plus grande sous-population de caribous migrateurs de l’Est) a diminué, et les menaces qui pèsent sur les sous-populations de la rivière George et de la rivière aux Feuilles sont considérées comme importantes.
Le nombre de caribous de la population des MT a été estimé à environ 5 000 dans les années 1980 et à 930 (dont 698 caribous matures) au printemps 2014, ce qui correspond à une réduction de plus de 80 % en 35 ans environ (approximativement 4 – 5 générations). Les connaissances traditionnelles autochtones corroborent ce déclin. Il n’existe aucune donnée sur les variations de population sur une période de trois générations.
Les caribous sont sensibles aux perturbations. Le développement industriel, et plus particulièrement l’exploitation minière et les réseaux routiers qui y sont associés, représente une menace pour les caribous ME. La récolte excessive de caribous ME et de caribous des MT contribue au déclin des populations. Les populations sont généralement restreintes par la disponibilité de la nourriture, mais la chasse de subsistance et la chasse sportive peuvent constituer un facteur limitatif lorsque les populations sont petites ou en déclin. Un parasite, le Besnoitia tarandi, est apparu dans les sous-populations de l’est de la population ME au milieu des années 2000 et pourrait avoir une incidence sur la productivité du caribou. Les changements climatiques, qui ont des effets sur la qualité de l’habitat et la disponibilité des ressources, semblent également constituer une menace pour les populations de caribous, compte tenu de l’augmentation du couvert arbustif dans la toundra. Selon le calculateur des menaces, l’impact des menaces est considéré comme « très élevé à élevé » pour le caribou ME, et « élevé » pour le caribou des MT.
Le COSEPAC a évalué la situation du caribou ME (en voie de disparition) en avril 2017, et la situation du caribou des MT (en voie de disparition) en novembre 2016. En 2016, l’UICN a modifié la cote attribuée à la population mondiale de caribous, la faisant passer de « préoccupation mineure » à « vulnérable ». La cote mondiale attribuée au caribou par NatureServe est G5 (non en péril; dernière mise à jour en 2012), mais aucune cote n’a été établie pour les différentes UD reconnues par le COSEPAC. La cote provisoire accordée en 2015 aux caribous du Labrador (principalement à la sous-population de la rivière George) est S1S2 (gravement en péril à en péril).
Source : COSEPAC. 2017. Évaluation et Rapport de situation du COSEPAC sur le caribou (Rangifer tarandus), population migratrice de l’Est et population des monts Torngat, au Canada. Comité sur la situation des espèces en péril au Canada, Ottawa, xix + 80 p.

Photo: © Thomas G. Barnes @ USDA-NRCS PLANTS Database
Description longue
Chimaphila maculata
Plantes vasculaires
Menacée
Ontario, Québec
Cette plante vivace basse est restreinte aux sols sablonneux dans le sud de l’Ontario. Depuis la dernière évaluation, cette espèce a été découverte dans deux nouveaux sites et est disparue de deux autres sites. L’ensemble de la population est demeuré relativement stable, mais les cinq sous-populations sont menacées par les activités récréatives et la possibilité de feu de friches.
La chimaphile maculée (Chimaphila maculata) est une petite plante vivace basse à feuilles persistantes qui est ligneuse à la base et se propage à l’aide de rhizomes pour former des colonies. Chaque tige porte des feuilles vert-bleu épaisses et dentées qui sont disposées en verticilles et dont la nervation est panachée de blanc. Le verticille de feuilles est surmonté d’une tige portant une à cinq fleurs blanches ou rosâtres à port retombant. Pour une année donnée, seules certaines tiges d’une sous-population produisent des fleurs. Les capsules arrondies se redressent après la floraison et contiennent de nombreuses graines minuscules.
La chimaphile maculée est présente dans l’est de l’Amérique du Nord, au Mexique et en Amérique centrale. Dans l’est de l’Amérique du Nord, on la trouve depuis le sud du Michigan et de l’Ontario jusqu’au sud du New Hampshire et du Maine, vers l’est, et jusqu’au Mississippi et au nord de la Floride, vers le sud. Par le passé, la chimaphile maculée était plus répandue dans le sud de l’Ontario et dans le sud-ouest du Québec. Aujourd’hui, il subsiste quelques sous-populations dans le sud de l’Ontario, et on la considère disparue du Québec.
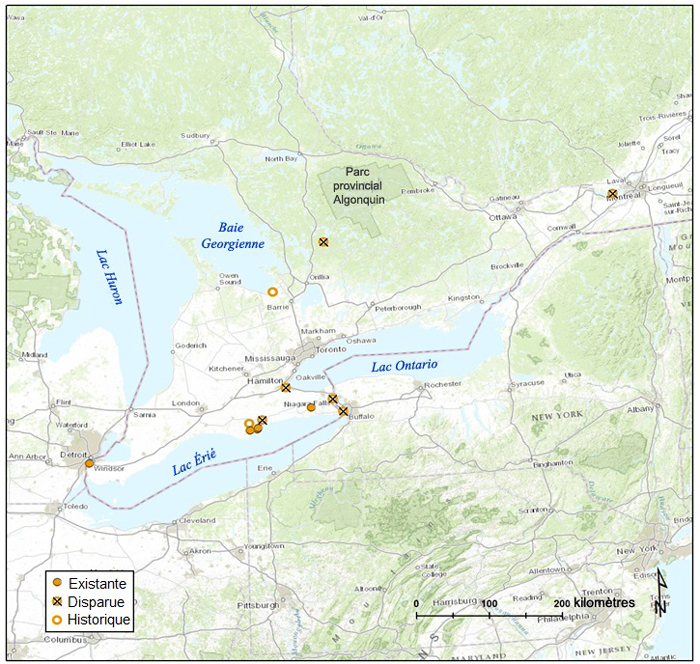
Sous-populations de chimaphile maculée au Canada. Cette figure illustre toutes les sous-populations répertoriées au Canada jusqu’à maintenant. Sources : NHIC, 2015; CDPNG, 2015.
La chimaphile maculée est une espèce du sous-étage typiquement associée aux forêts et aux boisés mixtes de chênes ou de chênes et de pins sur sol sec à frais. La plante pousse généralement dans un sol sableux bien drainé, exempt de gros fragments, pauvre en nutriments et dont la teneur en matière organique est faible.
La floraison de la chimaphile maculée se produit à la fin du mois de juillet et au début du mois d’août. Elle se reproduit par voie clonale ou à partir de graines. Comme les tiges proviennent de rhizomes traçants, les touffes ou les groupes contigus de tiges constituent probablement des ramets plutôt que des individus génétiquement distincts. Les graines minuscules de cette famille de plantes, semblables à des grains de poussière, sont surtout dispersées par le vent.
Au Canada, on compte actuellement cinq sous-populations existantes. Selon les relevés effectués entre 2011 et 2014, la population totale au Canada serait d’au moins 3 587 (~3 600) tiges. Le nombre d’individus génétiquement distincts n’est pas connu, mais on présume qu’il est inférieur à ce chiffre. Les populations déclarées antérieurement s’élevaient à quelques centaines de tiges, mais deux des sous-populations existantes (et plusieurs sites plus petits) ont été découvertes après la diffusion du dernier rapport de situation et sont toutes deux assez isolées des autres sites existants. Il ne s’agit probablement pas de sous-populations nouvellement établies; cette découverte pourrait découler de l’intensification des activités de recherche et de communication des observations. La plupart des sites connus depuis environ l’an 2000 sont demeurés au minimum stables, mais certains présentent une abondance et une étendue accrues, comme l’indique le suivi effectué régulièrement.
On compte en outre deux sous-populations historiques et six sous-populations disparues. Il est possible que des individus aient persisté à l’un ou l’autre des sites historiques. La plupart des mentions d’individus disparus n’ont été obtenues qu’à partir de données vagues sur leur localisation ou leur population et les individus n’ont jamais été retrouvés. Une petite sous-population découverte près de Montréal en 1992 pourrait avoir été plantée, et on croit aujourd’hui qu’elle a disparu.
Les activités récréatives représentent probablement la principale menace pesant sur les sous-populations existantes de chimaphile maculée, mais les incendies risquent d’avoir le plus de conséquences, car cette espèce ne semble pas persister après un feu. La plupart des sites existants sont de propriété publique et sont protégés des pertes attribuables au développement, mais de nombreux sites sont accessibles à la population, et il se peut que certains d’entre eux soient vulnérables aux dommages occasionnés par les VTT et au compactage du sol dans les sentiers pédestres adjacents. Beaucoup de sites ne semblent pas être menacés dans l’immédiat, bien que leur petite taille et leur étendue géographique les rendent vulnérables à des perturbations localisées. Des espèces envahissantes sont présentes sur quelques sites ou à proximité de ces derniers, mais ne semblent pas nuire au nombre de ramets (ou tiges) de ces sous-populations. La dégradation de l’habitat (p. ex. par le déversement de déchets) pourrait aussi avoir des effets limités sur certaines sous-populations de chimaphile maculée. Il se peut que cette espèce soit restreinte dans une certaine mesure en raison de sa dépendance aux champignons mycorhiziens du sol et de la biologie de sa reproduction.
La chimaphile maculée a été désignée « en voie de disparition » pour la première fois par le COSEPAC en 1987. Ce statut a été revu et confirmé en 1998 et en 2000. L’espèce est actuellement désignée « en voie de disparition » aux termes de la Loi sur les espèces en péril (LEP) et de la Loi sur les espèces en voie de disparition (LEVD) de l’Ontario. En Ontario, l’espèce et son habitat sont protégés en vertu de la LEVD. La cote de conservation mondiale de la chimaphile maculée est G5, soit « non en péril ». Au Canada, la chimaphile maculée est classée N2 (en péril). En Ontario, elle est classée S2 et au Québec, SX. La chimaphile maculée est considérée comme étant non en péril (N5) aux États-Unis, mais au sein même de ce pays, elle est désignée gravement en péril (S1) en Illinois, et en péril (S2) au Vermont, au Maine et au Mississippi. L’espèce est aussi protégée par la loi en Illinois, où elle a été désignée comme espèce en voie de disparition.
Source : COSEPAC. 2017. Évaluation et Rapport de situation du COSEPAC sur la chimaphile maculée (Chimaphila maculata) au Canada. Comité sur la situation des espèces en péril au Canada. Ottawa. xiv + 42 p.

Photo: © Tamra Feenstra
Description longue
Coccinella transversoguttata
Arthropodes
Préoccupante
Yukon, Territoires-du-Nord-Ouest, Nunavut, Colombie-Britannique, Alberta, Saskatchewan, Manitoba, Ontario, Québec, Nouveau-Brunswick, Île-du-Prince-Édouard, Nouvelle-Écosse, Terre-Neuve-et-Labrador
Cette espèce était autrefois commune et largement répartie dans la majeure partie du Canada. Les déclins ont débuté dans les années 1970, et l’espèce est maintenant absente du sud de l’Ontario et des Maritimes. Dans certaines parties de son aire de répartition occidentale et septentrionale, l’espèce est toujours couramment observée. La propagation de coccinelles non indigènes est considérée comme une des menaces possibles pesant sur l’espèce en raison de la compétition, de la prédation intraguilde ou de l’introduction de pathogènes. Les coccinelles non indigènes sont moins abondantes dans les endroits où l’espèce demeure.
La coccinelle à bandes transverses est un petit coléoptère au corps arrondi indigène en Amérique du Nord. Chez les adultes, les élytres sont orange à rouges, avec un motif distinctif constitué d’une bande noire et de quatre taches noires de forme allongée. Cette espèce charismatique était autrefois une des coccinelles les plus communes et les plus largement réparties en Amérique du Nord et jouait un rôle important à titre d’agent de lutte biologique contre des pucerons et d’autres insectes ravageurs.
La coccinelle à bandes transverses est présente dans tout le Canada et est largement répartie aux États-Unis. Au Canada, elle se rencontre depuis St. John’s, à Terre-Neuve, jusqu’à l’île de Vancouver, en Colombie-Britannique. Vers le nord, elle se rencontre jusqu’au Yukon et aux Territoires du Nord-Ouest et probablement jusqu’au Nunavut.
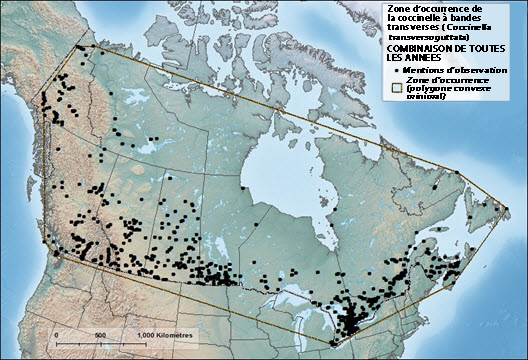
Répartition canadienne de la coccinelle à bandes transverses d’après les données de collecte de spécimens de musée et les résultats de relevés récents (1889-2015). La carte montre la zone d’occurrence, soit l’aire comprise dans un polygone sans angles concaves qui recouvre la distribution géographique de toutes les populations connues d’une espèce sauvage.
La coccinelle à bandes transverses est une généraliste de l’habitat qui se nourrit principalement de pucerons et vit dans divers types de milieux tels que des zones agricoles, des jardins suburbains, des parcs, des forêts conifériennes et décidues, des prairies, des prés, des zones riveraines et d’autres milieux naturels. La diversité des milieux dans laquelle elle se rencontre témoigne de sa capacité d’exploiter les fluctuations saisonnières de l’abondance des proies dans divers types de végétation.
Le cycle vital de la coccinelle à bandes transverses comporte quatre étapes, à savoir l’œuf, la larve, la nymphe et l’adulte. La coccinelle à bandes transverses peut avoir deux générations par année. Les adultes de la génération printanière peuvent entrer en estivation pour échapper aux chaleurs estivales et se reproduisent au début de l’automne. Les adultes de la génération automnale se rassemblent pour hiberner et entrent en diapause, puis redeviennent actifs et se reproduisent au début du printemps suivant lorsque les températures s’élèvent. Cette espèce occupe une large niche écologique dans un large éventail de milieux et de régimes de température au Canada. En général, les coccinelles sont des insectes très mobiles qui affichent une faible fidélité au site et qui se dispersent communément sur des distances allant de courtes (quelques centaines de mètres) à longues (18 à 120 km). La coccinelle à bandes transverses n’est pas migratrice. Tant au stade larvaire qu’au stade adulte, elle se nourrit principalement de pucerons. Elle sert elle-même de proie à d’autres invertébrés et à des vertébrés et est vulnérable à divers parasitoïdes et pathogènes.
La vaste répartition et l’abondance historiques de la coccinelle à bandes transverses tranchent avec sa répartition actuelle. Avant 1986, l’espèce était largement répartie et abondante à l’échelle de l’Amérique du Nord et y était une des espèces de coccinelles les plus fréquemment récoltées. Aujourd’hui, dans de nombreuses régions comprises dans son aire de répartition où elle était autrefois commune, elle est absente ou présente à des niveaux inférieurs au seuil de détection. Dans d’autres régions, elle se maintient à des densités très faibles. Au Yukon, dans les Territoires du Nord-Ouest et en Colombie-Britannique, elle semble toutefois abondante et commune. Ces régions présentent de plus faibles proportions de coccinelles non indigènes, lesquelles sont considérées comme une des menaces potentielles pour la coccinelle à bandes transverses et d’autres espèces de coccinelles indigènes.
Les causes précises du déclin de la coccinelle à bandes transverses à l’échelle de son aire de répartition sont actuellement inconnues. Au nombre des menaces possibles pour cette espèce figurent les relations interspécifiques négatives (en particulier la compétition, la prédation intraguilde ou les effets indirects de l’introduction de pathogènes) avec des espèces non indigènes récemment introduites en Amérique du Nord telles que la coccinelle à sept points et la coccinelle asiatique. D’autres menaces localisées et cumulatives possibles incluent les changements touchant l’utilisation des terres, tels les effets directs et indirects de l’utilisation de pesticides et d’autres produits chimiques agricoles contre des espèces-proies de la coccinelle à bandes transverses, la perte d’habitat causée par l’expansion urbaine, la conversion des terres agricoles en forêts et d’autres perturbations liées aux activités humaines.
La coccinelle à bandes transverses n’est protégée par aucune loi au Canada. Aucune cote de conservation mondiale ou nationale n’a encore été attribuée à l’espèce. Les divers Centres de données sur la conservation au Canada lui ont attribué les cotes suivantes : Yn = S4; T.N.-O. = S4S5; C.-B. = S5; Alb., Sask., Man. = S4S5; Ont. = S1; Qc = S4; N.-B., N.-É., Î.-P.-É. = SH; T.-N.-L. = SU; T.-N.-L. (Labrador seulement) = S5.
Source : COSEPAC. 2016. Évaluation et Rapport de situation du COSEPAC sur la coccinelle à bandes transverses (Coccinella transversoguttata) au Canada. Comité sur la situation des espèces en péril au Canada. Ottawa. xi + 64 p.

Photo: © Leagh Vermeylen
Description longue
Pituophis catenifer sayi
Reptiles
Préoccupante
Alberta, Saskatchewan
Comme les autres serpents de grande taille, cette espèce est touchée par la perte d’habitat et la mortalité routière et pourrait devenir « menacée » si les menaces ne sont pas atténuées. L’espèce dépend de gîtes d’hivernage communaux, qui semblent peu abondants dans le paysage. Bien que la gravité des menaces dans l’ensemble de l’aire de répartition de l’espèce ne soit pas entièrement comprise, l’impact de ces menaces est potentiellement significatif. L’espèce est particulièrement vulnérable à une mortalité accrue en raison de sa faible abondance, de sa maturité tardive et de son faible taux de productivité.
La couleuvre gaufre de Say (antérieurement appelée « couleuvre à nez mince des Prairies ») est l’une des trois sous-espèces de couleuvres à nez mince du Canada. Elle fait partie des plus grandes espèces de serpents du pays, avec une longueur excédant parfois 2 m; c’est pourquoi d’innombrables herpétologues s’y intéressent. Les adultes sont jaunâtres et leurs écailles dorsales et latérales comportent des taches noires, brunes ou brun rougeâtre. Les caractéristiques distinctives de l’espèce englobent une écaille étroite au bout du nez qui est soulevée par rapport aux écailles qui l’entourent, une ligne foncée qui traverse la tête à la hauteur des yeux, une bande foncée reliant l’oeil à l’arrière de la mâchoire, et une tache verticale foncée sous l’oeil. La couleuvre gaufre de Say n’est pas venimeuse.
L’aire de répartition de la couleuvre gaufre de Say en Amérique du Nord s’étend depuis l’Alberta et la Saskatchewan jusque dans le nord-est du Mexique, en passant par le centre des États-Unis. En Alberta, la couleuvre gaufre de Say est présente du nord et de l’ouest de Drumheller, le long du système de coulées de la rivière Red Deer, et elle est répartie principalement dans la région de prairie mixte des vallées du cours inférieur de la rivière Red Deer, de la rivière Saskatchewan Sud et de la rivière Milk. En Saskatchewan, l’aire de répartition de l’espèce s’étend vers l’est jusqu’à la vallée de la Big Muddy, et vers le nord, jusqu’à la rivière Saskatchewan Sud.
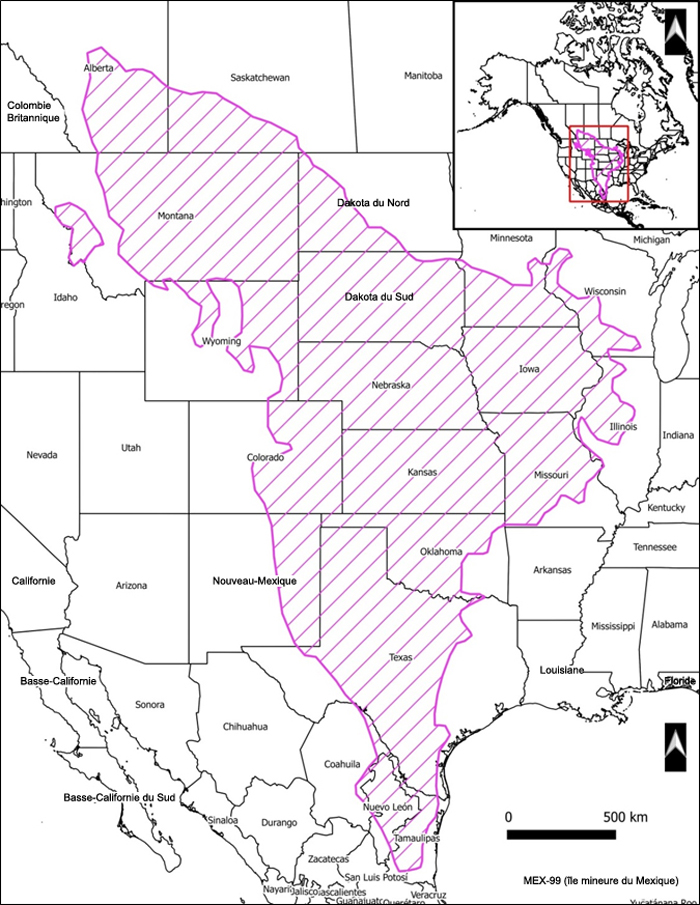
Aire de répartition nord-américaine de la couleuvre gaufre de Say. Adaptée de Conant et Collins (1998) et de Kissner et Nicholson (2003).
Au Canada, la couleuvre gaufre de Say se trouve dans les prairies à graminées courtes et mixtes, habituellement associées aux zones broussailleuses et sablonneuses et autour des badlands, le long des grandes vallées fluviales. Les serpents utilisent souvent des terriers de mammifères pour s’alimenter, se protéger des prédateurs, muer, réguler leur température et hiberner. La couleuvre gaufre de Say hiberne en groupe, souvent avec d’autres espèces de serpents, dans des terriers de mammifères, des blocs de glissement, des escarpements et des fissures de méandres, des dolines et des affleurements rocheux sur des pentes exposées au soleil. Pour la nidification, les couleuvres gaufres de Say femelles creusent un gîte ou modifient des terriers de mammifères existants dans des sols sablonneux ou friables sur des escarpements orientés vers le sud, dans les coulées et les gorges de vallées fluviales.
L’accouplement a habituellement lieu en mai, aussitôt que les individus émergent de l’hibernation. Les femelles peuvent se reproduire chaque année ou tous les deux ans, pondant en moyenne 16 oeufs en juin ou en juillet, et les oeufs éclosent entre la mi-août et la mi-septembre. L’âge de la maturité sexuelle est inconnu; toutefois, la couleuvre à nez mince du Grand Bassin, proche parente de la couleuvre gaufre de Say, ne se reproduit probablement pas avant l’âge de quatre ans. Chez la couleuvre gaufre de Say au Canada, la durée probable d’une génération est d’environ huit ans. L’espèce est active durant le jour et se nourrit principalement de petits mammifères. Elle a la capacité de grimper et peut également se nourrir d’oiseaux et d’oeufs d’oiseaux.
Les données accessibles sont insuffisantes pour décrire la taille ou les tendances des populations. Les déclins par rapport aux niveaux historiques sont inférés à partir des cas de mortalité routière et de la perte d’habitat. L’habitat dans les régions prairiaux est disparu ou s’est dégradé dans l’ensemble de l’aire de répartition de la couleuvre gaufre de Say en Alberta et en Saskatchewan. Toutefois, l’espèce semble persister dans l’ensemble de sa vaste aire de répartition canadienne.
Les menaces qui pèsent sur la couleuvre gaufre de Say englobent la mortalité routière, certains types de pratiques agricoles, le surpâturage et l’altération de l’habitat de prairie causée par le forage pétrolier et gazier. L’impact global des menaces sur la couleuvre gaufre de Say est considéré comme étant faible. Parmi les autres menaces dont l’impact global sur l’espèce est jugé négligeable, mais potentiellement important à l’échelle locale figurent : la persécution; la perturbation humaine sous forme d’activités récréatives et militaires; les modifications des systèmes naturels, comme les incendies de forêt; le développement résidentiel et commercial; la pollution, plus précisément les mesures de lutte contre les rongeurs. Les menaces potentielles ayant un impact inconnu sur la couleuvre gaufre de Say englobent les glissements de terrain et l’altération de l’habitat attribuable aux végétaux envahissants.
À l’échelle mondiale, NatureServe classe l’espèce comme étant non en péril (G5T5) et lui accorde les cotes infranationales S3 (vulnérable) en Alberta et S4 (apparemment non en péril) en Saskatchewan. En Alberta, la couleuvre gaufre de Say est désignée comme étant une espèce sensible par le ministère de l’Environnement et des Parcs de la province, et la population est décrite comme étant stable ou possiblement en déclin. La couleuvre gaufre de Say s’est vu accorder une protection générale à titre d’espèce sauvage indigène aux termes des lois sur les espèces sauvages de l’Alberta et de la Saskatchewan; les sites d’hibernation sont protégés selon les saisons aux termes du Wildlife Act provincial en Alberta. Dans les parcs nationaux et provinciaux, l’espèce et son habitat sont protégés aux termes de la Loi sur les parcs nationaux du Canada, du Provincial Parks Act (Alberta) et du Parks Act (Saskatchewan).
Source : COSEPAC. 2017. Évaluation et Rapport de situation du COSEPAC sur la Couleuvre gaufre de Say (Pituophis catenifer sayi) au Canada. Comité sur la situation des espèces en péril au Canada. Ottawa. xii + 39 p.

Photo: © Cory Sheffield
Description longue
Melanoplus madeleineae
Arthropodes
Préoccupante
Québec
Cette espèce endémique canadienne est restreinte aux îles de la Madeleine, au Québec, où elle a été observée dans sept des huit îles principales. Les menaces pesant sur l’espèce sont faibles, mais les activités récréatives, la mortalité attribuable à la circulation routière et la perte d’habitat due à une érosion côtière prévue pourrait avoir un impact sur l’espèce ou son habitat.
Le criquet des Îles-de-la-Madeleine (Melanoplus madeleineae) est une espèce de grande taille (entre 21 et 29 mm) sans caractéristique distinctive, qui est endémique aux îles de la Madeleine, archipel situé dans la province de Québec, au Canada. Le principal trait qui permet de l’identifier est son fémur postérieur, dont la surface inférieure est pourpre et la surface extérieure est uniformément noire (c.-à-d. sans bande).
Le criquet des Îles-de-la-Madeleine est un héritage de la glaciation du Wisconsin. L’espèce est peut-être dérivée du criquet boréal, une espèce étroitement apparentée, plus petite, mais morphologiquement similaire, qui est absente des îles de la Madeleine, mais qui est très répandue sur le continent.

Photo: © Cory Sheffield
Description longue
L’aire de répartition mondiale et canadienne du criquet des Îles-de-la-Madeleine est restreinte aux îles de la Madeleine, archipel situé dans le golfe du Saint-Laurent, au Québec. L’archipel des îles de la Madeleine comporte huit îles principales et plusieurs autres îles plus petites et inhabitées. Ce criquet a été observé sur sept îles principales. Six de ces îles (île du Havre Aubert, île d'Entrée, île du Cap aux Meules, Grosse Île, île du Havre aux Maisons et île de la Pointe-aux-Loups) sont reliées par des bancs de sable et des petites îles, tandis que l’île d'Entrée est séparée d’environ 4 km du groupe principal. Cette espèce n’a pas été observée à l’île Brion, qui est située à environ 13 km de la Grosse Île.
Répartition mondiale du criquet des Îles-de-la-Madeleine. La présence de l’espèce a récemment été confirmée à l’île du Havre aux Maisons et à l’île d’Entrée. Carte : GoogleEarth.
Le criquet des Îles-de-la-Madeleine est présent dans des prés maritimes dégagés et des milieux en pente abritant des communautés végétales (principalement des herbes ou du carex).
Le criquet des Îles-de-la-Madeleine hiverne à l’état d’œuf; la nymphe éclot au début du printemps. L’espèce pourrait avoir la capacité de demeurer en diapause durant deux ans, ce qui a déjà été observé chez son taxon sœur, le criquet boréal. La croissance s’effectue par métamorphose graduelle : la larve traverse cinq stades nymphaux et elle est progressivement plus grosse et présente des caractéristiques morphologiques adultes plus prononcées au fil des mues. Les nymphes et les adultes partagent les mêmes habitudes alimentaires. Les adultes sont actifs de la mi-juillet à la fin de septembre, jusqu’au moment de l’accouplement et de la ponte. Les femelles pondent leurs œufs dans un substrat de sol mou, potentiellement sur le sol nu (p. ex. sentiers, chemins de terre, etc.). Comme la plupart des représentants des Mélanoplinés, cette espèce se nourrit probablement d’un vaste éventail de plantes hôtes, bien que ses préférences alimentaires (le cas échéant) soient inconnues.
Il n’existe aucune information quant aux tendances et à la taille des sous-populations du criquet des Îles-de-la-Madeleine. Environ 80 spécimens ont été recueillis et conservés dans des musées en tant que spécimens témoins. Les relevés réalisés jusqu’à présent visaient surtout à consigner de nouvelles sous-populations, à recueillir des renseignements sur l’histoire naturelle et l’habitat et à étudier la génétique. Les relevés stratégiques de cette espèce ont surtout été réalisés à l’aide de filets fauchoirs dans des habitats convenables. Il est difficile de synchroniser les activités de collecte avec le moment culminant de l’émergence des adultes, ce qui donne à penser que le taux de détection et la perception de rareté varient considérablement.
Plusieurs menaces potentielles planent sur le criquet des Îles-de-la-Madeleine. La mortalité routière est potentiellement élevée chez les criquets, là où les routes traversent un habitat convenable ou lorsque les adultes pondent sur des routes de terre qui leur offrent un substrat mou. Les activités récréatives comme la conduite de véhicules tout terrain sur des routes qui sillonnent les prés peuvent entraîner une mortalité directe, une compaction du sol et un piétinement des plantes dont se nourrissent les criquets. L’espèce peut également être la proie d’une foule de prédateurs, de parasites et de pathogènes naturels qui régulent les populations d’orthoptères. Dans l’ensemble, l’impact des menaces est considéré comme faible.
Aucune loi fédérale ou provinciale ne protège en particulier le criquet des Îles-de-la-Madeleine, n’atténue les menaces propres aux criquets ou ne protège l’habitat de cette espèce. La cote de conservation mondiale est G2 (en péril), la cote de conservation nationale au Canada est N2 (en péril) et la cote provinciale au Québec est S2 (en péril). Environ 30 % de la superficie des îles principales des îles de la Madeleine est située sur les terres publiques. Par contre, on ignore dans quelle portion de ce territoire le criquet des Îles-de-la-Madeleine est présent.
Source : COSEPAC. 2016. Évaluation et Rapport de situation du COSEPAC sur le criquet des Îles-de-la-Madeleine (Melanoplus madeleineae) au Canada. Comité sur la situation des espèces en péril au Canada. Ottawa. xi + 49 p.

Photo: © Marc Jones
Description longue
Entosthodon rubiginosus
Mousses
Préoccupante
Colombie-Britannique, Saskatchewan
La répartition et l’abondance connues de cette mousse ont augmenté de façon significative en raison de la recherche sur le terrain et de la collecte depuis l’évaluation initiale de l’espèce par le COSEPAC en 2004, résultant ainsi à une diminution du risque d’extinction. L’espèce est maintenant observée en Colombie-Britannique et en Saskatchewan, et une quantité considérable d’habitat potentiel inexploré existe. De faibles déclins ont été observés, et des menaces potentielles, incluant la présence de bétail, les changements climatiques, la conversion de l’habitat naturel en zones agricoles, ainsi que les espèces envahissantes, ont été identifiées. L’espèce demeure en péril et pourrait devenir « menacée » à moins que les menaces soient atténuées avec une efficacité démontrée.
L’entosthodon rouilleux est une petite mousse vert pâle à vert moyen qui pousse en tiges isolées ou en petites touffes. Il mesure 2 ou 3 mm de hauteur, est difficile à apercevoir et est souvent caché parmi les autres mousses. L’entosthodon rouilleux est endémique à l’Amérique du Nord et est rare dans l’ensemble de son aire de répartition. Les occurrences canadiennes sont situées à l’extrémité nord de l’aire de répartition nord-américaine de l’espèce. Outre les occurrences canadiennes, il y a sept occurrences connues aux États-Unis (dont une historique). L’entosthodon rouilleux se distingue de l’Entosthodon fascicularis, espèce semblable, par des caractères microscopiques de la paroi de la capsule.
L’entosthodon rouilleux est endémique à l’ouest de l’Amérique du Nord et se rencontre en régions arides et semi-arides, en Colombie-Britannique, en Saskatchewan, au Montana, en Arizona, au Nouveau-Mexique, au Texas et dans l’État de Washington. Au Canada, l’entosthodon rouilleux a été trouvé dans 17 sites, soit 12 dans la région intérieure sud de la Colombie-Britannique et 5 dans le sud-ouest de la Saskatchewan.
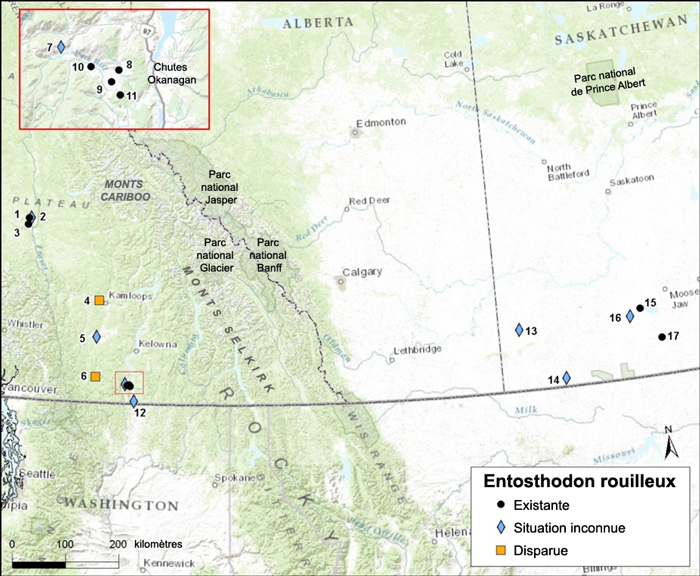
Répartition canadienne de l’entosthodon rouilleux. Sites : 1. lac Roundup; 2. lac Lost; 3. ruisseau Riske; 4. baie Cooney; 5. Quilchena; 6. Princeton; 7. lacs Twin; 8. Observatoire; 9. lac White; 10. ruisseau Park; 11. Grasslands; 12. ruisseau Strawberry; 13. ruisseau Maple; 14. Climax; 15. Courval; 16. Gravelbourg; 17. Lake of the Rivers.
Au Canada, l’entosthodon rouilleux pousse uniquement dans des sols salins et généralement limoneux ou argileux qui sont mouillés une partie de l’année et bordent les étangs, les lacs et les vasières, ou encore sur les pentes suintantes de milieux par ailleurs relativement secs. Il pousse sur le sol dénudé et tolère une certaine accumulation de litière et une certaine présence de plantes vasculaires. L’entosthodon rouilleux se rencontre le plus souvent dans une étroite bande entourant les milieux humides, en terrain plat ou en pente très douce. L’espèce n’a jamais été trouvée dans des milieux salins où dominent les grandes espèces de joncs et de cypéracées. La salinité de l’habitat est due à l’évaporation de l’eau durant les mois les plus chauds, qui laisse des minéraux dans le sol.
L’entosthodon rouilleux peut être une espèce annuelle ou une espèce vivace à courte durée de vie (~2 ans) et produit régulièrement des sporophytes. La dispersion à courte distance des spores, la persistance des spores dans le sol et la dispersion de fragments d’individus contribuent probablement toutes au maintien des sous-populations d’entosthodon rouilleux. L’entosthodon rouilleux présente des caractères physiologiques qui lui permettent de survivre dans les milieux arides et semi-arides, notamment sa capacité de demeurer en dormance durant des périodes prolongées, la marge enroulée de ses feuilles et la présence de soies à l’extrémité de celles-ci.
L’entosthodon rouilleux a été signalé dans 17 sites, soit 12 dans la région intérieure sud de la Colombie-Britannique et 5 dans le sud-ouest de la Saskatchewan. Il pourrait être disparu de deux sites en Colombie-Britannique. Les relevés continus des bryophytes ont permis une augmentation du nombre de sites connus : seulement quatre sites avaient été signalés au moment de la publication du premier rapport de situation sur l’espèce, en 2004. La plupart des sites connus renferment de petites touffes composées de moins de 10 individus, mais deux sites récemment découverts en Colombie-Britannique, au ruisseau Park, dans le bassin du lac White, et au lac Roundup, dans le secteur d’entraînement de Chilcotin, hébergent de grandes sous-populations comptant plus de 1 000 individus. D’après les nouveaux relevés, la plupart des sous-populations situées dans le bassin du lac White et dans la région de Chilcotin semblent être stables. Toutefois, plusieurs des petites sous-populations n’ont pas été retrouvées en 2015, de sorte qu’il est difficile d’estimer les tendances en matière d’abondance.
L’entosthodon rouilleux pousse uniquement dans des sols dénudés mouillés une partie de l’année et généralement associés à des lacs, à des étangs, à des vasières ou à des zones de suintement salins. Les menaces pesant sur l’espèce sont l’utilisation de l’habitat par le bétail, la modification des régimes hydrologiques associée aux changements climatiques, la conversion des milieux humides en terres agricoles, les espèces exotiques envahissantes, l’utilisation de véhicules hors route et les perturbations causées par la Bernache du Canada. L’utilisation intensive de l’habitat par le bétail, qui peut avoir des effets directs (piétinement des individus) et indirects (perturbation du sol) sur l’entosthodon rouilleux, représente une menace d’impact moyen à faible pour l’espèce. La plupart des sites connus sont accessibles au bétail, et l’utilisation de l’habitat par le bétail est plutôt intensive dans certains sites. On ignore quels sont les effets sur l’entosthodon rouilleux des modifications des régimes hydrologiques des milieux humides causés par les changements des températures et des précipitations. L’habitat de l’entosthodon rouilleux pourrait devenir plus sec et plus éphémère et être davantage exposé à des conditions météorologiques extrêmes à cause des changements climatiques. La conversion des milieux humides en terres agricoles représente une menace négligeable pour l’entosthodon rouilleux dans les sites des Prairies, mais aucun des sites connus en Saskatchewan ne semble actuellement être menacé par cette activité. Les autres menaces ont probablement un impact négligeable, ou leur impact est inconnu.
Le COSEPAC a classé l’entosthodon rouilleux espèce en voie de disparition, et l’espèce figure à ce titre à l’annexe 1 de la Loi sur les espèces en péril. NatureServe a attribué à l’entosthodon rouilleux la cote de conservation mondiale de G1G3 (gravement en péril à vulnérable; risque de disparition élevé à modéré). En Colombie-Britannique, l’espèce a été inscrite sur la liste bleue (taxon préoccupant particulièrement sensible ou vulnérable aux activités humaines ou aux phénomènes naturels) et s’est vu attribuer la cote de conservation de S2S3 (en péril à vulnérable; risque élevé à modéré de disparition) par le Conservation Data Centre de la province. L’espèce est considérée comme historique (SH, espèce pour laquelle il existe seulement des mentions datant de plus de 50 ans, mais susceptible d’être retrouvée) par le Montana Natural Heritage Program, et aucune cote ne lui a été attribuée en Arizona, au Nouveau-Mexique et dans l’État de Washington. Les occurrences qui se trouvent dans le secteur d’entraînement de Chilcotin et dans le bassin du lac White sont protégées dans une certaine mesure par les lignes directrices existantes en matière de gestion.
Source : COSEPAC. 2017. Évaluation et Rapport de situation du COSEPAC sur l’entosthodon rouilleux (Entosthodon rubiginosus) au Canada. Comité sur la situation des espèces en péril au Canada. Ottawa. xiii + 49 p.

Photo: © Annegret Nicolai
Description longue
Anguispira kochi kochi
Mollusques
En voie de disparition
Ontario
Ce grand escargot terrestre demeure dans de petites parcelles d’habitat isolées sur les îles Middle et Pelée, dans le lac Érié. La perte de sous-populations dans de plus petites îles était probablement attribuable à la destruction de l’habitat causée par la surabondance de Cormorans à aigrettes, lesquels ont colonisé les îles au début des années 1980, ainsi que par les activités anthropiques. La perte et l’altération de l’habitat sur l’île Pelée ont probablement mené à des déclins et à la fragmentation des sous-populations. Les changements climatiques constituent la menace la plus grave.
L’escargot-tigre à bandes est un grand escargot terrestre (diamètre de la coquille des adultes : 2,0 à 2,5 cm) à coquille globulaire jaune ou brune qui laisse voir une ouverture en son centre lorsqu’on l’observe du dessous et qui présente une bande spiralée claire bordée d’une bande plus foncée de chaque côté. Il peut y avoir des variations sur le plan de la taille, de l’épaisseur et de la couleur de la coquille, ainsi que de la visibilité des bandes. Deux sous-espèces sont actuellement reconnues : Anguispira kochi, sur les îles du lac Érié en Ontario, et A. k. occidentalis, en Colombie-Britannique. Les sous-espèces de l’Est et de l’Ouest font partie des espèces uniques des écosystèmes carolinien et du nord du bassin du Columbia, respectivement, et sont importantes pour la biodiversité, la recherche et la conservation. Comme membre de la communauté des gastéropodes dans les écosystèmes forestiers, l’escargot-tigre à bandes joue un rôle dans la décomposition de la litière et dans le cycle des éléments nutritifs.

Photo: © Annegret Nicolai
Description longue
L’aire de répartition de l’escargot-tigre à bandes est disjointe; elle est constituée de deux composantes nord-américaines, soit à l’est et à l’ouest, et s’étend vers le sud depuis le sud du Canada jusqu’au Tennessee dans l’est, et en Oregon dans l’ouest. Au Canada, les populations de l’Ontario et de la Colombie-Britannique sont séparées par une distance de plus de 2 000 km, sans connexion aux États-Unis. En Ontario, on sait que l’escargot-tigre à bandes de l’Est existe actuellement sur deux îles du lac Érié (îles Pelée et Middle). En Colombie-Britannique, l’escargot-tigre de l’Ouest est présent dans la partie sud-est de la province, la plupart des mentions provenant de la région de Kootenay-Ouest.
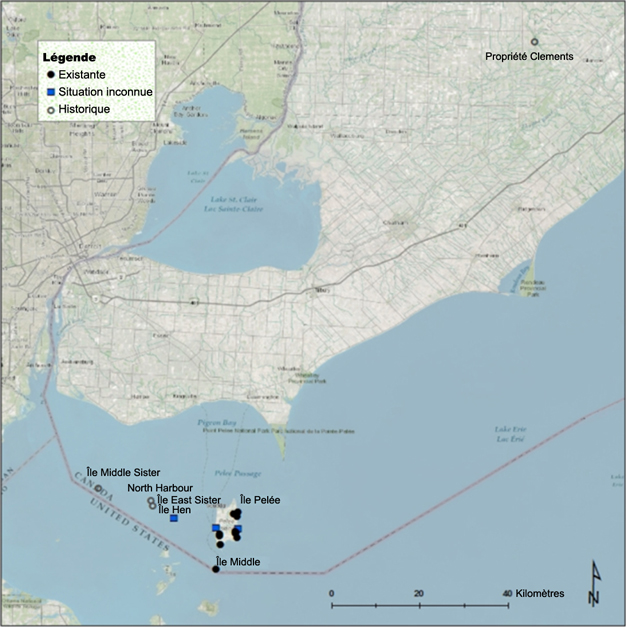
Répartition de l’escargot-tigre à bandes de l’Est en Ontario. Carte préparée par Alain Filion (Secrétariat du COSEPAC) d’après les mentions compilées aux fins du présent rapport.
En Ontario, l’escargot-tigre à bandes préfère les milieux suivants : alvar boisé à chêne jaune et ail penché, forêt décidue à micocoulier sur sol sec à frais, forêt décidue à érable à sucre et frêne blanc sur sol sec à frais et forêt clairsemée à chêne des teinturiers sur sol sec. Ces milieux, qui totalisent environ 98 ha, sont caractérisés par une forte proximité entre la terre végétale et un substrat calcaire ou par un sol sableux recouvert d’une importante couche de litière de feuilles. L’île Pelée est très utilisée pour l’agriculture; c’est pourquoi des superficies d’habitat ont été perdues par le passé. D’autres sont aujourd’hui touchées par des inondations et des mesures de gestion telles que la lutte contre les espèces envahissantes et les brûlages dirigés, ainsi que par l’érosion de la pointe Fish sur l’île Pelée. L’île Middle est inoccupée par les humains depuis les années 1980, mais l’habitat continue d’y être modifié par les tempêtes et la surabondance des Cormorans à aigrettes.
En Colombie-Britannique, l’escargot-tigre à bandes vit dans les forêts mixtes humides et denses, et on le trouve souvent dans les zones riveraines le long des lacs, des rivières et des ruisseaux, particulièrement dans les sites où l’on trouve des peupliers. Une litière de feuilles bien développée et les débris ligneux grossiers du sol forestier offrent des abris contre les prédateurs et le mauvais temps. Par le passé, la conversion des terres aux fins du développement résidentiel et commercial ainsi que pour l’agriculture a donné lieu à des pertes d’habitat dans les secteurs de faible altitude, particulièrement le long des vallées fluviales, des berges lacustres et des routes. L’habitat dans l’ensemble de l’aire de répartition de l’espèce continue d’être modifié et fragmenté par l’exploitation forestière, les réseaux routiers et l’expansion de l’aménagement urbain ainsi que par l’augmentation de la fréquence et de la durée des sécheresses qui est prévue dans le contexte des changements climatiques.
L’escargot-tigre à bandes est un escargot pulmoné (capable de respirer dans l’air), à hermaphrodisme simultané (possédant des organes reproducteurs mâle et femelle) et ovipare. On sait peu de choses au sujet du cycle vital de l’espèce au Canada. L’accouplement a probablement lieu au milieu du printemps et au milieu de l’été, et la ponte, à la fin du printemps et à la fin de l’été. L’hibernation s’effectue entre le début du mois d’octobre et le mois d’avril dans les régions tempérées. Les escargots sont vulnérables au gel en hiver et à la déshydratation en été. Ils ont besoin d’abris couverts et de couverture neigeuse pour s’isoler du gel durant l’hiver. En été, les individus peuvent entrer en dormance durant les périodes de sécheresse prolongée. La maturité sexuelle est vraisemblablement atteinte à l’âge de deux ou trois ans, et une génération dure probablement de cinq à six ans. La dispersion active, qui permet la colonisation de nouvelles zones, s’effectue sur une distance de quelques dizaines de mètres, au cours de plusieurs années. La dispersion passive, par l’inondation des cours d’eau ou le transport par les oiseaux, est possible sans toutefois avoir été documentée. Rien n’indique que l’espèce est transportée par les humains.
La présence de l’escargot-tigre à bandes de l’Est n’a pu être confirmée que sur les îles Middle et Pelée dans le cadre de travaux sur le terrain effectués entre 2013 et 2015; les perturbations historiques de l’habitat laissent croire à une réduction de l’effectif dans certains sites de ces îles. Il semble que l’espèce ait disparu de l’île Middle Sister, de l’île East Sister et d’une propriété à proximité d’Alvinston, dans le comté de Lambton, dans la partie continentale de l’Ontario. La persistance de l’espèce sur les îles Hen et North Harbour est incertaine. On estime que la population compte actuellement quelque 800 000 individus matures. Le recrutement a été observé dans la plupart des sites où l’espèce a été trouvée vivante. Une immigration de source externe n’est pas possible, en raison du lac Érié qui agit comme un obstacle.
On ne sait rien des densités et des tendances au sein de la population de l’escargot tigre à bandes de l’Ouest, mais il est probable que l’espèce ait été plus répandue et abondante par le passé qu’à l’heure actuelle, particulièrement dans les grandes vallées fluviales. La plupart des données sur la répartition sont récentes (recueillies depuis les années 1990), et les données historiques dont on dispose sont insuffisantes pour effectuer des comparaisons. Les menaces qui continuent de peser sur l’habitat proviennent de diverses sources et pourraient entraîner des baisses de la population à l’avenir. Plusieurs mentions de l’espèce ont été faites à proximité de la frontière canado-américaine et, aux endroits où l’habitat est continu, il existe une possibilité d’immigration de source externe. Cependant, en raison de la faible capacité de dispersion des escargots et de la fragmentation de leur habitat, l’immigration vers les sous-populations de la Colombie-Britannique depuis les États-Unis est limitée.
Au Canada, l’escargot-tigre à bandes se situe à la limite septentrionale de son aire de répartition. Sa faible capacité de dispersion et son faible degré de résistance physiologique face aux fluctuations de facteurs environnementaux comme la température et l’humidité sont considérés comme des facteurs limitatifs.
En Ontario, les changements climatiques représentent une menace importante, quoique mal comprise, pour les escargots en raison de l’augmentation des tempêtes sur l’île Middle et de l’érosion et des inondations des forêts sur l’île Pelée. En outre, les risques de sécheresse et de températures extrêmes, qui entraînent le gel au printemps, représentent une menace dans tous les sites. Parmi les autres menaces pesant sur l’espèce, on compte la concurrence avec les espèces introduites d’escargots et de limaces ainsi que la pression de prédation accrue découlant de l’introduction de Dindons sauvages et de Faisans de Colchide, des espèces omnivores, sur l’île Pelée. Sur l’île Middle, la nidification du Cormoran à aigrettes, une espèce indigène, a gravement modifié l’habitat par la modification des propriétés chimiques du sol, le dépérissement des arbres, la réduction de la richesse en espèces végétales et la propagation des espèces exotiques. Les plantes et les lombrics non indigènes sur l’île Pelée contribuent aussi à la modification de la structure de la couche de litière et de l’habitat. Les brûlages dirigés modifient aussi l’habitat potentiel de l’espèce.
En Colombie-Britannique, les menaces qui pèsent sur l’espèce comprennent la perte, l’altération et la fragmentation de l’habitat découlant de l’exploitation forestière, des routes, de l’aménagement urbain et des feux de friches ainsi que de la fréquence et de l’intensité accrues des sécheresses, des tempêtes et des inondations, comme prévu dans le contexte des changements climatiques. Les sécheresses estivales prolongées qui sont associées aux changements climatiques exacerberont vraisemblablement les effets de l’exploitation forestière et des feux de friches. Les changements climatiques et les perturbations des forêts pourraient en outre faciliter la propagation d’invertébrés introduits comme des limaces, des escargots et des carabes, qui peuvent entrer en concurrence avec les escargots-tigres ou s’en alimenter.
Aucune désignation juridique n’est attribuée à l’escargot-tigre à bandes. L’espèce est classée comme étant non en péril à l’échelle mondiale et non en péril à l’échelle nationale aux États-Unis, mais elle est classée comme étant vulnérable au Canada. Elle est classée comme étant en péril en Ontario et vulnérable en Colombie-Britannique. En Ontario, la majeure partie de l’aire de répartition de l’espèce est située sur des terres protégées gérées par Parcs Canada, Conservation de la nature Canada ou le ministère des Richesses naturelles et de la Foresterie de l’Ontario. En Colombie-Britannique, le régime foncier varie dans l’ensemble de l’aire de répartition de l’espèce, mais la plupart des mentions proviennent de terres provinciales non protégées et visées par l’exploitation forestière. En Colombie-Britannique, des mentions de l’espèce ont été faites dans cinq parcs provinciaux; plusieurs autres parcs provinciaux et aires protégées existent dans son aire de répartition.
Source : COSEPAC. 2017. Évaluation et Rapport de situation du COSEPAC sur l’escargot-tigre à bandes de l'Est (Anguispira kochi kochi) et l’escargot-tigre à bandes de l'Ouest (Anguispira kochi occidentalis), au Canada. Comité sur la situation des espèces en péril au Canada. Ottawa. xvi + 92 p.

Photo: © Carl Savignac
Description longue
Coccothraustes vespertinus
Oiseaux
Préoccupante
Yukon, Territoires-du-Nord-Ouest, Colombie-Britannique, Alberta, Saskatchewan, Manitoba, Ontario, Québec, Nouveau-Brunswick, Île-du-Prince-Édouard, Nouvelle-Écosse, Terre-Neuve-et-Labrador
Ce grand passereau est largement répandu dans les forêts du Canada, mais il présente des déclins à long terme significatifs (de 77 à 90 %) depuis 1970 dans la majeure partie de son aire de répartition. Au cours des dernières décennies, certaines données indiquent un nouveau déclin de près de 40 %, alors que d’autres données indiquent une stabilisation à un niveau inférieur. Les menaces qui pèsent sur l’espèce incluent une disponibilité réduite des forêts mixtes et conifériennes matures et anciennes, les collisions avec les fenêtres, et la mortalité liée à la consommation de gravier et de sel le long des routes en hiver.
Le Gros-bec errant est un oiseau chanteur trapu et coloré; son bec est fort et jaune verdâtre. Chez les mâles adultes, la tête est brun foncé avec un sourcil jaune vif; le brun de la tête se fond dans la couleur jaune des parties supérieures et du ventre, ce qui contraste avec la queue et les ailes noires et avec les secondaires qui sont blanches. Les femelles adultes et les juvéniles sont généralement de couleur brun grisâtre; les flancs et la nuque sont jaunâtres; les ailes et la queue sont blanches et noires. Durant l’été, l’espèce peut constituer l’un des principaux prédateurs de la tordeuse des bourgeons de l’épinette et contribuer à la lutte naturelle contre l’insecte ravageur. En hiver, le Gros-bec errant est un visiteur fréquent des mangeoires d’oiseaux.
Le Gros-bec errant niche au Canada, aux États-Unis et au Mexique. Au Canada, son aire de répartition englobe l’ensemble des provinces et des territoires, à l’exception du Nunavut. Aux États-Unis, l’espèce niche principalement dans le nord de la Nouvelle-Angleterre et dans certains États de l’ouest du pays. Durant l’hiver, le Gros-bec errant est nomade et peut se déplacer considérablement, selon la quantité de graines produites dans la forêt boréale. Par le passé, l’espèce était limitée à l’ouest de l’Amérique du Nord, mais elle a pris de l’expansion vers l’est à la fin du 19e siècle et au début du 20e siècle.
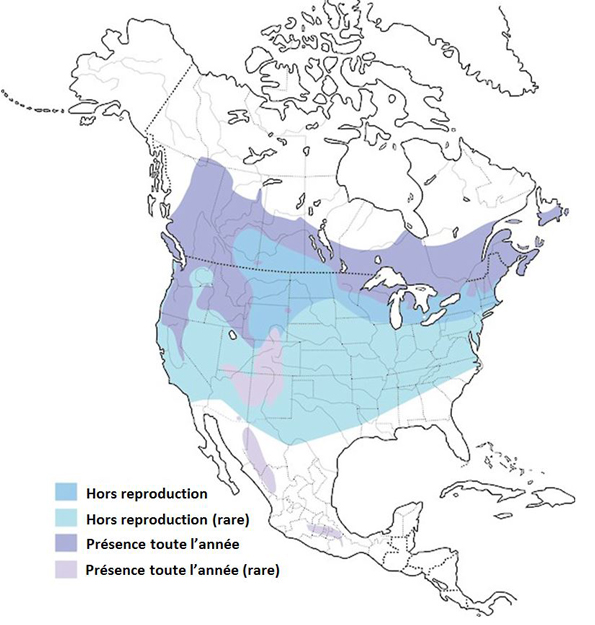
Répartition du Gros-bec errant en Amérique du Nord. Les aires de présence hors reproduction et de présence toute l’année sont représentées.
Source : Carte fournie par Birds of America online (Birds of North America), Cornell Lab of Ornithology.
L’habitat de nidification optimal du Gros-bec errant comprend généralement des forêts mixtes matures et ouvertes, dans lesquelles des espèces de sapins ou l’épinette blanche sont dominantes et où il y a abondance de tordeuses des bourgeons de l’épinette. En dehors de la période de nidification, l’espèce semble dépendre en grande partie des graines produites par divers arbres, comme les sapins et les épinettes dans la forêt boréale, et elle est attirée aussi par les arbres ornementaux qui produisent des graines ou des fruits et par les mangeoires d’oiseaux qui contiennent des graines de tournesol.
Le Gros-bec errant est une espèce monogame, qui est non territoriale durant la période de nidification. Les couples arrivent habituellement dans les lieux de nidification entre la mi-mai et la fin de mai, et la période de nidification peut s’étendre jusqu’au début de septembre. Le nid est une coupe faite de brindilles ou de radicelles et il est souvent installé de préférence à la cime d’un conifère. Le Gros-bec errant produit une nichée par année, contenant en moyenne 3 ou 4 œufs; il peut y avoir une seconde nichée après la perte d’un nid. La durée de l’incubation est habituellement de 12 à 14 jours, et les jeunes quittent le nid à l’âge de 13 ou 14 jours. L’âge à la première reproduction est de un an.
La population de Gros-becs errants au Canada est estimée à environ 2 200 000 individus matures. Bien qu’il soit difficile de déterminer les tendances des espèces nomades, les données du Recensement des oiseaux de Noël (RON) et du Relevé des oiseaux nicheurs (BBS, pour Breeding Bird Survey) indiquent des baisses de populations semblables à long terme. Les données du RON, dont les sites d’échantillonnage se trouvent dans l’ensemble de l’aire d’hivernage de l’espèce, montrent que les effectifs ont connu une baisse annuelle générale significative de 3,4 % de 1970 à 2012, ce qui correspond à une baisse cumulative de 76,6 %; cependant, une augmentation non significative des effectifs de 3,1 % par année a été décelée de 2002 à 2012. Les relevés du BBS, qui concernent principalement le sud de l’aire de nidification du Gros-bec errant, indiquent une baisse annuelle significative de 5,2 % entre 1970 et 2014, ce qui représente une baisse des effectifs de 90 % sur 44 ans. Les données du BBS relatives à la plus récente période de 10 ans (de 2004 à 2014) indiquent une baisse annuelle continue significative de 5,0 % au Canada, ce qui correspond à une baisse cumulative des effectifs de 42 %. Les tendances à court terme (2004-2014) du BBS sont aussi négatives dans l’ensemble des provinces, mais elles sont significatives seulement au Manitoba, en Ontario et au Québec. Les atlas des oiseaux nicheurs des provinces, l’Étude des populations d’oiseaux du Québec (ÉPOQ) et le projet FeederWatch montrent aussi des tendances générales à la baisse. Selon les données de l’Observatoire d’oiseaux de Tadoussac (Québec), les effectifs du Gros-bec errant ont été faibles de 1998 à 2011, puis ont augmenté considérablement de 2012 à 2015. Les résultats du projet de surveillance des oiseaux chanteurs de Fort Liard, mené dans le sud des Territoires du Nord-Ouest, indiquent une tendance à la stabilité de 1998 à 2011. Dans l’ensemble, les tendances à long terme sont très négatives selon de nombreuses sources de données; les tendances à court terme sont plus variables, certaines indiquant des baisses continues des effectifs, d’autres indiquant une stabilité ou une augmentation des effectifs dans certaines régions.
Les variations des populations de tordeuses des bourgeons de l’épinette, qui se produisent de manière naturelle à tous les 25 à 40 ans dans l’est du Canada et à tous les 26 ans dans l’ouest du pays, constituent probablement l’un des principaux facteurs ayant influé sur les variations des populations de Gros-becs errants depuis 1970. Les menaces pesant sur le Gros-bec errant sont notamment la mortalité associée aux collisions avec des fenêtres lorsque les individus viennent s’alimenter aux mangeoires durant l’hiver, la réduction de la superficie des forêts mixtes matures et anciennes qui résulte de l’exploitation forestière commerciale et la mortalité routière lorsque les individus se nourrissent de sels de voirie et de gravier sur les routes. La mortalité causée par l’ingestion de chlorure de sodium au bord des routes peut aussi constituer une menace pour l’espèce. À long terme, il pourrait y avoir contraction de l’habitat de nidification en raison des changements climatiques.
Au Canada, le Gros-bec errant, ses nids et ses œufs sont protégés en vertu de la Loi de 1994 sur la Convention concernant les oiseaux migrateurs. Selon NatureServe, l’espèce est non en péril au Canada, en péril à l’Île-du-Prince-Édouard et vulnérable au Yukon, au Manitoba et au Nouveau-Brunswick; dans les autres provinces et territoires, elle est considérée comme non en péril ou probablement non en péril.
Source : COSEPAC. 2016. Évaluation et Rapport de situation du COSEPAC sur le Gros-bec errant (Coccothraustes vespertinus) au Canada. Comité sur la situation des espèces en péril au Canada. Ottawa. x + 77 p.

Photo : © Tom Murray
Description longue
Polites sonora
Arthropodes
Non en péril
Colombie-Britannique
Ce papillon a une petite aire de répartition dans la partie méridionale de l’intérieur de la Colombie–Britannique. Depuis sa dernière évaluation, de nouvelles données ont été recueillies sur sa répartition, son habitat, ses plantes hôtes, son histoire naturelle et les menaces qui pèsent sur lui. L’espèce est maintenant connue dans un plus grand nombre de sites naturels et perturbés, incluant les prés, les bordures des routes et les zones de coupe à blanc où se trouvent généralement des suintements ou une forme d’eau stagnante. Elle a aussi de plus larges préférences en matière de plante hôte qu’on ne le croyait antérieurement ainsi qu’une certaine capacité à utiliser des espèces non indigènes pour compléter son cycle de vie. Les menaces demeurent faibles, et certains impacts potentiels tels que les coupes à blanc peuvent mener à la création d’habitat et à des corridors de dispersion pour ce papillon.
L’hespérie du Sonora (Polites sonora) appartient à la famille des Hespériidés (hespéries). Les adultes ont une envergure de 25 à 30 mm. Le dessus des ailes est orange rouille et brun avec les bordures noirâtres. Le dessous des ailes antérieures porte une tache basale noire, quelques zones fauves et pâles dans la portion médiane de l’aile et a une bordure brun foncé. Le dessous des ailes postérieures est brun ocre avec une bande semi-circulaire distincte composée de points pâles. L’hespérie du Sonora comprend au moins huit sous-espèces dans son aire de répartition. La population canadienne pourrait faire partie d’une neuvième sous-espèce qui n’est pas encore décrite, bien que le travail taxinomique ne soit pas terminé. Peu importe sa classification taxinomique, une seule sous-espèce existe au Canada, mais c’est l’espèce entière qui est le sujet du présent rapport de situation.
À titre d’espèce, l’hespérie du Sonora est largement répartie dans l’ouest de l’Amérique du Nord, depuis le sud de la Colombie-Britannique jusqu’en Basse-Californie vers le sud, et jusqu’au Wyoming et au Colorado (États-Unis) vers l’est. Au Canada, son aire de répartition a une étendue limitée; on peut la rencontrer dans le nord de la chaîne des Cascades et dans le plateau Thompson qui lui est adjacent, dans le sud de la Colombie-Britannique dans une zone adjacente à la frontière canado-états-unienne. On connaît 12 sous-populations existantes de l’hespérie du Sonora au Canada, certaines d’entre elles comprenant plusieurs sites.
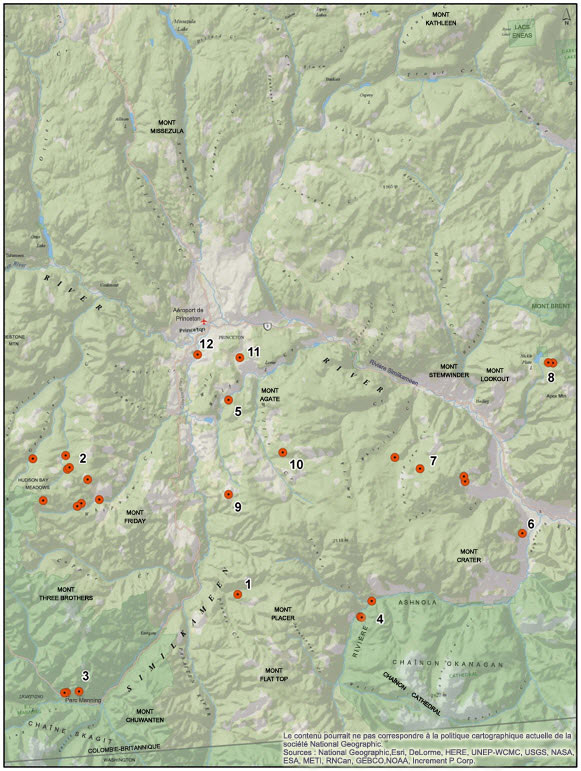
Répartition de l’hespérie du Sonora en Colombie-Britannique. Sous-populations : 1. Ruisseau Placer; 2. Ruisseau Corral (ruisseau Whipsaw); 3. Lac Twenty Minute, parc provincial E.C. Manning; 4. 2,6 km au nord du ruisseau McBride; 5. Ruisseau Verde (ruisseau Wolfe); 6. Lac Red Bridge (mont Crater); 7. Au nord du ruisseau Paul; 8. Mont Apex; 9. 1,8 km à l’est du Ruisseau Sunday; 10. Au sud-ouest des collines Wilbert; 11. Au sud du lac August; 12. Au nord-ouest d’Allenby.
L’hespérie du Sonora vit dans les clairières humides et herbeuses mésiques et les prés fleuris, les versants en pente douce, les zones dégagées en bordure des routes, les berges dégagées, les prés agricoles en jachère et les clairières herbeuses exposées au sud, dont certaines sont bordées de forêts, de zones de coupe à blanc ou d’une végétation plus dense. L’hespérie du Sonora a été observée dans des milieux anthropiques semi-naturels, comme les prairies de fauche et les anciennes zones de coupe qui sont devenues des prés. Les sites de l’espèce se trouvent généralement sur un terrain plat ou en pente douce, présentant des suintements et des eaux stagnantes (des mares, des bassins, des suintements où l’eau coule goutte à goutte).
Le cycle vital de l’hespérie du Sonora comporte quatre grandes étapes. L’espèce est univoltine (une génération par année), et la longévité des adultes varie de sept à dix jours. En Colombie-Britannique, des adultes ont été observés de la fin juin à la mi-août. Les femelles pondent leurs œufs pendant qu’elles volent près du sol à proximité immédiate de plantes hôtes. On n’a pas confirmé quelles sont les plantes hôtes des chenilles en Colombie-Britannique. Des femelles ont toutefois été observées alors qu’elles laissaient choir des œufs sur des agrostides blanches et des fléoles des prés, deux espèces non indigènes, dans un site en Colombie-Britannique. Ailleurs dans l’aire de répartition mondiale de l’hespérie du Sonora, des chenilles ont été élevées avec succès sur la sétaire glauque (non indigène), la fétuque d’Idaho (indigène), la fléole des prés (non indigène) et le pâturin des prés (indigène). Les œufs éclosent dans les 7 à 8 jours suivant la ponte. Les chenilles tissent des fourreaux de soie dans lesquels elles s’abritent, émergeant pour s’alimenter sur les plantes hôtes. Un nouveau fourreau est tissé à chaque stade. Les chenilles hibernent au quatrième stade, interrompent leur diapause au printemps (avril/mai) et continuent à se nourrir durant environ un mois avant d’atteindre la nymphose (cinquième stade).
À ce jour, les relevés de l’hespérie du Sonora se sont concentrés sur l’observation de nouvelles populations et la collecte de données sur l’histoire naturelle et l’habitat, et les données permettant d’estimer l’abondance, la taille ou les tendances des populations dans les sites existants de l’espèce sont peu nombreuses. La plupart des observations portent sur un ou deux individus. L’observation portant sur le plus grand nombre d’hespéries du Sonora a été enregistrée en 2014 dans un site le long du chemin de service forestier (CSF) Granite (Granite Forest Service Road) (n° 2, ruisseau Corral); 25 individus y ont été observés le 24 juillet 2014. Les fluctuations naturelles des populations de papillons résultent de facteurs comme les parasites, les prédateurs et les conditions météorologiques de l’année précédente. L’hespérie du Sonora ne subit probablement pas de fluctuations extrêmes, mais les données sont insuffisantes pour estimer les fluctuations ou les tendances des populations de l’espèce au Canada ou ailleurs dans son aire de répartition. De nombreux sites ont été visités sur plusieurs années pour confirmer la présence de l’espèce et enregistrer le nombre d’individus. Cependant, ces sites n’ont été visités qu’une ou deux fois au cours d’une saison de travail sur le terrain.
Les menaces pesant sur les sous-populations de l’hespérie du Sonora sont considérées comme faibles et propres aux sites, et il n’y a aucune menace immédiate à l’échelle de l’aire de répartition de l’espèce. Parmi ces menaces faibles, on compte plus précisément la perte d’habitat causée par l’aménagement de pistes de ski récréatives; l’époque de la fenaison, effectuée une ou deux fois par année et qui peut tuer à la fois les œufs et les chenilles; et les régimes de pâturage du bétail inadéquats.
La majeure partie de l’aire de répartition de l’hespérie du Sonora (excluant les parcs provinciaux) se trouve dans des zones d’approvisionnement forestier actives. La coupe à blanc pourrait créer un habitat temporaire (< 10 ans) pour l’espèce, pourvu que des plantes hôtes appropriées soient présentes et que le taux d’humidité soit convenable. L’habitat ainsi créé pourrait constituer des corridors vers d’autres habitats convenables ou des sous-populations isolées. Dans certains sites existants, la coupe a ouvert la forêt, qui ne s’est pas régénérée, et ces sites sont restés sous forme de prés humides, où des sous-populations de l’hespérie du Sonora sont toujours présentes.
Les sous-populations de l’hespérie du Sonora sont protégées dans le parc provincial E.C. Manning en vertu du Park Act de la Colombie-Britannique. L’hespérie du Sonora est inscrite comme espèce désignée (Identified Wildlife) dans le Forest and Range Practices Act de la Colombie-Britannique, de sorte qu’elle est protégée des menaces que représentent l’exploitation forestière et le pâturage, grâce à l’établissement d’aires d’habitat faunique (Wildlife Habitat Areas). L’espèce figure sur la liste des espèces préoccupantes de la Loi sur les espèces en péril (LEP) du gouvernement fédéral.
Source : COSEPAC. 2016. Évaluation et Rapport de situation du COSEPAC sur l’hespérie du Sonora (Polites sonora) au Canada. Comité sur la situation des espèces en péril au Canada. Ottawa. xii + 40 p.

Photo: © Figment Films; photo: John Mitchell
Description longue
Danaus plexippus
Arthropodes
En voie de disparition
Territoires-du-Nord-Ouest, Colombie-Britannique, Alberta, Saskatchewan, Manitoba, Ontario, Québec, Nouveau-Brunswick, Île-du-Prince-Édouard, Nouvelle-Écosse, Terre-Neuve-et-Labrador
Cette grande espèce remarquable est un des papillons les plus connus dans le monde. La population canadienne est migratrice et elle emprunte deux voies distinctes. Des menaces cumulatives pèsent sur les sites d’hivernage et le long des voies de migration. Le groupe migrateur à l’ouest des montagnes Rocheuses se déplace entre la côte de la Californie et le sud de la Colombie-Britannique. Le groupe à l’est des montagnes Rocheuses représente la vaste majorité de la population canadienne et se déplace entre la forêt de sapin oyamel du centre du Mexique et le sud du Canada à l’est de l’Alberta. Les sites d’hivernage dans le centre du Mexique sont extrêmement petits, et les menaces qui pèsent sur ces aires incluent l’exploitation forestière illégale et le développement agricole, ainsi qu’une augmentation de la fréquence et de la gravité des tempêtes pendant les périodes clés de rassemblement. Des déclins de plus de 50 % se sont produits au cours de la dernière décennie.
Le monarque est une espèce emblématique de la conservation et compte parmi les espèces de papillons les plus connues et les plus étudiées dans le monde. Le cycle vital du monarque comprend quatre stades. Le monarque adulte est un superbe et grand papillon (envergure de 93 à 105 mm) dont les ailes sont principalement orange et comportent une large bordure noire piquée de deux rangées de points circulaires blancs. La chenille, facilement reconnaissable, est annelée de blanc, de jaune et de noir et porte deux paires de filaments noirs, une au niveau de la tête et l’autre à l’extrémité de l’abdomen. La chrysalide est verte et dorée. L’œuf du monarque mesure environ 1 mm de longueur et est légèrement ovale, avec la base aplatie et le sommet formant une pointe arrondie.
Le monarque est l’une des rares espèces de papillons qui migrent, et sa migration depuis le sud du Canada jusqu’au Mexique est considérée comme un phénomène biologique en péril. Partout en Amérique du Nord, le monarque est utilisé dans les écoles pour enseigner aux enfants la biologie, la métamorphose et la conservation et leur faire apprécier la nature.
Le monarque est une espèce migratrice. L’aire de répartition indigène globale du monarque s’étend depuis l’Amérique centrale jusqu’au Canada, en passant par la partie continentale des États-Unis, et de la côte de l’Atlantique jusqu’à la côte du Pacifique. Au Canada, l’espèce se rencontre dans certaines portions des dix provinces et des Territoires du Nord-Ouest. L’espèce peut être divisée en deux sous-groupes, la population de l’est et la population de l’ouest, en fonction des voies migratoires et des sites d’hivernage des individus. L’aire de reproduction de la population de l’est s’étend depuis l’Alberta jusqu’à la Nouvelle-Écosse, et les individus de cette population migrent vers le sud pour aller hiverner dans les montagnes du centre du Mexique. Les individus de la population de l’ouest se reproduisent dans le sud de la Colombie-Britannique et migrent vers le sud jusqu’à leur aire d’hivernage, située sud les côtes de la Californie. L’aire de reproduction de l’espèce au Canada se situe au sud du 50e parallèle en Ontario, au Québec et dans les Maritimes et au sud du 54e parallèle au Manitoba, en Saskatchewan et en Alberta.
Le monarque est considéré comme formant une seule unité désignable au Canada aux fins de la présente évaluation. Des échanges d’individus ont été observés entre les populations de l’est et de l’ouest durant la migration, et aucune observation génétique ou morphologique n’indique qu’il pourrait y avoir deux sous-espèces.
Le monarque a colonisé l’Europe continentale, l’Afrique du Nord, l’Australie et de nombreuses îles du Pacifique au cours des 200 dernières années, mais les populations ainsi établies ne migrent pas.
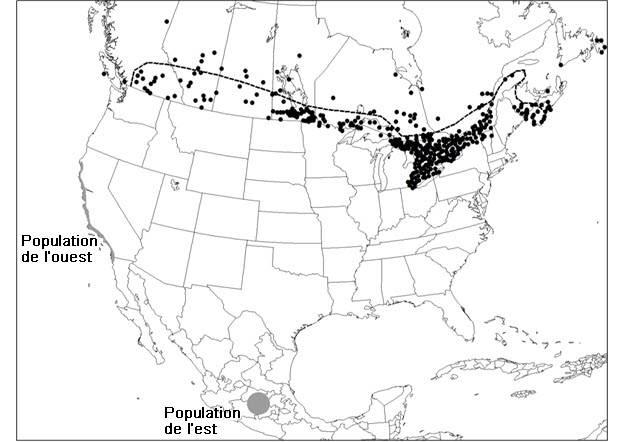
Aire de répartition canadienne du monarque (Danaus plexippus). La ligne tiretée représente la limite nord approximative des plantes hôtes de la chenille de l’espèce, soit l’asclépiade incarnate, l’asclépiade commune et la belle asclépiade. Les points situés au nord de cette ligne et dans la région côtière de la Colombie-Britannique représentent des individus errants non reproducteurs et les occurrences observées dans les parcelles isolées où des asclépiades ont été plantées à l’extérieur de leur aire de répartition indigène. Les zones d’hivernage des populations de l’est et de l’ouest sont indiquées en gris.
Les asclépiades (nombreuses espèces) sont les seules plantes dont se nourrit la chenille du monarque. Ces plantes poussent principalement dans les milieux dégagés et subissant périodiquement des perturbations, comme les bords de route, les champs, les milieux humides, les prairies et les forêts claires. Les asclépiades sont souvent plantées à l’extérieur de leur aire de répartition indigène, et des monarques errants sont parfois observés dans ces parcelles.
Pour l’hivernage, le monarque a besoin d’un microclimat frais et humide et d’être protégé du gel, d’une exposition excessive au soleil, du vent et des précipitations fortes. Il trouve ces conditions en Californie, dans la région de la côte du Pacifique, et dans le centre du Mexique, dans les forêts de haute altitude. Les individus de la population de l’est hivernent à des altitudes de 2 900 à 3 300 m, dans les forêts de sapin oyamel du Mexique. Ceux de la population de l’ouest hivernent à quelques kilomètres de la côte du Pacifique, en Californie, principalement dans des peuplements d’eucalyptus, arbres exotiques qui ont été plantés à partir des années 1850 pour remplacer les essences indigènes, dont les pins.
Le monarque a besoin d’aires de rassemblement où les individus peuvent se reposer, s’alimenter et s’abriter des intempéries durant la migration. Au Canada, on trouve ce type d’aires le long des rives nord des Grands Lacs, où les monarques se reposent sur les arbres avant de traverser ces vastes étendues d’eau libre.
Les adultes se reproduisent durant l’hiver et au début du printemps dans les sites d’hivernage du Mexique ou de la Californie, puis entreprennent leur migration vers le nord à la fin février ou au début mars. Environ 10 % des individus de la population de l’est font le voyage en entier jusqu’au Canada, mais la plupart des femelles qui quittent les sites d’hivernage se reproduisent dans le sud des États-Unis. La femelle du monarque pond 300 à 400 œufs, chaque œuf étant déposé individuellement sur la face inférieure des feuilles d’asclépiade. L’éclosion survient trois à huit jours après la ponte, puis la chenille se nourrit des feuilles d’asclépiade de façon presque continue, multipliant son poids corporel par 2 000. Après s’être alimentée durant 9 à 14 jours, la chenille se transforme en chrysalide, et l’adulte émerge 9 à 15 jours plus tard. Les adultes de la génération suivante poursuivent la migration vers le nord, et plusieurs d’entre eux se reproduisent dans le centre des États-Unis, donnant naissance à une nouvelle génération. La plupart des individus qui atteignent le Canada sont en fait les arrière-petits-enfants de ceux qui ont quitté le Mexique. Dans le sud de l’Ontario et du Québec, l’espèce produit chaque année deux ou trois générations, de juin à octobre. Dans le sud de la Colombie-Britannique, l’espèce produit au moins une génération chaque été. Les adultes estivaux ont une durée de vie de deux à cinq semaines, mais les adultes hivernants peuvent vivre jusqu’à neuf mois. Les adultes qui émergent à la fin de l’été migrent vers le Mexique ou la Californie, où ils hivernent avant d’entreprendre une nouvelle migration en sens inverse.
La chenille du monarque stocke les composés chimiques présents chez les asclépiades, ce qui rend l’espèce, également au stade adulte, non comestible pour la plupart des oiseaux et des autres vertébrés.
On ne dispose d’aucune estimation de la taille de la population de monarque au Canada. Chaque automne, des centaines de milliers de monarques migrent à partir de la région de Long Point, dans le sud de l’Ontario, mais on ignore quelle proportion de la population canadienne ces individus représentent. Une estimation de la population a été faite dans les sites d’hivernage, où se rassemblent les individus provenant du Canada et des États-Unis. L’effectif total de la population hivernant au Mexique (population de l’est) a été évalué à 66 millions d’individus en 2014-2015, et à 200 millions d’individus en 2015-2016. Une tempête survenue en mars 2016 a tué un grand nombre d’individus dans les sites d’hivernage de la population de l’est, mais on ignore l’ampleur exacte des pertes. Moins de 500 000 individus hivernent actuellement en Californie (population de l’ouest), et seulement un très faible pourcentage de ceux-ci se reproduisent au Canada. Certaines années, la population reproductrice de l’ouest (Colombie-Britannique) est si petite qu’elle n’est pas détectée.
La population hivernante du Mexique, dont la taille est mesurée d’après la superficie d’habitat occupée (hectares), a considérablement diminué au cours de la période de 1994 à 2015. Selon une régression linéaire logarithmique de cette série chronologique, la population a subi un déclin de 83 %. Les estimations pour la période 2012-2014 ont été les plus basses de cette série. La superficie d’habitat occupée en 2015 (4 ha) a été plus élevée que celle enregistrée les trois années précédentes, mais tout de même inférieure à la moyenne pour la série chronologique, qui est de 6 ha. Le taux de déclin de l’habitat occupé au cours d’une période de 10 ans a été calculé au moyen la pente de la régression linéaire logarithmique établie d’après la série chronologique entière, appliquée à une période de 10 ans. Le changement a ainsi été évalué à - 59 % sur une période de 10 ans.
Une étude à long terme sur la migration a été réalisée dans la région de Long Point, en Ontario; selon les données ajustées en fonction des conditions météorologiques, la population a connu un faible déclin. Toutefois, aucun signe de déclin n’a été observé dans le cadre d’études semblables menées à Cape May (New Jersey) et à Peninsula Point (Michigan).
Durant l’hiver, la majeure partie des monarques d’Amérique du Nord se concentrent sur seulement quelques hectares et sont donc vulnérables aux phénomènes météorologiques extrêmes, aux incendies, aux maladies, à la prédation et aux menaces anthropiques. L’habitat d’hivernage situé dans les forêts de sapin oyamel du Mexique a été fragmenté et dégradé par l’aménagement de terres agricoles, les incendies, l’exploitation forestière et les coupes d’éclaircie. Ces pratiques augmentent le risque d’exposition des individus hivernants aux tempêtes hivernales ainsi qu’aux conditions froides et humides, ce qui entraîne une hausse du taux de mortalité. Selon les modèles de changements climatiques, dans l’aire d’hivernage du Mexique, il y aura une diminution de la superficie de forêts convenant à l’espèce et une augmentation de la fréquence des tempêtes hivernales, ce qui entraînera une mortalité catastrophique. Dans le cas de la population de l’ouest, la dégradation de l’habitat d’hivernage résulte principalement du développement immobilier qui se poursuit le long de la côte de la Californie et de l’élimination des eucalyptus introduits sur lesquels les monarques se rassemblent pour hiverner.
L’utilisation accrue d’herbicides et les déclins connexes des asclépiades représentent une menace considérable pour le monarque dans l’ensemble de son aire de répartition nord-américaine. L’utilisation accrue d’herbicides peut également causer un déclin des plantes nectarifères dont les individus migrateurs ont besoin et ainsi réduire les taux de survie hivernale. Les pesticides de la catégorie des néonicotinoïdes sont une menace nouvelle, mais l’ampleur de leur impact est mal comprise.
Le monarque a été désigné espèce préoccupante par le COSEPAC en 1997. Son statut a été réexaminé et confirmé en 2001 et en 2010, et l’espèce a été désignée espèce en voie de disparition en 2016. Le monarque est considéré comme une espèce préoccupante aux termes la Loi de sur les espèces en voie de disparition de l’Ontario et de la Loi sur les espèces en péril du Nouveau-Brunswick. Il est « sous protection particulière » au Mexique, et il fait actuellement l’objet d’une évaluation en vue de son inscription à l’Endangered Species Act aux États-Unis. Les populations reproductrices du monarque sont classées apparemment non en péril (G4) à l’échelle mondiale et non en péril au Canada et aux États-Unis. Les zones de concentration d’individus migrateurs sont classées comme vulnérables à en péril aux États-Unis.
Source : COSEPAC. 2016. Évaluation et Rapport de situation du COSEPAC sur le monarque (Danaus plexippus) au Canada. Comité sur la situation des espèces en péril au Canada. Ottawa. xiv + 65 p.

Photo: © David Fraser
Description longue
Ardenna creatopus
Oiseaux
En voie de disparition
Colombie-Britannique, Océan Pacifique
Cet oiseau de mer longévif ne se reproduit que sur trois îles au large des côtes du Chili, où ses effectifs ont connu des déclins significatifs par suite de la prédation des nids par des prédateurs introduits, de l’exploitation par l’homme et de la dégradation de l’habitat. L’espèce connaît une mortalité par prise accessoire dans les pêches effectuées au sein de son aire de répartition, incluant d’importantes aires d’alimentation au large de la Colombie–Britannique. Le risque de prises accessoires dans les pêches a augmenté au cours des trois dernières générations. L’espèce est également vulnérable aux déversements d’hydrocarbures en mer.
Le Puffin à pieds roses est un oiseau de mer trapu de la taille d’un goéland moyen environ. En vol, il paraît lourd, et il alterne battements d’ailes laborieux et vol plané. Il se distingue des autres puffins présents dans le Pacifique Nord par la combinaison des caractéristiques suivantes : parties supérieures brun grisâtre, parties inférieures gris pâle et variablement tachetées, avec couvertures sous-alaires blanches, et tête sombre. Le plumage est semblable chez l’adulte et le juvénile et ne présente pas de variations saisonnières, et le mâle est en moyenne plus gros que la femelle. Le bec rosâtre teinté de jaune à bout foncé et les pattes et pieds roses sont distinctifs. Le Puffin à pieds roses, espèce menacée à l’échelle mondiale, ne compte que trois sites de reproduction connus dans le monde.

Photo: © Ben Lascelles
Description longue
Le Puffin à pieds roses est connu pour se reproduire dans trois îles situées au large de la côte chilienne, soit les îles Mocha, Robinson Crusoe et Santa Clara. En mer, l’espèce occupe principalement les eaux du talus continental, du rebord externe de la plate-forme continentale et de cette dernière dans l’est du Pacifique. Son aire de répartition s’étend depuis les îles où elle se reproduit vers le nord le long de la côte de l’Amérique du Sud et de l’Amérique du Nord jusque dans le golfe d’Alaska et le sud de la mer de Béring, mais on n’observe qu’un faible nombre d’individus au nord de Haida Gwaii. Au Canada, le Puffin à pieds roses n’est présent qu’au large de la côte de la Colombie-Britannique, les observations étant concentrées au large de la côte ouest de l’île de Vancouver, à l’entrée du détroit de Juan de Fuca et dans le bassin de la Reine-Charlotte. L’espèce est le plus nombreuse au pays de juin à octobre.
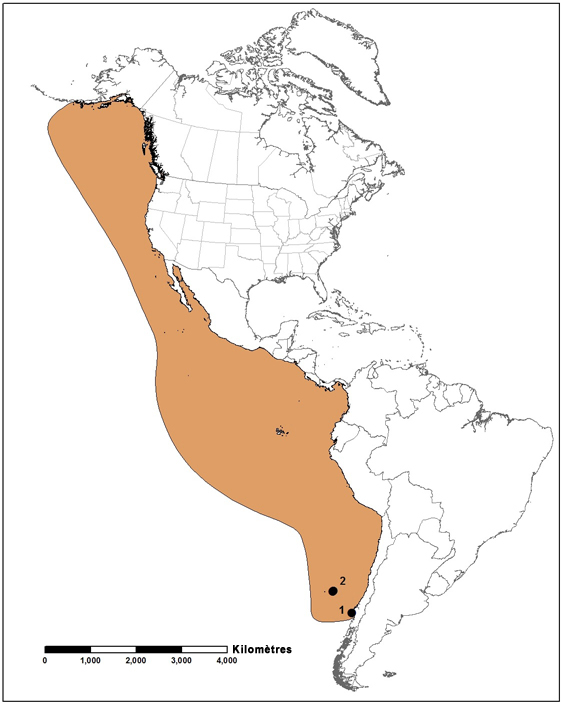
Répartition mondiale du Puffin à pieds roses (à l’est de la ligne), selon des cartes de BirdLife International (2003). 1 – colonie de l’île Mocha, 2 – colonies de l’archipel Juan Fernández (îles Robinson Crusoe et Santa Clara). L’espèce est aussi régulièrement signalée en Nouvelle-Zélande (non représentée ici; répartition inconnue jusqu’à cet endroit). Source des données : BirdLife International et NatureServe (2015). Carte dressée par Alain Filion, du COSEPAC.
Les Puffins à pieds roses nichent dans des terriers qu’ils creusent dans le sol de leurs colonies de nidification. À l’île Mocha, les terriers se trouvent en forêt indigène dans des hauts de pentes orientés vers la mer et sur des sommets de crêtes, tandis qu’aux îles Robinson Crusoe et Santa Clara, les nids sont situés dans des restes de forêt indigène ou en terrain dégagé à végétation herbeuse ou à sol dénudé. En milieu marin, les Puffins à pieds roses montrent une préférence pour les eaux biologiquement productives du talus continental, du rebord externe de la plate-forme continentale et de cette dernière.
Les Puffins à pieds roses se reproduisent durant le printemps et l’été austraux dans leurs colonies de nidification, où ils retournent du début au milieu d’octobre. Les femelles ne pondent qu’un seul œuf par année, entre la fin de novembre et la mi-décembre. Les œufs éclosent de la fin de janvier à la mi-février après une longue incubation, et les jeunes quittent le nid principalement en mai. L’incubation est assurée par les deux parents. Une fois les jeunes hors du nid, les parents migrent vers le nord dans leurs quartiers d’hiver au large du Pérou et de la côte ouest des États-Unis et du Canada.
La taille de la population mondiale du Puffin à pieds roses est estimée à 28 000 couples nicheurs. À l’île Mocha, on pense que la population a diminué considérablement au cours du 20e siècle en raison de la récolte illégale de poussins et des prédateurs introduits. Selon une étude qui y a été réalisée à la fin des années 1990, le nombre de couples nicheurs aurait fortement diminué (~40 %) par rapport à une estimation réalisée à la fin des années 1980, les méthodes utilisées dans les deux relevés ayant cependant été différentes. Des données montrent qu’il y a eu vraisemblablement baisse de l’effectif à l’île Robinson Crusoe au cours des 55 dernières années (3 générations) en raison de la prédation d’adultes et de poussins par les coatis et les chats féraux. Cependant, on pense que la population de l’île Robinson Crusoe est demeurée stable au cours des 15 dernières années, et le suivi effectué à l’île Mocha à partir de 2010 laisse penser que la population y est stable depuis. Les tendances des effectifs dans l’aire canadienne de l’espèce sont inconnues.
Les menaces pesant sur l’espèce à ses colonies comprennent l’exploitation et la perturbation par les humains, la prédation, la perturbation et la compétition exercées par des mammifères introduits, et la perte et la dégradation d’habitat, particulièrement par l’entremise de l’érosion accentuée par la perte de végétation. En mer, l’espèce est menacée par des interactions avec les pêches, la pollution par les hydrocarbures et autres, l’ingestion de plastique, et probablement par la compétition avec les humains pour des poissons proies.
Le Puffin à pieds roses est classé comme étant menacé au Canada, en voie de disparition au Chili, et vulnérable selon l’UICN. Le Conservation Data Centre de la Colombie-Britannique le classe comme étant vulnérable. En 2015, il a été ajouté à l’Annexe 1 de l’Accord sur la conservation des albatros et des pétrels, conclu aux termes de la Convention sur la conservation des espèces migratrices appartenant à la faune sauvage (Convention de Bonn), à laquelle l’espèce est également inscrite. L’archipel Juan Fernández est un parc national du Chili, et une réserve nationale protège la portion de l’île Mocha où niche des Puffins à pieds roses. Au Canada, l’espèce fréquente l’aire marine nationale de conservation Gwaii Haanas.
Source : COSEPAC. 2016. Évaluation et Rapport de situation du COSEPAC sur le Puffin à pieds roses (Ardenna creatopus) au Canada. Comité sur la situation des espèces en péril au Canada. Ottawa. xiv + 50 p.

Photo: © Atlantic Canada Conservation Data Centre
Description longue
Scirpus longii
Plantes vasculaires
Préoccupante
Nouvelle-Écosse
Cette plante des milieux humides, longévive et vulnérable à l’échelle mondiale, est confinée au Canada à une petite région de la Nouvelle-Écosse, qui abrite près de la moitié de la population mondiale. L’espèce est de plus en plus menacée par la compétition et l’ombrage exercés par le nerprun bourdaine, espèce envahissante, ainsi que par des arbustes indigènes. L’extraction de tourbe pourrait être une menace dans le futur. La reproduction sexuée limitée et l’hybridation pourraient également réduire la survie de ce carex.
Le scirpe de Long est un carex vivace robuste qui pousse dans les tourbières. Il produit des plaques clonales circulaires de pousses végétatives à partir de rhizomes souterrains robustes. Les tiges florifères, peu fréquemment produites dans la plupart des occurrences, sont longues de 100 à 180 cm et se terminent par une inflorescence fortement ramifiée comprenant jusqu’à 1 000 épillets, chacun composé de jusqu’à 60 fleurs minuscules prenant une apparence laineuse à maturité. L’inflorescence est sous-tendue par trois bractées foliacées, qui sont de couleur foncée et collantes à leur base. Le scirpe de Long se distingue des espèces apparentées cooccurrentes par ses bractées, ses rhizomes épais, sa grande taille ainsi que ses fruits brun-rouge (akènes semblables à des graines).
Le scirpe de Long est considéré comme vulnérable (G2G3) à l’échelle mondiale et possède une aire de répartition mondiale restreinte, et une responsabilité élevée pour la conservation de cette espèce incombe au Canada. Les occurrences canadiennes (46+ % des occurrences mondiales) se trouvent dans un paysage beaucoup moins perturbé que la plupart des occurrences des États-Unis, et elles pourraient revêtir une importance particulière parce qu’elles se trouvent à la limite nord de l’aire de répartition mondiale de l’espèce. Le scirpe de Long fait partie des nombreuses plantes de la plaine côtière de l’Atlantique rares au Canada qui comptent une population isolée et sont d’intérêt public dans le sud de la Nouvelle-Écosse. Le scirpe de Long est localement dominant dans des tourbières, et la longévité impressionnante de ses clones, qui peuvent vivre plus de 400 ans, est souvent mentionnée dans les interprétations de la nature portant sur la flore de la plaine côtière de l’Atlantique.
Le scirpe de Long a une aire de répartition mondiale limitée, qui s’étend depuis le sud du New Jersey, aux États-Unis, jusque dans le sud de la Nouvelle-Écosse, au Canada. Aucune mention ne se trouve à plus de 70 km de la côte. Les occurrences historiques de l’espèce au Connecticut et dans l’État de New York ont été détruites par le développement, ce qui a créé un trou de près de 300 km dans l’aire de répartition, entre le New Jersey et l’est de la Nouvelle-Angleterre, au Rhode Island, dans le sud du New Hampshire et dans le sud du Maine. Au Canada, 37 sous-populations sont connues dans une zone de 94 km sur 90 km dans le sud-ouest de la Nouvelle-Écosse, où tout porte à croire qu’il existe encore de nombreuses occurrences non découvertes.
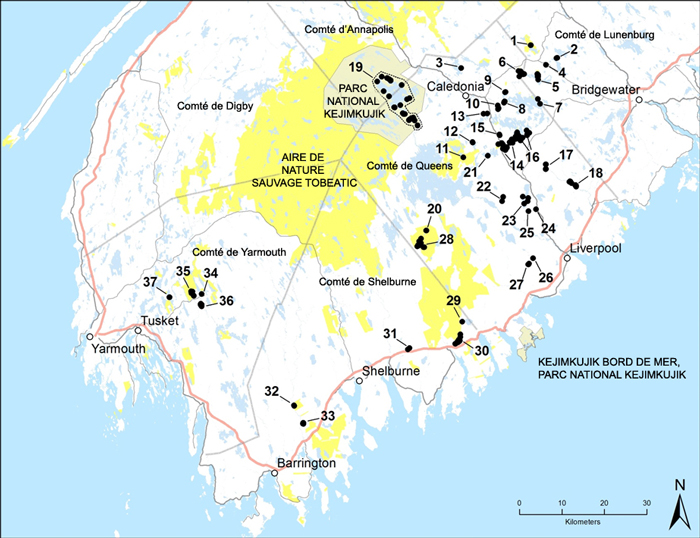
Occurrences canadiennes du scirpe de Long dans le sud de la Nouvelle-Écosse. Les aires protégées sont indiquées en jaune.
Le scirpe de Long pousse dans les tourbières dégagées, mouillées, acides, pauvres en éléments nutritifs et présentant une couverture limitée d’arbustes et d’arbres plus hauts que les pousses de l’espèce. L’espèce se rencontre particulièrement fréquemment dans les grandes tourbières inondées une partie de l’année par les ruisseaux, les rivières et les lacs adjacents, et les sous-populations sont généralement particulièrement grandes dans ces milieux, mais l’espèce est aussi observée dans des tourbières éloignées des cours et plans d’eau, le plus souvent dans des zones mouillées une partie de l’année où la biomasse sur pied est faible.
Le scirpe de Long est une espèce clonale vivace. Il se reproduit principalement par voie végétative au moyen de ses rhizomes, et ses clones peuvent avoir une très longue durée de vie, l’âge de certains grands clones étant estimé à plusieurs centaines d’années. La floraison est peu fréquente dans la plupart des sous-populations, et celle-ci est souvent induite par des perturbations telles que les incendies et la consommation des rhizomes par le rat musqué. L’espèce fleurit à la fin mai et en juin. Le pollen est dispersé par le vent, et peut-être aussi par les insectes. Le système de reproduction de l’espèce n’a pas été étudié, et on ignore si celle-ci est autocompatible. Les akènes arrivent à maturité au milieu ou à la fin de l’été et peuvent tout de suite germer. La germination des graines et l’établissement des semis sont limités, sauf en conditions écologiques atypiques, notamment lorsque les incendies réduisent la couverture de plantes et de litière. Les graines sont dispersées par le vent et par l’eau, principalement à la fin de l’été et en automne, et même jusqu’en hiver lorsque les tiges demeurent sur pied. La dispersion des graines par les oiseaux aquatiques, par voies interne ou externe, pourrait être importante pour la dispersion sur de longues distances. Il est probable que les individus mettent plusieurs années pour arriver à maturité, mais la floraison a été observée chez des individus de moins de un an au New Jersey. Le maintien à long terme de graines du scirpe de Long dans le réservoir de semences du sol pourrait être important étant donné la faible fréquence de la floraison et la faible fréquence potentielle des perturbations qui favorisent l’établissement des semis. La fragmentation des rhizomes par la glace ou par le rat musqué semble être importante pour la dispersion de l’espèce le long des cours d’eau, mais elle se produit probablement peu fréquemment dans les tourbières éloignées de cours d’eau.
Il est difficile de quantifier la taille de la population, car il est complexe de déterminer le nombre d’individus matures. La population canadienne connue est évaluée à 2 700 clones contenant 718 000 pousses, et le nombre d’individus matures devant être utilisé aux fins de l’évaluation de la situation de l’espèce se rapproche davantage de 2 700. Il est probable que les occurrences qui n’ont pas encore été découvertes dans le sud de la Nouvelle-Écosse renferment un nombre de clones et de pousses au moins équivalent à celui déjà connu.
La population canadienne semble être relativement stable. Toutes les sous-populations recensées dans le rapport de situation précédent existent encore, et aucune d’elle ne semble avoir subi de déclins considérables, sauf peut-être une. Le nerprun bourdaine, la succession végétale et peut-être les effets localisés des véhicules tout-terrain ou du développement causeront probablement des déclins de faible ampleur au cours des prochaines décennies.
Les principales menaces qui pèsent sur le scirpe de Long ont une évolution lente ou sont limitées sur le plan spatial. L’ombre créée par le nerprun bourdaine, espèce exotique envahissante, ne constitue pas encore une menace importante, mais elle représente la menace de la plus grande ampleur et la plus répandue à court terme, puisque 20 des 37 sous-populations se trouvent à moins de 15 km de sites où cette espèce envahissante est présente. Le nerprun bourdaine pousse tout juste en bordure d’au moins 4 de ces 20 sous-populations, et on peut s’attendre à ce qu’il se soit propagé à l’ensemble de l’aire de répartition canadienne du scirpe de Long (mais pas nécessairement dans tous les milieux occupés par l’espèce) d’ici une période correspondant à une à trois fois la durée présumée d’une génération du scirpe de Long.
L’hybridation du scirpe de Long avec le scirpe souchet, espèce indigène beaucoup plus abondante, a été constatée dans deux des cinq sous-populations ayant fait l’objet d’analyses génétiques, et on estime qu’elle représente une menace continue pour l’intégrité génétique du scirpe de Long. Cette menace est accentuée par la présence accrue du scirpe souchet dans les sites perturbés, comme les fossés des chemins forestiers, mais la longévité des clones du scirpe de Long et la floraison peu fréquente de ceux-ci limitent considérablement l’immédiateté de cette menace. L’inondation des berges causée par l’aménagement de barrages hydroélectriques a sans aucun doute causé la disparition de sous-populations de 1900 à 1950, mais on ne prévoit pas que cette activité fera d’autres dommages à court terme. L’utilisation de véhicules tout-terrain et la succession végétale constituent des menaces pour certaines sous-populations. L’extraction de tourbe pourrait devenir une menace dans le futur.
La faible fréquence de la floraison, qui fait en sorte que la production de graines, la dispersion de celles-ci et l’établissement de semis sont limités, représente un facteur limitatif. On ignore exactement dans quelle mesure la fréquence de la floraison a diminué au Canada par rapport à ce qu’elle était avant la colonisation européenne, à cause de la suppression anthropique des incendies et d’autres facteurs.
Le scirpe de Long est désigné espèce préoccupante aux termes de l’annexe 3 de la Loi sur les espèces en péril du Canada, et espèce vulnérable aux termes de l’Endangered Species Act de la Nouvelle-Écosse, mais ces deux désignations confèrent une protection limitée à l’espèce. Le scirpe de Long est protégé dans une certaine mesure par les lois sur les espèces en péril des États du New Jersey, du Rhode Island, du New Hampshire et du Massachusetts. Il est considéré comme une espèce préoccupante au Connecticut, où il est présumé disparu. NatureServe a attribué à l’espèce les cotes de G2G3 (en péril à vulnérable) à l’échelle mondiale, de N2 (en péril) aux États-Unis, de N2N3 (en péril à vulnérable) au Canada, de SX (présumée disparue) dans l’État de New York, de SH (potentiellement disparue) au Connecticut, de S1 (gravement en péril) au Rhode Island et au New Hampshire, de S2 (en péril) au New Jersey, au Massachusetts et au Maine et de S2S3 (en péril à vulnérable) en Nouvelle-Écosse.
Source : COSEPAC. 2017. Évaluation et Rapport de situation du COSEPAC sur le scirpe de Long (Scirpus longii) au Canada. Comité sur la situation des espèces en péril au Canada. Ottawa. xvii + 69 p.

Photo: © Sam Brinker
Description longue
Teloschistes chrysophthalmus
Lichens
Préoccupante
Manitoba, Ontario
Environ 99 % de la population connue de ce lichen se trouve à moins de 15 km de la forêt provinciale Spruce Woods, dans le centre–sud du Manitoba, mais des occurrences dispersées s’étendent depuis le sud du lac Winnipeg, au Manitoba, jusqu’au lac à la Pluie, dans le nord–ouest de l’Ontario. Les menaces pesant sur cette population incluent les changements dans la fréquence et la gravité des incendies, les changements climatiques, les activités récréatives et le pâturage du bétail. Ces menaces devraient contribuer à aggraver le déclin de ce lichen, de son habitat et de son hôte privilégié, l’épinette blanche.
Le téloschiste ocellé (Teloschistes chrysophthalmus) est un macrolichen arboricole dont la coloration distinctive varie de l’orange vif au gris verdâtre. Le thalle a un port en arbrisseau touffu et présente souvent des ramifications aplaties fixées au substrat par un crampon central. L’espèce se distingue des autres espèces du même genre par ses abondants organes de fructification (apothécies) aux marges ciliées et par l’absence de propagules végétatives comme des isidies ou des sorédies.
Au Canada, le téloschiste ocellé est présent dans certaines zones du centre-sud du Manitoba, du nord-ouest de l’Ontario et de la partie sud de la région des Grands Lacs, en Ontario. Aux États-Unis, on trouve l’espèce dans le Midwest, les Grandes Plaines jusqu’au Texas au sud et la région côtière de la Californie et au Mexique. Sur la côte est des États-Unis, il existe des mentions historiques de l’espèce depuis le Maine jusqu’au New Jersey, et on ne l’a observée récemment qu’en Caroline du Nord.
Le téloschiste ocellé est présent dans les hémisphères nord et sud, sur tous les continents à l’exception de l’Asie et de l’Antarctique. Il existe des mentions de l’espèce dans le sud de l’Australie et en Nouvelle-Zélande, en Afrique du Nord, aux îles Canaries et aux îles du Cap-Vert, ainsi que dans l’ouest, le centre et le sud de l’Europe. On en trouve également des occurrences éparses en Amérique du Sud, particulièrement en Argentine et au Chili.
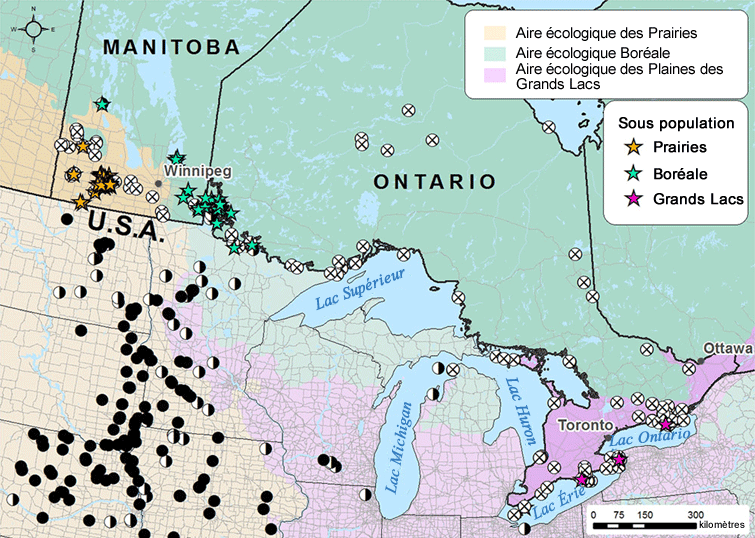
Activités de recherche et occurrences du téloschiste ocellé dans chacune de trois aires écologiques nationales du COSEPAC. Les étoiles (☆) indiquent les occurrences de l’espèce au Canada : les étoiles vertes et jaunes représentent la population boréale et des Prairies, et les étoiles rouges la population des Grands Lacs. Les cercles blancs avec un x (⊗) représentent les endroits où l’on a cherché en vain l’espèce au Canada de 2013 à 2015. Les cercles (●) indiquent les mentions récentes du téloschiste ocellé aux États-Unis, citées dans des publications. Les cercles à moitié blancs et à moitié noirs (◑) indiquent les mentions historiques (remontant à plus de 20 ans) du téloschiste ocellé aux États-Unis.
Le téloschiste ocellé a besoin d’un milieu humide et bien éclairé sous un climat tempéré ou de type méditerranéen, et on le trouve souvent en milieu riverain et dans des régions côtières. Au Canada, il occupe habituellement les branches et rameaux d’arbres hôtes de plusieurs espèces. Dans la région du delta glaciaire de l’Assiniboine, dans le centre-sud du Manitoba, des thalles de l’espèce poussent en abondance sur des épinettes blanches matures formant des peuplements clairs sur des sables calcaires, lesquels paraissent comme des « îles » dans la prairie mixte. Dans le sud-est du Manitoba et le nord-ouest de l’Ontario, ce lichen pousse en très faible densité sur l’épinette blanche, le peuplier faux-tremble, le pin gris, le sapin baumier et le chêne à gros fruits dans des forêts claires ou des landes rocheuses. Dans le sud de la région ontarienne des Grands Lacs, le seul site qui abrite encore le téloschiste ocellé se trouve dans une forêt ancienne composée d’érables à sucre, d’ostryers de Virginie et de chênes rouges poussant sur une fondation rocheuse calcaire, sur le littoral du lac Ontario. Dans ce site, le lichen pousse sur l’écorce bien éclairée du chêne rouge.
Le téloschiste ocellé se reproduit sexuellement par la dispersion de ses ascospores fongiques qui doivent germer et entrer en contact avec une algue verte compatible du genre Trebouxia. La dispersion à petite distance par reproduction asexuée, c’est-à-dire par fragmentation du thalle, est commune chez les lichens, et on présume qu’elle se produit aussi chez le téloschiste ocellé. Il s’agit d’une espèce mésotrophe qui tolère des concentrations d’azote modérées, mais pas les fortes concentrations tolérées par les lichens nitrophiles, comme le Xanthoria parietina qui lui est apparenté. Le téloschiste ocellé croît assez rapidement, sans doute parce qu’il préfère les substrats bien éclairés et relativement riches en éléments nutritifs. Il a d’ailleurs une durée de génération plus courte que bien d’autres espèces de lichen. Il est toutefois sensible aux précipitations acides et au dioxyde de soufre, en partie en raison de son port en arbrisseau qui lui confère un rapport surface/volume élevé.
Au Canada, 25 occurrences du téloschiste ocellé ont été documentées. Elles représentent trois sous-populations : la sous-population des Prairies (six occurrences), la sous-population boréale (14 occurrences, dont une est historique) et la sous-population des Grands Lacs (cinq occurrences, dont quatre sont historiques et sans doute disparues). La sous-population des Grands Lacs est considérée comme une unité désignable (UD) parce qu’elle est géographiquement isolée et écologiquement distincte des deux autres sous-populations, puisqu’elle pousse sur des arbres feuillus.
En 2013, l’abondance totale du téloschiste ocellé au Canada était estimée à plus de 15 millions d’individus. On a estimé le nombre de colonies du lichen sur les épinettes blanches en dénombrant les colonies sur certaines branches, puis en comptant sur chaque arbre le nombre de branches occupées par l’espèce. Ces données ont permis d’estimer que les arbres abritaient chacun entre 10 000 et 20 000 colonies. Ainsi, la population totale est peut-être très élevée, mais elle pourrait n’être répartie que sur 7 000 à 15 000 épinettes blanches.
Environ 99 % des effectifs connus de l’espèce au Canada appartiennent à la sous-population des Prairies et se trouvent à moins de 15 km de la forêt provinciale Spruce Woods, dans le centre-sud du Manitoba. Hors de cette zone principale, les occurrences sont peu nombreuses, petites et fragmentées; elles constituent sans doute ce qui reste de l’ancienne aire de répartition plus continue. Estimée à 5 000-7 000 individus, soit environ 0,03-0,05 % de la population totale au pays, la sous-population boréale est présente dans la région qui s’étend depuis le sud du lac Winnipeg jusqu’au lac des Bois et au lac à la Pluie, dans le nord-ouest de l’Ontario. La sous-population des Grands Lacs, qui constitue une UD distincte, ne consiste plus qu’en un seul individu présent dans le parc provincial Sandbanks, au bord du lac Ontario. Selon les rares données pouvant indiquer une tendance, l’espèce aurait toujours été rare dans la région des Grands Lacs, mais elle aurait aussi décliné en raison de facteurs anthropiques.
Selon l’évaluation effectuée au moyen du calculateur de menaces, les impacts des menaces qui pèsent sur le téloschiste ocellé sont considérés comme « moyens à élevés ». Les principales menaces qui pèsent sur la très grande sous-population des Prairies sont les incendies et la suppression des incendies, les changements climatiques, les activités récréatives et le pâturage de bétail. La sous-population boréale pourrait être touchée par la construction de chalets, tandis que la très petite sous-population des Grands Lacs, maintenant réduite à un seul arbre hôte, pourrait être touchée par plusieurs menaces, notamment un phénomène météorologique violent, des perturbations humaines, la pollution atmosphérique et des espèces envahissantes.
À l’heure actuelle, le téloschiste ocellé ne jouit d’aucune protection ou statut juridique au Canada et aux États-Unis. Il est coté G4G5 (apparemment non en péril à non en péril) à l’échelle mondiale et N3N4 (vulnérable à apparemment non en péril) à l’échelle nationale au Canada. À l’échelle provinciale, il est coté S2S3 (en péril à vulnérable) en Ontario, et S3S4 (vulnérable à apparemment non en péril) au Manitoba.
Sa plus grande sous-population au Canada est présente dans l’aire écologique des Prairies, plus précisément dans le centre-sud du Manitoba, où une grande partie de l’habitat convenable se trouve dans le parc provincial Spruce Woods et dans la forêt provinciale adjacente du même nom et y bénéficie d’une certaine protection. On trouve également une partie de cette sous-population sur la base des Forces canadiennes Shilo gérée par le gouvernement fédéral. La sous-population boréale occupe principalement des terres de la Couronne sur des rives lacustres et ne jouit d’aucune protection officielle. UD distincte située dans le parc provincial Sandbanks, la sous-population des Grands Lacs n’est représentée que par une seule occurrence actuelle qui jouit d’une certaine protection conférée par la Loi sur les parcs provinciaux et les réserves de conservation de l’Ontario, bien qu’aucun programme de surveillance officiel ne soit en place pour y évaluer l’impact des menaces ou la persistance du téloschiste ocellé.
Source : COSEPAC. 2016. Évaluation et Rapport de situation du COSEPAC sur le téloschiste ocellé (Teloschistes chrysophthalmus), population des Grands Lacs et population boréale et des Prairies, au Canada. Ottawa. vii + 46 p.

Photo: © Sam Brinker
Description longue
Teloschistes chrysophthalmus
Lichen
En voie de disparition
Ontario
Cette population se compose maintenant d’un seul individu sur un seul chêne rouge, qui se trouve dans le parc provincial Sandbanks, près du lac Ontario. Les données sur les tendances sont limitées, mais elles portent à croire que cette population, qui est associée aux arbres hôtes à feuilles caduques, a probablement toujours été rare dans cette province. Le nombre d’individus matures de ce lichen a connu un déclin en raison d’une combinaison de menaces, qui incluent la pollution atmosphérique, les perturbations anthropiques, les espèces envahissantes et les phénomènes météorologiques violents. Un seul événement naturel ou d’origine humaine pourrait entraîner la perte de toute la population.
Le téloschiste ocellé (Teloschistes chrysophthalmus) est un macrolichen arboricole dont la coloration distinctive varie de l’orange vif au gris verdâtre. Le thalle a un port en arbrisseau touffu et présente souvent des ramifications aplaties fixées au substrat par un crampon central. L’espèce se distingue des autres espèces du même genre par ses abondants organes de fructification (apothécies) aux marges ciliées et par l’absence de propagules végétatives comme des isidies ou des sorédies.
Au Canada, le téloschiste ocellé est présent dans certaines zones du centre-sud du Manitoba, du nord-ouest de l’Ontario et de la partie sud de la région des Grands Lacs, en Ontario. Aux États-Unis, on trouve l’espèce dans le Midwest, les Grandes Plaines jusqu’au Texas au sud et la région côtière de la Californie et au Mexique. Sur la côte est des États-Unis, il existe des mentions historiques de l’espèce depuis le Maine jusqu’au New Jersey, et on ne l’a observée récemment qu’en Caroline du Nord.
Le téloschiste ocellé est présent dans les hémisphères nord et sud, sur tous les continents à l’exception de l’Asie et de l’Antarctique. Il existe des mentions de l’espèce dans le sud de l’Australie et en Nouvelle-Zélande, en Afrique du Nord, aux îles Canaries et aux îles du Cap-Vert, ainsi que dans l’ouest, le centre et le sud de l’Europe. On en trouve également des occurrences éparses en Amérique du Sud, particulièrement en Argentine et au Chili.
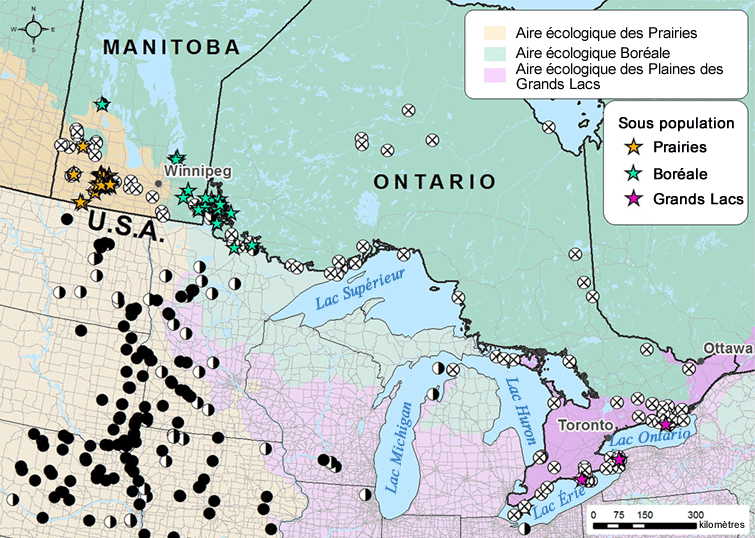
Activités de recherche et occurrences du téloschiste ocellé dans chacune de trois aires écologiques nationales du COSEPAC. Les étoiles (☆) indiquent les occurrences de l’espèce au Canada : les étoiles vertes et jaunes représentent la population boréale et des Prairies, et les étoiles rouges la population des Grands Lacs. Les cercles blancs avec un x (⊗) représentent les endroits où l’on a cherché en vain l’espèce au Canada de 2013 à 2015. Les cercles (●) indiquent les mentions récentes du téloschiste ocellé aux États-Unis, citées dans des publications. Les cercles à moitié blancs et à moitié noirs (◑) indiquent les mentions historiques (remontant à plus de 20 ans) du téloschiste ocellé aux États-Unis.
Le téloschiste ocellé a besoin d’un milieu humide et bien éclairé sous un climat tempéré ou de type méditerranéen, et on le trouve souvent en milieu riverain et dans des régions côtières. Au Canada, il occupe habituellement les branches et rameaux d’arbres hôtes de plusieurs espèces. Dans la région du delta glaciaire de l’Assiniboine, dans le centre-sud du Manitoba, des thalles de l’espèce poussent en abondance sur des épinettes blanches matures formant des peuplements clairs sur des sables calcaires, lesquels paraissent comme des « îles » dans la prairie mixte. Dans le sud-est du Manitoba et le nord-ouest de l’Ontario, ce lichen pousse en très faible densité sur l’épinette blanche, le peuplier faux-tremble, le pin gris, le sapin baumier et le chêne à gros fruits dans des forêts claires ou des landes rocheuses. Dans le sud de la région ontarienne des Grands Lacs, le seul site qui abrite encore le téloschiste ocellé se trouve dans une forêt ancienne composée d’érables à sucre, d’ostryers de Virginie et de chênes rouges poussant sur une fondation rocheuse calcaire, sur le littoral du lac Ontario. Dans ce site, le lichen pousse sur l’écorce bien éclairée du chêne rouge.
Le téloschiste ocellé se reproduit sexuellement par la dispersion de ses ascospores fongiques qui doivent germer et entrer en contact avec une algue verte compatible du genre Trebouxia. La dispersion à petite distance par reproduction asexuée, c’est-à-dire par fragmentation du thalle, est commune chez les lichens, et on présume qu’elle se produit aussi chez le téloschiste ocellé. Il s’agit d’une espèce mésotrophe qui tolère des concentrations d’azote modérées, mais pas les fortes concentrations tolérées par les lichens nitrophiles, comme le Xanthoria parietina qui lui est apparenté. Le téloschiste ocellé croît assez rapidement, sans doute parce qu’il préfère les substrats bien éclairés et relativement riches en éléments nutritifs. Il a d’ailleurs une durée de génération plus courte que bien d’autres espèces de lichen. Il est toutefois sensible aux précipitations acides et au dioxyde de soufre, en partie en raison de son port en arbrisseau qui lui confère un rapport surface/volume élevé.
Au Canada, 25 occurrences du téloschiste ocellé ont été documentées. Elles représentent trois sous-populations : la sous-population des Prairies (six occurrences), la sous-population boréale (14 occurrences, dont une est historique) et la sous-population des Grands Lacs (cinq occurrences, dont quatre sont historiques et sans doute disparues). La sous-population des Grands Lacs est considérée comme une unité désignable (UD) parce qu’elle est géographiquement isolée et écologiquement distincte des deux autres sous-populations, puisqu’elle pousse sur des arbres feuillus.
En 2013, l’abondance totale du téloschiste ocellé au Canada était estimée à plus de 15 millions d’individus. On a estimé le nombre de colonies du lichen sur les épinettes blanches en dénombrant les colonies sur certaines branches, puis en comptant sur chaque arbre le nombre de branches occupées par l’espèce. Ces données ont permis d’estimer que les arbres abritaient chacun entre 10 000 et 20 000 colonies. Ainsi, la population totale est peut-être très élevée, mais elle pourrait n’être répartie que sur 7 000 à 15 000 épinettes blanches.
Environ 99 % des effectifs connus de l’espèce au Canada appartiennent à la sous-population des Prairies et se trouvent à moins de 15 km de la forêt provinciale Spruce Woods, dans le centre-sud du Manitoba. Hors de cette zone principale, les occurrences sont peu nombreuses, petites et fragmentées; elles constituent sans doute ce qui reste de l’ancienne aire de répartition plus continue. Estimée à 5 000-7 000 individus, soit environ 0,03-0,05 % de la population totale au pays, la sous-population boréale est présente dans la région qui s’étend depuis le sud du lac Winnipeg jusqu’au lac des Bois et au lac à la Pluie, dans le nord-ouest de l’Ontario. La sous-population des Grands Lacs, qui constitue une UD distincte, ne consiste plus qu’en un seul individu présent dans le parc provincial Sandbanks, au bord du lac Ontario. Selon les rares données pouvant indiquer une tendance, l’espèce aurait toujours été rare dans la région des Grands Lacs, mais elle aurait aussi décliné en raison de facteurs anthropiques.
Selon l’évaluation effectuée au moyen du calculateur de menaces, les impacts des menaces qui pèsent sur le téloschiste ocellé sont considérés comme « moyens à élevés ». Les principales menaces qui pèsent sur la très grande sous-population des Prairies sont les incendies et la suppression des incendies, les changements climatiques, les activités récréatives et le pâturage de bétail. La sous-population boréale pourrait être touchée par la construction de chalets, tandis que la très petite sous-population des Grands Lacs, maintenant réduite à un seul arbre hôte, pourrait être touchée par plusieurs menaces, notamment un phénomène météorologique violent, des perturbations humaines, la pollution atmosphérique et des espèces envahissantes.
À l’heure actuelle, le téloschiste ocellé ne jouit d’aucune protection ou statut juridique au Canada et aux États-Unis. Il est coté G4G5 (apparemment non en péril à non en péril) à l’échelle mondiale et N3N4 (vulnérable à apparemment non en péril) à l’échelle nationale au Canada. À l’échelle provinciale, il est coté S2S3 (en péril à vulnérable) en Ontario, et S3S4 (vulnérable à apparemment non en péril) au Manitoba.
Sa plus grande sous-population au Canada est présente dans l’aire écologique des Prairies, plus précisément dans le centre-sud du Manitoba, où une grande partie de l’habitat convenable se trouve dans le parc provincial Spruce Woods et dans la forêt provinciale adjacente du même nom et y bénéficie d’une certaine protection. On trouve également une partie de cette sous-population sur la base des Forces canadiennes Shilo gérée par le gouvernement fédéral. La sous-population boréale occupe principalement des terres de la Couronne sur des rives lacustres et ne jouit d’aucune protection officielle. UD distincte située dans le parc provincial Sandbanks, la sous-population des Grands Lacs n’est représentée que par une seule occurrence actuelle qui jouit d’une certaine protection conférée par la Loi sur les parcs provinciaux et les réserves de conservation de l’Ontario, bien qu’aucun programme de surveillance officiel ne soit en place pour y évaluer l’impact des menaces ou la persistance du téloschiste ocellé.
Source : COSEPAC. 2016. Évaluation et Rapport de situation du COSEPAC sur le téloschiste ocellé (Teloschistes chrysophthalmus), population des Grands Lacs et population boréale et des Prairies, au Canada. Ottawa. vii + 46 p.

Photo: © Ryan M. Bolton
Description longue
Emydoidea blandingii
Reptiles
En voie de disparition
Ontario, Québec
Cette population, bien que dispersée, connaît un déclin en raison de plusieurs menaces observées, déduites et projetées. Les menaces les plus graves incluent les suivantes : la mortalité sur la route et les rails; la collecte illégale pour le commerce des animaux de compagnie, des aliments et des produits médicinaux traditionnels; la perte d’habitat causée par le roseau commun envahissant; le développement ainsi que la modification des milieux humides; l’augmentation du nombre de prédateurs. Les analyses quantitatives permettent d’estimer que le nombre total d’individus matures dans cette population a connu un déclin de plus de 60 % au cours des trois dernières générations (en raison du drainage de zones humides à grande échelle après l’arrivée des Européens) et subira un déclin de 50 % au cours des trois prochaines générations causée par la mortalité sur les routes seulement.
La tortue mouchetée (Emydoidea blandingii) est le seul représentant du genre Emydoidea. Il s’agit d’une tortue d’eau douce de taille moyenne dotée d’une gorge jaune vif facilement reconnaissable et d’une carapace formant un dôme prononcé, de couleur noire avec des taches et des mouchetures jaunâtres. Son aire de répartition mondiale est parmi les plus petites pour toutes les tortues nord-américaines, et environ 20 % de cette aire, seulement, se trouve au Canada.
Au Canada, la population de tortues mouchetées des Grands Lacs et du Saint-Laurent vit principalement dans le sud de l’Ontario (malgré des mentions isolées jusqu’à Timmins, au nord) et dans le sud du Québec (malgré des mentions isolées jusque dans l’Abitibi-Témiscamingue, au nord, et jusque dans la région de la Capitale-Nationale, à Québec, à l’est). La population de la Nouvelle-Écosse, beaucoup plus petite, est observée dans la partie sud de la province; il s’agit de la population la plus isolée au sein de l’aire de répartition de l’espèce.
Aux États-Unis, la tortue mouchetée est présente dans les États du nord-est, et en plus grandes concentrations autour des Grands Lacs. Elle a cependant été observée jusqu’au Nebraska et au Dakota du Sud à l’ouest, et de petites populations isolées existent le long de la côte de l’Atlantique dans les États de New York, du Massachusetts, du New Hampshire et du Maine.
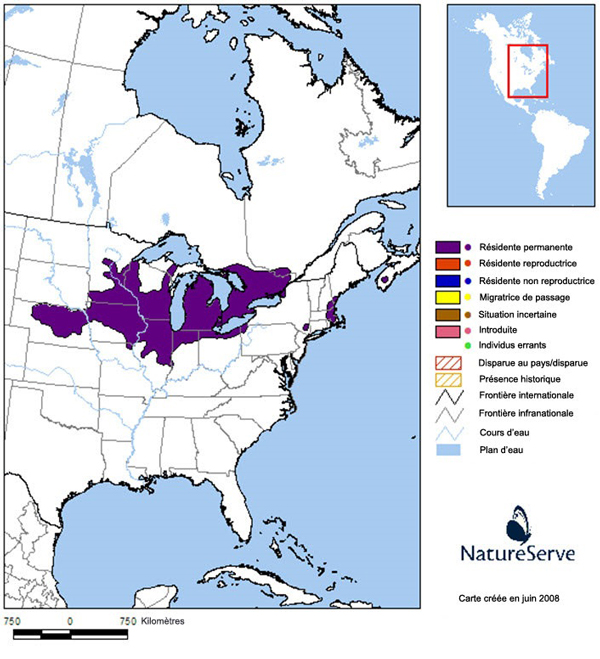
Répartition de la tortue mouchetée en Amérique du Nord.
Source : carte fournie par NatureServe, 2008.
En Nouvelle-Écosse, la tortue mouchetée montre une préférence pour les eaux foncées, associées à une productivité secondaire relativement élevée. La population des Grands Lacs et du Saint-Laurent, cependant, est souvent observée dans les milieux humides caractérisés par des eaux claires et eutrophes. L’espèce manifeste une grande fidélité aux sites qu’elle occupe, mais elle peut se déplacer entre plusieurs plans d’eau interreliés au cours de la saison active. Les individus de tout âge fréquentent principalement des habitats d’eau peu profonde. Les femelles creusent leur nid dans divers substrats : sable, sol organique, gravier, galets et crevasses emplies de terre sur des affleurements rocheux. Les adultes et les juvéniles hivernent dans divers plans d’eau permanents d’environ un mètre de profondeur, en moyenne; on a cependant vu des nouveau-nés passer leur premier hiver en milieu terrestre. La superficie moyenne du domaine vital de la tortue mouchetée se situe entre 10 et 60 ha (maximum de 382 ha) ou entre 1 000 et 2 500 m (maximum de 7 000 m). Toutefois, la plupart des études sous-estiment probablement la superficie du domaine vital de l’espèce puisque peu ont eu recours à des enregistreurs utilisant un système GPS pour assurer le suivi quotidien des déplacements pendant une ou plusieurs saisons actives.
La tortue mouchetée a une longévité exceptionnelle et une maturité particulièrement tardive, même par comparaison aux autres tortues. Elle met de 14 à 25 ans à atteindre la maturité et peut réussir à se reproduire jusqu’à au moins 75 ans. Les femelles matures produisent une couvée tous les un à trois ans, et la fécondité ainsi que la fréquence de reproduction sont positivement corrélées à l’âge des individus. Les femelles effectuent une migration de nidification sur une longue distance et peuvent alors parcourir plus de 10 km hors de l’eau. La capacité de la tortue mouchetée de se déplacer sur de grandes distances facilite le flux génique entre les milieux humides et augmente peut-être grandement le succès de reproduction. La durée moyenne d’une génération de cette espèce au Canada est d’environ 40 ans.
Dans toute son aire de répartition nord-américaine, la tortue mouchetée est principalement observée en petites sous-populations isolées regroupant de quelques dizaines à une centaine d’individus. Au Canada, la plupart des sous-populations ayant fait l’objet d’un suivi semblent comporter moins de 150 adultes; aucune n’en compte plus de 1 000.
La taille de la population de tortues mouchetées des Grands Lacs et du Saint-Laurent est impossible à estimer avec exactitude étant donné que très peu d’études par marquage-recapture ont été faites dans la région. On croit cependant qu’elle compte moins de 50 000 adultes. Selon les estimations, la population a connu un déclin de plus de 60 % au cours des 3 dernières générations en raison du drainage de zones humides à grande échelle après l’arrivée des Européens. Elle devrait subir un déclin de 50 % de plus au cours des 3 prochaines générations d’après les tendances observées dans les sous-populations faisant l’objet d’un suivi et les modèles de mortalité routière. Le programme de marquage-recapture de longue date mis en œuvre au Québec a permis de trouver, à ce jour, moins de 200 adultes. Si aucune tendance n’a été confirmée pour cette sous-population, elle a sans doute elle aussi connu un déclin étant donné la disparition historique des milieux humides et les menaces anthropiques qui se poursuivent.
Le nombre total de tortues mouchetées matures au sein de la population de la Nouvelle-Écosse est estimé à moins de 500. La sous-population étudiée depuis le plus longtemps arrive à maturité très tard (20 à 25 ans) et a une très grande longévité (plus de 70 ans). Si aucune mesure de gestion n’est prise, les modèles prédisent que cette population présente un risque élevé de disparition, même si elle vit dans une aire protégée.
Cette espèce fait l’objet de nombreuses menaces, dont les plus graves sont les suivantes :
- mortalité sur les routes et les voies ferrées, et effets connexes des routes;
- perte d’habitat causée par le roseau commun, une espèce envahissante, ainsi que par divers types de développement et la modification des milieux humides;
- collecte illégale pour le commerce des animaux de compagnie, des aliments et des produits médicinaux traditionnels;
- augmentation de la mortalité d’individus et de la destruction de nids par des prédateurs favorisés par les activités humaines.
Les autres menaces possibles incluent la mortalité causée par la production d’agrégats, l’exploitation forestière, la production d’énergie et les activités récréatives; la pollution des milieux humides; les changements climatiques; l’introduction d’autres espèces envahissantes. Les menaces les plus graves pour les sous-populations de tortues mouchetées sont celles qui causent la mortalité ou la perte d’adultes.
Les principaux facteurs limitatifs de l’espèce sont son cycle vital lent (longévité extrême, âge de maturité très élevé, faible efficacité annuelle de la reproduction, faible taux de recrutement des juvéniles et dépendance à un taux annuel élevé de survie des adultes) ainsi que les étés courts et frais à la périphérie septentrionale de son aire de répartition, ce qui réduit sa fréquence de reproduction et son succès de nidification. Ces facteurs limitatifs rendent la tortue mouchetée très vulnérable à toute hausse, même mineure (moins de 5 %), de la mortalité annuelle des adultes. Comme cette espèce met bien plus de temps à atteindre la maturité que les autres tortues qui vivent au Canada, sa vulnérabilité au déclin est aussi beaucoup plus grande. La stabilité et la persistance de la population dépendent donc en grande partie du taux de survie des adultes.
En 2016, le COSEPAC a désigné comme « en voie de disparition » la population de la Nouvelle-Écosse ainsi que la population des Grands Lacs et du Saint-Laurent. La tortue mouchetée est protégée en vertu de la Loi sur les espèces en péril du gouvernement fédéral (L.C. 2002, ch. 29), de la Loi de 2007 sur les espèces en voie de disparition de l’Ontario (S.O. 2007, c. 6), de la Loi de 1997 sur la protection du poisson et de la faune de l’Ontario (S.O. 1997, c. 41), de la Loi sur la conservation et la mise en valeur de la faune (2002) du Québec (RLRQ, c. C-61.1) et de l’Endangered Species Act (2000) de la Nouvelle-Écosse (1998, c. 11, s. 1). En 2013, l’espèce a été ajoutée à l’annexe II de la CITES; son commerce international est donc aujourd’hui réglementé.
La cote générale attribuée à la tortue mouchetée au Canada, en Ontario, au Québec et en Nouvelle-Écosse est « en péril ». À l’échelle des 18 administrations où elle est présente dans son aire de répartition nord-américaine, l’espèce n’est considérée comme « apparemment non en péril » (S4) que dans un État, le Nebraska, où elle profite d’une protection à grande échelle de l’habitat depuis près d’un siècle. La tortue mouchetée est désignée officiellement comme « en voie de disparition » ou « menacée » dans 13 des 18 provinces ou États où on la trouve; en 2010, l’Union internationale pour la conservation de la nature (en anglais, International Union for Conservation of Nature, ou IUCN) a élevé son statut à « en voie de disparition » puisque la taille de la population de l’espèce a décliné d’au moins 80 % à l’échelle mondiale dans les 3 dernières générations.
Source : COSEPAC. 2016. Évaluation et Rapport de situation du COSEPAC sur la tortue mouchetée (Emydoidea blandingii), population de la Nouvelle–Écosse et population des Grands Lacs et du Saint–Laurent au Canada. Comité sur la situation des espèces en péril au Canada. Ottawa. xxi + 124 p.

Photo: © Kym Welstead
Description longue
Chrysemys picta bellii
Reptiles
Menacée
Colombie-Britannique
La répartition de cette population chevauche une zone où la population humaine est dense dans le sud-ouest de la Colombie-Britannique, y compris la vallée du bas Fraser, où la perte de milieux humides est considérable. Dans l’ensemble de son aire de répartition, cette population continue de faire face à de multiples menaces résultant de la perte et de l’altération de l’habitat, de la mortalité routière et des espèces introduites, comme les ouaouarons et les tortues introduites. Les relevés effectués au cours des 10 dernières années ont révélé bon nombre de nouvelles localités, amenant le nombre total de plans d’eau occupés à plus de 80, répartis en 39 groupes. Toutefois, la population canadienne et les sous-populations locales sont petites, et nombre d’entre elles, particulièrement dans la vallée du bas Fraser, connaissent un déclin ou sont considérées comme non viables. La persistance à long terme de la population canadienne demeure précaire.
La tortue peinte de l’Ouest (Chrysemys picta bellii; Gray, 1831) est une tortue peinte de taille relativement grande; la dossière (partie dorsale de la carapace) des adultes peut atteindre une longueur de 25 cm. Cette sous-espèce possède un plastron (partie ventrale) orange vif distinctif, qui présente aussi un motif complexe de lignes noires réticulées.
Au Canada, la tortue peinte de l’Ouest est présente dans trois grandes régions distinctes, qui correspondent aux unités désignables suivantes : la population de la côte du Pacifique et la population intramontagnarde – des Rocheuses en Colombie-Britannique, et la population des Prairies/boréale de l’Ouest – Bouclier canadien à l’est des Rocheuses. Les populations de tortues peintes de l’Ouest en Colombie-Britannique affichent une forte différenciation génétique, parfois sur de courtes distances. Le présent rapport tient compte de cette différenciation, mais maintient les trois unités désignables établies dans l’évaluation précédente du COSEPAC (COSEWIC, 2006) en raison de considérations relatives au caractère distinct des unités et à l’importance des variations.
L’aire de répartition de la population des Prairies/boréale de l’Ouest – Bouclier canadien s’étend depuis la région d’Algoma, dans le nord de l’Ontario, jusqu’au sud-est de l’Alberta, en passant par le sud des Prairies. Son aire de répartition naturelle en Alberta se limite au bassin versant de la rivière Milk, mais il existe de nombreuses sous-populations introduites dont certaines sont bien établies depuis près d’un siècle, voire plus. La population intramontagnarde – des Rocheuses est surtout présente au fond des grandes vallées des chaînes de montagnes qui caractérisent l’intérieur méridional de la Colombie-Britannique. Parmi les centres de population les plus importants, on compte les vallées de la Thompson et de l’Okanagan, le sud du sillon de la région de Kootenay-Est et le sud de la région de Cariboo. La population de la côte du Pacifique est présente dans la vallée du bas Fraser, depuis le secteur de Chilliwack jusqu’au Grand Vancouver, depuis le nord de la Sunshine Coast jusqu’à la rivière Powell au nord, dans l’île Texada et dans certains secteurs de l’île de Vancouver, dont le district régional de la capitale, la région de Nanaimo et la vallée Alberni.
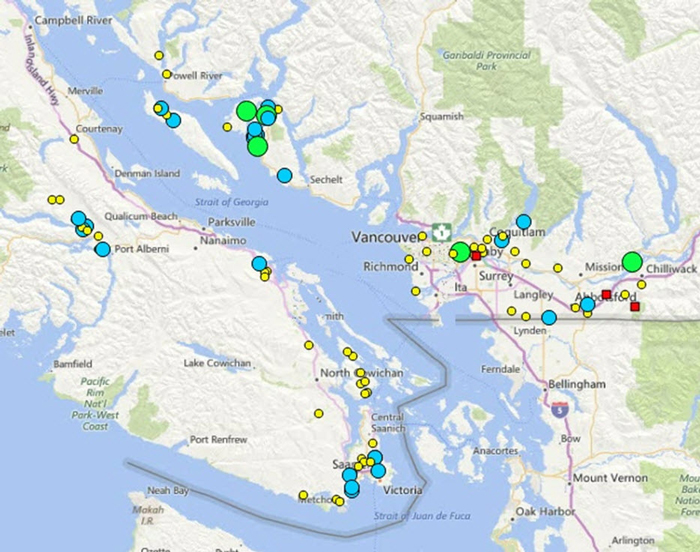
Répartition de la tortue peinte de l’Ouest de la population de la côte du Pacifique. Petit cercle jaune : < 10 individus; cercle bleu moyen : 10 à 100 individus; grand cercle vert : > 100 individus; carré rouge : disparue. À noter que la taille des populations est caractérisée par une forte incertitude, particulièrement dans l’île de Vancouver, au nord du district régional de la capitale.
La tortue peinte de l’Ouest est dans une très large mesure une espèce aquatique, présente dans les eaux peu profondes des étangs, des lacs, des méandres abandonnés et des marais, ainsi que dans les tronçons à faible débit et les bras morts de cours d’eau. Son habitat comporte généralement un substrat boueux, de la végétation aquatique émergente, des nattes racinaires exposées, des rondins flottants et des rives ouvertes. Les tortues peintes préfèrent les rondins flottants, les branches et d’autres objets émergents pour s’exposer au soleil. L’habitat de nidification se trouve dans les milieux terrestres adjacents à l’habitat aquatique utilisé pour la recherche de nourriture, habituellement à moins de 200 m du plan d’eau, sur des pentes douces orientées vers le sud. La ponte a lieu dans le sol, le sable ou le gravier, dans des sites bien drainés où la couverture végétale est minime ou absente.
Les tortues peintes de l’Ouest adultes sont omnivores et s’alimentent de plantes aquatiques, de charogne et de petites proies vivantes dans les eaux peu profondes durant la saison active, soit du printemps à l’automne. Les jeunes tortues tendent à être plus carnivores et s’alimentent d’une variété d’invertébrés et de têtards. Les œufs éclosent à l’automne, mais les nouveau-nés demeurent habituellement dans le nid durant leur premier hiver. Ces derniers peuvent tolérer le gel jusqu’à une température de -10 °C au moins. On considère que les tortues peintes comptent parmi les vertébrés les plus tolérants en conditions d’hypoxie (pauvres en oxygène). La prédation des œufs et des nouveau-nés peut être très élevée. On pense que l’âge des individus à la maturité varie entre 4 à 10 ans chez les mâles et de 6 à 15 ans chez les femelles. La durée d’une génération est estimée à quelque 25 à 30 ans pour la population de la côte du Pacifique et à entre 30 et 40 ans pour la population intramontagnarde – des Rocheuses et la population des Prairies/boréale de l’Ouest – Bouclier canadien.
On ne dispose d’aucune estimation précise quant à la taille des trois populations. La population de la côte du Pacifique contient probablement quelque 3 000 adultes ou moins. La population intramontagnarde – des Rocheuses pourrait compter entre 5 000 et 10 000 adultes, tandis que la population des Prairies/boréale de l’Ouest – Bouclier canadien pourrait compter des dizaines de milliers d’adultes. Aucune de ces estimations n’est toutefois fondée sur des méthodes robustes. On peut inférer, d’après les pertes d’habitat, que la population de la côte du Pacifique a subi une baisse par rapport à ses niveaux historiques, mais le pourcentage de ce déclin est inconnu. Grâce à des activités de recherche, le nombre de localités connues a grandement augmenté au cours des dix dernières années. Il est probable que la population intramontagnarde – des Rocheuses ait aussi subi une baisse par rapport à ses niveaux historiques, particulièrement dans la vallée de l’Okanagan, d’après les tendances en matière d’habitat. On ignore quelles sont les tendances en matière de population au sein de la population des Prairies/boréale de l’Ouest – Bouclier canadien, mais des baisses d’effectif sont probables à l’échelle locale.
Les principales menaces qui pèsent sur la tortue peinte de l’Ouest sont la perte et l’altération de l’habitat, ainsi que la mortalité routière. La perte et l’altération de l’habitat découlent de diverses menaces, dont le développement résidentiel et industriel, les activités agricoles associées au drainage ou au remblayage des plans d’eau et le bétail en liberté qui dégrade les plans d’eau. Les tortues sont exposées à la menace de la mortalité routière durant leurs migrations saisonnières, lorsque les femelles se déplacent depuis les cours d’eau jusqu’à leurs aires de nidification en milieu terrestre, et lorsque les mâles et les femelles se dispersent. Parmi les autres menaces qui pèsent sur l’espèce, on compte les espèces envahissantes comme le ouaouaron, qui s’alimente des nouveau-nés dans les zones côtières, ainsi que des plantes qui réduisent la qualité des aires de nidification. Les activités récréatives peuvent aussi perturber les tortues qui s’exposent au soleil ou nidifient. De plus, la conduite de véhicules hors route risque de dégrader les étangs et l’habitat riverain adjacent ou endommager les sites de nidification. Le ruissellement d’eaux polluées peut aussi réduire la qualité de l’eau; parmi les sources de pollution, on compte le ruissellement provenant des fosses septiques agricoles et les polluants industriels. L’impact global des menaces pesant sur la population de la côte du Pacifique a été calculé comme étant « très élevé », celui des menaces pesant sur la population intramontagnarde – des Rocheuses a été calculé comme étant « élevé », et celui des menaces pesant sur la population des Prairies/boréale de l’Ouest – Bouclier canadien a été calculé comme étant « moyen ».
Le COSEPAC a évalué la tortue peinte de l’Ouest en 2006 en tenant compte de trois populations : population de la côte du Pacifique – en voie de disparition; population intramontagnarde – des Rocheuses – préoccupante; population des Prairies/boréale de l’Ouest – Bouclier canadien – non en péril. La population de la côte du Pacifique et la population intramontagnarde – des Rocheuses ont été inscrites à l’annexe 1 de la Loi sur les espèces en péril (LEP) selon leurs désignations respectives. Un plan de rétablissement provincial ciblant la population de la côte du Pacifique a été achevé en juin 2016. La délimitation de l’habitat essentiel a été ébauchée, mais cet habitat n’a pas encore été désigné aux termes de la LEP. Aucune mesure de protection précise n’a été adoptée pour la tortue peinte de l’Ouest. L’espèce bénéficie de certaines mesures de planification municipale conçues pour conserver les zones écosensibles et certains plans d’eau, mais ces mesures ont une portée et une application limitées.
Source : COSEPAC. 2016. Évaluation et Rapport de situation du COSEPAC sur la tortue peinte de l'Ouest (Chrysemys picta bellii), population intramontagnarde – des Rocheuses et population des Prairies / boréal de l’Ouest- Bouclier canadien au Canada. Comité sur la situation des espèces en péril au Canada. Ottawa. xxiii + 116 p.